РОДСТВЕННЫЕ ЗАЯВКИ
[01] Данная заявка испрашивает приоритет по предварительной заявке USSN 62/405184, поданной 6 октября 2016 года, содержание которой полностью включено в настоящее описание путем ссылки.
ВКЛЮЧЕНИЕ СПИСКА ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[02] Содержание текстового файла, поданного под названием «ΡΟΊΉ-011_001WO__SeqList.txt», который был создан 6 октября 2017 года и имеет размер 61 КБ, полностью включено в данное описание путем ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[03] Изобретение относится к области молекулярной биологии, и еще, в частности, к композициям, содержащим по меньшей мере одну последовательность, кодирующую индуцируемый белок каспазу, а также к способам его получения и применения.
УРОВЕНЬ ТЕХНИКИ
[04] В данной области техники давно существует неудовлетворенная потребность в способе селективной индукции апоптоза в генетически модифицированных клетках, и, в частности, когда эти модифицированные клетки предназначены для введения субъекту, как, например, в адаптивной клеточной терапии. Изобретение относится к решению этой давно назревшей, но нерешенной проблеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[05] Изобретение относится к индуцируемому проапоптотическому полипептиду, функционально связанному с областью связывания лиганда, которая может быть оптимизирована, чтобы связывать химический индуктор димеризации. Когда область связывания лиганда специфично связывается с индуцирующим агентом, проапоптотические молекулы-мишени сшиваются и, таким образом, активируются, селективно индуцируя апоптоз в клетке, содержащей индуцируемый проапоптотический полипептид по изобретению. Предпочтительные индуцируемые проапоптотические полипептиды по изобретению включают, но не ограничиваются ими, индуцируемые полипептиды каспаз. Предпочтительные индуцируемые полипептиды каспаз по изобретению включают в себя, но не ограничиваются ими, индуцируемые полипептиды каспазы 9. Предпочтительные индуцируемые полипептиды каспазы 9 по настоящему изобретению могут содержать усеченный полипептид каспазы 9, кодируемый усеченной или модифицированной нуклеотидной последовательностью.
[06] Индуцируемые проапоптотические полипептиды по изобретению превосходят существующие индуцируемые полипептиды, поскольку индуцируемые проапоптотические полипептиды по изобретению являются гораздо менее иммуногенными. В то время как индуцируемые проапоптотические полипептиды по изобретению представляют собой рекомбинантные полипептиды и, таким образом, не встречаются в природе, последовательности, которые рекомбинируют для получения индуцируемых проапоптотических полипептидов по изобретению, не содержат не принадлежащие человеку последовательности, которые иммунная система хозяина человека может распознать как «несобственные» и, таким образом, индуцировать иммунный ответ у субъекта, получающего индуцируемый проапоптотический полипептид по изобретению, клетку, содержащую индуцируемый проапоптотический полипептид, либо композицию, содержащую индуцируемый проапоптотический полипептид или клетку, содержащую индуцируемый проапоптотический полипептид. Хотя последовательность линкера представляет собой искусственную последовательность, последовательность линкера не содержит не принадлежащие человеку последовательности. Например, последовательность линкера не содержит сайт рестрикции.
[07] Изобретение относится к индуцируемому проапоптотическому полипептиду, содержащему (а) область связывания лиганда, (b) линкер и (с) проапоптотический полипептид, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения, не принадлежащая человеку последовательность содержит сайт рестрикции. В некоторых вариантах осуществления изобретения область связывания лиганда может представлять собой область связывания мультимерного лиганда.
[08] Изобретение относится к индуцируемому полипептиду каспазы, содержащему (а) область связывания лиганда, (b) линкер и (с) полипептид каспазы, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения, не принадлежащая человеку последовательность содержит сайт рестрикции. В некоторых вариантах осуществления изобретения область связывания лиганда может представлять собой область связывания мультимерного лиганда.
[09] Изобретение относится к индуцируемую полипептиду каспазы, содержащему (а) область связывания лиганда, (b) линкер и (с) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения, не принадлежащая человеку последовательность содержит сайт рестрикции. В некоторых вариантах осуществления изобретения область связывания лиганда может представлять собой область связывания мультимерного лиганда.
[010] В некоторых вариантах индуцируемого полипептида каспазы область связывания лиганда может специфично связываться с индуцирующим агентом и активировать транскрипцию проапоптотического полипептида (например, полипептида каспазы) по изобретению. Например, область связывания лиганда не будет связывать терапевтический агент. Индуцирующие агенты, специфично связывающиеся с областью связывания лиганда индуцируемых полипептидов по изобретению, напрямую не индуцируют транскрипцию эндогенных генов.
[011] Индуцируемые проапоптотические полипептиды по изобретению (например, каспазы) могут находиться под контролем одного или несколько транскрипционных регуляторных элементов, включая, но не ограничиваясь ими, промотор, способный инициировать транскрипцию полипептида каспазы в клетке, модифицированной таким образом, чтобы она содержала индуцируемый полипептид каспазы по изобретению. Например, индуцируемые полипептиды каспаз по изобретению могут находиться под контролем одного или нескольких транскрипционных регуляторных элементов, включая, но не ограничиваясь ими, промотор из клеток млекопитающих, способный инициировать транскрипцию полипептида каспазы в клетке млекопитающего, модифицированной таким образом, чтобы она содержала индуцируемый полипептид каспазы по изобретению. Например, индуцируемые полипептиды каспаз по изобретению могут находиться под контролем одного или несколько транскрипционных регуляторных элементов, включая, но не ограничиваясь ими, гетерологичный или экзогенный промотор, способный инициировать транскрипцию полипептида каспазы в клетке млекопитающего, модифицированной таким образом, чтобы она содержала индуцируемый полипептид каспазы по изобретению. Предпочтительные клетки млекопитающих включают, но не ограничиваются ими, клетки человека.
[012] Изобретение относится к индуцируемому полипептиду каспазы, содержащему (а) область связывания лиганда, (b) линкер и (с) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения область связывания лиганда может представлять собой область связывания мультимерного лиганда.
[013] В некоторых вариантах индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспаз или усеченных полипептидов каспазы 9 по изобретению, область связывания лиганда может содержать полипептид FK506-связывающего белка 12 (FKBP12). В некоторых вариантах осуществления аминокислотная последовательность области связывания лиганда, которая содержит полипептид FK506-связывающего белка 12 (FKBP 12), может включать в себя модификацию последовательности в положении 36. Модификация может представлять собой замену валином (V) фенилаланина (F) в положении 36 (F36V). В некоторых вариантах осуществления полипептид FKBP 12 имеет аминокислотную последовательность, содержащую
GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO: 3). В некоторых вариантах осуществления полипептид FKBP12 кодируется нуклеотидной последовательностью, содержащей
GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGATGTGGAACTGCTGAAGCTGGAG (SEQ ID NO: 4). В некоторых вариантах осуществления индуцирующий агент, специфичный к области связывания лиганда, которая может содержать полипептид FK506-связывающего белка 12 (FKBP12), имеющий замену фенилаланина (F) на валин (V) в положении 36 (F36V), содержит AP20187 и/или AP1903 (Римидуцид), оба являющиеся синтетическими препаратами.
[014] В некоторых вариантах индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспаз или усеченных полипептидов каспазы 9 по изобретению, линкерная область имеет аминокислотную последовательность, содержащую GGGGS (SEQ ID NO: 5), или кодируется нуклеотидной последовательностью, содержащей GGAGGAGGAGGATCC (SEQ ID NO: 6). В некоторых вариантах осуществления нуклеотидная последовательность, кодирующая линкер, не содержит сайт рестрикции.
[015] В некоторых вариантах усеченных полипептидов каспазы 9 по изобретению, усеченный полипептид каспазы 9 имеет аминокислотную последовательность, которая не содержит аргинин (R) в положении 87 последовательности. В альтернативном или в дополнительном случае, в некоторых вариантах индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспаз или усеченных полипептидов каспазы 9 по изобретению, усеченный полипептид каспазы 9 имеет аминокислотную последовательность, которая не содержит аланин (А) в положении 282 последовательности. В некоторых вариантах индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспаз или усеченных полипептидов каспазы 9 по изобретению, усеченный полипептид каспазы 9 имеет аминокислотную последовательность, содержащую
GFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO: 7), или кодируется нуклеотидной последовательностью, содержащей
TTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO: 8).
[016] В некоторых вариантах индуцируемых проапоптотических полипептидов, где полипептид содержит усеченный полипептид каспазы 9, индуцируемый проапоптотический полипептид имеет аминокислотную последовательность, содержащую GVQVETISPGDGRTFPKR GQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLEGGGGSGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO: 9) или кодируется нуклеотидной последовательностью, содержащей GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGATGTGGAACTGCTGAAGCTGGAGGGAGGAGGAGGATCCGGATTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO: 10).
[017] Изобретение относится к композиции, содержащей индуцируемый проапоптотический полипептид, индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению.
[018] Изобретение относится к транспозону, содержащему индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению.
[019] Изобретение относится к транспозону, содержащему индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах транспозонов по изобретению, транспозон дополнительно содержит последовательность, кодирующую терапевтический белок. В некоторых вариантах осуществления терапевтический белок является природным белком. В некоторых вариантах осуществления терапевтический белок представляет собой эндогенный белок. В некоторых вариантах осуществления терапевтический белок представляет собой экзогенный белок.
[020] Изобретение относится к транспозону, содержащему индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах транспозонов по изобретению транспозон дополнительно содержит последовательность, кодирующую терапевтический белок. В некоторых вариантах осуществления терапевтический белок не является природным белком. В некоторых вариантах осуществления терапевтический белок представляет собой эндогенный белок. В некоторых вариантах осуществления терапевтический белок представляет собой экзогенный белок. В некоторых вариантах осуществления терапевтический белок представляет собой синтетический белок. В некоторых вариантах осуществления терапевтический белок представляет собой химерный или рекомбинантный белок. В некоторых вариантах осуществления терапевтический белок представляет собой слитый белок. В некоторых вариантах осуществления терапевтический белок является белком человека, белком дикого типа или его вариантом по последовательности.
[021] Изобретение относится к транспозону, содержащему индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах транспозонов по изобретению транспозон дополнительно содержит последовательность, кодирующую терапевтический белок. В некоторых вариантах осуществления терапевтический белок содержит белок клеточной поверхности, мембранно-связанный белок, внеклеточный мембранно-связанный белок, внутриклеточный мембранно-связанный белок, внутриклеточный белок, локализованный в ядре белок, ядерный белок, цитоплазматический белок, цитозольный белок, секретируемый белок, лизосомальный белок, эндосомальный белок, везикуло-ассоциированный белок, митохондриальный белок, белок эндоплазматического ретикулума, белок цитоскелета, белок, участвующий во внутриклеточной передаче сигнала и/или белок, участвующий во внеклеточной передаче сигнала.
[022] Изобретение относится к транспозону, содержащему индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах транспозонов по изобретению транспозон дополнительно содержит последовательность, кодирующую терапевтический белок. В некоторых вариантах осуществления терапевтический белок содержит рецептор антигена. В некоторых вариантах осуществления рецептор антигена содержит Т-клеточный рецептор. В некоторых вариантах осуществления рецептор антигена содержит рецептор, выделенный или полученный из Т-клеточного рецептора. В некоторых вариантах осуществления рецептор антигена содержит одну или несколько вариаций и/или мутаций в последовательности по сравнению с Т-клеточным рецептором дикого типа. В некоторых вариантах осуществления изобретения Т-клеточный рецептор представляет собой рекомбинантный Т-клеточный рецептор.
[023] Изобретение относится к транспозону, содержащему индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах транспозонов по изобретению транспозон дополнительно содержит последовательность, кодирующую терапевтический белок. В некоторых вариантах осуществления изобретения рецептор антигена представляет собой химерный рецептор антигена (CAR). В некоторых вариантах осуществления CAR включает в себя одну или несколько последовательностей Центирина (Centyrin). В некоторых вариантах осуществления CAR представляет собой CARTyrin. В некоторых вариантах осуществления CAR содержит одну или несколько последовательностей VHH. В некоторых вариантах осуществления CAR представляет собой VCAR.
[024] В некоторых вариантах осуществления транспозон по изобретению может дополнительно содержать по меньшей мере один саморасщепляющийся пептид. В некоторых вариантах осуществления транспозон по изобретению может содержать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид расположен между индуцируемым проапоптотическим полипептидом, индуцируемым полипептидом каспазы, индуцируемый полипептидом каспазы 9 и/или индуцируемым усеченным полипептидом каспазы 9 по изобретению и другой последовательностью в транспозоне. В некоторых вариантах осуществления транспозон по изобретению может содержать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид расположен перед индуцируемым проапоптотическим полипептидом, индуцируемым полипептидом каспазы, индуцируемый полипептидом каспазы 9 и/или индуцируемым усеченным полипептидом каспазы 9 по изобретению, а второй саморасщепляющийся пептид расположен после индуцируемого проапоптотического полипептида, индуцируемого полипептида каспазы, индуцируемого полипептида каспазы 9 и/или индуцируемого усеченного полипептида каспазы 9 по изобретению. В некоторых вариантах осуществления транспозон по изобретению может содержать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид расположен прямо перед индуцируемым проапоптотическим полипептидом, индуцируемым полипептидом каспазы, индуцируемым полипептидом каспазы 9 и/или индуцируемым усеченным полипептидом каспазы 9 по изобретению, а второй саморасщепляющийся пептид расположен сразу после индуцируемого проапоптотического полипептида, индуцируемого полипептида каспазы, индуцируемого полипептида каспазы 9 и/или индуцируемого усеченного полипептида каспазы 9 по изобретению. По меньшей мере один саморасщепляющийся пептид может содержать пептид T2A, пептид GSG-Т2А, пептид Е2А, пептид GSG-Е2А, пептид F2A, пептид GSG-F2A, пептид P2A или пептид GSG-P2A. В некоторых вариантах осуществления пептид Т2А содержит аминокислотную последовательность, содержащую EGRGSLLTCGDVEENPGP (SEQ ID NO: 11). В некоторых вариантах осуществления пептид GSG-Т2А содержит аминокислотную последовательность, содержащую GSGEGRGSLLTCGDVEENPGP (SEQ ID NO: 12). В некоторых вариантах осуществления пептид Е2А содержит аминокислотную последовательность, содержащую QCTNYALLKLAGDVESNPGP (SEQ ID NO: 13). В некоторых вариантах осуществления пептид GSG-Е2А содержит аминокислотную последовательность, содержащую GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO: 14). В некоторых вариантах осуществления пептид F2A содержит аминокислотную последовательность, содержащую VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO: 15). В некоторых вариантах осуществления пептид GSG-F2A содержит аминокислотную последовательность, содержащую GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO: 16). В некоторых вариантах осуществления пептид P2A содержит аминокислотную последовательность, содержащую ATNFSLLKQAGDVEENPGP (SEQ ID NO: 17). В некоторых вариантах осуществления пептид GSG-P2A содержит аминокислотную последовательность, содержащую GSGATNFSLLKQAGDVEENPGP (SEQ ID NO: 18).
[025] Изобретение относится к композиции, содержащей транспозон по изобретению. В некоторых вариантах содержащей транспозон композиции она может дополнительно содержать плазмиду, содержащую последовательность, кодирующую фермент транспозазу. Последовательность, кодирующая фермент транспозазу, может представлять собой последовательностью мРНК. В некоторых вариантах осуществления транспозон представляет собой транспозон piggyBac. В некоторых вариантах осуществления транспозон представляет собой транспозон piggyBac, а транспозаза представляет собой транспозазу Super piggyBac.
[026] Транспозоны по изобретению могут содержать транспозоны piggyBac. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления транспозон представляет собой транспозон piggyBac. Транспозазы по изобретению могут включать транспозазы piggyBac или совместимые ферменты. В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозон является транспозоном piggyBac, транспозаза представляет собой транспозазу piggyBac™ или Super piggyBac™ (SPB). В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозаза представляет собой транспозазу Super piggyBac™ (SPB), последовательность, кодирующая транспозазу, представляет собой последовательность мРНК.
[027] В некоторых вариантах осуществления способов по изобретению, фермент транспозаза представляет собой транспозазу piggyBac™ (PB). Транспозаза piggyBac (PB) может содержать или состоять из аминокислотной последовательности по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичной:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF (SEQ ID NO: 1).
[028] В некоторых вариантах осуществления способов по изобретению, фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющей аминокислотную замену в одном или нескольких из положений 30, 165, 282 или 538 в последовательности:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF (SEQ ID NO: 1).
[029] В некоторых вариантах осуществления фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющей аминокислотные замены по двум или нескольким положениям 30, 165, 282 или 538 в последовательности SEQ ID NO: 1. В некоторых вариантах осуществления фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющий аминокислотные замены в трех или большим числе положений 30, 165, 282 или 538 в последовательности SEQ ID NO: 1. В некоторых вариантах осуществления фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющей аминокислотные замены в каждом из следующих положений 30, 165, 282 и 538 в последовательности SEQ ID NO: 1. В некоторых вариантах осуществления изобретения, аминокислотной заменой в положении 30 последовательности SEQ ID NO: 1 является замена валином (V) изолейцина (I). В некоторых вариантах осуществления аминокислотной заменой в положении 165 последовательности SEQ ID NO: 1 является замена серином (S) глицина (G). В некоторых вариантах осуществления аминокислотной заменой в положении 282 последовательности SEQ ID NO: 1 является замена валином (V) метионина (М). В некоторых вариантах осуществления аминокислотной заменой в положении 538 последовательности из SEQ ID NO: 1 является замена лизином (K) аспарагина (N).
[030] В некоторых вариантах осуществления способов по изобретению фермент транспозаза представляет собой транспозазу Super piggyBac™ (SPB). В некоторых вариантах осуществления транспозазы Super piggyBac™ (SPB) по изобретению могут содержать или состоять из аминокислотной последовательности, имеющей последовательность SEQ ID NO: 1, где аминокислотная замена в положении 30 представляет собой замену валином (V) изолейцина (I), аминокислотная замена в положении 165 представляет собой замену серином (S) глицина (G), аминокислотная замена в положении 282 представляет собой замену валином (V) метионина (М), а аминокислотная замена в положении 538 представляет собой замену лизином (K) аспарагина (N). В некоторых вариантах осуществления изобретения транспозаза Super piggyBac™ (SPB) может содержать или состоять из аминокислотной последовательности по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичной:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTV RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF (SEQ ID NO: 2).
[031] В некоторых вариантах осуществления способов по настоящему изобретению, включая те варианты осуществления, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac™ или Super piggyBac™ может дополнительно содержать аминокислотные замены в одном или нескольких положениях 3, 46, 82, 103, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 258, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 486, 503, 552, 570 и 591 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления, включая те варианты осуществления, в которых транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac™ или Super piggyBac™ может дополнительно содержать аминокислотные замены в одном или нескольких положениях 46, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 485, 503, 552 и 570. В некоторых вариантах осуществления аминокислотная замена в положении 3 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аспарагином (N) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену серином (S) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену треонином (Т) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 82 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену триптофаном (W) изолейцина (I). В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 119 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) аргинина (R). В некоторых вариантах осуществления аминокислотная замена в положении 125 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (А) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 125 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену гистидином (H) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином (V) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 185 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 187 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 200 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену триптофаном (W) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 207 из SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 209 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 226 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 235 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аргинином (R) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 240 в SEQ ID NO: 1 или SEQ ID NO: 1 представляет собой замену лизином (K) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 241 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 243 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) пролина (Р). В некоторых вариантах осуществления аминокислотная замена в положении 258 из SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену серином (S) аспарагина (N). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену триптофаном (W) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену тирозином (Y) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 298 из SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) метионина (М). В некоторых вариантах осуществления замена аминокислоты в положении 298 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (А) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO: 1 ИЛИ SEQ ID NO: 2 представляет собой замену валином (V) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) пролина (Р). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином пролина (P). В некоторых вариантах осуществления аминокислотная замена в положении 315 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) аргинина (R). В некоторых вариантах осуществления аминокислотная замена в положении 319 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) треонина (Т). В некоторых вариантах осуществления аминокислотная замена в положении 327 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аргинином (R) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 328 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином (V) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 421 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену гистидином (H) аспарагиновой кислоты (D). В некоторых вариантах осуществления аминокислотная замена в положении 436 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 456 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену тирозином (Y) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 470 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 485 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 552 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 570 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену треонином (Т) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) глутамина (Q). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аргинином (R) глутамина (Q).
В некоторых вариантах осуществления способов по изобретению, включая те, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, транспозаза piggyBac™ может содержать, или транспозаза Super piggyBac™ может дополнительно содержать аминокислотные замены в одном или нескольких из положений 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления способов по изобретению, включая те, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, транспозаза piggyBac™ может содержать, или транспозаза Super piggyBac™ может дополнительно содержать аминокислотную замену в двух, трех, четырех, пяти, шести или большем числе положений 103, 194, 372, 375, 450, 509 и 570 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления, включая те, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, транспозаза piggyBac™ может содержать, или транспозаза Super piggyBac™ может дополнительно содержать аминокислотную замену в положениях 103, 194, 372, 375, 450, 509 и 570 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (P) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 194 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином (V) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 372 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (A) аргинина (R). В некоторых вариантах осуществления аминокислотная замена в положении 375 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (A) лизина (K). В некоторых вариантах осуществления аминокислотная замена в положении 450 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аспарагином (N) аспарагиновой кислоты (D). В некоторых вариантах осуществления аминокислотная замена в положении 509 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 570 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену серином (S) аспарагина (N). В некоторых вариантах осуществления транспозаза piggyBac™ может содержать замену валином (V) метионина (M) в положении 194 SEQ ID NO: 1. В некоторых вариантах осуществления, включая те варианты осуществления, в которых транспозаза piggyBac™ может содержать замену валином (V) метионина (М) в положении 194 SEQ ID NO: 1, транспозаза piggyBac™ может дополнительно содержать аминокислотную замену в положениях 372, 375 и 450 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления транспозаза piggyBac™ может содержать замену валином (V) метионина (M) в положении 194 SEQ ID NO: 1, замену аланином (A) аргинина (R) в положении 372 SEQ ID NO: 1 и замену аланином (A) лизина (K) в положении 375 SEQ ID NO: 1. В некоторых вариантах осуществления транспозаза piggyBac™ может содержать замену валином (V) метионина (М) в положении 194 SEQ ID NO: 1, замену аланином (A) аргинина (R) в положении 372 SEQ ID NO: 1, замену аланином (A) лизина (K) в положении 375 SEQ ID NO: 1 и замену аспарагином (N) аспарагиновой кислоты (D) в положении 450 SEQ ID NO: 1.
[032] Изобретение относится к композиции, содержащей транспозон по изобретению. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления композиции, содержащей транспозон, она может дополнительно содержать плазмиду, содержащую последовательность, кодирующую фермент транспозазу. Последовательность, кодирующая транспозазу, может представлять собой последовательностью мРНК. В некоторых вариантах осуществления транспозон представляет собой транспозон Sleeping Beauty. В некоторых вариантах осуществления транспозон представляет собой транспозон Sleeping Beauty, а транспозаза представляет собой транспозазу Sleeping Beauty или гиперактивную транспозазу Sleeping Beauty (SB100X).
[033] Транспозоны по изобретению могут содержать транспозоны Sleeping Beauty. В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозон представляет собой транспозон Sleeping Beauty, композиция дополнительно содержит плазмиду, содержащую последовательность, кодирующую транспозазу. В некоторых вариантах осуществления последовательность, кодирующая транспозазу, представляет собой последовательность, кодирующую транспозазу Sleeping Beauty или гиперактивную транспозазу Sleeping Beauty (SB100X). В некоторых вариантах осуществления последовательность, кодирующая транспозазу, представляет собой последовательность мРНК.
[034] В некоторых вариантах осуществления способов по изобретению, транспозаза Sleeping Beauty содержит аминокислотную последовательность по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичную:
1 MGKSKEISQD LRKKIVDLHK SGSSLGAISK RLKVPRSSVQ TIVRKYKHHG TTQPSYRSGR
61 RRVLSPRDER TLVRKVQINP RTTAKDLVKM LEETGTKVSI STVKRVLYRH NLKGRSARKK
121 PLLQNRHKKA RLRFATAHGD KDRTFWRNVL WSDETKIELF GHNDHRYVWR KKGEACKPKN
181 TIPTVKHGGG SIMLWGCFAA GGTGALHKID GIMRKENYVD ILKQHLKTSV RKLKLGRKWV
241 FQMDNDPKHT SKVVAKWLKD NKVKVLEWPS QSPDLNPIEN LWAELKKRVR ARRPTNLTQL
301 HQLCQEEWAK IHPTYCGKLV EGYPKRLTQV KQFKGNATKY (SEQ ID NO: 19).
[035] В некоторых вариантах осуществления способов по изобретению гиперактивная транспозаза Sleeping Beauty (SB100X) содержит аминокислотную последовательность по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичную:
1 MGKSKEISQD LRKRIVDLHK SGSSLGAISK RLAVPRSSVQ TIVRKYKHHG TTQPSYRSGR
61 RRVLSPRDER TLVRKVQINP RTTAKDLVKM LEETGTKVSI STVKRVLYRH NLKGHSARKK
121 PLLQNRHKKA RLRFATAHGD KDRTFWRNVL WSDETKIELF GHNDHRYVWR KKGEACKPKN
181 TIPTVKHGGG SIMLWGCFAA GGTGALHKID GIMDAVQYVD ILKQHLKTSV RKLKLGRKWV
241 FQHDNDPKHT SKVVAKWLKD NKVKVLEWPS QSPDLNPIEN LWAELKKRVR ARRPTNLTQL
301 HQLCQEEWAK IHPNYCGKLV EGYPKRLTQV KQFKGNATKY (SEQ ID NO: 20).
[036] Изобретение относится к композиции, содержащей транспозон по изобретению. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления композиции, содержащей транспозон, она может дополнительно содержать плазмиду, содержащую последовательность, кодирующую фермент транспозазу. Последовательность, кодирующая транспозазу, может представлять собой последовательностью мРНК. В некоторых вариантах осуществления транспозон представляет собой транспозон Helraiser. В некоторых вариантах осуществления транспозон представляет собой транспозон Helraiser, а транспозаза представляет собой транспозазу Helitron.
[037] Транспозоны по изобретению могут содержать транспозоны Helraiser. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления транспозон представляет собой транспозон Helraiser. В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозон представляет собой транспозон Helraiser, композиция дополнительно содержит плазмиду, содержащую последовательность, кодирующую транспозазу. В некоторых вариантах осуществления последовательность, кодирующая транспозазу, представляет собой последовательность, кодирующую транспозазу Helitron. В некоторых вариантах осуществления последовательность, кодирующая транспозазу, представляет собой последовательность мРНК.
[038] В некоторых вариантах осуществления транспозаза представляет собой транспозазу Helitron. Транспозаза генома Helitron мобилизует транспозон Heiraiser, древний элемент из летучей мыши, который был активен примерно от 30 до 36 миллионов лет назад. Типовой транспозон Heiraiser по изобретению включает в себя Helibat1, который содержит нуклеотидную последовательность, содержащую:
1 TCCTATATAA TAAAAGAGAA ACATGCAAAT TGACCATCCC TCCGCTACGC TCAAGCCACG
61 CCCACCAGCC AATCAGAAGT GACTATGCAA ATTAACCCAA CAAAGATGGC AGTTAAATTT
121 GCATACGCAG GTGTCAAGCG CCCCAGGAGG CAACGGCGGC CGCGGGCTCC CAGGACCTTC
181 GCTGGCCCCG GGAGGCGAGG CCGGCCGCGC CTAGCCACAC CCGCGGGCTC CCGGGACCTT
241 CGCCAGCAGA GAGCAGAGCG GGAGAGCGGG CGGAGAGCGG GAGGTTTGGA GGACTTGGCA
301 GAGCAGGAGG CCGCTGGACA TAGAGCAGAG CGAGAGAGAG GGTGGCTTGG AGGGCGTGGC
361 TCCCTCTGTC ACCCCAGCTT CCTCATCACA GCTGTGGAAA CTGACAGCAG GGAGGAGGAA
421 GTCCCACCCC CACAGAATCA GCCAGAATCA GCCGTTGGTC AGACAGCTCT CAGCGGCCTG
481 ACAGCCAGGA CTCTCATTCA CCTGCATCTC AGACCGTGAC AGTAGAGAGG TGGGACTATG
541 TCTAAAGAAC AACTGTTGAT ACAACGTAGC TCTGCAGCCG AAAGATGCCG GCGTTATCGA
601 CAGAAAATGT CTGCAGAGCA ACGTGCGTCT GATCTTGAAA GAAGGCGGCG CCTGCAACAG
661 AATGTATCTG AAGAGCAGCT ACTGGAAAAA CGTCGCTCTG AAGCCGAAAA ACAGCGGCGT
721 CATCGACAGA AAATGTCTAA AGACCAACGT GCCTTTGAAG TTGAAAGAAG GCGGTGGCGA
781 CGACAGAATA TGTCTAGAGA ACAGTCATCA ACAAGTACTA CCAATACCGG TAGGAACTGC
841 CTTCTCAGCA AAAATGGAGT ACATGAGGAT GCAATTCTCG AACATAGTTG TGGTGGAATG
901 ACTGTTCGAT GTGAATTTTG CCTATCACTA AATTTCTCTG ATGAAAAACC ATCCGATGGG
961 AAATTTACTC GATGTTGTAG CAAAGGGAAA GTCTGTCCAA ATGATATACA TTTTCCAGAT
1021 TACCCGGCAT ATTTAAAAAG ATTAATGACA AACGAAGATT CTGACAGTAA AAATTTCATG
1081 GAAAATATTC GTTCCATAAA TAGTTCTTTT GCTTTTGCTT CCATGGGTGC AAATATTGCA
1141 TCGCCATCAG GATATGGGCC ATACTGTTTT AGAATACACG GACAAGTTTA TCACCGTACT
1201 GGAACTTTAC ATCCTTCGGA TGGTGTTTCT CGGAAGTTTG CTCAACTCTA TATTTTGGAT
1261 ACAGCCGAAG CTACAAGTAA AAGATTAGCA ATGCCAGAAA ACCAGGGCTG CTCAGAAAGA
1321 CTCATGATCA ACATCAACAA CCTCATGCAT GAAATAAATG AATTAACAAA ATCGTACAAG
1381 ATGCTACATG AGGTAGAAAA GGAAGCCCAA TCTGAAGCAG CAGCAAAAGG TATTGCTCCC
1441 ACAGAAGTAA CAATGGCGAT TAAATACGAT CGTAACAGTG ACCCAGGTAG ATATAATTCT
1501 CCCCGTGTAA CCGAGGTTGC TGTCATATTC AGAAACGAAG ATGGAGAACC TCCTTTTGAA
1561 AGGGACTTGC TCATTCATTG TAAACCAGAT CCCAATAATC CAAATGCCAC TAAAATGAAA
1621 CAAATCAGTA TCCTGTTTCC TACATTAGAT GCAATGACAT ATCCTATTCT TTTTCCACAT
1681 GGTGAAAAAG GCTGGGGAAC AGATATTGCA TTAAGACTCA GAGACAACAG TGTAATCGAC
1741 AATAATACTA GACAAAATGT AAGGACACGA GTCACACAAA TGCAGTATTA TGGATTTCAT
1801 CTCTCTGTGC GGGACACGTT CAATCCTATT TTAAATGCAG GAAAATTAAC TCAACAGTTT
1861 ATTGTGGATT CATATTCAAA AATGGAGGCC AATCGGATAA ATTTCATCAA AGCAAACCAA
1921 TCTAAGTTGA GAGTTGAAAA ATATAGTGGT TTGATGGATT ATCTCAAATC TAGATCTGAA
1981 AATGACAATG TGCCGATTGG TAAAATGATA ATACTTCCAT CATCTTTTGA GGGTAGTCCC
2041 AGAAATATGC AGCAGCGATA TCAGGATGCT ATGGCAATTG TAACGAAGTA TGGCAAGCCC
2101 GATTTATTCA TAACCATGAC ATGCAACCCC AAATGGGCAG ATATTACAAA CAATTTACAA
2161 CGCTGGCAAA AAGTTGAAAA CAGACCTGAC TTGGTAGCCA GAGTTTTTAA TATTAAGCTG
2221 AATGCTCTTT TAAATGATAT ATGTAAATTC CATTTATTTG GCAAAGTAAT AGCTAAAATT
2281 CATGTCATTG AATTTCAGAA ACGCGGACTG CCTCACGCTC ACATATTATT GATATTAGAT
2341 AGTGAGTCCA AATTACGTTC AGAAGATGAC ATTGACCGTA TAGTTAAGGC AGAAATTCCA
2401 GATGAAGACC AGTGTCCTCG ACTTTTTCAA ATTGTAAAAT CAAATATGGT ACATGGACCA
2461 TGTGGAATAC AAAATCCAAA TAGTCCATGT ATGGAAAATG GAAAATGTTC AAAGGGATAT
2521 CCAAAAGAAT TTCAAAATGC GACCATTGGA AATATTGATG GATATCCCAA ATACAAACGA
2581 AGATCTGGTA GCACCATGTC TATTGGAAAT AAAGTTGTCG ATAACACTTG GATTGTCCCT
2641 TATAACCCGT ATTTGTGCCT TAAATATAAC TGTCATATAA ATGTTGAAGT CTGTGCATCA
2701 ATTAAAAGTG TCAAATATTT ATTTAAATAC ATCTATAAAG GGCACGATTG TGCAAATATT
2761 CAAATTTCTG AAAAAAATAT TATCAATCAT GACGAAGTAC AGGACTTCAT TGACTCCAGG
2821 TATGTGAGCG CTCCTGAGGC TGTTTGGAGA CTTTTTGCAA TGCGAATGCA TGACCAATCT
2881 CATGCAATCA CAAGATTAGC TATTCATTTG CCAAATGATC AGAATTTGTA TTTTCATACC
2941 GATGATTTTG CTGAAGTTTT AGATAGGGCT AAAAGGCATA ACTCGACTTT GATGGCTTGG
3001 TTCTTATTGA ATAGAGAAGA TTCTGATGCA CGTAATTATT ATTATTGGGA GATTCCACAG
3061 CATTATGTGT TTAATAATTC TTTGTGGACA AAACGCCGAA AGGGTGGGAA TAAAGTATTA
3121 GGTAGACTGT TCACTGTGAG CTTTAGAGAA CCAGAACGAT ATTACCTTAG ACTTTTGCTT
3181 CTGCATGTAA AAGGTGCGAT AAGTTTTGAG GATCTGCGAA CTGTAGGAGG TGTAACTTAT
3241 GATACATTTC ATGAAGCTGC TAAACACCGA GGATTATTAC TTGATGACAC TATCTGGAAA
3301 GATACGATTG ACGATGCAAT CATCCTTAAT ATGCCCAAAC AACTACGGCA ACTTTTTGCA
3361 TATATATGTG TGTTTGGATG TCCTTCTGCT GCAGACAAAT TATGGGATGA GAATAAATCT
3421 CATTTTATTG AAGATTTCTG TTGGAAATTA CACCGAAGAG AAGGTGCCTG TGTGAACTGT
3481 GAAATGCATG CCCTTAACGA AATTCAGGAG GTATTCACAT TGCATGGAAT GAAATGTTCA
3541 CATTTCAAAC TTCCGGACTA TCCTTTATTA ATGAATGCAA ATACATGTGA TCAATTGTAC
3601 GAGCAACAAC AGGCAGAGGT TTTGATAAAT TCTCTGAATG ATGAACAGTT GGCAGCCTTT
3661 CAGACTATAA CTTCAGCCAT CGAAGATCAA ACTGTACACC CCAAATGCTT TTTCTTGGAT
3721 GGTCCAGGTG GTAGTGGAAA AACATATCTG TATAAAGTTT TAACACATTA TATTAGAGGT
3781 CGTGGTGGTA CTGTTTTACC CACAGCATCT ACAGGAATTG CTGCAAATTT ACTTCTTGGT
3841 GGAAGAACCT TTCATTCCCA ATATAAATTA CCAATTCCAT TAAATGAAAC TTCAATTTCT
3901 AGACTCGATA TAAAGAGTGA AGTTGCTAAA ACCATTAAAA AGGCCCAACT TCTCATTATT
3961 GATGAATGCA CCATGGCATC CAGTCATGCT ATAAACGCCA TAGATAGATT ACTAAGAGAA
4021 ATTATGAATT TGAATGTTGC ATTTGGTGGG AAAGTTCTCC TTCTCGGAGG GGATTTTCGA
4081 CAATGTCTCA GTATTGTACC ACATGCTATG CGATCGGCCA TAGTACAAAC GAGTTTAAAG
4141 TACTGTAATG TTTGGGGATG TTTCAGAAAG TTGTCTCTTA AAACAAATAT GAGATCAGAG
4201 GATTCTGCTT ATAGTGAATG GTTAGTAAAA CTTGGAGATG GCAAACTTGA TAGCAGTTTT
4261 CATTTAGGAA TGGATATTAT TGAAATCCCC CATGAAATGA TTTGTAACGG ATCTATTATT
4321 GAAGCTACCT TTGGAAATAG TATATCTATA GATAATATTA AAAATATATC TAAACGTGCA
4381 ATTCTTTGTC CAAAAAATGA GCATGTTCAA AAATTAAATG AAGAAATTTT GGATATACTT
4441 GATGGAGATT TTCACACATA TTTGAGTGAT GATTCCATTG ATTCAACAGA TGATGCTGAA
4501 AAGGAAAATT TTCCCATCGA ATTTCTTAAT AGTATTACTC CTTCGGGAAT GCCGTGTCAT
4561 AAATTAAAAT TGAAAGTGGG TGCAATCATC ATGCTATTGA GAAATCTTAA TAGTAAATGG
4621 GGTCTTTGTA ATGGTACTAG ATTTATTATC AAAAGATTAC GACCTAACAT TATCGAAGCT
4681 GAAGTATTAA CAGGATCTGC AGAGGGAGAG GTTGTTCTGA TTCCAAGAAT TGATTTGTCC
4741 CCATCTGACA CTGGCCTCCC ATTTAAATTA ATTCGAAGAC AGTTTCCCGT GATGCCAGCA
4801 TTTGCGATGA CTATTAATAA ATCACAAGGA CAAACTCTAG ACAGAGTAGG AATATTCCTA
4861 CCTGAACCCG TTTTCGCACA TGGTCAGTTA TATGTTGCTT TCTCTCGAGT TCGAAGAGCA
4921 TGTGACGTTA AAGTTAAAGT TGTAAATACT TCATCACAAG GGAAATTAGT CAAGCACTCT
4981 GAAAGTGTTT TTACTCTTAA TGTGGTATAC AGGGAGATAT TAGAATAAGT TTAATCACTT
5041 TATCAGTCAT TGTTTGCATC AATGTTGTTT TTATATCATG TTTTTGTTGT TTTTATATCA
5101 TGTCTTTGTT GTTGTTATAT CATGTTGTTA TTGTTTATTT ATTAATAAAT TTATGTATTA
5161 TTTTCATATA CATTTTACTC ATTTCCTTTC ATCTCTCACA CTTCTATTAT AGAGAAAGGG
5221 CAAATAGCAA TATTAAAATA TTTCCTCTAA TTAATTCCCT TTCAATGTGC ACGAATTTCG
5281 TGCACCGGGC CACTAG (SEQ ID NO: 21).
[039] В отличии от других транспозаз транспозаза Helitron не содержит РНКазаH-подобный каталитический домен, но вместо этого содержит мотив RepHel, состоящий домена инициатора репликации (Rep) и домена ДНК геликазы. Rep-домен является нуклеазным доменом суперсемейства нуклеаз HUH.
[040] Типовая транспозаза Helitron по изобретению включает в себя аминокислотную последовательность, содержащую:
1 MSKEQLLIQR SSAAERCRRY RQKMSAEQRA SDLERRRRLQ QNVSEEQLLE KRRSEAEKQR
61 RHRQKMSKDQ RAFEVERRRW RRQNMSREQS STSTTNTGRN CLLSKNGVHE DAILEHSCGG
121 MTVRCEFCLS LNFSDEKPSD GKFTRCCSKG KVCPNDIHFP DYPAYLKRLM TNEDSDSKNF
181 MENIRSINSS FAFASMGANI ASPSGYGPYC FRIHGQVYHR TGTLHPSDGV SRKFAQLYIL
241 DTAEATSKRL AMPENQGCSE RLMININNLM HEINELTKSY KMLHEVEKEA QSEAAAKGIA
301 PTEVTMAIKY DRNSDPGRYN SPRVTEVAVI FRNEDGEPPF ERDLLIHCKP DPNNPNATKM
361 KQISILFPTL DAMTYPILFP HGEKGWGTDI ALRLRDNSVI DNNTRQNVRT RVTQMQYYGF
421 HLSVRDTFNP ILNAGKLTQQ FIVDSYSKME ANRINFIKAN QSKLRVEKYS GLMDYLKSRS
481 ENDNVPIGKM IILPSSFEGS PRNMQQRYQD AMAIVTKYGK PDLFITMTCN PKWADITNNL
541 QRWQKVENRP DLVARVFNIK LNALLNDICK FHLFGKVIAK IHVIEFQKRG LPHAHILLIL
601 DSESKLRSED DIDRIVKAEI PDEDQCPRLF QIVKSNMVHG PCGIQNPNSP CMENGKCSKG
661 YPKEFQNATI GNIDGYPKYK RRSGSTMSIG NKVVDNTWIV PYNPYLCLKY NCHINVEVCA
721 SIKSVKYLFK YIYKGHDCAN IQISEKNIIN HDEVQDFIDS RYVSAPEAVW RLFAMRMHDQ
781 SHAITRLAIH LPNDQNLYFH TDDFAEVLDR AKRHNSTLMA WFLLNREDSD ARNYYYWEIP
841 QHYVFNNSLW TKRRKGGNKV LGRLFTVSFR EPERYYLRLL LLHVKGAISF EDLRTVGGVT
901 YDTFHEAAKH RGLLLDDTIW KDTIDDAIIL NMPKQLRQLF AYICVFGCPS AADKLWDENK
961 SHFIEDFCWK LHRREGACVN CEMHALNEIQ EVFTLHGMKC SHFKLPDYPL LMNANTCDQL
1021 YEQQQAEVLI NSLNDEQLAA FQTITSAIED QTVHPKCFFL DGPGGSGKTY LYKVLTHYIR
1081 GRGGTVLPTA STGIAANLLL GGRTFHSQYK LPIPLNETSI SRLDIKSEVA KTIKKAQLLI
1141 IDECTMASSH AINAIDRLLR EIMNLNVAFG GKVLLLGGDF RQCLSIVPHA MRSAIVQTSL
1201 KYCNVWGCFR KLSLKTNMRS EDSAYSEWLV KLGDGKLDSS FHLGMDIIEI PHEMICNGSI
1261 IEATFGNSIS IDNIKNISKR AILCPKNEHV QKLNEEILDI LDGDFHTYLS DDSIDSTDDA
1321 EKENFPIEFL NSITPSGMPC HKLKLKVGAI IMLLRNLNSK WGLCNGTRFI IKRLRPNIIE
1381 AEVLTGSAEG EVVLIPRIDL SPSDTGLPFK LIRRQFPVMP AFAMTINKSQ GQTLDRVGIF
1441 LPEPVFAHGQ LYVAFSRVRR ACDVKVKVVN TSSQGKLVKH SESVFTLNVV YREILE (SEQ ID NO: 22).
[041] При транспозициях Helitron шпилька ближе к 3'-концу транспозона функционирует как терминатор. Однако транспозаза может обойти эта шпильку, что приводит в результате к трансдукции фланкирующих последовательностей. Кроме того, при транспозиции Helraiser генерируются ковалентно замкнутые кольцевые промежуточные продукты. Кроме того, при транспозиции Helitron может отсутствовать удвоение (дупликация) сайта-мишени. В последовательности Helraiser, транспозаза фланкирована левой и правой концевыми (терминальными) последовательностями, называемыми LTS и RTS. Эти последовательности заканчиваются консервативным мотивом 5'-TC/CTAG-3'. Палиндромная последовательность длиной 19 п.о., которая способна образовать структуру терминирующей шпильки, находится на 11 нуклеотидов выше RTS и состоит из последовательности GTGCACGAATTTCGTGCACCGGGCCACTAG (SEQ ID NO: 23).
[042] Изобретение относится к композиции, содержащей транспозон по изобретению. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления композиции, содержащей транспозон, она может дополнительно содержать плазмиду, содержащую последовательность, кодирующую фермент транспозазу. Последовательность, кодирующая транспозазу, может представлять собой последовательностью мРНК. В некоторых вариантах осуществления транспозон представляет собой транспозон Tol2. В некоторых вариантах осуществления транспозон представляет собой транспозон Tol2, а транспозаза представляет собой транспозазу Tol2.
[043] Транспозоны по изобретению могут содержать транспозоны Tol2. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон Tol2. В некоторых вариантах осуществления и, в частности, в тех, где транспозон представляет собой транспозон Tol2, композиция дополнительно содержит плазмиду, содержащую последовательность, кодирующую фермент транспозазу. В некоторых вариантах осуществления последовательность, кодирующая транспозазу, содержит последовательность, кодирующую транспозазу Tol2. В некоторых вариантах осуществления последовательность, кодирующая транспозазу, представляет собой последовательность мРНК.
[044] Транспозоны Tol2 могут быть выделены или получены из генома оризии, и могут быть аналогичны транспозонам семейства hAT. Типичные транспозоны Tol2 по изобретению кодируются последовательностью, содержащей около 4,7 т.п.о., и содержат ген, кодирующий транспозазу Tol2, который содержит четыре экзона. Типичная транспозаза Tol2 по изобретению включает в себя аминокислотную последовательность, содержащую нижеследующую последовательность:
1 MEEVCDSSAA ASSTVQNQPQ DQEHPWPYLR EFFSLSGVNK DSFKMKCVLC LPLNKEISAF
61 KSSPSNLRKH IERMHPNYLK NYSKLTAQKR KIGTSTHASS SKQLKVDSVF PVKHVSPVTV
121 NKAILRYIIQ GLHPFSTVDL PSFKELISTL QPGISVITRP TLRSKIAEAA LIMKQKVTAA
181 MSEVEWIATT TDCWTARRKS FIGVTAHWIN PGSLERHSAA LACKRLMGSH TFEVLASAMN
241 DIHSEYEIRD KVVCTTTDSG SNFMKAFRVF GVENNDIETE ARRCESDDTD SEGCGEGSDG
301 VEFQDASRVL DQDDGFEFQL PKHQKCACHL LNLVSSVDAQ KALSNEHYKK LYRSVFGKCQ
361 ALWNKSSRSA LAAEAVESES RLQLLRPNQT RWNSTFMAVD RILQICKEAG EGALRNICTS
421 LEVPMFNPAE MLFLTEWANT MRPVAKVLDI LQAETNTQLG WLLPSVHQLS LKLQRLHHSL
481 RYCDPLVDAL QQGIQTRFKH MFEDPEIIAA AILLPKFRTS WTNDETIIKR GMDYIRVHLE
541 PLDHKKELAN SSSDDEDFFA SLKPTTHEAS KELDGYLACV SDTRESLLTF PAICSLSIKT
601 NTPLPASAAC ERLFSTAGLL FSPKRARLDT NNFENQLLLK LNLRFYNFE (SEQ ID NO: 24).
[045] Типичный транспозон Tol2 по изобретению, включая инвертированные повторы, субконцевые последовательности и транспозазу Tol2, кодируется нуклеотидной последовательностью, содержащей нижеследующую последовательность:
1 CAGAGGTGTA AAGTACTTGA GTAATTTTAC TTGATTACTG TACTTAAGTA TTATTTTTGG
61 GGATTTTTAC TTTACTTGAG TACAATTAAA AATCAATACT TTTACTTTTA CTTAATTACA
121 TTTTTTTAGA AAAAAAAGTA CTTTTTACTC CTTACAATTT TATTTACAGT CAAAAAGTAC
181 TTATTTTTTG GAGATCACTT CATTCTATTT TCCCTTGCTA TTACCAAACC AATTGAATTG
241 CGCTGATGCC CAGTTTAATT TAAATGTTAT TTATTCTGCC TATGAAAATC GTTTTCACAT
301 TATATGAAAT TGGTCAGACA TGTTCATTGG TCCTTTGGAA GTGACGTCAT GTCACATCTA
361 TTACCACAAT GCACAGCACC TTGACCTGGA AATTAGGGAA ATTATAACAG TCAATCAGTG
421 GAAGAAAATG GAGGAAGTAT GTGATTCATC AGCAGCTGCG AGCAGCACAG TCCAAAATCA
481 GCCACAGGAT CAAGAGCACC CGTGGCCGTA TCTTCGCGAA TTCTTTTCTT TAAGTGGTGT
541 AAATAAAGAT TCATTCAAGA TGAAATGTGT CCTCTGTCTC CCGCTTAATA AAGAAATATC
601 GGCCTTCAAA AGTTCGCCAT CAAACCTAAG GAAGCATATT GAGGTAAGTA CATTAAGTAT
661 TTTGTTTTAC TGATAGTTTT TTTTTTTTTT TTTTTTTTTT TTTTTGGGTG TGCATGTTTT
721 GACGTTGATG GCGCGCCTTT TATATGTGTA GTAGGCCTAT TTTCACTAAT GCATGCGATT
781 GACAATATAA GGCTCACGTA ATAAAATGCT AAAATGCATT TGTAATTGGT AACGTTAGGT
841 CCACGGGAAA TTTGGCGCCT ATTGCAGCTT TGAATAATCA TTATCATTCC GTGCTCTCAT
901 TGTGTTTGAA TTCATGCAAA ACACAAGAAA ACCAAGCGAG AAATTTTTTT CCAAACATGT
961 TGTATTGTCA AAACGGTAAC ACTTTACAAT GAGGTTGATT AGTTCATGTA TTAACTAACA
1021 TTAAATAACC ATGAGCAATA CATTTGTTAC TGTATCTGTT AATCTTTGTT AACGTTAGTT
1081 AATAGAAATA CAGATGTTCA TTGTTTGTTC ATGTTAGTTC ACAGTGCATT AACTAATGTT
1141 AACAAGATAT AAAGTATTAG TAAATGTTGA AATTAACATG TATACGTGCA GTTCATTATT
1201 AGTTCATGTT AACTAATGTA GTTAACTAAC GAACCTTATT GTAAAAGTGT TACCATCAAA
1261 ACTAATGTAA TGAAATCAAT TCACCCTGTC ATGTCAGCCT TACAGTCCTG TGTTTTTGTC
1321 AATATAATCA GAAATAAAAT TAATGTTTGA TTGTCACTAA ATGCTACTGT ATTTCTAAAA
1381 TCAACAAGTA TTTAACATTA TAAAGTGTGC AATTGGCTGC AAATGTCAGT TTTATTAAAG
1441 GGTTAGTTCA CCCAAAAATG AAAATAATGT CATTAATGAC TCGCCCTCAT GTCGTTCCAA
1501 GCCCGTAAGA CCTCCGTTCA TCTTCAGAAC ACAGTTTAAG ATATTTTAGA TTTAGTCCGA
1561 GAGCTTTCTG TGCCTCCATT GAGAATGTAT GTACGGTATA CTGTCCATGT CCAGAAAGGT
1621 AATAAAAACA TCAAAGTAGT CCATGTGACA TCAGTGGGTT AGTTAGAATT TTTTGAAGCA
1681 TCGAATACAT TTTGGTCCAA AAATAACAAA ACCTACGACT TTATTCGGCA TTGTATTCTC
1741 TTCCGGGTCT GTTGTCAATC CGCGTTCACG ACTTCGCAGT GACGCTACAA TGCTGAATAA
1801 AGTCGTAGGT TTTGTTATTT TTGGACCAAA ATGTATTTTC GATGCTTCAA ATAATTCTAC
1861 CTAACCCACT GATGTCACAT GGACTACTTT GATGTTTTTA TTACCTTTCT GGACATGGAC
1921 AGTATACCGT ACATACATTT TCAGTGGAGG GACAGAAAGC TCTCGGACTA AATCTAAAAT
1981 ATCTTAAACT GTGTTCCGAA GATGAACGGA GGTGTTACGG GCTTGGAACG ACATGAGGGT
2041 GAGTCATTAA TGACATCTTT TCATTTTTGG GTGAACTAAC CCTTTAATGC TGTAATCAGA
2101 GAGTGTATGT GTAATTGTTA CATTTATTGC ATACAATATA AATATTTATT TGTTGTTTTT
2161 ACAGAGAATG CACCCAAATT ACCTCAAAAA CTACTCTAAA TTGACAGCAC AGAAGAGAAA
2221 GATCGGGACC TCCACCCATG CTTCCAGCAG TAAGCAACTG AAAGTTGACT CAGTTTTCCC
2281 AGTCAAACAT GTGTCTCCAG TCACTGTGAA CAAAGCTATA TTAAGGTACA TCATTCAAGG
2341 ACTTCATCCT TTCAGCACTG TTGATCTGCC ATCATTTAAA GAGCTGATTA GTACACTGCA
2401 GCCTGGCATT TCTGTCATTA CAAGGCCTAC TTTACGCTCC AAGATAGCTG AAGCTGCTCT
2461 GATCATGAAA CAGAAAGTGA CTGCTGCCAT GAGTGAAGTT GAATGGATTG CAACCACAAC
2521 GGATTGTTGG ACTGCACGTA GAAAGTCATT CATTGGTGTA ACTGCTCACT GGATCAACCC
2581 TGGAAGTCTT GAAAGACATT CCGCTGCACT TGCCTGCAAA AGATTAATGG GCTCTCATAC
2641 TTTTGAGGTA CTGGCCAGTG CCATGAATGA TATCCACTCA GAGTATGAAA TACGTGACAA
2701 GGTTGTTTGC ACAACCACAG ACAGTGGTTC CAACTTTATG AAGGCTTTCA GAGTTTTTGG
2761 TGTGGAAAAC AATGATATCG AGACTGAGGC AAGAAGGTGT GAAAGTGATG ACACTGATTC
2821 TGAAGGCTGT GGTGAGGGAA GTGATGGTGT GGAATTCCAA GATGCCTCAC GAGTCCTGGA
2881 CCAAGACGAT GGCTTCGAAT TCCAGCTACC AAAACATCAA AAGTGTGCCT GTCACTTACT
2941 TAACCTAGTC TCAAGCGTTG ATGCCCAAAA AGCTCTCTCA AATGAACACT ACAAGAAACT
3001 CTACAGATCT GTCTTTGGCA AATGCCAAGC TTTATGGAAT AAAAGCAGCC GATCGGCTCT
3061 AGCAGCTGAA GCTGTTGAAT CAGAAAGCCG GCTTCAGCTT TTAAGGCCAA ACCAAACGCG
3121 GTGGAATTCA ACTTTTATGG CTGTTGACAG AATTCTTCAA ATTTGCAAAG AAGCAGGAGA
3181 AGGCGCACTT CGGAATATAT GCACCTCTCT TGAGGTTCCA ATGTAAGTGT TTTTCCCCTC
3241 TATCGATGTA AACAAATGTG GGTTGTTTTT GTTTAATACT CTTTGATTAT GCTGATTTCT
3301 CCTGTAGGTT TAATCCAGCA GAAATGCTGT TCTTGACAGA GTGGGCCAAC ACAATGCGTC
3361 CAGTTGCAAA AGTACTCGAC ATCTTGCAAG CGGAAACGAA TACACAGCTG GGGTGGCTGC
3421 TGCCTAGTGT CCATCAGTTA AGCTTGAAAC TTCAGCGACT CCACCATTCT CTCAGGTACT
3481 GTGACCCACT TGTGGATGCC CTACAACAAG GAATCCAAAC ACGATTCAAG CATATGTTTG
3541 AAGATCCTGA GATCATAGCA GCTGCCATCC TTCTCCCTAA ATTTCGGACC TCTTGGACAA
3601 ATGATGAAAC CATCATAAAA CGAGGTAAAT GAATGCAAGC AACATACACT TGACGAATTC
3661 TAATCTGGGC AACCTTTGAG CCATACCAAA ATTATTCTTT TATTTATTTA TTTTTGCACT
3721 TTTTAGGAAT GTTATATCCC ATCTTTGGCT GTGATCTCAA TATGAATATT GATGTAAAGT
3781 ATTCTTGCAG CAGGTTGTAG TTATCCCTCA GTGTTTCTTG AAACCAAACT CATATGTATC
3841 ATATGTGGTT TGGAAATGCA GTTAGATTTT ATGCTAAAAT AAGGGATTTG CATGATTTTA
3901 GATGTAGATG ACTGCACGTA AATGTAGTTA ATGACAAAAT CCATAAAATT TGTTCCCAGT
3961 CAGAAGCCCC TCAACCAAAC TTTTCTTTGT GTCTGCTCAC TGTGCTTGTA GGCATGGACT
4021 ACATCAGAGT GCATCTGGAG CCTTTGGACC ACAAGAAGGA ATTGGCCAAC AGTTCATCTG
4081 ATGATGAAGA TTTTTTCGCT TCTTTGAAAC CGACAACACA TGAAGCCAGC AAAGAGTTGG
4141 ATGGATATCT GGCCTGTGTT TCAGACACCA GGGAGTCTCT GCTCACGTTT CCTGCTATTT
4201 GCAGCCTCTC TATCAAGACT AATACACCTC TTCCCGCATC GGCTGCCTGT GAGAGGCTTT
4261 TCAGCACTGC AGGATTGCTT TTCAGCCCCA AAAGAGCTAG GCTTGACACT AACAATTTTG
4321 AGAATCAGCT TCTACTGAAG TTAAATCTGA GGTTTTACAA CTTTGAGTAG CGTGTACTGG
4381 CATTAGATTG TCTGTCTTAT AGTTTGATAA TTAAATACAA ACAGTTCTAA AGCAGGATAA
4441 AACCTTGTAT GCATTTCATT TAATGTTTTT TGAGATTAAA AGCTTAAACA AGAATCTCTA
4501 GTTTTCTTTC TTGCTTTTAC TTTTACTTCC TTAATACTCA AGTACAATTT TAATGGAGTA
4561 CTTTTTTACT TTTACTCAAG TAAGATTCTA GCCAGATACT TTTACTTTTA ATTGAGTAAA
4621 ATTTTCCCTA AGTACTTGTA CTTTCACTTG AGTAAAATTT TTGAGTACTT TTTACACCTC
4681 TG (SEQ ID NO: 25).
[046] Изобретение относится к вектору, содержащему индуцируемый проапоптотический полипептид, индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах осуществления вектор представляет собой вирусный вектор.
[047] Вирусные векторы по изобретению могут содержать последовательность, выделенную или полученную из ретровируса, лентивируса, аденовируса, адено-ассоциированного вируса (AAV) или любой их комбинации. В некоторых вариантах осуществления изобретения вирусный вектор содержит последовательность, выделенную или полученную из ретровируса. В некоторых вариантах осуществления ретровирус представляет собой гаммаретровирус. В некоторых вариантах осуществления ретровирус представляет собой лентивирус. В некоторых вариантах осуществления вирусные векторы по изобретению могут являться рекомбинантными векторами.
[048] Вирусные векторы по изобретению могут содержать последовательность, выделенную или полученную из аденоассоциированного вируса (AAV). В некоторых вариантах осуществления AAV содержит AAV с серотипом AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, АА8, AAV9, AAV10 или AAV11. В некоторых вариантах осуществления AAV содержит последовательность из одного или нескольких из AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10 или AAV11. В некоторых вариантах осуществления AAV содержит последовательность, выделенную, полученную или рекомбинированную из одного или нескольких из AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8, AAV9, AAV10 или AAV11. В некоторых вариантах осуществления настоящего изобретения AAV содержит последовательность, выделенную, полученную или рекомбинированную из AAV2. В некоторых вариантах осуществления изобретения, включая те, в которых вектор пересекает гематоэнцефалический барьер (ГЭБ), AAV содержит последовательность, выделенную, полученную или рекомбинированную из AAV9. Типовые адено-ассоциированные вирусы и рекомбинантные адено-ассоциированные вирусы по изобретению содержат, но не ограничиваются ими, самокомплементарный AAV (scAAV) и гибриды AAV, содержащие геном одного серотипа и капсид от другого серотипа (например, AAV2/5, AAV-DJ и ААВ-DJ8). Примеры адено-ассоциированных вирусов и рекомбинантных аденоассоциированных вирусов по изобретению включают в себя, но не ограничиваются ими, rAAV-LK03, rAAV-NP59 и rAAV-NP84. В некоторых вариантах осуществления AAV содержит последовательность, выделенную или полученную из rAAV-LK03, rAAV-NP59 или rAAV-NP84. В некоторых вариантах осуществления вирусные векторы по изобретению могут представлять собой рекомбинантные векторы.
[049] Изобретение относится к вектору, содержащему индуцируемый проапоптотический полипептид, индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9, и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. В некоторых вариантах осуществления настоящего изобретения вектор представляет собой вектор в виде наночастиц.
[050] Векторы в виде наночастиц по изобретению могут содержать нуклеиновую кислоту, аминокислоту, полимер, мицеллу, липид, органическую молекулу, неорганическую молекулу или любую их комбинацию. Наночастицы могут состоять из полимеров, раскрытых, например, в международной патентной публикации № WO 2012/094679, международной патентной публикации № WO 2016/022805, международной патентной публикации № WO/2011/133635, международной патентной публикации № WO/2016/090111, международной патентной публикации № WO/2017/004498, WO/2017/004509, международной патентной публикации PCT/US2017/030271, патенте США № 6835394, патенте США № 7217427 и патенте США № 7867512.
[051] Векторы в виде наночастиц по изобретению могут дополнительно содержать по меньшей мере один саморасщепляющийся пептид. В некоторых вариантах осуществления вектор в виде наночастицы по изобретению может содержать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид, расположен между индуцируемым проапоптотическим полипептидом, индуцируемым полипептидом каспазы, индуцируемый полипептидом каспазы 9 и/или индуцируемым усеченным полипептидом каспазы 9 по изобретению и другой последовательностью, связанной с наночастицами. В некоторых вариантах осуществления вектор в виде наночастицы по изобретению может содержать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид расположен перед индуцируемым проапоптотическим полипептидом, индуцируемым полипептидом каспазы, индуцируемым полипептидом каспазы 9 и/или индуцируемым усеченным полипептидом каспазы 9 по изобретению, а второй саморасщепляющийся пептид расположен после индуцируемого проапоптотического полипептида, индуцируемого полипептида каспазы, индуцируемого полипептида каспазы 9 и/или индуцируемого усеченного полипептида каспазы 9 по изобретению. По меньшей мере один саморасщепляющийся пептид может содержать пептид T2A, пептид GSG-Т2А, пептид Е2А, пептид GSG-Е2А, пептид F2A, пептид GSG-F2A, пептид P2A или пептид GSG-P2A. В некоторых вариантах осуществления пептид Т2А содержит аминокислотную последовательность, содержащую EGRGSLLTCGDVEENPGP (SEQ ID NO: 11). В некоторых вариантах осуществления пептид GSG-Т2А содержит аминокислотную последовательность, содержащую GSGEGRGSLLTCGDVEENPGP (SEQ ID NO: 12). В некоторых вариантах осуществления пептид Е2А содержит аминокислотную последовательность, содержащую QCTNYALLKLAGDVESNPGP (SEQ ID NO: 13). В некоторых вариантах осуществления пептид GSG-Е2А содержит аминокислотную последовательность, содержащую GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO: 14). В некоторых вариантах осуществления пептид F2A содержит аминокислотную последовательность, содержащую VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO: 15). В некоторых вариантах осуществления пептид GSG-F2A содержит аминокислотную последовательность, содержащую GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO: 16). В некоторых вариантах осуществления пептид P2A содержит аминокислотную последовательность, содержащую ATNFSLLKQAGDVEENPGP (SEQ ID NO: 17). В некоторых вариантах осуществления пептид GSG-P2A содержит аминокислотную последовательность, содержащую GSGATNFSLLKQAGDVEENPGP (SEQ ID NO: 18).
[052] Изобретение относится к композиции, содержащей вектор по изобретению.
[053] Изобретение относится к клетке, содержащей индуцируемый проапоптотический полипептид, индуцируемый полипептид каспазы, индуцируемый полипептид каспазы 9 и/или индуцируемый усеченный полипептид каспазы 9 по изобретению. Изобретение относится к клетке, содержащей транспозон по изобретению. Изобретение относится к клетке, содержащей вектор по изобретению. В некоторых вариантах осуществления клетка экспрессирует индуцируемую каспазу по изобретению после контакта с индуцирующим агентом.
[054] В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой клетки человека.
[055] В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой иммунные клетки. Примеры иммунных клеток включают в себя, но не ограничиваются ими, Т-клетки, естественные клетки-киллеры (NK), клетки, подобные естественным клеткам-киллерам (NK), предшественники гемопоэтических клеток, полученные из периферической крови (РВ) Т-клетки и полученные из пуповинной крови (UCB) Т-клетки. В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой Т-клетки. В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой активированные Т-клетки. В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой активированные Т-клетки, которые экспрессируют последовательность iC9 по изобретению. В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой искусственные антигенпредставляющие клетки (АРС). Иммунные клетки по изобретению могут дополнительно включать любую доступную в продаже клеточную линию или модифицированную клеточную линию, включая, но не ограничиваясь ими, клеточные линии дендритных клеток, В-клеток, макрофагов и моноцитов.
[056] В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой иммунные клетки. Примеры иммунных клеток включают в себя, но не ограничиваются ими, Т-клетки, естественные клетки-киллеры (NK), клетки, подобные естественным клеткам-киллерам (NK), предшественники гемопоэтических клеток, полученные из периферической крови (РВ) Т-клетки и полученные из пуповинной крови (UCB) Т-клетки. В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой Т-клетки. В некоторых вариантах осуществления клетка представляет собой искусственную антигенпредставляющую клетку.
[057] В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой стволовые клетки. Стволовые клетки по изобретению могут представлять собой стволовые клетки человека. Стволовые клетки по изобретению могут представлять собой эмбриональные стволовые клетки или стволовые клетки взрослого человека. Стволовые клетки по изобретению могут быть тотипотентными, плюрипотентными или мультипотентными. В некоторых вариантах осуществления стволовые клетки по изобретению могут представлять собой индуцированные стволовые клетки (iPSC).
[058] В некоторых вариантах осуществления клетки по изобретению, которые содержат полипептид, транспозон или вектор по изобретению, могут представлять собой соматические клетки. Соматические клетки по изобретению могут быть выделены или получены из любой части тела и, предпочтительно, тела человека, включая, но не ограничиваясь ими, сердце, скелетную или гладкую мускулатуру, кровеносный сосуд, вену или капилляр, селезенку, щитовидную железу, лимфатический узел или лимфатический сосуд, кость или костный мозг, кожу или эндотелий, надпочечник, пищевод, гортань, головной или спинной мозг, периферическую нервную систему, глаз, гипоталамус, печень, обонятельную ткань, предстательную железу, желудок, толстый или тонкий кишечник, легкое или бронхи, почку, поджелудочную железу, тимус, мочеточник или уретру, мочевой пузырь, слуховую ткань, мочевой пузырь, паращитовидную железу, слюнную железу или трахею человека. Соматические клетки по изобретению могут быть выделены или получены из клетки-предшественника или стволовой клетки, которые могут дифференцироваться в любую часть тела и, предпочтительно, тела человека, включая, но не ограничиваясь этим, сердце, скелетную или гладкую мускулатуру, кровеносный сосуд, вену или капилляр, селезенку, щитовидную железу, лимфатический узел или лимфатический сосуд,, кость или костный мозг, кожу или эндотелий, надпочечник, пищевод, гортань, головной или спинной мозг, периферическую нервную систему, глаз, гипоталамус, печень, обонятельную ткань, предстательную железу, желудок, толстый или тонкий кишечник, легкое или бронхи, почку, поджелудочную железу, тимус, мочеточник или уретру, мочевой пузырь, слуховую ткань, мочевой пузырь, паращитовидную железу, слюнную железу или трахею человека. Соматические клетки по изобретению могут быть выделены или получены из трансдифференцированных клеток.
[059] Изобретение относится к композиции, содержащей клетку по изобретению, содержащую полипептид, транспозон или вектор по изобретению.
[060] Изобретение относится к применению композиций по изобретению для адаптивной клеточной терапии. В некоторых вариантах осуществления клетка композиции может быть аутологичной. В некоторых вариантах осуществления клетка композиции может быть аллогенной.
[061] Изобретение относится к применению композиций по изобретению для генной терапии ex vivo. В некоторых вариантах осуществления клетка композиции может быть аутологичной. В некоторых вариантах осуществления клетка композиции может быть аллогенной.
[062] Изобретение относится к применению композиции, содержащей клетку по изобретению, для генной терапии ex vivo. В некоторых вариантах применения композиции, содержащей клетку по изобретению, клетка является аутологичной. В некоторых вариантах осуществления клетка является аллогенной.
[063] Изобретение относится к способу модификации клеточной терапии у субъекта, нуждающегося в этом, включающему введение субъекту композиции, содержащей клетку, содержащую терапевтический агент и индуцируемый полипептид каспазы по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом.
[064] Изобретение относится к способу модификации клеточной терапии у субъекта, нуждающегося в этом, включающему введение субъекту композиции, содержащей клетку, содержащую терапевтический агент и композицию по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом.
[065] Изобретение относится к способу модификации клеточной терапии у субъекта, нуждающегося в этом, включающему введение субъекту композиции, содержащей клетку, содержащую терапевтический агент, транспозон по изобретению и композицию, содержащую транспозазу по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом.
[066] Изобретение относится к способу модификации клеточной терапии у субъекта, нуждающегося в этом, включающему введение субъекту композиции, содержащей клетку, содержащую терапевтический агент и вектор по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом.
[067] В некоторых вариантах осуществления способов модификации клеточной терапии по изобретению, клетки композиции могут быть аутологичными. В некоторых вариантах осуществления клетки композиции могут быть аллогенными. В некоторых вариантах осуществления этого способа клеточная терапия представляет собой адаптивную клеточную терапию. В некоторых вариантах осуществления терапевтический агент вводится с помощью генной терапии ex vivo. В некоторых вариантах осуществления терапевтический агент представляет собой последовательность, кодирующую модифицированный эндогенный ген, экзогенный ген или его участок. В некоторых вариантах осуществления этого способа модификацией клеточной терапии является прекращение клеточной терапии. В некоторых вариантах осуществления этого способа модификацией клеточной терапии является деплеция части клеток, представленных в клеточной терапии. Эта деплеция может являться временной или может поддерживаться в течение определенного периода времени, например, в период ремиссии заболевания или расстройства. В некоторых вариантах осуществления способ дополнительно включает в себя стадию введения ингибитора индуцирующего агента для ингибирования модификации клеточной терапии, тем самым восстанавливая функцию и/или эффективность клеточной терапии. Например, если заболевание или расстройство рецидивирует после ремиссии, или у субъекта возникают побочные реакции, то клеточная терапия может быть возобновлена путем введения субъекту ингибитора индуцирующего агента.
[068] Способы модификации клеточной терапии по изобретению могут использоваться для прекращения или ослабления терапии в ответ, например, на признак восстановления или признак снижения тяжести/развития заболевания, признак ремиссии/подавления заболевания и/или возникновение побочных эффектов. Клеточная терапия по изобретению может быть возобновлена путем ингибирования индуцирующего агента при повторном появлении признака или симптома либо увеличения степени тяжести заболевания, и/или после устранения побочного эффекта.
[069] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 2×105-5×108 клеток на килограмм веса тела пациента на одно введение, или любой их диапазон, значение или часть.
[070] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,2×106-20×106 клеток на килограмм веса тела пациента на одно введение. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,2×106 клеток на килограмм веса тела пациента на одно введение, 2×106 клеток на килограмм веса тела пациента на одно введение, 20×106 клеток на килограмм веса тела пациента на одно введение, или любое количество клеток на килограмм веса тела пациента на одно введение в этом диапазоне.
[071] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 1×106 клеток или около 1×106 клеток на килограмм веса тела пациента на одно введение.
[072] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 3×106 клеток или около 3×106 клеток на килограмм веса тела пациента на одно введение.
[073] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,7×106-6,7×106 клеток на килограмм веса тела пациента на одно введение. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,7×106 клеток на килограмм веса тела пациента на одно введение, 6,7×106 клеток на килограмм веса тела пациента на одно введение или любое количество клеток на килограмм веса тела пациента на одно введение в этом диапазоне.
[074] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,7×106-16×106 клеток на килограмм веса тела пациента на одно введение. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,7×106 клеток на килограмм веса тела пациента на одно введение, 2×106 клеток на килограмм веса тела пациента на одно введение, 6×106 клеток на килограмм веса тела пациента на одно введение, 10,7×106 клеток на килограмм веса тела пациента на одно введение, 16×106 клеток на килограмм веса тела пациента на одно введение, или любое количество клеток на килограмм веса тела пациента на одно введение в этом диапазоне.
[075] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 1,2×106-7,1×106 клеток на килограмм веса тела пациента на одно введение. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 1,2×106 клеток на килограмм веса тела пациента на одно введение, 7,1×106 клеток на килограмм веса тела пациента на одно введение или любое количество клеток на килограмм веса тела пациента на одно введение в этом диапазоне. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 2×106-3×106 клеток на килограмм веса тела пациента на одно введение.
[076] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 1×106-2×106 клеток на килограмм веса тела пациента на одно введение. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 1×106 клеток на килограмм веса тела пациента на одно введение, 2×106 клеток на килограмм веса тела пациента на одно введение или любое количество клеток на килограмм веса тела пациента на одно введение в этом диапазоне. В некоторых вариантах осуществления модифицированные клетки по изобретению вводятся пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,7×106-1,3×106 клеток на килограмм веса тела пациента на одно введение. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит 0,7×106 клеток на килограмм веса тела пациента на одно введение, 1,3×106 клеток на килограмм веса тела пациента на одно введение или любое количество клеток на килограмм веса тела пациента на одно введение в этом диапазоне.
[077] В некоторых вариантах осуществления композицию, содержащую клетку по изобретению или модифицированную клетку по изобретению, вводят пациенту с помощью инъекции или внутривенной инфузии. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит одну или несколько доз. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит дробную дозу. В некоторых вариантах осуществления терапевтически эффективная доза композиции по изобретению или композиций, содержащих модифицированные клетки по изобретению, содержит начальную дозу и поддерживающую дозу.
[078] Изобретение относится к способу лечения заболевания или расстройства у субъекта, нуждающегося в этом, включающему в себя введение субъекту композиции, содержащей клетку, содержащую кинетический агент и индуцируемый полипептид каспазы по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом, и где клетка, содержащая кинетический агент, индуцирует местную тканевую токсичность в ткани-мишени субъекта; и селективную индукцию апоптоза в клетке, содержащей кинетический агент, до индукции токсичности в не являющейся мишенью ткани субъекта, в результате чего воздействие элиминирует ткань-мишень при сохранении не являющейся мишенью ткани, и осуществляется лечение заболевания или расстройства у субъекта.
[079] В данном описании термин кинетический агент предназначен для описания терапевтического агента, имеющего специфичность к ткани-мишени, и либо известную/преднамеренную, либо неизвестную/непреднамеренную токсичность в отношении не являющейся мишенью ткани, которая в любом случае может контролироваться или может быть ограничена таким образом, что токсичность не оказывает существенного влияния на не являющуюся мишенью ткань. Кинетические агенты специфично нацелены на ткань, специфично и местно вызывают токсичность, но до того, как кинетический агент может вызывать значительную токсичность или повреждение не являющейся мишенью ткани, может быть введен индуцирующий агент по изобретению, чтобы уменьшить или предотвратить токсичность не являющейся мишенью ткани. Степень, в которой любая токсичность затрагивает не являющиеся мишенью ткани (например, повреждение не являющихся мишенью тканей) может быть ограничена введением индуцирующего агента и может соответствовать продолжительности воздействия кинетического агента на не являющуюся мишенью ткань. В некоторых вариантах осуществления изобретения клетки, содержащие терапевтический агент, могут реагировать как на мишень на клетке-опухоли, так и на мишень на неопухолевых клетках, одновременно и в нескольких различных тканях. Несущие мишень неопухолевые клетки сохраняются за счет активации индуцируемого полипептида каспазы по изобретению в клетках, содержащих терапевтический агент, элиминирующий клетки, содержащие индуцируемые полипептиды каспаз по изобретению, например, после элиминации опухоли. В некоторых вариантах осуществления эффекты в отношении не являющихся опухолевыми и не несущих мишень клеток могут являться следствием перекрестной реактивности кинетического агента. В некоторых вариантах осуществления, если неспецифичные эффекты слишком велики, то токсичность кинетического агента может быть ограничена или устранена путем введения индуцирующего агента до завершения лечения заболевания у субъекта.
[080] Изобретение относится к способу лечения заболевания или расстройства у субъекта, нуждающегося в этом, включающему в себя введение субъекту композиции, содержащей клетку, содержащую кинетический агент и композицию по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом, и где клетка, содержащая кинетический агент, индуцирует местную тканевую токсичность в ткани-мишени субъекта; и селективную индукцию апоптоза в клетке, содержащей кинетический агент, до индукции значительной токсичности в не являющейся мишенью ткани субъекта, в результате чего воздействие элиминирует ткань-мишень при сохранении не являющейся мишенью ткани, и осуществляется лечение заболевания или расстройства у субъекта.
[081] Изобретение относится к способу лечения заболевания или расстройства у субъекта, нуждающегося в этом, включающему в себя введение субъекту композиции, содержащей клетку, содержащую кинетический агент, транспозон по изобретению и композиции, содержащей транспозазу по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом, и где клетка, содержащая кинетический агент, индуцирует местную тканевую токсичность в ткани-мишени субъекта; и селективную индукцию апоптоза в клетке, содержащей кинетический агент, до индукции значительной токсичности в не являющейся мишенью ткани субъекта, в результате чего воздействие элиминирует ткань-мишень при сохранении не являющейся мишенью ткани, и осуществляется лечение заболевания или расстройства у субъекта.
[082] Изобретение относится к способу лечения заболевания или расстройства у субъекта, нуждающегося в этом, включающему в себя введение субъекту композиции, содержащей клетку, содержащую кинетический агент и вектор по изобретению, где апоптоз может селективно индуцироваться в клетке путем контактирования клетки с индуцирующим агентом, и где клетка, содержащая кинетический агент, индуцирует местную тканевую токсичность в ткани-мишени субъекта; и селективную индукцию апоптоза в клетке, содержащей кинетический агент, до индукции значительной токсичности в не являющейся мишенью ткани субъекта, в результате чего воздействие элиминирует ткань-мишень при сохранении не являющейся мишенью ткани, и осуществляется лечение заболевания или расстройства у субъекта.
[083] Термином «значительная токсичность в не являющейся мишенью ткани» может быть описан уровень токсичности, при котором клетка ткани мертва (например, погибла в результате некроза или апоптоза), стала в ином случае нежизнеспособной, или перестала выполнять одну или несколько существенных физиологических функций. В некоторых вариантах осуществления значительная токсичность означает необратимое повреждение клетки или ткани. В некоторых вариантах осуществления значительная токсичность обозначает временную потерю функции клетки или ткани. В некоторых вариантах осуществления значительная токсичность вызывает симптомы у субъекта, которые распознаются, соответственно, специалистом в данной области. В некоторых вариантах осуществления значительная токсичность приводит к смерти, уменьшает продолжительность жизни или снижает качество жизни субъекта.
[084] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляет собой пролиферативное расстройство или рак. В некоторых вариантах осуществления ткань-мишень включает опухоль. В некоторых вариантах осуществления опухоль является доброкачественной. В некоторых вариантах осуществления опухоль является злокачественной. В некоторых вариантах осуществления ткань-мишень включает открытую ткань или границу резекции опухоли. В некоторых вариантах осуществления ткань-мишень содержит участок вероятного метастазирования. В некоторых вариантах осуществления участок метастазирования включает один или несколько лимфатических узлов, лимфатическую жидкость, периферическую циркулирующую кровь, локальную циркулирующую кровь, кость, костный мозг и спинномозговую жидкость (CSF).
[085] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой воспалительное заболевание или расстройство. В некоторых вариантах осуществления ткань-мишень включает участок воспаления.
[086] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой иммунное или аутоиммунное заболевание или расстройство. В некоторых вариантах осуществления ткань-мишень содержит участок открытой или инфицированной ткани. В некоторых вариантах осуществления ткань-мишень содержит обожженные или раненые ткани.
[087] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляет собой инфекционное заболевание или расстройство. В некоторых вариантах осуществления ткань-мишень включает инфицированную ткань.
[088] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой генетическое или эпигенетическое заболевание или расстройство. В некоторых вариантах осуществления ткань-мишень включает одну или несколько клеток, содержащих генетическую или эпигенетическую модификацию по сравнению с диким типом клеток.
[089] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляет собой метаболическое нарушение. В некоторых вариантах осуществления ткань-мишень включает одну или несколько клеток с метаболическим нарушением.
[090] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой сосудистые заболевания. В некоторых вариантах осуществления ткань-мишень включает одну или несколько клеток из вены, кровеносного сосуда, капилляра или компонента циркулирующей крови.
[091] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой заболевание дыхательных путей. В некоторых вариантах осуществления ткань-мишень включает одну или несколько клеток из носового прохода, пищевода или легкого.
[092] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой фиброзное заболевание. В некоторых вариантах осуществления ткань-мишень включает фиброидную массу или клетку в непосредственной близости от фиброидной массы.
[093] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, адаптивная клеточная терапия включает клетку, содержащую кинетический агент. В некоторых вариантах осуществления клетка, содержащая кинетический агент, является аутологичной. В некоторых вариантах осуществления клетка, содержащая кинетический агент, является аллогенной. В некоторых вариантах осуществления клетка, содержащая кинетический агент, представляет собой Т-клетку. В некоторых вариантах осуществления кинетический агент представляет собой неприродный рецептор. В некоторых вариантах осуществления изобретения неприродный рецептор представляет собой синтетический, модифицированный, рекомбинантный или химерный рецептор. В некоторых вариантах осуществления изобретения химерный рецептор представляет собой химерный рецептор антигена (CAR).
[094] В некоторых вариантах осуществления способов лечения заболевания или расстройства по изобретению, заболевание или расстройство представляют собой пролиферативное расстройство или рак. В некоторых вариантах осуществления ткань-мишень включает опухоль. В некоторых вариантах осуществления лечение опухоли включает композицию, содержащую клетку, содержащую индуцируемый полипептид каспазы по изобретению. В некоторых вариантах осуществления композиция, содержащая клетку, содержащую индуцируемый полипептид каспазы по изобретению, дополнительно содержит химерный рецептор антигена (CAR). В некоторых вариантах осуществления изобретения химерный рецептор антигена (CAR) специфично связывает последовательность, экспрессирующуюся на опухолевой клетке, тем самым обеспечивая специфичность CAR к опухолевой клетке. В некоторых вариантах осуществления клетка, экспрессирующая CAR, который специфично связывается с опухолевой клеткой, является Т-клеткой, то есть представляет собой CAR-T, которая специфично связывается с опухолевой клеткой. В некоторых вариантах осуществления композиции, содержащие CAR-Т-клетки, специфично направленные на опухолевые клетки-мишени, будут избирательно убивать только те опухолевые клетки, которые экспрессируют последовательность антигена. Однако в некоторых вариантах осуществления опухолевый антиген может экспрессироваться в других здоровых тканях, приводя к мишень-специфичной активности CAR-T-клеток в отношении здоровых клеток в не являющихся мишенью тканях. Например, антиген может представлять собой CD19, и CD19 экспрессируется практически исключительно на В-клетках. В случае CD19, неспецифичная активность анти-CD-19 CAR-Т-клеток является минимальной. Однако, если, например, антигеном является PSMA (фолатгидролаза 1), а PSMA экспрессируется в нескольких здоровых типах клеток, анти-PSMA CAR-Т-клетки могут связываться со здоровыми клетками вместе с патологическими клетками-мишенями, и эта активность называется специфичной токсичностью в отношении здоровых клеток. В некоторых вариантах осуществления, как только патологические клетки-мишени по изобретению (например, опухолевые клетки) уничтожаются с помощью анти-PSMA CAR-Т-клеток, лечение субъекта индуцирующим агентом по изобретению, чтобы вызвать программируемую гибель клеток у анти-PSMA CAR-Т-клетках с использованием индуцируемых полипептидов каспаз по изобретению, устраняет специфичную токсичность в отношении здоровых клеток.
[095] В некоторых способах по изобретению, включая те, в которых адаптивная клеточная терапия включает в себя клетку, содержащую кинетический агент, кинетический агент содержит противораковый агент. В некоторых вариантах осуществления изобретения противораковый агент содержит анти-CD-19 агент. В некоторых вариантах осуществления изобретения противораковый агент содержит анти-ВСМА агент. В некоторых вариантах осуществления изобретения противораковый агент содержит анти-PSMA агент. В некоторых вариантах осуществления изобретения противораковый агент содержит анти-Muc1 агент. В некоторых вариантах осуществления кинетический агент представляет собой неприродный рецептор. В некоторых вариантах осуществления изобретения неприродный рецептор представляет собой синтетический, модифицированный, рекомбинантный или химерный рецептор. В некоторых вариантах осуществления изобретения химерный рецептор представляет собой химерный рецептор антигена (CAR). В некоторых вариантах осуществления CAR содержит одну или несколько последовательностей VHH. В некоторых вариантах осуществления CAR представляет собой VCAR. В некоторых вариантах осуществления кинетический агент индуцирует аплазию. В некоторых вариантах осуществления аплазия не является фатальной. В некоторых вариантах осуществления индуцирующий агент устраняет клетку, содержащую кинетическую агент. В некоторых вариантах осуществления клетка представляет собой Т-клетку. В некоторых вариантах осуществления индуцирующий агент устраняет или уменьшает признак или симптом аплазии. В некоторых вариантах осуществления CAR-Т-терапия элиминирует злокачественное заболевание, но продолжает воздействовать на здоровые В-клетки, так что субъект должен быть получать инфузии IVIg. В некоторых вариантах осуществления анти-ВСМА CAR-Т-терапия элиминирует собственные немутированные плазматические клетки субъекта, так что субъект также должен получать лечение IVIg. В некоторых вариантах осуществления CAR-Т, вызывающие аплазию, могут быть элиминированы с помощью полипептидов каспазы 9 по изобретению и индуцирующего агента. В некоторых вариантах осуществления лечение субъекта индуцирующим агентом по изобретению устраняет признак или симптом аплазии.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[096] Фигура 1 представляет собой схематическую диаграмму, иллюстрирующую типовой индуцируемый усеченный полипептид каспазы 9 по изобретению.
[097] Фигура 2 представляет собой серию диаграмм, полученных методом проточной цитометрии, отображающих множество клеток, двигающихся из области расположения живых клеток (нижний правый квадрант) в область, где располагаются апоптотические клетки (верхний левый квадрант), как функцию увеличения дозы индуцирующего агента (AP1903, также называемого Римидуцидом), в клетках модифицированных для экспрессии терапевтического агента (CARTyrin) отдельно или в комбинации с индуцируемым полипептидом каспазы по изобретению (кодируемым конструкцией iC9 (также известной как «защитный выключатель»), введенным в клетки с помощью транспозазы piggyBac (PB)) на 12-й день после нуклеофекции.
[098] Фигура 3 представляет собой серию диаграмм, полученных методом проточной цитометрии, отображающих множество клеток, двигающихся из области расположения живых клеток (нижний правый квадрант) в область, где располагаются апоптотические клетки (верхний левый квадрант), как функцию увеличения дозы индуцирующего агента (AP1903, также называемого Римидуцидом), в клетках модифицированных для экспрессии терапевтического агента (CARTyrin) отдельно или в комбинации с индуцируемым полипептидом каспазы по изобретению (кодируемым конструкцией iC9 (также известной как «защитный выключатель»), введенным в клетки с помощью транспозазы piggyBac (PB)) на 19-й день после нуклеофекции.
[099] Фигура 4 представляет собой пару графиков, отображающих количественную оценку агрегации, показанную либо на фиг. 2 (левый график) или 3 (правый график). В частности, эти графики показывают влияние защитного выключателя iC9 на процент жизнеспособных клеток в зависимости от концентрации индуцирующего агента (AP1903, также называемого Римидуцидом) защитного выключателя iC9 для каждого модифицированного типа клеток либо на 12-й день (фиг.2 и левый график), либо на 19-й день (фиг.3 и правый график).
[0100] Фигура 5 представляет собой диаграмму, показывающую временной график исследования и план исследования in vivo. Мышам NSG вводили внутривенной инъекцией клетки MM.1S/люцифераза+, мышей разделяли на 8-й день, вводили Т-клетки на 9-й день, и вводили AP1903 (Римидуцид) на 12-й день в указанных дозах. Через 24 ч мышей умерщвляли, и клетки крови, селезенки и костного мозга собирали и окрашивали на присутствие клеток huCD45+.
[0101] Фигура 6 представляет собой график, демонстрирующий высокую эффективность элиминации клеток, содержащих P-ВСМА-101 с использованием Римидуцида (AP1903) in vivo. На фигуре 6 показано наличие клеток CARTyrin+ в крови, селезенки и костного мозга после воздействия A1903. Клетки крови, селезенки и костного мозга анализировали с помощью проточной цитометрии на присутствие клеток huCD45+. Относительную жизнеспособность определяли по следующей формуле: ((число клеток huCD45/число клеток msCD45)/(среднее huCD45/msCD45 в группе воздействия))*100% на 1500 событий для каждого образца. Каждая точка данных представляет собой индивидуальную мышь. На оси х отложена процентная относительная жизнеспособность CAR-T от 0 до 175 с шагом 25. На оси у, слева направо на каждой панели указаны данные для крови, селезенки и костного мозга после воздействия AP1903 (Римидуцида). Повышение концентрации AP1903 (Римидуцида) идет на панели слева направо в следующем порядке: 0 мг/кг, 0,005 мг/кг, 0,05 мг/кг, 0,5 мг/кг, 5 мг/кг и 5 мг/кг в отсутствии гена iC9.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0102] Изобретение относится к индуцируемым проапоптотическим полипептидам, а также к транспозонам, векторам и клеткам, содержащим индуцируемые проапоптотические полипептиды по изобретению. Индуцируемые проапоптотические полипептиды по изобретению могут быть введены в клетку одновременно или последовательно с терапевтическим агентом. Например, индуцируемые проапоптотические полипептиды по изобретению могут быть введены в клетку одновременно или последовательно с одним или несколькими последовательностями, которые кодируют химерный рецептор антигена для получения модифицированной клетки по изобретению. Модифицированные клетки по изобретению могут быть использованы в клеточной терапии. Для того, чтобы контролировать активность модифицированных клеток по изобретению, содержащих индуцируемый проапоптотический полипептид и, необязательно, терапевтический агент, клетка и/или индуцируемый проапоптотический полипептид могут контактировать с индуцирующим агентом, который специфично связывается с областью связывания лиганда в индуцируемом проапоптотическом полипептиде, что в итоге приводит к инициации апоптоза в клетке, содержащей индуцируемый проапоптотический полипептид. Когда модифицированные клетки по изобретению используются в качестве клеточной терапии, индуцирующий агент может быть введен локально или системно субъекту, который получал клеточную терапию. Ингибитор индуцирующего агента может быть введен локально или системно субъекту, который получил клеточную терапию и индуцирующий агент.
[0103] В данном описании термин «терапевтический агент» может относиться к любой молекуле, органической или неорганической, которая при введении в клетку, предназначенной для клеточной терапии, модифицирует активность, сигнальный путь, сигнал и/или взаимодействие этой клетки с внутренним или внешним окружением клетки, включая, но не ограничиваясь этим, соседние клетки, внеклеточные лиганды и сигнальные молекулы, иммунную систему хозяина клетки или ее компоненты, инфекцию хозяина, больную клетку (например, раковую клетку) хозяина, внутриклеточные лиганды и сигнальные молекулы, эпигенетическую регуляцию, транскрипцию генов, регуляцию генов, транскриптом, трансляцию ДНК/РНК, белковый процессинг или секреторные процессы, и протеом. Терапевтические агенты включают, но не ограничиваются ими, рекомбинантные и/или химерные рецепторы клеточной поверхности, рекомбинантные и/или химерные трансмембранные рецепторы, рекомбинантные и/или химерные ионные каналы и рекомбинантные и/или химерные рецепторы антигенов. В некоторых вариантах осуществления терапевтический агент представляет собой химерный рецептор антигена (CAR) и, необязательно, химерный рецептор антигена, в котором область распознавания антигена содержит по меньшей мере один центирин (Centyrin). В данном описании CAR, содержащий центирин, называется CARTyrin.
[0104] Изобретение относится к индуцируемым проапоптотическим полипептидам, содержащим область связывания лиганда, линкер и проапоптотический пептид, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения, не принадлежащая человеку последовательность содержит сайт рестрикции. Индуцируемые проапоптотические полипептиды по изобретению димеризуются посредством взаимодействия с индуцирующим агентом. Димеризация первого индуцируемого проапоптотического полипептида и второго индуцируемого проапоптотического полипептид облегчает или активизирует взаимодействие, сшивку, перекрестную активацию или активацию полипептидов каспаз. Взаимодействие, сшивка, перекрестная активация или активация полипептидов каспаз инициирует апоптоз в клетке, содержащей индуцируемые проапоптотические полипептиды по изобретению или последовательности, кодирующей индуцируемые проапоптотические полипептиды по изобретению. Индуцируемые проапоптотические полипептиды по изобретению не инициируют апоптоз за исключением того случая, когда индуцируемый проапоптотический полипептид по изобретению контактирует с индуцирующим агентом. Контакт между индуцирующим агентом и индуцируемыми проапоптотическими полипептидами по изобретению может осуществляться in vivo, ex vivo или in vitro. Контакт между индуцирующим агентом и индуцируемыми проапоптотическими полипептидами по изобретению может осуществляться внутри клетки.
[0105] Для клеточной терапии в изобретении предложены модифицированные Т-клетки для адаптивной клеточной терапии, содержащие индуцируемый проапоптотический полипептид или последовательность, кодирующую индуцируемый проапоптотический полипептид по изобретению.
[0106] Модифицированные Т-клетки для адаптивной клеточной терапии могут быть аутологичными или аллогенными. Термин «аллогенная», используемый в данном описании, относится к локусам HLA или MHC, которые антигенно отличаются. Клетки или ткани, передаваемые из одного вида, могут отличаться по антигенным свойствам. Сингенные мыши могут отличаться по одному или нескольким локусам (конгенные), и аллогенные мыши могут иметь одно происхождение.
[0107] Модифицированные Т-клетки для адаптивной клеточной терапии, могут включать активированные Т-клетки. Т-клетки (называемые также Т-лимфоцитами) принадлежат к группе белых кровяных клеток, называемых лимфоцитами. Лимфоциты как правило участвуют в клеточно-опосредованном иммунитете. «Т» в «Т-клетках» относится к клеткам, полученным из тимуса, или чье созревание прошло в тимусе. T-клетки можно отличить от других типов лимфоцитов, таких как В-клетки и природные киллеры (NK), по присутствию белков клеточной поверхности, известных как Т-клеточные рецепторы. Термин «активированные Т-клетки», используемый в данном описании, относится к Т-клеткам, которые были стимулированы для получения иммунного ответа (например, клональной экспансии активированных Т-клеток) путем распознавания антигенной детерминанты, представленной в контексте маркера главного комплекса гистосовместимости (MHC) II класса. Т-клетки активируются в присутствии антигенной детерминанты, цитокинов и/или лимфокинов и белков клеточной поверхности кластера дифференцировки (например, CD3, CD4, CD8 и т.п., и их комбинации). Клетки, которые экспрессируют белок кластера дифференцировки, часто называются «положительными» по экспрессии этого белка на поверхности Т-клеток (например, клетки, положительные по экспрессии CD3 или CD4 указываются как CD3+ или CD4+). Белки CD3 и CD4 являются рецепторами на клеточной поверхности или корецепторами, которые могут прямо и/или косвенно участвовать в передаче сигнала в Т-клетках.
[0108] Модифицированные Т-клетки для адаптивной клеточной терапии могут включать в себя «пан-Т-клетки». В контексте изобретения пан-Т-клетки включают в себя все Т-лимфоциты, выделенные из биологического образца, без разделения по подтипу, состоянию активации, состоянию созревания или экспрессии маркеров клеточной поверхности.
[0109] Модифицированные Т-клетки для адаптивной клеточной терапии могут быть выделены и/или получены из, например, цельной крови, периферической крови, пуповинной крови, лимфатической жидкости, ткани лимфатических узлов, костного мозга и спинномозговой жидкости (CSF). Под «выделены и/или получены», например, в случае клеток подразумевается, что клетки или культуру клеток выделяют, очищают или частично очищают из источника, где источник может представлять собой, например, пуповинную кровь, костный мозг или периферическую кровь. Термины могут также применяться в случае, когда исходный источник или клеточная культура культивировались, и клетки реплицировались, и где из первоначального источника теперь получено потомство клеток. Термин «периферическая кровь», используемый в данном описании, относится к клеточным компонентам крови (например, эритроцитам, лейкоцитам и тромбоцитам), которые выделены или получены из циркулирующего пула крови и не находятся в пределах лимфатической системы, селезенки, печени или костного мозга. Пуповинная кровь отличается от периферической крови и крови, находящейся в пределах лимфатической системы, селезенки, печени или костного мозга. Термины «кровь из пуповины» или «пуповинная кровь», которые могут использоваться взаимозаменяемо, относятся к крови, которая остается в плаценте и в присоединенной пуповине после рождения ребенка. Пуповинная кровь часто содержит стволовые клетки, включая кроветворные клетки.
[0110] Изобретение относится к индуцируемым проапоптотическим полипептидам, содержащим область связывания лиганда, линкер и проапоптотический пептид, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения, не принадлежащая человеку последовательность содержит сайт рестрикции. В некоторых вариантах осуществления проапоптотический пептид представляет собой полипептид каспазы. В некоторых вариантах осуществления полипептид каспазы представляет собой полипептид каспазы 9. В некоторых вариантах осуществления полипептид каспазы 9 представляет собой усеченный полипептид каспазы 9. Индуцируемые проапоптотические полипептиды по изобретению могут быть неприродными.
[0111] Полипептиды каспаз по изобретению включают в себя, но не ограничиваются ими, каспазу 1, каспазу 2, каспазу 3, каспазу 4, каспазу 5, каспазу 6, каспазу 7, каспазу 8, каспазу 9, каспазу 10, каспазу 11, каспазы 12 и 14. Полипептиды каспаз по изобретению включают в себя, но не ограничиваются ими, полипептиды каспаз, ассоциированные с апоптозом, включая каспазу 2, каспазу 3, каспазу 6, каспазу 7, каспазу 8, каспазу 9 и каспазу 10. Полипептиды каспаз по изобретению включают в себя, но не ограничиваются ими, полипептиды каспаз, которые инициируют апоптоз, включая каспазу 2, каспазу 8, каспазу 9 и каспазу 10. Полипептиды каспаз по изобретению включают в себя, но не ограничиваются ими, полипептиды каспаз, которые осуществляют апоптоз, включая каспазу 3, каспазу 6 и каспазу 7.
[0112] Полипептиды каспаз по изобретению могут иметь аминокислотную последовательность или могут кодироваться нуклеотидной последовательностью, которые имеют одну или несколько модификаций по сравнению с аминокислотной или нуклеотидной последовательностью дикого типа. Нуклеотидная последовательность, кодирующая полипептид каспазы по изобретению, может быть оптимизирована по кодонам. Одна или несколько модификаций аминокислотной и/или нуклеотидной последовательности полипептида каспазы по изобретению могут повысить взаимодействие, сшивку, перекрестную активацию или активацию полипептида каспазы по изобретению по сравнению с аминокислотной и/или нуклеотидной последовательностью дикого типа. В качестве альтернативного или дополнительного варианта, одна или несколько модификаций аминокислотной и/или нуклеотидной последовательности полипептида каспазы по изобретению могут уменьшить иммуногенность полипептида каспазы по изобретению по сравнению с аминокислотной и/или нуклеотидной последовательностью дикого типа.
[0113] Полипептиды каспаз по изобретению могут быть укорочены по сравнению с полипептидами каспаз дикого типа. Например, полипептид каспазы может быть укорочен, чтобы исключить последовательность, кодирующую домен активации и рекрутинга каспаз (CARD), чтобы устранить или свести к минимуму возможность активации местного воспалительного ответа в дополнение к инициации апоптоза в клетке, содержащей индуцируемый полипептид каспазы по изобретению. Нуклеотидная последовательность, кодирующая полипептид каспазы по изобретению, может сплайсироваться с образованием варианта аминокислотной последовательности полипептида каспазы по изобретению по сравнению с полипептидом каспазы дикого типа. Полипептиды каспаз по изобретению могут кодироваться рекомбинантными и/или химерными последовательностями. Рекомбинантные и/или химерные полипептиды каспаз по изобретению могут включать в себя последовательность из одного или нескольких различных полипептидов каспаз. В качестве альтернативного или дополнительного варианта, рекомбинантные и/или химерные полипептиды каспаз по изобретению могут включать в себя последовательность из одного или нескольких биологических видов (например, последовательность, принадлежащая человеку, и не принадлежащая человеку последовательность). Полипептиды каспаз по изобретению могут быть неприродными.
[0114] Область связывания лиганда индуцируемого проапоптотического полипептида по изобретению может включать в себя любую полипептидную последовательность, которая облегчает или способствует димеризации первого индуцируемого проапоптотического полипептида по изобретению со вторым индуцируемым проапоптотическим полипептидом по изобретению, димеризация которых активирует или индуцирует сшивание проапоптотических полипептидов и инициацию апоптоза в клетке.
[0115] Область связывания лиганда («димеризации») может содержать любой полипептид или его функциональный домен, который позволяет индукцию с использованием природного или неприродного лиганда (т.е. индуцирующего агента), например, неприродного синтетического лиганда. Область связывания лиганда может являться внутренней или внешней по отношению к клеточной мембране в зависимости от природы индуцируемого проапоптотического полипептида и выбора лиганда (т.е. индуцирующего агента). Известны множество лиганд-связывающих полипептидов и функциональных доменов, включая рецепторы. Области связывания лиганда по изобретению могут включать в себя одну или несколько последовательностей из рецептора. Особый интерес представляют собой области связывания лиганда, для которых известны или могут быть легко получены лиганды (например, небольшие органические лиганды). Эти лиганд-связывающие области или рецепторы могут включать в себя, но не ограничиваются ими, рецепторы FKBP и циклофилина, стероидные рецепторы, рецептор тетрациклина и т.п., а также «неприродные» рецепторы, которые могут быть получены из антител, в частности, из их тяжелой или легкой цепи, их мутированный последовательности, случайной последовательности аминокислот, полученной с помощью стохастических процедур, комбинаторных синтезов и т.п. В некоторых вариантах осуществления область связывания лиганда выбрана из группы, состоящей из лиганд-связывающей области FKBP, лиганд-связывающей области рецептора циклофилина, лиганд-связывающей области стероидного рецептора, лиганд-связывающей области циклофилиновых рецепторов и лиганд-связывающей области тетрациклинового рецептора.
[0116] Область связывания лиганда, содержащая один или несколько доменов рецептора, может иметь по меньшей мере примерно 50 аминокислот и менее примерно 350 аминокислот, обычно менее 200 аминокислот, либо в виде природного домена, либо в виде усеченного его активного участка. Область связывания может, например, являться небольшой (<25 кДа, чтобы обеспечить эффективную трансфекцию в вирусных векторах), мономерной, неиммуногенной, может иметь легко синтезируемые искусственно, клеточнопроницаемые, нетоксичные лиганды, которые могут быть сконфигурированы для димеризации.
[0117] Лиганд-связывающие области, содержащие один или несколько доменов рецептора (рецепторов) могут быть внутриклеточными или внеклеточными в зависимости от конструкции индуцируемого проапоптотического полипептида и от доступности соответствующего лиганда (т.е. индуцирующего агента). Для гидрофобных лигандов область связывания может находиться по обе стороны мембраны, но для гидрофильных лигандов, в частности белковых лигандов, область связывания обычно будет находиться на внешней стороне клеточной мембраны, если нет транспортной системы для интернализации лиганда в том виде, в котором он доступен для связывания. Для внутриклеточного рецептора индуцируемый проапоптотический полипептид или транспозон или вектор, содержащий индуцируемый проапоптотический полипептид, могут содержать сигнальный пептид и трансмембранный домен в 5'- или 3'-положении от последовательности рецепторного домена, или может иметь липидную присоединенную сигнальную последовательность в 5'-положении от последовательности рецепторного домена. Если рецепторный домен находится между сигнальным пептидом и трансмембранным доменом, то рецепторный домен будет внеклеточным.
[0118] Антитело и субъединицы антител, например, тяжелая или легкая цепь, в частности, фрагменты, в частности, вся или часть вариабельной области, или слитые тяжелая и легкая цепи, могут быть использованы в качестве области связывания лиганда по изобретению для создания высокоаффинного связывания. Рассматриваемые антитела включают антитела, направленные на эктопически экспрессируемый продукт у человека, например, внеклеточный домен, который не будет инициировать иммунный ответ, и в общем не экспрессируется на периферии (то есть, за пределами области ЦНС/мозга). Такие примеры включают, но не ограничиваются этим, низкоаффинный рецептор фактора роста нервов (LNGFR) и эмбриональные поверхностные белки (то есть, карциноэмбриональный антиген). Однако, кроме этого, могут быть получены антитела против гаптеновых молекул, которые являются физиологически приемлемыми, а отдельные субъединицы антител скринированы на аффинность связывания. кДНК, кодирующая субъединицы, может быть выделена и модифицирована путем делеции константной области, участков вариабельной области, мутагенеза вариабельной области и т.п., чтобы получить связывающий домен, который имеет соответствующее сродство к лиганду. Таким образом, почти любое физиологически приемлемое гаптеновое соединение может быть использовано в качестве лиганда или дать эпитоп для лиганда. Вместо элементов антител могут быть использованы природные рецепторы, для которых известны область связывания или домен, и существует подходящий или известный лиганд для связывания.
[0119] Для мультимеризации рецептора, лиганд для области связывания лиганда/рецепторных доменов индуцируемых проапоптотических полипептидов может являться мультимерным в том смысле, что лиганд может иметь по меньшей мере два участка связывания, причем каждый из участков связывания способен связываться с областью связывания лиганда (т.е. лиганд имеет первый участок связывания, способный связывать область связывания лиганда первого индуцируемого проапоптотического полипептида, и второй участок связывания, способный связывать область связывания лиганда второго индуцируемого проапоптотического полипептида, где области связывания лиганда первого и второго индуцируемых проапоптотических полипептидов являются либо идентичными, или различными). Таким образом, используемый в данном описании термин «область связывания мультимерного лиганда» относится к области связывания лиганда индуцируемого проапоптотического полипептида по изобретению, которая связывается с мультимерным лигандом. Мультимерные лиганды по изобретению включают димерные лиганды. Димерный лиганд по изобретению может иметь два сайта связывания, способных связываться с доменом рецептора лиганда. В некоторых вариантах осуществления мультимерные лиганды по изобретению представляют собой димер или олигомер более высокого порядка (обычно не выше примерно тетрамера) небольших синтетических органических молекул, причем отдельные молекулы, как правило, имеют вес по меньшей мере примерно 150 Da и менее примерно 5 кДа, обычно менее примерно 3 кДа. Могут быть использованы различные пары синтетических лигандов и рецепторов. Например, в вариантах, включающих природные рецепторы, димерный FK506 может быть использован с рецептором FKBP12, димерный циклоспорин А может быть использован с рецептором циклофилина, димерный эстроген - с рецептором эстрогена, димерные глюкокортикоиды - с глюкокортикоидным рецептором, димерный тетрациклин - с тетрациклином рецептором, димерный витамин D - с рецептором витамина D и т.п. В качестве альтернативы могут быть использованы лиганды более высокого порядка, например, тримерные. Для вариантов осуществления, включающих неприродные рецепторы, например, субъединицы антител, модифицированные субъединицы антител, одноцепочечные антитела, состоящие из вариабельных областей тяжелых и легких цепей в тандеме, разделенных гибким линкером, или модифицированные рецепторы и их мутированные последовательности, и т.п., может использоваться любое множества соединений. Значимой характеристикой единиц, включающих мультимерный лиганд по изобретению, является то, что каждый сайт связывания способен связываться с рецептором с высокой аффинностью, и предпочтительно, что они могут быть димеризоваться химически. Кроме того, доступны способы для баланса гидрофобности/гидрофильности лигандов, так что они способны растворяться в сыворотке крови при функциональных концентрациях и одновременно способны диффундировать через плазматические мембраны для большинства вариантов применения.
[0120] Активация индуцируемых проапоптотических полипептидов по изобретению может быть осуществлена с помощью, например, химически индуцированной димеризации (CID), опосредованной индуцирующим агентом, с получением кондиционно контролируемого белка или полипептида. Проапоптотические полипептиды по изобретению не только являются индуцируемыми, но индукция этих полипептидов также является обратимой вследствие деградации лабильного димеризующего агента или введения мономерного конкурентного ингибитора.
[0121] В некоторых вариантах осуществления изобретения область связывания лиганда содержит полипептид FK506-связывающего белка 12 (FKBP12). В некоторых вариантах осуществления изобретения область связывания лиганда содержит полипептид FKBP12, имеющий замену валином (V) фенилаланина (F) в положении 36 (F36V). В некоторых вариантах осуществления, где область связывания лиганда содержит полипептид FKBP12, имеющий замену валином (V) фенилаланина (F) в положении 36 (F36V), индуцирующий агент может содержать AP1903 (Римидуцид), синтетический препарат (CAS-название: сложный эфир 2-пиперидинкарбоновой кислоты и 1-[(2S)-1-оксо-2-(3,4,5-триметоксифенил)бутил]-1,2-этандиилбис[имино(2-оксо-2,1-этандиил)окси-3,1-фенилен[(1R)-3-(3,4-диметоксифенил)пропилидена]], CID) регистрационный номер CAS: 195514-63-7; молекулярная формула: C78H98N4O20; молекулярный вес: 1411,65)). В некоторых вариантах осуществления, где область связывания лиганда содержит полипептид FKBP12, имеющий замену валином (V) фенилаланина (F) в положении 36 (F36V), индуцирующий агент может содержать AP1903 (регистрационный номер CAS: 195514-80-8 и молекулярная формула: C82H107N5O20). В некоторых вариантах осуществления индуцирующий агент является аналогом AP20187, таким, как, например, AP1510. Используемые в данном описании индуцирующие агенты AP20187, AP903 (Rim1iducid) и AP1510 могут использоваться взаимозаменяемо.
[0122] Активный фармацевтический ингредиент AP1903 (Римидуцид) производится компанией Alphora Research Inc., а лекарственный препарат AP1903 (Римидуцид) для инъекций изготавливается Formatech Inc. Он представлен в виде раствора 5 мг/мл AP1903 (Римидуцид) в 25%-м растворе неионогенного солюбилизатора Солютол HS 15 (250 мг/мл, компания BASF). При комнатной температуре эта композиция представляет собой прозрачный слегка желтоватый раствор. После охлаждения этот препарат претерпевает обратимый фазовый переход, в результате чего раствор приобретает молочный цвет. Этот фазовый переход обратим при повторном нагревании до комнатной температуры. Аликвоты составляют по 2,33 мл в 3-мл стеклянном флаконе (приблизительно всего 10 мг AP1903 (Римидуцида) для инъекций на флакон). При определении необходимости введения АР1903 (Римидуцида) пациенту могут вводить, например, одну фиксированную дозу AP1903 (Римидуцида) для инъекций (0,4 мг/кг) с помощью внутривенной инфузии в течение 2 часов, с использованием свободного от DEHP и этиленоксида, стерильного инфузионного набора. Доза AP1903 (Римидуцида) рассчитывается индивидуально для всех пациентов, и не пересчитывается, если вес тела не колеблется≥10%. Перед инфузией расчетную дозу разводят в 100 мл 0,9%-нормального солевого раствора. В предыдущей фазе I исследования AP1903 (Римидуцида), 24 здоровых добровольца получали однократные дозы AP1903 (Римидуцида) для инъекций в дозировке 0,01, 0,05, 0,1, 0,5 и 1,0 мг/кг путем инфузии в течение 2 часов. Уровни AP1903 (Римидуцида) в плазме были прямо пропорциональны дозировке, со средними значениями Cmax в интервале примерно 10-1275 нг/мл в диапазоне доз 0,01-1,0 мг/кг. После начального периода инфузии, концентрации в крови продемонстрировали фазу быстрого распределения, с уровнями в плазме, снижающимися приблизительно до 18, 7 и 1% от максимальной концентрации через 0,5, 2 и 10 ч после введения дозы, соответственно. Было показано, что AP1903 (Римидуцид) для инъекций является безопасным и хорошо переносится при всех дозировках, и продемонстрирован его положительный фармакокинетический профиль. Iuliucci J D, et al., J Clin Pharmacol. 41: 870-9, 2001.
[0123] Например, используемая фиксированная доза АР1903 (Римидуцида) для инъекций может составлять 0,4 мг/кг внутривенно в течение 2 часов. Количество AP1903 (Римидуцида), необходимое in vitro для эффективной передачи сигналов клеткам, составляет 10-100 нМ (мол. вес. 1600 Да). Это соответствует 16-160 мкг/л или приблизительно 0,016-1,6 мкг/кг (1,6-160 мкг/кг). Дозы до 1 мг/кг хорошо переносились в фазе I исследования AP1903 (Римидуцида), описанной выше. Таким образом, 0,4 мг/кг может быть безопасной и эффективной дозой АР1903 (Римидуцида) для этого исследования фазы I в сочетании с терапевтическими клетками.
[0124] Аминокислотная последовательность области связывания лиганда и/или кодирующая ее нуклеотидная последовательность, может содержать последовательность с одной или несколькими модификациями по сравнению с аминокислотной или нуклеотидной последовательностью дикого типа. Например, аминокислотная последовательность области связывания лиганда или кодирующая ее нуклеотидная последовательность по изобретению могут представлять собой оптимизированную по кодонам последовательность. Одна или несколько модификаций могут увеличивать аффинность связывания лиганда (например, индуцирующего агента) для области связывания лиганда по изобретению по сравнению с полипептидом дикого типа. В качестве альтернативы или в дополнение, одна или несколько модификаций могут снижать иммуногенность области связывания лиганда по изобретению по сравнению с полипептидом дикого типа. Области связывания лиганда по изобретению и/или индуцирующие агенты по изобретению могут быть неприродными.
[0125] Индуцируемые проапоптотические полипептиды по изобретению содержат область связывания лиганда, линкер и проапоптотический пептид, где индуцируемый проапоптотический полипептид не содержит не принадлежащую человеку последовательность. В некоторых вариантах осуществления изобретения, не принадлежащая человеку последовательность содержит сайт рестрикции. Линкер может включать любой органический или неорганический материал, который позволяет, при димеризации области связывания лиганда взаимодействие, сшивку, перекрестную активацию или активации проапоптотических полипептидов, так что взаимодействие или активация проапоптотических полипептидов инициирует апоптоз в клетка. В некоторых вариантах осуществления линкер представляет собой полипептид. В некоторых вариантах осуществления линкер представляет собой полипептид, содержащий богатую G/S-аминокислотами последовательность («GS»-линкер). В некоторых вариантах осуществления линкер представляет собой полипептид, содержащий аминокислотную последовательность GGGGS (SEQ ID NO: 5). В предпочтительных вариантах осуществления линкер представляет собой полипептид, а нуклеиновая кислота, кодирующая полипептид, не содержит сайт рестрикции для эндонуклеазы рестрикции. Линкеры по изобретению могут быть неприродными.
[0126] Индуцируемые проапоптотические полипептиды по изобретению могут экспрессироваться в клетке под транскрипционным контролем любого промотора, способного инициировать и/или регулировать экспрессию индуцируемого проапоптотического полипептида по изобретению в этой клетке. Термин «промотор», используемый в данном описании, относится к промотору, который действует в качестве исходного сайта связывания РНК-полимеразы для транскрипции ген. Например, индуцируемые проапоптотические полипептиды по изобретению могут экспрессироваться в клетках млекопитающих под транскрипционным контролем любого промотора, способного инициировать и/или регулировать экспрессию индуцируемого проапоптотического полипептида по изобретению в клетке млекопитающего, включая, но не ограничиваясь этим, нативные, эндогенные, экзогенные и гетерологичные промоторы. Предпочтительные клетки млекопитающих включают в себя клетки человека. Таким образом, индуцируемые проапоптотические полипептиды по изобретению могут экспрессироваться в клетке человека под транскрипционным контролем любого промотора, способного инициировать и/или регулировать экспрессию индуцируемого проапоптотического полипептида по изобретению в человеческой клетке, включая, но не ограничиваясь этим, промотор человека или вирусный промотор. Типичные промоторы для экспрессии в клетках человека включают в себя, но не ограничиваются этим, промотор раннего гена цитомегаловируса человека (CMV), ранний промотор SV40, длинный концевой повтор вируса саркомы Рауса, промотор β-актина, промотор инсулина крысы и промотор глицеральдегид-3-фосфат-дегидрогеназы, каждый из которых может использоваться для получения высокого уровня экспрессии индуцируемого проапоптотического полипептида по изобретению. Использование других промоторов из вирусов или клеток млекопитающих либо бактериальных фагов, которые хорошо известны в данной области техники, также предусмотрено для получения экспрессии индуцируемого проапоптотического полипептида по изобретению при условии, что уровни экспрессии достаточны для инициации апоптоза в клетке. После трансфекции или трансформации, используя промотор с хорошо известными свойствами, можно оптимизировать уровень и схему экспрессии белка, представляющего интерес.
[0127] Путем выбора промотора, который регулируется в ответ на специфические физиологические или синтетические сигналы, можно осуществить индуцируемую экспрессию индуцируемого проапоптотического полипептида по изобретению. Одной из таких систем является экдизоновая система (Invitrogen, Carlsbad, CA). Эта система предназначена для получения регулируемой экспрессии представляющего интерес гена в клетках млекопитающих. Она состоит из жестко регулируемого механизма экспрессии, который не позволяет практически никакого базального уровня экспрессии трансгена, но более чем 200-кратную индукцию. Система основана на гетеродимерном экдизоновом рецепторе из дрозофилы, и когда экдизон или его аналог, такой как муристерон А, связывается с рецептором, рецептор активирует промотор, запуская экспрессию расположенного после него трансгена, так что достигаются высокие уровни транскриптов мРНК. В этой системе оба мономера гетеродимерного рецептора экспрессируются с одного вектора, тогда как экдизон-чувствительный промотор, который стимулирует экспрессию представляющего интерес гена, находится в другой плазмиде. Поэтому, создание системы этого типа в представляющем интерес векторе может представлять собой полезным. Другой индуцируемый системой, которая может быть полезной, является система Tet-Off™ или Tet-On™ (Clontech, Palo Alto, CA), исходно разработанная Госсеном и Буярдом (Gossen and Bujard, Proc. Natl. Acad. Sci. USA, 89:5547-5551, 1992; Gossen et al., Science, 268:1766-1769, 1995). Эта система также обеспечивает высокие уровни экспрессии генов, регулируются в ответ на тетрациклин или производные тетрациклина, такие как доксициклин. В системе Tet-On™ экспрессия гена включается в присутствии доксициклина, тогда как в системе Tet-Off™ экспрессия гена включена в отсутствие доксициклина. Эти системы основаны на двух регуляторных элементах, полученных из оперона устойчивости к тетрациклину E. coli: последовательности тетрациклинового оператора (с которым связывается тетрациклиновый репрессор) и белке - тетрациклиновом репрессоре. Представляющий интерес ген клонируют в плазмиду после промотора, который имеет тетрациклиновые регуляторные элементы, присутствующие в нем. Вторая плазмида содержит регуляторный элемент, называемый тетрациклин-регулируемым трансактиватором, который состоит в системе Tet-Off™ из домена VP-16 из вируса простого герпеса и тетрациклинового репрессора дикого типа. Таким образом, в отсутствие доксициклина транскрипция конститутивно запущена. В системе Tet-On™ тетрациклиновый репрессор не является репрессором дикого типа и в присутствии доксициклина активирует транскрипцию. Для получения вектора для генной терапии система Tet-Off™ может использоваться таким образом, что клетки-продуценты могут выращиваться в присутствии тетрациклина или доксициклина, и экспрессия потенциально токсичного трансгена может быть блокирована, но когда вектор вводят пациенту, то экспрессия гена будет конститутивно запущена.
[0128] В некоторых случаях желательно регулировать экспрессию трансгена в векторе для генной терапии. Например, в зависимости от желаемого уровня экспрессии используются различные вирусные промоторы с разной силой активности. В клетках млекопитающих ранний часто используется промотор CMV, чтобы обеспечить сильную активацию транскрипции. Промотор CMV, описан в Donnelly, J. J., et al., 1997. Annu. Rev. Immunol. 15:617-48. Модифицированные версии промотора CMV, которые являются менее сильными, также используются, когда желательно снижение уровня экспрессии трансгена. Когда желательна экспрессия трансгена в кроветворных клетках, часто используются ретровирусные промоторы, такие как LTR из MLV или MMTV. Другие вирусные промоторы, которые используются в зависимости от желаемого эффекта, включают SV40, RSV LTR, LTR HIV-1 и HIV-2, аденовирусные промоторы, такие как промоторы области E1A, E2A или MLP, AAV LTR, HSV-TK и вируса саркомы птиц.
[0129] В других примерах могут быть выбраны промоторы, которые регулируются развитием организма и активны в конкретных дифференцированных клетках. Например, промотор может быть неактивным в плюрипотентных стволовых клетках, но, например, если плюрипотентные стволовые клетки дифференцируется в более зрелые клетки, промотор может затем активироваться.
[0130] Аналогичным образом, тканеспецифичные промоторы используются для осуществления транскрипции в определенных тканях или клетках таким образом, чтобы снизить потенциальную токсичность или нежелательные эффекты в нецелевых тканях. Эти промоторы могут дать снижение экспрессии по сравнению с более сильным промотором, таким как промотор CMV, но могут также дать более ограниченную экспрессию и иммуногенность (Bojak, A., et al., 2002. Vaccine. 20:1975-79; Cazeaux., N., et al., 2002. Vaccine 20:3322-31). Например, в случае необходимости могут быть использованы тканеспецифичные промоторы, такие как промотор PSA или гландулярного калликреина, или гена мышечной креатинкиназы.
[0131] Примеры тканеспецифичных или специфичных к дифференцировке промоторов включают, но не ограничиваются ими, промоторы следующих генов: B29 (В-клетки), CD14 (моноциты), CD43 (лейкоциты и тромбоциты), CD45 (кроветворные клетки), CD68 (макрофаги), десмина (мышцы), эластазы-1 (ацинарные клетки поджелудочной железы), эндоглина (эндотелиальные клетки), фибронектина (дифференцировка клеток, заживление тканей), Flt-1 (эндотелиальные клетки) и GFAP (астроциты).
[0132] При некоторых показаниях, желательно активировать транскрипцию в определенное время после введения вектора для генной терапии. Это осуществляется с помощью таких промоторов, которые регулируются гормонами или цитокинами. Промоторы, отвечающие на цитокины и воспалительные белки, которые могут быть использованы, включают промоторы генов K и T-кининогена (Kageyama et al., (1987) J. Biol. Chem., 262, 2345-2351), c-fos, TNF-альфа, C-реактивного белка (Arcone, et al., (1988) Nucl. Acids Res., 16(8), 3195-3207), гаптоглобина (Oliviero et al., (1987) EMBO J., 6, 1905-1912), сывороточного амилоида А2, С/ЕВР-альфа, IL-1, IL-6 (Poli and Cortese, (1989) Proc. Nat'l Acad. Sci. USA, 86, 8202-8206), белка С3 комплемента (Wilson et al., (1990) Mol. Cell. Biol., 6181-6191), IL-8, альфа-1 кислого гликопротеина (Prowse and Baumann, (1988) Mol Cell Biol, 8, 42-51), альфа-1 антитрипсина, липопротеинлипазы (Zechner et al., Mol. Cell. Biol., 2394-2401, 1988), ангиотензиногена (Рон, et al., (1991) Mol. Cell. Biol., 2887-2895), фибриногена, с-jun (индуцируемого форболовыми эфирами, TNF-альфа, УФ-излучением, ретиноевой кислотой и перекисью водорода), коллагеназы (индуцируемой форболовыми эфирами и ретиноевой кислотой), металлотионеина (индуцируемого тяжелыми металлами и глюкокортикоидами), стромелизина (индуцируемого форболовым эфиром, интерлейкином-1 и EGF), альфа-2 макроглобулина и альфа- 1 антихимотрипсина. Другие промоторы включают, например, промоторы SV40, MMTV, вируса иммунодефицита человека, вируса Молони (MV), ALV, вируса Эпштейна-Барра, вируса саркомы Рауса, актина, миозина, гемоглобина и креатин человека.
[0133] Предполагается, что любой из указанных выше промоторов, один или в комбинации с другим промотором, может быть полезен в зависимости от желаемого действия. Промоторы и другие регуляторные элементы выбирают таким образом, чтобы они функционировали в заданных клетках или ткани. Кроме того, этот список промоторов не должен истолковываться как исчерпывающий или ограничивающий - также предусмотрены другие промоторы, которые используются в сочетании с промоторами и способами, описанными в данном документе.
Молекулы нуклеиновых кислот
[0134] Молекулы нуклеиновых кислот по настоящему изобретению, включая последовательности, кодирующие индуцируемый полипептид по настоящему изобретению, могут находиться в форме РНК, такой как мРНК, гяРНК, тРНК, или в любой другой форме, или в форме ДНК, включая, но не ограничиваясь этим, кДНК и геномную ДНК, полученные путем клонирования или полученные синтетическим путем, или любой их комбинации. ДНК может быть трехцепочечной, двухцепочечной или одноцепочечной или любой их комбинацией. Любая участок по меньшей мере одной цепи ДНК или РНК может представлять собой кодирующую цепь, также известную как смысловая цепь, или он может быть некодирующей цепью, также называемой антисмысловой цепью.
[0135] Выделенные молекулы нуклеиновой кислоты по настоящему изобретению могут включать молекулы нуклеиновой кислоты, включающие открытую рамку считывания (ORF), необязательно, с одним или несколькими интронами, например, но не ограничиваясь по меньшей мере одним указанным участком по меньшей мере одной последовательности, кодирующей индуцируемый полипептид по изобретению; молекулы нуклеиновой кислоты, содержащие кодирующую последовательность для индуцируемого полипептида по изобретению; и молекулы нуклеиновой кислоты, которые содержат нуклеотидную последовательность, существенно отличающуюся от описанной выше, но которые, вследствие вырожденности генетического кода, все еще кодируют индуцируемый полипептид по изобретению, как описано в данном документе и/или как известно в данной области. Естественно, генетический код хорошо известен в данной области. Таким образом, для специалиста в данной области техники является рутинным создание таких вырожденных вариантов нуклеиновых кислот, которые кодируют индуцируемый полипептид по изобретению. См., Например, Ausubel et al., supra, и такие варианты нуклеиновых кислот включены в описание.
[0136] Как указано в настоящем описании, молекулы нуклеиновых кислот по изобретению, которые содержат нуклеиновую кислоту, кодирующую индуцируемый полипептид по изобретению, могут включать в себя, но не ограничиваются этим, молекулы, кодирующие аминокислотную последовательность самого индуцируемого полипептида или его фрагмента; кодирующую последовательность для всего индуцируемого полипептида или его участка; кодирующую последовательность для индуцируемого полипептида по изобретению, его фрагмента или участка, а также дополнительные последовательности, такие как последовательности, кодирующие по меньшей мере один лидерный сигнал или слитый пептид, с или без вышеуказанных дополнительных кодирующих последовательностей, таких как по меньшей мере один интрон, вместе с дополнительными некодирующими последовательностями, включая, но не ограничиваясь ими, некодирующие 5'- и 3'-последовательности, такие как транскрибируемые нетранслируемые последовательности, которые играют определенную роль в транскрипции и процессинге мРНК, включая сигналы сплайсинга и полиаденилирования (например, в связывании рибосомы и стабильности мРНК); дополнительную кодирующую последовательность, которая кодирует дополнительные аминокислоты, такие как те, которые обеспечивают дополнительные функциональные возможности. Таким образом, последовательность, кодирующая индуцируемый полипептид по настоящему изобретению, может быть слита с маркерной последовательностью, такой как последовательность, кодирующая пептид, который облегчает очистку слитого белкового каркаса, содержащего фрагмент или часть белкового каркаса.
Конструирование нуклеиновых кислот
[0137] Выделенные нуклеиновые кислоты по изобретению могут быть получены с использованием (а) рекомбинантных способов, (b) синтетических способов, (с) способов очистки, и/или (d) их комбинаций, которые хорошо известны в данной области техники.
[0138] Обычно нуклеиновые кислоты могут содержать другие последовательности в дополнение к последовательности, кодирующей индуцируемый полипептид по изобретению. Например, в нуклеиновую кислоту может быть вставлен сайт поликлонирования, включающий один или несколько сайтов рестрикции эндонуклеаз, чтобы облегчить выделение последовательности, кодирующей индуцируемый полипептид по изобретению. Кроме того, могут быть вставлены транслируемые последовательности, чтобы облегчить выделение транслируемого полинуклеотида по изобретению. Например, гексагистидиновая маркерная последовательность обеспечивает удобное средство для очистки каспаз по изобретению. Нуклеиновая кислота по изобретению, за исключением кодирующей последовательности, необязательно, представляет собой вектор, адаптер или линкер для клонирования и/или экспрессии последовательности, кодирующей индуцируемый полипептид по изобретению или индуцируемый полипептид по изобретению.
[0139] Дополнительные последовательности могут быть добавлены к таким клонируемым и/или экспрессирующимся последовательностям с целью оптимизации их функции при клонировании и/или экспрессии, чтобы облегчить выделение полинуклеотидной последовательности, кодирующей индуцируемый полипептид по изобретению, или для улучшения введения полинуклеотида, кодирующего последовательность индуцируемого полипептида по изобретению, в клетку. Использование векторов для клонирования, экспрессирующих векторов, адаптеров и линкеров хорошо известно в данной области техники. (См, например, Ausubel, supra; или Sambrook, supra).
Рекомбинантные способы конструирования нуклеиновых кислот
[0140] Выделенные композиции нуклеиновых кислот по изобретению, таких как РНК, кДНК, геномная ДНК или любые их комбинации, могут быть получены из биологических источников, с использованием любого числа методик клонирования, известных специалистам в данной области техники. В некоторых вариантах осуществления изобретения олигонуклеотидные зонды, которые селективно гибридизуются в жестких условиях с полинуклеотидами по настоящему изобретению, используются для идентификации желаемой последовательности в библиотеке кДНК или геномной ДНК. Выделение РНК, получение кДНК и геномных библиотек хорошо известны специалистам в данной области техники. (См., например, Ausubel, supra, или Sambrook, supra).
Способы скрининга и выделения нуклеиновых кислот
[0141] кДНК- или геномную библиотеку можно скринировать с использованием зонда на основании последовательности полинуклеотида по изобретению или его фрагмента. Зонды могут быть использованы для гибридизации с геномной ДНК или кДНК для выделения гомологичных генов в одних и тех же или разных организмов. Специалистам в данной области техники будет понятно, что в анализе могут использоваться различные степени жесткости гибридизации; и либо гибридизационная, либо промывочная среда может являться жесткой. Если условия для гибридизации становится более жестким, то должна быть большая степень комплементарности между зондом и мишенью для того, чтобы произошло образование дуплекса. Степень жесткости можно регулировать с помощью одного или нескольких из температуры, ионной силы, рН и присутствия частично денатурирующего растворителя, такого как формамид. Например, жесткость гибридизации удобно варьировать, изменяя полярность раствора реагента, например, меняя концентрацию формамида в диапазоне от 0% до 50%. Степень комплементарности (идентичности последовательностей), необходимая для детектируемого связывания, будет изменяться в соответствии с жесткостью гибридизационной среды и/или промывочной среды. Степень комплементарности оптимально будет составлять 100% или 70-100%, или любой диапазон или значение в вышеуказанном диапазоне. Однако следует понимать, что минорные вариации последовательности в пробах и праймерах может быть скомпенсирована жесткостью гибридизационной и/или промывочной среды.
[0142] Способы амплификации РНК или ДНК хорошо известны в данной области техники и могут быть использованы согласно изобретению без излишних экспериментов, на основе идей и руководства, представленных в данном описании.
[0143] Известные способы амплификации ДНК или РНК включают в себя, но не ограничиваются ими, полимеразную цепную реакцию (ПЦР) и родственные способы амплификации (см., например, патенты США №№ 4683195, 4683202, 4800159, 4965188, авторов Mullis, et al.; 4795699 и 4921794 авторов Tabor, et al.; 5142033 автора Innis; 5122464 авторов Wilson, et al.; 5091310 автора Innis; 5066584 авторов Gyllensten, et al.; 4889818 авторов Gelfand, et al; 4994370 авторов Silver, et al.; 4766067 автора Biswas; 4656134 автора Ringold), а также РНК-опосредованную амплификацию, в который используется анти-смысловая РНК к последовательности-мишени в качестве матрицы для синтеза двухцепочечной ДНК (патент США № 5130238 авторов Malek, et al., с торговым названием NASBA); причем полное содержание ссылок включено в настоящее описание путем ссылки. (См., например, Ausubel, supra; или Sambrook, supra).
[0144] Например, технологии полимеразной цепной реакции (ПЦР) могут использоваться для амплификации последовательностей полинуклеотидов по изобретению и связанных с ними генов непосредственно из библиотек геномной ДНК или кДНК. ПЦР и другие способы амплификации in vitro также могут использоваться, например, для клонирования последовательностей нуклеиновых кислот, которые кодируют белки, которые необходимо проэкспрессировать, для создания нуклеиновых кислот, чтобы использовать в качестве зондов для обнаружения присутствия желаемой мРНК в образцах, для секвенирования нуклеиновых кислот, или для других целей. Примеры методов, достаточных для ознакомления специалистов в данной области со способами амплификации in vitro можно найти в Berger, supra, Sambrook, supra и Ausubel, supra, а также в Mullis, et al., патенте США № 4683202 (1987); и в Innis, et al., PCR Protocols A Guide to Methods and Applications, Eds., Academic Press Inc., San Diego, Calif. (1990). Коммерчески доступные наборы для геномной ПЦР-амплификации известны в данной области техники. См., например, набор Advantage-GC Genomic PCR Kit (Clontech). Кроме того, например, ген белка 32 фага Т4 (Boehringer Mannheim) может быть использован для повышения выхода длинных продуктов ПЦР.
Синтетические способы конструирования нуклеиновых кислот
[0145] Выделенные нуклеиновые кислоты по изобретению могут быть также получены путем прямого химического синтеза известными способами (см., например, Ausubel, et al., supra). Химический синтез обычно дает одноцепочечный олигонуклеотид, который может быть превращен в двухцепочечную ДНК путем гибридизации с комплементарной последовательностью или путем полимеризации с помощью ДНК-полимеразы с использованием одной цепи в качестве матрицы. Специалисту в данной области техники будет понятно, что тогда как химический синтез ДНК может быть ограничен последовательностями, имеющими длину примерно 100, 500 и 1000 или большее число оснований, более длинные последовательности могут быть получены путем лигирования коротких последовательностей.
Рекомбинантные экспрессионные кассеты
[0146] Изобретение дополнительно относится к рекомбинантной экспрессионной кассете, содержащей нуклеиновую кислоту по изобретению. Последовательность нуклеиновой кислоты по изобретению, например, кДНК или геномная последовательность, кодирующая участок индуцируемого полипептида по изобретению, может быть использована для конструирования рекомбинантной экспрессионной кассеты, которая может быть введена по меньшей мере в одну желаемую клетку-хозяина. Рекомбинантная экспрессионная кассета, как правило, будет включать в себя полинуклеотид по изобретению, функционально связанный с регуляторными последовательностями инициации транскрипции, которые будут управлять транскрипцией полинуклеотида в предполагаемой клетке-хозяине. Как гетерологичный, так и негетерологичный (т.е. эндогенный) промоторы могут использоваться для управления экспрессией нуклеиновых кислот по изобретению.
[0147] В некоторых вариантах осуществления изобретения, выделенные нуклеиновые кислоты, которые служат в качестве промоторных, энхансерных или других элементов, могут быть введены в соответствующее положение (перед или после кодирующей последовательности, или в интронную область) негетерологичной формы полинуклеотида по изобретению таким образом, чтобы повышать или подавлять экспрессию полинуклеотида по изобретению. Например, эндогенные промоторы могут быть изменены in vivo или in vitro путем мутации, делеции и/или замены.
Векторы и клетки-хозяева
[0148] Настоящее изобретение также относится к векторам, которые включают последовательность, кодирующую индуцируемый полипептид по изобретению, клеткам-хозяевам, генетически модифицированным рекомбинантным векторами, и к получению по меньшей мере одного индуцируемого полипептида по изобретению с помощью рекомбинантных методик, хорошо известных в данной области техники. См., например, Sambrook, et al., supra; Ausubel, et al., supra; где каждый полностью включен в настоящее описание путем ссылки.
[0149] Полинуклеотиды, включающие последовательность, кодирующую индуцируемый полипептид по изобретению, необязательно может быть присоединены к вектору, содержащему селективный маркер для размножения в хозяине. Как правило, плазмидный вектор вводят в виде осадка, например, в виде осадка с фосфатом кальция, или в комплексе с заряженным липидом. Если вектор представляет собой вирус, он может быть упакован in vitro с использованием соответствующей паковочной клеточной линии, а затем трансдуцирован в клетки-хозяева.
[0150] Изобретение относится к композиции, содержащий транспозон по изобретению. В некоторых вариантах осуществления композиция может дополнительно содержать плазмиду, содержащую последовательность, кодирующую фермент транспозазу. Последовательность, кодирующая транспозазу, может представлять собой последовательностью мРНК.
[0151] Транспозоны по изобретению эписомно поддерживаются или интегрированы в геном рекомбинантной/модифицированной клетки. Транспозон может представлять собой часть двухкомпонентной системы, в которой используются транспозон PiggyBac и транспозаза для усиленного невирусного переноса генов. В некоторых вариантах осуществления этого способа транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления транспозон представляет собой транспозон piggyBac. В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозон является транспозоном piggyBac, транспозаза представляет собой транспозазу piggyBac™ или Super piggyBac™ (SPB)
[0152] Транспозоны по изобретению могут содержать транспозоны piggyBac. В некоторых вариантах осуществления этого способа по изобретению транспозон представляет собой транспозон в плазмидной ДНК с последовательностью, кодирующей индуцируемый полипептид каспазы по изобретению, фланкированный двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления транспозон представляет собой транспозон piggyBac. В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозон является транспозоном piggyBac, транспозаза представляет собой транспозазу piggyBac™ или Super piggyBac™ (SPB). В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозаза представляет собой транспозазу Super piggyBac™ (SPB), последовательность, кодирующая транспозазу, представляет собой последовательность мРНК.
[0153] В некоторых вариантах осуществления способов по изобретению, фермент транспозаза представляет собой транспозазу piggyBac™ (PB). Транспозаза piggyBac (PB) может содержать или состоять из аминокислотной последовательности по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичной:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF (SEQ ID NO: 1).
[0154] В некоторых вариантах осуществления способов по изобретению, фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющей аминокислотную замену в одном или нескольких из положений 30, 165, 282 или 538 в последовательности:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF (SEQ ID NO: 1).
[0155] В некоторых вариантах осуществления фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющей аминокислотные замены по двум или нескольким положениям 30, 165, 282 или 538 в последовательности SEQ ID NO: 1. В некоторых вариантах осуществления фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющий аминокислотные замены в трех или большим числе положений 30, 165, 282 или 538 в последовательности SEQ ID NO: 1. В некоторых вариантах осуществления фермент транспозаза представляет собой транспозазу piggyBac™ (PB), которая содержит или состоит из аминокислотной последовательности, имеющей аминокислотные замены в каждом из следующих положений 30, 165, 282 и 538 в последовательности SEQ ID NO: 1. В некоторых вариантах осуществления изобретения, аминокислотной заменой в положении 30 последовательности SEQ ID NO: 1 является замена валином (V) изолейцина (I). В некоторых вариантах осуществления аминокислотной заменой в положении 165 последовательности SEQ ID NO: 1 является замена серином (S) глицина (G). В некоторых вариантах осуществления аминокислотной заменой в положении 282 последовательности SEQ ID NO: 1 является замена валином (V) метионина (М). В некоторых вариантах осуществления аминокислотной заменой в положении 538 последовательности из SEQ ID NO: 1 является замена лизином (K) аспарагина (N).
[0156] В некоторых вариантах осуществления способов по изобретению фермент транспозаза представляет собой транспозазу Super piggyBac™ (SPB). В некоторых вариантах осуществления транспозазы Super piggyBac™ (SPB) по изобретению могут содержать или состоять из аминокислотной последовательности, имеющей последовательность SEQ ID NO: 1, где аминокислотная замена в положении 30 представляет собой замену валином (V) изолейцина (I), аминокислотная замена в положении 165 представляет собой замену серином (S) глицина (G), аминокислотная замена в положении 282 представляет собой замену валином (V) метионина (М), а аминокислотная замена в положении 538 представляет собой замену лизином (K) аспарагина (N). В некоторых вариантах осуществления изобретения транспозаза Super piggyBac™ (SPB) может содержать или состоять из аминокислотной последовательности по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичной:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTV RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF (SEQ ID NO: 2).
[0157] В некоторых вариантах осуществления способов по настоящему изобретению, включая те варианты осуществления, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac™ или Super piggyBac™ может дополнительно содержать аминокислотные замены в одном или нескольких положениях 3, 46, 82, 103, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 258, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 486, 503, 552, 570 и 591 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления, включая те варианты осуществления, в которых транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac™ или Super piggyBac™ может дополнительно содержать аминокислотные замены в одном или нескольких положениях 46, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 485, 503, 552 и 570. В некоторых вариантах осуществления аминокислотная замена в положении 3 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аспарагином (N) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену серином (S) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену треонином (Т) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 82 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену триптофаном (W) изолейцина (I). В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 119 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) аргинина (R). В некоторых вариантах осуществления аминокислотная замена в положении 125 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (А) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 125 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену гистидином (H) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином (V) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 185 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 187 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 200 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену триптофаном (W) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 207 из SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 209 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 226 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 235 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аргинином (R) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 240 в SEQ ID NO: 1 или SEQ ID NO: 1 представляет собой замену лизином (K) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 241 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) фенилаланина (F). В некоторых вариантах осуществления аминокислотная замена в положении 243 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) пролина (Р). В некоторых вариантах осуществления аминокислотная замена в положении 258 из SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену серином (S) аспарагина (N). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену триптофаном (W) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену тирозином (Y) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 298 из SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) метионина (М). В некоторых вариантах осуществления замена аминокислоты в положении 298 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (А) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO: 1 ИЛИ SEQ ID NO: 2 представляет собой замену валином (V) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) пролина (Р). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином пролина (P). В некоторых вариантах осуществления аминокислотная замена в положении 315 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) аргинина (R). В некоторых вариантах осуществления аминокислотная замена в положении 319 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) треонина (Т). В некоторых вариантах осуществления аминокислотная замена в положении 327 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аргинином (R) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 328 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином (V) тирозина (Y). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) цистеина (С). В некоторых вариантах осуществления аминокислотная замена в положении 421 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену гистидином (H) аспарагиновой кислоты (D). В некоторых вариантах осуществления аминокислотная замена в положении 436 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 456 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену тирозином (Y) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 470 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену фенилаланином (F) лейцина (L). В некоторых вариантах осуществления аминокислотная замена в положении 485 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лейцином (L) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену изолейцином (I) метионина (M). В некоторых вариантах осуществления аминокислотная замена в положении 552 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену лизином (K) валина (V). В некоторых вариантах осуществления аминокислотная замена в положении 570 в SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену треонином (Т) аланина (А). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (Р) глутамина (Q). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аргинином (R) глутамина (Q).
В некоторых вариантах осуществления способов по изобретению, включая те, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, транспозаза piggyBac™ может содержать, или транспозаза Super piggyBac™ может дополнительно содержать аминокислотные замены в одном или нескольких из положений 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления способов по изобретению, включая те, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, транспозаза piggyBac™ может содержать, или транспозаза Super piggyBac™ может дополнительно содержать аминокислотную замену в двух, трех, четырех, пяти, шести или большем числе положений 103, 194, 372, 375, 450, 509 и 570 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления, включая те, где транспозаза содержит описанные выше мутации в положениях 30, 165, 282 и/или 538, транспозаза piggyBac™ может содержать, или транспозаза Super piggyBac™ может дополнительно содержать аминокислотную замену в положениях 103, 194, 372, 375, 450, 509 и 570 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену пролином (P) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 194 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену валином (V) метионина (М). В некоторых вариантах осуществления аминокислотная замена в положении 372 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (A) аргинина (R). В некоторых вариантах осуществления аминокислотная замена в положении 375 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аланином (A) лизина (K). В некоторых вариантах осуществления аминокислотная замена в положении 450 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену аспарагином (N) аспарагиновой кислоты (D). В некоторых вариантах осуществления аминокислотная замена в положении 509 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену глицином (G) серина (S). В некоторых вариантах осуществления аминокислотная замена в положении 570 SEQ ID NO: 1 или SEQ ID NO: 2 представляет собой замену серином (S) аспарагина (N). В некоторых вариантах осуществления транспозаза piggyBac™ может содержать замену валином (V) метионина (M) в положении 194 SEQ ID NO: 1. В некоторых вариантах осуществления, включая те варианты осуществления, в которых транспозаза piggyBac™ может содержать замену валином (V) метионина (М) в положении 194 SEQ ID NO: 1, транспозаза piggyBac™ может дополнительно содержать аминокислотную замену в положениях 372, 375 и 450 в последовательности SEQ ID NO: 1 или SEQ ID NO: 2. В некоторых вариантах осуществления транспозаза piggyBac™ может содержать замену валином (V) метионина (M) в положении 194 SEQ ID NO: 1, замену аланином (A) аргинина (R) в положении 372 SEQ ID NO: 1 и замену аланином (A) лизина (K) в положении 375 SEQ ID NO: 1. В некоторых вариантах осуществления транспозаза piggyBac™ может содержать замену валином (V) метионина (М) в положении 194 SEQ ID NO: 1, замену аланином (A) аргинина (R) в положении 372 SEQ ID NO: 1, замену аланином (A) лизина (K) в положении 375 SEQ ID NO: 1 и замену аспарагином (N) аспарагиновой кислоты (D) в положении 450 SEQ ID NO: 1.
[0158] В некоторых вариантах осуществления изобретения транспозон является транспозоном Sleeping Beauty. В некоторых вариантах осуществления изобретения и, в частности, в тех, где транспозон представляет собой транспозон Sleeping Beauty, транспозазой является транспозаза Sleeping Beauty или гиперактивная транспозаза Sleeping Beauty (SB100X).
[0159] В некоторых вариантах осуществления способов по изобретению, транспозаза Sleeping Beauty содержит аминокислотную последовательность по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичную:
1 MGKSKEISQD LRKKIVDLHK SGSSLGAISK RLKVPRSSVQ TIVRKYKHHG TTQPSYRSGR
61 RRVLSPRDER TLVRKVQINP RTTAKDLVKM LEETGTKVSI STVKRVLYRH NLKGRSARKK
121 PLLQNRHKKA RLRFATAHGD KDRTFWRNVL WSDETKIELF GHNDHRYVWR KKGEACKPKN
181 TIPTVKHGGG SIMLWGCFAA GGTGALHKID GIMRKENYVD ILKQHLKTSV RKLKLGRKWV
241 FQMDNDPKHT SKVVAKWLKD NKVKVLEWPS QSPDLNPIEN LWAELKKRVR ARRPTNLTQL
301 HQLCQEEWAK IHPTYCGKLV EGYPKRLTQV KQFKGNATKY (SEQ ID NO: 19).
[0160] В некоторых вариантах осуществления способов по изобретению, гиперактивная транспозаза Sleeping Beauty (SB100X) содержит аминокислотную последовательность по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% (или на какой-либо процент между этими значениями) идентичную:
1 MGKSKEISQD LRKRIVDLHK SGSSLGAISK RLAVPRSSVQ TIVRKYKHHG TTQPSYRSGR
61 RRVLSPRDER TLVRKVQINP RTTAKDLVKM LEETGTKVSI STVKRVLYRH NLKGHSARKK
121 PLLQNRHKKA RLRFATAHGD KDRTFWRNVL WSDETKIELF GHNDHRYVWR KKGEACKPKN
181 TIPTVKHGGG SIMLWGCFAA GGTGALHKID GIMDAVQYVD ILKQHLKTSV RKLKLGRKWV
241 FQHDNDPKHT SKVVAKWLKD NKVKVLEWPS QSPDLNPIEN LWAELKKRVR ARRPTNLTQL
301 HQLCQEEWAK IHPNYCGKLV EGYPKRLTQV KQFKGNATKY (SEQ ID NO: 20).
[0161] В некоторых вариантах осуществления транспозаза представляет собой транспозазу Helitron. Транспозаза генома Helitron мобилизует транспозон Heiraiser, древний элемент из летучей мыши, который был активен примерно от 30 до 36 миллионов лет назад. Типовой транспозон Heiraiser по изобретению включает в себя Helibat1, который содержит нуклеотидную последовательность, содержащую:
1 TCCTATATAA TAAAAGAGAA ACATGCAAAT TGACCATCCC TCCGCTACGC TCAAGCCACG
61 CCCACCAGCC AATCAGAAGT GACTATGCAA ATTAACCCAA CAAAGATGGC AGTTAAATTT
121 GCATACGCAG GTGTCAAGCG CCCCAGGAGG CAACGGCGGC CGCGGGCTCC CAGGACCTTC
181 GCTGGCCCCG GGAGGCGAGG CCGGCCGCGC CTAGCCACAC CCGCGGGCTC CCGGGACCTT
241 CGCCAGCAGA GAGCAGAGCG GGAGAGCGGG CGGAGAGCGG GAGGTTTGGA GGACTTGGCA
301 GAGCAGGAGG CCGCTGGACA TAGAGCAGAG CGAGAGAGAG GGTGGCTTGG AGGGCGTGGC
361 TCCCTCTGTC ACCCCAGCTT CCTCATCACA GCTGTGGAAA CTGACAGCAG GGAGGAGGAA
421 GTCCCACCCC CACAGAATCA GCCAGAATCA GCCGTTGGTC AGACAGCTCT CAGCGGCCTG
481 ACAGCCAGGA CTCTCATTCA CCTGCATCTC AGACCGTGAC AGTAGAGAGG TGGGACTATG
541 TCTAAAGAAC AACTGTTGAT ACAACGTAGC TCTGCAGCCG AAAGATGCCG GCGTTATCGA
601 CAGAAAATGT CTGCAGAGCA ACGTGCGTCT GATCTTGAAA GAAGGCGGCG CCTGCAACAG
661 AATGTATCTG AAGAGCAGCT ACTGGAAAAA CGTCGCTCTG AAGCCGAAAA ACAGCGGCGT
721 CATCGACAGA AAATGTCTAA AGACCAACGT GCCTTTGAAG TTGAAAGAAG GCGGTGGCGA
781 CGACAGAATA TGTCTAGAGA ACAGTCATCA ACAAGTACTA CCAATACCGG TAGGAACTGC
841 CTTCTCAGCA AAAATGGAGT ACATGAGGAT GCAATTCTCG AACATAGTTG TGGTGGAATG
901 ACTGTTCGAT GTGAATTTTG CCTATCACTA AATTTCTCTG ATGAAAAACC ATCCGATGGG
961 AAATTTACTC GATGTTGTAG CAAAGGGAAA GTCTGTCCAA ATGATATACA TTTTCCAGAT
1021 TACCCGGCAT ATTTAAAAAG ATTAATGACA AACGAAGATT CTGACAGTAA AAATTTCATG
1081 GAAAATATTC GTTCCATAAA TAGTTCTTTT GCTTTTGCTT CCATGGGTGC AAATATTGCA
1141 TCGCCATCAG GATATGGGCC ATACTGTTTT AGAATACACG GACAAGTTTA TCACCGTACT
1201 GGAACTTTAC ATCCTTCGGA TGGTGTTTCT CGGAAGTTTG CTCAACTCTA TATTTTGGAT
1261 ACAGCCGAAG CTACAAGTAA AAGATTAGCA ATGCCAGAAA ACCAGGGCTG CTCAGAAAGA
1321 CTCATGATCA ACATCAACAA CCTCATGCAT GAAATAAATG AATTAACAAA ATCGTACAAG
1381 ATGCTACATG AGGTAGAAAA GGAAGCCCAA TCTGAAGCAG CAGCAAAAGG TATTGCTCCC
1441 ACAGAAGTAA CAATGGCGAT TAAATACGAT CGTAACAGTG ACCCAGGTAG ATATAATTCT
1501 CCCCGTGTAA CCGAGGTTGC TGTCATATTC AGAAACGAAG ATGGAGAACC TCCTTTTGAA
1561 AGGGACTTGC TCATTCATTG TAAACCAGAT CCCAATAATC CAAATGCCAC TAAAATGAAA
1621 CAAATCAGTA TCCTGTTTCC TACATTAGAT GCAATGACAT ATCCTATTCT TTTTCCACAT
1681 GGTGAAAAAG GCTGGGGAAC AGATATTGCA TTAAGACTCA GAGACAACAG TGTAATCGAC
1741 AATAATACTA GACAAAATGT AAGGACACGA GTCACACAAA TGCAGTATTA TGGATTTCAT
1801 CTCTCTGTGC GGGACACGTT CAATCCTATT TTAAATGCAG GAAAATTAAC TCAACAGTTT
1861 ATTGTGGATT CATATTCAAA AATGGAGGCC AATCGGATAA ATTTCATCAA AGCAAACCAA
1921 TCTAAGTTGA GAGTTGAAAA ATATAGTGGT TTGATGGATT ATCTCAAATC TAGATCTGAA
1981 AATGACAATG TGCCGATTGG TAAAATGATA ATACTTCCAT CATCTTTTGA GGGTAGTCCC
2041 AGAAATATGC AGCAGCGATA TCAGGATGCT ATGGCAATTG TAACGAAGTA TGGCAAGCCC
2101 GATTTATTCA TAACCATGAC ATGCAACCCC AAATGGGCAG ATATTACAAA CAATTTACAA
2161 CGCTGGCAAA AAGTTGAAAA CAGACCTGAC TTGGTAGCCA GAGTTTTTAA TATTAAGCTG
2221 AATGCTCTTT TAAATGATAT ATGTAAATTC CATTTATTTG GCAAAGTAAT AGCTAAAATT
2281 CATGTCATTG AATTTCAGAA ACGCGGACTG CCTCACGCTC ACATATTATT GATATTAGAT
2341 AGTGAGTCCA AATTACGTTC AGAAGATGAC ATTGACCGTA TAGTTAAGGC AGAAATTCCA
2401 GATGAAGACC AGTGTCCTCG ACTTTTTCAA ATTGTAAAAT CAAATATGGT ACATGGACCA
2461 TGTGGAATAC AAAATCCAAA TAGTCCATGT ATGGAAAATG GAAAATGTTC AAAGGGATAT
2521 CCAAAAGAAT TTCAAAATGC GACCATTGGA AATATTGATG GATATCCCAA ATACAAACGA
2581 AGATCTGGTA GCACCATGTC TATTGGAAAT AAAGTTGTCG ATAACACTTG GATTGTCCCT
2641 TATAACCCGT ATTTGTGCCT TAAATATAAC TGTCATATAA ATGTTGAAGT CTGTGCATCA
2701 ATTAAAAGTG TCAAATATTT ATTTAAATAC ATCTATAAAG GGCACGATTG TGCAAATATT
2761 CAAATTTCTG AAAAAAATAT TATCAATCAT GACGAAGTAC AGGACTTCAT TGACTCCAGG
2821 TATGTGAGCG CTCCTGAGGC TGTTTGGAGA CTTTTTGCAA TGCGAATGCA TGACCAATCT
2881 CATGCAATCA CAAGATTAGC TATTCATTTG CCAAATGATC AGAATTTGTA TTTTCATACC
2941 GATGATTTTG CTGAAGTTTT AGATAGGGCT AAAAGGCATA ACTCGACTTT GATGGCTTGG
3001 TTCTTATTGA ATAGAGAAGA TTCTGATGCA CGTAATTATT ATTATTGGGA GATTCCACAG
3061 CATTATGTGT TTAATAATTC TTTGTGGACA AAACGCCGAA AGGGTGGGAA TAAAGTATTA
3121 GGTAGACTGT TCACTGTGAG CTTTAGAGAA CCAGAACGAT ATTACCTTAG ACTTTTGCTT
3181 CTGCATGTAA AAGGTGCGAT AAGTTTTGAG GATCTGCGAA CTGTAGGAGG TGTAACTTAT
3241 GATACATTTC ATGAAGCTGC TAAACACCGA GGATTATTAC TTGATGACAC TATCTGGAAA
3301 GATACGATTG ACGATGCAAT CATCCTTAAT ATGCCCAAAC AACTACGGCA ACTTTTTGCA
3361 TATATATGTG TGTTTGGATG TCCTTCTGCT GCAGACAAAT TATGGGATGA GAATAAATCT
3421 CATTTTATTG AAGATTTCTG TTGGAAATTA CACCGAAGAG AAGGTGCCTG TGTGAACTGT
3481 GAAATGCATG CCCTTAACGA AATTCAGGAG GTATTCACAT TGCATGGAAT GAAATGTTCA
3541 CATTTCAAAC TTCCGGACTA TCCTTTATTA ATGAATGCAA ATACATGTGA TCAATTGTAC
3601 GAGCAACAAC AGGCAGAGGT TTTGATAAAT TCTCTGAATG ATGAACAGTT GGCAGCCTTT
3661 CAGACTATAA CTTCAGCCAT CGAAGATCAA ACTGTACACC CCAAATGCTT TTTCTTGGAT
3721 GGTCCAGGTG GTAGTGGAAA AACATATCTG TATAAAGTTT TAACACATTA TATTAGAGGT
3781 CGTGGTGGTA CTGTTTTACC CACAGCATCT ACAGGAATTG CTGCAAATTT ACTTCTTGGT
3841 GGAAGAACCT TTCATTCCCA ATATAAATTA CCAATTCCAT TAAATGAAAC TTCAATTTCT
3901 AGACTCGATA TAAAGAGTGA AGTTGCTAAA ACCATTAAAA AGGCCCAACT TCTCATTATT
3961 GATGAATGCA CCATGGCATC CAGTCATGCT ATAAACGCCA TAGATAGATT ACTAAGAGAA
4021 ATTATGAATT TGAATGTTGC ATTTGGTGGG AAAGTTCTCC TTCTCGGAGG GGATTTTCGA
4081 CAATGTCTCA GTATTGTACC ACATGCTATG CGATCGGCCA TAGTACAAAC GAGTTTAAAG
4141 TACTGTAATG TTTGGGGATG TTTCAGAAAG TTGTCTCTTA AAACAAATAT GAGATCAGAG
4201 GATTCTGCTT ATAGTGAATG GTTAGTAAAA CTTGGAGATG GCAAACTTGA TAGCAGTTTT
4261 CATTTAGGAA TGGATATTAT TGAAATCCCC CATGAAATGA TTTGTAACGG ATCTATTATT
4321 GAAGCTACCT TTGGAAATAG TATATCTATA GATAATATTA AAAATATATC TAAACGTGCA
4381 ATTCTTTGTC CAAAAAATGA GCATGTTCAA AAATTAAATG AAGAAATTTT GGATATACTT
4441 GATGGAGATT TTCACACATA TTTGAGTGAT GATTCCATTG ATTCAACAGA TGATGCTGAA
4501 AAGGAAAATT TTCCCATCGA ATTTCTTAAT AGTATTACTC CTTCGGGAAT GCCGTGTCAT
4561 AAATTAAAAT TGAAAGTGGG TGCAATCATC ATGCTATTGA GAAATCTTAA TAGTAAATGG
4621 GGTCTTTGTA ATGGTACTAG ATTTATTATC AAAAGATTAC GACCTAACAT TATCGAAGCT
4681 GAAGTATTAA CAGGATCTGC AGAGGGAGAG GTTGTTCTGA TTCCAAGAAT TGATTTGTCC
4741 CCATCTGACA CTGGCCTCCC ATTTAAATTA ATTCGAAGAC AGTTTCCCGT GATGCCAGCA
4801 TTTGCGATGA CTATTAATAA ATCACAAGGA CAAACTCTAG ACAGAGTAGG AATATTCCTA
4861 CCTGAACCCG TTTTCGCACA TGGTCAGTTA TATGTTGCTT TCTCTCGAGT TCGAAGAGCA
4921 TGTGACGTTA AAGTTAAAGT TGTAAATACT TCATCACAAG GGAAATTAGT CAAGCACTCT
4981 GAAAGTGTTT TTACTCTTAA TGTGGTATAC AGGGAGATAT TAGAATAAGT TTAATCACTT
5041 TATCAGTCAT TGTTTGCATC AATGTTGTTT TTATATCATG TTTTTGTTGT TTTTATATCA
5101 TGTCTTTGTT GTTGTTATAT CATGTTGTTA TTGTTTATTT ATTAATAAAT TTATGTATTA
5161 TTTTCATATA CATTTTACTC ATTTCCTTTC ATCTCTCACA CTTCTATTAT AGAGAAAGGG
5221 CAAATAGCAA TATTAAAATA TTTCCTCTAA TTAATTCCCT TTCAATGTGC ACGAATTTCG
5281 TGCACCGGGC CACTAG (SEQ ID NO: 21).
[0162] В отличии от других транспозаз транспозаза Helitron не содержит РНКазаH-подобный каталитический домен, но вместо этого содержит мотив RepHel, состоящий домена инициатора репликации (Rep) и домена ДНК геликазы. Rep-домен является нуклеазным доменом суперсемейства нуклеаз HUH.
[0163] Типовая транспозаза Helitron по изобретению включает в себя аминокислотную последовательность, содержащую:
1 MSKEQLLIQR SSAAERCRRY RQKMSAEQRA SDLERRRRLQ QNVSEEQLLE KRRSEAEKQR
61 RHRQKMSKDQ RAFEVERRRW RRQNMSREQS STSTTNTGRN CLLSKNGVHE DAILEHSCGG
121 MTVRCEFCLS LNFSDEKPSD GKFTRCCSKG KVCPNDIHFP DYPAYLKRLM TNEDSDSKNF
181 MENIRSINSS FAFASMGANI ASPSGYGPYC FRIHGQVYHR TGTLHPSDGV SRKFAQLYIL
241 DTAEATSKRL AMPENQGCSE RLMININNLM HEINELTKSY KMLHEVEKEA QSEAAAKGIA
301 PTEVTMAIKY DRNSDPGRYN SPRVTEVAVI FRNEDGEPPF ERDLLIHCKP DPNNPNATKM
361 KQISILFPTL DAMTYPILFP HGEKGWGTDI ALRLRDNSVI DNNTRQNVRT RVTQMQYYGF
421 HLSVRDTFNP ILNAGKLTQQ FIVDSYSKME ANRINFIKAN QSKLRVEKYS GLMDYLKSRS
481 ENDNVPIGKM IILPSSFEGS PRNMQQRYQD AMAIVTKYGK PDLFITMTCN PKWADITNNL
541 QRWQKVENRP DLVARVFNIK LNALLNDICK FHLFGKVIAK IHVIEFQKRG LPHAHILLIL
601 DSESKLRSED DIDRIVKAEI PDEDQCPRLF QIVKSNMVHG PCGIQNPNSP CMENGKCSKG
661 YPKEFQNATI GNIDGYPKYK RRSGSTMSIG NKVVDNTWIV PYNPYLCLKY NCHINVEVCA
721 SIKSVKYLFK YIYKGHDCAN IQISEKNIIN HDEVQDFIDS RYVSAPEAVW RLFAMRMHDQ
781 SHAITRLAIH LPNDQNLYFH TDDFAEVLDR AKRHNSTLMA WFLLNREDSD ARNYYYWEIP
841 QHYVFNNSLW TKRRKGGNKV LGRLFTVSFR EPERYYLRLL LLHVKGAISF EDLRTVGGVT
901 YDTFHEAAKH RGLLLDDTIW KDTIDDAIIL NMPKQLRQLF AYICVFGCPS AADKLWDENK
961 SHFIEDFCWK LHRREGACVN CEMHALNEIQ EVFTLHGMKC SHFKLPDYPL LMNANTCDQL
1021 YEQQQAEVLI NSLNDEQLAA FQTITSAIED QTVHPKCFFL DGPGGSGKTY LYKVLTHYIR
1081 GRGGTVLPTA STGIAANLLL GGRTFHSQYK LPIPLNETSI SRLDIKSEVA KTIKKAQLLI
1141 IDECTMASSH AINAIDRLLR EIMNLNVAFG GKVLLLGGDF RQCLSIVPHA MRSAIVQTSL
1201 KYCNVWGCFR KLSLKTNMRS EDSAYSEWLV KLGDGKLDSS FHLGMDIIEI PHEMICNGSI
1261 IEATFGNSIS IDNIKNISKR AILCPKNEHV QKLNEEILDI LDGDFHTYLS DDSIDSTDDA
1321 EKENFPIEFL NSITPSGMPC HKLKLKVGAI IMLLRNLNSK WGLCNGTRFI IKRLRPNIIE
1381 AEVLTGSAEG EVVLIPRIDL SPSDTGLPFK LIRRQFPVMP AFAMTINKSQ GQTLDRVGIF
1441 LPEPVFAHGQ LYVAFSRVRR ACDVKVKVVN TSSQGKLVKH SESVFTLNVV YREILE (SEQ ID NO: 22).
[0164] При транспозициях Helitron шпилька ближе к 3'-концу транспозона функционирует как терминатор. Однако транспозаза может обойти эта шпильку, что приводит в результате к трансдукции фланкирующих последовательностей. Кроме того, при транспозиции Helraiser генерируются ковалентно замкнутые кольцевые промежуточные продукты. Кроме того, при транспозиции Helitron может отсутствовать удвоение (дупликация) сайта-мишени. В последовательности Helraiser, транспозаза фланкирована левой и правой концевыми (терминальными) последовательностями, называемыми LTS и RTS. Эти последовательности заканчиваются консервативным мотивом 5'-TC/CTAG-3'. Палиндромная последовательность длиной 19 п.о., которая способна образовать структуру терминирующей шпильки, находится на 11 нуклеотидов выше от RTS и состоит из последовательности GTGCACGAATTTCGTGCACCGGGCCACTAG (SEQ ID NO: 23).
[0165] В некоторых вариантах осуществления способов по изобретению, транспозаза является транспозазой Tol2. Транспозоны Tol2 могут быть выделены или получены из генома оризии, и могут быть аналогичны транспозонам семейства hAT. Типичные транспозоны Tol2 по изобретению кодируются последовательностью, содержащей около 4,7 т.п.о., и содержат ген, кодирующий транспозазу Tol2, который содержит четыре экзона. Типичная транспозаза Tol2 по изобретению включает в себя аминокислотную последовательность, содержащую нижеследующую последовательность:
1 MEEVCDSSAA ASSTVQNQPQ DQEHPWPYLR EFFSLSGVNK DSFKMKCVLC LPLNKEISAF
61 KSSPSNLRKH IERMHPNYLK NYSKLTAQKR KIGTSTHASS SKQLKVDSVF PVKHVSPVTV
121 NKAILRYIIQ GLHPFSTVDL PSFKELISTL QPGISVITRP TLRSKIAEAA LIMKQKVTAA
181 MSEVEWIATT TDCWTARRKS FIGVTAHWIN PGSLERHSAA LACKRLMGSH TFEVLASAMN
241 DIHSEYEIRD KVVCTTTDSG SNFMKAFRVF GVENNDIETE ARRCESDDTD SEGCGEGSDG
301 VEFQDASRVL DQDDGFEFQL PKHQKCACHL LNLVSSVDAQ KALSNEHYKK LYRSVFGKCQ
361 ALWNKSSRSA LAAEAVESES RLQLLRPNQT RWNSTFMAVD RILQICKEAG EGALRNICTS
421 LEVPMFNPAE MLFLTEWANT MRPVAKVLDI LQAETNTQLG WLLPSVHQLS LKLQRLHHSL
481 RYCDPLVDAL QQGIQTRFKH MFEDPEIIAA AILLPKFRTS WTNDETIIKR GMDYIRVHLE
541 PLDHKKELAN SSSDDEDFFA SLKPTTHEAS KELDGYLACV SDTRESLLTF PAICSLSIKT
601 NTPLPASAAC ERLFSTAGLL FSPKRARLDT NNFENQLLLK LNLRFYNFE (SEQ ID NO: 24).
[0166] Типичный транспозон Tol2 по изобретению, включая инвертированные повторы, субконцевые последовательности и транспозазу Tol2, кодируется нуклеотидной последовательностью, содержащей нижеследующую последовательность:
1 CAGAGGTGTA AAGTACTTGA GTAATTTTAC TTGATTACTG TACTTAAGTA TTATTTTTGG
61 GGATTTTTAC TTTACTTGAG TACAATTAAA AATCAATACT TTTACTTTTA CTTAATTACA
121 TTTTTTTAGA AAAAAAAGTA CTTTTTACTC CTTACAATTT TATTTACAGT CAAAAAGTAC
181 TTATTTTTTG GAGATCACTT CATTCTATTT TCCCTTGCTA TTACCAAACC AATTGAATTG
241 CGCTGATGCC CAGTTTAATT TAAATGTTAT TTATTCTGCC TATGAAAATC GTTTTCACAT
301 TATATGAAAT TGGTCAGACA TGTTCATTGG TCCTTTGGAA GTGACGTCAT GTCACATCTA
361 TTACCACAAT GCACAGCACC TTGACCTGGA AATTAGGGAA ATTATAACAG TCAATCAGTG
421 GAAGAAAATG GAGGAAGTAT GTGATTCATC AGCAGCTGCG AGCAGCACAG TCCAAAATCA
481 GCCACAGGAT CAAGAGCACC CGTGGCCGTA TCTTCGCGAA TTCTTTTCTT TAAGTGGTGT
541 AAATAAAGAT TCATTCAAGA TGAAATGTGT CCTCTGTCTC CCGCTTAATA AAGAAATATC
601 GGCCTTCAAA AGTTCGCCAT CAAACCTAAG GAAGCATATT GAGGTAAGTA CATTAAGTAT
661 TTTGTTTTAC TGATAGTTTT TTTTTTTTTT TTTTTTTTTT TTTTTGGGTG TGCATGTTTT
721 GACGTTGATG GCGCGCCTTT TATATGTGTA GTAGGCCTAT TTTCACTAAT GCATGCGATT
781 GACAATATAA GGCTCACGTA ATAAAATGCT AAAATGCATT TGTAATTGGT AACGTTAGGT
841 CCACGGGAAA TTTGGCGCCT ATTGCAGCTT TGAATAATCA TTATCATTCC GTGCTCTCAT
901 TGTGTTTGAA TTCATGCAAA ACACAAGAAA ACCAAGCGAG AAATTTTTTT CCAAACATGT
961 TGTATTGTCA AAACGGTAAC ACTTTACAAT GAGGTTGATT AGTTCATGTA TTAACTAACA
1021 TTAAATAACC ATGAGCAATA CATTTGTTAC TGTATCTGTT AATCTTTGTT AACGTTAGTT
1081 AATAGAAATA CAGATGTTCA TTGTTTGTTC ATGTTAGTTC ACAGTGCATT AACTAATGTT
1141 AACAAGATAT AAAGTATTAG TAAATGTTGA AATTAACATG TATACGTGCA GTTCATTATT
1201 AGTTCATGTT AACTAATGTA GTTAACTAAC GAACCTTATT GTAAAAGTGT TACCATCAAA
1261 ACTAATGTAA TGAAATCAAT TCACCCTGTC ATGTCAGCCT TACAGTCCTG TGTTTTTGTC
1321 AATATAATCA GAAATAAAAT TAATGTTTGA TTGTCACTAA ATGCTACTGT ATTTCTAAAA
1381 TCAACAAGTA TTTAACATTA TAAAGTGTGC AATTGGCTGC AAATGTCAGT TTTATTAAAG
1441 GGTTAGTTCA CCCAAAAATG AAAATAATGT CATTAATGAC TCGCCCTCAT GTCGTTCCAA
1501 GCCCGTAAGA CCTCCGTTCA TCTTCAGAAC ACAGTTTAAG ATATTTTAGA TTTAGTCCGA
1561 GAGCTTTCTG TGCCTCCATT GAGAATGTAT GTACGGTATA CTGTCCATGT CCAGAAAGGT
1621 AATAAAAACA TCAAAGTAGT CCATGTGACA TCAGTGGGTT AGTTAGAATT TTTTGAAGCA
1681 TCGAATACAT TTTGGTCCAA AAATAACAAA ACCTACGACT TTATTCGGCA TTGTATTCTC
1741 TTCCGGGTCT GTTGTCAATC CGCGTTCACG ACTTCGCAGT GACGCTACAA TGCTGAATAA
1801 AGTCGTAGGT TTTGTTATTT TTGGACCAAA ATGTATTTTC GATGCTTCAA ATAATTCTAC
1861 CTAACCCACT GATGTCACAT GGACTACTTT GATGTTTTTA TTACCTTTCT GGACATGGAC
1921 AGTATACCGT ACATACATTT TCAGTGGAGG GACAGAAAGC TCTCGGACTA AATCTAAAAT
1981 ATCTTAAACT GTGTTCCGAA GATGAACGGA GGTGTTACGG GCTTGGAACG ACATGAGGGT
2041 GAGTCATTAA TGACATCTTT TCATTTTTGG GTGAACTAAC CCTTTAATGC TGTAATCAGA
2101 GAGTGTATGT GTAATTGTTA CATTTATTGC ATACAATATA AATATTTATT TGTTGTTTTT
2161 ACAGAGAATG CACCCAAATT ACCTCAAAAA CTACTCTAAA TTGACAGCAC AGAAGAGAAA
2221 GATCGGGACC TCCACCCATG CTTCCAGCAG TAAGCAACTG AAAGTTGACT CAGTTTTCCC
2281 AGTCAAACAT GTGTCTCCAG TCACTGTGAA CAAAGCTATA TTAAGGTACA TCATTCAAGG
2341 ACTTCATCCT TTCAGCACTG TTGATCTGCC ATCATTTAAA GAGCTGATTA GTACACTGCA
2401 GCCTGGCATT TCTGTCATTA CAAGGCCTAC TTTACGCTCC AAGATAGCTG AAGCTGCTCT
2461 GATCATGAAA CAGAAAGTGA CTGCTGCCAT GAGTGAAGTT GAATGGATTG CAACCACAAC
2521 GGATTGTTGG ACTGCACGTA GAAAGTCATT CATTGGTGTA ACTGCTCACT GGATCAACCC
2581 TGGAAGTCTT GAAAGACATT CCGCTGCACT TGCCTGCAAA AGATTAATGG GCTCTCATAC
2641 TTTTGAGGTA CTGGCCAGTG CCATGAATGA TATCCACTCA GAGTATGAAA TACGTGACAA
2701 GGTTGTTTGC ACAACCACAG ACAGTGGTTC CAACTTTATG AAGGCTTTCA GAGTTTTTGG
2761 TGTGGAAAAC AATGATATCG AGACTGAGGC AAGAAGGTGT GAAAGTGATG ACACTGATTC
2821 TGAAGGCTGT GGTGAGGGAA GTGATGGTGT GGAATTCCAA GATGCCTCAC GAGTCCTGGA
2881 CCAAGACGAT GGCTTCGAAT TCCAGCTACC AAAACATCAA AAGTGTGCCT GTCACTTACT
2941 TAACCTAGTC TCAAGCGTTG ATGCCCAAAA AGCTCTCTCA AATGAACACT ACAAGAAACT
3001 CTACAGATCT GTCTTTGGCA AATGCCAAGC TTTATGGAAT AAAAGCAGCC GATCGGCTCT
3061 AGCAGCTGAA GCTGTTGAAT CAGAAAGCCG GCTTCAGCTT TTAAGGCCAA ACCAAACGCG
3121 GTGGAATTCA ACTTTTATGG CTGTTGACAG AATTCTTCAA ATTTGCAAAG AAGCAGGAGA
3181 AGGCGCACTT CGGAATATAT GCACCTCTCT TGAGGTTCCA ATGTAAGTGT TTTTCCCCTC
3241 TATCGATGTA AACAAATGTG GGTTGTTTTT GTTTAATACT CTTTGATTAT GCTGATTTCT
3301 CCTGTAGGTT TAATCCAGCA GAAATGCTGT TCTTGACAGA GTGGGCCAAC ACAATGCGTC
3361 CAGTTGCAAA AGTACTCGAC ATCTTGCAAG CGGAAACGAA TACACAGCTG GGGTGGCTGC
3421 TGCCTAGTGT CCATCAGTTA AGCTTGAAAC TTCAGCGACT CCACCATTCT CTCAGGTACT
3481 GTGACCCACT TGTGGATGCC CTACAACAAG GAATCCAAAC ACGATTCAAG CATATGTTTG
3541 AAGATCCTGA GATCATAGCA GCTGCCATCC TTCTCCCTAA ATTTCGGACC TCTTGGACAA
3601 ATGATGAAAC CATCATAAAA CGAGGTAAAT GAATGCAAGC AACATACACT TGACGAATTC
3661 TAATCTGGGC AACCTTTGAG CCATACCAAA ATTATTCTTT TATTTATTTA TTTTTGCACT
3721 TTTTAGGAAT GTTATATCCC ATCTTTGGCT GTGATCTCAA TATGAATATT GATGTAAAGT
3781 ATTCTTGCAG CAGGTTGTAG TTATCCCTCA GTGTTTCTTG AAACCAAACT CATATGTATC
3841 ATATGTGGTT TGGAAATGCA GTTAGATTTT ATGCTAAAAT AAGGGATTTG CATGATTTTA
3901 GATGTAGATG ACTGCACGTA AATGTAGTTA ATGACAAAAT CCATAAAATT TGTTCCCAGT
3961 CAGAAGCCCC TCAACCAAAC TTTTCTTTGT GTCTGCTCAC TGTGCTTGTA GGCATGGACT
4021 ACATCAGAGT GCATCTGGAG CCTTTGGACC ACAAGAAGGA ATTGGCCAAC AGTTCATCTG
4081 ATGATGAAGA TTTTTTCGCT TCTTTGAAAC CGACAACACA TGAAGCCAGC AAAGAGTTGG
4141 ATGGATATCT GGCCTGTGTT TCAGACACCA GGGAGTCTCT GCTCACGTTT CCTGCTATTT
4201 GCAGCCTCTC TATCAAGACT AATACACCTC TTCCCGCATC GGCTGCCTGT GAGAGGCTTT
4261 TCAGCACTGC AGGATTGCTT TTCAGCCCCA AAAGAGCTAG GCTTGACACT AACAATTTTG
4321 AGAATCAGCT TCTACTGAAG TTAAATCTGA GGTTTTACAA CTTTGAGTAG CGTGTACTGG
4381 CATTAGATTG TCTGTCTTAT AGTTTGATAA TTAAATACAA ACAGTTCTAA AGCAGGATAA
4441 AACCTTGTAT GCATTTCATT TAATGTTTTT TGAGATTAAA AGCTTAAACA AGAATCTCTA
4501 GTTTTCTTTC TTGCTTTTAC TTTTACTTCC TTAATACTCA AGTACAATTT TAATGGAGTA
4561 CTTTTTTACT TTTACTCAAG TAAGATTCTA GCCAGATACT TTTACTTTTA ATTGAGTAAA
4621 ATTTTCCCTA AGTACTTGTA CTTTCACTTG AGTAAAATTT TTGAGTACTT TTTACACCTC
4681 TG (SEQ ID NO: 25).
[0167] ДНК-вставка должна быть функционально связана с соответствующим промотором. Экспрессирующие конструкции будут дополнительно содержать сайты инициации, терминации транскрипции и в транскрибируемой области - сайт связывания рибосомы для трансляции. Кодирующая часть зрелых транскриптов, экспрессируемых этими конструкциями, предпочтительно, будет включать в себя сайт инициации трансляции в начале и терминирующий кодон (например, UAA, UGA или UAG), соответствующим образом расположенный в конце мРНК, подлежащей трансляции, с предпочтительными UAA и UAG. для экспрессии в клетках млекопитающих или эукариотических клетках.
[0168] Экспрессионные векторы предпочтительно, но необязательно, включают по меньшей мере один селектируемый маркер. Такие маркеры включают, например, но не ограничиваются ими, гены резистентности к ампициллину, зеоцину (ген Sh bla), пуромицину (ген pac), гигромицину B (ген hygB), G418/генетицину (ген neo), микофеноловой кислоте и бластицидину (ген bsd) или глутаминсинтетазу (GS, патенты США №№ 5124644, 5770359, 5827739) для культуры эукариотических клеток, а также гены резистентности к ампициллину, зеоцину (ген Sh bla), пуромицину (ген pac), гигромицину B (ген hygB), G418/генетицину (ген neo), канамицину, спектиномицину, стрептомицину, карбенициллину, блеомицину, эритромицину, полимиксину B или тетрациклину для культивирования в E.coli и в других бактериях или прокариотах (вышеуказанные патенты полностью включены в настоящее описание посредством ссылки). Подходящие культуральные среды и условия для вышеописанных клеток-хозяев известны в данной области. Подходящие векторы будут очевидны для специалиста в данной области. Введение векторной конструкции в клетку-хозяина может осуществляться трансфекцией фосфатом кальция, опосредованной DEAE-декстраном трансфекцией, опосредованной катионными липидами трансфекцией, электропорацией, трансдукцией, инфекцией или другими известными способами. Такие способы описаны в данной области техники, например, в главах 1-4 и 16-18 из Sambrook, supra; главах 1, 9, 13, 15, 16 из Ausubel, supra.
[0169] Экспрессионные векторы предпочтительно, но необязательно, включают по меньшей мере один селектируемый маркер клеточной поверхности для выделения клеток, модифицированных композициями и способами по настоящему изобретению. Селектируемые маркеры клеточной поверхности по изобретению включают поверхностные белки, гликопротеины или группу белков, которые отличают клетку или подмножество клеток от другого определенного подмножества клеток. Предпочтительно, чтобы селектируемый маркер клеточной поверхности позволял отличать клетки, модифицированные композицией или способом по изобретению, от клеток, которые не модифицированы композицией или способом по изобретению. Такие маркеры клеточной поверхности включают, например, но не ограничиваются ими, белки «кластера назначения» или «классификационной детерминанты» (часто сокращенно обозначаемые как «CD»), такие как усеченная или полноразмерная форма CD19, CD271, CD34, CD22, CD20, CD33, CD52 или любая их комбинация. Маркеры клеточной поверхности дополнительно включают маркер суицидного гена RQR8 (Philip B et al. Blood. 2014 Aug 21; 124 (8): 1277-87).
[0170] Экспрессионные векторы предпочтительно, но необязательно, включают по меньшей мере один селектируемый маркер устойчивости к лекарственному средству для выделения клеток, модифицированных композициями и способами по настоящему изобретению. Селективные маркеры лекарственной устойчивости по изобретению могут содержать дикий тип или мутантный Neo, DHFR, TYMS, FRANCF, RAD51C, GCS, MDR1, ALDH1, NKX2.2 или любую их комбинацию.
[0171] По меньшей мере один индуцируемый полипептид по изобретению может экспрессироваться в модифицированной форме, такой как слитый белок, и может включать дополнительные гетерологичные функциональные области. Например, область дополнительных аминокислот, особенно заряженных аминокислот, может быть добавлена к N-концу белкового каркаса для улучшения стабильности и устойчивости в клетке-хозяине, во время очистки или во время последующей обработки и хранения. Также пептидные фрагменты могут быть добавлены в каркас белка по настоящему изобретению для облегчения очистки. Такие области могут быть удалены до окончательного получения индуцируемого полипептида или по меньшей мере одного его фрагмента. Такие способы описаны во многих стандартных лабораторных руководствах, таких как главы 17.29-17.42 и 18.1-18.74 в Sambrook, supra; главы 16, 17 и 18 в Ausubel, supra.
[0172] Специалистам в данной области техники известны многочисленные системы экспрессии, доступные для экспрессии нуклеиновой кислоты, кодирующей белок по настоящему изобретению. В качестве альтернативы нуклеиновые кислоты по изобретению могут быть экспрессированы в клетке-хозяине путем включения (манипуляции) в клетке-хозяине, которая содержит последовательность, кодирующую индуцируемый полипептид по изобретению. Такие способы хорошо известны в данной области, например, описаны в патенте США №№ 5580734, 5641670, 5733746 и 5733761, полностью включенных в настоящий документ путем ссылки.
[0173] Экспрессионные векторы для модифицированных клеток могут включать одну или несколько из следующих последовательностей регуляции экспрессии, таких как, но не ограниченных ими, точка инициации репликации; промотор (например, поздние или ранние промоторы SV40, промотор CMV (патенты США №№ 5168062, 5385839), промотор HSV tk, промотор pgk (фосфоглицераткиназы), промотор EF-1-альфа (патент США № 5266491), по меньшей мере один промотор гена человека, энхансер и/или сайты обработки информации, такие как сайты связывания рибосом, сайты сплайсинга РНК, сайты полиаденилирования (например, сайт присоединения большого Т-антигена вируса SV40) и последовательности терминатора транскрипции. См., например, Ausubel et al., supra; Sambrook, et al., supra. Другие клетки, подходящие для получения нуклеиновых кислот или белков по настоящему изобретению, известны и/или доступны, например, из Американского каталога коллекций типовых культур для клеточных линий и гибридом (www.atcc.org) или других известных или коммерческих источников.
[0174] При использовании эукариотических клеток-хозяев в вектор обычно включают последовательности терминатора полиаденилирования или транскрипции. Примером последовательности терминатора является последовательность полиаденилирования из гена гормона роста крупного рогатого скота. Также могут быть включены последовательности для точного сплайсинга транскрипта. Примером сплайсинговой последовательности является интрон VP1 из SV40 (Sprague, et al., J. Virol. 45: 773-781 (1983)). Кроме того, в вектор могут быть включены последовательности генов для регуляции репликации в клетке-хозяине, известные в данной области.
Коды аминокислот
[0175] Аминокислоты, из которых состоят каркасы белков по настоящему изобретению, часто указываются сокращенно. Аминокислоты могут указываться с помощью однобуквенного кода, трехбуквенного кода, названия или трехнуклеотидного кодона (кодонов), как хорошо известно в данной области (см. Alberts, B., et al., Molecular Biology of The Cell, Third Ed., Garland Publishing, Inc., New York, 1994). Индуцируемый полипептид по настоящему изобретению может включать одну или несколько аминокислотных замен, делеций или добавок либо в результате естественных мутаций, либо манипуляций человека, как указано в данном описании. Аминокислоты в индуцируемом полипептиде по изобретению, которые важны для функции, могут быть идентифицированы способами, известными в данной области, такими как сайт-направленный мутагенез или аланин-сканирующий мутагенез (например, главы 8, 15 в Ausubel, supra; Cunningham and Wells Science 244: 1081-1085 (1989). В последней процедуре одиночные мутации на аланин вводят по каждому остатку в молекуле. Полученные мутантные молекулы затем тестируют на биологическую активность, такую как, но не ограниченную этим, по меньшей мере одна нейтрализующая активность. Участки, которые являются критическими для функции (т.е. вызывают апоптоз), также могут быть идентифицированы структурным анализом, таким как кристаллизация, ядерный магнитный резонанс или фотоаффинное мечение (Smith, et al., J. Mol. Biol. 224: 899-904 (1992) и de Vos et al., Science 255: 306-312 (1992)).
[0176] Биологически активный индуцируемый полипептид по изобретению включает в себя один или несколько белков или ферментов (например, каспазу, такую как каспаза 9), способных индуцировать апоптоз в клетке с эффективностью, которая по меньшей мере на 20%, 30% или 40% и, предпочтительно, по меньшей мере 50%, 60% или 70% и, наиболее предпочтительно, по меньшей мере 80%, 90% или 95-99% или более превышает таковую при экспрессией или индукцией нативного (не синтетического), эндогенного или родственного и известного белка или фермента. Способы анализа и количественной оценки связывания белка и ферментативной активности хорошо известны специалистам в данной области.
Инфузия модифицированных клеток в качестве адаптивной клеточной терапии
[0177] Изобретение относится к модифицированным клеткам, которые экспрессируют один или несколько индуцируемых полипептидов по изобретению, которые были отобраны для введения субъекту, нуждающемуся в этом. Модифицированные клетки по изобретению могут быть подготовлены для хранения при любой температуре, включая комнатную температуру и температуру тела. Модифицированные клетки по изобретению могут быть подготовлены для криоконсервации и последующей разморозки. Модифицированные клетки по изобретению могут быть изготовлены в фармацевтически приемлемом носителе для прямого введения субъекту из стерильной упаковки.
ПРИМЕРЫ
Пример 1: экспрессия и функция встроенного с помощью piggyBac защитного выключателя iC9 в пан Т-клетки человека
[0178] Пан-Т-клетки человека были подвергнуты нуклеофекции с использованием нуклеофектора Amaxa 4D с одним из четырех транспозонов piggyBac. Модифицированные Т-клетки из «пустой» группы подвергались нуклеофекции с пустым транспозоном piggyBac. Модифицированные Т-клетки получали либо транспозазу piggyBac, содержащую только терапевтический агент (последовательность, кодирующую CARTyrin), либо транспозазу piggyBac, содержащую интегрированную последовательность iC9, и терапевтический агент (последовательность, кодирующую CARTyrin).
[0179] На фиг.1 представлена принципиальная схема защитного выключателя iC9, который содержит лиганд-связывающую область, линкер и усеченный полипептид каспазы 9. Конкретно, полипептид iC9 содержит лиганд-связывающую область, содержащую полипептид связывающего FK506 белка 12 (FKBP12), включающий замену валином (V) фенилаланина (F) в положении 36 (F36V). Полипептид FKBP12 полипептида iC9 имеет аминокислотную последовательность, содержащую:
GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO: 3). Полипептид FKBP12 полипептида iC9 кодируется нуклеотидной последовательностью, содержащей:
GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGAT GTGGAACTGCTGAAGCTGGAG (SEQ ID NO: 4). Область линкера в полипептиде iC9 имеет аминокислотную последовательность, содержащую GGGGS (SEQ ID NO: 5) и кодируется нуклеотидной последовательностью, содержащей GGAGGAGGAGGATCC (SEQ ID NO: 6). Аминокислотная последовательность полипептида iC9 содержит: GFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRES GLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO: 7). Нуклеотидная последовательность, кодирующая полипептид iC9, содержит следующую последовательность:
TTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO: 8).
[0180] Для тестирования защитного выключателя iC9 каждый из четырех типов модифицированных Т-клеток инкубировали в течение 24 часов в отсутствие и с 0,1 нМ, 1 нМ, 10 нМ, 100 нМ или 1000 нМ AP1903 (индуцирующего агента AP1903, также известного как Римидуцид). Жизнеспособность оценивали с помощью проточной цитометрии с использованием 7-аминоактиномицина D (7-AAD), флуоресцентного интеркалятора, в качестве маркера для апоптозирующих клеток.
[0181] Жизнеспособность клеток оценивали на 12-й день (см. фиг.2). Данные демонстрируют сдвиг клеточных популяций из нижнего правого в верхний левый квадранты с увеличением концентрации индуцирующего агента в клетках, содержащих конструкцию iC9; однако этот эффект не наблюдается в клетках, в которых отсутствует конструкция iC9 (те, которые получали только CARTyrin), в которых клетки равномерно распределены между этими двумя областями независимо от концентрации индуцирующего агента. Кроме того, жизнеспособность клеток оценивали на 19-й день (см. фиг.3). Данные показывают ту же тенденцию, что и на фиг.2 (12-й день после нуклеофекции); однако смещение популяции в верхний левый квадрант более выражено в этот более поздний момент времени (19-й день после нуклеофекции).
[0182] Была проведена количественная оценка агрегатов, которая приведена на фиг.4, которая показала значительное влияние защитного выключателя iC9 на процент жизнеспособных клеток в зависимости от концентрации индуцирующего агента (AP1903, также известного как Римидуцид) для защитного выключателя iC9 для каждого модифицированного типа клеток в день 12 (фиг.2 и левый график) или день 19 (фиг.3 и правый график). Наличие защитного выключателя iC9 вызывает апоптоз у значительного большинства клеток к 12-му дню, а эффект к 19-му дню становится еще более выраженным.
[0183] Результаты этого исследования показывают, что защитный выключатель iC9 чрезвычайно эффективен для удаления активных клеток при контакте с индуцирующим агентом (например, AP1903, также известным как Римидуцид), потому что AP1903 (Римидуцид) вызывает апоптоз даже при самых низких исследуемых концентрациях (0,1 нМ). Кроме того, защитный выключатель iC9 может быть функционально проэкспрессирован как часть трицистронного вектора.
Пример 2: высокоэффективное уничтожение клеток, содержащих P-BCMA-101, с использованием защитного выключателя iC9 у мышей NGS in vivo .
[0184] Мышам NSG вводили внутривенной инъекцией клетки MM.1S/люцифераза+, мышей разделяли на 8-й день, вводили Т-клетки на 9-й день, и вводили AP1903 (Римидуцид) на 12-й день в указанных дозах. Через 24 ч мышей умерщвляли, и клетки крови, селезенки и костного мозга собирали и окрашивали на присутствие клеток huCD45+ (фиг.5). Клетки крови, селезенки и костного мозга анализировали проточной цитометрией на наличие клеток huCD45+. Относительную жизнеспособность определяли путем деления числа клеток huCD45 на количество клеток msCD45 и нормализации на среднее значение huCD45/msCD45 для групп без обработки, и умножения 100% для 1500 событий для каждого образца. Каждая точка данных представляет отдельную мышь (фиг.6).
ВКЛЮЧЕНИЕ ПУТЕМ ССЫЛКИ
[0185] Каждый документ, цитируемый в данном документе, включая любые перекрестные ссылки или связанные патенты или заявки, тем самым включается в настоящий документ путем ссылки во всей своей полноте, если это явно не исключено или иным образом не ограничено. Цитирование любого документа не является признанием того, что он является прототипом в отношении любого изобретения, раскрытого или заявленного в настоящем документе, или что он сам по себе или в любой комбинации с любой другой ссылкой или ссылками, сообщает, предлагает или раскрывает любое такое изобретение. Кроме того, в той степени, в которой любое значение или определение термина в этом документе вступает в противоречие с любым значением или определением того же термина в документе, включенном путем ссылки, значение или определение, присвоенные этому термину в этом документе, должны превалировать.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0186] Хотя конкретные варианты осуществления изобретения были проиллюстрированы и описаны, различные другие изменения и модификации могут быть осуществлены без отклонения от сущности и объема изобретения. Объем прилагаемой формулы изобретения включает в себя все такие изменения и модификации, которые входят в объем данного изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> POSEIDA THERAPEUTICS, INC
OSTERTAG, Eric
SHEDLOCK, Devon
<120> ИНДУЦИРУЕМЫЕ КАСПАЗЫ И СПОСОБЫ ПРИМЕНЕНИЯ
<130> POTH-012/001WO
<150> 62/405,184
<151> 2016-10-06
<160> 25
<170> PatentIn version 3.5
<210> 1
<211> 594
<212> Белок
<213> Trichoplusia ni
<400> 1
Met Gly Ser Ser Leu Asp Asp Glu His Ile Leu Ser Ala Leu Leu Gln
1 5 10 15
Ser Asp Asp Glu Leu Val Gly Glu Asp Ser Asp Ser Glu Ile Ser Asp
20 25 30
His Val Ser Glu Asp Asp Val Gln Ser Asp Thr Glu Glu Ala Phe Ile
35 40 45
Asp Glu Val His Glu Val Gln Pro Thr Ser Ser Gly Ser Glu Ile Leu
50 55 60
Asp Glu Gln Asn Val Ile Glu Gln Pro Gly Ser Ser Leu Ala Ser Asn
65 70 75 80
Arg Ile Leu Thr Leu Pro Gln Arg Thr Ile Arg Gly Lys Asn Lys His
85 90 95
Cys Trp Ser Thr Ser Lys Ser Thr Arg Arg Ser Arg Val Ser Ala Leu
100 105 110
Asn Ile Val Arg Ser Gln Arg Gly Pro Thr Arg Met Cys Arg Asn Ile
115 120 125
Tyr Asp Pro Leu Leu Cys Phe Lys Leu Phe Phe Thr Asp Glu Ile Ile
130 135 140
Ser Glu Ile Val Lys Trp Thr Asn Ala Glu Ile Ser Leu Lys Arg Arg
145 150 155 160
Glu Ser Met Thr Gly Ala Thr Phe Arg Asp Thr Asn Glu Asp Glu Ile
165 170 175
Tyr Ala Phe Phe Gly Ile Leu Val Met Thr Ala Val Arg Lys Asp Asn
180 185 190
His Met Ser Thr Asp Asp Leu Phe Asp Arg Ser Leu Ser Met Val Tyr
195 200 205
Val Ser Val Met Ser Arg Asp Arg Phe Asp Phe Leu Ile Arg Cys Leu
210 215 220
Arg Met Asp Asp Lys Ser Ile Arg Pro Thr Leu Arg Glu Asn Asp Val
225 230 235 240
Phe Thr Pro Val Arg Lys Ile Trp Asp Leu Phe Ile His Gln Cys Ile
245 250 255
Gln Asn Tyr Thr Pro Gly Ala His Leu Thr Ile Asp Glu Gln Leu Leu
260 265 270
Gly Phe Arg Gly Arg Cys Pro Phe Arg Met Tyr Ile Pro Asn Lys Pro
275 280 285
Ser Lys Tyr Gly Ile Lys Ile Leu Met Met Cys Asp Ser Gly Thr Lys
290 295 300
Tyr Met Ile Asn Gly Met Pro Tyr Leu Gly Arg Gly Thr Gln Thr Asn
305 310 315 320
Gly Val Pro Leu Gly Glu Tyr Tyr Val Lys Glu Leu Ser Lys Pro Val
325 330 335
His Gly Ser Cys Arg Asn Ile Thr Cys Asp Asn Trp Phe Thr Ser Ile
340 345 350
Pro Leu Ala Lys Asn Leu Leu Gln Glu Pro Tyr Lys Leu Thr Ile Val
355 360 365
Gly Thr Val Arg Ser Asn Lys Arg Glu Ile Pro Glu Val Leu Lys Asn
370 375 380
Ser Arg Ser Arg Pro Val Gly Thr Ser Met Phe Cys Phe Asp Gly Pro
385 390 395 400
Leu Thr Leu Val Ser Tyr Lys Pro Lys Pro Ala Lys Met Val Tyr Leu
405 410 415
Leu Ser Ser Cys Asp Glu Asp Ala Ser Ile Asn Glu Ser Thr Gly Lys
420 425 430
Pro Gln Met Val Met Tyr Tyr Asn Gln Thr Lys Gly Gly Val Asp Thr
435 440 445
Leu Asp Gln Met Cys Ser Val Met Thr Cys Ser Arg Lys Thr Asn Arg
450 455 460
Trp Pro Met Ala Leu Leu Tyr Gly Met Ile Asn Ile Ala Cys Ile Asn
465 470 475 480
Ser Phe Ile Ile Tyr Ser His Asn Val Ser Ser Lys Gly Glu Lys Val
485 490 495
Gln Ser Arg Lys Lys Phe Met Arg Asn Leu Tyr Met Ser Leu Thr Ser
500 505 510
Ser Phe Met Arg Lys Arg Leu Glu Ala Pro Thr Leu Lys Arg Tyr Leu
515 520 525
Arg Asp Asn Ile Ser Asn Ile Leu Pro Asn Glu Val Pro Gly Thr Ser
530 535 540
Asp Asp Ser Thr Glu Glu Pro Val Met Lys Lys Arg Thr Tyr Cys Thr
545 550 555 560
Tyr Cys Pro Ser Lys Ile Arg Arg Lys Ala Asn Ala Ser Cys Lys Lys
565 570 575
Cys Lys Lys Val Ile Cys Arg Glu His Asn Ile Asp Met Cys Gln Ser
580 585 590
Cys Phe
<210> 2
<211> 594
<212> Белок
<213> Искусственная последовательность
<220>
<223> Транспозаза Super PiggyBac
<400> 2
Met Gly Ser Ser Leu Asp Asp Glu His Ile Leu Ser Ala Leu Leu Gln
1 5 10 15
Ser Asp Asp Glu Leu Val Gly Glu Asp Ser Asp Ser Glu Val Ser Asp
20 25 30
His Val Ser Glu Asp Asp Val Gln Ser Asp Thr Glu Glu Ala Phe Ile
35 40 45
Asp Glu Val His Glu Val Gln Pro Thr Ser Ser Gly Ser Glu Ile Leu
50 55 60
Asp Glu Gln Asn Val Ile Glu Gln Pro Gly Ser Ser Leu Ala Ser Asn
65 70 75 80
Arg Ile Leu Thr Leu Pro Gln Arg Thr Ile Arg Gly Lys Asn Lys His
85 90 95
Cys Trp Ser Thr Ser Lys Ser Thr Arg Arg Ser Arg Val Ser Ala Leu
100 105 110
Asn Ile Val Arg Ser Gln Arg Gly Pro Thr Arg Met Cys Arg Asn Ile
115 120 125
Tyr Asp Pro Leu Leu Cys Phe Lys Leu Phe Phe Thr Asp Glu Ile Ile
130 135 140
Ser Glu Ile Val Lys Trp Thr Asn Ala Glu Ile Ser Leu Lys Arg Arg
145 150 155 160
Glu Ser Met Thr Ser Ala Thr Phe Arg Asp Thr Asn Glu Asp Glu Ile
165 170 175
Tyr Ala Phe Phe Gly Ile Leu Val Met Thr Ala Val Arg Lys Asp Asn
180 185 190
His Met Ser Thr Asp Asp Leu Phe Asp Arg Ser Leu Ser Met Val Tyr
195 200 205
Val Ser Val Met Ser Arg Asp Arg Phe Asp Phe Leu Ile Arg Cys Leu
210 215 220
Arg Met Asp Asp Lys Ser Ile Arg Pro Thr Leu Arg Glu Asn Asp Val
225 230 235 240
Phe Thr Pro Val Arg Lys Ile Trp Asp Leu Phe Ile His Gln Cys Ile
245 250 255
Gln Asn Tyr Thr Pro Gly Ala His Leu Thr Ile Asp Glu Gln Leu Leu
260 265 270
Gly Phe Arg Gly Arg Cys Pro Phe Arg Val Tyr Ile Pro Asn Lys Pro
275 280 285
Ser Lys Tyr Gly Ile Lys Ile Leu Met Met Cys Asp Ser Gly Thr Lys
290 295 300
Tyr Met Ile Asn Gly Met Pro Tyr Leu Gly Arg Gly Thr Gln Thr Asn
305 310 315 320
Gly Val Pro Leu Gly Glu Tyr Tyr Val Lys Glu Leu Ser Lys Pro Val
325 330 335
His Gly Ser Cys Arg Asn Ile Thr Cys Asp Asn Trp Phe Thr Ser Ile
340 345 350
Pro Leu Ala Lys Asn Leu Leu Gln Glu Pro Tyr Lys Leu Thr Ile Val
355 360 365
Gly Thr Val Arg Ser Asn Lys Arg Glu Ile Pro Glu Val Leu Lys Asn
370 375 380
Ser Arg Ser Arg Pro Val Gly Thr Ser Met Phe Cys Phe Asp Gly Pro
385 390 395 400
Leu Thr Leu Val Ser Tyr Lys Pro Lys Pro Ala Lys Met Val Tyr Leu
405 410 415
Leu Ser Ser Cys Asp Glu Asp Ala Ser Ile Asn Glu Ser Thr Gly Lys
420 425 430
Pro Gln Met Val Met Tyr Tyr Asn Gln Thr Lys Gly Gly Val Asp Thr
435 440 445
Leu Asp Gln Met Cys Ser Val Met Thr Cys Ser Arg Lys Thr Asn Arg
450 455 460
Trp Pro Met Ala Leu Leu Tyr Gly Met Ile Asn Ile Ala Cys Ile Asn
465 470 475 480
Ser Phe Ile Ile Tyr Ser His Asn Val Ser Ser Lys Gly Glu Lys Val
485 490 495
Gln Ser Arg Lys Lys Phe Met Arg Asn Leu Tyr Met Ser Leu Thr Ser
500 505 510
Ser Phe Met Arg Lys Arg Leu Glu Ala Pro Thr Leu Lys Arg Tyr Leu
515 520 525
Arg Asp Asn Ile Ser Asn Ile Leu Pro Lys Glu Val Pro Gly Thr Ser
530 535 540
Asp Asp Ser Thr Glu Glu Pro Val Met Lys Lys Arg Thr Tyr Cys Thr
545 550 555 560
Tyr Cys Pro Ser Lys Ile Arg Arg Lys Ala Asn Ala Ser Cys Lys Lys
565 570 575
Cys Lys Lys Val Ile Cys Arg Glu His Asn Ile Asp Met Cys Gln Ser
580 585 590
Cys Phe
<210> 3
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Полученный из FKBP12 полипептид
<400> 3
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu
100 105
<210> 4
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, кодирующая полученный из FKBP12 полипептид
<400> 4
ggggtccagg tcgagactat ttcaccaggg gatgggcgaa catttccaaa aaggggccag 60
acttgcgtcg tgcattacac cgggatgctg gaggacggga agaaagtgga cagctccagg 120
gatcgcaaca agcccttcaa gttcatgctg ggaaagcagg aagtgatccg aggatgggag 180
gaaggcgtgg cacagatgtc agtcggccag cgggccaaac tgaccattag ccctgactac 240
gcttatggag caacaggcca cccagggatc attccccctc atgccaccct ggtcttcgat 300
gtggaactgc tgaagctgga g 321
<210> 5
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> линкер
<400> 5
Gly Gly Gly Gly Ser
1 5
<210> 6
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, кодирующая линкер
<400> 6
ggaggaggag gatcc 15
<210> 7
<211> 282
<212> Белок
<213> Искусственная последовательность
<220>
<223> Усеченная каспаза 9
<400> 7
Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly Asn Ala Asp
1 5 10 15
Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys Leu Ile Ile
20 25 30
Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr Arg Thr Gly
35 40 45
Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser Ser Leu His
50 55 60
Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys Met Val Leu
65 70 75 80
Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu Asp Cys Cys
85 90 95
Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His Leu Gln Phe
100 105 110
Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser Val Glu Lys
115 120 125
Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu Gly Gly Lys
130 135 140
Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln Lys Asp His
145 150 155 160
Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser Pro Gly Ser
165 170 175
Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu Arg Thr Phe
180 185 190
Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser Asp Ile Phe
195 200 205
Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg Asp Pro Lys
210 215 220
Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe Glu Gln Trp
225 230 235 240
Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val Ala Asn Ala
245 250 255
Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys Phe Asn Phe
260 265 270
Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
275 280
<210> 8
<211> 843
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Усеченная каспаза 9
<400> 8
tttggggacg tgggggccct ggagtctctg cgaggaaatg ccgatctggc ttacatcctg 60
agcatggaac cctgcggcca ctgtctgatc attaacaatg tgaacttctg cagagaaagc 120
ggactgcgaa cacggactgg ctccaatatt gactgtgaga agctgcggag aaggttctct 180
agtctgcact ttatggtcga agtgaaaggg gatctgaccg ccaagaaaat ggtgctggcc 240
ctgctggagc tggctcagca ggaccatgga gctctggatt gctgcgtggt cgtgatcctg 300
tcccacgggt gccaggcttc tcatctgcag ttccccggag cagtgtacgg aacagacggc 360
tgtcctgtca gcgtggagaa gatcgtcaac atcttcaacg gcacttcttg ccctagtctg 420
gggggaaagc caaaactgtt ctttatccag gcctgtggcg gggaacagaa agatcacggc 480
ttcgaggtgg ccagcaccag ccctgaggac gaatcaccag ggagcaaccc tgaaccagat 540
gcaactccat tccaggaggg actgaggacc tttgaccagc tggatgctat ctcaagcctg 600
cccactccta gtgacatttt cgtgtcttac agtaccttcc caggctttgt ctcatggcgc 660
gatcccaagt cagggagctg gtacgtggag acactggacg acatctttga acagtgggcc 720
cattcagagg acctgcagag cctgctgctg cgagtggcaa acgctgtctc tgtgaagggc 780
atctacaaac agatgcccgg gtgcttcaat tttctgagaa agaaactgtt ctttaagact 840
tcc 843
<210> 9
<211> 394
<212> Белок
<213> Искусственная последовательность
<220>
<223> Индуцируемый проапоптотический полипептид
<400> 9
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Gly Gly Gly Gly Ser
100 105 110
Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly Asn Ala Asp
115 120 125
Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys Leu Ile Ile
130 135 140
Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr Arg Thr Gly
145 150 155 160
Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser Ser Leu His
165 170 175
Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys Met Val Leu
180 185 190
Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu Asp Cys Cys
195 200 205
Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His Leu Gln Phe
210 215 220
Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser Val Glu Lys
225 230 235 240
Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu Gly Gly Lys
245 250 255
Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln Lys Asp His
260 265 270
Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser Pro Gly Ser
275 280 285
Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu Arg Thr Phe
290 295 300
Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser Asp Ile Phe
305 310 315 320
Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg Asp Pro Lys
325 330 335
Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe Glu Gln Trp
340 345 350
Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val Ala Asn Ala
355 360 365
Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys Phe Asn Phe
370 375 380
Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
385 390
<210> 10
<211> 1182
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Нуклеиновая кислота, кодирующая индуцируемый проапоптотический полипептид
<400> 10
ggggtccagg tcgagactat ttcaccaggg gatgggcgaa catttccaaa aaggggccag 60
acttgcgtcg tgcattacac cgggatgctg gaggacggga agaaagtgga cagctccagg 120
gatcgcaaca agcccttcaa gttcatgctg ggaaagcagg aagtgatccg aggatgggag 180
gaaggcgtgg cacagatgtc agtcggccag cgggccaaac tgaccattag ccctgactac 240
gcttatggag caacaggcca cccagggatc attccccctc atgccaccct ggtcttcgat 300
gtggaactgc tgaagctgga gggaggagga ggatccggat ttggggacgt gggggccctg 360
gagtctctgc gaggaaatgc cgatctggct tacatcctga gcatggaacc ctgcggccac 420
tgtctgatca ttaacaatgt gaacttctgc agagaaagcg gactgcgaac acggactggc 480
tccaatattg actgtgagaa gctgcggaga aggttctcta gtctgcactt tatggtcgaa 540
gtgaaagggg atctgaccgc caagaaaatg gtgctggccc tgctggagct ggctcagcag 600
gaccatggag ctctggattg ctgcgtggtc gtgatcctgt cccacgggtg ccaggcttct 660
catctgcagt tccccggagc agtgtacgga acagacggct gtcctgtcag cgtggagaag 720
atcgtcaaca tcttcaacgg cacttcttgc cctagtctgg ggggaaagcc aaaactgttc 780
tttatccagg cctgtggcgg ggaacagaaa gatcacggct tcgaggtggc cagcaccagc 840
cctgaggacg aatcaccagg gagcaaccct gaaccagatg caactccatt ccaggaggga 900
ctgaggacct ttgaccagct ggatgctatc tcaagcctgc ccactcctag tgacattttc 960
gtgtcttaca gtaccttccc aggctttgtc tcatggcgcg atcccaagtc agggagctgg 1020
tacgtggaga cactggacga catctttgaa cagtgggccc attcagagga cctgcagagc 1080
ctgctgctgc gagtggcaaa cgctgtctct gtgaagggca tctacaaaca gatgcccggg 1140
tgcttcaatt ttctgagaaa gaaactgttc tttaagactt cc 1182
<210> 11
<211> 18
<212> Белок
<213> Вирус Thosea asigna
<400> 11
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
1 5 10 15
Gly Pro
<210> 12
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<223> GSG-T2A
<400> 12
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1 5 10 15
Glu Asn Pro Gly Pro
20
<210> 13
<211> 20
<212> Белок
<213> Вирус Equine rhnitis A
<400> 13
Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp Val Glu Ser
1 5 10 15
Asn Pro Gly Pro
20
<210> 14
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<223> GSG-E2A
<400> 14
Gly Ser Gly Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp
1 5 10 15
Val Glu Ser Asn Pro Gly Pro
20
<210> 15
<211> 22
<212> Белок
<213> Вирус "болезни рук и ног" (тип 0)
<400> 15
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<210> 16
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> GSG-F2A
<400> 16
Gly Ser Gly Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala
1 5 10 15
Gly Asp Val Glu Ser Asn Pro Gly Pro
20 25
<210> 17
<211> 19
<212> Белок
<213> Porcine teschovirus-1
<400> 17
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 18
<211> 22
<212> Белок
<213> Искусственная последовательность
<220>
<223> GSG-P2A
<400> 18
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 19
<211> 340
<212> Белок
<213> Искусственная последовательность
<220>
<223> Транспозаза Sleeping Beauty
<400> 19
Met Gly Lys Ser Lys Glu Ile Ser Gln Asp Leu Arg Lys Lys Ile Val
1 5 10 15
Asp Leu His Lys Ser Gly Ser Ser Leu Gly Ala Ile Ser Lys Arg Leu
20 25 30
Lys Val Pro Arg Ser Ser Val Gln Thr Ile Val Arg Lys Tyr Lys His
35 40 45
His Gly Thr Thr Gln Pro Ser Tyr Arg Ser Gly Arg Arg Arg Val Leu
50 55 60
Ser Pro Arg Asp Glu Arg Thr Leu Val Arg Lys Val Gln Ile Asn Pro
65 70 75 80
Arg Thr Thr Ala Lys Asp Leu Val Lys Met Leu Glu Glu Thr Gly Thr
85 90 95
Lys Val Ser Ile Ser Thr Val Lys Arg Val Leu Tyr Arg His Asn Leu
100 105 110
Lys Gly Arg Ser Ala Arg Lys Lys Pro Leu Leu Gln Asn Arg His Lys
115 120 125
Lys Ala Arg Leu Arg Phe Ala Thr Ala His Gly Asp Lys Asp Arg Thr
130 135 140
Phe Trp Arg Asn Val Leu Trp Ser Asp Glu Thr Lys Ile Glu Leu Phe
145 150 155 160
Gly His Asn Asp His Arg Tyr Val Trp Arg Lys Lys Gly Glu Ala Cys
165 170 175
Lys Pro Lys Asn Thr Ile Pro Thr Val Lys His Gly Gly Gly Ser Ile
180 185 190
Met Leu Trp Gly Cys Phe Ala Ala Gly Gly Thr Gly Ala Leu His Lys
195 200 205
Ile Asp Gly Ile Met Arg Lys Glu Asn Tyr Val Asp Ile Leu Lys Gln
210 215 220
His Leu Lys Thr Ser Val Arg Lys Leu Lys Leu Gly Arg Lys Trp Val
225 230 235 240
Phe Gln Met Asp Asn Asp Pro Lys His Thr Ser Lys Val Val Ala Lys
245 250 255
Trp Leu Lys Asp Asn Lys Val Lys Val Leu Glu Trp Pro Ser Gln Ser
260 265 270
Pro Asp Leu Asn Pro Ile Glu Asn Leu Trp Ala Glu Leu Lys Lys Arg
275 280 285
Val Arg Ala Arg Arg Pro Thr Asn Leu Thr Gln Leu His Gln Leu Cys
290 295 300
Gln Glu Glu Trp Ala Lys Ile His Pro Thr Tyr Cys Gly Lys Leu Val
305 310 315 320
Glu Gly Tyr Pro Lys Arg Leu Thr Gln Val Lys Gln Phe Lys Gly Asn
325 330 335
Ala Thr Lys Tyr
340
<210> 20
<211> 340
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гиперактивная транспозаза Sleeping Beauty
<400> 20
Met Gly Lys Ser Lys Glu Ile Ser Gln Asp Leu Arg Lys Arg Ile Val
1 5 10 15
Asp Leu His Lys Ser Gly Ser Ser Leu Gly Ala Ile Ser Lys Arg Leu
20 25 30
Ala Val Pro Arg Ser Ser Val Gln Thr Ile Val Arg Lys Tyr Lys His
35 40 45
His Gly Thr Thr Gln Pro Ser Tyr Arg Ser Gly Arg Arg Arg Val Leu
50 55 60
Ser Pro Arg Asp Glu Arg Thr Leu Val Arg Lys Val Gln Ile Asn Pro
65 70 75 80
Arg Thr Thr Ala Lys Asp Leu Val Lys Met Leu Glu Glu Thr Gly Thr
85 90 95
Lys Val Ser Ile Ser Thr Val Lys Arg Val Leu Tyr Arg His Asn Leu
100 105 110
Lys Gly His Ser Ala Arg Lys Lys Pro Leu Leu Gln Asn Arg His Lys
115 120 125
Lys Ala Arg Leu Arg Phe Ala Thr Ala His Gly Asp Lys Asp Arg Thr
130 135 140
Phe Trp Arg Asn Val Leu Trp Ser Asp Glu Thr Lys Ile Glu Leu Phe
145 150 155 160
Gly His Asn Asp His Arg Tyr Val Trp Arg Lys Lys Gly Glu Ala Cys
165 170 175
Lys Pro Lys Asn Thr Ile Pro Thr Val Lys His Gly Gly Gly Ser Ile
180 185 190
Met Leu Trp Gly Cys Phe Ala Ala Gly Gly Thr Gly Ala Leu His Lys
195 200 205
Ile Asp Gly Ile Met Asp Ala Val Gln Tyr Val Asp Ile Leu Lys Gln
210 215 220
His Leu Lys Thr Ser Val Arg Lys Leu Lys Leu Gly Arg Lys Trp Val
225 230 235 240
Phe Gln His Asp Asn Asp Pro Lys His Thr Ser Lys Val Val Ala Lys
245 250 255
Trp Leu Lys Asp Asn Lys Val Lys Val Leu Glu Trp Pro Ser Gln Ser
260 265 270
Pro Asp Leu Asn Pro Ile Glu Asn Leu Trp Ala Glu Leu Lys Lys Arg
275 280 285
Val Arg Ala Arg Arg Pro Thr Asn Leu Thr Gln Leu His Gln Leu Cys
290 295 300
Gln Glu Glu Trp Ala Lys Ile His Pro Asn Tyr Cys Gly Lys Leu Val
305 310 315 320
Glu Gly Tyr Pro Lys Arg Leu Thr Gln Val Lys Gln Phe Lys Gly Asn
325 330 335
Ala Thr Lys Tyr
340
<210> 21
<211> 5296
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Транспозон Helraiser
<400> 21
tcctatataa taaaagagaa acatgcaaat tgaccatccc tccgctacgc tcaagccacg 60
cccaccagcc aatcagaagt gactatgcaa attaacccaa caaagatggc agttaaattt 120
gcatacgcag gtgtcaagcg ccccaggagg caacggcggc cgcgggctcc caggaccttc 180
gctggccccg ggaggcgagg ccggccgcgc ctagccacac ccgcgggctc ccgggacctt 240
cgccagcaga gagcagagcg ggagagcggg cggagagcgg gaggtttgga ggacttggca 300
gagcaggagg ccgctggaca tagagcagag cgagagagag ggtggcttgg agggcgtggc 360
tccctctgtc accccagctt cctcatcaca gctgtggaaa ctgacagcag ggaggaggaa 420
gtcccacccc cacagaatca gccagaatca gccgttggtc agacagctct cagcggcctg 480
acagccagga ctctcattca cctgcatctc agaccgtgac agtagagagg tgggactatg 540
tctaaagaac aactgttgat acaacgtagc tctgcagccg aaagatgccg gcgttatcga 600
cagaaaatgt ctgcagagca acgtgcgtct gatcttgaaa gaaggcggcg cctgcaacag 660
aatgtatctg aagagcagct actggaaaaa cgtcgctctg aagccgaaaa acagcggcgt 720
catcgacaga aaatgtctaa agaccaacgt gcctttgaag ttgaaagaag gcggtggcga 780
cgacagaata tgtctagaga acagtcatca acaagtacta ccaataccgg taggaactgc 840
cttctcagca aaaatggagt acatgaggat gcaattctcg aacatagttg tggtggaatg 900
actgttcgat gtgaattttg cctatcacta aatttctctg atgaaaaacc atccgatggg 960
aaatttactc gatgttgtag caaagggaaa gtctgtccaa atgatataca ttttccagat 1020
tacccggcat atttaaaaag attaatgaca aacgaagatt ctgacagtaa aaatttcatg 1080
gaaaatattc gttccataaa tagttctttt gcttttgctt ccatgggtgc aaatattgca 1140
tcgccatcag gatatgggcc atactgtttt agaatacacg gacaagttta tcaccgtact 1200
ggaactttac atccttcgga tggtgtttct cggaagtttg ctcaactcta tattttggat 1260
acagccgaag ctacaagtaa aagattagca atgccagaaa accagggctg ctcagaaaga 1320
ctcatgatca acatcaacaa cctcatgcat gaaataaatg aattaacaaa atcgtacaag 1380
atgctacatg aggtagaaaa ggaagcccaa tctgaagcag cagcaaaagg tattgctccc 1440
acagaagtaa caatggcgat taaatacgat cgtaacagtg acccaggtag atataattct 1500
ccccgtgtaa ccgaggttgc tgtcatattc agaaacgaag atggagaacc tccttttgaa 1560
agggacttgc tcattcattg taaaccagat cccaataatc caaatgccac taaaatgaaa 1620
caaatcagta tcctgtttcc tacattagat gcaatgacat atcctattct ttttccacat 1680
ggtgaaaaag gctggggaac agatattgca ttaagactca gagacaacag tgtaatcgac 1740
aataatacta gacaaaatgt aaggacacga gtcacacaaa tgcagtatta tggatttcat 1800
ctctctgtgc gggacacgtt caatcctatt ttaaatgcag gaaaattaac tcaacagttt 1860
attgtggatt catattcaaa aatggaggcc aatcggataa atttcatcaa agcaaaccaa 1920
tctaagttga gagttgaaaa atatagtggt ttgatggatt atctcaaatc tagatctgaa 1980
aatgacaatg tgccgattgg taaaatgata atacttccat catcttttga gggtagtccc 2040
agaaatatgc agcagcgata tcaggatgct atggcaattg taacgaagta tggcaagccc 2100
gatttattca taaccatgac atgcaacccc aaatgggcag atattacaaa caatttacaa 2160
cgctggcaaa aagttgaaaa cagacctgac ttggtagcca gagtttttaa tattaagctg 2220
aatgctcttt taaatgatat atgtaaattc catttatttg gcaaagtaat agctaaaatt 2280
catgtcattg aatttcagaa acgcggactg cctcacgctc acatattatt gatattagat 2340
agtgagtcca aattacgttc agaagatgac attgaccgta tagttaaggc agaaattcca 2400
gatgaagacc agtgtcctcg actttttcaa attgtaaaat caaatatggt acatggacca 2460
tgtggaatac aaaatccaaa tagtccatgt atggaaaatg gaaaatgttc aaagggatat 2520
ccaaaagaat ttcaaaatgc gaccattgga aatattgatg gatatcccaa atacaaacga 2580
agatctggta gcaccatgtc tattggaaat aaagttgtcg ataacacttg gattgtccct 2640
tataacccgt atttgtgcct taaatataac tgtcatataa atgttgaagt ctgtgcatca 2700
attaaaagtg tcaaatattt atttaaatac atctataaag ggcacgattg tgcaaatatt 2760
caaatttctg aaaaaaatat tatcaatcat gacgaagtac aggacttcat tgactccagg 2820
tatgtgagcg ctcctgaggc tgtttggaga ctttttgcaa tgcgaatgca tgaccaatct 2880
catgcaatca caagattagc tattcatttg ccaaatgatc agaatttgta ttttcatacc 2940
gatgattttg ctgaagtttt agatagggct aaaaggcata actcgacttt gatggcttgg 3000
ttcttattga atagagaaga ttctgatgca cgtaattatt attattggga gattccacag 3060
cattatgtgt ttaataattc tttgtggaca aaacgccgaa agggtgggaa taaagtatta 3120
ggtagactgt tcactgtgag ctttagagaa ccagaacgat attaccttag acttttgctt 3180
ctgcatgtaa aaggtgcgat aagttttgag gatctgcgaa ctgtaggagg tgtaacttat 3240
gatacatttc atgaagctgc taaacaccga ggattattac ttgatgacac tatctggaaa 3300
gatacgattg acgatgcaat catccttaat atgcccaaac aactacggca actttttgca 3360
tatatatgtg tgtttggatg tccttctgct gcagacaaat tatgggatga gaataaatct 3420
cattttattg aagatttctg ttggaaatta caccgaagag aaggtgcctg tgtgaactgt 3480
gaaatgcatg cccttaacga aattcaggag gtattcacat tgcatggaat gaaatgttca 3540
catttcaaac ttccggacta tcctttatta atgaatgcaa atacatgtga tcaattgtac 3600
gagcaacaac aggcagaggt tttgataaat tctctgaatg atgaacagtt ggcagccttt 3660
cagactataa cttcagccat cgaagatcaa actgtacacc ccaaatgctt tttcttggat 3720
ggtccaggtg gtagtggaaa aacatatctg tataaagttt taacacatta tattagaggt 3780
cgtggtggta ctgttttacc cacagcatct acaggaattg ctgcaaattt acttcttggt 3840
ggaagaacct ttcattccca atataaatta ccaattccat taaatgaaac ttcaatttct 3900
agactcgata taaagagtga agttgctaaa accattaaaa aggcccaact tctcattatt 3960
gatgaatgca ccatggcatc cagtcatgct ataaacgcca tagatagatt actaagagaa 4020
attatgaatt tgaatgttgc atttggtggg aaagttctcc ttctcggagg ggattttcga 4080
caatgtctca gtattgtacc acatgctatg cgatcggcca tagtacaaac gagtttaaag 4140
tactgtaatg tttggggatg tttcagaaag ttgtctctta aaacaaatat gagatcagag 4200
gattctgctt atagtgaatg gttagtaaaa cttggagatg gcaaacttga tagcagtttt 4260
catttaggaa tggatattat tgaaatcccc catgaaatga tttgtaacgg atctattatt 4320
gaagctacct ttggaaatag tatatctata gataatatta aaaatatatc taaacgtgca 4380
attctttgtc caaaaaatga gcatgttcaa aaattaaatg aagaaatttt ggatatactt 4440
gatggagatt ttcacacata tttgagtgat gattccattg attcaacaga tgatgctgaa 4500
aaggaaaatt ttcccatcga atttcttaat agtattactc cttcgggaat gccgtgtcat 4560
aaattaaaat tgaaagtggg tgcaatcatc atgctattga gaaatcttaa tagtaaatgg 4620
ggtctttgta atggtactag atttattatc aaaagattac gacctaacat tatcgaagct 4680
gaagtattaa caggatctgc agagggagag gttgttctga ttccaagaat tgatttgtcc 4740
ccatctgaca ctggcctccc atttaaatta attcgaagac agtttcccgt gatgccagca 4800
tttgcgatga ctattaataa atcacaagga caaactctag acagagtagg aatattccta 4860
cctgaacccg ttttcgcaca tggtcagtta tatgttgctt tctctcgagt tcgaagagca 4920
tgtgacgtta aagttaaagt tgtaaatact tcatcacaag ggaaattagt caagcactct 4980
gaaagtgttt ttactcttaa tgtggtatac agggagatat tagaataagt ttaatcactt 5040
tatcagtcat tgtttgcatc aatgttgttt ttatatcatg tttttgttgt ttttatatca 5100
tgtctttgtt gttgttatat catgttgtta ttgtttattt attaataaat ttatgtatta 5160
ttttcatata cattttactc atttcctttc atctctcaca cttctattat agagaaaggg 5220
caaatagcaa tattaaaata tttcctctaa ttaattccct ttcaatgtgc acgaatttcg 5280
tgcaccgggc cactag 5296
<210> 22
<211> 1496
<212> Белок
<213> Искусственная последовательность
<220>
<223> Транспозаза Helitron
<400> 22
Met Ser Lys Glu Gln Leu Leu Ile Gln Arg Ser Ser Ala Ala Glu Arg
1 5 10 15
Cys Arg Arg Tyr Arg Gln Lys Met Ser Ala Glu Gln Arg Ala Ser Asp
20 25 30
Leu Glu Arg Arg Arg Arg Leu Gln Gln Asn Val Ser Glu Glu Gln Leu
35 40 45
Leu Glu Lys Arg Arg Ser Glu Ala Glu Lys Gln Arg Arg His Arg Gln
50 55 60
Lys Met Ser Lys Asp Gln Arg Ala Phe Glu Val Glu Arg Arg Arg Trp
65 70 75 80
Arg Arg Gln Asn Met Ser Arg Glu Gln Ser Ser Thr Ser Thr Thr Asn
85 90 95
Thr Gly Arg Asn Cys Leu Leu Ser Lys Asn Gly Val His Glu Asp Ala
100 105 110
Ile Leu Glu His Ser Cys Gly Gly Met Thr Val Arg Cys Glu Phe Cys
115 120 125
Leu Ser Leu Asn Phe Ser Asp Glu Lys Pro Ser Asp Gly Lys Phe Thr
130 135 140
Arg Cys Cys Ser Lys Gly Lys Val Cys Pro Asn Asp Ile His Phe Pro
145 150 155 160
Asp Tyr Pro Ala Tyr Leu Lys Arg Leu Met Thr Asn Glu Asp Ser Asp
165 170 175
Ser Lys Asn Phe Met Glu Asn Ile Arg Ser Ile Asn Ser Ser Phe Ala
180 185 190
Phe Ala Ser Met Gly Ala Asn Ile Ala Ser Pro Ser Gly Tyr Gly Pro
195 200 205
Tyr Cys Phe Arg Ile His Gly Gln Val Tyr His Arg Thr Gly Thr Leu
210 215 220
His Pro Ser Asp Gly Val Ser Arg Lys Phe Ala Gln Leu Tyr Ile Leu
225 230 235 240
Asp Thr Ala Glu Ala Thr Ser Lys Arg Leu Ala Met Pro Glu Asn Gln
245 250 255
Gly Cys Ser Glu Arg Leu Met Ile Asn Ile Asn Asn Leu Met His Glu
260 265 270
Ile Asn Glu Leu Thr Lys Ser Tyr Lys Met Leu His Glu Val Glu Lys
275 280 285
Glu Ala Gln Ser Glu Ala Ala Ala Lys Gly Ile Ala Pro Thr Glu Val
290 295 300
Thr Met Ala Ile Lys Tyr Asp Arg Asn Ser Asp Pro Gly Arg Tyr Asn
305 310 315 320
Ser Pro Arg Val Thr Glu Val Ala Val Ile Phe Arg Asn Glu Asp Gly
325 330 335
Glu Pro Pro Phe Glu Arg Asp Leu Leu Ile His Cys Lys Pro Asp Pro
340 345 350
Asn Asn Pro Asn Ala Thr Lys Met Lys Gln Ile Ser Ile Leu Phe Pro
355 360 365
Thr Leu Asp Ala Met Thr Tyr Pro Ile Leu Phe Pro His Gly Glu Lys
370 375 380
Gly Trp Gly Thr Asp Ile Ala Leu Arg Leu Arg Asp Asn Ser Val Ile
385 390 395 400
Asp Asn Asn Thr Arg Gln Asn Val Arg Thr Arg Val Thr Gln Met Gln
405 410 415
Tyr Tyr Gly Phe His Leu Ser Val Arg Asp Thr Phe Asn Pro Ile Leu
420 425 430
Asn Ala Gly Lys Leu Thr Gln Gln Phe Ile Val Asp Ser Tyr Ser Lys
435 440 445
Met Glu Ala Asn Arg Ile Asn Phe Ile Lys Ala Asn Gln Ser Lys Leu
450 455 460
Arg Val Glu Lys Tyr Ser Gly Leu Met Asp Tyr Leu Lys Ser Arg Ser
465 470 475 480
Glu Asn Asp Asn Val Pro Ile Gly Lys Met Ile Ile Leu Pro Ser Ser
485 490 495
Phe Glu Gly Ser Pro Arg Asn Met Gln Gln Arg Tyr Gln Asp Ala Met
500 505 510
Ala Ile Val Thr Lys Tyr Gly Lys Pro Asp Leu Phe Ile Thr Met Thr
515 520 525
Cys Asn Pro Lys Trp Ala Asp Ile Thr Asn Asn Leu Gln Arg Trp Gln
530 535 540
Lys Val Glu Asn Arg Pro Asp Leu Val Ala Arg Val Phe Asn Ile Lys
545 550 555 560
Leu Asn Ala Leu Leu Asn Asp Ile Cys Lys Phe His Leu Phe Gly Lys
565 570 575
Val Ile Ala Lys Ile His Val Ile Glu Phe Gln Lys Arg Gly Leu Pro
580 585 590
His Ala His Ile Leu Leu Ile Leu Asp Ser Glu Ser Lys Leu Arg Ser
595 600 605
Glu Asp Asp Ile Asp Arg Ile Val Lys Ala Glu Ile Pro Asp Glu Asp
610 615 620
Gln Cys Pro Arg Leu Phe Gln Ile Val Lys Ser Asn Met Val His Gly
625 630 635 640
Pro Cys Gly Ile Gln Asn Pro Asn Ser Pro Cys Met Glu Asn Gly Lys
645 650 655
Cys Ser Lys Gly Tyr Pro Lys Glu Phe Gln Asn Ala Thr Ile Gly Asn
660 665 670
Ile Asp Gly Tyr Pro Lys Tyr Lys Arg Arg Ser Gly Ser Thr Met Ser
675 680 685
Ile Gly Asn Lys Val Val Asp Asn Thr Trp Ile Val Pro Tyr Asn Pro
690 695 700
Tyr Leu Cys Leu Lys Tyr Asn Cys His Ile Asn Val Glu Val Cys Ala
705 710 715 720
Ser Ile Lys Ser Val Lys Tyr Leu Phe Lys Tyr Ile Tyr Lys Gly His
725 730 735
Asp Cys Ala Asn Ile Gln Ile Ser Glu Lys Asn Ile Ile Asn His Asp
740 745 750
Glu Val Gln Asp Phe Ile Asp Ser Arg Tyr Val Ser Ala Pro Glu Ala
755 760 765
Val Trp Arg Leu Phe Ala Met Arg Met His Asp Gln Ser His Ala Ile
770 775 780
Thr Arg Leu Ala Ile His Leu Pro Asn Asp Gln Asn Leu Tyr Phe His
785 790 795 800
Thr Asp Asp Phe Ala Glu Val Leu Asp Arg Ala Lys Arg His Asn Ser
805 810 815
Thr Leu Met Ala Trp Phe Leu Leu Asn Arg Glu Asp Ser Asp Ala Arg
820 825 830
Asn Tyr Tyr Tyr Trp Glu Ile Pro Gln His Tyr Val Phe Asn Asn Ser
835 840 845
Leu Trp Thr Lys Arg Arg Lys Gly Gly Asn Lys Val Leu Gly Arg Leu
850 855 860
Phe Thr Val Ser Phe Arg Glu Pro Glu Arg Tyr Tyr Leu Arg Leu Leu
865 870 875 880
Leu Leu His Val Lys Gly Ala Ile Ser Phe Glu Asp Leu Arg Thr Val
885 890 895
Gly Gly Val Thr Tyr Asp Thr Phe His Glu Ala Ala Lys His Arg Gly
900 905 910
Leu Leu Leu Asp Asp Thr Ile Trp Lys Asp Thr Ile Asp Asp Ala Ile
915 920 925
Ile Leu Asn Met Pro Lys Gln Leu Arg Gln Leu Phe Ala Tyr Ile Cys
930 935 940
Val Phe Gly Cys Pro Ser Ala Ala Asp Lys Leu Trp Asp Glu Asn Lys
945 950 955 960
Ser His Phe Ile Glu Asp Phe Cys Trp Lys Leu His Arg Arg Glu Gly
965 970 975
Ala Cys Val Asn Cys Glu Met His Ala Leu Asn Glu Ile Gln Glu Val
980 985 990
Phe Thr Leu His Gly Met Lys Cys Ser His Phe Lys Leu Pro Asp Tyr
995 1000 1005
Pro Leu Leu Met Asn Ala Asn Thr Cys Asp Gln Leu Tyr Glu Gln
1010 1015 1020
Gln Gln Ala Glu Val Leu Ile Asn Ser Leu Asn Asp Glu Gln Leu
1025 1030 1035
Ala Ala Phe Gln Thr Ile Thr Ser Ala Ile Glu Asp Gln Thr Val
1040 1045 1050
His Pro Lys Cys Phe Phe Leu Asp Gly Pro Gly Gly Ser Gly Lys
1055 1060 1065
Thr Tyr Leu Tyr Lys Val Leu Thr His Tyr Ile Arg Gly Arg Gly
1070 1075 1080
Gly Thr Val Leu Pro Thr Ala Ser Thr Gly Ile Ala Ala Asn Leu
1085 1090 1095
Leu Leu Gly Gly Arg Thr Phe His Ser Gln Tyr Lys Leu Pro Ile
1100 1105 1110
Pro Leu Asn Glu Thr Ser Ile Ser Arg Leu Asp Ile Lys Ser Glu
1115 1120 1125
Val Ala Lys Thr Ile Lys Lys Ala Gln Leu Leu Ile Ile Asp Glu
1130 1135 1140
Cys Thr Met Ala Ser Ser His Ala Ile Asn Ala Ile Asp Arg Leu
1145 1150 1155
Leu Arg Glu Ile Met Asn Leu Asn Val Ala Phe Gly Gly Lys Val
1160 1165 1170
Leu Leu Leu Gly Gly Asp Phe Arg Gln Cys Leu Ser Ile Val Pro
1175 1180 1185
His Ala Met Arg Ser Ala Ile Val Gln Thr Ser Leu Lys Tyr Cys
1190 1195 1200
Asn Val Trp Gly Cys Phe Arg Lys Leu Ser Leu Lys Thr Asn Met
1205 1210 1215
Arg Ser Glu Asp Ser Ala Tyr Ser Glu Trp Leu Val Lys Leu Gly
1220 1225 1230
Asp Gly Lys Leu Asp Ser Ser Phe His Leu Gly Met Asp Ile Ile
1235 1240 1245
Glu Ile Pro His Glu Met Ile Cys Asn Gly Ser Ile Ile Glu Ala
1250 1255 1260
Thr Phe Gly Asn Ser Ile Ser Ile Asp Asn Ile Lys Asn Ile Ser
1265 1270 1275
Lys Arg Ala Ile Leu Cys Pro Lys Asn Glu His Val Gln Lys Leu
1280 1285 1290
Asn Glu Glu Ile Leu Asp Ile Leu Asp Gly Asp Phe His Thr Tyr
1295 1300 1305
Leu Ser Asp Asp Ser Ile Asp Ser Thr Asp Asp Ala Glu Lys Glu
1310 1315 1320
Asn Phe Pro Ile Glu Phe Leu Asn Ser Ile Thr Pro Ser Gly Met
1325 1330 1335
Pro Cys His Lys Leu Lys Leu Lys Val Gly Ala Ile Ile Met Leu
1340 1345 1350
Leu Arg Asn Leu Asn Ser Lys Trp Gly Leu Cys Asn Gly Thr Arg
1355 1360 1365
Phe Ile Ile Lys Arg Leu Arg Pro Asn Ile Ile Glu Ala Glu Val
1370 1375 1380
Leu Thr Gly Ser Ala Glu Gly Glu Val Val Leu Ile Pro Arg Ile
1385 1390 1395
Asp Leu Ser Pro Ser Asp Thr Gly Leu Pro Phe Lys Leu Ile Arg
1400 1405 1410
Arg Gln Phe Pro Val Met Pro Ala Phe Ala Met Thr Ile Asn Lys
1415 1420 1425
Ser Gln Gly Gln Thr Leu Asp Arg Val Gly Ile Phe Leu Pro Glu
1430 1435 1440
Pro Val Phe Ala His Gly Gln Leu Tyr Val Ala Phe Ser Arg Val
1445 1450 1455
Arg Arg Ala Cys Asp Val Lys Val Lys Val Val Asn Thr Ser Ser
1460 1465 1470
Gln Gly Lys Leu Val Lys His Ser Glu Ser Val Phe Thr Leu Asn
1475 1480 1485
Val Val Tyr Arg Glu Ile Leu Glu
1490 1495
<210> 23
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Палиндромная последовательность транспозона Helraiser
<400> 23
gtgcacgaat ttcgtgcacc gggccactag 30
<210> 24
<211> 649
<212> Белок
<213> Oryzias latipes
<400> 24
Met Glu Glu Val Cys Asp Ser Ser Ala Ala Ala Ser Ser Thr Val Gln
1 5 10 15
Asn Gln Pro Gln Asp Gln Glu His Pro Trp Pro Tyr Leu Arg Glu Phe
20 25 30
Phe Ser Leu Ser Gly Val Asn Lys Asp Ser Phe Lys Met Lys Cys Val
35 40 45
Leu Cys Leu Pro Leu Asn Lys Glu Ile Ser Ala Phe Lys Ser Ser Pro
50 55 60
Ser Asn Leu Arg Lys His Ile Glu Arg Met His Pro Asn Tyr Leu Lys
65 70 75 80
Asn Tyr Ser Lys Leu Thr Ala Gln Lys Arg Lys Ile Gly Thr Ser Thr
85 90 95
His Ala Ser Ser Ser Lys Gln Leu Lys Val Asp Ser Val Phe Pro Val
100 105 110
Lys His Val Ser Pro Val Thr Val Asn Lys Ala Ile Leu Arg Tyr Ile
115 120 125
Ile Gln Gly Leu His Pro Phe Ser Thr Val Asp Leu Pro Ser Phe Lys
130 135 140
Glu Leu Ile Ser Thr Leu Gln Pro Gly Ile Ser Val Ile Thr Arg Pro
145 150 155 160
Thr Leu Arg Ser Lys Ile Ala Glu Ala Ala Leu Ile Met Lys Gln Lys
165 170 175
Val Thr Ala Ala Met Ser Glu Val Glu Trp Ile Ala Thr Thr Thr Asp
180 185 190
Cys Trp Thr Ala Arg Arg Lys Ser Phe Ile Gly Val Thr Ala His Trp
195 200 205
Ile Asn Pro Gly Ser Leu Glu Arg His Ser Ala Ala Leu Ala Cys Lys
210 215 220
Arg Leu Met Gly Ser His Thr Phe Glu Val Leu Ala Ser Ala Met Asn
225 230 235 240
Asp Ile His Ser Glu Tyr Glu Ile Arg Asp Lys Val Val Cys Thr Thr
245 250 255
Thr Asp Ser Gly Ser Asn Phe Met Lys Ala Phe Arg Val Phe Gly Val
260 265 270
Glu Asn Asn Asp Ile Glu Thr Glu Ala Arg Arg Cys Glu Ser Asp Asp
275 280 285
Thr Asp Ser Glu Gly Cys Gly Glu Gly Ser Asp Gly Val Glu Phe Gln
290 295 300
Asp Ala Ser Arg Val Leu Asp Gln Asp Asp Gly Phe Glu Phe Gln Leu
305 310 315 320
Pro Lys His Gln Lys Cys Ala Cys His Leu Leu Asn Leu Val Ser Ser
325 330 335
Val Asp Ala Gln Lys Ala Leu Ser Asn Glu His Tyr Lys Lys Leu Tyr
340 345 350
Arg Ser Val Phe Gly Lys Cys Gln Ala Leu Trp Asn Lys Ser Ser Arg
355 360 365
Ser Ala Leu Ala Ala Glu Ala Val Glu Ser Glu Ser Arg Leu Gln Leu
370 375 380
Leu Arg Pro Asn Gln Thr Arg Trp Asn Ser Thr Phe Met Ala Val Asp
385 390 395 400
Arg Ile Leu Gln Ile Cys Lys Glu Ala Gly Glu Gly Ala Leu Arg Asn
405 410 415
Ile Cys Thr Ser Leu Glu Val Pro Met Phe Asn Pro Ala Glu Met Leu
420 425 430
Phe Leu Thr Glu Trp Ala Asn Thr Met Arg Pro Val Ala Lys Val Leu
435 440 445
Asp Ile Leu Gln Ala Glu Thr Asn Thr Gln Leu Gly Trp Leu Leu Pro
450 455 460
Ser Val His Gln Leu Ser Leu Lys Leu Gln Arg Leu His His Ser Leu
465 470 475 480
Arg Tyr Cys Asp Pro Leu Val Asp Ala Leu Gln Gln Gly Ile Gln Thr
485 490 495
Arg Phe Lys His Met Phe Glu Asp Pro Glu Ile Ile Ala Ala Ala Ile
500 505 510
Leu Leu Pro Lys Phe Arg Thr Ser Trp Thr Asn Asp Glu Thr Ile Ile
515 520 525
Lys Arg Gly Met Asp Tyr Ile Arg Val His Leu Glu Pro Leu Asp His
530 535 540
Lys Lys Glu Leu Ala Asn Ser Ser Ser Asp Asp Glu Asp Phe Phe Ala
545 550 555 560
Ser Leu Lys Pro Thr Thr His Glu Ala Ser Lys Glu Leu Asp Gly Tyr
565 570 575
Leu Ala Cys Val Ser Asp Thr Arg Glu Ser Leu Leu Thr Phe Pro Ala
580 585 590
Ile Cys Ser Leu Ser Ile Lys Thr Asn Thr Pro Leu Pro Ala Ser Ala
595 600 605
Ala Cys Glu Arg Leu Phe Ser Thr Ala Gly Leu Leu Phe Ser Pro Lys
610 615 620
Arg Ala Arg Leu Asp Thr Asn Asn Phe Glu Asn Gln Leu Leu Leu Lys
625 630 635 640
Leu Asn Leu Arg Phe Tyr Asn Phe Glu
645
<210> 25
<211> 4682
<212> ДНК
<213> Oryzias latipes
<400> 25
cagaggtgta aagtacttga gtaattttac ttgattactg tacttaagta ttatttttgg 60
ggatttttac tttacttgag tacaattaaa aatcaatact tttactttta cttaattaca 120
tttttttaga aaaaaaagta ctttttactc cttacaattt tatttacagt caaaaagtac 180
ttattttttg gagatcactt cattctattt tcccttgcta ttaccaaacc aattgaattg 240
cgctgatgcc cagtttaatt taaatgttat ttattctgcc tatgaaaatc gttttcacat 300
tatatgaaat tggtcagaca tgttcattgg tcctttggaa gtgacgtcat gtcacatcta 360
ttaccacaat gcacagcacc ttgacctgga aattagggaa attataacag tcaatcagtg 420
gaagaaaatg gaggaagtat gtgattcatc agcagctgcg agcagcacag tccaaaatca 480
gccacaggat caagagcacc cgtggccgta tcttcgcgaa ttcttttctt taagtggtgt 540
aaataaagat tcattcaaga tgaaatgtgt cctctgtctc ccgcttaata aagaaatatc 600
ggccttcaaa agttcgccat caaacctaag gaagcatatt gaggtaagta cattaagtat 660
tttgttttac tgatagtttt tttttttttt tttttttttt tttttgggtg tgcatgtttt 720
gacgttgatg gcgcgccttt tatatgtgta gtaggcctat tttcactaat gcatgcgatt 780
gacaatataa ggctcacgta ataaaatgct aaaatgcatt tgtaattggt aacgttaggt 840
ccacgggaaa tttggcgcct attgcagctt tgaataatca ttatcattcc gtgctctcat 900
tgtgtttgaa ttcatgcaaa acacaagaaa accaagcgag aaattttttt ccaaacatgt 960
tgtattgtca aaacggtaac actttacaat gaggttgatt agttcatgta ttaactaaca 1020
ttaaataacc atgagcaata catttgttac tgtatctgtt aatctttgtt aacgttagtt 1080
aatagaaata cagatgttca ttgtttgttc atgttagttc acagtgcatt aactaatgtt 1140
aacaagatat aaagtattag taaatgttga aattaacatg tatacgtgca gttcattatt 1200
agttcatgtt aactaatgta gttaactaac gaaccttatt gtaaaagtgt taccatcaaa 1260
actaatgtaa tgaaatcaat tcaccctgtc atgtcagcct tacagtcctg tgtttttgtc 1320
aatataatca gaaataaaat taatgtttga ttgtcactaa atgctactgt atttctaaaa 1380
tcaacaagta tttaacatta taaagtgtgc aattggctgc aaatgtcagt tttattaaag 1440
ggttagttca cccaaaaatg aaaataatgt cattaatgac tcgccctcat gtcgttccaa 1500
gcccgtaaga cctccgttca tcttcagaac acagtttaag atattttaga tttagtccga 1560
gagctttctg tgcctccatt gagaatgtat gtacggtata ctgtccatgt ccagaaaggt 1620
aataaaaaca tcaaagtagt ccatgtgaca tcagtgggtt agttagaatt ttttgaagca 1680
tcgaatacat tttggtccaa aaataacaaa acctacgact ttattcggca ttgtattctc 1740
ttccgggtct gttgtcaatc cgcgttcacg acttcgcagt gacgctacaa tgctgaataa 1800
agtcgtaggt tttgttattt ttggaccaaa atgtattttc gatgcttcaa ataattctac 1860
ctaacccact gatgtcacat ggactacttt gatgttttta ttacctttct ggacatggac 1920
agtataccgt acatacattt tcagtggagg gacagaaagc tctcggacta aatctaaaat 1980
atcttaaact gtgttccgaa gatgaacgga ggtgttacgg gcttggaacg acatgagggt 2040
gagtcattaa tgacatcttt tcatttttgg gtgaactaac cctttaatgc tgtaatcaga 2100
gagtgtatgt gtaattgtta catttattgc atacaatata aatatttatt tgttgttttt 2160
acagagaatg cacccaaatt acctcaaaaa ctactctaaa ttgacagcac agaagagaaa 2220
gatcgggacc tccacccatg cttccagcag taagcaactg aaagttgact cagttttccc 2280
agtcaaacat gtgtctccag tcactgtgaa caaagctata ttaaggtaca tcattcaagg 2340
acttcatcct ttcagcactg ttgatctgcc atcatttaaa gagctgatta gtacactgca 2400
gcctggcatt tctgtcatta caaggcctac tttacgctcc aagatagctg aagctgctct 2460
gatcatgaaa cagaaagtga ctgctgccat gagtgaagtt gaatggattg caaccacaac 2520
ggattgttgg actgcacgta gaaagtcatt cattggtgta actgctcact ggatcaaccc 2580
tggaagtctt gaaagacatt ccgctgcact tgcctgcaaa agattaatgg gctctcatac 2640
ttttgaggta ctggccagtg ccatgaatga tatccactca gagtatgaaa tacgtgacaa 2700
ggttgtttgc acaaccacag acagtggttc caactttatg aaggctttca gagtttttgg 2760
tgtggaaaac aatgatatcg agactgaggc aagaaggtgt gaaagtgatg acactgattc 2820
tgaaggctgt ggtgagggaa gtgatggtgt ggaattccaa gatgcctcac gagtcctgga 2880
ccaagacgat ggcttcgaat tccagctacc aaaacatcaa aagtgtgcct gtcacttact 2940
taacctagtc tcaagcgttg atgcccaaaa agctctctca aatgaacact acaagaaact 3000
ctacagatct gtctttggca aatgccaagc tttatggaat aaaagcagcc gatcggctct 3060
agcagctgaa gctgttgaat cagaaagccg gcttcagctt ttaaggccaa accaaacgcg 3120
gtggaattca acttttatgg ctgttgacag aattcttcaa atttgcaaag aagcaggaga 3180
aggcgcactt cggaatatat gcacctctct tgaggttcca atgtaagtgt ttttcccctc 3240
tatcgatgta aacaaatgtg ggttgttttt gtttaatact ctttgattat gctgatttct 3300
cctgtaggtt taatccagca gaaatgctgt tcttgacaga gtgggccaac acaatgcgtc 3360
cagttgcaaa agtactcgac atcttgcaag cggaaacgaa tacacagctg gggtggctgc 3420
tgcctagtgt ccatcagtta agcttgaaac ttcagcgact ccaccattct ctcaggtact 3480
gtgacccact tgtggatgcc ctacaacaag gaatccaaac acgattcaag catatgtttg 3540
aagatcctga gatcatagca gctgccatcc ttctccctaa atttcggacc tcttggacaa 3600
atgatgaaac catcataaaa cgaggtaaat gaatgcaagc aacatacact tgacgaattc 3660
taatctgggc aacctttgag ccataccaaa attattcttt tatttattta tttttgcact 3720
ttttaggaat gttatatccc atctttggct gtgatctcaa tatgaatatt gatgtaaagt 3780
attcttgcag caggttgtag ttatccctca gtgtttcttg aaaccaaact catatgtatc 3840
atatgtggtt tggaaatgca gttagatttt atgctaaaat aagggatttg catgatttta 3900
gatgtagatg actgcacgta aatgtagtta atgacaaaat ccataaaatt tgttcccagt 3960
cagaagcccc tcaaccaaac ttttctttgt gtctgctcac tgtgcttgta ggcatggact 4020
acatcagagt gcatctggag cctttggacc acaagaagga attggccaac agttcatctg 4080
atgatgaaga ttttttcgct tctttgaaac cgacaacaca tgaagccagc aaagagttgg 4140
atggatatct ggcctgtgtt tcagacacca gggagtctct gctcacgttt cctgctattt 4200
gcagcctctc tatcaagact aatacacctc ttcccgcatc ggctgcctgt gagaggcttt 4260
tcagcactgc aggattgctt ttcagcccca aaagagctag gcttgacact aacaattttg 4320
agaatcagct tctactgaag ttaaatctga ggttttacaa ctttgagtag cgtgtactgg 4380
cattagattg tctgtcttat agtttgataa ttaaatacaa acagttctaa agcaggataa 4440
aaccttgtat gcatttcatt taatgttttt tgagattaaa agcttaaaca agaatctcta 4500
gttttctttc ttgcttttac ttttacttcc ttaatactca agtacaattt taatggagta 4560
cttttttact tttactcaag taagattcta gccagatact tttactttta attgagtaaa 4620
attttcccta agtacttgta ctttcacttg agtaaaattt ttgagtactt tttacacctc 4680
tg 4682
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПЕЦИФИЧНЫЕ К MUC16 ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2795198C2 |
| Конструкции для направленного редактирования генов и способы с их применением | 2020 |
|
RU2832109C2 |
| УЛУЧШЕННЫЕ ЭКСПРЕССИЯ И ПРОЦЕССИНГ ТРАНСГЕНА | 2014 |
|
RU2711505C2 |
| ИНТЕГРАЦИЯ КОНСТРУКЦИЙ НУКЛЕИНОВОЙ КИСЛОТЫ В ЭУКАРИОТИЧЕСКИЕ КЛЕТКИ С ТРАНСПОЗАЗОЙ ИЗ ORYZIAS | 2020 |
|
RU2817770C2 |
| АНТИТЕЛА АНТИ-TNFRSF25 | 2017 |
|
RU2746314C2 |
| ТРАНСПОЗИЦИЯ КОНСТРУКЦИЙ НУКЛЕИНОВОЙ КИСЛОТЫ В ЭУКАРИОТИЧЕСКИЕ ГЕНОМЫ С ТРАНСПОЗАЗОЙ ИЗ AMYELOIS | 2020 |
|
RU2814721C2 |
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
| АНТИ-DR5-АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2735956C1 |
| РЕКОМБИНАНТНЫЕ КЛЕТКИ, ПРОДУЦИРУЮЩИЕ ГИАЛУРОНОВУЮ КИСЛОТУ | 2022 |
|
RU2839983C2 |
| СПОСОБ СНИЖЕНИЯ ОШИБОЧНОГО ВКЛЮЧЕНИЯ НЕКАНОНИЧЕСКИХ АМИНОКИСЛОТ С РАЗВЕТВЛЕННОЙ ЦЕПЬЮ | 2019 |
|
RU2816654C2 |
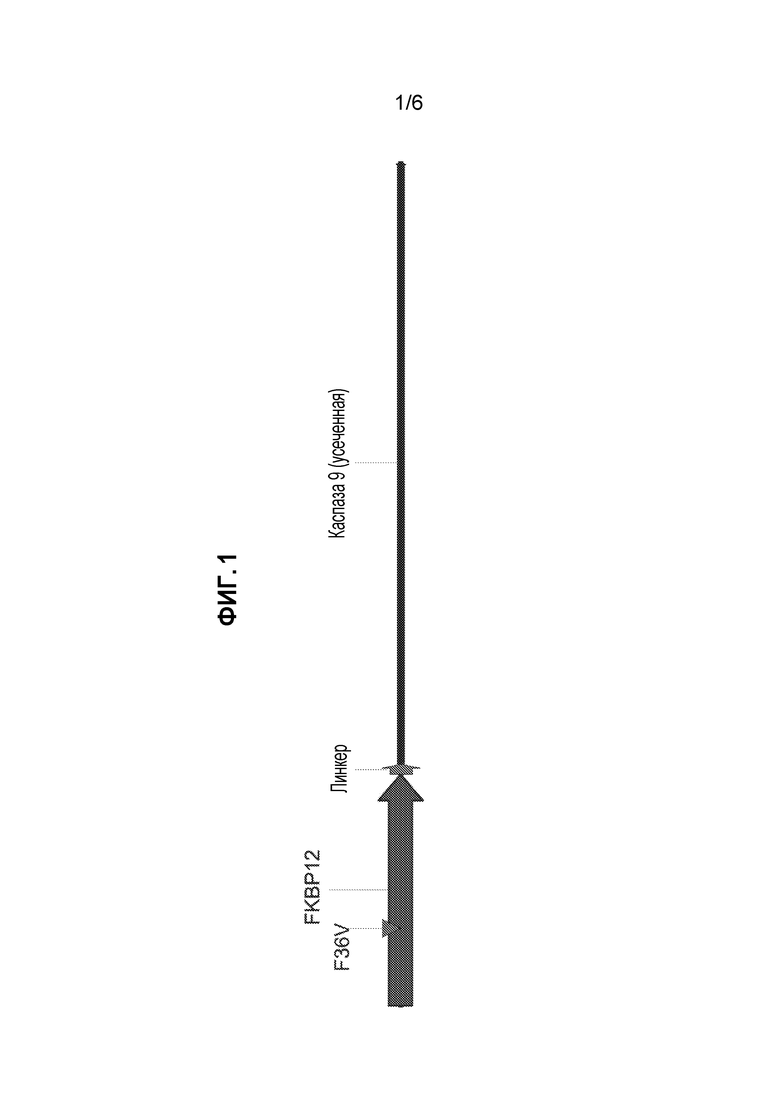
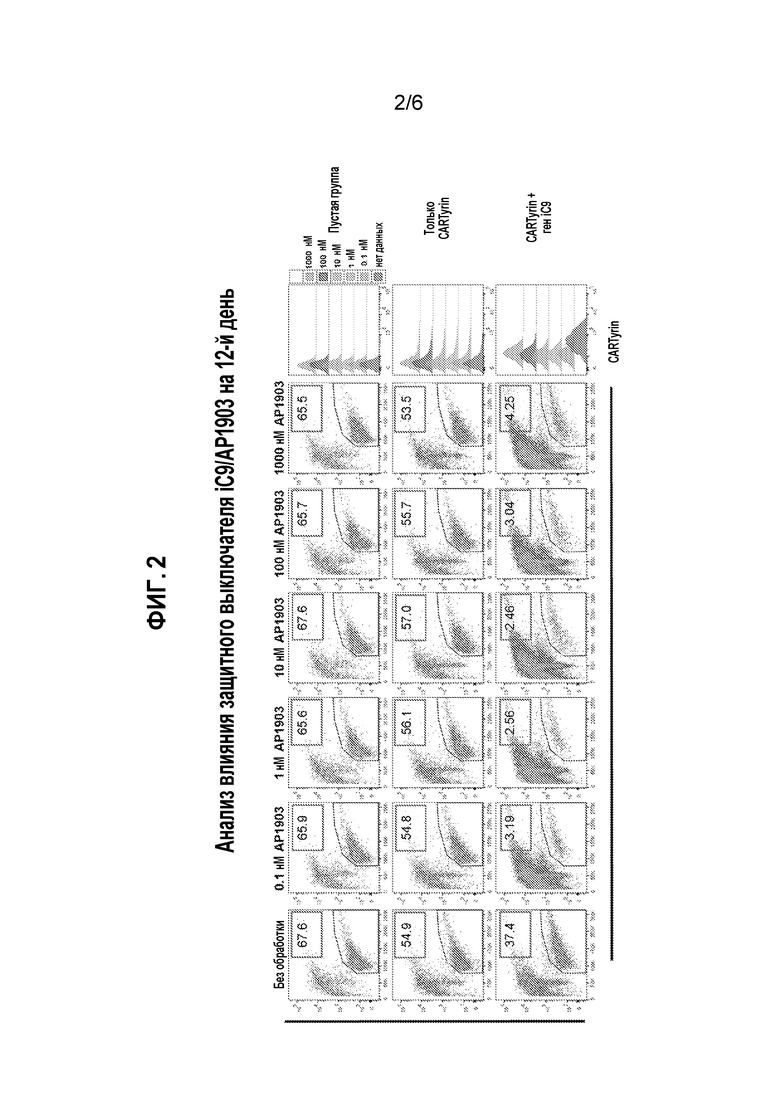
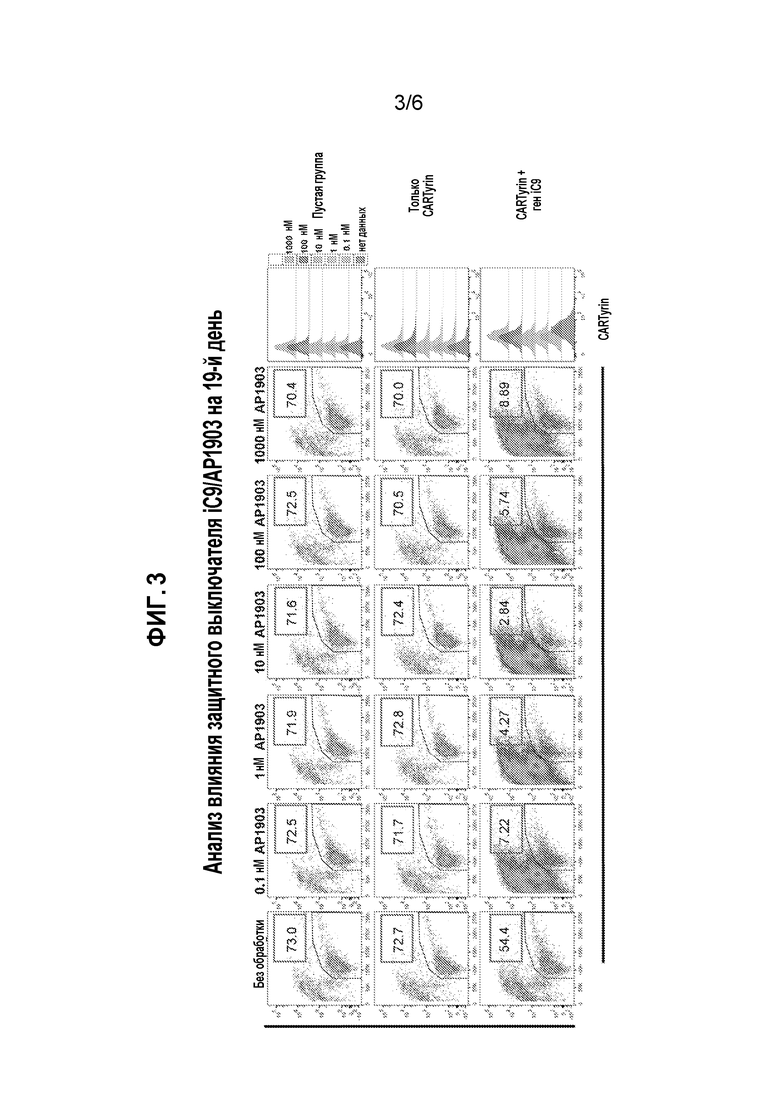
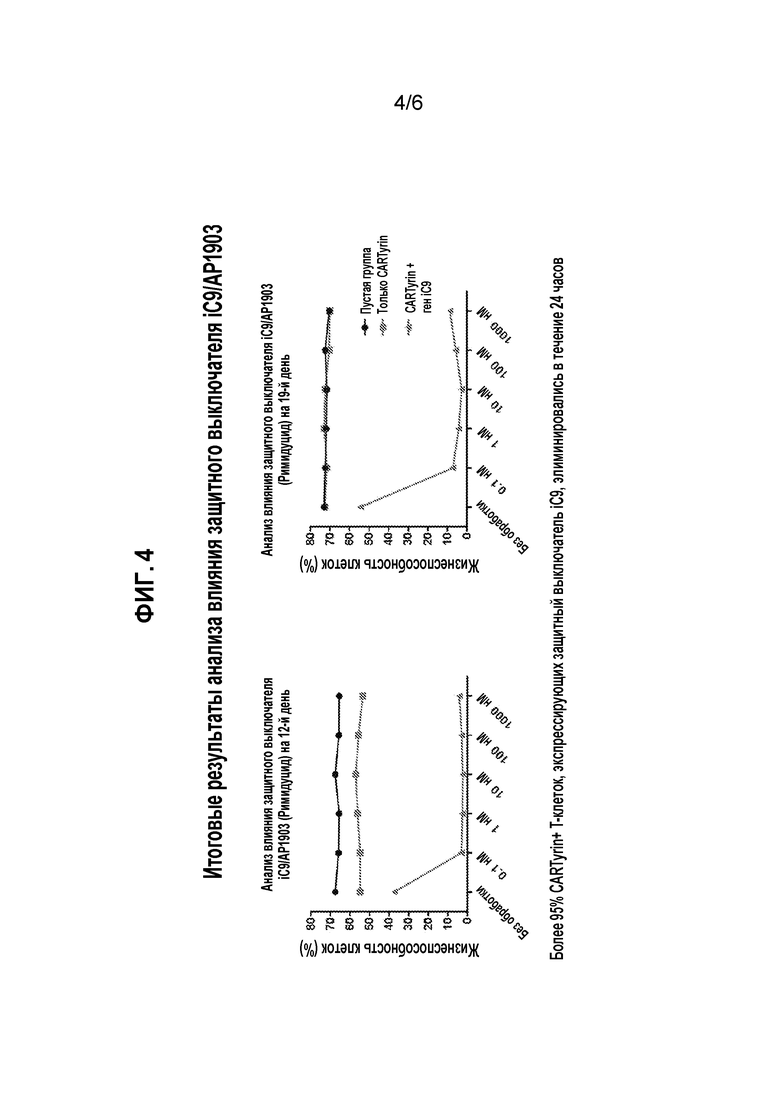
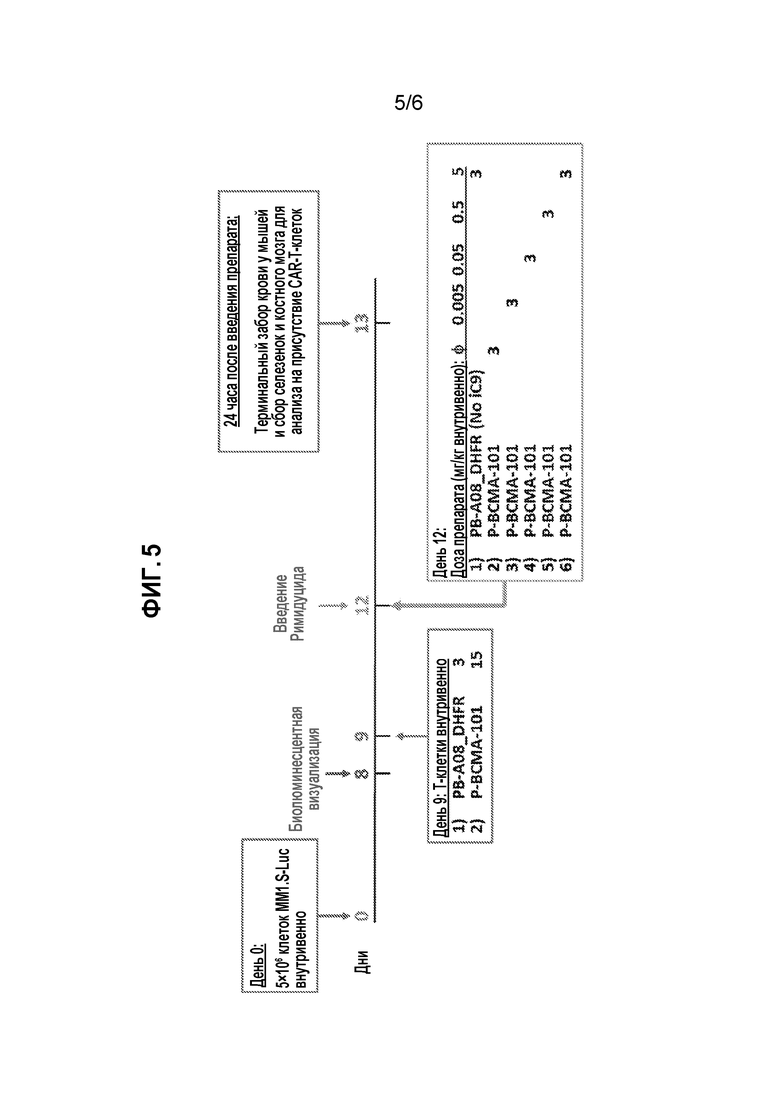
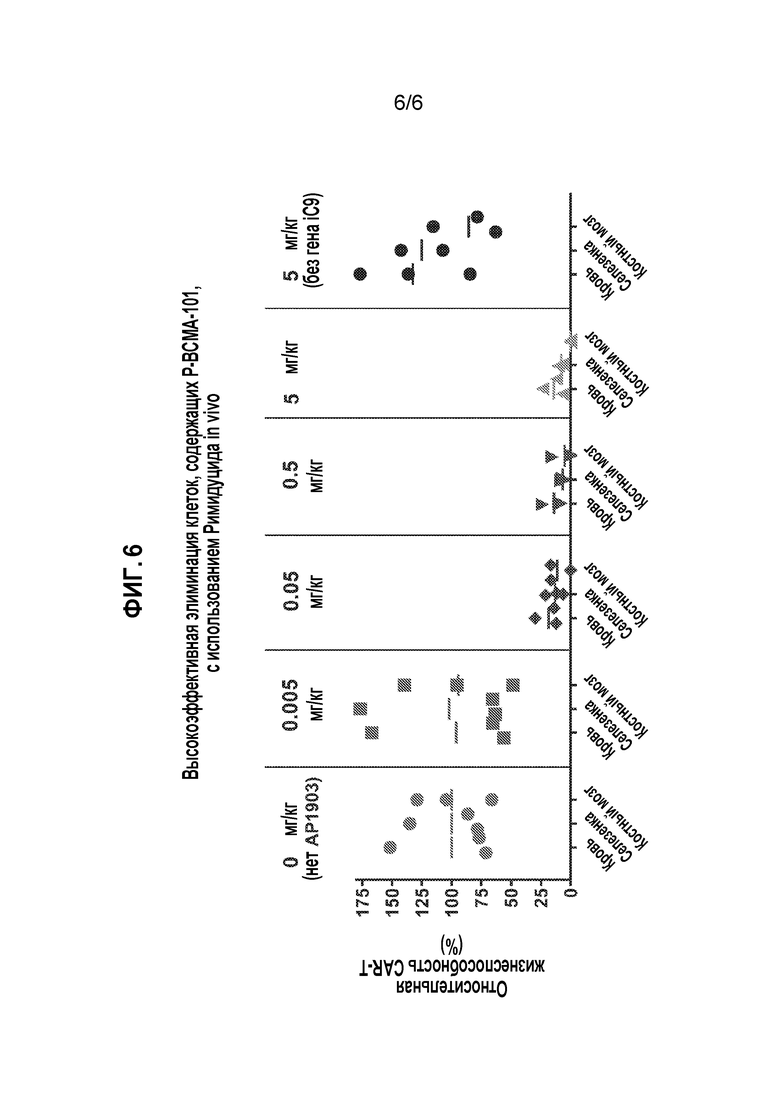
Изобретение относится к области биотехнологии, в частности к полинуклеотиду, кодирующему идуцируемый полипептид каспазы, к полинуклеотиду, содержащему нуклеотидную последовательность, кодирующую область связывания лиганда, нуклеотидную последовательность, кодирующую линкер, и нуклеотидную последовательность, кодирующую усеченный полипептид каспазы 9, а также к содержащей его композиции, вектору и клетке. Также раскрыт индуцируемый полипептид каспазы, а также способ модификации клеточной терапии у субъекта, нуждающегося в этом, включающий в себя введение субъекту вышеуказанной клетки. Изобретение также относится к способу лечения заболевания или расстройства у субъекта, предусматривающего введение субъекту вышеуказанного полинуклеотида. Изобретение позволяет селективно индуцировать апоптоз в генетически модифицированных клетках. 12 н. и 17 з.п. ф-лы, 6 ил., 2 пр.
1. Полинуклеотид, кодирующий индуцируемый полипептид каспазы, где полинуклеотид содержит:
a. нуклеотидную последовательность, кодирующую область связывания лиганда, где область связывания лиганда содержит полипептид связывающего FK506 белка 12 (FKBP12), где полипептид FKBP12 содержит аминокислотную последовательность SEQ ID NO:3;
b. нуклеотидную последовательность, кодирующую линкер, где линкер содержит аминокислотную последовательность SEQ ID NO: 5; и
c. нуклеотидную последовательность, кодирующую усеченный полипептид каспазы 9, где усеченный полипептид каспазы 9 содержит аминокислотную последовательность SEQ ID NO: 7.
2. Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую область связывания лиганда, нуклеотидную последовательность, кодирующую линкер, и нуклеотидную последовательность, кодирующую усеченный полипептид каспазы 9, где
a. нуклеотидная последовательность, кодирующая область связывания лиганда, содержит нуклеотидную последовательность SEQ ID NO: 4;
b. нуклеотидная последовательность, кодирующая линкер, содержит нуклеотидную последовательность SEQ ID NO: 6; и
c. нуклеотидная последовательность, кодирующая усеченный полипептид каспазы 9, содержит нуклеотидную последовательность SEQ ID NO: 8.
3. Индуцируемый полипептид каспазы, включающий:
a. область связывания лиганда, где область связывания лиганда содержит полипептид FKBP12, где полипептид FKBP12 содержит аминокислотную последовательность SEQ ID NO: 3;
b. линкер, содержащий аминокислотную последовательность SEQ ID NO: 5; и
c. усеченный полипептид каспазы 9, содержащий аминокислотную последовательность SEQ ID NO: 7.
4. Полипептид по п. 3, где полипептид содержит аминокислотную последовательность SEQ ID NO: 9.
5. Полинуклеотид по п. 1 или 2, где полинуклеотид содержит нуклеотидную последовательность SEQ ID NO: 10.
6. Композиция для введения в клетку, где композиция содержит транспозон и транспозазу, где транспозон содержит полинуклеотид по п. 1 или 2.
7. Композиция по п. 6, дополнительно содержащая нуклеотидную последовательность, кодирующую терапевтический белок.
8. Композиция по п. 7, где терапевтический белок содержит рецептор антигена, белок клеточной поверхности, мембранно-связанный белок, внеклеточный мембранно-связанный белок, внутриклеточный мембранно-связанный белок, внутриклеточный белок, локализованный в ядре белок, ядерный белок, цитоплазматический белок, цитозольный белок, секретируемый белок, лизосомальный белок, эндосомальный белок, везикуло-ассоциированный белок, митохондриальный белок, белок эндоплазматического ретикулума, белок цитоскелета, белок, участвующий во внутриклеточной передаче сигнала, белок, участвующий во внеклеточной передаче сигнала, или любую их комбинацию.
9. Композиция по п. 8, где рецептор антигена содержит Т-клеточный рецептор (TCR) или химерный рецептор антигена (CAR).
10. Композиция по п. 9, где CAR содержит одну или несколько последовательностей центиринов или CAR содержит одну или несколько последовательностей VHH.
11. Композиция по любому из пп. 6-10, где транспозон представляет собой транспозон piggyBac, транспозон Helraiser или транспозон Tol2.
12. Композиция по любому из пп. 6-11, где транспозаза представляет собой транспозазу piggyBac, транспозазу Super piggyBac (sPBo), транспозазу Sleeping Beauty, гиперактивную транспозазу Sleeping Beauty (SB100X), транспозазу Helitron или траспозазу Tol2.
13. Вектор, содержащий полинуклеотид по п. 1 или 2, для применения при трансдукции клетки-хозяина.
14. Вектор по п. 13, где вектор представляет собой вирусный вектор или вектор в виде наночастиц.
15. Вектор по п. 14, где вирусный вектор содержит последовательность, выделенную или полученную из ретровируса, лентивируса, аденовируса, аденоассоциированного вируса (AAV) или любой их комбинации.
16. Клетка, содержащая полинуклеотид по п. 1 или 2, для применения в клеточной терапии.
17. Клетка, содержащая композицию по любому из пп. 6-12, для применения в клеточной терапии.
18. Клетка, содержащая полипептид по п. 3 или 4, для применения в клеточной терапии.
19. Клетка, содержащая вектор по любому из пп. 13-15, для применения в клеточной терапии.
20. Клетка по любому из пп. 16-19, где клетка представляет собой клетку человека, иммунную клетку, искусственную антигенпредставляющую клетку или стволовую клетку.
21. Клетка по любому из пп. 16-20, где клетка представляет собой соматическую клетку, выделенную из сердца, скелетной или гладкой мускулатуры, кровеносного сосуда, вены или капилляра, селезенки, щитовидной железы, лимфатического узла или лимфатического сосуда, кости или костного мозга, кожи или эндотелия, надпочечника, пищевода, гортани, головного или спинного мозга, периферической нервной системы, глаза, гипоталамуса, печени, обонятельной ткани, предстательной железы, желудка, толстого или тонкого кишечника, легкого или бронхов, почки, поджелудочной железы, тимуса, мочеточника или уретры, мочевого пузыря, мочевого пузыря, слуховой ткани, паращитовидной железы, слюнной железы или трахеи человека.
22. Применение клетки по любому из пп. 16-21 для адаптивной клеточной терапии или для генной терапии ex vivo.
23. Применение по п. 22, где клетка является аутологичной.
24. Применение по п. 22, где клетка является аллогенной.
25. Способ модификации клеточной терапии у субъекта, нуждающегося в этом, включающий в себя введение субъекту клетку по любому из пп. 16-21, где апоптоз может селективно индуцироваться в клетке путем контакта клетки с индуцирующим агентом.
26. Способ по п. 25, где модификация представляет собой прекращение клеточной терапии или деплецию части клеток, обеспечиваемых клеточной терапией.
27. Способ по п. 25, дополнительно содержащий стадию введения ингибитора индуцирующего агента для ингибирования модификации клеточной терапии, в результате чего восстанавливаются функция и/или эффективность клеточной терапии.
28. Способ лечения заболевания или расстройства у субъекта, нуждающегося в этом, включающий в себя
a. введение субъекту композиции, содержащей клетку, содержащую кинетический агент и полинуклеотид по п. 1 или 2, где апоптоз может селективно индуцироваться в клетке путем контакта клетки с индуцирующим агентом, и где клетка, содержащая кинетический агент, вызывает локальную тканевую токсичность в ткани-мишени субъекта, и
b. селективную индукцию апоптоза в клетке, содержащей кинетический агент, до возникновения значительной токсичности в не являющейся мишенью ткани субъекта,
c. в результате чего воздействие элиминирует ткань-мишень при сохранении не являющейся мишенью ткани, и осуществляется лечение заболевания или расстройства у субъекта.
29. Способ по п. 28, где заболевание или расстройство представляет собой пролиферативное расстройство, рак, воспалительное заболевание или расстройство, иммунное или аутоиммунное заболевание или расстройство, инфекционное заболевание или расстройство, генетическое или эпигенетическое заболевание или расстройство, метаболическое нарушение, сосудистое заболевание, респираторное заболевание или фиброзное заболевание.
| WO 2016135470 A1, 01.09.2016 | |||
| WO 2015134877 A1, 11.09.2015 | |||
| KARIN C STRAATHOF ET AL, A inducible caspase 9 safety switch for T-cell therapy, BLOOD, 2005, vol | |||
| Транспортер для перевозки товарных вагонов по трамвайным путям | 1919 |
|
SU105A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Транспортер для волокон к трепальным машинам | 1926 |
|
SU4247A1 |
| TEY ET AL, Inducible Caspase 9 Suicide Gene to Improve the Safety of Allodepleted T Cells after Haploidentical Stem Cell Transplantation, BIOLOGY OF BLOOD AND | |||
Авторы
Даты
2021-10-11—Публикация
2017-10-06—Подача