Настоящее изобретение относится к определяемым в крови биомаркерам инсульта и областям их применения, в частности, для мониторинга эффективности терапии при ишемическом инсульте, для диагностических целей, краткосрочного и долгосрочного прогнозирования, а также оценки рисков.
В мире инсульт занимает второе место среди основных причин смертности и третье - среди основных причин наступления инвалидности (McKay & Mensah, 2005. The atlas of heart disease and stroke (1-е издание). Женева: Всемирная организация здравоохранения). Фокальная церебральная ишемия, т.е. ишемический инсульт, приводит к тяжелому и стремительно развивающемуся повреждению ткани в очаге инфаркта головного мозга. После первичного повреждения гибель клеток головного мозга прогрессирует медленно, распространяясь на гетерогенную зону, окружающую очаг и называемую «пенумбра» (ишемическая полутень) (Astrup и другие., 1977. Stroke. 8 (1):51-7). Спасение клеток ишемической полутени от необратимых изменений смягчает последствия в отношении наступления инвалидности (Emberson и другие., 2014. Lancet. 384(9958): 1929-35).
На сегодняшний день единственной неотложной терапевтической помощью является восстановление проходимости сосудов посредством тромболизиса и/или тромбэктомии. Однако вследствие серьезных временных ограничений на проведение медицинского вмешательства (<6 часов для восстановления проходимости сосудов и 4 часа 30 минут для тромболизиса) и риска геморрагической трансформации подобные методы лечения могут применяться лишь в отношении небольшого процента пациентов с острым ишемическим инсультом. Например, согласно оценкам, среди всех пациентов, доставленных в специализированный медицинский центр в течение 6 часов после развития инсульта, только 10,5% могут быть подвергнуты тромбэктомии, исходя из эндоваскулярных показателей в соответствии с критериями AHA/ASA (Vanacker и другие, 2016. Stroke. 47(7):1844-9).
Таким образом, разработка новой стратегии лечения, позволяющей расширить «терапевтическое окно», представляет собой важнейший вопрос в сфере общественного здравоохранения. Хотя многие клинические испытания ранее потерпели неудачу, после внедрения методов восстановления проходимости сосудов нейрозащита, в сочетании с восстановлением кровотока, остается потенциально перспективной стратегией расширения «терапевтического окна». Растущее число доказательств позволяет предположить, что периферические белки, нуклеиновые кислоты или липиды могут быть использованы для подтверждения диагноза «ишемический инсульт» и мониторинга прогрессирования заболевания. На данный момент, однако, ничто из упомянутого не было реализовано в клинической практике (Kim и другие, 2013. J Stroke. 15(1):27-37).
К анализам на биомаркеры относятся визуализация, химические или биологические тесты, которые могут применяться для качественной оценки или количественного измерения присутствия или отсутствия одного или нескольких маркеров, указывающих на наличие, прогрессирование или тяжесть заболевания или на определенные эффекты лечения. С одной стороны, достигнут огромный прогресс в методах визуализации центральной нервной системы (ЦНС), но, с другой стороны, технологии выявления периферических биологических маркеров развиты слабее. Определение в крови надежных биомаркеров, характеризующих заболевания или результаты терапии заболеваний ЦНС, является одной из наиболее важных проблем современной неврологии, поскольку кровь не вступает в прямой контакт с мозгом.
Определение содержания РНК в крови в качестве диагностического маркера представляет собой новую область, в поддержку которой выступают результаты клинического применения данного метода в диагностике онкологических заболеваний молочных желез, ишемической болезни сердца и инфекционных заболеваний (Rothstein & Jickling, 2013. Biomark Med. 7(1):37-47). Кроме того, определение содержания РНК в крови может быть использовано в качестве сопутствующей диагностики для оценки действия веществ-нейропротекторов на ранних стадиях клинических исследований. Исследования использования РНК как диагностического биомаркера при остром ишемическом инсульте немногочисленны и включают лишь небольшое число пациентов, среди которых только некоторые находились в острой фазе инфаркта головного мозга (Tang и др., 2006. J Cereb Blood Flow Metab. 26(8):1089-102; Stamova и др., 2010. Stroke. 41(10):2171-7) для определения кодирующих РНК. В последнее время наблюдается растущий интерес к некодирующим РНК в качестве потенциальных биомаркеров инсульта как фактора риска, но не в острой фазе инфаркта головного мозга (Mick и другие., 2017. Stroke. 48(4):828-834).
Транскриптомный анализ уже используется во многих экспериментальных исследованиях церебральной ишемии для выявления изменений в экспрессии генов. Большинство исследований с применением транскриптомного анализа выполнялось на крысах и мышах с использованием моделей фокальной или глобальной ишемии (обзор см. Cox-Limpens и другие., 2014. Brain Res. 1564:85-100). Кроме ишемии, прекондиционирование также использовалось в качестве инструмента для изучения эндогенной защиты мозга у грызунов. Результаты микроматричного анализа, исследовавшего транскриптом этих грызунов, показали, что в ходе церебральной ишемии наблюдались изменения экспрессии предранних генов, генов ответа на стресс, генов апоптоза, генов сигнальной трансдукции, генов нейротрансмиссии, генов ионных каналов, генов воспаления, генов цитоскелета, рибосомных генов, и генов нейротрофического фактора (Schmidt-Kastner и другие, 2002. Brain Res Mol Brain Res. 108(1-2):81-93; Büttner и другие, 2009. Brain Res. 1252:1-14; Wang и другие, 2011. Brain Res. 1372:13-21; Wang и другие, 2012. Neuroscience. 220:100-8; Lu и другие, 2004. J Neurosci Res. 77(6):843-57). Однако, насколько известно, было проведено лишь небольшое число экспериментов с участием приматов (Cook и другие, 2012. Nature. 483(7388):213-7; Cook & Tymianski, 2012. Neurotherapeutics, 9(2):371-9). Приматы являются уникальными моделями для изучения ишемии головного мозга из-за анатомического сходства с человеком и высокой степени схожести их генома с геномом человека. Например, как приматы, так и люди, в отличие от грызунов, имеют нелиссэнцефалический мозг (то есть, мозг, имеющий извилины в области коры - на поверхности больших полушарий). Более того, транскриптомы коры головного мозга у людей и у шимпанзе очень похожи и разнятся в большей степени между отдельными представителями, чем для разных участков у одного представителя (Khaitovich и другие, 2004. Genome Res. 14(8):1462-73).
Установлены четыре основные причины неудачи при переходе от изучения нейропротективной терапии на животных к ее применению у людей (Moretti и другие, 2015. Pharmacol Ther. 146:23-34; Timsit & Menn, 2012. Clin Pharmacol Ther. 91(2):327-32):
i) Низкое качество доклинических исследований:
Для клинических исследований проблема в данной области постепенно решается путем разработки критериев балльной оценки качества в ходе доклинических исследований, например, критериев STAIR (Stroke Therapy Academic Industry Roundtable - Круглый стол научного сообщества по вопросам терапии инсульта), 1999. Stroke. 30(12):2752-8; Fisher и другие, 2009. Stroke. 40(6):2244-50); и путем разработки рандомизированных слепых исследований на людях (Llovera и другие, 2015. Sci Transi Med. 7(299):299ra121).
ii) Отсутствие сопутствующих биологических маркеров фармакодинамики на ранних стадиях клинических испытаний:
Сопутствующие биомаркеры для разработки лекарственных средств сегодня используются все чаще. Для обретения уверенности в вопросе о том, можно ли достичь эффективного результата, у больных пациентов при помощи безопасных доз, перед существенными инвестициями, которых требуют более поздние стадии исследования, проводится относительно кратковременная фаза клинических исследований Ib при участии небольшого числа пациентов, имеющих соответствующее заболевание. Это наиболее важная область применения некоторых фармакодинамических биомаркеров (Zhao и другие, 2015. Clin Chem. 61(11):1343-53).
iii) Отсутствие прогностических томографических биомаркеров в фазе II исследований на людях для оценки пенумбры:
Как показывает исследование DAWN, отбор пациентов на основании визуализации головного мозга с целью выявления тех из них, кто, пригоден для тромбэктомии, сегодня играет решающую роль для спасения пенумбры у отобранных пациентов (Jovin и другие, 2017. Int J Stroke. 12(6):641-652; Chaisinanunkul и другие, 2015. Stroke. 46(8):2238-43; Nogueira и другие, 2018. N Engi J Med. 378(1):11-21). Отбор на основании характеристик пенумбры осуществлялся в ходе всего лишь нескольких исследований, посвященных нейрозащите (обзор см. Donnan и другие, 2009. Lancet Neurol. 8(3):261-9). Сегодня эта новая концепция может предложить полезный путь терапевтического вмешательства (Hillis & Baron, 2015. Front Neurol. 6:85) на период ожидания восстановления проходимости сосудов или реперфузии.
iv) Отсутствие возможности восстановления проходимости сосудов у большинства пациентов:
Тромбэктомия становится стандартным способом лечения во время острой фазы ишемического инсульта, хотя использование этого способа необходимо расширить. Согласно оценкам, только 10,5% от общего числа пациентов, в течение 6 часов после наступления инсульта прибывающих в специализированный медицинский центр, по эндоваскулярным показателям подходят, на основании критериев AHA/ASA, для проведения тромбэктомии (Vanacker и другие, 2016. Stroke. 47(7):1844-9).
Более глубокое понимание профилей экспрессии генов в ткани, пораженной церебральной ишемией, может содействовать совершенствованию методов диагностики. В данной работе изучали экспрессию генов после наступления церебральной ишемии, исследуя кровь и головной мозг. Микроматричный анализ экспрессии генов у макак, проведенный с использованием данных крови и мозга, показал, что образцы от животных с инсультом и без инсульта различаются профилем экспрессии, а большинство высокодифференциально экспрессируемых генов имеют повышенный уровень экспрессии при инсульте через 6 часов после его наступления. Сравнение дифференциально экспрессируемых генов в крови и в головном мозге выявило существенную степень частичного совпадения профилей экспрессии генов. К удивлению исследователей, данные свидетельствовали о наличии общей кодирующей сигнатуры для мозга и крови при инсульте, что говорит в пользу развития транскриптомики крови в качестве инструмента биопсийного транскриптомного профилирования экспрессии с целью характеризации пациентов с ишемическим инсультом и разработки сопутствующих биомаркеров, необходимых для оценки эффективности лекарств-нейропротекторов у пациентов.
Краткое описание сущности изобретения
Настоящее изобретение относится к способу диагностики инсульта у индивида, включающему:
i) Определение сигнатуры (профили экспрессии набора генов) в образце, полученном от индивида, путем измерения уровней экспрессии, как минимум, двух биомаркеров, выбранных из группы, состоящей из PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM,
предпочтительно с условием, что упомянутые выше, как минимум, два биомаркера, не состоят из DUSP1 и ADM;
ii) Сравнение сигнатуры, определенной на стадии i), с эталонной сигнатурой; и
iii) Диагностирование индивида как перенесшего инсульт, если уровни экспрессии упомянутых ранее, как минимум, двух биомаркеров в сигнатуре выше, чем уровни экспрессии тех же, как минимум, двух биомаркеров, в эталонной сигнатуре.
В одном варианте осуществления стадия i) данного способа диагностики инсульта у индивида включает измерение уровней экспрессии, как минимум, трех биомаркеров, выбранных из группы, состоящей из PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления стадия i) данного способа диагностики инсульта у индивида включает измерение уровней экспрессии PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления эталонную сигнатуру получают измерением уровней экспрессии биомаркеров у референтной группы по существу здоровых индивидов.
В одном варианте осуществления способ диагностики инсульта согласно настоящему изобретению направлен на дифференцирование инсульта и имитации инсульта.
Настоящее изобретение также относится к способу определения вероятности ответной реакции индивида, перенесшего инсульт, на лечение.
Метод включает:
i) Определение сигнатуры в образце, полученном от данного индивида, путем измерения уровней экспрессии, как минимум, двух биомаркеров, выбранных из группы, включающей: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
предпочтительно с условием, что упомянутые выше, как минимум, два биомаркера, не состоят из DUSP1 и ADM
ii) Сравнение сигнатуры, определенной на стадии i), с эталонной сигнатурой; и
iii) Вывод о том, что индивид демонстрирует ответную реакцию на лечение, если уровни экспрессии вышеупомянутых, как минимум, двух биомаркеров в сигнатуре ниже, чем уровни экспрессии тех же, как минимум, двух биомаркеров, в эталонной сигнатуре.
В одном варианте осуществления стадия i) рассматриваемого способа определения вероятности ответной реакции индивида, перенесшего инсульт, на лечение, включает измерение уровней экспрессии девяти биомаркеров, выбранных из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления эталонную сигнатуру получают путем измерения уровней экспрессии биомаркеров в образце, взятом у того же индивида до начала указанного лечения.
Настоящее изобретение относится к методу определения риска возникновения инсульта у индивида, включающему:
i) Определение сигнатуры в образце, полученном от данного индивида, путем измерения уровней экспрессии, как минимум, двух биомаркеров, выбранных из группы, включающей PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
предпочтительно с условием, что упомянутые выше, как минимум, два биомаркера, не состоят из DUSP1 и ADM
ii) Сравнение сигнатуры, определенной на стадии i), с эталонной сигнатурой; и
iii) Вывод о том, что у индивида присутствует риск возникновения инсульта, если уровни экспрессии ранее упомянутых, как минимум, двух биомаркеров в сигнатуре выше, чем уровни экспрессии тех же, как минимум, двух биомаркеров, в эталонной сигнатуре.
В одном варианте осуществлении стадия i) определения риска возникновения инсульта у индивида включает измерение уровней экспрессии девяти биомаркеров, выбранных из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления эталонную сигнатуру получают измерением уровней экспрессии данных биомаркеров у референтной группы по существу здоровых индивидов.
В одном варианте осуществления у индивида уже был инсульт, и метод определения риска возникновения у индивида инсульта направлен на определение риска возникновения у данного индивида повторного инсульта.
В одном варианте осуществления, относящемся к любому из методов по настоящему изобретению, инсульт представляет собой ишемический инсульт, транзиторную ишемическую атаку, или геморрагический инсульт.
В одном варианте осуществления, относящемся к любому из методов по настоящему изобретению, образец представляет собой образец крови, плазмы или сыворотки.
В одном варианте осуществления, относящемся к любому из методов по настоящему изобретению, образец не является образцом тканей головного мозга.
Определения
В настоящем изобретении нижеприведенные термины имеют следующие значения:
«Инсульт» в контексте настоящего документа означает любое патологическое состояние, возникающее в результате нарушения, снижения или остановки притока крови или кислорода к любой части головного мозга. В частности, термин «инсульт» включает, в числе прочего, ишемический инсульт, транзиторную ишемическую атаку (ТИА), геморрагический инсульт.
«Ишемический инсульт» (или «ИИ») это случай неврологической дисфункции, вызванной очаговой ишемией мозга, ишемией спинного мозга, или ишемией сетчатки с признаками острого инфаркта (Easton и другие, 2009. Stroke. 40(6):2276-2293). Существуют, по крайней мере, четыре причины нарушения кровообращения:
(1) Тромб в кровеносном сосуде;
(2) Тромб в дуральных венозных синусах, отводящих кровь от мозга;
(3) Закупорка кровеносного сосуда эмболом; и/или
(4) Внезапное и резкое понижение давления крови.
Симптомы инсульта могут сохраняться, и часто сохраняются, в течение более чем 24 часов, если пациент выживает при исходном нарушении.
«Транзиторная ишемическая атака» или «ТИА», также называемая микроинсультом, представляет собой преходящий случай неврологической дисфункции, вызванной очаговой ишемией мозга, ишемией спинного мозга, или ишемией сетчатки без признаков острого инфаркта. Симптомы ТИА могут изначально быть аналогичными симптомам инсульта, за исключением того, что они длятся недолго, обычно менее часа, максимум 24 часа. Даже несмотря на то, что ТИА носит временный характер и обычно не вызывает повреждения тканей головного мозга, пациентам, у которых случается ТИА, советуют немедленно обращаться за профессиональной помощью из-за схожести симптомов и из-за того, что ТИА является фактором риска возникновения впоследствии ишемического инсульта.
«Геморрагический инсульт» означает инсульт, являющийся результатом разрыва какого-либо элемента сосудистой сети головного мозга.
Примеры острых неврологических расстройств, которые включают инсульт или охватывают этиологию или симптоматику, наблюдаемую при инсульте, перечислены выше и состоят, помимо прочего, из церебральной ишемии или инфаркта головного мозга (в том числе, эмболической окклюзии и тромболитической окклюзии), реперфузии, следующей за острой ишемией, перинатальных гипоксическо-ишемических повреждений, остановки сердца, а также внутричерепных кровоизлияний (таких, например, как эпидуральное, субдуральное, субарахноидальное и внутримозговое).
«Индивид» в контексте настоящего документа означает лицо, диагностированное или получающее лечение в соответствии с методами по настоящему изобретению. К индивидам относятся, помимо прочих, млекопитающие (например, мышиные, обезьяны, лошадиные, бычьи, свиные, псовые, кошачьи, и другие), предпочтительно, приматы, наиболее предпочтительно, люди. В контексте настоящего изобретения термин «пациент» относится, в целом, к лицу, обратившемуся за диагнозом и лечением, или уже имеющему диагноз и получающему лечение в соответствии с методами по настоящему изобретению.
«Лечение» в контексте настоящего документа означает смягчение конкретного патологического состояния (например, инсульта), устранение или уменьшение симптоматики патологического состояния (например, инсульта), замедление или блокирование прогрессирования патологического состояния (например, инсульта), и предотвращение или откладывание первичного наступления патологического состояния (например, инсульта) у индивида, или предотвращение или откладывание повторного наступления патологического состояния (например, инсульта), ранее уже наблюдавшегося у индивида.
«Диагностика» или «диагноз» в контексте настоящего документа означает оценку развития или прогрессирования патологического состояния (например, инсульта). Как известно специалистам в данной области техники, точная оценка осуществима в отношении статистически значимого индивида, хотя предполагается, что она должна быть точной для 100% диагностируемых индивидов. Специалисту несложно установить статистическую значимость, используя методы, широко известные в данной области техники, например, определение доверительного интервала, определение p-уровня, критерий Стьюдента, критерий Манна-Уитни, и т.п. Предпочтительные значения доверительного интервала: 90% или выше, 95% или выше, 97% или выше, 98% или выше, и 99%. Предпочтительные значения p-уровня: 0,1; 0,05; 0,01; 0,005 или 0,0001. Предпочтительно, чтобы результат диагностики в соответствии с настоящим изобретением был точен для 60 или более процентов, 70 или более процентов, 80 или более процентов, или 90 или более процентов индивидов в составе группы.
«Прогнозирование» или «прогноз» в контексте настоящего документа означает предположение, на основании фактов, сделанное в отношении возможного результата для индивида, имеющего патологическое состояние (например, инсульт), по окончании конкретного лечения или вмешательства.
«Образец крови» в контексте настоящего документа означает любой образец крови, полученный или взятый у индивида. Отбор образцов крови может производиться методами, хорошо известными специалистам в данной области техники. В некоторых вариантах осуществления образец крови представляет собой образец цельной крови, образец сыворотки или образец плазмы крови.
«Биомаркер» в контексте настоящего документа означает набор продуктов экспрессии генов (например, мРНК и/или белок), который связан с повреждением тканей головного мозга или нервных клеток, и который может коррелировать с инсультом, но, предпочтительно, не коррелирует с другими типами повреждений. Подобные специфические биомаркеры инсульта, выделенные в крови Авторами изобретения, включают PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM. Данные специфические биомаркеры подробно описаны ниже в настоящем документе.
В настоящем описании название каждого из искомых генов означает международное название соответствующего гена в том виде, в котором оно фигурирует в международных базах данных последовательностей генов и последовательностей белков, в частности, в базе данных Комитета по номенклатуре генов в составе HUGO, которую можно найти в Интернете по следующему адресу: http://www.gene.ucl.ac.uk/nomenclature/index.html.
В настоящем описании название каждого из различных искомых биомаркеров может также означать международное название соответствующего гена в том виде, в котором оно фигурирует в международных базах данных последовательностей генов и последовательностей белков ENTRE ID, Genbank, TrEMBL или ENSEMBL. При помощи указанных международных баз данных последовательность нуклеиновых кислот, соответствующая каждому искомому гену, описанному в настоящем документе, может быть установлена специалистом в рассматриваемой области техники.
"PTG52" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген простагландин-эндопероксид-синтазы-2 (идентификационный номер (ID) гена: 5743). Типичная аминокислотная последовательность человека, кодируемая геном "PTGS2", представлена в виде стандартной последовательности NP_000954.1 (SEQ ID NO: 1) банка данных Национального центра биотехнологической информации (NCBI). Типичная последовательность человеческой мРНК гена "PTGS2" представлена в виде стандартной последовательности NM_000963.4 (SEQ ID NO: 2) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 134 до остатка 1948 последовательности SEQ ID NO: 2.
"HMOX1" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген гемоксигеназы-1 (ID гена: 3162). Типичная аминокислотная последовательность человека, кодируемая геном "НМОХ1" представлена в виде стандартной последовательности NP_002124.1 (SEQ ID NO: 3) банка данных NCBI. Типичная последовательность человеческой мРНК гена "HMOX1" представлена в виде стандартной последовательности NM_002133.3 (SEQ ID NO: 4) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 79 до остатка 945 последовательности SEQ IDNO: 4.
"LDLR" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген рецептора липопротеинов низкой плотности (ID гена: 3949). Типичная аминокислотная последовательность человека, кодируемая геном "LDLR", представлена в виде стандартной последовательности NP_000518.1 (SEQ ID NO: 5) банка данных NCBI. Типичная последовательность человеческой мРНК гена "LDLR" представлена в виде стандартной последовательности NM_000527.4 (SEQ ID NO: 6) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 188 до остатка 2770 последовательности SEQ ID NO: 6.
"HSPA1B" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген представителя семейства белков теплового шока A (Hsp70) 1B (ID гена: 3304). Типичная аминокислотная последовательность человека, кодируемая геном "HSPA1B", представлена в виде стандартной последовательности NP_005337.2 (SEQ ID NO: 7) банка данных NCBI. Типичная последовательность человеческой мРНК гена "HSPA1B" представлена в виде стандартной последовательности NM_005346.5 (SEQ ID NO: 8) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 214 до остатка 2139 последовательности SEQ ID NO: 8.
"G0S2" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген белка G0/G1 switch 2 (ID гена: 50486). Типичная аминокислотная последовательность человека, кодируемая геном "G0S2", представлена в виде стандартной последовательности NP_056529.1 (SEQ ID NO: 9) банка данных NCBI. Типичная последовательность человеческой мРНК гена "G0S2" представлена в виде стандартной последовательности NM_015714.4 (SEQ ID NO: 10) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 171 до остатка 482 последовательности SEQ ID NO: 10.
"BAG3" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген BCL2-ассоциированного атаногена 3 (ID гена: 9531). Типичная аминокислотная последовательность человека, кодируемая геном "BAG3", представлена в виде стандартной последовательности NP_004272.2 (SEQ ID NO: 11) банка данных NCBI. Типичная последовательность человеческой мРНК гена "BAG3" представлена в виде стандартной последовательности NM_004281.3 (SEQ ID NO: 12) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 307 до остатка 2034 последовательности SEQ ID NO: 12.
"TM4SF1" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген белка transmembrane 4-L-six family member-1 (ID гена: 4075). Типичная аминокислотная последовательность человека, кодируемая геном "TM4SF1", представлена в виде стандартной последовательности ХР_016861874.1 (SEQ ID NO: 13) банка данных NCBI. Типичная последовательность человеческой мРНК гена "TM4SF1" представлена в виде стандартной последовательности ХМ_017006385.2 (SEQ ID NO: 14) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 235 до остатка 954 последовательности SEQ ID NO: 14.
"DUSP1" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген фосфатазы с двойной специфичностью-1 (ID гена: 1843). Типичная аминокислотная последовательность человека, кодируемая геном "DUSP1", представлена в виде стандартной последовательности NP_004408.1 (SEQ ID NO: 15) банка данных NCBI. Типичная последовательность человеческой мРНК гена "DUSP1" представлена в виде стандартной последовательности NM_004417.4 (SEQ ID NO: 16) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 244 до остатка 1347 последовательности SEQ ID NO: 16.
"ADM" в контексте настоящего документа имеет свое общеупотребительное значение, принятое в данной области техники, и означает ген адреномедуллина (ID гена: 133). Типичная аминокислотная последовательность человека, кодируемая геном "ADM", представлена в виде стандартной последовательности NP_001115.1 (SEQ ID NO: 17) банка данных NCBI. Типичная последовательность человеческой мРНК гена "ADM" представлена в виде стандартной последовательности NM_001124.3 (SEQ ID NO: 18) банка данных NCBI, при этом кодирующая последовательность (CDS) находится в пределах от остатка 179 до остатка 736 последовательности SEQ IDNO: 18.
Подробное описание изобретения
Настоящее изобретение относится к сигнатуре инсульта, где указанная сигнатура содержит биомаркеры, уровни экспрессии которых специфичны для инсульта или указывают на инсульт. Такие биомаркеры далее будут именоваться "биомаркером инсульта".
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта. В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для ишемического инсульта, микроинсульта (также известного как транзиторная ишемическая атака (ТИА)) и/или геморрагического инсульта (в частности, геморрагического инсульта, вызванного внутримозговым кровоизлиянием). В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для ишемического инсульта. В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для транзиторной ишемической атаки. В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для геморрагического инсульта (в частности, геморрагического инсульта, вызванного внутримозговым кровоизлиянием).
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, один биомаркер инсульта. В одном варианте осуществления, сигнатура по настоящему изобретению содержит или включает, по меньшей мере, два биомаркера инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, три биомаркера инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, четыре биомаркера инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, пять биомаркеров инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, шесть биомаркеров инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, семь биомаркеров инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, восемь биомаркеров инсульта. В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, девять биомаркеров инсульта.
В одном варианте осуществления биомаркеры инсульта выбирают из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления биомаркеры инсульта выбирают из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления биомаркеры инсульта выбирают из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления, сигнатура по настоящему изобретению содержит или включает, по меньшей мере, один биомаркер инсульта, выбранный из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, один биомаркер инсульта, выбранный из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, один биомаркер инсульта, выбранный из группы, включающей или состоящей из; PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления биомаркеры инсульта выбирают из содержит или включает, по меньшей мере, два биомаркера инсульта, выбранные из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, два биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, два биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, два биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, при условии, что упомянутые выше, как минимум, два биомаркера, не состоят из DUSP1 and ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, три биомаркера инсульта, выбранные из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, три биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, три биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, четыре биомаркера инсульта, выбранные из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1 ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1. EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, четыре биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, четыре биомаркера инсульта, выбранные из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, пять биомаркеров инсульта, выбранные из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, пять биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, пять биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, шесть биомаркеров инсульта, выбранных из группы, включающей или состоящей из: HSPA1B, NFAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, шесть биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, шесть биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, семь биомаркеров инсульта, выбранных из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAGS, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, семь биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, семь биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, восемь биомаркеров инсульта, выбранные из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGSJ, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, восемь биомаркеров инсульта, выбранных из группы, включающей или состоящей из: PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, девять биомаркеров инсульта, выбранных из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2.
В одном варианте осуществления сигнатура по настоящему изобретению содержит или включает, по меньшей мере, девять биомаркеров инсульта, выбранные из группы, включающей или состоящей из: PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
Таким образом, настоящее изобретение также относится к сигнатуре инсульта, содержащей или включающей один или несколько биомаркеров, уровни экспрессии которого/которых различны у индивида, пораженного инсультом, и у по существу здорового индивида.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, одного биомаркера инсульта, выбранного из группы, включающей или состоящей из PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, одного биомаркера инсульта, выбранного из группы, включающей или состоящей из PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3 and TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, двух биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой; предпочтительно при условии, что упомянутые выше, как минимум, два биомаркера, не состоят из DUSP1 and ADM.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, двух биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 and TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, четырех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, четырех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, пяти биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, пяти биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, шести биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, шести биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, семи биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, семи биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPAJB, G0S2, BAG3 и TM4SF1, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, восьми биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления сигнатура по настоящему изобретению является специфической или показательной для инсульта, если уровень экспрессии, по меньшей мере, девяти биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, является повышенным по сравнению с эталонной сигнатурой.
В одном варианте осуществления уровень экспрессии биомаркеров инсульта по настоящему изобретению в образце, полученном от индивида, предпочтительно, образце физиологической жидкости, более предпочтительно, образце крови, может быть определен с использованием стандартных протоколов, известных в данной области техники.
В одном варианте осуществления уровень экспрессии биомаркеров инсульта по настоящему изобретению соответствует их уровням транскрипции (т.е. экспрессии мРНК) или их уровням трансляции (т.е. экспрессии белка).
В одном варианте осуществления уровень экспрессии биомаркеров инсульта в образце, предпочтительно в образце физиологической жидкости, наиболее предпочтительно, в образце крови, взятом у индивида, оценивают по уровню белка, то есть по уровню трансляции. В этом варианте осуществления сигнатуру по настоящему изобретению можно назвать протеомной сигнатурой.
Методы определения уровня белка в образце хорошо известны в данной области техники. Примеры таких методов включают, помимо прочих, иммуногистохимию, мультиплексные методы (Luminex), вестерн-блоттинг, твердофазный иммуноферментный анализ (ELISA), сэндвич-вариант ELISA, иммуноферментный анализ с флуоресцентным усилением (FLISA), иммуноферментный анализ (ИФА), радиоиммунологический анализ (РИА), масс-спектрометрию (МС), микроматричный анализ, и т.д., или любую их комбинацию.
Масс-спектрометрия (МС) может быть использована для разделения различных форм белка, потому что различные формы обычно имеют различные массы, которые могут быть разделены с помощью масс-спектрометрии. Соответственно, если одна форма полипептида или белка является лучшим биомаркером в отношении какого-либо заболевания, чем другая форма такого биомаркера, масс-спектрометрия может быть использована для целенаправленного обнаружения и количественной оценки полезной формы. МС может включать в себя времяпролетную (TOF) масс-спектрометрию (например, МС с использованием матрично-активированной лазерной десорбции/ионизации (MALDI)-TOF), MC с использованием лазерной десорбции/ионизации, усиленной поверхностью (MELDI), MC с ионизацией электрораспылением, или MC ионного циклотронного резонанса с Фурье-преобразованием (FTICRR).
Иммуноанализ обычно включает контакт образца с партнером по связыванию, способным избирательно взаимодействовать с конкретным биомаркером в образце. В некоторых вариантах осуществления партнерами по связыванию являются антитела, такие как, например, моноклональные антитела или даже аптамеры. Например, связывание может быть обнаружено при помощи конкурентного иммуноаналнза, системы неконкурентного анализа, использующей такие методы, как вестерн-блот, радиоиммунологнческого анализа, ELISA, "сэндвич"-варианта ИФА, анализа иммунопреципитации, реакции преципитации, реакции диффузной преципитации в геле, иммунодиффузионного анализа, реакции агглютинации, анализа фиксации комплемента, иммунорадиометрического анализа, флуоресцентного иммуноанализа, иммуноанализа белка А, иммуногистохимического анализа, конкурентного или сэндвич-ИФА, вестерн-блоттинга, иммуногистологического анализа, иммуноцитохимического анализа, дот-блоттинга, флуоресцентного поляризационного анализа, анализа сцинтилляционного анализа сближения, гомогенного флуоресцентного анализа с временным разрешением, анализа с использованием систем LAsys и BIAcore. Вышеупомянутые анализы обычно включают связывание партнера (т.е. антитела или аптамера) с твердым носителем. Твердые носители, которые могут использоваться в практике осуществления настоящего изобретения, включают такие субстраты, как нитроцеллюлоза (например, в виде мембраны или лунки микротитрационного планшета), поливинилхлорид (например, пластины или лунки микротитрационного планшета), полистирольный латекс (например, гранулы или микротитрационные планшеты), поливинилиденфторид, диазотированная бумага, найлоновые мембраны, активированные гранулы, магниточувствительные гранулы, и т.п.
Мультиплексный анализ может включать в себя технологию фагового дисплея, профилирование антител или анализ с использованием платформы Luminex. Микроматрица для анализа профиля полипептидов может включать в себя аналитические микроматрицы, микроматрицы функциональных белков или обращено-фазовые белковые микроматрицы. В некоторых случаях профиль полипептидов или белков может быть определен протеомным сканированием (например, полным протеомным сканированием) с использованием протеомного микрочипа.
В одном варианте осуществления, уровень экспрессии биомаркеров инсульта оценивают по уровню нуклеиновой кислоты (т.е. РНК), т.е. по уровню транскрипции, в образце, предпочтительно в образце физиологической жидкости, более предпочтительно, в образце крови, взятом у индивида. В этом варианте осуществления сигнатуру, согласно настоящему изобретению, можно назвать транскриптомной сигнатурой.
Способы оценки уровня транскрипции биомаркера хорошо известны в данной области техники. Примеры таких способов включают, в числе прочих, полимеразную цепную реакцию (ПЦР), ОТ-ПЦР, количественную ПЦР с обратной транскрипцией, нозерн-блот, методы гибридизации, например, использование микроматриц, и их комбинацию, включая, в числе прочих, гибридизацию ампликонов, полученных с помощью ОТ-ПЦР, секвенирование, например, секвенирование ДНК нового поколения (NGS) или РНК-секвенирование (также известное как «секвенирование полного транскриптома методом дробовика»), и т.п., или любую их комбинацию.
Общепринятые методы обычно включают полимеразную цепную реакцию (ПЦР). Например, патенты США US 4,683,202, US 4,683,195, US 4,800,159 и US 4,965,188 описывают общепринятые способы ПЦР. В методе ПЦР обычно используют два олигонуклеотидных праймера, которые связываются с выбранной последовательностью нуклеиновой кислоты-мишени. Праймеры, используемые в настоящем изобретении, включают олигонуклеотиды, способные действовать в качестве точки инициации синтеза нуклеиновой кислоты в пределах данной последовательности нуклеиновой кислоты-мишени. Праймер может быть очищен от фрагментов рестрикции стандартными методами или может быть получен синтетически. ПЦР включает использование термостабильной полимеразы. Термин "термостабильная полимераза" означает полимеразный фермент, который является термостойким, т.е. данный фермент катализирует образование продуктов удлинения праймера, комплементарных матрице, и не подвергается необратимой денатурации при воздействии повышенных температур в течение времени, необходимого для того, чтобы вызвать денатурацию двухцепочечных матричных нуклеиновых кислот. Термостабильные полимеразы были выделены из Thermusfiavus, Т. ruber, Т. thermophilus, Т. aquaticus, Т. lacteus, Т. rubens, Bacillus stearothermophilus и Methanothermus fervidus. Тем не менее, полимеразы, которые не являются термостабильными, также могут быть использованы в ПЦР-анализе при условии восполнения потерь фермента. Обычно в качестве такой полимеразы используется полимераза Taq (т.е. полимераза Thermus aquaticus).
Количественную ПЦР (кПЦР) обычно проводят в термоциклере, способном освещать каждый образец пучком света с заданной длиной волны и регистрировать флуоресценцию, испускаемую возбужденным флуорофором. Термоциклер также способен быстро нагревать и охлаждать образцы, тем самым используя преимущества физико-химических свойств нуклеиновых кислот и термополимеразы. Для обнаружения и измерения в образце количества ампликона (т.е. амплифицированной последовательности нуклеиновой кислоты-мишени) необходимо генерировать измеримый сигнал, который пропорционален количеству амплифицированного продукта. Все современные системы обнаружения используют флуоресцентные технологии. Некоторые из них являются неспецифическими и, следовательно, позволяют единовременно обнаруживать только одну цель.
В противоположность этому, специфические химические методы детекции могут различать неспецифическую амплификацию и целевую амплификацию. Эти специфические методы могут быть использованы для того, чтобы сделать анализ мультиплексным, т.е. способным обнаруживать нескольких различных мишеней в рамках одного и того же исследования. Данной цели могут служить, например, зонды SYBR® Green I, зонды для анализа кривых плавления с высоким разрешением, зонды TaqMan®, зонды LNA® и зонды для анализа методом молекулярных пучков. Зонды TaqMan® являются наиболее широко используемым типом зондов. Они были разработаны компаниями Roche (Базель, Швейцария) и ABI (Фостер-Сити, США) на основе анализа, в котором первоначально использовался радиомеченный зонд (Holland и др., 1991. Proc Nati Acad Sci USA. 88 (16): 7276-80), состоявший из одноцепочечной последовательности зонда, комплементарной одной из цепей ампликона. Флуорофор присоединен к 5'-концу зонда, а тушитель - к 3'-концу. Аппарат возбуждает флуорофор, который передает свою энергию на тушитель посредством резонансного переноса энергии флуоресценции (FRET). Традиционно FRET-пара конъюгирована с FAM в качестве флуорофора и TAMRA в качестве тушителя. В хорошо сконструированном зонде FAM не флуоресцирует, поскольку он передает свою энергию на TAMRA. Поскольку флуоресценция TAMRA обнаружима на длине волны, отличающейся от длины волны для FAM, фоновый уровень FAM низок. Зонд связывается с ампликоном на каждой стадии отжига в ходе ПЦР. Полимераза Taq протягивается от праймера, который связан с ампликоном, и замещает 5'-конец зонда, который затем разрушается 5'-3'-экзонуклеазой полимеразы Taq. Расщепление продолжается до тех пор, пока оставшийся зонд не расплавит ампликон. Этот процесс высвобождает флуорофор и тушитель в раствор, пространственно разделяя их (по сравнению с тем периодом, когда они удерживались вместе зондом). Это приводит к необратимому увеличению флуоресценции FAM и снижению флуоресценции TAMRA.
В некоторых вариантах осуществления уровень экспрессии биомаркеров инсульта по уровню нуклеиновых кислот (то есть, РНК) определяется методом секвенирования РНК. Используемый термин "секвенирование РНК'" или "секвенирование транскриптома" означает секвенирование РНК (или кДНК) вместо ДНК, где основная цель обычно состоит в измерении уровней экспрессии, обнаружении слитых транскриптов, альтернативного сплайсинга и других геномных изменений, которые лучше оценивать по РНК. Секвенирование РНК обычно включает секвенирование всего транскриптома. Используемый в настоящем документе термин "секвенирование всего транскриптома" означает использование высокопроизводительных технологий секвенирования для секвенирования всего транскриптома с целью получения информации о составе РНК в образце. Секвенирование всего транскриптома может быть выполнено с помощью различных платформ, например, анализатора генома (Illumina, Inc., Сан-Диего, Калифорния) и системы секвенирования SOLiD™ (Life Technologies, Карлсбад, Калифорния). В принципе, может быть использована любая платформа, пригодная для секвенирования всего транскриптома. Обычно РНК экстрагируют, и рибосомальную РНК можно удалить, как описано в патенте США US 9,005,891. С использованием имеющихся в продаже наборов, например, ScriptSeq™ M mRNA-Seq Library Preparation Kit (Epicenter Biotechnologies, Мадисон, Висконсин), могут быть подготовлены направленные одиночные и парно-концевые библиотеки кДНК для секвенирования. Библиотеки также могут быть баркодированы для мультиплексного секвенирования с использованием имеющихся в продаже праймеров для баркодирования, таких как RNA-Seq Barcode Primers компании Epicenter Biotechnologies (Мадисон, Висконсин). Затем проводят ПЦР для генерации второй цепи кДНК с целью включения баркодов и амплификации библиотек. После количественной характеризации библиотек можно секвенировать библиотеки для секвенирования. Технологии секвенирования нуклеиновых кислот являются подходящими способами для анализа экспрессии. Принцип, лежащий в основе этих методов, заключается в том, что количество раз, когда последовательность ДНК обнаруживается в образце, напрямую связано с относительными уровнями РНК, соответствующими этой последовательности. Эти способы иногда определяют термином "цифровая генная экспрессия" или DGE, чтобы отразить дискретное числовое свойство полученных данных. Одними из первых методов, применяющих этот принцип, были серийный анализ экспрессии генов (SAGE) и массивно-параллельное опознавательное секвенирование (MPSS). См., например, Brenner и др. (2000. Nat Biotechnol. 18(6):630-634). Обычно для секвенирования РНК используется секвенирование нового поколения (или NGS). Используемый в настоящем документе термин "секвенирование нового поколения" или "NGS" означает относительно новую методику секвенирования по сравнению с традиционной методикой секвенирования по Сенгеру. Обзор см. в Shendure и др. (2008. Nat Biotechol. 26(10):1135-45), включенный в настоящее изобретение посредством ссылки. Для целей настоящего изобретения NGS может включать, помимо прочего, параллельное циклическое секвенирование, секвенирование на основе микроэлектрофореза, секвенирование путем гибридизации. В типичном примере секвенирования нового поколения с использованием методов параллельного циклического секвенирования, сначала готовят геномную библиотеку или библиотеку кДНК, а затем может производиться лигирование распространенных адаптеров к фрагментированной геномной ДНК или кДНК. Для формирования прыгающих библиотек тегов спаренных концевых фрагментов с управляемым распределением расстояний могут использоваться различные протоколы. При помощи ПЦР создается матрица из миллионов пространственно иммобилизованных колоний или "полоний", при этом каждая полония состоит из множества копий одного фрагмента библиотеки, полученной методом дробовика. Поскольку полонии привязаны к планарной матрице, одного микролитрового объема реагента достаточно для одновременного изменения свойств матрицы, например, для гибридизации праймера или для осуществления реакций ферментативного удлинения. Обнаружение флуоресцентных меток, включенных в каждое удлинение, посредством визуализации, может использоваться для получения данных секвенирования по всем признакам одновременно. Последовательные циклы повтора ферментативных реакций и визуализации также могут быть использованы для создания непрерывной последовательности, или рида, для каждого свойства матрицы.
В одном варианте осуществления вывод о том, повышен ли уровень экспрессии определенного биомаркера инсульта в конкретном образце, предпочтительно образце физиологической жидкости, более предпочтительно, образце крови, делается по результатам сравнения с эталонной сигнатурой и/или предварительно установленным эталонным значением.
В одном варианте осуществления эталонная сигнатура содержит или включает предварительно установленные эталонные значения для каждого из искомых биомаркеров инсульта, предпочтительно, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из: HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, НМОХ1, LDLR, DNAJA4, МСЫ, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2, предпочтительно выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, предпочтительно при условии, что вышеупомянутые, по меньшей мере, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM.
Как правило, эталонная сигнатура либо реализована в программном обеспечении, либо получают общую медиану или другое среднее арифметическое значение по результатам измерений.
В одном варианте осуществления эталонная сигнатура получена по результатам предшествующего измерения уровней экспрессии биомаркеров инсульта по настоящему изобретению в эталонном образце, взятом у того же индивида, например, уровней экспрессии биомаркеров инсульта, измеренных за месяц до последующего измерения уровней экспрессии биомаркеров инсульта по изобретению, предпочтительно, за шесть месяцев, более предпочтительно, за один год или более до последующего измерения; или, например, уровней экспрессии биомаркеров инсульта, измеренных перед началом терапии.
В одном варианте осуществления эталонную сигнатуру получают путем измерения уровней экспрессии биомаркеров инсульта по настоящему изобретению у контрольной группы.
В одном варианте осуществления эталонная сигнатура соответствует сигнатуре, полученной в результате популяционных исследований, включая, в числе прочего, подобных индивидов, имеющих одинаковый возрастной диапазон, индивидов, относящихся к той же или сходной этнической группе, имеющих сходную историю онкологических заболеваний, и тому подобное.
В одном варианте осуществления эталонную сигнатуру получают путем измерения уровней экспрессии биомаркеров инсульта по настоящему изобретению в контрольном образце, полученном от одного или более по существу здоровых индивидов. Для целей настоящего документа, "по существу здоровому индивиду" ранее не ставился диагноз «инсульт», и он не был идентифицирован, как перенесший инсульт или страдающий от инсульта.
В одном варианте осуществления контрольная группа включает в себя по существу здоровых индивидов, предпочтительно, по меньшей мере, 50, более предпочтительно, по меньшей мере, 100, более предпочтительно, по меньшей мере, 200 и еще более предпочтительно, по меньшей мере, 500 по существу здоровых индивидов.
При наличии множества образцов, взятых у контрольной группы, можно рассчитать медианный и/или средний уровень экспрессии для каждого биомаркера инсульта, соответственно. Во взаимосвязи с полученными результатами биомаркер инсульта может отслеживаться как дифференциально экспрессируемый. В одном варианте осуществления эталонная сигнатура соответствует средним уровням экспрессии биомаркеров инсульта сигнатуры по настоящему изобретению, полученным в контрольной группе. В одном варианте осуществления эталонная сигнатура соответствует медианным уровням экспрессии биомаркеров инсульта сигнатуры по настоящему изобретению, полученным в контрольной группе.
В одном варианте осуществления эталонную сигнатуру получают с использованием алгоритмов и других методов статистической и структурной классификации. Образцы, полученные в контрольной группе, используют для определения среднего профиля (то есть эталонной сигнатуры), по меньшей мере, для одного биомаркера инсульта, предпочтительно, по меньшей мере, для 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта по настоящему изобретению.
В одном варианте осуществления биомаркер инсульта рассматривается как дифференциально экспрессированный у индивида, которому требуется диагностировать наличие или отсутствие инсульта, и у по существу здорового индивида, если диапазон изменения экспрессии, по меньшей мере, больше чем приблизительно |1,1|, предпочтительно, по меньшей мере, больше чем приблизительно |1,2|, приблизительно |1,3|, приблизительно 1,4|, приблизительно |1,5|, приблизительно |1,6|, приблизительно 1,7|, приблизительно |1,8|, приблизительно |1,9|, приблизительно [2,0|, приблизительно |2,1|, приблизительно |2,2|, приблизительно |2,3|, приблизительно |2,4|, приблизительно |2,5|, приблизительно [3,0|, приблизительно |4,0|, приблизительно |5,0| или более.
В одном варианте осуществления биомаркер инсульта рассматривается как дифференциально экспрессированный у индивида, которому требуется диагностировать наличие или отсутствие инсульта, и у по существу здорового индивида, если диапазон изменения экспрессии, по меньшей мере, больше чем приблизительно 1,1; предпочтительно, по меньшей мере, больше чем приблизительно 1,2; приблизительно 1,3; приблизительно 1,4; приблизительно 1,5; приблизительно 1,6; приблизительно 1,7; приблизительно 1,8; приблизительно 1,9; приблизительно 2,0; приблизительно 2,1; приблизительно 2,2; приблизительно 2,3; приблизительно 2,4; приблизительно 2,5; приблизительно 3,0; приблизительно 4,0; приблизительно 5,0 или более.
В одном варианте осуществления биомаркер инсульта рассматривается как дифференциально экспрессированный у индивида, которому требуется диагностировать наличие или отсутствие инсульта, и у по существу здорового индивида, если log2 диапазона изменения экспрессии, по меньшей мере, больше чем приблизительно |0,1|, предпочтительно, по меньшей мере, больше чем приблизительно |0,2|, приблизительно |0,3|, приблизительно |0,4|, приблизительно |0,5|, приблизительно |0,6|, приблизительно |0,7|, приблизительно |0,8|, приблизительно |0,9|, приблизительно |1,0|, приблизительно |1,1|, приблизительно |1,2|, приблизительно |1,3|, приблизительно |1,4|, приблизительно |1,5|, приблизительно |1,6|, приблизительно |1,7|, приблизительно 1,8|, приблизительно |1,9|, приблизительно |2,0|, приблизительно |2,1|, приблизительно |2,2|, приблизительно |2,3| или более.
В одном варианте осуществления биомаркер инсульта рассматривается как дифференциально экспрессированный у индивида, которому требуется диагностировать наличие или отсутствие инсульта, и у по существу здорового индивида, если log2 диапазона изменения экспрессии, по меньшей мере, больше чем приблизительно 0,1, предпочтительно, по меньшей мере, больше чем приблизительно 0,2; приблизительно 0,3; приблизительно 0,4; приблизительно 0,5; приблизительно 0,6; приблизительно 0,7; приблизительно 0,8; приблизительно 0,9; приблизительно 1,0; приблизительно 1,1; приблизительно 1,2; приблизительно 1,3; приблизительно 1,4; приблизительно 1,5; приблизительно 1,6; приблизительно 1,7; приблизительно 1,8; приблизительно 1,9; приблизительно 2,0; приблизительно 2,1; приблизительно 2,2; приблизительно 2,3; или более.
В одном варианте осуществления биомаркер инсульта рассматривается как дифференциально экспрессированный у индивида, которому требуется диагностировать наличие или отсутствие инсульта, и у, по существу, здорового индивида, если уровень экспрессии указанного биомаркера, по меньшей мере, приблизительно в 0,5; приблизительно в 1; приблизительно в 1,5; приблизительно в 2; приблизительно в 2,5; приблизительно в 3; приблизительно в 3,5; приблизительно в 4; приблизительно в 5; приблизительно в 6; приблизительно в 7; приблизительно в 8; приблизительно в 9; приблизительно в 10; приблизительно в 15; приблизительно в 20; приблизительно в 30; приблизительно в 40; приблизительно в 50 или приблизительно в 100 раз выше, чем уровень экспрессии того же самого биомаркера, определенного у по существу здорового индивида, предпочтительно, из контрольной группы.
В одном варианте осуществления, при определении уровня экспрессии более чем одного биомаркера инсульта в образце, предпочтительно образце физиологической жидкости, более предпочтительно, образце крови, полученном от индивида, которому требуется диагностировать наличие или отсутствие инсульта, может вычисляться балл, который представляет собой комплексный показатель указанных уровней экспрессии, и который затем сравнивается с предварительно установленным эталонным значением. В одном варианте осуществления балл, превышающий предварительно установленное эталонное значение, указывает на то, что у индивида развивается или ранее был инсульт.
Как правило, предварительно установленное эталонное значение является пороговым значением или значением отсечения. Как правило, "пороговое значение" или "значение отсечения" определяются экспериментально, эмпирически или теоретически. Пороговое значение также может быть выбрано произвольно, исходя из существующих экспериментальных и/или клинических условий, что понятно специалисту в соответствующей области техники. Например, для установления эталонной величины может быть использована ретроспективная количественная оценка отобранных ранее и надлежащим образом сохраняемых образцов индивида. Пороговое значение должно быть определено для достижения оптимальной чувствительности и специфичности в соответствии с функцией теста и балансом пользы/риска (клинические последствия ложноположительных и ложноотрицательных результатов). Как правило, оптимальная чувствительность и специфичность (и, следовательно, пороговое значение) могут быть определены с помощью кривой рабочих характеристик приемника (ROC-кривой) на основе экспериментальных данных. Например, после определения уровня экспрессии биомаркера по настоящему изобретению в контрольной группе, можно использовать алгоритмический анализ для статистической обработки уровней экспрессии, определенных в тестируемых образцах, и, таким образом, получить стандарт классификации, имеющий значимость для классификации образцов. Полное наименование ROC-кривой это кривая рабочих характеристик приемника, которая также известна как кривая зависимости чувствительности от частоты ложноположительных заключений. Она используется, в основном, в клинических тестах биохимической диагностики. ROC-кривая является комплексным показателем, который отражает непрерывные переменные для доли истинно положительных заключений (чувствительность) и доли ложноположительных заключений (1-специфичность). Она выявляет связь между чувствительностью и специфичностью методом совмещения визуализации. Для расчета ряда значений чувствительности и специфичности устанавливают ряд различных значений отсечения (пороговые или критические значения, граничные значения между нормальными и аномальными результатами диагностического теста) в виде непрерывных переменных. Затем чувствительность используют как вертикальную координату, а специфичность - как горизонтальную координату для построения кривой. Чем выше площадь под кривой (AUC), тем выше точность диагностики. На ROC-кривой точка, ближайшая к дальнему верхнему левому краю диаграммы координат, является критической точкой, имеющей как высокую чувствительность, так и высокие значения специфичности. Значение площади под ROC-кривой (AUC) лежит в диапазоне от 1,0 до 0,5. Когда AUC>0,5, результат диагностики улучшается по мере того, как значение AUC приближается к 1. Когда 0,5<AUC<0,7, точность низкая. При 0,7<AUC<0,9 точность является умеренной. Когда AUC<0,9, точность высокая. Этот алгоритмический метод предпочтительно реализуют с помощью компьютера. Для построения ROC-кривой могут использоваться существующие программы или системы, например: медицинское статистическое программное обеспечение MedCalc 9.2.0.1; SPSS 9,0; ROCKOWER.SAS; DESIGNROC.FOR; MULTIREADER POWER.SAS; CREATE-ROC.SAS; GB STAT VI0.0 (Dynamic Microsystems, Inc., Силвер-Спринг, Мэриленд, США), и др.
Настоящее изобретение, кроме того, относится к методам диагностики инсульта у индивида с использованием сигнатуры инсульта по настоящему изобретению.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению особенно хорошо подходит для диагностики ишемического инсульта, микроинсульта (или транзиторной ишемической атаки - ТИА) и/или геморрагического инсульта (в частности, геморрагического инсульта, вызванного внутримозговым кровоизлиянием).
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению особенно хорошо подходит для того, чтобы отличить инсульт от имитации инсульта, при которой могут наблюдаться некоторые или все симптомы инсульта, за исключением того, что это не инсульт и это не результат ишемического поражения мозга. Не ограничиваясь какой-либо теорией, отметим, что, поскольку повышенный уровень биомаркера является результатом инсульта, индивид, у которого имеет место имитация инсульта, не будет иметь повышенный уровень биомаркера (другими словами, поскольку сигнатура по настоящему изобретению является специфической или показательной для инсульта, индивид, у которого наблюдается имитация инсульта, не будет демонстрировать аналогичную сигнатуру).
К числу распространенных имитаторов инсульта относятся, в числе прочих, мигрень, синкопе, периферические вестибулярные расстройства и BPPV (доброкачественное пароксизмальное позиционное головокружение), судорожные припадки, функциональные проявления/тревожное расстройство, транзиторная глобальная амнезия, паралич Белла, заболевание/дисфункция периферической нервной системы, постуральная гипотония, опухоли, вирусные заболевания, сердечная аритмия, рассеянный склероз, побочные эффекты препаратов, гипогликемия, болезнь Паркинсона, заболевания сетчатки/глазные патологии, патологии позвоночника, невралгия тройничного нерва, инфекции мочевыводящих путей, делирий, мотонейронные болезни, субарахноидальное кровоизлияние, субдуральная гематома, и т.п. (см. Nadarajan и другие авторы., 2014. Pract Neurol. 14(1):23-31).
Соответственно, метод диагностики инсульта по настоящему изобретению обеспечивает преимущество в виде ранней и точной диагностики инсульта, которое может быть полезным индивиду с подозрением на инсульт, по меньшей мере, в следующих аспектах:
(1) может снизить частоту ложных диагнозов инсульта, и/или
(2) может ограничить масштаб поражения тканей путем назначения раннего и эффективного лечения у индивида, нуждающегося в медицинской помощи.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадию взятия образца у индивида, которому требуется диагностировать наличие или отсутствие инсульта.
Термин "образец", используемый в настоящем документе, в общем случае относится к любому образцу, который может быть протестирован с целью определения уровней экспрессии биомаркера, предпочтительно, маркеров инсульта по настоящему изобретению.
В одном варианте осуществления образец представляет собой образец физиологической жидкости. Примеры физиологических жидкостей включают, в числе прочих, кровь, плазму, сыворотку, лимфу, асцитическую жидкость, кистозная жидкость, мочу, желчь, слизь, серозную жидкость, секрет сальных желез, экссудат из сосков, синовиальную жидкость, жидкость бронхоальвеолярного лаважа, мокроту, амниотическую жидкость, перитонеальную жидкость, спинномозговую жидкость, плевральную жидкость, перикардиальную жидкость, слюну, сперму, слезную жидкость, выделения слизистых оболочек, пот, и альвеолярные макрофаги.
В одном варианте осуществления образец является образцом крови. Термин "образец крови", используемый в настоящем документе, включает образцы цельной крови, образцы сыворотки и образцы плазмы.
В одном варианте осуществления образец представляет собой образец цельной крови, плазмы или сыворотки.
В одном варианте осуществления образец не является образцом ткани организма. Примеры тканей организма включают, помимо прочих, головной мозг, мышцы, нервы, сердце, легкое, печень, поджелудочную железу, селезенку, вилочковую железу, пищевод, желудок, кишечник, почку, предстательную железу, яичко, яичник, волосы, кожу, кость, молочную железу, матку, мочевой пузырь и спинной мозг.
В одном варианте осуществления образец не является образцом ткани головного мозга. Следовательно, в соответствии с этим вариантом осуществления методы по настоящему изобретению не включают стадию получения образца ткани мозга индивида.
В одном варианте осуществления образец не является образцом, полученным в результате биопсии. В одном варианте осуществления образец не является образцом, полученным в результате биопсии мозга.
В одном варианте осуществления образец, предпочтительно, образец физиологической жидкости, более предпочтительно, образец крови, был взят у индивида ранее, то есть, метод диагностики инсульта по настоящему изобретению не включает стадию активного взятия образца у индивида. Следовательно, согласно этому варианту осуществления, метод по настоящему изобретению является неинвазивным методом, то есть, методом in vitro.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадию определения сигнатуры согласно настоящему изобретению в упомянутом выше образце, предпочтительно, образце физиологической жидкости, более предпочтительно, образце крови индивида.
Средства и методы определения сигнатуры согласно настоящему изобретению подробно описаны выше в настоящем документе.
В одном варианте осуществления стадия определения сигнатуры включает подстадию количественного определения уровня экспрессии, по меньшей мере, одного биомаркера инсульта, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта по настоящему изобретению.
В одном варианте осуществления уровень экспрессии, по крайней мере, одного биомаркера инсульта, предпочтительно, по крайней мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта, измеряется с использованием микроматрицы ДНК, чтобы уровни экспрессии каждого из биомаркеров инсульта сигнатуры по настоящему изобретению определялись одновременно.
В одном варианте осуществления уровень экспрессии, по меньшей мере, одного биомаркера инсульта, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта, измеряют с использованием методов секвенирования РНК.
В одном варианте осуществления уровень экспрессии, по меньшей мере, одного биомаркера инсульта, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта, измеряют с использованием кодового набора CodeSet. Специальные наборы кодов для конкретной панели маркеров (например, для рассматриваемых в настоящем изобретении биомаркеров инсульта) могут разрабатываться на коммерческой основе. Они включают, без ограничений, nCounter ® Custom CodeSets (NanoString) (Malkov и другие., 2009. ВМС Res Notes. 2:80; Kulkarni, 2011. Curr Protoc Mol Biol. Chapter 25:Unit 25B.10).
В одном варианте осуществления при определении уровня экспрессии для более чем одного биомаркера инсульта в упомянутом ранее образце, предпочтительно, в образце физиологической жидкости, более предпочтительно, в образце крови, взятом у индивида, которому требуется диагностировать наличие или отсутствие инсульта, вычисляют суммарный показатель указанных уровней экспрессии.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадию сравнения сигнатур, полученных при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, с эталонной сигнатурой, как описано выше.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадию сравнения сигнатур, полученных при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, с предварительно установленной эталонной величиной, как описано выше.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадию сравнения уровней экспрессии биомаркеров инсульта в сигнатуре, полученной при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно образца крови индивида, с уровнями экспрессии биомаркеров инсульта в эталонной сигнатуре, как описано выше.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадию диагностики инсульта у индивида на основе корреляции сигнатуры, полученной при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови упомянутого индивида по сравнению с эталонной сигнатурой.
В одном варианте осуществления пациенту диагностируется инсульт, когда сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, как определено выше.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если диапазон изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по меньшей мере, больше, чем приблизительно |1,1|, предпочтительно, по меньшей мере, больше чем приблизительно |1,2|, приблизительно |1,3|, приблизительно |1,4|, приблизительно |1,5|, приблизительно |1,6|, приблизительно |1,7|, приблизительно |1,8|, приблизительно |1,9|, приблизительно |2,0|, приблизительно |2,1|, приблизительно |2,2|, приблизительно |2,3|, приблизительно |2,4|, приблизительно |2,5|, приблизительно |3,0|, приблизительно |4,0|, приблизительно |5,0|, или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если диапазон изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по меньшей мере, больше, чем приблизительно 1,1; предпочтительно, по меньшей мере, больше чем приблизительно 1,2; приблизительно 1,3; приблизительно 1,4; приблизительно 1,5; приблизительно 1,6; приблизительно 1,7; приблизительно 1,8; приблизительно 1,9; приблизительно 2,0; приблизительно 2,1; приблизительно 2,2; приблизительно 2,3; приблизительно 2,4; приблизительно 2,5; приблизительно 3,0; приблизительно 4,0; приблизительно 5,0 или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если log2 диапазона изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по меньшей мере, больше, чем приблизительно |0,5|, предпочтительно, по меньшей мере, больше чем приблизительно |0,1|, приблизительно |0,2|, приблизительно |0,3|, приблизительно |0,4|, приблизительно |0,5|, приблизительно |0,6|, приблизительно |0,7|, приблизительно |0,8|, приблизительно |0,9|, приблизительно |1,0|, приблизительно |1,1|, приблизительно |1,2|, приблизительно |1,3|, приблизительно |1,4|, приблизительно |1,5|, приблизительно |1,6|, приблизительно |1,7|, приблизительно |1,8|, приблизительно |1,9|, приблизительно |2,0|, приблизительно |2,1|, приблизительно |2,2|, приблизительно |2,3| или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если log2 диапазона изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по меньшей мере, больше, чем приблизительно 0,5; предпочтительно, по меньшей мере, больше чем приблизительно 0,1; приблизительно 0,2; приблизительно 0,3; приблизительно 0,4; приблизительно 0,5; приблизительно 0,6; приблизительно 0,7; приблизительно 0,8; приблизительно 0,9; приблизительно 1,0; приблизительно 1,1; приблизительно 1,2; приблизительно 1,3; приблизительно 1,4; приблизительно 1,5; приблизительно 1,6; приблизительно 1,7; приблизительно 1,8; приблизительно 1,9; приблизительно 2,0; приблизительно 2,1; приблизительно 2,2; приблизительно 2,3 или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если уровень экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по меньшей мере, приблизительно в 0,5; приблизительно в 1; приблизительно в 1,5; приблизительно в 2; приблизительно в 2,5; приблизительно в 3; приблизительно в 3,5; приблизительно в 4; приблизительно в 5; приблизительно в 6; приблизительно в 7; приблизительно в 8; приблизительно в 9; приблизительно в 10; приблизительно в 15; приблизительно в 20; примерно в 30; приблизительно в 40; приблизительно в 50 или приблизительно в 100 раз выше уровня экспрессии того же самого биомаркера, определенного у по существу здорового индивида, предпочтительно, из контрольной группы.
В одном варианте осуществления, у индивида диагностируют инсульт, если уровень экспрессии, по меньшей мере, одного, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта по настоящему изобретению выше, чем уровень экспрессии того же биомаркера инсульта у по существу здорового индивида, предпочтительно, из контрольной группы.
В одном варианте осуществления у индивида диагностируется инсульт, если суммарный показатель, рассчитанный для уровней экспрессии более одного биомаркера инсульта, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, или 9 биомаркеров инсульта по настоящему изобретению, выше, чем предварительно установленное эталонное значение, то есть, суммарный показатель, рассчитанный для уровней экспрессии тех же биомаркеров у по существу здорового индивида, предпочтительно, из контрольной группы.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, которому требуется диагностировать наличие или отсутствие инсульта;
ii) определение сигнатуры по настоящему изобретению в указанном образце;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) диагностирование индивида как имеющего инсульт на основе корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод диагностики инсульта по по настоящему изобретению включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, которому требуется диагностировать наличие или отсутствие инсульта;
ii) определение сигнатуры в указанном образце, предпочтительно, путем измерения уровней экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2, предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) диагностирование индивида как имеющего инсульт на основе корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, которому требуется диагностировать наличие или отсутствие инсульта;
ii) определение сигнатуры в указанном образце, предпочтительно, путем измерения уровней экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM.
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой, и
iv) диагностирование индивида как имеющего инсульт на основе корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, которому требуется диагностировать наличие или отсутствие инсульта;
ii) определение сигнатуры в указанном образце, предпочтительно, путем измерения уровней экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой, и
iv) диагностирование индивида как имеющего инсульт на основе корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод диагностики инсульта по данному изобретению включает следующие шаги:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, которому требуется диагностировать наличие или отсутствие инсульта;
ii) определение сигнатуры в указанном образце, предпочтительно, путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) диагностирование индивида как имеющего инсульт на основе корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод диагностики инсульта по данному изобретению включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, которому требуется диагностировать наличие или отсутствие инсульта;
ii) определение сигнатуры в упомянутом образце, предпочтительно путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) диагностирование индивида как имеющего инсульт на основе корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению включает стадии i) определения уровня экспрессии, по меньшей мере, одного биомаркера, выбранного из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM в образце, предпочтительно, образце физиологической жидкости, более предпочтительно, образце крови, полученном от индивида ii) сравнения уровня, определенного на стадии i), с предварительно установленным эталонным значением, и iii) постановки диагноза «инсульт», когда уровень экспрессии, определенный на стадии i) выше предварительно установленного эталонного значения.
В одном варианте осуществления эталонную сигнатуру определяют или получают с использованием данных контрольной группы, предпочтительно, контрольной группы, включающей, по меньшей мере, одного, по существу, здорового индивида.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению применяется к индивиду, у которого наблюдаются симптомы инсульта, но который не проходил рутинное обследование с целью исключения всех возможных причин инсульта.
В одном варианте осуществления метод диагностики инсульта согласно настоящему изобретению может быть частью рутинного набора тестов, выполняемых в отношении индивида, который демонстрирует симптомы инсульта, включая, в числе прочего, потерю зрения на один глаз, слабость в одной руке или ноге, слабость в одной стороне тела, дурноту, головокружение, двоение в глазах, слабость в обеих сторонах тела, затрудненность речи, невнятную речь или потерю координации.
В одном варианте осуществления метод диагностики инсульта по настоящему изобретению может быть осуществлен в качестве дополнения к другим диагностическим инструментам, которые включают, в частности, компьютерную томографию (КТ) и магнитно-резонансную томографию (МРТ).
Настоящее изобретение, кроме того, относится к методу определения наличия у индивида, страдающего от инсульта, ответной реакции на проводимую терапию. Настоящее изобретение относится также к методу определения наличия у индивида, страдающего от инсульта, ответной реакции во время или после завершения терапии.
В одном варианте осуществления метод определения наличия у индивида, страдающего от инсульта, ответной реакции на терапию включает стадии i) определения уровня экспрессии, по меньшей мере, одного биомаркера по настоящему изобретению, выбранного из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, ii) сравнения уровня экспрессии, определенного на стадии i), с предварительно установленным эталонным значением, и iii) вынесения заключения о наличии у индивида ответной реакции, если уровень, определенный на стадии i), ниже предварительно установленного эталонного значения.
В одном варианте осуществления метод определения наличия у индивида, страдающего от инсульта, ответной реакции на терапию включает стадии взятия у индивида образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови; определения в указанном образце сигнатуры по настоящему изобретению, и сравнения упомянутой сигнатуры с эталонной сигнатурой. Эти стадии были подробно описаны выше в контексте метода диагностики инсульта и должны применяться к настоящему методу соответствующим образом.
В одном варианте осуществления метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры по настоящему изобретению;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о наличии у индивида ответной реакции на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровня экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о наличии у индивида ответной реакции на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровня экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о наличии у индивида ответной реакции на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение сигнатуры в упомянутом образце, предпочтительно, путем измерения уровня экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о наличии у индивида ответной реакции на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение сигнатуры в упомянутом образце, предпочтительно, путем измерения уровня экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о наличии у индивида ответной реакции на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение сигнатуры в упомянутом образце, предпочтительно, путем измерения уровня экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о наличии у индивида ответной реакции на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления эталонную сигнатуру определяют или получают по результатам предшествующего измерения уровней экспрессии биомаркеров инсульта по настоящему изобретению в эталонном образце, взятом у того же индивида, например, уровней экспрессии биомаркеров инсульта, измеренных до начала терапии.
В одном варианте осуществления делается вывод о наличии у индивида ответной реакции, если сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, как описано выше.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если диапазон изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по крайней мере, меньше, чем приблизительно |1,1|, предпочтительно, по крайней мере, меньше, чем приблизительно |1,2|, приблизительно |1,3|, приблизительно |1,4|, приблизительно |1,5|, приблизительно |1,6|, приблизительно |1,7|, приблизительно |1,8|, приблизительно |1,9|, приблизительно |2,0|, приблизительно |2,1|, приблизительно |2,2|, приблизительно |2,3|, приблизительно |2,4|, приблизительно |2,5|, приблизительно |3,0|, приблизительно |4,0|, приблизительно |5,0| или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если диапазон изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по крайней мере, меньше, чем приблизительно 1,1, предпочтительно, по крайней мере, меньше, чем приблизительно 1,2; приблизительно 1,3; приблизительно 1,4; приблизительно 1,5; приблизительно 1,6; приблизительно 1,7; приблизительно 1,8; приблизительно 1,9; приблизительно 2,0; приблизительно 2,1; приблизительно 2,2; приблизительно 2,3; приблизительно 2,4; приблизительно 2,5; приблизительно 3,0; приблизительно 4,0; приблизительно 5,0 или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если log2 диапазона изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по крайней мере, меньше, чем приблизительно |0,1|, предпочтительно, по крайней мере, меньше, чем приблизительно |0,2|, приблизительно |0,3|, приблизительно |0,4|, приблизительно |0,5|, приблизительно |0,6|, приблизительно |0,7|, приблизительно |0,8|, приблизительно |0,9|, приблизительно |1,0|, приблизительно |1,1|, приблизительно |1,2|, приблизительно |1,3|, приблизительно |1,4|, приблизительно |1,5|, приблизительно |1,6|, приблизительно |1,7|, приблизительно |1,8|, приблизительно |1,9|, приблизительно |2,0|, приблизительно |2,1|, приблизительно |2,2|, приблизительно |2,3| или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если log2 диапазона изменения экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по крайней мере, меньше, чем приблизительно 0,1; предпочтительно, по крайней мере, меньше, чем приблизительно 0,2; приблизительно 0,3; приблизительно 0,4; приблизительно 0,5; приблизительно 0,6; приблизительно 0,7; приблизительно 0,8; приблизительно 0,9; приблизительно 1,0; приблизительно 1,1; приблизительно 1,2; приблизительно 1,3; приблизительно 1,4; приблизительно 1,5; приблизительно 1,6; приблизительно 1,7; приблизительно 1,8; приблизительно 1,9; приблизительно 2,0; приблизительно 2,1; приблизительно 2,2; приблизительно 2,3 или более.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если уровень экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта согласно определению, приведенному в настоящем документе, по крайней мере, приблизительно в 0,5; приблизительно в 1; приблизительно в 1,5; приблизительно в 2; приблизительно в 2,5; приблизительно в 3; приблизительно в 3,5; приблизительно в 4; приблизительно в 5; приблизительно в 6; приблизительно в 7; приблизительно в 8; приблизительно в 9; приблизительно в 10; приблизительно в 15; приблизительно в 20; примерно в 30; приблизительно в 40; приблизительно в 50 или приблизительно в 100 раз ниже уровня экспрессии того же самого биомаркера, определенного у по существу здорового индивида, предпочтительно из контрольной группы.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если уровень экспрессии, по меньшей мере, 1, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8 или 9 биомаркеров инсульта по настоящему изобретению не выше уровня экспрессии того же биомаркера инсульта у по существу здорового субъекта, предпочтительно, из контрольной группы.
В одном варианте осуществления сигнатура, полученная при анализе образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, считается отличной от эталонной сигнатуры, если суммарный показатель, рассчитанный для уровней экспрессии более чем одного биомаркера инсульта, предпочтительно, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, или 9 биомаркеров инсульта по настоящему изобретению, не выше, чем предварительно установленное эталонное значение, то есть, суммарный показатель, рассчитанный для уровней экспрессии тех же биомаркеров у по существу здорового индивида, предпочтительно, из контрольной группы.
Таким образом, метод определения наличия у пациента, страдающего от инсульта, ответной реакции на терапию, в частности, подходит для дифференциации "респондентов" и "не респондентов".
В контексте настоящего документа термин "респондент" означает индивида или пациента, у которого будет наблюдаться терапевтический ответ, то есть, индивида, у которого наблюдается снижение, ослабление или излечение проявлений инсульта. Согласно настоящему изобретению, у респондентов наблюдается объективный ответ и, следовательно, данный термин не включает индивидов или пациентов, у которых инсульт стабилизирован, вследствие чего заболевание не прогрессирует после терапии.
Используемый здесь термин "не респондент" (или трудно поддающийся лечению) включает индивидов или пациентов, у которых не наблюдается снижение или улучшение проявлений инсульта после терапии. Согласно настоящему изобретению, термин "не респондент" включает также индивидов или пациентов со стабилизированным инсультом.
Как правило, характеризация индивида как респондента или не респондента может осуществляться путем соотнесения со стандартом или тренировочной выборкой. Стандартом может служить профиль индивида, который, как известно, является респондентом или не респондентом, или, в качестве альтернативы, стандартом может служить цифровой показатель. Подобные предварительно установленные стандарты могут быть представлены в любой подходящей форме, например, в виде распечатанного перечня или диаграммы, компьютерной программы или иного носителя информации. В некоторых вариантах осуществления предварительно установленной величиной является уровень экспрессии, определенный перед началом терапии. Когда делается вывод о том, что пациент является не респондентом, врач может принять решение о прекращении терапии во избежание любых дальнейших нежелательных побочных реакций.
В одном варианте осуществления, для целей мониторинга уровни экспрессии могут быть измерены в нескольких временных точках, например, дважды, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз или более. Таким образом, мониторинг уровней экспрессии в течение некоторого периода времени после или во время терапии может предоставить индикатор степени успеха лечения, поскольку следует ожидать, что уровни экспрессии будут снижаться быстрее у индивидов с успешным лечением по сравнению с индивидом, не получавшим лечение, у которого уровни экспрессии также могут снижаться, но медленнее.
Обычно терапия заключается в любом методе, хорошо известном специалисту в данной области техники. Варианты лечения включают, в числе прочего, эндоваскулярные процедуры и хирургическое вмешательство, например, тромбэктомию.
В контексте настоящего документа термин "тромбэктомия" означает любое хирургическое и/или механическое удаление или разрушение тромба. В целом, известны три класса устройств для проведения механической тромбэктомии: катетеры со спиралью, аспирационные аппараты и стент-ретриверы. Другие устройства и способы, разрабатываемые в настоящее время, также включены в определение тромбэктомии, используемое в настоящем документе. Обычно катетер направляют к участку блокирования кровотока для удаления тромба. В отношении пациента может применяться комбинация тромбэктомии и тромболизиса. Кроме того, ишемический инсульт можно лечить введением тромболитического агента для растворения тромба ("тромболизис").
Антитромботические средства далее подразделяют на следующие три подтипа: антикоагулянты, антитромбоцитарные препараты и тромболитические препараты.
Примеры антикоагулянтов включают, в числе прочих, кумарины, гепарин, варфарин, аценокумарол, фенпрокумон, атроментин, фениндион, фондапаринукс, идрапаринукс, прямых ингибиторов фактора Ха, прямых ингибиторов тромбина, антитромбиновые препараты, батроксобин и гементин.
Примеры антитромбоцитарных препаратов включают, в числе прочих, необратимых ингибиторов циклооксигеназы (например, аспирин или трифлузал), ингибиторов аденозиндифосфатных рецепторов (например, клопидогрел, прасугрел, тикагрелор или тиклопидин), ингибиторов фосфодиэстеразы (например, цилостазол), ингибиторов гликопротеина IIB/IIIA (например, абциксимаб, эптифибатид или тирофибан), ингибиторов обратного захвата аденозина (например, дипиридамол) и ингибиторов тромбоксана (например, ингибиторы тромбоксан синтазы или антагонисты тромбоксановых рецепторов).
Примеры тромболитических препаратов включают, в числе прочих, тканевой активатор плазминогена t-PA (альтеплаза и другие (десмотеплаза, ретеплаза, тенектеплаза, …), анистреплазу, стрептокиназу и урокиназу. t-PA может вводиться опционально во время эндоваскулярных процедур.
В одном варианте осуществления терапия заключается во введении нейропротективного средства.
Примеры нейропротективных средств, как правило, включают, без ограничений, средства, блокирующие свободные радикалы, антиглутаматные средства и ингибиторов циклинзависимых киназ.
В некоторых вариантах осуществления нейропротективным средством является ингибитор циклинзависимой киназы (CDK). Известные ингибиторы CDK могут быть классифицированы в соответствии с их способностью ингибировать циклинзависимые киназы, в общем, или согласно их селективности в отношении конкретной CDK. Например, флаворипидол действует как «пан»-антагонист CDK и не проявляет избирательной селективности в отношении какой-либо специфической циклинзависимой киназы (Dai & Grant, 2003. Curr Opin Pharmacol. 3(4):362-70). Ингибиторы CDK, в основе которых лежит пурин, такие, как оломоуцин, росковитин, пурванололы и CGP74514A, как известно, демонстрируют более высокую селективность в отношении циклинзависимых киназ 1, 2 и 5, но не оказывают ингибирующего воздействия на циклинзависимые киназы 4 и 6 (Dai & Grant, 2003. Curr Opin Pharmacol. 3(4):362-70). Кроме того, доказано, что ингибиторы цинклинзависимых киназ, в основе которых лежит пурин, например, S-росковитин, могут вызывать в нервной системе противоапоптозный эффект (О'Hare и др., 2002. Pharmacol Ther. 93(2-3):135-43; Timsit & Menn, 2012. Clin Pharmacol Ther. 91(2):327-32;  и др., 2017. J Cereb Blood Flow Metab. 37(6):2208-2223) или предотвращать гибель нейронов при таких нейродегенеративных заболеваниях, как болезнь Альцгеймера (Filgueira de Azevedo и др., 2002. Biochem Biophys Res Commun. 297(5):1154-8; Knockaert и др., 2002. Trends Pharmacol Sci. 23(9):417-25).
и др., 2017. J Cereb Blood Flow Metab. 37(6):2208-2223) или предотвращать гибель нейронов при таких нейродегенеративных заболеваниях, как болезнь Альцгеймера (Filgueira de Azevedo и др., 2002. Biochem Biophys Res Commun. 297(5):1154-8; Knockaert и др., 2002. Trends Pharmacol Sci. 23(9):417-25).
В некоторых вариантах осуществления терапия заключается в гипотермии (например, Kurisu & Yenari, 2018. Neuropharmacology. 134(Pt B):302-309).
Настоящее изобретение также относится к методу определения наличия риска инсульта для пациента, включающему стадии i) определения уровня экспрессии, по меньшей мере, одного биомаркера, выбранного из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM, в образце, предпочтительно, образце физиологической жидкости, более предпочтительно, образце крови, взятом у индивида ii) сравнения уровня, определенного на стадии i), с предварительно установленным эталонным значением и iii) вынесения заключения о том, что для индивида существует риск развития инсульта, если уровень экспрессии, определенный на стадии i) выше предварительно установленного эталонного значения.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает стадии получения образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида; определения в указанном образце сигнатуры по настоящему изобретению; и сравнения указанной сигнатуры с эталонной сигнатурой. Эти стадии были подробно описаны выше в контексте метода диагностики инсульта и должны применяться к настоящему методу соответствующим образом.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры по настоящему изобретению;
iii) сравнение сигнатуры, полученной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что для индивида существует риск развития инсульта, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида; ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровня экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
ii) сравнение сигнатуры, полученной на стадии ii), с эталонной сигнатурой; и
iii) вынесение заключения о том, что для индивида существует риск развития инсульта, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровня экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что для индивида существует риск развития инсульта, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровня экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что для индивида существует риск развития инсульта, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение сигнатуры в упомянутом образце, предпочтительно, путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что для индивида существует риск развития инсульта, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения наличия риска инсульта для пациента включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение сигнатуры в упомянутом образце, предпочтительно путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что для индивида существует риск развития инсульта, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления эталонную сигнатуру определяют или получают на основании данных контрольной группы, предпочтительно, включающей, по меньшей мере, одного по существу здорового индивида.
В одном варианте осуществления индивид страдает или страдал сердечно-сосудистым заболеванием, или у него диагностировано сердечнососудистое заболевание (например, атеросклероз, гипертония…), которое может привести к инсульту.
В одном варианте осуществления индивид пережил инсульт, и метод по настоящему изобретению подходит, в частности, для прогнозирования вероятности повторного инсульта.
Таким образом, метод определения наличия у индивида риска наступления инсульта подходит, в частности, для прогнозирования и, следовательно, выявления индивидов, находящихся в зоне риска, с последующим осуществлением всех возможных терапевтических вмешательств с целью предотвращения инсульта.
В контексте настоящего документа термин "риск" обозначает вероятность наступления события в течение определенного периода времени, и может означать "абсолютный риск" или "относительный риск" для индивида.
"Абсолютный риск" может быть оценен либо на основании фактического наблюдения по результатам измерений для соответствующей временной когорты, либо на основании индексных значений, полученных для статистически достоверных исторических когорт, которые наблюдались в течение надлежащего периода времени.
"Относительный риск" означает соотношение абсолютных рисков индивида и абсолютных рисков когорт с низким уровнем риска или среднего популяционного риска, что может варьироваться в зависимости от того, как оцениваются клинические факторы риска. Как правило, также используют соотношение шансов, то есть, отношение положительных и отрицательных событий для определенного результата теста (шансы вычисляют по формуле р/(1-р), где р - вероятность события, а (1-р) - вероятность отсутствия события) без конверсии.
"Оценка риска" в контексте настоящего изобретения включает прогнозирование вероятности, шансов или возможности наступления события или патологического состояния, скорости возникновения события или перехода от одного патологического состояния в другое (конверсии). Оценка риска также может включать прогнозирование будущих клинических параметров, значений традиционных лабораторных факторов риска, или других показателей рецидива, в абсолютном или относительном выражении по отношению к группе, в которой ранее проводились измерения.
Определение наличия у индивида риска наступления инсульта может быть использовано для проведения непрерывных или категориальных измерений риска конверсии, таким образом, осуществляя диагностику и определяя спектр риска в отношении категории индивидов, отнесенных в группу риска конверсии. В категориальном сценарии изобретение может быть использовано для различения нормальных и других групп индивидов с более высоким риском. В одном варианте осуществления настоящее изобретение может использоваться для дифференциации нормальных индивидов и индивидов, находящихся в группе риска.
Настоящее изобретение также относится к методу определения прогноза для индивида, страдающего от инсульта, включающему i) определение уровня экспрессии, по меньшей мере, одного биомаркера, выбранного из группы, состоящей из DUSP1, PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, ADM, и TM4SF1 в образце, предпочтительно образце физиологической жидкости, более предпочтительно, образце крови, полученном от субъекта ii) сравнение уровня, определенного на стадии i), с предварительно установленным эталонным значением и iii) вынесение заключения о том, что у пациента хороший прогноз, если уровень, определенный на стадии i), ниже, чем предварительно установленное эталонное значение, или вынесение заключения о том, что у пациента плохой прогноз, если уровень, определенный на стадии i), выше, чем предварительно установленное эталонное значение.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает стадии получения образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, определения в указанном образце сигнатуры по настоящему изобретению и сравнения указанной сигнатуры с эталонной сигнатурой. Эти стадии были подробно описаны выше в контексте метода диагностики инсульта и должны применяться к настоящему методу соответствующим образом.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры по настоящему изобретению;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что у пациента хороший прогноз, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что у пациента хороший прогноз, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что у пациента хороший прогноз, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что у пациента хороший прогноз, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1;
iii) сравнение сигнатуры, определенной на стадии ii) с эталонной сигнатурой; и
iv) вынесение заключения о том, что у пациента хороший прогноз, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления метод определения прогноза для индивида, страдающего от инсульта, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) вынесение заключения о том, что у пациента хороший прогноз, на основании корреляции сигнатуры с эталонной сигнатурой, как подробно описано выше.
В одном варианте осуществления эталонную сигнатуру определяют или получают на основании данных контрольной группы, предпочтительно, включающей, по меньшей мере, одного по существу здорового индивида.
В одном варианте осуществления эталонную сигнатуру определяют или получают на основании предыдущего измерения уровней экспрессии биомаркеров инсульта по настоящему изобретению в эталонном образце, полученном от того же индивида, например, уровней экспрессии биомаркеров инсульта, измеренных после наступления инсульта, предпочтительно, не менее чем через 6 часов, 12 часов, 18 часов, 24 часа, 36 часов, 48 часов, 60 часов, 72 часа, 84 часа или 96 часов после наступления инсульта.
В контексте настоящего документа термин "прогноз" означает предсказание вероятного исхода инсульта, т.е. течения инсульта или времени выживания пациента.
В контексте настоящего документа термин "хороший прогноз" означает  чем средняя, вероятность выживания пациента, страдающего инсультом, по сравнению с другими представителями того же пола, страдающими аналогичным заболеванием.
чем средняя, вероятность выживания пациента, страдающего инсультом, по сравнению с другими представителями того же пола, страдающими аналогичным заболеванием.
В контексте настоящего документа термин "плохой прогноз" означает меньшую, чем средняя, вероятность выживания пациента, страдающего инсультом, по сравнению с другими представителями того же пола, страдающими аналогичным заболеванием.
Настоящее изобретение также относится к методу лечения индивида, пораженного инсультом.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает стадии получения образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида, определения в указанном образце сигнатуры по настоящему изобретению и сравнения указанной сигнатуры с эталонной сигнатурой. Эти стадии были подробно описаны выше в контексте метода диагностики инсульта и должны применяться к настоящему методу соответствующим образом.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры по настоящему изобретению;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой; и
iv) диагностирование индивида как пораженного инсультом на основании корреляции полученной сигнатуры с эталонной сигнатурой, как подробно описано выше; и
v) лечение индивида, если на стадии iv) у него был диагностирован инсульт.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из HSPA1B, NPAS4, DNAJB1, ATF3, HSPB1, RRAD, NR4A1, CYR61, C-FOS, GADD45G, RGS1, ARC, EGR4, PTGS2, RGS2, CCL3, BAG3, EGR2, HSPA4L, ADM, TM4SF1, EGR1, DUSP1, BTG2, LOC715456, HMOX1, LDLR, DNAJA4, MCL1, HSPA6, GADD45B, IL6, ADFP, HES4, DUSP5, GEM и G0S2;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой;
iv) диагностирование индивида как пораженного инсультом на основании корреляции полученной сигнатуры с эталонной сигнатурой, как подробно описано выше; и
v) лечение индивида, если на стадии iv) у него был диагностирован инсульт.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9 или более биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
предпочтительно, с условием, что упомянутые выше, как минимум, один или два биомаркера инсульта не состоят из DUSP1 и/или ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой;
iv) диагностирование индивида как пораженного инсультом на основании корреляции полученной сигнатуры с эталонной сигнатурой, как подробно описано выше; и
v) лечение индивида, если на стадии iv) у него был диагностирован инсульт.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно путем измерения уровней экспрессии, по меньшей мере, трех биомаркеров инсульта, выбранных из группы, включающей или состоящей из PTGS2, HMOX1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой;
iv) диагностирование индивида как пораженного инсультом на основании корреляции полученной сигнатуры с эталонной сигнатурой, как подробно описано выше; и
v) лечение индивида, если на стадии iv) у него был диагностирован инсульт.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3 и TM4SF1;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой;
iv) диагностирование индивида как пораженного инсультом на основании корреляции полученной сигнатуры с эталонной сигнатурой, как подробно описано выше; и
v) лечение индивида, если на стадии iv) у него был диагностирован инсульт.
В одном варианте осуществления метод лечения индивида, пораженного инсультом, включает следующие стадии:
i) получение образца, предпочтительно, образца физиологической жидкости, более предпочтительно, образца крови индивида;
ii) определение в упомянутом образце сигнатуры, предпочтительно, путем измерения уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
iii) сравнение сигнатуры, определенной на стадии ii), с эталонной сигнатурой;
iv) диагностирование индивида как пораженного инсультом на основании корреляции полученной сигнатуры с эталонной сигнатурой, как подробно описано выше; и
v) лечение индивида, если на стадии iv) у него был диагностирован инсульт.
В одном варианте осуществления эталонную сигнатуру определяют или получают с использованием данных контрольной группы, предпочтительно, включающей, по меньшей мере, одного по существу здорового индивида.
Примеры подходящих способов лечения и терапии для индивидов, у которых диагностирован инсульт, хорошо известны в данной области техники и подробно описаны выше в настоящем документе.
Изобретение будет дополнительно проиллюстрировано нижеследующим примером и чертежами. Однако данный пример не должен интерпретироваться как каким-либо образом ограничивающий объем настоящего изобретения.
Краткое описание фигур
Фигура 1 представляет собой совокупность 3 графиков, демонстрирующих корреляцию между уровнями мРНК и значениями интенсивности сигнала микроматрицы для (a) HSPA1B, (b) GADD45G и (с) CDKN1A по результатам количественной ПЦР в реальном времени (qRT-PCR). На оси х показан log2 соотношения уровней мРНК (кПЦР в реальном времени), нормализованных по SMC2, а на оси у показан сигнал олигонуклеотидной микроматрицы. Р-величина взята из U-критерия Манна-Уитни.
Фигура 2 представляет собой совокупность двух диаграмм Венна для наиболее значительного перекрытия двух наборов генов, дифференциально экспрессируемых в головном мозге и в крови. На верхней панели представлены гены, снизившие экспрессию, а на нижней панели - гены, повысившие экспрессию.
Фигура 3 иллюстрирует кинетику интенсивности генов в крови для 9 наиболее дифференциально экспрессируемых генов у самца макаки-резус S1 в разные временные промежутки: до (Т0) и после (T1, Т2, Т3) ишемии.
Фигура 4 иллюстрирует кинетику интенсивности генов в крови для 9 наиболее дифференциально экспрессируемых генов у самцов макаки-резус S2 в разные временные промежутки: до (Т0) и после (T1, Т2, Т3) ишемии.
Примеры
Настоящее изобретение далее иллюстрируется следующими примерами.
Пример 1: определение общей сигнатуры для мозга с ишемическими повреждениями и крови на модели с участием макак-резус с тромбозом
Методы
Эксперимент на животных
Эксперименты проводились на 2 самцах вида Масаса mulatta возрастом 12-13 лет, с весом тела от 16,5 до 17,2 кг. В дальнейшем две указанные обезьяны будут обозначены как S1 и S2.
Протокол эксперимента был передан в Региональный комитет по контролю этических норм проведения экспериментов с участием животных (Нормандия), было получено разрешение на проведение данного исследования (номер для ссылок N/02-03-08/03/02-11). Эксперименты проводились исследователями, имеющими соответствующее разрешение (C.O.), в соответствии с законами в области этики и руководящими указаниями по обращению и использованию лабораторных животных, действующими во Франции и в Европе (Директива 2010/63/EU Европейского Парламента и Совета от 22 сентября 2010 года о защите животных, используемых в научных целях). В ходе настоящего исследования обезьяны содержались в исследовательском центре Cyceron Research Centre (Учреждение для проведения экспериментов над животными, соглашение № В14118001) в отдельных клетках с поддержанием в течение 24 часов 50% относительной влажности и цикла смены освещенности 12 часов день/12 часов ночь и питанием магазинным кормом с добавлением свежих фруктов и воды без ограничений. На всем протяжении настоящего исследования за состоянием животных наблюдал ветеринарный врач.
Модель эксперимента с участием животных
Модель с участием макак-резус с тромбозом
Эксперименты проводились в соответствии с представленным ранее описанием (Gauberti и др., 2012. Cerebrovasc Dis. 33(4):329-39).
После общего наркоза, после энуклеации, была обнажена правая средняя мозговая артерия (MCA). Были наложены два шва для изоляции ветви M1, в которую была вставлена микропипетка и произведена инъекция человеческого тромбина. Было введено приблизительно 600 мкл тромбина в концентрации 1 Ед/мкл. Первая инъекция содержала 100 мкл, за ней с 2-минутным интервалом следовали 6 инъекций по 50 мкл. Затем был удален проксимальный шов и введен оставшийся тромбин. Затем через 15 минут был снят дистальный шов.
Вся процедура инъекции тромбина заняла, в совокупности, около 30 минут.
Анестезия и контроль физиологических показателей
Животным в качестве транквилизатора вводили кетамин (0,1 мг/кг; IM; Imalgene®). Для ингаляционной анестезии использовался севофлуран (2,5%; Sevorane®) в 100% кислороде. Миорелаксация достигалась введением атракуриума (0,5 мг/кг; IV; Tracrium®) через подкожную вену.
Обезьяны находились на механической вентиляции с перемежающимся положительным давлением при фиксированной частоте дыхания 22 дыхательных движений в минуту. Дыхательный объем (VT) был отрегулирован для достижения нормокапнии ( =38-42 мм ртутного столба). Анестезия поддерживалась с помощью севофлурана с 66% закисью азота.
=38-42 мм ртутного столба). Анестезия поддерживалась с помощью севофлурана с 66% закисью азота.
Во время хирургического вмешательства концентрация севофлурана была увеличена до 3%, а затем уменьшена до 1,5-2% в ходе процедуры магнитно-резонансной томографии (МРТ). Внутривенная перфузия атракуриума осуществлялась при 0,75 мг/кг/ч. Перед проведением хирургического вмешательства животные были зафиксированы в стереотаксической раме.
Исследование методом MPT in vivo
Обезьян исследовали на клиническом томографе для 3Т MPT (Philips Sense Flex M).
Томография проводилась в аксиальной и корональной плоскости и включала следующие последовательности: 3D-времяпролетную ангиографию, Т2-взвешенное изображение с подавлением сигнала от свободной жидкости (FLAIR), диффузно-взвешенное изображение (DWI), и пре- и постконтрастное Т1-взвешенное и перфузионно-взвешенное изображение (PWI).
Образцы крови
Образцы тканей головного мозга
У каждой обезьяны было взято 12 образцов тканей головного мозга. У каждой обезьяны 6 образцов отбирались поблизости от очага инфаркта и 6 образцов отбирались из соответствующего участка в другом полушарии. Таким образом, в совокупности было проанализировано 12 ишемических и 12 неишемических образцов.
Две рассматриваемые обезьяны были прооперированы и умерщвлены приблизительно через 5,5 часов после закупорки артерии (S1: 5 ч 12 мин; S2: 5 ч 35 мин). МРТ проводилась в период между 3 и 4 часами после закупорки артерии (S1: 3ч 10 мин; S2: 3ч 05 мин). Животным вводили внутрисердечно после торактомии примерно 8 литров 4°С физ. раствора. Затем после краниотомии извлекали головной мозг и помещали его в форму, специально разработанную для получения фронтальных срезов головного мозга. Каждый срез помещали на сетку, чтобы иметь возможность определить координаты по осям х и у в ишемическом и неишемическом полушарии. На сетке в произвольном порядке римские цифры относились к правой, ишемической стороне, а арабские цифры - к левой, не ишемической стороне.
Ишемия была видна невооруженным глазом (данные не показаны) и подтверждалась наличием ишемической ткани с пониженным метаболизмом, обработанной тетразолием, которая выглядела белой по сравнению с розоватым окрашиванием, полученным для противоположного, неишемического полушария.
Было подготовлено по три образца коры головного мозга с ишемией от каждого животного: один потенциально соответствовал ядру и два - из краевых участков, потенциально соответствующие области пенумбры. Также для каждого животного были подготовлены три гомологичных образца тканей противоположного полушария.
Окрашивание ТТХ
Для оценки метаболической активности и, следовательно, ишемической ткани, ткани, прилегающие к образцам, подлежащим транскриптомному анализу, были окрашены 1%-м хлоридом тетразолия (ТТХ).
Экстракция суммарной РНК
Для выделения суммарной РНК из коры головного мозга использовали набор RNeasy Microarray Tissue kit в соответствии с инструкцией производителя (Qiagen). Целостность РНК оценивали с помощью анализатора Agilent 2100 BioAnalyzer (Agilent Technologies), измеряя число целостности РНК (RIN) (Schroeder и др., 2006. ВМС Mol Biol. 7:3). Полученное значение RTN находилось в диапазоне между 6,3 и 8,8.
Для выделения суммарной РНК из образцов крови использовали набор PAXgene Blood RNA Kit (PreAnalytix). Для отделения глобиновой мРНК от суммарной РНК использовали набор GlobinClear kit (Ambion). Полученное значение RIN находилось в диапазоне между 7,8 и 10.
Микроматрица экспрессии для макак и выбор образцов
Для мечения РНК из коры головного мозга (30 нг) и из образцов крови (30 нг) использовался набор Low Input Quick Amp WT Labeling kit (Agilent Technologies). Для корректировки возможных эффектов окрашивания использовали контроль пиковой РНК. РНК переводили в кДНК с помощью обратной транскриптазы и WT-праймеров (праймер с Т7 промотором и случайный праймер с Т7 промотором). Для синтеза и мечения кРНК с помощью Су3 использовали Т7 РНК-полимеразу. Флуоресцентно меченые кРНК-зонды очищали с использованием набора RNeasy mini kit (Qiagen).
Равное количество (3,75 мкг) кРНК-зондов, меченых Су3, гибридизовали на чипе 4х44К Agilent DNA chip (номер в каталоге: G2519F, Масасса mulatto). Гибридизацию проводили в течение 17 часов, при вращении со скоростью 10 об/мин при 65°С. Образцы затем промывали и высушивали в соответствии с инструкцией производителя.
Изображения после гибридизации получали с использованием сканера фирмы Agilent для ДНК-микрочипов, данные по интенсивности получали с использованием программного обеспечения Feature Extraction software (Agilent Technologies). Данная матрица содержит 43803 зондов макак-резус. Эти зонды получены из RefSeq (Release 37, октябрь 2009), Unigene (Release 13, октябрь 2009), UCSC MRNA (октябрь 2009), Ensembl (Release 56, сентябрь 2009), UCSC RheMac2 (январь 2006). Многие зонды спрогнозированы, исходя из ортологичных генов человека. Кроме того, некоторые зонды аннотированы только как кДНК Масаса mulatto, и в отношении их функции можно только строить предположения, исходя из гомологии с человеком. Анализ проводился в сотрудничестве с компанией Genosplice (Эври, Франция), которая специализируется на транскриптомном анализе.
Микроматричный анализ
Исследование дифференциальной экспрессии на основании данных микроматричного анализа экспрессии, полученных с использованием ресурсов фирмы Agilent, выполняли с помощью линейной модели для данных, полученных на микроматрице (LIMMA), использовавшейся в проекте Bioconductor (Smyth, 2004. Stat Appl Genet Mol Biol. 3: Article3). Первичные данные нормализовали, сначала путем коррекции фона, а затем путем нормализации между матрицами для всех образцов тканей мозга и крови также с использованием LIMMA. Зонды аннотировали с использованием информации для матриц Agilent, представленной на сайте Array Express (http://www.ebi.ac.uk/arrayexpress/arrays/A-GEOD-9861/?page=71&pagesize=100&sortby=organism&sortorder=descending) и информации по генам, предоставленной фирмой Genosplice.
Пакет LIMMA осуществляет анализ дифференциальной экспрессии, сначала приводя данные по экспрессии каждого гена в соответствие с линейной моделью. Затем он использует эмпирический подход Байеса (eBayes) для заимствования информации по всем генам, что позволяет нам осуществить анализ на небольшом количестве матриц.
Все анализы дифференциальной экспрессии на основании данных микроматричного анализа образцов тканей мозга были проведены с помощью LIMMA с использованием эмпирического метода Байеса (Smyth, 2005. limma: Linear Models for Microarray Data. In: Gentleman и др. (Eds), Bioinformatics and Computational Biology Solutions Using R and Bioconductor. Statistics for Biology and Health. New York, NY: Springer).
Статистика
Сравнение генов с высоким уровнем экспрессии в образцах головного мозга
Двух рассматриваемых обезьян анализировали отдельно. Гены считались «генами с высоким уровнем экспрессии», если величина диапазона изменения превышала 2 (то есть, log2 диапазона изменения был более 1) у обеих обезьян при сравнении образцов ишемических и неишемических тканей мозга, и если величина диапазона изменения была менее 2 при сравнении ишемических образцов разных обезьян или при сравнении неишемических образцов разных обезьян.
Сравнение генов с высоким уровнем экспрессии в образцах крови
Образцы крови анализировали путем сравнения образца до закупорки сосуда с каждым образцом после закупорки сосуда. Двух рассматриваемых обезьян анализировали отдельно. Момент времени с максимальным диапазоном изменения отбирался для последующего анализа и обозначался как "S1 макс, кровь" и "S2 макс, кровь" (Таблица 1). Гены считались «генами с высоким уровнем экспрессии», если величина диапазона изменения превышала 1,5 у обеих обезьян при сравнении образца до закупорки сосуда со значениями "S1 макс, кровь" и "S2 макс, кровь".
Для сравнения и выявления общих высокодифференциально экспрессируемых генов использовали только высокодифференциально экспрессируемые гены в образцах ишемических тканей мозга и в образцах крови, взятых после закупорки артерии, согласно определениям, приведенным выше.
Контроль качества данных
Внутренняя валидизация
Для валидизации результатов микроматричного анализа использовали зонд-специфичный двухэтапный тест TaqMan R Gene Expression Assay (Applied Biosystems). Гены для валидизации отбирались, исходя из ранжирования дифференциальной экспрессии и биологической аннотации, соответствующей ишемии. Мы выбрали SMC2 для нормализации всех целевых генов, поскольку этот ген продемонстрировал постоянный уровень экспрессии в образцах ишемических и неишемических тканей. Идентификаторы зонда для количественного анализа экспрессии генов: HSPA1B (А 01 Р010726), GADD45G (А 01 Р018040), CDKN1A (А 01 Р002585), SMC2 (А 01 Р019124).
100 нг суммарной РНК каждого образца использовали для генерации кДНК с помощью набора Superscript® III First-Strand Synthesis Kit (ThermoFisher scientific) в соответствии с протоколом производителя. Полимеразные цепные реакции в реальном времени проводились в системе Roche LightCycler R480. Сравнение экспрессии генов в образцах ишемических и неишемических тканей осуществлялось методом сравнения CT (метод ΔΔCT) с применением U-критерия Манна-Уитни (Wilcoxon), используя ПО Prism software v6.0c (GraphPad, LaJolla, CA).
Внешняя валидизация
Мы предприняли попытку верифицировать полученные нами результаты, используя данные исследования, проведенного Cook и другими учеными (Cook и др., 2012. Nature. 483(7388):213-7). В ходе этого исследования также изучалась транскриптомика инсульта у приматов, имеющих мозговые извилины на поверхности больших полушарий, однако в исследовании участвовали яванские макаки - близкие родственники Масаса mulaiia (Street и др., 2007. ВМС Genomics. 8:480). С целью валидизации результатов, Полученных для Масаса mulatto, мы анализировали транскриптомные данные Для плацебо и неишемических образцов из исследования Cook и соавторов. Данные по плацебо ишемическим и неишемическим образцам получены из банка данных GEO (номер доступа: GSE35589) и проанализированы с использованием вышеописанных методов.
Частичное совпадение результатов, полученных для тканей головного мозга и крови
При применении теста RRHO было обнаружено значительно перекрывание результатов анализа дифференциальной экспрессии генов в образцах крови и Головного мозга (Plaisier и др., 2010. Nucleic Acids Res. 38(17):e169). Этот метод применяет гипергеометрический тест ко всем возможным совпадениям ранжированных списков генов с целью выявить граничное значение, при котором перекрывание между двумя наборами генов является наиболее значительным. Полные списки генов были ранжированы по среднему значению логарифма диапазона изменения для двух обезьян. Для изучения конкретных генов, экспрессия которых изменилась в крови и в головном мозге, мы составили список высокодифференциально экспрессированных генов в образцах тканей головного мозга (см. методы, описанные выше), и вычислили максимальное значение диапазона изменения для каждого из этих генов в образцах крови.
Анализ обогащения набора генов
Анализ обогащения набора генов осуществлялся с использованием программы командной строки GSEA (Subramanian и др., 2005. Proc Natl Acad Sci U S А. 102(43): 15545-50). Данный инструмент содержит предварительно установленный набор генов и определяет, является ли обогащенным каждый набор в верхней или в нижней части ранжированного экспериментального списка, что служит индикатором фенотипической роли. Программа вычисляет показатель обогащения (ES) для каждого исследуемого набора генов. Этот показатель показывает степень, в которой набор является перепредставленным в верхней или нижней части ранжированного экспериментального списка генов. Нормализованный показатель обогащения (NES) является нормализованным по размеру набора генов.
Результаты анализа дифференциальной экспрессии для образцов тканей мозга и крови были ранжированы по логарифму диапазона изменения. Эти списки были введены в программу GSEA. Анализ проводился с использованием 100 пермутаций, и наборы генов, содержащие менее 10 генов, исключались. Итоговые наборы генов были ранжированы по значению NES. GSEA ES показывает степень перепредставленности набора генов в верней или нижней части ранжированного списка генов. Величина показателя обогащения (ES) рассчитывается посредством прохождения по списку сверху вниз и повышения показателя, если ген присутствует, или его снижения при отсутствии гена. Величина повышения показателя зависит от корреляции конкретного гена и фенотипа (предварительно установленный набор генов). ES представляет собой максимальное отклонение от 0, обнаруженное в ходе прохождения по списку. Положительное значение ES говорит об обогащении в верхней части списка (в генах с повышенным уровнем экспрессии), а отрицательное значение ES означает обогащение в нижней части списка. Нормализованное значение ES показывает разницу в размере наборов генов и корреляцию между наборами генов и данными экспрессии, предоставляя возможность сравнить наборы генов.
Отношения между генами в таких наборах были визуализированы с помощью базы данных STRING (Szklarczyk и др., 2015. Nucleic Acids Res. 43(Database issue):D447-52). Гены вводились в базу данных STRING, если диапазон изменения для них составлял, как минимум, 2 в случае тканей мозга, и 1,5 для крови. Толщина линий показывает достоверность наличия связи, а крупные узлы обозначают белки, для которых имеется информация о третичной структуре.
Результаты
Животные были умерщвлены через 5,5 часов после наступления ишемического поражения. Аксиальная диффузионно-взвешенная МРТ показала фокальную ишемию средней мозговой артерии у обоих животных (данные не показаны). Анализ объема ишемического поражения у двух разных животных показал, что объем инфаркта был крайне изменчивым: у животного S1 наблюдался заметно больший объем поражения, чем у животного S2. И у S1, и у S2 наблюдались поверхностный и глубокий инфаркты. Поражение было также отчетливо видно у обоих животных на Т2-взвешенных изображениях с подавлением сигнала от свободной жидкости. MP-ангиография виллизиева круга показала проксимальную закупорку средней мозговой артерии у S1, хотя в случае S2 это было не так очевидно. Инфаркт был также виден на Т1-последовательности на уровне базальных ядер и у S1, и у S2.
Изменение экспрессии генов: сравнение ишемической и неишемической ткани головного мозга
В настоящем исследовании изменения в экспрессии генов между ишемической и неишемической тканью головного мозга измерялись для отдельных генов, а эффект этих изменений изучался на уровне наборов генов. Анализ дифференциальной экспрессии осуществлялся посредством сравнения данных по экспрессии, полученных для ишемической ткани головного мозга, с данными для соответствующей области другого полушария, в котором не было ишемического поражения.
Указанный анализ установил, что профили экспрессии для ишемической и неишемической ткани мозга имеют отчетливые различия (данные не показаны). Гены считались высокодифференциально экспрессируемыми, если диапазон изменений для них был более 2 при сравнении образцов ишемической и неишемической ткани головного мозга у каждой обезьяны, и эти гены не являлись дифференциально экспрессируемыми при сравнении образцов ишемической ткани двух рассматриваемых обезьян и образцов не ишемической ткани двух рассматриваемых обезьян (диапазон изменения <2). При применении к указанным наиболее дифференциально экспрессируемым генам (37 генов) иерархической кластеризации образцы ишемической ткани и не ишемической ткани образовывали четкие независимые группы.
Все высокодифференциально экспрессируемые гены имели повышенный уровень экспрессии (Таблица 1).
Значения, приведенные в столбцах "S1 мозг" и "S2 мозг" представляют собой log2 диапазона изменения экспрессии этих генов в мозгу двух рассматриваемых обезьян.
В столбцах "S1 макс, кровь", "S1 момент времени", "S2 макс, кровь" и "S2 момент времени" показаны данные для крови тех же двух обезьян. Для каждой показан момент времени с максимальным значением log2 диапазона изменения.
Гены, высокодифференциально экспрессируемые в крови (диапазон изменения >|1,5|) выделены жирным шрифтом и серой заливкой.
HSPA1B и LOC720054(HSPA1B) являются репликатами зондов для различных областей одного и того же гена.
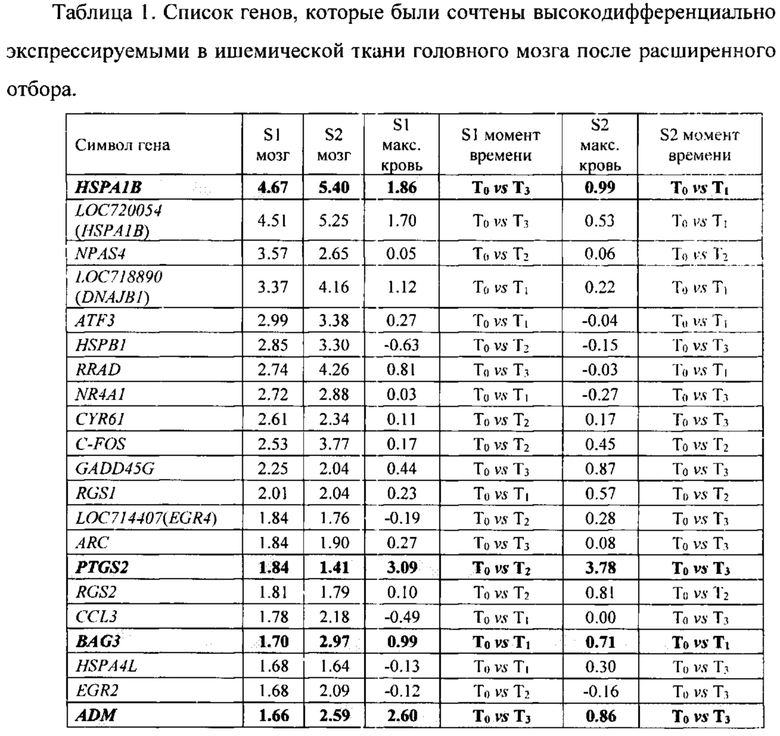
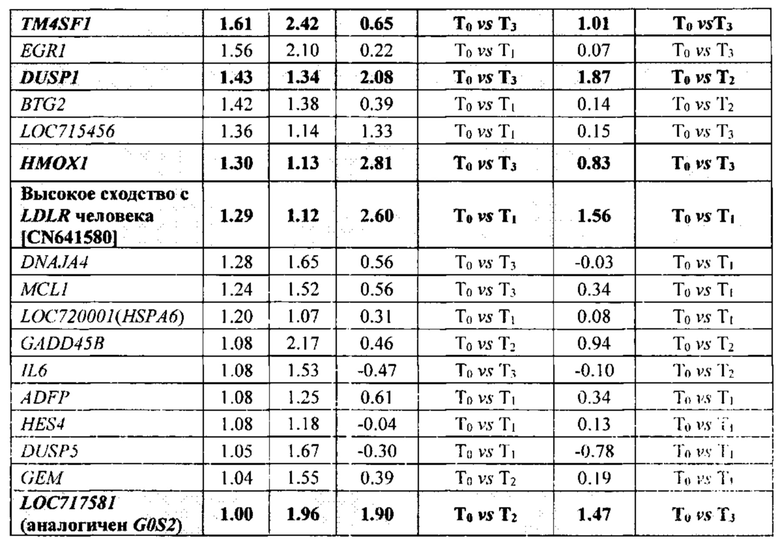
Внутренняя валидизация
Чтобы подтвердить надежность результатов микроматричного анализа, в образцах, полученных от исследуемых животных, методом количественной ПЦР в реальном времени были измерены уровни мРНК трех генов, чувствительных к ишемии (HSPA1B, GADD45G, CDKN1A). SMC2, который, как показали исследования, демонстрировал постоянный уровень экспрессии во всех тестируемых образцах, использовался в качестве внутреннего стандарта (ген домашнего хозяйства). Для каждого образца РНК было проведено три обратных транскрипции, после чего последовали три независимых цикла кПЦР, с повторными измерениями в отношении как целевых, так и референсных генов. Для всех генов направление и величина изменения в высокой степени соответствовали данным микроматричного анализа (Фигура 1 и Таблица 2).
Статистическая значимость: *р<0.05; **р<0.01; ***р<0.001. Результаты были нормализованы по SMC2.

Внешняя валидизация
Анализ транскриптомных данных, приведенный в исследовании инсульта, осуществленном Cook и соавторами (Cook и др., 2012. Nature. 483(7388):213-7) на макаках вида Масаса fascicularis, дал результаты, сильно отличающиеся от тех, что были описаны в настоящей работе. В то время как проведенный в ходе настоящей работы анализ данных для Масаса mulatta выявил множество генов с повышенным уровнем экспрессии в тканях, пораженных инсультом, данные, полученные для Масаса fascicularis, демонстрировали наличие, в основном, генов с пониженным уровнем экспрессии. Наиболее вероятная причина этого заключается в большой разнице методов, которыми вызывался инсульт у приматов. В исследовании Cook и соавторов использовалась хирургическая закупорка средней мозговой артерии, которая, как было известно авторам, вызывает более тяжелый инсульт, чем тот, который обычно наблюдается у людей. Вероятно, эта модель более тяжелого инсульта вызвала массовую гибель клеток, что привело в результате к обнаружению, в основном, генов с пониженным уровнем экспрессии.
Обогащение наборов генов
Идентификация генов, для которых наблюдалось обогащение в ишемической ткани головного мозга, проводилась методом анализа обогащения набора генов (GSEA) института Броуда (Subramanian и др., 2005. Proc Natl Acad Sci USA. 102(43): 15545-50). В число 5 наиболее обогащенных наборов генов из характеристических (Hallmark) наборов генов для GSEA вошли: сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би», апоптоз, путь Р53, гипоксия, и повышение экспрессии в ответ на УФ-облучение. Все - с повышенным уровнем экспрессии (Таблица 3).
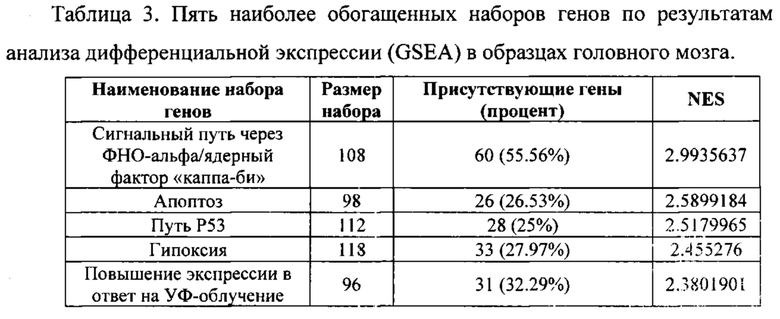
60 из 108 генов в наборе «Сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би»» являются ядром обогащения (наиболее обогащенной группой набора (NES=2,96).
Практически все гены в данном наборе, в отношении которых у нас имелись данные, имеют повышенный уровень экспрессии, и ни один не показывает значительного снижения уровня экспрессии: для 15 генов уровень экспрессии лишь немного снижен с максимальным диапазоном изменения, составляющим 1,17.
В наборе генов апоптоза 26 из 98 генов являются ядром обогащения (NES=2,57).
В наборе генов гипоксии 33 из 118 генов являются ядром обогащения (NES=2,38).
В наборе генов, повышающих экспрессию в ответ на УФ-облучение, 31 из 96 генов являются ядром обогащения (NES=2,3).
Наиболее значительно обогащенным набором генов с пониженным уровнем экспрессии являлись гены окислительного фосфорилирования. 84 из 120 генов данного набора являются обогащенной группой генов (NES=-2,57).
Взаимодействие генных продуктов
Для визуализации взаимодействия генных продуктов генов, высокодифференциально экспрессируемых в головном мозге и в крови и входящих в состав наиболее обогащенных наборов генов головного мозга (диапазон изменений ≥2 в образцах тканей головного мозга, диапазон изменений ≥1,5 в образцах крови), использовалась база данных STRING (Szklarczyk и др., 2015. Nucleic Acids Res. 43(Database issue):D447-52) (данные не показаны).
Было отмечено, что IL-6 имеет множество связей внутри сетей, формируемых генами апоптоза, гипоксии и сигнального пути через ФНО-альфа/ядерный фактор «каппа-би». Кроме того, во всех четырех указанных сетях присутствует CDKN1A. Взаимодействие CDKN1A с НМОХ1 наблюдается в сети с участием генов апоптоза, пути р53 и гипоксии. Ген ATF3 также присутствует во всех четырех указанных сетях, взаимодействуя с IL-6 в трех из них. Занимающий 5-е место набор генов головного мозга (Таблица 3) «Повышение экспрессии в ответ на УФ-облучение» не показан, поскольку ни один из наиболее дифференциально экспрессируемых генов этого набора не имеет каких-либо известных взаимодействий.
Изменение экспрессии генов: сравнение образцов крови, взятых до и после закупорки сосуда
Обнаружение в крови генов, дифференциально экспрессируемых в ходе ишемии головного мозга, осуществлялось путем сравнения всех образцов крови, взятых до закупорки артерии, со всеми образцами, взятыми после закупорки артерии. При применении в отношении дифференциально экспрессируемых генов иерархической кластеризации, образцы, взятые до и после закупорки сосуда, образуют отдельные группы (данные не показаны). Также, исходя из результатов кластеризации, по-видимому, имеют место различия в профилях экспрессии в крови двух изучаемых макак. У обезьяны S1 наблюдается более выраженное повышение уровней экспрессии указанных генов по сравнению с обезьяной S2. Эти различия между двумя обезьянами не наблюдаются с такой очевидностью в профилях экспрессии, полученных для образцов головного мозга (данные не показаны).
Как и в случае образцов головного мозга, методом GSEA были проанализированы результаты, касающиеся дифференциальной экспрессии в образцах крови. 5 наиболее обогащенных наборов генов: сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би», гипоксия, сигнальный путь hedgehog, воспалительная реакция, и ангиогенез (Таблица 4).
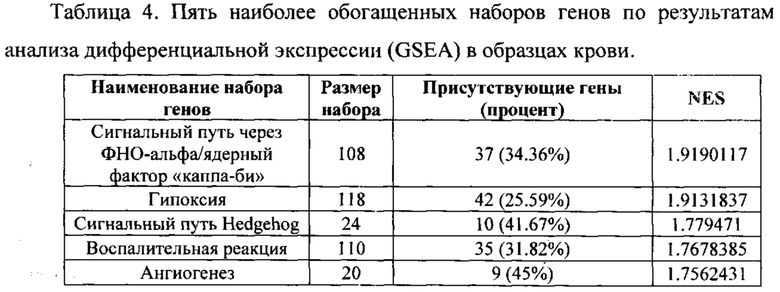
Наборы генов сигнального путь через ФНО-альфа/ядерный фактор «каппа-би» и гипоксии также вошли в число 5 основных наборов генов для образцов головного мозга (Таблица 4).
37 из 108 генов в наборе «Сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би»» являются ядром обогащения (NES=1,92).
В наборе генов гипоксии 42 из 118 генов являются ядром обогащения (NES=1,91).
В наборе генов сигнального пути Hedgehog 10 из 24 генов являются ядром обогащения (NES=1,77).
В наборе генов воспалительной реакции 35 из 110 генов являются ядром обогащения (NES=1,77).
В наборе генов ангиогенеза 9 из 20 генов являются ядром обогащения (NES=1,76).
Дифференциально экспрессируемые гены, общие для головного мозга и крови
Результаты, полученные для дифференциальной экспрессии генов в образцах тканей головного мозга и крови, исследовали на предмет наличия значительного перекрытия после ранжирования генов по диапазону изменения. Мы наглядно показываем, что два ранжированных набора генов в высокой степени аналогичны, в частности, в двух экстремумах: гены с наибольшим повышением и наибольшим снижением экспрессии в ходе ишемического поражения. Мы также показали перекрывающиеся гены, имеющие наибольшую значимость: 2156 генов с понижением экспрессии демонстрируют значительное сходство в образцах тканей головного мозга и крови, также в значительной степени совпадают результаты для 493 генов с повышенным уровнем регуляции (Фигура 2). Большинство указанных генов имеет сравнительно небольшой диапазон изменения экспрессии, однако степень совпадения дифференциально экспрессируемых генов в образцах тканей мозга и крови очень велика.
Хотя многие гены из этих перекрывающихся наборов не являлись высокодифференциально экспрессируемыми, но были и те, которые проявляли данную особенность, и нас в первую очередь интересовали гены с очень высоким значением изменения экспрессии в образцах тканей мозга. Из числа генов, идентифицированных как высокодифференциально экспрессируемые в тканях мозга, 9 входили также в число высокодифференциально экспрессируемых в крови (диапазон изменения ≥1,5; Таблица 1, выделены жирным шрифтом). Все 9 упомянутых генов попадали в область наиболее значительного гипергеометрического перекрытия (выделено жирным шрифтом). К указанным генам относятся: PTGS2, G0S2-подобный, DUSP1, LDLR-подобный, НМОХ1, HSPA1B, BAG3, ADM, и TM4SF1. Для большинства перечисленных генов наблюдалось резкое повышение уровней экспрессии в крови, которые со временем снижались (Фигуры 3 и 4).
Обсуждение
Для изучения изменения профилей экспрессии генов в ходе ишемического инсульта головного мозга использовалась модель эксперимента с участием нечеловекообразных приматов (Gauberti и др., 2012. Cerebrovasc Dis. 33(4):329-39), с введением человеческого тромбина в среднюю мозговую артерию. Это эмболическая модель фокальной ишемии с частичным ишемическим поражением средней мозговой артерии. Был использован временной интервал в 6 часов, поскольку именно он представляет собой временное окно, в течение которого возможно проведение терапевтического вмешательства у людней (тромболизис в период до 4 ч 30 мин; тромбэктомия в период до 6 часов после наступления инсульта).
Исследование данных микроматричного анализа экспрессии генов у макак в образцах тканей головного мозга и крови показало, что ишемические и неишемические образцы можно различать на основании профилей экспрессии, и что в случае инсульта большинство высокодифференциально экспрессируемых генов имеют повышенный уровень экспрессии через 6 часов после наступления ишемического поражения. Многие из этих генов с повышенным уровнем экспрессии участвуют в реализации метаболических путей, связанных с отмиранием клеток и «починкой» поврежденных ДНК. Сравнение генов, дифференциально экспрессируемых в головном мозге и в крови, установило значительное совпадение профилей экспрессии генов.
Полученные результаты свидетельствуют о потенциальной возможности выявления ишемического инсульта посредством транскриптомики образцов тканей головного мозга и крови.
Экспрессия генов в головном мозге, пораженном инсультом
Качество полученных данных подтверждено методом главных компонент (РСА), показавшим, что различение обеих обезьян, а также ишемии и не ишемии, возможно на основании данных экспрессии генов. Более того, полученные результаты в дальнейшем были подтверждены в ходе внутренней валидизации.
Иерархическая кластеризация данных, полученных для экспрессии генов в тканях головного мозга Масаса mulatta, выявила существенную независимую кластеризацию образцов тканей мозга, пораженных и не пораженных ишемией (данные не показаны). Эти результаты говорят о потенциальной возможности установить наличие ткани мозга, пораженной инсультом, исходя из профилей экспрессии генов. Наиболее существенно дифференциально экспрессируемые гены имели повышенный уровень экспрессии, что соответствует результатам многих проведенных ранее исследований ишемии у мышей (Büttner и др., 2009. Brain Res. 1252:1-14; Hori и др., 2012. Dis Model Mech. 5(2):270-83). В настоящем исследовании высокодифференциально экспрессируемые гены в тканях мозга определены как гены с диапазоном изменения не менее 2 у обеих обезьян, и гены не являются дифференциально экспрессируемыми при сравнении неишемических образцов двух указанных обезьян или при сравнении ишемических образцов двух указанных обезьян (диапазон изменения <2). Результаты проведенного нами анализа показали, что в тканях мозга 37 генов имели повышенный уровень экспрессии и ни один не имел пониженного уровня экспрессии. Эти результаты аналогичны результатам, полученным Büttner с коллегами, которые обнаружили через 6 часов 115 генов с повышенным и 19 генов с пониженным уровнем экспрессии (Büttner и др., 2009. Brain Res. 1252:1-14). То факт, что Büttner с коллегами обнаружили большее число генов, может объясняться использованием более объемной матрицы для профилирования экспрессии, а также различиями в экспрессии между видами животных.
Все высокодифференциально экспрессируемые гены в ткани мозга, пораженной ишемией, демонстрировали повышение уровня экспрессии. Многие из этих генов были ранее идентифицированы как гены, уровень экспрессии которых повышается при ишемическом инсульте в связи с рядом функций, в частности, стрессовой реакцией, апоптозом, и сигнальной трансдукцией.
В число генов стрессовой реакции, демонстрировавших повышенный уровень экспрессии, входили 7 белков теплового шока HSPA1B (Hsp70), HSP40, HSPB1, HSPA4L, и DNAJA4 (Hsp40-подобный) (Таблица 1). Повышенный уровень экспрессии белков теплового шока во время ишемии уже был отмечен в ходе многих исследований (Schmidt-Kastner и др., 2002. Brain Res Mol Brain Res. 108(l-2):81-93; Büttner и др., 2009. Brain Res. 1252:1-14; Kawahara и др., 2004. J Cereb Blood Flow Metab. 24(2):212-23;Tang и др., 2002. Eur J Neurosci. 15(12): 1937-52). Человеческий ортолог данного гена подробно описан как стрессиндуцированный ген, стабилизирующий белки для предотвращения их агрегации. Он также вовлечен в убиквитин-протеасомный метаболический путь (NCBI, Accession: NM 005346.5). Hsp70 является наиболее часто упоминаемым белком теплового шока с повышением уровня экспрессии при ишемическом инсульте (Cox-Limpens и др., 2014. Brain Res. 1564:85-100). У вида Масаса mulatta белок 1B (HSPA1B), входящий в семейство белков теплового шока А (Hsp70), является геном с наиболее повышенным уровнем экспрессии в ишемической ткани головного мозга. Исследования HSPA1B у мышей, использовавшие технологию генного нокаута, показали, что кардиомиоциты, в которых отсутствует данный ген, более подвержены разрушительному действию ишемии (Kim и др., 2006. Circulation. 113(22):2589-97). Исследования ишемии головного мозга установили, что у мышей с нокаутом генов hsp70 наблюдался более обширный инфаркт, чем у мышей дикого типа (Lee и др., 2004. Stroke. 35(9):2195-9), а у мышей со сверхэкспрессией Hsp70 наблюдались меньший размер инфаркта и улучшенная неврологическая функция (Zheng и др., 2008. J Cereb Blood Flow Metab. 28(1):53-63). Высокий уровень дифференциальной экспрессии HSPA1B у макак означает, что он, возможно, играет также нейропротективную роль в мозге приматов при ишемии. Также интересно отметить, что одним из наиболее дифференциально экспрессируемых генов по результатам данных микроматричных анализов является DNAJB1, гомолог белка теплового шока.
Еще один высокодифференциально экспрессируемый ген стрессовой реакции, это NPAS4, который, как известно, является также нейропротектором (Chby и др., 2015. Int J Mol Sci. 16(12):29011-28). Этот фактор транскрипции экспрессируется в нейронах головного мозга и играет роль в реакциях раннего ответа в возбуждающих и тормозящих нейронах. Экспрессия данного гена индуцируется рядом ситуаций, в которых нервные клетки испытывают стресс. В нашем исследовании log2 диапазона изменения для NPAS4 составил 3,57 у S1 и 2,65 у S2 (Таблица 1). Ген C-FOS, контролируемый NPAS4 (Ramamoorthi и др., 2011. Science. 334(6063): 1669-75), в нашем исследовании также является высокодифференциально экспрессируемым, с log2 диапазона изменения, равным 2,53 у S1 и 3,77 у S2. При развитии ишемии головного мозга уровень экспрессии гена C-FOS, как правило, повышается (Cox-Limpens и др., 2014. Brain Res. 1564:85-100).
Следующим среди наиболее дифференциально экспрессируемых генов идет ген активирующего фактора транскрипции 3 (ATF3). ATF3 кодирует одного из членов семейства транскрипционных факторов CREB. Он участвует в клеточном ответе на стресс. Для ATF3 получены следующие значения log2 диапазона изменения: 2,99 у S1 и 3,38 у S2 (Таблица 1). Кроме того, данный ген образует множество связей в рамках наборов наиболее дифференциально экспрессируемых генов GSEA (данные не показаны). Предшествующие эксперименты на мышах показали, что у особей с нокаутом ATF3 после ишемии головного мозга развивается более обширное поражение и ухудшается неврологическая функция (Wang и др., 2012. Neuroscience. 220:100-8).
Другими важными генами стрессовой реакции, для которых наблюдался повышенный уровень экспрессии в ишемических тканях головного мозга, являются два гена, активирующиеся при возникающем поражении, GADD45G и GADD45B (индуцируемые блокировкой роста и повреждением ДНК». Гены GADD45 вовлечены в репарацию ДНК. Для GADD45G получен log2 диапазона изменения экспрессии, равный 2,25 у S1 и 2,04 у S2, для GADD45B этот показатель составил 1,08 и 2,17, соответственно. Подобно белкам теплового Шока, семейство генов Gadd45 упоминалось, как повышающее уровень экспрессии, в ряде исследований, изучавших ишемию головного мозга на грызунах (Schmidt-Kastner и др., 2002. Brain Res Mol Brain Res. 108(l-2):81-93; 7-9, 20). Проведенный ранее анализ головного мозга крыс во время ишемической атаки показал, что экспрессия данных генов индуцируется транзиторной глобальной ишемией (Chen и др., 1998. J Cereb Blood Flow Metab. 18(6):646-57). Указанные исследователи пришли к заключению, что это может указывать на нейропротективную функцию рассматриваемых генов. Полученные нами результаты говорят, что подобная повышенная экспрессия при ишемии присутствует также и у приматов, вновь связывая роль рассматриваемых генов с клеточным ответом на ишемическое поражение.
Ген апоптоза BAG3 также демонстрировал значительное повышение уровня экспрессии в ишемической ткани головного мозга: log2 диапазона изменения составил 1,7 у S1 и 2,97 у S2. Изучение экспрессии генов при ишемии головного мозга у крыс также показало высокую степень повышения уровня экспрессии для данного гена (Schmidt-Kastner и др., 2002. Brain Res Mol Brain Res. 108(l-2):81-93). Известно, что после наступления ишемии происходит растворение белков, связанных с цитоскелетом (Lipton, 1999. Physiol Rev. 79(4): 1431-568). Интересно, что мы наблюдали повышенный уровень экспрессии гена белка ARC в ишемической ткани головного мозга (log2 диапазона изменения = 1,84 у S1 и 1,9 у S2). Повышение экспрессии ARC наблюдалось и в ходе проведенных ранее исследований ишемии головного мозга у крыс (Büttner и др., 2009. Brain Res. 1252:1-14).
Еще один класс генов, связываемый с ишемией головного мозга, это гены фосфатазы с двойной специфичностью (Dusp) (Wang и др., 2011. Brain Res. 1372:13-21). Продуцируемые ими белки способны инактивировать белки MAPK. В ходе нашего исследования высокую степень повышения экспрессии демонстрировали два гена Dusp: DUSP1 (log2 диапазона изменения = 1,43 у S1 и 1,43 у S2) и DUSP5 (log2 диапазона изменения = 1,05 у S1 и 1,67 у S2). Интересно, что, согласно выдвинутым ранее предположениям, Dusp5 является мишенью для р53 (Ueda и др., 2003. Oncogene. 22(36):5586-91).
Изменение экспрессии генов в крови
Профили экспрессии, наблюдавшиеся в крови, были аналогичны профилям экспрессии в тканях головного мозга, однако в данном исследовании имели место некоторые ограничения, касавшиеся транскриптомики крови. Вследствие относительно небольшого числа образцов (1 образец на каждый контрольный момент времени для каждой обезьяны), анализ временной динамики не представлялся возможным. Вместо анализа временной динамики образцы, взятые до закупорки артерии, попарно сравнивали с каждым образцом, взятым после закупорки. Для целей анализа набора генов полученные при сравнении результаты дифференциальной экспрессии, показавшие наибольшее изменение экспрессии, использовали в GSEA. Наборы генов, участвовавшие в данном анализе, продемонстрировали высокую степень корреляции с профилями экспрессии, полученными для образцов головного мозга.
Иерархическая кластеризация уровней экспрессии, определенных в образцах крови, показала, что образцы, взятые до и после закупорки сосуда, образуют независимые кластеры (данные не показаны). Хотя контраст не столь разителен, как в случае образцов тканей головного мозга, тем не менее, имеют место четкие различия в экспрессии генов до и после закупорки артерии. Эти результаты позволяют предположить, что дальнейшие эксперименты могли бы определить панель биомаркеров крови для использования в диагностике инсульта. Вследствие небольшого числа образцов и участников настоящего исследования точное установление выборки генов, которая могла бы использоваться для диагностики, оказалось затруднено, однако четко различимые профили позволяют предположить, что это станет возможным при большем количестве образцов.
Проведенный анализ дифференциально экспрессируемых генов в образцах крови макак с ишемией головного мозга показал, что, аналогично образцам тканей головного мозга, большинство транскриптов, обнаруживаемых в крови, имеют повышенный уровень экспрессии. При объединении данных для образцов от обеих обезьян и объединении данных для всех образцов, взятых после закупорки артерии, высокую степень дифференциальной экспрессии демонстрировал 651 ген (диапазон изменения больше 2), из которых 513 показали повышение уровня экспрессии.
Отдельного упоминания среди упомянутых дифференциально экспрессируемых генов заслуживают четыре гена S100: S100A8, S100A12, S100P, и S100A9. S100 представляют собой кальций-связывающие белки глиальных клеток. Наиболее высокодифференциально экспрессируемым членом данной группы является S100A8 (log2 диапазона изменения = 3,29; р = 0,027; данные не показаны), который тесно связан с провоспалительной функцией (Sedaghat & Notopoulos, 2008. Hippokratia. 12(4): 198-204).
Наборы генов, связанные с ишемией головного мозга
Головной мозг
Анализ обогащения набора генов для данных по экспрессии генов в образцах тканей головного мозга позволил выделить несколько наборов генов, вовлеченных в репарацию ДНК и апоптоз, которые демонстрировали повышенный уровень экспрессии в образцах ишемической ткани головного мозга. В число 5 наиболее обогащенных наборов генов вошли сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би», апоптоз, путь Р53, гипоксия, и повышение экспрессии в ответ на УФ-облучение. Некоторые из указанных метаболических путей уже были описаны в ранее проведенных исследованиях, как связанные с ишемией головного мозга.
Наибольшая степень обогащенности наблюдалась для набора генов «Сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би»». Цитокин ФНО-альфа активирует ядерный фактор «каппа-би», который участвует в воспалительном ответе. О повышении уровня экспрессии провоспалительных цитокинов сообщалось в ряде более ранних исследований (Schmidt-Kastner и др., 2002. Brain Res Mol Brain Res. 108(1-2):81-93; Lu и др., 2004. J Neurosci Res. 77(6):843-57; Broughton и др., 2009. Stroke. 40(5):e331-9).
Кроме того, повышение уровня экспрессии показали наборы генов, вовлеченных в апоптоз и метаболический путь р53. Эти пути активируются в случае клеточного стресса или повреждения ДНК, и повышенный уровень различных проапоптозных факторов был отмечен в предшествующих исследованиях (Büttner et al, 2009. Brain Res. 1252:1-14).
В дополнение, было показано, что метаболический путь через ядерный фактор «каппа-би» и путь р53 вносят свой вклад в нейрозащиту (Zhang и др., 2005. J Cereb Blood Flow Metab. 25(1):30-40; Chen и др., 2011. Antioxid Redox Signal. 14(8):1505-17).
Интересно отметить, что ген IL-6 является тесно связанным участником метаболических путей апоптоза, гипоксии и сигнального пути через ФИО-альфа/ядерный фактор «каппа-би» (данные не показаны), log2 диапазона изменения экспрессии для этого гена в образцах тканей головного мозга составил 1,08 и 1,53 у S1 и S2, соответственно. Кроме того, для нескольких наборов генов (апоптоз, путь р53 и гипоксия) отмечено взаимодействие CDKN1A и НМОХ1, при этом НМОХ1 демонстрирует значительное повышение уровня экспрессии.
Кровь
Анализ обогащения набора генов с использованием результатов, касающихся дифференциальной экспрессии генов в образцах крови, позволил выделить метаболические пути, связанные с сигнальной функцией, гипоксией и воспалительным ответом. 5 наиболее обогащенных наборов генов в образцах крови индивидов с ишемией головного мозга: сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би», гипоксия, сигнальный путь hedgehog, воспалительная реакция, и ангиогенез.
Интересно, что два наиболее обогащенных набора генов в образцах тканей головного мозга оказались также обогащенными в образцах крови: сигнальный путь через ФНО-альфа/ядерный фактор «каппа-би» и ответная реакция на гипоксию. Оба указанных метаболических пути соответствуют модели ответной реакции на ишемическое поражение. Для образцов крови, 37 из 108 генов сигнального пути через ФНО-альфа/ядерный фактор «каппа-би» относятся к обогащенной группе генов (NES=1,92), и 42 из 118 генов, входящих в набор генов ответной реакции на гипоксию, относятся к обогащенной группе генов (NES=1,91). Набор генов сигнального пути через ФНО-альфа/ядерный фактор «каппа-би», по-видимому, представляет собой метаболический путь, в наибольшей степени связанный с ишемическим поражением, при этом свыше 50% генов, входящих в данный набор, вносят ключевой вклад в показатель обогащения в случае тканей головного мозга, и свыше 30% - в случае образцов крови.
Дифференциально экспрессируемые гены, общие для головного мозга и крови
С целью сравнения дифференциальной экспрессии генов в тканях головного мозга и в крови все гены были ранжированы по диапазону изменения, было изучено каждое возможное гипергеометрическое перекрытие, и в результате обнаружено значительное частичное совпадение как для генов с повышенным, так и для генов с пониженным уровнем экспрессии, входящих в ранжированный список. Проведенный нами анализ наиболее значительного гипергеометрического перекрытия генов с повышенной и пониженной экспрессией показал, что перекрывающиеся области содержат, соответственно, 493 и 2156 генов (Фигура 2).
Кроме того, был проведен более точный анализ данных экспрессии для образцов крови, в рамках которого образцы, взятые у каждой из обезьян до и после закупорки артерии, сравнивались отдельно, и отбирался только контрольный момент времени с наибольшим значением диапазона изменения. Полученные результаты объединяли с данными по экспрессии, полученными для тканей головного мозга, и гены ранжировали по показателю дифференциальной экспрессии как для образцов головного мозга (диапазон изменения ≥2), так и для образцов крови (диапазон изменений ≥1,5). 9 генов были идентифицированы как высоко дифференциально экспрессируемые как в головном мозге, так и в крови (Таблица 1). Все 9 генов принадлежали области наиболее значительного гипергеометрического перекрытия, описанной выше.
В число 9-ти упомянутых генов входят: HSPA1B, PTGS2, BAG3, ADM, TM4SF1, DUSP1, НМОХ1, IDL-подобный, и G0S2. HSPA1B, BAG3, и DUSP1 были рассмотрены в предыдущем разделе. Большинство указанных генов демонстрируют резкое повышение уровня экспрессии, который со временем снижается (Фигуры 3 и 4).
Простагландин-эндопероксид-синтаза-2 (PTGS2/COX2) это энзим, играющий роль в биосинтезе простагландинов. Как известно, уровень экспрессии данного гена повышается при воспалении, и он является мишенью аспирина. Аспирин подавляет выделение простагландинов, и в определенных дозах снижает риск возникновения инсульта (Tohgi и др., 1992. Stroke. 23(10): 1400-3; Eikelboom и др., 2002. Circulation. 105(14): 1650-5).
Было показано, что уровни экспрессии гена адреномедуллина (ADM) в крови связаны со степенью тяжести ишемического инсульта (Liu и др., 2014. Int J Neurosci. 124(4):271-80). Liu и другие исследователи выдвинули предположение о том, что уровень экспрессии ADM в лейкоцитах периферической крови может указывать на тяжесть поражения ткани. Данная гипотеза соответствует полученным нами результатам, поскольку у обезьяны S1 наблюдалось более обширное поражение, что подтверждается результатами МРТ (данные не показаны), и у указанной особи был найден более высокий уровень экспрессии ADM в образцах крови по сравнению с S2. Хотя данный профиль экспрессии меняется на противоположный в тканях головного мозга.
Гемоксигеназа 1 (НМОХ1) является членом семейства белков теплового шока, которое мы рассматривали ранее. Полагают, что она входит в состав системы защиты клеток от поражения, вызываемого оксидативным стрессом, например, инсультом (Chen & Maines, 2000. Cell Mol Biol (Noisy-le-grand). 46(3):609-17). Кроме того, в ходе ранее проведенных исследований было обнаружено повышение уровня экспрессии НМОХ1 в головном мозге после наступления ишемии головного мозга (Zhao и др., 2017. J Stroke Cerebrovasc Dis. 26(7):1622-1634).
Заключение
Полученные нами данные показали наличие общей сигнатуры для головного мозга, затронутого ишемическим поражением, и крови, и говорят в пользу развития транскриптомики крови в качестве инструмента биопсийного транскриптомного профилирования экспрессии с целью характеризации пациентов с ишемическим инсультом и разработки сопутствующих биомаркеров, необходимых для оценки эффективности лекарств-нейропротекторов у пациентов.
Хотя известно, что внеклеточные некодирующие РНК плазмы (ex-RNA) представляют собой класс циркулирующих молекул РНК, которые непосредственно управляют сетями экспрессии генов в тканях-мишенях (Mick и др., 2017. Stroke. 48(4):828-834), обнаружение общего профиля кодирующей последовательности РНК в головном мозге и в крови было достаточно неожиданным. Этот профиль экспрессии генов, связанных с ишемией, наблюдаемый в крови пациентов с ишемией головного мозга, уже упоминался в исследовании, проведенном Moore и другими учеными (2005. Circulation. 111(2):212-21). Они обнаружили гены, связанные с гипоксией, в МКПК, даже несмотря на то, что непосредственно в МКПК гипоксии не наблюдалось, хотя мозг страдал от гипоксии. Полученные результаты подтверждают заключение Moore и других авторов о том, что кровь может быть использована в качестве диагностического инструмента для подтверждения наличия ишемического инсульта.
Пример 2
Протокол клинических исследований
Использовали модель с участием нечеловекообразных приматов (Gauberti et al., 2012. Cerebrovasc Dis. 33(4): 329-39), с инъекцией человеческого тромбина в среднюю мозговую артерию. Проведенное исследование показало, что ишемические и неишемические образцы можно различить на основании профилей экспрессии через 6 часов после наступления ишемии. Идентифицированные гены с повышенной экспрессией относятся к метаболическим путям, связанным с гибелью клеток и репарацией ДНК. Сравнение генов, дифференциально экспрессируемых в головном мозге и в крови, выявило значительное совпадение профилей экспрессии генов.
В совокупности эти результаты обозначили потенциал для выявления ишемического инсульта с помощью транскриптомного профилирования, проводимого в отношении образцов тканей головного мозга и крови.
Были определены и использованы далее в исследованиях на людях девять наиболее значительно перекрывающихся генов с повышенными уровнями экспрессии в головном мозге и в крови.
Предлагается экстраполировать данные, полученные для обезьян, на человека. Гены с повышенной экспрессией, идентифицированные как в ишемическом мозге, так и в периферической крови в модели ишемического инсульта с участием приматов, исследуются в образцах, взятых у 20 пациентов с ишемическим инсультом, 20 пациентов с геморрагическим инсультом, и у аналогичных контрольных групп. Затем смотрим на соответствующие белки, чтобы иметь возможность потенциально разработать экспресс-тест, подобный тем, которые уже существуют для других сердечно-сосудистых заболеваний.
Пилотное исследование "случай-контроль"
Исследование «случай-контроль» для случаев ишемического инсульта, случающегося впервые, с разбивкой по парам на основании возраста, пола и риска возникновения сердечно-сосудистых заболеваний, измеренного в баллах (European Heart Score), до индексного инсульта у пациентов.
Случаи ишемического инсульта взяты из реестра Brest stroke registry. Реестр включает 900 пациентов в год. Контрольная группа набирается из одного центра (Университетский госпиталь Бреста).
Основная цель:
Разработать тест на определение РНК-биомаркера в крови на основании идентифицированных генов, экспрессия которых значительно повышена.
План исследования:
Исследование «случай-контроль» для случаев ишемического инсульта, случающегося впервые, с разбивкой по парам на основании возраста, пола и риска возникновения сердечно-сосудистых заболеваний, измеренного в баллах (European Heart Score), до индексного инсульта у пациентов.
Первичная конечная точка:
Экспрессия (выраженная в виде log2) каждого из генов, измеренная через 6 часов после наступления ишемии.
Первичный статистический анализ:
Экспрессия каждого гена-кандидата сравнивается со случаем и с контролем при помощи парного критерия Стьюдента.
Вторичный статистический анализ:
Экспрессия каждого гена сравнивается для случаев между острой фазой ишемического инсульта и 3 месяцами после.
Оценка размера выборки для полного исследования:
Разница между случаем и контролем устанавливается в 1,5 раза для случаев по сравнению с контролем (Диапазон изменения ДИ=1,5 и log2ДИ=0,585), для стандартного отклонения log2 степени выраженности экспрессии менее 1 (персональные данные).
При указанных гипотезах (разность = 0,585 и стандартное отклонение = 1), мощности 90% и коррекции Бонферрони на множественность тестов расчетное количество требуемых индивидов составляет: 110 - случаи и 110 контроль. Данный расчет не учитывает эффект возможного увеличения мощности, обеспечиваемого попарным распределением, так как уровень корреляции ответной реакции неизвестен.
Критерии включения
Для пациентов:
Возраст >18-лет; начало ишемического инсульта сонной артерии менее 6 часов назад, возможность взятия образца крови в момент времени Т1 в период до 6 часов после наступления инсульта; подходящий кандидат для проведения тромболизиса или тромбэктомии.
Начальный балл NIHSS >0; пациенты с результатами КТ или МРТ, соответствующими картине ишемического инсульта; пациенты с мультимодальной визуализацией, позволяющей анализировать пенумбру с помощью перфузионной МРТ или КТ-перфузии надаортальных и внутримозговых сосудов (виллизиев круг).
Критерии исключения включают пациентов с внутримозговым кровоизлиянием.
Для контроля:
Возраст >18 лет; стандартизированная анкета без перенесенного инсульта; индивиды с высоким риском без сердечно-сосудистых заболеваний и без перенесенного инсульта.
Индивидуальная регистрационная форма (ИРФ):
Используя стандартизованную регистрационную форму реестра Brest Stroke registry, для каждого пациента и контроля регистрируют демографические и клинические характеристики, факторы риска возникновения сердечно-сосудистых заболеваний и получаемое лечение.
Визуализация головного мозга:
В острой фазе - перфузионная МРТ или КТ и MP-ангиография или сканирование сосудов
Клиническое наблюдение и мониторинг методами визуализации:
Для пациентов, оценка по шкале Рэнкина через 3 месяца ± 15 дней и МРТ головного мозга через 3 месяца ± 15 дней.
Количество образцов на одного пациента:
42 мл крови отбирают в 6 различных моментов времени: <6 часов, 12 часов ± 2 часа, 24 часа ± 4 часа, 48 часов ± 4 часа, 7 дней ± 2 дня и через 3 месяца ±15 дней после инсульта.
Количество проб на 1 участника контрольной группы: 42 мл крови отбирают один раз для каждого участника контрольной группы.
Количество пациентов и участников контрольных групп:
20 пациентов с ишемическим инсультом; 20 участников контрольной группы, совпадающих с пациентами с ишемическим инсультом по возрасту, полу и показателю European Heart score.
Пациенты с геморрагическим инсультом
Случаи геморрагического инсульта отбираются из реестра Brest stroke registry в виде отдельной группы с тем же количеством образцов на каждого пациента, что и в группе с ишемическим инсультом.
Критерии включения
Для пациентов:
Возраст > 18-лет; внутримозговое кровоизлияние, наступившее менее 6 часов назад; возможность взятия образца крови в момент времени Т1 в период до 6 часов после наступления инсульта.
Начальный балл NIHSS >0; пациенты с КТ или МРТ, совместимые с геморрагическим инсультом.
Критерии исключения включают пациентов с травматическим внутримозговым кровоизлиянием и пациентов с ишемическим инсультом.
Число пациентов
20 пациентов с геморрагическим инсультом. Этические аспекты:
Проект проводится в соответствии с принципами Хельсинкской декларации и требованиями надлежащей клинической практики (GCP - ICHE6). Он представляется на утверждение в Комитет по этике исследований на людях в соответствии с действующими во Франции положениями о проведении клинических испытаний. Каждый участник дает информированное согласие в письменной форме.
Управление данными и биобанкинг:
Ввод данных в базу данных, управляемую программным обеспечением Clinsight (Capture system), осуществляется специалистом по управлению данными. Биобанк хранится в центре биологических ресурсов (CRB - Centre de Resources Biologiques) при Университетской больнице Бреста, сертифицированная NFS 96-900.
Отбор пациентов и контроля
Центры для отбора:
Отбор пациентов и контрольной группы, а также взятие образцов крови осуществляются в Университетской больнице (CHRU) Бреста.
Характеризация изображений и централизованная последующая обработка данных
Целью первичной функциональной визуализации (перфузионная МРТ или КТ) является картирование ядра инфаркта и пенумбры, мониторинг изменений в обеих зонах проводится через 3 месяца посредством МРТ. Первоначальная визуализация учитывает проходимость сосуда. Программное обеспечение позволяет проводить стандартизированный перфузионный анализ изображений, полученных методами МРТ и КТ. Другое программное обеспечение позволяет оценить окончательный объем по результатам МРТ и сравнить с пенумброй, определенной при первой визуализации.
Платформы для обработки изображений:
Для первичной визуализации используется контрастная 64-рядная (или более) мультидетекторная КТ или сканнеры для МРТ 1.5 Tesla или 3.0 Tesla. Методы получения данных:
Любой из следующих:
- неконтрастная КТ головы; КТ-перфузия головного мозга; КТ-ангиография головы и шеи; или
- МРТ головного мозга, включая диффузно-взвешенную визуализацию (DWI), взвешенное изображение с подавлением сигнала от свободной жидкости (FLAIR) и градиент-восстановленное эхо (GRE), магнитно-резонансную времяпролетную ангиографию (MRA) головы, МРТ-перфузию мозга с динамическим контрастом восприимчивости (DSC), MP-ангиографию с гадолинием для дуги аорты и шейных артерий.
В группе КТ ишемическое ядро оценивается либо по относительному мозговому кровотоку, либо по церебральному объему крови (CBV). В группе пациентов, обследуемой методами МРТ, ишемическое ядро (ткань, которая считается необратимо поврежденной) оценивается на основе порога считается необратимо поврежденной) оценивается на основе порога внешнего коэффициента диффузии (ADC).
Ткань с критической гипоперфузией оценивается для групп, обследуемых методами МРТ и КТ, исходя из времени до максимального порогового значения сигнала на кривой интенсивности (Tmax) > 6 секунд. Для МРТ или КТ регистрируются, соответственно, объем поражения по данным DWI или показатель ASPECTS (Alberta Stroke Program Early CT Score). Также фиксируется местоположение окклюзии (внутренняя сонная артерия (ВСА), M1, М2, базилярная артерия или отсутствие окклюзии).
Через 3 месяца МРТ головного мозга, включая диффузно-взвешенную визуализацию (DWI), 3D Т2-взвешенное изображение с подавлением сигнала от свободной жидкости (3D T2-FLAIR) и 3D Т1-градиент-восстановленное эхо (GRE), Т2-градиент-восстановленное эхо, магнитно-резонансную времяпролетную ангиографию головы.
Последующая обработка изображений
Постпроцессинг необработанных данных перфузионной визуализации (КТ и МРТ) в формате DICOM производится с помощью программного обеспечения для анализа перфузионного дисбаланса. Окончательный объем инфаркта устанавливается посредством Т2-взвешенного изображения с подавлением сигнала от свободной жидкости (Т2 FLAIR) в соответствии с методами сегментации. В исследовании принимают участие инженеры Лаборатории обработки медицинской информации (LaTIM - INSERM UMR 1101 г. Брест, Франция).
--->
Перечень последовательностей
<110> СЕНТР ОСПИТАЛЬЕ РЕЖЬОНАЛЬ Э УНИВЕРСИТЕР ДЕ БРЕСТ [FR]
ЭСТАБЛИСМОН ФРАНСЕ ДЮ СОН [FR]
ИНСТИТЬЮТ НАСЬОНАЛ ДЕ ЛА САНТЕ ET DE LA РЕШЕРШ МЕДИКАЛЬ (ИНСЕРМ) [FR]
УНИВЕРСИТЕ ДЕ БРЕТАНЬ ОКСИДAНТАЛЬ [FR]
<120> Способы диагностики инсульта, эффективности терапии, определения риска
инсульта
<150> RU 2020140532
<160> 18
<170> BiSSAP 1.3.6
<210> 1
<211> 604
<212> PRT
<213> Homo sapiens
<223> PTGS2 – Номер доступа NP_000954.1
<400> 1
Met Leu Ala Arg Ala Leu Leu Leu Cys Ala Val Leu Ala Leu Ser His
1 5 10 15
Thr Ala Asn Pro Cys Cys Ser His Pro Cys Gln Asn Arg Gly Val Cys
20 25 30
Met Ser Val Gly Phe Asp Gln Tyr Lys Cys Asp Cys Thr Arg Thr Gly
35 40 45
Phe Tyr Gly Glu Asn Cys Ser Thr Pro Glu Phe Leu Thr Arg Ile Lys
50 55 60
Leu Phe Leu Lys Pro Thr Pro Asn Thr Val His Tyr Ile Leu Thr His
65 70 75 80
Phe Lys Gly Phe Trp Asn Val Val Asn Asn Ile Pro Phe Leu Arg Asn
85 90 95
Ala Ile Met Ser Tyr Val Leu Thr Ser Arg Ser His Leu Ile Asp Ser
100 105 110
Pro Pro Thr Tyr Asn Ala Asp Tyr Gly Tyr Lys Ser Trp Glu Ala Phe
115 120 125
Ser Asn Leu Ser Tyr Tyr Thr Arg Ala Leu Pro Pro Val Pro Asp Asp
130 135 140
Cys Pro Thr Pro Leu Gly Val Lys Gly Lys Lys Gln Leu Pro Asp Ser
145 150 155 160
Asn Glu Ile Val Glu Lys Leu Leu Leu Arg Arg Lys Phe Ile Pro Asp
165 170 175
Pro Gln Gly Ser Asn Met Met Phe Ala Phe Phe Ala Gln His Phe Thr
180 185 190
His Gln Phe Phe Lys Thr Asp His Lys Arg Gly Pro Ala Phe Thr Asn
195 200 205
Gly Leu Gly His Gly Val Asp Leu Asn His Ile Tyr Gly Glu Thr Leu
210 215 220
Ala Arg Gln Arg Lys Leu Arg Leu Phe Lys Asp Gly Lys Met Lys Tyr
225 230 235 240
Gln Ile Ile Asp Gly Glu Met Tyr Pro Pro Thr Val Lys Asp Thr Gln
245 250 255
Ala Glu Met Ile Tyr Pro Pro Gln Val Pro Glu His Leu Arg Phe Ala
260 265 270
Val Gly Gln Glu Val Phe Gly Leu Val Pro Gly Leu Met Met Tyr Ala
275 280 285
Thr Ile Trp Leu Arg Glu His Asn Arg Val Cys Asp Val Leu Lys Gln
290 295 300
Glu His Pro Glu Trp Gly Asp Glu Gln Leu Phe Gln Thr Ser Arg Leu
305 310 315 320
Ile Leu Ile Gly Glu Thr Ile Lys Ile Val Ile Glu Asp Tyr Val Gln
325 330 335
His Leu Ser Gly Tyr His Phe Lys Leu Lys Phe Asp Pro Glu Leu Leu
340 345 350
Phe Asn Lys Gln Phe Gln Tyr Gln Asn Arg Ile Ala Ala Glu Phe Asn
355 360 365
Thr Leu Tyr His Trp His Pro Leu Leu Pro Asp Thr Phe Gln Ile His
370 375 380
Asp Gln Lys Tyr Asn Tyr Gln Gln Phe Ile Tyr Asn Asn Ser Ile Leu
385 390 395 400
Leu Glu His Gly Ile Thr Gln Phe Val Glu Ser Phe Thr Arg Gln Ile
405 410 415
Ala Gly Arg Val Ala Gly Gly Arg Asn Val Pro Pro Ala Val Gln Lys
420 425 430
Val Ser Gln Ala Ser Ile Asp Gln Ser Arg Gln Met Lys Tyr Gln Ser
435 440 445
Phe Asn Glu Tyr Arg Lys Arg Phe Met Leu Lys Pro Tyr Glu Ser Phe
450 455 460
Glu Glu Leu Thr Gly Glu Lys Glu Met Ser Ala Glu Leu Glu Ala Leu
465 470 475 480
Tyr Gly Asp Ile Asp Ala Val Glu Leu Tyr Pro Ala Leu Leu Val Glu
485 490 495
Lys Pro Arg Pro Asp Ala Ile Phe Gly Glu Thr Met Val Glu Val Gly
500 505 510
Ala Pro Phe Ser Leu Lys Gly Leu Met Gly Asn Val Ile Cys Ser Pro
515 520 525
Ala Tyr Trp Lys Pro Ser Thr Phe Gly Gly Glu Val Gly Phe Gln Ile
530 535 540
Ile Asn Thr Ala Ser Ile Gln Ser Leu Ile Cys Asn Asn Val Lys Gly
545 550 555 560
Cys Pro Phe Thr Ser Phe Ser Val Pro Asp Pro Glu Leu Ile Lys Thr
565 570 575
Val Thr Ile Asn Ala Ser Ser Ser Arg Ser Gly Leu Asp Asp Ile Asn
580 585 590
Pro Thr Val Leu Leu Lys Glu Arg Ser Thr Glu Leu
595 600
<210> 2
<211> 4510
<212> ДНК
<213> Homo sapiens
<223> PTGS2 – Номер доступа NM_000963.4
<400> 2
aattgtcata cgacttgcag tgagcgtcag gagcacgtcc aggaactcct cagcagcgcc 60
tccttcagct ccacagccag acgccctcag acagcaaagc ctacccccgc gccgcgccct 120
gcccgccgct gcgatgctcg cccgcgccct gctgctgtgc gcggtcctgg cgctcagcca 180
tacagcaaat ccttgctgtt cccacccatg tcaaaaccga ggtgtatgta tgagtgtggg 240
atttgaccag tataagtgcg attgtacccg gacaggattc tatggagaaa actgctcaac 300
accggaattt ttgacaagaa taaaattatt tctgaaaccc actccaaaca cagtgcacta 360
catacttacc cacttcaagg gattttggaa cgttgtgaat aacattccct tccttcgaaa 420
tgcaattatg agttatgtgt tgacatccag atcacatttg attgacagtc caccaactta 480
caatgctgac tatggctaca aaagctggga agccttctct aacctctcct attatactag 540
agcccttcct cctgtgcctg atgattgccc gactcccttg ggtgtcaaag gtaaaaagca 600
gcttcctgat tcaaatgaga ttgtggaaaa attgcttcta agaagaaagt tcatccctga 660
tccccagggc tcaaacatga tgtttgcatt ctttgcccag cacttcacgc atcagttttt 720
caagacagat cataagcgag ggccagcttt caccaacggg ctgggccatg gggtggactt 780
aaatcatatt tacggtgaaa ctctggctag acagcgtaaa ctgcgccttt tcaaggatgg 840
aaaaatgaaa tatcagataa ttgatggaga gatgtatcct cccacagtca aagatactca 900
ggcagagatg atctaccctc ctcaagtccc tgagcatcta cggtttgctg tggggcagga 960
ggtctttggt ctggtgcctg gtctgatgat gtatgccaca atctggctgc gggaacacaa 1020
cagagtatgc gatgtgctta aacaggagca tcctgaatgg ggtgatgagc agttgttcca 1080
gacaagcagg ctaatactga taggagagac tattaagatt gtgattgaag attatgtgca 1140
acacttgagt ggctatcact tcaaactgaa atttgaccca gaactacttt tcaacaaaca 1200
attccagtac caaaatcgta ttgctgctga atttaacacc ctctatcact ggcatcccct 1260
tctgcctgac acctttcaaa ttcatgacca gaaatacaac tatcaacagt ttatctacaa 1320
caactctata ttgctggaac atggaattac ccagtttgtt gaatcattca ccaggcaaat 1380
tgctggcagg gttgctggtg gtaggaatgt tccacccgca gtacagaaag tatcacaggc 1440
ttccattgac cagagcaggc agatgaaata ccagtctttt aatgagtacc gcaaacgctt 1500
tatgctgaag ccctatgaat catttgaaga acttacagga gaaaaggaaa tgtctgcaga 1560
gttggaagca ctctatggtg acatcgatgc tgtggagctg tatcctgccc ttctggtaga 1620
aaagcctcgg ccagatgcca tctttggtga aaccatggta gaagttggag caccattctc 1680
cttgaaagga cttatgggta atgttatatg ttctcctgcc tactggaagc caagcacttt 1740
tggtggagaa gtgggttttc aaatcatcaa cactgcctca attcagtctc tcatctgcaa 1800
taacgtgaag ggctgtccct ttacttcatt cagtgttcca gatccagagc tcattaaaac 1860
agtcaccatc aatgcaagtt cttcccgctc cggactagat gatatcaatc ccacagtact 1920
actaaaagaa cgttcgactg aactgtagaa gtctaatgat catatttatt tatttatatg 1980
aaccatgtct attaatttaa ttatttaata atatttatat taaactcctt atgttactta 2040
acatcttctg taacagaagt cagtactcct gttgcggaga aaggagtcat acttgtgaag 2100
acttttatgt cactactcta aagattttgc tgttgctgtt aagtttggaa aacagttttt 2160
attctgtttt ataaaccaga gagaaatgag ttttgacgtc tttttacttg aatttcaact 2220
tatattataa gaacgaaagt aaagatgttt gaatacttaa acactgtcac aagatggcaa 2280
aatgctgaaa gtttttacac tgtcgatgtt tccaatgcat cttccatgat gcattagaag 2340
taactaatgt ttgaaatttt aaagtacttt tggttatttt tctgtcatca aacaaaaaca 2400
ggtatcagtg cattattaaa tgaatattta aattagacat taccagtaat ttcatgtcta 2460
ctttttaaaa tcagcaatga aacaataatt tgaaatttct aaattcatag ggtagaatca 2520
cctgtaaaag cttgtttgat ttcttaaagt tattaaactt gtacatatac caaaaagaag 2580
ctgtcttgga tttaaatctg taaaatcagt agaaatttta ctacaattgc ttgttaaaat 2640
attttataag tgatgttcct ttttcaccaa gagtataaac ctttttagtg tgactgttaa 2700
aacttccttt taaatcaaaa tgccaaattt attaaggtgg tggagccact gcagtgttat 2760
cttaaaataa gaatattttg ttgagatatt ccagaatttg tttatatggc tggtaacatg 2820
taaaatctat atcagcaaaa gggtctacct ttaaaataag caataacaaa gaagaaaacc 2880
aaattattgt tcaaatttag gtttaaactt ttgaagcaaa ctttttttta tccttgtgca 2940
ctgcaggcct ggtactcaga ttttgctatg aggttaatga agtaccaagc tgtgcttgaa 3000
taatgatatg ttttctcaga ttttctgttg tacagtttaa tttagcagtc catatcacat 3060
tgcaaaagta gcaatgacct cataaaatac ctcttcaaaa tgcttaaatt catttcacac 3120
attaatttta tctcagtctt gaagccaatt cagtaggtgc attggaatca agcctggcta 3180
cctgcatgct gttccttttc ttttcttctt ttagccattt tgctaagaga cacagtcttc 3240
tcatcacttc gtttctccta ttttgtttta ctagttttaa gatcagagtt cactttcttt 3300
ggactctgcc tatattttct tacctgaact tttgcaagtt ttcaggtaaa cctcagctca 3360
ggactgctat ttagctcctc ttaagaagat taaaagagaa aaaaaaaggc ccttttaaaa 3420
atagtataca cttattttaa gtgaaaagca gagaatttta tttatagcta attttagcta 3480
tctgtaacca agatggatgc aaagaggcta gtgcctcaga gagaactgta cggggtttgt 3540
gactggaaaa agttacgttc ccattctaat taatgccctt tcttatttaa aaacaaaacc 3600
aaatgatatc taagtagttc tcagcaataa taataatgac gataatactt cttttccaca 3660
tctcattgtc actgacattt aatggtactg tatattactt aatttattga agattattat 3720
ttatgtctta ttaggacact atggttataa actgtgttta agcctacaat cattgatttt 3780
tttttgttat gtcacaatca gtatattttc tttggggtta cctctctgaa tattatgtaa 3840
acaatccaaa gaaatgattg tattaagatt tgtgaataaa tttttagaaa tctgattggc 3900
atattgagat atttaaggtt gaatgtttgt ccttaggata ggcctatgtg ctagcccaca 3960
aagaatattg tctcattagc ctgaatgtgc cataagactg accttttaaa atgttttgag 4020
ggatctgtgg atgcttcgtt aatttgttca gccacaattt attgagaaaa tattctgtgt 4080
caagcactgt gggttttaat atttttaaat caaacgctga ttacagataa tagtatttat 4140
ataaataatt gaaaaaaatt ttcttttggg aagagggaga aaatgaaata aatatcatta 4200
aagataactc aggagaatct tctttacaat tttacgttta gaatgtttaa ggttaagaaa 4260
gaaatagtca atatgcttgt ataaaacact gttcactgtt ttttttaaaa aaaaaacttg 4320
atttgttatt aacattgatc tgctgacaaa acctgggaat ttgggttgtg tatgcgaatg 4380
tttcagtgcc tcagacaaat gtgtatttaa cttatgtaaa agataagtct ggaaataaat 4440
gtctgtttat ttttgtacta tttaaaaatt gacagatctt ttctgaagat aaactttgat 4500
tgtttctata 4510
<210> 3
<211> 288
<212> PRT
<213> Homo sapiens
<223> HMOX1 – Номер доступа NP_002124.1
<400> 3
Met Glu Arg Pro Gln Pro Asp Ser Met Pro Gln Asp Leu Ser Glu Ala
1 5 10 15
Leu Lys Glu Ala Thr Lys Glu Val His Thr Gln Ala Glu Asn Ala Glu
20 25 30
Phe Met Arg Asn Phe Gln Lys Gly Gln Val Thr Arg Asp Gly Phe Lys
35 40 45
Leu Val Met Ala Ser Leu Tyr His Ile Tyr Val Ala Leu Glu Glu Glu
50 55 60
Ile Glu Arg Asn Lys Glu Ser Pro Val Phe Ala Pro Val Tyr Phe Pro
65 70 75 80
Glu Glu Leu His Arg Lys Ala Ala Leu Glu Gln Asp Leu Ala Phe Trp
85 90 95
Tyr Gly Pro Arg Trp Gln Glu Val Ile Pro Tyr Thr Pro Ala Met Gln
100 105 110
Arg Tyr Val Lys Arg Leu His Glu Val Gly Arg Thr Glu Pro Glu Leu
115 120 125
Leu Val Ala His Ala Tyr Thr Arg Tyr Leu Gly Asp Leu Ser Gly Gly
130 135 140
Gln Val Leu Lys Lys Ile Ala Gln Lys Ala Leu Asp Leu Pro Ser Ser
145 150 155 160
Gly Glu Gly Leu Ala Phe Phe Thr Phe Pro Asn Ile Ala Ser Ala Thr
165 170 175
Lys Phe Lys Gln Leu Tyr Arg Ser Arg Met Asn Ser Leu Glu Met Thr
180 185 190
Pro Ala Val Arg Gln Arg Val Ile Glu Glu Ala Lys Thr Ala Phe Leu
195 200 205
Leu Asn Ile Gln Leu Phe Glu Glu Leu Gln Glu Leu Leu Thr His Asp
210 215 220
Thr Lys Asp Gln Ser Pro Ser Arg Ala Pro Gly Leu Arg Gln Arg Ala
225 230 235 240
Ser Asn Lys Val Gln Asp Ser Ala Pro Val Glu Thr Pro Arg Gly Lys
245 250 255
Pro Pro Leu Asn Thr Arg Ser Gln Ala Pro Leu Leu Arg Trp Val Leu
260 265 270
Thr Leu Ser Phe Leu Val Ala Thr Val Ala Val Gly Leu Tyr Ala Met
275 280 285
<210> 4
<211> 1554
<212> ДНК
<213> Homo sapiens
<223> HMOX1 – Номер доступа NM_002133.3
<400> 4
aacgcctgcc tcctctcgag cgtcctcagc gcagccgccg cccgcggagc cagcacgaac 60
gagcccagca ccggccggat ggagcgtccg caacccgaca gcatgcccca ggatttgtca 120
gaggccctga aggaggccac caaggaggtg cacacccagg cagagaatgc tgagttcatg 180
aggaactttc agaagggcca ggtgacccga gacggcttca agctggtgat ggcctccctg 240
taccacatct atgtggccct ggaggaggag attgagcgca acaaggagag cccagtcttc 300
gcccctgtct acttcccaga agagctgcac cgcaaggctg ccctggagca ggacctggcc 360
ttctggtacg ggccccgctg gcaggaggtc atcccctaca caccagccat gcagcgctat 420
gtgaagcggc tccacgaggt ggggcgcaca gagcccgagc tgctggtggc ccacgcctac 480
acccgctacc tgggtgacct gtctgggggc caggtgctca aaaagattgc ccagaaagcc 540
ctggacctgc ccagctctgg cgagggcctg gccttcttca ccttccccaa cattgccagt 600
gccaccaagt tcaagcagct ctaccgctcc cgcatgaact ccctggagat gactcccgca 660
gtcaggcaga gggtgataga agaggccaag actgcgttcc tgctcaacat ccagctcttt 720
gaggagttgc aggagctgct gacccatgac accaaggacc agagcccctc acgggcacca 780
gggcttcgcc agcgggccag caacaaagtg caagattctg cccccgtgga gactcccaga 840
gggaagcccc cactcaacac ccgctcccag gctccgcttc tccgatgggt ccttacactc 900
agctttctgg tggcgacagt tgctgtaggg ctttatgcca tgtgaatgca ggcatgctgg 960
ctcccagggc catgaacttt gtccggtgga aggccttctt tctagagagg gaattctctt 1020
ggctggcttc cttaccgtgg gcactgaagg ctttcagggc ctccagccct ctcactgtgt 1080
ccctctctct ggaaaggagg aaggagccta tggcatcttc cccaacgaaa agcacatcca 1140
ggcaatggcc taaacttcag agggggcgaa gggatcagcc ctgcccttca gcatcctcag 1200
ttcctgcagc agagcctgga agacacccta atgtggcagc tgtctcaaac ctccaaaagc 1260
cctgagtttc aagtatcctt gttgacacgg ccatgaccac tttccccgtg ggccatggca 1320
atttttacac aaacctgaaa agatgttgtg tcttgtgttt ttgtcttatt tttgttggag 1380
ccactctgtt cctggctcag cctcaaatgc agtatttttg ttgtgttctg ttgtttttat 1440
agcagggttg gggtggtttt tgagccatgc gtgggtgggg agggaggtgt ttaacggcac 1500
tgtggccttg gtctaacttt tgtgtgaaat aataaacaac attgtctgat agta 1554
<210> 5
<211> 860
<212> PRT
<213> Homo sapiens
<223> LDLR – Номер доступа NP_000518.1
<400> 5
Met Gly Pro Trp Gly Trp Lys Leu Arg Trp Thr Val Ala Leu Leu Leu
1 5 10 15
Ala Ala Ala Gly Thr Ala Val Gly Asp Arg Cys Glu Arg Asn Glu Phe
20 25 30
Gln Cys Gln Asp Gly Lys Cys Ile Ser Tyr Lys Trp Val Cys Asp Gly
35 40 45
Ser Ala Glu Cys Gln Asp Gly Ser Asp Glu Ser Gln Glu Thr Cys Leu
50 55 60
Ser Val Thr Cys Lys Ser Gly Asp Phe Ser Cys Gly Gly Arg Val Asn
65 70 75 80
Arg Cys Ile Pro Gln Phe Trp Arg Cys Asp Gly Gln Val Asp Cys Asp
85 90 95
Asn Gly Ser Asp Glu Gln Gly Cys Pro Pro Lys Thr Cys Ser Gln Asp
100 105 110
Glu Phe Arg Cys His Asp Gly Lys Cys Ile Ser Arg Gln Phe Val Cys
115 120 125
Asp Ser Asp Arg Asp Cys Leu Asp Gly Ser Asp Glu Ala Ser Cys Pro
130 135 140
Val Leu Thr Cys Gly Pro Ala Ser Phe Gln Cys Asn Ser Ser Thr Cys
145 150 155 160
Ile Pro Gln Leu Trp Ala Cys Asp Asn Asp Pro Asp Cys Glu Asp Gly
165 170 175
Ser Asp Glu Trp Pro Gln Arg Cys Arg Gly Leu Tyr Val Phe Gln Gly
180 185 190
Asp Ser Ser Pro Cys Ser Ala Phe Glu Phe His Cys Leu Ser Gly Glu
195 200 205
Cys Ile His Ser Ser Trp Arg Cys Asp Gly Gly Pro Asp Cys Lys Asp
210 215 220
Lys Ser Asp Glu Glu Asn Cys Ala Val Ala Thr Cys Arg Pro Asp Glu
225 230 235 240
Phe Gln Cys Ser Asp Gly Asn Cys Ile His Gly Ser Arg Gln Cys Asp
245 250 255
Arg Glu Tyr Asp Cys Lys Asp Met Ser Asp Glu Val Gly Cys Val Asn
260 265 270
Val Thr Leu Cys Glu Gly Pro Asn Lys Phe Lys Cys His Ser Gly Glu
275 280 285
Cys Ile Thr Leu Asp Lys Val Cys Asn Met Ala Arg Asp Cys Arg Asp
290 295 300
Trp Ser Asp Glu Pro Ile Lys Glu Cys Gly Thr Asn Glu Cys Leu Asp
305 310 315 320
Asn Asn Gly Gly Cys Ser His Val Cys Asn Asp Leu Lys Ile Gly Tyr
325 330 335
Glu Cys Leu Cys Pro Asp Gly Phe Gln Leu Val Ala Gln Arg Arg Cys
340 345 350
Glu Asp Ile Asp Glu Cys Gln Asp Pro Asp Thr Cys Ser Gln Leu Cys
355 360 365
Val Asn Leu Glu Gly Gly Tyr Lys Cys Gln Cys Glu Glu Gly Phe Gln
370 375 380
Leu Asp Pro His Thr Lys Ala Cys Lys Ala Val Gly Ser Ile Ala Tyr
385 390 395 400
Leu Phe Phe Thr Asn Arg His Glu Val Arg Lys Met Thr Leu Asp Arg
405 410 415
Ser Glu Tyr Thr Ser Leu Ile Pro Asn Leu Arg Asn Val Val Ala Leu
420 425 430
Asp Thr Glu Val Ala Ser Asn Arg Ile Tyr Trp Ser Asp Leu Ser Gln
435 440 445
Arg Met Ile Cys Ser Thr Gln Leu Asp Arg Ala His Gly Val Ser Ser
450 455 460
Tyr Asp Thr Val Ile Ser Arg Asp Ile Gln Ala Pro Asp Gly Leu Ala
465 470 475 480
Val Asp Trp Ile His Ser Asn Ile Tyr Trp Thr Asp Ser Val Leu Gly
485 490 495
Thr Val Ser Val Ala Asp Thr Lys Gly Val Lys Arg Lys Thr Leu Phe
500 505 510
Arg Glu Asn Gly Ser Lys Pro Arg Ala Ile Val Val Asp Pro Val His
515 520 525
Gly Phe Met Tyr Trp Thr Asp Trp Gly Thr Pro Ala Lys Ile Lys Lys
530 535 540
Gly Gly Leu Asn Gly Val Asp Ile Tyr Ser Leu Val Thr Glu Asn Ile
545 550 555 560
Gln Trp Pro Asn Gly Ile Thr Leu Asp Leu Leu Ser Gly Arg Leu Tyr
565 570 575
Trp Val Asp Ser Lys Leu His Ser Ile Ser Ser Ile Asp Val Asn Gly
580 585 590
Gly Asn Arg Lys Thr Ile Leu Glu Asp Glu Lys Arg Leu Ala His Pro
595 600 605
Phe Ser Leu Ala Val Phe Glu Asp Lys Val Phe Trp Thr Asp Ile Ile
610 615 620
Asn Glu Ala Ile Phe Ser Ala Asn Arg Leu Thr Gly Ser Asp Val Asn
625 630 635 640
Leu Leu Ala Glu Asn Leu Leu Ser Pro Glu Asp Met Val Leu Phe His
645 650 655
Asn Leu Thr Gln Pro Arg Gly Val Asn Trp Cys Glu Arg Thr Thr Leu
660 665 670
Ser Asn Gly Gly Cys Gln Tyr Leu Cys Leu Pro Ala Pro Gln Ile Asn
675 680 685
Pro His Ser Pro Lys Phe Thr Cys Ala Cys Pro Asp Gly Met Leu Leu
690 695 700
Ala Arg Asp Met Arg Ser Cys Leu Thr Glu Ala Glu Ala Ala Val Ala
705 710 715 720
Thr Gln Glu Thr Ser Thr Val Arg Leu Lys Val Ser Ser Thr Ala Val
725 730 735
Arg Thr Gln His Thr Thr Thr Arg Pro Val Pro Asp Thr Ser Arg Leu
740 745 750
Pro Gly Ala Thr Pro Gly Leu Thr Thr Val Glu Ile Val Thr Met Ser
755 760 765
His Gln Ala Leu Gly Asp Val Ala Gly Arg Gly Asn Glu Lys Lys Pro
770 775 780
Ser Ser Val Arg Ala Leu Ser Ile Val Leu Pro Ile Val Leu Leu Val
785 790 795 800
Phe Leu Cys Leu Gly Val Phe Leu Leu Trp Lys Asn Trp Arg Leu Lys
805 810 815
Asn Ile Asn Ser Ile Asn Phe Asp Asn Pro Val Tyr Gln Lys Thr Thr
820 825 830
Glu Asp Glu Val His Ile Cys His Asn Gln Asp Gly Tyr Ser Tyr Pro
835 840 845
Ser Arg Gln Met Val Ser Leu Glu Asp Asp Val Ala
850 855 860
<210> 6
<211> 5292
<212> ДНК
<213> Homo sapiens
<223> LDLR – Номер доступа NM_000527.4
<400> 6
ctcttgcagt gaggtgaaga catttgaaaa tcaccccact gcaaactcct ccccctgcta 60
gaaacctcac attgaaatgc tgtaaatgac gtgggccccg agtgcaatcg cgggaagcca 120
gggtttccag ctaggacaca gcaggtcgtg atccgggtcg ggacactgcc tggcagaggc 180
tgcgagcatg gggccctggg gctggaaatt gcgctggacc gtcgccttgc tcctcgccgc 240
ggcggggact gcagtgggcg acagatgcga aagaaacgag ttccagtgcc aagacgggaa 300
atgcatctcc tacaagtggg tctgcgatgg cagcgctgag tgccaggatg gctctgatga 360
gtcccaggag acgtgcttgt ctgtcacctg caaatccggg gacttcagct gtgggggccg 420
tgtcaaccgc tgcattcctc agttctggag gtgcgatggc caagtggact gcgacaacgg 480
ctcagacgag caaggctgtc cccccaagac gtgctcccag gacgagtttc gctgccacga 540
tgggaagtgc atctctcggc agttcgtctg tgactcagac cgggactgct tggacggctc 600
agacgaggcc tcctgcccgg tgctcacctg tggtcccgcc agcttccagt gcaacagctc 660
cacctgcatc ccccagctgt gggcctgcga caacgacccc gactgcgaag atggctcgga 720
tgagtggccg cagcgctgta ggggtcttta cgtgttccaa ggggacagta gcccctgctc 780
ggccttcgag ttccactgcc taagtggcga gtgcatccac tccagctggc gctgtgatgg 840
tggccccgac tgcaaggaca aatctgacga ggaaaactgc gctgtggcca cctgtcgccc 900
tgacgaattc cagtgctctg atggaaactg catccatggc agccggcagt gtgaccggga 960
atatgactgc aaggacatga gcgatgaagt tggctgcgtt aatgtgacac tctgcgaggg 1020
acccaacaag ttcaagtgtc acagcggcga atgcatcacc ctggacaaag tctgcaacat 1080
ggctagagac tgccgggact ggtcagatga acccatcaaa gagtgcggga ccaacgaatg 1140
cttggacaac aacggcggct gttcccacgt ctgcaatgac cttaagatcg gctacgagtg 1200
cctgtgcccc gacggcttcc agctggtggc ccagcgaaga tgcgaagata tcgatgagtg 1260
tcaggatccc gacacctgca gccagctctg cgtgaacctg gagggtggct acaagtgcca 1320
gtgtgaggaa ggcttccagc tggaccccca cacgaaggcc tgcaaggctg tgggctccat 1380
cgcctacctc ttcttcacca accggcacga ggtcaggaag atgacgctgg accggagcga 1440
gtacaccagc ctcatcccca acctgaggaa cgtggtcgct ctggacacgg aggtggccag 1500
caatagaatc tactggtctg acctgtccca gagaatgatc tgcagcaccc agcttgacag 1560
agcccacggc gtctcttcct atgacaccgt catcagcaga gacatccagg cccccgacgg 1620
gctggctgtg gactggatcc acagcaacat ctactggacc gactctgtcc tgggcactgt 1680
ctctgttgcg gataccaagg gcgtgaagag gaaaacgtta ttcagggaga acggctccaa 1740
gccaagggcc atcgtggtgg atcctgttca tggcttcatg tactggactg actggggaac 1800
tcccgccaag atcaagaaag ggggcctgaa tggtgtggac atctactcgc tggtgactga 1860
aaacattcag tggcccaatg gcatcaccct agatctcctc agtggccgcc tctactgggt 1920
tgactccaaa cttcactcca tctcaagcat cgatgtcaac gggggcaacc ggaagaccat 1980
cttggaggat gaaaagaggc tggcccaccc cttctccttg gccgtctttg aggacaaagt 2040
attttggaca gatatcatca acgaagccat tttcagtgcc aaccgcctca caggttccga 2100
tgtcaacttg ttggctgaaa acctactgtc cccagaggat atggttctct tccacaacct 2160
cacccagcca agaggagtga actggtgtga gaggaccacc ctgagcaatg gcggctgcca 2220
gtatctgtgc ctccctgccc cgcagatcaa cccccactcg cccaagttta cctgcgcctg 2280
cccggacggc atgctgctgg ccagggacat gaggagctgc ctcacagagg ctgaggctgc 2340
agtggccacc caggagacat ccaccgtcag gctaaaggtc agctccacag ccgtaaggac 2400
acagcacaca accacccgac ctgttcccga cacctcccgg ctgcctgggg ccacccctgg 2460
gctcaccacg gtggagatag tgacaatgtc tcaccaagct ctgggcgacg ttgctggcag 2520
aggaaatgag aagaagccca gtagcgtgag ggctctgtcc attgtcctcc ccatcgtgct 2580
cctcgtcttc ctttgcctgg gggtcttcct tctatggaag aactggcggc ttaagaacat 2640
caacagcatc aactttgaca accccgtcta tcagaagacc acagaggatg aggtccacat 2700
ttgccacaac caggacggct acagctaccc ctcgagacag atggtcagtc tggaggatga 2760
cgtggcgtga acatctgcct ggagtcccgt ccctgcccag aacccttcct gagacctcgc 2820
cggccttgtt ttattcaaag acagagaaga ccaaagcatt gcctgccaga gctttgtttt 2880
atatatttat tcatctggga ggcagaacag gcttcggaca gtgcccatgc aatggcttgg 2940
gttgggattt tggtttcttc ctttcctcgt gaaggataag agaaacaggc ccggggggac 3000
caggatgaca cctccatttc tctccaggaa gttttgagtt tctctccacc gtgacacaat 3060
cctcaaacat ggaagatgaa aggggagggg atgtcaggcc cagagaagca agtggctttc 3120
aacacacaac agcagatggc accaacggga ccccctggcc ctgcctcatc caccaatctc 3180
taagccaaac ccctaaactc aggagtcaac gtgtttacct cttctatgca agccttgcta 3240
gacagccagg ttagcctttg ccctgtcacc cccgaatcat gacccaccca gtgtctttcg 3300
aggtgggttt gtaccttcct taagccagga aagggattca tggcgtcgga aatgatctgg 3360
ctgaatccgt ggtggcaccg agaccaaact cattcaccaa atgatgccac ttcccagagg 3420
cagagcctga gtcactggtc acccttaata tttattaagt gcctgagaca cccggttacc 3480
ttggccgtga ggacacgtgg cctgcaccca ggtgtggctg tcaggacacc agcctggtgc 3540
ccatcctccc gacccctacc cacttccatt cccgtggtct ccttgcactt tctcagttca 3600
gagttgtaca ctgtgtacat ttggcatttg tgttattatt ttgcactgtt ttctgtcgtg 3660
tgtgttggga tgggatccca ggccagggaa agcccgtgtc aatgaatgcc ggggacagag 3720
aggggcaggt tgaccgggac ttcaaagccg tgatcgtgaa tatcgagaac tgccattgtc 3780
gtctttatgt ccgcccacct agtgcttcca cttctatgca aatgcctcca agccattcac 3840
ttccccaatc ttgtcgttga tgggtatgtg tttaaaacat gcacggtgag gccgggcgca 3900
gtggctcacg cctgtaatcc cagcactttg ggaggccgag gcgggtggat catgaggtca 3960
ggagatcgag accatcctgg ctaacacgtg aaaccccgtc tctactaaaa atacaaaaaa 4020
ttagccgggc gtggtggcgg gcacctgtag tcccagctac tcgggaggct gaggcaggag 4080
aatggtgtga acccgggaag cggagcttgc agtgagccga gattgcgcca ctgcagtccg 4140
cagtctggcc tgggcgacag agcgagactc cgtctcaaaa aaaaaaaaca aaaaaaaacc 4200
atgcatggtg catcagcagc ccatggcctc tggccaggca tggcgaggct gaggtgggag 4260
gatggtttga gctcaggcat ttgaggctgt cgtgagctat gattatgcca ctgctttcca 4320
gcctgggcaa catagtaaga ccccatctct taaaaaatga atttggccag acacaggtgc 4380
ctcacgcctg taatcccagc actttgggag gctgagctgg atcacttgag ttcaggagtt 4440
ggagaccagg cctgagcaac aaagcgagat cccatctcta caaaaaccaa aaagttaaaa 4500
atcagctggg tacggtggca cgtgcctgtg atcccagcta cttgggaggc tgaggcagga 4560
ggatcgcctg agcccaggag gtggaggttg cagtgagcca tgatcgagcc actgcactcc 4620
agcctgggca acagatgaag accctatttc agaaatacaa ctataaaaaa ataaataaat 4680
cctccagtct ggatcgtttg acgggacttc aggttctttc tgaaatcgcc gtgttactgt 4740
tgcactgatg tccggagaga cagtgacagc ctccgtcaga ctcccgcgtg aagatgtcac 4800
aagggattgg caattgtccc cagggacaaa acactgtgtc ccccccagtg cagggaaccg 4860
tgataagcct ttctggtttc ggagcacgta aatgcgtccc tgtacagata gtggggattt 4920
tttgttatgt ttgcactttg tatattggtt gaaactgtta tcacttatat atatatatat 4980
acacacatat atataaaatc tatttatttt tgcaaaccct ggttgctgta tttgttcagt 5040
gactattctc ggggccctgt gtagggggtt attgcctctg aaatgcctct tctttatgta 5100
caaagattat ttgcacgaac tggactgtgt gcaacgcttt ttgggagaat gatgtccccg 5160
ttgtatgtat gagtggcttc tgggagatgg gtgtcacttt ttaaaccact gtatagaagg 5220
tttttgtagc ctgaatgtct tactgtgatc aattaaattt cttaaatgaa ccaatttgtc 5280
taaaaaaaaa aa 5292
<210> 7
<211> 641
<212> PRT
<213> Homo sapiens
<223> HSPA1B – Номер доступа NP_005337.2
<400> 7
Met Ala Lys Ala Ala Ala Ile Gly Ile Asp Leu Gly Thr Thr Tyr Ser
1 5 10 15
Cys Val Gly Val Phe Gln His Gly Lys Val Glu Ile Ile Ala Asn Asp
20 25 30
Gln Gly Asn Arg Thr Thr Pro Ser Tyr Val Ala Phe Thr Asp Thr Glu
35 40 45
Arg Leu Ile Gly Asp Ala Ala Lys Asn Gln Val Ala Leu Asn Pro Gln
50 55 60
Asn Thr Val Phe Asp Ala Lys Arg Leu Ile Gly Arg Lys Phe Gly Asp
65 70 75 80
Pro Val Val Gln Ser Asp Met Lys His Trp Pro Phe Gln Val Ile Asn
85 90 95
Asp Gly Asp Lys Pro Lys Val Gln Val Ser Tyr Lys Gly Glu Thr Lys
100 105 110
Ala Phe Tyr Pro Glu Glu Ile Ser Ser Met Val Leu Thr Lys Met Lys
115 120 125
Glu Ile Ala Glu Ala Tyr Leu Gly Tyr Pro Val Thr Asn Ala Val Ile
130 135 140
Thr Val Pro Ala Tyr Phe Asn Asp Ser Gln Arg Gln Ala Thr Lys Asp
145 150 155 160
Ala Gly Val Ile Ala Gly Leu Asn Val Leu Arg Ile Ile Asn Glu Pro
165 170 175
Thr Ala Ala Ala Ile Ala Tyr Gly Leu Asp Arg Thr Gly Lys Gly Glu
180 185 190
Arg Asn Val Leu Ile Phe Asp Leu Gly Gly Gly Thr Phe Asp Val Ser
195 200 205
Ile Leu Thr Ile Asp Asp Gly Ile Phe Glu Val Lys Ala Thr Ala Gly
210 215 220
Asp Thr His Leu Gly Gly Glu Asp Phe Asp Asn Arg Leu Val Asn His
225 230 235 240
Phe Val Glu Glu Phe Lys Arg Lys His Lys Lys Asp Ile Ser Gln Asn
245 250 255
Lys Arg Ala Val Arg Arg Leu Arg Thr Ala Cys Glu Arg Ala Lys Arg
260 265 270
Thr Leu Ser Ser Ser Thr Gln Ala Ser Leu Glu Ile Asp Ser Leu Phe
275 280 285
Glu Gly Ile Asp Phe Tyr Thr Ser Ile Thr Arg Ala Arg Phe Glu Glu
290 295 300
Leu Cys Ser Asp Leu Phe Arg Ser Thr Leu Glu Pro Val Glu Lys Ala
305 310 315 320
Leu Arg Asp Ala Lys Leu Asp Lys Ala Gln Ile His Asp Leu Val Leu
325 330 335
Val Gly Gly Ser Thr Arg Ile Pro Lys Val Gln Lys Leu Leu Gln Asp
340 345 350
Phe Phe Asn Gly Arg Asp Leu Asn Lys Ser Ile Asn Pro Asp Glu Ala
355 360 365
Val Ala Tyr Gly Ala Ala Val Gln Ala Ala Ile Leu Met Gly Asp Lys
370 375 380
Ser Glu Asn Val Gln Asp Leu Leu Leu Leu Asp Val Ala Pro Leu Ser
385 390 395 400
Leu Gly Leu Glu Thr Ala Gly Gly Val Met Thr Ala Leu Ile Lys Arg
405 410 415
Asn Ser Thr Ile Pro Thr Lys Gln Thr Gln Ile Phe Thr Thr Tyr Ser
420 425 430
Asp Asn Gln Pro Gly Val Leu Ile Gln Val Tyr Glu Gly Glu Arg Ala
435 440 445
Met Thr Lys Asp Asn Asn Leu Leu Gly Arg Phe Glu Leu Ser Gly Ile
450 455 460
Pro Pro Ala Pro Arg Gly Val Pro Gln Ile Glu Val Thr Phe Asp Ile
465 470 475 480
Asp Ala Asn Gly Ile Leu Asn Val Thr Ala Thr Asp Lys Ser Thr Gly
485 490 495
Lys Ala Asn Lys Ile Thr Ile Thr Asn Asp Lys Gly Arg Leu Ser Lys
500 505 510
Glu Glu Ile Glu Arg Met Val Gln Glu Ala Glu Lys Tyr Lys Ala Glu
515 520 525
Asp Glu Val Gln Arg Glu Arg Val Ser Ala Lys Asn Ala Leu Glu Ser
530 535 540
Tyr Ala Phe Asn Met Lys Ser Ala Val Glu Asp Glu Gly Leu Lys Gly
545 550 555 560
Lys Ile Ser Glu Ala Asp Lys Lys Lys Val Leu Asp Lys Cys Gln Glu
565 570 575
Val Ile Ser Trp Leu Asp Ala Asn Thr Leu Ala Glu Lys Asp Glu Phe
580 585 590
Glu His Lys Arg Lys Glu Leu Glu Gln Val Cys Asn Pro Ile Ile Ser
595 600 605
Gly Leu Tyr Gln Gly Ala Gly Gly Pro Gly Pro Gly Gly Phe Gly Ala
610 615 620
Gln Gly Pro Lys Gly Gly Ser Gly Ser Gly Pro Thr Ile Glu Glu Val
625 630 635 640
Asp
<210> 8
<211> 2517
<212> ДНК
<213> Homo sapiens
<223> HSPA1B – Номер доступа NM_005346.5
<400> 8
aaacggccag cctgaggagc tgctgcgagg gtccgcttcg tctttcgaga gtgactcccg 60
cggtcccaag gctttccaga gcgaacctgt gcggctgcag gcaccggcgt gttgagtttc 120
cggcgttccg aaggactgag ctcttgtcgc ggatcccgtc cgccgtttcc agcccccagt 180
ctcagagcgg agcccacaga gcagggcacc ggcatggcca aagccgcggc gatcggcatc 240
gacctgggca ccacctactc ctgcgtgggg gtgttccaac acggcaaggt ggagatcatc 300
gccaacgacc agggcaaccg caccaccccc agctacgtgg ccttcacgga caccgagcgg 360
ctcatcgggg atgcggccaa gaaccaggtg gcgctgaacc cgcagaacac cgtgtttgac 420
gcgaagcggc tgatcggccg caagttcggc gacccggtgg tgcagtcgga catgaagcac 480
tggcctttcc aggtgatcaa cgacggagac aagcccaagg tgcaggtgag ctacaagggg 540
gagaccaagg cattctaccc cgaggagatc tcgtccatgg tgctgaccaa gatgaaggag 600
atcgccgagg cgtacctggg ctacccggtg accaacgcgg tgatcaccgt gccggcctac 660
ttcaacgact cgcagcgcca ggccaccaag gatgcgggtg tgatcgcggg gctcaacgtg 720
ctgcggatca tcaacgagcc cacggccgcc gccatcgcct acggcctgga cagaacgggc 780
aagggggagc gcaacgtgct catctttgac ctgggcgggg gcaccttcga cgtgtccatc 840
ctgacgatcg acgacggcat cttcgaggtg aaggccacgg ccggggacac ccacctgggt 900
ggggaggact ttgacaacag gctggtgaac cacttcgtgg aggagttcaa gagaaaacac 960
aagaaggaca tcagccagaa caagcgagcc gtgaggcggc tgcgcaccgc ctgcgagagg 1020
gccaagagga ccctgtcgtc cagcacccag gccagcctgg agatcgactc cctgtttgag 1080
ggcatcgact tctacacgtc catcaccagg gcgaggttcg aggagctgtg ctccgacctg 1140
ttccgaagca ccctggagcc cgtggagaag gctctgcgcg acgccaagct ggacaaggcc 1200
cagattcacg acctggtcct ggtcgggggc tccacccgca tccccaaggt gcagaagctg 1260
ctgcaggact tcttcaacgg gcgcgacctg aacaagagca tcaaccccga cgaggctgtg 1320
gcctacgggg cggcggtgca ggcggccatc ctgatggggg acaagtccga gaacgtgcag 1380
gacctgctgc tgctggacgt ggctcccctg tcgctggggc tggagacggc cggaggcgtg 1440
atgactgccc tgatcaagcg caactccacc atccccacca agcagacgca gatcttcacc 1500
acctactccg acaaccaacc cggggtgctg atccaggtgt acgagggcga gagggccatg 1560
acgaaagaca acaatctgtt ggggcgcttc gagctgagcg gcatccctcc ggcccccagg 1620
ggcgtgcccc agatcgaggt gaccttcgac atcgatgcca acggcatcct gaacgtcacg 1680
gccacggaca agagcaccgg caaggccaac aagatcacca tcaccaacga caagggccgc 1740
ctgagcaagg aggagatcga gcgcatggtg caggaggcgg agaagtacaa agcggaggac 1800
gaggtgcagc gcgagagggt gtcagccaag aacgccctgg agtcctacgc cttcaacatg 1860
aagagcgccg tggaggatga ggggctcaag ggcaagatca gcgaggcgga caagaagaag 1920
gttctggaca agtgtcaaga ggtcatctcg tggctggacg ccaacacctt ggccgagaag 1980
gacgagtttg agcacaagag gaaggagctg gagcaggtgt gtaaccccat catcagcgga 2040
ctgtaccagg gtgccggtgg tcccgggcct ggcggcttcg gggctcaggg tcccaaggga 2100
gggtctgggt caggccctac cattgaggag gtggattagg ggcctttgtt ctttagtatg 2160
tttgtctttg aggtggactg ttgggactca aggactttgc tgctgttttc ctatgtcatt 2220
tctgcttcag ctctttgctg cttcacttct ttgtaaagtt gtaacctgat ggtaattagc 2280
tggcttcatt atttttgtag tacaaccgat atgttcatta gaattctttg catttaatgt 2340
tgatactgta agggtgtttc gttcccttta aatgaatcaa cactgccacc ttctgtacga 2400
gtttgtttgt tttttttttt tttttttttt tttgcttggc gaaaacacta caaaggctgg 2460
gaatgtatgt ttttataatt tgtttattta aatatgaaaa ataaaatgtt aaacttt 2517
<210> 9
<211> 103
<212> PRT
<213> Homo sapiens
<223> G0S2 – Номер доступа NP_056529.1
<400> 9
Met Glu Thr Val Gln Glu Leu Ile Pro Leu Ala Lys Glu Met Met Ala
1 5 10 15
Gln Lys Arg Lys Gly Lys Met Val Lys Leu Tyr Val Leu Gly Ser Val
20 25 30
Leu Ala Leu Phe Gly Val Val Leu Gly Leu Met Glu Thr Val Cys Ser
35 40 45
Pro Phe Thr Ala Ala Arg Arg Leu Arg Asp Gln Glu Ala Ala Val Ala
50 55 60
Glu Leu Gln Ala Ala Leu Glu Arg Gln Ala Leu Gln Lys Gln Ala Leu
65 70 75 80
Gln Glu Lys Gly Lys Gln Gln Asp Thr Val Leu Gly Gly Arg Ala Leu
85 90 95
Ser Asn Arg Gln His Ala Ser
100
<210> 10
<211> 876
<212> ДНК
<213> Homo sapiens
<223> G0S2 – Номер доступа NM_015714.4
<400> 10
tgccagcggc ggagtctcca actgggagag ctgcagctgc cgagaggagg agaacgctga 60
ggtcggtcgg accaacggac gcgctgaccg ctgccaactg cagctcgcgc tgcctcctgc 120
tcgcgccgtg ccactaaggt cattcccgcc tccgagagcc cagagccgag atggaaacgg 180
tccaggagct gatccccctg gccaaggaga tgatggccca gaagcgcaag gggaagatgg 240
tgaagctgta cgtgctgggc agcgtgctgg ccctcttcgg cgtggtgctc ggcctgatgg 300
agactgtgtg cagccccttc acggccgcca gacgtctgcg ggaccaggag gcagccgtgg 360
cggagctgca ggccgccctg gagcgacagg ctctccagaa gcaagccctg caggagaaag 420
gcaagcagca ggacacggtc ctcggcggcc gggccctgtc caaccggcag cacgcctcct 480
aggaactgtg ggagaccagc ggagtgggag ggagacgcag tagacagaga cagaccgaga 540
gaggaatgga gagacagagg gggcgcgcgc acaggagcct gactccgctg ggagagtgca 600
ggagcacgtg ctgtttttta tttggactta acttcagaga aaccgctgac atctagaact 660
gacctaccac aagcatccac caaaggagtt tgggattgag ttttgctgct gtgcagcact 720
gcattgtcat gacatttcca acactgtgtg aattatctaa atgcgtctac cattttgcac 780
tagggaggaa ggataaatgc tttttatgtt attattatta attattacaa tgaccaccat 840
tttgcatttt gaaataaaaa aactttttat accata 876
<210> 11
<211> 575
<212> PRT
<213> Homo sapiens
<223> BAG3 – Номер доступа NP_004272.2
<400> 11
Met Ser Ala Ala Thr His Ser Pro Met Met Gln Val Ala Ser Gly Asn
1 5 10 15
Gly Asp Arg Asp Pro Leu Pro Pro Gly Trp Glu Ile Lys Ile Asp Pro
20 25 30
Gln Thr Gly Trp Pro Phe Phe Val Asp His Asn Ser Arg Thr Thr Thr
35 40 45
Trp Asn Asp Pro Arg Val Pro Ser Glu Gly Pro Lys Glu Thr Pro Ser
50 55 60
Ser Ala Asn Gly Pro Ser Arg Glu Gly Ser Arg Leu Pro Pro Ala Arg
65 70 75 80
Glu Gly His Pro Val Tyr Pro Gln Leu Arg Pro Gly Tyr Ile Pro Ile
85 90 95
Pro Val Leu His Glu Gly Ala Glu Asn Arg Gln Val His Pro Phe His
100 105 110
Val Tyr Pro Gln Pro Gly Met Gln Arg Phe Arg Thr Glu Ala Ala Ala
115 120 125
Ala Ala Pro Gln Arg Ser Gln Ser Pro Leu Arg Gly Met Pro Glu Thr
130 135 140
Thr Gln Pro Asp Lys Gln Cys Gly Gln Val Ala Ala Ala Ala Ala Ala
145 150 155 160
Gln Pro Pro Ala Ser His Gly Pro Glu Arg Ser Gln Ser Pro Ala Ala
165 170 175
Ser Asp Cys Ser Ser Ser Ser Ser Ser Ala Ser Leu Pro Ser Ser Gly
180 185 190
Arg Ser Ser Leu Gly Ser His Gln Leu Pro Arg Gly Tyr Ile Ser Ile
195 200 205
Pro Val Ile His Glu Gln Asn Val Thr Arg Pro Ala Ala Gln Pro Ser
210 215 220
Phe His Gln Ala Gln Lys Thr His Tyr Pro Ala Gln Gln Gly Glu Tyr
225 230 235 240
Gln Thr His Gln Pro Val Tyr His Lys Ile Gln Gly Asp Asp Trp Glu
245 250 255
Pro Arg Pro Leu Arg Ala Ala Ser Pro Phe Arg Ser Ser Val Gln Gly
260 265 270
Ala Ser Ser Arg Glu Gly Ser Pro Ala Arg Ser Ser Thr Pro Leu His
275 280 285
Ser Pro Ser Pro Ile Arg Val His Thr Val Val Asp Arg Pro Gln Gln
290 295 300
Pro Met Thr His Arg Glu Thr Ala Pro Val Ser Gln Pro Glu Asn Lys
305 310 315 320
Pro Glu Ser Lys Pro Gly Pro Val Gly Pro Glu Leu Pro Pro Gly His
325 330 335
Ile Pro Ile Gln Val Ile Arg Lys Glu Val Asp Ser Lys Pro Val Ser
340 345 350
Gln Lys Pro Pro Pro Pro Ser Glu Lys Val Glu Val Lys Val Pro Pro
355 360 365
Ala Pro Val Pro Cys Pro Pro Pro Ser Pro Gly Pro Ser Ala Val Pro
370 375 380
Ser Ser Pro Lys Ser Val Ala Thr Glu Glu Arg Ala Ala Pro Ser Thr
385 390 395 400
Ala Pro Ala Glu Ala Thr Pro Pro Lys Pro Gly Glu Ala Glu Ala Pro
405 410 415
Pro Lys His Pro Gly Val Leu Lys Val Glu Ala Ile Leu Glu Lys Val
420 425 430
Gln Gly Leu Glu Gln Ala Val Asp Asn Phe Glu Gly Lys Lys Thr Asp
435 440 445
Lys Lys Tyr Leu Met Ile Glu Glu Tyr Leu Thr Lys Glu Leu Leu Ala
450 455 460
Leu Asp Ser Val Asp Pro Glu Gly Arg Ala Asp Val Arg Gln Ala Arg
465 470 475 480
Arg Asp Gly Val Arg Lys Val Gln Thr Ile Leu Glu Lys Leu Glu Gln
485 490 495
Lys Ala Ile Asp Val Pro Gly Gln Val Gln Val Tyr Glu Leu Gln Pro
500 505 510
Ser Asn Leu Glu Ala Asp Gln Pro Leu Gln Ala Ile Met Glu Met Gly
515 520 525
Ala Val Ala Ala Asp Lys Gly Lys Lys Asn Ala Gly Asn Ala Glu Asp
530 535 540
Pro His Thr Glu Thr Gln Gln Pro Glu Ala Thr Ala Ala Ala Thr Ser
545 550 555 560
Asn Pro Ser Ser Met Thr Asp Thr Pro Gly Asn Pro Ala Ala Pro
565 570 575
<210> 12
<211> 2608
<212> ДНК
<213> Homo sapiens
<223> BAG3 – Номер доступа NM_004281.3
<400> 12
gcggagctcc gcatccaacc ccgggccgcg gccaacttct ctggactgga ccagaagttt 60
ctagccggcc agttgctacc tccctttatc tcctccttcc cctctggcag cgaggaggct 120
atttccagac acttccaccc ctctctggcc acgtcacccc cgcctttaat tcataaaggt 180
gcccggcgcc ggcttcccgg acacgtcggc ggcggagagg ggcccacggc ggcggcccgg 240
ccagagactc ggcgcccgga gccagcgccc cgcacccgcg ccccagcggg cagaccccaa 300
cccagcatga gcgccgccac ccactcgccc atgatgcagg tggcgtccgg caacggtgac 360
cgcgaccctt tgccccccgg atgggagatc aagatcgacc cgcagaccgg ctggcccttc 420
ttcgtggacc acaacagccg caccactacg tggaacgacc cgcgcgtgcc ctctgagggc 480
cccaaggaga ctccatcctc tgccaatggc ccttcccggg agggctctag gctgccgcct 540
gctagggaag gccaccctgt gtacccccag ctccgaccag gctacattcc cattcctgtg 600
ctccatgaag gcgctgagaa ccggcaggtg caccctttcc atgtctatcc ccagcctggg 660
atgcagcgat tccgaactga ggcggcagca gcggctcctc agaggtccca gtcacctctg 720
cggggcatgc cagaaaccac tcagccagat aaacagtgtg gacaggtggc agcggcggcg 780
gcagcccagc ccccagcctc ccacggacct gagcggtccc agtctccagc tgcctctgac 840
tgctcatcct catcctcctc ggccagcctg ccttcctccg gcaggagcag cctgggcagt 900
caccagctcc cgcgggggta catctccatt ccggtgatac acgagcagaa cgttacccgg 960
ccagcagccc agccctcctt ccaccaagcc cagaagacgc actacccagc gcagcagggg 1020
gagtaccaga cccaccagcc tgtgtaccac aagatccagg gggatgactg ggagccccgg 1080
cccctgcggg cggcatcccc gttcaggtca tctgtccagg gtgcatcgag ccgggagggc 1140
tcaccagcca ggagcagcac gccactccac tccccctcgc ccatccgtgt gcacaccgtg 1200
gtcgacaggc ctcagcagcc catgacccat cgagaaactg cacctgtttc ccagcctgaa 1260
aacaaaccag aaagtaagcc aggcccagtt ggaccagaac tccctcctgg acacatccca 1320
attcaagtga tccgcaaaga ggtggattct aaacctgttt cccagaagcc cccacctccc 1380
tctgagaagg tagaggtgaa agttccccct gctccagttc cttgtcctcc tcccagccct 1440
ggcccttctg ctgtcccctc ttcccccaag agtgtggcta cagaagagag ggcagccccc 1500
agcactgccc ctgcagaagc tacacctcca aaaccaggag aagccgaggc tcccccaaaa 1560
catccaggag tgctgaaagt ggaagccatc ctggagaagg tacaggggct ggagcaggct 1620
gtagacaact ttgaaggcaa gaagactgac aaaaagtacc tgatgatcga agagtatttg 1680
accaaagagc tgctggccct ggattcagtg gaccccgagg gacgagccga tgtgcgtcag 1740
gccaggagag acggtgtcag gaaggttcag accatcttgg aaaaacttga acagaaagcc 1800
attgatgtcc caggtcaagt ccaggtctat gaactccagc ccagcaacct tgaagcagat 1860
cagccactgc aggcaatcat ggagatgggt gccgtggcag cagacaaggg caagaaaaat 1920
gctggaaatg cagaagatcc ccacacagaa acccagcagc cagaagccac agcagcagcg 1980
acttcaaacc ccagcagcat gacagacacc cctggtaacc cagcagcacc gtagcctctg 2040
ccctgtaaaa atcagactcg gaaccgatgt gtgctttagg gaattttaag ttgcatgcat 2100
ttcagagact ttaagtcagt tggtttttat tagctgcttg gtatgcagta acttgggtgg 2160
aggcaaaaca ctaataaaag ggctaaaaag gaaaatgatg cttttcttct atattcttac 2220
tctgtacaaa taaagaagtt gcttgttgtt tgagaagttt aaccccgttg cttgttgttc 2280
tgcagccctg tctacttggg cacccccacc acctgttagc tgtggttgtg cactgtcttt 2340
tgtagctctg gactggaggg gtagatgggg agtcaattac ccatcacata aatatgaaac 2400
atttatcaga aatgttgcca ttttaatgag atgattttct tcatctcata attaaaatac 2460
ctgactttag agagagtaaa atgtgccagg agccatagga atatctgtat gttggatgac 2520
tttaatgcta cattttaaaa aaagaaaata aagtaataat ataactcaaa aaaaaaaaaa 2580
aaaaaaaaaa aaaaaaaaaa aaaaaaaa 2608
<210> 13
<211> 239
<212> PRT
<213> Homo sapiens
<223> TM4SF1 – Номер доступа XP_016861874.1
<400> 13
Met Cys Tyr Gly Lys Cys Ala Arg Cys Ile Gly His Ser Leu Val Gly
1 5 10 15
Leu Ala Leu Leu Cys Ile Ala Ala Asn Ile Leu Leu Tyr Phe Pro Asn
20 25 30
Gly Glu Thr Lys Tyr Ala Ser Glu Asn His Leu Ser Arg Phe Val Trp
35 40 45
Phe Phe Ser Gly Ile Val Gly Gly Gly Leu Leu Met Leu Leu Pro Ala
50 55 60
Phe Val Phe Ile Gly Leu Glu Gln Asp Asp Cys Cys Gly Cys Cys Gly
65 70 75 80
His Glu Asn Cys Gly Lys Arg Cys Ala Met Leu Ser Ser Val Leu Ala
85 90 95
Ala Leu Ile Gly Ile Ala Gly Ser Gly Tyr Cys Val Ile Val Ala Ala
100 105 110
Leu Gly Leu Ala Glu Gly Pro Leu Cys Leu Asp Ser Leu Gly Gln Trp
115 120 125
Asn Tyr Thr Phe Ala Ser Thr Glu Gly Gln Tyr Leu Leu Asp Thr Ser
130 135 140
Thr Trp Ser Glu Cys Thr Glu Pro Lys His Ile Val Glu Trp Asn Val
145 150 155 160
Ser Leu Phe Ser Ile Leu Leu Ala Leu Gly Gly Ile Glu Phe Ile Leu
165 170 175
Cys Leu Ile Gln Val Ile Asn Gly Val Leu Gly Gly Ile Cys Gly Phe
180 185 190
Cys Cys Ser His Gln Gln Val Arg Thr Cys Met Lys Ile Asn Met Thr
195 200 205
Ala Lys Arg Thr Asn Pro Gly Gln Ser His Asn Leu Pro Leu Phe His
210 215 220
Cys Asn Leu Tyr Ile Ser Leu Val Phe Ile Cys Lys Thr Leu Tyr
225 230 235
<210> 14
<211> 972
<212> ДНК
<213> Homo sapiens
<220>
<223> TM4SF1 – Номер доступа XM_017006385.2
<400> 14
aagggcggga cattccccct gcctcttcgc accacagcca gagcctgcca ttaggaccaa 60
tgaaagcaaa gtacctcatc ccctcagtga ctaagaatcg cagtatttaa gaggtagcag 120
gaatgggctg agagtggtgt ttgctttctc caccagaagg gcacactttc atctaatttg 180
gggtatcact gagctgaaga caaagagaag ggggagaaaa cctagcagac caccatgtgc 240
tatgggaagt gtgcacgatg catcggacat tctctggtgg ggctcgccct cctgtgcatc 300
gcggctaata ttttgcttta ctttcccaat ggggaaacaa agtatgcctc cgaaaaccac 360
ctcagccgct tcgtgtggtt cttttctggc atcgtaggag gtggcctgct gatgctcctg 420
ccagcatttg tcttcattgg gctggaacag gatgactgct gtggctgctg tggccatgaa 480
aactgtggca aacgatgtgc gatgctttct tctgtattgg ctgctctcat tggaattgca 540
ggatctggct actgtgtcat tgtggcagcc cttggcttag cagaaggacc actatgtctt 600
gattccctcg gccagtggaa ctacaccttt gccagcactg agggccagta ccttctggat 660
acctccacat ggtccgagtg cactgaaccc aagcacattg tggaatggaa tgtatctctg 720
ttttctatcc tcttggctct tggtggaatt gaattcatct tgtgtcttat tcaagtaata 780
aatggagtgc ttggaggcat atgtggcttt tgctgctctc accaacaggt aagaacctgc 840
atgaaaatca atatgactgc taaaagaacc aacccaggac agagccacaa tcttcctcta 900
tttcattgta atttatatat ttcacttgta ttcatttgta aaactttgta ttagtgtaac 960
atactcccca ca 972
<210> 15
<211> 367
<212> PRT
<213> Homo sapiens
<223> DUSP1 – Номер доступа NP_004408.1
<400> 15
Met Val Met Glu Val Gly Thr Leu Asp Ala Gly Gly Leu Arg Ala Leu
1 5 10 15
Leu Gly Glu Arg Ala Ala Gln Cys Leu Leu Leu Asp Cys Arg Ser Phe
20 25 30
Phe Ala Phe Asn Ala Gly His Ile Ala Gly Ser Val Asn Val Arg Phe
35 40 45
Ser Thr Ile Val Arg Arg Arg Ala Lys Gly Ala Met Gly Leu Glu His
50 55 60
Ile Val Pro Asn Ala Glu Leu Arg Gly Arg Leu Leu Ala Gly Ala Tyr
65 70 75 80
His Ala Val Val Leu Leu Asp Glu Arg Ser Ala Ala Leu Asp Gly Ala
85 90 95
Lys Arg Asp Gly Thr Leu Ala Leu Ala Ala Gly Ala Leu Cys Arg Glu
100 105 110
Ala Arg Ala Ala Gln Val Phe Phe Leu Lys Gly Gly Tyr Glu Ala Phe
115 120 125
Ser Ala Ser Cys Pro Glu Leu Cys Ser Lys Gln Ser Thr Pro Met Gly
130 135 140
Leu Ser Leu Pro Leu Ser Thr Ser Val Pro Asp Ser Ala Glu Ser Gly
145 150 155 160
Cys Ser Ser Cys Ser Thr Pro Leu Tyr Asp Gln Gly Gly Pro Val Glu
165 170 175
Ile Leu Pro Phe Leu Tyr Leu Gly Ser Ala Tyr His Ala Ser Arg Lys
180 185 190
Asp Met Leu Asp Ala Leu Gly Ile Thr Ala Leu Ile Asn Val Ser Ala
195 200 205
Asn Cys Pro Asn His Phe Glu Gly His Tyr Gln Tyr Lys Ser Ile Pro
210 215 220
Val Glu Asp Asn His Lys Ala Asp Ile Ser Ser Trp Phe Asn Glu Ala
225 230 235 240
Ile Asp Phe Ile Asp Ser Ile Lys Asn Ala Gly Gly Arg Val Phe Val
245 250 255
His Cys Gln Ala Gly Ile Ser Arg Ser Ala Thr Ile Cys Leu Ala Tyr
260 265 270
Leu Met Arg Thr Asn Arg Val Lys Leu Asp Glu Ala Phe Glu Phe Val
275 280 285
Lys Gln Arg Arg Ser Ile Ile Ser Pro Asn Phe Ser Phe Met Gly Gln
290 295 300
Leu Leu Gln Phe Glu Ser Gln Val Leu Ala Pro His Cys Ser Ala Glu
305 310 315 320
Ala Gly Ser Pro Ala Met Ala Val Leu Asp Arg Gly Thr Ser Thr Thr
325 330 335
Thr Val Phe Asn Phe Pro Val Ser Ile Pro Val His Ser Thr Asn Ser
340 345 350
Ala Leu Ser Tyr Leu Gln Ser Pro Ile Thr Thr Ser Pro Ser Cys
355 360 365
<210> 16
<211> 2013
<212> ДНК
<213> Homo sapiens
<223> DUSP1 – Номер доступа NM_004417.4
<400> 16
gcgaaggaca tttgggctgt gtgtgcgacg cgggtcggag gggcagtcgg gggaaccgcg 60
aagaagccga ggagcccgga gccccgcgtg acgctcctct ctcagtccaa aagcggcttt 120
tggttcggcg cagagagacc cgggggtcta gcttttcctc gaaaagcgcc gccctgccct 180
tggccccgag aacagacaaa gagcaccgca gggccgatca cgctgggggc gctgaggccg 240
gccatggtca tggaagtggg caccctggac gctggaggcc tgcgggcgct gctgggggag 300
cgagcggcgc aatgcctgct gctggactgc cgctccttct tcgctttcaa cgccggccac 360
atcgccggct ctgtcaacgt gcgcttcagc accatcgtgc ggcgccgggc caagggcgcc 420
atgggcctgg agcacatcgt gcccaacgcc gagctccgcg gccgcctgct ggccggcgcc 480
taccacgccg tggtgttgct ggacgagcgc agcgccgccc tggacggcgc caagcgcgac 540
ggcaccctgg ccctggcggc cggcgcgctc tgccgcgagg cgcgcgccgc gcaagtcttc 600
ttcctcaaag gaggatacga agcgttttcg gcttcctgcc cggagctgtg cagcaaacag 660
tcgaccccca tggggctcag ccttcccctg agtactagcg tccctgacag cgcggaatct 720
gggtgcagtt cctgcagtac cccactctac gatcagggtg gcccggtgga aatcctgccc 780
tttctgtacc tgggcagtgc gtatcacgct tcccgcaagg acatgctgga tgccttgggc 840
atcactgcct tgatcaacgt ctcagccaat tgtcccaacc attttgaggg tcactaccag 900
tacaagagca tccctgtgga ggacaaccac aaggcagaca tcagctcctg gttcaacgag 960
gccattgact tcatagactc catcaagaat gctggaggaa gggtgtttgt ccactgccag 1020
gcaggcattt cccggtcagc caccatctgc cttgcttacc ttatgaggac taatcgagtc 1080
aagctggacg aggcctttga gtttgtgaag cagaggcgaa gcatcatctc tcccaacttc 1140
agcttcatgg gccagctgct gcagtttgag tcccaggtgc tggctccgca ctgttcggca 1200
gaggctggga gccccgccat ggctgtgctc gaccgaggca cctccaccac caccgtgttc 1260
aacttccccg tctccatccc tgtccactcc acgaacagtg cgctgagcta ccttcagagc 1320
cccattacga cctctcccag ctgctgaaag gccacgggag gtgaggctct tcacatccca 1380
ttgggactcc atgctccttg agaggagaaa tgcaataact ctgggagggg ctcgagaggg 1440
ctggtcctta tttatttaac ttcacccgag ttcctctggg tttctaagca gttatggtga 1500
tgacttagcg tcaagacatt tgctgaactc agcacattcg ggaccaatat atagtgggta 1560
catcaagtcc atctgacaaa atggggcaga agagaaagga ctcagtgtgt gatccggttt 1620
ctttttgctc gcccctgttt tttgtagaat ctcttcatgc ttgacatacc taccagtatt 1680
attcccgacg acacatatac atatgagaat ataccttatt tatttttgtg taggtgtctg 1740
ccttcacaaa tgtcattgtc tactcctaga agaaccaaat acctcaattt ttgtttttga 1800
gtactgtact atcctgtaaa tatatcttaa gcaggtttgt tttcagcact gatggaaaat 1860
accagtgttg ggtttttttt tagttgccaa cagttgtatg tttgctgatt atttatgacc 1920
tgaaataata tatttcttct tctaagaaga cattttgtta cataaggatg acttttttat 1980
acaatggaat aaattatggc atttctattg aaa 2013
<210> 17
<211> 185
<212> PRT
<213> Homo sapiens
<223> ADM – Номер доступа NP_001115.1
<400> 17
Met Lys Leu Val Ser Val Ala Leu Met Tyr Leu Gly Ser Leu Ala Phe
1 5 10 15
Leu Gly Ala Asp Thr Ala Arg Leu Asp Val Ala Ser Glu Phe Arg Lys
20 25 30
Lys Trp Asn Lys Trp Ala Leu Ser Arg Gly Lys Arg Glu Leu Arg Met
35 40 45
Ser Ser Ser Tyr Pro Thr Gly Leu Ala Asp Val Lys Ala Gly Pro Ala
50 55 60
Gln Thr Leu Ile Arg Pro Gln Asp Met Lys Gly Ala Ser Arg Ser Pro
65 70 75 80
Glu Asp Ser Ser Pro Asp Ala Ala Arg Ile Arg Val Lys Arg Tyr Arg
85 90 95
Gln Ser Met Asn Asn Phe Gln Gly Leu Arg Ser Phe Gly Cys Arg Phe
100 105 110
Gly Thr Cys Thr Val Gln Lys Leu Ala His Gln Ile Tyr Gln Phe Thr
115 120 125
Asp Lys Asp Lys Asp Asn Val Ala Pro Arg Ser Lys Ile Ser Pro Gln
130 135 140
Gly Tyr Gly Arg Arg Arg Arg Arg Ser Leu Pro Glu Ala Gly Pro Gly
145 150 155 160
Arg Thr Leu Val Ser Ser Lys Pro Gln Ala His Gly Ala Pro Ala Pro
165 170 175
Pro Ser Gly Ser Ala Pro His Phe Leu
180 185
<210> 18
<211> 1492
<212> ДНК
<213> Homo sapiens
<223> ADM – Номер доступа NM_001124.3
<400> 18
actcagtggt ttcttggtga cactggatag aacagctcaa gccttgccac ttcgggcttc 60
tcactgcagc tgggcttgga cttcggagtt ttgccattgc cagtgggacg tctgagactt 120
tctccttcaa gtacttggca gatcactctc ttagcagggt ctgcgcttcg cagccgggat 180
gaagctggtt tccgtcgccc tgatgtacct gggttcgctc gccttcctag gcgctgacac 240
cgctcggttg gatgtcgcgt cggagtttcg aaagaagtgg aataagtggg ctctgagtcg 300
tgggaagagg gaactgcgga tgtccagcag ctaccccacc gggctcgctg acgtgaaggc 360
cgggcctgcc cagaccctta ttcggcccca ggacatgaag ggtgcctctc gaagccccga 420
agacagcagt ccggatgccg cccgcatccg agtcaagcgc taccgccaga gcatgaacaa 480
cttccagggc ctccggagct ttggctgccg cttcgggacg tgcacggtgc agaagctggc 540
acaccagatc taccagttca cagataagga caaggacaac gtcgccccca ggagcaagat 600
cagcccccag ggctacggcc gccggcgccg gcgctccctg cccgaggccg gcccgggtcg 660
gactctggtg tcttctaagc cacaagcaca cggggctcca gcccccccga gtggaagtgc 720
tccccacttt ctttaggatt taggcgccca tggtacaagg aatagtcgcg caagcatccc 780
gctggtgcct cccgggacga aggacttccc gagcggtgtg gggaccgggc tctgacagcc 840
ctgcggagac cctgagtccg ggaggcaccg tccggcggcg agctctggct ttgcaagggc 900
ccctccttct gggggcttcg cttccttagc cttgctcagg tgcaagtgcc ccagggggcg 960
gggtgcagaa gaatccgagt gtttgccagg cttaaggaga ggagaaactg agaaatgaat 1020
gctgagaccc ccggagcagg ggtctgagcc acagccgtgc tcgcccacaa actgatttct 1080
cacggcgtgt caccccacca gggcgcaagc ctcactatta cttgaacttt ccaaaaccta 1140
aagaggaaaa gtgcaatgcg tgttgtacat acagaggtaa ctatcaatat ttaagtttgt 1200
tgctgtcaag attttttttg taacttcaaa tatagagata tttttgtacg ttatatattg 1260
tattaagggc attttaaaag caattatatt gtcctcccct attttaagac gtgaatgtct 1320
cagcgaggtg taaagttgtt cgccgcgtgg aatgtgagtg tgtttgtgtg catgaaagag 1380
aaagactgat tacctcctgt gtggaagaag gaaacaccga gtctctgtat aatctattta 1440
cataaaatgg gtgatatgcg aacagcaaac caataaactg tctcaatgct ga 1492
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Выделенное антитело к CD45RC человека, нуклеиновая кислота, вектор экспрессии, клетка, фармацевтическая композиция, их применение, in vitro способ обнаружения hCD45RC | 2019 |
|
RU2826421C2 |
| ИНГИБИТОР ИММУНОСУПРЕССИИ, СВЯЗАННЫЙ С РАКОМ | 2018 |
|
RU2805232C2 |
| ИММУНОЦИТОКИНЫ НА ОСНОВЕ IL-15 И IL-15Rα ДОМЕНА SUSHI | 2012 |
|
RU2763298C2 |
| ВАРИАНТЫ КИСЛОЙ АЛЬФА-ГЛЮКОЗИДАЗЫ И ИХ ИСПОЛЬЗОВАНИЕ | 2017 |
|
RU2780410C2 |
| АНТИТЕЛА ПРОТИВ BTN3A И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ РАКА ИЛИ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2800726C2 |
| РЕКОМБИНАНТНЫЕ КЛЕТКИ ДРОЖЖЕЙ, ПРОДУЦИРУЮЩИЕ ПОЛИМОЛОЧНУЮ КИСЛОТУ, И ИХ ИСПОЛЬЗОВАНИЯ | 2016 |
|
RU2758138C2 |
| ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ С ВЫСОКОПЛОТНЫМ ПОКРЫТИЕМ ДЛЯ ИНДУКЦИИ ЭКСПРЕССИИ АНТИТЕЛ | 2017 |
|
RU2813282C2 |
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРЕДОТВРАЩЕНИЯ ИНСУЛЬТА | 2015 |
|
RU2744909C2 |
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2721916C2 |
| УЛУЧШЕННЫЙ БЕЛОК REP ДЛЯ ПРИМЕНЕНИЯ В ДИАГНОСТИЧЕСКИХ АНАЛИЗАХ | 2018 |
|
RU2736275C1 |

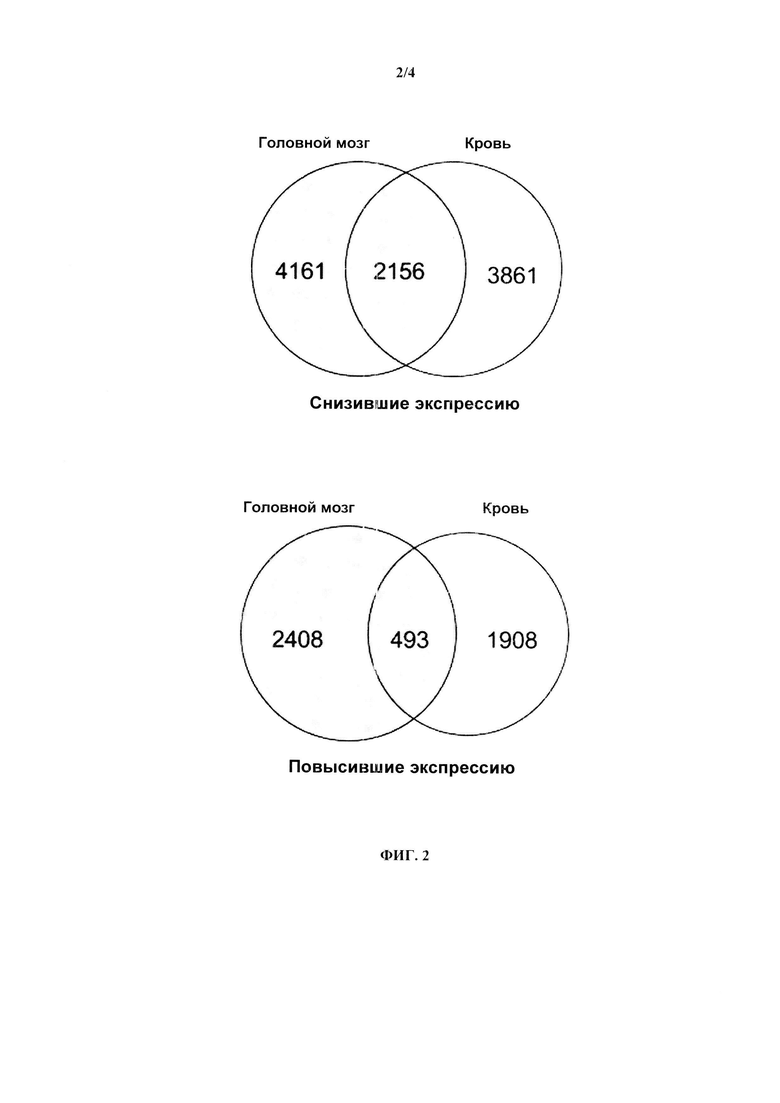

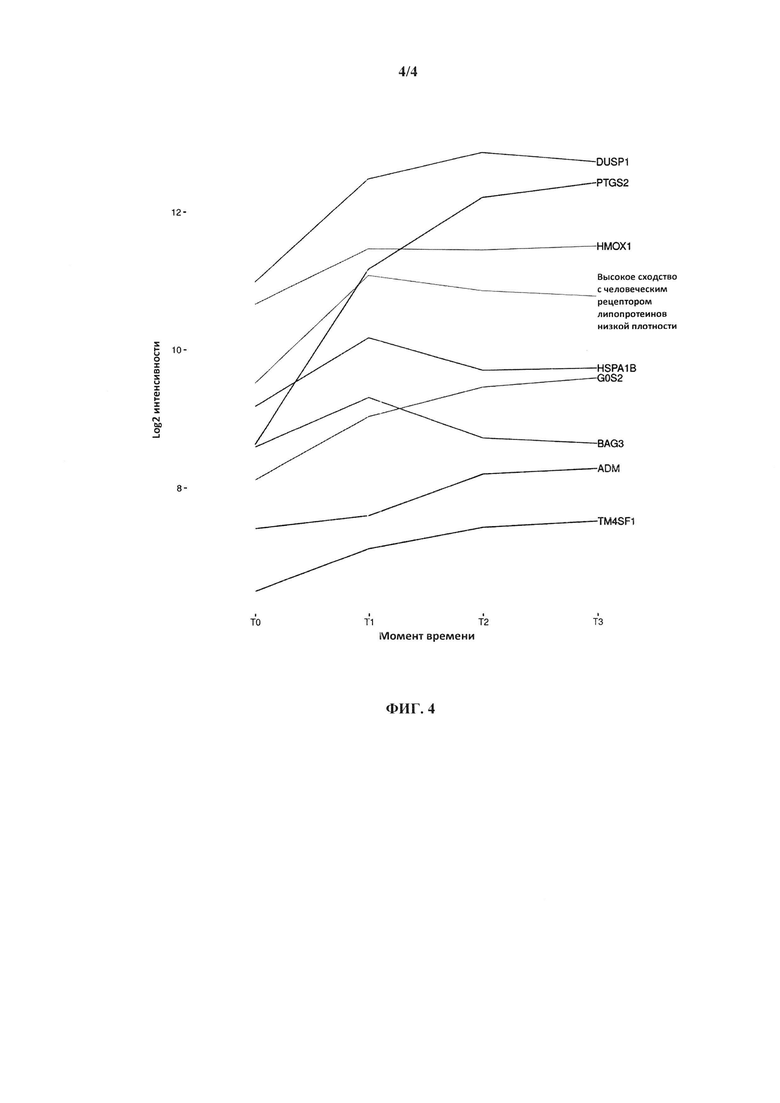
Предложенная группа изобретений относится к медицине, а именно к медицинской диагностике. Предложены способ диагностики и способ определения у индивида риска развития инсульта, включающие измерение уровней экспрессии как минимум трех биомаркеров, выбранных из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM. Предложен способ определения наличия у индивида, перенесшего инсульт, ответной реакции на терапию, включающий измерение уровней экспрессии как минимум двух биомаркеров, выбранных из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM. Предложенная группа изобретений обеспечивает характеризацию пациентов с ишемическим инсультом и разработку сопутствующих биомаркеров, необходимых для оценки эффективности лекарств-нейропротекторов у пациентов за счет определения общей кодирующей сигнатуры для головного мозга, затронутого ишемическим поражением, в образце, взятом у индивида. 3 н. и 18 з.п. ф-лы, 4 ил., 4 табл., 2 пр.
1. Способ диагностики инсульта у индивида, включающий:
i) определение сигнатуры в образце, взятом у индивида, путем измерения уровней экспрессии как минимум трех биомаркеров, выбранных из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
ii) сравнение сигнатуры, полученной на стадии i), с эталонной сигнатурой; и
iii) диагностирование индивида, как перенесшего инсульт, если уровни экспрессии как минимум трех биомаркеров в сигнатуре выше, чем уровни экспрессии тех же как минимум трех биомаркеров в эталонной сигнатуре.
2. Способ по п. 1, отличающийся тем, что стадия i) включает определение уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
3. Способ по п. 1, отличающийся тем, что эталонную сигнатуру получают путем измерения уровней экспрессии биомаркеров в контрольной группе, состоящей из по существу здоровых индивидов для дифференцирования инсульта и имитации инсульта, где по существу здоровые субъекты предварительно не диагностированы или не идентифицированы как имеющие или страдающие от инсульта.
4. Способ по п. 1 для дифференцирования инсульта и имитации инсульта.
5. Способ по п. 1, где инсульт является ишемическим инсультом, транзиторной ишемической атакой, или геморрагическим инсультом.
6. Способ по п. 1, где образец является образцом крови, плазмы или сыворотки.
7. Способ по п. 1, где образец не является образцом тканей головного мозга.
8. Способ определения наличия у индивида, перенесшего инсульт, ответной реакции на терапию, включающий:
i) определение сигнатуры в образце, взятом у индивида, путем измерения уровней экспрессии как минимум двух биомаркеров, выбранных из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
ii) сравнение сигнатуры, полученной на стадии i), с эталонной сигнатурой; и
iii) заключение о наличии у индивида ответной реакции, если уровни экспрессии упомянутых ранее как минимум двух биомаркеров в сигнатуре ниже, чем уровни экспрессии тех же как минимум двух биомаркеров в эталонной сигнатуре.
9. Способ по п. 8, где по крайней мере два биомаркера не состоят из DUSP1 и ADM.
10. Способ по п. 8, отличающийся тем, что стадия i) включает измерение уровней экспрессии PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
11. Способ по п. 8, отличающийся тем, что эталонную сигнатуру получают путем измерения уровней экспрессии биомаркеров в образце, взятом у того же индивида до начала указанной терапии.
12. Способ по п. 8, где инсульт является ишемическим инсультом, транзиторной ишемической атакой, или геморрагическим инсультом.
13. Способ по п. 8, где образец является образцом крови, плазмы или сыворотки.
14. Способ по п. 8, где образец не является образцом тканей головного мозга.
15. Способ определения у индивида риска развития инсульта, включающий:
i) определение сигнатуры в образце, взятом у индивида, путем измерения уровней экспрессии как минимум трех биомаркеров, выбранных из группы, состоящей из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM;
ii) сравнение сигнатуры, полученной на стадии i), с эталонной сигнатурой; и
iii) заключение о наличии у индивида риска развития инсульта, если уровни экспрессии как минимум трех биомаркеров в сигнатуре выше, чем уровни экспрессии тех же как минимум трех биомаркеров в эталонной сигнатуре.
16. Способ по п. 15, отличающийся тем, что стадия i) включает измерение уровней экспрессии девяти биомаркеров, выбранных из PTGS2, НМОХ1, LDLR, HSPA1B, G0S2, BAG3, TM4SF1, DUSP1 и ADM.
17. Способ по п. 15, отличающийся тем, что эталонную сигнатуру получают путем измерения уровней экспрессии биомаркеров в контрольной группе, состоящей из по существу здоровых индивидов, где по существу здоровые субъекты предварительно не диагностированы или идентифицированы как имеющие или страдающие от инсульта.
18. Способ по п. 15, отличающийся тем, что у индивида ранее уже был инсульт, и данный метод предназначен для определения у данного индивида риска наступления повторного инсульта.
19. Способ по п. 15, отличающийся тем, что инсульт представляет собой ишемический инсульт, транзиторную ишемическую атаку или геморрагический инсульт.
20. Способ по п. 15, отличающийся тем, что образец представляет собой образец крови, образец плазмы или образец сыворотки.
21. Способ по п. 15, отличающийся тем, что образец не является образцом тканей головного мозга.
| Способ определения индивидуального генетического риска развития ишемического инсульта | 2014 |
|
RU2612630C2 |
| WO 2018067571 A2, 12.04.2018 | |||
| WO 2015054700 A2, 16.04.2015 | |||
| US 2003104393 A1, 05.06.2003. | |||
Авторы
Даты
2024-06-26—Публикация
2019-05-16—Подача