ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[001] Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США №62/812,585, поданной 1 марта 2019 года, и предварительной заявки на патент США №62/969,976, поданной 4 февраля 2020 г., содержание всех из которых полностью включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[002] Данное изобретение относится к связывающим DLL3 агентам и химерным антигенным рецепторам (CAR), содержащим антигенсвязывающую молекулу, которая связывается с DLL3, кодирующим их полинуклеотидам и способам лечения рака у пациента с их применением.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[003] Данная заявка подается в электронном виде через EFS-Web и включает перечень последовательностей, подаваемый в электронном виде в формате .txt. Файл .txt содержит перечень последовательностей, озаглавленный «АТ-019_03US_SL», созданный 4 февраля 2020 г. и имеющий размер 1026798 байт. Перечень последовательностей, содержащийся в этом файле .txt, является частью описания и полностью включен в настоящий документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[004] Мелкоклеточный рак легкого (МРЛ) это агрессивная форма рака легкого с плохим прогнозом и ограниченными возможными вариантами лечения. МРЛ составляет около 10-15% всех новых диагностированных случаев рака легкого. По оценкам Американского онкологического общества, в 2018 году будет диагностировано около 234000 новых случаев рака легкого. Расчетная 5-летняя относительная выживаемость для МРЛ составляет 31% (для I стадии), 19% (для II стадии), 8% (для III стадии) и 2% (для IV стадии). Показатели выживаемости при МРЛ остаются низкими в течение нескольких десятилетий в значительной степени из-за отсутствия новых вариантов лечения этой формы рака легкого. Обычные терапевтические средства лечения рака включают химиотерапию и лучевую терапию. Пациенты обычно хорошо отвечают на применяемую в настоящее время терапию первой линии, включающую этопозид и цисплатин, но у них неизменно быстро развивается рецидив химиорезистентного заболевания. Прогноз при рецидиве рефрактерного заболевания крайне неблагоприятный, с быстрым прогрессированием заболевания и короткой медианной выживаемостью менее шести месяцев. Таким образом, сохраняется значительная необходимость в разработке более направленных и эффективных вариантов лечения пролиферативных нарушений.
[005] Адоптивный перенос иммунных клеток, генетически модифицированных для распознавания антигенов, связанных со злокачественными новообразованиями, является многообещающим новым подходом к лечению рака (см., например, Brenner et al., Current Opinion in Immunology, 22 (2): 251-257 (2010); Rosenberg et al., Nature Reviews Cancer, 8 (4): 299-308 (2008)). Иммунные клетки могут быть генетически модифицированы для экспрессии химерных антигенных рецепторов (CAR) слитых белков, состоящих из фрагмента, распознающего антиген DLL3, и доменов активации Т-клеток (см., например, Eshhar et al., Proc. Natl. Acad. Sci. USA, 90 (2): 720-724 (1993) и Sadelain et al., Curr. Opin. Immunol, 21 (2): 215-223 (2009)). Иммунные клетки, содержащие CAR, например, CAR-T-клетки (CAR-T), сконструированы так, чтобы придать им антигенную специфичность, сохраняя или повышая их способность распознавать и уничтожать клетку-мишень.
[006] DLL3 является неканоническим лигандом Notch, функционирующим автономно от клетки, ингибируя передачу сигналов Notch, тем самым блокируя межклеточные взаимодействия и интернализацию Notch в клетке-мишени. Дельта-подобный лиганд 3 (DLL3) является опухолевым маркером МРЛ и, как было обнаружено, связан с раковыми стволовыми клетками. Другие патологические состояния, в которых участвует DLL3, включают меланому, глиомы низкой степени злокачественности, глиобластому, медуллярный рак щитовидной железы, карциноиды, диспергированные нейроэндокринные опухоли поджелудочной железы, мочевого пузыря и предстательной железы, рак яичка и аденокарциномы легких с нейроэндокринными особенностями. Существует потребность в вариантах лечения рака и, в частности, злокачественных новообразований, связанных с аберрантной экспрессией DLL3. В настоящем документе предложены способы и композиции, которые удовлетворяют эту потребность.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[007] В настоящем документе предложены химерные антигенные рецепторы (CAR), содержащие антигенсвязывающий домен против DLL3, который специфически связывается с DLL3; и иммунные клетки, содержащие эти DLL3-специфичные CAR, например, CAR-T-клетки. Также предложены способы получения и применения этих DLL3-специфичных CAR и иммунных клеток, содержащих эти DLLS-специфичные CAR. Описанные в настоящем документе CAR-T-клетки, нацеленные на DLL-3, демонстрируют хорошую эффективность трансдукции, фенотип in vitro и высокую противоопухолевую активность in vitro и in vivo.
[008] В одном из аспектов настоящее изобретение относится к химерному антигенному рецептору, содержащему внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит по меньшей мере одну из следующих: (a) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 10, 19, 28, 37, 46, 55, 64, 73, 82, 91, 100, 109, 118, 127, 136, 145, 154, 163, 172, 181, 190, 199, 208, 217, 226, 235, 244, 253, 262, 271, 280, 289, 298, 307, 316, 325, 334, 343, 352, 361, 370, 379, 388, 397, 406, 415, 424, 433, 442, 451 и 460; (b) CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 2, 11, 20, 38, 47, 56, 65, 74, 83, 92, 101, 110, 119, 128, 137, 146, 155, 164, 173, 182, 191, 200, 209, 218, 227, 236, 245, 254, 263, 272, 281, 290, 299, 308, 317, 326, 335, 344, 353, 362, 371, 380, 389, 398, 407, 416, 425, 434, 443, 452, 461 и 695; (с) CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3, 12, 21, 30, 39, 48, 57, 66, 75, 84, 93, 102, 111, 120, 129, 138, 147, 156, 165, 174, 183, 192, 201, 210, 219, 228, 237, 246, 255, 264, 273, 282, 291, 300, 309, 318, 327, 336, 345, 354, 363, 372, 381, 390, 399, 408, 417, 426, 435, 444, 453 и 462; (d) CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 13, 22, 31, 40, 49, 58, 67, 85, 94, 103, 112, 121, 130, 139, 148, 157, 166, 175, 184, 193, 202, 211, 220, 229, 238, 247, 256, 265, 274, 283, 292, 301, 310, 319, 328, 337, 346, 355, 364, 373, 382, 391, 400, 409, 418, 427, 436, 445, 454, 463 и 696; (е) CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 5, 14, 23, 32, 41, 50, 59, 68, 77, 86, 95, 104, 113, 122, 131, 140, 149, 158, 167, 176, 185, 194, 203, 212, 221, 230, 239, 248, 257, 266, 275, 284, 293, 302, 311, 320, 329, 338, 347, 356, 365, 374, 383, 392, 401, 410, 419, 428, 437, 446, 455 и 464; и (f) CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 6, 15, 24, 33, 42, 51, 60, 69, 78, 87, 96, 105, 114, 123, 132, 141, 150, 159, 168, 177, 186, 195, 204, 213, 222, 231, 240, 249, 258, 267, 276, 285, 294, 303, 312, 321, 330, 339, 348, 357, 366, 375, 384, 393, 402, 411, 420, 429, 438, 447, 456 и 465.
[009] В еще одном аспекте настоящее изобретение относится к химерному антигенному рецептору, содержащему внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит: (a) CDR1 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 10, 19, 28, 37, 46, 55, 64, 73, 82, 91, 100, 109, 118, 127, 136, 145, 154, 163, 172, 181, 190, 199, 208, 217, 226, 235, 244, 253, 262, 271, 280, 289, 298, 307, 316, 325, 334, 343, 352, 361, 370, 379, 388, 397, 406, 415, 424, 433, 442, 451 и 460; (b) CDR2 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 2, 11, 20, 38, 47, 56, 65, 74, 83, 92, 101, 110, 119, 128, 137, 146, 155, 164, 173, 182, 191, 200, 209, 218, 227, 236, 245, 254, 263, 272, 281, 290, 299, 308, 317, 326, 335, 344, 353, 362, 371, 380, 389, 398, 407, 416, 425, 434, 443, 452 и 695461; и (с) CDR3 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3, 12,21,30,39, 48, 57, 66, 75, 84, 93, 102, 111, 120, 129, 138, 147, 156, 165, 174, 183, 192, 201, 210, 219, 228, 237, 246, 255, 264, 273, 282, 291, 300, 309, 318, 327, 336, 345, 354, 363, 372, 381, 390, 399, 408, 417, 426, 435, 444, 453 и 462.
[010] В одном из аспектов настоящее изобретение относится к химерному антигенному рецептору, содержащему внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит: (a) CDR1 вариабельной легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 13, 22, 31, 40, 49, 58, 67, 85, 94, 103, 112, 121, 130, 139, 148, 157, 166, 175, 184, 193, 202, 211, 220, 229, 238, 247, 256, 265, 274, 283, 292, 301, 310, 319, 328, 337, 346, 355, 364, 373, 382, 391, 400, 409, 418, 427, 436, 445, 454, 463 и 696; (b) CDR2 вариабельной легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 5, 14, 23, 32, 41, 50, 59, 68, 77, 86, 95, 104, 113, 122, 131, 140, 149, 158, 167, 176, 185, 194, 203, 212, 221, 230, 239, 248, 257, 266, 275, 284, 293, 302, 311, 320, 329, 338, 347, 356, 365, 374, 383, 392, 401, 410, 419, 428, 437, 446, 455 и 464; и (с) CDR3 вариабельной легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 6, 15,24,33,42, 51, 60, 69, 78, 87, 96, 105, 114, 123, 132, 141, 150, 159, 168, 177, 186, 195, 204, 213, 222, 231, 240, 249, 258, 267, 276, 285, 294, 303, 312, 321, 330, 339, 348, 357, 366, 375, 384, 393, 402, 411, 420, 429, 438, 447, 456 и 465.
[011] В еще одном аспекте настоящее изобретение относится к химерному антигенному рецептору, содержащему внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит по меньшей мере одну из: (а) вариабельной тяжелой цепи, содержащей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 7, 16, 25, 34, 43, 52, 61, 70, 79, 88, 97, 106, 115, 124, 133, 142, 151, 160, 169, 178, 187, 196, 205, 214, 223, 232, 241, 250, 259, 268, 277, 286, 295, 304, 313, 322, 331, 340, 349, 358, 367, 376, 385, 394, 403, 412, 421, 430, 439, 448, 457, 466; и (b) вариабельной легкой цепи, содержащей аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 8, 17, 26, 35, 44, 53, 62, 71, 80, 89, 98, 107, 116, 125, 134, 143, 152, 161, 170, 179, 188, 197, 206, 215, 224, 233, 242, 251, 260, 269, 278, 287, 296, 305, 314, 323, 332, 341, 350, 359, 368, 377, 386, 395, 404, 413, 422, 431, 440, 449, 458 и 467, где вариабельная тяжелая цепь и вариабельная легкая цепь связаны по меньшей мере одним линкером.
[012] В дополнительном настоящее изобретение относится к химерному антигенному рецептору, содержащему внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит: (а) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 7, 16, 25, 34, 43, 52, 61, 70, 79, 88, 97, 106, 115, 124, 133, 142, 151, 160, 169, 178, 187, 196, 205, 214, 223, 232, 241, 250, 259, 268, 277, 286, 295, 304, 313, 322, 331, 340, 349, 358, 367, 376, 385, 394, 403, 412, 421, 430, 439, 448, 457 и 466; и (b) вариабельную легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 8, 17, 26, 35, 44, 53, 62, 71, 80, 89, 98, 107, 116, 125, 134, 143, 152, 161, 170, 179, 188, 197, 206, 215, 224, 233, 242, 251, 260, 269, 278, 287, 296, 305, 314, 323, 332, 341, 350, 359, 368, 377, 386, 395, 404, 413, 422, 431, 440, 449, 458 и 467, где вариабельная тяжелая цепь и вариабельная легкая цепь связаны по меньшей мере одним линкером.
[013] В одном из аспектов настоящее изобретение относится к химерному антигенному рецептору, содержащему внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит последовательность, выбранную из группы, состоящей из scFv, представленных в таблице 1d.
[014] В еще одном аспекте настоящее изобретение относится к химерному антигенному рецептору, который специфически связывается с DLL3, где химерный антигенный рецептор содержит аминокислотную последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную любой из SEQ ID NO: 482-533 и 632-683. В некоторых вариантах осуществления химерный антигенный рецептор содержит аминокислотную последовательность любой из SEQ ID NO: 482-533 и 632-683.
[015] В некоторых вариантах осуществления настоящее изобретение относится к химерному антигенному рецептору, который специфически связывается с DLL3, где химерный антигенный рецептор содержит аминокислотную последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную любой из SEQ ID NO: 482-533 и 632-683, с сигнальной последовательностью или без нее. В некоторых вариантах осуществления химерный антигенный рецептор содержит аминокислотную последовательность любой из SEQ ID NO: 482-533 и 632-683, с сигнальной последовательностью или без нее.
[016] В некоторых вариантах осуществления внутриклеточный домен химерного антигенного рецептора содержит по меньшей мере один костимулирующий домен.
[017] В некоторых вариантах осуществления костимулирующий домен химерного антигенного рецептора представляет собой сигнальную область CD28, ОХ-40, 4-1BB/CD137, CD2, CD7, CD27, CD30, CD40, программируемую смерть-1 (PD-1), индуцибельный костимулятор Т-клеток (ICOS), антиген 1, связанный с функцией лимфоцитов (LFA-1 (CD1 1a/CD 18), CD3-гамма, CD3-дельта, CD3-эпсилон, CD247, CD276 (В7-Н3), LIGHT, (TNFSF14), NKG2C, Ig-альфа (CD79a), DAP-10, Fc-гамма-рецептор, молекулу МНС класса I, белки TNF-рецептора, белок иммуноглобулина, рецептор цитокинов, интегрины, сигнальные молекулы активации лимфоцитов (SLAM-белки), активирующие рецепторы NK-клеток, BTLA, лиганды Toll-рецепторов, ICAM-1, В7-Н3, CDS, ICAM-1, GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CD8-бета, IL-2R-бета, IL-2R-гамма, 1b-711-альфа, ITGA4, VLA1, CD49a, ITGA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD1 1d, ITGAE, CD103, ITGAL, CD1 1a, LFA-1, ITGAM, CD1 1b, ITGAX, CD1 1c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, TNFR2, TRANCE/RANKL, DNAMI (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRT AM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Lyl08), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a, лиганд, который специфически связывается с CD83, или любую их комбинацию.
[018] В некоторых вариантах осуществления костимулирующий домен содержит сигнальную область CD28.
[019] В некоторых вариантах осуществления костимулирующий домен CD28 содержит SEQ ID NO: 550.
[020] В некоторых вариантах осуществления костимулирующий домен содержит сигнальную область 4-1BB/CD137.
[021] В некоторых вариантах осуществления костимулирующий домен 4-1BB/CD137 содержит SEQ ID NO: 480.
[022] В некоторых вариантах осуществления внутриклеточный домен содержит по меньшей мере один активирующий домен.
[023] В некоторых вариантах осуществления активирующий домен содержит CD3.
[024] В некоторых вариантах осуществления CD3 включает CD3-дзета.
[025] В некоторых вариантах осуществления CD3-дзета содержит SEQ ID NO: 481.
[026] В некоторых вариантах осуществления химерный антигенный рецептор кодируется полинуклеотидной последовательностью любой из SEQ ID NO: 571-621 и 631.
[027] В некоторых вариантах осуществления химерный антигенный рецептор дополнительно содержит предохранительный переключатель.
[028] В некоторых вариантах осуществления предохранительный переключатель содержит мимотоп CD20 или эпитоп QBEND-10.
[029] В некоторых вариантах осуществления предохранительный переключатель содержит один или более мимотопов CD20, или один или более эпитопов QBEND-10, или их комбинации.
[030] В некоторых вариантах осуществления химерный антигенный рецептор содержит один или более предохранительных переключателей в формате QR3, SR2, RSR или R2S.
[031] В некоторых вариантах осуществления химерный антигенный рецептор содержит аминокислотную последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную любой из SEQ ID NO: 622-628, 474-476, 565 и 684-694.
[032] В некоторых вариантах осуществления химерный антигенный рецептор содержит аминокислотную последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную любой из SEQ ID NO: 622-628, 474-476, 565 и 684-694, с сигнальной последовательностью или без нее.
[033] В некоторых аспектах настоящее изобретение относится к выделенному полинуклеотиду, кодирующему любой из химерных антигенных рецепторов, описанных в настоящем документе.
[034] В еще одном аспекте настоящее изобретение относится к вектору, содержащему полинуклеотид, кодирующий любой из химерных антигенных рецепторов, описанных в настоящем документе.
[035] В некоторых вариантах осуществления вектор представляет собой ретровирусный вектор, ДНК-вектор, плазмиду, РНК-вектор, аденовирусный вектор, аденоассоциированный вирусный вектор, лентивирусный вектор или любую их комбинацию.
[036] В еще одном аспекте настоящее изобретение относится к сконструированной иммунной клетке, экспрессирующей химерные антигенные рецепторы, описанные в настоящем документе.
[037] В некоторых аспектах настоящее изобретение относится к сконструированной иммунной клетке, экспрессирующей полинуклеотид или вектор, кодирующий любой из химерных антигенных рецепторов, описанных в настоящем документе.
[038] В некоторых вариантах осуществления сконструированная иммунная клетка представляет собой Т-клетку, опухоль-инфильтрирующий лимфоцит (TIL), NK-клетку, TCR-экспрессирующую клетку, дендритную клетку или NK-T-клетку.
[039] В некоторых вариантах осуществления сконструированная иммунная клетка представляет собой аутологичную Т-клетку.
[040] В некоторых вариантах осуществления сконструированная иммунная клетка представляет собой аллогенную Т-клетку.
[041] В некоторых вариантах осуществления сконструированная иммунная клетка имеет нокаут TCR (например, TCRα, TCRβ).
[042] В одном из аспектов настоящее изобретение относится к фармацевтической композиции, содержащей сконструированную иммунную клетку, экспрессирующую химерные антигенные рецепторы, описанные в настоящем документе.
[043] В некоторых аспектах настоящее изобретение относится к способу лечения заболевания или нарушения у нуждающегося в этом субъекта, включающему введение указанному субъекту сконструированной иммунной клетки или фармацевтической композиции, содержащей сконструированную иммунную клетку, экспрессирующую химерные антигенные рецепторы, описанные в настоящем документе.
[044] В некоторых вариантах осуществления заболевание или нарушение представляет собой рак.
[045] В некоторых вариантах осуществления заболевание или нарушение представляет собой мелкоклеточный рак легкого.
[046] В некоторых аспектах настоящее изобретение относится к изделию, содержащему сконструированную иммунную клетку или фармацевтическую композицию, содержащую сконструированную иммунную клетку, экспрессирующую химерные антигенные рецепторы, описанные в настоящем документе.
[047] В некоторых аспектах настоящее изобретение относится к связывающему агенту против DLL3, раскрытому в настоящем документе.
[048] В некоторых вариантах осуществления связывающий агент против DLL3 представляет собой антитело, конъюгат антитела или его антигенсвязывающий фрагмент, необязательно F(ab’)2-фрагмент, Fab'-фрагмент, Fab-фрагмент, Fv-фрагмент, scFv-фрагмент, dsFv-фрагмент или dAb-фрагмент.
[049] В некоторых вариантах осуществления связывающий агент представляет собой моноклональное антитело, содержащее константную область IgG.
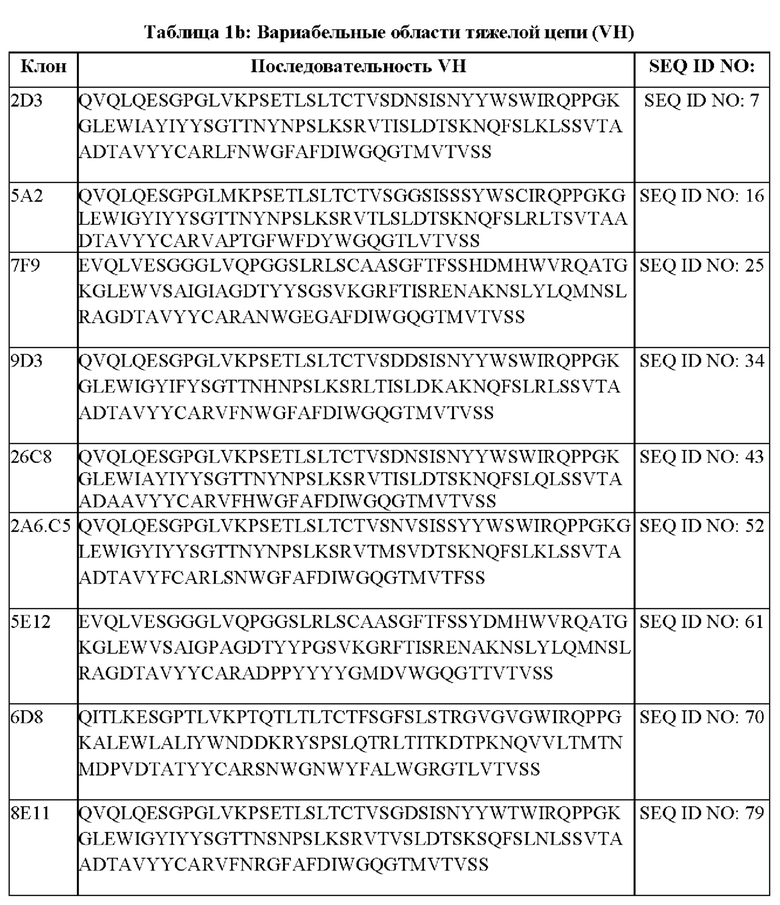
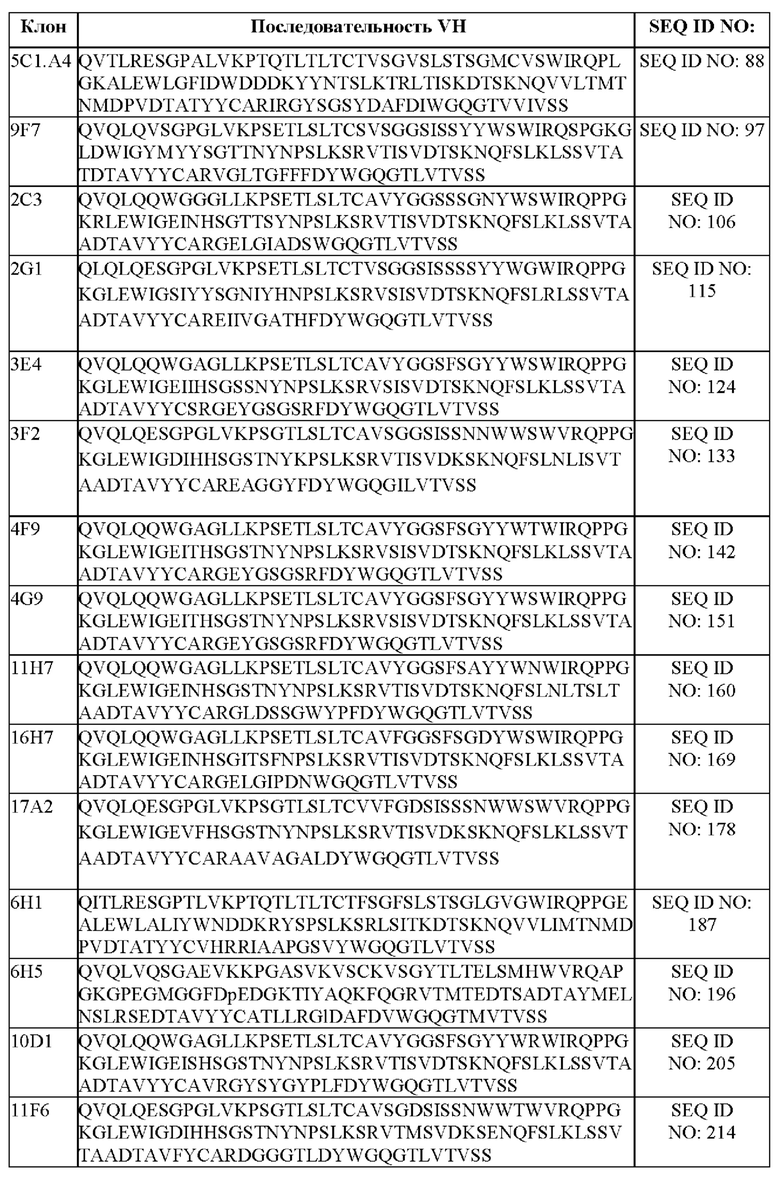
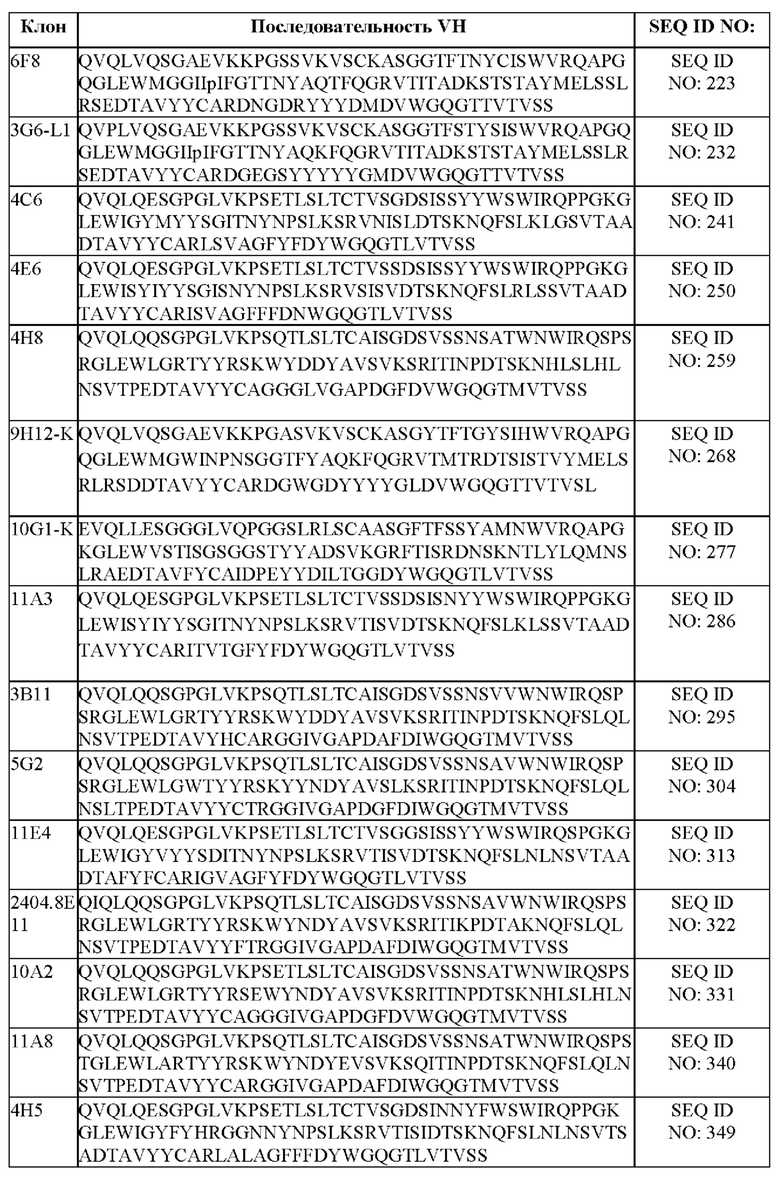
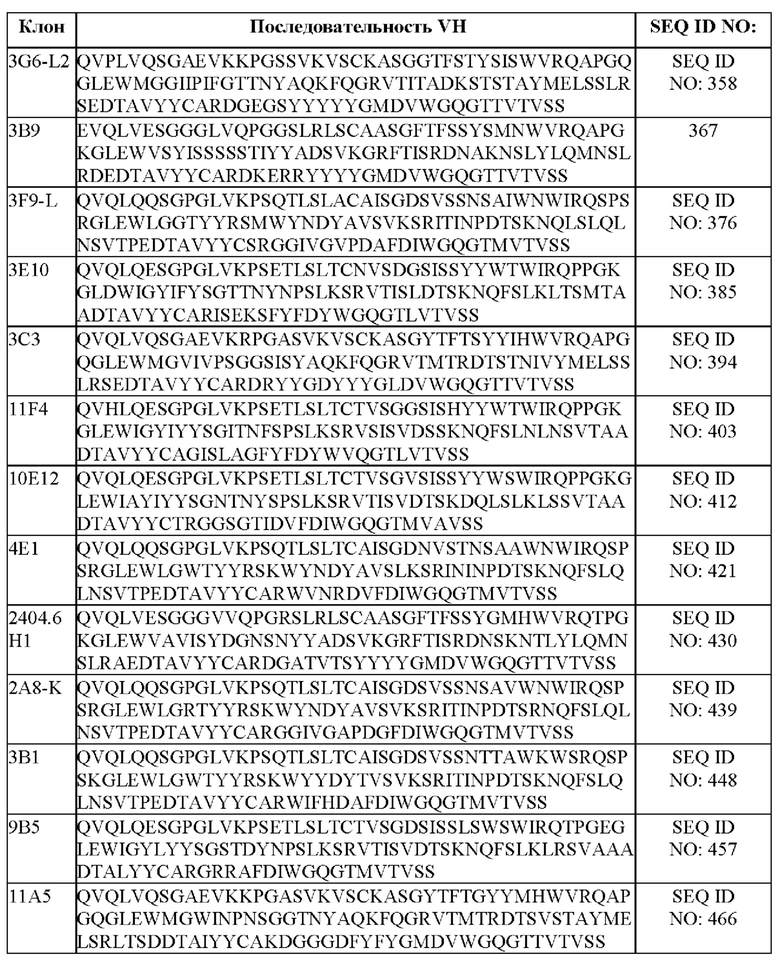
[050] В некоторых вариантах осуществления связывающий агент против DLL3 содержит последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную последовательности VH, представленной в таблице 1b.
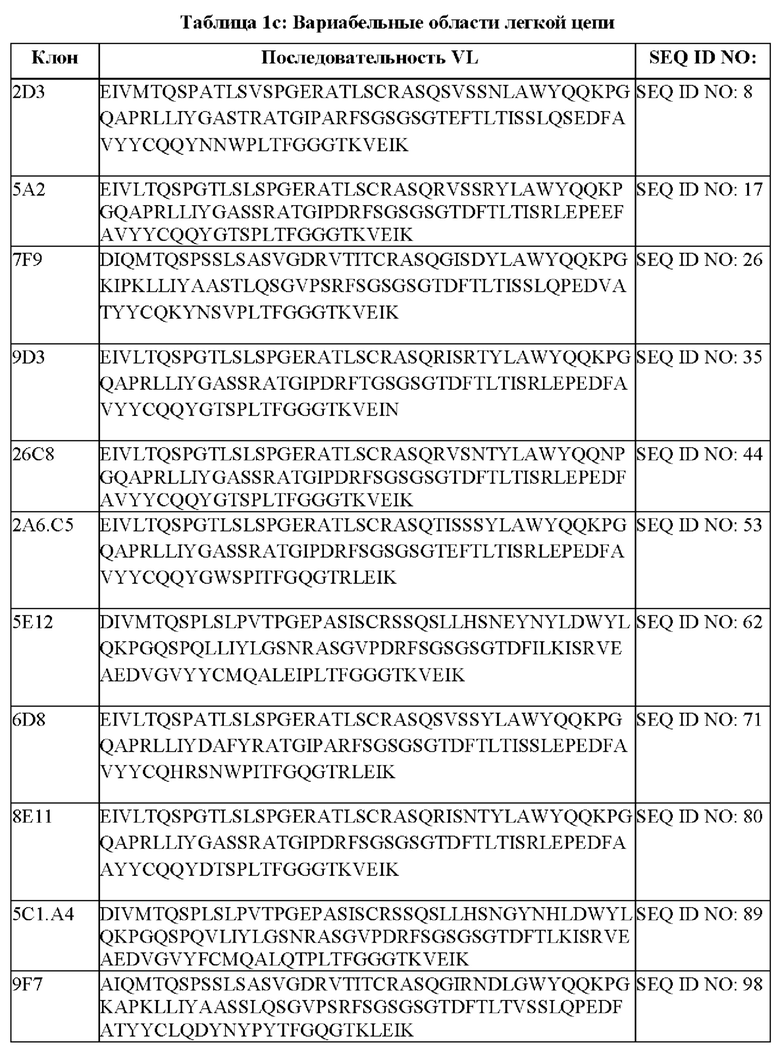
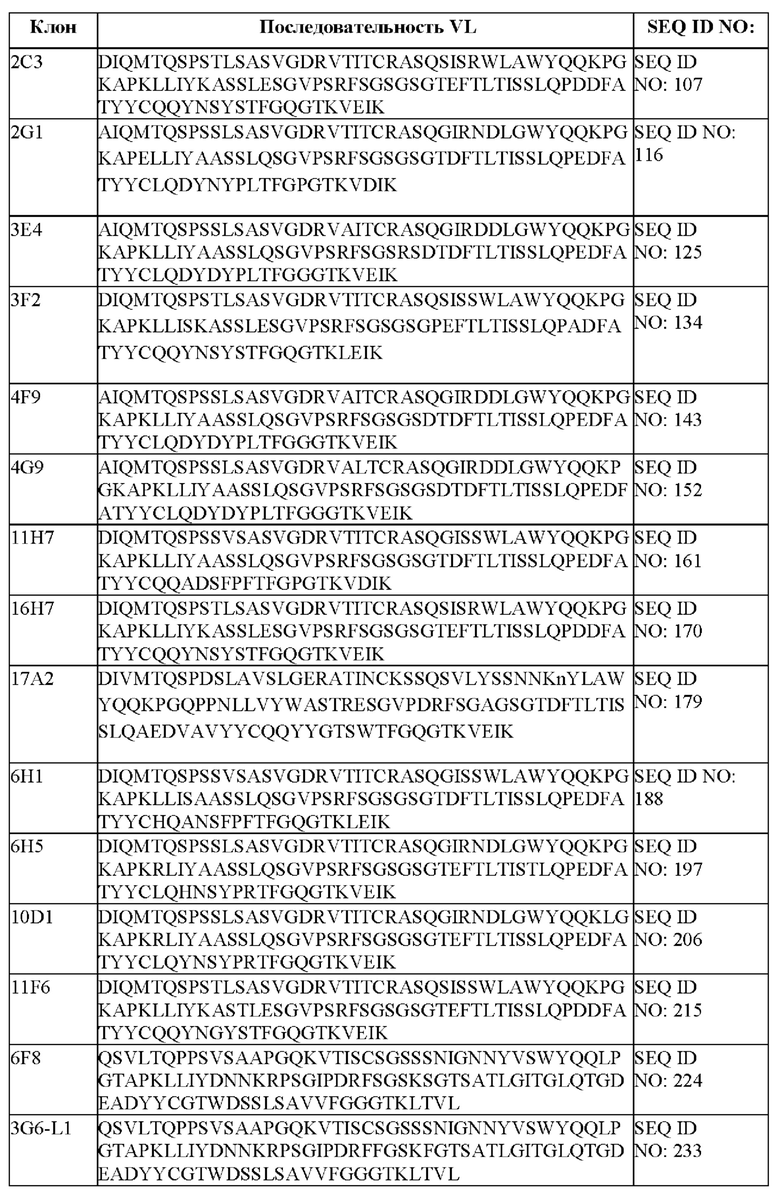
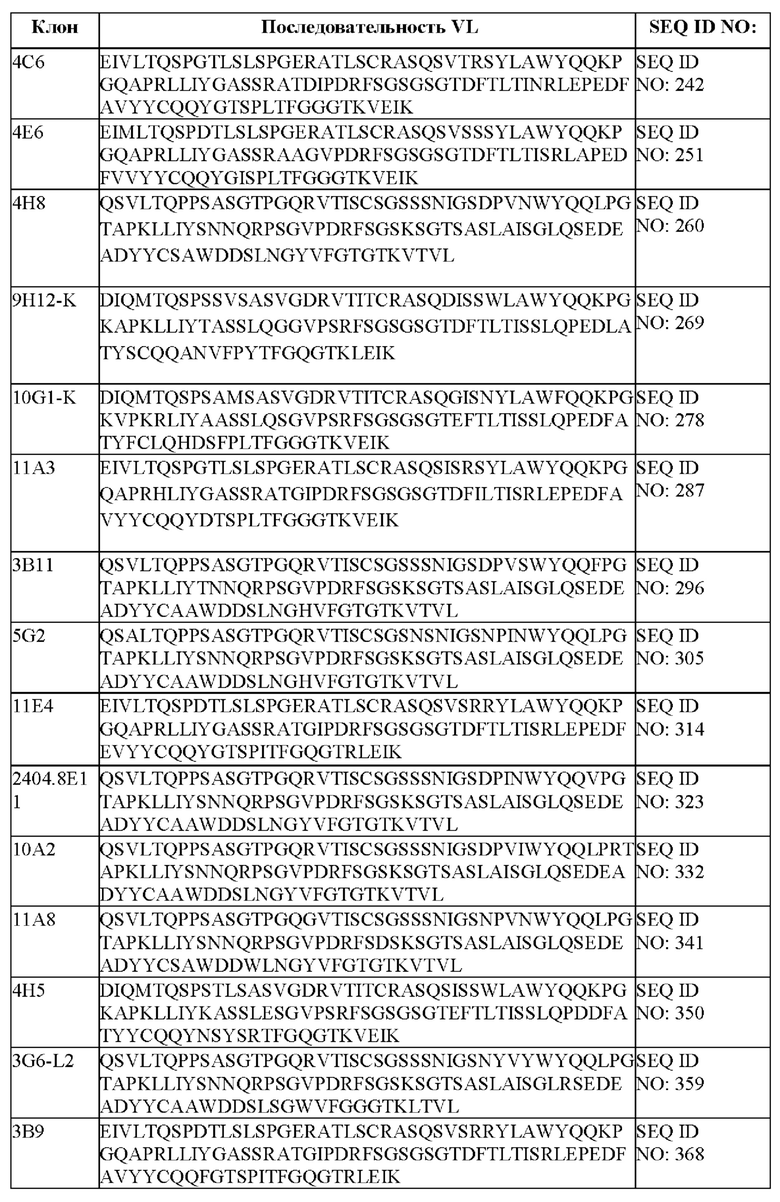
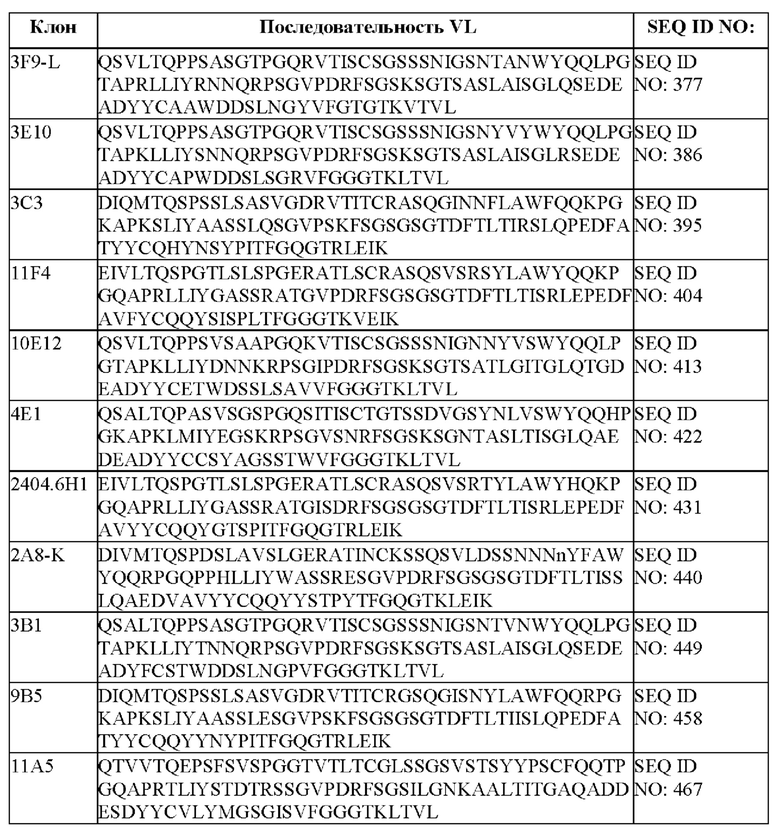
[051] В некоторых вариантах осуществления связывающий агент против DLL3 содержит последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную последовательности VL, представленной в таблице 1с.
[052] В некоторых вариантах осуществления связывающий агент против DLL3 содержит последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную последовательности scFv, представленной в таблице 1d.
[053] В некоторых вариантах осуществления связывающий агент против DLL3 представляет собой слитый белок, содержащий scFv-фрагмент, слитый с константной Fc-областью.
[054] В некоторых аспектах настоящее изобретение относится к фармацевтической композиции, содержащей связывающий агент против DLL3, раскрытый в настоящем документе, и фармацевтически приемлемое вспомогательное вещество.
[055] В некоторых аспектах настоящее изобретение относится к способу лечения заболевания или нарушения у нуждающегося в этом субъекта, включающему введение указанному субъекту связывающего агента против DLL3 или фармацевтической композиции, содержащей связывающий агент против DLL3, как раскрыто в настоящем документе.
[056] В некоторых вариантах осуществления заболевание или нарушение представляет собой рак.
[057] В некоторых вариантах осуществления заболевание или нарушение представляет собой мелкоклеточный рак легкого.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[058] ФИГ. 1А-1В представляют собой серию графиков, показывающих, что очищенные антитела против DLL3, описанные в настоящем документе, связываются с тремя линиями клеток мелкоклеточного рака легкого, экспрессирующих DLL3 (SHP-77, DMS 273 и DMS 454). Сплошная линия и пунктирная линия обозначают окрашивание антителами против DLL3 или контрольным мышиным антителом изотипа IgG2A, соответственно.
[059] ФИГ. 2A-2D демонстрируют результаты экспериментов по картированию эпитопов. ФИГ. 2А представляет собой схематическое изображение полноразмерных и усеченных белков DLL3 человека, экспрессируемых на клетках СНО для картирования эпитопа, и все белки были слиты на N-конце с НА-меткой для облегчения обнаружения. ФИГ. 2В и 2С демонстрируют аминокислотные последовательности полноразмерных и усеченных белков DLL3 человека, показанных на ФИГ. 2А. ФИГ. 2D представляет собой серию графиков, показывающих результаты картирования эпитопа антител против DLL3 и примеры антител против DLL3, распознающих домен DSL, EGF1 и EGF3, соответственно; по оси абсцисс показаны сигналы из канала РЕ, а по оси ординат счет клеток.
[060] ФИГ. 3А-3С представляют собой серию графиков и таблиц, показывающих структуру, эффективность трансдукции клеток от двух разных доноров и цитотоксическую активность анти-DLL3 CAR. ФИГ. 3А представляет собой схему конструкции, кодирующей анти-DLL3 CAR, содержащей, от N-конца к С-концу: scFv против DLL3, шарнирную и транс мембранную области из CD8α человека, цитоплазматическую область из 41ВВ человека и цитоплазматическую область из CD3ζ, человека. ФИГ. 3В демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR экспрессируются на поверхности первичных Т-клеток и могут распознавать рекомбинантный DLL3; графики гейтированы по живым CD3+ клеткам, а числа на графиках представляют собой процент клеток, экспрессирующих каждый анти-DLL3 CAR. ФИГ. 3С и 3D демонстрируют эффективность трансдукции анти-DLL3 CAR, содержащих последовательности scFv, описанные в настоящем документе.
[061] ФИГ. 4А-4С представляют собой серию графиков, демонстрирующих данные по уничтожению для некоторых анти-DLL3 CAR. ФИГ. 4А демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR-T-клетки специфически уничтожали клетки HEK-293Т, экспрессирующие DLL3 человека, но не родительские клетки HEK-293Т, в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор : мишень (Е:Т). Т-клетки, которые не экспрессировали анти-DLL3 CAR (помеченные как «пустой вектор»), использовали в качестве отрицательного контроля. ФИГ. 4В демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR-T-клетки уничтожали клетки SHP-77 и WM266.4, экспрессирующие эндогенный DLL3, в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор : мишень. ФИГ. 4С демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR-T-клетки уничтожали клетки мелкоклеточного рака легкого DMS 454 и DMS 273, экспрессирующие эндогенный DLL3, в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор : мишень. Для всех графиков на ФИГ. 4А-4С для оценки жизнеспособности клеток-мишеней была использована система анализа One-glo, n=3.
[062] ФИГ. 5 представляет собой серию гистограмм, показывающих, что анти-DLL3 CAR-T-клетки высвобождали цитокины после совместной инкубации с линией клеток SHP-77, экспрессирующей DLL3, когда CAR-T-клетки и клетки SHP-77 инкубировали при соотношении эффектор : мишень, равном 1:1 или 1:9, в течение 24 часов. Собирали супернатант и измеряли уровни IFN-γ, IL-2 и TNF-α с использованием набора proinflammory 9-plex от MSD, n=3.
[063] ФИГ. 6А-6В представляют собой графики, показывающие экспериментальные данные анализа последовательного уничтожения после многократного воздействия анти-DLL3 CAR-T-клеток на линию DLL3+ клеток. ФИГ. 6А демонстрирует последовательное уничтожение анти-DLL3 CAR-Т-клетками DLL3+ клеток WM266.4. Некоторые клоны оставались активными на 12-й день анализа. ФИГ. 6В демонстрирует последовательное уничтожение анти-DLL3 CAR-Т-клетками клеток DMS 454 и WM266.4. ФИГ. 6С демонстрирует последовательное уничтожение анти-DLL3 CAR-T линии мелкоклеточного рака легкого DMS 273. Для всех графиков на ФИГ. 6А-6С для оценки жизнеспособности клеток-мишеней была использована система анализа one-glo или CellTiter-glo, n=3-5.
[064] ФИГ. 7А-7В представляют собой графики, демонстрирующие, что анти-DLL3 CAR-T-клетки вызывали клиренс сформировавшихся подкожных опухолей мелкоклеточного рака легкого SHP-77 у мышей дозозависимым образом.
[065] ФИГ. 8 представляет собой график, демонстрирующий, что анти-DLL3 CAR-T-клетки 10G1-K ингибировали рост сформировавшихся внутривенно инъецированных опухолей мелкоклеточного рака легкого SHP-77 дозозависимым образом. Статистический анализ проводили с использованием ANOVA с повторными измерениями (множественные сравнения Даннета), день 14 - день 28, n=4-5. *, р<0,05. **, р<0,01.
[066] ФИГ. 9А-9С демонстрируют структуру, эффективность трансдукции первичных Т-клеток и цитотоксическую активность анти-DLL3 CAR с предохранительным переключателем. ФИГ. 9А представляет собой схемы, демонстрирующие структуру конструкций CAR с 4 различными предохранительными переключателями (QR3, SR2, RSR и R2S). ФИГ. 9В демонстрирует графики проточной цитометрии, показывающие, что анти-DLL3 CAR с предохранительными переключателями, показанными на ФИГ. 9А, экспрессируются на поверхности первичных Т-клеток и могут распознавать рекомбинантный DLL3. Графики гейтированы по живым CD3+ клеткам, а числа на графиках представляют собой процент клеток, экспрессирующих каждый анти-DLL3 CAR. ФИГ. 9С демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR с предохранительными переключателями активны в анализе последовательного уничтожения.
[067] ФИГ. 10А демонстрирует графики, показывающие, что две ксенотрансплантатные модели мелкоклеточного рака легкого, полученного от пациента (PDX), экспрессируют DLL3 на клеточной поверхности. Сплошная линия и пунктирная линия обозначают окрашивание антителами к DLL3 или флуоресценцию минус один (FMO), соответственно. ФИГ. 10В демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR проявляют цитотоксическую активность против тех же двух PDX-моделей.
[068] ФИГ. 11А-11В демонстрируют предохранительные переключатели, позволяющие обнаруживать и истощать DLL3 CAR-T-клетки с помощью ритуксимаба. ФИГ. 11А демонстрирует, что анти-DLL3 CAR-T-клетки 8E11-SR2 и 26C8-R2S окрашивали рекомбинантным DLL3 и РЕ-конъюгированным ритуксимабом через 14 дней после размножения и анализировали с помощью проточной цитометрии. Числа в квадрантах представляют процент от общего количества Т-клеток. ФИГ. 11В демонстрирует опосредованную ритуксимабом комплементзависимую цитотоксичность (КЗЦ) анти-DLL3 CAR-T-клеток 8Е11-SR2 и 26C8-R2S. CAR-T-клетки инкубировали в течение 3 часов с 25% комплемента крольчат и ритуксимабом, и оценивали цитотоксичность с помощью проточной цитометрии.
[069] ФИГ. 12А-12В демонстрируют графики, показывающие, что анти-DLL3 CAR-T-клетки с предохранительными переключателями подавляли рост опухолей мелкоклеточного рака легкого, вводимых подкожно или внутривенно. На ФИГ. 12А показано, что DLL3 CAR-T-клетки с предохранительными переключателями вызывали клиренс сформировавшихся подкожных опухолей мелкоклеточного рака легкого SHP-77 у мышей. ФИГ. 12В представляет собой график, демонстрирующий, что анти-DLL3 CAR-T-клетки ингибировали рост введенных в/в опухолей мелкоклеточного рака легкого DMS 273-DLL3.
[070] ФИГ. 13А демонстрирует репрезентативное изображение экспрессии РНК DLL3 мыши в головном мозге мышей NSG. Кружком обозначены кластеры РНК DLL3 мыши. ФИГ. 13В демонстрирует окрашивание антителом против человеческого CD3 образцов селезенки, гипофиза и мозга животных, которым вводили дозы нетрансдуцированных Т-клеток, DLL3 CAR-T-клеток 10G1-K или DLL3 CAR-T-клеток 2G1. Стрелки обозначают CD3-положительные клетки в образцах селезенки.
[071] ФИГ. 14A-14F демонстрируют план эксперимента и результаты исследования безопасности на мышах с использованием модели подкожной опухоли LN229-mDLL3. ФИГ. 14А демонстрирует экспериментальные группы и план эксперимента. ФИГ. 14В демонстрирует время сбора ткани и объем опухолей у животных, которые получали либо нетрансдуцированные Т-клетки, либо DLL3 CAR-T-клетки. ФИГ. 14С представляет собой таблицу, показывающую оценку окрашивания человеческого CD3 образцов головного мозга и гипофиза. ФИГ. 14D представляет собой таблицу, демонстрирующую гистологический анализ собранных образцов головного мозга и гипофиза. ФИГ. 14Е демонстрирует изображения образцов гипофиза, окрашенных антителом против вазопрессина. ФИГ. 14F демонстрирует изображения образцов гипофиза, окрашенных антителом против окситоцина.
[072] ФИГ. 15A-15D демонстрируют план эксперимента и результаты исследования безопасности на мышах с использованием модели внутричерепной опухоли LN229-mDLL3. ФИГ. 15А демонстрирует экспериментальные группы и план эксперимента. ФИГ. 15В демонстрирует время сбора ткани и объем опухолей у животных, которые получали нетрансдуцированные Т-клетки, DLL3 CAR-T-клетки или EGFRvIII CAR-T-клетки. ФИГ. 15С представляет собой таблицу, демонстрирующую оценку окрашивания человеческого CD45 образцов головного мозга, гипофиза и селезенки. ФИГ. 15D представляет собой таблицу, демонстрирующую гистологический анализ образцов головного мозга и гипофиза.
[073] ФИГ. 16А-16С демонстрируют экспериментальные данные по цитотоксичности in vitro диссоциированных клеток гипофиза мыши. ФИГ. 16А демонстрирует показатель цитотоксичности клеток-мишеней после 3-дневного совместного культивирования с DLL3 CAR-T-клетками, демонстрируя, что DLL3 CART не являются цитотоксичными в отношении клеток гипофиза мыши in vitro. ФИГ. 16В демонстрирует анализ методом проточной цитометрии окрашивания на поверхностные маркеры активации CD25 и 41ВВ Т-клеток, культивированных совместно с мишенями, демонстрирующий, что клетки гипофиза мыши не активируют DLL3 CAR-T in vitro. ФИГ. 16С демонстрирует цитокины, секретируемые в культуральной среде, проанализированные с помощью MSD, демонстрируя, что цитокины не секретируются после совместного культивирования клеток DLL3 CAR-T-клеток с клетками гипофиза мыши in vitro в течение 3 дней.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[074] В настоящем документе предложены DLL3-специфичные антитела и химерные антигенные рецепторы (CAR). DLL-3-специфичные CAR, описанные в настоящем документе, содержат внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и полинуклеотиды, кодирующие эти CAR. Также предложены иммунные клетки, содержащие эти DLL3-специфичные CAR, например, CAR-T-клетки, и фармацевтические композиции, содержащие эти иммунные клетки. Также раскрыты способы получения и применения этих DLL3-специфичных CAR и иммунных клеток, содержащих эти DLL3-специфичные CAR, например, для лечения рака.
I. Связывающие DLL-3 агенты
[075] В настоящем изобретении предложены связывающие DLL-3 агенты (например, молекулы, содержащие антигенсвязывающий домен против DLL3, антитела к DLL-3 или их фрагменты), которые специфически связываются с DLL-3. В контексте настоящего документа термин «антитело» относится к полипептиду, который включает элементы канонической последовательности иммуноглобулина, достаточные для обеспечения специфического связывания с определенным антигеном-мишенью (например, DLL-3). Как известно в данной области техники, интактные антитела, продуцируемые в природе, представляют собой тетрамерные агенты массой приблизительно 150 кДа, состоящие из двух идентичных полипептидов тяжелой цепи (приблизительно по 50 кДа каждый) и двух идентичных полипептидов легкой цепи (приблизительно по 25 кДа каждый), которые связываются друг с другом в то, что обычно называют «Y-образной» структурой. Каждая тяжелая цепь состоит из по меньшей мере доменов (каждый длиной приблизительно 110 аминокислот) - аминоконцевого вариабельного (VH) домена (расположенного на концах структуры Y), за которым следуют три константных домена: CH1, СН2 и карбоксиконцевой CH3 (расположенный в основании стебля Y). Короткая область, известная как «сайт переключения», соединяет вариабельную и константную области тяжелой цепи. «Шарнир» соединяет домены СН2 и СН3 с остальной частью антитела. Две дисульфидные связи в этой шарнирной области соединяют два полипептида тяжелой цепи друг с другом в интактном антителе. Каждая легкая цепь состоит из двух доменов - аминоконцевого вариабельного (VL) домена, за которым следует карбоксиконцевой константный (CL) домен, отделенных друг от друга еще одним «сайтом переключения». Специалисты в данной области хорошо знакомы со структурой антитела и элементами последовательностей, распознают «вариабельные» и «константные» области в предоставленных последовательностях и понимают, что может существовать некоторая гибкость в определении «границы» между такими доменами, так что разные представления одной и той же последовательности цепи антитела могут, например, указывать такую границу в месте, которое сдвинуто на один или несколько остатков относительно другого представления той же последовательности цепи антитела.
[076] Присвоение аминокислот каждому из каркасных, CDR и вариабельных доменов обычно соответствует схемам нумерации согласно Kabat (см., например, Kabat et al. in Sequences of Proteins of Immunological Interest, 5th Ed., NIH Publication 91-3242, Bethesda Md. 1991), Chothia (см., например, Chothia & Lesk, (1987), J Mol Biol 196: 901-917; Al-Lazikani et al., (1997) J Mol Biol 273: 927-948; Chothia et al., (1992) J Mol Biol 227: 799-817; Tramontano et al., (1990) J Mol Biol 215 (1): 175-82 и патент США №7709226), контактному определению или схеме AbM (Antibody Modeling program, Oxford Molecular).
[077] Соответственно, в некоторых вариантах осуществления CDR связывающих DLL3 агентов, предложенных в настоящем документе, пронумерованы в соответствии со схемой нумерации согласно Kabat. В других вариантах осуществления CDR связывающих DLL3 агентов, предложенных в настоящем документе, пронумерованы в соответствии со схемой нумерации согласно Chothia. В других вариантах осуществления CDR связывающих DLL3 агентов, предложенных в настоящем документе, пронумерованы в соответствии со схемой нумерации согласно контактному определению. В других вариантах осуществления CDR связывающих DLL3 агентов, предложенных в настоящем документе, пронумерованы в соответствии со схемой нумерации согласно AbM.
[078] Тетрамеры интактных антител состоят из двух димеров тяжелая цепь - легкая цепь, в которых тяжелая и легкая цепи связаны друг с другом одной дисульфидной связью; две другие дисульфидные связи соединяют шарнирные области тяжелой цепи друг с другом, так что димеры соединяются друг с другом и образуется тетрамер. Антитела, продуцируемые естественным путем, также гликозилируются, как правило, по СН2-домену. Каждый домен в природном антителе имеет структуру, характеризующуюся «иммуноглобулиновой складкой», образованной двумя бета-листами (например, 3-, 4- или 5-нитевыми листами), упакованными друг напротив друга в сжатый антипараллельный бета-цилиндр. Каждый вариабельный домен содержит три гипервариабельные петли, известные как «определяющие комплементарность области» (CDR1, CDR2 и CDR3), и четыре в некоторой степени инвариантные «каркасные» области (FR1, FR2, FR3 и FR4). Когда естественные антитела складываются, FR-области образуют бета-листы, которые обеспечивают структурную основу для доменов, а области петель CDR как тяжелой, так и легкой цепей объединяются в трехмерном пространстве, так что они создают единый гипервариабельный антигенсвязывающий сайт, расположенный на вершине Y-структуры. Fc-область природных антител связывается с элементами системы комплемента, а также с рецепторами на эффекторных клетках, включая, например, эффекторные клетки, которые опосредуют цитотоксичность. Как известно в данной области техники, аффинность и/или другие характеристики связывания Fc-областей с Fc-рецепторами можно модулировать посредством гликозилирования или другой модификации. В некоторых вариантах осуществления антитела, продуцируемые и/или используемые в соответствии с настоящим изобретением, включают гликозилированные Fc-домены, включая Fc-домены с модифицированным или сконструированным гликозилированием.
[079] В контексте настоящего изобретения в отдельных вариантах осуществления любой полипептид или комплекс полипептидов, который включает в себя достаточные последовательности иммуноглобулиновых доменов, которые содержатся в природных антителах, можно назвать и/или использовать как «антитело», независимо от того, продуцируется ли такой полипептид в естественных условиях (например, генерируется организмом, реагирующим на антиген), или получен методами рекомбинантной инженерии, химическим синтезом или путем другой искусственной системы или методики. В некоторых вариантах осуществления антитело является поликлональным; в некоторых вариантах осуществления антитело является моноклональным. В некоторых вариантах осуществления антитело имеет последовательности константной области, которые характерны для антител мыши, кролика, приматов или человека. В некоторых вариантах осуществления элементы последовательности антитела являются гуманизированными, приматизированными, химерными и т.д., как известно в данной области техники.
[080] Более того, в контексте настоящего документа термин «антитело» может относиться в соответствующих вариантах осуществления (если иное не указано или не следует из контекста) к любым из известных или разработанных конструкций или форматов для использования структурных и функциональных признаков антитела в альтернативном представлении. Например, в некоторых вариантах осуществления антитело, используемое в соответствии с настоящим изобретением, находится в формате, выбранном из, не ограничиваясь перечисленным, интактных антител IgA, IgG, IgE или IgM; би- или мультиспецифичных антител (например, Zybodies®, и т.д.); фрагментов антител, таких как Fab-фрагменты, Fab'-фрагменты, Е(ab’)2-фрагменты, Fd'-фрагменты, Fd-фрагменты и выделенные CDR или их наборы; одноцепочечных Fvs; слияний полипептид-Fc; однодоменных антител (например, однодоменных акульих антител, таких как IgNAR или их фрагментов); антител верблюдовых; маскированных антител (например, Probody®); иммунофармацевтических средств на основе модульного белка малого размера (SMIP™); одноцепочечных или тандемных диатела (TandAb®); VHH; Anticalin®; минител Nanobody®; BiTE®; белков с анкириновыми повторами или DARPIN®; Avimer®; DART; TCR-подобных антител; Adnectin®; Affilin®; Trans-body®; Affibody®; TrimerX®; MicroProtein; Fynomer®, Centyrin® и KALBITOR®. В некоторых вариантах осуществления в антителе может отсутствовать ковалентная модификация (например, присоединение гликана), которая бы в нем присутствовала, если бы оно было получено естественным путем. В некоторых вариантах осуществления антитело может содержать ковалентную модификацию (например, присоединение гликана, полезную нагрузку (например, детектируемый фрагмент, терапевтический фрагмент, каталитический фрагмент и т.д.) или другую боковую группу (например, полиэтиленгликоль и т.д.).
[081] Антитела включают фрагменты антител. Антитела также включают, не ограничиваясь перечисленным, поликлональные, моноклональные, химерные dAb (доменные антитела), одноцепочечные, Fab, Fa, F(ab)2-фрагменты, scFv и библиотеки экспрессии Fab. Антитело может представлять собой целое антитело, иммуноглобулин или фрагмент антитела.
[082] Как подробно описано выше, целые антитела состоят из двух пар «легкая цепь» (LC) и «тяжелая цепь» (НС) (такие пары легкой цепи (LC)/тяжелой цепи сокращенно обозначены в настоящем документе как LC/HC). Легкие и тяжелые цепи таких антител представляют собой полипептиды, состоящие из нескольких доменов. В целом антителе каждая тяжелая цепь содержит вариабельную область тяжелой цепи (сокращенно обозначаемую в настоящем документе как HCVR или VH) и константную область тяжелой цепи. Константная область тяжелой цепи содержит константные домены тяжелой цепи CH1, СН2 и СН3 (классы антител IgA, IgD и IgG) и необязательно константный домен тяжелой цепи СН4 (классы антител IgE и IgM). Каждая легкая цепь содержит вариабельный домен легкой цепи VL и константный домен легкой цепи CL. Вариабельные домены VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые определяющими комплементарность областями (CDR), перемежающиеся более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от аминоконца к карбоксиконцу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4 (Janeway, С.A., Jr, et al, (2001). knmunobiology., 5th ed., Garland Publishing; и Woof, J., Burton, D., Nat Rev Immunol 4 (2004) 89-99). Две пары тяжелой цепи и легкой цепи (HC/LC) способны специфично связываться с одним и тем же антигеном. Таким образом, указанное целое антитело представляет собой двухвалентное моноспецифическое антитело. Такие «антитела» включают, например, мышиные антитела, человеческие антитела, химерные антитела, гуманизированные антитела и геннетически модифицированные антитела (вариантные или мутантные антитела), при условии сохранения их характерных свойств. В некоторых вариантах осуществления антитела или связывающие агенты представляют собой гуманизированные антитела, особенно в виде рекомбинантных человеческих или гуманизированных антител.
[083] В некоторых вариантах осуществления антитело или связывающий агент могут быть «симметричными». Под «симметричным» подразумевается, что антитело или связывающий агент имеет один и тот же тип областей Fv (например, антитело имеет две области Fab). В некоторых вариантах осуществления антитело или связывающий агент могут быть «асимметричными». Под «асимметричным» подразумевается, что антитело или связывающий агент имеет по меньшей мере два различных типа областей Fv (например, антитело имеет: области Fab и scFv, области Fab и scFv2 или области Fab-VHH). В данной области техники известны различные асимметричные архитектуры антител или связывающих агентов (Brinkman and Kontermann et al. 2017 Mabs (9) (2): 182-212).
[084] В контексте настоящего документа термин «агент-антитело» относится к агенту, который специфично связывается с конкретным антигеном. В некоторых вариантах осуществления этот термин охватывает любой полипептид или полипептидный комплекс, который включает структурные элементы иммуноглобулина, достаточные для обеспечения специфичного связывания. Примеры агентов антител включают, не ограничиваясь перечисленным, моноклональные антитела или поликлональные антитела. В некоторых вариантах осуществления агент антитела может включать одну или более последовательностей константной области, которые характерны для антител мыши, кролика, приматов или человека. В некоторых вариантах осуществления агент антитела может включать один или более элементов последовательности, являющихся гуманизированными, приматизированными, химерными и т.д., как известно в данной области техники. Во многих вариантах осуществления термин «агент антитела» используется для обозначения одной или более известных из области техники или разработанных конструкций или форматов для использования структурных и функциональных характеристик антитела в альтернативном представлении. Например, агент антитела, используемый в соответствии с настоящим изобретением, находится в формате, выбранном из, не ограничиваясь перечисленным, интактных антител IgA, IgG, IgE или IgM; би- или мультиспецифичных антител (например, Zybodies®, и т.д.); фрагментов антител, таких как Fab-фрагменты, Fab'-фрагменты, Е(ab’)2-фрагменты, Fd'-фрагменты, Fd-фрагменты и выделенные CDR или их наборы; одноцепочечных Fvs; слияний полипептид-Fc; однодоменных антител (например, однодоменных акульих антител, таких как IgNAR или их фрагментов); антител верблюдовых; маскированных антител (например, Probody®); иммунофармацевтических средств на основе модульного белка малого размера (SMIP™); одноцепочечных или тандемных диател (TandAb®); VHH; Anticalin®; минител Nanobody®; BiTE®; белков с анкириновыми повторами или DARPIN®; Avimer®; DART; TCR-подобных антител; Adnectin®; Affilin®; Trans-body®; Affibody®; TrimerX®; MicroProtein; Fynomer®, Centyrin® и KALBITOR®.
[085] В некоторых вариантах осуществления в антителе может отсутствовать ковалентная модификация (например, присоединение гликана), которая бы в нем присутствовала, если бы оно было получено естественным путем. В некоторых вариантах осуществления антитело может содержать ковалентную модификацию (например, присоединение гликана, полезную нагрузку (например, детектируемый фрагмент, терапевтический фрагмент, каталитический фрагмент и т.д.) или другую боковую группу (например, полиэтиленгликоль и т.д.). Во многих вариантах осуществления агент антитела представляет собой или содержит полипептид, аминокислотная последовательность которого включает один или более структурных элементов, признанных специалистами в данной области техники определяющей комплементарность областью (CDR); в некоторых вариантах осуществления агент антитела представляет собой или содержит полипептид, аминокислотная последовательность которого включает по меньшей мере одну CDR (например, по меньшей мере одну CDR тяжелой цепи и/или по меньшей мере одну CDR легкой цепи), которая по существу идентична содержащейся в референсном антителе. В некоторых вариантах осуществления агент антитела представляет собой или содержит полипептид, аминокислотная последовательность которого включает структурные элементы, признанные специалистами в данной области вариабельным доменом иммуноглобулина. В некоторых вариантах осуществления агент антитела представляет собой полипептидный белок, имеющий связывающий домен, который гомологичен или в значительной степени гомологичен иммуноглобулин-связывающему домену.
[086] Антитело или антигенсвязывающая молекула, кодируемая согласно настоящему изобретению, может быть одноцепочечной или двухцепочечной. В некоторых вариантах осуществления антитело или антигенсвязывающая молекула является одноцепочечной. В некоторых вариантах осуществления антигенсвязывающая молекула выбрана из группы, состоящей из scFv, Fab, Fab', Fv, F(ab')2, dAb и любой их комбинации.
[087] В некоторых вариантах осуществления выделяют агент антитела против DLL-3. В некоторых вариантах осуществления агент антитела может быть очищен до чистоты более 95% или 99%, при определении, например, электрофоретическим методом (например, SDS-PAGE, изоэлектрическое фокусирование (IEF), капиллярный электрофорез) или хроматографией (например, ионообменной или обращенно-фазовой ВЭЖХ) (см., например, Flatman et al., J. Chromatogr., В 848: 79-87 (2007)). В некоторых аспектах настоящее изобретение относится к композиции, содержащей связывающий DLL-3 агент (например, антитело, специфичное к DLL3) и фармацевтически приемлемый носитель.
[088] В некоторых вариантах осуществления агент антитела против DLL-3 содержит Fc. Fc-домены могут взаимодействовать с рецепторами клеточной поверхности, что позволяет антителам активировать иммунную систему. В изотипах антител IgG, IgA и IgD Fc-область состоит из двух идентичных фрагментов белка, полученных из второго и третьего константных доменов двух тяжелых цепей антитела; Fc-области IgM и IgE содержат три константных домена тяжелой цепи (CH-домены 2-4) в каждой полипептидной цепи. Fc-области IgG могут нести высококонсервативный сайт N-гликозилирования (N297). Гликозилирование Fc-фрагмента может быть принципиально важным для активности, опосредованной Fc-рецептором. Присоединенные к этому сайту N-гликаны могут быть преимущественно фукозилированными по ядру диантенными структурами сложного типа.
[089] Хотя константные области легкой и тяжелой цепей могут не участвовать напрямую в связывании антитела с антигеном, константные области могут влиять на ориентацию вариабельных областей. Константные области могут также проявлять различные эффекторные функции, такие как участие в антителозависимом комплемент-опосредованном лизисе или антителозависимой клеточной токсичности через взаимодействия с эффекторными молекулами и клетками.
[090] Раскрытые агенты антител против DLL-3 могут быть антителами любого изотипа, включая изотип IgA, изотип IgD, изотип IgE, изотип IgG или изотип IgM. В некоторых вариантах осуществления антитело против DLL-3 содержит константный домен IgG1, IgG2, IgG3 или IgG4.
[091] В настоящем документе предложены связывающие DLL3 агенты (например, антитела), которые могут связываться с различными областями или доменами мишени DLL3. Эпитоп может представлять собой, например, смежные аминокислоты мишени DLL3 (линейный или непрерывный эпитоп) или быть составлен из двух или более несмежных областей мишени DLL3 (конформационный, нелинейный, прерывистый или несмежный эпитоп). Эпитоп, с которым связывается антигенсвязывающий домен против DLL3, может быть определен с помощью различных анализов, например, ЯМР-спектроскопии, рентгеноструктурных кристаллографических исследований, анализов ELISA, водородно-дейтериевого обмена в сочетании с масс-спектрометрией (например, жидкостной хроматографией с масс-спектрометрией с ионизацией электроспреем), основанных на матрице анализов олигопептидного сканирования, проточной цитометрии и/или картирования мутагенеза (например, картирования сайт-направленного мутагенеза).
[092] Иллюстративные области или домены DLL3 показаны на ФИГ. 2. Иллюстративные антитела против DLL3, описанные в настоящем документе, связываются с доменами DLL3, представленными в таблице 1а.

[093] В некоторых вариантах осуществления связывающий DLL3 агент содержит вариабельную тяжелую цепь (VH), где аминокислотная последовательность VH выбрана из последовательностей VH, представленных в таблице 1b. В некоторых вариантах осуществления связывающий агент против DLL-3 содержит тяжелую цепь иммуноглобулина, обладающую по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью аминокислотной последовательности, представленной в таблице 1b.
[094] В некоторых вариантах осуществления связывающий DLL3 агент содержит вариабельную легкую цепь (VL), где аминокислотная последовательность VL выбрана из последовательностей VL, представленных в таблице 1с. В некоторых вариантах осуществления связывающий агент против DLL-3 содержит легкую цепь иммуноглобулина, обладающую по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичностью аминокислотной последовательности, представленной в таблице 1 с.
[095] В настоящем документе предложены связывающие DLL3 агенты (например, антитела), где антигенсвязывающий домен против DLL3 содержит вариабельную тяжелую цепь (VH) и вариабельную легкую цепь, где аминокислотная последовательность VH выбрана из последовательностей VH, представленных в таблице 1b; и аминокислотная последовательность VL выбрана из последовательностей VL, представленных в таблице 1с.
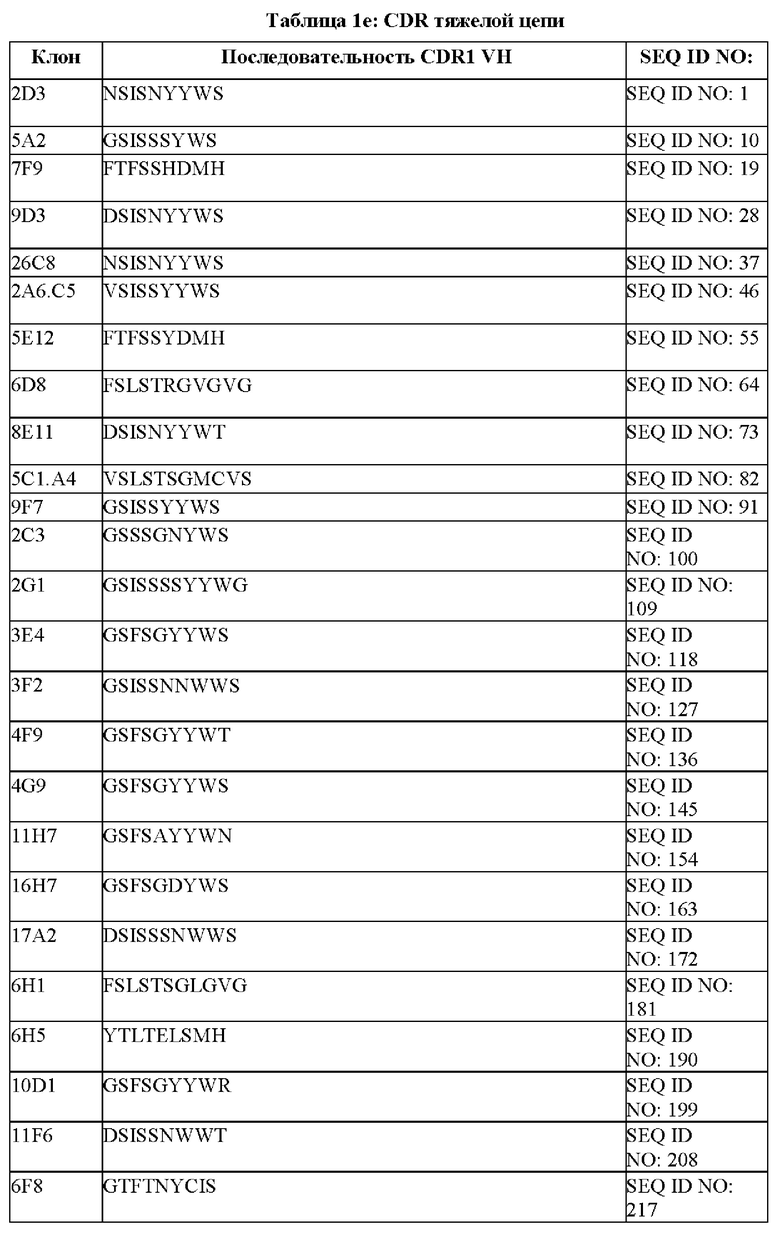
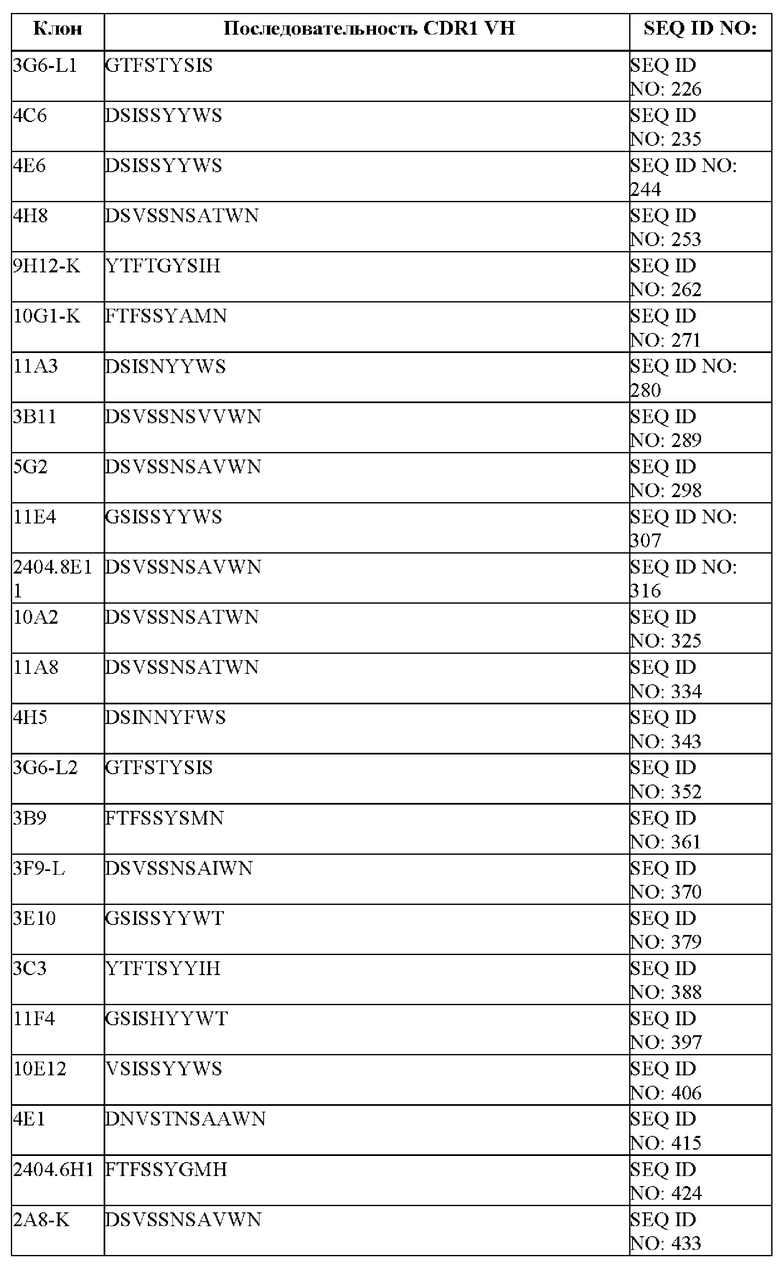
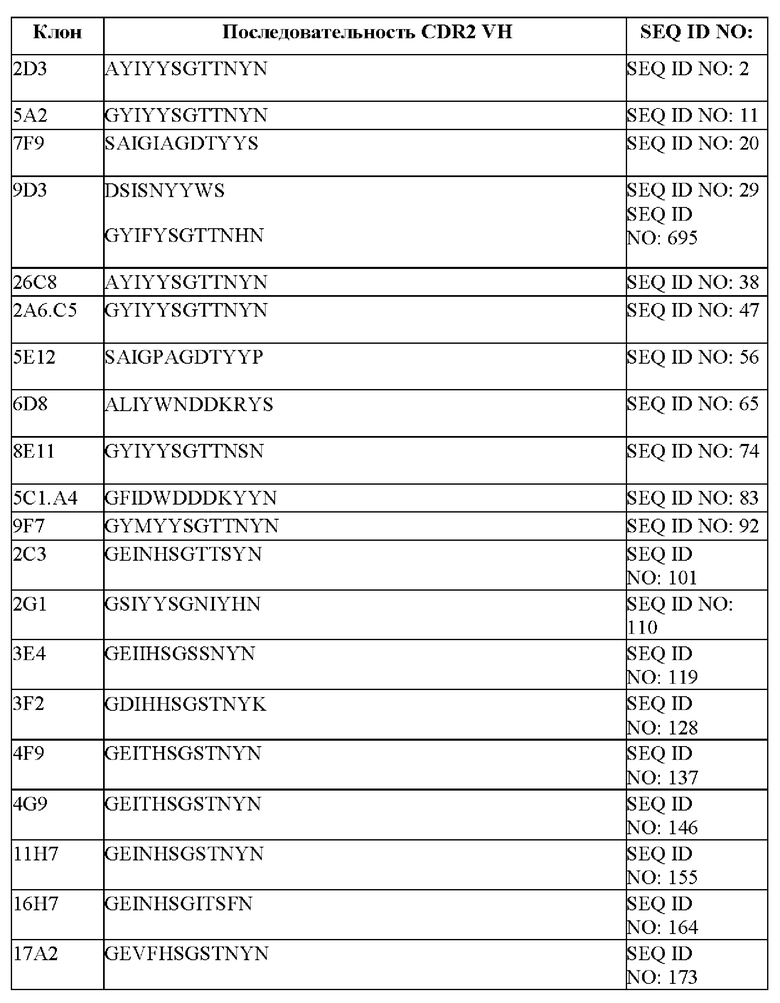
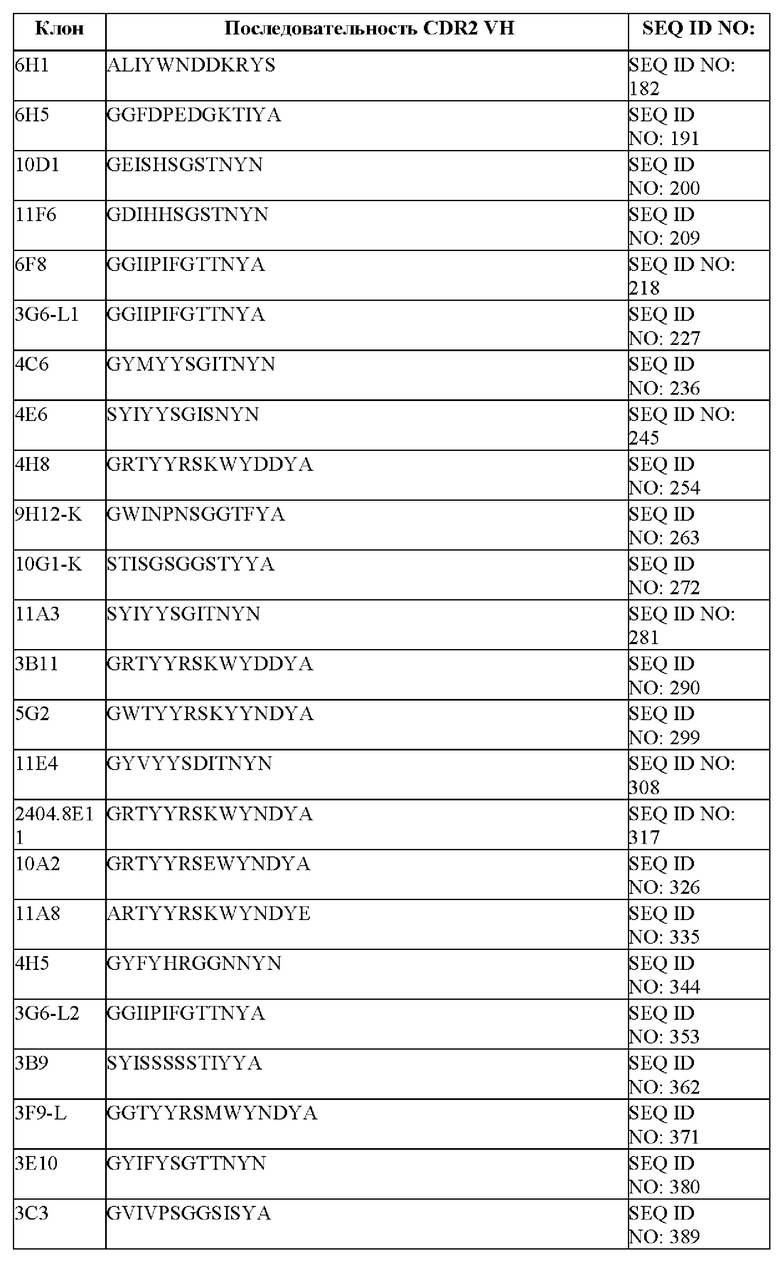
[096] В некоторых вариантах осуществления связывающий DLL-3 агент содержит CDR1, CDR2 и CDR3 тяжелой цепи. В некоторых вариантах осуществления последовательности CDR1, CDR2 и CDR3 тяжелой цепи выбраны из CDR тяжелой цепи, представленных в таблице 1е.

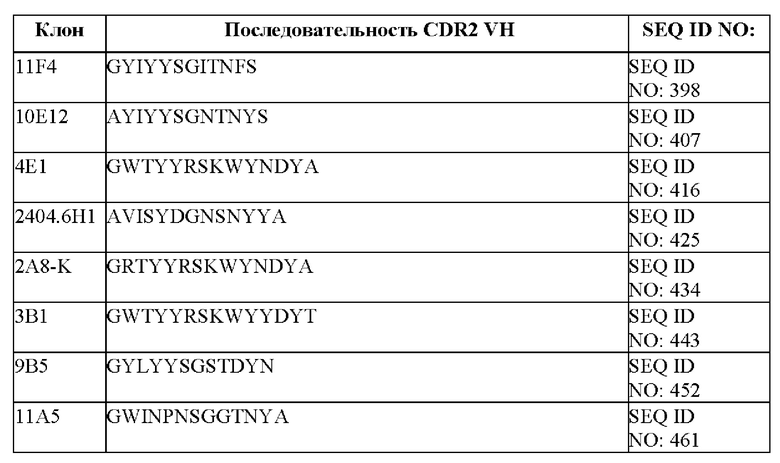
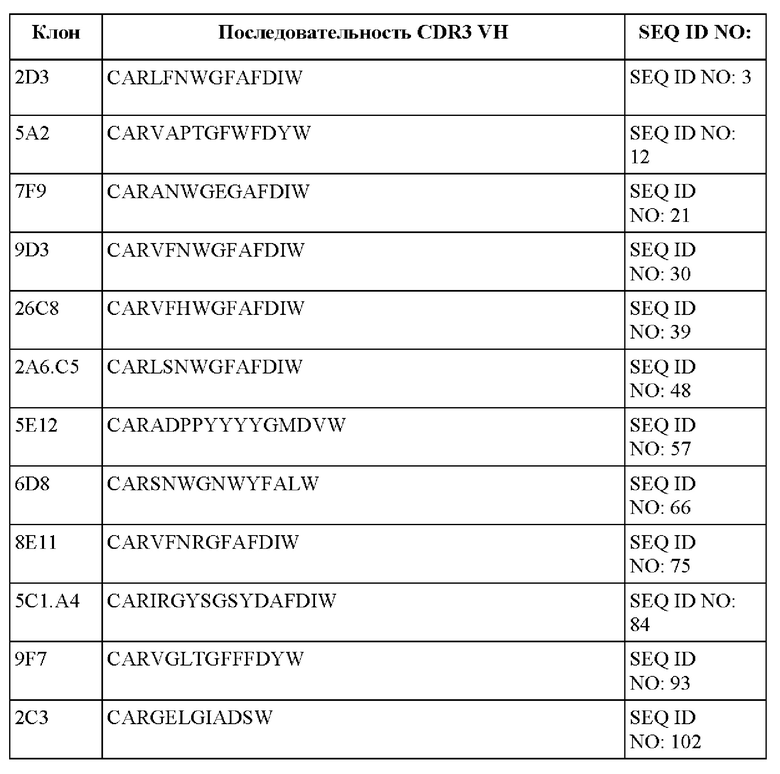
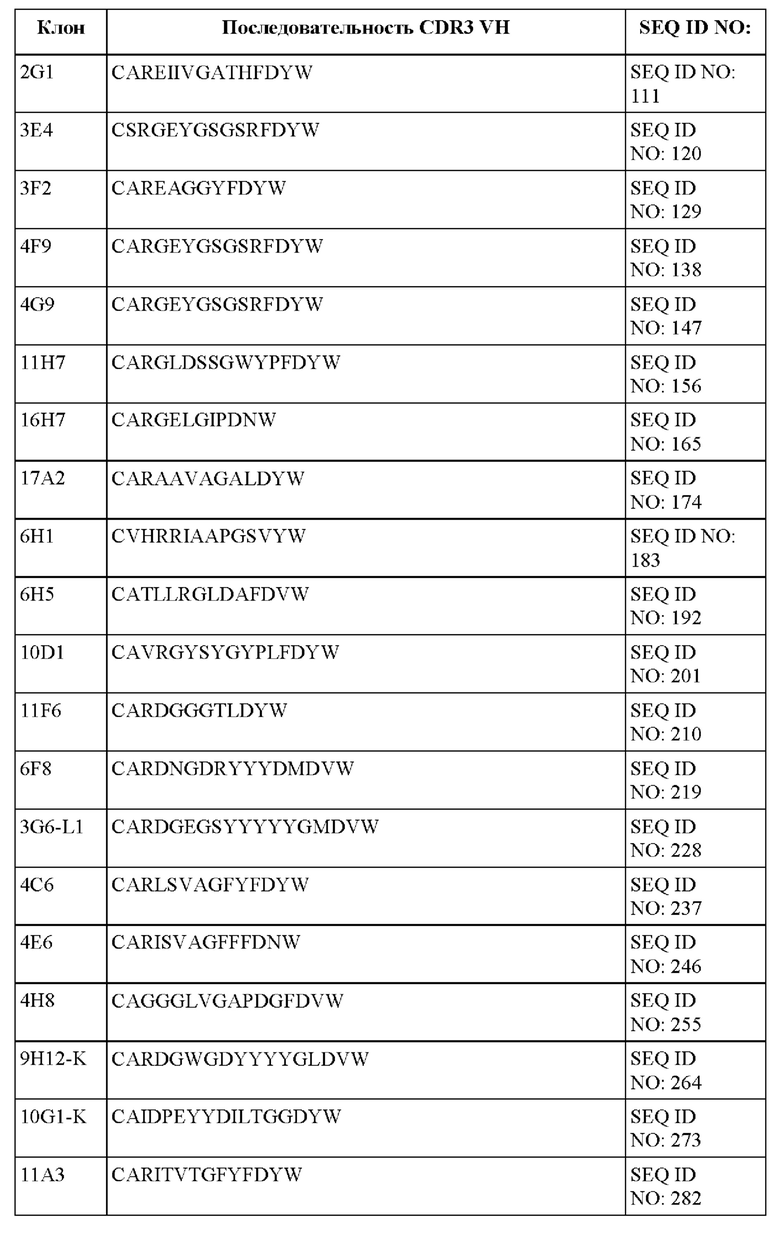
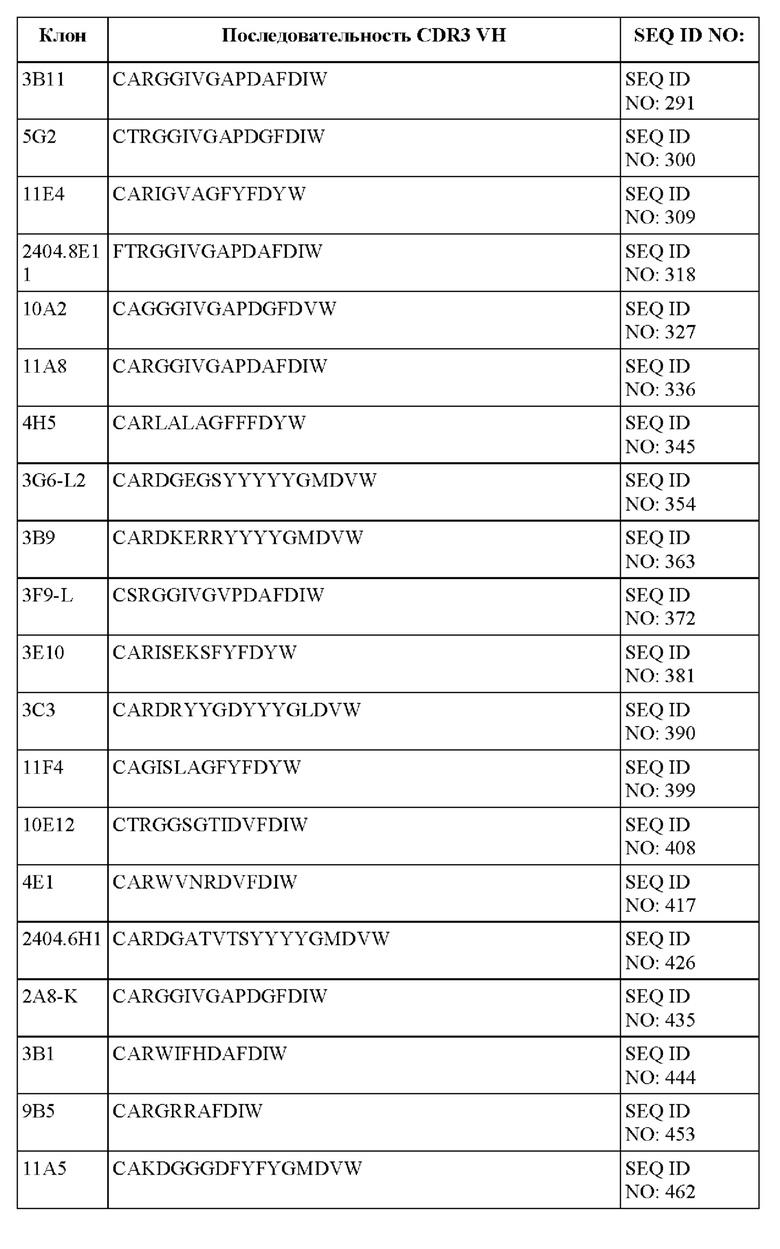
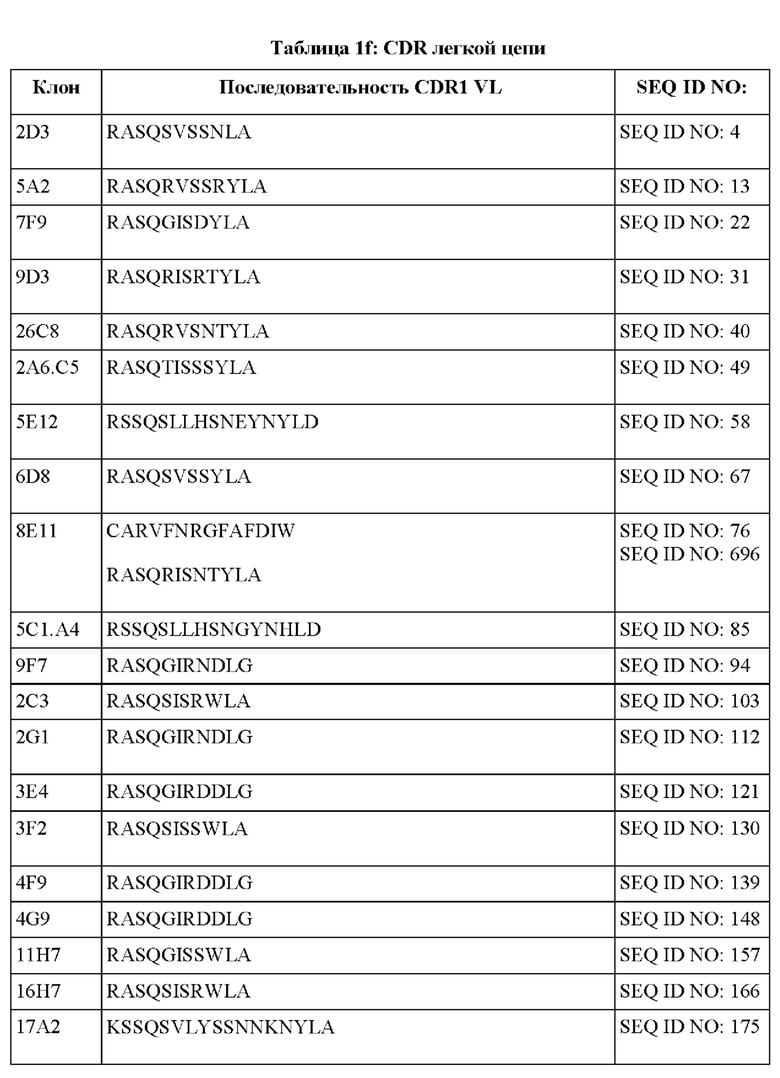
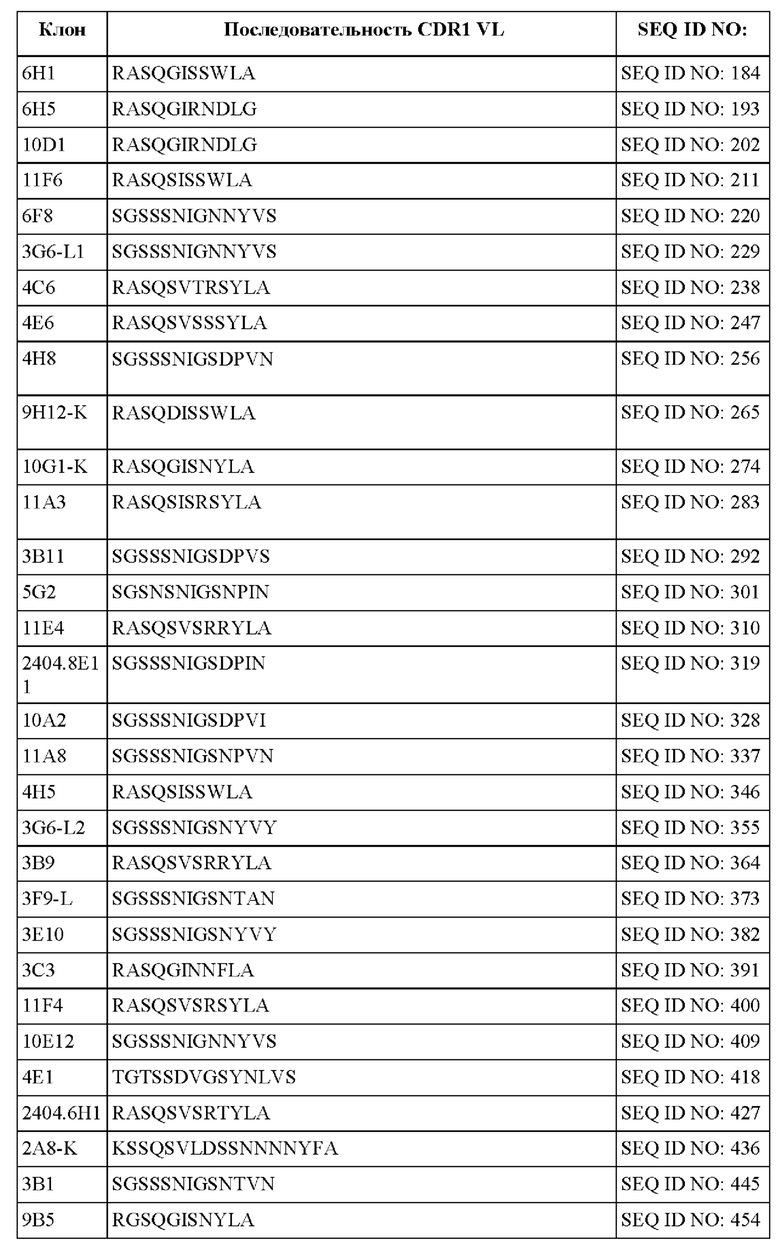
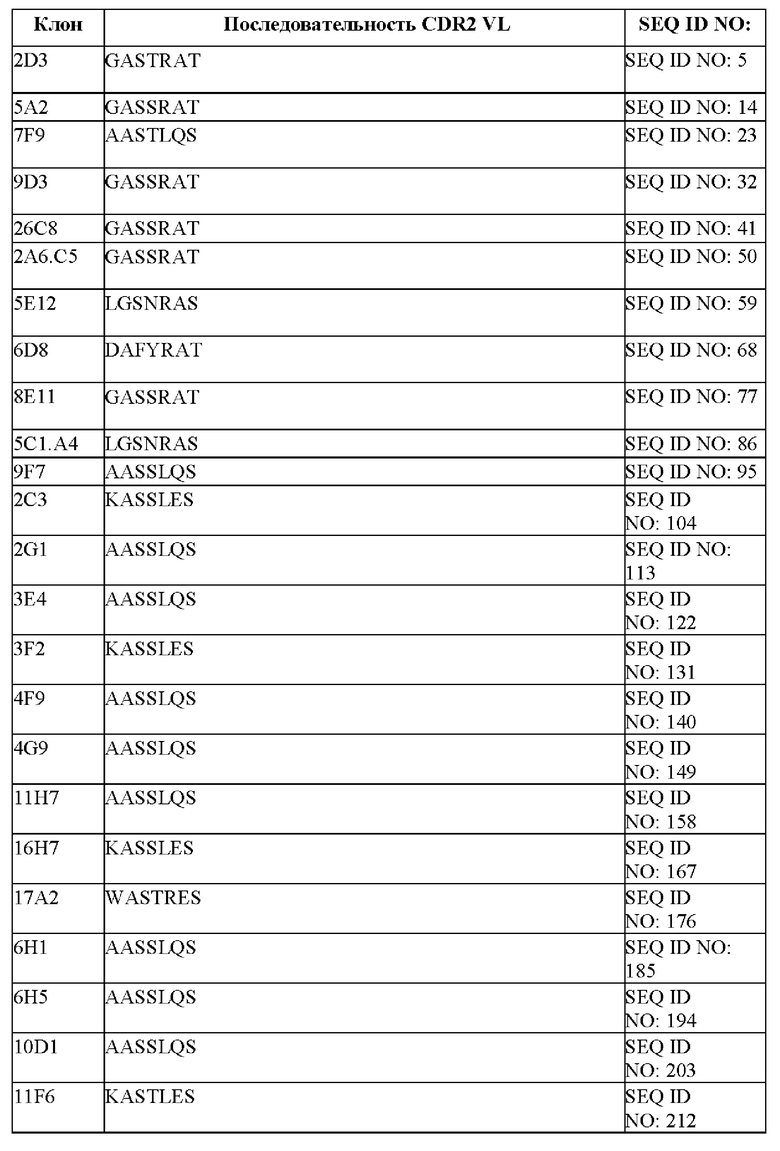
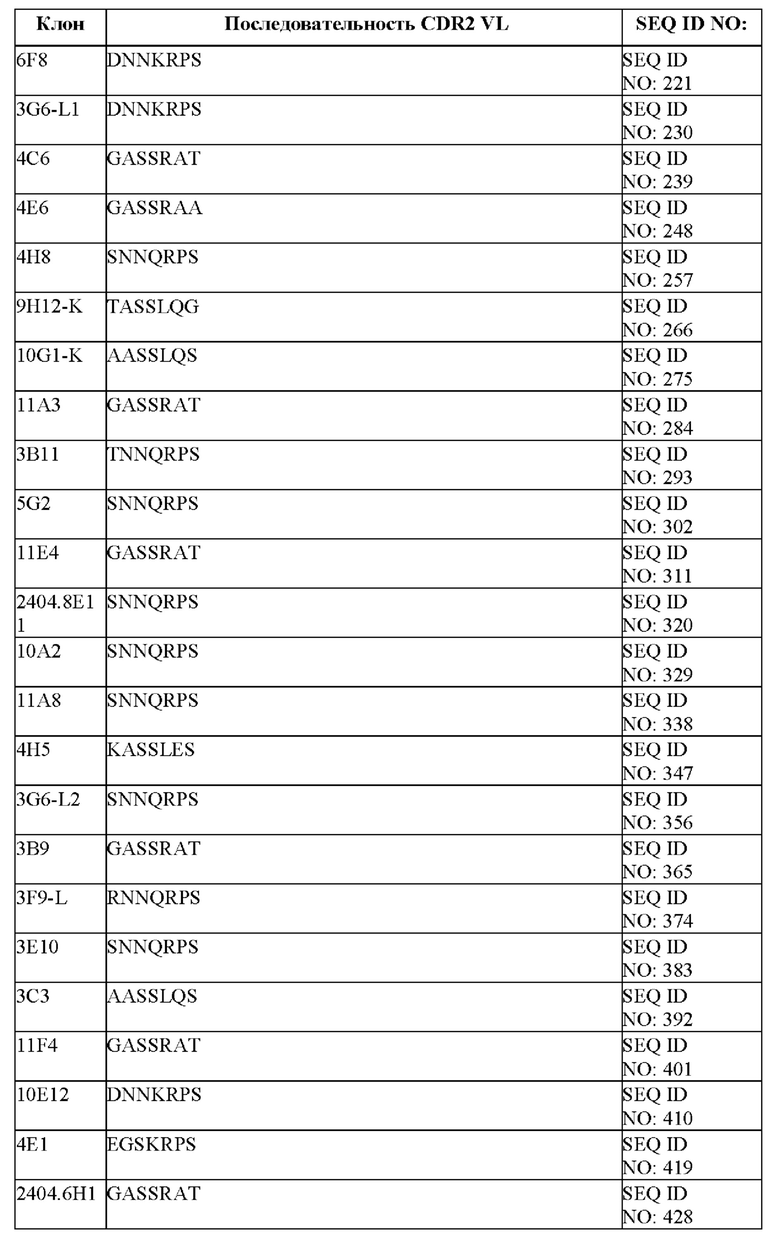
[097] В некоторых вариантах осуществления связывающий DLL-3 агент содержит CDR1, CDR2 и CDR3 легкой цепи. В некоторых вариантах осуществления последовательности CDR1, CDR2 и CDR3 легкой цепи выбраны из CDR легкой цепи, представленных в таблице 1f.



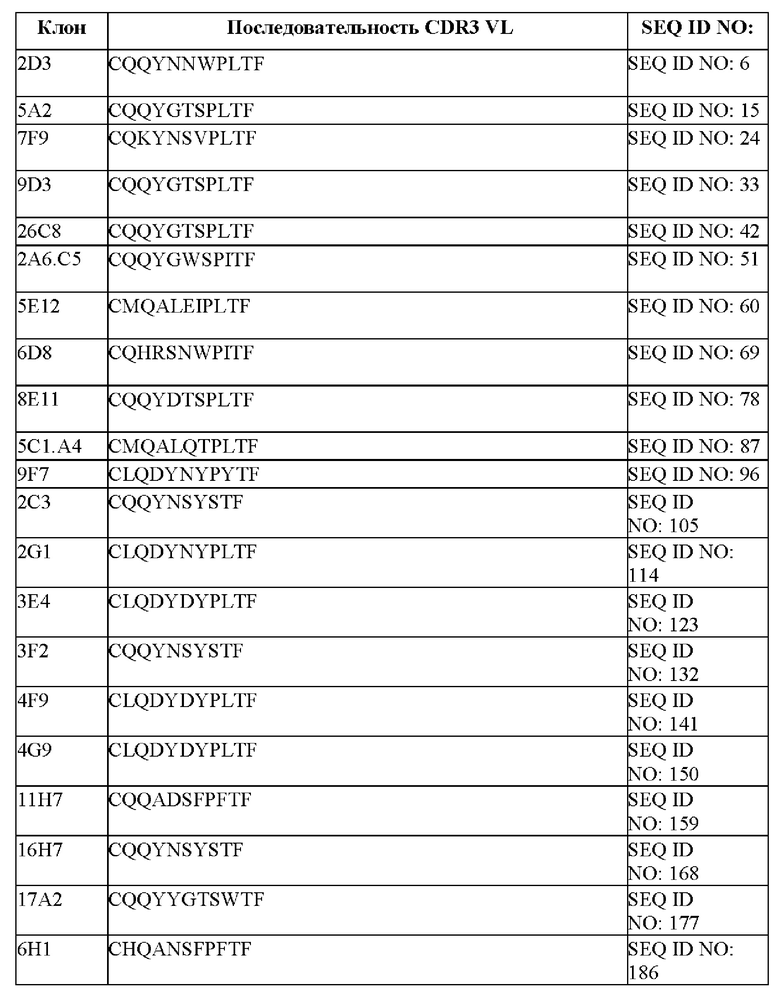
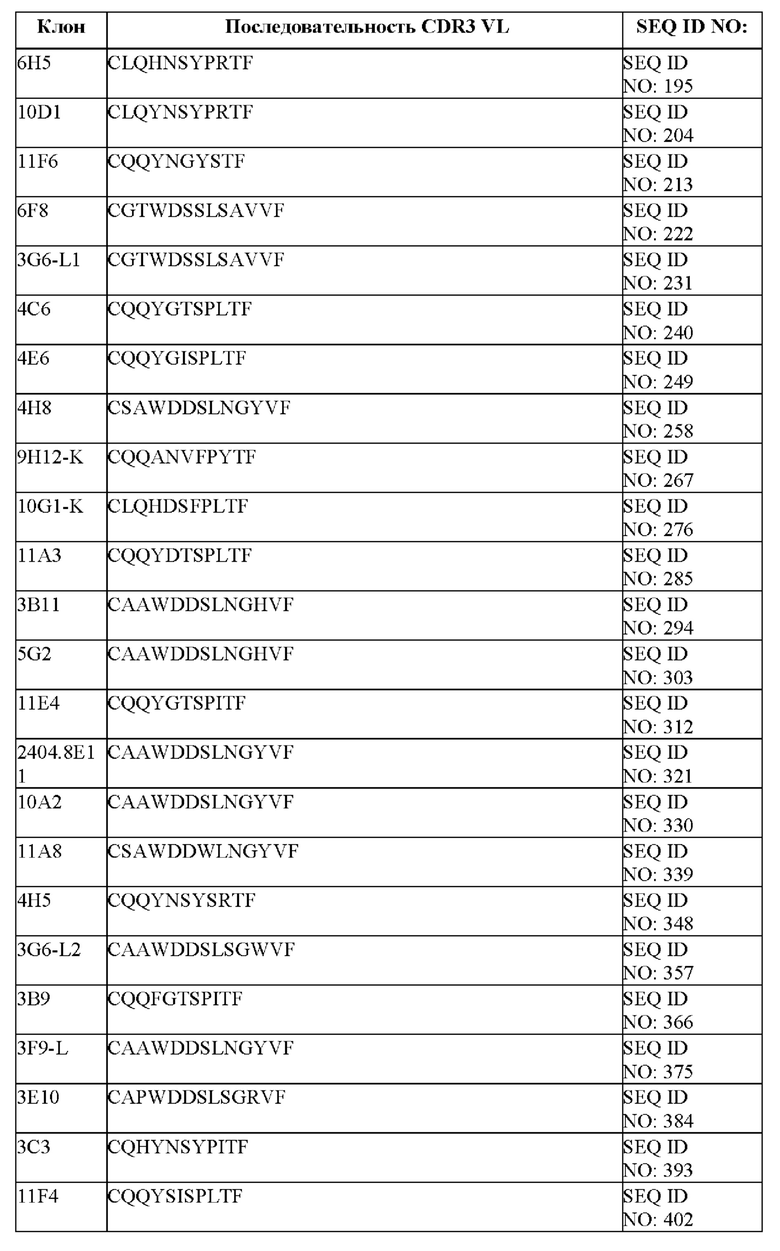
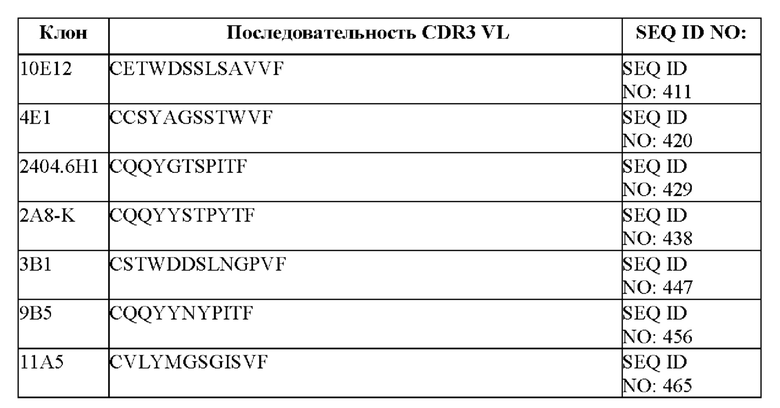
[098] Изобретение охватывает модификации агентов антитела против DLL3, содержащие последовательности, представленные в таблицах 1b-1е, включая функционально эквивалентные агенты антител против DLL3, имеющие модификации, которые по существу не влияют на их свойства, и варианты, которые обладают повышенной или пониженной активностью и/или аффинностью. Например, аминокислотная последовательность может быть мутирована для получения агента, связывающего антиген DLL3, с желаемой аффинностью связывания с DLL3. Модификация полипептидов является обычной практикой в данной области техники и нет необходимости в ее подробном описании в настоящем документе. Примеры модифицированных полипептидов включают полипептиды с консервативными заменами аминокислотных остатков, одной или более делециями или добавлениями аминокислот, которые по существу не оказывают отрицательного влияния на функциональную активность, или которые приводят к созреванию (повышению) аффинности полипептида к его лиганду, или использование химических аналогов.
[099] Инсерции в аминокислотной последовательности включают амино- и/или карбоксиконцевые слияния в диапазоне длины от одного остатка до полипептидов, содержащих сто или более остатков, а также вставки из одного или нескольких аминокислотных остатков внутри последовательности. Примеры вставок в концевой части последовательности включают антитело с N-концевым метионильным остатком или антитело, слитое с эпитопной меткой. Другие инсерционные варианты молекулы антитела включают слияние с N- или С-концом антитела фермента или полипептида, что увеличивает период полужизни антитела в кровотоке.
[0100] В вариантах с заменой по меньшей мере один аминокислотный остаток в антигенсвязывающем домене удален и на его место вставлен другой остаток. В некоторых вариантах осуществления сайты, представляющие интерес для замещающего мутагенеза, включают гипервариабельные области/CDR, но также рассматриваются изменения FR. Консервативные замены представлены в таблице 2 под заголовком «консервативные замены». Если такие замены приводят к изменению биологической активности, то могут быть внесены более существенные изменения, называемые «иллюстративными заменами» в таблице 2 или как дополнительно описано ниже в отношении классов аминокислот, и проведен скрининг продуктов.

i. Фрагменты антител
[0101] В одном из аспектов агент антитела против DLL-3 согласно любому из вышеуказанных вариантов осуществления может представлять собой фрагмент антитела. Фрагмент антитела содержит часть интактного антитела, такую как антигенсвязывающая или вариабельная область интактного антитела. Фрагменты антител включают, не ограничиваясь перечисленным, Fab, Fab', Fab'-SH, F(ab')2, Fv, диатело, линейные антитела, мультиспецифичные антитела, образованные из фрагментов антител, и scFv-фрагменты, а также другие фрагменты, описанные ниже. В некоторых вариантах осуществления антитело представляет собой полноразмерное антитело, например, интактное антитело IgG1 или другой класс или изотип антитела, как описано в настоящем документе. (См., например, Hudson et al., Nat. Med., 9: 129-134 (2003); Pluckthun, The Pharmacology of Monoclonal Antibodies, vol. 113, pp.269-315 (1994); Hollinger et al., Proc. Natl. Acad. Sci. USA, 90: 6444- 6448 (1993); WO93/01161; и патенты США №№5,571,894, 5,869,046, 6,248,516 и 5,587,458). Полноразмерное антитело, интактное антитело или целое антитело представляет собой антитело, имеющее структуру, по существу аналогичную структуре нативного антитела, или имеющее тяжелые цепи, содержащие Fc-область, как определено в настоящем документе. Фрагменты антител могут быть получены различными методами, включая, не ограничиваясь перечисленным, протеолитическое расщепление интактного антитела, а также продукцию рекомбинантными клетками-хозяевами (например, Е. coli или фагом), как известно в данной области техники.
[0102] Fv-фрагмент антитела содержит полный антигенраспознающий и антигенсвязывающий сайт. Этот фрагмент может содержать димер одного домена вариабельной области тяжелой цепи и одного домена вариабельной области легкой цепи, объединенных тесной нековалентной связью. В результате сворачивания этих двух доменов образуются шесть гипервариабельных петель (по три петли от Н- и L-цепи), которые вносят аминокислотные остатки для связывания антигена и придают антителу антигенсвязывающую специфичность. Однако даже одна вариабельная область (или половина Fv, содержащая только три CDR, специфичных к антигену) обладает способностью распознавать и связывать антиген, хотя и с более низкой аффинностью, чем весь связывающий сайт.
[0103] Диатело представляет собой небольшой фрагмент антитела, полученный путем конструирования sFv-фрагмента с коротким линкером (например, приблизительно 5-10 остатков) между доменами VH и VL, так что достигается межцепочечное, но не внутрицепочечное спаривание V-доменов, в результате образуется двухвалентный фрагмент. Биспецифические диатела представляют собой гетеродимеры двух sFv-фрагментов с перекрестным связыванием, в которых домены VH и VL двух антител присутствуют на разных полипептидных цепях (см., например, ЕР 404,097; WO 93/11161; и Hollinger et al, Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993)).
[0104] Доменные антитела (dAb), которые могут быть получены в полностью человеческой форме, представляют собой наименьшие из известных антигенсвязывающих фрагментов антител массой в диапазоне от приблизительно 11 кДа до приблизительно 15 кДа. dAb представляют собой устойчивые вариабельные области тяжелой и легкой цепей иммуноглобулинов (VH и VL, соответственно). Они на высоком уровне экспрессируются в культуре микробных клеток, демонстрируют благоприятные биофизические свойства, включая, например, не ограничиваясь перечисленным, растворимость и термическую стабильность, и хорошо подходят для отбора и созревания аффинности с помощью систем отбора in vitro, таких как, например, фаговый дисплей. dAb являются биоактивными в виде мономеров и, благодаря их небольшому размеру и свойственной им стабильности, могут быть преобразованы в более крупные молекулы для создания лекарственных средств с увеличенным периодом полужизни в сыворотке или другой фармакологической активностью. (См., например, W09425591 и US20030130496).
[0105] Fv и scFv представляют собой варианты, имеющие интактные связывающие сайты, лишенные константных областей. Таким образом, они могут подходить для снижения неспецифического связывания при применении in vivo. Одноцепочечный Fv (sFv или scFv) представляет собой фрагмент антитела, содержащий домены антитела VH и VL, соединенные в единую полипептидную цепь. Полипептид sFv может дополнительно содержать полипептидный линкер между доменами VH и VL, который позволяет sFv формировать желаемую структуру для связывания антигена (см., например, Pluckthun, The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., Springer- Verlag, New York, pp.269-315 (1994); Borrebaeck 1995, цитируемый ниже. Слитые белки scFv могут быть сконструированы для получения слияния эффекторного белка либо на амино-, либо на карбоксиконце sFv. Фрагмент антитела также может представлять собой «линейное антитело» (см., например, патент США №5,641,870). Такие линейные фрагменты антител могут быть моноспецифичными или биспецифичными. Иллюстративные scFv, специфичные к DLL3, представлены в таблице 1d.
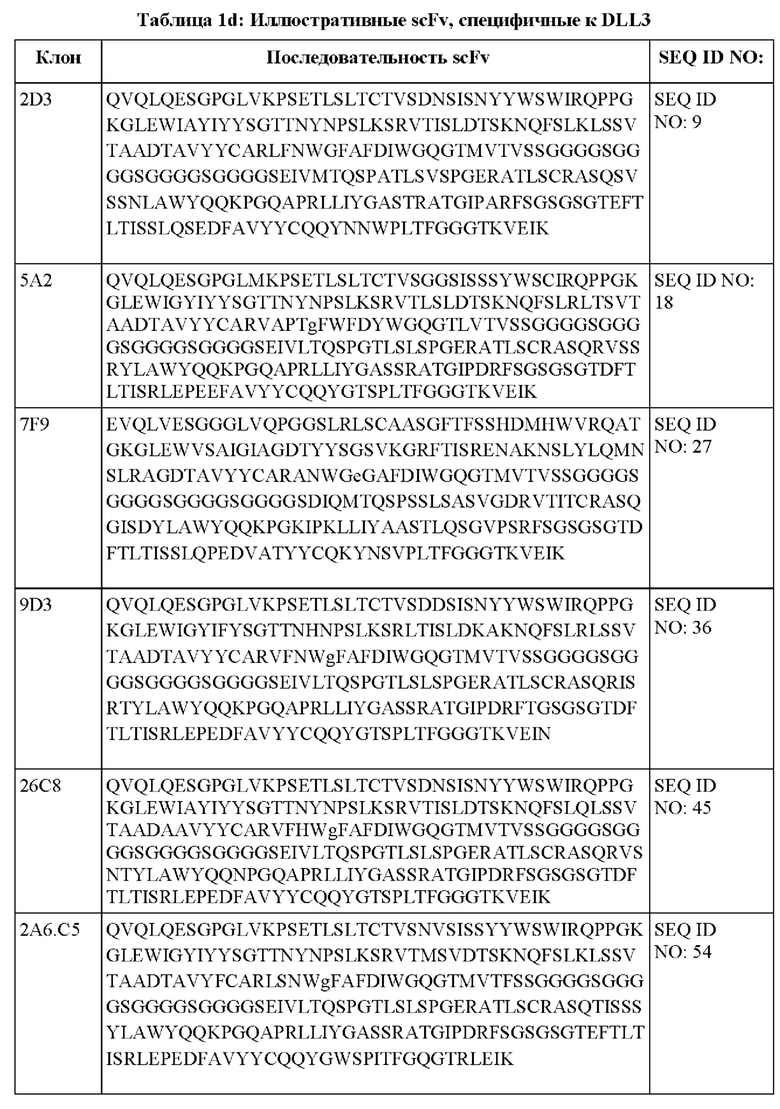
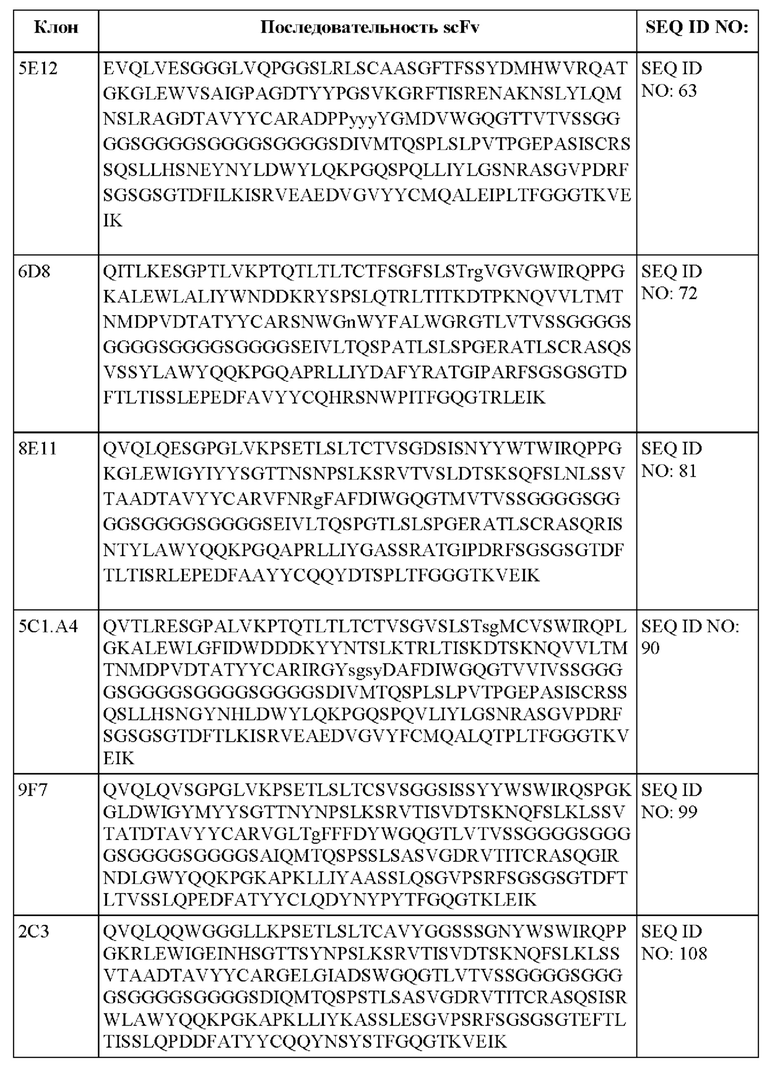

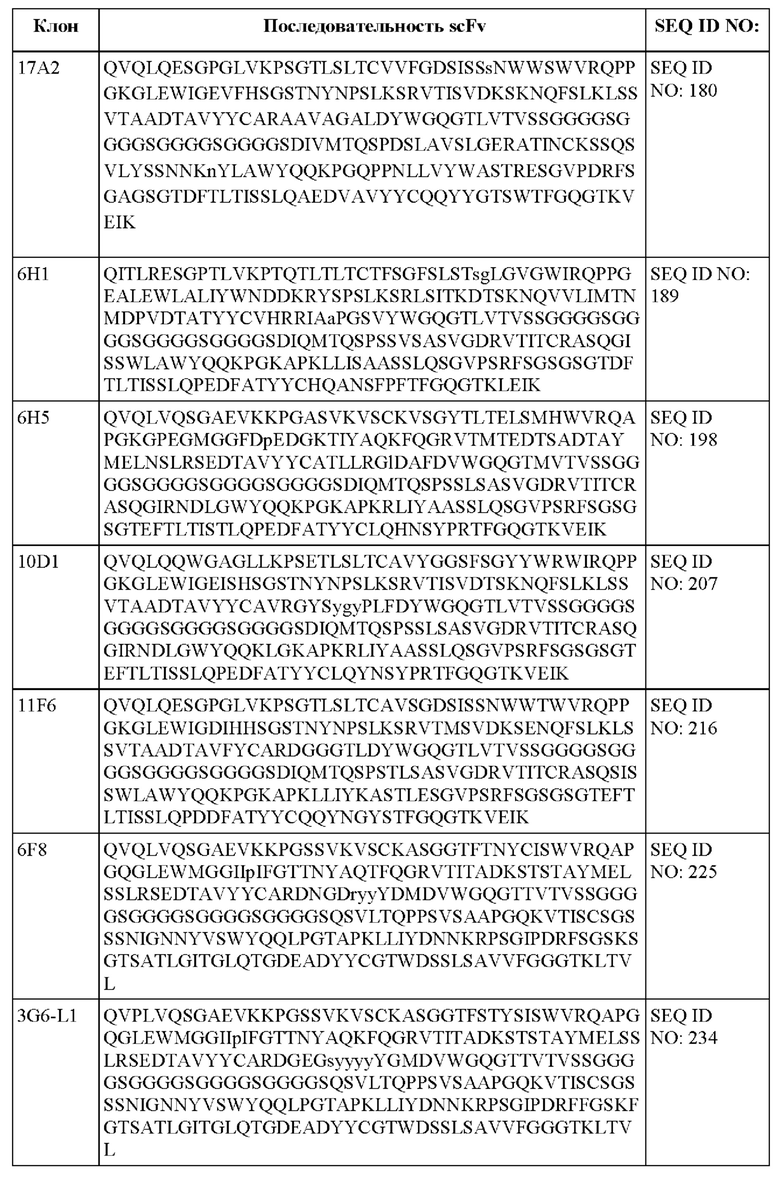

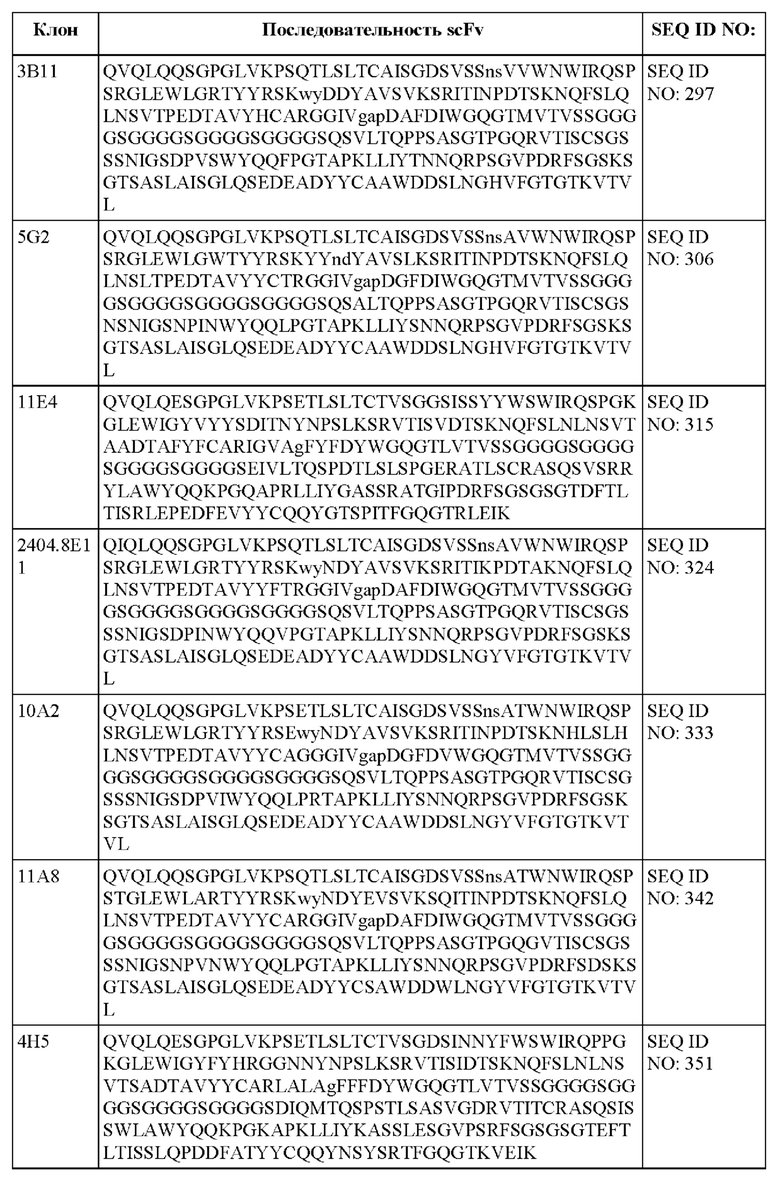
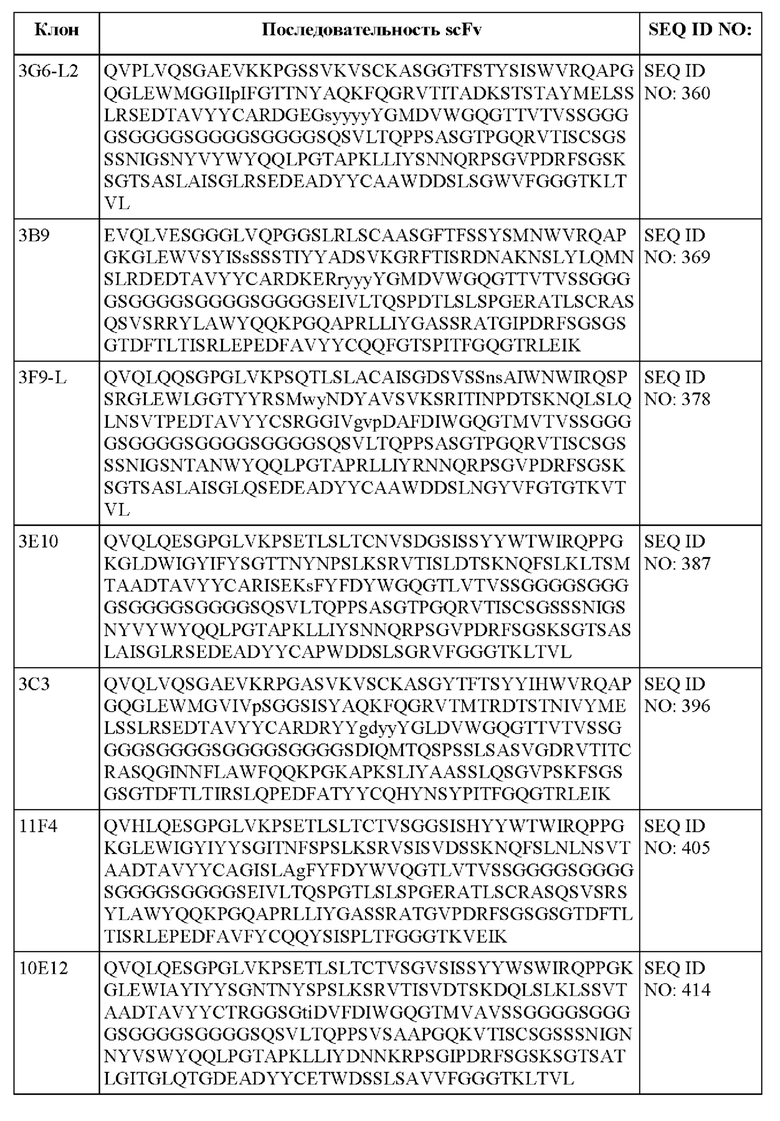

[0106] В некоторых вариантах осуществления антигенсвязывающий домен против DLL3 содержит scFv, содержащий вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH) DLL3-специфичного моноклонального антитела, соединенные гибким линкером. Одноцепочечные фрагменты вариабельной области могут быть получены путем связывания вариабельных областей легкой и/или тяжелой цепи с использованием связывающего пептида. Примером связывающего пептида является линкер GS, имеющий аминокислотную последовательность (GGGGS)x, где х равно 1, 2, 3, 4 или 5 (SEQ ID NO: 470). В некоторых вариантах осуществления х равно 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или любому целому числу меньше приблизительно 20. В некоторых вариантах осуществления линкер представляет собой (GGGGS)4 (SEQ ID NO: 478). В целом, линкеры могут представлять собой короткие гибкие полипептиды, которые в некоторых вариантах осуществления состоят из приблизительно 20 или менее аминокислотных остатков. Линкеры, в свою очередь, могут быть модифицированы для придания дополнительных функций, таких как присоединение лекарственных средств или присоединение к твердым подложкам. Одноцепочечные варианты могут быть получены либо рекомбинантно, либо путем синтеза. Для получения scFv путем синтеза может быть использован автоматический синтезатор. Для рекомбинантного получения scFv подходящая плазмида, содержащая полинуклеотид, кодирующий указанный scFv, может быть введена в подходящую клетку-хозяина, либо эукариотическую, такую как клетки дрожжей, растений, насекомых или млекопитающих, либо прокариотическую, такую как Е. coli. Полинуклеотиды, кодирующие представляющий интерес scFv, могут быть получены посредством рутинных манипуляций, таких как лигирование полинуклеотидов. Полученный scFv может быть выделен с использованием стандартных методов очистки белка, известных в данной области техники.
[0107] В иллюстративных вариантах осуществления в настоящем документе предложены антигенсвязывающие домены против DLL3, содержащие: область VH, содержащую CDR1 VH, CDR2 VH и CDR3 VH последовательности VH, представленной в таблице 1b, и/или область VL, содержащую CDR1 VL, CDR2 VL и CDR3 VL последовательности VL, представленной в таблице 1 с. В некоторых вариантах осуществления VH и VL связаны друг с другом линкером. В некоторых вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGSGGGGS (SEQ ID NO: 478). В некоторых вариантах осуществления линкер может быть кодирован последовательностью ДНК, содержащей GGCGGTGGAGGCTCCGGAGGGGGGGGCTCTGGCGGAGGGGGCTCC (SEQ ID NO: 564). В некоторых вариантах осуществления линкер может быть кодирован последовательностью ДНК,содержащей ggcggcggcggctctggaggaggaggcagcggcggaggaggctccggaggcggcggctct (SEQ ID NO: 630). В некоторых вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 534). В некоторых вариантах осуществления линкер представляет собой линкер scFv Whitlow, который может содержать аминокислотную последовательность GSTSGSGKPGSGEGSTKG (SEQ ID NO: 535). Линкер scFv Whitlow может быть кодирован последовательностью ДНК, содержащей GGGTCTACATCCGGCTCCGGGAAGCCCGGAAGTGGCGAAGGTAGTACAAAGGGG (SEQ ID NO: 566). В некоторых вариантах осуществления последовательности VH и VL раскрытых scFv могут быть ориентированы так, чтобы последовательность VH была расположена на N-конце scFv, за ней следовал линкер, а затем последовательность VL, тогда как в других вариантах осуществления scFv может быть ориентирован с последовательностью VL на N-конце, за которой следует линкер, а затем последовательность VH.
ii. Химерные и гуманизированные антитела
[0108] В некоторых вариантах осуществления агент антитела против DLL-3 представляет собой или содержит моноклональное антитело, включая химерное, гуманизированное или человеческое антитело.
[0109] В некоторых вариантах осуществления агент антитела против DLL-3, предложенный в настоящем документе, может представлять собой химерное антитело (см., например, патент США №4,816,567; и Morrison et al., Proc. Natl. Acad. Sci. USA, 81:6851-6855 (1984)). Химерное антитело может представлять собой антитело, в котором часть тяжелой и/или легкой цепи получена из определенного источника или вида, тогда как остальная часть тяжелой и/или легкой цепи получена из другого источника или вида. В одном примере химерное антитело может содержать вариабельную область нечеловеческого происхождения (например, вариабельную область, полученную от мыши, крысы, хомяка, кролика или отличного от человека примата, такого как обезьяна) и человеческую константную область. В дополнительном примере химерное антитело может представлять собой «изотип-переключенное» антитело, в котором класс или подкласс был изменен по сравнению с родительским антителом. Химерные антитела включают их антигенсвязывающие фрагменты.
[0110] В некоторых вариантах осуществления химерное антитело может представлять собой гуманизированное антитело (см., например, Almagro and Fransson, Front. Biosci., 13: 1619-1633 (2008); Riechmann et al., Nature, 332:323-329 (1988); Queen et al., Proc. Natl Acad. Sci. USA 86: 10029-10033 (1989); патенты США №№5,821,337, 7,527,791, 6,982,321 и 7,087,409; Kashmiri et al., Methods 36:25-34 (2005); Padlan, Mol. Immunol, 28:489-498 (1991); Dall'Acqua et al., Methods, 36:43-60 (2005); Osbourn et al., Methods, 36:61-68 (2005); и Klimka et al., Br. J. Cancer, 83:252-260 (2000)). Гуманизированное антитело представляет собой химерное антитело, содержащее аминокислотные остатки из гипервариабельных областей нечеловеческого происхождения и аминокислотные остатки из человеческих FR. В отдельных вариантах осуществления гуманизированное антитело будет содержать по существу все из по меньшей мере одного, и обычно двух вариабельных доменов, в которых все или по существу все гипервариабельные области (например, CDR) соответствуют таковым в антителе нечеловеческого происхождения, и все или по существу все FR соответствуют таковым в человеческом антителе. Гуманизированное антитело необязательно может содержать по меньшей мере часть константной области антитела, полученной из человеческого антитела.
[0111] Антитело нечеловеческого происхождения может быть гуманизировано для снижения иммуногенности для человека, сохраняя при этом специфичность и аффинность родительского антитела нечеловеческого происхождения. Гуманизированное антитело может содержать один или более вариабельных доменов, содержащих одну или более CDR или их частей, полученных из антитела нечеловеческого происхождения. Гуманизированное антитело может содержать один или более вариабельных доменов, содержащих один или более FR или их частей, полученных из последовательностей человеческого антитела. Гуманизированное антитело может необязательно содержать по меньшей мере часть человеческой константной области. В некоторых вариантах осуществления один или более остатков FR в гуманизированном антителе заменены соответствующими остатками антитела нечеловеческого происхождения (например, антитела, из которого получены остатки CDR) для восстановления или улучшения специфичности или аффинности антитела.
[0112] Человеческие каркасные области, которые могут быть использованы для гуманизации, включают, не ограничиваясь перечисленным: каркасные области, выбранные с использованием метода «наилучшего соответствия»; каркасные области, полученные из консенсусной последовательности человеческих антител конкретной подгруппы вариабельных областей легкой или тяжелой цепи; зрелые (соматически мутированные) человеческие каркасные области или каркасные области зародышевой линии человека; и каркасные области, полученные из скрининговых библиотек FR (см., например, Sims et al., J. Immunol, 151:2296 (1993); Carteret al., Proc. Natl. Acad. Sci. USA, 89:4285 (1992); Presta et al., J. Immunol, 151:2623 (1993); Bacaetal., J. Biol. Chem., 272: 10678-10684 (1997); и Rosok et al., J. Biol. Chem., 271:22611-22618 (1996)).
iii. Человеческие антитела
[0113] В некоторых вариантах осуществления агент антитела против DLL-3, предложенный в настоящем документе, представляет собой человеческое антитело. Человеческие антитела могут быть получены с использованием различных методик, известных в данной области техники (см., например, van Dijk and van de Winkel, Curr. Opin. Pharmacol, 5: 368-74 (2001); и Lonberg, Curr. Opin. Immunol, 20:450-459 (2008)). Человеческое антитело может представлять собой антитело, обладающее аминокислотной последовательностью, которая соответствует таковой для антитела, продуцируемого человеком или клеткой человека, или полученного из отличного от человека источника, в котором используется репертуар человеческих антител или другие последовательности, кодирующие человеческие антитела. Это определение человеческого антитела специально исключает гуманизированное антитело, содержащее антигенсвязывающие остатки нечеловеческого происхождения. Человеческие антитела могут быть получены путем введения иммуногена (например, белка DLL-3) трансгенному животному, которое было модифицировано для продуцирования интактных человеческих антител или интактных антител с человеческими вариабельными областями в ответ на антигенную стимуляцию (см., например, Lonberg, Nat. Biotech., 23: 1117-1125 (2005); патенты США №№6,075, 181, 6,150,584, 5,770,429 и 7,041,870; и публикация заявки на патент США US 2007/0061900). Человеческие вариабельные области из интактных антител, генерируемых такими животными, могут быть дополнительно модифицированы, например, путем комбинирования с другой человеческой константной областью.
[0114] Человеческие антитела также могут быть получены посредством гибридомной технологии. Например, человеческие антитела могут быть получены из клеточных линий миеломы человека и гетеромиеломы мыши и человека с использованием технологии гибридомы человеческих В-клеток и других методов (см., например, Kozbor, J. Immunol, 133: 3001 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications, pp.51-63 (1987); Boerner et al., J. Immunol, 147: 86 (1991); Li et al., Proc. Natl. Acad. Sci. USA, 103:3557-3562 (2006); патент США №7,189,826; Ni, Xiandai Mianyixue, 26(4): 265-268 (2006); Vollmers and Brandlein, Histology and Histopathology, 20(3): 927-937 (2005); и Vollmers and Brandlein, Methods and Findings in Experimental and Clinical Pharmacology, 27(3): 185-91 (2005)). Человеческие антитела также могут быть получены путем выделения последовательностей вариабельного домена клона Fv, выбранных из библиотек фагового дисплея человеческого происхождения. Такие последовательности вариабельного домена затем можно комбинировать с желаемой человеческой константной областью.
[0115] Модификации олигосахарида в антителе могут быть сделаны, например, для создания вариантов антитела с определенными улучшенными свойствами. Например, варианты гликозилирования антител могут иметь улучшенную функцию КЗЦ. В некоторых вариантах осуществления настоящего изобретения может рассматриваться вариант антитела, который обладает некоторыми, но не всеми эффекторными функциями, что делает его желательным кандидатом для применений, в которых период полужизни антитела in vivo важен, но при этом некоторые эффекторные функции (такие как комплемент) являются ненужными или вредными. Для подтверждения снижения/истощения активности КЗЦ могут быть проведены анализы цитотоксичности in vitro и/или in vivo.
iv. Производные антител
[0116] В некоторых вариантах осуществления агент антитела, предложенный в настоящем документе, может быть дополнительно модифицирован, чтобы он содержал дополнительные небелковые фрагменты, которые известны в данной области техники и легко доступны. Фрагменты, подходящие для дериватизации антитела, могут включать, не ограничиваясь перечисленным, водорастворимые полимеры. Неограничивающие примеры водорастворимых полимеров могут включать, не ограничиваясь перечисленным, полиэтиленгликоль (ПЭГ), сополимеры этиленгликоля/пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена/малеинового ангидрида, полиаминокислоты (либо гомополимеры, либо статистические сополимеры) и декстран или поли(н-винилпирролидон)полиэтиленгликоль, гомополимеры полипропиленгликоля, сополимеры полипропиленоксида/этиленоксида, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт и их смеси. Пропиональдегид полиэтиленгликоля может иметь преимущества при производстве из-за его стабильности в воде.
[0117] Полимер может иметь любую молекулярную массу и может быть разветвленным или неразветвленным. Количество полимеров, присоединенных к антителу, может варьироваться, и если присоединены два или более полимеров, они могут быть одинаковыми или разными молекулами.
[0118] В некоторых вариантах осуществления предложены конъюгаты антитела и небелкового фрагмента, которые можно избирательно нагревать под воздействием излучения. В некоторых вариантах осуществления небелковый фрагмент может представлять собой углеродную нанотрубку (см., например, Kam et al., Proc. Natl. Acad. Sci. USA, 102: 11600-11605 (2005)). Излучение может иметь любую длину волны и может включать, не ограничиваясь перечисленным, длины волн, которые не повреждают обычные клетки, но нагревают небелковый фрагмент до температуры, при которой гибнут клетки, находящиеся вблизи антитела-небелкового фрагмента.
[0119] Говорят, что связывающий DLL3 агент (например, молекула, содержащая антигенсвязывающий домен) «специфически связывает» свой антиген-мишень (например, DLL3 человека, яванского макака или мыши), когда равновесная константа диссоциации (Kd) составляет ~1 нМ. Антигенсвязывающий домен специфически связывает антиген с «высокой аффинностью», когда Kd составляет 1-5 нМ, и с «очень высокой аффинностью», когда Kd составляет 0,1-0,5 нМ. В одном из вариантов осуществления антигенсвязывающий домен имеет Kd ~1 нМ. В одном из вариантов осуществления константа диссоциации составляет <1×10-5. В других вариантах осуществления антигенсвязывающие домены будут связываться с DLL3 человека с Kd приблизительно от 1×10-7 М до 1×10-12 М, и еще в одном варианте осуществления антигенсвязывающие домены будут связываться с Kd приблизительно от 1×10-5 М до 1×10-12 М.
[0120] Как предусмотрено в настоящем документе, антигенсвязывающие домены согласно настоящему изобретению специфически связывают DLL3 млекопитающих (например, DLL3 человека, DLL3 яванского макака или DLL3 мыши). В отдельных вариантах осуществления антигенсвязывающий домен против DLL3 согласно настоящему изобретению связывает DLL3 млекопитающих с Kd менее 1×10-6 М, менее 1×10-7 М, менее 1×10-8 М или менее 1×10-9 М. В одном частном варианте осуществления антигенсвязывающие домены против DLL3 связывают DLL3 млекопитающих (например, DLL3 человека, DLL3 яванского макака или DLL3 мыши) с Kd менее 1×10-7 М. В еще одном варианте осуществления антигенсвязывающие домены против DLL3 связывают DLL3 млекопитающих (например, DLL3 человека, DLL3 яванского макака или DLL3 мыши) с Kd менее 1×10-8 М. В некоторых вариантах осуществления антигенсвязывающие домены против DLL3 связывают DLL3 млекопитающих (например, DLL3 человека, DLL3 яванского макака) с Kd приблизительно 1×10-7 М, приблизительно 2×10-7 М, приблизительно 3×10-7 М, приблизительно 4×10-7 М, приблизительно 5×10-7 М, приблизительно 6×10-7 М, приблизительно 7×10-7 М, приблизительно 8×10-7 М, приблизительно 9×10-7 М, приблизительно 1×10-8 М, приблизительно 2×10-8 М, приблизительно 3×10-8 М, приблизительно 4×10-8 М, приблизительно 5×10-8 М, приблизительно 6×10-8 М, приблизительно 7×10-8 М, приблизительно 8×10-8 М, приблизительно 9×10-8 М, приблизительно 1×10-9 М, приблизительно 2×10-9 М, приблизительно 3×10-9 М, приблизительно 4×10-9 М, приблизительно 5×10-9 М, приблизительно 6×10-9 М, приблизительно 7×10-9 М, приблизительно 8×10-9 М, приблизительно 9×10-9 М, приблизительно 1×10-10 М или приблизительно 5×10-10 М. В отдельных вариантах осуществления Kd рассчитывают как отношение Koff/Kon, а Kon и Koff определяют с использованием одновалентного антитела, такого как Fab-фрагмент, при измерении, например, с помощью технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления Kd рассчитывают как отношение Koff/Kon, а Kon и Koff определяют с использованием двухвалентного антитела, такого как Fab-фрагмент, при измерении, например, с помощью технологии поверхностного плазмонного резонанса BIAcore®.
[0121] В некоторых вариантах осуществления антигенсвязывающий домен против DLL3 связывает DLL3 млекопитающих (например, DLL3 человека, DLL3 яванского макака или DLL3 мыши) со скоростью ассоциации (kon) менее 1×10-4 М-1 с-1, менее 2×10-4 М-1 с-1, менее 3×10-4 М-1 с-1, менее 4×10-4 М-1 с-1, менее 5×10-4 М-1 с-1, менее 7×10-4 М-1 с-1, менее 8×10-4 М-1 с-1, менее 9×10-4 М-1 с-1, менее 1×10-5 М-1 с-1, менее 2×10-5 М-1 с-1, менее 3×10-5 М-1 с-1, менее 4×10-5 М-1 с-1, менее 5×10-5 М-1 с-1, менее 6×10-5 М-1 с-1, менее 7×10-5 М-1 с-1, менее 8×10-5 М-1 с-1, менее 9×10-5 М-1 с-1, менее 1×10-6 М-1 с-1, менее 2×10-6 М-1 с-1, менее 3×10-6 М-1 с-1, менее 4×10-6 М-1 с-1, менее 5×10-6 М-1 с-1, менее 6×10-6 М-1 с-1, менее 7×10-6 М-1 с-1, менее 8×10-6 М-1 с-1, менее 9×10-6 М-1 с-1 или менее 1×10-7 М-1 с-1. В отдельных вариантах осуществления kon определяют с использованием одновалентного антитела, такого как Fab-фрагмент, при измерении, например, с помощью технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления kon определяют с использованием двухвалентного антитела, при измерении, например, с помощью технологии поверхностного плазмонного резонанса BIAcore®.
[0122] В некоторых вариантах осуществления антигенсвязывающий домен против DLL3 связывает DLL3 млекопитающих (например, DLL3 человека, DLL3 яванского макака или DLL3 мыши) со скоростью диссоциации (koff) менее 1×10-2 с-1, менее 2×10-2 с-1, менее 3×10-2 с-1, менее 4×10-2 с-1, менее 5×10-2 с-1, менее 6×10-2 с-1, менее 7×10-2 с-1, менее 8×10-2 с-1, менее 9×10-2 с-1, менее 1×10-3 с-1, менее 2×10-3 с-1, менее 3×10-3 с-1, менее 4×10-3 с-1, менее 5×10-3 с-1, менее 6×10-3 с-1, менее 7×10-3 с-1, менее 8×10-3 с-1, менее 9×10-3 с-1, менее 1×10-4 с-1, менее 2×10-4 с-1, менее 3×10-4 с-1, менее 4×10-4 с-1, менее 5×10-4 с-1, менее 6×10-4 с-1 менее 7×10-4 с-1, менее 8×10-4 с-1, менее 9×10-4 с-1, менее 1×10-5 с-1 или менее 5×10-4 с-1. В отдельных вариантах осуществления koff определяют с использованием одновалентного антитела, такого как Fab-фрагмент, при измерении, например, с помощью технологии поверхностного плазмонного резонанса BIAcore®. В других вариантах осуществления koff определяют с использованием двухвалентного антитела, при измерении, например, с помощью технологии поверхностного плазмонного резонанса BIAcore®.
II. Химерные антигенные рецепторы
[0123] В контексте настоящего документа химерные антигенные рецепторы (CAR) представляют собой белки, которые специфически распознают антигены-мишени (например, антигены-мишени на раковых клетках). При связывании с антигеном-мишенью CAR может активировать иммунную клетку для атаки и разрушения клетки, несущей этот антиген (например, раковой клетки). CAR могут также включать костимулирующие или сигнальные домены для повышения их активности. См. Krause et al, J. Exp. Med., Volume 188, No. 4, 1998 (619-626); Finney et al, Journal of Immunology, 1998, 161: 2791-2797, Song et al, Blood 119:696-706 (2012); Kalos et al, Sci. Transl. Med. 3:95 (2011); Porter et al., N. Engl. J. Med. 365:725-33 (2011), и Gross et al, Annu. Rev. Pharmacol. Toxicol. 56:59-83 (2016); патенты США №№7,741,465 и 6,319,494.
[0124] Химерные антигенные рецепторы, описанные в настоящем документе, содержат внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3. В некоторых вариантах осуществления CAR, специфичный к DLL-3, содержит следующие элементы, в направлении от 5' к 3': сигнальную последовательность, антигенсвязывающий домен против DLL3 (например, scFv против DLL3), шарнирную и трансмембранную область и один или более последовательно расположенных сигнальных доменов. В отдельных вариантах осуществления CAR, специфичный к DLL-3, содержит следующие элементы, в направлении от 5' к 3': сигнальную последовательность CD8α, scFv против DLL3, содержащий вариабельную область тяжелой цепи и/или вариабельную область легкой цепи против DLL3, описанные в настоящем документе, шарнирную и трансмембранную область CD8α, цитоплазматический сигнальный домен 41ВВ и цитоплазматический сигнальный домен CD3ζ (ФИГ. 4, таблица 7).
[0125] В некоторых вариантах осуществления CAR, специфичные к DLL-3, дополнительно содержат предохранительные переключатели и/или эпитоп, специфичный к моноклональному антителу.
а. Антигенсвязывающий домен
[0126] Как обсуждалось выше, описанные в настоящем документе CAR против DLL3 содержат антигенсвязывающий домен. «Антигенсвязывающий домен» в контексте настоящего документа означает любой полипептид, который связывает определенный антиген-мишень, например, определенный антиген-мишень может представлять собой белок DLL3 (DLL-3) или его фрагмент (в настоящем документе взаимозаменяемо именуемый «антигеном DLL3», «антигеном-мишенью DLL3» или «мишенью DLL3»). В некоторых вариантах осуществления антигенсвязывающий домен связывается с антигеном DLL3 на опухолевой клетке. В некоторых вариантах осуществления антигенсвязывающий домен связывается с антигеном DLL3 на клетке, вовлеченной в гиперпролиферативное заболевание.
[0127] В некоторых вариантах осуществления антигенсвязывающий домен содержит вариабельную тяжелую цепь, вариабельную легкую цепь и/или одну или более CDR, описанных в настоящем документе. В некоторых вариантах осуществления антигенсвязывающий домен представляет собой одноцепочечный вариабельный фрагмент (scFv), содержащий CDR легкой цепи CDR1, CDR2 и CDR3, и CDR тяжелой цепи CDR1, CDR2 и CDR3.
[0128] В некоторых вариантах осуществления CAR, специфичные к DLL-3, содержат VH, представленную в таблице 1b. В некоторых вариантах осуществления CAR, специфичные к DLL-3, содержат VL, представленную в таблице 1. В некоторых вариантах осуществления CAR, специфичные к DLL-3, содержат CDR1, CDR2, CDR3 тяжелой цепи, представленные в таблице 1е. В некоторых вариантах осуществления CAR, специфичные к DLL-3, содержат CDR1, CDR2, CDR3 легкой цепи, представленные в таблице 1f.
[0129] Варианты антигенсвязывающих доменов (например, варианты CDR, VH и/или VL) также входят в объем настоящего изобретения, например, вариабельные легкие и/или вариабельные тяжелые цепи, каждая из которых обладает по меньшей мере 70-80%, 80-85%, 85-90%, 90-95%, 95-97%, 97-99% или более чем 99% идентичностью аминокислотным последовательностям последовательностей антигенсвязывающих доменов, описанных в настоящем документе. В некоторых случаях такие молекулы включают по меньшей мере одну тяжелую цепь и одну легкую цепь, тогда как в других случаях вариантные формы содержат две вариабельные легкие цепи и две вариабельные тяжелые цепи (или их составляющие части). Специалист сможет определить подходящие варианты антигенсвязывающих доменов, как изложено в настоящем документе, с использованием хорошо известных методик. В отдельных вариантах осуществления специалист в данной области техники может идентифицировать подходящие области молекулы, которые могут быть изменены без нарушения активности, путем нацеливания на области, которые, как считается, не являются важными для активности.
[0130] В отдельных вариантах осуществления полипептидная структура антигенсвязывающих доменов основана на антителах, включая, не ограничиваясь перечисленным, моноклональные антитела, биспецифичные антитела, минитела, доменные антитела, синтетические антитела (иногда называемые в настоящем документе «миметиками антител»), химерные антитела, гуманизированные антитела, человеческие антитела, слитые антитела (иногда называемые в настоящем документе «конъюгатами антител») и их фрагменты, соответственно. В некоторых вариантах осуществления антигенсвязывающий домен содержит авимеры или состоит из них.
[0131] Антигенсвязывающий домен против DLL3 считается «селективным», когда он связывается с одной мишенью более прочно, чем со второй мишенью.
[0132] В некоторых вариантах осуществления антигенсвязывающий домен против DLL3 представляет собой scFv. В некоторых вариантах осуществления CAR, специфичный к DLL3, содержит scFv, представленный в таблице 1d.
[0133] В некоторых вариантах осуществления CAR, специфичный к DLL3, содержит лидерный или сигнальный пептид; в некоторых вариантах осуществления лидерный пептид содержит аминокислотную последовательность, по меньшей мере приблизительно на 75%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или на 100% идентичную аминокислотной последовательности MALPVTALLLPLALLLHAARP (SEQ ID NO: 477). В некоторых вариантах осуществления лидерный пептид содержит аминокислотную последовательность SEQ ID NO: 477. В некоторых вариантах осуществления лидерный пептид кодируется последовательностью нуклеиновой кислоты, содержащей:
ATGGCACTCCCCGTAACTGCTCTGCTGCTGCCGTTGGCATTGCTCCTGCACGCCGCA CGCCCG (SEQ ID NO: 555).
[0134] В других вариантах осуществления изобретение относится к выделенным полинуклеотидам, кодирующим любой из описанных в настоящем документе антигенсвязывающих доменов против DLL3. В некоторых вариантах осуществления изобретение относится к выделенным полинуклеотидам, кодирующим DLL3 CAR, описанные в таблице 10. В настоящем документе также предложены векторы, содержащие указанные полинуклеотиды, и способы их получения.











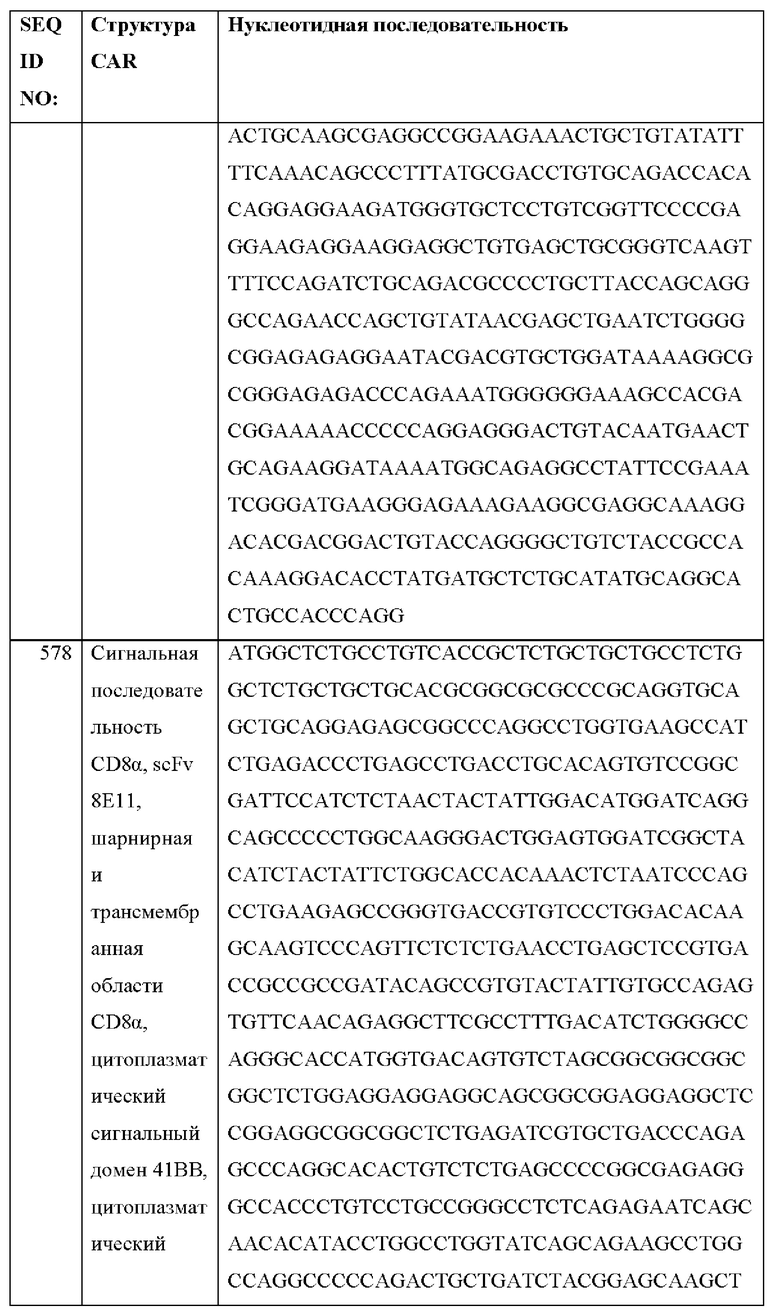











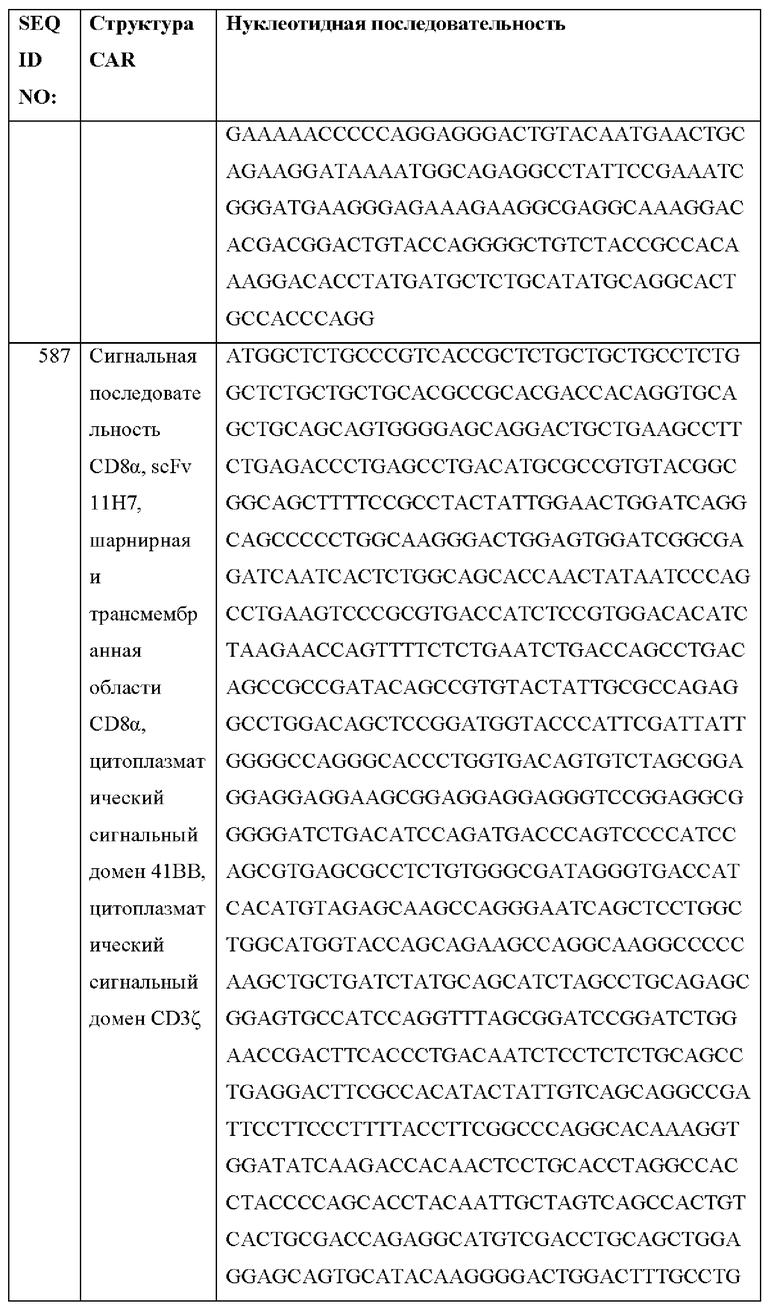
















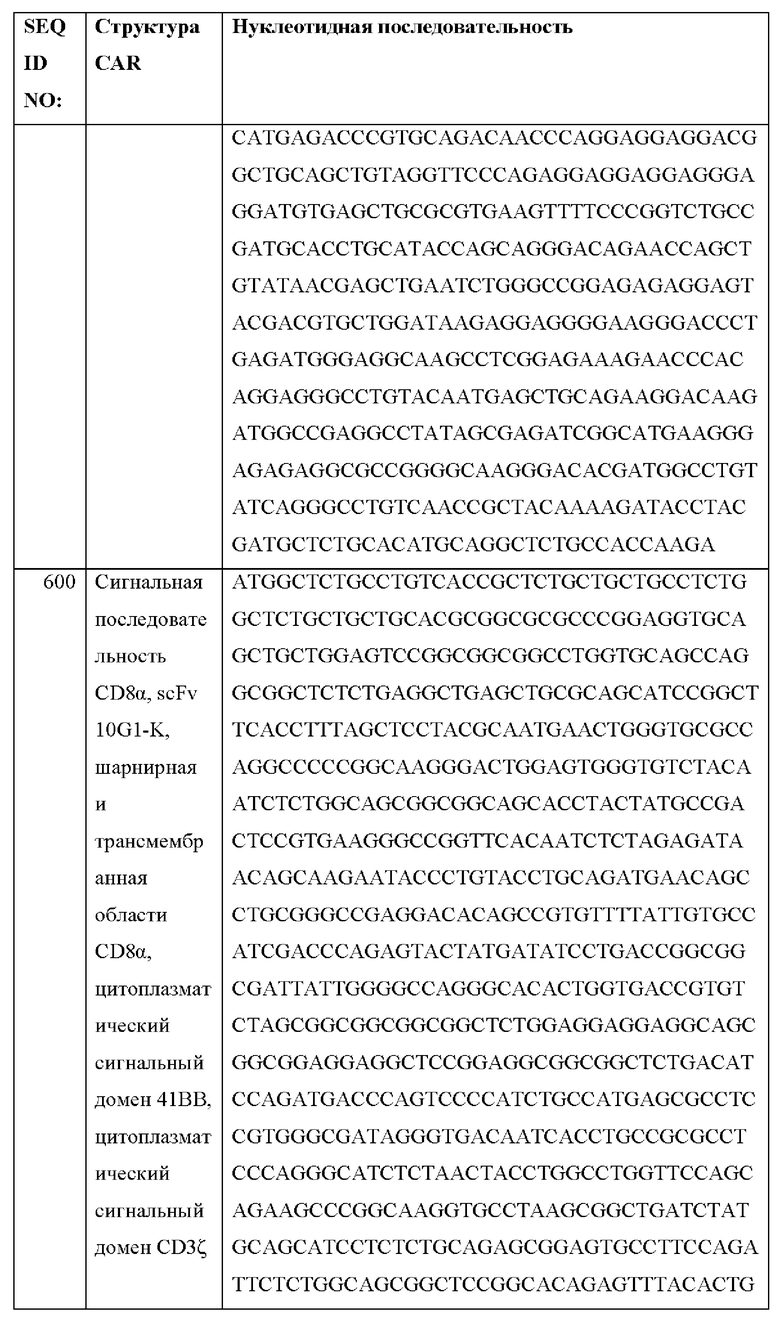











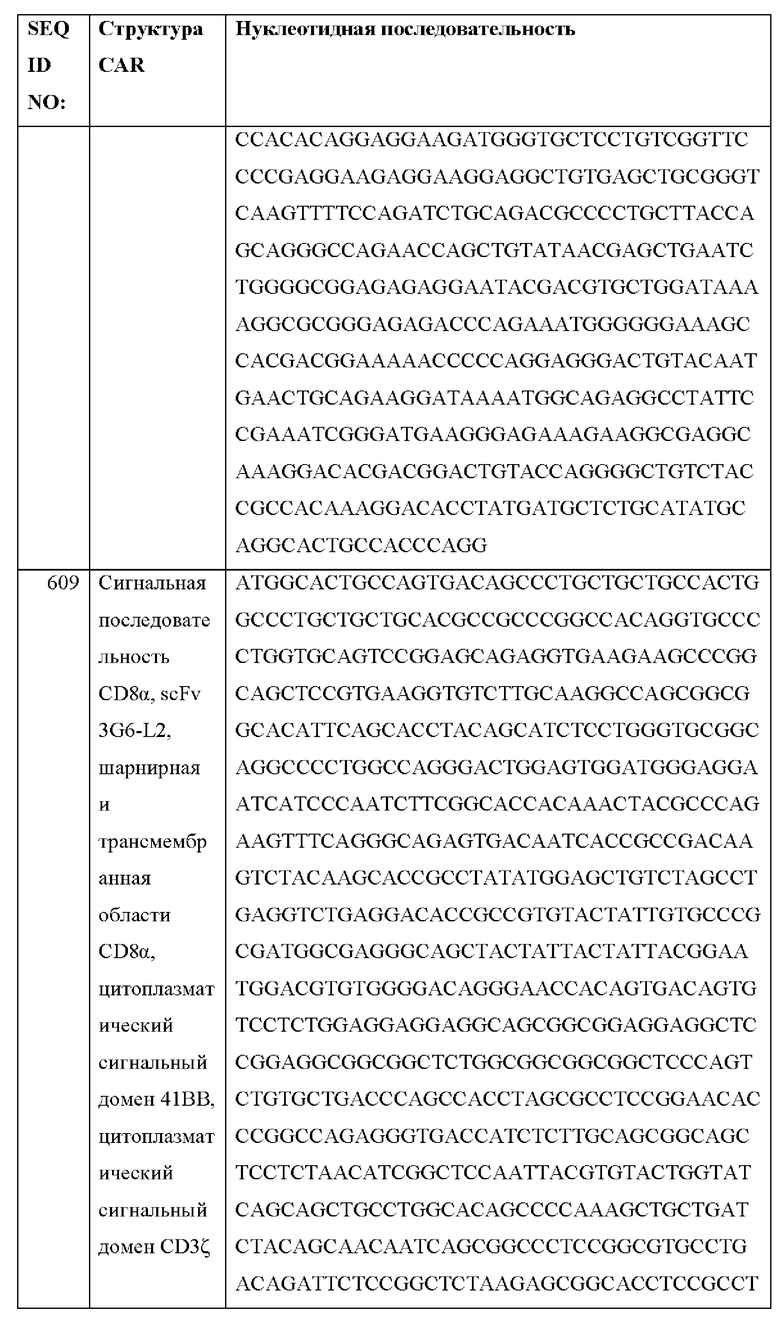

















b. Предохранительные переключатели и эпитопы, специфичные к моноклональным антителам
Предохранительные переключатели
[0135] Следует принимать во внимание, что побочные действия могут быть минимизированы путем трансдукции иммунных клеток (содержащих один или более CAR) «суицидальным» геном. Также может быть желательно включить в иммунные клетки индуцибельный «включающий» или «ускоряющий» переключатель. Подходящие методы включают использование индуцибельной каспазы-9 (заявка на патент США № 2011/0286980) или тимидинкиназы до, после или одновременно с трансдукцией клеток конструкцией CAR согласно настоящему изобретению. Дополнительные методы введения суицидальных генов и/или «включающих» переключателей включают TALEN, цинковые пальцы, РНКи, миРНК, кшРНК, антисмысловую технологию и другие методы, известные в данной области техники.
[0136] В соответствии с изобретением сюда могут быть включены дополнительные «включающие/выключающие» или другие типы методов переключения. В этих методах может применяться использование доменов димеризации и необязательных активаторов димеризации таких доменов. Эти методы включают, например, методы, описанные Wu et al., Science 2014 350 (6258) с использованием систем димеризации FKBP/рапалог в определенных клетках, содержание которых полностью включено в настоящий документ посредством ссылки. Дополнительная технология димеризации описана, например, в Fegan et al. Chem. Rev. 2010, 110, 3315-3336, а также патентах США №№5,830,462; 5,834,266; 5,869,337; и 6,165,787, содержание которых также полностью включено в настоящий документ посредством ссылки. Дополнительные пары димеризации могут включать циклоспорин-А/циклофилин, рецептор, эстроген/рецептор эстрогена (необязательно с использованием тамоксифена), глюкокортикоиды/рецептор глюкокортикоидов, тетрациклин/рецептор тетрациклина, витамин D/рецептор витамина D. Дополнительные примеры технологии димеризации можно найти, например, в WO 2014/127261, WO 2015/090229, US 2014/0286987, US 2015/0266973, US 2016/0046700, патенте США №8,486,693, US 2014/0171649 и US 2012/0130076, содержание которых полностью включено в настоящий документ посредством ссылки.
[0137] В некоторых вариантах осуществления CAR-иммунная клетка (например, CAR-Т-клетка) содержит полинуклеотид, кодирующий суицидальный полипептид, такой как, например, RQR8. См., например, WO 2013153391 A, полностью включенную в настоящий документ посредством ссылки. В CAR-иммунной клетке (например, CAR-T-клетке), клетках, содержащих полинуклеотид, суицидальный полипептид экспрессируется на поверхности CAR-иммунной клетки (например, CAR-T-клетки). В некоторых вариантах осуществления суицидальный полипептид содержит аминокислотную последовательность, представленную в SEQ ID NO: 552:
CPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLCSGGGGSPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHRNRRRVCKCPRPVV (SEQ ID NO: 552).
[0138] Суицидальный полипептид может также содержать сигнальный пептид на аминоконце, например, MGTSLLCWMALCLLGADHADA (SEQ ID NO: 553). В некоторых вариантах осуществления суицидальный полипептид содержит аминокислотную последовательность, представленную в SEQ ID NO: 554, которая включает сигнальную последовательность SEQ ID NO: 553:
MGTSLLCWMALCLLGADHADACPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLCSGGGGSPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHRNRRRVCKCPRPVV (SEQ ID NO: 554).
[0139] Когда суицидальный полипептид экспрессируется на поверхности CAR-иммунной клетки (например, CAR-T-клетки), связывание ритуксимаба с R эпитопами полипептида вызывает лизис клетки. Более чем одна молекула ритуксимаба может связываться с полипептидом, экспрессируемым на поверхности клетки. Каждый R эпитоп полипептида может связывать отдельную молекулу ритуксимаба. Удаление DLL3-специфичных CAR-иммунных клеток (например, CAR-T-клеток) может происходить in vivo, например, при введении пациенту ритуксимаба. Решение об удалении перенесенных клеток может быть принято при обнаружении у субъекта нежелательных эффектов, которые связывают с перенесенными клетками, например, при обнаружении неприемлемых уровней токсичности.
[0140] В некоторых вариантах осуществления суицидальный полипептид экспрессируется на поверхности клетки. В некоторых вариантах осуществления суицидальный полипептид включен в конструкцию CAR. В некоторых вариантах осуществления суицидальный полипептид не является частью конструкции DLL3 CAR.
[0141] В некоторых вариантах осуществления внеклеточный домен любого из CAR, специфичных к DLL3, раскрытых в настоящем документе, может содержать один или более эпитопов, специфичных к моноклональному антителу (специфически распознаваемых им). Эти эпитопы также называются в настоящем документе mAb-специфичными эпитопами. Иллюстративные mAb-специфичные эпитопы описаны в публикации международной патентной заявки WO 2016/120216, полностью включенной в настоящий документ. В этих вариантах осуществления внеклеточный домен CAR содержит антигенсвязывающие домены, которые специфично связываются с DLL3, и один или более эпитопов, которые связываются с одним или более моноклональными антителами (mAb). CAR, содержащие mAb-специфичные эпитопы, могут быть одноцепочечными или многоцепочечными.
[0142] Включение эпитопов, специфичных к моноклональным антителам, во внеклеточный домен CAR, описанных в настоящем документе, позволяет сортировать и истощать сконструированные иммунные клетки, экспрессирующие эти CAR. В некоторых вариантах осуществления эта особенность также способствует восстановлению эндогенных DLL3-экспрессирующих клеток, которые были истощены введением сконструированных иммунных клеток, экспрессирующих эти CAR. В некоторых вариантах осуществления возможность истощения обеспечивает предохранительный переключатель в случае возникновения пагубных эффектов, например, при введении субъекту.
[0143] Соответственно, в некоторых вариантах осуществления настоящее изобретение относится к способу сортировки и/или истощения сконструированных иммунных клеток, наделенных CAR, содержащими mAb-специфичные эпитопы, и способу стимулирования восстановления эндогенных DLL3-экспрессирующих клеток.
[0144] Несколько различных пар эпитоп-моноклональное антитело могут быть использованы для создания CAR, содержащих эпитопы, специфичные к моноклональным антителам; в частности, уже одобренные для медицинского применения, такие как, в качестве неограничивающего примера, эпитоп CD20/ритуксимаб.
[0145] Изобретение также включает способы сортировки сконструированных иммунных клеток, наделенных DLL3-специфичными CAR, экспрессирующими mAb-специфичный эпитоп(ы), и терапевтические методы, при которых активация сконструированных иммунных клеток, наделенных этими CAR, модулируется путем истощения клеток с использованием антитела, нацеленного на внешний лигандсвязывающий домен указанных CAR. В таблице 4 представлены иллюстративные последовательности мимотопов, которые могут быть вставлены во внеклеточные домены любого из CAR согласно изобретению.
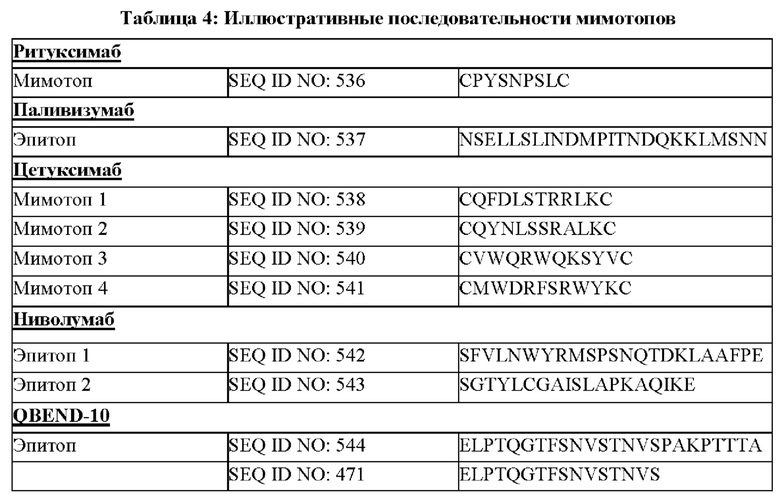

[0146] В некоторых вариантах осуществления внеклеточный связывающий домен CAR содержит следующую последовательность:
- V1-L1-V2-(L)x-Эпитоп-(L)x-;
- V1-L1-V2-(L)x-Эпитоп-(L)x-Эпитоп2-(L)x-;
- V1-L1-V2-(L)х-Эпитоп1-(L)x-Эпитоп2-(L)x-Эпитоп3-(L)x-;
- (L)x-Эпитоп-(L)x-V1-L1-V2;
- (L)x-Эпитоп-(L)x-Эпитоп2-(L)x-V1-L1-V2;
- Эпитоп1-(L)x-Эпитоп2-(L)x-Эпитоп3-(L)x-V1-L1-V2;
- (L)x-Эпитоп-(L)x-V1-L1-V2-(L)x-Эпитоп2-(L)x;
- (L)x-Эпитоп-(L)x-V1-L1-V2-(L)x-Эпитоп2-(L)x-Эпитоп3-(L)x-;
- (L)x-Эпитоп-(L)x-V1-L1-V2-(L)x-Эпитоп2-(L)x-Эпитоп3-(L)x-Эпитоп4-(L)x-;
- (L)x-Эпитоп-(L)x-Эпитоп2-(L)x-V1-L1-V2-(L)x-Эпитоп3-(L)x-;
- (L)x-Эпитоп-(L)x-Эпитоп2-(L)x-V1-L1-V2-(L)x-Эпитоп3-(L)x-Эпитоп4-(L)x-;
- V1-(L)x-Эпитоп-(L)x-V2;
- V1-(L)x-Эпитоп-(L)x-V2-(L)x-Эпитоп2-(L)x;
- V1-(L)x-Эпитоп-(L)x-V2-(L)x-Эпитоп2-(L)x-Эпитоп3-(L)x;
- V1-(L)x-Эпитоп-(L)x-V2-(L)x-Эпитоп2-(L)x-Эпитоп3-(L)x-Эпитоп4-(L)x;
- (L)x-Эпитоп-(L)x-V1-(L)x-Эпитоп2-(L)x-V2; или
- (L)x-Эпитоп-(L)x-V1-(L)x-Эпитоп2-(L)x-V2-(L)x-Эпитоп3-(L)x;
- где
- V1 представляет собой VL и V2 представляет собой VH, или V1 представляет собой VH и V2 представляет собой VL;
- L1 представляет собой линкер, подходящий для связывания цепи VH с цепью VL;
- Эпитоп 1, Эпитоп 2, Эпитоп 3 и Эпитоп 4 являются mAb-специфичными эпитопами и могут быть одинаковыми или
с. Шарнирный домен
[0147] Внеклеточный домен CAR согласно изобретению может содержать «шарнирный» домен (или шарнирную область). Этот термин в общем относится к любому полипептиду, функция которого заключается в связывании трансмембранного домена в CAR с внеклеточным антигенсвязывающим доменом в CAR. В частности, шарнирные домены могут быть использованы для обеспечения большей гибкости и доступности внеклеточного антигенсвязывающего домена.
[0148] Шарнирный домен может содержать до 300 аминокислот - в некоторых вариантах осуществления от 10 до 100 аминокислот, или, в некоторых вариантах осуществления, от 25 до 50 аминокислот. Шарнирный домен может быть получен из всех или части встречающихся в природе молекул, например, из всей или части внеклеточной области CD8, CD4, CD28, 4-1 ВВ или IgG (в частности, шарнирной области IgG; следует понимать, что шарнирная область может содержать часть или весь член семейства иммуноглобулинов, такой как IgG1, IgG2, IgG3, IgG4, IgA, IgD, IgE, IgM, или его фрагмент), или всей или части константной области тяжелой цепи антитела. В качестве альтернативы, домен А может представлять собой синтетическую последовательность, которая соответствует встречающейся в природе последовательности А, или может представлять собой полностью синтетическую последовательность А. В некоторых вариантах осуществления указанный домен А является частью цепи CD8α человека (например, NP_001139345.1). В еще одном частном варианте осуществления указанные транс мембранный и шарнирный домены содержат часть цепи CD8α человека. В некоторых вариантах осуществления шарнирный домен CAR, описанных в настоящем документе, содержит подпоследовательность CD8α, CD28, IgG1, IgG4, PD-1 или FcγRIIIα, в частности, шарнирную область любого из CD8α, CD28, IgG1, IgG4, PD-1 или FcγRIIIα. В некоторых вариантах осуществления шарнирный домен содержит шарнир CD8α человека, шарнир IgG1 человека, шарнир IgG4 человека, PD-1 человека или шарнир FcγRIIIα человека. В некоторых вариантах осуществления CAR, раскрытые в настоящем документе, содержат scFv, человеческие шарнирный и трансмембранный домены CD8α, сигнальный домен CD3C, и сигнальный домен 4-1ВВ. В таблице 5 представлены аминокислотные последовательности для иллюстративных шарниров, предложенных в настоящем документе.


[0149] В отдельных вариантах осуществления шарнирная область содержит аминокислотную последовательность, по меньшей мере приблизительно на 75%, по меньшей мере приблизительно на 80%, по меньшей мере приблизительно на 85%, по меньшей мере приблизительно на 90%, по меньшей мере приблизительно на 95%, по меньшей мере приблизительно на 96%, по меньшей мере приблизительно на 97%, по меньшей мере приблизительно на 98%, по меньшей мере приблизительно на 99% или на 100% идентичную аминокислотным последовательностям внеклеточного домена, приведенным в таблице 5 в настоящем документе.
d. Трансмембранный домен
[0150] CAR согласно изобретению сконструированы с трансмембранным доменом, который слит с внеклеточным доменом CAR. Аналогичным образом он может быть слит с внутриклеточным доменом CAR. В некоторых случаях транс мембранный домен может быть выбран или модифицирован путем аминокислотной замены, чтобы избежать связывания таких доменов с трансмембранными доменами тех же или других поверхностных мембранных белков, чтобы минимизировать взаимодействия с другими членами рецепторного комплекса. В некоторых вариантах осуществления короткие линкеры могут образовывать связи между любыми или некоторыми из внеклеточного, транс мембранного и внутриклеточного доменов CAR.
[0151] Подходящие трансмембранные домены для CAR, раскрытого в настоящем документе, обладают способностью (а) экспрессироваться на поверхности иммунной клетки, такой как, например, не ограничиваясь перечисленным, лимфоцит, такой как Т-хелперная (Th) клетка, цитотоксическая Т (Тс) -клетка, Т-регуляторная (Treg) клетка или естественная киллерная (NK) клетка, и/или (b) взаимодействовать с внеклеточным антигенсвязывающим доменом и внутриклеточным сигнальным доменом для направления клеточного ответа иммунной клетки против клетки-мишени.
[0152] Трансмембранный домен может быть получен либо из природного, либо из синтетического источника. Если источник является естественным, домен может быть получен из любого мембраносвязанного или трансмембранного белка.
[0153] Трансмембранные области, которые, в частности, находят применение в настоящем изобретении, могут быть получены из (содержать или соответствовать) CD28, ОХ-40, 4-1BB/CD137, CD2, CD7, CD27, CD30, CD40, программируемой смерти-1 (PD-1), индуцибельного костимулятора Т-клеток (ICOS), антигена 1, связанного с функцией лимфоцитов (LFA-1 (CD1-1a/CD18), CD-3-гамма, CD3-дельта, CD-3-эпсилон, CD247, CD276 (В7-Н3), LIGHT, (TNFSF14), NKG2C, Ig-альфа (CD79a), DAP-10, Fc-гамма-рецептора, молекулы МНС класса 1, белков TNF-рецептора, белка иммуноглобулина, рецептора цитокинов, интегринов, сигнальных молекул активации лимфоцитов (SLAM-белков), активирующих рецепторов NK-клеток, BTLA, лигандов Toll-рецепторов, ICAM-1, В7-Н3, CDS, ICAM-1, GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CDS-бета, IL-2R-бета, IL-2R-гамма, IL-7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD 18, LFA-1, ITGB7, NKG2D, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRT AM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD 19a, лиганда, который специфически связывается с CD83, или любой их комбинации.
[0154] В качестве неограничивающих примеров, трансмембранная область может быть получена из или может представлять собой субъединицу Т-клеточного рецептора, такую как α, β, γ или δ, полипептид, составляющий комплекс CD3, р55 (а-цепь), р75 (β-цепь) или γ-цепь рецептора IL-2, цепь субъединицы Fc-рецепторов, в частности, Fcγ-рецептора III, или белки CD. В качестве альтернативы, трансмембранный домен может быть синтетическим и может содержать преимущественно гидрофобные остатки, такие как лейцин и валин. В некоторых вариантах осуществления указанный трансмембранный домен получен из цепи CD8α человека (например, NP_001139345.1).
[0155] В некоторых вариантах осуществления трансмембранный домен в CAR согласно изобретению представляет собой трансмембранный домен CD8α. В некоторых вариантах осуществления трансмембранный домен в CAR согласно изобретению представляет собой транс мембранный домен CD8α, содержащий аминокислотную последовательность IYIWAPLAGTCGVLLLSLVIT (SEQ ID NO: 549). В некоторых вариантах осуществления транс мембранный домен CD8α содержит последовательность нуклеиновой кислоты, кодирующую трансмембранную аминокислотную последовательность SEQ ID NO: 549. В некоторых вариантах осуществления шарнирный и трансмембранный домен в CAR согласно изобретению представляет собой шарнирный и трансмембранный домен CD8α, содержащий аминокислотную последовательность SEQ ID NO: 479.
[0156] В некоторых вариантах осуществления трансмембранный домен в CAR согласно изобретению представляет собой трансмембранный домен CD28. В некоторых вариантах осуществления трансмембранный домен в CAR согласно изобретению представляет собой транс мембранный домен CD28, содержащий аминокислотную последовательность FWVLVVVGGVLACYSLLVTVAFIIFWV (SEQ ID NO: 550). В некоторых вариантах осуществления трансмембранный домен CD28 содержит последовательность нуклеиновой кислоты, которая кодирует трансмембранную аминокислотную последовательность SEQ ID NO: 550.
е. Внутриклеточный домен
[0157] Внутриклеточный (цитоплазматический) домен CAR согласно изобретению может обеспечивать активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, содержащей CAR, например, сигнала 1/активации и/или сигнала 2/костимуляции. Например, эффекторная функция Т-клетки может представлять собой цитолитическую активность или хелперную активность, включая секрецию цитокинов.
В некоторых вариантах осуществления активирующий внутриклеточный сигнальный домен для использования в CAR может представлять собой цитоплазматические последовательности, например, не ограничиваясь перечисленным, Т-клеточного рецептора и корецепторов, которые действуют согласованно, инициируя передачу сигнала после взаимодействия с антигенным рецептором, а также любое производное или вариант этих последовательностей и любую синтетическую последовательность, обладающую такой же функциональной способностью.
[0158] Следует принимать во внимание, что подходящие (например, активирующие) внутриклеточные домены включают, не ограничиваясь перечисленным, сигнальные домены, полученные из (или соответствующие) CD3-дзета, CD28, ОХ-40, 4-1BB/CD137, CD2, CD7, CD27, CD30, CD40, программируемой смерти-1 (PD-1), индуцибельного костимулятора Т-клеток (ICOS), антигена 1, связанного с функцией лимфоцитов (LFA-1 (CD1-1a/CD 18), CD3-гамма, CD3-дельта, CD3-эпсилон, CD247, CD276 (В7-Н3), LIGHT, (TNFSF14), NKG2C, Ig-альфа (CD79a), DAP-10, Fc-гамма-рецептора, молекулы МНС класса 1, белков TNF-рецептора, белка иммуноглобулина, рецептора цитокинов, интегринов, сигнальных молекул активации лимфоцитов (SLAM-белков), активирующих рецепторов NK-клеток, BTLA, лигандов Toll-рецепторов, ICAM-1, В7-НЗ, CDS, ICAM-1, GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CDS-бета, IL-2R-бета, IL-2R-гамма, IL-7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRT AM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a, лиганда, который специфически связывается с CD83, или любой их комбинации.
[0159] Внутриклеточные домены CAR согласно изобретению могут включать, в дополнение к активирующим доменам, описанным выше, костимулирующие сигнальные домены (взаимозаменяемо называемые в настоящем документе костимулирующими молекулами) для повышения их активности. Костимулирующие домены могут обеспечивать сигнал в дополнение к первичному сигналу, обеспечиваемому активирующей молекулой, как описано в настоящем документе.
[0160] Следует принимать во внимание, что подходящие костимулирующие домены в рамках настоящего изобретения могут быть получены из (или соответствовать), например, CD28, ОХ40, 4-1BB/CD137, CD2, CD3 (альфа, бета, дельта, эпсилон, гамма, дзета), CD4, CD5, CD7, CD9, CD16, CD22, CD27, CD30, CD33, CD37, CD40, CD45, CD64, CD80, CD86, CD 134, CD 137, CD 154, PD-1, ICOS, антигена 1, связанного с функцией лимфоцитов (LFA-1 (CD1 la/CD 18), CD247, CD276 (В7-Н3), LIGHT (член надсемейства факторов некроза опухоли 14; TNFSF14), NKG2C, Ig-альфа (CD79a), DAP-10, Fc-гамма-рецептора, молекулы МНС класса I, TNFR, интегрина, сигнальных молекул активации лимфоцитов, BTLA, лигандов Toll-рецепторов, ICAM-1, В7-Н3, CDS, ICAM-1, GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CDS-альфа, CDS-бета, IL-2R-бета, IL-2R-гамма, IL-7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD1-1d, ITGAE, CD 103, ITGAL, CD1-1a, LFA-1, ITGAM, CD1-1b, ITGAX, CD1-1c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRT AM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a, лиганда CD83, или их фрагментов или комбинаций. Следует принимать во внимание, что дополнительные ко стимулирующие молекулы или их фрагменты, не перечисленные выше, входят в объем изобретения.
[0161] В некоторых вариантах осуществления внутриклеточный/цитоплазматический домен CAR может быть сконструирован так, чтобы он содержал домен 41BB/CD137 сам по себе или в сочетании с любым другим желаемым внутриклеточным доменом(ами), применимым в контексте CAR согласно изобретению. Полная нативная аминокислотная последовательность 41BB/CD137 описана последовательностью под регистрационным номером NCBI: NP_ 001552.2. Полная нативная последовательность нуклеиновой кислоты 41BB/CD137 описана последовательностью под регистрационным номером NCBI: NM_001561.5.
[0162] В некоторых вариантах осуществления внутриклеточный/цитоплазматический домен CAR может быть сконструирован так, чтобы он содержал домен CD28 сам по себе или в сочетании с любым другим желаемым внутриклеточным доменом(ами), применимым в контексте CAR согласно изобретению. Полная нативная аминокислотная последовательность CD28 описана последовательностью под регистрационным номером NCBI: NP_006130.1. Полная нативная последовательность нуклеиновой кислоты CD28 описана последовательностью под регистрационным номером NCBI: NM_006139.1.
[0163] В некоторых вариантах осуществления внутриклеточный/цитоплазматический домен CAR может быть сконструирован так, чтобы он содержал домен CD3-дзета сам по себе или в сочетании с любым другим желаемым внутриклеточным доменом(ами), применимым в контексте CAR согласно изобретению. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR может содержать сигнальный домен CD3ζ, который имеет аминокислотную последовательность, по меньшей мере приблизительно на 70%, по меньшей мере на 80%, по меньшей мере на 90%, 95%, 97% или на 99% идентичную аминокислотной последовательности, представленной в SEQ ID NO: 481 в таблице 7. Например, внутриклеточный домен CAR может содержать часть дзета-цепи CD3 и часть костимулирующей сигнальной молекулы. Внутриклеточные сигнальные последовательности во внутриклеточной сигнальной части CAR согласно изобретению могут быть связаны друг с другом в случайном или заданном порядке. В некоторых вариантах осуществления внутриклеточный домен сконструирован так, чтобы он содержал активирующий домен CD3-дзета и сигнальный домен CD28. В некоторых вариантах осуществления внутриклеточный домен сконструирован так, чтобы он содержал активирующий домен CD3-дзета и ко стимулирующий/сигнальный домен 4-1 ВВ.
[0164] В некоторых вариантах осуществления 4-1ВВ (внутриклеточный домен) содержит аминокислотную последовательность KRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCEL (SEQ ID NO: 480). В некоторых вариантах осуществления 4-1 ВВ (внутриклеточный домен) кодируется последовательностью нуклеиновой кислоты: 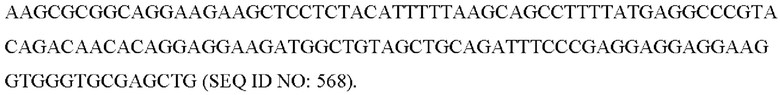
[0165] В некоторых вариантах осуществления внутриклеточный домен в CAR сконструирован так, чтобы он содержал часть CD28 и СО3-дзета, где внутриклеточный CD28 содержит последовательность нуклеиновой кислоты, представленную в SEQ ID NO: 567.
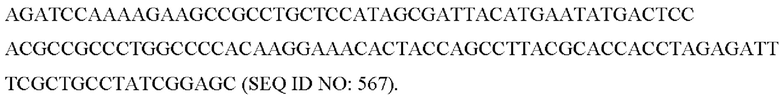
[0166] В некоторых вариантах осуществления внутриклеточный домен в CAR сконструирован так, чтобы он содержал аминокислотную последовательность RSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRS (SEQ ID NO: 551). Аминокислотная последовательность СО3-дзета может содержать SEQ ID NO: 481 или 469, а последовательность нуклеиновой кислоты может содержать SEQ ID NO: 569:
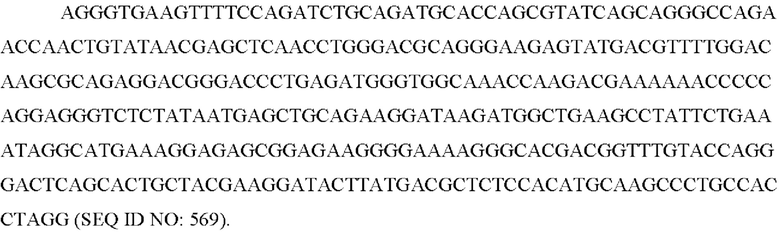
[0167] В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR согласно изобретению содержит домен костимулирующей молекулы. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR согласно изобретению содержит часть костимулирующей молекулы, выбранную из группы, состоящей из фрагмента 4-1 ВВ (GenBank: ААА53133.) и CD28 (NP_006130.1). В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR согласно изобретению содержит аминокислотную последовательность, которая по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, 95%, 97% или на 99% идентична аминокислотной последовательности, представленной в SEQ ID NO: 480 и SEQ ID NO: 551. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR согласно изобретению содержит аминокислотную последовательность, которая по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, 95%, 97% или на 99% идентична аминокислотной последовательности, представленной в SEQ ID NO: 480, и/или по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, 95%, 97% или на 99% идентична аминокислотной последовательности, представленной в SEQ ID NO: 551.
[0168] В иллюстративных вариантах осуществления CAR согласно изобретению содержит, от N-конца к С-концу: (отщепляемую) сигнальную последовательность CD8α, scFv против DLL3, шарнирную и трансмембранную область CD8α, цитоплазматический (костимулирующий) сигнальный домен 4-1 ВВ и цитоплазматический (стимулирующий) сигнальный домен CD3ζ.
III. Иммунные клетки, содержащие CAR
а. Иммунные клетки
[0169] В настоящем документе предложены сконструированные иммунные клетки, экспрессирующие CAR согласно изобретению (например, CAR-T-клетки).
[0170] В некоторых вариантах осуществления сконструированная иммунная клетка содержит популяцию CAR, содержащих различные внеклеточные антигенсвязывающие домены. В некоторых вариантах осуществления иммунная клетка содержит популяцию CAR, каждый из которых содержит один и тот же внеклеточный антигенсвязывающий домен.
[0171] Сконструированные иммунные клетки могут быть аллогенными или аутологичными.
[0172] В некоторых вариантах осуществления сконструированная иммунная клетка представляет собой Т-клетку (например, воспалительный Т-лимфоцит, цитотоксический Т-лимфоцит, регуляторный Т-лимфоцит (Treg), хелперный Т-лимфоцит, опухоль-инфильтрирующий лимфоцит (TIL)), естественную киллерную Т-клетку (NKT), TCR-экспрессирующую клетку, дендритную клетку, киллерную дендритную клетку, тучную клетку или В-клетку. В некоторых вариантах осуществления клетка может происходить из группы, состоящей из CD4+ Т-лимфоцитов и CD8+ Т-лимфоцитов. В некоторых иллюстративных вариантах осуществления иммунная клетка представляет собой Т-клетку. В некоторых иллюстративных вариантах осуществления сконструированная иммунная клетка представляет собой гамма-дельта-Т-клетку. В некоторых иллюстративных вариантах осуществления сконструированная иммунная клетка представляет собой макрофаг. В некоторых иллюстративных вариантах осуществления сконструированная иммунная клетка представляет собой естественную киллерную (NK) клетку.
[0173] В некоторых вариантах осуществления иммунная клетка может происходить, например, не ограничиваясь перечисленным, из стволовой клетки. Стволовые клетки могут представлять собой стволовые клетки взрослого, эмбриональные стволовые клетки нечеловеческого происхождения, в частности, стволовые клетки нечеловеческого происхождения, стволовые клетки пуповинной крови, клетки-предшественники, стволовые клетки костного мозга, индуцированные плюрипотентные стволовые клетки, тотипотентные стволовые клетки или гемопоэтические стволовые клетки.
[0174] В некоторых вариантах осуществления клетка получена или приготовлена из периферической крови. В некоторых вариантах осуществления клетка получена или приготовлена из мононуклеарных клеток периферической крови (МНПК). В некоторых вариантах осуществления клетка получена или приготовлена из костного мозга. В некоторых вариантах осуществления клетка получена или приготовлена из пуповинной крови. В некоторых вариантах осуществления клетка представляет собой клетку человека.
[0175] В некоторых вариантах осуществления клетку трансфицируют или трансдуцируют нуклеиново-кислотным вектором с использованием метода, выбранного из группы, состоящей из электропорации, сонопорации, биолистики (например, Gene Gun), липидной трансфекции, полимерной трансфекции, наночастиц, вирусной трансфекции (например, ретровирусом, лентивирусом, AAV) или полиплексов.
[0176] В некоторых вариантах осуществления сконструированные иммунные клетки, экспрессирующие на своей наружной клеточной мембране DLL3-специфичный CAR согласно изобретению, содержат процентную долю стволовых клеток памяти и клеток центральной памяти, превышающую 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%. В некоторых вариантах осуществления сконструированные иммунные клетки, экспрессирующие на своей наружной клеточной мембране DLL3-специфичный CAR согласно изобретению, содержат процентную долю стволовых клеток памяти и клеток центральной памяти от приблизительно 10% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 10% до приблизительно 60%, от приблизительно 10% до приблизительно 50%, от приблизительно 10% до приблизительно 40%, от приблизительно 10% до приблизительно 30%, от приблизительно 10% до приблизительно 20%, от приблизительно 15% до приблизительно 100%, от приблизительно 15% до приблизительно 90%, от приблизительно 15% до приблизительно 80%, от приблизительно 15% до приблизительно 70%, от приблизительно 15% до приблизительно 60%, от приблизительно 15% до приблизительно 50%, от приблизительно 15% до приблизительно 40%, от приблизительно 15% до приблизительно 30%, от приблизительно 20% до приблизительно 100%, от приблизительно 20% до приблизительно 90%, от приблизительно 20% до приблизительно 80%, от приблизительно 20% до приблизительно 70%, от приблизительно 20% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 20% до приблизительно 40%, от приблизительно 20% до приблизительно 30%, от приблизительно 30% до приблизительно 100%, от приблизительно 30% до приблизительно 90%, от приблизительно 30% до приблизительно 80%, от приблизительно 30% до приблизительно 70%, от приблизительно 30% до приблизительно 60%, от приблизительно 30% до приблизительно 50%, от приблизительно 30% до приблизительно 40%, от приблизительно 40% до приблизительно 100%, от приблизительно 40% до приблизительно 90%, от приблизительно 40% до приблизительно 80%, от приблизительно 40% до приблизительно 70%, от приблизительно 40% до приблизительно 60%, от приблизительно 40% до приблизительно 50%, от приблизительно 50% до приблизительно 100%, от приблизительно 50% до приблизительно 90%, от приблизительно 50% до приблизительно 80%, от приблизительно 50% до приблизительно 70%, от приблизительно 50% до приблизительно 60%, от приблизительно 60% до приблизительно 100%, от приблизительно 60% до приблизительно 90%, от приблизительно 60% до приблизительно 80%, от приблизительно 60% до приблизительно 70%, от приблизительно 70% до приблизительно 90%, от приблизительно 70% до приблизительно 80%, от приблизительно 80% до приблизительно 100%, от приблизительно 80% до приблизительно 90%, от приблизительно 90% до приблизительно 100%, от приблизительно 25% до приблизительно 50%, от приблизительно 75% до приблизительно 100% или от приблизительно 50% до приблизительно 75%.
[0177] В некоторых вариантах осуществления иммунная клетка представляет собой воспалительный Т-лимфоцит, экспрессирующий любой из CAR, описанных в настоящем документе. В некоторых вариантах осуществления иммунная клетка представляет собой цитотоксический Т-лимфоцит, экспрессирующий любой из CAR, описанных в настоящем документе. В некоторых вариантах осуществления иммунная клетка представляет собой регуляторный Т-лимфоцит, экспрессирующий любой из CAR, описанных в настоящем документе. В некоторых вариантах осуществления иммунная клетка представляет собой хелперный Т-лимфоцит, экспрессирующий любой из CAR, описанных в настоящем документе.
[0178] Перед размножением и генетической модификацией источник клеток может быть получен от субъекта с помощью множества неограничивающих способов. Клетки могут быть получены из ряда неограничивающих источников, включая мононуклеарные клетки периферической крови, костный мозг, ткань лимфатических узлов, пуповинную кровь, ткань тимуса, ткань из очага инфекции, асцит, плевральный выпот, ткань селезенки и опухоли. В некоторых вариантах осуществления может быть использовано любое количество линий Т-клеток, доступных и известных специалистам в данной области техники. В некоторых вариантах осуществления клетки могут быть получены от здорового донора, от субъекта, у которого диагностирован рак, или от субъекта, у которого диагностирована инфекция. В некоторых вариантах осуществления клетки могут быть частью смешанной популяции клеток, которые обладают разными фенотипическими характеристиками.
[0179] В настоящем документе также предложены линии клеток, полученные из трансформированной иммунной клетки (например, Т-клетки) в соответствии с любым из описанных выше способов. В настоящем документе также предложены модифицированные клетки, устойчивые к иммуносупрессивному лечению. В некоторых вариантах осуществления выделенная клетка согласно изобретению содержит полинуклеотид, кодирующий CAR.
[0180] Иммунные клетки согласно изобретению могут быть активированы и размножены до или после генетической модификации иммунных клеток с использованием общеизвестных способов. Как правило, сконструированные Т-клетки согласно изобретению могут быть размножены, например, путем приведения их в контакт с агентом, который стимулирует комплекс CD3 с TCR и костимулирующую молекулу на поверхности Т-клеток, создавая активирующий сигнал для Т-клетки. Например, для создания активирующего сигнала для Т-клетки могут быть использованы химические вещества, такие как кальциевый ионофор А23187, форбол-12-миристат 13-ацетат (РМА) или митогенные лектины, такие как фитогемагглютинин (РНА).
[0181] В некоторых вариантах осуществления популяции Т-клеток могут быть стимулированы in vitro путем приведения их в контакт, например, с антителом к CD3, таким как антитело ОКТ3, или его антигенсвязывающим фрагментом, или с антителом к CD28, иммобилизованным на поверхности, или путем приведения их в контакт с активатором протеинкиназы С (например, бриостатином) в сочетании с кальциевым ионофором. Для совместной стимуляции вспомогательной молекулы на поверхности Т-клеток используют лиганд, который связывает эту вспомогательную молекулу. Например, популяция Т-клеток может быть приведена в контакт с антителом к CD3 (например, антителом ОКТ3) и антителом к CD28 в условиях, подходящих для стимуляции пролиферации Т-клеток. Антитело к CD3 и антитело к CD28 могут быть расположены на шарике, таком как пластиковый или магнитный шарик, или планшете, или другом субстрате. Условия, подходящие для культуры Т-клеток, включают подходящую среду (например, минимальную питательную среду или среду RPMI 1640 или Х-vivo 15 (Lonza)), которая может содержать факторы, необходимые для пролиферации и жизнеспособности, включая сыворотку (например, эмбриональную телячью сыворотку или человеческую сыворотку, интерлейкин-2 (IL-2), инсулин, IFN-γ, IL-4, IL-7, ГМ-КСФ, IL-10, IL-2, IL-15, TGF-бета и TNF, или любые другие добавки для роста клеток, известные специалисту в данной области техники. Другие добавки для роста клеток включают, не ограничиваясь перечисленным, поверхностно-активное вещество, плазманат и восстанавливающие агенты, такие как N-ацетилцистеин и 2-меркаптоэтанол. Среда может включать RPMI 1640, A1M-V, DMEM, MEM, a- MEM, F-12, Х-Vivo 15 и Х-Vivo 20, Optimizer с добавками аминокислот, пирувата натрия и витаминов, бессывороточную или с добавлением соответствующего количества сыворотки (или плазмы), или определенного набора гормонов, и/или определенного количества цитокина(ов), достаточного для роста и размножения Т-клеток (например, IL-7 и/или IL-15). Антибиотики, например, пенициллин и стрептомицин, включают только в экспериментальные культуры, но не в культуры клеток, которые должны быть введены субъекту. Клетки-мишени поддерживают в условиях, необходимых для поддержания роста, например, при соответствующей температуре (например, 37°С) и атмосфере (например, воздух плюс 5% СО2). Т-клетки, подвергавшиеся стимуляции в течение разного количества времени, могут обладать разными характеристиками. В некоторых вариантах осуществления клетки согласно изобретению могут быть размножены путем совместного культивирования с тканью или клетками. Клетки также могут быть размножены in vivo, например, в крови субъекта после введения клетки субъекту.
[0182] В некоторых вариантах осуществления сконструированная иммунная клетка согласно изобретению может содержать один или более нарушенных или инактивированных генов. В некоторых вариантах осуществления сконструированная иммунная клетка согласно настоящему изобретению содержит один нарушенный или инактивированный ген, выбранный из группы, состоящей из CD52, DLL3, GR, PD-1, CTLA-4, LAG3, TIM3, BTLA, BY55, TIGIT, В7Н5, LAIR1, SIGLEC10, 2 В4, HLA, TCRα и TCRβ, и/или экспрессирует CAR, многоцепочечный CAR и/или трансген рТα. В некоторых вариантах осуществления выделенная клетка содержит полинуклеотиды, кодирующие полипептиды, содержащие многоцепочечный CAR. В некоторых вариантах осуществления выделенная клетка согласно настоящему изобретению содержит два нарушенных или инактивированных гена, выбранных из группы, состоящей из: CD52 и GR, CD52 и TCRα, CDR52 и TCRβ, DLL3 и CD52, DLL3 и TCRα, DLL3 и TCRβ, GR и TCRα, GR и TCRβ, TCRα и TCRβ, PD-1 и TCRα, PD-1 и TCRβ, CTLA-4 и TCRα, CTLA-4 и TCRβ, LAG3 и TCRα, LAG3 и TCRβ, TIM3 и TCRα, Tim3 и TCRβ, BTLA и TCRα, BTLA и TCRβ, BY55 и TCRα, BY55 и TCRβ, TIGIT и TCRα, TIGIT и TCRβ, B7H5 и TCRα, B7H5 и TCRβ, LAIR1 и TCRα, LAIR1 и TCRβ, SIGLEC10 и TCRα, SIGLEC10 и TCRβ, 2B4 и TCRα, 2B4 и TCRβ, и/или экспрессирует CAR, многоцепочечный CAR и трансген pTα. В некоторых вариантах осуществления способ включает нарушение или инактивацию одного или более генов путем введения в клетки эндонуклеазы, способной селективно инактивировать ген путем селективного расщепления ДНК. В некоторых вариантах осуществления эндонуклеаза может представлять собой, например, нуклеазу цинкового пальца (ZFN), нуклеазу megaTAL, мегануклеазу, эффекторную нуклеазу, подобную активатору транскрипции (TALE-нуклеазу/TALEN), или эндонуклеазу CRISPR (например, Cas9).
[0183] В некоторых вариантах осуществления TCR делают нефункциональным в клетках согласно изобретению путем нарушения или инактивации гена TCRα и/или гена (генов) TCRβ.В некоторых вариантах осуществления предложен способ получения модифицированных клеток, происходящих от индивидуума, согласно которому клетки могут пролиферировать независимо от пути передачи сигнала главного комплекса гистосовместимости (МНС). Модифицированные клетки, которые могут пролиферировать независимо от пути передачи сигнала МНС, которые могут быть получены этим способом, входят в объем настоящего изобретения. Раскрытые в настоящем документе модифицированные клетки можно применять для лечения отторжения «хозяин против трансплантата» (ХПТ) и реакции «трансплантат против хозяина» (РТПХ) у нуждающихся в этом пациентов; соответственно, в объем настоящего изобретения включен способ лечения нуждающихся в этом пациентов от отторжения «хозяин против трансплантата» (ХПТ) и реакции «трансплантат против хозяина» (РТПХ), включающий лечение указанного пациента путем введения указанному пациенту эффективного количества модифицированных клеток, содержащих нарушенные или инактивированные гены TCRα и/или TCRβ.
[0184] В некоторых вариантах осуществления иммунные клетки конструируют таким образом, чтобы они были устойчивыми к одному или более химиотерапевтическим лекарственным средствам. Химиотерапевтическое лекарственное средство может представлять собой, например, аналог пуринового нуклеотида (PNA), что таким образом делает иммунную клетку подходящей для лечения рака в комбинации с адоптивной иммунотерапией и химиотерапией. Примеры PNA включают, например, клофарабин, флударабин, циклофосфамид и цитарабин, по отдельности или в комбинации. PNA метаболизируются дезоксицитидинкиназой (dCK) в моно-, ди- и трифосфатные PNA. Их трифосфатные формы конкурируют с АТФ за синтез ДНК, действуют как проапоптотические агенты и являются мощными ингибиторами рибонуклеотидредуктазы (RNR), участвующей в образовании тринуклеотидов. В настоящем изобретении предложены DLLS-специфичные CAR-T-клетки, содержащие нарушенный или инактивированный ген dCK. В некоторых вариантах осуществления клетки с нокаутом dCK получают путем трансфекции Т-клеток с использованием полинуклеотидов, кодирующих специфическую TAL-нуклеазу, направленную против генов dCK, например, путем электропорации мРНК. DLL3-специфичные CAR-T-клетки с нокаутом dCK устойчивы к PNA, включая, например, клофарабин и/или флударабин, и сохраняют цитотоксическую активность Т-клеток в отношении DLL3-экспрессирующих клеток.
[0185] В некоторых вариантах осуществления выделенные клетки или линии клеток согласно изобретению могут содержать рТα или его функциональный вариант. В некоторых вариантах осуществления выделенная клетка или линия клеток может быть дополнительно генетически модифицирована путем нарушения или инактивации гена TCRα.
[0186] Согласно настоящему изобретению также предложены сконструированные иммунные клетки, содержащие любой из полинуклеотидов CAR, описанных в настоящем документе. В некоторых вариантах осуществления CAR могут быть введены в иммунную клетку в качестве трансгена с помощью плазмидного вектора. В некоторых вариантах осуществления плазмидный вектор может также содержать, например, маркер отбора, который обеспечивает возможность идентификации и/или отбора клеток, которые получили вектор.
[0187] Полипептиды CAR могут быть синтезированы in situ в клетке после введения в клетку полинуклеотидов, кодирующих полипептиды CAR. В качестве альтернативы, полипептиды CAR могут быть продуцированы вне клеток, а затем введены в клетки. Способы введения полинуклеотидной конструкции в клетки известны в данной области техники. В некоторых вариантах осуществления для интеграции полинуклеотидной конструкции в геном клетки могут быть использованы методы стабильной трансформации (например, с использованием лентивирусного вектора). В других вариантах осуществления могут быть использованы методы временной трансформации для временной экспрессии полинуклеотидной конструкции, и полинуклеотидная конструкция не будет интегрирована в геном клетки. В других вариантах осуществления могут быть использованы вирус-опосредованные методы. Полинуклеотиды могут быть введены в клетку любыми подходящими средствами, например, с использованием рекомбинантных вирусных векторов (например, ретровирусов, аденовирусов), липосом и тому подобного. Способы временной трансформации включают, например, не ограничиваясь перечисленным, микроинъекцию, электропорацию или бомбардировку частицами. Полинуклеотиды могут быть включены в векторы, такие как, например, плазмидные векторы или вирусные векторы.
[0188] В некоторых вариантах осуществления предложены выделенные нуклеиновые кислоты, содержащие промотор, функционально связанный с первым полинуклеотидом, кодирующим антигенсвязывающий домен DLL3, по меньшей мере одну костимулирующую молекулу и активирующий домен. В некоторых вариантах осуществления конструкция нуклеиновой кислоты содержится в вирусном векторе. В некоторых вариантах осуществления вирусный вектор выбран из группы, состоящей из ретровирусных векторов, векторов вируса мышиного лейкоза, векторов SFG, аденовирусных векторов, лентивирусных векторов, аденоассоциированных вирусных (AAV) векторов, герпесвирусных векторов и векторов вируса осповакцины. В некоторых вариантах осуществления нуклеиновая кислота содержится в плазмиде.
b. Способы получения
[0189] В настоящем документе предложены способы получения CAR и CAR-содержащих иммунных клеток согласно изобретению.
[0190] Для получения полинуклеотидов, полипептидов, векторов, антигенсвязывающих доменов, иммунных клеток, композиций и т.п.в соответствии с изобретением может быть использовано множество известных методик.
[0191] Перед манипуляциями in vitro или генетической модификацией иммунных клеток, описанных в настоящем документе, клетки могут быть получены от субъекта. Клетки, экспрессирующие DLL3 CAR, могут быть получены в результате аллогенного или аутологичного процесса.
i. Исходный материал
[0192] В некоторых вариантах осуществления иммунные клетки включают Т-клетки. Клетки могут быть получены из ряда источников, включая мононуклеарные клетки периферической крови (МНПК), костный мозг, ткань лимфатических узлов, пуповинную кровь, ткань тимуса, ткань из очага инфекции, асцит, плевральный выпот, ткань селезенки и опухоли. В отдельных вариантах осуществления Т-клетки могут быть получены из единицы крови, взятой у субъекта, с использованием любого количества методик, известных специалисту, таких как разделение FICOLL™.
[0193] Клетки могут быть получены из циркулирующей крови человека с помощью афереза. Продукт афереза обычно содержит лимфоциты, включая Т-клетки, моноциты, гранулоциты, В-клетки, другие ядросодержащие лейкоциты, эритроциты и тромбоциты. В отдельных вариантах осуществления клетки, собранные с помощью афереза, могут быть промыты для удаления фракции плазмы и помещены в подходящий буфер или среду для последующей обработки.
[0194] В некоторых вариантах осуществления Т-клетки выделяют из МНПК путем лизирования эритроцитов и истощения моноцитов, например, с помощью центрифугирования в градиенте PERCOLL™. Конкретная субпопуляция Т-клеток (например, CD28+, CD4+, CDS+, CD45RA-, CD45RO+, CDS+, CD62-, CD95-, CD95+, IL2Rβ+, IL2Rβ-, CCR7+, CCR7-, CDL-, CD62L+ и их комбинации) может быть дополнительно выделена методами положительного или отрицательного отбора, известными в данной области техники. В одном примере субпопуляция Т-клеток представляет собой CD45RA+, CD95-, IL-2Rβ-, CCR7+, CD62L+. В одном примере субпопуляция Т-клеток представляет собой CD45RA+, CD95+, IL-2Rβ+, CCR7+, CD62L+. В одном примере субпопуляция Т-клеток представляет собой CD45RO+, CD95+, IL-2Rβ+, CCR7+, CD62L+. В одном примере субпопуляция Т-клеток представляет собой CD45RO+, CD95+, IL-2Rβ+, CCR7-, CD62L-. В одном примере субпопуляция Т-клеток представляет собой CD45RA+, CD95+, IL-2Rβ+, CCR7-, CD62L-. Например, обогащение популяции Т-клеток путем отрицательного отбора может быть достигнуто с помощью комбинации антител, направленных на поверхностные маркеры, уникальные для отрицательно отобранных клеток. Одним из способов, подходящих для использования в настоящем изобретении, является сортировка и/или отбор клеток с помощью отрицательной магнитной иммуноадгезии или проточной цитометрии, в которой используется коктейль моноклональных антител, направленных на маркеры клеточной поверхности, присутствующие на отрицательно отобранных клетках. Например, для обогащения CD4+ клетками путем отрицательного отбора коктейль моноклональных антител обычно включает антитела к CD14, CD20, CD11b, CD16, HLA-DR и CD8. Проточная цитометрия и сортировка клеток также могут использоваться для выделения представляющих интерес популяций клеток для использования в настоящем изобретении.
[0195] МНПК могут быть использованы непосредственно для генетической модификации иммунными клетками (такими как CAR или TCR) с использованием способов, описанных в настоящем документе. В отдельных вариантах осуществления после выделения МНПК Т-лимфоциты могут быть дополнительно выделены, и как цитотоксические, так и хелперные Т-лимфоциты могут быть отсортированы на субпопуляции наивных Т-клеток, Т-клеток памяти и эффекторных Т-клеток либо до, либо после генетической модификации и/или размножения.
[0196] В некоторых вариантах осуществления CD8+ клетки дополнительно сортируют на наивные клетки, стволовые клетки памяти, клетки центральной памяти и эффекторные клетки путем идентификации характерных антигенов клеточной поверхности, которые связаны с каждым из этих типов CD8+ клеток. В некоторых вариантах осуществления экспрессия фенотипических маркеров Т-клеток центральной памяти включает CD45RO, CD62L, CCR7, CD28, CD3 и CD 127 и является отрицательной на гранзим В. В некоторых вариантах осуществления стволовые Т-клетки памяти представляют собой CD45RO-, CD62L+, CD8+Т-клетки. В некоторых вариантах осуществления Т-клетки центральной памяти представляют собой CD45RO+, CD62L+, CD8+Т-клетки. В некоторых вариантах осуществления эффекторные Т-клетки отрицательны на CD62L, CCR7, CD28 и CD 127 и положительны на гранзим В и перфорин.
[0197] В отдельных вариантах осуществления CD4+ Т-клетки дополнительно разделяют на субпопуляции. Например, CD4+ Т-хелперы могут быть отсортированы на наивные клетки, клетки центральной памяти и эффекторные клетки путем идентификации популяций клеток, имеющих характерные антигены клеточной поверхности.
iii. Иммунные клетки, полученные из стволовых клеток
[0198] В некоторых вариантах осуществления иммунные клетки могут быть получены из стволовых клеток, таких как клетка-предшественник, стволовая клетка костного кургана, индуцируемая плюрипотентная стволовая клетка, ИПСК, гемопоэтическая стволовая клетка и мезенхимальная стволовая клетка. ИПС-клетки и другие типы стволовых клеток могут представлять собой культивируемые иммортализованные линии клеток или могут быть выделены непосредственно от пациента. Различные способы выделения, разработки и/или культивирования стволовых клеток известны в данной области техники и могут быть использованы для практического осуществления настоящего изобретения.
[0199] В некоторых вариантах осуществления иммунная клетка представляет собой индуцированную плюрипотентную стволовую клетку (ИПСК), полученную из перепрограммированной Т-клетки. В некоторых вариантах реализации исходный материал может представлять собой индуцированную плюрипотентную стволовую клетку (ИПСК), полученную из Т-клетки или клетки, отличной от Т-клетки. В качестве альтернативы, исходный материал может представлять собой В-клетку или любую другую клетку из изолятов мононуклеарных клеток периферической крови, гемопоэтических предшественников, гематопоэтических стволовых клеток, мезенхимальных стволовых клеток, стволовых клеток жировой ткани или любого другого типа соматических клеток.
ii. Генетическая модификация выделенных клеток
[0200] Иммунные клетки, такие как Т-клетки, могут быть генетически модифицированы после выделения с использованием известных методов, или иммунные клетки могут быть активированы и размножены (или дифференцированы в случае предшественников) in vitro перед генетической модификацией. В некоторых вариантах осуществления выделенные иммунные клетки генетически модифицируют для снижения или устранения экспрессии эндогенных TCRα и/или CD52. В некоторых вариантах осуществления клетки генетически модифицируют с использованием технологии редактирования генов (например, CRISPR/Cas9, CRISPR/CAS12, нуклеазы цинкового пальца (ZFN), TALEN, MegaTAL, мегануклеазы) для снижения или устранения экспрессии эндогенных белков (например, TCRα и/или CD52). В еще одном варианте осуществления иммунные клетки, такие как Т-клетки, необязательно дополнительно генетически модифицируют описанными в настоящем документе химерными антигенными рецепторами (например, трансдуцируют вирусным вектором, содержащим одну или более нуклеотидных последовательностей, кодирующих CAR), а затем активируют и/или размножают in vitro.
[0201] Способы активации и размножения Т-клеток известны в данной области техники и описаны, например, в патенте США №6,905,874; патенте США №6,867,041; патенте США №6,797,514; и публикации заявки РСТ WO 2012/079000, содержание которых полностью включено в настоящий документ посредством ссылки. Обычно такие способы включают приведение МНПК или выделенных Т-клеток в контакт со стимулирующей молекулой и костимулирующей молекулой, такой как антитела против CD3 и против CD28, обычно прикрепленные к пластиковому или магнитному шарику или другой поверхности, в культуральной среде с соответствующими цитокинами, например, IL-2. Антитела против CD3 и против CD28, прикрепленные к одному и тому же шарику, служат «суррогатными» антигенпрезентирующими клетками (АПК). Одним из примеров является система Dynabeads®, которая представляет собой систему активатора/стимулятора CD3/CD28 для физиологической активации человеческих Т-клеток. В других вариантах осуществления Т-клетки могут быть активированы и стимулированы для пролиферации фидерными клетками и соответствующими антителами и цитокинами с использованием способов, таких как описанные в патенте США №6,040,177; патенте США №5,827,642; и WO 2012129514, содержание которых полностью включено в настоящий документ посредством ссылки.
[0202] Некоторые способы создания конструкций и сконструированных иммунных клеток согласно изобретению описаны в заявке РСТ PCT/US15/14520, содержание которой полностью включено в настоящий документ посредством ссылки.
[0203] Следует принимать во внимание, что МНПК могут дополнительно включать другие цитотоксические лимфоциты, такие как NK-клетки или NKT-клетки. Вектор экспрессии, несущий кодирующую последовательность химерного рецептора, как раскрыто в настоящем документе, может быть введен в популяцию донорских человеческих Т-клеток, NK-клеток или NKT-клеток. Успешно трансдуцированные Т-клетки, несущие вектор экспрессии, могут быть отсортированы с помощью проточной цитометрии для выделения CD3-положительных Т-клеток и затем дополнительно размножены для увеличения количества этих Т-клеток, экспрессирующих CAR, в дополнение к активации клеток с использованием антител к CD3 и IL-2 или других способов, известных в данной области техники, как описано в других местах в настоящем документе. Стандартные процедуры используют для криоконсервации Т-клеток, экспрессирующих CAR, для хранения и/или подготовки для применения у человека. В одном из вариантов осуществления трансдукцию, культивирование и/или размножение Т-клеток in vitro проводят в отсутствие продуктов, происходящих от животных, отличных от человека, таких как фетальная телячья сыворотка и фетальная бычья сыворотка. В одном из вариантов осуществления криоконсервация может включать замораживание в подходящей среде, такой как CryoStor® CS10, CryoStor® CS2 или CryoStor® CS5 (BioLife Solutions).
[0204] Для клонирования полинуклеотидов вектор может быть введен в клетку-хозяина (выделенную клетку-хозяина), чтобы обеспечить репликацию самого вектора и тем самым амплифицировать копии содержащегося в нем полинуклеотида. Клонирующие векторы могут содержать компоненты последовательности, как правило, включая, не ограничиваясь перечисленным, точку начала репликации, промоторные последовательности, последовательности инициации транскрипции, энхансерные последовательности и селектируемые маркеры. Эти элементы могут быть выбраны соответствующим образом специалистом в данной области техники. Например, точка начала репликации может быть выбрана так, чтобы способствовать автономной репликации вектора в клетке-хозяине.
[0205] В отдельных вариантах осуществления настоящее изобретение относится к выделенным клеткам-хозяевам, содержащим вектор, предложенный в настоящем документе. Клетки-хозяева, содержащие вектор, могут быть пригодны для экспрессии или клонирования полинуклеотида, содержащегося в векторе. Подходящие клетки-хозяева могут включать, не ограничиваясь перечисленным, прокариотические клетки, грибковые клетки, дрожжевые клетки или высшие эукариотические клетки, такие как клетки млекопитающих, и более конкретно клетки человека.
[0206] Вектор может быть введен в клетку-хозяина с использованием любых подходящих способов, известных в данной области техники, включая, не ограничиваясь перечисленным, доставку, опосредованную DEAE-декстраном, метод осаждения с фосфатом кальция, доставку, опосредованную катионными липидами, трансфекцию, опосредованную липосомами, электропорацию, бомбардировку микрочастицами, рецептор-опосредованную доставку гена, доставку, опосредованную полилизином, гистоном, хитозаном и пептидами. Стандартные методы вирусной трансфекции и трансформации клеток для экспрессии представляющего интерес вектора хорошо известны в данной области техники. В дополнительном варианте осуществления смесь различных векторов экспрессии может быть использована для генетической модификации донорской популяции иммунных эффекторных клеток, где каждый вектор кодирует отдельный CAR, как раскрыто в настоящем документе. Полученные трансдуцированные иммунные эффекторные клетки образуют смешанную популяцию сконструированных клеток, причем часть сконструированных клеток экспрессирует более одного разного CAR.
[0207] В одном из вариантов осуществления изобретение относится к способу хранения генетически модифицированных клеток, экспрессирующих CAR, нацеленных на белок DLL3. В одном из вариантов осуществления он включает криоконсервацию иммунных клеток таким образом, что клетки остаются жизнеспособными после размораживания. В одном из вариантов осуществления криоконсервация может включать замораживание в подходящей среде, такой как CryoStor® CS10, CryoStor® CS2 или CryoStor® CS5 (BioLife Solutions). Фракция иммунных клеток, экспрессирующих CAR, может быть криоконсервирована способами, известными в данной области техники, чтобы обеспечить постоянный источник таких клеток для будущего лечения пациентов, страдающих злокачественными новообразованиями. При необходимости криоконсервированные трансформированные иммунные клетки могут быть разморожены, выращены и размножены для получения большего количества таких клеток.
[0208] В некоторых вариантах осуществления клетки готовят, сначала собирая их из культуральной среды, а затем промывая и концентрируя клетки в среде и системе контейнеров, подходящих для введения («фармацевтически приемлемый» носитель), в эффективном для лечения количестве. Подходящей инфузионной средой может быть любой изотонический состав среды, обычно физиологический раствор, Normosol™ R (Abbott) или Plasma-Lyte™ A (Baxter), а также можно использовать 5% раствор декстрозы в воде или лактат Рингера. Инфузионная среда может быть дополнена человеческим сывороточным альбумином.
iv. Аллогенные CAR-T-клетки
[0209] Вкратце, процесс производства аллогенной CAR Т-терапии или AlloCARs™ включает сбор здоровых, отобранных, подвергнутых скринингу и протестированных Т-клеток от здоровых доноров. Аллогенные Т-клетки подвергают редактированию генов, чтобы снизить риск реакции «трансплантат против хозяина» (РТПХ) и предотвратить аллогенное отторжение. Выбранный ген Т-клеточного рецептора (например, TCRα, TCRβ) нокаутируют, чтобы избежать РТПХ. Ген CD52 также может быть отключен, чтобы сделать продукт CAR Т устойчивым к лечению антителом к CD52. Таким образом, лечение антителом к CD52 может быть использовано для лимфодеплеции иммунной системы хозяина и позволяет CAR Т-клеткам оставаться прижившимися для достижения полного терапевтического эффекта. Затем конструируют Т-клетки для экспрессии CAR, которые распознают определенные белки клеточной поверхности (например, DLL-3), которые экспрессируются в гематологических или солидных опухолях. Затем сконструированные Т-клетки проходят стадию очистки и в конечном итоге подвергаются криоконсервации во флаконах для доставки пациентам.
v. Аутологичные CAR-T-клетки
[0210] Терапия аутологичными Т-клетками с химерным антигенным рецептором (CAR) включает сбор собственных клеток пациента (например, лейкоцитов, включая Т-клетки) и генетическую модификацию Т-клеток для экспрессии CAR, которые распознают антиген-мишень, экспрессируемый на клеточной поверхности одной или более определенных раковых клеток, и уничтожают раковые клетки. Затем сконструированные клетки криоконсервируют, после чего вводят пациенту, клетки которого были изъяты для модификации.
IV. Способы лечения
[0211] Изобретение включает способы лечения или предупреждения состояния, связанного с нежелательными и/или повышенными уровнями DLL3 у пациента, включающие введение нуждающемуся в этом пациенту эффективного количества по меньшей мере одного CAR или иммунных клеток, содержащих CAR, описанный в настоящем документе.
[0212] Предложены способы лечения заболеваний или нарушений, включая рак. В некоторых вариантах осуществления изобретение относится к созданию опосредованного Т-клетками иммунного ответа у субъекта, включающему введение указанному субъекту эффективного количества сконструированных иммунных клеток согласно настоящей заявке. В некоторых вариантах осуществления опосредованный Т-клетками иммунный ответ направлен против клетки- или клеток-мишеней. В некоторых вариантах осуществления сконструированная иммунная клетка дополнительно содержит химерный антигенный рецептор (CAR). В некоторых вариантах осуществления клетка-мишень представляет собой опухолевую клетку. В некоторых аспектах изобретение включает способ лечения или предупреждения злокачественного новообразования, включающий введение нуждающемуся в этом субъекту эффективного количества по меньшей мере одного выделенного антигенсвязывающего домена, описанного в настоящем документе. В некоторых аспектах изобретение включает способ лечения или предупреждения злокачественного новообразования, включающий введение нуждающемуся в этом субъекту эффективного количества по меньшей мере одной иммунной клетки, где иммунная клетка содержит по меньшей мере один химерный антигенный рецептор и/или выделенный антигенсвязывающий домен, как описано в настоящем документе. CAR, содержащие иммунные клетки согласно изобретению, могут быть использованы для лечения злокачественных новообразований, связанных с аберрантной экспрессией DLL3. В некоторых вариантах осуществления CAR, содержащие иммунные клетки согласно изобретению, могут быть использованы для лечения таких злокачественных новообразований, как мелкоклеточный рак легкого, меланома, глиомы низкой степени злокачественности, глиобластома, медуллярный рак щитовидной железы, карциноиды, диспергированные нейроэндокринные опухоли поджелудочной железы, мочевого пузыря и предстательной железы, рак яичка и аденокарциномы легких с нейроэндокринными особенностями. В иллюстративных вариантах осуществления CAR-содержащие иммунные клетки, например, анти-DLL3 CAR-T-клетки согласно изобретению, применяют для лечения мелкоклеточного рака легкого.
[0213] Также предложены способы уменьшения размера опухоли у субъекта, включающие введение указанному субъекту сконструированной клетки согласно настоящему изобретению, где клетка содержит химерный антигенный рецептор, содержащий антигенсвязывающий домен против DLL3, и связывается с антигеном DLL3 на опухоли.
[0214] В некоторых вариантах осуществления субъект имеет солидную опухоль или гематологическое злокачественное новообразование, такое как лимфома или лейкоз. В некоторых вариантах осуществления сконструированная клетка доставляется в ложе опухоли, такое как ложе опухоли, которое имеет место при мелкоклеточном раке легкого. В некоторых вариантах осуществления рак имеет место в костном мозге субъекта. В некоторых вариантах осуществления сконструированные клетки представляют собой аутологичные иммунные клетки, например, аутологичные Т-клетки. В некоторых вариантах осуществления сконструированные клетки представляют собой аллогенные иммунные клетки, например, аллогенные Т-клетки. В некоторых вариантах осуществления сконструированные клетки представляют собой гетерологичные иммунные клетки, например, гетерологичные Т-клетки. В некоторых вариантах осуществления сконструированные клетки трансфицируют или трансдуцируют ex vivo. В контексте настоящего документа термин «клетка in vitro» относится к любой клетке, которую культивируют ex vivo.
[0215] «Терапевтически эффективное количество», «эффективная доза», «эффективное количество» или «терапевтически эффективная дозировка» терапевтического агента, например, сконструированных CAR-T-клеток, представляет собой любое количество, которое при использовании по отдельности или в комбинации с другим терапевтическим агентом защищает субъекта от начала заболевания или способствует регрессу заболевания, о чем свидетельствует уменьшение тяжести симптомов заболевания, увеличение частоты и продолжительности бессимптомных периодов заболевания или предотвращение ухудшения или потери трудоспособности из-за заболевания. Способность терапевтического агента способствовать регрессу заболевания может быть оценена с использованием различных методов, известных квалифицированному практикующему врачу (например, терапевту или клиницисту), например, у людей во время клинических исследований, в модельных системах на животных, предсказывающих эффективность у людей, или путем анализа активности агента в анализах in vitro.
[0216] Термины «пациент» и «субъект» используются взаимозаменяемо и включают субъектов-людей и животных, отличных от человека, а также лиц с официально диагностированными нарушениями, лиц без официально признанных нарушений, лиц, получающих медицинскую помощь, лиц с риском развития нарушений и т.д.
[0217] Термины «лечить» и «лечение» включают терапевтическое лечение, профилактическое лечение и применения, в которых снижается риск того, что у субъекта разовьется нарушение, или другой фактор риска. Лечение не требует полного излечения нарушения и охватывает варианты осуществления, в которых уменьшаются симптомы или основные факторы риска. Термин «предотвращать» не требует 100% исключения возможности события. Скорее, это означает, что вероятность возникновения события уменьшилась в присутствии соединения или способа.
[0218] Общее желаемое для лечения количество клеток в композиции включает по меньшей мере 2 клетки (например, по меньшей мере одну CD8+ Т-клетку и по меньшей мере одну CD4+ Т-клетку, или две CD8+ Т-клетки, или две CD4+ Т-клетки) или, как правило, составляет более 102 клеток и вплоть до 106, вплоть до и включая 108 или 109 клеток, и может составлять 1010 или 1012 или более клеток. Количество клеток будет зависеть от желаемого применения, для которого предназначена композиция, и типа клеток, включенных в нее. Плотность желаемых клеток обычно превышает 106 клеток/мл и обычно превышает 107 клеток/мл, обычно составляет 108 клеток/мл или более. Клинически значимое количество иммунных клеток может быть разделено на несколько инфузий, которые в совокупности равны или превышают 105, 106, 107, 108, 109, 1010, 1011 или 1012 клеток. В некоторых аспектах настоящего изобретения, в частности, поскольку все введенные с помощью инфузий клетки будут перенаправлены на конкретный антиген-мишень (например, DLL3), может быть введено меньшее количество клеток, в диапазоне 106/килограмм (106-1011 на пациента). Лечение CAR можно осуществлять несколько раз в дозировках в пределах этих диапазонов. Клетки могут быть аутологичными, аллогенными или гетерологичными по отношению к пациенту, проходящему терапию.
[0219] В некоторых вариантах осуществления терапевтически эффективное количество CAR-T-клеток составляет приблизительно 1 × 105 клеток/кг, приблизительно 2 × 105 клеток/кг, приблизительно 3 × 105 клеток/кг, приблизительно 4 × 105 клеток/кг, приблизительно 5 × 105 клеток/кг, приблизительно 6 × 105 клеток/кг, приблизительно 7 × 105 клеток/кг, приблизительно 8 × 105 клеток/кг, приблизительно 9 × 105 клеток/кг, 2 × 106 клеток/кг, приблизительно 3 × 106 клеток/кг, приблизительно 4 × 106 клеток/кг, приблизительно 5 × 106 клеток/кг, приблизительно 6 × 106 клеток/кг, приблизительно 7 × 106 клеток/кг, приблизительно 8 × 106 клеток/кг, приблизительно 9 × 106 клеток/кг, приблизительно 1 × 107 клеток/кг, приблизительно 2 × 107 клеток/кг, приблизительно 3 × 107 клеток/кг, приблизительно 4 × 107 клеток/кг, приблизительно 5 × 107 клеток/кг, приблизительно 6 × 107 клеток/кг, приблизительно 7 × 107 клеток/кг, приблизительно 8 × 107 клеток/кг или приблизительно 9 × 107 клеток/кг.
[0220] В некоторых вариантах осуществления целевые дозы для CAR+/CAR-T+ клеток находятся в диапазоне от приблизительно 1 × 106 до приблизительно 1 × 1010 клеток/кг, например, приблизительно 1× 106 клеток/кг, приблизительно 1 × 107 клеток/кг, приблизительно 1 × 108 клеток/кг, приблизительно 1 × 109 клеток/кг или приблизительно 1 × 1010 клеток/кг. Следует принимать во внимание, что дозы выше и ниже этого диапазона могут быть подходящими для отдельных субъектов, и подходящие уровни доз могут быть определены лечащим врачом по мере необходимости. Кроме того, в соответствии с изобретением может быть предоставлено несколько доз клеток.
[0221] В некоторых аспектах изобретение включает фармацевтическую композицию, содержащую по меньшей мере один антигенсвязывающий домен, как описано в настоящем документе, и фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах осуществления фармацевтическая композиция дополнительно содержит дополнительный активный агент.
[0222] Популяции клеток, экспрессирующих CAR, согласно изобретению могут быть введены либо отдельно, либо в виде фармацевтической композиции в комбинации с разбавителями и/или с другими компонентами, такими как IL-2 или другие цитокины или популяции клеток. Фармацевтические композиции согласно настоящему изобретению могут содержать популяцию клеток, экспрессирующих CAR, таких как Т-клетки, как описано в настоящем документе, в комбинации с одним или более фармацевтически или физиологически приемлемыми носителями, разбавителями или вспомогательными веществами. Такие композиции могут содержать буферы, такие как нейтральный забуференный физиологический раствор, натрий-фосфатный буфер, и тому подобное; углеводы, такие как глюкоза, манноза, сахароза или декстраны, маннит; белки; полипептиды или аминокислоты, такие как глицин; антиоксиданты; хелатирующие агенты, такие как ЭДТА или глутатион; адъюванты (например, гидроксид алюминия); и консерванты. Композиции согласно настоящему изобретению предпочтительно составляют для внутривенного введения.
[0223] Фармацевтические композиции (растворы, суспензии и т.п.) могут включать один или более из следующего: стерильные разбавители, такие как вода для инъекций, раствор хлорида натрия, предпочтительно физиологический раствор, раствор Рингера, изотонический хлорид натрия, нелетучие масла, такие как синтетические моно- или диглицериды, которые могут служить в качестве растворителя или суспендирующей среды, полиэтиленгликоли, глицерин, пропиленгликоль или другие растворители; антибактериальные агенты, такие как бензиловый спирт или метилпарабен; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатирующие агенты, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и агенты для регулирования тоничности, такие как хлорид натрия или декстроза. Парентеральный препарат может быть заключен в ампулы, одноразовые шприцы или многодозовые флаконы, изготовленные из стекла или пластика. Для терапевтическах применений фармацевтическая композиция для инъекций предпочтительно является стерильной.
[0224] В некоторых вариантах осуществления при введении пациенту сконструированные иммунные клетки, экспрессирующие на своей клеточной поверхности любой из DLLS-специфичных CAR, описанных в настоящем документе, могут уменьшать количество, уничтожать или лизировать эндогенные DLL3-экспрессирующие клетки пациента. В одном из вариантов осуществления процент уменьшения количества или лизиса эндогенных DLL3-экспрессирующих клеток или клеток линии клеток, экспрессирующих DLL3, сконструированными иммунными клетками, экспрессирующими любой из DLL3-специфичных CAR, описанных в настоящем документе, составляет по меньшей мере приблизительно или более 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95%. В одном из вариантов осуществления процент уменьшения количества или лизиса эндогенных DLL3-экспрессирующих клеток или клеток линии клеток, экспрессирующих DLL3, сконструированными иммунными клетками, экспрессирующими любой из DLL3-специфичных CAR, описанных в настоящем документе, составляет от приблизительно 5% до приблизительно 95%, от приблизительно 10% до приблизительно 95%, от приблизительно 10% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 10% до приблизительно 60%, от приблизительно 10% до приблизительно 50%, от приблизительно 10% до приблизительно 40%, от приблизительно 20% до приблизительно 90%, от приблизительно 20% до приблизительно 80%, от приблизительно 20% до приблизительно 70%, от приблизительно 20% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 75% или от приблизительно 25% до приблизительно 60%. В одном из вариантов осуществления эндогенные DLL3-экспрессирующие клетки представляют собой эндогенные DLL3-экспрессирующие клетки костного мозга.
[0225] В одном из вариантов осуществления процент уменьшения количества или лизиса клеток-мишеней, например, линии клеток, экспрессирующих DLL3, сконструированными иммунными клетками, экспрессирующими на своей наружной клеточной мембране DLLS-специфичный CAR согласно изобретению, может быть измерен с использованием анализа, раскрытого в настоящем документе.
[0226] Способы могут дополнительно включать введение пациенту одного или более химиотерапевтических агентов перед введением сконструированных клеток, предложенных в настоящем документе. В некоторых вариантах осуществления химиотерапевтический агент представляет собой лимфодеплетирующий химиотерапевтический агент (для прекондиционирования). Например, способы кондиционирования пациента, нуждающегося в Т-клеточной терапии, включают введение указанному пациенту определенных полезных доз циклофосфамида (от 200 мг/м2/сут до 2000 мг/м2/сут, от приблизительно 100 мг/м2/сут до приблизительно 2000 мг/м2/сут; например, приблизительно 100 мг/м2/сут, приблизительно 200 мг/м2/сут, приблизительно 300 мг/м2/сут, приблизительно 400 мг/м2/сут, приблизительно 500 мг/м2/сут, приблизительно 600 мг/м2/сут, приблизительно 700 мг/м2/сут, приблизительно 800 мг/м2/сут, приблизительно 900 мг/м2/сут, приблизительно 1000 мг/м2/сут, приблизительно 1500 мг/м2/сут или приблизительно 2000 мг/м2/сут) и указанных доз флударабина (от 20 мг/м2/до 900 мг/м2/сут, от приблизительно 10 мг/м2/сут до приблизительно 900 мг/м2/сут; например, приблизительно 10 мг/м2/сут, приблизительно 20 мг/м2/сут, приблизительно 30 мг/м2/сут, приблизительно 40 мг/м2/сут, приблизительно 40 мг/м2/сут, приблизительно 50 мг/м2/сут, приблизительно 60 мг/м2/сут, приблизительно 70 мг/м2/сут, приблизительно 80 мг/м2/сут, приблизительно 90 мг/м2/сут, приблизительно 100 мг/м2/сут, приблизительно 500 мг/м2/сут или приблизительно 900 мг/м2/сут). Иллюстративный режим дозирования включает лечение пациента, включающее ежедневное введение указанному пациенту приблизительно 300 мг/м2/сут циклофосфамида в комбинации или до или после введения приблизительно 30 мг/м2/сут флударабина в течение трех суток до введения указанному пациенту терапевтически эффективного количества сконструированных Т-клеток.
[0227] В некоторых вариантах осуществления, особенно в случае, когда сконструированные клетки, предложенные в настоящем документе, были подвергнуты редактированию генов для устранения или минимизации поверхностной экспрессии CD52, лимфодеплеция дополнительно включает введение антитела против CD52, такого как алемтузумаб. В некоторых вариантах осуществления антитело против CD52 вводят в дозе приблизительно 1-20 мг/сут в/в, например, приблизительно 13 мг/сут в/в, в течение 1, 2, 3 или более суток. Антитело может быть введено в комбинации с, до или после введения других элементов режима лимфодеплеции (например, циклофосфамида и/или флударабина).
[0228] В других вариантах осуществления каждый из антигенсвязывающего домена, трансдуцированных (или иным образом генетически модифицированных) клеток и химиотерапевтического агента вводят в количестве, эффективном для лечения заболевания или состояния у субъекта.
[0229] В отдельных вариантах осуществления композиции, содержащие CAR-экспрессирующие иммунные эффекторные клетки, раскрытые в настоящем документе, могут быть введены в сочетании с любым количеством химиотерапевтических агентов. Примеры химиотерапевтических агентов включают алкилирующие агенты, такие как тиотепа и циклофосфамид (CYTOXAN™); алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метиламеламины, включая алтретамин, триэтиле имел амин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилоломеламин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, гидрохлорид оксида мехлорэтамина, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урациловый иприт; нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин, ранимустин; антибиотики, такие как аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, калихеамицин, карабицин, карминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин, эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицины, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин, 5-FU; андрогены, такие как калустерон, дромостанолона пропионат, эпитиостанол, мепитиостан, тестолактон; средства, угнетающие функции надпочечников, такие как аминоглутетимид, митотан, трилостан; восполнитель фолиевой кислоты, такой как фолиниевая кислота; ацеглатон; гликозид альдофосфамида; аминолевулиновая кислота; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; элформитин; эллиптиния ацетат; этоглюцид; нитрат галлия; гидроксимочевину; лентинан; лонидамин; митогуазон; митоксантрон; мопидамол; нитракрин; пентостатин; фенамет; пирарубицин; подофиллиновую кислоту; 2-этилгидразид; прокарбазин; PSK®; разоксан; сизофиран; спирогерманий; тенуазоновую кислоту; триазиквон; 2,2',2''-трихлортриэтиламин; уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид («Ara-С»); циклофосфамид; тиотепу; таксоиды, например, паклитаксел (TAXOL™, Bristol-Myers Squibb) и доксетаксел (TAXOTERE®, Rhone-Poulenc Rorer); хлорамбуцил; гемцитабин; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин и карбоплатин; винбластин; платина; этопозид (VP-16); ифосфамид; митомицин С; митоксантрон; винкристин; винорелбин; навельбин; новантрон; тенипозид; дауномицин; аминоптерин; кселода; ибандронат; СРТ-11; ингибитор топоизомеразы RF S2000; дифторметилорнитин (DMFO); производные ретиноевой кислоты, такие как Targretin™ (бексаротен), Panretin™ (алитретиноин); ONTAK™ (денилейкин-дифтитокс); эсперамицины; капецитабин; и фармацевтически приемлемые соли, кислоты или производные любого из вышеперечисленных. В это определение также включены антигормональные агенты, которые регулируют или ингибируют действие гормонов на опухоли, такие как антиэстрогены, включая, например, тамоксифен, ралоксифен, 4(5)-имидазолы, ингибирующие ароматазу, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и торемифен (Fareston); и антиандрогены, такие как флутамид, нилутамид, бикалутамид, лейпролид и гозерелин; и фармацевтически приемлемые соли, кислоты или производные любых из вышеперечисленных. При необходимости также вводят комбинации химиотерапевтических агентов, включая, не ограничиваясь перечисленным, CHOP, т.е. циклофосфамид (Cytoxan®), доксорубицин (гидроксидоксорубицин), винкристин (Oncovin®) и преднизон.
[0230] В некоторых вариантах осуществления химиотерапевтический агент вводят в то же время или в течение одной недели после введения сконструированной клетки, полипептида или нуклеиновой кислоты. В других вариантах осуществления химиотерапевтический агент вводят в течение приблизительно 1-7 дней, от приблизительно 1 до приблизительно 4 недель или от приблизительно 1 недели до приблизительно 1 месяца, от приблизительно 1 недели до приблизительно 2 месяцев, от приблизительно 1 недели до приблизительно 3 месяцев, от приблизительно 1 недели до приблизительно 6 месяцев, от приблизительно 1 недели до приблизительно 9 месяцев или от приблизительно 1 недели до приблизительно 12 месяцев после введения сконструированной клетки, полипептида или нуклеиновой кислоты. В других вариантах осуществления химиотерапевтический агент вводят по меньшей мере за 1 месяц до введения клетки, полипептида или нуклеиновой кислоты. В некоторых вариантах осуществления способы дополнительно включают введение двух или более химиотерапевтических агентов.
[0231] В сочетании с композициями, описанными в настоящем документе, можно применять множество дополнительных терапевтических агентов. Например, потенциально полезные дополнительные терапевтические агенты включают ингибиторы PD-1, такие как ниволумаб (Opdivo®), пембролизумаб (Keytruda®), пембролизумаб, пидилизумаб и атезолизумаб.
[0232] Дополнительные терапевтические агенты, подходящие для применения в комбинации с изобретением, включают, не ограничиваясь перечисленным, ибрутиниб (Imbruvica®), офатумумаб (Arzerra®), ритуксимаб (Rituxan®), бевацизумаб (Avastin®), трастузумаб (Herceptin®), трастузумаб эмтанзин (KADCYLA®), иматиниб (Gleevec®), цетуксимаб (Erbitux®), панитумумаб (Vectibix®), катумаксомаб, ибритумомаб, офатумумаб, тозитумомаб, брентуксимаб, алемтузумаб, гемтузумаб, эрлотиниб, гефитиниб, вандетаниб, афатиниб, лапатиниб, нератиниб, акситиниб, мазатиниб, пазопаниб, сунитиниб, сорафениб, тоцераниб, лестауртиниб, акситиниб, цедираниб, ленватиниб, нинтеданиб, пазопаниб, регорафениб, семаксаниб, сорафениб, сунитиниб, тивозаниб, тоцераниб, вандетаниб, энтректиниб, кабозантиниб, иматиниб, дазатиниб, нилотиниб, понатиниб, радотиниб, бозутиниб, лестауртиниб, руксолитиниб, пакритиниб, кобиметиниб, селуметиниб, траметиниб, биниметиниб, алектиниб, церитиниб, кризотиниб, афлиберцепт, адипотид, денилейкин дифтитокс, ингибиторы mTOR, такие как эверолимус и темсиролимус, ингибиторы hedgehog, такие как сонидегиб и висмодегиб, ингибиторы CDK, такие как ингибитор CDK (палбоциклиб).
[0233] В некоторых вариантах осуществления композиция, содержащая CAR-содержащие иммунные клетки, может быть введена с терапевтическим режимом для предупреждения или снижения синдрома высвобождения цитокинов (CRS) или нейротоксичности. Терапевтический режим для предупреждения синдрома высвобождения цитокинов (CRS) или нейротоксичности может включать лензилумаб, тоцилизумаб, предсердный натрийуретический пептид (ПНП), анакинру, ингибиторы iNOS (например, L-NIL или 1400W). В дополнительных вариантах осуществления композиция, содержащая CAR-содержащие иммунные клетки, может быть введена с противовоспалительным агентом. Противовоспалительные агенты или лекарственные средства включают, не ограничиваясь перечисленным, стероиды и глюкокортикоиды (включая бетаметазон, будесонид, дексаметазон, ацетат гидрокортизона, гидрокортизон, гидрокортизон, метилпреднизолон, преднизолон, преднизон, триамцинолон), нестероидные противовоспалительные препараты (НПВП), включая аспирин, ибупрофен, напроксен, метотрексат, сульфасалазин, лефлуномид, препараты против TNF, циклофосфамид и микофенолят. Примеры НПВП включают ибупрофен, напроксен, напроксен натрия, ингибиторы Сох-2 и сиалилаты. Примеры анальгетиков включают ацетаминофен, оксикодон, трамадол или гидрохлорид пропоксифена. Примеры глюкокортикоидов включают кортизон, дексаметазон, гидрокортизон, метилпреднизолон, преднизолон или преднизон. Примеры модификаторов биологического ответа включают молекулы, направленные против маркеров клеточной поверхности (например, CD4, CD5 и т.д.), ингибиторы цитокинов, такие как антагонисты TNF (например, этанерцепт (ENBREL®), адалимумаб (HUMIRA®) и инфликсимаб (REMICADE®, ингибиторы хемокинов и ингибиторы молекул адгезии. Модификаторы биологического ответа включают моноклональные антитела, а также рекомбинантные формы молекул. Примеры DMARD включают азатиоприн, циклофосфамид, циклоспорин, метотрексат, пеницилламин, лефлуномид, сульфасалазин, гидроксихлорохин, золото (перорально (ауранофин) и внутримышечно) и миноциклин.
[0234] В некоторых вариантах осуществления описанные в настоящем документе композиции вводят вместе с цитокином. Примерами цитокинов являются лимфокины, монокины и традиционные полипептидные гормоны. В число цитокинов входят гормоны роста, такие как гормон роста человека, N-метионил гормон роста человека и гормон роста крупного рогатого скота; паратиреоидный гормон; тироксин; инсулин; проинсулин; релаксин; прорелаксин; гликопротеиновые гормоны, такие как фолликулостимулирующий гормон (ФСГ), тиреотропный гормон (ТТГ) и лютеинизирующий гормон (ЛГ); фактор роста гепатоцитов (HGF); фактор роста фибробластов (FGF); пролактин; плацентарный лактоген; мюллеров ингибирующий фактор; гонадотропин-ассоциированный пептид мыши; ингибин; активин; фактор роста эндотелия сосудов; интегрин; тромбопоэтин (ТПО); факторы роста нервов (NGF), такие как NGF-бета; фактор роста тромбоцитов; трансформирующие факторы роста (TGF), такие как TGF-альфа и TGF-бета; инсулиноподобный фактор роста-I и -II; эритропоэтин (ЭПО); остеоиндуктивные факторы; интерфероны, такие как интерферон-альфа, бета и гамма; колониестимулирующие факторы (КСФ), такие как макрофагальный КСФ (М-КСФ); гранулоцитарно-макрофагальный КСФ (ГМ-КСФ); и гранулоцитарный КСФ (Г-КСФ); интерлейкины (IL), такие как IL-1, IL-1-альфа, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12; IL-15, IL-21, фактор некроза опухоли, такой как TNF-альфа или TNF-бета; и другие полипептидные факторы, включая LIF и лиганд kit (KL). В контексте настоящего документа термин «цитокин» включает белки из природных источников или из культуры рекомбинантных клеток, а также биологически активные эквиваленты цитокинов с нативной последовательностью.
V. Способы сортировки и истощения
[0235] В некоторых вариантах осуществления предложены способы сортировки популяции иммунных клеток in vitro, где подмножество популяции иммунных клеток включает сконструированные иммунные клетки, экспрессирующие любой из DLL3-специфичных CAR, содержащих эпитопы, специфичные к моноклональным антителам (например, иллюстративные последовательности мимотопов). Указанный способ включает приведение популяции иммунных клеток в контакт с моноклональным антителом, специфичным к эпитопам, и отбор иммунных клеток, которые связываются с моноклональным антителом, с получением популяции клеток, обогащенных сконструированными иммунными клетками, экспрессирующими DLL3-специфичный CAR.
[0236] В некоторых вариантах осуществления указанное моноклональное антитело, специфичное к указанному эпитопу, необязательно конъюгировано с флуорофором. В этом варианте осуществления стадия отбора клеток, которые связываются с моноклональным антителом, может быть проведена с помощью сортировки клеток с активированной флуоресценцией (FACS).
[0237] В некоторых вариантах осуществления указанное моноклональное антитело, специфичное к указанному эпитопу, необязательно конъюгировано с магнитной частицей. В этом варианте осуществления стадия отбора клеток, которые связываются с моноклональным антителом, может быть проведена с помощью сортировки клеток с магнитной активацией (MACS).
[0238] В некоторых вариантах осуществления mAb, используемое в способе сортировки иммунных клеток, экспрессирующих CAR, выбрано из алемтузумаба, ибритумомаба тиуксетана, муромонаба-CD3, тозитумомаба, абциксимаба, базиликеимаба, брентуксимаба ведотина, цетуксимаба, инфликсимаба, ритуксимаба, бевацизумаба, цертолизумаба пэгол, даклизумаба, экулизумаба, эфализумаба, гемтузумаба, натализумаба, омализумаба, паливизумаба, ранибизумаба, тоцилизумаба, трастузумаба, ведолизумаба, адалимумаба, белимумаба, канакинумаба, деносумаба, голимумаба, ипилимумаба, офатумумаба, панитумумаба, QBEND-10 и/или устекинумаба. В некоторых вариантах осуществления указанное mAb представляет собой ритуксимаб. В еще одном варианте осуществления указанное mAb представляет собой QBEND-10.
[0239] В некоторых вариантах осуществления популяция CAR-экспрессирующих иммунных клеток, полученная при использовании описанного выше способа сортировки CAR-экспрессирующих иммунных клеток in vitro, содержит по меньшей мере 70%, 75%, 80%, 85%, 90%, 95 CAR-экспрессирующих иммунных клеток. В некоторых вариантах осуществления популяция CAR-экспрессирующих иммунных клеток, полученная при использовании способа сортировки CAR-экспрессирующих иммунных клеток in vitro, содержит по меньшей мере 85% CAR-экспрессирующих иммунных клеток.
[0240] В некоторых вариантах осуществления популяция CAR-экспрессирующих иммунных клеток, полученная при использовании способа сортировки CAR-экспрессирующих иммунных клеток in vitro, демонстрирует повышенную цитотоксическую активность in vitro по сравнению с исходной (несортированной) популяцией клеток. В некоторых вариантах осуществления указанная цитотоксическая активность in vitro увеличена на 10%, 20%, 30% или 50%. В некоторых вариантах осуществления иммунные клетки представляют собой Т-клетки.
[0241] В некоторых вариантах осуществления mAb предварительно связывают с подложкой или поверхностью. Неограничивающие примеры твердой подложки могут включать шарик, агарозный шарик, пластмассовый шарик, магнитный шарик, планшет с пластиковыми лунками, планшет со стеклянными лунками, планшет с керамическими лунками, колонку или мешок для культивирования клеток.
[0242] CAR-экспрессирующие иммунные клетки, вводимые реципиенту, могут быть обогащены in vitro из исходной популяции. Способы размножения исходных популяций могут включать отбор клеток, экспрессирующих антиген, такой как антиген CD34, с использованием комбинаций центрифугирования в градиенте плотности, очистки иммуномагнитными шариками, аффинной хроматографии и сортировки клеток с активированной флуоресценцией.
[0243] Проточная цитометрия может использоваться для количественной оценки определенных типов клеток в популяции клеток. В целом проточная цитометрия это метод количественной оценки компонентов или структурных особенностей клеток, в первую очередь с помощью оптических средств. Поскольку различные типы клеток можно различить путем количественной оценки структурных особенностей, проточная цитометрия и сортировка клеток могут использоваться для подсчета и сортировки клеток разных фенотипов в смеси.
[0244] Анализ методом проточной цитометрии включает два основных этапа: 1) мечение выбранных типов клеток одним или более маркерами для мечения и 2) определение количества меченых клеток по отношению к общему количеству клеток в популяции. В некоторых вариантах осуществления способ мечения типов клеток включает связывание меченых антител с маркерами, экспрессируемыми конкретным типом клеток. Антитела могут быть либо непосредственно мечены флуоресцентным соединением, либо опосредованно мечены с использованием, например, второго антитела с флуоресцентной меткой, которое распознает первое антитело.
[0245] В некоторых вариантах осуществления способ, используемый для сортировки Т-клеток, экспрессирующих CAR, представляет собой сортировку клеток с магнитной активацией (MACS). Сортировка клеток с магниной активацией (MACS) - это метод разделения различных популяций клеток в зависимости от их поверхностных антигенов (молекул CD) с использованием суперпарамагнитных наночастиц и колонок. MACS может применяться для получения чистой популяции клеток. Клетки в суспензии отдельных клеток могут быть магнитно мечены с помощью микрогранул. Образец наносят на колонку, состоящую из ферромагнитных сфер, покрытых не вредящим клеткам защитным покрытием, обеспечивающим быстрое и бережное разделение клеток. Немеченые клетки проходят, а клетки с магнитной меткой задерживаются внутри колонки. Проходящий поток может быть собран в виде немеченой клеточной фракции. После стадии промывки колонку удаляют из сепаратора, и клетки с магнитной меткой элюируются из колонки.
[0246] Подробный протокол очистки конкретной популяции клеток, такой как Т-клетки, можно найти в Basu S et al. (2010). (Basu S, Campbell HM, Dittel BN, Ray A. Purification of specific cell population by fluorescence activated cell sorting (FACS). J Vis Exp. (41): 1546).
[0247] В некоторых аспектах настоящее изобретение относится к способу истощения иммунных клеток, экспрессирующих CAR, специфичные к DLL3, путем истощения in vivo. Истощение in vivo может включать введение лечебного средства (например, молекулы, которая связывает эпитоп на CAR) в организм млекопитающего с целью остановить пролиферацию CAR-экспрессирующих иммунных клеток путем ингибирования или устранения.
[0248] Один из аспектов изобретения относится к способу истощения in vivo сконструированной иммунной клетки, экспрессирующей CAR против DLL3, содержащей mAb-специфичный эпитоп, включающему приведение указанной сконструированной иммунной клетки или указанной CAR-экспрессирующей иммунной клетки в контакт с по меньшей мере одним эпитоп-специфичным mAb. Еще один аспект изобретения относится к способу in vivo истощения CAR-экспрессирующей иммунной клетки, которая содержит химерный scFv (например, образованный путем вставки mAb-специфичного эпитопа), путем приведения указанной сконструированной иммунной клетки в контакт с эпитоп-специфичными антителами. В некоторых вариантах осуществления иммунные клетки представляют собой Т-клетки и/или антитела являются моноклональными.
[0249] Согласно одному из вариантов осуществления истощение in vivo иммунных сконструированных клеток проводят на сконструированных иммунных клетках, которые ранее были отсортированы с использованием способа in vitro согласно настоящему изобретению. В этом случае можно использовать те же вводимые с помощью инфузии mAb. В некоторых вариантах осуществления mAb-специфичный антиген представляет собой антиген CD20, а эпитоп-специфичное mAb представляет собой ритуксимаб. В некоторых вариантах осуществления изобретение относится к способу истощения in vivo сконструированной иммунной клетки, экспрессирующей CAR, содержащей mAb-специфичный эпитоп (CAR-экспрессирующей иммунной клетки), у пациента, включающему приведение указанной CAR-экспрессирующей иммунной клетки в контакт с по меньшей мере одним эпитоп-специфичным mAb.
[0250] В некоторых вариантах осуществления стадия приведения указанной сконструированной иммунной клетки или указанной CAR-экспрессирующей иммунной клетки в контакт с по меньшей мере одним эпитоп-специфичным mAb включает инфузию пациенту эпитоп-специфичного mAb (например, ритуксимаба). В некоторых вариантах осуществления количество эпитоп-специфичных mAb, вводимых пациенту, достаточно для устранения по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% CAR-экспрессирующих иммунных клеток в организме пациента.
[0251] В некоторых вариантах осуществления стадия приведения указанной сконструированной иммунной клетки или указанной CAR-экспрессирующей иммунной клетки в контакт с по меньшей мере одним эпитоп-специфичным mAb включает инфузию пациенту приблизительно 375 мг/м2 ритуксимаба один или несколько раз. В некоторых вариантах осуществления mAb (например, ритуксимаб) вводят один раз в неделю.
[0252] В некоторых вариантах осуществления, когда иммунные клетки, экспрессирующие CAR, содержащие mAb-специфичный эпитоп (CAR-экспрессирующие иммунные клетки), истощают в анализе комплементзависимой цитотоксичности (КЗЦ) с использованием эпитоп-специфичных mAb, количество жизнеспособных CAR-экспрессирующих иммунных клеток уменьшается. В некоторых вариантах осуществления количество жизнеспособных CAR-экспрессирующих иммунных клеток уменьшается по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90%. В некоторых вариантах осуществления указанный mAb-специфичный эпитоп представляет собой эпитоп или мимотоп CD20, и/или эпитоп-специфичное mAb представляет собой ритуксимаб.
[0253] В некоторых вариантах осуществления истощение in vivo модифицированных с помощью CAR иммунных клеток осуществляют путем инфузии биспецифичных антител. По определению, биспецифичное моноклональное антитело (BsAb) представляет собой искусственный белок, который состоит из фрагментов двух разных моноклональных антител и, следовательно, связывается с двумя разными типами антигена. Эти BsAb и их применение в иммунотерапии были рассмотрены в Muller D and Kontermann R.E. (2010) Bispecific Antibodies for Cancer Immunotherapy, BioDrugs 24 (2): 89-98.
[0254] Согласно еще одному частному варианту осуществления введенное с помощью инфузии биспецифичное mAb способно связывать как mAb-специфичный эпитоп, переносимый на сконструированных иммунных клетках, экспрессирующих химерный scFv, так и поверхностный антиген на эффекторной и цитотоксической клетке (например, иммунных клетках, таких как лимфоциты, макрофаги, дендритные клетки, естественные киллерные клетки (NK-клетки), цитотоксические Т-лимфоциты (CTL)). Таким образом, истощение сконструированных иммунных клеток, вызванное BsAb, может происходить из-за антителозависимой клеточной цитотоксичности (АЗКЦ). (Deo Y М, Sundarapandiyan K, Keler Т, Wallace PK, and Graziano RF, (2000), Journal of Immunology, 165 (10):5954-5961]).
[0255] В некоторых вариантах осуществления с эпитоп-специфичными mAb, которые можно использовать для истощения CAR-экспрессирующих иммунных клеток, связывают цитотоксическое лекарственное средство. Комбинируя способности нацеливания моноклональных антител со способностью цитотоксических лекарств уничтожать рак, конъюгат антитело-лекарственное средство (ADC) позволяет с высокой степенью чувствительности различать здоровую и больную ткань по сравнению с применением одного лекарственного средства. Получены одобрения для выпуска на рынок нескольких ADC; технология их получения, особенно на линкерах, описана в (Payne, G. (2003) Cancer Cell 3:207-212; Trail et al (2003) Cancer Immunol. Immunother. 52:328-337; Syrigos and Epenetos (1999) Anticancer Research 19:605-614; Niculescu-Duvaz and Springer (1997) Adv. Drug Del. Rev. 26:151-172; патент США №4,975,278).
[0256] В некоторых вариантах осуществления эпитоп-специфичное mAb, подлежащее инфузии, предварительно конъюгируют с молекулой, способной стимулировать комплементзависимую цитотоксичность (КЗЦ). Таким образом, система комплемента помогает или дополняет способность антител выводить патогены из организма. При стимуляции запускается каскад активации как массивное усиление ответа и активация комплекса, атакующего мембраны с уничтожением клеток. Для конъюгирования mAb можно использовать другую молекулу, такую как гликаны (Courtois, A, Gac-Breton, S., Berthou, С, Guezennec, J., Bordron, A. and Boisset, C. (2012), Complement dependent cytotoxicity activity of therapeutic antibody fragments may be acquired by immunogenic glycan coupling, Electronic Journal of Biotechnology ISSN: 0717-3458; http://www.ejbiotechnology.info DOI: 10.2225/voll5-issue5).
VI. Наборы и изделия
[0257] В настоящей заявке предложены наборы, содержащие любой из CAR, содержащих DLL3, или иммунных клеток, содержащих анти-DLL3 CAR, описанных в настоящем документе, и содержащие их фармацевтические композиции. В одном варианте осуществления набора сконструированные CAR-клетки замораживают в подходящей среде, такой как CryoStor® CS10, CryoStor® CS2 или CryoStor® CS5 (BioLife Solutions).
[0258] В некоторых иллюстративных вариантах осуществления набор согласно изобретению содержит аллогенные DLL3 CAR-содержащие Т-клетки и антитело к CD52 для введения субъекту режима лимфодеплеции и режима CAR-T.
[0259] В настоящей заявке также предложены изделия, содержащие любую из терапевтических композиций или наборов, описанных в настоящем документе. Примеры изделия включают флаконы (например, запечатанные флаконы).
ПРИМЕРЫ
Пример 1: Создание и тестирование антител, нацеленных на DLL3
[0260] Моноклональные антитела, используемые в соответствии с изобретением, могут быть получены гибридомным методом, впервые описанным Kohler and Milstein, Nature 256:495, 1975, или могут быть получены методами рекомбинантной ДНК, такими как описанные в патенте США №4,816,567. Антитела к DLL3 сначала подвергали скринингу в ELISA Flag-DLL3 (adipogen), а затем скринингу в FACS для определения связывания с клетками HEK-293Т, обладающими или не обладающими экспрессией DLL3 человека.
[0261] Чтобы проверить, могут ли DLL3-специфичные антитела распознавать клетки, экспрессирующие эндогенный DLL3, клетки DMS 273 (Sigma, кат. №95062830), DMS 454 (Sigma, кат. №95062832) и SHP-77 (АТСС, кат. № CRL-2195) окрашивали 2 мкг/мл очищенных антител к DLL3 с основной цепью мышиного IgG2A (mIgG2a) или контрольным антителом mIgG2a в PBS с добавлением 1% BSA. Связанные антитела к DLL3 определяли с помощью РЕ-меченого антитела против мышиного IgG (Biolegend, кат. №405307). Образцы анализировали методом проточной цитометрии. Репрезентативные изображения, демонстрирующие связывание антител к DLL3 с клетками DMS 273, DMS 454 и SHP-77, включены на ФИГ. 1.
Пример 2: Определение кинетики и аффинности антител к DLL3 по отношению к DLL3
[0262] В этом примере определяли кинетику связывания и аффинность различных антител к DLL3 при 37°С в виде как полноразмерных моноклональных антител (IgG), так и scFv, по отношению к DLL3 человека, яванского макака (cyno) и мыши. Для scFv вариабельные области антител к DLL3, полученных из их соответствующей гибридомы, клонировали, фланкируя линкер (GGGGS)3 (SEQ ID NO: 472) или (GGGGS)4 (SEQ ID NO: 478), за которым следовала часть шарнира и Fc из модифицированной последовательности человеческого IgG2, получая слияние scFv-Fc, которое экспрессировали с использованием Expi293. Внеклеточный домен (ECD) из DLL3 человека, яванского макака и мыши был слит с С-концевой эпитопной меткой 8×His (SEQ ID NO: 473) и меткой Avi, экспрессирован с использованием Expi293, затем очищен с помощью аффинной хроматографии на иммобилизованных ионах металла (IMAC) с последующей эксклюзионной хроматографией (SEC).
[0263] Кинетику связывания антител определяли с помощью поверхностного плазмонного резонанса (система поверхностного плазмонного резонанса (SPR) BiacoreTM, GE Healthcare Bio-Sciences, Питтсбург, Пенсильвания). Антитела, разведенные в подвижном буфере HBS-T+ (0,01 М HEPES рН 7,4, 0,15 М NaCl, 0,05% об./об. Tween20, 1 мг/мл BSA), были захвачены на чипе СМ4, иммобилизованном с помощью антитела, специфичного к константным доменам антитела к DLL3. Очищенный DLL3 последовательно разводили HBS-T+, вводили в течение 2 мин со скоростью 30 мкл/мин и временем диссоциации 10 мин, затем поверхность между введениями регенерировали либо 10 мМ глицин-HCl рН 1,7, либо фосфорной кислотой. Кинетические скорости ассоциации (kon) и скорости диссоциации (koff) получают одновременно путем аппроксимации данных в глобальном масштабе к модели связывания Ленгмюра 1:1 (Karlsson, R. Roos, Н. Fagerstam, L. Petersson, В. (1994). Methods Enzymology 6. 99-110) с помощью программы BIAevaluation. Значения равновесной константы диссоциации (Kd) рассчитывают как koff/kon.
[0264] Параметры кинетики и аффинности для протестированных антител к DLL3 приведены в таблице 8. В частности, в таблице 8 показана аффинность антител к DLL3 (в виде IgG или слияния scFv-Fc) к DLL3 человека, яванского макака и мыши. В последнем столбце показано, какой внеклеточный домен DLL3 человека распознает каждое из антител к DLL3.
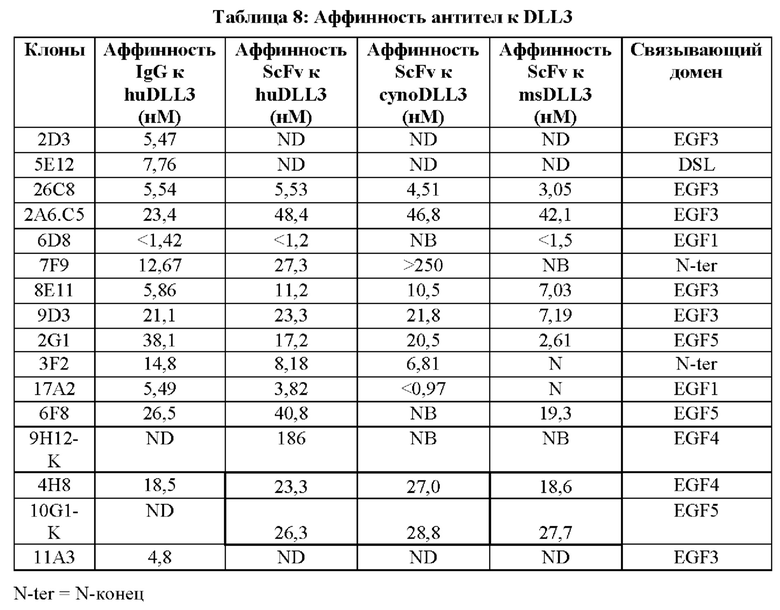
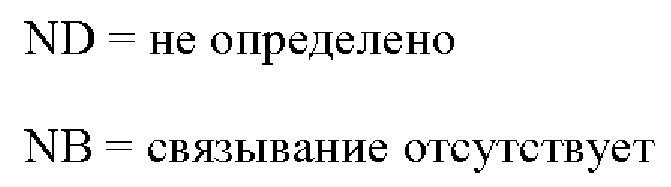
Пример 3: Создание клеток СНО, экспрессирующих полноразмерный и усеченный DLL3
[0265] Панель клеток СНО, экспрессирующих полноразмерный и различные усеченные DLL3 человека использовали для определения того, какой домен распознает каждое антитело, нацеленное на DLL3. Внеклеточный домен DLL3 человека можно подразделить на различные субдомены, которые определяются следующими аминокислотными положениями: сигнальный пептид: 1-26; N-конец (N-ter): 27-175; DSL: 176-215; EGF1: 215-249; EGF2: 274-310; EGF3: 312-351; EGF4: 353-389; EGF5: 391-427; и EGF6: 429-465.
[0266] Для создания усеченных белков DLL3, используемых для картирования эпитопов, последовательности соответствующих 8 внеклеточных доменов (сигнальный пептид плюс N-конец, DSL, EGF1, EGF2, EGF3, EGF4, EGF5 и EGF6) DLL3 человека были последовательно удалены из антигена, начиная с N-конца. В таблице 6 приведены усеченные белки DLL3, которые были созданы (также см. ФИГ. 2A-2D).

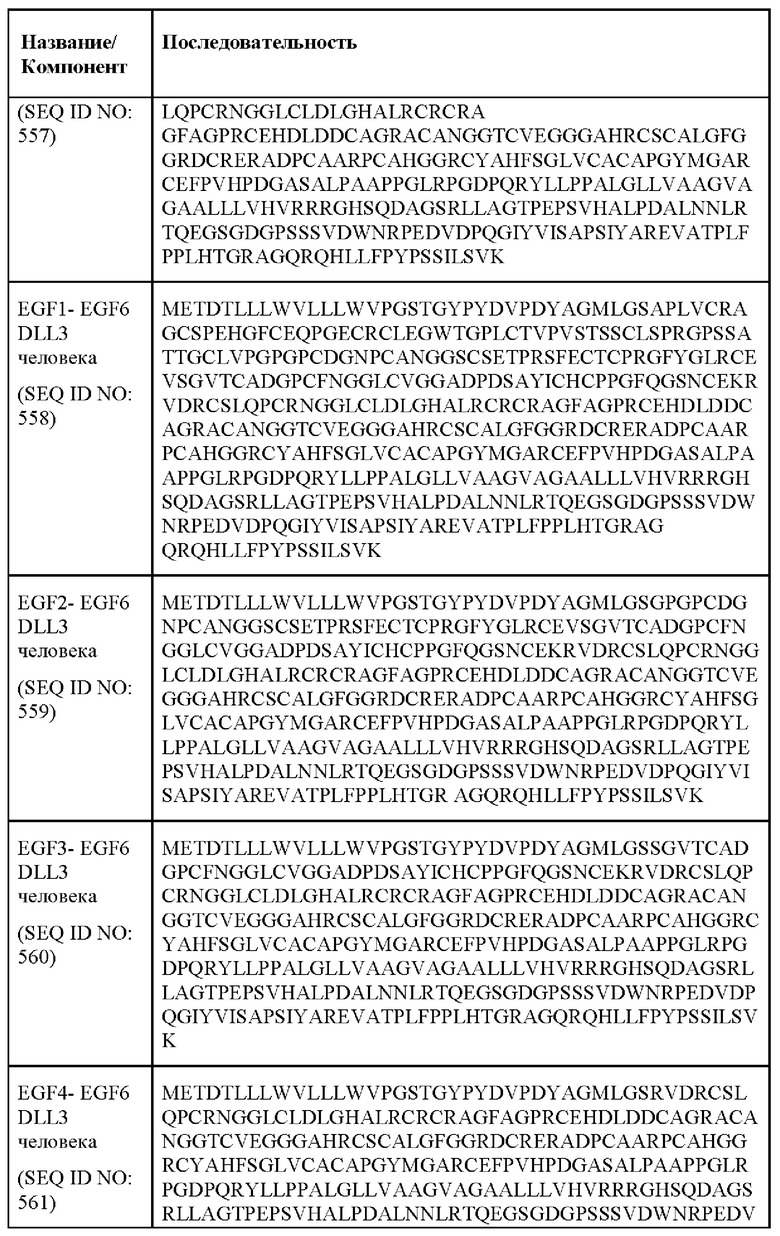

[0267] Для получения клеток СНО, экспрессирующих полноразмерный и усеченный DLL3 человека с N-концевой НА-меткой, кодирующие последовательности для полноразмерного DLL3 человека (SEQ ID NO: 556; запись в GeneBank NM_016941) и 7 усеченных НА-меченых DLL3 человека (SEQ ID NO: 557-563) клонировали в вектор pLVX-SFFV-Puro-P2A-TetO3G (Clontech). Лентивирус, кодирующий либо полноразмерные, либо усеченные DLL3 человека, получали путем котрансфекции клеток 293Т векторами pLVX-SFFV-Puro-P2A-TetO3G с векторами psPAX2 и pMD2G. Через два дня после трансфекции супернатант, содержащий вирусные частицы, собирали и использовали для трансдукции клеток СНО вместе с 5 мкг/мл полибрена.
[0268] Экспрессию полноразмерного и усеченного DLL3 проверяли с помощью FACS-анализа с использованием конъюгированного с РЕ антитела к НА (Biolegend, кат. №901518). В качестве отрицательного контроля клетки инкубировали с изотипически сходным и РЕ-меченым антителом (Biolegend, кат. №400111) вместо антитела к НА. На нижней панели ФИГ. 2А показана экспрессия полноразмерного и усеченного DLL3 на клетках СНО.
Пример 4: Картирование эпитопа антител, нацеленных на DLL3
[0269] Клетки СНО, экспрессирующие полноразмерный и усеченный DLL3, окрашивали супернатантом гибридомы или очищенными антителами к DLL3 в PBS+1% BSA. Связанные антитела к DLL3 определяли с помощью РЕ-меченого антитела против мышиного IgG (Biolegend, кат. №405307). Образцы анализировали методом проточной цитометрии. Связывающий домен для каждого клона определяли с использованием панели СНО, экспрессирующих полноразмерный или усеченный DLL3, описанной в примере 2. Анализ методом проточной цитометрии показал, что, например, если клон связывается со всеми усеченными белками, включая EGF3, но не с каким-либо усеченным белком без EGF3, то такой клон распознает EGF3. Как показано на репрезентативных изображениях на ФИГ. 2D, антитела к DLL3 распознают домены DSL, EGF1 и EGF3, соответственно. Сигналы из канала РЕ показаны по оси х, а счет клеток показан по оси у.
Пример 5: Получение DLL3-специфичных CAR-T-клеток
[0270] В этом примере описано конструирование химерных антигенных рецепторов (CAR) против DLL3.
[0271] Антитела к DLL3, перечисленные в таблице 1а, были переформатированы в CAR. Аминокислотные последовательности вариабельных областей тяжелой цепи и вариабельных областей легкой цепи этих антител (таблица 1b и таблица 1с) были использованы для конструирования одно цепочечных вариабельных фрагментов (scFv) (таблица 1d), имеющих следующую общую структуру: вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи. Линкер имел следующие аминокислотные последовательности:  (SEQ ID NO: 478).
(SEQ ID NO: 478).
[0272] Последовательности белков, кодирующие химерный антигенный рецептор, были сконструированы так, чтобы они содержали следующие элементы, в направлении от 5' к 3' (ФИГ. 3А, таблица 7): сигнальная последовательность CD8α (SEQ ID NO: 477), scFv против DLL3, шарнирная и трансмембранная области молекулы CD8α человека (SEQ ID NO: 479), цитоплазматическая часть молекулы 41ВВ (SEQ ID NO: 291) и цитоплазматическая часть молекулы CD3ζ (SEQ ID NO: 292).

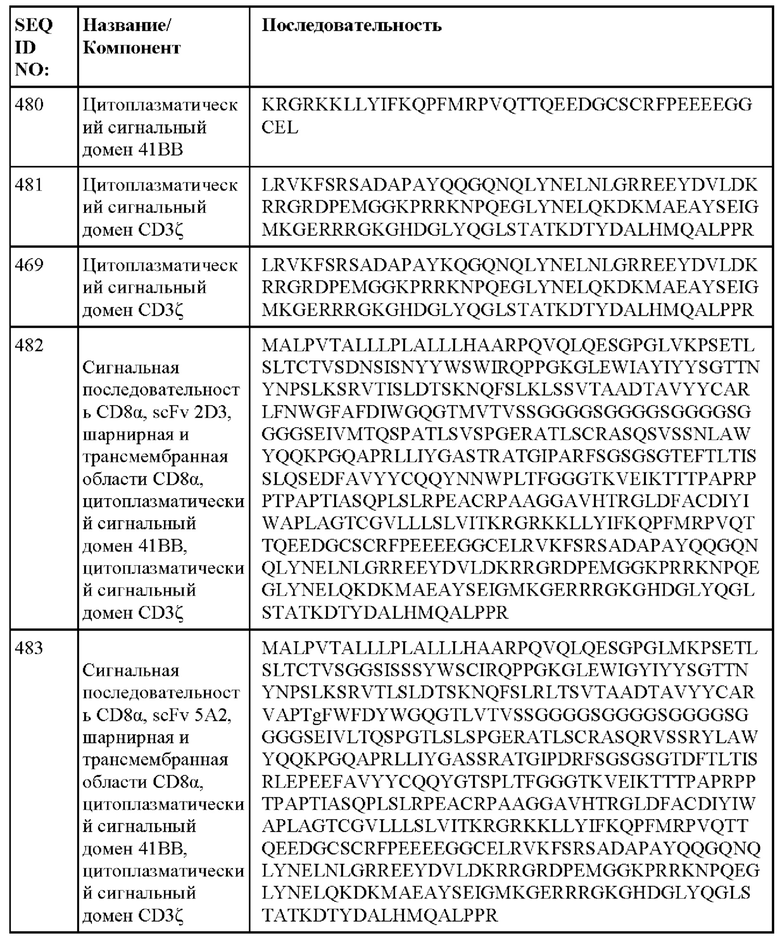
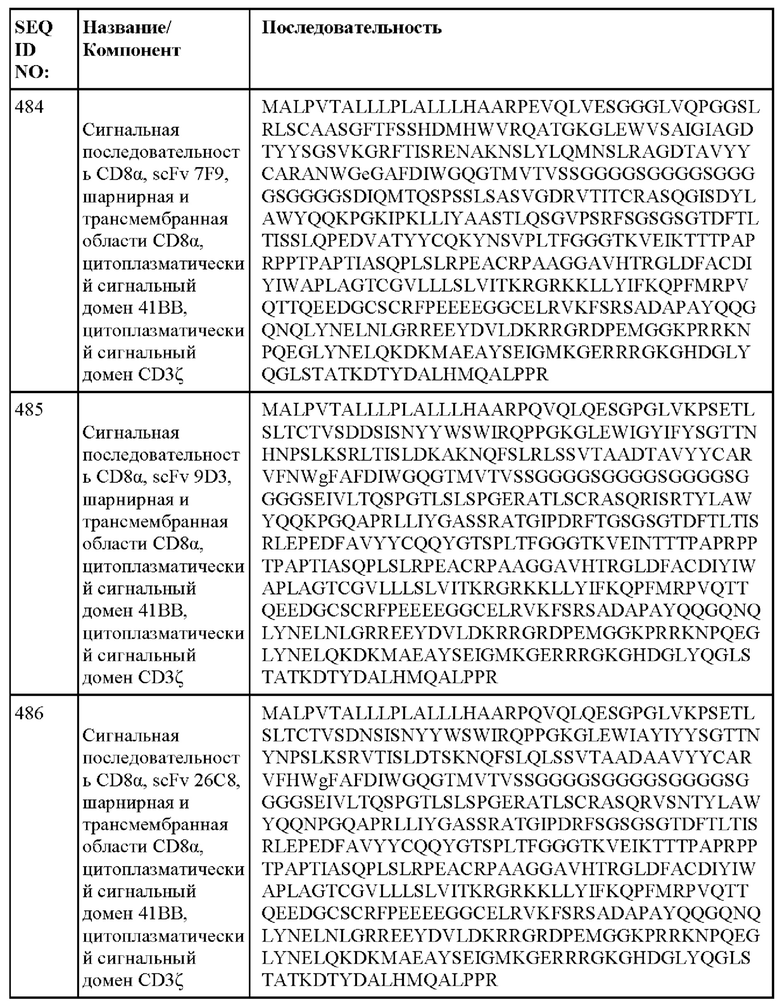
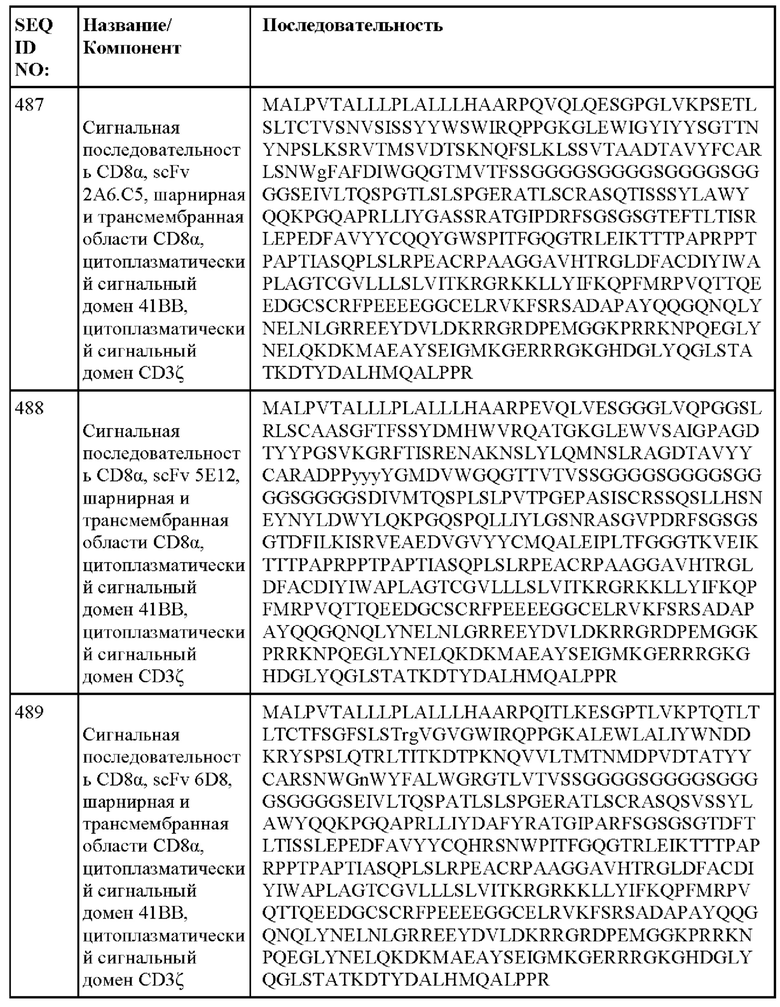
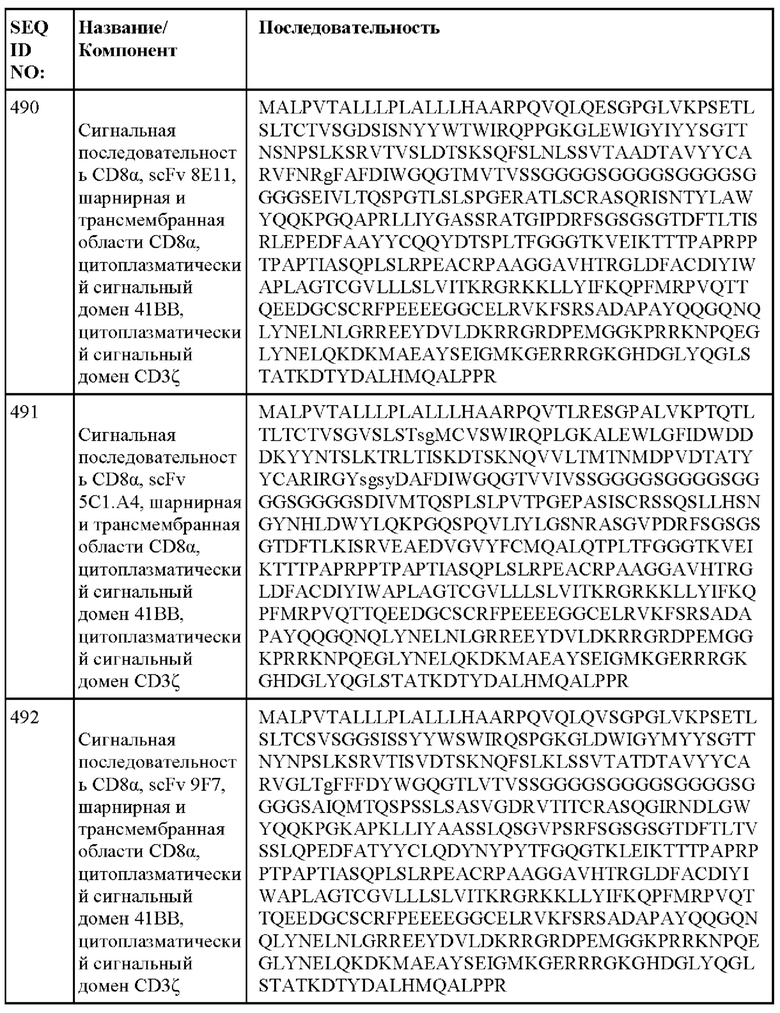
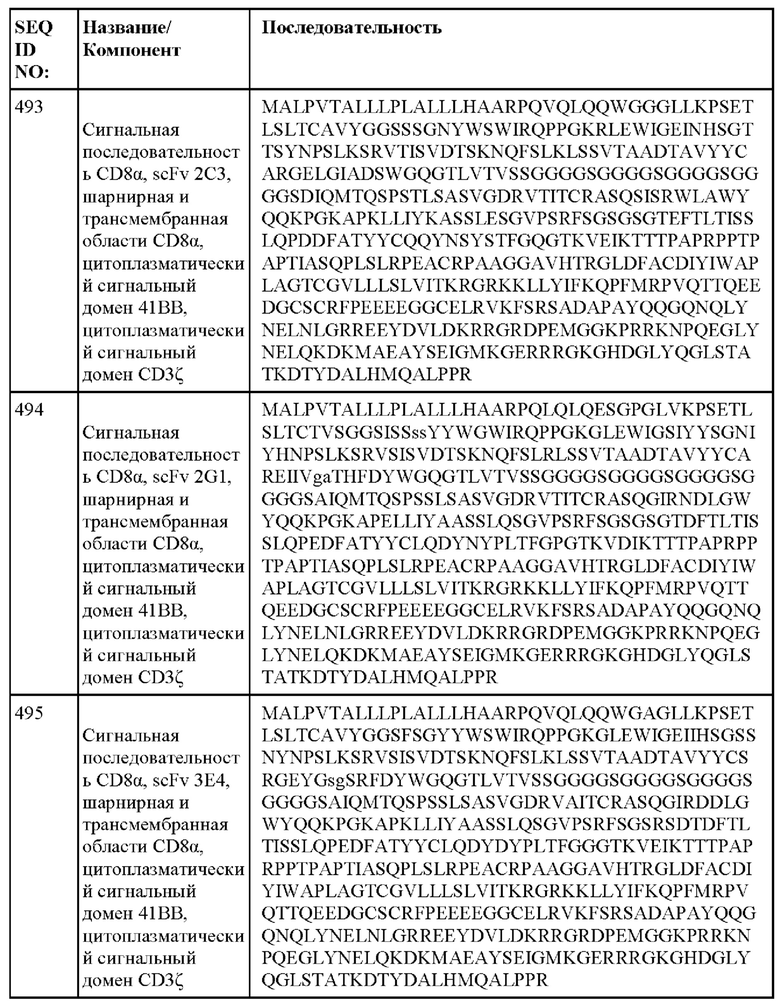
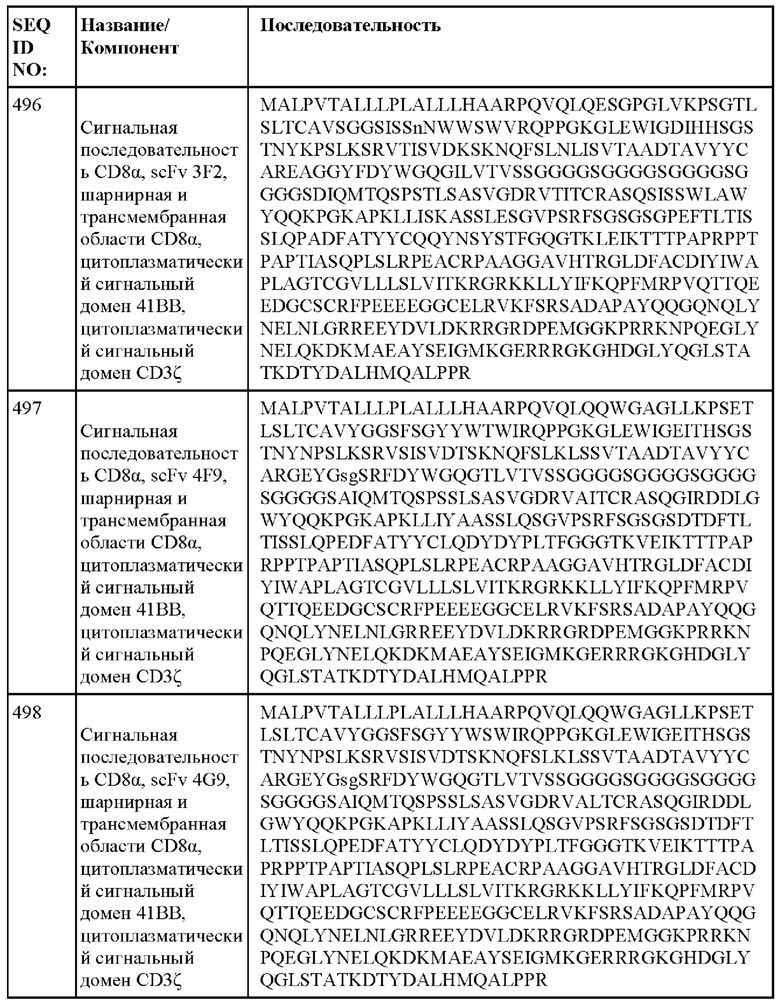
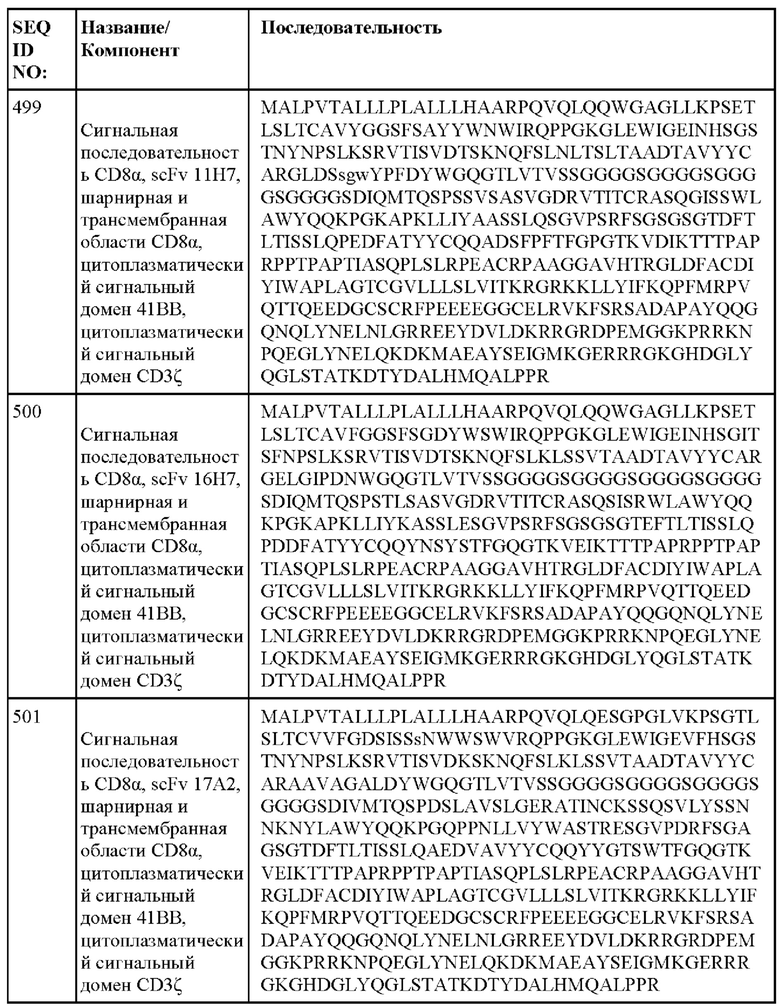
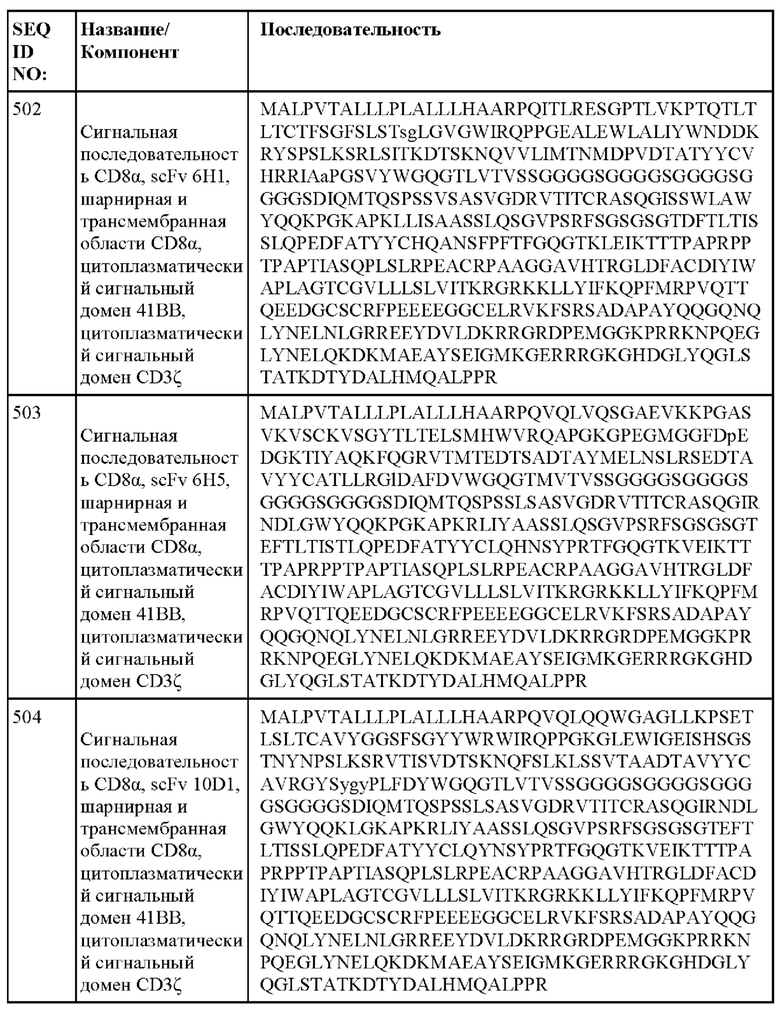
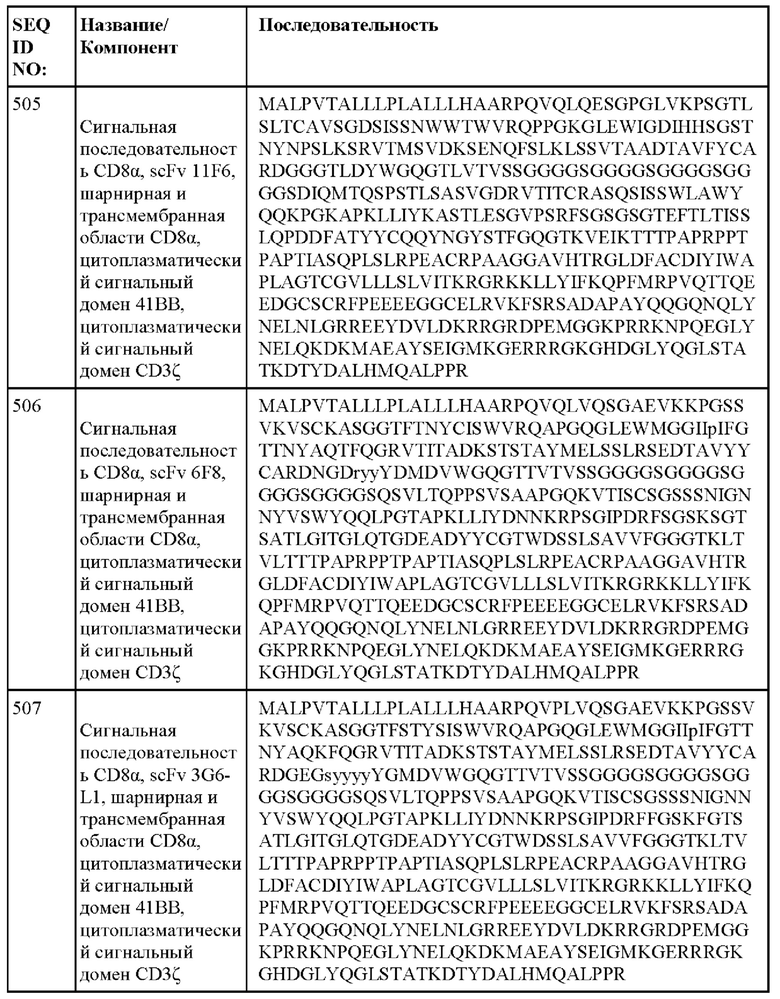
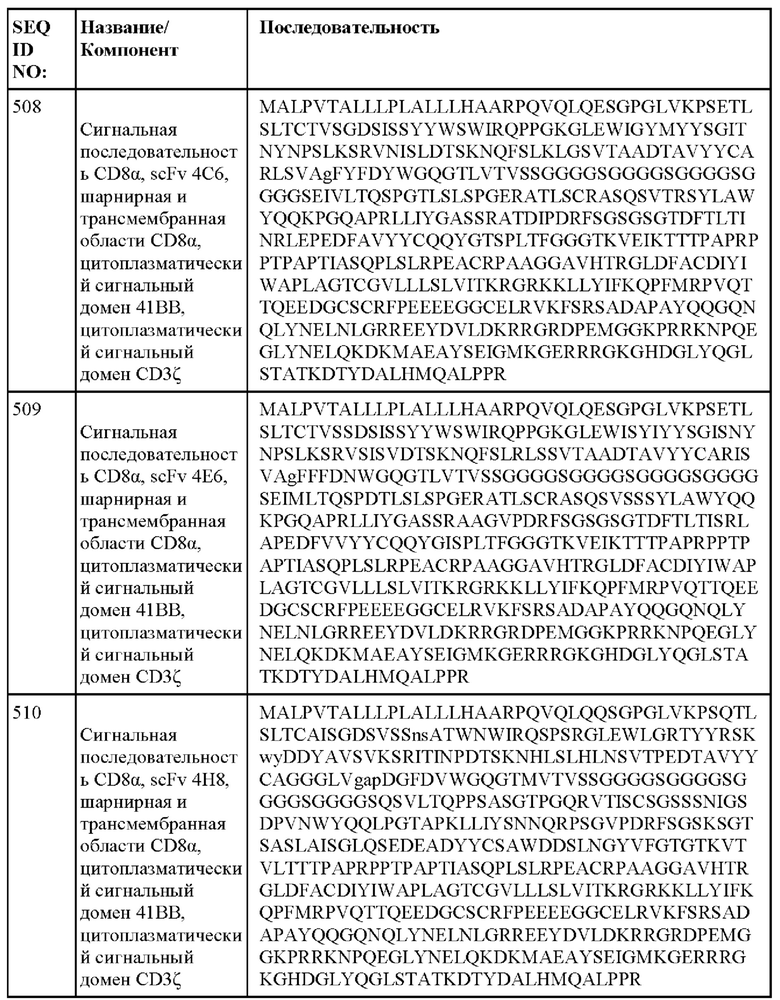
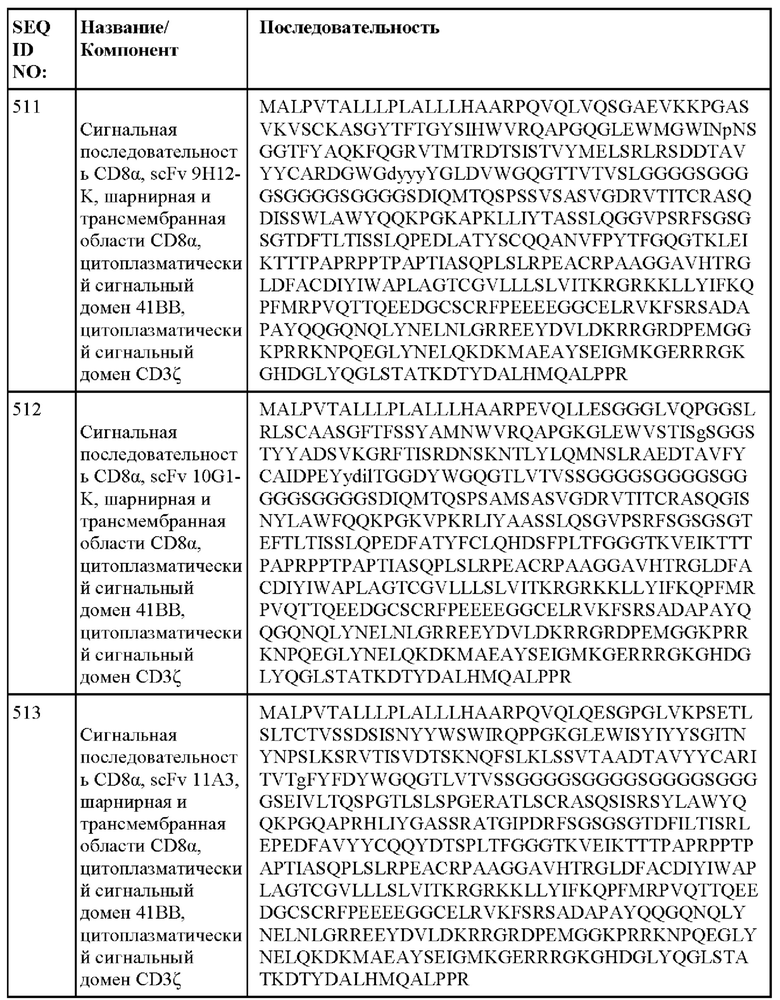
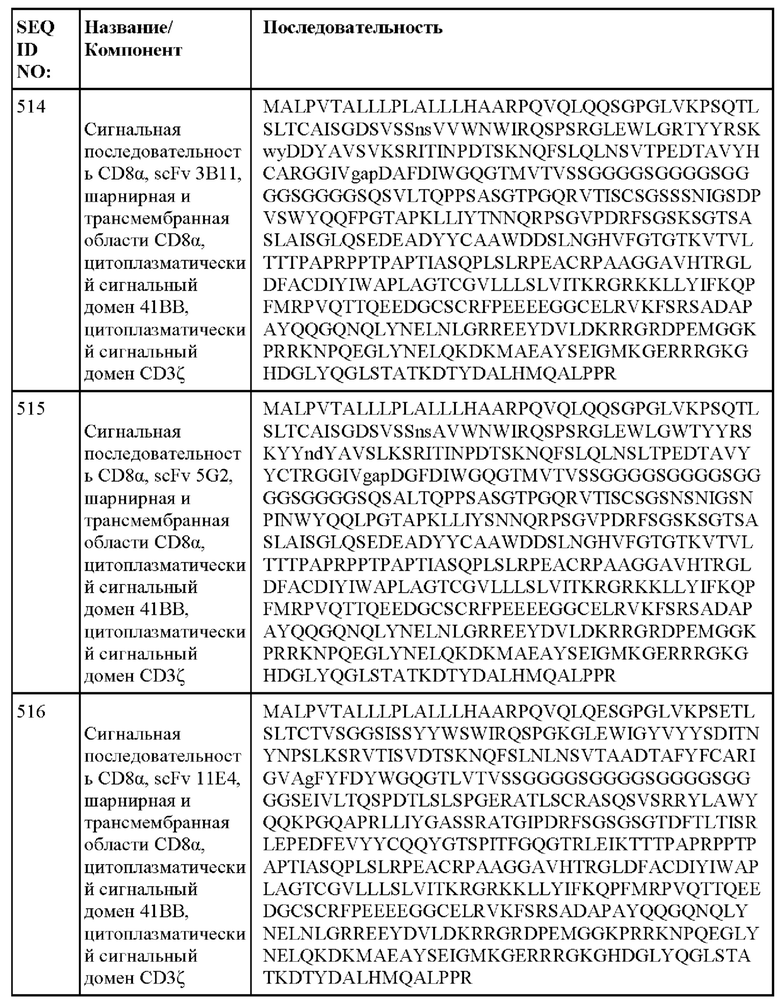
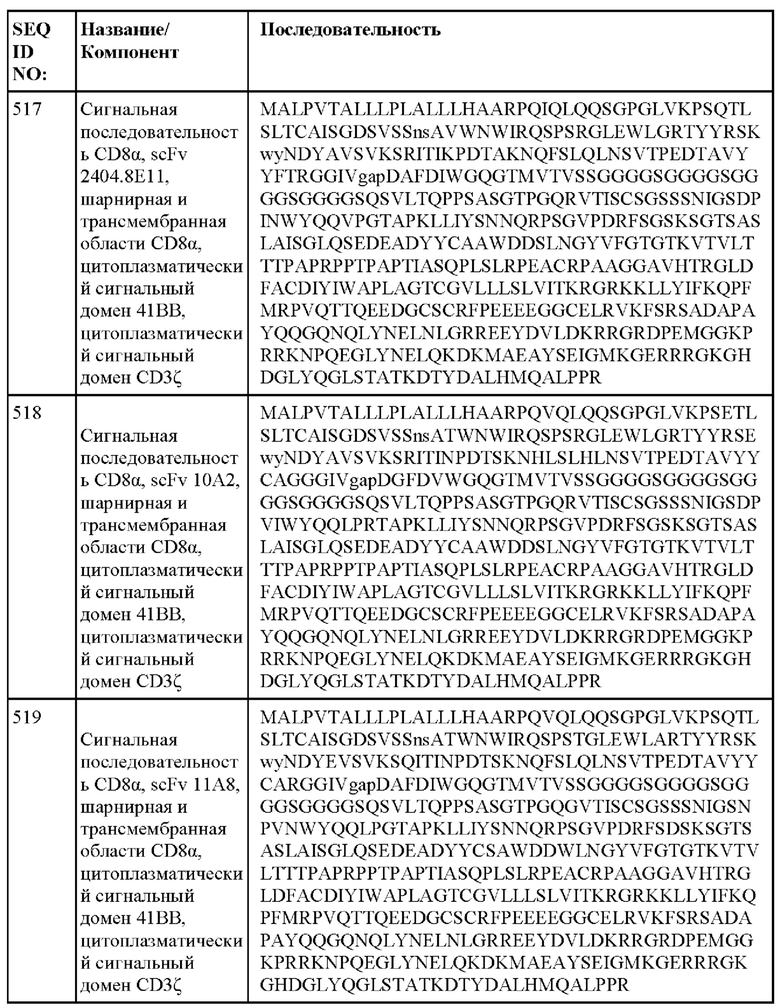
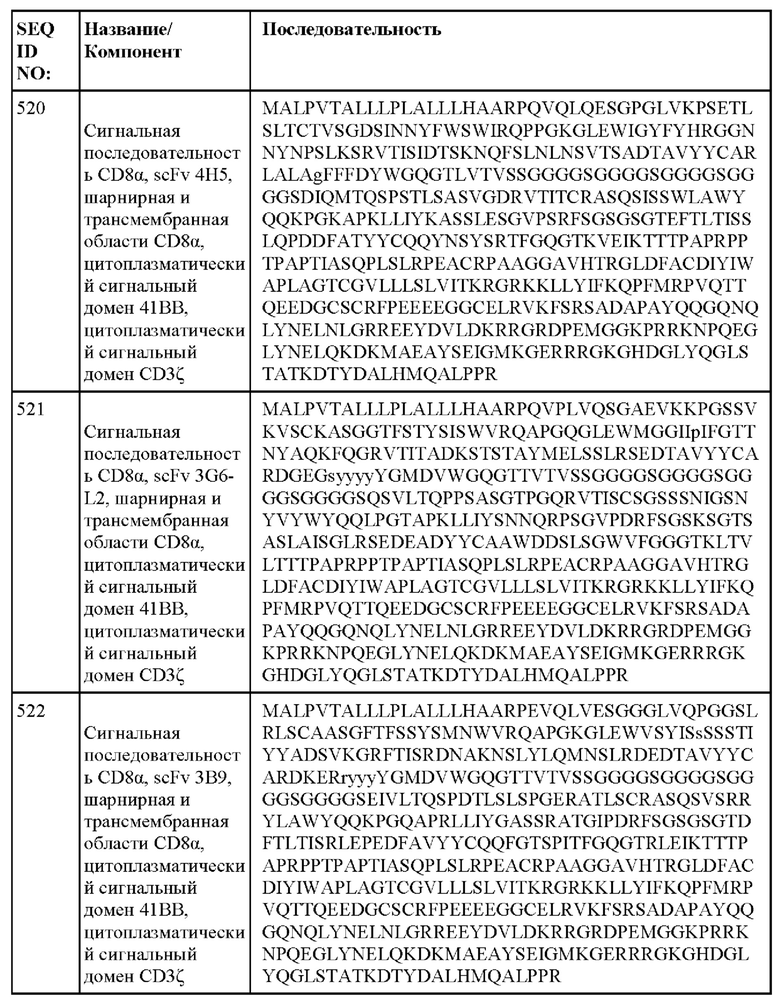
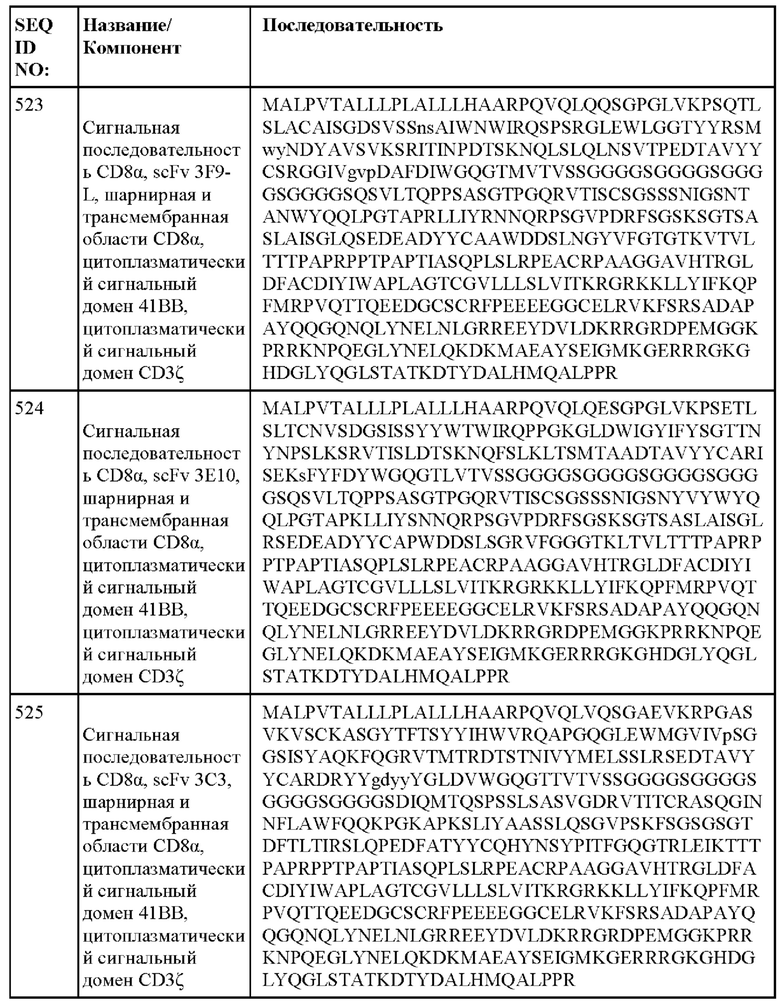
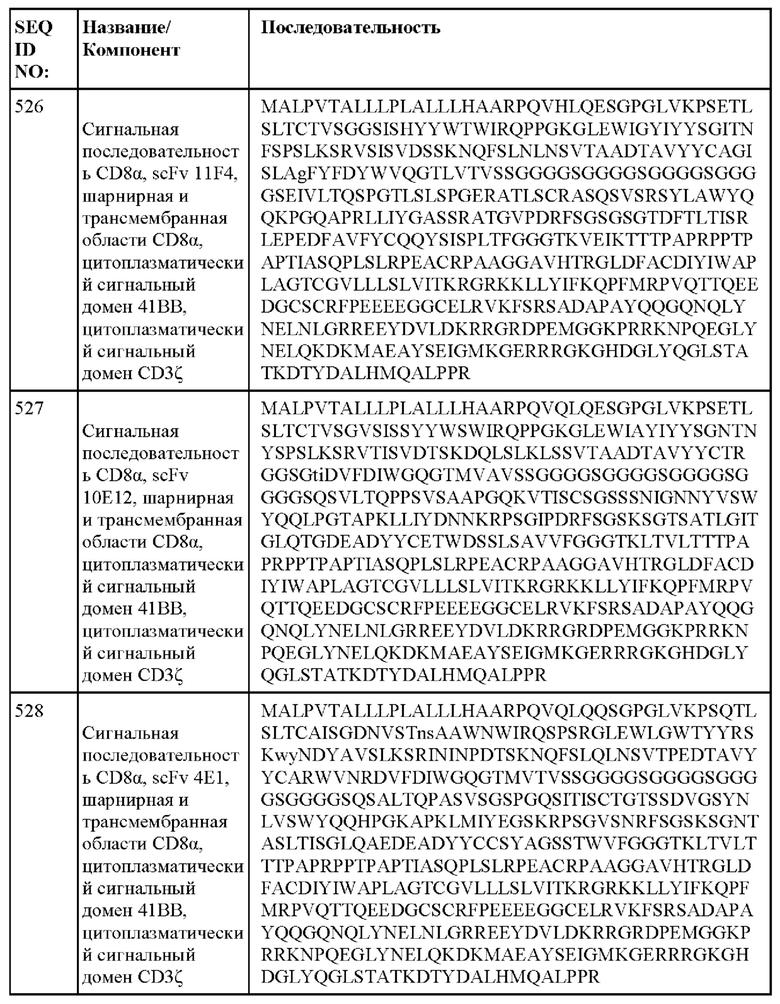
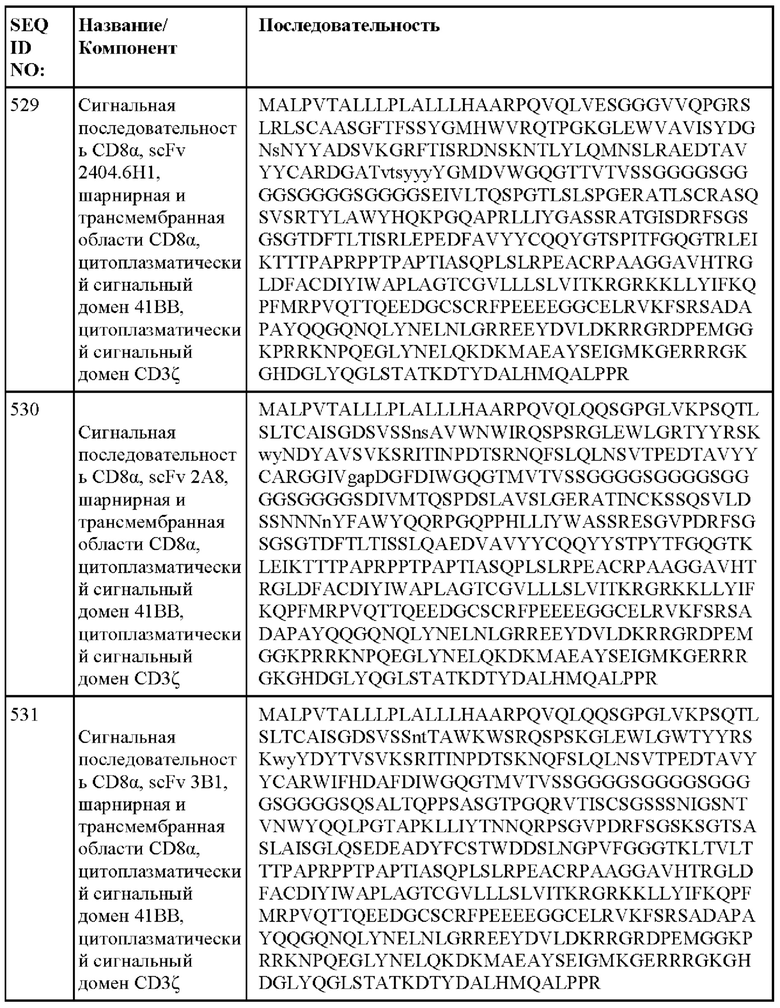
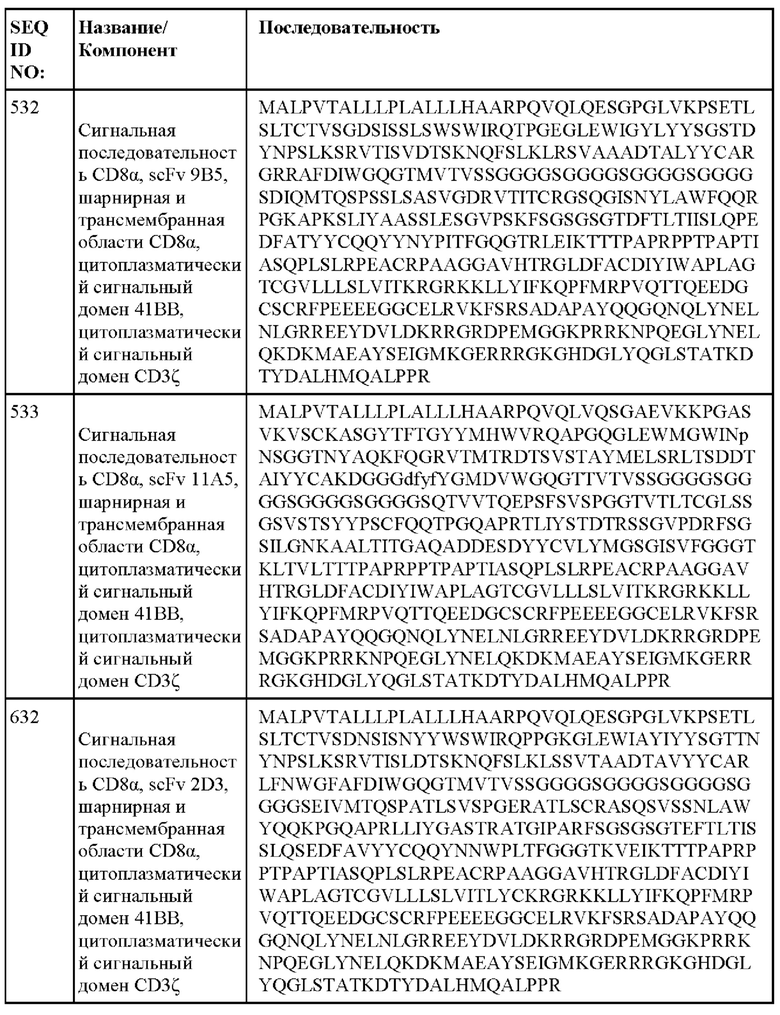
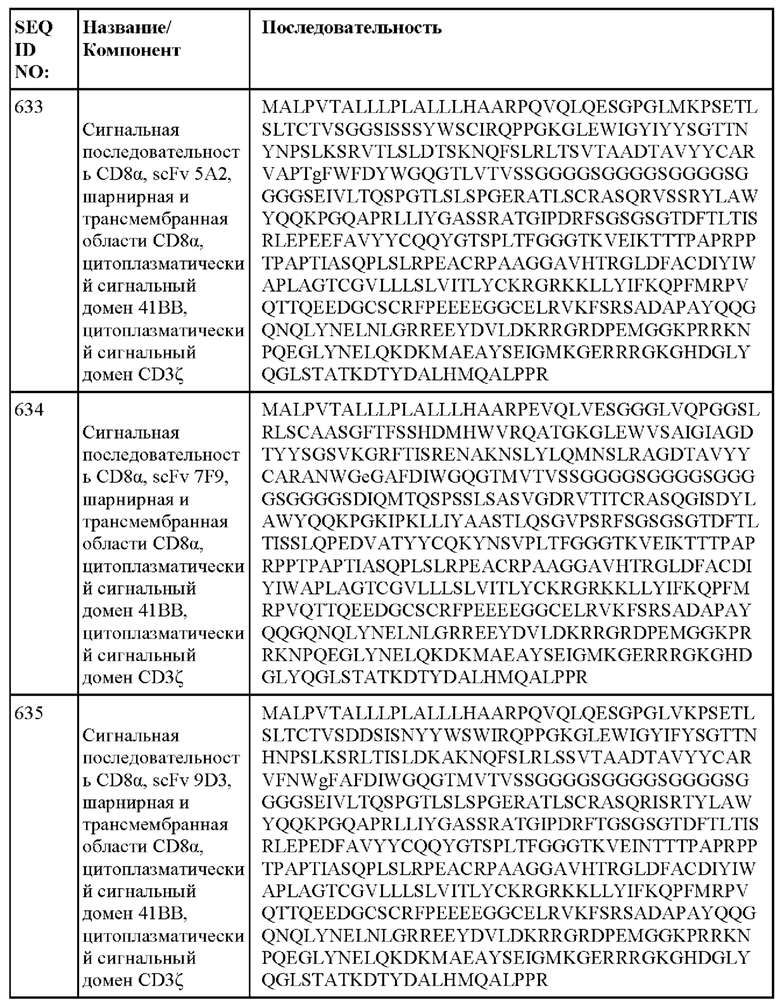
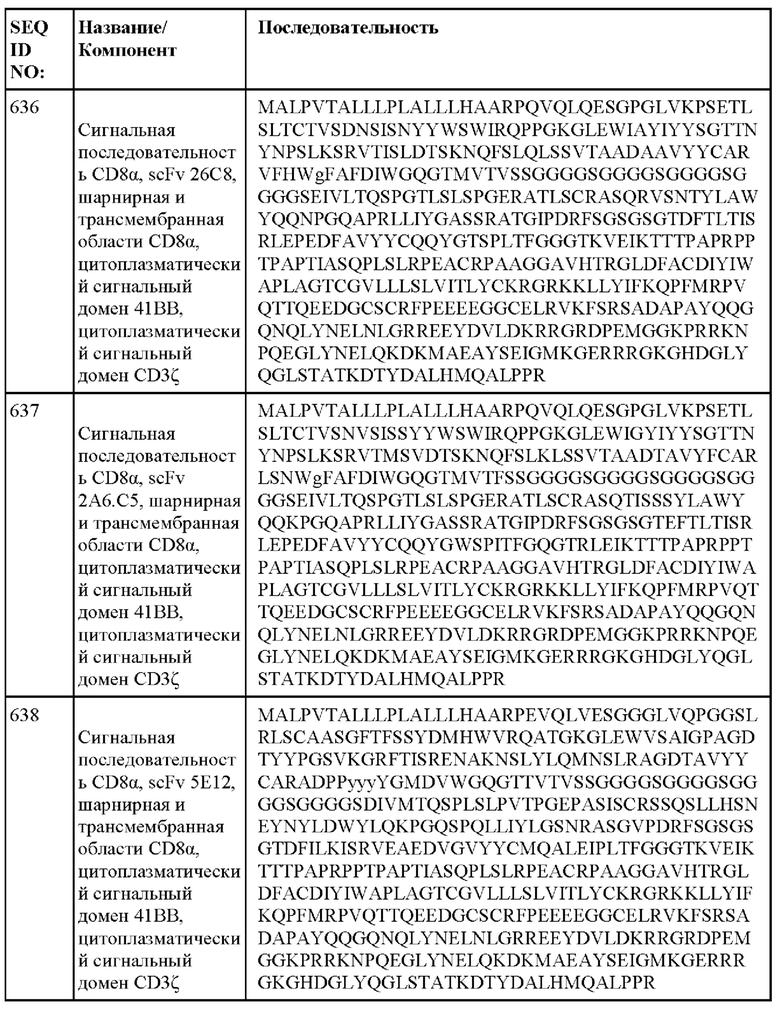
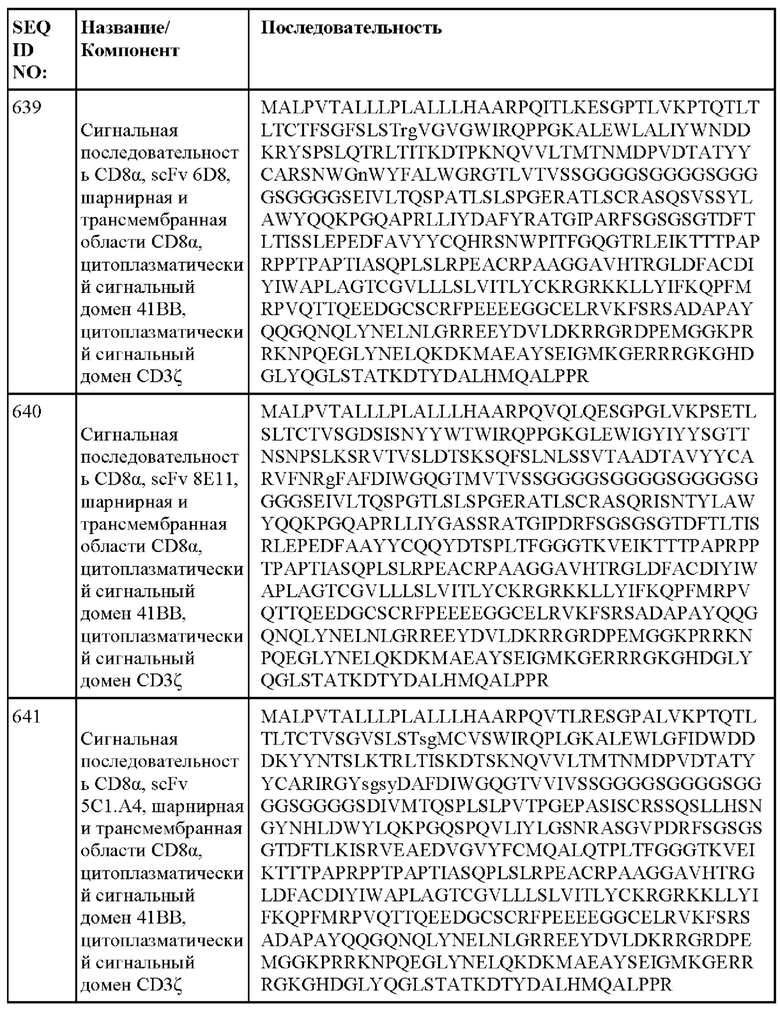
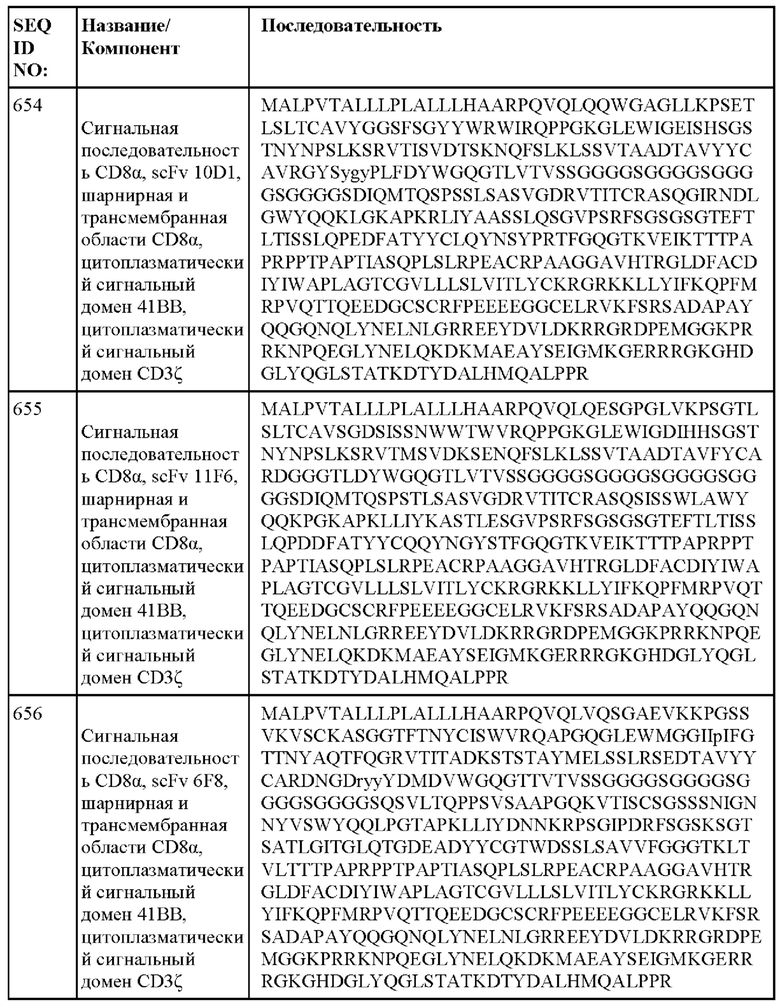
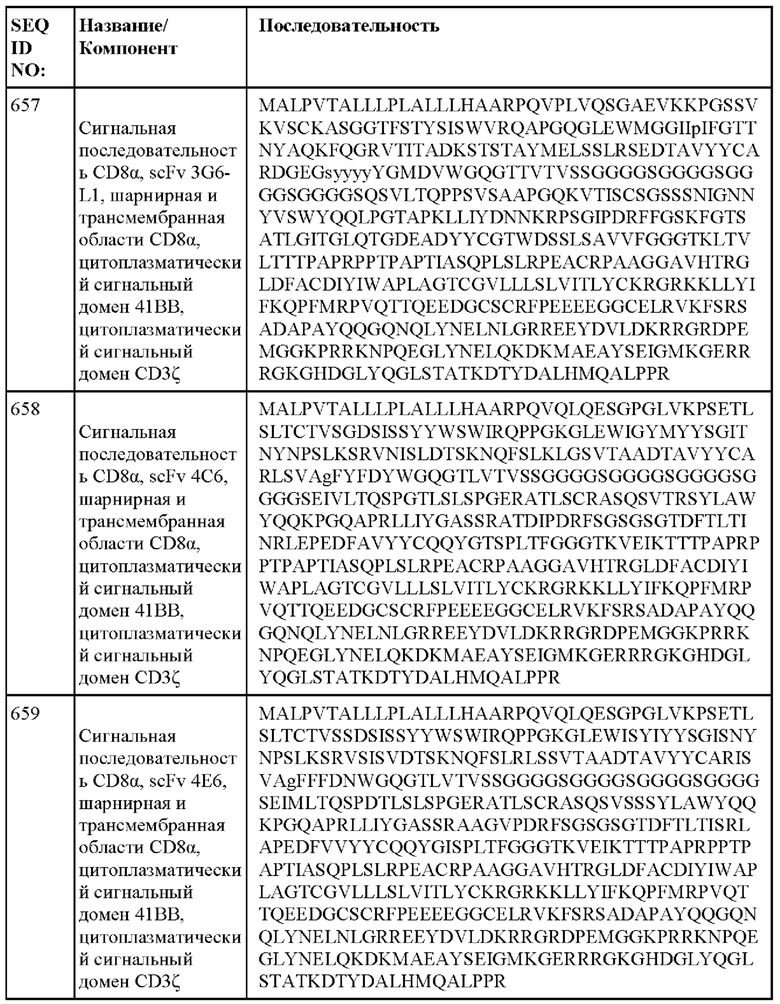
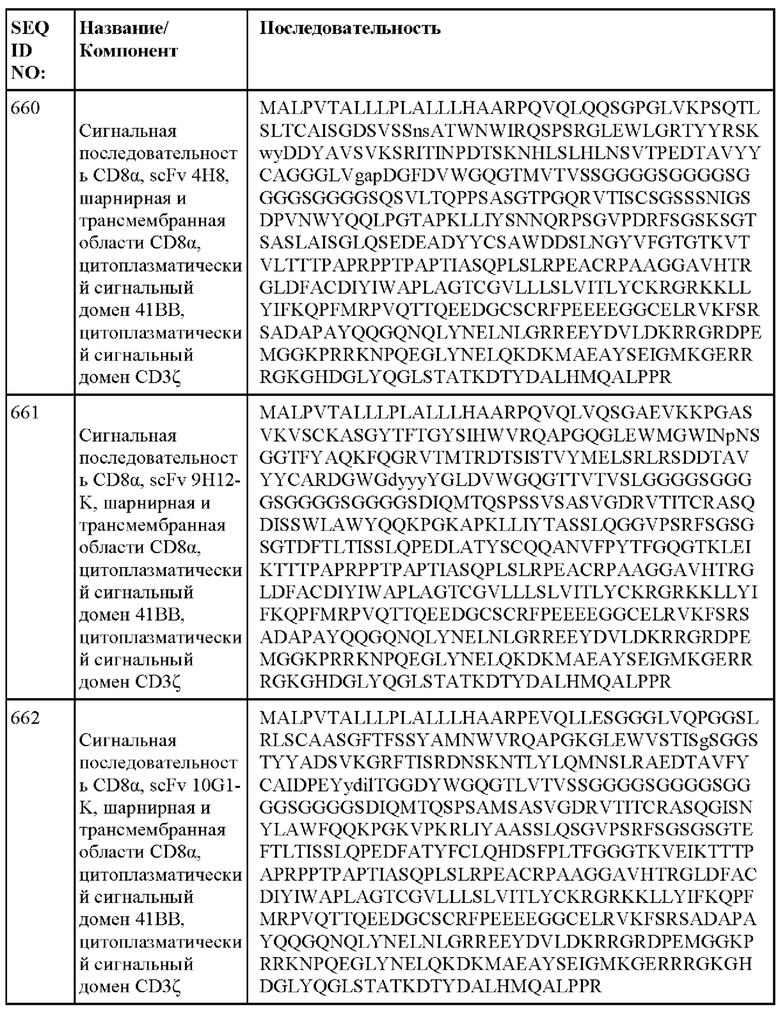
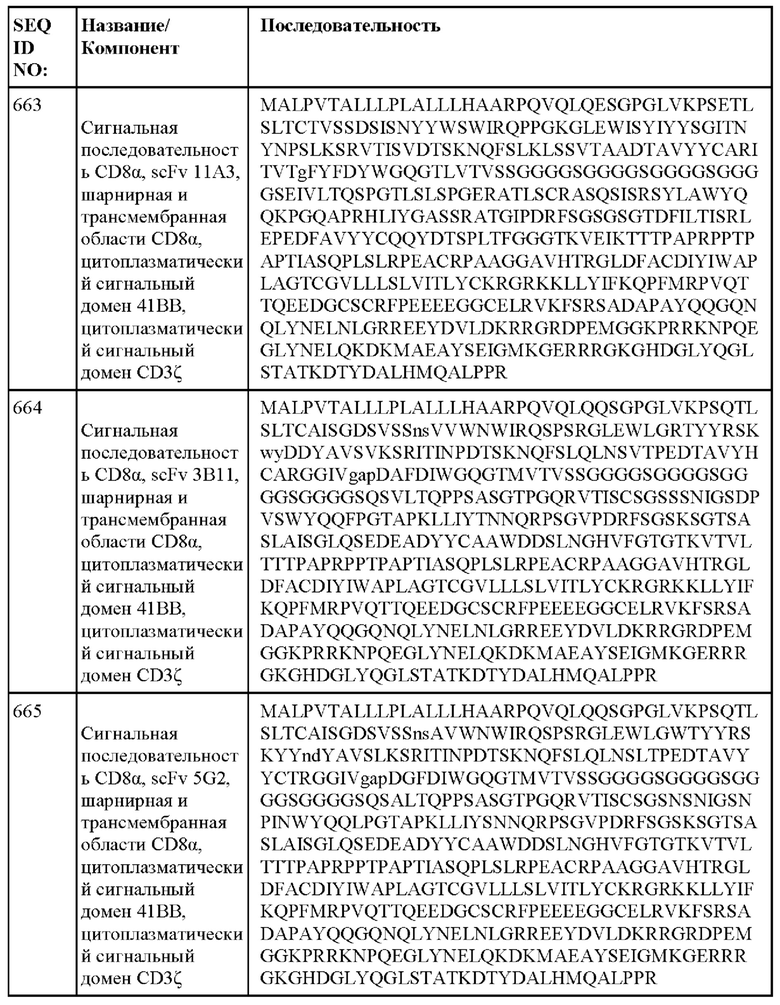
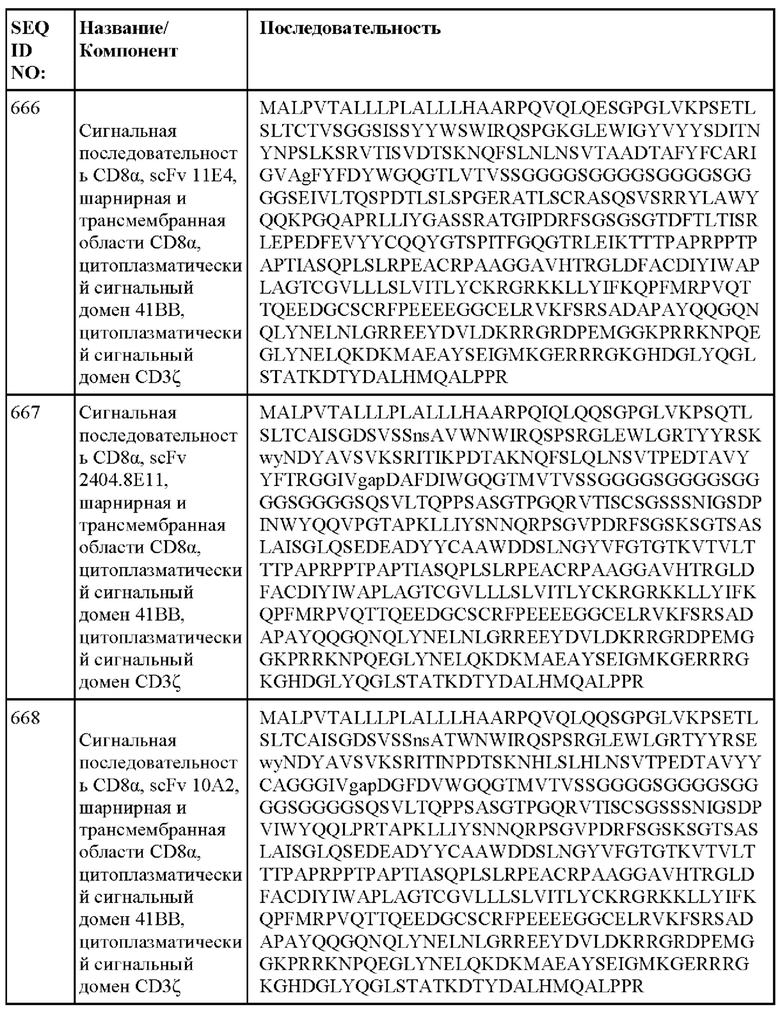
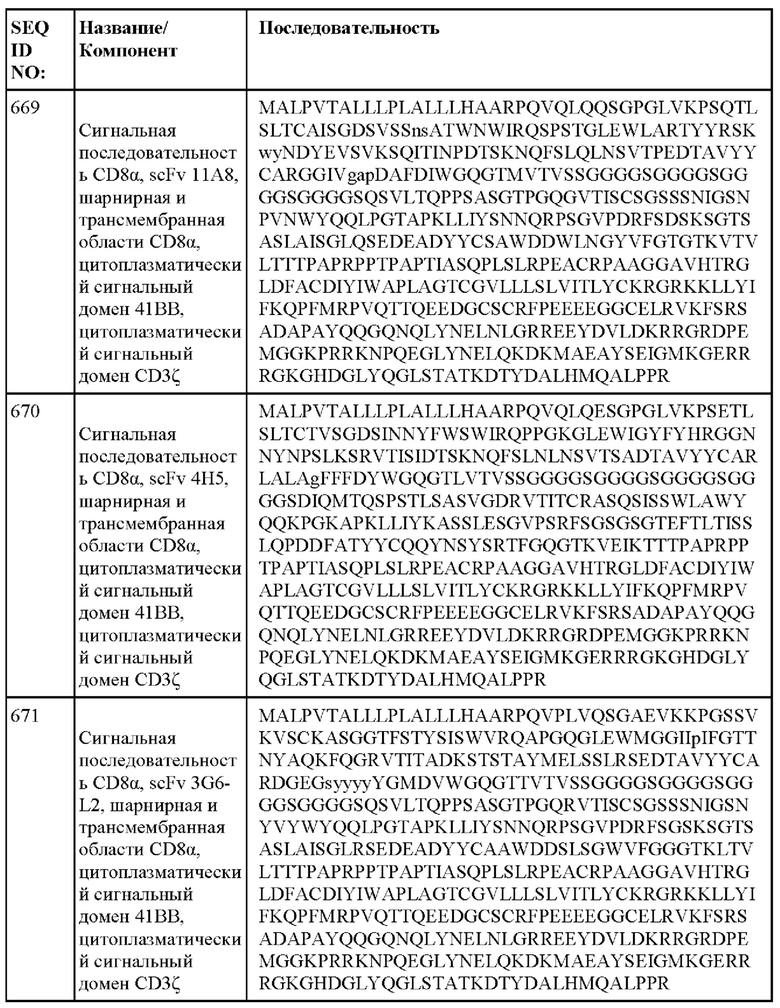
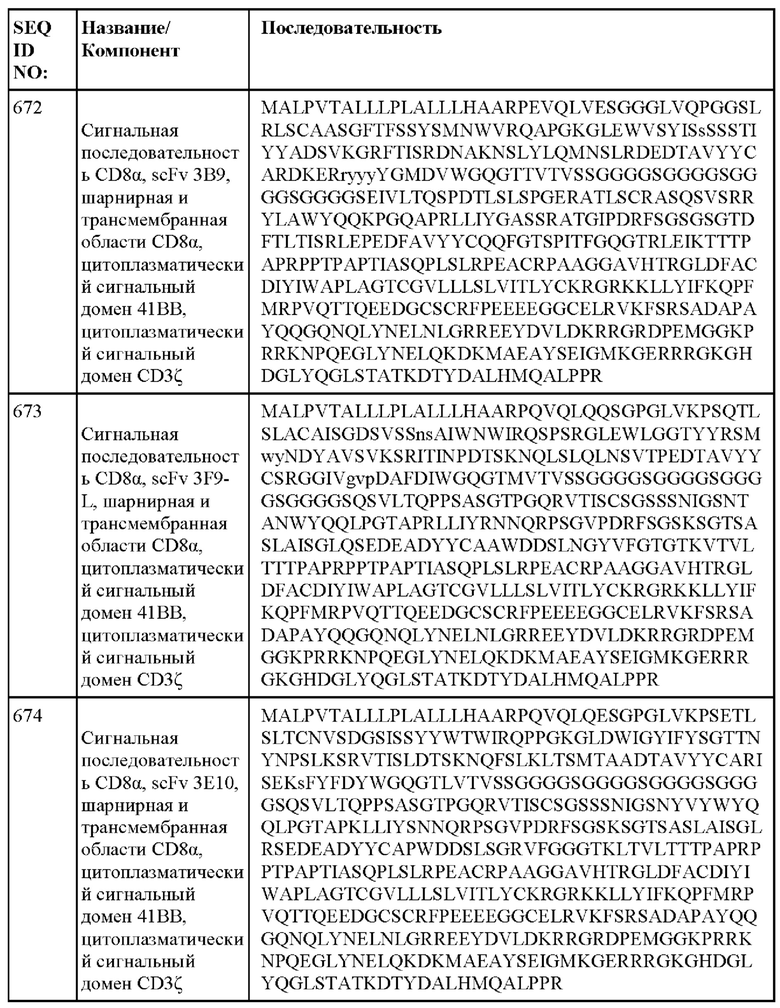
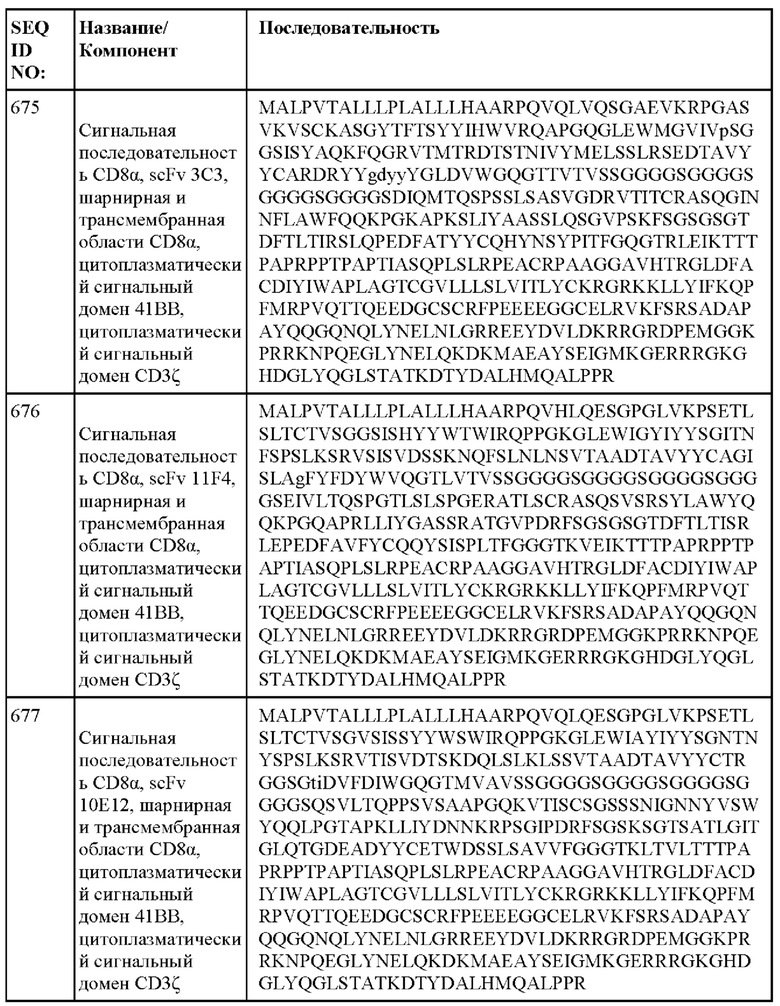
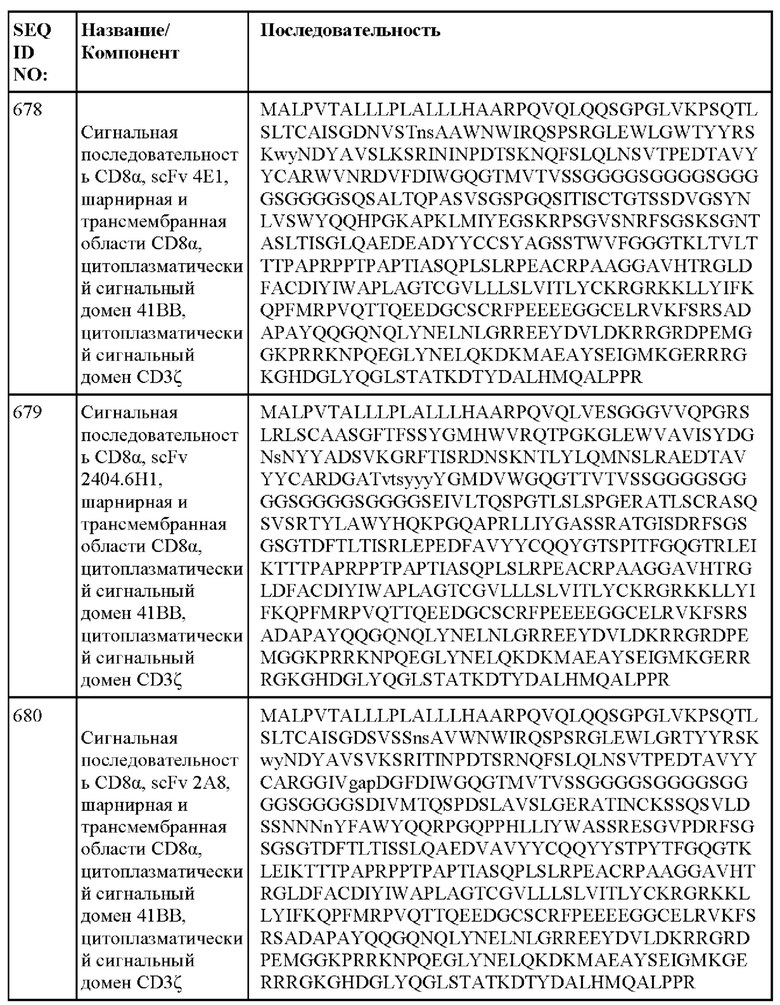
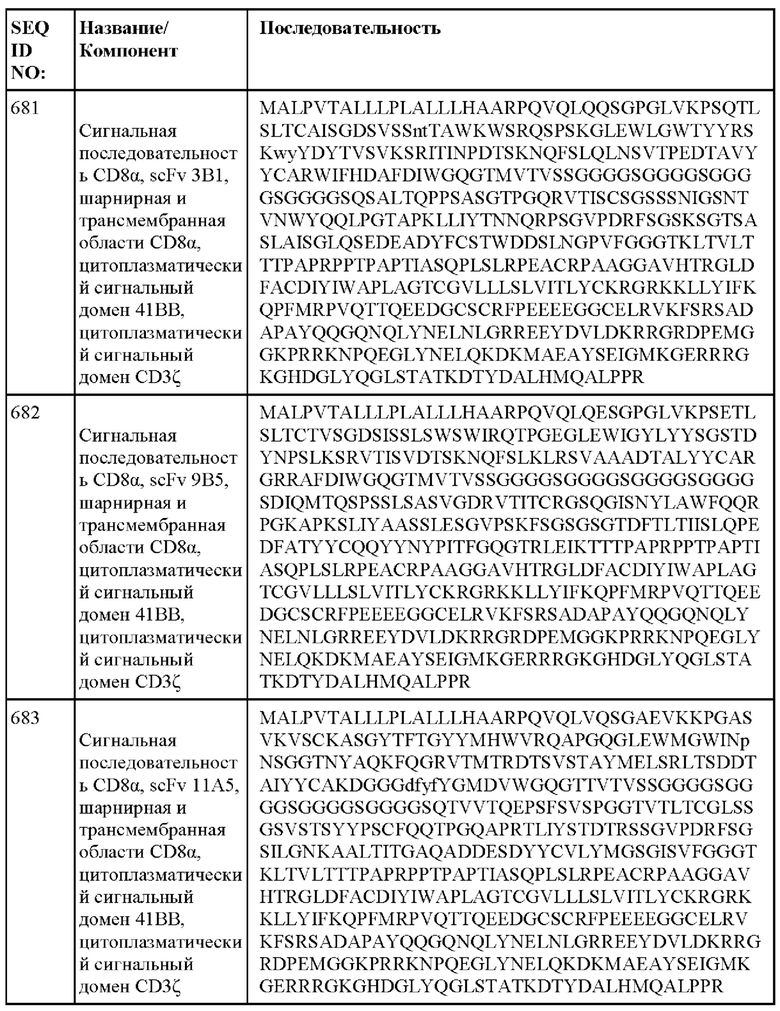
[0273] Схема структуры CAR представлена на ФИГ. 3А. Репрезентативные последовательности CAR, преобразованные из клонов против DLL3, включены в SEQ ID NO: 482-533. Оптимизированные по кодонам последовательности DLL3 CAR были синтезированы и субклонированы в следующие лентивирусные векторы pLVX-EF1a -DLL3 CAR (Clontech) с использованием сайтов рестрикции Xmal (5') и MluI (3').
[0274] Для создания клеток DLL3 CAR-T-клеток МНПК сначала очищали из образцов лейкоцитарной пленки, используя градиент плотности в среде Ficoll (Ficoll Paque PLUS / GE Healthcare Life Sciences). Т-клетки очищали из МНПК с использованием коммерчески доступного набора для выделения Т-клеток (Miltenyi Biotec, кат.№130-096-535). В качестве альтернативы, первичные человеческие Т-клетки могут быть очищены непосредственно из LeukoPak (StemCell Technologies).
[0275] Чтобы получить лентивирус, кодирующий DLL3 CAR, клетки HEK-293Т высевали из расчета 0,4 миллиона клеток на мл в 2 мл DMEM (Gibco) с добавлением 10% FBS (Hyclone) на лунку 6-луночного планшета в день 0. В день 1 получали лентивирус путем смешивания 1,5 мкг лентивирусных пакующих векторов psPAX2, 0,5 мкг pMD2G и 0,5 мкг подходящего вектора для переноса CAR в 250 мкл Opti-MEM (Gibco) на лунку 6-луночного планшета («смесь ДНК»). 10 мкл липофектамина 2000 (Invitrogen) в 250 мкл Opti-MEM инкубировали при комнатной температуре в течение 5 минут, а затем добавляли к смеси ДНК. Смесь инкубировали при комнатной температуре в течение 20 минут, и общий объем 500 мкл медленно добавляли по бокам лунок, содержащих HEK-293Т. Очищенные Т-клетки активировали в среде X-Vivo-15 (Lonza) с добавлением 100 МЕ/мл человеческого IL-2 (Miltenyi Biotec), 10% FBS (Hyclone) и TransAct для человеческих Т-клеток (Miltenyi Biotec, кат.№130-111-160, разведение 1:100). В день 2 среду из каждой лунки 6-луночного планшета заменяли 2 мл на лунку среды для трансдукции Т-клеток, т.е. X-Vivo-15 с добавлением 10% FBS. В день 3 Т-клетки ресуспендировали в количестве 0,5 миллиона клеток на мл в 1 мл среды для трансдукции Т-клеток на лунку планшета Grex-24 (Wilson Wolf, кат. №80192М). Лентивирусные супернатанты из клеток HEK293T собирали и пропускали через фильтр на 0,45 мкм (EMD Millipore) для удаления клеточного детрита, а затем добавляли к Т-клеткам вместе со 100 МЕ/мл человеческого IL-2. В день 5 в каждую лунку планшета Grex-24 добавляли 4,5 мл среды для размножения Т-клеток, т.е. X-Vivo-15 с добавлением 5% человеческой сыворотки группы АВ (Gemini Bio). В день 9 и день 13 определяли эффективность трансдукции путем определения процента Т-клеток, распознающих рекомбинантный DLL3 (Adipogen), с помощью проточной цитометрии. При необходимости клетки размножали в более крупных колбах или сосудах G-Rex (Wilson Wolf), используя среду для размножения Т-клеток. На 14 день клетки DLL3 CAR-T-клетки криоконсервировали. Процент клеток, окрашенных рекомбинантным DLL3, был нормирован по клонам непосредственно перед криоконсервацией.
[0276] Для определения процента Т-клеток, которые были успешно трансдуцированы DLL3 CAR, Т-клетки сначала инкубировали с 1 мкг/мл Flag-меченого рекомбинантного DLL3 (Adipogen) в PBS+1% BSA в течение 20 минут при 4°С.Затем клетки промывали PBS +1% BSA, окрашивали РЕ-мечеными антителами к Flag (Biolegend, кат.№637310) и анализировали с помощью проточной цитометрии.
[0277] Примеры DLL3 CAR-T-клеток показаны на ФИГ. 3В. ФИГ. 3В демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR экспрессируются на поверхности первичных Т-клеток и могут распознавать рекомбинантный DLL3. Графики гейтированы по живым CD3+ клеткам. Числа на графиках представляют собой процент клеток, экспрессирующих каждый анти-DLL3 CAR.
Пример 6: Определение характеристик in vitro
[0278] В этом примере описаны эксперименты, использованные для определения специфичности и активности CAR в отношении DLL3 in vitro.
[0279] SHP-77, WM266.4, DMS 454 и DMS 273 представляют собой линии DLL3+ клеток, которые были приобретены у АТСС или Sigma. HEK-293Т представляет собой DLL3-отрицательную линию клеток. Для экспрессии DLL3 человека в HEK-293Т использовали лентивирус, кодирующий полноразмерный DLL3 человека, для трансдукции клеток HEK-293Т.
[0280] Затем для тестирования DLL3-специфичного уничтожения клетки HEK-293Т, экспрессирующие люциферазу светлячков, обладающие или не обладающие экспрессией DLL3 человека, высевали с плотностью посева 5000 клеток на лунку в 96-луночные аналитические планшеты (Costar). DLL3 CAR-Т-клетки размораживали и добавляли к высеянным клеткам HEK-293Т, обладающим или не обладающим экспрессией DLL3 человека, при соотношении эффектор: мишень (Е:Т) в диапазоне от 1:9 до 9:1 в среде для размножения Т-клеток, т.е. X-Vivo-15 с добавлением 5% человеческой сыворотки группы АВ (Gemini Bio). Жизнеспособность клеток измеряли через 72 часа с использованием набора для анализа one-glo (Promega). Репрезентативные DLL3 CAR-T-клетки продемонстрировали эффективное уничтожение клеток HEK-293T-DLL3, но не проявили обнаружимой активности в отношении родительских клеток HEK-293Т (ФИГ. 4А).
[0281] Для тестирования цитотоксической активности DLL3 CAR-T-клеток в отношении линий клеток, экспрессирующих эндогенный DLL3, DLL3 CAR-T-клетки инкубировали с мечеными люциферазой светлячков DLL3+ клетками SHP-77, WM266.4, DMS 454 или DMS 273 при соотношении эффектор:мишень (Е:Т) от 1:9 до 9:1 в среде для размножения Т-клеток, т.е. X-Vivo-15 с добавлением 5% человеческой сыворотки группы AB (Gemini Bio). Жизнеспособность клеток измеряли через 72 часа с использованием набора для анализа one-glo (Promega). Каждое условие анализировали в 3 параллельных анализах. Наносили на график средний процент живых клеток и стандартное отклонение (ФИГ. 4В и ФИГ. 4С).
[0282] ФИГ. 4А демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR-T-клетки специфически уничтожали клетки HEK-293Т, экспрессирующие DLL3 человека, но не родительские клетки HEK-293Т, в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор:мишень. Т-клетки, которые не экспрессировали анти-DLL3 CAR (помеченные как «пустой вектор»), использовали в качестве отрицательного контроля.
[0283] ФИГ. 4В демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR-T-клетки уничтожали клетки SHP-77 и WM266.4, экспрессирующие эндогенный DLL3, в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор:мишень.
[0284] ФИГ. 4С демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR-T-клетки уничтожали клетки мелкоклеточного рака легкого DMS 454 и DMS 273, экспрессирующие эндогенный DLL3, в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор:мишень. Для всех графиков на ФИГ. 4С для оценки жизнеспособности клеток-мишеней была использована система анализа One-glo, n=3.
[0285] Для измерения цитокинов, секретируемых из DLL3 CAR-T-клеток, DLL3 CAR-T-клетки инкубировали с DLL3+клетками SHP-77 при соотношении эффектор:мишень (Е:Т) 1:1 или 1:9 в среде для размножения Т-клеток, т.е. X-Vivo-15 с добавлением 5% человеческой сыворотки группы AB (Gemini Bio). Через 24 часа собирали супернатант тканевой культуры и измеряли уровни 3 цитокинов [интерферона-гамма (IFN-γ), фактора некроза опухоли-альфа (TNF-α) и IL-2] в супернатантах с использованием 9-плексного анализа провоспалительной тканевой культуры человека (human proinflammatory tissue culture 9-plex assay) (MSD) в соответствии с протоколом производителя. На ФИГ. 5 показано, что анти-DLL3 CAR-T-клетки высвобождали цитокины после совместной инкубации с линией DLL3-экспрессирующих клеток SHP-77. CAR-T-клетки и клетки SHP-77 инкубировали при соотношении эффектор:мишень, равном 1:1 или 1:9, в течение 24 часов, n=3.
Пример 7: Анализ последовательного уничтожения
[0286] Анализ последовательного уничтожения включает многократное воздействие на CAR-T-клеток их мишени, в результате чего CAR-T-клетки подвергаются пролиферации и, в некоторых случаях, дифференцировке и истощению. Этот анализ использовали для выбора оптимальных клонов с высоким лизисом клеток-мишеней и пролиферативными способностями после нескольких циклов воздействия клеток-мишеней.
[0287] В первый день анализа 5000 меченых люциферазой светлячков клеток WM266.4, DMS 454 или DMS 273, которые, как известно, экспрессируют DLL3, высевали в 96-луночные планшеты с белыми стенками и плоским прозрачным дном в 100 мкл среды X-Vivo-15 с 5% человеческой сыворотки. После прикрепления клеток-мишеней ко дну планшетов DLL3 CAR-T-клетки размораживали и добавляли к высеянным клеткам-мишеням при соотношении эффектор:мишень (Е:Т) 1:1 в среде X-VIVO с 5% человеческой сыворотки. Каждые 2 дня после этого 100 мкл среды, содержащей DLL3 CAR-T-клетки, переносили к свежевысеянным клеткам-мишеням и определяли процент лизиса ранее высеянных клеток-мишеней с использованием системы анализа one-glo или системы CellTiter-glo (Promega). Каждое условие анализировали в 3-6 параллельных анализах. Наносили на график средний процент лизиса и среднеквадратическое отклонение (ФИГ. 6А-6С). Оптимальными клонами были клоны с наивысшим лизисом клеток-мишеней в течение всего анализа на 12 день. Эти данные показывают экспериментальные данные анализа последовательного уничтожения, демонстрирующие, что после многократного воздействия анти-DLL3 CAR-T-клеток на DLL3+ клетки WM266.4 некоторые из клонов оставались активными. Систему анализа One-glo или CellTiter-glo использовали в каждый указанный момент времени для оценки жизнеспособности клеток-мишеней, n=3-6.
Пример 8: Активность in vivo
[0288] Для тестирования противоопухолевой активности DLL3 CAR-T-клеток использовали мышей NSG, имеющих опухоль SHP-77. Клетки SHP-77 получали из пробирки с замороженным исходным продуктом, размораживали и подсчитывали в соответствии со стандартной процедурой. Клетки разводили до 50×106 жизнеспособных клеток/мл в полной питательной среде (RPMI+10% FBS). Суспензию клеток хранили на льду до имплантации. Непосредственно перед имплантацией клетки смешивали в соотношении 1:1 с BD Matrigel Matrix (кат.№354234) и каждой мыши подкожно вводили 200 мкл суспензии клетки/matrigel, содержащей 5×106 клеток SHP-77. Рост опухоли контролировали с помощью измерения штангенциркулем с использованием цифрового штангенциркуля, начиная с 5 дня после имплантации. Размер опухоли рассчитывали по формуле: объем опухоли=(ширина∧2×длина/2). Мышей рандомизировали на группы по 5 особей на основании объема опухоли примерно через две недели после имплантации. Средний объем опухоли на группу составлял 314 мм3 или меньше. Через день после рандомизации мышей нетрансдуцированные Т-клетки и DLL3 CAR-T-клетки размораживали и подсчитывали в соответствии со стандартной процедурой. Клетки ресуспендировали в RPMI +10% FBS и вводили в дозах 2 или 5 миллионов CAR+ клеток/мышь путем в/в инъекции в хвостовую вену в объеме 200 мкл/мышь. Затем опухоли продолжали контролировать каждые 3-4 дня до конца исследования. DLL3 CAR-T-клетки 26С8 и 10G1-K индуцировали ингибирование опухоли дозозависимым образом (ФИГ. 7А-7В). На ФИГ. 7А-7В показаны экспериментальные данные, демонстрирующие, что анти-DLL3 CAR-T-клетки могут вызывать клиренс сформировавшихся опухолей мелкоклеточного рака легкого у мышей дозозависимым образом.
[0289] Чтобы проверить противоопухолевую активность DLL3 CAR-T-клеток на моделях, которые демонстрируют метастазы, аналогичные заболеванию человека, были созданы опухоли SHP-77 с помощью инъекции в хвостовую вену. Опухоли наблюдались в легких, печени, головном мозге, почках и селезенке. В частности, клетки SHP-77 размораживали и разводили до 40×106 жизнеспособных клеток/мл в полной питательной среде (RPMI +10% FBS). Суспензию клеток хранили на льду до имплантации и в/в вводили 200 мкл суспензии клеток на мышь в хвостовую вену. На 7 день после имплантации вводили 200 мкл люциферина (15 мг/мл) и контролировали рост опухоли с помощью визуализации IVIS. Мышей рандомизировали на группы по 5 особей на основании общего потока фотонов на 11 день после имплантации. На 12 день после имплантации CAR-T размораживали и подсчитывали в соответствии со стандартной процедурой. Клетки ресуспендировали в RPMI +10% FBS и вводили 2 или 7 миллионов CAR+ клеток на мышь путем в/в инъекции в хвостовую вену в объеме 200 мкл на мышь. Затем опухоли продолжали контролировать каждые 3-4 дня до конца исследования. Как показано на ФИГ. 8, анти-DLL3 CAR-T-клетки 10G1-K могут ингибировать сформировавшиеся опухоли мелкоклеточного рака легкого у мышей дозозависимым образом.
Пример 9: Конструкции анти-DLL3 CAR с предохранительным переключателем
[0290] В этом примере описано конструирование, экспрессия и цитотоксическая активность анти-DLL3 CAR с предохранительным переключателем. Анти-DLL3 CAR в таблице 6 были переформатированы, чтобы включить в них различные конструкции предохранительных переключателей, перечисленные ниже (таблица 8).

[0291] Последовательности белков, кодирующие конструкции анти-DLL3 CAR, включающих предохранительный переключатель, приведены в таблице 9. Иллюстративные конструкции предохранительного переключателя могут содержать сигнальную последовательность CD8α (SEQ ID NO: 477), scFv против DLL3, описанный в настоящем документе, мимотоп CD20 (SEQ ID NO: 536), эпитоп QBEND-10 (SEQ ID NO: 544), шарнирную и транс мембранную области молекулы CD8α человека (SEQ ID NO: 479), цитоплазматическую часть молекулы 4-1 ВВ (SEQ ID NO: 291) и цитоплазматическую часть молекулы CD3C (SEQ ID NO: 292).


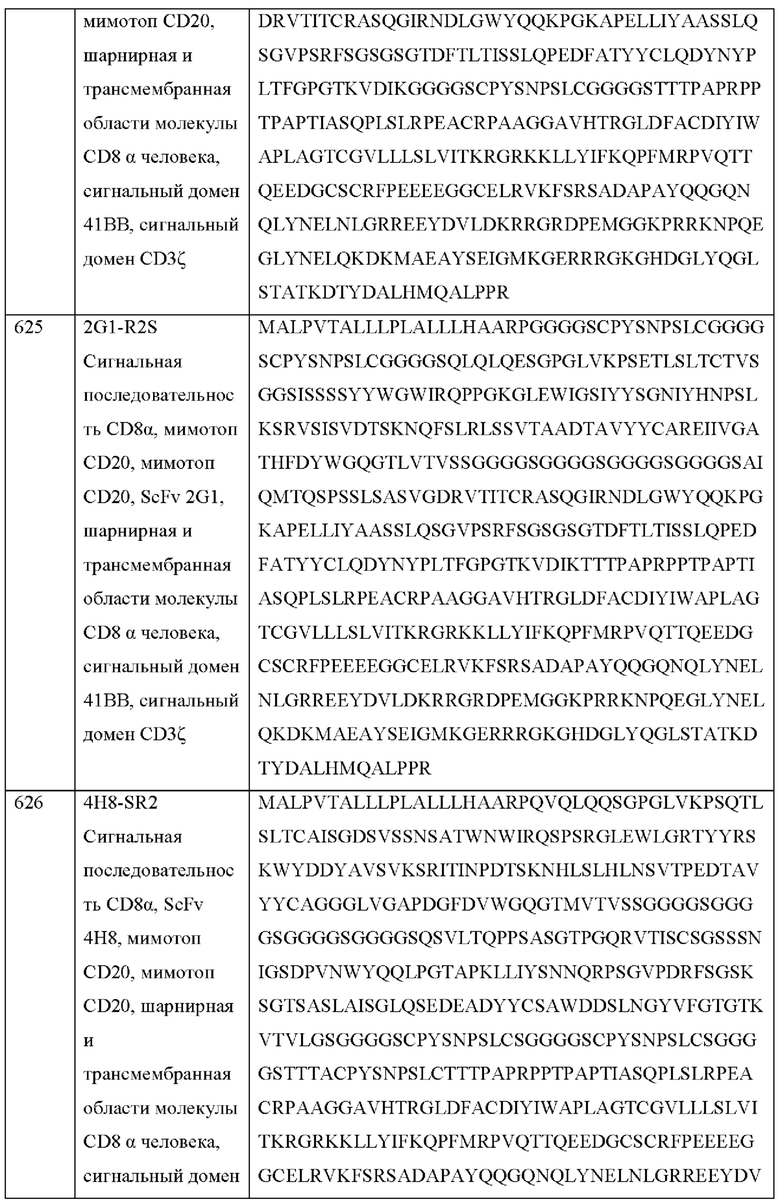

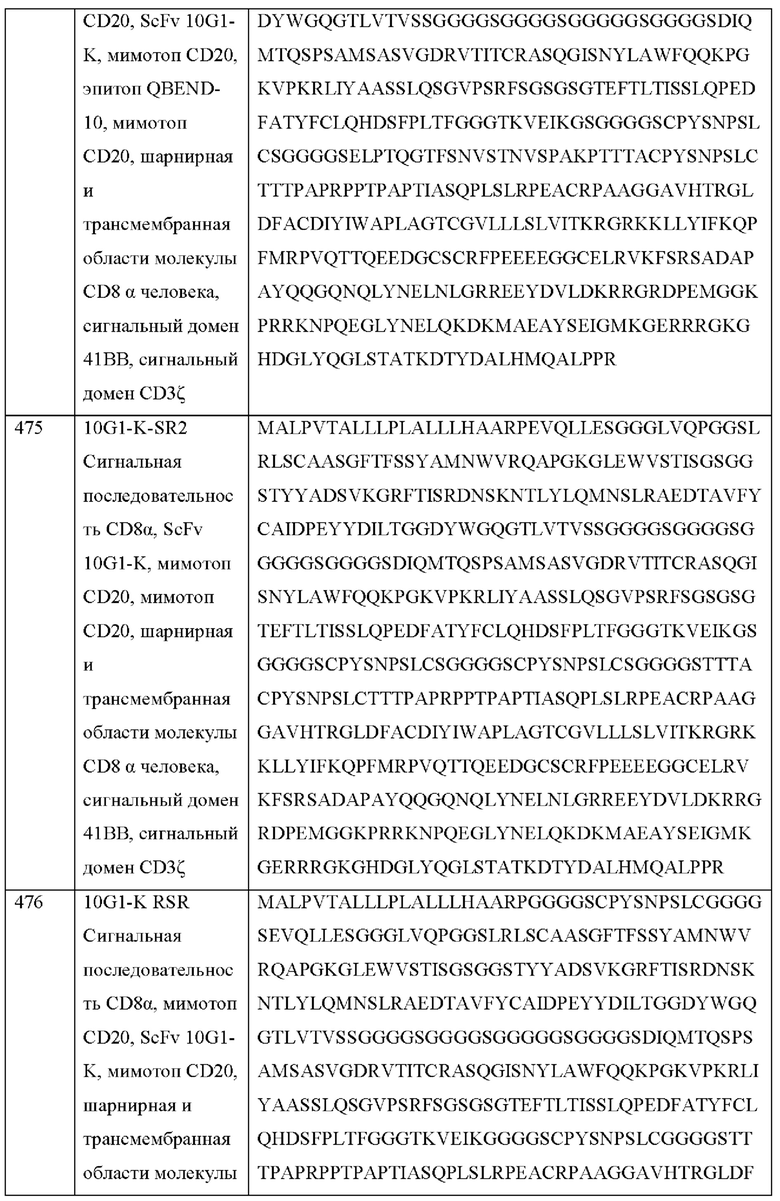

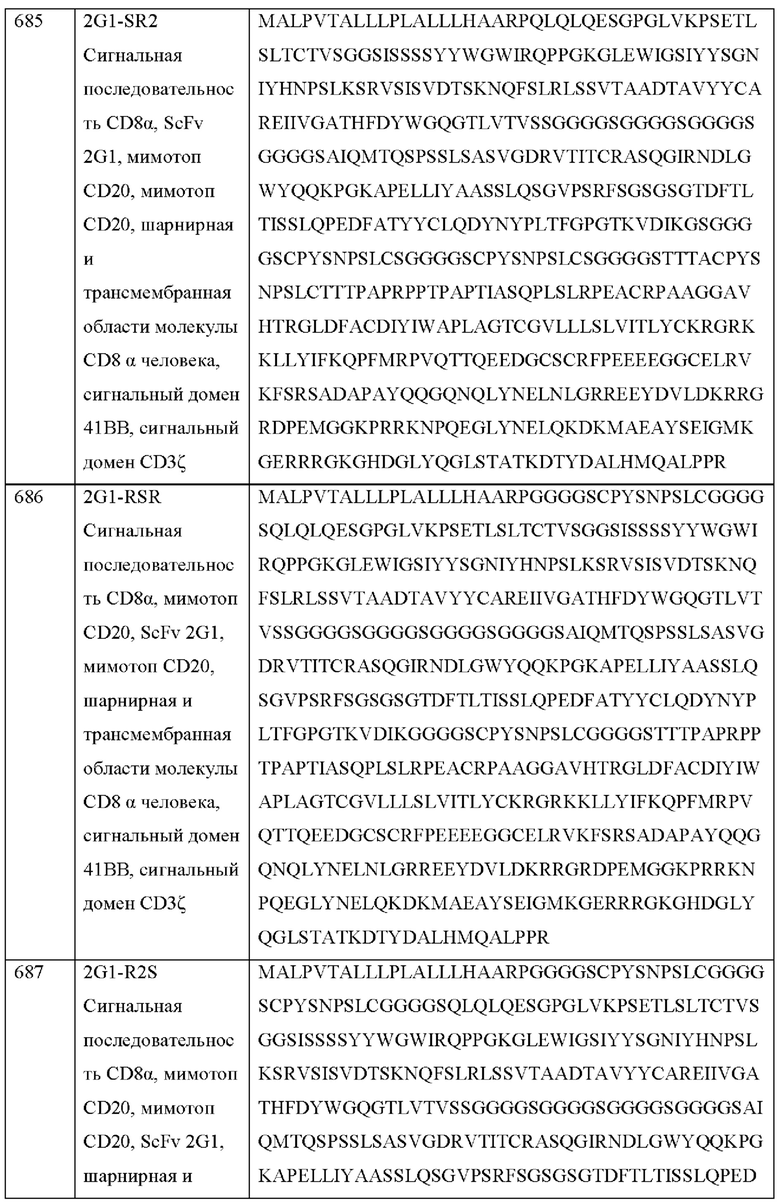
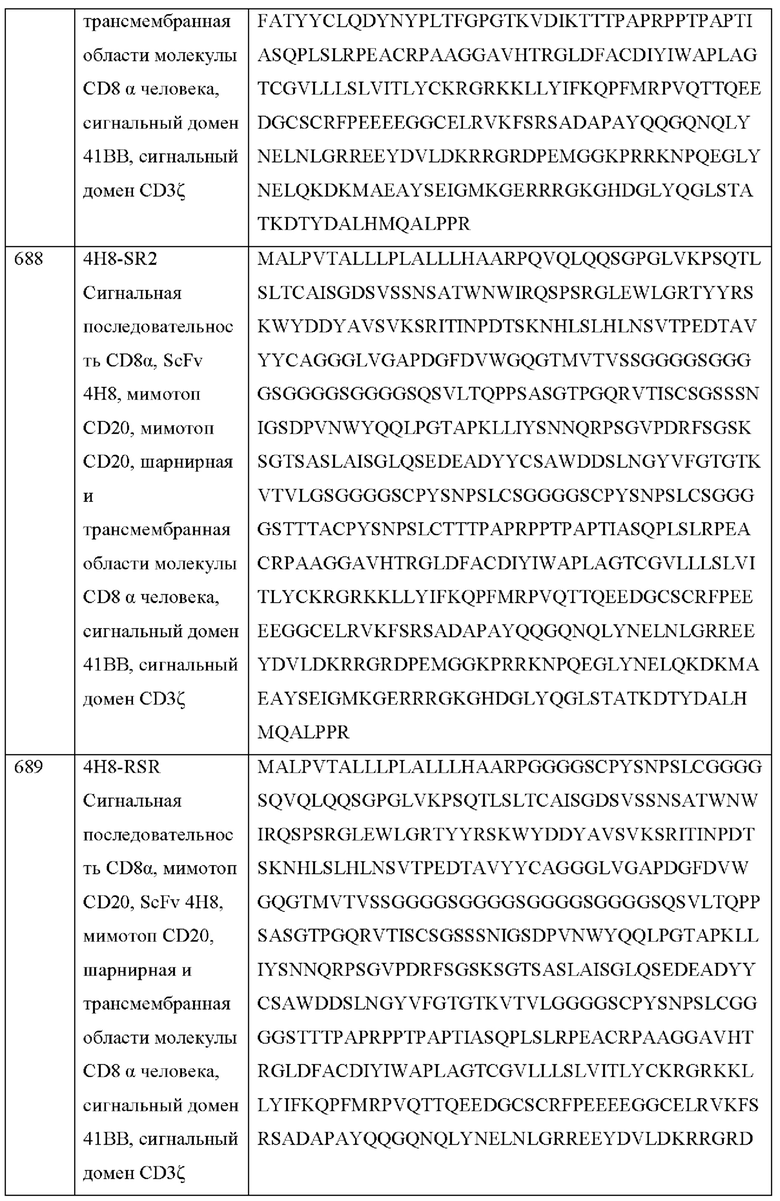
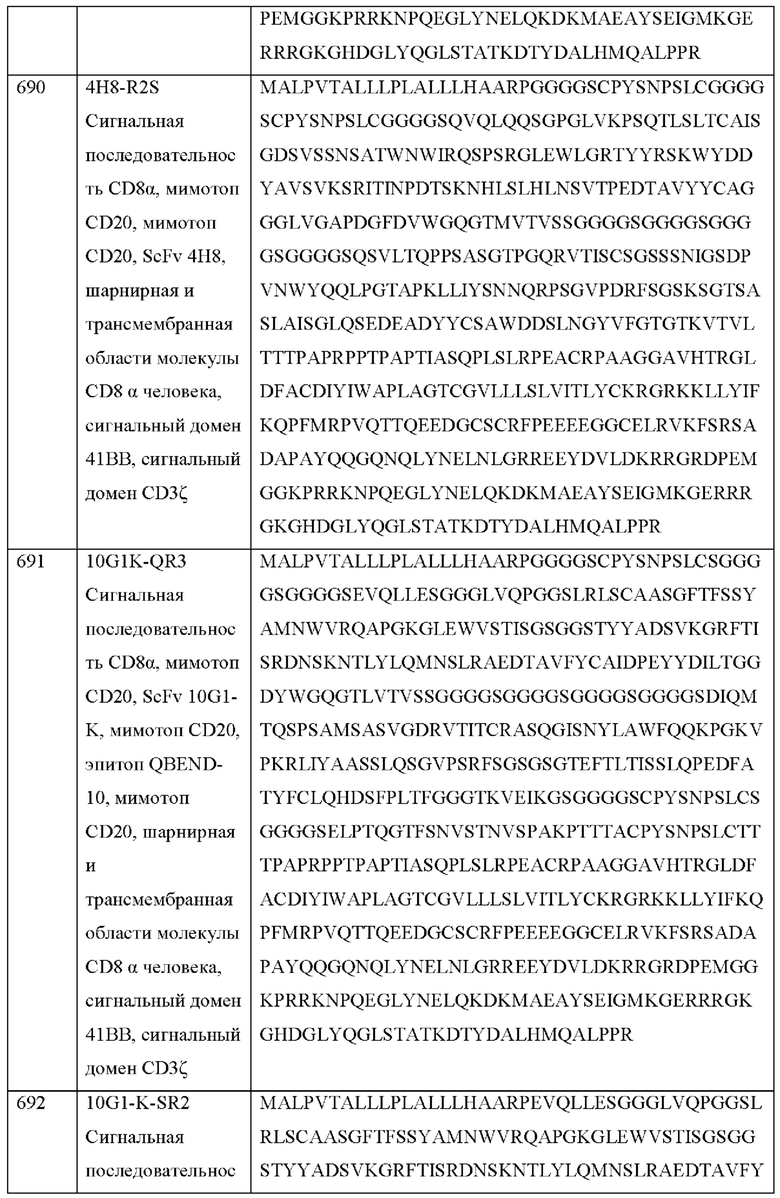
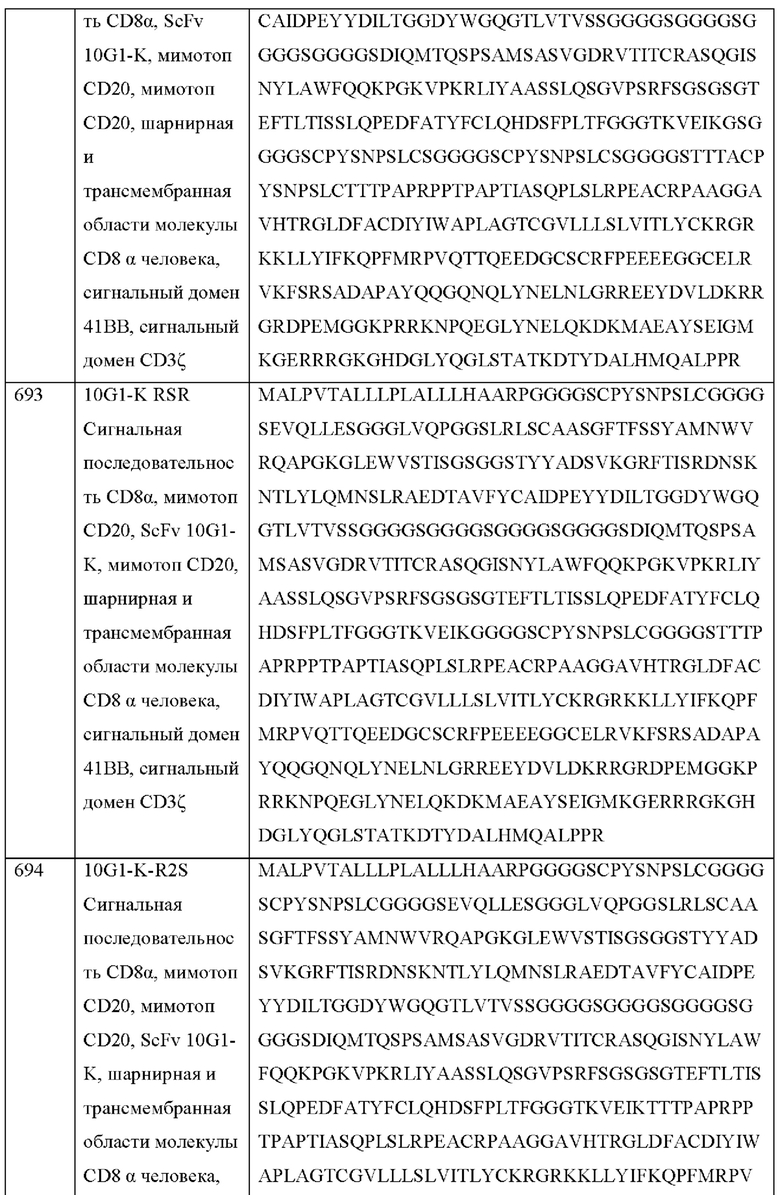

[0292] CAR-T были получены с использованием способов, описанных в примере 5, и их цитотоксическая активность была исследована с использованием способов, описанных в примере 7. ФИГ. 9А представляет собой графики, показывающие структуру четырех различных предохранительных переключателей. ФИГ. 9В демонстрирует экспериментальные данные проточной цитометрии, показывающие, что анти-DLL3 CAR 2G1, 4Н8 и 10G1-K с предохранительными переключателями экспрессировались на поверхности первичных Т-клеток и могут распознавать рекомбинантный DLL3. Графики гейтированы по живым CD3+ клеткам, а числа на графиках представляют собой процент клеток, экспрессирующих каждый анти-DLL3 CAR. ФИГ. 9С демонстрирует экспериментальные данные, показывающие, что анти-DLL3 CAR с предохранительными переключателями активны в анализе последовательного уничтожения линии DLL3+ клеток WM266.4.
Пример 10: Цитотоксичность на PDX-моделях мелкоклеточного рака легкого
[0293] PDX-модели мелкоклеточного рака легкого были приобретены у Crown Bioscience. Чтобы исследовать экспрессию DLL3 на поверхности клеток, замороженные флаконы с PDX-моделями размораживали, и для каждого окрашиваемого образца использовали 200000 клеток. Экспрессию DLL3 проверяли с помощью FACS-анализа с использованием конъюгированного с РЕ антитела к DLL3. Конъюгированные с бриллиантовым фиолетовым 421 антитела к CD45 человека и к CD45 мыши добавляли в один и тот же образец для окрашивания для исключения лимфоцитов человека и мыши. [0294] На ФИГ. 10А представлены экспериментальные данные, демонстрирующие, что DLL3 экспрессируется на поверхности двух PDX-моделей мелкоклеточного рака легкого. На ФИГ. 10В показаны экспериментальные данные, демонстрирующие, что анти-DLL3 CAR-T-клетки уничтожали клетки в тех же двух PDX-моделях мелкоклеточного рака легкого в 3-дневном анализе цитотоксичности при указанных соотношениях эффектор:мишень. Т-клетки, которые не экспрессировали анти-DLL3 CAR (помеченные как «пустой вектор»), использовали в качестве отрицательного контроля.
Пример 11: Обнаружение in vitro и истощение DLL3 CAR-T-клеток с помощью предохранительного переключателя на основе ритуксимаба
[0295] Чтобы истощить или выключить CAR-T-клетки в случае нежелательной активности, был разработан выключающий переключатель на основе ритуксимаба путем вставки мимотопов ритуксимаба в различные места внеклеточной области CAR, как описано в примере 9. Анализ комплементзависимой цитотоксичности использовали для оценки ритуксимаб-зависимого истощения in vitro DLL3 CAR-T-клеток. В этом анализе замороженные CAR-T-клетки размораживали и 1×105 клеток инкубировали в среде RPMI 1640 с добавлением 10% FBS в 96-луночных планшетах. Клетки инкубировали в течение 3 часов в отсутствие или в присутствии 25% комплемента крольчат (Cedarlane, CL3441-S) и антителами ритуксимабом (собственного производства; 100 мг/мл). Клетки окрашивали рекомбинантным DLL3 (Adipogen) и анализировали цитотоксичность с помощью проточной цитометрии. На ФИГ. 11А представлены экспериментальные данные, демонстрирующие, что анти-DLL3 CAR-T-клетки могут быть обнаружены как при окрашивании рекомбинантным DLL3, так и при окрашивании ритуксимабом. На ФИГ. 11В представлены экспериментальные данные, демонстрирующие, что DLL3 CAR-T-клетки истощались in vitro ритуксимаб-зависимым и комплемент-зависимым образом.
Пример 12: Активность in vivo анти-DLL3 CAR-T-клеток с предохранительным переключателем
[0296] Для тестирования противоопухолевой активности DLL3 CAR-T-клеток с предохранительным переключателем использовали мышей NSG, имеющих опухоль SHP-77. Клетки SHP-77 размораживали из замороженного флакона, подсчитывали и разводили. Каждой мыши подкожно вводили 50×106 жизнеспособных клеток/мл в суспензии среда RPMI/matrigel. Рост опухоли контролировали с помощью измерения штангенциркулем с использованием цифрового штангенциркуля, начиная с 5 дня после имплантации. Размер опухоли рассчитывали по формуле: объем опухоли=(ширина∧2×длина/2). Мышей рандомизировали на группы по 8 особей на основании объема опухоли примерно через 14 дней после имплантации. Средний объем опухоли на группу составлял 178 мм3. В этот же день после рандомизации мышей нетрансдуцированные Т-клетки и DLL3 CAR-T-клетки размораживали и подсчитывали в соответствии со стандартной процедурой. Клетки ресуспендировали в RPMI при 5×106 CAR+ клеток/мышь путем в/в инъекции в хвостовую вену в объеме 200 мкл/мышь. Опухоли продолжали контролировать каждые 3-4 дня до конца исследования. Все группы DLL3 CAR-T-клеток с предохранительным переключателем индуцировали значительное ингибирование опухоли и полный или почти полный клиренс обнаружимой опухоли к 50 дню (ФИГ. 12А).
[0297] Чтобы проверить противоопухолевую активность DLL3 CAR-T-клеток на моделях, которые демонстрируют метастазы, аналогичные заболеванию человека, были созданы мелкоклеточные опухоли легкого DMS 273, экспрессирующие экзогенный DLL3 (DMS 273-DLL3), с помощью инъекции в хвостовую вену. В частности, клетки DMS 273-DLL3 размораживали и разводили до 5×105 жизнеспособных клеток/мл в среде RPMI. 200 мкл суспензии клеток на мышь вводили в/в в хвостовую вену. На 3 день после имплантации мышей рандомизировали на группы по 9 особей. В тот же день DLL3 CAR-T размораживали, подсчитывали и ресуспендировали в среде RPMI при 5×106 CAR+ клеток на мышь с помощью в/в инъекции вхвостовую вену в объеме 200 мкл на мышь. Опухоли продолжали контролировать каждые 3-4 дня с помощью системы визуализации IVIS до конца исследования. Как показано на ФИГ. 12В, несколько различных DLL3 CAR с разными предохранительными переключателями на основе ритуксимаба были эффективны против метастатических опухолей.
Пример 13: Исследование безопасности на мышах с использованием животных, не имеющих опухолей
[0298] Сообщалось о РНК DLL3 в мозге и гипофизе человека (GTex). Точно так же сообщалось о РНК DLL3 мыши в гипофизе (Bio-GPS). Чтобы понять экспрессию РНК DLL3 в головном мозге мышей, головной мозг от трех мышей NSG фиксировали в 10% нейтральном забуференном формалине (NBF), заливали, последовательно нарезали на срезы по 4-6 мкм и анализировали в анализе RNAscope®LS Red ISH (ACDBio). РНК DLL3 была обнаружена на низких уровнях в образцах головного мозга мышей NSG. ФИГ. 13А демонстрирует репрезентативное изображение окрашивания РНК DLL3 мыши, наблюдаемого в этом анализе.
[0299] Чтобы понять потенциальную токсичность экспрессии РНК DLL3 в головном мозге и гипофизе, нетрансдуцированные Т-клетки, 8×106 клеток DLL3 CAR-T-клеток 10G1-K или 8×106 DLL3 CAR-T-клеток 2G1 внутривенно вводили мышам NSG. Через семь дней после инъекции собирали селезенки, головной мозг и гипофиз, фиксировали в 10% NBF, заливали, последовательно нарезали на срезы по 4-6 мкм и окрашивали антителом к CD3 человека (Abeam, ab52959, разведение 1:500) для обнаружения человеческих Т-клеток с помощью иммуногистохимии. Хотя Т-клетки были обнаружены в селезенках всех животных, они не были обнаружены в образцах головного мозга или гипофиза (ФИГ. 13В). Таким образом, хотя РНК DLL3 была обнаружена на низком уровне у мышей NSG, не имеющих опухолей, DLL3 CAR-T-клетки не были обнаружены в образцах головного мозга или гипофиза мышей.
Пример 14: Исследование безопасности на мышах с использованием животных, имеющих подкожную опухоль
[0300] Для дальнейшей оценки потенциальной токсичности для мозга и гипофиза DLL3 CAR-T-клетки вводили мышам NSG, имеющим подкожные опухоли LN229, которые экспрессируют экзогенный DLL3 мыши (LN229-mDLL3). В этой модели активация CAR-T опухолевыми клетками может приводить к повышенной чувствительности и активности в отношении потенциально нормальных тканей, экспрессирующих DLL3. План эксперимента показан на ФИГ. 14А. За три дня до имплантации опухоли (день -3) аденоассоциированные вирусы (AAV), кодирующие IL-7 и IL-15 (Vigene Biosciences), вводили через хвостовую вену для поддержки роста и устойчивости CAR-T-клеток. Затем клетки LN229-mDLL3 размораживали из замороженного флакона и разводили до 4,25×107 клеток/мл в полной питательной среде (RPMI +10% FBS). Суспензию клеток хранили на льду до имплантации. Непосредственно перед имплантацией клетки смешивали в соотношении 1:1 с BD Matrigel Matrix (кат.№354234) и каждой мыши подкожно вводили 200 мкл суспензии клетки/matrigel, содержащей 4,25×106 клеток LN229-mDLL3. Рост опухоли контролировали с помощью измерения штангенциркулем с использованием цифрового штангенциркуля, начиная с 8 дня после имплантации. Размер опухоли рассчитывали по формуле: объем опухоли=(ширина∧2×длина/2). На 22 день после имплантации мышей рандомизировали на группы по 5 особей в зависимости от объема опухоли и концентрации IL-7 и IL-15 в сыворотке. В тот же день (день 22) нетрансдуцированные Т-клетки и мышиные перекрестно-реактивные DLL3 CAR-T-клетки 10G1-K размораживали и ресуспендировали в RPMI +10% FBS и вводили из расчета 1×107 CAR+ клеток/мышь путем в/в инъекции в хвостовую вену в объеме 200 мкл/мышь. За опухолями продолжали наблюдать каждые 3-4 дня до конца исследования и наблюдали устойчивую противоопухолевую активность при лечении DLL3 CAR-T (ФИГ. 14В).
[0301] На 49 день, когда животные, получавшие DLL3 CAR-T-клетки, не имели опухолей, ткани головного мозга животных фиксировали в 10% NBF и заливали, чтобы выявить желудочковую систему, включая боковой, третий и четвертый желудочки, таким образом, чтобы три секции были помещены в единый блок, который последовательно нарезали на срезы по 4-6 мкм и окрашивали гематоксилином и эозином (Н&Е) или окрашивали для выявления специфических для человека CD3 (hCD3) с помощью иммуногистохимии. Образцы гипофиза фиксировали в 10% NBF, обрабатывали и окрашивали Н&Е или иммуногистохимически окрашивали для демонстрации hCD3. Окрашенные Н&Е срезы были исследованы под микроскопом, а гистопатологические данные были оценены патоморфологом с использованием стандартной системы. Введение DLL3 CAR-T-клеток приводило к обильному количеству Т-клеток с положительным окрашиванием на hCD3 в промежуточной и нервной частях гипофиза с относительно небольшим количеством Т-клеток в дистальной части (ФИГ. 14С и данные не показаны). Окрашивание Т-клеток на hCD3 от рассеянного до умеренно низкого или от умеренного до умеренно высокого присутствовало в нейропиле и сосудистой сети головного мозга (в виде циркулирующих Т-клеток) (ФИГ. 14С и данные не показаны). Никаких других изменений в гипофизе или головном мозге не наблюдалось (ФИГ. 14C-D). Чтобы понять функциональные последствия инфильтрации Т-клетками, два гормона, высвобождающиеся в нервной части, вазопрессин и окситоцин, были окрашены с помощью иммуногистохимии. Для обнаружения вазопрессина образцы окрашивали антителом к вазопрессину (ImmunoStar, 20069) в разведении 1/7000 в течение 1 часа при комнатной температуре, а затем Rabbit-on-Rodent HRP-Polymer (Biocare Medical) в течение 30 минут при комнатной температуре. Для обнаружения окситоцина образцы окрашивали антителом к окситоцину (ImmunoStar, 20068) в разведении 1/10000 в течение 15 минут при комнатной температуре, а затем Rabbit-on-Rodent HRP-Polymer (Biocare Medical) в течение 30 минут при комнатной температуре. Оба гормона могут быть обнаружены в нервных частях гипофиза животных, которым вводили нетрансдуцированные Т-клетки или DLL3 CAR-T-клетки, что позволяет предположить, что нейроны, продуцирующие гормон, в этой области оставались функциональными (ФИГ. 14E-F). Таким образом, на основании оценки патоморфологом и окрашивания гормонов в образцах не наблюдалось повреждения тканей.
Пример 15: Исследование безопасности на мышах с использованием животных с внутричерепными опухолями
[0302] Чтобы способствовать инфильтрации Т-лимфоцитов в головном мозге и для дальнейшего понимания потенциальной токсичности для головного мозга использовали мышей NSG, имеющих внутричерепные опухоли LN229, экспрессирующие экзогенный DLL3 мыши и EGFRvIII человека (LN229-mDLL3-vIII). План эксперимента показан на ФИГ. 15А. Клетки LN229-mDLL3 размораживали из замороженного флакона и разводили до 1×107 жизнеспособных клеток/мл в RPMI. Затем каждой мыши интракраниально инъецировали 3 мкл суспензии клеток, содержащей 3×104 клеток LN229-mDLL3. Рост опухоли контролировали с помощью системы визуализации IVIS. На 17 день после имплантации мышей рандомизировали на группы по 10 особей в зависимости от объема опухоли. В тот же день (день 17) нокаутированные по TCR, нетрансдуцированные Т-клетки, DLL3 CAR-T-клетки 10G1-K и EGFRvIII CAR-T-клетки размораживали, ресуспендировали в RPMI и вводили в количестве 1×107 CAR+ клеток/мышь с помощью в/в инъекции в хвостовую вену в объеме 200 мкл/мышь. EGFRvIII CAR-T-клетки были включены в качестве контроля для оценки потенциального воспаления, вызываемого лизисом опухоли в головном мозге. Для поддержки роста и устойчивости CAR-T-клеток каждому животному дважды в неделю, начиная с 17 дня и до конца исследования, давали 0,5 мкг IL-15 (Peprotech AF-200-15) и 3 мкг слитого белка IL-15Ra Fc (R&D Systems 7194-IR). За опухолями продолжали наблюдать каждые 3-4 дня до конца исследования, и не наблюдали явной противоопухолевой активности (ФИГ. 15В). На 22 и 38 день ткани головного мозга всех животных иссекали, обрабатывали и заливали, чтобы выявить желудочковую систему, включая боковой, третий и четвертый желудочки, таким образом, чтобы три секции были помещены в единый блок, который последовательно нарезали на срезы по 4-6 мкм и окрашивали Н&Е или окрашивали для выявления специфических для человека CD45 (hCD45) с помощью иммуногистохимии. Ткани гипофиза были обработаны, чтобы включить нервную часть, промежуточную часть и дистальную часть, и окрашивали Н&Е или иммуногистохимически окрашивали для обнаружения hCD45 в качестве маркера человеческих Т-клеток.
[0303] На 22 день у животных, которым вводили нетрансдуцированные Т-клетки или клетки DLL3 CAR-T-клетки 10G1-K, в головном мозге или гипофизе наблюдались редкие/рассеянные Т-клетки с окрашиванием на hCD45 (данные не показаны). С другой стороны, для животных, получавших EGFRvIII CAR-T-клетки, hCD45+ окрашивание варьировалось от редкого/рассеянного до умеренно низкого или от умеренного до умеренно высокого в областях инфильтрата/глиоза или глиомы, что соответствует противоопухолевой активности в этой группе (данные не показаны). На 38 день у животных, получавших нетрансдуцированные Т-клетки или EGFRvIII CAR-T-клетки, наблюдалось редкое/рассеянное hCD45+ окрашивание в головном мозге и гипофизе. Животные, получавшие DLL3 CAR-T-клетки 10G1-K, имели минимальный или умеренный инфильтрат мононуклеарных клеток в гипофизе, прежде всего в промежуточной и нервной частях (ФИГ. 15C-D). Кроме того, эти животные имели немного большее (умеренно низкое) hCD45+ окрашивание, связанное с небольшими очагами глиомы, по сравнению с редким/рассеянным окрашиванием в других областях головного мозга (сосудистой сети головного мозга, сосудистом сплетении и мозговых оболочках), что соответствовало противоопухолевой активности в этой группе, как показано на ФИГ. 15В.
Пример 16: Цитотоксичность диссоциированных клеток гипофиза мыши in vitro
[0304] Чтобы напрямую проверить, активны ли CART к DLL3 в отношении гипофиза, образцы гипофиза мышей NSG собирали в асептических условиях для анализа in vitro. Ткани диссоциировали с помощью 3 циклов инкубации при 37°С в 1 мл смеси для диссоциации [5 мл DMEM, высокое содержание глюкозы, GlutaMax (Gibco, кат. №10564), 50 мкл фермента Н, 5 мкл фермента R, 6,25 мкл фермента А (набор для диссоциации опухоли от Miltenyi №130-095-929)] с последующей механической диссоциацией с помощью растирания. Отдельные клетки переносили в полную среду (DMEM, высокое содержание глюкозы, GlutaMax, 20%, IX раствор инсулин-трансферрин-селен, IX раствор заменимых аминокислот MEM, IX пенициллин-стрептомицин) и объединяли после каждого цикла. Клетки осаждали и обрабатывали буфером для лизиса АСК в течение 3 минут при комнатной температуре с последующей нейтрализацией в полной среде. Суспензию клеток фильтровали через фильтр на 70 мкм и центрифугировали для удаления буфера. Клетки подсчитывали и высевали в 96-луночный планшет в полной среде из расчета 5×104 клеток на лунку и оставляли для восстановления в течение 3 дней перед добавлением CAR-T-клеток. В момент добавления CAR-T-клеток ожидаемая целевая плотность составляла 1×104 клеток на лунку. Для контролей DLL3+ клетки (DMS-273) и DLL3 клетки (293Т) высевали с одинаковой плотностью. DLL3 CAR-T-клетки 10G1-K и 2G1 добавляли при Е:Т=9:1, 3:1 и 1:1 и культивировали совместно с мишенями в течение 3 дней. По окончании 3-дневного совместного культивирования среду отделяли от лунок и центрифугировали для осаждения Т-клеток. Клетки-мишени обрабатывали 50 мкл/лунку Cell Titer Glo (Promega, G7570) в течение 10 минут и анализировали в планшет-ридере SpectraMax для определения цитотоксичности.
[0305] На ФИГ. 16А представлены экспериментальные данные, показывающие, что, хотя DLL3 CAR-T-клетки активны в отношении линии DLL3+ клеток DMS 273, они не являются цитотоксичными в отношении клеток гипофиза мыши in vitro. Т-клетки объединяли и окрашивали на маркеры активации (41ВВ и CD25) для анализа с помощью проточной цитометрии. На ФИГ. 16В показано, что клетки гипофиза мыши не активируют DLL3 CAR-T-клетки in vitro. Супернатант замораживали при -80°С, а затем размораживали для анализа цитокинов с использованием набора Human ТН1/ТН2 10-Р1ех Tissue Culture Kit (Meso Scale Discovery, K15010B). На ФИГ. 16C показано, что хотя и 10G1-K, и 2G1 DLL3 CAR-T-клетки секретируют интерферон-гамма (IFNγ), фактор некроза опухоли альфа (TNF-α) и IL-2 при совместном культивировании с линией DLL3+ клеток DMS 273, после совместного культивирования DLL3 CAR-T-клеток с клетками гипофиза мыши не происходит секреции цитокинов. Таким образом, DLL3 CAR-T-клетки не были цитотоксичными в отношении клеток гипофиза in vitro.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> АЛЛОДЖЕН ТЕРАПЬЮТИКС, ИНК.
ПФАЙЗЕР ИНК.
<120> ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И СВЯЗЫВАЮЩИЕ АГЕНТЫ, НАЦЕЛЕННЫЕ
НА DLL3
<130> AT-019/03WO
<140>
<141>
<150> 62/969,976
<151> 2020-02-04
<150> 62/812,585
<151> 2019-03-01
<160> 696
<170> PatentIn версии 3.5
<210> 1
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 1
Asn Ser Ile Ser Asn Tyr Tyr Trp Ser
1 5
<210> 2
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 2
Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn
1 5 10
<210> 3
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 3
Cys Ala Arg Leu Phe Asn Trp Gly Phe Ala Phe Asp Ile Trp
1 5 10
<210> 4
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 4
Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala
1 5 10
<210> 5
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 5
Gly Ala Ser Thr Arg Ala Thr
1 5
<210> 6
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 6
Cys Gln Gln Tyr Asn Asn Trp Pro Leu Thr Phe
1 5 10
<210> 7
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 7
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Leu Phe Asn Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 8
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 8
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 9
<211> 245
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 9
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Leu Phe Asn Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln
130 135 140
Ser Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg
180 185 190
Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser Glu Asp Phe Ala Val Tyr
210 215 220
Tyr Cys Gln Gln Tyr Asn Asn Trp Pro Leu Thr Phe Gly Gly Gly Thr
225 230 235 240
Lys Val Glu Ile Lys
245
<210> 10
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 10
Gly Ser Ile Ser Ser Ser Tyr Trp Ser
1 5
<210> 11
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 11
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn
1 5 10
<210> 12
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 12
Cys Ala Arg Val Ala Pro Thr Gly Phe Trp Phe Asp Tyr Trp
1 5 10
<210> 13
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 13
Arg Ala Ser Gln Arg Val Ser Ser Arg Tyr Leu Ala
1 5 10
<210> 14
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 14
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 15
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 15
Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe
1 5 10
<210> 16
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 16
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Met Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Tyr Trp Ser Cys Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Leu Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Ala Pro Thr Gly Phe Trp Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 17
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 17
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Ser Arg
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Glu Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 18
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 18
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Met Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Tyr Trp Ser Cys Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Leu Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Ala Pro Thr Gly Phe Trp Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Arg Val Ser Ser Arg Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Glu Phe Ala Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 19
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 19
Phe Thr Phe Ser Ser His Asp Met His
1 5
<210> 20
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 20
Ser Ala Ile Gly Ile Ala Gly Asp Thr Tyr Tyr Ser
1 5 10
<210> 21
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 21
Cys Ala Arg Ala Asn Trp Gly Glu Gly Ala Phe Asp Ile Trp
1 5 10
<210> 22
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 22
Arg Ala Ser Gln Gly Ile Ser Asp Tyr Leu Ala
1 5 10
<210> 23
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 23
Ala Ala Ser Thr Leu Gln Ser
1 5
<210> 24
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 24
Cys Gln Lys Tyr Asn Ser Val Pro Leu Thr Phe
1 5 10
<210> 25
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 25
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser His
20 25 30
Asp Met His Trp Val Arg Gln Ala Thr Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Ile Ala Gly Asp Thr Tyr Tyr Ser Gly Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ala Asn Trp Gly Glu Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 26
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 26
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asp Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 27
<211> 245
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser His
20 25 30
Asp Met His Trp Val Arg Gln Ala Thr Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Ile Ala Gly Asp Thr Tyr Tyr Ser Gly Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ala Asn Trp Gly Glu Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
130 135 140
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Gly Ile Ser Asp Tyr Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ile Pro Lys Leu Leu Ile Tyr Ala Ala Ser Thr Leu
180 185 190
Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr
210 215 220
Tyr Cys Gln Lys Tyr Asn Ser Val Pro Leu Thr Phe Gly Gly Gly Thr
225 230 235 240
Lys Val Glu Ile Lys
245
<210> 28
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 28
Asp Ser Ile Ser Asn Tyr Tyr Trp Ser
1 5
<210> 29
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 29
Asp Ser Ile Ser Asn Tyr Tyr Trp Ser
1 5
<210> 30
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 30
Cys Ala Arg Val Phe Asn Trp Gly Phe Ala Phe Asp Ile Trp
1 5 10
<210> 31
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 31
Arg Ala Ser Gln Arg Ile Ser Arg Thr Tyr Leu Ala
1 5 10
<210> 32
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 32
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 33
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 33
Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe
1 5 10
<210> 34
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 34
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn His Asn Pro Ser Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ser Leu Asp Lys Ala Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Phe Asn Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 35
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 35
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Arg Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Thr
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn
100 105
<210> 36
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 36
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn His Asn Pro Ser Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ser Leu Asp Lys Ala Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Phe Asn Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Arg Ile Ser Arg Thr Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Asn
245
<210> 37
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 37
Asn Ser Ile Ser Asn Tyr Tyr Trp Ser
1 5
<210> 38
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 38
Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn
1 5 10
<210> 39
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 39
Cys Ala Arg Val Phe His Trp Gly Phe Ala Phe Asp Ile Trp
1 5 10
<210> 40
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 40
Arg Ala Ser Gln Arg Val Ser Asn Thr Tyr Leu Ala
1 5 10
<210> 41
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 41
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 42
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 42
Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe
1 5 10
<210> 43
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 43
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Gln Leu Ser Ser Val Thr Ala Ala Asp Ala Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Phe His Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 44
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 44
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Asn Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Asn Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 45
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 45
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Gln Leu Ser Ser Val Thr Ala Ala Asp Ala Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Phe His Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Arg Val Ser Asn Thr Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Asn Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 46
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 46
Val Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5
<210> 47
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 47
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn
1 5 10
<210> 48
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 48
Cys Ala Arg Leu Ser Asn Trp Gly Phe Ala Phe Asp Ile Trp
1 5 10
<210> 49
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 49
Arg Ala Ser Gln Thr Ile Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 50
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 50
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 51
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 51
Cys Gln Gln Tyr Gly Trp Ser Pro Ile Thr Phe
1 5 10
<210> 52
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 52
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asn Val Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Phe Cys Ala
85 90 95
Arg Leu Ser Asn Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Phe Ser Ser
115
<210> 53
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 53
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Thr Ile Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Trp Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 54
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 54
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asn Val Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Phe Cys Ala
85 90 95
Arg Leu Ser Asn Trp Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Phe Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Thr Ile Ser Ser Ser Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Glu Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Trp Ser Pro Ile Thr Phe Gly Gln Gly
225 230 235 240
Thr Arg Leu Glu Ile Lys
245
<210> 55
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 55
Phe Thr Phe Ser Ser Tyr Asp Met His
1 5
<210> 56
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 56
Ser Ala Ile Gly Pro Ala Gly Asp Thr Tyr Tyr Pro
1 5 10
<210> 57
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 57
Cys Ala Arg Ala Asp Pro Pro Tyr Tyr Tyr Tyr Gly Met Asp Val Trp
1 5 10 15
<210> 58
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 58
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Glu Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 59
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 59
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 60
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 60
Cys Met Gln Ala Leu Glu Ile Pro Leu Thr Phe
1 5 10
<210> 61
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 61
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Thr Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Pro Ala Gly Asp Thr Tyr Tyr Pro Gly Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ala Asp Pro Pro Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 62
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 62
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Glu Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Glu Ile Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 63
<211> 252
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 63
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Thr Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Pro Ala Gly Asp Thr Tyr Tyr Pro Gly Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ala Asp Pro Pro Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met
130 135 140
Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser
145 150 155 160
Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn Glu Tyr Asn
165 170 175
Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu
180 185 190
Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Lys Ile Ser Arg Val Glu
210 215 220
Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Glu Ile Pro
225 230 235 240
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
245 250
<210> 64
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 64
Phe Ser Leu Ser Thr Arg Gly Val Gly Val Gly
1 5 10
<210> 65
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 65
Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser
1 5 10
<210> 66
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 66
Cys Ala Arg Ser Asn Trp Gly Asn Trp Tyr Phe Ala Leu Trp
1 5 10
<210> 67
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 67
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
1 5 10
<210> 68
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 68
Asp Ala Phe Tyr Arg Ala Thr
1 5
<210> 69
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 69
Cys Gln His Arg Ser Asn Trp Pro Ile Thr Phe
1 5 10
<210> 70
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 70
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Arg
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Gln Thr Arg Leu Thr Ile Thr Lys Asp Thr Pro Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ser Asn Trp Gly Asn Trp Tyr Phe Ala Leu Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 71
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 71
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Phe Tyr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Arg Ser Asn Trp Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 72
<211> 247
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 72
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Arg
20 25 30
Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Gln Thr Arg Leu Thr Ile Thr Lys Asp Thr Pro Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ser Asn Trp Gly Asn Trp Tyr Phe Ala Leu Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Phe
180 185 190
Tyr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
210 215 220
Val Tyr Tyr Cys Gln His Arg Ser Asn Trp Pro Ile Thr Phe Gly Gln
225 230 235 240
Gly Thr Arg Leu Glu Ile Lys
245
<210> 73
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 73
Asp Ser Ile Ser Asn Tyr Tyr Trp Thr
1 5
<210> 74
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 74
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Ser Asn
1 5 10
<210> 75
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 75
Cys Ala Arg Val Phe Asn Arg Gly Phe Ala Phe Asp Ile Trp
1 5 10
<210> 76
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 76
Cys Ala Arg Val Phe Asn Arg Gly Phe Ala Phe Asp Ile Trp
1 5 10
<210> 77
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 77
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 78
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 78
Cys Gln Gln Tyr Asp Thr Ser Pro Leu Thr Phe
1 5 10
<210> 79
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 79
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Ser Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Val Ser Leu Asp Thr Ser Lys Ser Gln Phe Ser Leu
65 70 75 80
Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Phe Asn Arg Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 80
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 80
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Asn Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Ala Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 81
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Ser Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Val Ser Leu Asp Thr Ser Lys Ser Gln Phe Ser Leu
65 70 75 80
Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Phe Asn Arg Gly Phe Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Arg Ile Ser Asn Thr Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Ala
210 215 220
Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 82
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 82
Val Ser Leu Ser Thr Ser Gly Met Cys Val Ser
1 5 10
<210> 83
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 83
Gly Phe Ile Asp Trp Asp Asp Asp Lys Tyr Tyr Asn
1 5 10
<210> 84
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 84
Cys Ala Arg Ile Arg Gly Tyr Ser Gly Ser Tyr Asp Ala Phe Asp Ile
1 5 10 15
Trp
<210> 85
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 85
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn His Leu Asp
1 5 10 15
<210> 86
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 86
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 87
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 87
Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe
1 5 10
<210> 88
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 88
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Val Ser Leu Ser Thr Ser
20 25 30
Gly Met Cys Val Ser Trp Ile Arg Gln Pro Leu Gly Lys Ala Leu Glu
35 40 45
Trp Leu Gly Phe Ile Asp Trp Asp Asp Asp Lys Tyr Tyr Asn Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ile Arg Gly Tyr Ser Gly Ser Tyr Asp Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Val Val Ile Val Ser Ser
115 120
<210> 89
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 89
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn His Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 90
<211> 255
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 90
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Val Ser Leu Ser Thr Ser
20 25 30
Gly Met Cys Val Ser Trp Ile Arg Gln Pro Leu Gly Lys Ala Leu Glu
35 40 45
Trp Leu Gly Phe Ile Asp Trp Asp Asp Asp Lys Tyr Tyr Asn Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ile Arg Gly Tyr Ser Gly Ser Tyr Asp Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Val Val Ile Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
130 135 140
Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu
145 150 155 160
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn
165 170 175
Gly Tyr Asn His Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
180 185 190
Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro Asp
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
210 215 220
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys Met Gln Ala Leu
225 230 235 240
Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
245 250 255
<210> 91
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 91
Gly Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5
<210> 92
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 92
Gly Tyr Met Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn
1 5 10
<210> 93
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 93
Cys Ala Arg Val Gly Leu Thr Gly Phe Phe Phe Asp Tyr Trp
1 5 10
<210> 94
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 94
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly
1 5 10
<210> 95
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 95
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 96
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 96
Cys Leu Gln Asp Tyr Asn Tyr Pro Tyr Thr Phe
1 5 10
<210> 97
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 97
Gln Val Gln Leu Gln Val Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Met Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Thr Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Gly Leu Thr Gly Phe Phe Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 98
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 98
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 99
<211> 245
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 99
Gln Val Gln Leu Gln Val Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Met Tyr Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Thr Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Gly Leu Thr Gly Phe Phe Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr Gln
130 135 140
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu
180 185 190
Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Val Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
210 215 220
Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Tyr Thr Phe Gly Gln Gly Thr
225 230 235 240
Lys Leu Glu Ile Lys
245
<210> 100
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 100
Gly Ser Ser Ser Gly Asn Tyr Trp Ser
1 5
<210> 101
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 101
Gly Glu Ile Asn His Ser Gly Thr Thr Ser Tyr Asn
1 5 10
<210> 102
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 102
Cys Ala Arg Gly Glu Leu Gly Ile Ala Asp Ser Trp
1 5 10
<210> 103
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 103
Arg Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala
1 5 10
<210> 104
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 104
Lys Ala Ser Ser Leu Glu Ser
1 5
<210> 105
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 105
Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe
1 5 10
<210> 106
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 106
Gln Val Gln Leu Gln Gln Trp Gly Gly Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Ser Ser Gly Asn
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Arg Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Thr Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Leu Gly Ile Ala Asp Ser Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 107
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 107
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 108
<211> 242
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 108
Gln Val Gln Leu Gln Gln Trp Gly Gly Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Ser Ser Gly Asn
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Arg Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Thr Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Leu Gly Ile Ala Asp Ser Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
195 200 205
Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 109
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 109
Gly Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly
1 5 10
<210> 110
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 110
Gly Ser Ile Tyr Tyr Ser Gly Asn Ile Tyr His Asn
1 5 10
<210> 111
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 111
Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His Phe Asp Tyr Trp
1 5 10 15
<210> 112
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 112
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly
1 5 10
<210> 113
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 113
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 114
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 114
Cys Leu Gln Asp Tyr Asn Tyr Pro Leu Thr Phe
1 5 10
<210> 115
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 115
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn Ile Tyr His Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 116
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 116
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Leu
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 117
<211> 248
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 117
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn Ile Tyr His Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln
130 135 140
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
145 150 155 160
Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu Leu Ile Tyr Ala Ala
180 185 190
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Leu Thr Phe Gly
225 230 235 240
Pro Gly Thr Lys Val Asp Ile Lys
245
<210> 118
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 118
Gly Ser Phe Ser Gly Tyr Tyr Trp Ser
1 5
<210> 119
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 119
Gly Glu Ile Ile His Ser Gly Ser Ser Asn Tyr Asn
1 5 10
<210> 120
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 120
Cys Ser Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp
1 5 10 15
<210> 121
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 121
Arg Ala Ser Gln Gly Ile Arg Asp Asp Leu Gly
1 5 10
<210> 122
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 122
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 123
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 123
Cys Leu Gln Asp Tyr Asp Tyr Pro Leu Thr Phe
1 5 10
<210> 124
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 124
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Ile His Ser Gly Ser Ser Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ser
85 90 95
Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 125
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 125
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 126
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 126
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Ile His Ser Gly Ser Ser Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ser
85 90 95
Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Ala Ile
145 150 155 160
Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp Leu Gly Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser
180 185 190
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Arg Ser Asp Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 127
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 127
Gly Ser Ile Ser Ser Asn Asn Trp Trp Ser
1 5 10
<210> 128
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 128
Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr Lys
1 5 10
<210> 129
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 129
Cys Ala Arg Glu Ala Gly Gly Tyr Phe Asp Tyr Trp
1 5 10
<210> 130
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 130
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 131
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 131
Lys Ala Ser Ser Leu Glu Ser
1 5
<210> 132
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 132
Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe
1 5 10
<210> 133
<211> 117
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 133
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser Ser Asn
20 25 30
Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr Lys Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Asn Leu Ile Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Gly Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Ile Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 134
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 134
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Pro Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Ala Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 135
<211> 243
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 135
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser Ser Asn
20 25 30
Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr Lys Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Asn Leu Ile Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Gly Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Ile Leu
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
130 135 140
Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
145 150 155 160
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Lys Ala Pro Lys Leu Leu Ile Ser Lys Ala Ser Ser Leu Glu
180 185 190
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Pro Glu Phe
195 200 205
Thr Leu Thr Ile Ser Ser Leu Gln Pro Ala Asp Phe Ala Thr Tyr Tyr
210 215 220
Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 136
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 136
Gly Ser Phe Ser Gly Tyr Tyr Trp Thr
1 5
<210> 137
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 137
Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr Asn
1 5 10
<210> 138
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 138
Cys Ala Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp
1 5 10 15
<210> 139
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 139
Arg Ala Ser Gln Gly Ile Arg Asp Asp Leu Gly
1 5 10
<210> 140
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 140
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 141
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 141
Cys Leu Gln Asp Tyr Asp Tyr Pro Leu Thr Phe
1 5 10
<210> 142
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 142
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 143
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 143
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 144
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 144
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Ala Ile
145 150 155 160
Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp Leu Gly Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser
180 185 190
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Asp Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 145
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 145
Gly Ser Phe Ser Gly Tyr Tyr Trp Ser
1 5
<210> 146
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 146
Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr Asn
1 5 10
<210> 147
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 147
Cys Ala Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp
1 5 10 15
<210> 148
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 148
Arg Ala Ser Gln Gly Ile Arg Asp Asp Leu Gly
1 5 10
<210> 149
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 149
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 150
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 150
Cys Leu Gln Asp Tyr Asp Tyr Pro Leu Thr Phe
1 5 10
<210> 151
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 151
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 152
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 152
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ala Leu Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 153
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 153
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Ala Leu
145 150 155 160
Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp Leu Gly Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser
180 185 190
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Asp Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 154
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 154
Gly Ser Phe Ser Ala Tyr Tyr Trp Asn
1 5
<210> 155
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 155
Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn
1 5 10
<210> 156
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 156
Cys Ala Arg Gly Leu Asp Ser Ser Gly Trp Tyr Pro Phe Asp Tyr Trp
1 5 10 15
<210> 157
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 157
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 158
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 158
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 159
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 159
Cys Gln Gln Ala Asp Ser Phe Pro Phe Thr Phe
1 5 10
<210> 160
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 160
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Ala Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Thr Ser Leu Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Leu Asp Ser Ser Gly Trp Tyr Pro Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 161
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 161
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asp Ser Phe Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 162
<211> 247
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 162
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Ala Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Thr Ser Leu Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Leu Asp Ser Ser Gly Trp Tyr Pro Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
130 135 140
Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser
180 185 190
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Ala Asp Ser Phe Pro Phe Thr Phe Gly Pro
225 230 235 240
Gly Thr Lys Val Asp Ile Lys
245
<210> 163
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 163
Gly Ser Phe Ser Gly Asp Tyr Trp Ser
1 5
<210> 164
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 164
Gly Glu Ile Asn His Ser Gly Ile Thr Ser Phe Asn
1 5 10
<210> 165
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 165
Cys Ala Arg Gly Glu Leu Gly Ile Pro Asp Asn Trp
1 5 10
<210> 166
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 166
Arg Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala
1 5 10
<210> 167
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 167
Lys Ala Ser Ser Leu Glu Ser
1 5
<210> 168
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 168
Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe
1 5 10
<210> 169
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 169
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Phe Gly Gly Ser Phe Ser Gly Asp
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Ile Thr Ser Phe Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Leu Gly Ile Pro Asp Asn Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 170
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 170
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 171
<211> 242
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 171
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Phe Gly Gly Ser Phe Ser Gly Asp
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Ser Gly Ile Thr Ser Phe Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Leu Gly Ile Pro Asp Asn Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
195 200 205
Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 172
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 172
Asp Ser Ile Ser Ser Ser Asn Trp Trp Ser
1 5 10
<210> 173
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 173
Gly Glu Val Phe His Ser Gly Ser Thr Asn Tyr Asn
1 5 10
<210> 174
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 174
Cys Ala Arg Ala Ala Val Ala Gly Ala Leu Asp Tyr Trp
1 5 10
<210> 175
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 175
Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser Asn Asn Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 176
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 176
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 177
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 177
Cys Gln Gln Tyr Tyr Gly Thr Ser Trp Thr Phe
1 5 10
<210> 178
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 178
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Val Val Phe Gly Asp Ser Ile Ser Ser Ser
20 25 30
Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Val Phe His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ala Val Ala Gly Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 179
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 179
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Asn Leu Leu Val Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ala Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Gly Thr Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 180
<211> 251
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 180
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Val Val Phe Gly Asp Ser Ile Ser Ser Ser
20 25 30
Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Val Phe His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ala Val Ala Gly Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln
130 135 140
Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn
145 150 155 160
Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser Asn Asn Lys Asn Tyr
165 170 175
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Asn Leu Leu Val
180 185 190
Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ala Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
210 215 220
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr Tyr Gly Thr Ser Trp
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
245 250
<210> 181
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 181
Phe Ser Leu Ser Thr Ser Gly Leu Gly Val Gly
1 5 10
<210> 182
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 182
Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser
1 5 10
<210> 183
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 183
Cys Val His Arg Arg Ile Ala Ala Pro Gly Ser Val Tyr Trp
1 5 10
<210> 184
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 184
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 185
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 185
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 186
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 186
Cys His Gln Ala Asn Ser Phe Pro Phe Thr Phe
1 5 10
<210> 187
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 187
Gln Ile Thr Leu Arg Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Leu Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Glu Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Ser Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Ile Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Val His Arg Arg Ile Ala Ala Pro Gly Ser Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 188
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 188
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys His Gln Ala Asn Ser Phe Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 189
<211> 247
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 189
Gln Ile Thr Leu Arg Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Leu Gly Val Gly Trp Ile Arg Gln Pro Pro Gly Glu Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys Arg Tyr Ser Pro Ser
50 55 60
Leu Lys Ser Arg Leu Ser Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Ile Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Val His Arg Arg Ile Ala Ala Pro Gly Ser Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
130 135 140
Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Ser Ala Ala Ser
180 185 190
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys His Gln Ala Asn Ser Phe Pro Phe Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 190
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 190
Tyr Thr Leu Thr Glu Leu Ser Met His
1 5
<210> 191
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 191
Gly Gly Phe Asp Pro Glu Asp Gly Lys Thr Ile Tyr Ala
1 5 10
<210> 192
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 192
Cys Ala Thr Leu Leu Arg Gly Leu Asp Ala Phe Asp Val Trp
1 5 10
<210> 193
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 193
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly
1 5 10
<210> 194
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 194
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 195
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 195
Cys Leu Gln His Asn Ser Tyr Pro Arg Thr Phe
1 5 10
<210> 196
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 196
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Tyr Thr Leu Thr Glu Leu
20 25 30
Ser Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Pro Glu Gly Met
35 40 45
Gly Gly Phe Asp Pro Glu Asp Gly Lys Thr Ile Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser Ala Asp Thr Ala Tyr
65 70 75 80
Met Glu Leu Asn Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Leu Leu Arg Gly Leu Asp Ala Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser
115
<210> 197
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 197
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 198
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 198
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Tyr Thr Leu Thr Glu Leu
20 25 30
Ser Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Pro Glu Gly Met
35 40 45
Gly Gly Phe Asp Pro Glu Asp Gly Lys Thr Ile Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser Ala Asp Thr Ala Tyr
65 70 75 80
Met Glu Leu Asn Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Leu Leu Arg Gly Leu Asp Ala Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser
180 185 190
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Glu Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Arg Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 199
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 199
Gly Ser Phe Ser Gly Tyr Tyr Trp Arg
1 5
<210> 200
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 200
Gly Glu Ile Ser His Ser Gly Ser Thr Asn Tyr Asn
1 5 10
<210> 201
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 201
Cys Ala Val Arg Gly Tyr Ser Tyr Gly Tyr Pro Leu Phe Asp Tyr Trp
1 5 10 15
<210> 202
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 202
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly
1 5 10
<210> 203
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 203
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 204
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 204
Cys Leu Gln Tyr Asn Ser Tyr Pro Arg Thr Phe
1 5 10
<210> 205
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 205
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Arg Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Ser His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Val Arg Gly Tyr Ser Tyr Gly Tyr Pro Leu Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 206
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 206
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Leu Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asn Ser Tyr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 207
<211> 247
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 207
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
20 25 30
Tyr Trp Arg Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Ser His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Val Arg Gly Tyr Ser Tyr Gly Tyr Pro Leu Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
130 135 140
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly Trp Tyr
165 170 175
Gln Gln Lys Leu Gly Lys Ala Pro Lys Arg Leu Ile Tyr Ala Ala Ser
180 185 190
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys Leu Gln Tyr Asn Ser Tyr Pro Arg Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Val Glu Ile Lys
245
<210> 208
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 208
Asp Ser Ile Ser Ser Asn Trp Trp Thr
1 5
<210> 209
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 209
Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr Asn
1 5 10
<210> 210
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 210
Cys Ala Arg Asp Gly Gly Gly Thr Leu Asp Tyr Trp
1 5 10
<210> 211
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 211
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 212
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 212
Lys Ala Ser Thr Leu Glu Ser
1 5
<210> 213
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 213
Cys Gln Gln Tyr Asn Gly Tyr Ser Thr Phe
1 5 10
<210> 214
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 214
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Asp Ser Ile Ser Ser Asn
20 25 30
Trp Trp Thr Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Met Ser Val Asp Lys Ser Glu Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Phe Tyr Cys Ala
85 90 95
Arg Asp Gly Gly Gly Thr Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 215
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 215
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Gly Tyr Ser Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 216
<211> 242
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 216
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Asp Ser Ile Ser Ser Asn
20 25 30
Trp Trp Thr Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Met Ser Val Asp Lys Ser Glu Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Phe Tyr Cys Ala
85 90 95
Arg Asp Gly Gly Gly Thr Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Thr Leu Glu Ser
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
195 200 205
Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Tyr Asn Gly Tyr Ser Thr Phe Gly Gln Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 217
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 217
Gly Thr Phe Thr Asn Tyr Cys Ile Ser
1 5
<210> 218
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 218
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala
1 5 10
<210> 219
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 219
Cys Ala Arg Asp Asn Gly Asp Arg Tyr Tyr Tyr Asp Met Asp Val Trp
1 5 10 15
<210> 220
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 220
Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser
1 5 10
<210> 221
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 221
Asp Asn Asn Lys Arg Pro Ser
1 5
<210> 222
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 222
Cys Gly Thr Trp Asp Ser Ser Leu Ser Ala Val Val Phe
1 5 10
<210> 223
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 223
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Thr Asn Tyr
20 25 30
Cys Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala Gln Thr Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asn Gly Asp Arg Tyr Tyr Tyr Asp Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 224
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 224
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 225
<211> 251
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 225
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Thr Asn Tyr
20 25 30
Cys Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala Gln Thr Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asn Gly Asp Arg Tyr Tyr Tyr Asp Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Val
130 135 140
Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln Lys Val Thr
145 150 155 160
Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser
165 170 175
Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Asp
180 185 190
Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Lys
195 200 205
Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln Thr Gly Asp
210 215 220
Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu Ser Ala Val
225 230 235 240
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 226
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 226
Gly Thr Phe Ser Thr Tyr Ser Ile Ser
1 5
<210> 227
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 227
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala
1 5 10
<210> 228
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 228
Cys Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr Tyr Gly Met Asp
1 5 10 15
Val Trp
<210> 229
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 229
Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser
1 5 10
<210> 230
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 230
Asp Asn Asn Lys Arg Pro Ser
1 5
<210> 231
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 231
Cys Gly Thr Trp Asp Ser Ser Leu Ser Ala Val Val Phe
1 5 10
<210> 232
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 232
Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Thr Tyr
20 25 30
Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr Tyr Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 233
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 233
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Phe
50 55 60
Gly Ser Lys Phe Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 234
<211> 253
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 234
Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Thr Tyr
20 25 30
Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr Tyr Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln Lys
145 150 155 160
Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr
165 170 175
Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile
180 185 190
Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Phe Gly
195 200 205
Ser Lys Phe Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln Thr
210 215 220
Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu Ser
225 230 235 240
Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 235
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 235
Asp Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5
<210> 236
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 236
Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Asn Tyr Asn
1 5 10
<210> 237
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 237
Cys Ala Arg Leu Ser Val Ala Gly Phe Tyr Phe Asp Tyr Trp
1 5 10
<210> 238
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 238
Arg Ala Ser Gln Ser Val Thr Arg Ser Tyr Leu Ala
1 5 10
<210> 239
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 239
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 240
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 240
Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe
1 5 10
<210> 241
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 241
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Asn Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Gly Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Leu Ser Val Ala Gly Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 242
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 242
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Arg Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Asp Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 243
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 243
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Asn Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Gly Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Leu Ser Val Ala Gly Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Ser Val Thr Arg Ser Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Asp Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp Phe Ala Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 244
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 244
Asp Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5
<210> 245
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 245
Ser Tyr Ile Tyr Tyr Ser Gly Ile Ser Asn Tyr Asn
1 5 10
<210> 246
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 246
Cys Ala Arg Ile Ser Val Ala Gly Phe Phe Phe Asp Asn Trp
1 5 10
<210> 247
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 247
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 248
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 248
Gly Ala Ser Ser Arg Ala Ala
1 5
<210> 249
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 249
Cys Gln Gln Tyr Gly Ile Ser Pro Leu Thr Phe
1 5 10
<210> 250
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 250
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Tyr Tyr Ser Gly Ile Ser Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ile Ser Val Ala Gly Phe Phe Phe Asp Asn Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 251
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 251
Glu Ile Met Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Ala Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Ala
65 70 75 80
Pro Glu Asp Phe Val Val Tyr Tyr Cys Gln Gln Tyr Gly Ile Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 252
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 252
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Tyr Tyr Ser Gly Ile Ser Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ile Ser Val Ala Gly Phe Phe Phe Asp Asn Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Met Leu Thr Gln
130 135 140
Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Ala Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Ala Pro Glu Asp Phe Val Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Ile Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 253
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 253
Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn
1 5 10
<210> 254
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 254
Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asp Asp Tyr Ala
1 5 10
<210> 255
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 255
Cys Ala Gly Gly Gly Leu Val Gly Ala Pro Asp Gly Phe Asp Val Trp
1 5 10 15
<210> 256
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 256
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp Pro Val Asn
1 5 10
<210> 257
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 257
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 258
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 258
Cys Ser Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe
1 5 10
<210> 259
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 259
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asp Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
His Leu Ser Leu His Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 260
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 260
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
20 25 30
Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 261
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 261
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asp Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
His Leu Ser Leu His Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
165 170 175
Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala Trp Asp Asp Ser Leu
225 230 235 240
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 262
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 262
Tyr Thr Phe Thr Gly Tyr Ser Ile His
1 5
<210> 263
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 263
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Phe Tyr Ala
1 5 10
<210> 264
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 264
Cys Ala Arg Asp Gly Trp Gly Asp Tyr Tyr Tyr Tyr Gly Leu Asp Val
1 5 10 15
Trp
<210> 265
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 265
Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu Ala
1 5 10
<210> 266
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 266
Thr Ala Ser Ser Leu Gln Gly
1 5
<210> 267
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 267
Cys Gln Gln Ala Asn Val Phe Pro Tyr Thr Phe
1 5 10
<210> 268
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 268
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Ser Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Phe Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Trp Gly Asp Tyr Tyr Tyr Tyr Gly Leu Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Leu
115 120
<210> 269
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 269
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Thr Ala Ser Ser Leu Gln Gly Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Leu Ala Thr Tyr Ser Cys Gln Gln Ala Asn Val Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 270
<211> 249
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 270
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Ser Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Phe Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Trp Gly Asp Tyr Tyr Tyr Tyr Gly Leu Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Leu Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Thr
180 185 190
Ala Ser Ser Leu Gln Gly Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Leu Ala Thr Tyr Ser Cys Gln Gln Ala Asn Val Phe Pro Tyr Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 271
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 271
Phe Thr Phe Ser Ser Tyr Ala Met Asn
1 5
<210> 272
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 272
Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala
1 5 10
<210> 273
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 273
Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr Gly Gly Asp Tyr
1 5 10 15
Trp
<210> 274
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 274
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala
1 5 10
<210> 275
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 275
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 276
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 276
Cys Leu Gln His Asp Ser Phe Pro Leu Thr Phe
1 5 10
<210> 277
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 277
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Phe Tyr Cys
85 90 95
Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr Gly Gly Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 278
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 278
Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp Ser Phe Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 279
<211> 250
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 279
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Phe Tyr Cys
85 90 95
Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr Gly Gly Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
130 135 140
Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp
145 150 155 160
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu
165 170 175
Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr
180 185 190
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
195 200 205
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
210 215 220
Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp Ser Phe Pro Leu Thr
225 230 235 240
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
245 250
<210> 280
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 280
Asp Ser Ile Ser Asn Tyr Tyr Trp Ser
1 5
<210> 281
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 281
Ser Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Tyr Asn
1 5 10
<210> 282
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 282
Cys Ala Arg Ile Thr Val Thr Gly Phe Tyr Phe Asp Tyr Trp
1 5 10
<210> 283
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 283
Arg Ala Ser Gln Ser Ile Ser Arg Ser Tyr Leu Ala
1 5 10
<210> 284
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 284
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 285
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 285
Cys Gln Gln Tyr Asp Thr Ser Pro Leu Thr Phe
1 5 10
<210> 286
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 286
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ile Thr Val Thr Gly Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 287
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 287
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Arg Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg His Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 288
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 288
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp Ser Ile Ser Asn Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ile Thr Val Thr Gly Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Ser Ile Ser Arg Ser Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg His Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Ile Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 289
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 289
Asp Ser Val Ser Ser Asn Ser Val Val Trp Asn
1 5 10
<210> 290
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 290
Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asp Asp Tyr Ala
1 5 10
<210> 291
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 291
Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp Ile Trp
1 5 10 15
<210> 292
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 292
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp Pro Val Ser
1 5 10
<210> 293
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 293
Thr Asn Asn Gln Arg Pro Ser
1 5
<210> 294
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 294
Cys Ala Ala Trp Asp Asp Ser Leu Asn Gly His Val Phe
1 5 10
<210> 295
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 295
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Val Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asp Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr His Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 296
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 296
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
20 25 30
Pro Val Ser Trp Tyr Gln Gln Phe Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly His Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 297
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 297
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Val Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asp Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr His Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
165 170 175
Pro Val Ser Trp Tyr Gln Gln Phe Pro Gly Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
225 230 235 240
Asn Gly His Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 298
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 298
Asp Ser Val Ser Ser Asn Ser Ala Val Trp Asn
1 5 10
<210> 299
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 299
Gly Trp Thr Tyr Tyr Arg Ser Lys Tyr Tyr Asn Asp Tyr Ala
1 5 10
<210> 300
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 300
Cys Thr Arg Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp Ile Trp
1 5 10 15
<210> 301
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 301
Ser Gly Ser Asn Ser Asn Ile Gly Ser Asn Pro Ile Asn
1 5 10
<210> 302
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 302
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 303
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 303
Cys Ala Ala Trp Asp Asp Ser Leu Asn Gly His Val Phe
1 5 10
<210> 304
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 304
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Tyr Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Leu Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Leu Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Thr Arg Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 305
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 305
Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Asn Ser Asn Ile Gly Ser Asn
20 25 30
Pro Ile Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly His Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 306
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 306
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Tyr Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Leu Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Leu Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Thr Arg Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Arg Val Thr Ile Ser Cys Ser Gly Ser Asn Ser Asn Ile Gly Ser Asn
165 170 175
Pro Ile Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
225 230 235 240
Asn Gly His Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 307
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 307
Gly Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5
<210> 308
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 308
Gly Tyr Val Tyr Tyr Ser Asp Ile Thr Asn Tyr Asn
1 5 10
<210> 309
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 309
Cys Ala Arg Ile Gly Val Ala Gly Phe Tyr Phe Asp Tyr Trp
1 5 10
<210> 310
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 310
Arg Ala Ser Gln Ser Val Ser Arg Arg Tyr Leu Ala
1 5 10
<210> 311
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 311
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 312
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 312
Cys Gln Gln Tyr Gly Thr Ser Pro Ile Thr Phe
1 5 10
<210> 313
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 313
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Val Tyr Tyr Ser Asp Ile Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Phe Tyr Phe Cys Ala
85 90 95
Arg Ile Gly Val Ala Gly Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 314
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 314
Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Arg
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Glu Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 315
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 315
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Val Tyr Tyr Ser Asp Ile Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Phe Tyr Phe Cys Ala
85 90 95
Arg Ile Gly Val Ala Gly Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Ser Val Ser Arg Arg Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Glu Val
210 215 220
Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Ile Thr Phe Gly Gln Gly
225 230 235 240
Thr Arg Leu Glu Ile Lys
245
<210> 316
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 316
Asp Ser Val Ser Ser Asn Ser Ala Val Trp Asn
1 5 10
<210> 317
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 317
Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
1 5 10
<210> 318
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 318
Phe Thr Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp Ile Trp
1 5 10 15
<210> 319
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 319
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp Pro Ile Asn
1 5 10
<210> 320
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 320
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 321
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 321
Cys Ala Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe
1 5 10
<210> 322
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 322
Gln Ile Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Lys Pro Asp Thr Ala Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Phe Thr Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 323
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 323
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
20 25 30
Pro Ile Asn Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 324
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 324
Gln Ile Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Lys Pro Asp Thr Ala Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Phe Thr Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
165 170 175
Pro Ile Asn Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
225 230 235 240
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 325
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 325
Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn
1 5 10
<210> 326
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 326
Gly Arg Thr Tyr Tyr Arg Ser Glu Trp Tyr Asn Asp Tyr Ala
1 5 10
<210> 327
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 327
Cys Ala Gly Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp Val Trp
1 5 10 15
<210> 328
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 328
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp Pro Val Ile
1 5 10
<210> 329
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 329
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 330
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 330
Cys Ala Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe
1 5 10
<210> 331
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 331
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Glu Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
His Leu Ser Leu His Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Gly Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 332
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 332
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
20 25 30
Pro Val Ile Trp Tyr Gln Gln Leu Pro Arg Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 333
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 333
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Glu Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
His Leu Ser Leu His Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Gly Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asp
165 170 175
Pro Val Ile Trp Tyr Gln Gln Leu Pro Arg Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
225 230 235 240
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 334
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 334
Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn
1 5 10
<210> 335
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 335
Ala Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Glu
1 5 10
<210> 336
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 336
Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp Ile Trp
1 5 10 15
<210> 337
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 337
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Pro Val Asn
1 5 10
<210> 338
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 338
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 339
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 339
Cys Ser Ala Trp Asp Asp Trp Leu Asn Gly Tyr Val Phe
1 5 10
<210> 340
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 340
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Thr Gly Leu Glu
35 40 45
Trp Leu Ala Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Glu
50 55 60
Val Ser Val Lys Ser Gln Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 341
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 341
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Gly Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Asp Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala Trp Asp Asp Trp Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 342
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 342
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Thr Gly Leu Glu
35 40 45
Trp Leu Ala Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Glu
50 55 60
Val Ser Val Lys Ser Gln Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Gly Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
165 170 175
Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Asp Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala Trp Asp Asp Trp Leu
225 230 235 240
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 343
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 343
Asp Ser Ile Asn Asn Tyr Phe Trp Ser
1 5
<210> 344
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 344
Gly Tyr Phe Tyr His Arg Gly Gly Asn Asn Tyr Asn
1 5 10
<210> 345
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 345
Cys Ala Arg Leu Ala Leu Ala Gly Phe Phe Phe Asp Tyr Trp
1 5 10
<210> 346
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 346
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 347
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 347
Lys Ala Ser Ser Leu Glu Ser
1 5
<210> 348
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 348
Cys Gln Gln Tyr Asn Ser Tyr Ser Arg Thr Phe
1 5 10
<210> 349
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 349
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Asn Asn Tyr
20 25 30
Phe Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Phe Tyr His Arg Gly Gly Asn Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ser Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Leu Ala Leu Ala Gly Phe Phe Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 350
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 350
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 351
<211> 245
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 351
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Asn Asn Tyr
20 25 30
Phe Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Phe Tyr His Arg Gly Gly Asn Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ser Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Leu Ala Leu Ala Gly Phe Phe Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
130 135 140
Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser Leu
180 185 190
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr
210 215 220
Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Arg Thr Phe Gly Gln Gly Thr
225 230 235 240
Lys Val Glu Ile Lys
245
<210> 352
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 352
Gly Thr Phe Ser Thr Tyr Ser Ile Ser
1 5
<210> 353
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 353
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala
1 5 10
<210> 354
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 354
Cys Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr Tyr Gly Met Asp
1 5 10 15
Val Trp
<210> 355
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 355
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr
1 5 10
<210> 356
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 356
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 357
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 357
Cys Ala Ala Trp Asp Asp Ser Leu Ser Gly Trp Val Phe
1 5 10
<210> 358
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 358
Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Thr Tyr
20 25 30
Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr Tyr Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 359
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 359
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Ser Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 360
<211> 253
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 360
Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Thr Tyr
20 25 30
Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr Tyr Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg
145 150 155 160
Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr
165 170 175
Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile
180 185 190
Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg Ser
210 215 220
Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu Ser
225 230 235 240
Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 361
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 361
Phe Thr Phe Ser Ser Tyr Ser Met Asn
1 5
<210> 362
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 362
Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala
1 5 10
<210> 363
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 363
Cys Ala Arg Asp Lys Glu Arg Arg Tyr Tyr Tyr Tyr Gly Met Asp Val
1 5 10 15
Trp
<210> 364
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 364
Arg Ala Ser Gln Ser Val Ser Arg Arg Tyr Leu Ala
1 5 10
<210> 365
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 365
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 366
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 366
Cys Gln Gln Phe Gly Thr Ser Pro Ile Thr Phe
1 5 10
<210> 367
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 367
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Lys Glu Arg Arg Tyr Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 368
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 368
Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Arg
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Thr Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 369
<211> 250
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 369
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Lys Glu Arg Arg Tyr Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Arg Tyr Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
180 185 190
Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
210 215 220
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly Thr Ser Pro Ile Thr
225 230 235 240
Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
245 250
<210> 370
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 370
Asp Ser Val Ser Ser Asn Ser Ala Ile Trp Asn
1 5 10
<210> 371
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 371
Gly Gly Thr Tyr Tyr Arg Ser Met Trp Tyr Asn Asp Tyr Ala
1 5 10
<210> 372
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 372
Cys Ser Arg Gly Gly Ile Val Gly Val Pro Asp Ala Phe Asp Ile Trp
1 5 10 15
<210> 373
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 373
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Thr Ala Asn
1 5 10
<210> 374
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 374
Arg Asn Asn Gln Arg Pro Ser
1 5
<210> 375
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 375
Cys Ala Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe
1 5 10
<210> 376
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 376
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Ala Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ile Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Gly Thr Tyr Tyr Arg Ser Met Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Leu Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ser Arg Gly Gly Ile Val Gly Val Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 377
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 377
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Ala Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 378
<211> 254
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 378
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Ala Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ile Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Gly Thr Tyr Tyr Arg Ser Met Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Leu Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ser Arg Gly Gly Ile Val Gly Val Pro Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
145 150 155 160
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
165 170 175
Thr Ala Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Arg Leu Leu
180 185 190
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
210 215 220
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
225 230 235 240
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 379
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 379
Gly Ser Ile Ser Ser Tyr Tyr Trp Thr
1 5
<210> 380
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 380
Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn Tyr Asn
1 5 10
<210> 381
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 381
Cys Ala Arg Ile Ser Glu Lys Ser Phe Tyr Phe Asp Tyr Trp
1 5 10
<210> 382
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 382
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr
1 5 10
<210> 383
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 383
Ser Asn Asn Gln Arg Pro Ser
1 5
<210> 384
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 384
Cys Ala Pro Trp Asp Asp Ser Leu Ser Gly Arg Val Phe
1 5 10
<210> 385
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 385
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Asn Val Ser Asp Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Met Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ile Ser Glu Lys Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 386
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 386
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Pro Trp Asp Asp Ser Leu
85 90 95
Ser Gly Arg Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 387
<211> 248
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 387
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Asn Val Ser Asp Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Met Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ile Ser Glu Lys Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln
130 135 140
Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys
145 150 155 160
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr Trp Tyr Gln
165 170 175
Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln
180 185 190
Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr
195 200 205
Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp
210 215 220
Tyr Tyr Cys Ala Pro Trp Asp Asp Ser Leu Ser Gly Arg Val Phe Gly
225 230 235 240
Gly Gly Thr Lys Leu Thr Val Leu
245
<210> 388
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 388
Tyr Thr Phe Thr Ser Tyr Tyr Ile His
1 5
<210> 389
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 389
Gly Val Ile Val Pro Ser Gly Gly Ser Ile Ser Tyr Ala
1 5 10
<210> 390
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 390
Cys Ala Arg Asp Arg Tyr Tyr Gly Asp Tyr Tyr Tyr Gly Leu Asp Val
1 5 10 15
Trp
<210> 391
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 391
Arg Ala Ser Gln Gly Ile Asn Asn Phe Leu Ala
1 5 10
<210> 392
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 392
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 393
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 393
Cys Gln His Tyr Asn Ser Tyr Pro Ile Thr Phe
1 5 10
<210> 394
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 394
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Val Ile Val Pro Ser Gly Gly Ser Ile Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Ile Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Tyr Tyr Gly Asp Tyr Tyr Tyr Gly Leu Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 395
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 395
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Asn Phe
20 25 30
Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Lys Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Asn Ser Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 396
<211> 249
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 396
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Val Ile Val Pro Ser Gly Gly Ser Ile Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Ile Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Tyr Tyr Gly Asp Tyr Tyr Tyr Gly Leu Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Asn Phe Leu Ala
165 170 175
Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile Tyr Ala
180 185 190
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Lys Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln His Tyr Asn Ser Tyr Pro Ile Thr Phe
225 230 235 240
Gly Gln Gly Thr Arg Leu Glu Ile Lys
245
<210> 397
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 397
Gly Ser Ile Ser His Tyr Tyr Trp Thr
1 5
<210> 398
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 398
Gly Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Phe Ser
1 5 10
<210> 399
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 399
Cys Ala Gly Ile Ser Leu Ala Gly Phe Tyr Phe Asp Tyr Trp
1 5 10
<210> 400
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 400
Arg Ala Ser Gln Ser Val Ser Arg Ser Tyr Leu Ala
1 5 10
<210> 401
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 401
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 402
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 402
Cys Gln Gln Tyr Ser Ile Ser Pro Leu Thr Phe
1 5 10
<210> 403
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 403
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser His Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Phe Ser Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Ser Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Gly Ile Ser Leu Ala Gly Phe Tyr Phe Asp Tyr Trp Val Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 404
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 404
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Phe Tyr Cys Gln Gln Tyr Ser Ile Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 405
<211> 246
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 405
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser His Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Phe Ser Pro Ser Leu Lys
50 55 60
Ser Arg Val Ser Ile Ser Val Asp Ser Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Gly Ile Ser Leu Ala Gly Phe Tyr Phe Asp Tyr Trp Val Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
130 135 140
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
145 150 155 160
Cys Arg Ala Ser Gln Ser Val Ser Arg Ser Tyr Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
180 185 190
Arg Ala Thr Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
210 215 220
Phe Tyr Cys Gln Gln Tyr Ser Ile Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 406
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 406
Val Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5
<210> 407
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 407
Ala Tyr Ile Tyr Tyr Ser Gly Asn Thr Asn Tyr Ser
1 5 10
<210> 408
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 408
Cys Thr Arg Gly Gly Ser Gly Thr Ile Asp Val Phe Asp Ile Trp
1 5 10 15
<210> 409
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 409
Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser
1 5 10
<210> 410
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 410
Asp Asn Asn Lys Arg Pro Ser
1 5
<210> 411
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 411
Cys Glu Thr Trp Asp Ser Ser Leu Ser Ala Val Val Phe
1 5 10
<210> 412
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 412
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Tyr Ser Gly Asn Thr Asn Tyr Ser Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asp Gln Leu Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Arg Gly Gly Ser Gly Thr Ile Asp Val Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Ala Val Ser Ser
115
<210> 413
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 413
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Glu Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 414
<211> 249
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 414
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Tyr Ser Gly Asn Thr Asn Tyr Ser Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asp Gln Leu Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Arg Gly Gly Ser Gly Thr Ile Asp Val Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Ala Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Val Leu Thr
130 135 140
Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln Lys Val Thr Ile Ser
145 150 155 160
Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser Trp Tyr
165 170 175
Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Asp Asn Asn
180 185 190
Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly
195 200 205
Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln Thr Gly Asp Glu Ala
210 215 220
Asp Tyr Tyr Cys Glu Thr Trp Asp Ser Ser Leu Ser Ala Val Val Phe
225 230 235 240
Gly Gly Gly Thr Lys Leu Thr Val Leu
245
<210> 415
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 415
Asp Asn Val Ser Thr Asn Ser Ala Ala Trp Asn
1 5 10
<210> 416
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 416
Gly Trp Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
1 5 10
<210> 417
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 417
Cys Ala Arg Trp Val Asn Arg Asp Val Phe Asp Ile Trp
1 5 10
<210> 418
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 418
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Leu Val Ser
1 5 10
<210> 419
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 419
Glu Gly Ser Lys Arg Pro Ser
1 5
<210> 420
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 420
Cys Cys Ser Tyr Ala Gly Ser Ser Thr Trp Val Phe
1 5 10
<210> 421
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 421
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Asn Val Ser Thr Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Leu Lys Ser Arg Ile Asn Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Trp Val Asn Arg Asp Val Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 422
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 422
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Leu Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Gly Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Cys Ser Tyr Ala Gly Ser
85 90 95
Ser Thr Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 423
<211> 251
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 423
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Asn Val Ser Thr Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Leu Lys Ser Arg Ile Asn Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Trp Val Asn Arg Asp Val Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Ala
130 135 140
Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln Ser Ile Thr
145 150 155 160
Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Leu Val
165 170 175
Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu Met Ile Tyr
180 185 190
Glu Gly Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe Ser Gly Ser
195 200 205
Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu Gln Ala Glu
210 215 220
Asp Glu Ala Asp Tyr Tyr Cys Cys Ser Tyr Ala Gly Ser Ser Thr Trp
225 230 235 240
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 424
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 424
Phe Thr Phe Ser Ser Tyr Gly Met His
1 5
<210> 425
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 425
Ala Val Ile Ser Tyr Asp Gly Asn Ser Asn Tyr Tyr Ala
1 5 10
<210> 426
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 426
Cys Ala Arg Asp Gly Ala Thr Val Thr Ser Tyr Tyr Tyr Tyr Gly Met
1 5 10 15
Asp Val Trp
<210> 427
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 427
Arg Ala Ser Gln Ser Val Ser Arg Thr Tyr Leu Ala
1 5 10
<210> 428
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 428
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 429
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 429
Cys Gln Gln Tyr Gly Thr Ser Pro Ile Thr Phe
1 5 10
<210> 430
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 430
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Asn Ser Asn Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ala Thr Val Thr Ser Tyr Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 431
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 431
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Thr
20 25 30
Tyr Leu Ala Trp Tyr His Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 432
<211> 252
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 432
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Asn Ser Asn Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ala Thr Val Thr Ser Tyr Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
145 150 155 160
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Thr
165 170 175
Tyr Leu Ala Trp Tyr His Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
180 185 190
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
210 215 220
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
225 230 235 240
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
245 250
<210> 433
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 433
Asp Ser Val Ser Ser Asn Ser Ala Val Trp Asn
1 5 10
<210> 434
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 434
Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
1 5 10
<210> 435
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 435
Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp Ile Trp
1 5 10 15
<210> 436
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 436
Lys Ser Ser Gln Ser Val Leu Asp Ser Ser Asn Asn Asn Asn Tyr Phe
1 5 10 15
Ala
<210> 437
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 437
Trp Ala Ser Ser Arg Glu Ser
1 5
<210> 438
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 438
Cys Gln Gln Tyr Tyr Ser Thr Pro Tyr Thr Phe
1 5 10
<210> 439
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 439
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Arg Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 440
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 440
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Asp Ser
20 25 30
Ser Asn Asn Asn Asn Tyr Phe Ala Trp Tyr Gln Gln Arg Pro Gly Gln
35 40 45
Pro Pro His Leu Leu Ile Tyr Trp Ala Ser Ser Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 441
<211> 257
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 441
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Arg Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala Pro Asp Gly Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
145 150 155 160
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Asp Ser
165 170 175
Ser Asn Asn Asn Asn Tyr Phe Ala Trp Tyr Gln Gln Arg Pro Gly Gln
180 185 190
Pro Pro His Leu Leu Ile Tyr Trp Ala Ser Ser Arg Glu Ser Gly Val
195 200 205
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
210 215 220
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
225 230 235 240
Tyr Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile
245 250 255
Lys
<210> 442
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 442
Asp Ser Val Ser Ser Asn Thr Thr Ala Trp Lys
1 5 10
<210> 443
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 443
Gly Trp Thr Tyr Tyr Arg Ser Lys Trp Tyr Tyr Asp Tyr Thr
1 5 10
<210> 444
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 444
Cys Ala Arg Trp Ile Phe His Asp Ala Phe Asp Ile Trp
1 5 10
<210> 445
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 445
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Thr Val Asn
1 5 10
<210> 446
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 446
Thr Asn Asn Gln Arg Pro Ser
1 5
<210> 447
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 447
Cys Ser Thr Trp Asp Asp Ser Leu Asn Gly Pro Val Phe
1 5 10
<210> 448
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 448
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Thr Thr Ala Trp Lys Trp Ser Arg Gln Ser Pro Ser Lys Gly Leu Glu
35 40 45
Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp Tyr Tyr Asp Tyr Thr
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Trp Ile Phe His Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 449
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 449
Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Phe Cys Ser Thr Trp Asp Asp Ser Leu
85 90 95
Asn Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 450
<211> 251
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 450
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Thr Thr Ala Trp Lys Trp Ser Arg Gln Ser Pro Ser Lys Gly Leu Glu
35 40 45
Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp Tyr Tyr Asp Tyr Thr
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Trp Ile Phe His Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Ala
130 135 140
Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg Val Thr
145 150 155 160
Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Thr Val Asn
165 170 175
Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Thr
180 185 190
Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys
195 200 205
Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln Ser Glu Asp
210 215 220
Glu Ala Asp Tyr Phe Cys Ser Thr Trp Asp Asp Ser Leu Asn Gly Pro
225 230 235 240
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 451
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 451
Asp Ser Ile Ser Ser Leu Ser Trp Ser
1 5
<210> 452
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 452
Gly Tyr Leu Tyr Tyr Ser Gly Ser Thr Asp Tyr Asn
1 5 10
<210> 453
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 453
Cys Ala Arg Gly Arg Arg Ala Phe Asp Ile Trp
1 5 10
<210> 454
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 454
Arg Gly Ser Gln Gly Ile Ser Asn Tyr Leu Ala
1 5 10
<210> 455
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 455
Ala Ala Ser Ser Leu Glu Ser
1 5
<210> 456
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 456
Cys Gln Gln Tyr Tyr Asn Tyr Pro Ile Thr Phe
1 5 10
<210> 457
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 457
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Leu
20 25 30
Ser Trp Ser Trp Ile Arg Gln Thr Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Leu Tyr Tyr Ser Gly Ser Thr Asp Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Ala Ala Ala Asp Thr Ala Leu Tyr Tyr Cys Ala
85 90 95
Arg Gly Arg Arg Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 458
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 458
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Gly Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Phe Gln Gln Arg Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Lys Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ile Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 459
<211> 242
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 459
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Leu
20 25 30
Ser Trp Ser Trp Ile Arg Gln Thr Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Leu Tyr Tyr Ser Gly Ser Thr Asp Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Ala Ala Ala Asp Thr Ala Leu Tyr Tyr Cys Ala
85 90 95
Arg Gly Arg Arg Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Gly
145 150 155 160
Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Arg Pro Gly
165 170 175
Lys Ala Pro Lys Ser Leu Ile Tyr Ala Ala Ser Ser Leu Glu Ser Gly
180 185 190
Val Pro Ser Lys Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ile Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln Tyr Tyr Asn Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu
225 230 235 240
Ile Lys
<210> 460
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 460
Tyr Thr Phe Thr Gly Tyr Tyr Met His
1 5
<210> 461
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 461
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala
1 5 10
<210> 462
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 462
Cys Ala Lys Asp Gly Gly Gly Asp Phe Tyr Phe Tyr Gly Met Asp Val
1 5 10 15
Trp
<210> 463
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 463
Gly Leu Ser Ser Gly Ser Val Ser Thr Ser Tyr Tyr Pro Ser
1 5 10
<210> 464
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 464
Ser Thr Asp Thr Arg Ser Ser
1 5
<210> 465
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 465
Cys Val Leu Tyr Met Gly Ser Gly Ile Ser Val Phe
1 5 10
<210> 466
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 466
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Thr Ser Asp Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Lys Asp Gly Gly Gly Asp Phe Tyr Phe Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 467
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 467
Gln Thr Val Val Thr Gln Glu Pro Ser Phe Ser Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Leu Ser Ser Gly Ser Val Ser Thr Ser
20 25 30
Tyr Tyr Pro Ser Cys Phe Gln Gln Thr Pro Gly Gln Ala Pro Arg Thr
35 40 45
Leu Ile Tyr Ser Thr Asp Thr Arg Ser Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Ile Leu Gly Asn Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Ala Asp Asp Glu Ser Asp Tyr Tyr Cys Val Leu Tyr Met Gly Ser
85 90 95
Gly Ile Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 468
<211> 252
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 468
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Val Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Thr Ser Asp Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Lys Asp Gly Gly Gly Asp Phe Tyr Phe Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Thr
130 135 140
Val Val Thr Gln Glu Pro Ser Phe Ser Val Ser Pro Gly Gly Thr Val
145 150 155 160
Thr Leu Thr Cys Gly Leu Ser Ser Gly Ser Val Ser Thr Ser Tyr Tyr
165 170 175
Pro Ser Cys Phe Gln Gln Thr Pro Gly Gln Ala Pro Arg Thr Leu Ile
180 185 190
Tyr Ser Thr Asp Thr Arg Ser Ser Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Ile Leu Gly Asn Lys Ala Ala Leu Thr Ile Thr Gly Ala Gln Ala
210 215 220
Asp Asp Glu Ser Asp Tyr Tyr Cys Val Leu Tyr Met Gly Ser Gly Ile
225 230 235 240
Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 469
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 469
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
1 5 10 15
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
20 25 30
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
35 40 45
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
50 55 60
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
65 70 75 80
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
85 90 95
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
100 105 110
Arg
<210> 470
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<220>
<221> SITE
<222> (1)..(25)
<223> /note="This sequence may encompass 1-5 'Gly Gly Gly Gly Ser'
repeating units"
<220>
<221> источник
<223> /note="See specification as filed for detailed description
of substitutions and preferred embodiments"
<400> 470
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 471
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 471
Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser
1 5 10 15
<210> 472
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 472
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 473
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
8xHis tag"
<400> 473
His His His His His His His His
1 5
<210> 474
<211> 571
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 474
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
35 40 45
Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
50 55 60
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Ala Met
65 70 75 80
Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Thr
85 90 95
Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly
100 105 110
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
115 120 125
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Phe Tyr Cys Ala Ile
130 135 140
Asp Pro Glu Tyr Tyr Asp Ile Leu Thr Gly Gly Asp Tyr Trp Gly Gln
145 150 155 160
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
180 185 190
Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp Arg Val
195 200 205
Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp
210 215 220
Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala
225 230 235 240
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
245 250 255
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
260 265 270
Ala Thr Tyr Phe Cys Leu Gln His Asp Ser Phe Pro Leu Thr Phe Gly
275 280 285
Gly Gly Thr Lys Val Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys
290 295 300
Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu
305 310 315 320
Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala
325 330 335
Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr
340 345 350
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
355 360 365
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
370 375 380
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
385 390 395 400
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
405 410 415
Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
420 425 430
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
435 440 445
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
450 455 460
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
465 470 475 480
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
485 490 495
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
500 505 510
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
515 520 525
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
530 535 540
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
545 550 555 560
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 475
<211> 541
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 475
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr
115 120 125
Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly
180 185 190
Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro
195 200 205
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp
245 250 255
Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly
260 265 270
Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser
275 280 285
Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
290 295 300
Gly Gly Gly Ser Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu
305 310 315 320
Cys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
325 330 335
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
340 345 350
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
355 360 365
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
370 375 380
Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
385 390 395 400
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
405 410 415
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
420 425 430
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
435 440 445
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
450 455 460
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
465 470 475 480
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
485 490 495
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
500 505 510
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
515 520 525
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
530 535 540
<210> 476
<211> 529
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 476
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly
35 40 45
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
50 55 60
Ser Gly Phe Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly
85 90 95
Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
100 105 110
Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala
115 120 125
Glu Asp Thr Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp
130 135 140
Ile Leu Thr Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
145 150 155 160
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
165 170 175
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
180 185 190
Ala Met Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
195 200 205
Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly
210 215 220
Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
225 230 235 240
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
245 250 255
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu
260 265 270
Gln His Asp Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu
275 280 285
Ile Lys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys
290 295 300
Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
305 310 315 320
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
325 330 335
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
340 345 350
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
355 360 365
Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr
370 375 380
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
385 390 395 400
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
405 410 415
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
420 425 430
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
435 440 445
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
450 455 460
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
465 470 475 480
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
485 490 495
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
500 505 510
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
515 520 525
Arg
<210> 477
<211> 21
<212> Белок
<213> Homo sapiens
<400> 477
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 478
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 478
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 479
<211> 66
<212> Белок
<213> Homo sapiens
<400> 479
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
35 40 45
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
50 55 60
Ile Thr
65
<210> 480
<211> 42
<212> Белок
<213> Homo sapiens
<400> 480
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 481
<211> 113
<212> Белок
<213> Homo sapiens
<400> 481
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
1 5 10 15
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
20 25 30
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
35 40 45
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
50 55 60
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
65 70 75 80
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
85 90 95
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
100 105 110
Arg
<210> 482
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 482
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Leu Phe Asn Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser Glu
225 230 235 240
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asn Trp Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 483
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 483
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Met Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Tyr Trp Ser Cys Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Leu Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Arg Leu Thr Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ala Pro Thr Gly Phe Trp Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Ser Arg Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Glu Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 484
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 484
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser His Asp Met His Trp Val Arg Gln Ala Thr Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Ile Ala Gly Asp Thr Tyr Tyr
65 70 75 80
Ser Gly Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys
85 90 95
Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ala Asn Trp Gly Glu Gly Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asp Tyr Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ile Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Val Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 485
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 485
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn His
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Leu Thr Ile Ser Leu Asp Lys Ala Lys
85 90 95
Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Phe Asn Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Arg Thr Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Thr Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 486
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 486
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Gln Leu Ser Ser Val Thr Ala Ala Asp Ala Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Phe His Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Asn Thr Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Asn Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 487
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 487
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asn Val
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Phe Cys Ala Arg Leu Ser Asn Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Phe Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Thr Ile Ser Ser Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Trp Ser Pro Ile
245 250 255
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 488
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 488
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Asp Met His Trp Val Arg Gln Ala Thr Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Pro Ala Gly Asp Thr Tyr Tyr
65 70 75 80
Pro Gly Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys
85 90 95
Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ala Asp Pro Pro Tyr Tyr Tyr Tyr Gly Met
115 120 125
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro
165 170 175
Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His
180 185 190
Ser Asn Glu Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln
195 200 205
Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Lys
225 230 235 240
Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln
245 250 255
Ala Leu Glu Ile Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
260 265 270
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 489
<211> 488
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 489
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Ser Thr Arg Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys
65 70 75 80
Arg Tyr Ser Pro Ser Leu Gln Thr Arg Leu Thr Ile Thr Lys Asp Thr
85 90 95
Pro Lys Asn Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ser Asn Trp Gly Asn Trp Tyr Phe
115 120 125
Ala Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser
180 185 190
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr Asp Ala Phe Tyr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Arg Ser Asn Trp Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 490
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 490
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Ser
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Val Ser Leu Asp Thr Ser Lys
85 90 95
Ser Gln Phe Ser Leu Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Phe Asn Arg Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Asn Thr Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Ala Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 491
<211> 496
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 491
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Ser Thr Ser Gly Met Cys Val Ser Trp Ile Arg Gln Pro Leu
50 55 60
Gly Lys Ala Leu Glu Trp Leu Gly Phe Ile Asp Trp Asp Asp Asp Lys
65 70 75 80
Tyr Tyr Asn Thr Ser Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Asn Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Gly Tyr Ser Gly Ser Tyr
115 120 125
Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Val Val Ile Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro
165 170 175
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser
180 185 190
Leu Leu His Ser Asn Gly Tyr Asn His Leu Asp Trp Tyr Leu Gln Lys
195 200 205
Pro Gly Gln Ser Pro Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala
210 215 220
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
225 230 235 240
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe
245 250 255
Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys
260 265 270
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 492
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 492
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Val Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ser Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys
50 55 60
Gly Leu Asp Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Thr Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Gly Leu Thr Gly Phe Phe Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu
180 185 190
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Tyr Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 493
<211> 483
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 493
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Gly Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Ser Ser Gly Asn Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Arg Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Thr Thr Ser Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Leu Gly Ile Ala Asp Ser Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala
195 200 205
Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 494
<211> 489
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 494
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn Ile
65 70 75 80
Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg
180 185 190
Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu
195 200 205
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr
245 250 255
Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 495
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 495
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Ile His Ser Gly Ser Ser Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ser Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Arg Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 496
<211> 484
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 496
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Asn Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Asp Ile His His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Lys Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Lys Asn Gln Phe Ser Leu Asn Leu Ile Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Glu Ala Gly Gly Tyr Phe Asp Tyr Trp
115 120 125
Gly Gln Gly Ile Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg
165 170 175
Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Ser Lys
195 200 205
Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Pro Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Ala Asp
225 230 235 240
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly
245 250 255
Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 497
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 497
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 498
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 498
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Ala Leu Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 499
<211> 488
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 499
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Ala Tyr Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Thr Ser Leu Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Leu Asp Ser Ser Gly Trp Tyr Pro Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser
180 185 190
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asp Ser Phe Pro
245 250 255
Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 500
<211> 483
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 500
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Phe Gly Gly
35 40 45
Ser Phe Ser Gly Asp Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ile Thr Ser Phe
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Leu Gly Ile Pro Asp Asn Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala
195 200 205
Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 501
<211> 492
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 501
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Val Val Phe Gly Asp
35 40 45
Ser Ile Ser Ser Ser Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Glu Val Phe His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ala Ala Val Ala Gly Ala Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu
165 170 175
Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser
180 185 190
Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
195 200 205
Pro Asn Leu Leu Val Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ala Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
225 230 235 240
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr
245 250 255
Tyr Gly Thr Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 502
<211> 488
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 502
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Thr Leu Arg Glu Ser Gly Pro Thr Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Ser Thr Ser Gly Leu Gly Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Glu Ala Leu Glu Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys
65 70 75 80
Arg Tyr Ser Pro Ser Leu Lys Ser Arg Leu Ser Ile Thr Lys Asp Thr
85 90 95
Ser Lys Asn Gln Val Val Leu Ile Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Val His Arg Arg Ile Ala Ala Pro Gly Ser
115 120 125
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser
180 185 190
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Ser Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys His Gln Ala Asn Ser Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 503
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 503
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Val Ser Gly Tyr
35 40 45
Thr Leu Thr Glu Leu Ser Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Pro Glu Gly Met Gly Gly Phe Asp Pro Glu Asp Gly Lys Thr Ile
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser
85 90 95
Ala Asp Thr Ala Tyr Met Glu Leu Asn Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Thr Leu Leu Arg Gly Leu Asp Ala Phe Asp
115 120 125
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Arg
245 250 255
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 504
<211> 488
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 504
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Arg Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Ser His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Val Arg Gly Tyr Ser Tyr Gly Tyr Pro Leu Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn
180 185 190
Asp Leu Gly Trp Tyr Gln Gln Lys Leu Gly Lys Ala Pro Lys Arg Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asn Ser Tyr Pro
245 250 255
Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 505
<211> 483
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 505
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Asp
35 40 45
Ser Ile Ser Ser Asn Trp Trp Thr Trp Val Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Met Ser Val Asp Lys Ser Glu
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Phe Tyr Cys Ala Arg Asp Gly Gly Gly Thr Leu Asp Tyr Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala
195 200 205
Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Gly Tyr Ser Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 506
<211> 492
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 506
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Thr Asn Tyr Cys Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn
65 70 75 80
Tyr Ala Gln Thr Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Asn Gly Asp Arg Tyr Tyr Tyr Asp
115 120 125
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro
165 170 175
Gly Gln Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
180 185 190
Asn Asn Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly
225 230 235 240
Leu Gln Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser
245 250 255
Ser Leu Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 507
<211> 494
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 507
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Thr Tyr Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr
115 120 125
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala
165 170 175
Ala Pro Gly Gln Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn
180 185 190
Ile Gly Asn Asn Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro
210 215 220
Asp Arg Phe Phe Gly Ser Lys Phe Gly Thr Ser Ala Thr Leu Gly Ile
225 230 235 240
Thr Gly Leu Gln Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp
245 250 255
Asp Ser Ser Leu Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 508
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 508
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Gly Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Leu Ser Val Ala Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Arg Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Asp Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 509
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 509
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ser Tyr Ile Tyr Tyr Ser Gly Ile Ser Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ile Ser Val Ala Gly Phe Phe Phe Asp Asn
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Met Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Ala Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Ala Pro
225 230 235 240
Glu Asp Phe Val Val Tyr Tyr Cys Gln Gln Tyr Gly Ile Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 510
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 510
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 511
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 511
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Ser Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Phe
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Trp Gly Asp Tyr Tyr Tyr Tyr
115 120 125
Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Leu Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile
180 185 190
Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Thr Ala Ser Ser Leu Gln Gly Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Leu Ala Thr Tyr Ser Cys Gln Gln Ala Asn Val
245 250 255
Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 512
<211> 491
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 512
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr
115 120 125
Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly
180 185 190
Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro
195 200 205
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp
245 250 255
Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 513
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 513
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ser Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ile Thr Val Thr Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Arg Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg His Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 514
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 514
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Val Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr His Cys Ala Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Ser Trp Tyr Gln Gln Phe Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly His Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 515
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 515
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Tyr
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Leu Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Leu Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Asn Ser
180 185 190
Asn Ile Gly Ser Asn Pro Ile Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly His Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 516
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 516
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Val Tyr Tyr Ser Asp Ile Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Phe Tyr Phe Cys Ala Arg Ile Gly Val Ala Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Arg Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Glu Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Ile
245 250 255
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 517
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 517
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Lys Pro
85 90 95
Asp Thr Ala Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Phe Thr Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Ile Asn Trp Tyr Gln Gln Val Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 518
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 518
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Glu Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Ile Trp Tyr Gln Gln Leu Pro Arg Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 519
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 519
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Thr Gly Leu Glu Trp Leu Ala Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Glu Val Ser Val Lys Ser Gln Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Gly Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asn Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Asp Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala
245 250 255
Trp Asp Asp Trp Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 520
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 520
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Asn Asn Tyr Phe Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Phe Tyr His Arg Gly Gly Asn Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Asn Ser Val Thr Ser Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Leu Ala Leu Ala Gly Phe Phe Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 521
<211> 494
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 521
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Thr Tyr Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr
115 120 125
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly
165 170 175
Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn
180 185 190
Ile Gly Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile
225 230 235 240
Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp
245 250 255
Asp Asp Ser Leu Ser Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 522
<211> 491
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 522
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Lys Glu Arg Arg Tyr Tyr Tyr Tyr
115 120 125
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val
180 185 190
Ser Arg Arg Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
195 200 205
Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
225 230 235 240
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly
245 250 255
Thr Ser Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 523
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 523
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Ala Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Ile Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Gly Thr Tyr Tyr Arg Ser Met Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Leu Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Gly Gly Ile Val Gly Val
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asn Thr Ala Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Arg Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 524
<211> 489
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 524
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Asn Val Ser Asp Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Asp Trp Ile Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Thr Ser Met Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ile Ser Glu Lys Ser Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
145 150 155 160
Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg
165 170 175
Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr
180 185 190
Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg Ser
225 230 235 240
Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Pro Trp Asp Asp Ser Leu Ser
245 250 255
Gly Arg Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 525
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 525
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Arg Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Val Ile Val Pro Ser Gly Gly Ser Ile Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Asn Ile Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Arg Tyr Tyr Gly Asp Tyr Tyr Tyr
115 120 125
Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile
180 185 190
Asn Asn Phe Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Ser Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Lys
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Asn Ser
245 250 255
Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 526
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 526
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser His Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Phe
65 70 75 80
Ser Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Ser Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Gly Ile Ser Leu Ala Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Val Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Phe Tyr Cys Gln Gln Tyr Ser Ile Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 527
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 527
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ala Tyr Ile Tyr Tyr Ser Gly Asn Thr Asn Tyr
65 70 75 80
Ser Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asp Gln Leu Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Thr Arg Gly Gly Ser Gly Thr Ile Asp Val Phe Asp
115 120 125
Ile Trp Gly Gln Gly Thr Met Val Ala Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
165 170 175
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
180 185 190
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
225 230 235 240
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Glu Thr Trp Asp Ser Ser Leu
245 250 255
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 528
<211> 492
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 528
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Asn Val Ser Thr Asn Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Leu Lys Ser Arg Ile Asn Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Trp Val Asn Arg Asp Val
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro
165 170 175
Gly Gln Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly
180 185 190
Ser Tyr Asn Leu Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro
195 200 205
Lys Leu Met Ile Tyr Glu Gly Ser Lys Arg Pro Ser Gly Val Ser Asn
210 215 220
Arg Phe Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser
225 230 235 240
Gly Leu Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Cys Ser Tyr Ala
245 250 255
Gly Ser Ser Thr Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 529
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 529
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Gly Met His Trp Val Arg Gln Thr Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Asn Ser Asn Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Ala Thr Val Thr Ser Tyr Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu
165 170 175
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
180 185 190
Ser Val Ser Arg Thr Tyr Leu Ala Trp Tyr His Gln Lys Pro Gly Gln
195 200 205
Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile
210 215 220
Ser Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
225 230 235 240
Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln
245 250 255
Tyr Gly Thr Ser Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile
260 265 270
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 530
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 530
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Arg Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu
165 170 175
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
180 185 190
Ser Val Leu Asp Ser Ser Asn Asn Asn Asn Tyr Phe Ala Trp Tyr Gln
195 200 205
Gln Arg Pro Gly Gln Pro Pro His Leu Leu Ile Tyr Trp Ala Ser Ser
210 215 220
Arg Glu Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
225 230 235 240
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
245 250 255
Tyr Tyr Cys Gln Gln Tyr Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly
260 265 270
Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
275 280 285
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
290 295 300
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
305 310 315 320
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
325 330 335
Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 531
<211> 492
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 531
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Thr Thr Ala Trp Lys Trp Ser Arg Gln Ser Pro
50 55 60
Ser Lys Gly Leu Glu Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Tyr Asp Tyr Thr Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Trp Ile Phe His Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
165 170 175
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
180 185 190
Ser Asn Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
225 230 235 240
Leu Gln Ser Glu Asp Glu Ala Asp Tyr Phe Cys Ser Thr Trp Asp Asp
245 250 255
Ser Leu Asn Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 532
<211> 483
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 532
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Ser Ser Leu Ser Trp Ser Trp Ile Arg Gln Thr Pro Gly Glu
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Leu Tyr Tyr Ser Gly Ser Thr Asp Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Ala Ala Ala Asp Thr Ala
100 105 110
Leu Tyr Tyr Cys Ala Arg Gly Arg Arg Ala Phe Asp Ile Trp Gly Gln
115 120 125
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Gly Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe
180 185 190
Gln Gln Arg Pro Gly Lys Ala Pro Lys Ser Leu Ile Tyr Ala Ala Ser
195 200 205
Ser Leu Glu Ser Gly Val Pro Ser Lys Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ile Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Tyr Pro Ile Thr Phe Gly Gln
245 250 255
Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 533
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 533
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Val Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Thr Ser Asp Asp Thr
100 105 110
Ala Ile Tyr Tyr Cys Ala Lys Asp Gly Gly Gly Asp Phe Tyr Phe Tyr
115 120 125
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gln Thr Val Val Thr Gln Glu Pro Ser Phe Ser Val Ser
165 170 175
Pro Gly Gly Thr Val Thr Leu Thr Cys Gly Leu Ser Ser Gly Ser Val
180 185 190
Ser Thr Ser Tyr Tyr Pro Ser Cys Phe Gln Gln Thr Pro Gly Gln Ala
195 200 205
Pro Arg Thr Leu Ile Tyr Ser Thr Asp Thr Arg Ser Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Ile Leu Gly Asn Lys Ala Ala Leu Thr Ile
225 230 235 240
Thr Gly Ala Gln Ala Asp Asp Glu Ser Asp Tyr Tyr Cys Val Leu Tyr
245 250 255
Met Gly Ser Gly Ile Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val
260 265 270
Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 534
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 534
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 535
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 535
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 536
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 536
Cys Pro Tyr Ser Asn Pro Ser Leu Cys
1 5
<210> 537
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 537
Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp
1 5 10 15
Gln Lys Lys Leu Met Ser Asn Asn
20
<210> 538
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 538
Cys Gln Phe Asp Leu Ser Thr Arg Arg Leu Lys Cys
1 5 10
<210> 539
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 539
Cys Gln Tyr Asn Leu Ser Ser Arg Ala Leu Lys Cys
1 5 10
<210> 540
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 540
Cys Val Trp Gln Arg Trp Gln Lys Ser Tyr Val Cys
1 5 10
<210> 541
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 541
Cys Met Trp Asp Arg Phe Ser Arg Trp Tyr Lys Cys
1 5 10
<210> 542
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 542
Ser Phe Val Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp
1 5 10 15
Lys Leu Ala Ala Phe Pro Glu Asp Arg
20 25
<210> 543
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 543
Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala Gln
1 5 10 15
Ile Lys Glu
<210> 544
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 544
Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser
1 5 10 15
Pro Ala Lys Pro Thr Thr Thr Ala
20
<210> 545
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 545
Gly Gln Asn Asp Thr Ser Gln Thr Ser Ser Pro Ser
1 5 10
<210> 546
<211> 16
<212> Белок
<213> Homo sapiens
<400> 546
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly Tyr Gln
1 5 10 15
<210> 547
<211> 45
<212> Белок
<213> Homo sapiens
<400> 547
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 548
<211> 231
<212> Белок
<213> Homo sapiens
<400> 548
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 549
<211> 21
<212> Белок
<213> Homo sapiens
<400> 549
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr
20
<210> 550
<211> 27
<212> Белок
<213> Homo sapiens
<400> 550
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 551
<211> 41
<212> Белок
<213> Homo sapiens
<400> 551
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 552
<211> 136
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 552
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu
1 5 10 15
Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro
20 25 30
Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys
35 40 45
Ser Gly Gly Gly Gly Ser Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
50 55 60
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
65 70 75 80
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
85 90 95
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
100 105 110
Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg Asn Arg Arg Arg Val
115 120 125
Cys Lys Cys Pro Arg Pro Val Val
130 135
<210> 553
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 553
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Ala
20
<210> 554
<211> 157
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 554
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
20 25 30
Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser
35 40 45
Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser
50 55 60
Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Pro Ala Pro Arg Pro
65 70 75 80
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
85 90 95
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
100 105 110
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
115 120 125
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg
130 135 140
Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val
145 150 155
<210> 555
<211> 63
<212> ДНК
<213> Homo sapiens
<400> 555
atggcactcc ccgtaactgc tctgctgctg ccgttggcat tgctcctgca cgccgcacgc
60
ccg
63
<210> 556
<211> 624
<212> Белок
<213> Homo sapiens
<400> 556
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Ala Gly Val Phe Glu Leu Gln Ile His Ser Phe Gly Pro Gly Pro Gly
35 40 45
Pro Gly Ala Pro Arg Ser Pro Cys Ser Ala Arg Leu Pro Cys Arg Leu
50 55 60
Phe Phe Arg Val Cys Leu Lys Pro Gly Leu Ser Glu Glu Ala Ala Glu
65 70 75 80
Ser Pro Cys Ala Leu Gly Ala Ala Leu Ser Ala Arg Gly Pro Val Tyr
85 90 95
Thr Glu Gln Pro Gly Ala Pro Ala Pro Asp Leu Pro Leu Pro Asp Gly
100 105 110
Leu Leu Gln Val Pro Phe Arg Asp Ala Trp Pro Gly Thr Phe Ser Phe
115 120 125
Ile Ile Glu Thr Trp Arg Glu Glu Leu Gly Asp Gln Ile Gly Gly Pro
130 135 140
Ala Trp Ser Leu Leu Ala Arg Val Ala Gly Arg Arg Arg Leu Ala Ala
145 150 155 160
Gly Gly Pro Trp Ala Arg Asp Ile Gln Arg Ala Gly Ala Trp Glu Leu
165 170 175
Arg Phe Ser Tyr Arg Ala Arg Cys Glu Pro Pro Ala Val Gly Thr Ala
180 185 190
Cys Thr Arg Leu Cys Arg Pro Arg Ser Ala Pro Ser Arg Cys Gly Pro
195 200 205
Gly Leu Arg Pro Cys Ala Pro Leu Glu Asp Glu Cys Glu Ala Pro Leu
210 215 220
Val Cys Arg Ala Gly Cys Ser Pro Glu His Gly Phe Cys Glu Gln Pro
225 230 235 240
Gly Glu Cys Arg Cys Leu Glu Gly Trp Thr Gly Pro Leu Cys Thr Val
245 250 255
Pro Val Ser Thr Ser Ser Cys Leu Ser Pro Arg Gly Pro Ser Ser Ala
260 265 270
Thr Thr Gly Cys Leu Val Pro Gly Pro Gly Pro Cys Asp Gly Asn Pro
275 280 285
Cys Ala Asn Gly Gly Ser Cys Ser Glu Thr Pro Arg Ser Phe Glu Cys
290 295 300
Thr Cys Pro Arg Gly Phe Tyr Gly Leu Arg Cys Glu Val Ser Gly Val
305 310 315 320
Thr Cys Ala Asp Gly Pro Cys Phe Asn Gly Gly Leu Cys Val Gly Gly
325 330 335
Ala Asp Pro Asp Ser Ala Tyr Ile Cys His Cys Pro Pro Gly Phe Gln
340 345 350
Gly Ser Asn Cys Glu Lys Arg Val Asp Arg Cys Ser Leu Gln Pro Cys
355 360 365
Arg Asn Gly Gly Leu Cys Leu Asp Leu Gly His Ala Leu Arg Cys Arg
370 375 380
Cys Arg Ala Gly Phe Ala Gly Pro Arg Cys Glu His Asp Leu Asp Asp
385 390 395 400
Cys Ala Gly Arg Ala Cys Ala Asn Gly Gly Thr Cys Val Glu Gly Gly
405 410 415
Gly Ala His Arg Cys Ser Cys Ala Leu Gly Phe Gly Gly Arg Asp Cys
420 425 430
Arg Glu Arg Ala Asp Pro Cys Ala Ala Arg Pro Cys Ala His Gly Gly
435 440 445
Arg Cys Tyr Ala His Phe Ser Gly Leu Val Cys Ala Cys Ala Pro Gly
450 455 460
Tyr Met Gly Ala Arg Cys Glu Phe Pro Val His Pro Asp Gly Ala Ser
465 470 475 480
Ala Leu Pro Ala Ala Pro Pro Gly Leu Arg Pro Gly Asp Pro Gln Arg
485 490 495
Tyr Leu Leu Pro Pro Ala Leu Gly Leu Leu Val Ala Ala Gly Val Ala
500 505 510
Gly Ala Ala Leu Leu Leu Val His Val Arg Arg Arg Gly His Ser Gln
515 520 525
Asp Ala Gly Ser Arg Leu Leu Ala Gly Thr Pro Glu Pro Ser Val His
530 535 540
Ala Leu Pro Asp Ala Leu Asn Asn Leu Arg Thr Gln Glu Gly Ser Gly
545 550 555 560
Asp Gly Pro Ser Ser Ser Val Asp Trp Asn Arg Pro Glu Asp Val Asp
565 570 575
Pro Gln Gly Ile Tyr Val Ile Ser Ala Pro Ser Ile Tyr Ala Arg Glu
580 585 590
Val Ala Thr Pro Leu Phe Pro Pro Leu His Thr Gly Arg Ala Gly Gln
595 600 605
Arg Gln His Leu Leu Phe Pro Tyr Pro Ser Ser Ile Leu Ser Val Lys
610 615 620
<210> 557
<211> 477
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 557
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Ala Arg Cys Glu Pro Pro Ala Val Gly Thr Ala Cys Thr Arg
35 40 45
Leu Cys Arg Pro Arg Ser Ala Pro Ser Arg Cys Gly Pro Gly Leu Arg
50 55 60
Pro Cys Ala Pro Leu Glu Asp Glu Cys Glu Ala Pro Leu Val Cys Arg
65 70 75 80
Ala Gly Cys Ser Pro Glu His Gly Phe Cys Glu Gln Pro Gly Glu Cys
85 90 95
Arg Cys Leu Glu Gly Trp Thr Gly Pro Leu Cys Thr Val Pro Val Ser
100 105 110
Thr Ser Ser Cys Leu Ser Pro Arg Gly Pro Ser Ser Ala Thr Thr Gly
115 120 125
Cys Leu Val Pro Gly Pro Gly Pro Cys Asp Gly Asn Pro Cys Ala Asn
130 135 140
Gly Gly Ser Cys Ser Glu Thr Pro Arg Ser Phe Glu Cys Thr Cys Pro
145 150 155 160
Arg Gly Phe Tyr Gly Leu Arg Cys Glu Val Ser Gly Val Thr Cys Ala
165 170 175
Asp Gly Pro Cys Phe Asn Gly Gly Leu Cys Val Gly Gly Ala Asp Pro
180 185 190
Asp Ser Ala Tyr Ile Cys His Cys Pro Pro Gly Phe Gln Gly Ser Asn
195 200 205
Cys Glu Lys Arg Val Asp Arg Cys Ser Leu Gln Pro Cys Arg Asn Gly
210 215 220
Gly Leu Cys Leu Asp Leu Gly His Ala Leu Arg Cys Arg Cys Arg Ala
225 230 235 240
Gly Phe Ala Gly Pro Arg Cys Glu His Asp Leu Asp Asp Cys Ala Gly
245 250 255
Arg Ala Cys Ala Asn Gly Gly Thr Cys Val Glu Gly Gly Gly Ala His
260 265 270
Arg Cys Ser Cys Ala Leu Gly Phe Gly Gly Arg Asp Cys Arg Glu Arg
275 280 285
Ala Asp Pro Cys Ala Ala Arg Pro Cys Ala His Gly Gly Arg Cys Tyr
290 295 300
Ala His Phe Ser Gly Leu Val Cys Ala Cys Ala Pro Gly Tyr Met Gly
305 310 315 320
Ala Arg Cys Glu Phe Pro Val His Pro Asp Gly Ala Ser Ala Leu Pro
325 330 335
Ala Ala Pro Pro Gly Leu Arg Pro Gly Asp Pro Gln Arg Tyr Leu Leu
340 345 350
Pro Pro Ala Leu Gly Leu Leu Val Ala Ala Gly Val Ala Gly Ala Ala
355 360 365
Leu Leu Leu Val His Val Arg Arg Arg Gly His Ser Gln Asp Ala Gly
370 375 380
Ser Arg Leu Leu Ala Gly Thr Pro Glu Pro Ser Val His Ala Leu Pro
385 390 395 400
Asp Ala Leu Asn Asn Leu Arg Thr Gln Glu Gly Ser Gly Asp Gly Pro
405 410 415
Ser Ser Ser Val Asp Trp Asn Arg Pro Glu Asp Val Asp Pro Gln Gly
420 425 430
Ile Tyr Val Ile Ser Ala Pro Ser Ile Tyr Ala Arg Glu Val Ala Thr
435 440 445
Pro Leu Phe Pro Pro Leu His Thr Gly Arg Ala Gly Gln Arg Gln His
450 455 460
Leu Leu Phe Pro Tyr Pro Ser Ser Ile Leu Ser Val Lys
465 470 475
<210> 558
<211> 437
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 558
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Ala Pro Leu Val Cys Arg Ala Gly Cys Ser Pro Glu His Gly
35 40 45
Phe Cys Glu Gln Pro Gly Glu Cys Arg Cys Leu Glu Gly Trp Thr Gly
50 55 60
Pro Leu Cys Thr Val Pro Val Ser Thr Ser Ser Cys Leu Ser Pro Arg
65 70 75 80
Gly Pro Ser Ser Ala Thr Thr Gly Cys Leu Val Pro Gly Pro Gly Pro
85 90 95
Cys Asp Gly Asn Pro Cys Ala Asn Gly Gly Ser Cys Ser Glu Thr Pro
100 105 110
Arg Ser Phe Glu Cys Thr Cys Pro Arg Gly Phe Tyr Gly Leu Arg Cys
115 120 125
Glu Val Ser Gly Val Thr Cys Ala Asp Gly Pro Cys Phe Asn Gly Gly
130 135 140
Leu Cys Val Gly Gly Ala Asp Pro Asp Ser Ala Tyr Ile Cys His Cys
145 150 155 160
Pro Pro Gly Phe Gln Gly Ser Asn Cys Glu Lys Arg Val Asp Arg Cys
165 170 175
Ser Leu Gln Pro Cys Arg Asn Gly Gly Leu Cys Leu Asp Leu Gly His
180 185 190
Ala Leu Arg Cys Arg Cys Arg Ala Gly Phe Ala Gly Pro Arg Cys Glu
195 200 205
His Asp Leu Asp Asp Cys Ala Gly Arg Ala Cys Ala Asn Gly Gly Thr
210 215 220
Cys Val Glu Gly Gly Gly Ala His Arg Cys Ser Cys Ala Leu Gly Phe
225 230 235 240
Gly Gly Arg Asp Cys Arg Glu Arg Ala Asp Pro Cys Ala Ala Arg Pro
245 250 255
Cys Ala His Gly Gly Arg Cys Tyr Ala His Phe Ser Gly Leu Val Cys
260 265 270
Ala Cys Ala Pro Gly Tyr Met Gly Ala Arg Cys Glu Phe Pro Val His
275 280 285
Pro Asp Gly Ala Ser Ala Leu Pro Ala Ala Pro Pro Gly Leu Arg Pro
290 295 300
Gly Asp Pro Gln Arg Tyr Leu Leu Pro Pro Ala Leu Gly Leu Leu Val
305 310 315 320
Ala Ala Gly Val Ala Gly Ala Ala Leu Leu Leu Val His Val Arg Arg
325 330 335
Arg Gly His Ser Gln Asp Ala Gly Ser Arg Leu Leu Ala Gly Thr Pro
340 345 350
Glu Pro Ser Val His Ala Leu Pro Asp Ala Leu Asn Asn Leu Arg Thr
355 360 365
Gln Glu Gly Ser Gly Asp Gly Pro Ser Ser Ser Val Asp Trp Asn Arg
370 375 380
Pro Glu Asp Val Asp Pro Gln Gly Ile Tyr Val Ile Ser Ala Pro Ser
385 390 395 400
Ile Tyr Ala Arg Glu Val Ala Thr Pro Leu Phe Pro Pro Leu His Thr
405 410 415
Gly Arg Ala Gly Gln Arg Gln His Leu Leu Phe Pro Tyr Pro Ser Ser
420 425 430
Ile Leu Ser Val Lys
435
<210> 559
<211> 379
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 559
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Gly Pro Gly Pro Cys Asp Gly Asn Pro Cys Ala Asn Gly Gly
35 40 45
Ser Cys Ser Glu Thr Pro Arg Ser Phe Glu Cys Thr Cys Pro Arg Gly
50 55 60
Phe Tyr Gly Leu Arg Cys Glu Val Ser Gly Val Thr Cys Ala Asp Gly
65 70 75 80
Pro Cys Phe Asn Gly Gly Leu Cys Val Gly Gly Ala Asp Pro Asp Ser
85 90 95
Ala Tyr Ile Cys His Cys Pro Pro Gly Phe Gln Gly Ser Asn Cys Glu
100 105 110
Lys Arg Val Asp Arg Cys Ser Leu Gln Pro Cys Arg Asn Gly Gly Leu
115 120 125
Cys Leu Asp Leu Gly His Ala Leu Arg Cys Arg Cys Arg Ala Gly Phe
130 135 140
Ala Gly Pro Arg Cys Glu His Asp Leu Asp Asp Cys Ala Gly Arg Ala
145 150 155 160
Cys Ala Asn Gly Gly Thr Cys Val Glu Gly Gly Gly Ala His Arg Cys
165 170 175
Ser Cys Ala Leu Gly Phe Gly Gly Arg Asp Cys Arg Glu Arg Ala Asp
180 185 190
Pro Cys Ala Ala Arg Pro Cys Ala His Gly Gly Arg Cys Tyr Ala His
195 200 205
Phe Ser Gly Leu Val Cys Ala Cys Ala Pro Gly Tyr Met Gly Ala Arg
210 215 220
Cys Glu Phe Pro Val His Pro Asp Gly Ala Ser Ala Leu Pro Ala Ala
225 230 235 240
Pro Pro Gly Leu Arg Pro Gly Asp Pro Gln Arg Tyr Leu Leu Pro Pro
245 250 255
Ala Leu Gly Leu Leu Val Ala Ala Gly Val Ala Gly Ala Ala Leu Leu
260 265 270
Leu Val His Val Arg Arg Arg Gly His Ser Gln Asp Ala Gly Ser Arg
275 280 285
Leu Leu Ala Gly Thr Pro Glu Pro Ser Val His Ala Leu Pro Asp Ala
290 295 300
Leu Asn Asn Leu Arg Thr Gln Glu Gly Ser Gly Asp Gly Pro Ser Ser
305 310 315 320
Ser Val Asp Trp Asn Arg Pro Glu Asp Val Asp Pro Gln Gly Ile Tyr
325 330 335
Val Ile Ser Ala Pro Ser Ile Tyr Ala Arg Glu Val Ala Thr Pro Leu
340 345 350
Phe Pro Pro Leu His Thr Gly Arg Ala Gly Gln Arg Gln His Leu Leu
355 360 365
Phe Pro Tyr Pro Ser Ser Ile Leu Ser Val Lys
370 375
<210> 560
<211> 341
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 560
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Ser Gly Val Thr Cys Ala Asp Gly Pro Cys Phe Asn Gly Gly
35 40 45
Leu Cys Val Gly Gly Ala Asp Pro Asp Ser Ala Tyr Ile Cys His Cys
50 55 60
Pro Pro Gly Phe Gln Gly Ser Asn Cys Glu Lys Arg Val Asp Arg Cys
65 70 75 80
Ser Leu Gln Pro Cys Arg Asn Gly Gly Leu Cys Leu Asp Leu Gly His
85 90 95
Ala Leu Arg Cys Arg Cys Arg Ala Gly Phe Ala Gly Pro Arg Cys Glu
100 105 110
His Asp Leu Asp Asp Cys Ala Gly Arg Ala Cys Ala Asn Gly Gly Thr
115 120 125
Cys Val Glu Gly Gly Gly Ala His Arg Cys Ser Cys Ala Leu Gly Phe
130 135 140
Gly Gly Arg Asp Cys Arg Glu Arg Ala Asp Pro Cys Ala Ala Arg Pro
145 150 155 160
Cys Ala His Gly Gly Arg Cys Tyr Ala His Phe Ser Gly Leu Val Cys
165 170 175
Ala Cys Ala Pro Gly Tyr Met Gly Ala Arg Cys Glu Phe Pro Val His
180 185 190
Pro Asp Gly Ala Ser Ala Leu Pro Ala Ala Pro Pro Gly Leu Arg Pro
195 200 205
Gly Asp Pro Gln Arg Tyr Leu Leu Pro Pro Ala Leu Gly Leu Leu Val
210 215 220
Ala Ala Gly Val Ala Gly Ala Ala Leu Leu Leu Val His Val Arg Arg
225 230 235 240
Arg Gly His Ser Gln Asp Ala Gly Ser Arg Leu Leu Ala Gly Thr Pro
245 250 255
Glu Pro Ser Val His Ala Leu Pro Asp Ala Leu Asn Asn Leu Arg Thr
260 265 270
Gln Glu Gly Ser Gly Asp Gly Pro Ser Ser Ser Val Asp Trp Asn Arg
275 280 285
Pro Glu Asp Val Asp Pro Gln Gly Ile Tyr Val Ile Ser Ala Pro Ser
290 295 300
Ile Tyr Ala Arg Glu Val Ala Thr Pro Leu Phe Pro Pro Leu His Thr
305 310 315 320
Gly Arg Ala Gly Gln Arg Gln His Leu Leu Phe Pro Tyr Pro Ser Ser
325 330 335
Ile Leu Ser Val Lys
340
<210> 561
<211> 300
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 561
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Arg Val Asp Arg Cys Ser Leu Gln Pro Cys Arg Asn Gly Gly
35 40 45
Leu Cys Leu Asp Leu Gly His Ala Leu Arg Cys Arg Cys Arg Ala Gly
50 55 60
Phe Ala Gly Pro Arg Cys Glu His Asp Leu Asp Asp Cys Ala Gly Arg
65 70 75 80
Ala Cys Ala Asn Gly Gly Thr Cys Val Glu Gly Gly Gly Ala His Arg
85 90 95
Cys Ser Cys Ala Leu Gly Phe Gly Gly Arg Asp Cys Arg Glu Arg Ala
100 105 110
Asp Pro Cys Ala Ala Arg Pro Cys Ala His Gly Gly Arg Cys Tyr Ala
115 120 125
His Phe Ser Gly Leu Val Cys Ala Cys Ala Pro Gly Tyr Met Gly Ala
130 135 140
Arg Cys Glu Phe Pro Val His Pro Asp Gly Ala Ser Ala Leu Pro Ala
145 150 155 160
Ala Pro Pro Gly Leu Arg Pro Gly Asp Pro Gln Arg Tyr Leu Leu Pro
165 170 175
Pro Ala Leu Gly Leu Leu Val Ala Ala Gly Val Ala Gly Ala Ala Leu
180 185 190
Leu Leu Val His Val Arg Arg Arg Gly His Ser Gln Asp Ala Gly Ser
195 200 205
Arg Leu Leu Ala Gly Thr Pro Glu Pro Ser Val His Ala Leu Pro Asp
210 215 220
Ala Leu Asn Asn Leu Arg Thr Gln Glu Gly Ser Gly Asp Gly Pro Ser
225 230 235 240
Ser Ser Val Asp Trp Asn Arg Pro Glu Asp Val Asp Pro Gln Gly Ile
245 250 255
Tyr Val Ile Ser Ala Pro Ser Ile Tyr Ala Arg Glu Val Ala Thr Pro
260 265 270
Leu Phe Pro Pro Leu His Thr Gly Arg Ala Gly Gln Arg Gln His Leu
275 280 285
Leu Phe Pro Tyr Pro Ser Ser Ile Leu Ser Val Lys
290 295 300
<210> 562
<211> 262
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 562
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Asp Leu Asp Asp Cys Ala Gly Arg Ala Cys Ala Asn Gly Gly
35 40 45
Thr Cys Val Glu Gly Gly Gly Ala His Arg Cys Ser Cys Ala Leu Gly
50 55 60
Phe Gly Gly Arg Asp Cys Arg Glu Arg Ala Asp Pro Cys Ala Ala Arg
65 70 75 80
Pro Cys Ala His Gly Gly Arg Cys Tyr Ala His Phe Ser Gly Leu Val
85 90 95
Cys Ala Cys Ala Pro Gly Tyr Met Gly Ala Arg Cys Glu Phe Pro Val
100 105 110
His Pro Asp Gly Ala Ser Ala Leu Pro Ala Ala Pro Pro Gly Leu Arg
115 120 125
Pro Gly Asp Pro Gln Arg Tyr Leu Leu Pro Pro Ala Leu Gly Leu Leu
130 135 140
Val Ala Ala Gly Val Ala Gly Ala Ala Leu Leu Leu Val His Val Arg
145 150 155 160
Arg Arg Gly His Ser Gln Asp Ala Gly Ser Arg Leu Leu Ala Gly Thr
165 170 175
Pro Glu Pro Ser Val His Ala Leu Pro Asp Ala Leu Asn Asn Leu Arg
180 185 190
Thr Gln Glu Gly Ser Gly Asp Gly Pro Ser Ser Ser Val Asp Trp Asn
195 200 205
Arg Pro Glu Asp Val Asp Pro Gln Gly Ile Tyr Val Ile Ser Ala Pro
210 215 220
Ser Ile Tyr Ala Arg Glu Val Ala Thr Pro Leu Phe Pro Pro Leu His
225 230 235 240
Thr Gly Arg Ala Gly Gln Arg Gln His Leu Leu Phe Pro Tyr Pro Ser
245 250 255
Ser Ile Leu Ser Val Lys
260
<210> 563
<211> 224
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 563
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gly Met Leu
20 25 30
Gly Ser Arg Ala Asp Pro Cys Ala Ala Arg Pro Cys Ala His Gly Gly
35 40 45
Arg Cys Tyr Ala His Phe Ser Gly Leu Val Cys Ala Cys Ala Pro Gly
50 55 60
Tyr Met Gly Ala Arg Cys Glu Phe Pro Val His Pro Asp Gly Ala Ser
65 70 75 80
Ala Leu Pro Ala Ala Pro Pro Gly Leu Arg Pro Gly Asp Pro Gln Arg
85 90 95
Tyr Leu Leu Pro Pro Ala Leu Gly Leu Leu Val Ala Ala Gly Val Ala
100 105 110
Gly Ala Ala Leu Leu Leu Val His Val Arg Arg Arg Gly His Ser Gln
115 120 125
Asp Ala Gly Ser Arg Leu Leu Ala Gly Thr Pro Glu Pro Ser Val His
130 135 140
Ala Leu Pro Asp Ala Leu Asn Asn Leu Arg Thr Gln Glu Gly Ser Gly
145 150 155 160
Asp Gly Pro Ser Ser Ser Val Asp Trp Asn Arg Pro Glu Asp Val Asp
165 170 175
Pro Gln Gly Ile Tyr Val Ile Ser Ala Pro Ser Ile Tyr Ala Arg Glu
180 185 190
Val Ala Thr Pro Leu Phe Pro Pro Leu His Thr Gly Arg Ala Gly Gln
195 200 205
Arg Gln His Leu Leu Phe Pro Tyr Pro Ser Ser Ile Leu Ser Val Lys
210 215 220
<210> 564
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
oligonucleotide"
<400> 564
ggcggtggag gctccggagg ggggggctct ggcggagggg gctcc
45
<210> 565
<211> 524
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 565
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly
50 55 60
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
65 70 75 80
Phe Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly
85 90 95
Lys Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr
100 105 110
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
115 120 125
Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
130 135 140
Thr Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu
145 150 155 160
Thr Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
165 170 175
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser
180 185 190
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met
195 200 205
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
210 215 220
Gly Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val
225 230 235 240
Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
245 250 255
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
260 265 270
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His
275 280 285
Asp Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
370 375 380
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
385 390 395 400
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
405 410 415
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
420 425 430
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
435 440 445
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
450 455 460
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
465 470 475 480
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
485 490 495
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
500 505 510
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 566
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
oligonucleotide"
<400> 566
gggtctacat ccggctccgg gaagcccgga agtggcgaag gtagtacaaa gggg
54
<210> 567
<211> 123
<212> ДНК
<213> Homo sapiens
<400> 567
agatccaaaa gaagccgcct gctccatagc gattacatga atatgactcc acgccgccct
60
ggccccacaa ggaaacacta ccagccttac gcaccaccta gagatttcgc tgcctatcgg
120
agc
123
<210> 568
<211> 126
<212> ДНК
<213> Homo sapiens
<400> 568
aagcgcggca ggaagaagct cctctacatt tttaagcagc cttttatgag gcccgtacag
60
acaacacagg aggaagatgg ctgtagctgc agatttcccg aggaggagga aggtgggtgc
120
gagctg
126
<210> 569
<211> 336
<212> ДНК
<213> Homo sapiens
<400> 569
agggtgaagt tttccagatc tgcagatgca ccagcgtatc agcagggcca gaaccaactg
60
tataacgagc tcaacctggg acgcagggaa gagtatgacg ttttggacaa gcgcagagga
120
cgggaccctg agatgggtgg caaaccaaga cgaaaaaacc cccaggaggg tctctataat
180
gagctgcaga aggataagat ggctgaagcc tattctgaaa taggcatgaa aggagagcgg
240
agaaggggaa aagggcacga cggtttgtac cagggactca gcactgctac gaaggatact
300
tatgacgctc tccacatgca agccctgcca cctagg
336
<210> 570
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 570
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtcc aggtgcagct gcaggagagc ggcccaggcc tggtgaagcc atctgagaca
120
ctgagcctga cctgcacagt gagcgataac tccatctcta attactattg gtcctggatc
180
aggcagcccc ctggcaaggg cctggagtgg atcgcctaca tctactattc tggcaccaca
240
aactataatc ccagcctgaa gtccagagtg accatctccc tggacacatc taagaaccag
300
ttctccctga agctgagctc cgtgaccgca gcagatacag ccgtgtacta ttgtgcccgg
360
ctgtttaatt ggggcttcgc ctttgacatc tggggccagg gcaccatggt gacagtgtct
420
agcggaggag gaggaagcgg aggaggaggg tccggaggcg ggggatctga gatcgtgatg
480
acccagtctc cagccacact gtccgtgtct cccggcgaga gggccaccct gagctgcaga
540
gccagccagt ccgtgagctc caacctggcc tggtaccagc agaagcctgg ccaggcacct
600
cggctgctga tctatggagc atccaccagg gccacaggaa tccctgcacg cttctctgga
660
agcggatccg gcacagagtt taccctgaca atctctagcc tgcagtctga ggacttcgcc
720
gtgtactatt gtcagcagta caacaattgg cccctgacct ttggcggcgg cacaaaggtg
780
gagatcaaga ccacaactcc tgcacctagg ccacctaccc cagcacctac aattgctagt
840
cagccactgt cactgcgacc agaggcatgt cgacctgcag ctggaggagc agtgcataca
900
aggggactgg actttgcctg cgatatctac atttgggctc ctctggcagg aacatgtggc
960
gtgctgctgc tgagcctggt catcactctg tactgcaagc gaggccggaa gaaactgctg
1020
tatattttca aacagccctt tatgcgacct gtgcagacca cacaggagga agatgggtgc
1080
tcctgtcggt tccccgagga agaggaagga ggctgtgagc tgcgggtcaa gttttccaga
1140
tctgcagacg cccctgctta ccagcagggc cagaaccagc tgtataacga gctgaatctg
1200
gggcggagag aggaatacga cgtgctggat aaaaggcgcg ggagagaccc agaaatgggg
1260
ggaaagccac gacggaaaaa cccccaggag ggactgtaca atgaactgca gaaggataaa
1320
atggcagagg cctattccga aatcgggatg aagggagaaa gaaggcgagg caaaggacac
1380
gacggactgt accaggggct gtctaccgcc acaaaggaca cctatgatgc tctgcatatg
1440
caggcactgc cacccagg
1458
<210> 571
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 571
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagga gtctggccca ggcctgatga agcccagcga gacactgtcc
120
ctgacctgca cagtgtctgg cggcagcatc agctcctctt actggagctg tatcaggcag
180
ccccctggca agggcctgga gtggatcggc tacatctact attccggcac cacaaactat
240
aatccttccc tgaagtctcg ggtgaccctg tctctggaca caagcaagaa ccagttctcc
300
ctgagactga cctctgtgac agccgccgat accgccgtgt actattgcgc cagagtggcc
360
cccacaggct tctggtttga ctattggggc cagggcaccc tggtgacagt gagctccgga
420
ggaggaggaa gcggaggagg agggtccgga ggcgggggat ctgagatcgt gctgacccag
480
tccccaggca cactgtccct gtctcccggc gagagagcca ccctgagctg cagggcctcc
540
cagagagtga gctccaggta cctggcctgg tatcagcaga agcctggcca ggcccccaga
600
ctgctgatct acggagcatc tagccgcgcc accggaatcc cagaccggtt cagcggatcc
660
ggatctggca cagacttcac cctgacaatc tctagactgg agcctgagga gttcgccgtg
720
tactattgtc agcagtatgg caccagccca ctgacatttg gcggcggcac aaaggtggag
780
atcaagacca caactcctgc acctaggcca cctaccccag cacctacaat tgctagtcag
840
ccactgtcac tgcgaccaga ggcatgtcga cctgcagctg gaggagcagt gcatacaagg
900
ggactggact ttgcctgcga tatctacatt tgggctcctc tggcaggaac atgtggcgtg
960
ctgctgctga gcctggtcat cactctgtac tgcaagcgag gccggaagaa actgctgtat
1020
attttcaaac agccctttat gcgacctgtg cagaccacac aggaggaaga tgggtgctcc
1080
tgtcggttcc ccgaggaaga ggaaggaggc tgtgagctgc gggtcaagtt ttccagatct
1140
gcagacgccc ctgcttacca gcagggccag aaccagctgt ataacgagct gaatctgggg
1200
cggagagagg aatacgacgt gctggataaa aggcgcggga gagacccaga aatgggggga
1260
aagccacgac ggaaaaaccc ccaggaggga ctgtacaatg aactgcagaa ggataaaatg
1320
gcagaggcct attccgaaat cgggatgaag ggagaaagaa ggcgaggcaa aggacacgac
1380
ggactgtacc aggggctgtc taccgccaca aaggacacct atgatgctct gcatatgcag
1440
gcactgccac ccagg
1455
<210> 572
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 572
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtcc agctggtcca gtcaggggcc gaggtgaaga aacctggggc ttctgtgaag
120
gtcagttgca aagctagtgg atactcattc cctgattact atatcaactg ggtgcgccag
180
gcaccaggac agggactgga gtggatggga tggatctact tcgctagcgg caactccgaa
240
tataatcaga agtttacagg cagagtgact atgaccaggg acacaagctc ctctactgcc
300
tatatggagc tgagttcact gcggagtgaa gataccgcag tgtacttctg cgcctctctg
360
tacgactatg attggtattt tgacgtctgg ggacagggca ctatggtgac cgtcagctcc
420
ggaggaggag gaagcggagg aggagggtcc ggaggcgggg gatctgatat cgtgatgaca
480
cagactcccc tgtcactgag cgtcactcca ggagagccag catccatttc ttgtaagtct
540
agtcagtcac tggtgcacag caacggaaat acctacctgc attggtatct gcagaagcct
600
ggccagagcc cacagctgct gatctacaaa gtgtccaata ggttctctgg cgtcccagac
660
cgctttagtg ggtcaggaag cggcgccgat ttcaccctga aaattagccg cgtggaggct
720
gaagacgtgg gcgtctacta ttgcgcagag acaagccacg tcccctggac ttttgggcag
780
ggaaccaagc tggaaatcaa aaccacaact cctgcaccta ggccacctac cccagcacct
840
acaattgcta gtcagccact gtcactgcga ccagaggcat gtcgacctgc agctggagga
900
gcagtgcata caaggggact ggactttgcc tgcgatatct acatttgggc tcctctggca
960
ggaacatgtg gcgtgctgct gctgagcctg gtcatcactc tgtactgcaa gcgaggccgg
1020
aagaaactgc tgtatatttt caaacagccc tttatgcgac ctgtgcagac cacacaggag
1080
gaagatgggt gctcctgtcg gttccccgag gaagaggaag gaggctgtga gctgcgggtc
1140
aagttttcca gatctgcaga cgcccctgct taccagcagg gccagaacca gctgtataac
1200
gagctgaatc tggggcggag agaggaatac gacgtgctgg ataaaaggcg cgggagagac
1260
ccagaaatgg ggggaaagcc acgacggaaa aacccccagg agggactgta caatgaactg
1320
cagaaggata aaatggcaga ggcctattcc gaaatcggga tgaagggaga aagaaggcga
1380
ggcaaaggac acgacggact gtaccagggg ctgtctaccg ccacaaagga cacctatgat
1440
gctctgcata tgcaggcact gccacccagg
1470
<210> 573
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 573
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagga gtctggccca ggcctggtga agccctctga gacactgagc
120
ctgacctgca cagtgagcga cgattccatc tctaactact attggtcctg gatcaggcag
180
ccccctggca agggcctgga gtggatcggc tacatcttct attccggcac cacaaaccac
240
aatcccagcc tgaagtcccg gctgacaatc tccctggaca aggccaagaa ccagttctct
300
ctgagactga gctccgtgac cgccgccgat acagccgtgt actattgtgc cagagtgttc
360
aactggggct tcgcctttga catctggggc cagggcacca tggtgacagt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctgag
480
atcgtgctga cccagtctcc aggcacactg tctctgagcc ccggcgagag ggccaccctg
540
agctgccgcg cctcccagcg gatctctaga acatacctgg cctggtatca gcagaagcct
600
ggccaggccc ccagactgct gatctacgga gcaagcagcc gggccaccgg aatccccgac
660
agattcaccg gctccggctc tggcacagac ttcaccctga caatcagcag actggagcct
720
gaggacttcg ccgtgtacta ttgtcagcag tatggcacct ccccactgac atttggcggc
780
ggcacaaagg tggagatcaa caccacaacc ccagcaccta ggccacctac acctgcacca
840
accatcgcca gccagcctct gtccctgaga ccagaggcct gtaggccagc agcaggagga
900
gcagtgcaca cccggggcct ggacttcgcc tgcgatatct acatctgggc accactggca
960
ggaacatgtg gcgtgctgct gctgtccctg gtcatcaccc tgtactgcaa gagaggcagg
1020
aagaagctgc tgtatatctt caagcagccc ttcatgagac ccgtgcagac aacccaggag
1080
gaggacggct gcagctgtag gttcccagag gaggaggagg gaggatgtga gctgcgcgtg
1140
aagttttccc ggtctgccga tgcacctgca taccagcagg gacagaacca gctgtataac
1200
gagctgaatc tgggccggag agaggagtac gacgtgctgg ataagaggag gggaagggac
1260
cctgagatgg gaggcaagcc tcggagaaag aacccacagg agggcctgta caatgagctg
1320
cagaaggaca agatggccga ggcctatagc gagatcggca tgaagggaga gaggcgccgg
1380
ggcaagggac acgatggcct gtatcagggc ctgtcaaccg ctacaaaaga tacctacgat
1440
gctctgcaca tgcaggctct gccaccaaga
1470
<210> 574
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 574
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagga gagcggccca ggcctggtga agccatctga gacactgagc
120
ctgacctgca cagtgagcga taactccatc tctaattact attggtcctg gatcaggcag
180
ccccctggca agggcctgga gtggatcgcc tacatctact attctggcac cacaaactat
240
aatcccagcc tgaagtccag agtgaccatc tccctggaca catctaagaa ccagttctcc
300
ctgcagctga gctccgtgac agcagcagat gcagccgtgt actattgtgc cagagtgttc
360
cactggggct tcgcctttga catctggggc cagggcacca tggtgacagt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctgag
480
atcgtgctga cccagagccc aggcacactg tctctgagcc ccggcgagag ggccaccctg
540
tcctgccggg cctctcagag agtgagcaac acatacctgg cctggtatca gcagaatccc
600
ggccaggccc ccagactgct gatctacgga gcaagctcca gggccaccgg aatcccagac
660
cgcttctccg gatctggaag cggcacagac ttcaccctga caatctcccg gctggagcct
720
gaggacttcg ccgtgtacta ttgtcagcag tatggcacct ctccactgac atttggcggc
780
ggcaccaagg tggagatcaa gaccacaacc ccagcaccta ggccacctac acctgcacca
840
accatcgcca gccagcctct gtccctgaga ccagaggcct gtaggccagc agcaggagga
900
gcagtgcaca cccggggcct ggacttcgcc tgcgatatct acatctgggc accactggca
960
ggaacatgtg gcgtgctgct gctgtccctg gtcatcaccc tgtactgcaa gagaggcagg
1020
aagaagctgc tgtatatctt caagcagccc ttcatgagac ccgtgcagac aacccaggag
1080
gaggacggct gcagctgtag gttcccagag gaggaggagg gaggatgtga gctgcgcgtg
1140
aagttttccc ggtctgccga tgcacctgca taccagcagg gacagaacca gctgtataac
1200
gagctgaatc tgggccggag agaggagtac gacgtgctgg ataagaggag gggaagggac
1260
cctgagatgg gaggcaagcc tcggagaaag aacccacagg agggcctgta caatgagctg
1320
cagaaggaca agatggccga ggcctatagc gagatcggca tgaagggaga gaggcgccgg
1380
ggcaagggac acgatggcct gtatcagggc ctgtcaaccg ctacaaaaga tacctacgat
1440
gctctgcaca tgcaggctct gccaccaaga
1470
<210> 575
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 575
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagga gagcggccca ggcctggtga agccatccga gaccctgtct
120
ctgacctgca cagtgagcaa cgtgtccatc agctcctact attggtcttg gatcaggcag
180
ccccctggca agggactgga gtggatcggc tacatctact atagcggcac cacaaactat
240
aatccctctc tgaagagcag agtgaccatg agcgtggaca catccaagaa ccagttctcc
300
ctgaagctgt ctagcgtgac cgccgccgat acagccgtgt acttttgtgc ccggctgtct
360
aattggggct tcgcctttga catctggggc cagggcacca tggtgacatt ctcctctgga
420
ggaggaggaa gcggaggagg agggtccgga ggcgggggat ctgagatcgt gctgacccag
480
tctccaggca cactgtctct gagccccggc gagagggcca ccctgtcctg cagagcctct
540
cagacaatca gctcctctta cctggcctgg tatcagcaga agcctggcca ggcacctcgg
600
ctgctgatct acggagcaag ctccagggcc accggaatcc cagaccgctt ctccggatct
660
ggaagcggca cagagtttac cctgacaatc agccggctgg agcctgagga tttcgccgtg
720
tactattgtc agcagtatgg ctggtcccca atcacctttg gccagggcac aaggctggag
780
atcaagacca caactcctgc acctaggcca cctaccccag cacctacaat tgctagtcag
840
ccactgtcac tgcgaccaga ggcatgtcga cctgcagctg gaggagcagt gcatacaagg
900
ggactggact ttgcctgcga tatctacatt tgggctcctc tggcaggaac atgtggcgtg
960
ctgctgctga gcctggtcat cactctgtac tgcaagcgag gccggaagaa actgctgtat
1020
attttcaaac agccctttat gcgacctgtg cagaccacac aggaggaaga tgggtgctcc
1080
tgtcggttcc ccgaggaaga ggaaggaggc tgtgagctgc gggtcaagtt ttccagatct
1140
gcagacgccc ctgcttacca gcagggccag aaccagctgt ataacgagct gaatctgggg
1200
cggagagagg aatacgacgt gctggataaa aggcgcggga gagacccaga aatgggggga
1260
aagccacgac ggaaaaaccc ccaggaggga ctgtacaatg aactgcagaa ggataaaatg
1320
gcagaggcct attccgaaat cgggatgaag ggagaaagaa ggcgaggcaa aggacacgac
1380
ggactgtacc aggggctgtc taccgccaca aaggacacct atgatgctct gcatatgcag
1440
gcactgccac ccagg
1455
<210> 576
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 576
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccagaggtgc agctggtgga gagcggagga ggactggtgc agcctggcgg atccctgagg
120
ctgtcttgcg cagcaagcgg cttcaccttt agctcctacg acatgcactg ggtgaggcag
180
gcaacaggca agggactgga gtgggtgtcc gccatcggac cagccggcga tacctactat
240
cccggctctg tgaagggccg gttcacaatc tccagagaga acgccaagaa ttctctgtat
300
ctgcagatga acagcctgag ggcaggcgac accgccgtgt actattgtgc cagagccgac
360
cccccttact attactatgg catggacgtg tggggccagg gcaccacagt gacagtgtct
420
agcggaggag gaggaagcgg aggaggaggg tccggaggcg ggggatctga catcgtgatg
480
acccagtccc ctctgtctct gcccgtgaca cctggcgagc cagcctctat cagctgcagg
540
agctcccaga gcctgctgca ctccaacgag tacaattatc tggattggta cctgcagaag
600
cctggccagt cccctcagct gctgatctat ctgggctcta acagggcaag cggagtgcca
660
gacagattct ccggctctgg cagcggcacc gacttcatcc tgaagatctc tcgggtggag
720
gcagaggacg tgggcgtgta ctattgtatg caggccctgg agatcccact gaccttcggc
780
ggaggaacaa aggtggagat caagaccaca actcctgcac ctaggccacc taccccagca
840
cctacaattg ctagtcagcc actgtcactg cgaccagagg catgtcgacc tgcagctgga
900
ggagcagtgc atacaagggg actggacttt gcctgcgata tctacatttg ggctcctctg
960
gcaggaacat gtggcgtgct gctgctgagc ctggtcatca ctctgtactg caagcgaggc
1020
cggaagaaac tgctgtatat tttcaaacag ccctttatgc gacctgtgca gaccacacag
1080
gaggaagatg ggtgctcctg tcggttcccc gaggaagagg aaggaggctg tgagctgcgg
1140
gtcaagtttt ccagatctgc agacgcccct gcttaccagc agggccagaa ccagctgtat
1200
aacgagctga atctggggcg gagagaggaa tacgacgtgc tggataaaag gcgcgggaga
1260
gacccagaaa tggggggaaa gccacgacgg aaaaaccccc aggagggact gtacaatgaa
1320
ctgcagaagg ataaaatggc agaggcctat tccgaaatcg ggatgaaggg agaaagaagg
1380
cgaggcaaag gacacgacgg actgtaccag gggctgtcta ccgccacaaa ggacacctat
1440
gatgctctgc atatgcaggc actgccaccc agg
1473
<210> 577
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 577
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacagatca cactgaagga gagcggccca accctggtga agcccaccca gacactgacc
120
ctgacatgca ccttctccgg cttttctctg agcaccagag gcgtgggagt gggatggatc
180
agacagcccc ctggcaaggc cctggagtgg ctggccctga tctactggaa cgacgataag
240
aggtattccc cttctctgca gacacgcctg acaatcacca aggacacccc aaagaaccag
300
gtggtgctga caatgaccaa tatggacccc gtggatacag ccacctacta ttgtgcccgg
360
tctaactggg gcaattggta cttcgcactg tggggaaggg gcacactggt gaccgtgagc
420
tccggaggag gaggaagcgg aggaggaggg tccggaggcg ggggatctga gatcgtgctg
480
acccagtctc cagccacact gtccctgtct cccggcgaga gggccaccct gagctgcaga
540
gccagccagt ccgtgagctc ctacctggcc tggtatcagc agaagcctgg ccaggcacct
600
cggctgctga tctacgacgc cttctatagg gccaccggca tcccagcacg cttctctgga
660
agcggatccg gcacagactt taccctgaca atctctagcc tggagcctga ggatttcgcc
720
gtgtactatt gtcagcaccg gtccaactgg ccaatcacct ttggccaggg cacaaggctg
780
gagatcaaga ccacaactcc tgcacctagg ccacctaccc cagcacctac aattgctagt
840
cagccactgt cactgcgacc agaggcatgt cgacctgcag ctggaggagc agtgcataca
900
aggggactgg actttgcctg cgatatctac atttgggctc ctctggcagg aacatgtggc
960
gtgctgctgc tgagcctggt catcactctg tactgcaagc gaggccggaa gaaactgctg
1020
tatattttca aacagccctt tatgcgacct gtgcagacca cacaggagga agatgggtgc
1080
tcctgtcggt tccccgagga agaggaagga ggctgtgagc tgcgggtcaa gttttccaga
1140
tctgcagacg cccctgctta ccagcagggc cagaaccagc tgtataacga gctgaatctg
1200
gggcggagag aggaatacga cgtgctggat aaaaggcgcg ggagagaccc agaaatgggg
1260
ggaaagccac gacggaaaaa cccccaggag ggactgtaca atgaactgca gaaggataaa
1320
atggcagagg cctattccga aatcgggatg aagggagaaa gaaggcgagg caaaggacac
1380
gacggactgt accaggggct gtctaccgcc acaaaggaca cctatgatgc tctgcatatg
1440
caggcactgc cacccagg
1458
<210> 578
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 578
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagga gagcggccca ggcctggtga agccatctga gaccctgagc
120
ctgacctgca cagtgtccgg cgattccatc tctaactact attggacatg gatcaggcag
180
ccccctggca agggactgga gtggatcggc tacatctact attctggcac cacaaactct
240
aatcccagcc tgaagagccg ggtgaccgtg tccctggaca caagcaagtc ccagttctct
300
ctgaacctga gctccgtgac cgccgccgat acagccgtgt actattgtgc cagagtgttc
360
aacagaggct tcgcctttga catctggggc cagggcacca tggtgacagt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctgag
480
atcgtgctga cccagagccc aggcacactg tctctgagcc ccggcgagag ggccaccctg
540
tcctgccggg cctctcagag aatcagcaac acatacctgg cctggtatca gcagaagcct
600
ggccaggccc ccagactgct gatctacgga gcaagctcca gggccaccgg aatcccagac
660
cgcttctccg gatctggaag cggcacagac ttcaccctga caatctccag gctggagcct
720
gaggacttcg cagcctacta ttgtcagcag tatgatacct ctccactgac atttggcggc
780
ggcaccaagg tggagatcaa gaccacaacc ccagcaccta ggccacctac acctgcacca
840
accatcgcca gccagcctct gtccctgaga ccagaggcct gtaggccagc agcaggagga
900
gcagtgcaca cccggggcct ggacttcgcc tgcgatatct acatctgggc accactggca
960
ggaacatgtg gcgtgctgct gctgtccctg gtcatcaccc tgtactgcaa gagaggcagg
1020
aagaagctgc tgtatatctt caagcagccc ttcatgagac ccgtgcagac aacccaggag
1080
gaggacggct gcagctgtag gttcccagag gaggaggagg gaggatgtga gctgcgcgtg
1140
aagttttccc ggtctgccga tgcacctgca taccagcagg gacagaacca gctgtataac
1200
gagctgaatc tgggccggag agaggagtac gacgtgctgg ataagaggag gggaagggac
1260
cctgagatgg gaggcaagcc tcggagaaag aacccacagg agggcctgta caatgagctg
1320
cagaaggaca agatggccga ggcctatagc gagatcggca tgaagggaga gaggcgccgg
1380
ggcaagggac acgatggcct gtatcagggc ctgtcaaccg ctacaaaaga tacctacgat
1440
gctctgcaca tgcaggctct gccaccaaga
1470
<210> 579
<211> 1482
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 579
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtga cactgaggga gtctggaccc gccctggtga agcctaccca gacactgacc
120
ctgacatgca ccgtgagcgg cgtgtctctg agcacctccg gcatgtgcgt gagctggatc
180
aggcagccac tgggcaaggc cctggagtgg ctgggcttca tcgattggga cgatgacaag
240
tactataaca caagcctgaa gacacgcctg accatctcca aggacacctc taagaaccag
300
gtggtgctga caatgaccaa tatggatccc gtggacacag ccacctacta ttgcgcccgg
360
atcagaggct actctggcag ctatgatgcc tttgacatct ggggccaggg caccgtggtc
420
atcgtgagct ccggaggagg aggaagcgga ggaggagggt ccggaggcgg gggatctgac
480
atcgtgatga cccagtcccc tctgtctctg cccgtgacac ctggcgagcc agcctctatc
540
agctgcagga gctcccagag cctgctgcac tccaacggct acaatcacct ggattggtat
600
ctgcagaagc ctggccagtc ccctcaggtg ctgatctacc tgggctctaa cagggcaagc
660
ggagtgccag acagattctc cggatctgga agcggaaccg acttcaccct gaagatctct
720
cgggtggagg cagaggacgt gggcgtgtat ttctgtatgc aggccctgca gacccccctg
780
acatttggcg gcggcaccaa ggtggagatc aagaccacaa ctcctgcacc taggccacct
840
accccagcac ctacaattgc tagtcagcca ctgtcactgc gaccagaggc atgtcgacct
900
gcagctggag gagcagtgca tacaagggga ctggactttg cctgcgatat ctacatttgg
960
gctcctctgg caggaacatg tggcgtgctg ctgctgagcc tggtcatcac tctgtactgc
1020
aagcgaggcc ggaagaaact gctgtatatt ttcaaacagc cctttatgcg acctgtgcag
1080
accacacagg aggaagatgg gtgctcctgt cggttccccg aggaagagga aggaggctgt
1140
gagctgcggg tcaagttttc cagatctgca gacgcccctg cttaccagca gggccagaac
1200
cagctgtata acgagctgaa tctggggcgg agagaggaat acgacgtgct ggataaaagg
1260
cgcgggagag acccagaaat ggggggaaag ccacgacgga aaaaccccca ggagggactg
1320
tacaatgaac tgcagaagga taaaatggca gaggcctatt ccgaaatcgg gatgaaggga
1380
gaaagaaggc gaggcaaagg acacgacgga ctgtaccagg ggctgtctac cgccacaaag
1440
gacacctatg atgctctgca tatgcaggca ctgccaccca gg
1482
<210> 580
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 580
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcaggt gtccggccct ggcctggtga agccttccga gacactgtct
120
ctgacctgca gcgtgtccgg cggctctatc agctcctact attggtcttg gatcaggcag
180
agcccaggca agggactgga ttggatcggc tacatgtact atagcggcac cacaaactat
240
aatccctctc tgaagagcag agtgacaatc agcgtggaca cctccaagaa ccagttttcc
300
ctgaagctgt ctagcgtgac cgccacagat accgccgtgt actattgtgc cagagtgggc
360
ctgacaggct tctttttcga ctactggggc cagggcacac tggtgaccgt gtcctctgga
420
ggaggaggaa gcggaggagg agggtccgga ggcgggggat ctgccatcca gatgacccag
480
tcccctagct ccctgagcgc ctccgtgggc gacagggtga ccatcacatg cagagcctct
540
cagggcatca ggaacgatct gggctggtat cagcagaagc ccggcaaggc ccctaagctg
600
ctgatctacg cagcatctag cctgcagtct ggagtgccaa gccggttctc tggaagcgga
660
tccggcaccg actttaccct gacagtgtcc tctctgcagc cagaggactt cgccacatac
720
tattgtctgc aggattacaa ttatccctac acctttggcc agggcacaaa gctggagatc
780
aagaccacaa ctcctgcacc taggccacct accccagcac ctacaattgc tagtcagcca
840
ctgtcactgc gaccagaggc atgtcgacct gcagctggag gagcagtgca tacaagggga
900
ctggactttg cctgcgatat ctacatttgg gctcctctgg caggaacatg tggcgtgctg
960
ctgctgagcc tggtcatcac tctgtactgc aagcgaggcc ggaagaaact gctgtatatt
1020
ttcaaacagc cctttatgcg acctgtgcag accacacagg aggaagatgg gtgctcctgt
1080
cggttccccg aggaagagga aggaggctgt gagctgcggg tcaagttttc cagatctgca
1140
gacgcccctg cttaccagca gggccagaac cagctgtata acgagctgaa tctggggcgg
1200
agagaggaat acgacgtgct ggataaaagg cgcgggagag acccagaaat ggggggaaag
1260
ccacgacgga aaaaccccca ggagggactg tacaatgaac tgcagaagga taaaatggca
1320
gaggcctatt ccgaaatcgg gatgaaggga gaaagaaggc gaggcaaagg acacgacgga
1380
ctgtaccagg ggctgtctac cgccacaaag gacacctatg atgctctgca tatgcaggca
1440
ctgccaccca gg
1452
<210> 581
<211> 1443
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 581
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagga ggactgctga agccctccga gaccctgtct
120
ctgacatgcg ccgtgtacgg aggaagctcc tctggaaact attggtcctg gatccggcag
180
ccccctggca agagactgga gtggatcggc gagatcaacc acagcggcac cacatcctac
240
aatccttctc tgaagagcag ggtgaccatc tctgtggaca caagcaagaa tcagttctcc
300
ctgaagctga gctccgtgac cgcagcagat acagccgtgt actattgcgc cagaggcgag
360
ctgggaatcg cagacagctg gggacagggc accctggtga cagtgtctag cggaggagga
420
ggaagcggag gaggagggtc cggaggcggg ggatctgata tccagatgac ccagtctccc
480
agcacactgt ccgcctctgt gggcgacagg gtgaccatca catgtcgcgc cagccagtcc
540
atctctcggt ggctggcctg gtaccagcag aagccaggca aggcccccaa gctgctgatc
600
tataaggcct cctctctgga gtccggcgtg ccttctagat tcagcggctc cggctctggc
660
accgagttta ccctgacaat cagctccctg cagccagacg atttcgccac ctactattgt
720
cagcagtaca acagctattc cacctttggc cagggcacaa aggtggagat caagaccaca
780
actcctgcac ctaggccacc taccccagca cctacaattg ctagtcagcc actgtcactg
840
cgaccagagg catgtcgacc tgcagctgga ggagcagtgc atacaagggg actggacttt
900
gcctgcgata tctacatttg ggctcctctg gcaggaacat gtggcgtgct gctgctgagc
960
ctggtcatca ctctgtactg caagcgaggc cggaagaaac tgctgtatat tttcaaacag
1020
ccctttatgc gacctgtgca gaccacacag gaggaagatg ggtgctcctg tcggttcccc
1080
gaggaagagg aaggaggctg tgagctgcgg gtcaagtttt ccagatctgc agacgcccct
1140
gcttaccagc agggccagaa ccagctgtat aacgagctga atctggggcg gagagaggaa
1200
tacgacgtgc tggataaaag gcgcgggaga gacccagaaa tggggggaaa gccacgacgg
1260
aaaaaccccc aggagggact gtacaatgaa ctgcagaagg ataaaatggc agaggcctat
1320
tccgaaatcg ggatgaaggg agaaagaagg cgaggcaaag gacacgacgg actgtaccag
1380
gggctgtcta ccgccacaaa ggacacctat gatgctctgc atatgcaggc actgccaccc
1440
agg
1443
<210> 582
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 582
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcagctgc agctgcagga gtccggccct ggcctggtga agccatccga gaccctgtct
120
ctgacctgca cagtgagcgg cggctccatc agctcctcta gctactattg gggctggatc
180
agacagcccc ctggcaaggg actggagtgg atcggcagca tctactattc cggcaacatc
240
taccacaatc cttctctgaa gagccgcgtg tctatcagcg tggacacctc caagaaccag
300
ttctctctga ggctgtcctc tgtgaccgca gcagatacag ccgtgtacta ttgcgccagg
360
gagatcatcg tgggagcaac ccactttgac tattggggcc agggcaccct ggtgacagtg
420
agctccggcg gcggcggctc tggaggagga ggcagcggcg gaggaggctc cggaggcggc
480
ggctctgcca tccagatgac acagtcccca tctagcctgt ccgcctctgt gggcgacagg
540
gtgaccatca catgtagagc cagccagggc atcaggaacg atctgggctg gtaccagcag
600
aagccaggca aggcccccga gctgctgatc tatgccgcct cctctctgca gtctggcgtg
660
ccaagcagat tcagcggctc cggctctggc accgacttta ccctgacaat cagctccctg
720
cagcccgagg acttcgccac atactattgt ctgcaggatt acaattatcc cctgaccttt
780
ggccctggca caaaggtgga tatcaagacc acaaccccag cacctaggcc acctacacct
840
gcaccaacca tcgccagcca gcctctgtcc ctgagaccag aggcctgtag gccagcagca
900
ggaggagcag tgcacacccg gggcctggac ttcgcctgcg atatctacat ctgggcacca
960
ctggcaggaa catgtggcgt gctgctgctg tccctggtca tcaccctgta ctgcaagaga
1020
ggcaggaaga agctgctgta tatcttcaag cagcccttca tgagacccgt gcagacaacc
1080
caggaggagg acggctgcag ctgtaggttc ccagaggagg aggagggagg atgtgagctg
1140
cgcgtgaagt tttcccggtc tgccgatgca cctgcatacc agcagggaca gaaccagctg
1200
tataacgagc tgaatctggg ccggagagag gagtacgacg tgctggataa gaggagggga
1260
agggaccctg agatgggagg caagcctcgg agaaagaacc cacaggaggg cctgtacaat
1320
gagctgcaga aggacaagat ggccgaggcc tatagcgaga tcggcatgaa gggagagagg
1380
cgccggggca agggacacga tggcctgtat cagggcctgt caaccgctac aaaagatacc
1440
tacgatgctc tgcacatgca ggctctgcca ccaaga
1476
<210> 583
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 583
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagca ggactgctga agccctccga gaccctgtct
120
ctgacatgcg ccgtgtacgg aggaagcttc tccggatact attggtcctg gatcaggcag
180
ccccctggca agggactgga gtggatcggc gagatcatcc actctggcag ctccaactat
240
aatccttctc tgaagagccg ggtgtctatc agcgtggaca cctctaagaa ccagttcagc
300
ctgaagctgt ctagcgtgac cgccgccgat acagccgtgt actattgctc cagaggcgag
360
tacggctccg gctctaggtt tgactattgg ggccagggca ccctggtgac agtgtcctct
420
ggaggaggag gaagcggagg aggagggtcc ggaggcgggg gatctgccat ccagatgacc
480
cagtccccaa gctccctgag cgcctccgtg ggcgataggg tggccatcac atgtagggca
540
agccagggaa tcagggacga tctgggctgg taccagcaga agccaggcaa ggcccccaag
600
ctgctgatct atgcagcatc tagcctgcag agcggagtgc catcccggtt ctctggaagc
660
agatccgaca ccgacttcac cctgacaatc tcctctctgc agcctgagga cttcgccaca
720
tactattgtc tgcaggacta cgattatcca ctgacctttg gcggcggcac aaaggtggag
780
atcaagacca caactcctgc acctaggcca cctaccccag cacctacaat tgctagtcag
840
ccactgtcac tgcgaccaga ggcatgtcga cctgcagctg gaggagcagt gcatacaagg
900
ggactggact ttgcctgcga tatctacatt tgggctcctc tggcaggaac atgtggcgtg
960
ctgctgctga gcctggtcat cactctgtac tgcaagcgag gccggaagaa actgctgtat
1020
attttcaaac agccctttat gcgacctgtg cagaccacac aggaggaaga tgggtgctcc
1080
tgtcggttcc ccgaggaaga ggaaggaggc tgtgagctgc gggtcaagtt ttccagatct
1140
gcagacgccc ctgcttacca gcagggccag aaccagctgt ataacgagct gaatctgggg
1200
cggagagagg aatacgacgt gctggataaa aggcgcggga gagacccaga aatgggggga
1260
aagccacgac ggaaaaaccc ccaggaggga ctgtacaatg aactgcagaa ggataaaatg
1320
gcagaggcct attccgaaat cgggatgaag ggagaaagaa ggcgaggcaa aggacacgac
1380
ggactgtacc aggggctgtc taccgccaca aaggacacct atgatgctct gcatatgcag
1440
gcactgccac ccagg
1455
<210> 584
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 584
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagga gtccggccct ggcctggtga agccaagcgg caccctgtcc
120
ctgacatgcg ccgtgtctgg cggcagcatc agctccaaca attggtggag ctgggtgagg
180
cagccccctg gcaagggact ggagtggatc ggcgacatcc accactccgg ctctaccaac
240
tacaagccat ccctgaagtc tcgcgtgaca atctctgtgg acaagagcaa gaaccagttc
300
tccctgaatc tgatcagcgt gaccgccgcc gatacagccg tgtactattg cgccagagag
360
gccggcggct actttgacta ttggggccag ggcatcctgg tgaccgtgtc tagcggcggc
420
ggcggctctg gaggaggagg cagcggcgga ggaggctccg gaggcggcgg ctctgatatc
480
cagatgaccc agagcccatc cacactgtct gccagcgtgg gcgacagggt gaccatcaca
540
tgtagagcct cccagtctat ctcctcttgg ctggcctggt atcagcagaa gccaggcaag
600
gcccccaagc tgctgatcag caaggcaagc tccctggagt ccggagtgcc atctaggttc
660
agcggatccg gctctggccc tgagtttacc ctgacaatct ctagcctgca gcctgccgat
720
ttcgccacct actattgtca gcagtacaat agctattcca cctttggcca gggcacaaag
780
ctggagatca agaccacaac cccagcacct aggccaccta cacctgcacc aaccatcgcc
840
agccagcctc tgtccctgag accagaggcc tgtaggccag cagcaggagg agcagtgcac
900
acccggggcc tggacttcgc ctgcgatatc tacatctggg caccactggc aggaacatgt
960
ggcgtgctgc tgctgtccct ggtcatcacc ctgtactgca agagaggcag gaagaagctg
1020
ctgtatatct tcaagcagcc cttcatgaga cccgtgcaga caacccagga ggaggacggc
1080
tgcagctgta ggttcccaga ggaggaggag ggaggatgtg agctgcgcgt gaagttttcc
1140
cggtctgccg atgcacctgc ataccagcag ggacagaacc agctgtataa cgagctgaat
1200
ctgggccgga gagaggagta cgacgtgctg gataagagga ggggaaggga ccctgagatg
1260
ggaggcaagc ctcggagaaa gaacccacag gagggcctgt acaatgagct gcagaaggac
1320
aagatggccg aggcctatag cgagatcggc atgaagggag agaggcgccg gggcaaggga
1380
cacgatggcc tgtatcaggg cctgtcaacc gctacaaaag atacctacga tgctctgcac
1440
atgcaggctc tgccaccaag a
1461
<210> 585
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 585
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagca ggactgctga agccctccga gaccctgtct
120
ctgacatgcg ccgtgtacgg cggctccttc tctggctact attggacctg gatcagacag
180
ccccctggca agggactgga gtggatcggc gagatcaccc acagcggctc cacaaactat
240
aatccttctc tgaagagcag ggtgtctatc agcgtggaca cctctaagaa ccagttcagc
300
ctgaagctga gctccgtgac cgcagcagat acagccgtgt actattgcgc cagaggcgag
360
tacggatccg gatctcggtt tgactattgg ggccagggca ccctggtgac agtgtctagc
420
ggaggaggag gaagcggagg aggagggtcc ggaggcgggg gatctgccat ccagatgacc
480
cagtccccat cctctctgag cgcctccgtg ggcgataggg tggcaatcac atgtagagcc
540
agccagggca tcagggacga tctgggctgg taccagcaga agccaggcaa ggcccccaag
600
ctgctgatct atgcagcaag ctccctgcag agcggagtgc catccagatt ctctggcagc
660
ggctccgaca ccgacttcac cctgacaatc tctagcctgc agcctgagga cttcgccaca
720
tactattgtc tgcaggacta cgattatcca ctgacctttg gcggcggcac aaaggtggag
780
atcaagacca caactcctgc acctaggcca cctaccccag cacctacaat tgctagtcag
840
ccactgtcac tgcgaccaga ggcatgtcga cctgcagctg gaggagcagt gcatacaagg
900
ggactggact ttgcctgcga tatctacatt tgggctcctc tggcaggaac atgtggcgtg
960
ctgctgctga gcctggtcat cactctgtac tgcaagcgag gccggaagaa actgctgtat
1020
attttcaaac agccctttat gcgacctgtg cagaccacac aggaggaaga tgggtgctcc
1080
tgtcggttcc ccgaggaaga ggaaggaggc tgtgagctgc gggtcaagtt ttccagatct
1140
gcagacgccc ctgcttacca gcagggccag aaccagctgt ataacgagct gaatctgggg
1200
cggagagagg aatacgacgt gctggataaa aggcgcggga gagacccaga aatgggggga
1260
aagccacgac ggaaaaaccc ccaggaggga ctgtacaatg aactgcagaa ggataaaatg
1320
gcagaggcct attccgaaat cgggatgaag ggagaaagaa ggcgaggcaa aggacacgac
1380
ggactgtacc aggggctgtc taccgccaca aaggacacct atgatgctct gcatatgcag
1440
gcactgccac ccagg
1455
<210> 586
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 586
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagca ggactgctga agccctccga gaccctgtct
120
ctgacatgcg ccgtgtacgg cggctccttc tctggctact attggtcctg gatcagacag
180
ccccctggca agggactgga gtggatcggc gagatcaccc acagcggctc cacaaactat
240
aatccttctc tgaagagcag ggtgtctatc agcgtggaca cctctaagaa ccagttcagc
300
ctgaagctga gctccgtgac cgcagcagat acagccgtgt actattgcgc cagaggcgag
360
tacggatccg gatctcggtt tgactattgg ggccagggca ccctggtgac agtgtctagc
420
ggaggaggag gaagcggagg aggagggtcc ggaggcgggg gatctgccat ccagatgacc
480
cagtccccat cctctctgag cgcctccgtg ggcgataggg tggccctgac atgtagagcc
540
agccagggca tcagggacga tctgggctgg taccagcaga agccaggcaa ggcccccaag
600
ctgctgatct atgcagcaag ctccctgcag agcggagtgc catccagatt ctctggcagc
660
ggctccgaca ccgacttcac cctgacaatc tctagcctgc agcctgagga cttcgccaca
720
tactattgtc tgcaggacta cgattatcca ctgacctttg gcggcggcac aaaggtggag
780
atcaagacca caactcctgc acctaggcca cctaccccag cacctacaat tgctagtcag
840
ccactgtcac tgcgaccaga ggcatgtcga cctgcagctg gaggagcagt gcatacaagg
900
ggactggact ttgcctgcga tatctacatt tgggctcctc tggcaggaac atgtggcgtg
960
ctgctgctga gcctggtcat cactctgtac tgcaagcgag gccggaagaa actgctgtat
1020
attttcaaac agccctttat gcgacctgtg cagaccacac aggaggaaga tgggtgctcc
1080
tgtcggttcc ccgaggaaga ggaaggaggc tgtgagctgc gggtcaagtt ttccagatct
1140
gcagacgccc ctgcttacca gcagggccag aaccagctgt ataacgagct gaatctgggg
1200
cggagagagg aatacgacgt gctggataaa aggcgcggga gagacccaga aatgggggga
1260
aagccacgac ggaaaaaccc ccaggaggga ctgtacaatg aactgcagaa ggataaaatg
1320
gcagaggcct attccgaaat cgggatgaag ggagaaagaa ggcgaggcaa aggacacgac
1380
ggactgtacc aggggctgtc taccgccaca aaggacacct atgatgctct gcatatgcag
1440
gcactgccac ccagg
1455
<210> 587
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 587
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagca ggactgctga agccttctga gaccctgagc
120
ctgacatgcg ccgtgtacgg cggcagcttt tccgcctact attggaactg gatcaggcag
180
ccccctggca agggactgga gtggatcggc gagatcaatc actctggcag caccaactat
240
aatcccagcc tgaagtcccg cgtgaccatc tccgtggaca catctaagaa ccagttttct
300
ctgaatctga ccagcctgac agccgccgat acagccgtgt actattgcgc cagaggcctg
360
gacagctccg gatggtaccc attcgattat tggggccagg gcaccctggt gacagtgtct
420
agcggaggag gaggaagcgg aggaggaggg tccggaggcg ggggatctga catccagatg
480
acccagtccc catccagcgt gagcgcctct gtgggcgata gggtgaccat cacatgtaga
540
gcaagccagg gaatcagctc ctggctggca tggtaccagc agaagccagg caaggccccc
600
aagctgctga tctatgcagc atctagcctg cagagcggag tgccatccag gtttagcgga
660
tccggatctg gaaccgactt caccctgaca atctcctctc tgcagcctga ggacttcgcc
720
acatactatt gtcagcaggc cgattccttc ccttttacct tcggcccagg cacaaaggtg
780
gatatcaaga ccacaactcc tgcacctagg ccacctaccc cagcacctac aattgctagt
840
cagccactgt cactgcgacc agaggcatgt cgacctgcag ctggaggagc agtgcataca
900
aggggactgg actttgcctg cgatatctac atttgggctc ctctggcagg aacatgtggc
960
gtgctgctgc tgagcctggt catcactctg tactgcaagc gaggccggaa gaaactgctg
1020
tatattttca aacagccctt tatgcgacct gtgcagacca cacaggagga agatgggtgc
1080
tcctgtcggt tccccgagga agaggaagga ggctgtgagc tgcgggtcaa gttttccaga
1140
tctgcagacg cccctgctta ccagcagggc cagaaccagc tgtataacga gctgaatctg
1200
gggcggagag aggaatacga cgtgctggat aaaaggcgcg ggagagaccc agaaatgggg
1260
ggaaagccac gacggaaaaa cccccaggag ggactgtaca atgaactgca gaaggataaa
1320
atggcagagg cctattccga aatcgggatg aagggagaaa gaaggcgagg caaaggacac
1380
gacggactgt accaggggct gtctaccgcc acaaaggaca cctatgatgc tctgcatatg
1440
caggcactgc cacccagg
1458
<210> 588
<211> 1443
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 588
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagca ggactgctga agccaagcga gaccctgtcc
120
ctgacatgcg ccgtgttcgg cggctctttt agcggcgact actggagctg gatcaggcag
180
ccccctggca agggactgga gtggatcggc gagatcaacc actctggcat caccagcttc
240
aatccctccc tgaagtctcg cgtgaccatc tccgtggaca catctaagaa ccagttttcc
300
ctgaagctga gctccgtgac cgcagcagat acagccgtgt actattgcgc cagaggcgag
360
ctgggcatcc ctgacaattg gggccagggc accctggtga cagtgtctag cggaggagga
420
ggaagcggag gaggagggtc cggaggcggg ggatctgata tccagatgac ccagtcccca
480
tctacactga gcgcctccgt gggcgatagg gtgaccatca catgtagagc ctctcagagc
540
atctcccggt ggctggcctg gtaccagcag aagccaggca aggcccccaa gctgctgatc
600
tataaggcat cctctctgga gagcggagtg ccatccaggt tctctggaag cggatccgga
660
accgagttta ccctgacaat cagctccctg cagcctgacg atttcgccac atactattgt
720
cagcagtaca actcttatag cacctttggc cagggcacaa aggtggagat caagaccaca
780
actcctgcac ctaggccacc taccccagca cctacaattg ctagtcagcc actgtcactg
840
cgaccagagg catgtcgacc tgcagctgga ggagcagtgc atacaagggg actggacttt
900
gcctgcgata tctacatttg ggctcctctg gcaggaacat gtggcgtgct gctgctgagc
960
ctggtcatca ctctgtactg caagcgaggc cggaagaaac tgctgtatat tttcaaacag
1020
ccctttatgc gacctgtgca gaccacacag gaggaagatg ggtgctcctg tcggttcccc
1080
gaggaagagg aaggaggctg tgagctgcgg gtcaagtttt ccagatctgc agacgcccct
1140
gcttaccagc agggccagaa ccagctgtat aacgagctga atctggggcg gagagaggaa
1200
tacgacgtgc tggataaaag gcgcgggaga gacccagaaa tggggggaaa gccacgacgg
1260
aaaaaccccc aggagggact gtacaatgaa ctgcagaagg ataaaatggc agaggcctat
1320
tccgaaatcg ggatgaaggg agaaagaagg cgaggcaaag gacacgacgg actgtaccag
1380
gggctgtcta ccgccacaaa ggacacctat gatgctctgc atatgcaggc actgccaccc
1440
agg
1443
<210> 589
<211> 1485
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 589
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagga gtccggccct ggcctggtga agccatccgg caccctgtct
120
ctgacatgcg tggtgttcgg cgacagcatc agctcctcta actggtggtc ctgggtgagg
180
cagccccctg gcaagggact ggagtggatc ggcgaggtgt tccactccgg ctctaccaac
240
tacaatccaa gcctgaagtc ccgcgtgaca atcagcgtgg ataagtccaa gaatcagttt
300
agcctgaagc tgagctccgt gaccgcagca gacacagccg tgtactattg cgccagagcc
360
gcagtggcag gcgccctgga ttattgggga cagggcaccc tggtgacagt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctgac
480
atcgtgatga cccagtctcc cgatagcctg gccgtgtctc tgggcgagag ggcaacaatc
540
aactgtaagt cctctcagag cgtgctgtac agctccaaca ataagaacta cctggcctgg
600
tatcagcaga agcctggcca gccacccaat ctgctggtgt attgggcctc taccagagag
660
agcggagtgc ctgacagatt ctccggagca ggatctggaa cagacttcac cctgacaatc
720
tctagcctgc aggccgagga cgtggccgtg tactattgtc agcagtacta tggcacctcc
780
tggacatttg gccagggcac caaggtggag atcaagacca caaccccagc acctaggcca
840
cctacacctg caccaaccat cgccagccag cctctgtccc tgagaccaga ggcctgtagg
900
ccagcagcag gaggagcagt gcacacccgg ggcctggact tcgcctgcga tatctacatc
960
tgggcaccac tggcaggaac atgtggcgtg ctgctgctgt ccctggtcat caccctgtac
1020
tgcaagagag gcaggaagaa gctgctgtat atcttcaagc agcccttcat gagacccgtg
1080
cagacaaccc aggaggagga cggctgcagc tgtaggttcc cagaggagga ggagggagga
1140
tgtgagctgc gcgtgaagtt ttcccggtct gccgatgcac ctgcatacca gcagggacag
1200
aaccagctgt ataacgagct gaatctgggc cggagagagg agtacgacgt gctggataag
1260
aggaggggaa gggaccctga gatgggaggc aagcctcgga gaaagaaccc acaggagggc
1320
ctgtacaatg agctgcagaa ggacaagatg gccgaggcct atagcgagat cggcatgaag
1380
ggagagaggc gccggggcaa gggacacgat ggcctgtatc agggcctgtc aaccgctaca
1440
aaagatacct acgatgctct gcacatgcag gctctgccac caaga
1485
<210> 590
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 590
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacagatca cactgaggga gagcggccct accctggtga agccaaccca gacactgacc
120
ctgacatgca ccttttccgg cttctccctg tctaccagcg gcctgggcgt gggatggatc
180
aggcagcccc ctggcgaggc cctggagtgg ctggccctga tctactggaa cgacgataag
240
cggtattccc cctctctgaa gtctagactg agcatcacaa aggacacctc caagaaccag
300
gtggtgctga tcatgacaaa tatggaccca gtggatacag ccacctacta ttgcgtgcac
360
aggagaatcg cagcccctgg cagcgtgtac tggggacagg gcacactggt gaccgtgagc
420
tccggaggag gaggaagcgg aggaggaggg tccggaggcg ggggatctga catccagatg
480
acccagtctc cttctagcgt gagcgcctcc gtgggcgata gggtgacaat cacctgtcgc
540
gccagccagg gcatctcctc ttggctggcc tggtatcagc agaagccagg caaggcacca
600
aagctgctga tcagcgccgc aagctccctg cagtccggag tgccatctcg gttttctggc
660
agcggctccg gcacagactt cacactgacc atctctagcc tgcagcccga ggattttgcc
720
acctactatt gtcaccaggc caattccttc ccttttacat tcggccaggg caccaagctg
780
gagatcaaga ccacaactcc tgcacctagg ccacctaccc cagcacctac aattgctagt
840
cagccactgt cactgcgacc agaggcatgt cgacctgcag ctggaggagc agtgcataca
900
aggggactgg actttgcctg cgatatctac atttgggctc ctctggcagg aacatgtggc
960
gtgctgctgc tgagcctggt catcactctg tactgcaagc gaggccggaa gaaactgctg
1020
tatattttca aacagccctt tatgcgacct gtgcagacca cacaggagga agatgggtgc
1080
tcctgtcggt tccccgagga agaggaagga ggctgtgagc tgcgggtcaa gttttccaga
1140
tctgcagacg cccctgctta ccagcagggc cagaaccagc tgtataacga gctgaatctg
1200
gggcggagag aggaatacga cgtgctggat aaaaggcgcg ggagagaccc agaaatgggg
1260
ggaaagccac gacggaaaaa cccccaggag ggactgtaca atgaactgca gaaggataaa
1320
atggcagagg cctattccga aatcgggatg aagggagaaa gaaggcgagg caaaggacac
1380
gacggactgt accaggggct gtctaccgcc acaaaggaca cctatgatgc tctgcatatg
1440
caggcactgc cacccagg
1458
<210> 591
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 591
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctggtgca gtccggagca gaggtgaaga agcctggcgc ctccgtgaag
120
gtgtcttgca aggtgagcgg ctacaccctg acagagctgt ctatgcactg ggtgcgccag
180
gcccccggca agggacctga gggaatggga ggattcgacc ctgaggatgg caagacaatc
240
tacgcccaga agtttcaggg ccgggtgacc atgacagagg acaccagcgc cgatacagcc
300
tatatggagc tgaactctct gcgcagcgag gacaccgccg tgtactattg cgccacactg
360
ctgaggggac tggacgcctt cgacgtgtgg ggacagggaa ccatggtgac agtgagctcc
420
ggaggaggag gaagcggagg aggagggtcc ggaggcgggg gatctgatat ccagatgacc
480
cagtctccat ctagcctgag cgcctccgtg ggcgacaggg tgaccatcac atgtagagcc
540
agccagggca tcaggaacga tctgggctgg taccagcaga agccaggcaa ggcccccaag
600
agactgatct atgcagcatc ctctctgcag tccggagtgc catctaggtt ctctggcagc
660
ggctccggca ccgagtttac cctgacaatc agcacactgc agcctgagga cttcgccacc
720
tactattgtc tgcagcacaa ttcctatcca cggacctttg gccagggcac aaaggtggag
780
atcaagacca caactcctgc acctaggcca cctaccccag cacctacaat tgctagtcag
840
ccactgtcac tgcgaccaga ggcatgtcga cctgcagctg gaggagcagt gcatacaagg
900
ggactggact ttgcctgcga tatctacatt tgggctcctc tggcaggaac atgtggcgtg
960
ctgctgctga gcctggtcat cactctgtac tgcaagcgag gccggaagaa actgctgtat
1020
attttcaaac agccctttat gcgacctgtg cagaccacac aggaggaaga tgggtgctcc
1080
tgtcggttcc ccgaggaaga ggaaggaggc tgtgagctgc gggtcaagtt ttccagatct
1140
gcagacgccc ctgcttacca gcagggccag aaccagctgt ataacgagct gaatctgggg
1200
cggagagagg aatacgacgt gctggataaa aggcgcggga gagacccaga aatgggggga
1260
aagccacgac ggaaaaaccc ccaggaggga ctgtacaatg aactgcagaa ggataaaatg
1320
gcagaggcct attccgaaat cgggatgaag ggagaaagaa ggcgaggcaa aggacacgac
1380
ggactgtacc aggggctgtc taccgccaca aaggacacct atgatgctct gcatatgcag
1440
gcactgccac ccagg
1455
<210> 592
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 592
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagca gtggggagca ggactgctga agccatccga gaccctgtct
120
ctgacatgcg ccgtgtatgg cggctccttc tctggctact attggcggtg gatcagacag
180
ccccctggca agggactgga gtggatcggc gagatcagcc actccggctc taccaactac
240
aatccctctc tgaagagccg cgtgaccatc agcgtggaca catccaagaa ccagttcagc
300
ctgaagctga gctccgtgac cgcagcagat acagccgtgt actattgcgc cgtgcggggc
360
tactcctatg gctaccccct gtttgactac tggggccagg gcaccctggt gacagtgtct
420
agcggaggag gaggaagcgg aggaggaggg tccggaggcg ggggatctga tatccagatg
480
acccagtccc cttcctctct gagcgcctcc gtgggcgaca gggtgaccat cacatgtcgc
540
gcctctcagg gcatccggaa cgatctgggc tggtatcagc agaagctggg caaggcccca
600
aagagactga tctacgcagc aagctccctg cagtctggag tgccaagcag gttctctgga
660
agcggatccg gaaccgagtt taccctgaca atctctagcc tgcagcctga ggacttcgcc
720
acatactatt gtctgcagta taatagctac ccacggacct ttggccaggg cacaaaggtg
780
gagatcaaga ccacaactcc tgcacctagg ccacctaccc cagcacctac aattgctagt
840
cagccactgt cactgcgacc agaggcatgt cgacctgcag ctggaggagc agtgcataca
900
aggggactgg actttgcctg cgatatctac atttgggctc ctctggcagg aacatgtggc
960
gtgctgctgc tgagcctggt catcactctg tactgcaagc gaggccggaa gaaactgctg
1020
tatattttca aacagccctt tatgcgacct gtgcagacca cacaggagga agatgggtgc
1080
tcctgtcggt tccccgagga agaggaagga ggctgtgagc tgcgggtcaa gttttccaga
1140
tctgcagacg cccctgctta ccagcagggc cagaaccagc tgtataacga gctgaatctg
1200
gggcggagag aggaatacga cgtgctggat aaaaggcgcg ggagagaccc agaaatgggg
1260
ggaaagccac gacggaaaaa cccccaggag ggactgtaca atgaactgca gaaggataaa
1320
atggcagagg cctattccga aatcgggatg aagggagaaa gaaggcgagg caaaggacac
1380
gacggactgt accaggggct gtctaccgcc acaaaggaca cctatgatgc tctgcatatg
1440
caggcactgc cacccagg
1458
<210> 593
<211> 1443
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 593
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccacaggtgc agctgcagga gagcggccct ggcctggtga agccatccgg caccctgtct
120
ctgacatgcg ccgtgagcgg cgactccatc agctccaact ggtggacatg ggtgaggcag
180
ccccctggca agggactgga gtggatcggc gatatccacc actccggctc taccaactac
240
aatccatctc tgaagagccg cgtgacaatg agcgtggaca agtccgagaa tcagttctcc
300
ctgaagctgt ctagcgtgac cgccgccgat acagccgtgt tttactgcgc cagagacgga
360
ggaggcaccc tggattattg gggccagggc accctggtga cagtgtcctc tggaggagga
420
ggaagcggag gaggagggtc cggaggcggg ggatctgaca tccagatgac ccagagccca
480
tccacactgt ctgccagcgt gggcgatcgg gtgaccatca catgtagagc ctcccagtct
540
atcagctcct ggctggcctg gtaccagcag aagccaggca aggcccccaa gctgctgatc
600
tataaggcat ctaccctgga gagcggagtg ccatccaggt tcagcggatc cggatctggc
660
acagagttta ccctgacaat ctctagcctg cagcctgacg atttcgccac ctactattgt
720
cagcagtaca acggctatag cacctttggc cagggcacaa aggtggagat caagaccaca
780
actcctgcac ctaggccacc taccccagca cctacaattg ctagtcagcc actgtcactg
840
cgaccagagg catgtcgacc tgcagctgga ggagcagtgc atacaagggg actggacttt
900
gcctgcgata tctacatttg ggctcctctg gcaggaacat gtggcgtgct gctgctgagc
960
ctggtcatca ctctgtactg caagcgaggc cggaagaaac tgctgtatat tttcaaacag
1020
ccctttatgc gacctgtgca gaccacacag gaggaagatg ggtgctcctg tcggttcccc
1080
gaggaagagg aaggaggctg tgagctgcgg gtcaagtttt ccagatctgc agacgcccct
1140
gcttaccagc agggccagaa ccagctgtat aacgagctga atctggggcg gagagaggaa
1200
tacgacgtgc tggataaaag gcgcgggaga gacccagaaa tggggggaaa gccacgacgg
1260
aaaaaccccc aggagggact gtacaatgaa ctgcagaagg ataaaatggc agaggcctat
1320
tccgaaatcg ggatgaaggg agaaagaagg cgaggcaaag gacacgacgg actgtaccag
1380
gggctgtcta ccgccacaaa ggacacctat gatgctctgc atatgcaggc actgccaccc
1440
agg
1443
<210> 594
<211> 1485
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 594
atggcactgc cagtgaccgc cctgctgctg cctctggccc tgctgctgca cgccgccagg
60
cctcaggtgc agctggtgca gtctggcgcc gaggtgaaga agccaggcag ctccgtgaag
120
gtgtcctgca aggcctctgg cggcacattc accaactatt gtatcagctg ggtgagacag
180
gccccaggcc agggactgga gtggatggga ggaatcatcc ccatcttcgg caccacaaat
240
tatgcccaga cctttcaggg ccgggtgaca atcaccgccg acaagtctac aagcaccgcc
300
tacatggagc tgtctagcct gagatccgag gatacagccg tgtactattg cgccagagac
360
aacggcgata gatactatta cgacatggac gtgtggggcc agggcaccac agtgaccgtg
420
tcctctggag gaggaggcag cggcggagga ggctccggag gcggcggctc tggcggcggc
480
ggctcccagt ctgtgctgac acagccacct agcgtgtccg ccgcccctgg ccagaaggtg
540
accatctctt gtagcggcag ctcctctaat atcggcaaca attacgtgag ctggtaccag
600
cagctgccag gcacagcccc caagctgctg atctacgaca acaataagag gcctagcggc
660
atcccagatc gcttctccgg ctctaagagc ggcacatccg ccaccctggg catcacagga
720
ctgcagaccg gcgacgaggc agattattac tgcggaacct gggacagctc cctgagcgcc
780
gtggtgtttg gaggaggcac aaagctgacc gtgctgacca caacccctgc ccctaggcca
840
cctaccccag cacctacaat tgctagtcag ccactgtcac tgcgaccaga ggcatgtcga
900
cctgcagctg gaggagcagt gcatacaagg ggactggact ttgcctgcga tatctacatt
960
tgggctcctc tggcaggaac atgtggcgtg ctgctgctga gcctggtcat cactctgtac
1020
tgcaagcgag gccggaagaa actgctgtat attttcaaac agccctttat gcgacctgtg
1080
cagaccacac aggaggaaga tgggtgctcc tgtcggttcc ccgaggaaga ggaaggaggc
1140
tgtgagctgc gggtcaagtt ttccagatct gcagacgccc ctgcttacca gcagggccag
1200
aaccagctgt ataacgagct gaatctgggg cggagagagg aatacgacgt gctggataaa
1260
aggcgcggga gagacccaga aatgggggga aagccacgac ggaaaaaccc ccaggaggga
1320
ctgtacaatg aactgcagaa ggataaaatg gcagaggcct attccgaaat cgggatgaag
1380
ggagaaagaa ggcgaggcaa aggacacgac ggactgtacc aggggctgtc taccgccaca
1440
aaggacacct atgatgctct gcatatgcag gcactgccac ccagg
1485
<210> 595
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 595
atggccctgc cagtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc ccctggtgca gagcggagca gaggtgaaga agcccggcag ctccgtgaag
120
gtgagctgca aggcctccgg cggcacattc tccacctatt ctatcagctg ggtgcggcag
180
gcccctggcc agggactgga gtggatggga ggaatcatcc caatcttcgg caccacaaac
240
tatgcccaga agtttcaggg cagggtgaca atcaccgccg acaagtccac atctaccgcc
300
tacatggagc tgtctagcct gaggtccgag gacacagccg tgtactattg tgcccgcgat
360
ggcgagggct cttactatta ctattacgga atggacgtgt ggggacaggg aaccacagtg
420
accgtgtcct ctggcggcgg cggctctgga ggaggaggca gcggcggagg aggctccgga
480
ggcggcggca gccagtccgt gctgacacag ccaccttctg tgagcgccgc ccctggccag
540
aaggtgacca tctcctgctc tggcagctcc tctaatatcg gcaacaatta tgtgagctgg
600
taccagcagc tgcctggcac agccccaaag ctgctgatct acgacaacaa taagcggccc
660
tccggcatcc ctgatagatt ctttggctct aagttcggca caagcgccac cctgggcatc
720
acaggactgc agaccggcga cgaggcagat tattactgtg gaacctggga cagctccctg
780
agcgccgtgg tgtttggagg aggcacaaag ctgaccgtgc tgaccacaac ccctgcccct
840
aggccaccta ccccagcacc tacaattgct agtcagccac tgtcactgcg accagaggca
900
tgtcgacctg cagctggagg agcagtgcat acaaggggac tggactttgc ctgcgatatc
960
tacatttggg ctcctctggc aggaacatgt ggcgtgctgc tgctgagcct ggtcatcact
1020
ctgtactgca agcgaggccg gaagaaactg ctgtatattt tcaaacagcc ctttatgcga
1080
cctgtgcaga ccacacagga ggaagatggg tgctcctgtc ggttccccga ggaagaggaa
1140
ggaggctgtg agctgcgggt caagttttcc agatctgcag acgcccctgc ttaccagcag
1200
ggccagaacc agctgtataa cgagctgaat ctggggcgga gagaggaata cgacgtgctg
1260
gataaaaggc gcgggagaga cccagaaatg gggggaaagc cacgacggaa aaacccccag
1320
gagggactgt acaatgaact gcagaaggat aaaatggcag aggcctattc cgaaatcggg
1380
atgaagggag aaagaaggcg aggcaaagga cacgacggac tgtaccaggg gctgtctacc
1440
gccacaaagg acacctatga tgctctgcat atgcaggcac tgccacccag g
1491
<210> 596
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 596
atggcactgc cagtgacagc cctgctgctg cctctggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagga gtccggccct ggcctggtga agccatctga gaccctgagc
120
ctgacatgta ccgtgtccgg cgattctatc agctcctact attggtcttg gatcaggcag
180
ccccctggca agggactgga gtggatcggc tacatgtact atagcggcat cacaaactat
240
aatcctagcc tgaagtcccg cgtgaacatc tccctggaca cctctaagaa tcagttcagc
300
ctgaagctgg gctccgtgac agcagcagat accgccgtgt actattgcgc aaggctgtcc
360
gtggcaggct tctactttga ctattggggc cagggcacac tggtgaccgt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggcggcgg cggctctgag
480
atcgtgctga cacagagccc aggcaccctg agcctgtccc ccggcgagcg ggccacactg
540
agctgtagag cctctcagag cgtgacccgg tcctacctgg cctggtatca gcagaagcca
600
ggccaggccc ccagactgct gatctacggc gcctcctcta gggccacaga catcccagat
660
cgcttctccg gctctggcag cggaaccgac tttacactga ccatcaacag actggagcct
720
gaggatttcg ccgtgtacta ttgccagcag tacggcacaa gcccactgac ctttggcggc
780
ggcaccaagg tggagatcaa gaccacaacc cctgccccta ggccacctac cccagcacct
840
acaattgcta gtcagccact gtcactgcga ccagaggcat gtcgacctgc agctggagga
900
gcagtgcata caaggggact ggactttgcc tgcgatatct acatttgggc tcctctggca
960
ggaacatgtg gcgtgctgct gctgagcctg gtcatcactc tgtactgcaa gcgaggccgg
1020
aagaaactgc tgtatatttt caaacagccc tttatgcgac ctgtgcagac cacacaggag
1080
gaagatgggt gctcctgtcg gttccccgag gaagaggaag gaggctgtga gctgcgggtc
1140
aagttttcca gatctgcaga cgcccctgct taccagcagg gccagaacca gctgtataac
1200
gagctgaatc tggggcggag agaggaatac gacgtgctgg ataaaaggcg cgggagagac
1260
ccagaaatgg ggggaaagcc acgacggaaa aacccccagg agggactgta caatgaactg
1320
cagaaggata aaatggcaga ggcctattcc gaaatcggga tgaagggaga aagaaggcga
1380
ggcaaaggac acgacggact gtaccagggg ctgtctaccg ccacaaagga cacctatgat
1440
gctctgcata tgcaggcact gccacccagg
1470
<210> 597
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 597
atggcactgc cagtgacagc cctgctgctg cctctggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagga gagcggccct ggcctggtga agccatctga gaccctgagc
120
ctgacatgta ccgtgagctc cgattccatc tctagctact attggtcttg gatcagacag
180
ccccctggca agggcctgga gtggatctcc tacatctact attccggcat ctctaactat
240
aatcctagcc tgaagagccg ggtgagcatc tctgtggaca cctccaagaa ccagttttct
300
ctgagactgt cctctgtgac agccgccgat accgccgtgt actattgcgc cagaatcagc
360
gtggccggct tctttttcga caattggggc cagggcacac tggtgaccgt gagctccgga
420
ggaggaggca gcggaggagg aggctccgga ggcggcggct ctggcggcgg cggcagcgag
480
atcatgctga cacagagccc agataccctg agcctgtccc ccggcgaaag ggccacactg
540
tcctgtagag cctctcagag cgtgtctagc tcctacctgg cctggtatca gcagaagcca
600
ggccaggcac ccaggctgct gatctacgga gcatctagca gggccgcagg agtgccagac
660
cgcttttccg gctctggcag cggcaccgat ttcacactga ccatctctcg cctggcccct
720
gaggactttg tggtgtacta ttgccagcag tatggcatct ccccactgac attcggcggc
780
ggcaccaagg tggagatcaa gaccacaacc cctgccccta ggccacctac cccagcacct
840
acaattgcta gtcagccact gtcactgcga ccagaggcat gtcgacctgc agctggagga
900
gcagtgcata caaggggact ggactttgcc tgcgatatct acatttgggc tcctctggca
960
ggaacatgtg gcgtgctgct gctgagcctg gtcatcactc tgtactgcaa gcgaggccgg
1020
aagaaactgc tgtatatttt caaacagccc tttatgcgac ctgtgcagac cacacaggag
1080
gaagatgggt gctcctgtcg gttccccgag gaagaggaag gaggctgtga gctgcgggtc
1140
aagttttcca gatctgcaga cgcccctgct taccagcagg gccagaacca gctgtataac
1200
gagctgaatc tggggcggag agaggaatac gacgtgctgg ataaaaggcg cgggagagac
1260
ccagaaatgg ggggaaagcc acgacggaaa aacccccagg agggactgta caatgaactg
1320
cagaaggata aaatggcaga ggcctattcc gaaatcggga tgaagggaga aagaaggcga
1380
ggcaaaggac acgacggact gtaccagggg ctgtctaccg ccacaaagga cacctatgat
1440
gctctgcata tgcaggcact gccacccagg
1470
<210> 598
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 598
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagca gagcggccct ggcctggtga agcctagcca gacactgtcc
120
ctgacctgtg ccatctctgg cgacagcgtg agctccaaca gcgccacatg gaattggatc
180
aggcagtccc catctcgcgg cctggagtgg ctgggacgga cctactatag atccaagtgg
240
tacgacgatt atgccgtgtc cgtgaagtct cgcatcacaa tcaaccctga cacctccaag
300
aatcacctgt ctctgcacct gaacagcgtg acaccagagg ataccgccgt gtactattgc
360
gcaggaggag gactggtggg cgcccctgac ggattcgacg tgtggggcca gggcacaatg
420
gtgaccgtgt ctagcggcgg cggcggctct ggaggaggag gcagcggcgg aggaggctcc
480
ggaggcggcg gctctcagtc cgtgctgaca cagccccctt ctgccagcgg aacacccggc
540
cagcgggtga ccatctcctg ttctggctcc tctagcaaca tcggctccga ccctgtgaat
600
tggtaccagc agctgccagg cacagccccc aagctgctga tctatagcaa caatcagcgg
660
ccttccggcg tgccagatag attcagcggc tccaagtctg gcaccagcgc ctccctggca
720
atctctggac tgcagagcga ggacgaggcc gattactatt gctccgcctg ggacgattct
780
ctgaatggct acgtgtttgg cacaggcacc aaggtgaccg tgctgaccac aaccccagca
840
cctaggccac ctacacctgc accaaccatc gccagccagc ctctgtccct gagaccagag
900
gcctgtaggc cagcagcagg aggagcagtg cacacccggg gcctggactt cgcctgcgat
960
atctacatct gggcaccact ggcaggaaca tgtggcgtgc tgctgctgtc cctggtcatc
1020
accctgtact gcaagagagg caggaagaag ctgctgtata tcttcaagca gcccttcatg
1080
agacccgtgc agacaaccca ggaggaggac ggctgcagct gtaggttccc agaggaggag
1140
gagggaggat gtgagctgcg cgtgaagttt tcccggtctg ccgatgcacc tgcataccag
1200
cagggacaga accagctgta taacgagctg aatctgggcc ggagagagga gtacgacgtg
1260
ctggataaga ggaggggaag ggaccctgag atgggaggca agcctcggag aaagaaccca
1320
caggagggcc tgtacaatga gctgcagaag gacaagatgg ccgaggccta tagcgagatc
1380
ggcatgaagg gagagaggcg ccggggcaag ggacacgatg gcctgtatca gggcctgtca
1440
accgctacaa aagataccta cgatgctctg cacatgcagg ctctgccacc aaga
1494
<210> 599
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 599
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctggtgca gagcggagca gaggtgaaga agcctggcgc cagcgtgaag
120
gtgtcctgca aggcctctgg ctacacattc accggctatt ctatccactg ggtgcgccag
180
gcccctggcc agggactgga gtggatgggc tggatcaacc caaatagcgg cggcaccttc
240
tacgcccaga agtttcaggg cagggtgaca atgacccgcg acacatctat cagcaccgtg
300
tatatggagc tgagccggct gagatccgac gatacagccg tgtactattg tgccagagac
360
ggctggggcg attactatta ctatggactg gacgtgtggg gacagggaac cacagtgacc
420
gtgtccctgg gcggcggcgg ctctggagga ggaggcagcg gcggaggagg ctccggaggc
480
ggcggctctg atatccagat gacacagagc cctagctccg tgtccgcctc tgtgggcgac
540
agggtgacaa tcacctgcag agcctcccag gatatctcta gctggctggc ctggtaccag
600
cagaagcccg gcaaggcccc taagctgctg atctataccg catcctctct gcagggagga
660
gtgccatccc ggttcagcgg ctccggctct ggaacagact ttacactgac catcagctcc
720
ctgcagccag aggatctggc cacctactct tgtcagcagg ccaacgtgtt cccctataca
780
tttggccagg gcaccaagct ggagatcaag accacaaccc cagcacctag gccacctaca
840
cctgcaccaa ccatcgccag ccagcctctg tccctgagac cagaggcctg taggccagca
900
gcaggaggag cagtgcacac ccggggcctg gacttcgcct gcgatatcta catctgggca
960
ccactggcag gaacatgtgg cgtgctgctg ctgtccctgg tcatcaccct gtactgcaag
1020
agaggcagga agaagctgct gtatatcttc aagcagccct tcatgagacc cgtgcagaca
1080
acccaggagg aggacggctg cagctgtagg ttcccagagg aggaggaggg aggatgtgag
1140
ctgcgcgtga agttttcccg gtctgccgat gcacctgcat accagcaggg acagaaccag
1200
ctgtataacg agctgaatct gggccggaga gaggagtacg acgtgctgga taagaggagg
1260
ggaagggacc ctgagatggg aggcaagcct cggagaaaga acccacagga gggcctgtac
1320
aatgagctgc agaaggacaa gatggccgag gcctatagcg agatcggcat gaagggagag
1380
aggcgccggg gcaagggaca cgatggcctg tatcagggcc tgtcaaccgc tacaaaagat
1440
acctacgatg ctctgcacat gcaggctctg ccaccaaga
1479
<210> 600
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 600
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccggaggtgc agctgctgga gtccggcggc ggcctggtgc agccaggcgg ctctctgagg
120
ctgagctgcg cagcatccgg cttcaccttt agctcctacg caatgaactg ggtgcgccag
180
gcccccggca agggactgga gtgggtgtct acaatctctg gcagcggcgg cagcacctac
240
tatgccgact ccgtgaaggg ccggttcaca atctctagag ataacagcaa gaataccctg
300
tacctgcaga tgaacagcct gcgggccgag gacacagccg tgttttattg tgccatcgac
360
ccagagtact atgatatcct gaccggcggc gattattggg gccagggcac actggtgacc
420
gtgtctagcg gcggcggcgg ctctggagga ggaggcagcg gcggaggagg ctccggaggc
480
ggcggctctg acatccagat gacccagtcc ccatctgcca tgagcgcctc cgtgggcgat
540
agggtgacaa tcacctgccg cgcctcccag ggcatctcta actacctggc ctggttccag
600
cagaagcccg gcaaggtgcc taagcggctg atctatgcag catcctctct gcagagcgga
660
gtgccttcca gattctctgg cagcggctcc ggcacagagt ttacactgac catcagctcc
720
ctgcagcccg aggacttcgc cacctacttt tgtctgcagc acgattcctt ccctctgaca
780
tttggcggcg gcaccaaggt ggagatcaag accacaaccc cagcacctag gccacctaca
840
cctgcaccaa ccatcgccag ccagcctctg tccctgagac cagaggcctg taggccagca
900
gcaggaggag cagtgcacac ccggggcctg gacttcgcct gcgatatcta catctgggca
960
ccactggcag gaacatgtgg cgtgctgctg ctgtccctgg tcatcaccct gtactgcaag
1020
agaggcagga agaagctgct gtatatcttc aagcagccct tcatgagacc cgtgcagaca
1080
acccaggagg aggacggctg cagctgtagg ttcccagagg aggaggaggg aggatgtgag
1140
ctgcgcgtga agttttcccg gtctgccgat gcacctgcat accagcaggg acagaaccag
1200
ctgtataacg agctgaatct gggccggaga gaggagtacg acgtgctgga taagaggagg
1260
ggaagggacc ctgagatggg aggcaagcct cggagaaaga acccacagga gggcctgtac
1320
aatgagctgc agaaggacaa gatggccgag gcctatagcg agatcggcat gaagggagag
1380
aggcgccggg gcaagggaca cgatggcctg tatcagggcc tgtcaaccgc tacaaaagat
1440
acctacgatg ctctgcacat gcaggctctg ccaccaaga
1479
<210> 601
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 601
atggctctgc ctgtcaccgc tctgctgctg cctctggctc tgctgctgca cgcggcgcgc
60
ccgcaggtgc agctgcagga gtccggccct ggcctggtga agccaagcga gaccctgtcc
120
ctgacatgta ccgtgagctc cgattctatc agcaactact attggagctg gatcaggcag
180
ccccctggca agggactgga gtggatctcc tacatctact attctggcat caccaactat
240
aatccttccc tgaagtctcg cgtgacaatc tctgtggaca ccagcaagaa tcagttcagc
300
ctgaagctgt ctagcgtgac agccgccgat accgccgtgt actattgcgc ccggatcaca
360
gtgaccggct tctactttga ctattggggc cagggcacac tggtgaccgt gtcctctggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctgag
480
atcgtgctga cacagtcccc aggcaccctg tccctgtctc ccggcgagcg ggccacactg
540
tcttgtagag ccagccagtc catctctcgg agctacctgg cctggtatca gcagaagcca
600
ggccaggccc ccagacacct gatctacgga gcaagctcca gggccaccgg catccccgac
660
cgcttctccg gctctggcag cggcacagac ttcatcctga ccatctccag actggagcct
720
gaggacttcg ccgtgtacta ttgccagcag tacgatacaa gcccactgac ctttggcggc
780
ggcaccaagg tggagatcaa gaccacaacc ccagcaccta ggccacctac acctgcacca
840
accatcgcca gccagcctct gtccctgaga ccagaggcct gtaggccagc agcaggagga
900
gcagtgcaca cccggggcct ggacttcgcc tgcgatatct acatctgggc accactggca
960
ggaacatgtg gcgtgctgct gctgtccctg gtcatcaccc tgtactgcaa gagaggcagg
1020
aagaagctgc tgtatatctt caagcagccc ttcatgagac ccgtgcagac aacccaggag
1080
gaggacggct gcagctgtag gttcccagag gaggaggagg gaggatgtga gctgcgcgtg
1140
aagttttccc ggtctgccga tgcacctgca taccagcagg gacagaacca gctgtataac
1200
gagctgaatc tgggccggag agaggagtac gacgtgctgg ataagaggag gggaagggac
1260
cctgagatgg gaggcaagcc tcggagaaag aacccacagg agggcctgta caatgagctg
1320
cagaaggaca agatggccga ggcctatagc gagatcggca tgaagggaga gaggcgccgg
1380
ggcaagggac acgatggcct gtatcagggc ctgtcaaccg ctacaaaaga tacctacgat
1440
gctctgcaca tgcaggctct gccaccaaga
1470
<210> 602
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 602
atggcactgc cagtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagca gagcggccct ggcctggtga agcctagcca gacactgtcc
120
ctgacctgtg ccatctctgg cgacagcgtg agctccaaca gcgtggtgtg gaattggatc
180
aggcagtccc catctcgcgg cctggagtgg ctgggacgga cctactatag atccaagtgg
240
tacgacgatt atgccgtgtc cgtgaagtct aggatcacaa tcaaccctga caccagcaag
300
aatcagttct ccctgcagct gaactctgtg acaccagagg ataccgccgt gtaccactgc
360
gccagaggcg gaatcgtggg cgcccctgac gcctttgata tctggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggcagc ggaggaggag gctccggagg cggcggctct
480
ggcggcggcg gcagccagtc cgtgctgacc cagccacctt ctgccagcgg aacacccggc
540
cagcgggtga ccatctcctg ttctggctcc tctagcaaca tcggctctga ccctgtgagc
600
tggtaccagc agttcccagg cacagccccc aagctgctga tctataccaa caatcagcgg
660
cctagcggcg tgccagatcg gttcagcggc tccaagtctg gcacaagcgc ctccctggca
720
atctccggac tgcagtctga ggacgaggcc gattactatt gcgccgcctg ggacgattcc
780
ctgaatggcc acgtgttcgg cacaggcacc aaggtgaccg tgctgaccac aacccccgcc
840
cctaggccac ctaccccagc acctacaatt gctagtcagc cactgtcact gcgaccagag
900
gcatgtcgac ctgcagctgg aggagcagtg catacaaggg gactggactt tgcctgcgat
960
atctacattt gggctcctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc
1020
actctgtact gcaagcgagg ccggaagaaa ctgctgtata ttttcaaaca gccctttatg
1080
cgacctgtgc agaccacaca ggaggaagat gggtgctcct gtcggttccc cgaggaagag
1140
gaaggaggct gtgagctgcg ggtcaagttt tccagatctg cagacgcccc tgcttaccag
1200
cagggccaga accagctgta taacgagctg aatctggggc ggagagagga atacgacgtg
1260
ctggataaaa ggcgcgggag agacccagaa atggggggaa agccacgacg gaaaaacccc
1320
caggagggac tgtacaatga actgcagaag gataaaatgg cagaggccta ttccgaaatc
1380
gggatgaagg gagaaagaag gcgaggcaaa ggacacgacg gactgtacca ggggctgtct
1440
accgccacaa aggacaccta tgatgctctg catatgcagg cactgccacc cagg
1494
<210> 603
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 603
atggccctgc cagtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagca gtccggccct ggcctggtga agccttctca gacactgagc
120
ctgacctgtg ccatctccgg cgactctgtg agctccaact ctgccgtgtg gaattggatc
180
agacagtccc cctctagagg cctggagtgg ctgggctgga catactatcg gagcaagtac
240
tataacgact acgccgtgag cctgaagtcc agaatcacaa tcaaccctga taccagcaag
300
aatcagttct ccctgcagct gaacagcctg acaccagagg ataccgccgt gtactattgc
360
accaggggcg gaatcgtggg cgcccctgac ggctttgata tctggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggcagc ggaggaggag gctccggagg cggcggctct
480
ggcggcggcg gcagccagtc cgccctgaca cagccacctt ctgccagcgg aacacccggc
540
cagcgcgtga ccatctcctg ttctggcagc aactccaata tcggctccaa ccctatcaat
600
tggtaccagc agctgccagg cacagccccc aagctgctga tctatagcaa caatcagagg
660
ccttccggcg tgccagaccg cttctctggc agcaagtccg gcacctctgc cagcctggca
720
atctccggac tgcagtctga ggacgaggcc gattactatt gcgcagcatg ggacgatagc
780
ctgaacggac acgtgtttgg cacaggcacc aaggtgaccg tgctgaccac aacccccgcc
840
cctaggccac ctaccccagc acctacaatt gctagtcagc cactgtcact gcgaccagag
900
gcatgtcgac ctgcagctgg aggagcagtg catacaaggg gactggactt tgcctgcgat
960
atctacattt gggctcctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc
1020
actctgtact gcaagcgagg ccggaagaaa ctgctgtata ttttcaaaca gccctttatg
1080
cgacctgtgc agaccacaca ggaggaagat gggtgctcct gtcggttccc cgaggaagag
1140
gaaggaggct gtgagctgcg ggtcaagttt tccagatctg cagacgcccc tgcttaccag
1200
cagggccaga accagctgta taacgagctg aatctggggc ggagagagga atacgacgtg
1260
ctggataaaa ggcgcgggag agacccagaa atggggggaa agccacgacg gaaaaacccc
1320
caggagggac tgtacaatga actgcagaag gataaaatgg cagaggccta ttccgaaatc
1380
gggatgaagg gagaaagaag gcgaggcaaa ggacacgacg gactgtacca ggggctgtct
1440
accgccacaa aggacaccta tgatgctctg catatgcagg cactgccacc cagg
1494
<210> 604
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 604
atggcactgc ctgtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccccaggtgc agctgcagga gagcggccca ggcctggtga agccaagcga gaccctgtcc
120
ctgacatgta ccgtgtctgg cggcagcatc agctcctact attggtcctg gatcagacag
180
tctcctggca agggcctgga gtggatcggc tacgtgtact attccgacat caccaactat
240
aatccatccc tgaagtctag agtgacaatc tctgtggata ccagcaagaa ccagttcagc
300
ctgaacctga acagcgtgac agccgccgac accgccttct acttttgcgc caggatcggc
360
gtggccggct tctactttga ttattggggc cagggcacac tggtgaccgt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggcggcgg cggctctgag
480
atcgtgctga cacagagccc agacaccctg agcctgtccc ctggcgagag ggccacactg
540
tcctgtaggg catctcagag cgtgtcccgg agatacctgg cctggtatca gcagaagcct
600
ggccaggcac ctcgcctgct gatctacgga gcatcctctc gggccacagg catccccgac
660
agattctctg gcagcggctc cggaaccgac ttcaccctga ccatctctag gctggagcca
720
gaggatttcg aggtgtacta ttgccagcag tatggcacat ccccaatcac ctttggccag
780
ggaacccgcc tggagatcaa gaccacaacc cctgccccta ggccacctac cccagcacct
840
acaattgcta gtcagccact gtcactgcga ccagaggcat gtcgacctgc agctggagga
900
gcagtgcata caaggggact ggactttgcc tgcgatatct acatttgggc tcctctggca
960
ggaacatgtg gcgtgctgct gctgagcctg gtcatcactc tgtactgcaa gcgaggccgg
1020
aagaaactgc tgtatatttt caaacagccc tttatgcgac ctgtgcagac cacacaggag
1080
gaagatgggt gctcctgtcg gttccccgag gaagaggaag gaggctgtga gctgcgggtc
1140
aagttttcca gatctgcaga cgcccctgct taccagcagg gccagaacca gctgtataac
1200
gagctgaatc tggggcggag agaggaatac gacgtgctgg ataaaaggcg cgggagagac
1260
ccagaaatgg ggggaaagcc acgacggaaa aacccccagg agggactgta caatgaactg
1320
cagaaggata aaatggcaga ggcctattcc gaaatcggga tgaagggaga aagaaggcga
1380
ggcaaaggac acgacggact gtaccagggg ctgtctaccg ccacaaagga cacctatgat
1440
gctctgcata tgcaggcact gccacccagg
1470
<210> 605
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 605
atggccctgc cagtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacagatcc agctgcagca gtccggccct ggcctggtga agcctagcca gacactgtcc
120
ctgacctgcg ccatctctgg cgacagcgtg agctccaact ctgccgtgtg gaattggatc
180
aggcagtccc catctcgcgg cctggagtgg ctgggaagga catactatag aagcaagtgg
240
tacaacgact atgccgtgtc cgtgaagtct aggatcacaa tcaagcctga taccgccaag
300
aaccagttct ccctgcagct gaacagcgtg acaccagagg ataccgccgt gtactatttc
360
acccgcggcg gaatcgtggg cgcccctgac gcctttgata tctggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggcagc ggaggaggag gctccggagg cggcggctct
480
ggcggcggcg gcagccagtc cgtgctgaca cagccccctt ctgccagcgg aacacccggc
540
cagcgggtga ccatctcctg ctctggctcc tctagcaaca tcggctccga ccctatcaat
600
tggtaccagc aggtgccagg cacagccccc aagctgctga tctatagcaa caatcagcgg
660
ccttccggcg tgccagatag attcagcggc tccaagtctg gcaccagcgc ctccctggca
720
atctctggac tgcagagcga ggacgaggcc gattactatt gtgccgcctg ggacgatagc
780
ctgaatggct acgtgtttgg cacaggcacc aaggtgaccg tgctgaccac aacccccgcc
840
cctaggccac ctaccccagc acctacaatt gctagtcagc cactgtcact gcgaccagag
900
gcatgtcgac ctgcagctgg aggagcagtg catacaaggg gactggactt tgcctgcgat
960
atctacattt gggctcctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc
1020
actctgtact gcaagcgagg ccggaagaaa ctgctgtata ttttcaaaca gccctttatg
1080
cgacctgtgc agaccacaca ggaggaagat gggtgctcct gtcggttccc cgaggaagag
1140
gaaggaggct gtgagctgcg ggtcaagttt tccagatctg cagacgcccc tgcttaccag
1200
cagggccaga accagctgta taacgagctg aatctggggc ggagagagga atacgacgtg
1260
ctggataaaa ggcgcgggag agacccagaa atggggggaa agccacgacg gaaaaacccc
1320
caggagggac tgtacaatga actgcagaag gataaaatgg cagaggccta ttccgaaatc
1380
gggatgaagg gagaaagaag gcgaggcaaa ggacacgacg gactgtacca ggggctgtct
1440
accgccacaa aggacaccta tgatgctctg catatgcagg cactgccacc cagg
1494
<210> 606
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 606
atggccctgc cagtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagca gagcggccct ggcctggtga agcctagcga gacactgtcc
120
ctgacctgtg ccatctctgg cgacagcgtg agctccaaca gcgccacatg gaattggatc
180
aggcagtccc catctcgcgg cctggagtgg ctgggacgga cctactatag atccgagtgg
240
tacaacgact atgccgtgtc cgtgaagtct cggatcacaa tcaaccctga tacctccaag
300
aatcacctgt ctctgcacct gaatagcgtg acaccagagg ataccgccgt gtactattgc
360
gcaggaggag gaatcgtggg cgcccctgac ggattcgacg tgtggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggctcc ggaggaggag gctctggcgg cggcggcagc
480
ggaggcggcg gcagccagtc cgtgctgaca cagccacctt ctgccagcgg aacacccggc
540
cagagggtga ccatctcctg ttctggctcc tctagcaaca tcggcagcga ccctgtgatc
600
tggtaccagc agctgccacg cacagccccc aagctgctga tctattccaa caatcagcgg
660
ccttctggcg tgccagatag attcagcggc tccaagtctg gcaccagcgc ctccctggca
720
atctctggac tgcagagcga ggacgaggcc gattactatt gcgccgcctg ggacgattcc
780
ctgaatggct acgtgtttgg cacaggcacc aaggtgaccg tgctgaccac aacccccgcc
840
cctaggccac ctaccccagc acctacaatt gctagtcagc cactgtcact gcgaccagag
900
gcatgtcgac ctgcagctgg aggagcagtg catacaaggg gactggactt tgcctgcgat
960
atctacattt gggctcctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc
1020
actctgtact gcaagcgagg ccggaagaaa ctgctgtata ttttcaaaca gccctttatg
1080
cgacctgtgc agaccacaca ggaggaagat gggtgctcct gtcggttccc cgaggaagag
1140
gaaggaggct gtgagctgcg ggtcaagttt tccagatctg cagacgcccc tgcttaccag
1200
cagggccaga accagctgta taacgagctg aatctggggc ggagagagga atacgacgtg
1260
ctggataaaa ggcgcgggag agacccagaa atggggggaa agccacgacg gaaaaacccc
1320
caggagggac tgtacaatga actgcagaag gataaaatgg cagaggccta ttccgaaatc
1380
gggatgaagg gagaaagaag gcgaggcaaa ggacacgacg gactgtacca ggggctgtct
1440
accgccacaa aggacaccta tgatgctctg catatgcagg cactgccacc cagg
1494
<210> 607
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 607
atggcactgc cagtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagca gagcggccct ggcctggtga agcctagcca gacactgtcc
120
ctgacctgtg ccatctctgg cgacagcgtg agctccaaca gcgccacctg gaattggatc
180
aggcagtccc catctacagg actggagtgg ctggcacgga cctactatag atccaagtgg
240
tacaacgact atgaggtgtc cgtgaagtct cagatcacaa tcaaccctga tacctccaag
300
aatcagttct ctctgcagct gaatagcgtg acaccagagg ataccgccgt gtactattgc
360
gccagaggcg gaatcgtggg cgcccctgac gcctttgata tctggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggctcc ggaggaggag gctctggcgg cggcggcagc
480
ggaggcggcg gcagccagtc cgtgctgaca cagccccctt ctgccagcgg aacacccggc
540
cagggagtga ccatctcctg ttctggctcc tctagcaaca tcggcagcaa ccctgtgaat
600
tggtaccagc agctgccagg cacagccccc aagctgctga tctattccaa caatcagagg
660
ccttctggcg tgccagaccg cttcagcgat tccaagtctg gcaccagcgc ctccctggca
720
atctctggac tgcagagcga ggacgaggcc gattactatt gctccgcctg ggacgattgg
780
ctgaatggct acgtgtttgg cacaggcacc aaggtgaccg tgctgaccac aacccccgcc
840
cctaggccac ctaccccagc acctacaatt gctagtcagc cactgtcact gcgaccagag
900
gcatgtcgac ctgcagctgg aggagcagtg catacaaggg gactggactt tgcctgcgat
960
atctacattt gggctcctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc
1020
actctgtact gcaagcgagg ccggaagaaa ctgctgtata ttttcaaaca gccctttatg
1080
cgacctgtgc agaccacaca ggaggaagat gggtgctcct gtcggttccc cgaggaagag
1140
gaaggaggct gtgagctgcg ggtcaagttt tccagatctg cagacgcccc tgcttaccag
1200
cagggccaga accagctgta taacgagctg aatctggggc ggagagagga atacgacgtg
1260
ctggataaaa ggcgcgggag agacccagaa atggggggaa agccacgacg gaaaaacccc
1320
caggagggac tgtacaatga actgcagaag gataaaatgg cagaggccta ttccgaaatc
1380
gggatgaagg gagaaagaag gcgaggcaaa ggacacgacg gactgtacca ggggctgtct
1440
accgccacaa aggacaccta tgatgctctg catatgcagg cactgccacc cagg
1494
<210> 608
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 608
atggcactgc cagtgacagc cctgctgctg cctctggccc tgctgctgca cgccgccagg
60
cctcaggtgc agctgcagga gtccggccct ggcctggtga agccatccga gaccctgtct
120
ctgacatgca ccgtgtccgg cgattctatc aacaattact tttggagctg gatcagacag
180
ccccctggca agggactgga gtggatcggc tacttctatc acaggggcgg caacaattat
240
aacccaagcc tgaagtcccg cgtgacaatc agcatcgaca cctccaagaa tcagttcagc
300
ctgaacctga acagcgtgac aagcgccgat accgccgtgt actattgtgc ccggctggcc
360
ctggccggct tctttttcga ctactggggc cagggcacac tggtgaccgt gagctccgga
420
ggaggaggct ccggcggcgg aggctctggc ggcggcggct ccggaggcgg cggcagcgac
480
atccagatga cacagtctcc aagcaccctg tccgcctctg tgggcgatag ggtgacaatc
540
acctgcagag ccagccagtc catctctagc tggctggcct ggtaccagca gaagccaggc
600
aaggccccca agctgctgat ctataaggcc tcctctctgg agtctggcgt gccaagccgg
660
ttttctggca gcggctccgg cacagagttc acactgacca tcagctccct gcagcccgac
720
gattttgcca cctactattg tcagcagtac aactcttata gcagaacatt cggccagggc
780
accaaggtgg agatcaagac cacaacccct gcccctaggc cacctacccc agcacctaca
840
attgctagtc agccactgtc actgcgacca gaggcatgtc gacctgcagc tggaggagca
900
gtgcatacaa ggggactgga ctttgcctgc gatatctaca tttgggctcc tctggcagga
960
acatgtggcg tgctgctgct gagcctggtc atcactctgt actgcaagcg aggccggaag
1020
aaactgctgt atattttcaa acagcccttt atgcgacctg tgcagaccac acaggaggaa
1080
gatgggtgct cctgtcggtt ccccgaggaa gaggaaggag gctgtgagct gcgggtcaag
1140
ttttccagat ctgcagacgc ccctgcttac cagcagggcc agaaccagct gtataacgag
1200
ctgaatctgg ggcggagaga ggaatacgac gtgctggata aaaggcgcgg gagagaccca
1260
gaaatggggg gaaagccacg acggaaaaac ccccaggagg gactgtacaa tgaactgcag
1320
aaggataaaa tggcagaggc ctattccgaa atcgggatga agggagaaag aaggcgaggc
1380
aaaggacacg acggactgta ccaggggctg tctaccgcca caaaggacac ctatgatgct
1440
ctgcatatgc aggcactgcc acccagg
1467
<210> 609
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 609
atggcactgc cagtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc ccctggtgca gtccggagca gaggtgaaga agcccggcag ctccgtgaag
120
gtgtcttgca aggccagcgg cggcacattc agcacctaca gcatctcctg ggtgcggcag
180
gcccctggcc agggactgga gtggatggga ggaatcatcc caatcttcgg caccacaaac
240
tacgcccaga agtttcaggg cagagtgaca atcaccgccg acaagtctac aagcaccgcc
300
tatatggagc tgtctagcct gaggtctgag gacaccgccg tgtactattg tgcccgcgat
360
ggcgagggca gctactatta ctattacgga atggacgtgt ggggacaggg aaccacagtg
420
acagtgtcct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctggc
480
ggcggcggct cccagtctgt gctgacccag ccacctagcg cctccggaac acccggccag
540
agggtgacca tctcttgcag cggcagctcc tctaacatcg gctccaatta cgtgtactgg
600
tatcagcagc tgcctggcac agccccaaag ctgctgatct acagcaacaa tcagcggccc
660
tccggcgtgc ctgacagatt ctccggctct aagagcggca cctccgcctc tctggcaatc
720
tccggactgc gctctgagga cgaggcagat tattactgtg cagcatggga cgatagcctg
780
tccggatggg tgtttggagg aggaacaaag ctgaccgtgc tgaccacaac ccctgcccct
840
aggccaccta ccccagcacc tacaattgct agtcagccac tgtcactgcg accagaggca
900
tgtcgacctg cagctggagg agcagtgcat acaaggggac tggactttgc ctgcgatatc
960
tacatttggg ctcctctggc aggaacatgt ggcgtgctgc tgctgagcct ggtcatcact
1020
ctgtactgca agcgaggccg gaagaaactg ctgtatattt tcaaacagcc ctttatgcga
1080
cctgtgcaga ccacacagga ggaagatggg tgctcctgtc ggttccccga ggaagaggaa
1140
ggaggctgtg agctgcgggt caagttttcc agatctgcag acgcccctgc ttaccagcag
1200
ggccagaacc agctgtataa cgagctgaat ctggggcgga gagaggaata cgacgtgctg
1260
gataaaaggc gcgggagaga cccagaaatg gggggaaagc cacgacggaa aaacccccag
1320
gagggactgt acaatgaact gcagaaggat aaaatggcag aggcctattc cgaaatcggg
1380
atgaagggag aaagaaggcg aggcaaagga cacgacggac tgtaccaggg gctgtctacc
1440
gccacaaagg acacctatga tgctctgcat atgcaggcac tgccacccag g
1491
<210> 610
<211> 1482
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 610
atggcactgc cagtgacagc cctgctgctg ccactggccc tgctgctgca cgccgccaga
60
cccgaggtgc agctggtgga gtccggagga ggactggtgc agcctggcgg ctccctgagg
120
ctgtcttgcg cagcaagcgg cttcaccttt agctcctaca gcatgaactg ggtgagacag
180
gcccccggca agggactgga gtgggtgtct tatatctcta gctcctctag cacaatctac
240
tatgccgaca gcgtgaaggg ccggttcacc atctctagag ataacgccaa gaatagcctg
300
tacctgcaga tgaacagcct gagggacgag gatacagccg tgtactattg tgcccgcgac
360
aaggagcgga gatactatta ctatggcatg gacgtgtggg gccagggcac cacagtgacc
420
gtgtcctctg gcggcggcgg ctccggaggc ggcggctctg gaggaggagg cagcggcgga
480
ggaggctccg agatcgtgct gacacagtcc cctgacaccc tgtctctgag cccaggcgag
540
agggccacac tgtcttgcag ggcatcccag tctgtgagca ggcgctacct ggcctggtat
600
cagcagaagc ctggccaggc ccccagactg ctgatctacg gagcaagcag ccgggccaca
660
ggcatccctg acagattctc cggctctggc agcggaaccg acttcaccct gaccatctcc
720
aggctggagc cagaggattt tgccgtgtac tattgtcagc agttcggcac aagcccaatc
780
acctttggcc agggaacccg cctggagatc aagaccacaa ccccagcccc taggccacct
840
accccagcac ctacaattgc tagtcagcca ctgtcactgc gaccagaggc atgtcgacct
900
gcagctggag gagcagtgca tacaagggga ctggactttg cctgcgatat ctacatttgg
960
gctcctctgg caggaacatg tggcgtgctg ctgctgagcc tggtcatcac tctgtactgc
1020
aagcgaggcc ggaagaaact gctgtatatt ttcaaacagc cctttatgcg acctgtgcag
1080
accacacagg aggaagatgg gtgctcctgt cggttccccg aggaagagga aggaggctgt
1140
gagctgcggg tcaagttttc cagatctgca gacgcccctg cttaccagca gggccagaac
1200
cagctgtata acgagctgaa tctggggcgg agagaggaat acgacgtgct ggataaaagg
1260
cgcgggagag acccagaaat ggggggaaag ccacgacgga aaaaccccca ggagggactg
1320
tacaatgaac tgcagaagga taaaatggca gaggcctatt ccgaaatcgg gatgaaggga
1380
gaaagaaggc gaggcaaagg acacgacgga ctgtaccagg ggctgtctac cgccacaaag
1440
gacacctatg atgctctgca tatgcaggca ctgccaccca gg
1482
<210> 611
<211> 1494
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 611
atggcactgc cagtgacagc cctgctgctg ccactggccc tgctgctgca cgccgccaga
60
ccccaggtgc agctgcagca gagcggccct ggcctggtga agcctagcca gaccctgtcc
120
ctggcctgtg ccatctctgg cgacagcgtg agctccaact ccgccatctg gaattggatc
180
aggcagtccc cttctcgcgg cctggagtgg ctgggaggaa catactatcg gtctatgtgg
240
tacaacgact atgccgtgtc cgtgaagtct agaatcacaa tcaaccctga tacctccaag
300
aatcagctgt ctctgcagct gaatagcgtg acaccagagg ataccgccgt gtactattgc
360
agccggggcg gaatcgtggg agtgccagac gccttcgata tctggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggctcc ggaggaggag gctctggcgg cggcggcagc
480
ggaggcggcg gcagccagtc cgtgctgacc cagccacctt ctgccagcgg aacacccggc
540
cagcgggtga ccatctcctg ttctggctcc tctagcaaca tcggcagcaa cacagccaat
600
tggtaccagc agctgccagg caccgcaccc aggctgctga tctatcggaa caatcagaga
660
ccttccggag tgccagaccg cttcagcggc tccaagtctg gcacaagcgc ctccctggcc
720
atctctggcc tgcagagcga ggacgaggcc gattactatt gcgccgcctg ggacgatagc
780
ctgaatggct acgtgtttgg cacaggcacc aaggtgaccg tgctgaccac aacccctgcc
840
cctaggccac ctaccccagc acctacaatt gctagtcagc cactgtcact gcgaccagag
900
gcatgtcgac ctgcagctgg aggagcagtg catacaaggg gactggactt tgcctgcgat
960
atctacattt gggctcctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc
1020
actctgtact gcaagcgagg ccggaagaaa ctgctgtata ttttcaaaca gccctttatg
1080
cgacctgtgc agaccacaca ggaggaagat gggtgctcct gtcggttccc cgaggaagag
1140
gaaggaggct gtgagctgcg ggtcaagttt tccagatctg cagacgcccc tgcttaccag
1200
cagggccaga accagctgta taacgagctg aatctggggc ggagagagga atacgacgtg
1260
ctggataaaa ggcgcgggag agacccagaa atggggggaa agccacgacg gaaaaacccc
1320
caggagggac tgtacaatga actgcagaag gataaaatgg cagaggccta ttccgaaatc
1380
gggatgaagg gagaaagaag gcgaggcaaa ggacacgacg gactgtacca ggggctgtct
1440
accgccacaa aggacaccta tgatgctctg catatgcagg cactgccacc cagg
1494
<210> 612
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 612
atggcactgc ctgtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagga gtccggccca ggcctggtga agccatctga gacactgagc
120
ctgacctgca acgtgtctga tggcagcatc agctcctact attggacctg gatcagacag
180
ccccctggca agggactgga ctggatcggc tatatcttct acagcggcac cacaaactat
240
aatccctccc tgaagtctag agtgacaatc tccctggaca cctctaagaa tcagttttct
300
ctgaagctga caagcatgac cgccgccgat acagccgtgt actattgcgc caggatcagc
360
gagaagtcct tctattttga ctactggggc cagggcacac tggtgaccgt gtctagcgga
420
ggaggaggct ccggaggagg aggctctggc ggcggcggca gcggaggcgg cggctcccag
480
tctgtgctga cccagccacc aagcgcctcc ggaacacctg gccagcgcgt gaccatctct
540
tgtagcggct cctctagcaa catcggctcc aattacgtgt attggtacca gcagctgcct
600
ggcacagccc caaagctgct gatctactcc aacaatcagc ggcccagcgg cgtgcctgat
660
agattctccg gctctaagag cggcacctcc gcctctctgg caatcagcgg actgaggtcc
720
gaggacgagg cagattacta ttgtgcacca tgggacgata gcctgtccgg ccgcgtgttt
780
ggaggaggaa caaagctgac cgtgctgacc acaacccctg cccctaggcc acctacccca
840
gcacctacaa ttgctagtca gccactgtca ctgcgaccag aggcatgtcg acctgcagct
900
ggaggagcag tgcatacaag gggactggac tttgcctgcg atatctacat ttgggctcct
960
ctggcaggaa catgtggcgt gctgctgctg agcctggtca tcactctgta ctgcaagcga
1020
ggccggaaga aactgctgta tattttcaaa cagcccttta tgcgacctgt gcagaccaca
1080
caggaggaag atgggtgctc ctgtcggttc cccgaggaag aggaaggagg ctgtgagctg
1140
cgggtcaagt tttccagatc tgcagacgcc cctgcttacc agcagggcca gaaccagctg
1200
tataacgagc tgaatctggg gcggagagag gaatacgacg tgctggataa aaggcgcggg
1260
agagacccag aaatgggggg aaagccacga cggaaaaacc cccaggaggg actgtacaat
1320
gaactgcaga aggataaaat ggcagaggcc tattccgaaa tcgggatgaa gggagaaaga
1380
aggcgaggca aaggacacga cggactgtac caggggctgt ctaccgccac aaaggacacc
1440
tatgatgctc tgcatatgca ggcactgcca cccagg
1476
<210> 613
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 613
atggccctgc cagtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgccagg
60
ccccaggtgc agctggtgca gagcggagca gaggtgaagc gccctggcgc aagcgtgaag
120
gtgtcctgca aggcctctgg ctatacattc accagctact atatccactg ggtgaggcag
180
gcccctggcc agggactgga gtggatgggc gtgatcgtgc catccggcgg ctctatcagc
240
tatgcccaga agtttcaggg cagggtgaca atgacccgcg acacaagcac caacatcgtg
300
tacatggagc tgagctccct gcggtccgag gatacagccg tgtactattg tgccagagac
360
agatactatg gcgattacta ttacggactg gacgtgtggg gacagggaac cacagtgacc
420
gtgtctagcg gcggcggcgg ctctggagga ggaggcagcg gcggaggagg ctccggcggc
480
ggcggctctg acatccagat gacacagtcc ccttcctctc tgtccgcctc tgtgggcgat
540
cgggtgacaa tcacctgcag agcctctcag ggcatcaaca atttcctggc ctggtttcag
600
cagaagcccg gcaaggcccc taagtccctg atctacgcag caagctccct gcagagcgga
660
gtgccatcca agttcagcgg ctccggctct ggcacagact ttacactgac catccggtct
720
ctgcagccag aggatttcgc cacctattac tgtcagcact ataatagcta ccccatcaca
780
tttggccagg gcaccagact ggagatcaag accacaaccc ccgcccctag gccacctacc
840
ccagcaccta caattgctag tcagccactg tcactgcgac cagaggcatg tcgacctgca
900
gctggaggag cagtgcatac aaggggactg gactttgcct gcgatatcta catttgggct
960
cctctggcag gaacatgtgg cgtgctgctg ctgagcctgg tcatcactct gtactgcaag
1020
cgaggccgga agaaactgct gtatattttc aaacagccct ttatgcgacc tgtgcagacc
1080
acacaggagg aagatgggtg ctcctgtcgg ttccccgagg aagaggaagg aggctgtgag
1140
ctgcgggtca agttttccag atctgcagac gcccctgctt accagcaggg ccagaaccag
1200
ctgtataacg agctgaatct ggggcggaga gaggaatacg acgtgctgga taaaaggcgc
1260
gggagagacc cagaaatggg gggaaagcca cgacggaaaa acccccagga gggactgtac
1320
aatgaactgc agaaggataa aatggcagag gcctattccg aaatcgggat gaagggagaa
1380
agaaggcgag gcaaaggaca cgacggactg taccaggggc tgtctaccgc cacaaaggac
1440
acctatgatg ctctgcatat gcaggcactg ccacccagg
1479
<210> 614
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 614
atggcactgc cagtgacagc cctgctgctg cctctggccc tgctgctgca cgccgcccgg
60
ccacaggtgc acctgcagga gtctggccct ggcctggtga agccatctga gacactgagc
120
ctgacatgta ccgtgagcgg cggcagcatc tcccactact attggacctg gatcaggcag
180
ccccctggca agggactgga gtggatcggc tacatctact attccggcat caccaacttc
240
tctcctagcc tgaagtctcg cgtgtccatc tctgtggaca gctccaagaa tcagttcagc
300
ctgaacctga acagcgtgac agccgccgat accgccgtgt actattgcgc cggcatctcc
360
ctggccggct tctactttga ctattgggtg cagggcacac tggtgaccgt gtctagcgga
420
ggaggaggca gcggaggagg aggctccgga ggcggcggct ctggcggcgg cggcagcgag
480
atcgtgctga cacagagccc aggcaccctg agcctgtccc ccggcgagcg ggccaccctg
540
tcctgtagag cctctcagag cgtgtcccgg tcttacctgg cctggtatca gcagaagcca
600
ggccaggccc ccagactgct gatctatgga gcatcctcta gggccacagg agtgccagac
660
cgcttcagcg gctccggctc tggaaccgac ttcaccctga ccatcagccg gctggagcct
720
gaggatttcg ccgtgtttta ctgccagcag tatagcatct ccccactgac attcggcggc
780
ggcaccaagg tggagatcaa gaccacaacc cctgccccta ggccacctac cccagcacct
840
acaattgcta gtcagccact gtcactgcga ccagaggcat gtcgacctgc agctggagga
900
gcagtgcata caaggggact ggactttgcc tgcgatatct acatttgggc tcctctggca
960
ggaacatgtg gcgtgctgct gctgagcctg gtcatcactc tgtactgcaa gcgaggccgg
1020
aagaaactgc tgtatatttt caaacagccc tttatgcgac ctgtgcagac cacacaggag
1080
gaagatgggt gctcctgtcg gttccccgag gaagaggaag gaggctgtga gctgcgggtc
1140
aagttttcca gatctgcaga cgcccctgct taccagcagg gccagaacca gctgtataac
1200
gagctgaatc tggggcggag agaggaatac gacgtgctgg ataaaaggcg cgggagagac
1260
ccagaaatgg ggggaaagcc acgacggaaa aacccccagg agggactgta caatgaactg
1320
cagaaggata aaatggcaga ggcctattcc gaaatcggga tgaagggaga aagaaggcga
1380
ggcaaaggac acgacggact gtaccagggg ctgtctaccg ccacaaagga cacctatgat
1440
gctctgcata tgcaggcact gccacccagg
1470
<210> 615
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 615
atggcactgc ctgtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccccaggtgc agctgcagga gtccggccca ggcctggtga agccaagcga gaccctgtcc
120
ctgacatgca ccgtgtccgg cgtgtctatc agctcctact attggagctg gatcaggcag
180
ccccctggca agggactgga gtggatcgcc tacatctact attccggcaa caccaattat
240
tctcctagcc tgaagtctcg cgtgacaatc tctgtggaca ccagcaagga tcagctgtct
300
ctgaagctgt ctagcgtgac agccgccgac accgccgtgt actattgcac aaggggcggc
360
agcggaacca tcgacgtgtt cgatatctgg ggacagggaa ccatggtggc cgtgtcctct
420
ggcggcggcg gctccggagg cggcggctct ggaggaggag gcagcggcgg aggaggctcc
480
cagtctgtgc tgacacagcc accaagcgtg tccgccgccc caggccagaa ggtgaccatc
540
tcttgtagcg gcagctcctc taacatcggc aacaattacg tgtcctggta tcagcagctg
600
cctggcacag ccccaaagct gctgatctac gacaacaata agcggcccag cggcatccct
660
gatagattct ccggctctaa gagcggcaca tccgccaccc tgggcatcac aggactgcag
720
accggcgacg aggcagatta ctattgtgag acctgggata gctccctgag cgccgtggtg
780
tttggaggag gcacaaagct gaccgtgctg accacaaccc ctgcccctag gccacctacc
840
ccagcaccta caattgctag tcagccactg tcactgcgac cagaggcatg tcgacctgca
900
gctggaggag cagtgcatac aaggggactg gactttgcct gcgatatcta catttgggct
960
cctctggcag gaacatgtgg cgtgctgctg ctgagcctgg tcatcactct gtactgcaag
1020
cgaggccgga agaaactgct gtatattttc aaacagccct ttatgcgacc tgtgcagacc
1080
acacaggagg aagatgggtg ctcctgtcgg ttccccgagg aagaggaagg aggctgtgag
1140
ctgcgggtca agttttccag atctgcagac gcccctgctt accagcaggg ccagaaccag
1200
ctgtataacg agctgaatct ggggcggaga gaggaatacg acgtgctgga taaaaggcgc
1260
gggagagacc cagaaatggg gggaaagcca cgacggaaaa acccccagga gggactgtac
1320
aatgaactgc agaaggataa aatggcagag gcctattccg aaatcgggat gaagggagaa
1380
agaaggcgag gcaaaggaca cgacggactg taccaggggc tgtctaccgc cacaaaggac
1440
acctatgatg ctctgcatat gcaggcactg ccacccagg
1479
<210> 616
<211> 1485
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 616
atggcactgc ctgtgacagc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
cctcaggtgc agctgcagca gagcggccca ggcctggtga agccatccca gacactgtct
120
ctgacctgcg ccatctccgg cgacaacgtg tccacaaatt ctgccgcctg gaactggatc
180
aggcagagcc catcccgcgg cctggagtgg ctgggctgga cctactatag gagcaagtgg
240
tacaatgact atgccgtgag cctgaagtcc cgcatcaaca tcaatccaga tacctccaag
300
aaccagttct ctctgcagct gaatagcgtg acacccgagg ataccgccgt gtactattgc
360
gcccggtggg tgaacagaga cgtgtttgat atctggggcc agggcacaat ggtgaccgtg
420
agctccggag gaggaggctc cggcggcgga ggctctggcg gcggcggcag cggaggcggc
480
ggctctcaga gcgccctgac acagccagca tccgtgtctg gcagccctgg ccagagcatc
540
accatctcct gtacaggcac ctctagcgac gtgggctcct acaatctggt gtcttggtat
600
cagcagcacc ccggcaaggc ccctaagctg atgatctacg agggcagcaa gaggccatct
660
ggcgtgagca acagattctc cggctctaag agcggcaata cagcctctct gaccatcagc
720
ggactgcagg cagaggacga ggcagattac tattgctgtt cctatgccgg ctcctctacc
780
tgggtgtttg gcggcggcac aaagctgacc gtgctgacca caacccctgc ccctaggcca
840
cctaccccag cacctacaat tgctagtcag ccactgtcac tgcgaccaga ggcatgtcga
900
cctgcagctg gaggagcagt gcatacaagg ggactggact ttgcctgcga tatctacatt
960
tgggctcctc tggcaggaac atgtggcgtg ctgctgctga gcctggtcat cactctgtac
1020
tgcaagcgag gccggaagaa actgctgtat attttcaaac agccctttat gcgacctgtg
1080
cagaccacac aggaggaaga tgggtgctcc tgtcggttcc ccgaggaaga ggaaggaggc
1140
tgtgagctgc gggtcaagtt ttccagatct gcagacgccc ctgcttacca gcagggccag
1200
aaccagctgt ataacgagct gaatctgggg cggagagagg aatacgacgt gctggataaa
1260
aggcgcggga gagacccaga aatgggggga aagccacgac ggaaaaaccc ccaggaggga
1320
ctgtacaatg aactgcagaa ggataaaatg gcagaggcct attccgaaat cgggatgaag
1380
ggagaaagaa ggcgaggcaa aggacacgac ggactgtacc aggggctgtc taccgccaca
1440
aaggacacct atgatgctct gcatatgcag gcactgccac ccagg
1485
<210> 617
<211> 1488
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 617
atggccctgc cagtgaccgc cctgctgctg cccctggccc tgctgctgca cgccgccagg
60
ccccaggtgc agctggtgga gtccggagga ggagtggtgc agcctggccg gtctctgaga
120
ctgagctgcg cagcatccgg cttcaccttc agctcctacg gaatgcactg ggtgcggcag
180
acccctggca agggactgga gtgggtggcc gtgatctcct atgacggcaa ctctaattac
240
tatgccgata gcgtgaaggg caggttcaca atctctcgcg acaacagcaa gaataccctg
300
tacctgcaga tgaactctct gcgggccgag gacacagccg tgtactattg tgccagagat
360
ggcgccacag tgaccagcta ctattactat ggcatggacg tgtggggcca gggcaccaca
420
gtgaccgtgt ctagcggagg aggaggcagc ggaggaggag gctccggagg cggcggctct
480
ggcggcggcg gcagcgagat cgtgctgaca cagtcccctg gcaccctgag cctgtcccca
540
ggcgagcggg ccacactgtc ttgcagagcc tctcagagcg tgtccaggac ctacctggcc
600
tggtatcacc agaagcctgg ccaggcacct cgcctgctga tctacggagc atcctctagg
660
gccacaggca tcagcgaccg cttctctggc agcggctccg gaaccgactt caccctgacc
720
atctcccggc tggagccaga ggacttcgcc gtgtactatt gtcagcagta tggcacatcc
780
cccatcacct ttggccaggg caccagactg gagatcaaga ccacaacccc cgcccctagg
840
ccacctaccc cagcacctac aattgctagt cagccactgt cactgcgacc agaggcatgt
900
cgacctgcag ctggaggagc agtgcataca aggggactgg actttgcctg cgatatctac
960
atttgggctc ctctggcagg aacatgtggc gtgctgctgc tgagcctggt catcactctg
1020
tactgcaagc gaggccggaa gaaactgctg tatattttca aacagccctt tatgcgacct
1080
gtgcagacca cacaggagga agatgggtgc tcctgtcggt tccccgagga agaggaagga
1140
ggctgtgagc tgcgggtcaa gttttccaga tctgcagacg cccctgctta ccagcagggc
1200
cagaaccagc tgtataacga gctgaatctg gggcggagag aggaatacga cgtgctggat
1260
aaaaggcgcg ggagagaccc agaaatgggg ggaaagccac gacggaaaaa cccccaggag
1320
ggactgtaca atgaactgca gaaggataaa atggcagagg cctattccga aatcgggatg
1380
aagggagaaa gaaggcgagg caaaggacac gacggactgt accaggggct gtctaccgcc
1440
acaaaggaca cctatgatgc tctgcatatg caggcactgc cacccagg
1488
<210> 618
<211> 1503
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 618
atggcactgc ctgtgacagc cctgctgctg ccactggccc tgctgctgca cgccgccagg
60
ccccaggtgc agctgcagca gagcggccca ggcctggtga agccatctca gacactgagc
120
ctgacctgcg ccatctctgg cgacagcgtg agctccaact ccgccgtgtg gaattggatc
180
aggcagagcc cttcccgcgg cctggagtgg ctgggacgga cctactatag atctaagtgg
240
tacaacgact atgccgtgtc cgtgaagtct aggatcacaa tcaaccccga tacctcccgc
300
aatcagttct ctctgcagct gaatagcgtg acacctgagg ataccgccgt gtactattgc
360
gccagaggcg gaatcgtggg cgccccagac ggctttgata tctggggcca gggcacaatg
420
gtgaccgtgt ctagcggagg aggaggctcc ggaggaggag gctctggcgg cggcggcagc
480
ggaggcggcg gctccgacat cgtgatgaca cagagccctg attccctggc cgtgtctctg
540
ggcgagaggg caaccatcaa ctgtaagtcc tctcagagcg tgctggacag ctccaacaat
600
aacaattact tcgcctggta tcagcagaga cctggccagc cccctcacct gctgatctac
660
tgggcatcta gccgggagag cggagtgcca gacagattct ctggcagcgg ctccggcaca
720
gacttcaccc tgaccatctc ctctctgcag gccgaggatg tggccgtgta ctattgtcag
780
cagtactatt ccacaccata tacctttggc cagggcacca agctggagat caagaccaca
840
acccccgccc ctaggccacc taccccagca cctacaattg ctagtcagcc actgtcactg
900
cgaccagagg catgtcgacc tgcagctgga ggagcagtgc atacaagggg actggacttt
960
gcctgcgata tctacatttg ggctcctctg gcaggaacat gtggcgtgct gctgctgagc
1020
ctggtcatca ctctgtactg caagcgaggc cggaagaaac tgctgtatat tttcaaacag
1080
ccctttatgc gacctgtgca gaccacacag gaggaagatg ggtgctcctg tcggttcccc
1140
gaggaagagg aaggaggctg tgagctgcgg gtcaagtttt ccagatctgc agacgcccct
1200
gcttaccagc agggccagaa ccagctgtat aacgagctga atctggggcg gagagaggaa
1260
tacgacgtgc tggataaaag gcgcgggaga gacccagaaa tggggggaaa gccacgacgg
1320
aaaaaccccc aggagggact gtacaatgaa ctgcagaagg ataaaatggc agaggcctat
1380
tccgaaatcg ggatgaaggg agaaagaagg cgaggcaaag gacacgacgg actgtaccag
1440
gggctgtcta ccgccacaaa ggacacctat gatgctctgc atatgcaggc actgccaccc
1500
agg
1503
<210> 619
<211> 1485
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 619
atggccctgc cagtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctgcagca gagcggccct ggcctggtga agcctagcca gacactgtcc
120
ctgacctgcg ccatctctgg cgacagcgtg agctccaaca ccacagcctg gaagtggagc
180
agacagtccc cctctaaggg cctggagtgg ctgggctgga catactatag gtccaagtgg
240
tactatgact acaccgtgtc cgtgaagtct cgcatcacaa tcaaccccga tacctccaag
300
aatcagttct ctctgcagct gaatagcgtg acacctgagg ataccgccgt gtactattgc
360
gccaggtgga tcttccacga cgcctttgat atctggggcc agggcacaat ggtgaccgtg
420
tctagcggag gaggaggctc cggaggagga ggctctggcg gcggcggcag cggaggcggc
480
ggcagccagt ccgccctgac acagccacct tctgccagcg gaacacctgg ccagagagtg
540
accatctcct gttctggctc ctctagcaac atcggcagca acaccgtgaa ttggtaccag
600
cagctgccag gcacagcccc caagctgctg atctatacca acaatcagag gccttccgga
660
gtgccagacc ggttcagcgg ctccaagtct ggcacaagcg cctccctggc catctctggc
720
ctgcagagcg aggacgaggc cgattatttc tgttccacct gggacgattc tctgaatgga
780
cccgtgttcg gaggaggaac aaagctgacc gtgctgacca caaccccagc ccctaggcca
840
cctaccccag cacctacaat tgctagtcag ccactgtcac tgcgaccaga ggcatgtcga
900
cctgcagctg gaggagcagt gcatacaagg ggactggact ttgcctgcga tatctacatt
960
tgggctcctc tggcaggaac atgtggcgtg ctgctgctga gcctggtcat cactctgtac
1020
tgcaagcgag gccggaagaa actgctgtat attttcaaac agccctttat gcgacctgtg
1080
cagaccacac aggaggaaga tgggtgctcc tgtcggttcc ccgaggaaga ggaaggaggc
1140
tgtgagctgc gggtcaagtt ttccagatct gcagacgccc ctgcttacca gcagggccag
1200
aaccagctgt ataacgagct gaatctgggg cggagagagg aatacgacgt gctggataaa
1260
aggcgcggga gagacccaga aatgggggga aagccacgac ggaaaaaccc ccaggaggga
1320
ctgtacaatg aactgcagaa ggataaaatg gcagaggcct attccgaaat cgggatgaag
1380
ggagaaagaa ggcgaggcaa aggacacgac ggactgtacc aggggctgtc taccgccaca
1440
aaggacacct atgatgctct gcatatgcag gcactgccac ccagg
1485
<210> 620
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 620
atggcactgc ctgtgacagc cctgctgctg ccactggccc tgctgctgca cgccgccaga
60
ccccaggtgc agctgcagga gtccggccca ggcctggtga agccaagcga gaccctgtcc
120
ctgacatgca ccgtgtctgg cgacagcatc agctccctgt cttggagctg gatcaggcag
180
acaccaggcg agggcctgga gtggatcggc tacctgtact attccggctc taccgactat
240
aacccctccc tgaagtctcg cgtgacaatc tctgtggata ccagcaagaa tcagttctct
300
ctgaagctgc ggagcgtggc tgccgccgac acagccctgt actattgcgc cagaggccgg
360
agagcctttg atatctgggg ccagggcaca atggtgaccg tgtctagcgg aggaggaggc
420
tccggaggag gaggctctgg cggcggcggc agcggaggcg gcggctccga catccagatg
480
acccagagcc cttcctctct gagcgcctcc gtgggcgata gggtgacaat cacctgtcgc
540
ggctcccagg gcatctctaa ctacctggca tggttccagc agcggcccgg caaggcacct
600
aagtctctga tctatgcagc aagctccctg gagagcggag tgccatccaa gttctctggc
660
agcggctccg gcacagactt tacactgacc atcatcagcc tgcagcccga ggatttcgcc
720
acctactatt gtcagcagta ctataattac cctatcacat ttggccaggg cacccggctg
780
gagatcaaga ccacaacccc tgcccctagg ccacctaccc cagcacctac aattgctagt
840
cagccactgt cactgcgacc agaggcatgt cgacctgcag ctggaggagc agtgcataca
900
aggggactgg actttgcctg cgatatctac atttgggctc ctctggcagg aacatgtggc
960
gtgctgctgc tgagcctggt catcactctg tactgcaagc gaggccggaa gaaactgctg
1020
tatattttca aacagccctt tatgcgacct gtgcagacca cacaggagga agatgggtgc
1080
tcctgtcggt tccccgagga agaggaagga ggctgtgagc tgcgggtcaa gttttccaga
1140
tctgcagacg cccctgctta ccagcagggc cagaaccagc tgtataacga gctgaatctg
1200
gggcggagag aggaatacga cgtgctggat aaaaggcgcg ggagagaccc agaaatgggg
1260
ggaaagccac gacggaaaaa cccccaggag ggactgtaca atgaactgca gaaggataaa
1320
atggcagagg cctattccga aatcgggatg aagggagaaa gaaggcgagg caaaggacac
1380
gacggactgt accaggggct gtctaccgcc acaaaggaca cctatgatgc tctgcatatg
1440
caggcactgc cacccagg
1458
<210> 621
<211> 1488
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 621
atggcactgc ctgtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg
60
ccacaggtgc agctggtgca gtctggagca gaggtgaaga agcctggcgc aagcgtgaag
120
gtgtcctgca aggcctctgg ctacacattc accggctact atatgcactg ggtgagacag
180
gcccctggcc agggactgga gtggatgggc tggatcaacc ctaatagcgg cggcaccaac
240
tacgcccaga agtttcaggg ccgggtgaca atgaccagag acaccagcgt gtccacagcc
300
tatatggagc tgagcaggct gacctccgac gatacagcca tctactattg tgccaaggac
360
ggcggcggcg atttctactt ttatggcatg gacgtgtggg gccagggcac cacagtgacc
420
gtgagctccg gcggcggcgg ctctggagga ggaggcagcg gcggaggagg ctccggagga
480
ggcggctctc agaccgtggt gacacaggag ccatctttca gcgtgtcccc cggcggaaca
540
gtgaccctga catgcggcct gtctagcggc tctgtgagca catcctacta tcctagctgt
600
ttccagcaga cccccggcca ggcacctaga acactgatct actccaccga cacaaggtcc
660
tctggcgtgc cagatcgctt ttctggcagc atcctgggca ataaggccgc cctgaccatc
720
acaggagcac aggccgacga tgagtccgac tactattgcg tgctgtatat gggctccgga
780
atcagcgtgt tcggaggagg caccaagctg acagtgctga ccacaacccc cgcccctagg
840
ccacctaccc cagcacctac aattgctagt cagccactgt cactgcgacc agaggcatgt
900
cgacctgcag ctggaggagc agtgcataca aggggactgg actttgcctg cgatatctac
960
atttgggctc ctctggcagg aacatgtggc gtgctgctgc tgagcctggt catcactctg
1020
tactgcaagc gaggccggaa gaaactgctg tatattttca aacagccctt tatgcgacct
1080
gtgcagacca cacaggagga agatgggtgc tcctgtcggt tccccgagga agaggaagga
1140
ggctgtgagc tgcgggtcaa gttttccaga tctgcagacg cccctgctta ccagcagggc
1200
cagaaccagc tgtataacga gctgaatctg gggcggagag aggaatacga cgtgctggat
1260
aaaaggcgcg ggagagaccc agaaatgggg ggaaagccac gacggaaaaa cccccaggag
1320
ggactgtaca atgaactgca gaaggataaa atggcagagg cctattccga aatcgggatg
1380
aagggagaaa gaaggcgagg caaaggacac gacggactgt accaggggct gtctaccgcc
1440
acaaaggaca cctatgatgc tctgcatatg caggcactgc cacccagg
1488
<210> 622
<211> 569
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 622
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Leu
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
50 55 60
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr
65 70 75 80
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
85 90 95
Gly Ser Ile Tyr Tyr Ser Gly Asn Ile Tyr His Asn Pro Ser Leu Lys
100 105 110
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
115 120 125
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
130 135 140
Arg Glu Ile Ile Val Gly Ala Thr His Phe Asp Tyr Trp Gly Gln Gly
145 150 155 160
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr
180 185 190
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
195 200 205
Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly Trp Tyr Gln
210 215 220
Gln Lys Pro Gly Lys Ala Pro Glu Leu Leu Ile Tyr Ala Ala Ser Ser
225 230 235 240
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
245 250 255
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
260 265 270
Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Leu Thr Phe Gly Pro Gly
275 280 285
Thr Lys Val Asp Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr
290 295 300
Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr
305 310 315 320
Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro
325 330 335
Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr
340 345 350
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
355 360 365
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
370 375 380
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
385 390 395 400
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 623
<211> 539
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 623
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn Ile
65 70 75 80
Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg
180 185 190
Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu
195 200 205
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr
245 250 255
Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Gly Ser Gly
260 265 270
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly
275 280 285
Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly
290 295 300
Gly Ser Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr
305 310 315 320
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
325 330 335
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
340 345 350
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
355 360 365
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
370 375 380
Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
385 390 395 400
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
405 410 415
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
420 425 430
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
435 440 445
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
450 455 460
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
465 470 475 480
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
485 490 495
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
500 505 510
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
515 520 525
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
530 535
<210> 624
<211> 527
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 624
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Leu Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg
65 70 75 80
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser
85 90 95
Gly Asn Ile Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser
100 105 110
Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr
115 120 125
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly
130 135 140
Ala Thr His Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
165 170 175
Gly Gly Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
180 185 190
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
195 200 205
Gly Ile Arg Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala
210 215 220
Pro Glu Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
225 230 235 240
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
245 250 255
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp
260 265 270
Tyr Asn Tyr Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
275 280 285
Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly
290 295 300
Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
305 310 315 320
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
325 330 335
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
340 345 350
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
355 360 365
Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 625
<211> 522
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 625
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly
65 70 75 80
Gly Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro
85 90 95
Pro Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn
100 105 110
Ile Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp
115 120 125
Thr Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala
130 135 140
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly Ala Thr
145 150 155 160
His Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
195 200 205
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile
210 215 220
Arg Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu
225 230 235 240
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
245 250 255
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
260 265 270
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn
275 280 285
Tyr Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr
290 295 300
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
305 310 315 320
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
325 330 335
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
340 345 350
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 626
<211> 545
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 626
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
275 280 285
Ser Leu Cys Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser
290 295 300
Leu Cys Ser Gly Gly Gly Gly Ser Thr Thr Thr Ala Cys Pro Tyr Ser
305 310 315 320
Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
325 330 335
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
340 345 350
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
355 360 365
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
370 375 380
Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr
385 390 395 400
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
405 410 415
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
420 425 430
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
435 440 445
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
450 455 460
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
465 470 475 480
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
485 490 495
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
500 505 510
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
515 520 525
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
530 535 540
Arg
545
<210> 627
<211> 533
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 627
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile
50 55 60
Ser Gly Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg
65 70 75 80
Gln Ser Pro Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg
85 90 95
Ser Lys Trp Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr
100 105 110
Ile Asn Pro Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser
115 120 125
Val Thr Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu
130 135 140
Val Gly Ala Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val
145 150 155 160
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro
180 185 190
Ser Ala Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly
195 200 205
Ser Ser Ser Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu
210 215 220
Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro
225 230 235 240
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala
245 250 255
Ser Leu Ala Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr
260 265 270
Cys Ser Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly
275 280 285
Thr Lys Val Thr Val Leu Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn
290 295 300
Pro Ser Leu Cys Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg
305 310 315 320
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
325 330 335
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
340 345 350
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
355 360 365
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys
370 375 380
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
385 390 395 400
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
405 410 415
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
420 425 430
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
435 440 445
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
450 455 460
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
465 470 475 480
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
485 490 495
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
500 505 510
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
515 520 525
Ala Leu Pro Pro Arg
530
<210> 628
<211> 528
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 628
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly
65 70 75 80
Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser
85 90 95
Pro Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys
100 105 110
Trp Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn
115 120 125
Pro Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr
130 135 140
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly
145 150 155 160
Ala Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val
165 170 175
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
180 185 190
Ser Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala
195 200 205
Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser
210 215 220
Ser Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly
225 230 235 240
Thr Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly
245 250 255
Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu
260 265 270
Ala Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser
275 280 285
Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys
290 295 300
Val Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
305 310 315 320
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
325 330 335
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
340 345 350
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
355 360 365
Leu Ser Leu Val Ile Thr Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
370 375 380
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
385 390 395 400
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
405 410 415
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
420 425 430
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
435 440 445
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
450 455 460
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
465 470 475 480
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
485 490 495
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
500 505 510
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 629
<211> 249
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 629
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Phe Tyr Cys
85 90 95
Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr Gly Gly Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala
165 170 175
Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr Ala
180 185 190
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Phe Cys Leu Gln His Asp Ser Phe Pro Leu Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 630
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
oligonucleotide"
<400> 630
ggcggcggcg gctctggagg aggaggcagc ggcggaggag gctccggagg cggcggctct
60
<210> 631
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полинуклеотид"
<400> 631
atggctctgc ccgtcaccgc tctgctgctg cctctggctc tgctgctgca cgccgcacga
60
ccagaggtgc agctggtgga gagcggagga ggcctggtgc agcctggcgg cagcctgagg
120
ctgtcctgcg cagcatctgg cttcaccttt agctcccacg acatgcactg ggtgaggcag
180
gcaacaggca agggcctgga gtgggtgtcc gccatcggaa tcgcaggcga tacctactat
240
tccggctctg tgaagggccg gttcacaatc agcagagaga acgccaagaa ttccctgtac
300
ctgcagatga actctctgag ggccggcgac accgccgtgt actattgtgc cagagccaat
360
tggggcgagg gcgcctttga tatctggggc cagggcacca tggtgacagt gtctagcggc
420
ggcggcggct ctggaggagg aggcagcggc ggaggaggct ccggaggcgg cggctctgac
480
atccagatga cacagtctcc tagctccctg tccgcctctg tgggcgaccg ggtgaccatc
540
acatgcagag ccagccaggg catctccgat tacctggcct ggtatcagca gaagcccggc
600
aagatcccta agctgctgat ctacgcagca tctaccctgc agagcggagt gccatcccgg
660
ttcagcggat ccggatctgg aacagacttt accctgacaa tctctagcct gcagccagag
720
gatgtggcca cctactattg tcagaagtat aactccgtgc cactgacctt cggcggagga
780
acaaaggtgg agatcaagac cacaactcct gcacctaggc cacctacccc agcacctaca
840
attgctagtc agccactgtc actgcgacca gaggcatgtc gacctgcagc tggaggagca
900
gtgcatacaa ggggactgga ctttgcctgc gatatctaca tttgggctcc tctggcagga
960
acatgtggcg tgctgctgct gagcctggtc atcactctgt actgcaagcg aggccggaag
1020
aaactgctgt atattttcaa acagcccttt atgcgacctg tgcagaccac acaggaggaa
1080
gatgggtgct cctgtcggtt ccccgaggaa gaggaaggag gctgtgagct gcgggtcaag
1140
ttttccagat ctgcagacgc ccctgcttac cagcagggcc agaaccagct gtataacgag
1200
ctgaatctgg ggcggagaga ggaatacgac gtgctggata aaaggcgcgg gagagaccca
1260
gaaatggggg gaaagccacg acggaaaaac ccccaggagg gactgtacaa tgaactgcag
1320
aaggataaaa tggcagaggc ctattccgaa atcgggatga agggagaaag aaggcgaggc
1380
aaaggacacg acggactgta ccaggggctg tctaccgcca caaaggacac ctatgatgct
1440
ctgcatatgc aggcactgcc acccagg
1467
<210> 632
<211> 489
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 632
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Leu Phe Asn Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser Glu
225 230 235 240
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asn Trp Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 633
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 633
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Met Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Tyr Trp Ser Cys Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Leu Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Arg Leu Thr Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ala Pro Thr Gly Phe Trp Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Ser Arg Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Glu Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 634
<211> 489
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 634
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser His Asp Met His Trp Val Arg Gln Ala Thr Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Ile Ala Gly Asp Thr Tyr Tyr
65 70 75 80
Ser Gly Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys
85 90 95
Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ala Asn Trp Gly Glu Gly Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asp Tyr Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ile Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Val Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 635
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 635
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn His
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Leu Thr Ile Ser Leu Asp Lys Ala Lys
85 90 95
Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Phe Asn Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Arg Thr Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Thr Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 636
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 636
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asn
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ala Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Gln Leu Ser Ser Val Thr Ala Ala Asp Ala Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Phe His Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ser Asn Thr Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Asn Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 637
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 637
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asn Val
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Phe Cys Ala Arg Leu Ser Asn Trp Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Phe Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Thr Ile Ser Ser Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Trp Ser Pro Ile
245 250 255
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 638
<211> 496
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 638
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Asp Met His Trp Val Arg Gln Ala Thr Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Pro Ala Gly Asp Thr Tyr Tyr
65 70 75 80
Pro Gly Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Glu Asn Ala Lys
85 90 95
Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Gly Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ala Asp Pro Pro Tyr Tyr Tyr Tyr Gly Met
115 120 125
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro
165 170 175
Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His
180 185 190
Ser Asn Glu Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln
195 200 205
Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Lys
225 230 235 240
Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln
245 250 255
Ala Leu Glu Ile Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
260 265 270
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 639
<211> 491
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 639
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Ser Thr Arg Gly Val Gly Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys
65 70 75 80
Arg Tyr Ser Pro Ser Leu Gln Thr Arg Leu Thr Ile Thr Lys Asp Thr
85 90 95
Pro Lys Asn Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ser Asn Trp Gly Asn Trp Tyr Phe
115 120 125
Ala Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser
180 185 190
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr Asp Ala Phe Tyr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Arg Ser Asn Trp Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 640
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 640
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Thr Thr Asn Ser
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Val Ser Leu Asp Thr Ser Lys
85 90 95
Ser Gln Phe Ser Leu Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Phe Asn Arg Gly Phe Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Asn Thr Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Ala Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 641
<211> 499
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 641
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Ser Thr Ser Gly Met Cys Val Ser Trp Ile Arg Gln Pro Leu
50 55 60
Gly Lys Ala Leu Glu Trp Leu Gly Phe Ile Asp Trp Asp Asp Asp Lys
65 70 75 80
Tyr Tyr Asn Thr Ser Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Asn Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Gly Tyr Ser Gly Ser Tyr
115 120 125
Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Val Val Ile Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro
165 170 175
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser
180 185 190
Leu Leu His Ser Asn Gly Tyr Asn His Leu Asp Trp Tyr Leu Gln Lys
195 200 205
Pro Gly Gln Ser Pro Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala
210 215 220
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
225 230 235 240
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe
245 250 255
Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys
260 265 270
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
340 345 350
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
355 360 365
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
370 375 380
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
385 390 395 400
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
405 410 415
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
420 425 430
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
435 440 445
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
450 455 460
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
465 470 475 480
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
485 490 495
Pro Pro Arg
<210> 642
<211> 489
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 642
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Val Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ser Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys
50 55 60
Gly Leu Asp Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Thr Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Gly Leu Thr Gly Phe Phe Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu
180 185 190
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Tyr Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 643
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 643
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Gly Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Ser Ser Gly Asn Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Arg Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Thr Thr Ser Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Leu Gly Ile Ala Asp Ser Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala
195 200 205
Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 644
<211> 492
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 644
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn Ile
65 70 75 80
Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg
180 185 190
Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu
195 200 205
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr
245 250 255
Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 645
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 645
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Ile His Ser Gly Ser Ser Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ser Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Arg Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 646
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 646
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Asn Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Asp Ile His His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Lys Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Lys Asn Gln Phe Ser Leu Asn Leu Ile Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Glu Ala Gly Gly Tyr Phe Asp Tyr Trp
115 120 125
Gly Gln Gly Ile Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg
165 170 175
Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Ser Lys
195 200 205
Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Pro Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Ala Asp
225 230 235 240
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly
245 250 255
Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 647
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 647
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 648
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 648
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Thr His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Tyr Gly Ser Gly Ser Arg Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Ala Leu Thr Cys Arg Ala Ser Gln Gly Ile Arg Asp Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Asp Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asp Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 649
<211> 491
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 649
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Ala Tyr Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Thr Ser Leu Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Leu Asp Ser Ser Gly Trp Tyr Pro Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser
180 185 190
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asp Ser Phe Pro
245 250 255
Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 650
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 650
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Phe Gly Gly
35 40 45
Ser Phe Ser Gly Asp Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ile Thr Ser Phe
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Leu Gly Ile Pro Asp Asn Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Arg Trp Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala
195 200 205
Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 651
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 651
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Val Val Phe Gly Asp
35 40 45
Ser Ile Ser Ser Ser Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Glu Val Phe His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ala Ala Val Ala Gly Ala Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu
165 170 175
Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser Ser
180 185 190
Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
195 200 205
Pro Asn Leu Leu Val Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ala Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
225 230 235 240
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr
245 250 255
Tyr Gly Thr Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 652
<211> 491
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 652
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Thr Leu Arg Glu Ser Gly Pro Thr Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Ser Thr Ser Gly Leu Gly Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Glu Ala Leu Glu Trp Leu Ala Leu Ile Tyr Trp Asn Asp Asp Lys
65 70 75 80
Arg Tyr Ser Pro Ser Leu Lys Ser Arg Leu Ser Ile Thr Lys Asp Thr
85 90 95
Ser Lys Asn Gln Val Val Leu Ile Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Val His Arg Arg Ile Ala Ala Pro Gly Ser
115 120 125
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser
180 185 190
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Ser Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys His Gln Ala Asn Ser Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 653
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 653
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Val Ser Gly Tyr
35 40 45
Thr Leu Thr Glu Leu Ser Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Pro Glu Gly Met Gly Gly Phe Asp Pro Glu Asp Gly Lys Thr Ile
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser
85 90 95
Ala Asp Thr Ala Tyr Met Glu Leu Asn Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Thr Leu Leu Arg Gly Leu Asp Ala Phe Asp
115 120 125
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
180 185 190
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Thr Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Arg
245 250 255
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 654
<211> 491
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 654
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Arg Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Ser His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Val Arg Gly Tyr Ser Tyr Gly Tyr Pro Leu Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn
180 185 190
Asp Leu Gly Trp Tyr Gln Gln Lys Leu Gly Lys Ala Pro Lys Arg Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asn Ser Tyr Pro
245 250 255
Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 655
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 655
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Asp
35 40 45
Ser Ile Ser Ser Asn Trp Trp Thr Trp Val Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Asp Ile His His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Met Ser Val Asp Lys Ser Glu
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Phe Tyr Cys Ala Arg Asp Gly Gly Gly Thr Leu Asp Tyr Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala
195 200 205
Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Gly Tyr Ser Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 656
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 656
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Thr Asn Tyr Cys Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn
65 70 75 80
Tyr Ala Gln Thr Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Asn Gly Asp Arg Tyr Tyr Tyr Asp
115 120 125
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro
165 170 175
Gly Gln Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
180 185 190
Asn Asn Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly
225 230 235 240
Leu Gln Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser
245 250 255
Ser Leu Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 657
<211> 497
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 657
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Thr Tyr Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr
115 120 125
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala
165 170 175
Ala Pro Gly Gln Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn
180 185 190
Ile Gly Asn Asn Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro
210 215 220
Asp Arg Phe Phe Gly Ser Lys Phe Gly Thr Ser Ala Thr Leu Gly Ile
225 230 235 240
Thr Gly Leu Gln Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp
245 250 255
Asp Ser Ser Leu Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 658
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 658
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Gly Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Leu Ser Val Ala Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Arg Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Asp Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 659
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 659
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ser Tyr Ile Tyr Tyr Ser Gly Ile Ser Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ile Ser Val Ala Gly Phe Phe Phe Asp Asn
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Met Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Ala Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Ala Pro
225 230 235 240
Glu Asp Phe Val Val Tyr Tyr Cys Gln Gln Tyr Gly Ile Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 660
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 660
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 661
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 661
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Ser Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Phe
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Trp Gly Asp Tyr Tyr Tyr Tyr
115 120 125
Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Leu Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile
180 185 190
Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Thr Ala Ser Ser Leu Gln Gly Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Leu Ala Thr Tyr Ser Cys Gln Gln Ala Asn Val
245 250 255
Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 662
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 662
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr
115 120 125
Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile
180 185 190
Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys
195 200 205
Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp Ser
245 250 255
Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 663
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 663
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Ser Asp
35 40 45
Ser Ile Ser Asn Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ser Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ile Thr Val Thr Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Arg Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg His Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asp Thr Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 664
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 664
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Val Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr His Cys Ala Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Ser Trp Tyr Gln Gln Phe Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly His Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 665
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 665
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Tyr
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Leu Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Leu Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Asn Ser
180 185 190
Asn Ile Gly Ser Asn Pro Ile Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly His Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 666
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 666
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Ser Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Val Tyr Tyr Ser Asp Ile Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Phe Tyr Phe Cys Ala Arg Ile Gly Val Ala Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Arg Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Glu Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro Ile
245 250 255
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 667
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 667
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Lys Pro
85 90 95
Asp Thr Ala Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Phe Thr Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Ile Asn Trp Tyr Gln Gln Val Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 668
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 668
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Glu Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Ile Trp Tyr Gln Gln Leu Pro Arg Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 669
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 669
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Thr Gly Leu Glu Trp Leu Ala Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Glu Val Ser Val Lys Ser Gln Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Gly Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asn Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Asp Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala
245 250 255
Trp Asp Asp Trp Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 670
<211> 489
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 670
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Asn Asn Tyr Phe Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Phe Tyr His Arg Gly Gly Asn Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Asn Ser Val Thr Ser Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Leu Ala Leu Ala Gly Phe Phe Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 671
<211> 497
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 671
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Pro Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Thr Tyr Ser Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Glu Gly Ser Tyr Tyr Tyr Tyr
115 120 125
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly
165 170 175
Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn
180 185 190
Ile Gly Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile
225 230 235 240
Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp
245 250 255
Asp Asp Ser Leu Ser Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 672
<211> 494
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 672
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Lys Glu Arg Arg Tyr Tyr Tyr Tyr
115 120 125
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Asp Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val
180 185 190
Ser Arg Arg Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
195 200 205
Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
225 230 235 240
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Gly
245 250 255
Thr Ser Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 673
<211> 498
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 673
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Ala Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Ile Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Gly Thr Tyr Tyr Arg Ser Met Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Leu Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ser Arg Gly Gly Ile Val Gly Val
115 120 125
Pro Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asn Thr Ala Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Arg Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 674
<211> 492
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 674
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Asn Val Ser Asp Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Asp Trp Ile Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Thr Ser Met Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ile Ser Glu Lys Ser Phe Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
145 150 155 160
Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg
165 170 175
Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr
180 185 190
Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg Ser
225 230 235 240
Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Pro Trp Asp Asp Ser Leu Ser
245 250 255
Gly Arg Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 675
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 675
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Arg Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Val Ile Val Pro Ser Gly Gly Ser Ile Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Asn Ile Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Arg Tyr Tyr Gly Asp Tyr Tyr Tyr
115 120 125
Gly Leu Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile
180 185 190
Asn Asn Phe Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Ser Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Lys
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Asn Ser
245 250 255
Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 676
<211> 490
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 676
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser His Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ile Thr Asn Phe
65 70 75 80
Ser Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Ser Ser Lys
85 90 95
Asn Gln Phe Ser Leu Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Gly Ile Ser Leu Ala Gly Phe Tyr Phe Asp Tyr
115 120 125
Trp Val Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
145 150 155 160
Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
165 170 175
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Arg Ser Tyr
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
195 200 205
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Val Phe Tyr Cys Gln Gln Tyr Ser Ile Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 677
<211> 493
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 677
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ala Tyr Ile Tyr Tyr Ser Gly Asn Thr Asn Tyr
65 70 75 80
Ser Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asp Gln Leu Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Thr Arg Gly Gly Ser Gly Thr Ile Asp Val Phe Asp
115 120 125
Ile Trp Gly Gln Gly Thr Met Val Ala Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
165 170 175
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
180 185 190
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Asn Asn Lys Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Lys Ser Gly Thr Ser Ala Thr Leu Gly Ile Thr Gly Leu Gln
225 230 235 240
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Glu Thr Trp Asp Ser Ser Leu
245 250 255
Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 678
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 678
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Asn Val Ser Thr Asn Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Leu Lys Ser Arg Ile Asn Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Trp Val Asn Arg Asp Val
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro
165 170 175
Gly Gln Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly
180 185 190
Ser Tyr Asn Leu Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro
195 200 205
Lys Leu Met Ile Tyr Glu Gly Ser Lys Arg Pro Ser Gly Val Ser Asn
210 215 220
Arg Phe Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser
225 230 235 240
Gly Leu Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Cys Ser Tyr Ala
245 250 255
Gly Ser Ser Thr Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 679
<211> 496
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 679
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Gly Met His Trp Val Arg Gln Thr Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Asn Ser Asn Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Ala Thr Val Thr Ser Tyr Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu
165 170 175
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
180 185 190
Ser Val Ser Arg Thr Tyr Leu Ala Trp Tyr His Gln Lys Pro Gly Gln
195 200 205
Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile
210 215 220
Ser Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
225 230 235 240
Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln
245 250 255
Tyr Gly Thr Ser Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile
260 265 270
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 680
<211> 501
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 680
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Val Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Arg Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Ile Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu
165 170 175
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
180 185 190
Ser Val Leu Asp Ser Ser Asn Asn Asn Asn Tyr Phe Ala Trp Tyr Gln
195 200 205
Gln Arg Pro Gly Gln Pro Pro His Leu Leu Ile Tyr Trp Ala Ser Ser
210 215 220
Arg Glu Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
225 230 235 240
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
245 250 255
Tyr Tyr Cys Gln Gln Tyr Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly
260 265 270
Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
275 280 285
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
290 295 300
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
305 310 315 320
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
325 330 335
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
340 345 350
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
355 360 365
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
370 375 380
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
385 390 395 400
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
405 410 415
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
420 425 430
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
435 440 445
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
450 455 460
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
465 470 475 480
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
485 490 495
Ala Leu Pro Pro Arg
500
<210> 681
<211> 495
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 681
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Thr Thr Ala Trp Lys Trp Ser Arg Gln Ser Pro
50 55 60
Ser Lys Gly Leu Glu Trp Leu Gly Trp Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Tyr Asp Tyr Thr Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Trp Ile Phe His Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gln Ser Ala Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
165 170 175
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
180 185 190
Ser Asn Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
225 230 235 240
Leu Gln Ser Glu Asp Glu Ala Asp Tyr Phe Cys Ser Thr Trp Asp Asp
245 250 255
Ser Leu Asn Gly Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 682
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 682
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp
35 40 45
Ser Ile Ser Ser Leu Ser Trp Ser Trp Ile Arg Gln Thr Pro Gly Glu
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Leu Tyr Tyr Ser Gly Ser Thr Asp Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Ala Ala Ala Asp Thr Ala
100 105 110
Leu Tyr Tyr Cys Ala Arg Gly Arg Arg Ala Phe Asp Ile Trp Gly Gln
115 120 125
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Gly Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe
180 185 190
Gln Gln Arg Pro Gly Lys Ala Pro Lys Ser Leu Ile Tyr Ala Ala Ser
195 200 205
Ser Leu Glu Ser Gly Val Pro Ser Lys Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ile Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Tyr Pro Ile Thr Phe Gly Gln
245 250 255
Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 683
<211> 496
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 683
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Val Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Thr Ser Asp Asp Thr
100 105 110
Ala Ile Tyr Tyr Cys Ala Lys Asp Gly Gly Gly Asp Phe Tyr Phe Tyr
115 120 125
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gln Thr Val Val Thr Gln Glu Pro Ser Phe Ser Val Ser
165 170 175
Pro Gly Gly Thr Val Thr Leu Thr Cys Gly Leu Ser Ser Gly Ser Val
180 185 190
Ser Thr Ser Tyr Tyr Pro Ser Cys Phe Gln Gln Thr Pro Gly Gln Ala
195 200 205
Pro Arg Thr Leu Ile Tyr Ser Thr Asp Thr Arg Ser Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Ile Leu Gly Asn Lys Ala Ala Leu Thr Ile
225 230 235 240
Thr Gly Ala Gln Ala Asp Asp Glu Ser Asp Tyr Tyr Cys Val Leu Tyr
245 250 255
Met Gly Ser Gly Ile Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val
260 265 270
Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 684
<211> 572
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 684
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Leu
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
50 55 60
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr
65 70 75 80
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
85 90 95
Gly Ser Ile Tyr Tyr Ser Gly Asn Ile Tyr His Asn Pro Ser Leu Lys
100 105 110
Ser Arg Val Ser Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
115 120 125
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
130 135 140
Arg Glu Ile Ile Val Gly Ala Thr His Phe Asp Tyr Trp Gly Gln Gly
145 150 155 160
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile Gln Met Thr
180 185 190
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
195 200 205
Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly Trp Tyr Gln
210 215 220
Gln Lys Pro Gly Lys Ala Pro Glu Leu Leu Ile Tyr Ala Ala Ser Ser
225 230 235 240
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
245 250 255
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
260 265 270
Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Leu Thr Phe Gly Pro Gly
275 280 285
Thr Lys Val Asp Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr
290 295 300
Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr
305 310 315 320
Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro
325 330 335
Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr
340 345 350
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
355 360 365
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
370 375 380
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
385 390 395 400
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
405 410 415
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
420 425 430
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
435 440 445
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
450 455 460
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
465 470 475 480
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
485 490 495
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
500 505 510
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
515 520 525
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
530 535 540
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
545 550 555 560
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 685
<211> 542
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 685
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn Ile
65 70 75 80
Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly Ala Thr His
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg
180 185 190
Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu
195 200 205
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr
245 250 255
Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Gly Ser Gly
260 265 270
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly
275 280 285
Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly
290 295 300
Gly Ser Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr
305 310 315 320
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
325 330 335
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
340 345 350
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
355 360 365
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
370 375 380
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
385 390 395 400
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
405 410 415
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
420 425 430
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
435 440 445
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
450 455 460
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
465 470 475 480
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
485 490 495
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
500 505 510
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
515 520 525
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
530 535 540
<210> 686
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 686
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Leu Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg
65 70 75 80
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser
85 90 95
Gly Asn Ile Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser
100 105 110
Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr
115 120 125
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly
130 135 140
Ala Thr His Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
165 170 175
Gly Gly Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
180 185 190
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
195 200 205
Gly Ile Arg Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala
210 215 220
Pro Glu Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
225 230 235 240
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
245 250 255
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp
260 265 270
Tyr Asn Tyr Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
275 280 285
Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly
290 295 300
Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
305 310 315 320
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
325 330 335
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
340 345 350
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
355 360 365
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
370 375 380
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
385 390 395 400
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
405 410 415
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
420 425 430
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
435 440 445
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
450 455 460
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
465 470 475 480
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
485 490 495
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
500 505 510
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
515 520 525
Pro Arg
530
<210> 687
<211> 525
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 687
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly
65 70 75 80
Gly Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro
85 90 95
Pro Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Asn
100 105 110
Ile Tyr His Asn Pro Ser Leu Lys Ser Arg Val Ser Ile Ser Val Asp
115 120 125
Thr Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala
130 135 140
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ile Ile Val Gly Ala Thr
145 150 155 160
His Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
195 200 205
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile
210 215 220
Arg Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu
225 230 235 240
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
245 250 255
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
260 265 270
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn
275 280 285
Tyr Pro Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr
290 295 300
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
305 310 315 320
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
325 330 335
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
340 345 350
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
355 360 365
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
370 375 380
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
385 390 395 400
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
405 410 415
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
420 425 430
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
435 440 445
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
450 455 460
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
465 470 475 480
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
485 490 495
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
500 505 510
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 688
<211> 548
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 688
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly Ala
115 120 125
Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ala
245 250 255
Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val
260 265 270
Thr Val Leu Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
275 280 285
Ser Leu Cys Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser
290 295 300
Leu Cys Ser Gly Gly Gly Gly Ser Thr Thr Thr Ala Cys Pro Tyr Ser
305 310 315 320
Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
325 330 335
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
340 345 350
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
355 360 365
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
370 375 380
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
385 390 395 400
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
405 410 415
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
420 425 430
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
435 440 445
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
450 455 460
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
465 470 475 480
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
485 490 495
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
500 505 510
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
515 520 525
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
530 535 540
Leu Pro Pro Arg
545
<210> 689
<211> 536
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 689
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile
50 55 60
Ser Gly Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg
65 70 75 80
Gln Ser Pro Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg
85 90 95
Ser Lys Trp Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr
100 105 110
Ile Asn Pro Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser
115 120 125
Val Thr Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu
130 135 140
Val Gly Ala Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val
145 150 155 160
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro
180 185 190
Ser Ala Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly
195 200 205
Ser Ser Ser Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu
210 215 220
Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro
225 230 235 240
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala
245 250 255
Ser Leu Ala Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr
260 265 270
Cys Ser Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly
275 280 285
Thr Lys Val Thr Val Leu Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn
290 295 300
Pro Ser Leu Cys Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg
305 310 315 320
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
325 330 335
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
340 345 350
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
355 360 365
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
370 375 380
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
385 390 395 400
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
405 410 415
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
420 425 430
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
435 440 445
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
450 455 460
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
465 470 475 480
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
485 490 495
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
500 505 510
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
515 520 525
His Met Gln Ala Leu Pro Pro Arg
530 535
<210> 690
<211> 531
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 690
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly
65 70 75 80
Asp Ser Val Ser Ser Asn Ser Ala Thr Trp Asn Trp Ile Arg Gln Ser
85 90 95
Pro Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys
100 105 110
Trp Tyr Asp Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn
115 120 125
Pro Asp Thr Ser Lys Asn His Leu Ser Leu His Leu Asn Ser Val Thr
130 135 140
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Gly Gly Leu Val Gly
145 150 155 160
Ala Pro Asp Gly Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val
165 170 175
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
180 185 190
Ser Gly Gly Gly Gly Ser Gln Ser Val Leu Thr Gln Pro Pro Ser Ala
195 200 205
Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser
210 215 220
Ser Asn Ile Gly Ser Asp Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly
225 230 235 240
Thr Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly
245 250 255
Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu
260 265 270
Ala Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ser
275 280 285
Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys
290 295 300
Val Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
305 310 315 320
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
325 330 335
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
340 345 350
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
355 360 365
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
370 375 380
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
385 390 395 400
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
405 410 415
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
420 425 430
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
435 440 445
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
450 455 460
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
465 470 475 480
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
485 490 495
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
500 505 510
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
515 520 525
Pro Pro Arg
530
<210> 691
<211> 573
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 691
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
35 40 45
Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
50 55 60
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Ala Met
65 70 75 80
Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Thr
85 90 95
Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly
100 105 110
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
115 120 125
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Phe Tyr Cys Ala Ile
130 135 140
Asp Pro Glu Tyr Tyr Asp Ile Leu Thr Gly Gly Asp Tyr Trp Gly Gln
145 150 155 160
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
180 185 190
Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp Arg Val Thr
195 200 205
Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe
210 215 220
Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala Ser
225 230 235 240
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
245 250 255
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
260 265 270
Thr Tyr Phe Cys Leu Gln His Asp Ser Phe Pro Leu Thr Phe Gly Gly
275 280 285
Gly Thr Lys Val Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro
290 295 300
Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro
305 310 315 320
Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys
325 330 335
Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr
340 345 350
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
355 360 365
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
370 375 380
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
385 390 395 400
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
405 410 415
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
420 425 430
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
435 440 445
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
450 455 460
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
465 470 475 480
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
485 490 495
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
500 505 510
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
515 520 525
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
530 535 540
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
545 550 555 560
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 692
<211> 543
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 692
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu Thr
115 120 125
Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile
180 185 190
Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys
195 200 205
Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp Ser
245 250 255
Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Ser
260 265 270
Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
275 280 285
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly
290 295 300
Gly Gly Ser Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys
305 310 315 320
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
325 330 335
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
340 345 350
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
355 360 365
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
370 375 380
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
385 390 395 400
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
405 410 415
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
420 425 430
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
435 440 445
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
450 455 460
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
465 470 475 480
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
485 490 495
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
500 505 510
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
515 520 525
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
530 535 540
<210> 693
<211> 531
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 693
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly
35 40 45
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
50 55 60
Ser Gly Phe Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly
85 90 95
Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
100 105 110
Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala
115 120 125
Glu Asp Thr Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp
130 135 140
Ile Leu Thr Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
145 150 155 160
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala
180 185 190
Met Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
195 200 205
Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys
210 215 220
Val Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
225 230 235 240
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr
245 250 255
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln
260 265 270
His Asp Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
275 280 285
Lys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly
290 295 300
Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
305 310 315 320
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
325 330 335
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
340 345 350
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
355 360 365
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
370 375 380
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
385 390 395 400
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
405 410 415
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
420 425 430
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
435 440 445
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
450 455 460
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
465 470 475 480
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
485 490 495
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
500 505 510
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
515 520 525
Pro Pro Arg
530
<210> 694
<211> 526
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
полипептид"
<400> 694
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Leu Glu Ser Gly Gly Gly
50 55 60
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
65 70 75 80
Phe Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly
85 90 95
Lys Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Ser Gly Gly Ser Thr
100 105 110
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
115 120 125
Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
130 135 140
Thr Ala Val Phe Tyr Cys Ala Ile Asp Pro Glu Tyr Tyr Asp Ile Leu
145 150 155 160
Thr Gly Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
165 170 175
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
180 185 190
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser
195 200 205
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly
210 215 220
Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro
225 230 235 240
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
245 250 255
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
260 265 270
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Asp
275 280 285
Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 695
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 695
Gly Tyr Ile Phe Tyr Ser Gly Thr Thr Asn His Asn
1 5 10
<210> 696
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note="Описание искусственной последовательности: Синтетический
пептид"
<400> 696
Arg Ala Ser Gln Arg Ile Ser Asn Thr Tyr Leu Ala
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ АНТИТЕЛА К STAPHYLOCOCCUS AUREUS С РИФАМИЦИНОМ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2731055C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2829097C2 |
| МОЛЕКУЛЫ, НАЦЕЛЕННЫЕ НА СИСТЕМУ СЕКРЕЦИИ ТИПА III | 2016 |
|
RU2759949C2 |
| ИММУНОГЛОБУЛИН С ТАНДЕМНЫМИ FAB-ФРАГМЕНТАМИ И ВАРИАНТЫ ЕГО ПРИМЕНЕНИЯ | 2017 |
|
RU2767329C2 |
| ИНДУЦИБЕЛЬНЫЕ ХИМЕРНЫЕ ЦИТОКИНОВЫЕ РЕЦЕПТОРЫ | 2019 |
|
RU2826155C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ НА ОСНОВЕ АКТИВИРУЮЩИХ Т-КЛЕТКИ БИСПЕЦИФИЧЕСКИХ АНТИГЕНСВЯЗЫВАЮЩИХ МОЛЕКУЛ ПРОТИВ CD3 И ФОЛАТНОГО РЕЦЕПТОРА 1 (FOLR1) И АНТАГОНИСТОВ, СВЯЗЫВАЮЩИХСЯ С ОСЬЮ PD-1 | 2015 |
|
RU2753902C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ЧЕЛОВЕЧЕСКИМ КАННАБИНОИДНЫМ РЕЦЕПТОРОМ 1 (СВ1) | 2015 |
|
RU2730674C2 |
| Антитела против CXCR2 и их применение | 2019 |
|
RU2807067C2 |
| МУЛЬТИВАЛЕНТНЫЕ И МУЛЬТИСПЕЦИФИЧЕСКИЕ 41BB-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ | 2017 |
|
RU2789648C2 |
| ТРАНСПОЗИЦИЯ КОНСТРУКЦИЙ НУКЛЕИНОВОЙ КИСЛОТЫ В ЭУКАРИОТИЧЕСКИЕ ГЕНОМЫ С ТРАНСПОЗАЗОЙ ИЗ AMYELOIS | 2020 |
|
RU2814721C2 |
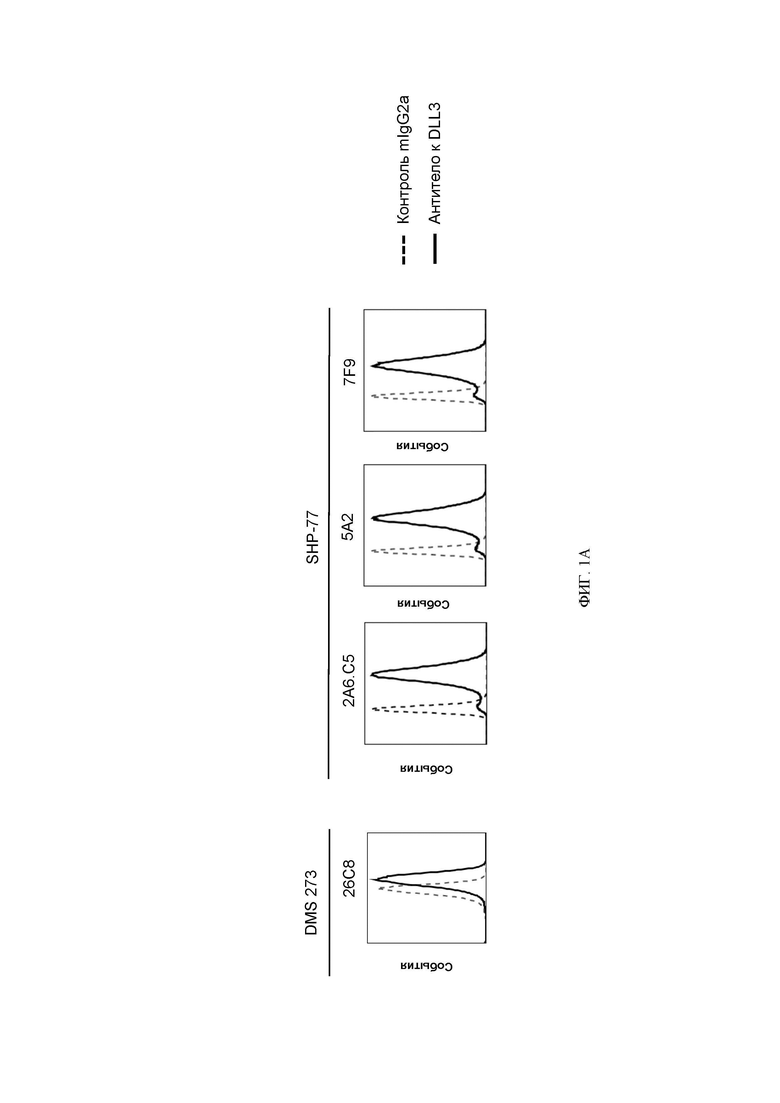
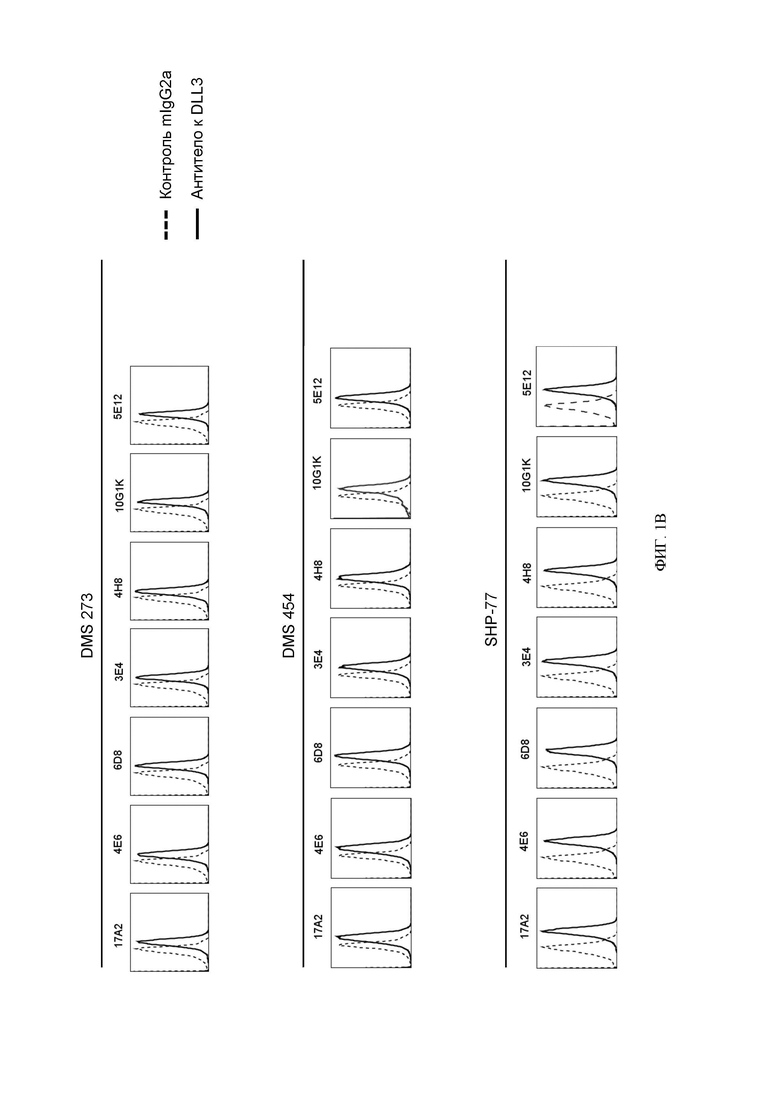
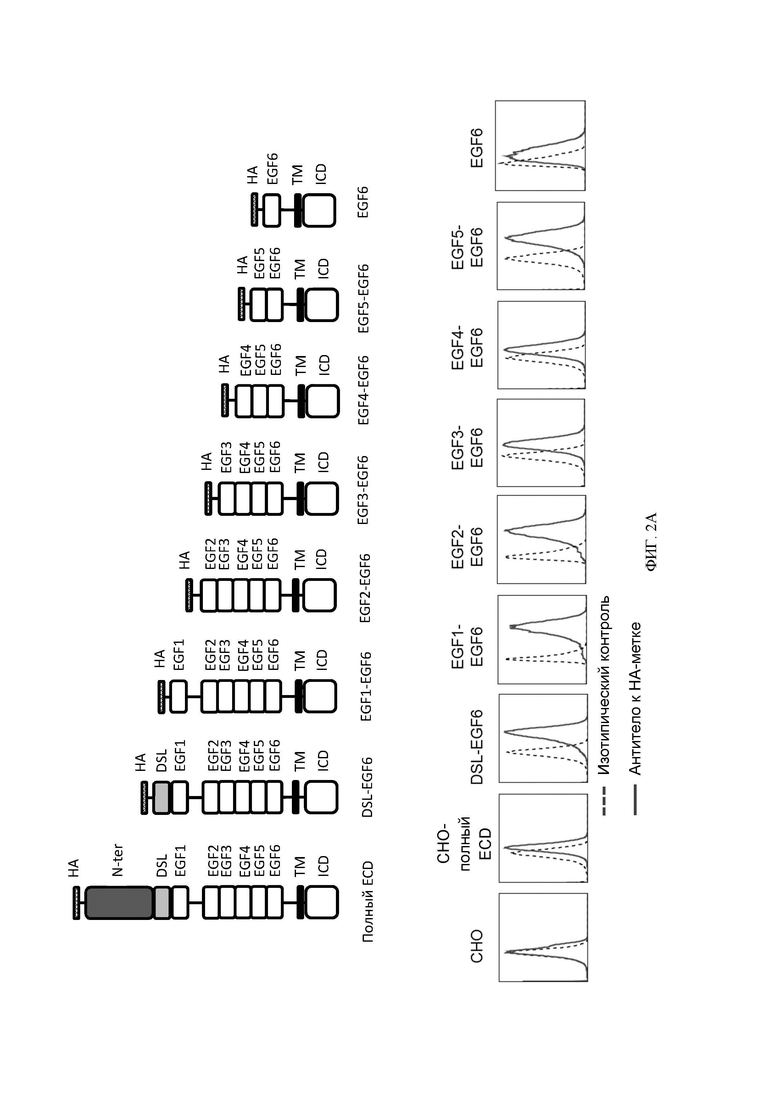

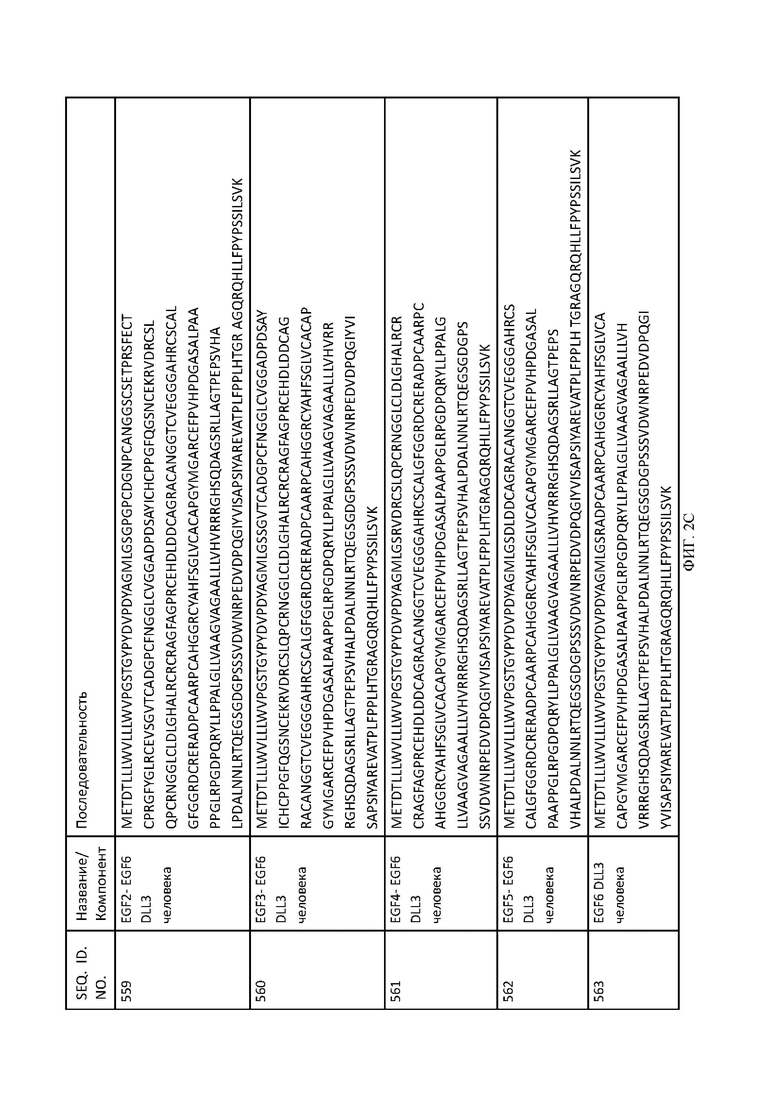
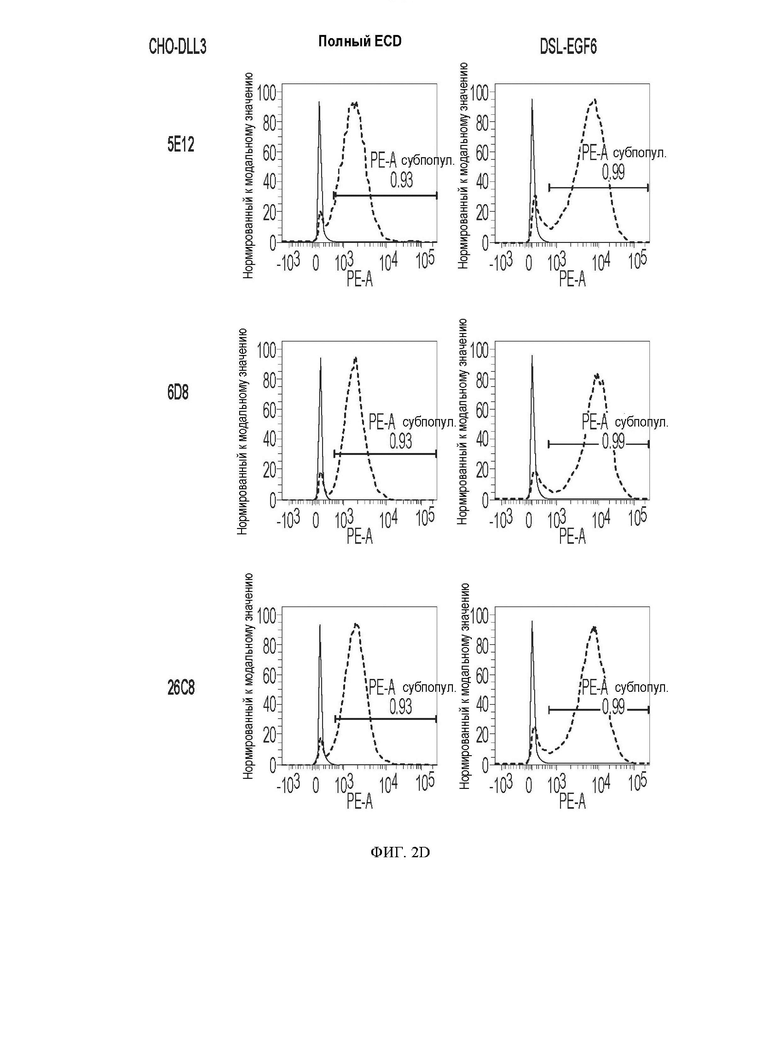
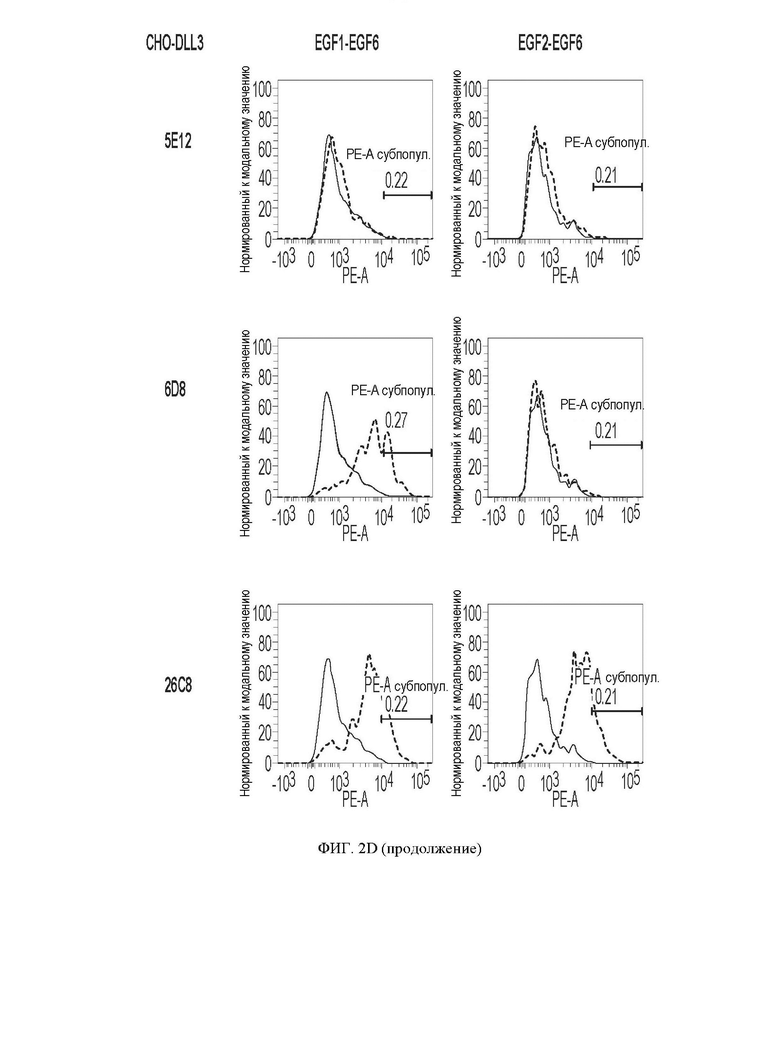
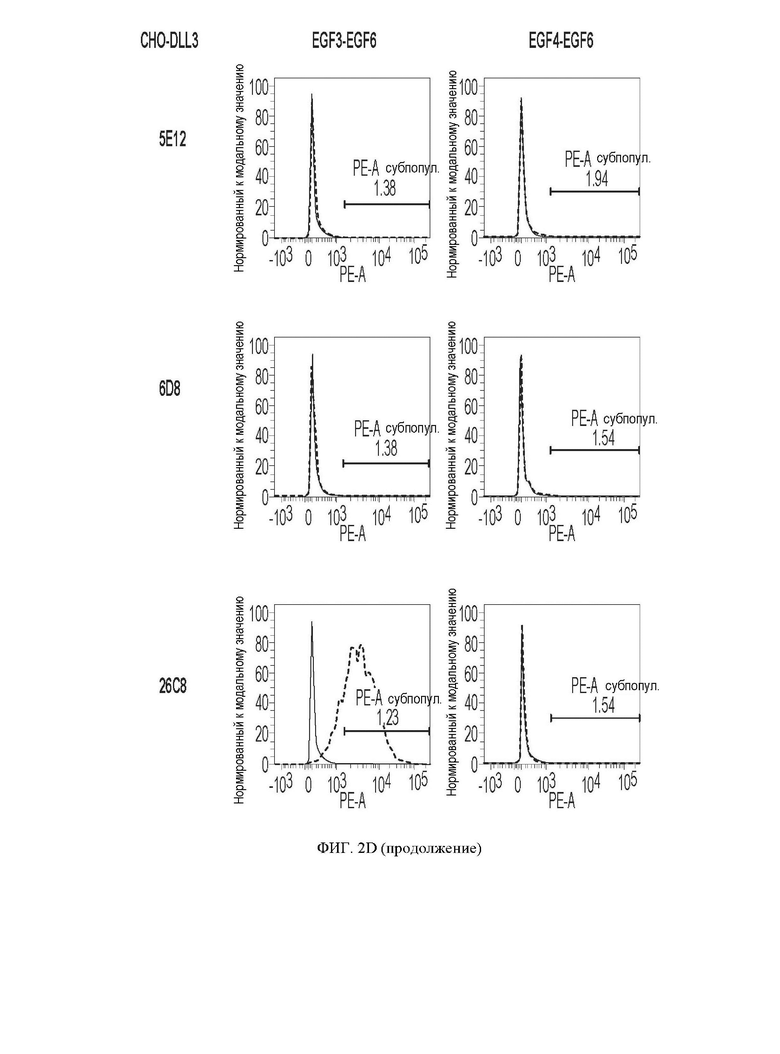
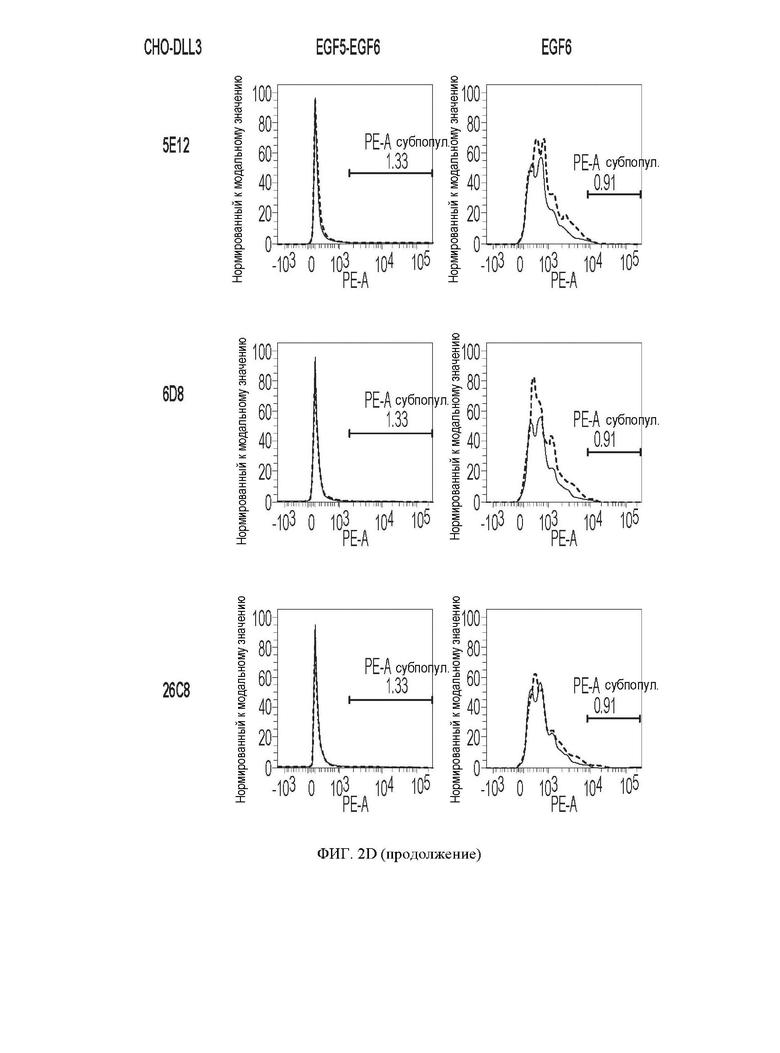
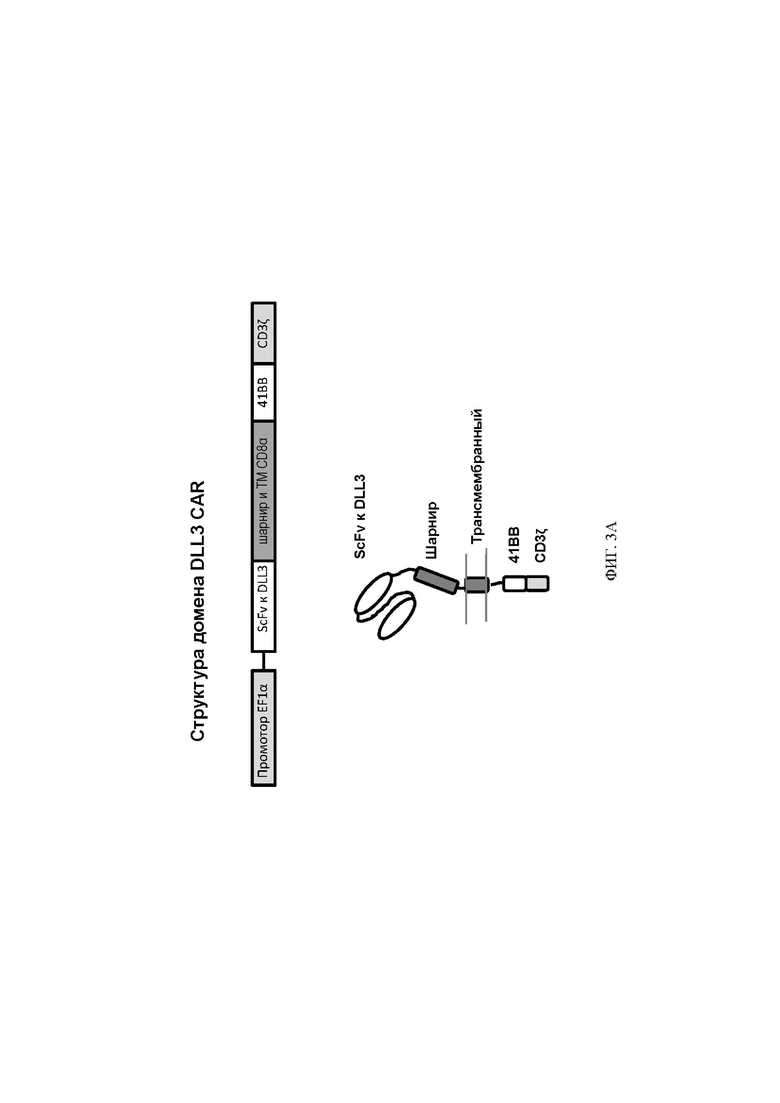


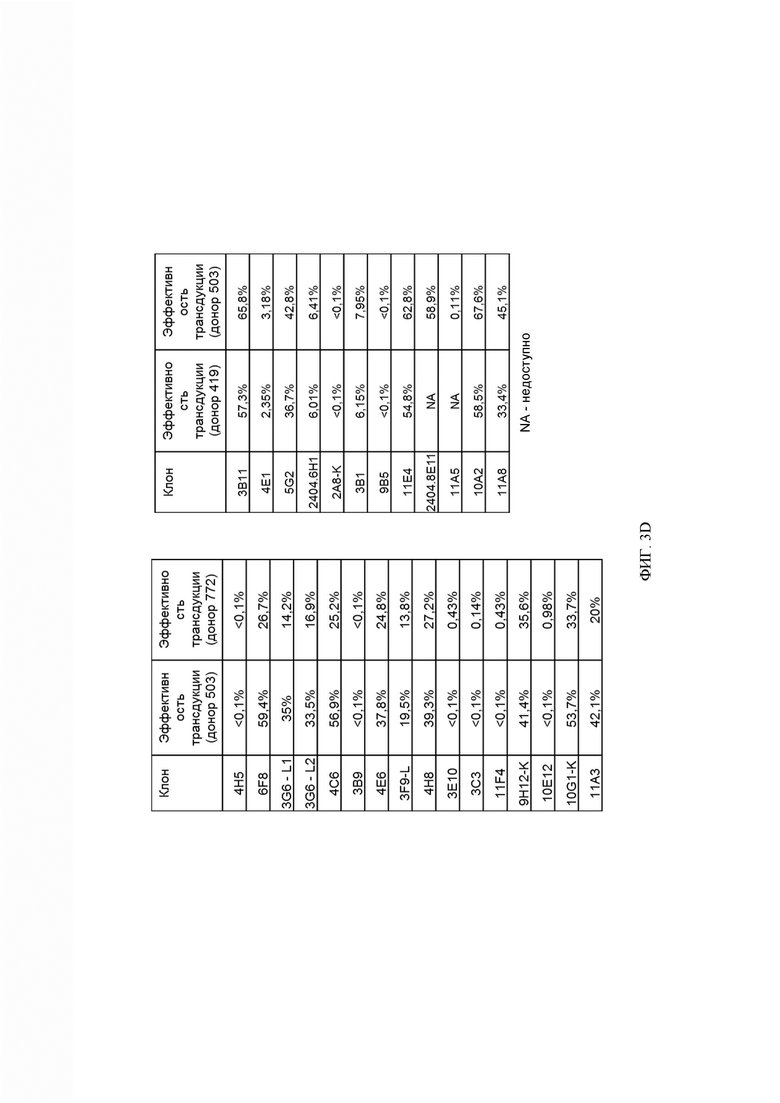
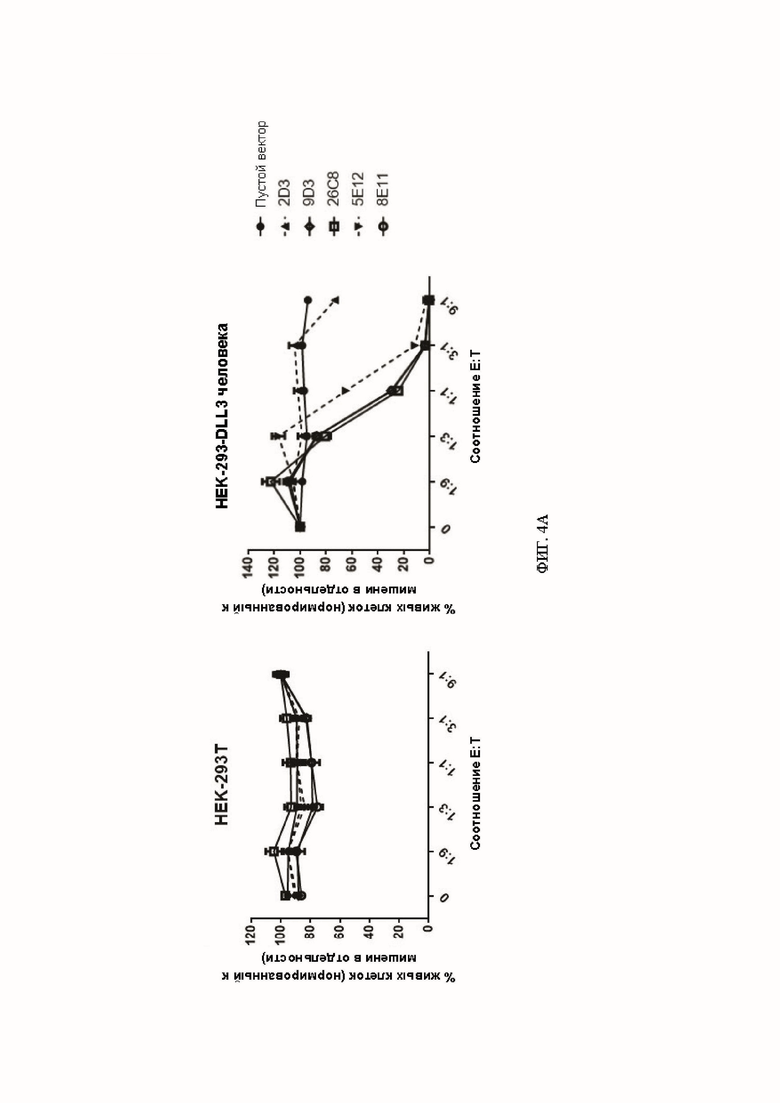
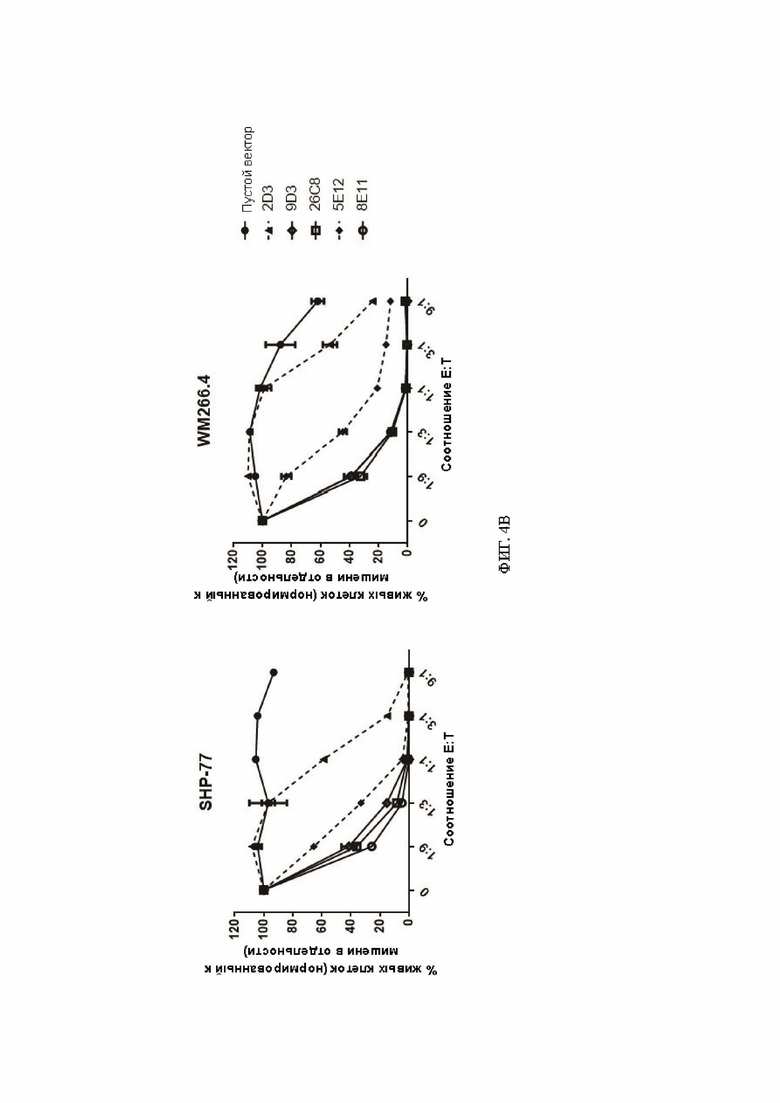
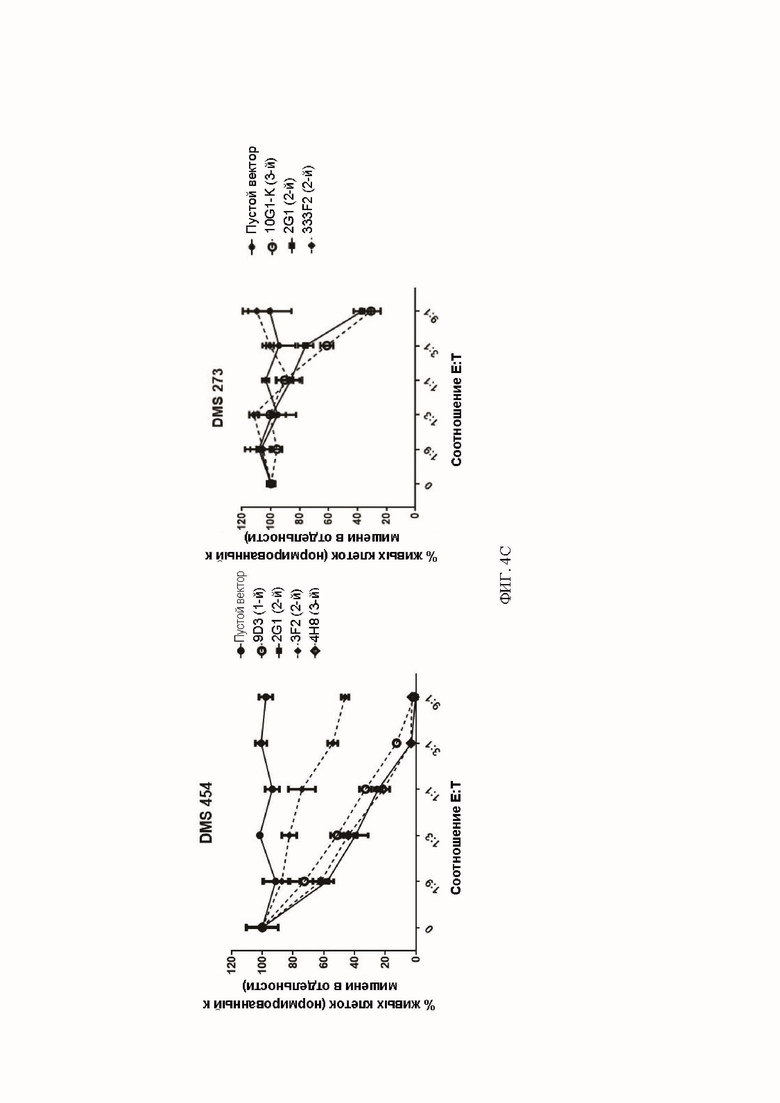
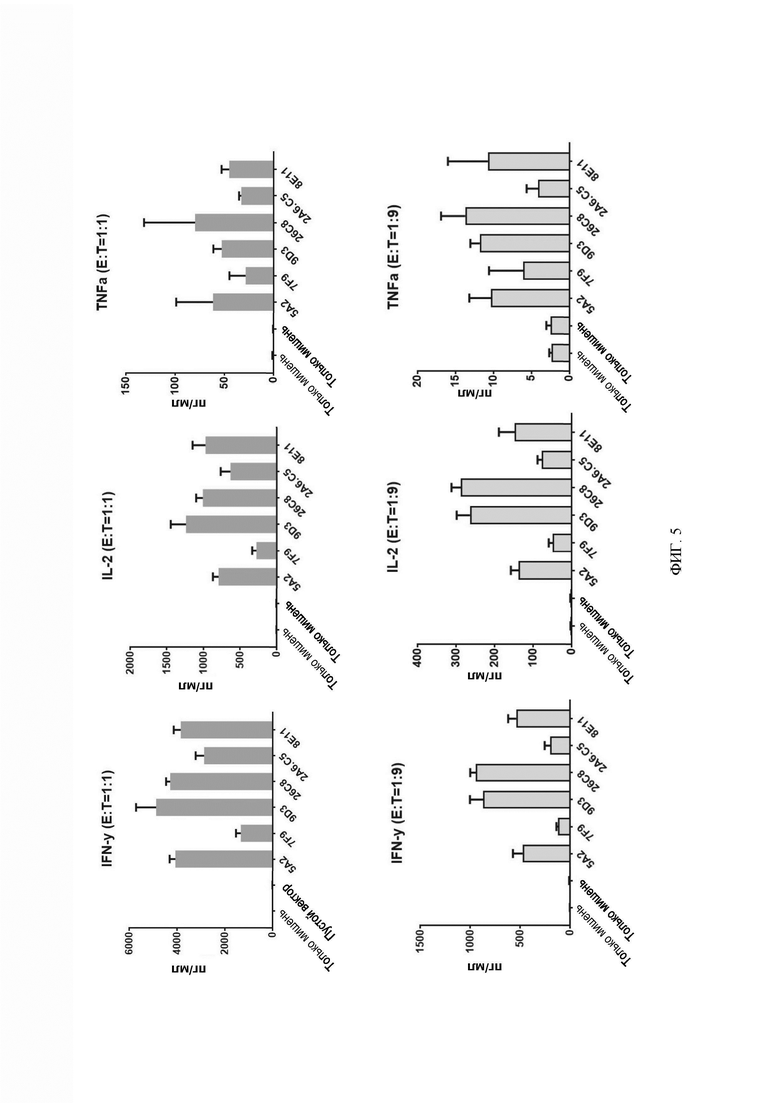
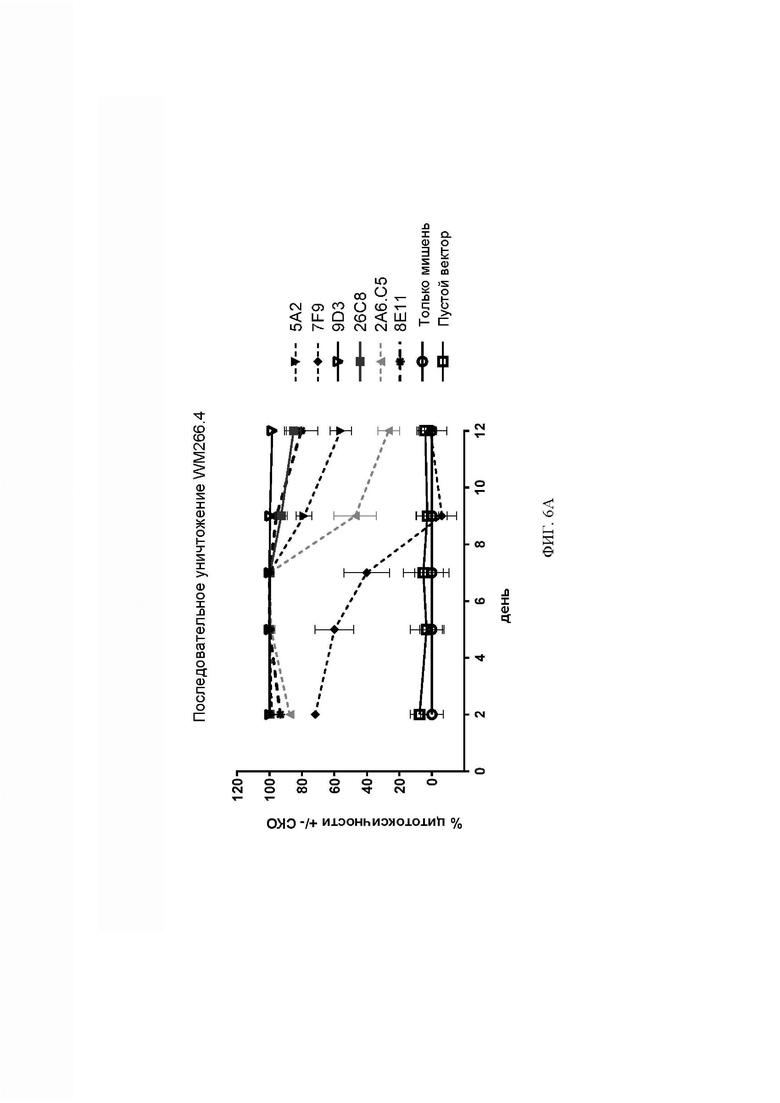
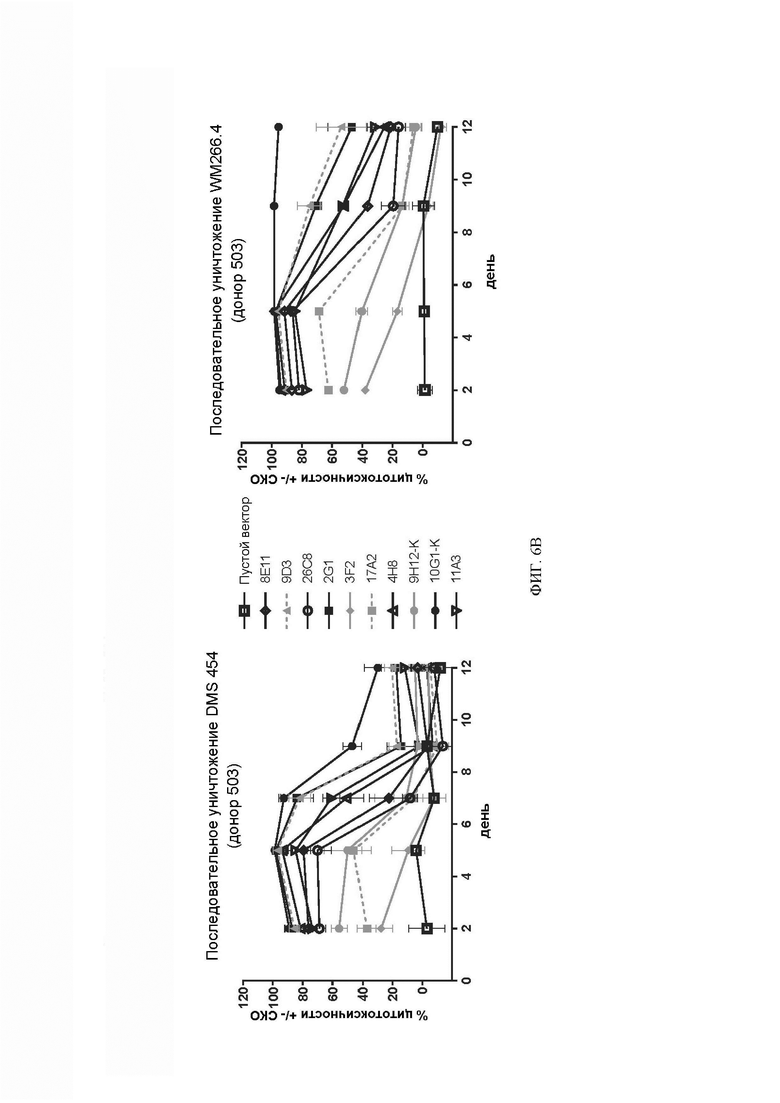
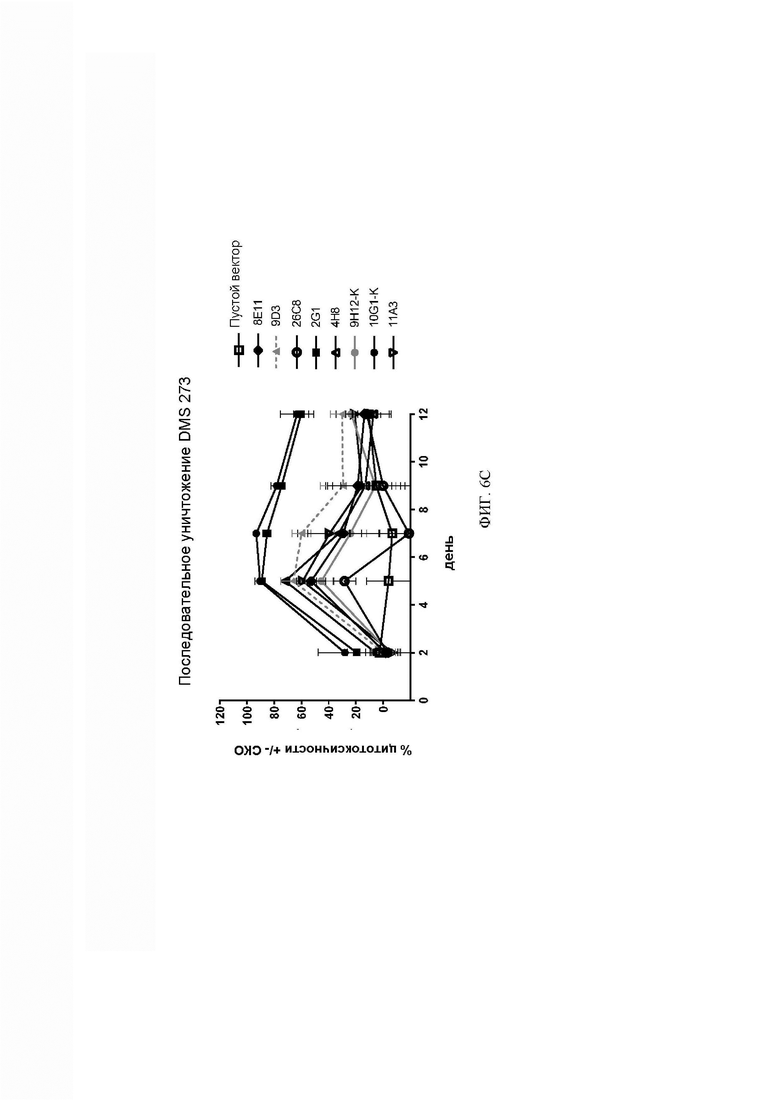
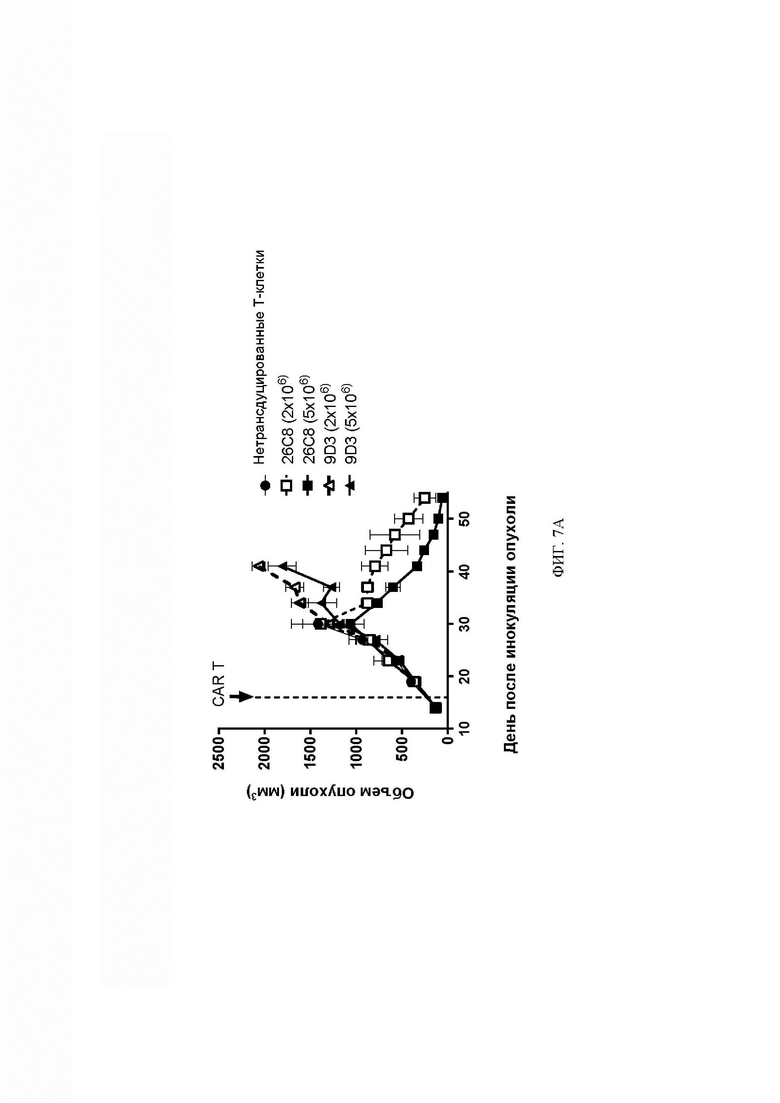
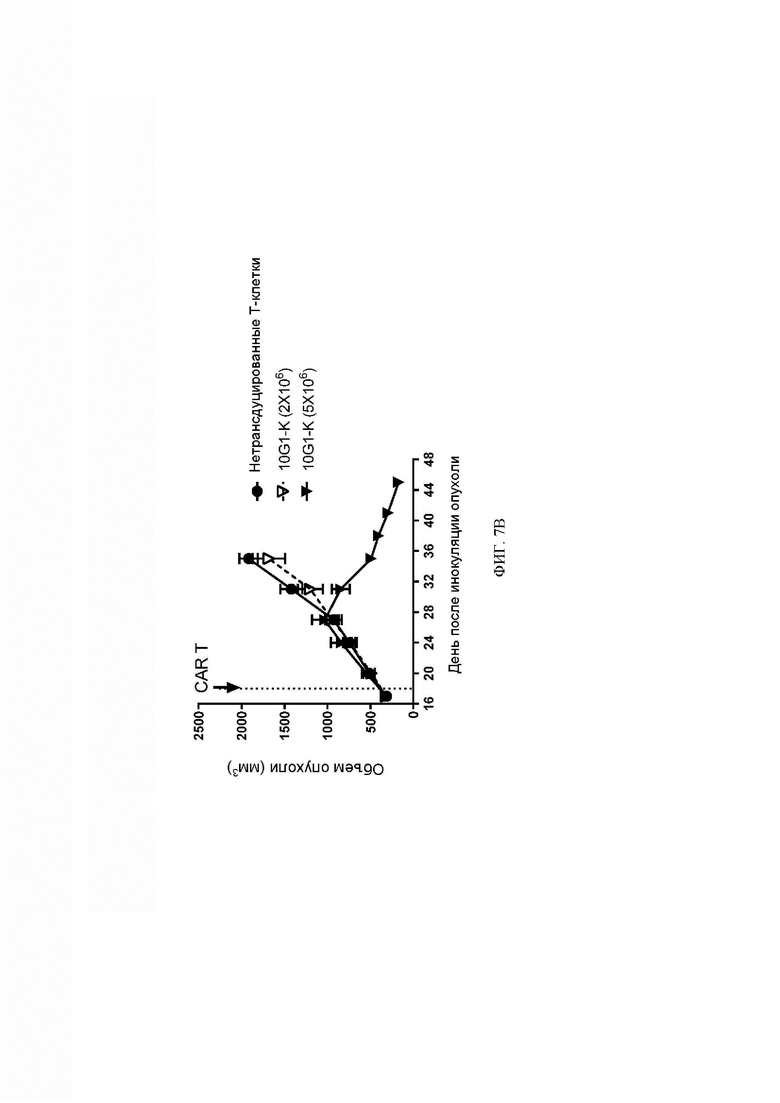
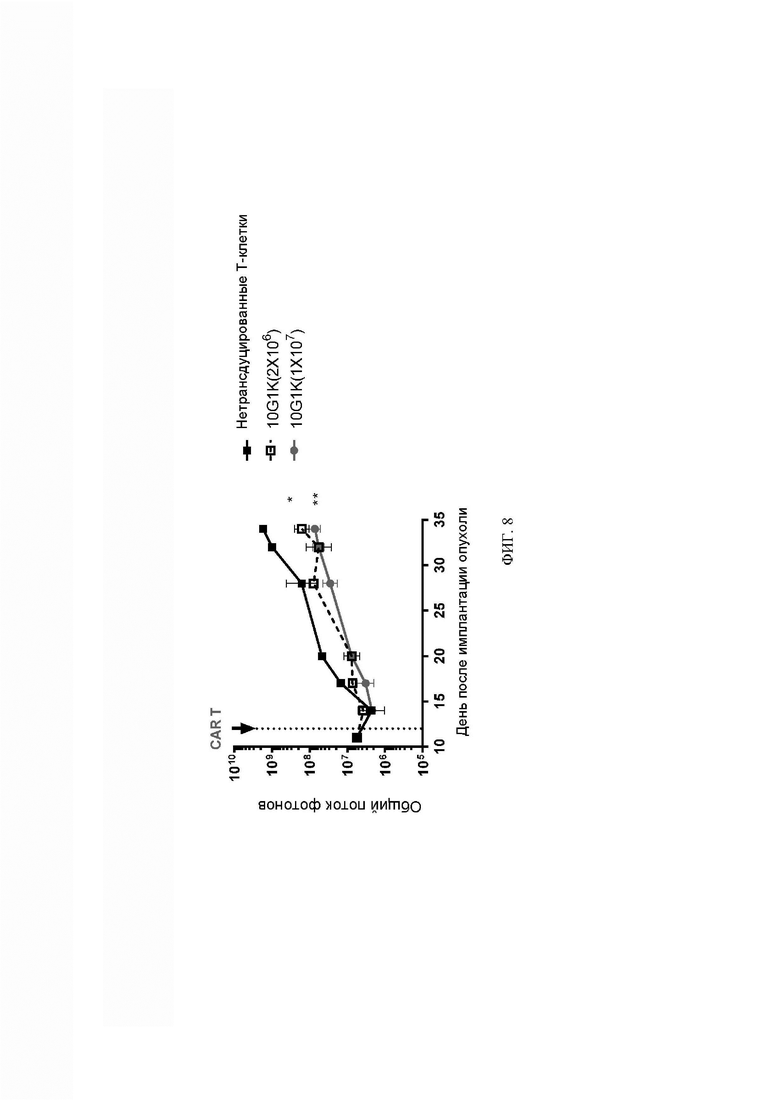
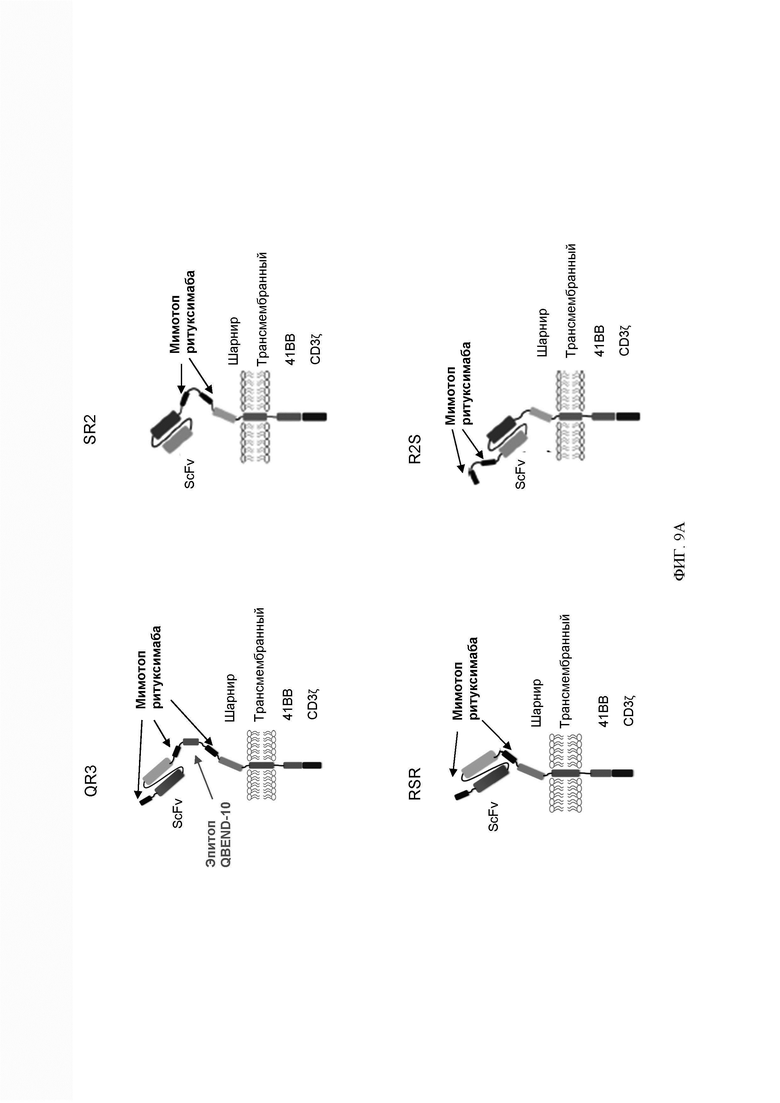
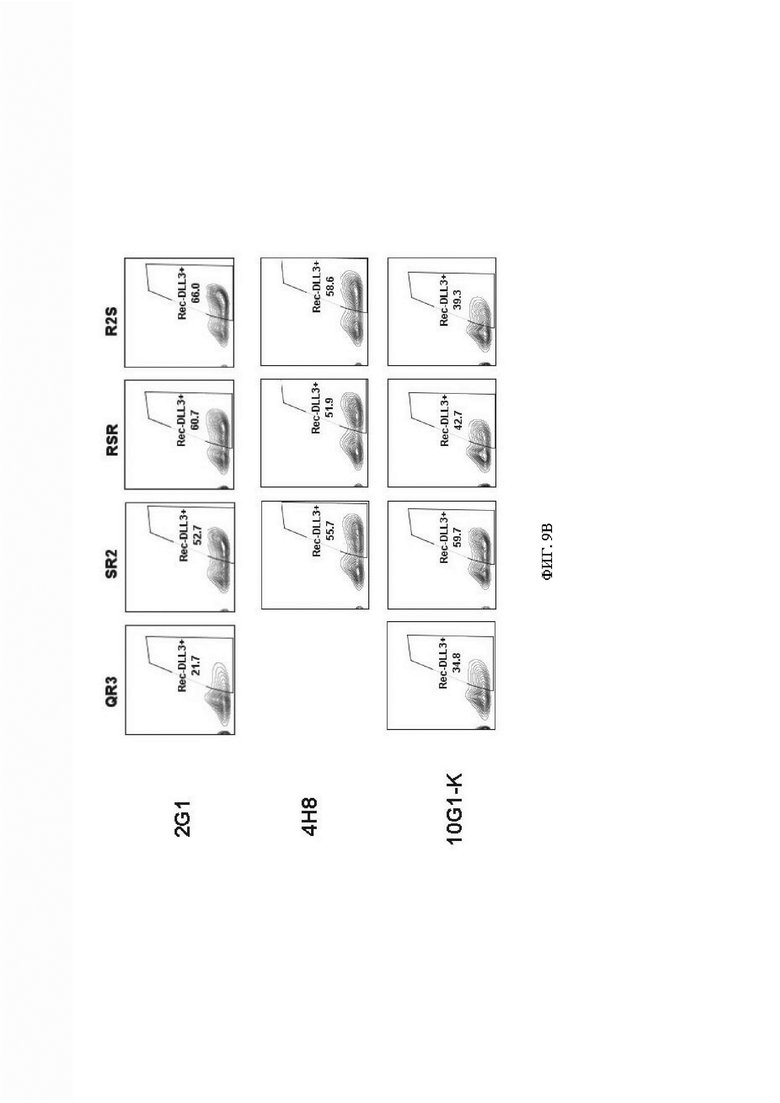
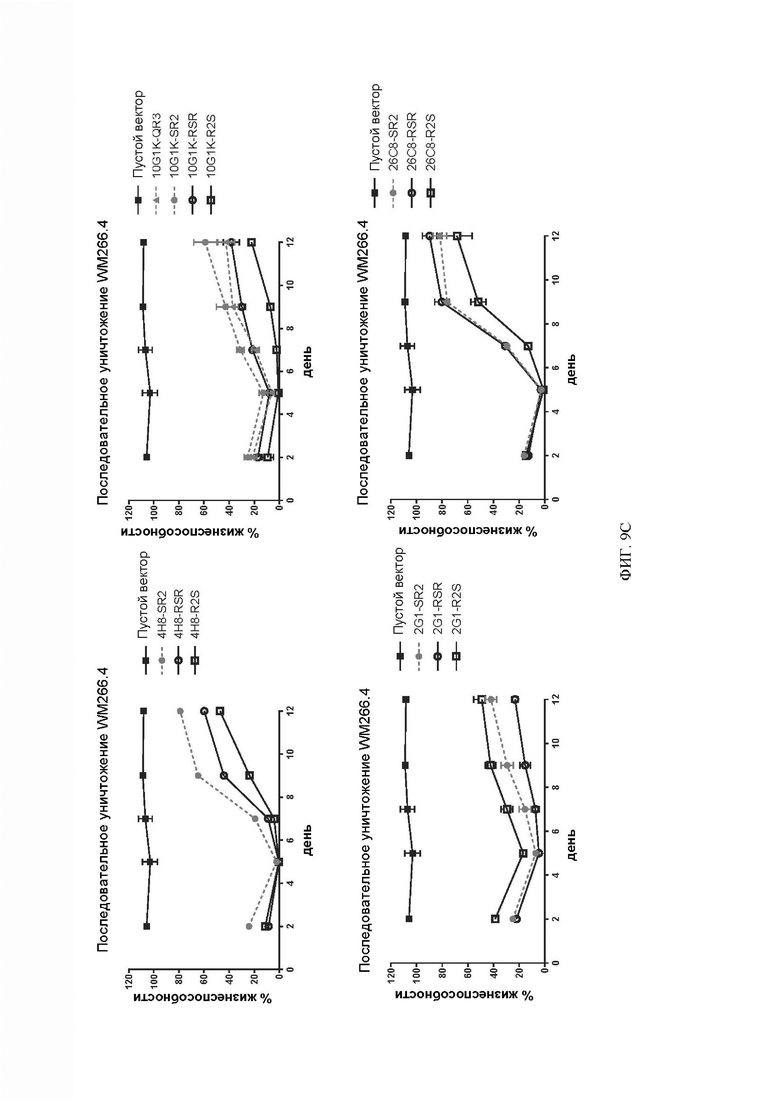
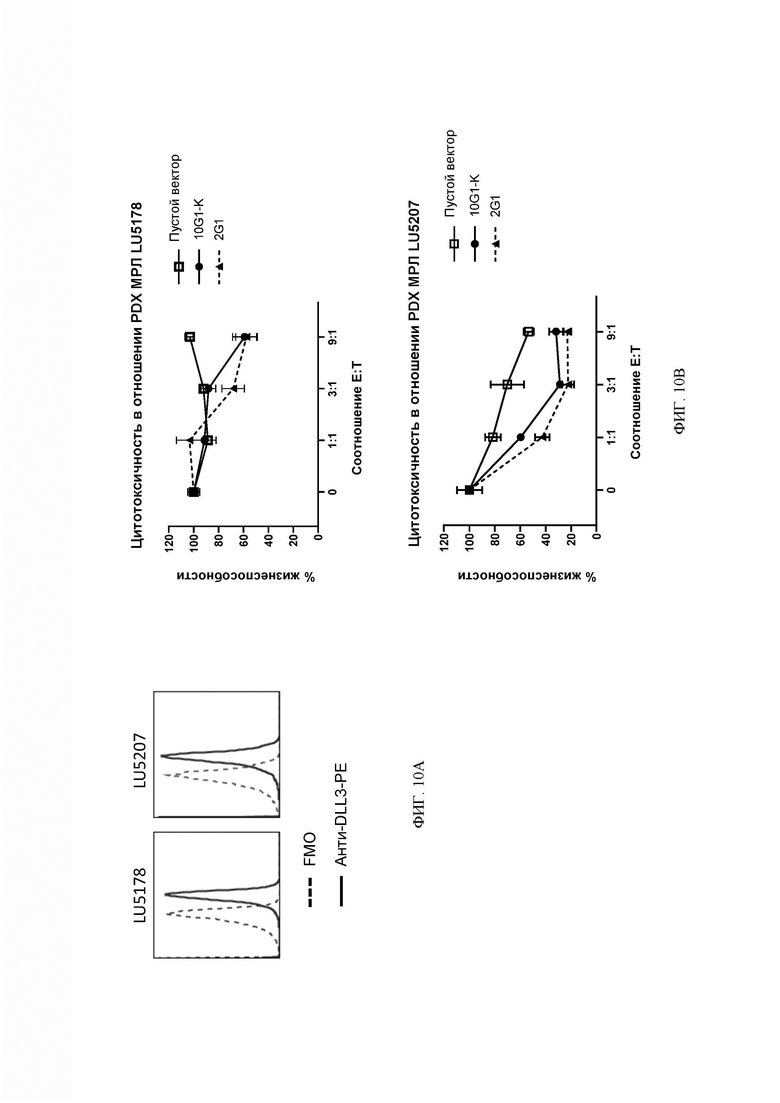
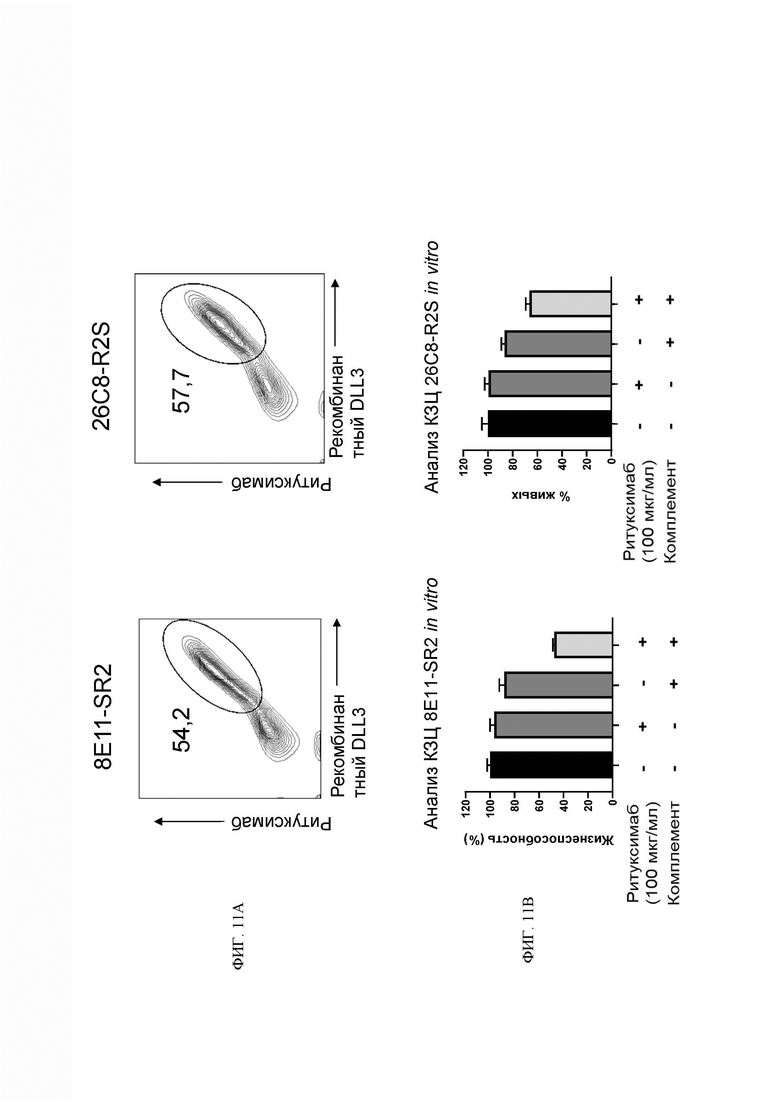
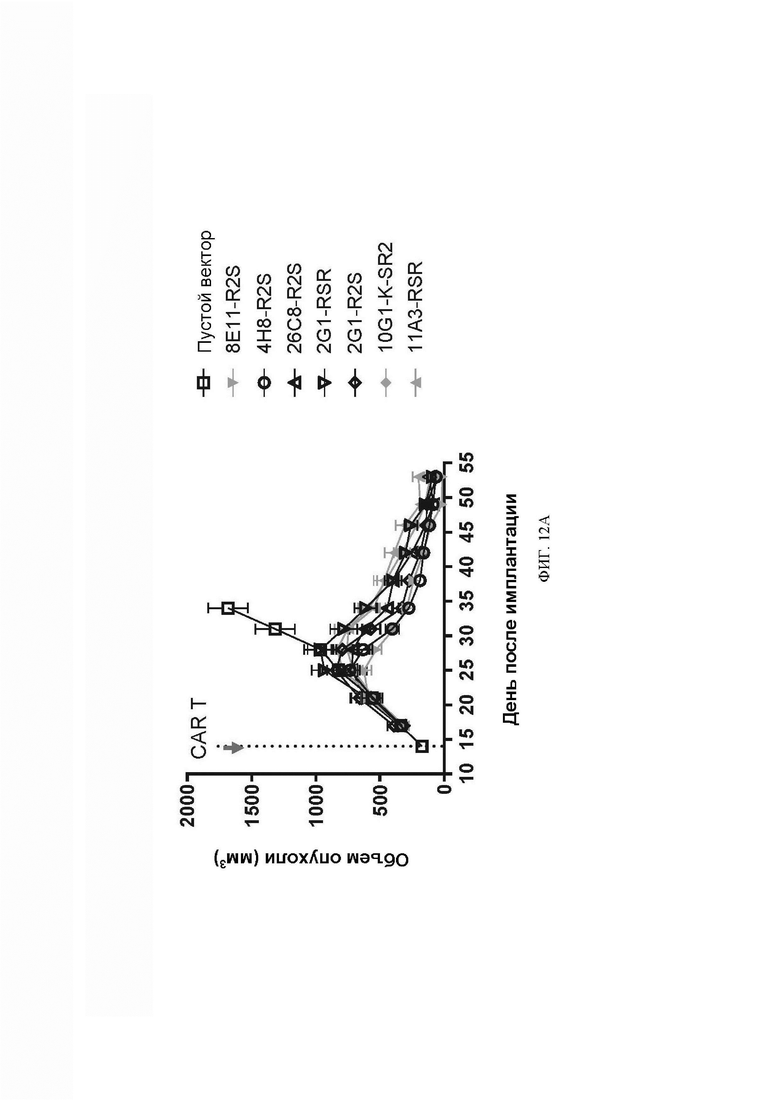
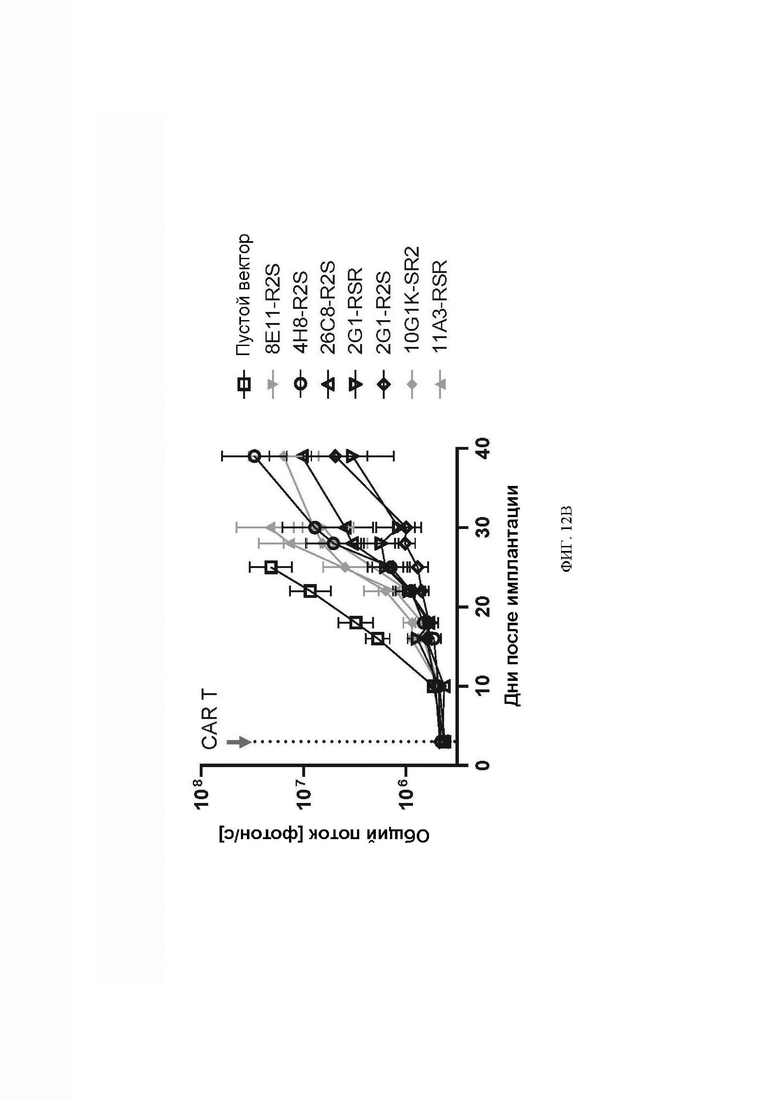
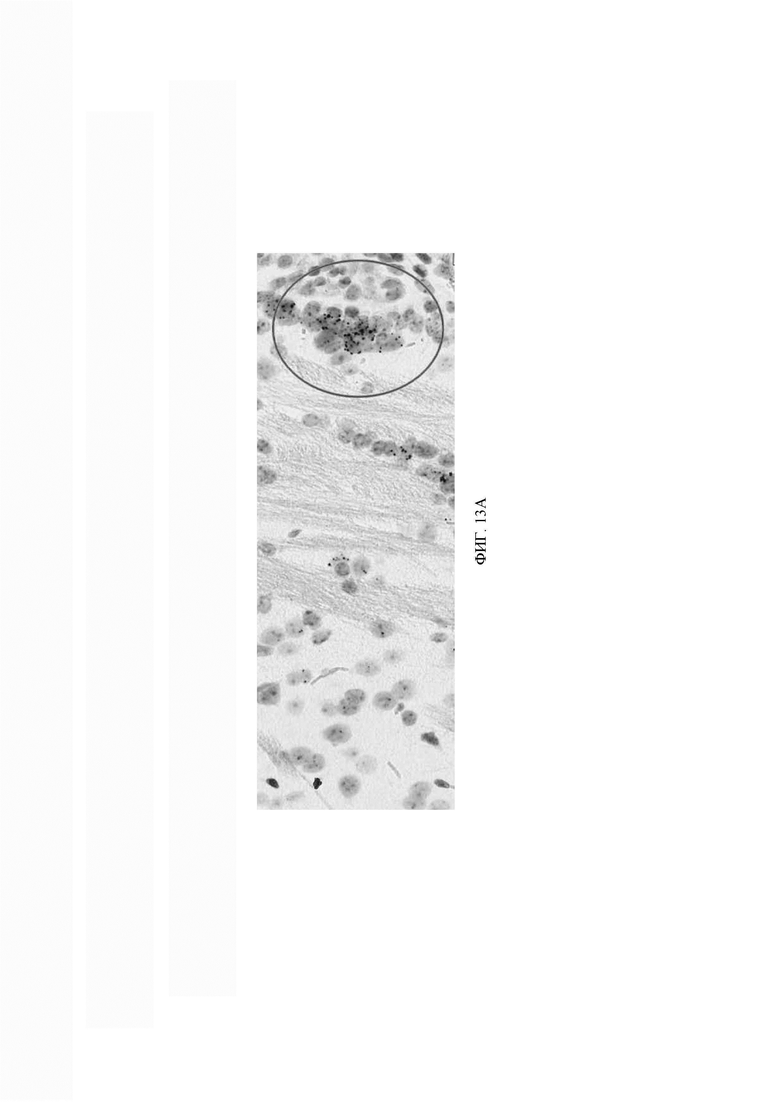
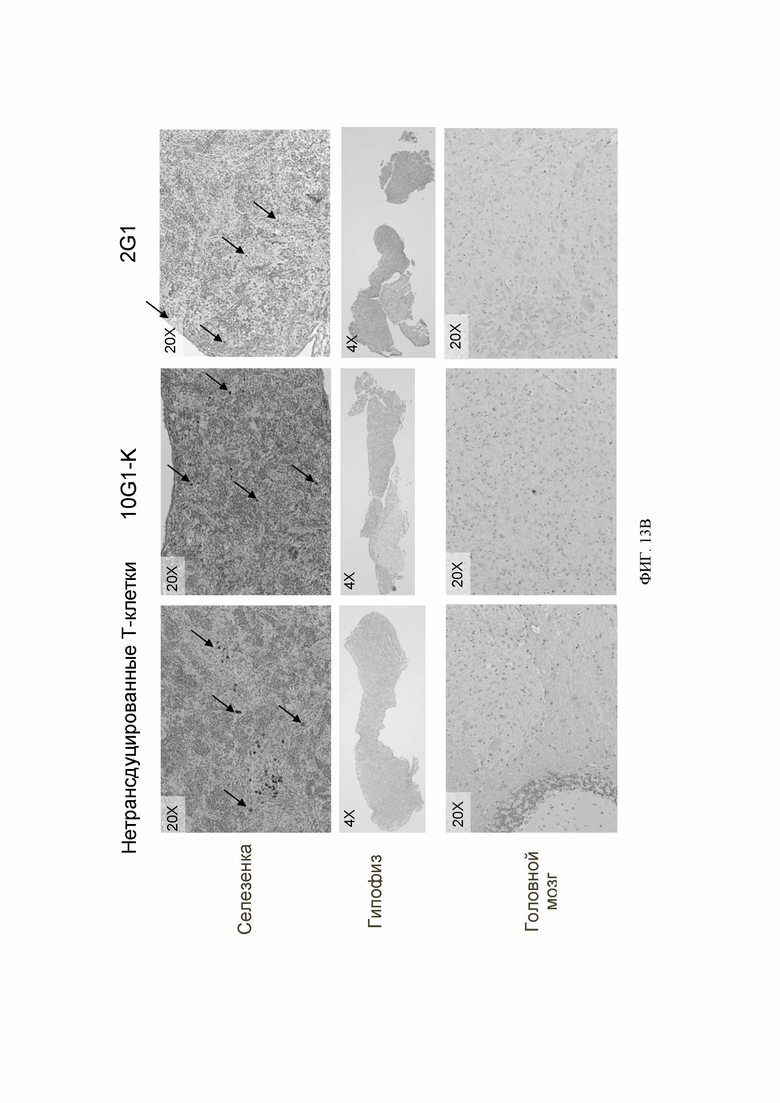
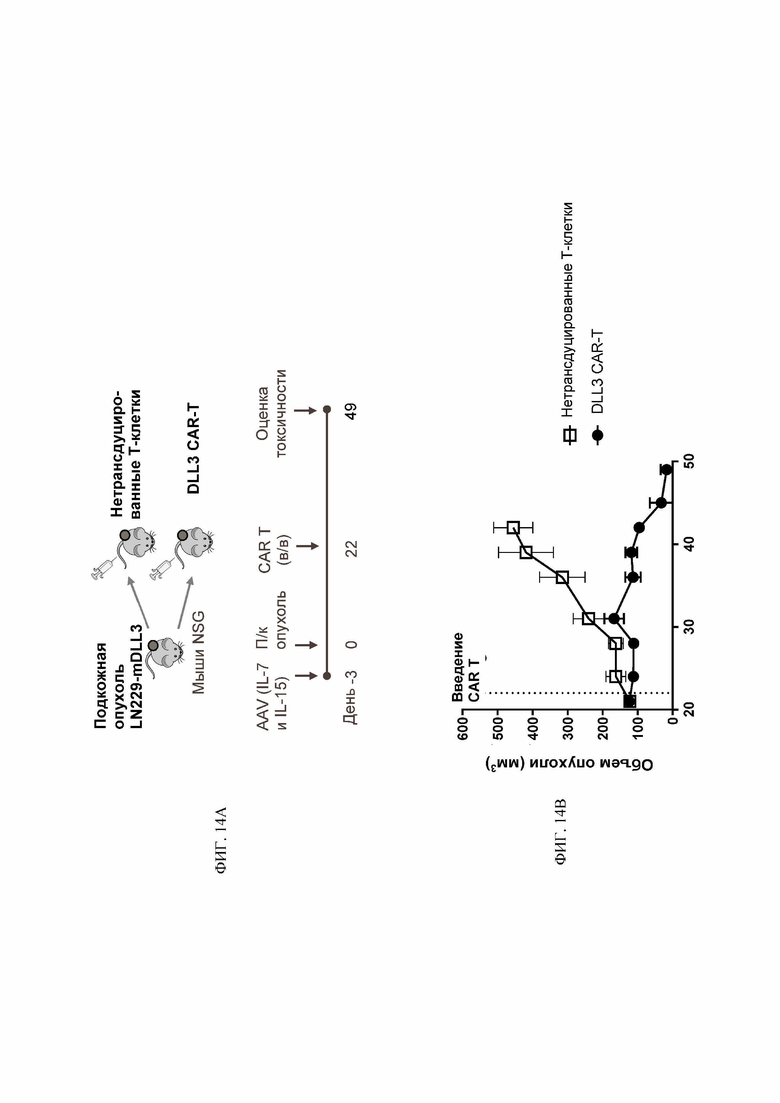


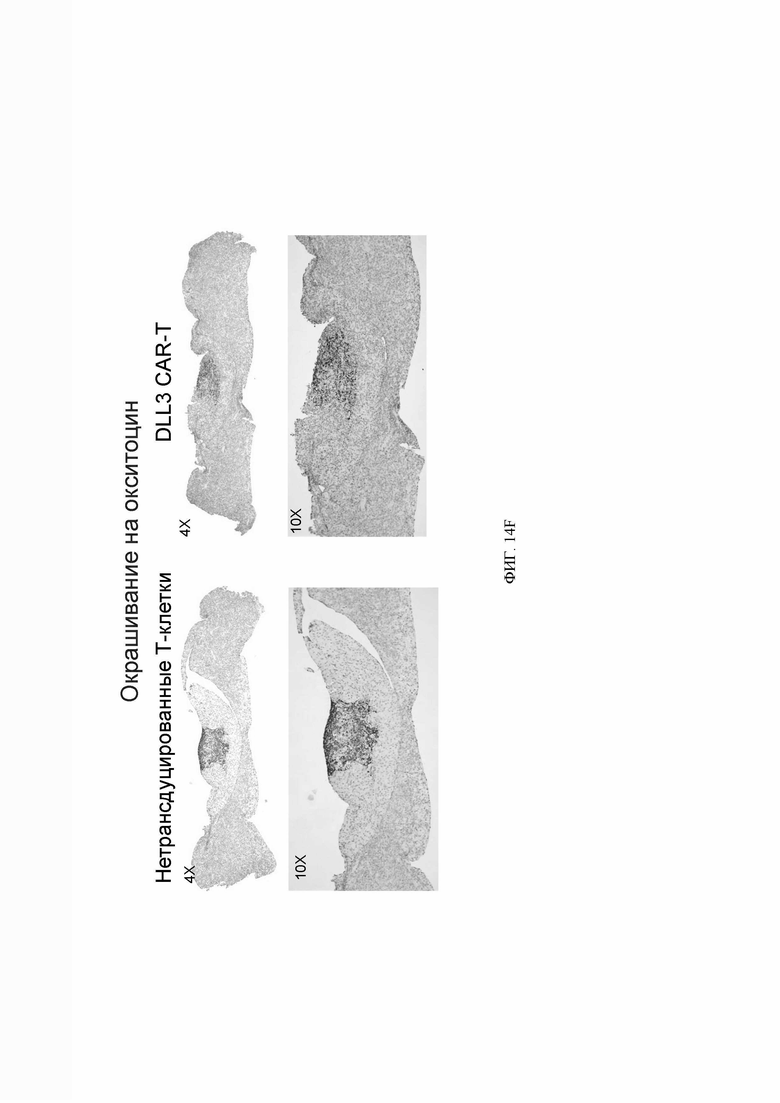
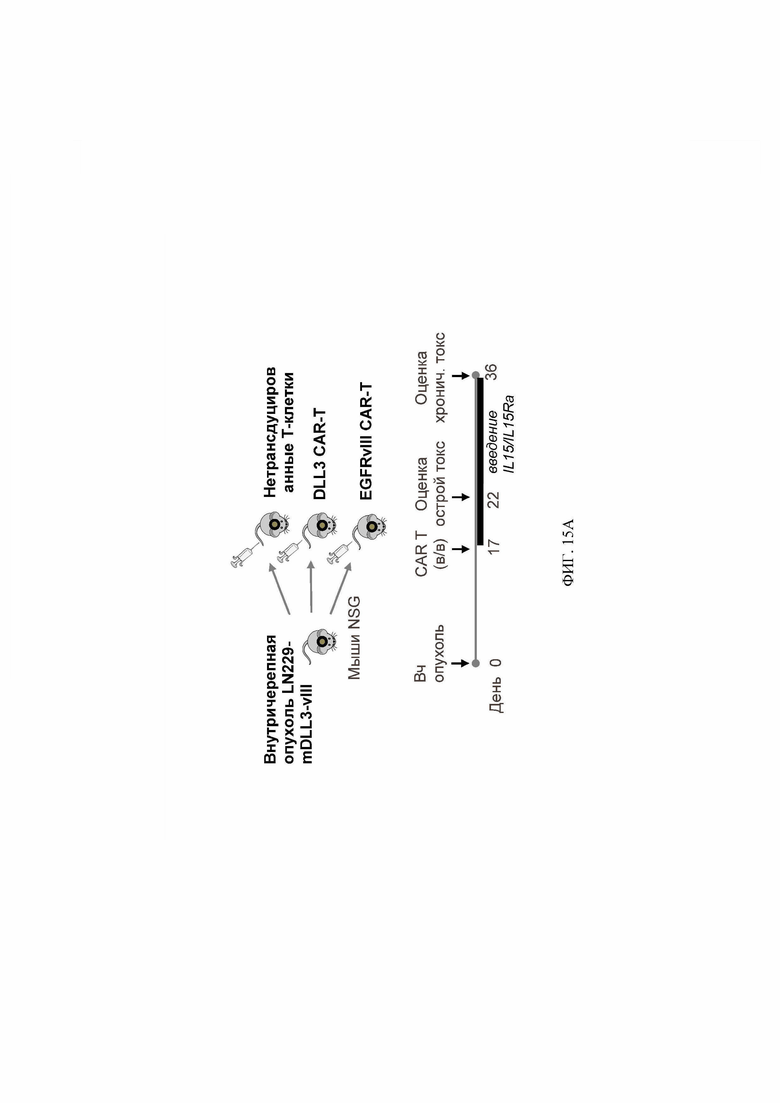
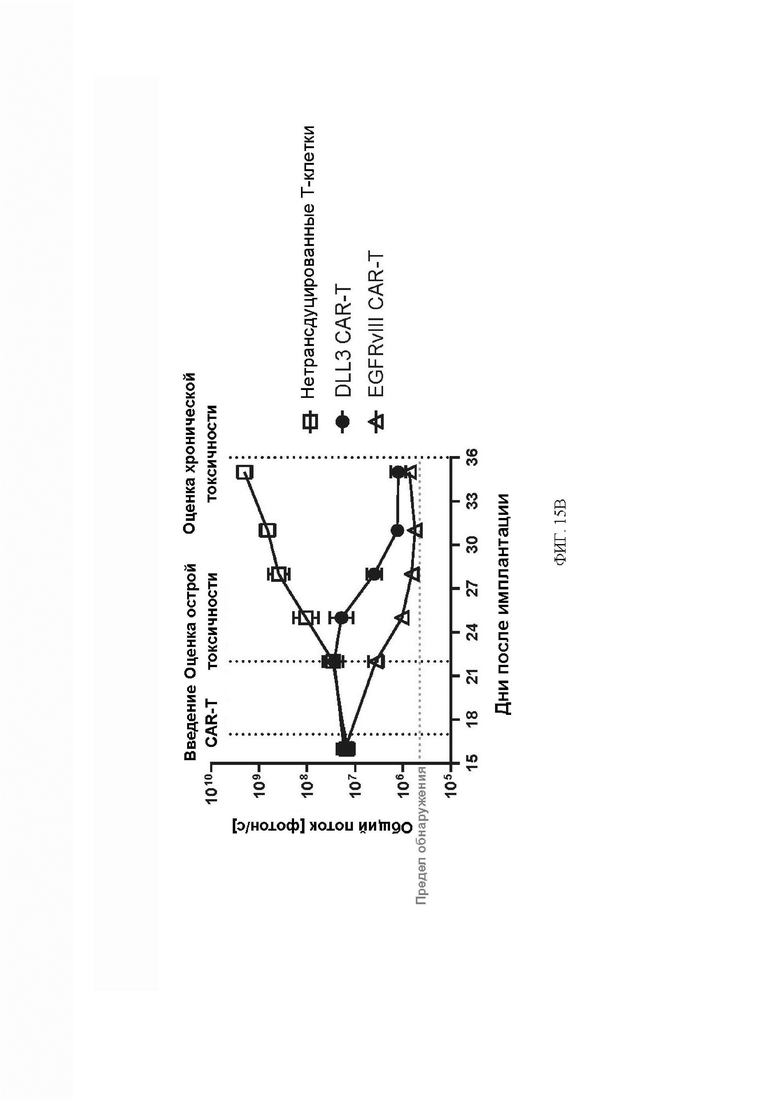

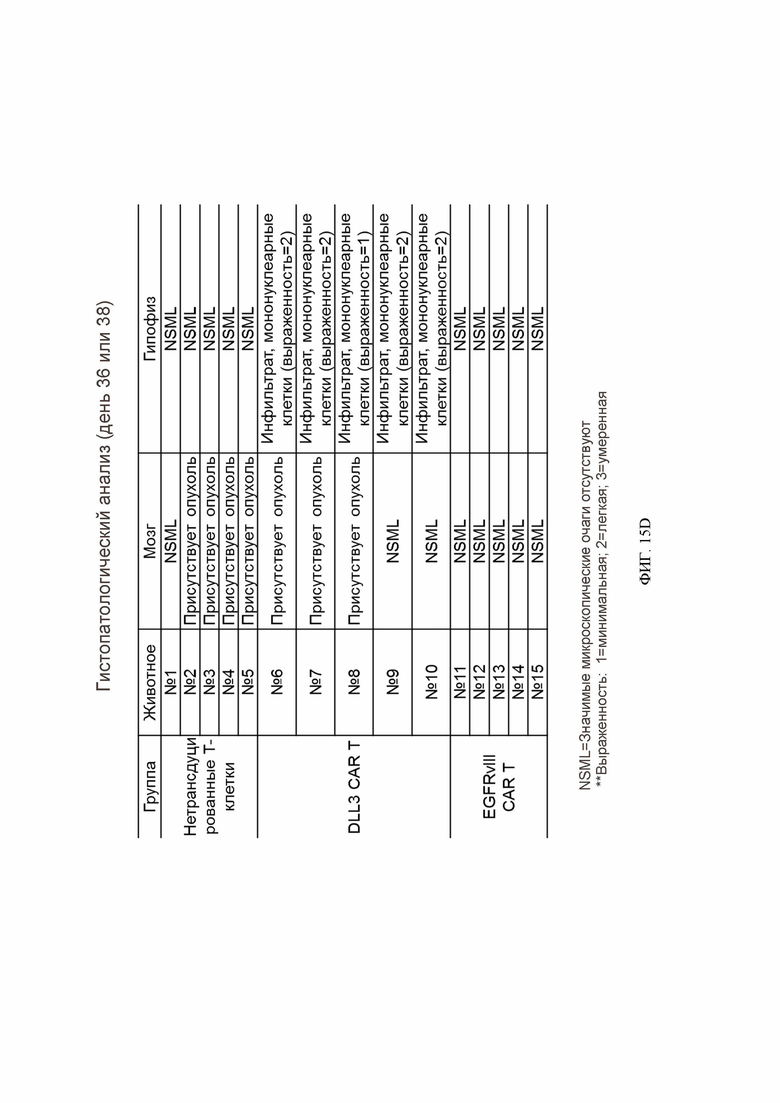
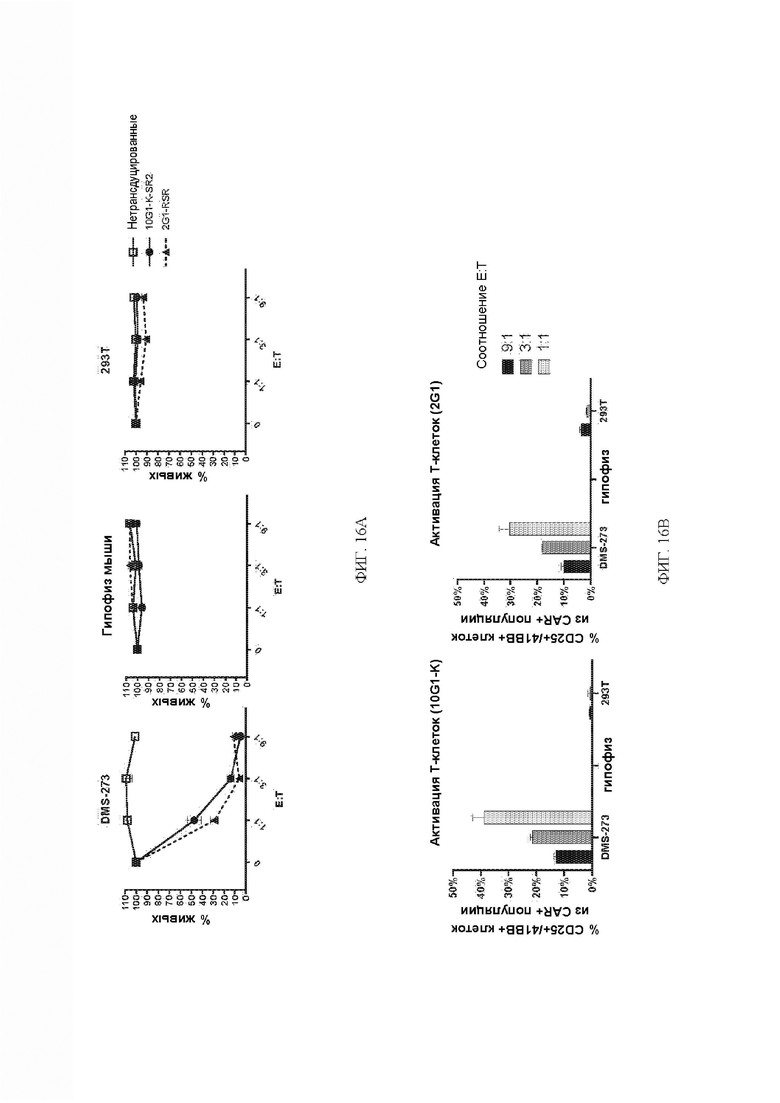
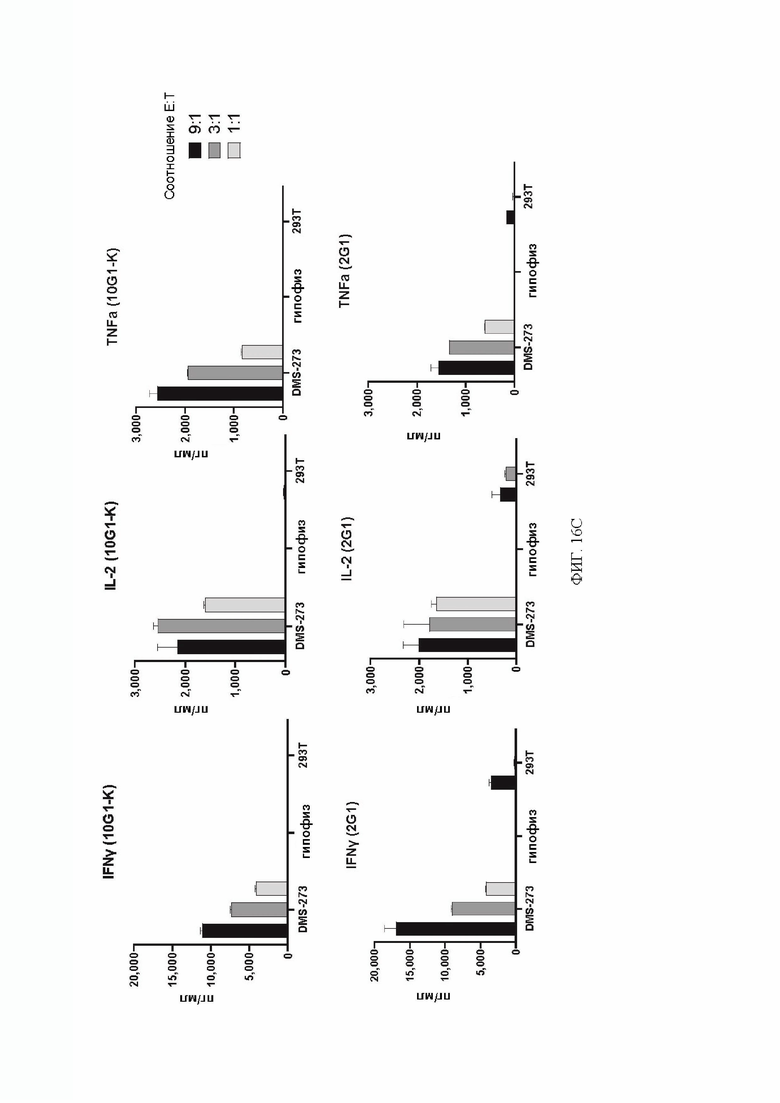
Изобретение относится к области биотехнологии, в частности к химерному антигенному рецептору, который специфически связывается с DLL3, выделенному полинуклеотиду, его кодирующему, а также к вектору и клетке, содержащим указанный полинуклеотид. Также раскрыты композиция и флакон, содержащие вышеуказанную клетку. Изобретение также относится к связывающему агенту против DLL3, а также к композиции, его содержащей. Изобретение эффективно для лечения или предупреждения состояния, связанного с нежелательными и/или повышенными уровнями DLL3. 23 н. и 36 з.п. ф-лы, 16 ил., 10 табл., 16 пр.
1. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит по меньшей мере одно из:
(a) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 109, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 110, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 111, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 112, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 113, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 114;
(b) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 253, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 254, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 255, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 256, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 257, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 258;
(c) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 271, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 272, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 273, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 274, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 275, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 276;
(d) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 217, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 218, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 219, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 220, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 221, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 222;
(e) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 262, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 263, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 264, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 265, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 266, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 267;
(f) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 37, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 38, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 39, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 40, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 41, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 42;
(g) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 28, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 29 или 695, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 30, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 31, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 32, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 33;
(h) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 73, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 74, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 75, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 76 или 696, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 77, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 78;
(i) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 280, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 281, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 282, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 283, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 284, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 285;
(j) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 1, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 2, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 3, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 4, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 5, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 6;
(k) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 46, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 47, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 48, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 49, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 50, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 51;
(l) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 64, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 65, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 66, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 67, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 68, CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 69;
(m) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 172, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 173, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 174, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 175, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 176, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 177;
(n) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 19, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 20, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 21, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 22, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 23, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 24;
(o) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 127, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 128, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 129, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 130, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 131, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 132; или
(p) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 55, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 56, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 57, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 58, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 59, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 60.
2. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит:
(a) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 109,
(b) CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 110,
(c) CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 111,
(d) CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 112,
(e) CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 113, и
(f) CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 114.
3. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит:
(a) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 253,
(b) CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 254,
(c) CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 255,
(d) CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 256,
(e) CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 257, и
(f) CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 258.
4. Химерный антигенный рецептор по любому из пп. 1-3, где вариабельная тяжелая цепь и вариабельная легкая цепь связаны по меньшей мере одним линкером.
5. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит:
(a) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 115, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 116;
(b) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 259, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 260;
(c) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 277, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 278;
(d) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 223, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 224;
(e) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 268, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 269;
(f) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 43, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 44;
(g) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 34, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 35;
(h) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 79, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 80;
(i) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 286, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 287;
(j) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 7, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 8;
(k) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 52, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 53;
(l) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 70, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 71;
(m) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 178, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 179;
(n) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 25, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 26;
(o) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 133, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 134; или
(p) вариабельную тяжелую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 61, и вариабельную легкую цепь, содержащую аминокислотную последовательность, как показано в SEQ ID NO: 62.
6. Химерный антигенный рецептор по п. 5, где вариабельная тяжелая цепь и вариабельная легкая цепь связаны по меньшей мере одним линкером.
7. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, где внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит последовательность, выбранную из группы, состоящей из SEQ ID NO: 117, SEQ ID NO: 261, SEQ ID NO: 9, SEQ ID NO: 18, SEQ ID NO: 27, SEQ ID NO: 36, SEQ ID NO: 45, SEQ ID NO: 54, SEQ ID NO: 63, SEQ ID NO: 72, SEQ ID NO: 81, SEQ ID NO: 90, SEQ ID NO: 99, SEQ ID NO: 108, SEQ ID NO: 126, SEQ ID NO: 135, SEQ ID NO: 144, SEQ ID NO: 153, SEQ ID NO: 162, SEQ ID NO: 171, SEQ ID NO: 180, SEQ ID NO: 189, SEQ ID NO: 198, SEQ ID NO: 207, SEQ ID NO: 216, SEQ ID NO: 225, SEQ ID NO: 234, SEQ ID NO: 243, SEQ ID NO: 252, SEQ ID NO: 270, SEQ ID NO: 279, SEQ ID NO: 288, SEQ ID NO: 297, SEQ ID NO: 306, SEQ ID NO: 315, SEQ ID NO: 324, SEQ ID NO: 333, SEQ ID NO: 342, SEQ ID NO: 351, SEQ ID NO: 360, SEQ ID NO: 369, SEQ ID NO: 378, SEQ ID NO: 387, SEQ ID NO: 396, SEQ ID NO: 405, SEQ ID NO: 414, SEQ ID NO: 423, SEQ ID NO: 432, SEQ ID NO: 441, SEQ ID NO: 450, SEQ ID NO: 459, SEQ ID NO: 468 и SEQ ID NO: 629.
8. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, причем внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит последовательность, показанную в SEQ ID NO: 117.
9. Химерный антигенный рецептор, который специфически связывается с DLL3, содержащий внеклеточный домен, трансмембранный домен и внутриклеточный домен, причем внеклеточный домен содержит антигенсвязывающий домен против DLL3, который специфически связывается с DLL3, и где антигенсвязывающий домен содержит последовательность, показанную в SEQ ID NO: 261.
10. Химерный антигенный рецептор, который специфически связывается с DLL3, где химерный антигенный рецептор содержит аминокислотную последовательность, выбранную из последовательностей SEQ ID NO: 482, 484-490, 492-494, 496, 501, 506, 510-513, 632, 634-640, 642, 644, 646, 651, 656 и 660-663.
11. Химерный антигенный рецептор, который специфически связывается с DLL3, где химерный антигенный рецептор содержит аминокислотную последовательностьSEQ ID NO: 686.
12. Химерный антигенный рецептор, который специфически связывается с DLL3, где химерный антигенный рецептор содержит аминокислотную последовательность SEQ ID NO: 690.
13. Химерный антигенный рецептор по любому из пп. 1-9, где внутриклеточный домен содержит по меньшей мере один костимулирующий домен.
14. Химерный антигенный рецептор по п. 13, где костимулирующий домен представляет собой сигнальную область CD28, OX-40, 4-1BB/CD137, CD2, CD7, CD27, CD30, CD40, программируемую смерть-1 (PD-1), индуцибельный костимулятор Т-клеток (ICOS), антиген 1, связанный с функцией лимфоцитов (LFA-1 (CD1 1a/CD18), CD3-гамма, CD3-дельта, CD3-эпсилон, CD247, CD276 (B7-H3), LIGHT, (TNFSF14), NKG2C, Ig-альфа (CD79a), DAP-10, Fc-гамма-рецептор, молекулу MHC класса I, белки TNF-рецептора, белок иммуноглобулина, рецептор цитокинов, интегрины, сигнальные молекулы активации лимфоцитов (SLAM-белки), активирующие рецепторы NK-клеток, BTLA, лиганды Toll-рецепторов, ICAM-1, B7-H3, CDS, ICAM-1, GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CD8-бета, IL-2R-бета, IL-2R-гамма, IL-7R-альфа, ITGA4, VLA1, CD49a, ITGA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD1 1d, ITGAE, CD103, ITGAL, CD1 1a, LFA-1, ITGAM, CD1 1b, ITGAX, CD1 1c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, TNFR2, TRANCE/RANKL, DNAMI (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRT AM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Lyl08), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a, лиганд, который специфически связывается с CD83, или любую их комбинацию.
15. Химерный антигенный рецептор по п. 14, где костимулирующий домен содержит сигнальную область 4-1BB/CD137.
16. Химерный антигенный рецептор по п. 15, где костимулирующий домен 4-1BB/CD137 содержит SEQ ID NO: 480 или ее фрагмент.
17. Химерный антигенный рецептор по любому из пп. 1-9 или 13-16, где внутриклеточный домен содержит по меньшей мере один активирующий домен.
18. Химерный антигенный рецептор по п. 17, где активирующий домен содержит CD3.
19. Химерный антигенный рецептор по п. 18, где CD3 включает CD3-дзета.
20. Химерный антигенный рецептор по п. 19, где CD3-дзета содержит SEQ ID NO: 481 или ее фрагмент.
21. Химерный антигенный рецептор по любому из пп. 1-9 или 17-20, где шарнирный домен выбран из CD8 шарнирного домена, CD4 шарнирного домена, CD28 шарнирного домена, 4-1BB шарнирного домена или IgG шарнирного домена.
22. Химерный антигенный рецептор по любому из пп. 1-9 или 17-20, где шарнирный домен представляет собой CD8 шарнирный домен.
23. Химерный антигенный рецептор по п. 22, где CD8 шарнирный домен представляет собой CD8-альфа шарнирный домен.
24. Химерный антигенный рецептор по любому из пп. 1-9 или 17-20, где шарнирный домен представляет собой CD28 шарнирный домен.
25. Химерный антигенный рецептор по любому из пп. 1-9 или 17-20, где трансмембранный домен выбран из CD8 трансмембранного домена, CD4 трансмембранного домена, CD28 трансмембранного домена или 4-1BB трансмембранного домена.
26. Химерный антигенный рецептор по любому из пп. 1-9 или 17-20, где трансмембранный домен представляет собой CD8 трансмембранный домен.
27. Химерный антигенный рецептор по п. 26, где CD8 трансмембранный домен представляет собой CD8-альфа трансмембранный домен.
28. Химерный антигенный рецептор по любому из пп. 1-9 или 17-20, где трансмембранный домен представляет собой CD28 трансмембранный домен.
29. Химерный антигенный рецептор по любому из пп. 1-28, где химерный антигенный рецептор кодируется полинуклеотидной последовательностью любой из SEQ ID NO: 570-621 и 631.
30. Химерный антигенный рецептор по любому из пп. 1-29, содержащий предохранительный переключатель.
31. Химерный антигенный рецептор по п. 30, где предохранительный переключатель содержит мимотоп CD20 или эпитоп QBEND-10.
32. Химерный антигенный рецептор по п. 31, где предохранительный переключатель содержит один или более мимотопов CD20, или один или более эпитопов QBEND-10, или их комбинации.
33. Химерный антигенный рецептор по любому из пп. 30-32, где химерный антигенный рецептор содержит один или более предохранительных переключателей в формате QR3, SR2, RSR или R2S.
34. Химерный антигенный рецептор по любому из пп. 30-33, где химерный антигенный рецептор содержит аминокислотную последовательность, по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную любой из SEQ ID NO: 622-628, 474-476, 565 и 684-694.
35. Выделенный полинуклеотид, кодирующий любой из химерных антигенных рецепторов по пп. 1-34.
36. Вектор экспрессии, содержащий полинуклеотид по п. 35.
37. Вектор по п. 36, где вектор представляет собой ретровирусный вектор, ДНК-вектор, плазмиду, РНК-вектор, аденовирусный вектор, аденоассоциированный вирусный вектор, лентивирусный вектор или любую их комбинацию.
38. Сконструированная иммунная Т-клетка для нацеливания на DLL3, содержащая любой из химерных антигенных рецепторов по пп. 1-34.
39. Сконструированная иммунная Т-клетка для нацеливания на DLL3, содержащая полинуклеотид по п. 35 или вектор по п. 36 или 37.
40. Сконструированная иммунная Т-клетка по п. 38 или 39, где клетка представляет собой аутологичную Т-клетку.
41. Сконструированная иммунная Т-клетка по п. 38 или 39, где клетка представляет собой аллогенную Т-клетку.
42. Фармацевтическая композиция для лечения или предупреждения состояния, связанного с нежелательными и/или повышенными уровнями DLL3, содержащая сконструированную иммунную клетку по любому из пп. 38-41 и фармацевтически приемлемое вспомогательное вещество.
43. Применение сконструированной иммунной клетки по любому из пп. 38-41 или фармацевтической композиции по п. 42 для лечения состояния, связанного с нежелательными и/или повышенными уровнями DLL3.
44. Применение по п. 43, где состояние представляет собой рак.
45. Применение по п. 43 или 44, где состояние представляет собой мелкоклеточный рак легкого.
46. Флакон для лечения или предупреждения состояния, связанного с нежелательными и/или повышенными уровнями DLL3, содержащий сконструированную иммунную клетку по любому из пп. 38-41 или фармацевтическую композицию по п. 42.
47. Связывающий агент против DLL3, содержащий:
(a) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 109, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 110, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 111, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 112, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 113, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 114;
(b) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 253, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 254, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 255, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 256, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 257, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 258;
(c) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 271, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 272, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 273, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 274, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 275, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 276;
(d) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 217, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 218, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 219, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 220, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 221, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 222;
(e) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 262, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 263, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 264, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 265, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 266, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 267;
(f) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 37, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 38, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 39, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 40, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 41, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 42;
(g) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 28, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 29 или 695, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 30, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 31, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 32, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 33;
(h) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 73, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 74, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 75, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 76 или 696, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 77, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 78;
(i) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 280, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 281, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 282, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 283, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 284, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 285;
(j) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 1, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 2, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 3, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 4, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 5, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 6;
(k) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 46, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 47, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 48, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 49, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 50, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 51;
(l) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 64, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 65, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 66, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 67, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 68, CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 69;
(m) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 172, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 173, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 174, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 175, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 176, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 177;
(n) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 19, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 20, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 21, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 22, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 23, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 24;
(o) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 127, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 128, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 129, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 130, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 131, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 132; или
(p) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 55, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 56, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 57, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 58, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 59, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 60.
48. Связывающий агент против DLL3, содержащий:
a) CDR1 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 109;
b) CDR2 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 110;
c) CDR3 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 111;
d) CDR1 вариабельной легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 112;
e) CDR2 вариабельной легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 113; и
f) CDR3 вариабельной легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 114.
49. Связывающий агент против DLL3, содержащий:
a) CDR1 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 253;
b) CDR2 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 254;
c) CDR3 вариабельной тяжелой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 255;
d) CDR1 вариабельной легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 256;
e) CDR2 вариабельной легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 257; и
f) CDR3 вариабельной легкой цепи, содержащую аминокислотную последовательность, показанную в SEQ ID NO: 258.
50. Связывающий DLL3 агент по любому из пп. 47-49, где связывающий агент представляет собой антитело или его антигенсвязывающий фрагмент, необязательно F(ab’)2-фрагмент, Fab’-фрагмент, Fab-фрагмент, Fv-фрагмент, scFv-фрагмент, dsFv-фрагмент или dAb-фрагмент.
51. Связывающий агент против DLL3, содержащий:
(a) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 109, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 110, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 111, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 112, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 113, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 114;
(b) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 253, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 254, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 255, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 256, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 257, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 258;
(c) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 271, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 272, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 273, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 274, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 275, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 276;
(d) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 217, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 218, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 219, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 220, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 221, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 222;
(e) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 262, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 263, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 264, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 265, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 266 и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 267;
(f) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 37, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 38, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 39, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 40, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 41, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 42;
(g) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 28, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 29 или 695, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 30, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 31, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 32, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 33;
(h) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 73, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 74, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 75, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 76 или 696, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 77, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 78;
(i) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 280, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 281, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 282, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 283, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 284, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 285;
(j) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 1, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 2, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 3, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 4, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 5, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 6;
(k) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 46, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 47, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 48, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 49, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 50, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 51;
(l) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 64, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 65, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 66, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 67, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 68, CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 69;
(m) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 172, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 173, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 174, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 175, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 176, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 177;
(n) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 19, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 20, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 21, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 22, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 23, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 24;
(o) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 127, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 128, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 129, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 130, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 131, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 132; или
(p) CDR1 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 55, CDR2 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 56, CDR3 вариабельной тяжелой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 57, CDR1 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 58, CDR2 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 59, и CDR3 вариабельной легкой цепи, содержащая аминокислотную последовательность, как показано в SEQ ID NO: 60,
где связывающий агент представляет собой конъюгат антитела с цитотоксическим лекарственным средством.
52. Связывающий агент против DLL3 по любому из пп. 47-50, где связывающий агент представляет собой моноклональное антитело, содержащее константную область IgG.
53. Связывающий агент против DLL3 по любому из пп. 47-52, содержащий:
(a) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 115, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 116;
(b) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 259, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 260;
(c) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 277, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 278;
(d) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 223, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 224;
(e) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 268, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 269;
(f) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 43, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 44;
(g) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 34, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 35;
(h) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 79, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 80;
(i) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 286, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 287;
(j) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 7, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 8;
(k) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 52, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 53;
(l) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 70, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 71;
(m) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 178, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 179;
(n) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 25, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 26;
(o) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 133, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 134; или
(p) последовательность вариабельной тяжелой цепи (VH), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 61, и последовательность вариабельной легкой цепи (VL), по меньшей мере приблизительно на 90%, 95%, 96%, 98%, 99% или на 100% идентичную SEQ ID NO: 62.
54. Связывающий агент против DLL3 по любому из пп. 47-53, где связывающий агент содержит последовательность, по меньшей мере приблизительно на 80%, 85%, 90%, 95%, 96%, 98%, 99% или на 100% идентичную последовательности scFv, выбранную из SEQ ID NO: 117, 261, 279, 225, 270, 45, 36, 81, 288, 9, 54, 72, 180, 27, 135 или 63.
55. Связывающий агент против DLL3 по любому из пп. 47-54, где связывающий агент представляет собой слитый белок, представляющий собой scFv-фрагмент, причем scFv-фрагмент дополнительно слит с константной Fc-областью.
56. Фармацевтическая композиция для лечения или предупреждения состояния, связанного с нежелательными и/или повышенными уровнями DLL3, содержащая связывающий агент против DLL3 по любому из пп. 47-55 и фармацевтически приемлемое вспомогательное вещество.
57. Применение связывающего агента против DLL3 по любому из пп. 47-55 или фармацевтической композиции по п. 56 для лечения состояния, связанного с нежелательными и/или повышенными уровнями DLL3.
58. Применение по п. 57, где состояние представляет собой рак.
59. Применение по п. 57 или 58, где состояние представляет собой мелкоклеточный рак легкого.
| WO 2016138038 A1, 01.09.2016 | |||
| WO 2017031458 A2, 23.02.2017 | |||
| LAURA R | |||
| SAUNDERS et al., A DLL3-targeted antibody-drug conjugate eradicates high-grade pulmonary neuroendocrine tumor-initiating cells in vivo, Science Translational Medicine, 2015, 7(302), 302ra136-302ra136 | |||
| SAI KIRAN SHARMA et al., Non-invasive Interrogation of DLL3 Expression in |
Авторы
Даты
2024-07-04—Публикация
2020-02-27—Подача