Область применения способа
Высокоэнтропийные сложные оксиды (ВСО) - однофазные оксидные системы, содержащие пять и более катионов в одной из подрешеток в эквимолярном или близком к эквимолярному соотношении, в результате чего конфигурационная энтропия таких соединений выше 1.5R (R - универсальная газовая постоянная). ВСО характеризуются высоким внутренним разупорядочением катионов по указанной подрешетке, что приводит к значительным искажениям кристаллической структуры. Образование ВСО описано для соединений со структурой каменной соли, флюорита, биксбиита, пирохлора, магнетоплюмбита, перовскита, шпинели и т.д., по химическому составу являющихся разнообразными силикатами, фосфатами, алюминатами, ферритами, ниобатами и т.д. [Sarkar A., Breitung B., Hahn H. High entropy oxides: The role of entropy, enthalpy and synergy // Scripta Materialia. 2020. V.187. P. 43-48; Xiang H., Xing Y., Dai F., Wang H., Su L., Miao L., Zhang G., Wang Y., Qi X., Yao L., Wang H., Zhao B., Li J., Zhou Y.. High-entropy ceramics: Present status, challenges, and a look forward // Journal of Advanced Ceramics. 2021, 10(3): 385-441].
В последние годы высокоэнтропийные керамические оксидные материалы вызывают значительный научный и практический интерес, т.к. высокая энтропия обеспечивает данному классу керамики термодинамическую стабильность, результируя высокую температуру плавления, термическую устойчивость, высокую вязкость разрушения, а также уникальные физико-химические характеристики. ВСО со структурой граната проявляют уникальные магнитные характеристики [D. Chen, Y. Yang, C.Chen, Y.Meng, Y. Zhang, C. Zhang Structure and magnetism of novel high-entropy rare-earth iron garnet ceramics // Ceramics International 49 (2023) 9862-9867 doi:10.1016/j.ceramint.2022.11.161].
Изобретение относится к способам получения однофазного высокоэнтропийного граната многокомпонентного состава (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12, где Ln1, Ln2, Ln3 Ln4, Ln5 - различные элементы из группы редкоземельных металлов (Y, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu) с возможностью получения нужных магнитных и диэлектрических свойств с последующим применением в радиочастотных, СВЧ и магнитных устройствах. Однофазность получаемого порошка определяет точность и воспроизводимость во времени функциональных характеристик заявленного материала и определяет стабильность работы указанных устройств.
Уровень техники
Аналог 1. Известен способ получения высокоэнтропийных гранатов состава (Gd0,2Dy0,2Y0,2Eu0,2M0,2)Fe5O12, где M - Sm, Tm или Yb [A type of magnetic high-entropy ceramics and a method for its production: пат.CN116605914A, 18.08.2023]. Способ получения заключается в следующем: берут оксиды исходных элементов в эквимолярном соотношении ионов металлов, смесь порошков помещают в камеру помола шаровой мельницы (диспергирующая жидкость - вода, 4-6 ч, 250 об/мин). В результате получают суспензию, которую помещают в печь для сушки и первичного отжига при температуре 1150°C (10 ч, скорость нагрева 3.5-4°C/мин). Полученный после первичного отжига порошок перетирают в ступке, затем осуществляют конечный отжиг на 1350°C на 10 ч. Продукт аттестуют методом рентгенофазового анализа и сканирующей электронной микроскопии и в результате получают высокоэнтропийный железоредкоземельный гранат. В качестве недостатков можно отметить использование дорогостоящего оборудования (шаровые мельницы) и высокие температуры первичного и конечного отжига, большое суммарное время синтеза (не менее 25 ч).
Аналог 2. Известен способ получения высокоэнтропийного граната с общей формулой (RexCeyEuyBizY3-x-2y-z) Fe5O12, где x, y, z>0, x+2y+z=1; Re=La, Yb, Tm, Er, Ho, Dy, Gd, Sm, Nd, Lu [High-entropy YIG-ferrite with high saturation magnetization and method of its preparation: пат.CN116514536A, 26.05.23]. Для синтеза стехиометрические количества порошков исходных оксидов соответствующих элементов помещают в камеру помола шаровой мельницы (диспергирующая жидкость - вода, время помола 20-24 ч, 250 об/мин, стальные мелющие тела). В результате получают суспензию, которую сушат в сушилке при температуре 135-165°C в течение 6-10 ч. Полученный в результате сушки порошок отжигают при температуре 950-1150°C в течение 2-4 ч. После отжига порошок опять подвергают измельчению в шаровых мельницах при тех же условиях в течение 24 ч, полученную после измельчения суспензию сушат при температуре 135-165°C в течение 6-10 ч. Полученный порошок прессуют в пеллет (давление 100-150 МПа, 5% водный раствор поливинилового спирта в качестве связки массой 10-15% от массы порошка). Спрессованный пеллет подвергают спеканию в муфельной печи по сложной программе отжига с максимальными температурами 1250-1400°C, например: нагрев от комнатной температуры до 120°C в течение 1 ч, нагрев до 330°C в течение 10 ч, нагрев до 1200°C в течение 10 ч, нагрев до 1250°C в течение 1 ч, удержание при 1250°C 2 ч, охлаждение до 1200°C в течение 1 ч, удержание при 1200°C 2 ч, охлаждение печи после достижения температуры 1100°C в течение 1 ч. Полученный продукт методом рентгенофазового анализа характеризуется как однофазный продукт со структурой граната. Недостатками данного метода синтеза можно отметить использования дорогостоящего оборудования (шаровые мельницы и прессы высокого давления), длительный высокотемпературный отжиги (суммарное время отжигов не менее 25 ч), большое суммарное время синтеза (не менее 90 ч).
Аналог 3. Известен способ получения высокоэнтропийного граната с формулой Li6,2La3(Zr0,2Hf0,2Ti0,2Nb0,2Ta0,2)2O12 [High-entropy garnet solid electrolyte ceramic and a method for its production: пат.CN116178012A, 30.05.23]. Способ получения заключается в следующем: стехиометрические количества порошков исходных оксидов или карбонатов соответствующих элементов помещают в камеру помола шаровой мельницы, при использовании карбоната лития берут 10% избыток вещества (покрытие камеры - тефлон, диспергирующая жидкость - изопропанол или этанол, время помола 12 ч, 400-500 об/мин, мелющие тела из диоксида циркония, помол в импульсном режиме - 5 мин релаксации на 30 мин помола). В результате получают суспензию, которую сушат в сушилке при температуре 80°C в течение 6 ч для получения прекурсора высокоэнтропийного граната. После сушки порошок отжигают в муфельной печи по программе при 750-900°C в течение 5-12 ч. Полученный порошок прессуют в пеллет (изостатическое холодное прессование, давление 4-8 МПа, 4% спиртовой раствор поливинилбутираля в качестве связки массой 2% от массы порошка). Спрессованный пеллет подвергают спеканию в муфельной печи с максимальными температурами 1200-1250°C, в течение 0.5-5 ч в магнезитовых тиглях с обязательной подложкой из слоя порошка этого же состава. Полученный продукт аттестовали методом рентгенофазового анализа и сканирующей электронной микроскопии как однофазный продукт со структурой граната. Недостатками данного метода синтеза можно отметить использование дорогостоящего оборудования (шаровые мельницы с камерой помола с тефлоновым покрытием и мелющими телами из диоксида циркония).
Аналог 4. Известен способ получения высокоэнтропийного граната состава (Y0,2Dy0,2Ho0,2Er0,2Yb0,2)3Al5O12 и (Y0,2Gd0,2Ho0,2Er0,2Yb0,2)3Al5O12 [Thermal photovoltaic rare earth high-entropy aluminate ceramic selective emitter and preparation method and a method for its production: пат.CN114573346A, 03.06.23]. Способ синтеза следующий: берут оксиды соответствующих элементов в стехиометрическом соотношении, помещают в камеру помола шаровой мельницы (покрытие камеры-тефлон, диспергирующая жидкость - этанол, суммарное время помола 5-10 ч, 360-500 об/мин, мелющие тела из диоксида циркония, работа в импульсном режиме - 1 мин релаксации на 4 мин помола). Полученную суспензию сушат в сушилке при 80°C в течение 12 ч. После сушки порошок просеивают через стандартное сито (200 меш), после чего прессуют в пеллеты под давлением в 10 МПа. Спрессованный пеллет подвергают отжигу в муфельной печи при температуре 1600-1650°C, в течение 2 ч (скорость нагрева 5°C/мин). Полученный высокоэнтропийный гранат однофазный: на полученной дифрактограмме нет примесных фаз. Недостатками данного метода синтеза являются использование дорогостоящего оборудования (шаровые мельницы с камерой помола с тефлоновым покрытием и мелющими телами из диоксида циркония, высокотемпературные печи), а также высокие температуры отжига, увеличивающие энергоемкость процесса.
Аналог 5. Известен способ синтеза гранатов с формулой (Gd0,2Dy0,2Er0,2Y0,2Re0,2)3Fe5O12(RE=Sm, Eu, Tm, Yb) [D. Chen, Y. Yang, C.Chen, Y.Meng, Y. Zhang, C. Zhang Structure and magnetism of novel high-entropy rare-earth iron garnet ceramics // Ceramics International 49 (2023) 9862-9867 doi:10.1016/j.ceramint.2022.11.161]. Для синтеза стехиометрические количества порошков исходных оксидов соответствующих элементов помещают в камеру помола планетарной мельницы (диспергирующая жидкость - вода, время помола 6 ч, частота оборотов, материал мелющих тел и размолочных стаканов не указан). Полученную суспензию сушат и отжигают в муфельной печи при 1150°C в течение 11 ч. Полученный в результате отжига порошок спекают в муфельной печи при конечной температуре 1350°C в течение 11 ч с последующим медленным охлаждением до комнатной температуры. Полученный продукт аттестуют методом рентгенофазового анализа и сканирующей электронной микроскопии как однофазный продукт со структурой граната. К недостаткам данного способа можно отнести использование дорогостоящего оборудования - планетарных мельниц.
Аналог 6 (прототип). Описан способ синтеза высокоэнтропийного железоредкоземельного граната состава (Dy0,2Er0,2Gd0,2Ho0,2Y0,2)3Fe5O12 и (Dy0,2Gd0,2Ho0,2Sm0,2Y0,2)3Fe5O12 по модифицированному методу Печини [Dabrova J., Cieslak J., Zajusz M., Mozdzierz M., Berent K., Mikuła A., Stępien A., Swierczek K. Structure and transport properties of the novel (Dy,Er,Gd,Ho,Y)3Fe5O12 and (Dy,Gd,Ho,Sm,Y)3Fe5O12 high entropy garnets // Journal of the European Ceramic Society, 2021, 41, 3844]. Для получения гранатов взвешивали азотнокислые соли соответствующих элементов в стехиометрическом количестве, лимонную кислоту и этиленгликоль в соотношении 1:2:4 по отношению ко всем катионам, т.е на 1 моль продукта брали 16 моль лимонной кислоты и 32 моля этиленгликоля. Смесь растворенных нитратов при постоянном перемешивании вносили в разогретую смесь лимонной кислоты и этиленгликоля (температура нагревателя 150°C, этерификационная стадия), а затем повышали температуру нагревателя до 300°C для начала поликонденсационной стадии и получения гелеобразного полупродукта. Гелеобразный продукт подвергали отжигу при 700°C в течение 6 часов в муфельной печи с последующим медленным охлаждением до комнатной температуры. Методом рентгенофазового анализа было установлено, что полученный порошок содержал желаемую фазу граната с примесями оксида железа Fe2O3. После первого отжига порошок прессовали в пеллет (сухое прессование, усилие 1-2 т), который спекали при температуре 1300°C в течение 36 часов с последующим медленным охлаждением до комнатной температуры. Продукт аттестовали методом рентгенофазового анализа и сканирующей электронной микроскопии; в результате был получен высокоэнтропийный железоредкоземельный гранат. В качестве недостатков данного метода можно отметить большое суммарное время синтеза (не менее 42 часа отжига); использование азотнокислых солей соответствующих элементов, что означает относительную дороговизну по сравнению с использованием оксидов соответствующих элементов, а также отсутствие стадии аттестации реального состава азотнокислых солей, являющихся кристаллогидратами.
Техническая задача заключается в создании способа получения однофазного высокоэнтропийного железоредкоземельного граната состава (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12, где Ln1, Ln2, Ln3 Ln4, Ln5 - различные элементы из группы редкоземельных металлов (Y, Eu, Gd, Dy, Ho, Er, Tb), с целью расширения арсенала средств, лишенного недостатков аналогов, а именно с использованием только доступного лабораторного оборудования, посуды и реактивов, без использования дорогостоящего оборудования, как шаровые или планетарные мельницы, снижение температуры конечного синтеза (до 1200°C), а также сокращение материалоемкости за счет использования только одного органического восстановителя - аминоуксусной кислоты.
Технический результат поставленной задачи достигается в предлагаемом способе получения высокоэнтропийного железоредкоземельного граната, заключающемся в глицин-нитратном синтезе граната и двухстадийной термической обработке.
Частицы порошка граната приготавливали с использованием прекурсора из оксидов редкоземельных элементов, растворимых в азотной кислоте, а также кристаллогидрата азотнокислого железа (III). Содержание основного вещества по металлическим примесям составило не менее 99.9% для всех реактивов. Фактическое содержание воды (n) в кристаллогидрате азотнокислого железа (III) Fe(NO3)3×nH2O, предварительно определяли гравиметрически, путем термического разложения известного количества указанной соли до оксида Fe2O3 (отжиг при 800°C в течение 5 часов в воздушной атмосфере). Число n рассчитывали по формуле (1):
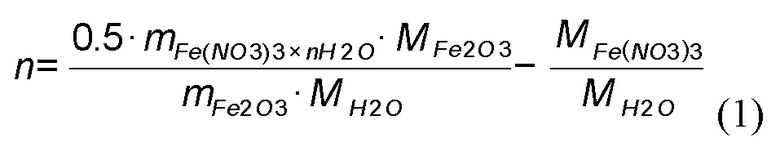
где M - молярные массы соответствующих соединений,
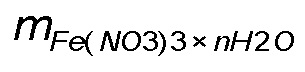 - масса вещества до термического разложения,
- масса вещества до термического разложения,
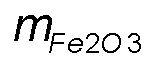 - масса вещества после термического разложения. Анализ проводили не менее чем в пяти параллелях, полученное значение n усредняли и учитывали в расчете с точностью до тысячных долей после запятой.
- масса вещества после термического разложения. Анализ проводили не менее чем в пяти параллелях, полученное значение n усредняли и учитывали в расчете с точностью до тысячных долей после запятой.
Взятие навесок стехиометрических количеств всех исходных веществ осуществляли на аналитических весах, затем оксиды редкоземельных элементов растворяли в стехиометрическом количестве азотной кислоты концентрацией 3-3.5М, при необходимости добавляя H2O2 (по каплям), азотнокислое железо растворяли в воде. Далее полученные растворы нитратов редкоземельных элементов и железа помещали в один сосуд и проводили обработку смеси погружным лабораторным ультразвуковым гомогенизатором (мощностью не менее 700 Вт) в течение 0.5 часа с использованием проточной охлаждающей водяной бани, обеспечивающей температуру смеси не более 30°С с целью получения полупродукта с равномерным распределением элементов. После ультразвуковой обработки реакционную смесь переносили в широкий термостойкий (фарфоровый или кварцевый) реакционный сосуд и добавляли аминоуксусную кислоту (глицин) с целью получения нитрат-органического прекурсора. Аминоуксусную кислоту брали в стехиометрическом количестве из расчета на полное восстановление нитрат-ионов в реакционной смеси до газообразного азота, согласно уравнению реакции (2), а именно брали 1.32 г аминоуксусной кислоты на 1 г расчетного количества продукта реакции - высокоэнтропийного железоредкоземельного граната.
1.8Ln1(NO3)3+1.8Ln2(NO3)3+1.8Ln3(NO3)3+1.8Ln4(NO3)3+1.8Ln5(NO3)3+15Fe(NO3)3+40C2H5NO2=3(Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12+100H2O+80CO2↑+56N2↑(2)
Затем полученный нитрат-органический прекурсор упаривали при интенсивном кипении (не более двух часов), вплоть до начала самопроизвольного пиролиза реакционной смеси. В результате пиролиза образовался ультрадисперсный порошок, являющийся полупродуктом. Данный полупродукт помещали в тигель для дальнейшей двухстадийной термической обработки: на воздухе при 750°C (отжиг) в течение 8 часов с последующим перемешиванием в ступке, а затем на воздухе при 1200°C (спекание) в течение 20 часов. Скорость нагрева образцов при термической обработке составляла 8°С/мин. Согласно результатам рентгенофазового анализа и сканирующей электронной микроскопии с энергодисперсионной приставкой, полученный продукт представляет собой однофазный высокоэнтропийный гранат многокомпонентного состава (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12, размер частиц около 2 мкм, форма частиц округлая, стержнеобразная.
Эффект (свойство), которое проявляется при осуществлении способа
Методы пиролиза нитрат-органических прекурсоров основаны на термообработке смесей необходимых исходных компонентов и органического восстановителя, в качестве которого используют аминоуксусную кислоту C2H5NO2. Эта кислота выступает в роли бидентантного лиганда, способного образовывать устойчивые комплексы, что повышает растворимость нитратов и предотвращает выпадение осадков при испарении воды. С другой стороны, аминоуксусная кислота в процессе пиролиза формирует пламя с наивысшей (по сравнению иными органическими восстановителями) температурой (до 1500°С), что способствует снижению конечной температуры синтеза. Большое количество газов, выделяющихся во время реакции пиролиза, приводит к диспергированию твердого продукта, и, соответственно, к равномерному распределению лантаноидов и железа по всему объему и увеличению реакционной площади частиц полупродукта. Поэтому получение порошкообразного материала после стадии пиролиза позволяет сократить количество стадий термической обработки, измельчения и перемешивания, понизить температуру конечного отжига, и использовать только доступное, типовое лабораторное оборудование, посуду и реактивы без использования дополнительных установок (шаровых или планетарных лабораторных мельниц).
Новизна предлагаемого способа
В сравнении с указанным прототипом авторы настоящей заявки использовали оксиды редкоземельных элементов вместо нитратов редкоземельных элементов. Ультразвуковая обработка реакционной смеси железа и редкоземельных элементов позволяла быстро и эффективно гомогенизировать ее и получить впоследствии полупродукт со статистическим распределением элементов. Авторы заявки использовали один органический восстановитель - аминоуксусную кислоту. За счет этого был получен более удобный для дальнейшей работы полупродукт - ультрадисперсный порошок вместо геля. Благодаря этому отпадает необходимость дополнительного прессования полупродукта после предварительного отжига, снижается температура и время конечного спекания полупродукта. В предлагаемом способе удается получить более чистый продукт со сравнительно меньшими трудовыми и временными затратами, чем в прототипе. Первая стадия термической обработки - отжиг при 750°С необходим в предлагаемом способе для полного удаления остатков органических веществ и формирования промежуточных фаз (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12, (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)FeO3 и Fe2O3. Последующая стадия термической обработки - спекание при 1200°С приводит к образованию однофазного продукта - высокоэнтропийного железоредкоземельного граната состава (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12. Основной особенностью предлагаемого метода является использование оптимального количества аминоуксусной кислоты и оптимальных режимов температурной обработки, за счет чего получают диспергированный твердый продукт, в котором редкоземельные элементы и железо равномерно распределены по всему объему, а природа восстановителя и размер зерен полупродукта, который обеспечивает большую реакционную площадь частиц, приводят к минимизации количества стадий термической обработки - его снижение до двух. Кроме того, предполагаемый метод позволяет уменьшить стоимость синтеза за счет использования оксидов редкоземельных элементов вместо более дорогостоящих нитратов редкоземельных элементов, использовать доступное лабораторное оборудование, посуду и реактивы, сократить энергоемкость за счет снижения температуры спекания до 1200°С, сократить материалоемкость за счет использования только одного органического восстановителя, а также уменьшить общие трудозатраты химика-синтетика. Предлагаемый метод позволяет получить однофазный гранат многокомпонентного состава (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12, проявляющий регулярные, воспроизводимые физико-химические и функциональные характеристики.
Общие технические характеристики способа
Осуществление заявляемого способа получения однофазного высокоэнтропийного железоредкоземельного граната многокомпонентного состава (Ln10,2Ln20,2Ln30,2Ln40,2Ln50,2)3Fe5O12 при помощи глицин-нитратного пиролиза не превышает 31 часа: 3 часа занимает получение ультрадисперсного порошка (полупродукта), в том числе ультразвуковая обработка в течение 0.5 часа, 8 часов занимает первая стадия термической обработки (отжиг) при 750°С, вторая стадия (спекание) при температуре 1200°С длится 20 часов, включая процессы нагрева и охлаждения, после чего, по данным рентгенофазового анализа, формируется однофазный железоредкоземельный гранат состава (Ln10.2Ln20.2Ln30.2Ln40.2Ln50.2)3Fe5O12. Расход сырья осуществлялся в соответствии с необходимым молярным соотношением реактивов оксидов редкоземельных элементов и азотнокислого железа n-водного (III) Fe(NO3)3 ×nH2O. По данным рентгеновской дифракции чистота продукта составляет 100%.
Общая характеристика продукции, полученной заявляемым способом
Образцы, изготовленные по заявляемому способу, приобретают кристаллическую структуру высокоэнтропийного железоредкоземельного граната многокомпонентного состава (Ln10.2Ln20.2Ln30.2Ln40.2Ln50.2)3Fe5O12. Примесных фаз не обнаружено.
Примеры осуществления способа
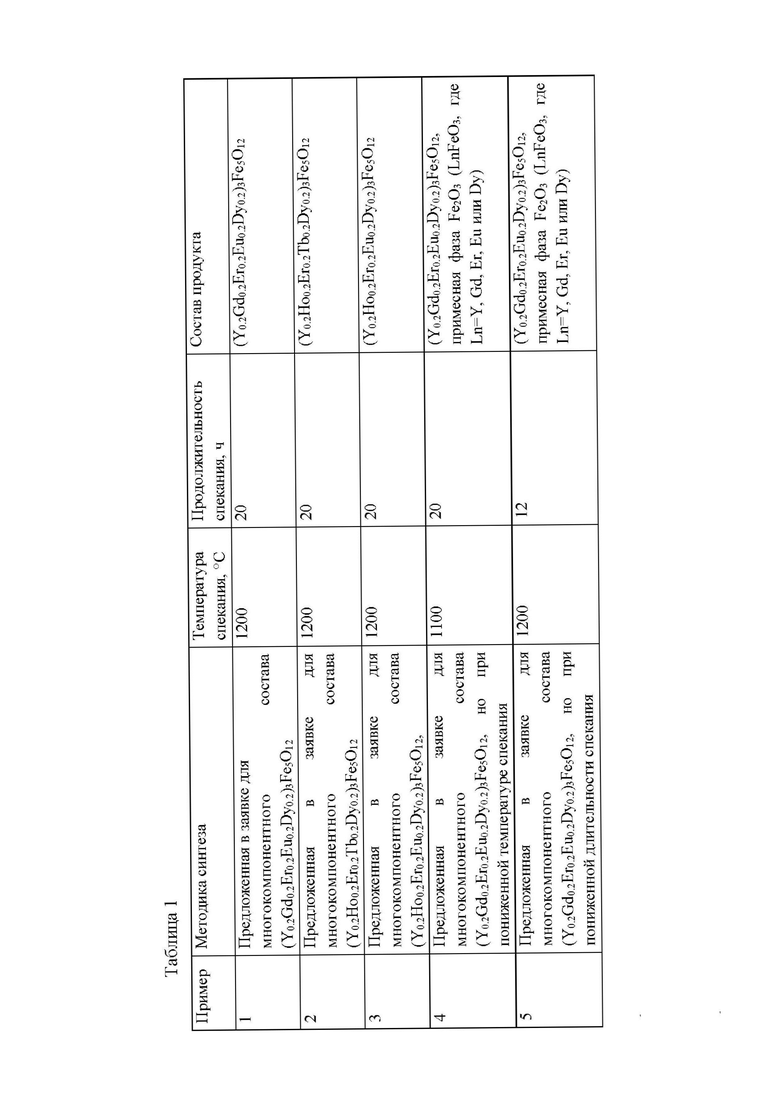
Осуществления способа синтеза высокоэнтропийного железоредкоземельного граната состава (Ln10.2Ln20.2Ln30.2Ln40.2Ln50.2)3Fe5O12 рассмотрены на нескольких примерах, основанных на изменении условий различных этапов синтеза (таблица 1).
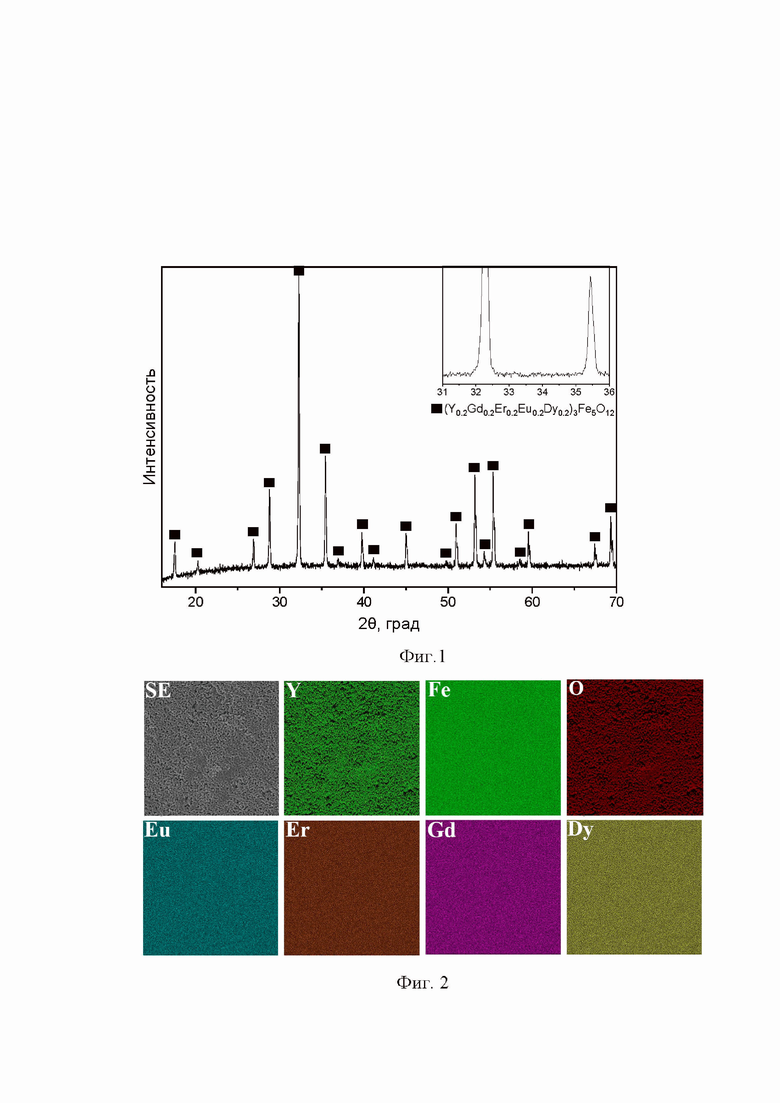
Пример 1: Синтез проводили по способу, описанному в заявке. В качестве исходных оксидов элементов брали оксиды иттрия, гадолиния, эрбия, европия, диспрозия. После отжига при 750°C в течение 8 часов с последующим перетиранием в ступке и спеканием при 1200°C в течение 20 часов образовался однофазный высокоэнтропийный железоредкоземельный гранат многокомпонентного состава (Y0.2Gd0.2Er0.2Eu0.2Dy0.2)3Fe5O12; размер частиц около 2 мкм; форма частиц округлая, стержнеобразная; частицы образуют агломераты (фиг. 1 и 2).
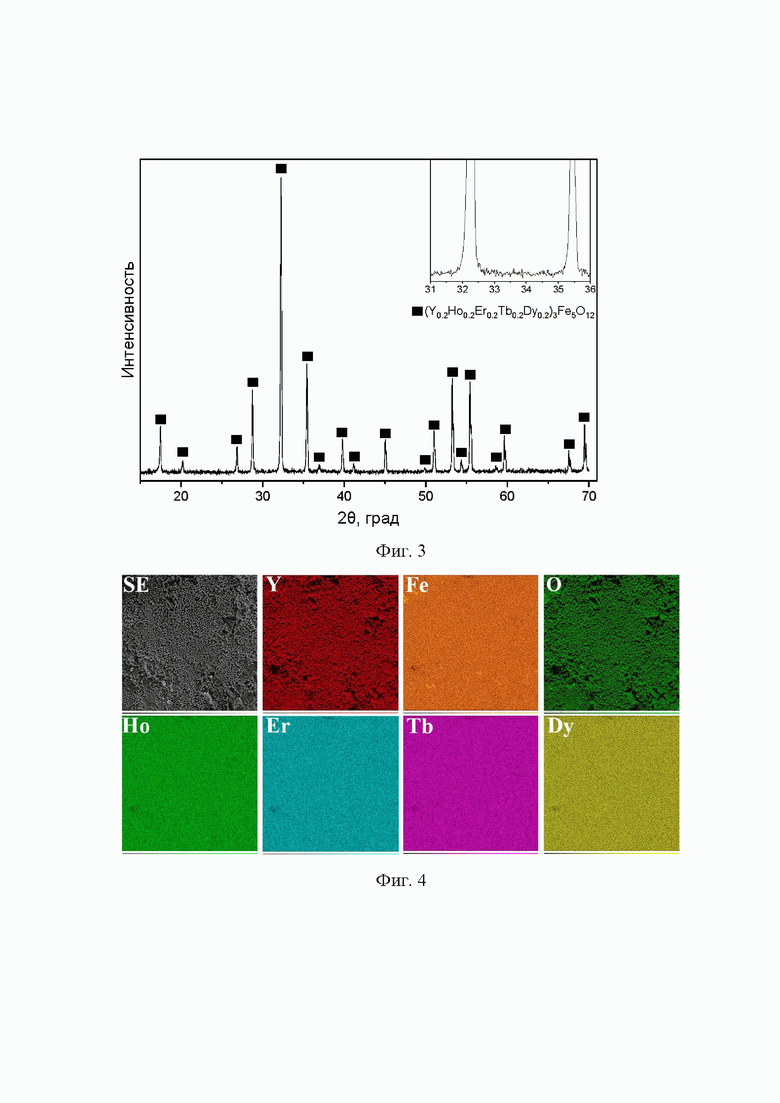
Пример 2: Синтез проводили по способу, описанному в заявке. В качестве исходных оксидов элементов брали оксиды иттрия, гольмия, эрбия, тербия, диспрозия. После отжига при 750°C в течение 8 часов с последующим перетиранием в ступке и спеканием при 1200°C в течение 20 часов образовался однофазный высокоэнтропийный железоредкоземельный гранат многокомпонентного состава (Y0.2Ho0.2Er0.2Tb0.2Dy0.2)3Fe5O12.
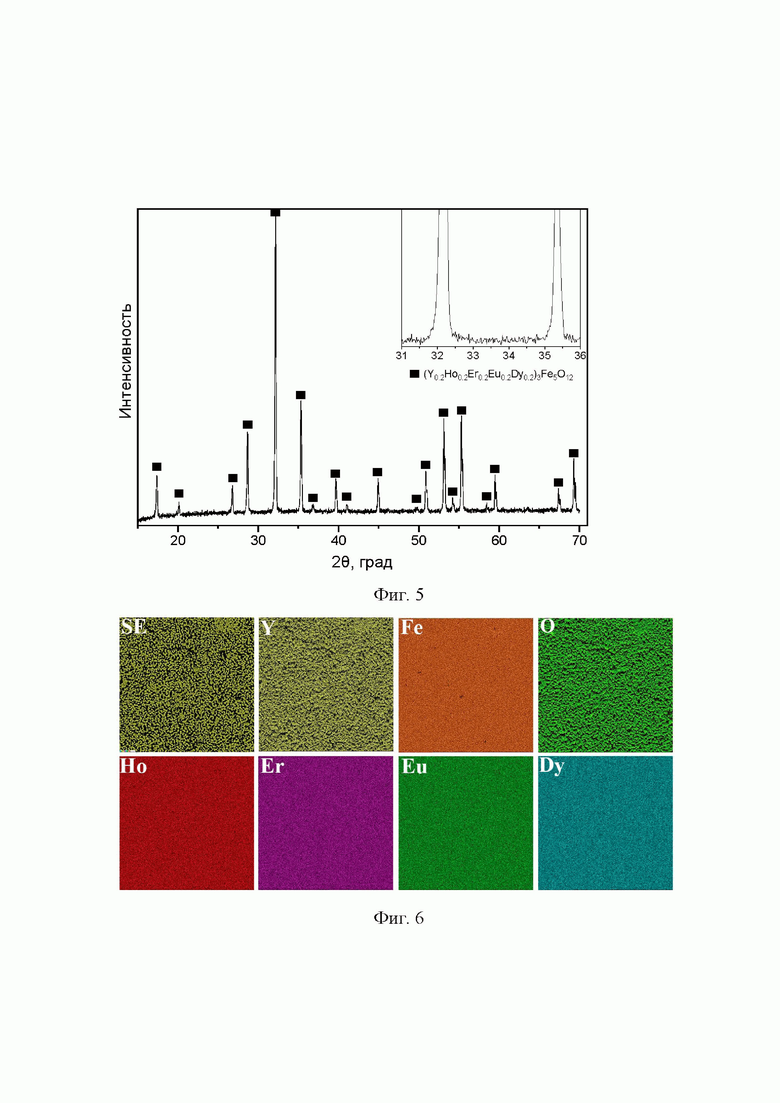
Пример 3: Синтез проводили по способу, описанному в заявке. В качестве исходных оксидов элементов брали оксиды иттрия, гольмия, эрбия, тербия, диспрозия. После отжига при 750°C в течение 8 часов с последующим перетиранием в ступке и спеканием при 1200°C в течение 20 часов образовался однофазный высокоэнтропийный железоредкоземельный гранат многокомпонентного состава (Y0.2Ho0.2Er0.2Eu0.2Dy0.2)3Fe5O12.
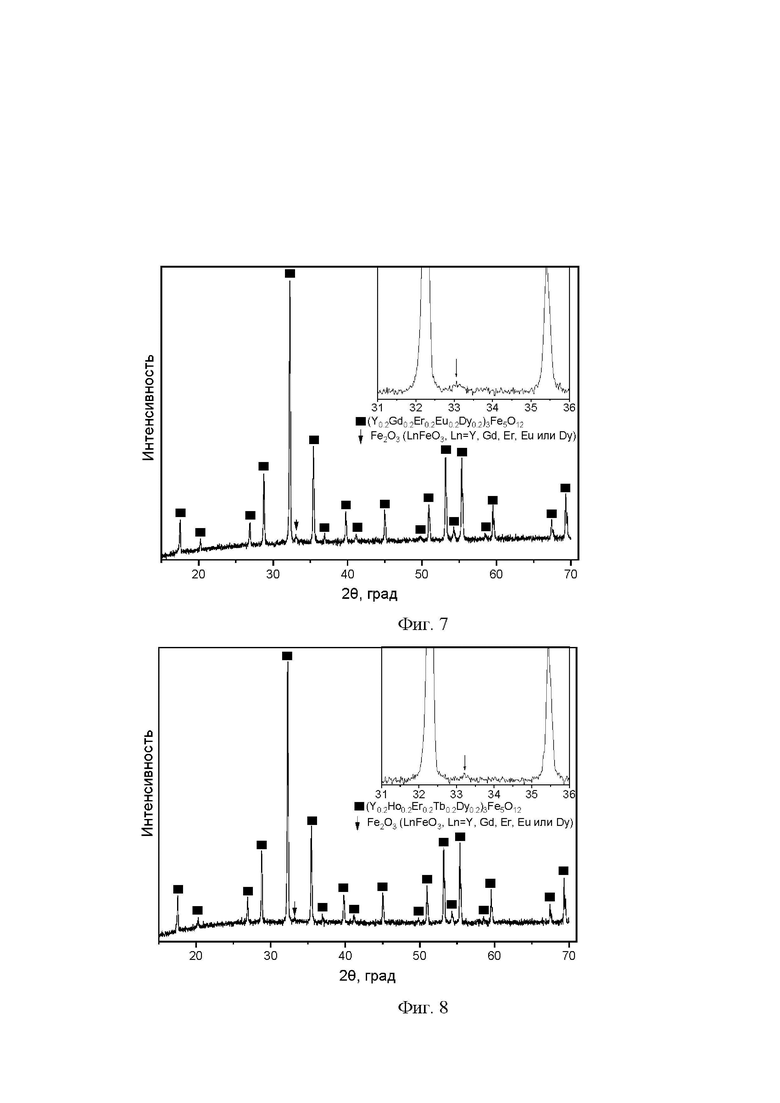
Пример 4: Синтез проводили по способу, описанному в заявке, однако была изменена температура спекания: она была снижена до 1100°C, при этом продолжительность спекания составляла 20 часов. В качестве исходных оксидов элементов брали оксиды иттрия, гадолиния, эрбия, европия, диспрозия. После отжига при 750°C в течение 8 часов с последующим перетиранием в ступке и спеканием при 1100°C в течение 20 часов образовался высокоэнтропийный железоредкоземельный гранат многокомпонентного состава (Y0.2Ho0.2Er0.2Eu0.2Dy0,2)3Fe5O12, присутствует примесная фаза оксида железа (возможно фаза ортоферрита соответствующего редкоземельного элемента).
Пример 5: Синтез проводили по способу, описанному в заявке, однако продолжительность спекания была понижена до 12 ч, его температура была 1200°C. В качестве исходных оксидов элементов брали оксиды иттрия, гадолиния, эрбия, европия, диспрозия. После отжига при 750°C в течение 8 часов с последующим перетиранием в ступке и спеканием при 1200°C в течение 12 часов образовался высокоэнтропийный железоредкоземельный гранат многокомпонентного состава (Y0,2Ho0,2Er0,2LnEu0,2Dy0,2)3Fe5O12, присутствует примесная фаза оксида железа (возможно фаза ортоферрита соответсвующего элемента).
Чертежи, поясняющие материалы, и их описание
Таблица 1. Описание особенностей синтеза железоредкоземельного граната по примерам (см. в графич. части).
Фиг. 1. Дифрактограмма продукта, полученного в рамках примера 1. Фиксируется только фаза граната состава (Y0.2Gd0.2Er0.2Eu0.2Dy0.2)3Fe5O12. Здесь и на фигурах 7, 8 черные квадраты - рефлексы (Y0.2Gd0.2Er0.2Eu0.2Dy0.2)3Fe5O12. Здесь и на фигурах 3, 5, 7, 8 на врезке - увеличенный в 3 раза по оси интенсивности фрагмент дифрактограммы в диапазоне 2θ=31-36°; порошковый дифрактометр XRD-7000, излучение Cu Ka.
Фиг. 2. Данные СЭМ - SE-изображения и карты распределения интенсивностей элементов продукта, полученного в рамках примера 1. Элементы равномерно распределены по поверхности образца. Здесь и на фигурах 2, 4, 6 размер карт 100×100 мкм, зерна преимущественно округлые, стержнеобразные, размером до 2 мкм; сканирующий электронный микроскоп JSM 6390LV с энергодисперсионной приставкой.
Фиг. 3. Дифрактограмма продукта, полученного в рамках примера 2. Фиксируется только фаза граната состава (Y0.2Ho0.2Er0.2Tb0.2Dy0,2)3Fe5O12. Черные квадраты - рефлексы (Y0.2Ho0.2Er0.2Tb0.2Dy0,2)3Fe5O12.
Фиг. 4. Данные СЭМ - SE-изображения и карты распределения интенсивностей элементов продукта, полученного в рамках примера 2. Все элементы распределены равномерно по поверхности образца
Фиг. 5. Дифрактограмма продукта, полученного в рамках примера 3. Фиксируется только фаза граната состава (Y0.2Ho0.2Er0.2Eu0.2Dy0,2)3Fe5O12. Черные квадраты - рефлексы (Y0.2Ho0.2Er0.2Eu0.2Dy0,2)3Fe5O12.
Фиг. 6. Данные СЭМ - SE-изображения и карты распределения интенсивностей элементов продукта, полученного в рамках примера 3. Практически все элементы равномерно распределены по поверхности образец, для Fe наблюдаются небольшие области изменения содержаний.
Фиг. 7. Дифрактограмма продукта, полученного в рамках примера 4. Фиксируются фазы граната состава (Y0.2Gd0.2Er0.2Eu0.2Dy0.2)3Fe5O12 и примесной фазы. Здесь и на фигуре 8 черная стрелка - рефлекс примесной фазы оксида железа Fe2O3 (возможно LnFeO3, где Ln=Y, Gd, Er, Eu или Dy).
Фиг. 8. Дифрактограмма продукта, полученного в рамках примера 5. Наряду с фазой граната состава (Y0.2Gd0.2Er0.2Eu0.2Dy0.2)3Fe5O12 фиксируется и примесная фаза.
Результаты получены в ЦКП «Геоаналитик» ИГГ УрО РАН в рамках проекта РНФ №24-17-00055, госзадания №123011800012-9, дооснащение ЦКП поддержано Минобрнауки РФ, соглашение №075-15-2021-680.
Литература
1. A type of magnetic high-entropy ceramics and a method for its production: patent №116605914A CN IPC C01G49/00 / Yang Y., Chen D., Chen C., Zhang Y., Meng Y.; applicant Anhui University. - № CN116605914A; application 11.05.2023; publication 18.08.2023. (https://worldwide.espacenet.com/patent/search/family/087679203/publication/CN116605914A?q=pn%3DCN116605914A)
2. High-entropy YIG-ferrite with high saturation magnetization and method of its preparation: patent №116514536 CN IPC C04B35/40, C04B35/622, H01F1/01 / Yang K., Miao Y., Zhang P., Yang Z., Yu X., Jia D.; applicant Jingdezhen Advanced Ceramics Research Co., Ltd. - №CN116514536A; application 26.05.2023; publication 01.08.2023 (https://worldwide.espacenet.com/patent/search/family/087401127/publication/CN116514536A?q=pn%3DCN116514536A)
3. High-entropy garnet solid electrolyte ceramic as well as preparation method and application thereof: patent №116178012 CN IPC C04B35/495, C04B35/50, C04B35/622, H01M10/0525, H01M10/0562 / Wang Y.; Han S.; Wang Y.; Wang X.; applicant UNIV TAIYUAN TECHNOLOGY. - № CN116178012A; application 02.03.2023; publication 30.05.2023. (https://worldwide.espacenet.com/patent/search/family/086446079/publication/CN116178012A?q=pn%3DCN116178012A)
4. Thermal photovoltaic rare earth high-entropy aluminate ceramic selective emitter and preparation method and application thereof: patent №114573346 CN IPC C04B35/44, C04B35/50, C04B35/622 / Li Z.; Yang F.; Chen H.; Xue L.; Wu J.; applicant XIAMEN RARE EARTH MATERIAL RES INSTITUTE. - № CN114573346A; application 08.04.2023; publication 03.06.2023. (https://worldwide.espacenet.com/patent/search/family/081783682/publication/CN114573346A?q=pn%3DCN114573346A)
5. Chen D., Yang Y., Chen C., Meng Y., Zhang Y., Zhang C. Structure and magnetism of novel high-entropy rare-earth iron garnet ceramics // Ceramic International, 2023, 49, 9862.
6. Dabrova J., Cieslak J., Zajusz M., Mozdzierz M., Berent K., Mikuła A., Stępien A., Swierczek K. Structure and transport properties of the novel (Dy, Er, Gd, Ho, Y)3Fe5O12 and (Dy, Gd, Ho, Sm, Y)3Fe5O12 high entropy garnets // Journal of the European Ceramic Society, 2021, 41, 3844.
7. Size-Dependent Structural, Magnetic and Magnetothermal Properties of Y3Fe5O12 Fine Particles Obtained by SCS // Nanomaterials, 2022, 12, 2733.
8. Xiang H., Xing Y., Dai F., Wang H., Su L., Miao L., Zhang G., Wang Y., Qi X., Yao L., Wang H., Zhao B., Li J., Zhou Y.. High-entropy ceramics: Present status, challenges, and a look forward // Journal of Advanced Ceramics. 2021, 10(3): 385-441.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения однофазного железоиттриевого граната YFeO | 2023 |
|
RU2819764C1 |
| Способ получения однофазного циркона | 2023 |
|
RU2819814C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЭНТРОПИЙНОГО КАРБИДА TiNbZrHfTaC | 2022 |
|
RU2806562C1 |
| Способ получения керамического материала на основе оксидов висмута-цинка-ниобия | 2023 |
|
RU2804938C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАТРИЙ - ИТТРИЕВЫХ СИЛИКАТОВ, ДОПИРОВАННЫХ РЕДКОЗЕМЕЛЬНЫМИ ЭЛЕМЕНТАМИ | 2023 |
|
RU2807989C1 |
| СОСТАВ И СПОСОБ СИНТЕЗА СЦИНТИЛЛЯЦИОННОЙ КЕРАМИКИ НА ОСНОВЕ НАНОПОРОШКА | 2020 |
|
RU2748274C1 |
| Способ синтеза наноразмерного порошкообразного материала на основе скандата лантана | 2017 |
|
RU2651009C1 |
| СПОСОБ ТВЁРДОФАЗНОГО СИНТЕЗА ЛЮМИНОФОРОВ БЕЛОГО СВЕЧЕНИЯ НА ОСНОВЕ РЕДКОЗЕМЕЛЬНЫХ ГРАНАТОВ | 2015 |
|
RU2582699C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДВОЙНОГО СИЛИКАТА NaYSiO | 2023 |
|
RU2819643C1 |
| Способ получения циркона | 2021 |
|
RU2776575C1 |
Изобретение относится к химической промышленности и может быть использовано при изготовлении радиочастотных, СВЧ и магнитных устройств. Для получения граната состава (Ln10,2Ln20.2Ln30,2Ln40,2Ln50,2)3Fe5O12, где Ln1, Ln2, Ln3 Ln4, Ln5 являются различными и выбраны из группы редкоземельных металлов, включающей Y, Eu, Gd, Dy, Но, Er и Tb, готовят реакционную смесь, содержащую оксиды указанных редкоземельных металлов, растворённые в азотной кислоте, и железосодержащее соединение - азотнокислое железо (III) n-водное, количество кристаллизационной воды в котором определяют гравиметрическим анализом. Полученную реакционную смесь гомогенизируют ультразвуковой обработкой при мощности не менее 700 Вт в течение 0,5 ч при поддержании температуры смеси не более 30°С. Затем получают нитрат-органический прекурсор, для чего в смесь вводят аминоуксусную кислоту в качестве органического восстановителя, необходимого для пиролиза указанного прекурсора. Полупродукт, полученный в результате пиролиза прекурсора, сначала отжигают при температуре 750°С в течение 8 ч и затем спекают при температуре 1200°С в течение 20 ч. При осуществлении способа по изобретению используют только доступное лабораторное оборудование, посуду и реактивы, снижается температура, сокращается материалоёмкость за счёт использования только одного органического восстановителя. Полученный продукт является однофазным. 8 ил., 1 табл., 5 пр.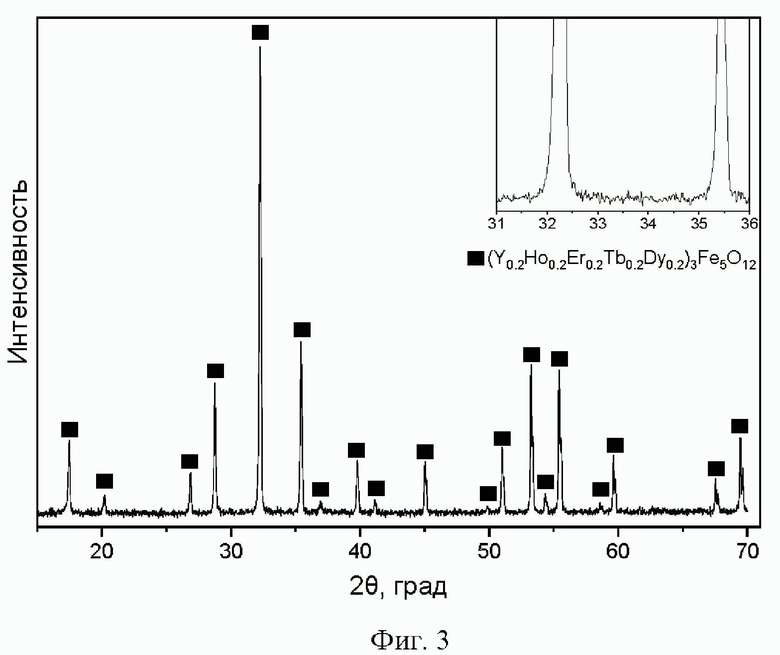
Способ получения высокоэнтропийного железоредкоземельного граната, включающий получение прекурсора из реакционной смеси, содержащей соединения редкоземельных металлов и железа, и термообработку полученного прекурсора, отличающийся тем, что для получения граната состава (Ln10,2Ln20.2Ln30,2Ln40,2Ln50,2)3Fe5O12, где Ln1, Ln2, Ln3 Ln4, Ln5 являются различными и выбраны из группы редкоземельных металлов, включающей Y, Eu, Gd, Dy, Но, Er и Tb, используют оксиды указанных редкоземельных металлов, растворённые в азотной кислоте, а в качестве железосодержащего соединения - азотнокислое железо (III) n-водное, количество кристаллизационной воды в котором определяют гравиметрическим анализом, реакционную смесь гомогенизируют ультразвуковой обработкой при мощности не менее 700 Вт в течение 0,5 ч при поддержании температуры смеси не более 30°С, для получения нитрат-органического прекурсора в смесь вводят аминоуксусную кислоту в качестве органического восстановителя, необходимого для пиролиза прекурсора, термообработку полученного прекурсора проводят путём его пиролиза, а полупродукт, полученный в результате пиролиза, сначала отжигают при температуре 750°С в течение 8 ч и затем спекают при температуре 1200°С в течение 20 ч.
| JULIUSZ DABROWA et al | |||
| Structure and transport properties of the novel (Dy,Er,Gd,Ho,Y)3Fe5O12 and (Dy,Gd,Ho,Sm,Y)3Fe5O12 high entropy garnets, J | |||
| of European Ceram | |||
| Soc., 2021, v | |||
| Механический грохот | 1922 |
|
SU41A1 |
| Водоочистительный аппарат при кипятильнике | 1925 |
|
SU3844A1 |
| УСТРОЙСТВА И СПОСОБ ИССЛЕДОВАНИЯ МАГНИТНЫХ СВОЙСТВ ОБЪЕКТОВ | 2001 |
|
RU2281557C2 |
| КОНТРАСТНЫЕ ВЕЩЕСТВА ДЛЯ ДЕТЕКЦИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2007 |
|
RU2450832C2 |
| CN 114573346 A, 03.06.2022 | |||
| CN 116178012 A, 30.05.2023 | |||
| CN 116514536 A, 01.08.2023 | |||
| CN | |||
Авторы
Даты
2024-07-08—Публикация
2023-12-13—Подача