Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицинской химии. В частности, настоящее изобретение относится к солям кетамина в кристаллической или аморфной форме и их фармацевтическому применению.
Уровень техники
Кетамин представляет собой рацемическую смесь, содержащую равные количества S-кетамина и R-кетамина, которые также называются S-изомером и R-изомером кетамина и которые представлены следующими структурными формулами:
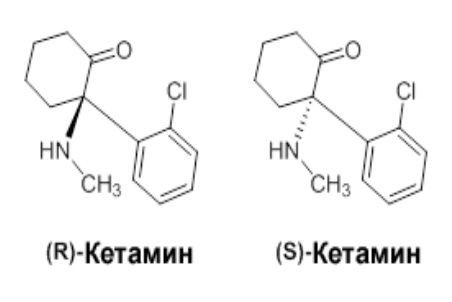
Кетамин является антагонистом рецептора N-метил-D-аспартата (NMDA) (NMDAR). Его фармакодинамическая характеристика описывается как анестезирующее, анальгезирующее или антидепрессантное действие, а также он имеет отношение к лечению некоторых заболеваний центральной нервной системы (ЦНС), таких как патогенез, связанный с NMDAR-опосредованной эксайтотоксичностью и воспалительными нейродегенеративными эффектами, которые включают в себя болезнь Альцгеймера, болезнь Паркинсона, инсульт, черепно-мозговую травму (ЧМТ) и рассеянный склероз (РС) [1-3].
Кетамин применялся в качестве обезболивающих препаратов и антидепрессантов. Кроме того, он также обладает специфической особенностью быстрого начала действия, которая может облегчить симптомы депрессии в течение 24 часов после начала лечения. Например, R,S-кетамин HCl присутствует на рынке с 1970 года как кеталар для инъекций (Pfizer) для применения в анестезии. Кроме того, интраназальный продукт S-кетамин HCl, назальный спрей Spravato, был одобрен Управлением по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) в 2019 году для лечения терапевтически резистентной депрессии (MS)(ТРД).
В настоящее время известно, что кетамин (включая S-изомер и R-изомер) не только применяется для анестезии, анальгезии, в качестве антидепрессанта и противовоспалительного агента [4], но и является одним из препаратов, привлекающих внимание для применения при больших депрессивных расстройствах (MDD)(БДР), БДР с неизбежным риском суицидальных мыслей, ТРД, биполярном расстройстве, обсессивно-компульсивном расстройстве, посттравматическом стрессовом расстройстве (PTSD)далее сокращенно ПТСР), расстройстве аутистического спектра, шуме в ушах, рефракторной хронической мигрени, астме, беспокойстве, расстройствах, связанных с употреблением психоактивных веществ, расстройствах, связанных с употреблением алкоголя, расстройствах пищевого поведения, рефракторном эпилептическом статусе и ишемии головного мозга, по данным клинических или доклинических исследований [5-23].
Однако у кетамина есть проблемы с побочными эффектами, включая психотические симптомы, такие как галлюцинации, бред, зависимость и склонность к злоупотреблениям. Обнаружены клинические побочные эффекты, включая психотические эффекты, такие как диссоциация, расстройства нервной системы, такие как головокружение и седативный эффект, нарушение памяти и когнитивных функций, прямые или косвенные периферические эффекты, такие как тахикардия, легкое угнетение дыхания, гипертония, ощущение сердцебиения, эффекты со стороны костно-мышечной системы (миоклонус, подергивания, спазмы, атаксия, фасцикуляция) и урологические осложнения (дизурия, учащенное мочеиспускание и позывы к мочеиспусканию, недержание мочи, боль, гематурия и язвенный цистит) [4, 24]. Наиболее частыми побочными эффектами являются расстройства психической и нервной системы, включая диссоциацию и седативный эффект [4]. Кроме того, связанные с кетамином токсикологические эффекты у животных включают нейротоксичность, токсичность для мочевого пузыря и почек, а также сердечную токсичность [25].
Таким образом, задачей настоящего изобретения является получение фармацевтической композиции, которая безопасна для пациентов и эффективно обеспечивает терапевтический эффект без неблагоприятного воздействия на функции организма пациентов.
Сущность изобретения
Ввиду вышеизложенного, настоящее изобретение относится к памоатным солям кетамина и их полиморфам. В одном варианте осуществления настоящего изобретения памоатная соль кетамина имеет стехиометрию 2:1 по отношению кетамина к памоату. В другом варианте осуществления изобретения кетамин может представлять собой S-кетамин, R-кетамин или R,S-кетамин (рацемическая смесь, содержащая равные количества S-кетамина и R-кетамина).
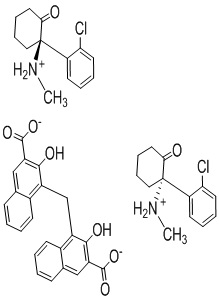
В одном варианте осуществления настоящего изобретения памоатная соль кетамина представляет собой R,S-кетамина памоат, S-кетамина памоат или R-кетамина памоат, которые представлены следующими структурными формулами (I), (II) и (III), соответственно:
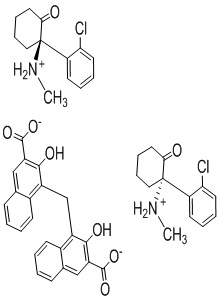 (I),
(I),
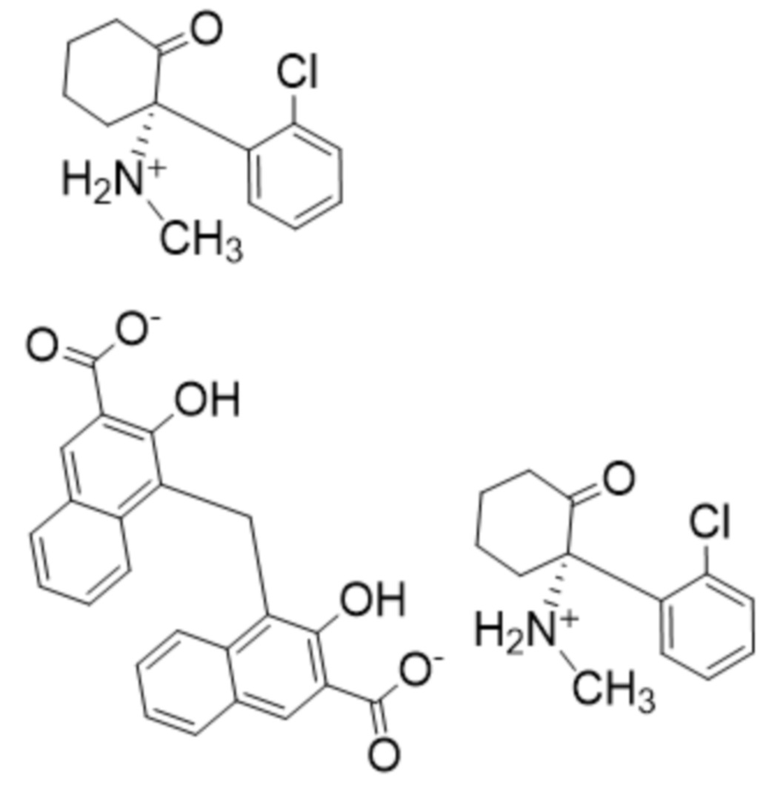 (II),
(II),
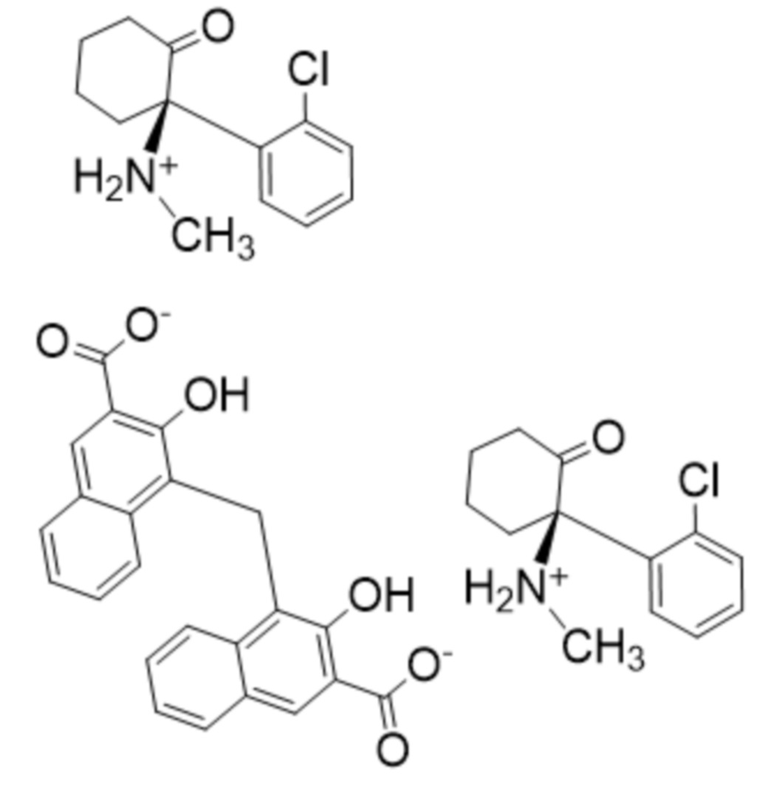 (III).
(III).
В одном варианте осуществления настоящего изобретения памоатная соль кетамина может быть аморфной или кристаллической. В другом варианте осуществления изобретения кристаллическая форма памоатной соли кетамина представлена порошковой рентгеновской дифрактограммой (XRPD), содержащей одно или несколько значений 2θ, выбранных из 6,0, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 19,6, 22,2, 25,2 и 30,3 (± 0,2 2θ).
В одном варианте осуществления настоящего изобретения памоатная соль кетамина представляет собой R,S-кетамина памоат в кристаллической форме, представленной дифрактограммой XRPD, содержащей одно или несколько значений 2θ, выбранных из 6,0, 8,6, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 15,3, 17,9, 18,6, 19,6, 20,0, 21,1, 21,6, 22,2, 23,3, 24,4, 25,2, 25,9, 26,9, 28,6, 29,7, 30,3, 32,4, 34,0 и 36,6 (± 0,2 2θ).
В одном варианте осуществления настоящего изобретения памоатная соль кетамина представляет собой S-кетамина памоат в кристаллической форме, представленной дифрактограммой XRPD, содержащей одно или несколько значений 2θ, выбранных из 6,0, 10,8, 11,7, 12,0, 12,6, 13,1, 14,6, 15,1, 18,2, 19,2, 19,7, 20,1, 22,0, 22,8, 23,3, 23,7, 24,1, 24,7, 25,2, 27,3, 30,1, 31,6, 45,4, 56,4 и 75,2 (± 0,2 2θ).
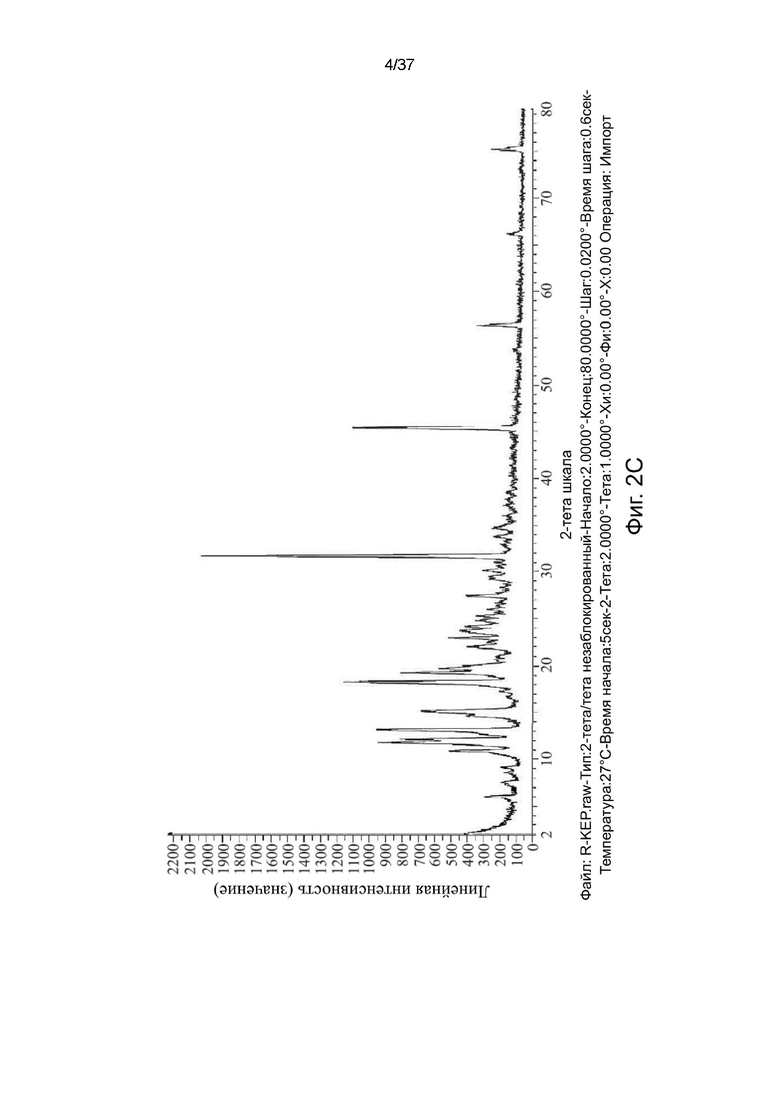
В одном варианте осуществления настоящего изобретения памоатная соль кетамина представляет собой R-кетамина памоат в кристаллической форме, представленной дифрактограммой XRPD, содержащей одно или несколько значений 2θ, выбранных из 6,0, 10,8, 11,7, 12,0, 12,6, 13,1, 14,6, 15,0, 18,2, 19,3, 19,7, 20,6, 22,0, 22,9, 23,6, 24,1, 24,7, 25,2, 25,9, 27,3, 30,1, 31,6, 45,4, 56,4 и 75,2 (± 0,2 2θ).
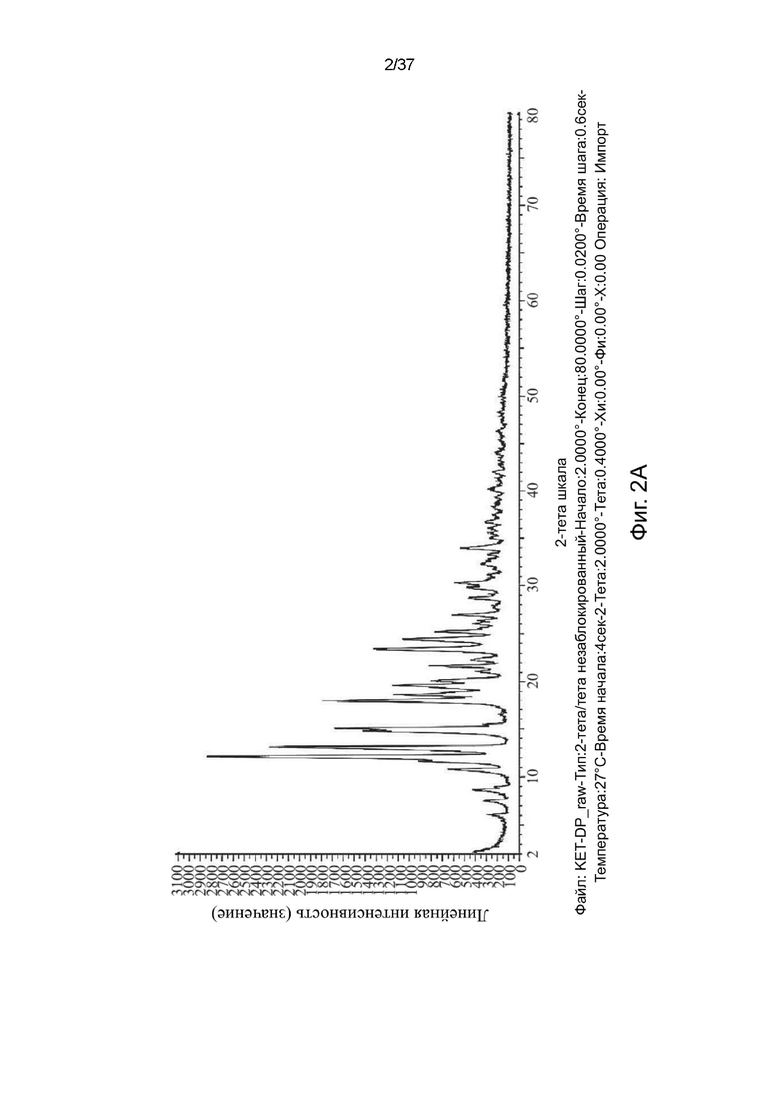
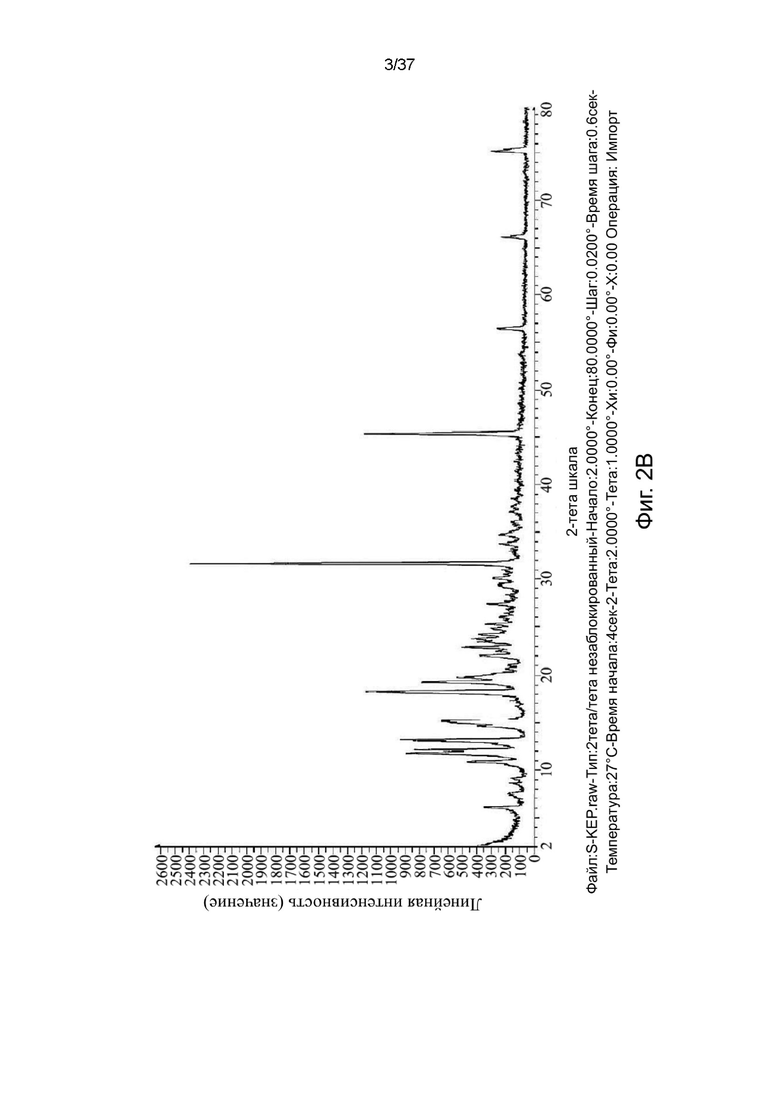
В одном варианте осуществления настоящего изобретения памоатная соль кетамина находится в кристаллической форме, представленной дифрактограммой XRPD, в значительной степени в соответствии с дифрактограммой, показанной на фигуре 2А, фигуре 2B или фигуре 2С.
В одном варианте осуществления настоящего изобретения памоатная соль кетамина имеет чистоту более 95%. В другом варианте осуществления изобретения памоатная соль кетамина имеет чистоту более 99%, например 99,5%, 99,6%, 99,7%, 99,8%, 99,9% и практически 100%.
Настоящее изобретение также относится к фармацевтической композиции, которая пригодна для применения в качестве антидепрессанта, противовоспалительного средства, анестетика и анальгетика. В одном варианте осуществления настоящего изобретения фармацевтическая композиция содержит указанную выше памоатную соль кетамина и её фармацевтически приемлемое вспомогательное вещество.
В одном варианте осуществления настоящего изобретения фармацевтическая композиция применяется для лечения заболевания ЦНС, где эффективное количество фармацевтической композиции вводят нуждающемуся в этом субъекту.
В одном варианте осуществления настоящего изобретения фармацевтическая композиция применяется для анестезии нуждающегося в этом субъекта эффективным количеством фармацевтической композиции, вводимой субъекту.
В одном варианте осуществления настоящего изобретения лечение заболевания ЦНС продолжается, по меньшей мере, 10 дней после введения фармацевтической композиции. В другом варианте осуществления изобретения фармацевтическая композиция может оказывать антидепрессивное, противовоспалительное, анестезирующее или обезболивающее действие, продолжающееся, по меньшей мере, примерно 10 дней.
Настоящее изобретение относится к памоатной соли кетамина и её полиморфу, которые могут применяться в качестве антидепрессанта, противовоспалительного средства, анестетика или анальгетика с большей безопасностью, чем кетамин или кетамин HCl, и, таким образом, могут преодолеть ограничения применения кетамина.
Таким образом, соли кетамина и их полиморфы, представленные в настоящем изобретении, обладают превосходными свойствами для фармацевтического применения.
Краткое описание чертежей
Настоящее изобретение можно более полно понять, прочитав следующие описания вариантов осуществления изобретения со ссылками на прилагаемые чертежи.
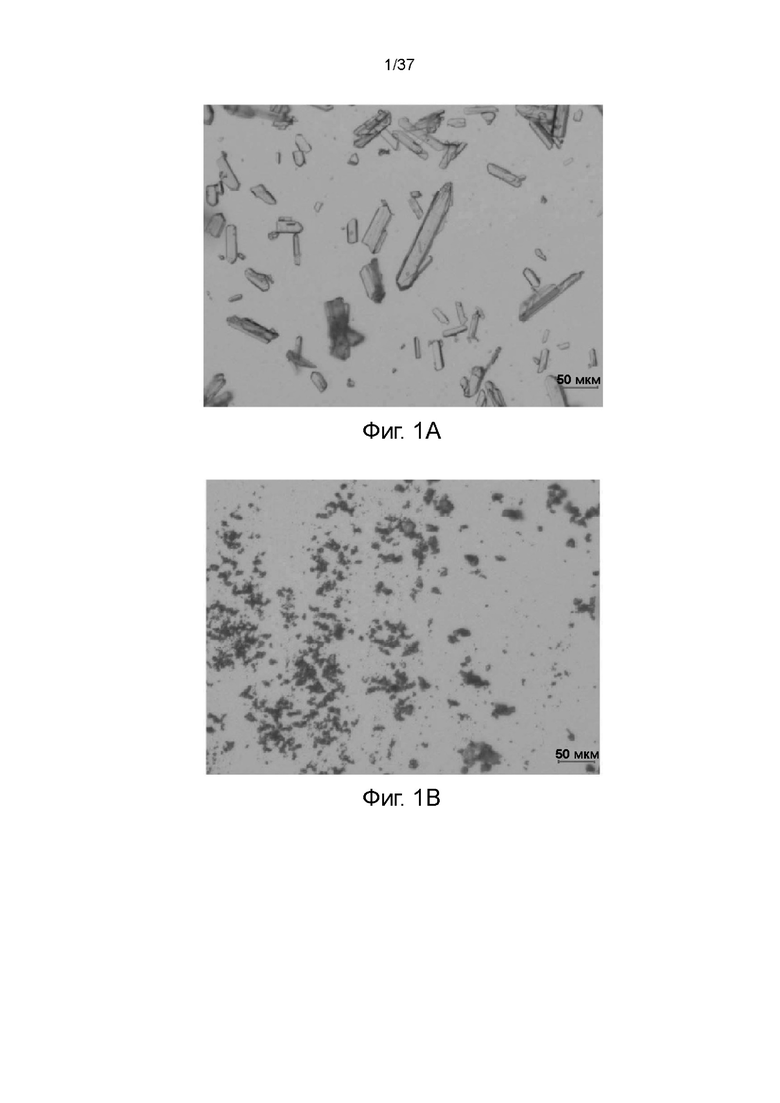
На фигурах 1A и 1B показаны изображения под микроскопом кристаллических и аморфных солей R,S-кетамина памоата, соответственно.
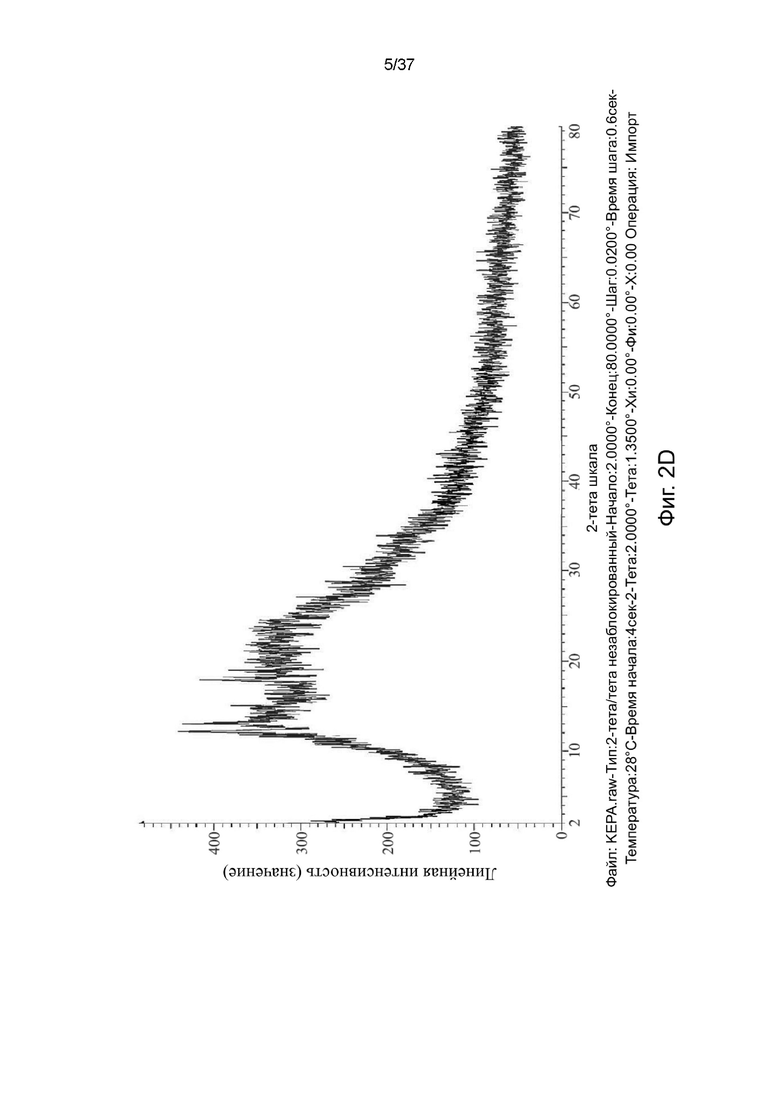
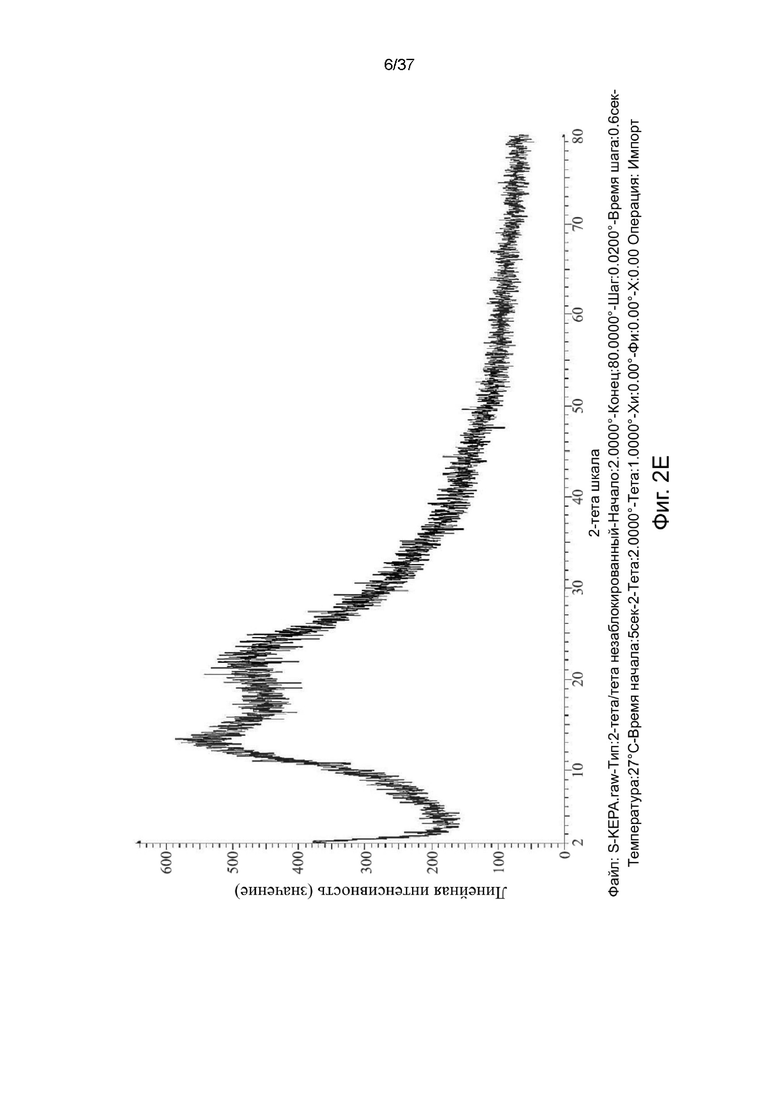
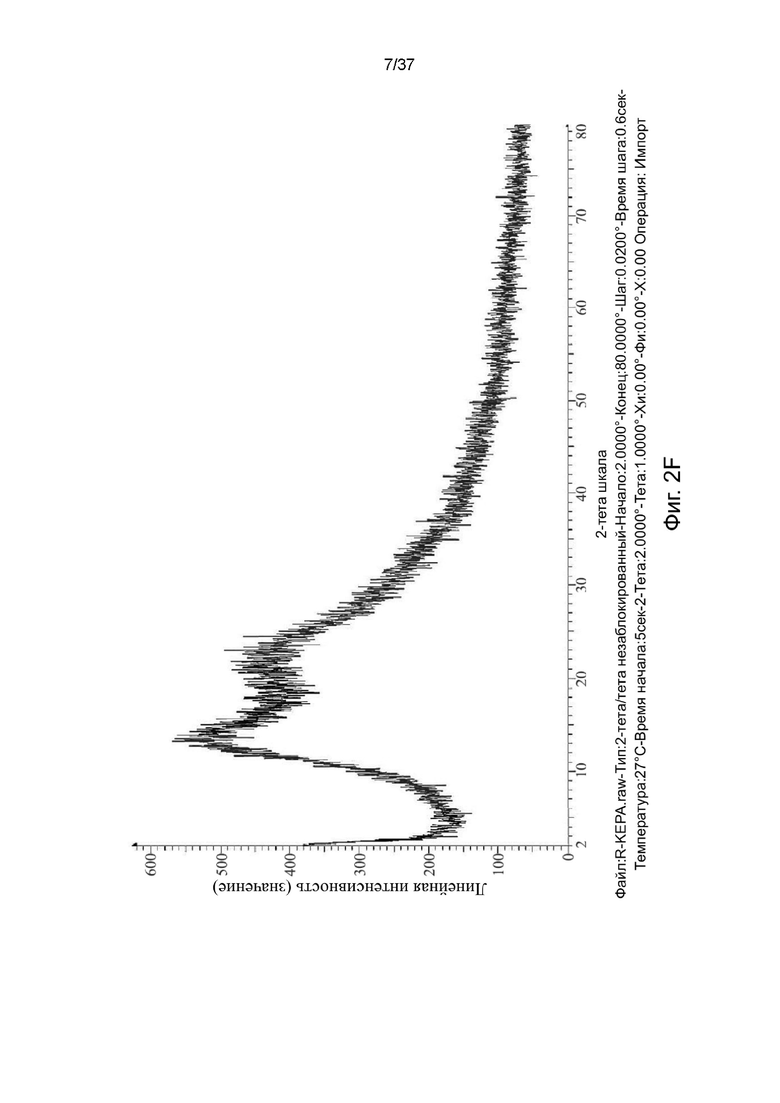
На фигурах 2A-2F показаны порошковые рентгеновские дифрактограммы R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата в кристаллической форме (Фигуры 2A-2C) или аморфной форме (Фигуры 2D-2F), соответственно.
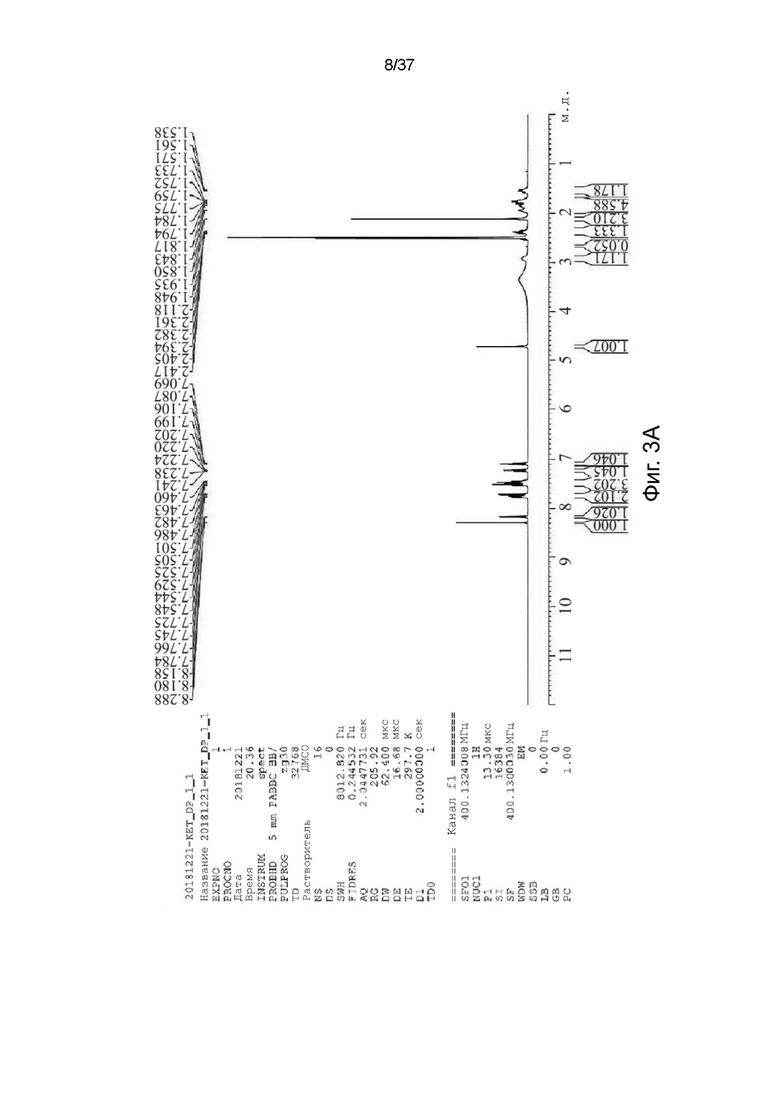
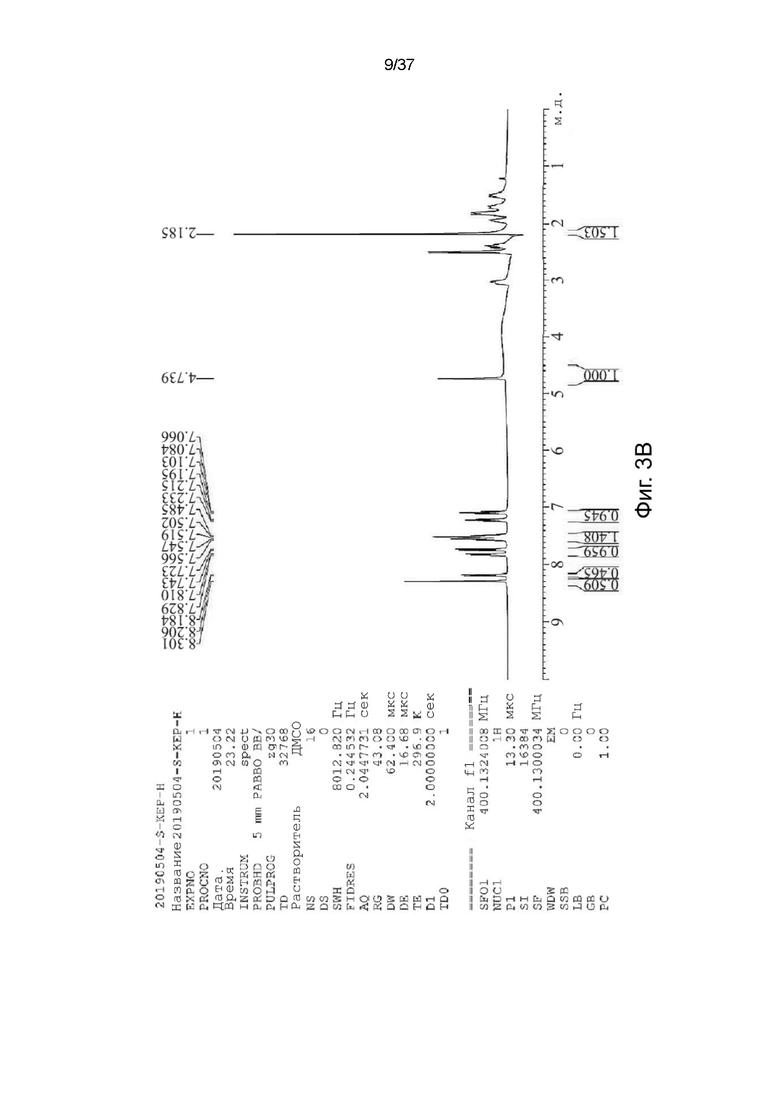
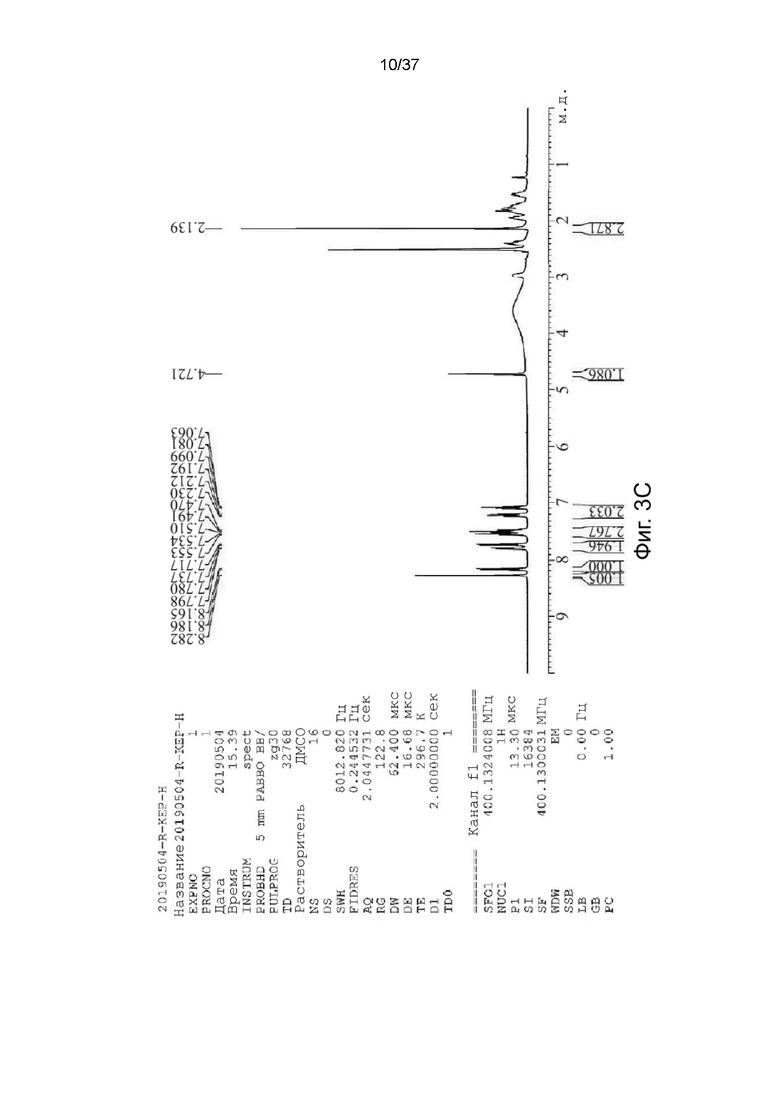
На фигурах 3A-3C показаны спектры 1H ядерного магнитного резонанса для R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата в кристаллической форме, соответственно.
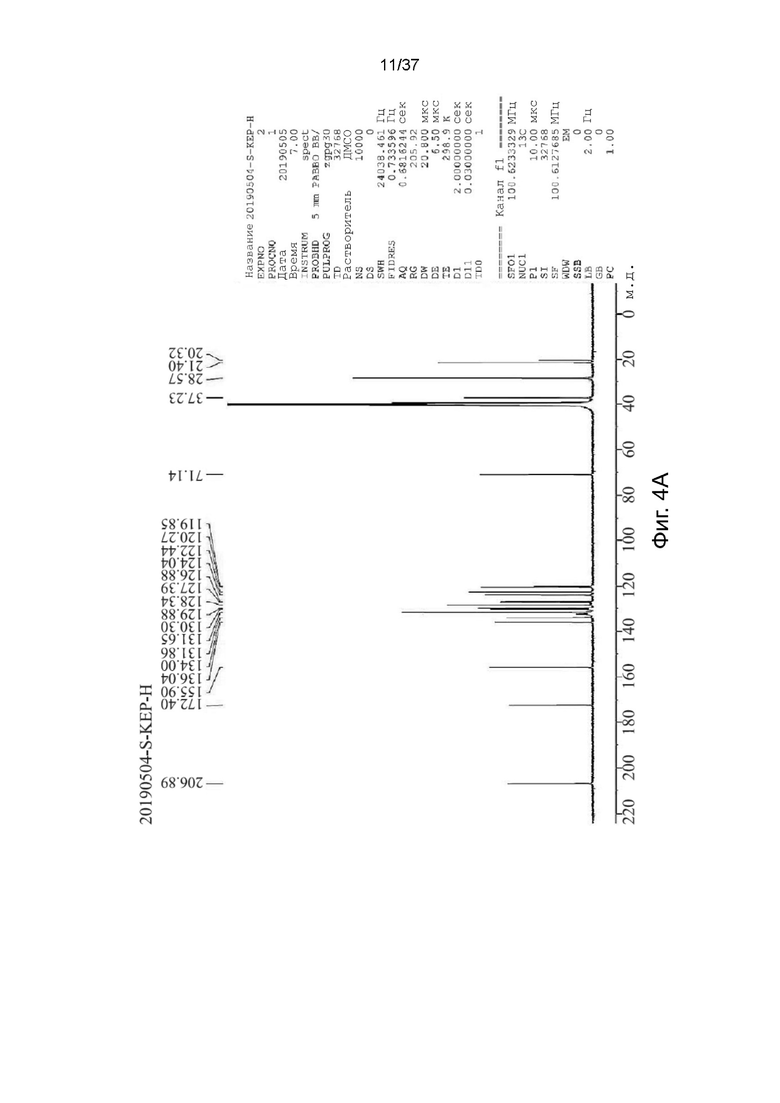
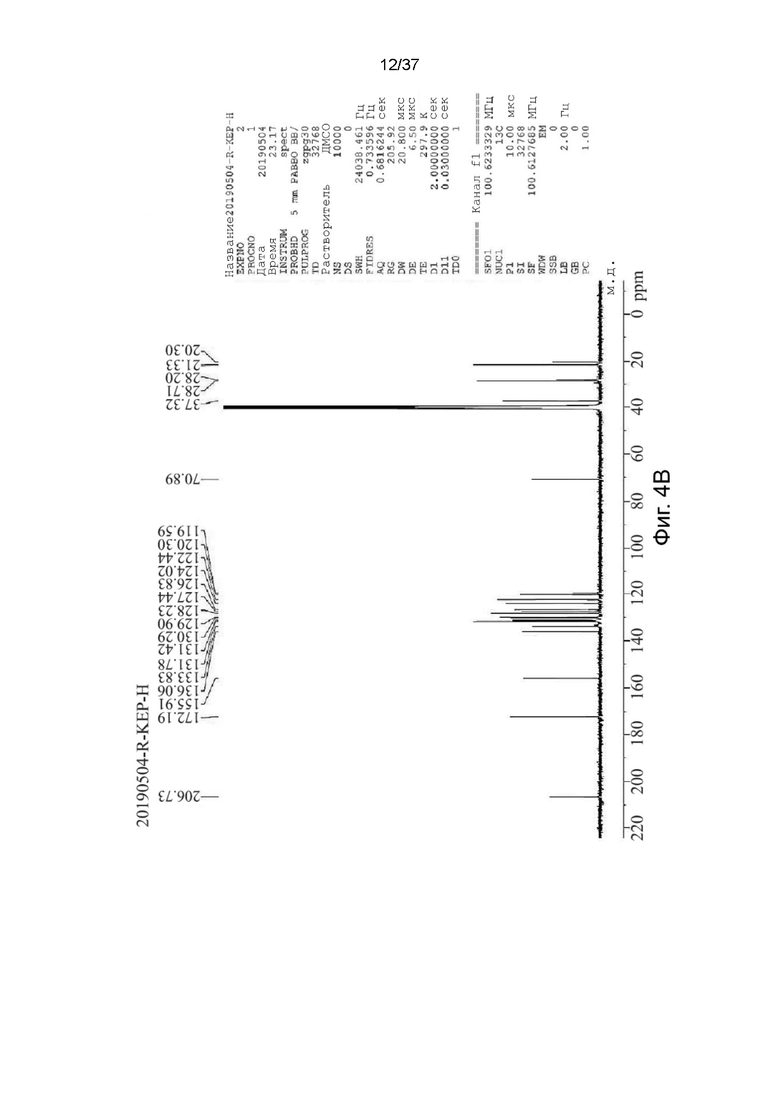
На фигурах 4A и 4B показаны спектры 13C ядерного магнитного резонанса S-кетамина памоата и R-кетамина памоата в кристаллической форме, соответственно.
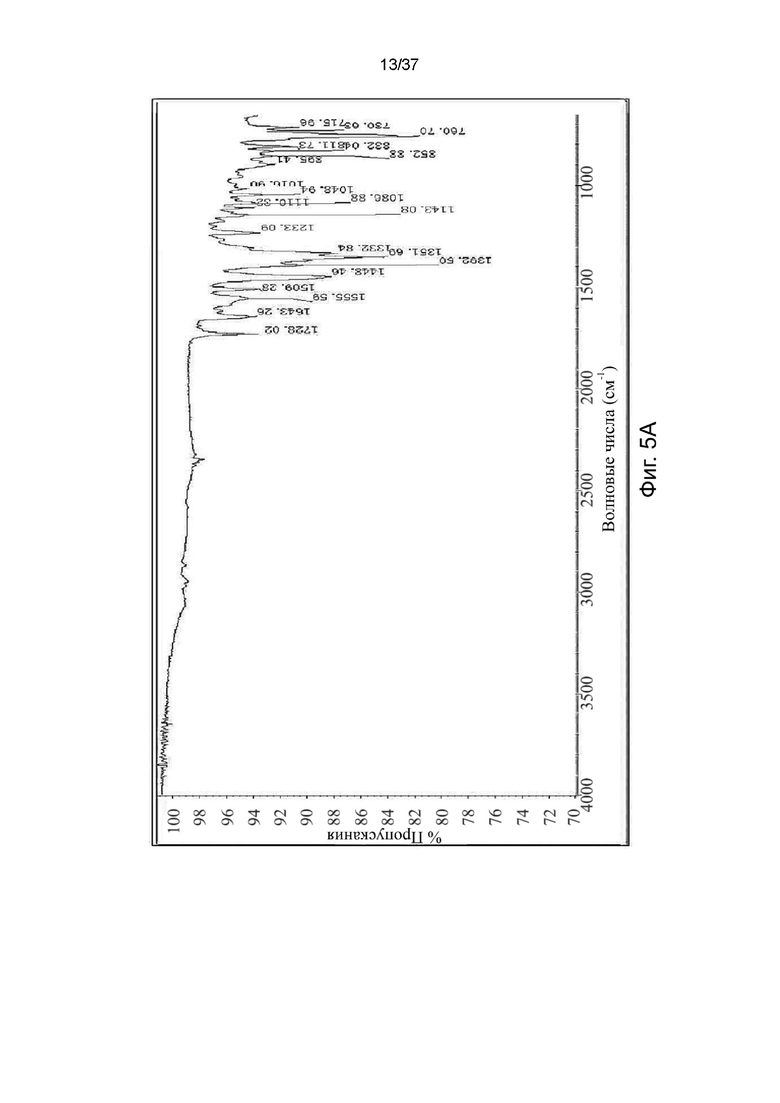
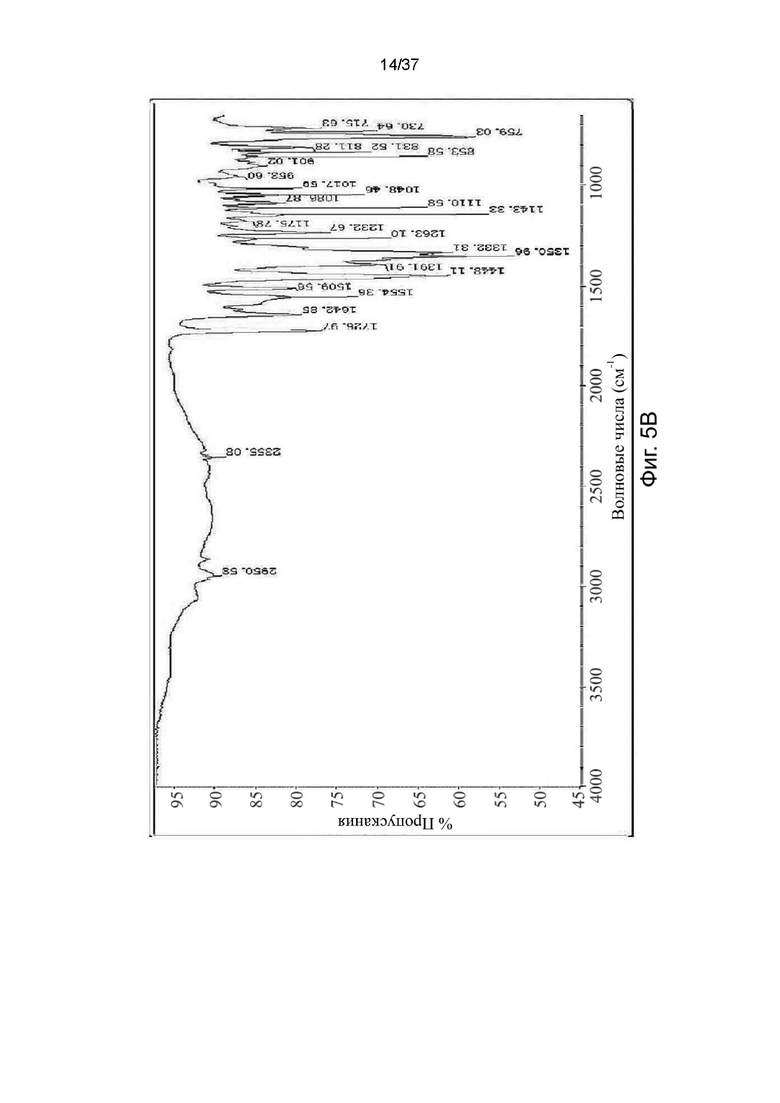
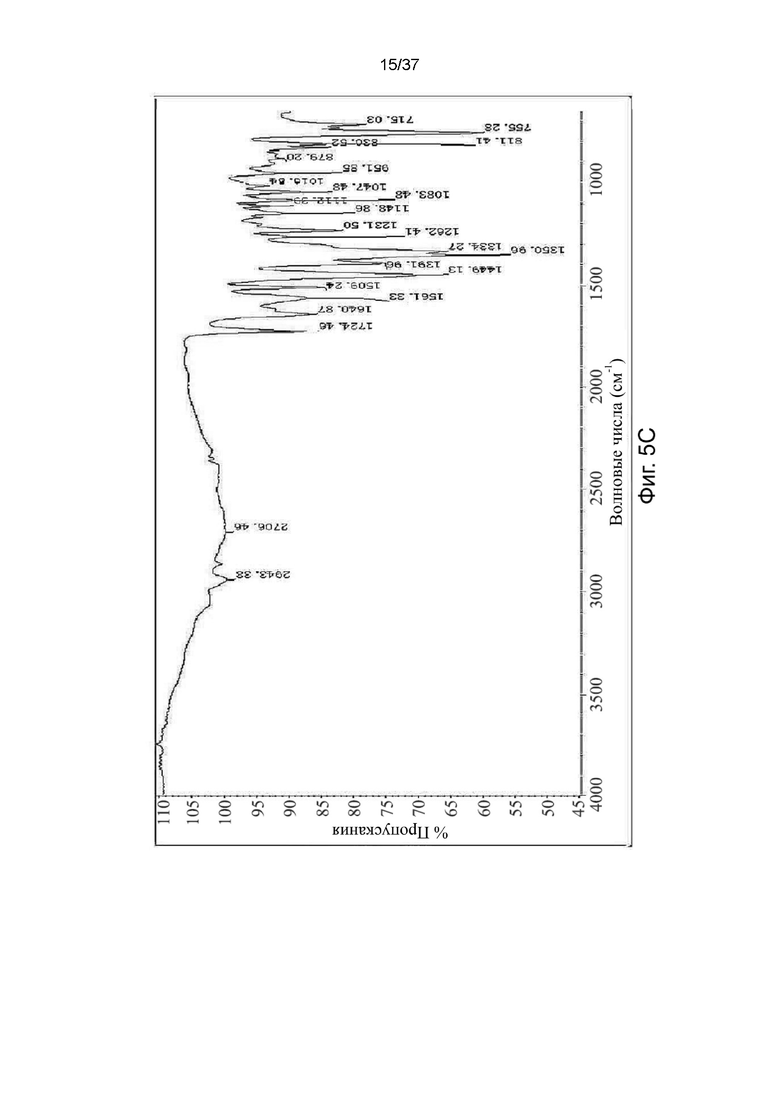
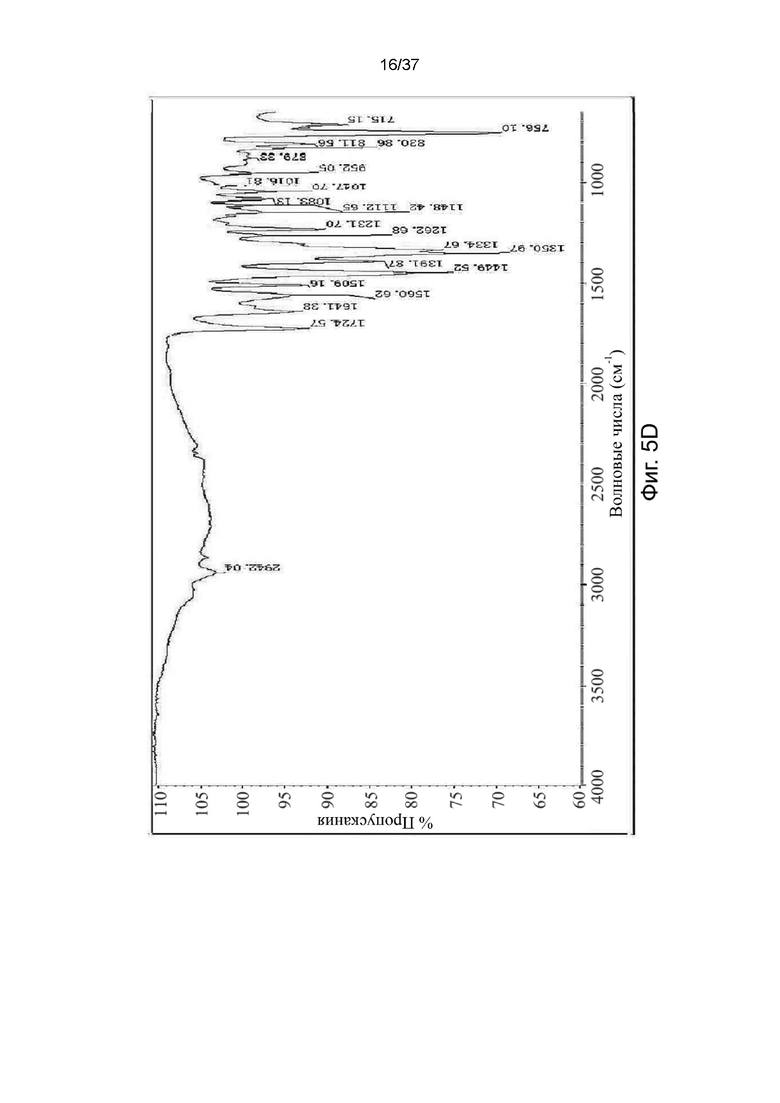
На фигурах 5A-5E показаны спектры инфракрасной спектроскопии с Фурье-преобразованием (Фурье-ИК) S-кетамина памоата и R-кетамина памоата в кристаллической форме (Фигуры 5A и 5B) или аморфной форме (Фигуры 5C и 5D) и R,S-кетамина памоата в аморфной форме (Фигура 5E), соответственно.
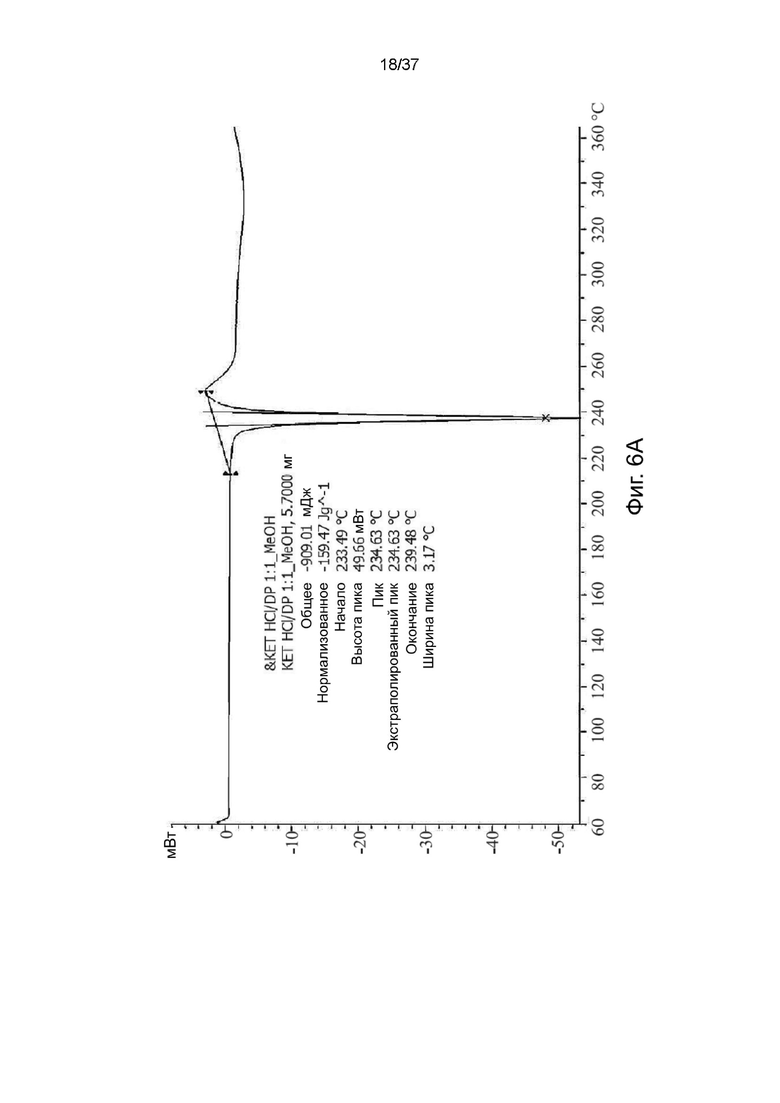
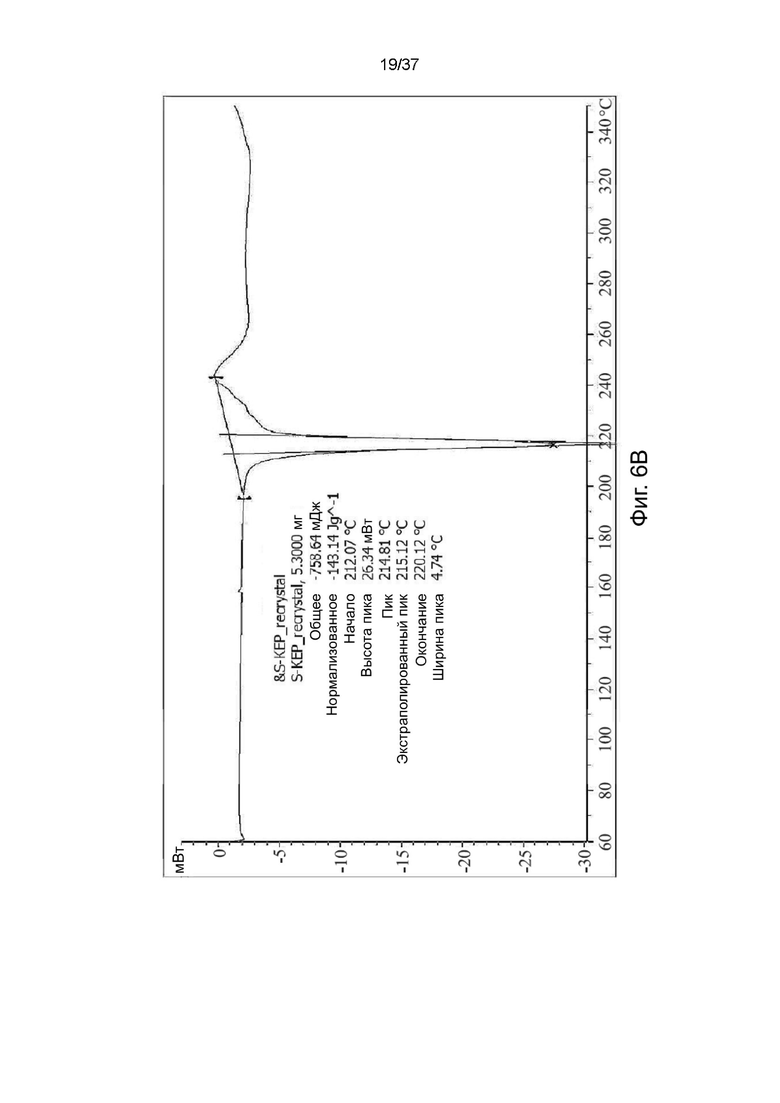
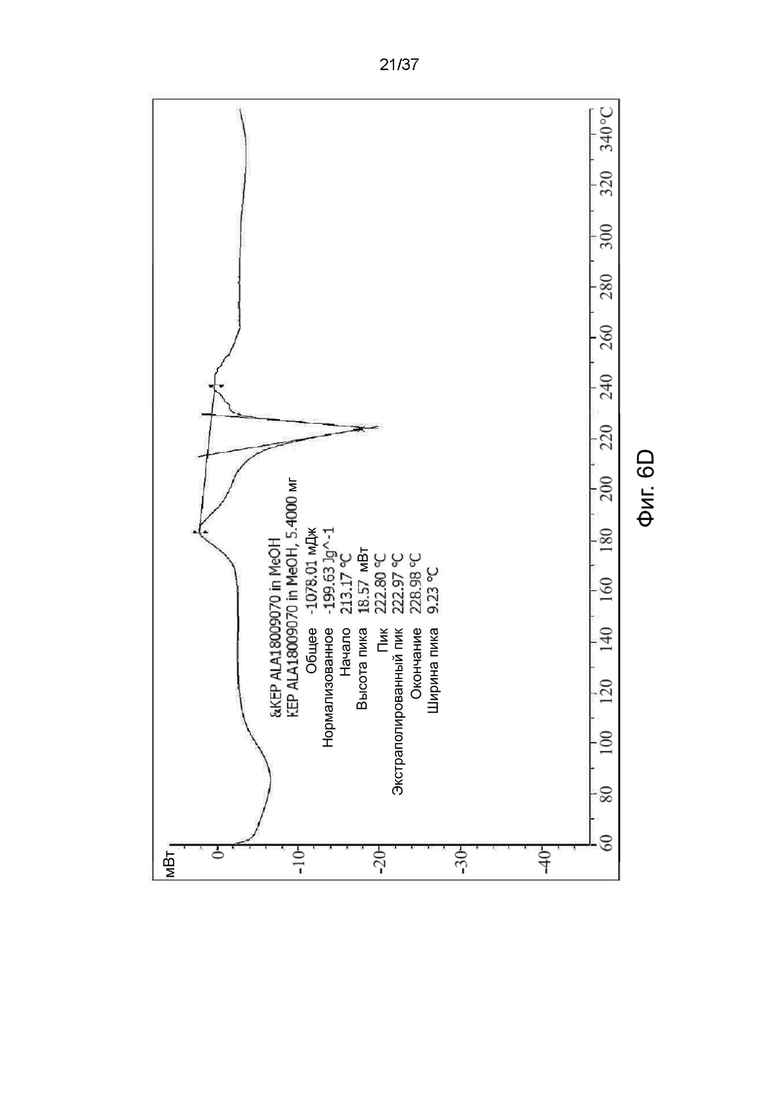
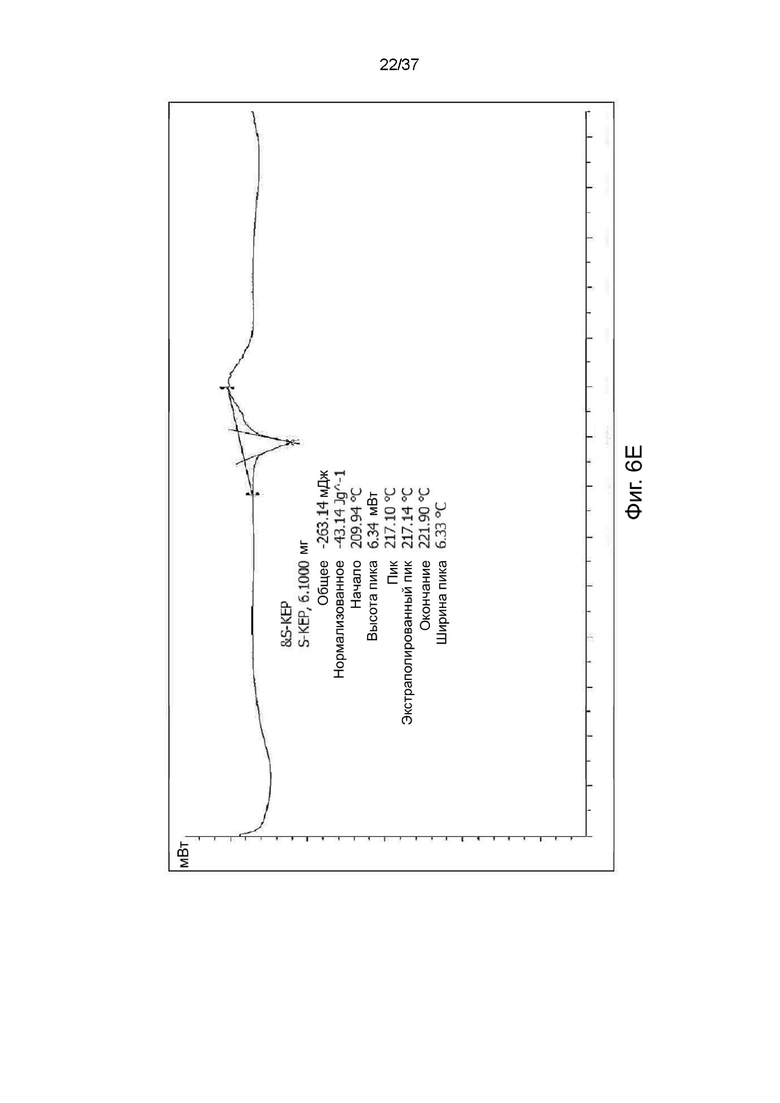
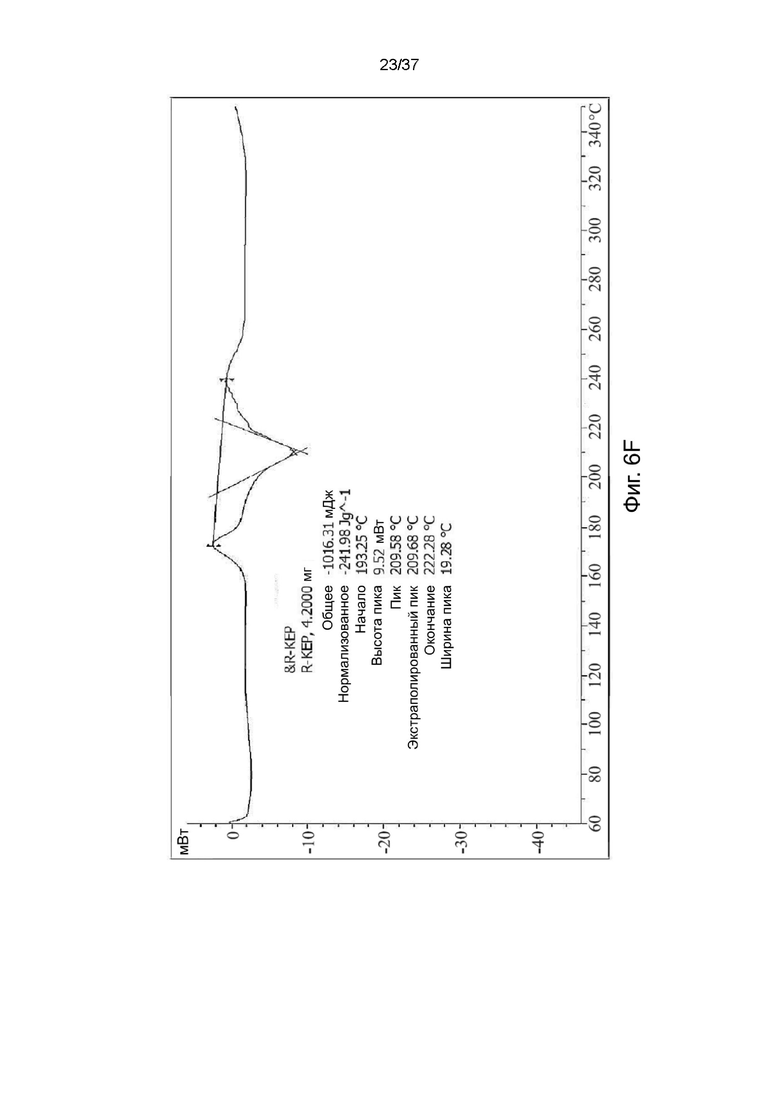
На фигурах 6A-6F показаны результаты дифференциальной сканирующей калориметрии R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата в кристаллической форме (Фигуры 6A-6C) или аморфной форме (Фигуры 6D-6F) соответственно.
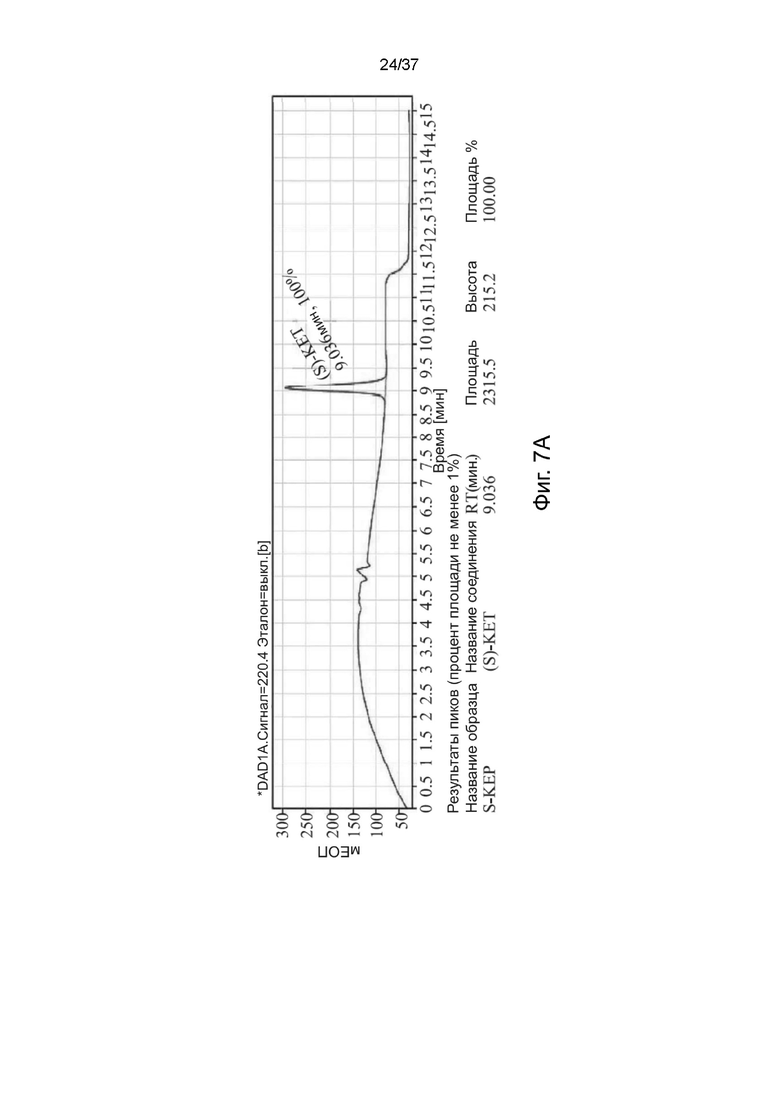
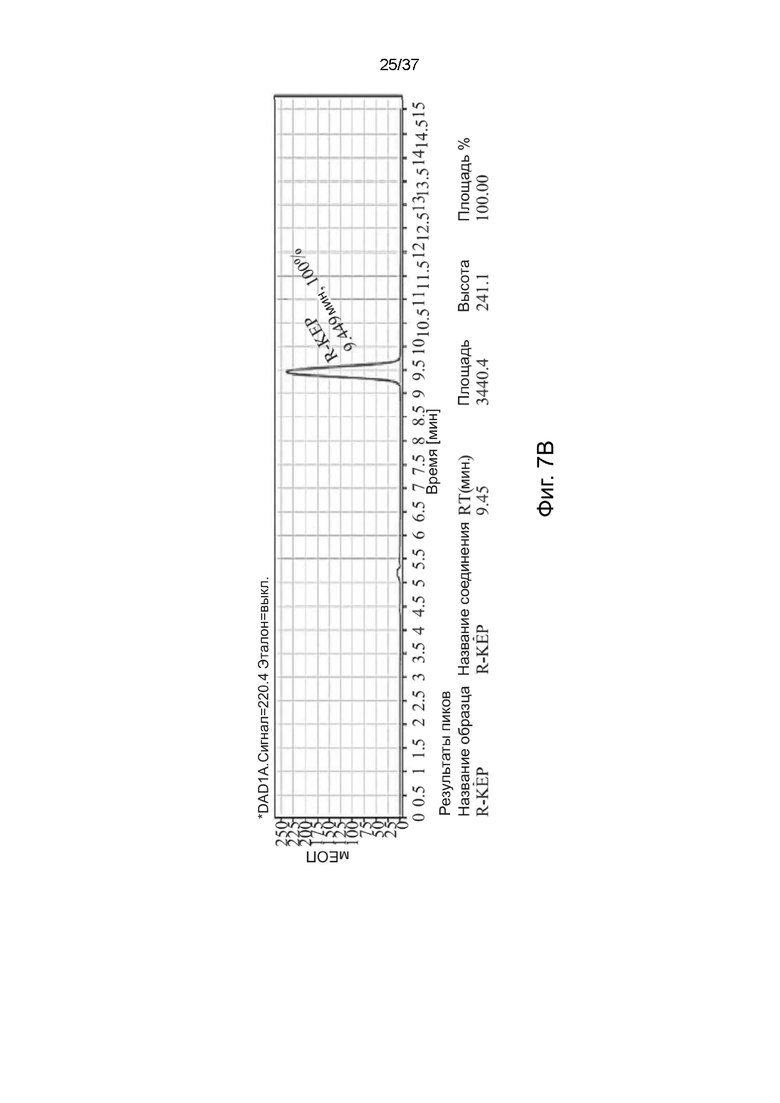
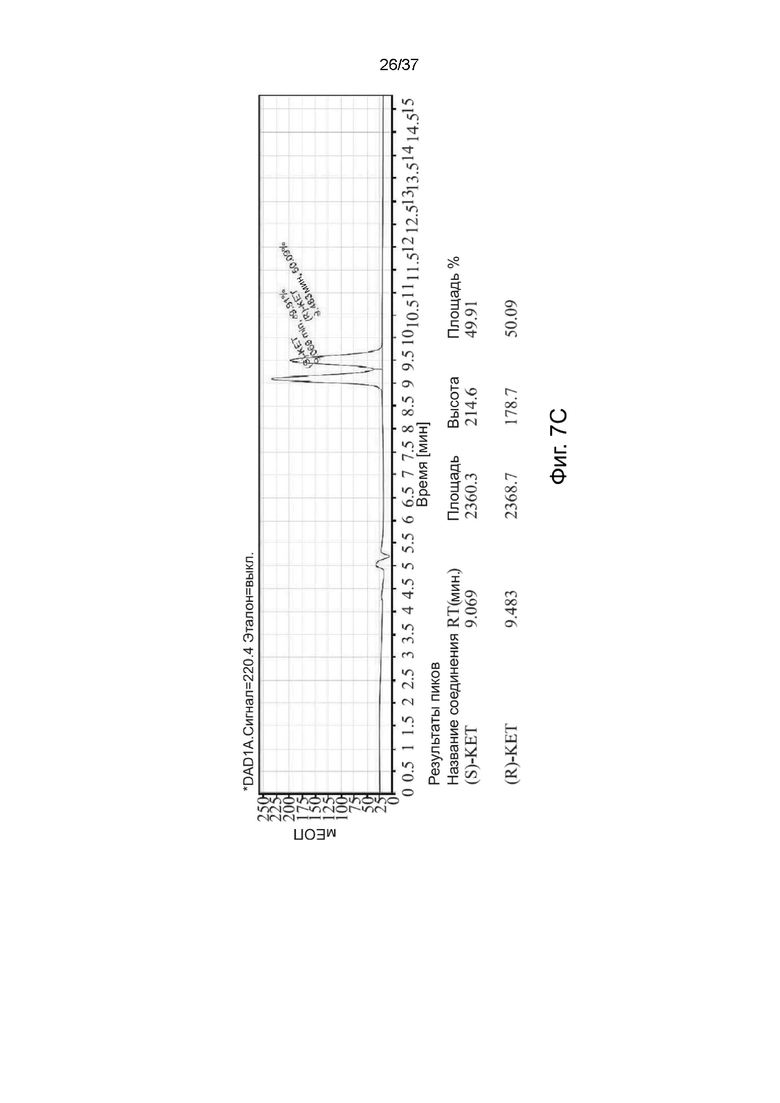
На фигурах 7A-7C показаны результаты анализа с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) кристаллического S-кетамина памоата и R-кетамина памоата и аморфного R,S-кетамина памоата, соответственно.
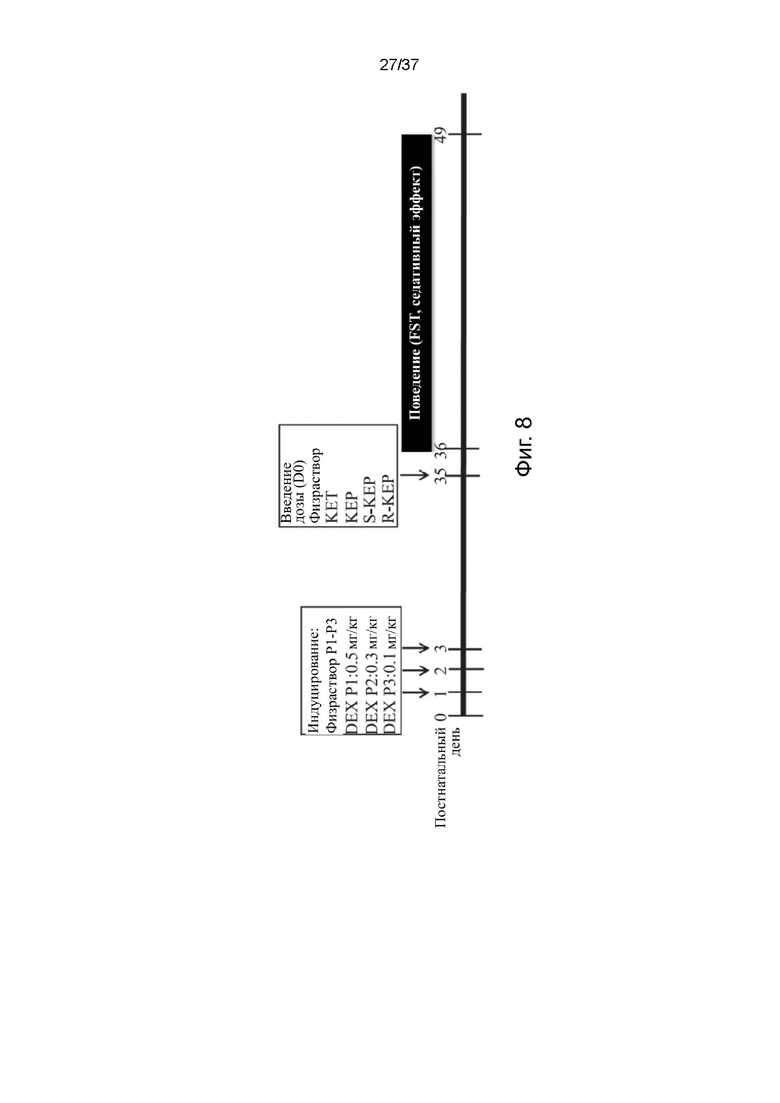
На фигуре 8 показана диаграмма, иллюстрирующая протокол использования животной модели индуцированного дексаметазоном (DEX) состояния подобного депрессии, для оценки антидепрессантных свойств кетамина HCl (KET), R,S-кетамина памоата (KEP), S-кетамина памоата (S-KEP) и R-кетамина памоата (R-KEP). Мышам ICR внутрибрюшинно вводили физиологический раствор или DEX в дни 1-3 после рождения (P1-P3) с уменьшением дозы до 0,5 мг/кг, 0,3 мг/кг и 0,1 мг/кг, соответственно. Лекарственные препараты для каждой группы или физиологический раствор вводили подкожно на 35-й день после рождения, P35 (т.е. день 0 введения дозы, D0), и тест принудительного плавания (FST) проводили в день 1 после введения дозы (D1, P36) и день 10 после введения дозы (P45) после введения препарата. Оценку седативного поведения также проводили по шкале оценки седативного эффекта от момента времени сразу после инъекции до дня 14 после введения дозы (P49) после введения лекарственного препарата.
На фигуре 9 представлена диаграмма, показывающая антидепрессантное действие кетамина HCl (KET), R,S-кетамина памоата (KEP), S-кетамина памоата (S-KEP) и R-кетамина памоата (R-KEP) в тесте принудительного плавания (FST) в день 1 и день 10 после введения препарата. *p < 0,05, **p < 0,01 и ***p < 0,001 указывают на значимые различия по сравнению с группой, получавшей физиологический раствор.
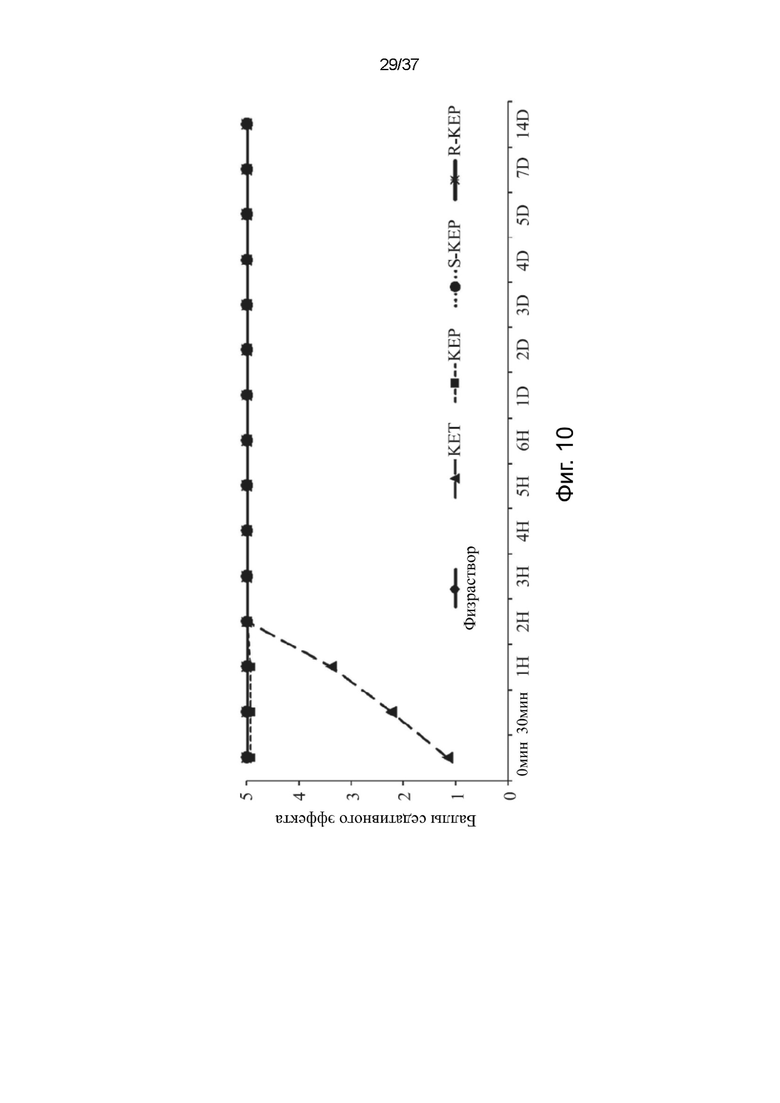
На фигуре 10 представлен график, показывающий балльную оценку седативного эффекта у мышей, получавших физиологический раствор (Физраствор), кетамин HCl (KET), R,S-кетамина памоат (KEP), S-кетамина памоат (S-KEP) и R-кетамина памоат (R -KEP) с момента сразу после инъекции до 14 дней.
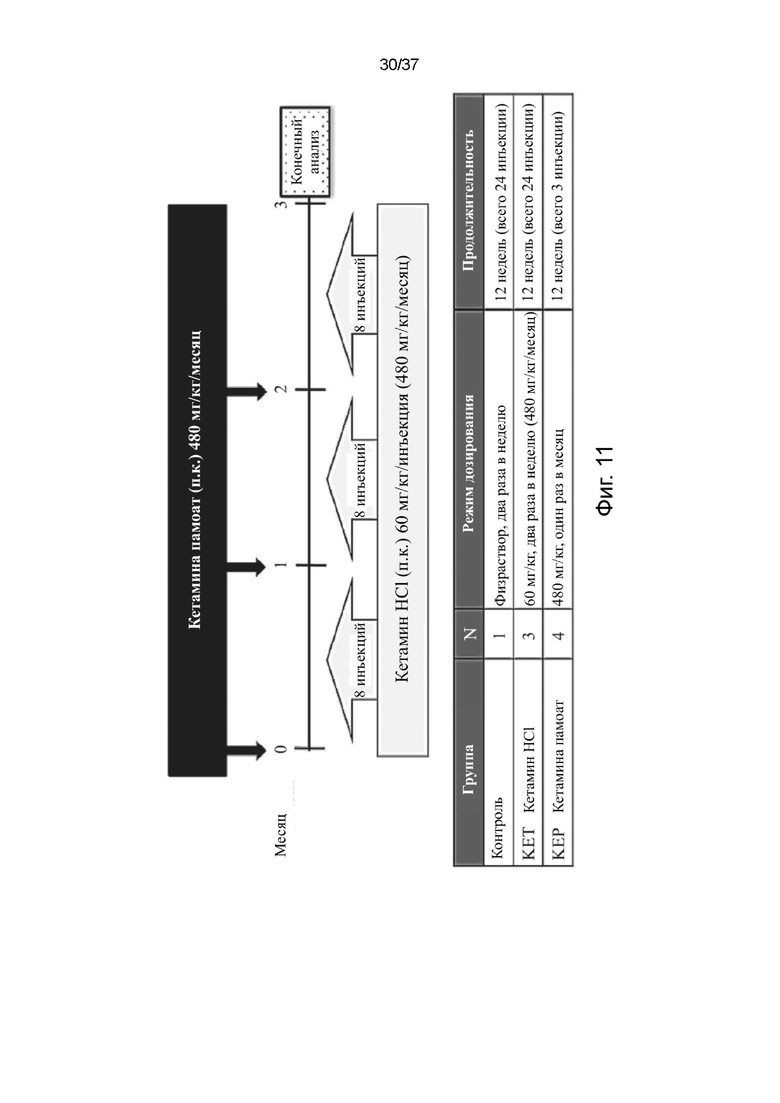
На фигуре 11 представлена схема, иллюстрирующая протокол 3-месячного токсикологического исследования с повторной дозой Контроля (физиологический раствор), кетамина HCl (KET) и R,S-кетамина памоата (KEP) у самок крыс линии Спрег-Доули (SD). Группе KET подкожно (п.к.) два раза в неделю вводили кетамин HCl в дозе 60 мг/кг массы тела, а группе KEP подкожно вводили R,S-кетамина памоат в дозе 480 мг/кг массы тела ежемесячно. На 84 день животных умерщвляли для гистопатологического анализа. INJs: инъекции.
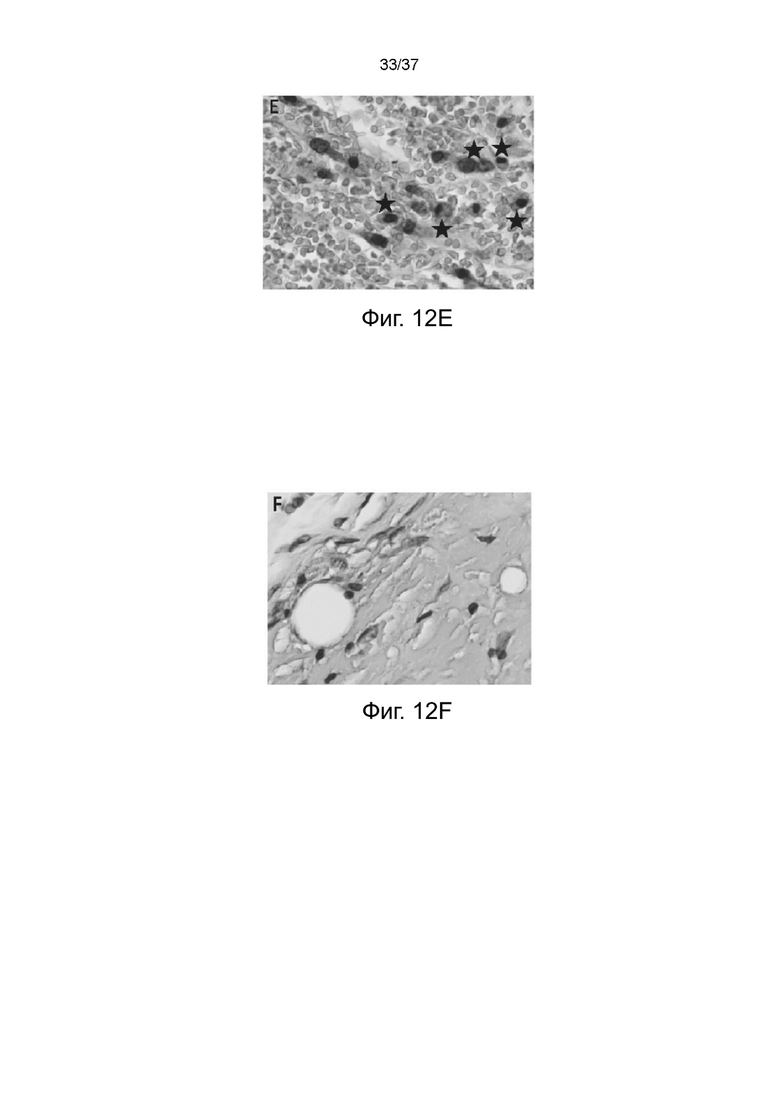
На фигурах 12A-12F показаны изображения окрашенных гематоксилином и эозином (HE) тканей в месте инъекции у крыс, где Фигуры 12A, 12C и 12E представляют собой репрезентативные изображения тканей в месте инъекции кетамина HCl при увеличении x40, x100 и x400, соответственно, а Фигуры 12B, 12D и 12F представляют собой репрезентативные изображения тканей в месте инъекции R,S-кетамина памоата при увеличении x40, x100 и x400, соответственно. Черными звездочками обозначены воспалительные клетки.
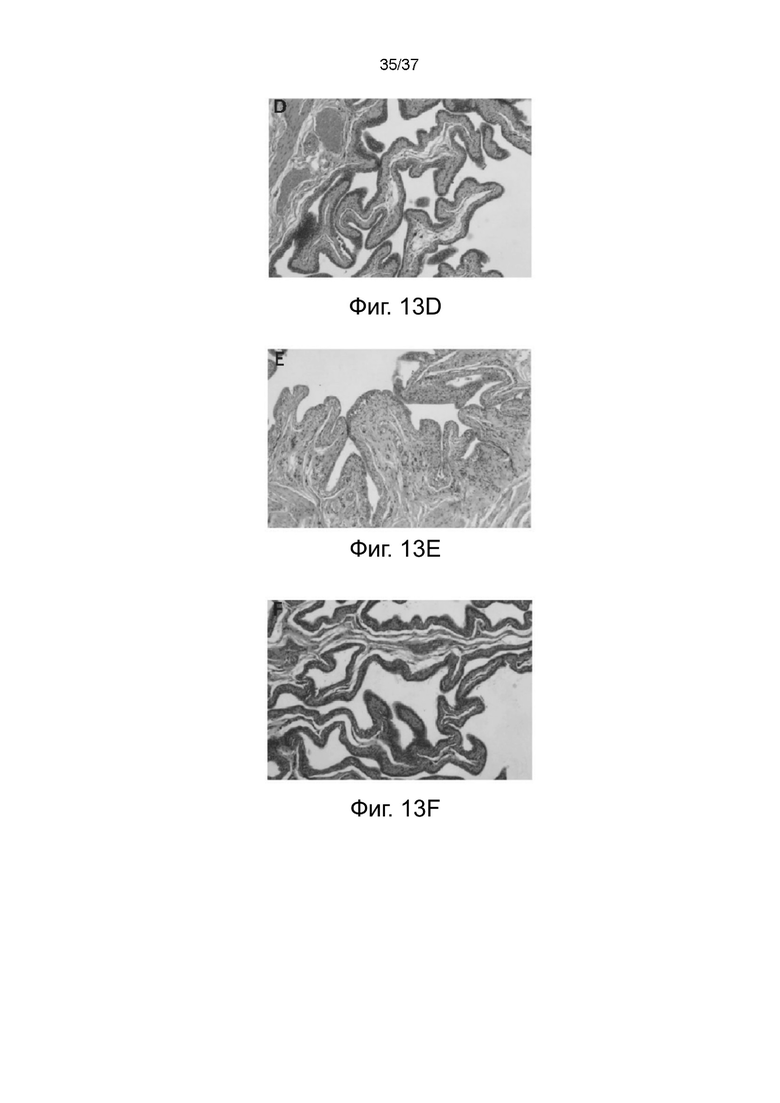
На фигурах 13A-13F показаны изображения окрашенных HE тканей мочевого пузыря крыс, где Фигуры 13A и 13D представляют собой репрезентативные изображения тканей мочевого пузыря контрольной крысы при увеличении x400 и x40 соответственно; Фигуры 13B и 13E представляют собой репрезентативные изображения тканей мочевого пузыря крысы, получавшей KET, при увеличении x400 и x40, соответственно; и Фигуры 13C и 13F представляют собой репрезентативные изображения тканей мочевого пузыря крысы, получавшей KEP, при увеличении x400 и x40, соответственно.
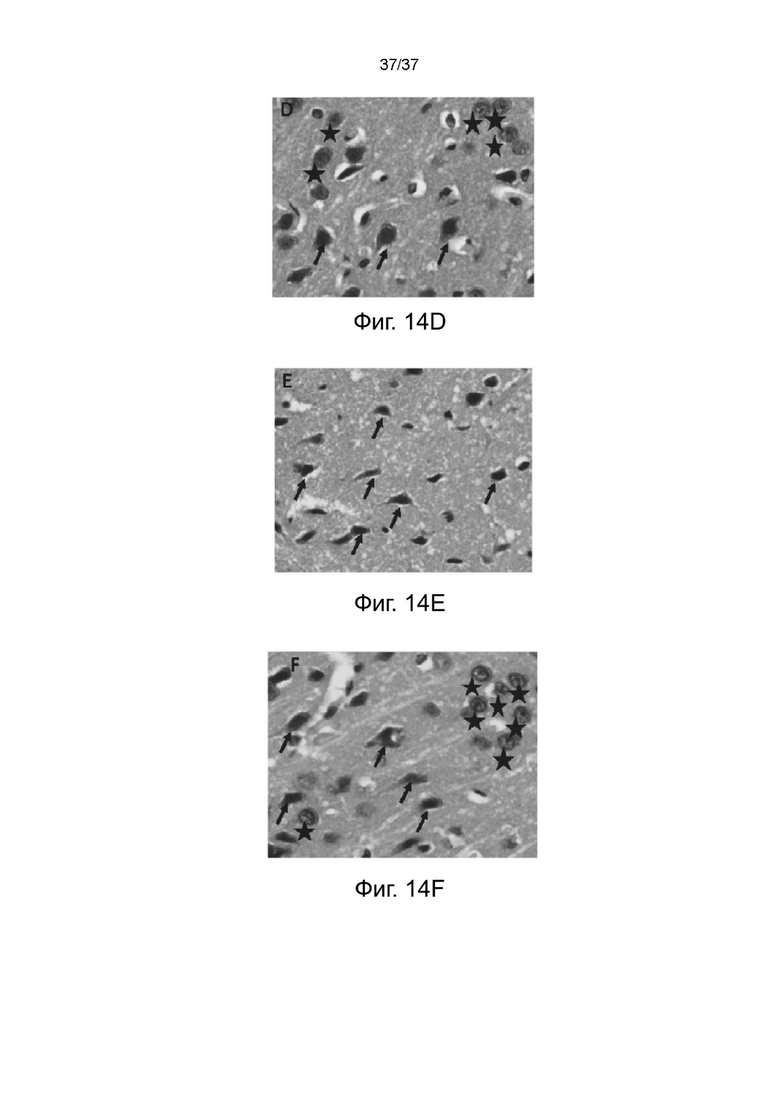
На фигурах 14A-14F показаны изображения окрашенных HE тканей головного мозга крыс в префронтальной коре головного мозга, где Фигуры 14A и 14D представляют собой репрезентативные изображения тканей мозга контрольной крысы при увеличении x100 и x400, соответственно; Фигуры 14B и 14E представляют собой репрезентативные изображения тканей мозга крысы, получавшей KET, при увеличении x100 и x400, соответственно; и Фигуры 14C и 14F представляют собой репрезентативные изображения тканей мозга крысы, получавшей KEP, при увеличении x100 и x400, соответственно. Черными звездочками обозначены гранулярные клетки. Черные стрелки указывают на пирамидные клетки.
Подробное описание изобретения
Следующие ниже примеры служат для иллюстрации настоящего изобретения. Специалист в данной области техники может легко представить себе другие преимущества и эффекты настоящего изобретения, основываясь на раскрытии описания. Настоящее изобретение также может быть реализовано или применено, как описано в различных примерах. Можно модифицировать или изменить приведенные выше примеры для реализации настоящего изобретения, не выходя за рамки его объема, для различных аспектов и применений.
Далее следует отметить, что используемые в тексте настоящего описания термины в форме единственного числа включают в себя формы множественного числа, если данный термин явно и недвусмысленно не ограничены единственным числом. Термин «или» используется взаимозаменяемо с термином «и/или», если из контекста явно не следует иное.
Настоящее изобретение относится к памоатной соли кетамина с соотношением кетамина и памоата 2:1.
В одном варианте осуществления изобретения памоатная соль кетамина может быть в аморфной или в кристаллической форме, характеризующейся дифрактограммой XRPD, содержащей одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 19,6, 22,2, 25,2 и 30,3 (± 0,2 2θ). В другом варианте осуществления изобретения значения 2θ измеряют с использованием излучения CuKα при комнатной температуре.
В одном варианте осуществления настоящее изобретение относится к кристаллической памоатной соли R,S-кетамина, которая имеет дифрактограмму XRPD, содержащую одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 19,6, 22,2, 25,2 и 30,3 (± 0,2 2θ), или одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 8,6, 15,3, 17,9, 18,6, 20,0, 21,1, 21,6, 23,4, 24,4, 25,9, 26,9, 28,6, 29,7, 32,4, 34,0 и 36,6 (± 0,2 2θ). В другом варианте осуществления изобретения кристаллическая памоатная соль R,S-кетамина имеет дифрактограмму XRPD, представленную, по меньшей мере, одним из следующего: (i) дифрактограмма XRPD, содержащая один, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 8,6, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 15,3, 17,9, 18,6, 19,6, 20,0, 21,1, 21,6, 22,2, 23,3, 24,4, 25,2, 25,9, 26,9, 28,6, 29,7, 30,3, 32,4, 34,0 и 36,6 (± 0,2 2θ); и (ii) дифрактограмма XRPD, показанная на фигуре 2А. Вещё одном варианте осуществления изобретения кристаллическая памоатная соль R,S-кетамина имеет дифрактограмму XRPD, как показано на фигуре 2А.
В одном варианте осуществления настоящее изобретение относится к кристаллической памоатной соли S-кетамина, которая имеет дифрактограмму XRPD, содержащую одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 10,8, 11,7, 12,0, 13,1, 14,6, 15,1, 19,7, 22,0, 25,2 и 30,1 (± 0,2 2θ) или одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 12,6 , 18,2, 19,2, 20,1, 22,8, 23,3, 23,7, 24,1, 24,7, 27,3, 31,6, 45,4, 56,4 и 75,2 (± 0,2 2θ). В другом варианте осуществления изобретения кристаллическая памоатная соль S-кетамина имеет дифрактограмму XRPD, представленную, по меньшей мере, одним из следующего: (i) дифрактограмма XRPD, содержащая один, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 10,8, 11,7, 12,0, 12,6, 13,1, 14,6, 15,1, 18,2, 19,2, 19,7, 20,1, 22,0, 22,8, 23,3, 23,7, 24,1, 24,7, 25,2, 27,3, 30,1, 31,6, 45,4, 56,4 и 75,2 (± 0,2 2θ); и (ii) дифрактограмма XRPD, показанная на фигуре 2B. Вещё одном варианте осуществления изобретения кристаллическая памоатная соль S-кетамина имеет дифрактограмму XRPD, как показано на фигуре 2B.
В одном варианте осуществления настоящее изобретение относится к кристаллической памоатной соли R-кетамина, которая имеет дифрактограмму XRPD, содержащую одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 10,8, 11,7, 12,0, 13,1, 14,6, 15,0, 19,7, 22,0, 25,2 и 30,1 (± 0,2 2θ) или одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 12,6 , 18,2, 19,3, 20,6, 22,9, 23,6, 24,1, 24,7, 25,9, 27,3, 31,6, 45,4, 56,4 и 75,2 (± 0,2 2θ). В другом варианте осуществления изобретения кристаллическая памоатная соль R-кетамина имеет дифрактограмму XRPD, представленную, по меньшей, мере одним из следующего: (i) дифрактограмма XRPD, содержащая один, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более значений 2θ, выбранных из 6,0, 10,8, 11,7, 12,0, 12,6, 13,1, 14,6, 15,0, 18,2, 19,3, 19,7, 20,6, 22,0, 22,9, 23,6, 24,1, 24,7, 25,2, 25,9, 27,3, 30,1, 31,6, 45,4, 56,4 и 75,2 (± 0,2 2θ); и (ii) дифрактограмма XRPD, показанная на фигуре 2С. Вещё одном варианте осуществления изобретения кристаллическая памоатная соль R-кетамина имеет дифрактограмму XRPD, как показано на фигуре 2С.
Настоящее изобретение также относится к способу лечения субъекта, страдающего заболеванием ЦНС, включающему в себя введение этому субъекту эффективного количества фармацевтической композиции, содержащей памоатную соль кетамина и её фармацевтически приемлемое вспомогательное вещество.
В одном из вариантов осуществления изобретения заболевание ЦНС может включать в себя без ограничений БДР, БДР с неизбежным риском суицидальных мыслей, ТРД, биполярное расстройство, обсессивно-компульсивное расстройство, ПТСР, расстройство аутистического спектра, шум в ушах, рефракторную хроническую мигрень, астму, тревожность, расстройства, связанные с употреблением психоактивных веществ, расстройство, связанное с употреблением алкоголя, расстройства пищевого поведения, рефракторный эпилептический статус, ишемию мозга, болезнь Альцгеймера, болезнь Паркинсона, инсульт, черепно-мозговые травмы, рассеянный склероз и боль.
Настоящее изобретение также относится к способу обезболивания нуждающегося в этом субъекта, включающему в себя введение этому субъекту эффективного количества фармацевтической композиции, содержащей памоатную соль кетамина и её фармацевтически приемлемое вспомогательное вещество.
Термин «пациент» или «субъект», используемый здесь взаимозаменяемо в контексте терапии, относится к человеку или животному, не являющемуся человеком, как получателю терапии или профилактики.
Используемый здесь термин «лечить» или «лечение» относится к введению эффективного количества памоатной соли кетамина, её полиморфа или содержащей её фармацевтической композиции нуждающемуся в этом субъекту для лечения, уменьшения, облегчения, излечения, ослабления или предотвращения заболевания, его симптома или предрасположенности к нему. Такой субъект может быть идентифицирован медицинским работником на основании результатов любого подходящего диагностического метода.
Используемый здесь термин «эффективное количество» относится к терапевтическому количеству, которое достаточно для предотвращения развития, рецидива или начала заболевания ЦНС и одного или нескольких его симптомов, усиления или улучшения профилактического эффекта другой терапии, уменьшения тяжести или продолжительности расстройства, облегчения одного или нескольких симптомов расстройства, предотвращения развития психотического расстройства или воспалительного расстройства и/или усиления или улучшения терапевтического эффекта другой терапии.
Используемый здесь термин «фармацевтически приемлемый» относится к веществу, которое приемлемо для использования в фармацевтике с токсикологической точки зрения и не взаимодействует отрицательно с активным ингредиентом.
В зависимости от типа фармацевтических композиций фармацевтически приемлемое вспомогательное вещество может быть выбрано из любого одного или комбинации вспомогательных веществ, известных в данной области техники. Выбор фармацевтически приемлемого вспомогательного вещества частично зависит от желаемого способа введения, который будет использоваться. Для фармацевтической композиции настоящего изобретения вспомогательное вещество следует выбирать так, чтобы в значительной степени поддерживать конкретную форму активного соединения (например, памоатной соли кетамина), независимо от того, является ли оно кристаллическим или нет. Другими словами, вспомогательное вещество существенно не изменяет форму активного соединения. Вспомогательное вещество также не может быть несовместимо с формой активного соединения, например, из-за того, что он вызывает какой-либо нежелательный биологический эффект или иным образом отрицательно взаимодействует с любым другим компонентом(ами) фармацевтической композиции.
В некоторых вариантах осуществления настоящего изобретения фармацевтическую композицию вводят субъекту перорально, внутривенно, внутримышечно, подкожно, внутрибрюшинно, внутрикожно, чрескожно, интраназально, ректально, интратекально, внутримукозально или внутриглазным способом.
В некоторых вариантах осуществления настоящего изобретения фармацевтическую композицию настоящего изобретения получают в форме, подходящей для перорального введения, и, таким образом, фармацевтическая композиция может вводиться субъекту перорально. Альтернативно, фармацевтическая композиция может быть получена в форме сухого порошка, таблетки, пастилки, капсулы, гранулы или драже.
Фармацевтическая композиция настоящего изобретения может содержать только памоатную соль кетамина в качестве активного ингредиента для применения в анестезии и лечения заболевания ЦНС. Другими словами, памоатная соль кетамина может служить единственным активным ингредиентом, который является анестетиком и предотвращает или лечит заболевание ЦНС в композиции. В этом варианте осуществления настоящее изобретение относится к безопасной и эффективной терапии для лечения заболевания ЦНС или анестезии с использованием только памоатной соли кетамина в качестве активного ингредиента. Альтернативно, в другом варианте осуществления изобретения фармацевтическая композиция может включать в себя или вводиться субъекту в комбинации с другим активным ингредиентом, при условии, что эффект настоящего изобретения не ингибируется.
В одном варианте осуществления изобретения терапевтический эффект, обеспечиваемый памоатными солями кетамина настоящего изобретения, наступает в течение 24 часов после введения фармацевтической композиции. В другом варианте осуществления изобретения памоатные соли кетамина настоящего изобретения проявляют терапевтический эффект, продолжающийся, по меньшей мере, 24 часа, по меньшей мере, два дня, по меньшей мере, одну неделю, по меньшей мере, десять дней или, по меньшей мере, две недели.
Для иллюстрации настоящего изобретения были использованы различные примеры. Приведенные ниже примеры не следует рассматривать как ограничение объема настоящего изобретения.
Примеры
Пример 1. Получение S- и R-энантиомеров кетамина памоата.
Процесс получения S-кетамина памоата и R-кетамина памоата показан на Схеме 1 ниже.
Схема 1:
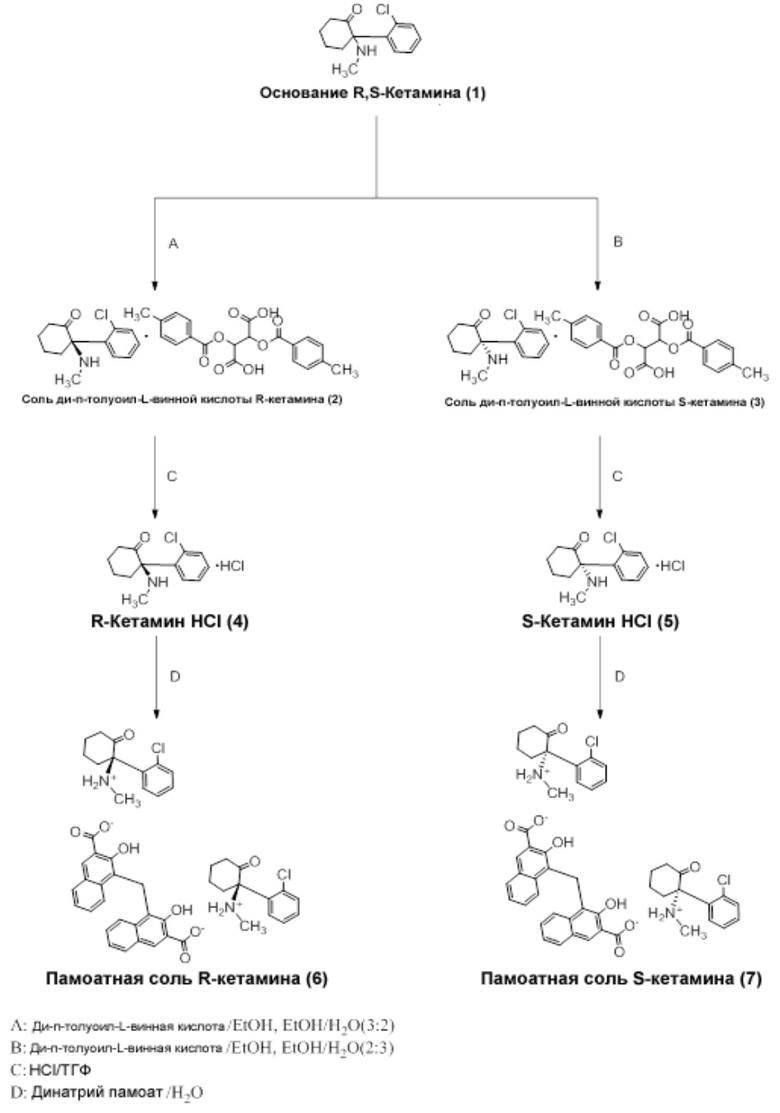
Пример 1-1. Получение свободного основания R,S-кетамина (1)
10 г R,S-кетамина гидрохлорида растворяли в 100 мл воды, а затем добавляли 150 мл насыщенного водного раствора бикарбоната натрия при перемешивании в течение 10 минут. Реакционную смесь экстрагировали дихлорметаном (100 мл × 2). Разделенные органические слои объединяли и перегоняли при пониженном давлении с получением свободного основания R,S-кетамина (1).
Пример 1-2. Получение соли (-)-O,O’-ди-п-толуоил-L-винной кислоты R-кетамина (2)
Ди-п-толуоил-L-винную кислоту (13 г, 33,6 ммоль) и свободное основание R,S-кетамина (8 г, 33,6 ммоль) растворяли в этаноле (EtOH, 160 мл) при перемешивании в течение 5 мин. К раствору по каплям добавляли 10 мл воды при комнатной температуре с последующим перемешиванием в течение 1 часа с получением осадка. Раствор фильтрата собирали после фильтрования с отсасыванием и сушили под вакуумом. Остаток растворяли в 100 мл 60% раствора этанола (т.е. EtOH:H2O = 3:2) при температуре 60°C и охлаждали до комнатной температуры в течение 1 часа с получением твердого вещества с последующей сушкой под вакуумом.
Полученный порошок анализировали с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ), дифференциальной сканирующей калориметрии (ДСК), оптического вращения, спектра ядерного магнитного резонанса (ЯМР) и информации из литературы. Характеристики соли (-)-O,O’-ди-п-толуоил-L-винной кислоты R-кетамина (2) были подтверждена удельным вращением плоскости поляризации, температурой плавления (т.пл.) и хиральной чистотой ВЭЖХ, как показано ниже:
т.пл. = 133,5-141,3°C, [α]25D = -75, c = 1,0, диметилформамид, хиральная чистота = 98,4%. 1H-ЯМР (ДМСО-d6): 7,87 (d, 4H, J = 8,0 Hz), 7,68 (d, 1H, J = 6,8 Hz), 7,44 (m, 3H), 7,36 (d, 4H, J = 8,0 Hz), 5,74 (s, 2H), 2,66-2,32 (m, 2H), 2,39 (s, 6H), 2,04 (s, 3H), 1,90-1,58 (m, 6H).
Пример 1-3. Получение соли (-)-O,O’-ди-п-толуоил-L-винной кислоты S-кетамина (3)
Осадок из Примера 1-2 сушили при пониженном давлении. Твердое вещество растворяли в 100 мл 40% раствора этанола (т.е. EtOH:H2O = 2:3) при температуре 60°C и охлаждали до комнатной температуры в течение 1 часа с получением твердого вещества с последующей сушкой в вакууме.
Полученный порошок анализировали с помощью ВЭЖХ, ДСК, оптического вращения, спектра ЯМР и информации из литературы. Характеристики соли (-)-O,O’-ди-п-толуоил-L-винной кислоты S-кетамина (3) были подтверждены удельным вращением плоскости поляризации, температурой плавления (т.пл.) и хиральной чистотой ВЭЖХ, как показано ниже:
т.пл. = 157,1-163,3°C, [α]25D = -108, c = 1,0, диметилформамид, хиральная чистота = 100%. 1H-ЯМР (ДМСО-d6): 7,87 (d, 4H, J = 7,6 Hz), 7,67 (d, 1H, J = 7,6 Hz), 7,44 (m, 3H), 7,36 (d, 4H, J = 8,0 Hz), 5,74 (s, 2H), 2,64-2,31 (m, 2H), 2,39 (s, 6H), 2,03 (s, 3H), 1,91-1,59 (m, 6H).
Пример 1-4. Получение R-кетамина памоата (6) (кристаллического)
Соль ди-п-толуоил-L-винной кислоты R-кетамина (2) растворяли в десятикратном количестве тетрагидрофурана (ТГФ) при перемешивании при температуре от 2°С до 10°С. К раствору добавляли соляную кислоту (37%), чтобы получить осадок, и осадок собирали фильтрованием с отсасыванием с получением R-кетамина гидрохлорида (4). R-кетамина гидрохлорид (4) и динатрий памоат растворяли отдельно в десятикратном количестве воды. После этого из реакционной смеси отгоняли воду декомпрессией. Остаток растворяли в этаноле при перемешивании при температуре 60°C и перекристаллизовывали при понижении температуры.
Полученный порошок анализировали с помощью ВЭЖХ, ДСК, инфракрасного анализа (ИК), порошковой рентгеновской дифракции (XRD) и ЯМР-спектров. Характеристики кристаллической формы R-кетамина памоата (6) были подтверждены результатами анализа и удельным вращением плоскости поляризации R-кетамина памоата (6) [α]25D = +67
Пример 1-5. Получение S-кетамина памоата (7) (кристаллического)
Соль ди-п-толуоил-L-винной кислоты S-кетамина (3) растворяли в десятикратном количестве тетрагидрофурана (ТГФ) при перемешивании при температуре от 2°С до 10°С. К раствору добавляли соляную кислоту (37%), чтобы получить осадок, и осадок собирали фильтрованием с отсасыванием с получением S-кетамина гидрохлорида (5). S-кетамина гидрохлорид (5) и динатрий памоат растворяли отдельно в десятикратном количестве воды. После этого из реакционной смеси отгоняли воду декомпрессией. Остаток перекристаллизовывали с этанолом при перемешивании при температуре 60°C и выделяли вакуумной фильтрацией.
Полученный порошок анализировали с помощью ВЭЖХ, ДСК, оптического вращения, ИК, XRD и ЯМР-спектров. Характеристики кристаллической формы S-кетамина памоата (7) были подтверждены результатами анализа и удельным вращением плоскости поляризации S-кетамина памоата (7) [α]25D = -67
Пример 1-6. Получение R-кетамина памоата (аморфного)
R-кетамина памоат (6) растворяли в метаноле и растворитель удаляли при пониженном давлении с получением аморфной формы R-кетамина памоата.
Полученный порошок анализировали с помощью ВЭЖХ, ДСК, оптического вращения, ИК, XRD и ЯМР-спектров. Характеристики аморфной формы R-кетамина памоата были подтверждены результатами анализа и удельным вращением плоскости поляризации R-кетамина памоата [α]25D = +67.
Пример 1-7. Получение памоатной соли S-кетамина (аморфной)
S-кетамина памоат (7) растворяли в метаноле и растворитель удаляли при пониженном давлении с получением аморфной формы S-кетамина памоата.
Полученный порошок анализировали с помощью ВЭЖХ, ДСК, оптического вращения, ИК, XRD и ЯМР-спектров. Характеристики аморфной формы S-кетамина памоата были подтверждены результатами анализа и удельным вращением плоскости поляризации S-кетамина памоата [α]25D = -67.
Пример 1-8. Получение R,S-кетамина памоата (кристаллического)
Кетамин HCl и деионизированную воду добавляли с образованием раствора, который добавляли по каплям к водному раствору моногидрата динатрия памоата при перемешивании в круглодонной колбе. Смесь постоянно перемешивали при комнатной температуре в течение 1 часа. Эту реакционную смесь фильтровали, порошок собирали и сушили при пониженном давлении. Полученный порошок анализировали с помощью ВЭЖХ, ДСК, ИК, XRD и ЯМР-спектров
Пример 1-9. Получение R,S-кетамина памоата (аморфного)
Порошки, собранные в Примере 1-8, растворяли в метаноле. Далее растворитель удаляли при пониженном давлении и сушили с получением аморфной формы R,S-кетамина памоата. Полученный порошок анализировали с помощью ВЭЖХ, ДСК, ИК, XRD и ЯМР-спектров
Пример 2. Характеристика кетамина памоата.
Памоатная соль кетамина памоата, полученная в примере 1, была кристаллической или аморфной. Полученные с помощью поляризационного микроскопа Olympus CX41 изображения таких плотных кристаллических и некристаллических порошков показаны на фигуре 1А и 1Б соответственно.
Кроме того, характеристики R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата в аморфной или кристаллической форме анализировали с помощью ВЭЖХ (HPLC), ДСК, ИК, XRD и ЯМР-спектров. Процесс таких анализов и характеристики кетамина памоата подробно описаны ниже
Пример 2-1. XRPD анализ
Порошковую рентгеновскую дифрактограмму (XRPD) получали на порошковом рентгеновском дифрактометре Bruker D8 Discover, оборудованном источником излучения CuKα с длиной волны (λ = 1,54056 Å), работающим при 40 кВ и 40 мА.
Каждый образец сканировали в диапазоне от 2 до 80 по 2θ, с шагом 0,02 по 2θ и скоростью сканирования 0,6 секунды/шаг. Положения угловых пиков в 2θ и соответствующие данные I/Io для всех кристаллических форм пиков кетамина памоата с интенсивностями, равными или превышающими 10% от наибольшего пика, приведены в Таблице 1 ниже.
Кристаллические формы и аморфные формы солей S-кетамина памоата, R-кетамина памоата и R,S-кетамина памоата были охарактеризованы методом XRD, и результаты представлены на фигурах 2A-2F.
Таблица 1. Пики дифракции рентгеновских лучей кристаллических форм R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата.
Пример 2-2. ЯМР анализ
Соли R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата растворяли в дейтериевом растворителе (ДМСО), и спектры ЯМР получали с использованием спектрометра ЯМР Bruker Ascend TM 400 МГц.
Характеристики солей R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата были подтверждены с помощью 1H-ЯМР-спектроскопии (как показано в Таблице 2 и на фигурах 3A-3C). Кроме того, S-кетамина памоат и R-кетамина памоат подвергали 13С-ЯМР-спектроскопии, и химические сдвиги были представлены в м.д. (как показано в Таблице 3 и на фигурах 4A и 4B).
Таблица 2. Данные 1H-ЯМР (400 МГц, ДМСО) для R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата
(Кристалл.)
(δм.д.)
Таблица 3. Данные 13С-ЯМР (100 МГц, ДМСО) для S-кетамина памоата и R-кетамина памоата
(Кристалл.)
(δ м.д.)
Пример 2-3. Анализ при помощи инфракрасной спектроскопии с Фурье-преобразованием (Фурье-ИК)
Полиморфы кетамина памоата были дополнительно охарактеризованы с помощью инфракрасной (ИК) спектроскопии, полученной на диске с использованием системы Bruker FPA-FTIR Vertex 70V, Hyperion 3000, и результаты показаны на фигурах 5А-5Е. ИК-поглощения (в волновых числах, см-1), достаточные для идентификации кристаллических и аморфных форм S-, R-энантиомеров кетамина памоата, представлены в Таблице 4 ниже.
Таблица 4. Пики Фурье-ИК S-кетамина памоата, R-кетамина памоата и R,S-кетамина памоата
см-1
см-1
см-1
см-1
см-1
Пример 2-4. ДСК анализ
Анализ методом дифференциальной сканирующей калориметрии (ДСК) образцов R,S-кетамина памоата, S-кетамина памоата и R-кетамина памоата показал стеклование при температуре примерно 233°С, 212°С и 214°С, что указывает на то, что такие образцы имели кристаллическую форму. (см. Фигуры 6A-6C). ДСК анализ образца R,S-кетамина памоата показал стеклование при температуре приблизительно 213°C, что указывает на то, что этот образец был аморфным (см. Фигуру 6D). ДСК анализ образцов S-кетамина памоата и R-кетамина памоата показал стеклование при температуре примерно 210°C и 193°C, что указывает на то, что эти образцы были аморфными (см. Фигуры 6E и 6F). ДСК анализ выполняли с использованием прибора Mettler Toledo DSC3 в стандартных условиях.
Результаты ДСК анализа кристаллических форм S-,R-энантиомеров и рацемической формы кетамина памоата приведены в Таблице 5 ниже.
Таблица 5. Пики ДСК анализа S-кетамина памоата и R-кетамина памоата
Пример 2-5. ВЭЖХ анализ
Хиральная чистота S-кетамина памоата или R-кетамина памоата была получена с использованием системы высокоэффективной жидкостной хроматографии (ВЭЖХ) Agilent 1260 Infinity II с хиральной колонкой (Agilent Poroshell 120 Chiral-V 2,7 мкм, 4,6 x 150 мм) в стандартных условиях. Для ВЭЖХ анализа хиральная чистота S-формы составляла 100% (время удерживания (RT): 9,0 мин), а хиральная чистота R-формы составляла 100% (RT: 9,5 мин). Результаты ВЭЖХ анализа S-кетамина памоата, R-кетамина памоата и R,S-кетамина памоата показаны на фигурах 7А-7С.
Пример 2-6. Анализ по методу Карла Фишера
Анализ титрованием по Карлу Фишеру показал, что образцы, использованные в этих примерах, не содержали воды и не были гидратированной формой (содержание воды: 0,329% для кетамина памоата). Анализ по методу Карла Фишера был выполнен с использованием прибора Metrohm 870 KF Titrino plus в стандартных условиях
Пример 3. Антидепрессантное действие in vivo.
Животную модель индуцированного дексаметазоном (далее сокращенно DEX) состояния подобного депрессии, использовали для оценки антидепрессантных свойств кетамина HCl (KET), R,S-кетамина памоата (KEP), S-кетамина памоата (S-KEP) и R-кетамина памоата (R-KEP) в эквивалентной дозе (120 мг/кг свободного основания кетамина). Протокол этого исследования показан на фигуре 8 и описан ниже.
Новорожденным мышам ICR (BioLASCO, Тайбэй, Тайвань) внутрибрюшинно вводили физиологический раствор или DEX в постнатальные дни 1, 2 и 3 (P1, P2 и P3) в дозах 0,5 мг/кг, 0,3 мг/кг и 0,1 мг/кг, соответственно. Мыши, получавшие физиологический раствор, были контрольной группой, и мышей, получавших DEX, разделили на группы KET, KEP, S-KEP, R-KEP и физиологический раствор (n = от 10 до 14 мышей в каждой группе). Затем мышам соответствующих групп подкожно вводили препараты на 35-й постнатальный день, в то время как мышам контрольной группы и группы физраствора вводили равные объемы 0,9% физиологического раствора. Препараты для введения готовили в фосфатно-солевом буфере (ФСБ), а затем перед инъекцией хорошо перемешивали на высокоскоростном вортексе.
Антидепрессантное действие оценивали с помощью теста принудительного плавания (FST), который выполняли в день 1 после введения препарата (P36) и день 10 после введения препарата (P45). Мышей всех групп перед введением препарата обучали плаванию. Во время FST мышей по отдельности помещали в стеклянные цилиндры объемом 5 л (высота 27 см, диаметр 18 см), наполненные 4 л воды (температура 23 ± 1°C). Наблюдалась общая продолжительность времени неподвижности в течение 5 минут в FST. Результаты представлены как среднее значение ± стандартная ошибка среднего. T-критерий Стьюдента использовали для анализа группы физиологического раствора (группа мышей, получавших DEX, которым вводили физиологический раствор), по сравнению с другими группами в каждый момент времени. *p<0,05, **p<0,01 и ***p<0,001 указывают на значимые различия по сравнению с группой, получавшей физиологический раствор.
Мыши, которые после рождения подверглись воздействию DEX, показали значительное увеличение времени неподвижности в FST по сравнению с контрольной группой. Результаты FST на фигуре 9 показывают, что все KET, KEP, S-KEP и R-KEP снижали время неподвижности в день 1 и день 10 после введения, которое было увеличено у мышей, получавших DEX.
Кроме того, седативное поведение также оценивали по балльной шкале седативного поведения у грызунов (Таблица 6) сразу после введения препарата в течение 14 дней. Как показано на фигуре 10, мыши в группе KET сразу после инъекции показали тяжелое седативное поведение, и этот эффект полностью восстановился через 2 часа после введения. Мыши, получавшие KEP, S-KEP и R-KEP, показали нормальное поведение в период от 0 до 14 дней после инъекции.
Таблица 6. Содержание балльной шкалы седативного поведения у грызунов.
Как следствие, все KET, KEP, S-KEP и R-KEP показали быстрое начало антидепрессивного действия в FST после однократной инъекции в эквивалентной дозе (120 мг/кг свободного основания кетамина), и этот эффект длился как минимум 10 дней у мышей, получавших DEX. Неожиданно, но в группах KEP, S-KEP и R-KEP седативный эффект или другие психотомиметические эффекты, связанные с кетамином, и расстройства нервной системы не возникали после введения, что означает, что KEP, S-KEP и R-KEP обладаютещё одним полезным свойством для применения в качестве антидепрессанта по сравнению с КЕТ
Пример 4. Токсикологическое исследование повторных доз in vivo
Было проведено трехмесячное токсикологическое исследование с повторной дозой у 10-недельных самок крыс линии Спрег-Доули (SD) (BioLASCO, Тайбэй, Тайвань) для оценки реакций токсичности кетамина HCl (KET) и R,S-кетамина памоата (KEP) в эквивалентной общей дозе (1440 мг/кг свободного основания кетамина) в течение 12 недель. Протокол этого исследования показан на фигуре 11 и описан ниже.
Крысам группы КЕТ подкожно вводили кетамин HCl в дозе 60 мг/кг массы тела два раза в неделю в течение 12 недель. Доза 60 мг/кг для подкожной инъекции была выбрана потому, что экспериментально было установлено, что более высокая доза является летальной для крыс. Крысам контрольной группы подкожно вводили эквивалентное количество (как в группе КЕТ) 0,9% физиологического раствора. Крысы группы КЕР получали подкожно R,S-кетамина памоат в дозе 480 мг/кг массы тела в месяц в течение 12 недель. Всех животных умерщвляли для окончательного токсикологического анализа.
При оценке места инъекции у крыс, получавших кетамин HCl, наблюдалась эритема в месте инъекции, которая постепенно превращалась в открытую рану после введения, тогда как крысы в контрольной группе и группе KEP имели нормальную поверхность кожи после инъекций.
При гистопатологическом анализе в местах инъекции KET выявили морфологические повреждения эпидермиса, дермы, подкожной ткани и мышечной ткани (Фигура 12A), а инфильтрация воспалительных клеток в соединительных тканях была обнаружена на изображениях с большим увеличением (Фигуры 12C и 12E). Для группы KEP гистопатологический анализ показал нормальную морфологию срезов кожи в местах инъекции (Фигура 12B). С помощью изображений с большим увеличением было также обнаружено, что KEP вызывает инфильтрацию воспалительных клеток в соединительных тканях; однако плотность воспалительных клеток в полях зрения микроскопа была намного меньше, чем в группе KET (Фигуры 12D и 12F). При 400-кратном увеличении поля (Фигура 12F) было обнаружено, что место инъекции в группе KEP имело некоторые очаговые пустые кистоподобные пространства, в которых могли существовать частицы R,S-кетамина памоата, которые были диффундированы или элиминированы в кровеносную систему. Частицы кетамина памоата не вызывали агрегации или инкапсуляции воспалительных клеток.
Сообщалось, что злоупотребление кетамином вызывает цистит мочевого пузыря [26]; поэтому в этом примере также был проведен гистопатологический анализ тканей мочевого пузыря. Эпителиальные поверхности апикальной части мочевого пузыря были шероховатыми в контрольной группе и группе KEP (Фигуры 13A и 13C; увеличение: x400), но гладкими в группе KET (Фигура 13B; увеличение: x400). Кроме того, контрольная группа и группа KEP имели тонкие складки слизистой оболочки (Фигуры 13D и 13F; увеличение: x40), тогда как группа KET имела выступающие и увеличенные складки слизистой оболочки (Фигура 13E; увеличение: x40), что указывает на распространение фиброза в соединительной ткани.
Для оценки центральной нервной системы срезы головного мозга крыс собирали для макроскопического патологического исследования. В префронтальной коре не было гранулярных клеток, и морфология пирамидных клеток у крыс группы KET изменилась на маленькие или сморщенные, как в процессе деградации (Фигуры 14B и 14E). С другой стороны, морфология нейронов в префронтальной коре головного мозга контрольных крыс и крыс группы KEP была нормальной (Фигуры 14A, 14C, 14D и 14F).
Как следствие, максимальная переносимая доза (МПД) KET при подкожной инъекции составляла 60 мг/кг свободного основания кетамина у крыс. Однократная подкожная инъекция KEP в концентрации 480 мг/кг свободного основания кетамина была выше, чем доза LD50 кетамина (229 мг/кг), и хорошо переносилась крысами. Субхроническое лечение высокими дозами KEP в течение 12 недель у крыс не вызывало патологических изменений мочевого пузыря и головного мозга, тогда как у крыс KET наблюдались изменения, включая фиброз мочевого пузыря и изменение морфологии нейронов в головном мозге. Согласно этим результатам, KEP определенно имел гораздо меньше токсических эффектов, чем KET в общей эквивалентной дозе
Пример 5. Оценка места инъекции in vivo
Целевое исследование in vivo для оценки реакции места инъекции KEP было проведено на собаках породы бигль (KITAYAMA LABES, CO., LTD. Ina, Япония). Четырем самцам собак вводили KEP в эквивалентной дозе (44 мг/кг свободного основания кетамина). Для оценки реакций в месте инъекции на 1, 2, 4, 8 и 15 день после введения KEP использовали шкалу оценки эритемы/струпа кожи Дрейза (Таблица 7 ниже).
Таблица 7. Шкала оценки эритемы/струпа кожи Дрейза
Предыдущее токсикологическое исследование повторной дозы на крысах доказало, что KEP имеет меньшую реакцию в месте инъекции как при местном наблюдении, так и при патологическом анализе. Этот пример продемонстрировал дополнительные подтверждающие доказательства безопасности KEP у собак в месте инъекции. По оценке по шкале Дрейза, у всех четырех собак породы бигль не наблюдалась эритема в местах инъекции с 1 по 15 день после введения однократной высокой дозы KEP (Таблица 8).
Таблица 8. Оценка места инъекции у отдельного животного по шкале оценки эритемы/струпа кожи Дрейза.
Исходя из вышеизложенного, соли кетамина, включая R,S-кетамина памоат, S-кетамина памоат и R-кетамина памоат, и их полиморфы, представленные в настоящем изобретении, обладают быстрым началом действия и аналогичным антидепрессантным действием, как кетамина гидрохлорид.
Неожиданно антидепрессантное действие не сопровождается седативным поведением у мышей, получавших R,S-кетамина памоат, S-кетамина памоат и R-кетамина памоат, тогда как седативный эффект сразу возникает у мышей, получавших кетамин HCl и длится в течение 2 часов после введения. Субхроническая токсичность введения R,S-кетамина памоата в течение 12 недель у крыс не вызывает патологических изменений мочевого пузыря и головного мозга, тогда как крысы, получавшие кетамина гидрохлорид, имеют изменения, включая фиброз мочевого пузыря и изменение морфологии нейронов в головном мозге. Кроме того, R,S-кетамина памоат имеет более мягкую реакцию в месте подкожной инъекции по сравнению с кетамина гидрохлоридом.
Эти результаты показывают, что соли кетамина и его полиморфы, представленные в настоящем изобретении, имеют меньше побочных эффектов и более высокую переносимую дозу, то есть имеют более высокую безопасность, чем кетамин HCl, и, таким образом, пригодны для фармацевтического применения.
Хотя некоторые из вариантов осуществления настоящего изобретения были подробно описаны выше, тем не менее, специалисты в данной области техники могут внести различные модификации и изменения в приведенные конкретные варианты осуществления изобретения без существенного отступления от идеи и преимуществ настоящего изобретения. Такие модификации и изменения входят в объем настоящего изобретения, как изложено в прилагаемой формуле изобретения.
Ссылки:
[1] Wang, R., Zhang, Z., Kumar, M., Xu, G., & Zhang, M. (2019) Neuroprotective potential of ketamine prevents developing brain structure impairment and alteration of neurocognitive function induced via isoflurane through the PI3K/AKT/GSK-3β pathway. Drug Design, Development and Therapy, 13: 501-512.
[2] Ferro, M.M., Angelucci, M.E.M., Anselmo-Franci, J.A., Canteras, N.S., & Da Cunha, C. (2007) Neuroprotective effect of ketamine/xylazine on two rat models of Parkinson’s disease. Brazilian Journal of Medical and Biological Research, 40(1): 89-96.
[3] Sakai, T., Ichiyama, T., Whitten, C.W., Giesecke A.H., & Lipton J.M. (2000) Ketamine suppresses endotoxin-induced NF-kB expression. Can. J. Anesth., 47: 1019-1024.
[4] Zanos, P., Moaddel, R., Morris, P.J., Riggs, L.M., Highland, J.N., Georgiou, P., Pereira E.F.R., Albuquerque E.X., & Thomas C.J., Zarate C.A. Jr., Gould T.D. (2018) Ketamine and Ketamine Metabolite Pharmacology: Insights into Therapeutic Mechanisms. Pharmacological Reviews, 70(3): 62-660.
[5] Kenji Hashimoto (2019) Application of R-ketamine and salt thereof as pharmaceuticals. US Patent No. 10,406,121 B2.
[6] Guitton M., Puel J.L., & Pujol R. (2012) Methods for the treatment of tinnitus induced by cochlear excitotoxicity. US Patent No. 8,268,866 B2.
[7] Diazgranados N., Ibrahim L., Brutsche N.E., Newberg A., Kronstein P., Khalife S., Kammerer W.A., Quezado Z., Luckenbaugh D.A., Salvadore G., Machado-Vieira R., Manji H.K., & Zarate C.A. Jr. (2010) A randomized add-on trial of an N-methyl-D-aspartate antagonist in treatment-resistant bipolar depression. Arch. Gen. Psychiatry, 67: 793-802.
[8] Bloch M.H., Wasylink S., Landeros-Weisenberger A., Panza K.E., Billingslea E., Leckman J.F., Krystal J.H., Bhagwagar Z., Sanacora G., & Pittenger C. (2012) Effects of ketamine in treatment-refractory obsessive-compulsive disorder. Biol. Psychiatry, 72(II): 964-970.
[9] Rodriguez C.I., Kegeles L.S., Levinson A., Feng T., Marcus S.M., Vermes D., Flood P., & Simpson H.B. (2013) Randomized controlled crossover trial of ketamine in obsessive-compulsive disorder: proof-of-concept. Neuropsychopharmacology, 38: 2475-83.
[10] Feder A., Parides M.K., Murrough J.W., Perez A.M., Morgan J.E., Saxena S., Kirkwood K., Aan Het Rot M., Lapidus K.A., Wan L.B., Losifescu D., & Charney D.S. (2014) Efficacy of intravenous ketamine for treatment of chronic posttraumatic stress disorder: a randomized clinical trial. JAMA Psychiatry, 71: 681-688.
[11] DiazGranados N., Ibrahim L.A., Brutsche N.E., Ameli R., Henter I.D., Luckenbaugh D.A., Machado-Vieira R., Zarate C.A. Jr. (2010) Rapid resolution of suicidal ideation after a single infusion of an N-methyl-D-aspartate antagonist in patients with treatment-resistant major depressive disorder. J. Clin. Psychiatry 71(12): 1605-1611.
[12] Wink L.K., O’Melia A.M., Shaffer R.C., Pedapati E., Friedmann K., Schaefer T., & Erickson C.A. (2014) Intranasal ketamine treatment in an adult with autism spectrum disorder. J. Clin. Psychiatry, 75(8): 835-836.
[13] Krystal J.H., Sanacora G., & Duman R.S. (2013) Rapid-acting glutamatergic antidepressants: the path to ketamine and beyond. Biol. Psychiatry, 73: 1133-1141.
[14] Domino E.F. (2010) Taming the ketamine tiger. 1965. Anesthesiology, 113: 678-686.
[15] Lauritsen, C., Mazuera, S., Lipton, R.B., & Ashina, S. (2016) Intravenous ketamine for subacute treatment of refractory chronic migraine: a case series. The Journal of Headache and Pain, 17(1): 106.
[16] Goyal, S. & Agrawal, A. (2013) Ketamine in status asthmaticus: A review. Indian journal of critical care medicine: peer-reviewed, official publication of Indian Society of Critical Care Medicine, 17(3): 154-161.
[17] Taylor, J.H., Landeros-Weisenberger, A., Coughlin, C., Mulqueen, J., Johnson, J. A., Gabriel, D., Reed M.O., Jakubovski E. & Bloch, M.H. (2018) Ketamine for social anxiety disorder: a randomized, placebo-controlled crossover trial. Neuropsychopharmacology, 43(2): 325-333.
[18] Jones, J.L., Mateus, C.F., Malcolm, R.J., Brady, K.T., & Back, S.E. (2018) Efficacy of ketamine in the treatment of substance use disorders: a systematic review. Frontiers in Psychiatry, 9: 277.
[19] Synowiec A.S., Singh D.S., Yenugadhati V., Valeriano J.P., Schramke C.J., & Kelly K.M. (2013) Ketamine use in the treatment of refractory status epilepticus. Epilepsy Research. 105(1-2): 183-188.
[20] Proescholdt M., Heimann A. & Kempski O. (2001). Neuroprotection of S(+) ketamine isomer in global forebrain ischemia. Brain Research, 904(2): 245-251.
[21] Mills, I., Park, G. & Manara, A. & Merriman, R. (1998). Treatment of compulsive behaviour in eating disorders with intermittent ketamine infusions. QJM: Monthly Journal of the Association of Physicians, 91: 493-503.
[22] Lascelles K., Marzano L., Brand F., Trueman H., McShane R.M.D., & Hawton K. (2019) Effects of ketamine treatment on suicidal ideation: a qualitative study of patients’ accounts following treatment for depression in a UK ketamine clinic. BMJ Open, 9: e029108.
[23] Canuso C.M., Singh J.B., Fedgchin M., Alphs L., Lane R., Lim P., Pinter C., Hough D., Sanacora G., Manji H. & Drevets W.C. (2018) Efficacy and safety of intranasal esketamine for the rapid reduction of symptoms of depression and suicidality in patients at imminent risk for suicide: results of a double-blind, randomized, placebo-controlled study. American Journal of Psychiatry, 175(7): 620-630.
[24] Jassen Research and Development, LLC. (2019). Esketamine nasal spray for patients with treatment-resistant depression. US FDA Advisory Committee Briefing Document.
[25] Li, Q., Chan, W.M., Rudd, J.A., Wang, C.M., Lam, P.Y., Wai, M.S., Wood, D.M., Dargan, P.I., & Yew, D.T. (2013). Novel psychoactive substances: classification, pharmacology and toxicology. Book 2013. Chapter 12 - Ketamine.
[26] Jhang, J., Hsu, Y. & Kuo, H. (2015) Possible pathophysiology of ketamine‐related cystitis and associated treatment strategies. Int. J. Urol., 22: 816-825.







Изобретение относится к памоатной соли кетамина, имеющей стехиометрическое отношениекетамина к памоату 2:1, которая представляет собой памоатную соль R,S-кетамина, представленную ниже структурной формулой (I), памоатную соль S-кетамина, представленную ниже структурной формулой (II), или памоатную соль R-кетамина, представленную ниже структурной формулой (III). Изобретение относится к способу лечения заболевания центральной нервной системы (ЦНС), включающему в себя введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции, где фармацевтическая композиция содержит памоатную соль кетамина по изобретению её фармацевтически приемлемое вспомогательное вещество. Также изобретение относится к способу анестезии нуждающегося в этом субъекта, включающий в себя введение субъекту эффективного количества фармацевтической композиции, где фармацевтическая композиция содержит памоатную соль кетамина по изобретению и её фармацевтически приемлемое вспомогательное вещество. Технический результат – памоатная соль кетамина для фармацевтического применения. 3 н. и 8 з.п. ф-лы, 14 ил., 8 табл., 5 пр.
 (I),
(I), 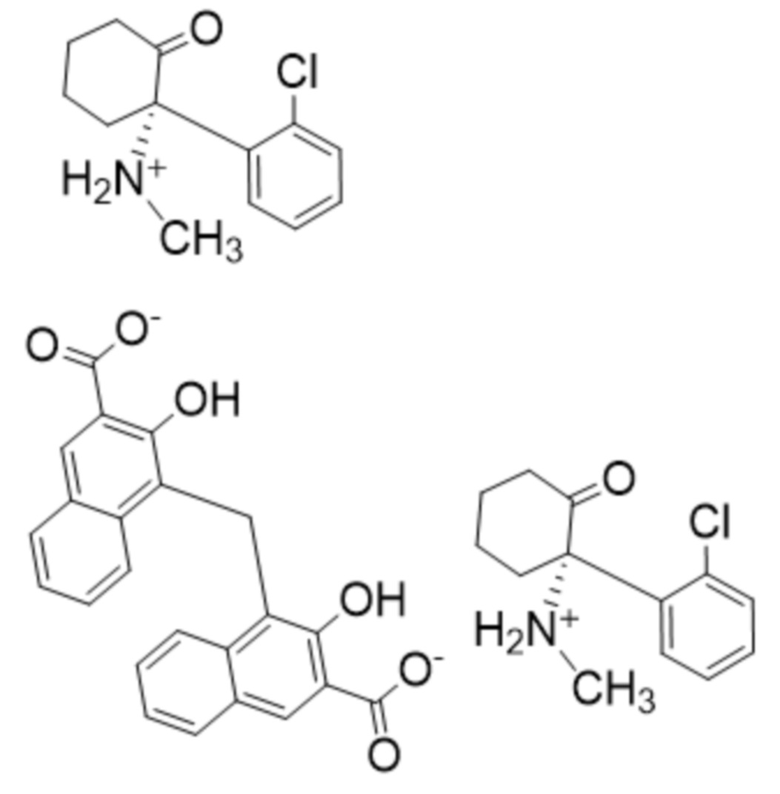 (II),
(II), 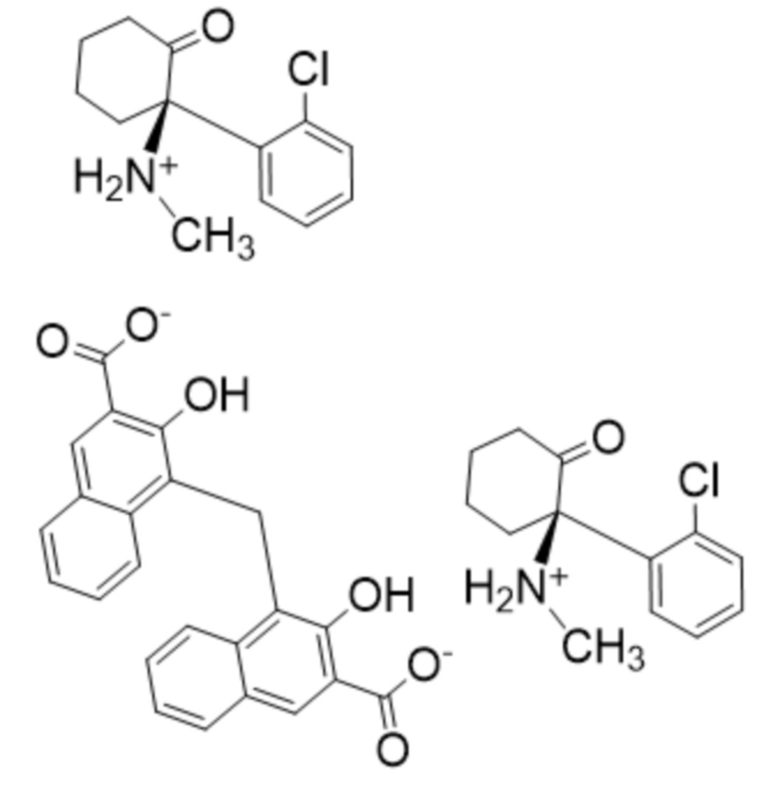
1. Памоатная соль кетамина, имеющая стехиометрическое отношение кетамина к памоату 2:1, которая представляет собой:
памоатную соль R,S-кетамина, представленную ниже структурной формулой (I):
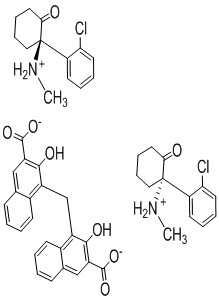 (I);
(I);
памоатную соль S-кетамина, представленную ниже структурной формулой (II):
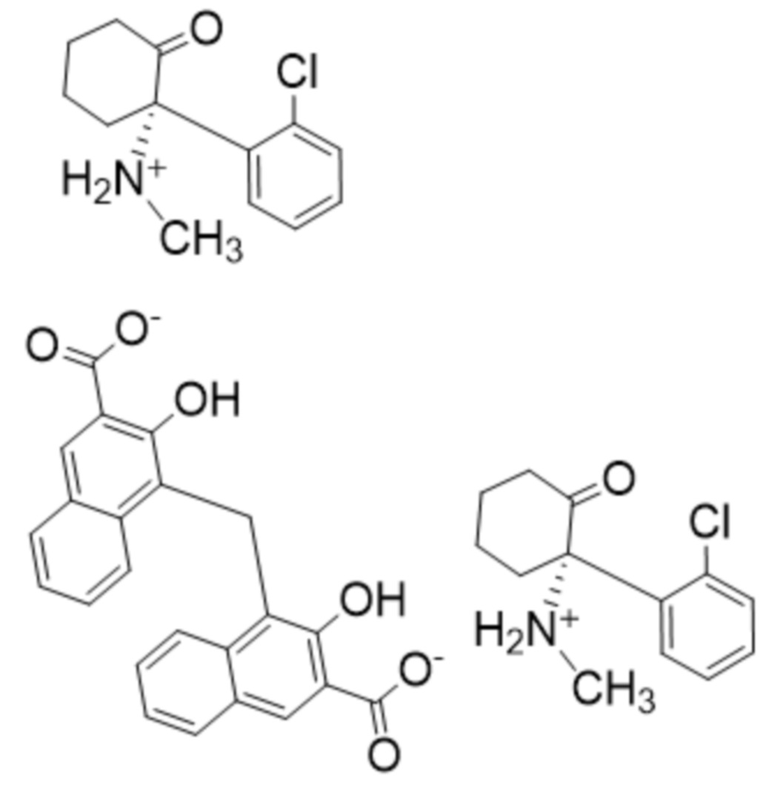 (II); или
(II); или
памоатную соль R-кетамина, представленную ниже структурной формулой (III):
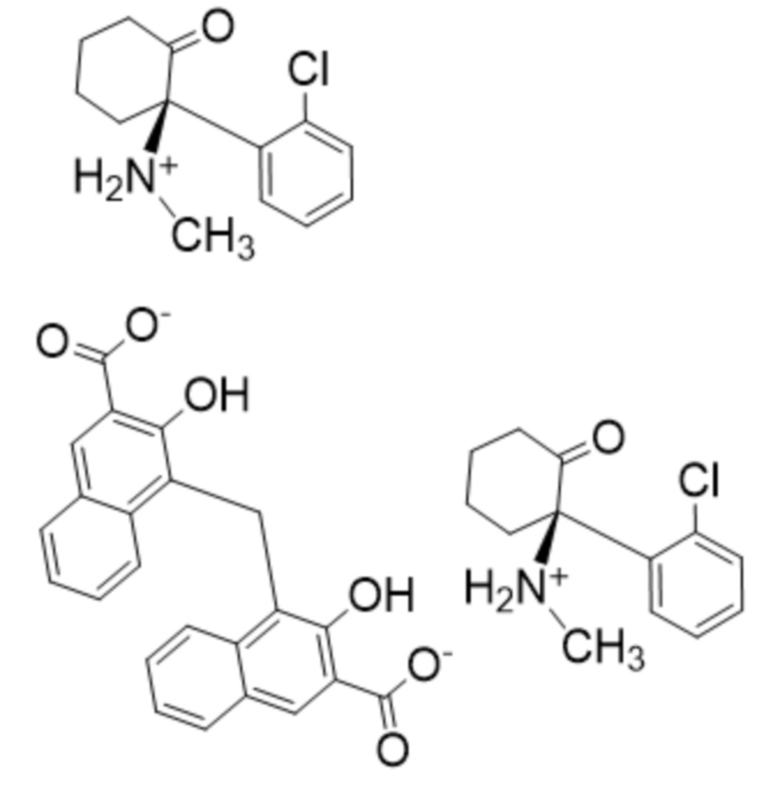 (III).
(III).
2. Памоатная соль кетамина по п. 1, которая является аморфной.
3. Памоатная соль кетамина по п. 1, которая является кристаллической, имеющей порошковую рентгеновскую дифрактограмму (XRPD), содержащую значения 2θ ± 0,2 2θ, выбранные из 6,0, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 19,6, 22,2, 25,2 и 30,3.
4. Памоатная соль кетамина по п. 1, где памоатная соль R,S-кетамина является кристаллической, имеющей дифрактограмму XRPD, представленную по меньшей мере одним из следующего:
(i) дифрактограмма XRPD, содержащая значения 2θ ± 0,2 2θ, выбранные из 6,0, 8,6, 10,7, 11,6, 12,0, 13,0, 14,7, 15,0, 15,3, 17,9, 18,6, 19,6, 20,0, 21,1, 21,6, 22,2, 23,3, 24,4, 25,2, 25,9, 26,9, 28,6, 29,7, 30,3, 32,4, 34,0 и 36,6; и
(ii) дифрактограмма XRPD, показанная на фигуре 2А.
5. Памоатная соль кетамина по п. 1, где памоатная соль S-кетамина является кристаллической, имеющей дифрактограмму XRPD, представленную по меньшей мере одним из следующего:
(i) дифрактограмма XRPD, содержащая значения 2θ ± 0,2 2θ, выбранные из 6,0, 10,8, 11,7, 12,0, 12,6, 13,1, 14,6, 15,1, 18,2, 19,2, 19,7, 20,1, 22,0, 22,8, 23,3, 23,7, 24,1, 24,7, 25,2, 27,3, 30,1, 31,6, 45,4, 56,4 и 75,2; и
(ii) дифрактограмма XRPD, показанная на фигуре 2B.
6. Памоатная соль кетамина по п. 1, где памоатная соль R-кетамина является кристаллической, имеющей дифрактограмму XRPD, представленную по меньшей мере одним из следующего:
(i) дифрактограмма XRPD, содержащая значения 2θ ± 0,2 2θ, выбранные из 6,0, 10,8, 11,7, 12,0, 12,6, 13,1, 14,6, 15,0, 18,2, 19,3, 19,7, 20,6, 22,0, 22,9, 23,6, 24,1, 24,7, 25,2, 25,9, 27,3, 30,1, 31,6, 45,4, 56,4 и 75,2; и
(ii) дифрактограмма XRPD, показанная на фигуре 2С.
7. Памоатная соль кетамина по любому из пп. 1-6, которая имеет чистоту более 95%.
8. Способ лечения заболевания центральной нервной системы (ЦНС), включающий в себя введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции, где фармацевтическая композиция содержит памоатную соль кетамина по любому из пп. 1-6 и её фармацевтически приемлемое вспомогательное вещество.
9. Способ по п. 8, где заболевание ЦНС выбрано из группы, состоящей из большого депрессивного расстройства (БДР), БДР с неизбежным риском суицидальных мыслей, терапевтически резистентной депрессии (ТРД), биполярного расстройства, обсессивно-компульсивного расстройства, посттравматического стрессового расстройства (ПТСР), расстройства аутистического спектра, шума в ушах, рефракторной хронической мигрени, астмы, беспокойства, расстройств, связанных с употреблением психоактивных веществ, расстройства, связанного с употреблением алкоголя, расстройств пищевого поведения, рефракторного эпилептического статуса, ишемии головного мозга, болезни Альцгеймера, болезни Паркинсона, инсульта, черепно-мозговой травмы, рассеянного склероза и боли.
10. Способ анестезии нуждающегося в этом субъекта, включающий в себя введение субъекту эффективного количества фармацевтической композиции, где фармацевтическая композиция содержит памоатную соль кетамина по любому из пп. 1-6 и её фармацевтически приемлемое вспомогательное вещество.
11. Способ по любому из пп. 8-10, где лечение заболевания ЦНС или начало действия анестезии наступает в течение 24 часов и продолжается в течение по меньшей мере 10 дней после введения фармацевтической композиции.
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| CN 106562952 A, 19.04.2017 | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Richard J.Bastin et al.: "Salt selection and Optimisation Procedures for Pharmaceutical New Chemical Entities", ORGANIC PROCESS RESEARCH & DEVELOPMENT, 2000, vol.4, p.427-435 | |||
| THACKABERRY E.A.et al.: "Non-clinical toxicological | |||
Авторы
Даты
2024-08-26—Публикация
2020-01-10—Подача