ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет предварительной заявки США № 62/833,875, поданной 15 апреля 2019 года, содержание которой включено в настоящий документ посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка содержит Перечень последовательностей, который был представлен в электронном виде в виде файла.txt под названием «2012538-0082_SL.txt». Файл.txt был создан 10 апреля 2020 года и имеет размер 26 104 байта. Все содержание Перечня последовательностей включено в настоящий документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0003] Существует ряд заболеваний человека, которые могут быть связаны с изменениями в ДНК, которые либо наследуются, либо приобретаются на ранних стадиях эмбрионального развития. Особый интерес для разработчиков генетической терапии (также называемой «генной терапией») представляют заболевания, вызванные мутацией в одном гене, известные как моногенные заболевания. Считается, что существует более 6 000 моногенных заболеваний. Как правило, каждое конкретное генетическое заболевание, вызванное наследственными мутациями, встречается относительно редко, но в совокупности число заболеваний, связанных с генетикой, велико. Известные генетические заболевания включают муковисцидоз, мышечную дистрофию Дюшенна, болезнь Хантингтона и серповидно-клеточную анемию. Другие классы генетических заболеваний включают нарушения обмена веществ, такие как органические ацидемии, и лизосомальные болезни накопления, когда дисфункциональные гены приводят к дефектам метаболических процессов и накоплению токсичных побочных продуктов, которые могут привести к серьезной заболеваемости и смертности как в краткосрочной, так и в долгосрочной перспективе.
[0004] В то время как генной терапии уделяется большое внимание в плане разработки терапевтических кандидатов, гораздо меньше внимания уделяется способам мониторинга и оценки эффективности и траектории генной терапии. Необходимы новые способы и композиции для обеспечения эффективного применения генной терапии, в том числе в сочетании с одним или несколькими дополнительными способами лечения.
Сущность изобретения
[0005] Настоящее раскрытие предоставляет, среди прочего, технологии для улучшения генной терапии. Среди прочего, настоящее раскрытие предоставляет технологии, позволяющие проводить мониторинг и/или оценку одной или более характеристик лечения генной терапией, таких как, например, степень, уровень и/или постоянство экспрессии полезной нагрузки. В некоторых вариантах реализации представленные технологии особенно полезны при интеграционной генной терапии.
[0006] Среди прочего, настоящее раскрытие демонстрирует, что определенные интеграционные технологии генной терапии могут генерировать новые биомаркеры, экспрессия и/или активность которых может высоко коррелировать с экспрессией и/или активностью интересующей полезной нагрузки (например, продукта, кодируемого трансгеном и/или экспрессируемого из него), доставляемой генной терапией. Более того, согласно настоящему раскрытию, такая генерация может обеспечить стратегии для мониторинга и/или иной оценки генной терапии и/или ее успеха, стабильности, поддержания и т.д.
[0007] Среди прочего, в некоторых вариантах реализации изобретения было обнаружено, что раскрытые в настоящее время биомаркеры могут быть оценены непосредственно из биологического образца, взятого неинвазивно у субъекта, получившего генную терапию, и что оценка таких биомаркеров может предоставить информацию о состоянии полезной нагрузки, для определения которой в противном случае потребовались бы более инвазивные процедуры. В качестве одного из примеров, настоящее раскрытие демонстрирует, что для определения доставки или экспрессии полезной нагрузки в ткани не обязательно проводить биопсию ткани. Скорее, анализ биомаркеров из кровообращения (например, через забор крови) может быть оценен для косвенного выявления одного или нескольких аспектов экспрессии и/или активности полезной нагрузки в ткани. Это может упростить и облегчить анализ полезной нагрузки, доставляемой во внутриклеточные локализации.
[0008] В некоторых вариантах реализации настоящее раскрытие предоставляет способы мониторинга генной терапии, способы включают этап обнаружения в биологическом образце от субъекта, который получил интеграционную генную терапию, уровня или активности биомаркера, созданного в результате интеграции интеграционной генной терапии, в качестве суррогата для одной или более характеристик статуса лечения генной терапией, где одна или более характеристик статуса лечения генной терапией выбрана из группы, состоящей из уровня полезной нагрузки, активности полезной нагрузки, уровня интеграции лечения генной терапией в популяцию клеток и их комбинаций.
[0009] В некоторых вариантах реализации настоящее раскрытие предоставляет способы мониторинга доставки, уровня и/или активности полезной нагрузки у субъекта, получившего генно-интеграционную композицию, которая доставляет полезную нагрузку, способы включают этап обнаружения в биологическом образце субъекта уровня или активности биомаркера, созданного в результате интеграции генно-интеграционной композиции, в качестве суррогата доставки, уровня и/или активности полезной нагрузки.
[00010] В некоторых вариантах реализации настоящее раскрытие предоставляет способы определения одной или более характеристик статуса лечения генной терапией у субъекта, который получил лечение средством интеграционной генной терапией, способы включают этапы: а) получение биологического образца от субъекта, b) определение уровня биомаркера, где биомаркер генерируется в результате интеграционной генной терапии в геном субъекта, и c) на основе определенного уровня биомаркера установления одной или более характеристик статуса лечения генной терапией у субъекта, где определенный уровень биомаркера соответствует одной или более характеристикам статуса лечения генной терапией.
[00011] В некоторых вариантах реализации настоящее раскрытие предоставляет способы доставки средства лечения генной терапией нуждающемуся в нем субъекту, включая этапы а) введения лечения интеграционной генной терапией субъекту и b) определения в биологическом образце субъекта уровня биомаркера, который образуется в результате интеграции лечения генной терапией в геном субъекта.
[00012] В некоторых вариантах реализации лечение средством интеграционной генной терапии или генно-интеграционная композиция обеспечивает интеграцию элемента нуклеиновой кислоты, включающего последовательность, которая кодирует полезную нагрузку, в целевой сайт в геноме субъекта. Специалисты в данной области оценят, что любой из множества целевых сайтов может быть подходящим для использования со способами и композициями, описанными в настоящем документе. Например, в некоторых вариантах реализации изобретения целевой сайт кодирует полипептид (например, альбумин). В некоторых вариантах реализации интеграция элемента нуклеиновой кислоты происходит на 5' или 3' конце гена, который кодирует полипептид. В некоторых вариантах реализации изобретения целевой сайт кодирует альбумин.
[00013] В соответствии с различными вариантами реализации изобретения, как описано в настоящем документе, может использоваться любая полезная нагрузка, подходящая для конкретного применения. В некоторых вариантах реализации полезная нагрузка представляет собой или состоит из пептида/полипептида/белка, нуклеиновой кислоты (например, кшРНК, микроРНК) и любой их комбинации. Например, в некоторых вариантах реализации полезная нагрузка представляет собой или включает пептид, экспрессируемый внутриклеточно. В некоторых вариантах реализации полезная нагрузка представляет собой или включает пептид, секретируемый внутриклеточно. В некоторых вариантах реализации полезная нагрузка представляет собой пептид, обладающий внутриклеточной или внеклеточной активностью, которая способствует биологическому процессу для лечения медицинского состояния. В некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в клетках печени. В некоторых вариантах реализации полезная нагрузка представляет собой пептид, который эктопически экспрессируется в клетках печени. В некоторых вариантах реализации полезная нагрузка представляет собой метилмалонил-КоА мутазу, альфа-1-антитрипсин или человеческий фактор IX.
[00014] Как описано в настоящем документе, многие варианты реализации включают использование одного или нескольких биологических образцов (например, образец жидкости или ткани, взятый у субъекта). В соответствии с настоящим раскрытием, любой из множества биологических образцов считается совместимым с различными вариантами реализации. Например, в некоторых вариантах реализации биологический образец представляет собой или включает волосы, кожу, кал, кровь, плазму, сыворотку, спинномозговую жидкость, мочу, слюну, слезы, стекловидное тело или слизь.
[00015] Как описано в настоящем документе, детектирование (например, детектирование сигнала, такого как биомаркер или детектируемый фрагмент), применительно к способам и композициям, описанным в настоящем документе, может быть достигнуто любым подходящим для применения способом. Например, в некоторых вариантах реализации изобретения этап обнаружения представляет собой или включает иммунологический анализ или анализ амплификации нуклеиновой кислоты.
[00016] В соответствии с настоящим раскрытием, использование множества биологических образцов считается совместимым с различными вариантами реализации. В некоторых вариантах реализации биомаркер представляет собой или включает детектируемый фрагмент, который после трансляции полипептида, кодируемого целевым сайтом, сливается с полипептидом, кодируемым целевым сайтом. В некоторых вариантах реализации биомаркер представляет собой или включает детектируемый фрагмент, который после трансляции полипептида, кодируемого целевым сайтом, сливается с полипептидом, кодируемым целевой нагрузкой. В некоторых вариантах реализации биомаркер представляет собой или включает 2А пептид. В некоторых вариантах реализации 2А пептид выбран из группы, состоящей из P2A, T2A, E2A и F2A. В некоторых вариантах реализации биомаркер может представлять собой или состоять из мотива расщепления фурином. В некоторых вариантах реализации детектируемый фрагмент может представлять собой или состоять из агента, который связывается с биомаркером (например, антителом или его фрагментом).
[00017] В некоторых вариантах реализации интеграция элемента нуклеиновой кислоты не нарушает существенно экспрессию полипептида, закодированного в целевом сайте (т.е. экспрессия полипептида в целевом сайте продолжается в основном так, как она продолжалась бы, если бы субъект не получал лечение интеграционной генной терапией или генно-интеграционную композицию). В некоторых вариантах реализации интеграция происходит без использования экзогенно поставляемой нуклеазы. В некоторых вариантах реализации интеграция происходит с использование одной или более экзогенно поставляемых нуклеаз.
[00018] В соответствии с различными вариантами реализации, способы и композиции, описанные в настоящем документе, считаются совместимыми с различными схемами генной терапии. Например, в некоторых вариантах реализации субъект получает одну дозу средства лечения генной терапией или генно-интеграционной композиции. В некоторых вариантах реализации субъект получает несколько доз средства лечения генной терапией или генно-интеграционной композиции (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более).
[00019] Кроме того, способы и композиции, описанные в настоящем документе, могут применяться в любой из множества моментов времени после лечения генной терапией (например, через несколько часов, дней, недель или месяцев после получения субъектом генной терапии). Соответственно, в некоторых вариантах реализации изобретения этап детекции выполняется через 1, 2, 3, 4, 5, 6, 7, 8 или более недель после того, как субъект получил лечение генной терапией или генно-интеграционную композицию. В некоторых вариантах реализации изобретения этап детекции выполняется в множественные временные точки после того, как субъект получил лечение генной терапией или генно-интеграционную композицию. В некоторых вариантах реализации изобретения этап детекции выполняется (например, множество раз) через по меньшей мере 3 месяца после того, как субъект получил лечение генной терапией или генно-интеграционную композицию.
[00020] Удивительно, но было обнаружено, что некоторые варианты реализации изобретения способны обеспечить пользу (например, облегчить мониторинг и/или корректировку терапии) субъекту, находящемуся на различных стадиях жизни при получении генной терапии, и, в некоторых вариантах осуществления изобретения, предлагаемые способы могут быть использованы при переходе субъекта от одной стадии жизни к другой. В некоторых вариантах реализации субъект получает лечение генной терапией или генно-интеграционную композицию в младенческом возрасте. В некоторых вариантах реализации субъект получает лечение генной терапией или генно-интеграционную композицию до достижения взрослого возраста (например, будучи ребенком). В некоторых вариантах реализации субъект получает лечение генной терапией или генно-интеграционную композицию во взрослом возрасте.
[00021] В частности, предполагается, что способы и композиции, описанные в настоящем документе, применимы к различным субъектам, каждый из которых потенциально имеет искажающие или осложняющие факторы/условия в дополнение к тем, которые требуют применения генной терапии. Кроме того, некоторые формы генной терапии известны или предполагаются как потенциально вызывающие проблемные реакции (например, аутоиммунные реакции, цитокиновые штормы и т.д.). Соответственно, в некоторых вариантах реализации представленные способы дополнительно включают мониторинг субъекта на предмет аутоиммунного ответа на генную терапию. В некоторых вариантах реализации представленные способы дополнительно включают мониторинг субъекта на предмет аномального ответа цитокинов на генную терапию (например, цитокиновый шторм).
[00022] Настоящее раскрытие также включает в себя признание того, что генная терапия может нуждаться в корректировке (например, усилении или подавлении), и предполагается, что различные варианты реализации являются преимущественными для мониторинга необходимости и/или успешного реализации таких корректировок. Соответственно, в некоторых вариантах реализации представленные способы дополнительно включают назначение субъекту дополнительного лечения (например, активирующего агента), если уровень биомаркера ниже, чем тот, который указывает на достижение терапевтически эффективного количества интеграционной генной терапии. Дополнительно или альтернативно, в некоторых вариантах реализации представленные способы дополнительно включают доставку субъекту дополнительного лечения (например, деактивирующего агента), которое снижает или ингибирует экспрессию полезной нагрузки, доставленной средством лечения генной терапией, если уровень биомаркера превышает уровень, который указывает на оптимальный или безопасный уровень полезной нагрузки.
[00023] В настоящей заявке термины «около» и «приблизительно» используются как эквивалентные. Любые ссылки на публикации, патенты или патентные заявки, приведенные в настоящем документе, включены в него посредством ссылки во всей своей полноте. Любые цифры, используемые в данной заявке с или без около/приблизительно, предназначены для охвата любых нормальных колебаний, оцененных человеком, обладающим обычными навыками в соответствующей области техники.
[00024] Другие признаки, объекты и преимущества настоящего изобретения очевидны из следующего подробного описания. Следует, однако, понимать, что подробное описание, указывая варианты реализации настоящего изобретения, приведено только в качестве иллюстрации, а не ограничения. Различные изменения и модификации в пределах объема изобретения станут очевидными для специалистов в данной области из подробного описания.
Краткое описание графических материалов
[00025] ФИГ. 1 демонстрирует схему конструкта GeneRide™ t (AAV) перед интеграцией и после интеграции, обусловленной гомологической рекомбинацией (ГР), в геном в целевой локус альбумина Alb. Экспрессия из отредактированного GeneRide™ локуса Alb может приводить к одновременной продукции альбумина-2A и трансгена как отдельных белков.
[00026] ФИГ. 2 изображает примерные споcобы анализа интеграции геномной ДНК (гДНК). Как показано, такие способы могут быть применены к анализу на гДНК, отредактированную с помощью GeneRide™ в локусе альбумина (Alb). На изображенном этапе 1 с помощью ПЦР длинных фрагментов (LR-PCR) амплифицируется продукт из выделенной гДНК с праймерами F1/R1. На изображенном этапе 2 очищенный продукт с этапа 1 амплифицируется с праймерами F2/R2 во вложенной кПЦР.
[00027] ФИГ. 3 представляет примерный подход для количественного определения эписомальной ДНК. Как показано, количество копий эписом можно определить методом кПЦР, используя стандартную кривую, построенную с помощью линеаризованной эписомной плазмиды.
[00028] ФИГ. 4 представляет примерный подход к анализу мРНК, включающей последовательность нуклеиновой кислоты, кодирующую 2А пептид. Число копий слитых мРНК определяется с помощью цифровой капельной ПЦР (цкПЦР) с набором праймеров Fwd/RF. Измеряется количество копий эндогенного Alb при помощи цкПЦР с набором праймеров Fwd/RE и используется для нормализации.
[00029] ФИГ. 5А-ФИГ. 5В представляют примерный подход для обнаружения и количественного определения полипептидов в плазме крови. Например, альбумин-2А в плазме крови может быть проанализирован с помощью проиллюстрированных способов. ФИГ.5А) изображает сэндвич-ИФА, включающий антитело захвата и антитело обнаружения. На иллюстрации представлены антитело анти-2А для захвата альбумина-2А и меченое антитело против альбумина для обнаружения. Для обнаружения других полипептидов, таких как альбумин, человеческий фактор IX и cyno A1AT, можно использовать антитела захвата и обнаружения, специфичные для других полипептидов в плазме. ФИГ 5В) изображает стандартные кривые, основанные на рекомбинантном мышином альбумине-2А в буфере PBST или 10% мышиной сыворотке.
[00030] ФИГ. 6A-ФИГ. 6C демонстрируют детекцию и анализ эписомальной ДНК in vivo. Новорожденным мышам (p2) вводили путем инъекции 1e14 гв/кг (геномов вектора на килограмм) hF9-DJ. ФИГ. 6A) Количество эписомальных копий уменьшается экспоненциально с течением времени после инъекции. ФИГ 6B) Инъекция не оказывала существенного влияния на рост печени у животных. ФИГ 6C) Инъекция не оказывала существенного влияния на увеличение веса тела у животных.
[00031] ФИГ. 7A-FIG. 7D демонстрирует детекцию in vivo , мониторинг и анализ биомаркера 2A с течением времени. Новорожденным мышам C57 в p2 вводили путем внутривенной инъекции 1e14 гв/кг hF9-DJ и отбирали ткани для анализа через 1, 2, 3, 4 и 8 недель после инъекции (n=5/группу). ФИГ. 7A) Интеграцию геномной ДНК биомаркера 2A в печень оценивали с применением ПЦР длинных фрагментов/кПЦР и выражали в виде процента эндогенного Alb. ФИГ. 7B-ФИГ. 7C) ALB-2A и общий мышиный альбумин в плазме измеряли с помощью ИФА. ФИГ. 7D) Корреляция данных, представленных на ФИГ. 7B и ФИГ. 7C. Анализ соотношения альбумина, меченого пептидом 2А, и общего альбумина в плазме подтверждает, что наблюдаемое повышение уровня ALB-2A в плазме связано с экспоненциальным увеличением эндогенного альбумина после рождения.
[00032] ФИГ. 8A-FIG. 8B демонстрируют детекцию in vivo , мониторинг и анализ полезной нагрузки, доставленной с биомаркером, с течением времени. Новорожденным мышам C57 в p2 вводили внутривенно путем инъекции 1e14 гв/кг hF9-DJ и отбирали ткани для анализа через 1, 2, 3, 4 и 8 недель после инъекции. ФИГ. 8A) Человеческий фактор IX количественно определяли в плазме крови мышей с помощью ИФА, специфичного для человеческого фактора IX. ФИГ 8B) Корреляция данных, представленных на ФИГ. 7B и ФИГ. 8А.
[00033] ФИГ. 9A-9E демонстрирует детекцию и анализ доставки биомаркеров и полезной нагрузки в двух дозах и двух возрастных группах. Новорожденным мышам C57 (р2) или молодым мышам (р21) вводили внутривенно путем инъекции 1e13 или 1e14 гв/кг hF9-DJ и отбирали ткани для анализа через 8 недель после инъекции (n=6-8/группу). На момент отбора для анализа возраст животных, получивших дозу в p2, составлял 8 недель, а животных, получивших дозу в p21, - 11 недель. ФИГ. 9A) ALB-2A в плазме, измеренный с помощью ИФА. ФИГ. 9В) Человеческий фактор IX в плазме, измеренный с помощью ИФА. ФИГ. 9C) Слитая мРНК в печени, определенная количественно с помощью цкПЦР и выраженная в процентах от эндогенной мРНК альбумина. ФИГ. 9D) Интеграцию геномной ДНК в печень оценивали с применением ПЦР длинных фрагментов/кПЦР и выражали в виде процента эндогенного Alb. ФИГ. 9E) Количество эписомальных копий на клетку, измеренное в печени методом кПЦР.
[00034] ФИГ. 10A-ФИГ. 10С демонстрируют детекцию in vivo, мониторинг и анализ полезной нагрузки, доставленной с биомаркером субъектам различных возрастных групп. Новорожденным мышам FvB/NJ (p2), молодым мышам (р21) или взрослым мышам (p42 и р63) вводили внутривенно 1e14 гв/кг hF9-DJ и отбирали ткани для анализа через 4 недели после инъекции (n=6-9/группу). На момент отбора для анализа возраст животных, получивших дозу в p2, составлял 4 недели, получивших дозу в p21-7 недель, получивших дозу в p42-11 недель и получивших дозу в p63-14 недель. ФИГ. 10А-ФИГ. 10В) ALB-2A и человеческий фактор IX в плазме измеряли с помощью ИФА. ФИГ. 10C) Линейная регрессия ALB-2A в плазме по сравнению с человеческим фактором IX составляет R2=0,93.
[00035] ФИГ. 11A-ФИГ. 11С демонстрирует детекцию in vivo, мониторинг и анализ полезной нагрузки, доставленной с биомаркером вирусными векторами, содержащими плечи различной гомологии для геномной интеграции. Новорожденным мышам FvB/NJ (р2) вводили путем внутривенной инъекции A1AT-DJ с конечной дозой 1e13 или 1e14 гв/кг. HA-750п.н. соответствует трансгену с 750п.н. с гомологичными плечами, а HA-1т.п.н. - трансгену с гомологичными плечами 1 т.п.н. Животных отбирали для анализа через 6 недель после инъекции (n=6-9/группу). ФИГ. 11А-ФИГ. 11В) ALB-2A и cyno A1AT в плазме измеряли с помощью ИФА. ФИГ. 11C) Линейная регрессия ALB-2A по сравнению с A1AT составляет R2=0,91.
[00036] ФИГ. 12A-ФИГ. 12В демонстрирует детекцию in vivo , мониторинг и анализ клеточной внутренней полезной нагрузки, доставленной с биомаркером, с течением времени. Новорожденным мышам Mut−/−;TgINS-MCK-Mut (p2) вводили внутривенно путем инъекции различные дозы DJ-hMUT (1e13, 3e13 или 1e14 вг/кг) и отбирали для анализа через 3 месяца. ФИГ. 12А) Интеграцию геномной ДНК в печень оценивали с применением ПЦР длинных фрагментов/кПЦР и выражали в виде процента эндогенного Alb. ALB-2A в плазме измеряли с помощью ИФА. ФИГ. 12B) Экспрессия белка интегрированного трансгена, человеческого MUT, была измерена методом вестерн-блота в лизатах печени мышей MCK-MUT. Оказалось, что циркулирующий ALB-2A линейно коррелирует с уровнями геномной интеграции в печени, а также с уровнями белка MUT.
[00037] ФИГ. 13A-ФИГ. 13B демонстрируют, что экспрессия полезной нагрузки может увеличиваться после однократного введения (т.е. селективной экспансии гепатоцитов, отредактированных GeneRide™) и что увеличение уровней полезной нагрузки можно отслеживать путем анализа уровней биомаркеров. Новорожденным мышам Mut−/−;TgINS-MCK-Mut (p2) вводили путем внутривенной инъекции 1e14 гв/кг DJ-hMUT и отбирали для анализа в течение 7 месяцев. ФИГ. 13A-13B) Белок MUT человека, экспрессированный из интегрированного трансгена в мышах MUT-/- был проанализирован в лизатах печени методом вестерн-блоттинга с использованием β-актина в качестве контроля нагрузки. В этих лизатах печени также были проанализированы ALB-2A (блоттинг для 2A) и общий альбумин. Мыши MUT+/- , обработанные носителем, и мыши В6 дикого типа служили в качестве контроля. Примечание: Белок MUT в гепацитах MUT-/- эекспрессированный из трансгена, является человеческим, в то время, как эндогенный белок в мышах MUT+/- и мышах дикого типа В6 является мышиным.
[00038] ФИГ. 14 демонстрирует стандартные кривые, основанные на рекомбинантном мышином ALB-2A, приготовленном только в разбавителе образца или 1% плазме мыши, с использованием оптимизированного метода ИФА для ALB-2A.
[00039] ФИГ. 15A-15B демонстрируют детекцию in vivo , мониторинг и анализ полезной нагрузки, доставленной с биомаркером, у мышей дикого типа и мышиной модели NAFLD (DIO). Взрослым мышам (возрастом ~9 недель) вводили путем внутривенной инъекции 1e14 гв/кг hF9-DJ, образцы плазмы собирались на первой неделе и далее раз в две недели в течение 16 недель. ALB-2A и человеческий фактор IX количественно определяли в плазме крови мышей методом ИФА.
[00040] ФИГ. 16A-16C демонстрирует детекцию и анализ доставки биомаркеров и полезной нагрузки дозозависимым образом. Новорожденным мышам FvB (р2) вводили внутривенно путем инъекции 4.1e12, 1.2e13, 3.7e13, 1.1e14, 3.3e14 и 1e15 гв/кг chA1AT-DJ и отбирали ткани для анализа через 4 недели после инъекции (n= 5/группу). ФИГ. 16A-B) показывают уровни ALB-2A и cA1AT в плазме, измеренные с помощью ИФА, соответственно. ФИГ. 16C) показывает, что линейная регрессия ALB-2A по сравнению с A1AT составляет R2 =0,97.
[00041] ФИГ. 17A-C демонстрирует детекцию и анализ интеграции гДНК и доставки полезной нагрузки дозозависимым образом. Новорожденным мышам Mut+/-; TgINS-MCK-Mut (p0) вводили путем внутривенной инъекции низкую, среднюю и высокую дозу DJ-mMUT (2.1e13, 6.7e13 или 2.0e14 гв/кг) и отбирали для анализа через 90 дней после дозирования. ФИГ. 17A показывает уровни ALB-2A в плазме, измеренный с помощью ИФА (n=18 низкая доза, n=19 средняя доза, n=19 высокая доза). ФИГ. 17 B показывает процент интеграции гДНК в печень (n=26 низкая доза, n=25 средняя доза, n=28 высокая доза). ФИГ. 17C показывает корреляцию ALB-2A и процента интеграции гДНК для животных с обоими анализами.
Определения
[00042] Для того чтобы настоящее изобретение было более понятным, ниже приведены определения некоторых терминов. Дополнительные определения следующих терминов и других терминов указаны по всей спецификации.
[00043] Около: Термин «около», когда он используется в настоящем документе в отношении значения, относится к значению, которое похоже в контексте на ссылаемое значение. В целом, специалисты в данной области, знакомые с контекстом, оценят соответствующую степень отклонения, охватываемую словом «около» в данном контексте. Например, в некоторых вариантах реализации термин «около» может охватывать диапазон значений, который находится в пределах 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или менее от указанного значения.
[00044] Активирующий агент: Как используется в настоящем документе, термин «активирующий агент» относится к агенту, присутствие или уровень которого коррелирует с повышенным уровнем или активностью мишени по сравнению с тем, что наблюдается в отсутствие агента (или с агентом на другом уровне). В некоторых вариантах реализации активирующий агент - это агент, присутствие или уровень которого коррелирует с целевым уровнем или активностью, которые сравнимы или превышают определенный эталонный уровень или активность (например, наблюдаемые в соответствующих эталонных условиях, таких как присутствие известного активирующего агента, например, положительного контроля). В некоторых вариантах реализации активирующий агент связывается или иным образом ассоциируется с активирующим элементом, чтобы оказать свое действие.
[00045] Взрослый: Как используется в настоящем документе, термин «взрослый» относится к человеку в возрасте восемнадцати лет и старше. В некоторых вариантах реализации взрослый человек имеет вес в диапазоне от около 90 фунтов до около 250 фунтов.
[00046] Связанные: Два события или сущности «связаны» друг с другом, как этот термин используется в данном документе, если присутствие, уровень и/или форма одного из них коррелируют с присутствием, уровнем и/или формой другого. Например, конкретный объект (например, полипептид, генетическая сигнатура, метаболит, микроб и т.д.) считается связанным с определенным заболеванием, расстройством или состоянием, если его присутствие, уровень и/или форма коррелируют с заболеваемостью и/или восприимчивостью к заболеванию, расстройству или состоянию (например, в соответствующей популяции). В некоторых вариантах реализации два или более субъектов физически «связаны» друг с другом, если они взаимодействуют, прямо или косвенно, так, что находятся и/или остаются в физической близости друг от друга. В некоторых вариантах реализации два или более субъектов, физически связанных друг с другом, ковалентно связаны друг с другом; в некоторых вариантах реализации два или более субъектов, физически связанных друг с другом, не ковалентно связаны друг с другом, а нековалентно связаны, например, посредством водородных связей, взаимодействия Ван-дер-Ваальса, гидрофобных взаимодействий, магнитных свойств и их комбинаций.
[00047] Биологический образец: Как используется в данном документе, термин «биологический образец» обычно относится к образцу, полученному или происходящему из биологического источника (например, ткани, организма или культуры клеток), представляющего интерес, как описано в данном документе. В некоторых вариантах реализации представляющий интерес источник включает организм, например, животное или человека. В некоторых вариантах реализации биологический образец представляет собой или включает биологическую ткань или жидкость.В некоторых вариантах реализации биологический образец может представлять собой или включать костный мозг; кровь; клетки крови; асцит; образцы тканей или тонкоигольной биопсии; жидкости организма, содержащие клетки; свободно плавающие нуклеиновые кислоты; мокроту; слюну; мочу; спинномозговую жидкость, перитонеальную жидкость; плевральную жидкость; кал; лимфу; гинекологические жидкости; кожные мазки; вагинальные мазки; мазки изо рта; мазки из носа; промывания или лаважи, такие как протоковый лаваж или бронхоальвеолярный лаваж; аспираты; соскобы; образцы костного мозга; образцы биопсии тканей; хирургические образцы; фекалии, другие жидкости организма, секреции и/или выделения; и/или клетки из них и т.д.В некоторых вариантах реализации биологический образец представляет собой или включает клетки, полученные от человека. В некоторых вариантах реализации изобретения полученные клетки представляют собой или включают клетки индивидуума, от которого получен образец. В некоторых вариантах реализации образец представляет собой «первичный образец», полученный непосредственно из представляющего интерес источника любым подходящим способом. Например, в некоторых вариантах реализации изобретения первичный биологический образец получают способами, выбранными из группы, состоящей из биопсии (например, тонкоигольной аспирации или биопсии ткани), хирургического вмешательства, сбора жидкости организма (например, крови, лимфы, кала и т.д.) и т.д. В некоторых вариантах реализации, как будет ясно из контекста, термин «образец» относится к препарату, который получают путем обработки (например, путем удаления одного или нескольких компонентов и/или добавления одного или нескольких агентов) первичного образца. Например, фильтрацией с использованием полупроницаемой мембраны. Такой «обработанный образец» может включать, например, нуклеиновые кислоты или белки, выделенные из образца или полученные путем подвергания первичного образца таким способам, как амплификация или обратная транскрипция мРНК, выделение и/или очистка определенных компонентов и т.д.
[00048] Биомаркер: Термин «биомаркер» используется в настоящем документе в соответствии с его использованием в данной области для обозначения соединения, присутствие, уровень или форма которого коррелирует с конкретным биологическим событием или состоянием, представляющим интерес, так что он считается «маркером» этого события или состояния. Среди прочего, настоящее раскрытие предоставляет биомаркеры для генной терапии (например, которые полезны для оценки одного или более признаков или характеристик лечения генной терапией, таких как, например, степень, уровень и/или постоянство экспрессии полезной нагрузки). В некоторых вариантах реализации биомаркер представляет собой маркер клеточной поверхности. В некоторых вариантах реализации биомаркер является внутриклеточным. В некоторых вариантах реализации биомаркер находится вне клеток (например, выделяется или иным образом образуется или присутствует вне клеток, например, в жидкости организма, такой как кровь, моча, слезы, слюна, спинномозговая жидкость и т.д.). В некоторых вариантах реализации настоящее раскрытие демонстрирует эффективность биомаркеров, которые могут быть обнаружены в образце, полученном от субъекта, получившего генную терапию, для использования в оценке одного или нескольких свойств или характеристик этой генной терапии; в некоторых таких вариантах реализации образец представляет собой клетки, ткань и/или жидкость, отличные от тех, в которые была доставлена генная терапия и/или от тех, в которых активна полезная нагрузка.
[00049] Детектируемый фрагмент: Используемый в настоящем документе термин «детектируемый фрагмент» относится к любому объекту (например, молекуле, комплексу или их части или компоненту). В некоторых вариантах реализации детектируемый фрагмент предоставляется и/или используется как отдельное молекулярное соединение; в некоторых вариантах реализации оно является частью и/или ассоциировано с другим молекулярным соединением. Примеры детектируемых фрагментов включают, но не ограничиваются: различными лигандами. радионуклидами (например, 3H, 14C, 18F, 19F, 32P, 35S, 135I, 125I, 123I, 64Cu, 187Re, 111In, 90Y, 99mTc, 177Lu, 89Zr и т.д.), флуоресцентными красителями (конкретные примеры флуоресцентных красителей см. ниже), хемилюминесцентными агентами (такие как, например, эфиры акридина, стабилизированные диоксетаны и т.п.), биолюминесцентными агентами, спектрально разрешимыми неорганическими флуоресцентными полупроводниковыми нанокристаллами (т.е. квантовые точки), наночастицами металлов (например, золота, серебра, меди, платины и т.д.), нанокластерами, ионами парамагнитных металлов, ферментами (конкретные примеры ферментов см. ниже), колориметрическими метками (такие как, например, красители, коллоидное золото и т.д.), биотином, диоксигенином, гаптенами, антителами и/или белками, для которых доступны антисыворотки или моноклональные антитела.
[00050] Ребенок: Как используется в настоящем документе, термин «ребенок» относится к человеку в возрасте от двух до 18 лет. Масса тела может сильно варьироваться в разных возрастах и у разных детей, при этом типичный диапазон составляет от 30 до 150 фунтов.
[00051] Комбинированная терапия: Как используется в настоящем документе, термин «комбинированная терапия» относится к ситуациям, в которых субъект одновременно подвергается воздействию двух или более терапевтических режимов (например, двух или более терапевтических агентов, например, способом воздействия генной терапии и не-генной терапии). В некоторых вариантах реализации два или более режима могут вводиться одновременно; в некоторых вариантах реализации такие режимы могут вводиться последовательно (например, все «дозы» первого режима вводятся до введения любых доз второго режима); в некоторых вариантах реализации такие агенты вводятся в перекрывающихся режимах дозирования. В некоторых вариантах реализации «введение» комбинированной терапии может включать введение одного или более агента(ов) или способа(ов) воздействия субъекту, получающему другой агент(ы) или способ(ы) воздействия в комбинации. Для ясности, комбинированная терапия не требует, чтобы отдельные агенты вводились вместе в одной композиции (или даже обязательно в одно и то же время).
[00052] Композиция: Специалисты в данной области оценят, что термин «композиция», как он используется в настоящем документе, может применяться для обозначения дискретного физического объекта, включающего один или несколько указанных компонентов. В общем, если не указано иное, композиция может иметь любую форму - например, газ, гель, жидкость, твердое вещество и т.д.
[00053] Дезактивирующий агент: Как используется в настоящем документе, термин «дезактивирующий агент» относится к агенту, присутствие или уровень которого коррелирует со сниженным уровнем или активностью мишени по сравнению с тем, что наблюдается в отсутствие агента (или с агентом на другом уровне). В некоторых вариантах реализации дезактивирующий агент - это агент, присутствие или уровень которого коррелирует с целевым уровнем или активностью, которые сравнимы с определенным эталонным уровнем или активностью или ниже их (например, наблюдаемые в соответствующих эталонных условиях, таких как присутствие известного активирующего агента, например, положительного контроля). В некоторых вариантах реализации дезактивирующий агент связывается или иным образом ассоциируется с дезактивирующим элементом, чтобы оказать свое действие.
[00054] Определять: Многие методологии, описанные в настоящем документе, включают этап «определения». Специалисты в данной области техники, прочитав настоящую спецификацию, поймут, что такое «определение» может быть использовано или выполнено с помощью любого из множества способов, доступных специалистам в данной области техники, включая, например, конкретные способы, явно указанные в настоящем документе. В некоторых вариантах реализации изобретения определение включает в себя манипуляцию с физическим образцом. В некоторых вариантах реализации изобретения определение включает в себя рассмотрение и/или манипулирование данными или информацией, например, с помощью компьютера или другого устройства обработки, приспособленного для выполнения соответствующего анализа. В некоторых вариантах реализации определение включает в себя получение соответствующей информации и/или материалов из источника. В некоторых вариантах реализации определение включает сравнение одной или нескольких характеристик образца или объекта с сопоставимым эталоном.
[00055] Ген: В настоящем документе термин «ген» относится к последовательности ДНК, которая кодирует генный продукт (например, продукт РНК и/или полипептидный продукт). В некоторых вариантах реализации ген включает кодирующую последовательность (например, последовательность, которая кодирует определенный продукт гена); в некоторых вариантах реализации ген включает некодирующую последовательность. В некоторых конкретных вариантах реализации ген может включать как кодирующие (например, экзонные), так и некодирующие (например, интронные) последовательности. В некоторых вариантах реализации ген может включать один или несколько регуляторных элементов (например, промоторы, энхансеры, сайленсеры, сигналы терминации), которые, например, могут контролировать или влиять на один или несколько аспектов экспрессии гена (например, экспрессия, специфичная для типа клеток, индуцибельная экспрессия). В некоторых вариантах реализации ген расположен или находится (или имеет нуклеотидную последовательность, идентичную расположенной или найденной) в геноме (например, в или на хромосоме или другой реплицирующейся нуклеиновой кислоте).
[00056] Продукт гена или продукт экспрессии: Как используется в настоящем документе, термин «продукт гена» или «продукт экспрессии» в целом относится к РНК, транскрибированной с гена (до и/или после процессинга), или полипептиду (до и/или после модификации), кодируемому РНК, транскрибированной с гена.
[00057] «Улучшить», «увеличить», «ингибировать» или «уменьшить»: как используется в настоящем документе, термины «улучшить», «увеличить», «ингибировать», «уменьшить» или их грамматические эквиваленты указывают на значения, которые относятся к исходному уровню или другому эталонному измерению. В некоторых вариантах реализации подходящее эталонное измерение может представлять собой или включать измерение в конкретной системе (например, у одного человека) в сопоставимых условиях без присутствия (например, до и/или после) конкретного агента или лечения или в присутствии соответствующего сопоставимого эталонного агента. В некоторых вариантах реализации подходящее эталонное измерение может представлять собой или включать измерение в сравниваемой системе, которая, как известно или ожидается, будет реагировать определенным образом в присутствии соответствующего агента или лечения.
[00058] Младенец: :Как используется в настоящем документе, термин «младенец» относится к человеку в возрасте до двух лет. Обычная масса тела младенца составляет от 3 фунтов до 20 фунтов.
[00059] Нуклеиновая кислота: Как используется здесь, в самом широком смысле относится к любому соединению и/или веществу, которое является или может быть включено в олигонуклеотидную цепь. В некоторых вариантах реализации нуклеиновая кислота представляет собой соединение и/или вещество, которое включено или может быть включено в олигонуклеотидную цепь через фосфодиэфирную связь. Как будет ясно из контекста, в некоторых вариантах реализации изобретения «нуклеиновая кислота» относится к отдельному остатку нуклеиновой кислоты (например, нуклеотиду и/или нуклеозиду); в некоторых вариантах реализации изобретения «нуклеиновая кислота» относится к олигонуклеотидной цепи, включающей отдельные остатки нуклеиновой кислоты. В некоторых вариантах реализации «нуклеиновая кислота» представляет собой или включает РНК; в некоторых вариантах реализации «нуклеиновая кислота» представляет собой или включает ДНК. В некоторых вариантах реализации нуклеиновая кислота представляет собой, включает или состоит из одного или нескольких остатков природных нуклеиновых кислот. В некоторых вариантах реализации нуклеиновая кислота представляет собой, включает или состоит из одного или нескольких аналогов нуклеиновой кислоты. В некоторых вариантах реализации аналог нуклеиновой кислоты отличается от нуклеиновой кислоты тем, что в нем не используется фосфодиэфирная основа. В некоторых вариантах реализации нуклеиновая кислота представляет собой, включает или состоит из одного или нескольких природных нуклеозидов (например, аденозин, тимидин, гуанозин, цитидин, уридин, дезоксиаденозин, дезокситимидин, дезоксигуанозин и дезоксицитидин). В некоторых вариантах реализации нуклеиновая кислота представляет собой, включает или состоит из одного или нескольких нуклеозидных аналогов (например, 2-аминоаденозин, 2-тиотимидин, инозин, пирролопиримидин, 3 -метил аденозин, 5-метилцитидин, С-5-пропинил-цитидин, С-5-пропинил-уридин, 2-аминоаденозин, С5-бромуридин, С5-фторуридин, С5-йодуридин, С5-пропинил-уридин, С5-пропинил-цитидин, С5-метилцитидин, 2-аминоаденозин, 7-дезааденозин, 7-дезагуанозин, 8-оксоаденозин, 8-оксогуанозин, 0(6)-метилгуанин, 2-тиоцитидин, метилированные основания, интеркалированные основания и их комбинации). В некоторых вариантах реализации нуклеиновая кислота имеет нуклеотидную последовательность, которая кодирует функциональный генный продукт, такой как РНК или белок. В некоторых вариантах реализации нуклеиновая кислота включает один или несколько интронов. В некоторых вариантах реализации нуклеиновые кислоты получают путем одного или более из выделения из природного источника, ферментативного синтеза путем полимеризации на основе комплементарного шаблона (in vivo или in vitro), воспроизведения в рекомбинантной клетке или системе и химического синтеза. В некоторых вариантах реализации изобретения нуклеиновая кислота представляет собой по меньшей мере длиной 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 1 10, 120, 130, 140, 150, 160, 170, 180, 190, 20, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 600, 700, 800, 900, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000 или более остатков. В некоторых вариантах реализации нуклеиновая кислота является частично или полностью одноцепочечной; в некоторых вариантах реализации нуклеиновая кислота является частично или полностью двухцепочечной. В некоторых вариантах реализации нуклеиновая кислота имеет нуклеотидную последовательность, включающую по меньшей мере один элемент, который кодирует или является комплементом последовательности, которая кодирует полипептид. В некоторых вариантах реализации нуклеиновая кислота обладает ферментативной активностью.
[00060] Пептид: Как используется в настоящем документе, термин «пептид» или «полипептид» относится к любой полимерной цепи аминокислот. В некоторых вариантах реализации пептид имеет аминокислотную последовательность, которая встречается в природе. В некоторых вариантах реализации пептид имеет аминокислотную последовательность, которая не встречается в природе. В некоторых вариантах реализации пептид имеет аминокислотную последовательность, которая является сконструированной, т.е. она разработана и/или получена в результате действия рук человека. В некоторых вариантах реализации пептид может состоять из природных аминокислот, неприродных аминокислот или и тех, и других. В некоторых вариантах реализации пептид может состоять только из природных аминокислот или только из неприродных аминокислот. В некоторых вариантах реализации пептид может включать D-аминокислоты, L-аминокислоты или и те, и другие. В некоторых вариантах реализации пептид может включать только D-аминокислоты. В некоторых вариантах реализации пептид может включать только L-аминокислоты. В некоторых вариантах реализации пептид является линейным. В некоторых вариантах реализации термин «пептид» может быть приложен к названию эталонного пептида, активности или структуры; в таких случаях он используется в настоящем документе для обозначения пептидов, которые обладают соответствующей активностью или структурой и, таким образом, могут рассматриваться как члены одного класса или семейства пептидов. Для каждого такого класса в настоящей спецификации приведены и/или специалистам в данной области будут известны примерные пептиды в пределах класса, аминокислотные последовательности и/или функции которых известны; в некоторых вариантах реализации такие примерные пептиды являются эталонными пептидами для класса или семейства пептидов. В некоторых вариантах реализации член класса или семейства пептидов показывает значительную гомологию или идентичность последовательности, имеет общий мотив последовательности (например, характерный элемент последовательности) и/или имеет общую активность (в некоторых вариантах реализации на сопоставимом уровне или в пределах обозначенного диапазона) с эталонным пептидом класса; в некоторых вариантах реализации со всеми пептидами класса). Например, в некоторых вариантах реализации изобретения пептид-член демонстрирует общую степень гомологии или идентичности последовательности с эталонным пептидом, которая составляет по меньшей мере около 30-40% и часто превышает около 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более и/или включает по меньшей мере одну область (например, консервативную область, которая в некоторых вариантах реализации может быть или состоять из характерного элемента последовательности), которая показывает очень высокую идентичность последовательности, часто более 90% или даже 95%, 96%, 97%, 98% или 99%. Такая консервативная область обычно охватывает по меньшей мере 3-4 и часто до 20 или более аминокислот; в некоторых вариантах реализации консервативная область охватывает по меньшей мере один участок из по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или более смежных аминокислот.
[00061] Полипептид: Как используется в данном документе, термин «полипептид» или «белок» относится к полимеру, состоящему по меньшей мере из трех аминокислотных остатков. В некоторых вариантах реализации полипептид включает одну или несколько, или все, природные аминокислоты. В некоторых вариантах реализации полипептид включает одну или несколько, или все, неприродные аминокислоты. В некоторых вариантах реализации полипептид включает одну или несколько, или все, D-аминокислоты. В некоторых вариантах реализации полипептид включает одну или несколько, или все, L-аминокислоты. В некоторых вариантах реализации полипептид включает одну или несколько боковых групп или других модификаций, например, модифицирующих или присоединенных к одной или нескольким боковым цепям аминокислот, на N-конце полипептида, на С-конце полипептида или в любой их комбинации. В некоторых вариантах реализации полипептид включает одну или несколько модификаций, таких как ацетилирование, амидирование, аминоэтилирование, биотинилирование, карбамилирование, карбонилирование, цитруллинирование, деамидирование, деэлиминирование, элиминирование, гликозилирование, липидирование, метилирование, пегилирование, фосфорилирование, сумоилирование или их комбинации. В некоторых вариантах реализации полипептид может участвовать в одной или нескольких внутри- или межмолекулярных дисульфидных связях. В некоторых вариантах реализации полипептид может быть циклическим и/или может включать циклическую часть. В некоторых вариантах реализации полипептид может быть нециклическим и/или не включает циклическую часть. В некоторых вариантах реализации полипептид является линейным. В некоторых вариантах реализации полипептид может включать сшитый полипептид. В некоторых вариантах реализации полипептид участвует в образовании нековалентного комплекса путем нековалентной или ковалентной ассоциации с одним или несколькими другими полипептидами (например, как в антителе). В некоторых вариантах реализации полипептид имеет аминокислотную последовательность, которая встречается в природе. В некоторых вариантах реализации полипептид имеет аминокислотную последовательность, которая не встречается в природе. В некоторых вариантах реализации полипептид имеет аминокислотную последовательность, которая является сконструированной, т.е. она разработана и/или получена в результате действия рук человека. В некоторых вариантах реализации термин «полипептид» может быть приложен к названию эталонного полипептида, активности или структуры; в таких случаях он используется в настоящем документе для обозначения полипептидов, которые обладают соответствующей активностью или структурой и, таким образом, могут рассматриваться как члены одного класса или семейства полипептидов. Для каждого такого класса в настоящей спецификации приведены и/или специалистам в данной области будут известны примерные полипептиды в пределах класса, аминокислотные последовательности и/или функции которых известны; в некоторых вариантах реализации такие примерные полипептиды являются эталонными полипептидами для класса или семейства полипептидов. В некоторых вариантах реализации член класса или семейства полипептидов показывает значительную гомологию или идентичность последовательности, имеет общий мотив последовательности (например, характерный элемент последовательности) и/или имеет общую активность (в некоторых вариантах реализации на сопоставимом уровне или в пределах обозначенного диапазона) с эталонным полипептидом класса; в некоторых вариантах реализации со всеми полипептидами класса). Например, в некоторых вариантах реализации изобретения полипептид-член демонстрирует общую степень гомологии или идентичности последовательности с эталонным полипептидом, которая составляет по меньшей мере около 30-40% и часто превышает около 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более и/или включает по меньшей мере одну область (например, консервативную область, которая в некоторых вариантах реализации может быть или состоять из характерного элемента последовательности), которая показывает очень высокую идентичность последовательности, часто более 90% или даже 95%, 96%, 97%, 98% или 99%. Такая консервативная область обычно охватывает по меньшей мере 3-4 и часто до 20 или более аминокислот; в некоторых вариантах реализации консервативная область охватывает по меньшей мере один участок из по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или более смежных аминокислот. В некоторых вариантах реализации полезный полипептид может включать фрагмент родительского полипептида. В некоторых вариантах реализации полезный полипептид может включать в себя множество фрагментов, каждый из которых находится в одном и том же родительском полипептиде в ином пространственном расположении относительно друг друга, чем в интересующем полипептиде (например, фрагменты, которые непосредственно связаны в родительском полипептиде, могут быть пространственно разделены в интересующем полипептиде или наоборот, и/или фрагменты могут присутствовать в ином порядке в интересующем полипептиде, чем в родительском), так что интересующий полипептид является производным от своего родительского полипептида.
[00062] Субъект: Как используется в настоящем документе, термин «субъект» означает организм, обычно млекопитающее (например, человек, в некоторых вариантах реализации, включая пренатальные формы человека). В некоторых вариантах реализации субъект страдает от соответствующего заболевания, расстройства или состояния. В некоторых вариантах реализации субъект восприимчив к заболеванию, расстройству или состоянию. В некоторых вариантах реализации субъект демонстрирует один или несколько симптомов или характеристик заболевания, расстройства или состояния. В некоторых вариантах реализации субъект не демонстрирует один или несколько симптомов или характеристик заболевания, расстройства или состояния. В некоторых вариантах реализации субъект - это человек с одним или несколькими признаками, характеризующими предрасположенность к заболеванию, расстройству или состоянию или имеет риск их возникновения. В некоторых вариантах реализации субъект является пациентом. В некоторых вариантах реализации субъект - это человек, которому проводится и/или назначается диагностика и/или терапия.
[00063] Существенно: Как используется в настоящем документе, термин «существенно» относится к качественному состоянию проявления полной или почти полной степени или уровня характеристики или свойства, представляющего интерес. Человек, обладающий обычными навыками в области биологии, поймет, что биологические и химические явления редко, если вообще когда-либо, доходят до завершения и/или протекают до полноты, или достигают или избегают абсолютного результата. Поэтому термин «существенно» используется в данном документе для отражения потенциального отсутствия полноты, присущего многим биологическим и химическим явлениям.
Детальное описание определенных вариантов реализации
[00064] Настоящее раскрытие предоставляет технологии для мониторинга и/или иной оценки генной терапии. Как описано в настоящем документе, настоящее раскрытие относится к обнаружению и оценке биомаркера(ов), которые образуются в результате лечения генно-интеграционной терапией, присутствие и относительные количества которого раскрывают информацию о полезной нагрузке, доставленной посредством лечения генной терапией, например, информацию о присутствии, количестве и/или кинетике доставленной полезной нагрузки. В одном аспекте настоящего раскрытия присутствие, количество и/или кинетика биомаркера действует как косвенный признак для определения присутствия, количества и/или кинетики доставленной полезной нагрузки. В некоторых вариантах реализации раскрытия изобретения биомаркер оценивается из биологического образца, взятого у субъекта, который получил лечение интеграционной генной терапией. В некоторых вариантах реализации раскрытия изобретения биомаркер может быть оценен в нетканевом биологическом образце, взятом у субъекта. В некоторых вариантах реализации раскрытия полезная нагрузка доставляется (например, посредством доставки соответствующего трансгена) и остается в ткани субъекта, получившего лечение интеграционной генной терапией.
Интеграционная генная терапия
[00065] Генная терапия вводит генетический материал в клетки субъекта, как правило, для экспрессии полезной нагрузки, которая может компенсировать аномальный ген или иным образом обеспечить благоприятный эффект для субъекта. Интеграционная генная терапия вводит генетический материал, который интегрируется в генетическую последовательность (т.е. целевой сайт), присутствующую в клетке-реципиенте.
[00066] Специалистам в данной области известно множество технологий для интеграции генетического материала в интересующий целевой сайт в клетке-реципиенте или организме. Такие интегрированные генетические элементы могут включать последовательность нуклеиновой кислоты (т.е. «трансген», как этот термин используется в настоящем документе), которая кодирует полезную нагрузку, доставляемую в клетку или организм хозяина. Как правило, трансген доставляется в контексте вектора; специалистам в данной области известны вирусные и невирусные векторные системы, которые могут быть успешно использованы для достижения интеграции трансгена.
[00067] Настоящее раскрытие обеспечивает выявление источника проблемы с помощью различных технологий интеграционной генной терапии.
[00068] Например, в настоящем раскрытии понимается, что малопроизводительная или неэффективная интеграция может ограничить полезность стратегий генной терапии. Если вектор не интегрируется, он обычно теряется при делении клеток в процессе роста или регенерации тканей, и все преимущества, которые дает или мог бы дать доставленный трансген (или полезная нагрузка), также будут потеряны. Аналогичная трудность возникает даже в том случае, когда интеграция изначально успешна, но впоследствии утрачена, например, в результате рекомбинации или гибели клетки-реципиента.
[00069] В настоящем раскрытии также отмечается, что многие технологии интеграции генов или события не могут вовсе или не могут точно контролировать целевой сайт интеграции, и что сайт интеграции может значительно влиять на степень и/или время экспрессии трансгена и/или может влиять на здоровье или даже жизнеспособность принимающей клетки. Кроме того, в настоящем раскрытии известно, что даже некоторые технологии «целенаправленной» интеграции генов могут быть подвержены негативному влиянию сайта интеграции, так что экспрессия трансгена может быть не в состоянии достигать и/или поддерживаться на желаемом уровне и/или в течение желаемого периода времени.
[00070] Настоящее раскрытие также принимает во внимание, что многие подходы генной терапии вводят трансген в оперативной ассоциации с промотором (например, экзогенным промотором), и что характеристики экспрессии такого промотора могут негативно влиять на клетки-реципиенты, в том числе потенциально увеличивая риск неконтролируемой пролиферации (например, рака), особенно для промоторов, которые обеспечивают высокий уровень экспрессии генов.
[00071] Таким образом, настоящее раскрытие позволяет понять, что источником одной из проблем многих лечений интеграционной генной терапией является неспособность или невозможность контролировать экспрессию соответствующей полезной нагрузки, особенно с течением времени. Учитывая, что многие полезные нагрузки являются или могут быть внутриклеточными и/или ткани, в которых они должны быть экспрессированы и/или активны, могут быть относительно недоступны, регулярный мониторинг часто не проводится.
[00072] Настоящее раскрытие способствует обнаружению того, что определенные технологии интеграции генов могут генерировать эффективный биомаркер для успешной интеграции трансгенов и экспрессии полезной нагрузки. Более того, настоящее раскрытие демонстрирует, что некоторые такие технологии генерируют биомаркер, который может быть оценен из легкодоступных биологических образцов (например, крови, мочи, слез и т.д.). Таким образом, настоящее раскрытие предоставляет технологии, которые улучшают интеграционную генную терапию, в частности, путем предоставления систем для мониторинга (например, обнаружения и/или количественного определения, во многих вариантах реализации во многих точках времени) биомаркера, созданного в результате успешной интеграции и отражающего экспрессию полезной нагрузки.
[00073] Предполагается, что может быть использована любая из множества технологий интеграционной генной терапии. В качестве неограничивающего примера, в некоторых вариантах реализации интеграционная генная терапия может представлять собой или включать использование системы на основе векторов (например, системы на основе вирусных векторов), системы на основе невирусных векторов, системы, опосредованной нуклеазой, и/или использование системы GENERIDE™, или любую их комбинацию.
Системы на основе вектора
[00074] В некоторых вариантах реализации интеграционная генная терапия может представлять собой или состоять из системы на основе вектора (например, вирусного вектора). Как правило, система на основе вектора включает вирус или вирусный генетический материал, в который может быть вставлен фрагмент чужеродной ДНК для переноса в клетку. Любой вирус, который включает стадию ДНК в своем жизненном цикле, может быть использован в качестве вирусного вектора в рамках объема некоторых вариантов реализации настоящего раскрытия. В качестве неограничивающего примера, система на основе вирусного вектора может представлять собой одноцепочечный ДНК-вирус, двухцепочечный ДНК-вирус, РНК-вирус, который имеет ДНК-стадию в своем жизненном цикле, например, ретровирусы. В некоторых вариантах реализации вирусный вектор может быть доставлен через фармацевтически приемлемую рецептуру, например, липосому или липидную частицу (например, микро- или наночастицу).
[00075] В качестве одного неограничивающего примера, одним из вирусов, представляющих интерес, является адено-ассоциированный вирус. Под адено-ассоциированным вирусом, или «AAV», подразумевается сам вирус или его производные. Термин охватывает все подтипы и как встречающиеся в природе, так и рекомбинантные формы, если не требуется иное, например, AAV тип 1 (AAV-1 ), AAV тип 2 (AAV-2), AAV тип 3 (AAV-3), AAV тип 4 (AAV-4), AAV тип 5 (AAV-5), AAV тип 6 (AAV-6), AAV тип 7 (AAV-7), AAV тип 8 (AAV-8), AAV тип 9 (AAV-9), AAV тип 10 (AAV-10), AAV тип 11 (AAV-11), птичий AAV, бычий AAV, AAV собак, лошадиный AAV, AAV приматов, AAV не-приматов, AAV овец, гибридный AAV (например, AAV, включающий капсидный белок одного подтипа AAV и геномный материал другого подтипа), AAV, включающий мутантный капсидный белок AAV или химерный капсидный белок AAV (т.е. капсидный белок с областями, доменами или отдельными аминокислотами, которые получены из двух или более различных серотипов AAV, например, AAV-DJ, AAV-LK3, AAV-LK19). « AAV приматов» относится к AAV, которые заражают приматов, «»AAV не-приматов» относится к AAV, которые заражают не-приматов, «бычий AAV» относится к AAV, которые заражают млекопитающих, относящихся к крупному рогатому скоту, и т.д.
[00076] Независимо от используемого вектора (например, вирусного), для продвижения направленной интеграции направленный вектор включает последовательности нуклеиновых кислот, которые допускают гомологичную рекомбинацию в месте интеграции, например, последовательности, которые допускают гомологичную рекомбинацию с геном альбумина, геном коллагена, геном актина и т.д.. Этот процесс требует гомологии нуклеотидной последовательности, используя молекулу «донора», например, направленный вектор, для матричной репарации молекулы «мишени», т.е. нуклеиновой кислоты, в которую интегрирована нуклеиновая кислота последовательности, например, целевого локуса в клеточном геноме, и приводит к переносу генетической информации от донора к мишени. Таким образом, в целевых векторах композиций по теме, трансген, который должен быть интегрирован в клеточный геном, может быть фланкирован последовательностями, которые содержат достаточную гомологию с геномной последовательностью в сайте расщепления, например, 70%, 80%, 85%, 90%, 95% или 100% гомологии с нуклеотидными последовательностями, фланкирующими сайт расщепления, например, в пределах около 50 оснований или менее от сайта расщепления, например, в пределах около 30 оснований, в пределах около 15 оснований, в пределах около 10 оснований, в пределах около 5 оснований или непосредственно фланкирующих целевой сайт интеграции, для поддержки гомологичной рекомбинации между ним и геномной последовательностью, к которой он имеет гомологию. Приблизительно 25, 50, 100, 250 или 500 нуклеотидов или более гомологии последовательности между донором и геномной последовательностью будут поддерживать гомологичную рекомбинацию между ними.
Не-вирусные векторные системы
[00077] В некоторых вариантах реализации интеграционная генная терапия может представлять собой или состоять из не-вирусной векторной системы. В некоторых вариантах реализации не-вирусная векторная система может представлять собой или состоять из плазмиды, частицы на основе полимера, зкДНК (дНК с закрытым концом), липосомы, миникольца и их комбинации. В некоторых вариантах реализации невирусная векторная система может представлять собой или включать использование химических носителей, электропорацию, использование баллистической ДНК (например, бомбардировка частицами), сонопорацию, фотопорацию, магнитофекцию, гидропорацию и любую их комбинацию.
[00078] Подобно приведенному выше описанию, независимо от типа (типов) используемой невирусной векторной системы (систем), для содействия направленной интеграции необходимо использовать/доставить в целевой сайт одну или несколько последовательностей нуклеиновых кислот, которые благоприятствуют гомологичной рекомбинации в сайте интеграции.
Интеграция, опосредованная нуклеазой
[00079] В соответствии с различными вариантами реализации, интеграция, опосредованная нуклеазой, использует одну или несколько нуклеаз - ферментов, которые были разработаны или первоначально идентифицированы в бактериях, которые разрезают ДНК. Как правило, интеграция, опосредованная нуклеазами, представляет собой двухэтапный процесс. Сначала экзогенная нуклеаза, способная разрезать одну или обе нити в двухцепочечной ДНК, направляется к нужному участку синтетической гидовой РНК и делает специфический разрез. После того, как нуклеаза делает нужный разрез или разрезы, активируется механизм репарации ДНК клетки и завершает процесс редактирования посредством NHEJ (негомологичное соединение концов) или, реже, HDR (гомологичная репарация).
[00080] В некоторых вариантах реализации NHEJ может происходить в отсутствие шаблона ДНК для копирования клеткой при восстановлении разреза ДНК. Это основной или стандартный путь, который используется клеткой для восстановления двухцепочечных разрывов. Механизм NHEJ может быть использован для введения небольших вставок или делеций, известных как инделы, что приводит к нарушению функции гена. NHEJ создает вставки и делеции в ДНК благодаря своему способу репарации, а также может привести к появлению нецелевых, нежелательных мутаций, включая хромосомные аберрации.
[00081] Нуклеаза-опосредованный HDR происходит при совместной доставке нуклеазы, направляющей РНК и шаблона ДНК, который похож на разрезанную ДНК. Следовательно, клетка может использовать этот шаблон для построения репаративной ДНК, что приводит к замене дефектных генетических последовательностей на правильные. В некоторых вариантах реализации механизм HDR является предпочтительным путем восстановления при использовании подхода на основе нуклеаз для вставки корректирующей последовательности из-за его высокой точности. Однако большая часть репарации генома после его разрезания нуклеазой продолжает использовать механизм NHEJ. Более частый путь репарации NHEJ потенциально может вызвать нежелательные мутации в месте разреза, что ограничивает круг заболеваний, на которые в настоящее время могут быть направлены любые подходы к интеграции, опосредованные нуклеазами.
Технологическая платформа GeneRide™
[00082] GeneRide™ представляет собой технологию редактирования генома, которая использует гомологичную рекомбинацию, или HR, естественный процесс восстановления ДНК, поддерживающий верность генома. Благодаря использованию HR, GeneRide™ позволяет вставлять полинуклеотиды в определенные целевые геномные участки без использования экзогенных нуклеаз. Направленная интеграция полинуклеотидов GeneRide™ предназначена для использования эндогенных промоторов в этих целевых участках для обеспечения высокого уровня тканеспецифической экспрессии генов без вредных проблем, связанных с использованием экзогенных промоторов. В некоторых вариантах реализации настоящего раскрытия GeneRide™ используется для доставки полинуклеотида, кодирующего полезную нагрузку, в клетку-хозяина или организм.
[00083] Технология GeneRide™ может быть использована для точной интеграции полинуклеотида, кодирующего терапевтическую полезную нагрузку, в геном пациента для обеспечения стабильного терапевтического эффекта. Поскольку GeneRide™ рассчитана на такой длительный терапевтический эффект, его можно применять для лечения целевых расстройств у педиатрических пациентов, когда очень важно обеспечить лечение на ранних этапах жизни пациента, пока не наступили необратимые патологические процессы.
[00084] В некоторых вариантах реализации GeneRide™ использует вектор AAV для доставки гена в ядро клетки. Затем она использует гомологичную рекомбинацию для стабильной интеграции корректирующего гена в геном реципиента в месте, где он регулируется эндогенным промотором, что позволяет производить белок в течение всей жизни, даже когда организм растет и меняется со временем.
[00085] GeneRide™ может обеспечить точную, сайт-специфическую, стабильную и долговечную интеграцию корректирующего гена в хромосому клетки-хозяина. В доклинических исследованиях на животных с использованием конструкций GeneRide наблюдается интеграция корректирующего гена в определенное место в геноме.
[00086] Модульная система GeneRide™ может быть применена для обеспечения надежной, тканеспецифической экспрессии генов, которая будет воспроизводима для различных терапевтических препаратов, доставляемых в одну или несколько тканей. Заменяя другой трансген в конструкте GeneRide™ , этот трансген может быть доставлен для решения новой терапевтической задачи при сохранении всех остальных компонентов конструкции. Такой подход позволит использовать общие производственные процессы и методы анализа аналитику для различных продуктов-кандидатов GeneRide™ и может сократить процесс разработки других программ лечения.
[00087] Предыдущие работы по неповреждающему генному таргетингу описаны в WO 2013/158309, включенном в настоящий документ посредством ссылки. Предыдущая работа по редактированию генома без использования нуклеаз описана в WO 2015/143177, включенном в настоящий документ посредством ссылки.
Целевой сайт
[00088] Интеграционная генная терапия для использования в соответствии с настоящим раскрытием желательно достигает интеграции, которая достигает функциональной ассоциации интегрированного трансгена с активным эндогенным промотором, так что транскрипция с промотора генерирует транскрипт, который распространяется через трансген. Более того, во многих вариантах реализации интеграция происходит в целевой сайт, выбранный таким образом, что такой транскрипт включает открытую рамку считывания, отличную от рамки считывания трансгена.
[00089] Во многих вариантах реализации интеграционная генная терапия для использования в соответствии с настоящим раскрытием достигает интеграции в целевой сайт в эндогенном гене (например, в определенное положение внутри или рядом с эндогенным геном) и распространяет транскрипт, генерируемый транскрипцией с промотора этого гена по меньшей мере в той степени, в которой он распространяется посредством трансгена.
[00090] В некоторых вариантах реализации лечение средством интеграционной генной терапии или генно-интеграционная композиция обеспечивает интеграцию элемента нуклеиновой кислоты, включающего последовательность, которая кодирует полезную нагрузку, в целевой сайт в геноме субъекта. Специалисты в данной области оценят, что любой из множества целевых сайтов может быть подходящим для использования со способами и композициями, описанными в настоящем документе. Например, в некоторых вариантах реализации изобретения целевой сайт кодирует полипептид. В некоторых вариантах реализации целевой сайт может кодировать полипептид, который высоко экспрессируется у субъекта (например, у субъекта, не страдающего заболеванием, расстройством или состоянием). В некоторых вариантах реализации интеграция элемента нуклеиновой кислоты происходит на 5' или 3' конце эндогенного гена, который кодирует полипептид. В качестве неограничивающего примера, в некоторых вариантах реализации изобретения целевой сайт кодирует альбумин.
[00091] Предполагается, что интеграционная доставка генетических элементов и/или трансгенов может быть осуществлена для любой ткани, включая, но не ограничиваясь этим, печень, центральную нервную систему (например, позвоночник), мышцы, почки, сетчатку глаза и кроветворные клетки костного мозга.
Полезные нагрузки
[00092] В соответствии с различными вариантами реализации изобретения, как описано в настоящем документе, может использоваться любая полезная нагрузка, подходящая для конкретного применения. В соответствии с различными вариантами реализации трансген кодирует одну или несколько полезных нагрузок. В настоящем документе термины «полезная нагрузка» и «представляющий интерес ген» (ПИГ) могут использоваться как взаимозаменяемые. В некоторых вариантах реализации полезная нагрузка представляет собой или состоит из пептида, нуклеиновой кислоты (например, кшРНК, микроРНК и/или нуклеиновой кислоты, кодирующей один или несколько пептидов) и любой их комбинации. В некоторых вариантах реализации лечения средством интеграционной генной терапии и/или генно-интеграционные композиции включают одну полезную нагрузку. В некоторых вариантах реализации лечения средством интеграционной генной терапии и/или генно-интеграционные композиции включают две или более полезные нагрузки (например, 3, 4, 5, 6, 7, 8, 9, 10 или более).
[00093] Например, в некоторых вариантах реализации полезная нагрузка представляет собой или включает пептид, экспрессируемый внутриклеточно, или последовательность нуклеиновой кислоты, кодирующую такой пептид (например, трансген). В качестве неограничивающего примера, внутриклеточно экспрессируемые пептиды включают метилмалонил-КоА мутазу (MUT), фенилаланин гидроксилазу (PAH), каталитическую субъединицу глюкого-6-фосфатазы (G6PC), пропионил-КоА карбоксилазу, субъединицу альфа (PCCA), кассетный транспортер, связывающий АТФ, подсемейство B член 11 (ABCB11), орнитин карбамоилтрансферазу (OTC), УДФ-глюкуронозилтрансферазу, семейство 1, член А1 (UGT1A1), кислую альфа-глюкозидазу (GAA), лизосомальную кислую глюкозилцерамидазу (GBA), фратаксин (FTX).
[00094] В некоторых вариантах реализации полезная нагрузка представляет собой или включает пептид, секретируемый внеклеточно, и/или последовательность нуклеиновой кислоты, кодирующую такой пептид (например, трансген). В качестве неограничивающего примера, секретируемые пептиды включают человеческий фактор IX (F9) и альфа-1-антитрипсин (SERPINA1).
[00095] В некоторых вариантах реализации полезная нагрузка представляет собой пептид, обладающий внутриклеточной или внеклеточной активностью, которая способствует биологическому процессу для лечения медицинского состояния.
[00096] В некоторых вариантах реализации полезная нагрузка может представлять собой или состоять из пептида, который обычно экспрессируется в одной или нескольких здоровых тканях, или последовательности нуклеиновой кислоты, кодирующей такой пептид. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в клетках печени, или последовательности нуклеиновой кислоты, кодирующей такой пептид. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в мышечных клетках. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в клетках центральной нервной системы. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в клетках глаза.
[00097] В некоторых вариантах реализации полезная нагрузка может представлять собой или состоять из пептида, который обычно не экспрессируется в одной или нескольких здоровых тканях (например, он экспрессируется эктопически), или последовательности нуклеиновой кислоты, кодирующей такой пептид. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который эктопически экспрессируется в клетках печени. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в мышечных клетках. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в клетках центральной нервной системы. Например, в некоторых вариантах реализации полезная нагрузка представляет собой пептид, который обычно экспрессируется в клетках глаза.
[00098] В некоторых вариантах реализации полезная нагрузка включает в себя активирующий элемент (например, активируемый активирующим агентом). В некоторых вариантах реализации полезная нагрузка включает в себя дезактивирующий элемент (например, активируемый дезактивирующим агентом). В некоторых вариантах реализации активирующий или дезактивирующий агент может представлять собой или состоять из малой молекулы,
Биомаркеры
[00099] Настоящее раскрытие предоставляет технологии интеграционной генной терапии, генерирующие детектируемый биомаркер, который может выступать в качестве косвенного показателя экспрессии полезной нагрузки.
[000100] В соответствии с настоящим раскрытием, экспрессия интегрированного трансгена включает производство транскрипта, включающего по меньшей мере одну транслируемую открытую рамку считывания, которая кодирует полипептид, отдельный или отделяемый от полезной нагрузки, кодируемой трансгеном. В некоторых вариантах реализации трансляция транскрипта генерирует один полипептид, который расщепляется для отделения полезной нагрузки от биомаркера; в некоторых вариантах реализации трансляция транскрипта генерирует отдельные полипептиды биомаркера и полезной нагрузки.
[000101] В соответствии с настоящим раскрытием, использование множества биологических образцов считается совместимым с различными вариантами реализации. В некоторых вариантах реализации биомаркер представляет собой или включает детектируемый фрагмент, который после трансляции полипептида, кодируемого целевым сайтом, сливается с полипептидом, кодируемым целевым сайтом. В некоторых вариантах реализации биомаркер представляет собой или включает детектируемый фрагмент, который после трансляции полипептида, кодируемого целевым сайтом, сливается с полипептидом, кодируемым полезной нагрузкой. В некоторых вариантах реализации изобретения связывание биомаркера с полезной нагрузкой может быть выгодным, например, когда полезная нагрузка представляет собой модифицированную форму эндогенного белка и поэтому в противном случае ее трудно или невозможно обнаружить отдельно от эндогенной версии. В некоторых вариантах реализации детектируемый фрагмент может представлять собой или состоять из агента, который связывается с биомаркером (например, антителом или его фрагментом, например, антителом, которое связывается с 2А пептидом).
[000102] В некоторых вариантах реализации биомаркер представляет собой или включает 2А пептид. В некоторых вариантах реализации 2A пептид выбран из группы, состоящей из P2A, T2A, E2A и F2A. В некоторых вариантах реализации биомаркер может представлять собой или состоять из мотива расщепления фурином. В качестве неограничивающего примера, массив мотивов расщепления фурином описан в Tian et al., FurinDB: A Databse of 20-Residue Furin Cleavage Site Motifs, Substrates and Their Associated Drugs, (2011), Int. J. Mol. Sci., vol. 12: 1060-1065. В качестве конкретного примера, в некоторых вариантах реализации 2А пептид может иметь или включать аминокислотную последовательность ATNFSLLKQAGDVEENPGP (SEQ ID NO: 1), а трансген, кодирующий такой 2А пептид, может иметь или включать нуклеотидную последовательность gccaccaacttcagcagcctgctgctgaaacaggccggcgacgtggaagagaaccctggccc (SEQ ID NO: 2). В некоторых вариантах реализации пептид 2A будет иметь последовательность, которая по меньшей мере на 80% идентична SEQ ID NO:1 или SEQ ID NO:2 (например, по меньшей мере на 85%, 90%, 95%, 99% идентична). В некоторых вариантах реализации 2А пептид или трансген, кодирующий 2А пептид, может являться или быть сгенерирован, как описано в Kim et al., (2011) High Cleavage Efficiency of a 2A Peptide Derived from Porcine Teschovirus-1 in Human Cell Lines, Zebrafish and Mice, PLoS ONE, vol. 6(4):e18556; Wang et al. (2015) 2A self-cleaving peptide-based multi-gene expression system in the silkworm Bombyx mori, Sci Rep., vol. 5: 16273; Yu et al. (2012) Use of Mutated Self-Cleaving 2A Peptides as a Molecular Rheostat to Direct Simultaneous Formation of Membrane and Secreted Anti-HIV Immunoglobulins. PLoS ONE 7(11): e50438; or Trichas et al. (2008), Use of the viral 2A peptide for bicistronic expression in transgenic mice, BMC Biology, vol. 6:40.
[000103] В некоторых вариантах реализации биомаркер может представлять собой или включать метку (например, иммунологическую метку), например, метку myc, HA, FLAG или другую метку. В некоторых вариантах реализации биомаркер может представлять собой или состоять из внутреннего сайта входа в рибосому (IRES).
Детектирование детектируемого фрагмента
[000104] Как описано в настоящем документе, детектирование (например, детектирование сигнала, такого как биомаркер или детектируемый фрагмент), применительно к способам и композициям, описанным в настоящем документе, может быть достигнуто любым подходящим для применения способом. Например, в некоторых вариантах реализации изобретения этап обнаружения представляет собой или включает иммунологический анализ или анализ амплификации нуклеиновой кислоты.
[000105] Как описано в данном документе, многие варианты реализации включают использование одного или нескольких биологических образцов (например, образец жидкости или ткани, взятый у субъекта), и способ обнаружения биомаркера может варьироваться в зависимости от биологического образца, используемого в конкретном варианте реализации. В соответствии с настоящим раскрытием, любой из множества биологических образцов считается совместимым с различными вариантами реализации. Например, в некоторых вариантах реализации биологический образец представляет собой или включает волосы, кожу, кал, кровь, плазму, сыворотку, спинномозговую жидкость, мочу, слюну, слезы, стекловидное тело или слизь.
[000106] В соответствии с различными вариантами реализации и в зависимости от конкретного используемого биомаркера (биомаркеров), специалист в данной области техники представляет себе один или несколько подходящих способов обнаружения или определения присутствия и/или количества/уровня биомаркера в биологическом образце. В некоторых вариантах реализации биомаркер может быть обнаружен с помощью любого из множества способов, включая флуоресценцию, радиоактивность, хемилюминесценцию, электрохемилюминесценцию, колориметрию, FRET, HTRF, изотопные методики, связывание партнеров (например, биотин/авидин, антитела, гибридизация) или любой другой известный способ обнаружения биомаркера. В некоторых вариантах реализации биомаркер может быть обнаружен путем связывания детектируемого фрагмента (например, экзогенно добавленной детектируемой молекулы), такого как антитело, включающее, например, метку в соответствии с одним или несколькими из вышеперечисленных способов, или фермента (например, люциферазы, β-гала).
Применения и дополнительные аспекты
[000107] Специалисты в данной области легко оценят, что способы, описанные в настоящем документе, могут быть полезны в различных областях применения, связанных с генной терапией. В некоторых вариантах реализации описанные здесь способы могут быть полезны для оценки того, является ли полезная нагрузка чрезмерно или недостаточно экспрессированной по сравнению с желаемым или «нормальным» уровнем экспрессии. В некоторых вариантах реализации описанные здесь способы могут быть использованы для прогнозирования или определения потенциальной неблагоприятной реакции на генную терапию (например, выработка вредного иммунного ответа, такого как антитела против препарата и/или цитокиновые штормы), что потенциально позволяет вмешаться и/или смягчить неблагоприятную реакцию.
[000108] В частности, предполагается, что способы и композиции, описанные в настоящем документе, применимы к любому из множества заболеваний, расстройств или состояний. В качестве неограничивающих примеров, некоторые варианты реализации могут быть полезны для мониторинга курса терапии или других параметров, среди прочих, ацидоза/ацидемии (например, метилмалоновой ацидемии), нарушения цикла мочевины, гемофилии, болезни Криглера-Найяра, острой печеночной порфирии, наследственного ATTR-амилоидоза и/или дефицита альфа-1 антитрипсина (A1ATD).
[000109] В соответствии с различными вариантами реализации, способы и композиции, описанные в настоящем документе, считаются совместимыми с различными схемами генной терапии. Например, в некоторых вариантах реализации субъект получает одну дозу средства лечения генной терапией или генно-интеграционной композиции. В некоторых вариантах реализации субъект получает несколько доз одного или более средств лечения генной терапией и/или генно-интеграционных композиций (например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более).
[000110] Кроме того, способы и композиции, описанные в настоящем документе, считаются применимыми в любой из множества моментов времени после лечения(ий) генной терапией(ями) (например, через несколько часов, дней, недель или месяцев после получения субъектом генной терапии). Соответственно, в некоторых вариантах реализации изобретения этап детекции выполняется через 1, 2, 3, 4, 5, 6, 7, 8 или более недель после того, как субъект получил лечение генной терапией или генно-интеграционную композицию. В некоторых вариантах реализации изобретения этап детекции выполняется в множественные временные точки после того, как субъект получил лечение генной терапией или генно-интеграционную композицию. В некоторых вариантах реализации изобретения этап детекции выполняется (например, множество раз) через по меньшей мере 3 месяца после того, как субъект получил лечение генной терапией или генно-интеграционную композицию.
[000111] Удивительно, но было обнаружено, что некоторые варианты реализации изобретения способны обеспечить пользу (например, облегчить мониторинг и/или корректировку терапии) субъекту, находящемуся на различных стадиях жизни при получении генной терапии, и, в некоторых вариантах осуществления изобретения, предлагаемые способы могут быть использованы при переходе субъекта от одной стадии жизни к другой. В некоторых вариантах реализации субъект получает лечение генной терапией или генно-интеграционную композицию в младенческом возрасте. В некоторых вариантах реализации субъект получает лечение генной терапией или генно-интеграционную композицию до достижения взрослого возраста (например, будучи ребенком). В некоторых вариантах реализации субъект получает лечение генной терапией или генно-интеграционную композицию во взрослом возрасте.
[000112] В частности, предполагается, что способы и композиции, описанные в настоящем документе, применимы к различным субъектам, каждый из которых потенциально имеет искажающие или осложняющие факторы/условия в дополнение к тем, которые требуют применения генной терапии. Кроме того, некоторые формы генной терапии известны или предполагаются как потенциально вызывающие проблемные реакции (например, аутоиммунные реакции, цитокиновые штормы и т.д.). Соответственно, в некоторых вариантах реализации представленные способы дополнительно включают мониторинг субъекта на предмет аутоиммунного ответа на генную терапию. В некоторых вариантах реализации изобретения, представленные способы дополнительно включают мониторинг субъекта на предмет аномального цитокинового ответа на генную терапию (например, цитокиновый шторм).
[000113] Настоящее раскрытие также включает в себя признание того, что генная терапия может нуждаться в корректировке (например, усилении или подавлении), и предполагается, что различные варианты реализации являются преимущественными для мониторинга необходимости и/или успешного реализации таких корректировок. Соответственно, в некоторых вариантах реализации представленные способы дополнительно включают назначение субъекту дополнительного лечения (например, активирующего агента), если уровень биомаркера ниже, чем тот, который указывает на достижение терапевтически эффективного количества интеграционной генной терапии. Дополнительно или альтернативно, в некоторых вариантах реализации представленные способы дополнительно включают доставку субъекту дополнительного лечения (например, деактивирующего агента), которое снижает или ингибирует экспрессию полезной нагрузки, доставленной средством лечения генной терапией, если уровень биомаркера превышает уровень, который указывает на оптимальный или безопасный уровень полезной нагрузки.
Примеры
Пример 1: Примерные способы обнаружения биомаркеров и полезной нагрузки
[000114] Настоящий пример демонстрирует примерные способы, которые могут быть применены для обнаружения, мониторинга и/или анализа биомаркера и/или полезной нагрузки в соответствии с настоящим раскрытием. В примерах 2-7 использовались способы и материалы, описанные в настоящем документе.
Анализ интеграции геномной ДНК (INT): кПЦР длинных фрагментов
[000115] Геномная ДНК (гДНК) была выделена из замороженной ткани печени мыши с помощью набора DNeasy компании Qiagen. Продукт ПЦР длинных фрагментов (LR-PCR), амплифицированный с праймерами F1/R1 (этап 1), был очищен с помощью магнитных бусин SPRI и использован во вложенной кПЦР (этап 2) с набором праймеров F2/R2 (ФИГ. 2). Для построения стандартной кривой использовалась синтетическая дцДНК, включающая фрагмент, расположенный выше по от 5' гомологического плеча представляющего интерес гена (ПИГ) (~2,1 т.п.н.). Стандарты проводились параллельно с образцами. Tfrc использовался в качестве контроля нагрузки для нормализации.
Анализ эписомальной ДНК
[000116] Геномная ДНК (гДНК) была выделена из печени мыши с помощью набора DNeasy компании Qiagen. Количество копий эписом определяли методом кПЦР (ФИГ. 3) с использованием стандартной кривой, построенной с помощью линеаризованной эписомной плазмиды. Tfrc использовался в качестве контроля нагрузки для нормализации. Из-за перекрестной реактивности праймеров с эндогенным геном Alb предел обнаружения анализа составляет 2, для 2 копий Alb в геноме.
Анализ слитой мРНК
[000117] РНК из печени мыши выделяли с помощью набора RNeasy от Qiagen. Число копий слитых мРНК определяется с помощью цкПЦР с набором праймеров Fwd/Rγ (ФИГ. 4). Измеряется количество копий Alb при помощи цкПЦР с набором праймеров Fwd/RE и используется для нормализации.
ИФА альбумина-2А
[000118] Альбумин-2А в плазме крови измеряли методом хемолюминесцентного ИФА, используя запатентованное кроличье поликлональное анти-2А антитело для захвата и меченное HRP поликлональное овечье антиальбуминовое антитело (BioRad AHP102P) для обнаружения (ФИГ. 5A). Рекомбинантный мышиный альбумин-2А, экспрессированный в клетках млекопитающих и аффинно очищенный, использовался для построения стандартной кривой в 10% плазме контрольной мыши для учета матричных эффектов (ФИГ. 5B). Казеин в концентрации 1% (Thermo 37528) использовался для блокирования и в концентрации 0,1% для разведения образцов в PBST.
ИФА альбумина
[000119] Общий мышиный альбумин в плазме измеряли методом хемолюминесцентного ИФА, используя поликлональное козье анти-мышиное альбуминовое антитело (abcam ab19194) для захвата и поликлональное овечье HRP-меченное анти-альбуминовое антитело (BioRad AHP102P) для обнаружения. Стандарт мышиного альбумина был приобретен у компании Sigma (SLBX6058). Казеин в концентрации 1% (Thermo 37528) использовался для блокирования и в концентрации 0,1% для разведения образцов в PBST.
Высокочувствительный ИФА альбумина-2А
[000120] Оригинальный протокол ИФА альбумина-2A был оптимизирован для повышения чувствительности анализа и минимизации матричных помех. Запатентованное рекомбинантное кроличье моноклональное анти-2А антитело было разработано и использовано для захвата и поликлональное козье антиальбуминовое антитело, меченное HRP (abcam ab19195), использовалось для обнаружения (ФИГ. 5A). Рекомбинантный мышиный альбумин-2А, экспрессированный в клетках млекопитающих и аффинно очищенный, с чистотой >95% использовался для построения стандартной кривой в ≤ 1% контрольной мышиной плазме или сыворотке (ФИГ. 14). Для блокирования использовался буфер, состоящий из 1% нежирного сухого молока, и образцы разводились в 1% BSA в PBST. Нижний предел обнаружения при использовании этого оптимизированного протокола составляет <1 нг/мл.
[000121]
ИФА человеческого фактора IX
[000122] Человеческий фактор IX в плазме измеряли методом хемолюминесцентного ИФА, используя моноклональные мышиные антитела против человеческого фактора IX (Sigma F2645) для захвата и козьи поликлональные HRP-меченые антитела против человеческого фактора IX (Affinity Biologicals GAFIX-APHRP) для обнаружения. Стандарт человеческого фактора IX был приобретен у abcam (ab62544), и стандартная кривая была построена в 6% плазме контрольной мыши для учета матричных эффектов. БСА в концентрации 3% использовался для блокирования и в концентрации 1% для разведения образцов в PBST.
ИФА сyno A1AT
[000123] Cyno A1AT в плазме измеряли методом хемолюминесцентного ИФА, используя козье поликлональное анти-A1AT антитело для захвата (MP Biomedical 55030) и овечье поликлональное HRP-меченное анти-A1AT антитело (abcam ab8768) для обнаружения. Рекомбинантный сyno A1AT, экспрессированный в клетках млекопитающих использовался для построения стандартной кривой в 10% контрольной мышиной плазме для учета матричных эффектов. БСА в концентрации 3% использовался для блокирования и в концентрации 1% для разведения образцов в PBST.
Вестерн-блот MUT
[000124] Замороженные ткани печени (~60 мг) гомогенизировали в буфере для лизиса (0,5% Igepal-630, 50 мМ Tris-HCl pH 7,5, 150 мМ NaCl, дополненный коктейлем ингибиторов протеаз Roche mini-tablet) с использованием MP Biomedicals Lysing Matrix D (#116913050) с двумя циклами разбивания шариками (20 сек при 3500 об/мин на цикл). Лизаты печени очищали центрифугированием и общий белок определяли количественно с помощью анализа BCA. Лизаты (6 мкг/дорожку) раскладывали на составляющие на 4-12% NuPAGE BisTris midi-gel (Life Technologies) с использованием MES буфера, перед переносом на нитроцеллюлозные мембраны на системе Trans-Turbo Blot (Bio-Rad). После блокирования в блокирующем буфере LI-COR Odyssey Buffer мембраны инкубировали с (a) кроличьим моноклональным анти-MUT антителом (abcam ab134956) и мышиным моноклональным анти-β-актином антителом (abcam ab14128) или (b) кроличьим поликлональным анти-2A антителом (запатентованным) и мышиным поликлональным антиальбумином (abcam ab19194). После инкубации со вторичными антителами (анти-кроличьими IRDye800CW и анти-мышиными IRDye680CT) блоты сканировались в системе LI-COR Odyssey, и изображения анализировались с помощью программного обеспечения ImageStudio.
Трансгены и векторы
[000125] Трансген человеческого фактора IX: Оптимизированная по кодонам кДНК человеческого фактора IX с кодирующей последовательностью P2A на 5'-конце, была фланкирована гомологичными плечами 1,3.п.н. в направлении против хода транскрипции и 1,4 т.п.н. в направлении по ходу транскрипции до стоп-кодона Alb (SEQ ID NO: 3).
[000126] Трансген человеческой метилмалонид-КоА мутазы: Оптимизированная по кодонам кДНК человеческая MUT с кодирующей последовательностью P2A на 5'-конце, была фланкирована гомологичными плечами 1 т.п.н. в направлении против хода транскрипции и 1 т.п.н. в направлении по ходу транскрипции до стоп-кодона Alb (SEQ ID NO: 4).
[000127] Трансген мышиной метилмалонил-КоА мутазы: Мышиная кДНК MUT с кодирующей последовательностью P2A на 5'-конце, была фланкирована гомологичными плечами 1 т.п.н. в направлении против хода транскрипции и 1 т.п.н. в направлении по ходу транскрипции до стоп-кодона Alb (SEQ ID NO: 5).
[000128] Трансген альфа-1-антитрипсина яванского макака (cyno-A1AT): Оптимизированная по кодонам кДНК SERPINA1 яванского макака с кодирующей последовательностью P2A на 5'-конце, была фланкирована гомологичными плечами 1 т.п.н. (SEQ ID NO: 6) или 750 п.н. (SEQ ID NO: 7) в направлении против хода и по ходу транскрипции до стоп-кодона Alb.
[000129] Подготовка векторов: Все плазмиды для получения rAAV были подготовлены с помощью набора EndoFree Plasmid Gigaprep Kit от Qiagen.
[000130] Векторы DJ были созданы в лабораторном масштабе с использованием тройной трансфекции в адгезивных клетках HEK-293 с очисткой градиентом CsCl для hF9 и MUT и с использованием тройной трансфекции в суспензионных клетках HEK-293F с аффинной очисткой с последующим градиентом йодиксанола для cyno-A1AT. Физические титры были определены количественно с помощью кПЦР
Исследования in vivo
[000131] Все процедуры с животными проводились в соответствии с рекомендациями Институционального комитета по уходу и использованию животных (IACUC) по уходу и использованию животных в исследованиях.
[000132] Мыши C57BL/6 и FvB/NJ были приобретены в лаборатории Jackson чтобы служить в качестве племенных пар для получения потомства для неонатальных (p2) и ювенильных (p21) инъекций. 2-дневным мышам вводили внутривенно путем инъекции в лицевую вену ~10 мкл вектора для конечной дозы 1e13 или 1e14 гв/кг, или PBS для группы носителя. 21-дневным мышам вводили внутривенно путем инъекции в хвостовую вену ~100 мкл вектора в конечной дозе 1e13 или 1e14 гв/кг, или PBS для группы носителя. Взрослым мышам (возраст >6-недель) вводили внутривенно путем инъекции в хвостовую вену ~200 мкл вектора для конечной дозы 1e13 или 1e14 гв/кг, или PBS для группы носителя. Вес животных контролировался еженедельно. Прижизненное взятие крови осуществлялось путем кровотечения из щеки, а терминальное кровотечение - путем пункции сердца, за исключением животных p7, которых обезглавливали. При отборе для анализа мышей подвергали эвтаназии путем вдыхания CO2 , печень собирали, разрезали и немедленно замораживали.
[000133] Мышиная модель MUT (Mut−/−;TgINS-MCK-Mut) была получена от доктора Чарльза Вендитти (Национальный институт исследования генома человека, Национальные институты здоровья). Новорожденным мышам (p1-2) вводили внутривенно путем инъекции в лицевую вену ~10 мкл вектора hMUT-DJ в конечной дозе 1e13, 3e13 или 1e14 гв/кг, или PBS в качестве носителя.
Пример 2: Обнаружение эписомальной ДНК
[000134] Настоящий пример демонстрирует применение обнаружения и анализа эписомальной ДНК в соответствии со способами, раскрытыми в настоящем документе.
[000135] Новорожденным мышам вводили внутривенно путем инъекции вирусный вектор, включающий кодирующую последовательность P2A и трансген человеческого фактора IX, разработанный для интеграции в эндогенный целевой сайт альбумина (см. трансген человеческого фактора IX, описанный в Примере 1).
[000136] Количество эписомальных копий уменьшалось экспоненциально с течением времени после инъекции (ФИГ. 6A). Уменьшение количества эписомальных копий наблюдалось одновременно с ростом печени (с 0,15 г в p7 до 1 г в возрасте 8 недель) (ФИГ. 6B). Несмотря на снижение количества эписомальных копий на клетку с течением времени, экспрессия трансгена оставалась высокой, что ожидается после стабильной интеграции трансгена в геном в течение первой недели, как это было достигнуто при использовании GeneRide™ (см., например, ФИГ. 7A и ФИГ. 8A).
[000137] Эти данные показывают, что количество эписомальной ДНК на клетку уменьшается с течением времени по мере роста печени. Эти данные дополнительно демонстрируют, что на рост и развитие животных не влияет дозирование высокого титра AAV, в данном случае 1e14 гв/кг (ФИГ. 6B-6C). Эти данные также демонстрируют, что количество эписомальных копий вирусного вектора, доставленного in vivo , может быть косвенным показателем дозировки и роста тканей. В частности, количество эписомальных копий пропорционально дозе, которую получало животное. Например, если животное дозировано неправильно (что может произойти при внутривенном введении новорожденным мышам), количество эписомальных копий для этого животного будет намного ниже, чем для животного, получившего полную дозу.
Пример 3: Обнаружение ALB-2A в плазме и корреляция с изменениями в экспрессии эндогенного альбумина
[000138] Настоящий пример демонстрирует обнаружение и мониторинг альбумина, меченного 2А-пептидом, после доставки in vivo элемента нуклеиновой кислоты, кодирующего 2А-пептид. Настоящий пример также демонстрирует, что изменения уровня ALB-2A в плазме могут быть связаны с изменениями экспрессии эндогенного альбумина.
[000139] Новорожденным мышам вводили внутривенно путем инъекции вирусный вектор, описанный в Примере 2. Геномная интеграция может быть обнаружена уже через 1 неделю после инъекции, а через 2 недели она уже достигла своего плато (ФИГ. 7А). Уровень ALB-2A в крови увеличивается в течение первых 3-4 недель, а затем стабилизируется (ФИГ. 7B). Наблюдаемое увеличение ALB-2A в плазме связано с экспоненциальным увеличением эндогенного альбумина после рождения (ФИГ. 7C и ФИГ. 7D).
[000140] Эти данные показывают, что способы, используемые в соответствии с настоящим раскрытием обеспечивают готовность к обнаружению и/или анализу ALB-2A в плазме, и что обнаружение и/или анализ ALB-2A в плазме могут быть достигнуты относительно рано (например, в течение 1 недели) после доставки in vivo элемента нуклеиновой кислоты, кодирующего пептид 2A. Эти данные также демонстрируют, что уровни ALB-2A в плазме можно отслеживать через множество временных интервалов после первоначальной доставки элемента нуклеиновой кислоты, кодирующего пептид 2A, и что уровни ALB-2A в плазме коррелируют с изменениями уровней эндогенного полипептида, который кодируется в целевом сайте для интеграции пептида 2A (например, целевой сайт альбумина).
Пример 4: Раннее обнаружение и анализ биомаркеров и полезной нагрузки
[000141] Настоящий пример демонстрирует, что способы, используемые в соответствии с настоящим раскрытием, позволяют проводить раннее обнаружение in vivo и анализ полезной нагрузки после доставки in vivo нуклеиновой кислоты, кодирующей полезную нагрузку, и нуклеиновой кислоты, кодирующей биомаркер. Настоящий пример также демонстрирует, что кинетика экспрессии полезной нагрузки имеет сходство с кинетикой экспрессии биомаркеров.
[000142] Новорожденным мышам вводили внутривенно путем инъекции вирусный вектор, описанный в Примере 2. Анализ уровня человеческого фактора IX в плазме крови, который экспрессируется из интегрированного трансгена, выявил сходную раннюю кинетику с ALB-2A (ФИГ. 8A-8B, соответственно). Подобно кинетике ALB-2A в плазме, уровень фактора IX увеличивался по мере увеличения эндогенного альбумина после рождения.
[000143] Эти данные демонстрируют, что экспрессия полезной нагрузки (например, фактора IX) может быть обнаружена и/или проанализирована относительно рано (например, в течение 1 недели) после доставки через вирусный вектор. Эти данные также демонстрируют сходную кинетику экспрессии полезной нагрузки и уровня в плазме крови биомаркера, доставленного вместе с полезной нагрузкой (например, пептида 2A) в течение множества временных интервалов после первоначальной доставки полезной нагрузки.
Пример 5: Возраст животных при дозировании не влияет на эффективность интеграции, ALB-2A в плазме и трансген
[000144] Настоящий пример демонстрирует, что способы, используемые в соответствии с настоящим раскрытием, могут применяться для средств лечения генной терапией, вводимых в различных возрастах субъектам, получающим такое лечение, в том числе на очень ранних (например, младенческих) и стадиях развития и до достижения взрослого возраста. Настоящий пример также демонстрирует, что описанные здесь способы могут быть применены для анализа генной терапии, которая доставляется в ткани с низким или высоким ростом.
[000145] Новорожденным (p2) или молодым (p21) мышам вводили внутривенно путем инъекции вирусный вектор, описанный в Примере 2, и отбирали для анализа через 8 недель после инъекции. Независимо от возраста при дозировке, легко обнаруживаются ALB-2A и человеческий фактор IX в плазме (ФИГ. 9A и 9B, соответственно), а также интеграция РНК биомаркера 2A (ФИГ. 9C). На эффективность интеграции в геномную ДНК не оказывает существенного влияния возраст, в котором животные получают дозу (ФИГ. 9D). Количество эписомальных копий после 8 недель после инъекции все еще высокое у животных, получивших дозу на уровне p21 (ФИГ. 9E), что соответствует более низкому росту печени у молодых животных.
[000146] Эти данные показывают, что экспрессия биомаркера (например, 2A) и полезной нагрузки (например, фактора IX) может быть обнаружена и/или проанализирована после доставки указанных биомаркера и полезной нагрузки субъекту на разных стадиях развития, в том числе в разном возрасте субъекта и/или на разных стадиях роста ткани при ткане-направленной доставке. В настоящем примере использование вектора DJ направлено на доставку нуклеиновой кислоты 2A и полезной нагрузки в печень.
Пример 6: Уровни биомаркеров как косвенный показатель уровня полезной нагрузки при введении препарата в различном возрасте
[000147] Настоящий пример демонстрирует, что способы, используемые в соответствии с настоящим раскрытием, позволяют обнаруживать и анализировать биомаркер в качестве косвенного показателя уровня полезной нагрузки. Настоящий пример также демонстрирует, что использование биомаркера в качестве косвенного показателя может практиковаться для доставки полезной нагрузки и биомаркера в различных возрастных группах субъектов.
[000148] Новорожденным (p2), молодым (р21) или взрослым мышам (p42 p63) вводили внутривенно путем инъекциии вирусный вектор, описанный в Примере 2, и отбирали для анализа через 4 недель после инъекции. Готовность к детекции ALB-2A (ФИГ. 10A) и человеческого фактора IX (ФИГ. 10B) в плазме наблюдалась в каждой возрастной группе по сравнению с обработкой носителем. Относительные уровни ALB-2A указывали на уровни человеческого фактора IX среди тестируемых возрастных групп (ФИГ. 10C).
[000149] Эти данные показывают, что обнаружение биомаркера (например, ALB-2A) свидетельствует об экспрессии полезной нагрузки (например, фактора IX). Эти данные дополнительно иллюстрируют, что обнаружение и анализ биомаркера может быть полезным в качестве косвенного показателя уровня полезной нагрузки, доставленной субъекту. Более того, такое измерение уровней биомаркеров в качестве косвенного показателя уровня полезной нагрузки может быть полезным для анализа полезной нагрузки, доставляемой субъектам в различных возрастных группах.
Пример 7: Уровни биомаркеров как косвенный показатель уровня полезной нагрузки, наблюдаемой при изменениях дизайна вектора
[000150] Новорожденным мышам вводили внутривенно путем инъекции вирусный вектор, включающий кодирующую последовательность P2A, кДНК SERPINA1 яванского макака и гомологичные плечи от 1 т.п.н. до 750 п.н., предназначенный для интеграции в эндогенный целевой сайт альбумина (см. трансген альфа-1-антитрипсин яванского макака (cyno-A1AT), описанный в Примере 1). Животных отбирали для анализа через 6 недель после инъекции. Уровни ALB-2A (ФИГ. 11A) в плазме крови были обнаружены после доставки вирусных векторов, содержащих гомологические плечи длиной 750 п.н. и 1 т.п.н. Уровни в плазме A1AT яванского макака, который экспрессируется из интегрированного трансгена, также легко обнаруживались в обоих наборах протестированных гомологичных плеч (ФИГ. 11B). Относительные уровни ALB-2A указывали на уровни A1AT яванского макака (ФИГ. 11C).
Пример 8: Уровни биомаркеров в плазме крови как косвенный показатель интеграции и экспрессии внутриклеточной полезной нагрузки
В настоящем примере была использована мышиная модель ММА, названная Mut-/-;TgINS-MCK-Mut мышами (упоминаемая здесь как MCK-Mut). В этой мышиной модели функциональная копия мышиного гена Mut находится под контролем промотора креатинкиназы, что позволяет экспрессировать Mut в мышечных клетках. Новорожденным мышам MCK-Mut (p2) вводили внутривенно путем инъекции различные дозы вирусного вектора, включающего кодирующую последовательность P2A и оптимизированную по кодонам кДНК MUT человека (см. трансген метилмалонил-КоА мутазы человека, описанный в Примере 1). Животных отбирали для анализа в течение 3 месяцев. Были легко обнаружены ALB-2A в плазме и геномная интеграция в печени (ФИГ. 12A). Относительные уровни ALB-2A в печени и в плазме крови указывали на уровень белка MUT в печени (ФИГ. 12B).
[000151] Эти данные показывают, что способы, используемые в соответствии с настоящим раскрытием , позволяют экспрессировать внутриклеточную полезную нагрузку (например, MUT), экспрессия которой может быть оценена путем обнаружения и анализа экспрессии детектируемого фрагмента, слитого с полипептидом, кодируемым геном сайта-мишени (например, ALB-2A). Эти данные также показывают, что изменения в экспрессии внутриклеточной полезной нагрузки (например, MUT) могут быть отражены в аналогичных изменениях в уровнях в плазме детектируемого фрагмента (например, пептида 2A), так что обнаружение уровней в плазме детектируемого фрагмента может действовать как косвенный показатель для обнаружения внутриклеточной полезной нагрузки. Кроме того, эти данные демонстрируют возможность мониторинга уровней внутриклеточной полезной нагрузки в режиме реального времени без необходимости обнаружения самой полезной нагрузки (например, с помощью биопсии печени).
Пример 9: Уровни биомаркеров как косвенный показатель изменяющихся уровней полезной нагрузки с течением времени
[000152] Новорожденным мышам MUT-MCK (p2) вводили внутривенно путем инъекции 1e14 гв/кг DJ-hMUT и мышей отбирали для анализа в течение 7 месяцев. Гепатоциты, отредактированные с помощью GeneRide, экспрессируют функциональный MUT, что дает им селективное преимущество в росте по сравнению с эндогенными гепатоцитами Mut-/-. В результате ожидается и наблюдается более быстрый рост популяции, подвергшейся генному редактированию. Эту экспансию можно обнаружить по повышенным уровням трансгена, а также ALB-2A (ФИГ. 13A-ФИГ. 13B).
[000153] Эти данные указывают, что уровни полезной нагрузки могут увеличиваться со временем после доставки однократной дозы в ткани, в которой отсутствует экспрессия белка дикого типа, соответствующего полипептиду, кодируемому полезной нагрузкой. Эти данные также демонстрируют, что повышение уровня биомаркера сопровождается повышением уровня полезной нагрузки. Специалист в данной области сможет применить способы, раскрытые в настоящем документе, для обнаружения и анализа биомаркера в плазме, такого как ALB-2A, в качестве косвенного показателя экспрессии внутриклеточной полезной нагрузки (например, MUT).
Пример 10: Долговременное обнаружение и анализ биомаркера и полезной нагрузки
[000154] Настоящий пример демонстрирует, что способы, используемые в соответствии с настоящим раскрытием, позволяют проводить длительное обнаружение in vivo и анализ полезной нагрузки после доставки in vivo нуклеиновой кислоты, кодирующей полезную нагрузку, и нуклеиновой кислоты, кодирующей биомаркер. Настоящий пример также демонстрирует валидацию теста в том смысле, что кинетика экспрессии полезной нагрузки имеет сходство с кинетикой экспрессии биомаркера.
[000155] Взрослым мышам вводили внутривенно вирусный вектор, описанный в Примере 2. Анализ уровня человеческого фактора IX в плазме крови, который экспрессируется из интегрированного трансгена, выявил сходную с ALB-2A кинетику с 1 по 16 неделю (ФИГ. 15A-15B), быстро увеличиваясь в течение первых недель после инъекции до достижения стабильного состояния.
[000156] Эти данные демонстрируют, что экспрессия полезной нагрузки (например, фактора IX) может оцениваться в течение длительного периода времени (например, до 16 недель) после доставки через вирусный вектор. Важно отметить, что эти данные подтверждают сходную кинетику экспрессии полезной нагрузки и уровня в плазме биомаркера, доставленного вместе с полезной нагрузкой (например, пептида 2A) в течение нескольких временных интервалов после первоначальной доставки полезной нагрузки.
Пример 11: Дозозависимое обнаружение и анализ биомаркера, гДНК и полезной нагрузки
[000157] Настоящий пример демонстрирует, что способы, используемые в соответствии с настоящим раскрытием, позволяют проводить дозозависимое обнаружение и анализ полезной нагрузки после доставки in vivo нуклеиновой кислоты, кодирующей биомаркер.
[000158] Эти данные показывают, что способы, используемые в соответствии с настоящим раскрытием, обеспечивают дозозависимую экспрессию полезной нагрузки, здесь внутриклеточной полезной нагрузки (например, mMUT) или секретируемой полезной нагрузки (например, cA1AT), экспрессия которых может быть оценена путем обнаружения и анализа экспрессии детектируемого фрагмента, слитого с полипептидом, кодируемым геном сайта-мишени (например, ALB-2A). Эти данные также демонстрируют, что дозозависимые изменения экспрессии секретируемой полезной нагрузки (например, cA1AT) могут быть отражены в аналогичных изменениях уровня в плазме детектируемого фрагмента (например, пептида 2A), так что обнаружение уровня в плазме детектируемого фрагмента может служить косвенным показателем для обнаружения секретируемой полезной нагрузки (ФИГ. 16A-C). Кроме того, эти данные демонстрируют, что уровни геномной интеграции для внутриклеточной полезной нагрузки могут также коррелировать с аналогичными изменениями в уровнях в плазме детектируемого фрагмента (ФИГ. 17A-C).
Эквиваленты и сфера применения
Специалисты в данной области признают или смогут установить с помощью не более чем обычного эксперимента множество эквивалентов конкретных вариантов реализации изобретения, описанных в настоящем документе. Объем настоящего изобретения не ограничивается приведенным выше описанием, а соответствует приведенной ниже формуле изобретения:
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> LogicBio Therapeutics, Inc.
<120> МОНИТОРИНГ ГЕННОЙ ТЕРАПИИ
<130> 2012538-0082
<150> 62/833875
<151> 15.04.2019
<160> 7
<170> Версия патентования 3.5
<210> 1
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетический полипептид
<400> 1
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 2
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 2
gccaccaact tcagcctgct gaaacaggcc ggcgacgtgg aagagaaccc tggcccc 57
<210> 3
<211> 4172
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 3
aggttcgaac cctgctgaag ggagaggttc caatactaca aaatgtagcg ggatattgtc 60
atcacctttg gggacatgtc atcatggtcc ccagacagag ttacaaaact catcccctac 120
acagcactat gtctctggta ctgtttgttc tacagatgtc aacaacagag gcccagccat 180
ctcctattgc ttggcttgtc agtctttcta gcctccccat tattaatttc aaatggggca 240
ggtgttagga gggcaaaaat ccacatatta agtgcaaagc ctttcaggag atttcctgaa 300
actagacaaa acccgtgtga ctggcatcga ttattctatt tgatctagct agtcctagca 360
aagtgacaac tgctactccc ctcctacaca gccaagattc ctaagttggc agtggcatgc 420
ttaatcctca aagccaaagt tacttggctc caagatttat agccttaaac tgtggcctca 480
cattccttcc tatcttactt tcctgcactg gggtaaatgt ctccttgctc ttcttgcttt 540
ctgtcctact gcagggctct tgctgagctg gtgaagcaca agcccaaggc tacagcggag 600
caactgaaga ctgtcatgga tgactttgca cagttcctgg atacatgttg caaggctgct 660
gacaaggaca cctgcttctc gactgaggtc agaaacgttt ttgcattttg acgatgttca 720
gtttccattt tctgtgcacg tggtcaggtg tagctctctg gaactcacac actgaataac 780
tccaccaatc tagatgttgt tctctacgta actgtaatag aaactgactt acgtagcttt 840
taatttttat tttctgccac actgctgcct attaaatacc tattatcact atttggtttc 900
aaatttgtga cacagaagag catagttaga aatacttgca aagcctagaa tcatgaactc 960
atttaaacct tgccctgaaa tgtttctttt tgaattgagt tattttacac atgaatggac 1020
agttaccatt atatatctga atcatttcac attccctccc atggcctaac aacagtttat 1080
cttcttattt tgggcacaac agatgtcaga gagcctgctt taggaattct aagtagaact 1140
gtaattaagc aatgcaaggc acgtacgttt actatgtcat tgcctatggc tatgaagtgc 1200
aaatcctaac agtcctgcta atacttttct aacatccatc atttctttgt tttcagggtc 1260
caaaccttgt cactagatgc aaagacgcct tagccggaag cggcgccacc aatttcagcc 1320
tgctgaaaca ggccggcgac gtggaagaga accctggccc tgctagccag cgcgtgaaca 1380
tgattatggc cgagagccct ggcctgatca ccatctgcct gctgggctac ctgctgagcg 1440
ccgagtgtac cgtgttcctg gaccacgaga acgccaacaa gatcctgaac agacccaaga 1500
gatacaacag cggcaagctg gaagagttcg tgcagggcaa cctggaacgc gagtgcatgg 1560
aagagaagtg cagcttcgaa gaggccagag aggtgttcga gaacaccgag agaaccaccg 1620
agttctggaa gcagtacgtg gacggcgacc agtgcgagag caacccttgt ctgaacggcg 1680
gcagctgcaa ggacgacatc aacagctacg agtgctggtg ccccttcggc ttcgagggca 1740
agaactgcga gctggacgtg acctgcaaca tcaagaacgg cagatgcgag cagttctgca 1800
agaacagcgc cgacaacaag gtcgtgtgct cctgcaccga gggctacaga ctggccgaga 1860
accagaagtc ctgcgagccc gctgtgcctt tcccatgcgg aagagtgtcc gtgtcccaga 1920
ccagcaagct gaccagagcc gagacagtgt tccccgacgt ggactacgtg aacagcaccg 1980
aggccgagac aatcctggac aacatcaccc agagcaccca gtccttcaac gacttcacca 2040
gagtcgtggg cggcgaggat gctaagcctg gccagttccc gtggcaggtg gtgctgaacg 2100
gaaaggtgga cgccttctgc ggcggctcca tcgtgaacga gaagtggatc gtgacagccg 2160
cccactgcgt ggaaaccggc gtgaagatca cagtggtggc cggcgagcac aacatcgagg 2220
aaaccgagca cacagagcag aaaagaaacg tgatcaggat catcccccac cacaactaca 2280
acgccgccat caacaagtac aaccacgata tcgccctgct ggaactggac gagcccctgg 2340
tgctgaatag ctacgtgacc cccatctgta tcgccgacaa agagtacacc aacatctttc 2400
tgaagttcgg cagcggctac gtgtccggct ggggcagagt gtttcacaag ggcagatccg 2460
ctctggtgct gcagtacctg agagtgcctc tggtggacag agccacctgt ctgagaagca 2520
ccaagttcac catctacaac aacatgttct gcgctggctt ccacgagggc ggcagagact 2580
cttgtcaggg cgattctggc ggccctcacg tgacagaggt ggaaggcacc agctttctga 2640
ccggcatcat cagctggggc gaggaatgcg ccatgaaggg gaagtacggc atctacacca 2700
aggtgtccag atacgtgaac tggatcaaag aaaagaccaa gctgacataa gctagcttag 2760
cctaaacaca tcacaaccac aaccttctca ggtaactata cttgggactt aaaaaacata 2820
atcataatca tttttcctaa aacgatcaag actgataacc atttgacaag agccatacag 2880
acaagcacca gctggcactc ttaggtcttc acgtatggtc atcagtttgg gttccatttg 2940
tagataagaa actgaacata taaaggtcta ggttaatgca atttacacaa aaggagacca 3000
aaccagggag agaaggaacc aaaattaaaa attcaaacca gagcaaagga gttagccctg 3060
gttttgctct gacttacatg aaccactatg tggagtcctc catgttagcc tagtcaagct 3120
tatcctctgg atgaagttga aaccatatga aggaatattt ggggggtggg tcaaaacagt 3180
tgtgtatcaa tgattccatg tggtttgacc caatcattct gtgaatccat ttcaacagaa 3240
gatacaacgg gttctgtttc ataataagtg atccacttcc aaatttctga tgtgccccat 3300
gctaagcttt aacagaattt atcttcttat gacaaagcag cctcctttga aaatatagcc 3360
aactgcacac agctatgttg atcaattttg tttataatct tgcagaagag aattttttaa 3420
aatagggcaa taatggaagg ctttggcaaa aaaattgttt ctccatatga aaacaaaaaa 3480
cttatttttt tattcaagca aagaacctat agacataagg ctatttcaaa attatttcag 3540
ttttagaaag aattgaaagt tttgtagcat tctgagaaga cagctttcat ttgtaatcat 3600
aggtaatatg taggtcctca gaaatggtga gacccctgac tttgacactt ggggactctg 3660
agggaccagt gatgaagagg gcacaactta tatcacacat gcacgagttg gggtgagagg 3720
gtgtcacaac atctatcagt gtgtcatctg cccaccaagt aacagatgtc agctaagact 3780
aggtcatgtg taggctgtct acaccagtga aaatcgcaaa aagaatctaa gaaattccac 3840
atttctagaa aataggtttg gaaaccgtat tccattttac aaaggacact tacatttctc 3900
tttttgtttt ccaggctacc ctgagaaaaa aagacatgaa gactcaggac tcatcttttc 3960
tgttggtgta aaatcaacac cctaaggaac acaaatttct ttaaacattt gacttcttgt 4020
ctctgtgctg caattaataa aaaatggaaa gaatctactc tgtggttcag aactctatct 4080
tccaaaggcg cgcttcaccc tagcagcctc tttggctcag aggaatccct gcctttcctc 4140
ccttcatctc agcagagaat gtagttccac at 4172
<210> 4
<211> 4312
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 4
actccatgaa agtggatttt attatcctca tcatgcagat gagaatattg agacttatag 60
cggtatgcct gagccccaaa gtactcagag ttgcctggct ccaagattta taatcttaaa 120
tgatgggact accatcctta ctctctccat ttttctatac gtgagtaatg ttttttctgt 180
tttttttttt tctttttcca ttcaaactca gtgcacttgt tgagcttgtg aaacacaagc 240
ccaaggcaac aaaagagcaa ctgaaagctg ttatggatga tttcgcagct tttgtagaga 300
agtgctgcaa ggctgacgat aaggagacct gctttgccga ggaggtacta cagttctctt 360
cattttaata tgtccagtat tcatttttgc atgtttggtt aggctagggc ttagggattt 420
atatatcaaa ggaggctttg tacatgtggg acagggatct tattttacaa acaattgtct 480
tacaaaatga ataaaacagc actttgtttt tatctcctgc tctattgtgc catactgtta 540
aatgtttata atgcctgttc tgtttccaaa tttgtgatgc ttatgaatat taataggaat 600
atttgtaagg cctgaaatat tttgatcatg aaatcaaaac attaatttat ttaaacattt 660
acttgaaatg tggtggtttg tgatttagtt gattttatag gctagtggga gaatttacat 720
tcaaatgtct aaatcactta aaattgccct ttatggcctg acagtaactt ttttttattc 780
atttggggac aactatgtcc gtgagcttcc gtccagagat tatagtagta aattgtaatt 840
aaaggatatg atgcacgtga aatcactttg caatcatcaa tagcttcata aatgttaatt 900
ttgtatccta atagtaatgc taatattttc ctaacatctg tcatgtcttt gtgttcaggg 960
taaaaaactt gttgctgcaa gtcaagctgc cttaggctta ggcagcggcg ccaccaactt 1020
cagcctgctg aaacaggccg gcgacgtgga agagaaccct ggccccctga gagccaaaaa 1080
ccagctgttc ctgctgagcc cccactatct gagacaggtc aaagaaagtt ccgggagtag 1140
actgatccag cagagactgc tgcaccagca gcagccactg catcctgagt gggccgctct 1200
ggccaagaaa cagctgaagg gcaaaaaccc agaagacctg atctggcaca ctccagaggg 1260
gatttcaatc aagcccctgt acagcaaaag ggacactatg gatctgccag aggaactgcc 1320
aggagtgaag cctttcaccc gcggacctta cccaactatg tatacctttc gaccctggac 1380
aattcggcag tacgccggct tcagtactgt ggaggaatca aacaagtttt ataaggacaa 1440
catcaaggct ggacagcagg gcctgagtgt ggcattcgat ctggccacac atcgcggcta 1500
tgactcagat aatcccagag tcagggggga cgtgggaatg gcaggagtcg ctatcgacac 1560
agtggaagat actaagattc tgttcgatgg aatccctctg gagaaaatgt ctgtgagtat 1620
gacaatgaac ggcgctgtca ttcccgtgct ggcaaacttc atcgtcactg gcgaggaaca 1680
gggggtgcct aaggaaaaac tgaccggcac aattcagaac gacatcctga aggagttcat 1740
ggtgcggaat acttacattt ttccccctga accatccatg aaaatcattg ccgatatctt 1800
cgagtacacc gctaagcaca tgcccaagtt caactcaatt agcatctccg ggtatcatat 1860
gcaggaagca ggagccgacg ctattctgga gctggcttac accctggcag atggcctgga 1920
atattctcga accggactgc aggcaggcct gacaatcgac gagttcgctc ctagactgag 1980
tttcttttgg ggaattggca tgaactttta catggagatc gccaagatga gggctggccg 2040
gagactgtgg gcacacctga tcgagaagat gttccagcct aagaactcta agagtctgct 2100
gctgcgggcc cattgccaga catccggctg gtctctgact gaacaggacc catataacaa 2160
tattgtcaga accgcaatcg aggcaatggc agccgtgttc ggaggaaccc agagcctgca 2220
cacaaactcc tttgatgagg ccctggggct gcctaccgtg aagtctgcta ggattgcacg 2280
caatacacag atcattatcc aggaggaatc cggaatccca aaggtggccg atccctgggg 2340
aggctcttac atgatggagt gcctgacaaa cgacgtgtat gatgctgcac tgaagctgat 2400
taatgaaatc gaggaaatgg ggggaatggc aaaggccgtg gctgagggca ttccaaaact 2460
gaggatcgag gaatgtgcag ctaggcgcca ggcacgaatt gactcaggaa gcgaagtgat 2520
cgtcggggtg aataagtacc agctggagaa agaagacgca gtcgaagtgc tggccatcga 2580
taacacaagc gtgcgcaatc gacagattga gaagctgaag aaaatcaaaa gctcccgcga 2640
tcaggcactg gccgaacgat gcctggcagc cctgactgag tgtgctgcaa gcggggacgg 2700
aaacattctg gctctggcag tcgatgcctc ccgggctaga tgcactgtgg gggaaatcac 2760
cgacgccctg aagaaagtct tcggagagca caaggccaat gatcggatgg tgagcggcgc 2820
ttatagacag gagttcgggg aatctaaaga gattaccagt gccatcaaga gggtgcacaa 2880
gttcatggag agagaagggc gacggcccag gctgctggtg gcaaagatgg gacaggacgg 2940
acatgatcgc ggagcaaaag tcattgccac cgggttcgct gacctgggat ttgacgtgga 3000
tatcggccct ctgttccaga caccacgaga ggtcgcacag caggcagtcg acgctgatgt 3060
gcacgcagtc ggagtgtcca ctctggcagc tggccataag accctggtgc ctgaactgat 3120
caaagagctg aactctctgg gcagaccaga catcctggtc atgtgcggcg gcgtgatccc 3180
accccaggat tacgaattcc tgtttgaggt cggggtgagc aacgtgttcg gaccaggaac 3240
caggatccct aaggccgcag tgcaggtcct ggatgatatt gaaaagtgtc tggaaaagaa 3300
acagcagtca gtgtaacatc acatttaaaa gcatctcagg taactatatt ttgaattttt 3360
taaaaaagta actataatag ttattattaa aatagcaaag attgaccatt tccaagagcc 3420
atatagacca gcaccgacca ctattctaaa ctatttatgt atgtaaatat tagcttttaa 3480
aattctcaaa atagttgctg agttgggaac cactattatt tctattttgt agatgagaaa 3540
atgaagataa acatcaaagc atagattaag taattttcca aagggtcaaa attcaaaatt 3600
gaaaccaaag tttcagtgtt gcccattgtc ctgttctgac ttatatgatg cggtacacag 3660
agccatccaa gtaagtgatg gctcagcagt ggaatactct gggaattagg ctgaaccaca 3720
tgaaagagtg ctttataggg caaaaacagt tgaatatcag tgatttcaca tggttcaacc 3780
taatagttca actcatcctt tccattggag aatatgatgg atctaccttc tgtgaacttt 3840
atagtgaaga atctgctatt acatttccaa tttgtcaaca tgctgagctt taataggact 3900
tatcttctta tgacaacatt tattggtgtg tccccttgcc tagcccaaca gaagaattca 3960
gcagccgtaa gtctaggaca ggcttaaatt gttttcactg gtgtaaattg cagaaagatg 4020
atctaagtaa tttggcattt attttaatag gtttgaaaaa cacatgccat tttacaaata 4080
agacttatat ttgtcctttt gtttttcagc ctaccatgag aataagagaa agaaaatgaa 4140
gatcaaaagc ttattcatct gtttttcttt ttcgttggtg taaagccaac accctgtcta 4200
aaaaacataa atttctttaa tcattttgcc tcttttctct gtgcttcaat taataaaaaa 4260
tggaaagaat ctaatagagt ggtacagcac tgttattttt caaagatgtg tt 4312
<210> 5
<211> 4307
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 5
ttacttggtg ggcagatgac acactgatag atgttgtgac accctctcac cccaactcgt 60
gcatgtgtga tataagttgt gccctcttca tcactggtcc ctcagagtcc ccaagtgtca 120
aagtcagggg tctcaccatt tctgaggacc tacatattac ctatgattac aaatgaaagc 180
tgtcttctca gaatgctaca aaactttcaa ttctttctaa aactgaaata attttgaaat 240
agccttatgt ctataggttc tttgcttgaa taaaaaaata agttttttgt tttcatatgg 300
agaaacaatt tttttgccaa agccttccat tattgcccta ttttaaaaaa ttctcttctg 360
caagattata aacaaaattg atcaacatag ctgtgtgcag ttggctatat tttcaaagga 420
ggctgctttg tcataagaag ataaattctg ttaaagctta gcatggggca catcagaaat 480
ttggaagtgg atcacttatt atgaaacaga acccgttgta tcttctgttg aaatggattc 540
acagaatgat tgggtcaaac cacatggaat cattgataca caactgtttt gacccacccc 600
ccaaatattc cttcatatgg tttcaacttc atccagagga taagcttgac taggctaaca 660
tggaggactc cacatagtgg ttcatgtaag tcagagcaaa accagggcta actcctttgc 720
tctggtttga atttttaatt ttggttcctt ctctccctgg tttggtctcc ttttgtgtaa 780
attgcattaa cctagacctt tatatgttca gtttcttatc tacaaatgga acccaaactg 840
atgaccatac gtgaagacct aagagtgcca gctggtgctt gtctgtatgg ctcttgtcaa 900
atggttatca gtcttgatcg ttttaggaaa aatgattatg attatgtttt ttaagtccca 960
agtatagtta cctgagaagg ttgtggttgt gatgtgttta cacagactgc tgcttctctg 1020
ccaaacactt ctcaatatca tcaagcactt ggacagcagc tcttggaatc cgggttccag 1080
gaccaaagac gttggaaaca ccaacttcat acagaaattc ataatcctgt ggtggaatca 1140
cgcccccaca catgacaagg atatctggcc gccccagggc ggtgagttct ttgataagct 1200
caggaacgag ggttttatga ccagcagcaa gtgtgctgac acccacagca tggacatctg 1260
catccacagc ttgctgcgcc acttcacggg gagtctgaaa aagagggcct atgtccacat 1320
caaaaccaag atcagcaaat cctgtagcaa tgaccttggc tcccctgtca tggccatctt 1380
gtcccatttt tgccacaaga agacgaggtc tgcgaccttc acgttccatg aatttattaa 1440
ctctcttgat ggcagatgtg atctctttac tttctccaaa ctcctgccga tatgctccac 1500
tcaccatacg atcattagct ttatgctcac caaatacttt tttcaaggca tccgtgattt 1560
ctccaactgt acatcttgca cgagctgcat ccactgccag agccagaata ttgccatctc 1620
cactggcagc acactgggta agtgcactga gacactgctc agccaaagct tgatccctgc 1680
tggatttaat cttcttgagt ttttcaatct gcttcttacg cactgaagtg ttgtcaatgg 1740
ccaggacctc cacagagtct tctttttcca actgatactt atttactcca acaattacct 1800
cagaaccaga atctattcta gcttgtcttc gggcagcaca ttcttcaatg cgaagtttag 1860
ggattccttc agctacagct ttggccattc cacccatttc ttcaacttca tatatcaact 1920
tcagagcagc ctcataaacg tcatttgtga gcgactccat catgtacgac cctccccaag 1980
gatccgccac tttggggatc ccagattctt cctgaatgat gatctgtgtg ttccgagcaa 2040
tccgggcact tttcacagtg ggcaaaccca gcgcttcatc aaaagagttc gtatgcaaag 2100
actgggttcc tccaaacaca gctgccatgg cttcgattgc agtgcggaca atgttattgt 2160
aaggatcctg ctcagtaagt gaccaccccg atgtctggca gtgtgctctt agaagaagag 2220
atttagagtt tttaggctgg aacatttttt ctattaagtg agcccacagt cttctcccag 2280
ctcgcatctt ggctatttcc atgtagaagt tcattccaat tccccagaag aaagacaacc 2340
ttggtgcaaa ttcatcaatt gtgagtccag cctggagtcc agttctgcag tactccaacc 2400
catctgcgat ggtataggcc agttctaaaa tggcatcagc tcctgcttcc tgcatatggt 2460
acccgctaat cgaaatggaa ttaaattttg gcatgtgctg tgctgtgtat tggaaaatgt 2520
cagcaataat tttcatcgat ggctctgggg gaaaaatata agtatttctg accataaact 2580
cctttaggat gtcattctga attgtgccag tgagcttctc cttcggcaca ccttgctctt 2640
ccccagttac tataaatgtt gccaggactg ggatgacagc tccgttcata gtcatggaaa 2700
cggacatttt ttctaaagga atgccatcaa ataggatttt ggtgtcttct acagtgtcaa 2760
tagcaactcc agccattcca acatctccac gaactctggg gttgtctgaa tcataaccac 2820
gatgtgttgc caagtcaaag gcaacagaca acccctgctg accagcctta atattgtcct 2880
tatagaattt attgctttct tccacagtac taaagcctgc atactgacgg atggtccagg 2940
gcctataggt atacatggta ggatatggtc cccgtgtgaa tggcttcact cctggaagtt 3000
cttcgggtaa gtccagagta tctgccctgg aatataaggg ctttatagag atcccttctg 3060
gggtgtgcca tataaggtcc tctgggtttt tgcctttcag ctgctttttg gccagtacag 3120
cccattctgg gtgaaggggt tgctgctggt gtagaaggcg tttccatctg gaagctgatg 3180
gaatgtttag ctgcttcagg taatggggcg atagcaaaaa aagttgattc ttagctctca 3240
aggggccagg gttctcttcc acgtcgccgg cctgtttcag caggctgaag ttggtggcgc 3300
cgctgccggc taaggcgtct ttgcatctag tgacaaggtt tggaccctga aaacaaagaa 3360
atgatggatg ttagaaaagt attagcagga ctgttaggat ttgcacttca tagccatagg 3420
caatgacata gtaaacgtac gtgccttgca ttgcttaatt acagttctac ttagaattcc 3480
taaagcaggc tctctgacat ctgttgtgcc caaaataaga agataaactg ttgttaggcc 3540
atgggaggga atgtgaaatg attcagatat ataatggtaa ctgtccattc atgtgtaaaa 3600
taactcaatt caaaaagaaa catttcaggg caaggtttaa atgagttcat gattctaggc 3660
tttgcaagta tttctaacta tgctcttctg tgtcacaaat ttgaaaccaa atagtgataa 3720
taggtattta ataggcagca gtgtggcaga aaataaaaat taaaagctac gtaagtcagt 3780
ttctattaca gttacgtaga gaacaacatc tagattggtg gagttattca gtgtgtgagt 3840
tccagagagc tacacctgac cacgtgcaca gaaaatggaa actgaacatc gtcaaaatgc 3900
aaaaacgttt ctgacctcag tcgagaagca ggtgtccttg tcagcagcct tgcaacatgt 3960
atccaggaac tgtgcaaagt catccatgac agtcttcagt tgctccgctg tagccttggg 4020
cttgtgcttc accagctcag caagagccct gcagtaggac agaaagcaag aagagcaagg 4080
agacatttac cccagtgcag gaaagtaaga taggaaggaa tgtgaggcca cagtttaagg 4140
ctataaatct tggagccaag taactttggc tttgaggatt aagcatgcca ctgccaactt 4200
aggaatcttg gctgtgtagg aggggagtag cagttgtcac tttgctagga ctagctagat 4260
caaatagaat aatcgatgcc agtcacacgg gttttgtcta gtttcag 4307
<210> 6
<211> 3344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 6
ctgaaactag acaaaacccg tgtgactggc atcgattatt ctatttgatc tagctagtcc 60
tagcaaagtg acaactgcta ctcccctcct acacagccaa gattcctaag ttggcagtgg 120
catgcttaat cctcaaagcc aaagttactt ggctccaaga tttatagcct taaactgtgg 180
cctcacattc cttcctatct tactttcctg cactggggta aatgtctcct tgctcttctt 240
gctttctgtc ctactgcagg gctcttgctg agctggtgaa gcacaagccc aaggctacag 300
cggagcaact gaagactgtc atggatgact ttgcacagtt cctggataca tgttgcaagg 360
ctgctgacaa ggacacctgc ttctcgactg aggtcagaaa cgtttttgca ttttgacgat 420
gttcagtttc cattttctgt gcacgtggtc aggtgtagct ctctggaact cacacactga 480
ataactccac caatctagat gttgttctct acgtaactgt aatagaaact gacttacgta 540
gcttttaatt tttattttct gccacactgc tgcctattaa atacctatta tcactatttg 600
gtttcaaatt tgtgacacag aagagcatag ttagaaatac ttgcaaagcc tagaatcatg 660
aactcattta aaccttgccc tgaaatgttt ctttttgaat tgagttattt tacacatgaa 720
tggacagtta ccattatata tctgaatcat ttcacattcc ctcccatggc ctaacaacag 780
tttatcttct tattttgggc acaacagatg tcagagagcc tgctttagga attctaagta 840
gaactgtaat taagcaatgc aaggcacgta cgtttactat gtcattgcct atggctatga 900
agtgcaaatc ctaacagtcc tgctaatact tttctaacat ccatcatttc tttgttttca 960
gggtccaaac cttgtcacta gatgcaaaga cgccttagcc ggcagcggcg ccaccaactt 1020
cagcctgctg aaacaggccg gcgacgtgga agagaaccct ggcccctctt ctgtctcatg 1080
gggcgtcctc ctgctggctg gcctgtgctg cctgctcccc ggctctctgg ctgaggatcc 1140
ccagggagat gctgcccaaa aaacggatac atccctccat gatcaagacc acccaaccct 1200
caacaagatc acccccagcc tggctgagtt cggcttcagc ctataccgcc agctggcaca 1260
ccagtccaac agcaccaata tcttcttctc cccagtgagc atcgctacag cctttgcaat 1320
gctctccctg gggaccaagg ctgacactca cagtgaaatc ctggagggcc tgaatttcaa 1380
cgtcacggag attccggagg ctcaggtcca tgaaggcttc caggaactcc tccataccct 1440
caacaagcca gacagccagc tccagctgac caccggcaac ggcctgttcc tcaacaagtc 1500
actcaaagta gtggataagt ttttggagga tgtcaaaaaa ctgtaccact cagaagcctt 1560
ctctgtcaac tttgaggaca ccgaagaggc caagaaacag atcaacaatt acgtggagaa 1620
ggaaactcaa gggaaaattg tggatttggt caaggagctt gacagagaca cagtttttgc 1680
tctggtgaat tacatcttct ttaaaggcaa atgggagaga ccctttgacg ttgaggccac 1740
caaggaagag gacttccacg tggaccaggc gaccaccgtg aaggtgccca tgatgaggcg 1800
tttaggcatg tttaacatct accactgtga gaagctgtcc agctgggtgc tgctgatgaa 1860
atacctgggc aatgccaccg ccatcttctt cctgcctgat gaggggaaac tgcagcacct 1920
ggaaaatgaa ctcacccatg atatcatcac caagttcctg gaaaatgaaa acagcaggtc 1980
tgccaactta catttaccca gactggccat tactggaacc tatgatctga agacagtcct 2040
gggccacctg ggtatcacta aggtcttcag caatggggct gacctctcag ggatcacgga 2100
ggaggcaccc ctgaagctct ccaaggccgt gcataaggct gtgctgacca tcgatgagaa 2160
agggactgaa gctgctgggg ccatgttttt agaggccata cccatgtcta ttccccccga 2220
ggtcaagttc aacaaaccct ttgtcttctt aatgattgaa caaaatacca agtctcccct 2280
cttcatggga aaagtggtga atcccaccca gaaagagcag aagctgatca gcgaggagga 2340
cctgtaaaca catcacaacc acaaccttct caggtaacta tacttgggac ttaaaaaaca 2400
taatcataat catttttcct aaaacgatca agactgataa ccatttgaca agagccatac 2460
agacaagcac cagctggcac tcttaggtct tcacgtatgg tcatcagttt gggttccatt 2520
tgtagataag aaactgaaca tataaaggtc taggttaatg caatttacac aaaaggagac 2580
caaaccaggg agagaaggaa ccaaaattaa aaattcaaac cagagcaaag gagttagccc 2640
tggttttgct ctgacttaca tgaaccacta tgtggagtcc tccatgttag cctagtcaag 2700
cttatcctct ggatgaagtt gaaaccatat gaaggaatat ttggggggtg ggtcaaaaca 2760
gttgtgtatc aatgattcca tgtggtttga cccaatcatt ctgtgaatcc atttcaacag 2820
aagatacaac gggttctgtt tcataataag tgatccactt ccaaatttct gatgtgcccc 2880
atgctaagct ttaacagaat ttatcttctt atgacaaagc agcctccttt gaaaatatag 2940
ccaactgcac acagctatgt tgatcaattt tgtttataat cttgcagaag agaatttttt 3000
aaaatagggc aataatggaa ggctttggca aaaaaattgt ttctccatat gaaaacaaaa 3060
aacttatttt tttattcaag caaagaacct atagacataa ggctatttca aaattatttc 3120
agttttagaa agaattgaaa gttttgtagc attctgagaa gacagctttc atttgtaatc 3180
ataggtaata tgtaggtcct cagaaatggt gagacccctg actttgacac ttggggactc 3240
tgagggacca gtgatgaaga gggcacaact tatatcacac atgcacgagt tggggtgaga 3300
gggtgtcaca acatctatca gtgtgtcatc tgcccaccaa gtaa 3344
<210> 7
<211> 2844
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 7
ctactgcagg gctcttgctg agctggtgaa gcacaagccc aaggctacag cggagcaact 60
gaagactgtc atggatgact ttgcacagtt cctggataca tgttgcaagg ctgctgacaa 120
ggacacctgc ttctcgactg aggtcagaaa cgtttttgca ttttgacgat gttcagtttc 180
cattttctgt gcacgtggtc aggtgtagct ctctggaact cacacactga ataactccac 240
caatctagat gttgttctct acgtaactgt aatagaaact gacttacgta gcttttaatt 300
tttattttct gccacactgc tgcctattaa atacctatta tcactatttg gtttcaaatt 360
tgtgacacag aagagcatag ttagaaatac ttgcaaagcc tagaatcatg aactcattta 420
aaccttgccc tgaaatgttt ctttttgaat tgagttattt tacacatgaa tggacagtta 480
ccattatata tctgaatcat ttcacattcc ctcccatggc ctaacaacag tttatcttct 540
tattttgggc acaacagatg tcagagagcc tgctttagga attctaagta gaactgtaat 600
taagcaatgc aaggcacgta cgtttactat gtcattgcct atggctatga agtgcaaatc 660
ctaacagtcc tgctaatact tttctaacat ccatcatttc tttgttttca gggtccaaac 720
cttgtcacta gatgcaaaga cgccttagcc ggcagcggcg ccaccaactt cagcctgctg 780
aaacaggccg gcgacgtgga agagaaccct ggcccctctt ctgtctcatg gggcgtcctc 840
ctgctggctg gcctgtgctg cctgctcccc ggctctctgg ctgaggatcc ccagggagat 900
gctgcccaaa aaacggatac atccctccat gatcaagacc acccaaccct caacaagatc 960
acccccagcc tggctgagtt cggcttcagc ctataccgcc agctggcaca ccagtccaac 1020
agcaccaata tcttcttctc cccagtgagc atcgctacag cctttgcaat gctctccctg 1080
gggaccaagg ctgacactca cagtgaaatc ctggagggcc tgaatttcaa cgtcacggag 1140
attccggagg ctcaggtcca tgaaggcttc caggaactcc tccataccct caacaagcca 1200
gacagccagc tccagctgac caccggcaac ggcctgttcc tcaacaagtc actcaaagta 1260
gtggataagt ttttggagga tgtcaaaaaa ctgtaccact cagaagcctt ctctgtcaac 1320
tttgaggaca ccgaagaggc caagaaacag atcaacaatt acgtggagaa ggaaactcaa 1380
gggaaaattg tggatttggt caaggagctt gacagagaca cagtttttgc tctggtgaat 1440
tacatcttct ttaaaggcaa atgggagaga ccctttgacg ttgaggccac caaggaagag 1500
gacttccacg tggaccaggc gaccaccgtg aaggtgccca tgatgaggcg tttaggcatg 1560
tttaacatct accactgtga gaagctgtcc agctgggtgc tgctgatgaa atacctgggc 1620
aatgccaccg ccatcttctt cctgcctgat gaggggaaac tgcagcacct ggaaaatgaa 1680
ctcacccatg atatcatcac caagttcctg gaaaatgaaa acagcaggtc tgccaactta 1740
catttaccca gactggccat tactggaacc tatgatctga agacagtcct gggccacctg 1800
ggtatcacta aggtcttcag caatggggct gacctctcag ggatcacgga ggaggcaccc 1860
ctgaagctct ccaaggccgt gcataaggct gtgctgacca tcgatgagaa agggactgaa 1920
gctgctgggg ccatgttttt agaggccata cccatgtcta ttccccccga ggtcaagttc 1980
aacaaaccct ttgtcttctt aatgattgaa caaaatacca agtctcccct cttcatggga 2040
aaagtggtga atcccaccca gaaagagcag aagctgatca gcgaggagga cctgtaaaca 2100
catcacaacc acaaccttct caggtaacta tacttgggac ttaaaaaaca taatcataat 2160
catttttcct aaaacgatca agactgataa ccatttgaca agagccatac agacaagcac 2220
cagctggcac tcttaggtct tcacgtatgg tcatcagttt gggttccatt tgtagataag 2280
aaactgaaca tataaaggtc taggttaatg caatttacac aaaaggagac caaaccaggg 2340
agagaaggaa ccaaaattaa aaattcaaac cagagcaaag gagttagccc tggttttgct 2400
ctgacttaca tgaaccacta tgtggagtcc tccatgttag cctagtcaag cttatcctct 2460
ggatgaagtt gaaaccatat gaaggaatat ttggggggtg ggtcaaaaca gttgtgtatc 2520
aatgattcca tgtggtttga cccaatcatt ctgtgaatcc atttcaacag aagatacaac 2580
gggttctgtt tcataataag tgatccactt ccaaatttct gatgtgcccc atgctaagct 2640
ttaacagaat ttatcttctt atgacaaagc agcctccttt gaaaatatag ccaactgcac 2700
acagctatgt tgatcaattt tgtttataat cttgcagaag agaatttttt aaaatagggc 2760
aataatggaa ggctttggca aaaaaattgt ttctccatat gaaaacaaaa aacttatttt 2820
tttattcaag caaagaacct atag 2844
<---
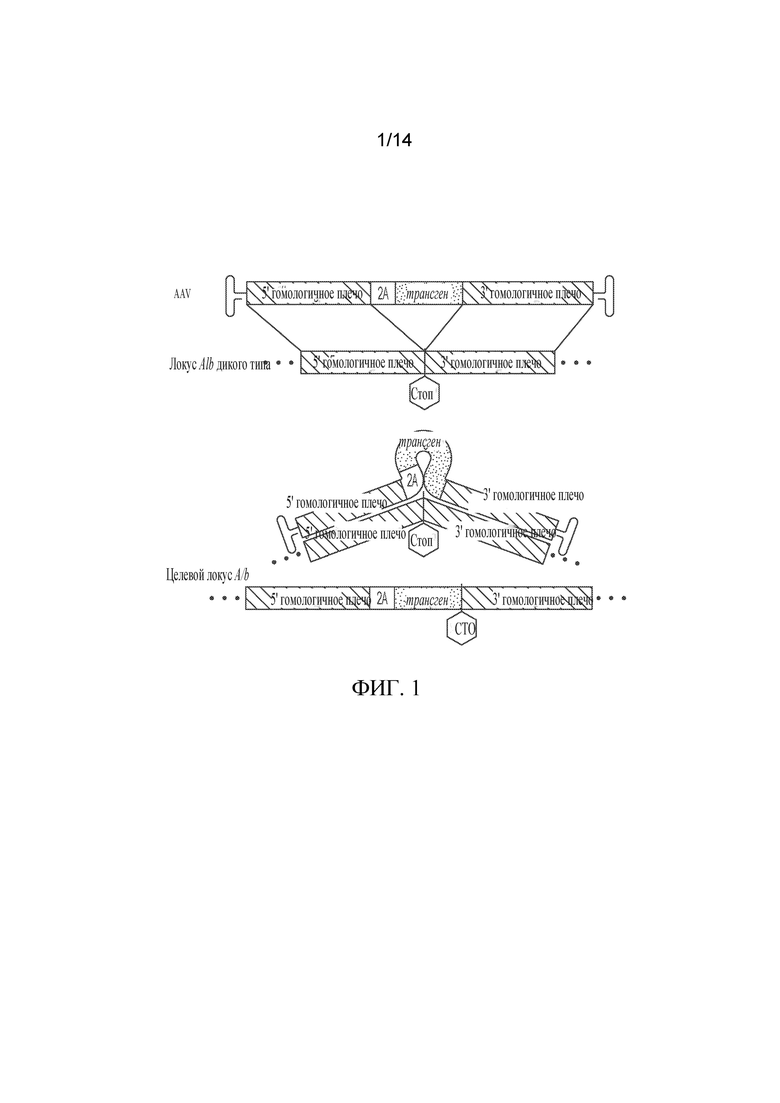
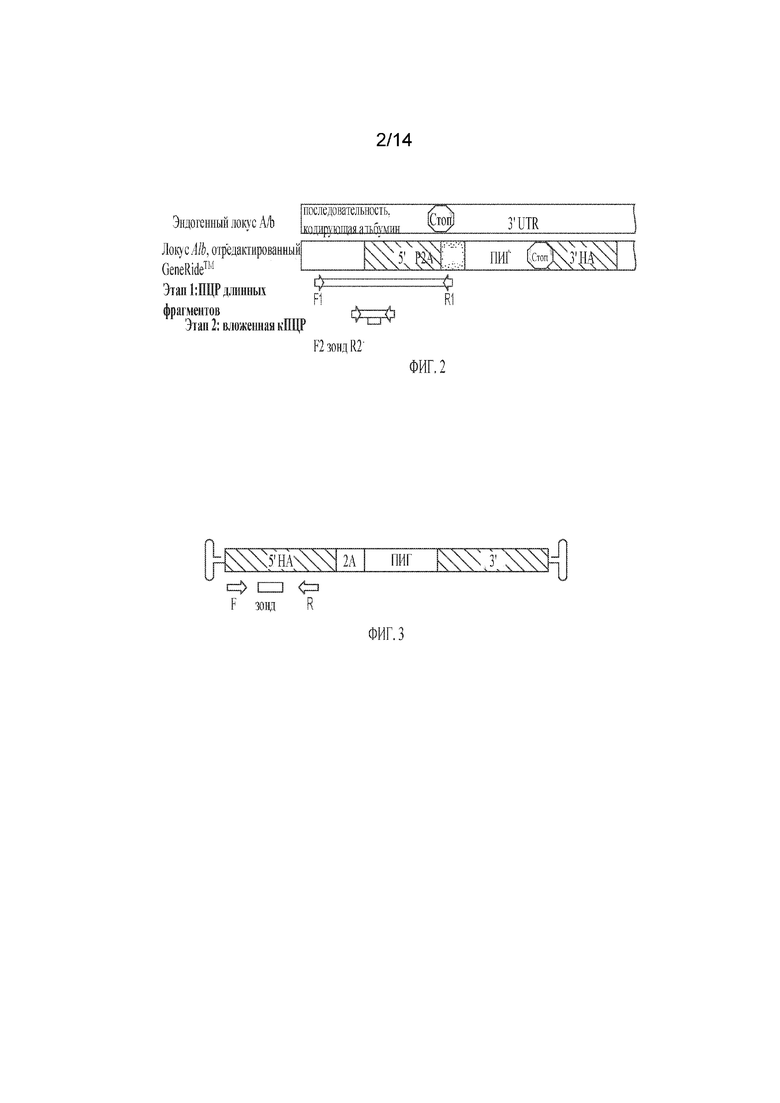
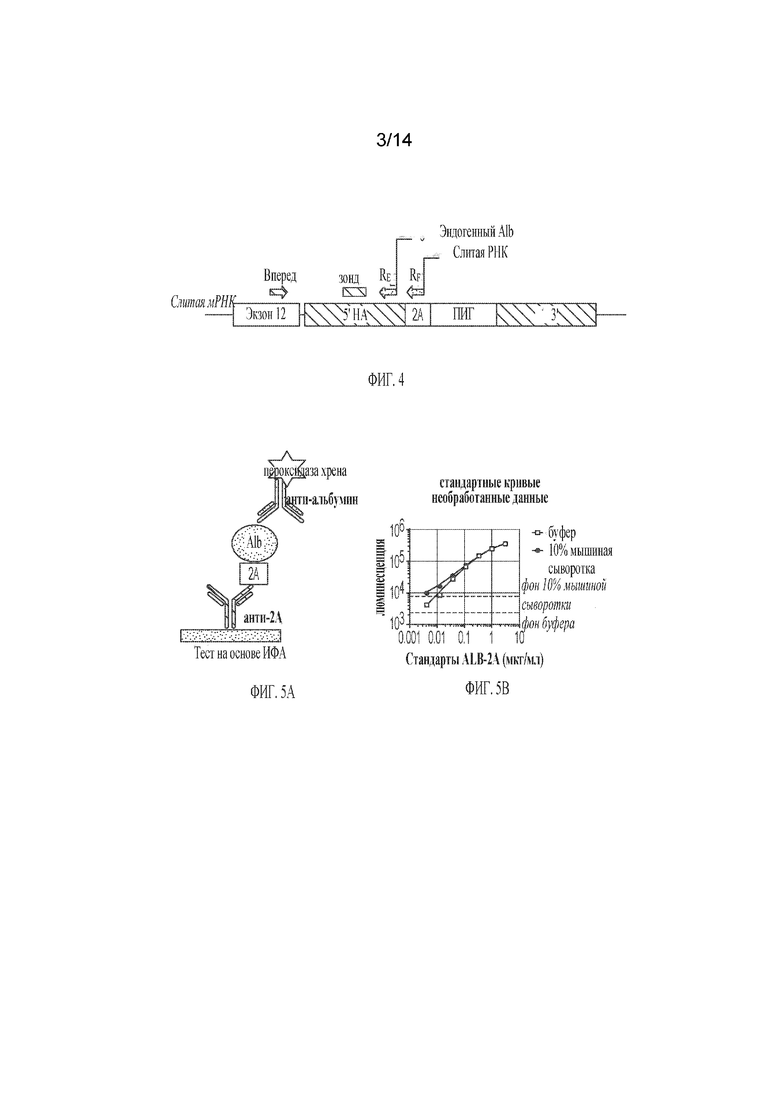
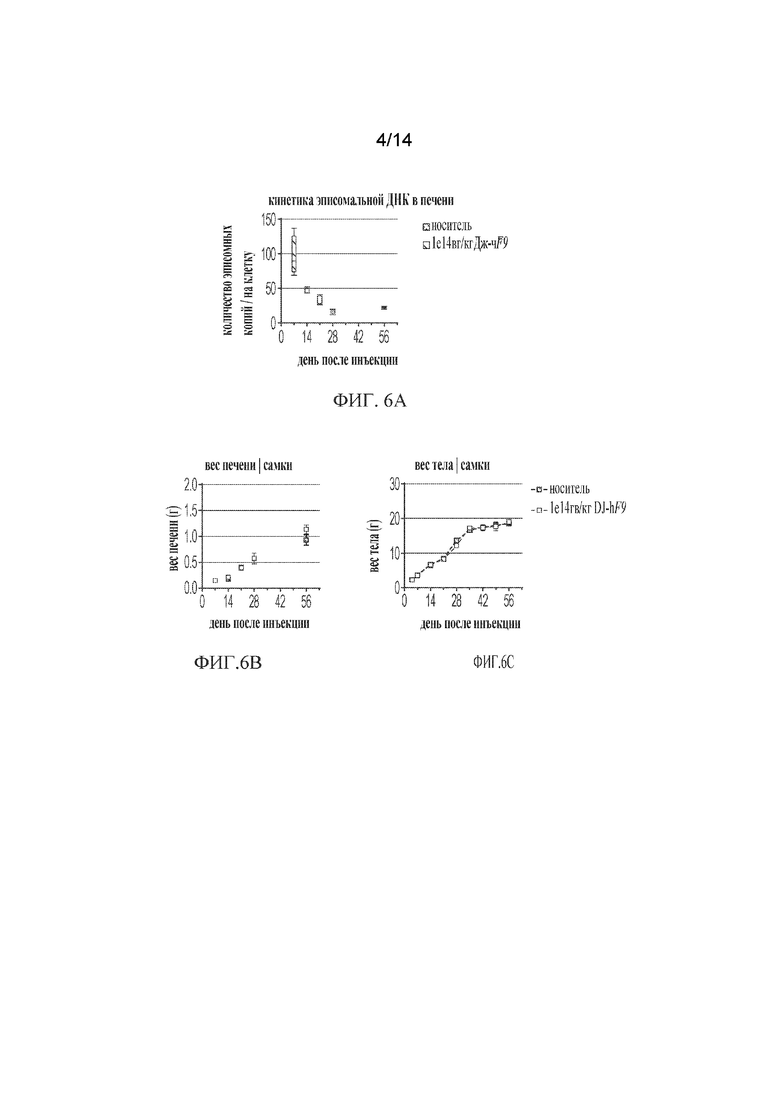
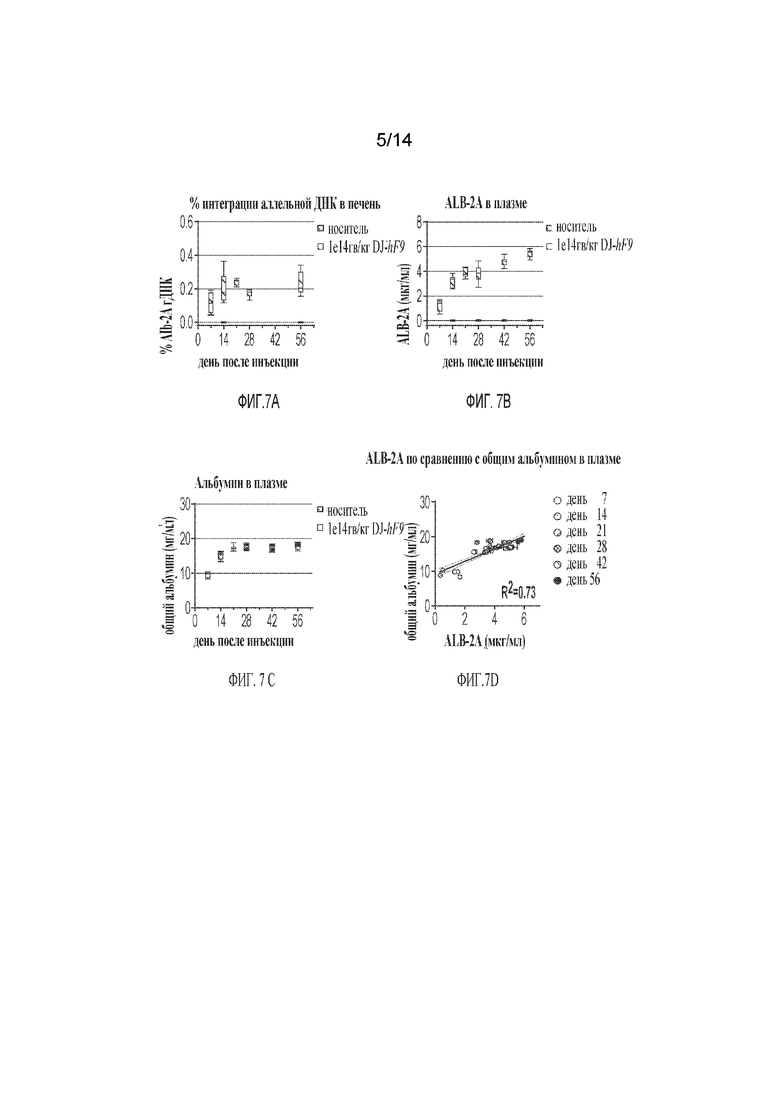
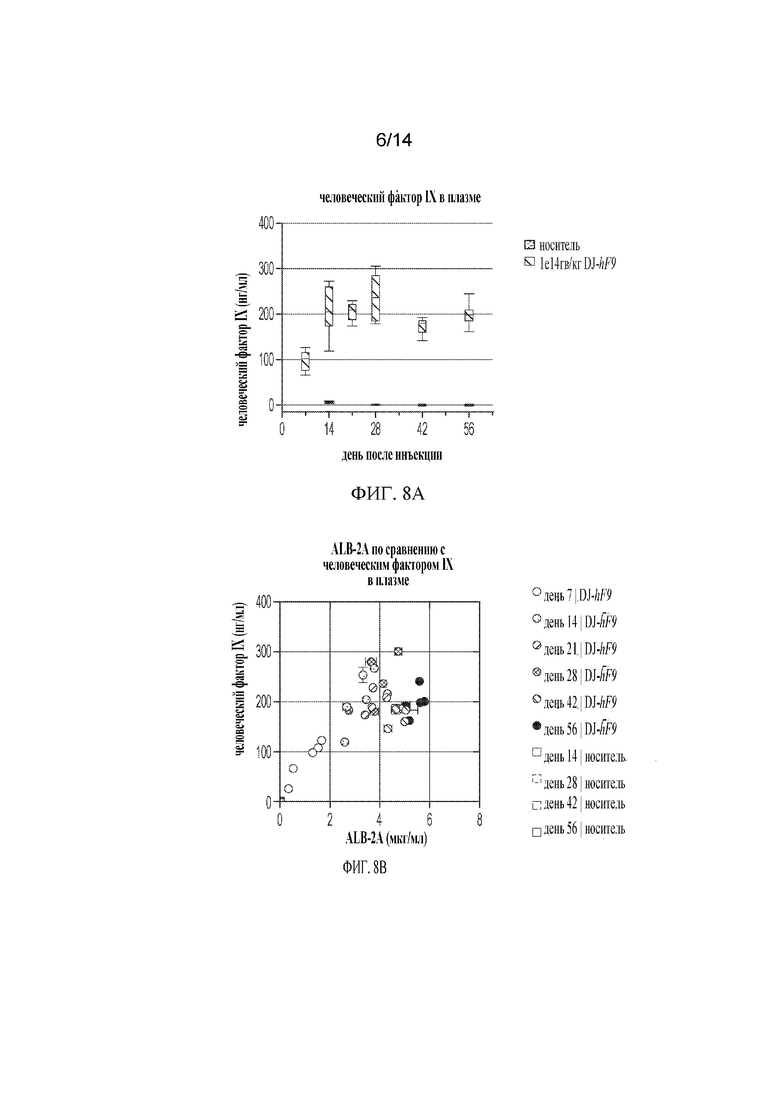
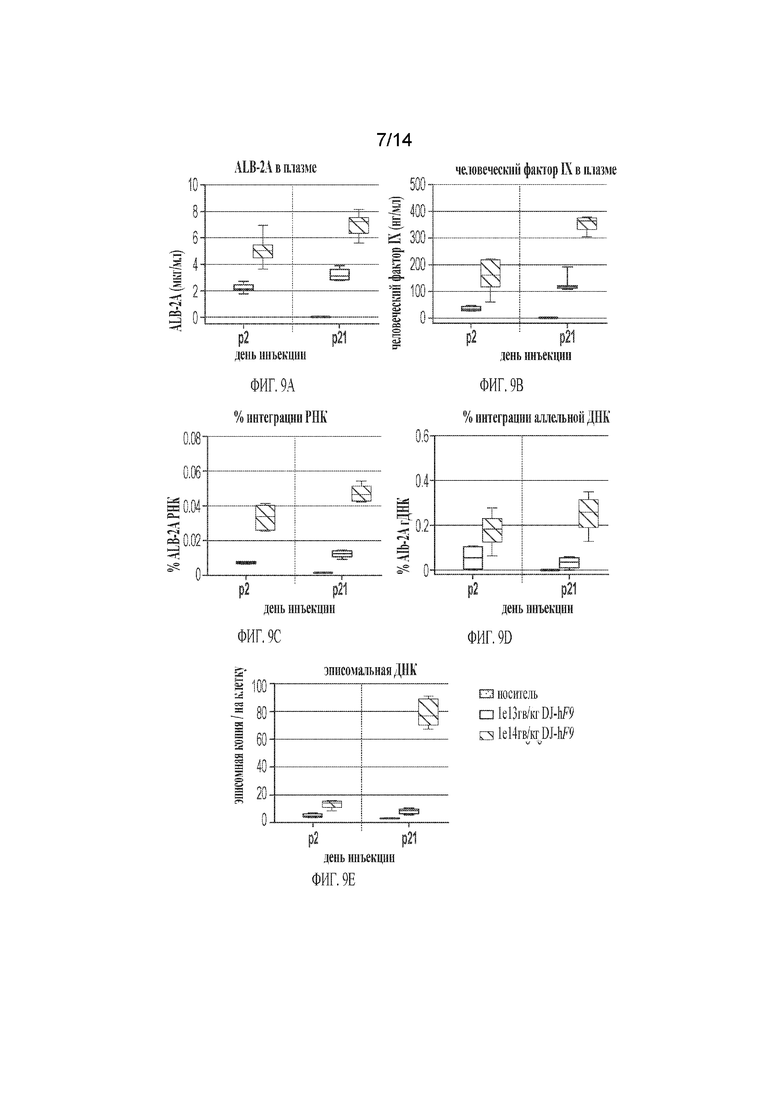
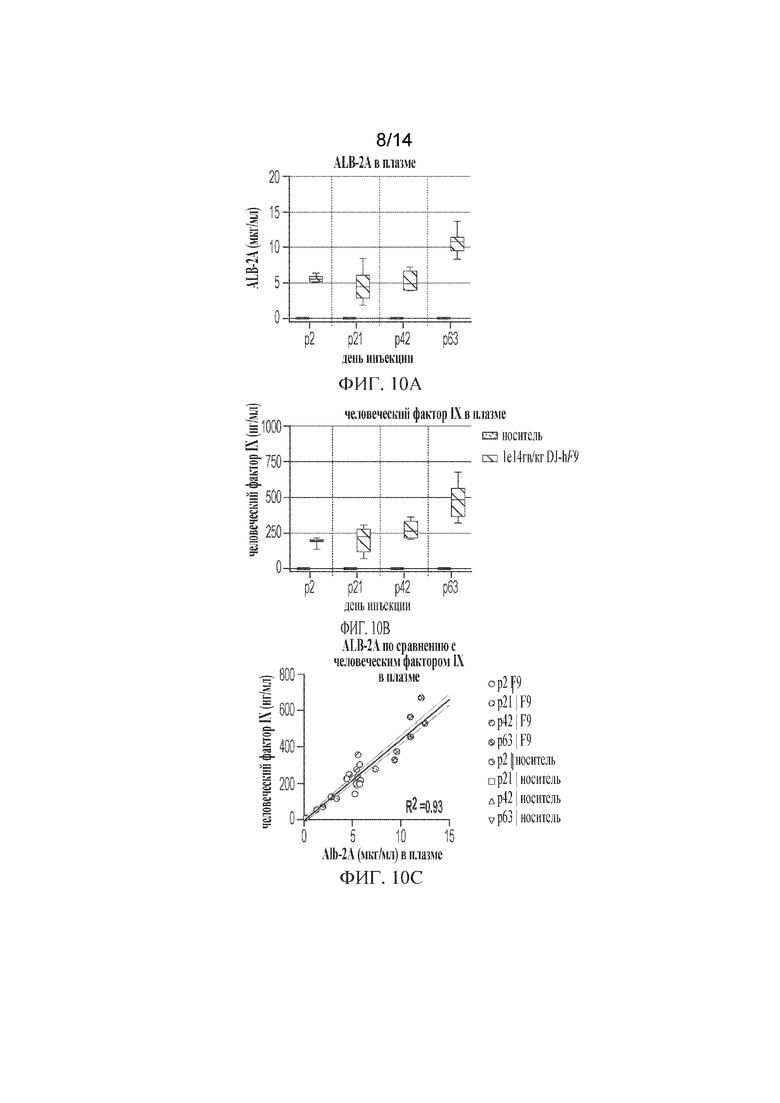
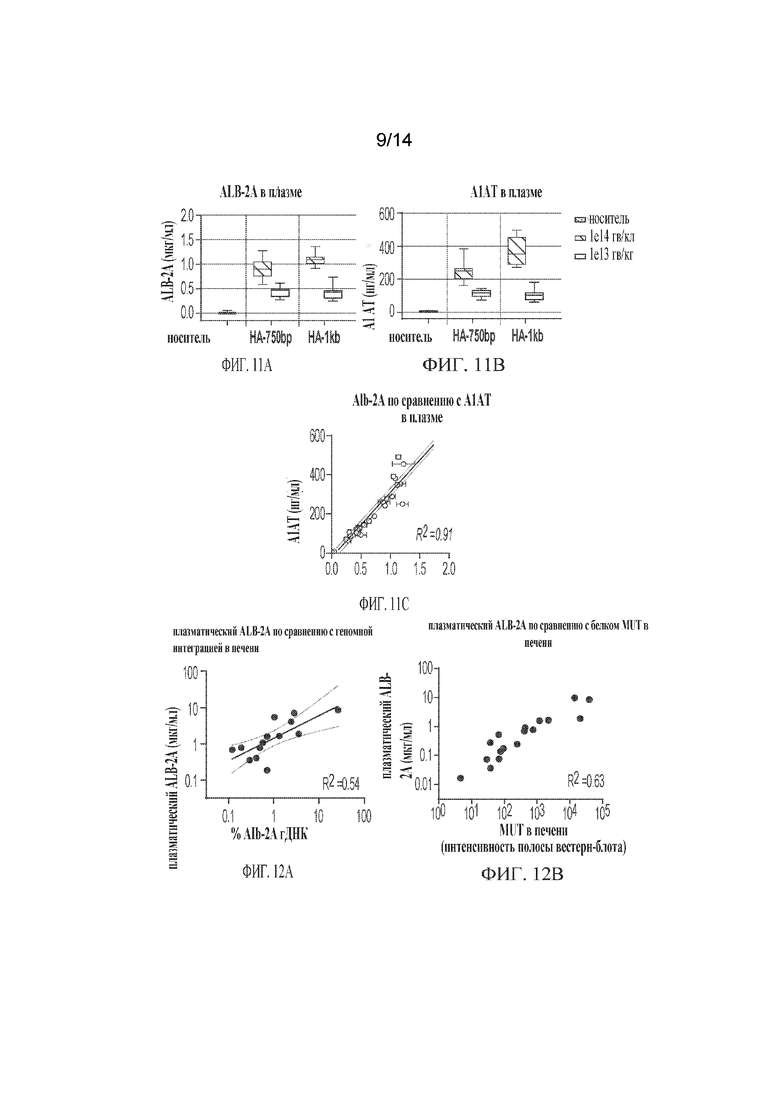
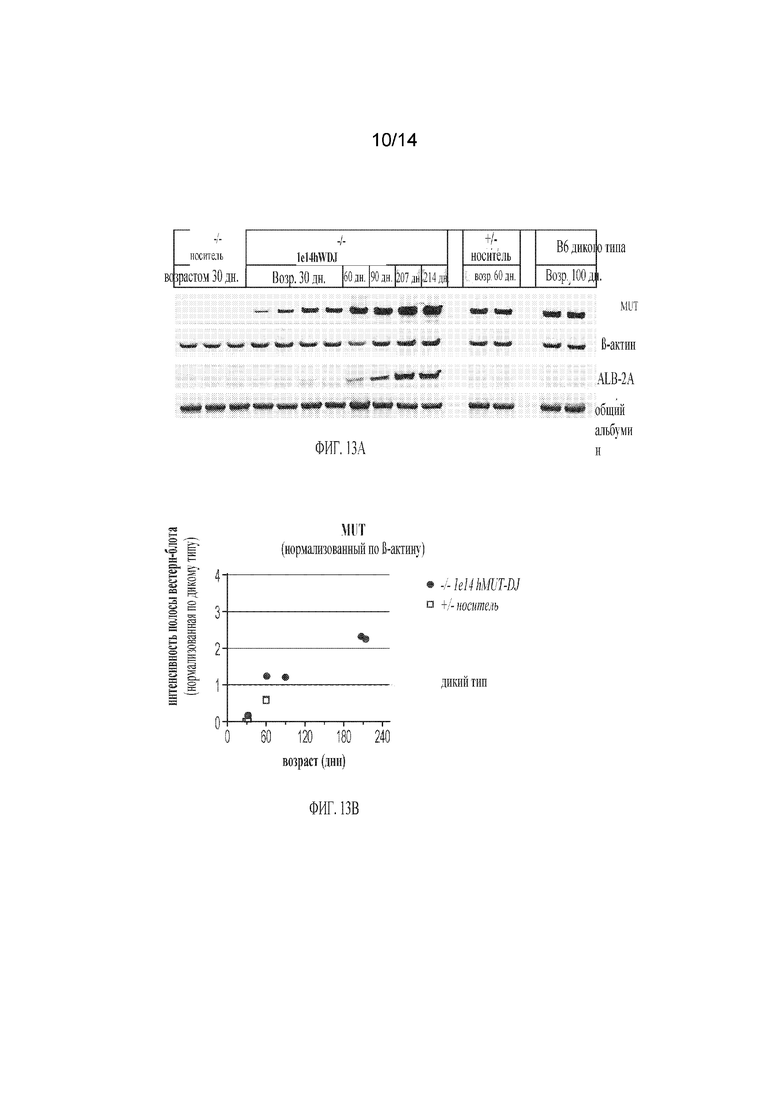
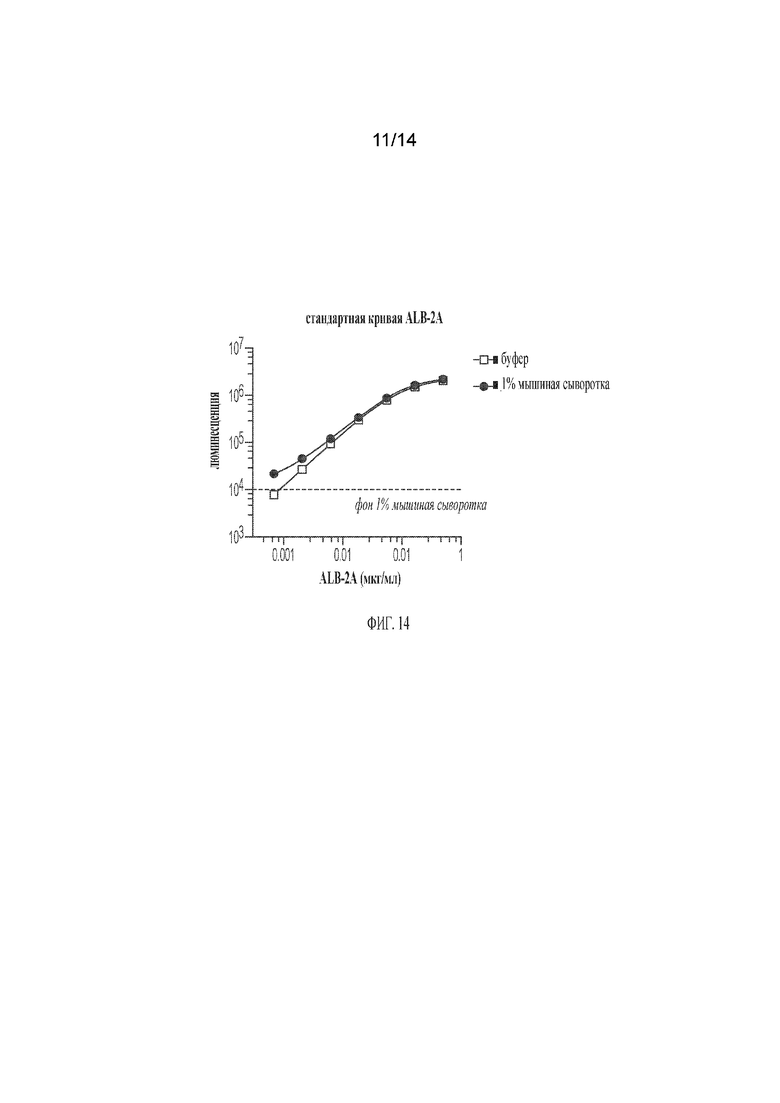
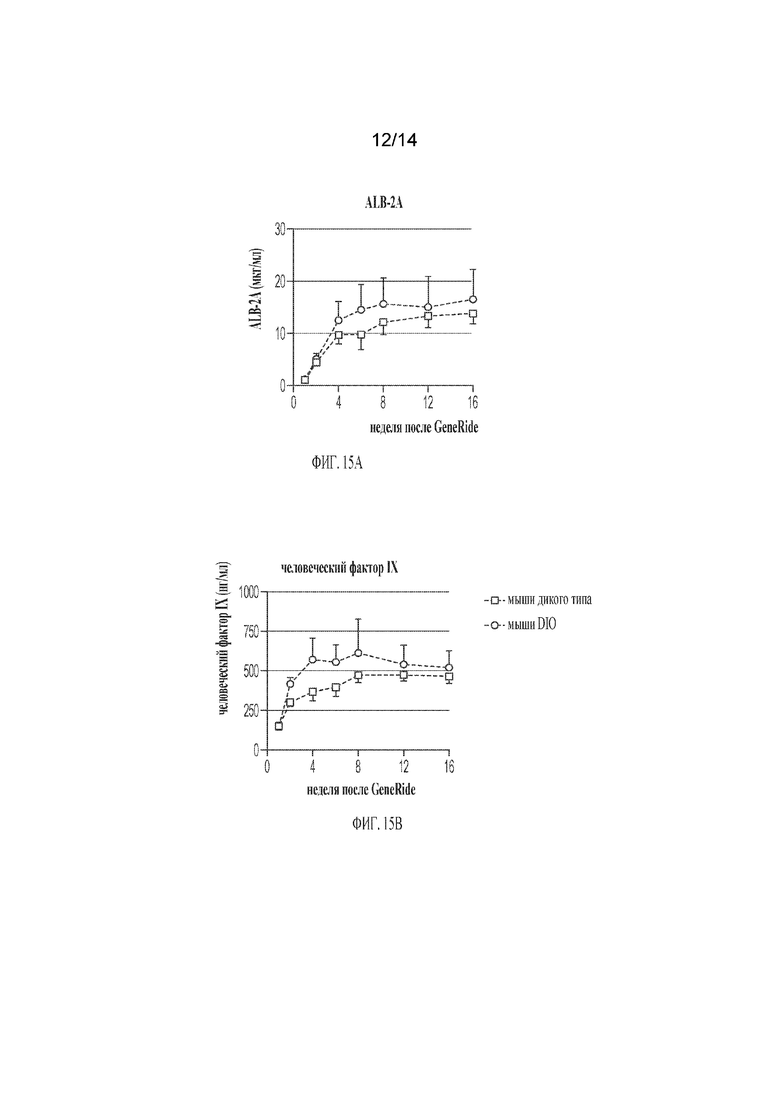
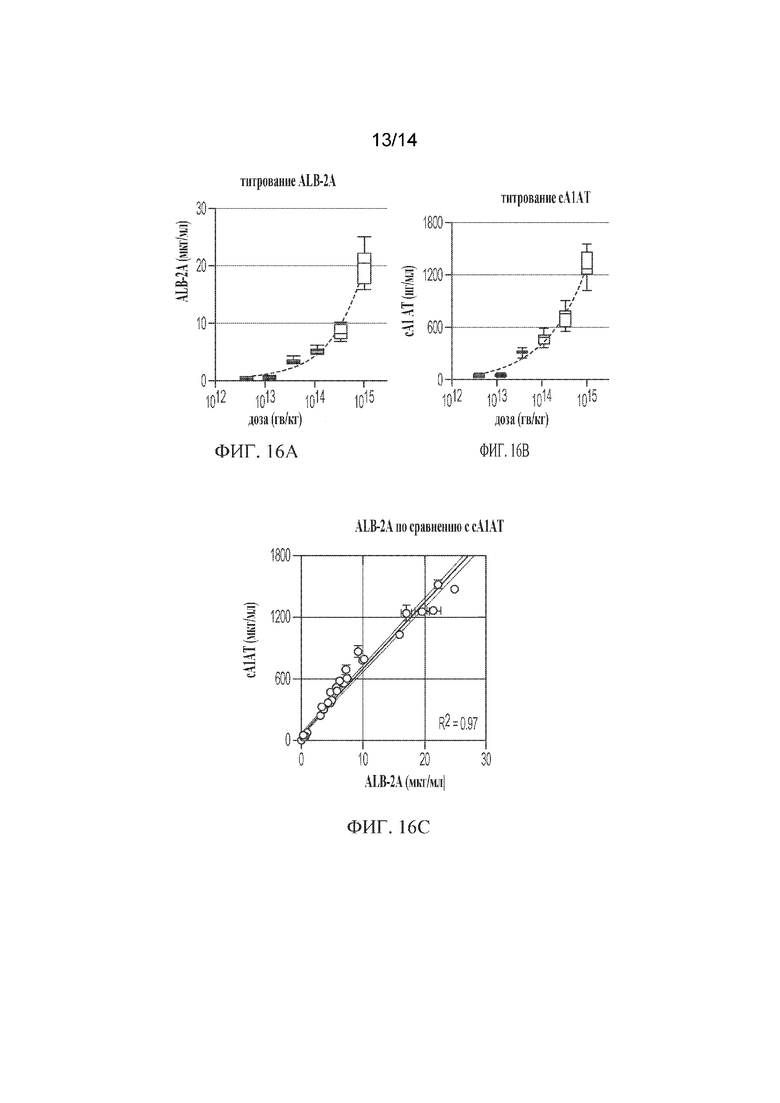
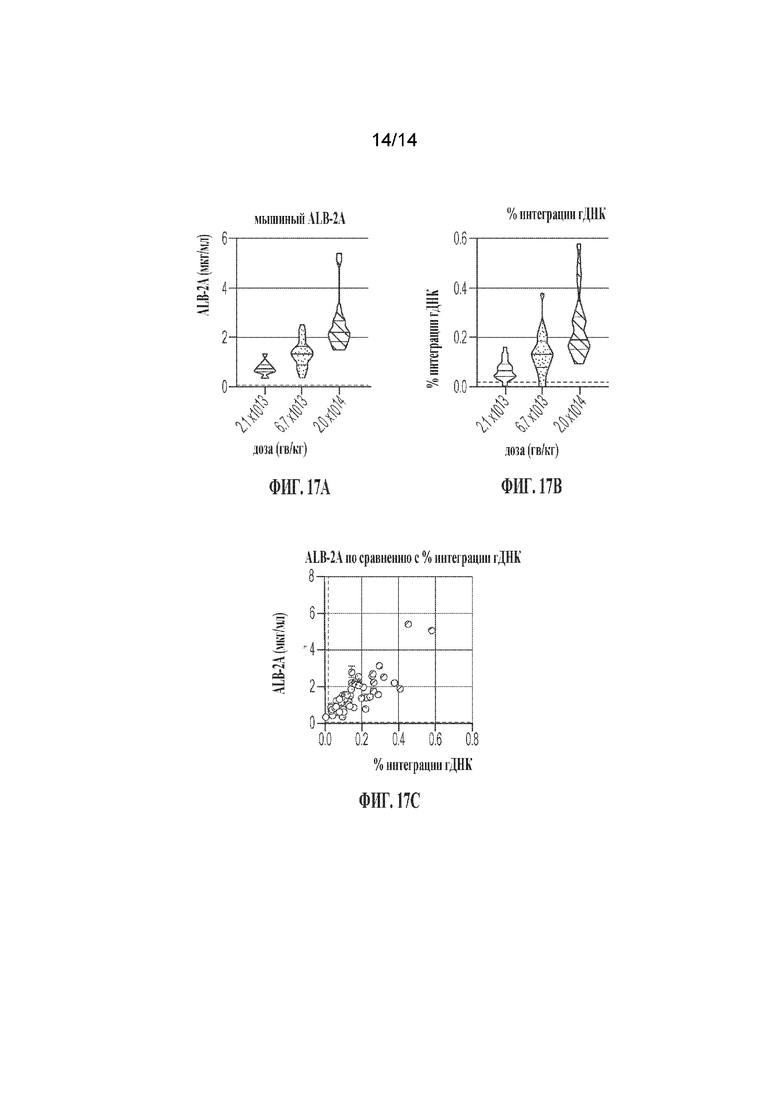
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая конструкцию для использования при измерении экспрессии терапевтической полезной нагрузки и способ мониторинга генной терапии. Конструкция содержит от 5' до 3' полинуклеотидную последовательность, кодирующую (а) 5'-гомологичное плечо, (б) кодирующую последовательность 2А, кодирующую пептид 2А, где кодирующая последовательность 2А содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 1, (c) терапевтическую полезную нагрузку и (d) 3'-гомологичное плечо, где указанная конструкция интегрируется в эндогенный сайт-мишень альбумина, так что локус альбумина транскрибируется с образованием альбумина-2А и терапевтической полезной нагрузки в виде отдельных белков. Изобретение расширяет арсенал средств для изменения экспрессии терапевтической полезной нагрузки. 2 н. и 18 з.п. ф-лы, 17 ил., 11 пр.
1. Конструкция для использования при измерении экспрессии терапевтической полезной нагрузки, содержащая от 5' до 3' полинуклеотидную последовательность, кодирующую (а) 5'-гомологичное плечо, (б) кодирующую последовательность 2А, кодирующую пептид 2А, где кодирующая последовательность 2А содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 1, (c) терапевтическую полезную нагрузку и (d) 3'-гомологичное плечо, где указанная конструкция интегрируется в эндогенный сайт-мишень альбумина, так что локус альбумина транскрибируется с образованием альбумина-2А и терапевтической полезной нагрузки в виде отдельных белков;
где пептид 2А функционирует как биомаркер для измерения экспрессии указанной терапевтической полезной нагрузки.
2. Конструкция для использования по п.1, где 5’- и 3’-гомологичные плечи конструкции имеют длину 1 т.о. каждое.
3. Конструкция для использования по п.1 или 2, где терапевтическая полезная нагрузка конструкции кодирует фенилаланин гидроксилазу (PAH), каталитическую субъединицу глюкого-6-фосфатазы (G6PC), пропионил-КоА карбоксилазу, субъединицу альфа (PCCA), кассетный транспортер, связывающий АТФ, член подсемейства B 11 (ABCB11), орнитин карбамоилтрансферазу (OTC), УДФ-глюкуронозилтрансферазу, семейство 1, член А1 (UGT1A1), кислую альфа-глюкозидазу (GAA), лизосомальную кислую глюкозилцерамидазу (GBA), фратаксин (FTX), фактор IX (F9), или альфа-1-антитрипсин (SERPINA1).
4. Конструкция для использования по любому из пп.1-3, где терапевтическая полезная нагрузка конструкции кодирует пептид, экспрессируемый внутриклеточно.
5. Конструкция для использования по любому из пп.1-4, где терапевтическая полезная нагрузка конструкции кодирует пептид, секретируемый внеклеточно.
6. Конструкция для использования по любому из пп.1-5, где терапевтическая полезная нагрузка конструкции кодирует пептид, обладающий внутриклеточной или внеклеточной активностью, который способствует биологическому процессу лечения медицинского состояния.
7. Конструкция для использования по любому из пп.1-6, где терапевтическая полезная нагрузка конструкции кодирует пептид, который обычно экспрессируется в клетках печени.
8. Конструкция для использования по любому из пп.1-7, где терапевтическая полезная нагрузка конструкции кодирует пептид, который эктопически экспрессируется в клетках печени.
9. Конструкция для использования по любому из пп.1-8, где интеграция конструкции существенно не нарушает экспрессию альбумина, кодируемого в сайте-мишени.
10. Конструкция для использования по любому из пп.1-9, где конструкция находится в AAV-векторе.
11. Способ мониторинга генной терапии, включающий:
(i) введение субъекту генотерапевтической конструкции, содержащей от 5' до 3' полинуклеотидную последовательность, кодирующую (а) 5'-гомологичное плечо, (б) кодирующую последовательность 2А, кодирующую пептид 2А, где кодирующая последовательность 2А содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO: 1, (c) терапевтическую полезную нагрузку и (d) 3'-гомологичное плечо, где указанная генотерапевтическая конструкция интегрируется в эндогенный сайт-мишень альбумина, так что локус альбумина транскрибируется с образованием альбумина-2А и терапевтической полезной нагрузки в виде отдельных белков; и
(ii) обнаружение экспрессии терапевтической полезной нагрузки путем измерения альбумина-2А в биологическом образце от субъекта, который получил геннотерапевтическую конструкцию,
где альбумин-2А служит биомаркером для мониторинга генной терапии.
12. Способ по п.11, где 5’- и 3’-гомологичные плечи имеют длину 1 т.о. каждое.
13. Способ по п.11 или 12, где терапевтическая полезная нагрузка геннотерапевтической конструкции кодирует фенилаланин гидроксилазу (PAH), каталитическую субъединицу глюкого-6-фосфатазы (G6PC), пропионил-КоА карбоксилазу, субъединицу альфа (PCCA), кассетный транспортер, связывающий АТФ, член подсемейства B 11 (ABCB11), орнитин карбамоилтрансферазу (OTC), УДФ-глюкуронозилтрансферазу, семейство 1, член А1 (UGT1A1), кислую альфа-глюкозидазу (GAA), лизосомальную кислую глюкозилцерамидазу (GBA), фратаксин (FTX), фактор IX (F9), или альфа-1-антитрипсин (SERPINA1).
14. Способ по любому из пп.11-13, где терапевтическая полезная нагрузка кодирует пептид, экспрессируемый внутриклеточно.
15. Способ по любому из пп.11-14, где терапевтическая полезная нагрузка кодирует пептид, секретируемый внеклеточно.
16. Способ по любому из пп.11-15, где терапевтическая полезная нагрузка кодирует пептид, обладающий внутриклеточной или внеклеточной активностью, который способствует биологическому процессу лечения медицинского состояния.
17. Способ по любому из пп.11-16, где терапевтическая полезная нагрузка кодирует пептид, который обычно экспрессируется в клетках печени.
18. Способ по любому из пп.11-17, где терапевтическая полезная нагрузка кодирует пептид, который эктопически экспрессируется в клетках печени.
19. Способ по любому из пп.11-18, где интеграция конструкции для генной терапии существенно не нарушает экспрессию альбумина, кодируемого в сайте-мишени.
20. Способ по любому из пп.11-19, где генотерапевтическая конструкция находится в AAV-векторе.
| US 6632800 B1, 14.10.2003 | |||
| WO 2018185468 A1, 11.10.2018 | |||
| ГЕНЕТИЧЕСКАЯ КОНСТРУКЦИЯ | 2016 |
|
RU2734678C2 |
Авторы
Даты
2024-09-02—Публикация
2020-04-14—Подача