РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка заявляет приоритет предварительной заявки США №62/671225, поданной
14 мая 2018 г., предварительной заявки США №62/756504, поданной 6 ноября 2018 г., и предварительной заявки США №62/756507, поданной 6 ноября 2018 г. Полное описание вышеуказанных заявок включено в данный документ посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка содержит Перечень последовательностей, который был подан в электронной форме в формате ASCII и в полном объеме включен в данный документ посредством ссылки. Указанная копия ASCII, созданная 14 мая 2019 г., называется 105365-0021_SL.txt и имеет размер 408319 байт.
УРОВЕНЬ ТЕХНИКИ
[1] Развитие зрелых иммунокомпетентных лимфоидных клеток из менее ко имитированных предшественников, их последующие антиген-обусловленные иммунные ответы и супрессия этих и нежелательных аутореактивных ответов сильно зависят от цитокинов и регулируются цитокинами (включая интерлейкин-2 [IL-2], IL-4, IL-7, IL-9, IL-15 и IL-21), которые используют рецепторы в общем семействе γ-цепей (γс) (Rochman et al., 2009), и представителями семейства, включающего IL-12, 18 и 23. IL-2 важен для развития клеток Treg в вилочковой железе и в значительной мере регулирует несколько ключевых аспектов зрелых периферических Treg и антиген-активируемых традиционных Т-клеток. Из-за его выраженной активности в качестве фактора роста Т-клеток in vitro, IL-2 широко изучают, частично вследствие этой активности, предоставляющей потенциальные средства для прямого повышения иммунитета, например, у пациентов со СПИД/ВИЧ, или мишень для антагонизации нежелательных ответов, например, отторжение трансплантата и аутоиммунные заболевания. Хотя in vitro исследования с IL-2 обеспечивают сильное обоснование для этих исследований, понятно, что функция IL-2 in vivo является намного сложнее, как было впервые продемонстрировано на мышах с дефицитом IL-2, у которых наблюдали быстрый летальный аутоиммунный синдром, а не отсутствие иммунитета (Sadlacket al., 1993, 1995). Сходные наблюдения были сделаны позже при индивидуальной абляции гена, кодирующего IL-2Rα (Il2ra) и IL-2Rβ (Il2rb) (Suzuki et al., 1995; Willerford et al., 1995).
[2] Данное изобретение относится к кондиционально активным и/или нацеленным цитокинам для применения в лечении рака и других заболеваний, зависимых от повышающей или понижающей регуляции иммунитета. Например, противоопухолевая активность некоторых цитокинов хорошо известна и описана, а некоторые цитокины уже используются в терапевтических целях для лечения людей. Такие цитокины, как интерлейкин-2 (IL-2), продемонстрировали положительную противоопухолевую активность у пациентов с разными типами опухолей, такими как метастатическая карцинома почки, волосатоклеточный лейкоз, саркома Капоши, меланома, множественная миелома и т.п. Другие цитокины, такие как IFNβ, фактор некроза опухоли (TNF) α, TNFβ, IL-1, 4, 6, 12, 15 и CSF демонстрировали определенную противоопухолевую активность в случае некоторых типов опухолей и, следовательно, являются предметом дополнительных исследований.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[3] В данном изобретении предложены терапевтические белки, нуклеиновые кислоты, которые кодируют белки, а также композиции и способы применения таких белков и нуклеиновых кислот для лечения заболевания или нарушения, такого как пролиферативное заболевание, опухолевое заболевание, воспалительное заболевание, иммунологическое нарушение, аутоиммунное заболевание, инфекционное заболевание, вирусное заболевание, аллергическая реакция, паразитарная реакция, болезнь «трансплантат против хозяина» и т.п.
[4] Данное изобретение относится к слитым белкам, которые являются кондиционально активными вариантами IL-2. В одном аспекте полноразмерные полипептиды по данному изобретению обладают сниженной или минимальной активностью активации рецептора IL-2 даже если они содержат функциональный полипептид цитокина. После активации, например, посредством расщепления линкера, который соединяет блокирующий фрагмент, например, стерически блокирующий полипептид, в последовательности с активным цитокином, IL-2 или его функциональным фрагментом или мутеином, может связывать свой рецептор и осуществлять сигнализацию. При необходимости полноразмерные полипептиды могут содержать блокирующий полипептидный фрагмент, который также обеспечивает дополнительные преимущественные свойства. Например, полноразмерный полипептид может блокирующий полипептидный фрагмент, который также продлевает сывороточное время полужизни и/или нацеливает полноразмерный полипептид на необходимый сайт активности IL-2. В альтернативном варианте полноразмерные слитые полипептиды могут содержать элемент продления сывороточного времени полужизни и/или нацеливающий домен, которые отличаются от блокирующего полипептидного фрагмента. Предпочтительно слитый белок содержит по меньшей мере один элемент, способный продлевать время полужизни в циркуляции in vivo. Предпочтительно этот элемент ферментативно удаляется в необходимом месте организма (например, за счет расщепления протеазой в микроокружении опухоли) с восстановлением фармакокинетических свойств нагрузочной молекулы (например, IL2 или IFNa), по существу сходных с нагрузочной молекулой природного происхождения. Предпочтительно слитые белки нацелены на необходимые клетку или ткань. Как описано в данном документе, нацеливание осуществляется посредством действия блокирующего полипептидного фрагмента, который также связывается с необходимой мишенью, или посредством нацеливающего домена. Домен, который распознает целевой антиген на предпочтительной мишени (например, опухолеспецифический антиген), может быть присоединен к цитокину посредством расщепляемого или нерасщепляемого линкера. При присоединении посредством нерасщепляемого линкера нацеливающий домен может дополнительно способствовать удержанию цитокина в опухоли и может считаться удерживающим доменом. Нацеливающий домен не обязательно должен быть напрямую связан с нагрузочной молекулой и может быть напрямую связан с другим элементом слитого белка. В особенности это справедливо для случаев, когда нацеливающий домен присоединен посредством расщепляемого линкера.
[5] В одном аспекте предложен слитый полипептид, содержащий полипептид IL-2 или его функциональный фрагмент или мутеин и блокирующий фрагмент, например, стерически блокирующий домен. Блокирующий фрагмент слит с полипептидом IL-2 напрямую или посредством линкера и может быть отделен от полипептида цитокина путем расщепления (например, опосредованного протеазой расщепления) слитого полипептида в или вблизи сайта слияния, или линкера, или в блокирующем фрагменте. Например, если полипептид цитокина слит с блокирующим фрагментом посредством линкера, который содержит сайт расщепления протеазой, полипептид цитокина отделяется от блокирующего фрагмента и может связывать свой рецептор после опосредованного протеазой расщепления линкера. Линкер сконструирован с возможностью расщепления в сайте необходимой цитокиновой активности, например, в микроокружении опухоли, с избежанием нецелевой цитокиновой активности и снижением общей токсичности цитокиновой терапии.
[6] Блокирующий фрагмент также может выполнять функцию элемента продления сывороточного времени полужизни. В некоторых вариантах осуществления слитый полипептид дополнительно содержит отдельный элемент продления сывороточного времени полужизни. В некоторых вариантах осуществления слитый полипептид дополнительно содержит нацеливающий домен. В различных вариантах осуществления элемент продления сывороточного времени полужизни представляет собой водорастворимый полипептид, такой как необязательно разветвленный или многозвеньевой полиэтиленгликоль (ПЭГ), полноразмерный человеческий сывороточный альбумин (ЧСА) или фрагмент, который сохраняет связывание с FcRn, Fc-фрагмент или нанотело, которое напрямую связывается с FcRn или с человеческим сывороточным альбумином.
[7] Помимо элементов продления сывороточного времени полужизни описанные в данном документе фармацевтические композиции предпочтительно содержат по меньшей мере один или более нацеливающих доменов, которые связываются с одним или более целевыми антигенами или одной или более областями на одном целевом антигене. В данном документе подразумевается, что полипептидная конструкция по изобретению расщепляется, например в патологическом микроокружении или в крови субъекта в сайте расщепления протеазой и что нацеливающий(ие) домен(ы) будет(ут) связываться с целевым антигеном на целевой клетке. По меньшей мере один целевой антиген вовлечен в процесс заболевания, нарушения или патологического состояния и/или связан с ним. Типовые антигены включают связанные с пролиферативным заболеванием, опухолевым заболеванием, воспалительным заболеванием, иммунологическим нарушением, аутоиммунным заболеванием, инфекционным заболеванием, вирусным заболеванием, аллергической реакцией, паразитарной реакцией, болезнью «трансплантат против хозяина» или болезнью «хозяин против трансплантата».
[8] В некоторых вариантах осуществления целевой антиген представляет собой молекулу клеточной поверхности, такую как белок, липид или полисахарид. В некоторых вариантах осуществления целевой антиген находится на опухолевой клетке, вирусно инфицированной клетке, бактериально инфицированной клетке, поврежденной красной кровяной клетке, клетке артериального тромбоцита или клетке фиброзной ткани.
[9] В некоторых случаях целевые антигены экспрессируются на поверхности патологической клетки или ткани, например, опухолевой или раковой клетки. Целевый антигены в случае опухолей включают, но не ограничиваются этим, белок активации фибробластов альфа (FAPa), гликопротеин трофобластов (5Т4), опухолеассоциированный трансдуктор кальциевого сигнала 2 (Trop2), EDB фибронектина (EDB-FN), домен EIIIB фибронектина, CGS-2, ЕрСАМ, EGFR, HER-2, HER-3, c-Met, FOLR1 и СЕА. Описанные в данном документе фармацевтические композиции также содержат белки, содержащие два антигенсвязывающих домена, которые связываются с двумя разными целевыми антигенами, которые, согласно известным данным, экспрессируются в патологической клетке или ткани. Примеры пар антигенсвязывающих доменов включают, но не ограничиваются этим, EGFR/CEA, ЕрСАМ/СЕА и HER-2/HER-3.
[10] В некоторых вариантах осуществления нацеливающие полипептиды независимо содержат scFv, VH-домен, VL-домен, не принадлежащий Ig домен или лиганд, который специфически связывается с целевым антигеном. В некоторых вариантах осуществления нацеливающие полипептиды специфически связываются с молекулой клеточной поверхности. В некоторых вариантах осуществления нацеливающие полипептиды специфически связываются с опухолевым антигеном. В некоторых вариантах осуществления нацеливающие полипептиды специфически и независимо связываются с опухолевым антигеном, выбранным по меньшей мере из одного из ЕрСАМ, EGFR, HER-2, HER-3, cMet, СЕА и FOLR1. В некоторых вариантах осуществления нацеливающие полипептиды специфически и независимо связываются с двумя разными антигенами, причем по меньшей мере один из антигенов представляет собой опухолевый антиген, выбранный из ЕрСАМ, EGFR, HER-2, HER-3, cMet, СЕА и FOLR1. В некоторых вариантах осуществления нацеливающий полипептид служит в качестве удерживающего домена и присоединен к цитокину посредством нерасщепляемого линкера.
[11] Как описано в данном документе, цитокин-блокирующий фрагмент может связываться с IL-2 и тем самым блокировать активацию когнатного рецептора IL-2.
[12] Данное описание также относится к нуклеиновым кислотам, например, ДНК, РНК, мРНК, которые кодируют описанные в данном документе кондиционально активные белки, а также векторам и клеткам-хозяевам, которые содержат такие нуклеиновые кислоты.
[13] Данное описание также относится к фармацевтическим композициям, которые содержат кондиционально активный белок, нуклеиновую кислоту, которая кодирует кондиционально активный белок, и векторы и клетки-хозяев, которые содержат такие нуклеиновые кислоты. Как правило, фармацевтическая композиция содержит один или более физиологически приемлемых носителей и/или эксципиентов.
[14] Данное описание также относится к терапевтическим способам, которые включают введение нуждающемуся в этом субъекту эффективного количества кондиционально активного белка, нуклеиновой кислоты, которая кодирует кондиционально активный белок, векторов или клеток-хозяев, которые содержат такую нуклеиновую кислоту, и фармацевтических композиций любых вышеприведенных компонентов. Как правило, субъект имеет или подвержен риску развития пролиферативного заболевания, опухолевого заболевания, воспалительного заболевания, иммунологического нарушения, аутоиммунного заболевания, инфекционного заболевания, вирусного заболевания, аллергической реакции, паразитарной реакции, болезни «трансплантат против хозяина» или болезни «хозяин против трансплантата».
[15] Данное описание также относится к применению кондиционально активного белка, нуклеиновой кислоты, которая кодирует кондиционально активный белок, векторов или клеток-хозяев, которые содержат такую нуклеиновую кислоту, и фармацевтических композиций любых вышеприведенных компонентов для лечения нуждающегося в этом субъекта. Как правило, субъект имеет или подвержен риску развития пролиферативного заболевания, опухолевого заболевания, воспалительного заболевания, иммунологического нарушения, аутоиммунного заболевания, инфекционного заболевания, вирусного заболевания, аллергической реакции, паразитарной реакции, болезни «трансплантат против хозяина» или болезни «хозяин против трансплантата».
[16] Данное описание также относится к применению кондиционально активного белка, нуклеиновой кислоты, которая кодирует кондиционально активный белок, векторов или клеток-хозяев, которые содержат такую нуклеиновую кислоту, для производства лекарственного средства для лечения заболевания, такого как пролиферативное заболевание, опухолевое заболевание, воспалительное заболевание, иммунологическое нарушение, аутоиммунное заболевание, инфекционное заболевание, вирусное заболевание, аллергическая реакция, паразитарная реакция, болезнь «трансплантат против хозяина» или болезнь «хозяин против трансплантата».
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[17] Фиг. 1а схематически иллюстрирует активируемый протеазой цитокин или хемокин, который содержит блокирующий фрагмент. Блокирующий фрагмент необязательно может выполнять функцию домена продления сывороточного времени полужизни. С левой стороны стрелки на изображении показано, что цитокин связан с блокирующим фрагментом посредством расщепляемого протеазой линкера, что блокирует его возможность связываться с рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере с высвобождением блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором.
[18] Фиг. 1b схематически иллюстрирует активируемый протеазой цитокин или хемокин, в котором ЧСА (блокирующий фрагмент) напрямую связан с представляющим интерес цитокином или хемокином, а сайт расщепления протеазой находится между ЧСА и представляющим интерес цитокином или хемокином. С левой стороны стрелки на изображении показано, что цитокин связан с блокирующим фрагментом посредством расщепляемого протеазой линкера, что блокирует его возможность связываться с рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере с высвобождением блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором.
[19] Фиг. 1с схематически иллюстрирует активируемый протеазой цитокин или хемокин, в котором более одного ЧСА (блокирующий фрагмент) напрямую связано с представляющей интерес молекулой. При необходимости один или более ЧСА могут быть связаны с цитокином или хемокином посредством линкера, такого как линкер, который содержит сайт расщепления протеазой. С левой стороны стрелки на изображении показано, что цитокин связан с блокирующим фрагментом посредством расщепляемого протеазой линкера, что блокирует его возможность связываться с рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере с высвобождением блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором. Теперь цитокин имеет аналогичные ФК-свойства по сравнению с нативным цитокином (например, имеет короткое время полужизни).
[20] Фиг. 1d схематически иллюстрирует активируемый протеазой цитокин или хемокин, содержащий более одного цитокина, одного типа или разного типа, каждый из которых связан со связывающим доменом посредством расщепляемого протеазой линкера. С левой стороны стрелки на изображении показано, что цитокин связан с блокирующим фрагментом посредством расщепляемого протеазой линкера, что блокирует его возможность связываться с рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере с высвобождением блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором.
[21] Фиг. 2 схематически иллюстрирует активируемый протеазой цитокин или хемокин, содержащий полипептид цитокина или хемокина, блокирующий фрагмент и домен для продления сывороточного времени полужизни, связанный посредством по меньшей мере одного расщепляемого протеазой линкера. С левой стороны стрелки на изображении показано, что цитокин связан с блокирующим фрагментом посредством расщепляемых протеазой линкеров, что блокирует его возможность связываться с рецептором. Также он связан с отдельным элементом для продления времени полужизни, который продлевает время полужизни в сыворотке. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере с высвобождением элемента для продления времени полужизни и блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором. Теперь цитокин имеет аналогичные ФК-свойства по сравнению с нативным цитокином (например, короткое время полужизни).
[22] Фиг. 3 схематически иллюстрирует активируемый протеазой цитокин или хемокин, содержащий полипептид цитокина или хемокина, блокирующий фрагмент и нацеливающий домен, связанный посредством по меньшей мере одного расщепляемого протеазой линкера. С левой стороны стрелки на изображении показано, что цитокин связан с блокирующим фрагментом и нацеливающим доменом посредством расщепляемого протеазой линкера, что блокирует его возможность связываться с рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере с высвобождением нацеливающего домена и блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором.
[23] Фиг. 4а схематически иллюстрирует активируемый протеазой цитокин или хемокин, содержащий полипептид цитокина или хемокина, блокирующий фрагмент, нацеливающий домен и домен для продления сывороточного времени полужизни, связанный посредством по меньшей мере одного расщепляемого протеазой линкера, причем полипептид цитокина и нацеливающий домен связаны посредством расщепляемого протеазой линкера. С левой стороны стрелки на изображении показано, что полипептид цитокинач связан с нацеливающим доменом, блокирующим фрагментом и элементом для продления времени полужизни посредством расщепляемого(ых) протеазой линкера(ов), что блокирует его возможность связываться с рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере(ах) с высвобождением элемента для продления времени полужизни, нацеливающего домена и блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором. Теперь цитокин имеет аналогичные ФК-свойства по сравнению с нативным цитокином (например, короткое время полужизни).
[24] Фиг. 4b схематически иллюстрирует активируемый протеазой цитокин или хемокин, содержащий полипептид цитокина или хемокина, блокирующий фрагмент, нацеливающий домен и домен для продления сывороточного времени полужизни, связанный посредством по меньшей мере одного расщепляемого протеазой линкера. С левой стороны стрелки на изображении показано, что цитокин связан с нацеливающим доменом, блокирующим фрагментом и элементом для продления времени полужизни посредством расщепляемого(ых) протеазой линкера(ов), что блокирует его возможность связываться со своим рецептором. С правой стороны стрелки на изображении показано, что в воспалительном или опухолевом окружении расщепление протеазой происходит в сайте расщепления протеазой на линкере(ах) с высвобождением элемента для продления времени полужизни и блокирующего фрагмента и обеспечением возможности цитокина связываться с рецептором. Нацеливающий фрагмент остается связанным, удерживая цитокин в микроокружении опухоли. Теперь цитокин имеет аналогичные ФК-свойства по сравнению с нативным цитокином (например, короткое время полужизни).
[25] Фиг. 5 схематически иллюстрирует структуру вариабельного домена молекулы иммуноглобулина. Вариабельные домены как легкой, так и тяжелой цепей иммуноглобулина содержат гипервариабельные петли или определяющие комплементарность области (CDR). Три CDR V-домена (CDR1, CDR2, CDR3) образуют кластер в одном конце бета-бочки. CDR представляют собой петли, которые соединяют бета-цепи В-С, С'-С'' и F-G укладки цепи иммуноглобулина, причем нижние петли, которые соединяют бета-цепи АВ, СС', С''-D и E-F укладки цепи иммуноглобулина, и верхняя петля, которая соединяет цепи D-E укладки цепи иммуноглобулина, представляют собой отличные от CDR петли.
[26] Фиг. 6 схематически иллюстрирует активируемый протеазой цитокин или хемокин, содержащий полипептид цитокина или хемокина, блокирующий фрагмент, который представляет собой домен, связывающий сывороточный альбумин (например, dAb), и расщепляемый протеазой линкер. В проиллюстрированном примере отличные от CDR петли в домене, связывающем сывороточный альбумин (например, sdAb), могут образовывать сайт связывания для цитокина IL-2. В этом примере сайт связывания для сывороточного альбумина может быть образован CDR домена, связывающего сывороточный альбумин.
[27] На Фиг. 7a-7h представлен ряд графиков, иллюстрирующих активность типовых слитых белков IL-2 в IL-2-зависимой линии клеток цитотоксических Т-лимфоцитов CTLL-2. На каждом графике проиллюстрированы результаты анализа пролиферации IL-2, количественно оцениваемой с помощью люминесцентного анализа жизнеспособности клеток CellTiter-Glo® (Promega). Каждый анализ пролиферации проводили с ЧСА (Фиг. 7b, 7d, 7f, 7h) или без него (Фиг. 7а, 7с, 7е, 7g). Каждый слитый белок содержит связывающий компонент против ЧСА, при этом в каждом анализе использовали как нерасщепленные, так и расщепленные протеазой ММР9 версии слитого белка.
[28] На Фиг. 8a-8f представлен ряд графиков, иллюстрирующих активность типовых слитых белков IL-2 в IL-2-зависимой линии клеток цитотоксических Т-лимфоцитов CTLL-2. На каждом графике проиллюстрированы результаты анализа пролиферации IL-2, количественно оцениваемой с помощью люминесцентного анализа жизнеспособности клеток CellTiter-Glo (Promega). В каждом анализе использовали как нерасщепленные, так и расщепленные протеазой ММР9 версии слитого белка.
[29] На Фиг. 9a-9z представлен ряд графиков, иллюстрирующих активность типовых слитых белков IL-2 в IL-2-зависимой линии клеток цитотоксических Т-лимфоцитов CTLL-2. На каждом графике проиллюстрированы результаты анализа пролиферации IL-2, количественно оцениваемой с помощью люминесцентного анализа жизнеспособности клеток CellTiter-Glo (Promega). В каждом анализе использовали как нерасщепленные, так и расщепленные протеазой ММР9 версии слитого белка.
[30] На Фиг. 10 проиллюстрированы результаты анализа расщепления белка, описанного в примере 2. Слитый белок ACP16 разделяли в геле ДСН-ПААГ в расщепленной и нерасщепленной форме. Как можно видеть в геле, расщепление было полным.
[31] На Фиг. 11а-11с представлен ряд графиков, иллюстрирующих результаты анализа IL-2 с репортером HEK-Blue, проведенного для слитых белков IL-2 и рекомбинантного человеческого IL2 (Rec hIL-2). Анализ проводили на основании количественной оценки активности секретируемой щелочной фосфатазы (SEAP), используя реагент QUANTI-Blue (InvivoGen).
[32] На Фиг. 12а-12b представлены два графика, иллюстрирующие анализ ACP16 (12а) и ACP124 (12b) в анализе IL-2 с репортером HEKBlue в присутствии ЧСА. Круги иллюстрируют активность нерасщепленного полипептида, квадраты иллюстрируют активность расщепленного полипептида. На Фиг. 12 с приведен график, иллюстрирующий результаты анализа пролиферации CTLL-2. Клетки CTLL2 (АТСС) высевали в суспензию в концентрации 500000 клеток/лунка в культуральную среду с 40 мг/мл человеческого сывороточного альбумина (ЧСА) или без него и стимулировали серией разведений активируемого hIL2 в течение 72 часов при 37°С и 5% СО2. Исследовали активность нерасщепленного и расщепленного активируемого ACP16. Расщепленный активируемый hIL2 получали путем инкубации с активной ММР9. Клеточную активность оценивали, используя люминесцентный анализ жизнеспособности клеток CellTiter-Glo (Promega). Круги иллюстрируют интактный слитый белок, а квадраты иллюстрируют расщепленный протеазой слитый белок.
[33] На Фиг. 13а-13с приведены три графика, иллюстрирующие результаты анализа АСР16, АСР124 в модели с ксенотрансплантатом опухоли. На Фиг. 13а проиллюстрирован объем опухолей в динамике по времени у мышей, обработанных 4,4 пг ACP16 (квадраты), 17 пг АСР16 (треугольники), 70 пг ACP16 (перевернутые треугольники), 232 пг АСР16 (темные круги) и 12 пг IL-2 дикого типа (пунктирная линия, треугольники) и 36 пг IL-2 дикого типа (пунктирная линия, ромбы) в целях сравнения. Один носитель показан большими незакрашенными кругами. Данные показывают, что у мышей, обработанный более высокими концентрациями ACP16, объем опухолей снижался со временем дозозависимым образом. На Фиг. 13b проиллюстрирован объем опухолей в динамике по времени у мышей, обработанных 17 мкг АСР124 (квадраты), 70 мкг АСР124 (треугольники), 230 мкг АСР124 (перевернутые треугольники) и 700 мкг АСР124. Один носитель показан большими незакрашенными кругами. На Фиг. 13 с проиллюстрирован объем опухолей в динамике по времени у мышей, обработанных 17 мкг ACP16 (треугольники), 70 мкг АСР16 (круги), 232 мкг АСР16 (темные круги) и 17 мкг АСР124 (пунктирная линия, треугольники), 70 мкг АСР124 (пунктирная линия, ромбы), 230 мкг АСР124 (пунктирная линия, ромбы) в целях сравнения. Один носитель показан темными перевернутыми треугольниками. Данные показывают, что у мышей, обработанных ACP16, но не АСР124, объем опухолей снижался со временем дозозависимым образом.
[34] На Фиг. 14а-14с приведен ряд «спагетти»-графиков, иллюстрирующих активность слитых белков в мышиной модели с ксенотрансплантатом МС38, соответствующих данным, проиллюстрированным на Фиг. 13. Каждая линия на графиках представляет одну мышь.
[35] На Фиг. 15 приведен график, иллюстрирующий объем опухолей в динамике по времени в мышиной модели с ксенотрансплантатом, иллюстрирующий рост опухолей у контрольных мышей (незакрашенные круги) и обработанных АР16 мышей (квадраты).
[36] На Фиг. 16a-16d приведен ряд графиков выживаемости, иллюстрирующих выживаемость мышей со временем после обработки расщепляемыми слитыми белками. На Фиг. 16а приведены данные для мышей, обработанных одним носителем (серая линия), 17 пг АСР16 (темная линия) и 1 пг АСР124 (пунктирная линия). На Фиг. 16b приведены данные для мышей, обработанных одним носителем (серая линия), 70 пг АСР16 (темная линия) и 70 пг АСР124 (пунктирная линия). На Фиг. 16 с приведены данные для мышей, обработанных одним носителем (серая линия), 232 пг АСР16 (темная линия) и 230 пг АСР124 (пунктирная линия). На Фиг. 16d приведены данные для мышей, обработанных одним носителем (серая линия), 232 пг ACP16 (темная линия) и 700 пг АСР124 (пунктирная линия).
[37] На Фиг. 17 приведен ряд «спагетти»-графиков, иллюстрирующих активность слитых белков в мышиной модели с ксенотрансплантатом МС38. Группам мышей давали всего по четыре дозы за исключением трех наибольших доз АРС132, в случае которых была зарегистрирована токсичность с летальным исходом через 1 неделю/две дозы. Проиллюстрированы: один носитель (вверху), 17, 55, 70 и 230 мкг АСР16 (полный верхний ряд), 9, 28, 36 и 119 мкг АСР132 (полный средний ряд) и 13, 42, 54 и 177 мкг АСР21 (полный нижний ряд). Каждая линия на графиках представляет отдельное животное.
[38] Фиг. 18-23 иллюстрируют свойства полипептидов TriTac, которые служат примерами расщепляемых протеазами слитых белков.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[39] В данном документе раскрыты способы и композиции для создания и применения конструкций, содержащих индуцибельные цитокины. Цитокины являются сильными иммунными агонистами, что позволяет рассматривать их в качестве перспективных терапевтических агентов для онкологии. Однако было доказано, что цитокины имеют очень узкое терапевтическое окно. Цитокины имеют короткое сывороточное время полужизни и также считаются очень сильнодействующими. Следовательно, терапевтическое введение цитокинов приводит к нежелательным системным эффектам и токсичности. Это усугублялось необходимостью введения больших количеств цитокинов с целью достижения необходимых уровней цитокинов в предполагаемом месте действия цитокинов (например, опухоли). К сожалению, вследствие биологии цитокинов и невозможности эффективно направлять и контролировать их активность, цитокины не оправдали надежд в отношении клинических преимуществ в лечении опухолей.
[40] В данном документе описаны слитые белки, для которых разрешены проблемы токсичности и короткого времени полужизни, которые сильно ограничивали клиническое применение цитокинов в онкологии. Это слитые белки содержат полипептиды цитокинов, которые обладают активностью агонистов рецепторов. Но в контексте слитого белка активность агониста рецептора цитокина ослаблена и продлено время полужизни в циркуляции. Эти слитые белки содержат сайты расщепления протеазами, которые расщепляются протеазами, ассоциированными с необходимым сайтом активности цитокина (например, опухолью), и как правило, обогащенными или избирательно присутствующими в сайте необходимой активности. Таким образом, слитые белки преимущественно (или избирательно) и эффективно расщепляются в необходимом сайте активности с ограничением активности цитокина по существу необходимым сайтом активности, таким как микроокружение опухоли. Расщепление протеазой в необходимом сайте активности, таком как микроокружение опухоли, приводит к высвобождению такой формы цитокина из слитого белка, которая является намного более активной в качестве агониста рецептора цитокина, чем слитый белок (как правило, по меньшей мере в около 100 раз более активной, чем слитый белок). Форма цитокина, которая высвобождается после расщепления слитого белка, как правило, имеет короткое время полужизни, которое часто по существу сходно со временем полужизни цитокина природного происхождения, дополнительно ограничивая активность цитокина микроокружением опухоли. Даже несмотря на то, что время полужизни слитого белка увеличено, токсичность сильно снижена или устранена, поскольку находящийся в циркуляции слитый белок ослаблен, а активный цитокин нацелен на микроокружение опухоли. Описанные в данном документе слитые белки впервые делают возможным введение эффективной терапевтической дозы цитокина для лечения опухолей, при этом активность цитокина по существу ограничена микроокружением опухоли, а нежелательные системные эффекты и токсичность цитокина сильно снижены или устранены.
[41] Если не указано иное, подразумевается, что все термины, присущие данной области техники, сокращения и другая научная терминология, используемые в данном документе, имеют значения, известные специалистам в области техники, к которой относится это изобретение. В некоторых случаях в данном документе приведены определения терминов, имеющих известное значение, в целях ясности и/или для удобства приведения ссылок, причем включение в данный документ таких определений не обязательно следует воспринимать, как представляющее разницу с тем, что в целом известно в данной области техники. Способы и процедуры, описанные или на которые приведены ссылки в данном документе, в целом хорошо известны и применимы специалистами в данной области техники с использованием традиционных методик, например таких, как широко используемые методики молекулярного клонирования, описанные в Sambrook et al., Molecular Cloning: A Laboratory Manual 4th ed. (2012) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY. В соответствующих случаях процедуры, включающие применение коммерчески доступных наборов и реагентов, в целом проводят в соответствии с определенными производителями протоколами и условиями, если не указано иное.
[42] «Цитокин» является хорошо известным термином в данной области техники, который относится к любому из класса иммунорегуляторных белков (таких как интерлейкины или интерфероны), которые секретируются клетками, в особенности иммунной системы, и которые являются модуляторами иммунной системы. Полипептиды цитокинов, которые можно использовать в описанных в данном документе слитых белках, включают, но не ограничиваются этим, трансформирующие факторы роста, такие как TGF-α и TGF-β (например, TGF-бета1, TGF-бета2, TGF-бета3); интерфероны, такие как интерферон-α, интерферон-β, интерферон-γ, интерферон-каппа и интерферон-омега; интерлейкины, такие как IL-1, IL-1α, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-21 и IL-25; факторы некроза опухолей, такие как фактор некроза опухолей альфа и лимфотоксин; хемокины (например, хемокин с мотивом С-Х-С 10 (CXCL10), CCL19, CCL20, CCL21) и гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CS), а также фрагменты таких полипептидов, которые активируют когнатные рецепторы для цитокина (т.е. функциональные фрагменты вышеприведенных молекул). «Хемокин» является термином в данной области техники, который относится к любому из семейства малых цитокинов со способностью индуцировать направленный хемотаксис в находящихся по близости чувствительных клетках.
[43] Хорошо известно, что хемокины имеют короткое время полужизни, которое часто составляет всего несколько минут или часов. Даже формы цитокинов, которые имеют измененные аминокислотные последовательности, предназначенные для продления сывороточного времени полужизни с сохранением активности агонистов рецепторов, как правило, также имеют короткое сывороточное время полужизни. В контексте данного документа «цитокин с коротким временем полужизни» относится к цитокину, который характеризуется по существу краткой циркуляцией в сыворотке субъекта, например, сывороточным временем полужизни, которое составляет менее 10, менее 15, менее 30, менее 60, менее 90, менее 120, менее 240 или менее 480 минут. В контексте данного документа цитокин с коротким временем полужизни включает цитокины, последовательности которых не были модифицированы с целью достижения большего чем обычно времени полужизни в организме субъекта, и полипептиды, которые имеют измененные аминокислотные последовательности, предназначенные для продления сывороточного времени полужизни с сохранением активности агонистов рецепторов. Как правило, полипептид цитокина с коротким временем полужизни, такой как полипептид IL-2, имеет сывороточное время полужизни, сравнимое с IL-2 природного происхождения, например, в пределах 5-кратного, 4-кратного, 3-кратного или 2-кратного превышения времени IL-2 природного происхождения. Этот последний случай не подразумевает добавление гетерологичных белковых доменов, таких как истинный элемент для продления времени полужизни, такой как сывороточный альбумин.
[44] «Сортазы» представляют собой транспозазы, которые модифицируют белки путем распознавания и расщепления карбокси-концевого сигнала сортировки, включенного в целевой белок или пептид или присоединенного в его конце. Сортаза А катализирует расщепление мотива LPXTG (SEQ ID NO: 125) (где X представляет собой любую стандартную аминокислоту) между остатками Thr и Gly в целевом белке с временным присоединением остатка Thr к активному сайту остатка Cys в ферменте с образованием промежуточного соединения фермент-тиоацил. Для завершения транспептидации и создания конъюгата пептид-мономер биомолекула с N-концевой нуклеофильной группой, как правило, олигоглициновым мотивом, атакует промежуточное соединение, вытесняя сортазу А и соединяя две молекулы.
[45] В контексте данного документа «стерический блокатор» относится полипептиду или полипептидному фрагменту, который может быть ковалентно связан с полипептидом цитокина, напрямую или ненапрямую посредством других фрагментов, таких как линкеры, например, в форме химерного полипептида (слитого белка), но никаким иным образом ковалентно не связывается с полипептидом цитокина. Стерический блокатор может связываться с полипептидом цитокина нековалентно, например, посредством электростатического, гидрофобного, ионного или водородного связывания. Стерический блокатор, как правило, ингибирует или блокирует активность цитокинового фрагмента вследствие своей близости к цитокиновому фрагменту и сопоставимого размера. Стерический блокатор также может блокировать посредством привлечения крупного белкового партнера по связыванию. Примером этого является антитело, которое связывается с сывороточным альбумином; тогда как само антитело может или нет быть достаточно крупным, чтобы блокировать активацию или связывание самому, привлечение альбумина делает возможным достаточное стерическое блокирование.
[46] В контексте данного документа и описания «элемент для продления времени полужизни» является частью химерного полипептида, которая повышает сывороточное время полужизни и улучшает ФК, например, путем изменения его размера (например, чтобы превышать порог почечной фильтрации), формы, гидродинамического радиуса, заряда или параметров всасывания, биораспределения, метаболизма и элиминации.
[47] В контексте данного документа термины «активируемый», «активировать», «индуцировать» и «индуцибельный» относятся к способности белка, т.е. цитокина, который является частью слитого белка, связывать его рецептор и осуществлять активность после расщепления дополнительных элементов из слитого белка.
[48] В контексте данного документа «плазмиды» или «вирусные векторы» представляют собой агенты, которые переносят описанные нуклеиновые кислоты в клетку, не разрушая ее, и содержат промотор, обеспечивающий экспрессию молекулы нуклеиновой кислоты и/или полипептида в клетках, в которые они были доставлены.
[49] В контексте данного документа термины «пептид», «полипептид» или «белок» используются в широком смысле для обозначения двух или более аминокислот, связанных пептидной связью. Белок, пептид и полипептид также взаимозаменяемо используются в данном документе для обозначения аминокислотных последовательностей. Следует понимать, что термин полипептид в контексте данного документа не предполагает конкретные размер или число аминокислот, составляющих молекулу, и что пептид по изобретению может содержать до нескольких аминокислотных остатков или более.
[50] В контексте данного документа «субъект» может представлять собой позвоночное, конкретнее млекопитающее (например, человека, лошадь, кошку, собаку, корову, свинью, овцу, козу, мышь, кролика, крысу и морскую свинку), птиц, рептилий, амфибий, рыб и любое другое животное. Этот термин не предполагает конкретный возрастили пол. Такими образом, подразумевается, что охвачены взрослые и новорожденные субъекты мужского и женского пола.
[51] В контексте данного документа термины «пациент» или «субъект» могут использоваться взаимозаменяемо и могут относиться к субъекту с заболеванием или нарушением (например, раком). Термин пациент или субъект включает людей и ветеринарных субъектов.
[52] В контексте данного документа термины «лечение» или «лечить» относятся к способу снижения действия заболевания или патологического состояния или симптома заболевания или патологического состояния. Таким образом, в описанном способе лечение может относиться к по меньшей мере около 10%, по меньшей мере около 20%, по меньшей мере около 30%, по меньшей мере около 40%, по меньшей мере около 50%, по меньшей мере около 60%, по меньшей мере около 70%, по меньшей мере около 80%, по меньшей мере около 90% или по существу полному снижению тяжести установленного заболевания или патологического состояния или симптома заболевания или патологического состояния. Например, способ лечения заболевания считается лечением, если наблюдается 10% снижение одного или более симптомов заболевания у субъекта по сравнению с контролем. Таким образом, снижение может составлять 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или любой процент снижения между 10% и 100% по сравнению с нативными или контрольными уровнями. Следует понимать, что лечение не обязательно относится к излечению или полному устранению заболевания, патологического состояния или симптомов заболевания или патологического состояния.
[53] В контексте данного документа термины «предотвращать» и «предотвращение» заболевания или нарушения относятся к действию, например, введению химерного полипептида или последовательности нуклеиновой кислоты, кодирующей химерный полипептид, которое происходит до или приблизительно в то же время, когда субъект начинает демонстрировать один или более симптомов заболевания или нарушения, которое ингибирует или замедляет начало или усугубление одного или более симптомов заболевания или нарушения.
[54] В контексте данного документа употребление терминов «снижение», «уменьшение» или «ингибирование» включает изменение, составляющее по меньшей мере около 10%, по меньшей мере около 20%, по меньшей мере около 30%, по меньшей мере около 40%, по меньшей мере около 50%, по меньшей мере около 60%, по меньшей мере около 70%, по меньшей мере около 80%, по меньшей мере около 90% или более по сравнению с подходящим контрольным уровнем. Такие термины могут включать, но необязательно включают полное устранение функции или свойства, такого как активность агониста.
[55] «Ослабленный агонист рецептора цитокина» относится к агонисту рецептора цитокина, который обладает сниженной активностью агониста рецептора по сравнению с агонистом рецептора цитокина природного происхождения. Ослабленный агонист рецептора цитокина может обладать по меньшей мере в около 10Х, по меньшей мере в около 50Х, по меньшей мере в около 100Х, по меньшей мере в около 250Х, по меньшей мере в около 500Х, по меньшей мере в около 1000Х или еще меньшей активностью агониста по сравнению с агонистом рецептора природного происхождения. Если слитый белок, который содержит полипептид цитокина, описанный в данном документе, описан как «ослабленный» или имеющий «ослабленную активность», это означает, что слитый белок представляет собой ослабленный агонист рецептора цитокина.
[56] «Интактный слитый белок» представляет собой слитый белок, в котором не было удалено ни одного домена, например, путем расщепления протеазой. Домен может быть удален расщеплением протеазой или посредством другой ферментативной активности, но когда слитый белок является «интактным», это еще не произошло.
[57] В контексте данного документа «фрагмент» относится к части молекулы, которая имеет отличную функцию в этой молекуле, и эта функция может осуществляться этим фрагментом в контексте другой молекулы. Фрагмент может представлять собой химическое соединение с конкретной функцией или часть биологической молекулы с конкретной функцией. Например, «блокирующий фрагмент» в слитом белке представляет собой часть слитого белка, которая способна блокировать активность некоторой части или всего слитого белка. Это может быть белковый домен, такой как сывороточный альбумин. Блокирование может осуществляться стерическим блокатором или специфическим блокатором. Стерический блокатор осуществляет блокирование за счет размера и положения, но не на основании специфического связывания; примером является сывороточный альбумин. Специфический блокатор осуществляет блокирование за счет специфических взаимодействий с предназначенный для блокирования фрагментом. Специфический блокатор должен быть подобран к конкретному цитокину или активному домену; стерический блокатор можно использовать вне зависимости от нагрузки при условии, что он является достаточно крупным.
[58] В целом, терапевтическое применение цитокинов сильно ограничено их системной токсичностью. Например, TNF изначально изучали вследствие его способности индуцировать геморрагический некроз некоторых опухолей и вследствие его in vitro цитотоксического эффекта на разные опухолевые линии, но впоследствии было доказано, что он обладает сильной противовоспалительной активностью, что может, в случае патологической сверхвыработки, представлять опасность для человеческого организма. Поскольку системная токсичность является фундаментальной проблемой для применения фармакологически активных количеств цитокинов людьми, на сегодня на апробации находятся новые производные и терапевтические стратегии, целью которых является снижение токсических эффектов этого класса биологических эффекторов с сохранением их терапевтической эффективности.
[59] IL-2 осуществляет как стимуляторные, так и регуляторные функции в иммунной системе и, наряду с другими представителями семейства цитокинов с общей γ-цепью (γс), является основополагающим для иммунного гемостаза. IL-2 опосредует его действие путем связывания с рецепторами IL-2 (IL-2R), состоящими из тримерных рецепторов, состоящих из цепей IL-2Rα (CD25), IL-2Rβ (CD122) и IL-2Rγ (γс, CD132), или димерных βγ IL-2R (1, 3). Оба варианта IL-2R способны передавать сигнал после связывания IL-2. Однако тримерные αβγ IL-2R имеют приблизительно в 10 100 раз большую аффинность в отношении IL-2, чем димерные βγ IL-2R (3), подразумевая, что CD25 обеспечивает высокоаффинное связывание IL-2 с его рецептором, но не является критически важным для передачи сигнала. Тримерные IL-2R находятся на активированных Т-клетках и CD4+ Т-регуляторных клетках (Treg) forkhead-бокс Р3 (FoxP3)+, которые являются чувствительными к IL-2 in vitro и in vivo. В отличие от этого, обученные антигеном клетки CD8+ (клетки памяти), CD8+ с высокими уровнями CD44 и фенотипом клеток памяти (MP) и естественные клетки-киллеры (NK) имеют высокие уровни димерных βγ IL-2R, и эти клетки также активно отвечают на IL-2 in vitro и in vivo.
[60] Экспрессия высокоаффинного IL-2R является важной для того, чтобы Т-клетки могли демонстрировать ответ на низкие концентрации IL-2, которые временно доступен in vivo. Экспрессия IL-2Rα отсутствует в наивных Т-клетках и Т-клетках памяти, но индуцируется после активации антигеном. IL-2Rβ конститутивно экспрессируется NK, NKT и CD8+ Т-клетками памяти, но также индуцируется в наивных Т-клетках после активации антигеном, ус регулируется намного менее жестко и конститутивно экспрессируется всеми лимфоидными клетками. После индукции высокоаффинного IL-2R антигеном сигнализация IL-2R повышает экспрессию IL-2Rα, частично посредством Stat5-зависимой регуляции транскрипции Il2ra (Kim et al., 2001). Этот процесс представляет механизм поддержания экспрессии высокоаффинного IL-2R и продолжения сигнализации IL-2 пока существует источник IL-2.
[61] IL-2Rα захватывает IL-2 посредством большой гидрофобной поверхности захвата, окруженной полярной периферией, что приводит к относительно слабому взаимодействию (Kd 10-8 М) с быстрой кинетикой ассоциации-диссоциации связывания. При этом бинарный комплекс IL-2Rα-IL-2 вызывает очень небольшое конформационное изменение в IL-2, которое способствует ассоциации с IL-2Rβ посредством отличного полярного взаимодействия между IL-2 и IL-2Rβ. Псевдовысокая аффинность тримерного комплекса IL2/α/β (т.е. Kd ~300 пМ) четко показывает, что тримерный комплекс является более стабильным, чем любой IL2, связанный только с α-цепью (Kd=10 нМ) или только с β-цепью (Kd=450 нМ), согласно данным Ciardelli. В любом случае тример IL2/α/β затем рекрутирует γ-цепь в четвертичный комплекс, способный осуществлять сигнализацию, что облегчается большим композитным сайтом связывания на IL2-связанной β-цепи на γ-цепи.
[62] Другими словами, тройной комплекс IL-2Rα-IL-2Rβ-IL-2 затем рекрутирует γс посредством слабого взаимодействия с IL-2 и более сильного взаимодействия с IL-2Rβ с образованием стабильного четвертичного высокоаффинного IL-2R (Kd 10-11 М, что составляет 10 пМ). Образование высокоаффинного четвертичного комплекса IL-2-IL-2R приводит к передаче сигнала через тирозинкиназы Jak1 и Jak3, которые связаны с IL-2Rβ и γс, соответственно (Nelson and Willerford, 1998). Четвертичный комплекс IL-2-IL-2R быстро интернализуется, при этом происходит быстрая деградация IL-2, IL-2Rβ и γс, но IL-2Rα возвращается обратно на клеточную поверхность ( et al., 1995; Yu and Malek, 2001). Таким образом, те виды функциональной активности, для которых необходима длительная сигнализация IL-2R, требуют постоянного источника IL-2 для привлечения IL-2Rα и образования дополнительных сигнальных комплексов IL-2-IL-2R.
et al., 1995; Yu and Malek, 2001). Таким образом, те виды функциональной активности, для которых необходима длительная сигнализация IL-2R, требуют постоянного источника IL-2 для привлечения IL-2Rα и образования дополнительных сигнальных комплексов IL-2-IL-2R.
[63] Регуляторные Т-клетки активно подавляют активацию иммунной системы и предотвращают патологическую аутореактивность и последующее развитие аутоиммунного заболевания. Разработка лекарственных препаратов и способов для избирательной активации Т-клеток для лечения аутоиммунных заболеваний является предметом интенсивный исследований и, до разработки данного изобретения, подходы, которые позволяют осуществлять избирательную доставку интерлейкинов в сайт воспаления, были в основном неуспешными. Регуляторные Т-клетки (Treg) представляют класс CD4+CD25+ Т-клеток, которые подавляют активность других иммунных клеток. Treg являются основополагающими для гомеостаза иммунной системы и играют основную роль в поддержании толерантности к собственным антигенам и модуляции иммунного ответа на чужеродные антигены. Было показано, что при многих аутоиммунных заболеваниях, включая диабет 1 типа(Д1Т), системную красную волчанку (СКВ) и болезнь «трансплантат против хозяина» (БТПХ), наблюдается дефицит числа клеток Treg или функции Treg.
[64] Следовательно, существует большая заинтересованность в разработке вариантов терапии и повышении числа и/или функции клеток Treg. Одним подходом к лечению аутоиммунных заболеваний, находящимся на стадии исследований, является трансплантация аутологичных, ех vivo-размноженных клеток Treg (Tang, Q., et al., 2013, Cold Spring Harb. Perspect. Med., 3:1-15). Хотя этот подход показал себя перспективным при лечении в животных моделях заболевания и на ранних стадиях нескольких клинических исследований на людях, для него необходимо персонализированное лечение собственными Т-клетками пациента, он является инвазивным и технически сложным. Другим подходом является лечение низкими дозами интерлейкина-2 (IL-2). Клетки Treg отличаются характерной экспрессией высоких конститутивных уровней высокоафинного рецептора IL-2, IL2Rαβγ, который состоит из субъединиц IL2Rα (CD25), IL2Rβ (CD122) и IL2Rγ (CD132), и было показано, что рост клеток Treg зависит от IL-2 (Malek, Т.R., et al., 2010, Immunity, 33:153-65).
[65] В свою очередь иммунную активацию также обеспечивали, используя IL-2, а рекомбинантный IL-2 (Proleukin®) был одобрен для лечения определенных видов рака. Высокие дозы IL-2 используют для лечения пациентов с метастатической меланомой и метастатической почечно-клеточной карциномой с долговременным воздействием на общую выживаемость.
[66] Клинические исследования лечения низкими дозами IL-2 пациентов с хронической БТПХ (Koreth, J., et al., 2011, N Engl J Med., 365:2055-66) и HCV-ассоциированного аутоиммунного васкулита (Saadoun, D., et al., 2011, N Engl J Med., 365:2067-77) продемонстрировали повышение уровней Treg и признаки клинической эффективности. Были начаты новые клинические исследования по изучению эффективности IL-2 при многих других аутоиммунных и воспалительных заболеваниях. Обоснованием для применения так называемых низких доз IL-2 было использование высокой аффинности IL-2 тримерного рецептора IL-2, который конститутивно экспрессируется на Treg, оставляя остальные Т-клетки, которые не экспрессируют высокоаффинный рецептор в инактивированном состоянии. Альдеслейкин (представленный на рынке как Proleukin® от Prometheus Laboratories, San Diego, CA), рекомбинантная форма IL-2, которую использовали в этих исследованиях, связан с высокой токсичностью. Альдеслейкин одобрен для лечения метастатической меланомы и метастатического почечного рака, но его побочные эффекты являются настолько тяжелыми, что его использование рекомендовано только в условиях госпитализации с доступом к отделению интенсивной терапии (веб-адрес: www.proleukin.com/assets/pdf/proleukin.pdf).
[67] В клинических исследованиях IL-2 при аутоиммунных заболеваниях исследовали низкие дозы IL-2 для нацеливания на клетки Treg, поскольку клетки Treg восприимчивы к более низким концентрациям IL-2, чем многие другие типы иммунных клеток благодаря экспрессии IL2R-альфа (Klatzmann D, 2015 Nat Rev Immunol. 15:283-94). Однако даже эти более низкие дозы приводили к проблемам с безопасностью и переносимостью, а в применяемых вариантах лечения использовали суточные подкожные инъекции, постоянно или интервальные 5-суточные курсы лечения. Следовательно, существует потребность в терапии аутоиммунных заболеваний, которая повышала бы число и функцию клеток Treg, которая нацелена на клетки Treg более специфичным образом, чем IL-2, которая является более безопасной и переносимой и которую применяют менее часто.
[68] Одним подходом, который был предложен для улучшения терапевтического индекса терапии на основе IL-2 для аутоиммунных заболеваний, является применение вариантов IL-2, которые являются избирательными в отношении клеток Treg относительно других иммунных клеток. Рецепторы IL-2 экспрессируются на ряде разных типов иммунных клеток, включая Т-клетки, NK-клетки, эозинофилы и моноциты, и этот широкий профиль экспрессии, вероятно, обуславливает его плейотропный эффект на иммунную систему и высокую системную токсичность. В частности, активированные Т-эффекторные клетки экспрессируют IL2Rαβγ, как и эпителиальные клетки легких. Но активация Т-эффекторных клеток прямо противоположна цели понижающей модуляции и регуляции иммунного ответа, а активация эпителиальных клеток легких приводит к известным дозолимитирующим побочным эффектам IL-2, включая отек легких. Действительно, основным побочным эффектом иммунотерапии высокими дозами IL-2 является синдром капиллярной утечки (СКУ), который приводит к накоплению внутрисосудистой жидкости в органах, таких как легкие и печень с последующим отеком легких и повреждением клеток печени. Не существует иного лечения СКУ, чем прекращение приема IL-2. Схемы применения низких доз IL-2 исследовали на пациентах, чтобы избежать СКУ, однако за счет субоптимальных терапевтических результатов.
[69] В соответствии с литературой считается, что СКУ вызывает высвобождение провоспалительных цитокинов из IL-2-активированных NK-клеток. При этом существуют явные свидетельства того, что отек легких является результатом прямого связывания IL-2 с эндотелиальными клетками легких, которые экспрессируют низкие или средние уровни функциональных αβγ IL-2R. Также отек легких, связанный с взаимодействием IL-2 с эндотелиальными клетками легких, подавлялся путем блокирования связывания с CD25 с помощью анти-CD25 моноклонального антитела (mAb) у мышей-хозяев с дефицитом CD25 или путем применения СВ122-специфических комплексов IL-2/анти-IL-2 mAb (IL-2/mAb) с предотвращением, таким образом, СКУ.
[70] Лечение цитокинами интерлейкинами, отличными от IL-2, является более ограниченным. IL-15 проявляет стимулирующую иммунные клетки активность, аналогично IL-2, но без таких же ингибирующих эффектов, что делает его перспективным иммунотерапевтическим кандидатом. Клинические исследования рекомбинантного человеческого IL-15 для лечения метастатической злокачественной меланомы или почечно-клеточного рака продемонстрировали существенные изменения в распределении, пролиферации и активации иммунных клеток и позволили предположить наличие потенциальной противоопухолевой активности (Conlon et. al., 2014). На данный момент IL-15 проходит клинические исследования для лечения различных форм рака. Однако известно, что терапия IL-15 связана с нежелательными и токсическими эффектами, такими как усугубление определенных видов лейкоза, болезни «трансплантат против хозяина», гипотензии, тромбоцитопении и поражения печени. (Mishra A., et al., Cance Cell, 2012, 22(5):645-55; Alpdogan O. et al., Blood, 2005, 105(2):866-73; Conlon KC et al., J Clin Oncol, 2015, 33(1):74-82.)
[71] Прямое применение IL-2 в качестве агониста для связывания IL-2R и модуляции иммунных ответов терапевтически является проблематичным вследствие широко описанных терапевтических рисков, например, его короткого сывороточного времени полужизни и высокой токсичности. Эти риски также ограничивают терапевтическую разработку и применение других цитокинов. Необходимы новые формы цитокинов, которые снижают эти риски. В данном документе описаны композиции и способы, включающие применение IL-2 и IL-15 и других цитокинов, функциональных фрагментов и мутеинов цитокинов, а также кондиционально активных цитокинов, разработанных для разрешения этих рисков и обеспечения необходимых иммуномодулирующих терапевтических средств.
[72] Данное изобретение разработано для разрешения недостатков прямой терапии IL-2 и терапии с применением других цитокинов, например, за счет применения блокирующих цитокины фрагментов, например, стерических блокирующих полипептидов, полипептидов для продления сывороточного времени полужизни, нацеливающих полипептидов, соединительных полипептидов, содержащих расщепляемые протеазами линкеры, и их комбинаций. Цитокины, включая интерлейкины (например, IL-2, IL-7, IL-12, IL-15, IL-18, IL-21 IL-23), интерфероны (IFN, включая IFN-альфа, IFN-бета и IFN-гамма), факторы некроза опухолей (например, TNF-альфа, лимфотоксин), трансформирующие факторы роста (например, TGF-бета1, TGF-бета2, TGF-бета3), хемокины (хемокин с мотивом С-Х-С 10 (CXCL10), CCL19, CCL20, CCL21) и гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CS) являются очень эффективными при введении пациентам. В контексте данного документа «хемокин» означает семейство малых цитокинов со способностью индуцировать направленный хемотаксис в находящихся по близости чувствительных клетках. Цитокины могут обеспечить мощную терапию, но она сопровождается нежелательными явлениями, которые трудно контролировать клинически и которые ограничивали клиническое применение цитокинов. Данное изобретение относится к новым формам цитокинов, которые можно применять на пациентах, со сниженными или устраненными нежелательными явлениями. В частности, данное изобретение относится к фармацевтическим композициям, содержащим химерные полипептиды (слитые белки), нуклеиновые кислоты, кодирующие слитые белки, и фармацевтическим составам вышеприведенного, которые содержат цитокины или активные фрагменты или мутеины цитокинов, которые имеют сниженную активность активации рецептора цитокина по сравнению с соответствующими цитокином. При этом в выбранных условиях или в выбранном биологическом окружении химерные полипептиды активируют свои когнатные рецепторы, часто с такой же или большей эффективностью, чем соответствующий цитокин природного происхождения. Как описано в данном документе, этого, как правило, достигают, используя блокирующий цитокин фрагмент, который блокирует или ингибирует рецептор-активирующую функцию цитокина, его активный фрагмент или мутеин, в общих условиях, но не в выбранных условиях, таких как существуют в необходимом сайте цитокиновой активности (например, сайте воспаления или опухоли).
[73] Химерные полипептиды и нуклеиновые кислоты, кодирующие химерные полипептиды, можно создавать, используя любой подходящий способ. Например, нуклеиновые кислоты, кодирующие химерный полипептид, можно создавать, используя технологии рекомбинантных ДНК, синтетической химии или комбинации этих способов, и экспрессировать в подходящей экспрессионной системе, например, в клетках СНО. Аналогично, химерные полипептиды можно создавать, например, путем экспрессии подходящей нуклеиновой кислоты, используя синтетические или полусинтетические химические способы и т.п. В некоторых вариантах осуществления блокирующий фрагмент может быть присоединен к полипептиду цитокина посредством опосредованной сортазой конъюгации. «Сортазы» представляют собой транспозазы, которые модифицируют белки путем распознавания и расщепления карбокси-концевого сигнала сортировки, включенного в целевой белок или пептид или присоединенного в его конце. Сортаза А катализирует расщепление мотива LPXTG (SEQ ID NO: 125) (где X представляет собой любую стандартную аминокислоту) между остатками Thr и Gly в целевом белке с временным присоединением остатка Thr к активному сайту остатка Cys в ферменте с образованием промежуточного соединения фермент-тиоацил. Для завершения транспептидации и создания конъюгата пептид-мономер биомолекула с N-концевой нуклеофильной группой, как правило, олигоглициновым мотивом, атакует промежуточное соединение, вытесняя сортазу А и соединяя две молекулы.
[74] Для образования слитого белка цитокин-блокирующий фрагмент полипептид цитокина сначала метят в N-конце полиглициновой последовательностью или, в альтернативном варианте, в С-конце мотивом LPXTG (SEQ ID NO: 125). Блокирующий фрагмент или другой элемент содержит соответствующие присоединенные пептиды, которые служат акцепторными сайтами для меченых полипептидов. Для конъюгации с доменами, несущими акцепторный пептид LPXTG (SEQ ID NO: 125), присоединенный в N-конце, полипептид метят N-концевым полиглициновым участком. Для конъюгации с доменом, несущим полиглициновый пептид, присоединенный в С-конце, полипептид метят в С-конце последовательностью распознавания сортазы LPXTG (SEQ ID NO: 125). Распознавая полиглициновую последовательность и LPXTG (SEQ ID NO: 125), сортаза образует пептидную связь между полимером-пептидом и мечеными полипептидами. Реакция с участием сортазы отщепляет остаток глицина в виде промежуточного соединения и происходит при комнатной температуре.
[75] Для устранения или снижения ингибирования, обусловленного блокирующим фрагментом, можно использовать ряд механизмов. Например, фармацевтические композиции могут содержать полипептид IL-2 и блокирующий фрагмент, например, стерический блокирующий фрагмент, причем между полипептидом IL-2 и блокирующим IL-2 фрагментом или в пределах блокирующего цитокин фрагмента расположен расщепляемый протеазой линкер, содержащий сайт расщепления протеазой. Если сайт расщепления протеазой расщеплен блокирующий фрагмент может диссоциировать от цитокина, а цитокин после этого может активировать рецептор цитокина. Цитокиновый фрагмент также можно блокировать специфическим блокирующим фрагментом, таким как антитело, которое связывает эпитоп, находящийся на соответствующем цитокине.
[76] Можно использовать любой подходящий линкер. Например, линкер может содержать глицин-глицин, мотив распознавания сортазы или мотив распознавания сортазы и пептидную последовательность (Gly4Ser)n (SEQ ID NO: 126) или (Gly3Ser)n, (SEQ ID NO: 127), где п равно 1, 2, 3, 4 или 5. Как правило, мотив распознавания сортазы содержит пептидную последовательность LPXTG (SEQ ID NO: 125), где X представляет собой любую аминокислоту. В некоторых вариантах осуществления ковалентная связь находится между реактивным остатком лизина, присоединенным к С-концу полипептида цитокина, и реактивным остатком аспарагиновой кислоты, присоединенным к N-концу блокатора или другого домена. В других вариантах осуществления ковалентная связь находится между реактивным остатком аспарагиновой кислоты, присоединенным к N-концу полипептида цитокина, и реактивным остатком лизина, присоединенным к С-концу указанного блокатора или другого домена.
[77] Соответственно, как подробно описано в данном документе, применяемые блокирующие цитокины фрагменты (например, блокирующие IL-2 фрагменты) могут быть стерическими блокаторами. В контексте данного документа «стерический блокатор» относится полипептиду или полипептидному фрагменту, который может быть ковалентно связан с полипептидом цитокина, напрямую или ненапрямую посредством других фрагментов, таких как линкеры, например, в форме химерного полипептида (слитого белка), но никаким иным образом ковалентно не связывается с полипептидом цитокина. Стерический блокатор может связываться с полипептидом цитокина нековалентно, например, посредством электростатического, гидрофобного, ионного или водородного связывания. Стерический блокатор, как правило, ингибирует или блокирует активность цитокинового фрагмента вследствие своей близости к цитокиновому фрагменту и сопоставимого размера. Стерическое ингибирование цитокина можно устранить путем пространственного отделения цитокинового фрагмента от стерического блокатора, например, путем ферментативного расщепления слитого белка, который содержит стерический блокатор и полипептид цитокина, в сайте между стерическим блокатором и полипептидом цитокина.
[78] Как более подробно описано в данном документе, функция блокирования может быть скомбинирована или обусловлена наличием дополнительных функциональных компонентов в фармацевтической композиции, таких как нацеливающий домен, элемент для продления сывороточного времени полужизни и расщепляемые протеазами связывающие полипептиды. Например, полипептид для продления сывороточного времени полужизни также может быть стерическим блокатором.
[79] Различные элементы гарантируют доставку и активность IL-2 преимущественно в сайте необходимой активности IL-2 и строгое ограничение системного воздействия интерлейкина посредством стратегии блокирования и/или нацеливания, преимущественно в связи со стратегией продления сывороточного времени полужизни. В этой стратегии продления сывороточного времени полужизни блокированная версия интерлейкина циркулирует в течение продленного времени (преимущественно 12 или более недель), но активированная версия имеет типичное сывороточное время полужизни интерлейкина.
[80] По сравнению с версией с продлением сывороточного времени полужизни сывороточное время полужизни вводимого внутривенно IL-2 составляет всего лишь ~10 из-за распределения по общему внеклеточному пространству организма, размер которого является большим и составляет ~15 л у среднестатического взрослого человека. Следовательно, IL-2 метаболизируется почками со временем полужизни ~2,5 часа. (Smith, K. "Interleukin 2 immunotherapy." Therapeutic Immunology 240 (2001)). Согласно другим измерениям IL-2 имеет очень короткое плазменное время полужизни, составляющее 85 минут для внутривенного введения и 3,3 часа для подкожного введения (Kirchner, G.I., et al., 1998, Br J Clin Pharmacol. 46:5-10). В некоторых вариантах осуществления этого изобретения элемент для продления времени полужизни связан с интерлейкином посредством линкера, который расщепляется в сайте действия (например, специфическими для воспаления или опухолеспецифическими протеазами) с высвобождением полной активности интерлейкина в необходимом сайте и также отделением его от элемента продления времени полужизни нерасщепленной версии. В таких вариантах осуществления полностью активный и свободный интерлейкин будет иметь очень отличные фармакокинетические (ФК) свойства - время полужизни, составляющее часы, вместо недель. Кроме того, воздействие активного цитокина ограничено местом необходимой цитокиновой активности (например, местом воспаления или опухолью), а системное воздействие активного цитокина и связанные с ним токсичность и побочные эффекты снижены.
[81] Другие цитокины, предусмотренные в этом изобретении, имеют сходную фармакологию (например, IL-15 по данным Blood 2011 117:4787-4795; doi: doi.org/10.1182/blood-2010-10-311456) с IL-2 и, соответственно, дизайн этого изобретения решает проблемы применения этих агентом напрямую и обеспечивает химерные полипептиды, которые могут иметь продленное время полужизни и/или быть нацелены на место необходимой активности (например, место воспаления или опухоль).
[82] При необходимости IL-2 может быть сконструирован так, чтобы связывать комплекс IL-2R в целом иди одну из трех субъединиц IL-2R, в частности, с аффинностью, которая отличается от аффинности соответствующего IL-2 дикого типа, например, для избирательной активации Tregs или Teff. Например, полипептиды IL-2, которые имеют большую аффинность в отношении тримерной формы рецептора IL-2 относительно димерной бета/гамма-формы рецептора Il-2 по сравнению с IL-2 дикого типа, могут иметь аминокислотную последовательность, которая содержит одну из следующих групп мутаций относительно SEQ ID NO: 1 (зрелый белок IL-2, содержащий аминокислоты 21-153 человеческого IL-2, имеющий номер доступа Uniprot № Р60568-1): (a) K64R, V69A и Q74P; (b) V69A, Q74P и Т101А; (с) V69A, Q74P и I128T; (d) N30D, V69A, Q74P и F103S; (е) K49E, V69A, A73V и K76E; (f) V69A, Q74P, Т101А и T133N; (g) N30S, V69A, Q74P и I128A; (h) V69A, Q74P, N88D и S99P; (i) N30S, V69A, Q74P и I128T; (j) K9T, Q11R, K35R, V69A и Q74P; (k) A1T, M46L, K49R, E61D, V69A и H79R; (1) K48E, E68D, N71T, N90H, F103S и I114V; (m) S4P, Т10А, Q11R, V69A, Q74P, N88D и Т133А; (n) E15K, N30S Y31H, K35R, K48E, V69A, Q74P и I92T; (о) N30S, E68D, V69A, N71A, Q74P, S75P, K76R и N90H; (р) N30S, Y31C, Т37А, V69A, A73V, Q74P, H79R и I128T; (q) N26D, N29S, N30S, K54R, E67G, V69A, Q74P и I92T; (r) K8R, Q13R, N26D, N30T, K35R, T37R, V69A, Q74P и I92T; и (s) N29S, Y31H, K35R, Т37А, K48E, V69A, N71R, Q74P, N88D и I89V. Этот подход также можно применять для получения мутеинов или других цитокинов, включая интерлейкины (например, IL-2, IL-7, IL-12, IL-15, IL-18, IL-23), интерфероны (IFN, включая IFN-альфа, IFN-бета и IFN-гамма), факторы некроза опухолей (например, TNF-альфа, лимфотоксин), трансформирующие факторы роста (например, TGF-бета1, TGF-бета2, TGF-бета3) и гранулоцитарно-макрофагальный колонне стимулирующий фактор (GM-CS). Например, можно получать мутеины, которые имеют необходимую аффинность связывания в отношении когнатного рецептора.
[83] Как указано выше, любые описанные в данном документе мутантные полипептиды IL-2 могут содержать описанные последовательности; также они могут быть ограничены последовательностями, описываемыми или иным образом идентичными SEQ ID NO: 1. Кроме того, любой из описанных в данном документе мутантных полипептидов IL-2, необязательно, может содержать замену остатка цистеина в позиции 125 другим остатком (например, серина) и/или может, необязательно, содержать делецию остатка аланина в позиции 1 SEQ ID NO: 1.
[84] Другим подходом улучшения терапевтического индекса терапии на основе IL-2 является оптимизация фармакокинетики молекулы для максимальной активации клеток Treg. Ранние исследования действия IL-2 продемонстрировали, что для стимуляции IL-2 пролиферации человеческих Т-клеток in vitro необходимо минимум 5-6-часовое воздействие эффективных концентрация IL-2 (Cantrell, D.A., et. al., 1984, Science, 224: 1312-1316). При введения пациентам-людям IL-2 имеет очень короткое плазменное время полужизни, составляющее 85 минут для внутривенного введения и 3,3 часа для подкожного введения (Kirchner, G.I., et al., 1998, Br J Clin Pharmacol. 46:5-10). Из-за его короткого времени полужизни поддержание IL-2 в циркуляции на уровне или вблизи уровня, необходимого для стимуляции пролиферации Т-клеток в течение необходимого времени, требуются высокие дозы, которые приводят к пиковым уровням IL-2, существенно превышающим ЕС50 для клеток Treg, или требуют частого введения. Эти высокие пиковые уровни IL-2 могут активировать рецепторы IL2Rβγ и имеют другие непредполагаемые или нежелательные эффекты, например, СКУ, как указано выше. Аналог IL-2 или многофункциональный белок с IL-2, присоединенным к домену, который обеспечивает связывание с FcRn-рецептором, с большим временем полужизни в циркуляции, чем IL-2, может обеспечивать целевую концентрацию лекарственного препарата в течение определенного периода времени в более низкой дозе, чем IL-2, и с более низкими пиковыми уровнями. Следовательно, для такого аналога IL-2 будут необходимы более низкие дозы или менее частое введение, чем для IL-2, для эффективной стимуляции клеток Treg. Менее частое подкожное введение лекарственного препарата IL-2 также будет лучше переноситься пациентами. Терапевтическое средством с такими характеристиками будет клинически транслироваться в улучшенную фармакологическую эффективность, сниженную токсичность и лучшее соблюдение пациентами режима терапии. В альтернативном варианте IL-2 или мутеины IL-2 (в данном документе «IL-2*») могут быть избирательно нацелены на предполагаемое место действия (например, места воспаления). Это нацеливание может быть обеспечено одной из нескольких стратегий, включая добавление к вводимому агенту доменов, которые содержат блокаторы IL-2 (или мутеинов), которые отщепляются, или с помощью нацеливающих доменов, или с применением обоих вариантов.
[85] В некоторых вариантах осуществления частичные агонисты IL-2* могут быть созданы с расчетом на связывание с большей или меньшей аффинностью в зависимости от необходимой мишени; например, IL-2* может быть сконструирован с расчетом на связывание с повышенной аффинностью с одной или более субъединицами рецептора, но не с другими. Эти типы частичных агонистов, в отличие от полных агонистов или абсолютных агонистов, обеспечивают возможность изменения свойств сигнализации до амплитуды, которая обеспечивает необходимые функциональные свойства, не доходя до границ нежелательных свойств. С учетом разной активности частичных агонистов может быть сконструирован репертуар вариантов IL-2, который демонстрирует даже большую степень отличаемой сигнальной активности в диапазоне от практически полного агонизма до полного антагонизма.
[86] В некоторых вариантах осуществления IL-2* характеризуется измененной аффинностью в отношении IL-2Rα. В некоторых вариантах осуществления IL-2* характеризуется большей аффинностью в отношении IL-2Rα чем IL-2 дикого типа. В других вариантах осуществления IL-2* характеризуется измененной аффинностью в отношении IL-2Rβ. В одном варианте осуществления IL-2* характеризуется повышенной аффинностью связывания в отношении IL-2Rβ, например, N-конца IL-2Rβ, что устраняет функциональную необходимость в IL-2Rα. В другом варианте осуществления создан IL-2*, который характеризуется повышенной аффинностью связывания в отношении IL-2Rβ, но демонстрирует сниженное связывание с IL-2Rγ, и, следовательно, является дефектным в отношении гетеродимеризации и сигнализации IL-2Rβγ.
[87] Блокирующие фрагменты, дополнительно подробно описанные ниже, также можно использовать, чтобы способствовать связыванию или активации одного или более рецепторов. В одном варианте осуществления блокирующие фрагменты добавлены таким образом, чтобы блокировать связывание или активацию IL-2Rβγ, но не изменять связывание или активацию IL-2Rα. В другом варианте осуществления блокирующие фрагменты добавлены таким образом, чтобы снизить связывание или активацию IL-2Rα. В другом варианте осуществления блокирующие фрагменты добавлены таким образом, чтобы ингибировать связывание или активацию всех трех рецепторов. Это блокирование можно снимать путем удаления блокирующих фрагментов в конкретном окружении, например, за счет протеолитического расщепления линкеры, связывающего один или более блокирующих фрагментов с цитокином.
[88] Сходный подход можно применять для усовершенствования других цитокинов, в частности, для их применения в качества иммуностимулирующих агентов, например, для лечения рака. Например, в этом аспекте фармакокинетику и/или фармакодинамику цитокина (например, IL-2, IL-7, IL-12, IL-15, IL-18, IL-21 IL-23, IFN-альфа, IFN-бета, IFN-гамма, TNF-альфа, лимфотоксина, TGF-бета1, TGF-бета2, TGF-бета3, GM-CSF, CXCL10, CCL19, CCL20 и CCL21) можно подбирать в расчете на максимальную активацию эффекторных клеток (например, воздействие на Т-клетки, NK-клетки) и/или цитотоксических клеток, стимулирующих иммунный ответ (например, индукция созревания дендритных клеток) в месте необходимой активности, таком как опухоль, но предпочтительно не систематически.
[89] Таким образом, в данном документе предложены фармацевтические композиции, содержащие по меньшей мере один полипептид цитокина, такой как интерлейкины (например, IL-2, IL-7, IL-12, IL-15, IL-18, IL-21, IL-23), интерфероны (IFN, включая IFN-альфа, IFN-бета и IFN-гамма), факторы некроза опухолей (например, TNF-альфа, лимфотоксин), трансформирующие факторы роста (например, TGF-бета1, TGF-бета2, TGF-бета3), хемокины (например, CXCL10, CCL19, CCL20, CCL21) и гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CS) или функциональный фрагмент или мутеин любого из вышеприведенного. Полипептид, как правило, также содержит по меньшей мере одну линкерную аминокислотную последовательность, причем аминокислотная последовательность, в определенных вариантах осуществления, может расщепляться эндогенной протеазой. В одном варианте осуществления линкер содержит аминокислотную последовательность HSSKLQ (SEQ ID NO: 25), GPLGVRG (SEQ ID NO: 128), IPVSLRSG (SEQ ID NO: 129), VPLSLYSG (SEQ ID NO. 130) или SGESPAYYTA (SEQ ID NO: 131). В других вариантах осуществления химерный полипептид дополнительно содержит блокирующий фрагмент, например, стерический блокирующий полипептидный фрагмент, способный блокировать активность полипептида интерлейкина. Блокирующий фрагмент, например, может содержать связывающий домен человеческого сывороточного альбумина (ЧСА) или необязательно разветвленный или многозвеньевой полиэтиленгликоль (ПЭГ). В альтернативном варианте фармацевтическая композиция содержит первый полипептид цитокина или его фрагмент и блокирующий фрагмент, например, стерический блокирующий полипептидный фрагмент, причем блокирующий фрагмент блокирует активность полипептида цитокина или рецептора цитокина и при этом, в определенных вариантах осуществления, блокирующий фрагмент содержит расщепляемый протеазой домен. В некоторых вариантах осуществления блокирование и снижение активности цитокина достигается просто за счет присоединения дополнительных доменов с очень короткими линкерами к N- или С-концу домена интерлейкина. В таких вариантах осуществления предполагается, что блокирование снимается расщеплением протеазой блокирующего фрагмента или короткого линкера, который связывает блокатор с интерлейкином. После отсечения или освобождения домена он более не способен блокировать активность цитокина.
[90] Фармацевтическая композиция, например, химерный полипептид, может содержать два или более цитокинов, которые могут представлять собой полипептид одного и того же цитокина или полипептиды разных цитокинов. Например, два или более типов цитокинов имеют взаимодополняющие функции. В некоторых примерах первым цитокином является IL-2, а вторым цитокином является IL-12. В некоторых вариантах осуществления каждый из полипептидов двух или более разных типов цитокинов обладает активностью, которая модулирует активность полипептидов других цитокинов. В некоторых примерах химерных полипептидов, которые содержат полипептиды двух цитокинов, полипептид первого цитокина активирует Т-клетки, а полипептид второго цитокина не активирует Т-клетки. В некоторых примерах химерных полипептидов, которые содержат полипептиды двух цитокинов, первый цитокин является хемоатрактантом, например, CXCL10, а второй цитокин является активатором иммунных клеток.
[91] Предпочтительно полипептиды цитокинов (включая их функциональные фрагменты), которые входят в состав описанных в данном документе слитых белков, не мутированы и не сконструированы так, чтобы изменять свойства цитокина природного происхождения, включая аффинность и специфичность связывания рецептора или сывороточное время полужизни. При этом изменения в аминокислотной последовательности относительно цитокина природного происхождения (включая дикий тип) являются приемлемыми, например, для облегчения клонирования и обеспечения необходимых уровней экспрессии.
Связывание CD25
[92] В модифицированных конструкциях IL-2 часто ослаблено связывание CD25. В противоположность этому, описанные в данном документе полипептиды IL-2 предпочтительно не модифицированы для предотвращения связывания CD25. Предпочтительно описанные в данном документе полипептиды IL-2 связывают CD25. Как правило, описанные в данном документе слитые белки IL-2 способны связывать CD25, а блокирование направлено на взаимодействия с IL-2R-бета и гамма (CD 122 и CD 132).
Блокирующий фрагмент
[93] Блокирующий фрагмент может представлять собой любой фрагмент, который ингибирует способность цитокина связывать и/или активировать его рецептор. Блокирующий фрагмент может ингибировать способность цитокина связывать и/или активировать его рецептор за счет стерического блокирования и/или нековалентного связывания цитокина. Примеры подходящих блокирующих фрагментов включают полноразмерный или цитокин-связывающий фрагмент или мутеин когнатного рецептора цитокина. Также можно использовать антитела и их фрагменты, включая поликлональное антитело, рекомбинантное антитело, человеческое антитело, гуманизированное антитело, одноцепочечный вариабельный фрагмент (scFv), однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен нанотела верблюжьих (VHH), dAb и т.п., которые связывают цитокин. Другие антигенсвязывающие домены, которые связывают цитокин и которые можно использовать, включают отличные от иммуноглобулинов белки, которые имитируют связывание и/или структуру антитела, такие как антикалины, аффилины, молекулы аффител, аффимеры, аффитины, альфатела, авимеры, дарпины, финомеры, пептиды доменов Куница, монотела и связывающие домены на основе других сконструированных остовов, таких как остовы SpA, GroEL, фибронектина, липокалина и CTLA4. дополнительные примеры подходящих блокирующих полипептидов включают полипептиды, которые стерически ингибируют или блокируют связывание цитокина с его когнатным рецептором. Преимущественно такие фрагменты могут также выполнять функцию элементов продления времени полужизни. Например, пептид, модифицированный путем конъюгации с водорастворимым полимером, таким как ПЭГ, может стерически ингибировать или предотвращать связывание цитокина с его рецептором. Также можно использовать полипептиды или их фрагменты, которые имеют длительное сывороточное время полужизни, такие как сывороточный альбумин (человеческий сывороточный альбумин), Fc иммуноглобулина, трансферрин и т.п., а также фрагменты и мутеины таких полипептидов. Антитела и антигенсвязывающие домены, которые связываются, например, с белком с длительным сывороточным временем полужизни, таким как ЧСА, иммуноглобулин или трансферрин, или с рецептором, который возвращается на плазматическую мембрану, таким как FcRn или рецептор трансферрина, также могут ингибировать цитокин, в частности при связывании с антигеном. Примеры таких антигенсвязывающих полипептидов включают одноцепочечный вариабельный фрагмент (scFv), однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен нанотела верблюжьих (VHH), dAb и т.п. Другие подходящие антигенсвязывающие домены, которые связывают цитокин и которые также можно использовать, включают отличные от иммуноглобулинов белки, которые имитируют связывание и/или структуру антитела, такие как антикалины, аффилины, молекулы аффител, аффимеры, аффитины, альфатела, авимеры, дарпины, финомеры, пептиды доменов Куница, монотела и связывающие домены на основе других сконструированных остовов, таких как остовы SpA, GroEL, фибронектина, липокалина и CTLA4.
[94] В иллюстративных примерах, если IL-2 является цитокином в химерном полипептиде, блокирующий фрагмент может быть полноразмерным рецептором или фрагментом или мутеином альфа-цепи рецептора IL-2 (IL-2Rα) или бета- (IL-2Rβ) или гамма-цепи рецептора IL-2 (IL-2Rγ), однодоменным анти-IL-2 антителом (dAb) или scFv, Fab, анти-CD25 антителом или его фрагментом и анти-HAS dAb или scFv, и т.п.
Дополнительные аспекты данного изобретения
1. Слитый белок, содержащий цитокиновый фрагмент, который функционально связан со связывающим фрагментом, причем связывающий фрагмент содержит отличную от CDR петлю и расщепляемый линкер, при этом связывающий фрагмент способен маскировать связывание цитокина с его рецептором и/или активацию рецептора цитокином.
2. Слитый белок по аспекту 1, отличающийся тем, что связывающий фрагмент представляет собой природный пептид, синтетический пептид, сконструированный остов или сконструированный общий сывороточный белок.
3. Слитый белок по аспекту 1 или 2, отличающийся тем, что сконструированный остов содержит sdAb, scFv, Fab, VHH, домен фибронектина типа III, иммуноглобулин-подобный остов, дарпин, пептид цистинового узла, липокалин, трехспиральный остов, родственный протеину G альбумин-связывающий модуль или остов ДНК- или РНК-аптамера.
4. Слитый белок по любому из аспектов 1-2, отличающийся тем, что связывающий фрагмент способен связываться с общим сывороточным белком.
5. Слитый белок по любому из аспектов 1-3, отличающийся тем, что отличная от CDR петля получена из вариабельного домена, константного домена, домена С1-типа, домена С2-типа, I-домена или любых их комбинаций.
6. Слитый белок по любому из аспектов 1-4, отличающийся тем, что связывающий фрагмент дополнительно содержит определяющие комплементарность области (CDR).
7. Слитый белок по аспекту 5, отличающийся тем, что связывающий фрагмент способен связываться с общим сывороточным белком.
8. Слитый белок по аспекту 6, отличающийся тем, что общий сывороточный белок представляет собой белок, продлевающий время полужизни.
9. Слитый белок по аспекту 6 или 7, отличающийся тем, что общий сывороточный белок представляет собой альбумин, трансферрин, фактор XIII или фибриноген.
10. Слитый белок по любому из аспектов 5-8, отличающийся тем, что петля CDR обеспечивает сайт связывания, специфический в отношении общего сывороточного белка или легкой цепи иммуноглобулина, или любой их комбинации.
11. Слитый белок по любому из аспектов 19, отличающийся тем, что расщепляемый линкер содержит сайт расщепления.
12. Слитый белок по аспекту 10, отличающийся тем, что сайт расщепления распознается протеазой.
13. Слитый белок по аспекту 11, отличающийся тем, что связывающий фрагмент связан с цитокином.
14. Слитый белок по аспекту 11, отличающийся тем, что связывающий фрагмент ковалентно связан с цитокином.
15. Слитый белок по аспекту 11 или 14, отличающийся тем, что связывающий фрагмент способен маскировать связывание цитокина с его мишенью посредством специфических межмолекулярных взаимодействий между связывающим фрагментом и цитокином.
16. Слитый белок по любому из аспектов 11-14, отличающийся тем, что отличная от CDR петля обеспечивает сайт связывания, специфический в отношении связывания фрагмента с цитокином.
17. Слитый белок по любому из аспектов 11-15, отличающийся тем, что после расщепления расщепляемого линкера происходит отделение связывающего фрагмента от цитокина, а цитокин связывается со своей мишенью.
18. Слитый белок по любому из аспектов 1-16, отличающийся тем, что цитокин связывается с рецептором цитокина.
19. Слитый белок по аспекту 17, отличающийся тем, что рецептор цитокина включает рецептор цитокина типа I, рецептор IL типа I, рецептор IL типа II, рецептор хемокина или рецептор суперсемейства факторов некроза опухолей.
20. Слитый белок по любому из аспектов 1-18, отличающийся тем, что расщепляемый линкер содержит сайт расщепления.
21. Слитый белок по аспекту 20, отличающийся тем, что сайт расщепления распознается протеазой.
22. Слитый белок по аспекту 21, отличающийся тем, что сайт расщепления протеазой распознается сериновой протеазой, цистеиновой протеазой, аспартатной протеазой, треониновой протеазой, глутаминовой кислой протеазой, металлопротеиназой, желатиназой или аспарагиновой пептид-лиазой.
23. Слитый белок по аспекту 21, отличающийся тем, что сайт расщепления протеазой распознается катепсином В, катепсином С, катепсином D, катепсином Е, катепсином K, катепсином L, калликреином, hK1, hK10, hK15, плазмином, коллагеназой, коллагеназой типа IV, стромелизином, фактором Ха, химотрипсин-подобной протеазой, трипсин-подобной протеазой, эластазо-подобной протеазой, субтилизин-подобной протеазой, актинидаином, бромелаином, кальпаином, каспазой, каспазой-3, Mir1-CP, папаином, ВИЧ-1-протеазой, ВПГ-протеазой, ЦМВ-протеазой, химозином, ренином, пепсином, матриптазой, легумаином, плазмепсином, непентезином, металлоэкзо пептидазой, металлоэндопептидазой, матриксной металлопротеиназой (ММР), ММР1, ММР2, ММР3, ММР8, ММР9, ММР10, ММР11, ММР12, ММР13, ММР14, ADAM10, ADAM17, ADAM12, активатором плазминогена урокиназного типа (uPA), энтерокиназой, простат-специфической мишенью (PSA, hK3), интерлейкин-1β-конвертирующим ферментом, тромбином, FAP (FAP-α), дипептидилпептидазой или дипептидилпептидазой IV (DPPIV/CD26), трансмембранной сериновой протеазой типа II (TTSP), эластазой нейтрофилов, катепсином G, протеиназой 3, сериновой протеазой нейтрофилов 4, химазой тучных клеток, триптазой тучных клеток, дипептидилпептидазой и дипептидилпептидазой IV (DPPIV/CD26).
24. Кондиционально активный связывающий белок, содержащий связывающий фрагмент (М), который содержит отличную от CDR петлю, цитокин и расщепляемый линкер (L), причем отличная от CDR петля способна связываться с цитокином, а связывающий фрагмент способен ингибировать связыванием цитокина с его рецептором и/или ингибировать активацию рецептора цитокином.
25. Кондиционально активный связывающий белок по аспекту 24, отличающийся тем, что связывающий фрагмент способен связываться с белком, продлевающим время полужизни.
26. Кондиционально активный связывающий белок по аспекту 24 или 25, отличающийся тем, что связывающий фрагмент представляет собой природный пептид, синтетический пептид, сконструированный остов или сконструированный общий сывороточный белок.
27. Кондиционально активный связывающий белок по аспекту 26, отличающийся тем, что сконструированный остов содержит sdAb, scFv, Fab, VHH, домен фибронектина типа III, иммуноглобулин-подобный остов, дарпин, пептид цистинового узла, липокалин, трехспиральный остов, родственный протеину G альбумин-связывающий модуль или остов ДНК- или РНК-аптамера.
28. Кондиционально активный связывающий по любому из аспектов 24-27, отличающийся тем, что отличная от CDR петля получена из вариабельного домена, константного домена, домена С1-типа, домена С2-типа, I-домена или любых их комбинаций.
29. Кондиционально активный связывающий белок по любому из аспектов 24-28, отличающийся тем, что связывающий фрагмент дополнительно содержит определяющие комплементарность области (CDR).
30. Кондиционально активный связывающий белок по любому из аспектов 24-29, отличающийся тем, что связывающий фрагмент содержит сайт связывания, специфический в отношении общего сывороточного белка.
31. Кондиционально активный связывающий белок по аспекту 30, отличающийся тем, что общий сывороточный белок представляет собой альбумин, трансферрин, фактор XIII или фибриноген.
32. Кондиционально активный связывающий белок по любому из аспектов 29-31, отличающийся тем, что CDR обеспечивают сайт связывания, специфический в отношении общего сывороточного белка или легкой цепи иммуноглобулина, или любой их комбинации.
33. Кондиционально активный связывающий белок по любому из аспектов 29-32, отличающийся тем, что связывающий фрагмент способен маскировать связывание цитокина с его мишенью посредством специфических межмолекулярных взаимодействий между связывающим фрагментом и цитокином.
34. Кондиционально активный связывающий белок по любому из аспектов 29-33, отличающийся тем, что отличная от CDR петля обеспечивает сайт связывания, специфический в отношении связывания связывающего фрагмента с цитокином.
35. Кондиционально активный связывающий белок по любому из аспектов 24-34, отличающийся тем, что цитокин связывается с рецептором цитокина.
36. Кондиционально активный связывающий белок по аспекту 35, отличающийся тем, что рецептор цитокина включает рецептор цитокина типа I, рецептор IL типа I, рецептор IL типа II, рецептор хемокина или рецептор суперсемейства факторов некроза опухолей.
37. Кондиционально активный связывающий белок по любому из аспектов 24-36, отличающийся тем, что расщепляемый линкер содержит сайт расщепления.
38. Кондиционально активный связывающий белок по аспекту 37, отличающийся тем, что сайт расщепления распознается протеазой.
39. Кондиционально активный связывающий белок по аспекту 38, отличающийся тем, что сайт расщепления протеазой распознается сериновой протеазой, цистеиновой протеазой, аспартатной протеазой, треониновой протеазой, глутаминовой кислой протеазой, металлопротеиназой, желатиназой или аспарагиновой пептид-лиазой.
40. Кондиционально активный связывающий белок по аспекту 38, отличающийся тем, что сайт расщепления протеазой распознается катепсином В, катепсином С, катепсином D, катепсином Е, катепсином K, катепсином L, калликреином, hK1, hK10, hK15, плазмином, коллагеназой, коллагеназой типа IV, стромелизином, фактором Ха, химотрипсин-подобной протеазой, трипсин-подобной протеазой, эластазо-подобной протеазой, субтилизин-подобной протеазой, актинидаином, бромелаином, кальпаином, каспазой, каспазой-3, Mir1-CP, папаином, ВИЧ-1-протеазой, ВПГ-протеазой, ЦМВ-протеазой, химозином, ренином, пепсином, матриптазой, легумаином, плазмепсином, непентезином, металлоэкзопептидазой, металлоэндопептидазой, матриксной металлопротеиназой (ММР), ММР1, ММР2, ММР3, ММР8, ММР9, ММР10, ММР11, MMP12, MMP13, MMP14, ADAM10, ADAM17, ADAM12, активатором плазминогена урокиназного типа (uPA), энтерокиназой, простат-специфической мишенью (PSA, hK3), интерлейкин-1β-конвертирующим ферментом, тромбином, FAP (FAP-α), дипептидилпептидазой или дипептидилпептидазой IV (DPPIV/CD26), трансмембранной сериновой протеазой типа II (TTSP), эластазой нейтрофилов, катепсином G, протеиназой 3, сериновой протеазой нейтрофилов 4, химазой тучных клеток, триптазой тучных клеток, дипептидилпептидазой и дипептидилпептидазой IV (DPPIV/CD26).
41. Кондиционально активный связывающий белок по аспекту 24, дополнительно содержащий домен для продления времени полужизни, связанный со связывающим фрагментом, причем домен для продления времени полужизни обеспечивает связывающий белок переключателем безопасности, и при этом после расщепления линкера происходит активация связывающего белка путем отделения связывающего фрагмента и домена для продления времени полужизни от цитокина и, таким образом, происходит отделение связывающего белка от переключателя безопасности.
42. Кондиционально активный связывающий белок по аспекту 41, отличающийся тем, расщепление линкера происходит в микроокружении опухоли.
43. Кондиционально активный связывающий белок, содержащий связывающий фрагмент, который связывает цитокин посредством отличной от CDR петли в связывающем фрагменте, причем связывающий фрагмент дополнительно связан с доменом для продления времени полужизни и содержит расщепляемый линкер, причем связывающий фрагмент имеет продленное время полужизни до его активации путем расщепления линкера, а после активации происходит отделение связывающего фрагмента и домена для продления времени полужизни от цитокина, и связывающий белок в активированном состоянии не обладает продленным временем полужизни.
44. Кондиционально активный связывающий белок по аспекту 43, отличающийся тем, расщепление линкера происходит в микроокружении опухоли.
Элементы для продления времени полужизни in vivo
[95] Предпочтительно химерные полипептиды содержат элемент для продления времени полужизни in vivo. Повышение времени полужизни терапевтических молекул in vivo с природно короткими временами полужизни позволяет реализовывать более приемлемые и поддающиеся коррекции схемы введения доз, не жертвуя эффективностью. В контексте данного документа «элемент для продления времени полужизни» является частью химерного полипептида, которая повышает время полужизни in vivo и улучшает ФК, например, путем изменения его размера (например, чтобы превышать порог почечной фильтрации), формы, гидродинамического радиуса, заряда или параметров всасывания, биораспределения, метаболизма и элиминации. Типовым способом улучшения ФК полипептида является экспрессия в полипептидной цепи элемента, который связывается с рецепторами, которые подвергаются рециклингу в плазматическую мембрану клеток, а не деградации в лизосомах, такими как FcRn-рецептор на эндотелиальных клетках и рецептор трансферрина. Три типа белков, например, человеческие IgG, ЧСА (или его фрагменты) и трансферрин присутствуют в человеческой сыворотке в течение намного большего времени, чем можно было спрогнозировать по их размеру, что является функцией их способности связываться с рецепторами, которые подвергаются рециклингу, а не деградации в лизосоме. Эти белки или их фрагменты, которые сохраняют свойство связывания FcRn, обычно связывают с другими полипептидами для продления их сывороточного времени полужизни. В одном варианте осуществления элементом для продления времени полужизни является связывающий домен человеческого сывороточного альбумина (ЧСА). ЧАС (SEQ ID NO: 2) также может быть напрямую связан с фармацевтическими композициями или связан посредством короткого линкера. Также можно использовать фрагменты ЧСА. ЧСА и его фрагменту могут осуществлять функцию как блокирующего фрагмента, так и элемента для продления времени полужизни. Человеческие IgG и Fc-фрагменты также могут осуществлять сходную функцию.
[96] Элементом продления сывороточного времени полужизни также может быть антигенсвязывающий полипептид, который связывается с белком с большим сывороточным временем полужизни, таким как сывороточный альбумин, трансферрин и т.п. Примеры таких полипептидов включают антитела и их фрагменты, включая поликлональное антитело, рекомбинантное антитело, человеческое антитело, гуманизированное антитело, одноцепочечный вариабельный фрагмент (scFv), однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен нанотела верблюжьих (VHH), dAb и т.п. Другие подходящие антигенсвязывающие домены включают отличные от иммуноглобулинов белки, которые имитируют связывание и/или структуру антитела, такие как антикалины, аффилины, молекулы аффител, аффимеры, аффитины, альфатела, авимеры, дарпины, финомеры, пептиды доменов Куница, монотела и связывающие домены на основе других сконструированных остовов, таких как остовы SpA, GroEL, фибронектина, липокалина и CTLA4. Дополнительные примеры антигенсвязывающих полипептидов включают лиганд для необходимого рецептора, лиганд-связывающую часть рецептора, лектин и пептиды, которые связываются или ассоциируют с одним или более целевыми антигенами.
[97] Некоторые предпочтительные элементы для продления сывороточного времени полужизни представляют собой полипептиды, которые содержат определяющие комплементарность области (CDR) и, необязательно, отличные от CDR петли. Преимущественно такие элементы для продления сывороточного времени полужизни могут продлевать сывороточное время полужизни цитокина, а также осуществлять функцию ингибиторов цитокина (например, посредством стерического блокирования, нековалентного взаимодействия или их комбинации) и/или нацеливающих доменов. В некоторых случаях элементы для продления сывороточного времени полужизни представляют собой домены, полученные из молекулы иммуноглобулина (Ig-молекулы) или сконструированные белковые каркасы, которые имитируют структуру и/или активность связывания антитела. Ig может принадлежать любому классу или подклассу (IgG1, IgG2, IgG3, IgG4, IgA, IgE, IgM и т.д.). Полипептидная цепь Ig-молекулы свернута в ряд параллельных бета-цепей, соединенных петлями. В вариабельной области три петли составляют «определяющие комплементарность области» (CDR), которые определяют антигенсвязывающую специфичность молекулы. Молекула IgG содержит по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, связанные между собой дисульфидными связями, или их антигенсвязывающий фрагмент. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно называемой в данном документе VH) и константной области тяжелой цепи. Константная область тяжелой цепи содержит три домена - CH1, СН2 и СН3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно называемой в данном документе VL) и константной области легкой цепи. Константная область легкой цепи содержит один домен - CL. VH- и VL-области можно дополнительно разделить на области гипервариабельности, называемые определяющими комплементарность областями (CDR), которые являются гипервариабельными по последовательности и/или участвуют в распознавании антигена, и/или обычно образуют структурно определенные петли, которые перемежаются более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. В некоторых вариантах осуществления этого изобретения по меньшей мере некоторые или все аминокислотные последовательности FR1, FR2, FR3 и FR4 являются частью «отличной от CDR петли» связывающих фрагментов, описанных в данном документе. Как проиллюстрировано на Фиг. 5, вариабельный домен молекулы иммуноглобулина имеет несколько бета-цепей, которые расположены двумя складками. Вариабельные домены как легкой, так и тяжелой цепей иммуноглобулина содержат гипервариабельные петли или определяющие комплементарность области (CDR). Три CDR V-домена (CDR1, CDR2, CDR3) образуют кластер в одном конце бета-бочки. CDR представляют собой петли, которые соединяют бета-цепи В-С, С'-С'' и F-G укладки цепи иммуноглобулина, причем нижние петли, которые соединяют бета-цепи АВ, СС', С''-D и E-F укладки цепи иммуноглобулина, и верхняя петля, которая соединяет цепи D-E укладки цепи иммуноглобулина, представляют собой отличные от CDR петли. В некоторых вариантах осуществления этого изобретения по меньшей мере некоторые аминокислотные остатки константного домена, CH1, СН2 и СН3, являются частью «отличной от CDR петли» связывающих фрагментов, описанных в данном документе. Отличные от CDR петли, в некоторых вариантах осуществления, включают одну или более из петель АВ, CD, EF и DE домена С1-типа Ig или Ig-подобной молекулы; петель АВ, СС', EF, FG, ВС и ЕС' домена С2-типа Ig или Ig-подобной молекулы; петель DE, BD, GF, А(А1А2)В и EF домена I(промежуточного)-типа Ig или Ig-подобной молекулы.
[98] В пределах вариабельного домена считается, что CDR отвечают за распознавание и связывание антигена, тогда как остатки FR считаются каркасом для CDR. Однако в определенных случаях некоторые из остатков FR играют важную роль в распознавании и связывании антигена. Каркасные области, которые влияют на связывание антигена, делятся на две категории. К первой относятся остатки FR, которые контактируют с антигеном и, таким образом, являются частью сайта связывания, а некоторые из этих остатков в последовательности расположены близко к CDR. Другими остатками являются те, которые расположены далеко от CDR в последовательности, но находятся в непосредственной близости к ним в 3-D структуре молекулы, например, в петле в тяжелой цепи. Домен для продления сывороточного времени полужизни (например, домен, который содержит CDR) может содержать по меньшей мере одну отличную от CDR петлю. В некоторых вариантах осуществления отличная от CDR петля обеспечивает сайт связывания для связывания с цитокином, общим сывороточным белком или другим целевым антигеном.
[99] Элемент для продления сывороточного времени полужизни помимо того, что содержит CDR, дополнительно или в качестве альтернативы содержит отличную от CDR петлю. В некоторых вариантах осуществления отличная от CDR петля модифицирована с целью создания антигенсвязывающего сайте, специфического в отношении необходимого целевого антигена, такого как общий сывороточный белок, такой как альбумин, или в отношении цитокинового фрагмента или другого целевого антигена. Подразумевается, что для модификации отличной от CDR петли можно использовать различные способы, например, сайт-направленный мутагенез, случайный мутагенез, вставку по меньшей мере одной кислоты, которая является чужеродной для аминокислотной последовательности отличной от CDR петли, аминокислотную замену. В некоторых примерах пептид антигена вставлен в отличную от CDR петлю. В некоторых примерах антигенный пептид замещает отличную от CDR петлю. Модификацией для создания антигенсвязывающего сайта в некоторых случаях является только одна отличная от CDR петля. В других случаях модифицировано более одной отличной от CDR петли. Например, модификация может присутствовать в любой из отличных от CDR петель, проиллюстрированных на Фиг. 5, т.е. АВ, СС', С'' D, EF и D-E. В некоторых случаях модификация находится в петле DE. В других случаях модификации находятся во всех четырех петлях из АВ, СС', С''-D, E-F.
[100] В некоторых примерах элемент для продления сывороточного времени полужизни имеет двойную специфичность связывания и содержит CDR, которые специфически связывают общие сывороточные белки, такие как сывороточный альбумин, и отличные от CDR петли, которые специфически связывают и блокируют цитокиновый домен. В других примерах элемент для продления сывороточного времени полужизни содержит CDR, которые специфически связывают целевой антиген, такой как цитокиновый домен или другой целевой антиген, и отличные от CDR петли, которые специфически связывают общий сывороточный белок, такой как сывороточный альбумин. Предпочтительно элемент для продления сывороточного времени полужизни ингибирует связывание цитокинового домена с когнатным рецептором цитокина, например, посредством стерического затруднения, посредством специфических межмолекулярных взаимодействий или их комбинации.
[101] В некоторых вариантах осуществления элемент для продления сывороточного времени полужизни напрямую нековалентно связывается с цитокином и ингибирует его активность.
[102] В определенных примерах связывающий фрагмент связывается с цитокином посредством одной или более из петель АВ, СС', С'' D и E-F и связывается с общим сывороточным белком, таким как альбумин, посредством одной или более из петель ВС, С'С'' и FG. В определенных примерах связывающий фрагмент связывается с общим сывороточным белком, таким как альбумин, посредством петли АВ, СС', С'' D или EF и связывается с цитокином посредством петли ВС, С'С'' или FG. В определенных примерах связывающий фрагмент связывается с общим сывороточным белком, таким как альбумин, посредством петли АВ, СС', С'' D и EF и связан с цитокином посредством петли ВС, С'С'' и FG. В определенных примерах связывающий фрагмент связывается с общим сывороточным белком, таким как альбумин, посредством одной или более из петель АВ, СС', С'' D и E-F и связывается с цитокином посредством одной или более из петель ВС, С'С'' и FG.
[103] Связывающие фрагменты представляют собой любые виды полипептидов. Например, в определенных случаях связывающие фрагменты представляют собой природные пептиды, синтетические пептиды или фибронектиновые остовы, или сконструированные общие сывороточные белки. Общие сывороточные белки включают, например, альбумин, фибриноген или глобулин. В некоторых вариантах осуществления связывающие фрагменты представляют собой сконструированные остовы. Сконструированные остовы включают, например, sdAb, scFv, Fab, VHH, домен фибронектина типа III, иммуноглобулин-подобный остов (предложенный в Halaby et al., 1999. Prot Eng 12(7): 563-571), дарпин, пептид цистинового узла, липокалин, трехспиральный остов, родственный протеину G альбумин-связывающий модуль или остов ДНК- или РНК-аптамера.
[104] В некоторых случаях элемент для продления сывороточного времени полужизни связывается с цитокиновым доменом посредством отличных от CDR петель, а цитокиновый домен дополнительно соединен с нацеливающим доменом, как описано в данном документе. В некоторых случаях элемент для продления сывороточного времени полужизни содержит сайт связывания для общего сывороточного белка. В некоторых вариантах осуществления CDR обеспечивают сайт связывания для общего сывороточного белка. В некоторых примерах общий сывороточный белок представляет собой глобулин, альбумин, трансферрин, IgG1, IgG2, IgG4, IgG3, мономер IgA, фактор XIII, фибриноген, IgE или пентамерный IgM. В некоторых вариантах осуществления CDR образует сайт связывания для легкой цепи иммуноглобулина, такой как свободная легкая цепь Igκ или свободная легкая цепь Igλ.
[105] Один типовой кондиционально активный белок представлен на Фиг. 6. В проиллюстрированном примере отличные от CDR петли в домене, связывающем сывороточный альбумин (например, dAb), могут образовывать сайт для цитокина IL-2. В этом примере сайт связывания для сывороточного альбумина может быть образован CDR домена, связывающего сывороточный альбумин.
[106] Элемент для продления сывороточного времени полужизни может представлять собой любой тип связывающего домена, включая, но не ограничиваясь этим, домены из моноклонального антитела, поликлонального антитела, рекомбинантного антитела, человеческого антитела, гуманизированного антитела. В некоторых вариантах осуществления связывающий фрагмент представляет собой одноцепочечный вариабельный фрагмент (scFv), однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен нанотела верблюжьих (VHH). В других вариантах осуществления связывающие фрагменты представляют собой отличные от Ig связывающие домены, т.е. миметики антител, такие как антикалины, аффилины, молекулы аффител, аффимеры, аффитины, альфатела, авимеры, дарпины, финомеры, пептиды доменов Куница и монотела.
[107] В других вариантах осуществления элемент для продления сывороточного времени полужизни может представлять собой водорастворимый полимер или пептид, который конъюгирован к водорастворимому полимеру, такому как ПЭГ. В контексте данного документе «ПЭГ», «полиэтиленгликоль» и «поли(этиленгликоль» являются взаимозаменяемыми терминами и охватывают любой непептидный водорастворимый поли(этиленоксид). Термин «ПЭГ» также обозначает полимер, который содержит большинство, то есть более 50%, повторяющихся субъединиц -ОСН2СН2-. Что до конкретных форм, то ПЭГ может иметь любое число или любой ряд значений молекулярной массы, а также структур или геометрий, например, «разветвленную», «линейную», «раздвоенную», «многофункциональную» и т.п., что более подробно описано ниже. ПЭГ не ограничен конкретной структурой и может быть линейным (например, кэпированным в конце, например, алкокси-ПЭГ или бифункциональный ПЭГ), разветвленным или многозвеньевым (например, раздвоенный ПЭГ или ПЭГ, присоединенный к полиоловой сердцевине), иметь дендритную (или в форме звезды) архитектуру, в каждом случае с одной или более разлагаемыми связями или без них. Кроме того, внутренняя структура ПЭГ может иметь организацию, соответствующую любому числу повторяющихся схем, и может быть выбрана из группы, состоящей из гомополимера, чередующегося сополимера, случайного сополимера, блок-сополимера, чередующегося триполимера, случайного триполимера и блок-триполимера. ПЭГ можно конъюгировать к полипептидам и пептидам любым подходящим способом. Как правило, реакционноспособное производное ПЭГ, такое как N-гидроксисукцинимидиловый сложный эфир ПЭГ, приводят в реакцию с пептидом или полипептидом, который содержит аминокислоты с боковой цепью, которая содержит функциональную группу амина, сульфгидрила, карбоновой кислоты или гидроксила, такие как цистеин, лизин, аспарагин, глутамин, треонин, тирозин, серии, аспарагиновая кислота и глутаминовая кислота.
Нацеливающие домены и домены удержания
[108] В определенных применениях может существовать необходимость минимизировать количество времени нахождения конструкции в необходимом месте в организме. Это можно обеспечить путем включения в химерный полипептид (слитый белок) одного дополнительного домена, который влиял бы на его перемещение в организме. Например, химерные нуклеиновые кислоты могут кодировать домен, который направляет полипептид к месту в организме, например, к опухолевым клеткам или месту воспаления; этот домен называется «нацеливающим доменом», и/или кодировать домен, который удерживает полипептид в определенном месте в организме, например, в опухолевых клетках или месте воспаления; этот домен называется «доменом удержания». В некоторых вариантах осуществления домен может функционировать сразу как нацеливающий домен и домен удержания. В некоторых вариантах осуществления нацеливающий домен и/или домен удержания специфичны к богатому протеазами окружению. В некоторых вариантах осуществления кодируемые нацеливающий домен и/или домен удержания специфичны в отношении регуляторных Т-клеток (Treg), например, нацелены на рецепторы CCR4 или CD39. Другие подходящие нацеливающий домен и/или домен удержания включают те, которые имеют когнатный лиганд, характеризующийся сверхэкспрессией в воспаленной ткани, например, рецептор IL-1 или рецептор IL-6. В других вариантах осуществления подходящие нацеливающий домен и/или домен удержания включают те, которые имеют когнатный лиганд, характеризующийся сверхэкспрессией в опухолевой ткани, например, Epcam, CEA или мезотелин. В некоторых вариантах осуществления нацеливающий домен связан с интерлейкином посредством линкера, который расщепляется в месте действия (например, воспалительными или специфическими для рака протеазами) с высвобождением полной активности интерлейкина в необходимом месте. В некоторых вариантах осуществления нацеливающий домен и/или домен удержания связаны с интерлейкином посредством линкера, который не расщепляется в месте действия (например, воспалительными или специфическими для рака протеазами), что приводит к удержанию цитокина в необходимом месте.
[109] Предпочтительные антигены в некоторых случаях экспрессируются на поверхности патологической клетки или ткани, например, опухолевой или раковой клетки. Антигены, применимые для нацеливания на опухоль и удержания в ней, включают, но не ограничиваются этим, ЕрСАМ, EGFR, HER-2, HER-3, c-Met, FOLR1 и CEA. Описанные в данном документе фармацевтические композиции также содержат белки, содержащие два нацеливающих домена и/или домена удержания, которые связываются с двумя разными целевыми антигенами, которые, согласно известным данным, экспрессируются в патологической клетке или ткани. Примеры пар антигенсвязывающих доменов включают, но не ограничиваются этим, EGFR/CEA, ЕрСАМ/СЕА и HER-2/HER-3.
[110] Подходящие нацеливающие домены и/или домены удержания включают антигенсвязывающие домены, такие как антитела и их фрагменты, включая поликлональное антитело, рекомбинантное антитело, человеческое антитело, гуманизированное антитело, одноцепочечный вариабельный фрагмент (scFv), однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен нанотела верблюжьих (VHH), dAb и т.п. Другие подходящие антигенсвязывающие домены включают отличные от иммуноглобулинов белки, которые имитируют связывание и/или структуру антитела, такие как антикалины, аффилины, молекулы аффител, аффимеры, аффитины, альфатела, авимеры, дарпины, финомеры, пептиды доменов Куница, монотела и связывающие домены на основе других сконструированных остовов, таких как остовы SpA, GroEL, фибронектина, липокалина и CTLA4. Дополнительные примеры антигенсвязывающих полипептидов включают лиганд для необходимого рецептора, лиганд-связывающую часть рецептора, лектин и пептиды, которые связываются или ассоциируют с одним или более целевыми антигенами.
[111] В некоторых вариантах осуществления нацеливающие домены и/или домены удержания специфически связываются с молекулой клеточной поверхности. В некоторых вариантах осуществления нацеливающие домены и/или домены удержания специфически связываются с опухолевым антигеном. В некоторых вариантах осуществления нацеливающие полипептиды специфически и независимо связываются с опухолевым антигеном, выбранным из по меньшей мере одного из активирующего фибробласты белка альфа (FAPa), гликопротеина трофобластов (5Т4), опухолеассоциированного трансдуктора кальциевого сигнала 2 (Trop2), EDB фибронектина (EDB-FN), домена EIIIB фибронектина, CGS-2, EpCAM, EGFR, HER-2, HER-3, cMet, CEA и FOLR1. В некоторых вариантах осуществления нацеливающие полипептиды специфически и независимо связываются с двумя разными антигенами, причем по меньшей мере один из антигенов представляет собой опухолевый антиген, выбранный из активирующего фибробласты белка альфа (FAPa), гликопротеина трофобластов (5Т4), опухолеассоциированного трансдуктора кальциевого сигнала 2 (Trop2), EDB фибронектина (EDB-FN), домена EIIIB фибронектина, CGS-2, EpCAM, EGFR, HER-2, HER-3, cMet, CEA и FOLR1.
[112] Нацеливающий антиген и/или антиген удержания могут представлять собой опухолевый антиген, экспрессируемый на опухолевой клетке. Опухолевые антигены хорошо известны в данной области техники и включают, например, EpCAM, EGFR, HER-2, HER-3, c-Met, FOLR1, PSMA, CD38, ВСМА и CEA. 5Т4, AFP, B7-H3, Cadherm-6, CAIX, CD117, CD123, CD138, CD166, CD19, CD20, CD205, CD22, CD30, CD33, CD352, CD37, CD44, CD52, CD56, CD70, CD71, CD74, CD79b, DLL3, EphA2, FAP, FGFR2, FGFR3, GPC3, gpA33, FLT-3, gpNMB, HPV-16 E6, HPV-16 E7, ITGA2, ITGA3, SLC39A6, MAGE, мезотелин, Muc1, Muc16, NaPi2b, нектин-4, Р-кадгерин, NY-ESO-1, PRLR, PSCA, PTK7, ROR1, SLC44A4, SLTRK5, SLTRK6, STEAP1, TIM1, Trop2, WT1.
[113] Нацеливающий антиген и/или антиген удержания могут представлять собой белок иммунной контрольной точки. Примеры белков иммунных контрольных точек включают, но не ограничиваются этим, CD27, CD137, 2В4, TIGIT, CD155, ICOS, HVEM, CD40L, LIGHT, TIM-1, 0Х40, DNAM-1, PD-L1, PD1, PD-L2, CTLA-4, CDS, CD40, CEACAM1, CD48, CD70, A2AR, CD39, CD73, B7-H3, B7-H4, BTLA, IDO1, IDO2, TDO, KIR, LAG-3, TIM-3 или VISTA.
[114] Нацеливающий антиген и/или антиген удержания могут представлять собой молекулу клеточной поверхности, такую как белок, липид или полисахарид. В некоторых вариантах осуществления нацеливающий антиген и/или антиген удержания находятся на опухолевой клетке, вирусно инфицированной клетке, бактериально инфицированной клетке, поврежденной красной кровяной клетке, клетке артериального тромбоцита, клетке воспаленной или фиброзной ткани. Нацеливающий антиген и/или антиген удержания могут включать модулятор иммунного ответа. Примеры модуляторов иммунного ответа включают, но не ограничиваются этим, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), макрофагальный колониестимулирующий фактор (M-CSF), гранулоцитарный колониестимулирующий фактор (G-CSF), интерлейкин 2 (IL-2), интерлейкин 3 (IL-3), интерлейкин 12 (IL-12), интерлейкин 15 (IL-15), B7-1 (CD80), В7-2 (CD86), GITRL, CD3 или GITR.
[115] Нацеливающий антиген и/или антиген удержания могут представлять собой рецептор цитокина. Примеры рецепторов цитокинов включают, но не ограничиваются этим, рецепторы цитокинов типа I, такие как рецептор GM-CSF, рецептор G-CSF, рецепторы IL типа I, рецептор Еро, рецептор LIF, рецептор CNTF, рецептор ТРО; рецепторы цитокинов типа II, такие как рецептор IFN-альфа (IFNAR1, IFNAR2), рецептор IFB-бета, рецептор IFN-гамма (IFNGR1, IFNGR2), рецепторы IL типа II; рецепторы хемокинов, такие как рецепторы хемокинов СС, рецепторы хемокинов СХС, рецепторы хемокинов СХ3С, рецепторы хемокинов ХС; рецепторы суперсемейства факторов некроза опухолей, такие как TNFRSF5/CD40, TNFRSF8/CD30, TNFRSF7/CD27, TNFRSF1A/TNFR1/CD120a, TNFRSF1B/TNFR2/CD120b; рецепторы TGF-бета, такие как рецептор TGF-бета 1, рецептор TGF-бета 2; рецепторы суперсемейства Ig, такие как рецепторы IL-1, CSF-1R, PDGFR (PDGFRA, PDGFRB), SCFR.
Линкеры
[116] Как указано выше, фармацевтические композиции содержат одну или более линкерных последовательностей. Линкерная последовательность служит для обеспечения гибкости между полипептидами так, чтобы, например, блокирующий фрагмент был способен ингибировать активность полипептида цитокина. Линкерная последовательность может быть расположена между любыми или всеми компонентами из полипептида цитокина, элемента для продления сывороточного времени полужизни и/или блокирующего фрагмента. Как описано в данном документе, по меньшей мере один из линкеров расщепляется протеазой и содержит (один или более) сайты расщепления для (одной или более) необходимых протеаз. Предпочтительно необходимая протеаза обогащена или избирательно присутствует в необходимом сайте цитокиновой активности (например, микроокружении опухоли). Таким образом, слитый белок преимущественно или избирательно расщепляется в сайте необходимой цитокиновой активности.
[117] Подходящие линкеры могут иметь любую длину, такую как от 1 аминокислоты (например, Gly) до 20 аминокислот, от 2 аминокислот до 15 аминокислот, от 3 аминокислот до 12 аминокислот, в том числе от 4 аминокислот до 10 аминокислот, аминокислот до 9 аминокислот, от 6 аминокислот до 8 аминокислот или от 7 аминокислот до 8 аминокислот, и могут составлять 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59 или 60 аминокислот.
[118] Ориентация компонентов фармацевтической композиции по большому счету зависит от выбора дизайна и понятно, что возможны многие варианты ориентации и предполагается, что они все охвачены этим изобретением. Например, блокирующий фрагмент может быть расположен со стороны С-конца или N-конца полипептида цитокина.
[119] Протеазы, которые, как известно, ассоциированы с патологическими клетками или тканями, включают, но не ограничиваются этим, сериновые протеазы, цистеиновые протеазы, аспартатные протеазы, треониновые протеазы, глутаминовые кислые протеазы, металлопротеиназы, аспарагиновые пептид-лиазы, сывороточные протеазы, катепсины, катепсин В, катепсин С, катепсин D, катепсин Е, катепсин K, катепсин L, калликреины, hK1, hK10, hK15, плазмин, коллагеназу, коллагеназу типа IV, стромелизин, фактор Ха, химотрипсин-подобную протеазу, трипсин-подобную протеазу, эластазо-подобную протеазу, субтилизин-подобную протеазу, актинидаин, бромелаин, кальпаин, каспазу, каспазу-3, Mir1-CP, папаин, ВИЧ-1-протеазу, ВПГ-протеазу, ЦМВ-протеазу, химозин, ренин, пепсин, матриптазу, легумаин, плазмепсин, непентезин, металлоэкзопептидазы, металлоэндопептидазы, матриксные металлопротеиназы (ММР), ММР1, ММР2, ММР3, ММР8, ММР9, ММР13, ММР11, ММР14, активатор плазминогена урокиназного типа (uPA), энтерокиназу, простат-специфический антиген (PSA, hK3), интерлейкин-1β-конвертирующий фермент, тромбин, FAP (FAP-α), дипептидилпептидазу, меприны, гранзимы и дипептидилпептидазу IV (DPPIV/CD26). Протеазы, способные расщеплять аминокислотные последовательности, кодируемые химерными последовательностями нуклеиновых кислот, предложенными в данном документе, могут, например, быть выбраны из группы, состоящей из простат-специфического антигена (PSA), матриксной металлопротеиназы (ММР), дизинтегрина и металле протеиназы (ADAM), активатора плазминогена, катепсина, каспазы, поверхностной протеазы опухолевых клеток и эластазы. ММР может, например, представлять собой матриксную металле протеиназу 2 (ММР2) или матриксную металле протеиназу 9 (ММР9).
[120] Протеазы, применимые в описанных в данном документе способах, представлены в таблице 1, а типовые протеазы и их сайты расщепления представлены в таблице 1а:

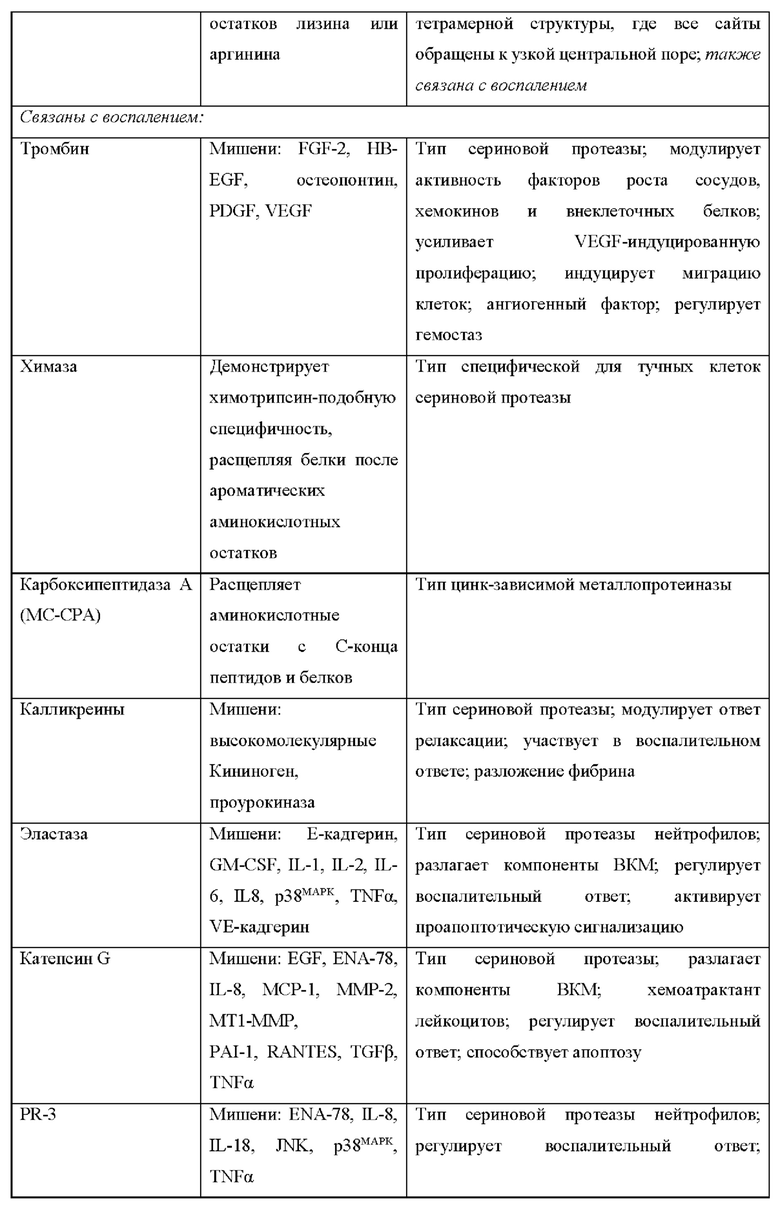
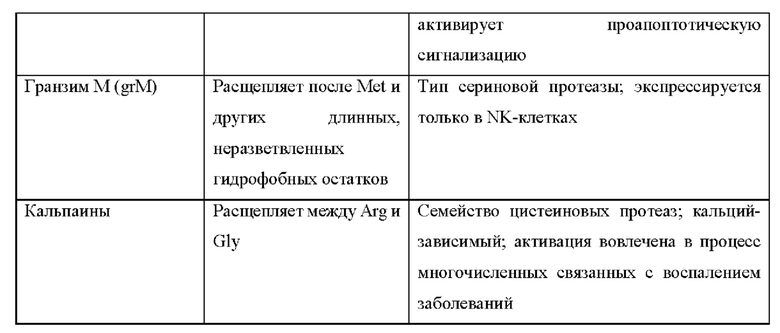
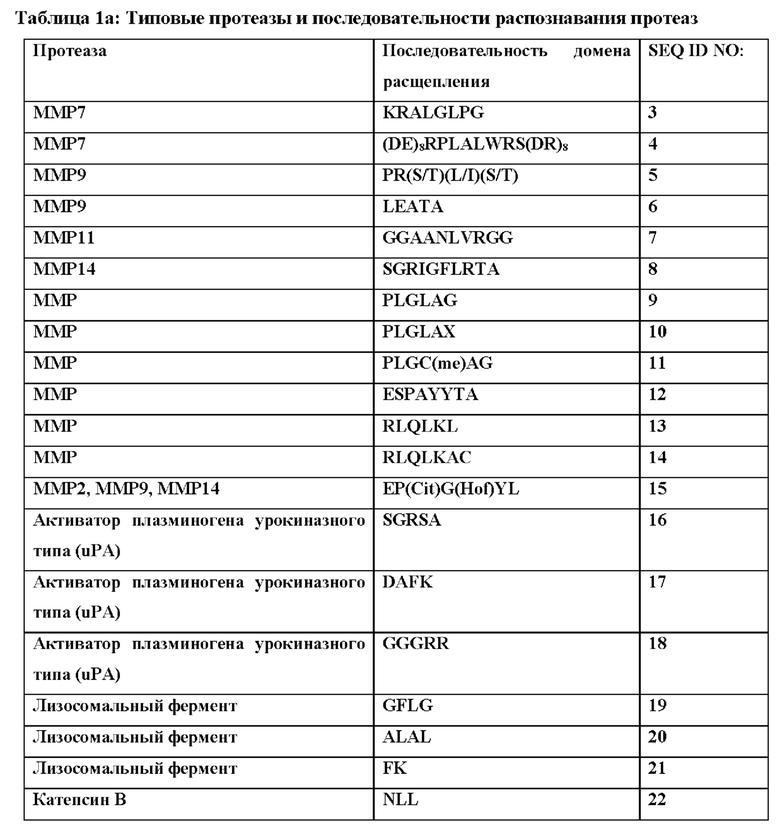

[121] В данном документе предложены фармацевтические композиции, содержащие полипептидные последовательности. Как и в случае всех пептидов, полипептидов и белков, включая их фрагменты, понятно, что могут присутствовать дополнительные модификации аминокислотной последовательности химерных полипептидов (варианты аминокислотной последовательности), которые не меняют природу или функцию пептидов, полипептидов или белков. Такие модификации включают консервативные аминокислотные замены и более подробно обсуждаются ниже.
[122] Предложенные в данном документе композиции имеют необходимую функуию. Указанные композиции состоят из по меньшей мере полипептида IL-2, блокирующего фрагмента, например, стерического блокирующего полипептида, и необязательного элемента для продления сывороточного времени полужизни и необязательного нацеливающего полипептида, причем каждый полипептид в композиции соединяют один или более линкеров. Первый полипептид, например, мутеин IL-2, предложен в качестве активного агента. Блокирующий фрагмент предложен с целью блокирования активности интерлейкина. Линкерный полипептид, например, расщепляемый протеазой полипептид, предложен с целью расщепления протеазой, которая специфически экспрессируется в предполагаемой мишени активного агента. Необязательно, блокирующий фрагмент блокирует активность первого полипептида путем связывания полипептида интерлейкина. В некоторых вариантах осуществления блокирующий фрагмент, например, стерический блокирующий пептид, связан с интерлейкином посредством расщепляемого протеазой линкера, который расщепляется в месте действия (например, воспалительными или опухолеспецифическими протеазами) с высвобождением полной активности цитокина в необходимом месте.
[123] Сайт расщепления протеазой может представлять собой сайт расщепления протеазой природного происхождения или искусственно сконструированный сайт расщепления протеазой. Искусственно сконструированный сайт расщепления протеазой может расщепляться более чем одной протеазой, специфической для необходимого окружения, в котором будет происходить расщепление, например, для опухоли. Сайт расщепления протеазой может расщепляться по меньшей мере одной протеазой, по меньшей мере двумя протеазами, по меньшей мере тремя протеазами или по меньшей мере четырьмя протеазами.
[124] В некоторых вариантах осуществления линкер содержит глицин-глицин, мотив распознавания сортазы или мотив распознавания сортазы и пептидную последовательность (Gly4Ser)n (SEQ ID NO: 126) или (Gly3Ser)n, (SEQ ID NO: 127), где n равно 1, 2, 3, 4 или 5. В одном варианте осуществления мотив распознавания сортазы содержит пептидную последовательность LPXTG (SEQ ID NO: 125), где X представляет собой любую аминокислоту. В одном варианте осуществления ковалентная связь находится между реактивным остатком лизина, присоединенным к С-концу полипептида цитокина, и реактивным остатком аспарагиновой кислоты, присоединенным к N-концу блокирующего или другого фрагмента. В одном варианте осуществления ковалентная связь находится между реактивным остатком аспарагиновой кислоты, присоединенным к N-концу полипептида цитокина, и реактивным остатком лизина, присоединенным к С-концу блокирующего или другого фрагмента.
Расщепление и индуцибельность
[125] Как описано в данном документе, активность полипептида цитокина в контексте слитого белка ослаблена, а расщепление протеазой в необходимом месте активности, таком как микроокружение опухоли, приводит к высвобождению из слитого белка формы цитокина, которая является намного более активной в качестве агониста рецептора цитокина, чем слитый белок. Например, активирующая (агонистическая) рецептор цитокина активность слитого полипептида может быть по меньшей мере в около 10 раз, по меньшей мере в около 50 раз, по меньшей мере в около 100 раз, по меньшей мере в около 250 раз, по меньшей мере в около 500 раз или по меньшей мере в около 1000 раз меньшей, чем активирующая рецептор цитокина активность полипептида цитокина в виде отдельной молекулы. Полипептид цитокина, который является частью слитого белка, существует в виде отдельной молекулы, когда он содержит аминокислоты, которые по существу идентичны полипептиду цитокина, и практически не содержит дополнительные аминокислоты и не связан (ковалентными или нековалентными связями) с другими молекулами. При необходимости полипептид цитокина в виде отдельной молекулы может содержать некоторые дополнительные аминокислотные последовательности, такие как метки или короткие последовательности, которые способствуют экспрессии и/или очистке.
[126] В других примерах активирующая (агонистическая) рецептор цитокина активность слитого полипептида является по меньшей мере в около 10 раз, по меньшей мере в около 50 раз, по меньшей мере в около 100 раз, по меньшей мере в около 250 раз, по меньшей мере в около 500 раз или в около 1000 раз меньшей, чем активирующая рецептор цитокина активность полипептида, который содержит полипептид цитокина, образованный вследствие расщепления расщепляемым протеазой линкером в слитом белке. Другими словами, активирующая (агонистическая) рецептор цитокина активность полипептида, который содержит полипептид цитокина, образованный вследствие расщепления расщепляемым протеазой линкером в слитом белке, является по меньшей мере в около 10 раз, по меньшей мере в около 50 раз, по меньшей мере в около 100 раз, по меньшей мере в около 250 раз, по меньшей мере в около 500 раз или по меньшей мере в около 1000 раз большей, чем активирующая рецептор цитокина активность слитого белка.
Полипептидные замены
[127] Описанные в данном документе полипептиды могут содержать компоненты (например, цитокин, блокирующий фрагмент), которые имеют такую же аминокислотную последовательность, что и соответствующий белок природного происхождения (например, IL-2, IL-15, ЧСА), или могут иметь аминокислотную последовательность, которая отличается от белка природного происхождения, при условии сохранения необходимой функции. Понятно, что один из способов определения любых модификаций и производных описанных белков и кодирующих их нуклеиновых кислот, известных или тех, которые могут возникнуть, состоит в определении вариантов последовательности в терминах идентичности с конкретными известными референсными последовательностями. В частности, описаны полипептиды и нуклеиновые кислоты, которые имеют по меньшей мере 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 процентов идентичности с предложенными в данном документе химерными полипептидами. Например, предложены полипептиды или нуклеиновые кислоты, которые имеют по меньшей мере 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 процентов идентичности с последовательностью любой из нуклеиновых кислот или любого из полипептидов, описанных в данном документе. Специалистам в данной области техники известно, как определять идентичность двух полипептидов или двух нуклеиновых кислот. Например, идентичность можно рассчитать после выравнивания двух последовательностей так, чтобы идентичность была на самом высоком уровне.
[128] Другой способ расчета идентичности может быть осуществлен по опубликованным в литературе алгоритмам. Оптимальное выравнивание последовательностей для сравнения можно проводить с помощью алгоритма локальной идентичности Смита и Уотермана (Smith and Waterman Adv. Appl. Math. 2:482 (1981)), с помощью алгоритма выравнивания Нидлмана и Вунша (Needleman and Wunsch, J. Mol. Biol. 48:443 (1970)), с помощью способа поиска сходства Пирсона и Липмана (Proc. Natl. Acad. Sci. USA 85:2444 (1988)), с помощью компьютеризованных версий этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в пакете программного обеспечения Wisconsin Genetics, Genetics Computer Group, 575 Science Dr., Madison, Wis.) или путем визуальной оценки.
[129] Те же типы идентичности можно получить для нуклеиновых кислот, например, с помощью алгоритмов, описанных в Zuker, Science 244:48-52 (1989); Jaeger et al., Proc. Natl. Acad. Sci. USA 86:7706-7710 (1989); Jaeger et al., Methods Enzymol. 183:281-306 (1989), которые включены посредством ссылки в отношении по меньшей мере материала, относящегося к выравниванию нуклеиновых кислот. Понятно, что обычно можно использовать любые из способов и что в определенных случаях результаты этих различных способов могут отличаться, но специалисту в данной области техники понятно, что в случае обнаружения идентичности по меньшей мере одним из этих способов будет считаться, что последовательности имеют указанную идентичности и описаны в данном документе.
[130] Белковые модификации включают модификации аминокислотной последовательности. Модификации в аминокислотной последовательности могут возникать естественным образом в виде аллельных вариаций (например, вследствие генетического полиморфизма), могут возникать вследствие влияния окружающей среды (например, за счет воздействия ультрафиолетового света) или могут быть созданы вследствие вмешательства человека (например, с помощью мутагенеза клонированных последовательностей ДНК), например, индуцированные точечные, делеционные, инсерционные и заместительные мутанты. Эти модификации могут приводить к изменениям в аминокислотной последовательности, обеспечивать молчащие мутации, модифицировать сайт рестрикции или обеспечивать другие специфические мутации. Модификации аминокислотной последовательности, как правило, относятся к одному или более из трех классов: заместительные, инсерционные или делеционные модификации. Вставки (инсерции) включают амино- и/или карбокси-концевые слияния, а также вставки внутри последовательности одного или нескольких аминокислотных остатков. Вставки обычно являются меньшими вставками, чем в случае амино- или карбокси-концевых слияний, например, порядка от одного до четырех остатков. Делеции характеризуются удалением одного или более аминокислотных остатков из белковой последовательности. Как правило, в любом сайте в белковой молекуле удаляют не более чем около 2-6 остатков. Аминокислотные замены, как правило, относятся к единичным остаткам, но могут быть внесены сразу в ряд разных локаций; вставки обычно имеют порядок от 1 до 10 аминокислотных остатков; а делеции имеют диапазон от 1 до 30 остатков. Делеции и вставки предпочтительно проводят в соседних парах, т.е. делецию 2 остатков или вставку 2 остатков. Замены, делеции, вставки или любые их комбинации можно комбинировать, чтобы получить конечную конструкцию. Мутации не должны вытеснять последовательность из рамки считывания и предпочтительно не создают комплементарные области, которые могут привести к образованию вторичной структуры мРНК. Заместительными модификациями являются те, в которых по меньшей мере один остаток был удален и на его место вставлен другой остаток. Такие замены в целом проводят в соответствии с нижеприведенной таблицей 2 и считаются консервативными заменами.
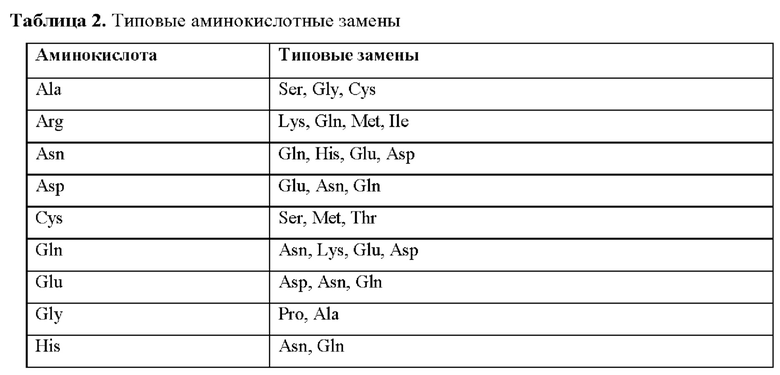

[131] Модификации, включая конкретные аминокислотные замены, осуществляют известными способами. Например, модификации можно осуществлять с помощью сайт-специфического мутагенеза нуклеотидов в ДНК, кодирующей полипептид, с получением, таким образом, ДНК, кодирующей модификацию, и экспрессии после этого ДНК в рекомбинантной клеточной культуре. Способы создания заместительных мутаций в заданных сайтах в ДНК, имеющих известную последовательность, хорошо известны, например, это мутагенез с праймерами М13 и ПЦР-мутагенез.
[132] Модификации можно выбирать, чтобы оптимизировать связывание. Например, можно использовать методы созревания аффинности для изменения связывания scFv путем внесения случайных мутаций в определяющие комплементарность области (CDR). Такие случайные мутации можно вносить с помощью ряда способов, включая облучение, химические мутагены или ПЦР с внесением ошибок. Множественные раунды мутации и отбора можно проводить, используя, например, фаговый дисплей.
[133] Данное изобретение также относится к нуклеиновым кислотам, которые кодируют описанные в данном документе химерные полипептиды, и к применению таких нуклеиновых кислот для получения химерных полипептидов в терапевтических целях. Например, данное изобретение включает молекулы ДНК и РНК (например, мРНК, самореплицирующаяся РНК), которые кодируют химерный полипептид, и к терапевтическому применению таких молекул ДНК и РНК.
Типовые композиции
[134] В типовых слитых белках по данному изобретению вышеописанные элементы скомбинированы в ряде вариаций. Описанные в данном разделе вариации подразумеваются как примеры и не считаются ограничивающими.
[135] В некоторых вариантах осуществления слитый белок содержит полипептид IL-2, блокирующий фрагмент и элемент для продления времени полужизни. В некоторых вариантах осуществления полипептид IL-2 расположен между элементом для продления времени полужизни и блокирующим фрагментом. В некоторых вариантах осуществления полипептид IL-2 расположен со стороны N-конца относительно блокирующего фрагмента и элемента для продления времени полужизни. В некоторых таких вариантах осуществления полипептид IL-2 расположен вблизи блокирующего фрагмента; в некоторых таких вариантах осуществления цитокин расположен вблизи элемента для продления времени полужизни. По меньшей мере один расщепляемый протеазой линкер должен быть включен во всех вариантах осуществления, чтобы полипептид IL-2 мог становиться активным после расщепления. В некоторых вариантах осуществления полипептид IL-2 расположен со стороны С-конца относительно блокирующего фрагмента и элемента для продления времени полужизни. Дополнительные элементы могут быть присоединены один к другому посредством расщепляемого линкера, нерасщепляемого линкера или путем прямого слияния. В некоторых случаях целесообразно включать два одинаковых цитокина, чтобы облегчить димеризацию.
[136] В некоторых вариантах осуществления используемые блокирующие домены способны продлевать время полужизни, а полипептид IL-2 расположен между двумя такими блокирующими доменами. В некоторых вариантах осуществления полипептид IL-2 расположен между двумя блокирующими доменами, один из которых способен продлевать время полужизни.
[137] В некоторых вариантах осуществления в одну конструкцию включены два цитокина, по меньшей мере один из которых представляет собой IL-2. В некоторых вариантах осуществления каждый из цитокинов соединен с двумя блокирующими доменами (всего три в одной молекуле) с блокирующим доменом между двумя цитокинами. В некоторых вариантах осуществления могут быть включены один или более дополнительных доменов для продления времени полужизни, чтобы оптимизировать фармакокинетические свойства.
[138] В некоторых вариантах осуществления в одну конструкцию включены три цитокина. В некоторых вариантах осуществления третий цитокин может иметь функцию блокирования двух других вместо блокирующего домена между двумя цитокинами.
[139] Предпочтительными элементами для продления времени полужизни для применения в слитых белках являются человеческий сывороточный альбумин (ЧСА), антитело или фрагмент антитела (например, scFV, dAb), которые связывают сывороточный альбумин, человеческий или гуманизированный IgG или фрагмент любого из вышеприведенного. В некоторых предпочтительных вариантах осуществления блокирующим фрагментом является человеческий сывороточный альбумин (ЧСА) или антитело или фрагмент антитела, которые связывают сывороточный альбумин, антитело, которое связывает цитокин и предотвращает активацию связывания или активацию рецептора цитокина, другой цитокин или фрагмент любого из вышеприведенного. В предпочтительных вариантах осуществления, включающий применение дополнительного нацеливающего домена, нацеливающий домен представляет собой антитело, которое связывается с белком клеточной поверхности, который обогащен на поверхности раковых клеток, таким как ЕрСАМ, FOLR1 и фибронектин.
Способы лечения и фармацевтические композиции
[140] Дополнительно предложены способы лечения субъекта, который имеет или подвержен риску развития заболевания или нарушения, такого как пролиферативное заболевание, опухолевое заболевание, воспалительное заболевание, иммунологическое нарушение, аутоиммунное заболевание, инфекционное заболевание, вирусное заболевание, аллергическая реакция, паразитарная реакция или болезнь «трансплантат против хозяина». Способы введения нуждающемуся в этом субъекту эффективного количества описанного в данном документе слитого белка, который, как правило, вводят в виде фармацевтической композиции. В некоторых вариантах осуществления способ дополнительно включает отбор субъекта, который имеет или подвержен риску развития такого заболевания или нарушения. Фармацевтическая композиция предпочтительно содержит заблокированный цитокин, его фрагмент или мутеин, который активируется в месте воспаления или в опухоли. В одном варианте осуществления химерный полипептид содержит полипептид цитокина, его фрагмент или мутеин и элемент для продления сывороточного времени полужизни. В другом варианте осуществления химерный полипептид содержит полипептид цитокина, его фрагмент или мутеин и блокирующий фрагмент, например, стерический блокирующий полипептид, причем стерический блокирующий полипептид способен стерически блокировать активность полипептида цитокина, его фрагмента или мутеина. В другом варианте осуществления химерный полипептид содержит полипептид цитокина, его фрагмент или мутеин, блокирующий фрагмент и элемент для продления сывороточного времени полужизни.
[141] Воспаление является частью комплексного биологического ответа тканей организма на вредоносные стимулы, такие как патогены, поврежденные клетки или раздражители, я является защитным ответом, в котором участвуют иммунные клетки, кровяные сосуды и молекулярные медиаторы. Функцией воспаления является устранение изначальной причины повреждения клеток, выведение некротических клеток и тканей, поврежденных вследствие исходного воздействия и воспалительного процесса, и инициация восстановления тканей. Воспаление может возникать из-за инфекции, как симптом заболевания, например, рака, атеросклероза, аллергий, миопатий, ВИЧ, ожирения или аутоиммунного заболевания. Аутоиммунное заболевание представляет собой хроническое патологическое состояние, возникающее из-за аномального иммунного ответа на собственные антигены. Аутоиммунные заболевания, которые можно лечить описанными в данном документе полипептидами, включают, но не ограничиваются этим, волчанку, глютеновую болезнь, сахарный диабет 1 типа, болезнь Грейвса, воспалительное заболевание кишечника, множественный склероз, псориаз, ревматоидный артрит и системную красную волчанку.
[142] Фармацевтическая композиция может содержать одну или более расщепляемых протеазами последовательностей. Линкерная последовательность служит для обеспечения гибкости между полипептидами так, чтобы каждый полипептид был способен ингибировать активность первого полипептида. Линкерная последовательность может быть расположена между любыми или всеми из полипептида цитокина, его фрагмента или мутеина, блокирующего фрагмента и элемента для продления сывороточного времени полужизни. Необязательно, композиция содержит две, три, четыре или пять линкерных последовательностей. Линкерная последовательность, две, три или четыре линкерные последовательности могут быть одинаковыми или разными линкерными последовательностями. В одном варианте осуществления линкерная последовательность содержит GGGGS (SEQ ID NO: 132), GSGSGS (SEQ ID NO: 133) или G(SGGG)2SGGT (SEQ ID NO: 134). В другом варианте осуществления линкер содержит расщепляемую протеазой последовательность, выбранную из группы, состоящей из HSSKLQ (SEQ ID NO: 25), GPLGVRG (SEQ ID NO: 128), IPVSLRSG (SEQ ID NO: 129), VPLSLYSG (SEQ ID NO: 130) и SGESPAYYTA (SEQ ID NO: 131).
[143] В некоторых вариантах осуществления линкер расщепляется протеазой, выбранной из группы, состоящей из калликреина, тромбина, химазы, карбоксипептидазы А, катепсина G, эластазы, PR-3, гранзима М, кальпаина, матриксной металлопротеиназы (ММР), активатора плазминогена, катепсина, каспазы, триптазы или поверхностной протеазы опухолевых клеток.
[144] Подходящие линкеры могут иметь любую длину, такую как от 1 аминокислоты (например, Gly) до 20 аминокислот, от 2 аминокислот до 15 аминокислот, от 3 аминокислот до 12 аминокислот, в том числе от 4 аминокислот до 10 аминокислот, аминокислот до 9 аминокислот, от 6 аминокислот до 8 аминокислот или от 7 аминокислот до 8 аминокислот, и могут составлять 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59 или 60 аминокислот.
[145] Дополнительно предложены способы лечение субъекта, которые имеет или подвержен риску развития рака. Указанные способы включают введение нуждающемуся в этом субъекту эффективного количества описанного в данном документе химерного полипептида (слитого белка), который, как правило, вводят в виде фармацевтической композиции. В некоторых вариантах осуществления способ дополнительно включает отбор субъекта, который имеет или подвержен риску развития рака. Фармацевтическая композиция предпочтительно содержит заблокированный цитокин, его фрагмент или мутеин, который активируется в месте опухоли. Предпочтительно опухоль является солидной опухолью. Рак может представлять собой, но не ограничивается этим, рак толстой кишки, рак легкого, меланому, саркому, почечно-клеточную карциному и рак молочной железы.
[146] Указанный способ может дополнительно включать введение одного или более дополнительных агентов для лечения рака, таких как химиотерапевтические агенты (например, адриамицин, церубидин, блеомицин, алкеран, велбан, онковин, фторурацил, тиотепа, метотрексат, бисантрен, ноантрон, тиогуанин, цитарабин, прокарбазин), иммуноонкологические агенты (например, анти-PD-L1, анти-СТ1А4, анти-PD-1, анти-CD47, анти-GD2), клеточная терапия (например, CAR-T, Т-клеточная терапия), онколитические вирусы и т.п.
[147] В данном документе предложены фармацевтические составы или композиции, содержащие химерные полипептиды и фармацевтически приемлемый носитель. Предложенные в данном документе композиции подходят для введения in vitro или in vivo. Под фармацевтически приемлемым носителем подразумевается материал, который не является биологически или иным образом нежелательным, т.е. материал, вводимый субъекту, не вызывает нежелательных биологических эффектов или не взаимодействует вредоносным образом с другими компонентами фармацевтического состава или композиции, в которой он находится. Носитель выбирают так, чтобы минимизировать деградацию активного ингредиента и минимизировать нежелательные побочные эффекты у субъекта.
[148] Подходящие носители и их составы описаны в Remington: The Science and Practice of Pharmacy, 21st Edition, David B. Troy, ed., Lippicott Williams & Wilkins (2005). Как правило, в составе используют соответствующее количество фармацевтически приемлемой соли, чтобы сделать состав изотоническим, хотя состав может быть гипертоническим или гипотоническим при необходимости. Примеры фармацевтически приемлемых носителей включают, но не ограничиваются этим, стерильную воду, солевой раствор, забуференные растворы, такие как раствор Рингера и раствор декстрозы. рН раствора в общем случае составляет от около 5 до около 8 или от около 7 до 7,5. Другие носители включают препараты для замедленного высвобождения, такие как полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие иммуногенные полипептиды. Матрицы имеют вид формованных изделий, например, пленок, липосом или микрочастиц. Определенные носители могут быть более предпочтительными в зависимости от, например, пути введения и концентрации вводимой композиции. Носители подходят для введения химерных полипептидов иди последовательностей нуклеиновых кислот, кодирующих химерные полипептиды, людям или другим субъектам.
[149] Фармацевтические составы или композиции вводят рядом способов в зависимости от того, необходимо местное или системное лечение, и от подлежащего лечению участка. Композиции вводят любым из нескольких путей введения, включая местный, пероральный, парентеральный, внутривенный, внутрисуставной, внутрибрюшинный, внутримышечный, подкожный, внутриполостной, трансдермальный, внутрипеченочный, внутричерепной, путем распыления/ингаляции или с помощью бронхоскопии. В некоторых вариантах осуществления композиции вводят местно (не систематически), в том числе интратуморально, внутрисуставно, интратекально и т.д.
[150] Препараты для парентерального введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и инъекционные органические сложные эфиры, такие как этилолеат. Водные носители включают воду, спиртово-водные растворы, эмульсии или суспензии, включая солевой раствор и забуференную среду. Парентеральные носители включают раствор хлорида натрия, декстрозу Рингера, декстрозу и хлорид натрия, лактат Рингера или жирные масла. Внутривенные носители включают пополнители жидкости и питательных веществ, пополнители электролитов (например, на основе декстрозы Рингера) и т.п. Необязательно присутствуют консерванты и другие добавки, такие как, например, противомикробные препараты, антиоксиданты, хелатирующие агенты и инертные газы и т.п.
[151] Составы для местного введения включают мази, лосьоны, кремы, гели, капли, суппозитории, спреи, жидкости и порошки. Традиционные фармацевтические носители, водные, порошковые или масляные основы, загустители и т.п. являются необязательными или необходимыми.
[152] Композиции для перорального введения включают порошки или гранулы, суспензии или растворы в воде или неводных средах, капсулы, саше или таблетки. Необязательно, необходимы загустители, ароматизаторы, разбавители, эмульгаторы, диспергирующие агенты или связующие вещества.
[153] Необязательно, химерные полипептиды или последовательности нуклеиновых кислот, кодирующие химерные полипептиды, вводят с помощью вектора. Существует ряд композиций и способов, которые можно использовать для доставки молекул нуклеиновых кислот и/или полипептидов в клетки, как in vitro, так и in vivo, например, экспрессионные векторы. Эти способы и композиции можно в целом поделить на два класса: системы на основе вирусной доставки и системы на основе невирусной доставки. Такие способы хорошо известны в данной области техники и легко адаптируются для применения с описанными в данном документе способами и композициями. Такие композиции и способы можно использовать для трансфекции или трансдукции клеток in vitro или in vivo, например, для получения линий клеток, которые экспрессируют и, предпочтительно, секретируют кодируемый химерный полипептид, или для терапевтической доставки нуклеиновых кислот субъекту. Компоненты описанных в данном документе нуклеиновых кислот, как правило, функционально связаны в рамке считывания, чтобы кодировать слитый белок.
[154] В контексте данного документа плазмиды или вирусные векторы представляют собой агенты, которые переносят описанные нуклеиновые кислоты в клетку, не разрушая ее, и содержат промотор, обеспечивающий экспрессию молекулы нуклеиновой кислоты и/или полипептида в клетках, в которые они были доставлены. Вирусными векторам являются, например, аденовирус, аденоассоциированный вирус, вирус герпеса, вирус осповакцины, полиовирус, вирус Синдбис и другие РНК-вирусы, включая вирусы с остовом ВИЧ. Также предпочтительными являются любые семейства вирусов, которые имеют свойства тех вирусов, которые делают их подходящими для применения в качестве векторов. Ретровирусные векторы в целом описаны в Coffin et al., Retroviruses, Cold Spring Harbor Laboratory Press (1997), которая включена в данный документ посредством ссылки в отношении векторов и способов их создания. Было описано конструирование дефективных по репликации аденовирусов (Berkner et al., J. Virol. 61:1213-20 (1987); Massie et al., Mol. Cell. Biol. 6:2872-83 (1986); Haj-Ahmad et al., J. Virol. 57:267-74 (1986); Davidson et al., J. Virol. 61:1226-39 (1987); Zhang et al., BioTechniques 15:868-72 (1993)). Преимуществом применения этих вирусов в качестве векторов является то, что они ограничены по степени, в которой они могут распространяться по другим типам клеток, то есть, они могут реплицироваться в исходной инфицированной клетке, но не способны образовывать новые инфекционные вирусные частицы. Было показано, что рекомбинантные вирусы обеспечивают высокую эффективность после прямой in vivo доставки в эпителий дыхательных путей, гепатоциты, сосудистый эндотелий, паренхиму ЦНС и ряд других тканевых сайтов. Другие применимые системы включают, например, векторы на основе реплицирующегося и ограниченного по организму-хозяину нереплицирующегося вируса осповакцины.
[155] Предложенные полипептиды и/или молекулы нуклеиновых кислот можно доставлять посредством вирусоподобных частиц. Вирусоподобные частицы (ВПЧ) состоят из вирусных белков, полученных из структурных белков вируса. Способы создания и применения вирусоподобных частиц описаны, например, в Garcea and Gissmann, Current Opinion in Biotechnology 15:513-7 (2004).
[156] Предложенные полипептиды можно доставлять с помощью субвирусных плотных телец (ПТ). ПТ переносят белки в целевые клетки посредством мембранного слияния. Способы создания и применения ПТ описаны, например, в Pepperl-Klindworth et al., Gene Therapy 10:278-84 (2003).
[157] Предложенные полипептиды можно доставлять посредством тегументных агрегатов. Способы создания и применения тегументных агрегатов описаны в международной публикации № WO 2006/110728.
[158] Способы на основе невирусной доставки могут включать применение экспрессионных векторов, содержащих молекулы нуклеиновых кислот и последовательности нуклеиновых кислот, кодирующие полипептиды, причем нуклеиновые кислоты функционально связаны с экспрессионной регуляторной последовательностью. Подходящие векторные остовы включают, например, те, которые обычно используют в данной области техники, такие как плазмиды, искусственные хромосомы, ВАС, YAC или РАС. Ряд векторов и экспрессионных систем коммерчески доступны от таких корпораций, kbks Novagen (Madison, Wis.), Clonetech (Pal Alto, Calif.), Stratagene (La Jolla, Calif.) и Invitro gen/Life Technologies (Carlsbad, Calif), векторы, как правило, содержат одну или более регуляторных областей. Регуляторные области включают, без ограничения, промоторные последовательности, энхансерные последовательности, элементы ответа, белок-распознающие сайты, индуцибельные элементы, белок-связывающие последовательности, 5' и 3' нетранслируемые области (НТО), сайты инициации транскрипции, последовательности терминации, последовательности полиаденилирования и интроны. Такие векторы также можно использовать для создания химерных полипептидов путем экспрессии в подходящей клетке-хозяине, такой как клетки СНО.
[159] Предпочтительные промоторы, регулирующие транскрипцию из векторов в клетках-хозяевах млекопитающих, можно получать из различных источников, например, геномов вирусов, таких как вирус полиомы, вирус обезьян 40 (SV40), аденовирус, ретровирус, вирус гепатита В и, наиболее предпочтительно, цитомегаловирус (ЦМВ), или из гетерологичных промоторов млекопитающих, например, промотора β-актина или промотора EF1α, или из гибридных химерных промоторов (например, промотора ЦМВ, слитого с промотором р-актина). Конечно, в контексте данного документа также применимы промоторы из клетки-хозяина или родственных видов.
[160] Энхансер в общем случае относится к последовательности ДНК; которая не функционирует на каком-либо фиксированном расстоянии от сайта инициации транскрипции и может находиться как 5', так и 3' относительно транскрипционной единицы. Кроме того, энхансеры могут находиться в интроне, а также в самой кодирующей последовательности. Обычно их длина составляет от 10 до 300 пар оснований (п.о.), и они функционируют в цис-форме. Функцией энхансера обычно является повышение транскрипции из расположенных рядом промоторов. Энхансеры также могут содержать элементы ответа, которые опосредуют регуляцию транскрипции. Хотя известны последовательности многих энхансеров из генов млекопитающих (глобина, эластазы, альбумина, фетопротеина и инсулина), как правило, для общей экспрессии используют энхансер из вируса эукариотической клетки. Предпочтительными примерами являются энхансер SV40 на поздней стороне точки начала репликации, энхансер раннего промотора цитомегаловируса, энхансер вируса полиомы на поздней стороне точки начала репликации и энхансеры аденовирусов.
[161] Промотор и/или энхансер может быть индуцибельным (например, регулироваться химически или физически). Химически регулируемый промотор и/или энхансер может, например, регулироваться наличием спирта, тетрациклина, стероида или металла. Физически регулируемый промотор и/или энхансер может, например, регулироваться факторами окружающей среды, такими как температура и освещение. Необязательно, область промотора и/или энхансера может действовать как конститутивный промотор и/или энхансер, чтобы максимизировать экспрессию области транскрипционной единицы, предназначенной для транскрипции. В определенных векторах область промотора и/или энхансера может быть активной образом, специфическим в отношении типа клеток. Необязательно, в определенных векторах область промотора и/или энхансера может быть активной в эукариотических клетках, независимо от типа клеток. Предпочтительными промоторами этого типа являются промотор ЦМВ, промотор SV40, промотор β-актина, промотор EF1α и ретровирусный длинный концевой повтор (ДКП).
[162] Векторы также могут содержать, например, точки начала репликации и/или маркеры. Маркерный ген может придавать клетке селективный фенотип, например, устойчивость к антибиотику. Маркерный продукт использую для определения, был ли вектор доставлен в клетку и экспрессируется ли он после доставки. Примерами селективных маркером для клеток млекопитающих являются дигидрофолатредуктаза (DHFR), тимидинкиназа, неомицин, аналог неомицина G418, гигромицин, пуромицин и бластицидин. В случае успешного переноса таких селективных маркеров в клетку-хозяина млекопитающего, трансформированная клетка-хозяин млекопитающего способна выжить при помещении в условия селективного давления. Примеры других маркеров включают, например, ген lacZ E.coli, зеленый флуоресцентный белок (ЗФБ) и люциферазу. Кроме того, экспрессионный вектор может содержать последовательность метки, предназначенную для облегчения обнаружения (например, очистки или локализации) экспрессируемого полипептида. Последовательности меток, такие как последовательности ЗФБ, глутатион S-трансферазы (GST), полигистидина, с-myc, гемагглютинина или метки FLAG™ (Kodak; New Haven, Conn.), как правило, экспрессируются в виде слияния с кодируемым полипептидом. Такие метки могут быть вставлены в любом месте в полипептиде, в том числе в карбокси- или амино-конце.
[163] В контексте данного документа термины пептид, полипептид или белок используются в широком смысле для обозначения двух или более аминокислот, связанных пептидной связью. Белок, пептид и полипептид также взаимозаменяемо используются в данном документе для обозначения аминокислотных последовательностей. Следует понимать, что термин полипептид в контексте данного документа не предполагает конкретные размер или число аминокислот, составляющих молекулу, и что пептид по изобретению может содержать до нескольких аминокислотных остатков или более. В контексте данного документа субъект может представлять собой позвоночное, конкретнее млекопитающее (например, человека, лошадь, кошку, собаку, корову, свинью, овцу, козу, мышь, кролика, крысу и морскую свинку), птиц, рептилий, амфибий, рыб и любое другое животное. Этот термин не предполагает конкретный возраст или пол. Такими образом, подразумевается, что охвачены взрослые и новорожденные субъекты мужского и женского пола. В контексте данного документа термины пациент или субъект могут использоваться взаимозаменяемо и могут относиться к субъекту с заболеванием или нарушением (например, раком). Термин пациент или субъект включает людей и ветеринарных субъектов.
[164] Субъект, подверженный риску развития заболевания или нарушения, может быть генетически предрасположен к заболеванию или нарушению, например, иметь семейный анамнез или иметь мутацию в гене, которая вызывает заболевание или нарушение, или демонстрировать ранние признаки или симптомы заболевания или нарушения. Субъект, который на данный момент имеет заболевание или нарушение, имеет один или более одного симптомы заболевания или нарушения, и у него может быть диагностировано заболевание или нарушение.
[165] Описанные в данном документе способы и агенты применимы в качестве как профилактического, так и терапевтического лечения. В случае профилактического применения терапевтически эффективное количество химерных полипептидов или последовательностей химерных нуклеиновых кислот, кодирующих химерные полипептиды, описанных в данном документе, вводят субъекту до начала (например, до появления очевидных симптомов рака или воспаления) или во время раннего начала (например, после появления начальных симптомов и симптомов рака или воспаления). Профилактическое введение может продолжаться в течение времени от нескольких суток до нескольких лет до проявления симптомов рака или воспаления. Профилактическое лечение можно применять, например, при превентивном лечении субъектов, у которых была диагностирована генетическая предрасположенность к раку. Терапевтическое лечение включает введение субъекту терапевтически эффективного количества химерных полипептидов или последовательностей химерных нуклеиновых кислот, кодирующих химерные полипептиды, описанных в данном документе, после диагностирования или развития рака или воспаления (например, аутоиммунного заболевания). Профилактическое применение также можно использовать, когда пациент проходит лечение, например, химиотерапию, при котором ожидаемо воспаление.
[166] В соответствии с описанными в данном документе способами субъекту вводят эффективное количество агента (например, химерного полипептида). Термины эффективное количество и эффективная дозировка используются взаимозаменяемо. Термин эффективное количество определяется как любое количество, необходимое для получения желаемого физиологического ответа. Эффективные количества и режимы введения агента можно определять эмпирически, и такие определения находятся в компетенции специалиста в данной области техники. Диапазоны дозировок для введения являются достаточно большими, чтобы привести к необходимому эффекту, при котором один или более симптомов заболевания или нарушения подвергаются изменению (например, снижаются или замедляются). Дозировка не должна быть настолько большой, чтобы вызвать существенные нежелательные побочные эффекты, такие как нежелательные перекрестные реакции, анафилактические реакции и т.п. В общем случае дозировка будет варьироваться в зависимости от возраста, патологического состояния, пола, типа заболевания, степени заболевания или нарушения, пути введения или того, включены ли в схему другие лекарственные препараты, и может быть определена специалистом в данной области техники. Дозировка может корректироваться индивидуальным лечащим врачом в случае любых противопоказаний. Дозировки могут варьироваться, и их можно вводить за одно или более введений дозы ежесуточно в течение одних или нескольких суток. Руководство в отношении соответствующих дозировок для заданных классов фармацевтических продуктов можно найти в литературе.
[167] В контексте данного документа термины лечение или лечить относятся к способу снижения действия заболевания или патологического состояния или симптома заболевания или патологического состояния. Таким образом, в описанном способе лечение может относиться к 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% снижению тяжести установленного заболевания или патологического состояния или симптома заболевания или патологического состояния. Например, способ лечения заболевания считается лечением, если наблюдается 10% снижение одного или более симптомов заболевания у субъекта по сравнению с контролем. Таким образом, снижение может составлять 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или любой процент снижения между 10% и 100% по сравнению с нативными или контрольными уровнями. Следует понимать, что лечение не обязательно относится к излечению или полному устранению заболевания, патологического состояния или симптомов заболевания или патологического состояния.
[168] В контексте данного документа термины предотвращать и предотвращение заболевания или нарушения относятся к действию, например, введению химерного полипептида или последовательности нуклеиновой кислоты, кодирующей химерный полипептид, которое происходит до или приблизительно в то же время, когда субъект начинает демонстрировать один или более симптомов заболевания или нарушения, которое ингибирует или замедляет начало или усугубление одного или более симптомов заболевания или нарушения. В контексте данного документа употребление терминов снижение, уменьшение или ингибирование включает изменение, составляющее 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более по сравнению с контрольным уровнем. Такие термины могут включать, но не обязательно включают полное устранение.
[169] Были разработаны варианты IL-2, которые являются избирательными в отношении IL2Rαβγ по сравнению с IL2Rβγ (Shanafelt, А.В., et al., 2000, Nat Biotechnol. 18:1197-202; Cassell, D. J., et. al., 2002, Curr Pharm Des., 8:2171-83). Эти варианты имеют аминокислотных замены, которые снижают их аффинность в отношении IL2Rβ. Поскольку IL-2 имеет необнаруживаемую аффинность в отношении IL2Rγ, эти варианты, следовательно, имеют сниженную аффинность в отношении комплекса рецептора IL2Rβγ и сниженную способность активировать IL2Rβγ-экспрессирующие клетки, но сохраняют способность связывать IL2Rα и способность связывать и активировать комплекс рецептора IL2Rαβγ.
[170] Один из этих вариантов, IL2/N88R (Bay 50-4798), клинически исследовали как низкотоксичную версию IL-2 в качестве стимулятора иммунной системы на основании гипотезы, что IL2Rβγ-экспрессирующие NK-клетки вносят основной вклад в токсичность. Было показано, что Bay 50-4798 избирательно стимулирует пролиферацию активированных Т-клеток относительно NK-клеток, и был оценен в клинических исследованиях фазы 1/11 на раковых пациентах (Margolin, K., et. а1., 2007, din Cancer Res., 13:3312-9) и пациентах с ВИЧ (Davey, R. Т., et. а1., 2008, J Interferon Cytokine Res., 28:89-100). Эти клинические исследования показали, что Bay 50-4798 был значительно безопаснее и более переносим, чем альдеслейкин, и также показали, что он повышал уровни CD4+CD25+ Т-клеток, клеточной популяции, обогащенной в клетках Treg. После этих испытаний исследования в данной области позволили в более полной мере установить идентичность клеток Treg и продемонстрировали, что клетки Treg избирательно экспрессируют IL2Rapy (обзор в Maiek, Т.R., et al., 2010, Immunity, 33:153-65).
[171] Кроме того, можно создавать мутантов, которые избирательно меняют аффинность в отношении цепи CD25 по сравнению с нативным IL-2.
[172] IL-2 можно сконструировать так, чтобы получить мутантов, которые связывают комплекс IL-2R в целом или субъединицу IL-2Rα в частности с аффинностью, которая отличается от соответствующего IL-2 дикого типа или доступного в настоящее время мутанта (называемого C125S, поскольку цистеин в позиции 125 замещен остатком серина).
[173] Соответственно данное изобретение относится к мутантным полипептидам интерлейкина-2 (IL-2*), которые содержат аминокислотную последовательность, являющуюся по меньшей мере на 80% идентичной IL-2 дикого типа (например, на 85, 87, 90, 95, 97, 98 или 99% идентичной) и которая связывается, по сравнению с IL-2 ДТ с большей аффинностью с тримерным рецептором IL-2 по сравнению с димерным рецептором IL-2. Как правило, мутеины также связывают α-субъединицу рецептора IL-2 (IL-2Rα) с аффинностью, которая превышает аффинность, с которой IL-2 дикого типа связывает IL-2Rα. Аминокислотная последовательность в пределах мутантных полипептидов IL-2 может варьироваться от SEQ ID NO: 1 (номер доступа UniProtKB Р60568) за счет содержания (или только содержания) одной или более аминокислотных замен, которые могут считаться консервативными или неконсервативными заменами. Также могут быть включены аминокислоты неприродного происхождения. В альтернативном варианте аминокислотная последовательность может варьироваться от SEQ ID NO: 1 (которая может считаться «референсной последовательностью) за счет содержания и добавления и/или удаления одного или более аминокислотных остатков. В частности, аминокислотная последовательность может отличаться от SEQ ID NO: 1 за счет мутации в по меньшей мере одной из следующих позиций SEQ ID NO: 1: 1, 4, 8, 9, 10, 11, 13, 15, 26, 29, 30, 31, 35, 37, 46, 48, 49, 54, 61, 64, 67, 68, 69, 71, 73, 74, 75, 76, 79, 88, 89, 90, 92, 99, 101, 103, 114, 125, 128 или 133 (или их комбинаций). Как указано, по меньшей мере одна из этих позиций может быть изменена, как могут и две, три, четыре, пять, шесть, семь, восемь, девять, десять или 11 или более (вплоть до всех) позиций. Например, аминокислотная последовательность может отличаться от SEQ ID NO: 1 в позициях 69 и 74 и дополнительно одной или более из позиций 30, 35 и 128. Аминокислотная последовательность также может отличаться от SEQ ID NO: 2 (описанной в US 7569215, включенном в данный документ посредством ссылки) в одной из следующих групп позиций: (а) позиции 64, 69 и 74; (b) позиции 69, 74 и 101; (с) позиции 69, 74 и 128; (d) позиции 30, 69, 74 и 103; (е) позиции 49, 69, 73 и 76; (f) позиции 69, 74, 101 и 133; (g) позиции 30, 69, 74 и 128; (h) позиции 69, 74, 88 и 99; (i) позиции 30, 69, 74 и 128; (j) позиции 9, 11, 35, 69 и 74; (k) позиции 1, 46, 49, 61, 69 и 79; (l) позиции 48, 68, 71, 90, 103 и 114; (m) позиции 4, 10, 11, 69, 74, 88 и 133; (n) позиции 15, 30 31, 35, 48, 69, 74 и 92; (o) позиции 30, 68, 69, 71, 74, 75, 76 и 90; (р) позиции 30, 31, 37, 69, 73, 74, 79 и 128; (q) позиции 26, 29, 30, 54, 67, 69, 74 и 92; (r) позиции 8, 13, 26, 30, 35, 37, 69, 74 и 92; и (s) позиции 29, 31, 35, 37, 48, 69, 71, 74, 88 и 89. Помимо мутаций в этих позициях аминокислотная последовательность мутантного полипептида IL-2 в остальном может быть идентичной SEQ ID NO: 1. В отношении конкретных замен аминокислотная последовательность может отличаться от SEQ ID NO: 1 за счет наличия одной или более из следующих мутаций: А1Т, S4P, K8R, K9T, Т10А, Q11R, Q13R, E15K, N26D, N29S, N30S, N30D, N30T, Y31H, Y31C, K35R, Т37А, T37R, M46L, K48E, K49R, K49E, K54R, E61D, K64R, E67G, E68D, V69A, N71T, N71A, N71R, A73V, Q74P, S75P, K76E, K76R, H79R, N88D, I89V, N90H, I92T, S99P, Т101А, F103S, I114V, I128T, I128A, Т133А или T133N. Наша номенклатура соответствует принятой в научной литературе, в которой за однобуквенным кодом аминокислоты в последовательности дикого типа или референсной последовательности следует ее позиция в последовательности, а затем - однобуквенный код аминокислоты, которой ее замещают. Таким образом, А1Т обозначает замену остатка аланина в позиции 1 треонином. Другие мутантные полипептиды, входящие в объем данного изобретения, включают содержащие мутант SEQ ID NO: 2, имеющий замены в V69 (например. А) и Q74 (например, Р). Например, аминокислотная последовательность может содержать одну из следующих групп мутаций по сравнению с SEQ ID NO: 2: (а) K64R, V69A и Q74P; (b) V69A, Q74P и Т101А; (с) V69A, Q74P и I128T; (d) N30D, V69A, Q74P и F103S; (е) K49E, V69A, A73V и K76E; (f) V69A, Q74P, Т101А и T133N; (g) N30S, V69A, Q74P и I128A; (h) V69A, Q74P, N88D и S99P; (i) N30S, V69A, Q74P и I128T; (j) K9T, Q11R, K35R, V69A и Q74P; (k) А1Т, M46L, K49R, E61D, V69A и H79R; (l) K48E, E68D, N71T, N90H, F103S и I114V; (m) S4P, Т10А, Q11R, V69A, Q74P, N88D и Т133А; (n) E15K, N30S Y31H, K35R, K48E, V69A, Q74P и I92T; (о) N30S, E68D, V69A, N71A, Q74P, S75P, K76R и N90H; (р) N30S, Y31C, Т37А, V69A, A73V, Q74P, H79R и I128T; (q) N26D, N29S, N30S, K54R, E67G, V69A, Q74P и I92T; (r) K8R, Q13R, N26D, N30T, K35R, T37R, V69A, Q74P и I92T; и (s) N29S, Y31H, K35R, Т37А, K48E, V69A, N71R, Q74P, N88D и I89V. SEQ ID NO: 2 описана в US 7569215, который включен в данный документ посредством ссылки в качестве типовой последовательности полипептида IL-2, которую можно использовать в данном изобретении.
[174] Как указано выше, любые описанные в данном документе мутантные полипептиды IL-2 могут содержать описанные последовательности; также они могут быть ограничены последовательностями, описываемыми или иным образом идентичными SEQ ID NO: 1. Кроме того, любой из описанный в данном документе мутантных полипептидов IL-2, необязательно, может содержать замену остатка цистеина в позиции 125 другим остатком (например, серина) и/или может, необязательно, содержать делецию остатка аланина в позиции 1 SEQ ID NO: 1.
[175] Описанные в данном документе мутантные полипептиды IL-2 могут связываться с субъединицей IL-2Rα Kd менее чем около 28 нМ (например, менее чем около 25 нМ; менее чем около 5 нМ; около 1 нМ; менее чем около 500 пМ; или менее чем около 100 пМ). В частности, мутантный полипептид IL-2 может иметь аффинную равновесную константу менее 1,0 нМ (например, около 0,8, 0,6, 0,4 или 0,2 нМ). Аффинность также можно выразить как относительную скорость диссоциации от субъединицы IL-2Rα или от комплекса рецептора IL-2 (например, комплекса, экспрессируемого на поверхности клетки или иным образом мембраносвязанного). Например, мутантные полипептиды IL-2 могут диссоциировать от, например, IL-2Rα, со сниженной скоростью по сравнению с полипептидом дикого типа или с терапевтическим средством на основе IL-2, например, IL-2*. В альтернативном варианте, аффинность можно охарактеризовать как время или среднее время, в течение которого полипептид IL-2* присутствует, например, на поверхности клетки, экспрессирующей IL-2R. Например, полипептид IL-2* может присутствовать на рецепторе в течение времени, по меньшей мере в около 2, 5, 10, 50, 100 или 250 раз (или более) большего.
[176] Описаны материалы, композиции и компоненты, которые можно использовать для, можно использовать в сочетании, можно использовать при приготовлении или которые являются продуктами описанных способов и композиций. Эти и другие материалы описаны в данном документе; понятно, что если описаны комбинации, подгруппы, взаимодействия, группы и т.д. этих материалов, несмотря на то, что конкретная ссылка на каждую из различных индивидуальных и коллективных комбинаций и перестановок этих соединений может быть явным образом не описана, каждая отдельно предусмотрена и описана в данном документе. Например, если описан и обсуждается способ и обсуждается ряд модификаций, которые могут быть осуществлены в отношении рада молекул, включая способ, каждая и любая комбинация и перестановка способа и модификации, которые возможны, явным образом предусмотрены, если явным образом не указано иное. Аналогично, любая их подгруппа или комбинация также явным образом предусмотрена и описана. Эта концепция относится ко всем аспектам изобретения, включая, но не ограничиваясь этим, этапы в способах с применением описанных композиций. Таким образом, при наличии рада дополнительных этапов, которые можно проводить, следует понимать, что каждый из этих дополнительных этапов можно проводить, используя любые конкретные этапы способа или комбинацию этапов способа описанных способов, и что каждая такая комбинация или подгруппа комбинаций явным образом предусмотрена и считается описанной.
[177] Цитируемые в данном документе публикации и материалы, в отношении которых они цитируются, в полном объеме и явным образом включены в данный документ посредством ссылки.
ПРИМЕРЫ
[178] Ниже приведены примеры способов и композиций по данному изобретению. Следует понимать, что на практике можно реализовать различные другие варианта осуществления с учетом описания, предложенного в данном документе.
Пример 1: Обнаружение IL-2, мутеина IL-2, IL-2Rα и IL-2Rγ в слитых белках методом ИФА
[179] Обнаружение мутеина IL-2 проводят с помощью коммерчески доступного антитела, например, анти-1b-2 моноклонального антитела (JES6-1A12) (BD Pharmingen; San Jose, Calif.). Положительный контроль используют, чтобы продемонстрировать, распознает ли моноклональное антитело цитокин или мутеин. Также можно использовать антитела против цепи IL-2Rα и IL-2Rγ. Лунки 96-луночного планшета покрывают антителом (2,5 мкг/мл) в ФСБ. Лунки блокируют 5% нежирным молоком в ФСБ с 0,2% Твин®20 (PBS-M-Tw), а слитые белки добавляют в течение 12 часов при 37°С. После промывки добавляют анти-IL-2 биотин-меченное антитело, например, JES5H4 (BD Pharmingen) и проводят обнаружение связывания, используя стрептавидин-HRP (Southern Biotechnology Associates; Birmingham, Ala.). Реакцию в ИФА-планшете инициировали добавлением 50 мкл O-фенилендиамина (ОФД) (Sigma-Aldrich) в 0,1 М цитрате, рН 4,5, и 0,04% H2O2, останавливали добавлением 50 мкл/лунка 2N H2SO4 и считывали поглощение на 490 нм.
Пример 2: Расщепление слитого белка протеазой ММР9
[180] Специалисту в данной области техники должны быть известны способы проведения анализа расщепления белка. 100 мкг белка в 1хФСБ, рН 7,4, расщепляли 1 мкг активной ММР9 (каталог Sigma, № SAE0078-50 или каталог Enzo, BML-SE360) и инкубировали при комнатной температуре в течение до 16 часов. После этого расщепленный белок использовали в функциональном анализе или хранили при -80°С до исследования. Степень расщепления отслеживали с помощью ДСН-ПААГ, используя методы, известные в данной области техники. Как проиллюстрировано на Фиг. 10, наблюдается полное расщепление слитых белков протеазой ММР9.
Пример 3: Анализ CTLL-2
[181] Клетки CTLL2 (АТСС) высевали в суспензию в концентрации 500000 клеток/лунка в культуральную среду с 40 мг/мл человеческого сывороточного альбумина (ЧСА) или без него и стимулировали серией разведении рекомбинантного hIL2 или активируемого hIL2 в течение 72 часов при 37°С и 5% CO2. Исследовали активность нерасщепленного и расщепленного активируемого hIL2. Расщепленный активируемый hIL2 получали путем инкубации с активной ММР9. Активность клеток оценивали, используя люминесцентный анализ жизнеспособности клеток CellTiter-Glo (Promega). Результаты приведены на Фиг. 7-9.
Пример 4: Расщепление протеазой химерного полипептида IL-1/IL-1Rα/IL-1Rγ приводит к повышению доступности для антител и биологически активному мутеину IL-2
[182] Биохимические характеристики слитых белков мутеина IL-2 получают до и после расщепления протеазой, например, PSA. Иммуноблот-анализ покажет, что слитые белки могут расщепляться PSA и что наблюдается повышение интенсивности предсказанного низкомолекулярного продукта расщепления массой приблизительно 20 кДа, вступающего в реакцию с анти-IL-2 антителом, после обработки образцов PSA. Степень расщепления зависит от количества PSA, а также от времени инкубации. Интересно, что когда слитый белок анализируют до и после расщепления PSA методом ИФА, было обнаружено, что кажущееся количество IL-2 повышается после расщепления PSA. В этом эксперименте наблюдается приблизительно 2- или 4-кратное повышение кажущегося количества IL-2, обнаруженное с помощью сандвич-ИФА, в зависимости от конструкции, что позволяет предположить, что связывание с антителом частично затруднено в интактном слитом белке. Аликвоты тех же образцов также анализируют после обработки PSA, используя линию клеток CTLL-2, для роста и выживаемости которой необходим IL-2, а в жизнеспособности клеток можно убедиться, используя колориметрический анализ МТТ. В этом анализе чем больше можно развести супернатант, тем больше биологически активного IL-2 он содержит; и наблюдается повышение количества биологически активного IL-2 после расщепления PSA. Повышение количества мутеина IL-2 позволит предположить, что после расщепления PSA наблюдается повышение количества предсказанного низкомолекулярного фрагмента расщепления массой приблизительно 20 кДа, вступающего в реакцию с анти-IL-2 антителом, повышение доступности для антитела и, что наиболее важно, повышение количества биологически активного мутеина IL-2.
Пример 5. In vivo доставка активированного протеазой слитого белка приводит к снижению роста опухоли
[183] Химерные полипептиды исследовали, чтобы определить, могут ли они оказывать биологические эффекты in vivo. В этих экспериментах используют систему, в которой опухолевые клетки, вводимые внутрибрюшинно, быстро и преимущественно присоединяются и растут изначально на молочных пятнах, ряде организованных иммунных агрегатов, встречающихся в сальниках (Gerber et al., Am. J. Pathol. 169:1739-52 (2006)). Эта система предлагает удобный способ для изучения эффектов обработки слитым белком на рост опухоли, поскольку слитые белки можно многократно доставлять внутрибрюшинно, а рост опухоли можно анализировать, изучая диссоциированные клетки сальника. Для этих экспериментов можно использовать линию клеток толстой кишки 38, быстро растущую опухолевую линию клеток, которая экспрессирует как ММР2, так и ММР9 in vitro. Ткань сальника обычно экспрессирует относительно небольшое количество ММР2 и ММР9, но когда опухоль толстой кишки 38 присутствует на сальнике, уровни ММР повышаются. Используя эту опухолевую модель, исследуют способность слитых белков мутеина IL-2 влиять на рост опухоли. Клетки толстой кишки 38 инъецируют внутрибрюшинно, позволяют им присоединиться и расти в течение 1 суток, а затем ежесуточно внутрибрюшинно обрабатывают слитым белком. На 7 сутки животных умерщвляют и исследуют сальники в отношении роста опухоли, используя проточную цитометрию и с помощью анализа образования колоний.
Пример 6: Конструирование типового активируемого белка IL2, нацеленного на CD20 Создание активируемого домена IL2.
[184] Полипептид IL-2, способный связываться с полипептидом CD20, присутствующим в опухоли или на опухолевой клетке, получают следующим образом. Получают нуклеиновую кислоту, которая содержит последовательности нуклеиновой кислоты: (1) кодирующие последовательность полипептида IL-2 и (2) один или более полипептидных линкеров. Плазмидные конструкции активируемого интерлейкина могут иметь необязательные Flag, His или другие аффинные метки, их электропорируют в HEK293 или другие подходящие линии клеток человека или млекопитающих и очищают. Валидационный анализ включает анализ активации Т-клеток с использованием Т-клеток, восприимчивых к стимуляции IL-2 в присутствии протеазы.
Создание CD20-связывающего домена scFv
[185] CD20 является одним из белков клеточной поверхности, присутствующих на В-лимфоцитах. Антиген CD20 встречается в нормальных и злокачественных пре-В и зрелых В-лимфоцитах, в том числе в более 90% В-клеток неходжкинских лимфом (НХЛ). Этот антиген отсутствует в гемопоэтических стволовых клетках, активированных В-лимфоцитах (плазматических клетках) и нормальной ткани. В связи с этим было описано несколько антител, преимущественно мышиного происхождения: 1F5, 2В8/С2В8, 2Н7 и 1Н4.
[186] Следовательно, человеческие или гуманизированные анти-CD20 антитела используют для создания последовательностей scFv для доменов связывания CD20 активируемого белка интерлейкина. Получают последовательности ДНК, кодирующие человеческие или гуманизированные VL- и VH-домены, а кодоны конструкций, необязательно, оптимизируют для экспрессии в клетках от Homo sapiens. Порядок, в котором VL- и VH-домены находятся в scFv, варьируется (т.е. ориентация VL-VH или VH-VL), а три копии «G4S» или субъединицы «G4S» (G4S)3 соединяют вариабельные домены с созданием домена scFv. Плазмидные конструкции анти-CD20 scFv могут иметь необязательные Flag, His или другие аффинные метки, их электропорируют в HEK293 или другие подходящие линии клеток человека или млекопитающих и очищают. Валидационный анализ включает анализ связывания методом FACS, кинетический анализ с помощью Proteon и окрашивание CD20-экспрессирующих клеток.
Клонирование экспрессионных конструкций ДНК, кодирующих активируемый белок IL2
[187] Активируемую конструкцию IL2 с доменами сайта расщепления протеазой используют для конструирования активируемого белка интерлейкина в комбинации с анти-CD20 scFv-доменом и элементом для продления сывороточного времени полужизни (например, ЧСА-связывающим пептидом или VH-доменом). Для экспрессии активируемого белка интерлейкина в клетках СНО кодирующие последовательности всех белковых доменов клонируют в экспрессионную векторную систему млекопитающих. Вкратце, генные последовательности, кодирующие домен активируемого белка интерлейкина, элемент для продления сывороточного времени полужизни и CD20-связывающий домен наряду с пептидными линкерами L1 и L2, синтезируют отдельно и субклонируют. Полученные в результате конструкции лигируют вместе в порядке CD20-связывающий домен - L1 - субъединица 1 IL2 - L2 - домен расщепления протеазой - L3 -субъединица 2 IL2 - L4 - анти-CD20 scFv - L5 - элемент для продления сывороточного времени полужизни для получения конечной конструкции. Все экспрессионные конструкции содержат кодирующие последовательности для N-концевого сигнального пептида и С-концевой гексагистидиновой (6xHis)-метки для облегчения секреции и очистки белка, соответственно.
Экспрессия активируемых белков IL2 в стабильно трансфицированных клетках СНО
[188] Используя экспрессионную систему на основе клеток СНО (F1p-In®, Life Technologies), производное клеток яичника китайского хомяка СНО-K1 (АТСС, CCL-61) (Kao and Puck, Proc. Natl. Acad Sci USA 1968;60(4):1275-81). Адгезивные клетки субкультивируют в соответствии со стандартными протоколами клеточного культивирования, предоставленными Life Technologies.
[189] Для адаптации для роста в суспензии клетки отделяют от пробирок для тканевых культур и помещают в бессывороточную среду. Адаптированные к суспензии клетки криоконсервируют в среде с 10% ДМСО.
[190] Рекомбинантные линии клеток СНО, стабильно экспрессирующие секретируемые активируемые белки интерлейкина, создают путем трансфекции адаптированных к суспензии клеток. Во время селекции с использованием антибиотика гигромицина В плотность жизнеспособных клеток измеряют дважды в неделю, клетки центрифугируют и ресуспендируют в свежей селекционной среде при максимальной плотности 0,1×106 жизнеспособных клеток/мл. Пулы клеток, стабильно экспрессирующих активируемые белки интерлейкина, восстанавливают через 23 недели селекции и в этот момент времени клетки переносят в стандартную культуральную среду во встряхиваемые пробирки. Экспрессию рекомбинантных секретируемых белков подтверждают путем проведения гель-электрофореза или проточной цитометрии. Стабильные пулы клеток криоконсервируют в среде, содержащей ДМСО.
[191] Активируемые белки IL2 получают в 10-суточных подпитываемых культурах стабильно трансфицированных линий клеток СНО путем секреции в клеточный культуральный супернатант. Клеточные культуральные супернатанты собирают через 10 суток при жизнеспособности культур обычно >75%. Образцы отбирают из вырабатывающих культур через сутки и оценивают жизнеспособность и плотность клеток. В день сбора клеточные культуральные супернатанты осветляют путем центрифугирования и вакуумной фильтрации перед дальнейшим использованием.
[192] Титры белковой экспрессии и целостность продуктов в клеточных культуральных супернатантах анализируют методом ДСН-ПААГ.
Очистка активируемых белков IL2
[193] Активируемые белки IL2 очищают из клеточных культуральных супернатантов СНО с помощью двухэтапной процедуры. На первом этапе конструкции подвергают аффинной хроматографии, за которой следуют эксклюзионная хроматография (ЭХ) на Superdex 200 на втором этапе. В образцах проводят замену буфера и концентрируют их путем ультрафильтрации до типичной концентрации >1 мг/мл. Чистоту и гомогенность (обычно >90%) конечных образцов оценивают методом ДСН-ПААГ в восстанавливающих и невосстанавливающих условиях с последующим иммуноблоттингом с использованием анти-ЧСА или анти-идиотипического антитела, а также методом аналитической ЭХ, соответственно. Очищенные белки хранят в аликвотах при -80°С до использования.
Пример 7: Определение аффинности к антигену методом проточной цитометрии
[194] Активируемые белки IL2 из примера 6 исследуют в отношении аффинности связывания с CD20+ клетками человека и CD20+ клетками яванского макака.
[195] Клетки CD20+ инкубируют со 100 мкл серийных разведении активируемых белков интерлейкина из примера 6 и по меньшей мере одной протеазой. После промывки три раза буфером FACS клетки инкубируют с ОД мл 10 мкг/мл мышиного моноклонального анти-идиотипического антитела в том же самом буфере в течение 45 мин на льду. После второго цикла промывки клетки инкубируют с ОД мл 15 мкг/мл ФИТЦ-конъюгированных козьих антимышиных антител IgG в тех же условиях, что и ранее. В качестве контроля клетки инкубируют с анти-His IgG, после этого - с ФИТЦ-конъюгированными козьими антимышиными антителами IgG без активируемых белков IL2. Клетки снова промывали и ресуспендировали в 0,2 мл буфера FACS, содержащего 2 мкг/мл пропидий йодида (ПИ), чтобы исключить мертвые клетки. Флуоресценцию 1×104 живых клеток измеряли, используя проточный цитометр Beckman-Coulter FC500 MPL и программное обеспечение МХР (Beckman-Coulter, Krefeld, Germany) или проточный цитометр Millipore Guava EasyCyte и программное обеспечение Incyte (Merck Millipore, Schwalbach, Germany). Среднюю интенсивность флуоресценции образцов клеток рассчитывали, используя программное обеспечение СХР (Beckman-Coulter, Krefeld, Germany) или программное обеспечение Incyte (Merck Millipore, Schwalbach, Germany). После вычитания значений интенсивности флуоресценции клеток, окрашенных только вторичными и третичными реагентами, эти значения затем используют для расчета значений kd с помощью уравнения для односайтового связывания (гипербола) в GraphPad Prism (версия 6.00 для Windows, GraphPad Software, La Jolla California USA).
[196] Связывание CD20 и перекрестную реактивность оценивают на линиях опухолевых клеток CD20+ человека. Отношение kd перекрестной реактивности рассчитывают, используя значения kd, определенные в линиях клеток СНО, экспрессирующих рекомбинантные антигены человека или рекомбинантные антигены яванского макака.
Пример 8: Анализ цитотоксичности
[197] Активируемый белок IL2 из примера 6 оценивают in vitro в отношении его опосредования иммунного ответа на целевые клетки CD20+.
[198] Флуоресцентно меченные клетки CD20+ REC-1 (линия клеток мантийно клеточной лимфомы, АТСС CRL-3004) инкубируют с выделенными МКПК от случайных доноров или СВ 15 Т-клетками (стандартизированная линия Т-клеток) в качестве эффекторных клеток в присутствии активируемого белка IL2 из примера 6 и по меньшей мере одной протеазы. После инкубации в течение 4 ч при 37°С в увлажненном инкубаторе определяют высвобождение флуоресцентного красителя из целевых клеток в супернатант в спектрофлуориметре. Целевые клетки, которые инкубировали без активируемого белка IL2 из примера 6, и целевые клетки, полностью лизированные путем добавления сапонина в конце инкубации, служат в качестве отрицательного и положительного контролей, соответственно.
[199] На основании измеренных оставшихся живых целевых клеток рассчитывают процент специфического клеточного лизиса в соответствии со следующей формулой: [1-(число живых мишеней (образец)/число живых мишеней(спонтанных))] × 100%. Сигмоидальные кривые доза-ответ и значения ЕС50 рассчитывают с помощью нелинейной регрессионной/4-параметрической логистической аппроксимации, используя программное обеспечение GraphPad. Значения лизиса, полученные для заданной концентрации антитела, используют для расчета сигмоидальных кривых доза-ответ с помощью анализа 4-параметрической логистической аппроксимации, используя программное обеспечение Prism.
Пример 9: Фармакокинетика активируемых белков IL2
[200] Активируемый белок IL2 из примера 6 оценивают в отношении периода полувыведения в исследованиях на животных.
[201] Активируемый белок IL2 вводят яванским макакам в виде 0,5 мг/кг болюсной инъекции в подкожную вену. Другая группа яванских макаков получает сравнимую по размеру конструкцию IL2, но в которой отсутствует элемент продления сывороточного времени полужизни. Третья и четвертая группы получают конструкцию IL2 с элементом для продления сывороточного времени полужизни и цитокин с CD20 и элементом для продления сывороточного времени полужизни, соответственно, оба сравнимые по размеру с активируемым белком интерлейкина. Каждая исследуемая группа состоит из 5 обезьян. Образцы сыворотки получают в указанные моменты времени, проводят серийное разведение и определяют концентрацию белков, используя ИФА связывания с CD20.
[202] Анализ фармакокинетики проводят, используя плазменные концентрации исследуемого препарата. Средние по группе плазменные данные для каждого исследуемого препарата соответствуют мультиэкспоненциальному профилю при построении зависимости от времени после введения дозы. Данные аппроксимируют стандартной двухкомпартментной моделью с болюсным вводом и константами скорости первого порядка для фаз распределения и выведения. Общим уравнением для наилучшей аппроксимации данных для в/в введения является: с(t)=Ае-αt+Ве-βt, где c(t) - плазменная концентрация в момент времени t, А и В - пересечения с осью Y, а α и β - кажущиеся константы скорости первого порядка для фаз распределения и выведения, соответственно. α-фаза представляет собой начальную фазу выведения и отображает распределение белка во всей внеклеточной жидкости животного, тогда как вторая часть или β-фаза спадающей кривой представляет истинное плазменное выведение. Способы аппроксимации таких уравнений хорошо известны в данной области техники. Например, A=D/V(α-k21)/(α-β), B=D/V(β-k21)/(α-β), а α и β (для α>β) являются корнями квадратного уравнения: r2+(k12+k21+k10)r+k21k10=0 с использованием оценочных параметров V - объем распределения, k10 - скорость выведения, k12 - скорость переноса из компартмента 1 в компартмент 2, а k21 - скорость переноса из компартмента 2 в компартмент 1, и D - вводимая доза.
[203] Анализ данных: Графики зависимости концентрации от временного профиля строят, используя KaleidaGraph (KaleidaGraph™ V. 3.09 Copyright 1986-1997. Synergy Software. Reading, Pa.). Значения, представленные как «меньше подлежащего представлению» (МПП) не включены в анализ ФК и не представлены графически. Фармакокинетические параметры определяют с помощью компартментного анализа, используя программное обеспечение WinNonlin (WinNonlin® Professional V. 3.1 WinNonlin™ Copyright 1998-1999. Pharsight Corporation. Mountain View, Calif.). Фармакокинетические параметры рассчитывают, как описано в Ritschel W A and Keams G L, 1999, в: Handbook Of Basic Pharmacokinetics Including Clinical Applications, 5th edition, American Pharmaceutical Assoc., Washington, D.C.
[204] Ожидается, что активируемый белок IL2 из примера 6 имеет улучшенные фармакокинетические параметры, такие как повышение времени полувыведения, по сравнению с белками, в которых отсутствует элемент для продления сывороточного времени полужизни.
Пример 10: Модель с ксенотрансплантатом опухоли
[205] Активируемый белок IL2 из примера 6 оценивают в модели с ксенотрансплантатом.
[206] Самок иммунодефицитных мышей NOD/scid облучают сублетальной дозой (2 грэй) и подкожно инокулируют 4×106 клеток Ramos RA1 в верхнюю часть правого бока. Когда опухоли достигают 100-200 мм3, животных распределяют по 3 группам обработки. Группам 2 и 3 (по 8 животных в каждой) внутрибрюшинно инъецируют 1,5×107 активированных человеческих Т-клеток. Через трое суток животных из группы 3 последовательно обрабатывают в целом 9 внутривенными дозами 50 мкг активируемого белка интерлейкина из примера 1 (один раз в сутки х 9 с). Группы 1 и 2 обрабатывают только носителем. Массу тела и объем опухолей определяют в течение 30 суток.
[207] Ожидается, что животные, обработанные активируемым белком IL2 из примера 6, имеют статически значимое замедление роста опухоли по сравнению с соответствующей обработанной носителем контрольной группой.
[208] Хотя предпочтительные варианты осуществления данного изобретения были проиллюстрированы и описаны в данном документе, для специалистов в данной области техники очевидно, что такие варианты осуществления приведены исключительно в качестве примера. Теперь специалистам в данной области техники станут понятны многочисленные вариации, изменения и замещения, не выходящие за пределы объема изобретения. Следует понимать, что при практической реализации изобретения можно применять различные альтернативы вариантам осуществления изобретения, описанным в данном документе. Предполагается, что нижеприведенная формула изобретения определяет объем изобретения и что она охватывает способы и структуры в пределах объема этой формулы изобретения, а также их эквиваленты.
Пример 11: Анализ HEK Blue
[209] Клетки HEK-Blue IL2 (InvivoGen) высевали в суспензию в концентрации 50000 клеток/лунка в культуральную среду с 15-40 мг/мл человеческого сывороточного альбумина (ЧСА) или без него и стимулировали серией разведении рекомбинантного hIL2 или активируемого hIL2 в течение 24 часов при 37°С и 5% CO2. Исследовали активность нерасщепленного и расщепленного активируемого hIL2. Расщепленный индуцибельный hIL2 получали путем инкубации с активной ММР9. Активность IL12 оценивали на основании количественной оценки активности секретируемой щелочной фосфатазы (SEAP), используя реагент QUANTI-Blue (InvivoGen), колориметрический анализ. Результаты проиллюстрированы на Фиг. 11.
Пример 12: Эксперименты МС38
[210] Использовали линию клеток МС38, быстро растущую линию клеток аденокарциномы толстой кишки, которая экспрессирует ММР9 in vitro. Используя эту опухолевую модель, исследовали способность слитых белков влиять на рост опухоли.
Пример 12а: МС38 IL-2POC Агенты и обработка:
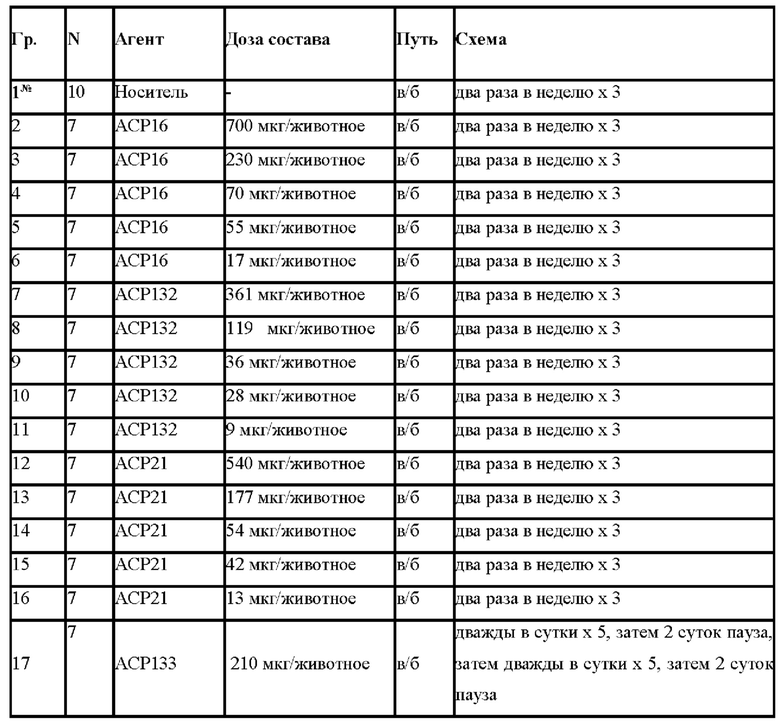

Пример 12b: MC38 IL-2 Агенты и обработка:

Пример 12с: Обработка АСР16, АСР132 и АСР21
Мышей анестезировали изофлураном для имплантации клеток для снижения изъязвлений. CR самкам мышей линии C57BL/6 п/к вводили 5×105 МС38 опухолевых клеток в 0% матригеле в бок. Объем инъекции клеток составлял 0,1 мл/мышь. Возраст мышей на дату начала составлял 8-12 недель. Проводили совмещение пар, когда опухоли достигали среднего объема 100-150 мм3, и начинали обработку. АСР16 вводили в дозе 17, 55, 70 или 230 мкг/животное; АСР132 вводили в дозе 9, 28, 36 или 119 мкг/животное; АСР21 вводили в дозе 13, 42, 54 или 177 мкг/животное. Массу тела измеряли на момент начала, и после этого - два раза в неделю до конца. Измерения кронциркулем проводили два раза в неделю до конца. О любых нежелательных реакциях следовало незамедлительно сообщать. Любое отдельное животное с одним наблюдением >30% потери массы тела или тремя последовательными измерениями >25% потери массы тела умерщвляли. В любой группе со средней потерей массы тела >20% или >10% введение доз прекращали; группу не умерщвляли и оставляли восстанавливаться. В группах с потерей массы >20% умерщвляли животных, достигших индивидуального конечного показателя потери массы тела. Если связанная с обработкой потеря массы тела в группе восстанавливалась до 10% от исходных значений массы, введение доз возобновляли в меньшей дозе или по схеме с менее частым введением. Исключения для не обусловленного лечением восстановления % массы тела допускались в зависимости от конкретного случая. Конечным результатом было замедление роста опухоли (ЗРО). За животными наблюдали индивидуально. Конечным результатом эксперимента был объем опухоли 1500 мм3 или 45 суток, в зависимости от того, что произойдет быстрее. За демонстрирующими ответ животными наблюдали дольше. При достижении конечного результата животных необходимо умертвить. Результаты проиллюстрированы на Фиг. 17.
Пример 12d: повторная стимуляция МС38
Излеченных мышей (обработанных АСР16) из примера 12b повторно стимулировали, имплантируя опухоли, чтобы определить, сформировалась ли противоопухолевая память после начальной обработки.
Агенты и обработка:


Процедуры:
Мышей анестезировали изофлураном для имплантации клеток для снижения изъязвлений. Эту часть исследования начинали на сутки имплантации (1 сутки). Группа 1 состояла из 33 CR самок мышей линии C57BL/6, которым подкожно вводили 5×105 МС38 опухолевых клеток в 0% матригеле в бок. Группы 2-6 состояли из 33 CR самок мышей линии C57BL/6, которым п/к вводили 5×105 МС38 опухолевых клеток в 0% матригеле в бок. Опухоли из предыдущего эксперимента МС38 (пример 12b) имплантировали в правый бок каждого животного. Объем инъекции клеток составлял 0,1 мл/мышь. Возраст контрольных мышей на момент начала составлял 1417 недель. Эти мыши совпадали по возрасту с мышами из предыдущего эксперимента МС38 (пример 12b). Во время повторной стимуляции не проводили введение активного агента. Массу тела измеряли два раза в неделю до конца, как и измерения кронциркулем. О любых нежелательных реакциях или смерти незамедлительно сообщали. Любое отдельное животное с одним наблюдением >30% потери массы тела или тремя последовательными измерениями >25% потери массы тела умерщвляли. Конечным результатом было замедление роста опухоли (ЗРО). За животными наблюдали индивидуально. Конечным результатом эксперимента был объем опухоли 1000 мм3 или 45 суток, в зависимости от того, что произойдет быстрее. При возможности демонстрирующих ответ животных наблюдали дольше. При достижении конечного результата животных умерщвляли. Результаты проиллюстрированы на Фиг. 15.
Пример 13. Кондиционально активные слитые белки, которые содержат блокирующий фрагмент, который представляет собой связывающий сывороточный альбумин фрагмент
[211] В этом примере описаны получение и активность слитых белков, предпочтительно цитокинов, которые обладают индуцибельной активностью, т.е. они неактивны до индукции, как правило, за счет отделения блокирующего фрагмента от активного фрагмента после расщепления линкера между блокирующим фрагментом и активным фрагментом. Слитые белки содержат один вариабельный домен антитела (dAb), который связывает сывороточный альбумин посредством петель CDR, и связывается с активным фрагментом (в данном случае анти-CD3 scFV) посредством одной или более отличных от CDR петель (например, петли С). Связывающий сывороточный альбумин блокирующий фрагмент функционально связан с активным фрагментом посредством расщепляемого протеазой линкера, а активный фрагмент функционально связан с нацеливающим доменом (в данном случае dAb против рецептора эпидермального фактора роста (EGFR) или dAb против простат-специфического мембранного антигена (PSMA)) посредством линкера, которые не расщепляется протеазой. Эти слитые белки можно вводить в виде неактивных белков, которые активируются после расщепления расщепляемого протеазой линкера и последующего высвобождения ингибирующего альбумин-связывающего домена. Анти-CD3 scFV в слитых белках является суррогатом необходимого цитокина в слитых белках, описанных в этом изобретении. Аналогичные слитые белки, которые содержат необходимый цитокин (например, IL-2, IL-12, интерферон) или его функциональный фрагмент или мутеин, нацеливающий домен и альбумин-связывающий dAb, который также связывает и ингибирует цитокин или его функциональный фрагмент или мутеин, можно получать, используя способы, описанные и проиллюстрированные в данном документе. dAb против сывороточного альбумина, который связывает и ингибирует активность необходимого цитокина или его функционального фрагмента или мутеина, может обеспечить как стерическую маскировку цитокина (за счет близости цитокина к связанному сывороточному альбумину), так и специфическую маскировку цитокина (за счет связывания с цитокином посредством отличной от CDR петли (например, петли С)). dAb против сывороточного альбумина, который связывает и ингибирует активность необходимого цитокина или его функционального фрагмента или мутеина, можно получать, используя подходящие способы, например, путем внесения разнообразия аминокислотной последовательности в отличные от CDR петли (например, петлю С) связывающего dAb против сывороточного альбумина, и проведения скрининга в отношении связывания с необходимым цитокином. Для проведения отбора можно использовать любые подходящие способы, такие как фаговый дисплей. Например, типовой dAb против сывороточного альбумина, который можно использовать, имеет следующую последовательность, а аминокислотную последовательность петли С (выделена жирным и подчеркиванием) можно диверсифицировать (например, рандомизировать), и провести скрининг полученных в результате dAb в отношении связывания с сывороточным альбумином посредством взаимодействия CDR и с цитокином посредством взаимодействия отличной от CDR петли. При необходимости аминокислотную последовательность известного цитокин-связывающего пептида можно привить в петлю С.
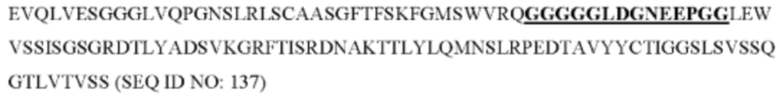
А. Активация протеазой ProTriTAC приводит к существенно повышенной активности in vitro
[212] Очищенный ProTriTAC (пролекарство), нерасщепляемый ProTriTAC [пролекарство (нерасщепляемый)] и рекомбинантный активный лекарственный фрагмент, имитирующий активность активированного протеазой ProTriTAC (активное лекарство) исследовали в отношении связывания с рекомбинантным человеческим CD3 в анализе ИФА, связывания с очищенными человеческими первичными Т-клетками в анализе проточной цитометрии и функциональной эффективности в Т-клеточно-зависимом анализе клеточной цитотоксичности.
[213] Для ИФА растворимые белки ProTriTAC в указанных концентрациях инкубировали с иммобилизованным рекомбинантным человеческим CD3e (R&D Systems) в течение 1 ч при комнатной температуре в ФСБ, дополненном 15 мг/мл человеческого сывороточного альбумина. Планшеты блокировали, используя SuperBlock (Thermo Fisher), промывали, используя ФСБ с 0,05% Твин-20, и проводили обнаружение, используя неконкурентное анти-CD3 идиотипическое моноклональное антитело 11D3, а после него - меченное пероксидазой вторичное антитело и раствор субстрата ТМБ-ИФА (Thermo Fisher).
[214] Для проточной цитометрии растворимые белки ProTriTAC в указанных концентрациях инкубировали с очищенными человеческими первичными Т-клетками в течение 1 ч при 4°С в присутствии ФСБ с 2% фетальной бычьей сыворотки и 15 мг/мл человеческого сывороточного альбумина. Планшеты промывали ФСБ с 2% фетальной бычьей сыворотки, проводили обнаружение, используя AlexaFluor 647-меченное неконкурентное анти-CD3 идиотипическое моноклональное антитело 11D3, а данные анализировали, используя FlowJo 10 (FlowJo, LLC).
[215] Для определения функциональной эффективности в Т-клеточно-зависимом анализе клеточной цитотоксичности растворимые белки ProTriTAC в указанных концентрациях инкубировали с очищенными покоящимися человеческими Т-клетками (эффекторные клетки) и раковыми клетками НСТ116 (целевые клетки) в соотношении 10:1 эффекторные щелевые клетки в течение 48 ч при 37°С. Линию целевых клеток НСТ116 стабильно трансфицировали репортерным геном люциферазы, чтобы провести измерение опосредованного Т-клетками уничтожения клеток с помощью ONE-Glo (Promega).
B. ProTriTAC демонстрирует сильную, протеазо-зависимую противоопухолевую активность в модели с ксенотрансплантатом опухоли у грызунов
[216] ProTriTAC оценивали в отношении их противоопухолевой активности in vivo в подкожной ксенотрансплантатной опухоли НСТ116 с добавленными размноженными человеческими Т-клетками у иммунодефицитных мышей NCG. В частности, 5×106 клеток НСТ116 смешивали с 2,5×106 размноженных Т-клеток на мышь на сутки 0. Введение доз ProTriTAC проводили, начиная со следующих суток по схеме каждые сутки × 10 посредством внутрибрюшинной инъекции. Объем опухолей определяли, используя проводимые с помощью кронциркуля измерения, и рассчитывали, используя формулу V = (длина × ширина × ширина)/2 в указанные моменты времени.
C. Экспрессия, очистка и стабильность типовых триспецифических молекул ProTriTAC
Выработка белка
[217] Последовательности, кодирующие молекулы индуцибельного слитого белка, клонировали в экспрессионный вектор млекопитающих pcDNA 3.4 (bivitrogen), перед ними находилась лидерная последовательность, а за ними - 6х гистидиновая метка (SEQ ID NO: 136). Клетки Expi293F (Life Technologies A14527) поддерживали в суспензии в пробирках для оптимального роста (Thomson) от 0,2 до 8 × 1е6 клеток/мл в среде Expi 293. Очищенную плазмидную ДНК трансфицировали в клетки Expi293 в соответствии с протоколами набора с экспрессионной системой для Expi293 (Life Technologies, А14635) и поддерживали в течение 4-6 суток после трансфекции. В альтернативном варианте последовательности, кодирующие молекулы слитого белка, клонировали в экспрессионный вектор млекопитающих pDEF38 (CMC ICOS), трансфицировали в клетки CHO-DG44 dhfr-, создавали стабильные пулы и культивировали в среде для выработки в течение до 12 суток перед очисткой. Количество типовых слитых белков в кондиционированной среде оценивали, используя прибор Octet RED 96 с наконечниками с протеином A (ForteBio/Pall), используя контрольный слитый белок для стандартной кривой. Кондиционированную среду из любых клеток-хозяев фильтровали и частично очищали с помощью аффинной и обессоливающей хроматографии. После этого слитые белки полировали с помощью ионообменной хроматографии и после объединения фракций вмешивали в нейтральный буфер, содержащий вспомогательный вещества. Конечную степень чистоты оценивали с помощью ДСН-ПААГ и аналитической ЭХ, используя колонку Acquity ВЕН SEC 200 1,7 мкм 4,6 × 150 мм (Waters Corporation), разрешали в водной/органической подвижной фазе со вспомогательными веществами при нейтральном рН на системе 1290 LC и интегрировали пики с помощью программного обеспечения Chemstation CDS (Agilent). Слитые белки, очищенные из клеток СНО, приведены на ДСН-ПААГ, проиллюстрированном ниже.
Оценка стабильности
[218] Очищенные слитые белки в двух составах субаликвотировали в стерильные пробирки и подвергали стрессовым условиями посредством пяти циклов замораживания-размораживания, каждый из которых включал более 1 часа при -80°С и комнатной температуре, или посредством инкубации при 37°С в течение 1 недели. Подвергнутые стрессу образцы оценивали в отношении концентрации и мутности с помощью УФ0спектрометрии, используя УФ-прозрачные 96-луночные планшеты (Corning 3635), с помощью программного обеспечения SpectraMax М2 и SoftMaxPro (Molecular Devices), ДСН-ПААГ и аналитической ЭХ, и сравнивали с таким же анализом контрольных не подвергнутых стрессу образцов. Наложение хроматограмм аналитической ЭХ контрольных и подвергнутых стрессу образцов для одной типовой молекулы ProTriTAC, очищенной из клеток-хозяев 293, проиллюстрировано ниже.
[219] Результаты показывают, что ProTriTAC вырабатывались на сравнимом уровне с регулярными TriTAC из стабильных пулов СНО; и что свойства белков были стабильными после повторяемых циклов замораживания-размораживания и 37°С в течение 1 недели.
D. Демонстрация функциональной маскировки и стабильности ProTriTAC in vivo в трехнедельном исследовании фармакокинетики на яванских макаках
[220] Одну дозу нацеленного на PSMA ProTriTAC (SEQ ID NO: 119), нерасщепляемого ProTriTAC (SEQ ID NO: 120), немаскированного/нерасщепляемого TriTAC (SEQ ID NO: 123) и активного лекарства, имитирующего активированный протеазой ProTriTAC (SEQ ID NO: 121) вводили яванским макакам в дозе 0,1 мг/кг путем внутривенной инъекции. Образцы плазмы получали в указанные моменты времени. Концентрации ProTriTAC определяли, используя анализ связывания лиганда с биотинилированным рекомбинантным человеческим PSMA (R&D systems) и сульфо-меченным анти-CD3 идиотипическим антителом 11D3 в анализе MSD (Meso Scale Diagnostic, LLC). Фармакокинетические параметры оценивали, используя программное обеспечение для фармакокинетики Phoenix WinNonlin и некомпартментный подход, согласующийся с внутривенным болюсным путем введения.
[221] Чтобы рассчитать скорость in vivo превращения пролекарства, оценивали концентрацию активного лекарства в циркуляции путем решения следующей системы дифференциальных уравнений, где Р - концентрация пролекарства, А - концентрация активного лекарства, ka - скорость активации пролекарства в циркуляции, kc,P - скорость выведения пролекарства, а kc,A - скорость выведения активного лекарства.


[222] Скорость выведения пролекарства, активного лекарства и нерасщепляемого контрольного пролекарства (kc,NCLV) определяли эмпирически у яванских макаков. Чтобы оценить скорость активации пролекарства в циркуляции, мы предположили, что разница между скоростью выведения расщепляемого пролекарства и нерасщепляемого пролекарства возникает исключительно вследствие неспецифической активации в циркуляции. Следовательно, скорость превращения пролекарства в активное лекарство в циркуляции оценивали путем вычитания скорости выведения расщепляемого пролекарства из нерасщепляемого пролекарства.
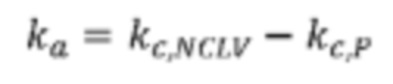
[223] Исходную концентрацию пролекарства в циркуляции определяли эмпирически, а исходную концентрацию активного лекарства приняли за ноль.
Результаты и обсуждение
[224] Результаты примера 13 показывают, что можно получать слитые белки, которые содержат полипептид с необходимой терапевтической активностью, такой как цитокин или его функциональный фрагмент или мутеин, или анти-CD3 scFV, в которых терапевтическая активность маскируется маскирующим доменом, который связывается как с сывороточным альбумином, так и с активным полипептидом. Маскирующий домен функционально связан с активным доменом посредство расщепляемого протеазой линкера. Результаты показывают, что этот тип слитого белка можно вводить в виде неактивного белка, который активируется после расщепления протеазой в необходимом месте терапевтической активности, таком как опухоль.
[225] Аминокислотные последовательности слитых белков из примера 13 приведены как SEQ ID NO: 116-123.
[226] Примеры конструкций слитых белков подробно описаны в таблице 3. В таблице 3 «L» является сокращением «линкера», а «расщепл. линк.» является сокращением «расщепляемого линкера». Другие сокращения: «mIFNg» обозначает мышиный интерферон гамма (IFNg); «hAlbumin» обозначает человеческий сывороточный альбумин (ЧСА); «mAlbumin» обозначает мышиный сывороточный альбумин.

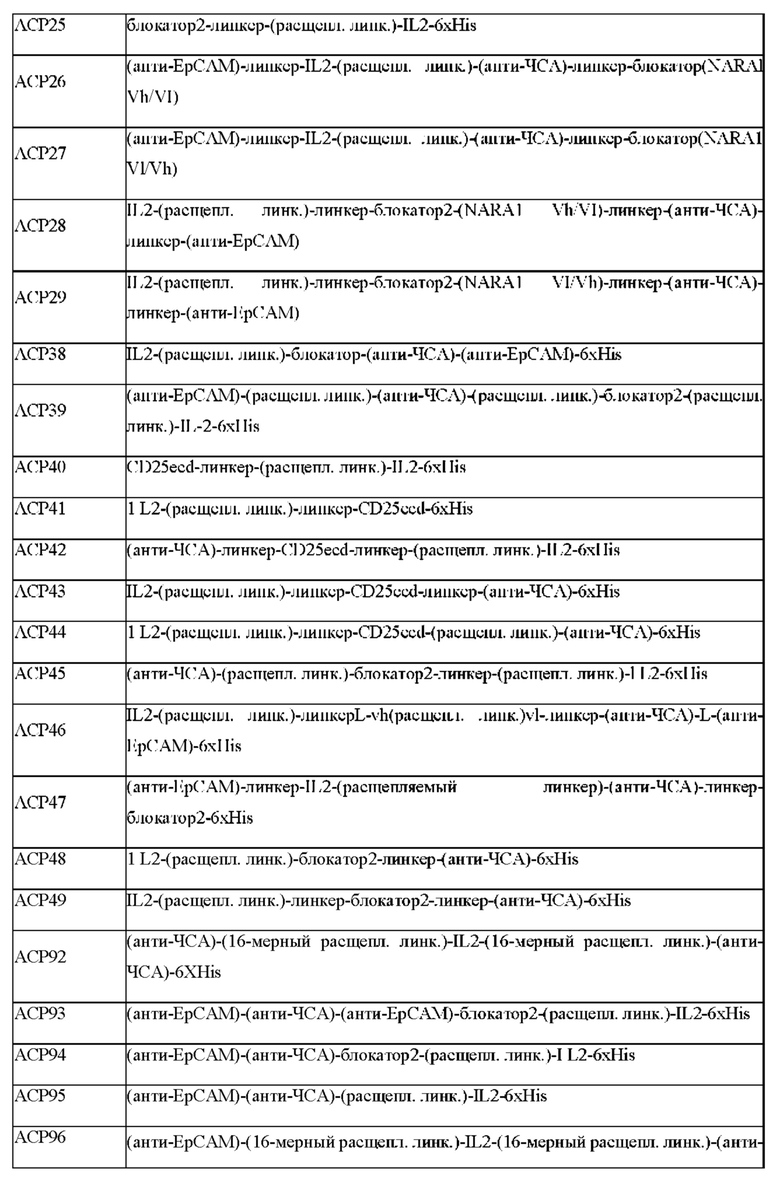







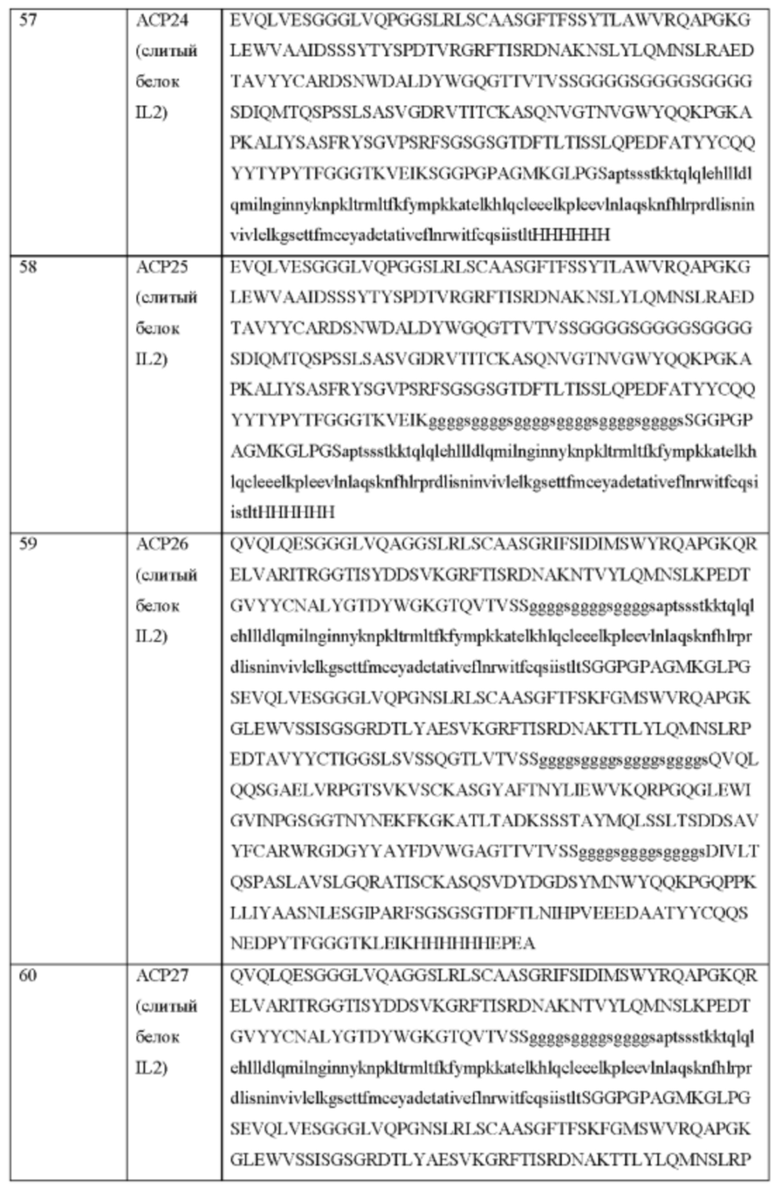



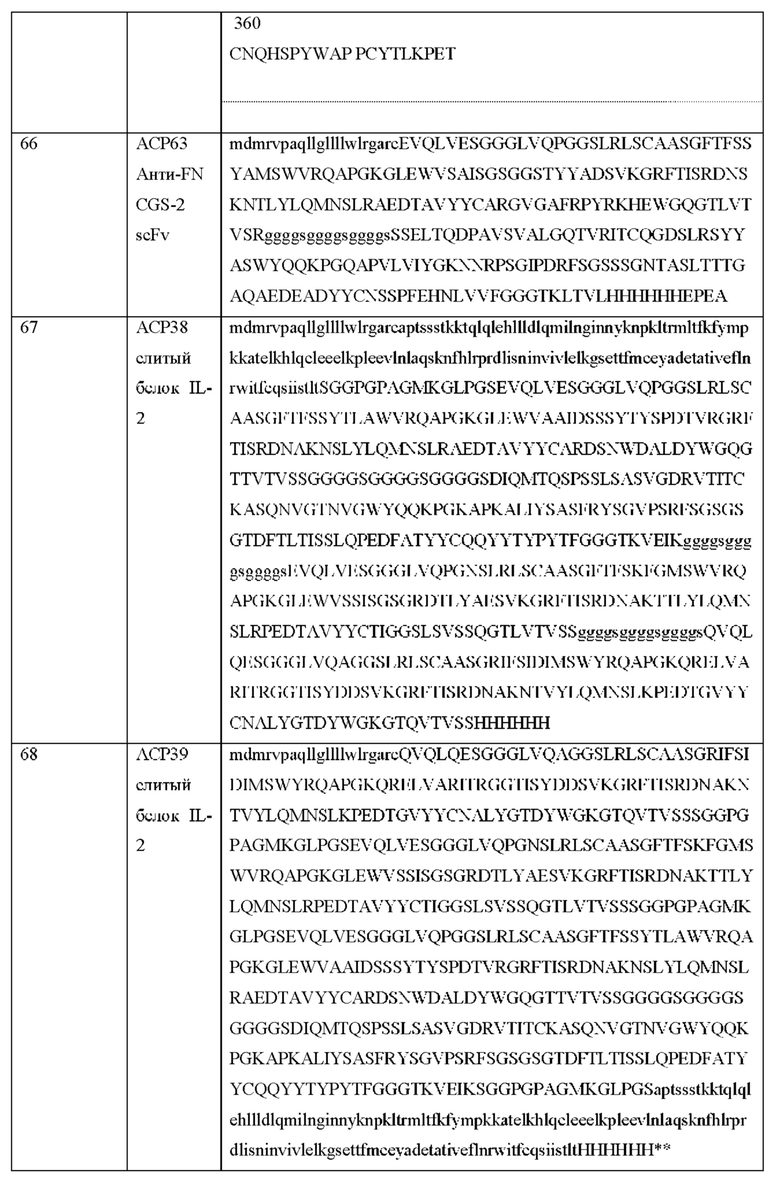


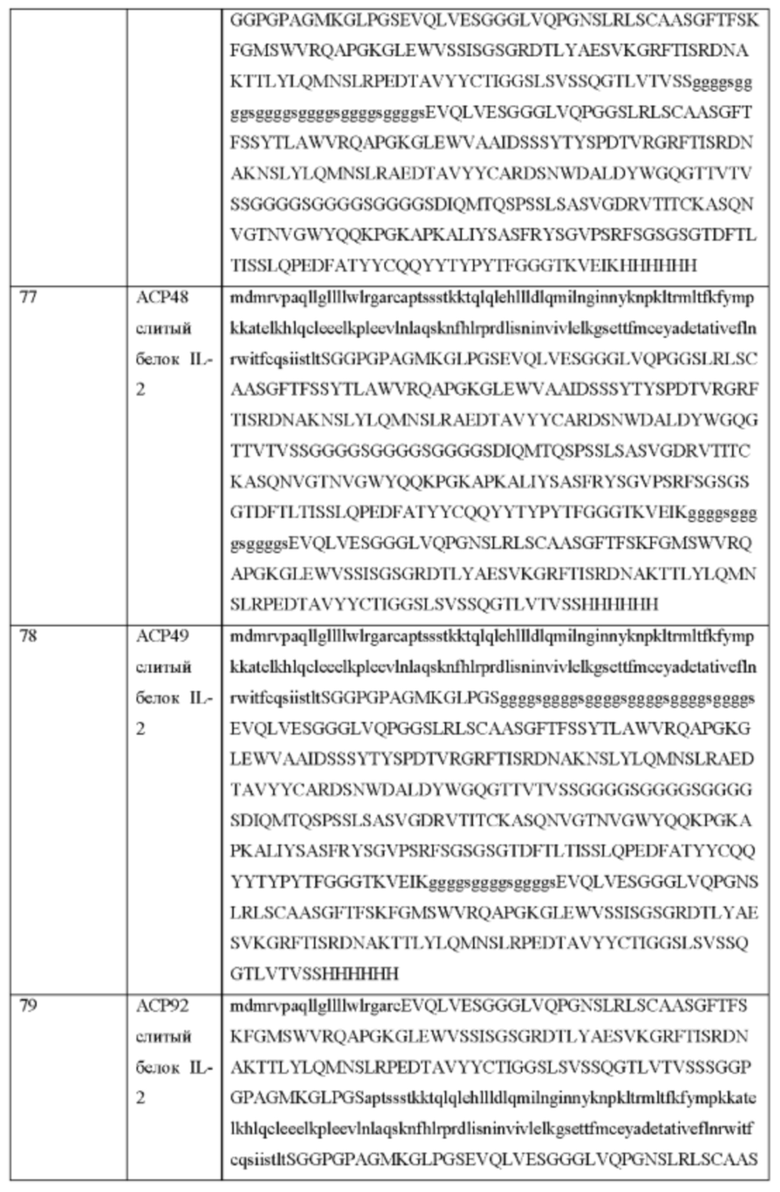





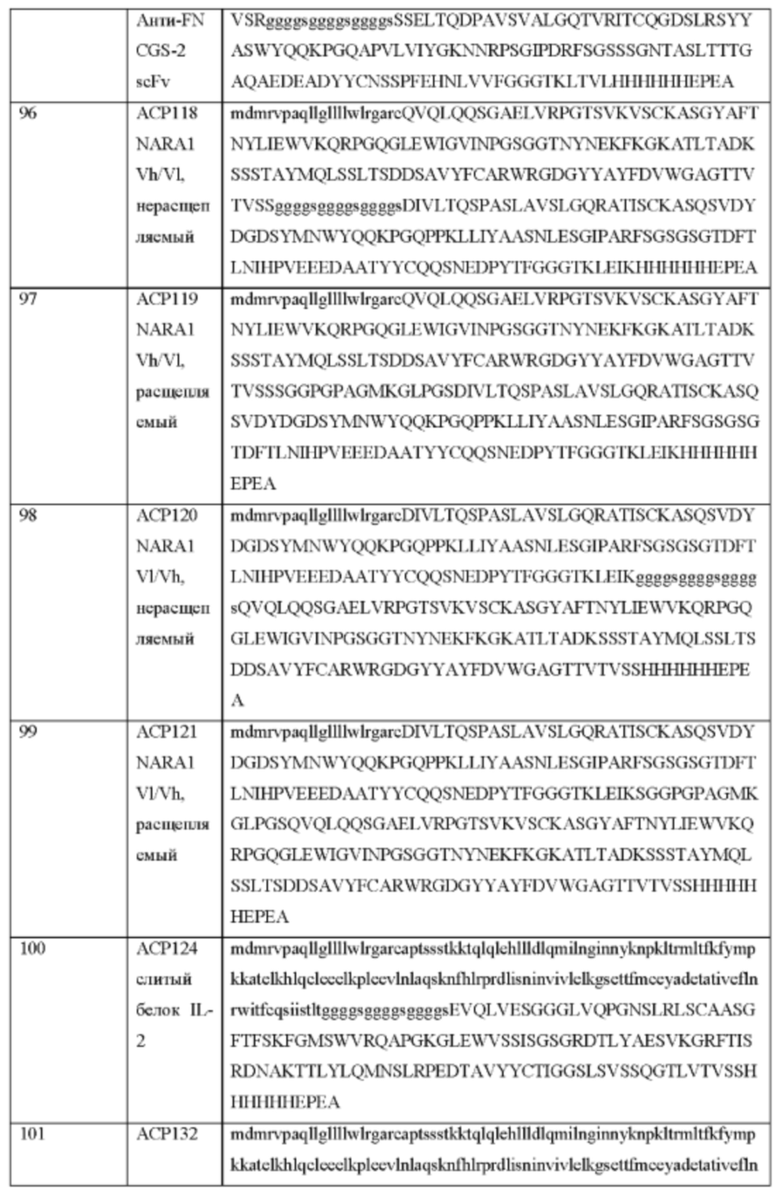





ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[227] Полное содержание всех патентных и непатентных публикаций, цитируемых в данном документе, включено посредством ссылки в полном объеме и во всех целях.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[228] Вышеприведенное описание может охватывать многие отличные изобретения с независимым применением. Хотя каждое из этих изобретений было описано в предпочтительной(ых) форме(ах), конкретные варианты их осуществления, описанные и проиллюстрированные в данном документе, не следует воспринимать в ограничительном смысле, поскольку возможны много численные вариации. Предмет данного изобретения включает все новые и неочевидные комбинации и подкомбинации различных элементов, признаков, функций и/или свойств, описанных в данном документе. В частности, в нижеприведенной формуле изобретения указаны определенные комбинации и подкомбинации, считающиеся новыми и неочевидными. Изобретения, осуществленные в других комбинациях и подкомбинациях признаков, функций, элементов и/или свойств, могут быть заявлены в данной заявке, в заявках, заявляющих приоритет по данной заявке, или в родственных заявках. Такие заявляемые пункты, относящиеся к другому изобретению или к одному и тому же изобретению, и имеющий более широкий, более узкий, эквивалентный или отличный объем по сравнению с оригинальными заявляемыми пунктами, также считаются включенными в предмет изобретение данного описания.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ВЕРВУЛФ ТЕРАПЬЮТИКС, ИНК.
<120> АКТИВИРУЕМЫЕ ПОЛИПЕПТИДЫ ИНТЕРЛЕЙКИНА-2 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> 105365-0021
<140>
<141>
<150> 62/756507
<151> 2018-11-06
<150> 62/756504
<151> 2018-11-06
<150> 62/671225
<151> 2018-05-14
<160> 137
<170> PatentIn, версия 3.5
<210> 1
<211> 153
<212>Белок
<213> Homo sapiens
<400> 1
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1 5 10 15
Val Thr Asn Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu
20 25 30
Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile
35 40 45
Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe
50 55 60
Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu
65 70 75 80
Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys
85 90 95
Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile
100 105 110
Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala
115 120 125
Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe
130 135 140
Cys Gln Ser Ile Ile Ser Thr Leu Thr
145 150
<210> 2
<211> 609
<212>Белок
<213> Homo sapiens
<400> 2
Met Lys Trp Val Thr Phe Ile Ser Leu Leu Phe Leu Phe Ser Ser Ala
1 5 10 15
Tyr Ser Arg Gly Val Phe Arg Arg Asp Ala His Lys Ser Glu Val Ala
20 25 30
His Arg Phe Lys Asp Leu Gly Glu Glu Asn Phe Lys Ala Leu Val Leu
35 40 45
Ile Ala Phe Ala Gln Tyr Leu Gln Gln Cys Pro Phe Glu Asp His Val
50 55 60
Lys Leu Val Asn Glu Val Thr Glu Phe Ala Lys Thr Cys Val Ala Asp
65 70 75 80
Glu Ser Ala Glu Asn Cys Asp Lys Ser Leu His Thr Leu Phe Gly Asp
85 90 95
Lys Leu Cys Thr Val Ala Thr Leu Arg Glu Thr Tyr Gly Glu Met Ala
100 105 110
Asp Cys Cys Ala Lys Gln Glu Pro Glu Arg Asn Glu Cys Phe Leu Gln
115 120 125
His Lys Asp Asp Asn Pro Asn Leu Pro Arg Leu Val Arg Pro Glu Val
130 135 140
Asp Val Met Cys Thr Ala Phe His Asp Asn Glu Glu Thr Phe Leu Lys
145 150 155 160
Lys Tyr Leu Tyr Glu Ile Ala Arg Arg His Pro Tyr Phe Tyr Ala Pro
165 170 175
Glu Leu Leu Phe Phe Ala Lys Arg Tyr Lys Ala Ala Phe Thr Glu Cys
180 185 190
Cys Gln Ala Ala Asp Lys Ala Ala Cys Leu Leu Pro Lys Leu Asp Glu
195 200 205
Leu Arg Asp Glu Gly Lys Ala Ser Ser Ala Lys Gln Gly Leu Lys Cys
210 215 220
Ala Ser Leu Gln Lys Phe Gly Glu Arg Ala Phe Lys Ala Trp Ala Val
225 230 235 240
Ala Arg Leu Ser Gln Arg Phe Pro Lys Ala Glu Phe Ala Glu Val Ser
245 250 255
Lys Leu Val Thr Asp Leu Thr Lys Val His Thr Glu Cys Cys His Gly
260 265 270
Asp Leu Leu Glu Cys Ala Asp Asp Arg Ala Asp Leu Ala Lys Tyr Ile
275 280 285
Cys Glu Asn Gln Asp Ser Ile Ser Ser Lys Leu Lys Glu Cys Cys Glu
290 295 300
Lys Pro Leu Leu Glu Lys Ser His Cys Ile Ala Glu Val Glu Asn Asp
305 310 315 320
Glu Met Pro Ala Asp Leu Pro Ser Leu Ala Ala Asp Phe Val Gly Ser
325 330 335
Lys Asp Val Cys Lys Asn Tyr Ala Glu Ala Lys Asp Val Phe Leu Gly
340 345 350
Met Phe Leu Tyr Glu Tyr Ala Arg Arg His Pro Asp Tyr Ser Val Val
355 360 365
Leu Leu Leu Arg Leu Ala Lys Thr Tyr Glu Thr Thr Leu Glu Lys Cys
370 375 380
Cys Ala Ala Ala Asp Pro His Glu Cys Tyr Ala Lys Val Phe Asp Glu
385 390 395 400
Phe Lys Pro Leu Val Glu Glu Pro Gln Asn Leu Ile Lys Gln Asn Cys
405 410 415
Glu Leu Phe Glu Gln Leu Gly Glu Tyr Lys Phe Gln Asn Ala Leu Leu
420 425 430
Val Arg Tyr Thr Lys Lys Val Pro Gln Val Ser Thr Pro Thr Leu Val
435 440 445
Glu Val Ser Arg Asn Leu Gly Lys Val Gly Ser Lys Cys Cys Lys His
450 455 460
Pro Glu Ala Lys Arg Met Pro Cys Ala Glu Asp Cys Leu Ser Val Phe
465 470 475 480
Leu Asn Gln Leu Cys Val Leu His Glu Lys Thr Pro Val Ser Asp Arg
485 490 495
Val Thr Lys Cys Cys Thr Glu Ser Leu Val Asn Gly Arg Pro Cys Phe
500 505 510
Ser Ala Leu Glu Val Asp Glu Thr Tyr Val Pro Lys Glu Phe Asn Ala
515 520 525
Glu Thr Phe Thr Phe His Ala Asp Ile Cys Thr Leu Ser Glu Lys Glu
530 535 540
Arg Gln Ile Lys Lys Gln Thr Ala Leu Val Glu Leu Val Lys His Lys
545 550 555 560
Pro Lys Ala Thr Lys Glu Gln Leu Lys Ala Val Met Asp Asp Phe Ala
565 570 575
Ala Phe Val Glu Lys Cys Cys Lys Ala Asp Asp Lys Glu Thr Cys Phe
580 585 590
Ala Glu Glu Gly Lys Lys Leu Val Ala Ala Ser Gln Ala Ala Leu Gly
595 600 605
Leu
<210> 3
<211> 8
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP7"
<400> 3
Lys Arg Ala Leu Gly Leu Pro Gly
1 5
<210> 4
<211> 40
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP7"
<400> 4
Asp Glu Asp Glu Asp Glu Asp Glu Asp Glu Asp Glu Asp Glu Asp Glu
1 5 10 15
Arg Pro Leu Ala Leu Trp Arg Ser Asp Arg Asp Arg Asp Arg Asp Arg
20 25 30
Asp Arg Asp Arg Asp Arg Asp Arg
35 40
<210> 5
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP9"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Thr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ile"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Thr"
<220>
<221> SITE
<222> (1)..(5)
<223> /примечание="Вариантные остатки, приведенные в последовательности,
не имеют преимущества относительно находящихся в
обозначениях для вариантных позиций"
<400> 5
Pro Arg Ser Leu Ser
1 5
<210> 6
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP9"
<400> 6
Leu Glu Ala Thr Ala
1 5
<210> 7
<211> 10
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP11"
<400> 7
Gly Gly Ala Ala Asn Leu Val Arg Gly Gly
1 5 10
<210> 8
<211> 10
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP14"
<400> 8
Ser Gly Arg Ile Gly Phe Leu Arg Thr Ala
1 5 10
<210> 9
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP"
<400> 9
Pro Leu Gly Leu Ala Gly
1 5
<210> 10
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP"
<220>
<221> МОД_ОСТ
<222> (6)..(6)
<223> Любая аминокислота
<400> 10
Pro Leu Gly Leu Ala Xaa
1 5
<210> 11
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP"
<220>
<221> МОД_ОСТ
<222> (4)..(4)
<223> Cys(me)
<400> 11
Pro Leu Gly Xaa Ala Gly
1 5
<210> 12
<211> 8
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP"
<400> 12
Glu Ser Pro Ala Tyr Tyr Thr Ala
1 5
<210> 13
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP"
<400> 13
Arg Leu Gln Leu Lys Leu
1 5
<210> 14
<211> 7
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность домена расщепления MMP"
<400> 14
Arg Leu Gln Leu Lys Ala Cys
1 5
<210> 15
<211> 7
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
MMP2, MMP9, последовательность домена расщепления MMP14"
<220>
<221> МОД_ОСТ
<222> (3)..(3)
<223> Cit
<220>
<221> МОД_ОСТ
<222> (5)..(5)
<223> Hof
<400> 15
Glu Pro Xaa Gly Xaa Tyr Leu
1 5
<210> 16
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления активатора
плазминогена урокиназного типа (uPA)"
<400> 16
Ser Gly Arg Ser Ala
1 5
<210> 17
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления активатора
плазминогена урокиназного типа (uPA)"
<400> 17
Asp Ala Phe Lys
1
<210> 18
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления активатора
плазминогена урокиназного типа (uPA)"
<400> 18
Gly Gly Gly Arg Arg
1 5
<210> 19
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления лизосомального фермента"
<400> 19
Gly Phe Leu Gly
1
<210> 20
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления лизосомального фермента"
<400> 20
Ala Leu Ala Leu
1
<210> 21
<211> 2
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления лизосомального фермента"
<400> 21
Phe Lys
1
<210> 22
<211> 3
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления катепсина B"
<400> 22
Asn Leu Leu
1
<210> 23
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления катепсина D"
<220>
<221>МОД_ОСТ
<222> (3)..(3)
<223> Cys(et)
<400> 23
Pro Ile Xaa Phe Phe
1 5
<210> 24
<211> 8
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления катепсина K"
<400> 24
Gly Gly Pro Arg Gly Leu Pro Gly
1 5
<210> 25
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления простат-специфического антигена"
<400> 25
His Ser Ser Lys Leu Gln
1 5
<210> 26
<211> 7
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления простат-специфического антигена"
<400> 26
His Ser Ser Lys Leu Gln Leu
1 5
<210> 27
<211> 9
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления простат-специфического антигена"
<400> 27
His Ser Ser Lys Leu Gln Glu Asp Ala
1 5
<210> 28
<211> 10
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления протеазой вируса простого
герпеса"
<400> 28
Leu Val Leu Ala Ser Ser Ser Phe Gly Tyr
1 5 10
<210> 29
<211> 10
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления протеазой ВИЧ"
<400> 29
Gly Val Ser Gln Asn Tyr Pro Ile Val Gly
1 5 10
<210> 30
<211> 10
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления протеазой ЦМВ"
<400> 30
Gly Val Val Gln Ala Ser Cys Arg Leu Ala
1 5 10
<210> 31
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления тромбина"
<220>
<221> МОД_ОСТ
<222> (2)..(2)
<223> 2-карбоксипиперидин
<400> 31
Phe Xaa Arg Ser
1
<210> 32
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления тромбина"
<400> 32
Asp Pro Arg Ser Phe Leu
1 5
<210> 33
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления тромбина"
<400> 33
Pro Pro Arg Ser Phe Leu
1 5
<210> 34
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления каспазы-3"
<400> 34
Asp Glu Val Asp
1
<210> 35
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления каспазы-3"
<400> 35
Asp Glu Val Asp Pro
1 5
<210> 36
<211> 8
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления каспазы-3"
<400> 36
Lys Gly Ser Gly Asp Val Glu Gly
1 5
<210> 37
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления
интерлейкин 1-бета-конвертирующего фермента"
<400> 37
Gly Trp Glu His Asp Gly
1 5
<210> 38
<211> 7
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления энтерокиназы"
<400> 38
Glu Asp Asp Asp Asp Lys Ala
1 5
<210> 39
<211> 9
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления FAP"
<400> 39
Lys Gln Glu Gln Asn Pro Gly Ser Thr
1 5
<210> 40
<211> 6
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления калликреина 2"
<400> 40
Gly Lys Ala Phe Arg Arg
1 5
<210> 41
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления плазмина"
<400> 41
Asp Ala Phe Lys
1
<210> 42
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления плазмина"
<400> 42
Asp Val Leu Lys
1
<210> 43
<211> 4
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления плазмина"
<400> 43
Asp Ala Phe Lys
1
<210> 44
<211> 7
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность домена расщепления TOP"
<400> 44
Ala Leu Leu Leu Ala Leu Leu
1 5
<210> 45
<211> 652
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 45
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp
20 25 30
Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu
130 135 140
His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
145 150 155 160
Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro
165 170 175
Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu
180 185 190
Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His
195 200 205
Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu
210 215 220
Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr
225 230 235 240
Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser
245 250 255
Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
260 265 270
Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
275 280 285
Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
290 295 300
Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys
305 310 315 320
Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu
325 330 335
Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
340 345 350
Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr
355 360 365
Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly
405 410 415
Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser
420 425 430
Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro
435 440 445
Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr
450 455 460
Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn
465 470 475 480
Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
485 490 495
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
515 520 525
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
530 535 540
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
545 550 555 560
Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln
565 570 575
Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe
580 585 590
Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
595 600 605
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
610 615 620
Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly
625 630 635 640
Thr Lys Val Glu Ile Lys His His His His His His
645 650
<210> 46
<211> 652
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 46
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp
20 25 30
Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser
145 150 155 160
Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val
180 185 190
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
260 265 270
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln
275 280 285
Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala
290 295 300
Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro
305 310 315 320
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
325 330 335
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr
340 345 350
Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
355 360 365
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
370 375 380
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser
385 390 395 400
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly
405 410 415
Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
420 425 430
Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys
435 440 445
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu
450 455 460
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr
465 470 475 480
Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val
485 490 495
Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly
500 505 510
Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu
515 520 525
His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
530 535 540
Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro
545 550 555 560
Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu
565 570 575
Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His
580 585 590
Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu
595 600 605
Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr
610 615 620
Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser
625 630 635 640
Ile Ile Ser Thr Leu Thr His His His His His His
645 650
<210> 47
<211> 553
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 47
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn
145 150 155 160
Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr
210 215 220
Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly
225 230 235 240
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly
260 265 270
Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser
275 280 285
Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
290 295 300
Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu
305 310 315 320
Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu
325 330 335
Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu
340 345 350
Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp
355 360 365
Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu
370 375 380
Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu
385 390 395 400
Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu
405 410 415
Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser
420 425 430
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
435 440 445
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
450 455 460
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
465 470 475 480
Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val
485 490 495
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr
500 505 510
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
515 520 525
Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr
530 535 540
Val Ser Ser His His His His His His
545 550
<210> 48
<211> 553
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 48
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn
145 150 155 160
Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr
210 215 220
Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly
225 230 235 240
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln
260 265 270
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg
275 280 285
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser
290 295 300
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile
305 310 315 320
Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg
325 330 335
Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met
340 345 350
Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly
355 360 365
Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser
370 375 380
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser
385 390 395 400
Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro
405 410 415
Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu
420 425 430
Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro
435 440 445
Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala
450 455 460
Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu
465 470 475 480
Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro
485 490 495
Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly
500 505 510
Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile
515 520 525
Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser
530 535 540
Thr Leu Thr His His His His His His
545 550
<210> 49
<211> 553
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 49
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
165 170 175
Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr
195 200 205
Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
210 215 220
Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
260 265 270
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
275 280 285
Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
290 295 300
Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
305 310 315 320
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
325 330 335
Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly
340 345 350
Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro
355 360 365
Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn
370 375 380
Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
385 390 395 400
Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly
405 410 415
Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
420 425 430
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
435 440 445
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys
450 455 460
Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro
465 470 475 480
Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser
485 490 495
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
500 505 510
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
515 520 525
Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val
530 535 540
Glu Ile Lys His His His His His His
545 550
<210> 50
<211> 682
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 50
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp
20 25 30
Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu
130 135 140
His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
145 150 155 160
Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro
165 170 175
Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu
180 185 190
Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His
195 200 205
Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu
210 215 220
Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr
225 230 235 240
Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser
245 250 255
Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
260 265 270
Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
275 280 285
Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
290 295 300
Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys
305 310 315 320
Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu
325 330 335
Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
340 345 350
Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr
355 360 365
Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
420 425 430
Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
435 440 445
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
450 455 460
Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys
465 470 475 480
Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser
485 490 495
Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
500 505 510
Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
515 520 525
Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp
530 535 540
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
545 550 555 560
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
565 570 575
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
580 585 590
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys
595 600 605
Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr
610 615 620
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
625 630 635 640
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
645 650 655
Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys
660 665 670
Val Glu Ile Lys His His His His His His
675 680
<210> 51
<211> 667
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 51
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp
20 25 30
Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu
130 135 140
His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
145 150 155 160
Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro
165 170 175
Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu
180 185 190
Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His
195 200 205
Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu
210 215 220
Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr
225 230 235 240
Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser
245 250 255
Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
260 265 270
Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
275 280 285
Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
290 295 300
Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys
305 310 315 320
Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu
325 330 335
Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
340 345 350
Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr
355 360 365
Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
420 425 430
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
435 440 445
Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly
450 455 460
Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr
465 470 475 480
Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
485 490 495
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
500 505 510
Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr
515 520 525
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ser Gly Gly Pro Gly
530 535 540
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Asp Ile Gln Met Thr Gln
545 550 555 560
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
565 570 575
Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln
580 585 590
Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg
595 600 605
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
610 615 620
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
625 630 635 640
Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
645 650 655
Lys Val Glu Ile Lys His His His His His His
660 665
<210> 52
<211> 682
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 52
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
180 185 190
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
195 200 205
Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
210 215 220
Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr
225 230 235 240
Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu
245 250 255
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
260 265 270
Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly
275 280 285
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
305 310 315 320
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser
325 330 335
Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys
340 345 350
Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val
355 360 365
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
370 375 380
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
385 390 395 400
Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
405 410 415
Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
420 425 430
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
435 440 445
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
450 455 460
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
465 470 475 480
Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val
485 490 495
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr
500 505 510
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
515 520 525
Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr
530 535 540
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
545 550 555 560
Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala
565 570 575
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser
580 585 590
Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu
595 600 605
Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser
610 615 620
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val
625 630 635 640
Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr
645 650 655
Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val
660 665 670
Thr Val Ser Ser His His His His His His
675 680
<210> 53
<211> 393
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 53
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr
165 170 175
Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro
195 200 205
Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn
210 215 220
Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly
245 250 255
Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
260 265 270
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
275 280 285
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys
290 295 300
Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro
305 310 315 320
Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser
325 330 335
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
340 345 350
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
355 360 365
Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val
370 375 380
Glu Ile Lys His His His His His His
385 390
<210> 54
<211> 423
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 54
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
180 185 190
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
195 200 205
Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
210 215 220
Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr
225 230 235 240
Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu
245 250 255
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
260 265 270
Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly
275 280 285
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
305 310 315 320
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser
325 330 335
Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys
340 345 350
Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val
355 360 365
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
370 375 380
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
385 390 395 400
Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
405 410 415
Lys His His His His His His
420
<210> 55
<211> 682
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 55
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
180 185 190
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
195 200 205
Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
210 215 220
Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr
225 230 235 240
Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu
245 250 255
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
260 265 270
Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly
275 280 285
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
305 310 315 320
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser
325 330 335
Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys
340 345 350
Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val
355 360 365
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
370 375 380
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
385 390 395 400
Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
405 410 415
Lys Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser
420 425 430
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
435 440 445
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
450 455 460
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
465 470 475 480
Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val
485 490 495
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr
500 505 510
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
515 520 525
Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr
530 535 540
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
545 550 555 560
Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala
565 570 575
Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser
580 585 590
Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu
595 600 605
Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser
610 615 620
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val
625 630 635 640
Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr
645 650 655
Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val
660 665 670
Thr Val Ser Ser His His His His His His
675 680
<210> 56
<211> 682
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 56
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Ala Gln Ala Gly Gly
1 5 10 15
Ser Leu Ser Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Asn Ser
20 25 30
Val Met Ala Trp Tyr Arg Gln Thr Pro Gly Lys Gln Arg Glu Phe Val
35 40 45
Ala Ile Ile Asn Ser Val Gly Ser Thr Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Val Cys Asn
85 90 95
Arg Asn Phe Asp Arg Ile Tyr Trp Gly Gln Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly
115 120 125
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
130 135 140
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser
145 150 155 160
Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
165 170 175
Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val
180 185 190
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
195 200 205
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
210 215 220
Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
260 265 270
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln
275 280 285
Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala
290 295 300
Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro
305 310 315 320
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
325 330 335
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr
340 345 350
Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
355 360 365
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
370 375 380
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly
385 390 395 400
Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln
405 410 415
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg
420 425 430
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser
435 440 445
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile
450 455 460
Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg
465 470 475 480
Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met
485 490 495
Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly
500 505 510
Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser
515 520 525
Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala
530 535 540
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
545 550 555 560
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
565 570 575
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
580 585 590
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
595 600 605
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
610 615 620
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
625 630 635 640
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
645 650 655
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
660 665 670
Ser Thr Leu Thr His His His His His His
675 680
<210> 57
<211> 393
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 57
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn
145 150 155 160
Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr
210 215 220
Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Ser
225 230 235 240
Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro
245 250 255
Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu
260 265 270
Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro
275 280 285
Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala
290 295 300
Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu
305 310 315 320
Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro
325 330 335
Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly
340 345 350
Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile
355 360 365
Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser
370 375 380
Thr Leu Thr His His His His His His
385 390
<210> 58
<211> 423
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 58
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Leu Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn
145 150 155 160
Val Gly Thr Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr
210 215 220
Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly
225 230 235 240
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
245 250 255
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly
260 265 270
Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser
275 280 285
Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp
290 295 300
Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu
305 310 315 320
Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu
325 330 335
Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu
340 345 350
Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp
355 360 365
Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu
370 375 380
Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu
385 390 395 400
Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu
405 410 415
Thr His His His His His His
420
<210> 59
<211> 669
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 59
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp
20 25 30
Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu
130 135 140
His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
145 150 155 160
Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro
165 170 175
Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu
180 185 190
Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His
195 200 205
Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu
210 215 220
Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr
225 230 235 240
Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser
245 250 255
Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
260 265 270
Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
275 280 285
Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
290 295 300
Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys
305 310 315 320
Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu
325 330 335
Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
340 345 350
Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr
355 360 365
Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu
405 410 415
Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Thr Ser Val Lys Val
420 425 430
Ser Cys Lys Ala Ser Gly Tyr Ala Phe Thr Asn Tyr Leu Ile Glu Trp
435 440 445
Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Val Ile Asn
450 455 460
Pro Gly Ser Gly Gly Thr Asn Tyr Asn Glu Lys Phe Lys Gly Lys Ala
465 470 475 480
Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser
485 490 495
Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Phe Cys Ala Arg Trp Arg
500 505 510
Gly Asp Gly Tyr Tyr Ala Tyr Phe Asp Val Trp Gly Ala Gly Thr Thr
515 520 525
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
530 535 540
Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala
545 550 555 560
Val Ser Leu Gly Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser
565 570 575
Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro
580 585 590
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser
595 600 605
Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
610 615 620
Leu Asn Ile His Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys
625 630 635 640
Gln Gln Ser Asn Glu Asp Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu
645 650 655
Glu Ile Lys His His His His His His Glu Pro Glu Ala
660 665
<210> 60
<211> 669
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 60
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp
20 25 30
Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val
35 40 45
Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu
130 135 140
His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr
145 150 155 160
Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro
165 170 175
Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu
180 185 190
Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His
195 200 205
Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu
210 215 220
Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr
225 230 235 240
Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser
245 250 255
Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
260 265 270
Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
275 280 285
Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
290 295 300
Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys
305 310 315 320
Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu
325 330 335
Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
340 345 350
Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr
355 360 365
Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu
405 410 415
Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly Gln Arg Ala Thr
420 425 430
Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr
435 440 445
Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
450 455 460
Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala Arg Phe Ser Gly
465 470 475 480
Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val Glu Glu
485 490 495
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn Glu Asp Pro Tyr
500 505 510
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
515 520 525
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln
530 535 540
Ser Gly Ala Glu Leu Val Arg Pro Gly Thr Ser Val Lys Val Ser Cys
545 550 555 560
Lys Ala Ser Gly Tyr Ala Phe Thr Asn Tyr Leu Ile Glu Trp Val Lys
565 570 575
Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Val Ile Asn Pro Gly
580 585 590
Ser Gly Gly Thr Asn Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu
595 600 605
Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu
610 615 620
Thr Ser Asp Asp Ser Ala Val Tyr Phe Cys Ala Arg Trp Arg Gly Asp
625 630 635 640
Gly Tyr Tyr Ala Tyr Phe Asp Val Trp Gly Ala Gly Thr Thr Val Thr
645 650 655
Val Ser Ser His His His His His His Glu Pro Glu Ala
660 665
<210> 61
<211> 689
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 61
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln
165 170 175
Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Thr Ser Val Lys
180 185 190
Val Ser Cys Lys Ala Ser Gly Tyr Ala Phe Thr Asn Tyr Leu Ile Glu
195 200 205
Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Val Ile
210 215 220
Asn Pro Gly Ser Gly Gly Thr Asn Tyr Asn Glu Lys Phe Lys Gly Lys
225 230 235 240
Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu
245 250 255
Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Phe Cys Ala Arg Trp
260 265 270
Arg Gly Asp Gly Tyr Tyr Ala Tyr Phe Asp Val Trp Gly Ala Gly Thr
275 280 285
Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
290 295 300
Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu
305 310 315 320
Ala Val Ser Leu Gly Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln
325 330 335
Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys
340 345 350
Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu
355 360 365
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
370 375 380
Thr Leu Asn Ile His Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr
385 390 395 400
Cys Gln Gln Ser Asn Glu Asp Pro Tyr Thr Phe Gly Gly Gly Thr Lys
405 410 415
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
420 425 430
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
435 440 445
Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
450 455 460
Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
465 470 475 480
Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala
485 490 495
Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr
500 505 510
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val
515 520 525
Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr
530 535 540
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
545 550 555 560
Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu
565 570 575
Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg
580 585 590
Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys
595 600 605
Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr
610 615 620
Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
625 630 635 640
Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly
645 650 655
Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly
660 665 670
Thr Gln Val Thr Val Ser Ser His His His His His His Glu Pro Glu
675 680 685
Ala
<210> 62
<211> 689
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 62
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val
165 170 175
Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly Gln Arg Ala
180 185 190
Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser
195 200 205
Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu
210 215 220
Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala Arg Phe Ser
225 230 235 240
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val Glu
245 250 255
Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn Glu Asp Pro
260 265 270
Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly
275 280 285
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
290 295 300
Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Thr Ser Val Lys Val Ser
305 310 315 320
Cys Lys Ala Ser Gly Tyr Ala Phe Thr Asn Tyr Leu Ile Glu Trp Val
325 330 335
Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Val Ile Asn Pro
340 345 350
Gly Ser Gly Gly Thr Asn Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr
355 360 365
Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser
370 375 380
Leu Thr Ser Asp Asp Ser Ala Val Tyr Phe Cys Ala Arg Trp Arg Gly
385 390 395 400
Asp Gly Tyr Tyr Ala Tyr Phe Asp Val Trp Gly Ala Gly Thr Thr Val
405 410 415
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
420 425 430
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
435 440 445
Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
450 455 460
Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
465 470 475 480
Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala
485 490 495
Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr
500 505 510
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val
515 520 525
Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr
530 535 540
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
545 550 555 560
Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu
565 570 575
Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg
580 585 590
Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly Lys
595 600 605
Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser Tyr
610 615 620
Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys
625 630 635 640
Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly
645 650 655
Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys Gly
660 665 670
Thr Gln Val Thr Val Ser Ser His His His His His His Glu Pro Glu
675 680 685
Ala
<210> 63
<211> 272
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность IL2Ra"
<400> 63
Met Asp Ser Tyr Leu Leu Met Trp Gly Leu Leu Thr Phe Ile Met Val
1 5 10 15
Pro Gly Cys Gln Ala Glu Leu Cys Asp Asp Asp Pro Pro Glu Ile Pro
20 25 30
His Ala Thr Phe Lys Ala Met Ala Tyr Lys Glu Gly Thr Met Leu Asn
35 40 45
Cys Glu Cys Lys Arg Gly Phe Arg Arg Ile Lys Ser Gly Ser Leu Tyr
50 55 60
Met Leu Cys Thr Gly Asn Ser Ser His Ser Ser Trp Asp Asn Gln Cys
65 70 75 80
Gln Cys Thr Ser Ser Ala Thr Arg Asn Thr Thr Lys Gln Val Thr Pro
85 90 95
Gln Pro Glu Glu Gln Lys Glu Arg Lys Thr Thr Glu Met Gln Ser Pro
100 105 110
Met Gln Pro Val Asp Gln Ala Ser Leu Pro Gly His Cys Arg Glu Pro
115 120 125
Pro Pro Trp Glu Asn Glu Ala Thr Glu Arg Ile Tyr His Phe Val Val
130 135 140
Gly Gln Met Val Tyr Tyr Gln Cys Val Gln Gly Tyr Arg Ala Leu His
145 150 155 160
Arg Gly Pro Ala Glu Ser Val Cys Lys Met Thr His Gly Lys Thr Arg
165 170 175
Trp Thr Gln Pro Gln Leu Ile Cys Thr Gly Glu Met Glu Thr Ser Gln
180 185 190
Phe Pro Gly Glu Glu Lys Pro Gln Ala Ser Pro Glu Gly Arg Pro Glu
195 200 205
Ser Glu Thr Ser Cys Leu Val Thr Thr Thr Asp Phe Gln Ile Gln Thr
210 215 220
Glu Met Ala Ala Thr Met Glu Thr Ser Ile Phe Thr Thr Glu Tyr Gln
225 230 235 240
Val Ala Val Ala Gly Cys Val Phe Leu Leu Ile Ser Val Leu Leu Leu
245 250 255
Ser Gly Leu Thr Trp Gln Arg Arg Gln Arg Lys Ser Arg Arg Thr Ile
260 265 270
<210> 64
<211> 551
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность IL2Rb"
<400> 64
Met Ala Ala Pro Ala Leu Ser Trp Arg Leu Pro Leu Leu Ile Leu Leu
1 5 10 15
Leu Pro Leu Ala Thr Ser Trp Ala Ser Ala Ala Val Asn Gly Thr Ser
20 25 30
Gln Phe Thr Cys Phe Tyr Asn Ser Arg Ala Asn Ile Ser Cys Val Trp
35 40 45
Ser Gln Asp Gly Ala Leu Gln Asp Thr Ser Cys Gln Val His Ala Trp
50 55 60
Pro Asp Arg Arg Arg Trp Asn Gln Thr Cys Glu Leu Leu Pro Val Ser
65 70 75 80
Gln Ala Ser Trp Ala Cys Asn Leu Ile Leu Gly Ala Pro Asp Ser Gln
85 90 95
Lys Leu Thr Thr Val Asp Ile Val Thr Leu Arg Val Leu Cys Arg Glu
100 105 110
Gly Val Arg Trp Arg Val Met Ala Ile Gln Asp Phe Lys Pro Phe Glu
115 120 125
Asn Leu Arg Leu Met Ala Pro Ile Ser Leu Gln Val Val His Val Glu
130 135 140
Thr His Arg Cys Asn Ile Ser Trp Glu Ile Ser Gln Ala Ser His Tyr
145 150 155 160
Phe Glu Arg His Leu Glu Phe Glu Ala Arg Thr Leu Ser Pro Gly His
165 170 175
Thr Trp Glu Glu Ala Pro Leu Leu Thr Leu Lys Gln Lys Gln Glu Trp
180 185 190
Ile Cys Leu Glu Thr Leu Thr Pro Asp Thr Gln Tyr Glu Phe Gln Val
195 200 205
Arg Val Lys Pro Leu Gln Gly Glu Phe Thr Thr Trp Ser Pro Trp Ser
210 215 220
Gln Pro Leu Ala Phe Arg Thr Lys Pro Ala Ala Leu Gly Lys Asp Thr
225 230 235 240
Ile Pro Trp Leu Gly His Leu Leu Val Gly Leu Ser Gly Ala Phe Gly
245 250 255
Phe Ile Ile Leu Val Tyr Leu Leu Ile Asn Cys Arg Asn Thr Gly Pro
260 265 270
Trp Leu Lys Lys Val Leu Lys Cys Asn Thr Pro Asp Pro Ser Lys Phe
275 280 285
Phe Ser Gln Leu Ser Ser Glu His Gly Gly Asp Val Gln Lys Trp Leu
290 295 300
Ser Ser Pro Phe Pro Ser Ser Ser Phe Ser Pro Gly Gly Leu Ala Pro
305 310 315 320
Glu Ile Ser Pro Leu Glu Val Leu Glu Arg Asp Lys Val Thr Gln Leu
325 330 335
Leu Leu Gln Gln Asp Lys Val Pro Glu Pro Ala Ser Leu Ser Ser Asn
340 345 350
His Ser Leu Thr Ser Cys Phe Thr Asn Gln Gly Tyr Phe Phe Phe His
355 360 365
Leu Pro Asp Ala Leu Glu Ile Glu Ala Cys Gln Val Tyr Phe Thr Tyr
370 375 380
Asp Pro Tyr Ser Glu Glu Asp Pro Asp Glu Gly Val Ala Gly Ala Pro
385 390 395 400
Thr Gly Ser Ser Pro Gln Pro Leu Gln Pro Leu Ser Gly Glu Asp Asp
405 410 415
Ala Tyr Cys Thr Phe Pro Ser Arg Asp Asp Leu Leu Leu Phe Ser Pro
420 425 430
Ser Leu Leu Gly Gly Pro Ser Pro Pro Ser Thr Ala Pro Gly Gly Ser
435 440 445
Gly Ala Gly Glu Glu Arg Met Pro Pro Ser Leu Gln Glu Arg Val Pro
450 455 460
Arg Asp Trp Asp Pro Gln Pro Leu Gly Pro Pro Thr Pro Gly Val Pro
465 470 475 480
Asp Leu Val Asp Phe Gln Pro Pro Pro Glu Leu Val Leu Arg Glu Ala
485 490 495
Gly Glu Glu Val Pro Asp Ala Gly Pro Arg Glu Gly Val Ser Phe Pro
500 505 510
Trp Ser Arg Pro Pro Gly Gln Gly Glu Phe Arg Ala Leu Asn Ala Arg
515 520 525
Leu Pro Leu Asn Thr Asp Ala Tyr Leu Ser Leu Gln Glu Leu Gln Gly
530 535 540
Gln Asp Pro Thr His Leu Val
545 550
<210> 65
<211> 369
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Последовательность IL2Rg"
<400> 65
Met Leu Lys Pro Ser Leu Pro Phe Thr Ser Leu Leu Phe Leu Gln Leu
1 5 10 15
Pro Leu Leu Gly Val Gly Leu Asn Thr Thr Ile Leu Thr Pro Asn Gly
20 25 30
Asn Glu Asp Thr Thr Ala Asp Phe Phe Leu Thr Thr Met Pro Thr Asp
35 40 45
Ser Leu Ser Val Ser Thr Leu Pro Leu Pro Glu Val Gln Cys Phe Val
50 55 60
Phe Asn Val Glu Tyr Met Asn Cys Thr Trp Asn Ser Ser Ser Glu Pro
65 70 75 80
Gln Pro Thr Asn Leu Thr Leu His Tyr Trp Tyr Lys Asn Ser Asp Asn
85 90 95
Asp Lys Val Gln Lys Cys Ser His Tyr Leu Phe Ser Glu Glu Ile Thr
100 105 110
Ser Gly Cys Gln Leu Gln Lys Lys Glu Ile His Leu Tyr Gln Thr Phe
115 120 125
Val Val Gln Leu Gln Asp Pro Arg Glu Pro Arg Arg Gln Ala Thr Gln
130 135 140
Met Leu Lys Leu Gln Asn Leu Val Ile Pro Trp Ala Pro Glu Asn Leu
145 150 155 160
Thr Leu His Lys Leu Ser Glu Ser Gln Leu Glu Leu Asn Trp Asn Asn
165 170 175
Arg Phe Leu Asn His Cys Leu Glu His Leu Val Gln Tyr Arg Thr Asp
180 185 190
Trp Asp His Ser Trp Thr Glu Gln Ser Val Asp Tyr Arg His Lys Phe
195 200 205
Ser Leu Pro Ser Val Asp Gly Gln Lys Arg Tyr Thr Phe Arg Val Arg
210 215 220
Ser Arg Phe Asn Pro Leu Cys Gly Ser Ala Gln His Trp Ser Glu Trp
225 230 235 240
Ser His Pro Ile His Trp Gly Ser Asn Thr Ser Lys Glu Asn Pro Phe
245 250 255
Leu Phe Ala Leu Glu Ala Val Val Ile Ser Val Gly Ser Met Gly Leu
260 265 270
Ile Ile Ser Leu Leu Cys Val Tyr Phe Trp Leu Glu Arg Thr Met Pro
275 280 285
Arg Ile Pro Thr Leu Lys Asn Leu Glu Asp Leu Val Thr Glu Tyr His
290 295 300
Gly Asn Phe Ser Ala Trp Ser Gly Val Ser Lys Gly Leu Ala Glu Ser
305 310 315 320
Leu Gln Pro Asp Tyr Ser Glu Arg Leu Cys Leu Val Ser Glu Ile Pro
325 330 335
Pro Lys Gly Gly Ala Leu Gly Glu Gly Pro Gly Ala Ser Pro Cys Asn
340 345 350
Gln His Ser Pro Tyr Trp Ala Pro Pro Cys Tyr Thr Leu Lys Pro Glu
355 360 365
Thr
<210> 66
<211> 276
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 66
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr
65 70 75 80
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
85 90 95
Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Val Gly Ala Phe Arg Pro Tyr
115 120 125
Arg Lys His Glu Trp Gly Gln Gly Thr Leu Val Thr Val Ser Arg Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser
145 150 155 160
Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val
165 170 175
Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Lys
195 200 205
Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser Ser
210 215 220
Gly Asn Thr Ala Ser Leu Thr Thr Thr Gly Ala Gln Ala Glu Asp Glu
225 230 235 240
Ala Asp Tyr Tyr Cys Asn Ser Ser Pro Phe Glu His Asn Leu Val Val
245 250 255
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu His His His His His His
260 265 270
Glu Pro Glu Ala
275
<210> 67
<211> 674
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 67
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
210 215 220
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
225 230 235 240
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
245 250 255
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
260 265 270
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
275 280 285
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
290 295 300
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
305 310 315 320
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
325 330 335
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
340 345 350
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
355 360 365
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
370 375 380
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
385 390 395 400
Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
420 425 430
Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala
435 440 445
Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala
450 455 460
Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg
465 470 475 480
Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
485 490 495
Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
500 505 510
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val
515 520 525
Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
530 535 540
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
545 550 555 560
Ser Gly Gly Gly Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys
565 570 575
Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg
580 585 590
Gln Ala Pro Gly Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly
595 600 605
Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
610 615 620
Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys
625 630 635 640
Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp
645 650 655
Tyr Trp Gly Lys Gly Thr Gln Val Thr Val Ser Ser His His His His
660 665 670
His His
<210> 68
<211> 674
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 68
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly
130 135 140
Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly
145 150 155 160
Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser
165 170 175
Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro
180 185 190
Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp
195 200 205
Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
210 215 220
Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu
225 230 235 240
Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser
245 250 255
Ser Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro
260 265 270
Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser
325 330 335
Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala
355 360 365
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala
370 375 380
Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala
450 455 460
Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly
500 505 510
Gly Gly Thr Lys Val Glu Ile Lys Ser Gly Gly Pro Gly Pro Ala Gly
515 520 525
Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
530 535 540
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
545 550 555 560
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
565 570 575
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
580 585 590
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
595 600 605
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
610 615 620
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
625 630 635 640
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
645 650 655
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr His His His His
660 665 670
His His
<210> 69
<211> 425
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 69
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Leu Cys Asp Asp Asp Pro Pro Glu Ile
20 25 30
Pro His Ala Thr Phe Lys Ala Met Ala Tyr Lys Glu Gly Thr Met Leu
35 40 45
Asn Cys Glu Cys Lys Arg Gly Phe Arg Arg Ile Lys Ser Gly Ser Leu
50 55 60
Tyr Met Leu Cys Thr Gly Asn Ser Ser His Ser Ser Trp Asp Asn Gln
65 70 75 80
Cys Gln Cys Thr Ser Ser Ala Thr Arg Asn Thr Thr Lys Gln Val Thr
85 90 95
Pro Gln Pro Glu Glu Gln Lys Glu Arg Lys Thr Thr Glu Met Gln Ser
100 105 110
Pro Met Gln Pro Val Asp Gln Ala Ser Leu Pro Gly His Cys Arg Glu
115 120 125
Pro Pro Pro Trp Glu Asn Glu Ala Thr Glu Arg Ile Tyr His Phe Val
130 135 140
Val Gly Gln Met Val Tyr Tyr Gln Cys Val Gln Gly Tyr Arg Ala Leu
145 150 155 160
His Arg Gly Pro Ala Glu Ser Val Cys Lys Met Thr His Gly Lys Thr
165 170 175
Arg Trp Thr Gln Pro Gln Leu Ile Cys Thr Gly Glu Met Glu Thr Ser
180 185 190
Gln Phe Pro Gly Glu Glu Lys Pro Gln Ala Ser Pro Glu Gly Arg Pro
195 200 205
Glu Ser Glu Thr Ser Cys Leu Val Thr Thr Thr Asp Phe Gln Ile Gln
210 215 220
Thr Glu Met Ala Ala Thr Met Glu Thr Ser Ile Phe Thr Thr Glu Tyr
225 230 235 240
Gln Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser
260 265 270
Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro
275 280 285
Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu
290 295 300
Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro
305 310 315 320
Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala
325 330 335
Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu
340 345 350
Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro
355 360 365
Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly
370 375 380
Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile
385 390 395 400
Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser
405 410 415
Thr Leu Thr His His His His His His
420 425
<210> 70
<211> 425
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 70
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Gly Gly Gly Gly Ser Glu Leu Cys Asp Asp Asp Pro Pro
195 200 205
Glu Ile Pro His Ala Thr Phe Lys Ala Met Ala Tyr Lys Glu Gly Thr
210 215 220
Met Leu Asn Cys Glu Cys Lys Arg Gly Phe Arg Arg Ile Lys Ser Gly
225 230 235 240
Ser Leu Tyr Met Leu Cys Thr Gly Asn Ser Ser His Ser Ser Trp Asp
245 250 255
Asn Gln Cys Gln Cys Thr Ser Ser Ala Thr Arg Asn Thr Thr Lys Gln
260 265 270
Val Thr Pro Gln Pro Glu Glu Gln Lys Glu Arg Lys Thr Thr Glu Met
275 280 285
Gln Ser Pro Met Gln Pro Val Asp Gln Ala Ser Leu Pro Gly His Cys
290 295 300
Arg Glu Pro Pro Pro Trp Glu Asn Glu Ala Thr Glu Arg Ile Tyr His
305 310 315 320
Phe Val Val Gly Gln Met Val Tyr Tyr Gln Cys Val Gln Gly Tyr Arg
325 330 335
Ala Leu His Arg Gly Pro Ala Glu Ser Val Cys Lys Met Thr His Gly
340 345 350
Lys Thr Arg Trp Thr Gln Pro Gln Leu Ile Cys Thr Gly Glu Met Glu
355 360 365
Thr Ser Gln Phe Pro Gly Glu Glu Lys Pro Gln Ala Ser Pro Glu Gly
370 375 380
Arg Pro Glu Ser Glu Thr Ser Cys Leu Val Thr Thr Thr Asp Phe Gln
385 390 395 400
Ile Gln Thr Glu Met Ala Ala Thr Met Glu Thr Ser Ile Phe Thr Thr
405 410 415
Glu Tyr Gln His His His His His His
420 425
<210> 71
<211> 555
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 71
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
65 70 75 80
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
85 90 95
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Glu Leu Cys Asp Asp Asp Pro Pro
145 150 155 160
Glu Ile Pro His Ala Thr Phe Lys Ala Met Ala Tyr Lys Glu Gly Thr
165 170 175
Met Leu Asn Cys Glu Cys Lys Arg Gly Phe Arg Arg Ile Lys Ser Gly
180 185 190
Ser Leu Tyr Met Leu Cys Thr Gly Asn Ser Ser His Ser Ser Trp Asp
195 200 205
Asn Gln Cys Gln Cys Thr Ser Ser Ala Thr Arg Asn Thr Thr Lys Gln
210 215 220
Val Thr Pro Gln Pro Glu Glu Gln Lys Glu Arg Lys Thr Thr Glu Met
225 230 235 240
Gln Ser Pro Met Gln Pro Val Asp Gln Ala Ser Leu Pro Gly His Cys
245 250 255
Arg Glu Pro Pro Pro Trp Glu Asn Glu Ala Thr Glu Arg Ile Tyr His
260 265 270
Phe Val Val Gly Gln Met Val Tyr Tyr Gln Cys Val Gln Gly Tyr Arg
275 280 285
Ala Leu His Arg Gly Pro Ala Glu Ser Val Cys Lys Met Thr His Gly
290 295 300
Lys Thr Arg Trp Thr Gln Pro Gln Leu Ile Cys Thr Gly Glu Met Glu
305 310 315 320
Thr Ser Gln Phe Pro Gly Glu Glu Lys Pro Gln Ala Ser Pro Glu Gly
325 330 335
Arg Pro Glu Ser Glu Thr Ser Cys Leu Val Thr Thr Thr Asp Phe Gln
340 345 350
Ile Gln Thr Glu Met Ala Ala Thr Met Glu Thr Ser Ile Phe Thr Thr
355 360 365
Glu Tyr Gln Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
370 375 380
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
385 390 395 400
Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser
405 410 415
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
420 425 430
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
435 440 445
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
450 455 460
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
465 470 475 480
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
485 490 495
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
500 505 510
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
515 520 525
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
530 535 540
Ile Ser Thr Leu Thr His His His His His His
545 550 555
<210> 72
<211> 555
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 72
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Gly Gly Gly Gly Ser Glu Leu Cys Asp Asp Asp Pro Pro
195 200 205
Glu Ile Pro His Ala Thr Phe Lys Ala Met Ala Tyr Lys Glu Gly Thr
210 215 220
Met Leu Asn Cys Glu Cys Lys Arg Gly Phe Arg Arg Ile Lys Ser Gly
225 230 235 240
Ser Leu Tyr Met Leu Cys Thr Gly Asn Ser Ser His Ser Ser Trp Asp
245 250 255
Asn Gln Cys Gln Cys Thr Ser Ser Ala Thr Arg Asn Thr Thr Lys Gln
260 265 270
Val Thr Pro Gln Pro Glu Glu Gln Lys Glu Arg Lys Thr Thr Glu Met
275 280 285
Gln Ser Pro Met Gln Pro Val Asp Gln Ala Ser Leu Pro Gly His Cys
290 295 300
Arg Glu Pro Pro Pro Trp Glu Asn Glu Ala Thr Glu Arg Ile Tyr His
305 310 315 320
Phe Val Val Gly Gln Met Val Tyr Tyr Gln Cys Val Gln Gly Tyr Arg
325 330 335
Ala Leu His Arg Gly Pro Ala Glu Ser Val Cys Lys Met Thr His Gly
340 345 350
Lys Thr Arg Trp Thr Gln Pro Gln Leu Ile Cys Thr Gly Glu Met Glu
355 360 365
Thr Ser Gln Phe Pro Gly Glu Glu Lys Pro Gln Ala Ser Pro Glu Gly
370 375 380
Arg Pro Glu Ser Glu Thr Ser Cys Leu Val Thr Thr Thr Asp Phe Gln
385 390 395 400
Ile Gln Thr Glu Met Ala Ala Thr Met Glu Thr Ser Ile Phe Thr Thr
405 410 415
Glu Tyr Gln Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
435 440 445
Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
450 455 460
Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
465 470 475 480
Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu
485 490 495
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr
500 505 510
Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr
515 520 525
Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu
530 535 540
Val Thr Val Ser Ser His His His His His His
545 550 555
<210> 73
<211> 555
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 73
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Gly Gly Gly Gly Ser Glu Leu Cys Asp Asp Asp Pro Pro
195 200 205
Glu Ile Pro His Ala Thr Phe Lys Ala Met Ala Tyr Lys Glu Gly Thr
210 215 220
Met Leu Asn Cys Glu Cys Lys Arg Gly Phe Arg Arg Ile Lys Ser Gly
225 230 235 240
Ser Leu Tyr Met Leu Cys Thr Gly Asn Ser Ser His Ser Ser Trp Asp
245 250 255
Asn Gln Cys Gln Cys Thr Ser Ser Ala Thr Arg Asn Thr Thr Lys Gln
260 265 270
Val Thr Pro Gln Pro Glu Glu Gln Lys Glu Arg Lys Thr Thr Glu Met
275 280 285
Gln Ser Pro Met Gln Pro Val Asp Gln Ala Ser Leu Pro Gly His Cys
290 295 300
Arg Glu Pro Pro Pro Trp Glu Asn Glu Ala Thr Glu Arg Ile Tyr His
305 310 315 320
Phe Val Val Gly Gln Met Val Tyr Tyr Gln Cys Val Gln Gly Tyr Arg
325 330 335
Ala Leu His Arg Gly Pro Ala Glu Ser Val Cys Lys Met Thr His Gly
340 345 350
Lys Thr Arg Trp Thr Gln Pro Gln Leu Ile Cys Thr Gly Glu Met Glu
355 360 365
Thr Ser Gln Phe Pro Gly Glu Glu Lys Pro Gln Ala Ser Pro Glu Gly
370 375 380
Arg Pro Glu Ser Glu Thr Ser Cys Leu Val Thr Thr Thr Asp Phe Gln
385 390 395 400
Ile Gln Thr Glu Met Ala Ala Thr Met Glu Thr Ser Ile Phe Thr Thr
405 410 415
Glu Tyr Gln Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro
420 425 430
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
435 440 445
Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser
450 455 460
Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
465 470 475 480
Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu
485 490 495
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr
500 505 510
Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr
515 520 525
Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu
530 535 540
Val Thr Val Ser Ser His His His His His His
545 550 555
<210> 74
<211> 575
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 74
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
65 70 75 80
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
85 90 95
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala
130 135 140
Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly
145 150 155 160
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
165 170 175
Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala
180 185 190
Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr
195 200 205
Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp
210 215 220
Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
225 230 235 240
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu
245 250 255
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly
260 265 270
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
275 280 285
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
290 295 300
Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr
305 310 315 320
Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser
325 330 335
Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
340 345 350
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
355 360 365
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly
370 375 380
Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly
385 390 395 400
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
405 410 415
Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
420 425 430
Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu
435 440 445
Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile
450 455 460
Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe
465 470 475 480
Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu
485 490 495
Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys
500 505 510
Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile
515 520 525
Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala
530 535 540
Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe
545 550 555 560
Cys Gln Ser Ile Ile Ser Thr Leu Thr His His His His His His
565 570 575
<210> 75
<211> 704
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 75
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
195 200 205
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
210 215 220
Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala
225 230 235 240
Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr
245 250 255
Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp
260 265 270
Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
275 280 285
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu
290 295 300
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ser Gly Gly
305 310 315 320
Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Asp Ile Gln Met
325 330 335
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
340 345 350
Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr
355 360 365
Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser
370 375 380
Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
385 390 395 400
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
405 410 415
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly
420 425 430
Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly
435 440 445
Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
450 455 460
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
465 470 475 480
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
485 490 495
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
500 505 510
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
515 520 525
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
545 550 555 560
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
565 570 575
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
580 585 590
Gly Gly Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
595 600 605
Ser Gly Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala
610 615 620
Pro Gly Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr
625 630 635 640
Ile Ser Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
645 650 655
Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu
660 665 670
Asp Thr Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp
675 680 685
Gly Lys Gly Thr Gln Val Thr Val Ser Ser His His His His His His
690 695 700
<210> 76
<211> 689
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 76
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
435 440 445
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
450 455 460
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp
465 470 475 480
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp
485 490 495
Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr
500 505 510
Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser
515 520 525
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn
530 535 540
Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
565 570 575
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
580 585 590
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
595 600 605
Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile
610 615 620
Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
625 630 635 640
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
645 650 655
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr
660 665 670
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His
675 680 685
His
<210> 77
<211> 545
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 77
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
210 215 220
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
225 230 235 240
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
245 250 255
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
260 265 270
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
275 280 285
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
290 295 300
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
305 310 315 320
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
325 330 335
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
340 345 350
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
355 360 365
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
370 375 380
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
385 390 395 400
Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
420 425 430
Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala
435 440 445
Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala
450 455 460
Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg
465 470 475 480
Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
485 490 495
Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
500 505 510
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val
515 520 525
Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser His His His His His
530 535 540
His
545
<210> 78
<211> 575
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 78
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
195 200 205
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
210 215 220
Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala
225 230 235 240
Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr
245 250 255
Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp
260 265 270
Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
275 280 285
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu
290 295 300
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly
305 310 315 320
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
325 330 335
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
340 345 350
Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr
355 360 365
Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser
370 375 380
Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
385 390 395 400
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
405 410 415
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly
420 425 430
Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly
435 440 445
Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
450 455 460
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
465 470 475 480
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
485 490 495
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
500 505 510
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
515 520 525
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
545 550 555 560
Gln Gly Thr Leu Val Thr Val Ser Ser His His His His His His
565 570 575
<210> 79
<211> 421
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 79
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
65 70 75 80
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
85 90 95
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala
130 135 140
Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys
145 150 155 160
Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile
165 170 175
Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu
180 185 190
Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu
195 200 205
Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu
210 215 220
Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn
225 230 235 240
Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met
245 250 255
Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg
260 265 270
Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly
275 280 285
Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu
290 295 300
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu
305 310 315 320
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp
325 330 335
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser
340 345 350
Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe
355 360 365
Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn
370 375 380
Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly
385 390 395 400
Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser His
405 410 415
His His His His His
420
<210> 80
<211> 806
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 80
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Ser Gly Ser Gly Ser Gly Ser
130 135 140
Gly Ser Gly Ser Gly Ser Gly Ser Glu Val Gln Leu Val Glu Ser Gly
145 150 155 160
Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala
165 170 175
Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala
180 185 190
Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg
195 200 205
Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
210 215 220
Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
225 230 235 240
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val
245 250 255
Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Ser Gly Ser Gly
260 265 270
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gln Val Gln Leu Gln
275 280 285
Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser
290 295 300
Cys Ala Ala Ser Gly Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr
305 310 315 320
Arg Gln Ala Pro Gly Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg
325 330 335
Gly Gly Thr Ile Ser Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile
340 345 350
Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu
355 360 365
Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr
370 375 380
Asp Tyr Trp Gly Lys Gly Thr Gln Val Thr Val Ser Ser Gly Ser Gly
385 390 395 400
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Glu Val Gln
405 410 415
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg
420 425 430
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala
435 440 445
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile
450 455 460
Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe
465 470 475 480
Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn
485 490 495
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser
500 505 510
Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
515 520 525
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
530 535 540
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
545 550 555 560
Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr
565 570 575
Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu
580 585 590
Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser
595 600 605
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
610 615 620
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro
625 630 635 640
Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Ser Gly Gly Pro
645 650 655
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser
660 665 670
Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu
675 680 685
Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr
690 695 700
Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu
705 710 715 720
Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val
725 730 735
Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu
740 745 750
Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr
755 760 765
Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe
770 775 780
Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr
785 790 795 800
His His His His His His
805
<210> 81
<211> 676
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 81
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Ser Gly Ser Gly Ser Gly Ser
130 135 140
Gly Ser Gly Ser Gly Ser Gly Ser Glu Val Gln Leu Val Glu Ser Gly
145 150 155 160
Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala
165 170 175
Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala
180 185 190
Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg
195 200 205
Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
210 215 220
Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
225 230 235 240
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val
245 250 255
Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Ser Gly Ser Gly
260 265 270
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Glu Val Gln Leu Val
275 280 285
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
290 295 300
Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val
305 310 315 320
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser
325 330 335
Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile
340 345 350
Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu
355 360 365
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp
370 375 380
Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
405 410 415
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
420 425 430
Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val
435 440 445
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr
450 455 460
Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
465 470 475 480
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
485 490 495
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr
500 505 510
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Ser Gly Gly Pro Gly Pro
515 520 525
Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr
530 535 540
Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met
545 550 555 560
Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met
565 570 575
Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His
580 585 590
Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn
595 600 605
Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser
610 615 620
Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe
625 630 635 640
Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn
645 650 655
Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr His His
660 665 670
His His His His
675
<210> 82
<211> 421
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 82
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Ser Gly Ser Gly Ser Gly Ser
130 135 140
Gly Ser Gly Ser Gly Ser Gly Ser Glu Val Gln Leu Val Glu Ser Gly
145 150 155 160
Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala
165 170 175
Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala
180 185 190
Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg
195 200 205
Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
210 215 220
Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
225 230 235 240
Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val
245 250 255
Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly
260 265 270
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser
275 280 285
Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln
290 295 300
Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg
305 310 315 320
Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys
325 330 335
His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu
340 345 350
Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile
355 360 365
Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr
370 375 380
Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu
385 390 395 400
Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr His
405 410 415
His His His His His
420
<210> 83
<211> 420
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 83
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly
130 135 140
Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser His His
405 410 415
His His His His
420
<210> 84
<211> 550
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 84
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly
145 150 155 160
Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser
165 170 175
Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro
180 185 190
Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp
195 200 205
Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
210 215 220
Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu
225 230 235 240
Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser
245 250 255
Ser Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro
260 265 270
Ala Gly Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr
275 280 285
Lys Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met
290 295 300
Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met
305 310 315 320
Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His
325 330 335
Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn
340 345 350
Leu Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser
355 360 365
Asn Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe
370 375 380
Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn
385 390 395 400
Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly
405 410 415
Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln
420 425 430
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg
435 440 445
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser
450 455 460
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile
465 470 475 480
Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg
485 490 495
Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met
500 505 510
Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly
515 520 525
Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser
530 535 540
His His His His His His
545 550
<210> 85
<211> 420
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 85
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser His His
405 410 415
His His His His
420
<210> 86
<211> 290
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 86
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr His His His His
275 280 285
His His
290
<210> 87
<211> 291
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 87
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser His His His
275 280 285
His His His
290
<210> 88
<211> 689
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 88
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly
130 135 140
Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
435 440 445
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
450 455 460
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp
465 470 475 480
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp
485 490 495
Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr
500 505 510
Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser
515 520 525
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn
530 535 540
Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
565 570 575
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
580 585 590
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
595 600 605
Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile
610 615 620
Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
625 630 635 640
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
645 650 655
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr
660 665 670
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His
675 680 685
His
<210> 89
<211> 704
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 89
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
180 185 190
Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
195 200 205
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
210 215 220
Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala
225 230 235 240
Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr
245 250 255
Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp
260 265 270
Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu
275 280 285
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu
290 295 300
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly
305 310 315 320
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
325 330 335
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
340 345 350
Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr
355 360 365
Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser
370 375 380
Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
385 390 395 400
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
405 410 415
Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly
420 425 430
Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly
435 440 445
Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
450 455 460
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
465 470 475 480
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
485 490 495
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
500 505 510
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
515 520 525
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
545 550 555 560
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
565 570 575
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
580 585 590
Gly Gly Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala
595 600 605
Ser Gly Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr
610 615 620
Pro Gly Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser
625 630 635 640
Thr Asn Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
645 650 655
Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu
660 665 670
Asp Thr Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp
675 680 685
Gly Gln Gly Thr Gln Val Thr Val Ser Ser His His His His His His
690 695 700
<210> 90
<211> 674
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 90
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr Pro Gly
50 55 60
Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser Thr Asn
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu Asp Thr
100 105 110
Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp Gly Gln
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Ala Pro Thr Ser Ser Ser Thr Lys
130 135 140
Lys Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile
145 150 155 160
Leu Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu
165 170 175
Thr Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu
180 185 190
Gln Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu
195 200 205
Ala Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn
210 215 220
Ile Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met
225 230 235 240
Cys Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg
245 250 255
Trp Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly
260 265 270
Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu
275 280 285
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu
290 295 300
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp
305 310 315 320
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser
325 330 335
Gly Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe
340 345 350
Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn
355 360 365
Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly
370 375 380
Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln
420 425 430
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg
435 440 445
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala
450 455 460
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile
465 470 475 480
Asp Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe
485 490 495
Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn
500 505 510
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser
515 520 525
Asn Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
530 535 540
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
545 550 555 560
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
565 570 575
Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr
580 585 590
Asn Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu
595 600 605
Ile Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser
610 615 620
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
625 630 635 640
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro
645 650 655
Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His
660 665 670
His His
<210> 91
<211> 704
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 91
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr
65 70 75 80
Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
145 150 155 160
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
165 170 175
Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg
195 200 205
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
245 250 255
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
275 280 285
Gly Gly Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro
290 295 300
Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu
305 310 315 320
Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn
325 330 335
Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met
340 345 350
Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu
355 360 365
Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe
370 375 380
His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu
385 390 395 400
Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu
405 410 415
Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln
420 425 430
Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly Pro Ala Gly Met
435 440 445
Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
450 455 460
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
465 470 475 480
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
485 490 495
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
500 505 510
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
515 520 525
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
545 550 555 560
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
565 570 575
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
580 585 590
Gly Gly Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala
595 600 605
Ser Gly Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr
610 615 620
Pro Gly Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser
625 630 635 640
Thr Asn Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
645 650 655
Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu
660 665 670
Asp Thr Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp
675 680 685
Gly Gln Gly Thr Gln Val Thr Val Ser Ser His His His His His His
690 695 700
<210> 92
<211> 704
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 92
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr Pro Gly
50 55 60
Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser Thr Asn
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu Asp Thr
100 105 110
Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp Gly Gln
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly
145 150 155 160
Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser
165 170 175
Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro
180 185 190
Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp
195 200 205
Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
210 215 220
Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu
225 230 235 240
Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser
245 250 255
Ser Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro
260 265 270
Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser
325 330 335
Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala
355 360 365
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala
370 375 380
Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala
450 455 460
Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly
500 505 510
Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly
515 520 525
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
530 535 540
Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
545 550 555 560
Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln
565 570 575
Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly
580 585 590
Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys
595 600 605
Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu
610 615 620
Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser
625 630 635 640
Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val
645 650 655
Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr
660 665 670
Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr
675 680 685
Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr His His His His His His
690 695 700
<210> 93
<211> 689
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 93
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr
65 70 75 80
Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
145 150 155 160
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
165 170 175
Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg
195 200 205
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
245 250 255
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
275 280 285
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
290 295 300
Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
305 310 315 320
Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
325 330 335
Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala
340 345 350
Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr
355 360 365
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val
370 375 380
Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr
385 390 395 400
Leu Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly Met Lys
405 410 415
Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln
420 425 430
Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly
435 440 445
Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys
450 455 460
Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu
465 470 475 480
Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser
485 490 495
Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val
500 505 510
Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr
515 520 525
Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr
530 535 540
Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Gly Gly Gly Gly Ser Gly
545 550 555 560
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
565 570 575
Gly Gly Gly Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala
580 585 590
Ala Ser Gly Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln
595 600 605
Thr Pro Gly Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly
610 615 620
Ser Thr Asn Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
625 630 635 640
Asp Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro
645 650 655
Glu Asp Thr Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr
660 665 670
Trp Gly Gln Gly Thr Gln Val Thr Val Ser Ser His His His His His
675 680 685
His
<210> 94
<211> 700
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 94
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Arg Gly Glu Thr Gly
290 295 300
Pro Ala Ala Pro Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly
305 310 315 320
Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
325 330 335
Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg Gln Ala Pro Gly
340 345 350
Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr
355 360 365
Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
370 375 380
Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp
385 390 395 400
Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser Val Ser Ser
405 410 415
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
420 425 430
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
435 440 445
Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly
450 455 460
Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser
465 470 475 480
Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro
485 490 495
Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr
500 505 510
Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn
515 520 525
Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp
545 550 555 560
Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
565 570 575
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
580 585 590
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
595 600 605
Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln
610 615 620
Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe
625 630 635 640
Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
645 650 655
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
660 665 670
Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly
675 680 685
Thr Lys Val Glu Ile Lys His His His His His His
690 695 700
<210> 95
<211> 276
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 95
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr
65 70 75 80
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
85 90 95
Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Val Gly Ala Phe Arg Pro Tyr
115 120 125
Arg Lys His Glu Trp Gly Gln Gly Thr Leu Val Thr Val Ser Arg Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser
145 150 155 160
Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val
165 170 175
Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Lys
195 200 205
Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser Ser
210 215 220
Gly Asn Thr Ala Ser Leu Thr Thr Thr Gly Ala Gln Ala Glu Asp Glu
225 230 235 240
Ala Asp Tyr Tyr Cys Asn Ser Ser Pro Phe Glu His Asn Leu Val Val
245 250 255
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu His His His His His His
260 265 270
Glu Pro Glu Ala
275
<210> 96
<211> 279
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 96
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Gln Ser Gly Ala Glu
20 25 30
Leu Val Arg Pro Gly Thr Ser Val Lys Val Ser Cys Lys Ala Ser Gly
35 40 45
Tyr Ala Phe Thr Asn Tyr Leu Ile Glu Trp Val Lys Gln Arg Pro Gly
50 55 60
Gln Gly Leu Glu Trp Ile Gly Val Ile Asn Pro Gly Ser Gly Gly Thr
65 70 75 80
Asn Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys
85 90 95
Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Asp Asp
100 105 110
Ser Ala Val Tyr Phe Cys Ala Arg Trp Arg Gly Asp Gly Tyr Tyr Ala
115 120 125
Tyr Phe Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly Gln Arg
165 170 175
Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp
180 185 190
Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu
195 200 205
Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val
225 230 235 240
Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn Glu Asp
245 250 255
Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys His His His
260 265 270
His His His Glu Pro Glu Ala
275
<210> 97
<211> 279
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 97
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Gln Ser Gly Ala Glu
20 25 30
Leu Val Arg Pro Gly Thr Ser Val Lys Val Ser Cys Lys Ala Ser Gly
35 40 45
Tyr Ala Phe Thr Asn Tyr Leu Ile Glu Trp Val Lys Gln Arg Pro Gly
50 55 60
Gln Gly Leu Glu Trp Ile Gly Val Ile Asn Pro Gly Ser Gly Gly Thr
65 70 75 80
Asn Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys
85 90 95
Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Asp Asp
100 105 110
Ser Ala Val Tyr Phe Cys Ala Arg Trp Arg Gly Asp Gly Tyr Tyr Ala
115 120 125
Tyr Phe Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser Ser
130 135 140
Gly Gly Pro Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Asp Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly Gln Arg
165 170 175
Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp
180 185 190
Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu
195 200 205
Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val
225 230 235 240
Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn Glu Asp
245 250 255
Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys His His His
260 265 270
His His His Glu Pro Glu Ala
275
<210> 98
<211> 279
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 98
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Asp Ile Val Leu Thr Gln Ser Pro Ala Ser
20 25 30
Leu Ala Val Ser Leu Gly Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser
35 40 45
Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu
65 70 75 80
Glu Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Asn Ile His Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr
100 105 110
Tyr Cys Gln Gln Ser Asn Glu Asp Pro Tyr Thr Phe Gly Gly Gly Thr
115 120 125
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val
145 150 155 160
Arg Pro Gly Thr Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ala
165 170 175
Phe Thr Asn Tyr Leu Ile Glu Trp Val Lys Gln Arg Pro Gly Gln Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Asn Pro Gly Ser Gly Gly Thr Asn Tyr
195 200 205
Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser
210 215 220
Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala
225 230 235 240
Val Tyr Phe Cys Ala Arg Trp Arg Gly Asp Gly Tyr Tyr Ala Tyr Phe
245 250 255
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser His His His
260 265 270
His His His Glu Pro Glu Ala
275
<210> 99
<211> 279
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 99
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Asp Ile Val Leu Thr Gln Ser Pro Ala Ser
20 25 30
Leu Ala Val Ser Leu Gly Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser
35 40 45
Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu
65 70 75 80
Glu Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Asn Ile His Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr
100 105 110
Tyr Cys Gln Gln Ser Asn Glu Asp Pro Tyr Thr Phe Gly Gly Gly Thr
115 120 125
Lys Leu Glu Ile Lys Ser Gly Gly Pro Gly Pro Ala Gly Met Lys Gly
130 135 140
Leu Pro Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val
145 150 155 160
Arg Pro Gly Thr Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ala
165 170 175
Phe Thr Asn Tyr Leu Ile Glu Trp Val Lys Gln Arg Pro Gly Gln Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Asn Pro Gly Ser Gly Gly Thr Asn Tyr
195 200 205
Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser
210 215 220
Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala
225 230 235 240
Val Tyr Phe Cys Ala Arg Trp Arg Gly Asp Gly Tyr Tyr Ala Tyr Phe
245 250 255
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser His His His
260 265 270
His His His Glu Pro Glu Ala
275
<210> 100
<211> 295
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 100
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser His His His
275 280 285
His His His Glu Pro Glu Ala
290 295
<210> 101
<211> 765
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 101
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ala His Lys Ser Glu
165 170 175
Val Ala His Arg Phe Lys Asp Leu Gly Glu Glu Asn Phe Lys Ala Leu
180 185 190
Val Leu Ile Ala Phe Ala Gln Tyr Leu Gln Gln Cys Pro Phe Glu Asp
195 200 205
His Val Lys Leu Val Asn Glu Val Thr Glu Phe Ala Lys Thr Cys Val
210 215 220
Ala Asp Glu Ser Ala Glu Asn Cys Asp Lys Ser Leu His Thr Leu Phe
225 230 235 240
Gly Asp Lys Leu Cys Thr Val Ala Thr Leu Arg Glu Thr Tyr Gly Glu
245 250 255
Met Ala Asp Cys Cys Ala Lys Gln Glu Pro Glu Arg Asn Glu Cys Phe
260 265 270
Leu Gln His Lys Asp Asp Asn Pro Asn Leu Pro Arg Leu Val Arg Pro
275 280 285
Glu Val Asp Val Met Cys Thr Ala Phe His Asp Asn Glu Glu Thr Phe
290 295 300
Leu Lys Lys Tyr Leu Tyr Glu Ile Ala Arg Arg His Pro Tyr Phe Tyr
305 310 315 320
Ala Pro Glu Leu Leu Phe Phe Ala Lys Arg Tyr Lys Ala Ala Phe Thr
325 330 335
Glu Cys Cys Gln Ala Ala Asp Lys Ala Ala Cys Leu Leu Pro Lys Leu
340 345 350
Asp Glu Leu Arg Asp Glu Gly Lys Ala Ser Ser Ala Lys Gln Arg Leu
355 360 365
Lys Cys Ala Ser Leu Gln Lys Phe Gly Glu Arg Ala Phe Lys Ala Trp
370 375 380
Ala Val Ala Arg Leu Ser Gln Arg Phe Pro Lys Ala Glu Phe Ala Glu
385 390 395 400
Val Ser Lys Leu Val Thr Asp Leu Thr Lys Val His Thr Glu Cys Cys
405 410 415
His Gly Asp Leu Leu Glu Cys Ala Asp Asp Arg Ala Asp Leu Ala Lys
420 425 430
Tyr Ile Cys Glu Asn Gln Asp Ser Ile Ser Ser Lys Leu Lys Glu Cys
435 440 445
Cys Glu Lys Pro Leu Leu Glu Lys Ser His Cys Ile Ala Glu Val Glu
450 455 460
Asn Asp Glu Met Pro Ala Asp Leu Pro Ser Leu Ala Ala Asp Phe Val
465 470 475 480
Glu Ser Lys Asp Val Cys Lys Asn Tyr Ala Glu Ala Lys Asp Val Phe
485 490 495
Leu Gly Met Phe Leu Tyr Glu Tyr Ala Arg Arg His Pro Asp Tyr Ser
500 505 510
Val Val Leu Leu Leu Arg Leu Ala Lys Thr Tyr Glu Thr Thr Leu Glu
515 520 525
Lys Cys Cys Ala Ala Ala Asp Pro His Glu Cys Tyr Ala Lys Val Phe
530 535 540
Asp Glu Phe Lys Pro Leu Val Glu Glu Pro Gln Asn Leu Ile Lys Gln
545 550 555 560
Asn Cys Glu Leu Phe Glu Gln Leu Gly Glu Tyr Lys Phe Gln Asn Ala
565 570 575
Leu Leu Val Arg Tyr Thr Lys Lys Val Pro Gln Val Ser Thr Pro Thr
580 585 590
Leu Val Glu Val Ser Arg Asn Leu Gly Lys Val Gly Ser Lys Cys Cys
595 600 605
Lys His Pro Glu Ala Lys Arg Met Pro Cys Ala Glu Asp Tyr Leu Ser
610 615 620
Val Val Leu Asn Gln Leu Cys Val Leu His Glu Lys Thr Pro Val Ser
625 630 635 640
Asp Arg Val Thr Lys Cys Cys Thr Glu Ser Leu Val Asn Arg Arg Pro
645 650 655
Cys Phe Ser Ala Leu Glu Val Asp Glu Thr Tyr Val Pro Lys Glu Phe
660 665 670
Asn Ala Glu Thr Phe Thr Phe His Ala Asp Ile Cys Thr Leu Ser Glu
675 680 685
Lys Glu Arg Gln Ile Lys Lys Gln Thr Ala Leu Val Glu Leu Val Lys
690 695 700
His Lys Pro Lys Ala Thr Lys Glu Gln Leu Lys Ala Val Met Asp Asp
705 710 715 720
Phe Ala Ala Phe Val Glu Lys Cys Cys Lys Ala Asp Asp Lys Glu Thr
725 730 735
Cys Phe Ala Glu Glu Gly Lys Lys Leu Val Ala Ala Ser Gln Ala Ala
740 745 750
Leu Gly Leu His His His His His His Glu Pro Glu Ala
755 760 765
<210> 102
<211> 765
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 102
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ala His Lys Ser Glu
165 170 175
Val Ala His Arg Phe Lys Asp Leu Gly Glu Glu Asn Phe Lys Ala Leu
180 185 190
Val Leu Ile Ala Phe Ala Gln Tyr Leu Gln Gln Cys Pro Phe Glu Asp
195 200 205
His Val Lys Leu Val Asn Glu Val Thr Glu Phe Ala Lys Thr Cys Val
210 215 220
Ala Asp Glu Ser Ala Glu Asn Cys Asp Lys Ser Leu His Thr Leu Phe
225 230 235 240
Gly Asp Lys Leu Cys Thr Val Ala Thr Leu Arg Glu Thr Tyr Gly Glu
245 250 255
Met Ala Asp Cys Cys Ala Lys Gln Glu Pro Glu Arg Asn Glu Cys Phe
260 265 270
Leu Gln His Lys Asp Asp Asn Pro Asn Leu Pro Arg Leu Val Arg Pro
275 280 285
Glu Val Asp Val Met Cys Thr Ala Phe His Asp Asn Glu Glu Thr Phe
290 295 300
Leu Lys Lys Tyr Leu Tyr Glu Ile Ala Arg Arg His Pro Tyr Phe Tyr
305 310 315 320
Ala Pro Glu Leu Leu Phe Phe Ala Lys Arg Tyr Lys Ala Ala Phe Thr
325 330 335
Glu Cys Cys Gln Ala Ala Asp Lys Ala Ala Cys Leu Leu Pro Lys Leu
340 345 350
Asp Glu Leu Arg Asp Glu Gly Lys Ala Ser Ser Ala Lys Gln Arg Leu
355 360 365
Lys Cys Ala Ser Leu Gln Lys Phe Gly Glu Arg Ala Phe Lys Ala Trp
370 375 380
Ala Val Ala Arg Leu Ser Gln Arg Phe Pro Lys Ala Glu Phe Ala Glu
385 390 395 400
Val Ser Lys Leu Val Thr Asp Leu Thr Lys Val His Thr Glu Cys Cys
405 410 415
His Gly Asp Leu Leu Glu Cys Ala Asp Asp Arg Ala Asp Leu Ala Lys
420 425 430
Tyr Ile Cys Glu Asn Gln Asp Ser Ile Ser Ser Lys Leu Lys Glu Cys
435 440 445
Cys Glu Lys Pro Leu Leu Glu Lys Ser His Cys Ile Ala Glu Val Glu
450 455 460
Asn Asp Glu Met Pro Ala Asp Leu Pro Ser Leu Ala Ala Asp Phe Val
465 470 475 480
Glu Ser Lys Asp Val Cys Lys Asn Tyr Ala Glu Ala Lys Asp Val Phe
485 490 495
Leu Gly Met Phe Leu Tyr Glu Tyr Ala Arg Arg His Pro Asp Tyr Ser
500 505 510
Val Val Leu Leu Leu Arg Leu Ala Lys Thr Tyr Glu Thr Thr Leu Glu
515 520 525
Lys Cys Cys Ala Ala Ala Asp Pro His Glu Cys Tyr Ala Lys Val Phe
530 535 540
Asp Glu Phe Lys Pro Leu Val Glu Glu Pro Gln Asn Leu Ile Lys Gln
545 550 555 560
Asn Cys Glu Leu Phe Glu Gln Leu Gly Glu Tyr Lys Phe Gln Asn Ala
565 570 575
Leu Leu Val Arg Tyr Thr Lys Lys Val Pro Gln Val Ser Thr Pro Thr
580 585 590
Leu Val Glu Val Ser Arg Asn Leu Gly Lys Val Gly Ser Lys Cys Cys
595 600 605
Lys His Pro Glu Ala Lys Arg Met Pro Cys Ala Glu Asp Tyr Leu Ser
610 615 620
Val Val Leu Asn Gln Leu Cys Val Leu His Glu Lys Thr Pro Val Ser
625 630 635 640
Asp Arg Val Thr Lys Cys Cys Thr Glu Ser Leu Val Asn Arg Arg Pro
645 650 655
Cys Phe Ser Ala Leu Glu Val Asp Glu Thr Tyr Val Pro Lys Glu Phe
660 665 670
Asn Ala Glu Thr Phe Thr Phe His Ala Asp Ile Cys Thr Leu Ser Glu
675 680 685
Lys Glu Arg Gln Ile Lys Lys Gln Thr Ala Leu Val Glu Leu Val Lys
690 695 700
His Lys Pro Lys Ala Thr Lys Glu Gln Leu Lys Ala Val Met Asp Asp
705 710 715 720
Phe Ala Ala Phe Val Glu Lys Cys Cys Lys Ala Asp Asp Lys Glu Thr
725 730 735
Cys Phe Ala Glu Glu Gly Lys Lys Leu Val Ala Ala Ser Gln Ala Ala
740 745 750
Leu Gly Leu His His His His His His Glu Pro Glu Ala
755 760 765
<210> 103
<211> 765
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 103
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Asp Ala His Lys Ser Glu
165 170 175
Val Ala His Arg Phe Lys Asp Leu Gly Glu Glu Asn Phe Lys Ala Leu
180 185 190
Val Leu Ile Ala Phe Ala Gln Tyr Leu Gln Gln Cys Pro Phe Glu Asp
195 200 205
His Val Lys Leu Val Asn Glu Val Thr Glu Phe Ala Lys Thr Cys Val
210 215 220
Ala Asp Glu Ser Ala Glu Asn Cys Asp Lys Ser Leu His Thr Leu Phe
225 230 235 240
Gly Asp Lys Leu Cys Thr Val Ala Thr Leu Arg Glu Thr Tyr Gly Glu
245 250 255
Met Ala Asp Cys Cys Ala Lys Gln Glu Pro Glu Arg Asn Glu Cys Phe
260 265 270
Leu Gln His Lys Asp Asp Asn Pro Asn Leu Pro Arg Leu Val Arg Pro
275 280 285
Glu Val Asp Val Met Cys Thr Ala Phe His Asp Asn Glu Glu Thr Phe
290 295 300
Leu Lys Lys Tyr Leu Tyr Glu Ile Ala Arg Arg His Pro Tyr Phe Tyr
305 310 315 320
Ala Pro Glu Leu Leu Phe Phe Ala Lys Arg Tyr Lys Ala Ala Phe Thr
325 330 335
Glu Cys Cys Gln Ala Ala Asp Lys Ala Ala Cys Leu Leu Pro Lys Leu
340 345 350
Asp Glu Leu Arg Asp Glu Gly Lys Ala Ser Ser Ala Lys Gln Arg Leu
355 360 365
Lys Cys Ala Ser Leu Gln Lys Phe Gly Glu Arg Ala Phe Lys Ala Trp
370 375 380
Ala Val Ala Arg Leu Ser Gln Arg Phe Pro Lys Ala Glu Phe Ala Glu
385 390 395 400
Val Ser Lys Leu Val Thr Asp Leu Thr Lys Val His Thr Glu Cys Cys
405 410 415
His Gly Asp Leu Leu Glu Cys Ala Asp Asp Arg Ala Asp Leu Ala Lys
420 425 430
Tyr Ile Cys Glu Asn Gln Asp Ser Ile Ser Ser Lys Leu Lys Glu Cys
435 440 445
Cys Glu Lys Pro Leu Leu Glu Lys Ser His Cys Ile Ala Glu Val Glu
450 455 460
Asn Asp Glu Met Pro Ala Asp Leu Pro Ser Leu Ala Ala Asp Phe Val
465 470 475 480
Glu Ser Lys Asp Val Cys Lys Asn Tyr Ala Glu Ala Lys Asp Val Phe
485 490 495
Leu Gly Met Phe Leu Tyr Glu Tyr Ala Arg Arg His Pro Asp Tyr Ser
500 505 510
Val Val Leu Leu Leu Arg Leu Ala Lys Thr Tyr Glu Thr Thr Leu Glu
515 520 525
Lys Cys Cys Ala Ala Ala Asp Pro His Glu Cys Tyr Ala Lys Val Phe
530 535 540
Asp Glu Phe Lys Pro Leu Val Glu Glu Pro Gln Asn Leu Ile Lys Gln
545 550 555 560
Asn Cys Glu Leu Phe Glu Gln Leu Gly Glu Tyr Lys Phe Gln Asn Ala
565 570 575
Leu Leu Val Arg Tyr Thr Lys Lys Val Pro Gln Val Ser Thr Pro Thr
580 585 590
Leu Val Glu Val Ser Arg Asn Leu Gly Lys Val Gly Ser Lys Cys Cys
595 600 605
Lys His Pro Glu Ala Lys Arg Met Pro Cys Ala Glu Asp Tyr Leu Ser
610 615 620
Val Val Leu Asn Gln Leu Cys Val Leu His Glu Lys Thr Pro Val Ser
625 630 635 640
Asp Arg Val Thr Lys Cys Cys Thr Glu Ser Leu Val Asn Arg Arg Pro
645 650 655
Cys Phe Ser Ala Leu Glu Val Asp Glu Thr Tyr Val Pro Lys Glu Phe
660 665 670
Asn Ala Glu Thr Phe Thr Phe His Ala Asp Ile Cys Thr Leu Ser Glu
675 680 685
Lys Glu Arg Gln Ile Lys Lys Gln Thr Ala Leu Val Glu Leu Val Lys
690 695 700
His Lys Pro Lys Ala Thr Lys Glu Gln Leu Lys Ala Val Met Asp Asp
705 710 715 720
Phe Ala Ala Phe Val Glu Lys Cys Cys Lys Ala Asp Asp Lys Glu Thr
725 730 735
Cys Phe Ala Glu Glu Gly Lys Lys Leu Val Ala Ala Ser Gln Ala Ala
740 745 750
Leu Gly Leu His His His His His His Glu Pro Glu Ala
755 760 765
<210> 104
<211> 708
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 104
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
275 280 285
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly
305 310 315 320
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
325 330 335
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
340 345 350
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
355 360 365
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
370 375 380
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
385 390 395 400
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
405 410 415
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
420 425 430
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
435 440 445
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
450 455 460
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
465 470 475 480
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
485 490 495
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
500 505 510
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
515 520 525
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
530 535 540
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
545 550 555 560
Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
565 570 575
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
580 585 590
Gly Gly Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala
595 600 605
Ser Gly Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr
610 615 620
Pro Gly Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser
625 630 635 640
Thr Asn Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
645 650 655
Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu
660 665 670
Asp Thr Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp
675 680 685
Gly Gln Gly Thr Gln Val Thr Val Ser Ser His His His His His His
690 695 700
Glu Pro Glu Ala
705
<210> 105
<211> 708
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 105
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr Pro Gly
50 55 60
Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser Thr Asn
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu Asp Thr
100 105 110
Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp Gly Gln
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro
435 440 445
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser
500 505 510
Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile
515 520 525
Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu
530 535 540
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp
545 550 555 560
Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
580 585 590
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
595 600 605
Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val
610 615 620
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr
625 630 635 640
Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
645 650 655
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
660 665 670
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr
675 680 685
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His
690 695 700
Glu Pro Glu Ala
705
<210> 106
<211> 708
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 106
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Ala Gln Ala Gly Gly Ser Leu Ser Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Val Ser Asn Ser Val Met Ala Trp Tyr Arg Gln Thr Pro Gly
50 55 60
Lys Gln Arg Glu Phe Val Ala Ile Ile Asn Ser Val Gly Ser Thr Asn
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Asn Leu Lys Pro Glu Asp Thr
100 105 110
Ala Val Tyr Val Cys Asn Arg Asn Phe Asp Arg Ile Tyr Trp Gly Gln
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly
130 135 140
Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro
435 440 445
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser
500 505 510
Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile
515 520 525
Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu
530 535 540
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp
545 550 555 560
Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
580 585 590
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
595 600 605
Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val
610 615 620
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr
625 630 635 640
Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
645 650 655
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
660 665 670
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr
675 680 685
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His
690 695 700
Glu Pro Glu Ala
705
<210> 107
<211> 161
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 107
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr His His His His His
145 150 155 160
His
<210> 108
<211> 708
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 108
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
275 280 285
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly
305 310 315 320
Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val Glu
325 330 335
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
340 345 350
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
355 360 365
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
370 375 380
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
385 390 395 400
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
405 410 415
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
420 425 430
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
435 440 445
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
450 455 460
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
465 470 475 480
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
485 490 495
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
500 505 510
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
515 520 525
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
530 535 540
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
545 550 555 560
Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
565 570 575
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
580 585 590
Gly Gly Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala
595 600 605
Ser Gly Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala
610 615 620
Pro Gly Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr
625 630 635 640
Ile Ser Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
645 650 655
Asn Ala Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu
660 665 670
Asp Thr Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp
675 680 685
Gly Lys Gly Thr Gln Val Thr Val Ser Ser His His His His His His
690 695 700
Glu Pro Glu Ala
705
<210> 109
<211> 708
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 109
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro
435 440 445
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser
500 505 510
Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile
515 520 525
Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu
530 535 540
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp
545 550 555 560
Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
580 585 590
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
595 600 605
Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val
610 615 620
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr
625 630 635 640
Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
645 650 655
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
660 665 670
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr
675 680 685
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His
690 695 700
Glu Pro Glu Ala
705
<210> 110
<211> 708
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 110
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Gln Val Gln Leu Gln Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Ala Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Arg Ile Phe Ser Ile Asp Ile Met Ser Trp Tyr Arg Gln Ala Pro Gly
50 55 60
Lys Gln Arg Glu Leu Val Ala Arg Ile Thr Arg Gly Gly Thr Ile Ser
65 70 75 80
Tyr Asp Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Asn Ala Leu Tyr Gly Thr Asp Tyr Trp Gly Lys
115 120 125
Gly Thr Gln Val Thr Val Ser Ser Ser Gly Gly Pro Gly Pro Ala Gly
130 135 140
Met Lys Gly Leu Pro Gly Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys
145 150 155 160
Thr Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu
165 170 175
Asn Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr
180 185 190
Phe Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln
195 200 205
Cys Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala
210 215 220
Gln Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile
225 230 235 240
Asn Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys
245 250 255
Glu Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp
260 265 270
Ile Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro
275 280 285
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
290 295 300
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
305 310 315 320
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
325 330 335
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
340 345 350
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
355 360 365
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
370 375 380
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
385 390 395 400
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
420 425 430
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro
435 440 445
Gly Pro Ala Gly Met Lys Gly Leu Pro Gly Ser Glu Val Gln Leu Val
450 455 460
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
465 470 475 480
Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val
485 490 495
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser
500 505 510
Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile
515 520 525
Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu
530 535 540
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp
545 550 555 560
Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
580 585 590
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
595 600 605
Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val
610 615 620
Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr
625 630 635 640
Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
645 650 655
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
660 665 670
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr
675 680 685
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His
690 695 700
Glu Pro Glu Ala
705
<210> 111
<211> 579
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 111
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Gly
145 150 155 160
Pro Ala Gly Leu Tyr Ala Gln Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
275 280 285
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Gly
305 310 315 320
Pro Ala Gly Leu Tyr Ala Gln Pro Gly Ser Glu Val Gln Leu Val Glu
325 330 335
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
340 345 350
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
355 360 365
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
370 375 380
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
385 390 395 400
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
405 410 415
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
420 425 430
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
435 440 445
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
450 455 460
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
465 470 475 480
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
485 490 495
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
500 505 510
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
515 520 525
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
530 535 540
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
545 550 555 560
Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His Glu
565 570 575
Pro Glu Ala
<210> 112
<211> 579
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 112
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Pro
145 150 155 160
Gly Gly Pro Ala Gly Ile Gly Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
275 280 285
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Pro
305 310 315 320
Gly Gly Pro Ala Gly Ile Gly Pro Gly Ser Glu Val Gln Leu Val Glu
325 330 335
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
340 345 350
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
355 360 365
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
370 375 380
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
385 390 395 400
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
405 410 415
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
420 425 430
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
435 440 445
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
450 455 460
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
465 470 475 480
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
485 490 495
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
500 505 510
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
515 520 525
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
530 535 540
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
545 550 555 560
Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His Glu
565 570 575
Pro Glu Ala
<210> 113
<211> 579
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 113
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Ala
145 150 155 160
Leu Phe Lys Ser Ser Phe Pro Pro Gly Ser Glu Val Gln Leu Val Glu
165 170 175
Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser Cys
180 185 190
Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val Arg
195 200 205
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser
210 215 220
Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile
225 230 235 240
Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu
245 250 255
Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu
260 265 270
Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
275 280 285
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
290 295 300
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro Ala
305 310 315 320
Leu Phe Lys Ser Ser Phe Pro Pro Gly Ser Glu Val Gln Leu Val Glu
325 330 335
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
340 345 350
Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg
355 360 365
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser
370 375 380
Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser
385 390 395 400
Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg
405 410 415
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp
420 425 430
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
435 440 445
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
450 455 460
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
465 470 475 480
Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly
485 490 495
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser
500 505 510
Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
515 520 525
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
530 535 540
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe
545 550 555 560
Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His His Glu
565 570 575
Pro Glu Ala
<210> 114
<211> 581
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 114
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Pro
145 150 155 160
Leu Ala Gln Lys Leu Lys Ser Ser Pro Gly Ser Glu Val Gln Leu Val
165 170 175
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
180 185 190
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
195 200 205
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
210 215 220
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
225 230 235 240
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
245 250 255
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
260 265 270
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
275 280 285
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
290 295 300
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro
305 310 315 320
Pro Leu Ala Gln Lys Leu Lys Ser Ser Pro Gly Ser Glu Val Gln Leu
325 330 335
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
340 345 350
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp
355 360 365
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp
370 375 380
Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr
385 390 395 400
Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser
405 410 415
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn
420 425 430
Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
435 440 445
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
450 455 460
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
465 470 475 480
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
485 490 495
Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile
500 505 510
Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
515 520 525
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
530 535 540
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr
545 550 555 560
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His
565 570 575
His Glu Pro Glu Ala
580
<210> 115
<211> 613
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 115
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr
20 25 30
Gln Leu Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn
35 40 45
Gly Ile Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe
50 55 60
Lys Phe Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys
65 70 75 80
Leu Glu Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln
85 90 95
Ser Lys Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn
100 105 110
Val Ile Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu
115 120 125
Tyr Ala Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile
130 135 140
Thr Phe Cys Gln Ser Ile Ile Ser Thr Leu Thr Ser Gly Gly Pro Pro
145 150 155 160
Gly Gly Pro Ala Gly Ile Gly Ala Leu Phe Lys Ser Ser Phe Pro Pro
165 170 175
Leu Ala Gln Lys Leu Lys Ser Ser Pro Gly Ser Glu Val Gln Leu Val
180 185 190
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu Ser
195 200 205
Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp Val
210 215 220
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser Gly
225 230 235 240
Ser Gly Arg Asp Thr Leu Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr
245 250 255
Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser
260 265 270
Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser
275 280 285
Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
290 295 300
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
305 310 315 320
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gly Gly Pro
325 330 335
Pro Gly Gly Pro Ala Gly Ile Gly Ala Leu Phe Lys Ser Ser Phe Pro
340 345 350
Pro Leu Ala Gln Lys Leu Lys Ser Ser Pro Gly Ser Glu Val Gln Leu
355 360 365
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
370 375 380
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp
385 390 395 400
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Ala Ile Asp
405 410 415
Ser Ser Ser Tyr Thr Tyr Ser Pro Asp Thr Val Arg Gly Arg Phe Thr
420 425 430
Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser
435 440 445
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn
450 455 460
Trp Asp Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser
465 470 475 480
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
485 490 495
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
500 505 510
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
515 520 525
Val Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile
530 535 540
Tyr Ser Ala Ser Phe Arg Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
545 550 555 560
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
565 570 575
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr
580 585 590
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys His His His His His
595 600 605
His Glu Pro Glu Ala
610
<210> 116
<211> 534
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 116
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Gly Gly Gly Gly Gly Leu Asp Gly Asn
35 40 45
Glu Glu Pro Gly Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly
50 55 60
Arg Asp Thr Leu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
65 70 75 80
Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
85 90 95
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser
100 105 110
Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Lys Pro Leu Gly Leu Gln Ala Arg Val Val Gly Gly Gly Gly Thr Gln
130 135 140
Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr
145 150 155 160
Val Thr Leu Thr Cys Ala Ser Ser Thr Gly Ala Val Thr Ser Gly Asn
165 170 175
Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu
180 185 190
Ile Gly Gly Thr Lys Phe Leu Val Pro Gly Thr Pro Ala Arg Phe Ser
195 200 205
Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val Gln
210 215 220
Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Thr Leu Trp Tyr Ser Asn Arg
225 230 235 240
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly
245 250 255
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
260 265 270
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser
275 280 285
Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr Ala Ile Asn Trp Val
290 295 300
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Ser
305 310 315 320
Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Gln Val Lys Asp Arg
325 330 335
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met
340 345 350
Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His
355 360 365
Ala Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr Trp Gly Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
405 410 415
Gly Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser
420 425 430
Tyr Ala Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
435 440 445
Val Val Ala Ile Asn Trp Ala Ser Gly Ser Thr Tyr Tyr Ala Asp Ser
450 455 460
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
465 470 475 480
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
485 490 495
Cys Ala Ala Gly Tyr Gln Ile Asn Ser Gly Asn Tyr Asn Phe Lys Asp
500 505 510
Tyr Glu Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
515 520 525
His His His His His His
530
<210> 117
<211> 534
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 117
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Gly Gly Gly Gly Gly Leu Asp Gly Asn
35 40 45
Glu Glu Pro Gly Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly
50 55 60
Arg Asp Thr Leu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
65 70 75 80
Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
85 90 95
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser
100 105 110
Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Val Val Gly Gly Gly Gly Thr Gln
130 135 140
Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr
145 150 155 160
Val Thr Leu Thr Cys Ala Ser Ser Thr Gly Ala Val Thr Ser Gly Asn
165 170 175
Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu
180 185 190
Ile Gly Gly Thr Lys Phe Leu Val Pro Gly Thr Pro Ala Arg Phe Ser
195 200 205
Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val Gln
210 215 220
Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Thr Leu Trp Tyr Ser Asn Arg
225 230 235 240
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly
245 250 255
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
260 265 270
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser
275 280 285
Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr Ala Ile Asn Trp Val
290 295 300
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Ser
305 310 315 320
Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Gln Val Lys Asp Arg
325 330 335
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met
340 345 350
Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His
355 360 365
Ala Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr Trp Gly Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
405 410 415
Gly Ser Leu Thr Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser
420 425 430
Tyr Ala Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
435 440 445
Val Val Ala Ile Asn Trp Ala Ser Gly Ser Thr Tyr Tyr Ala Asp Ser
450 455 460
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
465 470 475 480
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
485 490 495
Cys Ala Ala Gly Tyr Gln Ile Asn Ser Gly Asn Tyr Asn Phe Lys Asp
500 505 510
Tyr Glu Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
515 520 525
His His His His His His
530
<210> 118
<211> 398
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 118
Val Val Gly Gly Gly Gly Thr Gln Thr Val Val Thr Gln Glu Pro Ser
1 5 10 15
Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys Ala Ser Ser
20 25 30
Thr Gly Ala Val Thr Ser Gly Asn Tyr Pro Asn Trp Val Gln Gln Lys
35 40 45
Pro Gly Gln Ala Pro Arg Gly Leu Ile Gly Gly Thr Lys Phe Leu Val
50 55 60
Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala
65 70 75 80
Ala Leu Thr Leu Ser Gly Val Gln Pro Glu Asp Glu Ala Glu Tyr Tyr
85 90 95
Cys Thr Leu Trp Tyr Ser Asn Arg Trp Val Phe Gly Gly Gly Thr Lys
100 105 110
Leu Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
145 150 155 160
Asn Lys Tyr Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
165 170 175
Glu Trp Val Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr
180 185 190
Tyr Ala Asp Gln Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser
195 200 205
Lys Asn Thr Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Val Arg His Ala Asn Phe Gly Asn Ser Tyr Ile
225 230 235 240
Ser Tyr Trp Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
260 265 270
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Thr Leu Ser Cys Ala
275 280 285
Ala Ser Gly Arg Thr Phe Ser Ser Tyr Ala Met Gly Trp Phe Arg Gln
290 295 300
Ala Pro Gly Lys Glu Arg Glu Phe Val Val Ala Ile Asn Trp Ala Ser
305 310 315 320
Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
325 330 335
Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
340 345 350
Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Ala Gly Tyr Gln Ile Asn
355 360 365
Ser Gly Asn Tyr Asn Phe Lys Asp Tyr Glu Tyr Asp Tyr Trp Gly Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser His His His His His His
385 390 395
<210> 119
<211> 518
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 119
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Gly Gly Gly Gly Gly Leu Asp Gly Asn
35 40 45
Glu Glu Pro Gly Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly
50 55 60
Arg Asp Thr Leu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
65 70 75 80
Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
85 90 95
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser
100 105 110
Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Lys Pro Leu Gly Leu Gln Ala Arg Val Val Gly Gly Gly Gly Thr Gln
130 135 140
Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr
145 150 155 160
Val Thr Leu Thr Cys Ala Ser Ser Thr Gly Ala Val Thr Ser Gly Asn
165 170 175
Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu
180 185 190
Ile Gly Gly Thr Lys Phe Leu Val Pro Gly Thr Pro Ala Arg Phe Ser
195 200 205
Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val Gln
210 215 220
Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Thr Leu Trp Tyr Ser Asn Arg
225 230 235 240
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly
245 250 255
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
260 265 270
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser
275 280 285
Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr Ala Ile Asn Trp Val
290 295 300
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Ser
305 310 315 320
Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Gln Val Lys Asp Arg
325 330 335
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met
340 345 350
Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His
355 360 365
Ala Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr Trp Gly Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
405 410 415
Gly Ser Leu Thr Leu Ser Cys Ala Ala Ser Arg Phe Met Ile Ser Glu
420 425 430
Tyr His Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
435 440 445
Val Ser Thr Ile Asn Pro Ala Gly Thr Thr Asp Tyr Ala Glu Ser Val
450 455 460
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
465 470 475 480
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
485 490 495
Asp Ser Tyr Gly Tyr Arg Gly Gln Gly Thr Gln Val Thr Val Ser Ser
500 505 510
His His His His His His
515
<210> 120
<211> 518
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 120
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Gly Gly Gly Gly Gly Leu Asp Gly Asn
35 40 45
Glu Glu Pro Gly Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly
50 55 60
Arg Asp Thr Leu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
65 70 75 80
Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
85 90 95
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser
100 105 110
Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Val Val Gly Gly Gly Gly Thr Gln
130 135 140
Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr
145 150 155 160
Val Thr Leu Thr Cys Ala Ser Ser Thr Gly Ala Val Thr Ser Gly Asn
165 170 175
Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu
180 185 190
Ile Gly Gly Thr Lys Phe Leu Val Pro Gly Thr Pro Ala Arg Phe Ser
195 200 205
Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val Gln
210 215 220
Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Thr Leu Trp Tyr Ser Asn Arg
225 230 235 240
Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly
245 250 255
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
260 265 270
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser
275 280 285
Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr Ala Ile Asn Trp Val
290 295 300
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Ser
305 310 315 320
Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Gln Val Lys Asp Arg
325 330 335
Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met
340 345 350
Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His
355 360 365
Ala Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr Trp Gly Gln
370 375 380
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
405 410 415
Gly Ser Leu Thr Leu Ser Cys Ala Ala Ser Arg Phe Met Ile Ser Glu
420 425 430
Tyr His Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
435 440 445
Val Ser Thr Ile Asn Pro Ala Gly Thr Thr Asp Tyr Ala Glu Ser Val
450 455 460
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
465 470 475 480
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
485 490 495
Asp Ser Tyr Gly Tyr Arg Gly Gln Gly Thr Gln Val Thr Val Ser Ser
500 505 510
His His His His His His
515
<210> 121
<211> 382
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 121
Val Val Gly Gly Gly Gly Thr Gln Thr Val Val Thr Gln Glu Pro Ser
1 5 10 15
Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys Ala Ser Ser
20 25 30
Thr Gly Ala Val Thr Ser Gly Asn Tyr Pro Asn Trp Val Gln Gln Lys
35 40 45
Pro Gly Gln Ala Pro Arg Gly Leu Ile Gly Gly Thr Lys Phe Leu Val
50 55 60
Pro Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala
65 70 75 80
Ala Leu Thr Leu Ser Gly Val Gln Pro Glu Asp Glu Ala Glu Tyr Tyr
85 90 95
Cys Thr Leu Trp Tyr Ser Asn Arg Trp Val Phe Gly Gly Gly Thr Lys
100 105 110
Leu Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
130 135 140
Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
145 150 155 160
Asn Lys Tyr Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
165 170 175
Glu Trp Val Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr
180 185 190
Tyr Ala Asp Gln Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser
195 200 205
Lys Asn Thr Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Val Arg His Ala Asn Phe Gly Asn Ser Tyr Ile
225 230 235 240
Ser Tyr Trp Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser
260 265 270
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Thr Leu Ser Cys Ala
275 280 285
Ala Ser Arg Phe Met Ile Ser Glu Tyr His Met His Trp Val Arg Gln
290 295 300
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Thr Ile Asn Pro Ala Gly
305 310 315 320
Thr Thr Asp Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
325 330 335
Asp Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Pro
340 345 350
Glu Asp Thr Ala Val Tyr Tyr Cys Asp Ser Tyr Gly Tyr Arg Gly Gln
355 360 365
Gly Thr Gln Val Thr Val Ser Ser His His His His His His
370 375 380
<210> 122
<211> 503
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 122
Gln Val Gln Leu Val Glu Ser Gly Gly Ala Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Pro Val Asn Arg Tyr
20 25 30
Ser Met Arg Trp Tyr Arg Gln Ala Pro Gly Lys Glu Arg Glu Trp Val
35 40 45
Ala Gly Met Ser Ser Ala Gly Asp Arg Ser Ser Tyr Glu Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ala Arg Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Asn Val Asn Val Gly Phe Glu Tyr Trp Gly Gln Gly Thr Gln Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Glu Val Gln Leu
115 120 125
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn Ser Leu Arg Leu
130 135 140
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe Gly Met Ser Trp
145 150 155 160
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ser Ile Ser
165 170 175
Gly Ser Gly Arg Asp Thr Leu Tyr Ala Asp Ser Val Lys Gly Arg Phe
180 185 190
Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn
195 200 205
Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly
210 215 220
Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser Gly
225 230 235 240
Gly Gly Gly Ser Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
245 250 255
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala
260 265 270
Ser Gly Phe Thr Phe Asn Lys Tyr Ala Ile Asn Trp Val Arg Gln Ala
275 280 285
Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Ser Lys Tyr Asn
290 295 300
Asn Tyr Ala Thr Tyr Tyr Ala Asp Gln Val Lys Asp Arg Phe Thr Ile
305 310 315 320
Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Asn Leu
325 330 335
Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Ala Asn Phe
340 345 350
Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr Trp Gly Gln Gly Thr Leu
355 360 365
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
370 375 380
Gly Gly Gly Ser Gln Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val
385 390 395 400
Ser Pro Gly Gly Thr Val Thr Leu Thr Cys Ala Ser Ser Thr Gly Ala
405 410 415
Val Thr Ser Gly Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln
420 425 430
Ala Pro Arg Gly Leu Ile Gly Gly Thr Lys Phe Leu Val Pro Gly Thr
435 440 445
Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr
450 455 460
Leu Ser Gly Val Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Thr Leu
465 470 475 480
Trp Tyr Ser Asn Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val
485 490 495
Leu His His His His His His
500
<210> 123
<211> 509
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 123
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Gly Ser Gly Arg Asp Thr Leu Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Thr Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Ile Gly Gly Ser Leu Ser Val Ser Ser Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Val
115 120 125
Val Gly Gly Gly Gly Thr Gln Thr Val Val Thr Gln Glu Pro Ser Leu
130 135 140
Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr Cys Ala Ser Ser Thr
145 150 155 160
Gly Ala Val Thr Ser Gly Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro
165 170 175
Gly Gln Ala Pro Arg Gly Leu Ile Gly Gly Thr Lys Phe Leu Val Pro
180 185 190
Gly Thr Pro Ala Arg Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala
195 200 205
Leu Thr Leu Ser Gly Val Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys
210 215 220
Thr Leu Trp Tyr Ser Asn Arg Trp Val Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
245 250 255
Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro
260 265 270
Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn
275 280 285
Lys Tyr Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
290 295 300
Trp Val Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr
305 310 315 320
Ala Asp Gln Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys
325 330 335
Asn Thr Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala
340 345 350
Val Tyr Tyr Cys Val Arg His Ala Asn Phe Gly Asn Ser Tyr Ile Ser
355 360 365
Tyr Trp Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
370 375 380
Gly Gly Gly Ser Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly
385 390 395 400
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Thr Leu Ser Cys Ala Ala
405 410 415
Ser Arg Phe Met Ile Ser Glu Tyr His Met His Trp Val Arg Gln Ala
420 425 430
Pro Gly Lys Gly Leu Glu Trp Val Ser Thr Ile Asn Pro Ala Gly Thr
435 440 445
Thr Asp Tyr Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
450 455 460
Asn Ala Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu
465 470 475 480
Asp Thr Ala Val Tyr Tyr Cys Asp Ser Tyr Gly Tyr Arg Gly Gln Gly
485 490 495
Thr Gln Val Thr Val Ser Ser His His His His His His
500 505
<210> 124
<211> 267
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 124
Met Asp Met Arg Val Pro Ala Gln Leu Leu Gly Leu Leu Leu Leu Trp
1 5 10 15
Leu Arg Gly Ala Arg Cys Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Ser Ser Tyr Thr Leu Ala Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ala Ala Ile Asp Ser Ser Ser Tyr Thr Tyr
65 70 75 80
Ser Pro Asp Thr Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Ser Asn Trp Asp Ala Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
145 150 155 160
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
165 170 175
Cys Lys Ala Ser Gln Asn Val Gly Thr Asn Val Gly Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Lys Ala Pro Lys Ala Leu Ile Tyr Ser Ala Ser Phe Arg
195 200 205
Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Tyr Thr Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
245 250 255
Lys Val Glu Ile Lys His His His His His His
260 265
<210> 125
<211> 5
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
Сайт расщепления сортазой A"
<220>
<221> МОД_ОСТ
<222> (3)..(3)
<223> Любая аминокислота
<400> 125
Leu Pro Xaa Thr Gly
1 5
<210> 126
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> SITE
<222> (1)..(25)
<223> /примечание="Эта последовательность может содержать 1-5 повторяющихся
звеньев 'Gly Gly Gly Gly Ser'"
<400> 126
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 127
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<220>
<221> SITE
<222> (1)..(20)
<223> /примечание=" Эта последовательность может содержать 1-5 повторяющихся
звеньев 'Gly Gly Gly Ser'"
<400> 127
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Ser
20
<210> 128
<211> 7
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
расщепляемая протеазой последовательность"
<400> 128
Gly Pro Leu Gly Val Arg Gly
1 5
<210> 129
<211> 8
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
расщепляемая протеазой последовательность"
<400> 129
Ile Pro Val Ser Leu Arg Ser Gly
1 5
<210> 130
<211> 8
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
расщепляемая протеазой последовательность"
<400> 130
Val Pro Leu Ser Leu Tyr Ser Gly
1 5
<210> 131
<211> 10
<212> Белок
<213> Неизвестная последовательность
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
расщепляемая протеазой последовательность"
<400> 131
Ser Gly Glu Ser Pro Ala Tyr Tyr Thr Ala
1 5 10
<210> 132
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 132
Gly Gly Gly Gly Ser
1 5
<210> 133
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 133
Gly Ser Gly Ser Gly Ser
1 5
<210> 134
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 134
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Thr
1 5 10
<210> 135
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 135
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 136
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетическая
метка 6xHis"
<400> 136
His His His His His His
1 5
<210> 137
<211> 124
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 137
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Phe
20 25 30
Gly Met Ser Trp Val Arg Gln Gly Gly Gly Gly Gly Leu Asp Gly Asn
35 40 45
Glu Glu Pro Gly Gly Leu Glu Trp Val Ser Ser Ile Ser Gly Ser Gly
50 55 60
Arg Asp Thr Leu Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser
65 70 75 80
Arg Asp Asn Ala Lys Thr Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
85 90 95
Pro Glu Asp Thr Ala Val Tyr Tyr Cys Thr Ile Gly Gly Ser Leu Ser
100 105 110
Val Ser Ser Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АКТИВИРУЕМЫЕ ПОЛИПЕПТИДЫ ИНТЕРЛЕЙКИНА 12 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2826183C2 |
| СЛИТЫЕ СЕРПИНОВЫЕ ПОЛИПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2728861C1 |
| СЛИТЫЕ СЕРПИНОВЫЕ ПОЛИПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2698655C2 |
| СЛИТЫЕ СЕРПИНОВЫЕ ПОЛИПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2746550C2 |
| ИММУНОЦИТОКИНЫ И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2818371C1 |
| ХИМЕРНЫЙ ЦИТОКИНОВЫЙ РЕЦЕПТОР | 2016 |
|
RU2826122C1 |
| ЛИГАНДСВЯЗЫВАЮЩАЯ МОЛЕКУЛА С РЕГУЛИРУЕМОЙ ЛИГАНДСВЯЗЫВАЮЩЕЙ АКТИВНОСТЬЮ | 2017 |
|
RU2803067C2 |
| ВАРИАНТНЫЕ МОЛЕКУЛЫ IL-10 И СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2020 |
|
RU2836849C2 |
| СЛИТЫЕ БЕЛКИ С АЛЬБУМИН-СВЯЗЫВАЮЩИМИ ДОМЕНАМИ | 2018 |
|
RU2786444C2 |
| АНТИТЕЛА, СОДЕРЖАЩИЕ ПОЛИПЕПТИД, ВСТРОЕННЫЙ В УЧАСТОК КАРКАСНОЙ ОБЛАСТИ 3 | 2019 |
|
RU2796254C2 |
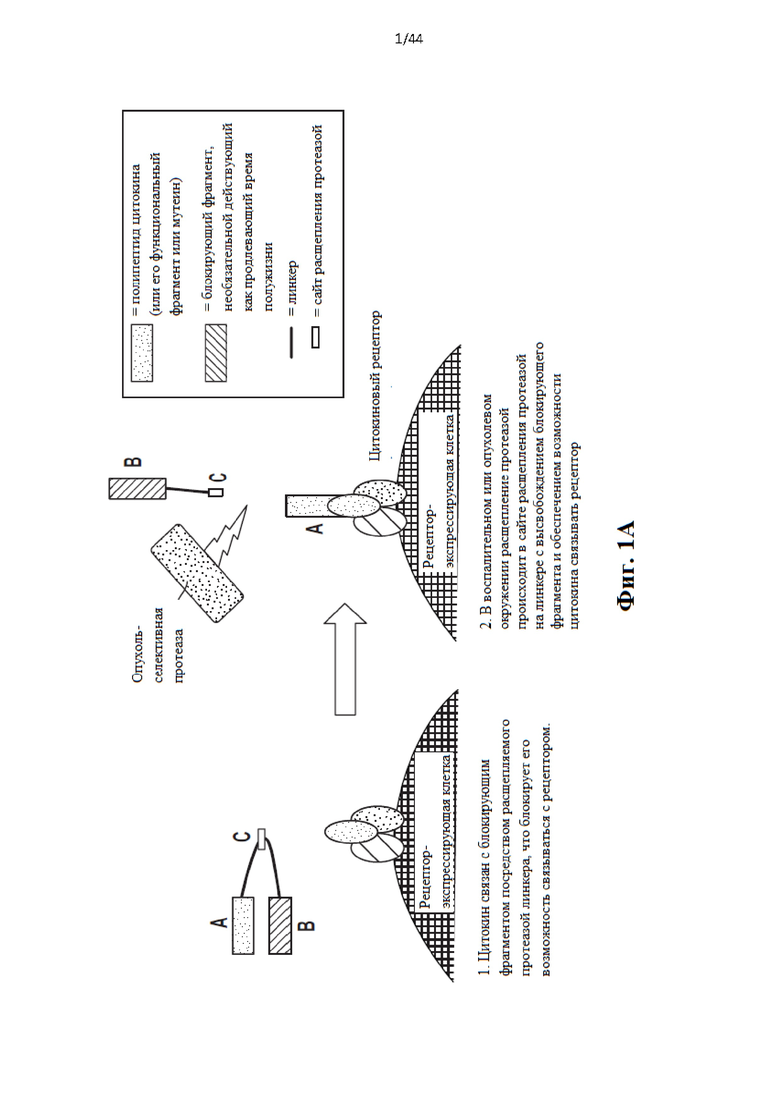
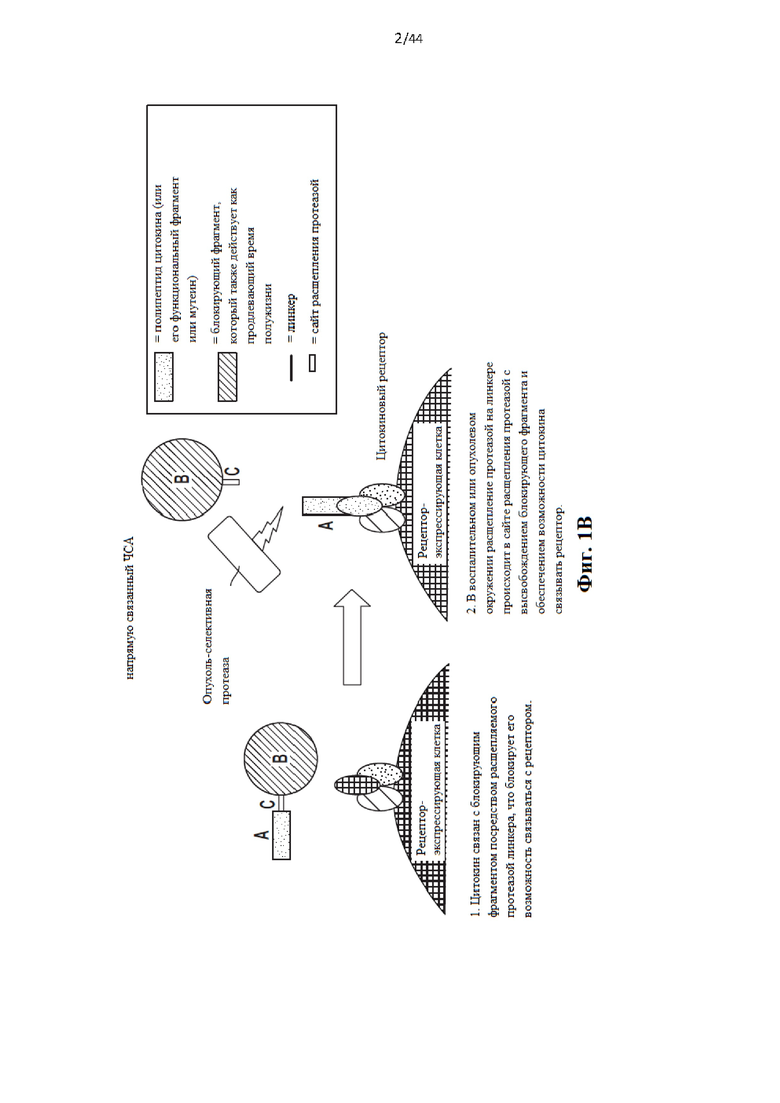

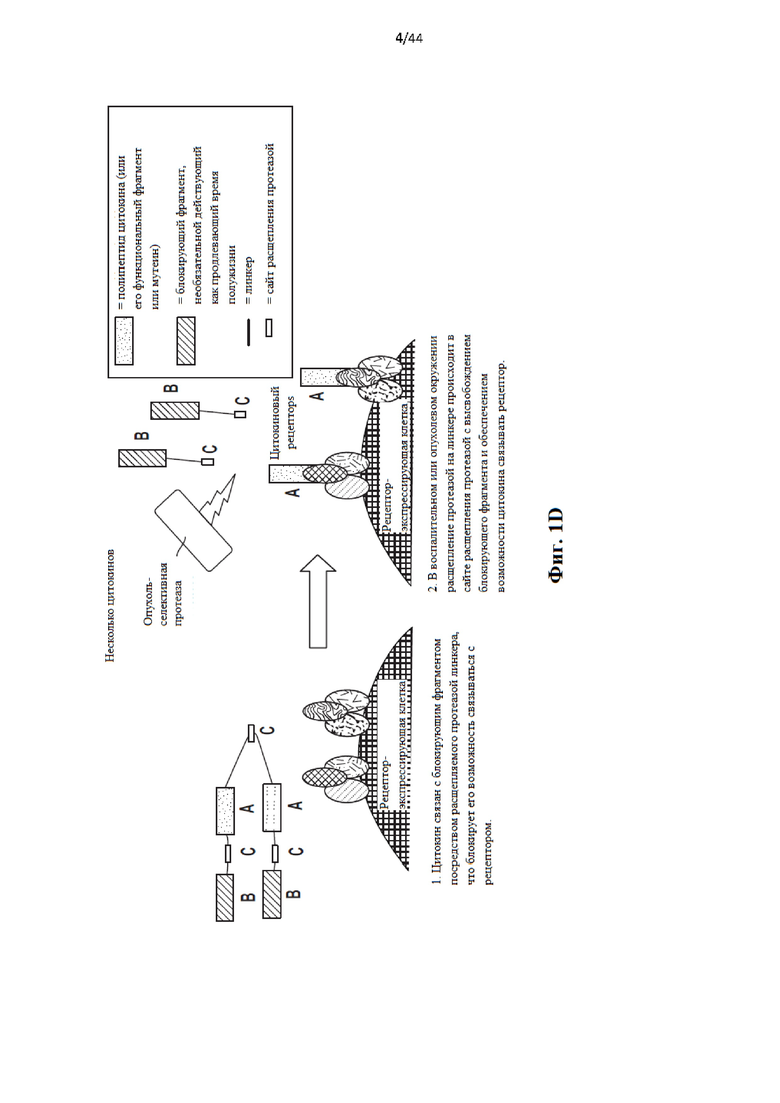
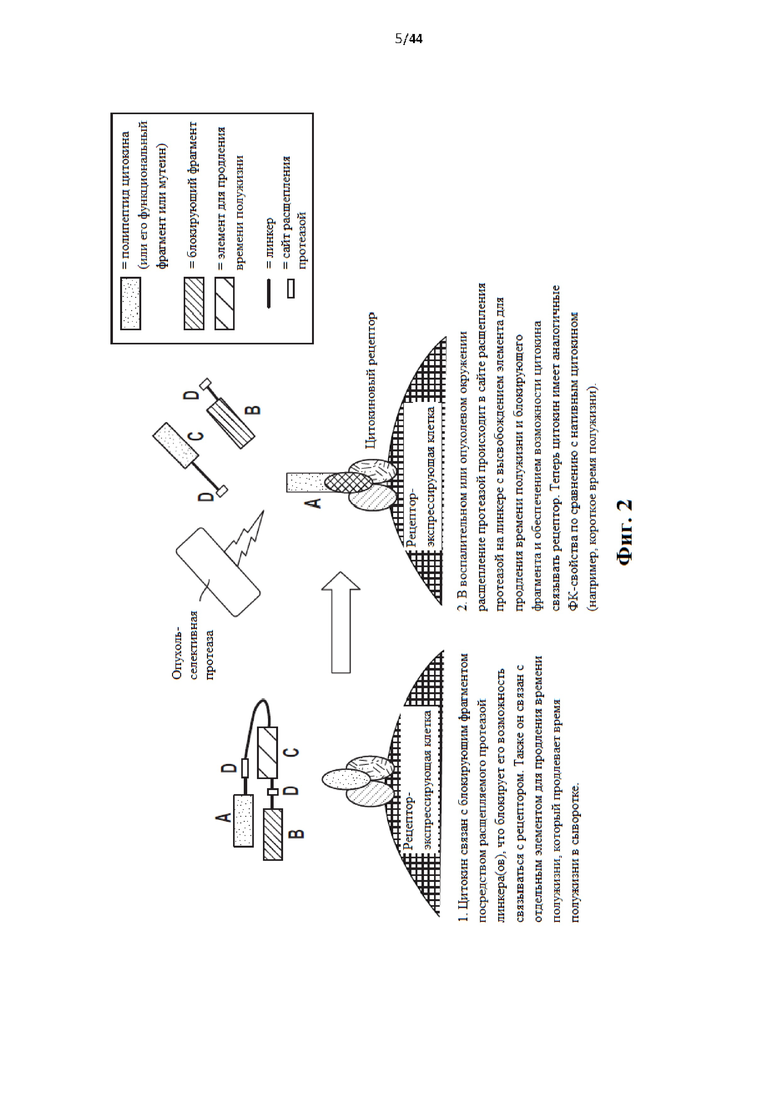

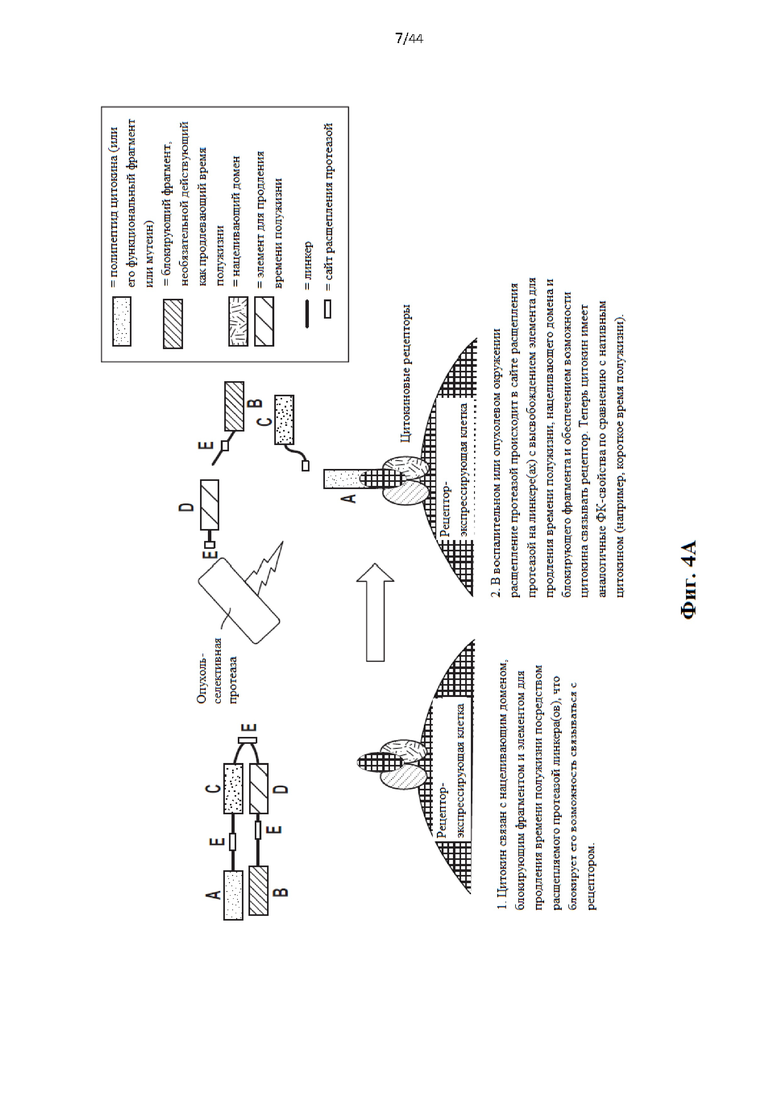
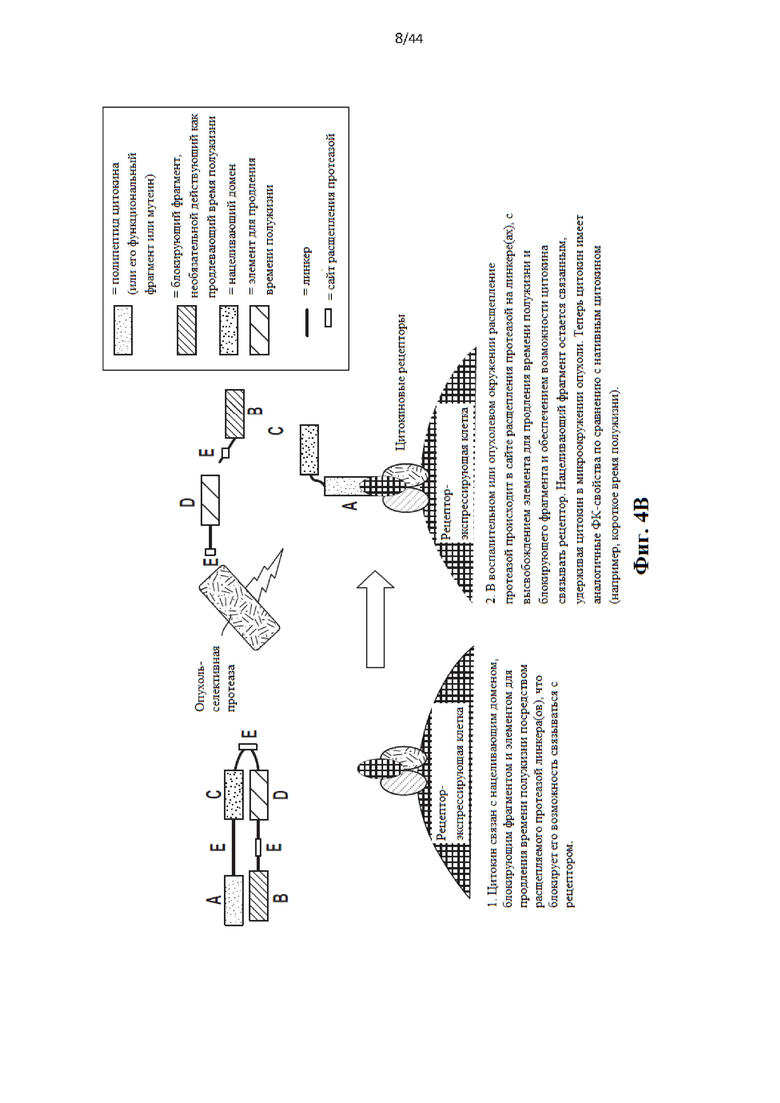
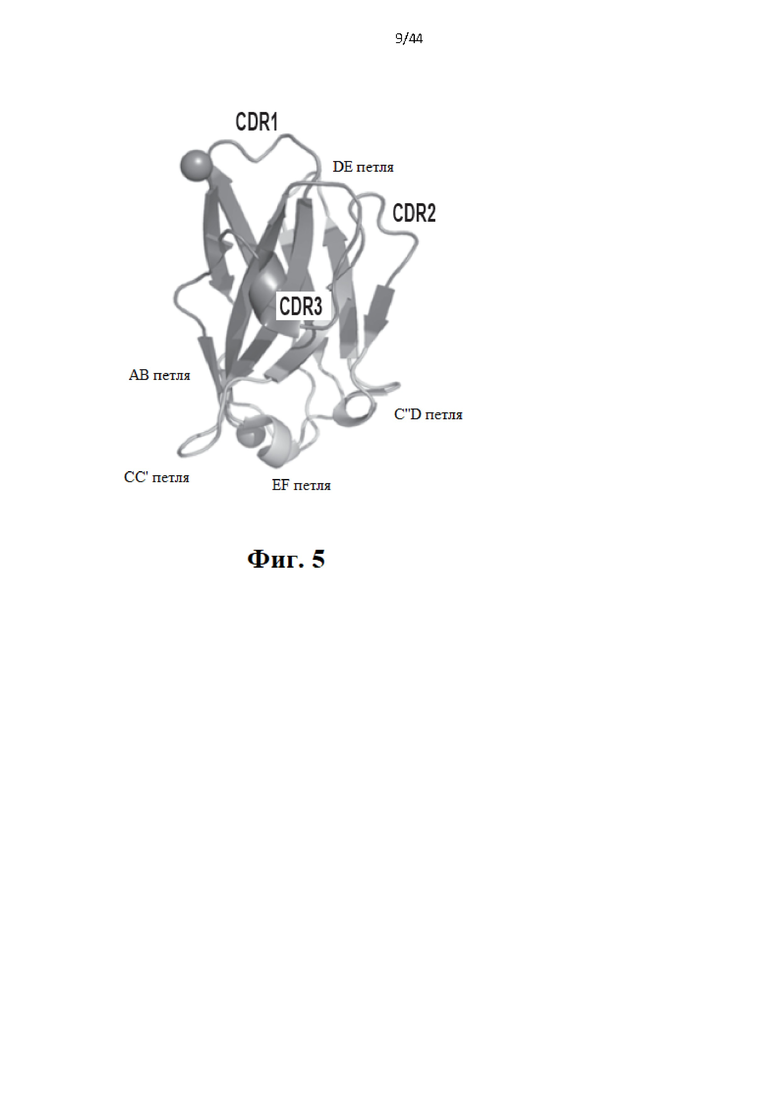
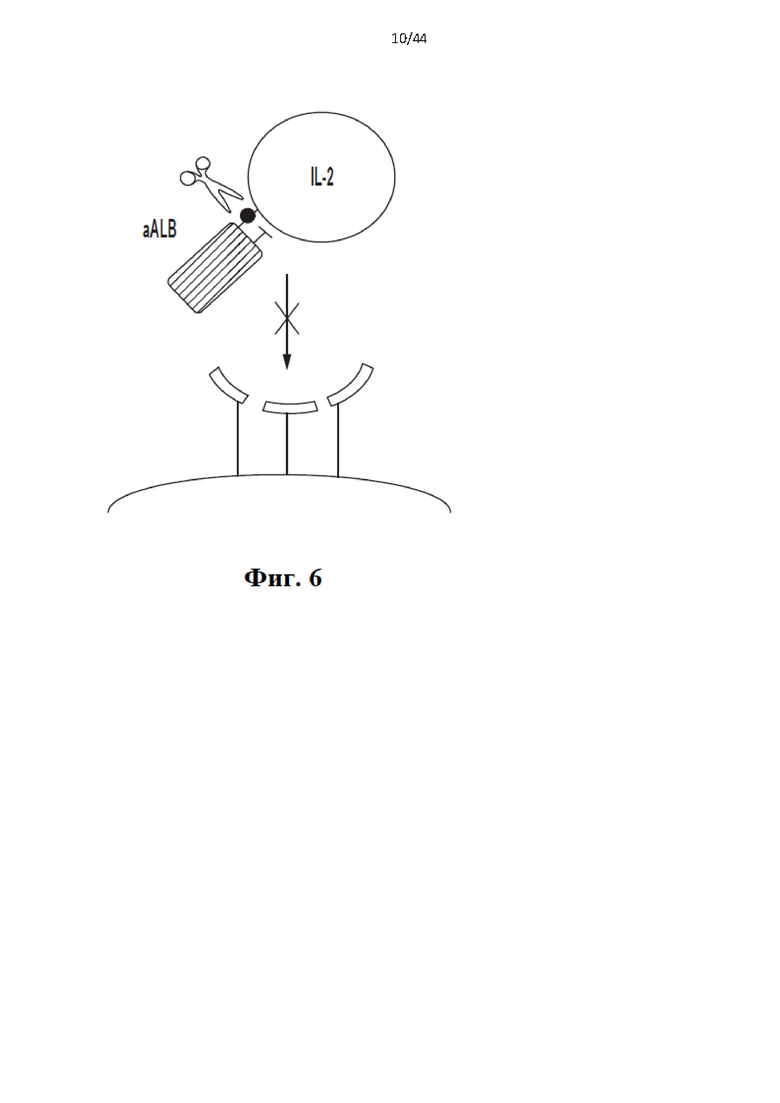
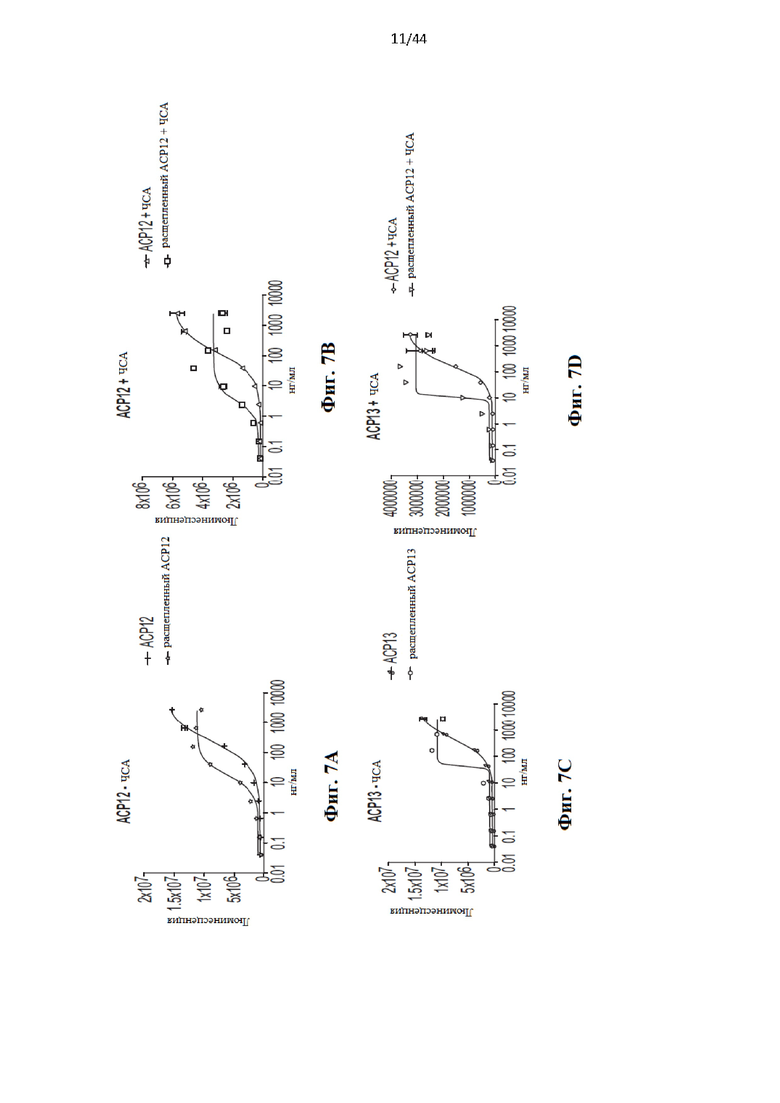




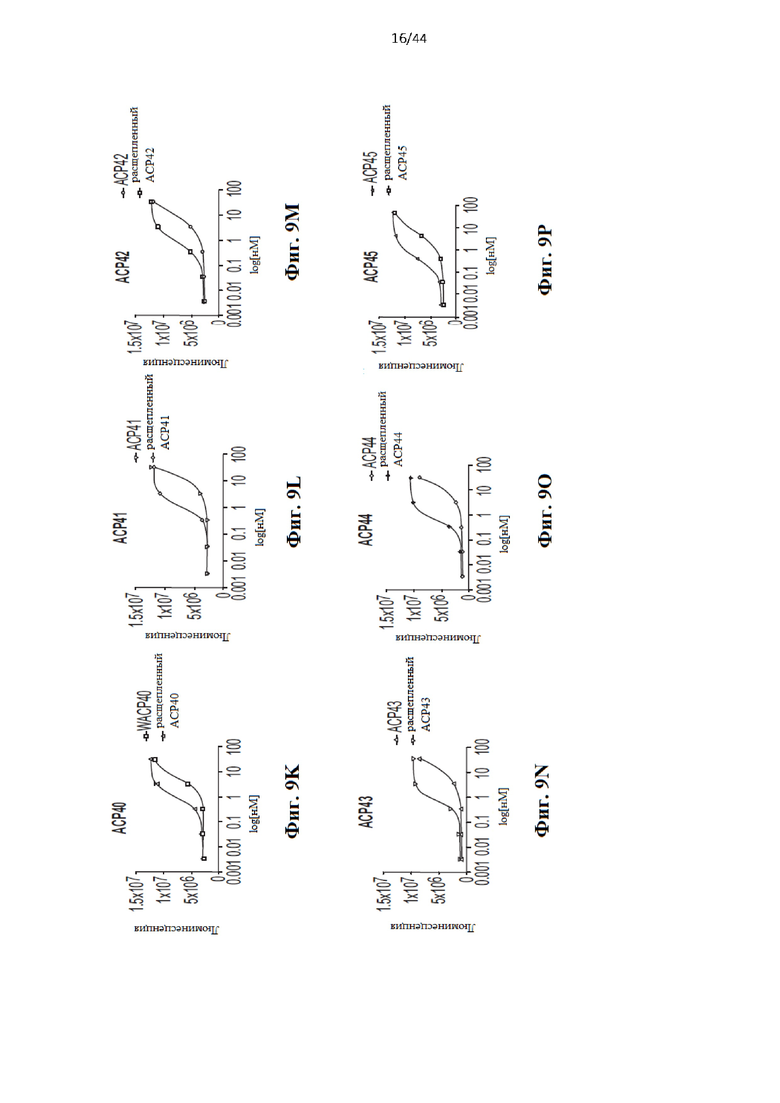
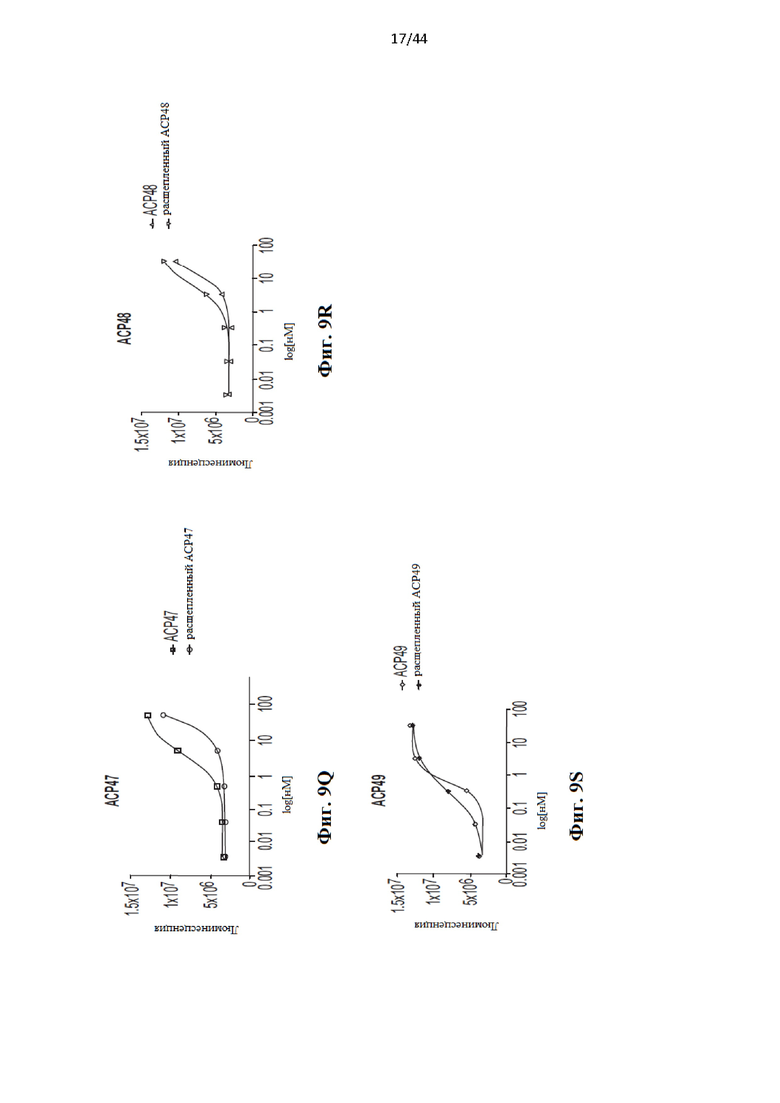

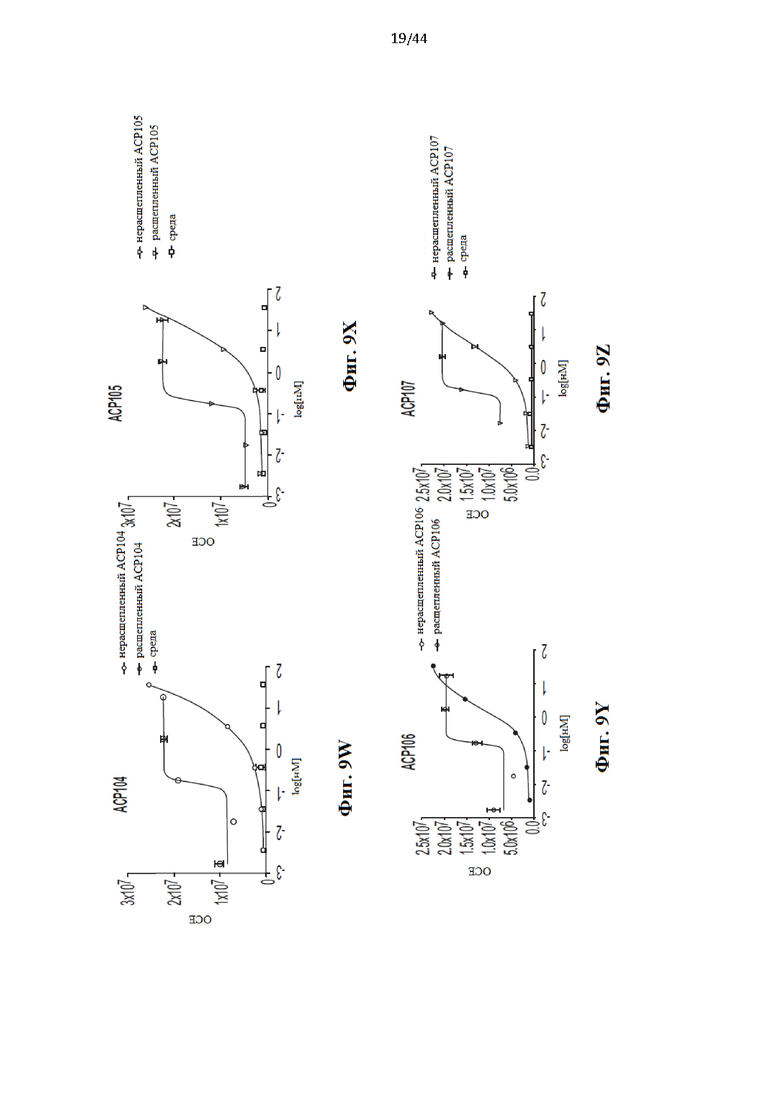


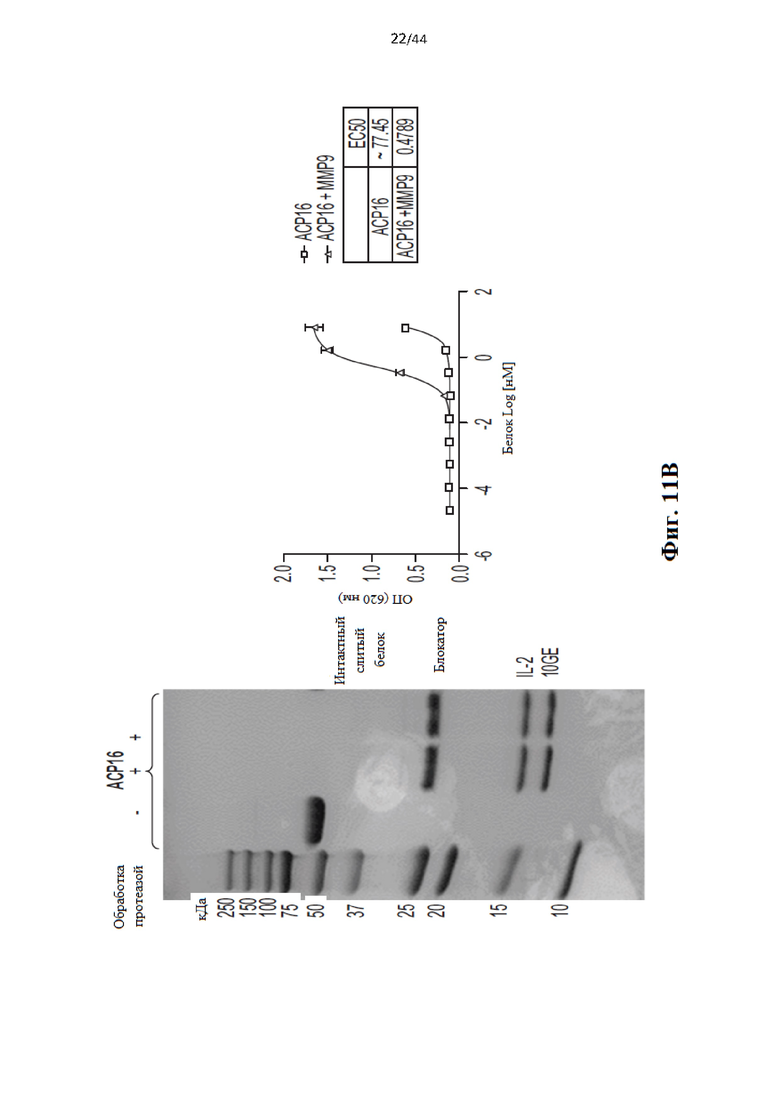





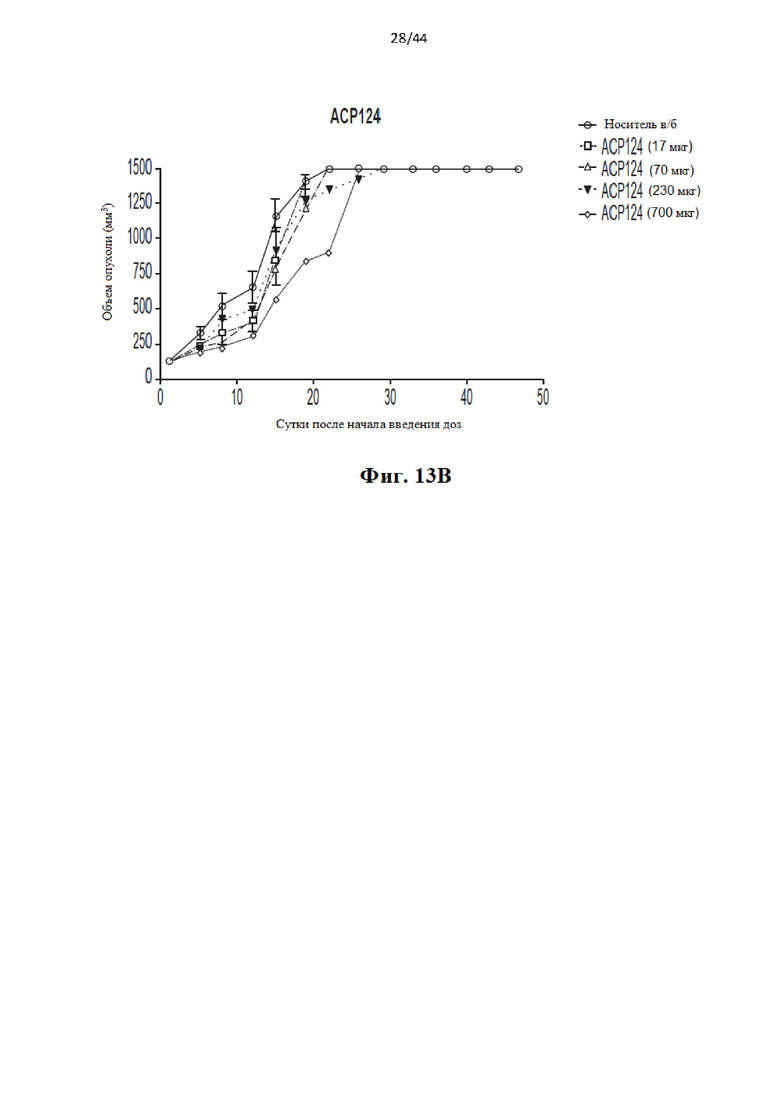



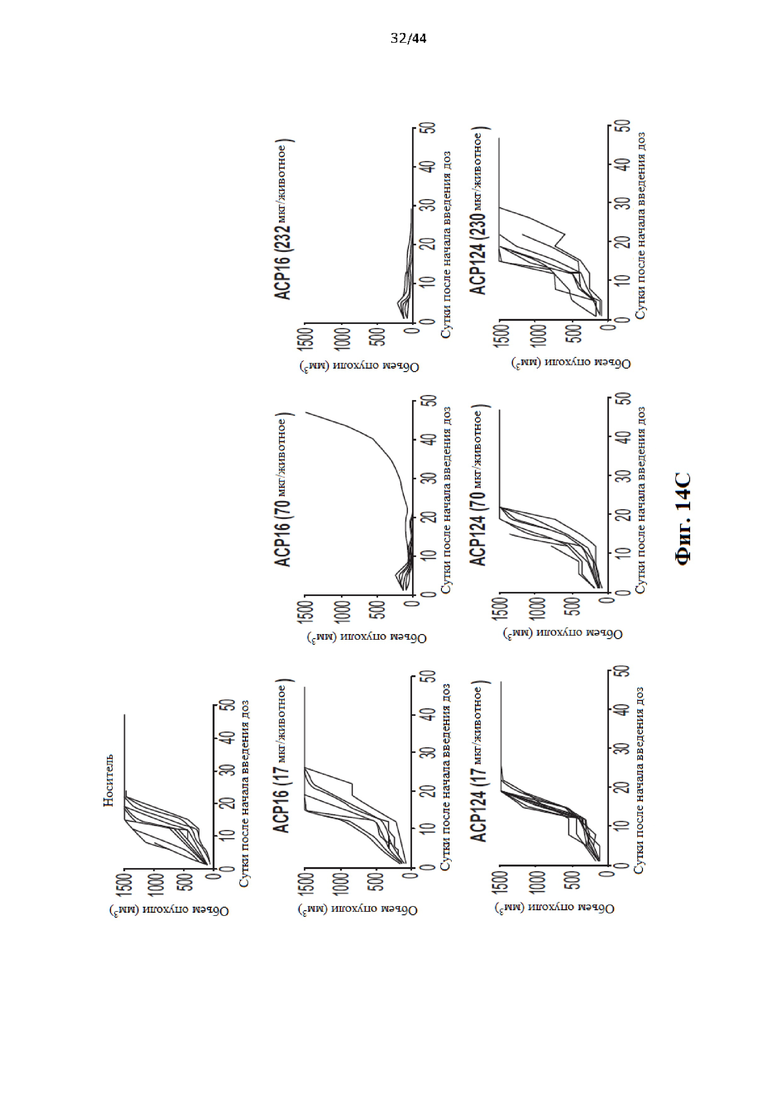





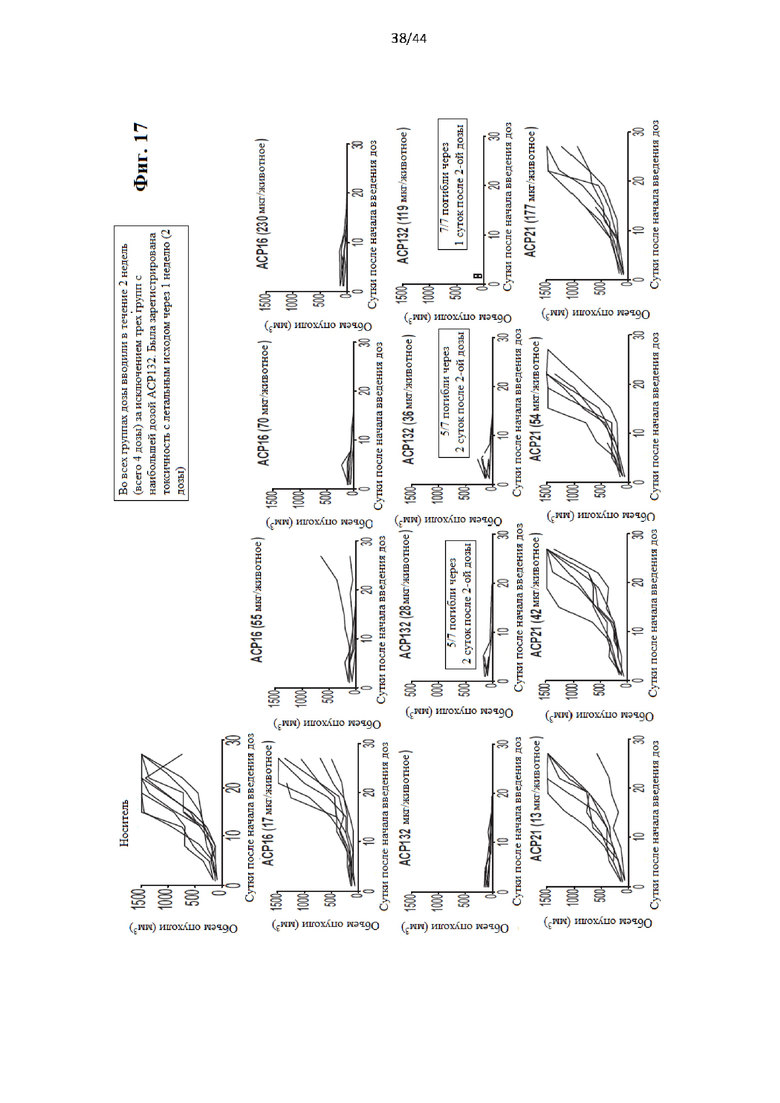

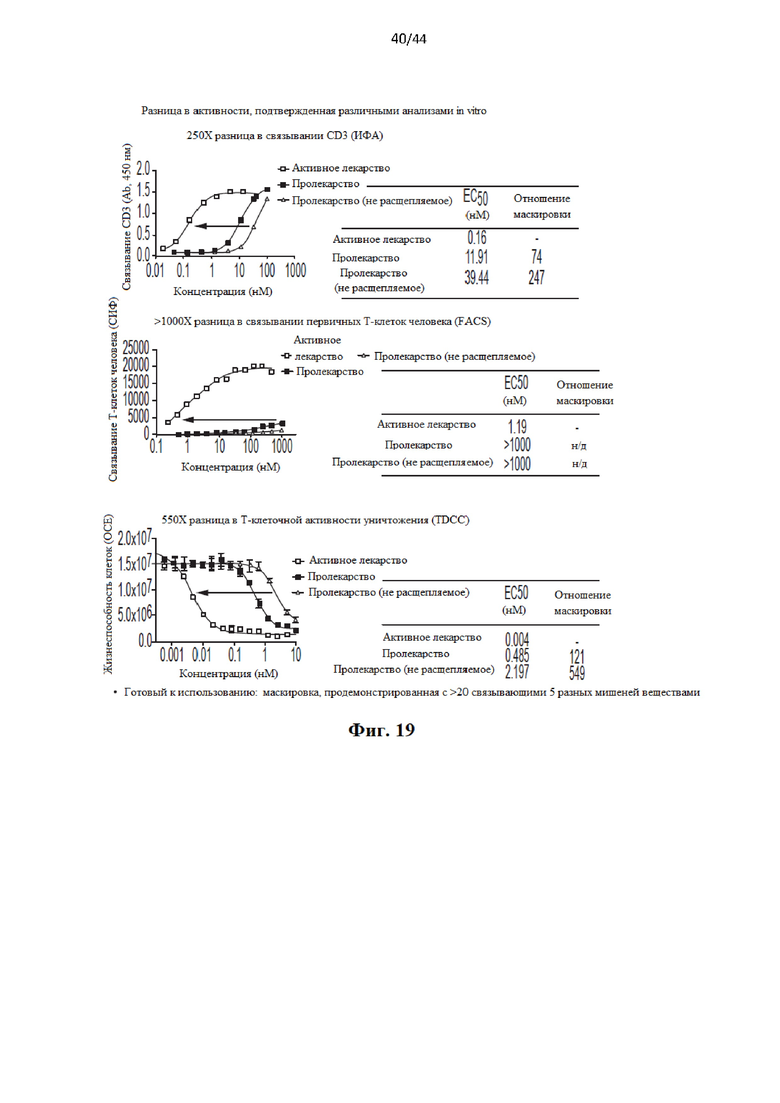
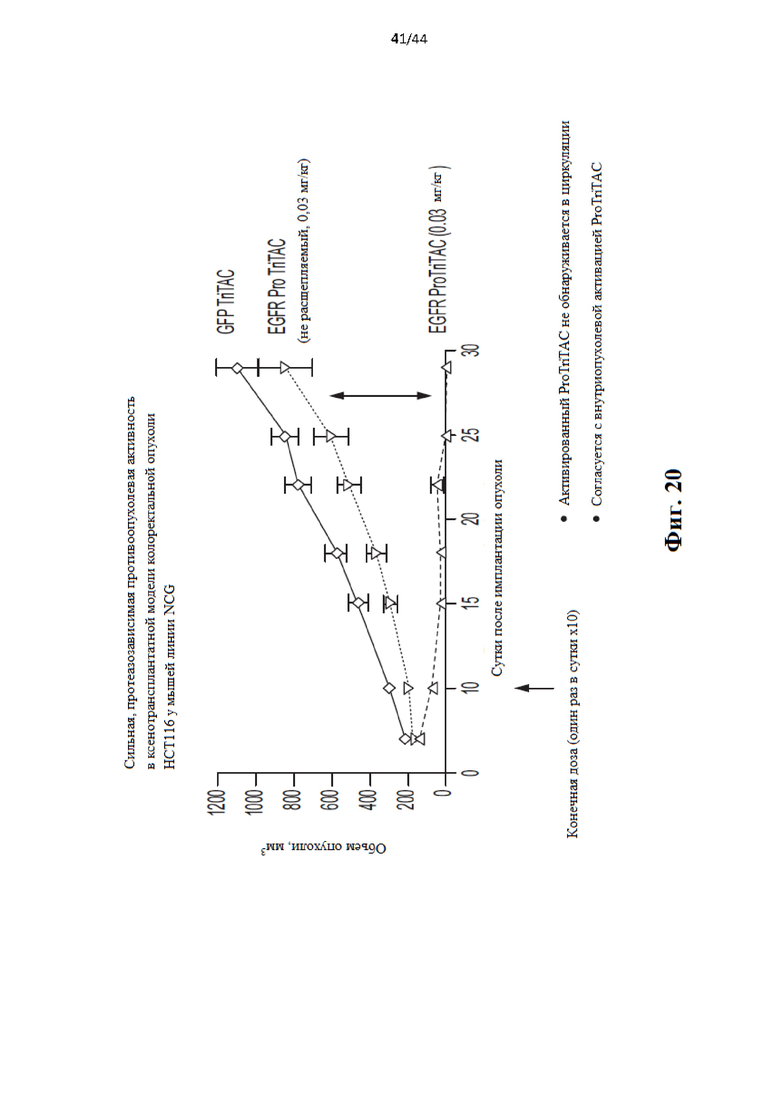
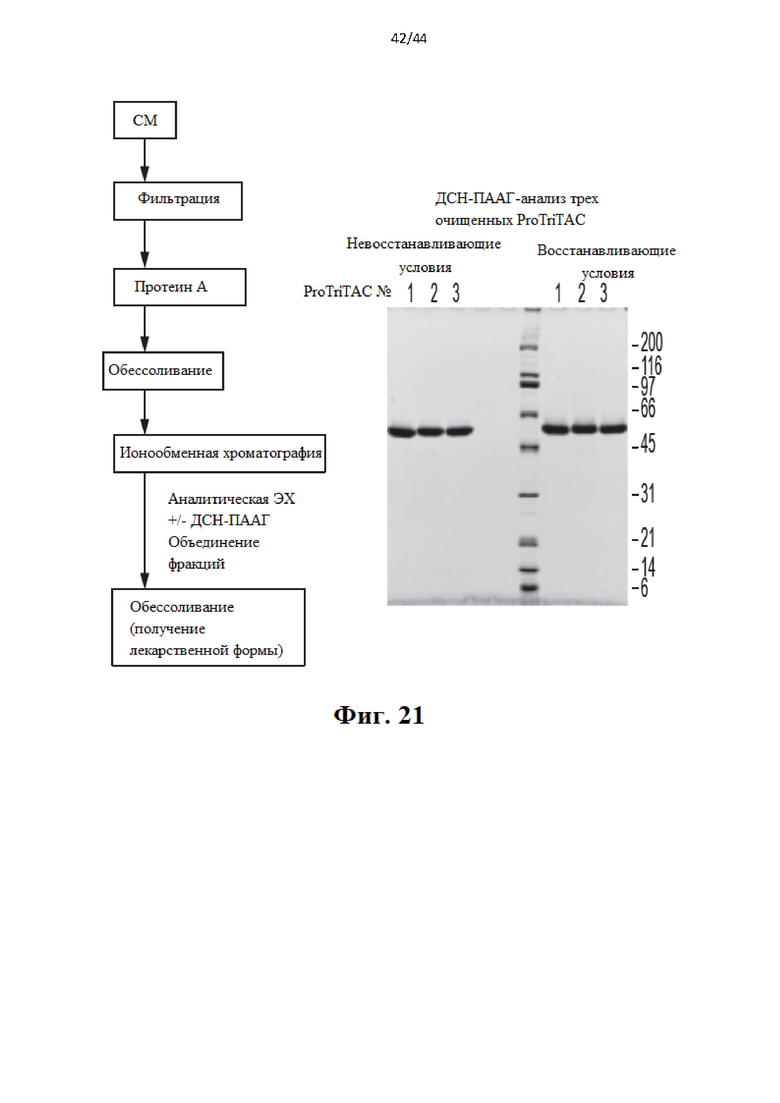


Изобретение относится к области биотехнологии, конкретно к получению слитых белков, которые являются кондиционально активными вариантами интерлейкина 2 (IL-2), и может быть использовано в медицине для лечения опухоли. Предложен кондиционально активный IL-2, содержащий слитый полипептид, в состав которого входит полипептид IL-2, элемент для продления времени полужизни и блокирующий IL-2 фрагмент, соединенные линкерами. Изобретение обеспечивает получение кондиционально активного пролекарства IL-2 с увеличенным периодом полужизни, которое доставляет активный IL-2 после расщепления протеазой, в частности, в желаемые места активности, такие как микроокружение опухоли. 4 н. и 6 з.п. ф-лы, 23 ил., 3 табл., 13 пр.
1. Кондиционально активный IL-2, содержащий слитый полипептид формулы:
[A]-[L1]-[B]-[L2]-[D] или [A]-[L1]-[D]-[L2]-[B] или [D]-[L2]-[B]-[L1]-[A] или
[B]-[L2]-[D]-[L1]-[A] или [D]-[L1]-[B]-[L1]-[A] или [B]-[L1]-[D]-[L1]-[A] или
[B]-[L1]-[A]-[L1]-[D] или [D]-[L1]-[A]-[L1]-[B]
где
[A] представляет собой полипептид интерлейкина 2 (IL-2);
[B] представляет собой элемент для продления времени полужизни, причем элемент для продления времени полужизни представляет собой человеческий сывороточный альбумин или антигенсвязывающий полипептид, который связывается с сывороточным альбумином, или Fc иммуноглобулина;
каждый из [L1] и [L2] независимо представляет собой полипептидный линкер, причем [L1] представляет собой расщепляемый протеазой полипептидный линкер, который содержит по меньшей мере одну последовательность, которая является расщепляемой протеазой, а [L2] является необязательно расщепляемым протеазой полипептидным линкером, и где расщепляемый протеазой линкер [L2] содержит по меньшей мере одну последовательность, которая является расщепляемой протеазой, причем для каждого из [L1] и [L2] независимо протеаза выбрана из группы, состоящей из калликреина, тромбина, химазы, карбоксипептидазы A, эластазы, PR-3, гранзима M, кальпаина, матриксной металлопротеиназы (MMP), белка активации фибробластов (FAP), металлопротеиназы ADAM, активатора плазминогена, катепсина, триптазы и поверхностной протеазы опухолевых клеток;
[D] представляет собой блокирующий IL-2 фрагмент, причем блокирующий IL-2 фрагмент представляет собой антитело или его антигенсвязывающий фрагмент, которое связывается с IL-2 или лигандсвязывающий домен, или фрагмент когнатного рецептора для полипептидаIL-2; и
при этом кондиционально активный IL-2 имеет ослабленную активирующую рецептор IL-2 активность, при этом активирующая рецептор IL-2 активность слитого полипептида является по меньшей мере в около 10 раз меньшей, чем активирующая рецептор IL-2 активность полипептида, который содержит полипептид IL-2, получаемый вследствие расщепления расщепляемого протеазой линкера L1, или, когда L2 является расщепляемым протеазой, вследствие расщепления как L1, так и L2, и причем активирующая рецептор IL-2 активность оценивается с использованием анализа пролиферации CTLL-2, ИФА фосфо-STAT, клеточного анализа с репортером HEK Blue, с эквивалентными молярными количествами полипептида IL-2 и слитого полипептида.
2. Кондиционально активный IL-2 по п. 1, отличающийся тем, что блокирующий фрагмент IL-2 ингибирует активацию рецептора IL-2 альфа/бета/гамма (IL-2Rαβγ) и рецептора IL-2 бета/гамма (IL-2Rβγ) полипептидом IL-2 в нерасщепленном слитом полипептиде.
3. Кондиционально активный IL-2 по п. 1, отличающийся тем, что [L2] является расщепляемым протеазой полипептидным линкером.
4. Кондиционально активный IL-2 по п. 1, отличающийся тем, что блокирующий IL-2 фрагмент нековалентно связывается с полипептидом IL-2.
5. Кондиционально активный IL-2 по п. 1, отличающийся тем, что блокирующий IL-2 фрагмент представляет собой фрагмент антитела, который связывается с полипептидом IL- 2, и фрагмент антитела представляет собой однодоменное антитело, Fab или scFv.
6. Кондиционально активный IL-2 по п. 1, отличающийся тем, что катепсин представляет собой катепсин В, катепсин С, катепсин D, катепсин Е, катепсин K, катепсин L или катепсин G.
7. Кондиционально активный IL-2 по п. 1, отличающийся тем, что матриксная металлопротеиназа (MMP) представляет собой MMP1, MMP2, MMP3, MMP8, MMP9, MMP10, MMP11, MMP12, MMP13 или MMP14.
8. Способ лечения опухоли, включающий введение нуждающемуся в этом субъекту эффективного количества кондиционально активного IL-2 по любому из пп. 1-7.
9. Применение кондиционально активного IL-2 по любому из пп. 1-7 для лечения опухоли у нуждающегося в этом субъекта.
10. Фармацевтическая композиция для лечения опухоли у нуждающегося в этом субъекта, содержащая в качестве активного ингредиента кондиционально активный IL-2 по любому из пп. 1-7.
| НУКЛЕИНОВО-КИСЛОТНЫЙ КОНСТРУКТ ДЛЯ ЭКСПРЕССИИ АКТИВНЫХ ВЕЩЕСТВ, КОТОРЫЕ МОГУТ БЫТЬ АКТИВИРОВАНЫ ПРОТЕАЗАМИ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ | 1998 |
|
RU2204414C2 |
| WO 2011123683 A2, 06.10.2011 | |||
| PUSKAS J | |||
| et al., Development of an attenuated interleukin-2 fusion protein that can be activated by tumour-expressed proteases, IMMUNOLOGY, 2011, v.133, n.2, p.206-220 | |||
| SKROMBOLAS D | |||
| et al., Challenges and developing solutions for increasing the benefits of IL-2 treatment in tumor | |||
Авторы
Даты
2024-09-11—Публикация
2019-05-14—Подача