ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к замещенному полипептидному соединению, обладающему эффектом ингибирования матриксной металлопротеазы 2 (далее подходящим образом сокращаемой как «ММР2»).
УРОВЕНЬ ТЕХНИКИ
Матриксная металлопротеаза представляет собой эндопептидазу с активным центром цинка, для которой известно 24 гена. ММР разрушает внеклеточный матрикс, включая коллаген и желатин, таким образом участвуя не только в физиологических реакциях, таких как ремоделирование кости и заживление ран, но и в патологических процессах, таких как воспаление и прогрессирование рака (см. NPTL 1).
Клинические испытания нескольких ингибиторов ММР ранее проводились с акцентом на противораковый эффект ингибирования ММР, но были прекращены из-за побочных эффектов, таких как боль в скелетных мышцах и возможное стимулирование метастазирования рака, которые, как предполагается, вызваны ингибирующим действием относительно не селективным в отношении подтипов MMP (см. NPTL 2 и 3).
Сообщалось, что активация MMP2 играет важную роль в инфильтрации и метастазировании раковых клеток. Инфильтрация и метастазирование раковых клеток являются ключевыми факторами, связанными с прогнозом злокачественной опухоли, и ингибирование активности MMP2 может служить эффективным терапевтическим средством для контроля рака. Рост рака подавляется у животных с нокаутом гена MMP2, и, как сообщается, MMP2 играет важную роль в росте рака (см. NPTL 4). Кроме того, было описано, что ММР2 ассоциируется с прогрессированием патологического состояния у пациентов с различными видами рака, такими как рак молочной железы, рак поджелудочной железы, рак мочевого пузыря, колоректальный рак, рак яичников, рак предстательной железы, опухоль головного мозга, рак желудка, гепатоцеллюлярная карцинома, рак головы и шеи, меланома, рак матки, рак пищевода, почечно-клеточная карцинома, рак легких и глиома (см. NPTL 5 и 6). Кроме того, было описано, что ММР2 вовлечена в образование патологического состояния даже при неопухолевых заболеваниях.
Сообщалось, что при хроническом заболевании почек, MMP2 вызывает эпителиально-мезенхимальный переход почечных канальцев путем преобразования структуры базальной мембраны канальцев, вызывая атрофию канальцев, фиброгенез и почечную дисфункцию (см. NPTL 7). Концентрации MMP2 в крови были обнаружены у пациентов с хроническим заболеванием почек (см. NPTL 8 и 9). Кроме того, сообщалось, что почечный фиброз, вызванный односторонней обструкцией мочеточника, подавляется у животных с нокаутом гена MMP2 (см. NPTL 10 и 11). В свете этого, ингибирование активности ММР2 для регуляции прогрессирования патологического состояния хронической болезни почек может служить эффективным терапевтическим средством.
Повышенная экспрессия MMP2 была обнаружена в альвеолярных эпителиальных клетках, фибробластах и макрофагах при идиопатическом фиброзе легких, и, в частности, повышенная экспрессия MMP2 в жидкости альвеолярного лаважа была обнаружена у пациентов с быстро прогрессирующим идиопатическим легочным фиброзом (см. NPTL 12 и 13). Кроме того, было описано влияние неселективного ингибитора ММР на снижение содержания коллагена в легких у мышей с индуцированным блеомицином легочным фиброзом (см. NPTL 14) и на предотвращение трансформации легочных паренхиматозных фибробластов, индуцированных TGF (см. NPTL 15). В свете этого, ингибирование активности MMP2 для регуляции прогрессирования патологического состояния идиопатического легочного фиброза может служить эффективным терапевтическим средством.
Кроме того, сообщалось о взаимосвязи между MMP2 и неопухолевыми заболеваниями, где неопухолевые заболевания включают рассеянный склероз, инфаркт головного мозга, атеросклероз, аневризму брюшной аорты, перитонеальный склероз, инфаркт миокарда, острое повреждение почек, диабетическую нефропатию, нефросклероз, гломерулонефрит, поликистоз почек, поликистоз печени, алкогольную болезнь печени, неалкогольный стеатогепатит, холестатическое поражение печени, хроническую обструктивную болезнь легких, интерстициальную пневмонию, диабетическую ретинопатию, возрастную дегенерацию желтого пятна, синдром Шегрена, менингит, мышечную дистрофию, склеродермию, воспалительные заболевания кишечника, и туберкулез (см. NPTL 16).
В свете вопросов, описанных выше, поиск средств для селективного ингибирования MMP2 представляет собой подход с высокой вероятностью создания эффективного терапевтического метода для заболеваний, в которые вовлечена MMP2.
Соединение с гидроксамовой кислотой или карбоновой кислотой, введенное в качестве хелатора цинка, было описано как низкомолекулярное соединение, обладающее эффектом ингибирования ММР2, однако не было известно ни о каком соединении, обладающем селективным ингибирующим эффектом к ММР2 (например, см. NPTL 17 и 18).
Сообщалось, что «β-амилоидный белок-предшественник (APP-IP, IIe-Ser-Tyr-Gly-Asn-Asp-Ala-Leu-Met-Pro)», пептидное соединение, состоящее из 10 природных аминокислот, проявляет селективный ингибирующий эффект к MMP2 (см. NPTL 19). Однако пептидные соединения, как правило, быстро метаболизируются и выводятся in vivo, поэтому известно, что даже при введении пептидного соединения, ожидаемый фармакологический эффект не сохраняется.
ПЕРЕЧЕНЬ ЦИТАТ
НЕ ПАТЕНТНАЯ ЛИТЕРАТУРА
NPL 1: H. J. Ra and W. C. Parks Matrix Biol., 2007, 26(8), 587-596.
NPL 2: A. H. Drummond et al. Ann N Y Acad Sci., 1999, 878, 228-235.
NPL 3: A. D. Baxter et al. Bioorg Med Chem Lett., 2001, 11, 1465-1468.
NPL 4: T. Itoh et al. Cancer Res., 1998, 58, 1048-1051.
NPL 5: R. Roy et al. J Clin Oncol., 2009, 27, 5287-5297.
NPL 6: T. Turpeenniemi-Hujanen Biochimie., 2005, 87, 287-297.
NPL 7: S. Cheng et al. FASEB J., 2006, 20, 1898-1900.
NPL 8: K. Pawlak et al. Clin Biochem., 2011, 44, 838-843.
NPL 9: H. R. Chang et al. Clin Chim Acta., 2006, 366, 243-248.
NPL 10: X. Du et al. Lab Invest., 2012, 92, 1149-1160.
NPL 11: M. K. Tveitaras et al. PLoS One., 2015, 10, e0143390.
NPL 12: M. Selman et al. Am J Physiol Lung Cell Mol Physiol., 2000, 279, L562-L574.
NPL 13: M. Suga et al. Am J Respir Crit Care Med., 2000, 162, 1949-1956.
NPL 14: M. Corbel et al. J Pathol., 2001, 193, 538-545.
NPL 15: J. Michael et al. Am J Respir Cell Mol Biol., 2009, 41, 731-741.
NPL 16: A. Tokito et al. Int J Mol Sci., 2016, 17, E1178.
NPL 17: D. E. Levy et al. J Med Chem., 1998, 41, 199-223.
NPL 18: Y. Tamura et al. J Med Chem., 1998, 41, 640-649.
NPL 19: S. Higashi et al. J Biol Chem., 2003, 278, 14020-14028.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ПРОБЛЕМА
Объектом настоящего изобретения является предоставление нового ингибитора MMP2.
РЕШЕНИЕ ПРОБЛЕМЫ
Авторы настоящего изобретения тщательно исследовали, чтобы достичь цели, и обнаружили, что соединение, представленное формулой [I'] (далее иногда называемое соединением [I']), обладает эффектом ингибирования ММР2.
Далее настоящее изобретение описывается подробно.
Более конкретно, варианты осуществления настоящего изобретения являются следующими.
(1) В качестве варианта осуществления по настоящему изобретению представлен замещенный полипептид, представленный формулой [I']:
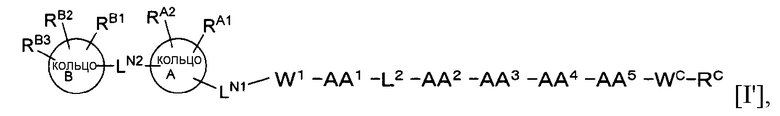
или его фармацевтически приемлемая соль,
где
AA1 представляет собой:
Asp,
β-Asp, β-(d)-Asp, γ-Glu или γ-(d)-Glu;
AA2 представляет собой одну группу, выбранную из группы, состоящей из:
Ala,
группы, представленной любой из формул [IV-7], [IV-8], [IV-9], [IV-11], [IV-12] и [IV-13]:
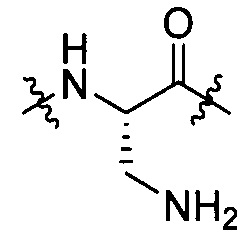 [IV-7],
[IV-7], 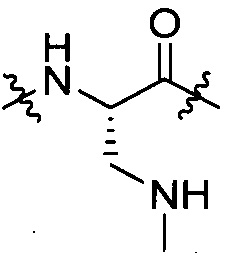 [IV-8],
[IV-8],  [IV-9],
[IV-9], 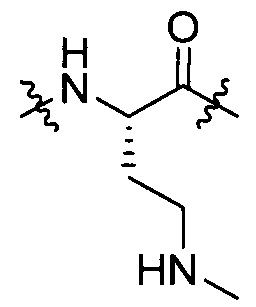 [IV-11],
[IV-11], 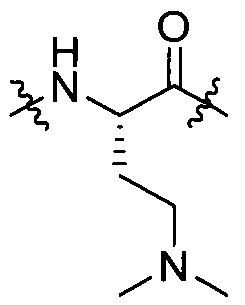 [IV-12],
[IV-12], 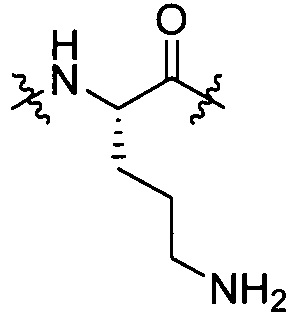 [IV-13]
[IV-13]
группы, представленной формулой [IV-27]:
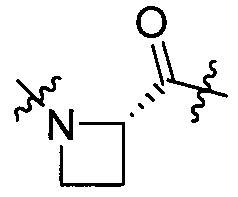 [IV-27]
[IV-27]
Pro и группы, представленной любой из формул [II-1] и [II-2]:
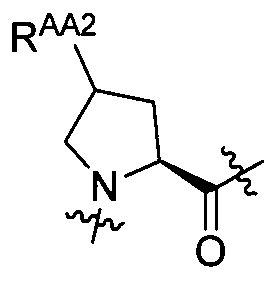 [II-1],
[II-1], 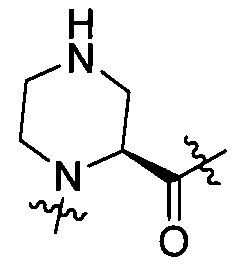 [II-2]
[II-2]
где RAA2 представляет собой гидрокси или амино; или
AA1 и AA2 могут быть взяты вместе с образованием структуры формулы [IV-32]:
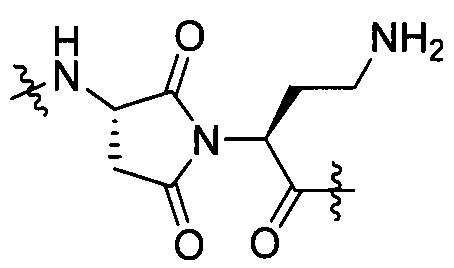 [IV-32];
[IV-32];
AA3 представляет собой одну группу, выбранную из группы, состоящей из:
Val, Leu, Ile, группы, представленной формулой [IV-2]:
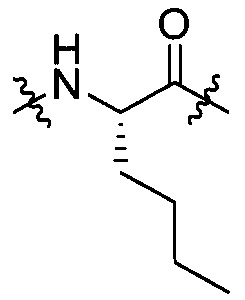 [IV-2]
[IV-2]
Phe, Trp,
Tyr, Lys, группы, представленной любой из формул [IV-3], [IV-4] и [IV-5]:
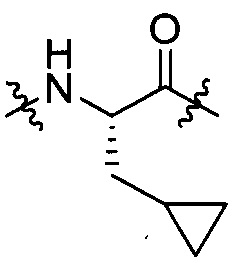 [IV-3],
[IV-3], 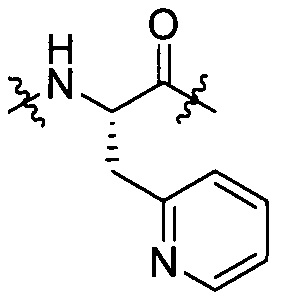 [IV-4],
[IV-4], 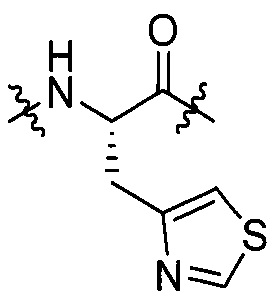 [IV-5]
[IV-5]
и
группы, представленной формулой [IV-9]:
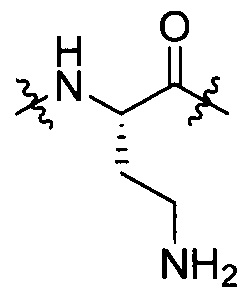 [IV-9];
[IV-9];
AA4 представляет собой одну группу, выбранную из группы, состоящей из:
одинарной связи,
Gly, (d)-Ala, (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile,
Pro, (d)-Pro,
(N-Me)Phe, (d)-Phe,
(N-Me)Tyr, (d)-Tyr,
(N-Me)Ser, (d)-Ser, гомоSer, (d)-Thr,
Met, (N-Me)Met,
(N-Me)Asp, Glu, (N-Me)Glu, (d)-(N-Me)Glu, гомоGlu,
(N-Me)Asn,
(N-Me)Arg, (d)-Arg,
группы, представленной любой из формул [IV-7], [IV-9] и [IV-13]:
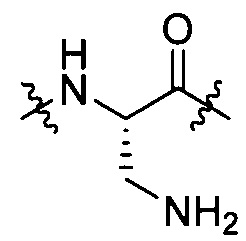 [IV-7],
[IV-7], 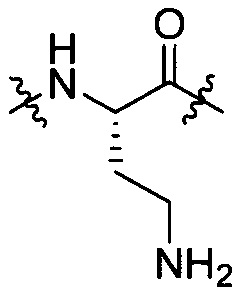 [IV-9],
[IV-9], 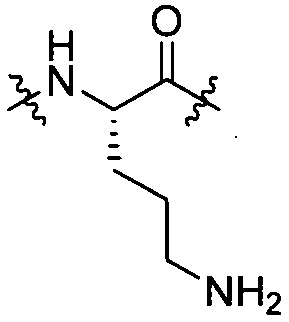 [IV-13]
[IV-13]
Lys и (N-Me)Lys,
где если AA4 представляет собой Lys, то
амино на боковой цепи Lys необязательно замещен C2-16 алкилкарбонилом, замещенным на конце карбокси;
AA5 представляет собой одну группу, выбранную из группы, состоящей из:
одинарной связи,
Ala, группы, представленной формулой [IV-1]:
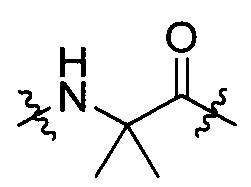 [IV-1]
[IV-1]
группы, представленной любой из формул [IV-27], [IV-28] и [IV-29]:
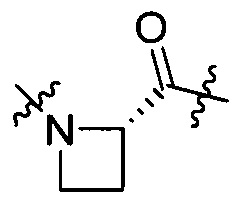 [IV-27],
[IV-27], 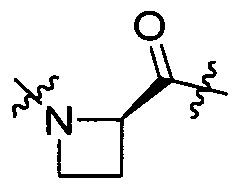 [IV-28],
[IV-28], 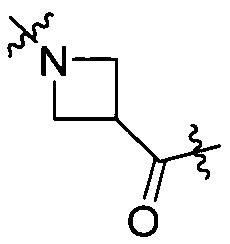 [IV-29]
[IV-29]
Pro, (d)-Pro, β-гомоPro, гомоPro, группы, представленной формулой [II-1']:
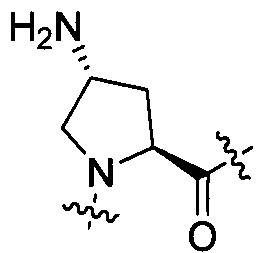 [II-1']
[II-1']
Phe, His,
Thr,
Arg, (d)-Arg,
группы, представленной любой из формул [IV-7], [IV-9] и [IV-13]:
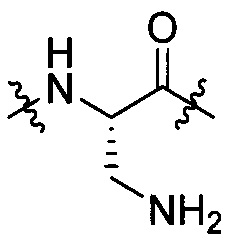 [IV-7],
[IV-7], 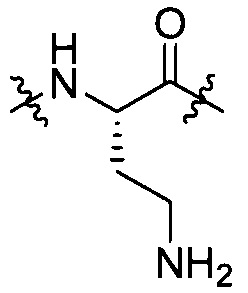 [IV-9],
[IV-9], 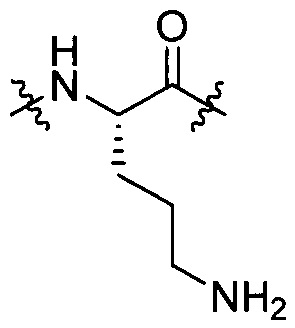 [IV-13]
[IV-13]
Lys, (d)-Lys,
β-Ala, (N-Me)-β-Ala, GABA, Ape, Acp,
группы, представленной любой из формул [III-6] и [III-13]:
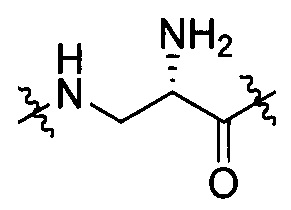 [III-6],
[III-6],  [III-7],
[III-7], 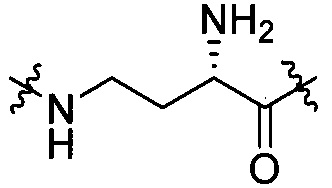 [III-8],
[III-8], 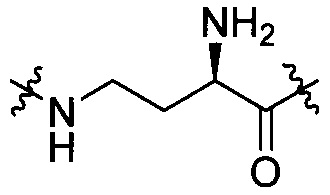 [III-9],
[III-9],  [III-10],
[III-10], 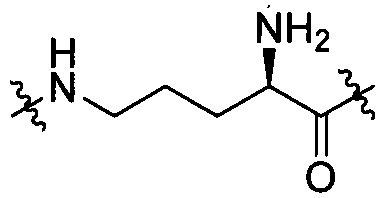 [III-11],
[III-11], 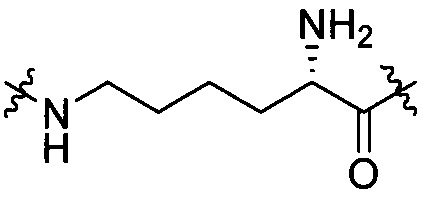 [III-12],
[III-12], 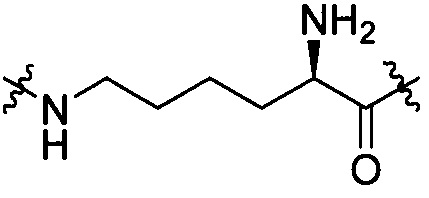 [III-13]
[III-13]
и
группы, представленной любой из формул [IV-25] и [IV-26]:
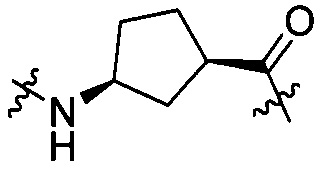 [IV-25],
[IV-25], 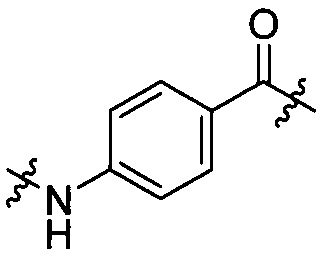 [IV-26];
[IV-26];
W1 представляет собой -L1- или -L1'-L1"-; где
L1 представляет собой одинарной связи; и
L1' представляет собой одну группу, выбранную из группы, состоящей из:
одинарной связи,
β-Ala, GABA, (N-Me)GABA, Ape, Acp,
группы, представленной любой из формул [III-6] - [III-13]
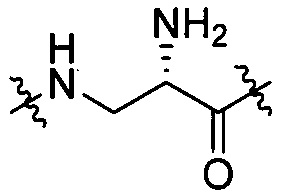 [III-6],
[III-6], 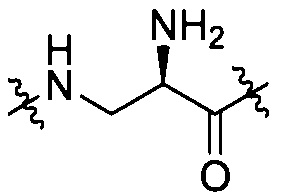 [III-7],
[III-7], 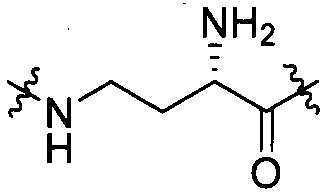 [III-8],
[III-8],  [III-9],
[III-9], 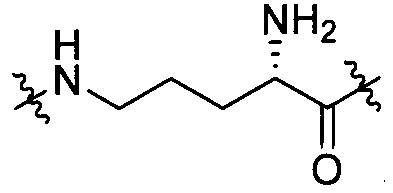 [III-10],
[III-10], 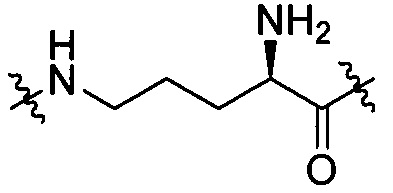 [III-11],
[III-11], 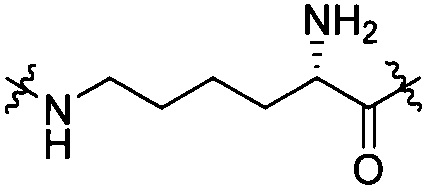 [III-12],
[III-12], 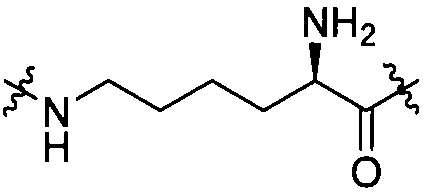 [III-13]
[III-13]
и
группы, представленной любой из формул [IV-23] и [IV-24]:
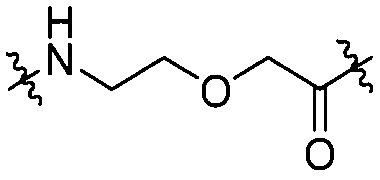 [IV-23],
[IV-23], 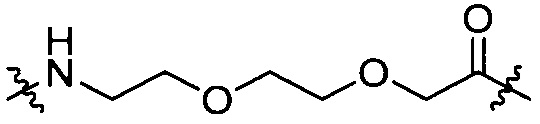 [IV-24];
[IV-24];
и
L1" представляет собой одну группу, выбранную из группы, состоящей из:
одинарной связи,
Gly, (N-Me)Gly,
Ala, (N-Me)Ala, (d)-Ala, Val, (N-Me)Val, (N-Me)Leu, (N-Me)Ile,
группы, представленной формулой [IV-27]:
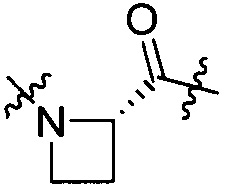 [IV-27]
[IV-27]
Pro, (d)-Pro, гомоPro, Phe, (N-Me)Phe, (d)-Phe,
His, (d)-His, Trp, (N-Me)Trp, (d)-Trp,
Tyr, (N-Me)Tyr, (d)-Tyr,
(d)-Ser, гомоSer, Thr, (N-Me)Thr, (d)-Thr,
Cys, (d)-Cys, Met, (N-Me)Met,
(N-Me)Asp, Glu, (N-Me)Glu, (d)-Glu,
Asn, (N-Me)Asn, (d)-Asn, Gln, (N-Me)Gln, (d)-Gln,
Arg, (N-Me)Arg, (d)-Arg, Cit, (d)-Cit,
группы, представленной любой из формул [IV-7], [IV-9], [IV-10] и [IV-13]:
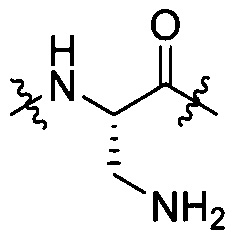 [IV-7],
[IV-7],  [IV-9],
[IV-9], 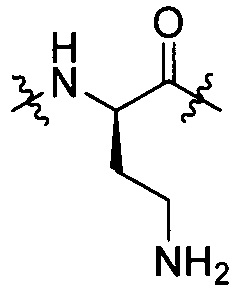 [IV-10],
[IV-10],
 [IV-13]
[IV-13]
Lys, (N-Me)Lys, (d)-Lys, группы, представленной формулой [IV-14]:
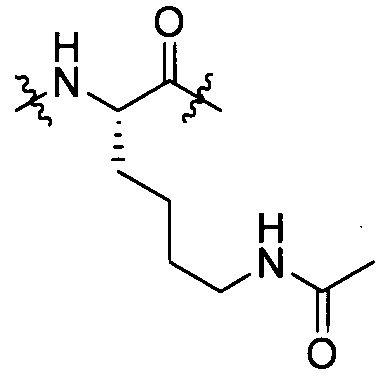 [IV-14]
[IV-14]
β-Ala,
β-Asp, β-(d)-Asp, и
группы, представленной любой из формул [III-6] и [III-7]:
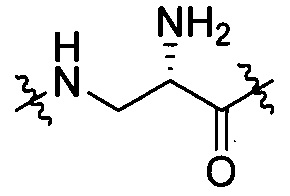 [III-6],
[III-6], 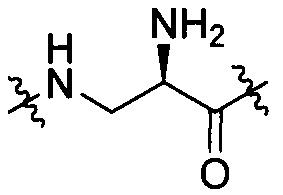 [III-7];
[III-7];
где если L1" представляет собой Lys или (d)-Lys, то
амино на боковой цепи Lys или (d)-Lys необязательно замещен группой, представленной формулой [VII-1]:
FAN-AAN5-AAN4-AAN3-AAN2-AAN1- [VII-1]
где
FAN представляет собой C2-16 алкилкарбонил, замещенный на конце карбокси;
AAN5 представляет собой:
одинарную связь,
Arg, (d)-Arg,
Lys, (d)-Lys,
γ-Glu, или
группу, представленную формулой [IV-24]:
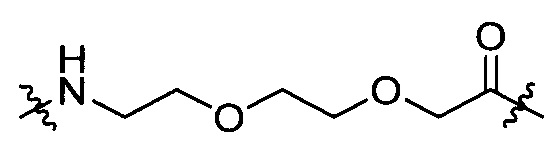 [IV-24];
[IV-24];
AAN4 представляет собой:
одинарную связь,
Arg, (d)-Arg,
Lys, (d)-Lys, или
группу, представленную формулой [IV-24]:
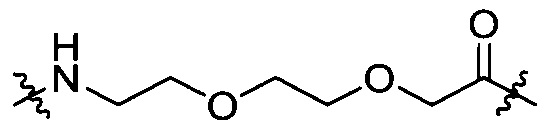 [IV-24];
[IV-24];
AAN3 представляет собой:
одинарную связь,
Arg, (d)-Arg,
Lys, (d)-Lys,
γ-Glu, или
группу, представленную формулой [IV-24]:
 [IV-24];
[IV-24];
AAN2 представляет собой:
одинарную связь, или
(d)-Lys; и
AAN1 представляет собой:
одинарную связь, или
(d)-Lys;
где если L1" представляет собой Glu и AA3 представляет собой Lys, то
соединение, представленное формулой [I'] может быть взято вместе с L3, присоединенным к каждой из функциональных групп на боковых цепях двух аминокислот с образованием циклической структуры, как представлено формулой [I'-α]:
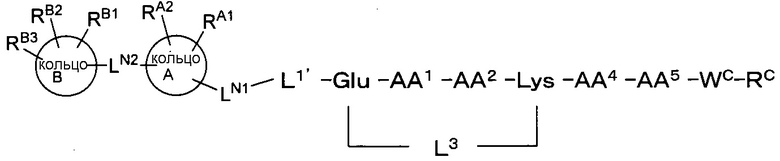 [I'-α]
[I'-α]
где L3 представляет собой Gly, β-Ala или GABA;
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-;
LN2 представляет собой:
одинарную связь,
C1-3 алкандиил,
C2-3 алкендиил,
этиндиил,
формулу -O-,
формулу -C(=O)-, формулу -C(=O)-NH-, или
триазолдиил;
L2 представляет собой одинарную связь;
кольцо A представляет собой ароматическое кольцо или гетероароматическое кольцо;
RA1 и RA2 каждый независимо представляет собой:
атом водорода,
атом галогена,
C1-6 алкил, или
C1-6 алкокси;
кольцо B представляет собой:
арил или гетероарил;
RB1, RB2 и RB3 каждый независимо представляет собой:
атом водорода,
карбамоил,
циано,
атом галогена,
C1-6 алкил, необязательно замещенный одним гидрокси, галоген C1-6 алкилом,
C1-6 алкокси, необязательно замещенный одним гидрокси, галоген C1-6 алкокси,
C1-6 алкилкарбонил,
C1-6 алкилкарбониламино,
моно C1-6 алкиламинокарбонил, ди C1-6 алкиламинокарбонил, где алкил в каждом из моно C1-6 алкиламинокарбонила и ди C1-6 алкиламинокарбонила необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, карбокси, карбамоила и амино,
C1-6 алкилсульфонил, или
арил;
WC представляет собой одинарную связь или линкер, состоящий из одной-трех аминокислот, где одна-три аминокислоты, образующие линкер, являются одинаковыми или разными, и каждая выбрана из группы, состоящей из:
Gly,
Pro,
Arg, (d)-Arg,
Lys, (d)-Lys,
β-Ala, GABA и Ape,
где если Lys или (d)-Lys включена в группу, представленную WC, то
амино на боковой цепи Lys или (d)-Lys необязательно замещен:
C2-16 алкилкарбонилом, замещенным на конце карбокси,
Lys, где амино на боковой цепи Lys необязательно замещен C2-16 алкилкарбонилом, замещенным на конце карбокси, или
(d)-Lys, где амино на боковой цепи (d)-Lys необязательно замещен C2-16 алкилкарбонилом, замещенным на конце карбокси; и
RC представляет собой:
формулу -OH, формулу -NH2,
C1-6 алкиламино, где C1-6 алкил из C1-6 алкиламино необязательно замещен одну группу, выбранную из группы, состоящей из гидрокси, амино, C1-6 алкокси и четырех-семи-членного насыщенного гетероциклила, содержащего один атом азота и необязательно другой, содержащий один гетероатом, или
четырех-семи-членного насыщенного гетероциклила, содержащего один атом азота и необязательно другой, содержащий один гетероатом, где четырех-семи-членный насыщенный гетероциклил, содержащий один атом азота и необязательно другой, содержащий один гетероатом, необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, амино и C1-6 алкила, где C1-6 алкил необязательно замещен одним карбамоилом; и два атома углерода в четырех-семи-членном насыщенном гетероциклиле, содержащем один атом азота и необязательно другой, содержащий один гетероатом, необязательно перекрестно сшит с C1-4 алкандиилом.
(2) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно (1), где
WC представляет собой:
одинарную связь,
Pro,
Arg, (d)-Arg,
Lys, (d)-Lys,
β-Ala, GABA, Ape,
Gly-(d)-Lys, Gly-(d)-Lys-(d)-Lys, Gly-(d)-Lys-(d)-Arg, Gly-(d)-Arg-(d)-Lys,
Lys-Lys, (d)-Lys-(d)-Lys, (d)-Lys-(d)-Lys-(d)-Lys,
Arg-Arg, (d)-Arg-(d)-Arg, (d)-Arg-(d)-Lys,
Lys-(d)-Lys-(d)-Lys, (d)-Lys-Lys-(d)-Lys, (d)-Lys-(d)-Lys-Lys,
β-Ala-(d)-Lys, β-Ala-(d)-Lys-(d)-Arg, β-Ala-(d)-Arg-(d)-Lys или β-Ala-(d)-Arg-(d)-Arg
где если Lys содержится в группе, представленной WC,
то амино на боковой цепи Lys необязательно замещен:
C2-16 алкилкарбонилом, замещенным на конце карбокси, или
(d)-Lys, где амино на боковой цепи (d)-Lys необязательно замещен C2-16 алкилкарбонилом, замещенным на конце карбокси.
(3) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно (1) или (2), где
кольцо A представляет собой бензольное кольцо, тиофеновое кольцо или пиридиновое кольцо;
RA1 и RA2 каждый независимо представляет собой:
атом водорода, или
атом галогена;
кольцо B представляет собой:
фенил, оксазолил, тиадиазолил, пиридил или бензофуранил;
RB1, RB2 и RB3 каждый независимо представляет собой:
атом водорода,
карбамоил,
циано,
атом галогена,
C1-6 алкил, где C1-6 алкил необязательно замещен одним гидрокси,
галоген C1-6 алкил,
C1-6 алкокси, где C1-6 алкокси необязательно замещен одним гидрокси,
галоген C1-6 алкокси,
C1-6 алкилкарбонил,
моно C1-6 алкиламинокарбонил, ди C1-6 алкиламинокарбонил, где алкил в каждом из моно C1-6 алкиламинокарбонила и ди C1-6 алкиламинокарбонила необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, карбокси, карбамоила и амино, или
C1-6 алкилсульфонил; и
RC представляет собой:
формулу -OH, формулу -NH2,
C1-6 алкиламино, где C1-6 алкил из C1-6 алкиламино необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, амино, C1-6 алкокси и морфолинила, или
азетидинил, пирролидинил, пиперидинил, морфолинил или пиперазинил, где азетидинил, пирролидинил, пиперидинил, морфолинил или пиперазинил необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, амино и C1-6 алкила, где C1-6 алкил необязательно замещен одним карбамоилом, где
два атома углерода в азетидиниле, пирролидиниле, пиперидиниле, морфолиниле или пиперазиниле необязательно перекрестно сшиты с C1-4 алкандиилом.
(4) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (3), где в замещенном полипептиде, представленном формулой [I'],
кольцо A представляет собой бензольное кольцо;
кольцо B представляет собой фенил;
L1" представляет собой одну группу, выбранную из группы, состоящей из:
одинарной связи,
Gly, (N-Me)Gly,
Ala, (N-Me)Ala, (d)-Ala, Val, (N-Me)Val, (N-Me)Leu, (N-Me)Ile,
группы, представленной формулой [IV-27]:
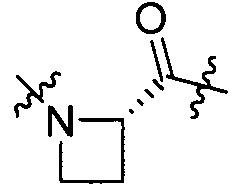 [IV-27]
[IV-27]
Pro, (d)-Pro, гомоPro, Phe, (N-Me)Phe, (d)-Phe,
His, (d)-His, Trp, (N-Me)Trp, (d)-Trp,
Tyr, (N-Me)Tyr, (d)-Tyr,
(d)-Ser, гомоSer, Thr, (N-Me)Thr, (d)-Thr,
Cys, (d)-Cys, Met, (N-Me)Met,
(N-Me)Asp, Glu, (N-Me)Glu, (d)-Glu,
Asn, (N-Me)Asn, (d)-Asn, Gln, (N-Me)Gln, (d)-Gln,
Arg, (N-Me)Arg, (d)-Arg, Cit, (d)-Cit,
группы, представленной любой из формул [IV-7], [IV-9], [IV-10] и [IV-13]:
 [IV-7],
[IV-7],  [IV-9],
[IV-9], 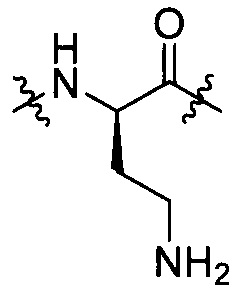 [IV-10],
[IV-10],  [IV-13]
[IV-13]
Lys, (N-Me)Lys, (d)-Lys, группы, представленной формулой [IV-14]:
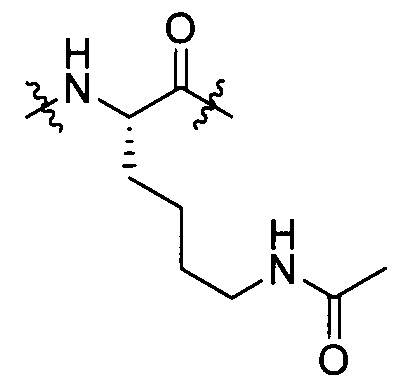 [IV-14]
[IV-14]
β-Ala,
β-Asp, β-(d)-Asp, и
группы, представленной любой из формул [III-6] и [III-7]:
 [III-6],
[III-6], 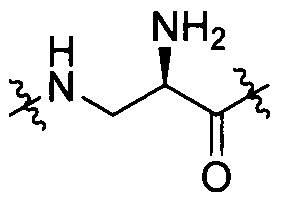 [III-7];
[III-7];
и
WC представляет собой:
одинарную связь,
Pro,
Arg, (d)-Arg,
Lys, (d)-Lys,
β-Ala, GABA, Ape,
Gly-(d)-Lys, Gly-(d)-Lys-(d)-Lys, Gly-(d)-Lys-(d)-Arg, Gly-(d)-Arg-(d)-Lys,
Lys-Lys, (d)-Lys-(d)-Lys, (d)-Lys-(d)-Lys-(d)-Lys,
Arg-Arg, (d)-Arg-(d)-Arg, (d)-Arg-(d)-Lys,
Lys-(d)-Lys-(d)-Lys, (d)-Lys-Lys-(d)-Lys, (d)-Lys-(d)-Lys-Lys,
β-Ala-(d)-Lys, β-Ala-(d)-Lys-(d)-Arg,
β-Ala-(d)-Arg-(d)-Lys или β-Ala-(d)-Arg-(d)-Arg.
(5) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (4), где в замещенном полипептиде, представленном формулой [I'],
AA2 представляет собой одну группу, выбранную из группы, состоящей из:
группы, представленной формулой [II-1]:
 [II-1]
[II-1]
и
группы, представленной любой из формул [IV-7], [IV-8], [IV-9], [IV-11] и [IV-12]:
 [IV-7],
[IV-7],  [IV-8],
[IV-8],  [IV-9],
[IV-9],  [IV-11],
[IV-11],  [IV-12]
[IV-12]
где RAA2 представляет собой амино;
AA3 представляет собой Val, Leu, Ile, Phe или Trp;
AA4 представляет собой (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Asp или (N-Me)Glu;
AA5 представляет собой β-Ala, GABA, Ape, Acp, Pro, (d)-Pro или β-гомоPro;
WC представляет собой одинарную связь, Arg, (d)-Arg, Lys или (d)-Lys; и
RC представляет собой формулу -OH или формулу -NH2.
(6) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (5), где в замещенном полипептиде, представленном формулой [I'],
W1 представляет собой -L1'-L1"-;
L2 представляет собой одинарную связь;
AA1 представляет собой Asp;
L1' представляет собой одну группу, выбранную из группы, состоящей из β-Ala, GABA, Ape, Acp и группы, представленной любой из формул [IV-23] и [IV-24]:
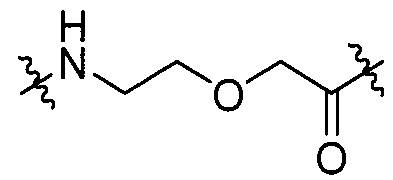 [IV-23],
[IV-23], 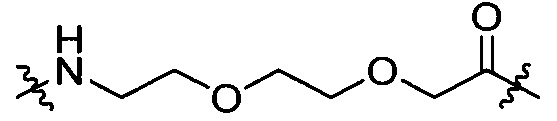 [IV-24];
[IV-24];
L1" представляет собой одинарную связь, Asn, (d)-Ser, (d)-Thr или Glu;
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-;
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-;
RA1 и RA2 каждый представляет собой атом водорода; и
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси.
(7) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (5), где в замещенном полипептиде, представленном формулой [I'],
W1 представляет собой -L1-, где L1 представляет собой одинарную связь;
L2 представляет собой одинарную связь;
AA1 представляет собой β-Asp, β-(d)-Asp, γ-Glu или γ-(d)-Glu;
AA2 представляет собой одну группу, выбранную из группы, состоящей из:
группы, представленной формулой [II-1]:
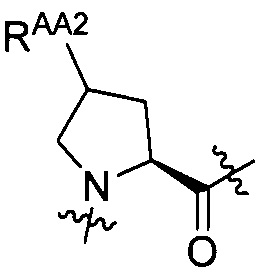 [II-1]
[II-1]
и
группы, представленной любой из формул [IV-7], [IV-8], [IV-9], [IV-11] и [IV-12]:
 [IV-7],
[IV-7],  [IV-8],
[IV-8],  [IV-9],
[IV-9],  [IV-11],
[IV-11],  [IV-12]
[IV-12]
где RAA2 представляет собой амино;
AA3 представляет собой Val, Leu, Ile, Phe или Trp;
AA4 представляет собой (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Asp или (N-Me)Glu;
AA5 представляет собой β-Ala, GABA, Ape, Acp или β-гомоPro;
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-;
LN2 представляет собой одинарную связь, формулу -O- или формулу -C(=O)-NH-;
RA1 и RA2 каждый представляет собой атом водорода; и
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси.
(8) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (4), где замещенный полипептид, представленный формулой [I'] представляет собой замещенный полипептид, представленный формулой [1]:
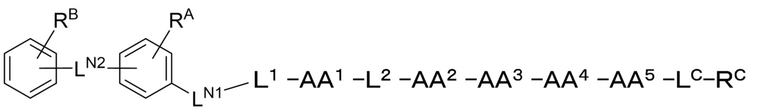 [1]
[1]
где
AA1 представляет собой β-Asp, γ-Glu или γ-(d)-Glu;
AA2 представляет собой группы, представленной формулой [II-1] или формулой [II-2]:
 [II-1],
[II-1], 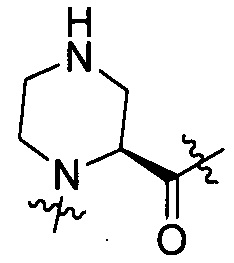 [II-2]
[II-2]
где RAA2 представляет собой гидрокси или амино;
AA3 представляет собой Val, Leu, Ile, Phe или Trp;
AA4 представляет собой одинарную связь, Pro, (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Asp или (N-Me)Glu;
AA5 представляет собой одинарную связь, Pro, (d)-Pro, β-гомоPro, Arg, (d)-Arg, Lys, (d)-Lys, β-Ala, GABA, Ape или Acp;
L1 представляет собой одинарную связь;
L2 представляет собой одинарную связь;
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-;
LN2 представляет собой одинарную связь, C1-3 алкандиил, формулу -O- или формулу -C(=O)-NH-;
RA представляет собой атом водорода, атом галогена, C1-6 алкил или C1-6 алкокси;
RB представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкил или C1-6 алкокси;
LC представляет собой одинарную связь, Pro, Arg, (d)-Arg, Lys, (d)-Lys или (d)-Lys-(d)-Lys; и
RC представляет собой формулу -OH или формулу -NH2.
(9) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (5), где в замещенном полипептиде, представленном формулой [I'],
AA1 представляет собой Asp, β-(d)-Asp или γ-(d)-Glu;
AA2 представляет собой одну группу, выбранную из группы, состоящей из:
группы, представленной формулой [II-1]:
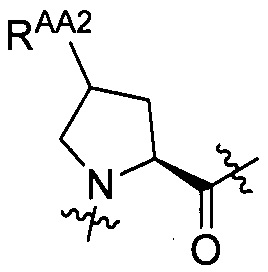 [II-1]
[II-1]
и
группы, представленной любой из формул [IV-7] и [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
где RAA2 представляет собой амино;
AA3 представляет собой Val, Leu или Ile;
AA4 представляет собой (N-Me)Ile или (N-Me)Glu;
AA5 представляет собой Ape или β-гомоPro;
W1 представляет собой -L1- или -L1'-L1"-,
где
L1 представляет собой одинарную связь,
L1' представляет собой GABA или Ape, и
L1" представляет собой Asn, (d)-Ser, (d)-Thr или Glu;
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-;
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-;
RA1 и RA2 каждый представляет собой атом водорода;
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси;
WC представляет собой одинарную связь или (d)-Lys; и
RC представляет собой формулу -NH2.
(10) В качестве другого варианта осуществления настоящего изобретения представлен замещенный полипептид или его фармацевтически приемлемая соль согласно любому из (1) - (5), где замещенный полипептид выбран из соединений, показанных в следующих:
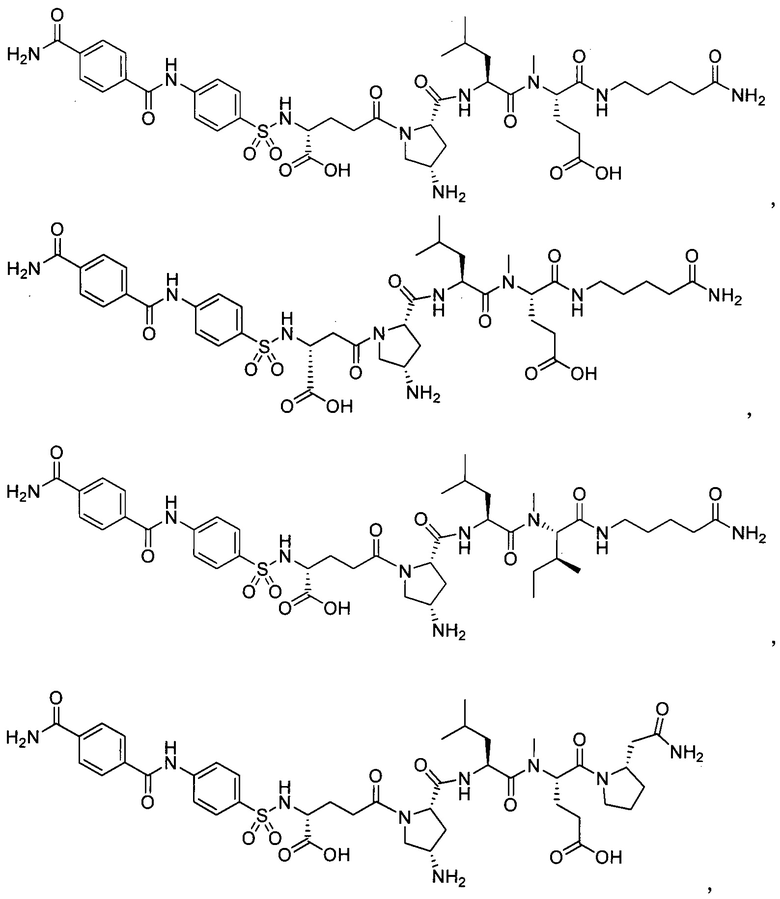
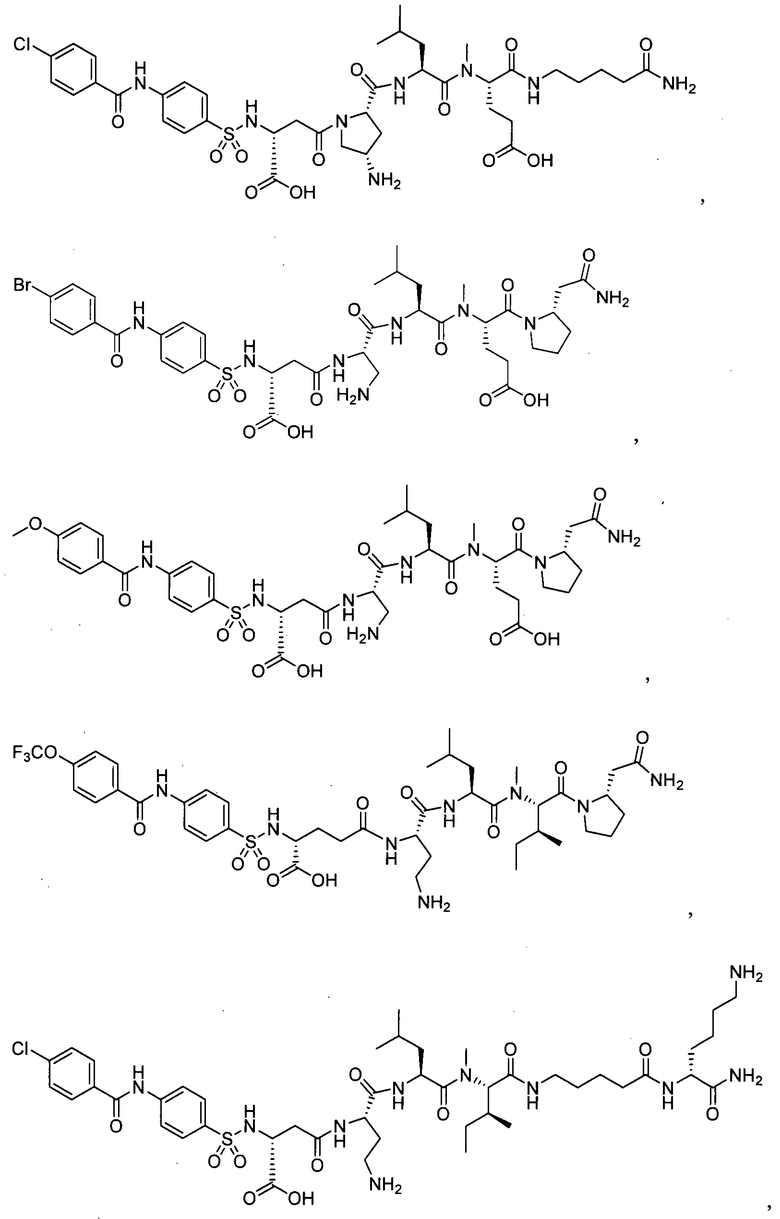
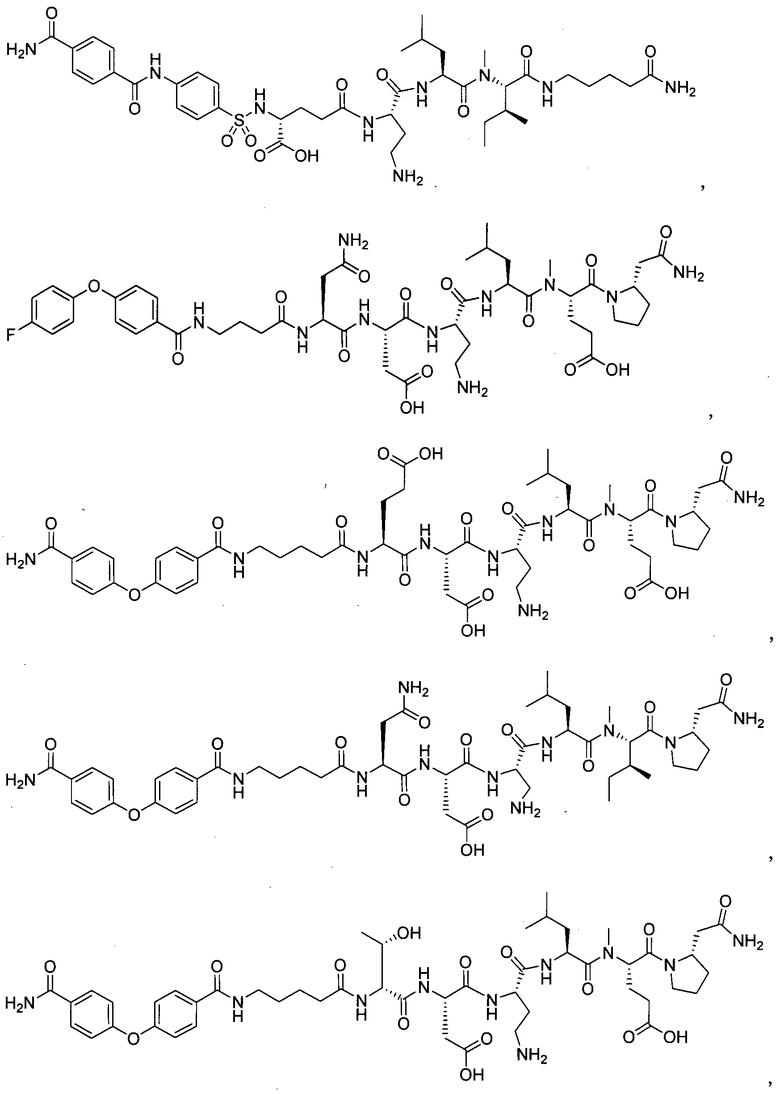
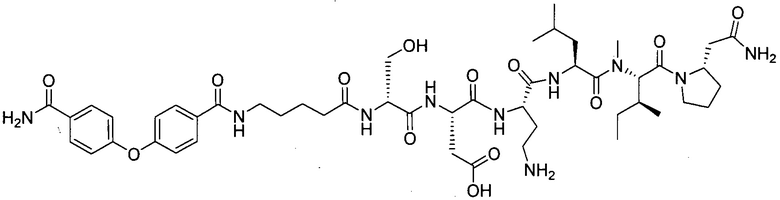
(11) В качестве другого варианта осуществления настоящего изобретения, представлен фармацевтический препарат, содержащий замещенный полипептид или его фармацевтически приемлемую соль по любому из (1) - (10) в качестве активного ингредиента.
(12) В качестве другого варианта осуществления настоящего изобретения, представлен ингибитор MMP2, содержащий замещенный полипептид или его фармацевтически приемлемую соль по любому из (1) - (10) в качестве активного ингредиента.
(13) В качестве другого варианта осуществления настоящего изобретения, представлен агент для подавления роста, инфильтрации или метастазирования раковых клеток, содержащий замещенный полипептид или его фармацевтически приемлемую соль по любому из (1) - (10) в качестве активного ингредиента.
(14) В качестве другого варианта осуществления настоящего изобретения, предложен агент для подавления фиброгенеза, содержащий замещенный полипептид или его фармацевтически приемлемую соль по любому из (1) - (10) в качестве активного ингредиента.
(15) В качестве другого варианта осуществления настоящего изобретения, представлено лекарственное средство для профилактики или лечения ракового заболевания или фиброза органов, или симптома, связанного с раковым заболеванием или фиброзом органов, содержащее замещенный полипептид или его фармацевтически приемлемую соль согласно любому из (1) - (10) в качестве активного ингредиента.
ПРЕИМУЩЕСТВА ИЗОБРЕТЕНИЯ
Соединения по настоящему изобретению (далее иногда называемые «соединениями по настоящему изобретению») обладают эффектом ингибирования ММР2. Некоторые из соединений по настоящему изобретению обладают эффектом селективного ингибирования ММР2.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение представляет замещенный полипептид, представленный формулой [I'] или его фармацевтически приемлемую соль, обладающую эффектом ингибирования MMP2.
Соединения по настоящему изобретению будут описаны более подробно ниже, однако настоящее изобретение не ограничивается приведенными в качестве примеров соединениями.
В настоящем документе «аминокислота» в широком смысле означает органическое соединение, имеющее две функциональные группы: амино и карбокси, в узком смысле (в частности, в области биохимии) «аминокислота» означает «α-аминокислоту». (α-аминокислота представляет собой аминокислоту, в которой аминогруппа связана с атомом углерода, с которым связан карбокси (α углерод)), которая служит составной единицей биогенных белков.
Примеры аминокислот в настоящем описании включают природные протеогенные L-аминокислоты; природные не протеогенные аминокислоты и аминокислоты не природного происхождения. Примеры аминокислот не природного происхождения включают D-формы природных протеогенных L-аминокислот; химически модифицированные аминокислоты, такие как аминокислоты варианты и производные; и химически синтезированные соединения, обладающие свойствами, характерными для аминокислот, и известные в данной области техники.
В настоящем документе, когда «аминокислота» представлена в виде ее названия без сокращения, например, в виде трехбуквенного кода или однобуквенного кода, где название указывает на аминокислоту в L-форме, D-форме или в обеих формах.
В настоящем документе, когда «аминокислота» представлена в виде сокращения, например, в трехбуквенном коде или однобуквенном коде, сокращение означает аминокислоту в L-форме. «L» или «l» иногда добавляют непосредственно перед «аминокислотой», чтобы явно показать, что аминокислота находится в L-форме.
В настоящем документе «D» или «d», добавленные непосредственно перед «аминокислотой», указывают, что аминокислота находится в D-форме.
В настоящем документе «природная протеогенная L-аминокислота» представляет собой встречающуюся в природе аминокислоту в L-форме, которая составляет белки, и ее примеры включают Gly, Ala, Val, Leu, Ile, Pro, Phe, His, Trp, Tyr, Ser, Thr, Met, Cys, Asp, Glu, Asn, Gln, Lys и Arg.
В настоящем документе «D-форма природной протеогенной L-аминокислоты» относится к энантиомеру природной протеогенной L-аминокислоты. Каждая из природных протеогенных L-аминокислот, за исключением глицина, имеет, по меньшей мере, один асимметричный углерод, поэтому они являются оптически активными. Аминокислоты классифицируются на L-формы и D-формы на основании строения L-формы и D-формы глицеральдегида.
Аминокислоты, отличные от природных протеогенных L-аминокислот, также могут иметь D-формы.
В настоящем документе «природная не протеогенная аминокислота» представляет собой встречающуюся в природе аминокислоту, которая не образует белков, и ее примеры включают L-норлейцин (далее также обозначаемый как Nle; далее «код, следующий в скобках» показывает сокращение), β-аланин (β-Ала) и L-орнитин (Orn).
Если природная не протеогенная аминокислота имеет асимметричный углерод, то существуют L-форма и D-форма для аминокислоты. Также могут существовать L-формы и D-формы для аминокислот, отличных от природных не протеогенных аминокислот.
В настоящем документе, «аминокислота не природного происхождения» относится к аминокислоте, которая не составляет белки и в основном продуцируется искусственно, будучи аминокислотой, не включенной в описанную выше «природную протеогенную L-аминокислоту и природную не протеогенную аминокислоту». Примеры аминокислот не природного происхождения включают D-формы природных протеогенных L-аминокислот (таких как D-Cys, D-Ser); α-метиламинокислоты (такие как 2-аминоизомасляная кислота (Aib)); аминокислоты с избытком метилена в боковой цепи («гомо» аминокислоты, такие как L-β-гомопролин (β-Hep или β-гомоPro), L-гомосерин (Hes или гомоSer), L-гомоцистеин (Hec или гомоCys), L-гомопролин (гомоPro), L-гомоглутаминовая кислота (гомоGlu)); аминокислоты, в которых боковая цепь аминокислоты с функциональной группой карбоксильной кислоты замещена группой сульфоновой кислоты (например, L-цистеиновая кислота); химически модифицированные аминокислоты, такие как варианты и производные аминокислот (такие как гидроксипролин, L-2,3-диаминопропионовая кислота (Dap), L-2,4-диаминомасляная кислота (Dab), N-метилглицин); и химически синтезированные соединения, обладающие свойствами, характерными для аминокислот, и известные в данной области техники (такие как 4-аминобензойная кислота).
Если аминокислота не природного происхождения имеет асимметричный углерод, существуют L-форма и D-форма аминокислоты.
Конкретные примеры «аминокислоты не природного происхождения» в настоящем описании включают следующие:
- (d)-Pro, (d)-Ser, (d)-Thr, (d)-Asp, (d)-Glu, (d)-Arg, (d)-Lys
- β-гомоPro
- β-Ala, GABA, Ape, Acp
- (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me) Asp, (N-Me) Glu
- группу, представленную формулой [II-1] или формулой [II-2]:
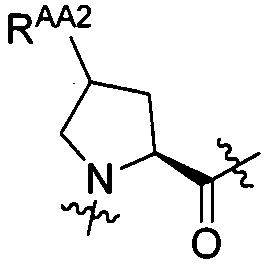 [II-1],
[II-1], 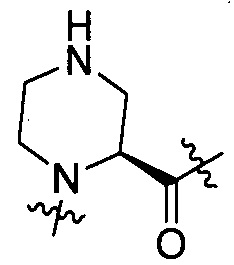 [II-2]
[II-2]
где RAA2 представляет собой гидрокси или амино; и
- аминокислоты, перечисленные далее в Таблице 1 и Таблице 2
Атом азота, участвующий в пептидной связи в любой аминокислоте в настоящем описании, может быть алкилирован. В этом случае, аминокислота также называется «N-алкиламинокислота». Примеры алкила включают метил и этил.
В настоящем документе выражение «β-Asp» означает аспарагиновую кислоту, участвующую в амидном связывании основной цепи через карбокси в боковой цепи, как показано в структуре, представленной формулой [III-1]. Аналогично, выражения «β-(d)-Asp», «γ-Glu» и «γ-(d)-Glu» означают структуры, представленные от формулы [III-2] до формулы [III-4].
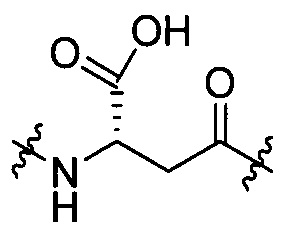 [III-1],
[III-1], 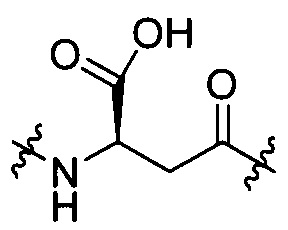 [III-2],
[III-2], 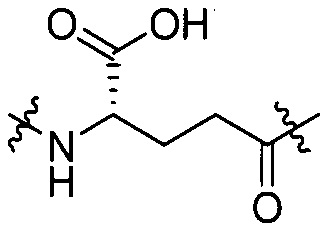 [III-3],
[III-3], 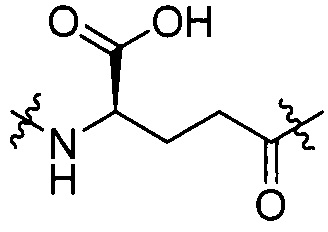 [III-4].
[III-4].
Выражение «(N-Me)Glu(OtBu)» означает N-метильную форму аминокислоты (Glu(OtBu)), как показано в структуре, представленной формулой [III-5].
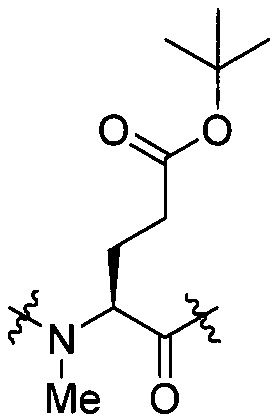 [III-5]
[III-5]
Выражение «(2S,4S)-(4-амино)Pro» по структуре, соответствующее AA2, означает структуру, представленную формулой [II-3]. Аналогично, выражения «(2S,4R)-(4-амино)Pro», «(2S,4S)-(4-гидрокси)Pro» и «(2S,4R)-(4-гидрокси)Pro» означают структуры, представленные формулами от [II-4] до формулы [II-6]. Кроме того, выражение «(S)-пиперазин» означает структуру, представленную формулой [II-2].
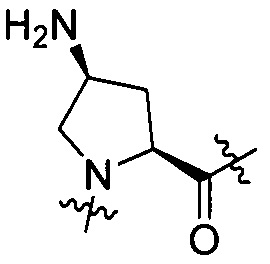 [II-3],
[II-3], 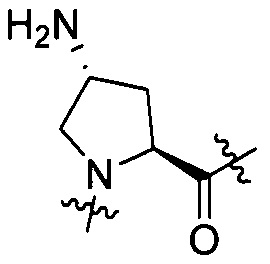 [II-4],
[II-4], 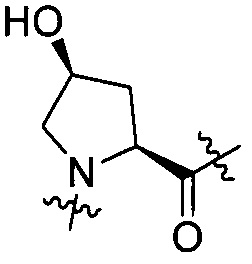 [II-5],
[II-5], 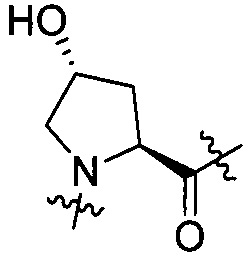 [II-6],
[II-6], 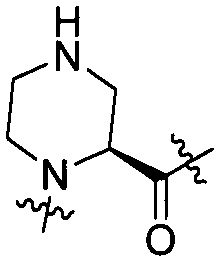 [II-2]
[II-2]
В настоящем документе, «n» обозначает нормальный, «i» обозначает изо, «s» обозначает вторичный, «t» и «трет» каждый обозначает третичный, «с» обозначает цикло, «о» обозначает орто, «м» обозначает мета и «р» означает пара.
«Атом галогена» относится к атому фтора, атому хлора, атому брома или атому йода.
«С1-6 алкил» относится к линейному или разветвленному алкилу, содержащему от одного до шести атомов углерода. Примеры «С1-6 алкила» включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил и н-гексил.
«Галоген C1-6 алкил» относится к линейному или разветвленному алкилу, имеющему от одного до шести атомов углерода и замещенному атомом галогена. Предпочтительное число атомов галогена составляет от одного до пяти, и предпочтительный атом галогена представляет собой атом фтора. Примеры «галоген C1-6 алкила» включают монофторметил, дифторметил, трифторметил, 1-фторэтил, 1,1-дифторэтил, 1,1,2,2-тетрафторэтил, 1,1,2,2,2-пентафторэтил, 2-фторэтил, 2-фтор-2-метилпропил, 2,2-дифторпропил, 1-фтор-2-метилпропан-2-ил, 1,1-дифтор-2-метилпропан-2-ил, 1-фторпентил, 1-фторгексил и 2,2,2-трифтор-1-метилэтил.
«Арил» относится к моноциклической ароматической углеводородной группе или конденсированной полициклической ароматической углеводородной группе, имеющей от 6 до 14 атомов углерода. Примеры «арила» включают фенил, нафтил и антрил.
«Ароматическое кольцо» относится к моноциклической ароматической углеводородной группе или конденсированной полициклической ароматической углеводородной группе, имеющей от 6 до 14 атомов углерода. Примеры «ароматического кольца» включают бензольное кольцо, нафталиновое кольцо и антраценовое кольцо.
Частично насыщенный арил также включен в понятие «арил». То же самое относится к ароматическим кольцам. «Частично насыщенный арил» и соответствующее ароматическое кольцо, «частично насыщенное ароматическое кольцо» относятся к группе, в которой моноциклическая ароматическая углеводородная группа или конденсированная полициклическая ароматическая углеводородная группа, содержащая от 6 до 14 атомов углерода, является частично насыщенной, и кольцо имеет такую структуру, например, дигидроинденильное и дигидроинденовое кольцо.
«Гетероарил» относится к пяти-семичленной моноциклической ароматической гетероциклической группе, состоящей из одного-шести атомов углерода и одного или нескольких атомов, одинаковых или разных, и выбранных из группы, состоящей из атома кислорода, атома серы и атома азота, или конденсированной полициклической ароматической гетероциклической группы, состоящей из 9-14 атомов, в частности, состоящей из 1-13 атомов углерода и одного или нескольких одинаковых или разных атомов, выбранных из группы, состоящей из атома кислорода, атома серы и атома азота. Примеры «гетероарила» включают имидазолил, пиразолил, тиенил, тиазолил, изотиазолил, тиадиазолил, оксазолил, изооксазолил, оксадиазолил, пирролил, триазолил, тетразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, индолил, бензопиразолил, бензотриазолил, бензофуранил, бензотиофенил, хинолил, изохинолил и хиноксалил.
«Гетероароматическое кольцо» относится к пяти-семичленному моноциклическому ароматическому гетероциклу, состоящему из одного-шести атомов углерода и одного или нескольких атомов, одинаковых или разных и выбранных из группы, состоящей из атома кислорода, атома серы и атома азота, или конденсированному полициклическому ароматическому гетероциклу, состоящему из 9-14 атомов, в частности, состоящему из 1-13 атомов углерода и одного или нескольких одинаковых или разных атомов, выбранных из группы, состоящей из атома кислорода, атома серы и атома азота. Примеры «гетероароматического кольца» включают имидазольное кольцо, пиразольное кольцо, тиофеновое кольцо, тиазольное кольцо, изотиазольное кольцо, тиадиазольное кольцо, оксазольное кольцо, изоксазольное кольцо, оксадиазольное кольцо, пиррольное кольцо, триазольное кольцо, теразольное кольцо, пиридиновое кольцо, пиримидиновое кольцо, пиразиновое кольцо, пиридазиновое кольцо, триазиновое кольцо, индольное кольцо, бензопиразольное кольцо, бензотриазольное кольцо, бензофурановое кольцо, бензотиофеновое кольцо, хинолиновое кольцо, изохинолиновое кольцо и хиноксалиновое кольцо.
Частично насыщенный гетероарил также включен в понятие «гетероарил». То же самое относится к гетероароматическим кольцам. «Частично насыщенный гетероарил» и соответствующее гетероароматическое кольцо, «частично насыщенное гетероароматическое кольцо» относится к пяти-семи-членной частично насыщенной моноциклической гетероциклической группе, состоящей из одного-шести атомов углерода и одного или нескольких атомов, одинаковых или разных, и выбранной из группы, состоящей из атома кислорода, атома серы и атома азота, или частично насыщенной конденсированной полициклической гетероциклической группе, состоящей из 9-14 атомов, в частности, состоящей из 1-13 атомов углерода и одного или нескольких атомов, одинаковых или разных и выбранных из группы, состоящей из атома кислорода, атома серы и атома азота, и кольца, имеющего такую структуру. Примеры таких соединений включают оксазолидинил, тиазолинил, дигидропиридинил, дигидробензофуранил, хроманил, дигидропиранопиридинил, дигидрофуропиридинил, тетрагидрохинолил, дигидробензодиоксинил, тетрагидротриазолоазепинил, оксазолидиновое кольцо, тиазолиновое кольцо, дигидропиридиновое кольцо, дигидробензофурановое кольцо, хромановое кольцо, дигидропиранопиридиновое кольцо, дигидрофуропиридиновое кольцо, тетрагидрохинолиновое кольцо, тетрагидрохинолиновое кольцо, дигидробензодиоксиновое кольцо и тетрагидротриазолоазепиновое кольцо.
«Четырех-семичленный насыщенный гетероциклил, содержащий атом азота» относится к четырех-семичленной моноциклической насыщенной гетероциклической группе, состоящей из одного атома азота и трех-шести атомов углерода, и может дополнительно содержать, помимо атома азота, один атом, выбранный из группы, состоящей из атома кислорода, атома серы и атома азота. Примеры «четырех-семичленного насыщенного гетероциклила, содержащего атом азота» включают азетидинил, пиролидинил, пиперидинил, азепанил, морфолинил, тиоморфолинил и пиперазинил.
«Четырех-семи-членный насыщенный гетероциклил, содержащий один атом азота и необязательно дополнительно содержащий один гетероатом» относится к четырех-семичленной моноциклической насыщенной гетероциклической группе, состоящей из одного атома азота и трех-шести атомов углерода, и может дополнительно содержать, в дополнение к атому азота, один атом, выбранный из группы, состоящей из атома кислорода, атома серы и атома азота. Примеры «четырех-семи-членного насыщенного гетероциклила, содержащего один атом азота и необязательно дополнительно содержащего один гетероатом» включают азетидинил, пирролидинил, пиперидинил, азепанил, морфолинил, тиоморфолинил и пиперазинил.
Примеры «четырех-семи-членного насыщенного гетероциклила, содержащего один атом азота и необязательно дополнительно содержащего один гетероатом, и необязательно перекрестно-сшитого с C1-4 алкандиилом» включают 8-окса-3-азабицикло[3,2,1]октан-3-ил (группа представлена формулой [VI-16]) и 3,8-диазабицикло[3,2,1]октан-3-ил (группа представлена формулой [VI-18]):
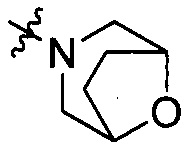 [VI-16],
[VI-16], 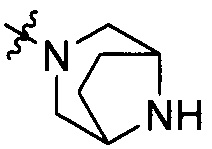 [VI-18]
[VI-18]
«С1-6 алкокси» относится к линейному или разветвленному алкокси, имеющему от одного до шести атомов углерода. Примеры «С1-6 алкокси» включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси и н-гексилокси.
«Галоген C1-6 алкокси» относится к линейному или разветвленному алкокси, содержащему от одного до шести атомов углерода и замещенному атомом галогена. Предпочтительное количество атомов галогена в качестве заместителей составляет от одного до пяти, и предпочтительным атомом галогена является атом фтора. Примеры «галоген C1-6 алкокси» включает монофторметокси, дифторметокси, трифторметокси, 1-фторэтокси, 1,1-дифторэтокси, 1,1,2,2-тетрафторэтокси, 2-фторэтокси, 2,2,2-трифторэтокси, 3,3,3-трифторпропокси, 1,3-дифторпропан-2-илокси, 2-фтор-2-метилпропокси, 2,2-дифторпропокси, 1-фтор-2-метилпропан-2-илокси, 1,1-дифтор-2-метилпропокси-2-илокси и 4,4,4-трифторбутокси.
«С1-6 алкилкарбонил» относится к группе, в которой «С1-6 алкил», описанный выше, и карбонил связаны вместе. Примеры «С1-6 алкилкарбонила» включают метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, н-бутилкарбонил, изобутилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, н-пентилкарбонил и н-гексилкарбонил.
«C1-6 алкилкарбониламино» относится к группе, в которой «C1-6 алкилкарбонил», описанный выше, и аминогруппа связаны вместе. Примеры «C1-6 алкилкарбониламино» включают метилкарбониламино, этилкарбониламино, н-пропилкарбониламино, изопропилкарбониламино, н-бутилкарбониламино, изобутилкарбониламино, втор-бутилкарбониламино, трет-бутилкарбониламино, н-пентилкарбониламино и н-гексилкарбониламино.
«С1-6 алкиламино» относится к аминогруппе, имеющей один или два «С1-6 алкила», описанных выше, в качестве заместителей, которые являются одинаковыми или разными. Примеры «С1-6 алкиламино» включают метиламино, этиламино, н-пропиламино, изопропиламино, н-бутиламино, изобутиламино, втор-бутиламино, трет-бутиламино, н-пентиламино, н-гексиламино, диметиламино, диэтиламино, ди(н-пропил)амино, ди(изопропил)амино, этилметиламино и метил(н-пропил)амино.
«Моно C1-6 алкиламино» относится к амино, имеющему в качестве замены один «C1-6 алкил», описанный выше. Примеры «моно C1-6 алкиламино» включают метиламино, этиламино, н-пропиламино, изопропиламино, н-бутиламино, изобутиламино, втор-бутиламино, трет-бутиламино, н-пентиламино и н-гексиламино.
«Ди C1-6 алкиламино» относится к амино, имеющему два «C1-6 алкила», описанных выше, в качестве заместителей, которые являются одинаковыми или разными. Примеры «ди C1-6 алкиламино» включают диметиламино, диэтиламино, ди(н-пропил)амино, ди(изопропил)амино, этилметиламино и метил(н-пропил)амино.
«Моно C1-6 алкиламинокарбонил» относится к группе, в которой «моно C1-6 алкиламино», описанные выше, и карбонил, связаны вместе. Примеры «моно C1-6 алкиламинокарбонила» включают метиламинокарбонил, этиламинокарбонил, н-пропиламинокарбонил, изопропиламинокарбонил н-бутиламинокарбонил, изобутиламинокарбонил, н-пентиламинокарбонил и н-гексиламинокарбонил.
«Ди-С1-6 алкиламинокарбонил» относится к группе, в которой «ди-С1-6 алкиламино», описанные выше, и карбонил связаны вместе. Примеры «ди-С1-6 алкиламинокарбонила» включают диметиламинокабинил, диэтиаминокарбонил, ди(н-пропил)аминокарбонил, ди(изопропил)аминокарбонил, этилметиламинокарбонил и метил(н-пропил)аминокарбонил.
«С1-6 алкилкарбонил» относится к группе, в которой «С1-6 алкил», описанный выше, и карбонил связаны вместе. Примеры «С1-6 алкилкарбонила» включают метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, н-бутилкарбонил, изобутилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, н-пентилкарбонил и н-гексилкарбонил.
«C2-16 алкилкарбонил» относится к группе, в которой линейный или разветвленный алкил, содержащий от 2 до 16 атомов углерода, и карбонил связаны вместе. Примеры «C2-16 алкилкарбонила» включают этилкарбонил, н-пропилкарбонил, изопропиларбонил, н-бутилкарбонил, изобутилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, н-децилкарбонил (ундеканоил), н-додецилкарбонил (тридеканоил) и н-тетрадецилкарбонил (пентадеканоил).
«C2-16 алкилкарбонил, замещенный на конце карбокси» относится к группе, в которой конец «C2-16 алкила» в «C2-16 алкилкарбониле», описанном выше, замещен карбокси. Примеры «C2-16 алкилкарбонила, замещенного на конце карбокси» включает 11-карбоксиундеканоил, 13-карбокситридеканоил и 15-карбоксипентадеканоил.
«С1-6 алкилсульфонил» относится к группе, в которой «С1-6 алкил», описанный выше, и сульфонил связаны друг с другом. Примеры «С1-6 алкилсульфонила» включают метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, втор-бутилсульфонил, трет-бутилсульфонил, н-пентилсульфонил и н-гексилсульфонил.
«С1-3 алкандиил» относится к двухвалентному углеводороду, образованному удалением одного атома водорода из алкила, содержащего от одного до трех атомов углерода. Примеры «С1-3 алкандиила» включают метандиил, этан-1,1-диил, этан-1,2-диил, пропан-1,1-диил, пропан-1,3-диил и пропан-2,2-диил.
«С1-4 алкандиил» относится к двухвалентному углеводороду, образованному удалением одного атома водорода из алкила, содержащего от одного до четырех атомов углерода. Примеры «С1-4 алкандиила» включают метандиил, этан-1,1-диил, этан-1,2-диил, пропан-1,1-диил, пропан-1,3-диил, пропан-2,2-диил и бутан-1,4-диил.
«С2-3 алкендиил» относится к двухвалентному ненасыщенному углеводороду, образованному удалением одного атома водорода из алкенила, имеющего два или три атома углерода. Примеры «С2-3 алкендиила» включают этен-1,1-диил, этен-1,2-диил, проп-1-ен-1,1-диил, проп-2-ен-1,1-диил, проп-1-ен-1,3-диил, проп-2-ен-1,3-диил и проп-1-ен-2,2-диил.
«Триазолдиил» относится к двухвалентному триазолу, образованному путем удаления двух атомов водорода из триазольного кольца. Примеры «триазолдиила» включают структуры, представленные формулами [VIII-1] - [VIII-5]:
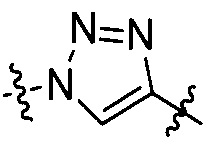 [VIII-1],
[VIII-1], 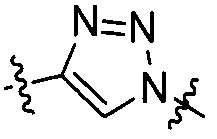 [VIII-2],
[VIII-2], 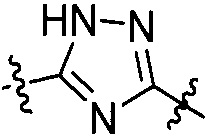 [VIII-3],
[VIII-3], 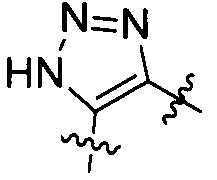 [VIII-4],
[VIII-4], 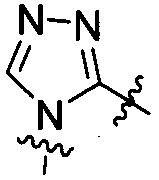 [VIII-5]
[VIII-5]
Используемые в настоящем документе сокращения обозначают структуры, перечисленные в таблице 1 по таблицу 4.
[Таблица 1-1]
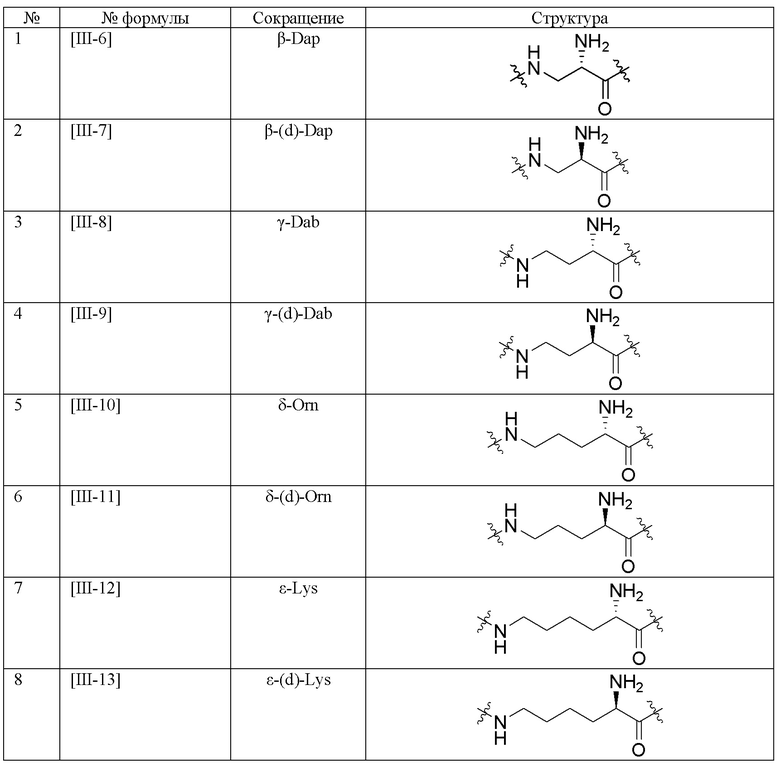
[Таблица 2-1]
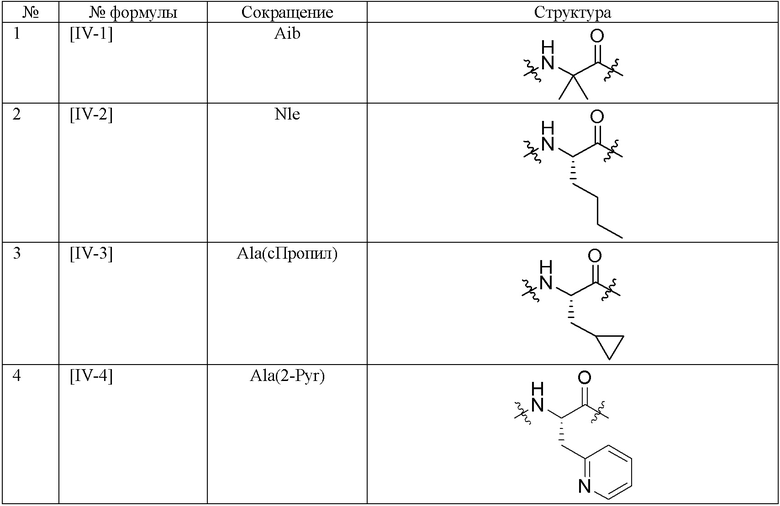
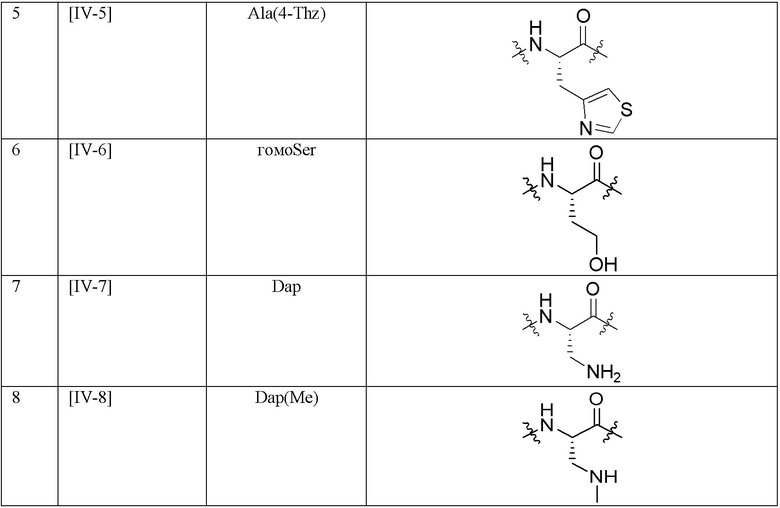
[Таблица 2-2]


[Таблица 2-3]
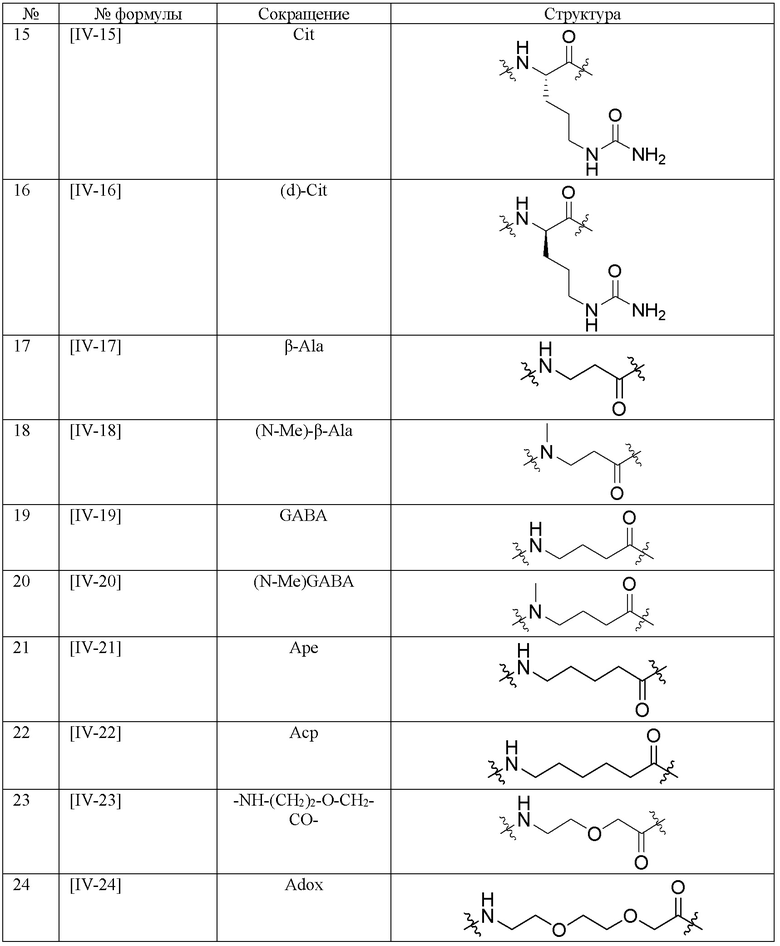
[Таблица 2-4]

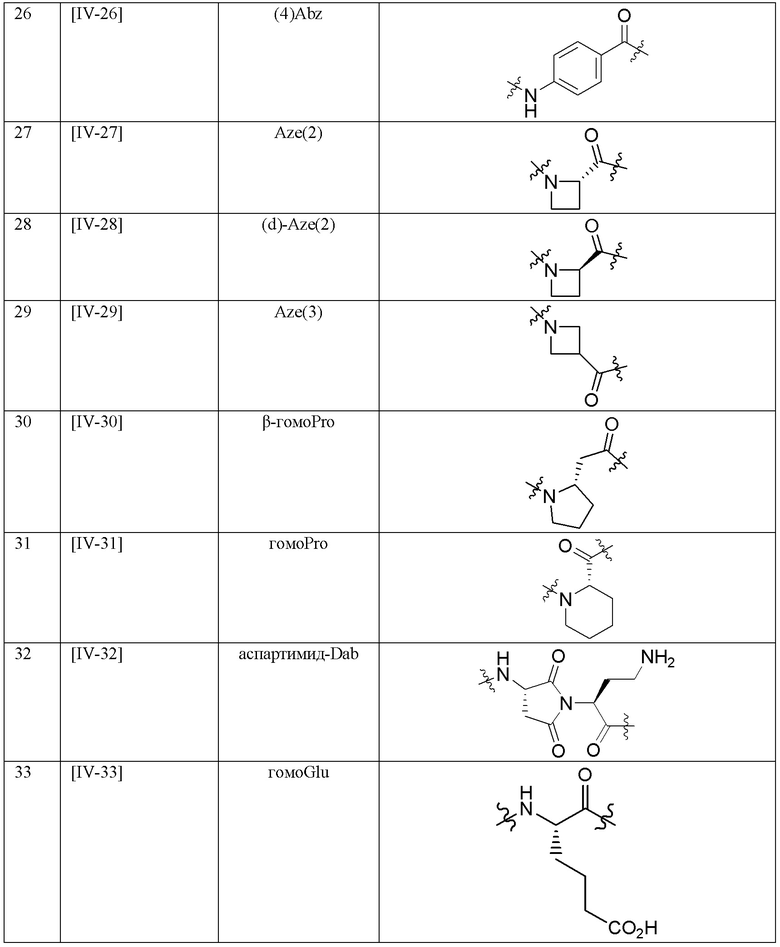
[Таблица 3-1]
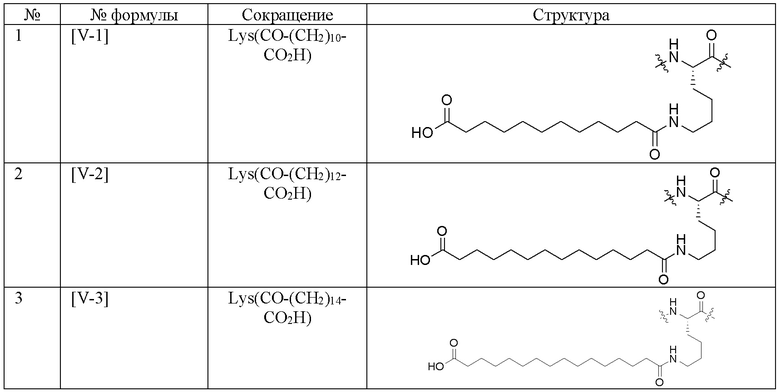
[Таблица 4-1]
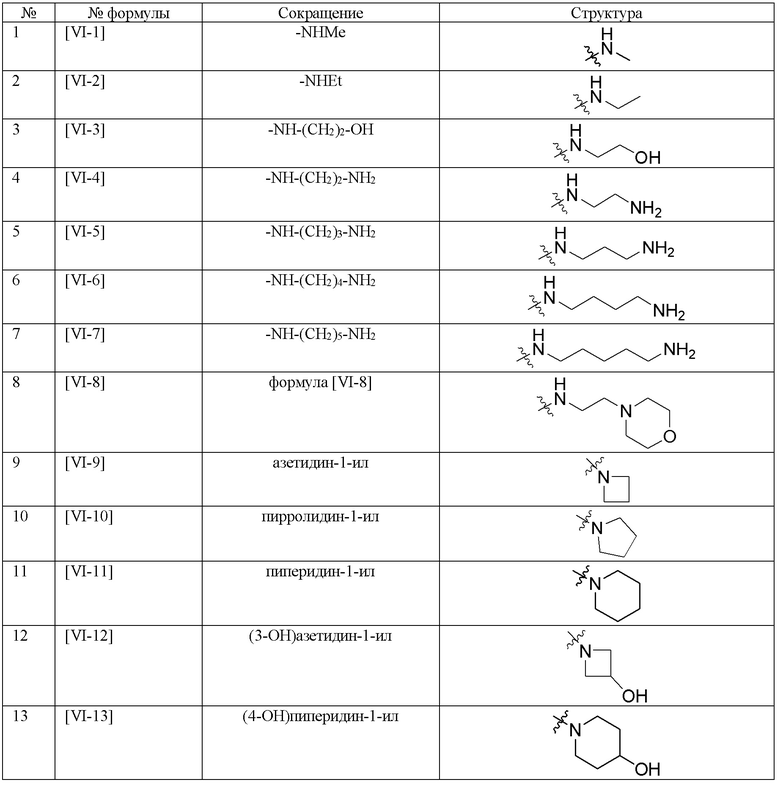
[Таблица 4-2]

Предпочтительные варианты осуществления замещенного полипептида, представленного формулой [I'], или его фармацевтически приемлемой соли по настоящему изобретению следующие.
Предпочтительно, AA1 представляет собой Asp, β-Asp, β-(d)-Asp, γ-Glu или γ-(d)-Glu,
более предпочтительно, AA1 представляет собой β-Asp, γ-Glu или γ-(d)-Glu,
где еще более предпочтительно, AA1 представляет собой γ-(d)-Glu,
в другом более предпочтительно, AA1 представляет собой β-(d)-Asp или γ-(d)-Glu,
где еще более предпочтительно, AA1 представляет собой β-(d)-Asp, и
в другом более предпочтительно, AA1 представляет собой Asp.
Предпочтительно, AA2 представляет собой группу, представленную формулой [II-1] или формулой [II-2]:
 [II-1],
[II-1],  [II-2]
[II-2]
группу, представленную формулой [IV-7], [IV-8], [IV-9], [IV-11] или [IV-12]:
 [IV-7],
[IV-7],  [IV-8],
[IV-8],  [IV-9],
[IV-9],  [IV-11],
[IV-11],  [IV-12]
[IV-12]
Ala,
группу, представленную формулой [IV-27]:
 [IV-27]
[IV-27]
или
Pro,
где, предпочтительно, RAA2 представляет собой гидрокси или амино,
более предпочтительно, AA2 представляет собой группу, представленную формулой [II-1]:
 [II-1]
[II-1]
или группы, представленной формулой [IV-7], [IV-8], [IV-9], [IV-11] или [IV-12]:
 [IV-7],
[IV-7],  [IV-8],
[IV-8],  [IV-9],
[IV-9],  [IV-11],
[IV-11],  [IV-12]
[IV-12]
где предпочтительно, RAA2 представляет собой амино,
еще более предпочтительно, AA2 представляет собой
группу, представленную формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
или группу, представленную формулой [II-1]:
 [II-1]
[II-1]
где предпочтительно, RAA2 представляет собой амино,
особенно предпочтительно, AA2 представляет собой
группу, представленную формулой [II-1]:
 [II-1]
[II-1]
где предпочтительно, RAA2 представляет собой амино, и
в другом особенно предпочтительно, AA2 представляет собой
группу, представленную формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9].
[IV-9].
Предпочтительно, AA3 представляет собой Val, Leu, Ile, группу, представленную формулой [IV-2]:
 [IV-2]
[IV-2]
Phe, группу, представленную формулой [IV-3], [IV-4] или [IV-5]:
 [IV-3],
[IV-3],  [IV-4],
[IV-4],  [IV-5]
[IV-5]
или Trp,
более предпочтительно, AA3 представляет собой Val, Leu, Ile, Phe или Trp,
еще более предпочтительно, AA3 представляет собой Val, Leu или Ile,
особенно предпочтительно, AA3 представляет собой Val,
в другом особенно предпочтительно, AA3 представляет собой Leu, и
в другом особенно предпочтительно, AA3 представляет собой Ile.
Предпочтительно, AA4 представляет собой одинарную связь, Pro, Gly, гомоSer, Met, Glu, (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Met, (N-Me)Asp, (N-Me)Glu, (d)-Pro, (d)-Ala, (d)-Phe, (d)-Tyr, (d)-Ser, (d)-Thr или (d)-(N-Me)Glu,
более предпочтительно, AA4 представляет собой (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Met, (N-Me)Asp, (N-Me)Glu, (d)-Pro, (d)-Ala, (d)-Phe, (d)-Tyr, (d)-Ser, (d)-Thr или (d)-(N-Me)Glu,
еще более предпочтительно, AA4 представляет собой (N-Me)Glu или (N-Me)Asp,
где особенно предпочтительно, AA4 представляет собой (N-Me)Glu, и
еще более предпочтительно, AA4 представляет собой (N-Me)Ile, (N-Me)Val или (N-Me)Leu,
где особенно предпочтительно, AA4 представляет собой (N-Me)Ile.
Предпочтительно, AA5 представляет собой β-Ala, GABA, Ape, Acp, Pro, (d)-Pro, β-гомоPro, одинарную связь, Arg, (d)-Arg,
группу, представленную [IV-7], [IV-9] или [IV-13]:
 [IV-7],
[IV-7],  [IV-9],
[IV-9],  [IV-13]
[IV-13]
Lys, (d)-Lys,
Ala, группы, представленной формулой [IV-1]:
 [IV-1]
[IV-1]
группы, представленной формулой [IV-27], [IV-28] или [IV-29]:
 [IV-27],
[IV-27],  [IV-28],
[IV-28],  [IV-29]
[IV-29]
Phe, His, Thr, или
группы, представленной любой из формул [III-6] - [III-13]:
 [III-6],
[III-6],  [III-7],
[III-7],  [III-8],
[III-8],  [III-9],
[III-9],  [III-10],
[III-10],  [III-11],
[III-11],  [III-12],
[III-12],  [III-13]
[III-13]
более предпочтительно, AA5 представляет собой β-Ala, GABA, Ape, Acp, Pro, (d)-Pro, β-гомоPro, одинарную связь, Arg, (d)-Arg,
группу, представленную формулой [IV-7], [IV-9] или [IV-13]:
 [IV-7],
[IV-7],  [IV-9],
[IV-9],  [IV-13]
[IV-13]
Lys или (d)-Lys,
еще более предпочтительно, AA5 представляет собой β-Ala, GABA, Ape, Acp, Pro, (d)-Pro или β-гомоPro, и
особенно предпочтительно, AA5 представляет собой β-Ala, GABA, Ape, Acp или β-гомоPro.
Предпочтительно, W1 представляет собой -L1- или -L1'-L1"-,
где L1 представляет собой одинарную связь,
L1' выбран из группы, состоящей из β-Ala, GABA, Ape, Acp,
группы, представленной любой из формул [III-6] - [III-13]:
 [III-6],
[III-6],  [III-7],
[III-7],  [III-8],
[III-8],  [III-9],
[III-9],  [III-10],
[III-10],  [III-11],
[III-11],  [III-12],
[III-12],  [III-13]
[III-13]
и группы, представленной любой из формул [IV-23] и [IV-24]:
 [IV-23],
[IV-23],  [IV-24];
[IV-24];
и L1" представляет собой одинарную связь, Asn, (d)-Ser, (d)-Thr, Lys, Arg или Glu,
более предпочтительно, W1 представляет собой -L1- или -L1'-L1"-,
где L1 представляет собой одинарную связь,
L1' представляет собой β-Ala, GABA, Ape, Acp, или
группы, представленной любой из формул [III-6] - [III-13]:
 [III-6],
[III-6],  [III-7],
[III-7],  [III-8],
[III-8],  [III-9],
[III-9],  [III-10],
[III-10],  [III-11],
[III-11],  [III-12],
[III-12],  [III-13]
[III-13]
и L1" представляет собой Asn, (d)-Ser, (d)-Thr или Glu,
где еще более предпочтительно, W1 представляет собой -L1- или -L1'-L1"-,
где L1 представляет собой одинарную связь,
L1' представляет собой β-Ala, GABA, Ape или Acp, и
L1" представляет собой Asn, (d)-Ser, (d)-Thr или Glu,
где особенно предпочтительно, W1 представляет собой -L1-,
где L1 представляет собой одинарную связь, и
в другом более предпочтительно, W1 представляет собой -L1'-L1"-,
где L1' представляет собой группы, представленной формулой [IV-23] или [IV-24]:
 [IV-23],
[IV-23],  [IV-24];
[IV-24];
и L1" представляет собой одинарную связь.
Предпочтительно, L2 представляет собой одинарную связь.
Предпочтительно, LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
более предпочтительно, LN1 представляет собой формулу -C(=O)-, и
в другом более предпочтительно, LN1 представляет собой формулу -S(=O)2-.
Предпочтительно, LN2 представляет собой одинарную связь, формулу -O- или формулу -C(=O)-NH-,
более предпочтительно, LN2 представляет собой формулу -O- или формулу -C(=O)-NH-,
еще более предпочтительно, LN2 представляет собой формулу -O-, и
еще более предпочтительно, LN2 представляет собой формулу -C(=O)-NH-.
Предпочтительно, кольцо A представляет собой бензольное кольцо или пиридиновое кольцо,
более предпочтительно, кольцо A представляет собой бензольное кольцо,
предпочтительно, RA1 и RA2 каждый независимо представляет собой атом водорода или атом галогена, и
более предпочтительно, RA1 и RA2 каждый представляет собой атом водорода.
Предпочтительно, кольцо B представляет собой фенил или пиридил,
более предпочтительно, кольцо B представляет собой фенил,
предпочтительно, RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкил, галоген C1-6 алкил, C1-6 алкокси или галоген C1-6 алкокси, и
более предпочтительно, RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси.
Предпочтительно, WC представляет собой одинарную связь или линкер, состоящий из одной или нескольких аминокислот, где
одна-три аминокислоты, образующие линкер, не ограничены, но, предпочтительно, являются одинаковыми или разными, и каждая выбрана из группы, состоящей из: Gly, Pro, Arg, (d)-Arg, Lys, (d)-Lys, β-Ala, GABA и Ape, где
если Lys или (d)-Lys включена в группу, представленную WC,
то амино на боковой цепи Lys или (d)-Lys необязательно замещен:
C2-16 алкилкарбонилом, замещенным на конце карбокси,
Lys, где амино на боковой цепи Lys необязательно замещен C2-16 алкилкарбонилом, замещенным на конце карбокси, или
(d)-Lys, где амино на боковой цепи (d)-Lys необязательно замещен C2-16 алкилкарбонилом, замещенным на конце карбокси,
более предпочтительно, WC представляет собой одинарную связь, Pro, Arg, (d)-Arg, Lys, (d)-Lys или (d)-Lys-(d)-Lys,
еще более предпочтительно, WC представляет собой одинарную связь, Arg, (d)-Arg, Lys или (d)-Lys,
особенно предпочтительно, WC представляет собой одинарную связь, и
в другом особенно предпочтительно, WC представляет собой (d)-Lys.
Предпочтительно, RC представляет собой:
формулу -OH, формулу -NH2,
C1-6 алкиламино, где C1-6 алкил из C1-6 алкиламино необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, амино и четырех-семи-членного насыщенного гетероциклила, содержащего один атом азота, или
четырех-семи-членного насыщенного гетероциклила, содержащего один атом азота и необязательно другой, содержащий один гетероатом, где четырех-семи-членный насыщенный гетероциклил, содержащий один атом азота и необязательно другой, содержащий один гетероатом необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси и C1-6 алкила, где C1-6 алкил необязательно замещен одним карбамоилом; и два атома углерода в четырех-семи-членном насыщенном гетероциклиле, содержащем один атом азота и необязательно другой, содержащий один гетероатом, необязательно перекрестно сшиты с C1-4 алкандиилом,
более предпочтительно, RC представляет собой формулу -OH или формулу -NH2, и
еще более предпочтительно, RC представляет собой формулу -NH2.
Другим предпочтительным вариантом осуществления соединений по настоящему изобретению является замещенный полипептид, представленный формулой [I'], или его фармацевтически приемлемая соль, где
AA1 представляет собой β-Asp, γ-Glu или γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [II-1] или формулой [II-2]:
 [II-1],
[II-1],  [II-2]
[II-2]
где RAA2 представляет собой гидрокси или амино,
AA3 представляет собой Val, Leu, Ile, Phe или Trp,
AA4 представляет собой одинарную связь, Pro, (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Asp или (N-Me)Glu,
AA5 представляет собой одинарную связь, Pro, (d)-Pro, β-гомоPro, Arg, (d)-Arg, Lys, (d)-Lys, β-Ala, GABA, Ape или Acp,
W1 представляет собой L1 и L1 представляет собой одинарную связь,
L2 представляет собой одинарную связь,
LN1 представляет собой формулу -S(=O)2-,
LN2 представляет собой одинарную связь, формулу -O- или формулу -C(=O)-NH-,
кольцо A представляет собой бензольное кольцо,
RA1 и RA2 каждый представляет собой атом водорода,
кольцо B представляет собой фенил,
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена или C1-6 алкокси,
WC представляет собой одинарную связь, Pro, Arg, (d)-Arg, Lys, (d)-Lys или (d)-Lys-(d)-Lys, и
RC представляет собой формулу -NH2.
Другим предпочтительным вариантом осуществления по настоящему изобретению является замещенный полипептид, представленный формулой [I'], или его фармацевтически приемлемая соль, где
AA1 представляет собой β-Asp, γ-Glu или γ-(d)-Glu,
где еще более предпочтительно, AA1 представляет собой γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [II-1]:
 [II-1]
[II-1]
где RAA2 представляет собой амино,
AA3 представляет собой Val, Leu или Ile,
где еще более предпочтительно, AA3 представляет собой Val,
еще более предпочтительно, AA3 представляет собой Leu, и
еще более предпочтительно, AA3 представляет собой Ile,
AA4 представляет собой (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Asp или (N-Me)Glu,
где еще более предпочтительно, AA4 представляет собой (N-Me)Val, (N-Me)Leu или (N-Me)Ile,
где особенно предпочтительно, AA4 представляет собой (N-Me)Ile,
еще более предпочтительно, AA4 представляет собой (N-Me)Asp или (N-Me)Glu,
где особенно предпочтительно, AA4 представляет собой (N-Me)Glu,
AA5 представляет собой Pro, (d)-Pro, β-гомоPro, β-Ala, GABA, Ape или Acp,
где еще более предпочтительно, AA5 представляет собой Pro, (d)-Pro или β-гомоPro,
где особенно предпочтительно, AA5 представляет собой β-гомоPro,
еще более предпочтительно, AA5 представляет собой β-Ala, GABA, Ape или Acp,
где особенно предпочтительно, AA5 представляет собой β-Ala, GABA или Ape,
W1 представляет собой L1,
L1 представляет собой одинарную связь,
L2 представляет собой одинарную связь,
LN1 представляет собой формулу -S(=O)2-,
LN2 представляет собой одинарную связь, формулу -O- или формулу -C(=O)-NH-,
где еще более предпочтительно, LN1 представляет собой формулу -C(=O)-, и
еще более предпочтительно, LN1 представляет собой формулу -S(=O)2-,
кольцо A представляет собой бензольное кольцо,
RA1 и RA2 каждый представляет собой атом водорода,
кольцо B представляет собой фенил,
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена или C1-6 алкокси,
WC представляет собой одинарную связь или (d)-Lys,
где еще более предпочтительно, WC представляет собой одинарную связь, и
еще более предпочтительно, WC представляет собой (d)-Lys, и
RC представляет собой формулу -NH2.
Другим предпочтительным вариантом осуществления соединений по настоящему изобретению является замещенный полипептид или его фармацевтически приемлемая соль, где
W1 представляет собой -L1'-L1»-,
L2 представляет собой одинарную связь, и
полипептид представлен формулой [I'-A]:
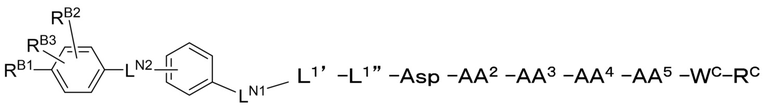 [I'-A],
[I'-A],
где предпочтительно, варианты осуществления AA2, AA3, AA4, AA5, L1', L1", LN1, LN2, RB1, RB2, RB3, WC и RC такие, как описаны выше.
В более предпочтительном варианте осуществления полипептида, представленного формулой [I'-A] или его фармацевтически приемлемой соли,
AA2 представляет собой группу, представленную формулой [II-1]:
 [II-1]
[II-1]
или группы, представленной формулой [IV-7], [IV-8], [IV-9], [IV-11] или [IV-12]:
 [IV-7],
[IV-7],  [IV-8],
[IV-8],  [IV-9],
[IV-9],  [IV-11],
[IV-11],  [IV-12]
[IV-12]
где RAA2 представляет собой амино,
AA3 представляет собой Val, Leu, Ile, Phe или Trp,
AA4 представляет собой (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Asp или (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape, Acp, Pro, (d)-Pro или β-гомоPro,
L1' представляет собой β-Ala, GABA, Ape, Acp или группу, представленную формулой [IV-23] или [IV-24]:
 [IV-23],
[IV-23],  [IV-24];
[IV-24];
L1" представляет собой одинарную связь, Asn, (d)-Ser, (d)-Thr или Glu,
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-,
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси,
WC представляет собой одинарную связь, Arg, (d)-Arg, Lys или (d)-Lys, и
RC представляет собой формулу -OH или формулу -NH2.
В еще более предпочтительном варианте осуществления полипептида, представленного формулой [I'-A] или его фармацевтически приемлемой соли,
AA2 представляет собой группу, представленную формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
AA3 представляет собой Val, Leu или Ile,
AA4 представляет собой (N-Me)Ile или (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape, Acp или β-гомоPro,
L1' представляет собой GABA или Ape,
L1" представляет собой Asn, Glu, (d)-Ser или (d)-Thr,
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-,
RB1 представляет собой карбамоил или атом фтора,
RB2 представляет собой атом водорода,
RB3 представляет собой атом водорода,
WC представляет собой одинарную связь, и
RC представляет собой формулу -NH2.
Особенно предпочтительный режим настоящего варианта осуществления следующий.
В полипептиде, представленном формулой [I'-A] или его фармацевтически приемлемой соли,
AA2 представляет собой группу, представленную формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
AA3 представляет собой Val,
AA3 может быть Leu,
AA3 может быть Ile,
AA4 представляет собой (N-Me)Ile,
AA4 может быть (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape или Acp,
AA5 может быть β-гомоPro,
L1' представляет собой GABA или Ape,
L1" представляет собой Asn, Glu, (d)-Ser или (d)-Thr,
комбинация L1' и L1" предпочтительно представляет собой GABA-Asn, Ape-Asn, Ape-Glu, Ape-(d)-Ser или Ape-(d)-Thr,
LN1 представляет собой формулу -C(=O)-,
LN1 может быть формулой -S(=O)2-,
LN2 представляет собой формулу -O- и LN2 может быть формулой -C(=O)-NH-,
RB1 представляет собой карбамоил или атом фтора,
RB2 представляет собой атом водорода,
RB3 представляет собой атом водорода,
WC представляет собой одинарную связь, и
RC представляет собой формулу -NH2.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-A] представляет собой любой из следующих:
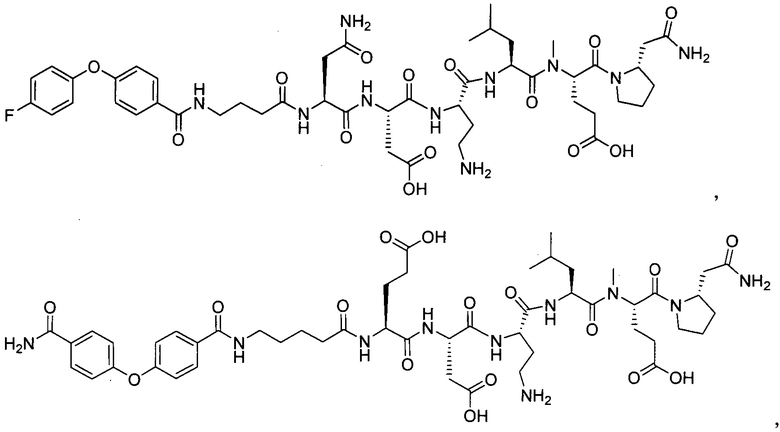
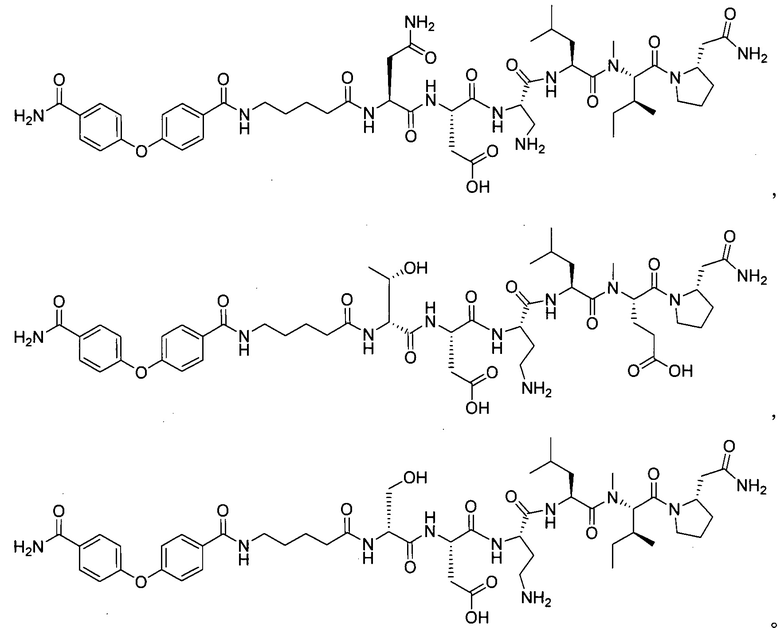
Другим предпочтительным вариантом осуществления соединений по настоящему изобретению является замещенный полипептид или его фармацевтически приемлемая соль,
где W1 представляет собой -L1-, где L1 представляет собой одинарную связь,
L2 представляет собой одинарную связь, и
замещенный полипептид представлен формулой [I'-B]:
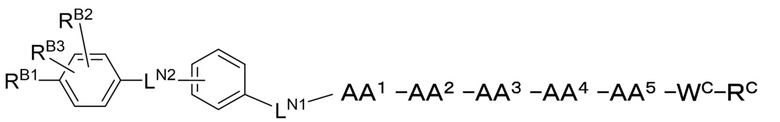 [I'-B],
[I'-B],
где предпочтительно, варианты осуществления AA1, AA2, AA3, AA4, AA5, LN1, LN2, RB1, RB2, RB3, WC и RC такие, как описаны выше.
В более предпочтительном варианте осуществления полипептида, представленного формулой [I'-B] или его фармацевтически приемлемой соли,
AA1 представляет собой β-Asp, β-(d)-Asp, γ-Glu или γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [II-1]:
 [II-1]
[II-1]
или группы, представленной формулой [IV-7], [IV-8], [IV-9], [IV-11] или [IV-12]:
 [IV-7],
[IV-7],  [IV-8],
[IV-8],  [IV-9],
[IV-9],  [IV-11],
[IV-11],  [IV-12]
[IV-12]
где RAA2 представляет собой амино,
AA3 представляет собой Val, Leu, Ile, Phe или Trp,
AA4 представляет собой (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Asp или (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape, Acp или β-гомоPro,
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
LN2 представляет собой одинарную связь, формулу -O- или формулу -C(=O)-NH-,
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси,
WC представляет собой одинарную связь, Arg, (d)-Arg, Lys или (d)-Lys, и
RC представляет собой формулу -OH или формулу -NH2.
В еще более предпочтительном варианте осуществления полипептида, представленного формулой [I'-B] или его фармацевтически приемлемой соли,
AA1 представляет собой β-(d)-Asp или γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [II-1]:
 [II-1]
[II-1]
или группы, представленной формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
где RAA2 представляет собой амино,
AA3 представляет собой Val, Leu или Ile,
AA4 представляет собой (N-Me)Ile или (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape, Acp или β-гомоPro,
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-,
RB1 представляет собой карбамоил, атом хлора, атом брома, метокси или трифторметокси,
RB2 представляет собой атом водорода,
RB3 представляет собой атом водорода,
WC представляет собой одинарную связь или (d)-Lys, и
RC представляет собой формулу -NH2.
Особенно предпочтительный режим настоящего варианта осуществления следующий.
В полипептиде, представленном формулой [I'-B] или его фармацевтически приемлемой соли,
AA1 представляет собой β-(d)-Asp,
AA1 может быть γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [II-1]:
 [II-1]
[II-1]
где RAA2 представляет собой амино,
AA2 может быть группой, представленной формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
AA3 представляет собой Val,
AA3 может быть Leu,
AA3 может быть Ile,
AA4 представляет собой (N-Me)Ile,
AA4 может быть (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape или Acp,
AA5 может быть β-гомоPro,
LN1 представляет собой формулу -C(=O)-,
LN1 может быть формулой -S(=O)2-,
LN2 представляет собой формулу -O-,
LN2 может быть формулой -C(=O)-NH-,
RB1 представляет собой карбамоил, атом хлора, атом брома, метокси или трифторметокси,
RB2 представляет собой атом водорода,
RB3 представляет собой атом водорода,
WC представляет собой одинарную связь,
WC может быть (d)-Lys, и
RC представляет собой формулу -NH2.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-B] представляет собой любой из следующих:

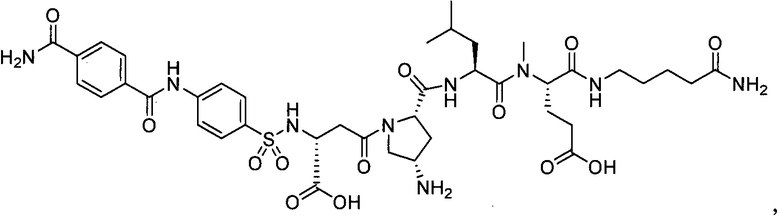
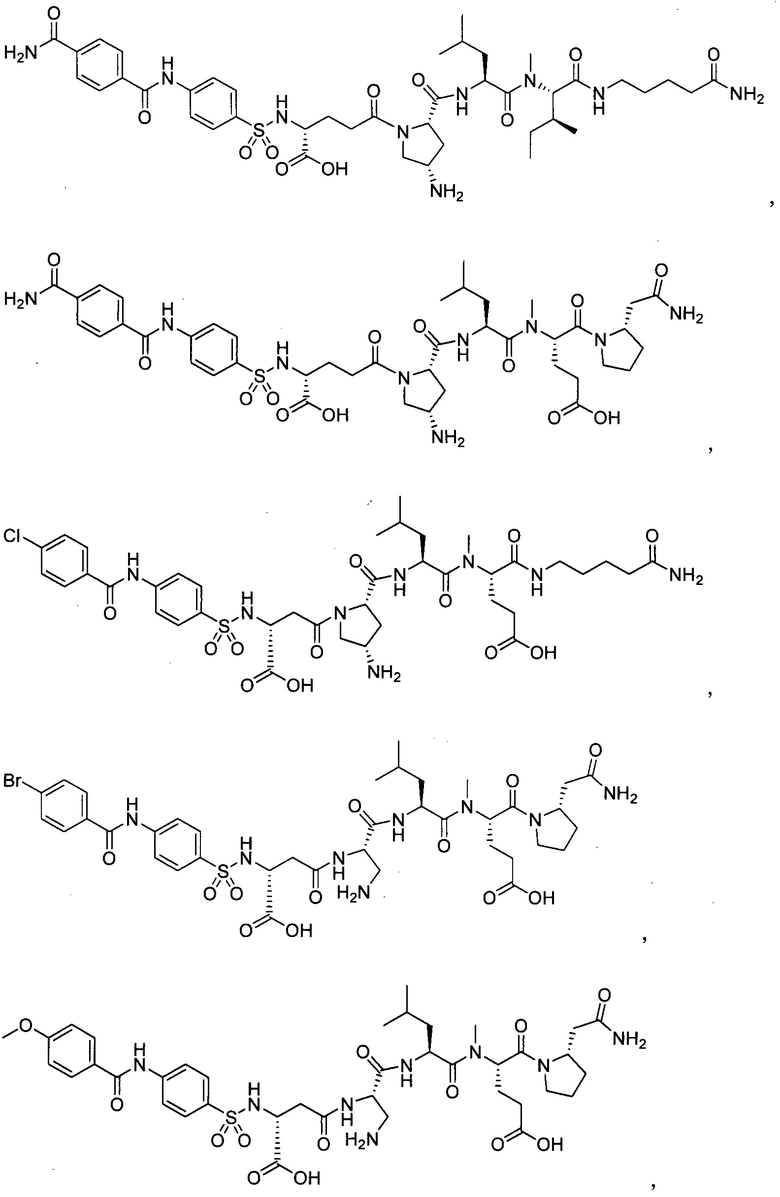
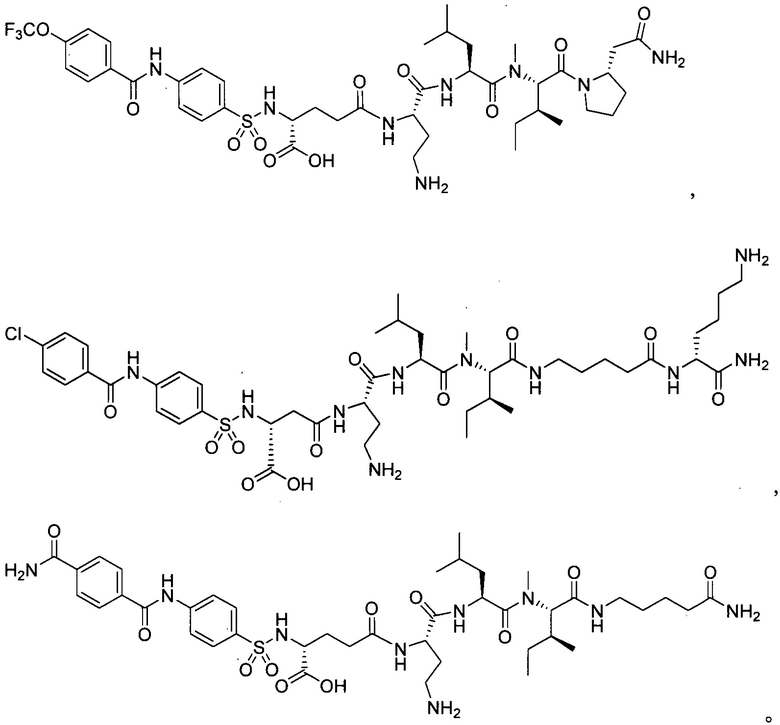
Другим предпочтительным вариантом осуществления соединений по настоящему изобретению является замещенный полипептид или его фармацевтически приемлемая соль,
где L2 представляет собой одинарную связь и
замещенный полипептид представлен формулой [I'-C]:
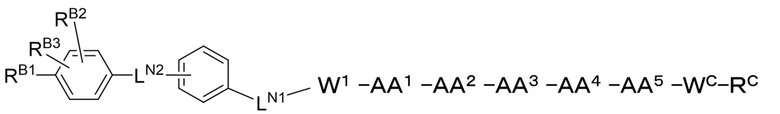 [I'-C],
[I'-C],
где
предпочтительно, варианты AA1, AA2, AA3, AA4, AA5, W1, LN1, LN2, RB1, RB2, RB3, WC и RC такие, как описаны выше.
В более предпочтительном варианте осуществления полипептида, представленного формулой [I'-C] или его фармацевтически приемлемой соли,
AA1 представляет собой Asp, β-(d)-Asp или γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
или группы, представленной формулой [II-1]:
 [II-1]
[II-1]
где RAA2 представляет собой амино,
AA3 представляет собой Val, Leu или Ile,
AA4 представляет собой (N-Me)Ile или (N-Me)Glu,
AA5 представляет собой Ape или β-гомоPro,
W1 представляет собой -L1- или -L1'-L1»-,
где L1 представляет собой одинарную связь,
L1' is GABA или Ape, и
L1" представляет собой Asn, (d)-Ser, (d)-Thr или Glu,
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-,
RB1, RB2 и RB3 каждый независимо представляет собой атом водорода, карбамоил, атом галогена, C1-6 алкокси или галоген C1-6 алкокси,
WC представляет собой одинарную связь или (d)-Lys, и
RC представляет собой формулу -NH2.
В еще более предпочтительном варианте осуществления полипептида, представленного формулой [I'-C] или его фармацевтически приемлемой соли,
AA1 представляет собой Asp,
AA1 может быть β-(d)-Asp,
AA1 может быть γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [IV-7] или [IV-9]:
 [IV-7],
[IV-7],  [IV-9]
[IV-9]
AA2 может быть группы, представленной формулой [II-1']:
 [II-1']
[II-1']
где RAA2 представляет собой амино,
AA3 представляет собой Val,
AA3 может быть Leu,
AA3 может быть Ile,
AA4 представляет собой (N-Me)Ile,
AA4 может быть (N-Me)Glu,
AA5 представляет собой Ape,
AA5 может быть β-гомоPro,
W1 представляет собой -L1- или -L1'-L1"-,
L1 представляет собой одинарную связь,
комбинация L1' и L1" (-L1'-L1"-) представляет собой GABA-Asn, Ape-Asn, Ape-Glu, Ape-(d)-Ser или Ape-(d)-Thr,
LN1 представляет собой формулу -C(=O)-,
LN1 может быть формулой -S(=O)2-,
LN2 представляет собой формулу -O-,
LN2 может быть формулой -C(=O)-NH-,
RB1 представляет собой карбамоил, атом хлора, атом брома, метокси или трифторметокси,
RB2 представляет собой атом водорода,
RB3 представляет собой атом водорода,
WC представляет собой одинарную связь,
WC может быть (d)-Lys, и
RC представляет собой формулу -NH2.
В особенно предпочтительном режиме настоящего изобретения,
замещенный полипептид, представленный формулой [I'-C] представляет собой любой из следующих:
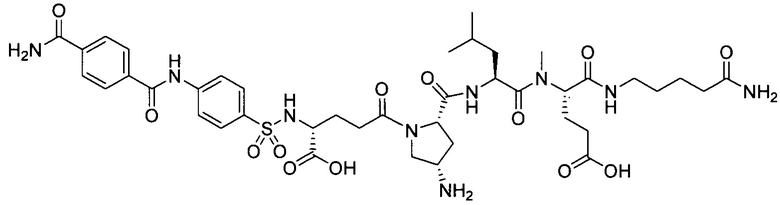 ,
,
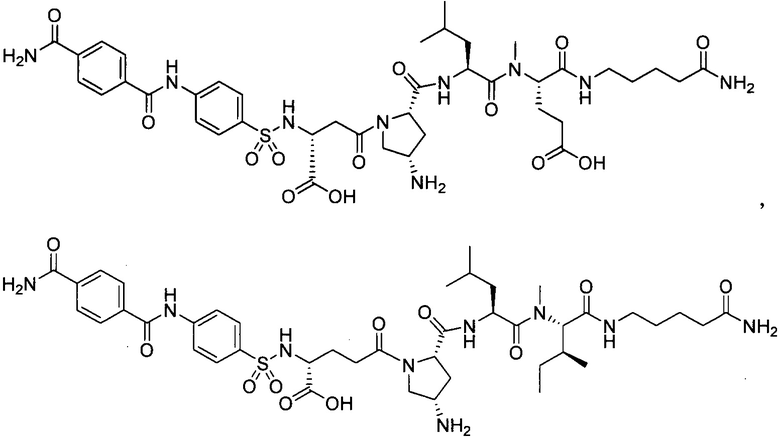 ,
,
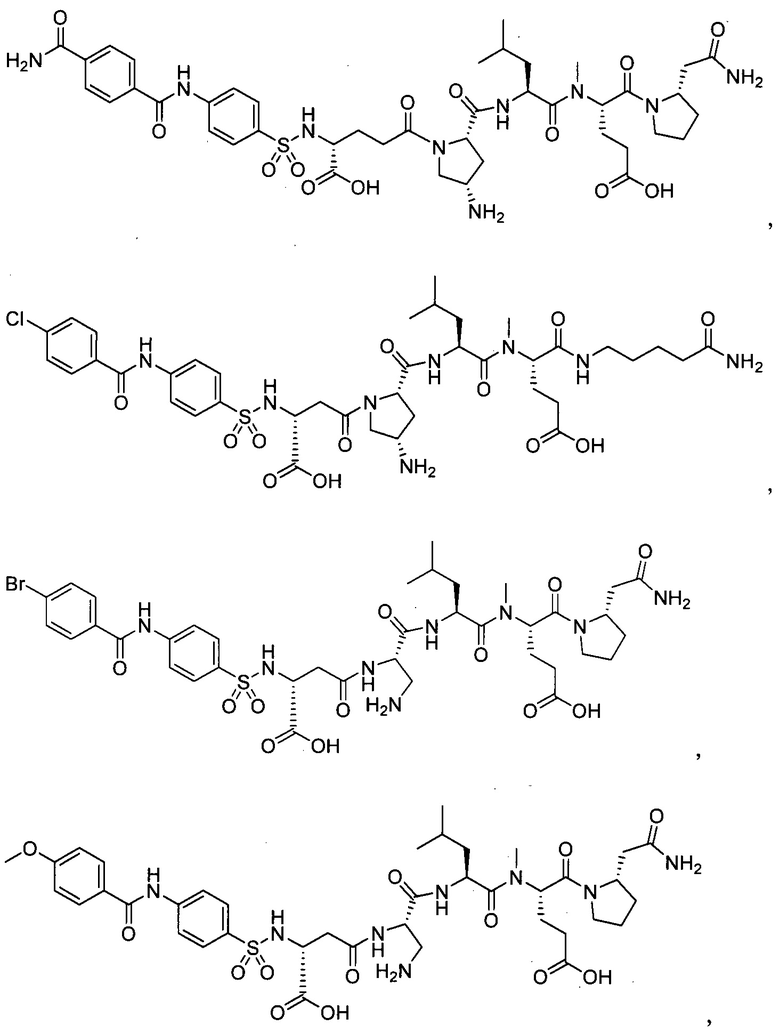
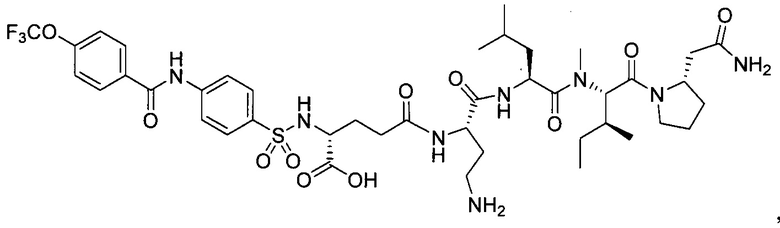
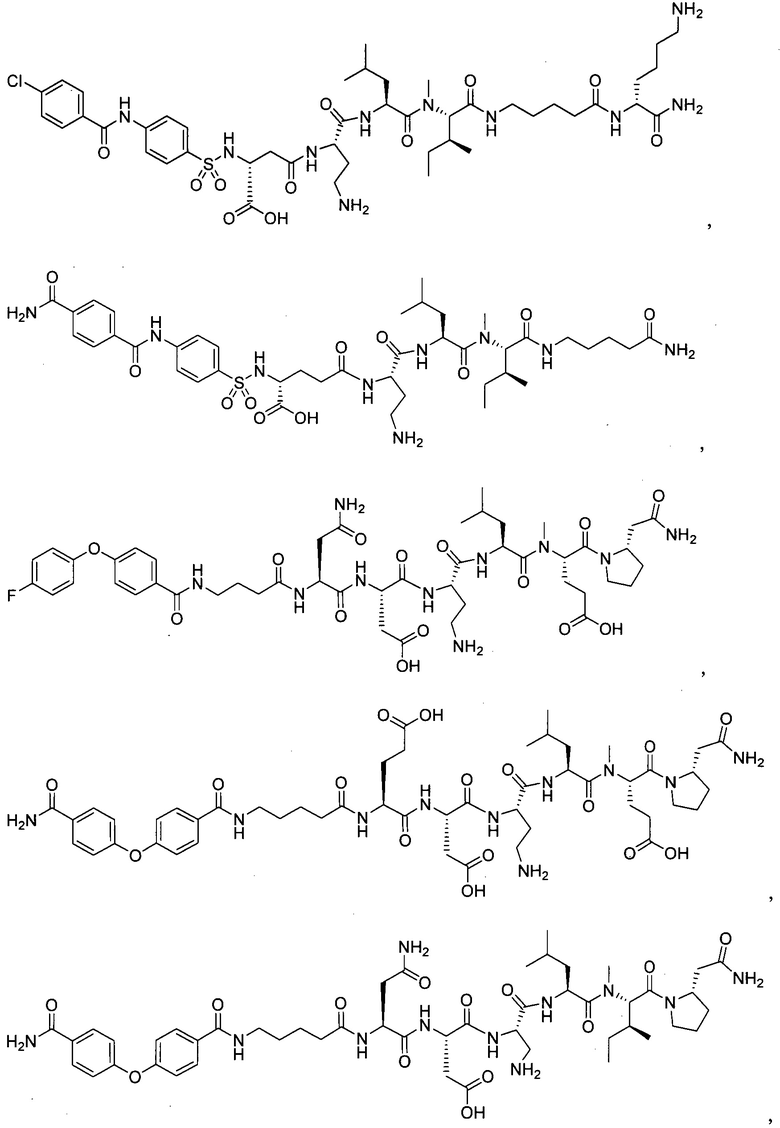
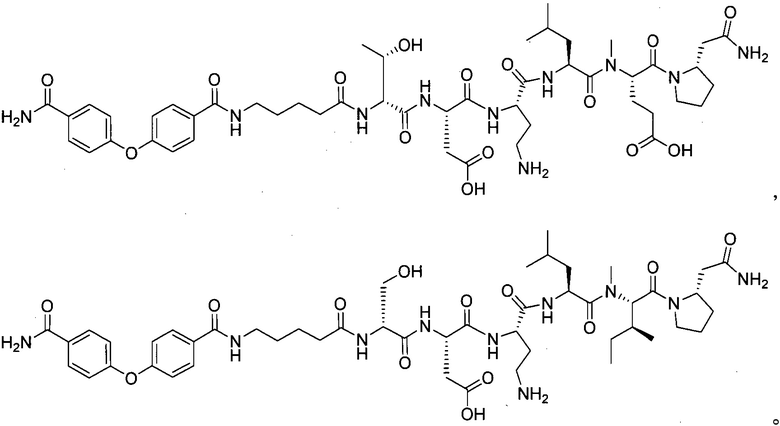
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-C], следующий:
 .
.
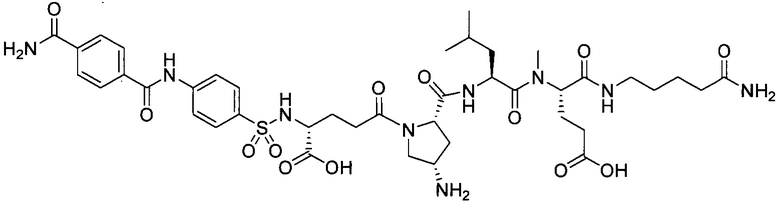
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-C], следующий:
 .
.
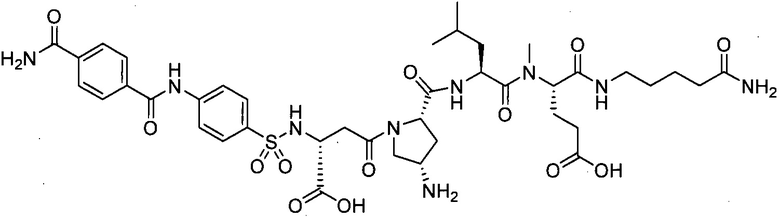
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-C], следующий:
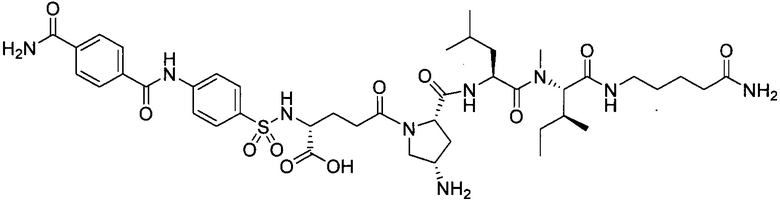 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-C], следующий:
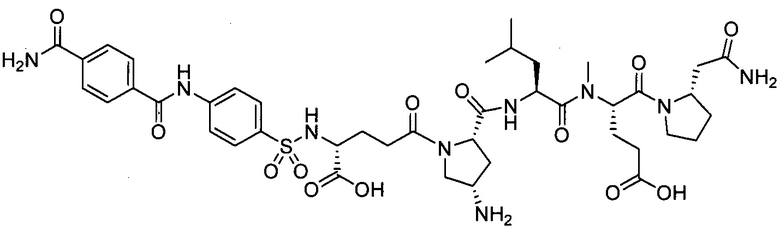 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I'-C], следующий:
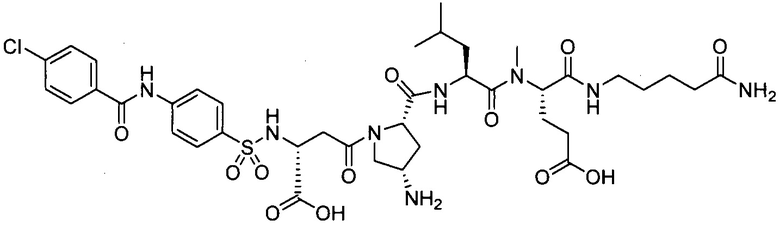 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
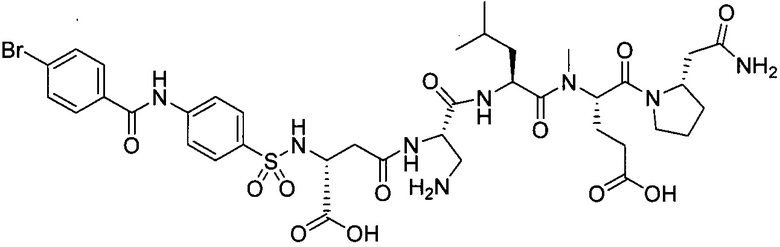 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
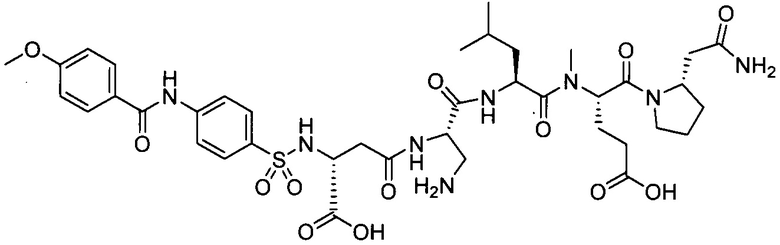 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
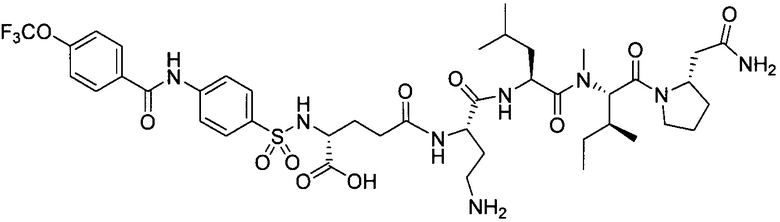 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
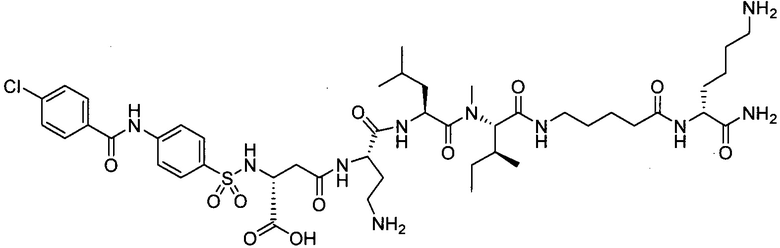 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
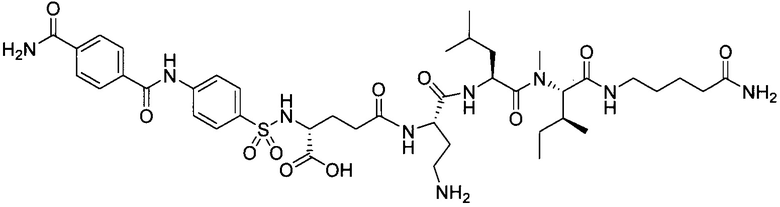 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
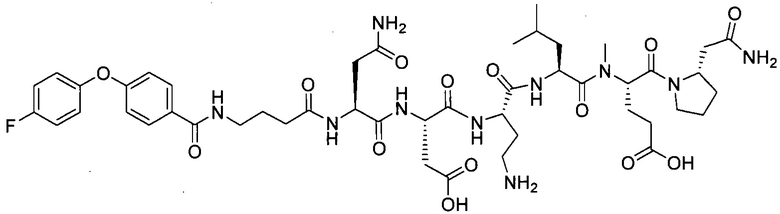 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
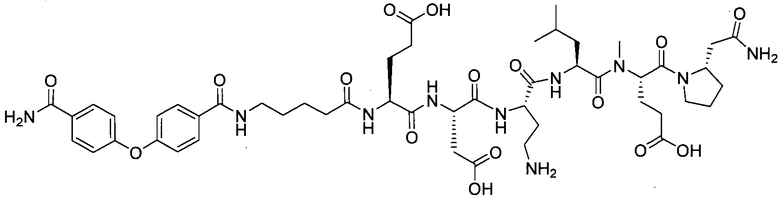 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
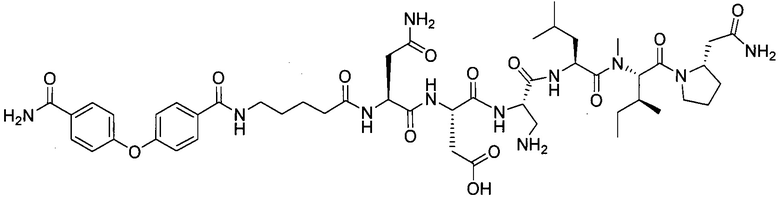 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
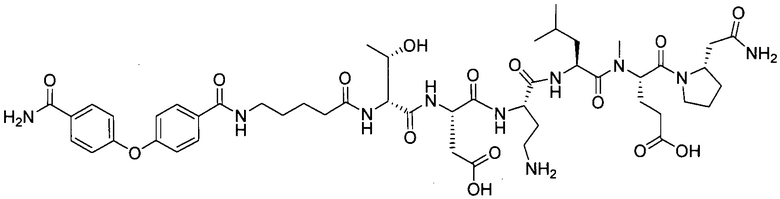 .
.
В другом особенно предпочтительном режиме настоящего варианта осуществления,
замещенный полипептид, представленный формулой [I’-C], следующий:
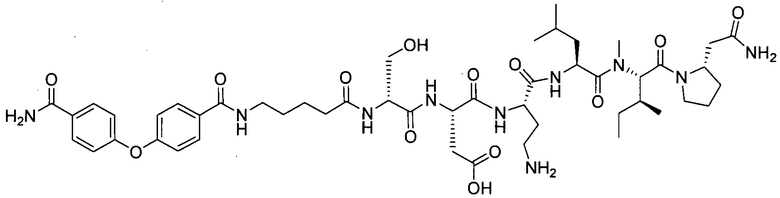 .
.
Другим предпочтительным вариантом осуществления соединений по настоящему изобретению является замещенный полипептид, представленный формулой [1], или его фармацевтически приемлемая соль, где
AA1 представляет собой β-Asp, γ-Glu или γ-(d)-Glu,
AA2 представляет собой группу, представленную формулой [II-1] или формулой [II-2]:
 [II-1],
[II-1],  [II-2]
[II-2]
где RAA2 представляет собой гидрокси или амино,
AA3 представляет собой Val, Leu, Ile, Phe или Trp,
AA4 представляет собой одинарную связь, Pro, (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Asp или (N-Me)Glu,
AA5 представляет собой одинарную связь, Pro, (d)-Pro, β-гомоPro, Arg, (d)-Arg, Lys, (d)-Lys, β-Ala, GABA, Ape или Acp,
L1 представляет собой одинарную связь,
L2 представляет собой одинарную связь,
LN1 представляет собой формулу -S(=O)2-,
LN2 представляет собой одинарную связь, формулу -O- или формулу -C(=O)-NH-,
RA представляет собой атом водорода,
RB представляет собой атом водорода, карбамоил, атом галогена или C1-6 алкокси,
LC представляет собой одинарную связь, Pro, Arg, (d)-Arg, Lys, (d)-Lys или (d)-Lys-(d)-Lys, и
RC представляет собой формулу -NH2.
Каждое из соединений по настоящему изобретению представляет собой соединение, имеющее основной остов полипептида, состоящего из трех-семи аминокислот и дополнительно имеющего замещенный бензоил или замещенный фенилсульфонил, и может быть в форме его фармацевтически приемлемой соли.
Примеры фармацевтически приемлемой соли включают: соли неорганических кислот, такие как гидрохлориды, гидробромиды, гидройодиды, фосфаты, сульфаты и нитраты; кислотно-аддитивные соли, такие как сульфонаты, включая метансульфонаты, этансульфонаты, бензолсульфонаты, п-толуолсульфонаты и трифторметансульфонаты и соли органических кислот, включая оксалаты, тартраты, цитраты, малеаты, сукцинаты, ацетаты, трифторацетаты, бензоаты, миндаляты, аскорбаты, лактаты, глюконаты и малаты; соли аминокислот, такие как глицинаты, лизинаты, аргинаты, орнитинаты, глутаматы и аспартаты; неорганические соли, такие как соли лития, соли натрия, соли калия, соли кальция и соли магния; и соли с органическим основанием, такие как соли аммония, соли триэтиламина, соли диизопропиламина и соли циклогексиламина. Соли включают гидратные соли.
Каждое из соединений по настоящему изобретению может иметь асимметричный центр и в этом случае для него существуют различные оптические изомеры. Таким образом, каждое из соединений по настоящему изобретению может существовать как индивидуальное оптически активное вещество в любой из (R)-формы и (S)- форме или в виде рацемата или смеси (RS). Для соединения, имеющего два или несколько асимметричных центров, дополнительно существуют диастереомеры из-за их оптической изомерии. Объем соединений по настоящему изобретению также включает смеси, содержащие все формы в любом соотношении. Например, диастереомеры могут быть разделены с помощью метода, хорошо известного специалистам в данной области техники, такого как метод фракционной кристаллизации, и оптически активные вещества могут быть получены с помощью метода органической химии, хорошо известного специалистам в данной области техники для этой цели. В дополнение, геометрические изомеры, такие как цис форма и транс форма, могут существовать для каждого из соединений по настоящему изобретению. Более того, каждое из соединений по настоящему изобретению проявляет таутомерию и существуют различные их таутомеры. Объем соединений по настоящему изобретению также включает эти изомеры и смеси, содержащие их, в любом соотношении.
Кроме того, если любое из соединений по настоящему изобретению или их соль образует гидрат или сольват, гидрат или сольват также входят в объем соединений по настоящему изобретению или их солей.
«Матричная металлопротеаза 2 (ММР2)» представляет собой одну из эндопептидаз, имеющих активный центр цинка.
Как описано выше, MMP2 разрушает внеклеточный матрикс, включая коллаген и желатин, и, следовательно, участвует в инфильтрации и миграции клеток, метастазировании и т.д., таким образом, участвуя в патологических состояниях раковых заболеваний, фиброзе органов и так далее.
Следовательно, раковое заболевание и фиброз органов и симптомы, относящиеся к раковому заболеванию и фиброзу органов, можно предотвратить или лечить путем ингибирования MMP2.
Соединения по настоящему изобретению обладают эффектом ингибирования ММР2. Соответственно, соединения по настоящему изобретению можно использовать в качестве ингибитора ММР 2 или активного ингредиента лекарственного средства для профилактики или лечения раковых заболеваний или фиброза органов.
Кроме того, соединения по настоящему изобретению можно использовать в качестве активного ингредиента лекарственного средства для профилактики или лечения симптомов, связанных с раковым заболеванием и фиброзом органов.
Примеры «раковых заболеваний» включают рак молочной железы, рак поджелудочной железы, рак мочевого пузыря, колоректальный рак, рак яичников, рак предстательной железы, опухоль головного мозга, рак желудка, гепатоцеллюлярную карциному, рак головы и шеи, меланому, рак матки, рак пищевода, почечно-клеточную карциному, рак легкого и глиому. Примеры «симптомов, относящихся к раковому заболеванию» включают боль, связанную с размножением опухолевых клеток или ростом опухоли, потерю массы тела и паранеопластический синдром.
Примеры «фиброза органов» включают хроническую болезнь почек, интерстициальную пневмонию и идиопатический фиброз легких. Примеры «симптомов, относящихся к фиброзу органов» включают протеинурию, дисфункцию почек и так далее при хронической болезни почек, и одышку при физической нагрузке, сухой кашель и так далее при интерстициальной пневмонии и идиопатическом фиброзе легких.
Оценку действия любого из соединений по настоящему изобретению по ингибированию ММР2 можно проводить с помощью известной процедуры, такой как способ, описанный ниже в Экспериментальных примерах в настоящем описании.
Для фармацевтических препаратов в соответствии с настоящим изобретением, соединение, обладающее эффектом ингибирования ММР2, представляющее собой любое из соединений по настоящему изобретению, содержащееся в фармацевтических препаратах, или его фармацевтические приемлемой соли, может вводиться отдельно или вместе с фармацевтически приемлемой добавкой.
В качестве средства можно использовать обычный эксципиент или разбавитель и, при необходимости, связующее, разрыхлитель, смазывающий агент, агент для покрытия, агент для сахарного покрытия, регулятор pH и солюбилизатор или водный или неводный растворитель, который обычно используется в качестве добавки. Конкретные примеры добавок могут включать воду, лактозу, декстрозу, фруктозу, сахарозу, сорбит, маннит, полиэтиленгликоль, пропиленгликоль, крахмал, кукурузный крахмал, камедь, желатин, аргинат, силикат кальция, фосфат кальция, целлюлозу, водный сироп, метилцеллюлозу, поливинилпирролидон, алкилпара-гидроксибензоат, тальк, стеариновую кислоту, стеарат магния, агар, пектин, аравийскую камедь, глицерин, кунжутное масло, оливковое масло, соевое масло, масло какао, этиленгликоль, низковязкую гидроксипропилцеллюлозу (HPC-L), микрокристаллическую целлюлозу, карбоксиметилцеллюлозу (CMC), карбоксиметилцеллюлозу натрия (CMC-Na) и другие распространенные добавки.
Фармацевтический препарат по настоящему изобретению может быть в любой форме твердых композиций, жидких композиций и других композиций, и оптимальная форма выбирается по необходимости.
Фармацевтический препарат по настоящему изобретению может быть приготовлен, например, в виде таблетки, пилюли, капсулы, гранулы, порошкового агента, порошка, раствора, эмульсии, суспензии или инъекции с помощью обычной технологии приготовления с добавлением вышеупомянутой добавки к любому из соединений по настоящему изобретению.
Фармацевтический препарат по настоящему изобретению может быть составлен путем образования клатратного соединения с любым из соединений по настоящему изобретению и α-, β- или γ-циклодекстрином или метилированным циклодекстрином.
Что касается соединений, которые можно использовать в комбинации с любым из соединений по настоящему изобретению, фармацевтические препараты по настоящему изобретению могут быть приготовлены в виде одного состава (комбинированного лекарственного средства) или двух или нескольких составов (сопутствующих лекарственных средств), полученных путем раздельного составления.
Если эти соединения составлены по-отдельности в два или несколько составов, отдельные составы можно вводить одновременно или по-отдельности через определенные промежутки времени. В последнем случае, любой состав можно вводить первым. Два или несколько составов можно вводить в разном количестве доз в сутки. Два или несколько составов можно вводить разными путями.
Если эти соединения составлены по-отдельности в два или несколько составов, их можно вводить одновременно или по отдельности через очень короткие промежутки времени, и следует указать, как использовать их в комбинации с помощью документа, такого как сопроводительный документ или рекламный проспект коммерчески доступного фармацевтического препарата.
Также необходимо отдельно составлять эти активные ингредиенты в виде набора, состоящего из двух составов.
Форма введения, когда любое из соединений по настоящему изобретению используется в качестве ингибитора MMP2 или подобного, не ограничивается, и любое из соединений по настоящему изобретению можно вводить прямо перорально или парентерально. Альтернативно, средство, содержащий любое из соединений по настоящему изобретению в качестве активного ингредиента может вводиться перорально или парентерально.
Также в случае, когда любое из соединений по настоящему изобретению используется в качестве средства для профилактики или лечения ракового заболевания или фиброза органов или симптомов, связанных с раковым заболеванием или фиброзом органов, любое из соединений по настоящему изобретению можно вводить непосредственно перорально или парентерально. Альтернативно, агент, содержащий любое из соединений по настоящему изобретению в качестве активного ингредиента, может вводиться перорально или парентерально.
При парентеральном введении, предпочтительно осуществлять внутривенное введение, подкожное введение или чрескожное введение.
Примеры дозированной формы для парентерального введения включают инъекцию, капельную инфузию, имплантат с лекарственным средством, трансдермальное лекарственное средство, трансмукозальное лекарственное средство и пластырь, и дозированная форма может представлять собой состав в виде микросфер.
Доза любого из соединений по настоящему изобретению различается в зависимости от субъектов, путей введения, заболеваний-мишеней, симптомов и так далее, и обычно желательно пероральное или парентеральное введение взрослому пациенту для введения разовой дозы от 0,1 мг до 1000 мг, предпочтительно, от 1 мг до 200 мг, от одного до трех раз в сутки или один раз каждые 2-3 дня.
Примеры получения составов соединений по настоящему изобретению будут показаны ниже.
Пример получения 1
Получают гранулу, содержащую следующие компоненты.
Компоненты: соединение, представленное общей формулой [I'], лактоза и кукурузный крахмал, HPC-L.
Соединение, представленное общей формулой [I'] и лактозу просеивают. Кукурузный крахмал просеивают. Их смешивают с помощью миксера. К перемешанному порошку добавляют водный раствор HPC-L и полученную смесь замешивают, гранулируют (экструзионная грануляция) и затем сушат. Полученную сухую гранулу просеивают через вибросито с получением гранулы.
Пример получения 2
Получают порошок для инкапсулирования, содержащий следующие компоненты.
Компоненты: соединение, представленное общей формулой [I'], лактоза и кукурузный крахмал, стеарат магния.
Соединение, соединение, представленное общей формулой [I'] и лактозу просеивают. Кукурузный крахмал просеивают. Их смешивают вместе со стеаратом магния с помощью миксера с получением порошка. Полученный порошок может быть инкапсулирован.
Пример получения 3
Получают гранулу для инкапсулирования, содержащую следующие компоненты.
Компоненты: соединение, представленное общей формулой [I'], лактоза и кукурузный крахмал, HPC-L.
Соединение, представленное общей формулой [I'] и лактозу просеивают. Кукурузный крахмал просеивают. Их смешивают с помощью миксера. К перемешанному порошку добавляют водный раствор HPC-L, полученную смесь замешивают, гранулируют и затем сушат. Полученные сухие гранулы просеивают через вибросито для регулирования размера частиц и получают гранулы. Полученные гранулы могут быть инкапсулированы.
Пример получения 4
Получают таблетки, содержащие следующие компоненты.
Компоненты: соединение, представленное общей формулой [I'], лактоза, микрокристаллическая целлюлоза, стеарат магния и CMC-Na.
Соединение, представленное общей формулой [I'], лактозу, микрокристаллическую целлюлозу и CMC-Na просеивают и смешивают вместе. Стеарат магния добавляют к смешанному порошку для получения смешанного порошка для состава. Этот смешанный порошок подвергают прямому прессованию с получением таблетки.
Пример получения 5
Получают инъекцию, содержащую следующие компоненты.
Компоненты: соединение, представленное общей формулой [I'], очищенный лецитин яичного желтка, олеиновая кислота, очищенное соевое масло, глицерин и вода для инъекций.
Соединение, представленное общей формулой [I'], очищенный лецитин яичного желтка и олеиновую кислоту добавляют к очищенному соевому маслу для растворения в нем, затем добавляют воду для инъекций, смешанную с глицерином, и полученную смесь эмульгируют с помощью эмульгатора. Туда же добавляют воду для инъекций и полученную смесь разливают по аликвотам в ампулы, которые запаивают и стерилизуют для получения инъекций.
Способы получения соединения [I'] в соответствии с настоящим изобретением будут подробно описаны ниже, но получение не ограничивается приведенными в качестве примеров способами получения. Растворитель, используемый для получения, может быть любым растворителем, который не ингибирует отдельные реакции, и не ограничивает следующее описание.
При получении соединения [I'] порядок стадий получения может быть соответствующим образом изменен.
При получении каждое исходное соединение может быть использовано в виде его соли, и примеры таких солей включают «фармацевтически приемлемую соль», представленную выше.
Соединение [I'] может быть получено с помощью твердофазного синтеза, жидкофазного синтеза или их комбинации Примеры получения твердофазным синтезом будут показаны в следующих способах получения.
Соединение [I'] может быть получено способами, показанными на любой из схем 1-9, или любой их комбинацией.
Боковая цепь каждой аминокислоты, образующая полипептидную группу соединения [I'], может иметь функциональную группу, и функциональная группа может быть защищена защитной группой. Примеры защитной группы включают tBu для карбокси, Trt для карбамоила, tBu для гидрокси, tBu для фенольного гидроксида, tBu для тиола (сульфанила), Boc для амино, Trt для имидазолила, Boc для индолила и Pbf для гуанидино. Каждая из этих защитных групп может быть подвергнута снятию защиты путем обработки кислотой.
Каждая из аминокислот может быть использована для производства, даже если функциональная группа в боковой цепи не защищена.
Способ A: способ получения соединения [1-f], соединения, в котором амино N-концевой аминокислоты полипептидной группы сульфонилировано, и карбокси C-концевой аминокислоты амидировано (-CONH2)
Соединение [1-f] может быть получено, например, с помощью твердофазного синтеза, сущность которого описана ниже (схема 1).
Схема 1

где
RA1, RA2, RB1, RB2, RB3, LN2, кольцо A и кольцо B имеют такие же определения, как описаны выше,
H-Zx-OH представляет собой аминокислоту,
x представляет собой целое число от 1 до m,
m представляет собой целое число от 2 до 15,
где Zx соответствует AAx, L2, W1 или Wc в соединении, представленном формулой [I'] и может представлять одинарную связь, и
PGx представляет собой липорастворимую защитную группу, защищающую амино аминокислоты (H-Zx-OH).
(1) [Стадия 1-1]
Смолу, имеющую амино, защищенную Fmoc (соединение [1-a]) подвергают снятию Fmoc с применением основания.
(2) [Стадия 1-2]
Смолу, полученную в (1) подвергают взаимодействию с аминокислотой, амино которой замещена липорастворимой защитной группой (PGx) (соединение [1-b]) для реакции амидирования между свободной амино в смоле и карбокси в соединении [1-b].
(3) [Стадия 1-3]
Липорастворимую защитную группу амино N-концевой аминокислоты полипептидной группы в соединении, полученном в (2), подвергают снятию защиты.
(4)
При повторении стадий (2) и (3) два или несколько раз может быть получено соединение [1-c], в котором карбокси C-концевой аминокислоты полипептидной группы связана со смолой, и амино N-концевой аминокислоты свободна.
(5) [Стадия 1-4]
Соединение [1-e] может быть получено реакцией соединения [1-c], полученного в (4), с соединением [1-d] для сульфонилирования свободной амино в соединении [1-c].
(6) [Стадия 1-5]
Соединение [1-f], одно из соединений по настоящему изобретению, может быть получено путем использования кислоты на соединении [1-e], полученном в (5), для расщепления связи со смолой. Примеры кислоты, применимой на настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует в боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [1-f], полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на Схеме 1, смола [1-a], соединение [1-b] и соединение [1-d], используемые в качестве исходных соединений, могут быть получены путем получения известным способом, или путем приобретения коммерчески доступных продуктов из них.
Способ B: способ получения соединения [2-c], соединения, в котором амино N-концевой аминокислоты полипептидной группы ацилирована, и карбокси C-концевой аминокислоты амидирована (-CONH2)
Соединение [2-c] может быть получено, например, посредством твердофазного синтеза, сущность которого описана ниже (схема 2), с использованием соединения [1-c] в качестве исходного материала.
Схема 2
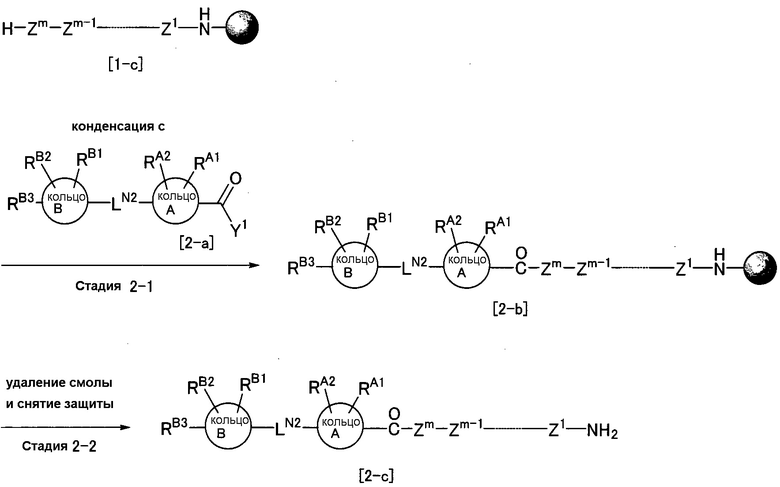
где
RA1, RA2, RB1, RB2, RB3, LN2, кольцо A, кольцо B, H-Zx-OH, x, m и Zx имеют такие же определения, как описаны выше, и
Y1 представляет собой гидрокси или атом хлора.
(1) [Стадия 2-1]
Соединение [2-b] может быть получено, позволяя соединению [2-a] воздействовать на соединение [1-c] для реакции амидирования.
(2) [Стадия 2-2]
Соединение [2-c], одно из соединений по настоящему изобретению, может быть получено путем использования кислоты на соединении [2-b], полученном в (1), для расщепления связи со смолой. Примеры кислот, применимых в настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [2-c], полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на Схеме 2, соединение [2-a], используемое в качестве исходного материала, может быть получено путем получения известным способом или путем приобретения коммерчески доступного его продукта. Соединение [1-c] может быть получено способом, описанным на схеме 1.
Способ C-1: способ получения соединения [3-h], соединения, в котором аминогруппа N-концевой аминокислоты полипептидной части сульфонилирована или ацилирована, и карбоксигруппа C-концевой аминокислоты вторично- или третично-амидирована.
Соединение [3-h] может быть получено, например, с помощью твердофазного синтеза, сущность которого описано ниже (схема 3).
Примеры смолы (смола [3-а]), применяемой в настоящем способе получения, могут включать хлортритилхлоридную смолу и смолу Ванга.
Схема 3
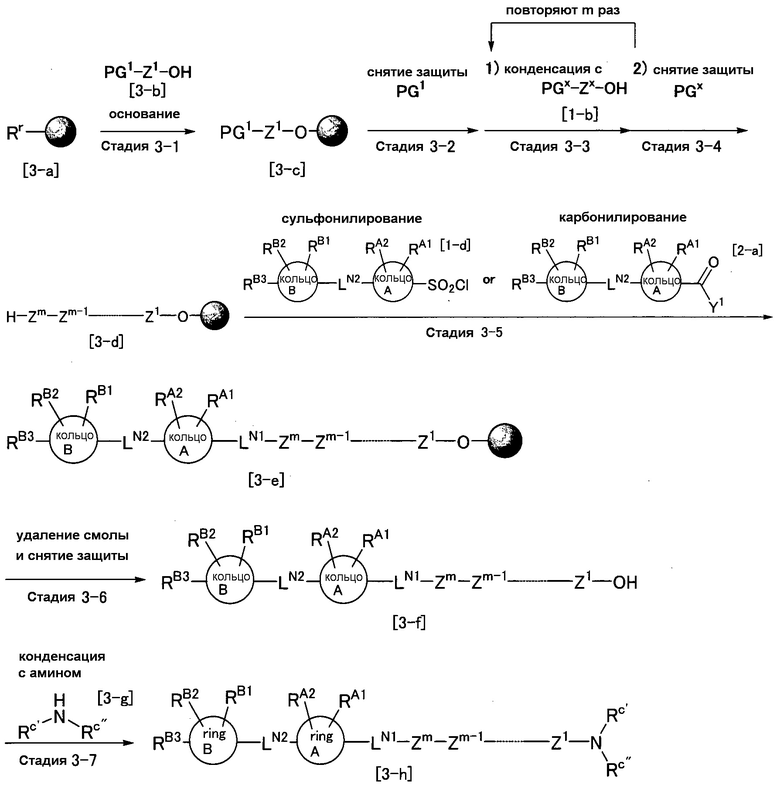
где
RA1, RA2, RB1, RB2, RB3, LN1, LN2, кольцо A, кольцо B, H-Zx-OH, x, m, Zx, PGx и Y1 имеют такие же определения, как описаны выше,
Rr представляет собой гидрокси или атом хлора,
Rc' и Rc" являются одинаковыми или разными и каждый представляет атом водорода или C1-6 алкил, где C1-6 алкил необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, амино и C1-6 алкокси,
Rc' и Rc" могут быть взяты вместе с соседним атомом азота с образованием четырех-семи-членного насыщенного гетероцикла, содержащего атом азота, где
четырех-семи-членный насыщенный гетероцикл, содержащий атом азота, образованный Rc' и Rc" взятыми вместе с соседним атомом азота, необязательно замещен одной группой, выбранной из группы, состоящей из гидрокси, амино, C1-6 алкила и C1-6 алкокси, и
два атома углерода в четырех-семи-членном насыщенным гетероцикле, содержащем атом азота, образованным Rc' и Rc" взятыми вместе с соседним атомом азота, необязательно перекрестно сшиты с C1-4 алкандиилом.
(1) [Стадия 3-1]
Соединение [3-c] может быть получено взаимодействием смолы (соединение [3-a]) с аминокислотой, амино которой замещена липорастворимой защитной группой (PG1) (соединение [3-b]).
(2) [Стадия 3-2]
Липорастворимую защитную группу (PG1) в соединении [3-c], полученном в (1) подвергают снятию защиты.
(3) [Стадия 3-3]
Соединение, полученное в (2) подвергают взаимодействию с аминокислотой, амино которой замещена липорастворимой защитной группой (PGx) (соединение [1-b]) для реакции амидирования между свободной амино в соединении, полученном в (1), и карбокси в соединении [1-b].
(4) [Стадия 3-4]
Липорастворимую защитную группу амино N-концевой аминокислоты полипептидной группы в соединении, полученном в (3), подвергают снятию защиты.
(5)
При повторении стадий (3) и (4) два или несколько раз, может быть получено соединение [3-d], в котором карбокси C-концевой аминокислоты полипептидной группы связана со смолой, и амино N-концевой аминокислоты является свободной.
(6) [Стадия 3-5]
Соединение [3-e] может быть получено реакцией соединения [3-d], полученного в (5) с соединением [1-d] или соединением [2-a] для сульфонирования или ацилирования свободной амино в соединении [3-d].
(7) [Стадия 3-6]
Соединение [3-f], в котором карбокси C-концевой аминокислоты полипептидной группы является свободной, может быть получено с применением кислоты на соединении [3-e], полученном в (6) для отщепления связи со смолой. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
(8) [Стадия 3-7]
Соединение [3-h], одно из соединений настоящего изобретения, может быть получено, позволяя соединению [3-g] действовать на соединение [3-f] полученное в (7) для реакции амидирования.
Соединение [3-h] полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 3, соединение [3-a], соединение [3-b], соединение [1-b], соединение [1-d], соединение [2-a] и [3-g] применяемые в качестве исходных соединений могут быть получены известным способом или путем приобретения коммерчески доступных их продуктов.
Способ C-2: способ получения соединения [4-e], соединения, в котором амино N-концевой аминокислоты полипептидной группы сульфонилирована или ацилирована, и карбокси C-концевой аминокислот вторично- или третично-амидирована
Альтернативно, соединение [4-e] может быть получено, например, твердофазным синтезом, сущность которого описана далее (Схема 4).
На схеме 4, в качестве примера представлен способ получения соединения, где функциональная группа присутствует в боковой цепи m-ной аминокислоты, считаемой от C-концевой аминокислоты полипептидной группы в соединении [4-e].
Примеры смолы, применяемой в настоящем способе получения, могут включать, как и на схеме 3, хлортритилхлоридную смолу и смолу Ванга.
Схема 4
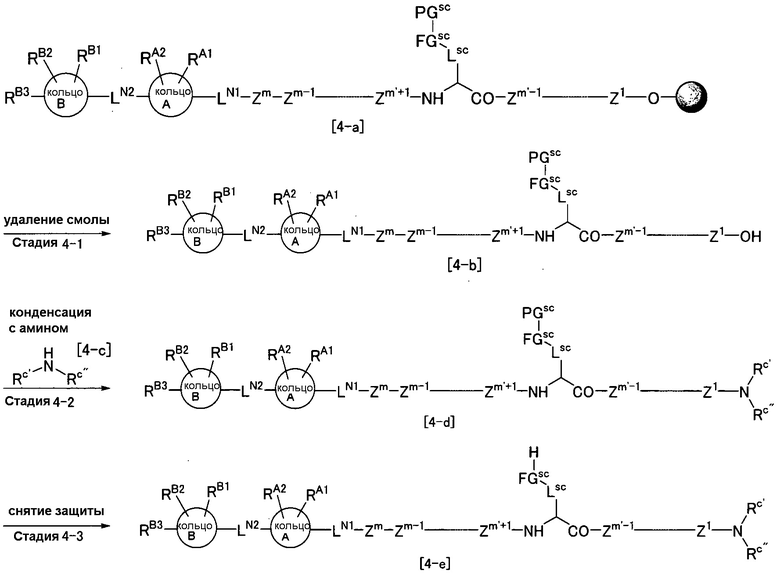
где
RA1, RA2, RB1, RB2, RB3, LN1, LN2, кольцо A, кольцо B, H-Zx-OH, x, m, Zx, Rc' и Rc» имеют такие же определения, как описаны выше,
m' представляет собой целое число от 1 до 15, при условии, что отношение «m'≤m» удовлетворяется,
Lsc представляет собой C1-4 алкандиил,
FGsc представляет собой вышеуказанную функциональную группу, присутствующую на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты полипептидной группы,
где примеры функциональной группы могут включать формулу -O- (формулу -OH), формулу -S- (формулу -SH), формулу -NH- (формулу -NH2), формулу -C(=O)O- (формулу -C(=O)OH), формулу -C(=O)NH- (формулу -C(=O)NH2) и формулу -NHC(=NH)NH- (-NHC(=NH)NH2), и
PGsc представляет собой защитную группу для функциональной группы,
где примеры функциональной группы могут включать, как описано выше, tBu, Trt, Boc и Pbf.
(1) [Стадия 4-1]
Соединение [4-b], в котором карбокси C-концевой аминокислоты полипептидной группы является свободной, может быть получено с применением кислоты на соединении [4-a] для отщепления связи со смолой.
В то же время, снятие защитной группы (PGsc), присутствующей на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты, может предотвращаться с применением слабой кислоты в качестве кислоты. Примеры слабой кислоты могут включать HFIP, уксусную кислоту и разведенную ТФК.
(2) [Стадия 4-2]
Соединение [4-d] может быть получено позволяя соединению «4-c» действовать на соединение [4-b], полученное в (1), для реакции амидирования между свободной карбокси в соединении [4-b] и амино в соединении [4-c].
(3) [Стадия 4-3]
Соединение [4-e], одно из соединений настоящего изобретения, может быть получено с применением кислоты для снятия вышеуказанной защитной группы (PGsc) присутствующей на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК.
Соединение [4-e] полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 4, соединение [4-c], применяемое в качестве исходного соединения, может быть получено путем получения известным способом или путем приобретения коммерчески доступного его продукта. Соединение [4-a] может быть получено способом, описанным на схеме 3.
Способ D: способ получения соединения [5-f], в котором функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, функциональная группа замещена полипептидным линкером, и амино N-концевой аминокислоты полипептидного линкера заменена на «C1-20 алкилкарбонил, замещенный карбокси»
Соединение [5-f] может быть получено твердофазным синтезом, сущность которого описана далее (Схема 5).
В настоящем документе, полипептидный линкер состоит из одной-пяти аминокислот.
На схеме 5, в качестве примера представлен способ получения соединения, где функциональная группа присутствует на боковой цепи m-ной аминокислоты, считая от С-концевой аминокислоты полипептидной группы в соединении [5-f], функциональная группа замещена полипептидным линкером, и амино N-концевой аминокислоты полипептидного линкера замещена «C1-20 алкилкарбонилом, замещенным карбокси».
Схема 5
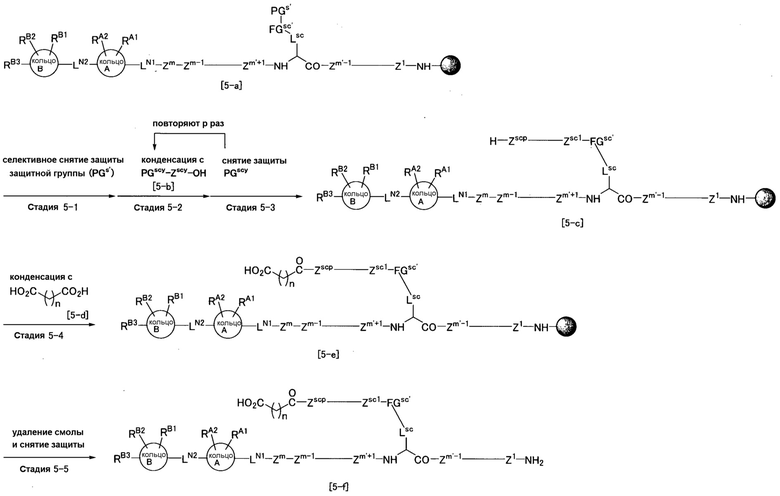
где
RA1, RA2, RB1, RB2, RB3, LN1, LN2, кольцо A, кольцо B, H-Zx-OH, x, m, m', Zx и Lsc имеют такие же определения, как описаны выше,
PGs' представляет собой защитную группу для вышеуказанной функциональной группы (FGsc'), присутствующей на боковой цепи аминокислоты, где примеры защитной группы включают Dde, ivDde, Alloc и Mtt для амино,
H-Zsc y-OH представляет собой аминокислоту, образующую полипептидный линкер, присоединенный к функциональной группе (FGsc'),
y представляет собой целое число от 1 до p,
p представляет собой целое число от 0 до 5,
PGsc y представляет собой липорастворимую защитную группу, защищающую амино аминокислоты (H-Zsc y-OH),
FGsc' представляет собой функциональную группу, присутствующую на боковой цепи аминокислоты; примеры функциональной группы могут включать формулу -NH- (формулу -NH2) и формулу -COO- (формулу -COOH); Схема 5 показывает случай, где FGsc' представляет собой формулу -NH- (формулу -NH2), и
n представляет собой целое число от 1 до 20.
(1) [Стадия 5-1]
Защитную группу (PGS') для функциональной группы, присутствующей на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты полипептидной группы в соединении [5-a] подвергают селективному снятию защиты.
(2) [Стадия 5-2]
Соединение, полученное в (1) подвергают взаимодействию с аминокислотой, амино которой замещена липорастворимой защитной группой (PGsc y) (соединение [5-b]) для реакции амидирования между свободной функциональной группой (FGsc') в соединении, полученном в (1), и карбокси в соединении [5-b].
(3) [Стадия 5-3]
Липорастворимую защитную группу (PGsc y) подвергают снятию защиты.
(4)
При повторении стадий (2) и (3) один или несколько раз, может быть получено соединение [5-c], в котором карбокси C-концевой аминокислоты полипептидной группы связана со смолой, функциональной группой присутствующей на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты, замещена полипептидным линкером, амино N-концевой аминокислоты полипептидного линкера является свободной.
(5) [Стадия 5-4]
Соединение [5-e] может быть получено реакцией соединения [5-c], полученного в (4), с соединением [5-d], которое представляет собой алкандикарбоновую кислоту, для реакции амидирования свободной амино в соединении [5-c] с одной карбокси в соединении [5-d].
(6) [Стадия 5-5]
Соединение [5-f], одно из соединений настоящего изобретения, может быть получено с применением кислоты на соединении [5-e], полученном в (5), для отщепления связи со смолой. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [5-f] полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 5, соединение [5-b] и соединение [5-d] применяемые в качестве исходных соединений могут быть получены известным способом или путем приобретения коммерчески доступных их продуктов. Соединение [5-a] может быть получено способом, описанным на схеме 1 или схеме 2 или, или способом, аналогичным любому из них.
Способ E: способ получения соединения [6-c], в котором функциональная группа присутствует на боковой цепи каждой из двух аминокислот из аминокислот, образующих полипептидную группу, и функциональные группы замещены одним и тем же полипептидным линкером (-Zsc 1-Zsc 2-…-Zsc y'-) с образованием кольца.
Соединение [6-c] может быть получено, например, твердофазным синтезом, сущность которого описана далее (Схема 6).
В настоящем документе, полипептидный линкер состоит из одной-пяти аминокислот.
На схеме 6, в качестве примера представлен способ получения соединения, где функциональная группа присутствует на боковой цепи m-ной и m"-ной аминокислоты, считая от С-концевой аминокислоты полипептидной группы, и функциональные группы замещены одним и тем же полипептидным линкером с образованием кольца.
Схема 6
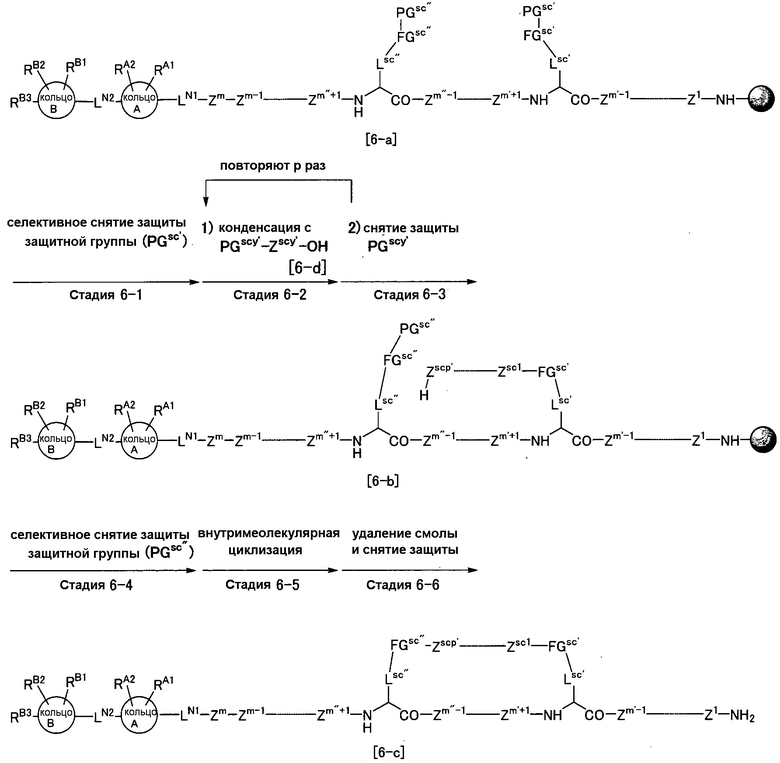
где
RA1, RA2, RB1, RB2, RB3, LN1, LN2, кольцо A, кольцо B, H-Zx-OH, x, m, m', Zx и Lsc имеют такие же определения, как описаны выше,
m" представляет собой целое число от 2 до 15, при условии, что отношение «m'<m"≤m» удовлетворяется,
полипептидный линкер (-Zsc 1-Zsc 2-…-Zsc y'-) в соединении [6-c] соответствует L3 в соединении, представленном формулой [I'], где L3 представляет собой Gly, β-Ala или GABA,
y' представляет собой целое число от 1 до p',
p' представляет собой целое число от 1 до 4,
Lsc' и Lsc" каждый представляет собой C1-4 алкандиил,
FGsc' и FGsc" каждый представляет собой функциональную группу, присутствующую на боковой цепи аминокислоты, где функциональная группа представляет собой формулу -O- (формулу -OH), формулу -S- (формулу -SH), формулу -NH- (формулу -NH2), формулу -C(=O)O- (формулу -C(=O)OH) или формулу -C(=O)NH- (формулу -C(=O)NH2), и
PGsc' и PGsc" каждый представляет собой защитную группу для функциональной группы, присутствующей на боковой цепи аминокислоты, где функциональной группой является, например, Dde, ivDde, Alloc или аллил.
(1) [Стадия 6-1]
Защитную группу (PGsc') для функциональной группы, присутствующей на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты полипептидной группы в соединении [6-a] подвергают селективному снятию защиты.
(2) [Стадия 6-2]
Соединение, полученное в (1), подвергают взаимодействию с аминокислотой, амино которой замещена липорастворимой защитной группой (PGsc y') (соединение [6-d]) для реакции амидирования между свободной функциональной группой (FGsc') в соединении, полученном в (1), и карбокси в соединении [6-d], амино которой защищена липорастворимой защитной группой.
(3) [Стадия 6-3]
Липорастворимую защитную группу подвергают снятию защиты.
(4)
При повторении стадий (2) и (3) один или неколько раз, может быть получено соединение [6-b], в котором функциональная группа, присутствующая на боковой цепи м-ной аминокислоты, считая от C-концевой аминокислоты полипептидной группы, замещена полипептидным линкером, амино N-концевой аминокислоты полипептидного линкера является свободной, и функциональная группа (FGsc") присутствующая на боковой цепи m"-ной аминокислоты, считая от C-концевой аминокислоты, защищена защитной группой (PGsc").
(5) [Стадия 6-4]
Защитную группу (PGsc"), присутствующую на боковой цепи m"-ной аминокислоты, считая от C-концевой аминокислоты полипептидной группы в соединении [6-b], подвергают селективному снятию защиты.
(6) [Стадия 6-5]
«Свободная функциональная группа (FGsc")» и «свободная амино в Zscp'» в соединении, полученном в (5), взаимодействуют для внутримолекулярной реакции циклизации.
(7) [Стадия 6-6]
Соединение [6-c], одно из соединений настоящего изобретения, может быть получено с применением кислоты на соединении, полученном в (6), для отщепления связи со смолой. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [6-c], полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 6, соединение [6-d], применяемое в качестве исходного соединения, может быть получено путем получения известным способом или путем приобретения коммерчески доступного его продукта. Соединение [6-a] может быть получено способом, описанным на схеме 1 или схеме 2 или способом, аналогичным любому из этих.
Способ F: способ получения соединения [7-f], который имеет заместитель, «алкиламинокарбонил, замещенный функциональной группой», на кольце B
Соединение [7-f] может быть получено, например, твердофазным синтезом, сущность которого описана далее (Схема 7).
Схема 7
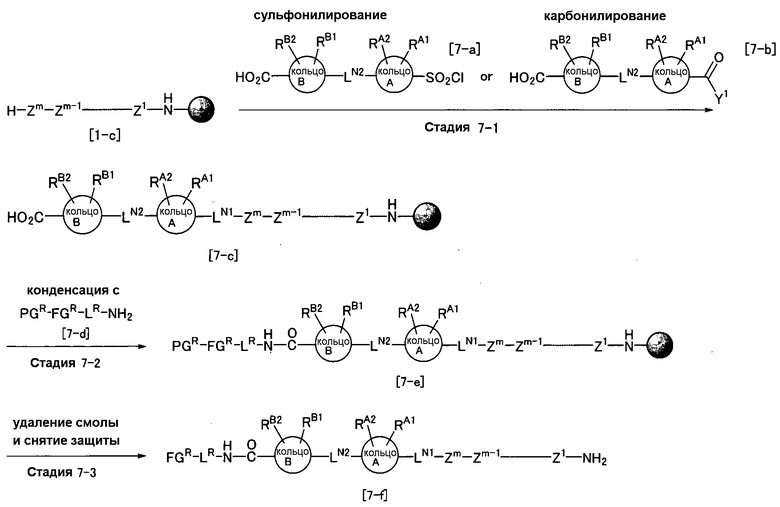
где
RA1, RA2, RB1, RB2, LN1, LN2, кольцо A, кольцо B, H-Zx-OH, x, m, Zx и Y1 имеют такие же определения, как описаны выше,
LR представляет собой C1-4 алкандиил,
FGR представляет собой функциональную группу, присоединенную к «алкил (LR)» «алкиламинокарбонил (LR-NHC(=O)-)», заместитель, присутствующий на кольце B и его примеры могут включать формулу -O- (формулу -OH), формулу -S- (формулу -SH), формулу -NH- (формулу -NH2), формулу -C(=O)O- (формулу -C(=O)OH) и формулу -C(=O)NH- (формулу -C(=O)NH2),
PGR представляет собой защитную группу для функциональной группы (FGR), где примеры защитной группы включают tBu для карбокси, Trt для карбамоила, tBu для гидрокси, tBu для тиола (сульфанила) и Boc для амино, и каждая из этих защитных групп может быть лишена защиты обработкой кислотой.
(1) [Стадия 7-1]
Соединение [7-c], которое имеет карбокси на кольце B, может быть получено реакцией соединения [1-c] с соединением [7-a] или соединением [7-b] для сульфонирования или ацилирования свободной амино N-концевой аминокислоты полипептидной группы в соединении [1-c].
(2) [Стадия 7-2]
Соединение [7-e] может быть получено реакцией соединения [7-c] с соединением [7-d] для реакции амидирования между карбокси в соединении [7-c] и амино в соединении [7-d].
(3) [Стадия 7-3]
Соединение [7-f], одно из соединений настоящего изобретения, может быть получено с применением кислоты на соединении [7-e], полученном в (2), для отщепления связи со смолой и одновременного снятия защитной группы (PGR) функциональной группы «алкиламинокарбонила, замещенного функциональной группой (FGR)», присутствующего на кольце B. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК. В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [7-f] полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 7, соединение [7-a], соединение [7-b] и соединение [7-d] применяемые в качестве исходных соединений, могут быть получены известным способом или путем приобретения коммерчески доступных их продуктов. Соединение [1-c] может быть получено способом, описанным на схеме 1 или аналогичным способом.
Способ G: способ получения соединения [8-f], в котором кольцо A непосредственно замещено кольцом B
Соединение [8-f] может быть получено, например, твердофазным синтезом, сущность которого описана далее (Схема 8).
Схема 8
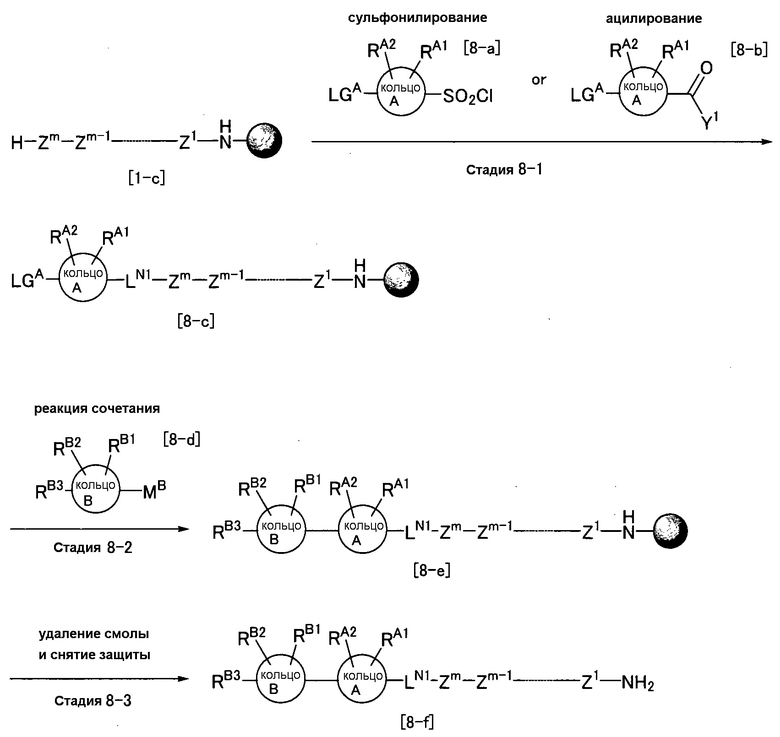
где
RA1, RA2, RB1, RB2, RB3, LN1, кольцо A, кольцо B, H-Zx-OH, x, m, Zx и Y1 имеют такие же определения, как описаны выше,
LGA представляет собой уходящую группу, где примеры уходящей группы могут включать атом хлора, атом брома, атом йода и галоген C1-6 алкилсульфонилокси, и
MB представляет собой бороновую кислоту, сложный эфир бороновой кислоты, алкилолово, алкилсилан или алкоксисилан.
(1) [Стадия 8-1]
Соединение [8-c] может быть получено реакцией соединения [1-c] с соединением [8-a] или соединением [8-b] для сульфонирования или ацилирования свободной амино N-концевой аминокислоты полипептидной группы в соединении [1-c].
(2) [Стадия 8-2]
Соединение [8-e], в котором кольцо A непосредственно замещено кольцом B, может быть получено реакцией сочетания соединения [8-c] с соединением [8-d] в присутствии металлического катализатора и основания. Примеры металлического катализатора могут включать тетракис(трифенилфосфин)палладий, ацетат палладия и трис(дибензилиденацетон)дипалладий. Примеры основания могут включать карбонаты металла, такие как карбонат цезия, карбонат калия и карбонат натрия и фосфат калия, фторид цезия и фторид тетрабутиламмония.
(3) [Стадия 8-3]
Соединение [8-f], одно из соединений настоящего изобретения, может быть получено с применением кислоты на соединении [8-e], полученном в (2), для отщепления связи со смолой. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [8-f] полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 8, соединение [8-a], соединение [8-b] и соединение [8-d] применяемые в качестве исходных соединений могут быть получены известным способом или путем приобретения коммерчески доступных их продуктов. Соединение [1-c] может быть получено способом, описанным на схеме 1 или аналогичным способом.
Способ H: способ получения соединения [9-f], которое имеет заместитель «арилкарбониламино (формула кольца B-C(=O)NH-)» на кольце A
Соединение [9-f] может быть получено, например, твердофазным синтезом, сущность которого описана далее (Схема 9).
Схема 9
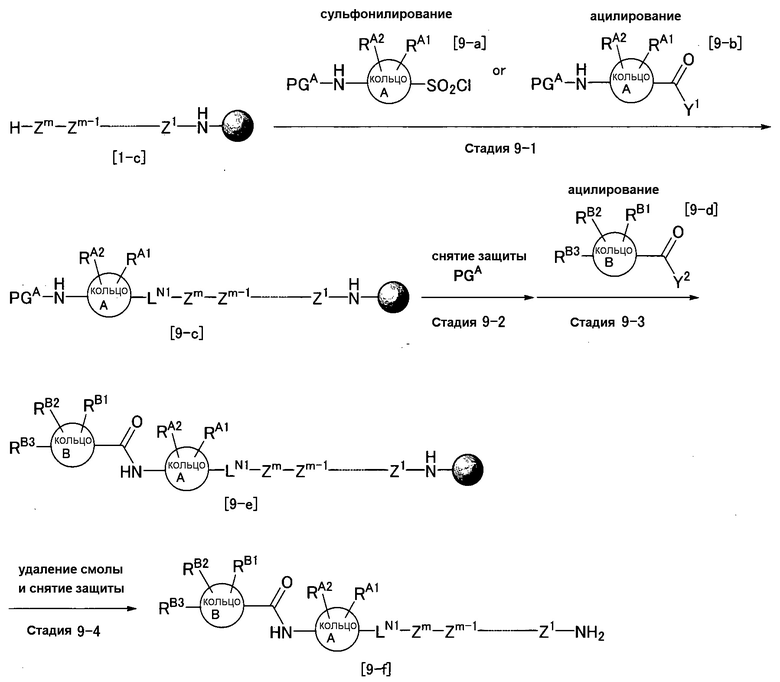
где
RA1, RA2, RB1, RB2, RB3, LN1, кольцо A, кольцо B, H-Zx-OH, x, m, Zx и Y1 имеют такие же определения, как описаны выше,
Y2 представляет собой гидрокси или атом хлора, и
PGA представляет собой липорастворимую защитную группу, защищающую амино, присутствующую на кольце A,
где примеры липорастворимой группы могут включать Fmoc.
(1) [Стадия 9-1]
Как на стадии 8-1 со схемы 8, соединение [9-c] может быть получено реакцией соединения [1-c] с соединением [9-a] или соединением [9-b] для сульфонирования или ацилирования свободной амино N-концевой аминокислоты полипептидной группы в соединении [1-c].
(2) [Стадия 9-2]
Липорастворимую защитную группу (PGA) в соединении [9-c], полученном в (1), подвергают снятию защиты.
(3) [Стадия 9-3]
Соединение [9-e] может быть получено реакцией соединения, полученного в (2), с соединением [9-d] для реакции амидирования (ацилирования) между свободной амино в соединении, полученном в (2), и карбокси в соединении [9-d].
(4) [Стадия 9-4]
Соединение [9-f], одно из соединений настоящего изобретения, может быть получено с применением кислоты на соединении [9-e], полученном в (3), для отщепления связи со смолой. Примеры кислоты, применяемой на настоящей стадии, могут включать ТФК.
В то же время, если защищенная функциональная группа присутствует на боковой цепи аминокислоты, образующей полипептидную группу, защитная группа функциональной группы может быть одновременно лишена защиты.
Соединение [9-f] полученное описанным способом, можно выделить/очистить с помощью известных средств разделения/очистки, таких как концентрирование, концентрирование при пониженном давлении, переосаждение, экстракция растворителем, кристаллизация и хроматография.
В способе, описанном на схеме 9, соединение [9-a], соединение [9-b] и соединение [9-d] применяемые в качестве исходных соединений, могут быть получены известным способом или путем приобретения коммерчески доступных их продуктов. Соединение [1-c] может быть получено способом, описанным на схеме 1 или аналогичным способом.
Все виды аминокислот могут применяться в качестве аминокислот в способах, показанных на схемах 1-9 для получения соединения [I'] по настоящему изобретению, и примеры аминокислот включают природные протеогенные L-аминокислоты: Gly, Ala, Val, Leu, Ile, Pro, Phe, His, Trp, Tyr, Ser, Thr, Met, Cys, Asp, Glu, Asn, Gln, Lys и Arg.
Кроме того, аминокислоты не природного происхождения, включая природные не протеогенные аминокислоты и D-формы природных протеогенных L-аминокислот, описанные выше, могут применяться в настоящих способах получения.
В настоящем документе, примеры аминокислот не природного происхождения, применяемые в настоящих способах получения, включают следующие:
- (d)-Pro, (d)-Ser, (d)-Thr, (d)-Asp, (d)-Glu, (d)-Arg, (d)-Lys
- β-гомоPro
- β-Ala, GABA, Ape, Acp
- (N-Me)Ala, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Asp, (N-Me)Glu
- группу, представленную формулой [II-1] или формулой [II-2]:
 [II-1],
[II-1],  [II-2]
[II-2]
где RAA2 представляет собой гидрокси или амино; и
- аминокислоты, перечисленные в таблице 1 и таблице 2
Примеры жирорастворимых защитных групп могут включать карбонатные защитные группы, амидные защитные группы и алкильные защитные группы, такие как 9-флуоренилметоксикарбонил (Fmoc), трет-бутилоксикарбонил (Boc), бензил (Bn), аллил (Аллил), аллилоксикарбонил (Alloc) и ацетил (Ac). Введение жирорастворимой защитной группы в аминокислоту, например, введение Fmoc, может быть достигнуто добавлением 9-флуоренилметил-N-сукцинидилкарбоната и гидрокарбоната натрия для реакции. Рекомендуется проводить реакцию при температуре от 0 до 50°C, предпочтительно при комнатной температуре, примерно от 1 до 5 часов.
Могут быть использованы коммерчески доступные аминокислоты, защищенные жирорастворимой защитной группой. Их примеры могут включать Fmoc-Ser-OH, Fmoc-Asn-OH, Fmoc-Val-OH, Fmoc-Leu-OH, Fmoc-Ile-OH, Fmoc-Ala-OH, Fmoc-Tyr-OH, Fmoc-Gly-OH, Fmoc-Lys-OH, Fmoc-Arg-OH, Fmoc-His-OH, Fmoc-Asp-OH, Fmoc-Glu-OH, Fmoc-Gln-OH, Fmoc-Thr-OH, Fmoc-Cys-OH, Fmoc-Met-OH, Fmoc-Phe-OH, Fmoc-Trp-OH и Fmoc-Pro-OH.
Примеры аминокислот, защищенных жирорастворимой защитной группой и имеющих защитную группу, введенную в боковую цепь, могут включать Fmoc-Arg(Pbf)-OH, Fmoc-Asn(Trt)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Cys(tBu)-OH, Fmoc-Glu(OtBu)-OH, Fmoc-Gln(Trt)-OH, Fmoc-His(Trt)-OH, Fmoc-Lys(Boc)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Trp(Boc)-OH и Fmoc-Tyr(tBu)-OH.
Смола может представлять собой любую смолу, обычно используемую для твердофазного синтеза, и, например, применима 2-хлортритилхлоридную смолу, которая функционализирована атомом хлора, смолу Ванга, смолу HMPA-PEGA и смолу амино-PEGA, которая функционализирована амино.
Твердофазный синтез с использованием смолы для амидного синтеза рекомендуется в качестве способа получения амида, образованного на С-конце пептида. Например, может применяться смола Rink-Amide-AM, смола SAL-PEG, смола SAL-MBHA или смола Rink-Amide-PEGA. Амид, образованный на С-конце пептида, может быть получен путем отщепления пептида от смолы.
Для связывания аминокислоты, амино которой замещена жирорастворимой защитной группой, со смолой, например, в случае, если используют смолу, содержащую гидрокси, или смолу, функционализированную атомом хлора, связывание может проводиться через связывание карбокси аминокислоты со смолой с образованием сложной эфирной связи.
В случае использования смолы, функционализированной амино, связывание может быть достигнуто за счет образования карбоксигруппой аминокислоты амидной связи со смолой.
В случае использования 2-хлортритилхлоридной смолы, эстерификацию можно проводить с использованием таких веществ, как диизопропилэтиламин (DIPEA), триэтиламин, пиридин и 2,4,6-коллидин.
В случае использования смолы, содержащей гидрокси, известный дегидратирующий/конденсирующий агент, такой как 1-(мезитилен-2-сульфонил)-3-нитро-1,2,4,-триазол (MSNT), дициклогексилкарбодиимид (DCK) и диизопропилкарбодиимид (DIC) можно использовать в качестве катализатора эстерификации. Что касается соотношения использования аминокислоты и дегидратирующего/конденсирующего агента, количество последнего обычно составляет от 1 до 10 эквивалентов и, предпочтительно, от 2 до 5 эквивалентов на эквивалент первого.
Например, обычно проводят реакцию эстерификации таким образом, что смолу помещают в твердофазную колонку, эту смолу промывают растворителем, и затем к ней добавляют раствор аминокислоты. Примеры промывочного растворителя могут включать хлороформ, диметилформамид (ДМФ), 2-пропанол и дихлорметан. Примеры растворителя для растворения аминокислот в настоящем документе включают хлороформ, диметилсульфоксид (ДМСО), ДМФ и дихлорметан. Реакцию эстерификации рекомендуется проводить при температуре от 0 до 50°C, предпочтительно при комнатной температуре в течение примерно от 10 минут до 30 часов, предпочтительно, в течение примерно от 15 минут до 24 часов.
В то же время также предпочтительно ацетилировать непрореагировавший гидрокси на твердой фазе с использованием уксусного ангидрида или подобного для блокирования.
Удаление жирорастворимой защитной группы можно проводить, например, обработкой основанием. Примеры основания могут включать пиперидин и морфолин. При этом, предпочтительно проводить удаление в присутствии растворителя. Примеры растворителя может включать ДМФ, ДМСО и метанол.
Предпочтительно проводить реакцию амидирования между высвобождающимися амино и карбокси любой аминокислоты, амино которой замещена жирорастворимой защитной группой в присутствии активатора и растворителя.
Примеры активаторов могут включать дициклогексилкарбодиимид (DCK), 1-этил-3-(диметиламинопропил)карбодиимид гидрохлорид (WSC/HCl), дифенилфосфорилазид (DPPA), карбонилдиимидазол (CDI), диэтилцианофосфонат (DEPC), бензотриазол-1-илокси-триспирролидинофосфоний. (DIPCI), гексафторфосфат бензотриазол-1-илокси-триспирролидинофосфония (PyBOP), 1-гидроксибензотриазол (HOBt), гидроксисукцинимид (HOSu), диметиламинопиридин (DMAP), 1-гидрокси-7-азабензотриазол (HOAt), гидроксифталимид (HOPht), пентафторфенол (Pfp-OH), гексафторфосфат 2-(1H-бензотриазол-1-ил)-1,1,3,3,-тетраметилурония (HBTU), 3-оксид гексафторфосфат 1-[бис(диметиламино)метилен]-5-хлор-1H-бензотриазола (HCTU), гексафторфосфонат O-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония (HATU), тетрафторборат О-бензотриазол-1-ил-1,1,3,3-тетраметилурония (TBTU), 3,4-дигидро-3-гидроди-4-окса-1,2,3-бензотриазин (Dhbt), гексафторфосфат N-[1-(циано-2-этокси-2-оксоэтилиденаминоокси)диметиламино(морфолино)]урония (COMU) и этилциано(гидроксиимино)ацетат (Oxyma).
Необходимо установить количество используемого активатора от 1 до 20 эквивалентов, предпочтительно, от 1 до 10 эквивалентов, более предпочтительно от 1 до 5 эквивалентов по отношению к любой аминокислоте, аминогруппа которой защищена защитной группой, обладающей жирорастворимостью.
Примеры растворителей могут включать ДМФ, ДМСО и дихлорметан. Рекомендуется проводить реакцию при температуре от 0 до 50°С, предпочтительно, при комнатной температуре, в течение примерно от 10 минут до 30 часов, предпочтительно, примерно от 15 минут до 2 часов.
Отщепление пептидной цепи от смолы можно осуществить обработкой кислотой. Примеры кислот могут включать трифторуксусную кислоту (ТФК) и фтористый водород (HF). Рекомендуется проводить реакцию отделения от смолы при температуре от 0 до 50°C, предпочтительно, при комнатной температуре, в течение от примерно 10 минут до 10 часов, предпочтительно, в течение от примерно 30 минут до 4 часов.
Настоящее изобретение более подробно описано со ссылкой на приведенные ниже примеры, эталонные примеры и экспериментальные примеры, однако они не ограничивают настоящее изобретение, и могут быть сделаны любые модификации без отклонения от объема настоящего изобретения.
Сокращения в настоящей спецификации показаны ниже.
ХИАД: химическая ионизация при атмосферном давлении
Arg (Pbf): Nω-2,2,4,6,7-пентаметилдигидробензофурансульфониларгинин
Bu: бутил
BuOH: бутанол
Dde: 1-(4,4-диметил-2,6-диоксоциклогексилиден)-3-этил
ДМСО-d6: гексадейтрированный диметилсульфоксид
ИСРД: испарительный светорассеивающий детектор
ИЭР: ионизация электрораспылением
ВЭЖХ: высокоэффективная жидкостная хроматография
ivDde: 1-(4,4-диметил-2,6-диоксоциклогексилиден)-3-метилбутил
ЖХМС: жидкостная хроматография/масс-спектрометрия
NMP: 1-метил-2-пирролидон
Trt: тритил
УФ: ультрафиолетовые лучи
В настоящем документе «комнатная температура» относится к температуре от 20 до 30°C, если не указано иное.
«Охлаждение льдом» относится к температуре от 0 до 5°C, если не указано иное.
В настоящем документе Biotage (зарегистрированный товарный знак) SNAP Ultra производства Biotage AB, или REVELERIS (зарегистрированный товарный знак) Silica 40 мкм производства BUCHI Labortechnik AG используют в качестве «картриджа с силикагелем» при очистке с помощью колоночной хроматографии.
При очистке с помощью колоночной хроматографии с обращенной фазой (здесь и далее иногда называемой препаративной ЖХМС), подходящие условия выбирают из двух условий, показанных ниже, и проводят очистку.
Аппарат для разделения: используют Agilent 1260 Infinity и Agilent 6130 (метод ионизации: ионизация электронным распылением: ИЭР) или Agilent 385-ELSD, когда используют датчик ИСРД, каждый аппарат от Agilent Technologies.
Растворитель: раствор А; вода с 0,1% муравьиной кислоты, раствор В; ацетонитрил с 0,1% муравьиной кислотой.
Скорость потока: 50 мл/мин
Применяют одну из следующих колонок.
Waters XBridge Prep C18, 5 мкм, 30×50 мм
Waters XSelect CSH C18, 5 мкм, 30×50 мм
(Условия разделения A)
0,0-0,5 мин (раствор A/раствор B=90/10)
0,5-7,5 мин (раствор A/раствор B=90/10-20/80)
7,5-7,95 мин (раствор A/раствор B=20/80)
7,95-8,0 мин (раствор A/раствор B=20/80-5/95)
8,0-9,0 мин (раствор A/раствор B=5/95)
(Условия разделения B)
0,0-0,5 мин (раствор A/раствор B=95/5)
0,5-7,5 мин (раствор A/раствор B=95/5-50/50)
7,5-7,95 мин (раствор A/раствор B=50/50)
7,95-8,0 мин (раствор A/раствор B=50/50-5/95)
8,0-9,0 мин (раствор A/раствор B=5/95)
Результаты измерений, показанные в настоящем документе, определяют с помощью следующих инструментов.
Микроволновый реактор: Initiator (Biotage AB)
ЯМР спектр: [1H-ЯМР] 600 МГц: JNM-ECA600 (JEOL Ltd.), 400 МГц: AVANCE III HD 400 (Bruker)
Масс спектр высокоэффективной жидкостной хроматографии (ЖХМС) и время удержания (ВУ) в настоящей спецификации определяют в условиях, показанных далее.
Аппарат для измерения: LCMS-2010EV, Shimadzu Corporation
Колонка: Shimadzu XR-ODS, 2,2 мкм, 2,0×30 мм
Способ ионизации: ИЭР/ХИАД двойной источник
Растворитель: раствор A; вода с 0,1% муравьиной кислоты, раствор B; ацетонитрил с 0,1% муравьиной кислоты.
Скорость потока: 0,6 мл/мин, способ определения: УФ 210 нм, 254 нм
(Условия анализа A)
0,0-1,0 мин (раствор A/раствор B=90/10-60/40)
1,0-2,0 мин (раствор A/раствор B=60/40-1/99)
2,0-2,6 мин (раствор A/раствор B=1/99)
(Условия анализа B)
0,0-0,5 мин (раствор A/раствор B=90/10)
0,5-1,5 мин (раствор A/раствор B=90/10-70/30)
1,5-2,5 мин (раствор A/раствор B=70/30-1/99)
2,5-5,0 мин (раствор A/раствор B=1/99)
Названия соединений в примерах получения, эталонных примерах и примерах даны в соответствии с «ACD/Name 2019,1,2 (ACD Labs 2019,1,2, Advanced Chemistry Development Inc.)».
Эталонный пример 1. 4-(4-Карбамоилбензамид)бензолсульфонил хлорид
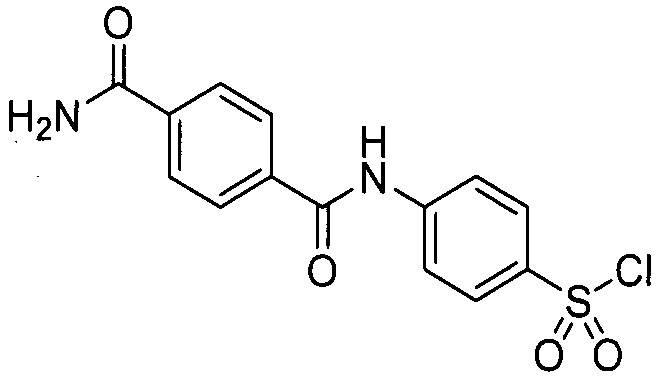
К раствору 4-карбамоилбензойной кислоты (150 г) в ДМФ (180 мл), добавляют WSC моногидрохлорид (209 г), HOBt моногидрат (167 г) и DIPEA (380 мл). После перемешивания при комнатной температуре в течение 5 минут, добавляют анилин (99 мл) и продукт перемешивают при комнатной температуре в течение 72 часов. К реакционному раствору добавляют воду, и твердый осадок собирают фильтрацией с получением N-фенилтерефталамида (147 г) в виде желтого аморфного вещества.
К полученному N-фенилтерефталамиду добавляют хлорсульфоновую кислоту (407 мл) и продукт перемешивают при 60°C в течение 1 часа при нагревании. Реакционную смесь охлаждают на льду и затем добавляют в ледяную воду. Твердый осадок собирают фильтрацией, промывают водой и затем сушат с получением указанного в заголовке соединения (198 г) в виде светло-желтого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6) δ ч./млн. 7,54 (шс, 1 H), 7,62 (д, J=8,2 Гц, 2 H), 7,79 (д, J=8,2 Гц, 2 H), 7,96-8,09 (м, 4 H), 8,14 (шс, 1 H), 10,46 (с, 1 H)
Эталонный пример 2. 4-(4-(Трифторметокси)бензамид)бензолсульфонил хлорид
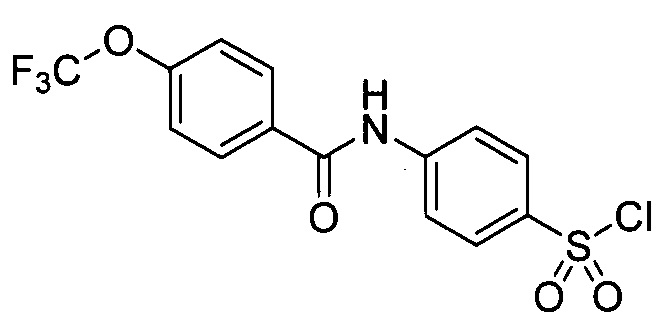
По методике эталонного примера 1, указанное в заголовке соединение получают в виде желтого твердого вещества из соответствующего исходного материала.
1H ЯМР (400 МГц, ДМСО-d6) δ ч./млн. 7,52 (д, J=8,3 Гц, 2 H), 7,58 (д, J=8,3 Гц, 2 H), 7,72 (д, J=8,3 Гц, 2 H), 8,08 (д, J=8,3 Гц, 2 H), 10,42 (с, 1 H)
Эталонный пример 3. 4-(4-(Метилкарбамоил)бензамид)бензолсульфонил хлорид
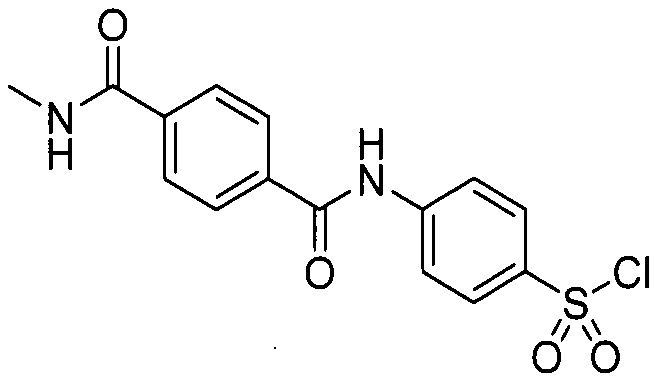
По методике эталонного примера 1, указанное в заголовке соединение получают в виде серого твердого вещества из соответствующего исходного материала.
1H ЯМР (600 МГц, ДМСО-d6) δ ч./млн. 2,81 (д, J=4,1 Гц, 3 H), 7,57-7,61 (м, 2 H), 7,72-7,78 (м, 2 H), 7,96 (д, J=8,7 Гц, 2 H), 8,03 (д, J=8,7 Гц, 2 H), 8,62 (кв, J=4,1, 1 H), 10,42 (с, 1 H)
Эталонный пример 4. 4-(4-(Диметилкарбамоил)бензамид)бензолсульфонил хлорид
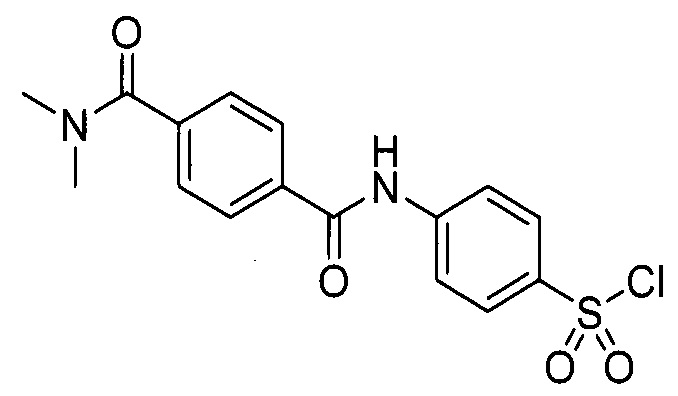
По методике эталонного примера 1, указанное в заголовке соединение получают в виде коричневого твердого вещества из соответствующего исходного материала.
1H ЯМР (600 МГц, ДМСО-d6) δ ч./млн. 2,91 (с, 3 H), 3,01 (с, 3 H), 7,54 (д, J=8,3 Гц, 2 H), 7,58 (д, J=8,3 Гц, 2 H), 7,74 (д, J=8,3 Гц, 2 H), 8,01 (д, J=8,3 Гц, 2 H), 10,41 (с, 1 H)
Эталонный пример 5. 4-(4-(Трифторметил)бензамид)бензолсульфонил хлорид
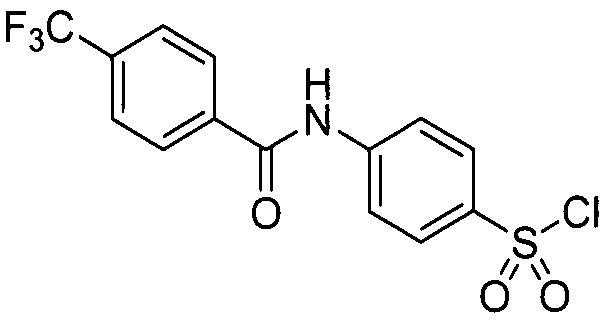
По методике эталонного примера 1, указанное в заголовке соединение получают в виде белого твердого вещества из соответствующего исходного материала.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ч./млн. 7,81 (д, J=8,2 Гц, 2 H), 7,93 (д, J=8,1 Гц, 2 H), 8,01 (д, J=8,2 Гц, 2 H), 8,08 (д, J=8,1 Гц, 3 H)
Эталонный пример 6. 4-(4-Цианобензамид)бензолсульфонил хлорид

По методике эталонного примера 1, указанное в заголовке соединение получают в виде светло-коричневого твердого вещества из соответствующего исходного материала.
1H ЯМР (600 МГц, ДМСО-d6) δ ч./млн. 7,58 (д, J=8,3 Гц, 2 H), 7,74 (д, J=8,3 Гц, 2 H), 7,99 (д, J=8,3 Гц, 2 H), 8,01 (д, J=8,3 Гц, 2 H), 10,42 (с, 1 H)
Эталонный пример 7. 4-(4-(1,1,2,2-Тетрафторэтокси)бензамид)бензолсульфонил хлорид
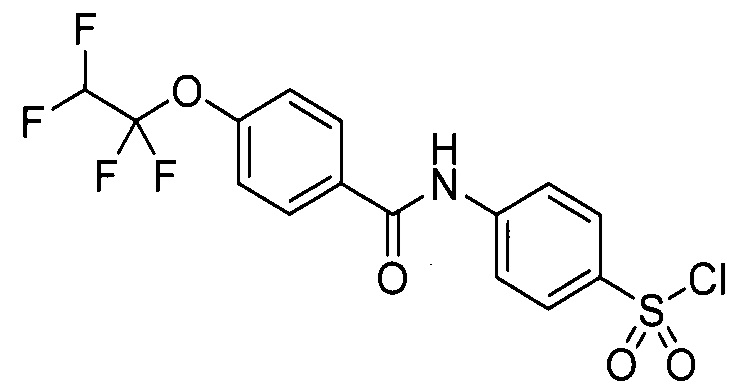
По методике эталонного примера 1, указанное в заголовке соединение получают в виде желтого твердого вещества из соответствующего исходного материала.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ч./млн. 5,95 (тт, J=53,2 Гц, 2,8 Гц, 1 H), 7,37 (д, J=8,6 Гц, 2 H), 7,92 (д, J=7,2 Гц, 2 H), 7,94 (д, J=7,2 Гц, 2 H), 8,05 (д, J=8,6 Гц, 2 H), 8,12 (с, 1 H)
Эталонный пример 8. 4-(2-Фторбензамид)бензолсульфонил хлорид
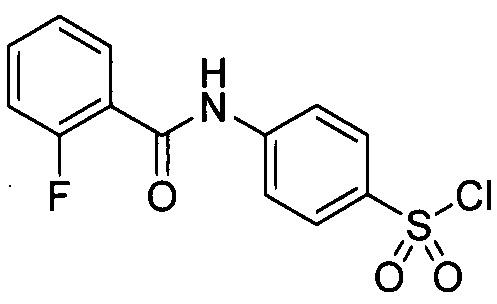
По методике эталонного примера 1, указанное в заголовке соединение получают в виде белого твердого вещества из соответствующего исходного материала.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ч./млн. 7,20-7,27 (м, 1 H), 7,37 (дд, J=7,6 Гц, 7,6 Гц, 1 H), 7,56-7,63 (м, 1 H), 7,95 (д, J=9,1 Гц, 2 H), 8,06 (д, J=9,1 Гц, 2 H), 8,20 (тд, J=8,0 Гц, 1,8 Гц, 1 H), 8,75 (д, J=16,9 Гц, 1 H)
Эталонный пример 9. 2-Фтор-4-феноксибензойной кислоты
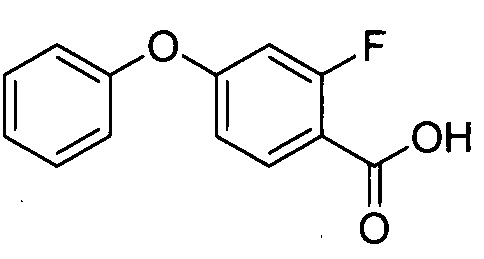
К раствору 2,4-дифторбензальдегида (250 мг) и фенола (199 мг) в ДМФ (10 мл), добавляют карбонат калия (535 мг), и продукт перемешивают при 120°C в течение 4 часов при нагревании. После охлаждения до комнатной температуры, реакционный раствор разбавляют этилацетатом и промывают водой. Органический слой сушат над безводным сульфатом магния и концентрируют при пониженном давлении с получением 2-фтор-4-феноксибензальдегида.
В тетрагидрофуране (5 мл) и воде (5 мл), полученный 2-фтор-4-феноксибензальдегид растворяют, туда добавляют дигидрофосфат натрия (844 мг), 2-метил-2-бутен (1,49 мл) и хлорит натрия (636 мг), и продукт перемешивают при комнатной температуре в течение 3 часов. Хлороформ добавляют к реакционному раствору, который промывают водой. Органический слой пропускают через разделитель фаз и концентрируют при пониженном давлении с получением указанного в заголовке соединения (182 мг) в виде белого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6) δ ч./млн. 6,75-6,92 (м, 2 H), 7,17 (д, J=7,5 Гц, 2 H), 7,24-7,33 (м, 1 H), 7,43-7,55 (м, 2 H), 7,83-7,97 (м, 1 H), 13,0 (шс, 1 H)
Эталонный пример 10. 4-(4-Карбамоил-2-фторфенокси)бензойной кислоты

По методике эталонного примера 9, указанное в заголовке соединение получают в виде белого твердого вещества из соответствующего исходного материала.
1H ЯМР (400 МГц, ДМСО-d6) δ ч./млн. 7,12 (д, J=8,4 Гц, 1 H), 7,19 (д, J=8,4 Гц, 2 H), 7,40 (т, J=8,3 Гц, 1 H), 7,53 (шс, 1 H), 7,82 (т, J=8,3 Гц, 1 H), 7,90-8,00 (м, 2 H), 8,07 (шс, 1 H), 9,95 (с, 1 H)
Эталонный пример 11. 3-Фтор-4-(2-фторфенокси)бензойной кислоты
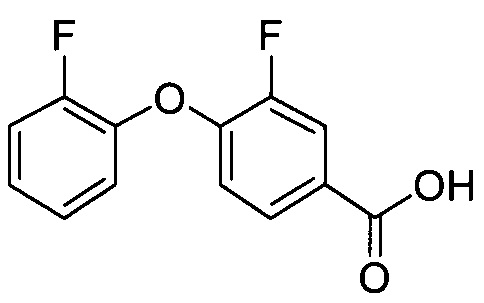
По методике эталонного примера 9, указанное в заголовке соединение получают в виде белого твердого вещества из соответствующего исходного материала.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ч./млн. 6,89 (т, J=8,1 Гц, 1 H), 7,10-7,25 (м, 4H), 7,80 (д, J=8,4 Гц, 1 H), 7,89 (д, J=11,3 Гц, 1 H)
Эталонный пример 12. 5-((4-(4-Карбамоилфенокси)фенил)сульфонамид)пентановая кислота
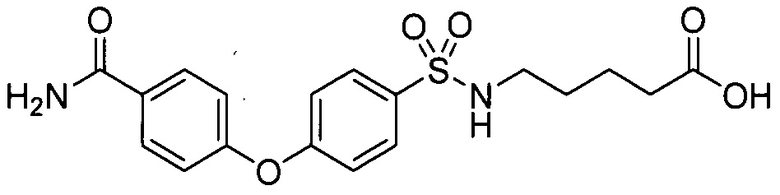
(1)
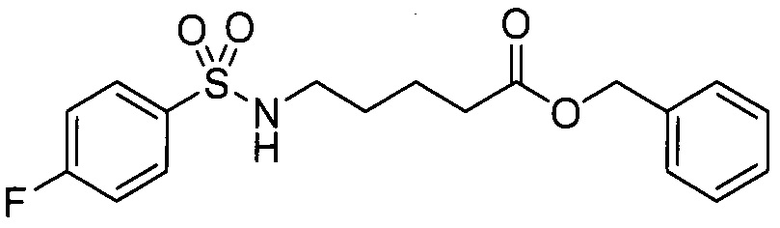
К раствору бензил 5-аминопентаноата тозилата (1,48 г) в хлороформе (20 мл), добавляют триэтиламин (2,3 мл) и 4-фторбензолсульфонилхлорид (800 мг) при охлаждении на льду, и продукт перемешивают при охлаждении на льду в течение 1 часа. После завершения реакции, насыщенный водный раствор гидрокарбоната натрия добавляют к реакционной смеси, и экстрагирование проводят с хлороформом. Органический слой пропускают через разделитель фаз и концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией (картридж с силикагелем, гексан:этилацетат=80:20-50:50) с получением бензил 5-((4-фторфенил)сульфонамид)пентаноата (1,24 г) в виде бесцветного маслянистого вещества.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ч./млн. 1,46-1,56 (м, 2 H), 1,58-1,68 (м, 2 H), 2,33 (т, J=7,0 Гц, 2 H), 2,96 (кв, J=6,5 Гц, 2 H), 4,40-4,47 (м, 1 H), 5,09 (с, 2 H), 7,18 (т, J=8,2 Гц, 2 H), 7,31-7,39 (м, 5 H), 7,86 (дд, J=7,6 Гц, 5,3 Гц, 2 H)
(2)
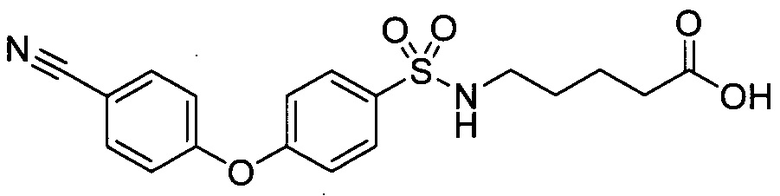
К раствору бензил 5-((4-фторфенил)сульфонамид)пентаноата (500 мг), полученному в (1), в ДМФ (13 мл), добавляют 4-гидроксибензонитрил (179 мг), и карбонат калия (567 мг) и продукт перемешивают под облучением микроволнами при 180°C в течение 1 часа. После охлаждения реакционного раствора, этилацетат и воду добавляют к реакционной смеси для жидкостного разделения. После промывания водного слоя этилацетатом, pH доводят до 1 с 1 M водным раствором хлористоводородной кислоты и экстрагирование проводят со смешанным растворителем этилацетат/толуол. Органический слой промывают водой, затем сушат над безводным сульфатом магния и концентрируют при пониженном давлении с получением 5-((4-(4-цианофенокси)фенил)сульфонамид)пентановой кислоты (285 мг) в виде белого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6) δ ч./млн. 1,32-1,49 (м, 4 H), 2,10-2,17 (м, 2 H), 2,69-2,78 (м, 2 H), 7,23-7,31 (м, 2 H), 7,43 (т, J=8,7 Гц, 2 H), 7,59-7,66 (м, 1 H), 7,81-7,87 (м, 3 H), 7,91 (д, J=8,3 Гц, 1 H)
(3)
К раствору 5-((4-(4-цианофенокси)фенил)сульфонамид)пентановой кислоты (100 мг), полученному в (2), в ДМСО (2 мл), добавляют карбонат калия (81 мг) и 30% раствор перекиси водорода (0,15 мл), и продукт перемешивают при комнатной температуре в течение 2 часов. После завершения реакции, добавляют водный раствор тиосульфата натрия и 1 M водный раствор хлористоводородной кислоты, и экстрагирование проводят с этилацетатом. Органический слой промывают водой, затем сушат над безводным сульфатом магния и концентрируют при пониженном давлении с получением указанного в заголовке соединения (89 мг) в виде белого твердого вещества.
1H ЯМР (400 МГц, ДМСО-d6) δ ч./млн. 1,32-1,50 (м, 4 H), 2,10-2,18 (м, 2 H), 2,69-2,78 (м, 2 H), 7,16 (д, J=8,2 Гц, 1 H), 7,19 (д, J=8,6 Гц, 1 H), 7,34 (шс, 1 H), 7,43 (т, J=8,6 Гц, 2 H), 7,52-7,58 (м, 1 H), 7,59-7,66 (м, 1 H), 7,86- 7,79 (м, 3 H), 7,96 (д, J=7,7 Гц, 1 H), 12,0 (шс, 1 H)
Пример 1. Синтез соединения №1: (N-[4-(4-карбамоилбензамидо)бензол-1-сульфонил]-D-γ-глутамил-(4S)-4-амино-L-пролил-L-лейцил-N-(5-амино-5-оксопентил)-N2-метил-L-α-глутамин)
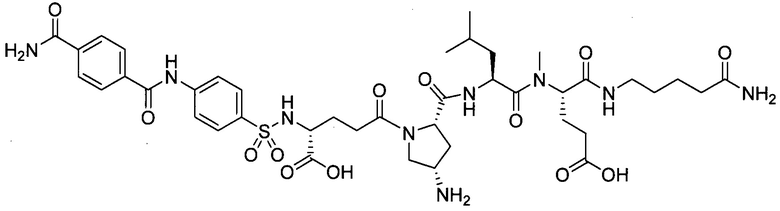
(1)
Смолу Fmoc-Rink Amide AM (0,10 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,6 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,6 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-Ape-OH (0,40 ммоль) в ДМФ (0,8 мл), раствор COMU (0,40 ммоль) и Oxyma (0,40 ммоль) в ДМФ (0,8 мл) и раствор DIPEA (0,80 ммоль) в NMP (0,4 мл) и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка Аре. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Glu(OtBu)-OH, Fmoc-Leu-OH, Fmoc-(2S,4S)-(4-NHBoc)Pro-OH и Fmoc-(d)-Glu-OtBu последовательно конденсируют, где снятие защиты проводят для N-концевой Fmoc, образованной в смоле после каждой конденсации при обработке пиперидин/ДМФ по указанной выше методике, и синтезируют H-γ-(d)-Glu(OtBu)-(2S,4S)-(4-NHBoc)Pro-Leu-(N-Me)Glu(OtBu)-Ape-Rink Amide AM смолу.
(2)
К смоле, полученной в (1), добавляют раствор 4-(4-карбамоилбензамид)бензолсульфонилхлорида (0,30 ммоль), полученного в эталонном примере 1, и DIPEA (0,60 ммоль) в ДМФ (3 мл), и смесь встряхивают при комнатной температуре в течение 1 часа. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза) и хлороформом (3 мл х три раза).
(3)
К смоле, полученной в (2), добавляют ТФК:воду:триизопропилсилан (92,5:2,5:5, 4 мл), смесь встряхивают при комнатной температуре в течение 1,5 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения B). Элюат фракционируют с применением тестовых пробирок и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (46 мг) в виде белого порошка.
Пример 2. Синтез соединения №106: (N2-[4-(4-феноксибензамидо)бутаноил]-L-аспарагинил-N-[(2S)-4-амино-1-({(2S)-1-[{(2S,3S)-1-[(2S)-2-(2-амино-2-оксоэтил)пирролидин-1-ил]-3-метил-1-оксопентан-2-ил}(метил)амино]-4-метил-1-оксопентан-2-ил}амино)-1-оксобутан-2-ил]-L-α-аспарагин)
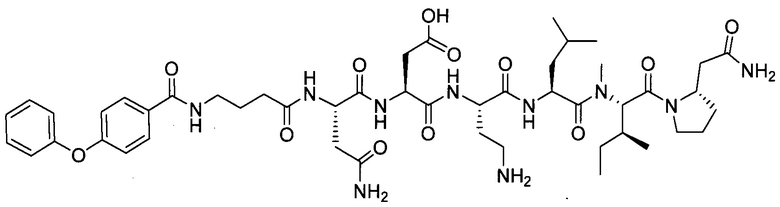
(1)
Смолу Fmoc-NH-SAL-PEG (0,12 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,9 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,9 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-β-гомоPro-OH (0,48 ммоль) в ДМФ (1,0 мл), раствор COMU (0,48 ммоль) и Oxyma (0,48 ммоль) в ДМФ (1,0 мл) и раствор DIPEA (0,96 ммоль) в NMP (0,48 мл), и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка β-гомоPro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Ile-OH, Fmoc-Leu-OH, Fmoc-Dab(Boc)-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asn(Trt)-OH, Fmoc-GABA-OH и 4-феноксибензойную кислоту последовательно конденсируют, и синтезируют смолу Ph-O-Ph-CO-GABA-Asn(Trt)-Asp(OtBu)-Dab(Boc)-Leu-(N-Me)Ile-β-гомоPro-NH-SAL-PEG. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза) и хлороформ (3 мл х три раза).
(2)
К смоле, полученной в (1), добавляют ТФК:воду:триизопропилсилан:дитиотреитол (90:2,5:5:2,5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (14 мг) в виде белого порошка.
Пример 3. Синтез соединения №177: (N2-(4-{4-[4-(метилкарбамоил)фенокси]бензамидо}бутаноил)-L-аспарагинил-L-α-аспартил-L-аланил-L-лейцил-L-метионил-L-пролинамид)
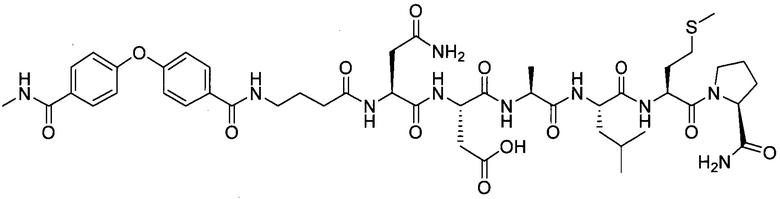
(1)
Смолу Fmoc-NH-SAL-PEG (0,10 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,6 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,6 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-Pro-OH (0,40 ммоль) в ДМФ (0,8 мл), раствор COMU (0,40 ммоль) и Oxyma (0,40 ммоль) в ДМФ (0,8 мл) и раствор DIPEA (0,80 ммоль) в NMP (0,4 мл) и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка Pro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-Met-OH, Fmoc-Leu-OH, Fmoc-Ala-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asn(Trt)-OH и Fmoc-GABA-OH последовательно конденсируют, где снятие защиты проводят для N-концевой Fmoc, образованной в смоле после каждой конденсации при обработке пиперидином/ДМФ по указанной выше методике, и синтезируют смолу H-GABA-Asn(Trt)-Asp(OtBu)-Ala-Leu-Met-Pro-NH-SAL-PEG.
(2)
К смоле, полученной в (1), раствор добавляют 4,4'-оксибисбензойной кислоты (0,75 ммоль), HATU (0,15 ммоль) и DIPEA (2,0 ммоль) в ДМФ (3 мл), и смесь встряхивают при комнатной температуре в течение 2 часов. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза).
(3)
К смоле, полученной в (2), добавляют раствор HATU (0,30 ммоль), DIPEA (0,60 ммоль) и раствор метиламина в метаноле (концентрация: 9,8 моль/л, 0,30 ммоль) в ДМФ (3 мл) и смесь перемешивают при комнатной температуре в течение 4 часов. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза) и хлороформом (3 мл х три раза).
(4)
К смоле, полученной в (3), добавляют ТФК:воду:триизопропилсилан:дитиотреитол (90:2,5:5:2,5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (30 мг) в виде белого порошка.
Пример 4. Синтез соединения №587: (N-{5-[(4-метилфенил)этинил]тиофен-2-сульфонил}-β-аланил-L-аспарагинил-L-α-аспартил-L-аланил-L-лейцил-N-метил-L-метионил-L-пролинамид)
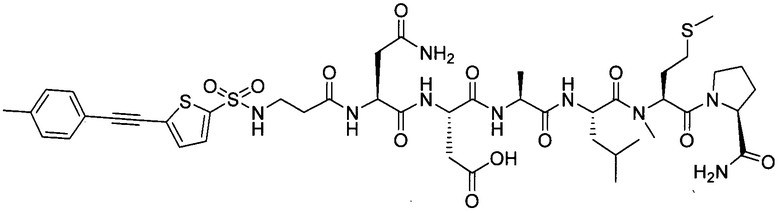
(1)
Смолу Fmoc-NH-SAL-PEG (0,10 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,6 мл) в течение 3 минут, и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,6 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-Pro-OH (0,40 ммоль) в ДМФ (0,8 мл) раствор, раствор COMU (0,40 ммоль) и Oxyma (0,40 ммоль) в ДМФ (0,8 мл) и раствор DIPEA (0,80 ммоль) в NMP (0,4 мл), и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка Pro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Met-OH, Fmoc-Leu-OH, Fmoc-Ala-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Asn(Trt)-OH и Fmoc-β-Ala-OH последовательно конденсируют, где снятие защиты проводят для N-концевой Fmoc, образованной в смоле, после каждой конденсации при обработке пиперидином/ДМФ по указанной выше методике и синтезируют смолу H-β-Ala-Asn(Trt)-Asp(OtBu)-Ala-Leu-(N-Me)Met-Pro-NH-SAL-PEG.
(2)
К смоле, полученной в (1), добавляют раствор 5-бромтиофен-2-сульфонилхлорид (0,20 ммоль) и DIPEA (0,40 ммоль) в ДМФ (3 мл) и смесь встряхивают при комнатной температуре в течение 2 часов. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза) и хлороформом (3 мл х три раза).
(3)
К смоле, полученной в (2), добавляют ТФК:воду:триизопропилсилан:дитиотреитол (90:2,5:5:2,5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения B). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением 5-Br-тиофен-2-SO2-β-Ala-Asn-Asp-Ala-Leu-(N-Me)Met-Pro-NH2 (27 мг) в виде белого порошка.
(4)
Соединение, полученное в (3), растворяют в ДМФ (0,5 мл), туда добавляют 4-этинилтолуол (0,30 ммоль), дихлорбис(трифенилфосфин)палладий(II) (0,01 ммоль), триэтиламин (0,18 ммоль) и йодид меди (0,01 ммоль), и смесь перемешивают в атмосфере азота при 50°C в течение 5 часов при нагревании. После охлаждения до комнатной температуры, реакционный раствор разбавляют ДМСО, фильтруют и очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (4 мг) в виде белого порошка.
Пример 5. Синтез соединения №608: (N-[(2S)-4-амино-1-({(2S)-1-[{(2S,3S)-1-[(2S)-2-(2-амино-2-оксоэтил)пирролидин-1-ил]-3-метил-1-оксопентан-2-ил}(метил)амино]-4-метил-1-оксопентан-2-ил}амино)-1-оксобутан-2-ил]-N2-[4-(1-фенил-1H-1,2,3-триазол-4-ил)бензол-1-сульфонил]-D-глутамин)
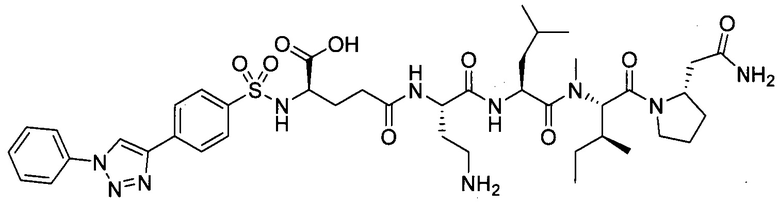
(1)
Смолу Fmoc-Rink Amide AM (0,10 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,6 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,6 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-β-гомоPro-OH (0,40 ммоль) в ДМФ (0,8 мл), раствор COMU (0,40 ммоль) и Oxyma (0,40 ммоль) в ДМФ (0,8 мл) и раствор DIPEA (0,80 ммоль) в NMP (0,4 мл), и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка β-гомоPro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Ile-OH, Fmoc-Leu-OH, Fmoc-Dab(Boc)-OH и Fmoc-(d)-Glu-OtBu последовательно конденсируют, где снятие защиты проводят для N-концевой Fmoc, образованной в смоле после каждой конденсации при обработке пиперидином/ДМФ по указанной выше методике и синтезируют смолу H-γ-(d)-Glu(OtBu)-Dab(Boc)-Leu-(N-Me)Ile-β-гомоPro-Rink Amide AM.
(2)
К смоле, полученной в (1), добавляют раствор 4-бромбензолсульфонил хлорид (0,30 ммоль) и DIPEA (0,60 ммоль) в ДМФ (2 мл), и смесь встряхивают при комнатной температуре в течение 2 часов. После завершения реакции, полученную смолу промывают ДМФ (2 мл х три раза).
(3)
К смоле, полученной в (2), добавляют раствор триметилсилилацетилен (0,30 ммоль), дихлорбис(трифенилфосфин)палладий(II) (0,03 ммоль) и йодид меди (0,03 ммоль) в ДМФ (2 мл), и смесь перемешивают под облучением микроволнами при 80°C в течение 30 минут при нагревании. После завершения реакции, полученную смолу промывают ДМФ (2 мл х три раза) и хлороформом (2 мл х три раза).
К полученной смоле, добавляют раствор фторида тетрабутиламмония в тетрагидрофуране (концентрация: 0,33 моль/л, 0,50 ммоль), и смесь встряхивают при комнатной температуре в течение 1 часа. После завершения реакции, полученную смолу промывают ДМФ (2 мл х три раза) и хлороформ (2 мл х три раза).
(4)
К смоле, полученной в (3), добавляют раствор азидобензола (0,20 ммоль), пентагидрат сульфата меди(II) (0,40 ммоль) и аскорбиновой кислоты (0,40 ммоль) в воде (2 мл) и tBuOH (1 мл) и смесь перемешивают под облучением микроволнами при 60°C в течение 1 часа при нагревании. После завершения реакции, полученную смолу промывают ДМФ (2 мл х три раза) и хлороформом (2 мл х три раза).
(5)
К смоле, полученной в (4), добавляют ТФК:воду:триизопропилсилан (92,5:2,5:5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (12 мг) в виде белого порошка.
Пример 6. Синтез соединения №634: (N2-(4'-ацетил[1,1'-бифенил]-4-сульфонил)-N-[(2S)-1-({(2S)-1-[{(2S,3S)-1-[(2S)-2-(2-амино-2-оксоэтил)пирролидин-1-ил]-3-метил-1-оксопентан-2-ил}(метил)амино]-4-метил-1-оксопентан-2-ил}амино)-1-оксопропан-2-ил]-D-аспарагин)
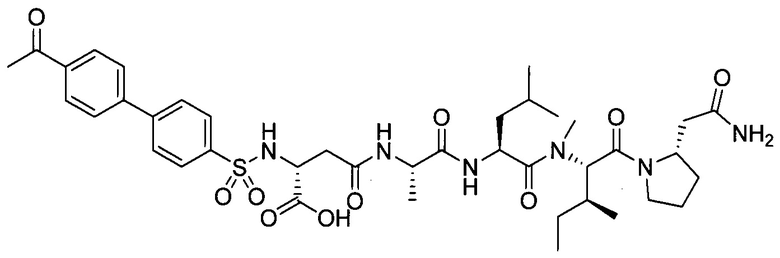
(1)
Смолу Fmoc-NH-SAL-PEG (0,10 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,6 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,6 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-β-гомоPro-OH (0,40 ммоль) в ДМФ (0,8 мл), раствор COMU (0,40 ммоль) и Oxyma (0,40 ммоль) в ДМФ (0,8 мл) и раствор DIPEA (0,80 ммоль) в NMP (0,4 мл) и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка β-гомоPro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Ile-OH, Fmoc-Leu-OH, Fmoc-Ala-OH и Fmoc-(d)-Asp-OtBu последовательно конденсируют, снятие защиты проводят для N-концевой Fmoc, образованной в смоле, после каждой конденсации при обработке пиперидином/ДМФ по указанной выше методике и синтезируют смолой H-β-(d)-Asp(OtBu)-Ala-Leu-(N-Me)Ile-β-гомоPro-NH-SAL-PEG.
(2)
К смоле, полученной в (1), добавляют раствор 4-йодбензолсульфонилхлорида (0,30 ммоль) и DIPEA (0,60 ммоль) в ДМФ (2 мл), и смесь встряхивают при комнатной температуре в течение 2 часов. После завершения реакции, полученную смолу промывают ДМФ (2 мл х три раза) и хлороформом (2 мл х три раза).
(3)
К смоле, полученной в (2), добавляют раствор 4-ацетилфенилбороновой кислоты (0,40 ммоль), тетракис(трифенилфосфин)палладий(0) (0,03 ммоль) и фосфат калия (0,50 ммоль) в 1,4-диоксане (1,5 мл) и воде (1,5 мл), и смесь перемешивают под облучением микроволнами при 100°C в течение 30 минут при нагревании. После завершения реакции, полученную смолу промывают ДМФ (2 мл х три раза) и хлороформом (2 мл х три раза).
(4)
К смоле, полученной в (3), добавляют ТФК:воду:триизопропилсилан (92,5:2,5:5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (8 мг) в виде белого порошка.
Пример 7. Синтез соединения №692: (N-[(2S)-3-амино-1-({(2S)-1-[{(2S,3S)-1-[(2S)-2-(2-амино-2-оксоэтил)пирролидин-1-ил]-3-метил-1-оксопентан-2-ил}(метил)амино]-4-метил-1-оксопентан-2-ил}амино)-1-оксопропан-2-ил]-N2-[4-(4-метоксибензамидо)бензол-1-сульфонил]-D-аспарагин)
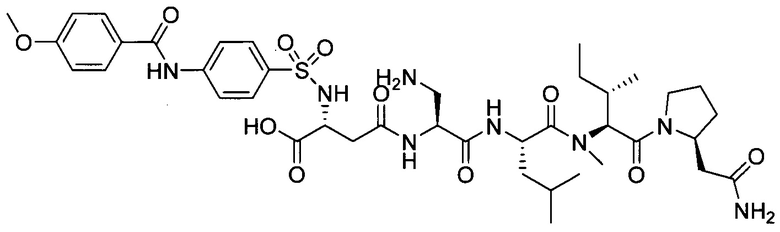
(1)
Смолу Fmoc-Rink Amide AM (0,10 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,6 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,6 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-β-гомоPro-OH (0,40 ммоль) в ДМФ (0,8 мл), раствор COMU (0,40 ммоль) и Oxyma (0,40 ммоль) в ДМФ (0,8 мл) и раствор DIPEA (0,80 ммоль) в NMP (0,4 мл), и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка β-гомоPro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Ile-OH, Fmoc-Leu-OH, Fmoc-Dap(Boc)-OH и Fmoc-(d)-Asp-OtBu последовательно конденсируют, снятие защиты проводят для N-концевой Fmoc, образованной в смоле после каждой конденсации, при обработке пиперидином/ДМФ по указанной выше методике, и синтезируют смолу H-γ-(d)-Asp(OtBu)-Dap(Boc)-Leu-(N-Me)Ile-β-гомоPro-Rink Amide AM.
(2)
К смоле, полученной в (1), добавляют раствор (9H-флуорен-9-ил)метил (4-(хлорсульфонил)фенил)карбамат (0,30 ммоль) и DIPEA (0,60 ммоль) в 1,4-диоксане (3 мл), и смесь встряхивают при комнатной температуре в течение 1 часа. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза). Затем, добавляют раствор пиперидина в ДМФ (концентрация: 20%, 3 мл) и Oxyma (0,01 ммоль), и продукт встряхивают при комнатной температуре в течение 10 минут.
(3)
К смоле, полученной в (2), добавляют раствор 4-метоксибензоилхлорида (0,30 ммоль) и DIPEA (0,60 ммоль) в 1,4-диоксане (2 мл), и смесь встряхивают при комнатной температуре в течение 3 часов. После завершения реакции, полученную смолу промывают хлороформом (3 мл х три раза).
(4)
К смоле, полученной в (3), добавляют ТФК:воду:триизопропилсилан:дитиотреитол (90:2,5:5:2,5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (12 мг) в виде белого порошка.
Пример 8. Синтез соединения №892: ([(2S,5S,8S,20S)-8-[{(2S,3S)-1-[(2S)-2-(2-амино-2-оксоэтил)пирролидин-1-ил]-3-метил-1-оксопентан-2-ил}(метил)карбамоил]-5-метил-3,6,14,17,21-пентаоксо-20-{4-[(4-феноксибензол-1-сульфонил)амино]бутанамидо}-1,4,7,13,16-пентаазациклогенкозан-2-ил]уксусная кислота)
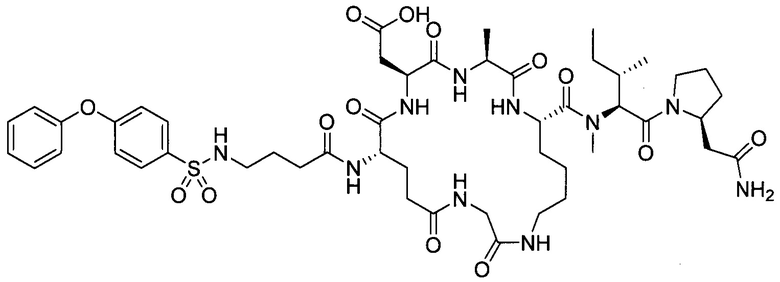 (1)
(1)
Смолу Fmoc-NH-SAL-PEG (0,12 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,9 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,9 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-β-гомоPro-OH (0,48 ммоль) в ДМФ (1,0 мл), раствор COMU (0,48 ммоль) и Oxyma (0,48 ммоль) в ДМФ (1,0 мл) и раствор DIPEA (0,96 ммоль) в NMP (0,48 мл) и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка β-гомоPro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Ile-OH, Fmoc-Lys(Dde)-OH, Fmoc-Ala-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Glu(OAllyl)-OH и Fmoc-GABA-OH последовательно конденсируют, снятие защиты проводят для N-концевой Fmoc, образованной в смоле, после каждой конденсации при обработке пиперидином/ДМФ по указанной выше методике, и синтезируют смолу H-GABA-Glu(OAllyl)-Asp(OtBu)-Ala-Lys(Dde)-(N-Me)Ile-β-гомоPro-SAL-PEG.
(2)
К смоле, полученной в (1), добавляют раствор 4-феноксибензолсульфонилхлорида (0,36 ммоль) и DIPEA (0,72 ммоль) в ДМФ (3 мл), и смесь встряхивают при комнатной температуре в течение 1,5 часов. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза).
(3)
К смоле, полученной в (2), добавляют раствор моногидрата гидразина в ДМФ (концентрация: 5%, 3 мл) и аллиловый спирт (3,1 ммоль) и смесь встряхивают при комнатной температуре в течение 30 минут для снятия защиты Dde с Lys боковой цепи. Затем, добавляют раствор Fmoc-Gly-OH (0,48 ммоль), COMU (0,48 ммоль), Oxyma (0,48 ммоль) и DIPEA (0,96 ммоль) в ДМФ (3 мл) и смесь встряхивают при комнатной температуре в течение 30 минут для введения остатка Gly. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза) и хлороформом (3 мл х три раза).
(4)
К смоле, полученной в (3), добавляют раствор тетракис(трифенилфосфин)палладия(0) (0,12 ммоль) и фенилсилана (0,60 ммоль) в хлороформе (4 мл), и смесь встряхивают при комнатной температуре в течение 1,5 часов для снятия защиты Аллил с Glu боковой цепи. Затем, добавляют раствор пиперидина в ДМФ (концентрация: 20%, 3 мл), и смесь встряхивают при комнатной температуре в течение 30 минут для снятия защиты Fmoc. После завершения реакции, полученный остаток промывают ДМФ (3 мл х пять раз).
(5)
К смоле, полученной в (4), добавляют раствор PyBOP (0,36 ммоль) и DIPEA (0,12 ммоль) в ДМФ (4 мл), и смесь встряхивают при комнатной температуре в течение 2 часов. После завершения реакции, полученный остаток промывают ДМФ (3 мл х три раза) и хлороформом (3 мл х три раза).
(6)
К смоле, полученной в (5), добавляют ТФК:воду:триизопропилсилан:дитиотреитол (90:2,5:5:2,5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (10 мг) в виде белого порошка.
Пример 9. Синтез соединения №903: ((2S,5S,32R)-2-{[(2S)-1-({(2S)-1-[{(2S,3S)-1-[(2S)-2-(2-амино-2-оксоэтил)пирролидин-1-ил]-3-метил-1-оксопентан-2-ил}(метил)амино]-4-метил-1-оксопентан-2-ил}амино)-1-оксопропан-2-ил]карбамоил}-4,11,20,29,34-пентаоксо-5-{4-[(4-феноксибензол-1-сульфонил)амино]бутанамидо}-13,16,22,25-тетраокса-3,10,19,28,33-пентаазаоктатетраконтан-1,32,48-трикарбоновая кислота)
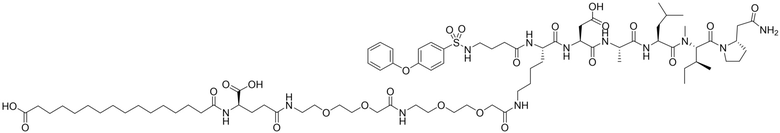 (1)
(1)
Смолу Fmoc-Rink Amide AM (0,12 ммоль) обрабатывают раствором пиперидина в ДМФ (концентрация: 40%, 1,9 мл) в течение 3 минут и затем обрабатывают раствором пиперидина в ДМФ (концентрация: 20%, 1,9 мл) в течение 12 минут для снятия защиты Fmoc на смоле. Затем, добавляют раствор Fmoc-β-гомоPro-OH (0,48 ммоль) в ДМФ (1,0 мл), раствор COMU (0,48 ммоль) и Oxyma (0,48 ммоль) в ДМФ (1,0 мл) и раствор DIPEA (0,96 ммоль) в NMP (0,48 мл), и смесь встряхивают при комнатной температуре в течение 40 минут для введения остатка β-гомоPro. По той же методике, повторяют снятие защиты Fmoc и конденсацию: более конкретно, Fmoc-(N-Me)Ile-OH, Fmoc-Leu-OH, Fmoc-Ala-OH, Fmoc-Asp(OtBu)-OH, Fmoc-Lys(Dde)-OH и Fmoc-GABA-OH последовательно конденсируют, где снятие защиты проводят для N-концевой Fmoc, образованной в смоле, после каждой конденсации при обработке пиперидином/ДМФ по указанной выше методике и синтезируют смолу H-GABA-Lys(Dde)-Asp(OtBu)-Ala-Leu-(N-Me)Ile-β-гомоPro-Rink Amide AM.
(2)
К смоле, полученной в (1), добавляют раствор 4-феноксибензолсульфонилхлорида (0,36 ммоль) и DIPEA (0,72 ммоль) в ДМФ (3 мл), и смесь встряхивают при комнатной температуре в течение 2 часов. После завершения реакции, полученную смолу промывают ДМФ (3 мл х три раза).
(3)
К смоле, полученной в (2), добавляют ДМФ раствор моногидрата гидразина (концентрация: 5%, 3 мл) и смесь встряхивают при комнатной температуре в течение 30 минут.Эту операцию повторяют четыре раза для снятия защиты Dde с Lys боковой цепи. Для полученной смолы, конденсацию и деFmoc проводят повторно: более конкретно, Fmoc-Adox-OH, Fmoc-Adox-OH и Fmoc-Glu-OtBu последовательно конденсируют для продления Lys боковой цепи с пептидом. Снятие защиты проводят для N-концевой Fmoc с Lys боковой цепи при обработке пиперидином/ДМФ.
(4)
К смоле, полученной в (3), раствор добавляют гексадекандикислоту (0,96 ммоль), COMU (0,18 ммоль), Oxyma (0,18 ммоль) и DIPEA (0,96 ммоль) в ДМФ (3 мл), и смесь встряхивают при комнатной температуре в течение 1 часа. После завершения реакции, полученную смолу промывают ДМФ (3 мл х четыре раза) и хлороформом (3 мл х три раза).
(5)
К смоле, полученной в (4), добавляют ТФК:воду:триизопропилсилан:дитиотреитол (90:2,5:5:2,5, 4 мл), смесь встряхивают при комнатной температуре в течение 2 часов и смолу удаляют фильтрацией. Операцию, в которой охлажденный диэтиловый эфир добавляют к фильтрату, полученный белый порошок осаждают центрифугированием и диэтиловый эфир удаляют декантированием, повторяют три раза с получением неочищенного продукта пептида. Полученный неочищенный продукт очищают препаративной ЖХМС (условия разделения A). Элюат фракционируют с применением тестовых пробирок, и элюированные фракции, содержащие целевой продукт, собирают и лиофилизируют с получением указанного в заголовке соединения (29 мг) в виде белого порошка.
Структуры соединений, представленных формулой [I'-1], которые синтезируют в примере 1 или по способу, как в примере 1, показаны в следующей таблице.
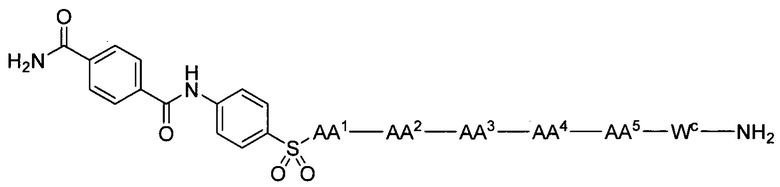 [I'-1]
[I'-1]
[Таблица 5]
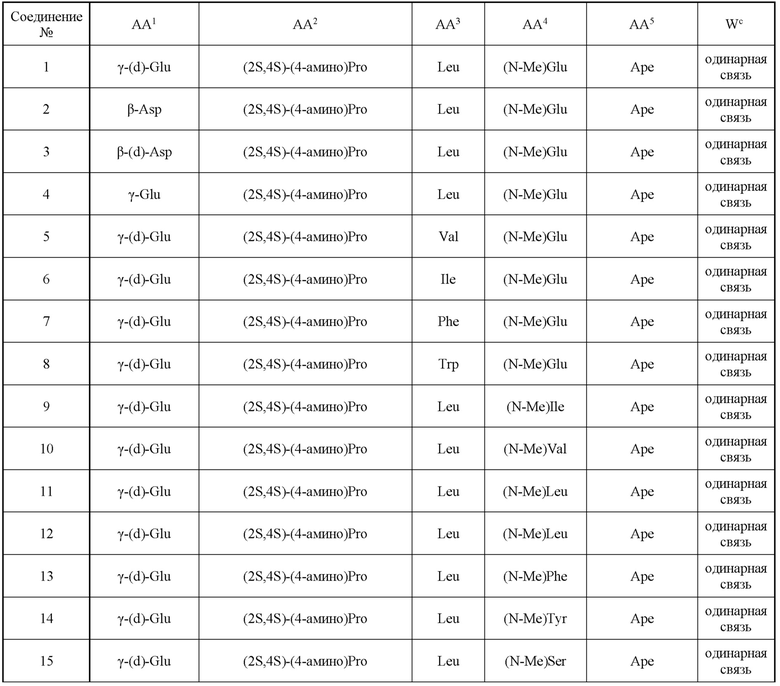
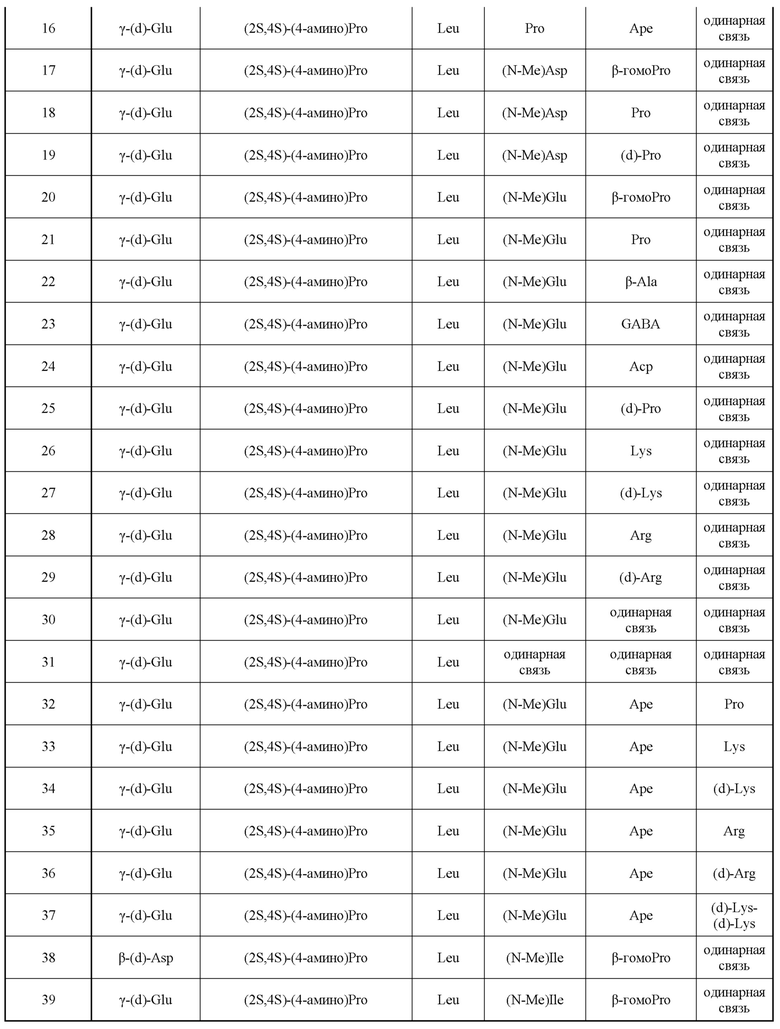
Структура соединения, представленного формулой [I'-2], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
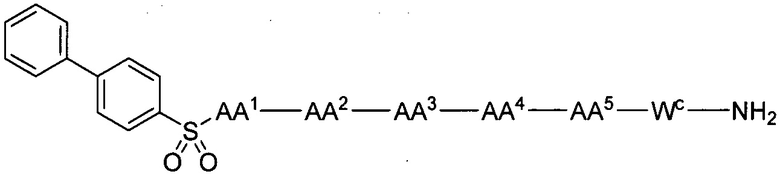 [I'-2]
[I'-2]
[Таблица 6]

Структура соединения, представленного формулой [I'-3], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
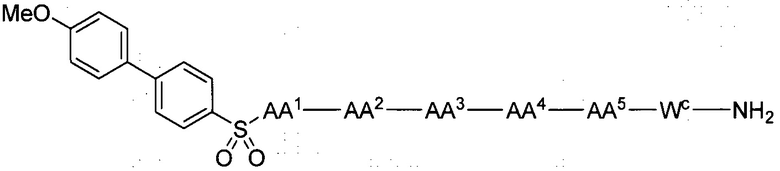 [I'-3]
[I'-3]
[Таблица 7]

Структура соединения, представленного формулой [I'-4], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
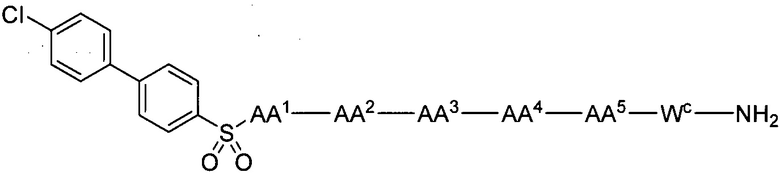 [I'-4]
[I'-4]
[Таблица 8]

Структура соединения, представленного формулой [I'-5], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
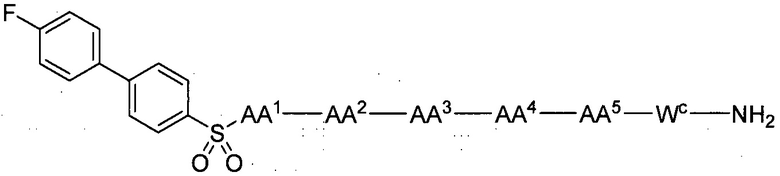 [I'-5]
[I'-5]
[Таблица 9]

Структура соединения, представленного формулой [I'-6], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
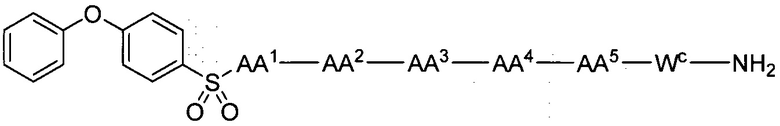 [I'-6]
[I'-6]
[Таблица 10]

Структуры соединений, представленных формулой [I'-7], которое синтезируют по способу, как в примере 1, показаны в следующей таблице.
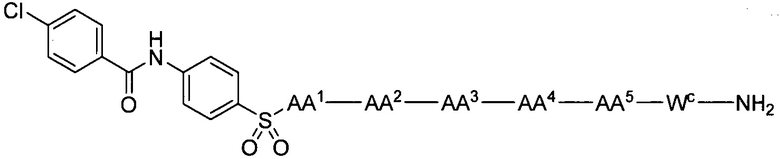 [I'-7]
[I'-7]
[Таблица 11]
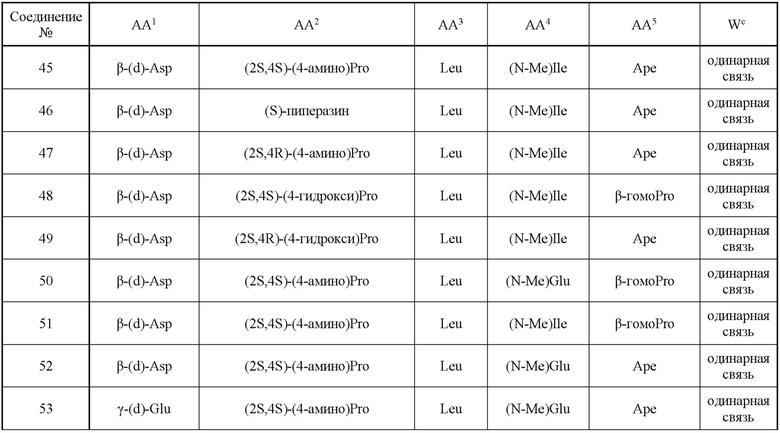

Структуры соединений, представленных формулой [I'-8], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
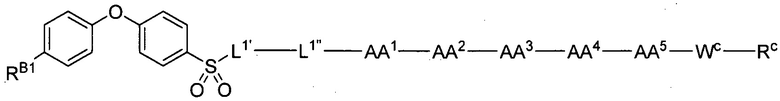 [I'-8]
[I'-8]
[Таблица 12]
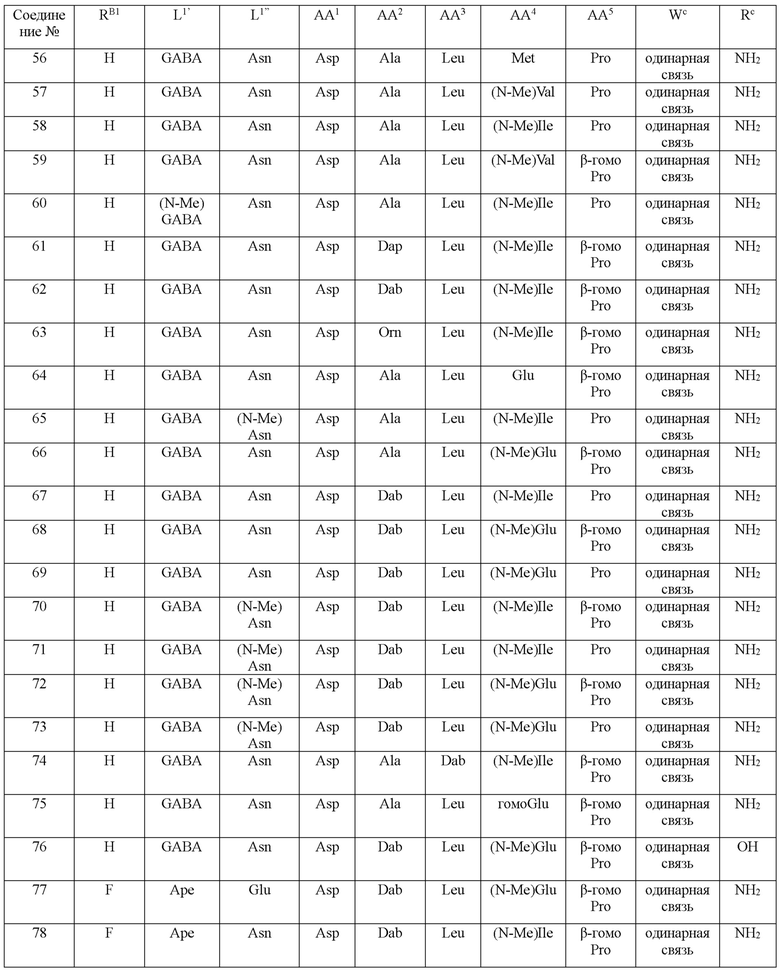
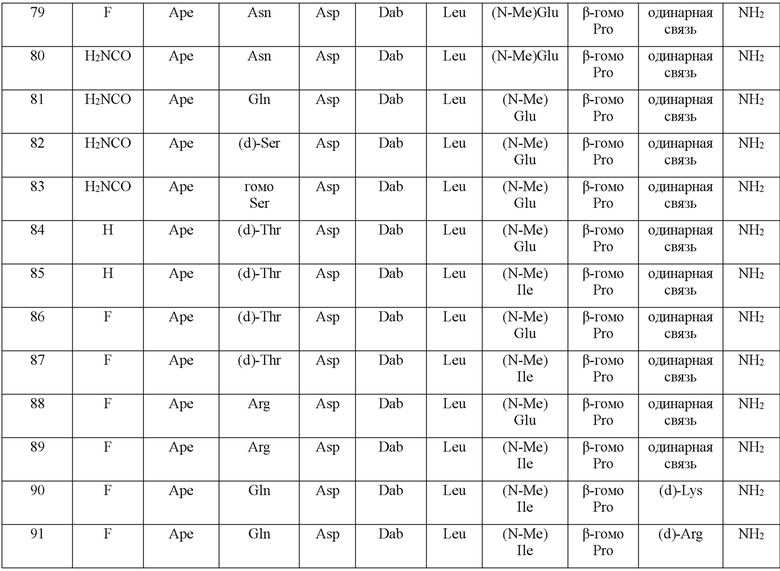
Структуры соединений, представленных формулой [I'-9], которые синтезируют в примере 2 или по способу, как в примере 2, показаны в следующей таблице.
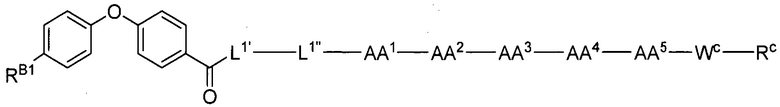 [I'-9]
[I'-9]
[Таблица 13]
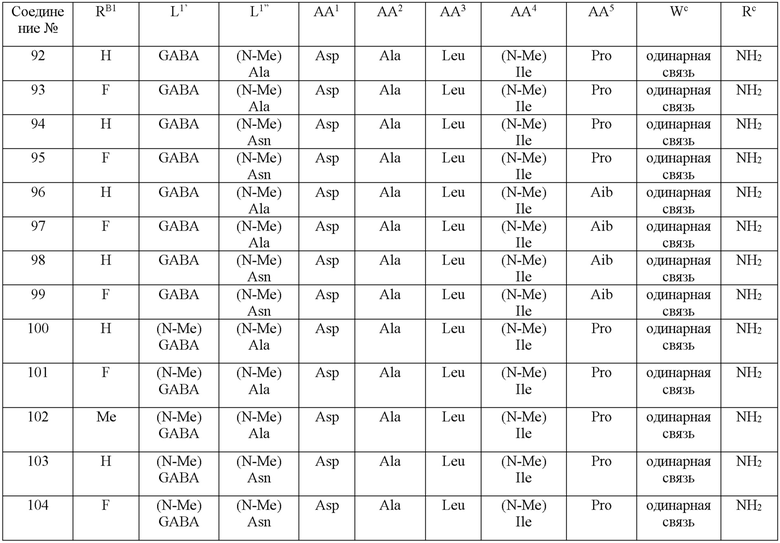
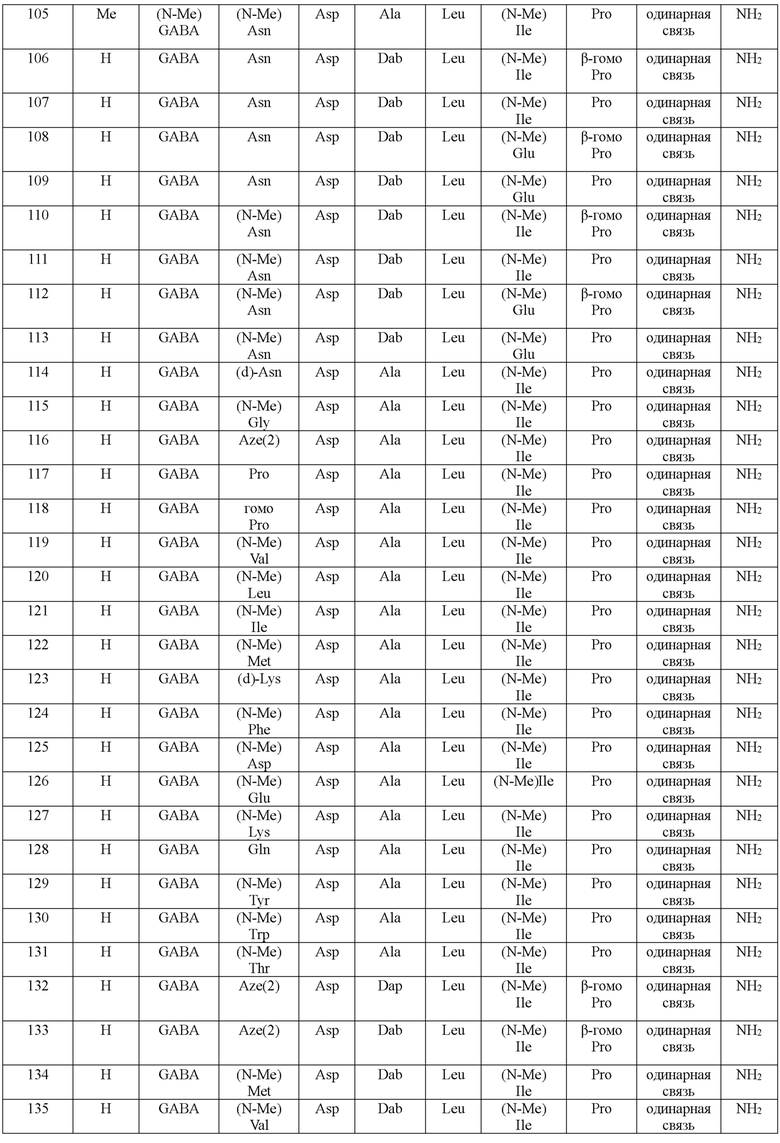

Структуры соединений, представленных формулой [I'-10], которые синтезируют по способу, как в примере 9, показаны в следующей таблице.
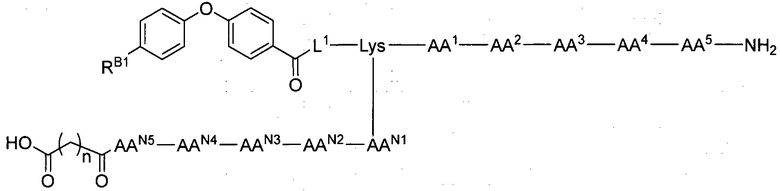 [I'-10]
[I'-10]
[Таблица 14]
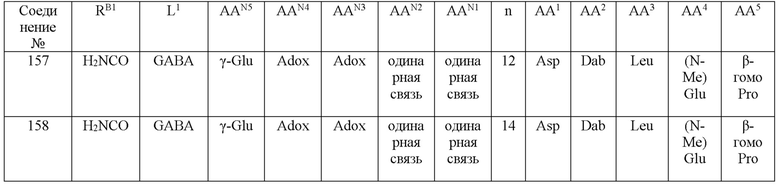

Структуры соединений, представленных формулой [I'-9], которые синтезируют в примере 2 или по способу, как в примере 2, показаны в следующей таблице.
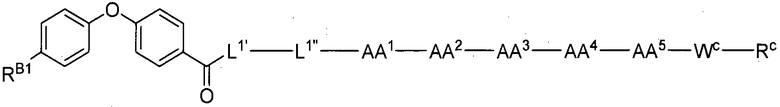 [I'-9]
[I'-9]
[Таблица 15]
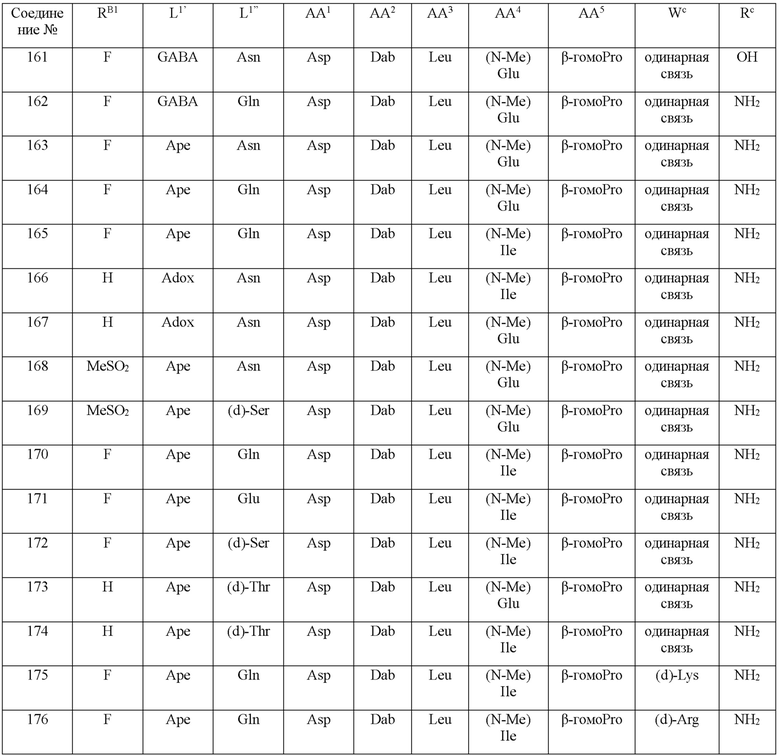
Структуры соединений, представленных формулой [I'-9], которые синтезируют в примере 3 или по способу, как в примере 3, показаны в следующей таблице.
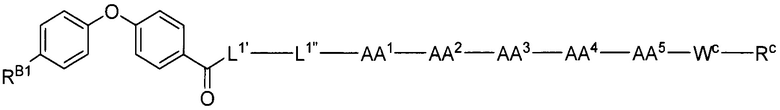 [I'-9]
[I'-9]
[Таблица 16]
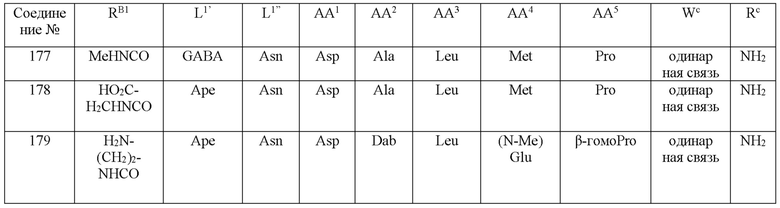
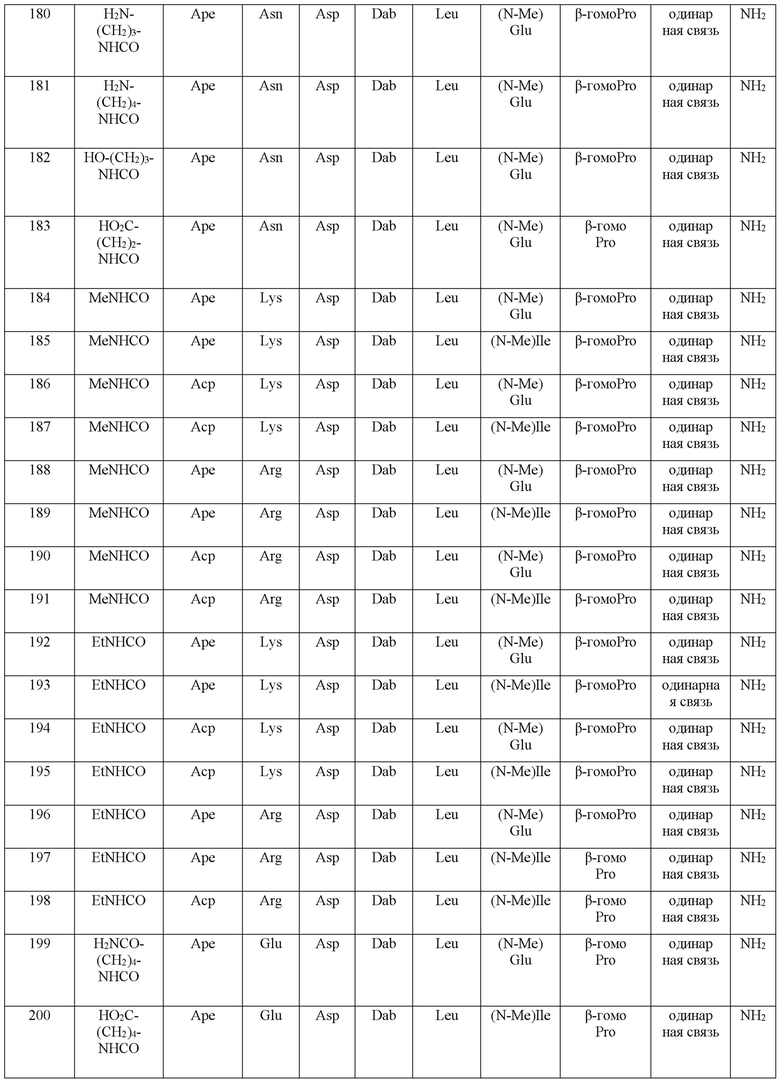

Структура соединения, представленного формулой [I'-11], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
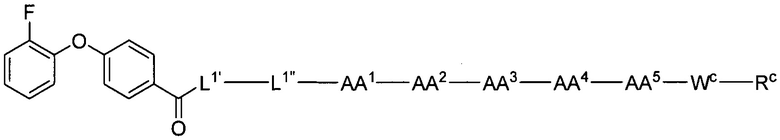 [I'-11]
[I'-11]
[Таблица 17]

Структуры соединений, представленных формулой [I'-12], которые синтезируют по способу, как в примере 2, показаны в следующей таблице.
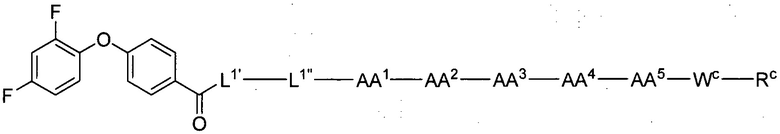 [I'-12]
[I'-12]
[Таблица 18]
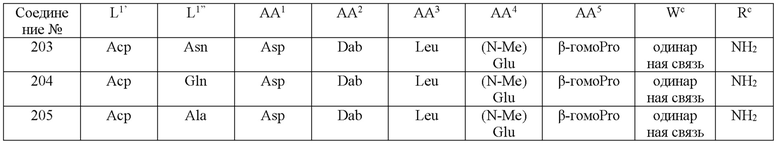
Структуры соединений, представленных формулой [I'-13], которые синтезируют по способу, как в примере 2, показаны в следующей таблице.
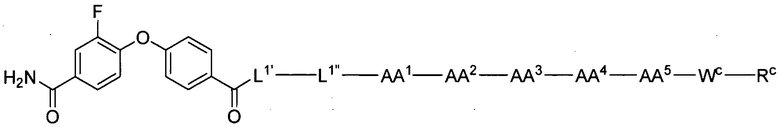 [I'-13]
[I'-13]
[Таблица 19]
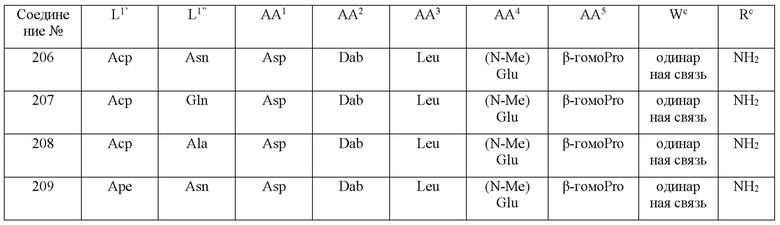
Структуры соединений, представленных формулой [I'-14], которые синтезируют по способу, как в примере 2, показаны в следующей таблице.
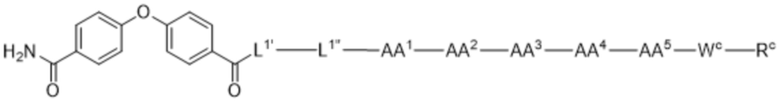 [I'-14]
[I'-14]
[Таблица 20]
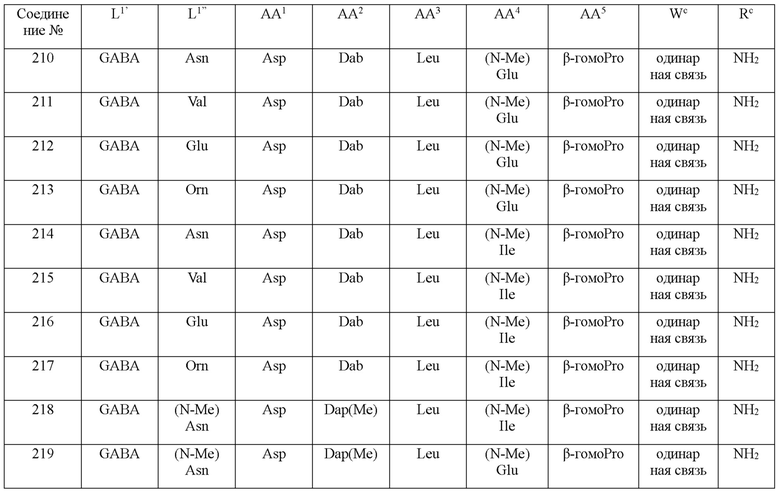
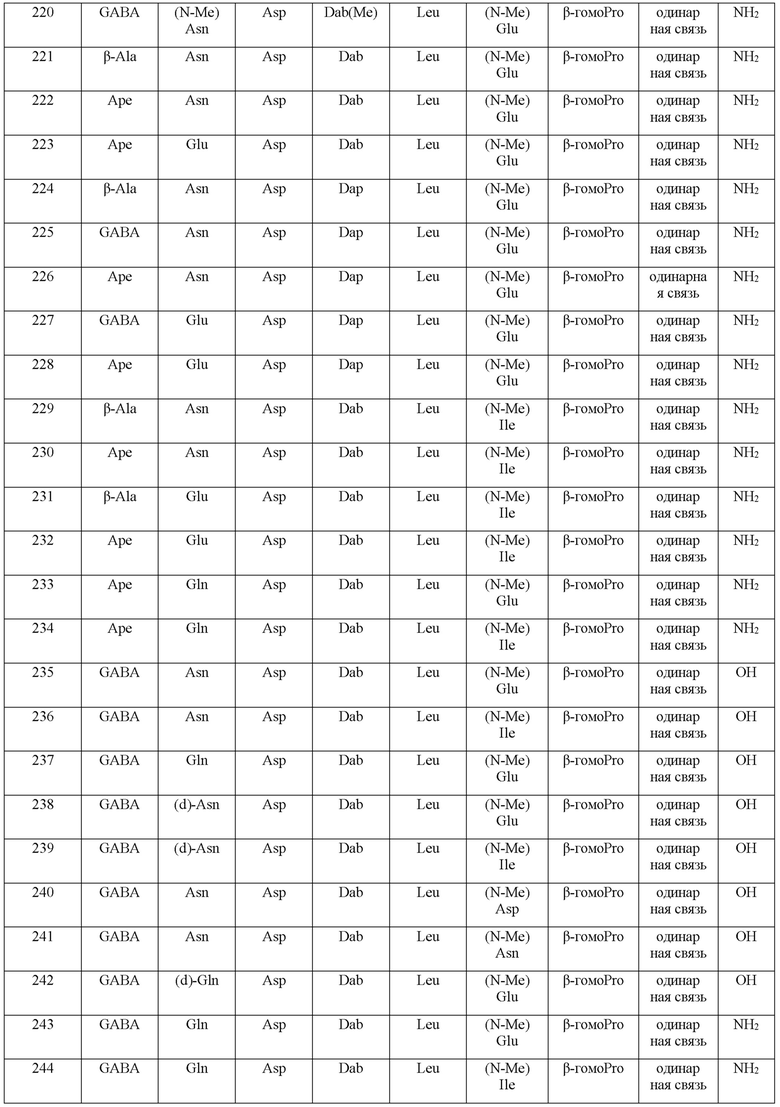
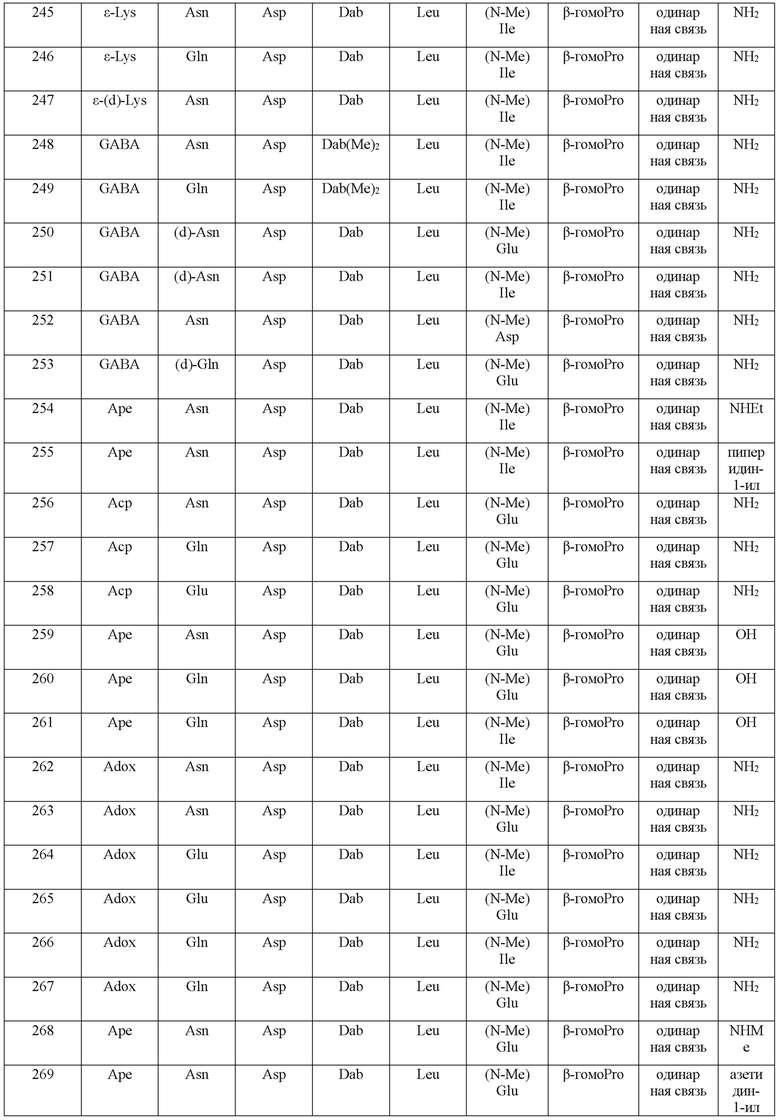
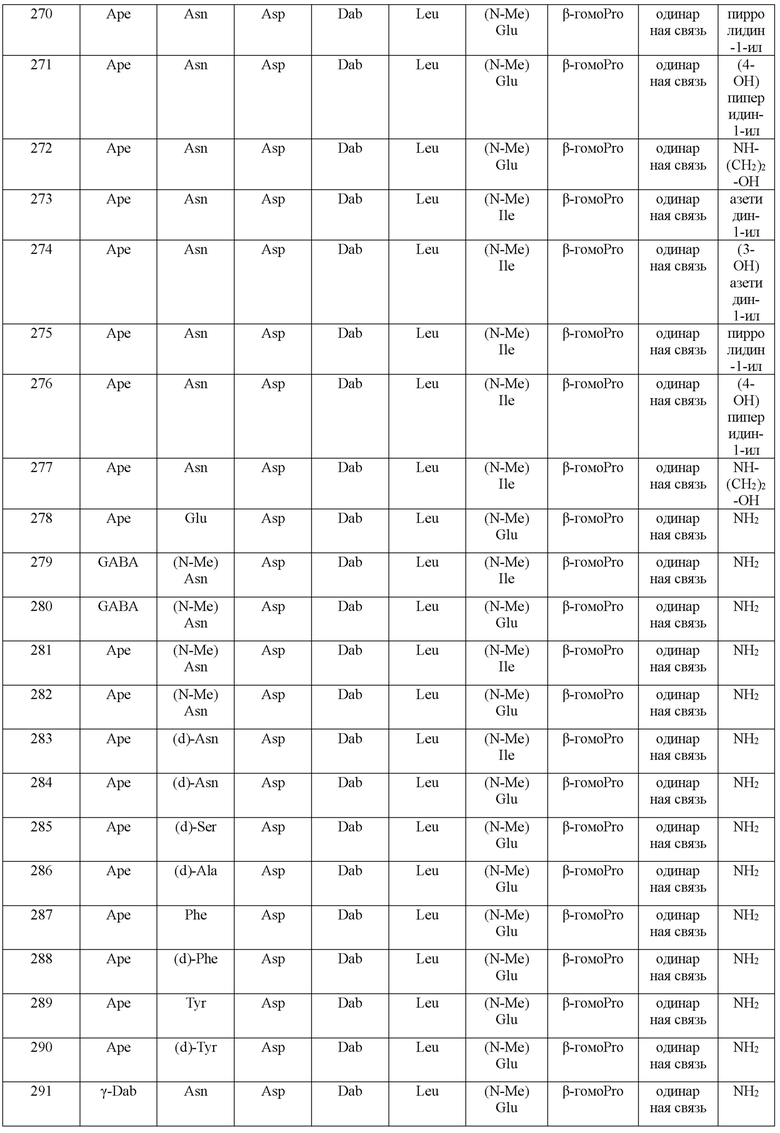
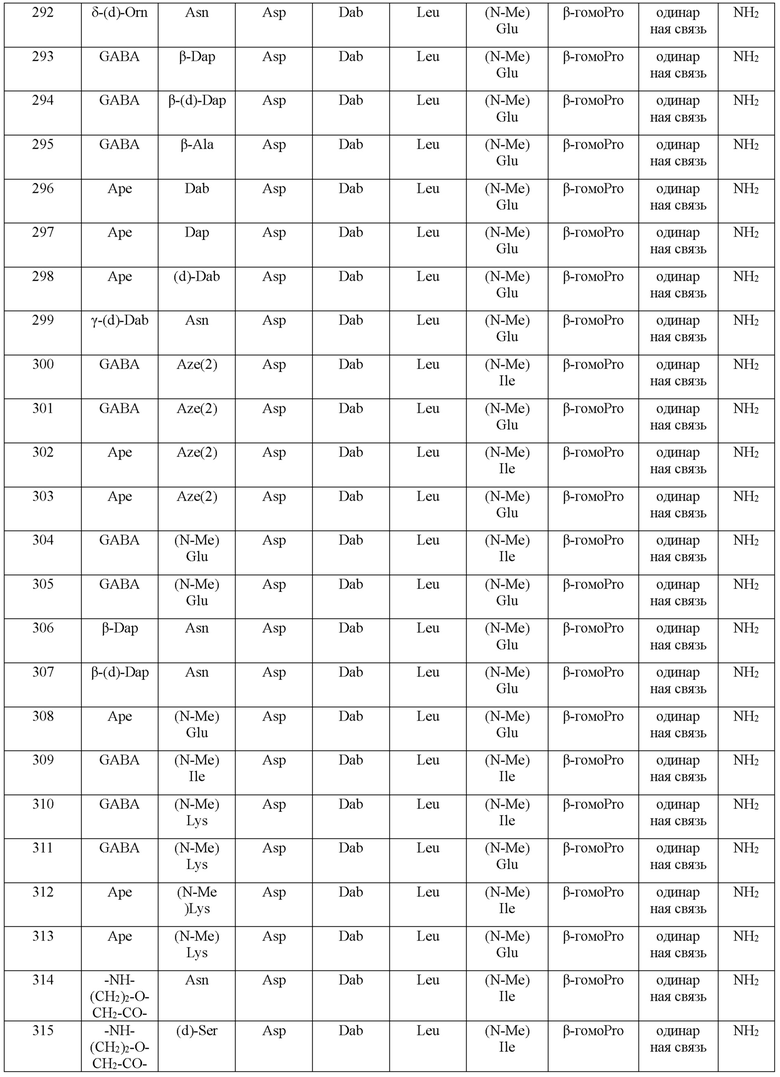
Структуры соединений, представленных формулой [I'-15], которые синтезируют по способу, как в примере 2, показаны в следующей таблице.
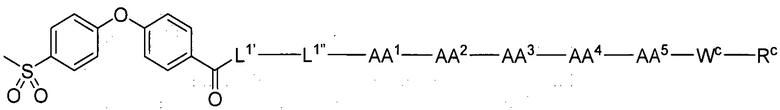 [I'-15]
[I'-15]
[Таблица 21]
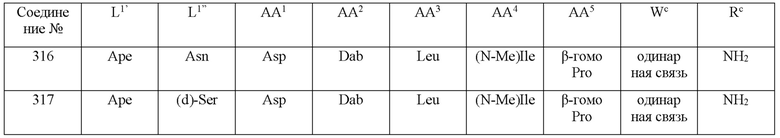
Структуры соединений, представленных формулой [I'-14], которые синтезируют по способу, как в примере 2, показаны в следующей таблице.
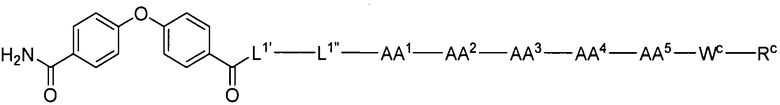 [I'-14]
[I'-14]
[Таблица 22]
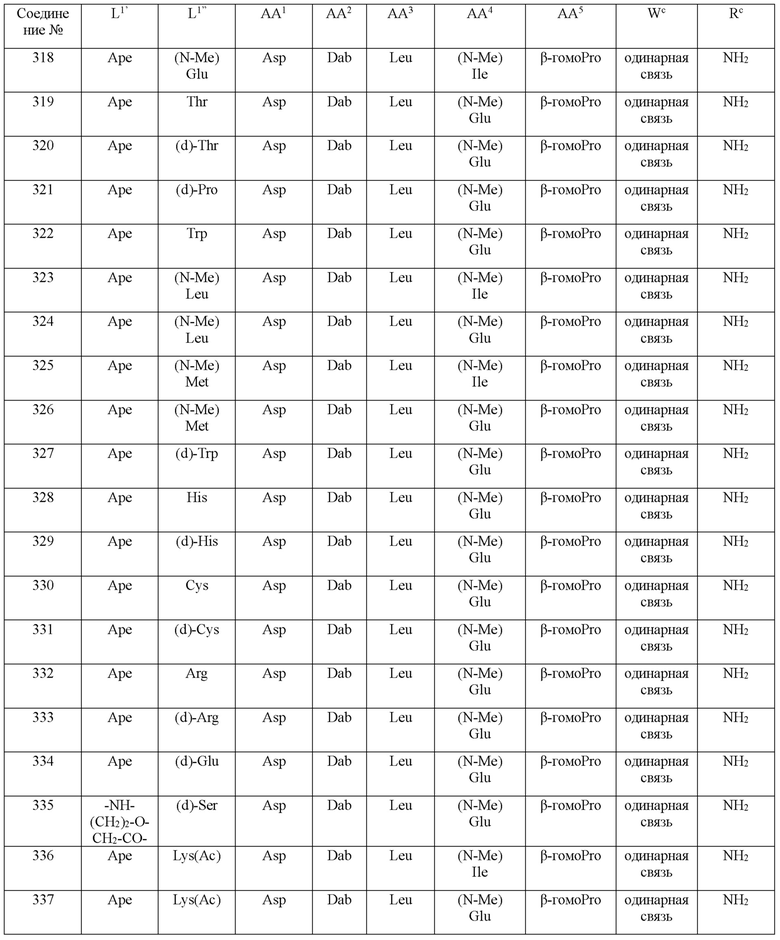

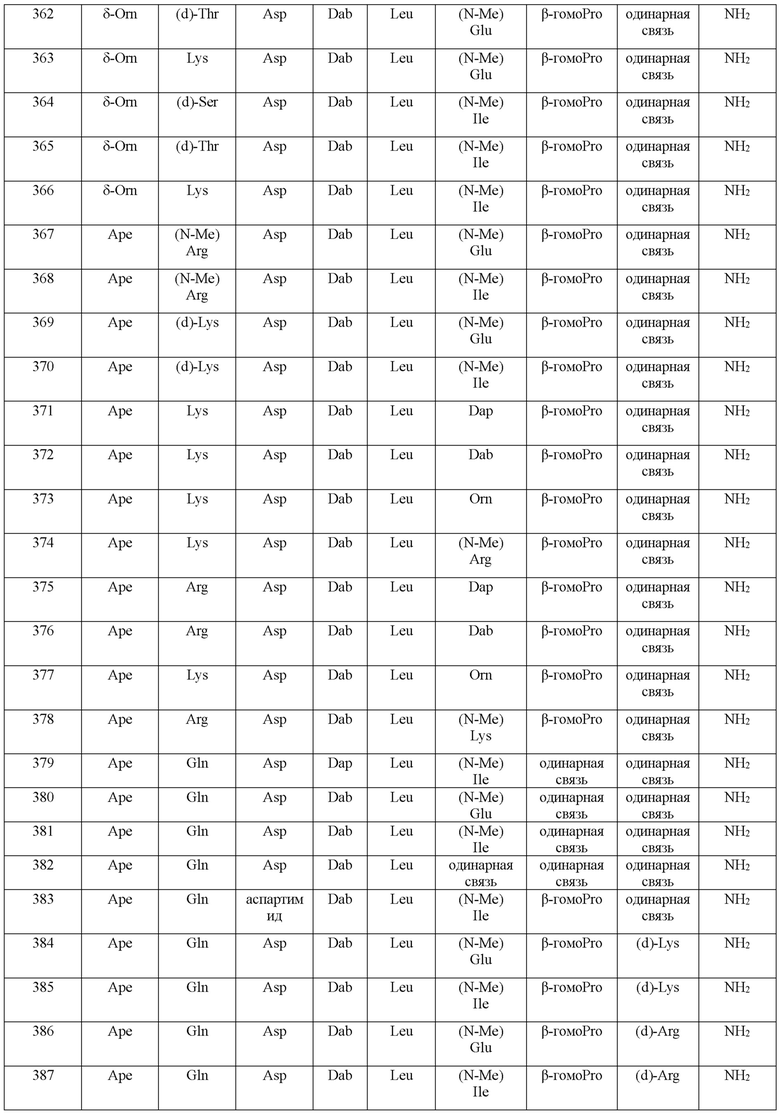
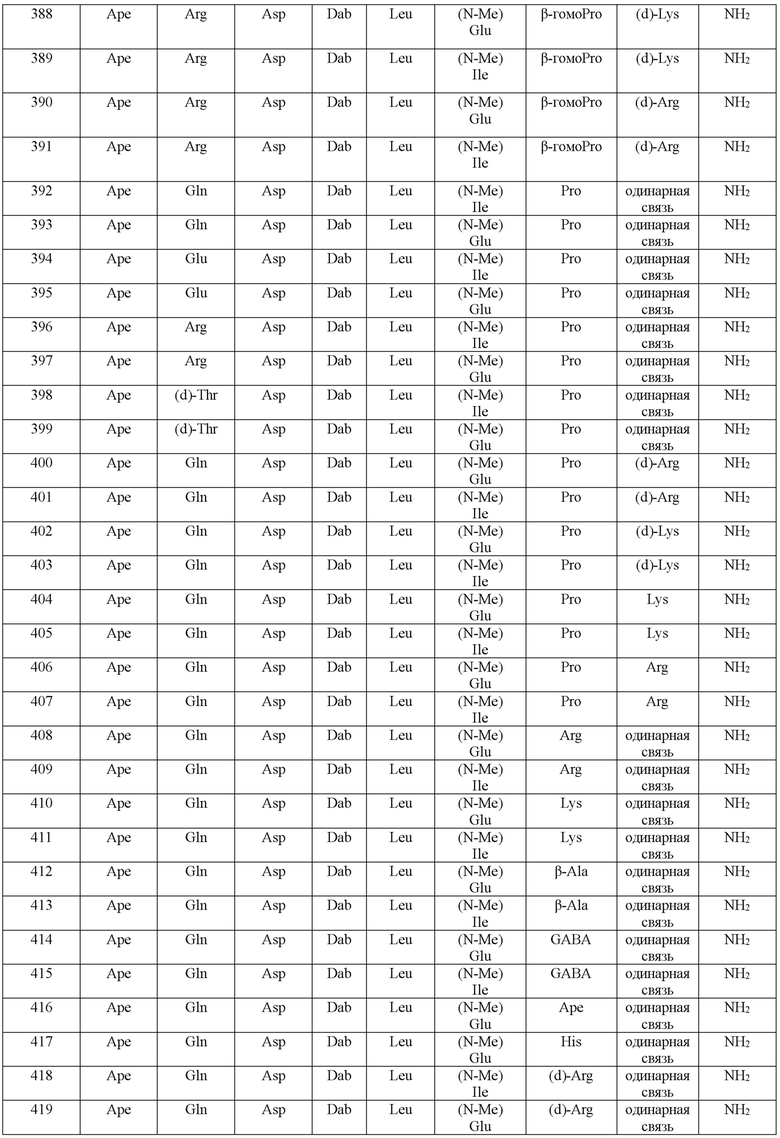
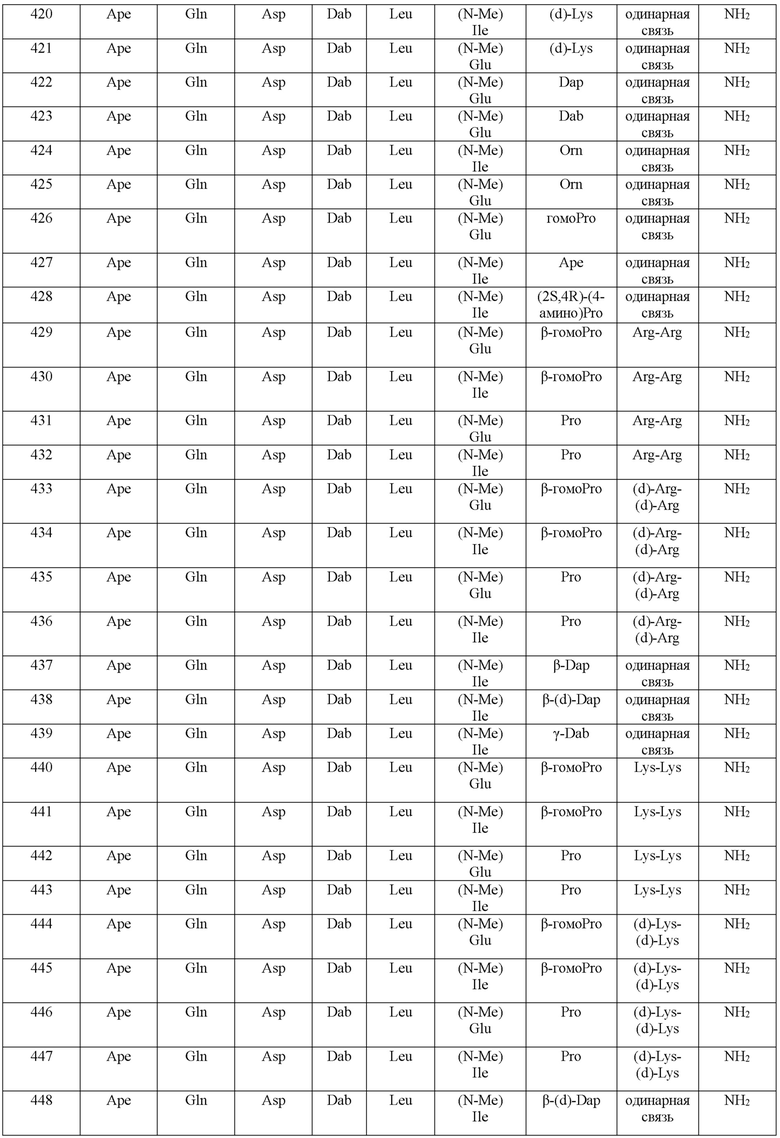
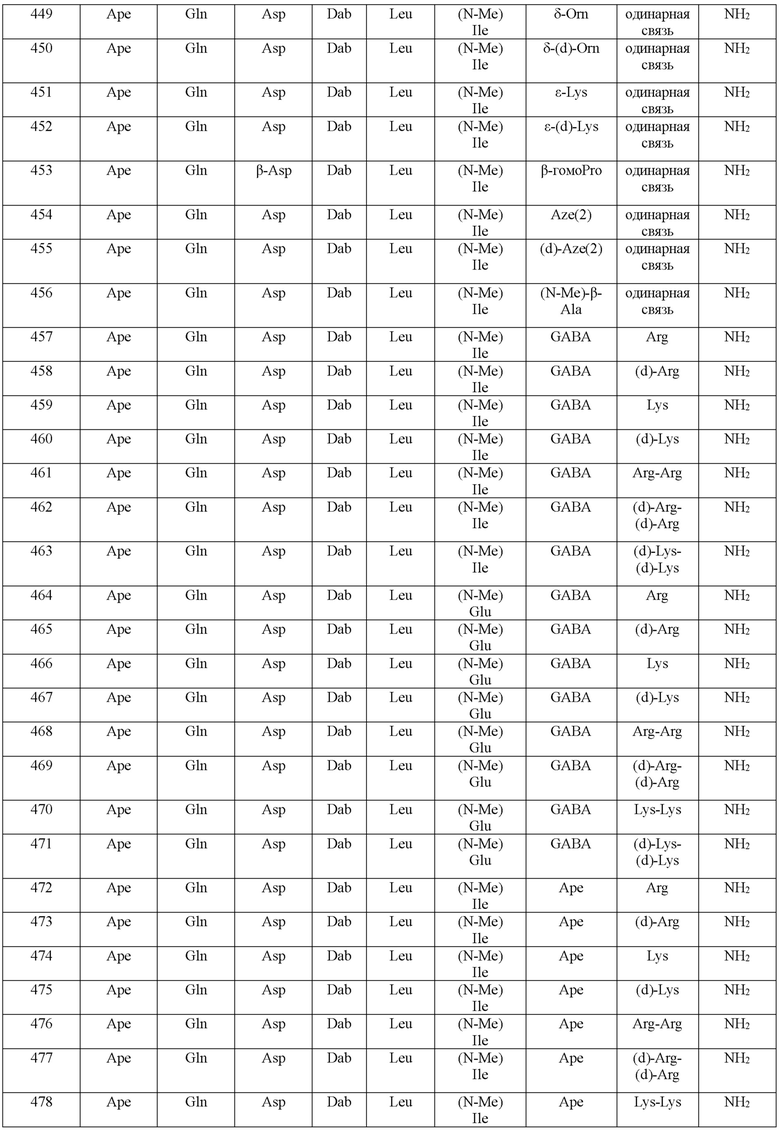
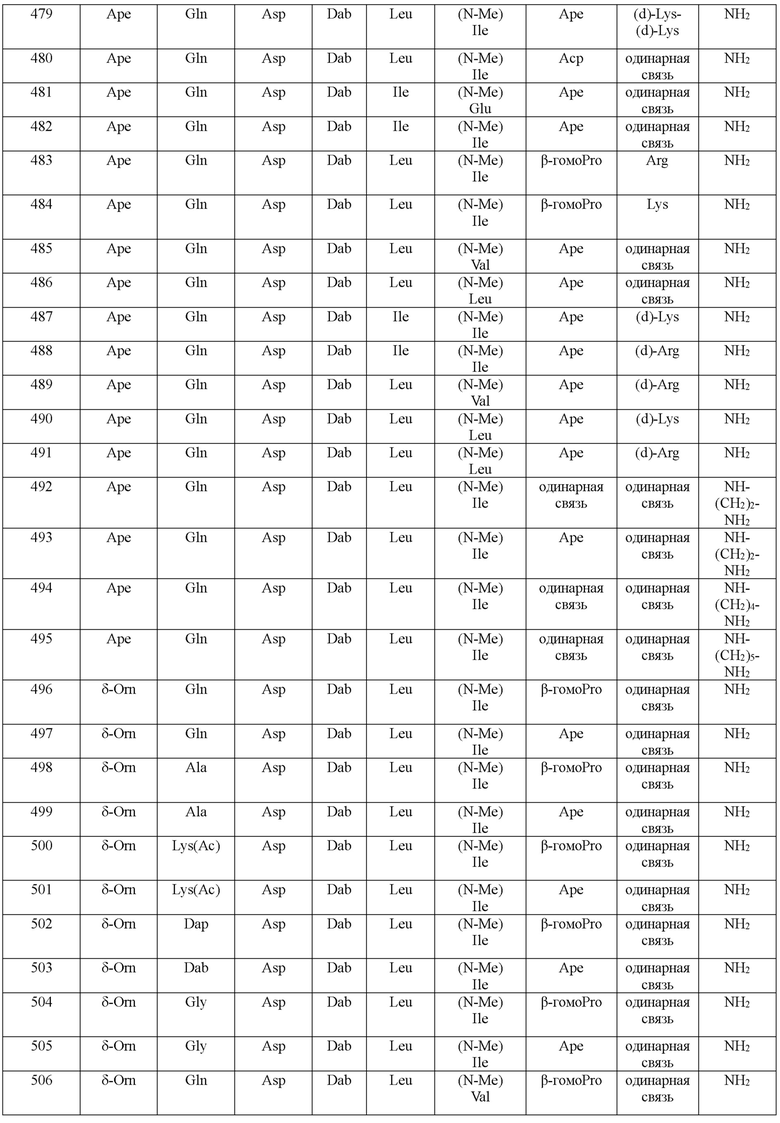
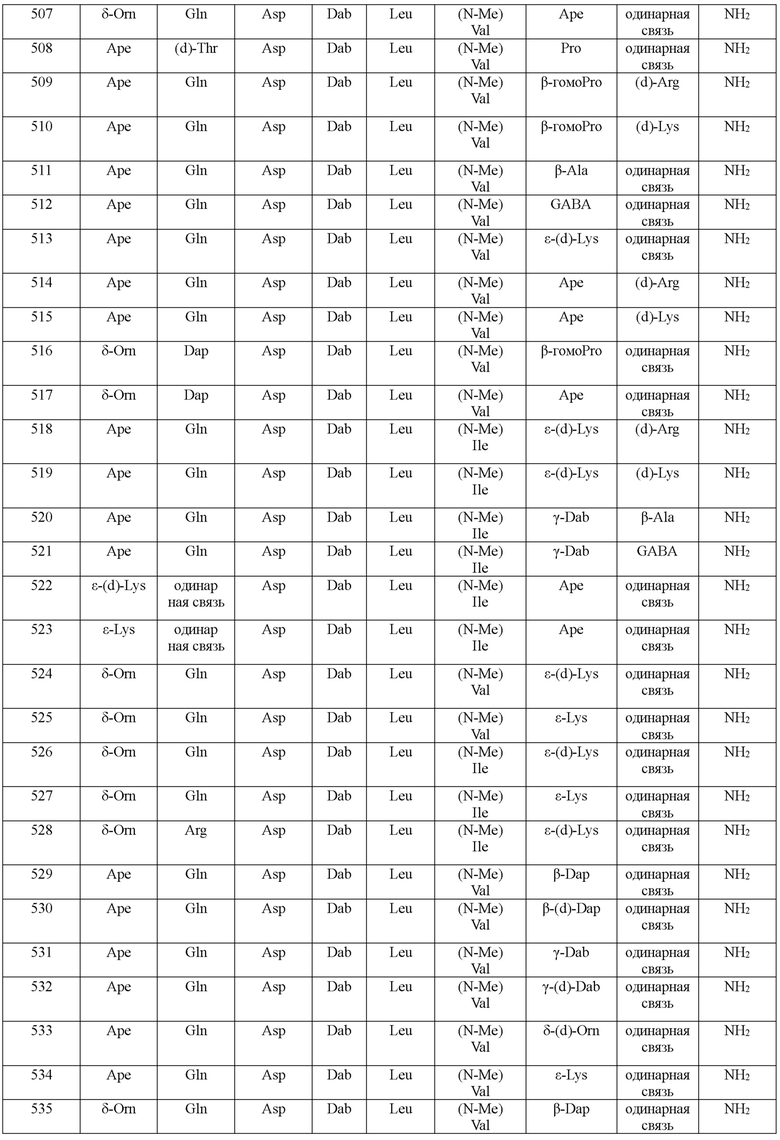
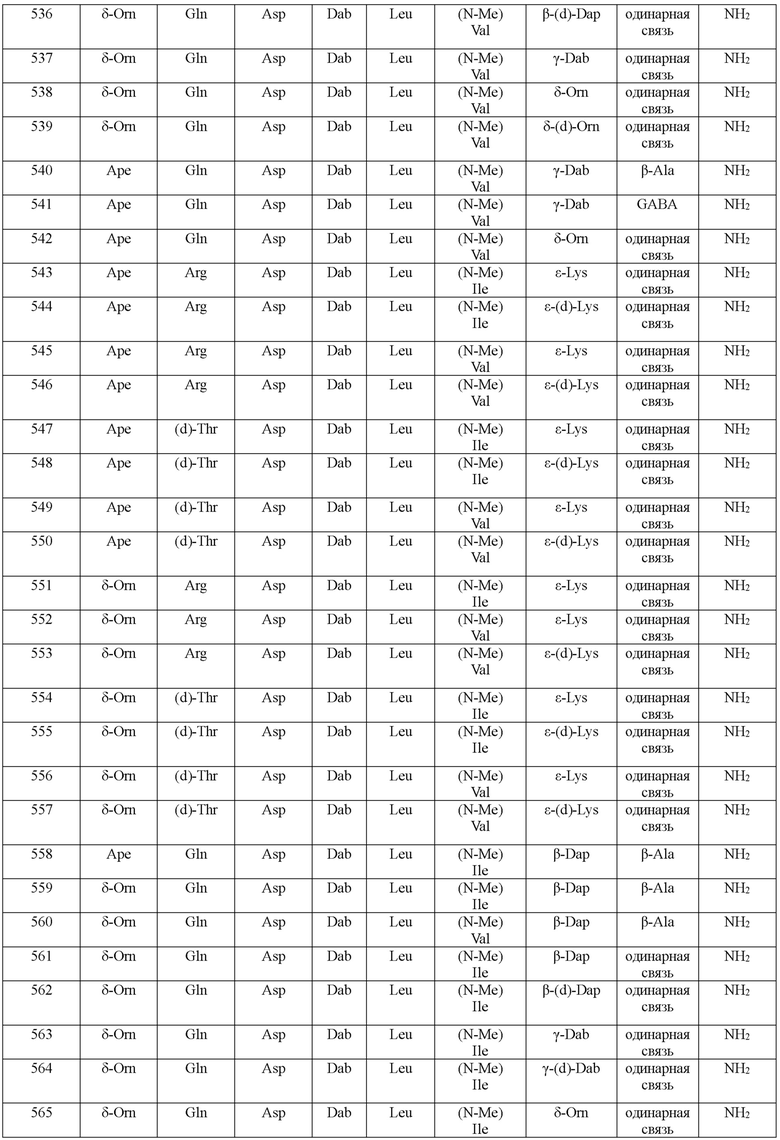
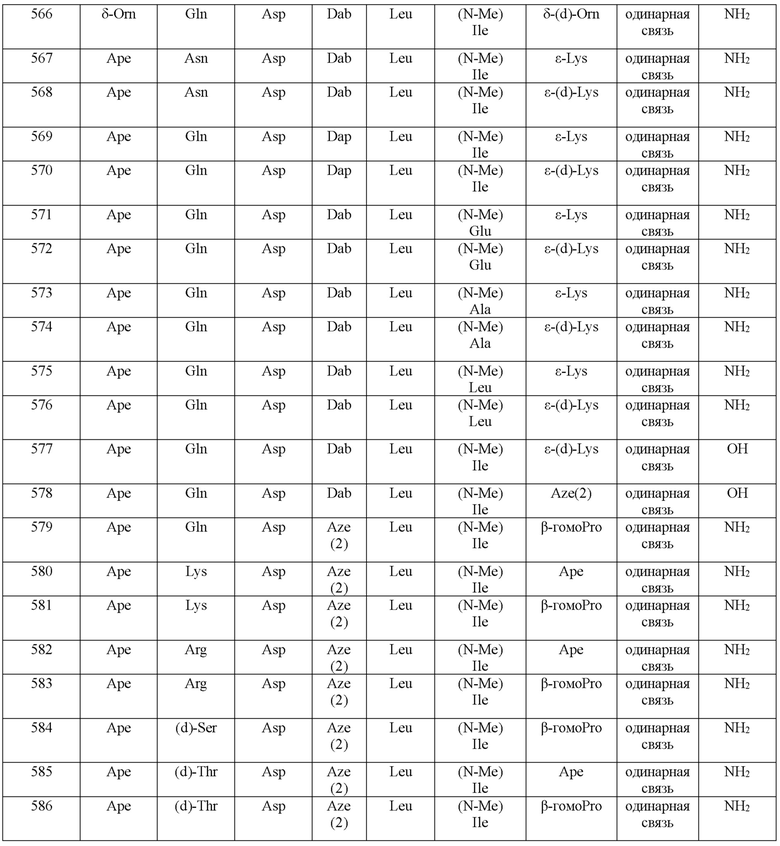
Структуры соединений, представленных формулой [I'-16], которые синтезируют в примере 4 или по способу, как в примере 4, показаны в следующей таблице.
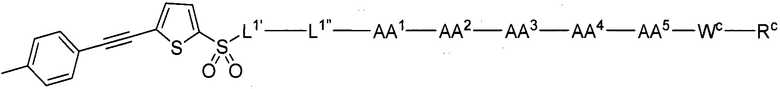 [I'-16]
[I'-16]
[Таблица 23]
Структура соединения, представленного формулой [I'-17], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
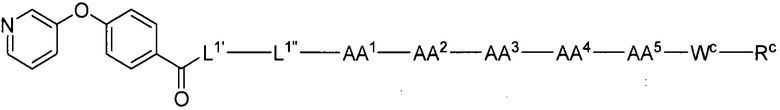 [I'-17]
[I'-17]
[Таблица 24]

Структура соединения, представленного формулой [I'-18], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
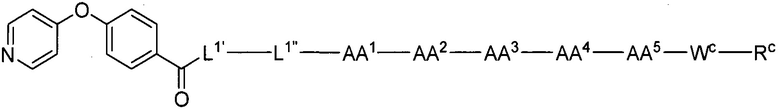 [I'-18]
[I'-18]
[Таблица 25]

Структура соединения, представленного формулой [I'-19], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
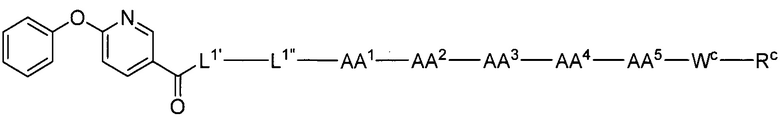 [I'-19]
[I'-19]
[Таблица 26]

Структура соединения, представленного формулой [I'-20], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
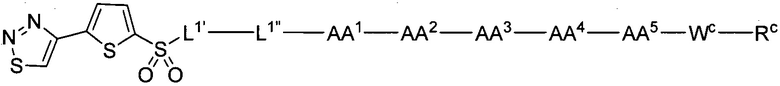 [I'-20]
[I'-20]
[Таблица 27]

Структуры соединений, представленных формулой [I'-21], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
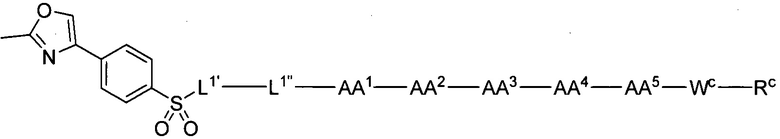 [I'-21]
[I'-21]
[Таблица 28]
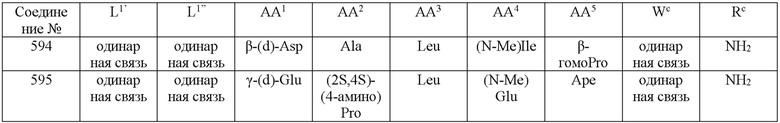
Структура соединения, представленного формулой [I'-22], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
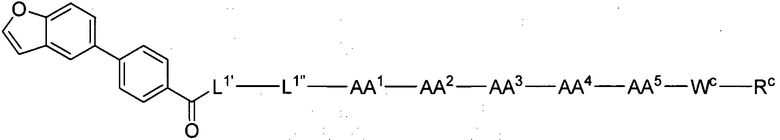 [I'-22]
[I'-22]
[Таблица 29]

Структура соединения, представленного формулой [I'-23], синтезируют по способу, как в примере 2, показана в следующей таблице.
 [I'-23]
[I'-23]
[Таблица 30]

Структура соединения, представленного формулой [I'-24], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
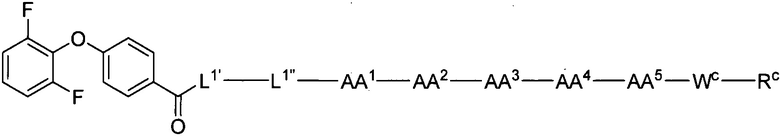 [I'-24]
[I'-24]
[Таблица 31]

Структура соединения, представленного формулой [I'-25], которое синтезируют по способу, как в примере 2, показана в следующей таблице.
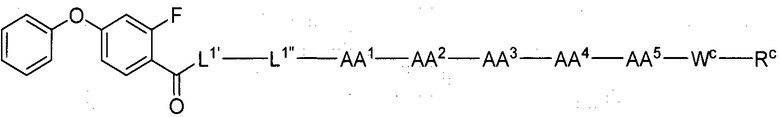 [I'-25]
[I'-25]
[Таблица 32]

Структуры соединений, представленных формулой [I'-26], которые синтезируют по способу, как в примере 2, показаны в следующей таблице.
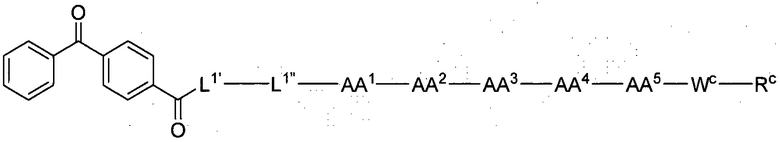 [I'-26]
[I'-26]
[Таблица 33]
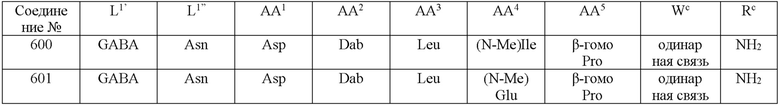
Структуры соединений, представленных формулой [I'-27], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
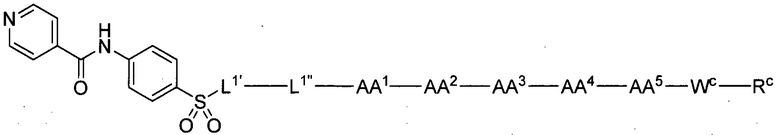 [I'-27]
[I'-27]
[Таблица 34]
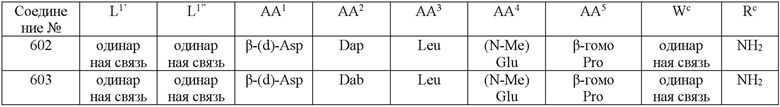

Структура соединения, представленного формулой [I'-28], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
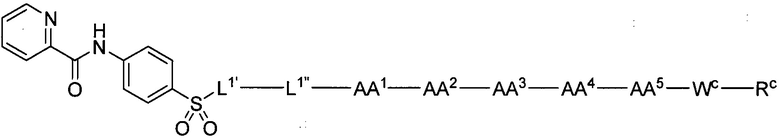 [I'-28]
[I'-28]
[Таблица 35]
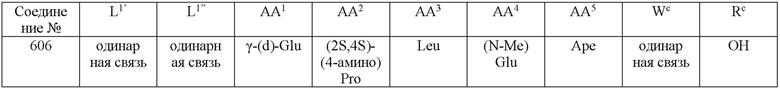
Структура соединения, представленного формулой [I'-29], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
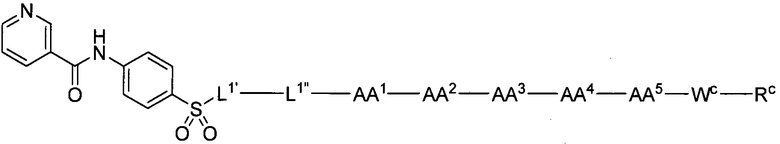 [I'-29]
[I'-29]
[Таблица 36]
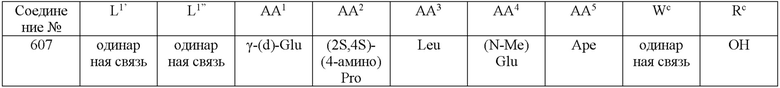
Структура соединения, представленного формулой [I'-30], которое синтезируют по способу, как в примере 5, показана в следующей таблице.
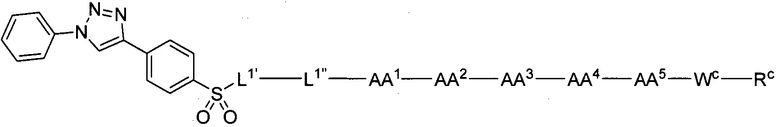 [I'-30]
[I'-30]
[Таблица 37]

Структура соединения, представленного формулой [I'-31], которое синтезируют по способу, как в примере 5, показана в следующей таблице.
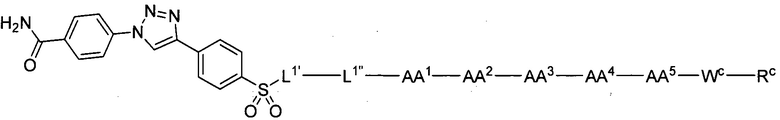 [I'-31]
[I'-31]
[Таблица 38]

Структуры соединений, представленных формулой [I'-32], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
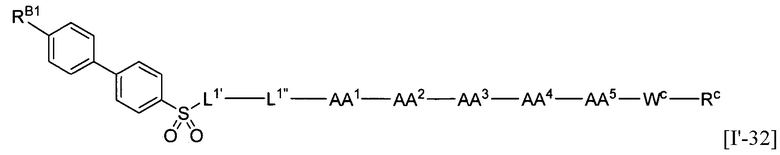
[Таблица 39]
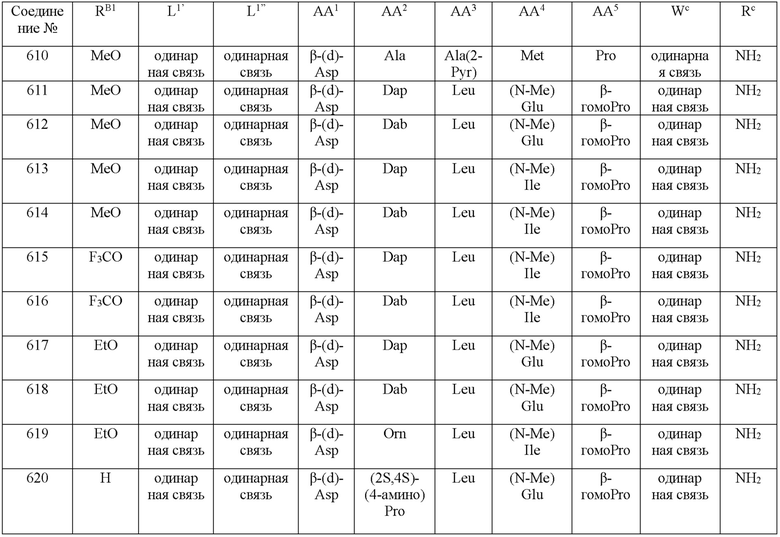
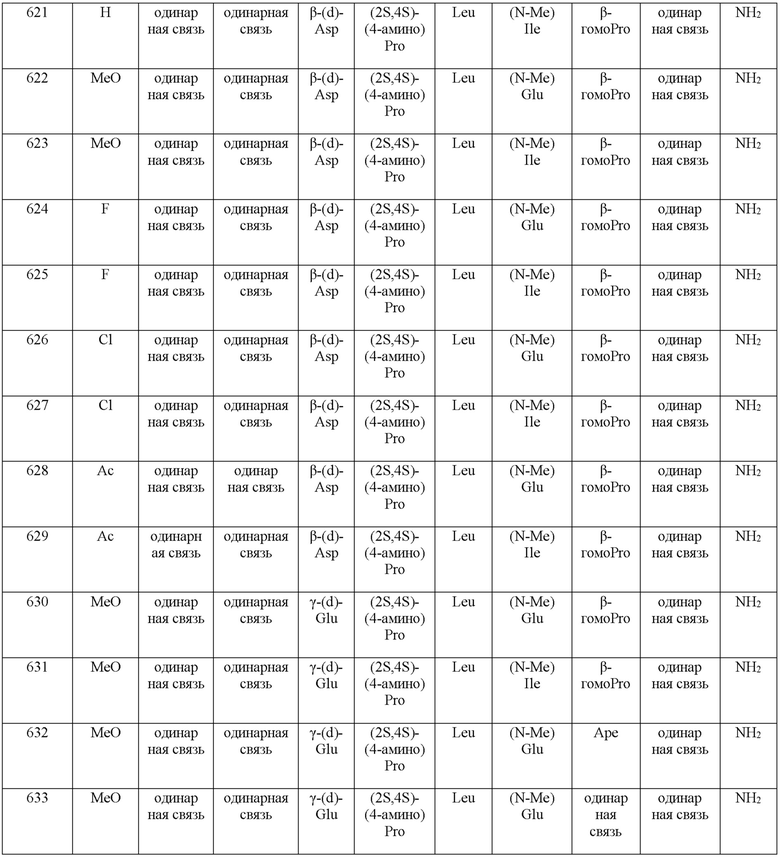
Структуры соединений, представленных формулой [I'-32], которые синтезируют в примере 6 или по способу, как в примере 6, показаны в следующей таблице.
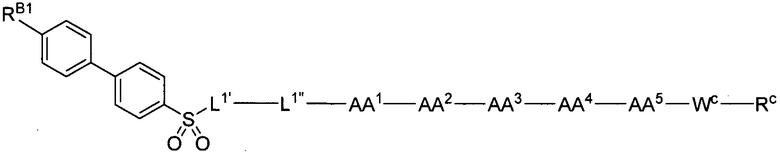 [I'-32]
[I'-32]
[Таблица 40]
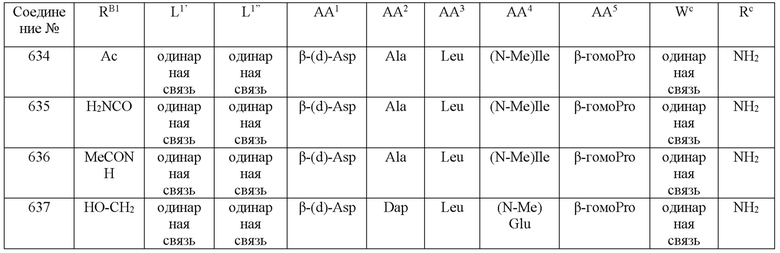
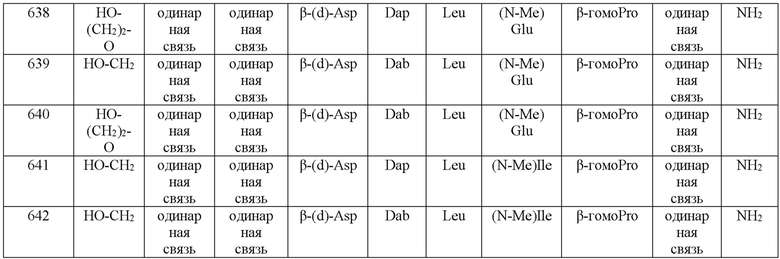
Структура соединения, представленного формулой [I'-33], которое синтезируют по способу, как в примере 1, показана в следующей таблице.
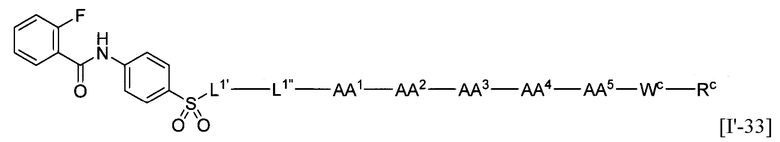
[Таблица 41]
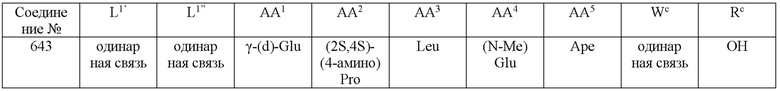
Структуры соединений, представленных формулой [I'-34], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
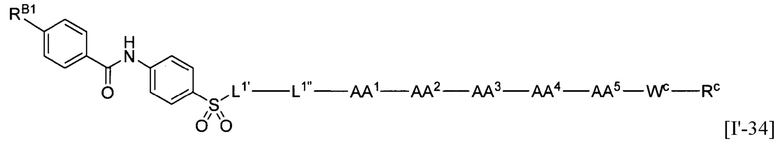
[Таблица 42]
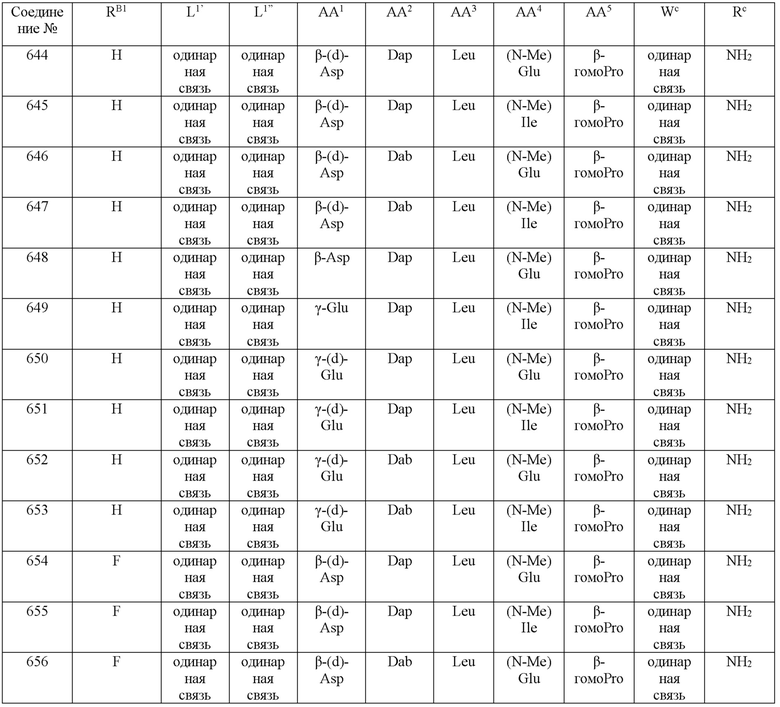
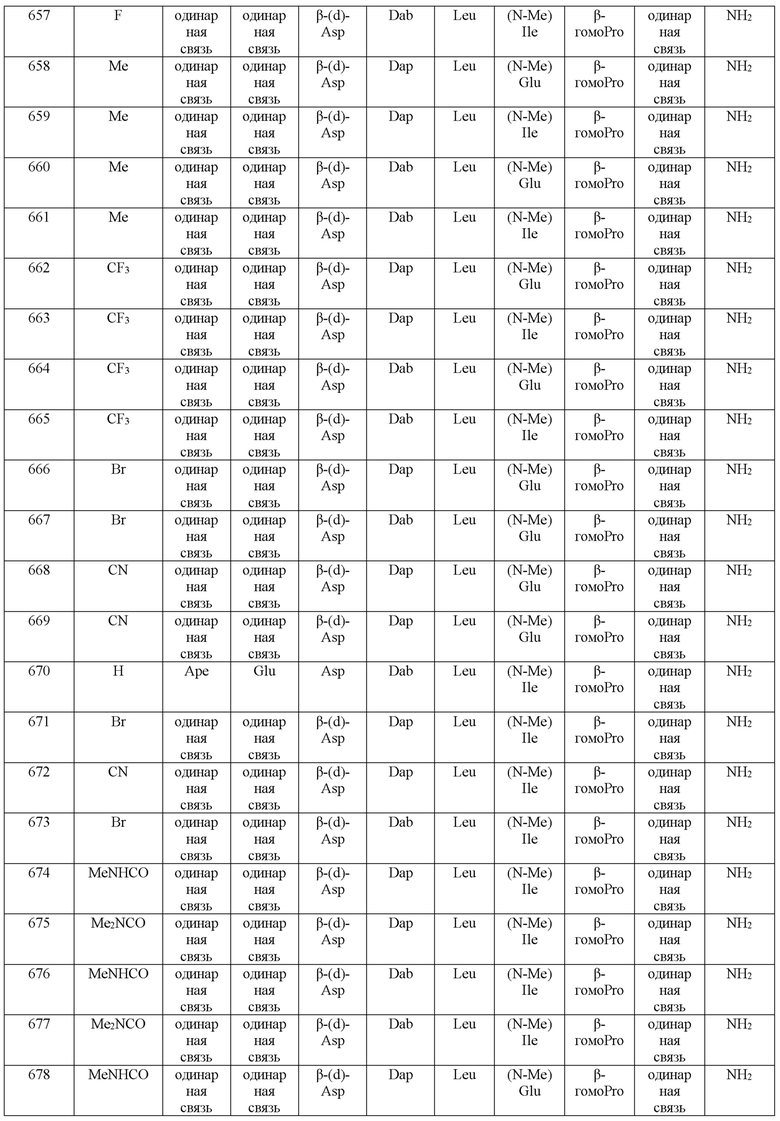
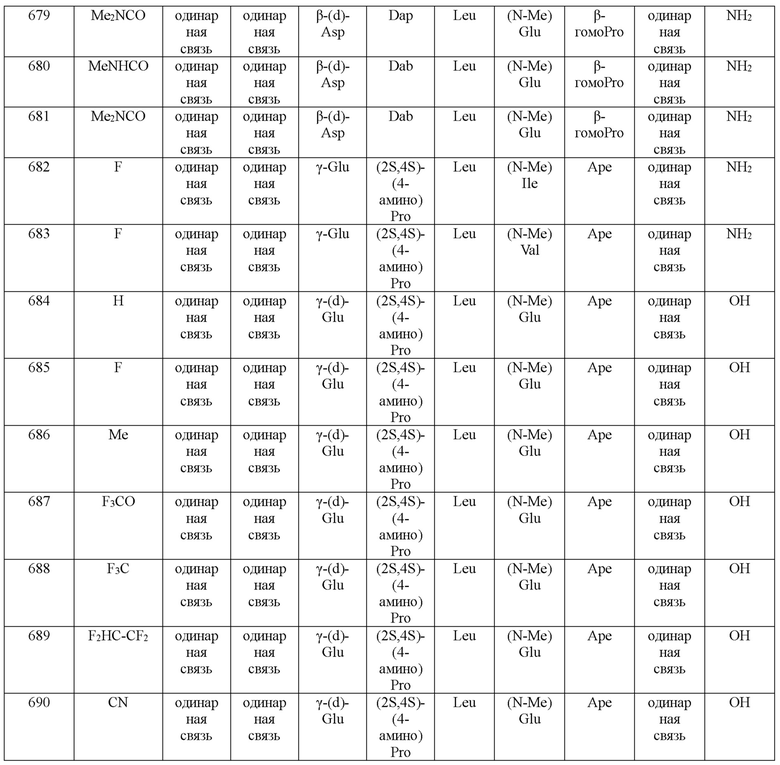
Структуры соединений, представленных формулой [I'-34], которые синтезируют в примере 7 или по способу, как в примере 7, показаны в следующей таблице.
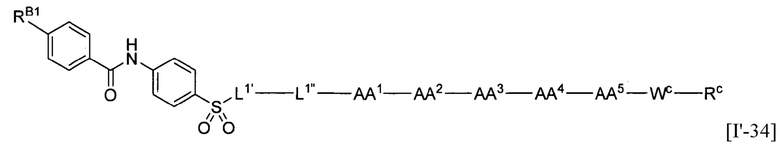
[Таблица 43]
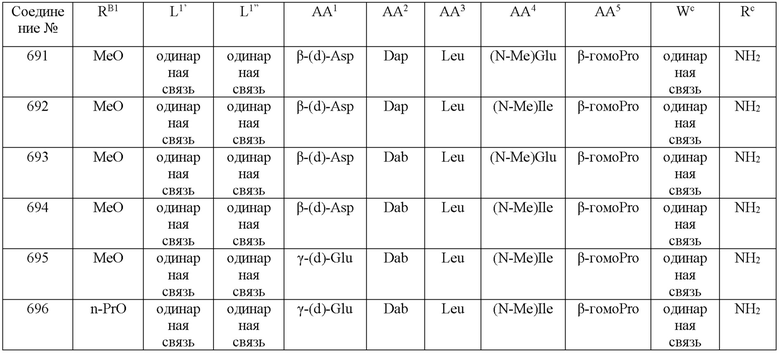
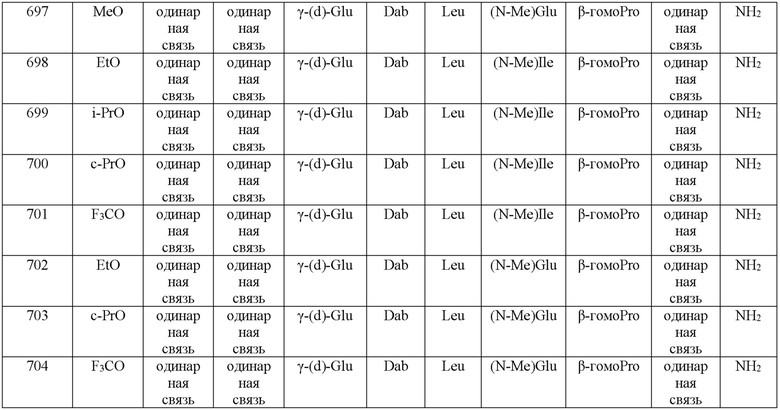
Структуры соединений, представленных формулой [I'-35], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
 [I'-35]
[I'-35]
[Таблица 44]
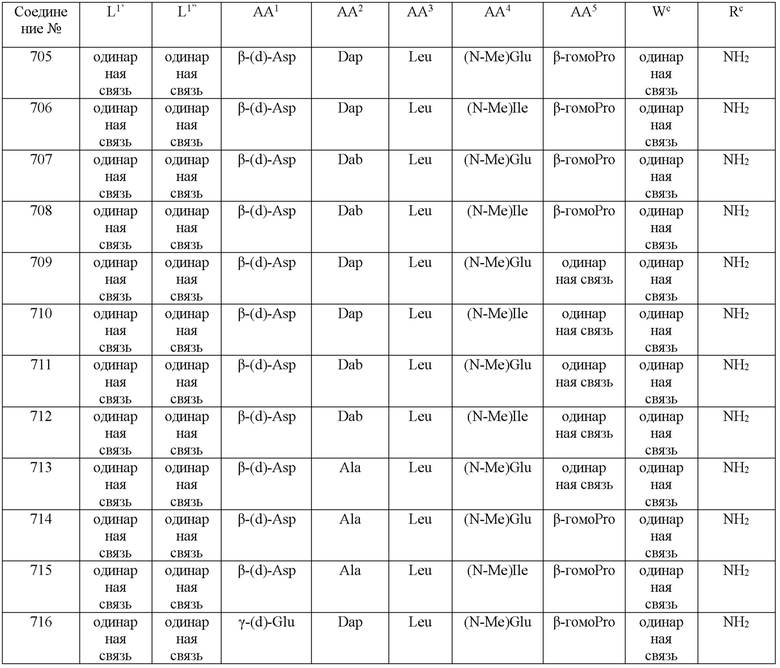
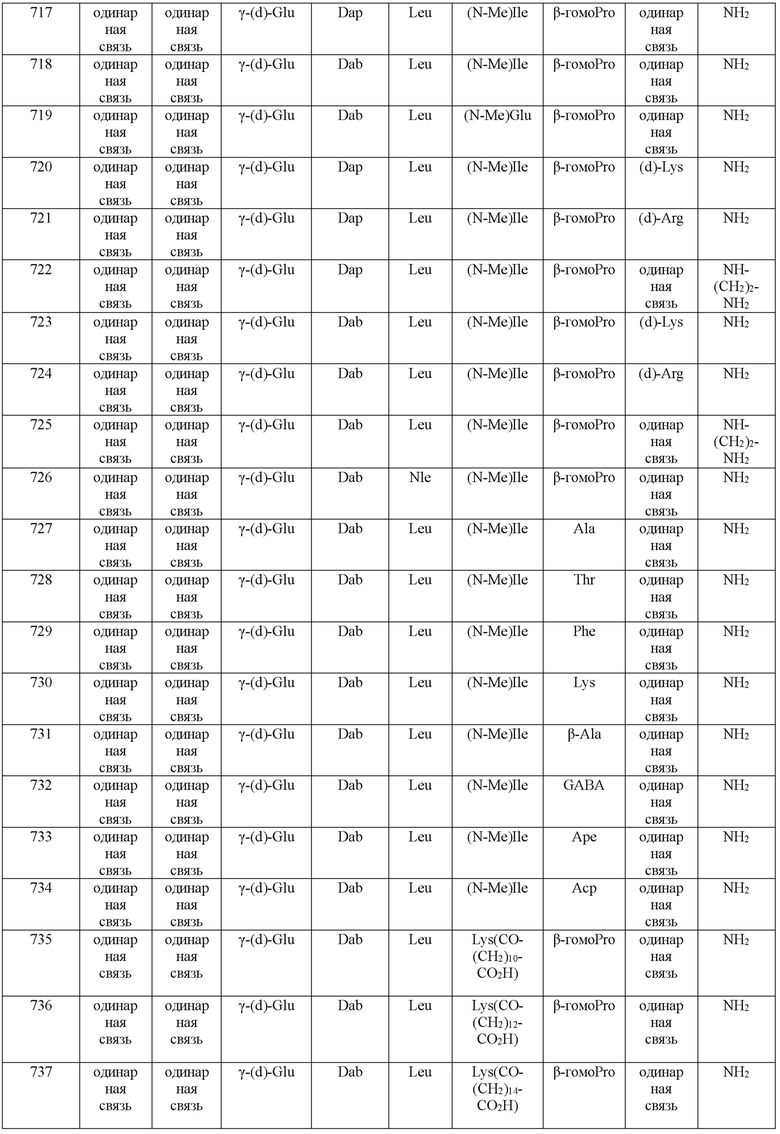
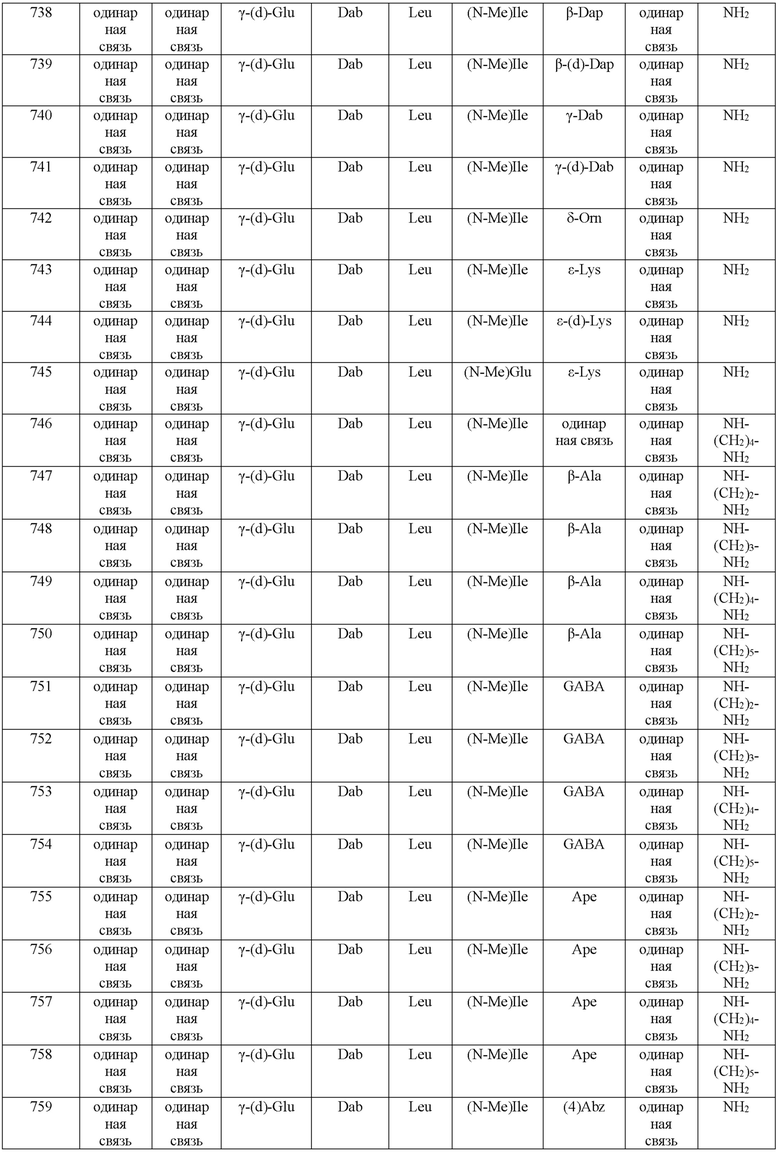
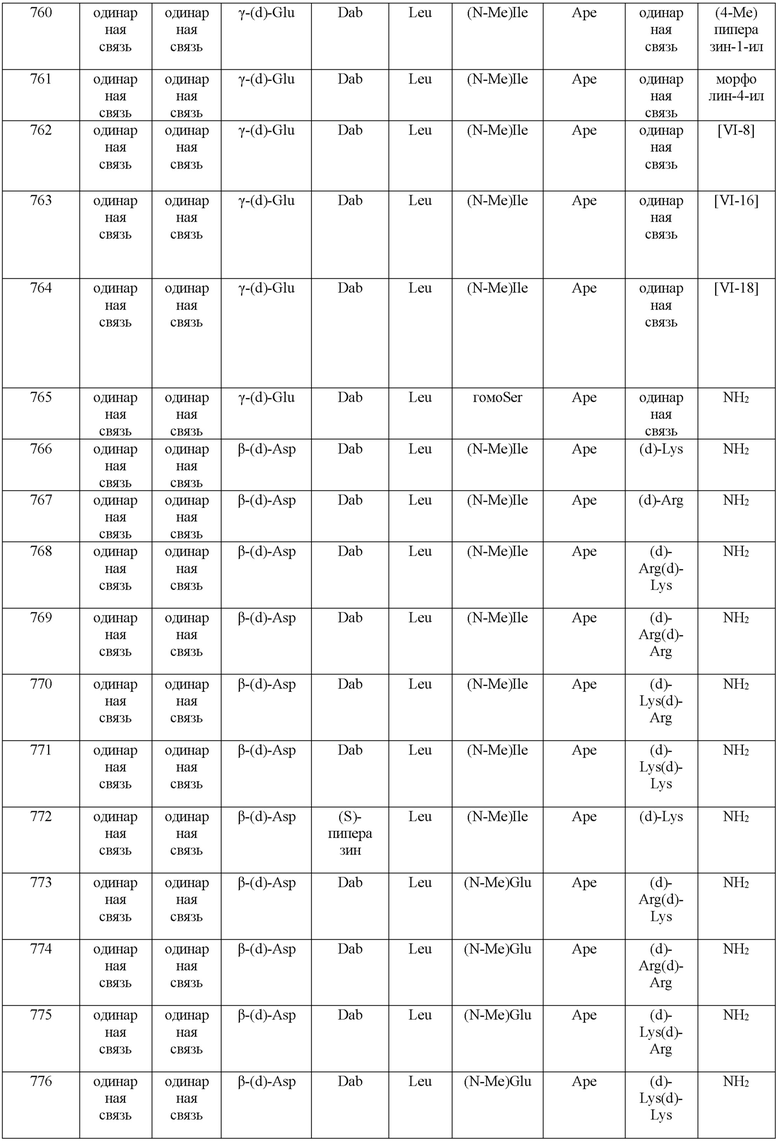
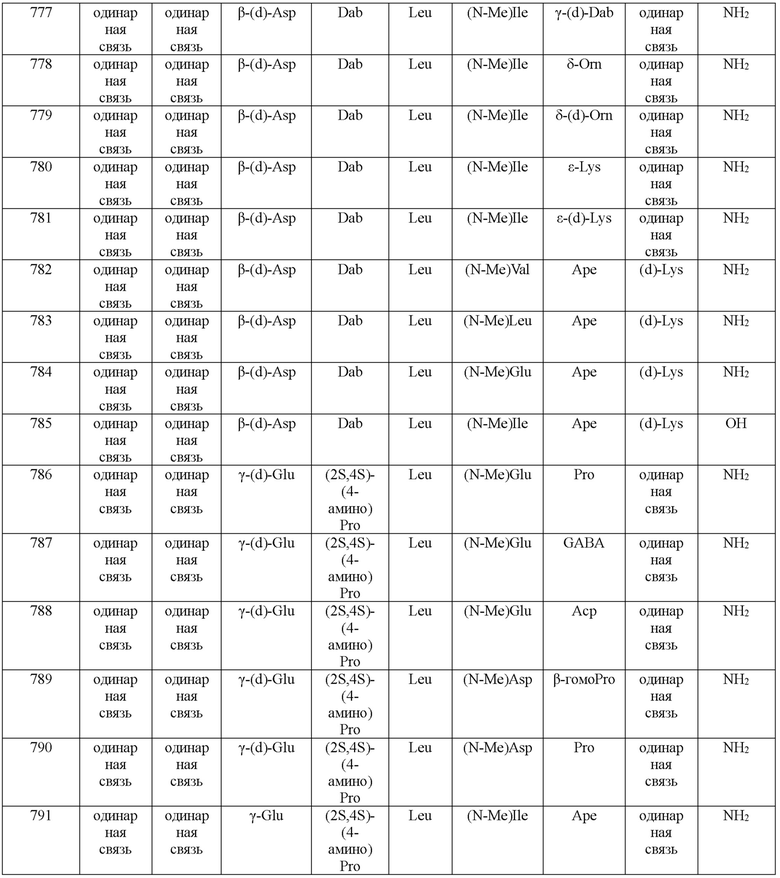
Структуры соединений, представленных формулой [I'-36], которые синтезируют по способу, как в примере 1, показаны в следующей таблице.
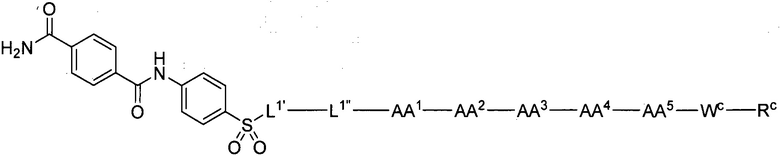 [I'-36]
[I'-36]
[Таблица 45]

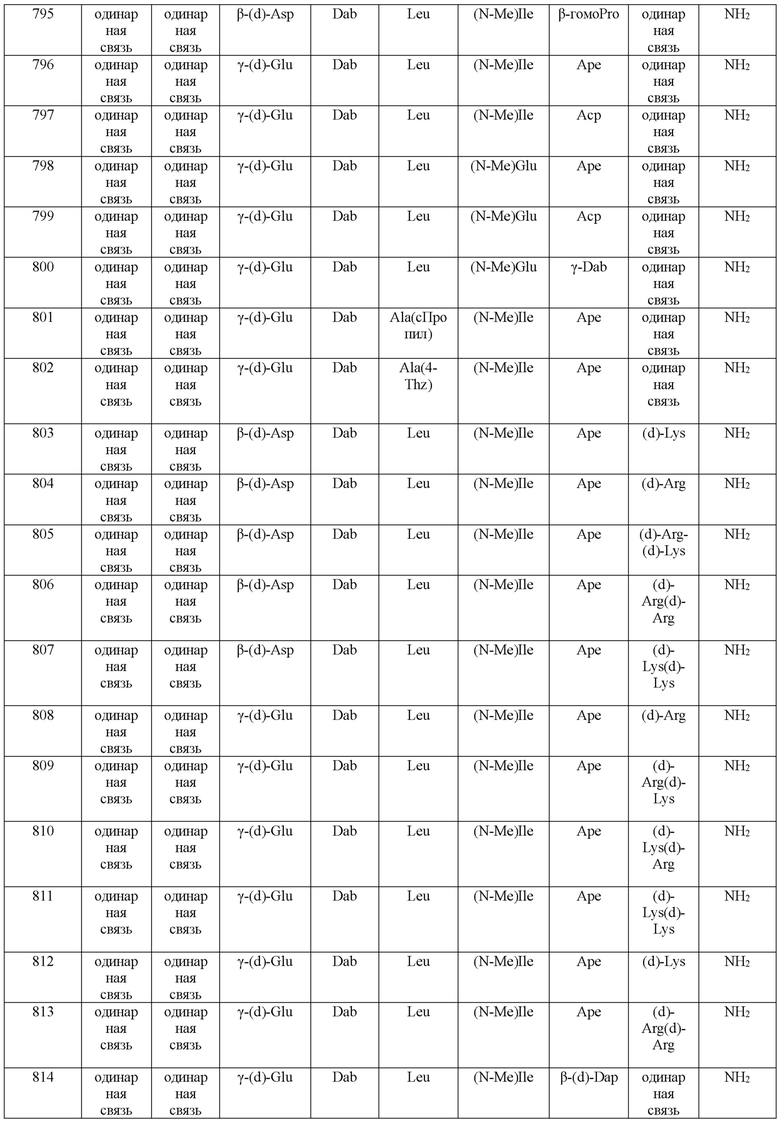
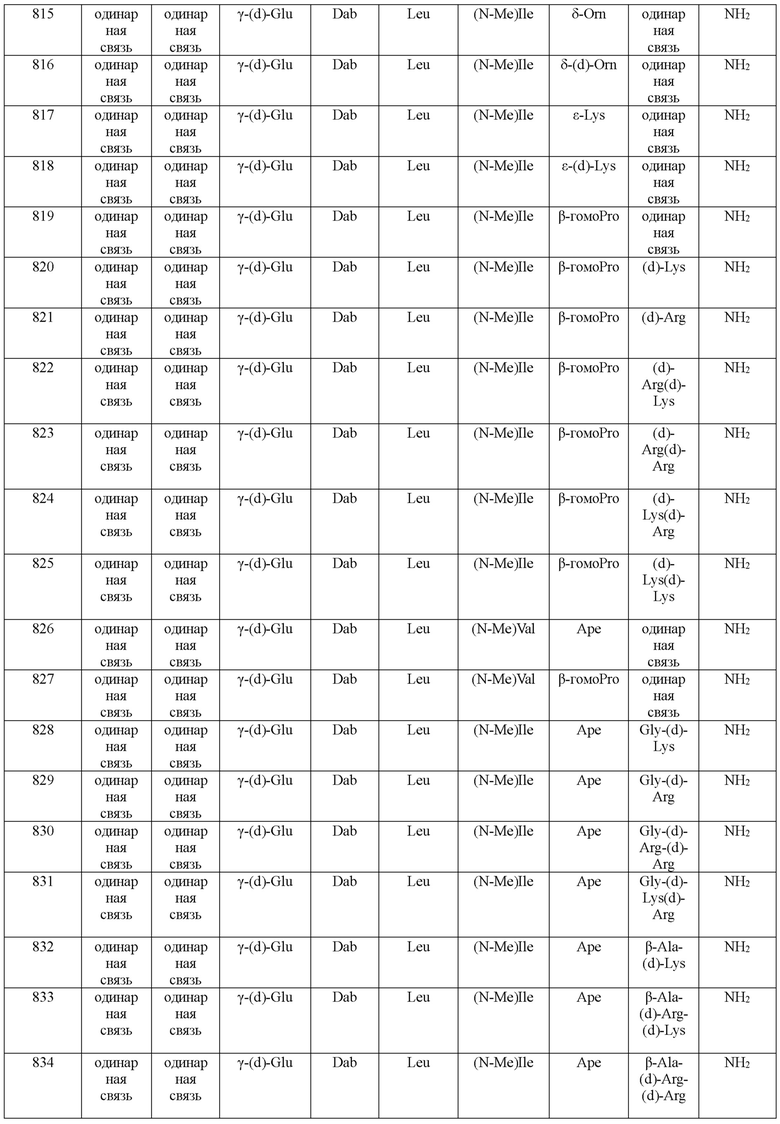
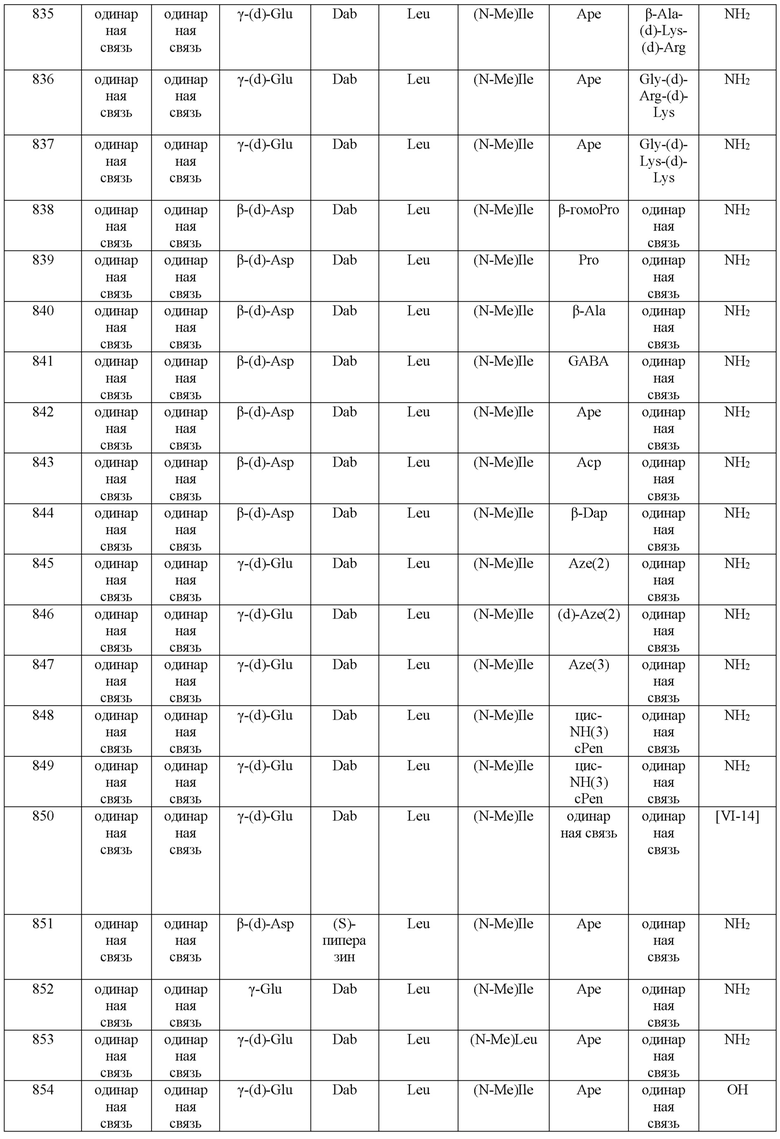
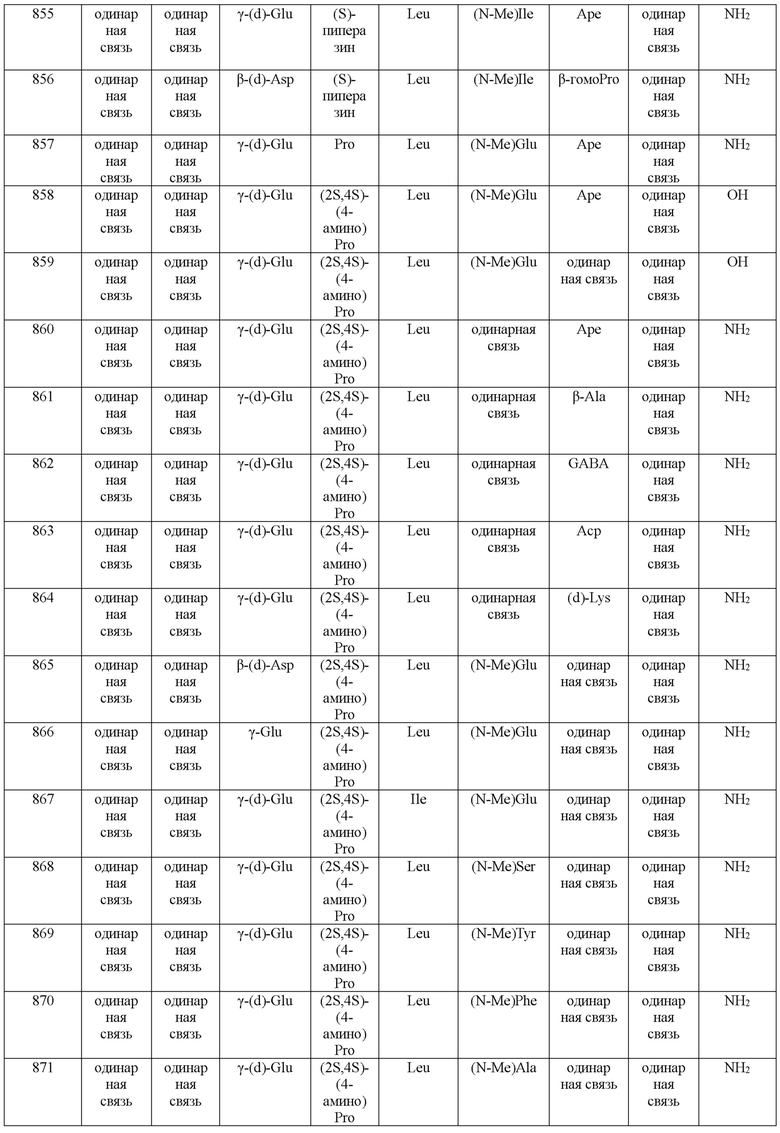
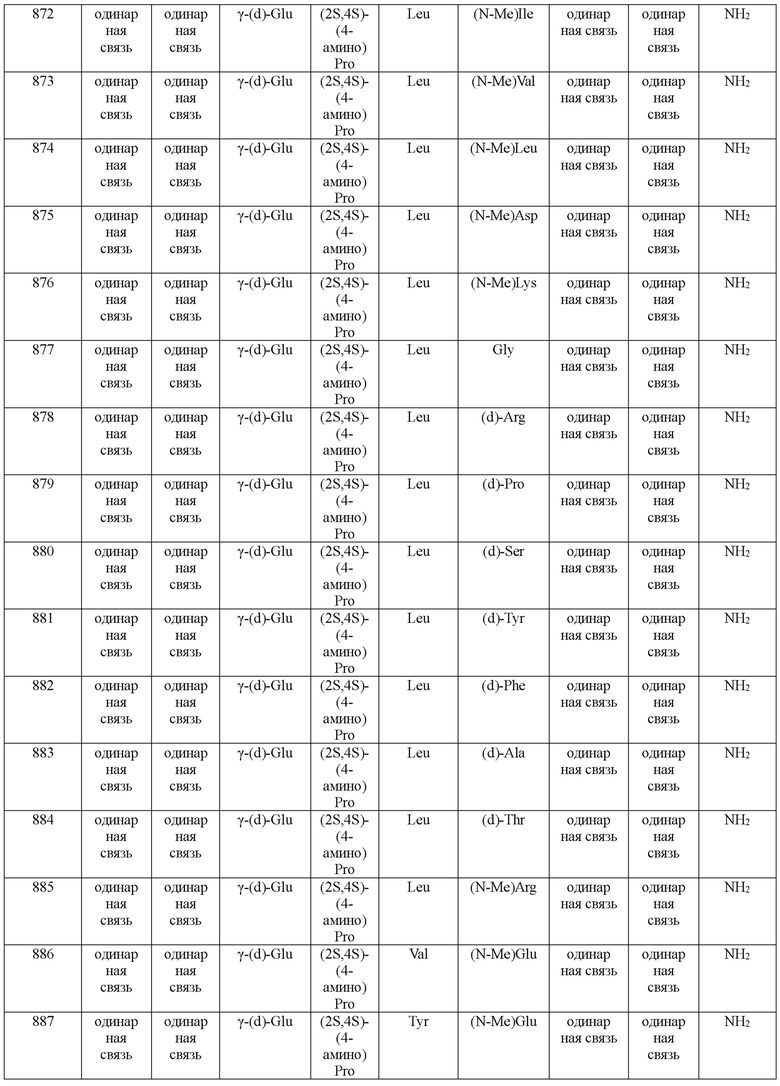
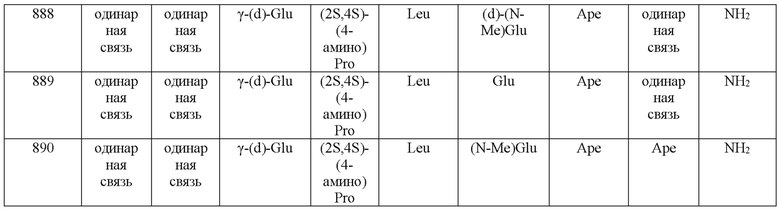
Структуры соединений, представленных формулой [I'-37], которые синтезируют в примере 8 или по способу, как в примере 8, показаны в следующей таблице.
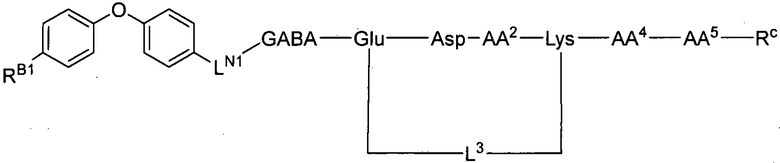 [I'-37]
[I'-37]
[Таблица 46]
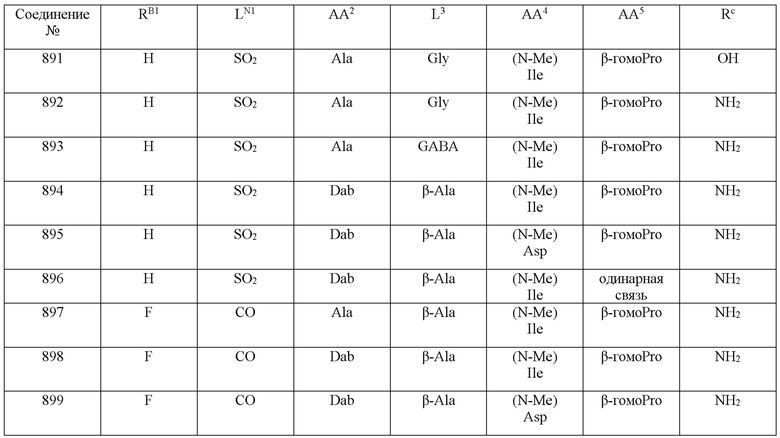
Структуры соединений, представленных формулой [I'-38], которые синтезируют в примере 9 или по способу, как в примере 9, показаны в следующей таблице.
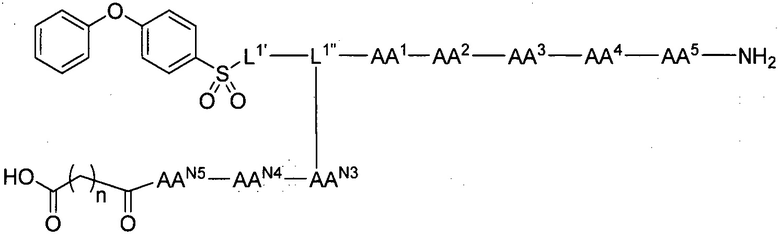 [I'-38]
[I'-38]
[Таблица 47]
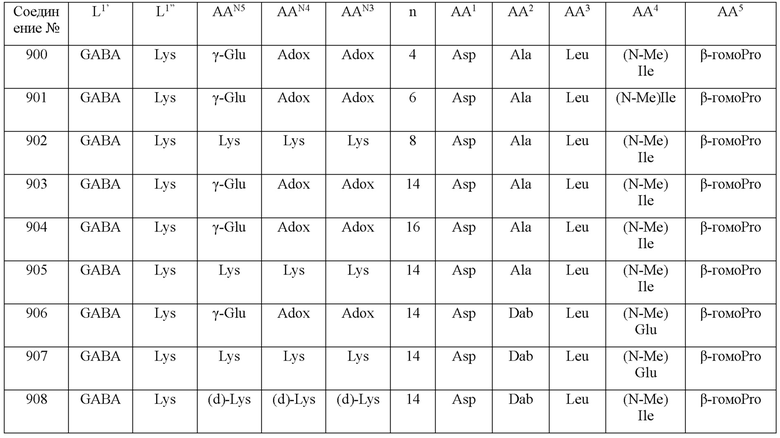
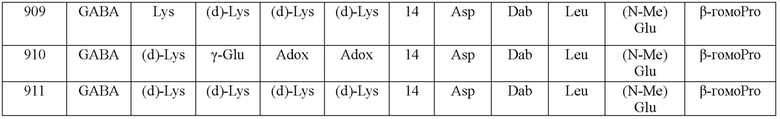
Структуры соединений, представленных формулой [I'-39], которые синтезируют по способу, как в примере 9, показаны в следующей таблице.
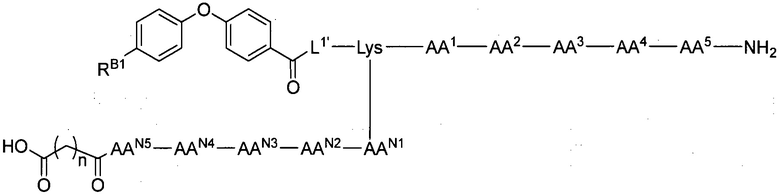 [I'-39]
[I'-39]
[Таблица 48]
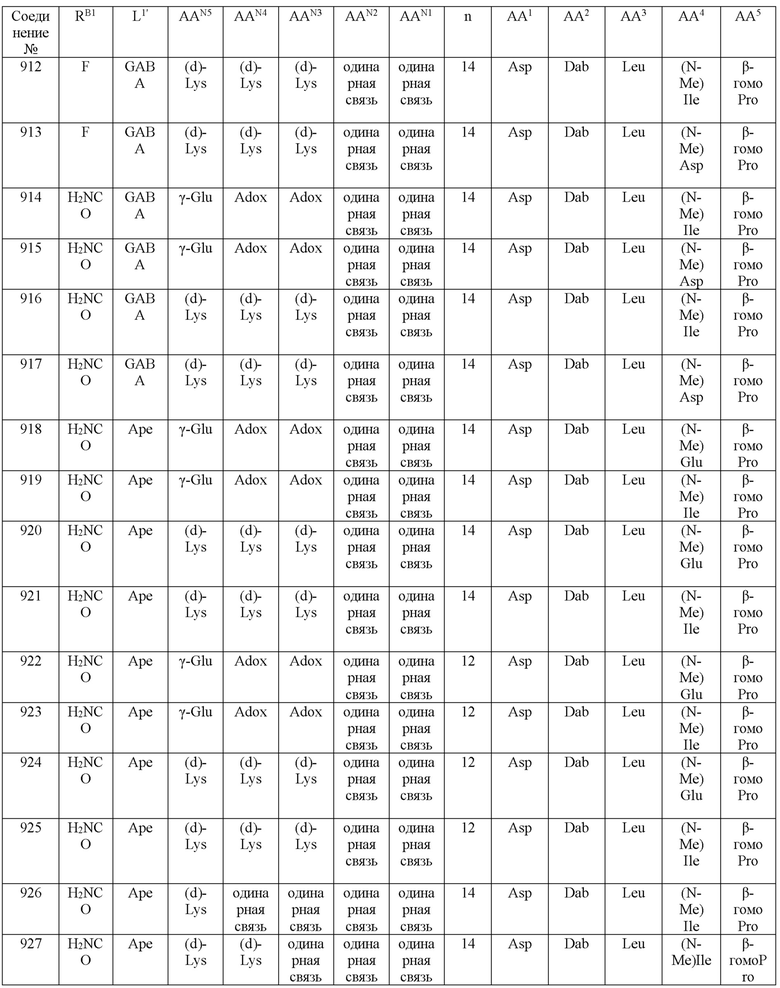
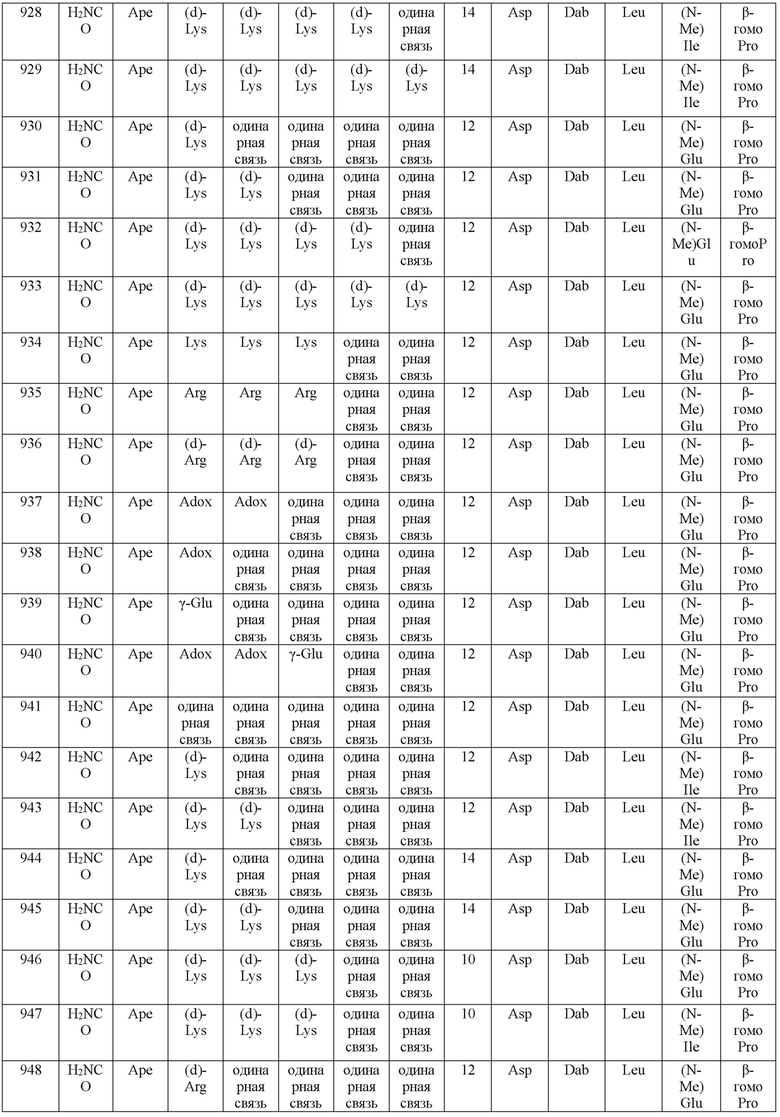
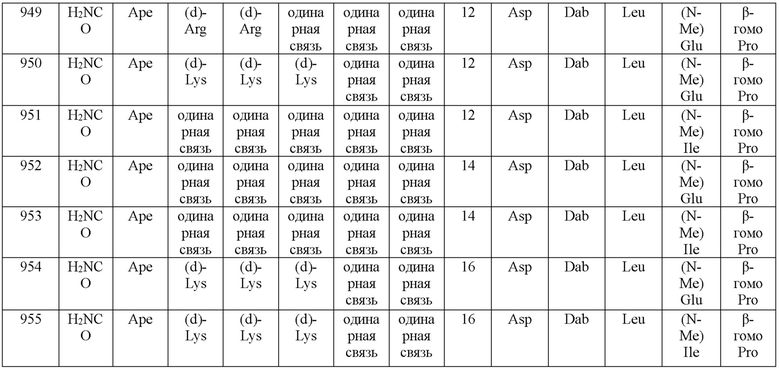
Структуры соединений, представленных формулой [I'-40], которые синтезируют по способу, как в примере 9, показаны в следующей таблице:
 [I'-40]
[I'-40]
где
структура, представленная формулой [VII-2]:
-AAWC1-AAWC2-AAWC3-AAWC4-AAWC5- [VII-2]
соответствует WC, который является «линкером, состоящем из одно-трех аминокислот» в соединении, представленном формулой [I'],
где
AAWC1, AAWC2, AAWC4 и AAWC5 являются одинаковыми или разными, и каждый выбран из группы, состоящей из одинарной связи и (d)-Lys,
AAWC3 представляет собой Lys или (d)-Lys, и
AAWCS представляет собой одинарную связь или (d)-Lys.
[Таблица 49]
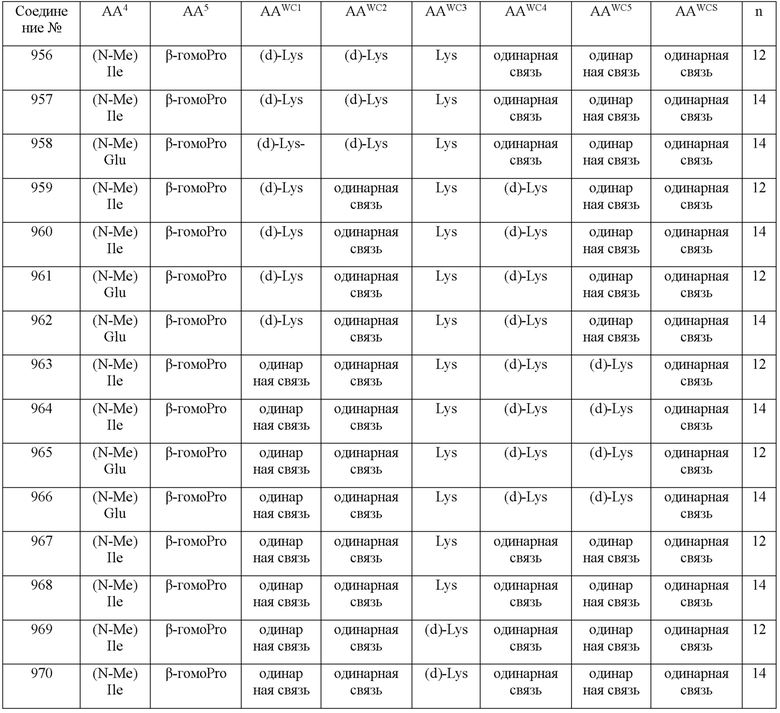

Масс спектры высокоэффективной жидкостной хроматографией (ЖХМС), время удержания (RT) и условия анализа для соединений по настоящему изобретению показаны в следующей таблице.
[Таблица 50]
(найдено)
(рассчитано)
Ингибирующее действие соединений по настоящему изобретению на MMP2 определяют методом, описанным в примерах испытаний 1-1 и 1-2, показанных ниже.
Экспериментальный пример 1-1: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP2 человека (способ 1)
Действие соединений по ингибированию MMP2 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 100 мкг/мл рекомбинантного фермента MMP2 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 60 минут.ММР2 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 0,7 или 7 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 5 или 16 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 2 часов измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Экспериментальный пример 1-2: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP2 человека (способ 2)
Действие соединений по ингибированию MMP2 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23] перемешивают 12,5 мкг/мл рекомбинантного фермента MMP2 человека и 1 ммоль/л ацетата 4-аминофенилртути, и подвергают взаимодействию при 37°C в течение 60 минут.MMP2 человека, активированный в результате реакции, выливают в 384-луночный микропланшет для достижения конечной концентрации 7 или 2,8 нг/мл. Затем, соединения по настоящему изобретению, которые были разведены до различных концентраций, добавляют и выстаивают при температуре в течение 10 минут, затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 16 или 5 мкмоль/L и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1-2 часов измеряют интенсивность флуоресценции (Ex 320 нм/Em 405 нм) с помощью микропланшетного ридера. Степени ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Результаты ингибирующего действия соединений по настоящему изобретению на активность фермента MMP2 человека представлены в следующих таблицах.
[Таблица 51-1]
[Таблица 51-2]
[Таблица 51-3]
[Таблица 51-4]
[Таблица 51-5]
[Таблица 51-6]
[Таблица 51-7]
[Таблица 51-8]
[Таблица 51-9]
[Таблица 51-10]
[Таблица 51-11]
[Таблица 51-12]
[Таблица 51-13]
[Таблица 51-14]
[Таблица 51-15]
[Таблица 51-16]
[Таблица 51-17]
Ингибирующее действие соединений по изобретению на разные типы MMP может быть определено способами, описанными в экспериментальных примерах 2-9.
Экспериментальный пример 2: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP1 человека
Действие соединений по ингибированию MMP1 человека определяют с помощью ферментативного анализа с использованием MOCAc-Lys-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 50 мкг/мл рекомбинантного фермента MMP1 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 120 минут.ММР1 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 8 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Lys-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 11 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Экспериментальный пример 3: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP3 человека
Действие соединений по ингибированию MMP3 человека определяют с помощью ферментативного анализа с использованием MOCAc-Arg-Pro-Lys-Pro-Val-Glu-Nva-Trp-Arg-Lys(Dnp)-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 3 мкг/мл рекомбинантного фермента MMP3 человека и 5 мг/мл химотрипсина. После взаимодействия при 37°C в течение 30 минут добавляют 2 ммоль/л PMSF, тем самым останавливая реакцию. ММР3 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 52 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Arg-Pro-Lys-Pro-Val-Glu-Nva-Trp-Arg-Lys(Dnp)-NH2 до достижения конечной концентрации 26 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Экспериментальный пример 4: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP7 человека
Действие соединений по ингибированию MMP7 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 50 мкг/мл рекомбинантного фермента MMP7 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 60 минут.ММР7 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 18 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 22 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Экспериментальный пример 5: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP8 человека
Действие соединений по ингибированию MMP8 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 100 мкг/мл рекомбинантного фермента MMP8 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 60 минут.ММР8 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 149 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 25 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Экспериментальный пример 6: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP9 человека
Действие соединений по ингибированию MMP9 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 50 мкг/мл рекомбинантного фермента MMP9 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 24 часов. ММР9 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 58 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 3 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Экспериментальный пример 7: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP12 человека
Действие соединений по ингибированию MMP12 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 50 мкг/мл рекомбинантного фермента MMP12 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 4 или 24 часов. ММР12 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 17 или 5,2 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 5 или 14 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Результаты ингибирующего действия соединение по изобретению на ферментную активность MMP12 человека показаны в следующей таблице.
[Таблица 52]
Экспериментальный пример 8: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP13 человека
Действие соединений по ингибированию MMP13 человека определяют с помощью ферментативного анализа с использованием MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 150 ммоль/л NaCl, 10 ммоль/л CaCl2, 0,05% Brij L23], смешивают 50 мкг/мл рекомбинантного фермента MMP13 человека и 1 ммоль/л ацетата 4-аминофенилртути и подвергают взаимодействию при 37°C в течение 2 часов. ММР13 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 5 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут. Затем добавляют MOCAc-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 6 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения
Результаты ингибирующего действия соединение по изобретению на ферментную активность MMP13 человека показаны в следующей таблице.
[Таблица 53]
Экспериментальный пример 9: Оценочный тест ингибирующего действия соединений по настоящему изобретению на MMP14 человека
Действие соединений по ингибированию MMP14 человека определяют с помощью ферментативного анализа с использованием MOCAc-Lys-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 в качестве субстрата. В реакционном растворе [50 ммоль/л Tris-HCl (pH 7,5), 200 ммоль/л NaCl, 5 ммоль/л CaCl2, 20 мкмоль/л ZnSO4, 0,05% Brij L23], смешивают 100 мкг/мл рекомбинантного фермента MMP14 человека и 5 мг/мл трипсина. После взаимодействия при комнатной температуре в течение 25 минут добавляют ингибитор трипсина для достижения 25 мкг/мл, тем самым останавливая реакцию. ММР14 человека, активированную в ходе реакции, выливают в 96-луночный микропланшет для достижения конечной концентрации 6 нг/мл. Кроме того, соединения по настоящему изобретению, которые были разведены до различных концентрации, добавляют и выстаивают при комнатной температуре в течение 15 минут.Затем добавляют MOCAc-Lys-Pro-Leu-Gly-Leu-A2pr(Dnp)-Ala-Arg-NH2 до достижения конечной концентрации 5 мкмоль/л и инициируют ферментативную реакцию. После взаимодействия при комнатной температуре в течение 1 часа измеряют интенсивность флуоресценции (Ex 320 нм/Em 400 нм) с помощью микропланшетного ридера. Степень ингибирования фермента (%) рассчитывают с помощью измеренных значений флуоресценции в соответствии со следующей формулой, и рассчитывают 50% ингибирующие концентрации (значения IC50) соединений по изобретению.
Степень ингибирования фермента (%)=[1-(A-B)/(C-B)] * 100
A: Значение флуоресценции с добавлением соединения
B: Значение флуоресценции без добавления соединения и фермента.
C: Значение флуоресценции без добавления соединения/
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Соединения по настоящему изобретению обладают превосходным эффектом ингибирования MMP2, и настоящее изобретение может обеспечить фармацевтический продукт, эффективный для профилактики или лечения ракового заболевания и фиброза органов и симптомов, связанных с раковым заболеванием и фиброзом органов, и, как ожидается, уменьшит нагрузку на пациентов, тем самым способствуя к развитию фармацевтической промышленности.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> TAISHO PHARMACEUTICAL CO., LTD.
<120> ПОЛИПЕПТИД, ИМЕЮЩИЙ ММР-2 ИНГИБИРУЮЩЕЕ ДЕЙСТВИЕ
<130> FA0061-20155
<150> JP 2019-203338
<151> 2019-11-08
<160> 47
<170> PatentIn version 3.5
<210> 1
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-1]: Соединение № 1-39
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-(d)-Glu, бета-Asp, бета-(d)-Asp или гамма-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu, Val, Ile, Phe или Trp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Glu, (N-Me)Ile, (N-Me)Val, (N-Me)Leu, (N-Me)Phe, (N-Me)Tyr,
(N-Me)Ser, Pro, (N-Me)Asp или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape, бета-гомоPro, Pro, (d)-Pro, бета-Ala, GABA, Acp, Lys,
(d)-Lys, Arg, (d)-Arg или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь, Pro, Lys, (d)-Lys, Arg, (d)-Arg (d)-Lys-(d)-Lys
<400> 1
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 2
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-2]: Соединение № 40
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь
<400> 2
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 3
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-3]: Соединение № 41
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь
<400> 3
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 4
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-4]: Соединение № 42
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь
<400> 4
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 5
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-5]: Соединение № 43
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь
<400> 5
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 6
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-6]: Соединение № 44
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь
<400> 6
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 7
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-7]: Соединение № 45-55
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> бета-(d)-Asp, гамма-(d)-Glu или гамма-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (2S,4S)-(4-амино)Pro, (S)-пиперазин, (2S,4R)-(4-амино)Pro,
(2S,4S)-(4-гидрокси)Pro или (2S,4R)-(4-гидрокси)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (N-Me)Ile или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ape или бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> одинарная связь
<400> 7
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 8
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-8]: Соединение № 56-91
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA, (N-Me)GABA или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn, (N-Me)Asn, Glu, Gln, (d)-Ser, гомоSer, (d)-Thr или Arg
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala, Dap, Dab или Orn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met, (N-Me)Val, (N-Me)Ile, Glu, (N-Me)Glu или гомоGlu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro или Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь, (d)-Lys или (d)-Arg
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2 или -OH
<400> 8
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 9
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-9]: Соединение № 92-156
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA или (N-Me)GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (N-Me)Ala, (N-Me)Asn, Asn, (d)-Asn, (N-Me)Gly, Aze(2), Pro,
гомоPro, (N-Me)Val, (N-Me)Leu, (N-Me)Ile, (N-Me)Met, (d)-Lys,
(N-Me)Phe, (N-Me)Asp, (N-Me)Glu, (N-Me)Lys, Gln, (N-Me)Tyr,
(N-Me)Trp, (N-Me)Thr, Val, Glu или Orn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala, Dab, Dap или Dap(Me)
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile, (N-Me)Glu или (N-Me)Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Aib, Pro или бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 9
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 10
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-10]: Соединение № 157-160
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-Glu или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Adox или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Adox или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (10)..(10)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (11)..(11)
<223> бета-гомоPro
<400> 10
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<210> 11
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-9]: Соединение № 161-176
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA, Ape или Adox
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn, Gln, (d)-Ser, Glu или (d)-Thr
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu или (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь, (d)-Lys или (d)-Arg
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2 или -OH (только соединение № 161)
<400> 11
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-9]: Соединение № 177-201
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA, Ape или Acp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn, Lys, Arg или Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met, (N-Me)Glu или (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro или бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 12
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 13
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-11]: Соединение № 202
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 13
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 14
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-12]: Соединение № 203-205
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Acp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn, Gln или Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 14
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 15
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-13]: Соединение № 206-209
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Acp или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn, Gln или Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 15
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 16
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-14]: Соединение № 210-315
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA, бета-Ala, Ape, эпсилон-Lys, эпсилон-(d)-Lys, Acp, Adox,
гамма-Dab, дельта-(d)-Orn, гамма-(d)-Dab, бета-Dap, бета-(d)-Dap
или -NH-(CH2)2-O-CH2-CO-
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn, Val, Glu, Orn, (N-Me)Asn, Gln, (d)-Asn, (d)-Gln, (d)-Ser,
(d)-Ala, Phe, (d)-Phe, Tyr, (d)-Tyr, бета-Dap, бета-(d)-Dap,
бета-Ala, Dab, Dap, (d)-Dab, Aze(2), (N-Me)Glu, (N-Me)Ile или
(N-Me)Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab, Dap, Dap(Me), Dab(Me) или Dab(Me)2
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu, (N-Me)Ile, (N-Me)Asp или (N-Me)Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> NH2, OH, NHEt, пиперидин-1-ил, NHMe, азетидин-1-ил,
пирролидин-1-ил, (4-OH)пиперидин-1-ил, NH-(CH2)2-OH или
(3-OH)азетидин-1-ил
<400> 16
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 17
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-15]: Соединение № 316-317
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn или (d)-Ser
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 17
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 18
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-14]: Соединение № 318-586
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Ape, -NH-(CH2)2-O-CH2-CO-, Adox, GABA, Acp, дельта-Orn,
эпсилон-(d)-Lys или эпсилон-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (N-Me)Glu, Thr, (d)-Thr, (d)-Pro, Trp, (N-Me)Leu, (N-Me)Met,
(d)-Trp, His, (d)-His, Cys, (d)-Cys, Arg, (d)-Arg, (d)-Glu,
(d)-Ser, Lys(Ac), Cit, (d)-Cit, бета-Asp, бета-(d)-Asp, Lys, Met,
одинарная связь, (N-Me)Gln, Asn, (N-Me)Arg, (d)-Lys, Gln, Glu, Ala,
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Dap, Dab или Gly
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp, аспартимид или бета-Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab, Dap или Aze(2)
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu, Phe или Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile, (N-Me)Glu, Dap, Dab, Orn, (N-Me)Arg, (N-Me)Lys,
одинарная связь, (N-Me)Val, (N-Me)Ala или (N-Me)Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro, одинарная связь, Pro, Arg, Lys, бета-Ala, GABA, Ape,
His, (d)-Arg, (d)-Lys, Dap, Dab, Orn, гомоPro,
(2S,4R)-(4-амино)Pro, бета-Dap, бета-(d)-Dap, гамма-Dab,
дельта-Orn, дельта-(d)-Orn, эпсилон-Lys, эпсилон-(d)-Lys, Aze(2),
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> (d)-Aze(2), (N-Me)бета-Ala, Acp или гамма-(d)-Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь, (d)-Lys-(d)-Lys-(d)-Lys, (d)-Lys, (d)-Arg, Lys, Arg,
Arg-Arg, (d)-Arg-(d)-Arg, Lys-Lys, (d)-Lys-(d)-Lys, бета-Ala или
GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2, -OH, -NH-(CH2)2-NH2, -NH-(CH2)4-NH2 или -NH-(CH2)5-NH2
<400> 18
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 19
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-16]: Соединение № 587-589
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> бета-Ala или GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Met или (N-Me)Val
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 19
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 20
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-17]: Соединение № 590
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 20
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 21
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-18]: Соединение № 591
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 21
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 22
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-19]: Соединение № 592
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 22
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 23
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-20]: Соединение № 593
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 23
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 24
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-21]: Соединение № 594-595
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp или гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala или (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 24
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 25
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-22]: Соединение № 596
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 25
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 26
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-23]: Соединение № 597
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 26
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 27
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-24]: Соединение № 598
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 27
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 28
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-25]: Соединение № 599
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 28
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 29
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-26]: Соединение № 600-601
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Asn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 29
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 30
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-27]: Соединение № 602-605
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dap или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu или (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 31
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-28]: Соединение № 606
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -OH
<400> 31
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 32
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-29]: Соединение № 607
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -OH
<400> 32
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 33
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-30]: Соединение № 608
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 33
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 34
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-31]: Соединение № 609
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 34
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 35
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-32]: Соединение № 610-633
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp или гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala, Dap, Dab, Orn или (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Ala(2-Pyr) или Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Met, (N-Me)Ile или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Pro, бета-гомоPro, Ape или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 35
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 36
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-32]: Соединение № 634-642
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala, Dap или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu или (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 36
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 37
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-33]: Соединение № 643
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -OH
<400> 37
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 38
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-34]: Соединение № 644-690
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь или Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp, бета-Asp, гамма-Glu, гамма-(d)-Glu или Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dap, Dab или (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu, (N-Me)Ile или (N-Me)Val
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2 или -OH
<400> 38
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 39
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-34]: Соединение № 691-704
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp или гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dap или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu или (N-Me)Ile
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> -NH2
<400> 39
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 40
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-35]: Соединение № 705-791
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp, гамма-(d)-Glu или гамма-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dap, Dab, Ala, (S)-пиперазин или (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu или Nle
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu, (N-Me)Ile, Lys(CO-(CH2)10-CO2H), Lys(CO-(CH2)12-CO2H),
Lys(CO-(CH2)14-CO2H), гомоSer, (N-Me)Val, (N-Me)Leu или (N-Me)Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro, одинарная связь, Ala, Thr, Phe, Lys, бета-Ala, GABA,
Ape, Acp, бета-Dap, бета-(d)-Dap, гамма-Dab, гамма-(d)-Dab,
дельта-Orn, эпсилон-Lys, эпсилон-(d)-Lys, (4)Abz, Pro или
дельта-(d)-Orn
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь, (d)-Lys, (d)-Arg, (d)-Arg-(d)-Lys,
(d)-Arg-(d)-Arg, (d)-Lys-(d)-Arg или (d)-Lys-(d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> NH2, NH-(CH2)2-NH2, NH-(CH2)3-NH2, NH-(CH2)4-NH2, NH-(CH2)5-NH2,
(4-Me)пиперазин-1-ил, морфолин-4-ил, [VI-8], [VI-16], [VI-18] или
OH
<400> 40
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 41
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-36]: Соединение № 792-890
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> бета-(d)-Asp, гамма-(d)-Glu или гамма-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dap, Dab, (S)-пиперазин, Pro или (2S,4S)-(4-амино)Pro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Leu, Ala(cПропил), Ala(4-Thz), Ile, Val или Tyr
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Glu, (N-Me)Ile, (N-Me)Val, (N-Me)Leu, одинарная связь,
(N-Me)Ser, (N-Me)Tyr, (N-Me)Phe, (N-Me)Ala, (N-Me)Asp, (N-Me)Lys,
Gly, (d)-Arg, (d)-Pro, (d)-Ser, (d)-Tyr, (d)-Phe, (d)-Ala,
(d)-Thr, (N-Me)Arg, (d)-(N-Me)Glu или Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro, Ape, Acp, гамма-Dab, бета-(d)-Dap, дельта-Orn,
дельта-(d)-Orn, эпсилон-Lys, эпсилон-(d)-Lys, Pro, бета-Ala, GABA,
бета-Dap, Aze(2), (d)-Aze(2), Aze(3), cis-NH(3)cPen,
одинарная связь или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> одинарная связь, (d)-Lys, (d)-Arg, (d)-Arg-(d)-Lys,
(d)-Arg-(d)-Arg, (d)-Lys-(d)-Lys, (d)-Lys-(d)-Arg, Gly-(d)-Lys,
Gly-(d)-Arg, Gly-(d)-Arg-(d)-Arg, Gly-(d)-Lys-(d)-Arg,
бета-Ala-(d)-Lys, бета-Ala-(d)-Arg-(d)-Lys,
бета-Ala-(d)-Arg-(d)-Arg,
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> бета-Ala-(d)-Lys-(d)-Arg, Gly-(d)-Arg-(d)-Lys,
Gly-(d)-Lys-(d)-Lys или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> NH2, [VI-14] или OH
<400> 41
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 42
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-37]: Соединение № 891-899
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> перекрестно сшитый с Lys в положении 5 через Gly, GABA или
бета-Ala
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Ala или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile или (N-Me)Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> -OH или -NH2
<400> 42
Xaa Glu Asp Xaa Lys Xaa Xaa Xaa
1 5
<210> 43
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-38]: Соединение № 900-911
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> гамма-Glu, Lys или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> Adox, Lys или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> Adox, Lys или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Lys или (d)-Lys
<220>
<221> MOD_RES
<222> (4)..(4)
<223> GABA
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Ala или Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> (N-Me)Ile или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> бета-гомоPro
<400> 43
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 44
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-39]: Соединение № 912-955
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> (d)-Lys, гамма-Glu, Lys, Arg, (d)-Arg, Adox или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> (d)-Lys, Adox, одинарная связь, Lys, Arg или (d)-Arg
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> (d)-Lys, Adox, одинарная связь, Lys, Arg, (d)-Arg или гамма-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Одинарная связь или (d)-Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Одинарная связь или (d)-Lys
<220>
<221> MOD_RES
<222> (6)..(6)
<223> GABA или Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> Asp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> Leu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (10)..(10)
<223> (N-Me)Ile, (N-Me)Asp или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (11)..(11)
<223> бета-гомоPro
<400> 44
Xaa Xaa Xaa Xaa Xaa Lys Xaa Xaa Xaa Xaa Xaa
1 5 10
<210> 45
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'-40]: Соединение № 956-972
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> Dab
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> (N-Me)Ile или (N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> бета-гомоPro
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> (d)-Lys или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> (d)-Lys или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (10)..(10)
<223> Lys или (d)-Lys
<220>
<221> MOD_RES
<222> (10)..(10)
<223> (d)-Lys или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (11)..(11)
<223> (d)-Lys или одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (12)..(12)
<223> (d)-Lys или одинарная связь
<400> 45
Xaa Glu Asp Xaa Leu Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<210> 46
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I'] указанная в п.1
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> L(N1):-C(=O)- или -S(=O)2-
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> W(1):L1 или L1'-L1''; L1 представляет собой одинарную связь, и
L1' представляет собой одинарную связь, бета-Ala, GABA,
(N-Me)GABA, Ape, Acp, [III-6], [III-7], [III-8], [III-9],
[III-10], [III-11], [III-12], [III-13], [IV-23] или [IV-24]
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> W(1):L1 или L1'-L1''; L1'' представляет собой одинарную связь,
Gly, (N-Me)Gly, Ala, (N-Me)Ala, (d)-Ala, Val, (N-Me)Val,
(N-Me)Leu, (N-Me)Ile, [IV-27], Pro, (d)-Pro, гомоPro, Phe,
(N-Me)Phe, (d)-Phe, His, (d)-His, Trp, (N-Me)Trp, (d)-Trp, Tyr,
(N-Me)Tyr, (d)-Tyr,
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> W(1):L1 или L1'-L1''; L1'' представляет собой Thr, (N-Me)Thr,
(d)-Thr, Cys, (d)-Cys, Met, (N-Me)Met, (N-Me)Asp, Glu, (N-Me)Glu,
(d)-Glu, Asn, (N-Me)Asn, (d)-Asn, Gln, (N-Me)Gln, (d)-Gln, Arg,
(N-Me)Arg, (d)-Arg, Cit, (d)-Cit, [IV-7], [IV-9], [IV-10],
[IV-13], Lys,
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> W(1):L1 или L1'-L1''; L1'' представляет собой (N-Me)Lys, (d)-Lys,
[IV-14], бета-Ala、бета-Asp、бета-(d)-Asp, [III-6], [III-7],
(d)-Ser или гомоSer
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> AA1: Asp, бета-Asp, бета-(d)-Asp, гамма-Glu или гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> L2: одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> AA2: Ala, [IV-7], [IV-8], [IV-9], [IV-11], [IV-12], [IV-13],
[IV-27], Pro, [II-1] или [II-2]
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> AA3: Val, Leu, Ile, [IV-2], Phe, Trp, Tyr, Lys, [IV-3], [IV-4],
[IV-5] или [IV-9]
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> AA4: Одинарная связь, Gly, (d)-Ala, (N-Me)Ala, (N-Me)Val,
(N-Me)Leu, (N-Me)Ile, Pro, (d)-Pro, (N-Me)Phe, (d)-Phe, (N-Me)Tyr,
(d)-Tyr, (N-Me)Ser, (d)-Ser, гомоSer, (d)-Thr, Met, (N-Me)Met,
(N-Me)Asp, Glu, (N-Me)Glu, (d)-(N-Me)Glu, гомоGlu, (N-Me)Asn,
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> AA4: ... (N-Me)Arg, (d)-Arg, [IV-7], [IV-9], [IV-13], Lys или
(N-Me)Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> AA5: Одинарная связь, Ala, [IV-1], [IV-27], [IV-28], [IV-29], Pro,
(d)-Pro, бета-гомоPro, гомоPro, [II-1'], Phe, His, Thr, Arg,
(d)-Arg, [IV-7], [IV-9], [IV-13], Lys, (d)-Lys, бета-Ala,
(N-Me)-бета-Ala, GABA, Ape, Acp, [III-6], [III-7], [III-8],
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> AA5: ...[III-9], [III-10], [III-11], [III-12], [III-13], [IV-25]
или[IV-26]
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> Wc: одинарная связь или линкер, состоящий из 1 - 3 аминокислот,
где 1 - 3 аминокислолты могут быть одинаковыми или разными, и
выбраны из группы, состоящей из Gly, Pro,
Arg, (d) -Arg, Lys, (d) -Lys, бета-Ala, GABA и Ape
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (10)..(10)
<223> Rc: -OH, -NH2, C1-6 алкиламино или 4-7-членный насыщенный
гетероциклил, содержащий один азот и, необязательно, один
гетероатом.
<400> 46
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<210> 47
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> пептидная цепь [I] указанная в п. 8
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> L(N1):-C(=O)- или -S(=O)2-
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (2)..(2)
<223> L1: одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (3)..(3)
<223> AA1: бета-Asp, гамма-Glu или гамма-(d)-Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (4)..(4)
<223> L2: одинарная связь
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> AA2: [II-1] или [II-2]
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> AA3: Val, Leu, Ile, Phe или Trp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (7)..(7)
<223> AA4: Одинарная связь, Pro, (N-Me)Ala, (N-Me)Val, (N-Me)Leu,
(N-Me)Ile, (N-Me)Phe, (N-Me)Tyr, (N-Me)Ser, (N-Me)Asp или
(N-Me)Glu
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (8)..(8)
<223> AA5: Одинарная связь, Pro, (d)-Pro, бета-гомоPro, Arg, (d)-Arg,
Lys, (d)-Lys, бета-Ala, GABA, Ape или Acp
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (9)..(9)
<223> Lc: одинарная связь, Pro, Arg, (d) -Arg, Lys, (d) -Lys или (d)
-Lys-(d) -Lys
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (10)..(10)
<223> Rc: -OH или -NH2
<400> 47
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОАГОНИСТЫ РЕЦЕПТОРОВ ГЛЮКАГОНА И GLP-1 ДЛИТЕЛЬНОГО ДЕЙСТВИЯ | 2018 |
|
RU2779314C2 |
| СОЕДИНЕНИЯ-АГОНИСТЫ GIP И СПОСОБЫ | 2015 |
|
RU2716985C2 |
| НОВЫЕ АНТИ-PD-L1 АНТИТЕЛА | 2017 |
|
RU2744959C2 |
| НОВЫЕ АНТИ-PD-L1 АНТИТЕЛА | 2017 |
|
RU2776121C2 |
| ПЕПТИДНЫЕ ИНГИБИТОРЫ РЕЦЕПТОРА ИНТЕРЛЕЙКИНА-23 ДЛЯ ПЕРОРАЛЬНОГО ПРИЕМА И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ КИШЕЧНИКА | 2015 |
|
RU2736637C2 |
| ИСКУССТВЕННЫЕ НЕИЗБИРАТЕЛЬНЫЕ ЭПИТОПЫ КЛЕТОК Т-ХЕЛПЕРОВ КАК ИММУННЫЕ СТИМУЛЯТОРЫ ДЛЯ СИНТЕТИЧЕСКИХ ПЕПТИДНЫХ ИММУНОГЕНОВ | 2019 |
|
RU2839585C2 |
| ВАРИАНТЫ СВИНОГО G-CSF И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2823074C2 |
| БЛОКАТОРЫ Kv1.3 | 2020 |
|
RU2825633C1 |
| КОНСТРУКЦИИ, ИМЕЮЩИЕ SIRP-АЛЬФА ДОМЕН ИЛИ ЕГО ВАРИАНТ | 2016 |
|
RU2740672C2 |
| СУБСТРАТЫ МАТРИКСНОЙ МЕТАЛЛОПРОТЕИНАЗЫ И ДРУГИЕ РАСЩЕПЛЯЕМЫЕ ФРАГМЕНТЫ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2832636C2 |
Изобретение относится к замещенному полипептиду формулы I’-B, где AA1-AA5, WC, RC определены в формуле изобретения, или его фармацевтически приемлемой соли, который обладает ингибирующим действием MMP2. Также предложены фармацевтический препарат, ингибитор MMP2 и лекарственное средство, обладающее ингибирующей MMP2 активностью. 4 н. и 1 з.п. ф-лы, 53 табл., 9 пр.

1. Замещенный полипептид, представленный формулой [I'-B]:
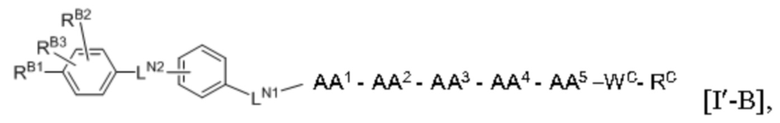
или его фармацевтически приемлемая соль,
где
AA1 представляет собой β-(d)-Asp или γ-(d)-Glu;
AA2 представляет собой группу, представленную формулой [II-1]:
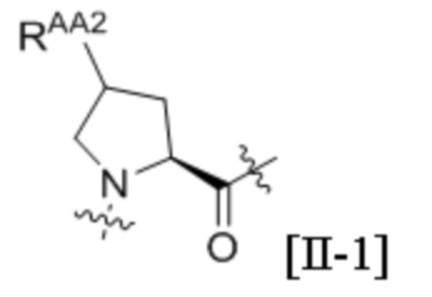
или группу, представленную формулой [IV-7] или [IV-9]:
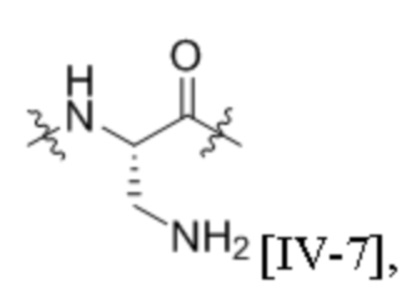
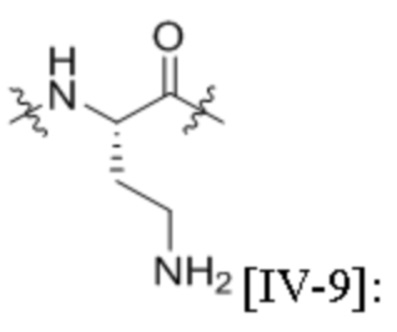
где RAA2 представляет собой амино,
AA3 представляет собой Val, Leu или Ile,
AA4 представляет собой (N-Me)Ile или (N-Me)Glu,
AA5 представляет собой β-Ala, GABA, Ape, Acp или β-гомоPro,
LN1 представляет собой формулу -C(=O)- или формулу -S(=O)2-,
LN2 представляет собой формулу -O- или формулу -C(=O)-NH-,
RB1 представляет собой карбамоил, атом хлора, атом брома, метокси или трифторметокси,
RB2 представляет собой атом водорода,
RB3 представляет собой атом водорода,
представляет собой атом водорода,
WC представляет собой одинарную связь или (d)-Lys, и
RC представляет собой формулу -NH2.
2. Замещенный полипептид или его фармацевтически приемлемая соль по п. 1, где замещенный полипептид выбран из соединений, показанных в следующих:
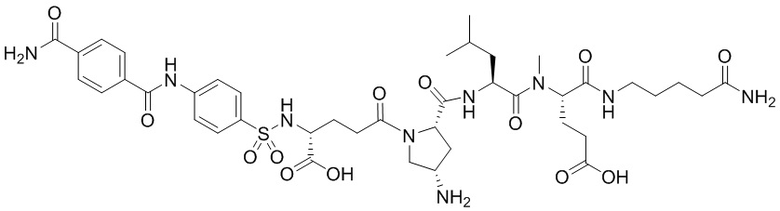 ,
,
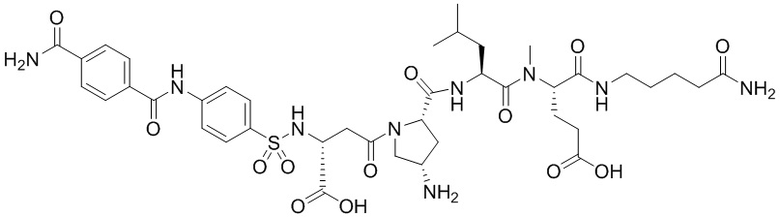 ,
,
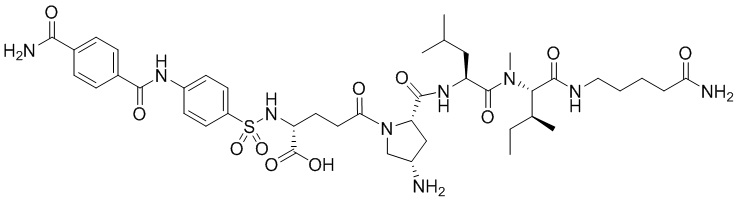 ,
,
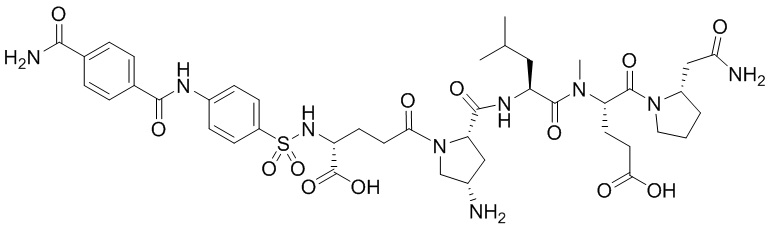 ,
,
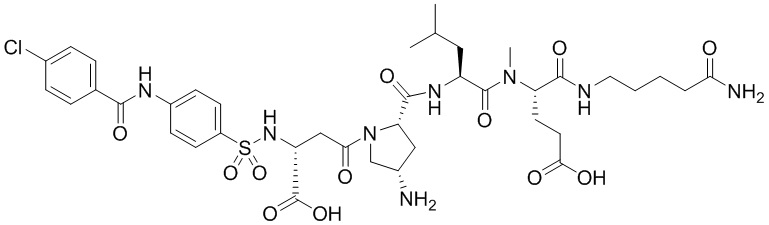 ,
,
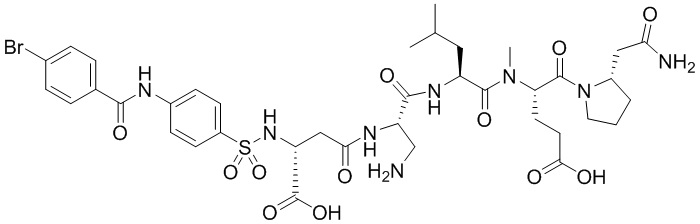 ,
,
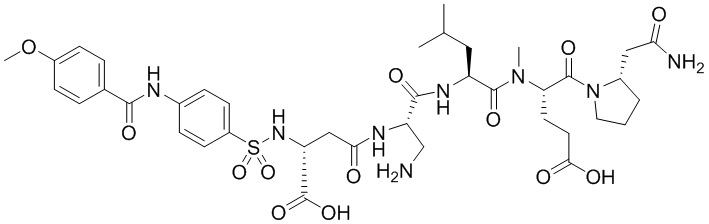 ,
,
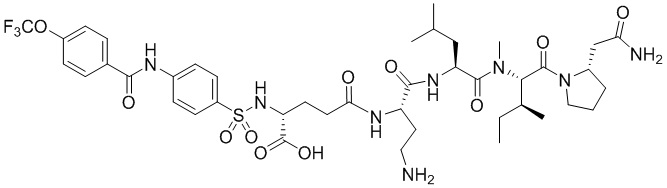 ,
,
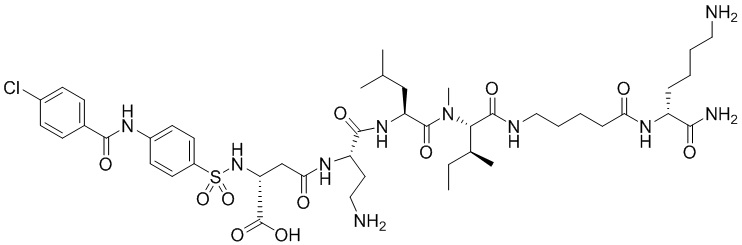 ,
,
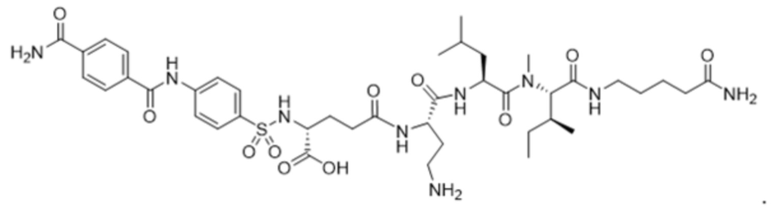
3. Фармацевтический препарат, обладающий ингибирующей MMP2 активностью, содержащий замещенный полипептид или его фармацевтически приемлемую соль по п. 1 или 2 в качестве активного ингредиента.
4. Ингибитор MMP2, содержащий замещенный полипептид или его фармацевтически приемлемую соль по п. 1 или 2 в качестве активного ингредиента.
5. Лекарственное средство, обладающее ингибирующей MMP2 активностью, для профилактики или лечения ракового заболевания или фиброза органов, или симптома, связанного с раковым заболеванием или фиброзом органов, содержащее замещенный полипептид или его фармацевтически приемлемую соль по п. 1 или 2 в качестве активного ингредиента.
| US 20110171133 A1, 14.07.2011 | |||
| SANTOS, M | |||
| AMELIA et al., "Design, synthesis and molecular modeling study of iminodiacetyl monohydroxamic acid derivatives as MMP inhibitors", Bioorganic & Medicinal Chemistry, 2006, vol | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| ПРИСПОСОБЛЕНИЕ К ТКАЦКОМУ СТАНКУ ДЛЯ ВТАЛКИВАНИЯ В ЧЕЛНОК ШПУЛИ | 1926 |
|
SU7539A1 |
| HIGASHI, SHOUICHI et al., "Identification of a Region of beta-Amyloid Precursor Protein Essential for Its | |||
Авторы
Даты
2024-10-08—Публикация
2020-11-06—Подача