Настоящее изобретение относится к области лечения кариеса, в частности минимально-инвазивного или неинвазивного лечения разрушения зубов. Оно относится к композиции и набору, содержащему самособирающийся пептид, например, самособирающийся пептид P11-4 или P11-8, и стоматологическое вещество, а именно стоматологический герметик, например, герметик на основе цемента, например, герметик на основе стеклоиономерного цемента или герметик на основе полимера, фтористый лак, или связывающее вещество, или другой реставрационный стоматологический материал. Изобретение, кроме того, относится к композиции и набору, содержащему самособирающийся пептид и стоматологическое вещество, для использования в лечении кариозного поражения, предпочтительно кариозного поражения, протекающего с образованием полости. Кариозные поражения могут представлять собой первичный или вторичный кариес. Первичный кариес не связан с предыдущей реставрацией. И наоборот, вторичный кариес определяется как поражение, связанное со стоматологическими реставрациями или герметиками. В контексте изобретения самособирающийся пептид препятствует вторичному кариесу после разрушения стоматологического вещества, используемого в лечении кариеса, сопровождающегося образованием полости, особенно в случае нарушения взаимодействия между реставрацией, выполненной с помощью стоматологического вещества, и зубом. Композиция и набор по настоящему изобретению могут также использоваться для защитного покрытия пульпы.
Разрушение зуба, также известное как зубной кариес, представляет собой одну из наиболее распространенных бактериальных инфекций в мире. Он представляет собой разложение зубного вещества из-за бактериальных метаболитов, главным образом, кислот, производимых бактериями, когда они разрушают пищевые остатки или сахар на поверхности или в биопленке зубов. Это приводит к нарушению равновесия между процессами деминерализации и реминерализации. Твердые структуры зубов, то есть, эмаль, дентин и цемент, повреждаются при постоянной деминерализации, что приводит к кариозным повреждениям и, в конечном итоге, к появлению кариозных полостей. Наиболее ранним сигналом нового кариозного повреждения является появление меловидного белого пятна на поверхности зуба, так называемого поражения по типу белого пятна (также называемого начальным кариозным поражением), то есть подповерхностное поражение. При прогрессировании деминерализации минерализованная поверхность поражения (частично) разрушается, и образуется микрополость или полость, отверстие в зубе. Это называется (частично) кариозным поражением, протекающим с образованием полости, или кариозным поражением, протекающим с образованием полости.
Были описаны подходы к профилактике кариеса, включающие в себя местное лечение фторидами и применение стоматологических герметиков, также известных как герметики для ямок и фиссур. Применение герметика заключается во введении герметиков в ямки и/или фиссуры склонных к кариесу зубов. Основными типами герметизирующих материалов на рынке в настоящее время являются герметики на основе полимера и герметики на основе стеклоиономерного цемента (Naaman и др., 2017, Dent J., 5, 34). Свойство высвобождения фторидов рассматривается как одно из преимуществ стеклоиономерных цементов (Sidhu и Nicholson, 2016, J Funct Biomater, 7, 16), которые, таким образом, объединяют реминерализующее действие фторида и защитное действие герметиков на ямках и фиссурах.
На сегодняшний день лечение кариеса обычно зависит от того, имеется или нет кариозная полость при кариозном поражении. Неинвазивные подходы предложены для некариозных поражений, протекающих с образованием полости, то есть подповерхностных поражений. Например, предпринимаются попытки реминерализации посредством аппликации фторида на место поражения.
Кроме того, производные эмалевой матрицы или самособирающиеся пептиды продемонстрировали эффективность в реминерализации подповерхностных кариозных поражений (Ruan и др., 2013. Acta Biomater.9 (7): 7289-97; Ruan и др. , 2014. J Vis Exp. 10 (89), doi 10.379151606; Schmidlin и др., 2016, J Appl Oral Sci. 24 (1), 31-36; Alkilzy и др., 2018, Adv Dent Res. 29 (1), 42-47; Brunton и др., 2013, Br Dent J, 215:E6; Kind и др., 2017, J Dent Res., 96 (7), 790-797; Kirkham и др., 2007, J Dent Res., 86, 426-430). В патентной заявке WO 2014/027012 A1 описан способ целевой доставки самособирающегося пептида к подповерхностному зубному поражению с целью реминерализации кариозных поражений (Alkilzy и др., 2018, см. выше) обнаружили дополнительное действие аппликации P11-4, самособирающегося пептида, на начальные кариозные поражения, в сочетании с фторидами, по сравнению со фторидом самим по себе.
Подход к восстановлению зуба на основе биоминерализации, основанной на амелогенине, был описан в контексте гиперчувствительности дентина, отбеливания или осветления зубов, и при лечении кариеса в патентных заявках WO 2017/123986 A1, 2014/0186273 A1 и 2017/0007737 A1.
В патентной заявке WO 2017/168183 A1 биоподобная минерализованная апатитная структура, основанная на эластино-подобных пептидах, описана для использования в качестве стоматологического реставрационного материала, в частности, для восстановления эмали и для использования при лечении стоматологических заболеваний, например, зубного кариеса.
Кроме того, для реминерализации эмали и профилактики и/или лечения кариеса или эрозии зуба были разработаны стратегии на основе казеина (например, патентные заявки WO 00/06108 A1 и WO 2010/042754 A2). Казеиновые фосфопептидные аморфные кальцийфосфатные комплексы (CPP-ACP) и CPP-стабилизированные аморфные кальцийфторидфосфатные комплексы описаны в сочетании со стеклоиономерным цементом в качестве реминерализующих стоматологических реставрационных материалов, например, в патентной заявке WO 02/094204 A1. Некоторые исследования также показали, что прогрессирование кариеса замедляется или прекращается под герметиками, при наложении на кариозные поражения, протекающие без образования полости (Griffin S.O. и др., 2008, J Dent Res., 87 (2), 169-174).
Как только при кариозном поражении образуется полость и возникает отверстие в зубе, общее лечение, применяемое на сегодняшний день, является инвазивным, поскольку реминерализация при этой стадии является значительно более затруднительной, чем для кариозных поражений, протекающих без образования полости. Разрушенные ткани обычно удаляются посредством использования, например, стоматологического наконечника ("сверла"). Альтернативно для удаления зубного кариеса могут использоваться лазер, экскаватор или химико-механическая система.
После удаления (то есть экскавации) поврежденной кариесом эмали утраченная зубная ткань требует стоматологической реставрации с использованием стоматологических реставрационных материалов, например, герметиков, амальгамы, стоматологических композитов, керамики или золота. Это традиционное инвазивное лечение кариеса, протекающего с образованием полости, связано с рядом недостатков.
Во-первых, естественная зубная ткань серьезно повреждается, поскольку во время процесса удаления поврежденной зубной ткани также удаляется здоровая зубная ткань. Процесс удаления кариозной ткани обычно связан с болью и тревогой, которые обычно должны облегчаться посредством применения местных анестетиков. Кроме того, из-за удаления пораженной кариесом эмали затрагивается соседняя зубная ткань.
Кроме того, реставрации, в частности герметиками или композитами, часто оказываются неудачными, и пломбу в конечном счете приходится переделывать, что приводит к дополнительной потере зубной ткани. Неудача может быть связана с наличием или образованием щелей между зубом и реставрацией, и/или герметик частично или полностью выпадает. Такая неудача часто связана со вторичным кариесом (также называемым повторным кариесом или CARS (кариес рядом с реставрациями и герметиками)). Место пломбирования является уязвимым для дальнейшего повреждения (Burke и Lucarotti 2018. Полное руководство по долговечности реставраций в Англии и Уэльсе. Часть 3: Стеклоиономерные реставрации - время до следующего вмешательства и удаления реставрированного зуба. Br Dent J. 224 (10): 789-800; Nedeljkovic и др., 2015. Dental Materials 31 (11): 247-277).
Таким образом, существует необходимость в усовершенствованном лечении кариеса, протекающего с образованием полости, преодолевающем по меньшей мере некоторые из указанных недостатков способов предшествующего уровня техники, в частности, не допускающем развития вторичного кариеса. Эта проблема решается посредством настоящего изобретения, в частности, объекта изобретения согласно формуле. Авторы настоящего изобретения неожиданно обнаружили, что самособирающиеся пептиды могут эффективно использоваться в сочетании с традиционными стоматологическими веществами, а именно, стоматологическим герметиком, например, стеклоиономерным цементом, фтористым лаком или связывающим веществом, для преимущественного лечения кариозных поражений, протекающих с образованием полости.
Настоящее изобретение, таким образом, относится к композиции, содержащей (a) самособирающийся пептид и (b) стоматологическое вещество, выбранное из группы, состоящей из стоматологического реставрационного материала, например, стоматологического герметика, фтористого лака и связывающего вещества, при этом предпочтительно указанное стоматологическое вещество представляет собой стоматологический герметик, например, герметик на основе цемента, наиболее предпочтительно - герметик на основе стеклоиономера. Композиция может представлять собой фармацевтическую композицию.
Предпочтительно в композиции по изобретению самособирающийся пептид и стоматологическое вещество находятся в гомогенно смешанном виде. "Гомогенно смешанный" означает, что указанная композиция представляет собой смесь из этих компонентов. Таким образом, композиция по настоящему изобретению предпочтительно имеет в основном одинаковые пропорции своих компонентов в любом данном образце.
Кроме того, настоящее изобретение обеспечивает набор, содержащий (a) самособирающийся пептид и (b) стоматологическое вещество, при этом указанное стоматологическое вещество представляет собой герметик на основе стеклоиономера. Указанный набор может представлять собой фармацевтический набор.
Указанный набор содержит компоненты композиции по настоящему изобретению в раздельном виде, например, в раздельных баночках, флаконах, шприцах, аппликаторах или других контейнерах. В наборе по настоящему изобретению самособирающийся пептид может содержаться в композиции, которая может, кроме того, содержать растворитель, например, воду и/или буфер. Альтернативно могут использоваться неполярные или полярные органические растворители. В контексте изобретения, если не указано иное, слово в единственном числе интерпретируется как означающее "один или более". Набор может также содержать дополнительные компоненты, например, более одного из стоматологических веществ, определенных в настоящем документе. Например, набор может содержать, помимо самособирающегося пептида, композит и связывающее вещество, подходящее для связывания с композитом. Дополнительные необязательные компоненты представляют собой, например, вещество для травления и/или буфер, способный обеспечивать кальций, фторид и/или фосфат.
Набор по настоящему изобретению может содержать (a) композицию, содержащую самособирающийся пептид и (b) по меньшей мере одно стоматологическое вещество, как определено в настоящем документе, при этом указанная композиция и указанное стоматологическое вещество находятся в раздельном виде. Альтернативно, указанный самособирающийся пептид и указанный растворитель, например, вода, могут находиться в раздельном виде, например, в отдельных отсеках аппликационного устройства (например, таких, как предлагаемый на рынке Curodont® Repair, credentis AG, Windisch, CH). Самособирающийся пептид может быть в высушенном, буферизованном виде, как описано в патентной заявке WO 2014/027012.
"Композиция или набор, содержащий самособирающийся пептид" означает, что композиция может содержать один тип самособирающихся пептидов или два или более, например, три, четыре или пять и т.д. различных типов самособирающихся пептидов. Например, как подробно описано ниже, указанная композиция может содержать два комплементарных пептида, которые в сочетании самособираются.
Термин "содержащий" при использовании в настоящем документе включает в себя значение "состоящий из".
Настоящее изобретение дополнительно обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) стоматологическое вещество, как определено в настоящем документе, для использования в лечении кариозного поражения. Кариозное поражение предпочтительно представляет собой кариозное поражение, протекающее с образованием полости, более предпочтительно активное кариозное поражение, например, активное кариозное поражение, протекающее с образованием полости, при этом указанная композиция или набор предпочтительно представляет собой композицию или набор по настоящему изобретению, например, набор, содержащий самособирающийся пептид и стоматологический герметик.
Изобретение также обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) стоматологическое вещество, выбранное из группы, состоящей из стоматологического герметика, фтористого лака и стоматологического связывающего вещества, для использования в профилактике вторичного кариеса после неудачного лечения стоматологическим веществом при лечении кариозного поражения, протекающего с образованием полости. Предпочтительно, стоматологическое вещество представляет собой стоматологический герметик, предпочтительно, герметик на основе стеклоиономерного цемента.
В контексте настоящего изобретения термин "кариес" (или "кариозное поражение") относится к локализованной деструкции твердых зубных тканей кислотными побочными продуктами бактериальной ферментации поступающих с пищей углеводов. Кариес может быть определен как микробное заболевание кальцифицированных тканей зубов, характеризующееся деминерализацией неорганической части и деструкцией органических веществ зуба. Указанный термин включает в себя, например, кариес эмали, кариес цемента и кариес дентина. В контексте изобретения подвергаемые лечению поражения представляют собой обычно кариозные поражения эмали. Кариозные поражения могут подразделяться на не образующие полости, или подповерхностные кариозные поражения, и кариозные поражения, протекающие с образованием полости. Кариозные поражения, подлежащие лечению по изобретению, могут представлять собой первичные или вторичные кариозные поражения.
Термин "кариозное поражение, протекающее с образованием полости" относится к кариозному поражению, которое приводит к тому, что зубная поверхность перестает быть интактной, то есть имеет место по меньшей мере частичное разрушение поверхности зубной ткани в области кариозного поражения, например, отверстие, например, локализованное разрушение эмали.
Существуют индексы, используемые в стоматологии для бальной оценки тяжести и активности кариозных поражений. В контексте настоящего изобретения предпочтительно используется клиническая система бальной оценки ICDAS (Международная система обнаружения и оценки кариеса), предпочтительно система ICDAS-II. Информацию по бальной оценке и критерию активности кариозных поражений согласно ICDAS-II можно найти, например, в Dikmen (2015, J Istanbul Univ Fac Dent 49 (3): 63-72) или по ссылке www.icdas.org. В общих чертах стадии ICDAS-II описывают стоматологический статус следующим образом: ICDAS-II стадия 0: неповрежденный; ICDAS-II стадия 1: первое видимое изменение в эмали; ICDAS-II стадия 2: выраженное изменение в эмали; ICDAS-II стадия 3: локализованное разрушение эмали (без клинически заметных признаков вовлечения дентина); ICDAS-II стадия 4: подлежащая темная зона от дентина; ICDAS-II стадия 5: выраженная полость с видимым дентином; ICDAS-II стадия 6: обширная выраженная полость с видимым дентином. Система ICDAS также используется для оценки активности поражения (LAA), которая обычно основывается на объединенном знании клинического вида поражения, есть или нет поражение в области накопления бляшки, и тактильное ощущение, когда шаровидный на конце зонд WHO осторожно проходит по поверхности зуба. Дополнительная информация о LAA может быть найдена, например, в статье Ekstrand и др. (2007, Oper Dent. 32 (3): 225-235) или статье Nyvad и др., 2018. Caries Res. 52 (5): 397-405).
В предпочтительном варианте осуществления композиция или набор для использования по настоящему изобретению предназначен для использования при лечении кариозного поражения стадии 3-6 по ICDAS-II, например, стадии 3 по ICDAS-II, стадии 4 по ICDAS-II, стадии 5 по ICDAS-II или стадии 6 по ICDAS-II, предпочтительно стадий 3-5, еще более стадий 3-4 по ICDAS-II. Предпочтительно кариозное поражение представляет собой активное кариозное поражение.
Обнаружение и оценка кариозного поражения может выполняться посредством традиционных способов обнаружения и оценки кариеса. Например, широко используется визуальный осмотр, например, с помощью зонда, например, зонда с шаровидным концом, или радиографические способы или сочетание перечисленного. В контексте настоящего изобретения "кариозное поражение, протекающее с образованием полости," может представлять собой кариозное поражение, которое может быть обнаружено с помощью зонда с шаровидным концом, например, зонда, имеющего на конце сферу диаметром 0,5 мм (например WHO-зонд). Информацию по диагностике и оценке кариозных поражений зубов можно обнаружить, например, в статье Braga и др. (2010, Dent Clin N Am 54: 479-493).
Таким образом, например, настоящее изобретение обеспечивает композицию, содержащую (a) самособирающийся пептид и (b) стоматологическое вещество, как определено в настоящем документе, для использования в лечении кариозного поражения, например, стадии 1, 2, 3, 4 или 5 по ICDAS-II, предпочтительно кариозного поражения, протекающего с образованием полости, более предпочтительно кариозного поражения стадии 3, 4 или 5 по ICDAS-II, еще более предпочтительно кариозного поражения стадии 3 или 4 по ICDAS-II. Кроме того настоящее изобретение обеспечивает, например, набор, содержащий (a) самособирающийся пептид и (b) стоматологический герметик на основе стеклоиономерного цемента для использования при лечении кариозного поражения, протекающего с образованием полости, то есть, кариозного поражения стадии 3, 4, 5 или 6 по ICDAS-II, более предпочтительно кариозного поражения стадии 3, 4 или 5 по ICDAS-II, еще более предпочтительно кариозного поражения стадии 3 или 4 по ICDAS-II, при этом предпочтительно кариозное поражение является активным.
Профилактика вторичного кариеса после неудачного лечения кариозного поражения, протекающего с образованием полости, с использованием стоматологического вещества, означает снижение частоты возникновения вторичного кариеса. Вторичный кариес обычно возникает под реставрациями или у краев реставраций. Неудачное лечение с использованием стоматологического вещества может быть связано с наличием или образованием щелей между стоматологическим веществом, использованным для реставрации кариозного поражения, протекающего с образованием полости, (частичная неудача). Оно может также представлять собой истирание или выпадение стоматологического вещества или реставрации частично или полностью (полная неудача). В одном варианте осуществления лечение, как описано в настоящем документе, не только снижает частоту возникновения вторичного кариеса после неудачного лечения с использованием стоматологического вещества, но также увеличивает время до частичной или полной неудачи в использовании стоматологического вещества, поскольку вторичный кариес, например, на краях реставрации, также может вызвать такую неудачу. Это, однако, не является обязательным, и достаточно того, что не допускается вторичный кариес после частичного или полного неудачного использования стоматологического вещества.
Реставрации классически изготовленные с помощью стоматологических веществ, определенных в настоящем документе, обычно приходят в негодность через относительно короткий промежуток времени, что в уровне техники часто связывают со вторичным кариесом. Например, фтористый лак обычно удерживается до 3 дней при условиях, имеющихся в полости рта, включая истирание при жевании. В защищенных областях лак может также оставаться дольше. Герметики, например, герметики на основе стеклоиономерного цемента, обычно медленно приходят в негодность течение 2-10 лет. Связывающие вещества обычно используются для связывания реставрации, например, композита, или коронки, с зубной поверхностью. Негодность связывающего вещества и реставрации обычно связаны друг с другом. Период времени до прихода в негодность стоматологического вещества также зависит от нескольких факторов, помимо материала, а именно, от пациента (например, история обширного стоматологического лечения в связи с частым неудачным лечением), гигиены, технической квалификации стоматолога, расположения и т.д.
В контексте изобретения заявители обнаружили, что сочетание стоматологического вещества с самособирающимся пептидом не допускает вторичного кариеса, поэтому при неудачном лечении с использованием стоматологического вещества, например, образовании щели между реставрацией из стоматологического вещества или истиранием/выпадением стоматологического вещества или реставрации, связанной с зубом стоматологическим веществом, матрица, образованная самособирающимся пептидом, которая обеспечивает реминерализацию, защищает зуб от развития вторичного кариеса. Реминерализация матрицы, образованной самособирающимся пептидом, уже может начинаться, когда зуб (то есть, полость) контактирует с самособирающимся пептидом, и, в зависимости от доступности ионов (например, выходящих из стоматологического материала и/или слюны), под покрытием из стоматологического материала. В любом случае при неудачном лечении с использованием стоматологического материала, например, когда образуется щель между материалом и зубом, матрица, образованная самособирающимися пептидами, может реминерализоваться и защищать зуб от вторичного кариеса. Самособирающийся пептид может также собираться вокруг краев реставрации, выполненной с помощью стоматологического материала, и защищать эти места, которые также имеют высокий риск развития вторичного кариеса.
Если указанный самособирающийся пептид и указанное стоматологическое вещество смешиваются, стоматологическое вещество может дополнительно служить резервуаром отсроченного высвобождения самособирающегося пептида.
Предварительная обработка самособирающимися пептидами использовалась для увеличения силы сцепления на деминерализованном дентине (Barbosa-Martins и др., 2018. J Mech Behav Biomed Mater 81:214-221). Из уровня техники известно, что связывание реставраций, в частности, композитов с дентином является проблематичным, поскольку, по сравнению с эмалью, в качестве органического компонента присутствует коллаген, и содержание воды в дентине значительно выше, и концентрация ионов значительно меньше, чем в эмали. Barbosa-Martins и др. проверяли, увеличивает ли предварительная обработка самособирающимися пептидами сцепление для двух адгезионных систем, Adper Single Bond (SB) и Clearfil SE Bond (CSE). Оба вещества представляют собой композиты на основе полимера. Преимущества были обнаружены для сцепления с SB, но не с CSE. Предполагается, что это происходит из-за того, что SB требует протравливания фосфорной кислотой, что, как предполагается, улучшает сборку самособирающегося пептида. И наоборот, CSE представляет собой самопротравливающуюся систему, у которой pH значительно ниже. Из-за значительных различий поверхностей дентина и эмали, эта публикация обеспечивает вывод только для поражений дентина, но не для поражений эмали. Поражения эмали являются предпочтительными для данного изобретения. Указанная публикация также не содержит указаний, применимы ли указанные результаты также к стоматологическим веществам, отличным от композитов. В одном варианте осуществления изобретения стоматологическое вещество не является композитом на основе полимера. В действительности другие стоматологические вещества, например, герметики на основе стеклоиономерного цемента, имеют преимущественные свойства в сочетании с самособирающимися пептидами, как описано в настоящем документе.
Стоматологические вещества, как определено в настоящем документе, хорошо известны специалисту в данной области техники, и они обычно имеются на рынке. Стоматологические вещества включают в себя стоматологические герметики, стоматологические лаки, например, фтористые лаки, и стоматологические связывающие вещества. Таким образом, настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) стоматологическое вещество, выбранное из группы, состоящей из стоматологических реставрационных материалов, например, стоматологических герметиков, стоматологических лаков и стоматологических связывающих веществ (в случае набора-герметик на основе стеклоиономерного цемента), предпочтительно для использования в лечении кариозного поражения стадии 1-6 по ICDAS-II, более предпочтительно для использования при лечении кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадии 3, 4 или 5 по ICDAS-II, как описано выше, в частности, для использования в профилактике вторичного кариеса.
Стоматологическое вещество, используемое в настоящем изобретении, может содержать кислотный полимер, выбранный из группы, содержащей акрилат и метакрилат, иономер, гиомер, ормокер® и любой другой подходящий полимер и/или его мономерную форму. Предпочтительно, указанное стоматологическое вещество содержит компоненты, которые способны полимеризоваться, например, в кариозном поражении, протекающем с образованием полости, или перед заполнением такого поражения. Таким образом, компоненты стоматологического вещества могут первоначально находиться в мономерном виде и могут образовывать реставрацию (в частности, в случае герметика) или защитный слой (в частности, в случае лака), или использоваться для связывания реставрации (в частности, в случае связывающего вещества) при полимеризации указанных мономерных компонентов. Указанное стоматологическое вещество может представлять собой материал, подходящий для отверждения видимым светом, самополимеризующийся материал или материал, подходящий для отверждения УФ-светом, предпочтительно, материал, подходящий для отверждения видимым светом.
В одном варианте осуществления настоящего изобретения стоматологическое вещество представляет собой стоматологический лак, например, фтористый лак. Фтористые лаки хорошо известны специалисту в данной области техники и представлены на рынке. Традиционный фтористый лак обычно содержит фторид в виде соли или силанового препарата в высокой концентрации в адгезивном растворе, например, в быстро сохнущем спирте и растворе на основе полимера. Концентрация, вид фторида и способ подачи различается в зависимости от производителя. Обычные концентрации составляют 2,5-5% фторида натрия или приблизительно 1% дифторсилана, например, в полиуретане, полиакрилате, канифоли или шеллачной основании. Лаки могут содержать CPP-ACP, например, MI Varnish (GC, Japan). Дополнительно подходящие фтористые лаки включают в себя, например, суспензию Durophat® (Gaba Schweiz AG), Profluoride Varnish и Bifluorid 12 (Voco, Cuxhaven, Германия), Fluor Protector (Ivoclar/Vivadent, Amherst NY), Duraflor (PharmaScience, Монреаль, Канада), CavityShield (OMNII Oral Pharmaceuticals, West Palm Beach, Флорида, США) и Carex (Voss,Норвегия). Информацию по фтористым лакам можно найти, например, у Chu и Lo (Gen Dent. Jul-Aug 2006; 54 (4): 247-253).
В предпочтительном варианте осуществления стоматологическое вещество представляет собой стоматологический герметик. Стоматологические герметики, также известные как герметики для ямок и фиссур, хорошо известные специалисту в данной области техники, широко используются в области стоматологии и имеются на рынке. Информацию по стоматологическим герметикам можно обнаружить, например, в Naaman и др. (Dent J. 2017, 5, 34). В контексте настоящего изобретения стоматологические герметики могут быть выбраны из группы, содержащей герметики на основе стеклоиономерного цемента, герметики на основе полимера и модифицированные керамические материалы (например, Ormocer®). Герметики на основе стеклоиономерного цемента содержат стеклоиономерные цементы, полимер-модифицированные стеклоиономерные цементы. Герметики на основе полимера содержат поликислотно-модифицированные композитные полимеры (также называемые "компомерами") и композиты на основе полимеров (также называемые композитными полимерами), например, текучие композитные полимеры.
Предпочтительно, указанный стоматологический герметик представляет собой герметик на основе цемента, в частности, герметик на основе стеклоиономерного цемента. Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) герметик на основе стеклоиономерного цемента, например, стеклоиономерный цемент, полимер-модифицированный стеклоиономерный цемент или материал стеклоиономерного типа. Указанная композиция или набор может использоваться при лечении кариозного поражения, например, стадий 1-6 по ICDAS-II. Герметики обычно используются для лечения некариозных поражений, протекающих с образованием полости, и могут использоваться с этой целью в сочетании с самособирающимися пептидами, например, P11-4, в смешанном виде или в виде набора, при этом самособирающийся пептид может наноситься первым, после чего следует нанесение герметика.
Настоящее изобретение дополнительно открывает возможность лечения кариозных поражений, протекающих с образованием полости, например, стадии 3-5 по ICDAS-II, в частности, 3-4, с помощью герметиков на основе стеклоиономерного цемента в сочетании с самособирающимися пептидами, например, P11-4. Преимущество этого состоит в том, что в сочетании с самособирающимся пептидом не допускается вторичного кариеса (или снижается частота возникновения вторичного кариеса).
Стеклоиономерные цементы принадлежат к классу материалов, известных как цементы на основе кислоты, и они широко используются в области стоматологии и доступны на рынке. Информацию по стеклоиономерным цементам можно найти, например, у Sidhu и Nicholson (J Funct Biomater. 2016, 7, 16). Термин "стеклоиономерный цемент" и "стеклоиономер" используются взаимозаменяемым образом. Другой термин, который используется для стеклоиономерных цементов в стоматологии - это "стеклополиалкеноатный цемент". Основная часть ингредиентов стеклоиономерного цемента составляют полимерная водорастворимая кислота, щелочное (выщелачиваемое) стекло и вода. Полимеры, обычно используемые в стеклоиономерных цементах, представляют собой полиалкеновые кислоты. Стекло, используемое для стеклоиономерных цементов, является щелочным стеклом и, таким образом, способно реагировать с кислотой с образованием соли, например, часто используется алюмосиликатное стекло со фтористыми и фосфатными добавками. Представленное на рынке стекло для стеклоиономерных цементов обычно основано на соединениях кальция и стронция и содержит фторид. Стеклоиономерные цементы обычно затвердевают в течение 2-3 минут от начала смешивания посредством кислотно-основной реакции и прикрепляются к зубной поверхности посредством химического связывания за счет ионных связей, образуемых между карбоксилатными группами на молекулах поликислоты и ионах кальция в зубной поверхности.
В контексте настоящего изобретения "Glass Carbomer®" (GCP Dental, Нидерланды) также охватывается термином "герметик на основе стеклоиономерного цемента". Он представляет собой новый коммерческий материал стеклоиономерного типа, который включает в себя вещества, которые часто не включаются в стеклоиономерные соединения, например, силиконовое масло, содержащее полидиметилсилоксан. Аналогично, "Activa" представляет собой вулканизированный стеклоиономерный цемент на основе герметика и также охватывается термином "герметик на основе стеклоиономерного цемента".
Полимер-модифицированные стеклоиономерные цементы могут также использоваться в качестве стоматологического герметика по настоящему изобретению. Эти материалы содержат такие же главные компоненты, что и традиционные стеклоиономеры (порошок щелочного стекла, вода, поликислота), но также включают в себя мономерный компонент и связанную инициирующую композицию. Мономер обычно представляет собой 2- гидроксиэтилметакрилат (HEMA), а инициатор может представлять собой карбохинон или другие подходящие фотоинициаторы.
В другом варианте осуществления в качестве стоматологического герметика по настоящему изобретению используются герметики на основе полимера, то есть стоматологические герметики на полимерной основе. Герметики на основе полимера хорошо известны в области стоматологии и обычно основаны на олигомерной матрице, содержащей компоненты, такие как Bisphenol A-гликодилметакрилат (bisGMA), уретандиметакрилат (UDMA) или другие диметакрилатные мономеры (например, TEGMA или HDDMA), или на полукристаллической поликерамике (PEX). Они могут подразделяться на четыре поколения, в зависимости от способа полимеризации. Первое поколение полимеризовалось под действием ультрафиолетовых лучей. Второе поколение представляло собой самополимеризующиеся герметики на основе полимера или химически отверждаемые герметики. В этом случае третичный амин (активатор) добавляется к одному компоненту и смешивается с другим компонентом. Реакция между этими двумя компонентами создает свободные радикалы, которые инициируют полимеризацию полимерного герметизирующего материала. Третье поколение содержит полимеризуемые видимым светом герметики на основе полимера, таким образом, видимый свет, обычно в диапазоне длины волны приблизительно 470 нм, активирует фотоинициаторы (например, как объяснено в настоящем документе), которые присутствуют в герметизирующем материале. Четвертое поколение герметиков на основе полимера представляют собой фтористые герметики на основе полимера, которые являются продуктом, получающимся в результате добавления фторвысвобождающих частиц в традиционные герметики на основе полимера. Герметики на основе полимера могут быть наполненными или ненаполненными, то есть герметики на основе полимера могут содержать наполнитель, например, как описано для композитов на основе полимера в настоящем документе. Обычно ненаполненные герметики на основе полимера демонстрируют более низкую вязкость. Подходящие, доступные на рынке герметики на основе полимера включают в себя Clinpro™ (3M-ESPE, St. Paul, MN, США), Delton® FS (Dentsply-De Trey, Konstanz, Германия), Estiseal® F (Heraerus-Kulzer, Hanau, Германия) и Guardian Seal™ (Kerr, Orange, CA, США). Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) герметик на основе полимера, например, для использования при лечении кариозного поражения. Герметики на основе полимера обычно используются для лечения некариозных поражений, протекающих с образованием полости, и могут использоваться с этой целью в сочетании с самособирающимися пептидами, например, P11-4.
Настоящее изобретение дополнительно открывает возможность лечения кариозных поражений, протекающих с образованием полости, например, стадий 3-5 по ICDAS-II, в частности, 3-4, с помощью герметиков на основе полимера в сочетании с самособирающимися пептидами, таким как P11-4. Указанное преимущество состоит в том, что в сочетании с самособирающимся пептидом не допускается вторичный кариес (или снижается частота возникновения вторичного кариеса).
При использовании в настоящем документе "герметики на основе полимера" также включают в себя композиты на основе полимера, предпочтительно, текучие композиты на основе полимера (также известные как текучие полимерные композиты). Таким образом, композиты на основе полимера, предпочтительно текучие композиты на основе полимера, могут использоваться в настоящем изобретении в качестве стоматологических герметиков или профилактических полимерных реставраций. В настоящем документе термины "композиты на основе полимера" и "композитные полимеры" используются взаимозаменяемым образом. Композиты на основе полимера представляют собой типы синтетических полимеров, которые широко используются в стоматологии в качестве реставрационного материала, стоматологических адгезивов и герметиков. Традиционные композиты на основе полимера содержат олигомерную матрицу на основе полимера и наполнитель, например, на основе стекла или керамических материалов. В качестве олигомерной матрицы на основе полимера используются, например, бисфенол A-глицидилметакрилат (bisGMA), уретандиметакрилат (UDMA) или другие диметакрилатные мономеры (например, TEGMA или HDDMA), или полукристаллическая поликерамика (PEX). Стеклянные наполнители обычно изготавливаются из кристаллического кварца, диоксида кремния, литий/барий-алюминиевого стекла или боросиликатного стекла, содержащего цинк/стронций/литий. Керамические наполнители включают в себя оксид циркония-оксид кремния и оксид циркония. Композитные полимеры обычно также содержат инициирующую систему, например, фотоинициатор, например, камфорохинон, фенилпропандион (PPD) и люкрин (TPO). Эти инициирующие системы начинают реакцию полимеризации полимеров при применении синего света. Они представляют собой также химически отвержаемые полимерные композитные системы (также известные как "самополимеризующиеся " герметики на основе полимера), обычно выпускаемые в виде системы из 2 паст (базовая и катализатор), которые начинают твердеть при смешивании указанных базы и катализатора. Могут добавляться различные добавки, например, для управления скоростью реакции или физическими характеристиками стоматологических композитных полимеров, например, диметилгликсомин, который может добавляться для достижения определенной текучести. Материалы для стоматологических композитов демонстрируют возможность адгезии к зубной структуре за счет микромеханического связывания, которое усиливается посредством кислотного протравливания. Очень высокая прочность соединения с зубной структурой может достигаться посредством дополнительного нанесения стоматологических связывающих веществ.
Композиты на основе полимера могут подразделяться по способу обращения с ними на категории "текучий" и "пакуемый". Обычно текучие полимерные композиты демонстрируют содержание наполнителя ниже 60% по объему, например, около 35-55% по объему. Пакуемые полимерные композиты обычно демонстрируют более высокое содержание наполнителя, например, выше 60% по объему. Текучие полимерные композиты в целом демонстрируют более низкую вязкость и, следовательно, подходящие смачивающие свойства и легкую обрабатываемость по сравнению с пакуемыми композитами на основе полимера.
Подходящие имеющиеся на рынке композитные полимеры включают в себя, например, Metafil (Sun Medical, Moriyama, Япония), Heliomolar® (Ivoclar-Vivadent, Лихтенштейн), Solitaire® (Heraeaus Kulzer, Hanau, Германия), Arabesk (Vocvo, Cuxhaven, Германия), и Charisma® (Heraeaus Kulzer, Hanau, Германия). Примерами подходящих имеющихся на рынке текучих полимерных композитов являются Admira® Flow (Voco, Cuxhaven, Германия), Filtek™ Supreme (3M-ESPE, St. Paul, MN,США), FlowLine (Heraeus-Kulzer, Hanau, Германия), Grandio® Flow (Voco, Cuxhaven, Германия), Point-4™ Flowable (Kerr, Orange, CA,США), Premise™ Flowable (Kerr, Orange, CA,США), Revolution™ Formula 2 (Kerr, Orange, CA,США) и X-Flow™ (Dentsply-De Trey, Konstanz, Германия). Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) композит на основе полимера, предпочтительно текучий композит на основе полимера, предпочтительно для использования при лечении кариозного поражения, более предпочтительно для использования при лечении кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадий 3, 4 или 5 по ICDAS-II, как описано в настоящем документе.
Герметики на основе полимера, при использовании в настоящем документе, также включают в себя поликислотно-модифицированные полимерные композитные полимеры (также называемые "компомеры"). Таким образом, стоматологический герметик, используемый в настоящем изобретении, может представлять собой поликислотно-модифицированный композитный полимер (также именуемый "компомер"). Компомеры имеют сходство с традиционными композитными полимерами, в том, что их реакция отверждения представляет собой обычно добавочную полимеризацию, в том, что они не содержат воды, и в том, что большинство компонентов являются идентичными. Обычно они представляют собой объемные макромономеры, например, бисглицедидиловый эфир диметакрилат (bisGMA) или его производные, и/или уретандиметилакрилат, который смешивается со снижающими вязкость растворителями, например, триэтиленгликольдиметакрилатом (TEGDMA). Эти полимерные системы наполнены нереактивными неорганическими порошками, например, кварцем или силикатным стеклом, например, SrAlFSiO4. Эти порошки обычно покрыты силаном для содействия соединению между наполнителем и матрицей в отвержденном материале. Компомеры обычно содержат добавочные мономеры, которые отличаются от таковых в традиционных композитах, которые содержат кислотные функциональные группы, например, диэфир 2-гидроксиметилметакрилата в бутантетракарбоксиловой кислоте (TGB). Реакция отверждения обычно является светозапускаемой, но существуют также системы, где отверждение происходит в результате смешивания двух паст, каждая из которых содержит компонент свободно радикальной инициирующей системы. Примеры подходящих представленных на рынке компомеров включают в себя Ana Compomer (Nordiska Dental, Швеция), Dyract® (Dentsply, Konstanz, Германия), Compoglass® (Ivoclar-Vivadent, Лихтенштейн), F2000 Compomer (3M-ESPE, St. Paul's, MN, США), Freedom (SDI, Bayswater, Victoria, Австралия), Hytac® (3M-ESPE, Seefeld, Германия), MagicFil (Zenith, Englewood, NJ,США), Twinky Star (Voco, Cuxhaven, Германия). Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) поликислотно-модифицированный композитный полимер, предпочтительно, для использования при лечении кариозного поражения, более предпочтительно для использования при лечении кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадий 3, 4 или 5 по ICDAS-II, как описано в настоящем документе.
В другом варианте осуществления стоматологическое вещество, используемое в настоящем изобретении, представляет собой стоматологическое связывающее вещество, также называемое "дентин-связывающими веществами". Стоматологические связывающие вещества хорошо известны в области стоматологии и обычно представляют собой полимерные материалы, которые традиционно используются для обеспечения прочной адгезиии стоматологического композитного пломбировочного материала как с дентином, так и с эмалью. Стоматологические связывающие вещества часто представляют собой метакрилаты с некоторым летучим носителем и растворителем, подобным ацетону или этанолу/воде. В качестве адгезивов обычно используются BisGMA или TEGMA. Нанесение стоматологических веществ обычно требует использования протравок, например, фосфорной кислоты, лимонной кислоты/хлорида кальция, или щавелевой кислоты/нитрата алюминия и т.д., использования праймера, например, NTG-GMMA/BPDM, HEMA/GPDM или 4META. Существуют доступные стоматологические связывающие системы, которые объединяют все необходимые компоненты в одной композиции. Другие обеспечивают компоненты по отдельности. Подходящие имеющиеся на рынке стоматологические связывающие вещества включают в себя 3M™ Scotchbond™ Universal Adhesive (3M ESPE, St. Paul, MN,США), ACE® ALL-BOND (BISCO Dental Products, Schaumburg, IL,США), Admira Bond (VOCO, Cuxhaven, Германия), Адгезив 7 поколения BeautiBond (Shofu Dental Corporation, Ratingen, Германия), CLEARFIL SE Bond 2 (Kuraray America Inc., Houston, TX,США), Futurabond U (VOCO, Cuxhaven, Германия), G-Premio BOND™ (GC America Inc., Alisp, IL,США), и Prelude™ (Zest Dental Solutions, Carlsbad, CA,США).Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид и (b) стоматологическое связывающее вещество, предпочтительно для использования при лечении кариозного поражения, более предпочтительно для использования при лечении кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадии 3, 4 или 5 по ICDAS-II, как описано в настоящем документе.
В настоящей заявке может использоваться более одного типа стоматологического вещества. Например, набор по настоящей заявке может содержать стоматологический герметик на основе стеклоиономерного цемента и фтористый лак. Таким образом, например, при использовании такого набора для лечения кариозного поражения самособирающийся пептид может наноситься сначала на указанную необязательно очищенную и/или обработанную зубную поверхность, например, поверхность кариозного поражения (или перед фтористым лаком или в одной композиции со фтористым лаком), а стеклоиономерный цемент может наноситься после аппликации фтористого лака.
В одном варианте осуществления изобретения фтористый лак не наносится.
В контексте настоящего изобретения предпочтительно, что указанное стоматологическое вещество, например, стеклоиономерный цемент, кальций-силикатный цемент, поликислотно-модифицированный композитный полимер или герметик на основе полимера, способно высвобождать фториды. В особенно предпочтительном варианте осуществления стоматологическое вещество способно высвобождать кальций и фторид. Например, стеклоиономерные цементы имеют оба свойства, поскольку они основаны на порошке кальцийалюмофторсиликатного стекла или стронциевом стекле и кислоте, обычно полиакриловой кислоте. Стоматологическое вещество может также, или альтернативно, быть проницаемым для ионов, например, из слюны, в частности, после нанесения на зуб. Соответственно, вещества, присутствующие в слюне, такие как кальций или фосфаты, могут проникать в стоматологическое вещество. Эти две характеристики улучшают реминерализацию поверхности зуба, в частности полости, еще до выпадения стоматологического вещества, и, таким образом, улучшают защиту.
Существуют стоматологические вещества, например, стоматологические герметики, которые имеют щелочной pH, и существуют стоматологические вещества, например, стоматологические герметики, которые имеют нейтральный или кислый pH. pH стоматологического вещества может определяться перед отверждением материала, в частности, в водной среде. Например, многие цементы, например, Portland-цемент, являются щелочными. В контексте изобретения могут использоваться и щелочные, и нейтральные или кислотные стоматологические вещества, но это может влиять на тип используемого самособирающегося пептида, как более подробно объяснено ниже.
Portland-цемент является примером кальций-силикатного цемента, который может использоваться в контексте изобретения. Предпочтительно используется для дентинных реставраций в непосредственной близости к зубной пульпе из-за относительно длинного времени отверждения. Например, может использоваться минеральный триоксидагрегат (MTA), например, быстротвердеющий минерал триоксидагрегат, такой как Biodentine (Septodont, Saint Maur des Fosses, Франция), который отверждается в течение приблизительно 12 минут или меньше; Watson и др. , 2014. Dental Mater. 30 (1): 50-61).
Самособирающиеся пептиды, используемые в настоящем изобретении, представляют собой пептиды, способные к образованию трехмерных "каркасов", таким образом способствуя регенерации тканей. Они могут собираться в одном измерении с образованием бета-структуры, и в структуры более высокого порядка, например, в лентовидные сборки. Могут быть образованы трехмерные надмолекулярные структуры самособирающийся белков, которые имеют способность к связыванию с фосфатом кальция.
В контексте настоящего изобретения самособирающиеся пептиды могут быть способны самособираться сами по себе, как в случае, например, с пептидами P11-4, P11-8, P11-2, P11-5, упомянутыми ниже, но они могут альтернативно быть способны к самосборке в сочетании двух самособирающихся пептидов, как в случае, например, с пептидами P11-13/P11-14 и P11-28/P11-29, P11-30/ P11-31, упомянутыми ниже.
В контексте настоящего изобретения предпочтительны самособирающиеся пептиды, информация о которых находится в патентных заявках WO 2004/007532 A1, US10/521628, US12/729046, US13/551878, US 14/062768 или WO2014/027012 A1, которые полностью включены в настоящий документ посредством ссылки. В частности, самособирающиеся пептиды, имеющие суммарный заряд +2 или -2 при pH 7,5, могут использоваться в мономерном или собранном виде.
Самособирающиеся пептиды, используемые в настоящем изобретении, предпочтительно содержат последовательность формулы X1-X2-X1-X2-X1, при этом X1 представляет собой аминокислоту, имеющую кислую боковую цепь, а X2 представляет собой аминокислоту, имеющую гидрофобную боковую цепь. Например, самособирающийся пептид, использованный в настоящем изобретении, содержит обобщающую типичную последовательность SEQ ID NO: 1, X1-X2-X1-X2-X1,при этом X1 независимо выбиратся из группы, состоящей из глутаминовой кислоты, аспарагиновой кислоты, глутамина и орнитина, а X2 независимо выбирается из группы, состоящей из аланина, валина, изолейцина, лейцина, метионина, фенилаланина, тирозина, триптофана и глутамина, или аминокислотную последовательность по меньшей мере на 80% идентичную этой последовательности. Независимо выбранное означает, что, например, X1 в положениях 1, 3 или 5 последовательности, указанной выше, могут отличаться друг от друга. Разумеется, они также могут быть идентичны.
Предпочтительно, самособирающиеся пептиды, используемые в изобретении, содержат SEQ ID NO: 2, X1-X2-X1-X2-X1, при этом X1 независимо выбирается из группы, состоящей из глутаминовой кислоты и орнитина, а X2 независимо выбирается из группы, состоящей из триптофана и фенилаланина.
В дополнительном варианте осуществления самособирающиеся пептиды, используемые в изобретении, могут содержать SEQ ID NO: 3, X3-F-X1-W-X1-F-X1, при этом X1 независимо выбирается из группы, состоящей из глутаминовой кислоты и орнитина, а X3 выбирается из группы, состоящей из аргинина, глутаминовой кислоты и орнитина, при этом X3 предпочтительно представляет собой аргинин.
Кроме того, самособирающиеся пептиды, используемые в изобретении, могут содержать SEQ ID NO: 4 или, предпочтительно, состоять из: X4-X4-X3-F-X1-W-X1-F-X1-X4-X4, при этом X1 независимо выбирается из группы, состоящей из глутаминовой кислоты и орнитина, X3 выбирается из группы, состоящей из аргинина, глутаминовой кислоты и орнитина, а X4 независимо выбирается из группы, состоящей из глутамина, глутаминовой кислоты, серина, треонина и орнитина. X3 предпочтительно представляет собой аргинин. Независимо X4 предпочтительно представляет собой глутамин.
Самособирающиеся пептиды по изобретению могут содержать SEQ ID NO: 5, или, предпочтительно, состоять из: Q-Q-R-F-X1-W-X1-F-X1-Q-Q, при этом X1 независимо выбирается из группы, состоящей из глутаминовой кислоты и орнитина.
Предпочтительно, самособирающиеся пептиды, используемые в настоящем изобретении, содержат или состоят из последовательностей, выбранных из обобщающих типичных последовательностей, перечисленных ниже в Табл. 1.
Наиболее предпочтительно, указанные пептиды содержат определенные пептиды, перечисленные в Табл. 2, или соcтоят из них. Разумеется, самособирающиеся пептиды, собранные в сочетании с другим самособирающимся пептидом, например, как раскрыто в настоящем документе, могут быть включены в один наборе или в одну композицию.
Пептиды SEQ ID NO: 6, 9, 11, 12, 16 или 17 являются особенно предпочтительными, например, поскольку они могут использоваться в относительно низких концентрациях, они хорошо совместимы с клетками и имеют выгодное распределение заряда.
Предпочтительно самособирающийся пептид содержит последовательность SEQ ID NO: 6 или состоит из нее. Пептид, состоящий из последовательности SEQ ID NO: 6, также обозначается P11-4 и является предпочтительным для всего изобретения. В другом предпочтительном варианте осуществления самособирающийся пептид содержит последовательность SEQ ID NO: 9 или состоит из нее (P11-8).
Набор или композиция по изобретению может также содержать по меньшей мере один самособирающийся пептид, имеющий последовательность, по меньшей мере на 45% идентичную пептиду, состоящему из SEQ ID NO: 6. Предпочтительно, указанный пептид имеет последовательность, по меньшей мере на 54%, по меньшей мере на 63%, по меньшей мере на 72%, по меньшей мере на 81% или по меньшей мере на 90% идентичную пептиду, состоящему из SEQ ID NO: 6, или представляет собой указанный пептид. Пептиды по изобретению представляют собой, например, 11 аминокислот в длину.
Самособирающиеся пептиды могут представлять собой модифицированные пептиды, содержащие Ac-N-концевой остаток и/или NH2-C-концевой остаток, предпочтительно, оба, или немодифицированные пептиды. Поскольку неблокированные формы имеют тенденцию начинать реакцию деаминизации, концевые остатки всех самособирающихся пептидов последовательности SEQ ID NO: 1 предпочтительно блокируются для увеличения стабильности. В частности, пептиды последовательности SEQ ID NO: 6, 9, 11, 12, 16 и 17 могут содержать Ac-N-концевой остаток и NH2-C-концевой остаток. Последовательность SEQ ID NO: 18-29 соответствует модифицированным пептидам по изобретению.
Таблица 1: Обобщающие типичные последовательности предпочтительных самособирающихся пептидов
где X1 независимо выбирается из группы, состоящей из глутаминовой кислоты и орнитина, X3 выбирается из группы, состоящей из аргинина, глутаминовой кислоты и орнитина, X4 независимо выбирается из группы, состоящей из глутамина, глутаминовой кислоты, серина, треонина и орнитина. X3 предпочтительно представляет собой аргинин. Независимо X4 предпочтительно представляет собой глутамин.
Таблица 2: Предпочтительные самособирающиеся пептиды. Положения X1 подчеркнуты
Указанные самособирающиеся пептиды предпочтительно не имеют участков рестрикции для эндопептидаз пациента. Им также не нужно содержать специального мотива распознавания для клеток.
В одном варианте осуществления в наборе или композиции по настоящему изобретению самособирающийся пептид находится преимущественно в мономерном виде, например, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90% самособирающихся пептидов присутствуют в мономерном состоянии. С этой целью, если пептид собирается при pH около или ниже 7,5, pH указанной композиции может быть выше указанного pH, при этом пептиды начинают претерпевать самосборку (например, pH 7,5 для P11-4), предпочтительно, на 0,1-0,5 pH единиц выше указанного pH, или более чем на 0,5 pH единиц выше указанного pH. Указанный pH может буферизироваться, чтобы избежать быстрой аггрегации. Может быть выгодно, если аггрегация и образование гидрогеля начинается вскоре после нанесения на кариозную полость. Соответственно, указанный pH может быть на 0,1-0,5 pH единиц выше pH, при котором пептид начинает подвергаться самосборке без буферизации. В одном варианте осуществления указанная композиция может содержать высушенный пептид, например, полученный согласно WO 2014/027012.
В другом варианте осуществления набор или композиция по изобретению содержит самособирающиеся пептиды в преимущественно собранном виде, например, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90% присутствуют в собранном виде, или в основном в собранном виде, и буфер (при pH, стабилизирующем собранный вид). Собранный самособирающийся пептид обычно образует гидрогель.
Выбор состояния сборки белка зависит от нескольких факторов. Преимущественно мономерная форма самособирающегося пептида улучшает диффузию мономера в деминерализованную эмаль, и может быть особенно предпочтительна для меньших по размеру поражений, проходящих с образованием полости, например, поражений с частичным образованием полости или поражения с микрополостями (например, 1-3 по ICDAS). Преимущественно собранная форма может приводить к более быстрому действию пептида и, таким образом, улучшать функцию, в частности, для полостей большего размера (например, 4, 5 или 6 по ICDAS). Если самособирающийся пептид и стоматологическое вещество смешиваются, pH, который требуется стоматологическому веществу для отверждения, и ионная сила, обычно имеют решающее значение. В случае композиции, содержащей и стоматологическое вещество, и самособирающийся пептид, при соответствующем pH может использоваться или преимущественно мономерный самособирающийся пептид или преимущественно полимерный самособирающийся пептид.
Сочетания комплементарных самособирающихся пептидов, например, P11-4 и P11-8, обеспечивает значительно более быструю сборку, приводящую к более быстрому нанесению и стабильности из-за их притяжения друг к другу.
Например, по настоящему изобретению обеспечивается композиция или набор, содержащий (a) самособирающийся пептид, содержащий обобщающую типичную последовательность согласно SEQ ID Nos: 1-5, например, обобщающую типичную последовательность согласно SEQ ID NO: 1, предпочтительно обобщающую типичную последовательность по SEQ ID NO: 2, более предпочтительно обобщающую типичную последовательность согласно SEQ ID NO: 3, еще более предпочтительно обобщающую типичную последовательность согласно SEQ ID NO: 4, и наиболее предпочтительно обобщающую типичную последовательность согласно SEQ ID NO: 5, и (b) стоматологическое вещество, например, стоматологический герметик, предпочтительно герметик на основе стеклоиономерного цемента, например, для использования при лечении кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадии 4 или 5 по ICDAS-I, как описано выше. В частности это может быть использовано для профилактики вторичного кариеса.
В предпочтительном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид, содержащий, предпочтительно состоящий из, последовательность, выбранную из последовательностей согласно SEQ ID NO: 6-17 и 30-33, или последовательности, по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% идентичные указанной последовательности, предпочтительно последовательности согласно SEQ ID NO: 6 или последовательности по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% идентичной ей, и (b) стоматологическое вещество, например, стоматологический герметик, предпочтительно герметик на основе стеклоиономерного цемента, предпочтительно для использования при лечении кариозного поражения, как раннего, так и развившегося кариозного поражения, более предпочтительно для использования при лечении кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадии 3-5 по ICDAS-II, как описано выше. P-11 является наиболее предпочтительным для использования в контексте настоящего изобретения. В частности, он может использоваться для профилактики вторичного кариеса.
В особенно предпочтительном варианте осуществления настоящее изобретение обеспечивает композицию или набор, содержащий (a) самособирающийся пептид, содержащий, предпочтительно состоящий из, последовательность согласно SEQ ID NO: 6, и (b) герметик на основе стеклоиономерного цемента, предпочтительно для использования при лечении кариозного поражения, более предпочтительно для использования при лечении кариозного поражения стадий 3-5 по ICDAS-II, например, 4 или 5, как описано выше. В частности, он может использоваться для профилактики вторичного кариеса.
В контексте изобретения используемый самособирающийся пептид, например, P11-4, может подвергаться самосборке при низком pH, в частности, при pH ниже 7,5. Кариозные поражения обычно имеют кислый pH, который обеспечивает сборку самособирающегося пептида в месте поражения. Предпочтительным пептидом, который подвергается самосборке при низком pH, в частности, при pH ниже 7,5, является P11-4.
Выражение, что самособирающиеся пептиды (SAP) подвергаются самосборке при pH ниже 7,5, означает, что они обладают способностью к самосборке при pH ниже 7,5. Ионная сила также оказывает влияние на состояние сборки выбранного самособирающегося пептида. Предпочтительно, самособирающиеся пептиды, используемые в настоящем изобретении, способны к самосборке при pH ниже 7,5 и по меньшей мере физиологической ионной силе. Самособирающиеся пептиды способны к самосборке при pH ниже 7,5 и по меньшей мере при физиологической ионной силе могут начать подвергаться самосборке при указанном pH, как происходит, например, в случае с предпочтительным пептидом, P11-4, но это необязательно. Они могут также быть способны находиться в самособранном состоянии при более высоком или более низком pH.
Специалисту в данной области техники известно, как определить и измерить ионную силу раствора. Ионная сила I в целом вычисляется по формуле I=½∑ zi2bi, где z - валентность и bi - моляльная концентрация [mol/kg{H2O}] i-ой ионной концентрации. Суммирование ∑, берется по всем ионам в растворе. Например, ионная сила 150 мМольного раствора NaCl составляет приблизительно 0,15 моль/л. Это также приблизительно равно ионной силе крови. Ионная сила слюны, имеющейся в полости рта, обычно значительно ниже, например, приблизительно 0,04 моль/л. В контексте изобретения ионная сила в физиологическом диапазоне принимается соответствующей ионной силе, равной 0,15 моль/л.
При необходимости на механические характеристики можно влиять концентрацией самособирающегося пептида и дополнительно - типом молекул и ионов, присутствующих в композиции. Композиция, содержащая самособирающийся пептид, используемая в изобретении, может, например, содержать NaCl и, необязательно, биологически подходящий буфер, например, Tris.
В одном варианте осуществления собранное состояние самособирающегося пептида может также управляться ионной силой, например, сборка может вызываться сочетанием с буфером, имеющим высокую ионную силу (например, выше 0,15 моль/л), который может дополнительно содержать ионы кальция, фосфата и/или фтора.
pH в месте повреждения (или между поверхностью кариозного поражения, протекающего с образованием полости, и стоматологическим веществом) может зависеть от pH стоматологического вещества. Большая часть стоматологических веществ имеет нейтральный или кислый pH, например, хитозан-аргинин-амид.
Альтернативно, в контексте изобретения используемый самособирающийся пептид может альтернативно подвергаться самосборке при высоком pH, в частности, при pH, составляющем по меньшей мере 7,5. В этом случае стоматологическое вещество, например, Portland- цемент или любой материал на основе гидроксида кальция, обычно имеет pH, составляющий по меньшей мере 7,5. Предпочтительным пептидом, который подвергается самосборке при высоком pH, в частности, при pH, составляющем по меньшей мере 7,5, является P11-8.
Один аспект настоящего изобретения представляет собой композицию или набор по настоящему изобретению для использования при лечении кариозного поражения, протекающего с образованием полости, как описано выше, предпочтительно, кариозного поражения, протекающего с образованием полости в эмали, в частности, для использования в недопущении или уменьшении частоты возникновения вторичного кариеса после неудачного использования стоматологического вещества. Соответственно, первичное кариозное поражение может подвергаться лечению, при котором частота возникновения вторичного кариеса снижается посредством лечения по изобретению. Лечение кариозного поражения в контексте настоящего изобретения обычно выполняется врачом-стоматологом.
Лечение может содержать этапы, на которых (a) очищают зубную поверхность, (b) необязательно, высушивают зубную поверхность, (c) необязательно, протравливают зубную поверхность, (d) наносят композицию или компоненты набора на кариозное поражение, и (e) необязательно, отверждают, при этом этапы (b) и (c), если имеются, могут выполняться в любом порядке.
Обычно этап (a) предшествует этапам (b-e) лечебной процедуры. Этапы (b-d) являются более гибкими в смысле их последовательности при нанесении, а этап (e) обычно следует за этапами (b-d). Таким образом, например, протравливание (если применяется) может выполняться перед или после высушивания или в середине этапа (d) и т.д. Последовательность и применение указанных этапов обычно зависит от типа стоматологического вещества, используемого в настоящем изобретении, и соответствует последовательности и применению этапов, обычно применяемым для указанного стоматологического вещества, если указанное стоматологическое вещество используется без самособирающегося пептида. Например, если герметик на основе полимера используется в качестве стоматологического вещества, предпочтительно, что поверхность зуба протравливается перед нанесением герметика на основе полимера. Герметики на основе полимера также более чувствительны к влажности, чем стеклоиономерные цементы. Таким образом, в случае нанесения герметиков на основе полимера, высушивание зубной поверхности является предпочтительным. Предпочтительно, в этом случае зуб и высушивают и протравливают. Стоматолог осведомлен о рекомендуемых этапах лечения для различных стоматологических веществ.
Этап (a), "очистка зубной поверхности", означает, что по меньшей мере поверхность кариозного поражения очищается, то есть вещества, например, частицы пищи, зубной налет, зубная бляшка или зубные пленки и т.д., удаляются с зубной поверхности, по меньшей мере с поверхности кариозного поражения, подходящими способами. Такие способы очистки могут включать в себя обработку традиционной зубной щеткой, обработку специальными зубными щетками, например, щетками для удаления зубной бляшки, обработки стоматологическими скалерами и кюретажными ложками, применение полоскания для полости рта, например, использование антибактериальных полосканий для полости рта, и т.д. Очистка предпочтительно включает удаление бляшки. Очистка может дополнительно включать частичное или полное удаление разрушенных кариесом тканей, например, посредством очистки, сверления, пескоструйной обработки или лазерного выжигания, посредством применения стоматологического экскаватора, или посредством химико-механического удаления (например, с использованием системы Carisolv®). Удаление разрушенных кариесом зубных тканей в целом не требуется в контексте изобретения, и, предпочтительно, не выполняется сверление.
При этом, в случае кариозных поражений на более выраженных стадиях кариеса например, кариозных поражениях стадий 3, 4, 5 и 6 по ICDAS-II, может быть предпочтительно по меньшей мере частичное удаление разрушенной зубной ткани. В случае выполнения удаления разрушенной зубной ткани предпочтительно, что кариозные зубные ткани удаляются посредством "щадящего" способа, например, посредством использования стоматологического экскаватора или химико-механического способа удаления, но не сверления. Авторы изобретения обнаружили, что, в контексте поражений эмали без вовлечения дентина (как предпочтительно в настоящем документе), не является обязательным полное удаление кариозной ткани. Особенно предпочтительно, чтобы в процессе удаления кариозных тканей не удалялись интактные ткани, что является обычным в случае, когда используется сверление в качестве техники удаления. В случае поражений с вовлечением дентина кариозная ткань предпочтительно удаляется.
Как описано выше, применение этапа (b), то есть, высушивание зубной поверхности, может быть предпочтительным для применения конкретных стоматологических веществ, например, герметиков на основе полимера, стоматологических связывающих веществ или композитов на основе полимера. Высушивание может выполняться перед протравливанием (если протравливание выполняется), после протравливания, или в контексте этапа (d), например, между нанесением самособирающегося пептида и нанесением стоматологического вещества. Высушивание зубных поверхностей обычно выполняется с помощью струи воздуха.
Кроме того, этап (c), то есть протравливание зубной поверхности, может являться выгодным для нанесения конкретных стоматологических веществ, например, герметиков на основе полимера, стоматологических связывающих веществ или композитов на основе полимера. Протравливание представляет собой стандартный способ, традиционно используемый в процедуре стоматологического пломбирования. "Протравливание" означает создание микроскопической пористости на зубной поверхности, в которую может течь самособирающийся пептид и/или стоматологическое вещество, например, стоматологический герметизирующий материал, увеличивая, таким образом, ретенцию, увеличивая площадь поверхности и увеличивая силу связывания между стоматологическим веществом и зубной поверхностью. Вещества для травления, которые могут использоваться в контексте настоящего изобретения, содержат малеиновую кислоту, EDTA, лимонную кислоту, тартаровую кислоту, фосфорную кислоту, азотную кислоту и полиакриловую кислоту. Особенно предпочтительным веществом для травления является фосфорная кислота, которая часто также называется кондиционирующим веществом. Обычно вещество для травления наносится на очищенную и необязательно высушенную зубную поверхность на период времени, составляющий 10-60 секунд, например, на 15-30 секунд. После протравливания зубная поверхность предпочтительно промывается, например, водой. В зависимости от нанесенного стоматологического вещества зубная поверхность высушивается после необязательного этапа промывания перед нанесением стоматологического вещества, например, в случае герметиков на основе полимера. В одном варианте осуществления протравливание выполняется после нанесения самособирающегося пептида и перед нанесением стоматологического вещества.
Этап (d) включает в себя нанесение композиции или компонентов набора на кариозное поражение, предпочтительно кариозное поражение, протекающее с образованием полости. Это означает, что композиция или компоненты набора наносятся на кариозное поражение подходящими способами, известными стоматологу, например, посредством пломбирования. Когда набор по изобретению используется для лечения кариозного поражения, предпочтительно этап (d) включает (i) нанесение самособирающегося пептида или композиции, содержащей самособирающийся пептид (содержащийся в наборе), на кариозное поражение, и затем (ii) нанесение стоматологического вещества на кариозное поражение. "Нанесение стоматологического вещества" обычно относится к нанесению, когда оно профессионально и традиционно выполняется врачом-стоматологом, например, согласно инструкции изготовителя. Самособирающийся пептид может наноситься, например, как раствор в подходящем буфере. Самособирающийся пептид может наноситься на кариозное поражение посредством любого подходящего аппликатора, например, шприца, губки и т.д. Например, может выполняться нанесение с использованием в Curodont® Repair. Набор предпочтительно также содержит аппликатор.
В одном варианте осуществления этап (d) включает нанесение смеси самособирающегося пептида и стоматологического вещества на кариозное поражение, протекающее с образованием полости. Эта смесь может представлять собой композицию по настоящему изобретению или компоненты набора по настоящему изобретению, смешанные перед или при нанесении. Смесь может наноситься так, как это традиционно выполняется в области стоматологии для соответствующего стоматологического вещества, например, согласно инструкциям изготовителя.
Применение необязательного этапа (e), то есть отверждения, зависит от используемого стоматологического вещества. Большинство стоматологических веществ требуют какого-либо вида отверждения. Термин "отверждение" относится к процессу, во время которого происходит химическая реакция (например, полимеризация) или физическое действие (например, испарение), приводящие к более жесткой, прочной или более устойчивой связи (например, связыванию) или веществу (например, отвержденному полимеру). Типичным отверждением для стоматологического материала является химическое отверждение, отверждение посредством применения света, термическое отверждение или их сочетание.
Таким образом, настоящее изобретение обеспечивает, например, композицию или набор по настоящему изобретению для использования при лечении кариозного поражения, предпочтительно кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадии 3, 4 или 5 по ICDAS-II, как описано выше, при этом лечение кариозного поражения содержит этапы, на которых (i) очищают зубную поверхность, удаляя бляшку, в частности, очищают поверхность кариозного поражения, необязательно, включая полное или частичное удаление пораженных тканей, при этом предпочтительно не выполняется сверление, (ii) наносят композицию, содержащую самособирающийся пептид, как описано выше, на кариозное поражение, например, самособирающийся пептид, содержащий обобщающую типичную последовательность согласно SEQ ID Nos: 1-5 (например, P11-4), (iii) наносят стоматологическое вещество на кариозное поражение, например, герметик на основе стеклоиономерного цемента или фтористый лак, и (iv) отверждают фтористый лак, например, посредством высушивания, или герметик на основе стеклоиономерного цемента, например, посредством химического отверждения или сочетания химического отверждения и отверждения видимым светом. Последовательность этапов может быть от (i) до (iv).
Другой пример для композиции или набора для использования по настоящему изобретению представляет собой композицию или набор по настоящему изобретению для использования при лечении кариозного поражения, предпочтительно кариозного поражения, протекающего с образованием полости, например, кариозного поражения стадии 3, 4 или 5 по ICDAS-II, как описано выше, при этом лечение кариозного поражения содержит этапы, на которых (i) очищают зубную поверхность, удаляя бляшку, в частности, необязательно, очищают поверхность кариозного поражения, что включает удаление пораженных тканей частично или полностью, при этом предпочтительно не выполняется сверление, (ii) необязательно высушивают поверхность кариозного поражения, (iii) наносят вещество для травления, например, фосфорную кислоту, на поверхность кариозного поражения на подходящее время и, таким образом, протравливают поверхность зуба, имеющего кариозное поражение, (iv) удаляют вещество для травления, например, посредством смывания, (v) наносят композицию, содержащую самособирающийся пептид, как описано выше, на кариозное поражение, например, самособирающийся пептид, содержащий обобщающую типичную последовательность согласно SEQ ID NOs: 1-5 (например, P11-4), (vi) высушивают поверхность зуба, имеющего кариозное поражение, (vii) наносят герметик на основе полимера, предпочтительно согласно инструкциям изготовителя, и (viii) отверждают герметик на основе полимера подходящим способом отверждения.
Выбор стоматологических веществ в контексте изобретения может зависеть от типа кариозного поражения, подлежащего лечению. Например, изобретение преимущественно обеспечивает возможность использования стоматологического герметика для кариозных поражений, протекающих с образованием полости любых размеров или для окклюзионных кариозных поражений в ямках и/или фиссурах зуба.
Дополнительно настоящее изобретение обеспечивает способ лечения кариозного поражения, протекающего с образованием полости, содержащий этап, на котором наносят указанные компоненты набора или композицию по изобретению на указанное кариозное поражение. Например, указанный способ может содержать этапы (a) - (e), как описано выше, то есть, (a) очищают зубную поверхность, (b) необязательно, высушивают зубную поверхность, (c) необязательно, протравливают или кондиционируют зубную поверхность, (d) наносят композицию или компоненты набора на кариозное поражение, и (e) необязательно, отверждают, как описано выше для композиции и набора для использования при лечении кариозного поражения.
Настоящее изобретение, кроме того, решает дополнительную техническую проблему. В частности, во время удаления кариозного дентина из кариозного поражения, зубная пульпа может обнажиться или может оказаться вблизи поражения, растет риск пульпита или ретракции пульпы из-за неблагоприятной реакции пульпы на стоматологический материал (герметик, связывающее вещество, пломбирующее вещество, полимер и т.д.). Авторы изобретения неожиданно обнаружили, что для недопущения повреждения пульпы при расположении зубной реставрации вблизи пульпы стоматолог может использовать набор или композицию по изобретению. Таким образом, изобретение обеспечивает композицию или набор по настоящему изобретению для использования при покрытии пульпы. Стоматологический материал может представлять собой стоматологические вещества, как описано выше, например, стоматологический герметик или связывающее вещество, или пломбирующее вещество и т.д. Он может представлять собой герметик на основе стеклоиономерного цемента, выбранный из группы, содержащей стеклоиономерные цементы и полимерно-модифицированные стеклоиономерные цементы, или герметик на основе полимера, выбранный из группы, содержащей поликислотномодифицированные композитные полимеры и композиты на основе полимера. В этом контексте композиты на основе полимера являются предпочтительными стоматологическими материалами.
Например, если, в контексте очистки, в частности, удаления дентина из кариозного поражения, пульпа обнажается или близка к обнажению (до степени, которая, как может обнаружить специалист в данной области техники, увеличивает риск ретракции пульпы или пульпита), самособирающийся пептид (например, P11-4 или смесь P11-4 и P11-8, предпочтительно, P11-4) в растворе может наноситься для защиты пульпы и улучшения реминерализации, и затем наносится стоматологический материал, например, стоматологический герметик.
Альтернативно, самособирающийся пептид (например, P11-4 или смесь P11-4 и P11-8, предпочтительно, P11-4) и стоматологический материал могут смешиваться перед нанесением, что является наиболее подходящим, если стоматологический материал также биосовместим с пульпой (например, MTA).
Композиция или набор по настоящему изобретению может использоваться для покрытия пульпы.
Покрытие пульпы может представлять собой прямое или непрямое покрытие пульпы. Реминерализация тонкого слоя размягченного дентина особенно предпочтительна для непрямого покрытия пульпы, которое может улучшиться за счет самособирающегося пептида, используемого в контексте изобретения. Стеклоиономер или полимерномодифицированные стеклоиономеры могут также использоваться в контексте покрытия пульпы по изобретению, в частности, для непрямого покрытия пульпы. При необходимости поверх покрытия пульпы могут наноситься различные слои стоматологического герметика.
Если самособирающийся пептид располагается поверх пульпы для защиты пульпы от ретракции из-за токсичности стоматологического пломбировочного материала, один источник ионов кальция для реминерализации может представлять собой пульпу. В случае покрытия пульпы ионы для реминерализации происходят из пульпы (или доставляются в пульпу кровью), и реминерализация может начинаться сразу после размещения (без/перед неудачным пломбированием или образованием микрощелей или микротечей). Разумеется, дополнительные ионы, включающие в себя фториды, могут происходить из стоматологического материала. Таким образом, высвобождающие фторид стоматологические материалы, например, стеклоиономерные цементы, также предпочтительны в этом контексте.
Настоящее изобретение иллюстрируется, но без ограничения, следующими примерами. Все цитируемые ссылки в настоящем документе полностью включены в него.
Описание чертежей
Фиг. 1.1. Лечение кариозного поражения, протекающего с частичным образованием полости, (класс 3 по ICDAS).
A: Поперечный разрез зуба с частичным образованием полости слева.
B: После очистки, в данном случае, без удаления размягченного дентина, нанесение раствора, в основном мономерного самособирающегося пептида (например, P11-4, полосы), на зубную поверхность. Самособирающийся пептид начинает диффундировать в полость.
C: Самособирающийся пептид, например, P11-4, собирается в полости благодаря низкому pH, создаваемому матрицей.
D: Зубная поверхность высушена, оставляя ленты & волокна собранного P11-4 внутри повреждения.
E: После поглощения раствора в полости наносится герметик, например, стеклоиономерный цемент (GIC), обеспечивающий диффузию ионов (кальция и фосфата) из слюны и из стеклоиономерного цемента в место поражения.
F: Минерализация (шестиугольники) в повреждении защищают поврежденный герметик, что приводит к минерализованной структуре под повреждением (защищенной герметиком, например, GIC).
После повреждения GIC остается полностью регенерированная зубная поверхность и структура.
Фиг. 1.2:
A: Поперечный разрез зуба с частично образованной полостью слева.
B: Кариозное поражение после удаления размягченного дентина.
C: Нанесение мономерного P11-4 (полосы) или одновременно с пломбировочным материалом, или последовательно.
D: Зуб после удаления размягченного дентина с пломбировочным материалом (серый) и фибриллярным P11-4 (более длинные полосы) на границе между зубом и пломбировочным материалом.
E: Минерализация (шестиугольники) в микрощелях между пломбировочным материалом и зубом. Фосфат кальция поступает или из пломбировочного материала (в случае стеклоиономерного цемента), слюны или из пульпы (посредством зубной лимфы).
Фиг. 2. Лечение кариозного поражения, протекающего с образованием полости, (класс 4 по ICDAS) с помощью композиции по изобретению в модели кариеса, как описано в Пр. 2. В правой и левой колонке представлены два характерных примера.
A, B: Сверление искусственной полости.
C, D: Нанесение 1 капли P11-4, 10 мг/мл, pH 8.
E, F: Нанесение стеклоиономерного цемента (Aqual Ionofill Plus, VOCO).
Фиг. 3. Лечение кариозного поражения, протекающего с образованием полости, (класс 4 по ICDAS) с помощью набора по изобретению в модели кариеса, как описано в Пр. 3. В правой и левой колонке представлены два характерных примера.
A, B: Сверление искусственной полости.
C, D: Нанесение стеклоиономерного цемента (Aqual Ionofill Plus, VOCO), смешанного с 1 каплей P11-4, 10 мг/мл, pH 8.
Фиг. 4. Кривая высвобождения модельного вещества Congo Red и P11-4 из лака, стеклоиономерного цемента и Paro-Amin Fluor Gelée. Эксперимент был проведен так, как указано в Примерах 6 и 7. Высвобождение измерялось, как описано, и выражалось в произвольных единицах (AU). На фиг. 4A представлено высвобождение Congo Red из лака Duraphat (образец A1) и стеклоиономерного цемента Aqua Ionofil Plus (образец B1), а на фиг. 4B представлено высвобождение Congo Red из paro Amin Fluor Gelée (Образец 2). На фиг. 4C представлено высвобождение мономерного P11-4 из лака Duraphat (образец AP) и стеклоиономерного цемента Aqua Ionofil Plus (образец BP).
Примеры
Пример 1
Поражение с частичным образованием полости (класс 3 по ICDAS) очищается. Это происходит или с удалением кариозного дентина, (фиг. 1.2) или без него (фиг. 1.1). После очистки, необязательно включающей в себя удаление размягченного дентина, самособирающийся пептид (например, P11-4) наносится на очищенную поверхность зуба, в частности, в полость. Самособирающийся пептид начинает диффундировать в полость. При этом самособирающийся пептид собирается благодаря низкому pH, создавая матрицу. После впитывания раствора в дентин или эмаль (10 сек-5 мин, в зависимости, например, от поверхности, (в дентине происходит более быстрое впитывание, чем в эмали), наносится герметик, например, стеклоиономерный цемент, обеспечивающий диффузию ионов (Ca и фосфата) из слюны или стеклоиономера в место повреждения. Это обеспечивает начало минерализации в матрице, защищенной герметиком. После утраты герметика зубом, обычно после нескольких месяцев или лет, остается полностью регенерированная зубная поверхность и структура, при отсутствии вторичного кариеса.
Пример 2
Искусственное повреждение класса 4 по ICDAS, созданное посредством сверления в удаленном резце быка, было обработано с помощью набора по изобретению, в частности, посредством аппликации 1 капли P11-4, 10 мг/мл, pH 8, а затем стеклоиономерным цементом (Aqual Ionofill Plus, VOCO) согласно инструкциям производителя. В кратком изложении, кондиционер полиакриловой кислоты был нанесен на 10 секунд, смыт, слегка подсушен, нанесен стеклоиономер и материал выдержали перед заключительными процедурами. Главные этапы представлены на фиг. 2. Стеклоиономерный цемент, отверждался с получения твердой реставрации, неотличимой от реставрации, нанесенной без сочетания с P11-4 (данные не представлены). В пределах недели после нанесения различий обнаружить не смогли.
Пример 3
Искусственное повреждение класса 4 по ICDAS, созданное посредством сверления в удаленном бычьем резце, было обработано с помощью композиции по изобретению. Порошок стеклоиономерного цемента (Aqual Ionofill Plus, VOCO) был подготовлен согласно инструкциям изготовителя. Был добавлен 1 мг P11-4 на 100 мг (10 мг на 1 мл порошка) и смешан с водой. Порошок был разведен согласно рекомендациям изготовителя. Раствор смешивался в течении 30 с и наносился на зубную поверхность, как рекомендовано изготовителем (как описано выше). Основные этапы представлены на фиг. 3.
Стеклоиономерный цемент отверждали с получением твердой реставрации, неотличимой от реставрации, нанесенной без сочетания с P11-4 (данные не представлены). Невозможно было обнаружить различия в течение одной недели после нанесения.
Пример 4 - Профилактика вторичного кариеса
Зубы, имеющие искусственные повреждения класса 4 по ICDAS, выполненные посредством сверления в удаленном бычьем резце, были обработаны стоматологическим герметиком (например, стеклоиономером (например, Aqual Ionofill Plus, VOCO)) в отсутствии или присутствии P11-4 согласно трем различным протоколам:
1) Стоматологический герметик наносится на очищенную поверхность полости согласно инструкциям изготовителя.
2) Капля P11-4, 10 мг/мл, pH 8, наносится на очищенную поверхность полости так, чтобы покрыть указанную поверхность полости. После впитывания по существу раствора зубной поверхностью на очищенную поверхность полости наносился стоматологический герметик согласно инструкциям изготовителя.
3) Порошок стеклоиономерного цемента (Aqual Ionofill Plus, VOCO) подготавливали согласно инструкциям изготовителя. 1 мг P11-4 на 100 мг добавляли (10 мг на 1 мл порошка) и смешивали с водой. Порошок растворяли согласно рекомендациям изготовителя. Раствор смешивали в течение 30 с и наносили на зубную поверхность согласно рекомендациям изготовителя (как описано выше).
Зубы сохраняли в дистилированной воде в течение 24 часов. Затем зубы были подвержены циклической термообработке (500 циклов, 5-55°C), погружены в щелочной фукцин, выполнены срезы и проведен анализ на проникновение красителя и реминерализацию с использованием стереомикроскопа (например, как описано Hepdeniz и др., 2016. Eur J Dent. 10 (2): 163-169).
Образование микрощелей или микропротечек и усадка стоматологического герметика отслеживалась во времени, и реминерализация в месте микротрещин анализировалась. Различные группы сравнивались.
Пример 5 - Покрытие пульпы - реминерализация благодаря пульпе и фосфату кальция из крови
Полость, имеющая из-за зубного кариеса обнаженную пульпу, была очищена посредством экскаватора. Пульпа была покрыта раствором P11-4 (например, 100 мкл, 10 мг/мл pH 8) перед размещением стоматологического материала, например, полимерного композита согласно инструкциям производителя (например, нанесение слоями и отверждение светом, в зависимости от требований).
Отсутствие симптомов со стороны пульпы (то есть нет пульпита), и при последующем рентгенологическом исследовании через 1 год оценивали ретракцию пульпы.
Пример 6 - Кривая высвобождения
Как хорошо известно специалисту в данной области техники, кривая высвобождения вещества, то есть фторида или самособирающегося пептида, зависит от матрицы материала (Mousavinasab и др., 2009, Dent Res J (Isfahan) 6 (2): 75-81). В следующем эксперименте кривая высвобождения модельного вещества, имитирующего самособирающийся пептид, Congo Red, была оценена после включения в стоматологический материал.
Указанный материал был приготовлен и нанесен согласно инструкции для использования (IFU), обычно описывающей использование 0,5-0,75 мл соответствующих продуктов. Для имитации слюны был использован натрий- фосфатный буфер (PBS). PBS соответствует осмолярности и концентрации ионов человеческого организма - он является изотоническим. Для имитации постоянного потока слюны взятое количество было помещено в раствор, эквивалентный потоку слюны за 1 час, который составил 20 мл. Диффузия материала оценивалась при 500 нм с помощью фотометра.
Материал
(Duraphat® зубная суспензия, лак)
(стеклоиономерный реставрационный материал)
Кривая высвобождения
Приготовление лака (Duraphat) и paro Amin Fluor Gelée
Согласно поставщикам IFU, рекомендуется добавить 0,5-1 мл лака на место кариеса. Концентрация Congo Red была выбрана для получения отчетливого сигнала в ультрафиолетовых Vi.
Поместили 12 мг Congo Red в 2 мл пробирку Эппендорфа.
Добавили 2 мл лака непосредственно в пробирку с помощью шприца.
Энергично смешивали Congo Red и лак до тех пор, пока содержимое не стало однородным.
Набрали продукт с помощью шприца.
Поместили 0,5-0,75 мл продукта на предметное стекло в качестве тонкой пленки - как рекомендовано согласно IFU.
Дали высохнуть на воздухе - согласно IFU.
Приготовление Ionofil (стеклоиономерного реставрационного материала).
Поместили 12 мг Congo Red непосредственно в стоматологическую чашечку.
Добавили 2 ложки Ionofil Plus согласно IFU.
Добавили 2 капли воды и смешали согласно IFU.
Поместили количество продукта на предметное стекло.
Выдерживание.
Приготовили раствор PBS с 1% EtOH для консервации.
Поместили стекло в 50 мл трубку для центрифугирования.
Добавили 20 мл PBS.
Поместили на карусельный стол.
Измерение и вычисление.
Непосредственно отфильтровали 1 мл выдержанной жидкости в UV-Cell.
Измерили при 500 нм, контроль/образец=PBS с 1% EthOH.
Вычли контроль без Congo Red из измеренного значения.
Результаты и обсуждение
Независимо от состава материала модельное вещество легко включалось в продукты. Это представлено посредством визуальной оценки однородности содержимого, поскольку гомогенное распределение красный/коричневый является заметным.
Модельное вещество также способно диффундировать из всех трех фторсодержащих препаратов в искусственную слюну. В зависимости от состава кривая высвобождения отдельных составов различалась.
Модельное вещество Congo red высвобождалось из лака Duraphat и стеклоиономерного цемента (фиг. 4A), а также из paro Amin Fluor Gelée, используемого для сравнения (фиг. 4B). Высвобождение из лака происходило быстрее, чем из стеклоиономерного цемента. Можно видеть, что высвобождение из стеклоиономерного цемента было постоянным и увеличивалось с течением времени.
Пример 7 - Кривая высвобождения P11-4
Пример 7 в целом выполнялся как Пример 6, но с самособирающимся пептидом P11-4, если не было описано иного. 12 мг P11-4 (credentis AG) в мономерном виде было добавлено или к лаку Duraphat (ID образца: AP), или к стекоиономерному цементу Aqua Ionofil Plus (ID образца: BP) в количествах и при условиях, описанных выше. Выдерживание выполнялось неподвижным способом при комнатной температуре. Измерение выполнялось при 280 нм, и контрольное значение для буфера без пептида вычиталось из измеренного значения.
Результаты представлены на фиг. 4C. В подтверждение ранее полученных данных эксперимент показал неожиданно хорошую диффузию пептида из тестируемой матрицы, то есть Duraphat (образец AP) или Aqua Ionofil Plus (BP), подтверждая данные, полученные с модельным веществом.
P11-4 медленно и по существу постоянно высвобождался и из лака, и из стеклоиономерного цемента. Количество высвобождаемого пептида увеличивалось во времени, что измерялось в течение нескольких дней. Высвобождение из лака происходило быстрее, чем высвобождение из стеклоиономерного цемента. Таким образом, в зависимости от состава, медленное высвобождение было получено при использовании герметика, например, стеклоиономерного цемента, или “быстрое” высвобождение посредством использования лака, например, канифольсодержащего состава.
Быстрое высвобождение, как видно при использовании лака, например, Duraphat, может иметь выгодное воздействие на эффективность действия пептида вскоре после аппликации, что может быть особенно полезным, например, для реминерализации повреждений, покрытых лаком.
С другой стороны, более длительное высвобождение может дополнительно быть особенно выгодным для профилактики или лечения вторичных поражений - которые могут развиваться во времени медленно - под или на краях герметика на вылеченных (запломбированных) поражениях. Можно сделать разумный вывод, что вещество будет высвобождаться из герметика, например, стеклоиономерного цемента, в течение более длительного периода, чем из лака. Это подходит, поскольку среднее время нахождения герметика, например, стеклоиономерного цемента, на зубе также больше, чем для лака. Кроме того, самособирающийся пептид, высвобожденный из пломбы, может оставаться на нужном месте в течение длительного времени.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> credentis AG
<120> Самособирающиеся пептиды в профилактике и лечении кариозных поражений,
сопровождающихся образованием полостей
<130> 11753 P 6575 EP
<160> 33
<170> BiSSAP 1.3
<210> 1
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> обобщающая типичная последовательность 1 самособирающихся пептидов
<220>
<221> ВАРИАНТ
<222> 1..1
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глуттаминовой кислоты, аспарагиновой кислоты, глутамина и орнитина
<220>
<221> ВАРИАНТ
<222> 2..2
<223> аминокислота X2 независимо выбирается из группы, состоящей из
аланина, валина, изолейцина, лейцина, метионина,
фенилаланина, тирозина, триптофана и глутамина
<220>
<221> ВАРИАНТ
<222> 3..3
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты, аспарагиновой кислоты, глутамина и орнитина
<220>
<221> ВАРИАНТ
<222> 4..4
<223> аминокислота X2 независимо выбирается из группы, состоящей из
аланина, валина, изолейцина, лейцина, метионин,
фенилаланина, тирозина, триптофана и глутамина
<220>
<221> ВАРИАНТ
<222> 5..5
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты, аспарагиновой кислоты, глутамина и орнитина
<400> 1
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 2
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> обобщающая типичная последовательность 2 самособирающихся пептидов
<220>
<221> ВАРИАНТ
<222> 1..1
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 2..2
<223> аминокислота X2 независимо выбирается из группы, состоящей из
фенилаланина и триптофана
<220>
<221> ВАРИАНТ
<222> 3..3
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 4..4
<223> аминокислота X2 независимо выбирается из группы, состоящей из
фенилаланина и триптофана
<220>
<221> ВАРИАНТ
<222> 5..5
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<400> 2
Xaa Xaa Xaa Xaa Xaa
1 5
<210> 3
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> обобщающая типичная последовательность 3 самособирающихся пептидов
<220>
<221> ВАРИАНТ
<222> 1..1
<223> аминокислота X3 независимо выбирается из группы, состоящей из
аргинина, глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 3..3
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 5..5
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<400> 3
Xaa Phe Xaa Trp Xaa
1 5
<210> 4
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> обобщающая типичная последовательность 4 самособирающихся пептидов
<220>
<221> ВАРИАНТ
<222> 1..1
<223> аминокислота X4 независимо выбирается из группы, состоящей из
глутамина, глутаминовой кислоты, серина, треонина и орнитина
<220>
<221> ВАРИАНТ
<222> 2..2
<223> аминокислота X4 независимо выбирается из группы, состоящей из
глутамина, глутаминовой кислоты, серина, треонина и орнитина
<220>
<221> ВАРИАНТ
<222> 3..3
<223> аминокислота X3 независимо выбирается из группы, состоящей из
аргинина, глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 5..5
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 7..7
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 9..9
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 10..10
<223> аминокислота X4 независимо выбирается из группы, состоящей из
глутамина, глутаминовой кислоты, серина, треонина и орнитина
<220>
<221> ВАРИАНТ
<222> 11..11
<223> аминокислота X4 независимо выбирается из группы, состоящей из
глутамина, глутаминовой кислоты, серина, треонина и орнитина
<400> 4
Xaa Xaa Xaa Phe Xaa Trp Xaa Phe Xaa Xaa Xaa
1 5 10
<210> 5
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> обобщающая типичная последовательность 5 самособирающихся пептидов
<220>
<221> ВАРИАНТ
<222> 5..5
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 7..7
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<220>
<221> ВАРИАНТ
<222> 9..9
<223> аминокислота X1 независимо выбирается из группы, состоящей из
глутаминовой кислоты и орнитина
<400> 5
Gln Gln Arg Phe Xaa Trp Xaa Phe Xaa Gln Gln
1 5 10
<210> 6
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-4
<400> 6
Gln Gln Arg Phe Glu Trp Glu Phe Glu Gln Gln
1 5 10
<210> 7
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-2
<400> 7
Gln Gln Arg Phe Gln Trp Gln Phe Glu Gln Gln
1 5 10
<210> 8
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-5
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<400> 8
Gln Gln Arg Phe Xaa Trp Xaa Phe Gln Gln Gln
1 5 10
<210> 9
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-8
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<400> 9
Gln Gln Arg Phe Xaa Trp Xaa Phe Glu Gln Gln
1 5 10
<210> 10
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-12
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<400> 10
Ser Ser Arg Phe Xaa Trp Xaa Phe Glu Ser Ser
1 5 10
<210> 11
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-13
<400> 11
Glu Gln Glu Phe Glu Trp Glu Phe Glu Gln Glu
1 5 10
<210> 12
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-14
<220>
<221> MOD_RES
<222> 3..3
<223> орнитин
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 9..9
<223> орнитин
<400> 12
Gln Gln Xaa Phe Xaa Trp Xaa Phe Xaa Gln Gln
1 5 10
<210> 13
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-17
<400> 13
Thr Thr Arg Phe Glu Trp Glu Phe Glu Thr Thr
1 5 10
<210> 14
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-19
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<400> 14
Gln Gln Arg Gln Xaa Gln Xaa Gln Glu Gln Gln
1 5 10
<210> 15
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-20
<400> 15
Gln Gln Arg Gln Glu Gln Glu Gln Glu Gln Gln
1 5 10
<210> 16
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> орнитин
<220>
<223> P11-28
<220>
<221> MOD_RES
<222> 3..3
<223> орнитин
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 9..9
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> орнитин
<400> 16
Xaa Gln Xaa Phe Xaa Trp Xaa Phe Xaa Gln Xaa
1 5 10
<210> 17
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-29
<400> 17
Gln Gln Glu Phe Glu Trp Glu Phe Glu Gln Gln
1 5 10
<210> 18
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-4mod
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 18
Gln Gln Arg Phe Glu Trp Glu Phe Glu Gln Gln
1 5 10
<210> 19
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-2mod
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 19
Gln Gln Arg Phe Gln Trp Gln Phe Glu Gln Gln
1 5 10
<210> 20
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-5mod
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 20
Gln Gln Arg Phe Xaa Trp Xaa Phe Gln Gln Gln
1 5 10
<210> 21
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-8mod
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 21
Gln Gln Arg Phe Xaa Trp Xaa Phe Glu Gln Gln
1 5 10
<210> 22
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-12mod
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 22
Ser Ser Arg Phe Xaa Trp Xaa Phe Glu Ser Ser
1 5 10
<210> 23
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-13mod
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 23
Glu Gln Glu Phe Glu Trp Glu Phe Glu Gln Glu
1 5 10
<210> 24
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-14mod
<220>
<221> MOD_RES
<222> 3..3
<223> орнитин
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 9..9
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 24
Gln Gln Xaa Phe Xaa Trp Xaa Phe Xaa Gln Gln
1 5 10
<210> 25
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-17mod
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 25
Thr Thr Arg Phe Glu Trp Glu Phe Glu Thr Thr
1 5 10
<210> 26
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-19mod
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 26
Gln Gln Arg Gln Xaa Gln Xaa Gln Glu Gln Gln
1 5 10
<210> 27
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-20mod
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 27
Gln Gln Arg Gln Glu Gln Glu Gln Glu Gln Gln
1 5 10
<210> 28
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<221> MOD_RES
<222> 1..1
<223> орнитин
<220>
<223> P11-28mod
<220>
<221> MOD_RES
<222> 3..3
<223> орнитин
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7..7
<223> орнитин
<220>
<221> MOD_RES
<222> 9..9
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> орнитин
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 28
Xaa Gln Xaa Phe Xaa Trp Xaa Phe Xaa Gln Xaa
1 5 10
<210> 29
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> MOD_RES
<222> 1..1
<223> АЦЕТИЛИРОВАНИЕ
<220>
<223> P11-29mod
<220>
<221> MOD_RES
<222> 11..11
<223> АМИДИРОВАНИЕ
<400> 29
Gln Gln Glu Phe Glu Trp Glu Phe Glu Gln Gln
1 5 10
<210> 30
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-16
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7
<223> орнитин
<400> 30
Asn Asn Arg Phe Xaa Trp Xaa Phe Glu Asn Asn
1 5 10
<210> 31
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-18
<220>
<221> MOD_RES
<222> 5..5
<223> орнитин
<220>
<221> MOD_RES
<222> 7
<223> орнитин
<400> 31
Thr Thr Arg Phe Xaa Trp Xaa Phe Glu Thr Thr
1 5 10
<210> 32
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-26
<220>
<221> MOD_RES
<222> 3
<223> орнитин
<220>
<221> MOD_RES
<222> 5
<223> орнитин
<220>
<221> MOD_RES
<222> 7
<223> орнитин
<220>
<221> MOD_RES
<222> 9
<223> орнитин
<400> 32
Gln Gln Xaa Gln Xaa Gln Xaa Gln Xaa Gln Gln
1 5 10
<210> 33
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> P11-31
<220>
<221> MOD_RES
<222> 3
<223> орнитин
<220>
<221> MOD_RES
<222> 5
<223> орнитин
<220>
<221> MOD_RES
<222> 7
<223> орнитин
<220>
<221> MOD_RES
<222> 9
<223> орнитин
<400> 33
Ser Ser Xaa Phe Xaa Trp Xaa Phe Xaa Ser Ser
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДЫ И ПЕПТИДОМИМЕТИКИ В КОМБИНАЦИИ С АГЕНТАМИ, ИНГИБИРУЮЩИМИ КОНТРОЛЬНЫЕ ТОЧКИ, ДЛЯ ЛЕЧЕНИЯ РАКА | 2016 |
|
RU2739201C2 |
| ПЕПТИДЫ И ПЕПТИДОМИМЕТИКИ ДЛЯ КОМБИНИРОВАННОГО ПРИМЕНЕНИЯ И ЛЕЧЕНИЯ В СУБПОПУЛЯЦИЯХ ПАЦИЕНТОВ С РАКОВЫМИ ЗАБОЛЕВАНИЯМИ | 2014 |
|
RU2732440C2 |
| ПЕПТИДНЫЙ АНАЛОГ АЦИЛИРОВАННОГО ОКСИНТОМОДУЛИНА | 2018 |
|
RU2752787C1 |
| ПОЛИПЕПТИДЫ АНАЛОГА АМИЛИНА ЧЕЛОВЕКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2839688C2 |
| ПЭГИЛИРОВАННЫЕ БИОЛОГИЧЕСКИ АКТИВНЫЕ ПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2748576C2 |
| ДВОЙНОЙ АГОНИСТ РЕЦЕПТОРОВ ГЛЮКАГОНОПОДОБНОГО ПЕПТИДА-1 И ГЛЮКАГОНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ | 2021 |
|
RU2799327C1 |
| УЛУЧШЕННЫЕ ПЕПТИДНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ NASH И ДРУГИХ РАССТРОЙСТВ | 2019 |
|
RU2790209C2 |
| ИНДИВИДУАЛЬНОЕ СРЕДСТВО УХОДА ЗА ЗУБАМИ ДЛЯ ПРЕДОТВРАЩЕНИЯ ДЕМИНЕРАЛИЗАЦИИ | 2020 |
|
RU2834399C1 |
| СОЕДИНЕНИЯ-АГОНИСТЫ GIP И СПОСОБЫ | 2015 |
|
RU2716985C2 |
| КОНСТРУКЦИИ, ИМЕЮЩИЕ SIRP-АЛЬФА ДОМЕН ИЛИ ЕГО ВАРИАНТ | 2016 |
|
RU2740672C2 |
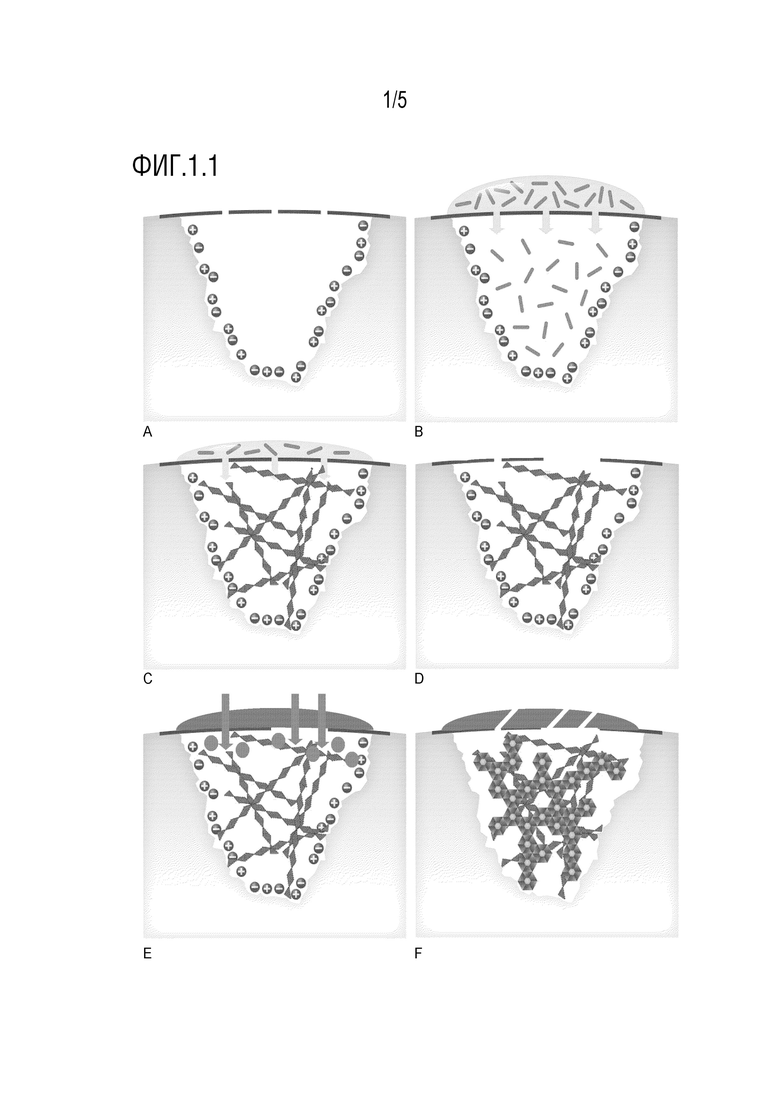
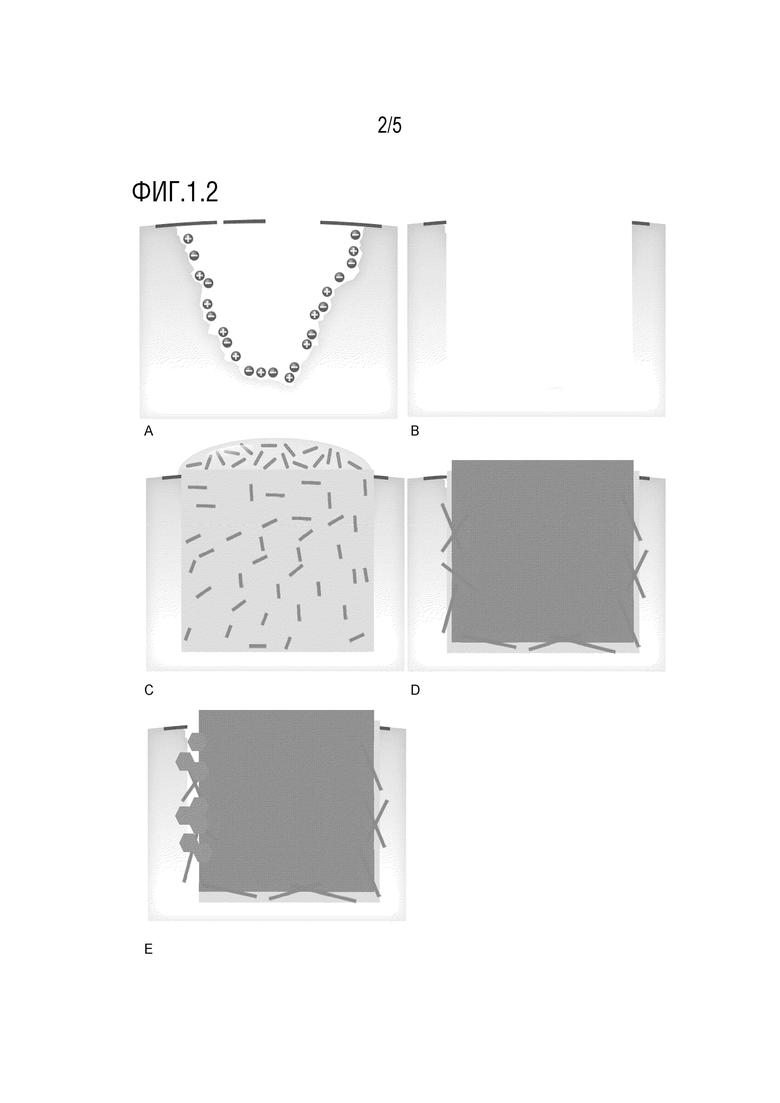
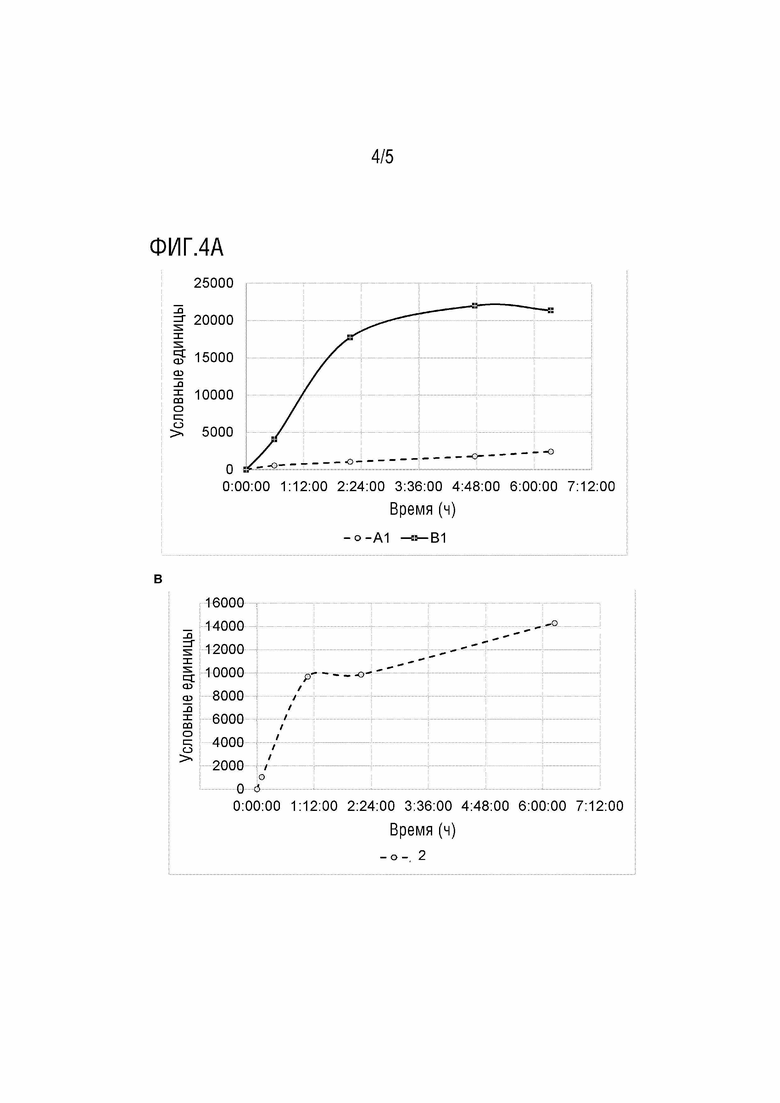
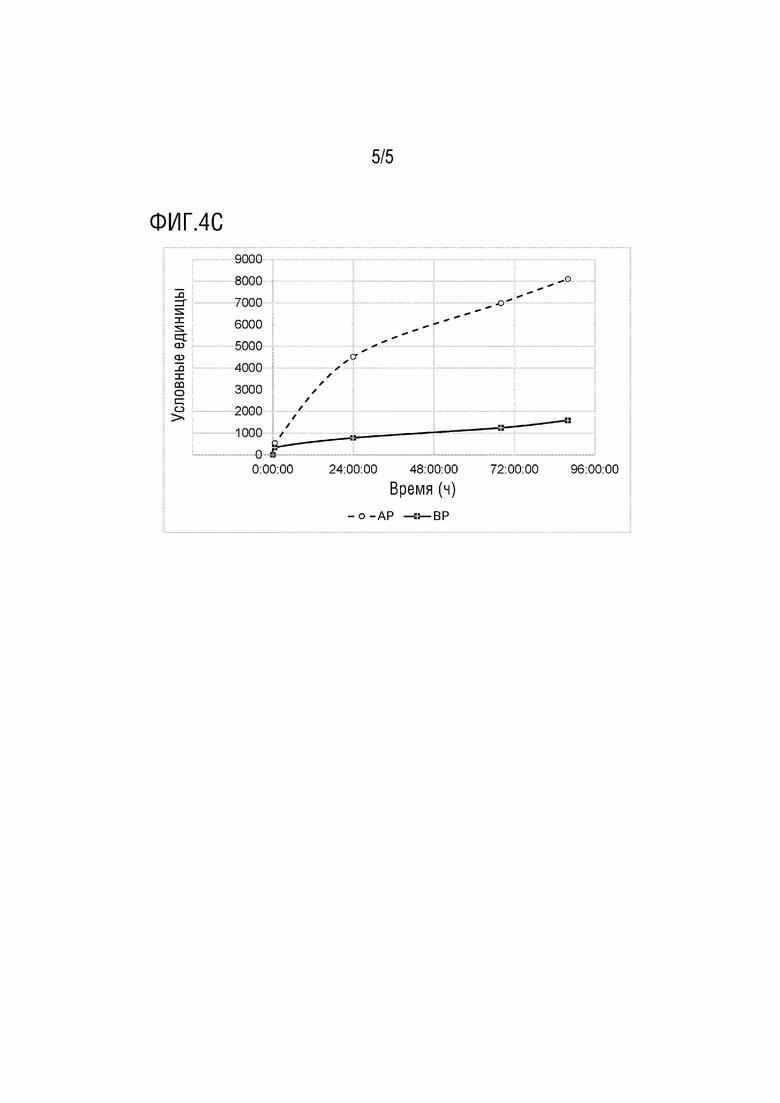
Группа изобретений относится к области средств для профилактики и лечения кариеса, в частности минимально-инвазивного или неинвазивного лечения кариеса, и касается композиции и набора, а также их применения. Предлагаемые композиция и набор содержат: a) самособирающийся пептид, представляющий собой P11-4, имеющий SEQ ID NO: 6, и b) стоматологическое вещество; при этом набор содержит указанные выше компоненты в раздельном виде. В качестве стоматологического вещества в составе композиции используют: стоматологический герметик, выбранный из группы стеклоиономерных цементов и полимер-модифицированных стеклоиономерных цементов; или фтористый лак, содержащий этиловый спирт в качестве растворителя в сочетании с канифолью или шеллачным основанием; в составе набора - стоматологический герметик на основе стеклоиономерного цемента, выбранный из группы, содержащей стеклоиономерные цементы и полимер-модифицированные стеклоиономерные цементы. Предлагается также применение указанных выше композиции или набора в профилактике вторичного кариеса после неудачного использования стоматологического вещества при лечении кариозного поражения, протекающего с образованием полости, а также в защитном покрывании пульпы. Использование самособирающегося пептида P11-4 в составе указанных выше композиции и набора обеспечивает предотвращение вторичного кариеса после неудачного использования стоматологического вещества, используемого при лечении кариеса, сопровождающегося образованием полости, особенно в случае нарушения границы между реставрацией, выполненной из указанного стоматологического вещества, и зубом, и, кроме того, эффективно для защитного покрытия пульпы. 4 н. и 11 з.п. ф-лы, 7 ил., 2 табл., 7 пр.
1. Композиция для профилактики вторичного кариеса после неудачного использования стоматологического вещества при лечении кариозного поражения, протекающего с образованием полости, содержащая:
a) самособирающийся пептид, где указанный самособирающийся пептид представляет собой P11-4, имеющий SEQ ID NO: 6, и
b) стоматологическое вещество, выбранное из группы, состоящей из стоматологического герметика, выбранного из группы стеклоиономерных цементов и полимер-модифицированных стеклоиономерных цементов, содержащих акрилатный полимеризующий компонент, и фтористого лака, где указанный фтористый лак содержит этиловый спирт в качестве растворителя в сочетании с канифолью или шеллачным основанием.
2. Композиция по п. 1, где указанная композиция представляет собой фармацевтическую композицию.
3. Композиция по п. 1, где стоматологическое вещество представляет собой фтористый лак.
4. Набор для профилактики вторичного кариеса после неудачного использования стоматологического вещества при лечении кариозного поражения, протекающего с образованием полости, содержащий в раздельном виде:
a) самособирающийся пептид, где указанный самособирающийся пептид представляет собой P11-4, имеющий SEQ ID NO: 6, и
b) стоматологическое вещество, которое представляет собой стоматологический герметик на основе стеклоиономерного цемента, выбранный из группы, состоящей из стеклоиономерных цементов и полимер-модифицированных стеклоиономерных цементов, содержащих акрилатный полимеризующий компонент.
5. Набор по п. 4, где указанный набор представляет собой фармацевтический набор.
6. Набор по п. 4, где стоматологическое вещество содержит неполярный или полярный органический растворитель.
7. Композиция по любому из пп. 1-3 или набор по любому из пп. 4-6, где указанное стоматологическое вещество обладает способностью высвобождать ионы фтора, где предпочтительно указанное стоматологическое вещество также обладает способностью высвобождать ионы кальция.
8. Композиция по любому из пп. 1-3 или 7 или набор по любому из пп. 4-7, где стоматологическое вещество проницаемо для ионов и в ионы.
9. Композиция по любому из пп. 1-3 или 7-8 или набор по любому из пп. 4-8, где самособирающийся пептид находится, главным образом, в виде мономера.
10. Применение композиции по любому из пп. 1-3 или 7-9 или набора по любому из пп. 4-9 в профилактике вторичного кариеса после неудачного использования стоматологического вещества при лечении кариозного поражения, протекающего с образованием полости.
11. Применение по п. 10, где лечение кариозного поражения включает этапы:
a) очищения зубной поверхности,
b) необязательно, высушивания зубной поверхности,
c) необязательно, протравливания зубной поверхности,
d) нанесения указанной композиции или указанных компонентов набора на кариозное поражение,
e) необязательно, отверждения.
12. Применение композиции по любому из пп. 1-3 или 7-9 или набора по любому из пп. 4-9 в защитном покрывании пульпы.
13. Применение по п. 12, где указанная композиция или указанные компоненты набора наносятся на кариозное поражение при контакте с пульпой.
14. Применение по любому из пп. 10 или 12, 13, где нанесение указанных компонентов набора на кариозное поражение включает нанесение самособирающегося пептида на кариозное поражение и затем нанесение указанного стоматологического вещества на кариозное поражение.
15. Применение по любому из пп. 10 или 12, 13, где нанесение указанных компонентов набора на кариозное поражение включает нанесение смеси указанного самособирающегося пептида и указанного стоматологического вещества на кариозное поражение.
| ALKILZY M | |||
| et al | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Journal of dental research, 2018, V | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Раздвижной паровозный золотник с подвижными по его скалке поршнями между упорными шайбами | 1922 |
|
SU148A1 |
| Найдено в PubMed, PMID: 28892645, DOI: 10.1177/0022034517730531 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| СТОМАТОЛОГИЧЕСКИЙ ПРОДУКТ ДЛЯ ОТБЕЛИВАНИЯ ЗУБОВ | 2014 |
|
RU2673820C2 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
Авторы
Даты
2024-10-09—Публикация
2020-07-09—Подача