Область техники
Настоящее изобретение относится к области биоаналитических систем, к массивам меченых микрочастиц, применяемых в мультиплексных анализах, в частности в областях проточной цитометрии и флуоресцентной микроскопии. Наборы микрочастиц, несущих уникальные флуоресцентные метки/коды, и соответствующие этим меткам функциональные молекулы, используются в биоаналитике. Изобретение относится к способам синтеза больших наборов микрочастиц с заранее заданными свойствами.
Уровень техники
Наборы микрочастиц, несущих уникальные флуоресцентные метки, и соответствующие этим меткам функциональные молекулы, активно используются в биоаналитике. Известны мультиплексные проточные цитометрические анализы на основе частиц для биомедицинских исследований и медицинской диагностики (Дарио А.А. Виньяли. Мультиплексные проточные цитометрические анализы на основе частиц. Журнал иммунологических методов. Том 243, выпуски 1-2, 21 сентября 2000 г., стр. 243-255. Режим доступа https://www.sciencedirect.com/science/article/pii/S0022175900002386). Известны массивы на основе микросфер, закодированных наночастицами, для высокопроизводительного мультиплексного обнаружения (Юанькуй Ленг , Кан Сунь, Сяоюань Чен, Ванван Ли. Подвесные массивы на основе микросфер, закодированных наночастицами, для высокопроизводительного мультиплексного обнаружения. Обзоры химического общества. Выпуск 15, 2015 г. Режим доступа https://pubs.rsc.org/en/content/articlelanding/2015/cs/c4cs00382a). Известны флуоресцентные микрогранулы, кодируемые нанокристаллами, для мультиплексной визуализации и диагностики рака (Sukhanova A. and I. Nabiev. Fluorescent nanocrystal-encoded microbeads for multiplexed cancer imaging and diagnosis. Crit Rev Oncol Hematol, 2008. 68 (1): p. 39-59).
В настоящее время на рынке представлены наборы микрочастиц Luminex (https://www.thermofisher.com/ru/ru/home/life-science/antibodies/immunoassays/procartaplex-assays-luminex.html), содержащие порядка 100 независимых меток. Магнитные частицы представляют собой семейство (https://www.luminexcorp.com/xmap-technology/#microspheres), включающее порядка 80 флуоресцентно-меченных микросфер, с диаметром 6.45 мкм, необходимых как для идентификации, так и в качестве твердой поверхности для нанесения образца. Классические агарозные микросферы - семейство, включающее порядка 500 флуоресцентно-меченных полистироловых микросфер, с диаметром 5.6 мкм, необходимых как для идентификации, так и в качестве твердой поверхности для нанесения образцов.
Используемая последовательная иммобилизация заранее синтезированных функциональных молекул на частицы с каждой меткой, при числе независимых меток более 100 трудозатратна, и неприменима для генерации большего числа комплексов метка-функциональная молекула.
Представленные на рынке наборы микрочастиц формируются с использованием комбинаций двух флуорофоров в нескольких концентрациях. Тем не менее, количество уникальных меток в наборе микрочастиц может быть расширено почти неограниченно, при использовании дополнительных флуоресцентных меток. Известные цитометры позволяют проводить одновременный анализ до 12-16 флуорофоров, комбинирование которых в разных концентрациях даёт множество, миллиарды и более, уникальных кодов.
До недавнего времени такие большие наборы микрочастиц не были востребованы по вышеуказанной причине.
Известно изготовление и использование расширенных наборов микрочастиц c одновременной функционализацией каждой частицы своей последовательностью нуклеотидов, где наборы микрочастиц несут уникальную для каждой метки, известную, но случайно выбранную олигонуклеотидную последовательность (система и способ для анализа фенотипа и полинуклеотидного секвенирования биологических частиц с использованием детерминированного штрихкодирования патент RU 2756306, Andreyev D.; Zybailov B. Integration of flow cytometry and single cell sequencing. Trends Biotechnol., 2020. 38 (2), p. 133-136).
Однако нет способов и устройств для синтеза заранее заданных пользователем олигонуклеотидных последовательностей, для обычных и расширенных наборов микрочастиц в одном общем синтезе, где количество синтезируемых последовательностей и их длина не ограничены, при количестве одновременно синтезируемых последовательностей до миллиона и более.
Сущность изобретения
Технический результат, обеспечиваемый способом, - получение набора микрочастиц, несущих уникальные флуоресцентные метки, и олигоуклеотид, либо полинуклеотид, либо аптамер с заранее задаваемой пользователем последовательностью, уникальной для каждой метки. Причем обеспечивается возможность одновременного синтеза миллионов последовательностей.
Технический результат достигается тем, что в способе модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, включающий формирование нуклеотидной последовательности на микрочастице на каждой микрочастице формируют олигонуклеотид, либо аптамер, либо полинуклеотид с предварительно заданной последовательностью нуклеотидов, уникальной для каждой флуоресцентной метки микрочастиц, осуществляют синтез олигонуклеотида, либо аптамера, либо полинуклеотида циклически, с применением сортировки микрочастиц по флуоресцентной метке на каждом цикле синтеза, на каждом цикле к каждой из микрочастиц добавляется один нуклеотид, заранее определённой уникальной последовательности, выбранной для соответствующей уникальной флуоресцентной метки каждой микрочастицы.
Предусмотрено, что сортировку набора меченых микрочастиц на каждом цикле синтеза выполняют, применяя сортировщик клеток, активируемый флуоресценцией (FACS), сортировку набора меченых микрочастиц производят в четыре реактора A,T,G,C, в каждом из реакторов к микрочастицам добавляют один из четырёх олигонуклеотидов A,T,G,C, после добавления нуклеотида, содержимое реакторов объединяют, перемешивают миксером и отправляют на следующий цикл сортировки и синтеза, причем сортировку и синтез производят с использованием управляемых компьютером сортировщика клеток, активируемого флуоресценцией, миксера, ректоров.
Предусмотрено, что приёмник сортируемой микрочастицы определяют по соотношению интенсивностей флуоресцентных сигналов каждой микрочастицы, в соответствии с программно задаваемой таблицей метка-приёмник.
Предусмотрено, что приёмник сортируемой микрочастицы определяют по соотношению интенсивностей сигналов комбинаторной метки каждой микрочастицы, в соответствии с программно задаваемой таблицей метка-приёмник.
Предусмотрено, что иммобилизацию и наращивание олигонуклеотида, либо аптамера, либо полинуклеотида производят на поверхности микрочастицы.
Устройство для модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, содержит компьютер, четыре реактора A, T, G, C, сортировщик клеток по сигналам флуоресцентной метки, миксер. В другом варианте устройство для модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, содержит компьютер, ДНК-синтезатор, сортировщик клеток по сигналам флуоресцентной метки, миксер.
Способ позволяет на каждой микрочастице выращивать свою, заданную пользователем, последовательность нуклеотидов.
Изобретение поясняется графическими материалами:
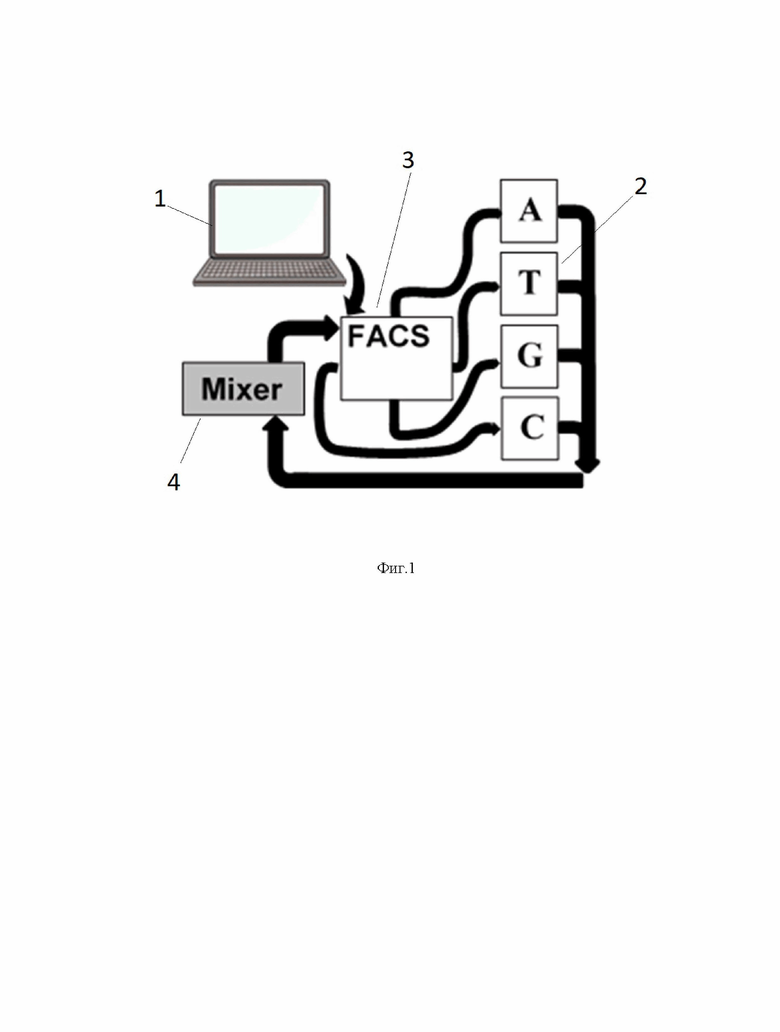
фиг. 1. Схема устройства для синтеза заданных для каждой метки микрочастиц олиго/полинуклеотидных последовательностей.
На графических материалах обозначены следующие позиции:
1 - компьютер;
2 - реактор;
3 - сортировщик клеток (FACS);
4 - миксер.
Осуществление изобретения
В способе модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, включающем формирование нуклеотидной последовательности на микрочастице на каждой микрочастице формируют олигонуклеотид либо аптамер либо полинуклеотид с предварительно заданной последовательностью нуклеотидов, уникальной (индивидуальной) для каждой флуоресцентной метки микрочастиц. Осуществляют синтез олигонуклеотида либо аптамера либо полинуклеотида циклически, с применением сортировки микрочастиц по флуоресцентной метке на каждом цикле (этапе) синтеза. На каждом цикле к каждой из микрочастиц добавляется один нуклеотид, заранее определённой уникальной последовательности, выбранной для соответствующей уникальной флуоресцентной метки каждой микрочастицы.
Сортировку набора меченых микрочастиц на каждом цикле синтеза выполняют, применяя сортировщик клеток, активируемый флуоресценцией (FACS), сортировку набора меченых микрочастиц производят в четыре реактора A, T, G, C, в каждом из реакторов к микрочастицам добавляют один из четырёх олигонуклеотидов A, T, G, C, после добавления нуклеотида, содержимое реакторов объединяют, перемешивают миксером и отправляют на следующий цикл сортировки и синтеза, причем сортировку и синтез производят с использованием управляемых компьютером сортировщика клеток, активируемого флуоресценцией, миксера, ректоров.
Приёмник сортируемой микрочастицы определяют по соотношению интенсивностей флуоресцентных сигналов каждой микрочастицы, в соответствии с программно задаваемой таблицей метка-приёмник.
Как вариант предусмотрено, что приёмник сортируемой микрочастицы определяют по соотношению интенсивностей сигналов комбинаторной метки каждой микрочастицы, в соответствии с программно задаваемой таблицей метка-приёмник.
Как вариант предусмотрено, что иммобилизацию и наращивание олигонуклеотида, либо аптамера, либо полинуклеотида производят на поверхности микрочастицы.
Устройство для модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, содержит компьютер 1, четыре реактора 2 A,T,G,C, сортировщик клеток 3 по сигналам флуоресцентной метки, миксер 4.
В другом варианте устройство для модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, содержит компьютер 1, ДНК-синтезатор (не показан), сортировщик клеток 3 по сигналам флуоресцентной метки, миксер 4.
Применение способа
Способ модификации больших наборов микрочастиц предназначен для получения наборов микрочастиц несущих уникальные флуоресцентные метки, олиго- либо полинуклеотидами/аптамерами с задаваемой пользователем последовательностью, уникальной для каждой метки.
Способ включает нанесение нуклеотидов на микрочастицы. Выполняют синтез олигонуклеотидов с заранее заданной уникальной последовательностью для каждой уникальной метки микрочастиц с применением сортировки микрочастиц по сигналам метки на каждом этапе синтеза. Синтез состоит из последовательности шагов (циклов), на каждом из которых к каждой из микрочастиц добавляется один нуклеотид, заранее определённый уникальной последовательностью, выбранной для соответствующей уникальной флуоресцентной метки каждой микрочастицы. Для этого на каждом шаге, с использованием сортировщика клеток, активируемого флуоресценцией производят сортировку набора меченых микрочастиц в четыре реактора A, T, G, C, в каждом из реакторов к микрочастицам добавляют один из четырёх олигонуклеотидов A, T, G, C, после добавления нуклеотида, содержимое реакторов объединяют, перемешивают миксером 4 и отправляют в следующий цикл сортировки и синтеза, причем сортировка и синтез производят с использованием управляемых компьютером 1 сортировщика 3 клеток, активируемого флуоресценцией, миксера 4, ректоров 2 (фиг. 1).
Способ и устройство реализуются на аппаратной базе сортировщика клеток, активируемый флуоресценцией FACS (где FACS - флуоресцентно-активируемый клеточный сортировщик, обеспечивает сортировку биологических частиц с флуоресцентной активацией на основе проточной цитометрии) и позволяют создавать большие, на миллион и более заранее заданных вариантов, наборы аптамеров, для использования в аффинных аналитических системах.
Способ предлагает синтез заранее заданных пользователем нуклеотидных последовательностей для обычных и расширенных наборов микрочастиц в одном общем синтезе, где количество синтезируемых последовательностей и их длина не ограничены.
Синтез основан на использовании аппаратной базы флуоресцентно-активируемых клеточных сортировщиков (FACS) и специализированного алгоритма сортировки, обеспечивающих заявленный результат.
Производительность современных FACS позволяет производить синтез миллионов последовательностей олиго- либо полинуклеотидов одновременно, за время, сравнимое с традиционным синтезом одного олиго/полинуклеотида, и с использованием тех же расходников и оборудования.
Для получения наборов микрочастиц в качестве твёрдофазного носителя используют микрочастицы, несущие уникальные флуоресцентные метки (коды). Способы создания оптически кодированных полимерных микросфер, получаемых путем включения в их состав органических флуоресцентных красителей известны (WO 2006115870, US 7445844 В2, US 6268222, RU 2624853). В качестве твёрдофазного носителя в способе используются микросферы, например полимерные микросферы с размером от 2 до 10 мкм, изготовленные из материалов с надлежащей плотностью, полистироловые, меламиновые, полистереновые, полиметилметакрилатные и др. (например, см. шарики Luminex https://www.sciencedirect.com/science/article/pii/S0022175900002386 или https://pubs.rsc.org/en/content/articlelanding/2015/cs/c4cs00382a).
Для синтеза олиго- либо полинуклеотидов на микрочастице в способе применяют известные способы синтеза олиго- либо полинуклеотидов на твердофазном носителе, стандартные подходы известны (https://en.wikipedia.org/wiki/Oligonucleotide_synthesis).
Микрочастицы с флуоресцентными метками идентифицируются и сортируются на каждом шаге синтеза посредством FACS (флуоресцентно-активируемой сортировки частиц на базе проточной цитометрии https://en.wikipedia.org/wiki/Flow_cytometry#Cell_sorting_by_flow_cytometry), что позволяет на каждой микрочастице выращивать свою, заданную пользователем, последовательность.
Способ модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, олиго- либо полинуклеотидами/аптамерами с задаваемой пользователем последовательностью включает синтез олигонуклеотидов с заранее заданной уникальной последовательностью для каждой уникальной метки микрочастиц с применением сортировки микрочастиц по сигналам метки на каждом этапе синтеза. Синтез состоит из последовательности шагов, на каждом из которых к каждой из микрочастиц добавляется один нуклеотид, заранее определённый уникальной последовательностью, выбранной для соответствующей уникальной флуоресцентной метки каждой микрочастицы. Для этого на каждом шаге производится сортировка набора меченых микрочастиц в четыре реактора 2 A, T, G, C (фиг. 1), в каждом из реакторов 2 производится добавление одного из четырёх олигонуклеотидов, идентичное традиционно применяемому в ДНК-синтезаторах. После добавления нуклеотида, содержимое реакторов 2 объединяется, перемешивается миксером 4 и отправляется в следующий цикл сортировки и синтеза.
В способе применяют алгоритм сортировки, определяющий приёмник сортируемой микрочастицы по соотношению интенсивностей флуоресцентных или иных сигналов (комбинаторной метки) каждой микрочастицы, в соответствии с программно задаваемой таблицей метка-приёмник. Обрабатывают независимо миллионы и более различных групп микрочастиц по соотношению интенсивностей флуоресцентных или иных сигналов (комбинаторной метки) каждой частицы, характерной для группы.
Способ синтеза олигонуклеотидов с заранее заданной последовательностью для каждой уникальной метки микрочастиц на основе сортировки частиц по сигналам метки на каждом этапе синтеза предусматривает использование традиционных способов синтеза поли- и олигонуклеотидов, где иммобилизация и рост поли- и олигонуклеотидов производится на поверхности микрочастиц.
Способ предлагает использование устройства для синтеза олигонуклеотидов с заранее заданной последовательностью для каждой уникальной метки микрочастиц на основе сортировки частиц на аппаратной базе (hardware) коммерчески доступных сортировщиков (FACS) или иных аналогичных сортировщиков по сигналам метки на каждом этапе синтеза, при количестве одновременно синтезируемых последовательностей до миллиона и более.
Способ предлагает использование устройства для синтеза олигонуклеотидов с заранее заданной последовательностью для каждой уникальной метки микрочастиц на основе сортировки частиц на аппаратной базе (hardware) коммерчески доступных сортировщиков (FACS) или иных аналогичных сортировщиков по сигналам метки на каждом этапе синтеза, где введение нуклеотидов производится на аппаратной базе (hardware) коммерчески доступных ДНК-синтезаторов или аналогичных устройств, при количестве одновременно синтезируемых последовательностей до миллиона и более.
Способ предлагает сортировку микрочастиц по сигналу комбинаторной метки с использованием аппаратной базы коммерчески доступных сортировщиков (FACS) или иных аналогичных сортировщиков.
Возможно проведение смешанного анализа, сочетающего анализ последовательностей ДНК/РНК и аффинный анализ, посредством одновременного выращивания заранее заданных для каждой метки олигонуклеотидов и аптамеров в наборах частиц с уникальными метками.
Возможно проведение синтеза экспонирующих заранее заданные нуклеотидные последовательности микрочастиц с функциональными свойствами, соответствующими метке - такими как магнитные свойства, загрузка реагентом, проводимость, плазмонные и оптические свойства, для наноинженерных задач.
Возможно проведение синтеза экспонирующих заранее заданные нуклеотидные последовательности микрочастиц с функциональными свойствами, соответствующими метке - такими как магнитные свойства, загрузка реагентом, проводимость, плазмонные и оптические свойства, для биоинженерных задач.
Возможно проведение синтеза олиго/полинуклеотидов с множеством последовательностей, до миллиона и более - в одном синтезе, с последующим высвобождением выбранных целевых олиго/полинуклеотидов с отсортированных микрочастиц, тогда и там, где синтезированные олиго/полинуклеотиды требуются.
Синтез состоит из последовательности шагов, на каждом из которых к каждой из частиц добавляется один нуклеотид, заранее определённый последовательностью, выбранной для соответствующей метки каждой частицы. Для этого в каждом шаге производится сортировка набора меченых частиц в 4 реактора (фиг. 1 (A, T, G, C)), а каждом из которых производится добавление одного из четырёх олигонуклеотидов, идентичное традиционно применяемому в ДНК-синтезаторах. После добавления нуклеотида, содержимое реакторов объединяется и отправляется в следующий цикл сортировки и синтеза.
Микрочастицы полученные заявленным способом применимы в системах многокомпонентного анализа олиго и полинуклеотидов, системах требующих анализа множества, от сотен до миллионов, различных анализируемых молекул в одном эксперименте. Включая генетическое картирование высокого разрешения, секвенирование, диагностику мутаций, детекцию патогенов по ДНК и РНК, системах основанных на аффинности к аптамерам, в том числе традиционно использующих антитела, системах требующих множества заданных нуклеотидных последовательностей на индивидуальных носителях, в том числе для моделирования биосистем, ДНК-наноинженерии, скринирования последовательностей в разработке биопродуцентов и лекарственных препаратов.
Способ позволяет модифицировать неограниченное количество микрочастиц с уникальными оптическими метками, каждая из которых несёт уникальную, заданную пользователем олиго или полинуклеотидную последовательность. В частности, позволяет создавать наборы микрочастиц, определяющие присутствие и концентрацию миллионов и более различных олигонуклеотидных последовательностей и аффинных к аптамерам веществ.
Производительность современных FACS-ов позволяет производить синтез миллионов последовательностей одновременно, за время, сравнимое с традиционным синтезом одного олиго/полинуклеотида, и с использованием тех же расходников и оборудования.
Большинство представленных на рынке сортировщиков поддерживают сортировку именно в 4 раздельных ёмкости, и требуют лишь программной модификации - изменения алгоритма сортировки в соответствии с таблицей соответствия код-нуклеотид для каждой стадии синтеза.
Аналогичного результата возможно достигнуть иммобилизацией меченых микрочастиц на 2D-матрице ловушек, с последующим проведением фотолитографии, как ранее описано нами для немеченых частиц в RU 2020111673 и Andreyev D.; Zybailov B. Integration of flow cytometry and single cell sequencing. Trends Biotechnol., 2020. 38 (2), p. 133-136. Но подход с иммобилизацией уступает сортировочному, поскольку требует более дорогой и менее надёжной фотохимии, сложен для модификации противоположной от источника света и доступа реагентов стороны иммобилизованных частиц, и отчасти ограничен разрешением литографа для очень больших количеств последовательностей.
Также аналогичного результата возможно достичь иммобилизацией меченых микрочастиц на 2D-матрице ловушек, содержащей совмещённый с ловушками массив микроэлектродов, с последующим проведением электрохимического синтеза (например, электрохимический синтез ДНК-матриц используют GeneScript Inc, CustomArray Inc). Такой подход частично устраняет ограничения фотохимического подхода, но также уступает сортировочному подходу по цене, производительности и надёжности.
Способ обеспечивает проведение аффинных анализов, в том числе аналогичных иммуноглобулиновым, посредством выращивания наборов аптамеров с аффинностью к анализируемым веществам и количеством уникальных, различимых аптамеров в миллионы и более.
Наборы микрочастиц, несущих уникальные флуоресцентные метки, олиго- либо полинуклеотидами/аптамерами с задаваемой пользователем последовательностью, уникальной для каждой метки, применимы в системах и способах анализа олиго- и полинуклеотидов, включая генетическое картирование, секвенирование, диагностику мутаций, детекцию патогенов по ДНК и РНК, многокомпонентном анализе, основанном на аффинности к аптамерам, для моделирования биосистем, в ДНК-наноинженерии, скринировании последовательностей, в разработке биопродуцентов и лекарственных препаратов.
Изобретение относится к области биотехнологии. Описан способ модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, включающий формирование нуклеотидной последовательности на микрочастице. Технический результат - получение набора микрочастиц с уникальными флуоресцентными метками, несущих заранее заданные пользователем последовательности нуклеотидов на каждой микрочастице, последовательности, индивидуальные для каждой метки. 1 ил.
Способ модификации больших наборов микрочастиц, несущих уникальные флуоресцентные метки, включающий формирование нуклеотидной последовательности на микрочастице, характеризующийся тем, что на каждой микрочастице формируют олигонуклеотид, либо аптамер, либо полинуклеотид с предварительно заданной последовательностью нуклеотидов, уникальной для каждой флуоресцентной метки микрочастиц, осуществляют синтез олигонуклеотида, либо аптамера, либо полинуклеотида циклически с применением сортировки микрочастиц по флуоресцентной метке на каждом цикле синтеза, на каждом цикле к каждой из микрочастиц добавляется один нуклеотид заранее определённой уникальной последовательности, выбранной для соответствующей уникальной флуоресцентной метки каждой микрочастицы, сортировку набора меченых микрочастиц на каждом цикле синтеза выполняют применяя сортировщик клеток, активируемый флуоресценцией, сортировку набора меченых микрочастиц производят в четыре реактора A, T, G, C, в каждом из реакторов к микрочастицам добавляют один из четырёх олигонуклеотидов A, T, G, C, после добавления нуклеотида содержимое реакторов объединяют, перемешивают миксером и отправляют на следующий цикл сортировки и синтеза, причем сортировку и синтез производят с использованием управляемых компьютером сортировщика клеток, активируемого флуоресценцией, миксера, реакторов.
Авторы
Даты
2024-10-30—Публикация
2022-02-11—Подача