Область техники, к которой относится изобретение
По настоящей заявке испрашивается преимущество по заявке Кореи № 10-2020-0044598, поданной 13 апреля 2020 г., и по заявке Кореи № 10-2021-0036863, поданной 22 марта 2021 г. в Патентное ведомство Кореи , раскрытия которых во всей их полноте включены в настоящее изобретение в качестве ссылки.
Настоящее изобретение относится к производному пиразола, применимому для предупреждения или лечения фиброза легких, способу его получения, и содержащей его фармацевтической композиции.
Уровень техники
Фиброз легких (PF) представляет собой тип хронического интерстициального заболевания легких и характеризуется инфильтрацией воспалительных клеток, таких как лимфоциты и макрофаги в интерстициальную ткань легких, пролиферацией фибробластов и осаждение волокнистой соединительной ткани в интерстициальной ткани легких. Фиброз легких вызван разными внутренними и внешними этиологическими причинами и является результатом хронического поражения легких или заболевания, прогрессирующего до конца, и серьезно угрожает здоровью человека.
Этиология фиброза легких включает такие факторы, как нарушение иммунитета, вирусная или бактериальная инфекция, лекарственные средства и химикаты, радиация и загрязнение воздуха (смог, сигаретный дым, пыль и т. п.).
Как отмечено выше, имеются пациенты, у которых можно выявить ясные причины фиброза легких, но также имеются случаи, когда причину невозможно выяснить, и такие случаи называются идиопатическим фиброзом легких (IPF). Идиопатический фиброз легких является типом интерстициальной пневмонии, при которой фиброз паренхимы легких постепенно прогрессирует, и известно, что существует риск смерти вследствие нарушения дыхания в течение нескольких лет после постановки диагноза и с очень плохим прогнозом. 5-Летняя выживаемость составляет примерно 20%, аналогично раку легких. Кроме того, частота и распространенность фиброза легких быстро увеличиваются при старении населения.
Фиброз легких является сложным патологическим и психофизическим процессом, при котором на ранней стадии большое количество воспалительных клеток инфильтруются вокруг центра воспаления легких и вызывают хроническое утолщение стенок альвеол и на средней/терминальной стадии нормальная структура ткани легких разрушается вследствие избыточного роста, деформации альвеол, затвердевания и рубцевание ткани легких, вызванного чрезмерным осаждением элементов внеклеточного матрикса, таких как коллаген, фибробластами, что приводит к потере функции.
Фибробласты играют роль в поступлении иммунных клеток в центры воспаления и повреждение тканей. Кроме того, фибробласты продуцируют многие воспалительные цитокины и реагируют на них. таким образом, фибробласты могут вносить вклад в хроническое воспаление и, напротив, воспалительные цитокины стимулируют превращение фибробластов в миофибробласты, тем самым стимулируя фиброз. Поэтому поражение или воспаление ткани легких может привести к фиброзу легких.
Трансплантация легкого является единственным способом восстановления ткани легких с прогрессирующим фиброзом вследствие фиброза легких и 5-летняя выживаемость после диагностики составляет лишь 43%.
Хотя проведены многие клинические исследования для разработки терапевтического средства для фиброза легких, пока еще нет терапевтического средства для фиброза легких, и в качестве средства первой линии в основном используют иммуносупрессанты, которые является стероидными или цитотоксичными лекарственными средствами. Из стероидных и цитотоксичных лекарственных средств, первыми используют стероиды и в настоящее время используют комбинированную терапию из стероидов и азатиоприна или циклофосфамида.
Кроме того, пирфенидон и нинтеданиб являются единственными лекарственными средствами, утвержденными для лечения фиброза легких. Сообщали, что пирфенидон оказывает умеренное терапевтическое воздействие и используется в очень большой дозе, равной примерно 2,4 г/сутки, но наблюдается небольшое увеличение продолжительности жизни или нет значительного его увеличения и, поскольку он проявляет тенденцию к ухудшению качестве жизни пациентов вследствие тяжелых побочных эффектов, таких как желудочно-кишечные нарушения (тошнота, диарея, диспепсия), нарушений кожи (светочувствительная сыпь) и метаболические нарушения и нарушения питания (анорексия, отсутствие аппетита) и ослабляет функцию печени, постоянное введение затруднительно. Сообщали, что нинтеданиб используют в дозе, равной от 200 до 400 мг/сутки и от уменьшает частоту сильных обострений при идиопатическом фиброзе легких от умеренного до тяжелого, но постоянное введение затруднительно вследствие многих побочных эффектов и желудочно-кишечных побочных эффектов.
Поэтому, настоятельно необходима разработка новых лекарственных средств, которые могут лечить лежащую в основе причине, а не облегчать прогрессирование симптомов заболевания.
Хотя проведено много исследований причин фиброза легких, патогенез все еще неясен, что затрудняет разработку терапевтических средств, но опубликованы результаты исследований, что важную роль в прогрессировании и обострении фиброза легких играет окислительный стресс, вызванный образованием чрезмерного количества активированного кислорода в соответствии с изменениями окислительно-восстановительного гомеостаза in vivo.
Окислительный стресс означает поражение тканей, вызванное относительно избыточным образованием реакционноспособных кислородсодержащих частиц, поскольку нарушается баланс между образованием реакционноспособных кислородсодержащих частиц (ROS) и антиоксидантным защитным механизмом для биомолекул, клеток и тканей. В частности, сообщали, что окислительный стресс, проявляющийся в ткани легких, вызывает и ухудшает фиброз легких. Сообщали, что стимулирование посредством TGF-β в ткани легких пациентов с прогрессирующим фиброзом легких вызывает усиление образования реакционноспособных кислородсодержащих частиц и увеличивает экспрессию коллагена и α-актина гладких мышц (α-SMA), которые важны для фиброза. В частности, сообщали, что фиброз легких ухудшается вследствие реакционноспособных кислородсодержащих частиц в ткани легких пациентов с идиопатическим фиброзом легких.
Инфекция RNA-вирусом или DNA-вирусом также вызывает неизлечимое поражение легких посредством пневмонии и фиброза легких, приводящее к смерти. Сообщали, что, когда однонитевые вирусы (коронавирус, вирус гриппа, респираторно-синцитиальный вирус, риновирус, вирус денге, HIV и т. п.) и DNA-вирусы (аденовирус, вирус вакцины, вирус простого герпеса и т. п.) проникают в клетки и образуют эндосомы, образуются реакционноспособные кислородсодержащие частицы для стимулирования репликации вируса и быстро амплифицированный вирус проникате в ткань легких и вызывает поражение легких, стимулируя воспаление и фиброз.
В настоящее время в случае вирусной инфекции быстрая амплификация в теле человека быстро вызывает поражение легких, делая лечение затруднительным, и таким образом, если терапевтическое средство для подавления образования реакционноспособных кислородсодержащих частиц и противовирусное средство используют в комбинации для лечения и облегчения протекания поражения легких, вызванного вирусной инфекцией и быстрой амплификацией, будет возможно более эффективно лечить пневмонию и фиброз легких. В этом случае в качестве противовирусных средств, которые можно использовать в комбинации, типичные лекарственные средства включают ремдесивир, ритонавир, лопинавир, фавилавир и т. п.
Сообщали, что стимулирование посредством TGF-β в ткани легких пациентов с прогрессирующим фиброзом легких вызывает усиление образования реакционноспособных кислородсодержащих частиц и увеличивает экспрессию коллагена и α-актина гладких мышц (α-SMA), которые важны для фиброза, и сообщали, что фиброз легких ухудшается вследствие реакционноспособных кислородсодержащих частиц в ткани легких пациентов с идиопатическим фиброзом легких.
С другой стороны, ни в одном из документов предшествующего уровня техники не раскрыто, что соединение на основе пиразола, предлагаемое в настоящем изобретении, эффективно для предупреждения и лечения фиброза легких.
[Документы предшествующего уровня техники]
(Патентный документ 1) Korean Patent No. 10-1280160
(Патентный документ 2) Korean Patent Application Laid-Open No. 10-2019-0122806
(Патентный документ 3) Korean Patent Application Laid-Open No. 10-2019-0136079
(Непатентный документ 1) Gabriel Laghlali, et al. Respiratory 2019, 13629.
(Непатентный документ 2) Eunice E. To et al. Nature communications, 8(69), 1-17.
(Непатентный документ 3) Alessandro G. Fois, Panagiotis Paligiannis et al., Respir Res. 2018, 19:51.
Раскрытие
Техническая задача
Задачей настоящего изобретения является получение фармацевтической композиции, содержащей соединение формулы 1 или его фармацевтически приемлемую соль.
Другой задачей настоящего изобретения является получение фармацевтической композиции для эффективного подавления образования реакционноспособных кислородсодержащих частиц, содержащей соединение формулы 1 или его фармацевтически приемлемую соль.
Другой задачей настоящего изобретения является получение фармацевтической композиции для лечения или предупреждения фиброза легких, содержащей соединение формулы 1 или его фармацевтически приемлемую соль.
Другой задачей настоящего изобретения является разработка способа предупреждения или лечения фиброза легких путем введения индивидууму соединения формулы 1 или его фармацевтически приемлемой соли.
Другой задачей настоящего изобретения является разработка применения соединения формулы 1 или его фармацевтически приемлемой соли для предупреждения или лечения фиброза легких.
Другой задачей настоящего изобретения является получение фармацевтической композиции для лечения и предупреждения фиброза легких, дополнительно содержащей соединение формулы 1 или его фармацевтически приемлемую соль и антибиотик, фунгицидный агент, противовирусное средство, противовоспалительное средство или любую их комбинацию.
Другой задачей настоящего изобретения является разработка способа предупреждения или лечения фиброза легких путем дополнительного введения индивидууму соединения формулы 1 или его фармацевтически приемлемой соли и антибиотика, фунгицидного агента, противовирусного средства, противовоспалительного средства или любой их комбинации.
Другой задачей настоящего изобретения является разработка применения соединения формулы 1 или его фармацевтически приемлемой соли и антибиотика, фунгицидного агента, противовирусного средства, противовоспалительного средства или любой их комбинации для предупреждения или лечения фиброза легких.
Другой задачей настоящего изобретения является получение противовирусного средства, содержащего соединение формулы 1 или его фармацевтически приемлемую соль.
Другой задачей настоящего изобретения является разработка способа предупреждения или лечения вирусного заболевания путем введения индивидууму соединения формулы 1 или его фармацевтически приемлемой соли.
Другой задачей настоящего изобретения является разработка применения соединения формулы 1 или его фармацевтически приемлемой соли для предупреждения или лечения вирусного заболевания.
Техническое решение
Для решения указанных выше задач настоящее изобретение относится к композиции для предупреждения или лечения фиброза легких или вирусного заболевания, содержащей соединение на основе пиразола, описывающееся следующей формулой 1, или его фармацевтически приемлемую соль:
Формула11
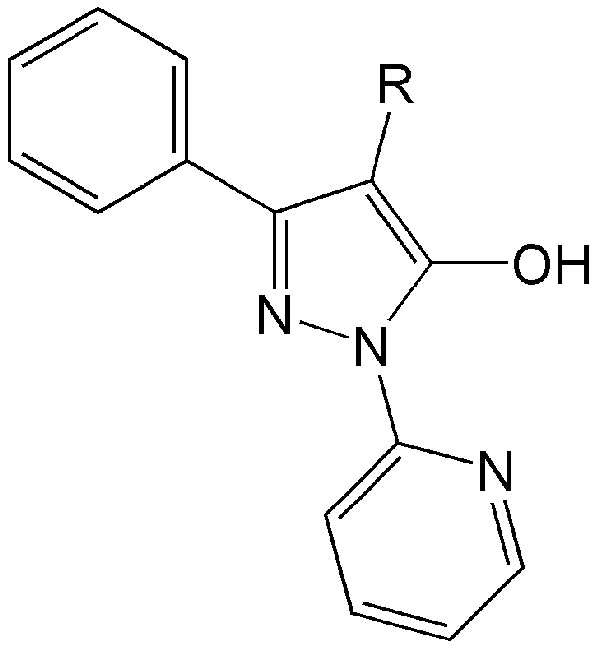
где R означает линейную или разветвленную алкильную группу, содержащую от 1 до 10 атомов углерода.
Полезные эффекты
Соединение на основе пиразола, предлагаемое в настоящем изобретении, или его фармацевтически приемлемая соль может эффективно подавлять образование реакционноспособных кислородсодержащих частиц, образующихся в легких, и таким образом может успешно использоваться для предупреждения или лечения вызванного окислительным стрессом фиброз легких без каких-либо существенных побочных эффектов.
Кроме того, соединение на основе пиразола, предлагаемое в настоящем изобретении, или его фармацевтически приемлемая соль обладает противовирусной активностью, и таким образом может с успехом применяться для предупреждения или лечения вирусного заболевания.
Описание чертежей
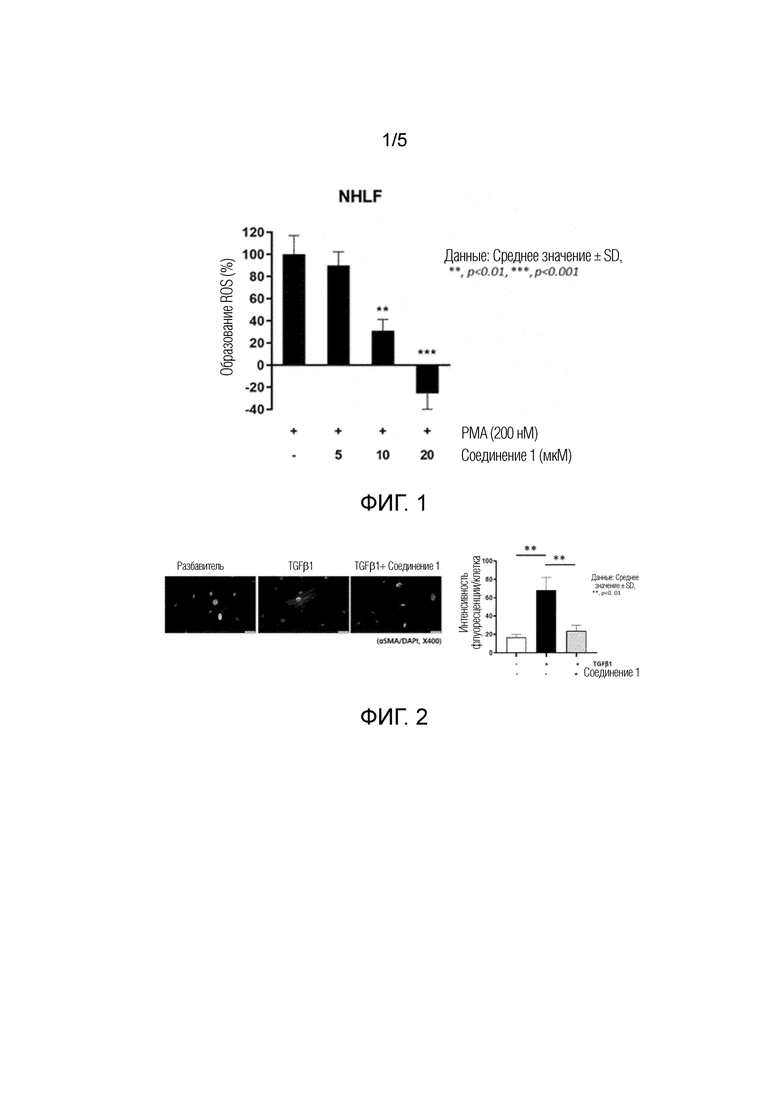
На фиг. 1 приведен результат эффективного подавления при обработке соединением 1 вызванной стимулированием посредством PMA экспрессии реакционноспособных кислородсодержащих частиц в нормальных фибробластах легких человека (NHLFs).
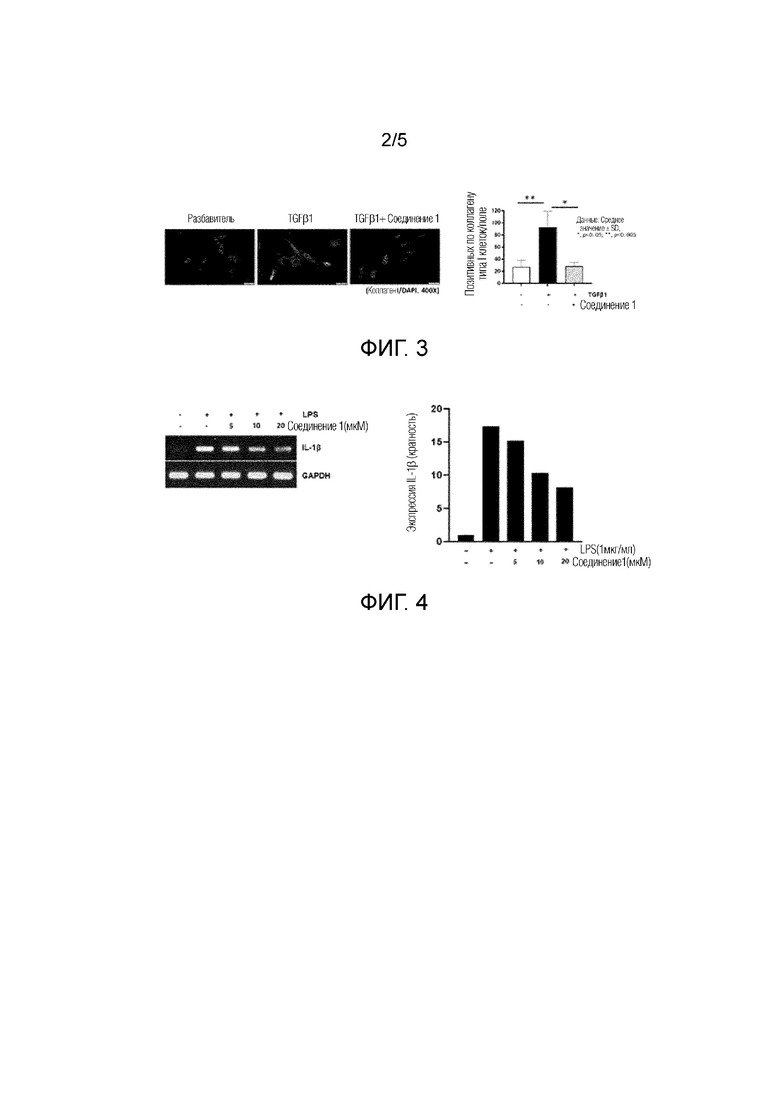
На фиг. 2 приведены результаты подавления при обработке соединением 1 вызванной посредством TGF-β1 экспрессии αSMA во время дифференциации нормальных фибробластов легких человека в миофибробласты.
На фиг. 3 приведены результаты подавления при обработке соединением 1 вызванной посредством TGF-β1 экспрессии коллагена I во время дифференциации нормальных фибробластов легких человека в миофибробласты.
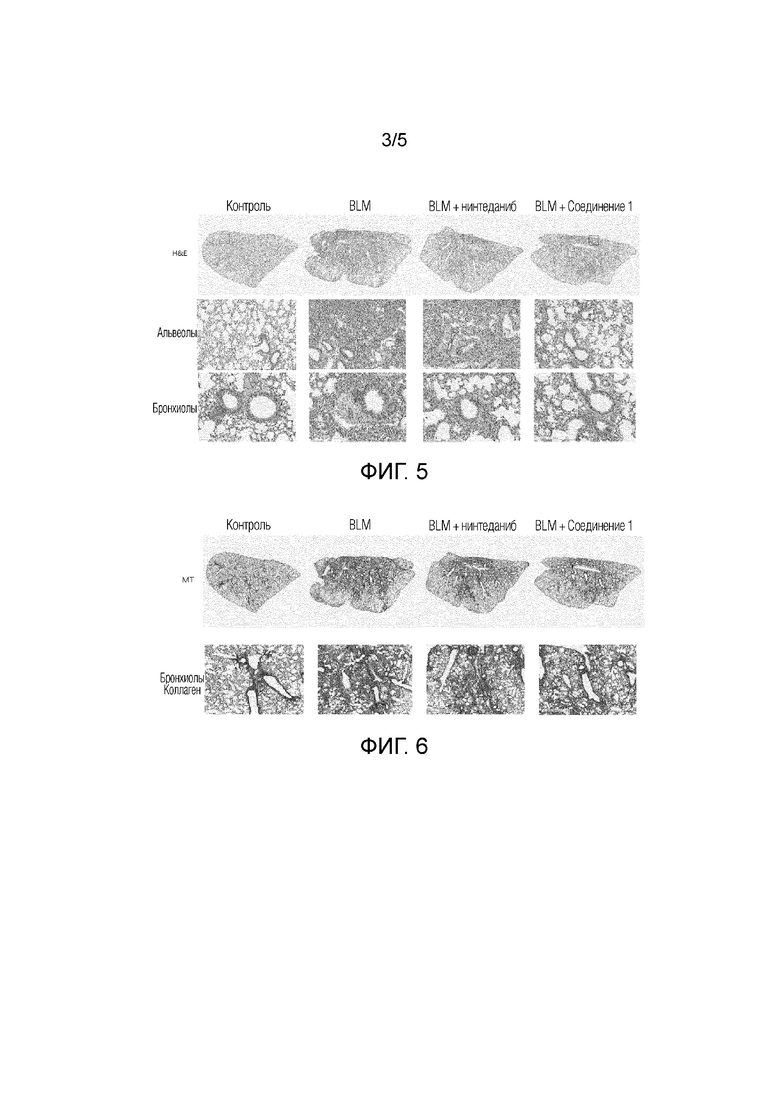
На фиг. 4 приведен результат эффективного подавления при обработке соединением 1 вызванной посредством LPS экспрессии IL-1β в нормальных фибробластах легких человека.
На фиг. 5 приведены фотографии, демонстрирующие окрашивание с помощью H&E альвеол и бронхиол при обработке нинтеданибом или соединением 1 в модели на животных с вызванным блеомицином фиброзом легких (BLM) и приведены данные по уменьшению количества иммунных клеток, проникших в альвеолы и бронхиолы при введении соединения 1.
На фиг. 6 приведены фотографии, демонстрирующие осаждение коллагена в бронхиолах по данным окрашивания при введении нинтеданиба или соединения 1 в модели на животных с вызванным блеомицином фиброзом легких (BLM) и приведены данные по уменьшению осаждения коллагена при введении соединения 1.
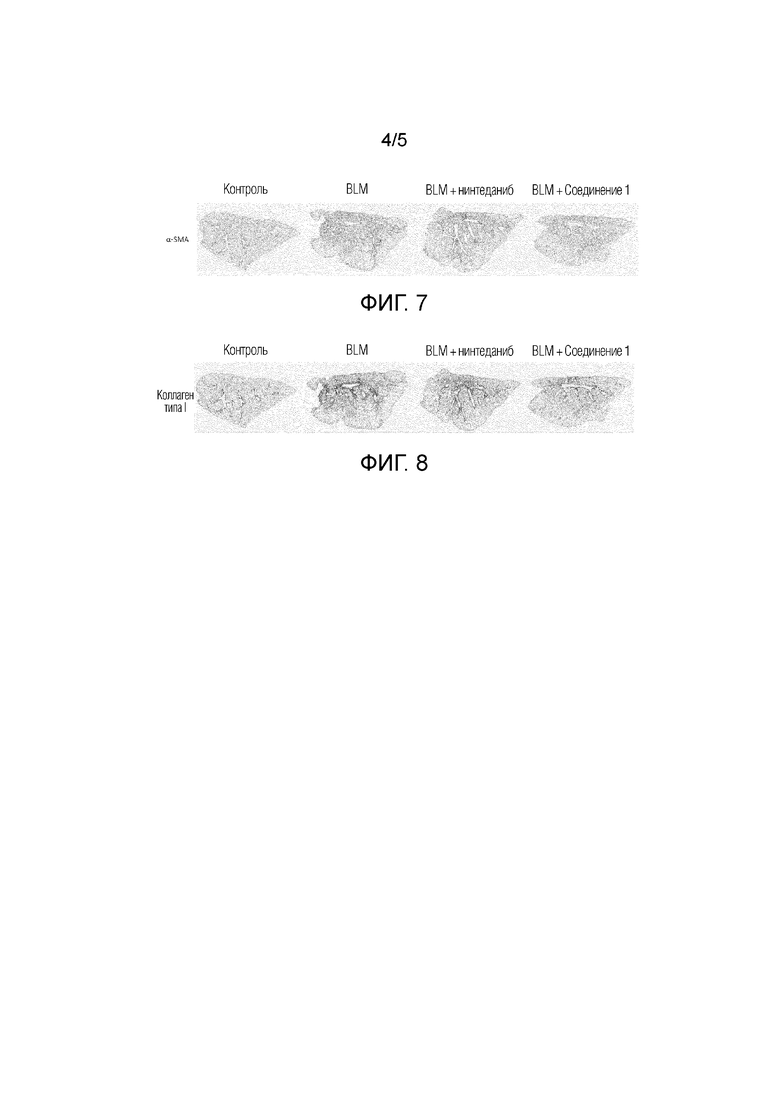
На фиг. 7 приведены фотографии, демонстрирующие окрашивание αSMA при введении нинтеданиба или соединения 1 в модели на животных с вызванным блеомицином фиброзом легких (BLM) и показано уменьшение экспрессии αSMA при введении соединения 1.
На фиг. 8 приведены фотографии, демонстрирующие окрашивание коллаген Iа при введении нинтеданиба или соединения 1 в модели на животных с вызванным блеомицином фиброзом легких (BLM) и показано уменьшение экспрессии коллагена I при введении соединения 1.
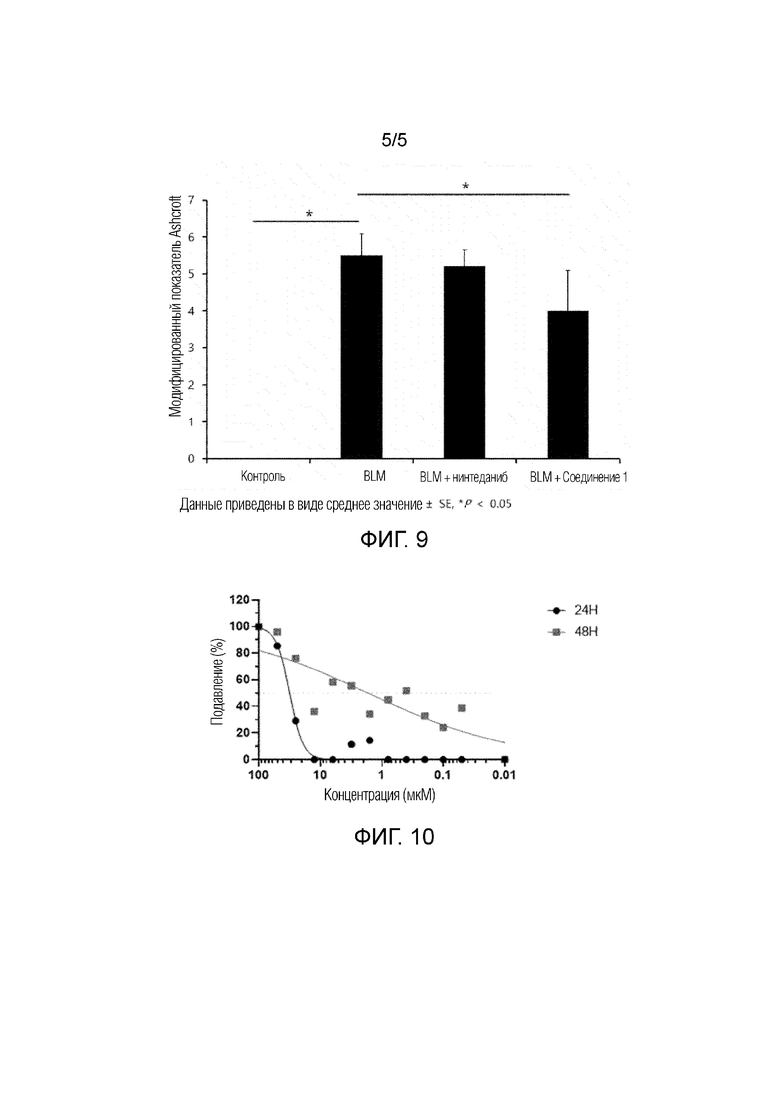
На фиг. 9 приведен результат количественного определения степени фиброза легких по улучшенной шкале Ashcroft при введении нинтеданиба или соединения 1 в модели на животных с вызванным блеомицином фиброзом легких (BLM) и показано эффективное улучшение состояния фиброза легких при введении соединения 1 по сравнению со случаем введения нинтеданиба.
На фиг. 10 показано, что для эпителиальных клеток легких человека противовирусная эффективность является превосходной и цитотоксичность является низкой при введении соединения 1.
Наилучший вариант осуществления
Ниже настоящее изобретение подробнее описано со ссылкой на варианты осуществления.
Однако настоящее изобретение не ограничивается вариантами осуществления, которые приведены в качестве примера, и настоящее изобретение определяется объемом прилагаемой формулы изобретения. Кроме того, даже если имеется положение, существенное для практического осуществления настоящего изобретения, опущено специальное описание этого положения, которое может легко осуществить специалист в данной области техники.
Термины и слова, использующиеся в настоящем описании и формуле изобретения не следует считать ограниченными обычными или приведенными в словарях значениями, а следует считать согласующимися со значениями и понятиями технической идеи настоящего изобретения, основанной на принципе, которым автор настоящего изобретения может надлежащим образом определить понятие термина для наилучшего описания его собственного изобретения.
Термины, использующиеся в настоящем изобретении, предназначены только для описания конкретного варианта осуществления и не предназначены для ограничения настоящего изобретения. Термины в единственном числа включают термины во множественном числа, если из контекста явно не следует иное. В настоящем изобретении такие термины, как "включает" и "содержит" предназначены для указания того, что имеется признак, количество, стадия, операция, компонент, часть или их комбинация, описанные в описании, и следует понимать, что термины заранее не исключают возможность наличия или добавления одного или большего количества других признаков, количеств, стадий, операций, компонентов, частей или их комбинации.
Фиброз легких является фиброз паренхимы легких, вызванный инфильтрацией воспалительных клеток в интерстициальную ткань легких, пролиферацией фибробластов и осаждение волокнистой соединительной ткани в интерстициальной ткани легких вследствие воспаления легких, и нормальная структура ткани легких разрушается, что приводит к потере функции легких. Таким образом, фиброз легких вызван разными внутренними и внешними этиологическими причинами и является результатом хронического поражения легких или заболевания, прогрессирующего до конца, и частота и распространенность фиброза легких быстро увеличиваются в соответствии с современной тенденции к старению населения. Недавно проблемой стал, в частности, идиопатический фиброз легких неизвестной причины.
Трансплантация легкого является единственным способом восстановления ткани легких с прогрессирующим фиброзом вследствие фиброза легких и пирфенидон и нинтеданиб являются единственными лекарственными средствами, утвержденными для лечения фиброза легких, оба лекарственные средства сопряжены с тем затруднением, что постоянное введение трудно проводить вследствие множества побочных эффектов и желудочно-кишечных нарушении.
Поэтому методикой лечения фиброза легких обычно является симптоматическая терапия для смягчения симптомов с использованием стероидов или иммуносупрессантов, но необходим основополагающий способ лечения.
В результате исследований, основанных на том факте, что терапевтическое средство для фиброза легких можно разработать, если эффективно подавить возникновение окислительного стресса в ткани легких, авторы настоящего изобретения завершили его путем установления того, что производное пиразола, предлагаемое в настоящем изобретении, уменьшает вызванное введением блеомицина поражение легких и подавляет вызванный накоплением αSMA и коллагена I фиброз легких, тем самым уменьшая фиброз легких, и подтвердили, что его можно использовать в качестве терапевтического средства для фиброза легких.
Соответственно, настоящее изобретение относится к фармацевтической композиции, способной предупреждать или лечить фиброз легких, содержащей одно или большее количество соединений, выбранное из группы, включающей соединение на основе пиразола, описывающееся формулой 1, или его фармацевтически приемлемую соль.
Кроме того, настоящее изобретение относится к фармацевтической композиции, способной предупреждать или лечить идиопатический фиброз легких, содержащей одно или большее количество соединений, выбранное из группы, включающей соединение на основе пиразола, описывающееся формулой 1, или его фармацевтически приемлемую соль.
Соединение на основе пиразола, применяющееся в настоящем изобретении, описывается следующей формулой 1:
<Формула 1>

где R означает линейную или разветвленную алкильную группу, содержащую от 1 до 10 атомов углерода.
Фармацевтически приемлемая соль соединения на основе пиразола, включенная в фармацевтическую композицию, предлагаемую в настоящем изобретении, относится к солям, которые сохраняют биологическую эффективность и характеристики исходного соединения и не вредны биологически или в другом отношении при введении в разовой дозе. Кроме того, она означает соль, обычно использующуюся в фармацевтической промышленности.
В частности, фармацевтически приемлемые соли присоединения с основанием можно получить из неорганических и органических оснований. Соли, образованные из неорганических оснований, могут включать, но не ограничиваются только ими, соли натрия, калия, лития, аммония, кальция и магния. Соли, образованные из органических оснований, включают, но не ограничиваются только ими, соли первичных, вторичных и третичных аминов; замещенных аминов, включая природные замещенные амины; и изопропиламина, триметиламина, диэтиламина, триэтиламина, трипропиламина, этаноламина, 2-диметиламиноэтанола, трометамина, лизина, аргинина, гистидина, кофеина, прокаина, гидрабамина, холина, бетаина, этилендиамина, глюкозамина, N-алкилглюкамина, теобромина, пурина, пиперазина, пиперидина и/или циклических аминов, включая N-этилпиперидин.
Также следует понимать, что другие производные карбоновых кислот, в частности, амиды карбоновых кислот, включая карбоксамиды, низшие алкилкарбоксамиды, ди(низший алкил)карбоксамиды и т. п., также применимы при практическом осуществлении настоящего изобретения.
Кроме того, фармацевтически приемлемые соли присоединения с кислотами можно получить из неорганических и органических кислот. Соли, образованные из неорганических кислот, включают соли хлористоводородной кислоты, бромистоводородной кислоты, серной кислоты, азотной кислоты, фосфорной кислоты, хрорной кислоты, йодной кислоты, винной кислоты и т. п. Соли, образованные из органических кислот могут включать, но не ограничиваются только ими, соли уксусной кислоты, трифторуксусной кислоты, пропионовой кислоты, гликолевой кислоты, глюконовой кислоты, галактуроновой кислоты, глутаминовой кислоты, глутаровой кислоты, глюкуроновой кислоты, аспарагиновой кислоты, аскорбиновой кислоты, угольной кислоты, ванильной кислоты, йодистоводородной кислоты, пировиноградной кислоты, щавелевой кислоты, яблочной кислоты, малоновой кислоты, молочной кислоты, янтарной кислоты, малеиновой кислоты, фумаровой кислоты, винной кислоты, лимонной кислоты, бензойной кислоты, коричной кислоты, миндальной кислоты, метансульфоновой кислоты, этансульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты, нафталинсульфоновой кислоты и/или салициловой кислоты и т. п.
Фармацевтически приемлемой солью может быть гидрохлорид.
Примером соединения на основе пиразола, описывающегося формулой 1, или его фармацевтически приемлемой соли, включенного в фармацевтическую композицию, предлагаемую в настоящем изобретении, являются следующие:
3-фенил-4-метил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-этил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-изопропил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-бутил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-трет-бутил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-пентил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-гексил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид.
В частности, соединением на основе пиразола, включенным в фармацевтическую композицию, предлагаемую в настоящем изобретении, может быть 3-фенил-4-н-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид.
Соединение формулы 1, предлагаемое в настоящем изобретении, может подавлять образование реакционноспособных кислородсодержащих частиц.
В настоящем изобретении окислительный стресс означает поражение тканей, вызванное относительно избыточным образованием реакционноспособных кислородсодержащих частиц, поскольку нарушается баланс между образованием реакционноспособных кислородсодержащих частиц (ROS) и антиоксидантным защитным механизмом для биомолекул, клеток и тканей. В этом случае "реакционноспособные кислородсодержащие частицы" могут означать активированный кислород, активный кислород и активированные кислородсодержащие частицы, что означает одно и то же вещество.
Соединение на основе пиразола, предлагаемое в настоящем изобретении, в частности, гидрохлорид 3-фенил-4-н-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ола (соединение 1) эффективно снижает содержание реакционноспособных кислородсодержащих частиц в эпителиальных клетках легких человека, и эффективно подавляет экспрессию αSMA и коллагена I, которые являются маркерами дифференциации миофибробластов, когда фибробласты легких дифференцируются в миофибробласты.
Кроме того, как подтверждено экспериментами в моделях на животных с вызванным введением блеомицина фиброзом легких, соединение, предлагаемое в настоящем изобретении, уменьшает инфильтрацию воспалительных клеток в ткань легких, снижает гипертрофию эпителиальных клеток легких, снижает деформацию структуры легких и уменьшает участок аномального осаждения в ткани по сравнению с нинтеданибом, который утвержден в качестве обычного терапевтического средства для фиброза легких.
Соединение, предлагаемое в настоящем изобретении, снижает экспрессию и накопление коллагена I и αSMA в ткани легких и также снижает экспрессию реакционноспособных кислородсодержащих частиц в ткани легких по сравнению с нинтеданибом. На основании этих результатов при использовании количественной оценки тяжести фиброза по улучшенной шкале Ashcroft продемонстрирован заметный эффект улучшения фиброза легких по сравнению со случаем использования нинтеданиба, который утвержден в качестве обычного терапевтического средства для фиброза легких.
Поэтому подтверждено, что соединение, предлагаемое в настоящем изобретении, не только подавляет воспалительный ответ путем подавления реакционноспособных кислородсодержащих частиц в клетках ткани легких человека и в моделях фиброза легких, но и также предупреждает или облегчает фиброз легких путем снижения экспрессии и накопления коллагена I и αSMA.
Фиброз легких может быть вызван воспалительным фиброзом легких, хроническим обструктивным заболеванием легких (COPD), объединенным с фиброзом легких, идиопатическим фиброзом легких (IPF) или астмой.
Кроме того, пневмония, которую можно назвать основной причиной фиброза легких, может быть вызвана вирусной пневмонией, бактериальной пневмонией, грибковой пневмонией, гиперчувствительным пневмонитом, аспирационной пневмонией, интерстициальным заболеванием легких, пневмокониозом и т. п.
Вирусная пневмония может быть вызвана вирусом, выбранным из группы, состоящей из следующих: аденовирус, вирус вакцины, вирус простого герпеса, паравирус гриппа, риновирус, вирус ветряной оспы, вирус кори, респираторно-синцитиальный вирус, вирус денге, вирус иммунодефицита человека (HIV), вирус гриппа, коронавирус, связанный с тяжелым острым респираторным синдромом коронавирус (SARS-CoV), связанный с тяжелым острым респираторным синдромом коронавирус 2 (SARS-CoV2), связанный с ближневосточным респираторным синдромом коронавирус (MERS-CoV) или вариантными вирусами этих вирусов.
Фармацевтическая композиция, предлагаемая в настоящем изобретении, в дополнение к соединению формулы 1 или его соли может дополнительно содержать антибиотик, фунгицидный агент, противовирусное средство, противовоспалительное средство или любую их комбинацию в качестве второго терапевтического средства.
В частности, антибиотик, включенный во второе терапевтическое средство, представляет собой гентамицин, канамицин, стрептомицин, амикацин, неомицин и т. п. из аминогликозидных антибиотиков; эритромицин, азитромицин, кларитромицин и т. п. из макролидных антибиотиков; пенициллин, цефалоспорин, карбапенем, монобактам и т. п. из бета-лактамных антибиотиков; клиндамицин и т. п. в качестве линкомициновых антибиотиков; линезолид и т. п. в качестве оксазолидиноновых антибиотиков; ципрофлоксацин, левофлоксацин, моксифлоксацин, фторхинолон и т. п. в качестве хинолонового антибиотика; тетрациклин, доксициклин, тигециклин и т. п. в качестве тетрациклиновых антибиотиков; триметоприм/сульфаметоксазол (TMX/SMX) в качестве сульфонамидных антибиотиков; или их комбинацию.
Противовирусное средство, включенное во второе терапевтическое средство, представляет собой тиосемикарбазон, метисазон, ацикловир, ремдецивир, ритонавир, лопинавир, фавиравир, идоксуридин, видарабин, рибавирин, ганцикловир, фамцикловир, валацикловир, цидофовир, валганцикловир, бривудин, рибавирин, римантадин, тромантадин, фоскарнет, саквинавир, индинавир, нелфинавир, ампренавир, фосампренавир, атазанавир, типранавир, зидовудин, диданозин, залцитабин, ставудин, ламивудин, абакавир, тенофовир дизопроксил, адефовир дизопроксил, эмтрицитабин, энтекавир, невирапин, делавирдин, эфавиренз, занамивир, осельтамивир, инозин pranobex, плеконарил, энфувиртид или их комбинацию.
Фунгицидный агент, включенный во второе терапевтическое средство, представляет собой аллиламин, тербинафин, 5-фторцитозин, флуконазол, итраконазол, кетоконазол, равуконазол, позаконазол, вориконазол, каспофунгин, микафунгин, анидулафунгин, амфотерицин B, липидный комплекс амфотерицина B (ABLC), коллоидную дисперсию амфотерицина B (ABCD), липосомный амфотерицин B (L-AMB), липосомный нистатин, гризеофульвин или их комбинацию.
Соединение формулы 1, предлагаемое в настоящем изобретении, обладает противовирусной активностью по отношению к разным вирусам и таким образом соединение, предлагаемое в настоящем изобретении, само можно использовать, как противовирусное средство. Соответственно, соединение формулы 1, предлагаемое в настоящем изобретении, может быть эффективно для предупреждения или лечения вирусного заболевания. Вирусное заболевание может быть вызвано вирусом, выбранным из группы, состоящей из следующих, но не ограничивается только ими, аденовирус, вирус вакцины, вирус простого герпеса, паравирус гриппа, риновирус, вирус ветряной оспы, вирус кори, респираторно-синцитиальный вирус, вирус денге, вирус иммунодефицита человека (HIV), вирус гриппа, коронавирус, тяжелый острый респираторный синдром коронавирус (SARS-CoV), связанный с тяжелым острым респираторным синдромом коронавирус 2 (SARS-CoV2), связанный с ближневосточным респираторным синдромом коронавирус (MERS-CoV) или вариантными вирусами этих вирусов. В частности, соединение 1, предлагаемое в настоящем изобретении, может эффективно подавлять пролиферацию связанного с тяжелым острым респираторным синдромом коронавируса 2 (SARS-CoV2) и поэтому также может подавлять пролиферацию его родственных вирусов, SARS-CoV, MERS-CoV или вариантных вирусов этих коронавирусов.
Фармацевтическая композиция, предлагаемая в настоящем изобретении, может содержать фармацевтически приемлемый носитель в количестве, не ухудшающем эффекты настоящего изобретения.
"Фармацевтически приемлемый носитель" включает любые и все типы растворителей, дисперсионных сред, покрытий, поверхностно-активных веществ, антиоксидантов, консервантов (антибактериальных или фунгицидных средств), изотонических агентов, разбавителей, агентов, задерживающих всасывание, солей, консервантов, стабилизаторов, связующих, инертных наполнителей, разрыхлителей, смазывающих веществ, подсластителей, вкусовых добавок, красителей и т. п. и их комбинации, известные специалистам в данной области техники. За исключением случаев, когда любой обычный носитель несовместим с активным ингредиентом, подразумевается его применение в терапевтической или фармацевтические композиции.
Разбавитель можно выбрать из группы, состоящей из следующих, но не ограничивается только ими, микрокристаллическая целлюлоза, моногидрат лактозы, лактоза ангидрид, лактоза, крахмал, маннит, карбоксиметилцеллюлоза, сорбит и их комбинации.
Разрыхлитель можно выбрать из группы, состоящей из следующих, но не ограничивается только ими, гидроксипропилцеллюлоза низкой степени замещения, кросповидон, натриевая соль кроскармеллозы, натриевая соль гликолята крахмала, F-melt и их комбинации.
Связующее можно выбрать из группы, состоящей из следующих, но не ограничивается только ими, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, гипромеллоза, поливинилуксусная кислота, повидон, поливинилпирролидон, коповидон, макрогол, лаурилсульфат натрия, легкая безводная кремниевая кислота, синтетический силикат алюминия, производные силикатов, такие как силикат кальция или метасиликат-алюминат магния, фосфаты, такие как гидрофосфат кальция, карбонаты, такие как карбонат кальция, предварительно желатинизированные крахмалы, камеди, такие как камедь акации, желатин, производные целлюлозы, такие как этилцеллюлоза, и их смеси.
Смазывающее вещество можно выбрать из группы, состоящей из следующих, но не ограничивается только ими, стеарат магния, диоксид кремния, тальк, легкая безводная кремниевая кислота, стеарилфумарат натрия и их комбинации.
В качестве агента, регулирующего pH, можно использовать подкисляющий агент, такой как уксусная кислота, адипиновая кислота, аскорбиновая кислота, аскорбат натрия, эфират натрия, яблочная кислота, янтарная кислота, винная кислота, фумаровая кислота и лимонная кислота, и подщелачивающий агент, такой как водный раствор аммиака, карбонат натрия, оксид магния, карбонат магния, цитрат натрия и трехосновной фосфат кальция.
В качестве антиоксиданта можно использовать дибутилгидрокситолуол, бутилированный гидроксианизол, токоферолацетат, токоферол, пропилгаллат, гидросульфит натрия, пиросульфит натрия и т. п.
Кроме того, агенты, предлагаемые в настоящем изобретении, можно приготовить путем выборочного использования разных добавок, выбранных из числа красителей и вкусовых добавок в качестве фармацевтически приемлемых добавок.
В настоящем изобретении на количество добавок не налагаются ограничения и их можно включать в количестве, находящемся в нормальном диапазоне, путем выборочного использования добавок.
Фармацевтическую композицию, предлагаемую в настоящем изобретении, можно приготовить и использовать в виде пероральных препаратов, таких как порошки, гранулы, таблетки, капсулы, суспензии, эмульсии, сиропы и аэрозоли, наружные препараты, суппозитории или растворы для инъекции.
Одним объектом настоящего изобретения может быть фармацевтическая композиция для предупреждения, улучшения протекания или лечения фиброза легких, содержащая активный ингредиент в диапазоне от 0,00001 до 100 мас.%, от 0,0001 до 95 мас.% или от 0,001 до 90 мас.% в пересчете на полную массу фармацевтической композиции.
В терапевтическим средстве для предупреждения или лечения фиброза легких, предлагаемом в настоящем изобретении, доза соединения на основе пиразола, описывающегося формулой 1, или его фармацевтически приемлемой соли может быть надлежащим образом изменена в зависимости от возраста и массы тела пациента, симптомов, пути введения и т. п.
Доза соединения на основе пиразола, описывающегося формулой 1, или его фармацевтически приемлемой соли, предлагаемого в настоящем изобретении, может равняться от 0,00001 мг/кг/сутки до 2000 мг/кг/сутки, от 0,0001 мг/кг/сутки до 1000 мг/кг/сутки, от 0,001 мг/кг/сутки до 800 мг/кг/сутки, от 0,001 мг/кг/сутки до 500 мг/кг/сутки, от 0,001 мг/кг/сутки до 100 мг/кг/сутки, от 0,001 мг/кг/сутки до 80 мг/кг/сутки или от 0,01 мг/кг/сутки до 70 мг/кг/сутки.
Содержание соединения на основе пиразола, описывающегося формулой 1, или его фармацевтически приемлемой соли, предлагаемого в настоящем, изобретении в разовой дозированной форме может равняться от 0,00001 до 100 мас.%, от 0,0001 до 95 мас.%, от 0,0001 до 90 мас.%, от 0,001 до 70 мас.% или от 0,001 до 50 мас.%.
При введении концентрация соединения на основе пиразола, описывающегося формулой 1, или его фармацевтически приемлемой соли, предлагаемого в настоящем изобретении, может равняться от 0,0001 до 500 мкМ, от 0,001 до 300 мкМ, от 0,001 до 150 мкМ, от 0,001 до 130 мкМ, от 0,001 до 100 мкМ, 0,001 до 80 мкМ или от 0,01 до 70 мкМ.
Фармацевтическую композицию, предлагаемую в настоящем изобретении, можно вводить вместе с контрастным веществом или отдельно от него обычным путем и ее можно специально приготовить для внутримышечного, интратекального, проводимого в пищеварительный тракт, внутрисердечно-сосудистого, внутрипочечного или внутривенного введения. В качестве методик приготовления используются обычные методики, известные специалистам в данной области техники.
Обычная композиция для внутримышечного или интратекального введения может состоять из следующих, но не ограничивается только ими, например, активный ингредиент и стерильный изотонический водный раствор, содержащий декстрозу, хлорид натрия или и декстрозу, и хлорид натрия. Другие примеры включают, но не ограничиваются только ими, лактат Рингера для инъекции, лактат Рингера для инъекции+декстроза для инъекции, Normosol-M и декстроза, Isolyte E, активированный раствор Рингера для инъекции и т. п. Предлагаемый препарат необязательно может содержать, но не ограничивается только ими, сорастворитель, такой как полиэтиленгликоль; хелатные агенты, такие как этилендиаминтетрауксусная кислота; и антиоксиданты, такие как метабисульфит натрия. Необязательно без наложения ограничений раствор можно лиофилизировать и затем непосредственно перед введением восстановить с помощью подходящего растворителя.
Предпочтительные примеры приведены для лучшего понимания настоящего изобретения. Следующие примеры не для ограничения настоящего изобретения, а для облегчения понимания настоящего изобретения.
Вариант осуществления изобретения
<Пример синтеза 1> Синтез 3-фенил-4-этил-1-(пиридин-2-ил)-1H-пиразол-5-ола
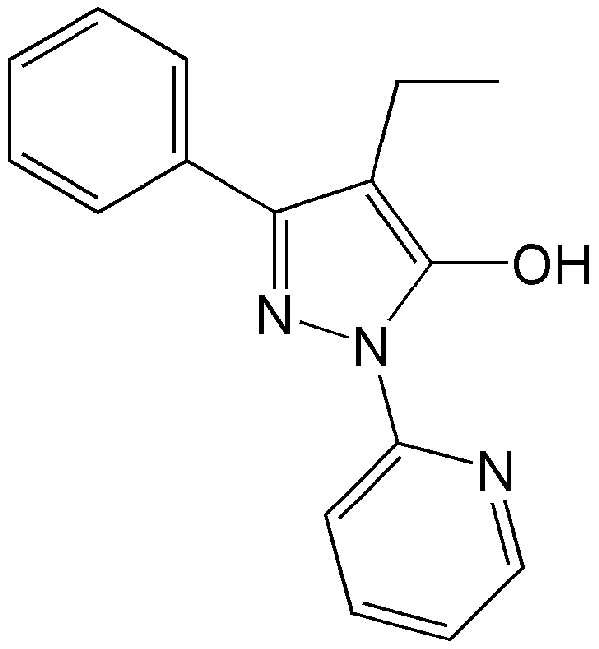
В круглодонной колбе этиловый эфир 2-этил-3-оксо-3-фенилпропионовой кислоты (10,7 г, 49 ммоля) и 2-гидразинопиридин (5,6 г, 51,4 ммоля) кипятили с обратным холодильником в атмосфере азота без растворителя в течение 1 дня. Полученное твердое вещество очищали гексаном и этилацетатом и затем сушили в вакууме и получали искомое соединение с выходом 70%.
1H NMR(300 MHz, DMSO-d6) δ 8,25-8,24(1H, d), 8,00-7,97(1H, d), 7,84-7,82(1H, t), 7,73-7,71(2H, m), 7,46-7,37(3H, m) 7,12-7,11(1H, t), 2,62-2,57(2H, m), 1,23-1,17(3H, m); ESI(m/z) 266,1[M+H]+
<Пример синтеза 2> Синтез 3-фенил-4-бутил-1-(пиридин-2-ил)-1H-пиразол-5-ола
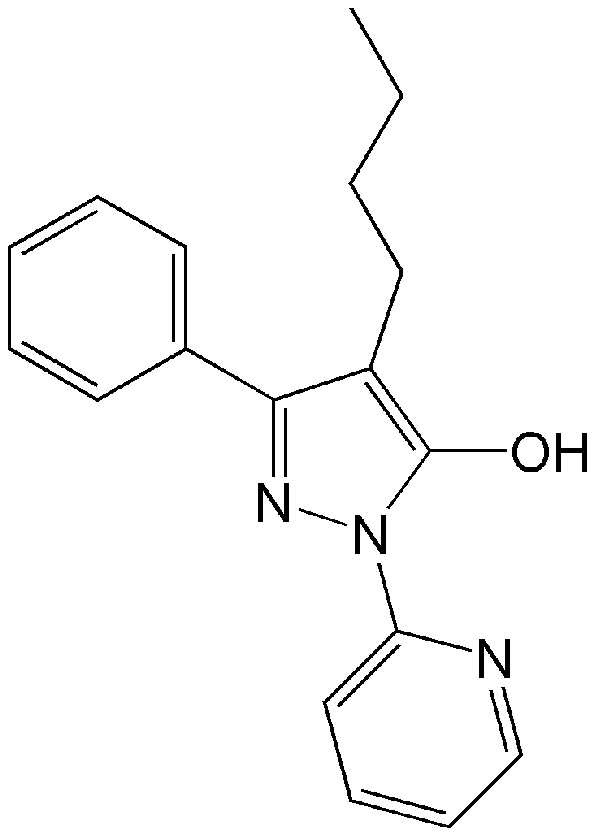
В круглодонной колбе этиловый эфир 2-бутил-3-оксо-3-фенилпропионовой кислоты (12,1 г, 49 ммоля) и 2-гидразинопиридин (5,6 г, 51,4 ммоля) кипятили с обратным холодильником в атмосфере азота без растворителя в течение 1 дня. Полученное твердое вещество очищали гексаном и этилацетатом и затем сушили в вакууме и получали искомое соединение с выходом 75%.
1H NMR(300 MHz, DMSO-d6) δ 8,25-8,24(1H, d), 8,03-8,02(1H, d), 7,85-7,83(1H, t), 7,70-7,69(2H, m), 7,44-7,35(3H, m) 7,12-7,11(1H, t), 2,56-2,53(2H, t), 1,58-1,52(2H, m), 1,38-1,24(2H, m), 0,89-0,86(3H, t); ESI(m/z) 294,0[M+H]+
<Пример синтеза 3> Синтез 3-фенил-4-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ола
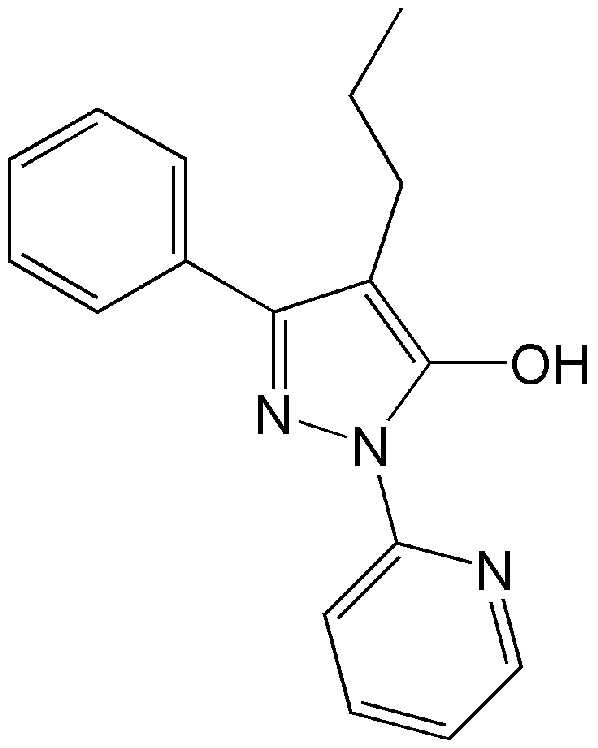
Этиловый эфир 2-пропил-3-оксо-3-фенилпропионовой кислоты (2,52 г, 10,7 ммоля) и 10 мл этанола помещали в круглодонную колбу и затем медленно по каплям к нему при 0°C добавляли раствор 2-гидразинопиридина (1,29 г, 1,18 ммоля), в 3 мл этанола. Его кипятили с обратным холодильником при 100°C в течение 3 дней. Растворитель удаляли путем отгонки при пониженном давлении и полученное твердое вещество промывали гексаном и этилацетатом и затем сушили в вакууме и получали искомое соединение с выходом 82%.
1H NMR(300 MHz, CDCl3) δ 12,50(1H, s), 8,27-8,25(1H, m), 8,01(1H, d, J=8,5 Hz), 7,81(1H, m), 7,69(2H, m), 7,48-7,34(3H, m), 7,12-7,10(1H, m), 2,54(2H, d, J=7,5 Hz), 1,64(2H, m), 0,93(3H, t, J=7,3 Hz); EIMS(70 eV) m/z(rel intensity) 279(M+, 37), 250(100)
<Пример синтеза 4> Синтез гидрохлорида 3-фенил-4-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ола (соединение 1)
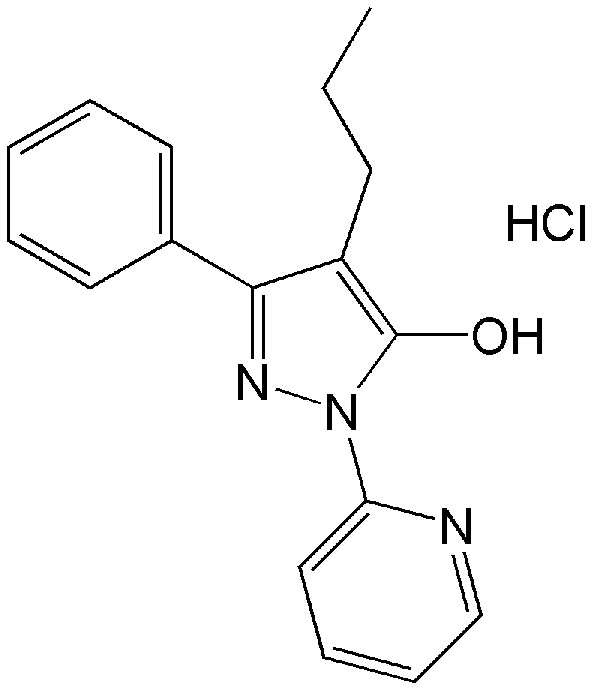
3-Фенил-4-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ол (280 мг, 1,0 ммоля), полученный выше в примере синтеза 3, растворяли в 4 мл этилового эфира в круглодонной колбе и затем к нему медленно по каплям добавляли при 0°C 0,55 мл этилового эфира, растворенного в 2 M HCl. Твердое вещество, образовавшееся из раствора реакционной смеси, отфильтровывали при пониженном давлении, растворитель удаляли, промывали гексаном и этилацетатом и затем сушили в вакууме и получали искомое соединение (270 мг, 0,85 ммоля).
1H NMR(300 MHz, CDCl3) δ 8,44(1H, d, J=4,2 Hz), 8,0-8,03(2H, m), 7,66-7,64(2H, m), 7,48-7,42(3H, m), 7,34-7,30(1H, m), 2,49(2H, brs), 2,43(2H, t, J=7,5 Hz), 1,48(2H, m), 0,48(3H, t, J=7,3 Hz)
< Пример 1> Анализ изменений количества образующихся реакционноспособных кислородсодержащих частиц в нормальных фибробластах легких человека
Для подтверждения влияния соединений примеров синтеза на образование реакционноспособных кислородсодержащих частиц в фибробластах легких образование реакционноспособных кислородсодержащих частиц было вызвано стимулированием посредством PMA в нормальных фибробластах легких человека (NHLFs, Lonza) и при этих условиях наблюдали эффект подавления соединением 1 образования реакционноспособных кислородсодержащих частиц.
Все клетки, суспендированные в культуральной среде, содержащей 10% FBS, высевали в 96-луночный планшет и выращивали в течение 24 ч при условиях 5% CO2 и 37°C. После предварительной обработки соединением 1 в течение от 30 мин до 1 ч стимулирование посредством TGF-β1 или форбол-12-миристат-13-ацетатом (PMA) проводили в каждой лунке, содержащей клетки и лекарственные средства. После дополнительного выращивания в течение 30 мин или 48 ч степень образования реакционноспособных кислородсодержащих частиц подтверждали с помощью 8-амино-5-хлор-7-фенил-2,3-дигидропиридо[3,4-d]пиридазин-1,4-диона (L-012) или диацетата 2',7'-дихлордигидрофлуоресцеина (DCF-DA).
Было подтверждено, что при обработке соединением 1 образование вызванных стимулированием посредством PMA реакционноспособных кислородсодержащих частиц подавлялось зависимым от концентрации образом (фиг. 1).
< Пример 2> Вызванная посредством TGF-β1 экспрессия αSMA и коллагена типа I в нормальных фибробластах легких человека
Для анализа влияния соединения 1 на дифференциацию фибробластов легких в миофибробласты наблюдали подавляющее воздействие соединения 1 на увеличение вызванной TGF-β1 экспрессии α-актина гладких мышц (αSMA) и коллагена типа I (коллаген I) в нормальных фибробластах легких человека (NHLFs, Lonza). Клетки NHLF суспендировали в культуральной среде (FGM-2 Bulletkit media, Lonza) и инокулировали в концентрации 1×104 клеток/лунка в 4-луночную слайд-камеру (Nunc).
После выращивания в течение 24 ч в инкубаторе с CO2 среду заменяли на бессывороточную среду и дополнительно выращивали в течение 12 ч. Затем проводили предварительную обработку разбавителем и с помощью и 2 мМ соединения 1 в соответствующих лунках в течение 1 ч и затем проводили обработку с помощью 10 нг/мл TGF-β1 в каждой лунке кроме лунки с отрицательным контролем (группа с введением разбавителя) в течение 72 ч.
Подтверждение экспрессии αSMA и коллагена I в приготовленных клетках проводили с помощью иммуноцитохимического анализа следующим образом. Клетки фиксировали в 4% параформальдегида в течение 10 мин и пропитывали с помощью 0,1% Triton X-100 и первичных антител (антитела к αSMA Ab, 1:200; антитела к коллагену I Ab, 1:500, реакцию проводили в течение 3 ч при комнатной температуре) и вторичных антител (с Alexa-594 конъюгированный Ab, 1:1000, реакцию проводили в течение 1 ч при комнатной температуре) последовательно проводили процесс обработки и затем экспрессию αSMA и коллагена I исследовали с помощью флуоресцентного микроскопа.
На этом этапе для количественного подтверждения степени экспрессии αSMA и коллагена I подсчитывали количество DAPI (маркер окрашивания ядер клеток)-позитивных клеток и αSMA- и коллаген I-позитивных клеток а каждом поле соответственно и затем рассчитывали содержание в процентах αSMA- и коллаген I-позитивных клеток проводили сопоставление по следующей формуле:
% αSMA (или коллаген I)-позитивных клеток/в поле=αSMA(или коллаген I)-позитивных клеток/DAPI-позитивных клеток×100/поле
Как показано на фиг. 2 и 3, обнаружено, что экспрессия αSMA и коллагена I значительно увеличивалась по сравнению с контрольной группой, когда NHLFs обрабатывали с помощью 10 нг/мл TGF-β1, и увеличение экспрессии обоих маркеров заметно подавлялось, когда обрабатывали соединением 1.
На основании этих результатов подтверждено, что соединение 1 может эффективно подавлять дифференциацию фибробластов легких в миофибробласты, вызванную обработкой с помощью TGF-β1 (см. фиг. 2 и 3).
< Пример 3> Анализ изменений вызванной посредством LPS экспрессии IL-1β
Для подтверждения влияния соединений примеров синтеза, приведенных в настоящем изобретении, на воспалительный ответ в нормальных фибробластах легких (NHLFs, Lonza), исследовали, подавляет ли соединение 1 вызванную посредством LPS увеличенную экспрессию IL-1β
2×105 Клеток инокулировали в 6-луночный планшет, выращивали в течение 24 ч и дополнительно выращивали в течение 16 ч в бессывороточной культуральной среде, и затем предварительно обрабатывали соединением 1 в течение 30 мин при каждый условиях и посредством LPS вызывали воспалительный ответ в течение 6 ч. Экспрессию IL-1β подтверждали с помощью RT-PCR. Полную RNA выделяли из клеток с использованием мини-набора RNeasy (Qiagen) и cDNA синтезировали из 2 мкг выделенной RNA с использованием набора для синтеза PrimeScriptTM II однонитевой cDNA (TaKaRa) и затем для амплификации гена проводили PCR с помощью AccuPower® PCR PreMix (Bioneer). Базовая последовательность для целевого праймера является следующей: IL-1β (прямая: 5′-CCACAGACCTTCCAGGAGAATG-3′, обратная: 5′-GTGCAGTTCAGTGATCGTACAGG-3′); GAPDH (прямая: 5′-GTGGCTGGCTCAGAAAAAGG-3′, обратная: 5′-GGTGGTCCAGGGGTCTTACT-3′); β-актин (прямая: 5′-CACCATTGGCAATGAGCGGTTC-3′, обратная: 5′-AGGTCTTTGCGGATGTCCACGT-3′. Продукт PCR подтверждали электрофорезом на 1,5% агарозном геле.
Как можно видеть на фиг. 4, в результате эксперимента обнаруживается, что при обработке соединением 1 вызванная посредством LPS экспрессия IL-1β эффективно подавлялась зависимым от концентрации образом (см. фиг. 4).
< Пример 4> Подтверждение терапевтического эффекта для фиброза легких в модели на мышах вызванного блеомицином фиброза легких
В модели на мышах вызванного блеомицином фиброза легких использовали самцов мышей C57BL/6J в возрасте 5 недель с массой тела 20 г. Мышей C57BL/6J анестезировали внутрибрюшинной инъекцией пентобарбитала (40 мг/кг), кожу передней части или середины шеи разрезали, трахею обнажали с помощью самоудерживающегося ранорасширителя и затем с затылочной стороны в легкие вставляли микрошприц для медленного введения блеомицина (2 мг/кг), проверяя состояние дыхания. Сразу после инъекции кожу на разрезанной передней части или середины шеи зашивали и затем их содержали в стерильной камере для животных при постоянной температуре (22-26°C) и постоянной влажности (55-60%). При использовании этой методики в легких образовывался заметный фиброз, обычно после 3 недель обработки.
В каждой группе было 7 животных и эксперимент проводили, разделяя из на следующие группы: контрольная группа (контроль) с пероральным введением дистиллированной воды, группа (BLM) с вызванным блеомицином фиброзом легких, экспериментальная группа в качестве положительной контрольной группы (BLM+нинтеданиб) с пероральным введением 100 мг/кг нинтеданиба ежедневно в течение 3 недель после введения блеомицина и экспериментальная группа (BLM+соединение 1) с пероральным введением 60 мг/кг соединения 1 ежедневно в течение 3 недель после введения блеомицина.
Нинтеданиб и соединение 1 вводили перорально один раз в сутки в течение 28 дней. Через день после последнего введения нинтеданиба или соединения 1 каждого животного анестезировали и затем иглой для пункции сердца отбирали кровь и умерщвляли.
Ткани легких вылущивали у всех животных для гистопатологического исследования. Вылущенную ткань легких фиксировали в 10% нейтральном забуференном формалине (NBF). Фиксированную ткань легких включали в парафин и нарезали толщиной 4 мкм для приготовления препаратов тканей.
Препараты тканей окрашивали гематоксилином и эозином (H&E), которые использую для окраски клеток и окрашивали трихромом по Массон (MT) для подтверждения фиброза. Результаты гистопатологического исследования приготовленных препаратов тканей подтверждали с помощью оптического микроскопа (Carl Zeiss, Oberkochen, Germany). Тяжесть фиброза оценивали с помощью модифицированной шкалы Ashcroft, которую использовали для полуколичественной гистопатологической оценки.
Для иммуногистохимического окрашивания полученные выше препараты тканей обеспарафинивали и затем в качестве первичных антител использовали кроличьи антитела к α-актину гладких мышц (SMA) или кроличьи антитела к коллагену типа I. И для подтверждения экспрессии антигена, взаимодействующего с каждыми антителами использовали набор Vectastatin ABC (Vector Laboratories, Inc, Burlingame, CA).
После реакции в течение 5 мин с использованием 3,3'-диаминобензидина (DAB) в качестве субстрата для пероксидазы их исследовали при увеличении 400× с помощью оптического микроскопа. Если при рассмотрении результатов окрашивания цитоплазма полностью или частично обладает красновато-коричневым цветом, считается, что имеется иммунная реакция и она считается положительной.
По экспериментальным данным среднее значение и стандартное отклонение получали с помощью статистической программы SPSS ver. 22.0 (SPSS Inc., Chicago, IL, USA) и значимость различий между экспериментальными группами проверяли при p<0,05 с помощью t-критерия Стьюдента.
В результате гистологического анализа с помощью окрашивания посредством H&E для экспериментальной группы (BLM) с вызванным блеомицином фиброзом легких, положительной контрольной группы (BLM+нинтеданиб) с введением нинтеданиба и группы с введением соединения 1 (BLM+соединение 1) подтверждено, что в группе с введением соединения 1 (BLM+соединение 1) степень инфильтрации воспалительных клеток в альвеолы и бронхиолы была значительно меньше, чем в экспериментальной группе и положительной контрольной группе. Кроме того, подтверждено, что содержание гипертрофированных эпителиальных клеток было снижено, деформация структуры легких уменьшилась и уменьшился участок аномального осаждения ткани (см. фиг. 5).
На фиг. 6 степень фиброза легких в группе с введением соединения 1 (BLM+соединение 1) сопоставлена с данными для экспериментальной группы с вызванным блеомицином фиброзом легких (BLM) и положительной контрольной группы с введением нинтеданиба (BLM+нинтеданиб) с помощью методики окрашивания трихромом по Массон (MT), специфической для фиброза легких. В результате подтверждено, что размеры фиброзного участка и участка осаждения коллагена вследствие фиброза заметно уменьшились в группе с введением соединения 1 (BLM+соединение 1) по сравнению с данными для экспериментальной группы и положительной контрольной группы.
По данным, приведенным на фиг. 7 и 8, можно подтвердить, что экспрессия α-SMA уменьшается в группе с введением соединения 1 (BLM+соединение 1) по сравнению с данными для экспериментальной группы с вызванным блеомицином фиброзом легких (BLM) и положительной контрольной группы с введением нинтеданиба (BLM+нинтеданиб) (фиг. 7), и подтверждено, что экспрессия коллагена типа I (коллаген I) также заметно уменьшена в группе с введением соединения 1 (BLM+соединение 1) по сравнению с данными для экспериментальной группы (BLM) и положительной контрольной группы (BLM+нинтеданиб) (фиг. 8).
В итоге на основании количественных гистологических и иммунологических данных с использованием модифицированной шкалы Ashcroft, широко применяющейся в области гистологии фиброза легких, тяжесть фиброза легких в группе с введением соединения 1 (BLM+соединение 1) сопоставлена с данными для отрицательной контрольной группы (контроль), экспериментальной группы (BLM) и положительной контрольной группы (BLM+нинтеданиб) соответственно.
Как показано на фиг. 9, показатель равнялся 0 для отрицательной контрольной группы (PBS), что является нормальным результатом, и показатель равнялся 5,5±0,8 для экспериментальной группы (BLM) с вызванным блеомицином фиброзом легких. Улучшенный показатель по шкале Ashcroft для положительной контрольной группы с введением нинтеданиба (BLM+нинтеданиб) снижался до 5,2±0,45 и улучшенный показатель по шкале Ashcroft для экспериментальной группы с введением соединения 1 (BLM+соединение 1) равнялся 4,0±1,1 и, таким образом, подтверждено, что соединение, предлагаемое в настоящем изобретении, эффективно улучшает состояние фиброза легких по сравнению со случаем введения нинтеданиба, который использовали в качестве обычного терапевтического средства для идиопатического фиброза легких.
< Пример 5> Подтверждение эффекта подавления вирусов в эпителиальных клетках легких человека
Для анализа противовирусной активности соединений примеров синтеза проводили qRT-PCR в реальном масштабе времени (количественный RT-PCR) с использованием связанного с тяжелым острым респираторным синдромом коронавируса 2 (SARS-CoV2) и клеток Calu-3, которые являются эпителиальными клетками легких человека (Calu-3), которые выращивали в модифицированной Дульбекко среде Игла (DMEM) при 37°C в 5% CO2. Концентрация соединения 1 равнялась 15, 12,5, 6,25, 3,125, 1,563, 0,781, 0,391, 0,195, 0,098, 0,049, 0,024, 0,012 мкМ. Противовирусную эффективность (IC50; 50% ингибирующая концентрация) и токсичность для клеток (CC50; 50% цитотоксичная концентрация), соответствующие концентрации лекарственного средства, определяли через 24 ч и 48 ч после обработки клеток при указанных концентрациях и они приведены в таблице 1 и на фиг. 10.
Таблица 1
Как показано в таблице 1 и на фиг. 10, противовирусная эффективность характеризуется значением IC50, равным 1,67 мкМ через 48 ч, и цитотоксичность является очень низкой и характеризуется значением CC50, равным 164,5 мкМ через 48 ч. Поэтому подтверждено, что соединение 1 может подавлять репликацию SARS-CoV-2 и является лекарственным средством, обладающим очень низкой цитотоксичностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТРОГО ПОРАЖЕНИЯ ПОЧЕК, ВЫЗВАННОГО КОНТРАСТНЫМ ВЕЩЕСТВОМ | 2021 |
|
RU2817980C1 |
| Новые производные пиразола | 2022 |
|
RU2816835C1 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2018 |
|
RU2723686C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ СИСТЕМНОГО СКЛЕРОЗА | 2022 |
|
RU2834641C2 |
| Фармацевтическая композиция для предупреждения или лечения фиброза | 2022 |
|
RU2829908C2 |
| ИНГИБИТОРЫ HDAC ДЛЯ ЛЕЧЕНИЯ ИДИОПАТИЧЕСКОГО ЛЕГОЧНОГО ФИБРОЗА И ДРУГИХ ВОСПАЛИТЕЛЬНЫХ НАРУШЕНИЙ ЛЕГКИХ | 2021 |
|
RU2833349C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛИНДИОНА КАК ИНГИБИТОРЫ НАДФН-ОКСИДАЗЫ | 2010 |
|
RU2569855C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА | 2021 |
|
RU2803733C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ВОЗРАСТНЫХ И ДИАБЕТИЧЕСКИХ СОСУДИСТЫХ ОСЛОЖНЕНИЙ | 2002 |
|
RU2291154C2 |
| ПРОИЗВОДНЫЕ 2-ПИРАЗИНОНА ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ИЛИ СОСТОЯНИЯ, ПРИ КОТОРЫХ ПОЛЕЗНО ИНГИБИРОВАНИЕ АКТИВНОСТИ НЕЙТРОФИЛЬНОЙ ЭЛАСТАЗЫ | 2007 |
|
RU2448098C2 |
Изобретение относится к органической химии и фармацевтической промышленности, а именно к применению фармацевтической композиции, содержащей соединение формулы 1 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель, для предупреждения или лечения фиброза легких, где соединение формулы 1 имеет структуру
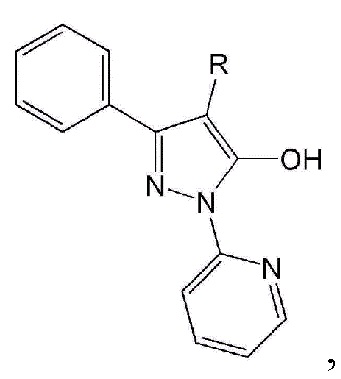
в которой R – линейная или разветвленная алкильная группа, содержащая 1-10 атомов углерода. Изобретение обеспечивает предупреждение или лечение вызванного окислительным стрессом фиброза легких без каких-либо существенных побочных эффектов. 7 з.п. ф-лы, 10 ил., 1 табл., 9 пр.
1. Применение фармацевтической композиции для предупреждения или лечения фиброза легких, содержащей соединение следующей формулы 1 или его фармацевтически приемлемую соль:
Формула 1
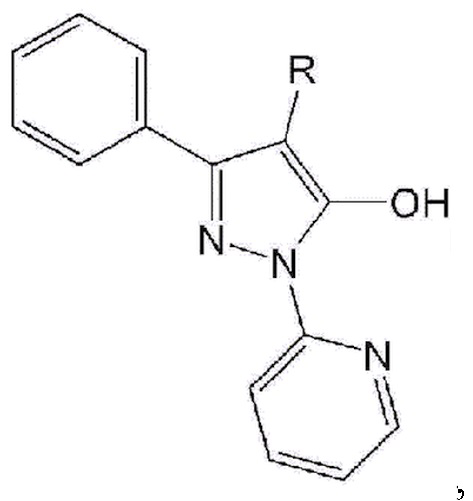
где R означает линейную или разветвленную алкильную группу, содержащую от 1 до 10 атомов углерода,
где фармацевтическая композиция дополнительно включает фармацевтически приемлемый носитель или наполнитель.
2. Применение по п. 1, где в формуле 1 R означает линейную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода.
3. Применение по п. 2, где соединением формулы 1 является:
3-фенил-4-метил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-этил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-изопропил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-бутил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-трет-бутил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид;
3-фенил-4-н-пентил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид; или
3-фенил-4-н-гексил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид.
4. Применение по п. 3, где соединением формулы 1 является 3-фенил-4-н-пропил-1-(пиридин-2-ил)-1H-пиразол-5-ол или его гидрохлорид.
5. Применение по пп. 1-4, где фиброз легких вызван воспалительным фиброзом легких, хроническим обструктивным заболеванием легких (COPD), объединенным с фиброзом легких, идиопатическим фиброзом легких (IPF) или астмой.
6. Применение по п. 5, где воспалительный фиброз легких вызван любым одним или комбинацией следующих: вирусная пневмония, бактериальная пневмония, грибковая пневмония, микоплазменная пневмония, гиперчувствительный пневмонит, аспирационная пневмония, интерстициальное заболевание легких и пневмокониоз.
7. Применение по п. 6, где вирусная пневмония вызвана вирусом, выбранным из аденовируса, вируса вакцины, вируса простого герпеса, паравируса гриппа, риновируса, вируса ветряной оспы, вируса кори, респираторно-синцитиального вируса, вируса денге, вируса иммунодефицита человека (HIV), вируса гриппа, коронавируса, связанного с тяжелым острым респираторным синдромом коронавируса 2 (SARS-CoV2), связанного с ближневосточным респираторным синдромом коронавируса (MERS-CoV) или вариантных вирусов этих вирусов.
8. Применение по п. 5, где фиброз легких вызван идиопатическим фиброзом легких.
| WO 2019088444 A1, 09.05.2019 | |||
| EP 3613733 A1, 26.02.2020 | |||
| Seung-Woo Hong et al | |||
| Ударно-долбежная врубовая машина | 1921 |
|
SU115A1 |
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| КОЛОСНИКОВАЯ РЕШЕТКА | 1924 |
|
SU1136A1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ФИБРОЗНЫХ ЗАБОЛЕВАНИЙ ЛЕГКИХ | 2010 |
|
RU2561672C2 |
Авторы
Даты
2024-04-23—Публикация
2021-03-23—Подача