Данная заявка испрашивает приоритет по предварительной заявке США №62/476,054, поданной 24 марта 2017 года.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к области антагонистов активин-рецептора II типа (ActRII), например, молекул, способных противодействовать связыванию активинов, белков growth differentiation factor (GDF), костных морфогенных белков (BMP) и миостатина с рецептором человека ActII, например, антитело-антагонист к ActRII А и/или ActRII В, например, бимагрумаб. В частности, оно относится к профилактике и/или лечению сердечной недостаточности, включая сердечную недостаточность со сниженной фракцией выброса (HFrEF) и сердечную недостаточности с сохраненной фракцией выброса (HFpEF), и к лечению структурных и/или функциональных нарушений сердца, связанных с этим состоянием, таких как порок сердца, ишемическая болезнь сердца, гипертензия, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсический или инфекционный агент, и генетические или идиопатические дилатированные кардиомиопатии путем введения субъекту терапевтически эффективного количества антагониста рецептора ActRII. Следует отметить, что эти состояния охватывают клинические синдромы, которые часто сосуществуют, но могут возникать изолированно, и их иногда называют систолической и/или диастолической сердечной недостаточностью, левосторонней и/или правосторонней сердечной недостаточностью и застойной сердечной недостаточностью.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Активин-рецептор IIB типа (ActRIIB) является сигнальным рецептором для различных членов суперсемейства трансформирующего ростового фактора-бета (TGF-P). Члены этого семейства включают активин A, nodal, ВМР2, ВМР6, ВМР7, ВМР9, GDF5, GDF8 (миостатин) и GDF11, которые участвуют в негативной регуляции мышц (Akpan et al., 2009).
Миостатин (GDF8) действует через активин-рецептор II типа (главным образом через ActRIIВ), и его предполагаемая передача сигналов осуществляется через путь SMAD 2/3, который участвует в ингибировании синтеза белка, а также дифференциации и пролиферации миоцитов. Ингибирование или генетическая абляция миостатина увеличивают мышечную массу и силу (Lee et al., 2005, Lee and McPherron 2001, Whittemore et al., 2003).
Бимагрумаб, также известный как BYM338, представляет собой моноклональное антитело, разработанное для конкурентного связывания с активин-рецептором II типа (ActRII) с большей аффинностью, чем миостатин или активин, его природные лиганды. Бимагрумаб раскрыт в WO 2010/12003, который включен сюда посредством ссылки, как если бы он был полностью изложен. Бимагрумаб представляет собой полностью человеческое антитело (модифицированный IgG1,234-235-Ala-Ala, Xi), которое связывается с лиганд-связывающим доменом ActRII А и В, тем самым предотвращая связывание и последующую передачу сигналов его лигандов, включая миостатин и активин, которые действуют как природные ингибиторы роста скелетных мышц. Бимагрумаб является перекрестно-реагирующим с ActRIIB человека и мыши и эффективен на клетках скелетных мышц человека, яванского макаки, мыши и крысы. ActRIIB широко распространен в скелетных мышцах, жировой ткани и различных органах, включая сердце (Rebbapragada et al., 2003).
Сердечная недостаточность представляет собой клинический синдром, при котором нарушения сердечной функции приводят к неадекватной системной перфузии для удовлетворения метаболических потребностей организма. Сердечная недостаточность подразделяется на два основных типа: (1) сердечная недостаточность со сниженной фракцией выброса (HFrEF) (также известная как «систолическая сердечная недостаточность») и (2) сердечная недостаточность с сохраненной фракцией выброса (HFpEF) (также известная как «диастолическая» сердечная недостаточность»). При HFrEF снижение сократимости сердца является основным механизмом, который ухудшает сердечный выброс и приводит к системной недостаточной перфузии. При HFpEF сократимость сердца в покое в целом сохраняется. Тем не менее, множество других дефектов сердечной функции, включая сердечные резервы и диастолическую функцию, ухудшают функциональные показатели сердца, что приводит к сходным фенотипам клинической сердечной недостаточности. Различные условия могут повредить или ослабить сердце и привести к сердечной недостаточности, включая, например, порок сердца, ишемическую болезнь сердца, гипертонию, диабет, старение, аритмию, кардиомиопатия при родах, стрессовую кардиомиопатию, токсические или инфекционные агенты и генетические и/или идиопатические дилатированные кардиомиопатии.
Сердечная недостаточность связанную с такими состояниями, как диабет, старение, гипертония, ишемическая болезнь сердца, коронарное заболевание сердца, порок сердца и генетические и идиопатические кардиомиопатии, является основной причиной заболеваемости и смертности во всем мире. Существуют ограниченные фармакологические методы лечения, доступные для этого распространяющегося заболевания. Стандарт лечения сердечной недостаточности включает в себя несколько лекарственных препаратов, которые нацелены на различные механизмы, вовлеченные в сложную патофизиологию этого заболевания. К сожалению, даже при ориентированной на рекомендации терапии прогноз для этих пациентов остается плохим, с 5-летним уровнем смертности, приближающимся к 50%. При прогрессирующей систолической сердечной недостаточности пациенты часто могут не переносить обычную пероральную лекарственную терапию из-за гемодинамических, нефрогенных и аритмогенных побочных эффектов или могут не достичь достаточного облегчения от такой терапии. Для этих пациентов передовые методы лечения, такие как внутривенное введение инотропов, механические устройства поддержки и трансплантация сердца, очень ограничены, дороги и связаны со значительными рисками.
До настоящего изобретения целевое ингибирование активин-рецепторов II типа (ActRIIA/В) не исследовалось как профилактическое средство или терапия сердечной недостаточности или вышеупомянутых состояний, которые могут привести к сердечной недостаточности. Как раскрыто в данном документе, в настоящее время имеются доказательства того, что системное введение антагониста рецептора ActRIIA/В, такого как CDD866, который является муринизированной версией BYM338 (где область Fc антитела человека была заменена Fc мыши), оказывает значительное благоприятное влияние на функцию сердца у мышей, подвергшихся поперечному сужению аорты (ТАС). ТАС является широко используемой экспериментальной моделью гипертрофии сердца и сердечной недостаточности, вызванной перегрузкой давлением. Впервые подтвержденная Rockman et al., 1991, модель ТАС мышей с тех пор широко использовалась в качестве ценного инструмента для имитации сердечно-сосудистых заболеваний человека и понимания фундаментальных сигнальных процессов, связанных с гипертрофическим откликом сердца и развитием сердечной недостаточности (deAlmeida et al., 2010). Как раскрыто в данном документе, CDD866 не только предотвращает ТАС-опосредованную сердечную дисфункцию, но также способен восстанавливать сердечную функцию после установленной сердечной недостаточности в течение 1-2 недель после введения лекарственного средства. Он также увеличивает рост скелетных мышц, которые часто атрофируются при запущенных формах сердечной недостаточности, и вызывает минимальные сердечные эффекты у контролируемых мышей, не подверженных патологическому стрессу/повреждению ТАС.
В данном документе раскрыты антагонисты рецептора ActRII для применения при лечении и/или предупреждения сердечной недостаточности, включая сердечную недостаточность, вызванную или связанную с таким состоянием, как порок сердца, ишемическая болезнь сердца, коронарная болезнь сердца, гипертония, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсические или инфекционные агенты и генетические и/или идиопатические дилатированные кардиомиопатии. Также раскрыты антагонисты рецептора ActRII для применения при лечении структурной и/или функциональной аномалии сердца, связанной с вышеупомянутым состоянием. Также предложены методы, использующие такие антагонисты ActRII для лечения и/или предотвращения сердечной недостаточности и для лечения структурной и/или функциональной аномалии сердца, связанной с вышеупомянутым состоянием.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
В данном документе раскрыты антагонисты рецептора ActRII для применения при лечении и/или профилактике сердечной недостаточности. Сердечная недостаточность может быть вызвана или связана с различными состояниями, такими как, например, заболевание клапанов, такое как аортальный стеноз, заболевание коронарной артерии, гипертензия, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсические или инфекционные агенты и генетические или идиопатические дилатированные кардиомиопатии. Как сердечная недостаточность со сниженной фракцией выброса (HFrEF), так и сердечная недостаточность с сохраненной фракцией выброса (HFpEF) включены сюда.
В данном документе также раскрыты антагонисты рецептора ActRII для применения при лечении структурных и/или функциональных нарушений сердца, связанных с такими состояниями, как клапанная болезнь сердца, ишемическая болезнь сердца, гипертония, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсические или инфекционные агенты и генетические или идиопатические дилатированные кардиомиопатии. В некоторых случаях кардиомиопатия при родах возникает во время поздней беременности или через 6 месяцев после родов. Стрессовая кардиомиопатия часто возникает у пожилых женщин после менопаузы. Примером порока сердца является аортальный стеноз, который может сопровождаться слабостью и/или саркопенией. Стрессовая кардиомиопатия может возникнуть после психологического, патологического или физического стресса.
В данном документе раскрыты методы лечения и/или профилактики сердечной недостаточности. Способы включают введение субъекту, у которого сердечная недостаточность или кто подвержен риску развития сердечной недостаточности, терапевтически эффективного количества антагониста рецептора ActRII, такого как, например, бимагрумаб. Как сердечная недостаточность со сниженной фракцией выброса (HFrEF), так и сердечная недостаточность с сохраненной фракцией выброса (HFpEF) включены сюда. Сердечная недостаточность может быть диагностирована у пациента с использованием хорошо известных методов, включая, например, измерение мозгового натрийуретического пептида с последующим ультразвуковым исследованием сердца, если оно положительное, и визуализацию, такую как эхокардиография.
Субъект подвержен риску развития сердечной недостаточности, когда у него или нее есть такое состояние, как клапанная болезнь сердца, ишемическая болезнь сердца (включая перенесенный инфаркт миокарда), гипертония, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия и генетические или идиопатические дилатированные кардиомиопатии.
В данном документе также раскрыты методы лечения структурной и/или функциональной аномалии сердца, связанной с таким состоянием, как клапанная болезнь сердца, ишемическая болезнь сердца, гипертония, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсический или инфекционный агент и генетические или идиопатические дилатированные кардиомиопатии. Способы включают введение субъекту, имеющему такую структурную и/или функциональную аномалию сердца, связанную с таким состоянием, эффективного количества антагониста рецептора ActRII.
Примером антагониста рецептора ActRII для использования или в способе, описанном в настоящем документе, является молекула, связывающая рецептор ActRII, которая может блокировать доступ лигандов, взаимодействующих с ActRII, таких как миостатин, GDF11 и активин А, к ActRII. Связывающая рецептор ActRII молекула может связываться с рецептором ActRIIА и/или с ActRIIВ. Примеры молекул, связывающих ActRII, включают, но не ограничиваются ими, антитела, которые связываются с рецептором ActRIIA и/или ActRIIB, например, антитело против рецептора ActRII. Предпочтительно антитело против рецептора ActRII представляет собой BYM338, также известный как бимагрумаб.
Дополнительным примером антагониста рецептора ActRII для использования в способе, описанном в настоящем документе, является растворимая форма внеклеточного домена рецептора ActRIIA или ActRIIB, который может связывать ActRII-взаимодействующие лиганды, такие как миостатин, GDF11 и активин А. Это «рецепторное тело» ингибирует функцию связанных с клетками рецепторов ActRII, конкурируя с их лигандами.
В данном документе раскрыты антагонисты рецептора ActRII для применения или использования в способе, описанном здесь, где антагонист рецептора ActRII представляет собой антитело против ActRII, которое связывается с эпитопом 5 ActRIIB, состоящим из аминокислот 19-134 SEQ ID NO: 181 (SEQ ID NO: 182).
В данном документе раскрыты антагонисты рецептора ActRII для применения или использования в способе, описанном здесь, где антитело против ActRII связывается с эпитопом ActRIIB, включающим или состоящим из:
(a) аминокислот 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID NO: 188);
(b) аминокислот 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID NO: 186);
(c) аминокислот 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID NO: 190);
(d) аминокислот 52-56 SEQ ID NO: 181 (EQDKR-SEQ ID N0: 189);
(e) аминокислот 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW - SEQ ID NO: 187);
(f) аминокислот 29-41 SEQ ID NO: 181 (CIYYNANWELERT - SEQ ID N0: 191);
(g) аминокислот 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID N0: 192); или
(h) аминокислот 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислот 52-56 SEQ ID NO: 181 (EQDKR).
Другие антитела против ActRII В для использования или в способе, описанном в настоящем документе, включают, например,
a) антитело против ActRII В, которое связывается с эпитопом ActRII В, содержащее:
(a) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID N0: 188);
(b) аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID N0: 186);
(c) аминокислоты 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID N0: 190);
(d) аминокислоты 52-56 SEQ ID NO: 181 (EQDKR-SEQ ID NO: 189);
(e) аминокислоты 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW-SEQ ID NO: 187);
(f) аминокислоты 29-41 SEQ ID NO: 181 (CIYYNANWELERT-SEQ ID NO: 191);
(g) аминокислоты 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID N0: 192); или
(h) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислоты 52- 56 SEQ ID NO: 181 (EQDKR); и
b) антитело-антагонист к ActRIIB, которое связывается с эпитопом ActRIIB, содержащее
(a) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID N0: 188);
(b) аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID N0: 186);
(c) аминокислоты 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID N0: 190);
(d) аминокислоты 52-56 SEQ ID NO: 181 (EQDKR-SEQ ID NO: 189);
(e) аминокислоты 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW - SEQ ID NO: 187);
(f) аминокислоты 29-41 SEQ ID NO: 181 (CIYYNANWELERT- SEQ ID NO: 191);
(g) аминокислоты 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID NO: 192); или
(h) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислоты 52-56 SEQ ID NO: 181 (EQDKR), причем антитело имеет KD около 2 пМ.
В одном варианте осуществления антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, представляет собой антитело, которое связывается с ActRIIB примерно с 10-кратной или большей аффинностью, чем оно связывается c ActRIIA.
Антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело, содержащее вариабельную область тяжелой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-14; вариабельную область тяжелой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-28; вариабельную область тяжелой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 29-42; вариабельную область легкой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 43-56; вариабельную область легкой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 57-70; и вариабельную область легкой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 71-84.
Антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело, содержащее:
(a) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 1; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 15; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 29; вариабельную область легкой цепи CDR1 SEQ ID NO: 43; вариабельную область легкой цепи CDR2 SEQ ID NO: 57; и вариабельную область легкой цепи CDR3 SEQ ID NO: 71,
(b) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 2; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 16; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 30; вариабельную область легкой цепи CDR1 SEQ ID NO: 44; вариабельную область легкой цепи CDR2 SEQ ID NO: 58; и вариабельную область легкой цепи CDR3 SEQ ID NO: 72,
(c) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 3; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 17; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 31; вариабельную область легкой цепи CDR1 SEQ ID NO: 45; вариабельную область легкой цепи CDR2 SEQ ID NO: 59; и вариабельную область легкой цепи CDR3 SEQ ID NO: 73,
(d) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 4; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 18; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 32; вариабельную область легкой цепи CDR1 SEQ ID NO: 46; вариабельную область легкой цепи CDR2 SEQ ID NO: 60; и вариабельную область легкой цепи CDR3 of SEQ ID NO: 74,
(e) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 5; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 19; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 33; вариабельную область легкой цепи CDR1 SEQ ID NO: 47; вариабельную область легкой цепи CDR2 SEQ ID NO: 61; и вариабельную область легкой цепи CDR3 SEQ ID NO: 75,
(f) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 6; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 20; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 34; вариабельную область легкой цепи CDR1 SEQ ID NO: 48; вариабельную область легкой цепи CDR2 SEQ ID NO: 62; и вариабельную область легкой цепи CDR3 SEQ ID NO: 76,
(g) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 7; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 21; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 35; вариабельную область легкой цепи CDR1 SEQ ID NO: 49; вариабельную область легкой цепи CDR2 SEQ ID NO: 63; и вариабельную область легкой цепи CDR3 SEQ ID NO: 77,
(h) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 8; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 22; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 36; вариабельную область легкой цепи CDR1 SEQ ID NO: 50 вариабельную область легкой цепи CDR2 SEQ ID NO: 64; и вариабельную область легкой цепи CDR3 SEQ ID NO: 78,
(i) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 9; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 23; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 37; вариабельную область легкой цепи CDR1 SEQ ID NO: 51; вариабельную область легкой цепи CDR2 SEQ ID NO: 65; и вариабельную область легкой цепи CDR3 SEQ ID NO: 79,
(j) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 10; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 24; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 38; вариабельную область легкой цепи CDR1 SEQ ID NO: 52; вариабельную область легкой цепи CDR2 SEQ ID NO: 66; и вариабельную область легкой цепи CDR3 SEQ ID NO: 80,
(k) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 11; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 25; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 39; вариабельную область легкой цепи CDR1 SEQ ID NO: 53; вариабельную область легкой цепи CDR2 SEQ ID NO: 67; и вариабельную область легкой цепи CDR3 SEQ ID NO: 81,
(l) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 12; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 26; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 40; вариабельную область легкой цепи CDR1 SEQ ID NO: 54; вариабельную область легкой цепи CDR2 SEQ ID NO: 68; и вариабельную область легкой цепи CDR3 SEQ ID NO: 82,
(m) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 13; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 27; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 41; вариабельную область легкой цепи CDR1 SEQ ID NO: 55; вариабельную область легкой цепи CDR2 SEQ ID NO: 69; и вариабельную область легкой цепи CDR3 SEQ ID NO: 83, или
(n) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 14; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 28; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 42; вариабельную область легкой цепи CDR1 SEQ ID NO: 56; вариабельную область легкой цепи CDR2 SEQ ID NO: 70; и вариабельную область легкой цепи CDR3 SEQ ID NO: 84.
В другом варианте осуществления антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело, содержащее полную длину аминокислотной последовательности тяжелой цепи, имеющую по меньшей мере 95%-ную идентичность последовательности по меньшей мере с одной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 146-150 и 156-160.
Антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело, содержащее полную длину аминокислотной последовательности легкой цепи, имеющую по меньшей мере 95%-ную идентичность последовательности по меньшей мере с одной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 141-145 и 151-155.
Антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело, содержащее:
(a) вариабельную последовательность тяжелой цепи SEQ ID NO: 99 и вариабельную последовательность легкой цепи SEQ ID NO: 85;
(b) вариабельную последовательность тяжелой цепи SEQ ID NO: 100 и вариабельную последовательность легкой цепи SEQ ID NO: 86;
(c) вариабельную последовательность тяжелой цепи SEQ ID NO: 101 и вариабельную последовательность легкой цепи SEQ ID NO: 87;
(d) вариабельную последовательность тяжелой цепи SEQ ID NO: 102 и вариабельную последовательность легкой цепи SEQ ID NO: 88;
(e) вариабельную последовательность тяжелой цепи SEQ ID NO: 103 и вариабельную последовательность легкой цепи SEQ ID NO: 89;
(f) вариабельную последовательность тяжелой цепи SEQ ID NO: 104 и вариабельную последовательность легкой цепи SEQ ID NO: 90;
(g) вариабельную последовательность тяжелой цепи SEQ ID NO: 105 и вариабельную последовательность легкой цепи SEQ ID NO: 91;
(h) вариабельную последовательность тяжелой цепи SEQ ID NO: 106 и вариабельную последовательность легкой цепи SEQ ID NO: 92;
(i) вариабельную последовательность тяжелой цепи SEQ ID NO: 107 и вариабельную последовательность легкой цепи SEQ ID NO: 93;
(j) вариабельную последовательность тяжелой цепи SEQ ID NO: 108 и вариабельную последовательность легкой цепи SEQ ID NO: 94;
(k) вариабельную последовательность тяжелой цепи SEQ ID NO: 109 и вариабельную последовательность легкой цепи SEQ ID NO: 95;
(l) вариабельную последовательность тяжелой цепи SEQ ID NO: 110 и вариабельную последовательность легкой цепи SEQ ID NO: 96;
(m) вариабельную последовательность тяжелой цепи SEQ ID NO: 111 и вариабельную последовательность легкой цепи SEQ ID NO: 97; или
(n) вариабельную последовательность тяжелой цепи SEQ ID NO: 112 и вариабельную последовательность легкой цепи SEQ ID NO: 98.
Антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело, содержащее:
(a) последовательность тяжелой цепи SEQ ID NO: 146 и последовательность легкой цепи SEQ ID NO: 141;
(b) последовательность тяжелой цепи SEQ ID NO: 147 и последовательность легкой цепи SEQ ID NO: 142;
(c) последовательность тяжелой цепи SEQ ID NO: 148 и последовательность легкой цепи SEQ ID NO: 143;
(d) последовательность тяжелой цепи SEQ ID NO: 149 и последовательность легкой цепи ID NO: 144;
(e) последовательность тяжелой цепи SEQ ID NO: 150 и последовательность легкой цепи SEQ ID NO: 145;
(f) последовательность тяжелой цепи SEQ ID NO: 156 и последовательность легкой цепи SEQ ID NO: 151;
(g) последовательность тяжелой цепи SEQ ID NO: 157 и последовательность легкой цепи SEQ ID NO: 152;
(h) последовательность тяжелой цепи SEQ ID NO: 158 и последовательность легкой цепи SEQ ID NO: 153;
(i) последовательность тяжелой цепи SEQ ID NO: 159 и последовательность легкой цепи SEQ ID NO: 154; или
(j) последовательность тяжелой цепи SEQ ID NO: 160 и последовательность легкой цепи SEQ ID NO: 155.
В данном документе также раскрыты антагонисты рецептора ActRII для применения или использования в способе, описанном здесь, которые представляют собой антитела против рецептора ActRII, которые перекрестно блокируют или перекрестно блокируются по меньшей мере одним антителом, описанным выше.
Антагонист рецептора ActRII для применения или использования в способе, описанном в настоящем документе, может представлять собой антитело против рецептора ActRII, обладающее измененной эффекторной функцией в результате мутации области Fc.
Примерами антител для применения или использования в способе, описанном в настоящем документе, являются антитела против ActRII, кодируемые pBW522 (DSM22873) или pBW524 (DSM22874).
В приведенных здесь демонстрационных примерах используется CDD866, который представляет собой муринизированную версию BYM338, где Fc-область антитела человека была заменена Fc мыши.
Однако предпочтительным антителом для применения или использования в способе, описанном в настоящем документе, является бимагрумаб (BYM338), который является полностью человеческим антителом (модифицированный IgG1, 234-235-Ala-Ala, λ2).
Термин «молекула, связывающая ActRII» означает любую молекулу, способную связываться с человеческим рецептором ActRII (ActRII А и/или ActRIIB) либо отдельно, либо с другими молекулами. Реакция связывания может быть показана стандартными способами (качественные анализы), включая, например, анализ связывания, конкурентный анализ или биоанализ для определения ингибирования связывания рецептора ActRII с миостатином или анализа связывания любого типа со ссылкой на отрицательный контрольный тест, в котором используется антитело с неродственной специфичностью, но в идеале того же изотипа, например, антитело против CD25. Неограничивающие примеры молекул, связывающих рецептор ActRII, включают небольшие молекулы, такие как аптамеры или другие молекулы нуклеиновой кислоты, сконструированные и/или подверженные связыванию с рецептором, ложные ловушки и антитела к рецептору ActRII, продуцируемые В-клетками или гибридомами и химерными структурами, CDR-привитые или человеческие антитела или любой их фрагмент, например F(ab')2 и Fab-фрагменты, а также одноцепочечные или однодоменные антитела. Предпочтительно молекула, связывающая рецептор ActRII, противодействует (например, уменьшает, ингибирует, снижает, задерживает) связывание природных лигандов с рецептором ActRII. В некоторых вариантах способов, схем, наборов, процессов, применений и композиций, раскрытых в данном документе, используется молекула, связывающая рецептор ActRIIB.
В другом варианте осуществления композиция содержит антитело против ActRII, которое связывается с доменом связывания, состоящим из аминокислот 19-134 SEQ ID NO: 181 (SEQ ID NO: 182), или с эпитопом, включающим или состоящим из (а) аминокислот 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID NO: 188); (b) аминокислот 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID NO: 186); (с) аминокислот 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID NO: 190); (d) аминокислот 52-56 SEQ ID NO: 181 (EQDKR - SEQ ID NO: 189); (e) аминокислот 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW - SEQ ID NO: 187); (f) аминокислот 29-41 SEQ ID NO: 181 (CIYYNANWELERT-SEQ ID NO: 191); (g) аминокислот 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID NO: 192); или (h) аминокислот 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислот 52-56 SEQ ID NO: 181 (EQDKR).
В еще одном альтернативном варианте осуществления вышеупомянутые композиции содержат антитело против ActRII, которое связывается с ActRIIB с 10-кратной или большей аффинностью, по сравнению cActRIIA.
Кроме того, изобретение относится к композиции, в которой антитело против ActRII В содержит вариабельную область тяжелой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-14; вариабельную область тяжелой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-28; вариабельную область тяжелой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 29-42; вариабельную область легкой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 43-56; вариабельную область легкой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 57-70; и вариабельную область легкой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 71-84.
В некоторых вариантах осуществления настоящее изобретение относится к композициям, в которых антитело против ActRII содержит: (а) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 1; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 15; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 29; вариабельную область легкой цепи CDR1 SEQ ID NO: 43; вариабельную область легкой цепи CDR2 SEQ ID NO: 57; и вариабельную область легкой цепи CDR3 SEQ ID NO: 71, (b) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 2; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 16; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 30; вариабельную область легкой цепи CDR1 SEQ ID NO: 44; вариабельную область легкой цепи CDR2 SEQ ID NO: 58; и вариабельную область легкой цепи CDR3 SEQ ID NO: 72, (с) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 3; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 17; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 31; вариабельную область легкой цепи CDR1 SEQ ID NO: 45; вариабельную область легкой цепи CDR2 SEQ ID NO: 59; и вариабельную область легкой цепи CDR3 SEQ ID NO: 73, (d) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 4; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 18; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 32; вариабельную область легкой цепи CDR1 SEQ ID NO: 46; вариабельную область легкой цепи CDR2 SEQ ID NO: 60; и вариабельную область легкой цепи CDR3 SEQ ID NO: 74, (е) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 5; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 19; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 33; вариабельную область легкой цепи CDR1 SEQ ID NO: 47; вариабельную область легкой цепи CDR2 SEQ ID NO: 61; и вариабельную области легкой цепи CDR3 SEQ ID NO: 75, (f) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 6; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 20; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 34; вариабельную область легкой цепи CDR1 SEQ ID NO: 48; вариабельную область легкой цепи CDR2 SEQ ID NO: 62; и вариабельную область легкой цепи CDR3 SEQ ID NO: 76, (g) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 7; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 21; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 35; вариабельную область легкой цепи CDR1 SEQ ID NO: 49; вариабельную область легкой цепи CDR2 SEQ ID NO: 63; и вариабельную область легкой цепи CDR3 SEQ ID NO: 77, (h) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 8; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 22; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 36; вариабельную область легкой цепи CDR1 SEQ ID NO: 50 вариабельную область легкой цепи CDR2 SEQ ID NO: 64; и вариабельную область легкой цепи CDR3 SEQ ID NO: 78, (i) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 9; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 23; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 37; вариабельную область легкой цепи CDR1 SEQ ID NO: 51; вариабельную область легкой цепи CDR2 SEQ ID NO: 65; и вариабельную области легкой цепи CDR3 SEQ ID NO: 79, (j) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 10; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 24; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 38; вариабельную область легкой цепи CDR1 SEQ ID NO: 52; вариабельную область легкой цепи CDR2 SEQ ID NO: 66; и вариабельную область легкой цепи CDR3 SEQ ID NO: 80, (k) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 11; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 25; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 39; вариабельную область легкой цепи CDR1 SEQ ID NO: 53; вариабельную область легкой цепи CDR2 SEQ ID NO: 67; и вариабельную области легкой цепи CDR3 SEQ ID NO: 81, (l) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 12; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 26; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 40; вариабельную область легкой цепи CDR1 SEQ ID NO: 54; вариабельную область легкой цепи CDR2 SEQ ID NO: 68; и вариабельную область легкой цепи CDR3 SEQ ID NO: 82, (m) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 13; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 27; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 41; вариабельную область легкой цепи CDR1 SEQ ID NO: 55; вариабельную область легкой цепи CDR2 SEQ ID NO: 69; и вариабельную область легкой цепи CDR3 SEQ ID NO: 83 или (n) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 14; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 28; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 42; вариабельную область легкой цепи CDR1 SEQ ID NO: 56; вариабельную область легкой цепи CDR2 SEQ ID NO: 70; и вариабельную область легкой цепи CDR3 SEQ ID NO: 84.
В еще одном варианте осуществления вышеупомянутое антитело против ActRII содержит (i) полную длину аминокислотной последовательности тяжелой цепи, имеющую по меньшей мере 95%-ную идентичность последовательности по меньшей мере с одной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 146-150, и 156-160, (ii) полную длину аминокислотной последовательности легкой цепи, имеющую по меньшей мере 95%-ную идентичность последовательности по меньшей мере с одной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 141-145 и 151-155, или (iii) (а) вариабельную последовательность тяжелой цепи SEQ ID NO: 99 и вариабельную последовательность легкой цепи SEQ ID NO: 85; (b) вариабельную последовательность тяжелой цепи SEQ ID NO: 100 и вариабельную последовательность легкой цепи SEQ ID NO: 86; (с) вариабельную последовательность тяжелой цепи SEQ ID NO: 101 и вариабельную последовательность легкой цепи SEQ ID NO: 87; (d) вариабельную последовательность тяжелой цепи SEQ ID NO: 102 и вариабельную последовательность легкой цепи SEQ ID NO: 88; (е) вариабельную последовательность тяжелой цепи SEQ ID NO: 103 и вариабельную последовательность легкой цепи SEQ ID NO: 89; (f) вариабельную последовательность тяжелой цепи SEQ ID NO: 104 и вариабельную последовательность легкой цепи SEQ ID NO: 90; (g) вариабельную последовательность тяжелой цепи SEQ ID NO: 105 и вариабельную последовательность легкой цепи SEQ ID NO: 91; (h) вариабельную последовательность тяжелой цепи SEQ ID NO: 106 и вариабельную последовательность легкой цепи SEQ ID NO: 92; (i) вариабельную последовательность тяжелой цепи SEQ ID NO: 107 и вариабельную последовательность легкой цепи SEQ ID NO: 93; (j) вариабельную последовательность тяжелой цепи SEQ ID NO: 108 и вариабельную последовательность легкой цепи SEQ ID NO: 94; (k) вариабельную последовательность тяжелой цепи SEQ ID NO: 109 и вариабельную последовательность легкой цепи SEQ ID NO: 95; (l) вариабельную последовательность тяжелой цепи SEQ ID NO: 110 и вариабельную последовательность легкой цепи SEQ ID NO: 96; (m) вариабельную последовательность тяжелой цепи SEQ ID NO: 111 и вариабельную последовательность легкой цепи SEQ ID NO: 97; или (n) вариабельную последовательность тяжелой цепи SEQ ID NO: 112 и вариабельную последовательность легкой цепи SEQ ID NO: 98.
В определенных аспектах изобретение относится к вышеописанным композициям, в которых антитело против ActRII содержит (а) последовательность тяжелой цепи SEQ ID NO: 146 и последовательность легкой цепи SEQ ID NO: 141; (b) последовательность тяжелой цепи SEQ ID NO: 147 и последовательность легкой цепи SEQ ID NO: 142; (с) последовательность тяжелой цепи SEQ ID NO: 148 и последовательность легкой цепи SEQ ID NO: 143; (d) последовательность тяжелой цепи SEQ ID NO: 149 и последовательность легкой цепи SEQ ID NO: 144; (е) последовательность тяжелой цепи SEQ ID NO: 150 и последовательность легкой цепи SEQ ID NO: 145; (f) последовательность тяжелой цепи SEQ ID NO: 156 и последовательность легкой цепи SEQ ID NO: 151; (g) последовательность тяжелой цепи SEQ ID NO: 157 и последовательность легкой цепи SEQ ID NO: 152; (h) последовательность тяжелой цепи SEQ ID NO: 158 и последовательность легкой цепи SEQ ID NO: 153; (i) последовательность тяжелой цепи SEQ ID NO: 159 и последовательность легкой цепи SEQ ID NO: 154; или (j) последовательность тяжелой цепи SEQ ID NO: 160 и последовательность легкой цепи SEQ ID NO: 155.
Дополнительный предмет изобретения относится к композиции, в которой (i) антитело против ActRII перекрестно блокирует или перекрестно блокируется одним из вышеописанных антител, (ii) изменяет эффекторную функцию посредством мутации области Fc и/или (iii) связывается с эпитопом, распознаваемым одним из вышеописанных антител.
В еще одном альтернативном варианте осуществления вышеупомянутые композиции содержат антитело против ActRII, которое связывается с ActRII В с 10-кратной или большей аффинностью, по сравнению c ActRIIA.
В еще одном варианте осуществления композиция по изобретению содержит антитело против ActRII, кодируемое pBW522 (DSM22873) или pBW524 (DSM22874).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1А представлены измеренные уровни CDD866 в плазме у мышей дикого типа C57BL/6, которым вводили либо еженедельные CDD866, либо изотропные контрольные инъекции Ab в течение восьми недель.
На фиг. 1В представлено отношение массы сердца к длине большеберцовой кости (HW/ TL) как для мышей контрольной группы, изотип Ab (n=3) серая линия, так и для мышей экспериментальной группы CDD866 Ab (n=3) * р<0,05, черная линия, что указывает на то, что CDD866 незначительно увеличивает массу сердца у взрослых мышей C57BL/6 дикого типа.
На фиг. 1С представлена гистограмма, показывающая % фиброза как у мышей контрольной группы (изотип Ab, серая линия), так и у мышей экспериментальной группы (CDD866 Ab [n=3]. * Р<0,05, черная линия). CDD866 уменьшает фиброз миокарда, хотя у взрослых мышей дикого типа C57BL/6 процент фиброза был заметно низким в начале исследования.
На фиг. 1D представлены типичные микрофотоснимки окрашенного PAS миокарда с выделением размера кардиомиоцитов.
На фиг. 1Е представлено обнаружение того, что CDD866 незначительно увеличивает размер кардиомиоцитов у животных дикого типа. Данные представлены как среднее + стандартное отклонение. Серый = контрольная группа, изотип Ab (n=3). Черный = Экспериментальная группа, CDD866Ab (n=3). * р<0,05
На фиг. 2А представлено то, что систолическая функция, измеренная с помощью % фракции сокращения (FS), как ожидается, уменьшается с ТАС (горизонтальная линия), но сохраняется у животных, обработанных CDD866, подвергнутых ТАС (диагональная линия). SHAM + изотип Ab (n=7), черная линия; SHAM + CDD866 Ab (n=7), серая линия; ТАС + изотип Ab (n=10), горизонтальная линия; ТАС + CDD866Ab (n=10), диагональная линия. #р<0,01.
На фиг. 2В представлены типичные эхокардиографические изображения через 11 недель после операции SHAM или ТАС, а также продемонстрировано сохранение систолической функции у животных ТАС, получавших CDD866.
На фиг. 2С представлено отношение массы легких к длине большеберцовой кости (LW/ TL) для мышей в разных группах лечения. SHAM + изотип Ab (n=7), черная линия; SHAM + CDD866 Ab (n=7), серая линия; ТАС + изотип Ab (n=10), горизонтальная линия; ТАС + CDD866 Ab (n=10), диагональная линия. *р<0,01. Существует тенденция к снижению массы легких у животных, получавших CDD866, и указывающая на меньшую легочную гиперемию (суррогат сердечной недостаточности на моделях мышей).
На фиг. 2D представлено значительное снижение основного конечного показателя (выживаемость или %FS<20%) при лечении CDD866.
На фиг. 3А представлены уровни CDD866 в плазме для различных групп лечения: ТАС + изотип; ТАС + CDD866; SHAM + изотип; и SHAM + CDD866.
На фиг. 3В представлена гистограмма, показывающая, что сердечная фоллистатин-подобная экспрессия 3 (FSTL3) увеличивается с ТАС, что указывает на то, что передача сигналов ActRII-A/B сердца увеличивается в этой модели повреждения сердца. Лечение CDD866 снижает сердечную экспрессию FSTL3, указывая на то, что оно эффективно блокирует ТАС-индуцированную передачу сигналов ActRII-A/B в сердце. Черный = SHAM + изотип Ab (n=7). Серый = SHAM + CDD866 Ab (n=7). Горизонтальная линия = ТАС + изотип Ab (n=10). Диагональная линия = ТАС + CDD866Ab (n=10). *р<0,05. #р<0,01.
На фиг. 3С представлено то, что относительная экспрессия мРНК генов патологической сердечной гипертрофии уменьшается при лечении CDD866. ANP (предсердный натрийуретический пептид); BNP (мозговой натрийуретический пептид); аМНС (тяжелая цепь альфа-миозина); bMHC (тяжелая цепь бета-миозина). Черный = SHAM + изотип Ab (n=7). Серый = SHAM + CDD866 Ab (n=7). Горизонтальная линия = ТАС + изотип Ab (n=10). Диагональная линия = ТАС + CDD866Ab (n=10). *р<0,05. #р<0,01.
На фиг. 3D представлена гистограмма, иллюстрирующая, что относительная экспрессия мРНК генов патологического фиброза сердца при ТАС-индуцированной сердечной недостаточности снижается при лечении CDD866. COL1 (коллаген типа 1); CTGF (фактор роста соединительной ткани). Черный = SHAM + изотип Ab (n=7). Серый = SHAM + CDD866 Ab (n=7). Горизонтальная линия = ТАС + изотип Ab (n=10). Диагональная линия = ТАС + CDD866 Ab (n=10). *р<0,05. #р<0,01.
На фиг. 4А представлены измеренные уровни CDD866 в плазме у мышей, у которых после ТАС развилась систолическая функция, и затем им вводили еженедельные инъекции CDD866 в течение восьми недель.
На фиг. 4В представлена гистограмма, показывающую относительный уровень экспрессии мРНК для FSTL3 (фоллистатин-подобный 3), Активин-А, MSTN (миостатин), ACVR2A (активин-рецептор А типа 2А) и ACVR2B (активин-рецептор А типа 2В). Этот график демонстрирует, что подход к лечению с помощью CDD866 может снизить сердечную экспрессию FSTL3, указывая на то, что CDD866 может эффективно блокировать ТАС-индуцированную передачу сигналов ActRII-A/B в сердце.
На фиг. 4С представлен график зависимости % фракции сокращения от времени в неделях, показывающий, что CDD866 устраняет систолическую дисфункцию при ТАС-индуцированной сердечной недостаточности уже через 1 неделю после лечения с постоянным улучшением.
На фиг. 4D представлено то, что CDD866 также уменьшает соотношение массы легких к длине большеберцовой кости, суррогатного маркера сердечной недостаточности в мышиной модели. Серый = ТАС + изотип Ab. Черный = ТАС + CDD866 Ab. *р<0,05. #р<0,01. LW/TL (отношение массы легкого к длине большеберцовой кости).
На фиг. 5А представлен график зависимости толщины стенок от недель после ТАС, показывающий, что толщина стенок постепенно увеличивается при обработке CDD866. Стрелка указывает на инициацию CDD866.
На фиг. 5В представлена серия эхо-изображений частей среднего желудочка во время курса лечения, демонстрирующие различия в росте сердца у изотипов по сравнению с животными, получавшими CDD866. CDD866-опосредованный рост сердца предотвращает эксцентрическую коррекцию, связанную с прогрессирующей систолической дисфункцией.
На фиг. 5С представлен график, на котором показано отношение массы сердца к длине большеберцовой кости (HW/TL) для мышей, обработанных ТАС + изотипом Ab (серая линия) и ТАС + CDD866 Ab (черная линия), что указывает на то, что CDD866 увеличивает массу сердца в модели ТАС.* р<0,05. # р<0,01.
На фиг. 5D представлены микрофотографии окрашенного PAS миокарда с выделением размера кардиомиоцитов для мышей, обработанных ТАС + изотипом Ab и ТАС + CDD866 Ab.
На фиг. 5Е представлен график, на котором показана площадь поперечного сечения кардиомиоцитов у мышей, обработанных как ТАС + изотипом Ab (серый), так и ТАС + CDD866 Ab (черный), что указывает на то, что CDD866 увеличивает рост кардиомиоцитов в ТАС. *р<0,05. #р<0,01.
На фиг. 6А представлен график, показывающий, что экспрессия мРНК генов, связанных с патологической гипертрофией, снижается при лечении CDD866. ANP (предсердный натрийуретический пептид); BNP (мозговой натрийуретический пептид); аМНС (тяжелая цепь альфа-миозина); рМНС (тяжелая цепь бета-миозина). Показаны ТАС + изотип Ab (серый); ТАС + CDD866 Ab (черный). * р<0,05. #р<0,01.
На фиг. 6В представлены графики фракции сокращения, толщины стенок и массы тела мышей в зависимости от времени в неделях. Стрелка = время однократного приема; пунктирная линия = ожидаемая траектория без лечения CDD866. Графики демонстрируют, что влияние CDD866 на сердечный рост и массу тела проявляется быстро, и является временным и обратимым. Влияние однократной дозы CDD866 также проявляется в течение 1-2 недель и сохраняется в течение не менее 6 недель.
На фиг. 6С представлены микрофотоснимки миокарда, окрашенного трихромом по Массону (синий = фиброз; красный = мышца), демонстрирующие снижение фиброза сердца у мышей ТАС, получавших CDD866.
Ha фиг. 6D представлена гистограмма, показывающая % фиброза с ТАС + изотипом Ab (серый) и ТАС+ CDD866 Ab (черный), демонстрируя тенденцию к уменьшению фиброза миокарда при лечении CDD866. *р<0,05. # р<0,01.
На фиг. 7А представлен вестерн-блот образцов икроножной мышцы, исследованных антителами p-SMAD3 и GAPDH. Образцы собирали у мышей C57BL/6 с подтвержденной сердечной дисфункцией после ТАС и последующих 8 недель лечения либо CDD866 (от ТТ-2 до ТТ-10), либо с контролем изотипа Ab (от ТТ-11 до ТТ-20). Эта фигура в целом демонстрирует, что CDD866 уменьшает передачу сигналов ActRII-A/B в скелетных мышцах в мышиной модели ТАС-опосредованной сердечной недостаточности. Стимуляция MSTN в клетках С2С12 была использована в качестве положительного контроля для анализа.
На фиг. 7В представлен график, на котором процентное изменение веса мышей по сравнению с исходным уровнем измеряется в сравнении с неделями после лечения. Точки на графике в виде ромба (красный) указывают на ТАС + изотип Ab. Точки на графике в виде квадрата (синие) обозначают ТАС + CDD866 Ab. * р<0,05. # р<0,01. CDD866 постепенно увеличивает общую массу тела, вероятно, за счет увеличения мышечной массы.
На фиг. 7С представлен % изменения по сравнению с контролем мышечной массы для различных групп скелетных мышц; EDL (длинный разгибатель пальцев), икроножные мышцы и большеберцовые кости. Красный цвет обозначает ТАС + изотип Ab. Синий цвет обозначает ТАС + CDD866 Ab. * р<0,05. # р<0,01. CDD866 в целом увеличивает массу трех групп скелетных мышц.
На фиг. 7D представлен график, на котором % распределения волокон строится по серии гистологических срезов, указывая, что CDD866 увеличивает размер скелетных миоцитов. Красный цвет указывает на лечение ТАС + изотипом Ab. Синий указывает на лечение ТАС + CDD866Ab. * р<0,05. # р<0,01.
На фиг. 7Е представлены четыре графика, на которых % распределения волокон строится по серии гистологических срезов, что указывает на то, что CDD866 индуцирует переключение нескольких типов волокон в скелетных мышцах. Красный цвет указывает на лечение ТАС + изотипом Ab. Синий указывает на лечение ТАС + CDD866 Ab.
На фиг. 8А представлен график, показывающий изменения в % фракции сокращения (FS) в зависимости от времени у мышей с миссенс-мутацией (F764L) в гене аМНС (мышиная модель дилатированной кардиомиопатии). Двенадцать недель лечения CDD866 привели к умеренной тенденции к увеличению систолической функции. Серый = Изотип Ab. Черный = CDD866Ab. * р<0,05. # р<0,01.
На фиг. 8В представлена гистограмма, показывающая относительные уровни экспрессии мРНК различных генов, имеющих отношение к ходу ActRII в сердечной ткани, у этих мышей, которым вводили либо CDD866 (черный), либо изотип Ab (серый). Существует тенденция к снижению сердечной экспрессии FSTL3 с CDD866, что свидетельствует об ингибировании передачи сигналов рецептора ActRII в сердце. *р<0,05. # р<0,01.
На фиг. 8С представлена гистограмма, показывающая относительные уровни экспрессии мРНК генов, связанных с патологической гипертрофией, у мышей, которых лечили изотипом Ab или CDD866Ab. *р<0,05. #р<0,01. Серый = Изотип Ab. Черный = CDD866Ab. *р<0,05. #р<0,01. ANP (предсердный натрийуретический пептид); BNP (мозговой натрийуретический пептид); аМНС (тяжелая цепь альфа-миозина); рМНС (тяжелая цепь бета-миозина). Существенных различий в профилях экспрессии генов патологической гипертрофии нет.
ОПРЕДЕЛЕНИЯ
Для более легкого понимания настоящего изобретения сначала определяются основные термины. Дополнительные определения приведены далее в подробном описании.
Термин «содержащий» означает «включающий», например, композиция, "содержащая" X, может состоять исключительно из X или может включать в себя что-то дополнительное, например, X+Y.
Термин «примерно» по отношению к числовому значению х означает, например, х+10%.
Далее приведены примеры возможных доклинических режимов лечения для оценки возможных эффектов лечения молекулой, связывающей ActRII, более предпочтительно антителом-антагонистом к ActRII, например, бимагрумабом.
Примером такого лечения является использование мышей, подвергшихся поперечному сужению аорты (ТАС), обычно используемой экспериментальной модели гипертрофии сердца и сердечной недостаточности, вызванной перегрузкой давлением. Специалист в данной области знает, как установить подходящие эксперименты или режимы дозирования для других видов, в частности для людей. Для исследований на приматах антитело против ActRII, например, бимагрумаб, можно вводить один раз в неделю на срок до 3 месяцев самцам и самкам яванского макаки путем внутривенной инъекции. 32 яванских макаки (16/пол) могут быть отнесены к одной из четырех групп лечения (от 3 до 5 животных/пол/группа), и им могут вводиться внутривенно инъекции либо носителя, либо антитела ActRIIB, например, BYM338, в 10, 30 или 100 мг/кг один раз в неделю в течение 13 недель (всего 14 доз; дозы должны подбираться на основе симптоматики сердечнососудистых заболеваний).
Термины «ActRIIA» и «ActRIIB» относятся к активин-рецепторам. Активины передают сигналы через гетеродимерный комплекс рецептора сериновых киназ, которые включают по меньшей мере два рецептора типа I (I и IB) и два рецептора типа II (IIA и IIB, также известные как ACVR2A и ACVR2B). Все эти рецепторы являются трансмембранными белками, состоящими из лигандсвязывающего внеклеточного домена с цистеин-богатой областью, трансмембранного домена и цитоплазматического домена с ожидаемой серии/ треониновой специфичностью. Рецепторы типа I необходимы для передачи сигналов, тогда как рецепторы типа II необходимы для связывания лигандов и для биосинтеза/ накопления рецепторов типа I. Рецепторы типа I и II образуют стабильный комплекс после связывания лиганда, что приводит к фосфорилированию рецепторов типа I рецепторами типа II. Активин-рецептор IIB (ActRIIB) является рецептором миостатина. Активин-рецептор IIA (Act RIIA) также является рецептором мизостатина. Термин рецептор ActRIIB или ActIIB относится к ActRIIB человека, как определено в SEQ ID NO: 181 (ААС64515.1, GI: 3769443). В данной области известны поликлональные и моноклональные антитела против ActRIIB исследовательского уровня, такие как R&D Systems®, MN, USA. Конечно, антитела против ActRIIB могут быть получены от других видов и могут использоваться для лечения патологических состояний у этих видов.
Термин «иммунная реакция» относится к действию, например, лимфоцитов, антиген-презентирующих клеток, фагоцитарных клеток, гранулоцитов и растворимых макромолекул, продуцируемых вышеуказанными клетками или печенью (например, антител, цитокинов и комплемента), которое приводит к селективному повреждению, уничтожению или удалению из организма человека инвазивных агентов, клеток или тканей, инфицированных патогенами, раковыми клетками или, в случае аутоиммунитета или патологического воспаления, нормальных клеток или тканей человека.
Термин «сигнальная активность» относится к биохимической причинно-следственной связи, обычно инициируемой межбелковым взаимодействием, таким как связывание фактора роста с рецептором, что приводит к передаче сигнала от одной части клетки к другой части клетки. В целом, передача включает специфическое фосфорилирование одного или нескольких остатков тирозина, серина или треонина в одном или нескольких белках в серии реакций, вызывающих передачу сигнала. Предпоследние процессы обычно включают ядерные превращения, приводящие к изменению экспрессии генов.
Термин «антитело» в контексте настоящего изобретения включает полные антитела и любой антигенсвязывающий фрагмент (то есть «антигенсвязывающую часть») или их отдельные цепи. Встречающееся в природе «антитело» представляет собой гликопротеин, содержащий по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, связанные между собой дисульфидными связями. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно обозначенной здесь как VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов, СН1, СН2 и СН3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно обозначенной здесь как VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена, CL. Области VH и VL могут быть далее подразделены на области гипервариабельности, называемые областями, определяющими комплементарность (CDR), чередующиеся с областями, которые являются более консервативными, называемыми каркасными областями (FR). Каждый VH и VL состоит из трех CDR и четырех FR, расположенных от аминоконца до карбоксиконца в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат домен связывания, который взаимодействует с антигеном. Константные области антител могут быть промежуточным звеном в связывании иммуноглобулина с тканями или факторами организма, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (Clq) классической системы комплемента.
Термин «антигенсвязывающая часть» антитела (или просто «часть антигена») в контексте настоящего изобретения относится к полноразмерному или одному или нескольким фрагментам антитела, которые сохраняют способность специфически связываться с антигеном (например, часть ActRIIB). Было показано, что антигенсвязывающая функция антитела может выполняться фрагментами полноразмерного антитела. Примеры связывающих фрагментов, охватываемых термином «антигенсвязывающая часть» антитела, включают фрагмент Fab, одновалентный фрагмент, состоящий из доменов VL, VH, CL и СН1; фрагмент F(ab)2, двухвалентный фрагмент, содержащий два фрагмента Fab, каждый из которых связывается с одним и тем же антигеном, связанным дисульфидным мостиком в шарнирной области; фрагмент Fd, состоящий из доменов VH и СН1; фрагмент Fv, состоящий из доменов VL и VH одного плеча антитела; фрагмент dAb (Ward et al., 1989 Nature 341: 544-546), который состоит из домена VH; и изолированная область, определяющая комплементарность (CDR).
Кроме того, хотя два домена фрагмента Fv, VL и VH кодируются отдельными генами, они могут быть объединены с использованием рекомбинантных методов с помощью синтетического линкера, который позволяет им образовать единую белковой цепи, в которой VL и VH области соединяются с образованием одновалентных молекул (известных как одноцепочечные Fv (scFv); см., например, Bird et al., 1988 Science 242: 423-426; и Huston et al., 1988 Proc. Natl. Acad. Sci. 85: 5879. - 5883). Такие одноцепочечные антитела также предназначены для включения в термин «антигенсвязывающая область» антитела. Эти фрагменты антител получают с использованием общепринятых методик, известных специалистам в данной области, и фрагменты проверяют на пригодность таким же образом, как и интактные антитела.
«Изолированное антитело», в контексте настоящего изобретения, относится к антителу, которое по существу не содержит других антител, обладающих различной антигенной специфичностью (например, изолированное антитело, которое специфически связывает ActRIIB, по существу не содержит антител, которые специфически связывают антигены, отличные от ActRIIB). Однако выделенное антитело, которое специфически связывает ActRIIB, может иметь перекрестную реактивность с другими антигенами, такими как молекулы ActRIIB от других видов. Кроме того, выделенное антитело может быть практически свободным от других клеточных материалов и/или химических веществ.
Термины «перекрестное блокирование», «перекрестно блокирующий» и «перекрестно блокированный» используются здесь взаимозаменяемо для обозначения способности антитела или другого связывающего агента препятствовать связыванию других антител или связывающих агентов с ActRIIB, в частности лиганд-связывающий домен, в стандартном конкурентном анализе связывания.
Используемые здесь термины «моноклональное антитело» или «композиция моноклонального антитела» относятся к приготовлению молекул антитела с одной молекулярной композицией. Композиция моноклонального антитела проявляет одну специфичность связывания и сродство к конкретному эпитопу.
Термин «человеческое антитело», используемый в данном документе, предназначен для включения антител, имеющих вариабельные области, в которых как каркасные области, так и области CDR получены из последовательностей человеческого происхождения. Кроме того, если антитело содержит константную область, константная область также получена из таких последовательностей человека, например, последовательности зародышевой линии человека или мутированные версии последовательностей зародышевой линии человека или антитела, содержащие консенсусные каркасные последовательности, полученные из анализа каркасных последовательностей человека, например, как описано в Knappik, et al. (2000. J Mol. Biol. 296, 57-86). Антитела человека по настоящему изобретению могут включать в себя аминокислотные остатки, не кодируемые человеческими последовательностями (например, мутации, введенные путем случайного или сайт-направленного мутагенеза in vitro или соматической мутацией in vivo). Однако термин «человеческое антитело», как используется в данном документе, не предназначен для включения антител, в которых последовательности CDR, полученные из зародышевой линии другого вида млекопитающих, таких как мышь, были привиты на каркасные последовательности человека.
Термин «человеческое моноклональное антитело» относится к антителам, обладающим единственной специфичностью связывания, которые имеют вариабельные области, в которых как каркасные области, так и области CDR получены из последовательностей человека. В одном варианте осуществления человеческие моноклональные антитела продуцируются гибридомой, которая включает В-клетку, полученную от трансгенного нечеловекоподобного животного, например, трансгенная мышь, имеющая геном, содержащий трансген тяжелой цепи человека и трансген легкой цепи, слитый с иммортализованной клеткой.
Термин «рекомбинантное человеческое антитело» в контексте настоящего изобретения включает все человеческие антитела, которые получают, экспрессируют, создают или выделяют рекомбинантными способами, такие как антитела, выделенные от животного (например, мыши), которое является трансгенным или трансхромосомным для генов человеческого иммуноглобулина, или полученные из них гибридомы, антитела, выделенные из клетки-хозяина, трансформированной для экспрессии человеческого антитела, например, из трансфектомы, антитела, выделенные из рекомбинантной, комбинаторной библиотеки антител человека, и антитела, полученные, экспрессированные, созданные или выделенные любыми другими способами, которые включают сплайсинг всего или части гена человеческого иммуноглобулина, последовательностей в другие последовательности ДНК. Такие рекомбинантные человеческие антитела имеют вариабельные области, в которых каркасные области и области CDR получены из последовательностей иммуноглобулина зародышевой линии человека. Однако в некоторых вариантах осуществления такие рекомбинантные человеческие антитела могут быть подвергнуты мутагенезу in vitro (или, когда используется трансгенное по человеческим Ig-последовательностям животное, соматическому мутагенезу in vivo) и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител представляют собой последовательности, которые, хотя и получены из последовательностей VH и VL зародышевой линии человека и связаны с ними, в естественных условиях не могут существовать в репертуаре зародышевой линии человеческого антитела in vivo.
Используемый здесь термин «изотип» относится к классу антител (например, IgM, IgE, IgG, таких как IgG1 или IgG2), который обеспечивается генами константной области тяжелой цепи.
Фразы «антитело, распознающее антиген» и «антитело, специфичное к антигену» используются здесь взаимозаменяемо с термином «антитело, которое специфически связывается с антигеном».
Используемый здесь термин антитело, которое «специфически связывается с полипептидом ActRIIB» предназначен для обозначения антитела, которое связывается с полипептидом ActRIIB человека с KD около 100 нМ или менее, около 10 нМ или менее, около 1 нМ или менее. Предполагается, что антитело, которое «перекрестно реагирует с антигеном, отличным от ActRIIB», относится к антителу, которое связывает этот антиген с KD около 10×10-9 М или менее, около 5×10-9 М или менее или около 2×10-9 М или менее. Предполагается, что антитело, которое «не вступает в перекрестную реакцию с конкретным антигеном», относится к антителу, которое связывается с этим антигеном, с KD около 1,5×10-8 М или более или с KD около 5-10×10-8 М или около 1×10-7 М или более. В некоторых вариантах осуществления такие антитела, которые не вступают в перекрестную реакцию с антигеном, проявляют по существу невыявленное связывание с этими белками в стандартных анализах связывания. KD может быть определено с использованием биосенсорной системы, такой как система Biacore®, или равновесного титрования в растворе.
Используемый здесь термин «антитело-антагонист» предназначен для обозначения антитела, которое ингибирует индуцированную ActRIIB сигнальную активность в присутствии миостатина или других лигандов ActRIIB, таких как активины или GDF-11, и/или антитела, которое ингибируют индуцированную ActRIIA сигнальную активность в присутствии миостатина или других лигандов ActRIIA, таких как активины или GDF-11. Примеры анализа для выявления этого включают ингибирование передачи сигналов, индуцированных миостатином (например, анализом Smad-зависимого гена-репортера), ингибирование индуцированного миостатином фосфорилирования Smad (P-Smad ELISA) и ингибирование индуцированного миостатином ингибирования дифференциации клеток скелетных мышц (например, анализ креатинкиназы).
В некоторых вариантах осуществления антитела ингибируют индуцированную миостатином передачу сигналов, измеренную анализом Smad-зависимого гена-репортера при IC50 около 10 нМ или менее, около 1 нМ или менее или около 100 пМ или менее.
Используемый здесь термин «не обладающий агонистической активностью» предназначен для обозначения антитела, которое незначительно повышает активность передачи сигналов, опосредованных ActRIIB, в отсутствие миостатина в анализе на основе клеток, таком как ингибирование передачи сигналов, индуцированной миостатином (например, анализ Smad-зависимого гена-репортера), ингибирование индуцированного миостатином фосфорилирования Smad (P-Smad ELISA) и ингибирование индуцированного миостатином ингибирования дифференциации клеток скелетных мышц (например, анализ креатинкиназы).
Термин «Kassoc» или «Ка», как используется в данном документе, предназначен для обозначения скорости ассоциации конкретного взаимодействия антитело-антиген, тогда как термин «Kdis» или «Kd», как используется в данном документе, предназначен для обозначения скорость диссоциации конкретного взаимодействия антитело-антиген. Используемый здесь термин «KD» предназначен для обозначения константы диссоциации, которая получается из отношения Kd к Ka (т.е. Kd/Ka) и выражается в виде молярной концентрации (М). Значения KD для антител могут быть определены с использованием методов, хорошо известных в данной области. Методом определения KD антитела является использование поверхностного плазмонного резонанса, такого как биосенсорная система Biacore®, или равновесного титрования раствора (SET) (см. Friguet et al. (1985) J. Immunol Methods; 77 (2): 305-319 и Hanel C. et al. (2005) Anal Biochem; 339 (1): 182-184).
Используемый здесь термин «аффинность» относится к силе взаимодействия между антителом и антигеном в отдельных иммунодоминантных сайтах. Внутри каждого иммунодоминантного сайта вариабельная область «плеча» антитела взаимодействует посредством слабых нековалентных связей с антигеном в многочисленных участках; чем больше взаимодействий, тем сильнее сродство.
Используемый здесь термин «авидность» относится к информативному показателю общей стабильности или силы комплекса антитело-антиген. Он контролируется тремя основными факторами: аффинностью антител к эпитопу; валентностью как антигена, так и антитела; и структурным расположением взаимодействующих частей. В конечном итоге эти факторы определяют специфичность антитела, то есть вероятность того, что конкретное антитело связывается сточным эпитопом антигена.
Используемый здесь термин активность «ADCC» или «антитело-зависимая клеточная цитотоксичность» относится к активности, истощающей клетки В человека. Активность ADCC может быть измерена с помощью анализов истощения В-клеток человека, известных в данной области.
Для того, чтобы получить образец с более высокой авидностью, может быть сконструирован димерный конъюгат (две молекулы белка антитела, связанных с маркером FACS), что делает взаимодействие с низкой аффинностью (например, с антителом зародышевой линии) более легко обнаруживаемым с помощью FACS. Кроме того, другое средство для увеличения авидности связывания антигена включает генерирование димеров, тримеров или мультимеров любой из описанных здесь конструкций антител против ActRIIB. Такие мультимеры могут быть получены посредством ковалентного связывания между отдельными модулями, например, путем имитации естественного связывания C-N-конца или путем имитации димеров антител, которые удерживаются вместе через их константные области. Связи, созданные на границе раздела Fc/Fc, могут быть ковалентными или нековалентными. Кроме того, партнеры димеризации или мультимеризации, отличные от Fc, могут использоваться в гибридах ActRIIB для создания таких структур более высокого порядка. Например, можно использовать домены мультимеризации, такие как домен тримеризации, описанный в WO 2004/039841, или домен пентамеризации, описанный в WO 98/18943.
Используемый здесь термин «селективность» для антитела относится к антителу, которое связывается с определенной полипептидной мишенью, но не с близко родственными полипептидами.
Используемый здесь термин «высокая аффинность» для антитела относится к антителу, имеющему KD 1 нМ или менее для целевого антигена. Используемый здесь термин «субъект» включает любого человека или нечелевокоподобное животное.
Термин "нечеловекоподобное животное" включает всех позвоночных животных, например, млекопитающие и немлекопитающие, такие как нечеловекоподобные приматы, овцы, собаки, кошки, мыши, лошади, коровы, цыплята, земноводные, рептилии и т.д.
Используемый здесь термин «оптимизированный» означает, что нуклеотидная последовательность была изменена для кодирования аминокислотной последовательности с использованием кодонов, которые являются предпочтительными в клетке-продуценте или организме, обычно в эукариотической клетке, например, в клетке Pichia, клетке Trichoderma, клетке яичника китайского хомячка (СНО) или клетке человека. Оптимизированная нуклеотидная последовательность разработана таким образом, чтобы полностью или в максимально возможной степени сохранить аминокислотную последовательность, первоначально кодируемую исходной нуклеотидной последовательностью, которая также известна как «родительская» последовательность. Оптимизированные последовательности здесь сконструированы так, чтобы иметь кодоны, которые являются предпочтительными в клетках СНО млекопитающих, однако здесь также предусматривается оптимизированная экспрессия этих последовательностей в других эукариотических клетках. Аминокислотные последовательности, кодируемые оптимизированными нуклеотидными последовательностями, также называют оптимизированными.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Было обнаружено, что антитела, направленные на рецепторы ActRII, например, бимагрумаб, могут снижать передачу сигналов через эти рецепторы и использоваться при профилактике и/или лечении заболеваний сердца.
Следовательно, в одном аспекте настоящее изобретение относится к композиции, содержащей молекулу, связывающую ActRII А или ActRIIB, например, бимагрумаб, или функциональный белок, содержащий антигенсвязывающую часть указанного антитела. Связывающая молекула может быть связывающей ActRIIB молекулой, например, ActRIIB человека. Полипептидная последовательность человеческого ActRIIВ приведена в SEQ ID NO: 181 (ААС64515.1, GI: 3769443). В одном варианте осуществления антитело или функциональный белок происходит от млекопитающего, такого как человек или верблюд. Таким образом, антитело, содержащееся в раскрытой композиции, может представлять собой химерное, человеческое или гуманизированное антитело. В конкретном варианте осуществления антитело против ActRIIB, содержащееся в раскрытой композиции, характеризуется как имеющее антигенсвязывающую область, которая специфична для белка-мишени ActRIIB и связывается с ActRIIВ или фрагментом ActRIIB.
В одном варианте осуществления антитела, содержащиеся в раскрытой композиции, являются антагонистами ActRII, не обладающими или обладающими низкой агонистической активностью. В другом варианте осуществления антитело или функциональный фрагмент, содержащийся в раскрытой композиции, связывает целевой белок ActRII и уменьшает связывание миостатина с ActRII до базального уровня. В дополнительном аспекте этого варианта осуществления антитело или функциональный фрагмент, содержащийся в раскрытой композиции, полностью предотвращает связывание миостатина с ActRII. В дополнительном варианте осуществления антитело или функциональный фрагмент, содержащийся в раскрытой композиции, ингибируют активацию Smad. В дополнительном варианте осуществления антитело или функциональный фрагмент, содержащийся в раскрытой композиции, ингибирует активин-рецептор типа IIB, опосредованный миостатин-индуцированным ингибированием скелетной дифференциации через Smad-зависимый путь.
Связывание может быть определено одним или несколькими анализами, которые можно использовать для измерения активности, которая представляет собой либо антагонизм, либо агонизм антитела. Предпочтительно, анализы измеряют по меньшей мере одно из влияний антитела на ActRIIB, которое включает: ингибирование связывания миостатина с ActRIIB с помощью ELISA, ингибирование индуцированной миостатином передачи сигналов (например, с помощью анализа Smad-зависимого гена-репортера), ингибирование индуцированного миостатином фосфорилирования Smad (P-Smad ELISA) и ингибирование индуцированного миостатином ингибирования дифференциации клеток скелетных мышц (например, анализом креатинкиназы).
В одном из вариантов осуществления настоящее изобретение относится к композициям, содержащим антитела, которые специфически связываются с миостатин-связывающей областью (т.е. лиганд-связывающим доменом) ActRIIB. Этот лиганд-связывающий домен состоит из аминокислот 19-134 SEQ ID NO: 181 и ему присвоен SEQ ID NO: 182 в настоящем документа. Домен связывания лиганда содержит несколько описанных ниже эпитопов.
В одном из вариантов осуществления изобретения антитела, содержащиеся в раскрытой здесь композиции, связываются с ActRIIB с KD около 100 нМ или менее, около 10 нМ или менее, около 1 нМ или менее. Предпочтительно антитела, содержащиеся в раскрытой композиции, связываются с ActRIIB с аффинностью 100 пМ или менее (т.е. около 100 пМ, около 50 пМ, около 10 пМ, около 2 пМ, около 1 пМ или менее). В одном варианте осуществления антитела, содержащиеся в раскрытой композиции, связываются с ActRIIB с аффинностью от около 1 до около 10 пМ.
В одном варианте осуществления изобретения антитела, содержащиеся в раскрытой здесь композиции, не перекрестно реагируют с белком, связанным с ActRIIB, в частности, не перекрестно реагируют с ActRIIA человека (NP_001607.1, GL4501897). В другом варианте осуществления антитела, содержащиеся в раскрытой композиции, перекрестно реагируют с ActRIIA и связываются с ActRIIB с эквивалентной аффинностью или примерно в 1, 2, 3,4 или 5-кратно большей аффинностью, чем они связываются с ActRIIA, более предпочтительно примерно в 10 раз большей, еще более предпочтительно примерно в 20, 30, 40 или 50 раз, еще более предпочтительно примерно в 100 раз.
В одном варианте осуществления изобретения антитела, содержащиеся в раскрытой в в настоящем изобретении композиции, связываются с ActRIIA с аффинностью 100 пМ или более (т.е. около 250 пМ, около 500 пМ, около 1 нМ, около 5 нМ или более).
В одном варианте осуществления изобретения антитела, содержащиеся в описанной композиции, имеют изотип IgG2.
В другом варианте осуществления изобретения антитела, содержащиеся в описанной композиции, имеют изотип IgG1. В дополнительном варианте осуществления антитела, содержащиеся в раскрытой композиции, имеют изотип IgG1 и имеют измененную эффекторную функцию благодаря мутации области Fc. Указанная измененная эффекторная функция может быть сниженной активностью ADCC и CDC. В одном варианте осуществления указанная измененная эффекторная функция представляет собой отключенную активность ADCC и CDC.
В другом сходном варианте осуществления антитела, содержащиеся в раскрытой композиции, являются полностью человеческими или гуманизированными антителами IgG1, не обладающими активностью в отношении антителозависимой клеточной цитотоксичности (ADCC) или активностью CDC, и связываются с областью ActRIIB, состоящей из аминокислот 19-134 SEQ ID N0: 181.
В другом сходном варианте осуществления антитела, содержащиеся в раскрытой композиции, представляют собой полностью человеческие или гуманизированные антитела IgG1 с пониженной активностью антителозависимой клеточной цитотоксичности (ADCC) или активностью CDC и связываются с областью ActRIIB, состоящей из аминокислот 19-134 SEQ ID N0: 181.
Настоящее изобретение также относится к композициям, содержащим человеческие или гуманизированные антитела против ActRIIB для применения в профилактике и/или лечении сердечных заболеваний, таких как сердечные заболевания, описанные выше.
В определенных вариантах осуществления антитела, содержащиеся в раскрытой композиции, получены из конкретных последовательностей тяжелой и легкой цепей и/или содержат конкретные структурные признаки, такие как области CDR, содержащие конкретные аминокислотные последовательности. Изобретение обеспечивает изолированные антитела против ActRIIB, способы получения таких антител, иммуноконъюгаты и поливалентные или полиспецифичные молекулы, содержащие такие антитела, и фармацевтические композиции, содержащие антитела, иммуноконъюгаты или биспецифичные молекулы.
В альтернативных вариантах осуществления, описанное изобретение относится к следующим аспектам:
1. Антагонист рецептора ActRII для использования в лечении и/или профилактике сердечной недостаточности, включая сердечную недостаточность, связанную с или вызванную, гипертонией, заболеванием коронарной артерии, диабет, старением, аритмией, кардиомиопатией при родах, стрессовой кардиомиопатией, токсическими или инфекционными агентами и другими формами генетической или идиопатической кардиомиопатии.
2. Антагонист рецептора ActRII для применения в соответствии с аспектом 1, причем антагонист ActRII следует вводить нуждающемуся в этом пациенту в дозе примерно 3-10 мг/кг.
3. Антагонист рецептора ActRII для применения в соответствии с аспектом 2, причем указанный антагонист миостатина следует вводить в дозе примерно 3 или примерно 10 мг/кг массы тела.
В альтернативном варианте, антагонист рецептора ActRII следует вводить в дозе примерно 3, 4, 5, 6, 7, 8, 9 или примерно 10 мг/кг массы тела.
4. Антагонист рецептора ActRII для применения в соответствии с аспектами 1-3, причем указанный антагонист рецептора ActRII следует вводить внутривенно или подкожно.
5. Антагонист рецептора ActRII для применения по любому из аспектов 1-4, причем указанный антагонист рецептора ActRII следует вводить каждые четыре недели.
В альтернативном варианте, антагонист рецептора ActRII можно вводить каждые 8 недель.
6. Антагонист рецептора ActRII для применения по любому из аспектов 1-5, причем указанный антагонист рецептора ActRII следует вводить в течение по меньшей мере 3 месяцев.
7. Антагонист рецептора ActRII для применения по любому из аспектов 1-6, причем указанный антагонист рецептора ActRII следует вводить в течение срока до 12 месяцев.
Предпочтительно антагонист рецептора ActRII следует вводить в течение, по меньшей мере, или до 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 месяцев.
8. Способ лечения и/или профилактики сердечной недостаточности, причем указанный способ включает введение эффективного количества антагониста рецептора ActRII субъекту, у которого есть сердечная недостаточность или кто подвержен риску развития сердечной недостаточности.
Во многих случаях сердечная недостаточность может быть вызвана или связана с таким состоянием, как порок сердца, ишемическая болезнь сердца, гипертензия, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, воздействие токсических и инфекционных агентов и другие формы генетической или идиопатической кардиомиопатии. Пациент с риском развития сердечной недостаточности может иметь одно или несколько из этих состояний.
9. Способ лечения структурной и/или функциональной аномалии сердца, связанной с состоянием, выбранным из группы, состоящей из порока сердца, гипертонии, заболевания коронарной артерии, диабета, старения, аритмии, кардиомиопатии при родах, стрессовой кардиомиопатии, токсических и инфекционных агентов и других форм генетической или идиопатической кардиомиопатии, причем указанный способ включает введение эффективного количества антагониста рецептора ActRII субъекту, у которого указанная структурная и/или функциональная аномалия сердца связана с указанным состоянием.
10. Способ в соответствии с аспектами 8 или 9, включающий введение антагониста рецептора ActRII нуждающемуся в этом пациенту в дозе примерно 3-10 мг/кг.
11. Способ в соответствии с аспектами 8 или 9, включающий введение антагониста рецептора ActRII нуждающемуся в этом пациенту в дозе примерно 3 или примерно 10 мг/кг массы тела.
12. Способ в соответствии с аспектами 8 или 9, включающий введение антагониста рецептора ActRII внутривенно или подкожно.
13. Способ в соответствии с аспектами 8-10, включающий введение антагониста рецептора ActRII каждые четыре недели.
14. Способ в соответствии с аспектами 8-13, включающий введение антагониста рецептора ActRII в течение по меньшей мере 3 месяцев.
15. Способ в соответствии с аспектом 14, включающий введение антагониста рецептора ActRII на срок до 12 месяцев.
16. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 1-15, причем антагонист рецептора ActRII представляет собой антитело против рецептора ActRII.
17. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 1-15, причем антитело против рецептора ActRII представляет собой бимагрумаб.
18. Антагонист рецептора ActRII для применения или способ в соответствии с аспектом 17, где антагонист рецептора ActRII представляет собой антитело против ActRII, которое связывается с эпитопом ActRIIB, состоящим из аминокислот 19-134 SEQ ID NO: 181 (SEQ ID NO: 182).
19. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-18, где антитело против ActRII связывается с эпитопом ActRIIB, включающим или состоящим из:
(а) аминокислоты 78-83 последовательности SEQ ID NO: 181 (WLDDFN - SEQ ID N0: 188);
(b) аминокислоты 76-84 последовательности SEQ ID NO: 181 (GCWLDDFNC - SEQ ID N0: 186);
(с) аминокислоты 75-85 последовательности SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID N0: 190);
(d)(d) аминокислоты 52-56 последовательности SEQ ID NO: 181 (EQDKR-SEQ ID N0: 189);
(е) аминокислоты 49-63 последовательности SEQ ID NO: 181 (CEGEQDKRLHCYASW - SEQ ID NO: 187);
(f) аминокислоты 29-41 последовательности SEQ ID NO: 181 (CIYYNANWELERT- SEQ ID N0: 191);
(g) аминокислоты 100-110 последовательности SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID N0: 192); или
(h) аминокислоты 78-83 последовательности SEQ ID NO: 181 (WLDDFN) и аминокислоты 52-56 SEQ ID NO: 181 (EQDKR).
20. Антагонист рецептора ActRII для применения в соответствии с аспектами 16-19, причем антитело против ActRIIB выбрано из группы, состоящей из:
а) антитело против ActRIIB, которое связывается с эпитопом ActRIIB, содержащее:
(a) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID N0: 188);
(b) аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID N0: 186);
(c) аминокислоты 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID N0: 190);
(d) аминокислоты 52-56 SEQ ID NO: 181 (EQDKR-SEQ ID N0: 189);
(e) аминокислоты 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW-SEQ ID NO: 187);
(e) аминокислоты 29-41 SEQ ID NO: 181 (CIYYNANWELERT-SEQ ID N0: 191);
(f) аминокислоты 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID N0: 192); или
(h) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислоты 52-56 SEQ ID NO: 181 (EQDKR);
и b) антитело-антагонист к ActRIIB, которое связывается с эпитопом ActRIIB, содержащим аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID N0: 188);
(b) аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID N0: 186);
(c) аминокислоты 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID N0: 190);
(d) аминокислоты 52-56 SEQ ID NO: 181 (EQDKR-SEQ ID N0: 189);
(e) аминокислоты 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW - SEQ ID N0: 187);
(f) аминокислоты 29-41 SEQ ID NO: 181 (CIYYNANWELERT- SEQ ID N0: 191);
(g) аминокислоты 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID N0: 192); или
(h) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислоты 52-56 SEQ ID NO: 181 (EQDKR), причем антитело имеет KD около 2 пМ.
21. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-20, причем антитело связывается с ActRIIB с аффинностью в 10 или более раз больше, чем оно связывается с ActRIIA.
22.Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-21, где антитело содержит вариабельную область тяжелой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-14; вариабельную область тяжелой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-28; вариабельную область тяжелой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 29-42; вариабельную область легкой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 43-56; вариабельную область легкой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 57-70; и вариабельную область легкой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 71-84.
23. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-22, где антитело содержит:
(a) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 1; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 15; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 29; вариабельную область легкой цепи CDR1 SEQ ID NO: 43; вариабельную область легкой цепи CDR2 SEQ ID NO: 57; и вариабельную область легкой цепи CDR3 SEQ ID NO: 71,
(b) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 2; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 16; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 30; вариабельную область легкой цепи CDR1 SEQ ID NO: 44; вариабельную область легкой цепи CDR2 SEQ ID NO: 58; и вариабельную область легкой цепи CDR3 SEQ ID NO: 72,
(c) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 3; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 17; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 31; вариабельную область легкой цепи CDR1 SEQ ID NO: 45; вариабельную область легкой цепи CDR2 SEQ ID NO: 59; и вариабельную область легкой цепи CDR3 SEQ ID NO: 73,
(d) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 4; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 18; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 32; вариабельную область легкой цепи CDR1 SEQ ID NO: 46; вариабельную область легкой цепи CDR2 SEQ ID NO: 60; и вариабельную область легкой цепи CDR3 of SEQ ID NO: 74,
(e) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 5; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 19; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 33; вариабельную область легкой цепи CDR1 SEQ ID NO: 47; вариабельную область легкой цепи CDR2 SEQ ID NO: 61; и вариабельную область легкой цепи CDR3 SEQ ID NO: 75,
(f) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 6; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 20; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 34; вариабельную область легкой цепи CDR1 SEQ ID NO: 48; вариабельную область легкой цепи CDR2 SEQ ID NO: 62; и вариабельную область легкой цепи CDR3 SEQ ID NO: 76,
(g) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 7; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 21; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 35; вариабельную область легкой цепи CDR1 SEQ ID NO: 49; вариабельную область легкой цепи CDR2 SEQ ID NO: 63; и вариабельную область легкой цепи CDR3 of SEQ ID NO: 77,
(h) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 8; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 22; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 36; вариабельную область легкой цепи CDR1 SEQ ID NO: 50; вариабельную область легкой цепи CDR2 SEQ ID NO: 64; и вариабельную область легкой цепи CDR3 SEQ ID NO: 78,
(i) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 9; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 23; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 37; вариабельную область легкой цепи CDR1 SEQ ID NO: 51; вариабельную область легкой цепи CDR2 SEQ ID NO: 65; и вариабельную область легкой цепи CDR3 SEQ ID NO: 79,
(j) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 10; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 24; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 38; вариабельную область легкой цепи CDR1 SEQ ID NO: 52; вариабельную область легкой цепи CDR2 SEQ ID NO: 66; и вариабельную область легкой цепи CDR3 SEQ ID NO: 80,
(k) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 11; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 25; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 39; вариабельную область легкой цепи CDR1 SEQ ID NO: 53; вариабельную область легкой цепи CDR2 SEQ ID NO: 67; и вариабельную область легкой цепи CDR3 SEQ ID NO: 81,
(l) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 12; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 26; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 40; вариабельную область легкой цепи CDR1 SEQ ID NO: 54; вариабельную область легкой цепи CDR2 SEQ ID NO: 68; и вариабельную область легкой цепи CDR3 SEQ ID NO: 82,
(m) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 13; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 27; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 41; вариабельную область легкой цепи CDR1 SEQ ID NO: 55; вариабельную область легкой цепи CDR2 SEQ ID NO: 69; и вариабельную область легкой цепи CDR3 SEQ ID NO: 83, или
(n) вариабельную область тяжелой цепи CDR1 SEQ ID NO: 14; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 28; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 42; вариабельную область легкой цепи CDR1 SEQ ID NO: 56; вариабельную область легкой цепи CDR2 SEQ ID NO: 70; и вариабельную область легкой цепи CDR3 SEQ ID NO: 84.
24. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-23, причем антитело содержит полноразмерную аминокислотную последовательность тяжелой цепи, имеющую по меньшей мере 95%-ную идентичность последовательности по меньшей мере с одной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 146-150 и 156-160.
25. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-24, причем антитело содержит полноразмерную аминокислотную последовательность легкой цепи, имеющую по меньшей мере 95%-ную идентичность последовательности по меньшей мере с одной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 141-145 и 151-155.
26. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-25, где антитело содержит:
(a) вариабельную последовательность тяжелой цепи SEQ ID NO: 99 и вариабельную последовательность легкой цепи SEQ ID NO: 85;
(b) вариабельную последовательность тяжелой цепи SEQ ID NO: 100 и вариабельную последовательность легкой цепи SEQ ID NO: 86;
(c) вариабельную последовательность тяжелой цепи SEQ ID NO: 101 и вариабельную последовательность легкой цепи SEQ ID NO: 87;
(d) вариабельную последовательность тяжелой цепи SEQ ID NO: 102 и вариабельную последовательность легкой цепи SEQ ID NO: 88;
(e) вариабельную последовательность тяжелой цепи SEQ ID NO: 103 и вариабельную последовательность легкой цепи SEQ ID NO: 89;
(f) вариабельную последовательность тяжелой цепи SEQ ID NO: 104 и вариабельную последовательность легкой цепи SEQ ID NO: 90;
(g) вариабельную последовательность тяжелой цепи SEQ ID NO: 105 и вариабельную последовательность легкой цепи SEQ ID NO: 91;
(h) вариабельную последовательность тяжелой цепи SEQ ID NO: 106 и вариабельную последовательность легкой цепи SEQ ID NO: 92;
(i) вариабельную последовательность тяжелой цепи SEQ ID NO: 107 и вариабельную последовательность легкой цепи SEQ ID NO: 93;
(j) вариабельную последовательность тяжелой цепи SEQ ID NO: 108 и вариабельную последовательность легкой цепи SEQ ID NO: 94;
(k) вариабельную последовательность тяжелой цепи SEQ ID NO: 109 и вариабельную последовательность легкой цепи SEQ ID NO: 95;
(l) вариабельную последовательность тяжелой цепи SEQ ID NO: 110 и вариабельную последовательность легкой цепи SEQ ID NO: 96;
(m) вариабельную последовательность тяжелой цепи SEQ ID NO: 111 и вариабельную последовательность легкой цепи SEQ ID NO: 97; или
(n) вариабельную последовательность тяжелой цепи SEQ ID NO: 112 и вариабельную последовательность легкой цепи SEQ ID NO: 98.
27. Антагонист рецептора ActRII для применения или способ в соответствии с аспектами 16-26, где антитело содержит:
(а) последовательность тяжелой цепи SEQ ID NO: 146 и последовательность легкой цепи SEQ ID NO: 141;
(b) последовательность тяжелой цепи SEQ ID NO: 147 и последовательность легкой цепи SEQ ID NO: 142;
(c) последовательность тяжелой цепи SEQ ID NO: 148 и последовательность легкой цепи SEQ ID NO: 143;
(d) последовательность тяжелой цепи SEQ ID NO: 149 и последовательность легкой цепи SEQ ID NO: 144;
(e) последовательность тяжелой цепи SEQ ID NO: 150 и последовательность легкой цепи SEQ ID NO: 145;
(f) последовательность тяжелой цепи SEQ ID NO: 156 и последовательность легкой цепи SEQ ID NO: 151;
(g) последовательность тяжелой цепи SEQ ID NO: 157 и последовательность легкой цепи SEQ ID NO: 152;
(h) последовательность тяжелой цепи SEQ ID NO: 158 и последовательность легкой цепи SEQ ID NO: 153;
(i) последовательность тяжелой цепи SEQ ID NO: 159 и последовательность легкой цепи SEQ ID NO: 154; или
(j) последовательность тяжелой цепи SEQ ID NO: 160 и последовательность легкой цепи SEQ ID NO: 155.
28. Антагонист рецептора ActRII для применения в соответствии с аспектами 16-27, где антитело, содержащееся в указанной композиции, перекрестно блокирует или перекрестно блокируется по меньшей мере одним антителом аспекта 27 от связывания с ActRIIB.
29. Антагонист рецептора ActRII для применения в соответствии с аспектами 16-28, где антитело, содержащееся в указанной композиции, изменяет эффекторную функцию посредством мутации области Fc.
30. Антагонист рецептора ActRII для применения в соответствии с аспектами 16-29, где антитело, содержащееся в указанной композиции, связывается с эпитопом, распознаваемым антителом, перечисленным в аспектах 26-27.
31. Антагонист рецептора ActRII для применения в соответствии с аспектами 16-30, где антитело кодируется pBW522 (DSM22873) или pBW524 (DSM22874).
32. Бимагрумаб для применения при лечении и/или профилактике сердечной недостаточности или для применения при лечении структурных и/или функциональных нарушений сердца, связанных с состоянием, выбранным из группы, состоящей из порока сердца, гипертонии, заболевания коронарной артерии, диабета, старения, аритмии, кардиомиопатия при родах, стрессовой кардиомиопатия, токсических и инфекционных агентов и других форм генетической или идиопатической кардиомиопатии, где бимагрумаб следует вводить внутривенно в дозе примерно 3-10 мг/кг массы тела каждые четыре недели.
33. Композиция, содержащая 150 мг/мл бимагрумаба, для применения при лечении и/или профилактике сердечной недостаточности или для лечения структурных и/или функциональных нарушений сердца, связанных с состоянием, выбранным из группы, состоящей из порока сердца, гипертонии, заболевания коронарной артерии, диабета, старения, аритмии, кардиомиопатии при родах, стрессовой кардиомиопатии, токсических и инфекционных агентов и других форм генетической или идиопатической кардиомиопатии.
34. Стандартная лекарственная форма, содержащая 150 мг/мл бимагрумаба.
В других вариантах осуществления стандартная лекарственная форма, то есть флакон, содержит 100-200 мг/мл бимагрумаба, предпочтительно 100, 105, 110, 115, 120, 125, 130, 135, 140, 145, 150, 155, 160, 165 170, 175, 180, 185, 190, 195, 200 мг/мл бимагрумаба.
35. Инфузионный пакет, содержащий соответствующее количество бимагрумаба из одного или нескольких флаконов, разбавленный раствором. Раствор предпочтительно представляет собой раствор D-глюкозы.
В некоторых других вариантах осуществления антагонист рецептора ActRII или антитело против ActRII, такое как бимагрумаб, следует вводить в дозе примерно 1, 2, 3, 4, 5, 5, 6, 7, 8, 9, 10 мг/кг массы тела.
Раскрытые в данном изобретении антагонисты рецептора ActRII для изготовления лекарственного средства для лечения и/или профилактики сердечной недостаточности и для лечения структурной и/или функциональной аномалии сердца, связанной с таким состоянием, как порок сердца, гипертония, заболевание коронарной артерии, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия и другие формы генетической или идиопатической дилатационной кардиомиопатии.
В дополнительных вариантах осуществления, все аспекты, раскрытые в данном изобретении, могут использоваться в сочетании любого одного с любым другим.
Различные аспекты изобретения описаны более подробно в следующих подразделах.
Стандартные анализы для оценки способности антител связываться с ActRII различных видов известны в данной области, включая, например, ELISA, вестерн-блоты и RIA. Аффинность связывания антител также можно оценивать с помощью стандартных анализов, известных в данной области, таких как анализ Biacore или титрование в равновесном растворе. Методы, основанные на поверхностном плазмонном резонансе, такие как Biacore, могут определять кинетику связывания, что позволяет рассчитывать аффинность связывания.
Соответственно, антитело, которое «ингибирует» одно или несколько из этих функциональных свойств ActRII (например, биохимическую, иммунохимическую, клеточную, физиологическую или другую биологическую активность или тому подобное), как определено в соответствии с методологиями, известными в данной области техники и описанными здесь, будет пониматься как относящееся к статистически значимому снижению конкретной активности по сравнению с тем, что наблюдается в отсутствие антитела (например, или когда присутствует контрольное антитело нерелевантной специфичности). Антитело, которое ингибирует активность ActRII, оказывает такое статистически значимое снижение, по меньшей мере, на 10% измеренного параметра, по меньшей мере, на 50%, 80% или 90%, и в некоторых вариантах осуществления антитело по изобретению может ингибировать более 95%, 98% или 99% от функциональной активности ActRII В.
Способность или степень, в которой антитело или другой связывающий агент способны влиять на связывание другого антитела или связывающей молекулы с ActRII, и, следовательно, можно ли сказать, что он перекрестно блокируется в соответствии с изобретением, может быть определена с использованием стандартных анализов конкурентного связывания связывания. Один подходящий анализ включает использование технологии Biacore (например, с использованием прибора BIAcore (Biacore, Упсала, Швеция)), которая может измерять степень взаимодействий с использованием технологии поверхностного плазмонного резонанса. Другой анализ для измерения перекрестной блокировки использует подход, основанный на ELISA. В дальнейших испытаниях используется анализ FACS, в котором тестируют конкуренцию различных антител за связывание с клетками, экспрессирующими ActRIIB.
В соответствии с настоящим изобретением перекрестно блокирующее антитело или другой связывающий агент в соответствии с настоящим изобретением связывается с ActRII в описанном анализе перекрестного блокирования BIAcore таким образом, что зарегистрированное связывание комбинации (смеси) антител или связывающих агентов составляет от 80% до 0,1% (например, от 80% до 4%) от максимального теоретического связывания, в частности, от 75% до 0,1% (например, от 75% до 4%) от максимального теоретического связывания, и более конкретно, от 70% до 0,1% (например, от 70% до 4%) и еще более конкретно от 65% до 0,1% (например, от 65% до 4%) от максимального теоретического связывания (как определено выше) двух антител или связывающих агентов в комбинации.
Антитело определяется как перекрестно блокирующее антитело против ActRIIB по изобретению в анализе ELISA, если тестируемое антитело способно вызывать снижение связывания антитела против ActRIIB с ActRIIB от 60% до 100%, конкретнее от 70% до 100%, а точнее от 80% до 100%, по сравнению с лунками положительного контроля (т.е. тем же антителом против ActRIIB и ActRIIB, но без «тестового» перекрестно блокирующего антитела). Примерами перекрестно блокирующих антител, которые цитируются в данном документе, являются MOR08159 и MOR08213 (раскрытые в WO 2010/12003). Таким образом, изобретение обеспечивает композиции, содержащие перекрестно блокирующие антитела MOR08159 или MOR08213 для связывания с ActRIIB.
Рекомбинантные антитела
Антитела, например, антитела-антагонисты к ActRII, такие как бимагрумаб, содержащиеся в композициях, используемых в данном описании, включают рекомбинантные антитела человека, выделенные и структурно охарактеризованные, как описано здесь. Аминокислотные последовательности VH антител, содержащихся в композициях по изобретению, показаны в SEQ ID NO: 99-112. Аминокислотные последовательности VL антител, содержащихся в композициях по изобретению, показаны в SEQ ID NO: 85-98 соответственно. Примеры предпочтительных полноразмерных аминокислотных последовательностей тяжелых цепей антител, содержащихся в композициях по изобретению, показаны в SEQ ID NO: 146-150 и 156-160. Примеры предпочтительных полноразмерных аминокислотных последовательностей легкой цепи антител, содержащихся в композициях по изобретению, показаны в SEQ ID NO: 141-145 и 151-155 соответственно. Другие антитела, входящие в состав композиций по изобретению, включают аминокислоты, которые были мутированы путем делеции, вставки или замены аминокислот, но при этом имеют по меньшей мере 60, 70, 80, 90, 95, 97 или 99-процентную идентичность в областях CDR с областями CDR, изображенными в последовательностях, описанных выше. В некоторых вариантах осуществления они включает мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были мутированы путем делеции, вставки или замены аминокислот в областях CDR по сравнению с областями CDR, изображенными в последовательности, описанной выше.
Кроме того, вариабельные родительские нуклеотидные последовательности тяжелой цепи показаны в SEQ ID NO: 127-140. Вариабельные нуклеотидные последовательности легкой цепи представлены в SEQ ID NO: 113-126. Полноразмерные нуклеотидные последовательности легкой цепи, оптимизированные для экспрессии в клетке млекопитающего, показаны в SEQ ID NO: 161-165 и 171-175. Полноразмерные нуклеотидные последовательности тяжелой цепи, оптимизированные для экспрессии в клетке млекопитающего, показаны в SEQ ID NO: 166-170 и 176-180. Другие антитела, входящие в состав композиций по изобретению, включают аминокислоты или кодируются нуклеиновыми кислотами, которые были мутированы, но имеют по меньшей мере 60 или более (то есть 80, 90, 95, 97, 99 или более) % идентичности с последовательностями, описанными выше. В некоторых вариантах осуществления они включает мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были мутированы путем делеции, вставки или замены аминокислоты в вариабельных областях по сравнению с вариабельными областями, представленными в последовательности, описанной выше.
Так как каждое из этих антител связывает один и тот же эпитоп и является потомками одного и того же родительского антитела, последовательности VH, VL, полной длины легкой цепи и полной длины тяжелой цепи (нуклеотидные последовательности и аминокислотные последовательности) можно «смешивать и сопоставлять» с получением других анти-ActRIIB-связывающих молекул по изобретению. Связывание ActRIIB с такими «смешанными и подобранными» антителами можно тестировать, используя анализы связывания, описанные выше, и хорошо известные способы, такие как, например, ELISA. Когда эти цепи смешаны и сопоставлены, последовательность VH из определенного объединения VH/VL должна быть заменена структурно подобной последовательностью VH. Аналогично, полноразмерная последовательность тяжелой цепи из конкретного объединения тяжелой цепи/легкой цепи полной длины должна быть заменена структурно подобной последовательностью тяжелой цепи полной длины. Аналогично, последовательность VL из определенной пары VH/VL должна быть заменена структурно подобной последовательностью VL. Аналогичным образом полноразмерная последовательность легкой цепи из конкретного объединения тяжелой цепи/легкой цепи полной длины должна быть заменена структурно подобной полноразмерной последовательностью легкой цепи. Соответственно, в одном аспекте настоящее изобретение относится к композициям, содержащим рекомбинантное антитело против ActRII или его антигенсвязывающую область, имеющую: вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 99-112; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 85-98.
В другом аспекте изобретение относится к композициям, содержащим:
(i) изолированное рекомбинантное антитело против ActRII, имеющее: полноразмерную тяжелую цепь, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 99-112; и полноразмерную легкую цепь, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 85-98, или
(ii) функциональный белок, содержащий его антигенсвязывающую часть.
В другом аспекте изобретение относится к композициям, содержащим:
(i) изолированное рекомбинантное антитело против ActRII, имеющее полноразмерную тяжелую цепь, кодируемую нуклеотидной последовательностью, которая была оптимизирована для экспрессии в клетке млекопитающего, выбранной из группы, состоящей из SEQ ID NO: 127-140, и полноразмерную легкую цепь, кодируемую нуклеотидной последовательностью, которая была оптимизирована для экспрессии в клетке млекопитающего, выбранной из группы, состоящей из SEQ ID NO: 113-126, или
(ii) функциональный белок, содержащий его антигенсвязывающую часть.
Примеры аминокислотных последовательностей CDR1 VH антител, содержащихся в композициях по изобретению, показаны в SEQ ID NO: 1-14. Аминокислотные последовательности VH CDR2 антител показаны в SEQ ID NO: 15-28. Аминокислотные последовательности VH CDR3 антител показаны в SEQ ID NO: 29-42. Аминокислотные последовательности VL CDR1 антител показаны в SEQ ID NO: 43-56. Аминокислотные последовательности VL CDR2S антител показаны в SEQ ID NO: 57-70. Аминокислотные последовательности VL CDR3 антител показаны в SEQ ID NO: 71-84. Области CDR изображаются с использованием системы Kabat (Kabat, Е.А., et al., 1991. Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242). Альтернативный способ определения областей CDR использует метод, разработанный Chothia (Chothia et al. 1989, Nature, 342: 877-883). Определение Chothia основано на расположении областей структурной петли. Однако из-за изменений в системе нумерации, используемой Chothia (см., например, http:// www.biochem.ucl.ac.uk/~martin/abs/Generallnfo.html и http://www.bioinf.ora.uk/abs/). эта система сейчас используется реже. Существуют и другие системы определения CDR, которые также упоминаются на этих двух веб-сайтах.
Учитывая, что каждое из этих антител может связываться с ActRII и что антигенсвязывающая специфичность обеспечивается в основном областями CDR1, 2 и 3, последовательности VH CDR1, 2 и 3 и последовательности VL CDR1, 2 и 3 могут быть «смешаны и соединены» (т.е. CDR от разных антител могут быть смешаны и соединены так, что каждое антитело, содержащее CDR1, 2 и 3 VH и CDR1, 2 и 3 VL, создает другие анти-ActRII-связывающие молекулы по настоящему изобретению). Связывание ActRII с такими «смешанными и соединенными» антителами может быть протестировано, используя тесты связывания, описанные выше и в примерах (например, ELISA). Когда последовательности CDR VH смешивают и сопоставляют, последовательности CDR1, CDR2 и/или CDR3 из каждой определенной последовательности VH следует заменить структурно сходной последовательностью(-ями) CDR. Аналогично, когда последовательности CDR VL смешиваются и сопоставляются, последовательность CDR1, CDR2 и/или CDR3 из определенной последовательности VL должна быть заменена структурно сходной последовательностью(-ями) CDR. Специалисту в данной области техники будет очевидно, что новые последовательности VH и VL могут быть созданы путем замены одной или нескольких последовательностей областей CDR VH и/или VL структурно сходными последовательностями из последовательностей CDR, показанных в данном документе, для моноклональных антител.
Антитело против ActRII, содержащееся в раскрытых здесь композициях, или его антигенсвязывающая область имеет: вариабельную область тяжелой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-14; вариабельную область тяжелой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-28; вариабельную область тяжелой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 29-42; вариабельную область легкой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 43-56; вариабельную область легкой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 57-70; и вариабельную область легкой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 71-84.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 1; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 15; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 29; вариабельную область легкой цепи CDR1 SEQ ID NO: 43; вариабельную область легкой цепи CDR2 SEQ ID NO: 57; и вариабельную область легкой цепи CDR3 SEQ ID NO: 71.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 2 вариабельную область тяжелой цепи CDR2 SEQ ID NO: 16; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 30; вариабельную область легкой цепи CDR1 SEQ ID NO: 44; вариабельную область легкой цепи CDR2 SEQ ID NO: 58; и вариабельную область легкой цепи CDR3 SEQ ID NO: 72.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 3; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 17; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 31; вариабельную область легкой цепи CDR1 SEQ ID NO: 45; вариабельную область легкой цепи CDR2 SEQ ID NO: 59; и вариабельную область легкой цепи CDR3 SEQ ID NO: 73.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 4; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 18; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 32; вариабельную область легкой цепи CDR1 SEQ ID NO: 46; вариабельную область легкой цепи CDR2 SEQ ID NO: 60; и вариабельную область легкой цепи CDR3 SEQ ID NO: 74.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 5; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 19; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 33; вариабельную область легкой цепи CDR1 SEQ ID NO: 47; вариабельную область легкой цепи CDR2 SEQ ID NO: 61; и вариабельную область легкой цепи CDR3 SEQ ID NO: 75.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 6; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 20; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 34; вариабельную область легкой цепи SEQ ID NO: 48; вариабельную область легкой цепи CDR2 SEQ ID NO: 62; и вариабельную область легкой цепи CDR3 SEQ ID NO: 76.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 7; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 21; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 35; вариабельную область легкой цепи CDR1 SEQ ID NO: 49; вариабельную область легкой цепи CDR2 SEQ ID NO: 63; и вариабельную область легкой цепи CDR3 SEQ ID NO: 77.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 8; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 22; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 36; вариабельную область легкой цепи CDR1 SEQ ID NO: 50 вариабельную область легкой цепи CDR2 SEQ ID NO: 64; и вариабельную область легкой цепи CDR3 SEQ ID NO: 78.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 9; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 23; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 37; вариабельную область легкой цепи CDR1 SEQ ID NO: 51; вариабельную область легкой цепи CDR2 SEQ ID NO: 65; и вариабельную область легкой цепи CDR3 SEQ ID NO: 79.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 10; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 24; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 38; вариабельную область легкой цепи CDR1 SEQ ID NO: 52; вариабельную область легкой цепи CDR2 SEQ ID NO: 66; и вариабельную область легкой цепи CDR3 SEQ ID NO: 80.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 11; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 25; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 39; вариабельную область легкой цепи CDR1 SEQ ID NO: 53; вариабельную область легкой цепи CDR2 SEQ ID NO: 67; и вариабельную область легкой цепи CDR3 SEQ ID NO: 81.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 12; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 26; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 40; вариабельную область легкой цепи CDR1 SEQ ID NO: 54; вариабельную область легкой цепи CDR2 SEQ ID NO: 68; и вариабельную область легкой цепи CDR3 SEQ ID NO: 82.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 13; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 27; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 41; вариабельную область легкой цепи CDR1 SEQ ID NO: 55; вариабельную область легкой цепи CDR2 SEQ ID NO: 69; и вариабельную область легкой цепи CDR3 SEQ ID NO: 83.
В одном варианте осуществления антитело, содержащееся в композиции по изобретению, содержит: вариабельную область тяжелой цепи CDR1 SEQ ID NO: 14; вариабельную область тяжелой цепи CDR2 SEQ ID NO: 28; вариабельную область тяжелой цепи CDR3 SEQ ID NO: 42; вариабельную область легкой цепи CDR1 SEQ ID NO: 56; вариабельную область легкой цепи CDR2 SEQ ID NO: 70; и вариабельную область легкой цепи CDR3 SEQ ID NO: 84.
В одном варианте осуществления настоящее изобретение относится к композиции, содержащей антитело, содержащее: (а) вариабельную последовательность тяжелой цепи SEQ ID NO: 85 и вариабельную последовательность легкой цепи SEQ ID NO: 99; (b) вариабельную последовательность тяжелой цепи SEQ ID NO: 86 и вариабельную последовательность легкой цепи SEQ ID NO: 100; (с) вариабельную последовательность тяжелой цепи SEQ ID NO: 87 и вариабельную последовательность легкой цепи SEQ ID NO: 101; (d) вариабельную последовательность тяжелой цепи SEQ ID NO: 88 и вариабельную последовательность легкой цепи SEQ ID NO: 102; (е) вариабельную последовательность тяжелой цепи SEQ ID NO: 89 и вариабельную последовательность легкой цепи SEQ ID NO: 103; (f) вариабельную последовательность тяжелой цепи SEQ ID NO: 90 и вариабельную последовательность легкой цепи SEQ ID NO: 104; (g) вариабельную последовательность тяжелой цепи SEQ ID NO: 91 и вариабельную последовательность легкой цепи SEQ ID NO: 105; (h) вариабельную последовательность тяжелой цепи SEQ ID NO: 92 и вариабельную последовательность легкой цепи SEQ ID NO: 106; (i) вариабельную последовательность тяжелой цепи SEQ ID NO: 93 и вариабельную последовательность легкой цепи SEQ ID NO: 107; (j) вариабельную последовательность тяжелой цепи SEQ ID NO: 94 и вариабельную последовательность легкой цепи SEQ ID NO: 108; (k) вариабельную последовательность тяжелой цепи SEQ ID NO: 95 и вариабельную последовательность легкой цепи SEQ ID NO: 109; (l) вариабельную последовательность тяжелой цепи SEQ ID NO: 96 и вариабельную последовательность легкой цепи SEQ ID NO: 110; (m) вариабельную последовательность тяжелой цепи SEQ ID NO: 97 и вариабельную последовательность легкой цепи SEQ ID NO: 111; или (n) вариабельную последовательность тяжелой цепи SEQ ID NO: 98 и вариабельную последовательность легкой цепи SEQ ID NO: 112.
В одном варианте осуществления настоящее изобретение относится к композиции, содержащей антитело, содержащее: (а) последовательность тяжелой цепи SEQ ID NO: 146 и последовательность легкой цепи SEQ ID NO: 141; (b) последовательность тяжелой цепи SEQ ID NO: 147 и последовательность легкой цепи SEQ ID NO: 142; (с) последовательность тяжелой цепи SEQ ID NO: 148 и последовательность легкой цепи SEQ ID NO: 143; (d) последовательность тяжелой цепи SEQ ID NO: 149 и последовательность легкой цепи SEQ ID NO: 144; (е) последовательность тяжелой цепи SEQ ID NO: 150 и последовательность легкой цепи SEQ ID NO: 145; (f) последовательность тяжелой цепи SEQ ID NO: 156 и последовательность легкой цепи SEQ ID NO: 151; (g) последовательность тяжелой цепи SEQ ID NO: 157 и последовательность легкой цепи SEQ ID NO: 152; (h) последовательность тяжелой цепи SEQ ID NO: 158 и последовательность легкой цепи SEQ ID NO: 153; (i) последовательность тяжелой цепи SEQ ID NO: 159 и последовательность легкой цепи SEQ ID NO: 154; или (j) последовательность тяжелой цепи SEQ ID NO: 160 и последовательность легкой цепи SEQ ID NO: 155.
Как раскрыто в данном документе, человеческое антитело содержит вариабельные области тяжелой или легкой цепи, или полноразмерные тяжелые или легкие цепи, которые являются «продуктом» или «получены из» определенной последовательности зародышевой линии, если вариабельные области или полноразмерные цепи антитела получены из системы, которая использует гены человеческого иммуноглобулина зародышевой линии. Такие системы включают иммунизацию трансгенной мыши, несущей гены иммуноглобулина человека с интересующим антигеном, или скрининг фаговой библиотеки генов иммуноглобулина человека с интересующим антигеном. Антитело человека, которое является «продуктом» или «получено из» последовательности иммуноглобулина зародышевой линии человека, можно идентифицировать как таковое путем сравнения аминокислотной последовательности антитела человека с аминокислотными последовательностями иммуноглобулинов зародышевой линии человека и выбора последовательности иммуноглобулина зародышевой линии человека, которая наиболее близка по последовательности (т.е. наибольший % идентичности) к последовательности человеческого антитела. Человеческое антитело, которое является «продуктом» или «получено из» определенной последовательности человеческого иммуноглобулина зародышевой линии, может содержать аминокислотные различия по сравнению с последовательностью зародышевой линии, например, из-за встречающихся в природе соматических мутаций или преднамеренного введения сайт-направленной мутации. Однако выбранное человеческое антитело, как правило, по меньшей мере на 90% идентично аминокислотной последовательности, кодируемой геном иммуноглобулина человеческой зародышевой линии, и содержит аминокислотные остатки, которые идентифицируют антитело как человеческое по сравнению с аминокислотной последовательностью иммуноглобулина зародышевой линии других видов (например, последовательности зародышевой линии мыши). В определенных случаях человеческое антитело может быть, по меньшей мере, на 80%, 90% или, по меньшей мере, на 95%, или даже, по меньшей мере, на 96, 97, 98 или 99% идентичным аминокислотной последовательности, кодируемой геном иммуноглобулина зародышевой линии. Как правило, человеческое антитело, полученное из определенной последовательности человеческой зародышевой линии, будет проявлять не более 10 аминокислотных различий от аминокислотной последовательности, кодируемой геном иммуноглобулина человеческой зародышевой линии. В определенных случаях человеческое антитело может демонстрировать не более 5 или даже не более 4, 3, 2 или 1 аминокислотного различия с аминокислотной последовательностью, кодируемой геном иммуноглобулина зародышевой линии.
В одном варианте осуществления изобретения антитело, содержащееся в композициях по настоящему изобретению, является антителом, кодируемым pBW522 или pBW524 (депонировано в DSMZ, Inhoffenstr. 7В, D-38124 Брауншвейг, Германия, 18 августа 2009 г. с номерами депонирования DSM22873 и DSM22874, соответственно).
Гомологичные антитела
В еще одном варианте осуществления антитело, содержащееся в композиции по изобретению, имеет полноразмерные аминокислотные последовательности тяжелой и легкой цепи; нуклеотидные полноразмерные последовательности тяжелой и легкой цепи, нуклеотидные последовательности тяжелой и легкой цепи вариабельной области или аминокислотные последовательности тяжелой и легкой цепи вариабельной области, которые гомологичны аминокислотным и нуклеотидным последовательностям антител, описанных в настоящем документе, и где антитела сохраняют требуемые функциональные свойства антител против ActRIIB по изобретению.
Например, настоящее изобретение относится к композиции, содержащей изолированное рекомбинантное антитело против ActRIIB (или функциональный белок, содержащий его антигенсвязывающую часть), содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, где: вариабельная область тяжелой цепи содержит аминокислотную последовательность, которая, по меньшей мере, на 80% или, по меньшей мере, на 90% (предпочтительно, по меньшей мере, на 95, 97 или 99%) идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 99-112; вариабельная область легкой цепи содержит аминокислотную последовательность, которая, по меньшей мере, на 80% или, по меньшей мере, на 90% (предпочтительно, по меньшей мере, на 95, 97 или 99%) идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 85-98; в альтернативном варианте, композиции содержат рекомбинантное антитело против ActRIIB (или функциональный белок, содержащий его антигенсвязывающую часть), содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, где: вариабельная область тяжелой цепи содержит не более 5, или не более 4, или не более 3, или не более 2 или не более 1 изменения аминокислоты по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 99-112; вариабельная область легкой цепи содержит не более 5, или не более 4, или не более 3, или не более 2 или не более 1 изменения аминокислоты по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 85-98, и антитело проявляет по меньшей мере одно из следующих функциональных свойств: (i) оно ингибирует связывание миостатина in vitro или in vivo, (ii) уменьшает ингибирование дифференциации мышц посредством Smad-зависимого направления и/или (iii) не вызывает гематологических изменений, в частности никаких изменений в эритроцитах. В этом контексте термин «изменение» относится к вставкам, удалениям и/или заменам.
В еще одном примере изобретение раскрывает композицию, содержащую изолированное рекомбинантное антитело против ActRII (или функциональный белок, содержащий его антигенсвязывающую часть), содержащее полноразмерную тяжелую цепь и полноразмерную легкую цепь, где: тяжелая полная длина цепь содержит аминокислотную последовательность, которая, по меньшей мере, на 80% или, по меньшей мере, на 90% (предпочтительно, по меньшей мере, на 95, 97 или 99%) идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 146-150 и 156-160; полноразмерная легкая цепь содержит аминокислотную последовательность, которая, по меньшей мере, на 80% или, по меньшей мере, на 90% (предпочтительно, по меньшей мере, на 95, 97 или 99%) идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 141-145 и 151-155; в альтернативном варианте, композиции содержат рекомбинантное антитело против ActRII (или функциональный белок, содержащий его антигенсвязывающую часть), содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, где: вариабельная область тяжелой цепи содержит не более 5, или не более 4, или не более 3, или не более 2 или не более 1 изменений аминокислоты по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 146-150 и 156-160; вариабельная область легкой цепи содержит не более 5, или не более 4, или не более 3, или не более 2 или не более 1 изменений аминокислоты по сравнению с аминокислотной последовательностью, выбранной из группа, состоящая из SEQ ID NO: 141-145 и 151-155, и антитело проявляет, по меньшей мере, одно из следующих функциональных свойств: (i) оно ингибирует связывание миостатина in vitro или in vivo, (ii) уменьшает ингибирование дифференциации мышц посредством Smad-зависимого направления и/или (iii) не вызывает гематологических изменений, в частности, никаких изменений в эритроцитах. Предпочтительно такое антитело связывается с лиганд-связывающим доменом ActRIIB и/или ActRIIA. В этом контексте термин «изменение» относится к вставкам, удалениям и/или заменам.
В другом примере настоящее изобретение относится к композиции, содержащей изолированное рекомбинантное антитело против ActRII (или функциональный белок, содержащий его антигенсвязывающую часть), содержащее тяжелую цепь полной длины и легкую цепь полной длины, где: тяжелая цепь полной длины кодируется нуклеотидной последовательностью, которая, по меньшей мере, на 80% или, по меньшей мере, на 90% (предпочтительно, по меньшей мере, на 95, 97 или 99%) идентична нуклеотидной последовательности, выбранной из группы, состоящей из SEQ ID NO: 166-170 и 176-180; легкая цепь полной длины кодируется нуклеотидной последовательностью, которая, по меньшей мере, на 80% или, по меньшей мере, на 90% (предпочтительно, по меньшей мере, на 95, 97 или 99%) идентична нуклеотидной последовательности, выбранной из группы, состоящей из SEQ ID NO: 161-165 и 171-175; в альтернативном варианте, композиции содержат рекомбинантное антитело против ActRIIB (или функциональный белок, содержащий его антигенсвязывающую часть), содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, где: вариабельная область тяжелой цепи содержит не более 5, или не более 4, или не более 3, или не более 2 или не более 1 изменений аминокислоты по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 166-170 и 176-180; вариабельная область легкой цепи содержит не более 5, или не более 4, или не более 3, или не более 2 или не более 1 изменений аминокислоты по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 161-165 и 171-175, и антитело проявляет по меньшей мере одно из следующих функциональных свойств: (i) оно ингибирует связывание миостатина in vitro или in vivo, (ii) уменьшает ингибирование дифференциации мышц посредством Smad-зависимого направления и/или (iii) не вызывает гематологических изменений, в частности, никаких изменений в эритроцитах. Предпочтительно такое антитело связывается с лиганд-связывающим доменом ActRIIB. В этом контексте термин «изменение» относится к вставкам, удалениям и/или заменам.
В различных вариантах осуществления антитело, содержащееся в композиции по изобретению, может проявлять одно или более, два или более, или три из функциональных свойств, обсужденных выше. Антитело может представлять собой, например, антитело человека, гуманизированное антитело или антитело химерной структуры. Предпочтительно антитело представляет собой полностью человеческое антитело IgG1
В других вариантах осуществления аминокислотные последовательности VH и/или VL могут быть, по меньшей мере, на 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным выше. В других вариантах осуществления аминокислотные последовательности VH и/или VL могут быть идентичными, за исключением аминокислотного замещения не более, чем в 1, 2, 3, 4 или 5 положениях. Антитело, имеющее области VH и VL, имеющие высокую (т.е. 80% или более) идентичность с областями VH и VL SEQ ID NO: 99-112 и SEQ ID NO: 85-98 соответственно, может быть получено мутагенезом (например, сайт-направленным или PCR-опосредованным мутагенезом) молекул нуклеиновой кислоты SEQ ID NO: 127-140 и 113-126 соответственно с последующим тестированием кодированного измененного антитела на сохраненную функцию (т.е. функции, изложенные выше) с использованием функциональных анализов, описанных в настоящем документе.
В других вариантах осуществления полноразмерные аминокислотные последовательности тяжелой цепи и/или легкой цепи могут быть, по меньшей мере, на 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным выше или могут быть идентичными, за исключением аминокислотного замещения не более, чем в 1, 2, 3, 4 или 5 положениях. Антитело, имеющее полноразмерную тяжелую цепь и полноразмерную легкую цепь, имеющее высокую (т.е. по меньшей мере, 80% или более) идентичность полноразмерным тяжелым цепям любой из SEQ ID NO: 146-150 и 156-160 и полноразмерным легким цепям любой из SEQ ID NO: 141-145 и 151-155 соответственно может быть получено путем мутагенеза (например, сайт-направленного или PCR-опосредованного мутагенеза) молекул нуклеиновой кислоты SEQ ID NO: 166-170 и 176-180 и SEQ ID NO: 161-165 и 171-175, соответственно, с последующим тестированием кодированного измененного антитела на сохраненную функцию (т.е. функции, изложенные выше) с использованием функциональных анализов, описанных в настоящем документе.
В других вариантах осуществления полноразмерные нуклеотидные последовательности тяжелой цепи и/или легкой цепи могут быть по меньшей мере на 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, указанным выше.
В других вариантах осуществления вариабельные области нуклеотидных последовательностей тяжелой цепи и/или легкой цепи могут быть по меньшей мере на 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным выше, или могут быть идентичными, за исключением аминокислотного замещения не более, чем в 1, 2, 3, 4 или 5 положениях.
Как используется в данном документе, процент идентичности между двумя последовательностями является функцией количества идентичных позиций, совместно используемых последовательностями (т.е. % идентичности = количество идентичных положений/общее количество положений × 100), принимая во внимание количество промежутков и длину каждого промежутка, которые необходимо ввести для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями может быть выполнено с использованием математического алгоритма, как описано ниже.
Процент идентичности между двумя аминокислотными последовательностями можно определить, используя алгоритм Э. Мейерса и У. Миллера (Comput. Appl. Biosci., 4:11-17, 1988), который был включен в программу ALIGN (версия 2.0). с использованием таблицы весов замен остатков РАМ 120, надбавка за длину промежутка 12 и надбавка за промежуток 4. Кроме того, процент идентичности между двумя аминокислотными последовательностями можно определить с помощью алгоритма Нидлемана и Вунша (J. Mol, Biol. 48: 444 -453, 1970), который был включен в программу GAP в программном пакете GCG (доступен по адресу http://www.qcg.com), используя либо матрицу Blossom 62, либо матрицу РАМ250, и надбавка за промежуток 16, 14, 12, 10, 8, 6 или 4, а за длину промежутка 1, 2, 3, 4, 5 или 6.
Антитела с консервативными модификациями
В некоторых вариантах осуществления антитело, содержащееся в композиции по изобретению, имеет вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, где одна или несколько из этих последовательностей CDR имеют указанные аминокислотные последовательности на основе антител, описанных в настоящем документе, или их вариантные последовательности, содержащие 1, 2, 3, 4 или 5 изменений аминокислот или их консервативные модификации, и где антитела сохраняют желаемые функциональные свойства антител против ActRIIB по изобретению. Соответственно, настоящее изобретение относится к композициям, содержащим изолированное рекомбинантное антитело против ActRIIB или функциональный белок, содержащий его антигенсвязывающую часть, состоящую из вариабельной области тяжелой цепи, содержащей последовательности CDR1, CDR2 и CDR3, и вариабельной области легкой цепи, содержащей CDR1, CDR2 и CDR3, где: аминокислотные последовательности CDR1 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 1-14 или ее вариантных последовательностей, содержащих 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативные модификации; аминокислотные последовательности CDR2 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 15-28 или ее вариантных последовательностей, содержащих 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативных модификаций; аминокислотные последовательности CDR3 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 29-42 или ее вариантных последовательностей, содержащих 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативных модификаций; аминокислотные последовательности CDR1 вариабельных областей легкой цепи выбраны из группы, состоящей из SEQ ID NO: 43-56 или их вариантных последовательностей, содержащих 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативных модификаций; аминокислотные последовательности CDR2 вариабельных областей легкой цепи выбраны из группы, состоящей из SEQ ID NO: 57-70 или ее вариантных последовательностей, содержащих 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативных модификаций; вариабельные области легкой цепи аминокислотных последовательностей CDR3 выбраны из группы, состоящей из SEQ ID NO: 71-84 или ее вариантных последовательностей, содержащих 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативных модификаций. Предпочтительно антитело проявляет, по меньшей мере, одно из следующих функциональных свойств: (i) оно ингибирует связывание миостатина in vitro или in vivo, (ii) уменьшает ингибирование мышечной дифференциации посредством Smad-зависимого направления и/или (iii) не вызывает гематологические изменения, в частности, изменения в эритроцитах.
В различных вариантах осуществления антитело может проявлять одно или все из функциональных свойств, перечисленных выше. Такими антителами могут быть, например, антитела человека, гуманизированные антитела или антитела химерной структуры.
В других вариантах осуществления антитело, содержащееся в композиции по изобретению, оптимизированной для экспрессии в клетке млекопитающего, имеет полноразмерную последовательность тяжелой цепи и полноразмерную последовательность легкой цепи, где одна или несколько из этих последовательностей имеют определенные аминокислотные последовательности на основе описанных в данном документе антител или их консервативные модификации, и где антитела сохраняют желательные функциональные свойства антител против ActRIIB по изобретению. Соответственно, настоящее изобретение относится к композициям, содержащим изолированное моноклональное антитело против ActRII, оптимизированное для экспрессии в клетке млекопитающего, состоящей из полноразмерной тяжелой цепи и полноразмерной легкой цепи, где: тяжелая цепь полной длины имеет аминокислотные последовательности, выбранные из группы SEQ ID NO: 146-150 и 156-160 или их вариантные последовательности, содержащие 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативные модификации; и легкая цепь полной длины имеет аминокислотные последовательности, выбранные из группы SEQ ID NO: 141-145 и 151-155 или их вариантные последовательности, содержащие 1, 2, 3, 4 или 5 изменений аминокислот, и их консервативные модификации; и антитело проявляет, по меньшей мере, одно из следующих функциональных свойств: (i) оно ингибирует связывание миостатина in vitro или in vivo, (ii) уменьшает ингибирование мышечной дифференциации посредством Smad-зависимого направления и/или (iii) не вызывает гематологические изменения, в частности, изменения в эритроцитах..
В различных вариантах осуществления антитело может проявлять одно или все из функциональных свойств, перечисленных выше. Такими антителами могут быть, например, антитела человека, гуманизированные антитела или химерные антитела.
Используемый здесь термин «модификации консервативных последовательностей» предназначен для обозначения модификаций аминокислот, которые не оказывают существенного влияния или не изменяют характеристики связывания антитела, содержащего аминокислотную последовательность. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации могут быть введены в антитело по изобретению стандартными способами, известными в данной области, такими как сайт-направленный мутагенез и PCR-опосредованный мутагенез.
Консервативные аминокислотные изменения представляют собой замены, в которых аминокислотный остаток заменен аминокислотным остатком, имеющим сходную боковую цепь. Семейства аминокислотных остатков, имеющих сходные боковые цепи, были определены в данной области. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотные боковые цепи (например, аспарагиновая кислота, глутаминовая кислота), незаряженные полярные боковые цепи (например, глицин, аспарагин, глутамин, серии, треонин, тирозин, цистеин, триптофан), неполярные боковые цепи (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленные боковые цепи (например, треонин, валин, изолейцин) и ароматические боковые цепи (например, тирозин, фенилаланин, триптофан, гистидин), Таким образом, один или несколько аминокислотных остатков в областях CDR антитела по настоящему изобретению могут быть заменены другими аминокислотными остатками из того же семейства боковых цепей, и измененное антитело может быть проверено на сохраненную функцию с использованием функциональных анализов, описанных в настоящем документе.
Антитела, которые связываются с тем же эпитопом. что и антитела против ActRII. содержащиеся в раскрытой композиции
В другом варианте осуществления настоящее изобретение относится к композициям, содержащим антитела, которые связываются с тем же эпитопом, что и различные специфические антитела против ActRII, описанные здесь. Все антитела, описанные в примерах, которые способны блокировать связывание миостатина с ActRIIA и ActRIIB, связываются с одним из эпитопов в ActRIIA и ActRIIB с высокой аффинностью, причем указанный эпитоп находится между аминокислотами 19-134 SEQ ID NO: 181.
Следовательно, дополнительные антитела могут быть идентифицированы на основе их способности к перекрестной конкуренции (например, конкурентно ингибировать связывание статистически значимым образом) с другими антителами по изобретению в стандартных анализах связывания ActRIIB. Способность тестируемого антитела ингибировать связывание антител, содержащихся в композициях по изобретению, с ActRIIB человека, демонстрирует, что тестируемое антитело может конкурировать с указанным антителом за связывание с ActRIIB человека; такое антитело может, в соответствии с теорией, не имеющей ограничительного характера, связываться с тем же или связанным (например, структурно сходным или пространственно близким) эпитопом на ActRIIB человека, что и антитело, с которым оно конкурирует. В определенном варианте осуществления антитело, которое связывается с тем же эпитопом на ActRIIA и ActRIIA человека, что и антитела, содержащиеся в композициях по изобретению, представляет собой человеческое рекомбинантное антитело. Такие человеческие рекомбинантные антитела могут быть получены и выделены, как описано в примерах. Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым и/или конкурирующим за связывание с антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 85, и вариабельную последовательность легкой цепи, приведенную в SEQ. ID NO: 99.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 86, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 100.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 87, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 101.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 88, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 102.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 89, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 103.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 90, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 104.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 91, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 105.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 92, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 106.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 93, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 107.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 94, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 108.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 95, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 109.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 96, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 110.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 97, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 111.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, распознаваемым антителом, имеющим вариабельную последовательность тяжелой цепи, приведенную в SEQ ID NO: 98, и вариабельную последовательность легкой цепи, приведенную в SEQ ID NO: 112.
После более детальных экспериментов по картированию эпитопов были более четко определены области связывания предпочтительных антител по композициям изобретения.
Таким образом, настоящее изобретение относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID NO: 188). Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID NO: 186).
Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим аминокислоты 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID NO: 190).
Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим аминокислоты 52-56 SEQ ID NO: 181 (EQDKR - SEQ ID NO: 189). Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим аминокислоты 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW -SEQ ID NO: 187).
Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим или состоящим из аминокислот 29-41 SEQ ID NO: 181 (CIYYNANWELERT-SEQ ID NO: 191).
Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим или состоящим из аминокислот 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID NO: 192).
Изобретение также относится к композиции, содержащей антитела, которые связываются с эпитопами, состоящими из этих последовательностей, или эпитопами, содержащими комбинации этих областей эпитопа.
Таким образом, Изобретение также относится к композиции, содержащей антитело, которое связывается с эпитопом, содержащим или состоящим из аминокислот 78-83 SEQ ID NO: 181 (WLDDFN) и аминокислот 52-56 SEQ ID NO: 181 (EQDKR).
Сконструированные и модифицированные антитела
Антитело, содержащееся в композициях по изобретению, дополнительно может быть получено с использованием антитела, имеющего одну или несколько последовательностей VH и/или VL, показанных в данном документе, в качестве исходного материала для конструирования модифицированного антитела, причем это модифицированное антитело может иметь измененные свойства по сравнению с исходным антителом. Антитело может быть сконструировано путем модификации одного или нескольких остатков в одной или обеих вариабельных областях (то есть VH и/или VL), например, в одной или нескольких областях CDR и/или в одной или нескольких каркасных областях. В дополнительном или альтернативном варианте, антитело может быть сконструировано путем модификации остатков в константной области (областях), например, для изменения эффекторной функции (функций) антитела.
Одним из типов конструирования вариабельной области, которое может быть выполнено, является пересадка CDR. Антитела взаимодействуют с антигенами-мишенями преимущественно через аминокислотные остатки, которые расположены в шести областях, определяющих комплементарность тяжелой и легкой цепей (CDR). По этой причине аминокислотные последовательности в CDR более разнообразны между отдельными антителами, чем последовательности вне CDR. Поскольку последовательности CDR ответственны за большинство взаимодействий антитело-антиген, то можно экспрессировать рекомбинантные антитела, которые имитируют свойства специфических встречающихся в природе антител, путем конструирования векторов экспрессии, которые включают последовательности CDR из специфического встречающегося в природе антитела, пересаженные на каркасные последовательности из другого антитела с другими свойствами (см., например, Riechmann, L. et al., 1998 Nature 332: 323-327; Jones, P. et al., 1986 Nature 321: 522-525; Queen, C. et al., 1989 Proc. Natl. Acad Sci. USA 86: 10029-10033; U.S. Patent No. 5,225,539 to Winter, and U.S. Patent Nos. 5,530,101; 5,585,089; 5,693,762 и 6,180,370 to Queen et al.).
Соответственно, другой вариант осуществления изобретения относится к композициям, содержащим моноклональное антитело против ActRII или функциональный белок, содержащий его антигенсвязывающую часть, содержащее вариабельную область тяжелой цепи, содержащую последовательности CDR1, имеющие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID №: 1-14; последовательности CDR2, имеющие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-28; последовательности CDR3, имеющие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 29-42 соответственно; и вариабельную область легкой цепи, имеющую последовательности CDR1, имеющие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 43-56; последовательности CDR2, имеющие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 57-70; и последовательности CDR3, состоящие из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 71-84, соответственно. Таким образом, такие антитела содержат последовательности CDR VH и VL моноклональных антител, но могут содержать различные каркасные последовательности из этих антител.
Такие каркасные последовательности могут быть получены из общедоступных баз данных ДНК или опубликованных ссылок, которые включают последовательности генов антител зародышевой линии. Например, последовательности ДНК зародышевой линии для генов вариабельной области тяжелой и легкой цепи человека можно найти в базе данных последовательностей зародышевой линии человека «VBase» (доступной в Интернете по адресу www mrc- cpe.cam.ac.uk/vbase). также как и в Kabat, Е. A., et al, [supra]]Tomlinson, I.M., et al, 992 J. fol. Biol. 227:776-798; и Cox, J. P. L. et al, 1994 Eur. J Immunol. 24:827-836. Примером каркасных последовательностей для использования в антителах по изобретению являются те, которые структурно аналогичны каркасным последовательностям, используемым выбранными антителами по изобретению, например, консенсусные последовательности и/или каркасные последовательности, используемые моноклональными антителами по изобретению. Последовательности CDR1, 2 и 3 VH и последовательности CDR1, 2 и 3 VL могут быть пересажены к каркасным областям, которые имеют идентичную последовательность, которая обнаружена в гене иммуноглобулина зародышевой линии, из которого происходит каркасная последовательность, или последовательности CDR могут быть пересажены к каркасным областям, которые содержат одну или несколько мутаций по сравнению с последовательностями зародышевой линии. Например, было обнаружено, что в некоторых случаях полезно мутировать остатки в каркасных областях для поддержания или усиления антигенсвязывающей способности антитела (см., например, U.S. Patents. 5,530,101; 5,585,089; 5,693,762 и 6,180,370 to Queen et al).
Другой тип модификации вариабельной области заключается в мутировании аминокислотных остатков в областях VH и/или VL CDR1, CDR2 и/или CDR3, чтобы тем самым улучшить одно или несколько свойств связывания (например, аффинность) целевого антитела, известного как «созревание аффинности». Для введения мутации (мутаций) могут быть выполнены сайт-направленный мутагенез или PCR-опосредованный мутагенез, и влияние на связывание антител или другое интересующее функциональное свойство может быть оценено в анализах in vitro или in vivo, как описано в настоящем документе, и представлено в примерах. Могут быть введены консервативные модификации (как обсуждалось выше). Мутации могут быть заменами, добавлениями или делециями аминокислот. Кроме того, обычно изменяются не более одного, двух, трех, четырех или пяти остатков в области CDR.
Соответственно, в другом варианте осуществления настоящее изобретение относится к изолированным моноклональным антителам против ActRII или функциональному белку, содержащему его антигенсвязывающую часть, состоящим из вариабельной области тяжелой цепи, имеющей: область VH CDR1, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-14 или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 1-14; область VH CDR2, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15-28, или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 15-28; область CDR3 VH, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 29-42, или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 29-42; область VL CDR1, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 43-56, или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 43-56; область VL CDR2, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 52-70, или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 52-70; и область VL CDR3, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 71-84, или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 71-84.
Верблюжьи антитела
Белки антител, полученные от представителей семейств верблюдов и дромадеров (Camelus bactrianus и Camelus dromaderius), включая новых представителей, таких как виды лам (Lama paccos, Lama glama и Lama vicugna), были охарактеризованы с точки зрения размера, структурной сложности и антигенности для субъекта-человека. Некоторые антитела IgG из этого семейства млекопитающих, обнаруженные в природе, лишены легких цепей и, таким образом, структурно отличаются от типичной четырехцепочечной четвертичной структуры, имеющей две тяжелые и две легкие цепи, для антител от других животных (см. WO 94 / 04678).
Область антитела верблюда, которая представляет собой небольшой единственный вариабельный домен, идентифицированный как VHH, может быть получена генной инженерией для получения небольшого белка, имеющего высокую аффинность к мишени, что приводит к низкомолекулярному белку, полученному из антитела, известному как «верблюжье нанотело» (см. US 5,759,808; Stijlemans, В. et al., 2004 J Biol Chem 279: 1256-1261; Dumoulin, M. et al., 2003 Nature 424: 783-788; Pleschberger, M. et al. 2003 Bioconjugate Chem 14: 440-448; Cortez-Retamozo, V. et al. 2002 Int J Cancer 89: 456- 62; и Lauwereys, M. et al. 1998 EMBO J 17: 3512-3520). Разработанные библиотеки антител верблюдов и фрагментов антител коммерчески доступны, например, от Ablynx, Ghent, Belgium. Как и в случае с другими антителами нечеловеческого происхождения, аминокислотная последовательность антитела верблюда может быть рекомбинантно изменена для получения последовательности, более близкой к человеческой последовательности, то есть нанотело может быть «гуманизированным». Таким образом, естественная низкая антигенность верблюжьих антител для людей может быть дополнительно снижена.
Нано-тело верблюда имеет молекулярную массу примерно в десять раз меньше, чем молекула человека IgG, а физический диаметр белка составляет всего несколько нанометров. Одним из следствий небольшого размера является способность нанотела верблюдов связываться с антигенными областями, которые функционально невидимы для более крупных белков антител, т.е. нанотела верблюдов полезны в качестве реагентов для обнаружения антигенов, которые в противном случае являются скрытыми, с использованием классических иммунологических методов, и в качестве возможных терапевтических агентов. Таким образом, еще одно следствие небольшого размера состоит в том, что нанотело верблюда может ингибировать в результате связывания с конкретным участком в бороздке или узкой щели белка-мишени, и, следовательно, может служить в качестве, которое более близко напоминает функцию классического низкомолекулярного препарата, чем классического антитела.
Низкая молекулярная масса и компактный размер также приводят к тому, что нанотела верблюдов являются чрезвычайно термостабильными, устойчивыми к экстремальным значениям рН и протеолитическому расщеплению, а также являются мало аллергенными. Еще одно последствие заключается в том, что нанотела верблюдов легко перемещаются из кровеносной системы в ткани и даже преодолевают гематоэнцефалический барьер и могут лечить нарушения, влияющие на нервную ткань. Нанотела могут дополнительно облегчать перенос лекарств через гематоэнцефалический барьер (см. US 2004/0161738). Эти особенности в сочетании с низкой антигенностью для человека указывают на большой терапевтический потенциал. Кроме того, эти молекулы могут полностью экспрессироваться в прокариотических клетках, таких как E. coli, и экспрессируются в виде слияния белков с бактериофагом, и являются функциональными
Соответственно, в одном варианте осуществления настоящее изобретение относится к композиции, содержащей антитело или нанотело верблюда, имеющее высокое сродство к ActRIIB. В некоторых вариантах осуществления настоящего изобретения антитело или нанотело верблюда естественным образом продуцируется у животного-верблюда, то есть продуцируется верблюдом после иммунизации ActRIIB или его пептидным фрагментом с использованием методик, описанных здесь для других антител. В альтернативном варианте, нанотело верблюда против ActRIIB конструируют, то есть получают путем отбора, например, из библиотеки фагов, отображающих подходящим образом мутагенизированные белки нанотела верблюда, используя процедуры пэннинга с ActRIIB в качестве мишени, как описано в приведенных здесь примерах. Сконструированные нанотела могут быть дополнительно адаптированы с помощью генной инженерии для того, чтобы иметь период полураспада у субъекта-реципиента от 45 минут до двух недель. В конкретном варианте осуществления антитело или нанотело верблюда получают пересадкой последовательностей CDR тяжелой или легкой цепи антител человека по настоящему изобретению в каркасные последовательности нанотрубок или однодоменных антител, как описано, например, в WO 94 / 04678.
Каркас, не принадлежащий к антителу
Известные неиммуноглобулиновые каркасы или скаффолды включают, но не ограничиваются ими, аднектины (фибронектин) (Compound Therapeutics, Inc., Waltham, MA), анкирин (Molecular Partners AG, Цюрих, Швейцария), доменные антитела (Domantis, Ltd (Кембридж)., MA) и Ablynx nv (Zwijnaarde, Бельгия)), липокалин (Anticalin) (Pieris Proteolab AG, Freising, Германия), небольшие модульные иммуно-фармацевтические препараты (Trubion Pharmaceuticals Inc., Сиэтл, штат Вашингтон), макситела (Avidia, Inc. (Mountain View, CA)), протеин A (Affibody AG, Швеция) и аффилин (гамма-кристаллин или убиквитин) (Scil Proteins GmbH, Галле, Германия), миметики белковых эпитопов (Polyphor Ltd, Allschwil, Швейцария).
(i) Скаффолд фибронектина
Скаффолды фибронектина основаны предпочтительно на домене фибронектина типа III (например, на десятом модуле фибронектина типа III (домен 10 Fn3)). Домен фибронектина типа III имеет 7 или 8 бета-цепей, которые распределены между двумя бета-структурами, которые сами упаковываются друг с другом, образуя ядро белка, и дополнительно содержат петли (аналогично CDR), которые соединяют бета-цепи друг с другом и подвергаются воздействию растворителя. На каждом краю «сэндвича» бета-структуры имеется по меньшей мере три таких петли, где край является границей белка, перпендикулярной направлению бета-цепей (US 6,818,418).
Эти каркасы, основанные на фибронектине, не являются иммуноглобулином, хотя общая структура тесно связана с наименьшим функциональным фрагментом антитела, вариабельной областью тяжелой цепи, которая включает всю единицу распознавания антигена в IgG верблюда и ламы. Из-за этой структуры неиммуноглобулиновое антитело имитирует антигенсвязывающие свойства, которые сходны по природе и сродству со свойствами антител. Эти каркасы могут быть использованы в стратегии тасовки и шаффлинга петель in vitro, которая аналогична процессу созревания аффинности антител in vivo. Эти молекулы на основе фибронектина могут быть использованы в качестве каркасов, где петлевые области молекулы могут быть заменены CDR по изобретению с использованием стандартных методов клонирования.
(ii) Анкирин-молекулярные партнеры
Технология основана на использовании белков с повторяющимися модулями, полученными из анкирина, в качестве каркаса для несущих вариабельных областей, которые можно использовать для связывания с различными мишенями. Анкирин с повторяющимися модулями представляет собой полипептид из 33 аминокислот, состоящий из двух антипараллельных а-спиралей и р-витка. Связывание вариабельных областей в основном оптимизируется с помощью рибосомного дисплея.
(iii) Макситела/Авимеры - Avidia
Авимеры получают из природного белка, содержащего А-домен, такого как LRP-1. Эти домены используются природой для межбелковых взаимодействий, и у человека более 250 белков структурно основаны на А-доменах. Авимеры состоят из ряда различных мономеров «А-домена» (от 2 до 10), связанных через аминокислотные линкеры. Могут быть созданы авимеры, которые могут связываться с антигеном-мишенью с использованием методологии, описанной, например, в US 2004/0175756; US 2005/0053973; US 2005/0048512; и US 2006/0008844.
(vi) Белок А - Affibody
Аффинные лиганды Affibody® представляют собой небольшие простые белки, состоящие из трехспирального пучка на основе каркаса одного из IgG-связывающих доменов белка А. Белок А представляет собой поверхностный белок из бактерии Staphylococcus aureus. Этот каркасный домен состоит из 58 аминокислот, 13 из которых расположены в случайном порядке для получения библиотек Affibody® с большим количеством вариантов лигандов (см., например, US 5,831,012). Молекулы Affibody® имитируют антитела, они имеют молекулярную массу 6 кДа по сравнению с молекулярной массой антитела, которая составляет 150 кДа. Несмотря на небольшой размер, участок связывания молекул Affibody® похож на участок связывания антитела.
(v) Anticalins - Pieris
Anticalins® представляют собой продукты, разработанные компанией Pieris ProteoLab AG. Они получены из липокалинов, широко распространенной группы небольших и устойчивых белков, которые обычно участвуют в физиологическом переносе или хранении химически чувствительных или нерастворимых соединений. Несколько природных липокалинов встречаются в тканях человека или жидкостях организма.
Структура белка напоминает иммуноглобулины с гипервариабельными петлями поверх жесткого каркаса. Однако, в отличие от антител или их рекомбинантных фрагментов, липокалины состоят из одной полипептидной цепи с 160-180 аминокислотными остатками, лишь незначительно превышающей один домен иммуноглобулина.
Набор из четырех петель, из которых состоит связывающий карман, проявляет ярко выраженную структурную пластичность и переносит различные боковые цепи. Таким образом, участок связывания может быть изменен в запатентованном процессе для распознавания предписанных молекул-мишеней различной формы с высокой аффинностью и специфичностью.
Один белок семейства липокалинов, билин-связывающий белок (ВВР) Pieris brassicae, был использован для выработки антикалинов путем мутагенизации набора из четырех петель. Одним примером патентной заявки, описывающей «антикалины», является W0 1999/16873.
(vi) Affilin - Scil Proteins
Молекулы AFFILIN™ представляют собой небольшие неиммуноглобулиновые белки, которые предназначены для специфического сродства к белкам и небольшим молекулам. Новые молекулы AFFILIN™ могут быть очень быстро выбраны из двух библиотек, каждая из которых основана на различном каркасном белке человеческого происхождения.
Молекулы AFFILIN™ не проявляют какой-либо структурной гомологии с белками иммуноглобулина. В Scil Proteins используются два каркаса AFFILIN™, один из которых является гамма-кристаллическим, структурным белком глазных линз человека, а другой является белком суперсемейства «убиквитин». Оба человеческих каркаса очень малы, обладают высокой температурной стабильностью и почти устойчивы к изменениям рН и денатурирующим агентам. Эта высокая стабильность в основном обусловлена расширенной структурой белков бета-структуры. Примеры белков, полученных из гамма-кристаллов, описаны в WO 2001/004144, а примеры «убиквитиноподобных» белков описаны в WO 2004/106368.
(vii) Миметики белковых эпитопов (РЕМ)
РЕМ представляют собой циклические пептидоподобные молекулы среднего размера (молекулярная масса 1-2 кДа), имитирующие вторичные структуры бета-шпилек белков, которые являются основной вторичной структурой, участвующей в межбелковых взаимодействиях.
Пересадка антигенсвязывающих доменов в альтернативные каркасы или скаффолды
Можно использовать широкий спектр каркасов или скаффолдов антител/ иммуноглобулинов, если полученный полипептид включает, по меньшей мере, одну область связывания, которая специфически связывается с ActRIIB. Такие каркасы или скаффолды включают в себя 5 основных идиотипов иммуноглобулинов человека или их фрагментов (таких, как раскрытые в настоящем документе) и включают иммуноглобулины других видов животных, предпочтительно имеющие гуманизированные аспекты. В этом отношении особый интерес представляют отдельные антитела тяжелой цепи, такие как антитела, идентифицированные у верблюдов. Новые структуры, каркасы и фрагменты продолжают обнаруживаться и развиваться специалистами в данной области.
В одном аспекте композиции по настоящему изобретению могут содержаться неиммуноглобулиновые антитела с использованием неиммуноглобулиновых каркасов, на которые могут быть пересажены CDR антител, раскрытых в данном документе. Могут быть использованы известные или будущие неиммуноглобулиновые каркасы и скаффолды, если они содержат область связывания, специфичную для целевого белка SEQ ID NO: 181 (предпочтительно, его лиганд-связывающий домен, как показано в SEQ ID NO: 182). Такие соединения известны здесь как «полипептиды, содержащие область специфического связывания мишени». Примеры неиммуноглобулинового каркаса дополнительно описаны в следующих разделах (антитела верблюда и каркас, не принадлежащий к антителу).
Каркас или получение Fc
Сконструированные антитела, содержащиеся в композициях по настоящему изобретению, включают антитела, в которых были сделаны модификации для каркасных остатков в VH и/или VL, например, улучшение свойства антитела. Как правило, такие модификации каркаса сделаны для снижения иммуногенности антитела. Например, один из подходов заключается в том, чтобы «мутировать к первоначальному виду» один или несколько каркасных остатков в соответствующую последовательность зародышевой линии. Более конкретно, антитело, которое подверглось соматической мутации, может содержать каркасные остатки, которые отличаются от последовательности зародышевой линии, из которой получено антитело. Такие остатки могут быть идентифицированы путем сравнения каркасных последовательностей антитела с последовательностями зародышевой линии, из которых получено антитело. Чтобы вернуть последовательности каркасной области в их конфигурацию зародышевой линии, соматические мутации могут быть «мутированы к первоначальному виду» в последовательность зародышевой линии, например, с помощью сайт-направленного мутагенеза или PCR-опосредованного мутагенеза. Такие «обратно мутированные» антитела также могут содержаться в композициях по изобретению.
Другой тип модификации каркаса включает в себя мутацию одного или нескольких остатков внутри каркасной области или даже внутри одной или нескольких областей CDR для удаления Т-клеточных эпитопов, чтобы тем самым снизить потенциальную иммуногенность антитела. Этот подход также упоминается как «деиммунизация», и описан более подробно в US 2003/0153043.
В дополнение или в качестве альтернативного варианта модификациям, сделанным в каркасных или CDR-областях, антитела по изобретению могут быть сконструированы так, чтобы включать модификации в Fc-области, обычно для изменения одного или нескольких функциональных свойств антитела, таких как период полураспада в сыворотке, фиксация комплемента связывания с Fc-рецептором и/или антиген-зависимая клеточная цитотоксичность. Кроме того, антитело, содержащееся в композициях по настоящему изобретению, может быть химически модифицировано (например, одна или несколько химических групп могут быть присоединены к антителу) или модифицировано для изменения его гликозилирования, снова, чтобы изменить одно или несколько функциональных свойств антитела. Каждый из этих вариантов осуществления описан более подробно ниже. Нумерация остатков в области Fc соответствует индексу ЕС по Кабату.
В одном варианте осуществления шарнирную область СН1 модифицируют таким образом, что количество остатков цистеина в шарнирной области изменяется, например, увеличивается или уменьшается. Этот подход описан далее в US 5677425. Количество остатков цистеина в шарнирной области СН1 изменяется, например, для облегчения сборки легких и тяжелых цепей или для увеличения или уменьшения стабильности антитела.
В другом варианте осуществления шарнирную область Fc антитела мутируют для уменьшения биологического периода полураспада антитела. Более конкретно, одну или несколько аминокислотных мутаций вводят в область поверхностного участка домена СН2-СН3 фрагмента Fc-шарнира так, что антитело нарушает связывание белка А Staphylococcyl (SpA) относительно связывания природного домена Fc-шарнира SpA. Этот подход более подробно описан в документе US 6,165,745.
В другом варианте осуществления антитело модифицировано для увеличения его биологического периода полураспада. Возможны разные подходы. Например, может быть введена одна или несколько из следующих мутаций: T252L, T254S, T256F, как описано в US 6,277,375. В альтернативном варианте, для увеличения биологического периода полураспада, антитело может быть изменено в пределах области СН1 или CL, чтобы оно содержало эпитоп, связывающий рецептор реутилизации, взятый из двух петель домена СН2 области Fc IgG, как описано в US 5869,046 и US 6,121,022.
В других вариантах осуществления область Fc изменяется путем замены, по меньшей мере, одного аминокислотного остатка другим аминокислотным остатком для изменения эффекторных функций антитела. Например, одна или несколько аминокислот могут быть заменены другим аминокислотным остатком так, что антитело имеет измененное сродство к эффекторному лиганду, но сохраняет антигенсвязывающую способность родительского антитела. Эффекторный лиганд, к которому изменяется аффинность, может представлять собой, например, рецептор Fc или компонент С1 комплемента. Этот подход более подробно описан в US 5624821 и US 5664260, Winter et al. В частности, остатки 234 и 235 могут быть мутированными. В частности, эти мутации могут быть связаны с аланином. Таким образом, в одном варианте осуществления антитело, содержащееся в композициях по настоящему изобретению, имеет мутацию в области Fc одной или обеих аминокислот 234 и 235. В другом варианте осуществления одна или обе аминокислоты 234 и 235 могут быть замещены аланином. Замена обеих аминокислот 234 и 235 на аланин приводит к снижению активности ADCC.
В другом варианте осуществления одну или несколько аминокислот, выбранных из аминокислотных остатков описанных антител, можно заменить другим аминокислотным остатком так, чтобы антитело изменило связывание C1q и/или уменьшило или отменило зависимую от комплемента цитотоксичность (CDC). Этот подход более подробно описан в патенте США 6,194,551.
В другом варианте осуществления один или несколько аминокислотных остатков описанных антител изменены, чтобы тем самым изменить способность антитела фиксировать комплемент. Этот подход описан далее в WO 94/29351.
В еще одном варианте осуществления область Fc описанных антител модифицируется для увеличения способности антитела опосредовать антитело-зависимую клеточную цитотоксичность (ADCC) и/или для увеличения аффинности антитела к рецептору Fey путем модификации одной или нескольких аминокислот. Этот подход описан далее в WO 00/42072. Кроме того, области связывания на человеческом IgG1 для FcyRI, FcyRII, FcyRIII и FcRn были локализованы, и были описаны варианты с улучшенным связыванием (см. Shields, R.L et al., 2001 J. Biol. Chen. 276: 6591-6604).
В еще одном варианте осуществления гликозилирования антитела, содержащегося в композициях по изобретению, модифицировано. Например, может быть получено агликозилированное антитело (т.е. антитело не имеет гликозилирования). Гликозилирование может быть изменено, например, для увеличения аффинности антитела к антигену. Такие модификации углеводов могут быть выполнены с помощью, например, изменения одного или нескольких участков гликозилирования в последовательности антитела. Например, могут быть сделаны одна или несколько аминокислотных замен, которые приводят к удалению одного или нескольких участков гликозилирования каркасной области вариабельной области, чтобы тем самым устранить гликозилирование в этом участке. Такое агликозилирование может увеличивать сродство антитела к антигену. Такой подход более подробно описан в патентах США №5714350 и 6 350 861, Со et al.
В дополнительном или альтернативном варианте, можно использовать антитело, которое имеет измененный тип гликозилирования, такое как гипофукозилированное антитело, имеющее уменьшенные количества фукозильных остатков, или антитело, имеющее увеличенные структуры GIcNac в точках ветвления. Было показано, что такие измененные профили гликозилирования увеличивают способность антител к ADCC. Такие модификации углеводов могут быть выполнены, например, путем экспрессии антитела в клетке-хозяине с измененным механизмом гликозилирования. Клетки с измененным механизмом гликозилирования были описаны в данной области техники и могут использоваться в качестве клеток-хозяев, в которых экспрессируются раскрытые рекомбинантные антитела, чтобы тем самым продуцировать антитело с измененным гликозилированием. Например, ЕР 1176195, Hang et al. описывает клеточную линию с функционально нарушенным геном FUT8, который кодирует фукозилтрансферазу так, что антитела, экспрессируемые в такой клеточной линии, обнаруживают гипофукозилирование. Следовательно, в одном варианте осуществления антитела, содержащиеся в композициях по изобретению, продуцируются рекомбинантной экспрессией в клеточной линии, которая демонстрирует способ гипофукозилирования, например, в клеточной линии млекопитающего с недостаточной экспрессией гена FUT8, кодирующего фукозилтрансферазу. В WO 03/035835 описан вариант клеточной линии СНО, клетки LecI3, со сниженной способностью присоединять фукозу к связанным с Asn (297) углеводам, что также приводит к гипофукозилированию антител, экспрессируемых в этой клетке-хозяине (см. также Shields, RL et al., 2002 J Biol. Chem. 277: 26733-26740). В WO 99/54342 описаны клеточные линии, сконструированные для экспрессии гликопротеин-модифицирующих гликозилтрансфераз (например, бета (1,4) -N-ацетилглюкозаминилтрансферазы III (GnTIII)) так, что антитела, экспрессируемые в сконструированных клеточных линиях, проявляют усиление структур GlcNac в точках ветвления, что приводит к увеличению активности ADCC антител (см. также Umana et al., 1999 Nat. Biotech. 17: 176-180). В альтернативном варианте, антитела, содержащиеся в композициях по настоящему изобретению, могут быть получены в дрожжах или нитевидных грибах, сконструированных для профиля гликозилирования, подобного млекопитающему, и способных продуцировать антитела, лишенные фукозы, в качестве профиля гликозилирования (см., например, ЕР 1297172 В1).
Другой модификацией антител в данном документе, которая рассматривается в настоящем описании, является пегилирование. Антитело может быть пегилировано, например, для увеличения биологического (например, в сыворотке) периода полураспада антитела. Для пегилирования антитело или его фрагмент обычно подвергают взаимодействию с полиэтиленгликолем (ПЭГ), таким как реакционноспособное эфирное или альдегидное производное ПЭГ, в условиях, в которых одна или несколько групп ПЭГ присоединяются к антителу или фрагменту антитела. Пегилирование может быть осуществлено с помощью реакции ацилирования или реакции алкилирования с реакционноспособной молекулой ПЭГ (или аналогичным реакционноспособным водорастворимым полимером). Используемый здесь термин «полиэтиленгликоль» предназначен для охвата любой из форм ПЭГ, которые были использованы для дериватизации других белков, таких как моно (С1-С10) алкокси- или арилокси-полиэтиленгликоль или полиэтиленгликоль-малеимид. В определенных вариантах осуществления используемое антитело, подлежащее пегилированию, представляет собой агликозилированное антитело. Способы пегилирования белков известны в данной области и могут применяться к антителам, раскрытым в данном документе (см., например, ЕР 0154316 и ЕР 0401384).
Другой возможностью является слияние, по меньшей мере, антигенсвязывающей области антитела, содержащейся в композиции по изобретению, с белками, способными связываться с сывороточными белками, такими как сывороточный альбумин человека, для увеличения периода полураспада получающейся в результате молекулы (см., например, ЕР 0486525).
Методы конструирования модифицированных антител
Как обсуждалось выше, антитела против ActRIIB, имеющие последовательности CDR, последовательности VH и VL или полноразмерные последовательности тяжелой и легкой цепи, показанные в данном документе, могут быть использованы для создания новых антител против ActRIIB путем модификации полноразмерных CDR-последовательностей тяжелой цепи и/или легкой цепи, последовательности VH и/или VL или константных областей, к которым они присоединены. Таким образом, в другом аспекте изобретения структурные признаки антитела против ActRIIB, содержащегося в композициях по настоящему изобретению, используются для создания структурно родственных антител против ActRIIB, которые сохраняют, по меньшей мере, одно функциональное свойство антител, содержащихся в композициях изобретения, такое как связывание с ActRIIB человека, но также ингибирование одного или нескольких функциональных свойств ActRIIB (например, ингибирование активации Smad).
Например, одну или несколько областей CDR антител, содержащихся в композициях по настоящему изобретению, или их мутации, можно рекомбинантно комбинировать с известными каркасными областями и/или другими CDR для создания дополнительных рекомбинантных сконструированных антител против ActRIIB, содержащихся в составах изобретения, как обсуждено выше. Другие типы модификаций включают в себя те, которые описаны в предыдущем разделе. Исходным материалом для способа конструирования является одна или несколько последовательностей VH и/или VL, представленных в настоящем документе, или одна или несколько их областей CDR. Для того, чтобы создать сконструированное антитело, нет необходимости фактически получать (т.е. экспрессировать в виде белка) антитело, имеющее одну или несколько последовательностей VH и/или VL, представленных в настоящем документе, или одну или несколько его областей CDR. Скорее, информация, содержащаяся в последовательности (ях), используется в качестве исходного материала для создания последовательности (ей) «второго поколения», полученной из исходной (ых) последовательности (ей), и затем готовится последовательность (последовательности) «второго поколения» и экспрессируется в виде белка.
Измененную последовательность антител также можно получить путем скрининга библиотек антител, имеющих фиксированные последовательности CDR3, выбранные из группы, состоящей из SEQ ID NO: 29-42 и SEQ ID NO: 71-84, или минимально необходимых эпитопов связывания, как описано в US 2005/0255552, и разнообразия на последовательностях CDR1 и CDR2. Скрининг может быть выполнен в соответствии с любой технологией скрининга, подходящей для скрининга антител из библиотек антител, такой как технология фагового дисплея.
Стандартные методы молекулярной биологии могут быть использованы для получения и экспрессии измененной последовательности антитела. Антитело, кодируемое измененной последовательностью (последовательностями) антитела, представляет собой антитело, которое сохраняет одно, некоторые или все функциональные свойства антител против ActRIIB, описанных в настоящем документе, причем эти функциональные свойства включают, но не ограничиваются этим, специфическое связывание с человеческим ActRIIB и ингибирование активации Smad.
Измененное антитело может проявлять одно или несколько, два или более, три или более функциональных свойств, обсужденных выше.
Функциональные свойства измененных антител могут быть оценены с использованием стандартных анализов, доступных в данной области техники и/или описанных здесь, таких как те, которые приведены в примерах (например, ELISA).
Мутации могут быть введены случайным образом или селективно по всей или части кодирующей последовательности антитела против ActRIIB, и полученные модифицированные антитела против ActRIIB могут быть подвергнуты скринингу на активность связывания и/или другие функциональные свойства, как описано в настоящем документе. Мутационные методы были описаны в данной области техники. Например, в WO 02/092780 описаны способы создания и скрининга мутаций антител с использованием мутагенеза с насыщением, синтетической лигированной сборки или их комбинации. В альтернативном варианте, в WO 03/074679 описаны способы использования методов компьютерного скрининга для оптимизации физико-химических свойств антител.
Молекулы нуклеиновой кислоты, кодирующие антитела, содержащиеся в описанных композициях
Примеры полноразмерных нуклеотидных последовательностей легкой цепи, оптимизированных для экспрессии в клетке млекопитающего, показаны в SEQ ID NO: 161-165 и 171-175. Примеры полноразмерных нуклеотидных последовательностей тяжелой цепи, оптимизированных для экспрессии в клетке млекопитающего, показаны в SEQ ID NO: 166-170 и 176-180.
Нуклеиновые кислоты могут присутствовать в целых клетках, в клеточном лизате или могут представлять собой нуклеиновые кислоты в частично очищенной или по существу чистой форме. Нуклеиновая кислота является «изолированной» или «сделанной по существу чистой», когда она очищена от других клеточных компонентов или других загрязнений, например, других клеточных нуклеиновых кислот или белков, стандартными методами, включая обработку щелочью/SDS, разделение в CsCl, колоночную хроматографию, электрофорез в агарозном геле и другие, хорошо известные в данной области. См. F. Ausubel, et al., Ed. 1987 Current Protocols in Molecular Biology, Greene Publishing and Wiley Interscience, New York. Нуклеиновые кислоты могут быть получены с использованием стандартных методов молекулярной биологии. Для антител, экспрессируемых гибридомами (например, гибридомами, полученными от трансгенных мышей, несущих гены иммуноглобулина человека, как описано далее), кДНК, кодирующие легкие и тяжелые цепи антитела, полученные гибридомой, можно получить стандартными методами PCR-амплификации или клонирования кДНК. Для антител, полученных из библиотеки генов иммуноглобулина (например, с использованием методов фагового дисплея), нуклеиновую кислоту, кодирующую антитело, можно извлечь из различных клонов фагов, которые являются членами библиотеки.
После получения фрагментов ДНК, кодирующих сегменты VH и VL, этими фрагментами ДНК можно дополнительно манипулировать с помощью стандартных методов рекомбинантной ДНК, например, для преобразования генов вариабельной области в гены цепи полноразмерных антител, в гены Fab-фрагмента или в ген scFv. В этих манипуляциях фрагмент ДНК, кодирующий VL или VH, оперативно связан с другой молекулой ДНК или с фрагментом, кодирующим другой белок, такой как константная область антитела или гибкий линкер. Термин «функционально связанный», используемый в данном контексте, предназначен для обозначения того, что два фрагмента ДНК функционально связаны, например, так, что аминокислотные последовательности, кодируемые этими двумя фрагментами ДНК, остаются внутри рамки считывания, или так, что белок экспрессируется под контролем желаемого промотора.
Изолированная ДНК, кодирующая область VH, может быть преобразована в полноразмерный ген тяжелой цепи путем оперативного связывания ДНК, кодирующей VH, с другой молекулой ДНК, кодирующей константные области тяжелой цепи (СН1, СН2 и СН3). Последовательности генов константной области тяжелой цепи человека известны в данной области (см., например, Kabat, Е.А., et al. [Supra]), и фрагменты ДНК, охватывающие эти области, могут быть получены с помощью стандартной амплификации PCR. Константная область тяжелой цепи может быть константной областью IgG1, IgG2, IgG3, IgG4, IgA, IgE, IgM или IgD. Константная область тяжелой цепи может быть выбрана среди изотипов IgG1. Для гена тяжелой цепи Fab-фрагмента ДНК, кодирующая VH, может быть функционально связана с другой молекулой ДНК, кодирующей только константную область СН1 тяжелой цепи.
Изолированная ДНК, кодирующая область VL, может быть преобразована в полноразмерный ген легкой цепи (а также в ген легкой цепи Fab) путем оперативного связывания VL-кодирующей ДНК с другой молекулой ДНК, кодирующей константную область легкой цепи, CL. Последовательности генов константной области легкой цепи человека известны в данной области (см., например, Kabat, Е.А., et al. [Supra]), и фрагменты ДНК, охватывающие эти области, могут быть получены с помощью стандартной амплификации PCR. Константная область легкой цепи может быть константной областью каппа или лямбда.
Для создания гена scFv фрагменты ДНК, кодирующие VH и VL, оперативно связаны с другим фрагментом, кодирующим гибкий линкер, например, кодирующий аминокислотную последовательность (Gly4 -Ser)3 так, что последовательности VH и VL могут быть экспрессированы в виде непрерывного одноцепочечного белка, причем области VL и VH соединены гибким линкером (см., например, Bird et al., 1988 Science 242: 423-426; Huston et al., 1988 Proc. Natl. Acad. Sci. USA, 85: 5879-5883; McCafferty et al., 1990 Nature 348: 552-554).
Получение моноклональных антител
Моноклональные антитела (mAb) могут быть получены различными способами, включая обычную методологию моноклональных антител, например, стандартную методику гибридизации соматических клеток Колера и Мильштейна (1975, Nature 256: 495). Можно использовать много способов для получения моноклональных антител, например, вирусную или онкогенную трансформация В-лимфоцитов.
Животной системой для получения гибридом является мышиная система. Производство гибридомы у мыши является хорошо отработанной процедурой. Протоколы и методы иммунизации для выделения иммунизированных спленоцитов для слияния известны в данной области. Партнеры по слиянию (например, клетки миеломы мыши) и процедуры слияния также известны.
Химерные или гуманизированные антитела, содержащиеся в композициях по настоящему изобретению, могут быть получены на основе последовательности мышиного моноклонального антитела, полученного, как описано выше. ДНК, кодирующая иммуноглобулины тяжелой и легкой цепей, может быть получена из мышиной гибридомы, представляющей интерес, и сконструирована так, чтобы содержать последовательности немышиного (например, человека) иммуноглобулина с использованием стандартных методов молекулярной биологии. Например, чтобы создать химерное антитело, вариабельные области мыши могут быть связаны с константными областями человека с использованием способов, известных в данной области (см., например, US 4816567). Для создания гуманизированного антитела мышиные области CDR могут быть вставлены в человеческий каркас с использованием способов, известных в данной области (см., например, патент США №5225539; 5530101; 5585089; 5693762 и 6180370).
В определенном варианте осуществления антитела, содержащиеся в композициях по изобретению, представляют собой человеческие моноклональные антитела. Такие человеческие моноклональные антитела, направленные против ActRIIB, могут быть получены с использованием трансгенных или трансхромосомных мышей, несущих части иммунной системы человека, а не мыши. Эти трансгенные и трансхромосомные мыши включают в себя мышей, называемых в данном документе мышами HuMAb и мышами KM, соответственно, и в совокупности упоминаются здесь как «мыши Ig человека».
Мышь HuMAb® (Medarex, Inc.) содержит минилокусы человеческого гена иммуноглобулина, которые кодируют неупорядоченные последовательности тяжелой (μ и у) и k легкой цепи человеческого иммуноглобулина, а также мутации-мишени, которые инактивируют эндогенные локусы цепи μ и k (см., например, Lonberg, et al., 1994 Nature 368 (6474): 856-859). Соответственно, у мышей наблюдается пониженная экспрессия мышиного IgM или k, и в ответ на иммунизацию введенные человеческие трансгены тяжелой и легкой цепи подвергаются переключению классов и соматической мутации с образованием высокоаффинного человеческого моноклонального IgGk (Lonberg, N. et al., 1994 [supra]] reviewed in Lonberg, N., 1994 Handbook of Experimental Pharmacology 113:49-101; Lonberg, N. and Huszar, D., 1995 Intern. Rev. Immunol.13: 65-93, and Harding, F. and Lonberg, N., 1995 Ann. N. Y. Acad. Sci. 764:536-546). Получение и использование мышей HuMAb и геномные модификации, которые несут такие мыши, дополнительно описаны в Taylor, L. et al., 1992 Nucleic Acids Research 20:6287-6295; Chen, J. et al., International Immunology 5: 647-656; Tuaillon et al., 1993 Proc. Natl. Acad. Sci. USA 94:3720-3724; Choi et al., 1993 Nature Genetics 4:117-123; Chen, J. et al., 1993 EMBO J. 12: 821-830; Tuaillon et al., 1994 J. Immunol. 152:2912-2920; Taylor, L. et al., 1994 International Immunology 579-591; и Fishwild, D. et al., 1996 Nature Biotechnology 14: 845-851, содержание которых полностью включено в настоящее описание в качестве ссылки. См. далее патенты США №5545806; 5569825; 5625126; 5633425; 5789650; 5877397; 5661016; 5814318; 5874299; 5770429; и 5545807; а также WO 92/103918, WO 93/12227, WO 94/25585, WO 97 /113852, WO 98/24884; WO 99/45962; и WO 01/14424.
В другом варианте осуществления антитела человека, содержащиеся в композициях по настоящему изобретению, могут быть получены с использованием мыши, которая несет последовательности иммуноглобулина человека на трансгенах и трансхромосомах, такой как мышь, которая несет трансген тяжелой цепи человека и трансхромосому легкой цепи человека. Такие мыши, называемые здесь «мышами КМ», подробно описаны в WO 02/43478.
Кроме того, в данной области доступны альтернативные системы трансгенных животных, экспрессирующих гены иммуноглобулина человека, и их можно использовать для получения антител против ActRIIB по настоящему изобретению. Например, можно использовать альтернативную трансгенную систему, называемую Xenomouse (Abgenix, Inc.). Такие мыши описаны, например, в патентах США №№5,939,598; 6,075,181; 6,114,598; 6,150,584 и 6,162,963.
Кроме того, альтернативные трансхромосомные системы животных, экспрессирующие гены иммуноглобулина человека, доступны в данной области и могут быть использованы для получения антител против ActRIIB по изобретению. Например, можно использовать мышей, несущих как транхромосому тяжелой цепи человека, так и транхромосому легкой цепи человека, называемых «мышами ТС»; такие мыши описаны в Tomizuka et al., 2000 Proc. Natl. Акад. Sci. США 97: 722-727. Кроме того, коровы, несущие трансхромосомы человека с тяжелой и легкой цепью, были описаны в данной области (Kuroiwa et al., 2002 Nature Biotechnology 20: 889-894) и могут быть использованы для получения антител против ActRIIB.
Человеческие рекомбинантные антитела, содержащиеся в композициях по изобретению, также могут быть получены с использованием методов фагового дисплея для скрининга библиотек генов иммуноглобулина человека. Такие методы фагового дисплея для выделения антител человека установлены в данной области или описаны в приведенных ниже примерах. См., например: патенты США №№5,223,409; 5,403,484; 5,571,698; 5,427,908; 5,580,717; 5,969,108; 6,172,197; 5,885,793; 6,521,404; 6,544,731; 6,555,313; 6,582,915 и 6,593,081.
Моноклональные антитела человека, содержащиеся в композициях по настоящему изобретению, также могут быть получены с использованием мышей SCID, в которых человеческие иммунные клетки были восстановлены таким образом, что при иммунизации может быть получен отклик человеческого антитела. Такие мыши описаны, например, в патентах США №№5479996 и 5698767.
Генерация гибридом, продуцирующих человеческие моноклональные антитела
Для создания гибридом, продуцирующих человеческие моноклональные антитела, содержащиеся в композициях по изобретению, спленоциты и/или клетки лимфатических узлов от иммунизированных мышей могут быть выделены и слиты с соответствующей иммортализованной клеточной линией, такой как клеточная линия миеломы мыши. Полученные гибридомы могут быть подвергнуты скринингу на продуцирование антигенспецифических антител. Например, одноклеточные суспензии лимфоцитов селезенки от иммунизированных мышей могут быть слиты с 1/6 количества несекретирующих клеток миеломы мыши P3X63-Ag8.653 (АТСС, CRL 1580) с 50% ПЭГ. Клетки высевают примерно 2 раза по 145 в планшеты для микротитрования с плоским дном с последующей двухнедельной инкубацией в селективной среде, содержащей 20% эмбриональной клоновой сыворотки, 18% кондиционированной среды "653", 5% origen (IGEN), 4 мМ L- глутамина, 1 мМ пирувата натрия, 5 мМ HEPES, 0:055 мМ 2-меркаптоэтанола, 50 ед/мл пенициллина, 50 мг/мл стрептомицина, 50 мг/мл гентамицина и 1Х HAT (Sigma; HAT добавляется через 24 часа после слияния). Примерно через две недели клетки можно культивировать в среде, в которой HAT заменяется на НТ. Индивидуальные лунки могут затем быть подвергнуты скринингу с помощью ELISA на человеческие моноклональные антитела IgM и IgG. После обширного роста гибридомы среду обычно можно наблюдать через 10-14 дней. Секретирующие антитела гибридомы могут быть воспроизведены, подвергнуты повторному скринингу, и, если они все еще позитивны в отношении человеческого IgG, моноклональные антитела могут быть субклонированы, по меньшей мере, дважды путем предельного разведения. Стабильные субклоны могут затем культивироваться in vitro для генерирования небольших количеств антител в тканевой культурной среде для характеристики. Для очистки человеческих моноклональных антител отобранные гибридомы могут быть выращены в двухлитровых вращающихся колбах для очистки моноклональных антител. Супернатанты могут быть отфильтрованы и сконцентрированы перед аффинной хроматографией с белком А-сефарозой (Pharmacia). Элюированный IgG можно проверить гель-электрофорезом и высокоэффективной жидкостной хроматографией для обеспечения чистоты. Буферный раствор можно обменять на PBS, а концентрацию можно определить по OD280, используя коэффициент экстинкции 1,43. Моноклональные антитела можно разделить на аликвоты и хранить при -80°С.
Генерация трансфектом, продуцирующих моноклональные антитела
Антитела, содержащиеся в композициях по изобретению, также могут быть получены в трансфектоме клетки-хозяина с использованием, например, комбинации методов рекомбинантной ДНК и методов генной трансфекции, как это хорошо известно в данной области (например, Morrison S. (1985) Science 229:1202).
Например, для экспрессии антител или их фрагментов антител ДНК, кодирующие частичные или полноразмерные легкие и тяжелые цепи, могут быть получены стандартными методами молекулярной биологии (например, амплификация PCR или клонирование кДНК с использованием гибридомы, которая экспрессирует интересующее антитело), и ДНК могут быть встроены в векторы экспрессии так, что гены функционально связаны с последовательностями контроля транскрипции и трансляции. В этом контексте термин «функционально связанный» предназначен для обозначения того, что ген антитела лигируется в вектор так, что транскрипционные и трансляционные контрольные последовательности в векторе выполняют свою намеченную функцию регуляции транскрипции и трансляции гена антитела. Вектор экспрессии и последовательности контроля экспрессии выбирают так, чтобы они были совместимы с используемой клеткой-хозяином экспрессии. Ген легкой цепи антитела и ген тяжелой цепи антитела могут быть вставлены в отдельный вектор или, что более типично, оба гена вставлены в один и тот же вектор экспрессии. Гены антитела встраивают в вектор экспрессии стандартными методами (например, лигированием комплементарных участков рестрикции на фрагменте и векторе гена антитела или лигированием тупого конца, если участков рестрикции нет). Вариабельные области легкой и тяжелой цепей антител, описанные в настоящем документе, можно использовать для создания полноразмерных генов антител любого изотипа антитела путем их вставки в векторы экспрессии, уже кодирующие константные области тяжелой цепи и константные области легкой цепи желаемого изотипа, так что VH сегмент функционально связан с сегментом (ами) СН в векторе, а сегмент VL функционально связан с сегментом CL в векторе. В дополнительном или альтернативном варианте рекомбинантный вектор экспрессии может кодировать сигнальный пептид, который облегчает секрецию цепи антитела из клетки-хозяина. Ген цепи антитела может быть клонирован в векторе таким образом, что сигнальный пептид связан в рамке с аминоконцом гена цепи антитела. Сигнальный пептид может быть сигнальным пептидом иммуноглобулина или гетерогенным сигнальным пептидом (т.е. сигнальным пептидом из белка, не являющегося иммуноглобулином). В дополнение к генам цепи антител рекомбинантные векторы экспрессии по настоящему изобретению несут регуляторные последовательности, которые контролируют экспрессию генов цепи антител в клетке хозяине. Предполагается, что термин «регуляторная последовательность» включает промоторы, энхансеры и другие элементы контроля экспрессии (например, сигналы полиаденилирования), которые контролируют транскрипцию или трансляцию генов цепи антитела. Такие регуляторные последовательности описаны, например, в Goeddel (Gene Expression Technology. Methods in Enzymology 185, Academic Press, San Diego, CA 1990). Специалистам в данной области будет понятно, что конструкция вектора экспрессии, включая выбор регуляторных последовательностей, может зависеть от таких факторов, как выбор клетки-хозяина, подлежащей трансформации, желаемый уровень экспрессии белка и т.д. Регуляторные последовательности для экспрессии клеток-хозяев млекопитающих включают вирусные элементы, которые управляют высокими уровнями экспрессии белка в клетках млекопитающих, такие как промоторы и/или энхансеры, полученные из цитомегаловируса (CMV), вируса Simian Virus 40 (SV40), аденовируса (например, главного позднего промотора аденовируса (AdMLP) и полиома. В альтернативном варианте, можно использовать невирусные регуляторные последовательности, такие как промотор убиквитина или промотор Р-глобина. Кроме того, регуляторные элементы состоят из последовательностей из разных источников, таких как промоторная система SRa, которая содержит последовательности раннего промотора SV40 и длинный концевой повтор вируса Т-клеточного лейкоза человека типа 1 (Takebe, Y. et al., 1988 Mol. Cell. Biol. 8: 466-472).
В дополнение к генам цепей антител и регуляторным последовательностям рекомбинантные векторы экспрессии могут нести дополнительные последовательности, такие как последовательности, которые регулируют репликацию вектора в клетках-хозяевах (например, происхождение репликации) и селектируемые маркерные гены. Селектируемый маркерный ген облегчает отбор клеток-хозяев, в которые был введен вектор (см., например, патенты США №№4,399,216, 4,634,665 и 5,179,017). Например, обычно селектируемый маркерный ген придает устойчивость к лекарствам, таким как G418, гигромицин или метотрексат, клетке-хозяину, в которую был введен вектор. Селектируемые маркерные гены включают ген дигидрофолатредуктазы (DHFR) (для использования в клетках-хозяевах dhfr с селекцией/амплификацией метотрексата) и ген neo (для селекции G418).
Для экспрессии легкой и тяжелой цепей вектор (ы) экспрессии, кодирующий тяжелую и легкую цепи, трансфицируют в клетку-хозяина стандартными методами. Предполагается, что различные формы термина «трансфекция» охватывают широкий спектр методов, обычно используемых для введения экзогенной ДНК в прокариотическую или эукариотическую клетку-хозяина, например, электропорация, осаждение фосфата кальция, трансфекция DEAE-декстраном и тому подобное. Теоретически возможно экспрессировать антитела по изобретению либо в прокариотических, либо в эукариотических клетках-хозяевах. Экспрессия антител в эукариотических клетках, в частности в клетках-хозяевах млекопитающих, обсуждается потому, что такие эукариотические клетки и, в частности, клетки млекопитающих, с большей вероятностью, чем прокариотические клетки, собирают и секретируют правильно свернутое и иммунологически активное антитело. Сообщалось, что прокариотическая экспрессия генов антител неэффективна для получения активных антител с высоким выходом (Boss, М.А. and Wood, C.R., 1985 Immunology Today 6: 12-13).
Клетки-хозяева млекопитающих для экспрессии рекомбинантных антител, содержащихся в композициях по изобретению, включают яичник китайского хомячка (клетки СНО) (включая клетки dhfr-CHO, описанные Urlaub и Chasin, 1980 Proc. Natl. Acad. Sci. USA 77: 4216-4220, используемые с селектируемым маркером DH FR, например, как описано в RJ Kaufman and PA Sharp, 1982 Mol. Biol. 159: 601-621), клетками миеломы NSO, клетки COS и клетки SP2. В одном варианте осуществления клетки-хозяева представляют собой клетки СНО K1PD. В частности, для использования с клетками миеломы NSO другой системой экспрессии является система экспрессии гена GS, показанная в WO 87/04462, WO 89/01036 и ЕР 338,841. Клетки-хозяева млекопитающих для экспрессии рекомбинантных антител, содержащихся в композициях по изобретению, включают клеточные линии млекопитающих, дефицитные по экспрессии гена FUT8, например, как описано в US 6946292 В2. Когда рекомбинантные векторы экспрессии, кодирующие гены антител, вводят в клетки-хозяева млекопитающих, антитела получают путем культивирования клеток-хозяев в течение периода времени, достаточного для обеспечения возможности экспрессии антитела в клетках-хозяевах или секреции антитела в культурную среду, в которой клетки-хозяева выращивают. Антитела могут быть выделены из культуральной среды с использованием стандартных методов очистки белка.
Иммуноконъюгаты
В другом аспекте настоящее раскрытие относится к композициям, содержащим антитело против ActRIIB или его фрагмент, конъюгированный с терапевтическим фрагментом, таким как цитотоксин, лекарственное средство (например, иммунодепрессант) или радиотоксин. Такие конъюгаты упоминаются здесь как «иммуноконъюгаты». Иммуноконъюгаты, которые включают один или несколько цитотоксинов, называются «иммунотоксинами». Цитотоксин или цитотоксический агент включает в себя любой агент, который наносит вред (например, убивает) клеткам.
Цитотоксины могут быть конъюгированы с антителами по изобретению с использованием линкерной технологии, доступной в данной области. Примеры типов линкеров, которые были использованы для конъюгирования цитотоксина с антителом, включают, но не ограничиваются ими, гидразоны, тиоэфиры, сложные эфиры, дисульфиды и пептидсодержащие линкеры. Может быть выбран линкер, который, например, подвержен расщеплению при низком рН в лизосомальном компартменте или подвержен расщеплению протеазами, такими как протеазы, преимущественно экспрессируемые в опухолевой ткани, такие как катепсины (например, катепсины В, С, D).
Для дальнейшего обсуждения типов цитотоксинов, линкеров и способов конъюгирования терапевтических агентов с антителами см. также Saito, G. et al., 2003 Adv. Drug Deliv. Rev. 55: 199-215; Trail. P.A. et al., 2003, Cancer Immunol. Immunother. 52: 328-337; Payne, G. 2003 Cancer Cell 3: 207 212; Allen T.M., 2002 Nat. Rev. Cancer 2: 750-763; Pastan, I. and Kreitman, R.J., 2002 Curr. Opin. Investig. Drugs 3: 1089-1091; Senter, P.D. и Springer, C.J., 2001 Adv. Drug Deliv. Rev. 53: 247-264.
Антитела, содержащиеся в композициях по настоящему изобретению, также могут быть конъюгированы с радиоактивным изотопом для получения цитотоксических радиофармацевтических препаратов, также называемых радиоиммуноконъюгатами. Примеры радиоактивных изотопов, которые могут быть конъюгированы с антителами для диагностического или терапевтического использования, включают, но не являются ограниченными, йод131, индий111, иттрий90 и лютеций177. Способы получения радиоиммунконъюгатов установлены в данной области. Примеры радиоиммуноконъюгатов являются коммерчески доступными, включая Zevalin™ (DEC Pharmaceuticals) и Bexxar™ (Corixa Pharmaceuticals), и аналогичные способы могут быть использованы для получения радиоиммуноконъюгатов с использованием антител, описанных в настоящем описании.
Конъюгаты антител, содержащиеся в композициях по настоящему изобретению, можно использовать для модификации данного биологического отклика, и фрагмент лекарственного средства не следует истолковывать как ограниченный классическими химическими терапевтическими агентами. Например, лекарственная составляющая может представлять собой белок или полипептид, обладающий желаемой биологической активностью. Такие белки могут включать, например, ферментативно активный токсин или его активный фрагмент, такой как абрин, рицин А, экзотоксин синегнойной палочки или токсин дифтерии; белок, такой как фактор некроза опухоли или интерферон-у; или модификаторы биологического отклика, такие как, например, лимфокины, интерлейкин-1 («IL-1»), интерлейкин-2 («IL-2»), интерлейкин-6 («IL-6»), гранулоцитарный макрофагальные колониестимулирующий фактор («GM-CSF»), гранулоцитарный колониестимулирующий фактор («G-CSF») или другие факторы роста.
Способы конъюгирования такого терапевтического фрагмента с антителами хорошо известны, см., например, Amon et al., "Monoclonal Antibodies For Immunotargering Of Drugs In Cancer Therapy", in Monoclonal Antibodies and Cancer Therapy, Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc., 1985); Hellstrom et al., «Antibodies For Drug Delivery», in Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp. 623-53 (Marcel Dekker, Inc. 1987); Thorpe, «Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Rewiew», in Monoclonal Antibodies '84: Biological and Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985); «Analysis, Results, and Future Prospective Of The Therapeutic Use Of Radiolabeted Antibody In Cancer Therapy», in Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), pp. 303-16 (Academic Press 1985) и Thorpe et al., "The Preparation And Cytotoxic Properties Of Antibody-Toxin Conjugates", Inmunol. Rev., 62: 119-58 (1982).
Биспецифичные молекулы
В другом аспекте настоящее раскрытие относится к композициям, содержащим биспецифичные или мультиспецифичные молекулы, содержащие антитело против ActRIIB или его фрагмент, раскрытия. Антитело, содержащееся в композициях по изобретению, или его антигенсвязывающие области, может быть дериватизировано или связано с другой функциональной молекулой, например, другой пептид или белок (например, другое антитело или лиганд для рецептора) для генерирования биспецифической молекулы, которая связывается по меньшей мере с двумя различными сайтами связывания или молекулами-мишенями.
Антитело по настоящему изобретению может быть на самом деле получено или связано с более чем одной другой функциональной молекулой для генерации мультиспецифических молекул, которые связываются с более чем двумя различными участками связывания и/или молекулами-мишенями; такие мультиспецифичные молекулы также предназначены для охвата термином «биспецифичная молекула», как используется в данном документе. Для того, чтобы создать биспецифическую молекулу по изобретению, антитело по изобретению может быть функционально связано (например, путем химического связывания, генетического слияния, нековалентной ассоциации или иным образом) с одной или несколькими другими связывающими молекулами, такими как другое антитело, фрагмент антитела, пептид или миметик связывания так, что получается биспецифическая молекула.
Соответственно, настоящее изобретение включает композиции, содержащие биспецифичные молекулы, содержащие, по меньшей мере, одну первую специфичность связывания для ActRIIB и вторую специфичность связывания для второго эпитопа-мишени. Например, второй эпитоп-мишень может представлять собой другой эпитоп ActRIIB, отличный от первого эпитопа-мишени.
Кроме того, для композиций, в которых биспецифичная молекула является мультиспецифичной, молекула может дополнительно включать третью специфичность связывания, в дополнение к первому и второму целевому эпитопу.
В одном варианте осуществления биспецифичные молекулы раскрытых композиций содержат в качестве специфичности связывания, по меньшей мере, одно антитело или его фрагмент антитела, включая, например, Fab, Fab', F(ab')2, Fv или одиночную цепь Fv. Антитело также может представлять собой димер легкой цепи или тяжелой цепи или любой их минимальный фрагмент, такой как Fv или одноцепочечная конструкция, как описано в Ladner et al. US 4946778, содержание которого специально включено в качестве ссылки.
Другими антителами, которые можно использовать в биспецифических молекулах, являются мышиные, химерные и гуманизированные моноклональные антитела.
Биспецифичные молекулы, содержащиеся в композициях по настоящему изобретению, могут быть получены путем конъюгирования специфичностей связывания компонентов с использованием способов, известных в данной области. Например, каждую специфичность связывания биспецифической молекулы можно генерировать отдельно и затем конъюгировать друг с другом. Когда специфичностями связывания являются белки или пептиды, для ковалентной конъюгации можно использовать различные связывающие или сшивающие агенты. Примеры сшивающих агентов включают белок А, карбодиимид, N-сукцинимидил-S-ацетилтиоацетат (SATA), 5,5'-дитиобис(2-нитробензойную кислоту) (DTNB), о-фенилендималеимид (oPDM), N- сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) и сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC) (см., например, Karpovsky et al., 1984 J. Exp. Med. 160: 1686).; Li, MA et al., 1985, Proc. Natl. Acad. Sci. USA, 82: 8648). Другие методы включают методы, описанные в Paulus, 1985, Behring Ins. Mitt. №78,118-132; Brennan et al., 1985 Science 229: 81-83) и Glennie et al., 1987 J. Immunol. 139: 2367-2375). Конъюгирующими агентами являются SATA и сульфо-SMCC, оба доступны в Pierce Chemical Co. (Rockford, IL).
Когда специфичности связывания представляют собой антитела, они могут быть конъюгированы сульфгидрильной связью С-конца шарнирных областей двух тяжелых цепей. В конкретном варианте осуществления шарнирную область модифицируют так, чтобы она содержала нечетное количество сульфгидрильных остатков, например, один, до конъюгации.
Альтернативно, обе специфичности связывания могут быть закодированы в одном и том же векторе и экспрессированы и собраны в одной и той же клетке-хозяине. Этот способ особенно полезен, когда биспецифическая молекула представляет собой слитый белок mAb × mAb, mAb × Fab, Fab × F(ab')2 или лиганд × Fab. Биспецифичная молекула, содержащаяся в композициях по изобретению, может представлять собой одноцепочечную молекулу, содержащую одно одноцепочечное антитело и эпитоп связывания, или одноцепочечную биспецифичную молекулу, содержащую два эпитопа связывания. Биспецифичные молекулы могут содержать, по меньшей мере, две одноцепочечные молекулы. Способы получения биспецифичных молекул описаны, например, в патентах США №№5260203; 5455030; 4881175; 5132405; 5091513; 5476786; 5013653; 5258498; и 5,482,858.
Связывание биспецифичных молекул с их конкретными мишенями может быть подтверждено, например, с помощью иммуноферментного анализа (ELISA), радиоиммуноанализа (RIA), анализа FACS, биоанализа (например, ингибирования роста) или анализа Вестерн-блоттинга. Каждый из этих анализов обычно обнаруживает присутствие комплексов белок-антитело, представляющих особый интерес, с использованием меченого реагента (например, антитела), специфичного для представляющего интерес комплекса.
Поливалентные антитела
В другом аспекте настоящее изобретение относится к композициям, содержащим поливалентные антитела, содержащие, по меньшей мере, две идентичные или разные антигенсвязывающие части раскрытых антител, связывающихся с ActRIIB. В одном варианте осуществления поливалентные антитела обеспечивают, по меньшей мере, две, три или четыре антигенсвязывающих части антител. Антигенсвязывающие части могут быть связаны вместе посредством слияния белков или ковалентной или нековалентной связи. В альтернативном варианте, способы связывания были описаны для биспецифичных молекул. В различных вариантах осуществления композиция может быть моно-, двух- или поливалентной (например, способной связываться с одним, двумя или несколькими антигенами) и/или моно-, би- или мультиспецифичной (например, имеющей область связывания, способную связываться с одним, двумя или несколькими различными антигенами), композиция может представлять собой любую их комбинацию, например моновалентную и моноспецифичную (имеющую одну область связывания, которая связывается с одним антигеном или эпитопом); или двухвалентную и двухспецифичную (имеющую две области связывания, каждая из которых связывается с различным эпитопом или антигеном); или двухвалентную и моноспецифичную (имеющую две области связывания, каждая из которых связывается с одним и тем же эпитопом или антигеном); или поливалентную и моноспецифичную (имеющий несколько областей связывания, которые все связываются с одним и тем же антигеном или эпитопом); или поливалентную и мультиспецифичную (имеющую несколько областей связывания, которые связываются с несколькими различными антигенами или эпитопами).
Фармацевтические композиции
В другом аспекте настоящего изобретение представлена композиция, например, фармацевтическая композиция, содержащая одно или комбинацию описанных выше антител/моноклональных антител или их антигенсвязывающей части (частей), приготовленную вместе с фармацевтически приемлемым носителем. Такие композиции могут включать одно или комбинацию (например, два или более разных) описанных антител, или иммуноконъюгатов, или биспецифичных молекул. Например, фармацевтическая композиция по изобретению может содержать комбинацию антител, которые связываются с различными эпитопами на антигене-мишени или которые обладают комплементарными активностями.
Фармацевтические композиции по изобретению также могут применяться при комбинированной терапии, т.е. в сочетании с другими агентами. Например, комбинированная терапия может включать антитело против ActRII по настоящему изобретению в сочетании, по меньшей мере, с одним другим агентом, увеличивающим мышечную массу/силу, например, IGF-1, IGF-2 или варианты IGF-1 или IGF-2, антитело против миостатина, пропептид миостатина, белок-ловушка миостатина, который связывает ActRIIB, но не активирует его, агонист бета 2, агонист грелина, SARM, агонисты/ миметики GH или фоллистатин. Примеры терапевтических агентов, которые можно использовать в комбинированной терапии, более подробно описаны ниже в разделе об использовании антител по настоящему изобретению.
Используемый здесь термин «фармацевтически приемлемый носитель» включает любые и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и замедляющие абсорбцию агенты и тому подобные, которые являются физиологически совместимыми. Носитель должен быть подходящим для внутривенного, внутримышечного, подкожного, парентерального, вертебрального или эпидермального введения (например, путем инъекции или инфузии), предпочтительно для внутривенной инъекции или инфузии. В зависимости от пути введения активное соединение, то есть антитело, иммуноконъюгированная или биспецифическая молекула, может быть покрыто материалом, защищающим соединение от действия кислот и других природных условий, которые могут инактивировать соединение.
Фармацевтические композиции по настоящему изобретению могут включать одну или несколько фармацевтически приемлемых солей. «Фармацевтически приемлемая соль» относится к соли, которая сохраняет желаемую биологическую активность исходного соединения и не вызывает каких-либо нежелательных токсикологических эффектов (см., Например, Berge, SM, et al., 1977 J. Pharm. Sci. 66: 1-19). Примеры таких солей включают соли присоединения кислоты и соли присоединения основания, соли присоединения кислоты включают соли, полученные из нетоксичных неорганических кислот, таких как соляная, азотная, фосфорная, серная, бромистоводородная, йодистоводородная, фосфорная и тому подобное, а также из нетоксичных органических кислот, таких как алифатические моно- и дикарбоновые кислоты, фенил- замещенные алкановые кислоты, гидроксиалкановые кислоты, ароматические кислоты, алифатические и ароматические сульфокислоты и тому подобное. Соли присоединения оснований включают соли, полученные из щелочноземельных металлов, таких как натрий, калий, магний, кальций и тому подобное, а также из нетоксичных органических аминов, таких как N, N'-дибензилэтилендиамин, N-метилглюкамин, хлорпрокаин, холин, диэтаноламин. этилендиамин, прокаин и тому подобное.
Фармацевтическая композиция по изобретению также может включать фармацевтически приемлемый антиоксидант. Примеры фармацевтически приемлемых антиоксидантов включают: водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфит натрия, сульфит натрия и тому подобное; маслорастворимые антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, альфа-токоферол и тому подобное; и металлхелатирующие агенты, такие как лимонная кислота, этилендиаминтетрауксусная кислота (ЭДТА), сорбит, винная кислота, фосфорная кислота и тому подобное.
Примеры подходящих водных и неводных носителей, которые могут использоваться в фармацевтических композициях по изобретению, включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и тому подобное) и их подходящие смеси, растительные масла, такие как оливковое масло и инъецируемые органические сложные эфиры, такие как этилолеат. Желаемая текучесть может поддерживаться, например, путем использования материалов для покрытия, таких как лецитин, путем поддержания требуемого размера частиц в случае дисперсий и путем использования поверхностно-активных веществ.
Эти композиции могут также содержать адъюванты, такие как консерванты, смачивающие агенты, эмульгирующие агенты и диспергирующие агенты. Предотвращение присутствия микроорганизмов может быть обеспечено как процедурами стерилизации, выше, так и включением различных антибактериальных и противогрибковых агентов, например, парабена, хлорбутанола, фенолсорбиновой кислоты и тому подобного. Также желательно включить в композиции изотонические агенты, такие как сахара, хлорид натрия и тому подобное. Кроме того, пролонгированное всасывание инъецируемой фармацевтической формы может быть вызвано включением агентов, которые замедляют всасывание, таких как моностеарат алюминия и желатин. Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии и стерильные порошки для немедленного приготовления стерильных инъекционных растворов или дисперсий. Использование таких сред и агентов для фармацевтически активных веществ известно в данной области. За исключением случаев, когда какой-либо обычный носитель или агент несовместим с активным соединением, предполагается его применение в фармацевтических композициях по изобретению. Дополнительные активные соединения также могут быть включены в композиции.
Терапевтические композиции обычно должны быть стерильными и стабильными в условиях производства и хранения. Композиция может быть составлена в виде раствора, микроэмульсии, липосомы или другой упорядоченной структуры, подходящей для высокой концентрации лекарственного средства. Носителем может быть растворитель или дисперсионная среда, содержащая, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и тому подобное) и их подходящие смеси. Желаемая текучесть может поддерживаться, например, путем использования покрытия, такого как лецитин, путем поддержания требуемого размера частиц в случае дисперсии и путем использования поверхностно-активных веществ. Во многих случаях в композицию можно включать изотонические агенты, например, сахара, полиспирты, такие как маннит, сорбит или хлорид натрия. Длительная абсорбция инъецируемых композиций может быть достигнута включением в композицию агента, который задерживает абсорбцию, например, моностеаратных солей и желатина.
Стерильные растворы для инъекций могут быть приготовлены путем включения активного соединения в необходимом количестве в подходящем растворителе с одним или комбинацией перечисленных выше агентов, как требуется, с последующей стерилизационной микрофильтрацией. Обычно дисперсии готовят путем включения активного соединения в стерильный носитель, который содержит основную дисперсионную среду и требуемые другие агенты из перечисленных выше. В случае стерильных порошков для приготовления стерильных растворов для инъекций методы приготовления представляют собой вакуумную сушку и сушку замораживанием (лиофилизация), которые дают порошок активного агента плюс любой дополнительный желаемый агент из его предварительно стерильно отфильтрованного раствора.
Количество активного агента, которое можно комбинировать с материалом-носителем для получения единичной дозированной формы, будет варьироваться в зависимости от субъекта, которого лечат, и конкретного способа введения. Количество активного агента, которое можно комбинировать с материалом-носителем для получения единичной дозированной формы, обычно будет таким количеством композиции, которое оказывает терапевтический эффект. Как правило, из ста процентов это количество будет находиться в диапазоне от 0,01 до девяноста девяти процентов активного агента, от 0,1 до 70 процентов или от 1 до 30 процентов активного агента в сочетании с фармацевтически приемлемым носителем.
Режимы и дозировки подбираются так, чтобы обеспечить оптимальный желаемый отклик (например, терапевтический ответ). Например, может быть введена одна таблетка, несколько разделенных доз могут вводиться в течении определенного времени, или доза может быть пропорционально уменьшена или увеличена, как показано в зависимости от терапевтической ситуации. Особенно эффективно составлять парентеральные композиции в единичной дозированной форме для простоты введения и единообразия дозировки. Используемая здесь единичная лекарственная форма относится к физически дискретным единицам, подходящим в качестве единичных доз для субъектов, подлежащих лечению; каждая единица содержит заданное количество активного соединения, рассчитанное для получения желаемого терапевтического эффекта в сочетании с необходимым фармацевтическим носителем. Технические требования для единичных дозированных форм раскрытия изобретения продиктованы и напрямую зависят от уникальных характеристик активного соединения и конкретного терапевтического эффекта, который должен быть достигнут, а также от ограничений, присущих технике приготовления такого активного соединения для лечения чувствительность у людей.
В содержащей антитело композиции для введения дозировка антитела составляет от около 0,0001 до около 100 мг/кг, и более предпочтительно от около 0,01 до около 30 мг/кг массы тела хозяина. Например, дозировки составляют около 1 мг/кг массы тела, около 3 мг/кг массы тела, около 5 мг/кг массы тела или около 10 мг/кг массы тела в пределах диапазонов около 1-10 мг/кг, например, около 1,2, 3, 4, 5, 6, 7, 8, 9, 10 мг/кг массы тела. Дозировки повторяются по мере необходимости и могут находиться в диапазоне от примерно одного раза в неделю до примерно одного раза каждые 10 недель, например, одного раза каждые 4-8 недель. Однако, в зависимости от состояния, может использоваться пульс-терапия, где, например, одна инъекция антагониста рецептора Actll вводится пациенту с острым обострением сердечной недостаточности, например, в отделении неотложной помощи.
Введение предпочтительно проводится внутривенно. Режимы дозировок для антитела против ActRII по изобретению, например, бимагрумаба, включают примерно 1 мг/кг массы тела, или примерно 3 мг/кг массы тела, или примерно 10 мг/кг массы тела, один раз каждые четыре недели при внутривенном введении.
В некоторых способах в композициях по изобретению содержатся два или более моноклональных антитела с различной специфичностью связывания и, таким образом, вводятся одновременно, и в этом случае дозировка каждого вводимого антитела попадает в указанные диапазоны. Антитело обычно вводят несколько раз. Интервалы между однократными дозами могут составлять, например, еженедельно, ежемесячно, каждые три месяца, каждые шесть месяцев или ежегодно. Интервалы также могут быть нерегулярными, на что указывает измерение уровня антител в крови к целевому антигену у пациента. В некоторых способах дозу корректируют до достижения концентрации антител в плазме от примерно 1 до примерно 1000 мкг/мл, а в некоторых способах от примерно 25 до примерно 300 мкг/мл. Например, антитело ActRII по изобретению может быть введено совместно с антителом против миостатина.
Дозировка и частота варьируются в зависимости от периода полураспада антитела у конкретного пациента. В целом, человеческие антитела показывают самый длинный период полураспада, за которым следуют гуманизированные антитела, химерные антитела и антитела нечеловеческого происхождения. Дозировка и частота введения могут варьироваться в зависимости от того, является ли лечение профилактическим или терапевтическим. В профилактических целях относительно низкие дозы вводятся с относительно редкими интервалами в течение длительного периода времени. Некоторые пациенты продолжают получать лечение до конца своей жизни. В терапевтических применениях иногда требуется относительно высокая доза с относительно короткими интервалами до тех пор, пока прогрессирование заболевания не уменьшится или не прекратится, или пока пациент не покажет частичное или полное улучшение симптомов заболевания. После этого пациенту может быть назначен профилактический режим.
Введение «терапевтически эффективной дозировки» антитела против ActRII, содержащегося в композициях по настоящему изобретению, может привести к уменьшению выраженности симптомов заболевания, увеличению частоты и продолжительности периодов без симптомов заболевания или предотвращению нарушения или инвалидности из-за болезни, то есть увеличению сердечной функции.
Активные соединения могут быть получены с носителями, которые будут защищать соединение от быстрого высвобождения, такими как состав с контролируемым высвобождением, включая имплантаты, трансдермальные пластыри и микрокапсулированные системы доставки. Могут быть использованы биоразлагаемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие способы получения таких составов запатентованы или общеизвестны специалистам в данной области. Смотрите, например, Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
Терапевтические композиции можно вводить с помощью медицинских устройств, известных в данной области.
Применение и используемые методы
Композиции по настоящему изобретению и описанные антитела имеют терапевтическое применение, поскольку они оказывают влияние на лечение заболеваний сердца или на улучшение состояния пациентов, пораженных заболеваниями сердца, или на уменьшение симптомов, связанных с заболеванием сердца.
Термин «субъект» или «индивидуум», используемый в данном документе, предназначен для обозначения человека и нечеловекоподобных животных. К нечеловекоподобным животным относятся все позвоночные, например, млекопитающие и не млекопитающие, такие как нечеловекоподобные приматы, овцы, собаки, кошки, мыши, коровы, лошади, цыплята, земноводные и рептилии.
Следовательно, изобретение также относится к способам лечения, в которых композиции по изобретению или описанные антагонисты рецептора ActRII, например, молекулы, связывающие ActRII, более предпочтительно антитела к ActRII, например, бимагрумаб или BYM338, ингибируют, т.е. противодействуют функции ActRII и тем самым приводят к улучшению состояния при различных видах сердечных заболеваний. Раскрытие изобретения предлагает способ предотвращения и/или лечения сердечнососудистых заболеваний, включающий введение терапевтически эффективного количества антагониста рецептора ActRII, например, предпочтительно молекулы, связывающей ActRIIB, более предпочтительно антитела-антагониста к ActRIIB, например бимагрумаба или BYM338, или описанных композиций пациенту.
Примерами антагонистов рецепторов ActRII, например, связывающих ActRII молекул, предпочтительно антител антагонистов к ActRIIB, например, бимагрумаба или BYM338, которые можно использовать в раскрытых способах лечения, являются те, которые раскрыты или подробно описаны выше. В определенных вариантах осуществления антитела к ActRII (например, бимагрумаб или BYM338) содержатся в раскрытых здесь композициях изобретения.
Изобретение также относится к применению антагониста рецептора ActRII, например, молекулы, связывающей рецептор ActRIIA или ActRIIB, предпочтительно антитела-антагониста к ActRII, например BYM338, в производстве лекарственного средства для лечения различных форм заболеваний сердца, как описано выше.
Связывающая ActRII молекула, предпочтительно антитело-антагонист к ActRII, например, бимагрумаб или BYM338, может вводиться в качестве единственного активного агента или в сочетании с, например, в качестве адъюванта или в сочетании с другими лекарственными средствами, например IGF-1, IGF-2 или вариантами IGF-1 или IGF-2, антимиостатиновыми антителами, миостатиновым пропептидом, миостатиновым белком-ловушкой, который связывает ActRIIB, но не активирует его, агонистом бета 2, агонистом грелина, SARM, агонистами/миметиками GH или фоллистатином. Например, антагонисты изобретения могут быть использованы в комбинации с миметиком IGF-1, как раскрыто в WO 2007/146689.
В соответствии с вышеизложенным настоящее раскрытие изобретения обеспечивает в еще одном дополнительном аспекте способ или использование, как определено выше, включающее совместное управление, например, одновременно или последовательно терапевтически эффективного количества антагониста рецептора ActRII, предпочтительно молекулы, связывающей ActRII, более предпочтительно антитела-антагониста к ActRII, например бимагрумаба или BYM338, и по меньшей мере одного второго лекарственного вещества, причем указанное второе лекарственное вещество представляет собой IGF-1, IGF-2 или варианты IGF-1 или IGF-2, анти-миостатиновые антитела, миостатиновый пропептид, миостатиновый белок-ловушка, который связывает ActRII, но не активирует его, агонист бета 2, агонист грелина, SARM, агонисты/миметики GH или фоллистатин.
Наборы
Изобретение также охватывает наборы, которые могут содержать антагонист рецептора ActRII, например, связывающую рецептор ActRII молекулу (например, антитело рецептора ActRII или его антигенсвязывающий фрагмент, например, бимагрумаб или BYM338) или связывающую рецептор ActRII (т.е. рецептор ActRII В) молекулу (например, антитела против ActRIIB или его антигенсвязывающий фрагмент) (например, в жидкой или лиофилизированной форме) или фармацевтическую композицию, содержащую антагонист рецептора ActRII (описано выше). Кроме того, такие наборы могут содержать средства для введения антагониста ActRII (например, шприц и флакон, предварительно заполненный шприц, предварительно заполненный шприц-флакон) и инструкции по применению. Эти наборы могут содержать дополнительные терапевтические агенты (описанные выше), например, для доставки в комбинации с прилагаемым антагонистом ActRII, например, BYM338.
Фраза «средство для введения» используется для обозначения любого доступного инструмента для системного введения лекарственного средства пациенту, включая, но не ограничиваясь этим, предварительно заполненный шприц, флакон и шприц, инъекционную ручку, автоинъектор, внутривенную капельница и сумку, насос и т.д. С такими предметами пациент может самостоятельно вводить лекарство (т.е. вводить лекарство от своего имени), или лекарство может ввести врач.
Каждый компонент набора обычно заключен в отдельный контейнер, и все различные контейнеры находятся в одной упаковке вместе с инструкциями по применению.
ПОСЛЕДОВАТЕЛЬНОСТИ
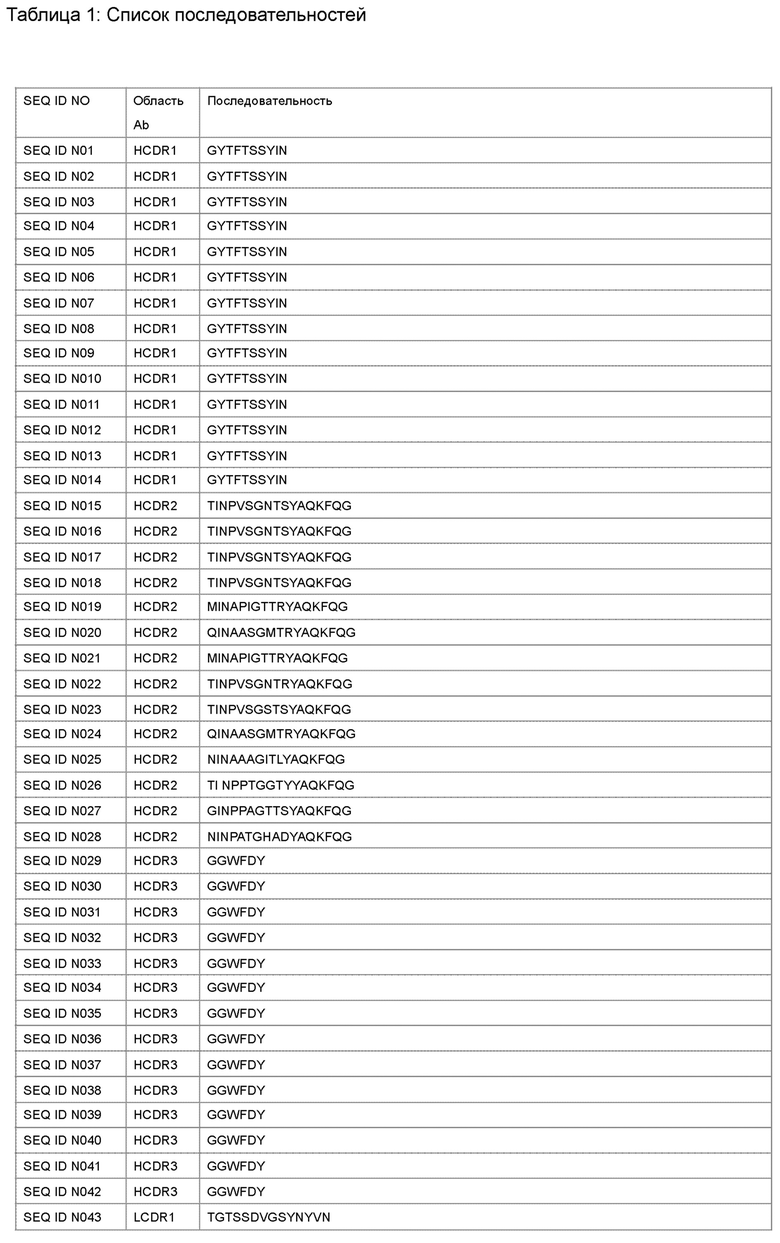
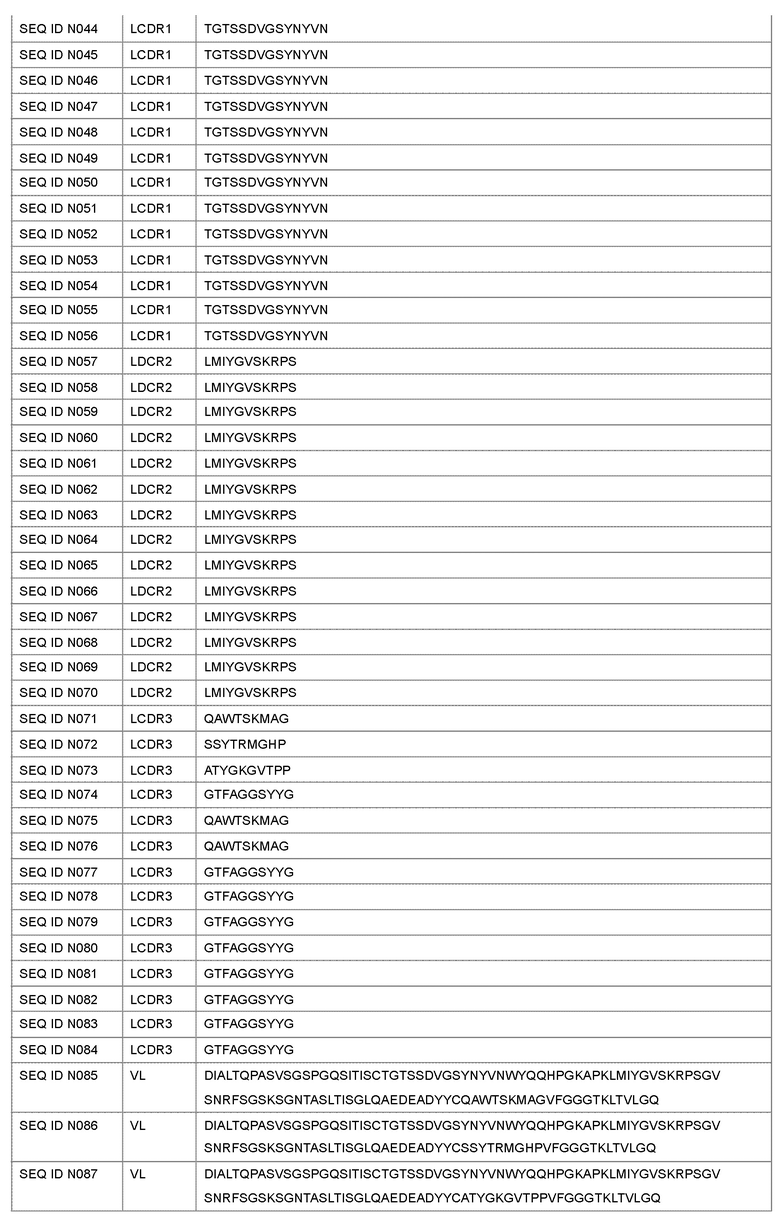
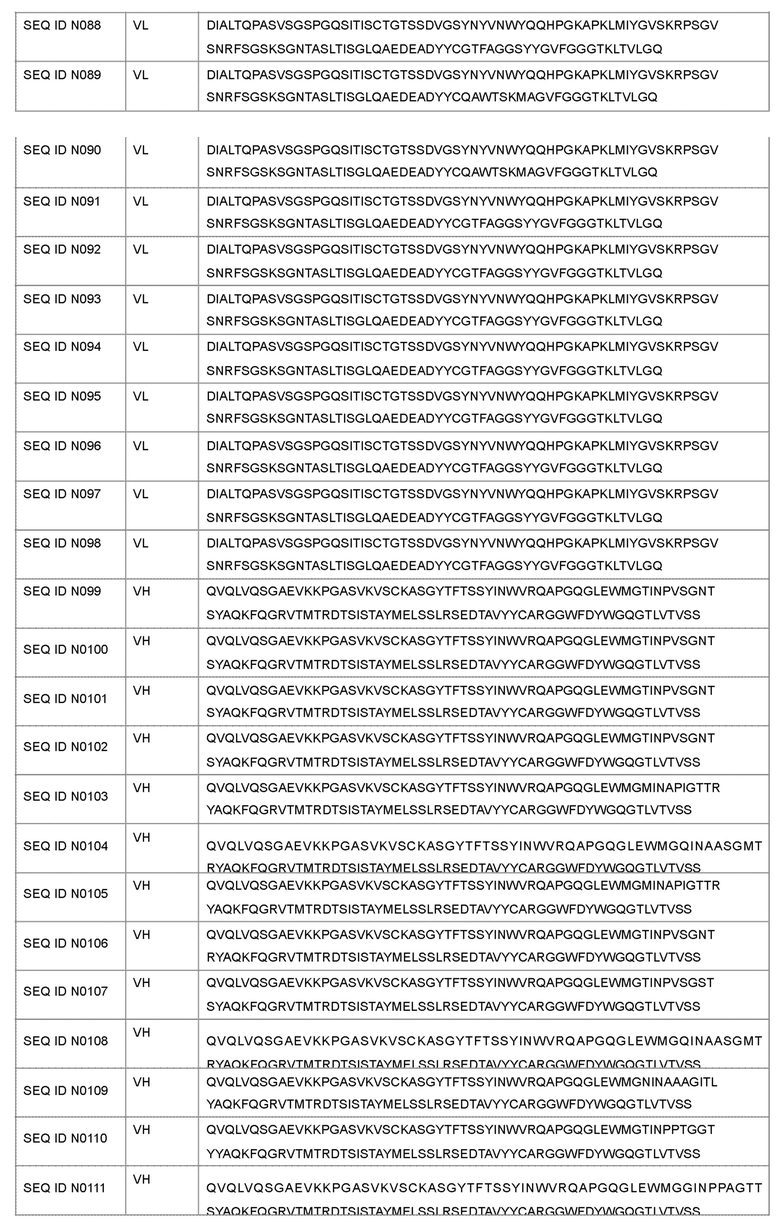
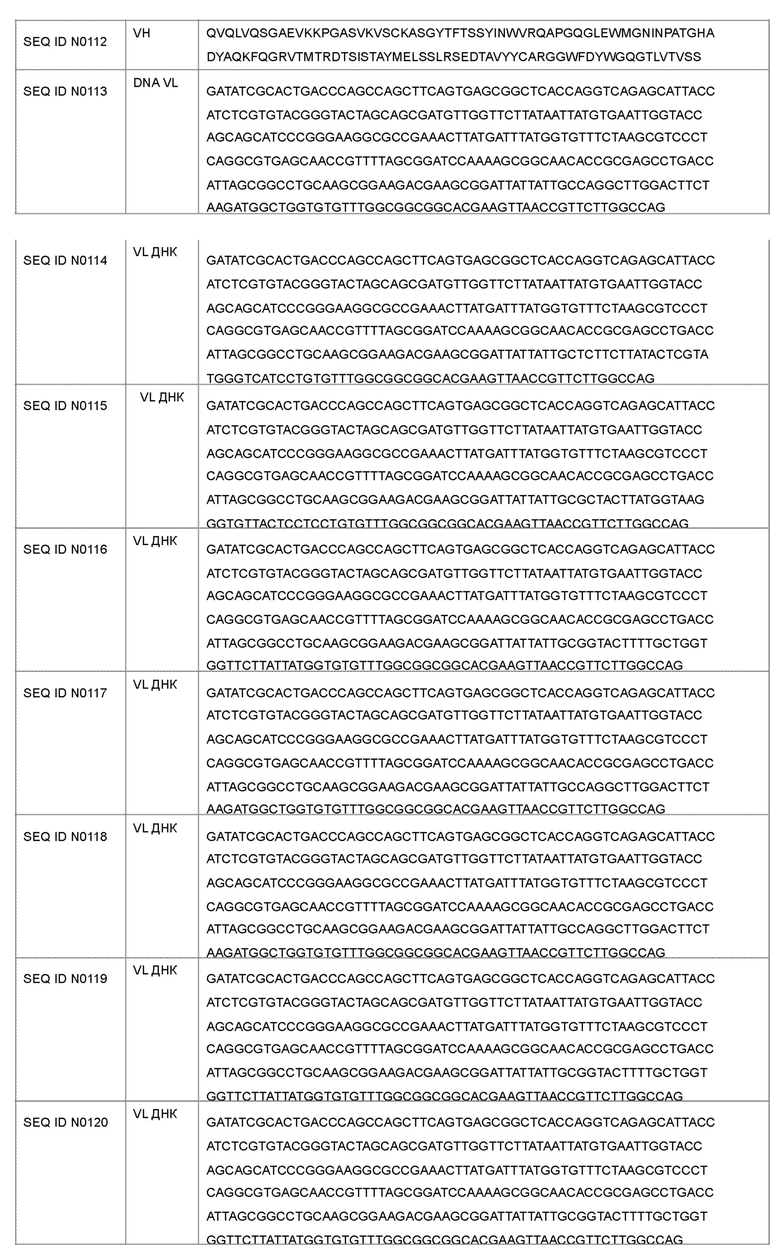
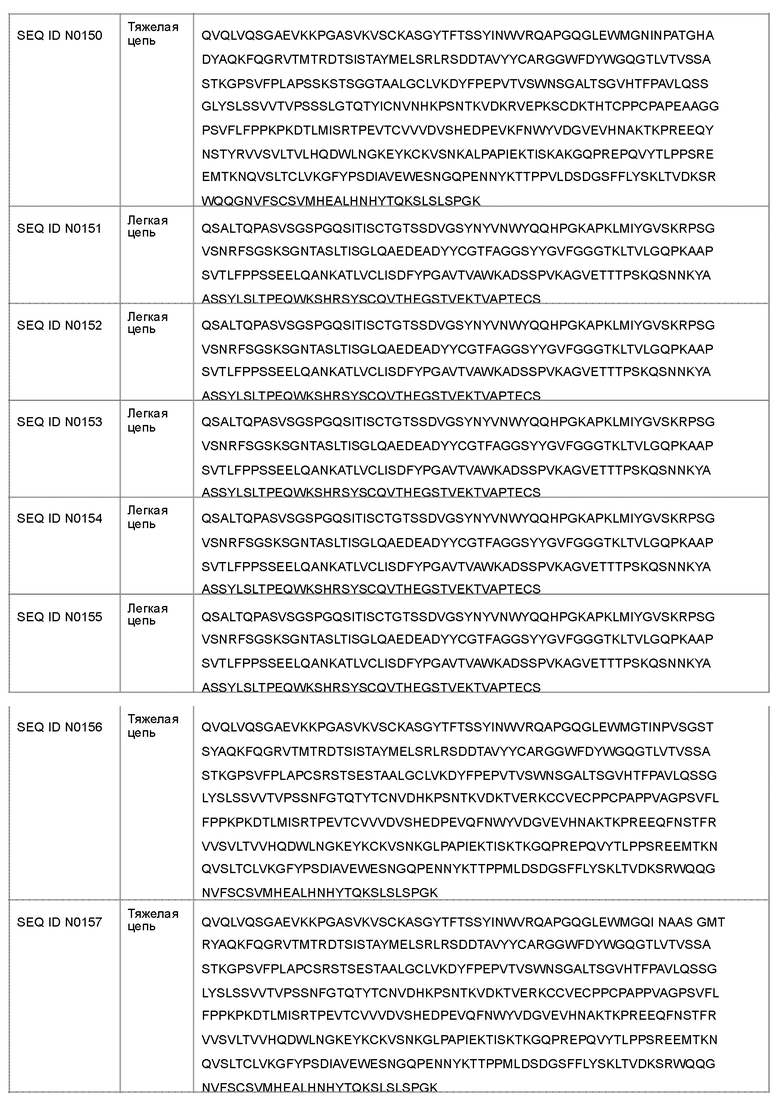
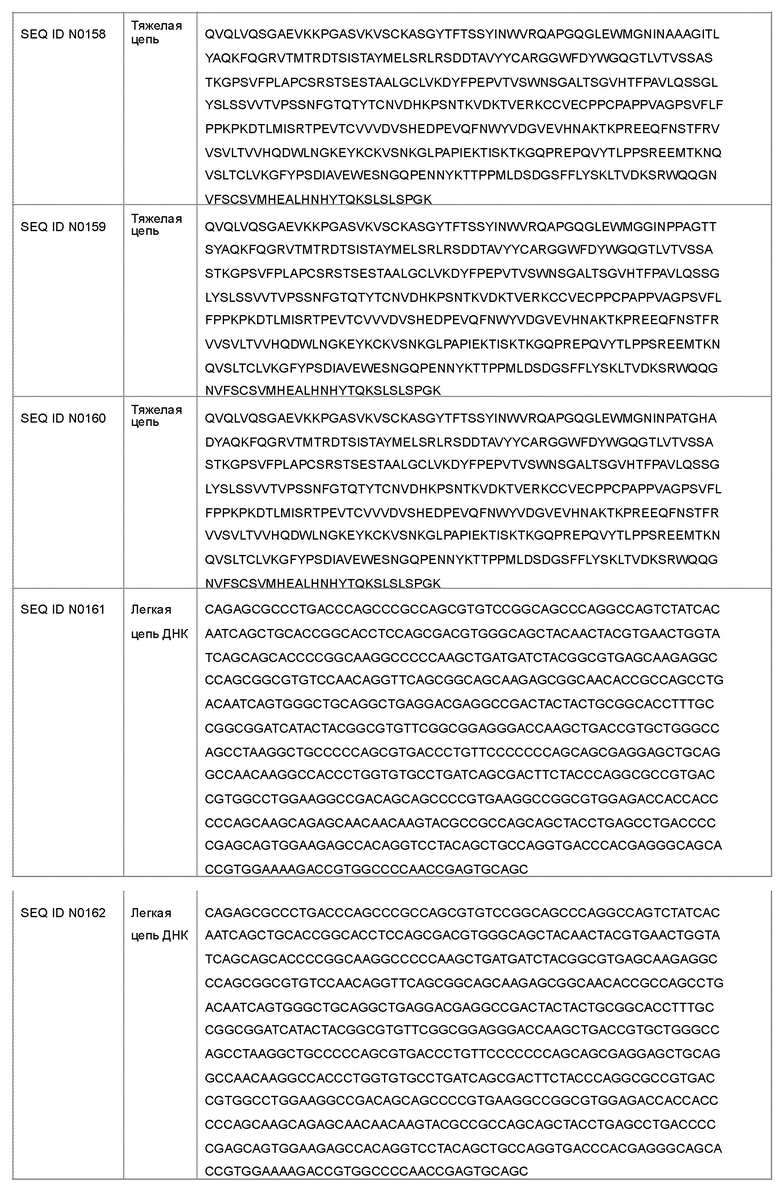
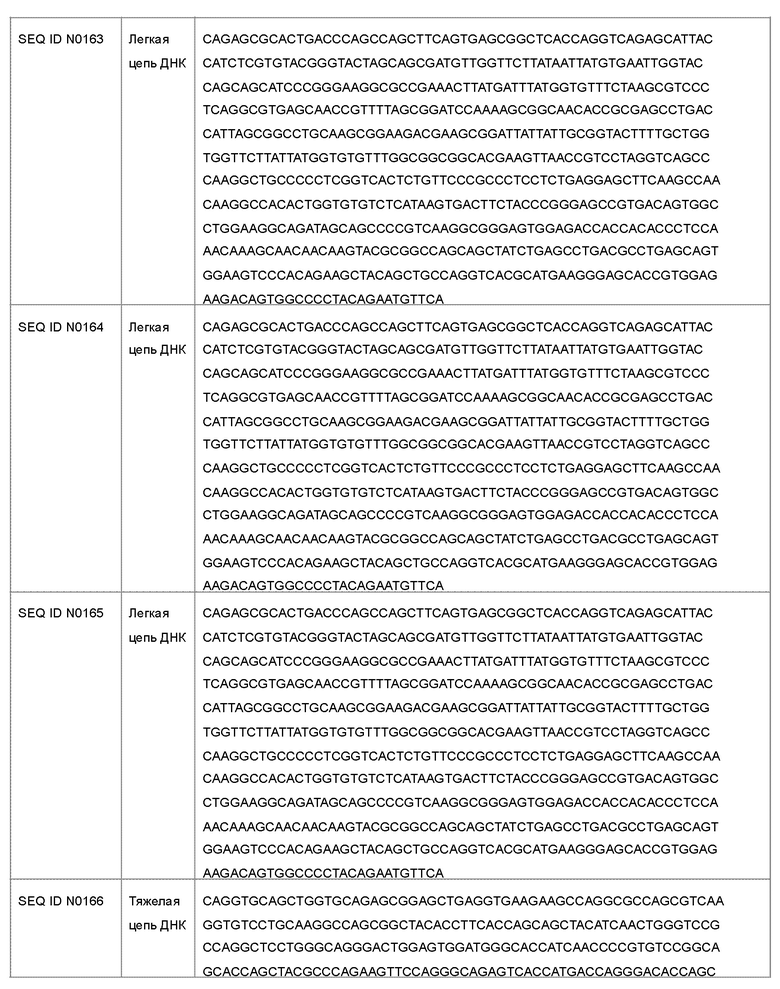


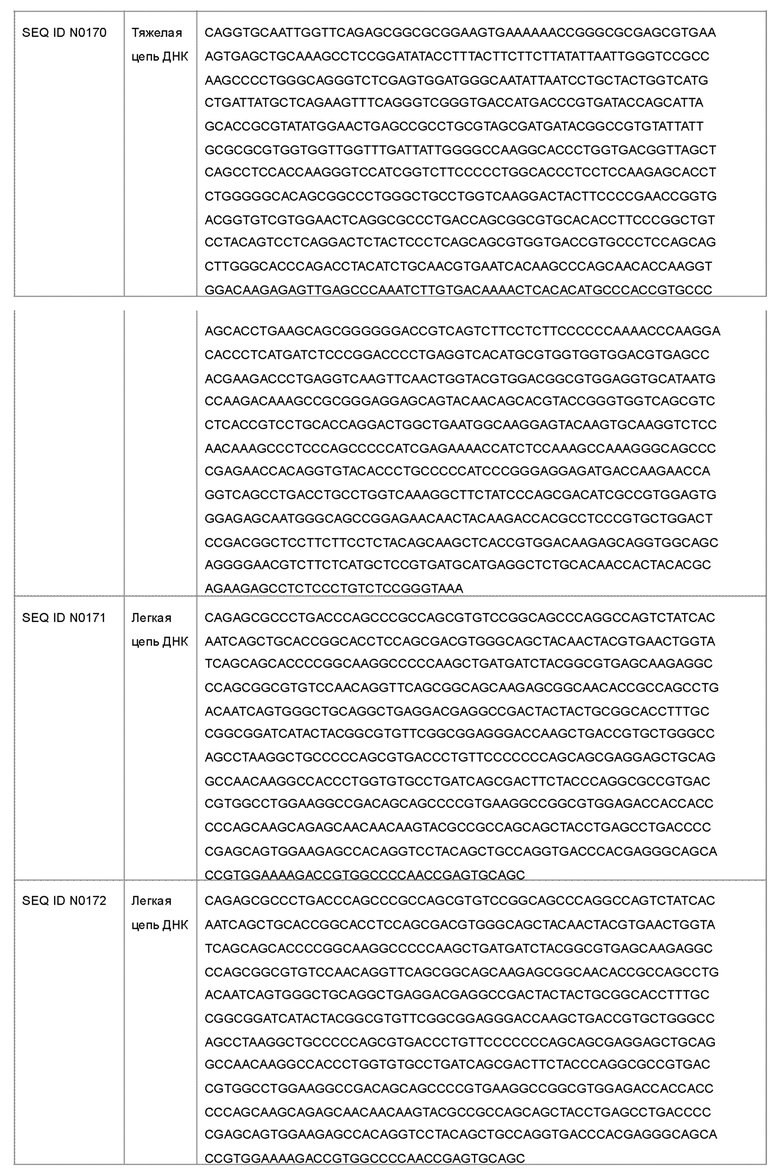


В вариантах осуществления описанных методов, способов лечения, режимов, применений и наборов по изобретению используется антагонист рецептора ActRII, например, связывающая молекула ActRIIB. В других вариантах осуществления связывающая ActRIIB молекула представляет собой антитело-антагонист к ActRIIB.
В некоторых вариантах осуществления описанных методов, способов лечения, режимов, применений и наборов антитело против ActRIIB выбрано из группы, состоящей из:
а) антитела против ActRIIB, которое связывается с эпитопом ActRIIB, содержащим SEQ ID NO: аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID NO: 188);
(b) аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID NO: 186);
(c) аминокислоты 75-85 SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID NO: 190);
(d) аминокислоты 52-56 SEQ ID NO: 181 (EQDKR-SEQ ID NO: 189);
(e) аминокислоты 49-63 SEQ ID NO: 181 (CEGEQDKRLHCYASW - SEQ ID NO: 187);
(f) аминокислоты 29-41 SEQ ID NO: 181 (CIYYNANWELERT- SEQ ID NO: 191);
(g) аминокислоты 100-110 SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID NO: 192); или же
(h) аминокислоты 78-83 of SEQ ID NO: 181 (WLDDFN) и аминокислоты 52-56 SEQ ID NO: 181 (EQDKR); а также
b) антитела-антагониста к ActRIIB, которое связывается с эпитопом ActRIIB, содержащим аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN - SEQ ID NO: 188);
(b) аминокислоты 76-84 SEQ ID NO: 181 (GCWLDDFNC - SEQ ID NO: 186);
(c) аминокислоты 75-85 of SEQ ID NO: 181 (KGCWLDDFNCY - SEQ ID NO: 190);
(e) аминокислоты 52-56 of SEQ ID NO: 181 (EQDKR-SEQ ID NO: 189);
(f) аминокислоты 49-63 of SEQ ID NO: 181 (CEGEQDKRLHCYASW-SEQ ID NO: 187);
(f) аминокислоты 29-41 of SEQ ID NO: 181 (CIYYNANWELERT-SEQ ID NO: 191);
(g) аминокислоты 100-110 of SEQ ID NO: 181 (YFCCCEGNFCN - SEQ ID NO: 192); или же
(h) аминокислоты 78-83 SEQ ID NO: 181 (WLDDFN) and аминокислоты 52-56 SEQ ID NO: 181 (EQDKR), где антитело имеет KD около 2 пМ.
В некоторых вариантах воплощения методов, способов лечения, режимов, применений и наборов по изобретению антитело-антагонист к ActRIIB представляет собой человеческое антитело.
В некоторых вариантах воплощения методов, способов лечения, режимов, применений и наборов по изобретению антитело представляет собой бимагрумаб или BYM338.
Детали одного или нескольких вариантов осуществления изобретения изложены в прилагаемом описании выше. Любые способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе, могут быть использованы на практике или при тестировании настоящего изобретения. Другие признаки, объекты и преимущества изобретения будут очевидны из описания и формулы изобретения. В описании и прилагаемой формуле изобретения формы единственного числа включают ссылки на множественное число, если контекст явно не предписывает иное. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области техники, к которой относится это изобретение. Все патенты и публикации, процитированные в описании, включены в настоящее изобретение посредством ссылки. Следующие примеры предназначены, чтобы более полно проиллюстрировать раскрытие изобретения и никоим образом не ограничивают его объем.
ПРИМЕРЫ
Общая методология
Антитела ActRIIB, их характеристика и связанные с ними методы, такие как (i) функциональные анализы, (ii) анализы по гену REPORTER (RGA), (iii) культивирование клеточных линий HEK293T/17, (iv) анализы генов репортерной люциферазы, индуцированной миостатином, (v) СПЕЦИФИЧНОСТЬ ELISA, (vi) ELISA взаимодействия связывания ActRIIB / Fc-миостатина, (vii) Титрование FACS на клетках, экспрессирующих hActRIIB- и hActRIIA, (viii) Связывание с первичными клетками скелетных мышц человека, (ix) Определение аффинности выбранных анти-человеческих фабов ActRIIB с использованием поверхностного плазмонного резонанса (Biacore), (х) СК-АНАЛИЗ, (xi) Модели на животных, (xii) ПРОТОКОЛЫ ЛЕЧЕНИЯ, (xiii) Статистический анализ, (xiiii) пэннинг, (xv) идентификация и характеристика антител, (xvi) Оптимизация антител, полученных из первого созревания аффинности, (xvii) Конверсия IgG2 фабов с созревшей аффинностью (1-е созревание), (XVIII) Второе созревание аффинности, (хх) конверсия IgG2 и характеристика IgG2 (2-е созревание), (xxi) Характеристика антитела против ActRIIB в исследовании мышей in vivo, (xxii) подтверждение сродства с помощью SET, (xxiii) исследования перекрестного блокирования и (xxiv) детали и технологии картирования эпитопов были раскрыты в WO 2010/125003.
Экспериментальная модель ТАС (поперечное сужение аорты) у мыши является широко используемой экспериментальной моделью для гипертрофии сердца и сердечной недостаточности, вызванной перегрузкой давлением, и описана, например, в Rockman et al. (1991) и deAlmeida et al. (2010), которые включены сюда посредством ссылки, как если бы они были полностью изложены в данном документе.
Пример 1: Исследование по профилактике ТАС
Материалы и методы:
В этом исследовании проверяется, предотвращает ли CDD866 развитие сердечной дисфункции в используемой мышиной модели сердечной недостаточности с поперечным сужением аорты (ТАС).
Следующие 4 группы самцов в возрасте 16-недель C57BL/6 мышей (n=7-10/группе) являются частью исследования:
1. SHAM + Изотип Ab
2. SHAM + CDD866 Ab
3. TAC + Изотип Ab
4. TAC + CDD866 Ab
Антитело вводят подкожно (SQ), 20 мг/кг, один раз в неделю, причем последняя доза вводится менее чем за 24 часа до умерщвления.
Эхокардиография проводится каждые две недели.
Основной конечный показатель: предварительно заданный конечный показатель 11-недельного периода после ТАС или % фракции сокращения (FS)<20%.
Результаты:
Как показано на фигурах 1А-1Е, лечение Ab CDD866 имеет минимальные сердечные эффекты у мышей дикого типа C57BL/6. В частности, как показано на фиг. 1А, измеренные уровни CDD866 в плазме подтверждают, что лекарственное средство вводили надлежащим образом. CDD866 несущественно увеличивает сердечную массу (Фигура 1 В). CDD866 уменьшает фиброз миокарда (фиг. 1С), хотя % фиброза был заметно низким в начале исследования у здоровых контролей дикого типа.
Репрезентативные микрофотографии окрашенного PAS миокарда (фиг. 1D) подчеркивают размер кардиомиоцитов. Фигура 1Е наглядно изображает обнаружение того, что CDD866 незначительно увеличивает размер кардиомиоцитов у животных дикого типа. Данные представлены как среднее + стандартное отклонение. Серый = контрольная группа, изотип Ab (n=3). Черный = Экспериментальная группа, CDD866 Ab (n=3). * р<0,05
Как показано на фиг. 2A-2D, лечение CDD866 предотвращает ТАС-индуцированную сердечную недостаточность у мышей. На фиг. 2А наглядно изображено, что систолическая функция (измеренная в % от полной шкалы), как ожидается, уменьшается с ТАС (горизонтальная полоса), но сохраняется у животных, обработанных CDD866, подвергнутых ТАС (диагональная полоса). Фиг. 2В - репрезентативные эхокардиографические изображения после 11 недель операции SHAM или ТАС, которые демонстрируют сохранение систолической функции у животных ТАС, получавших CDD866. Существует тенденция к снижению веса легких у животных, получавших CDD866, что указывает на меньшую легочную гиперемию (суррогат сердечной недостаточности на мышиной модели (фиг. 2С)). При лечении CDD866 наблюдается значительное снижение основного конечного показателя (выживаемость или % FS <20%). (фиг. 2D). Данные представлены в виде среднего + стандартное отклонение. Черный = SHAM + изотип Ab (n=7). Серый = SHAM + CDD866 Ab (n=7). Горизонтальная полоса = ТАС + изотип Ab (n=10 Диагональная полоса = ТАС + CDD866 Ab (n=10). * р<0,05. # р <0,01 (черный цвет обозначает сравнение с группой SHAM + изотип, красный цвет обозначает сравнение с группой ТАС + изотип.
Как показано на фиг. 3A-3D, CDD866 Ab эффективно блокирует передачу сигналов ActRII-A/B в модели ТАС при сердечной недостаточности. На фиг. 3 (А) измеренные уровни CDD866 в плазме указывают на то, что лекарственное средство вводят надлежащим образом. Сердечная фоллистатиноподобная экспрессия 3 (FSTL3) увеличивается с ТАС, указывая на то, что передача сигналов ActRII-A/B сердца увеличивается в этой модели повреждения сердца. Лечение CDD866 снижает сердечную экспрессию FSTL3, указывая на то, что оно эффективно блокирует ТАС-индуцированную передачу сигналов ActRII-A/B в сердце (фиг. 3В). Экспрессия патологических генов гипертрофии сердца уменьшается при лечении CDD866 (фиг. 3С). Как показано на фигуре 3D, патологический профиль фиброза сердца при ТАС-индуцированной сердечной недостаточности снижается при лечении CDD866. Данные представлены как среднее + стандартное отклонение
Черный = SHAM + изотип Ab (n=7). Серый = SHAM + CDD866 Ab (n=7). Горизонтальная линия = ТАС + изотип Ab (n=10). Диагональная линия = ТАС + CDD866 Ab (n=10). * р<0,05. # р<0,01 (черный цвет обозначает сравнение с группой SHAM + изотип, красный цвет обозначает сравнение с группой ТАС + изотип.
Подводя итог, (i) CDD866 оказывает минимальное влияние на сердечный рост/функцию в контроле дикого типа; (ii) CDD866 эффективно предотвращает развитие сердечной недостаточности, вызванной ТАС, и (iii) CDD866 улучшает общую выживаемость в модели сердечной недостаточности ТАС.
Пример 2: Исследование по лечению ТАС
Материалы и методы:
В этом исследовании проверяется, может ли CDD866 спасти животных от сердечной недостаточности путем устранения установленной сердечной дисфункции у животных, подвергшихся воздействию ТАС.
Были исследованы следующие 2 группы 16-недельных самцов мышей C57BL/6 (n=10 / группа):
ТАС + Изотип Ab
ТАС + CDD866 Ab
Лечение антителами начинают только после уменьшения % дробного сокращения >4 стандартных отклонений.
Антитело вводят SQ, 20 мг/кг/нед., в течение 8 недель (последняя доза вводится менее чем за 24 часа до умерщвления).
Эхокардиография проводится каждые две недели.
Основной конечный показатель: предварительно заданный показатель 8-недельного лечения или % FS <25%.
Результаты:
На фиг. 4A-4D показано, что лечение CDD866 восстанавливает сердечную функцию и спасает животных от ТАС-индуцированной сердечной недостаточности. Измеренные уровни CDD866 в плазме указывают на то, что лекарственное средство вводится надлежащим образом с систолической функцией (фиг. 4А). 4В наглядно изображает обнаружение того, что сердечная экспрессия FSTL3 снижается при обработке CDD866, указывая на то, что она эффективно блокирует ТАС-индуцированную передачу сигналов ActRII-A/B в сердце. CDD866 устраняет систолическую дисфункцию при ТАС-индуцированной сердечной недостаточности, и это наблюдается уже через 1 неделю после лечения с прогрессирующим улучшением (фиг. 4С). CDD866 также уменьшает вес легких, суррогатный маркер сердечной недостаточности на мышиной модели (фиг. 4D). Данные представлены как среднее + стандартное отклонение. Серый = ТАС + изотип Ab Черный = ТАС + CDD866 Ab. * р <0,05. # р <0,01.
Лечение CDD866 вызывает сердечный рост в модели ТАС. На фиг. 5А наглядно изображено, что при обработке CDD866 толщина стенки постепенно увеличивается (черная стрелка указывает на начало Rx). На фиг. 5В показаны последовательные эхо-изображения срезов, имеющим отношение к средним отделам желудочка во время курса лечения, демонстрирующие различия в росте сердца у изотипов по сравнению с животными, получавшими CDD866. CDD866 увеличивает сердечную массу в модели ТАС, как показано на фиг. 5С. На фиг. 5D представлены микрофотографии окрашенного PAS миокарда с выделением размера кардиомиоцитов. CDD866 также увеличивает рост кардиомиоцитов в ТАС (фиг. 5Е). Данные представлены как среднее + стандартное отклонение. Серый = ТАС + изотип Ab. Черный = ТАС + CDD866 Ab. * р <0,05. # р <0,01.
Результаты также показывают, что CDD866 индуцирует физиологический рост сердца, который является защитным средством при сердечной недостаточности. На фиг. 6А показано, что экспрессия генов, связанных с патологической гипертрофией, снижается при лечении CDD866. Эффекты CDD866 на сердечный рост и массу тела являются временными и обратимыми, как показано на фиг. 6В. Улучшения сердечной функции, вызванные однократной дозой CDD866, сохраняются в течение не менее 6 недель. (Стрелка на фиг. 6В = время приема одной дозы; пунктирная линия = ожидаемая траектория без лечения CDD866). На фиг. 6С представлены микрофотоснимки миокарда, окрашенного трихромом по Массону (синий = фиброз; красный = мышца). Существует тенденция к снижению фиброза миокарда при лечении CDD866, как показано на фиг. 6D. Данные представлены как среднее + стандартное отклонение. Серый = ТАС + изотип Ab. Черный = ТАС + CDD866 Ab. * р <0,05. # р <0,01.
CDD866 индуцирует рост скелетных мышц при ТАС-опосредованной сердечной недостаточности, как показано на фиг. 7А-7Е. CDD866 снижает экспрессию p-SMAD3 в скелетных мышцах, указывая на то, что он эффективно блокирует передачу сигналов ActRII А/В в скелетных мышцах в этой модели сердечной недостаточности (фиг. 7А). CDD866 постепенно увеличивает общую массу тела; скорее всего, через увеличение мышечной массы (фиг. 7В). На фиг. 7С показано, что CDD866 увеличивает общую массу различных групп скелетных мышц (EDL, gas, ТС). Размер скелетных миоцитов также увеличивается с помощью CDD866 (фиг. 7D). Переключение типа волокна в скелетных мышцах также индуцируется CDD866 (фиг. 7Е). Красный = ТАС + изотип Ab. Синий = ТАС + CDD866 Ab. * р <0,05. # р <0,01.
Подводя итог, CDD866 эффективно устраняет установленную систолическую дисфункцию, вызванную ТАС. CDD866 увеличивает сердечный рост и уменьшает фиброз миокарда, данные указывают на физиологическую гипертрофию сердца, которая является защитной при сердечной недостаточности.
CDD866 увеличивает рост скелетных мышц в модели ТАС сердечной недостаточности, указывая на его использование для улучшения сердечного истощения при распространенной сердечной недостаточности.
Пример 3: исследование временной точки MHCF764L
Материалы и методы:
Это исследование проверяет, может ли CDD866 улучшить сердечную функцию в генетической модели дилатационной кардиомиопатии (MHCF764L).
Исследованы 2 группы мышей-самцов МНС F764L +/- в возрасте 14-24 недель:
Изотип Ab (n=3)
CDD866 Ab (n=3)
Антитело вводят SQ, 20 мг/кг/нед в течение 12 недель (последняя доза вводится менее чем за 24 часа до умерщвления).
Эхокардиография проводится каждые две недели (q2wk).
Основной конечный показатель: предварительно определенный показатель 12-недельного лечения или % FS <20%
Результаты:
CDD866 обладает минимальными сердечными эффектами в модели генетической дилатационной кардиомиопатии (хотя умеренный фенотип сердца только на начальном уровне). На фиг. 8А наглядно изображено, что CDD866 индуцирует тенденцию к умеренно повышенной систолической функции у мышей MHCF74L. Фиг. 8В иллюстрирует тенденцию к снижению экспрессии FSTL3 в сердце при лечении CDD866, указывая на то, что он эффективно блокирует передачу сигналов ActRII-A/B в сердце. Как показано на фиг. 8С, значительного различия в профиле экспрессии гена патологической гипертрофии не наблюдается. Данные представлены как среднее + стандартное отклонение. Серый = Изотип Ab. Черный = CDD866 Ab. * р <0,05. # р <0,01.
Подводя итог, можно сказать, что при лечении CDD866 наблюдается небольшое увеличение систолической функции. Существенных различий в профилях экспрессии генов сердечной недостаточности не обнаружено.
Список литературы
Akpan I, Goncalves MD, Dihr R, Yin X, Pistilli E, Bogdanovich S, Khurana, T, Ucran, J, Lachey, J, Ahima, RS. The effects of a soluble activin type 11В receptor on obesity and insulin sensitivity. Int J Obes (Lond) 2009 Nov; 33(11):1265-1273.
deAlmeida AC, van Oort RJ, Wehrens XH. Transverse aortic constriction in mice. J Vis Exp 2010 Apr 21; (38). http://www.iove.com/detaiis.php?id=1729. doi: 10.3791/1729.
Lee SJ, McPherron AC. Regulation of myostatin activity and muscle growth. Proc Natl Acad Sci USA. 2001 Jul 31; 98(16):9306-11.
Lee SJ, Reed LA, Davies MV, Girgenrath S, Goad ME, Tomkinson KN, Wright JF, Barker C, Ehrmantraut G, Holmstrom J, Trowell B, Gertz B, Jiang MS, Sebald SM, Matzuk M, Li E, Liang LF, Quattlebaum E, Stotish RL, Wolfman NM. Regulation of muscle growth by multiple ligands signaling through activin type II receptors. Proc Natl Acad Sci USA. 2005 Dec 13; 102(50): 18117-22.
Rebbapragada A, Benchabane H, Wrana JL, Celeste AJ, Attisano L. Myostatin signals through a transforming growth factor beta-like signaling pathway to block adipogenesis. Mol Cell Biol. 2003; 23:7230-7242.
Rockman HA, Ross RS, Harris AN, Knowlton KU, Steinhelper ME, Field LJ, Ross Jr. J, Chien KR. Segregation of atrial-specific and inducible expression of an atrial natriuretic factor transgene in an in vivo murine model of cardiac hypertrophy. Proc Natl Acad Sci USA. 1991 September; 88:8277-8281.
Whittemore LA, Song K, Li X, Aghajanian J, Davies M, Girgenrath S, Hill JJ, Jalenak M, Kelley P, Knight A, Maylor R, O'Hara D, Pearson A, Quazi A, Ryerson S, Tan XY, Tomkinson KN, Veldman GM, Widom A, Wright JF, Wudyka S, Zhao L, Wolfman NM. Inhibition of myostatin in adult mice increases skeletal muscle mass and strength. Biochem Biophys Res Commun. 2003 Jan 24; 300(4):965-71.
--->
Перечень последовательностей
SEQUENCE LISTING
<110> Novartis AG
Beth Israel Deaconess Medical Center, Inc
<120> Methods for Preventing and Treating Heart Disease
<130> 057695
<141> 2018-03-20
<150> US 62/476,054
<151> 2017-03-24
<160> 194
<170> PatentIn version 3.5
<210> 1
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 1
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 2
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 2
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 3
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 3
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 4
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 4
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 5
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 5
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 6
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 6
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 7
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 7
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 8
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 8
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 9
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 9
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 10
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 10
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 11
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 11
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 12
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 12
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 13
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 13
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 14
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 14
Gly Tyr Thr Phe Thr Ser Ser Tyr Ile Asn
1 5 10
<210> 15
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 15
Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 16
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 16
Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 17
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 17
Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 18
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 18
Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 19
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 19
Met Ile Asn Ala Pro Ile Gly Thr Thr Arg Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 20
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 20
Gln Ile Asn Ala Ala Ser Gly Met Thr Arg Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 21
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 21
Met Ile Asn Ala Pro Ile Gly Thr Thr Arg Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 22
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 22
Thr Ile Asn Pro Val Ser Gly Asn Thr Arg Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 23
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 23
Thr Ile Asn Pro Val Ser Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 24
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 24
Gln Ile Asn Ala Ala Ser Gly Met Thr Arg Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 25
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 25
Asn Ile Asn Ala Ala Ala Gly Ile Thr Leu Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 26
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 26
Thr Ile Asn Pro Pro Thr Gly Gly Thr Tyr Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 27
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 27
Gly Ile Asn Pro Pro Ala Gly Thr Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 28
<211> 17
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 28
Asn Ile Asn Pro Ala Thr Gly His Ala Asp Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 29
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 29
Gly Gly Trp Phe Asp Tyr
1 5
<210> 30
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 30
Gly Gly Trp Phe Asp Tyr
1 5
<210> 31
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 31
Gly Gly Trp Phe Asp Tyr
1 5
<210> 32
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 32
Gly Gly Trp Phe Asp Tyr
1 5
<210> 33
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 33
Gly Gly Trp Phe Asp Tyr
1 5
<210> 34
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 34
Gly Gly Trp Phe Asp Tyr
1 5
<210> 35
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 35
Gly Gly Trp Phe Asp Tyr
1 5
<210> 36
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 36
Gly Gly Trp Phe Asp Tyr
1 5
<210> 37
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 37
Gly Gly Trp Phe Asp Tyr
1 5
<210> 38
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 38
Gly Gly Trp Phe Asp Tyr
1 5
<210> 39
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 39
Gly Gly Trp Phe Asp Tyr
1 5
<210> 40
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 40
Gly Gly Trp Phe Asp Tyr
1 5
<210> 41
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 41
Gly Gly Trp Phe Asp Tyr
1 5
<210> 42
<211> 6
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 42
Gly Gly Trp Phe Asp Tyr
1 5
<210> 43
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 43
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 44
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 44
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 45
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 45
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 46
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 46
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 47
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 47
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 48
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 48
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 49
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 49
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 50
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 50
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 51
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 51
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 52
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 52
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 53
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 53
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 54
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 54
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 55
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 55
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 56
<211> 14
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 56
Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr Asn Tyr Val Asn
1 5 10
<210> 57
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 57
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 58
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 58
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 59
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 59
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 60
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 60
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 61
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 61
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 62
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 62
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 63
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 63
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 64
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 64
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 65
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 65
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 66
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 66
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 67
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 67
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 68
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 68
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 69
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 69
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 70
<211> 11
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 70
Leu Met Ile Tyr Gly Val Ser Lys Arg Pro Ser
1 5 10
<210> 71
<211> 9
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 71
Gln Ala Trp Thr Ser Lys Met Ala Gly
1 5
<210> 72
<211> 9
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 72
Ser Ser Tyr Thr Arg Met Gly His Pro
1 5
<210> 73
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 73
Ala Thr Tyr Gly Lys Gly Val Thr Pro Pro
1 5 10
<210> 74
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 74
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 75
<211> 9
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 75
Gln Ala Trp Thr Ser Lys Met Ala Gly
1 5
<210> 76
<211> 9
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 76
Gln Ala Trp Thr Ser Lys Met Ala Gly
1 5
<210> 77
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 77
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 78
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 78
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 79
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 79
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 80
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 80
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 81
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 81
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 82
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 82
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 83
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 83
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 84
<211> 10
<212> PRT
<213> Artificial
<220>
<223> CDR
<400> 84
Gly Thr Phe Ala Gly Gly Ser Tyr Tyr Gly
1 5 10
<210> 85
<211> 112
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 85
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Thr Ser Lys
85 90 95
Met Ala Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln
100 105 110
<210> 86
<211> 112
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 86
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Arg Met
85 90 95
Gly His Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln
100 105 110
<210> 87
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 87
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Tyr Gly Lys Gly
85 90 95
Val Thr Pro Pro Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 88
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 88
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 89
<211> 112
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 89
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Thr Ser Lys
85 90 95
Met Ala Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln
100 105 110
<210> 90
<211> 112
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 90
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Thr Ser Lys
85 90 95
Met Ala Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln
100 105 110
<210> 91
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 91
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 92
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 92
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 93
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 93
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 94
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 94
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 95
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 95
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 96
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 96
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 97
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 97
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 98
<211> 113
<212> PRT
<213> Artificial
<220>
<223> VL
<400> 98
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln
<210> 99
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 99
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 100
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 100
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 101
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 101
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 102
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 102
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Asn Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 103
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 103
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asn Ala Pro Ile Gly Thr Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 104
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 104
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gln Ile Asn Ala Ala Ser Gly Met Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 105
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 105
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asn Ala Pro Ile Gly Thr Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 106
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 106
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Asn Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 107
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 107
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 108
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 108
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gln Ile Asn Ala Ala Ser Gly Met Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 109
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 109
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asn Ala Ala Ala Gly Ile Thr Leu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 110
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 110
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Pro Thr Gly Gly Thr Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 111
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 111
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Pro Ala Gly Thr Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 112
<211> 115
<212> PRT
<213> Artificial
<220>
<223> VH
<400> 112
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asn Pro Ala Thr Gly His Ala Asp Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 113
<211> 336
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 113
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc caggcttgga cttctaagat ggctggtgtg 300
tttggcggcg gcacgaagtt aaccgttctt ggccag 336
<210> 114
<211> 336
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 114
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc tcttcttata ctcgtatggg tcatcctgtg 300
tttggcggcg gcacgaagtt aaccgttctt ggccag 336
<210> 115
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 115
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc gctacttatg gtaagggtgt tactcctcct 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 116
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 116
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 117
<211> 336
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 117
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc caggcttgga cttctaagat ggctggtgtg 300
tttggcggcg gcacgaagtt aaccgttctt ggccag 336
<210> 118
<211> 336
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 118
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc caggcttgga cttctaagat ggctggtgtg 300
tttggcggcg gcacgaagtt aaccgttctt ggccag 336
<210> 119
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 119
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 120
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 120
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 121
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 121
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 122
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 122
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 123
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 123
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 124
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 124
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtactg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 125
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 125
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 126
<211> 339
<212> DNA
<213> Artificial
<220>
<223> VL
<400> 126
gatatcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtt cttggccag 339
<210> 127
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 127
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact atcaatccgg tttctggcaa tacgtcttac 180
gcgcagaagt ttcagggccg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 128
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 128
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact atcaatccgg tttctggcaa tacgtcttac 180
gcgcagaagt ttcagggccg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 129
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 129
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact atcaatccgg tttctggcaa tacgtcttac 180
gcgcagaagt ttcagggccg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 130
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 130
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact atcaatccgg tttctggcaa tacgtcttac 180
gcgcagaagt ttcagggccg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 131
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 131
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcatg attaatgctc ctattggtac tactcgttat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 132
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 132
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggccag attaatgctg cttctggtat gactcgttat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 133
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 133
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcatg attaatgctc ctattggtac tactcgttat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 134
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 134
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact atcaatccgg tttctggcaa tacgcgttac 180
gcgcagaagt ttcagggccg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 135
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 135
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact atcaatccgg tttctggctc tacgtcttac 180
gcgcagaagt ttcagggccg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 136
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 136
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggccag attaatgctg cttctggtat gactcgttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 137
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 137
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcaat attaatgctg ctgctggtat tactctttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 138
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 138
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcact attaatcctc ctactggagg tacttattat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 139
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 139
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcggt attaatcctc ctgctggtac tacttcttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 140
<211> 345
<212> DNA
<213> Artificial
<220>
<223> VH
<400> 140
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcaat attaatcctg ctactggtca tgctgattat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gcagcctgcg tagcgaagat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctca 345
<210> 141
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 141
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 142
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 142
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 143
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 143
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 144
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 144
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 145
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 145
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 146
<211> 445
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 146
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 147
<211> 445
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 147
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gln Ile Asn Ala Ala Ser Gly Met Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 148
<211> 445
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 148
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asn Ala Ala Ala Gly Ile Thr Leu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 149
<211> 445
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 149
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Pro Ala Gly Thr Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 150
<211> 445
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 150
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asn Pro Ala Thr Gly His Ala Asp Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 151
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 151
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 152
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 152
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 153
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 153
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 154
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 154
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 155
<211> 217
<212> PRT
<213> Artificial
<220>
<223> light chain
<400> 155
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 156
<211> 441
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 156
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
210 215 220
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
225 230 235 240
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
245 250 255
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
260 265 270
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
275 280 285
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
290 295 300
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
305 310 315 320
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
325 330 335
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
340 345 350
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
355 360 365
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
370 375 380
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
385 390 395 400
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
405 410 415
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
420 425 430
Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 157
<211> 441
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 157
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gln Ile Asn Ala Ala Ser Gly Met Thr Arg Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
210 215 220
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
225 230 235 240
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
245 250 255
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
260 265 270
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
275 280 285
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
290 295 300
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
305 310 315 320
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
325 330 335
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
340 345 350
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
355 360 365
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
370 375 380
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
385 390 395 400
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
405 410 415
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
420 425 430
Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 158
<211> 441
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 158
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asn Ala Ala Ala Gly Ile Thr Leu Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
210 215 220
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
225 230 235 240
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
245 250 255
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
260 265 270
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
275 280 285
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
290 295 300
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
305 310 315 320
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
325 330 335
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
340 345 350
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
355 360 365
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
370 375 380
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
385 390 395 400
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
405 410 415
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
420 425 430
Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 159
<211> 441
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 159
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Pro Ala Gly Thr Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
210 215 220
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
225 230 235 240
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
245 250 255
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
260 265 270
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
275 280 285
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
290 295 300
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
305 310 315 320
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
325 330 335
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
340 345 350
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
355 360 365
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
370 375 380
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
385 390 395 400
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
405 410 415
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
420 425 430
Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 160
<211> 441
<212> PRT
<213> Artificial
<220>
<223> heavy chain
<400> 160
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asn Pro Ala Thr Gly His Ala Asp Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
210 215 220
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
225 230 235 240
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
245 250 255
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
260 265 270
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
275 280 285
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
290 295 300
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
305 310 315 320
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
325 330 335
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
340 345 350
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
355 360 365
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
370 375 380
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
385 390 395 400
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
405 410 415
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
420 425 430
Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 161
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 161
cagagcgccc tgacccagcc cgccagcgtg tccggcagcc caggccagtc tatcacaatc 60
agctgcaccg gcacctccag cgacgtgggc agctacaact acgtgaactg gtatcagcag 120
caccccggca aggcccccaa gctgatgatc tacggcgtga gcaagaggcc cagcggcgtg 180
tccaacaggt tcagcggcag caagagcggc aacaccgcca gcctgacaat cagtgggctg 240
caggctgagg acgaggccga ctactactgc ggcacctttg ccggcggatc atactacggc 300
gtgttcggcg gagggaccaa gctgaccgtg ctgggccagc ctaaggctgc ccccagcgtg 360
accctgttcc cccccagcag cgaggagctg caggccaaca aggccaccct ggtgtgcctg 420
atcagcgact tctacccagg cgccgtgacc gtggcctgga aggccgacag cagccccgtg 480
aaggccggcg tggagaccac cacccccagc aagcagagca acaacaagta cgccgccagc 540
agctacctga gcctgacccc cgagcagtgg aagagccaca ggtcctacag ctgccaggtg 600
acccacgagg gcagcaccgt ggaaaagacc gtggccccaa ccgagtgcag c 651
<210> 162
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 162
cagagcgccc tgacccagcc cgccagcgtg tccggcagcc caggccagtc tatcacaatc 60
agctgcaccg gcacctccag cgacgtgggc agctacaact acgtgaactg gtatcagcag 120
caccccggca aggcccccaa gctgatgatc tacggcgtga gcaagaggcc cagcggcgtg 180
tccaacaggt tcagcggcag caagagcggc aacaccgcca gcctgacaat cagtgggctg 240
caggctgagg acgaggccga ctactactgc ggcacctttg ccggcggatc atactacggc 300
gtgttcggcg gagggaccaa gctgaccgtg ctgggccagc ctaaggctgc ccccagcgtg 360
accctgttcc cccccagcag cgaggagctg caggccaaca aggccaccct ggtgtgcctg 420
atcagcgact tctacccagg cgccgtgacc gtggcctgga aggccgacag cagccccgtg 480
aaggccggcg tggagaccac cacccccagc aagcagagca acaacaagta cgccgccagc 540
agctacctga gcctgacccc cgagcagtgg aagagccaca ggtcctacag ctgccaggtg 600
acccacgagg gcagcaccgt ggaaaagacc gtggccccaa ccgagtgcag c 651
<210> 163
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 163
cagagcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtc ctaggtcagc ccaaggctgc cccctcggtc 360
actctgttcc cgccctcctc tgaggagctt caagccaaca aggccacact ggtgtgtctc 420
ataagtgact tctacccggg agccgtgaca gtggcctgga aggcagatag cagccccgtc 480
aaggcgggag tggagaccac cacaccctcc aaacaaagca acaacaagta cgcggccagc 540
agctatctga gcctgacgcc tgagcagtgg aagtcccaca gaagctacag ctgccaggtc 600
acgcatgaag ggagcaccgt ggagaagaca gtggccccta cagaatgttc a 651
<210> 164
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 164
cagagcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtc ctaggtcagc ccaaggctgc cccctcggtc 360
actctgttcc cgccctcctc tgaggagctt caagccaaca aggccacact ggtgtgtctc 420
ataagtgact tctacccggg agccgtgaca gtggcctgga aggcagatag cagccccgtc 480
aaggcgggag tggagaccac cacaccctcc aaacaaagca acaacaagta cgcggccagc 540
agctatctga gcctgacgcc tgagcagtgg aagtcccaca gaagctacag ctgccaggtc 600
acgcatgaag ggagcaccgt ggagaagaca gtggccccta cagaatgttc a 651
<210> 165
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 165
cagagcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtc ctaggtcagc ccaaggctgc cccctcggtc 360
actctgttcc cgccctcctc tgaggagctt caagccaaca aggccacact ggtgtgtctc 420
ataagtgact tctacccggg agccgtgaca gtggcctgga aggcagatag cagccccgtc 480
aaggcgggag tggagaccac cacaccctcc aaacaaagca acaacaagta cgcggccagc 540
agctatctga gcctgacgcc tgagcagtgg aagtcccaca gaagctacag ctgccaggtc 600
acgcatgaag ggagcaccgt ggagaagaca gtggccccta cagaatgttc a 651
<210> 166
<211> 1335
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 166
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggcgccag cgtcaaggtg 60
tcctgcaagg ccagcggcta caccttcacc agcagctaca tcaactgggt ccgccaggct 120
cctgggcagg gactggagtg gatgggcacc atcaaccccg tgtccggcag caccagctac 180
gcccagaagt tccagggcag agtcaccatg accagggaca ccagcatcag caccgcctac 240
atggagctgt ccaggctgag aagcgacgac accgccgtgt actactgcgc caggggcggc 300
tggttcgact actggggcca gggcaccctg gtgaccgtgt cctcagctag caccaagggc 360
cccagcgtgt tccccctggc ccccagcagc aagagcacct ccggcggcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag cccgtgaccg tgtcctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
tccagcgtgg tgacagtgcc cagcagcagc ctgggcaccc agacctacat ctgcaacgtg 600
aaccacaagc ccagcaacac caaggtggac aagagagtgg agcccaagag ctgcgacaag 660
acccacacct gccccccctg cccagccccc gaagctgcag gcggcccttc cgtgttcctg 720
ttccccccca agcccaagga caccctgatg atcagcagga cccccgaggt gacctgcgtg 780
gtggtggacg tgagccacga ggacccagag gtgaagttca actggtacgt ggacggcgtg 840
gaggtgcaca acgccaagac caagcccaga gaggagcagt acaacagcac ctacagggtg 900
gtgtccgtgc tgaccgtgct gcaccaggac tggctgaacg gcaaagaata caagtgcaag 960
gtctccaaca aggccctgcc tgcccccatc gaaaagacca tcagcaaggc caagggccag 1020
ccacgggagc cccaggtgta caccctgccc ccttctcggg aggagatgac caagaaccag 1080
gtgtccctga cctgtctggt gaagggcttc taccccagcg acatcgccgt ggagtgggag 1140
agcaacggcc agcccgagaa caactacaag accacccccc cagtgctgga cagcgacggc 1200
agcttcttcc tgtacagcaa gctgaccgtg gacaagagca ggtggcagca gggcaacgtg 1260
ttcagctgca gcgtgatgca cgaggccctg cacaaccact acacccagaa gagcctgagc 1320
ctgtcacccg gcaag 1335
<210> 167
<211> 1335
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 167
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggcgccag cgtcaaggtg 60
tcctgcaagg ccagcggcta caccttcacc agcagctaca tcaactgggt gcgccaggct 120
ccagggcagg gactggagtg gatgggccag atcaacgccg ccagcggcat gaccagatac 180
gcccagaagt tccagggcag agtcacaatg accagggaca cctctatcag caccgcctac 240
atggagctgt ccaggctgag aagcgacgac accgccgtgt actactgcgc caggggcggc 300
tggttcgact actggggcca gggcaccctg gtgaccgtgt cctcagctag caccaagggc 360
cccagcgtgt tccccctggc ccccagcagc aagagcacct ccggcggcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag cccgtgaccg tgtcctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
tccagcgtgg tgacagtgcc cagcagcagc ctgggcaccc agacctacat ctgcaacgtg 600
aaccacaagc ccagcaacac caaggtggac aagagagtgg agcccaagag ctgcgacaag 660
acccacacct gccccccctg cccagccccc gaagctgcag gcggcccttc cgtgttcctg 720
ttccccccca agcccaagga caccctgatg atcagcagga cccccgaggt gacctgcgtg 780
gtggtggacg tgagccacga ggacccagag gtgaagttca actggtacgt ggacggcgtg 840
gaggtgcaca acgccaagac caagcccaga gaggagcagt acaacagcac ctacagggtg 900
gtgtccgtgc tgaccgtgct gcaccaggac tggctgaacg gcaaagaata caagtgcaag 960
gtctccaaca aggccctgcc tgcccccatc gaaaagacca tcagcaaggc caagggccag 1020
ccacgggagc cccaggtgta caccctgccc ccttctcggg aggagatgac caagaaccag 1080
gtgtccctga cctgtctggt gaagggcttc taccccagcg acatcgccgt ggagtgggag 1140
agcaacggcc agcccgagaa caactacaag accacccccc cagtgctgga cagcgacggc 1200
agcttcttcc tgtacagcaa gctgaccgtg gacaagagca ggtggcagca gggcaacgtg 1260
ttcagctgca gcgtgatgca cgaggccctg cacaaccact acacccagaa gagcctgagc 1320
ctgtcacccg gcaag 1335
<210> 168
<211> 1335
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 168
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcaat attaatgctg ctgctggtat tactctttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gccgcctgcg tagcgatgat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctcagcctc caccaagggt 360
ccatcggtct tccccctggc accctcctcc aagagcacct ctgggggcac agcggccctg 420
ggctgcctgg tcaaggacta cttccccgaa ccggtgacgg tgtcgtggaa ctcaggcgcc 480
ctgaccagcg gcgtgcacac cttcccggct gtcctacagt cctcaggact ctactccctc 540
agcagcgtgg tgaccgtgcc ctccagcagc ttgggcaccc agacctacat ctgcaacgtg 600
aatcacaagc ccagcaacac caaggtggac aagagagttg agcccaaatc ttgtgacaaa 660
actcacacat gcccaccgtg cccagcacct gaagcagcgg ggggaccgtc agtcttcctc 720
ttccccccaa aacccaagga caccctcatg atctcccgga cccctgaggt cacatgcgtg 780
gtggtggacg tgagccacga agaccctgag gtcaagttca actggtacgt ggacggcgtg 840
gaggtgcata atgccaagac aaagccgcgg gaggagcagt acaacagcac gtaccgggtg 900
gtcagcgtcc tcaccgtcct gcaccaggac tggctgaatg gcaaggagta caagtgcaag 960
gtctccaaca aagccctccc agcccccatc gagaaaacca tctccaaagc caaagggcag 1020
ccccgagaac cacaggtgta caccctgccc ccatcccggg aggagatgac caagaaccag 1080
gtcagcctga cctgcctggt caaaggcttc tatcccagcg acatcgccgt ggagtgggag 1140
agcaatgggc agccggagaa caactacaag accacgcctc ccgtgctgga ctccgacggc 1200
tccttcttcc tctacagcaa gctcaccgtg gacaagagca ggtggcagca ggggaacgtc 1260
ttctcatgct ccgtgatgca tgaggctctg cacaaccact acacgcagaa gagcctctcc 1320
ctgtctccgg gtaaa 1335
<210> 169
<211> 1335
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 169
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcggt attaatcctc ctgctggtac tacttcttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gccgcctgcg tagcgatgat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctcagcctc caccaagggt 360
ccatcggtct tccccctggc accctcctcc aagagcacct ctgggggcac agcggccctg 420
ggctgcctgg tcaaggacta cttccccgaa ccggtgacgg tgtcgtggaa ctcaggcgcc 480
ctgaccagcg gcgtgcacac cttcccggct gtcctacagt cctcaggact ctactccctc 540
agcagcgtgg tgaccgtgcc ctccagcagc ttgggcaccc agacctacat ctgcaacgtg 600
aatcacaagc ccagcaacac caaggtggac aagagagttg agcccaaatc ttgtgacaaa 660
actcacacat gcccaccgtg cccagcacct gaagcagcgg ggggaccgtc agtcttcctc 720
ttccccccaa aacccaagga caccctcatg atctcccgga cccctgaggt cacatgcgtg 780
gtggtggacg tgagccacga agaccctgag gtcaagttca actggtacgt ggacggcgtg 840
gaggtgcata atgccaagac aaagccgcgg gaggagcagt acaacagcac gtaccgggtg 900
gtcagcgtcc tcaccgtcct gcaccaggac tggctgaatg gcaaggagta caagtgcaag 960
gtctccaaca aagccctccc agcccccatc gagaaaacca tctccaaagc caaagggcag 1020
ccccgagaac cacaggtgta caccctgccc ccatcccggg aggagatgac caagaaccag 1080
gtcagcctga cctgcctggt caaaggcttc tatcccagcg acatcgccgt ggagtgggag 1140
agcaatgggc agccggagaa caactacaag accacgcctc ccgtgctgga ctccgacggc 1200
tccttcttcc tctacagcaa gctcaccgtg gacaagagca ggtggcagca ggggaacgtc 1260
ttctcatgct ccgtgatgca tgaggctctg cacaaccact acacgcagaa gagcctctcc 1320
ctgtctccgg gtaaa 1335
<210> 170
<211> 1335
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 170
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcaat attaatcctg ctactggtca tgctgattat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gccgcctgcg tagcgatgat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctcagcctc caccaagggt 360
ccatcggtct tccccctggc accctcctcc aagagcacct ctgggggcac agcggccctg 420
ggctgcctgg tcaaggacta cttccccgaa ccggtgacgg tgtcgtggaa ctcaggcgcc 480
ctgaccagcg gcgtgcacac cttcccggct gtcctacagt cctcaggact ctactccctc 540
agcagcgtgg tgaccgtgcc ctccagcagc ttgggcaccc agacctacat ctgcaacgtg 600
aatcacaagc ccagcaacac caaggtggac aagagagttg agcccaaatc ttgtgacaaa 660
actcacacat gcccaccgtg cccagcacct gaagcagcgg ggggaccgtc agtcttcctc 720
ttccccccaa aacccaagga caccctcatg atctcccgga cccctgaggt cacatgcgtg 780
gtggtggacg tgagccacga agaccctgag gtcaagttca actggtacgt ggacggcgtg 840
gaggtgcata atgccaagac aaagccgcgg gaggagcagt acaacagcac gtaccgggtg 900
gtcagcgtcc tcaccgtcct gcaccaggac tggctgaatg gcaaggagta caagtgcaag 960
gtctccaaca aagccctccc agcccccatc gagaaaacca tctccaaagc caaagggcag 1020
ccccgagaac cacaggtgta caccctgccc ccatcccggg aggagatgac caagaaccag 1080
gtcagcctga cctgcctggt caaaggcttc tatcccagcg acatcgccgt ggagtgggag 1140
agcaatgggc agccggagaa caactacaag accacgcctc ccgtgctgga ctccgacggc 1200
tccttcttcc tctacagcaa gctcaccgtg gacaagagca ggtggcagca ggggaacgtc 1260
ttctcatgct ccgtgatgca tgaggctctg cacaaccact acacgcagaa gagcctctcc 1320
ctgtctccgg gtaaa 1335
<210> 171
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 171
cagagcgccc tgacccagcc cgccagcgtg tccggcagcc caggccagtc tatcacaatc 60
agctgcaccg gcacctccag cgacgtgggc agctacaact acgtgaactg gtatcagcag 120
caccccggca aggcccccaa gctgatgatc tacggcgtga gcaagaggcc cagcggcgtg 180
tccaacaggt tcagcggcag caagagcggc aacaccgcca gcctgacaat cagtgggctg 240
caggctgagg acgaggccga ctactactgc ggcacctttg ccggcggatc atactacggc 300
gtgttcggcg gagggaccaa gctgaccgtg ctgggccagc ctaaggctgc ccccagcgtg 360
accctgttcc cccccagcag cgaggagctg caggccaaca aggccaccct ggtgtgcctg 420
atcagcgact tctacccagg cgccgtgacc gtggcctgga aggccgacag cagccccgtg 480
aaggccggcg tggagaccac cacccccagc aagcagagca acaacaagta cgccgccagc 540
agctacctga gcctgacccc cgagcagtgg aagagccaca ggtcctacag ctgccaggtg 600
acccacgagg gcagcaccgt ggaaaagacc gtggccccaa ccgagtgcag c 651
<210> 172
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 172
cagagcgccc tgacccagcc cgccagcgtg tccggcagcc caggccagtc tatcacaatc 60
agctgcaccg gcacctccag cgacgtgggc agctacaact acgtgaactg gtatcagcag 120
caccccggca aggcccccaa gctgatgatc tacggcgtga gcaagaggcc cagcggcgtg 180
tccaacaggt tcagcggcag caagagcggc aacaccgcca gcctgacaat cagtgggctg 240
caggctgagg acgaggccga ctactactgc ggcacctttg ccggcggatc atactacggc 300
gtgttcggcg gagggaccaa gctgaccgtg ctgggccagc ctaaggctgc ccccagcgtg 360
accctgttcc cccccagcag cgaggagctg caggccaaca aggccaccct ggtgtgcctg 420
atcagcgact tctacccagg cgccgtgacc gtggcctgga aggccgacag cagccccgtg 480
aaggccggcg tggagaccac cacccccagc aagcagagca acaacaagta cgccgccagc 540
agctacctga gcctgacccc cgagcagtgg aagagccaca ggtcctacag ctgccaggtg 600
acccacgagg gcagcaccgt ggaaaagacc gtggccccaa ccgagtgcag c 651
<210> 173
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 173
cagagcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtc ctaggtcagc ccaaggctgc cccctcggtc 360
actctgttcc cgccctcctc tgaggagctt caagccaaca aggccacact ggtgtgtctc 420
ataagtgact tctacccggg agccgtgaca gtggcctgga aggcagatag cagccccgtc 480
aaggcgggag tggagaccac cacaccctcc aaacaaagca acaacaagta cgcggccagc 540
agctatctga gcctgacgcc tgagcagtgg aagtcccaca gaagctacag ctgccaggtc 600
acgcatgaag ggagcaccgt ggagaagaca gtggccccta cagaatgttc a 651
<210> 174
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 174
cagagcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtc ctaggtcagc ccaaggctgc cccctcggtc 360
actctgttcc cgccctcctc tgaggagctt caagccaaca aggccacact ggtgtgtctc 420
ataagtgact tctacccggg agccgtgaca gtggcctgga aggcagatag cagccccgtc 480
aaggcgggag tggagaccac cacaccctcc aaacaaagca acaacaagta cgcggccagc 540
agctatctga gcctgacgcc tgagcagtgg aagtcccaca gaagctacag ctgccaggtc 600
acgcatgaag ggagcaccgt ggagaagaca gtggccccta cagaatgttc a 651
<210> 175
<211> 651
<212> DNA
<213> Artificial
<220>
<223> light chain
<400> 175
cagagcgcac tgacccagcc agcttcagtg agcggctcac caggtcagag cattaccatc 60
tcgtgtacgg gtactagcag cgatgttggt tcttataatt atgtgaattg gtaccagcag 120
catcccggga aggcgccgaa acttatgatt tatggtgttt ctaagcgtcc ctcaggcgtg 180
agcaaccgtt ttagcggatc caaaagcggc aacaccgcga gcctgaccat tagcggcctg 240
caagcggaag acgaagcgga ttattattgc ggtacttttg ctggtggttc ttattatggt 300
gtgtttggcg gcggcacgaa gttaaccgtc ctaggtcagc ccaaggctgc cccctcggtc 360
actctgttcc cgccctcctc tgaggagctt caagccaaca aggccacact ggtgtgtctc 420
ataagtgact tctacccggg agccgtgaca gtggcctgga aggcagatag cagccccgtc 480
aaggcgggag tggagaccac cacaccctcc aaacaaagca acaacaagta cgcggccagc 540
agctatctga gcctgacgcc tgagcagtgg aagtcccaca gaagctacag ctgccaggtc 600
acgcatgaag ggagcaccgt ggagaagaca gtggccccta cagaatgttc a 651
<210> 176
<211> 1323
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 176
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggcgccag cgtcaaggtg 60
tcctgcaagg ccagcggcta caccttcacc agcagctaca tcaactgggt ccgccaggct 120
cctgggcagg gactggagtg gatgggcacc atcaaccccg tgtccggcag caccagctac 180
gcccagaagt tccagggcag agtcaccatg accagggaca ccagcatcag caccgcctac 240
atggagctgt ccaggctgag aagcgacgac accgccgtgt actactgcgc caggggcggc 300
tggttcgact actggggcca gggcaccctg gtgaccgtgt cctcagctag caccaagggc 360
cccagcgtgt tccccctggc cccctgcagc agaagcacca gcgagagcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag ccagtgaccg tgtcctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
tccagcgtgg tgaccgtgcc cagcagcaac ttcggcaccc agacctacac ctgcaacgtg 600
gaccacaagc ccagcaacac caaggtggac aagaccgtgg agaggaagtg ctgcgtggag 660
tgccccccct gcccagcccc cccagtggcc ggaccctccg tgttcctgtt cccccccaag 720
cccaaggaca ccctgatgat cagcaggacc cccgaggtga cctgcgtggt ggtggacgtg 780
agccacgagg acccagaggt gcagttcaac tggtacgtgg acggcgtgga ggtgcacaac 840
gccaagacca agcccagaga ggaacagttt aacagcacct tcagggtggt gtccgtgctg 900
accgtggtgc accaggactg gctgaacggc aaagagtaca agtgcaaggt ctccaacaag 960
ggcctgccag cccccatcga gaaaaccatc agcaagacca agggccagcc acgggagccc 1020
caggtgtaca ccctgccccc cagccgggag gaaatgacca agaaccaggt gtccctgacc 1080
tgtctggtga agggcttcta ccccagcgac atcgccgtgg agtgggagag caacggccag 1140
cccgagaaca actacaagac cacccccccc atgctggaca gcgacggcag cttcttcctg 1200
tacagcaagc tgacagtgga caagagcagg tggcagcagg gcaacgtgtt cagctgcagc 1260
gtgatgcacg aggccctgca caaccactac acccagaaga gcctgagcct gtcccccggc 1320
aag 1323
<210> 177
<211> 1323
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 177
caggtgcagc tggtgcagag cggagctgag gtgaagaagc caggcgccag cgtcaaggtg 60
tcctgcaagg ccagcggcta caccttcacc agcagctaca tcaactgggt gcgccaggct 120
ccagggcagg gactggagtg gatgggccag atcaacgccg ccagcggcat gaccagatac 180
gcccagaagt tccagggcag agtcacaatg accagggaca cctctatcag caccgcctac 240
atggagctgt ccaggctgag aagcgacgac accgccgtgt actactgcgc caggggcggc 300
tggttcgact actggggcca gggcaccctg gtgaccgtgt cctcagctag caccaagggc 360
cccagcgtgt tccccctggc cccctgcagc agaagcacca gcgagagcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag ccagtgaccg tgtcctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
tccagcgtgg tgaccgtgcc cagcagcaac ttcggcaccc agacctacac ctgcaacgtg 600
gaccacaagc ccagcaacac caaggtggac aagaccgtgg agaggaagtg ctgcgtggag 660
tgccccccct gcccagcccc cccagtggcc ggaccctccg tgttcctgtt cccccccaag 720
cccaaggaca ccctgatgat cagcaggacc cccgaggtga cctgcgtggt ggtggacgtg 780
agccacgagg acccagaggt gcagttcaac tggtacgtgg acggcgtgga ggtgcacaac 840
gccaagacca agcccagaga ggaacagttt aacagcacct tcagggtggt gtccgtgctg 900
accgtggtgc accaggactg gctgaacggc aaagagtaca agtgcaaggt ctccaacaag 960
ggcctgccag cccccatcga gaaaaccatc agcaagacca agggccagcc acgggagccc 1020
caggtgtaca ccctgccccc cagccgggag gaaatgacca agaaccaggt gtccctgacc 1080
tgtctggtga agggcttcta ccccagcgac atcgccgtgg agtgggagag caacggccag 1140
cccgagaaca actacaagac cacccccccc atgctggaca gcgacggcag cttcttcctg 1200
tacagcaagc tgacagtgga caagagcagg tggcagcagg gcaacgtgtt cagctgcagc 1260
gtgatgcacg aggccctgca caaccactac acccagaaga gcctgagcct gtcccccggc 1320
aag 1323
<210> 178
<211> 1323
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 178
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcaat attaatgctg ctgctggtat tactctttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gccgcctgcg tagcgatgat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctcagcttc caccaagggc 360
cccagcgtgt tccccctggc cccctgcagc agaagcacca gcgagagcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag cccgtgaccg tgagctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
agcagcgtgg tgaccgtgcc cagcagcaac ttcggcaccc agacctacac ctgcaacgtg 600
gaccacaagc ccagcaacac caaggtggac aagaccgtgg agcggaagtg ctgcgtggag 660
tgccccccct gccctgcccc tcctgtggcc ggaccctccg tgttcctgtt cccccccaag 720
cccaaggaca ccctgatgat cagccggacc cccgaggtga cctgcgtggt ggtggacgtg 780
agccacgagg accccgaggt gcagttcaac tggtacgtgg acggcgtgga ggtgcacaac 840
gccaagacca agccccggga ggaacagttc aacagcacct tccgggtggt gtccgtgctg 900
accgtggtgc accaggactg gctgaacggc aaagaataca agtgcaaggt gtccaacaag 960
ggcctgcctg cccccatcga gaaaaccatc agcaagacaa agggccagcc cagggaaccc 1020
caggtgtaca ccctgccccc cagccgggag gaaatgacca agaaccaggt gtccctgacc 1080
tgtctggtga agggcttcta ccccagcgac atcgccgtgg agtgggagag caacggccag 1140
cccgagaaca actacaagac cacccccccc atgctggaca gcgacggcag cttcttcctg 1200
tacagcaagc tgacagtgga caagagccgg tggcagcagg gcaacgtgtt cagctgcagc 1260
gtgatgcacg aggccctgca caaccactac acccagaaga gcctgagcct gtcccccggc 1320
aaa 1323
<210> 179
<211> 1323
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 179
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcggt attaatcctc ctgctggtac tacttcttat 180
gctcagaagt ttcagggtcg ggtcaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gccgcctgcg tagcgatgat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctcagcttc caccaagggc 360
cccagcgtgt tccccctggc cccctgcagc agaagcacca gcgagagcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag cccgtgaccg tgagctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
agcagcgtgg tgaccgtgcc cagcagcaac ttcggcaccc agacctacac ctgcaacgtg 600
gaccacaagc ccagcaacac caaggtggac aagaccgtgg agcggaagtg ctgcgtggag 660
tgccccccct gccctgcccc tcctgtggcc ggaccctccg tgttcctgtt cccccccaag 720
cccaaggaca ccctgatgat cagccggacc cccgaggtga cctgcgtggt ggtggacgtg 780
agccacgagg accccgaggt gcagttcaac tggtacgtgg acggcgtgga ggtgcacaac 840
gccaagacca agccccggga ggaacagttc aacagcacct tccgggtggt gtccgtgctg 900
accgtggtgc accaggactg gctgaacggc aaagaataca agtgcaaggt gtccaacaag 960
ggcctgcctg cccccatcga gaaaaccatc agcaagacaa agggccagcc cagggaaccc 1020
caggtgtaca ccctgccccc cagccgggag gaaatgacca agaaccaggt gtccctgacc 1080
tgtctggtga agggcttcta ccccagcgac atcgccgtgg agtgggagag caacggccag 1140
cccgagaaca actacaagac cacccccccc atgctggaca gcgacggcag cttcttcctg 1200
tacagcaagc tgacagtgga caagagccgg tggcagcagg gcaacgtgtt cagctgcagc 1260
gtgatgcacg aggccctgca caaccactac acccagaaga gcctgagcct gtcccccggc 1320
aaa 1323
<210> 180
<211> 1323
<212> DNA
<213> Artificial
<220>
<223> heavy chain
<400> 180
caggtgcaat tggttcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cctccggata tacctttact tcttcttata ttaattgggt ccgccaagcc 120
cctgggcagg gtctcgagtg gatgggcaat attaatcctg ctactggtca tgctgattat 180
gctcagaagt ttcagggtcg ggtgaccatg acccgtgata ccagcattag caccgcgtat 240
atggaactga gccgcctgcg tagcgatgat acggccgtgt attattgcgc gcgtggtggt 300
tggtttgatt attggggcca aggcaccctg gtgacggtta gctcagcttc caccaagggc 360
cccagcgtgt tccccctggc cccctgcagc agaagcacca gcgagagcac agccgccctg 420
ggctgcctgg tgaaggacta cttccccgag cccgtgaccg tgagctggaa cagcggagcc 480
ctgaccagcg gcgtgcacac cttccccgcc gtgctgcaga gcagcggcct gtacagcctg 540
agcagcgtgg tgaccgtgcc cagcagcaac ttcggcaccc agacctacac ctgcaacgtg 600
gaccacaagc ccagcaacac caaggtggac aagaccgtgg agcggaagtg ctgcgtggag 660
tgccccccct gccctgcccc tcctgtggcc ggaccctccg tgttcctgtt cccccccaag 720
cccaaggaca ccctgatgat cagccggacc cccgaggtga cctgcgtggt ggtggacgtg 780
agccacgagg accccgaggt gcagttcaac tggtacgtgg acggcgtgga ggtgcacaac 840
gccaagacca agccccggga ggaacagttc aacagcacct tccgggtggt gtccgtgctg 900
accgtggtgc accaggactg gctgaacggc aaagaataca agtgcaaggt gtccaacaag 960
ggcctgcctg cccccatcga gaaaaccatc agcaagacaa agggccagcc cagggaaccc 1020
caggtgtaca ccctgccccc cagccgggag gaaatgacca agaaccaggt gtccctgacc 1080
tgtctggtga agggcttcta ccccagcgac atcgccgtgg agtgggagag caacggccag 1140
cccgagaaca actacaagac cacccccccc atgctggaca gcgacggcag cttcttcctg 1200
tacagcaagc tgacagtgga caagagccgg tggcagcagg gcaacgtgtt cagctgcagc 1260
gtgatgcacg aggccctgca caaccactac acccagaaga gcctgagcct gtcccccggc 1320
aaa 1323
<210> 181
<211> 512
<212> PRT
<213> Homo sapiens
<400> 181
Met Thr Ala Pro Trp Val Ala Leu Ala Leu Leu Trp Gly Ser Leu Cys
1 5 10 15
Ala Gly Ser Gly Arg Gly Glu Ala Glu Thr Arg Glu Cys Ile Tyr Tyr
20 25 30
Asn Ala Asn Trp Glu Leu Glu Arg Thr Asn Gln Ser Gly Leu Glu Arg
35 40 45
Cys Glu Gly Glu Gln Asp Lys Arg Leu His Cys Tyr Ala Ser Trp Arg
50 55 60
Asn Ser Ser Gly Thr Ile Glu Leu Val Lys Lys Gly Cys Trp Leu Asp
65 70 75 80
Asp Phe Asn Cys Tyr Asp Arg Gln Glu Cys Val Ala Thr Glu Glu Asn
85 90 95
Pro Gln Val Tyr Phe Cys Cys Cys Glu Gly Asn Phe Cys Asn Glu Arg
100 105 110
Phe Thr His Leu Pro Glu Ala Gly Gly Pro Glu Val Thr Tyr Glu Pro
115 120 125
Pro Pro Thr Ala Pro Thr Leu Leu Thr Val Leu Ala Tyr Ser Leu Leu
130 135 140
Pro Ile Gly Gly Leu Ser Leu Ile Val Leu Leu Ala Phe Trp Met Tyr
145 150 155 160
Arg His Arg Lys Pro Pro Tyr Gly His Val Asp Ile His Glu Asp Pro
165 170 175
Gly Pro Pro Pro Pro Ser Pro Leu Val Gly Leu Lys Pro Leu Gln Leu
180 185 190
Leu Glu Ile Lys Ala Arg Gly Arg Phe Gly Cys Val Trp Lys Ala Gln
195 200 205
Leu Met Asn Asp Phe Val Ala Val Lys Ile Phe Pro Leu Gln Asp Lys
210 215 220
Gln Ser Trp Gln Ser Glu Arg Glu Ile Phe Ser Thr Pro Gly Met Lys
225 230 235 240
His Glu Asn Leu Leu Gln Phe Ile Ala Ala Glu Lys Arg Gly Ser Asn
245 250 255
Leu Glu Val Glu Leu Trp Leu Ile Thr Ala Phe His Asp Lys Gly Ser
260 265 270
Leu Thr Asp Tyr Leu Lys Gly Asn Ile Ile Thr Trp Asn Glu Leu Cys
275 280 285
His Val Ala Glu Thr Met Ser Arg Gly Leu Ser Tyr Leu His Glu Asp
290 295 300
Val Pro Trp Cys Arg Gly Glu Gly His Lys Pro Ser Ile Ala His Arg
305 310 315 320
Asp Phe Lys Ser Lys Asn Val Leu Leu Lys Ser Asp Leu Thr Ala Val
325 330 335
Leu Ala Asp Phe Gly Leu Ala Val Arg Phe Glu Pro Gly Lys Pro Pro
340 345 350
Gly Asp Thr His Gly Gln Val Gly Thr Arg Arg Tyr Met Ala Pro Glu
355 360 365
Val Leu Glu Gly Ala Ile Asn Phe Gln Arg Asp Ala Phe Leu Arg Ile
370 375 380
Asp Met Tyr Ala Met Gly Leu Val Leu Trp Glu Leu Val Ser Arg Cys
385 390 395 400
Lys Ala Ala Asp Gly Pro Val Asp Glu Tyr Met Leu Pro Phe Glu Glu
405 410 415
Glu Ile Gly Gln His Pro Ser Leu Glu Glu Leu Gln Glu Val Val Val
420 425 430
His Lys Lys Met Arg Pro Thr Ile Lys Asp His Trp Leu Lys His Pro
435 440 445
Gly Leu Ala Gln Leu Cys Val Thr Ile Glu Ala Cys Trp Asp His Asp
450 455 460
Ala Glu Ala Arg Leu Ser Ala Gly Cys Val Glu Glu Arg Val Ser Leu
465 470 475 480
Ile Arg Arg Ser Val Asn Gly Thr Thr Ser Asp Cys Leu Val Ser Leu
485 490 495
Val Thr Ser Val Thr Asn Val Asp Leu Pro Pro Lys Glu Ser Ser Ile
500 505 510
<210> 182
<211> 116
<212> PRT
<213> Homo sapiens
<400> 182
Ser Gly Arg Gly Glu Ala Glu Thr Arg Glu Cys Ile Tyr Tyr Asn Ala
1 5 10 15
Asn Trp Glu Leu Glu Arg Thr Asn Gln Ser Gly Leu Glu Arg Cys Glu
20 25 30
Gly Glu Gln Asp Lys Arg Leu His Cys Tyr Ala Ser Trp Arg Asn Ser
35 40 45
Ser Gly Thr Ile Glu Leu Val Lys Lys Gly Cys Trp Leu Asp Asp Phe
50 55 60
Asn Cys Tyr Asp Arg Gln Glu Cys Val Ala Thr Glu Glu Asn Pro Gln
65 70 75 80
Val Tyr Phe Cys Cys Cys Glu Gly Asn Phe Cys Asn Glu Arg Phe Thr
85 90 95
His Leu Pro Glu Ala Gly Gly Pro Glu Val Thr Tyr Glu Pro Pro Pro
100 105 110
Thr Ala Pro Thr
115
<210> 183
<211> 15
<212> PRT
<213> Homo sapiens
<400> 183
Ile Glu Leu Val Lys Lys Gly Ser Trp Leu Asp Asp Phe Asn Ser
1 5 10 15
<210> 184
<211> 15
<212> PRT
<213> Homo sapiens
<400> 184
Val Lys Lys Gly Ser Trp Leu Asp Asp Phe Asn Ser Tyr Asp Arg
1 5 10 15
<210> 185
<211> 15
<212> PRT
<213> Homo sapiens
<400> 185
Gly Ser Trp Leu Asp Asp Phe Asn Ser Tyr Asp Arg Gln Glu Ser
1 5 10 15
<210> 186
<211> 9
<212> PRT
<213> Homo sapiens
<400> 186
Gly Cys Trp Leu Asp Asp Phe Asn Cys
1 5
<210> 187
<211> 15
<212> PRT
<213> Homo sapiens
<400> 187
Cys Glu Gly Glu Gln Asp Lys Arg Leu His Cys Tyr Ala Ser Trp
1 5 10 15
<210> 188
<211> 6
<212> PRT
<213> Homo sapiens
<400> 188
Trp Leu Asp Asp Phe Asn
1 5
<210> 189
<211> 5
<212> PRT
<213> Homo sapiens
<400> 189
Glu Gln Asp Lys Arg
1 5
<210> 190
<211> 11
<212> PRT
<213> Homo sapiens
<400> 190
Lys Gly Cys Trp Leu Asp Asp Phe Asn Cys Tyr
1 5 10
<210> 191
<211> 13
<212> PRT
<213> Human
<400> 191
Cys Ile Tyr Tyr Asn Ala Asn Trp Glu Leu Glu Arg Thr
1 5 10
<210> 192
<211> 11
<212> PRT
<213> Human
<400> 192
Tyr Phe Cys Cys Cys Glu Gly Asn Phe Cys Asn
1 5 10
<210> 193
<211> 216
<212> PRT
<213> Artificial Sequence
<220>
<223> Light Chain
<400> 193
Asp Ile Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Ser Tyr
20 25 30
Asn Tyr Val Asn Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Lys Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Phe Ala Gly Gly
85 90 95
Ser Tyr Tyr Gly Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Gln Pro Lys Ser Thr Pro Thr Leu Thr Val Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Lys Glu Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asn Phe
130 135 140
Ser Pro Ser Gly Val Thr Val Ala Trp Lys Ala Asn Gly Thr Pro Ile
145 150 155 160
Thr Gln Gly Val Asp Thr Ser Asn Pro Thr Lys Glu Gly Asn Lys Phe
165 170 175
Met Ala Ser Ser Phe Leu His Leu Thr Ser Asp Gln Trp Arg Ser His
180 185 190
Asn Ser Phe Thr Cys Gln Val Thr His Glu Gly Asp Thr Val Glu Lys
195 200 205
Ser Leu Ser Pro Ala Glu Cys Leu
210 215
<210> 194
<211> 445
<212> PRT
<213> Artificial
<220>
<223> Heavy Chain
<400> 194
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ser
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Thr Ile Asn Pro Val Ser Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Lys Thr Thr Ala Pro Ser Val Tyr Pro Leu Ala Pro
115 120 125
Val Cys Gly Asp Thr Thr Gly Ser Ser Val Thr Leu Gly Cys Leu Val
130 135 140
Lys Gly Tyr Phe Pro Glu Pro Val Thr Leu Thr Trp Asn Ser Gly Ser
145 150 155 160
Leu Ser Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Asp Leu
165 170 175
Tyr Thr Leu Ser Ser Ser Val Thr Val Thr Ser Ser Thr Trp Pro Ser
180 185 190
Gln Ser Ile Thr Cys Asn Val Ala His Pro Ala Ser Ser Thr Lys Val
195 200 205
Asp Lys Lys Ile Glu Pro Arg Gly Pro Thr Ile Lys Pro Cys Pro Pro
210 215 220
Cys Lys Cys Pro Ala Pro Asn Ala Ala Gly Gly Pro Ser Val Phe Ile
225 230 235 240
Phe Pro Pro Lys Ile Lys Asp Val Leu Met Ile Ser Leu Ser Pro Ile
245 250 255
Val Thr Cys Val Val Val Asp Val Ser Glu Asp Asp Pro Asp Val Gln
260 265 270
Ile Ser Trp Phe Val Asn Asn Val Glu Val His Thr Ala Gln Thr Gln
275 280 285
Thr His Arg Glu Asp Tyr Asn Ser Thr Leu Arg Val Val Ser Ala Leu
290 295 300
Pro Ile Gln His Gln Asp Trp Met Ser Gly Lys Glu Phe Lys Cys Lys
305 310 315 320
Val Asn Asn Lys Asp Leu Pro Ala Pro Ile Glu Arg Thr Ile Ser Lys
325 330 335
Pro Lys Gly Ser Val Arg Ala Pro Gln Val Tyr Val Leu Pro Pro Pro
340 345 350
Glu Glu Glu Met Thr Lys Lys Gln Val Thr Leu Thr Cys Met Val Thr
355 360 365
Asp Phe Met Pro Glu Asp Ile Tyr Val Glu Trp Thr Asn Asn Gly Lys
370 375 380
Thr Glu Leu Asn Tyr Lys Asn Thr Glu Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Tyr Phe Met Tyr Ser Lys Leu Arg Val Glu Lys Lys Asn Trp Val
405 410 415
Glu Arg Asn Ser Tyr Ser Cys Ser Val Val His Glu Gly Leu His Asn
420 425 430
His His Thr Thr Lys Ser Phe Ser Arg Thr Pro Gly Lys
435 440 445
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2020 |
|
RU2835543C1 |
| АНТИТЕЛО, СПОСОБНОЕ СВЯЗЫВАТЬСЯ С ТИМИЧЕСКИМ СТРОМАЛЬНЫМ ЛИМФОПОЭТИНОМ, И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2825304C2 |
| АНТИТЕЛО ПРОТИВ ФАКТОРА РОСТА СОЕДИНИТЕЛЬНОЙ ТКАНИ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2819228C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| ТЕРАПЕВТИЧЕСКИЕ АНТИТЕЛА ПРОТИВ ЛИГАНДА CD40 | 2018 |
|
RU2770209C2 |
| АНТИТЕЛО К CLDN-18.2 И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2829997C1 |
| ПРОКОАГУЛЯНТНЫЕ АНТИТЕЛА | 2018 |
|
RU2810094C2 |
| АНТИ-PCSK9 АНТИТЕЛО, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2739208C2 |
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| АНТИТЕЛО К B7-H4, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2792748C2 |
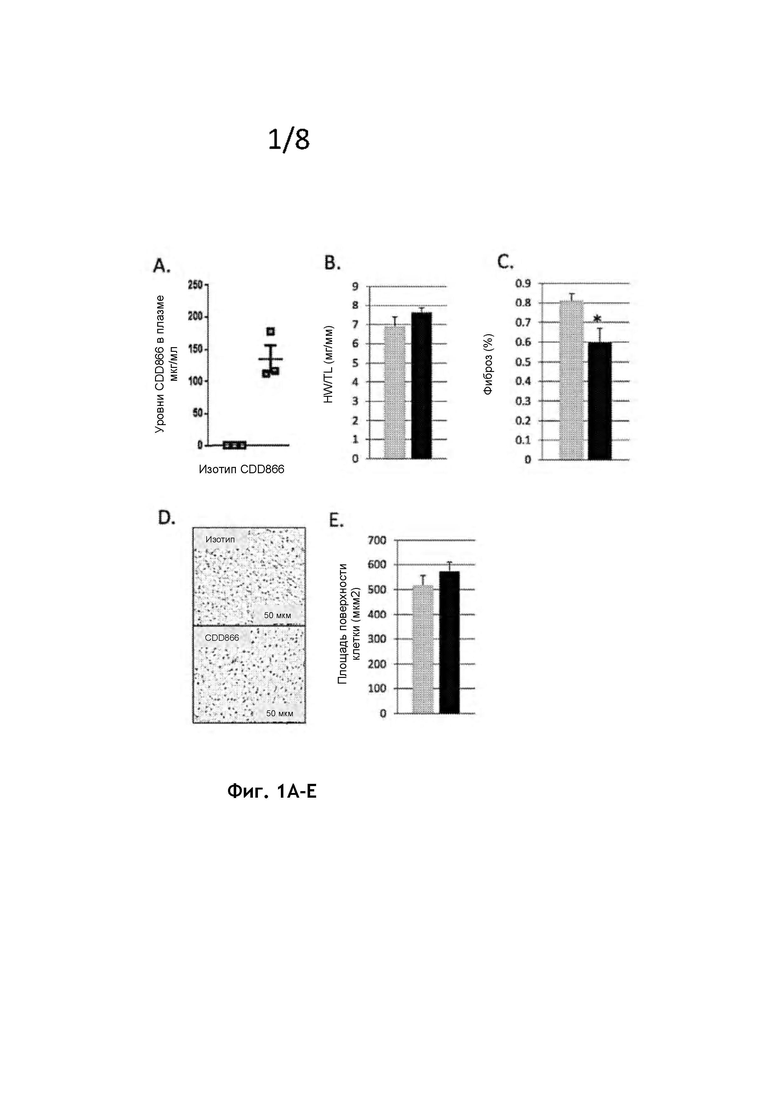
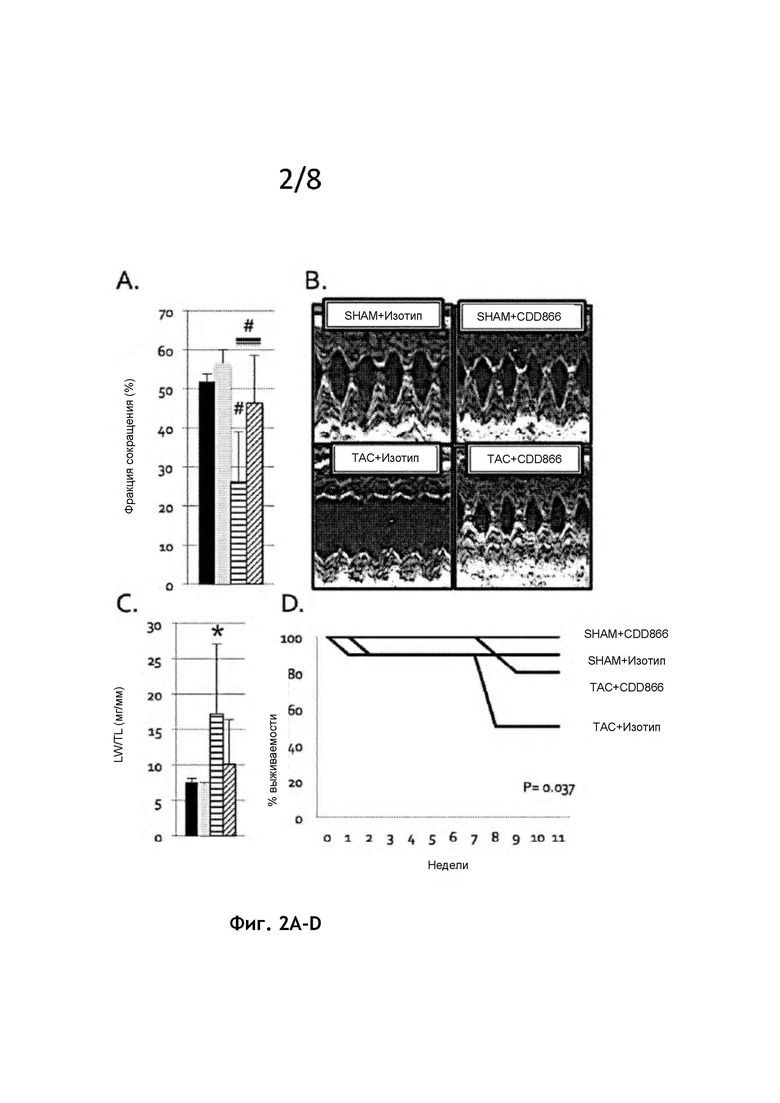
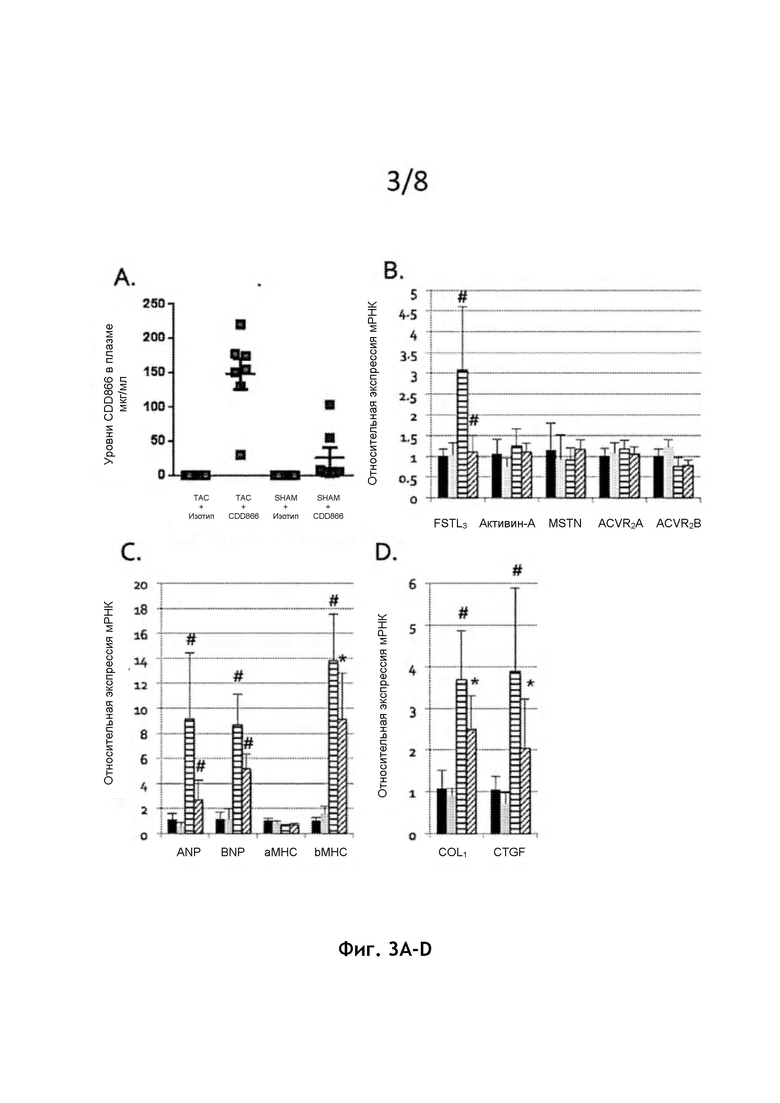
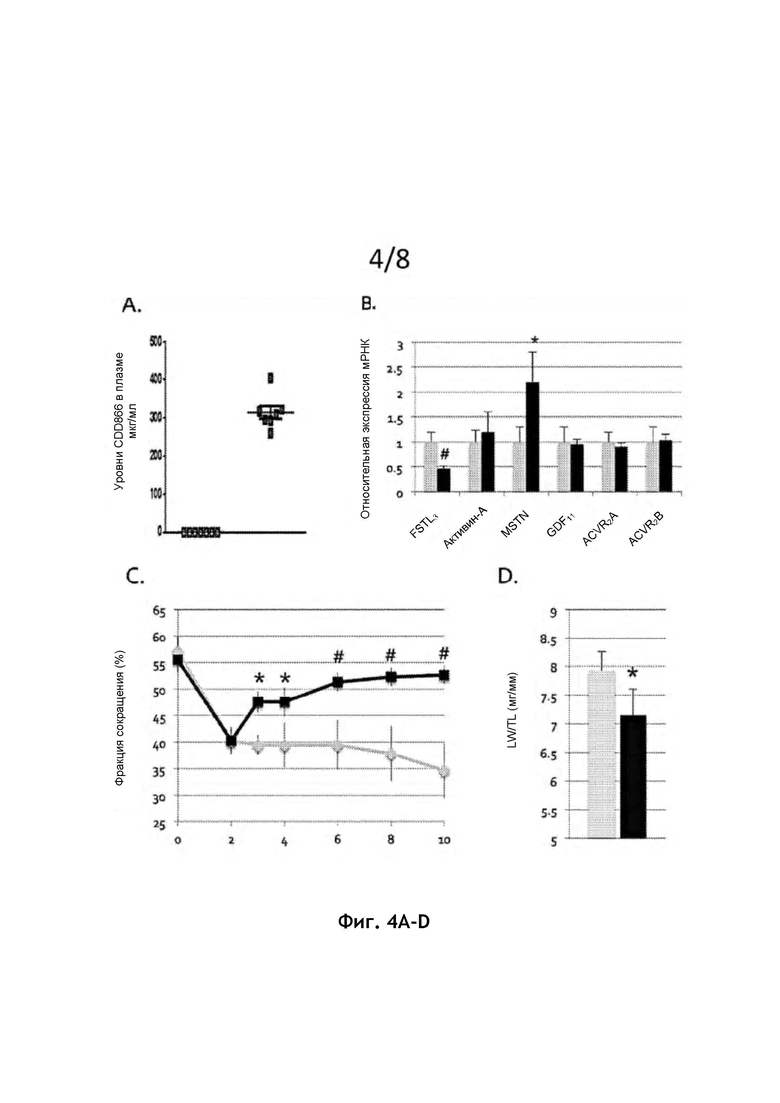
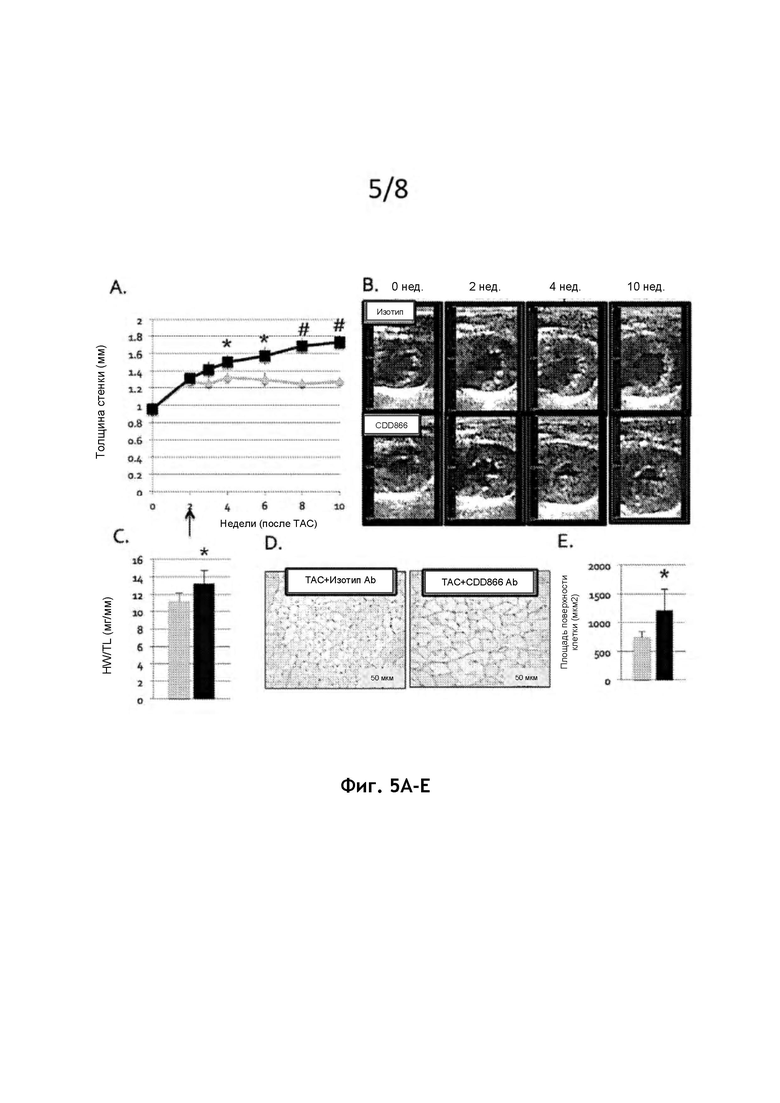
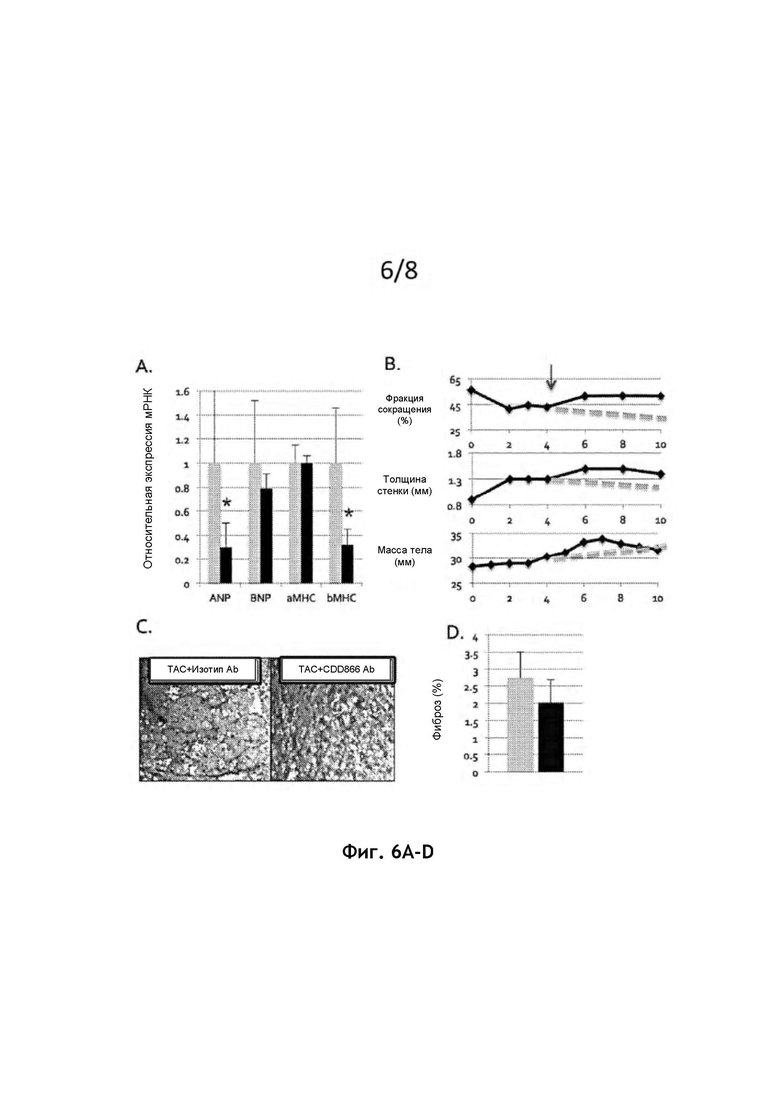
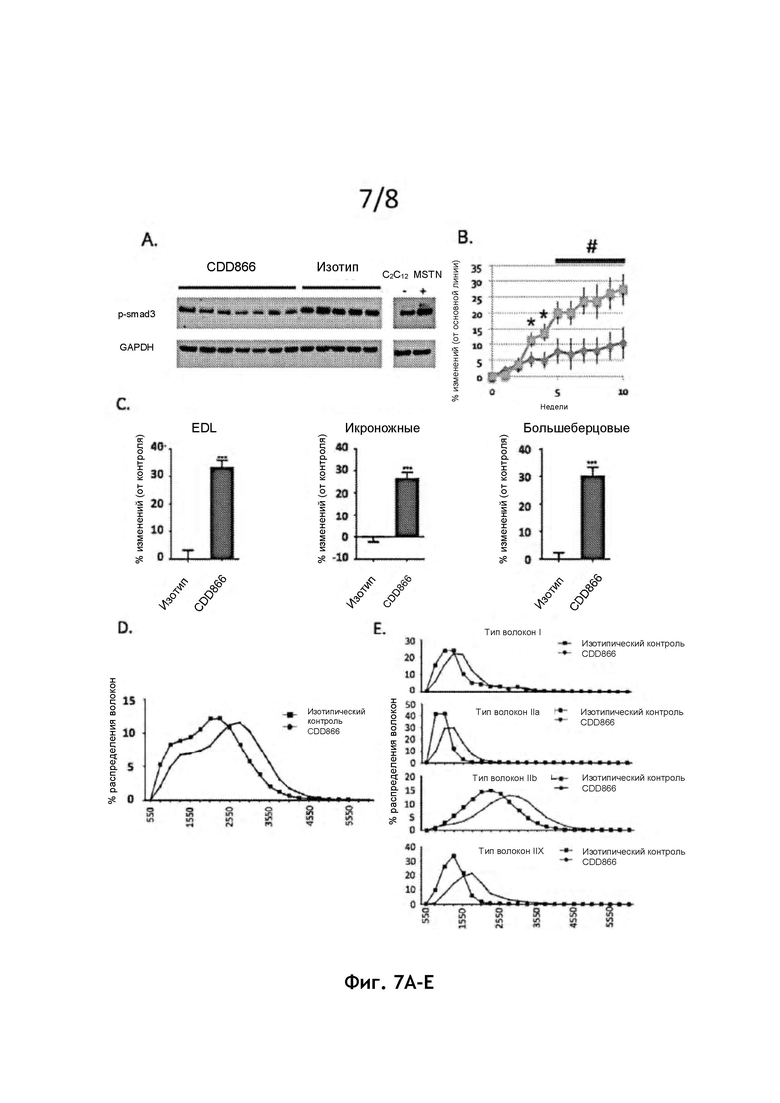
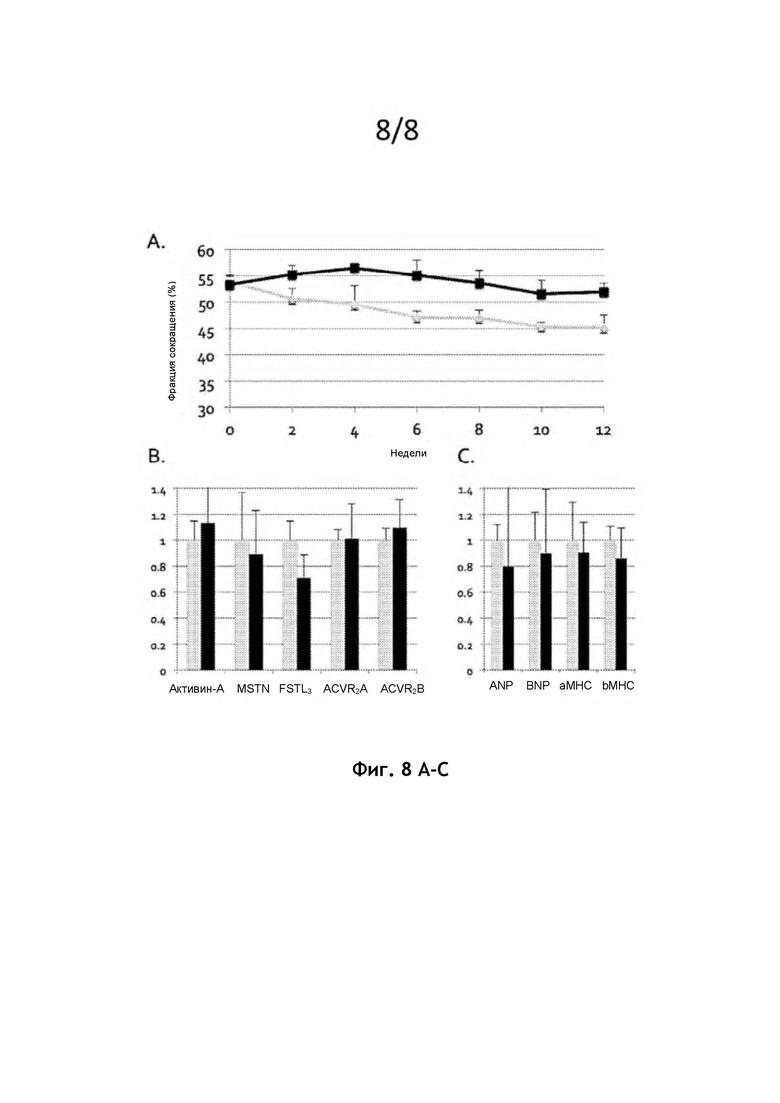
Группа изобретений относится к области биотехнологии, а именно к новым применениям и методам профилактики или лечения сердечной недостаточности. Предложены применения антитела против рецептора ActRII для лечения или профилактики сердечной недостаточности или для изготовления лекарственного средства для лечения или профилактики сердечной недостаточности. Антитело против рецептора ActRII содержит CDR1-3 тяжелой цепи c SEQ ID NO: 9, 23, 37 соответственно, и CDR1-3 легкой цепи c SEQ ID NO: 51, 65, 79 соответственно. Сердечная недостаточность вызвана или связана по меньшей мере с одним из следующих состояний: порок сердца, ишемическая болезнь сердца, гипертония, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсические или инфекционные агенты, генетическая кардиомиопатия или идиопатическая дилатационная кардиомиопатия. Изобретения приводят к улучшению сердечной функции при различных видах сердечных заболеваний. 2 н. и 6 з.п. ф-лы, 8 ил, 3 пр.
1. Применение антитела против рецептора ActRII для лечения или профилактики сердечной недостаточности, при котором сердечная недостаточность вызвана или связана по меньшей мере с одним из следующих состояний: порок сердца, ишемическая болезнь сердца, гипертония, диабет, старение, аритмия, кардиомиопатия при родах, стрессовая кардиомиопатия, токсические или инфекционные агенты, генетическая кардиомиопатия или идиопатическая дилатационная кардиомиопатия, где антитело против рецептора ActRII содержит вариабельную область CDR1 тяжелой цепи c SEQ ID NO: 9, вариабельную область CDR2 тяжелой цепи c SEQ ID NO: 23, вариабельную область CDR3 тяжелой цепи c SEQ ID NO: 37, вариабельную область CDR1 легкой цепи c SEQ ID NO: 51, вариабельную область CDR2 легкой цепи c SEQ ID NO: 65 и вариабельную область CDR3 легкой цепи c SEQ ID NO: 79.
2. Применение антитела против рецептора ActRII для изготовления лекарственного средства для лечения или профилактики сердечной недостаточности, где антитело против рецептора ActRII содержит вариабельную область CDR1 тяжелой цепи c SEQ ID NO: 9, вариабельную область CDR2 тяжелой цепи c SEQ ID NO: 23, вариабельную область CDR3 тяжелой цепи c SEQ ID NO: 37, вариабельную область CDR1 легкой цепи c SEQ ID NO: 51, вариабельную область CDR2 легкой цепи c SEQ ID NO: 65 и вариабельную область CDR3 легкой цепи c SEQ ID NO: 79.
3. Применение антитела против рецептора ActRII для лечения или профилактики сердечной недостаточности по п. 1, где указанный порок сердца представляет собой аортальный стеноз.
4. Применение антитела против рецептора ActRII по любому из пп. 1-3, где антитело против рецептора ActRII связывается с эпитопом ActRII В, состоящим из аминокислот 19-134 SEQ ID NO: 181, которому присвоен SEQ ID NO: 182.
5. Применение антитела против рецептора ActRII по любому из пп. 1-4, где антитело содержит полноразмерную аминокислотную последовательность тяжелой цепи, имеющую по меньшей мере 95% идентичность последовательности SEQ ID NO: 146.
6. Применение антитела против рецептора ActRII по любому из пп. 1-5, где антитело содержит полноразмерную аминокислотную последовательность легкой цепи, имеющую по меньшей мере 95% идентичность последовательности SEQ ID NO: 141.
7. Применение антитела против рецептора ActRII по любому из пп. 1-6, в котором антитело против рецептора ActRII представляет собой бимагрумаб.
8. Применение антитела против рецептора ActRII для изготовления лекарственного средства для лечения или профилактики сердечной недостаточности по п. 2, при котором сердечная недостаточность вызвана или связана с пороком сердца, где указанный порок сердца представляет собой аортальный стеноз.
| Токарный резец | 1924 |
|
SU2016A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
| WO 2010125003 A1, 04.11.2010 | |||
| WO 2015022658 A2, 19.02.2015 | |||
| RU 2015120804 A, 27.12.2016. | |||
Авторы
Даты
2024-11-18—Публикация
2018-03-20—Подача