ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[1] Настоящее изобретение относится к применению антител, биспецифических антител и их антигенсвязывающих фрагментов, а также конъюгатов антитело-лекарственное средство таких антител, которые специфически связывают рецептор фактора роста гепатоцитов (c-Met или MET) и модулируют передачу сигнала MET, для лечения рака глаза, включая увеальную меланому.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[2] Официальная копия перечня последовательностей подана одновременно с описанием в электронном виде через EFS-Web в виде перечня последовательностей в формате ASCII с именем файла 10548WO01_SEQ_LIST_ST25.TXT, дата создания 20 февраля 2020 г., и размером приблизительно 140 килобайт. Перечень последовательностей, содержащийся в данном документе в формате ASCII, является частью настоящего описания и включен в данный документ посредством ссылки во всей своей полноте.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[3] Увеальная меланома является наиболее распространенной первичной внутриглазной злокачественной опухолью у взрослых, составляя 79-81% всех случаев поражения меланомой глаза. Показатели заболеваемости в США оцениваются в 5 на миллион населения, в то время как показатели заболеваемости в Европе находятся в диапазоне от 2 до 8 на миллион населения в зависимости от широты, со снижением заболеваемости с севера на юг. Увеальная меланома характеризуется высокой тенденцией к метастазированию, что приводит к неблагоприятному долгосрочному прогнозу, при этом смерть наступает более чем в 50% случаев.
[4] Фактор роста гепатоцитов (HGF) (иначе называемый рассеивающим фактором [SF]) представляет собой гетеродимерный паракринный фактор роста, который проявляет свою активность посредством взаимодействия с рецептором HGF (HGFR). HGFR является продуктом онкогена c-Met и также известен как MET. MET представляет собой рецепторную тирозинкиназу, состоящую из трансмембранной бета-цепи, связанной посредством дисульфидного мостика с внеклеточной альфа-цепью. Связывание HGF с MET активирует киназную каталитическую активность MET, что приводит к фосфорилированию Tyr 1234 и Tyr 1235 бета-цепи и последующей активации нижележащих сигнальных путей.
[5] Линии опухолевых клеток, характеризующиеся амплификацией гена MET, в высокой степени зависят от MET в отношении роста и выживания. Различные моновалентные блокирующие МЕТ антитела находятся в клинической разработке для лечения различных видов рака (см. патенты США №№5686292; 5646036; 6099841; 7476724; 9260531; и 9328173; и публикации заявок на патент США №2014/0349310 и №2005/0233960). Такие антитела включают онартузумаб (MetMab) и эмибетузумаб (Xiang et al., Clin. Cancer Res. 19(18): 5068-78, 2013, и Rosen et al., Clin. Cancer Res., опубликовано 10 октября 2016 г., doi: 10.1158/1078-0432.CCR-16-1418). Некоторые из данных антител блокируют лиганд-зависимую передачу сигнала MET, но не так эффективны в блокировании лиганд-независимой активации MET.
[6] Опухоли при увеальной меланоме характеризуются мутациями в G-белках (GNAQ и GNA11) и высокой экспрессией c-Met. Нацеливание на c-Met при увеальной меланоме приводит к подавлению инвазии клеток и метастазирования, однако не супрессирует рост опухоли. Показатель локального контроля опухоли и сохранения глазного яблока со временем улучшился, но показатель выживаемости остается относительно неизменным. Конъюгаты антитело-лекарственное средство (ADC) были усовершенствованы в последние годы, некоторые из них одобрены FDA для применения, но до настоящего времени ни один из них не был разработан для лечения увеальной меланомы. Остается значительная неудовлетворенная медицинская потребность в улучшенных противораковых лекарственных средствах для применения в лечении рака глазного яблока, включая увеальную меланому, которые эффективно блокируют как лиганд-зависимую, так и лиганд-независимую передачу сигнала МЕТ.
КРАТКОЕ ОПИСАНИЕ
[7] В настоящем документе предусмотрены способы лечения рака глаза, такого как увеальная меланома, орбитальная лимфома, ретинобластома и медуллоэпителиома. Способы включают лечение с помощью антител, антигенсвязывающих фрагментов антител, комбинаций бивалентных моноспецифических антител или биспецифических антител, которые связывают рецепторный белок c-Met человека (MET x MET). Антитела к MET и их антигенсвязывающие части можно использовать отдельно в немодифицированной форме или можно включать в качестве части конъюгата антитело-лекарственное средство (ADC) или биспецифического антитела. Антитела и ADC применимы, inter alia, для нацеливания на опухолевые клетки, которые экспрессируют MET, и, таким образом, применимы в способах лечения рака глаза, раскрытых в данном документе.
[8] Другие варианты осуществления будут очевидны из обзора следующего подробного описания.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[9] На фигуре 1 представлена матрица, иллюстрирующая компоненты 272 иллюстративных биспецифических антител к MET x MET, раскрытых в данном документе. Каждая пронумерованная ячейка матрицы идентифицирует уникальное биспецифическое антитело, содержащее антигенсвязывающий домен «D1» и антигенсвязывающий домен «D2», где антигенсвязывающий домен D1 содержит вариабельный домен иммуноглобулина (пара аминокислотных последовательностей HCVR/LCVR) или CDR из соответствующего антитела к MET, указанные вдоль оси Y, и где антигенсвязывающий домен D2 содержит вариабельный домен иммуноглобулина (пара аминокислотных последовательностей HCVR/LCVR) или CDR из соответствующего антитела к MET, указанные вдоль оси X.
[10] На фигуре 2 представлена схема репортерного анализа с применением люциферазы, используемого для оценки индуцируемой антителом активации пути MET или блокады антителом индуцированной HGF активации пути в клетках HEK293T, содержащих конструкцию на основе репортерного гена SRE-люцифераза.
[11] На фигуре 3 представлен линейный график, демонстрирующий единицы относительной светимости (RLU), представляющие экспрессию гена SRE-люцифераза, в зависимости от концентрации антитела, выраженной посредством логарифма молей на литр. Закрашенные квадраты (■) представляют собой исходное бивалентное моноспецифическое антитело H4H13306P2, закрашенные пирамиды (▲) представляют собой исходное бивалентное моноспецифическое антитело H4H13312P2, закрашенные круги (•) представляют собой моновалентное антитело, закрашенные ромбы (♦) представляют собой изотипический контроль, а закрашенные перевернутые пирамиды (▼) представляют собой отсутствие лиганда. На фигуре 3A показано только антитело без лиганда HGF. На фигуре 3B показаны антитела плюс лиганд HGF.
[12] На фигуре 4 представлен линейный график, демонстрирующий единицы относительной светимости (RLU), представляющие экспрессию гена SRE-люцифераза, в зависимости от концентрации антитела, выраженной посредством логарифма молей на литр. Закрашенные квадраты (■) представляют собой моновалентное антитело к MET, закрашенные круги (●) представляют собой биспецифическое антитело к MET x MET, а закрашенные ромбы (♦) представляют собой исходное антитело H4H13312P2. На фигуре 4A показано только антитело без лиганда HGF. На фигуре 4B показаны антитела плюс лиганд HGF.
[13] На фигуре 5 представлена столбчатая диаграмма, демонстрирующая относительный клеточный рост клеток SNU5 рака желудка с амплификацией MET в зависимости от обработки с помощью человеческих бивалентных моноспецифических антител к MET 1-18, контрольного антитела и моновалентного антитела к MET. В целях сравнения, антитело 8 (абсцисса) является исходным антителом H4H13306P2, а антитело 11 (абсцисса) является исходным антителом H4H13312P2.
[14] На фигуре 6 представлены столбчатые диаграммы, демонстрирующие относительный клеточный рост клеток с амплификацией MET в зависимости от обработки с помощью биспецифического антитела к MET x MET, контрольного антитела и моновалентного антитела к MET. На фигуре 6A показан относительный рост клеток SNU5 в зависимости от обработки с помощью контрольного антитела, моновалентного антитела при 0,1, 1 и 10 мкг/мл и биспецифического антитела к MET x MET при 0,1, 1 и 10 мкг/мл. На фигуре 6B показан относительный рост клеток EBC-1 в зависимости от обработки с помощью контрольного антитела и биспецифического антитела к MET x MET при 0,1 и 1 мкг/мл.
[15] На фигуре 7 показаны результаты иммуноблоттинга pMET (фосфорилированного MET), MET, pErk (фосфорилированного Erk) и тубулина (для контроля нагрузки), выделенных из клеток Hs746T после обработки с помощью контрольного антитела и биспецифического антитела к MET x MET (фигура 7A), а также экспрессии MET (и тубулина в качестве контроля нагрузки) в клетках Hs746T после обработки с помощью биспецифического антитела к MET x MET в течение 0, 2 и 6 часов (фигура 7B).
[16] На фигуре 8 показан результат иммуноблоттинга pMET, MET, pErk и тубулина (для контроля нагрузки), выделенных из клеток Hs746T после обработки с помощью контрольного антитела, биспецифического антитела к MET x MET, моноспецифического бивалентного исходного антитела 1 к MET, моноспецифического бивалентного исходного антитела 2 к MET и комбинации исходных антител 1 и 2.
[17] На фигуре 9 показан результат иммуноблоттинга экспрессии MET (и тубулина в качестве контроля нагрузки) в клетках Hs746T после обработки с помощью контрольного антитела и биспецифического антитела к MET x MET в течение 2, 6 и 18 часов.
[18] На фигуре 10 показаны результаты иммуноблоттинга pMET, MET, pErk и тубулина (для контроля нагрузки), выделенных из клеток SNU5 после обработки с помощью контрольного антитела и биспецифического антитела к MET x MET (фигура 10A); и экспрессия MET (и тубулина в качестве контроля нагрузки) в клетках SNU5 после обработки с помощью контрольного антитела и моновалентного антитела к MET (фигура 10B).
[19] На фигуре 11 показан результат иммуноблоттинга pMET, MET, pErk и тубулина (для контроля нагрузки), выделенных из клеток EBC-1 после обработки с помощью контрольного антитела и биспецифического антитела к MET x MET.
[20] На фигуре 12 представлен линейный график, демонстрирующий изменение объема опухоли EBC-1 в кубических миллиметрах в зависимости от времени в днях после имплантации клеток EBC-1 животным, обработанным с помощью контрольного антитела (закрашенный квадрат ■), моновалентного антитела к MET (закрашенный кружок •) или биспецифического антитела к MET x MET (закрашенный ромб ♦).
[21] На фигуре 13 представлены столбчатые диаграммы, демонстрирующие относительный клеточный рост клеток с амплификацией MET в зависимости от обработки с помощью биспецифического антитела к MET x MET, контрольного антитела и моновалентного антитела к MET. На фигуре 13A показан относительный рост клеток Hs746T в зависимости от обработки с помощью контрольного антитела, биспецифического антитела к MET x MET, исходного моноспецифического антитела 1 к MET x MET, исходного моноспецифического антитела 2 к MET x MET и комбинации исходных антител 1 и 2. На фигуре 13B показан относительный рост клеток Hs746T в зависимости от обработки с помощью контрольного антитела, моновалентного антитела при 1, 10 и 25 мкг/мл и биспецифического антитела к MET x MET при 1, 10 и 25 мкг/мл.
[22] На фигуре 14 представлена столбчатая диаграмма, демонстрирующая относительный клеточный рост клеток NCI-H596 в зависимости от обработки с помощью контрольного антитела (C), биспецифического антитела к MET x MET (MM), исходного моноспецифического антитела 1 к MET x MET (M1), исходного моноспецифического антитела 2 к MET x MET (M2), комбинации исходных антител 1 и 2 (M1M2) и фактора роста гепатоцитов (HGF), являющегося агонистом MET.
[23] На фигуре 15 представлен линейный график, демонстрирующий изменение объема опухоли Hs746T в кубических миллиметрах в зависимости от времени в днях после имплантации клеток Hs746T животным, которых обрабатывали с помощью контрольного антитела (закрашенный квадрат ■), моновалентного антитела к MET (закрашенный кружок •) или биспецифического антитела к MET x MET (закрашенный ромб ♦).
[24] На фигуре 16A представлен линейный график, демонстрирующий изменение объема опухоли SNU5 в кубических миллиметрах в зависимости от времени в днях после имплантации клеток SNU5 животным, обработанным с помощью контрольного антитела (закрашенный квадрат ■), моновалентного антитела к MET при 1 мг/мл (закрашенный круг •), моновалентного антитела к MET при 10 мг/мл (незакрашенный круг ○), биспецифического антитела к MET x MET при 1 мг/мл (закрашенный ромб ♦) или биспецифического антитела к MET x MET при 10 мг/мл (незакрашенный ромб ◊).
[25] На фигуре 16B представлен результат иммуноблоттинга pMET, MET и тубулина (контроль нагрузки), выделенных из опухоли SNU5, удаленной из мышиной модели ксенотрансплантата, после обработки с помощью контрольного антитела, 10 мг/кг моновалентного антитела к MET и 10 мг/кг биспецифического антитела к MET x MET.
[26] На фигуре 17 представлен линейный график, демонстрирующий изменение объема опухоли U87-MG в кубических миллиметрах в зависимости от времени в днях после имплантации клеток U87-MG животным, обработанным с помощью контрольного антитела (закрашенный квадрат ■), моновалентного антитела к MET (закрашенный кружок •) или биспецифического антитела к MET x MET (закрашенный ромб ♦).
[27] На фигуре 18 представлен линейный график, демонстрирующий изменение объема опухоли U118-MG в кубических миллиметрах в зависимости от времени в днях после имплантации клеток U118-MG животным, обработанным с помощью контрольного антитела (закрашенный квадрат ■), моновалентного антитела к MET (закрашенный кружок •) или биспецифического антитела к MET x MET (незакрашенный ромб ◊).
[28] На фигуре 19 представлена схема, иллюстрирующая синтез майтанзиноида 6.
[29] На фигуре 20 представлена схема, иллюстрирующая синтез промежуточного соединения 1 майтанзиноида.
[30] На фигуре 21A, фигуре 21B, фигуре 21C и фигуре 21D представлены линейные графики, демонстрирующие изменение жизнеспособности клеток в четырех линиях клеток увеальной меланомы, экспрессирующих c-Met, обработанных с помощью двух разных концентраций биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B (закрашенный круг •), по сравнению с изотипическим антителом, конъюгированным с майтанзиноидом B (закрашенный треугольник ▲), в течение 7 дней.
[31] На фигуре 22A и фигуре 22B представлены линейные графики, демонстрирующие изменение жизнеспособности клеток OMM1.3, экспрессирующих c-Met, по сравнению с c-Met-отрицательными клетками OCM3 при обработке с помощью биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B (от 0,3 до 10 нМ) (линия с поперечными штрихами), или изотипического антитела, конъюгированного с майтанзиноидом B (закрашенный квадрат ■), в течение 7 дней.
[32] На фигуре 23 и фигуре 24 представлены столбчатые диаграммы, демонстрирующие процент апоптоза, обусловленного обработкой клеток увеальной меланомы с помощью двух разных концентраций (1,25 нМ, фигура 23; 2,5 нМ, фигура 24) биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B, по сравнению с изотипическим антителом, конъюгированным с майтанзиноидом B.
[33] На фигуре 25, фигуре 26 и фигуре 27 представлены гистограммы (со вставленными графиками бокового светорассеяния), демонстрирующие распределение клеток в каждой из фаз роста после обработки с помощью биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B, по сравнению с изотипическим антителом, конъюгированным с майтанзиноидом B. Тестировали две линии c-Met-положительных клеток, OMM1.3 (фигура 25) и Mel202 (фигура 26), и сравнивали с линией c-Met-отрицательных клеток OCM3 (фигура 27).
[34] На фигуре 28 представлено изображение результатов вестерн-блоттинга, демонстрирующее уровни экспрессии c-Met в нескольких линиях клеток увеальной меланомы, а также SNU-5, линии клеток карциномы желудка в качестве положительного контроля, известной высокой экспрессией c-Met, и A549, линии клеток карциномы легкого, которая также экспрессирует c-Met.
[35] На фигуре 29 представлено изображение результатов вестерн-блоттинга, демонстрирующее расщепление PARP и фосфорилирование гистона H3 в трех линиях клеток увеальной меланомы после 24 часов обработки с помощью биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B, по сравнению с изотипическим антителом, конъюгированным с майтанзиноидом B.
[36] На фигуре 30 представлено изображение результатов вестерн-блоттинга, демонстрирующее зависимую от времени индукцию расщепления PARP, экспрессию белка c-Met и фосфорилирование гистона H3 в c-Met-положительной линии клеток OMM1.3 по сравнению с c-Met-отрицательной линией клеток OCM3 после обработки с помощью биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B, по сравнению с изотипическим антителом, конъюгированным с майтанзиноидом B.
[37] На фигуре 31 проиллюстрирован спектр ‘H-NMR майтанзин-3-N-метил-L-аланин-пропанамидил-3-тио-3-сукцинимидил-N-метилциклогексил-4-транс-карбоксисукцината. Спектр не усложнен резонансами, присущими смеси, и соответствует одному диастереомеру, присутствующему в по меньшей мере 95% диастереомерном избытке.
[38] На фигуре 32 представлены изображения, демонстрирующие подавление клеточной инвазии для клеток OMM1.3, обработанных с помощью увеличивающихся доз контрольного антитела, контрольного ADC, MET x MET и MET x MET-ADC при применении 50 нг/мл HGF в качестве хемоаттрактанта. Антитело к MET x MET и MET x MET-ADC эффективно подавляют инвазию клеток в пикомолярных дозах, при которых жизнеспособность клеток не нарушается.
[39] На фигуре 33 проиллюстрировано дозозависимое снижение жизнеспособности клеток увеальной меланомы, обработанных с помощью биспецифического антитела к c-Met, конъюгированного с майтанзиноидом B, по сравнению с изотипическим антителом, конъюгированным с майтанзиноидом B.
ПОДРОБНОЕ ОПИСАНИЕ
[40] Перед описанием настоящего изобретения необходимо понимать, что настоящее изобретение не ограничивается конкретными описанными способами и условиями экспериментов, поскольку такие способы и условия могут варьироваться. Также следует понимать, что терминология, используемая в данном документе, предназначена только для целей описания конкретных вариантов осуществления и не предназначена для ограничения, поскольку объем настоящего изобретения будет ограничиваться только прилагаемой формулой изобретения.
[41] Если не указано иное, то все технические и научные термины, используемые в данном документе, имеют такое же значение, как это обычно понимает специалист в области техники, к которой принадлежит данная технология. Используемый в данном документе термин «приблизительно» при использовании в отношении конкретного указанного числового значения означает, что значение может отличаться от указанного значения на не более чем 1%. Например, используемое в данном документе выражение «приблизительно 100» включает 99 и 101 и все значения между ними (например, 99,1, 99,2, 99,3, 99,4 и т.д.).
[42] Хотя при практическом осуществлении или тестировании настоящего изобретения можно применять любые способы и материалы, сходные с описанными в данном документе или эквивалентные им, в данном документе описаны только предпочтительные способы и материалы. Все патенты, заявки на патент и непатентные публикации, упомянутые в данном описании, включены в данный документ посредством ссылки во всей своей полноте.
БЕЛОК MET
[43] Выражения «MET,» «c-Met» и тому подобные, используемые в данном документе, относятся к трансмембранной рецепторной тирозинкиназе человека, содержащей (1) аминокислотную последовательность, указанную под SEQ ID NO:145, и/или характеризующуюся аминокислотной последовательностью, указанной в NCBI под номером доступа NM_001127500.2, представляющую собой непроцессированный препробелок изоформы «a», (2) аминокислотную последовательность, указанную под SEQ ID NO:146, и/или характеризующуюся аминокислотной последовательностью, указанной в NCBI под номером доступа NM_000236.2, представляющую собой непроцессированный препробелок изоформы «b», (3) аминокислотную последовательность, указанную под SEQ ID NO:147, и/или характеризующуюся аминокислотной последовательностью, указанной в NCBI под номером доступа NM_001311330.1, представляющую собой непроцессированный препробелок изоформы «c», и/или (3) зрелый белок, содержащий цитоплазматическую альфа-субъединицу (SEQ ID NO:148), общую для всех трех изоформ, и трансмембранную бета-субъединицу (SEQ ID NO:149, 150 или 151 для изоформ a, b и c соответственно). Выражение «MET» включает как мономерные, так и мультимерные молекулы МЕТ. Используемое в данном документе выражение «мономерный MET человека» означает белок МЕТ или его часть, которые не содержат или не имеют в своем составе каких-либо доменов мультимеризации и которые существуют в нормальных условиях в виде одной молекулы MET без непосредственного физического соединения с другой молекулой MET. Иллюстративной мономерной молекулой MET является молекула, называемая в данном документе «hMET.mmh», содержащая аминокислотную последовательность под SEQ ID NO:152 (см., например, пример 3 в данном документе). Используемое в данном документе выражение «димерный МЕТ человека» означает конструкцию, содержащую две молекулы МЕТ, соединенные друг с другом посредством линкера, ковалентной связи, нековалентной связи или посредством домена мультимеризации, такого как Fc-домен антитела. Иллюстративной димерной молекулой MET является молекула, называемая в данном документе «hMET.mFc», содержащая аминокислотную последовательность под SEQ ID NO:153 (см., например, пример 3 в данном документе).
[44] Все ссылки на белки, полипептиды и фрагменты белка в данном документе относятся к человеческой версии соответствующего белка, полипептида или фрагмента белка, если явно не указано, что они получены от видов, отличных от человека. Таким образом, выражение «MET» означает MET человека, если не указано, что он получен от видов, отличных от человека, например, «MET мыши», «MET обезьяны» и т.д.
[45] Используемое в данном документе выражение «MET, экспрессируемый на клеточной поверхности», означает один или более белков МЕТ или его внеклеточный домен, которые экспрессируются на поверхности клетки in vitro или in vivo таким образом, что по меньшей мере часть белка МЕТ располагается на внеклеточной стороне клеточной мембраны и доступна для антигенсвязывающей части антитела. «MET, экспрессируемый на клеточной поверхности», может содержать белок МЕТ, экспрессируемый на поверхности клетки, которая обычно экспрессирует белок МЕТ, или состоять из него. В качестве альтернативы, «MET, экспрессируемый на клеточной поверхности», может содержать белок MET, экспрессируемый на поверхности клетки, которая обычно не экспрессирует MET человека на своей поверхности, но была искусственно сконструирована для экспрессии МЕТ на своей поверхности, или состоять из него.
ТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ ЛЕЧЕНИЯ РАКА ГЛАЗА
[46] В данном документе предусмотрены способы лечения рака глаза, такого как, например, увеальная меланома, орбитальная лимфома, ретинобластома и медуллоэпителиома. В некоторых аспектах способ включает введение субъекту, нуждающемуся в этом, терапевтической композиции, содержащей антитело к MET или биспецифическую антигенсвязывающую молекулу MET x MET (например, антитело к MET, содержащее любую из последовательностей HCVR/LCVR или CDR, указанных в таблице 1 в данном документе, или биспецифическую антигенсвязывающую молекулу MET x MET, содержащую любой из компонентов D1 и D2, указанных в таблице 5 в данном документе, или антитело к MET, выбранное из группы, состоящей из онартузумаба, эмибетузумаба, телизотузумаба, SAIT301, ARGX-111, Sym015, HuMax-cMet и CE-355621). В некоторых вариантах осуществления антитело к MET или биспецифическая антигенсвязывающая молекула MET x MET конъюгированы с цитотоксическим соединением, таким как майтанзиноид, как подробно описано ниже. Терапевтическая композиция может содержать любое из антител к MET или биспецифических антигенсвязывающих молекул MET x MET, раскрытых в данном документе, включая ADC к MET или биспецифическую антигенсвязывающую молекулу MET x MET, конъюгированную с цитотоксическим средством, и фармацевтически приемлемый носитель или разбавитель.
[47] Увеальная меланома является наиболее распространенной злокачественной первичной внутриглазной опухолью у взрослых. Данные опухоли могут возникать в сосудистой оболочке, радужной оболочке и цилиарном теле и иногда называются меланомами радужной оболочки или цилиарного тела. Увеальная меланома является в высокой степени метастатической. Другие виды рака глаза включают орбитальную лимфому, ретинобластому и медуллоэпителиому, последняя из которых может возникать в цилиарном теле и сосудистой оболочке глазного яблока. Предполагается, что способы, раскрытые в данном документе, применимы в лечении видов рака глаза, таких как орбитальная лимфома, ретинобластома и медуллоэпителиома. В некоторых аспектах лечение включает подавление или снижение инвазии и/или метастазирования из первичной опухоли.
[48] Антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET, а также их конъюгаты с лекарственным средством применимы, inter alia, для лечения, предупреждения и/или снижения симптомов любого заболевания или нарушения, ассоциированного с экспрессией, передачей сигнала или активностью MET или опосредованного ими, или поддающегося лечению посредством блокирования взаимодействия между MET и HGF или подавления активности и/или передачи сигнала MET иным образом, и/или посредством стимуляции интернализации рецептора и/или снижения количества рецепторов на поверхности клетки. В частности, антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET, а также их конъюгаты с лекарственным средством применимы в лечении увеальной меланомы. Лечение включает снижение интенсивности роста опухоли при увеальной меланоме и/или инициацию регрессии увеальной меланомы у субъекта. Лечение также включает подавление или снижение инвазии клеток увеальной меланомы или подавление или снижение метастазирования увеальной меланомы из первичной опухоли.
[49] Например, антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET по настоящему изобретению применимы для лечения опухолей при увеальной меланоме, которые экспрессируют (или сверхэкспрессируют) MET. Например, антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET можно использовать для лечения первичных и/или метастатических опухолей, возникающих в глазу.
[50] Таким образом, в данном документе предусмотрен способ лечения рака глазного яблока, снижения интенсивности роста рака глазного яблока, подавления или снижения инвазии и/или метастазирования и/или индукции регрессии рака глазного яблока у субъекта. Например, в данном документе предусмотрен способ лечения увеальной меланомы, снижения интенсивности роста опухоли при увеальной меланоме, подавления или снижения инвазии и/или метастазирования и/или индукции регрессии увеальной меланомы у субъекта. В некоторых аспектах при раке глазного яблока, например увеальной меланоме, экспрессируется MET. В некоторых аспектах способ включает введение субъекту, нуждающемуся в этом, конъюгата антитело-лекарственное средство (ADC), содержащего биспецифическую антигенсвязывающую молекулу и цитотоксин, где биспецифическая антигенсвязывающая молекула содержит первый антигенсвязывающий домен (D1) и второй антигенсвязывающий домен (D2), где D1 специфически связывает первый эпитоп МЕТ человека, и где D2 специфически связывает второй эпитоп МЕТ человека.
[51] Дополнительно в данном документе предусмотрен способ подавления пролиферации, подавления инвазии, инициации апоптоза и/или снижения жизнеспособности клетки увеальной меланомы. В некоторых вариантах осуществления способ включает приведение клетки в контакт с конъюгатом антитело-лекарственное средство (ADC), содержащим биспецифическую антигенсвязывающую молекулу и цитотоксин. В некоторых вариантах осуществления биспецифическая антигенсвязывающая молекула содержит первый антигенсвязывающий домен (D1) и второй антигенсвязывающий домен (D2), где D1 специфически связывает первый эпитоп МЕТ человека, и где D2 специфически связывает второй эпитоп МЕТ человека.
[52] Также дополнительно в данном документе предусмотрен способ индукции остановки митоза клетки увеальной меланомы. В некоторых вариантах осуществления способ включает приведение клетки в контакт с конъюгатом антитело-лекарственное средство (ADC), содержащим биспецифическую антигенсвязывающую молекулу и цитотоксин, где биспецифическая антигенсвязывающая молекула содержит первый антигенсвязывающий домен (D1) и второй антигенсвязывающий домен (D2), где D1 специфически связывает первый эпитоп МЕТ человека, и где D2 специфически связывает второй эпитоп МЕТ человека.
[53] Также в данном документе предусмотрен способ лечения рака глазного яблока у субъекта, пораженного опухолью, экспрессирующей c-Met. В некоторых вариантах осуществления способ включает введение субъекту биспецифической антигенсвязывающей молекулы, содержащей первый антигенсвязывающий домен (D1) и второй антигенсвязывающий домен (D2), где D1 специфически связывает первый эпитоп МЕТ человека, и где D2 специфически связывает второй эпитоп МЕТ человека. В некоторых аспектах биспецифическая антигенсвязывающая молекула конъюгирована с цитотоксином с образованием конъюгата антитело-лекарственное средство (ADC). В некоторых аспектах цитотоксин представляет собой майтанзиноид.
[54] Различные аспекты биспецифической антигенсвязывающей молекулы и различные аспекты цитотоксина представлены в следующих абзацах, хотя более подробно они описаны в другом месте данного документа.
[55] В некоторых аспектах D1 и D2 не конкурируют друг с другом за связывание с МЕТ человека. В некоторых аспектах первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO: 155. В некоторых аспектах второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO: 155. В некоторых аспектах первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO: 155; и второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO: 155.
[56] В некоторых вариантах осуществления D1 содержит три определяющие комплементарность области тяжелой цепи (HCDR1, HCDR2 и HCDR3) в пределах вариабельной области тяжелой цепи (HCVR), содержащей аминокислотную последовательность под SEQ ID NO: 58 или SEQ ID NO: 18, и три определяющие комплементарность области легкой цепи (LCDR1, LCDR2 и LCDR3) в пределах вариабельной области легкой цепи (LCVR), содержащей аминокислотную последовательность под SEQ ID NO:138. В некоторых вариантах осуществления D2 содержит три определяющие комплементарность области тяжелой цепи (HCDR1, HCDR2 и HCDR3) в пределах вариабельной области тяжелой цепи (HCVR), содержащей аминокислотную последовательность под SEQ ID NO: 82, и три определяющие комплементарность области легкой цепи (LCDR1, LCDR2 и LCDR3) в пределах вариабельной области легкой цепи (LCVR), содержащей аминокислотную последовательность под SEQ ID NO: 138.
[57] В некоторых вариантах осуществления биспецифическая антигенсвязывающая молекула содержит CDR в пределах аминокислотной последовательности D1-HCVR под SEQ ID NO: 58 и CDR в пределах аминокислотной последовательности D2-HCVR под SEQ ID NO: 82. В некоторых вариантах осуществления биспецифическая антигенсвязывающая молекула содержит CDR в пределах аминокислотной последовательности D1-HCVR под SEQ ID NO: 18 и CDR в пределах аминокислотной последовательности D2-HCVR под SEQ ID NO: 82.
[58] В некоторых аспектах D1 биспецифической антигенсвязывающей молекулы содержит три определяющие комплементарность области тяжелой цепи (HCDR1, HCDR2 и HCDR3) в пределах вариабельной области тяжелой цепи (HCVR), содержащей аминокислотную последовательность под SEQ ID NO:58 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей, и три определяющие комплементарность области легкой цепи (LCDR1, LCDR2 и LCDR3) в пределах вариабельной области легкой цепи (LCVR), содержащей аминокислотную последовательность под SEQ ID NO:138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей.
[59] В некоторых аспектах HCDR1 D1 содержит аминокислотную последовательность под SEQ ID NO:60; HCDR2 содержит аминокислотную последовательность под SEQ ID NO:62; HCDR3 содержит аминокислотную последовательность под SEQ ID NO:64; LCDR1 содержит аминокислотную последовательность под SEQ ID NO:140; LCDR2 содержит аминокислотную последовательность под SEQ ID NO:142, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO:144.
[60] В некоторых аспектах D1 биспецифической антигенсвязывающей молекулы содержит HCVR, содержащую аминокислотную последовательность под SEQ ID NO: 58 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей, и LCVR, содержащую аминокислотную последовательность под SEQ ID NO: 138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей.
[61] В некоторых аспектах D1 биспецифической антигенсвязывающей молекулы содержит HCVR, содержащую аминокислотную последовательность под SEQ ID NO: 58, и LCVR, содержащую аминокислотную последовательность под SEQ ID NO: 138.
[62] В некоторых аспектах D2 биспецифической антигенсвязывающей молекулы содержит три определяющие комплементарность области тяжелой цепи (HCDR1, HCDR2 и HCDR3) в пределах вариабельной области тяжелой цепи (HCVR), содержащей аминокислотную последовательность под SEQ ID NO: 82 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей, и три определяющие комплементарность области легкой цепи (LCDR1, LCDR2 и LCDR3) в пределах вариабельной области легкой цепи (LCVR), содержащей аминокислотную последовательность под SEQ ID NO: 138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей.
[63] В некоторых аспектах HCDR1 D2 биспецифической антигенсвязывающей молекулы содержит аминокислотную последовательность под SEQ ID NO: 84; HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 86; HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 88; LCDR1 содержит аминокислотную последовательность под SEQ ID NO:140; LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 142, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 144.
[64] В некоторых аспектах D2 биспецифической антигенсвязывающей молекулы содержит HCVR, содержащую аминокислотную последовательность под SEQ ID NO: 82 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей, и LCVR, содержащую аминокислотную последовательность под SEQ ID NO: 138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична ей.
[65] В некоторых аспектах D2 биспецифической антигенсвязывающей молекулы содержит HCVR, содержащую аминокислотную последовательность под SEQ ID NO: 82, и LCVR, содержащую аминокислотную последовательность под SEQ ID NO: 138.
[66] В некоторых вариантах осуществления способов, предусмотренных в данном документе, цитотоксин выбран из группы, состоящей из биотоксинов, химиотерапевтических средств и радиоактивных изотопов. Например, цитотоксин может быть выбран из группы, состоящей из майтанзиноидов, ауристатинов, томаймицинов, дуокармицинов, 225Ac, 227Th и любых их производных. В некоторых аспектах цитотоксин конъюгирован с биспецифической антигенсвязывающей молекулой посредством линкера.
[67] Иллюстративный цитотоксин представляет собой:
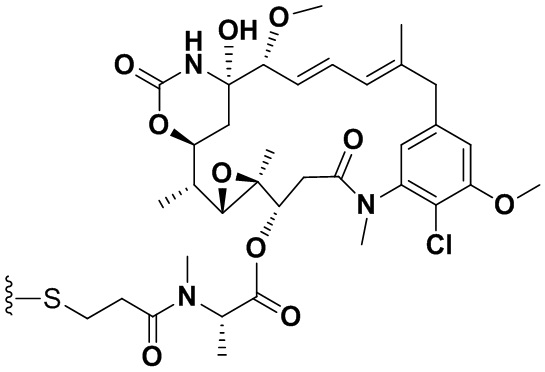
где 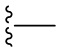 представляет собой связь с линкером. В некоторых аспектах линкер представляет собой:
представляет собой связь с линкером. В некоторых аспектах линкер представляет собой:
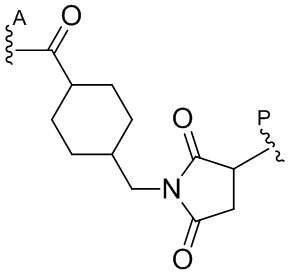
где связь, отмеченная с помощью  , представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью
, представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью  , представляет собой связь с цитотоксином.
, представляет собой связь с цитотоксином.
[68] Дополнительный иллюстративный цитотоксин представляет собой:
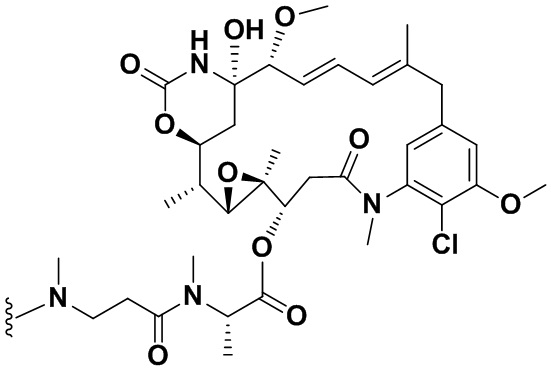
где  представляет собой связь с линкером. В некоторых аспектах линкер представляет собой
представляет собой связь с линкером. В некоторых аспектах линкер представляет собой
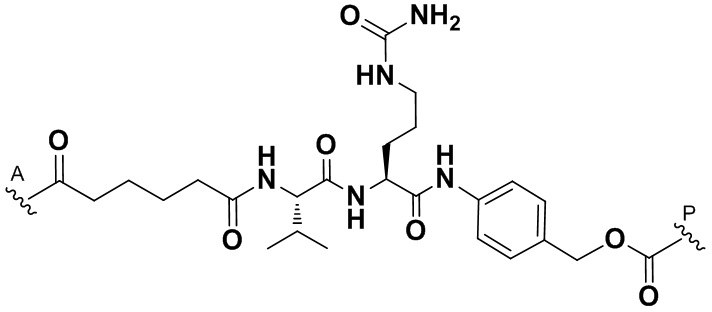
где связь, отмеченная с помощью  , представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью
, представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью  , представляет собой связь с цитотоксином.
, представляет собой связь с цитотоксином.
[69] Способы, предусмотренные в данном документе, применимы в лечении рака глаза или рака глазного яблока. В некоторых вариантах осуществления рак глазного яблока выбран из группы, состоящей из увеальной меланомы, орбитальной лимфомы, ретинобластомы и медуллоэпителиомы.
[70] В контексте способов лечения, описанных в данном документе, антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET и их конъюгаты с лекарственным средством можно вводить в виде монотерапии (т.е. в качестве единственного терапевтического средства) или в комбинации с одним или более дополнительными терапевтическими средствами (примеры которых описаны в другом месте в данном документе).
АНТИТЕЛА К MET И ИХ АНТИГЕНСВЯЗЫВАЮЩИЕ ФРАГМЕНТЫ
[71] Более подробно и в соответствии с одним аспектом антитела к MET, применимые в соответствии со способами, предусмотренными в данном документе, перечислены в таблицах 1 и 2 в данном документе. В таблице 1 указаны идентификаторы аминокислотных последовательностей вариабельных областей тяжелой цепи (HCVR), вариабельных областей легкой цепи (LCVR), определяющих комплементарность областей тяжелой цепи (HCDR1, HCDR2 и HCDR3) и определяющих комплементарность областей легкой цепи (LCDR1, LCDR2 и LCDR3) иллюстративных антител к MET, из которых могут быть получены раскрытые в данном документе биспецифические антигенсвязывающие молекулы (используемые в данном документе взаимозаменяемо с биспецифическим антигенсвязывающим белком). В таблице 2 указаны идентификаторы последовательностей нуклеиновых кислот HCVR, LCVR, HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3 иллюстративных антител к MET.
[72] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела к MET, выбранные из группы, состоящей из онартузумаба, эмибетузумаба, телизотузумаба, SAIT301, ARGX-111, Sym015, HuMax-cMet и CE-355621.
[73] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET и выступают в качестве агонистов (например, активируют) сигнального пути MET в клетках, а также применение таких антител в планах терапии, где активация передачи сигнала MET может быть полезной или терапевтически применимой. Неограничивающие примеры таких агонистических антител к MET включают антитело, называемое в данном документе «H4H14636D», а также антитела и их антигенсвязывающие фрагменты, содержащие CDR тяжелой и легкой цепей (SEQ ID NO: 28, 30, 32, 140, 142, 144) и/или их вариабельные домены тяжелой и легкой цепей (SEQ ID NO: 26/138).
[74] Применимыми в соответствии с данным документом являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие HCVR, содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCVR, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[75] Применимыми в соответствии с данным документом являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие LCVR, содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCVR, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[76] Применимыми в соответствии с данным документом являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие пару аминокислотных последовательностей HCVR и LCVR (HCVR/LCVR), содержащую любую из аминокислотных последовательностей HCVR, перечисленных в таблице 1, в паре с любой из аминокислотных последовательностей LCVR, перечисленных в таблице 1. В соответствии с определенными вариантами осуществления антитела или их антигенсвязывающие фрагменты содержат пару аминокислотных последовательностей HCVR/LCVR, содержащуюся в любом из иллюстративных антител к MET, перечисленных в таблице 1. В определенных вариантах осуществления пара аминокислотных последовательностей HCVR/LCVR выбрана из группы, состоящей из: SEQ ID NO: 2/138, 10/138, 18/138, 26/138, 34/138, 42/138, 50/138, 58/138, 66/138, 74/138, 82/138, 90/138, 98/138, 106/138, 114/138, 122/138 и 130/138.
[77] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCDR1, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[78] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCDR2, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[79] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCDR3, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[80] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCDR1, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[81] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие пару аминокислотных последовательностей HCDR1 и LCDR1 (HCDR1/LCDR1), содержащую любую из аминокислотных последовательностей HCDR1, перечисленных в таблице 1, в паре с любой из аминокислотных последовательностей LCDR1, перечисленных в таблице 1. В соответствии с определенными вариантами осуществления антитела или их антигенсвязывающие фрагменты содержат пару аминокислотных последовательностей HCDR3/LCDR3, содержащуюся в любом из иллюстративных антител к MET, перечисленных в таблице 1. В определенных вариантах осуществления пара аминокислотных последовательностей HCDR1/LCDR1 выбрана из группы, состоящей из: SEQ ID NO: 4/140, 12/140, 20/140, 28/140, 36/140, 44/140, 52/140, 60/140, 68/140, 76/140, 84/140, 92/140, 100/140, 108/140, 116/140, 124/140 и 132/140.
[82] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCDR2, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[83] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие пару аминокислотных последовательностей HCDR2 и LCDR2 (HCDR2/LCDR2), содержащую любую из аминокислотных последовательностей HCDR2, перечисленных в таблице 1, в паре с любой из аминокислотных последовательностей LCDR2, перечисленных в таблице 1. В соответствии с определенными вариантами осуществления антитела или их антигенсвязывающие фрагменты содержат пару аминокислотных последовательностей HCDR2/LCDR2, содержащуюся в любом из иллюстративных антител к MET, перечисленных в таблице 1. В определенных вариантах осуществления пара аминокислотных последовательностей HCDR2/LCDR2 выбрана из группы, состоящей из: SEQ ID NO: 6/142, 14/142, 22/142, 30/142, 38/142, 46/142, 54/142, 62/142, 70/142, 78/142, 86/142, 94/142, 102/142, 110/142, 118/142, 126/142 и 134/142.
[84] Также применимыми являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCDR3, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[85] Также применимыми в соответствии с данным документом являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие пару аминокислотных последовательностей HCDR3 и LCDR3 (HCDR3/LCDR3), содержащую любую из аминокислотных последовательностей HCDR3, перечисленных в таблице 1, в паре с любой из аминокислотных последовательностей LCDR3, перечисленных в таблице 1. В соответствии с определенными вариантами осуществления антитела или их антигенсвязывающие фрагменты содержат пару аминокислотных последовательностей HCDR3/LCDR3, содержащуюся в любом из иллюстративных антител к MET, перечисленных в таблице 1. В определенных вариантах осуществления пара аминокислотных последовательностей HCDR3/LCDR3 выбрана из группы, состоящей из: SEQ ID NO: 8/144, 16/144, 24/144, 32/144, 40/144, 48/144, 56/144, 64/144, 72/144, 80/144, 88/144, 96/144, 104/144, 112/144, 120/144, 128/144 и 136/144.
[86] Также применимыми в соответствии с данным документом являются антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержащие набор из шести CDR (т.е. HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащихся в любом из иллюстративных антител к MET, перечисленных в таблице 1. В определенных вариантах осуществления набор аминокислотных последовательностей HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3 выбран из группы, состоящей из: SEQ ID NO: 4-6-8-140-142-144, 12-14-16-140-142-144, 20-22-24-140-142-144, 28-30-32-140-142-144, 36-38-40-140-142-144, 44-44-48-140-142-144, 52-54-56-140-142-144, 60-62-64-140-142-144, 68-70-72-140-142-144, 76-78-80-140-142-144, 84-86-88-140-142-144, 92-94-96-140-142-144, 100-102-104-140-142-144, 108-110-112-140-142-144, 116-118-120-140-142-144, 124-126-128-140-142-144 и 132-134-136-140-142-144.
[87] В связанном варианте осуществления антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET и являются применимыми в способах, раскрытых в данном документе, содержат набор из шести CDR (т.е. HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащихся в паре аминокислотных последовательностей HCVR/LCVR, которая определена для любого из иллюстративных антител к MET, перечисленных в таблице 1. Например, антитела или их антигенсвязывающие фрагменты, которые специфически связывают MET, содержат набор аминокислотных последовательностей HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3, содержащихся в паре аминокислотных последовательностей HCVR/LCVR, выбранных из группы, состоящей из: SEQ ID NO: 4-6-8-140-142-144, 12-14-16-140-142-144, 20-22-24-140-142-144, 28-30-32-140-142-144, 36-38-40-140-142-144, 44-44-48-140-142-144, 52-54-56-140-142-144, 60-62-64-140-142-144, 68-70-72-140-142-144, 76-78-80-140-142-144, 84-86-88-140-142-144, 92-94-96-140-142-144, 100-102-104-140-142-144, 108-110-112-140-142-144, 116-118-120-140-142-144, 124-126-128-140-142-144 и 132-134-136-140-142-144.
[88] Способы и методики идентификации CDR в пределах аминокислотных последовательностей HCVR и LCVR хорошо известны в данной области техники и могут применяться для идентификации CDR в пределах указанных аминокислотных последовательностей HCVR и/или LCVR, раскрытых в данном документе. Иллюстративные общепринятые способы, которые можно использовать для идентификации границ CDR, включают, например, определение согласно Kabat, определение согласно Chothia и определение согласно AbM. В общих чертах, определение согласно Kabat основано на вариабельности последовательности, определение согласно Chothia основано на расположении структурных областей петли, а определение согласно AbM является компромиссным решением между подходами согласно Kabat и Chothia. См., например, Kabat, «Sequences of Proteins of Immunological Interest», National Institutes of Health, Bethesda, Md. (1991); Al-Lazikani et al., J. Mol. Biol. 273:927-948 (1997); и Martin et al., Proc. Natl. Acad. Sci. USA 86:9268-9272 (1989). Также для идентификации последовательностей CDR в антителе доступны базы данных общего пользования.
[89] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела к MET, характеризующиеся модифицированным профилем гликозилирования. В некоторых вариантах осуществления может быть применима модификация для удаления нежелательных сайтов гликозилирования или антитело, лишенное фукозного фрагмента, присутствующего в олигосахаридной цепи, например, для повышения функции антителозависимой клеточной цитотоксичности (ADCC) (см. Shield et al. (2002) JBC 277:26733). В других путях применения модификацию галактозилирования можно осуществлять для изменения комплементзависимой цитотоксичности (CDC).
БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ MET x MET
[90] Авторы настоящего изобретения наблюдали, что определенные моноспецифические антигенсвязывающие молекулы к MET, которые блокируют связывание HGF с MET, проявляют тенденцию к эффективной активации передачи сигнала MET (нежелательное последствие для терапевтической молекулы). Однако авторы настоящего изобретения обнаружили, что биспецифические антигенсвязывающие молекулы, которые одновременно связываются с двумя отдельными эпитопами на внеклеточном домене белка MET, являются эффективными при блокировании связывания лиганда с MET, обусловливая при этом небольшой агонизм передачи сигнала MET. Кроме того, авторы настоящего изобретения обнаружили, что биспецифические антигенсвязывающие молекулы исключительно подходят для лечения рака глаза, такого как увеальная меланома, орбитальная лимфома, ретинобластома и медуллоэпителиома, и/или подавления или снижения метастазирования.
[91] Соответственно, применимыми в соответствии с описанными в данном документе способами являются биспецифические антигенсвязывающие молекулы, содержащие первый антигенсвязывающий домен (также называемый в данном документе «D1») и второй антигенсвязывающий домен (также называемый в данном документе «D2»). Одновременное связывание двух отдельных эпитопов MET с помощью биспецифической антигенсвязывающей молекулы приводит к эффективному блокированию лиганда с минимальной активацией передачи сигнала MET.
[92] Биспецифические антигенсвязывающие молекулы, которые содержат первый антигенсвязывающий домен (D1), который специфически связывает первый эпитоп MET человека, и второй антигенсвязывающий домен (D2), который специфически связывает второй эпитоп MET человека, могут называться в данном документе как «биспецифические антитела к MET x MET», «MET x MET» или другими сходными терминами. В некоторых вариантах осуществления первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO:155. В некоторых вариантах осуществления второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO:155. В некоторых вариантах осуществления первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO:155; и второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO:155.
[93] В определенных вариантах осуществления домены D1 и D2 биспецифического антитела к MET x MET не конкурируют друг с другом. Отсутствие конкуренции между D1 и D2 за связывание с MET означает, что соответствующие моноспецифические антигенсвязывающие белки, из которых получены D1 и D2, не конкурируют друг с другом за связывание с MET человека. Из уровня техники известны иллюстративные анализы конкуренции антигенсвязывающих белков, неограничивающие примеры которых описаны в другом месте в данном документе.
[94] В определенных вариантах осуществления D1 и D2 связываются с разными (например неперекрывающимися или частично перекрывающимися) эпитопами на MET, как описано в другом месте в данном документе.
[95] Биспецифические антигенсвязывающие молекулы MET x MET могут быть сконструированы с применением антигенсвязывающих доменов двух отдельных моноспецифических антител к MET. Например, коллекцию моноклональных моноспецифических антител к MET можно получить с применением стандартных способов, известных из уровня техники. Полученные таким образом отдельные антитела можно тестировать попарно друг против друга в отношении перекрестной конкуренции за связывание с белком MET. Если два разных антитела к MET способны одновременно связываться с MET (т.е., не конкурируют друг с другом), то из антигенсвязывающего домена первого антитела к MET и антигенсвязывающего домена второго неконкурентного антитела к MET можно сконструировать одно биспецифическое антитело к MET x MET в соответствии с настоящим изобретением.
[96] В соответствии с настоящим изобретением биспецифическая антигенсвязывающая молекула может представлять собой один многофункциональный полипептид или может представлять собой мультимерный комплекс из двух или более полипептидов, которые ковалентно или нековалентно ассоциированы друг с другом. Как станет очевидно из настоящего изобретения, любая антигенсвязывающая конструкция, которая обладает способностью одновременно связывать два отдельных неидентичных эпитопа молекулы MET, рассматривается как биспецифическая антигенсвязывающая молекула. Любые из описанных в данном документе биспецифических антигенсвязывающих молекул или их вариантов можно конструировать с применением стандартных молекулярно-биологических методик (например технологии рекомбинантных ДНК и экспрессии белков), известных специалисту в данной области техники.
АНТИГЕНСВЯЗЫВАЮЩИЕ ДОМЕНЫ
[97] Биспецифические антигенсвязывающие молекулы, применимые в способах, раскрытых в данном документе, содержат два отдельных антигенсвязывающих домена (D1 и D2). Используемое в данном документе выражение «антигенсвязывающий домен» означает любой пептид, полипептид, молекулу нуклеиновой кислоты, молекулу каркасного типа, молекулу пептидного дисплея или конструкцию, содержащую полипептид, которые способны специфически связывать конкретный представляющий интерес антиген (например MET человека). Термин «специфически связывает» или подобный, используемый в данном документе, означает, что антигенсвязывающий домен образует комплекс с определенным антигеном, характеризующийся константой диссоциации (KD), составляющей 500 пМ или меньше, и не связывает другие неродственные антигены в обычных условиях тестирования. «Неродственные антигены» представляют собой белки, пептиды или полипептиды, которые характеризуются менее чем 95% идентичностью аминокислот по отношению друг к другу.
[98] Иллюстративные категории антигенсвязывающих доменов, которые можно использовать в контексте настоящего изобретения, включают антитела, антигенсвязывающие части антител, пептиды, которые специфически взаимодействуют с конкретным антигеном (например пептитела), рецепторные молекулы, которые специфически взаимодействуют с конкретным антигеном, белки, содержащие лигандсвязывающую часть рецептора, которая специфически связывает конкретный антиген, антигенсвязывающие каркасы (например, DARPin, белки с повторами HEAT, белки с повторами ARM, белки с тетратрикопептидными повторами и другие каркасы на основе встречающихся в природе белков с повторами и т.п. [см., например, Boersma and Pluckthun, 2011, Curr. Opin. Biotechnol. 22:849-857, и ссылки, цитируемые в нем]), а также аптамеры или их части.
[99] Способы определения наличия специфического связывания двух молекул друг с другом хорошо известны из уровня техники и включают, например, равновесный диализ, поверхностный плазмонный резонанс и т.п. Например, антигенсвязывающий домен, используемый в контексте настоящего изобретения, включает полипептиды, которые связывают конкретный антиген (например молекулу-мишень [T] или интернализующий эффекторный белок [E]) или его часть с KD, составляющей менее чем приблизительно 500 пМ, менее чем приблизительно 400 пМ, менее чем приблизительно 300 пМ, менее чем приблизительно 200 пМ, менее чем приблизительно 100 пМ, менее чем приблизительно 90 пМ, менее чем приблизительно 80 пМ, менее чем приблизительно 70 пМ, менее чем приблизительно 60 пМ, менее чем приблизительно 50 пМ, менее чем приблизительно 40 пМ, менее чем приблизительно 30 пМ, менее чем приблизительно 20 пМ, менее чем приблизительно 10 пМ, менее чем приблизительно 5 пМ, менее чем приблизительно 4 пМ, менее чем приблизительно 2 пМ, менее чем приблизительно 1 пМ, менее чем приблизительно 0,5 пМ, менее чем приблизительно 0,2 пМ, менее чем приблизительно 0,1 пМ или менее чем приблизительно 0,05 пМ, как измерено в анализе поверхностного плазмонного резонанса.
[100] Термин «поверхностный плазмонный резонанс», используемый в данном документе, относится к оптическому явлению, которое обеспечивает возможность анализа взаимодействий в реальном времени посредством выявления изменений значений концентрации белков в биосенсорной матрице, например с применением системы BIAcore™ (подразделение Biacore Life Sciences в GE Healthcare, Пискатауэй, Нью-Джерси).
[101] Термин «KD», используемый в данном документе, означает равновесную константу диссоциации конкретного белок-белкового взаимодействия (например взаимодействия антитело-антиген). Если не указано иное, значения KD, раскрытые в данном документе, относятся к значениям KD, определенным посредством анализа поверхностного плазмонного резонанса при 25°C.
[102] Как указано выше, «антигенсвязывающий домен» (D1 и/или D2) может содержать антитело или антигенсвязывающий фрагмент или состоять из них. Термин «антитело», используемый в данном документе, означает любую антигенсвязывающую молекулу или молекулярный комплекс, содержащий по меньшей мере одну определяющую комплементарность область (CDR), которая специфически связывается или взаимодействует с конкретным антигеном (например MET человека). Термин «антитело» включает молекулы иммуноглобулина, содержащие четыре полипептидные цепи, две тяжелые (H) цепи и две легкие (L) цепи, соединенные между собой дисульфидными связями, а также их мультимеры (например IgM). Каждая тяжелая цепь содержит вариабельную область тяжелой цепи (сокращенно обозначенную в данном документе как HCVR или VH) и константную область тяжелой цепи. Константная область тяжелой цепи содержит три домена, CH1, CH2 и CH3. Каждая легкая цепь содержит вариабельную область легкой цепи (сокращенно обозначенную в данном документе как LCVR или VL) и константную область легкой цепи. Константная область легкой цепи содержит один домен (CL1). Области VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые определяющими комплементарность областями (CDR), чередующиеся с более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от аминоконца к карбоксиконцу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. В различных вариантах осуществления FR антител, предусмотренных в данном документе (или их антигенсвязывающей части), могут быть идентичны последовательностям зародышевого типа человека или могут быть модифицированы естественным или искусственным путем. Консенсусную аминокислотную последовательность можно определить на основании анализа на основе прямого сравнения двух или более CDR.
[103] Компоненты D1 и/или D2 биспецифических антигенсвязывающих молекул, предусмотренных в данном документе, могут содержать антигенсвязывающие фрагменты полных молекул антител или состоять из них. Термины «антигенсвязывающая часть» антитела, «антигенсвязывающий фрагмент» антитела и т.п., используемые в данном документе, включают любой встречающийся в природе, получаемый ферментативным путем, синтетический или генетически сконструированный полипептид или гликопротеин, который специфически связывает антиген с образованием комплекса. Антигенсвязывающие фрагменты антитела могут быть получены, например, из молекул полного антитела с применением любых подходящих стандартных методик, таких как протеолитическое расщепление или рекомбинантные методики генной инженерии, включающие манипуляцию с ДНК, кодирующей вариабельные и необязательно константные домены антител, и ее экспрессию. Такая ДНК известна и/или легко доступна, например, из коммерческих источников, библиотек ДНК (включая, например, фаговые библиотеки антител), или может быть синтезирована. ДНК можно секвенировать и с ней можно проводить химические манипуляции или манипуляции с применением методик молекулярной биологии, например, для расположения одного или более вариабельных и/или константных доменов в подходящей конфигурации или для введения кодонов, включения остатков цистеина, модификации, добавления или удаления аминокислот и т.д.
[104] Неограничивающие примеры антигенсвязывающих фрагментов включают (i) Fab-фрагменты; (ii) F(ab')2-фрагменты; (iii) Fd-фрагменты; (iv) Fv-фрагменты; (v) одноцепочечные молекулы Fv (scFv); (vi) dAb-фрагменты и (vii) минимальные распознающие единицы, состоящие из аминокислотных остатков, которые имитируют гипервариабельную область антитела (например, выделенная определяющая комплементарность область (CDR), такая как пептид CDR3), или пептид FR3-CDR3-FR4 c ограниченной конформационной свободой. Другие сконструированные молекулы, такие как домен-специфические антитела, однодоменные антитела, антитела с удаленным доменом, химерные антитела, антитела с привитой CDR, диатела, триатела, тетратела, минитела, нанотела (например, моновалентные нанотела, двухвалентные нанотела и т.д.), иммунофармацевтические средства на основе небольшого модульного белка (SMIP) и вариабельные домены IgNAR акулы также охватываются выражением «антигенсвязывающий фрагмент», используемым в данном документе.
[105] Антигенсвязывающий фрагмент антитела обычно будет содержать по меньшей мере один вариабельный домен. Вариабельный домен может быть любого размера или аминокислотного состава и будет, как правило, содержать по меньшей мере одну CDR, которая находится в смежном положении или в одной рамке считывания с одной или более каркасными последовательностями. В антигенсвязывающих фрагментах, содержащих домен VH, ассоциированный с доменом VL, домены VH и VL могут располагаться друг относительно друга в любом подходящем порядке. Например, вариабельная область может быть димерной и содержать димеры VH-VH, VH-VL или VL-VL. В качестве альтернативы, антигенсвязывающий фрагмент антитела может содержать мономерный домен VH или VL.
[106] В определенных вариантах осуществления антигенсвязывающий фрагмент антитела может содержать по меньшей мере один вариабельный домен, ковалентно связанный с по меньшей мере одним константным доменом. Неограничивающие иллюстративные конфигурации вариабельных и константных доменов, которые могут находиться в пределах антигенсвязывающего фрагмента антитела по настоящему изобретению, включают (i) VH-CH1; (ii) VH-CH2; (iii) VH-CH3; (iv) VH-CH1-CH2; (v) VH-CH1-CH2-CH3; (vi) VH-CH2-CH3; (vii) VH-CL; (viii) VL-CH1; (ix) VL-CH2; (x) VL-CH3; (xi) VL-CH1-CH2; (xii) VL-CH1-CH2-CH3; (xiii) VL-CH2-CH3 и (xiv) VL-CL. В любой конфигурации вариабельных и константных доменов, в том числе любой из иллюстративных конфигураций, перечисленных выше, вариабельные и константные домены могут быть либо непосредственно соединены друг с другом, либо могут быть соединены посредством целой шарнирной или линкерной области или ее части. Шарнирная область может состоять из по меньшей мере 2 (например, 5, 10, 15, 20, 40, 60 или больше) аминокислот, которые обеспечивают образование гибкой или полугибкой связи между смежными вариабельными и/или константными доменами в одной молекуле полипептида. Более того, антигенсвязывающий фрагмент может содержать гомодимер или гетеродимер (или другой мультимер) из любых конфигураций вариабельных и константных доменов, изложенных выше, нековалентно связанных друг с другом и/или с одним или более мономерными доменами VH или VL (например, с помощью дисульфидной связи(связей)).
[107] Биспецифические антигенсвязывающие молекулы, применимые в способах, предусмотренных в данном документе, могут содержать человеческие антитела и/или рекомбинантные человеческие антитела или их фрагменты или состоять из них. Термин «человеческое антитело», используемый в данном документе, включает антитела, содержащие вариабельные и константные области, полученные из человеческих последовательностей иммуноглобулинов зародышевого типа. Человеческие антитела могут, тем не менее, содержать аминокислотные остатки, не кодируемые человеческими последовательностями иммуноглобулинов зародышевого типа (например за счет мутаций, вводимых посредством случайного или сайт-специфического мутагенеза in vitro, или посредством введения соматической мутации in vivo), например в CDR, и, в частности, в CDR3. Однако подразумевается, что термин «человеческое антитело», используемый в данном документе, не включает антитела, в которых последовательности CDR, полученные из последовательностей зародышевого типа другого вида млекопитающего, такого как мышь, привиты на человеческие каркасные последовательности.
[108] Биспецифические антигенсвязывающие молекулы, применимые в способах, предусмотренных в данном документе, могут содержать рекомбинантные человеческие антитела или их антигенсвязывающие фрагменты или состоять из них. Подразумевается, что термин «рекомбинантное человеческое антитело», используемый в данном документе, включает все человеческие антитела, получаемые, экспрессируемые, создаваемые или выделяемые рекомбинантными способами, такие как антитела, экспрессируемые с применением рекомбинантного вектора экспрессии, трансфицированного в клетку-хозяина (дополнительно описанные ниже), антитела, выделяемые из рекомбинантной комбинаторной библиотеки человеческих антител (дополнительно описанные ниже), антитела, выделяемые из организма животного (например мыши), которое является трансгенным по генам человеческих иммуноглобулинов (см., например, Taylor et al. (1992) Nucl. Acids Res. 20:6287-6295), или антитела, получаемые, экспрессируемые, создаваемые или выделяемые любыми другими способами, которые включают сплайсинг последовательностей генов человеческих иммуноглобулинов с другими последовательностями ДНК. Такие рекомбинантные человеческие антитела содержат вариабельные и константные области, полученные из человеческих последовательностей иммуноглобулинов зародышевого типа. Однако в определенных вариантах осуществления такие рекомбинантные человеческие антитела подвергаются мутагенезу in vitro (или если используется животное, трансгенное по последовательностям человеческого Ig, соматическому мутагенезу in vivo) и, следовательно, аминокислотные последовательности областей VH и VL рекомбинантных антител представляют собой последовательности, которые, хотя и получены из человеческих последовательностей VH и VL зародышевого типа и родственны им, могут не существовать в природе в репертуаре человеческих антител зародышевого типа in vivo.
[109] Способы получения биспецифических антител известны из уровня техники и могут применяться для конструирования раскрытых в данном документе биспецифических антигенсвязывающих молекул. Иллюстративные биспецифические форматы, которые можно использовать в контексте настоящего изобретения, включают без ограничения, например, биспецифические форматы на основе scFv или диател, слитых белков IgG-scFv, двойной вариабельный домен (DVD)-Ig, квадрому, «выступы-в углубления», обычную легкую цепь (например общую легкую цепь со структурой выступы-в-углубления и т.п.), CrossMab, CrossFab, (SEED)-антитело, «лейциновую застежку», дуотело, IgG1/IgG2, Fab (DAF)-IgG двойного действия и биспецифические форматы Mab2 (для обзора вышеизложенных форматов см., например, Klein et al. 2012, mAbs 4:6, 1-11, и цитируемые в нем ссылки).
[110] Иллюстративные антигенсвязывающие домены (D1 и D2), которые могут быть включены в биспецифические антигенсвязывающие молекулы MET x MET, предусмотренные в данном документе, включают антигенсвязывающие домены, полученные из любого из антител к MET, раскрытых в данном документе. Например, биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий HCVR, содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCVR, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней, применимы в способах лечения увеальной меланомы, описанных в данном документе.
[111] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий LCVR, содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCVR, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности с ней.
[112] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий пару аминокислотных последовательностей HCVR и LCVR (HCVR/LCVR), содержащую любую из аминокислотных последовательностей HCVR, перечисленных в таблице 1, в паре с любой из аминокислотных последовательностей LCVR, перечисленных в таблице 1. В соответствии с определенными вариантами осуществления применимые биспецифические антигенсвязывающие молекулы MET x MET содержат антигенсвязывающий домен D1 или D2, содержащий пару аминокислотных последовательностей HCVR/LCVR, содержащуюся в любом из иллюстративных антител к MET, перечисленных в таблице 1.
[113] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCDR1, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности.
[114] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCDR2, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности.
[115] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей HCDR3, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности.
[116] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCDR1, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности.
[117] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCDR2, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности.
[118] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность, выбранную из любой из аминокислотных последовательностей LCDR3, перечисленных в таблице 1, или практически аналогичную ей последовательность, характеризующуюся по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности.
[119] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий пару аминокислотных последовательностей HCDR3 и LCDR3 (HCDR3/LCDR3), содержащую любую из аминокислотных последовательностей HCDR3, перечисленных в таблице 1, в паре с любой из аминокислотных последовательностей LCDR3, перечисленных в таблице 1. В соответствии с определенными вариантами осуществления настоящее изобретение предусматривает антитела или их антигенсвязывающие фрагменты, содержащие пару аминокислотных последовательностей HCDR3/LCDR3, содержащуюся в любом из иллюстративных антител к MET, перечисленных в таблице 1.
[120] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий набор из шести CDR (т.е. HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащихся в любом из иллюстративных антител к MET, перечисленных в таблице 1.
[121] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие молекулы MET x MET, содержащие антигенсвязывающий домен D1 или D2, содержащий набор из шести CDR (т.е. HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащихся в паре аминокислотных последовательностей HCVR/LCVR, определенной для любого из иллюстративных антител к MET, перечисленных в таблице 1.
[122] Биспецифические антигенсвязывающие молекулы MET x MET, применимые в способах, предусмотренных в данном документе, могут содержать антигенсвязывающий домен D1, полученный из любого из антител к MET из таблицы 1, и антигенсвязывающий домен D2, полученный из любого другого антитела к MET из таблицы 1. Неограничивающие примеры биспецифических антител к MET x MET изображены на фигуре 1. На фигуре 1 представлена матрица, иллюстрирующая компоненты 272 иллюстративных биспецифических антител к MET x MET. Каждая пронумерованная ячейка матрицы (нумерация от 1 до 272) идентифицирует уникальное биспецифическое антитело, содержащее антигенсвязывающий домен «D1» и антигенсвязывающий домен «D2», где антигенсвязывающий домен D1 содержит вариабельный домен иммуноглобулина (пара аминокислотных последовательностей HCVR/LCVR) или CDR из соответствующего антитела к MET, указанные вдоль оси Y, и где антигенсвязывающий домен D2 содержит вариабельный домен иммуноглобулина (пара аминокислотных последовательностей HCVR/LCVR) или CDR из соответствующего антитела к MET, указанные вдоль оси X. Таким образом, например, биспецифическая антигенсвязывающая молекула MET x MET «номер 10», показанная в матрице, содержит антигенсвязывающий домен D1, содержащий пару HCVR/LCVR или набор 6-CDR из иллюстративного антитела к MET H4H13290P2, и антигенсвязывающий домен D2, содержащий пару HCVR/LCVR или набор 6-CDR из иллюстративного антитела к MET H4H13321P2. Дополнительные примеры биспецифических антител к МЕТ x МЕТ, предусмотренных в данном документе, описаны в примере 4 в данном документе.
[123] Иллюстративная биспецифическая антигенсвязывающая молекула MET x MET, применимая в соответствии со способами, предусмотренными в данном документе, содержит антигенсвязывающий домен D1 и антигенсвязывающий домен D2, где антигенсвязывающий домен D1 содержит пару аминокислотных последовательностей HCVR/LCVR под SEQ ID NO: 58/138 или набор CDR тяжелой и легкой цепей (HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащий SEQ ID NO: 60-62-64-140-142-144, и где антигенсвязывающий домен D2 содержит пару аминокислотных последовательностей HCVR/LCVR под SEQ ID NO: 82/138 или набор CDR тяжелой и легкой цепей (HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащий SEQ ID NO: 84-86-88-140-142-144. Иллюстративное биспецифическое антитело к MET x MET, обладающее такими характеристиками последовательностей, представляет собой биспецифическое антитело, обозначенное H4H14639D, также называемое биспецифическим антителом №122, которое содержит D1, полученный из H4H13306P2, и D2, полученный из H4H13312P2 (см. пример 4, таблицу 5 в данном документе).
[124] В качестве дополнительного неограничивающего иллюстративного примера биспецифические антигенсвязывающие молекулы MET x MET, применимые в соответствии с данным документом, содержат антигенсвязывающий домен D1 и антигенсвязывающий домен D2, где антигенсвязывающий домен D1 содержит пару аминокислотных последовательностей HCVR/LCVR под SEQ ID NO: 18/138 или набор CDR тяжелой и легкой цепей (HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащий SEQ ID NO: 20-22-24-140-142-144, и где антигенсвязывающий домен D2 содержит пару аминокислотных последовательностей HCVR/LCVR под SEQ ID NO: 82/138 или набор CDR тяжелой и легкой цепей (HCDR1-HCDR2-HCDR3-LCDR1-LCDR2-LCDR3), содержащий SEQ ID NO: 84-86-88-140-142-144. Иллюстративное биспецифическое антитело к MET x MET, обладающее такими характеристиками последовательностей, представляет собой биспецифическое антитело, обозначенное H4H14635D, также называемое биспецифическим антителом № 42, которое содержит D1, полученный из H4H13295P2, и D2, полученный из H4H13312P2 (см. пример 4, таблицу 5 в данном документе).
КОМПОНЕНТЫ МУЛЬТИМЕРИЗАЦИИ
[125] Биспецифические антигенсвязывающие молекулы, применимые в соответствии со способами, предусмотренными в данном документе, в определенных вариантах осуществления могут также содержать один или более компонентов мультимеризации. Компоненты мультимеризации могут выполнять функцию поддержания связи между антигенсвязывающими доменами (D1 и D2). Используемый в данном документе термин «компонент мультимеризации» представляет собой любую макромолекулу, белок, полипептид, пептид или аминокислоту, которые обладают способностью связываться со вторым компонентом мультимеризации такой же или подобной структуры или состава. Например, компонент мультимеризации может представлять собой полипептид, содержащий домен CH3 иммуноглобулина. Неограничивающим примером компонента мультимеризации является Fc-часть иммуноглобулина, например Fc-домен IgG, выбранного из изотипов IgG1, IgG2, IgG3 и IgG4, а также любого аллотипа в пределах каждой группы изотипов. В определенных вариантах осуществления компонент мультимеризации представляет собой Fc-фрагмент или аминокислотную последовательность длиной от 1 до приблизительно 200 аминокислот, содержащую по меньшей мере один остаток цистеина. В других вариантах осуществления компонент мультимеризации представляет собой остаток цистеина или короткий цистеин-содержащий пептид. Другие домены мультимеризации включают пептиды или полипептиды, содержащие лейциновую застежку, мотив спираль-петля или мотив суперспираль, или состоящие из них.
[126] В определенных вариантах осуществления биспецифические антигенсвязывающие молекулы содержат два домена мультимеризации, M1 и M2, где D1 присоединен к M1, а D2 присоединен к M2, и где ассоциация M1 с M2 способствует физической связи D1 и D2 друг с другом в одной биспецифической антигенсвязывающей молекуле. В определенных вариантах осуществления M1 и M2 идентичны друг другу. Например, M1 может представлять собой Fc-домен, содержащий определенную аминокислотную последовательность, а M2 представляет собой Fc-домен с той же аминокислотной последовательностью, что и M1. В качестве альтернативы, M1 и M2 могут отличаться друг от друга по одному или более аминокислотным положениям. Например, M1 может содержать CH3-домен первого иммуноглобулина (Ig), и M2 может содержать CH3-домен второго Ig, где CH3-домены первого и второго Ig отличаются друг от друга по меньшей мере одной аминокислотой, и где отличие в по меньшей мере одну аминокислоту снижает степень связывания нацеливающейся конструкции с белком А по сравнению с эталонной конструкцией, содержащей идентичные последовательности М1 и М2. В одном варианте осуществления CH3-домен Ig в M1 связывает белок A, а CH3-домен Ig в M2 содержит мутацию, которая снижает или устраняет связывание белка A, такую как модификация H95R (нумерация экзонов согласно IMGT; нумерация H435R согласно EU). CH3 M2 может дополнительно содержать модификацию Y96F (согласно IMGT; Y436F согласно EU). Дополнительные модификации, которые могут присутствовать в пределах CH3 M2, включают D16E, L18M, N44S, K52N, V57M и V82I (согласно IMGT; D356E, L358M, N384S, K392N, V397M и V422I согласно EU) в случае Fc-домена IgG1; N44S, K52N и V82I (IMGT; N384S, K392N и V422I согласно EU) в случае Fc-домена IgG2 и Q15R, N44S, K52N, V57M, R69K, E79Q и V82I (согласно IMGT; Q355R, N384S, K392N, V397M, R409K, E419Q и V422I согласно EU) в случае Fc-домена IgG4.
[127] Биспецифические антигенсвязывающие молекулы, применимые в соответствии со способами, предусмотренными в данном документе, могут быть «выделенными». Используемый в данном документе термин «выделенная биспецифическая антигенсвязывающая молекула» означает биспецифическую антигенсвязывающую молекулу, которая была идентифицирована, отделена и/или извлечена из по меньшей мере одного компонента ее природного окружения. Например, биспецифическое антитело, которое было отделено или удалено из по меньшей мере одного компонента организма или из ткани или клетки, в которых антитело продуцируется, является «выделенным биспецифическим антителом» для целей настоящего изобретения. Выделенная биспецифическая антигенсвязывающая молекула также включает молекулы in situ в рекомбинантной клетке. Выделенные биспецифические антигенсвязывающие молекулы представляют собой молекулы, которые были подвергнуты по меньшей мере одной стадии очистки или выделения. В соответствии с определенными вариантами осуществления выделенная биспецифическая антигенсвязывающая молекула может практически не содержать другого клеточного материала и/или химических веществ.
[128] Биспецифические антигенсвязывающие молекулы, применимые в соответствии со способами, предусмотренными в данном документе, или их антигенсвязывающие домены (D1 и/или D2) могут содержать одну или несколько аминокислотных замен, вставок и/или делеций в каркасных областях и/или CDR вариабельных доменов тяжелой и легкой цепей по сравнению с соответствующими последовательностями зародышевого типа, из которых были получены антигенсвязывающие белки или антигенсвязывающие домены. Такие мутации можно легко определить посредством сравнения аминокислотных последовательностей, раскрытых в данном документе, с последовательностями зародышевого типа, доступными, например, из общедоступных баз данных последовательностей антител. Биспецифические антигенсвязывающие молекулы или их антигенсвязывающие домены (D1 и/или D2) получают из любых аминокислотных последовательностей, раскрытых в данном документе, где одна или более аминокислот в пределах одной или более каркасных областей и/или CDR подвергнуты мутации с получением соответствующего остатка(остатков) последовательности зародышевого типа, из которой получено антитело, или с получением соответствующего остатка(остатков) другой человеческой последовательности зародышевого типа, или с получением консервативной аминокислотной замены соответствующего остатка(остатков) зародышевого типа (такие изменения последовательностей называются в данном документе в совокупности «мутациями зародышевого типа»).
[129] Специалист в данной области техники, исходя из раскрытых в данном документе последовательностей вариабельных областей тяжелой и легкой цепей может легко получить многочисленные биспецифические антигенсвязывающие молекулы или их антигенсвязывающие домены (D1 и/или D2), которые содержат одну или более отдельных мутаций зародышевого типа или их комбинации. В определенных вариантах осуществления все остатки из каркасной области и/или CDR в пределах доменов VH и/или VL подвергнуты обратной мутации до остатков, находящихся в первоначальной последовательности зародышевого типа, из которой было получено антитело. В других вариантах осуществления только определенные остатки подвергнуты обратной мутации до первоначальной последовательности зародышевого типа, например только подвергнутые мутации остатки, находящиеся в пределах первых 8 аминокислот FR1 или в пределах последних 8 аминокислот FR4, или только подвергнутые мутации остатки, находящиеся в пределах CDR1, CDR2 или CDR3. В других вариантах осуществления один или более остатков каркасного участка и/или CDR подвергнуты мутации до соответствующего остатка(остатков) другой последовательности зародышевого типа (т.е. последовательности зародышевого типа, которая отличается от последовательности зародышевого типа, из которой первоначально было получено антитело).
[130] Кроме того, биспецифические антигенсвязывающие молекулы или их антигенсвязывающие домены (D1 и/или D2), применимые в соответствии с данным документом, могут содержать любую комбинацию двух или более мутаций зародышевого типа в пределах каркасных областей и/или CDR, например, где определенные отдельные остатки подвергаются мутации с получением соответствующего остатка конкретной последовательности зародышевого типа, в то время как определенные другие остатки, которые отличаются от исходной последовательности зародышевого типа, сохраняются или подвергаются мутации с получением соответствующего остатка другой последовательности зародышевого типа. После получения биспецифические антигенсвязывающие молекулы или их антигенсвязывающие домены (D1 и/или D2), которые содержат одну или более мутаций зародышевого типа, можно легко протестировать в отношении одного или более требуемых свойств, таких как улучшение специфичности связывания, повышение аффинности связывания, улучшение или усиление антагонистических или агонистических биологических свойств (в случае необходимости), снижение иммуногенности и т.п. Биспецифические антигенсвязывающие молекулы или их антигенсвязывающие домены (D1 и/или D2), полученные таким общим образом, рассматриваются как применимые в данном документе.
ВАРИАНТЫ
[131] Также применимыми в соответствии с данным документом являются антитела к MET и биспецифические антигенсвязывающие молекулы, содержащие варианты любых из аминокислотных последовательностей HCVR, LCVR и/или CDR, раскрытых в данном документе. Иллюстративные варианты, включенные в данный аспект, включают варианты любых из аминокислотных последовательностей HCVR, LCVR и/или CDR, раскрытых в данном документе, содержащие одну или более консервативных замен. Например, настоящее изобретение включает антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET, содержащие аминокислотные последовательности HCVR, LCVR и/или CDR, например, с 10 или меньше, 8 или меньше, 6 или меньше, 4 или меньше и т.д. консервативными аминокислотными заменами относительно любой из аминокислотных последовательностей HCVR, LCVR и/или CDR, указанных в таблице 1 в данном документе.
[132] Иллюстративные варианты включают варианты, характеризующиеся существенной идентичностью последовательности с любой из аминокислотных последовательностей HCVR, LCVR и/или CDR, раскрытых в данном документе. Используемый в данном документе в контексте аминокислотных последовательностей термин «существенная идентичность» или «практически идентичный» означает, что две аминокислотные последовательности при оптимальном выравнивании, например, с помощью программ GAP или BESTFIT с применением значений штрафа за открытие гэпа по умолчанию, характеризуются по меньшей мере 95%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательностей. В определенных вариантах осуществления положения остатков, которые не являются идентичными, отличаются по консервативным аминокислотным заменам. «Консервативная аминокислотная замена» представляет собой замену, при которой аминокислотный остаток заменяется другим аминокислотным остатком, содержащим боковую цепь (R-группу) со сходными химическими свойствами (например зарядом или гидрофобностью). Как правило, консервативная аминокислотная замена практически не будет изменять функциональные свойства белка. В случаях, если две или более аминокислотные последовательности отличаются друг от друга консервативными заменами, процентную идентичность последовательностей или степень сходства можно регулировать в сторону повышения для коррекции консервативного характера замены. Средства для осуществления такой коррекции хорошо известны специалистам в данной области техники. См, например, Pearson (1994) Methods Mol. Biol. 24: 307-331, которая включена в данный документ посредством ссылки. Примеры групп аминокислот, которые содержат боковые цепи со сходными химическими свойствами, включают (1) алифатические боковые цепи: глицин, аланин, валин, лейцин и изолейцин; (2) алифатические боковые цепи с гидроксильными группами: серин и треонин; (3) амид-содержащие боковые цепи: аспарагин и глутамин; (4) ароматические боковые цепи: фенилаланин, тирозин и триптофан; (5) основные боковые цепи: лизин, аргинин и гистидин; (6) кислые боковые цепи: аспартат и глутамат и (7) серосодержащие боковые цепи: цистеин и метионин. Предпочтительными группами консервативных аминокислотных замен являются валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин. В качестве альтернативы, консервативной заменой является любое изменение, характеризующееся положительным значением в матрице логарифмической функции правдоподобия РАМ250, раскрытой в Gonnet et al. (1992) Science 256: 1443-1445, которая включена в данный документ посредством ссылки. «Умеренно консервативная» замена представляет собой любое изменение, характеризующееся неотрицательным значением в матрице логарифмической функции правдоподобия PAM250.
[133] Идентичность последовательностей двух различных аминокислотных последовательностей обычно измеряется с применением программного обеспечения для анализа последовательностей. Программное обеспечение для анализа последовательностей сопоставляет сходные последовательности с применением показателей сходства, присваиваемых различным заменам, делециям и другим модификациям, включая консервативные аминокислотные замены. Например, программное обеспечение GCG включает программы, такие как Gap и Bestfit, которые можно использовать с параметрами по умолчанию для определения гомологии последовательностей или идентичности последовательностей у близкородственных полипептидов, таких как гомологичные полипептиды из различных видов организмов, или белка дикого типа и его мутеина. См., например, GCG версии 6.1. Полипептидные последовательности также можно сравнивать с помощью FASTA с применением параметров по умолчанию или рекомендованных параметров; программа в GCG версии 6.1. FASTA (например FASTA2 и FASTA3) обеспечивает выравнивания и расчет процента идентичности последовательностей в областях с наибольшим перекрыванием между запрашиваемой и найденной последовательностями (Pearson (2000), выше). Другим предпочтительным алгоритмом при сравнении предусмотренной в данном документе последовательности с базой данных, содержащей большое количество последовательностей от разных организмов, является компьютерная программа BLAST, в частности BLASTP или TBLASTN, с применением параметров по умолчанию. См., например, Altschul et al. (1990) J. Mol. Biol. 215:403-410 и Altschul et al. (1997) Nucleic Acids Res. 25:3389-402, каждая из которых включена в данный документ посредством ссылки.
Антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET, содержащие варианты Fc
[134] В соответствии с определенными вариантами осуществления, предусмотренными в данном документе, антитела к MET и биспецифические антигенсвязывающие белки MET x MET, применимые в соответствии с данным документом, содержат Fc-домен, содержащий одну или более мутаций, которые усиливают или ослабляют связывание антитела с рецептором FcRn, например, при кислотном pH по сравнению с нейтральным pH. Например, такие варианты включают антитела к MET и биспецифические антигенсвязывающие белки MET x MET, содержащие мутацию в области CH2 или CH3 Fc-домена, где мутация(мутации) повышает аффинность Fc-домена к FcRn в кислотной среде (например в эндосоме, где pH находится в диапазоне от приблизительно 5,5 до приблизительно 6,0). Результатом таких мутаций может быть увеличение периода полужизни антитела в сыворотке крови при введении животному. Неограничивающие примеры таких модификаций Fc включают, например, модификацию в положении 250 (например E или Q); 250 и 428 (например L или F); 252 (например L/Y/F/W или T), 254 (например S или T) и 256 (например S/R/Q/E/D или T), или модификацию в положении 428 и/или 433 (например H/L/R/S/P/Q или K), и/или 434 (например H/F или Y); или модификацию в положении 250 и/или 428, или модификацию в положении 307 или 308 (например, 308F, V308F) и 434. В одном варианте осуществления модификация включает модификацию 428L (например M428L) и 434S (например N434S); модификацию 428L, 259I (например V259I) и 308F (например V308F); модификацию 433K (например H433K) и 434 (например 434Y); модификацию 252, 254 и 256 (например, 252Y, 254T и 256E); модификацию 250Q и 428L (например T250Q и M428L); и модификацию 307 и/или 308 (например 308F или 308P).
[135] Соответственно, применимыми в соответствии с данным документом являются антитела к MET и биспецифические антигенсвязывающие белки MET x MET, содержащие Fc-домен, содержащий одну или более пар или групп мутаций, выбранных из группы, состоящей из 250Q и 248L (например T250Q и M248L); 252Y, 254T и 256E (например M252Y, S254T и T256E); 428L и 434S (например M428L и N434S); а также 433K и 434F (например H433K и N434F). Объемом настоящего изобретения предусмотрены все возможные комбинации вышеупомянутых мутаций в Fc-домене и другие мутации в пределах вариабельных доменов антитела, раскрытых в данном документе.
Биологические характеристики антигенсвязывающих молекул, применимых в соответствии с данным документом
[136] Применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела и их антигенсвязывающие фрагменты, а также ADC, содержащие антитела и антигенсвязывающие фрагменты, которые подавляют пролиферацию, подавляют инвазию, вызывают апоптоз и/или снижают жизнеспособность клетки увеальной меланомы.
[137] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела и их антигенсвязывающие фрагменты, а также ADC, содержащие антитела и антигенсвязывающие фрагменты, которые влияют на клеточный цикл клетки увеальной меланомы. В некоторых аспектах клетка подвергается остановке митоза. В некоторых аспектах клетка остается в фазе SubG1, что указывает на то, что клетка претерпевает апоптоз.
[138] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела и их антигенсвязывающие фрагменты, а также ADC, содержащие антитела и антигенсвязывающие фрагменты, которые вызывают апоптоз в клетке увеальной меланомы. В некоторых аспектах клетка увеальной меланомы демонстрирует расщепление PARP. В некоторых аспектах клетка увеальной меланомы демонстрирует фосфорилирование гистона H3.
[139] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела и их антигенсвязывающие фрагменты, которые связывают мономерный MET человека с высокой аффинностью. Например, настоящее изобретение включает антитела к MET, которые связывают мономерный MET человека (например hMET.mmh) с KD, составляющей менее чем приблизительно 230 нМ, измеренной посредством поверхностного плазмонного резонанса при 25°C или 37°C, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа. В соответствии с определенными вариантами осуществления предусмотрены антитела к MET, которые связывают мономерный MET человека при 37°C с KD, составляющей менее чем приблизительно 230 нМ, менее чем приблизительно 200 нМ, менее чем приблизительно 150 нМ, менее чем приблизительно 100 нМ, менее чем приблизительно 50 нМ, менее чем приблизительно 25 нМ, менее чем приблизительно 20 нМ, менее чем приблизительно 10 нМ, менее чем приблизительно 8 нМ, менее чем приблизительно 6 нМ, менее чем приблизительно 5 нМ, менее чем приблизительно 4 нМ или менее чем приблизительно 3 нМ, измеренной посредством поверхностного плазмонного резонанса, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа.
[140] Такие антитела и их антигенсвязывающие фрагменты связывают мономерный MET человека (например hMET.mmh) с периодом полудиссоциации (t½), составляющим более чем приблизительно 1 минуту, измеренным посредством поверхностного плазмонного резонанса при 25°C или 37°C, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа. Такие антитела к MET связывают мономерный MET человека при 37°C с t½, составляющим более чем приблизительно 1 минуту, более чем приблизительно 2 минуты, более чем приблизительно 4 минуты, более чем приблизительно 6 минут, более чем приблизительно 8 минут, более чем приблизительно 10 минут, более чем приблизительно 12 минут, более чем приблизительно 14 минут, более чем приблизительно 16 минут, более чем приблизительно 18 минут или более чем приблизительно 20 минут или больше, измеренным посредством поверхностного плазмонного резонанса, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа.
[141] Такие антитела и их антигенсвязывающие фрагменты связывают димерный МЕТ человека (например hMET.mFc) с высокой аффинностью. Например, антитела к MET связывают димерный MET человека с KD, составляющей менее чем приблизительно 3 нМ, измеренной посредством поверхностного плазмонного резонанса при 25°C или 37°C, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа. В соответствии с определенными вариантами осуществления антитела к MET связывают димерный MET человека при 37ºC с KD, составляющей менее чем приблизительно 3 нМ, менее чем приблизительно 2 нМ, менее чем приблизительно 1 нМ, менее чем приблизительно 0,9 нМ, менее чем приблизительно 0,8 нМ, менее чем приблизительно 0,7 нМ, менее чем приблизительно 0,6 нМ, менее чем приблизительно 0,5 нМ, менее чем приблизительно 0,4 нМ, менее чем приблизительно 0,3 нМ или менее чем приблизительно 0,25 нМ, измеренной посредством поверхностного плазмонного резонанса, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа.
[142] Такие антитела и их антигенсвязывающие фрагменты могут связывать димерный MET человека (например hMET.mFc) с периодом полудиссоциации (t½), составляющим более чем приблизительно 4 минуты, измеренным посредством поверхностного плазмонного резонанса при 25°C или 37°C, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа. В соответствии с определенными вариантами осуществления антитела к MET могут связывать димерный МЕТ человека при 37°C с t½, составляющим более чем приблизительно 4 минуты, более чем приблизительно 5 минут, более чем приблизительно 10 минут, более чем приблизительно 20 минут, более чем приблизительно 30 минут, более чем приблизительно 40 минут, более чем приблизительно 50 минут, более чем приблизительно 60 минут, более чем приблизительно 70 минут, более чем приблизительно 80 минут, более чем приблизительно 90 минут, более чем приблизительно 100 минут, более чем приблизительно 105 минут или больше, измеренным посредством поверхностного плазмонного резонанса, например с применением формата анализа, определенного в примере 3 в данном документе, или практически аналогичного анализа.
[143] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются биспецифические антигенсвязывающие белки MET x MET, которые связывают димерный MET человека (например hMET.mFc) с периодом диссоциации (t½), составляющим более чем приблизительно 10 минут, измеренным посредством поверхностного плазмонного резонанса при 25°C или 37°C, например с применением формата анализа, определенного в примере 5 в данном документе, или практически аналогичного анализа. В соответствии с определенными вариантами осуществления биспецифические антигенсвязывающие белки MET x MET связывают димерный MET человека при 37°C с t½, составляющим более чем приблизительно 10 минут, более чем приблизительно 20 минут, более чем приблизительно 30 минут, более чем приблизительно 40 минут, более чем приблизительно 50 минут, более чем приблизительно 60 минут, более чем приблизительно 70 минут, более чем приблизительно 80 минут, более чем приблизительно 90 минут, более чем приблизительно 100 минут, более чем приблизительно 200 минут, более чем приблизительно 300 минут, более чем приблизительно 400 минут, более чем приблизительно 500 минут, более чем приблизительно 600 минут, более чем приблизительно 700 минут, более чем приблизительно 800 минут, более чем приблизительно 900 минут, более чем приблизительно 1000 минут, более чем приблизительно 1100 минут или дольше, измеренным посредством поверхностного плазмонного резонанса, например с применением формата анализа, определенного в примере 5 в данном документе, или практически аналогичного анализа.
[144] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела к MET и биспецифические антигенсвязывающие белки MET x MET, которые блокируют взаимодействие между HGF и MET, например в анализе связывания лиганда in vitro. В соответствии с определенными вариантами осуществления, предусмотренными в данном документе, биспецифические антигенсвязывающие белки MET x MET блокируют связывание HGF с клетками, экспрессирующими MET человека, и индуцируют или не индуцируют минимальную активацию MET в отсутствие передачи сигнала HGF. Например, биспецифические антигенсвязывающие белки MET x MET демонстрируют степень агонистической активности в отношении MET в клеточном репортерном анализе активности MET, которая составляет менее чем 50%, менее чем 40%, менее чем 30%, менее чем 20%, менее чем 10%, менее чем 5%, менее чем 3%, менее чем 2% или менее чем 1% от агонистической активности в отношении MET, наблюдаемой в эквивалентном репортерном анализе активности с применением моноспецифического антитела, содержащего только D1 или D2.
[145] Антитела и антигенсвязывающие белки, применимые в соответствии с настоящим изобретением, могут обладать одной или более из вышеупомянутых биологических характеристик или любой их комбинацией. Приведенный выше перечень биологических характеристик антител не является исчерпывающим. Другие биологические характеристики предусмотренных в данном документе антител будут очевидны специалисту в данной области техники из обзора настоящего изобретения, включая предусмотренные в данном документе практические примеры.
КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННЫЕ СРЕДСТВО (ADC)
[146] Применимыми в соответствии со способами, предусмотренными в данном документе, являются конъюгаты антитело-лекарственное средство (ADC), содержащие антитело к MET или биспецифический антигенсвязывающий белок MET x MET, конъюгированные с терапевтическим фрагментом, таким как цитотоксическое средство, химиотерапевтическое лекарственное средство или радиоактивный изотоп.
[147] Цитотоксические средства включают любое средство, которое оказывает негативное воздействие на рост, жизнеспособность или размножение клеток, включая без ограничения средства, взаимодействующие с тубулином, и средства, повреждающие ДНК. Примеры подходящих цитотоксических средств и химиотерапевтических средств, которые можно конъюгировать с антителами к MET в соответствии с данным аспектом настоящего изобретения, включают, например, 1-(2-хлорэтил)-1,2-диметансульфонилгидразид, 1,8-дигидроксибицикло[7.3.1]тридека-4,9-диен-2,6-диин-13-он, 1-дегидротестостерон, 5-фторурацил, 6-меркаптопурин, 6-тиогуанин, 9-аминокамптотецин, актиномицин D, аманитины, аминоптерин, ангуидин, антрациклин, антрамицин (AMC), ауристатины, блеомицин, бусульфан, масляную кислоту, калихеамицины (например калихеамицин γ1), камптотецин, карминомицины, кармустин, цемадотины, цисплатин, колхицин, комбретастатины, циклофосфамид, цитарабин, цитохалазин B, дактиномицин, даунорубицин, декарбазин, диацетоксипентилдоксорубицин, дибромманнит, дигидроксиантрациндион, дисоразолы, доластатин (например доластатин 10), доксорубицин, дуокармицин, эхиномицины, элеутеробины, эметин, эпотилоны, эсперамицин, эстрамустины, бромид этидия, этопозид, фторурацилы, гелданамицины, грамицидин D, глюкокортикоиды, иринотеканы, ингибиторы белка кинезина веретена (KSP), лептомицины, лейрозины, лидокаин, ломустин (CCNU), майтанзиноиды, мехлорэтамин, мелфалан, меркатопурины, метоптерины, метотрексат, митрамицин, митомицин, митоксантрон, N8-ацетилспермидин, подофиллотоксины, прокаин, пропранолол, птеридины, пуромицин, пирролобензодиазепины (PBD), ризоксины, стрептозотоцин, таллизомицины, таксол, тенопозид, тетракаин, тиоэпахлорамбуцил, томаймицины, топотеканы, тубулизин, винбластин, винкристин, виндезин, винорелбины и производные любого из вышеперечисленных. В соответствии с определенными вариантами осуществления цитотоксическое средство, которое конъюгировано с антителом к MET, представляет собой майтанзиноид, такой как DM1 или DM4, производное томаймицина или производное доластатина. В соответствии с определенными вариантами осуществления цитотоксическое средство, которое конъюгировано с антителом к MET, представляет собой ауристатин, такой как MMAE, MMAF или его производные. Другие цитотоксические средства, известные из уровня техники, рассматриваются в пределах объема настоящего изобретения, включая, например, белковые токсины, такие как рицин, токсин C. difficile, экзотоксин синегнойной палочки, рицин, дифтерийный токсин, ботулинический токсин, бриодин, сапорин, токсины фитолакки (т.е. фитолаккатоксин и фитолакцигенин) и другие, например, изложенные в Sapra et al., Pharmacol. & Therapeutics, 2013, 138:452-469.
[148] В определенных вариантах осуществления цитотоксическое средство представляет собой майтанзиноид, например производное майтанзина. Подходящие майтанзиноиды включают DM1, DM4 или их производные, стереоизомеры или изотопологи. Подходящие майтанзиноиды также включают без ограничения майтанзиноиды, раскрытые в WO 2014/145090A1, WO 2015/031396A1, US 2016/0375147A1 и US 2017/0209591A1, включенные в данный документ посредством ссылки во всей своей полноте.
[149] В некоторых вариантах осуществления майтанзиноид характеризуется следующей структурой:
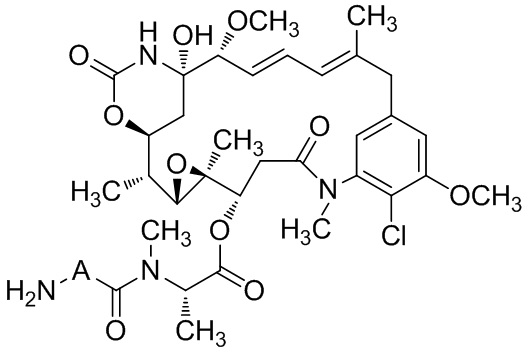
где A представляет собой необязательно замещенный арилен или гетероарилен.
[150] В некоторых вариантах осуществления майтанзиноид характеризуется следующей структурой:
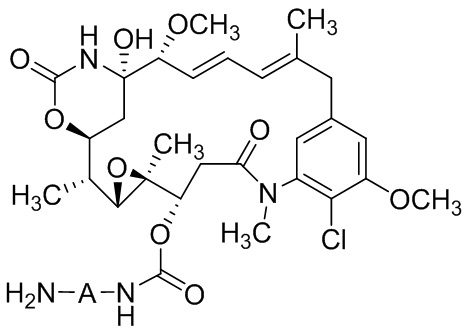
где A представляет собой необязательно замещенный арилен или гетероарилен.
[151] В некоторых вариантах осуществления майтанзиноид характеризуется следующей структурой:
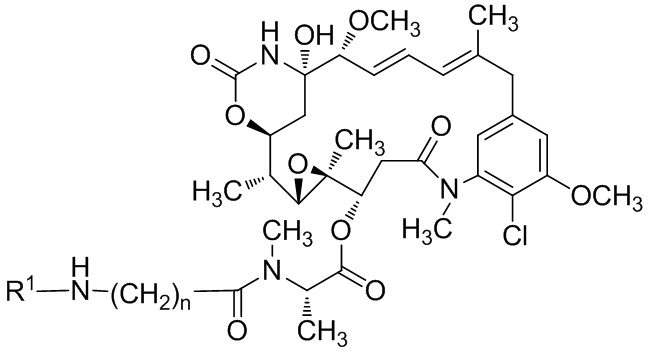
где n представляет собой целое число от 1 до 12, а R1 представляет собой алкил.
[152] В некоторых вариантах осуществления майтанзиноид представляет собой:
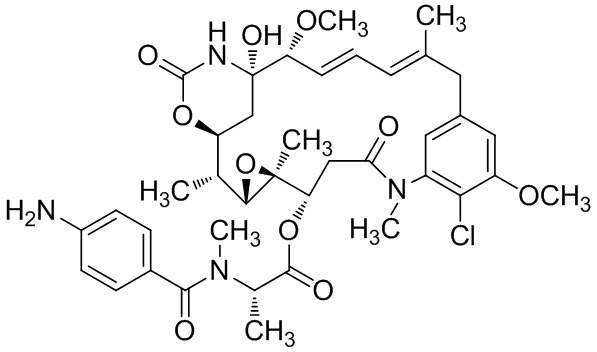 ,
, 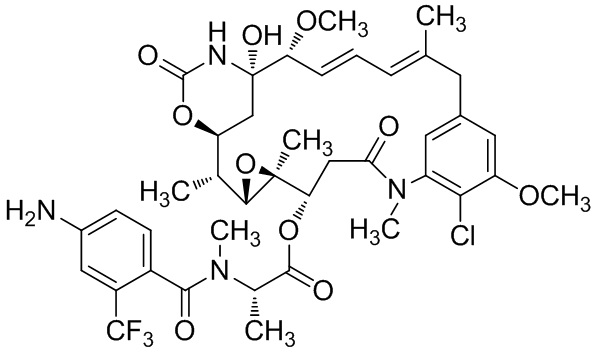 ,
, 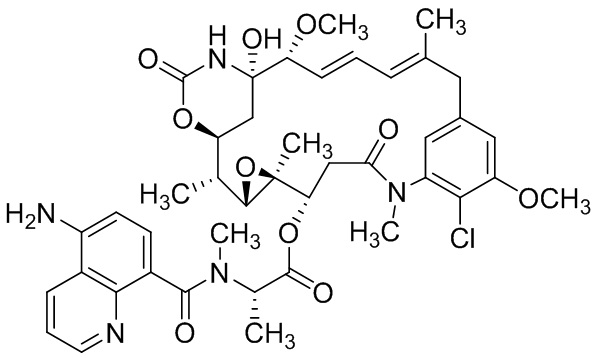 ,
, 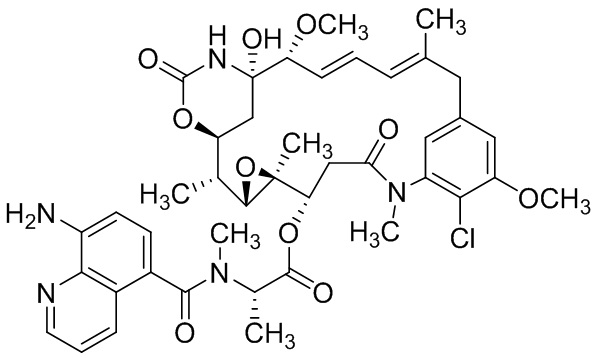 ,
,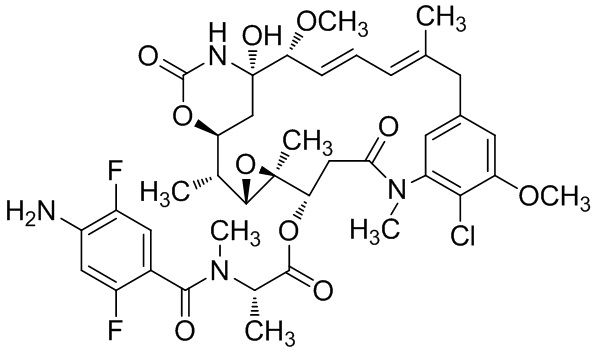 ,
, 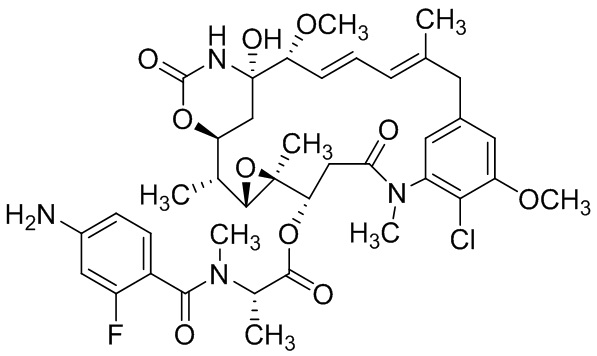 ,
, 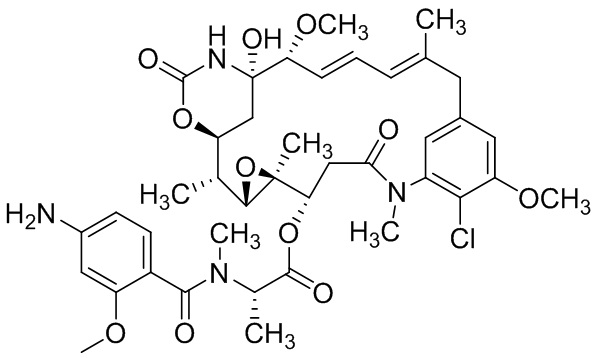 ,
, 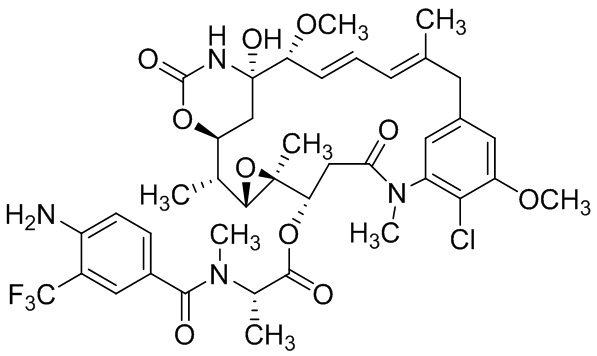 ,
, 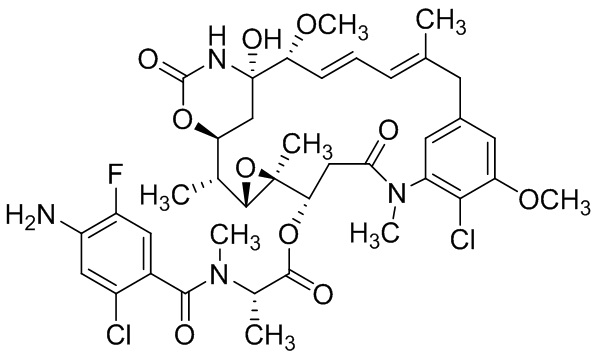 ,
, 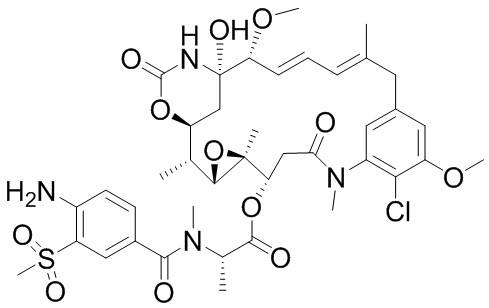 ,
, 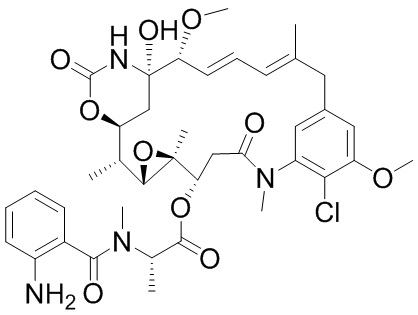 ,
, 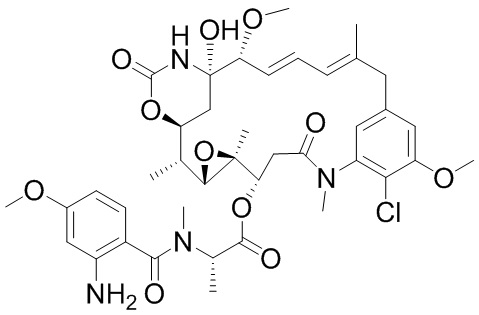 ,
, 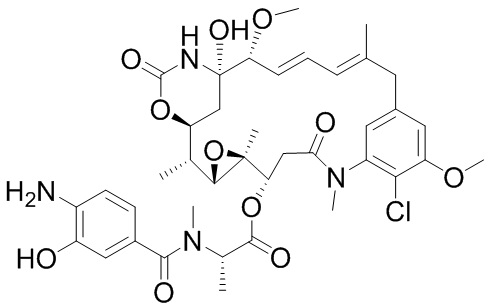 ,
,  .
.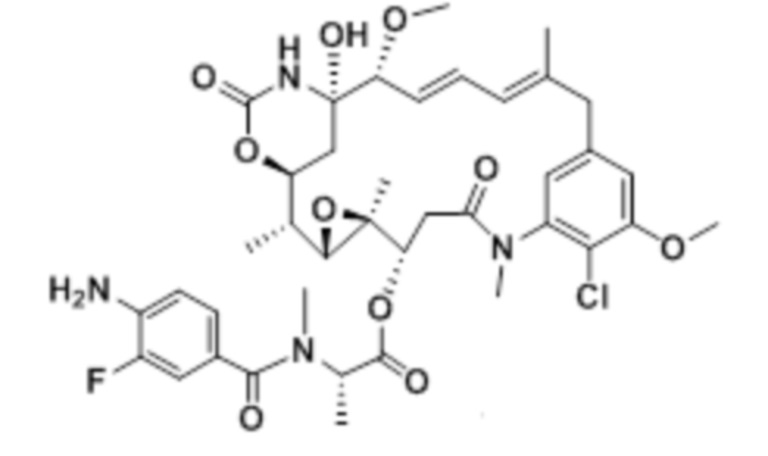 ,
, 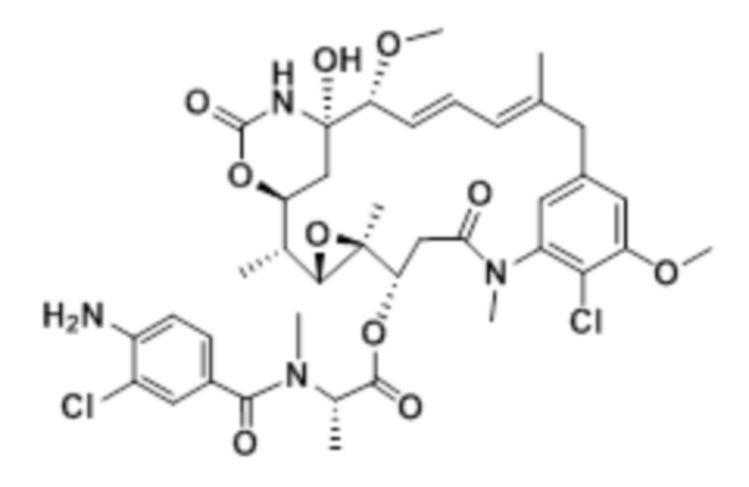 ,
, 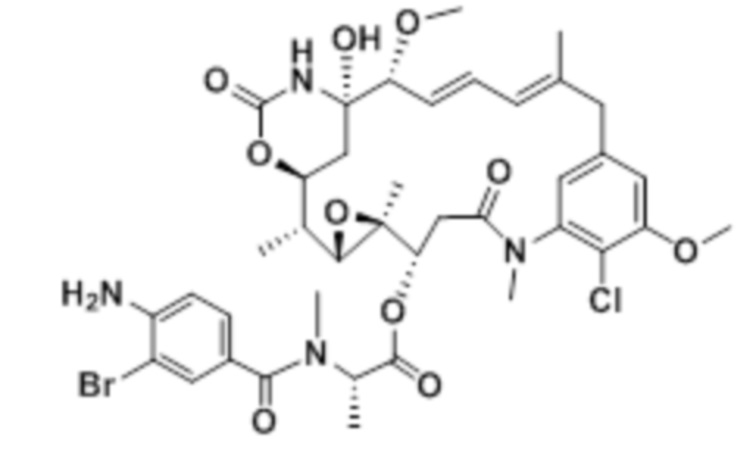 ,
, 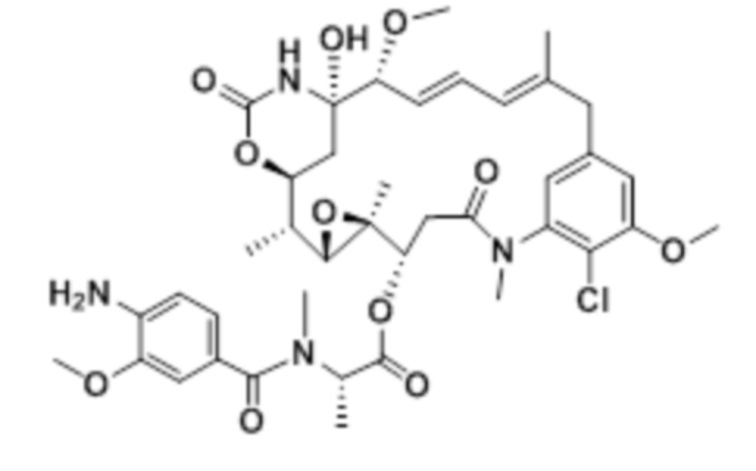 ,
, 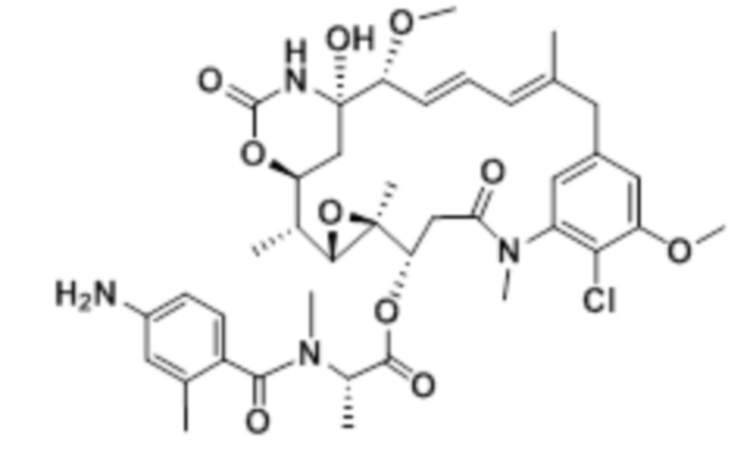 ,
, 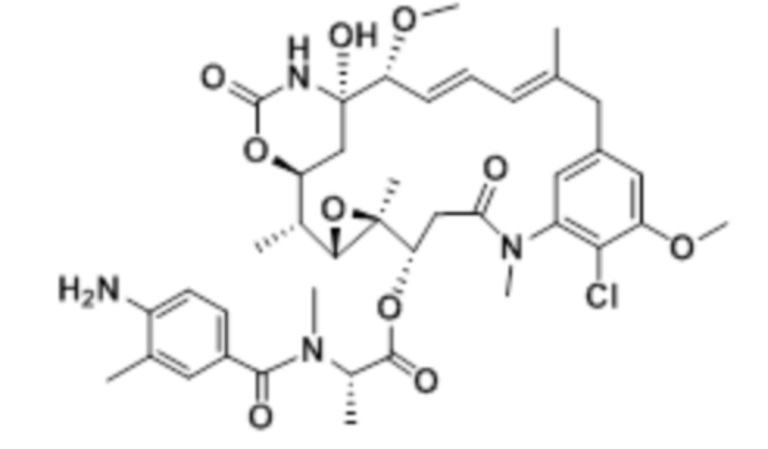 ,
, 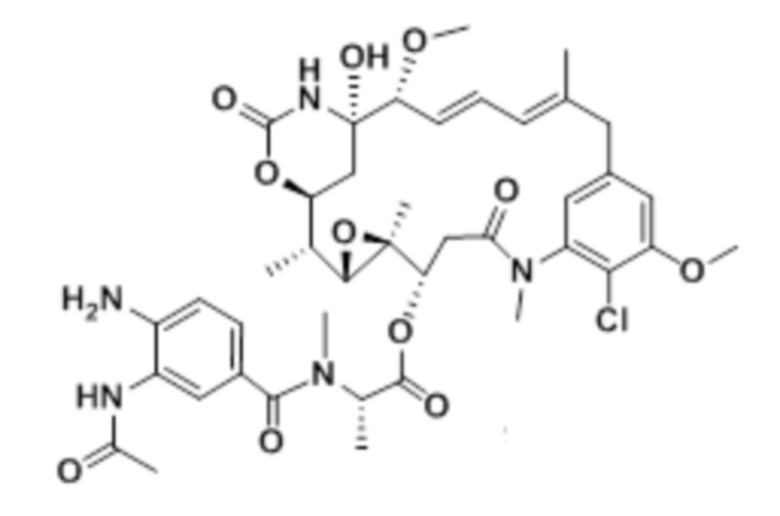 ,
, 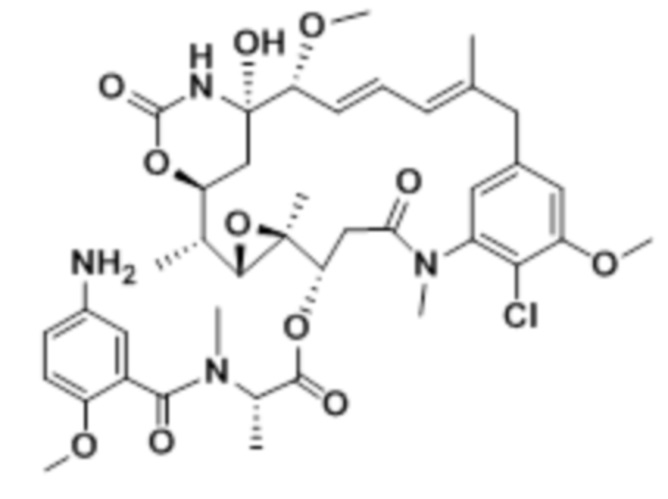 ,
, 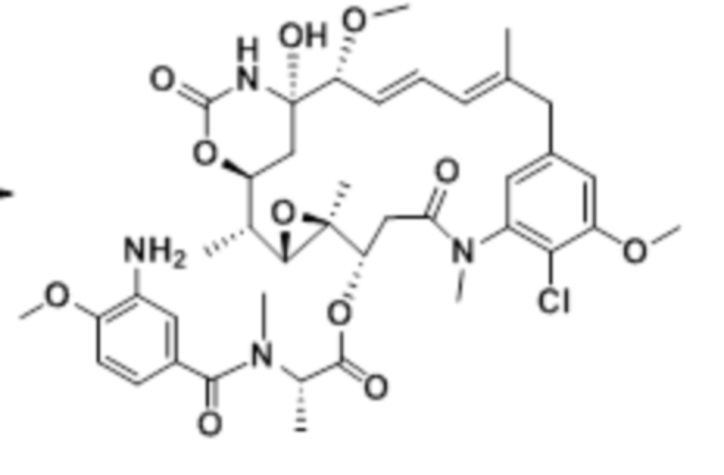 ,
, 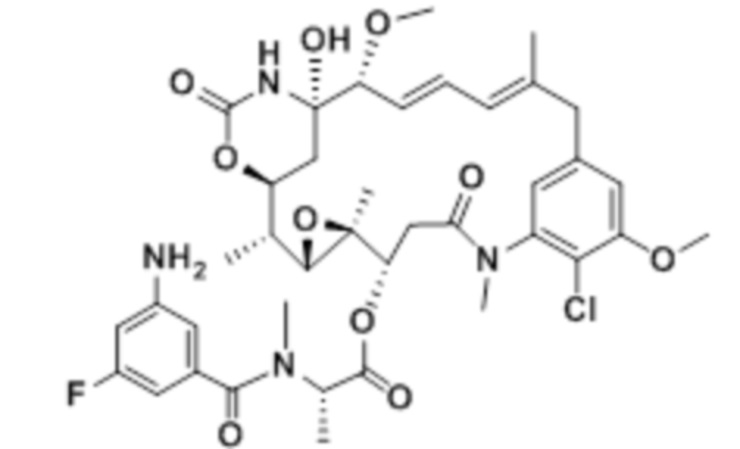 ,
, 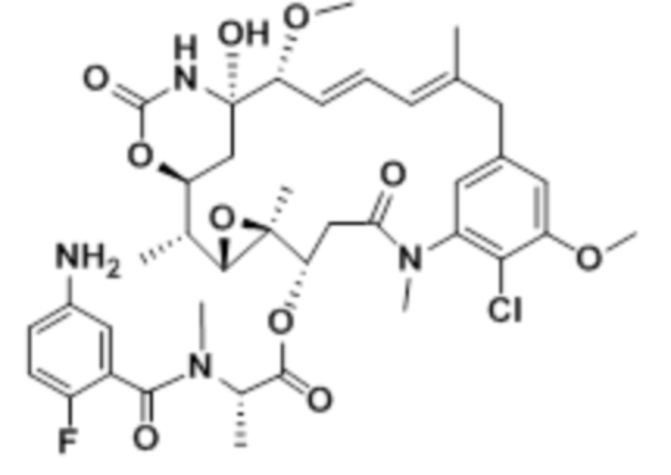 ,
,  ,
, 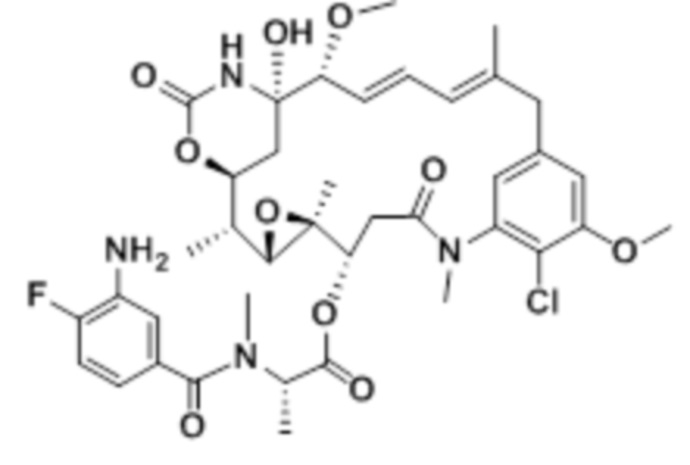 ,
, 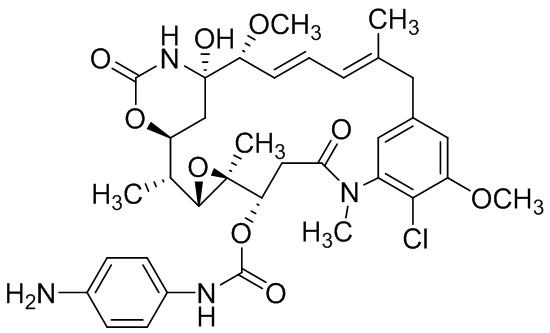 ,
,
 ,
, 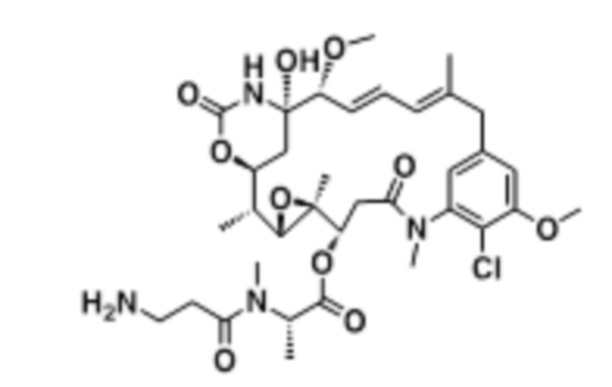 ,
, 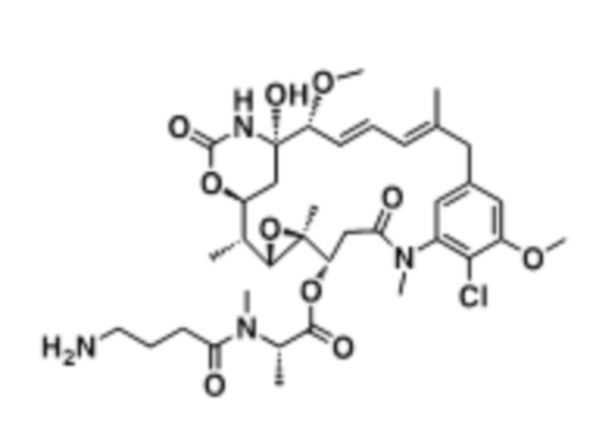 ,
, 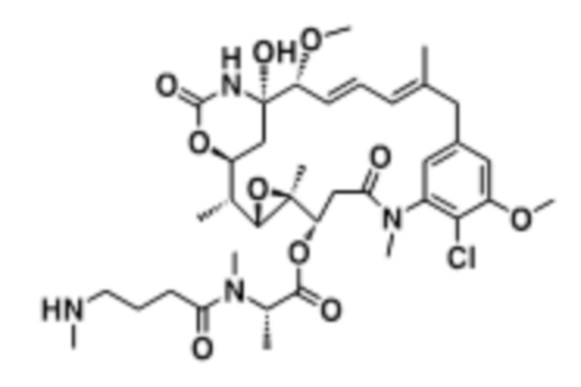 ,
, 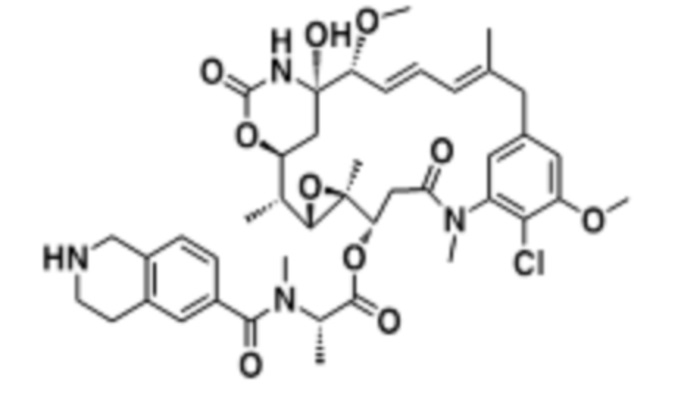 или
или 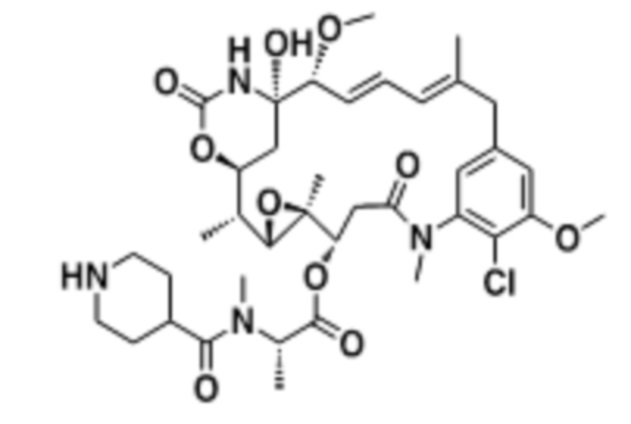 .
.
[153] В некоторых вариантах осуществления майтанзиноид представляет собой:
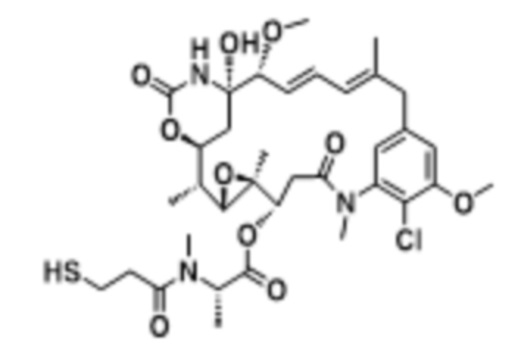 .
.
[154] В некоторых вариантах осуществления майтанзиноид представляет собой:
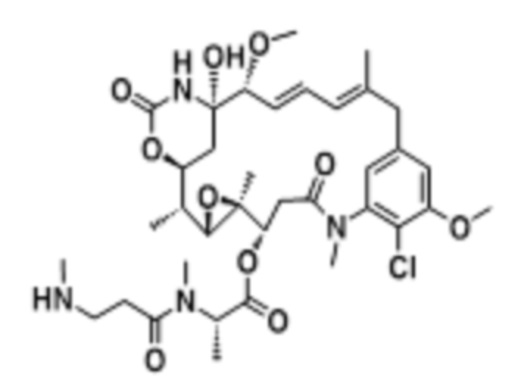 .
.
[155] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются конъюгаты антитело-радионуклид (ARC), содержащие антитела к MET, конъюгированные с одним или более радионуклидами. Иллюстративные радионуклиды, которые можно применять в контексте данного аспекта настоящего изобретения, включают без ограничения, например, 225Ac, 212Bi, 213Bi, 131I, 186Re, 227Th, 222Rn, 223Ra, 224Ra и 90Y.
[156] В определенных вариантах осуществления ADC содержат антитело к MET или биспецифический антигенсвязывающий белок MET x MET, конъюгированный с цитотоксическим средством (например любым из цитотоксических средств, раскрытых выше) посредством линкерной молекулы. Линкеры представляют собой любую группу или фрагмент, которые сшивают, соединяют или связывают антитело или антигенсвязывающие белки, описанные в данном документе, с терапевтическим фрагментом, например цитотоксическим средством. Подходящие линкеры можно найти, например, в Antibody-Drug Conjugates and Immunotoxins; Phillips, G. L., Ed.; Springer Verlag: New York, 2013; Antibody-Drug Conjugates; Ducry, L., Ed.; Humana Press, 2013; Antibody-Drug Conjugates; Wang, J., Shen, W.-C., and Zaro, J. L., Eds.; Springer International Publishing, 2015, содержание каждого из которых включено в данный документ посредством ссылки во всей своей полноте. В целом, подходящими линкерами связывающих средств для конъюгатов на основе антител, описанных в данном документе, являются линкеры, которые достаточно стабильны для применения периода полужизни антитела в кровотоке и в то же время способны высвобождать свою нагрузку после опосредованной антигеном интернализации конъюгата. Линкеры могут быть расщепляемыми или нерасщепляемыми. Расщепляемые линкеры включают линкеры, которые расщепляются посредством внутриклеточного метаболизма после интернализации, например расщепляются посредством гидролиза, восстановления или ферментативной реакции. Нерасщепляемые линкеры включают линкеры, которые высвобождают присоединенную нагрузку посредством лизосомной деградации антитела после интернализации. Подходящие линкеры включают без ограничения кислотонеустойчивые линкеры, неустойчивые к гидролизу линкеры, ферментативно расщепляемые линкеры, неустойчивые к восстановлению линкеры, саморасщепляющиеся линкеры и нерасщепляемые линкеры. Подходящие линкеры также включают без ограничения линкеры, которые представляют собой пептиды, глюкурониды, тиоэфиры сукцинимида, звенья полиэтиленгликоля (PEG), гидразоны, звенья малкапроила, дипептидные звенья, звенья валин-цитруллина и звенья парааминобензила (PAB), или содержат их.
[157] Любую линкерную молекулу или линкерную технологию, известную из уровня техники, можно использовать для получения или конструирования ADC, применимого в соответствии с настоящим изобретением. В определенных вариантах осуществления линкер представляет собой расщепляемый линкер. В соответствии с другими вариантами осуществления линкер представляет собой нерасщепляемый линкер. Иллюстративные линкеры, которые можно использовать в контексте настоящего изобретения, включают линкеры, которые содержат, например, MC (6-малеимидокапроил), MP (малеимидопропаноил), val-cit (валин-цитруллин), val-ala (валин-аланин), дипептидный сайт в расщепляемом протеазой линкере, ala-phe (аланин-фенилаланин), дипептидный сайт в расщепляемом протеазой линкере, PAB (п-аминобензилоксикарбонил), SPP (N-сукцинимидил-4-(2-пиридилтио)пентаноат), SMCC (N-сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат), SIAB (N-сукцинимидил-(4-йодацетил)аминобензоат) и их варианты и комбинации, или состоят из них. Дополнительные примеры линкеров, которые можно использовать в контексте настоящего изобретения, предусмотрены, например, в US 7754681 и в Ducry, Bioconjugate Chem., 2010, 21:5-13, и ссылках, цитируемых в них, содержание которых включено в данный документ посредством ссылки во всей своей полноте.
[158] В определенных вариантах осуществления линкеры являются стабильными в физиологических условиях. В определенных вариантах осуществления линкеры являются расщепляемыми, например способными высвобождать по меньшей мере часть нагрузки в присутствии фермента или при определенном диапазоне или значении pH. В некоторых вариантах осуществления линкер содержит расщепляемый ферментом фрагмент. Иллюстративные расщепляемые ферментом фрагменты включают без ограничения пептидные связи, сложноэфирные связи, гидразоны и дисульфидные связи. В некоторых вариантах осуществления линкер содержит расщепляемый катепсином линкер.
[159] В некоторых вариантах осуществления линкер содержит нерасщепляемый фрагмент.
[160] Подходящие линкеры также включают без ограничения линкеры, которые химически связаны с двумя остатками цистеина одного связывающего средства, например антитела. Такие линкеры могут служить для имитации дисульфидных связей антитела, которые разрушаются в результате процесса конъюгации.
[161] В некоторых вариантах осуществления линкер содержит одну или более аминокислот. Подходящие аминокислоты включают природные, неприродные, стандартные, нестандартные, протеиногенные, непротеиногенные и L- или D-αаминокислоты. В некоторых вариантах осуществления линкер содержит аланин, валин, глицин, лейцин, изолейцин, метионин, триптофан, фенилаланин, пролин, серин, треонин, цистеин, тирозин, аспарагин, глутамин, аспарагиновую кислоту, глутаминовую кислоту, лизин, аргинин, гистидин или цитруллин, их производное или их комбинацию. В определенных вариантах осуществления одна или более боковых цепей аминокислот связаны с группой боковой цепи, описанной ниже. В некоторых вариантах осуществления линкер содержит валин и цитруллин. В некоторых вариантах осуществления линкер содержит лизин, валин и цитруллин. В некоторых вариантах осуществления линкер содержит лизин, валин и аланин. В некоторых вариантах осуществления линкер содержит валин и аланин.
[162] В некоторых вариантах осуществления линкер содержит саморасщепляющуюся группу. Саморасщепляющаяся группа может представлять собой любую такую группу, известную специалистам в данной области техники. В конкретных вариантах осуществления саморасщепляющаяся группа представляет собой п-аминобензил (PAB) или его производное. Применимые производные включают п-аминобензилоксикарбонил (PABC). Специалистам в данной области техники будет понятно, что саморасщепляющаяся группа способна осуществлять химическую реакцию, которая приводит к освобождению оставшихся атомов линкера от нагрузки.
[163] В некоторых вариантах осуществления линкер представляет собой:
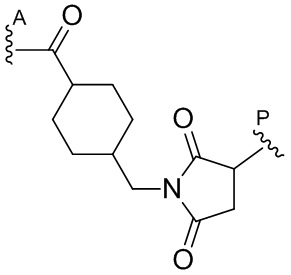
где  представляет собой связь с антителом или антигенсвязывающим белком (например посредством остатка лизина), и
представляет собой связь с антителом или антигенсвязывающим белком (например посредством остатка лизина), и 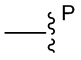 представляет собой связь с цитотоксическим средством (например DM1). В некоторых вариантах осуществления линкер представляет собой:
представляет собой связь с цитотоксическим средством (например DM1). В некоторых вариантах осуществления линкер представляет собой:
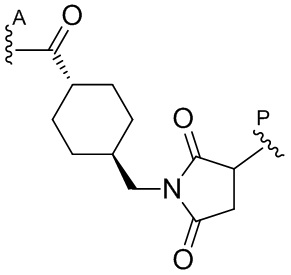
где  представляет собой связь с антителом или антигенсвязывающим белком (например посредством остатка лизина), и
представляет собой связь с антителом или антигенсвязывающим белком (например посредством остатка лизина), и 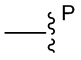 представляет собой связь с цитотоксическим средством (например DM1). В определенных вариантах осуществления линкер представляет собой:
представляет собой связь с цитотоксическим средством (например DM1). В определенных вариантах осуществления линкер представляет собой:
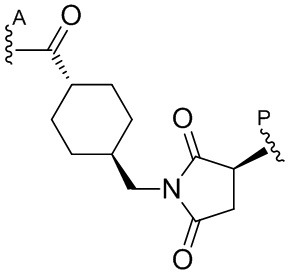 .
.
[164] В определенных вариантах осуществления линкер представляет собой:
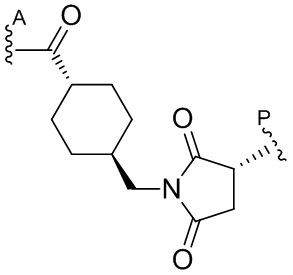 .
.
[165] В некоторых вариантах осуществления линкер представляет собой производное малеимидилметил-4-транс-циклогексанкарбоксисукцината:
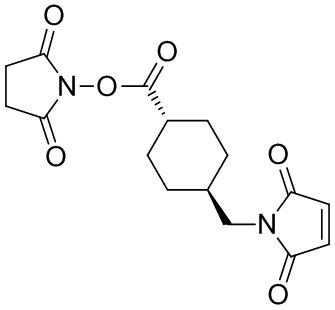 .
.
[166] В некоторых вариантах осуществления линкер представляет собой:
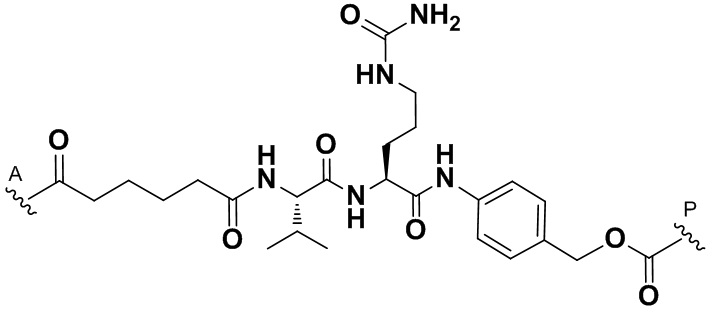
где  представляет собой связь с антителом или антигенсвязывающим белком (например посредством остатка лизина), и
представляет собой связь с антителом или антигенсвязывающим белком (например посредством остатка лизина), и 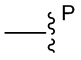 представляет собой связь с цитотоксическим средством (например соединением, характеризующимся следующей формулой:
представляет собой связь с цитотоксическим средством (например соединением, характеризующимся следующей формулой:
 ).
).
[167] Молекулы, применимые в соответствии с раскрытыми способами, включают ADC, в которых линкер соединяет антитело к MET или биспецифический антигенсвязывающий белок MET x MET с лекарственным средством или цитотоксином посредством присоединения к конкретной аминокислоте в антителе или антигенсвязывающей молекуле. Иллюстративные присоединения аминокислот, которые можно использовать в контексте данного аспекта, включают, например, лизин (см., например, US 5208020; US 2010/0129314; Hollander et al., Bioconjugate Chem., 2008, 19:358-361; WO 2005/089808; US 5714586; US 2013/0101546 и US 2012/0585592), цистеин (см., например, US 2007/0258987; WO 2013/055993; WO 2013/055990; WO 2013/053873; WO 2013/053872; WO 2011/130598; US 2013/0101546; и US 7750116), селеноцистеин (см., например, WO 2008/122039 и Hofer et al., Proc. Natl. Acad. Sci., USA, 2008, 105:12451-12456), формилглицин (см., например, Carrico et al., Nat. Chem. Biol., 2007, 3:321-322; Agarwal et al., Proc. Natl. Acad. Sci., USA, 2013, 110:46-51, и Rabuka et al., Nat. Protocols, 2012, 10:1052-1067), неприродные аминокислоты (см., например, WO 2013/068874 и WO 2012/166559) и кислые аминокислоты см., например, WO 2012/05982). Линкеры также могут быть конъюгированы с антигенсвязывающим белком посредством присоединения к углеводам (см., например, US 2008/0305497, WO 2014/065661 и Ryan et al., Food & Agriculture Immunol., 2001, 13:127-130) и посредством дисульфидных линкеров (см., например, WO 2013/085925, WO 2010/010324, WO 2011/018611 и Shaunak et al., Nat. Chem. Biol., 2006, 2:312-313). Методики сайт-специфической конъюгации также можно использовать для непосредственной конъюгации с конкретными остатками антитела или антигенсвязывающего белка (см., например, Schumacher et al. J Clin Immunol (2016) 36(Suppl 1): 100). Методики сайт-специфической конъюгации включают без ограничения конъюгацию с глутамином с помощью трансглутаминазы (см., например, Schibli, Angew Chemie Inter Ed. 2010, 49 ,9995).
[168] В соответствии с определенными вариантами осуществления ADC, применимые в соответствии со способами, предусмотренными в данном документе, содержат антитело к MET или биспецифический антигенсвязывающий белок MET x MET, конъюгированный с композицией линкер-лекарственное средство, изложенной в международной патентной публикации WO2014/145090, (например соединение «7», также называемое в данном документе «M0026»и изображенное ниже), раскрытие которой включено в данный документ посредством ссылки во всей своей полноте:
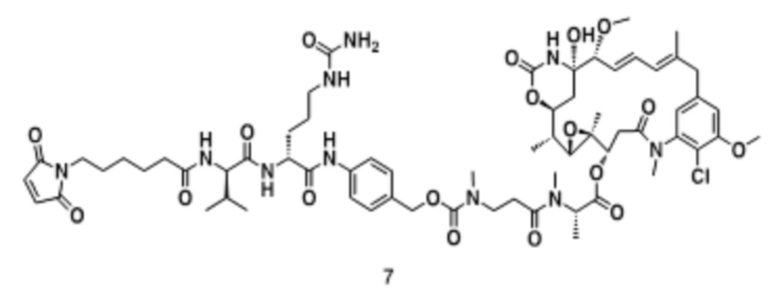 .
.
[169] Также применимыми в соответствии со способами, предусмотренными в данном документе, являются конъюгаты антитело-лекарственное средство, содержащие моноспецифические антитела к MET и биспецифические антитела к MET x MET, где указанное антитело к MET или биспецифическое антитело к MET x MET конъюгировано с цитотоксическим средством. В определенных вариантах осуществления цитотоксическое средство представляет собой майтанзиноид. В определенных вариантах осуществления майтанзиноид представляет собой соединение, характеризующееся следующей формулой:

где n представляет собой целое число от 1 до 12, а R1 представляет собой алкил. В определенных вариантах осуществления майтанзиноид представляет собой
 или
или  .
.
В определенных вариантах осуществления цитотоксическое средство представляет собой майтанзиноид, и майтанзиноид ковалентно присоединен к антителу посредством нерасщепляемого линкера. В определенных вариантах осуществления цитотоксическое средство представляет собой майтанзиноид, и майтанзиноид ковалентно присоединен к антителу посредством расщепляемого линкера.
[170] В одном варианте осуществления антитело конъюгировано с:
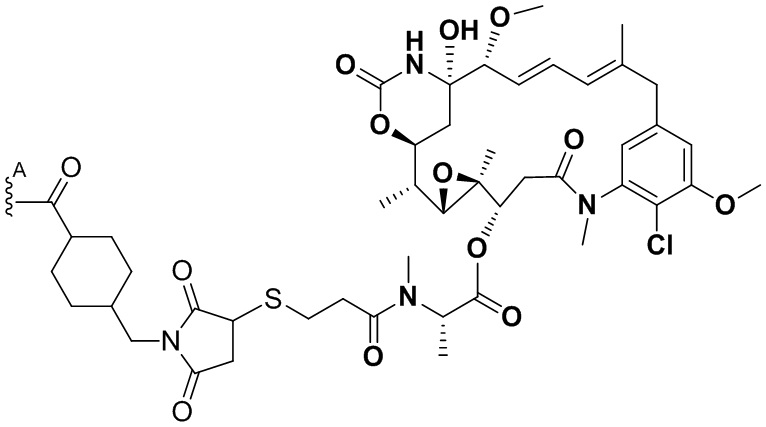 .
.
где  представляет собой связь с антителом.
представляет собой связь с антителом.
[171] В одном варианте осуществления антитело конъюгировано с:
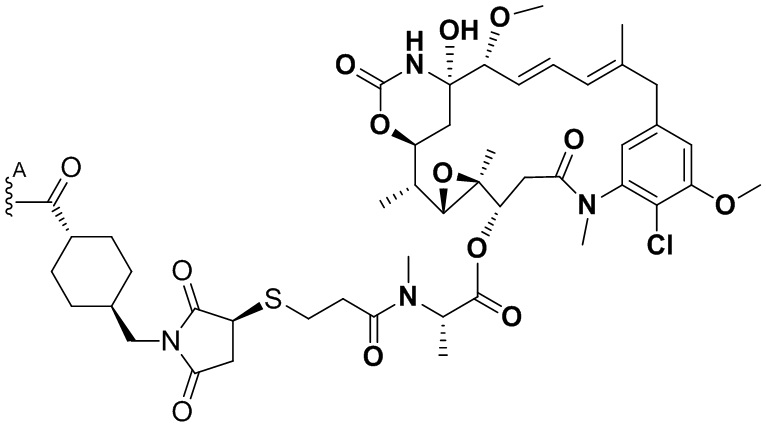
где  представляет собой связь с антителом.
представляет собой связь с антителом.
[172] В одном варианте осуществления антитело конъюгировано с:
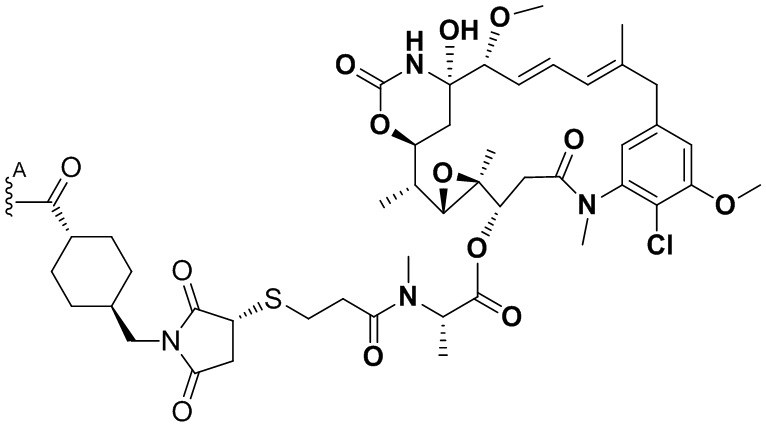
где  представляет собой связь с антителом.
представляет собой связь с антителом.
[173] В одном варианте осуществления антитело конъюгировано с:
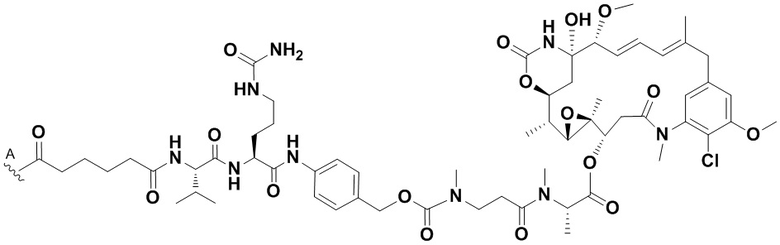
где  представляет собой связь с антителом.
представляет собой связь с антителом.
[174] В одном варианте осуществления антитело конъюгировано с диастереомером соединения, характеризующегося следующей структурой
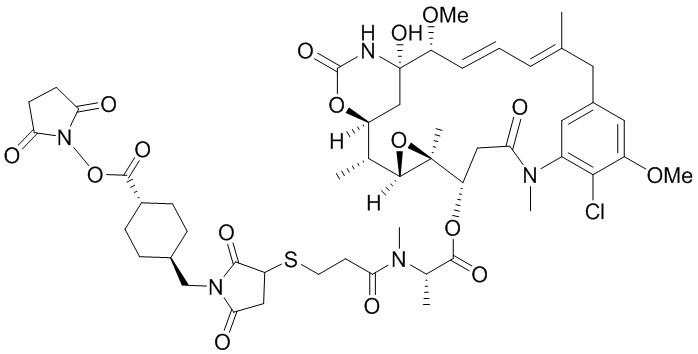
где диастереомер характеризуется 1H ЯМР, характеризующимся дельта-сдвигами (300 МГц, CDCl3) δ 6,85 (d, 1H, J = 4 Гц), 6,72 (m, 1H), 6,65 (d, 1H, J = 4 Гц), 6,44 (dd, 1H, J = 15 Гц, 11 Гц), 6,25 (s, 1H), 5,67 (dd, 1H, J = 16 Гц, 9 Гц), 5,41 (m, 1H), 4,79 (d, 1H, J = 11 Гц), 4,30 (t, 1H, J = 11 Гц), 3,72 (m, 2H), 3,51 (d, 1H, J = 9 Гц), 3,37 (m, 4H), 3,27 (m, 1H), 3,23 (s, 3H), 3,16-2,99 (m, 4H), 2,85 (m, 7H), 2,62 (m, 3H), 2,39 (ddd, 1H, J = 19 Гц, 12 Гц, 4 Гц), 2,18 (br m, 2H), 1,77 (br m, 3H), 1,66 (s, 3H), 1,60-1,47 (m, 4H), 1,31 (m, 6H), 1,05 (m, 2H) и 0,82 (s, 3H).
[175] В одном варианте осуществления антитело конъюгировано с диастереомером соединения, характеризующегося следующей структурой

где диастереомер характеризуется 1H ЯМР, в значительной степени сходным с показанным на фигуре 31.
[176] В одном варианте осуществления антитело конъюгировано с соединением, характеризующимся следующей структурой:

(I);
полученным посредством способа, включающего стадии приведения в контакт:
(i) соединения формулы III:
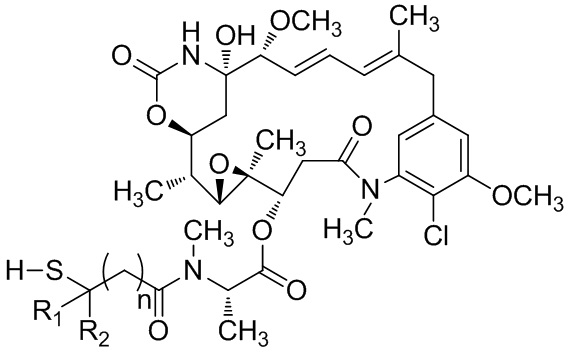
III;
(ii) соединения формулы IV:

IV,
(iii) силикагеля и
(iv) разбавителя, содержащего органический растворитель и воду.
[177] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n
где
Ab представляет собой антитело к MET или биспецифический антигенсвязывающий белок MET x MET, описанные в данном документе;
L представляет собой линкер;
Pay представляет собой цитотоксическое средство, и
n представляет собой целое число от 1 до 10.
[178] В некоторых вариантах осуществления Ab представляет собой антитело к MET, содержащее CDR в пределах пары аминокислотных последовательностей HCVR/LCVR под SEQ ID NO: 82/138. В некоторых вариантах осуществления Ab представляет собой антитело к MET, содержащее аминокислотную последовательность HCVR под SEQ ID NO: 82 и аминокислотную последовательность LCVR под SEQ ID NO: 138.
[179] В некоторых вариантах осуществления Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий CDR в пределах аминокислотной последовательности D1-HCVR под SEQ ID NO: 58 и CDR в пределах аминокислотной последовательности D2-HCVR под SEQ ID NO: 82. В некоторых аспектах биспецифический антигенсвязывающий белок MET x MET дополнительно содержит CDR в пределах аминокислотной последовательности LCVR под SEQ ID NO: 138. В некоторых вариантах осуществления Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 58 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82. В некоторых аспектах биспецифический антигенсвязывающий белок MET x MET дополнительно содержит аминокислотную последовательность LCVR под SEQ ID NO: 138.
[180] В некоторых вариантах осуществления Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий CDR в пределах аминокислотной последовательности D1-HCVR под SEQ ID NO: 18 и CDR в пределах аминокислотной последовательности D2-HCVR под SEQ ID NO: 82. В некоторых аспектах биспецифический антигенсвязывающий белок MET x MET дополнительно содержит CDR в пределах аминокислотной последовательности LCVR под SEQ ID NO: 138. В некоторых вариантах осуществления Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 18 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82.
[181] В некоторых вариантах осуществления L представляет собой расщепляемый линкер. В некоторых вариантах осуществления L представляет собой нерасщепляемый линкер. В некоторых вариантах осуществления L содержит дипептид. В некоторых вариантах осуществления L содержит фрагмент PAB.
[182] В некоторых вариантах осуществления L содержит фрагмент, характеризующийся следующей структурой:
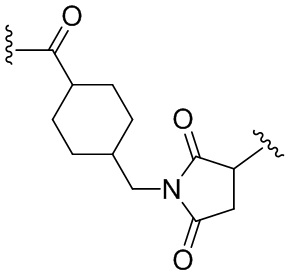 .
.
[183] В некоторых вариантах осуществления L содержит фрагмент, характеризующийся следующей структурой:
 .
.
[184] В некоторых вариантах осуществления L содержит фрагмент, характеризующийся следующей структурой:
 .
.
[185] В некоторых вариантах осуществления L содержит фрагмент, характеризующийся следующей структурой:
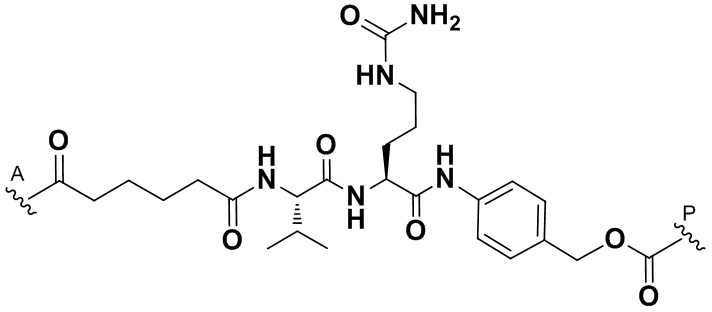 .
.
[186] В некоторых вариантах осуществления Pay представляет собой майтанзиноид.
[187] В некоторых вариантах осуществления Pay представляет собой:
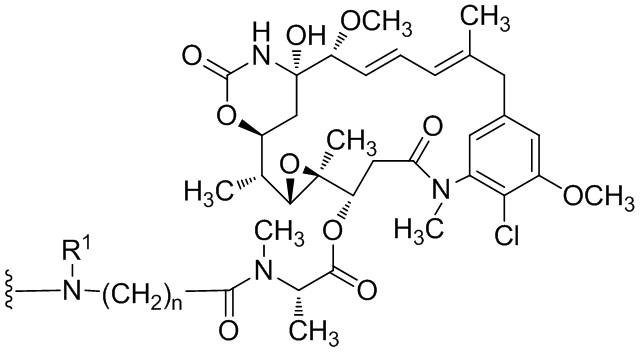
где R1 представляет собой алкил.
[188] В некоторых вариантах осуществления Pay представляет собой:
 .
.
[189] В некоторых вариантах осуществления Pay представляет собой:
 .
.
[190] В некоторых вариантах осуществления n представляет собой целое число от 2 до 5.
[191] В некоторых вариантах осуществления -L-Pay представляет собой:
 .
.
где  представляет собой связь с антителом.
представляет собой связь с антителом.
[192] В некоторых вариантах осуществления -L-Pay представляет собой:

где  представляет собой связь с антителом.
представляет собой связь с антителом.
[193] В некоторых вариантах осуществления -L-Pay представляет собой

где  представляет собой связь с антителом.
представляет собой связь с антителом.
[194] В некоторых вариантах осуществления -L-Pay представляет собой:

где  представляет собой связь с антителом.
представляет собой связь с антителом.
[195] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой антитело к MET, содержащее аминокислотную последовательность HCVR под SEQ ID NO: 82 и аминокислотную последовательность LCVR под SEQ ID NO: 138;
L-Pay представляет собой

где  представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
[196] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой антитело к MET, содержащее аминокислотную последовательность HCVR под SEQ ID NO: 82 и аминокислотную последовательность LCVR под SEQ ID NO: 138;
L-Pay представляет собой

где  представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
[197] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой антитело к MET, содержащее аминокислотную последовательность HCVR под SEQ ID NO: 82 и аминокислотную последовательность LCVR под SEQ ID NO: 138;
L-Pay представляет собой

где  представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
[198] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой антитело к MET, содержащее аминокислотную последовательность HCVR под SEQ ID NO: 82 и аминокислотную последовательность LCVR под SEQ ID NO: 138;
L-Pay представляет собой

где  представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
представляет собой связь с антителом, и n представляет собой целое число от 2 до 5.
[199] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 58 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[200] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 58 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[201] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 58 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[202] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 58 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[203] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 18 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[204] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 18 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[205] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 18 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[206] В некоторых вариантах осуществления конъюгаты характеризуются следующей структурой:
Ab-[L-Pay]n,
где
Ab представляет собой биспецифический антигенсвязывающий белок MET x MET, содержащий аминокислотную последовательность D1-HCVR под SEQ ID NO: 18 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82;
L-Pay представляет собой

где  представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
представляет собой связь с антигенсвязывающим белком, и n представляет собой целое число от 2 до 5.
[207] Конъюгаты антитело-лекарственное средство, применимые в соответствии с данным документом, можно получать с применением условий конъюгации, известных специалистам в данной области техники (см., например, Doronina et al. Nature Biotechnology 2003, 21, 7, 778, которая включена в данный документ посредством ссылки во всей своей полноте). В некоторых вариантах осуществления конъюгат антитело-лекарственное средство на основе антитела к MET или биспецифического антигенсвязывающего белка MET x MET получают посредством приведения в контакт антитела к MET или биспецифического антигенсвязывающего белка MET x MET, описанного в данном документе, с соединением, содержащим требуемый линкер и цитотоксическое средство, где указанный линкер содержит фрагмент, который реагирует с антителом или антигенсвязывающим белком, например по требуемому остатку антитела или антигенсвязывающего белка.
[208] В некоторых вариантах осуществления способы получения конъюгата антитело-лекарственное средство, применимого в соответствии со способами, предусмотренными в данном документе, включают приведение в контакт антитела к MET или биспецифического антигенсвязывающего белка MET x MET, описанных в данном документе, с соединением, характеризующимся следующей формулой A1:
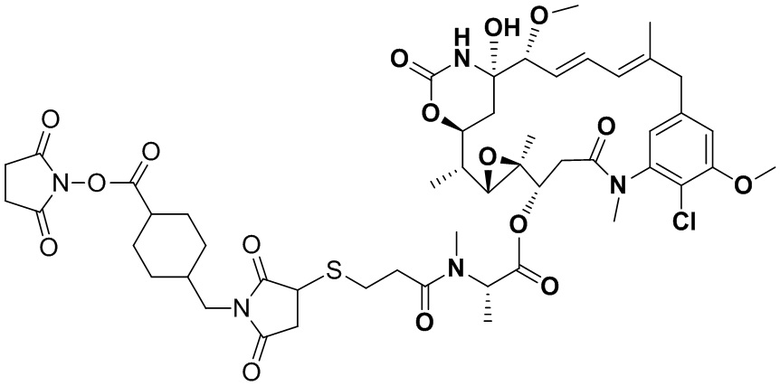
A1,
и водным разбавителем.
[209] В некоторых вариантах осуществления соединение формулы A1 присутствует в стехиометрическом избытке. В некоторых вариантах осуществления соединение формулы A1 присутствует в 5-6-кратном стехиометрическом избытке. В некоторых вариантах осуществления водный разбавитель содержит HEPES. В некоторых вариантах осуществления водный разбавитель содержит DMA.
[210] В некоторых вариантах осуществления соединение формулы A1 представляет собой соединение формулы A2 или A3:
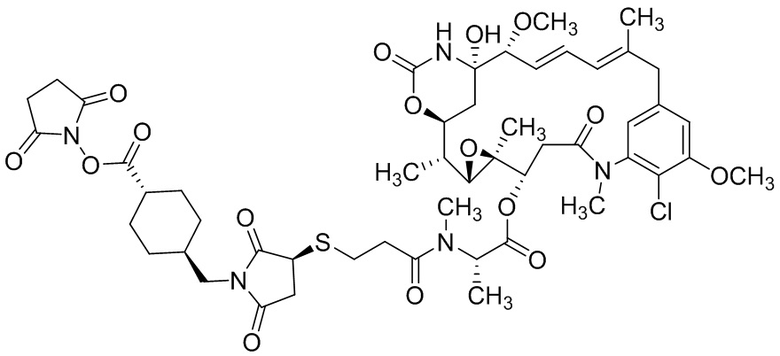
A2,
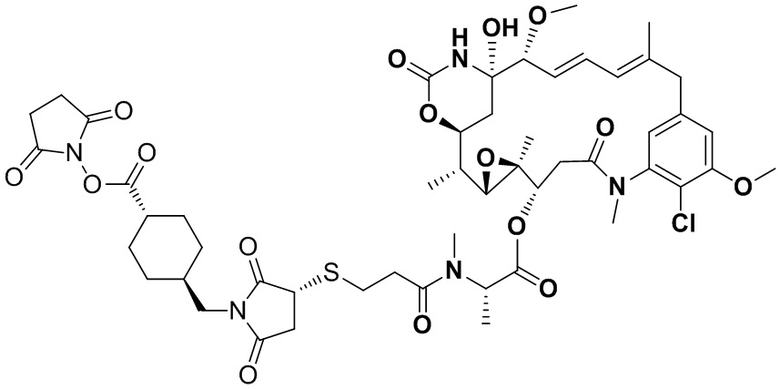
A3.
[211] В некоторых вариантах осуществления соединение формулы A2 или A3 является стереометрически чистым. В некоторых вариантах осуществления соединение формулы A1 содержит соединение формулы A2 или A3, где соединение A2 или A3 присутствует в диастереомерном избытке, составляющем более чем 50%. В определенных вариантах осуществления диастереомерный избыток составляет более чем 70%. В определенных вариантах осуществления диастереомерный избыток составляет более чем 90%. В определенных вариантах осуществления диастереомерный избыток составляет более чем 95%.
[212] Термин «диастереомерный избыток» относится к разнице между молярной долей одного требуемого диастереомера по сравнению с остальными диастереомерами в композиции. Диастереомерный избыток рассчитывается следующим образом: (количество одного диастереомера)-(количество других диастереомеров)/1. Например, композиция, которая содержит 90% 1 и 10% 2, 3, 4 или их смеси, характеризуется диастереомерным избытком, составляющим 80% [(90-10)/1]. Композиция, которая содержит 95% 1 и 5% 2, 3, 4 или их смеси, характеризуется диастереомерным избытком, составляющим 90% [(95-5)/1]. Композиция, которая содержит 99% 1 и 1% 2, 3, 4 или их смеси, характеризуется диастереомерным избытком, составляющим 98% [(99-1)/1]. Диастереомерный избыток аналогичным образом можно рассчитать для любого из 1, 2, 3 или 4.
[213] В некоторых вариантах осуществления соединение формулы A1 получают посредством приведения в контакт соединения формулы (a):
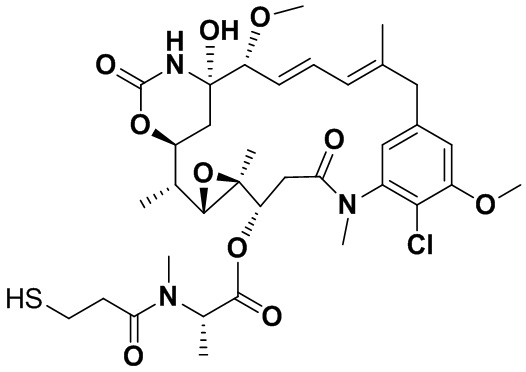
(a),
с соединением формулы (b)
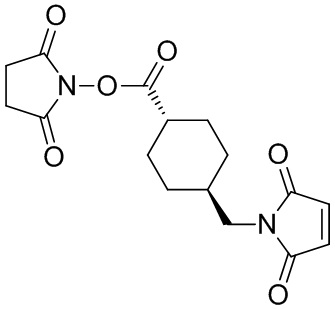
(b),
в присутствии силикагеля и разбавителя. В некоторых вариантах осуществления разбавитель содержит органический растворитель и воду.
[214] В данном документе также предусмотрен продукт, получаемый посредством способа:
(i) приведения в контакт соединения формулы (a):

(a),
с соединением формулы (b):
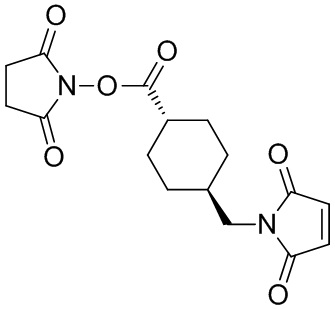
(b),
в присутствии силикагеля и разбавителя с синтезом промежуточного соединения, и
(ii) приведения в контакт антитела к MET или биспецифического антигенсвязывающего белка MET x MET, описанных в данном документе, с промежуточным соединением и водным разбавителем.
[215] В некоторых вариантах осуществления в данном документе предусмотрены способы получения конъюгата антитело-лекарственное средство, включающие приведение в контакт антитела к MET или биспецифического антигенсвязывающего белка MET x MET, описанного в данном документе, с соединением, характеризующимся следующей формулой B:
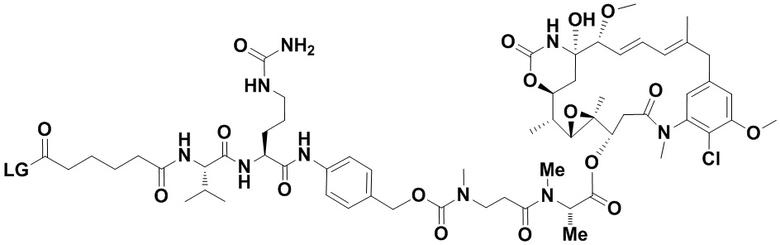
B,
где LG представляет собой уходящую группу, и водным разбавителем.
[216] В некоторых вариантах осуществления соединение формулы B присутствует в стехиометрическом избытке. В некоторых вариантах осуществления соединение формулы B присутствует в 5-6-кратном стехиометрическом избытке. В некоторых вариантах осуществления водный разбавитель содержит HEPES. В некоторых вариантах осуществления водный разбавитель содержит DMA. В некоторых вариантах осуществления -C(O)-LG представляет собой сложный эфир, например NHS или сложный трифторфениловый эфир.
[217] В некоторых вариантах осуществления соединение формулы B представляет собой соединение формулы B1:
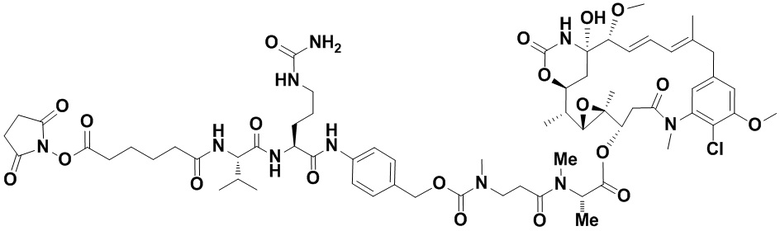 .
.
B1.
[218] В некоторых вариантах осуществления соединение формулы B1 получают посредством приведения в контакт соединения формулы C:
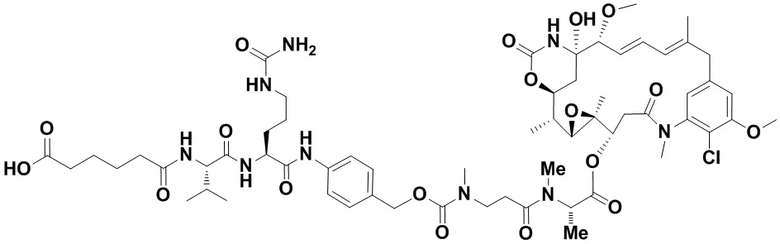
C,
с N-гидроксисукцинимидом (NHS), реагентом для образования пептидной связи и органическим разбавителем. Подходящие реагенты для образования пептидной связи включают реагенты, которые активируют, т.е. делают реакционноспособными остатки карбоновой кислоты для реакции с нуклеофилом. В определенных вариантах осуществления реагент для образования пептидной связи представляет собой гидрохлорид N-(3-диметиламинопропил)-N’-этилкарбодиимида (EDC). В некоторых вариантах осуществления органический растворитель представляет собой дихлорметан.
[219] В некоторых вариантах осуществления соединение формулы C получают посредством приведения в контакт соединения формулы D:
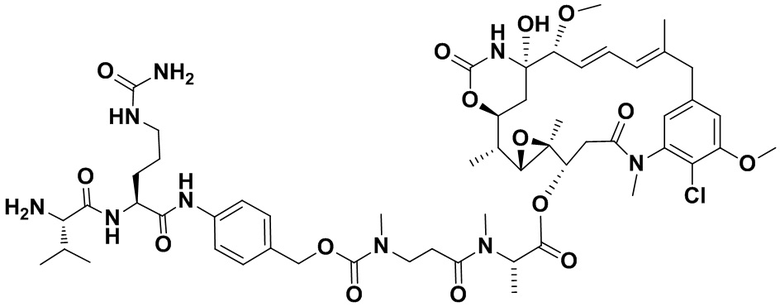
D,
с адипиновой кислотой, средством для образования пептидной связи и органическим растворителем. В определенных вариантах осуществления средство для образования пептидной связи представляет собой 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин (EEDQ). В определенных вариантах осуществления органический растворитель содержит дихлорметан. Соединение D можно получать, как описано в WO2014/145090.
Эпитопное картирование и связанные с ним технологии
[220] Эпитоп, с которым связываются антитела и антигенсвязывающие домены, может состоять из одной непрерывной последовательности из 3 или более (например, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более) аминокислот белка MET. В качестве альтернативы, рассматриваемый эпитоп может состоять из множества несмежных аминокислот (или аминокислотных последовательностей) MET. В некоторых вариантах осуществления эпитоп расположен на лиганд-связывающем домене MET или рядом с ним. В других вариантах осуществления эпитоп расположен за пределами лиганд-связывающего домена MET, например в месте на поверхности MET, в котором антитело при связывании с таким эпитопом не препятствует связыванию HGF с MET.
[221] Как описано в другом месте в данном документе, отдельные антигенсвязывающие домены (D1 и D2) биспецифических антигенсвязывающих молекул MET x MET могут связываться с отличающимися, или неперекрывающимися, или частично перекрывающимися по отношению друг к другу эпитопами. Используемый в данном документе термин «частично перекрывающиеся эпитопы» означает, что первый и второй эпитопы содержат менее чем 5, менее чем 4, менее чем 3 или только одну общую аминокислоту, как определено посредством любой методики эпитопного картирования, известной из уровня техники (например, рентгенокристаллографии, аланин-сканирующего мутагенеза, водородно-дейтериевого обмена [HDX], обмена доменами и т.д.). Домены D1 и D2 могут не конкурировать друг с другом. Например, в определенных вариантах осуществления связывание домена D1 конкретной биспецифической антигенсвязывающей молекулы MET x MET с ее эпитопом на MET не подавляет (или только минимально подавляет) связывание домена D2 биспецифической антигенсвязывающей молекулы MET x MET с ее эпитопом на MET. В связи с неперекрывающимся (или, как максимум, частично перекрывающимся) характером соответствующих эпитопов компонентов D1 и D2 биспецифические антигенсвязывающие молекулы MET x MET способны связываться с одной молекулой MET на поверхности клетки.
[222] Для определения эпитопа на МЕТ, с которым взаимодействуют антитела и антигенсвязывающие домены, применимые в соответствии с данным документом, можно использовать различные методики, известные специалистам в данной области техники. Иллюстративные методики, которые можно использовать для определения эпитопа или связывающего домена конкретного антитела или антигенсвязывающего домена, включают, например, точечный мутагенез (например, аланин-сканирующий мутагенез, аргинин-сканирующий мутагенез и т.д.), анализ посредством пептидного блоттинга (Reineke, 2004, Methods Mol Biol 248:443-463), защиту от протеаз и анализ расщепления пептидов. Кроме того, можно применять такие способы, как вырезание эпитопа, выделение эпитопа и химическая модификация антигенов (Tomer, 2000, Protein Science 9:487-496). Другим способом, который можно использовать для идентификации аминокислот в пределах полипептида, с которым взаимодействует антитело, является водородно-дейтериевый обмен, выявляемый посредством масс-спектрометрии. В общих чертах метод водородно-дейтериевого обмена включает мечение дейтерием представляющего интерес белка с последующим связыванием антитела с белком, меченным дейтерием. Затем комплекс белок/антитело переносится в воду с обеспечением осуществления водородно-дейтериевого обмена по всем остаткам, за исключением остатков, защищенных антителом (которые остаются меченными дейтерием). После диссоциации антитела целевой белок подвергается расщеплению протеазами и анализу посредством масс-спектрометрии, за счет чего выявляются остатки, меченные дейтерием, которые соответствуют конкретным аминокислотам, с которыми взаимодействует антитело. См., например, Ehring (1999) Analytical Biochemistry 267(2):252-259; Engen and Smith (2001) Anal. Chem. 73:256A-265A. Для идентификации аминокислот в пределах полипептида, с которым взаимодействует антитело, также можно использовать рентгеноструктурный анализ.
[223] Применимыми в соответствии со способами, предусмотренными в данном документе, являются антитела к MET (включая биспецифические антитела), которые связываются с тем же эпитопом, что и любое из специфических иллюстративных антител или антигенсвязывающих доменов, описанных в данном документе (например антитела, содержащие любую из аминокислотных последовательностей, представленных в таблице 1 в данном документе). Аналогичным образом, в данном документе также предусмотрены антитела к MET, которые конкурируют за связывание с MET с любым из специфических иллюстративных антител, описанных в данном документе (например антитела, содержащие любую из аминокислотных последовательностей, представленных в таблице 1 в данном документе). В некоторых вариантах осуществления эпитоп MET человека, с которым связываются антитела к MET, содержит аминокислоты 192-204, аминокислоты 305-315 и/или аминокислоты 421-455 из SEQ ID NO:155. В некоторых вариантах осуществления первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO:155; и второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO:155.
[224] Используя стандартные способы, известные из уровня техники и представленные в данном документе в примерах, можно легко определить, связывается ли антитело с тем же самым эпитопом, что и эталонное антитело к MET, или конкурирует с ним за связывание. Например, чтобы определить, связывается ли тестируемое антитело с тем же самым эпитопом, что и эталонное антитело к MET, предусмотренное в данном документе, обеспечивается возможность связывания эталонного антитела с белком MET. Затем оценивается способность тестируемого антитела связываться с молекулой MET. Если тестируемое антитело способно связываться с MET после насыщающего связывания с эталонным антителом к MET, то можно сделать вывод, что тестируемое антитело связывается с другим эпитопом, отличным от того эпитопа, с которым связывается эталонное антитело к MET. С другой стороны, если тестируемое антитело не способно связываться с молекулой MET после насыщающего связывания с эталонным антителом к MET, то тестируемое антитело может связываться с тем же эпитопом, что и эпитоп, связанный с эталонным антителом к MET. Затем можно провести дополнительные стандартные эксперименты (например анализы с внесением в пептиды мутаций и анализы связывания) для того, чтобы подтвердить, действительно ли наблюдаемое отсутствие связывания тестируемого антитела обусловлено связыванием с тем же эпитопом, как у эталонного антитела, или что причиной отсутствия наблюдаемого связывания является стерическое блокирование (или другое явление). Эксперименты такого типа можно проводить с применением ELISA, RIA, Biacore, проточной цитометрии или любого другого количественного или качественного анализа связывания антитела, доступного в данной области техники. В соответствии с определенными вариантами осуществления два антитела связываются с одним и тем же (или перекрывающимся) эпитопом, если, например, 1-, 5-, 10-, 20- или 100-кратный избыток одного антитела подавляет связывание другого на по меньшей мере 50%, но предпочтительно 75%, 90% или даже 99%, при измерении посредством анализа конкурентного связывания (см., например, Junghans et al., Cancer Res. 1990:50:1495-1502). В качестве альтернативы, считается, что два антитела связываются с одним и тем же эпитопом, если практически все аминокислотные мутации в антигене, которые ослабляют или устраняют связывание одного антитела, ослабляют или устраняют связывание другого антитела. Считается, что два антитела имеют «перекрывающиеся эпитопы», если только часть аминокислотных мутаций, которые ослабляют или устраняют связывание одного антитела, ослабляют или устраняют связывание другого антитела.
[225] Для определения того, конкурирует ли антитело за связывание (или перекрестно конкурирует за связывание) с эталонным антителом к MET, описанная выше методика исследования связывания осуществляется в двух направлениях: в первом направлении обеспечивается возможность связывания эталонного антитела с белком MET в условиях насыщения с последующей оценкой связывания тестируемого антитела с молекулой MET. Во втором направлении обеспечивается возможность связывания тестируемого антитела с молекулой MET в условиях насыщения с последующей оценкой связывания эталонного антитела с молекулой MET. Если в обоих направлениях только первое (насыщающее) антитело способно к связыванию с молекулой MET, то делается заключение, что тестируемое антитело и эталонное антитело конкурируют за связывание с MET. Специалисту в данной области техники будет понятно, что антитело, которое конкурирует за связывание с эталонным антителом, необязательно может связываться с тем же эпитопом, что и эталонное антитело, но может стерически блокировать связывание эталонного антитела за счет связывания перекрывающегося или смежного эпитопа.
Получение человеческих антител
[226] Антитела к MET и биспецифические антитела к MET x MET, применимые в соответствии со способами, предусмотренными в данном документе, могут быть полностью человеческими антителами. Способы получения моноклональных антител, включая полностью человеческие моноклональные антитела, известны из уровня техники. Любые такие известные способы можно использовать в контексте настоящего изобретения для получения человеческих антител, которые специфически связываются с MET человека.
[227] Используя, например, технологию VELOCIMMUNE™ или любой другой аналогичный известный способ получения полностью человеческих моноклональных антител, первоначально выделяются высокоаффинные химерные антитела к MET, содержащие человеческую вариабельную область и мышиную константную область. Как показано в приведенном ниже экспериментальном разделе, антитела подвергаются анализу характеристик и отбору в отношении требуемых характеристик, включая аффинность, активность блокирования лиганда, селективность, эпитоп и т.д. При необходимости мышиные константные области заменяются требуемой человеческой константной областью, например из IgG1 или IgG4 дикого типа или из модифицированных IgG1 или IgG4, с получением полностью человеческого антитела к MET. Хотя отобранная константная область может варьироваться в зависимости от конкретного применения, характеристики, касающиеся высокой аффинности связывания антигена или специфичности к мишени, присущи вариабельной области. В определенных случаях полностью человеческие антитела к MET выделяются непосредственно из антиген-положительных В-клеток.
Биоэквиваленты
[228] Антитела к MET и фрагменты антител, применимые в соответствии со способами, предусмотренными в данном документе, охватывают белки, содержащие аминокислотные последовательности, которые отличаются от последовательностей описанных антител, но которые сохраняют способность связывать MET человека. Такие варианты антител и фрагментов антител содержат одно или более добавлений, делеций или замен аминокислот при сравнении с исходной последовательностью, но проявляют биологическую активность, которая практически эквивалентна активности описанных антител. Аналогичным образом, последовательности ДНК по настоящему изобретению, кодирующие антитело к MET, охватывают последовательности, которые содержат одно или более добавлений, делеций или замен нуклеотидов при сравнении с раскрытой последовательностью, но которые кодируют антитело к MET или фрагмент антитела, которые практически являются биоэквивалентами антитела к MET или фрагмента антитела по настоящему изобретению. Примеры таких вариантов аминокислотных последовательностей и последовательностей ДНК обсуждались выше.
[229] Два антигенсвязывающих белка или антитела считаются биоэквивалентами, если, например, они являются фармацевтическими эквивалентами или фармацевтическими альтернативами, скорость и/или степень поглощения которых значимо не отличаются при введении при одинаковой молярной дозе в сходных экспериментальных условиях, как в случае однократной дозы, так и в случае нескольких доз. Некоторые антитела будут считаться эквивалентами или фармацевтическими альтернативами, если они являются эквивалентами по степени их поглощения, но не по скорости их поглощения, и все же могут считаться биоэквивалентами, поскольку такие различия в скорости поглощения являются предусмотренными и отражены в информации по лекарственному препарату, не являются необходимыми для достижения в организме эффективных концентраций лекарственного средства, например при длительном применении, и считаются не значимыми с медицинской точки зрения в случае конкретного исследуемого лекарственного продукта.
[230] В одном варианте осуществления два антигенсвязывающих белка являются биоэквивалентами, если отсутствуют клинически значимые различия в отношении их безопасности, чистоты и эффективности.
[231] В одном варианте осуществления два антигенсвязывающих белка являются биоэквивалентами, если пациента можно перевести один или более раз с эталонного продукта на биологический продукт без ожидаемого повышения риска возникновения побочных эффектов, в том числе значимого с клинической точки зрения изменения иммуногенности или снижения эффективности по сравнению с таковой при продолжении терапии без такого перевода.
[232] В одном варианте осуществления два антигенсвязывающих белка являются биоэквивалентами, если они оба действуют согласно общему механизму или механизмам действия при условии или условиях применения, в том объеме, в котором такие механизмы известны.
[233] Биоэквивалентность можно продемонстрировать посредством способов in vivo и in vitro. Измерения степени биоэквивалентности включают, например, (a) тест in vivo у людей или других млекопитающих, в котором концентрация антитела или его метаболитов измеряется в крови, плазме крови, сыворотке крови или других биологических жидкостях в виде зависимости от времени; (b) тест in vitro, который коррелировал с данными биодоступности in vivo у человека и с достаточной точностью предсказывал их; (c) тест in vivo у людей или других млекопитающих, у которых соответствующий ранний фармакологический эффект антитела (или его мишени) измеряется в виде зависимости от времени; и (d) строго контролируемое клиническое испытание, в котором устанавливается безопасность, эффективность, или биодоступность, или биоэквивалентность антитела.
[234] Биоэквивалентные варианты антител к MET, предусмотренные в данном документе, можно конструировать посредством, например, осуществления различных замен остатков или последовательностей или делеции концевых или внутренних остатков или последовательностей, которые не являются необходимыми для биологической активности. Например, остатки цистеина, не являющиеся необходимыми для биологической активности, можно подвергнуть делеции или заменить другими аминокислотами для предупреждения образования нежелательных или несоответствующих внутримолекулярных дисульфидных мостиков при ренатурации. В других ситуациях биоэквивалентные антитела могут включать варианты антител к MET, содержащие аминокислотные изменения, которые модифицируют характеристики гликозилирования антител, например мутации, которые обеспечивают устранение или удаление гликозилирования.
Видовая селективность и межвидовая перекрестная реактивность
[235] Настоящее изобретение в соответствии с определенными вариантами осуществления предусматривает антитела к MET (и антигенсвязывающие молекулы, содержащие антигенсвязывающие домены к MET), которые связываются с MET человека, но не с MET других видов, и применимы в лечении видов рака глазного яблока, таких как увеальная меланома, орбитальная лимфома, ретинобластома и медуллоэпителиома. Настоящее изобретение также включает антитела к MET (и антигенсвязывающие молекулы, содержащие антигенсвязывающие домены к MET), которые связываются с MET человека и с MET одного или более видов, отличных от человека, и применимы в лечении видов рака глазного яблока, таких как увеальная меланома, орбитальная лимфома, ретинобластома и медуллоэпителиома. Например, антитела к MET и антигенсвязывающие молекулы могут связываться с MET человека и могут связываться или не связываться, в зависимости от конкретного случая, с одним или более из МЕТ мыши, крысы, морской свинки, хомяка, песчанки, свиньи, кошки, собаки, кролика, козы, овцы, коровы, лошади, верблюда, яванского макака, мартышки, макака-резуса или шимпанзе. В соответствии с определенными иллюстративными вариантами осуществления предусмотрены антитела и антигенсвязывающие молекулы к MET, которые специфически связывают MET человека и MET яванского макака (например Macaca fascicularis). Другие антитела и антигенсвязывающие молекулы к МЕТ связывают МЕТ человека, но не связывают или связывают, но слабо, МЕТ яванского макака.
Полиспецифические антитела
[236] Как описано в другом месте в данном документе, пригодными в соответствии с настоящим изобретением являются биспецифические антигенсвязывающие молекулы, содержащие два разных антигенсвязывающих домена, где первый антигенсвязывающий домен (D1) связывает первый эпитоп на MET, и где второй антигенсвязывающий домен (D2) связывает второй эпитоп на MET. В определенных вариантах осуществления первый и второй эпитопы на MET, с которыми связываются домены D1 и D2, отличаются, или не перекрываются, или частично перекрываются. В соответствии с данным аспектом домен D1 может содержать любую из аминокислотных последовательностей HCVR/LCVR или CDR, представленных в таблице 1 в данном документе, а домен D2 может содержать любую другую из аминокислотных последовательностей HCVR/LCVR или CDR, представленных в таблице 1 в данном документе (при условии, что специфичность связывания домена D1 отличается от специфичности связывания домена D2, и/или антигенсвязывающий белок, из которого получен D1, не конкурирует за связывание с MET с антигенсвязывающим белком, из которого получен D2). В некоторых вариантах осуществления эпитоп MET человека, с которым связываются антитела к MET, содержит аминокислоты 192-204, аминокислоты 305-315 и/или аминокислоты 421-455 из SEQ ID NO:155. В некоторых вариантах осуществления первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO:155; и второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO:155.
[237] В соответствии с отдельным аспектом также предусмотрены традиционные биспецифические антитела, которые применимы в соответствии с данным документом, где одно плечо биспецифического антитела связывается с эпитопом на МЕТ человека, а другое плечо биспецифического антитела связывается со вторым антигеном, отличным от МЕТ. МЕТ-связывающее плечо может содержать любую из аминокислотных последовательностей HCVR/LCVR или CDR, представленных в таблице 1 в данном документе. В определенных вариантах осуществления МЕТ-связывающее плечо связывает MET человека и блокирует связывание HGF с MET. В других вариантах осуществления МЕТ-связывающее плечо связывает MET человека, но не блокирует связывание HGF с МЕТ.
[238] Иллюстративный формат биспецифического антитела, который можно использовать в контексте настоящего изобретения, включает применение CH3-домена первого иммуноглобулина (Ig) и CH3-домена второго Ig, где п CH3-домены первого и второго Ig отличаются друг от друга по меньшей мере одной аминокислотой, и где отличие в по меньшей мере одну аминокислоту ослабляет связывание биспецифического антитела с белком A по сравнению с биспецифическим антителом, в котором отсутствует отличие по аминокислотам. В одном варианте осуществления CH3-домен первого Ig связывает белок A, а CH3-домен второго Ig содержит мутацию, которая ослабляет или устраняет связывание белка A, такую как модификация H95R (нумерация экзонов согласно IMGT; нумерация H435R согласно EU). Второй CH3 может дополнительно содержать модификацию Y96F (согласно IMGT; Y436F согласно EU). Дополнительные модификации, которые могут присутствовать в пределах второго CH3, включают D16E, L18M, N44S, K52N, V57M и V82I (согласно IMGT; D356E, L358M, N384S, K392N, V397M и V422I согласно EU) в случае антител IgG1; N44S, K52N и V82I (IMGT; N384S, K392N и V422I согласно EU) в случае антител IgG2; и Q15R, N44S, K52N, V57M, R69K, E79Q и V82I (согласно IMGT; Q355R, N384S, K392N, V397M, R409K, E419Q и V422I согласно EU) в случае антител IgG4. Варианты формата биспецифических антител, описанные выше, рассматриваются в пределах объема настоящего изобретения.
[239] Другие иллюстративные биспецифические форматы, которые можно использовать в контексте настоящего изобретения, включают без ограничения, например, биспецифические форматы на основе scFv или диател, слитых белков IgG-scFv, двойной вариабельный домен (DVD)-Ig, квадрому, «выступы-в углубления», обычную легкую цепь (например общую легкую цепь со структурой выступы-в-углубления и т.п.), CrossMab, CrossFab, (SEED)-антитело, «лейциновую застежку», дуотело, IgG1/IgG2, Fab (DAF)-IgG двойного действия и биспецифические форматы Mab2 (для обзора вышеизложенных форматов см., например, Klein et al. 2012, mAbs 4:6, 1-11, и цитируемые в нем ссылки). Биспецифические антитела также можно конструировать с применением конъюгации пептид/нуклеиновая кислота, например, где не встречающиеся в природе аминокислоты с ортогональной химической реактивностью используются для получения сайт-специфических конъюгатов антитело-олигонуклеотид, которые затем самостоятельно собираются в мультимерные комплексы с определенными составом, валентностью и геометрической формой. (См., например, Kazane et al., J. Am. Chem. Soc. [Epub: Dec. 4, 2012]).
Составление и введение средства терапии
[240] В данном документе предусмотрены фармацевтические композиции, содержащие антитела к MET или биспецифические антигенсвязывающие молекулы MET x MET, применимые в соответствии со способами, описанными в данном документе. Фармацевтические композиции можно составлять с подходящими носителями, вспомогательными веществами и другими средствами, которые обеспечивают улучшение переноса, доставки, переносимости и т.п.
[241] В некоторых аспектах фармацевтические композиции, содержащие антитела к MET или биспецифические антигенсвязывающие молекулы MET x MET, составлены для введения в глаз для лечения рака глазного яблока, такого как увеальная меланома, орбитальная лимфома, ретинобластома или медуллоэпителиома.
[242] В данном документе предусмотрены способы, в которых антитела к MET или биспецифические антигенсвязывающие молекулы MET x MET, которые вводят пациенту, содержатся в фармацевтическом составе. Фармацевтический состав может содержать антитело к MET или биспецифическую антигенсвязывающую молекулу MET x MET вместе с по меньшей мере одним неактивным ингредиентом, таким как, например, фармацевтически приемлемый носитель. В фармацевтическую композицию можно включать другие средства для обеспечения улучшенного переноса, доставки, переносимости и т. п. Термин «фармацевтически приемлемый» означает одобренный регулирующим органом федерального правительства или правительства штата или перечисленный в фармакопее США или другой общепризнанной фармакопее для применения у животных и, в частности, у людей. Термин «носитель» относится к разбавителю, адъюванту, вспомогательному веществу или среде-носителю, с которыми вводится антитело. Множество подходящих составов можно найти в справочнике, хорошо известном всем химикам-фармацевтам: Remington's Pharmaceutical Sciences (15th ed, Mack Publishing Company, Easton, Pa., 1975), в частности, глава 87, написанная Blaug, Seymour. Данные составы включают, например, порошки, пасты, мази, желе, воски, масла, липиды, везикулы, содержащие липиды (катионные или анионные) (такие как LIPOFECTIN.TM.), конъюгаты ДНК, безводные абсорбционные пасты, эмульсии типа масло в воде и вода в масле, эмульсии на основе карбовакса (полиэтиленгликоли с различной молекулярной массой), полутвердые гели и полутвердые смеси, содержащие карбовакс. Любая из вышеуказанных смесей может быть подходящей в контексте способов по настоящему изобретению при условии, что антитело к MET или биспецифическая антигенсвязывающая молекула MET x MET не инактивируются составом, и состав является физиологически совместимым и переносимым при определенном пути введения. См. также Powell et al. PDA (1998) J Pharm Sci Technol. 52:238-311 и ссылки в них для получения дополнительной информации, относящейся к вспомогательным веществам и носителям, хорошо известным химикам-фармацевтам.
[243] Фармацевтические составы, применимые для введения путем инъекции в контексте настоящего изобретения, можно получать посредством растворения, суспендирования или эмульгирования антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET в стерильной водной среде или масляной среде, обычно используемых для инъекций. В качестве водной среды для инъекций используются, например, физиологический солевой раствор, изотонический раствор, содержащий глюкозу и другие вспомогательные средства и т. п., которые можно использовать в комбинации с подходящим солюбилизирующим средством, таким как спирт (например этанол), многоатомный спирт (например, пропиленгликоль, полиэтиленгликоль), неионогенное поверхностно-активное вещество [например, полисорбат 80, HCO-50 (полиоксиэтиленовый (50 моль) аддукт гидрогенизированного касторового масла)] и т. п. В качестве масляной среды можно применять, например, кунжутное масло, соевое масло и т. п., которые можно использовать в комбинации с солюбилизирующим средством, таким как бензилбензоат, бензиловый спирт и т.п. Полученным таким способом инъекционным составом при необходимости можно наполнять подходящую ампулу.
Способы введения
[244] Антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET (или фармацевтический состав, содержащий антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET) можно вводить пациенту с помощью любой известной системы доставки и/или способа введения. В определенных вариантах осуществления антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET вводятся пациенту путем глазной, внутриглазной, интравитреальной или субконъюнктивальной инъекции. В других вариантах осуществления антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET можно вводить пациенту посредством местного применения, например, с помощью глазных капель или другой жидкости, геля, мази или лосьона, которые содержат антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET и могут наноситься непосредственно на глаз. Другие возможные пути введения включают, например, внутрикожный, внутримышечный, интраперитонеальный, внутривенный, подкожный, интраназальный, эпидуральный и пероральный.
Комбинированные средства терапии и составы
[245] В данном документе предусмотрены композиции и терапевтические составы, содержащие любые из антител к MET и биспецифических антигенсвязывающих молекул MET x MET, описанных в данном документе, в комбинации с одним или несколькими дополнительными терапевтически активными компонентами, и способы лечения, включающие введение таких комбинаций субъектам, нуждающимся в этом.
[246] Антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET можно объединять в состав и/или вводить в комбинации с одним или более дополнительными терапевтически активными компонентами, выбранными из группы, состоящей из антагониста MET (например антитела к MET [например, онартузумаба, эмибетузумаба, телизотузумаба, SAIT301, ARGX-111, Sym015, HuMax-cMet, CE-355621 и H4H14639D] или низкомолекулярного ингибитора MET), антагониста EGFR (например антитела к EGFR [например цетуксимаба или панитумумаба] или низкомолекулярного ингибитора EGFR [например гефитиниба или эрлотиниба]), антагониста другого представителя семейства EGFR, такого как Her2/ErbB2, ErbB3 или ErbB4 (например антитела к ErbB2 [например трастузумаба или T-DM1 {KADCYLA®}], антитела к ErbB3, или антитела к ErbB4, или низкомолекулярного ингибитора активности ErbB2, ErbB3 или ErbB4), антагониста EGFRvIII (например антитела к EGFRvIII), антагониста IGF1R (например антитела к IGF1R), ингибитора B-raf (например, вемурафениба, сорафениба, GDC-0879, PLX-4720), ингибитора PDGFR-α (например антитела к PDGFR-α), ингибитора PDGFR-β (например антитела к PDGFR-β или низкомолекулярного ингибитора киназ, такого как, например, мезилат иматиниба или малат сунитиниба), ингибитора лиганда PDGF (например, антитела к PDGF-A, -B, -C или -D, аптамера, siRNA и т.д.), антагониста VEGF (например VEGF-Trap, такой как афлиберцепт, см., например, US 7087411 (также называемой в данном документе «слитый белок, ингибирующий VEGF»), антитела к VEGF (например бевацизумаба), низкомолекулярного ингибитора киназы рецептора VEGF (например, сунитиниба, сорафениба или пазопаниба)), антагониста DLL4 (например антитела к DLL4, раскрытого в US 2009/0142354, такого как REGN421), антагониста Ang2 (например антитела к Ang2, раскрытого в US 2011/0027286, такого как H1H685P), антагониста FOLH1 (например антитела к FOLH1), антагониста STEAP1 или STEAP2 (например антитела к STEAP1 или антитела к STEAP2), антагониста TMPRSS2 (например антитела к TMPRSS2), антагониста MSLN (например антитела к MSLN), антагониста CA9 (например антитела к CA9), антагониста уроплакина (например антитела к уроплакину [например антитела к UPK3A]), антагониста MUC16 (например антитела к MUC16), антагониста антигена Tn (например антитела к Tn), антагониста CLEC12A (например антитела к CLEC12A), антагониста TNFRSF17 (например антитела к TNFRSF17), антагониста LGR5 (например антитела к LGR5), моновалентного антагониста CD20 (например моновалентного антитела к CD20, такого как ритуксимаб), биспецифического антитела к CD20 x CD3, средства, блокирующего PD-1 (например антитела к PD-1, такого как пембролизумаб или ниволумаб) и т.д. Другие средства, которые можно эффективно вводить в комбинации с антителами, предусмотренными в данном документе, включают, например, тамоксифен, ингибиторы ароматазы и ингибиторы цитокинов, включая низкомолекулярные ингибиторы цитокинов и антитела, которые связываются с цитокинами, такими как IL-1, IL-2, IL- 3, IL-4, IL-5, IL-6, IL-8, IL-9, IL-11, IL-12, IL-13, IL-17, IL-18, или с их соответствующими рецепторами.
[247] В качестве иллюстрации, ингибитор PD-1, такой как антитело к PD-1, можно комбинировать с конъюгатом антитело к МЕТ-лекарственное средство, описанным в данном документе. Целевая популяция пациентов включает, в частности, пациентов с опухолями, у которых сверхэкспрессируется c-Met с мутацией, таких как пациент с увеальной меланомой, при которой сверхэкспрессируется c-Met, или немелкоклеточным раком легкого, при котором экспрессируется c-Met.
[248] В данном документе предусмотрены композиции и терапевтические составы, содержащие любые из антител к MET и биспецифических антигенсвязывающих молекул MET x MET, описанных в данном документе, в комбинации с одним или более химиотерапевтическими средствами. Примеры химиотерапевтических средств включают алкилирующие средства, такие как тиотепа и циклофосфамид (Cytoxan™; алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метиламеламины, включая альтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилоломеламин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлорэтамин, гидрохлорид мехлорэтаминоксида, мелфалан, новэмбихин, фенестерин, преднимустин, трофосфамид, урациловый иприт; нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин, ранимустин; антибиотики, такие как аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, калихеамицин, карабицин, карминомицин, карзинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин, эпирубицин, эзорубицин, идарубицин, марцелломицин, митомицины, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, циностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурина, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, пропионат дромостанолона, эпитиостанол, мепитиостан, тестолактон; средства, угнетающие функции надпочечников, такие как аминоглутетимид, митотан, трилостан; пополнитель фолиевой кислоты, такой как фролиновая кислота; ацеглатон; гликозид альдофосфамида; аминолевулиновую кислоту; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; эльфорнитин; ацетат эллиптиния; этоглюцид; нитрат галлия; гидроксимочевину; лентинан; лонидамин; митогуазон; митоксантрон; мопидамол; нитракрин; пентостатин; фенамет; пирарубицин; подофиллиновую кислоту; 2-этилгидразид; прокарбазин; PSK™; разоксан; сизофиран; спирогерманий; тенуазоновую кислоту; триазиквон; 2,2',2''-трихлортриэтиламин; уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид («Ara-C»); циклофосфамид; тиотепу; таксаны, например паклитаксел (Taxol™, Bristol-Myers Squibb Oncology, Принстон, Нью-Джерси) и доцетаксел (Taxotere™; Aventis Antony, Франция); хлорамбуцил; гемцитабин; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин и карбоплатин; винбластин; платину; этопозид (VP-16); ифосфамид; митомицин C; митоксантрон; винкристин; винорелбин; навельбин; новантрон; тенипозид; дауномицин; аминоптерин; кселода; ибандронат; CPT-11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноевую кислоту; эсперамицины; капецитабин; и фармацевтически приемлемые соли, кислоты или производные любого из вышеперечисленных. В данное определение также включены антигормональные средства, которые регулируют или подавляют действие гормонов на опухоли, такие как антиэстрогены, включая, например, тамоксифен, ралоксифен, 4(5)-имидазолы, ингибирующие ароматазу, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY 117018, онапристон и торемифен (фарестон); и антиандрогены, такие как флутамид, нилутамид, бикалутамид, лейпролид и гозерелин; и фармацевтически приемлемые соли, кислоты или производные любого из вышеперечисленных.
[249] Антитела к MET и биспецифические антигенсвязывающие молекулы MET x MET также можно вводить и/или объединять в состав в комбинации с противовирусными средствами, антибиотиками, анальгетиками, кортикостероидами, стероидами, кислородом, антиоксидантами, ингибиторами COX, кардиопротекторами, хелаторами металлов, IFN-гамма и/или NSAID.
[250] Дополнительный терапевтически активный компонент(компоненты), например любое из перечисленных выше средств или их производных, можно вводить непосредственно перед антителом к MET или биспецифической антигенсвязывающей молекулой MET x MET, одновременно с ними или вскоре после их введения; (для целей настоящего изобретения такие режимы введения рассматриваются как введение антитела «в комбинации с» дополнительным терапевтически активным компонентом). Настоящее изобретение включает фармацевтические композиции, в которых антитело к MET или биспецифическая антигенсвязывающая молекула MET x MET объединены в состав с одним или более дополнительным терапевтически активным компонентом(компонентами), описанным в другом месте в данном документе.
Режимы введения
[251] В соответствии с определенными вариантами осуществления многократные дозы антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET (или фармацевтической композиции, содержащей комбинацию антитела к МЕТ или биспецифической антигенсвязывающей молекулы MET x MET и любого из дополнительных терапевтических средств, упомянутых в данном документе) можно вводить субъекту в течение определенного периода времени. Способы в соответствии с данным аспектом включают последовательное введение субъекту многократных доз антитела к МЕТ или биспецифической антигенсвязывающей молекулы MET x MET, предусмотренных в данном документе. Используемый в данном документе термин «последовательное введение» означает, что каждая доза антитела вводится субъекту в отдельный момент времени, например в разные дни, разделенные предварительно определенным интервалом (например, часы, дни, недели или месяцы). Настоящее изобретение включает способы, которые включают последовательное введение пациенту одной начальной дозы антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET, затем одной или более вторичных доз антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET, а затем необязательно одной или более третичных доз антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET.
[252] Термины «начальная доза», «вторичные дозы» и «третичные дозы» относятся к временной последовательности введения антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET. Таким образом, «начальная доза» представляет собой дозу, которая вводится в начале режима лечения (также обозначена как «исходная доза»); «вторичные дозы» представляют собой дозы, которые вводятся после начальной дозы; и «третичные дозы» представляют собой дозы, которые вводятся после вторичных доз. Все из начальной, вторичной и третичной доз могут содержать одинаковое количество антитела к MET или биспецифической антигенсвязывающей молекулы MET x MET, но, как правило, могут отличаться друг от друга частотой введения. Однако в определенных вариантах осуществления количества антитела, содержащегося в начальной, вторичной и/или третичной дозах, отличаются друг от друга (например, при необходимости корректируются в сторону повышения или понижения) на протяжении курса лечения. В определенных вариантах осуществления две или более (например, 2, 3, 4 или 5) доз вводятся в начале режима лечения в качестве «нагрузочных доз» с последующим введением последующих доз, которые вводятся с меньшей частотой (например «поддерживающие дозы»).
Пути применения антител в диагностике
[253] Антитело к MET или биспецифическую антигенсвязывающую молекулу MET x MET по настоящему изобретению также можно использовать для выявления и/или измерения содержания MET или MET-экспрессирующих клеток в образце, например для диагностических целей. Например, антитело к MET или его фрагмент можно использовать для диагностики состояния или заболевания, характеризующихся аберрантной экспрессией (например, сверхэкспрессией, недостаточной экспрессией, отсутствием экспрессии и т.д.) MET. Иллюстративные диагностические анализы в отношении MET могут предусматривать, например, приведение образца, полученного от пациента, в контакт с антителом к MET или биспецифической антигенсвязывающей молекулой MET x MET, где антитело помечено выявляемой меткой или репортерной молекулой. В качестве альтернативы, немеченое антитело к MET или биспецифическую антигенсвязывающую молекулу MET x MET можно использовать в диагностике в комбинации с вторичным антителом, которое само помечено выявляемой меткой. Выявляемая метка или репортерная молекула могут представлять собой радиоизотоп, такой как 3H, 14C, 32P, 35S или 125I, флуоресцентный или хемилюминесцентный фрагмент, такой как флуоресцеин или родамин, или фермент, такой как щелочная фосфатаза, бета-галактозидаза, пероксидаза хрена или люцифераза. Конкретные иллюстративные анализы, которые можно использовать для выявления или измерения содержания MET в образце, включают твердофазный иммуноферментный анализ (ELISA), радиоиммуноанализ (RIA), иммуно-PET (например, 89Zr, 64Cu, и т. д.) и сортировку клеток с активацией флуоресценции (FACS).
[254] Образцы, которые можно использовать в диагностических анализах MET в соответствии с настоящим изобретением, включают любой образец ткани или жидкости, получаемый от пациента, в частности, ткани или жидкости, находящихся в глазу или глазнице. Обычно для первоначального определения исходного или стандартного уровня MET будут измеряться уровни MET в конкретном образце, полученном от здорового пациента (например пациента, не страдающего заболеванием или состоянием, ассоциированными с аномальными уровнями или активностью MET). Затем этот исходный уровень МЕТ можно сравнивать с уровнями МЕТ, измеренными в образцах, полученных от индивидуумов с подозрением на наличие заболевания или состояния, связанных с МЕТ.
ПРИМЕРЫ
[255] Следующие примеры представлены с тем, чтобы обеспечить специалистов средней квалификации в данной области техники полным раскрытием и описанием того, как осуществлять и применять способы и получать и применять композиции, предусмотренные в данном документе, и они не предполагают ограничение объема того, что авторы настоящего изобретения рассматривают в качестве своего изобретения. Были приложены усилия для обеспечения точности в отношении используемых чисел (например, количеств, температуры и т. п.), однако необходимо учитывать некоторые экспериментальные погрешности и отклонения. Если не указано иное, то части являются частями по массе, молекулярная масса является средней молекулярной массой, температура представлена в градусах Цельсия, а давление является атмосферным или близким к атмосферному.
Пример 1. Получение антител к MET
[256] Антитела к MET получали посредством иммунизации генетически модифицированной мыши, содержащей ДНК, кодирующую вариабельные области тяжелой и легкой каппа-цепи иммуноглобулина человека, иммуногеном, содержащим внеклеточный домен рекомбинантного MET человека, слитый с Fc человека (R&D Systems, номер по каталогу 358-MT, Миннеаполис, Миннесота). Мыши, использованные для иммунизации, экспрессируют «универсальную легкую цепь». То есть антитела, продуцируемые этой мышью, содержат разные вариабельные области тяжелой цепи, но практически идентичные вариабельные домены легкой цепи.
[257] Мониторинг опосредованного антителами иммунного ответа осуществляли с помощью МЕТ-специфического иммуноанализа. После достижения требуемого иммунного ответа собирали спленоциты и сливали их с клетками миеломы мыши для сохранения их жизнеспособности и формирования клеточных линий гибридом. Клеточные линии гибридомы подвергали скринингу и отбирали для идентификации клеточных линий, продуцирующих МЕТ-специфические антитела. Посредством применения данной методики получали несколько химерных антител к MET (т.е., антител, имеющих вариабельные домены человека и константные домены мыши). В дополнение несколько полностью человеческих антител к MET выделяли непосредственно из антиген-положительных В-клеток без слияния с клетками миеломы, как описано в US 2007/0280945A1.
[258] Определенные биологические свойства иллюстративных антител к MET, полученных в соответствии со способами из данного примера, и биспецифических антител, сконструированных на их основе, подробно описаны в примерах, изложенных ниже.
Пример 2. Аминокислотные последовательности и последовательности нуклеиновых кислот вариабельных областей тяжелой и легкой цепи
[259] В таблице 1 представлены идентификаторы аминокислотных последовательностей вариабельных областей тяжелой и легкой цепи и CDR выбранных антител к MET, описанных в данном документе. (Как отмечалось выше, все антитела, полученные в примере 1, имеют одинаковую вариабельную область легкой цепи и, следовательно, одинаковые последовательности CDR легкой цепи). Соответствующие идентификаторы последовательностей нуклеиновых кислот представлены в таблице 2.
[260] В данном документе антитела обычно называются в соответствии со следующей номенклатурой: после префикса, обозначающего Fc (например «H4H»), следует числовой идентификатор (например «13290», «13291», «13295» и т.д.), за которым следует суффикс «P2», как показано в таблицах 1 и 2. Таким образом, в соответствии с данной номенклатурой в данном документе антитело может называться, например, «H4H13290P2», «H4H13291P2», «H4H13295P2» и т.д. Используемые в данном документе префиксы в обозначениях антител указывают на конкретный изотип Fc-области антитела. В частности, антитело «H4H» содержит Fc IgG4 человека (все вариабельные области являются полностью человеческими, на что указывает первая буква 'H' в обозначении антитела). Специалисту средней квалификации в данной области техники будет понятно, что антитело, содержащее антитело с Fc конкретного изотипа, можно превращать в антитело, содержащее Fc другого изотипа (например, антитело с Fc из IgG4 мыши можно превращать в антитело с Fc из IgG1 человека и т.д.), но в любом случае вариабельные домены (в том числе CDR), которые обозначены числовыми идентификаторами, показанными в таблицах 1 и 2, останутся такими же, и при этом ожидается, что свойства связывания будут идентичными или практически сходными независимо от природы Fc-домена.
Пример 3. Полученные с помощью поверхностного плазмонного резонанса значения аффинности связывания и кинетические константы моноклональных антител к MET (моноспецифических) человека
[261] Значения аффинности связывания и кинетические константы антител к MET человека определяли с помощью поверхностного плазмонного резонанса (в системе Biacore 4000 или T-200) при 37°C. Антитела к Met, протестированные в данном примере, являлись бивалентными моноспецифическими связывающимися с MET молекулами. Антитела, экспрессируемые как IgG4 человека (обозначенные «H4H»), захватывались сенсорной поверхностью Biacore CM4 или CM5, дериватизированной посредством иммобилизации по аминогруппе моноклонального мышиного антитела к Fc человека (GE, BR-1008-39). Различные концентрации растворимых мономерных (Met.mmh человека (h); SEQ ID NO: 152; Met.mmh яванского макака (mf) ; SEQ ID NO: 154) или димерных (hMet.mFc; SEQ ID NO: 153) белков Met вносили на поверхность с захваченными антителами к MET со скоростью потока 30 или 50 мкл/минуту. Мониторинг ассоциации hMET.mmh или hMET.mFc с захваченным моноклональным антителом осуществляли в течение 4 или 5 минут, а мониторинг диссоциации hMET.mmh или hMET.mFc в подвижном буфере HBS-ET (0,01 M HEPES с pH 7,4, 0,15 M NaCl, 3 мМ EDTA, 0,05% об./об. поверхностно-активного вещества P20) или PBS-P (0,01 M фосфата натрия с pH 7,4, 0,15 M NaCl, 0,05% об./об. поверхностно-активного вещества P20) осуществляли в течение 10 минут.
Кинетические константы скорости ассоциации (ka) и скорости диссоциации (kd) определяли посредством аппроксимации сенсограмм в реальном времени по модели связывания 1:1 с применением программного обеспечения для аппроксимации кривой Scrubber 2.0c. Равновесную константу диссоциации связывания (KD) и значение полупериода диссоциации (t½) рассчитывали исходя из кинетических констант скоростей следующим образом:
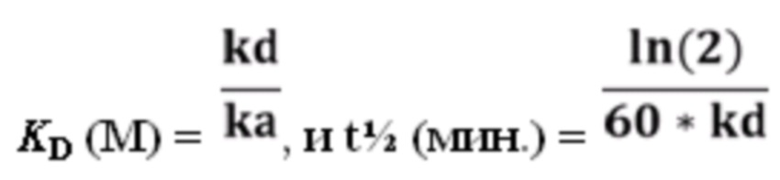
[262] Кинетические параметры связывания моноспецифических антител к Met с мономерным и димерным белком Met показаны ниже в таблице 3.
NB= в используемых условиях связывание не наблюдали
[263] Как показано в таблице 3, некоторые антитела демонстрировали связывание с высокой аффинностью с белком MET человека и обезьяны.
Пример 4. Антитела к Met связываются с отдельными эпитопами рецептора Met
[264] Для оценки того, способны ли два антитела к Met конкурировать друг с другом за связывание со своими соответствующими эпитопами на MET, проводили анализ конкурентного связывания с применением безметочной биослойной интерферометрии (BLI) в режиме реального времени на биосенсоре OCTET® HTX (FortéBio Corp., Менло-Парк, Калифорния).
[265] Вкратце, сначала внеклеточный домен МЕТ человека, экспрессируемый с применением C-концевой myc-myc-гексагистидиновой метки (hMet.mmh), в количестве приблизительно 0,25 нМ захватывался биосенсорами OCTET®, покрытыми антителом к пента-His (FortéBio Corp., № 18-5079), посредством погружения биосенсоров на 5 минут в лунки, содержащие раствор hMET.mmh с концентрацией 20 мкг/мл. Затем биосенсоры с захваченным антигеном насыщали первым моноклональным антителом к MET (далее называемым mAb-1) посредством погружения в лунки, содержащие раствор с концентрацией 50 мкг/мл mAb-1, на 5 минут. Затем биосенсоры погружали в лунки, содержащие раствор с концентрацией 50 мкг/мл второго моноклонального антитела к MET (далее называемого mAb-2), на 3 минуты. Все биосенсоры промывали в буфере OCTET®, содержащем HEPES-забуференный физиологический раствор-EDTA с полисорбатом 20 (HBS-EP), после каждой стадии эксперимента. Мониторинг реакции связывания в реальном времени осуществляли в течение эксперимента и регистрировали ответ связывания в конце каждой стадии. Сравнивали ответ связывания mAb-2 с предварительно образованным комплексом антигена MET и mAb-1 и определяли конкурентный/неконкурентный характер связывания различных моноклональных антител к MET с применением 50% порога подавления. В таблице 4 явно определены взаимодействия антител, конкурирующих в обоих направлениях, независимо от порядка связывания.
(mAb-1), захваченное с применением биосенсоров Octet, покрытых антителом к пента-His
(mAb-1), захваченное с применением биосенсоров Octet, покрытых антителом к пента-His
Пример 5. Конструирование биспецифических антител, содержащих два разных антигенсвязывающих домена, специфичных для разных эпитопов MET
[266] В данном примере описано конструирование биспецифических антител, содержащих два разных антигенсвязывающих домена (D1 и D2), где D1 и D2 получены из разных антител к MET и, следовательно, связываются с отдельными эпитопами на внеклеточном домене MET.
[267] Отдельные антигенсвязывающие домены к MET, используемые для конструирования биспецифических антител в данном примере, получали из различных бивалентных моноспецифических антител к MET, описанных в примерах с 1 по 3 в данном документе. Все описанные в данном документе антитела к MET содержат одну и ту же («общую») легкую цепь (содержащую аминокислотную последовательность вариабельной области легкой цепи [LCVR] под SEQ ID NO:138 и аминокислотные последовательности CDR легкой цепи [LCDR1, LCDR2 и LCDR3] под SEQ ID NO: 140, 142 и 144). В дополнение, все биспецифические антитела, проиллюстрированные в данном примере, содержат плечо «D2», полученное из иллюстративного антитела к MET H4H13312P2. Таким образом, оба антигенсвязывающих домена (D1 и D2) всех биспецифических антител, описанных в данном примере, содержат данную общую вариабельную область легкой цепи, и все связывающие плечи D2 содержат вариабельную область тяжелой цепи из H4H13312P2; однако биспецифические антитела отличаются друг от друга с точки зрения их вариабельных областей тяжелой цепи D1 (HCVR) и CDR тяжелой цепи (HCDR). Компоненты биспецифических антител из данного примера приведены в таблице 5.
(№219)
(№235)
Пример 6. Полученные с помощью поверхностного плазмонного резонанса значения аффинности связывания и кинетические константы человека биспецифических моноклональных антител к MET x MET человека
[268] Значения аффинности связывания и кинетические константы биспецифических антител к MET x MET, сконструированных в соответствии с приведенным в данном документе примером 4, определяли с помощью поверхностного плазмонного резонанса (в системах Biacore 4000 или T-200) при 37°C. Биспецифические антитела, экспрессируемые как IgG4 человека (обозначенные «H4H»), захватывали на сенсорной поверхности Biacore CM4 или CM5, дериватизированной посредством иммобилизации по аминогруппе моноклональных мышиных антител к Fc человека (GE, BR-1008-39). Различные концентрации растворимого мономерного белка MET (hMet.mmh, SEQ ID NO: 152) вносили на поверхность с захваченными биспецифическими антителами к MET x MET при скорости потока 30 или 50 мкл/минуту. Мониторинг ассоциации аналита с захваченным биспецифическим антителом осуществляли в течение 4 или 5 минут, а мониторинг диссоциации аналита в подвижном буфере HBS-ET (0,01 M HEPES с pH 7,4, 0,15 M NaCl, 3 мМ EDTA, 0,05% об./об. поверхностно-активного вещества P20) или PBS-P (0,01 M фосфата натрия с pH 7,4, 0,15 M NaCl, 0,05% об./об. поверхностно-активного вещества P20) осуществляли в течение 10 минут.
[269] Кинетические константы скоростей ассоциации (ka) и диссоциации (kd) определяли, как описано в примере 3.
[270] Кинетические параметры связывания биспецифических антител к Met с мономерным белком Met (hMET.mmh) показаны в таблице 6.
[271] Как показано в таблице 6, биспецифические антитела к «MET x MET», описываемые в данном документе, показали значения T ½, составляющие более чем 1155 минут.
[272] Как показано в таблице 7, скорость диссоциации биспецифического антитела H4H14639D является значительно ниже, чем значения скорости диссоциации каждого из его исходных антител, H4H13306P2 и H4H13312P2.
Пример 7. Антитела к Met блокируют HFG-опосредованную активацию Met в биологическом репортерном анализе с применением SRE-люциферазы
[273] Способность антител к MET блокировать активацию MET, опосредованную фактором роста гепатоцитов (HGF), изучали с помощью репортерного анализа с применением люциферазы. Фактор роста HGF связывается с внеклеточным доменом своего рецептора c-Met (MET), запуская быструю гомодимеризацию и активируя несколько нижележащих сигнальных каскадов. Антитела к MET, протестированные в данном примере, представляли собой бивалентные моноспецифические связывающие MET молекулы или «биспецифические» антитела к MET, в которых каждое плечо биспецифического антитела связано с различным и отличающимся эпитопом на MET.
[274] Репортерный анализс применением люциферазы на основе генетически сконструированных клеток (фигура 2) применяли для определения способность антител к MET активировать передачу сигналов MET (фигура 3, панель A; таблица 8, столбцы 3 и 4) и блокировать лиганд-опосредованную активацию MET (фигура 3, панель B; таблица 8, столбцы 1 и 2). Вкратце, для получения клеток HEK293/SRE-Luc использовали набор CIGNAL™ Lenti SRE Reporter (luc) (SABiosciences, Хильден, Германия). Клетки HEK293 (почки эмбриона человека) выбрали, поскольку они эндогенно экспрессируют c-Met. Клетки HEK293/SRE-Luc стабильно включали репортерный ген люциферазы, зависимой от элемента сывороточного ответа (SRE) (Luc) (см. Dinter et al., PLoS ONE 10(2): e0117774, 2015). Клетки HEK293/SRE-Luc культивировали в среде DMEM с добавлением 10% фетальной бычьей сыворотки (FBS), пенициллина/стрептомицина/глутамина и 1 мкг/мл пуромицина.
[275] Затем 2,0×105 клеток HEK293/SRE-Luc высевали в среду для анализа с применением люциферазы в 96-луночные планшеты и инкубировали в течение ночи при 37°C в 5% CO2. Кривые зависимости ответа от дозы фактора роста гепатоцитов (HGF) получали посредством добавления к клеткам серийно разведенного HGF (от 0,01 нМ до 1,0 нМ) и регистрации сигнала люциферазы после инкубации при 37°C в течение от четырех часов до шести часов в отсутствие антител. Для построения кривых подавления антител клетки предварительно инкубировали в течение одного часа при 37°C с серийно разведенными антителами к МЕТ человека (от 1,1 пМ до 200 нМ). Затем добавляли HGF в концентрации 73 пМ или 100 пМ в течение дополнительных от четырех часов до шести часов перед регистрацией сигнала. Отдельно также оценивали способность антител активировать c-Met в отсутствие лиганда.
[276] Активность люциферазы выявляли с помощью системы люциферазного анализа ONE-Glo™ (Promega, Мадисон, Висконсин), а излучаемый свет измеряли с помощью люминометра Victor или Envision (Perkin Elmer, Шелтон, Коннектикут) и выражали в относительных световых единицах (RLU). Значения EC50/IC50 определяли с помощью четырехпараметрического логистического уравнения по 12-точечной кривой ответа с применением программного обеспечения GRAPHPAD PRISM®. Сообщалось о проценте блокирования HGF и кратности активации MET (только mAb) для наивысшей дозы антител. Результаты представлены в таблице 8.
NT = не тестировалось; ND = EC50/IC50 не определено в связи с несигмоидальными кривыми или неполным блокированием.
[277] Как приведено в таблице 8, большинство антител подавляли активацию репортера SRE со значениями IC50, варьирующими от < 2,0 пМ до приблизительно 1,0 нМ. Несколько иллюстративных моноспецифических бивалентных антител к MET, таких как H4H13306P2 и H4H13309P2, являлись сильными ингибиторами активации SRE-luc с процентными значениями подавления, составляющими 67% и 77%, соответственно. Биспецифические антитела к MET (MET x MET) в целом проявляли большую степень подавления активации SRE-luc. Например, биспецифическое антитело к MET x MET H4H14639D демонстрировало 95-процентное подавление. Дополнительно, несколько блокирующих антител являлись слабо активирующими в отсутствие лиганда с кратностью активационных ответов, варьирующей от 0,8 до 14,4 выше исходных уровней.
[278] Также, как показано на фигуре 3, каждое из бивалентных моноспецифических антител H41413306P2 и H4H13312P2 активирует путь Met в отсутствие лиганда HGF (панель A), а также блокирует HGF-активацию Met (панель B).
[279] Влияние биспецифического антитела к MET x MET (например, H4H14639D) на HGF-зависимую и HGF-независимую активацию MET также оценивали с применением системы HEK293/SRE-Luc. SRE-управляемую люциферазную активность измеряли в клетках HEK293T, обработанных антителами к MET H4H14639D (биспецифическое антитело к MET x MET), моновалентным антителом к MET и исходным для H4H14639D антителом H4H13312P2 в различных концентрациях для определения уровня HGF-независимого агонизма MET. В то время как исходное моноспецифическое бивалентное антитело к MET проявляло активность агониста MET, ни моновалентное, ни биспецифическое антитело к MET x MET не проявляли активности агониста MET (фигура 4, панель A).
[280] SRE-управляемую люциферазную активность измеряли в клетках HEK293T, обработанных антителами к MET H4H14639D (биспецифическое антитело к MET x MET), моновалентным антителом к MET и исходным для H4H14639D антителом H4H13312P2 в различных концентрациях для определения уровня подавления или блокирования HGF-зависимого агонизма МЕТ. В то время как исходное моноспецифическое бивалентное антитело к MET проявляло некоторую активность блокирования HGF, как моновалентное, так и биспецифическое антитело к MET x MET проявляли большую степень блокирования HGF (фигура 4, панель B).
[281] Биспецифическое антитело к MET x MET блокирует передачу сигналов HGF и демонстрирует низкую агонистическую активность в отношении MET.
Пример 8. Антитела к Met подавляют рост клеток с амплификацией MET
[282] Затем выбранные антитела к Met тестировали на способность подавлять рост клеток SNU5 с амплификацией MET. Вкратце, 2,5×103 клеток карциномы желудка человека (SNU5) высевали в полные среды для выращивания в присутствии антител к MET в концентрациях, варьирующих от 1,5 пМ до 100 нМ. Полные среды для выращивания SNU5 содержали среду Дульбекко в модификации Искова, 10% FBS и пенициллин/стрептомицин/глутамин. Клетки инкубировали в течение 5 дней и количество жизнеспособных клеток определяли с применением набора для люминесцентного анализа жизнеспособности клеток CELLTITER-GLO® (Promega, Мадисон, Висконсин) в соответствии с инструкциями производителя.
[283] Как приведено в таблице 9, несколько антител к MET, таких как H4H13312P2 и H4H13325P2, блокировали рост SNU5 более чем на 50%, с общими значениями IC50, варьирующими от 44 пМ до 780 пМ.
[284] На фигуре 5 изображен относительный рост клеток SNU5, обработанных различными бивалентными моноспецифическими антителами к MET (т.е., обычными антителами). Субпопуляция обычных антител к MET подавляет рост SNU5 клеток рака желудка с амплификацией MET (фигура 5). Клетки SNU5 в 96-луночных планшетах обрабатывали с применением каждого антитела в концентрации 10 мкг/мл и рост клеток определяли через 5 дней посредством восстановления реагента alamarBlue® (Thermo Fisher Scientific, Уолтем, Массачусетс). Моновалентное антитело к MET (столбец 2, фигура 5) получали с применением вариабельных последовательностей тяжелой и легкой цепей антитела MetMab, как изложено в патенте США №7892550 B2, который включен в данный документ посредством ссылки во всей своей полноте. Обычное антитело 8 представляет собой H4H13306P2, а обычное антитело 11 представляет собой H4H13312P2, которые использовали для конструирования биспецифического антитела к MET x MET H4H14639D.
[285] В отдельном анализе роста блокирующую активность биспецифического антитела к MET x MET (т.е., H4H14639D) оценивали как в линии клеток SNU5, так и в линии клеток немелкоклеточного рака легкого (NSCLC) EBC-1, которая также характеризуется амплифицированным геном Met и сверхэкспрессирует МЕТ (Lutterbach et al., Cancer Res. 67(5): 2081-2088, 2007). Полные среды для выращивания клеток EBC-1 содержали MEM с солями Эрла, 10% фетальную бычью сыворотку (FBS), пенициллин/стрептомицин/глутамин и заменимые аминокислоты для MEM. H4H14369D продемонстрировало наибольшее процентное значение подавления активности МЕТ согласно регистрируемым показателям SRE-люциферазы. В текущем эксперименте 3,0×103 клеток SNU5 или EBC-1 высевали в полные среды для выращивания в присутствии H4H14639D в концентрациях, варьирующих от 15 пМ до 100 нМ. Клетки инкубировали в течение 3 дней при 37°C в 5% CO2. Затем клетки фиксировали в 4% формальдегиде и окрашивали с применением 3 мкг/мл красителя Hoechst 33342 для мечения ядер. Изображения получали с применением комплекса IMAGEXPRESS® Micro XL (Molecular Devices, Саннивейл, Калифорния), а количество ядер определяли с помощью программного обеспечения для анализа изображений METAXPRESS® (Molecular Devices, Саннивейл, Калифорния). Фоновые количества ядер клеток, обработанных 40 нМ дигитонином, вычитали из количества во всех лунках, и жизнеспособность выражали в виде процента от необработанных контролей. Значения IC50 определяли с помощью четырехпараметрического логистического уравнения по 10-точечной кривой ответа (GRAPHPAD PRISM®). Значения IC50 и процентный показатель уничтожения клеток показаны в таблице 9.
ND = IC50 не определено в связи с несигмоидальными кривыми или неполным блокированием
[286] Как приведено в таблице 10 ниже, биспецифическое антитело H4H14639D к MET x MET подавляло рост клеток EBC-1 и SNU5 на 37 и 40 процентов, а IC50 составляли 0,82 нМ и 0,3 нМ, соответственно.
[287] Клетки SNU5 (желудочные) в 96-луночных планшетах обрабатывали контрольным антителом, моновалентным антителом к MET или биспецифическим антителом к MET x MET в концентрации 0,1 мкг/мл, 1 мкг/мл или 10 мкг/мл. Рост клеток определяли через 5 дней с помощью восстановления реагента ALAMARBLUE® (Thermo Fisher Scientific, Уолтем, Массачусетс). Биспецифическое антитело к MET x MET значительно снижало относительный рост клеток SNU5 по сравнению с контрольным и моновалентным антителом (фигура 6, панель A).
[288] Аналогичным образом оценивали влияние биспецифического антитела к MET x MET на рост клеток EBC-1. 2500 клеток EBC-1 высевали в 96-луночный планшет и культивировали в среде Дульбекко с добавлением 10% FBS. Клетки обрабатывали контрольным антителом или биспецифическим антителом к MET x MET в концентрации 0,1 мкг/мл или 1 мкг/мл, а затем инкубировали с 5% CO2 при 37°C. Через 5 дней определяли относительный рост клеток посредством измерения восстановления индикаторного красителя ALAMARBLUE® до его высокофлуоресцентной формы в планшет-ридере Spectramax® M3 (Molecular Devices, LLC, Саннивейл, Калифорния). Результаты показаны в таблице 11 и на фигуре 6, панель B. Биспецифическое антитело к MET x MET (H4H14639D) значительно снижает относительный рост клеток EBC-1 по сравнению с контрольным антителом (фигура 6, панель B).
[289] Некоторые антитела к MET, как бивалентные моноспецифические, так и бивалентные антитела к MET x MET, являются сильными ингибиторами активации SRE-Luc и ингибируют рост клеточных линий с амплификацией Met и сверхэкспрессирующих MET клеточных линий.
Пример 9. Биспецифическое антитело к MET x MET индуцирует умеренную и временную активность пути MET в клетках NCI-H596 NSCLC
[290] Влияние биспецифических антител к MET x MET на путь MET в клетках аденосквамозной карциномы легкого человека оценивали in vitro.
[291] 250000 клеток NCI-H596 высевали в 12-луночный планшет и культивировали в среде RPMI с добавлением 10% FBS. Клетки обрабатывали фактором роста гепатоцитов (HGF) в концентрации 50 нг/мл или биспецифическим антителом к MET x MET H4H14639D в концентрации 10 мкг/мл в двух повторностях. Затем клетки инкубировали в 5% CO2 при 37°C. Через 0, 2, 6 или 18 часов получали клеточные лизаты, нормализовали содержание белка и проводили иммуноблот-анализ. Фосфорилирование МЕТ и фосфорилирование ERK количественно оценивали с помощью программы обработки изображений ImageJ (T. Collins, BioTechniques 43: S25-S30, 2007). Уровни фосфорилирования нормализовали к тубулину в качестве контроля нагрузки и выражали как кратное изменение относительно контрольной обработки. Результаты приведены в таблице 12.
[292] Обработка клеток NCI-H596 с применением HGF индуцировала сильную активацию MET и ERK, которая достигала пика через 2 часа и сохранялась через 18 часов. При обработке биспецифическим антителом H4H14636D обнаруживали умеренное фосфорилирование MET и ERK, которое возвращалось к исходным уровням через 18 или 6 часов соответственно.
Пример 10. Биспецифическое антитело к MET x MET индуцирует разрушение MET и подавляет активность метаболического пути более эффективно, чем моноспецифические антитела в клетках рака желудка Hs746T
[293] Влияние биспецифического антитела к MET x MET на активность MET в клетках карциномы желудка человека оценивали in vitro. 250000 клеток карциномы желудка человека Hs746T (H. Smith, J. Nat’l. Cancer Inst. 62(2): 225-230, 1979) высевали в 12-луночный планшет и культивировали в модифицированной среде Дульбекко с добавлением 10% FBS. Клетки обрабатывали с применением (1) 5 мкг/мл контрольной молекулы hFc, (2) 5 мкг/мл исходного бивалентного моноспецифического антитела к MET H4H13306P2, (3) 5 мкг/мл исходного бивалентного моноспецифического антитела к MET H4H13312P2, (4) комбинации 2,5 мкг/мл H4H13306P2 и 2,5 мкг/мл H4H13312P2 или (5) 5 мкг/мл биспецифического антитела к MET x MET H4H14639D. Затем клетки инкубировали с 5% CO2 при 37°C. Через 18 часов получали клеточные лизаты, нормализовали содержание белка и проводили иммуноблот-анализ. Экспрессию MET, фосфорилирование MET и фосфорилирование ERK количественно оценивали с помощью программы обработки изображений ImageJ (T. Collins, BioTechniques 43: S25-S30, 2007). Результаты приведены в таблице 13 и на фигуре 7, панель A, на которой представлены необработанные данные иммуноблот-анализа. На панели B фигуры 7 представлена экспрессия белка MET в клетках, обработанных биспецифическим антителом к MET x MET в концентрации 10 мкг/мл в течение 0, 2 или 6 часов. Общие уровни MET в клетках Hs747T со временем снижались после обработки биспецифическим антителом к MET x MET. Аналогичные результаты получили для линии клеток папиллярной аденокарциномы человека с амплификацией MET NCI-H820, (Bean et al., «MET amplification occurs with or without T790M mutations in EGFR mutant lung tumors with acquired resistance to getfitnib or erlotinib,» Proc. Natl. Acad. Sci. 2007 Dec 26, 104(52): 20932-20937).
[294] Биспецифическое антитело H4H14639D индуцировало разрушение MET более эффективно, чем его исходные обычные антитела. Фосфорилирование как MET, так и ERK более эффективно подавлялось посредством обработки с применением H4H14636D, чем с применением исходных антител или комбинации исходных антител.
[295] Клетки рака желудка Hs746T обрабатывали с применением контрольного антитела, биспецифического антитела к MET x MET H4H14639D, исходного антитела к MET H4H13306P2, исходного антитела к MET H4H13312P2 и комбинации исходных антител 1 и 2 с концентрацией каждого антитела 10 мкг/мл или комбинации исходных антител с концентрацией каждого антитела по 5 мкг/мл в течение 18 часов. Экспрессию MET (MET) и активацию пути (pMET и pErk) определяли посредством иммуноблоттинга с указанными антителами (фигура 8). Биспецифическое антитело к MET x MET подавляет активацию пути MET более эффективно, чем его исходные антитела в клетках рака желудка Hs746T.
Пример 11. Биспецифическое антитело к MET x MET индуцирует разрушение MET более эффективно, чем моноспецифические антитела в клетках рака легких NCI-H596
[296] Оценивали влияние биспецифических антител к MET x MET и исходных бивалентных моноспецифических антител к MET на уровни экспрессии рецептора фактора роста гепатоцитов (HGFR или MET) на клетках аденосквамозной карциномы легких человека. 250000 клеток аденосквамозной карциномы легких человека NCI-H596 высевали в 12-луночный планшет и культивировали в среде RPMI с добавлением 10% FBS. Клетки обрабатывали с применением (1) 5 мкг/мл контрольной молекулы hFc, (2) 5 мкг/мл исходного бивалентного моноспецифического антитела к MET H4H13306P2, (3) 5 мкг/мл исходного бивалентного моноспецифического антитела к MET H4H13312P2, (4) комбинации 2,5 мкг/мл H4H13306P2 и 2,5 мкг/мл H4H13312P2 или (5) 5 мкг/мл биспецифического антитела к MET x MET H4H14639D. Затем клетки инкубировали с 5% CO2 при 37°C. Через 18 часов получали клеточные лизаты, нормализовали содержание белка и проводили иммуноблот-анализ. Экспрессию MET количественно оценивали с помощью программы обработки изображений ImageJ (T. Collins, BioTechniques 43: S25-S30, 2007). Результаты приведены в таблице 14.
[297] Клетки рака легких NCI-H596 (мутация MET с пропуском экзона 14) также обрабатывали с применением контрольных или биспецифических антител к MET x MET в концентрации 10 мкг/мл в течение 2, 6 или 18 часов. Экспрессию MET определяли посредством иммуноблоттинга (фигура 9), который показывает индуцированное биспецифическими антителами к MET x MET разрушение MET при увеличении времени обработки.
[298] Биспецифическое антитело H4H14636D индуцирует разрушение MET более эффективно, чем его исходные обычные антитела в клетках рака легких NCI-H596.
Пример 12. Биспецифические антитела к MET x MET индуцируют разрушение MET и подавляют активность метаболического пути более эффективно, чем моноспецифические антитела в клетках рака желудка SNU5
[299] Оценивали влияние бивалентного моноспецифического антитела к MET и нескольких биспецифических антител к MET x MET на уровни экспрессии рецептора фактора роста гепатоцитов (HGFR или MET) на клетках карциномы желудка. Клетки карциномы желудка человека SNU5 высевали в среду Искова, содержащую 20% FBS с добавлением пенициллина-стрептомицина-глутамина. Через 24 часа после посева клетки обрабатывали с применением контрольного hFc, исходного бивалентного моноспецифического антитела к MET H4H13312P2 или биспецифических антител к MET x MET (H4H14634D, H4H14635D, H4H14636D, H4H14637D, H4H14638D, H4H14639D, H4H14640D, H4H14641D) в течение 18 часов. Затем получали лизаты клеток и анализировали с помощью вестерн-блоттинга. Иммуноблоты исследовали с помощью зондов на МЕТ и тубулин. Уровень экспрессии белка МЕТ количественно определяли и нормализовали относительно тубулина в качестве контроля нагрузки. Результаты представлены в таблице 15 и на фигуре 10, панель B.
[300] Опухолевые клетки SNU5 обрабатывали с применением контрольного антитела, биспецифического антитела к MET x MET или моновалентного антитела MET в концентрации 10 мкг/мл в течение 18 часов, как описано выше. Экспрессию MET (фигура 10, панели A и B) и активацию пути (т.е., pMET и pERK; панель A) определяли посредством иммуноблоттинга с указанными антителами. Результаты иммуноблотинга показаны на фигуре 10.
[301] Обработка клеток SNU5 биспецифическими антителами к MET x MET индуцировала более сильное разрушение MET, чем обработка бивалентным моноспецифическим антителом к MET (H4H13312P2) (фигура 10, панель B), моновалентным антителом к MET или контрольным hFc. Обработка клеток SNU5 биспецифическим антителом к MET x MET подавляла нижележащие эффекторы пути MET. Аналогичные результаты получили для линии клеток аденокарциномы немелкоклеточного рака легкого NCI-H1993 с амплификацией MET (Kubo et al., «MET gene amplification or EGFR mutation activate MET in lung cancers untreated with EGFR tyrosine kinase inhibitors,» Int. J. Cancer 2009 Apr 15; 124(8): 1778-1784).
Пример 13. Биспецифическое антитело к MET x MET индуцирует разрушение MET, подавляет активность метаболического пути и подавляет рост опухоли более эффективно, чем моноспецифические антитела в клетках EBC-1
[302] Клетки EBC-1 плоскоклеточной карциномы легких человека с амплификацией MET (Lutterbach et al., «Lung cancer cell lines harboring MET gene amplification are dependent on Met for growth and survival,» Cancer Res. 2007 Mar 1;67(5):2081-8) обрабатывали с применением контрольного антитела или биспецифического антитела к MET x MET в концентрации 10 мкг/мл в течение 18 часов, как описано выше. Экспрессию МЕТ и активацию пути МЕТ, установленную по экспрессии pMET и pErk, определяли посредством иммуноблоттинга с указанными антителами. Результаты иммуноблотинга показаны на фигуре 11.
[303] Обработка клеток EBC-1, которые имеют амплификацию гена MET, биспецифическими антителами к MET x MET индуцировала более сильное разрушение MET, чем обработка контрольным антителом. Обработка клеток EBC-1 биспецифическим антителом к MET x MET подавляла нижележащие эффекторы пути MET.
[304] В другом эксперименте 5 миллионов клеток EBC-1 имплантировали подкожно в область бока мышей SCID C.B.-17. Когда объемы опухоли достигал примерно 150 мм3, мышей рандомизировали на группы по 6 особей и два раза в неделю обрабатывали контрольным антителом при 25 мг/кг или биспецифическим антителом к MET x MET H4H14639D при 25 мг/кг. Рост опухоли контролировали в течение 30 дней после имплантации, и объем опухоли (мм3) измеряли в каждой экспериментальной группе с течением времени. Результаты представлены в таблице 16 и на фигуре 12, где продемонстрировано, что биспецифическое антитело к MET x MET значительно подавляет рост опухолей EBC-1.
(среднее значение ± SEM)
Пример 14. Биспецифическое антитело к MET x MET подавляет in vitro рост клеток рака желудка Hs746T более эффективно, чем моноспецифические антитела
[305] Влияние биспецифического антитела к MET x MET на рост клеток карциномы желудка человека оценивали in vitro. 2500 клеток карциномы желудка человека Hs746T (H. Smith, J. Nat'l. Cancer Inst. 62(2): 225-230, 1979) высевали в 96-луночный планшет и культивировали в модифицированной среде Дульбекко с добавлением 10% FBS. Клетки обрабатывали с применением (1) отдельных бивалентных моноспецифических антител к MET (H4H13306P2 или H4H13312P2) в концентрации 5 мкг/мл, (2) комбинации двух бивалентных моноспецифических исходных антител к MET (H4H13306P2 и H4H13312P2) с концентрацией каждого 2,5 мкг/мл или (3) биспецифического антитела, содержащего одно связывающее плечо от H4H13306P2 и другое связывающее плечо от H4H13312P2 (H4H14639D) в концентрации 5 мкг/мл. Затем клетки инкубировали с 5% CO2 при 37°C. Через 5 дней определяли относительный рост клеток посредством измерения восстановления индикаторного красителя Alamar blue® (ThermoFischer Scientific, Уолтем, Массачусетс) до его высокофлуоресцентной формы в планшет-ридере Spectramax® M3 (Molecular Devices, Саннивейл, Калифорния). Увеличение уровня флуоресценции коррелирует с ростом клеток. В таблице 17 показан относительный рост клеток Hs746T в случае каждой обработки антителом, нормализованный к контрольному (без обработки) росту клеток Hs746T. Биспецифическое антитело H4H14639D подавляет пролиферацию клеток Hs746T более эффективно, чем его исходные моноспецифические антитела по отдельности или в комбинации.
[306] Клетки рака желудка Hs746T обрабатывали с применением контрольного антитела, биспецифического антитела к MET x MET H4H14639D, исходного антитела к MET H4H13306P2, исходного антитела к MET H4H13312P2 и комбинации исходных антител 1 и 2, с концентрацией каждого антитела 2 мкг/мл. Рост клеток определяли через 5 дней с помощью восстановления реагента ALAMAR BLUE® (фигура 13, панель A). Биспецифическое антитело к MET x MET подавляло рост клеток по сравнению с исходными антителами, используемыми по отдельности или в комбинации, и подавляло активацию пути MET более эффективно, чем его исходные антитела в клетках рака желудка Hs746T.
[307] Клетки рака желудка Hs746T в 96-луночных планшетах обрабатывали с применением контрольного антитела в концентрации 25 мкг/мл, моновалентного антитела к MET в концентрации 1 мкг/мл, 10 мкг/мл или 25 мкг/мл или биспецифического антитела к MET x MET в концентрации 1 мкг/мл, 10 мкг/мл или 25 мкг/мл. Рост клеток рака желудка Hs746T определяли через 5 дней с помощью восстановления реагента alamarBlue® (фигура 13, панель B). Биспецифическое антитело к MET x MET эффективно подавляет рост клеток с амплификацией MET.
Пример 15. Биспецифическое антитело к MET x MET не индуцирует рост клеток рака легких NCI-H596 in vitro
[308] Влияние биспецифического антитела к MET x MET на рост клеток немелкоклеточного рака легких (NSCLC) человека (NCI-H596) оценивали in vitro. 10000 клеток аденосквамозной карциномы легких NCI-H596 (Nair et al., J. Nat’l. Cancer Inst. 86(5): 378-383, 1994) высевали в 96-луночные планшеты на слой 0,66% агара в среде с добавлением 1% фетальной бычьей сыворотки (FBS). Клетки культивировали в среде RPMI 1640 с добавлением 1% FBS с 0,3% агарозы. Клетки обрабатывали с применением (1) отдельных исходных бивалентных моноспецифических антител к MET (H4H13306P2 или H4H13312P2) в концентрации 5 мкг/мл, (2) комбинации двух исходных бивалентных моноспецифических антител к MET (H4H13306P2 и H4H13312P2) с концентрацией каждого 2,5 мкг/мл, (3) биспецифического антитела, содержащего одно связывающее плечо от H4H13306P2 и другое связывающее плечо от H4H13312P2 (H4H14639D) в концентрации 5 мкг/мл, или (4) фактора роста гепатоцитов (HGF) в концентрации 100 нг/мл. Затем клетки инкубировали с 5% CO2 при 37°C. Через две недели определяли относительный рост клеток посредством измерения восстановления индикаторного красителя Alamar blue® (Thermo Fischer Scientific, Уолтем, Массачусетс) до его высокофлуоресцентной формы в планшет-ридере Spectramax® M3 (Molecular Devices, Саннивейл, Калифорния). Увеличение уровня флуоресценции коррелирует с ростом клеток. В таблице 18 и на фигуре 14 показан относительный рост клеток NCI-H596 в случае каждой обработки антителом, нормализованный к контрольному (без обработки) росту клеток NCI-H596. Обработка клеток рака легких NCI-H596 с применением HGF приводила к сильному индуцированию роста в мягком агаре. Биспецифическое антитело к MET x MET H4H14639D (MM на фигуре 14) не вносило значительных изменений в рост по сравнению с контрольными обработанными клетками. Умеренное индуцирование роста клеток наблюдали в случае с каждым исходным бивалентным моноспецифическим антителом H4H13306P2 (M1) или H4H13312P2 (M2) по отдельности или в комбинации (H4H13306P2 и H4H13312P2) (M1M2).
Пример 16. Биспецифическое антитело к MET x MET подавляет in vitro рост клеток рака желудка SNU5 более эффективно, чем моноспецифические антитела
[309] Влияние биспецифического антитела к MET x MET на рост клеток карциномы желудка человека оценивали in vitro. 2500 клеток карциномы желудка человека SNU5 (Ku and Park, Cancer Res. Treat. 37(1): 1-19, 2005) высевали в 96-луночный планшет и культивировали в среде Дульбекко в модификации Искова с добавлением 20% FBS. Клетки обрабатывали с применением (1) отдельных бивалентных моноспецифических антител к MET (H4H13306P2 или H4H13312P2) в концентрации 5 мкг/мл, (2) комбинации двух бивалентных моноспецифических антител к MET (H4H13306P2 и H4H13312P2) с концентрацией каждого 2,5 мкг/мл или (3) биспецифического антитела, содержащего одно связывающее плечо от H4H13306P2 и другое связывающее плечо от H4H13312P2 (H4H14639D) в концентрации 5 мкг/мл. Затем клетки инкубировали с 5% CO2 при 37°C. Через 5 дней определяли относительный рост клеток посредством измерения восстановления индикаторного красителя Alamar blue® (Thermo Fischer Scientific, Уолтем, Массачусетс) до его высокофлуоресцентной формы в планшет-ридере Spectramax® M3 (Molecular Devices, Саннивейл, Калифорния). Увеличение уровня флуоресценции коррелирует с ростом клеток. В таблице 19 показан относительный рост клеток SNU5 в случае каждой обработки антителом, нормализованный к контрольному (без обработки) росту клеток SNU5. Биспецифическое антитело H4H14639D подавляет пролиферацию клеток SNU5 более эффективно, чем его исходные моноспецифические антитела.
Пример 17. Биспецифическое антитело к MET x MET индуцирует регрессию опухолевого ксенотрансплантата Hs746T
[310] Оценивали влияние биспецифического антитела к MET x MET на опухоль карциномы желудка человека на мышиной модели с нарушенной иммунологической реактивностью. Три миллиона клеток карциномы желудка человека Hs746T имплантировали подкожно в область бока мышей SCID CB-17 (Bancroft et al., J. Immunol. 137(1): 4-9, 1986). Когда объем опухоли достигал приблизительно 200 мм3, мышей рандомизировали на группы по шесть особей и дважды в неделю обрабатывали контрольным антителом в дозе 25 мг/кг или биспецифическим антителом к MET x MET (H4H14639D) в дозе 25 мг/кг. В контрольной группе рост опухоли контролировали в течение 16 дней после имплантации, когда опухоли, которые обрабатывали контролем, достигли предельных размеров, соответствующих протоколу. В группе, которую обрабатывали H4H14639, рост опухоли контролировали в течение 30 дней после имплантации.
[311] Обработка опухолей биспецифическим антителом к MET x MET индуцировала регрессию размера опухоли в течение 21 дня относительно начала обработки. Опухоли, которые обрабатывали контролем, показали среднее увеличение объема приблизительно в 12 раз за 16 дней роста (таблица 20). Объем опухоли с течением времени, который демонстрирует регрессию опухоли Hs746T, обусловленную биспецифическим антителом к MET x MET, показан на фигуре 15.
Пример 18. Биспецифическое антитело к MET x MET индуцирует регрессию опухолевого ксенотрансплантата SNU5
[312] Оценивали влияние биспецифического антитела к MET x MET на опухоль карциномы желудка человека на мышиной модели с нарушенной иммунологической реактивностью. Десять миллионов клеток карциномы желудка человека SNU5 имплантировали подкожно в область бока мышей SCID CB-17. Когда объем опухоли достигал приблизительно 500 мм3, мышей рандомизировали на группы по пять особей и дважды в неделю обрабатывали контрольным антителом в дозе 10 мг/кг или биспецифическим антителом к MET x MET (H4H14639D) в дозе либо 1 мг/кг, либо 10 мг/кг. Рост опухоли контролировали в течение 81 дня после имплантации, когда опухоли, которые обрабатывали контролем, достигли предельных размеров, соответствующих протоколу.
[313] Опухоли у мышей, которых обрабатывали с применением антитела к MET x MET в дозе 1 мг/кг или 10 мг/кг, демонстрировали среднее уменьшение размера приблизительно на 95% или 98% соответственно. Опухоли, которые обрабатывали контролем, показали среднее увеличение объема приблизительно в 12 раз от начала обработок (таблица 21).
[314] Подкожно имплантированные опухоли SNU5 обрабатывали дважды в неделю контрольным антителом, моновалентным антителом к MET в дозе 1 мг/кг или 10 мг/кг или биспецифическим антителом к MET x MET в дозе 1 мг/кг или 10 мг/кг. Сильно выраженную и устойчивую регрессию опухолей SNU5 с амплификацией MET (т.е., уменьшение объема опухоли) наблюдали с течением времени у тех мышей, которых обрабатывали с применением биспецифического антитела к MET x MET (фигура 16, панель A). Из опухолей в конце исследования экстрагировали белок, а экспрессию MET и активацию метаболического пути, о которой свидетельствовало фосфорилирование MET (экспрессия pMET), определяли посредством иммуноблоттинга. Мыши (опухоли), обработанные антителом к MET x MET, показали снижение экспрессии MET и pMET по сравнению с контрольными (фигура 16, панель B). Биспецифическое антитело к MET x MET является сильным ингибитором опухолей, имеющих амплификацию MET.
Пример 19. Биспецифическое антитело к MET x MET индуцирует регрессию опухолевого ксенотрансплантата U87-MG
[315] Оценивали влияние биспецифического антитела к MET x MET на опухоль глиобластомы человека на мышиной модели с нарушенной иммунологической реактивностью. Пять миллионов клеток глиобластомы человека U87-MG (Vordermark and Brown, Int. J. Radiation Biol. 56(4): 1184-1193, 2003) имплантировали подкожно в область бока мышей SCID CB-17. Модели ксенотрансплантатов глиобластомы U87-MG контролируются посредством аутокринной передачи сигналов HGF. Когда объем опухоли достигал приблизительно 100 мм3, мышей рандомизировали на группы по шесть особей и обрабатывали контрольным антителом или биспецифическим антителом к MET x MET (H4H14639D). Каждой мыши дважды в неделю вводили антитело (контрольное или MET x MET) в дозе 25 мг/кг. Рост опухоли контролировали в течение 29 дней после имплантации, когда опухоли, которые обрабатывали контролем, достигли предельных размеров, соответствующих протоколу.
[316] Опухоли мышей, обработанные антителом к MET x MET, продемонстрировали среднее уменьшение размера приблизительно на 38%, тогда как опухоли, обработанные контрольным антителом, показали среднее увеличение объема приблизительно в 19 раз за 29 дней роста (таблица 22). Объем опухоли с течением времени, который демонстрирует регрессию опухоли U87-MG, обусловленную биспецифическим антителом к MET x MET, показан на фигуре 17.
Пример 20. Биспецифическое антитело к MET x MET подавляет рост опухолевого ксенотрансплантата U118-MG
[317] Оценивали влияние биспецифического антитела к MET x MET на опухоль глиобластомы человека на мышиной модели с нарушенной иммунологической реактивностью. Модели ксенотрансплантатов глиобластомы U118-MG контролируются посредством аутокринной передачи сигналов HGF. Пять миллионов клеток глиобластомы человека U118-MG (Olopade et al., Cancer Research 52: 2523-2529, 1992) имплантировали подкожно в область бока мышей SCID CB-17. Когда объем опухоли достигал приблизительно 100 мм3, мышей рандомизировали на группы по шесть особей и обрабатывали контрольным антителом или биспецифическим антителом к MET x MET (H4H14639D). Каждой мыши дважды в неделю вводили антитело (контрольное или MET x MET) в дозе 25 мг/кг. Рост опухоли контролировали в течение 72 дней после имплантации.
[318] Антитело к MET подавляло рост опухоли на 99% в течение 72 дней (таблица 23).
(мг/кг)
[319] В другом эксперименте подкожно имплантированные опухоли глиобластомы U118-MG у мышей обрабатывали два раза в неделю контрольным антителом, моновалентным антителом к MET или биспецифическим антителом к MET x MET в дозе 25 мг/кг. Объем опухоли (мм3) измеряли для каждой экспериментальной группы с течением времени. Результаты представлены на фигуре 18, где продемонстрировано, что биспецифическое антитело к MET x MET подавляет рост опухолей U118-MG.
Пример 21. Синтез майтанзиноидов
[320] Майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин-карбамил-(п-амино)бензил-цитруллин-валин-адипоил-сукцинат (соединение 1 на фигуре 20) синтезировали из соединения 2 (фигура 19), как описано ниже.
[321] Майтанзин-3-N-метил-L-аланин-Fmoc-N-Me-бета-аланин (соединение 3, фигура 19). Дезацетилмайтанзин (соединение 2, фигура 19, 0,433 г, 0,666 ммоль), Fmoc-N-Me-бета-Ala (0,434 г, 1,33 ммоль) и HATU (0,757 г, 1,99 ммоль) отвешивали в сухую колбу, растворяли в безводном DMF (9 мл) и подвергали воздействию 4-метилморфолина (0,300 мл, 2,73 ммоль). Колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды. Через 3 дня смесь выпаривали до маслянистого состояния, растворяли в ацетонитриле и воде и очищали посредством флэш-хроматографии на колонке с силикагелем 275 г C18 (30 - 90% ацетонитрила в воде в течение 20 минут, 0,05% уксусной кислоты в обеих фазах). Посредством лиофилизации фракций продукта получали указанное в заголовке соединение в виде белого твердого вещества. Неочищенный продукт очищали на колонке с силикагелем 80 г (EtOAc - 5:5:1 EtOAc:DCM:MeOH в течение 17 минут). Чистые фракции объединяли, выпаривали и высушивали in vacuo в течение ночи с получением указанного в заголовке соединения в виде белого твердого вещества (0,424 г, 66%). MS (ESI, полож.): рассчитывали C51H61ClN4O12, 956,4; определили 956,9 (M+H), 979,0 (M+Na), 939,0 (M-H2O+H).
[322] Сукцинатный эфир N-трет-бутоксикарбонил-N-метил-бета-аланина (соединение 4, фигура 19). Указанное в заголовке соединение получали из коммерческого Boc-N-Me-бета-Ala-OH с помощью способа, хорошо известного в данной области техники (см. Widdison et al., J. Med. Chem., 2006, 49 (14), 4401). 1H ЯМР (300 МГц, CDCl3): δ 3,62 (bm, 2H), 2,88 (m, 9H), 1,47 (s, 9H).
[323] Майтанзин-3-N-метил-L-аланин-Boc-N-Me-бета-аланин (соединение 5, фигура 19). Способ A. Продукт из предыдущей стадии (соединение 4, фигура 19, 0,453 г, 1,51 ммоль) и дезацетилмайтанзин (соединение 2, фигура 19, 0,304 г, 0,468 ммоль) растворяли в смеси ацетонитрил: вода 3:1 (8 мл), подвергали воздействию 1 М водного NaHCO3 (0,5 мл) и перемешивали при температуре окружающей среды в течение 18 часов. Когда реакция была завершена, что определили с помощью TLC, продукт затем перемешивали с солевым раствором в течение 10 минут и трижды экстрагировали этилацетатом (EtOAc). Затем объединенные органические слои высушивали над Na2SO4, фильтровали и фильтрат концентрировали и высушивали in vacuo до образования сиропа золотого цвета, который очищали посредством колоночной флэш-хроматографии на картридже с 20 г силикагеля (0 - 10% MeOH в EtOAc в течение 15 минут) с получением указанного в заголовке соединения в виде белого твердого вещества (0,084 г, 43%). MS (ESI, полож.): рассчитывали C41H59ClN4O12, 834,4; определили 835,2 (M+H), 857,2 (M+Na), 817,4 (M-H2O+H).
[324] Способ B. Boc-N-Me-бета-Ala-OH (0,294 г, 1,45 ммоль) растворяли в безводном DMF (5 мл), подвергали воздействию пентафторфенилдифенилфосфината (FDPP, 0,555 г, 1,44 ммоль) и реакционную смесь перемешивали при температуре окружающей среды в течение 30 минут. Затем смесь переносили в колбу большего размера, содержащую смесь дезацетилмайтанзина (соединение 2, фигура 19, 0,462 г, 0,711 ммоль) и диизопропилэтиламина (DIEA, 0,250 мл, 1,44 ммоль) в безводном DMF (7 мл), колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь снова перемешивали при температуре окружающей среды. Через 24 часа реакционную смесь концентрировали in vacuo до маслянистого состояния, растворяли в этилацетате (EtOAc, 2 мл) и очищали на картридже с 40 г силикагеля (EtOAc - 5:5:1 EtOAc/DCM/MeOH в течение 15 минут) с получением указанного в заголовке соединения в виде бледно-желтого твердого вещества (0,468 г, 79%). MS (ESI, полож.): рассчитывали C41H59ClN4O12, 834,4; определили 857,2 (M+Na), 817,2 (M-H2O+H).
[325] Майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин (соединение 6, фигура 19). Способ A. Майтанзин-N-Me-L-Ala-Boc-N-Me-бета-Ala (соединение 5, фигура 19, 0,464 г, 0,555 ммоль) растворяли в смеси ацетонитрил/вода/трифторуксусная кислота 3:1:1 (7 мл), колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды в течение 24 часов, затем закрывали крышкой и хранили при -20°C в течение 3 дней. Неочищенную реакционную смесь нагревали до температуры окружающей среды в течение 2 часов, в течение непродолжительного времени концентрировали in vacuo, очищали на колонке RediSep Gold со 100 г C18 (20 - 80% ацетонитрила в воде в течение 25 минут, 0,1% TFA в обоих растворителях) и объединенные чистые фракции частично выпаривали при температуре окружающей среды, замораживали на бане с сухим льдом и лиофилизировали с получением указанного в заголовке соединения в виде бледно-желтого твердого вещества (0,295 г, 63%). MS (ESI, полож.): рассчитывали C36H51ClN4O10, 734,3; определили 735,7 (M+H), 1471,3 (2M+H).
[326] Способ B. Майтанзин-N-Me-L-Ala-Fmoc-бета-Ala (соединение 3, фигура 19, 0,422 г, 0,441 ммоль) растворяли в 5% пиперидине в DMF (6,00 мл, 3,04 ммоль), реакционную колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды. Через 3 часа реакцию завершали посредством LCMS, поэтому продукт концентрировали in vacuo, герметично закрывали и хранили при -20°C в течение ночи. Неочищенный продукт нагревали до температуры окружающей среды, подвергали воздействию ацетонитрила и 10% водного раствора уксусной кислоты (3 мл каждого) и очищали посредством флэш-хроматографии на колонке с силикагелем 275 г C18 (10 - 90% ацетонитрила в воде в течение 20 минут, 0,05% уксусная кислота в обоих растворителях). Посредством лиофилизации фракций продукта получали указанное в заголовке соединение в виде белого твердого вещества. Твердое вещество трижды растирали с сухим диэтиловым эфиром, фильтровали, твердые частицы смывали с фильтра с помощью DCM, фильтрат выпаривали и высушивали in vacuo с получением указанного в заголовке соединения в виде белого твердого вещества (0,311 г, 89%). MS (ESI, полож.): рассчитывали C36H51ClN4O10, 734,3; определили 735,0 (M+H).
[327] Майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин-карбамил-(п-амино)бензил-цитруллин-валин-Fmoc (соединение 7, фигура 20). Стадия 1. Продукт из предыдущей стадии (соединение 6, фигура 19, 0,310 г, 0,390 ммоль), 1-гидрокси-7-азабензотриазол (HOAT, 0,164 г, 1,20 ммоль), бикарбонат натрия (0,138 г, 1,64 ммоль) и Fmoc-валин-цитруллин-(п-амино)бензил-(п-нитрофенил)карбонат (0,595 г, 0,776 ммоль, полученный спомощью способа, известного в данной области техники (см. Gangwar et al., патент США № 7714016 B2), растворяли в безводном DMF (10 мл), реакционную колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды. Через 24 часа реакционную смесь частично выпаривали in vacuo до приблизительно 2-3 мл, подвергали воздействию 10% водного раствора уксусной кислоты и воды (приблизительно 1 мл каждого), растворяли в ацетонитриле (приблизительно 6 мл) и очищали посредством флэш-хроматографии на колонке с силикагелем 275 г C18 (30-90% ацетонитрила в воде в течение 20 минут, 0,05% уксусная кислота в обоих растворителях). Посредством частичного выпаривания, замораживания и лиофилизации получали указанное в заголовке соединение в виде белого твердого вещества (0,362 г, 68%). MS (ESI, полож.): рассчитывали C70H88ClN9O17, 1361,6; определили 1362,1 (M+H), 1384,1 (M+Na), 1344,1 (M-H2O+H).
[328] Стадия 2. Продукт из предыдущей стадии (0,360 г, 0,264 ммоль) растворяли в 5% пиперидине в DMF (7 мл), реакционную колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды. Через 3 часа реакционную смесь выпаривали in vacuo, остаток подвергали воздействию 10% водного раствора уксусной кислоты (2 мл), растворяли в ацетонитриле (4 мл) и очищали посредством флэш-хроматографии на колонке с силикагелем 275 г C18 (10 - 70% ацетонитрила в воде в течение 20 минут, 0,05% уксусной кислоты в обоих растворителях). Чистые фракции объединяли, хранили при -20°C в течение ночи, частично выпаривали in vacuo при 25 - 30°C, замораживали на сухом льду и лиофилизировали в течение 6 дней с получением указанного в заголовке соединения в виде бледно-желтого твердого вещества (0,303 г, 95%). MS (ESI, полож.): рассчитывали C15H78ClN9O15, 1139,5; определили 1140,1 (M+H), 1162,0 (M+Na).
[329] Майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин-карбамил-(п-амино)бензил-цитруллин-валин-адипиновая кислота (соединение 8, фигура 20). Продукт из предыдущей стадии (соединение 7, фигура 20, 0,205 г, 0,171 ммоль), адипиновую кислоту (0,258 г, 1,77 ммоль) и 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин (EEDQ, 0,215 г, 0,869 ммоль) растворяли в сухом DCM (10 мл) и безводном метаноле (5 мл), реакционную колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды. Через 21 час реакционную смесь выпаривали in vacuo, остаток растворяли в нескольких мл ацетонитрила/воды и очищали посредством флэш-хроматографии на колонке с силикагелем 150 г C18 (20 - 80% ацетонитрила в воде в течение 17 минут, 0,05% уксусной кислоты в обоих растворителях). Посредством частичного выпаривания, замораживания и лиофилизации чистых фракций в течение 18 часов получали указанное в заголовке соединение в виде белого твердого вещества (0,140 г, 65%). MS (ESI, полож.): рассчитывали C61H86ClN9O18, 1267,6; определили 1268,9 (M+H), 1290,9 (M+Na).
[330] Майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин-карбамил-(п-амино)бензил-цитруллин-валин-адипоилсукцинат (соединение 1, фигура 20). Продукт из предыдущей стадии (соединение 8, фигура 20, 0,061 г, 0,048 ммоль), N-гидроксисукцинимид (0,063 г, 0,55 ммоль) и гидрохлорид N-(3-диметиламинопропил)-N'-этилкарбодиимида (EDC-HCl, 0,071 г, 0,37 ммоль) растворяли в сухом DCM (7 мл), реакционную колбу закрывали резиновой перегородкой, продували аргоном и реакционную смесь перемешивали при температуре окружающей среды. Через 5 дней реакционную смесь выпаривали in vacuo, остаток растворяли в нескольких мл ацетонитрила/воды и очищали посредством флэш-хроматографии на колонке с силикагелем 100 г C18 (30-90% ацетонитрила в воде в течение 15 минут, 0,05% уксусной кислоты в обоих растворителях). Посредством частичного выпаривания, замораживания и лиофилизации наиболее чистых фракций продукта в течение 18 часов получали указанное в заголовке соединение в виде белого твердого вещества (0,044 г, 67%). MS (ESI, полож.): рассчитывали C65H89ClN10O20, 1364,6; определили 1365,7 (M+H), 1387,7 (M+Na), 1347,7 (M-H2O+H). 1H-ЯМР (500 МГц; CDCl3): δ 7,56 (d, J = 8,3 Гц, 2H), 7,20 (d, J=8,7 Гц, 1H), 6,80 (s, 1H), 6,71 (m, 1H), 6,62 (d, J = 10,0 Гц, 1H), 6,39 (dd, J = 15,1, 11,3 Гц, 1H), 5,68 (dd, J = 15,3, 9,1 Гц, 1H), 5,38-5,32 (m, 1H), 5,03 (t, J=15,1 Гц, 1H), 4,88 (d, J = 12,3 Гц, 1H), 4,73 (d, J = 11,3 Гц, 1H), 4,61 (dd, J = 9,1, 3,6 Гц, 1H), 4,26 (d, J = 7,0 Гц, 1H), 4,17 (t, J = 7,1 Гц, 1H), 3,95 (s, 3H), 3,61 (d, J = 11,7 Гц, 1H), 3,57 (d, J = 12,4 Гц, 1H), 3,46 (d, J = 9,1 Гц, 2H), 3,33 (s, 3H), 3,27 (t, J = 6,9 Гц, 1H), 3,17-3,07 (m, 5H), 2,97 (dd, J = 16,6, 9,9 Гц, 1H), 2,88 (d, J = 11,7 Гц, 3H), 2,84 (s, 4H), 2,77 (s, 2H), 2,66 (s, 2H), 2,62 (t, J=4,8 Гц, 2H), 2,56 (d, J = 13,1 Гц, 1H), 2,32 (t, J = 6,6 Гц, 2H), 2,15 (d, J=14,0 Гц, 1H), 2,10 (q, J = 6,8 Гц, 1H), 1,92 (s, 4H), 1,75 (m, 5H), 1,61 (s, 3H), 1,52 (s, 3H), 1,27 (d, J = 6,3 Гц, 3H), 1,22 (dt, J = 12,7, 6,3 Гц, 6H), 0,95 (t, J = 5,9 Гц, 7H), 0,78 (s, 3H).
[331] DM1 синтезировали в виде одного диастереомера на основе методик, описанных в WO 2015/031396 (например, пример 2, абзац [00106]), включенном в данный документ посредством ссылки во всей своей полноте.
Пример 22. Конъюгирование антител и определение характеристик конъюгатов
[332] Конъюгирование антител
[333] Антитела (H4H14639D, H4H13312P, H4H14635D и изотипический контроль; 10-20 мг/мл) в 50 мМ HEPES, 150 мМ NaCl, pH 8,0 и 10-15% (об./об.) DMA конъюгировали с 5-6 кратным избытком диастереомера SMCC-DM1, полученного, как описано в примере 21 (майтанзиноид A), или майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин-карбамил-(п-амино)бензил-цитруллин-валин-адипоилсукцината (соединение 1, фигура 20) (майтанзиноид B) в течение 2 часов при температуре окружающей среды. Конъюгаты очищали посредством эксклюзионной хроматографии по размеру или экстенсивной ультрафильтрации и стерилизовали фильтрованием. Концентрации белков определяли посредством УФ-спектрального анализа. Посредством эксклюзионной HPLC установили, что все использованные конъюгаты являлись на >90% мономерными, а посредством RP-HPLC установили, что нагрузка неконъюгированного линкера составляла <1%. Все конъюгированные антитела анализировали с помощью УФ-анализов для определения значений содержания нагрузки линкера в соответствии с Hamblett et al. (American Association for Cancer Research. 2004 Oct 15;10(20):7063-70) и/или с помощью различия по массам нативных по сравнению с конъюгированными. Отношения нагрузки к антителам представлены в таблице 24.
REGN1945-майтанзиноид B
REGN1945-майтанзиноид A
Определение характеристик конъюгатов с применением жидкостной хроматографии-масс-спектрометрии
[334] Для определения содержания нагрузки линкера на антитело конъюгаты дегликозилировали и анализировали посредством LC-MS.
[335] Для анализа 50 мкг конъюгата разбавляли водой milli-Q до конечной концентрации 1 мг/мл. Десять мкл раствора PNGазы F [раствор PNGазы F получали посредством добавления 150 мкл исходного раствора PNGазы F (New England Biolabs, № по каталогу P0704L) к 850 мкл воды milli-Q и тщательного перемешивания] добавляли к разбавленному раствору конъюгата, а затем инкубировали при 37°C в течение ночи. Пробы по 5 мкл каждого образца вводили в LC-MS (система Waters Synat G2-Si) и элюировали со скоростью 0,1 мл/минуту с помощью градиента концентрации подвижной фазы 20-40% в течение 25 минут (подвижная фаза A: 0,1% об./об. FA в H2O; подвижная фаза B: 0,1% об./об. FA в ацетонитриле). LC-разделение осуществляли на колонке Waters Acquity BEH C4 (1,0 X 50 мМ, 1,7 мкМ) при 80°C.
[336] Спектры, полученные при масс-спектрометрии, подвергали деконволюции с применением программного обеспечения Masslynx, а отношение лекарственного средства к антителу (DAR) рассчитывали с применением следующих уравнений.
1. Относительный процент (%) лекарственного средства (Dn) по максимуму интенсивности распределения (PI):
Dn% = PIn /Ʃ(PI0+PI1+PI2…….+PIi)×100
(n= 0,1,2,3,…,i).
2. Расчет среднего DAR:
DAR=Ʃ(1×D1%+2×D2%+3×D3%+……+i×Di%).
Пример 23. Полученные с помощью поверхностного плазмонного резонанса значения аффинности связывания и кинетические константы конъюгированных моноклональных антител к MET (моноспецифических и биспецифических) человека
[337] Равновесные константы диссоциации (значения KD) связывания MET с антителами к MET, конъюгированными либо с диастереомером MCC-DM1 (майтанзиноид A), либо с майтанзин-3-N-метил-L-аланин-N-Me-бета-аланин-карбамил-(п-амино)бензил-цитруллин-валин-адипоилсукцинатом (соединение 1, фигура 20) (майтанзиноид B), определяли с применением биосенсорного анализа поверхностного плазмонного резонанса в реальном времени на приборе Biacore 2000. Поверхность сенсора Biacore дериватизировали посредством иммобилизации по аминогруппе моноклонального мышиного антитела к Fc человека (GE Healthcare, № по каталогу BR-1008-39) для захвата ADC к MET и исходных немодифицированных антител, экспрессируемых с константными областями человека. Исследования связывания с помощью прибора Biacore проводили в подвижном буфере, состоящем из забуференного HEPES физиологического раствора (HBS)-EP (0,01 M HEPES, pH 7,4, 0,15 M NaCl, 3 мМ EDTA, 0,05% об./об. поверхностно-активного вещества P20). MET человека получали самостоятельно с экспрессией С-концевой myc-myc-гексагистидиновой метки (hMET-mmh). Различные концентрации (3-кратные разведения) hMET-mmh (в диапазоне от 30 нМ до 1,1 нМ), полученного в подвижном буфере HBS-EP, вносили на поверхность с захваченным ADC или антителом к MET со скоростью потока 40 мкл/мин. Мониторинг ассоциации hMET-mmh с каждым из захваченных ADC и моноклональных антител осуществляли в течение 4 минут. Затем осуществляли мониторинг диссоциации hMET-mmh в течение 6 минут в подвижном буфере HBS-EP. Поверхность с антителом к Fc человека регенерировали посредством кратковременного внесения 20 мМ H3PO4. Все эксперименты по кинетике связывания проводили при 25°C.
[338] Кинетические константы скорости ассоциации (ka) и скорости диссоциации (kd) определяли посредством аппроксимации сенсограмм в реальном времени по модели связывания 1:1 с применением программного обеспечения для аппроксимации кривой Scrubber 2.0c. На всех сенсограммах осуществляли вычитание двух опорных сигналов посредством вычитания сигнала на сенсограмме от внесения буфера из соответствующей сенсограммы аналита, тем самым удаляя артефакты, полученные в результате диссоциации антитела от поверхности захвата. Равновесные константы диссоциации связывания (KD) и полупериоды диссоциации (t½) рассчитывали исходя из кинетических констант скоростей следующим образом:
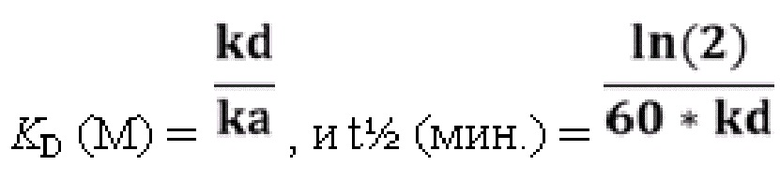
[339] Кинетические параметры связывания для моноспецифических и биспецифических антител к Met, конъюгированных с майтанзиноидом A или майтанзиноидом B, показаны ниже в таблице 25, при этом некоторые эксперименты осуществляли в двух повторностях.
Пример 24. Эффективность конъюгатов антитело к MET-лекарственное средство (ADC) In Vitro
[340] Для определения относительной эффективности конъюгатов антитело к MET-лека×ственное средство (ADC), описанных в данном документе, в отношении уничтожения клеток проводили анализы уничтожения клеток на множестве клеточных линий, экспрессирующих различные уровни эндогенного MET. Линии клеток EBC-1 (Riken Cell Bank; № по каталогу RBRC-RCB1965), MKN-45 (JCRB; № по каталогу JCRB0254), NCI-H1993 (ATCC; № по каталогу CRL-5909) и J.RT3 (ATCC; № по каталогу TIB-153) поддерживали в RPMI + 10% FBS + 1X пенициллина/стрептомицина/L-глутамина (P/S/G), SNU-5 (ATCC; № по каталогу CRL-5973) поддерживали в среде Искова + 10% FBS + 1X P/S/G, Hs746t (ATCC; № по каталогу HTB-135) и HEK293 (ATCC; № по каталогу 003041) поддерживали в DME + 10% FBS + 1X P/S/G, MDA-MB-231 (ATCC; № по каталогу HTB-26) поддерживали в среде Лейбовица L-15 + 10% FBS + 1X P/S/G + 1X заменимых аминокислот (NEAA) без CO2, U87MG (ATCC; № по каталогу HTB-14) поддерживали в MEM с солями Эрла, + 15% FBS + 1X P/S/G + 1X NEAA, T47D (ATCC; № по каталогу HTB-133) поддерживали в RPM1 1640 + 10% FBS + 1X P/S/G + 10 мМ HEPES + 1мМ пируват натрия + 10 мкг/мл бычьего инсулина и A549 (ATCC; № по каталогу CCL-185) поддерживали в питательной смеси Каигхн (Kaighn) F-12 (среда Хэма F-12K) + 10% FBS + 1X P/S/G.
[341] Первоначально относительное связывание антител к MET оценивали с помощью неконъюгированных антител H4H14635D, H4H14639D и H4H13312P2 в пределах всей панели клеточных линий посредством проточной цитометрии. Вкратце, 1×106 клеток инкубировали с антителом H4H14635D, H4H14639D, H4H13312P2 или антителом изотипического контроля (REGN1945) в концентрации 10 мкг/мл в течение 30 минут на льду в PBS + 2% FBS (буфер FACS). После одного промывания буфером FACS клетки инкубировали с конъюгированным с красителем Alexa647 вторичным антителом к антителам человека (Jackson ImmunoResearch, № по каталогу 109-606-170) в концентрации 10 мкг/мл в течение 30 минут на льду. После одного дополнительного промывания буфером FACS образцы фиксировали с помощью реагента Cytofix (BD Biosciences, № по каталогу 554655), фильтровали с применением буфера FACS и анализировали на проточном цитометре iQue (Intelicyte). Данные о средней интенсивности флуоресценции (MFI) определяли с применением программного обеспечения FlowJo (FlowJo LLC). Связывание с помощью FACS выражали как кратность значения MFI связывания выше уровней изотипического контроля, и результаты представлены в таблице 26. Относительное связывание трех антител к Met являлось сопоставимым для каждой линии клеток и в 447-7 раз превышало показатели изотипических контролей. На клетках T47D, HEK293 или J.RT3 не наблюдали обнаруживаемого связывания какого-либо из 3 протестированных антител к MET.
[342] Для измерения цитотоксичности ADC к MET in vitro оценивали количество ядер после 3- или 6-дневной обработки с помощью ADC. Вкратце, клетки высевали в 96-луночные планшеты, покрытые коллагеном (Greiner, VWR; № по каталогу 82050-812), в количестве 750 - 3000 клеток/лунка в полную среду для роста и выращивали в течение ночи при 37°C, 5% CO2. Для получения кривых жизнеспособности клеток к клеткам добавляли серийно разведенные ADC, неконъюгированные антитела или свободные нагрузки в конечных концентрациях в диапазоне от 100 нМ до 0,01 нМ (в зависимости от концентрации токсина) и инкубировали в течение 3 или 6 дней при 37°C в 5% CO2. Затем клетки обрабатывали с помощью ядерного красителя Hoechst 33342 в концентрации 3 мкг/мл (Invitrogen, № по каталогу H3570), фиксируя с помощью 4% формальдегида. Изображения получали с применением комплекса ImageXpress micro XL (Molecular Devices, Саннивейл, Калифорния), а количество ядер определяли с помощью программного обеспечения для анализа изображений MetaXpress (Molecular Devices, Саннивейл, Калифорния). Фоновые количества ядер клеток, обработанных 40 нМ дигитонином, вычитали из количества во всех лунках, и жизнеспособность выражали в виде процента от необработанных контролей. Значения IC50 определяли с помощью четырехпараметрического логистического уравнения по 10-точечной кривой ответа (GraphPad Prism). Условие отсутствия обработки для каждой кривой зависимости ответа от дозы также включено в анализ и представлено в виде самой низкой дозы. Значения IC50 и процентный показатель уничтожения клеток представлены в таблицах 27 и 28.
[343] Как приведено в таблице 27, конъюгат антитело к MET-лекарственное средство, H4H14639D-майтанзиноид A, специфически снижал жизнеспособность клеток в теневых фенотипах EBC-1, SNU-5, MKN-45, NCI-H1993 и Hs746t с амплификацией Met со значениями IC50, варьирующими от 0,35 нМ до 0,96 нМ. Процентный показатель уничтоженных клеток (макс. % уничтожения) варьировал от 73% до 100%. H4H14639D-майтанзиноид A также специфически уничтожал 84% клеток A549 со значениями IC50, составляющими 13,91 нМ. Значения IC50 конъюгата H4H14639D-майтанзиноид A превышали 37 нМ в линиях клеток с низкой экспрессией (MDA-MB-231 и U87MG) и с отсутствием экспрессии (T47D, HEK293 и J.RT3). Аналогичным образом конъюгированное антитело изотипического контроля уничтожало все клеточные линии со значениями IC50, превышающими 35 нМ. Метилдисульфидная версия DM1 (MeS-DM1) уничтожала все тестируемые линии со значениями IC50, варьирующими от 0,07 нМ до 2,86 нМ.
[344] В отдельном эксперименте три антитела к Met (H4H14639D, H4H14635D и H4H13312P2) конъюгировали с майтанзиноидными нагрузками майтанзиноида A или майтанзиноида B, и цитотоксичность in vitro оценивали в клетках EBC-1, Hs746t, A549 и T47D после 6-дневной обработки. Как приведено в таблице 28, все конъюгаты антитело к MET-лекарственное средство в значительной степени и специфически снижают клеточную жизнеспособность Met-положительных клеток со значениями IC50 вплоть до 10 пМ в клетках EBC-1, 0,82 нМ в клетках Hs746t и 3,5 нМ в клетках A549. Процентный показатель уничтоженных клеток составлял более 95% в клетках EBC-1, более 86% в клетках Hs746t и более 72% в клетках A549. Клетки T47D (Met-отрицательные) не подвергались специфическому уничтожению с помощью ADC к Met. Аналогичным образом конъюгированные антитела изотипического контроля снижали жизнеспособность клеток во всех тестируемых клеточных линиях со значениями IC50, составляющими более 5 нМ в клетках EBC-1, более 33 нМ в клетках Hs746t и более 90 нМ в клетках A549 и T47D. Неконъюгированное антитело H4H14639D снижало клеточную жизнеспособность в клетках EBC-1, Hs746t и A549, но с более низким процентным показателем, чем конъюгированные антитела. Неконъюгированные антитела H4H14635D и H4H13312P2 практически не влияли на жизнеспособность любой из протестированных линий клеток. Метилдисульфидная версия DM1 (MeS-DM1) уничтожала все тестируемые линии со значениями IC50, варьирующими от 0,12 нМ до 1,39 нМ. Напротив, M24 (нагрузка, отсоединяемая от майтанзиноида B) уничтожала клетки со значениями IC50 >100 нМ.
(Изотипический контроль)
Пример 25. Эффективность In Vivo в отношении клеток рака желудка
[345] 3 миллиона клеток рака желудка Hs746T имплантировали подкожно в область бока мышей SCID C.B.-17. Когда объемы опухоли достигали примерно 150 мм3 мышей рандомизировали на группы по 6 особей и обрабатывали конъюгатом контрольных антител REGN1945-майтанзиноид B, или конъюгатом REGN1945-майтанзиноид A при 10 мг/кг, или конъюгатом H4H14639D-майтанзиноид A, или конъюгатом H4H14639D-майтанзиноид B при 3 или 10 мг/кг. Все антитела вводили три раза с частотой один раз в неделю. Рост опухоли контролировали в течение 37 дней после имплантации.
[346] Оценивали влияние конъюгатов H4H14639D-майтанзиноид A или H4H14639D-майтанзиноид B на рост ксенотрансплантатов опухоли человека у мышей с ослабленной иммунной системой и результаты приведены в таблице 29. Опухоли, обработанные конъюгатами контрольных антител, REGN1945-майтанзиноид B или REGN1945-майтанзиноид A, росли до достижения пределов размера, соответствующих протоколу, в течение 20 дней. Опухоли, обработанные конъюгатом H4H14639D-майтанзиноид A в дозе 3 мг/кг, росли до достижения пределов размера, соответствующих протоколу, в течение 27 дней. Рост опухолей, обработанных конъюгатом H4H14639D-майтанзиноид B в дозе 3 мг/кг, подавлялся в течение всего периода проведения эксперимента. Обработка опухолей конъюгатами H4H14639D-майтанзиноид A или H4H14639D-майтанзиноид B при 10 мг/кг индуцировала уменьшение размера опухоли относительно начала обработки.
конъюгата H4H14639D-майтанзиноид A
конъюгата H4H14639D-майтанзиноид B
конъюгата H4H14639D-майтанзиноид B
Пример 26. Эффективность in vivo в отношении клеток рака легкого
[347] 5 миллионов клеток рака легкого EBC1 имплантировали подкожно в область бока мышей SCID C.B.-17. Когда объемы опухоли достигали примерно 170 мм3 мышей рандомизировали на группы по 6 особей и обрабатывали конъюгатом контрольного антитела REGN1945-майтанзиноид B при 15 мг/кг или конъюгатом H4H14639D-майтанзиноид B при 2,5, 5, 10 или 15 мг/кг. Антитела вводили два раза с частотой один раз в неделю. Рост опухоли контролировали в течение 73 дней после имплантации.
[348] Оценивали влияние H4H14639D на рост ксенотрансплантатов опухоли человека у мышей с ослабленной иммунной системой. Опухоли, обработанные конъюгатом контрольного антитела, REGN1945-майтанзиноид B, росли до достижения пределов размера, соответствующих протоколу, в течение 24 дней (протоколы IACUC требуют умерщвления животных с опухолями диаметром более 2 см, примерно 1500 мм3). Обработка опухолей конъюгатом H4H14639D-майтанзиноид B при 2,5, 5, 10 или 15 мг/кг индуцировала уменьшение размера опухоли относительно начала обработки. Результаты показаны в таблице 30.
конъюгата REGN1945-майтанзиноид B
H4H14639D-майтанзиноид B
Пример 27. Эффективность in vivo в отношении опухолей NSCLC, полученных от пациентов
[349] Met-экспрессирующие опухоли NSCLC, полученные от пациента CTG-0165, имплантировали подкожно в область бока бестимусных мышей nu/nu. Когда объемы опухоли достигали примерно 150 мм3 мышей рандомизировали на группы по 6 особей и обрабатывали конъюгатом контрольных антител REGN1945-майтанзиноид B, или конъюгатом REGN1945-майтанзиноид A при 10 мг/кг, или конъюгатом H4H14639D-майтанзиноид A, или конъюгатом H4H14639D-майтанзиноид B при 3 или 10 мг/кг. Все антитела вводили три раза с частотой один раз в неделю. Рост опухоли контролировали в течение 61 дня после имплантации.
[350] Оценивали влияние конъюгатов H4H14639D-майтанзиноид A или H4H14639D-майтанзиноид B на рост ксенотрансплантатов опухоли человека у мышей с ослабленной иммунной системой. Опухоли, обработанные конъюгатами контрольных антител REGN1945-майтанзиноид A или REGN1945-майтанзиноид B, росли до достижения пределов размера, соответствующих протоколу, в течение 27 дней. Рост опухолей, обработанных конъюгатами H4H14639D-майтанзиноид A или H4H14639D-майтанзиноид B при 3 мг/кг, подавляли в течение 27 дней. Обработка опухолей конъюгатами H4H14639D-майтанзиноид A или H4H14639D-майтанзиноид B при 10 мг/кг индуцировала уменьшение размера опухоли относительно начала обработки. Данные представлены в таблице 31.
Пример 28. Эпитопное картирование на основании водородно-дейтериевого (H/D) обмена. Эпитопное картирование антител к Met H4H13312P2, H4H13306P2 и H4H14639D, связывающихся с MET человека
[351] Проводили эксперименты для определения специфических областей эктодомена рецептора фактора роста гепатоцитов человека (SEQ ID NO:155: изоформа 1 Met человека (Uniprot ID: P08581), экспрессируемого с myc-myc-гексагистидиновой (.mmh) меткой; далее в данном документе называемого hMet), с которыми взаимодействуют антитела к Met H4H13312P2, H4H13306P2 и H4H14639D. H4H13312P2 и H4H13306P2 представляют собой бивалентные моноспецифические антитела к Met; H4H14639D представляет собой биспецифическое антитело, содержащее две тяжелые цепи, связывающиеся с отдельными эпитопами на Met, каждая из H4H13312P2 и H4H13306P2 соответственно, и универсальную легкую цепь. (См. пример 5).
[352] Эпитопное картирование на основании водородно-дейтериевого (H/D) обмена с масс-спектрометрией (HDX-MS) использовали для определения связываемых эпитопов антител, упомянутых выше. Общее описание способа HDX приведено, например, в Ehring (1999) Analytical Biochemistry 267(2):252-259; и Engen and Smith (2001) Anal. Chem. 73:256A-265A.
Порядок проведения эксперимента
[353] Для картирования связываемого эпитопа(эпитопов) антител к Met H4H13312P2, H4H13306P2 и H4H14639D на hMET посредством HDX отдельные антитела по отдельности ковалентно присоединяли к гранулам NHS-активированной сефарозы 4 Fast Flow (GE Healthcare, Питтсбург, Пенсильвания). Для подтверждения связываемых эпитопов антител к Met использовали два способа, «на антигене» и «на комплексе», которые описаны ниже.
[354] В экспериментальных условиях «на антигене» hMET дейтерировали в течение 5,0 мин или 10,0 мин в буфере PBS, полученном с D2O. Дейтерированный антиген связывали с гранулами с присоединенными антителами H4H13312P2 или H4H13306P2 посредством короткой инкубации и затем элюировали с гранул ледяным буфером с низким pH для гашения реакции. Элюированный образец вручную загружали в систему Waters H/DX-MS, включающую интегрированное поточное расщепление пептидов, улавливание, разделение посредством жидкостной хроматографии (LC) в течение 9,0 минут и сбор данных MS с помощью Synapt G2-Si.
[355] В экспериментальных условиях «на комплексе» hMET сначала связывали с гранулами с присоединенными H4H13312P2 или H4H13306P2 и затем дейтерировали в течение 5,0 или 10,0 мин посредством инкубации в буфере PBS, полученном с D2O. Дейтерированный hMET элюировали и анализировали с помощью системы Waters H/DX-MS, как упомянуто выше.
[356] Для идентификации расщепленных пептидов из hMET данные LC- MSE, полученные для недейтерированного образца, обрабатывали и выполняли поиск в отношении MET человека с применением программного обеспечения Waters ProteinLynx Global Server (PLGS). Идентифицированные пептиды импортировали в программное обеспечение DynamX 3.0 и отфильтровывали по двум следующим критериям: 1) минимальное количество продуктов на аминокислоту составляет 0,3; 2) пороговое значение повторов файлов составляет 3,0. Программное обеспечение DynamX 3.0 в дальнейшем автоматически рассчитывало разницу в захвате дейтерия каждым идентифицированным пептидом в способах «на антигене» и «на комплексе» в обеих временных точках дейтерирования, составляющих 5 мин и 10 мин. Отдельный изотопный пик каждого пептида, полученный с помощью программного обеспечения DynamX для расчета центроидного значения, также анализировали вручную для подтверждения точности расчета захвата дейтерия.
[357] В целом, значения дельта для дейтерирования, превышающие 0,2, использовали в качестве точки отсечки для определения специфического связываемого эпитопа.
Результаты
[358] Используя поточное расщепление пепсином на колонке Waters Enzymate™ BEH с пепсином (2,1×30 мм, 5 мкм) в сочетании со сбором данных с помощью LC-MSE в течение 9,0 минут в общей сложности 162 расщепленных пептида из MET человека воспроизводимо идентифицировали с применением отслеживаемого захвата дейтерия как в эксперименте «на антигене», так и в эксперименте «на комплексе» при применении гранул с присоединенным антителом H4H13312P2. Эти пептиды представляют 55,7% покрытие последовательности. Было обнаружено, что среди всех данных пептидов только пять характеризовались значительно сниженным захватом при дейтерировании после связывания H4H13312P2 («на комплексе») по сравнению с дейтерированием только антигена («на антигене»). Центроидные значения для данных пяти пептидов в обоих экспериментальных условиях проиллюстрированы в таблице 32. Область, соответствующая остаткам 192-204, которая покрывается данными пятью пептидами, была определена как связываемый эпитоп для антитела H4H13312P2 на основании данных HDX.
Центроид MH+
Центроид MH+
Центроид MH+
[359] В случае эксперимента HDX, проводимого с применением гранул с присоединенным антителом H4H13306P2, в общей сложности 98 расщепленных пептидов из hMET воспроизводимо идентифицировали с применением отслеживаемого захвата дейтерия как в эксперименте «на антигене», так и в эксперименте «на комплексе». Эти 98 пептидов представляют 52,1% покрытие последовательности. Было обнаружено, что среди всех данных пептидов двенадцать характеризовались сниженным и значительно сниженным захватом при дейтерировании после связывания H4H13306P2 («на комплексе») по сравнению с дейтерированием только антигена («на антигене»). Центроидные значения для данных двенадцати пептидов в обоих экспериментальных условиях проиллюстрированы в таблице 33. Области, соответствующие остаткам 305-315 и остаткам 421-455, которые покрываются данными пептидами, были определены как связываемый эпитоп для антитела H4H13306P2 на основании данных HDX.
Центроид MH+
Центроид MH+
Центроид MH+
Центроид MH+
[360] Ту же методику, которая изложена выше, применяли для определения связываемых эпитопов для биспецифического антитела к MET H4H14639D. Связываемые H4H14639D эпитопы на hMET, определенные посредством данной методики, соответствуют эпитопам, определенным для исходных антител.
[361] Связываемый эпитоп антитела к MET H4H13312P2: AA 192-204: VRRLKETKDGFMF (SEQ ID NO: 156) из SEQ ID NO: 155.
[362] Связываемый эпитоп антитела к MET H4H13306P2: AA 305-315: LARQIGASLND (SEQ ID NO: 157) из SEQ ID NO: 155 и AA 421-455: FIKGDLTIANLGTSEGRFMQVVVSRSGPSTPHVNF (SEQ ID NO: 158) из SEQ ID NO: 155.
Пример 29. Подавление пролиферации клеток и жизнеспособности клеток с помощью ADC на основе биспецифических антител к MET x MET в линиях клеток увеальной меланомы
[363] Биспецифическое антитело к c-Met H4H14639D, конъюгированное с одной из двух нагрузок, представляющих собой майтанзиноид, и обозначенное как конъюгат H4H14639D-майтанзиноид A и конъюгат H4H14639D-майтанзиноид B, тестировали на линиях клеток увеальной меланомы для определения влияния на пролиферацию клеток и жизнеспособность клеток относительно экспрессии c-Met в линиях клеток.
[364] В первом эксперименте клетки увеальной меланомы OMM1.3, Mel202, Mel270 и MP65, которые экспрессируют c-Met, высевали на ночь в 96-луночные планшеты в количестве 1000 клеток на лунку в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2. Клетки обрабатывали в течение семи дней возрастающими дозами REGN1945, конъюгата REGN1945-майтанзиноид A, конъюгата REGN1945-майтанзиноид B, H4H14639D, конъюгата H4H14639D-майтанзиноид A и конъюгата H4H14639D-майтанзиноид B, составляющими от 0,01 нМ до 100 нМ. Через 7 дней относительную жизнеспособность клеток определяли посредством измерения снижения WST-8 в колориметрическом анализе с помощью набора Dojindo Cell Counting Kit 8 с применением устройства для считывания микропланшетов Emax Plus (Molecular Devices).
[365] Во втором эксперименте клетки увеальной меланомы OMM1.3, которые экспрессируют c-Met, а также c-Met-отрицательные клетки OCM3, высевали на ночь в 96-луночные планшеты в количестве 1000 клеток на лунку в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2. Клетки обрабатывали возрастающими дозами REGN1945, конъюгата REGN1945-майтанзиноид B, H4H14639D и конъюгата H4H14639D-майтанзиноид B, составляющими от 0,3125 нМ до 10 нМ. Через 7 дней относительную жизнеспособность клеток определяли посредством измерения снижения WST-8 в колориметрическом анализе с помощью набора Dojindo Cell Counting Kit 8 с применением устройства для считывания микропланшетов Emax Plus (Molecular Devices).
[366] В таблицах 34-38 и на фигурах 21 и 22 показано, что биспецифическое антитело к c-Met, конъюгированное с нагрузкой, представляющей собой майтанзиноид, H4H14639D-майтанзиноид B, снижает жизнеспособность клеток увеальной меланомы, которые экспрессируют белок c-Met, по сравнению с контрольными обработками. Конъюгат H4H14639D-майтанзиноид B не оказывал влияния на жизнеспособность c-Met-отрицательной линии клеток. На фигуре 21 на логарифмической шкале показано влияние на жизнеспособность клеток при более низких концентрациях ADC. Данные для конъюгата H4H14639D-майтанзиноид A также показаны на фигуре 21. Неконъюгированное антитело H4H14639D практически не снижало жизнеспособность экспрессирующих c-Met клеток увеальной меланомы, что указывает на то, что выживание данных клеток не зависит от передачи сигнала Met. Данные из третьего эксперимента, в котором тринадцать линий клеток обрабатывали возрастающими дозами REGN1945, конъюгата REGN1945-майтанзиноид B, H4H14639D и конъюгата H4H14639D-майтанзиноид B в течение 3 дней, показаны на фигуре 33. Конъюгат H4H14639D-майтанзиноид B снижает жизнеспособность экспрессирующих MET линий клеток увеальной меланомы дозозависимым образом с IC50, составляющей менее чем 1 нМ.
Пример 30. ADC на основе биспецифического антитела к MET x MET индуцирует апоптоз клеток увеальной меланомы
[367] Клетки увеальной меланомы OMM1.3 и Mel202, которые экспрессируют c-Met, а также линию c-Met-отрицательных клеток OCM3 высевали на ночь в планшеты объемом 60 мм3 в количестве 800000 клеток на планшет в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2. Клетки обрабатывали с помощью 1,25, 2,5 нМ или 10 нМ REGN1945 (антитело изотипического контроля), конъюгата REGN1945-майтанзиноид A, H4H14639D или конъюгата H4H14639D-майтанзиноид B в течение 48 часов. Затем клетки собирали с помощью трипсина, промывали с помощью PBS, фиксировали 4% параформальдегидом в течение 30 минут при комнатной температуре и окрашивали с помощью DAPI в течение ночи при 4°C. Клетки помещали на предметное стекло микроскопа и заключали в Cytoseal 40. Количество апоптотических клеток определяли под микроскопом с UV-излучением для возбуждения флуоресценции DAPI.
[368] Биспецифическое антитело к c-Met, конъюгированное с нагрузкой, представляющей собой майтанзиноид, конъюгат H4H14639D-майтанзиноид B, в значительной степени индуцировал апоптоз экспрессирующих белок c-Met клеток увеальной меланомы дозозависимым образом (см. таблицы 39 и 40) по сравнению с контрольными обработками и c-Met-отрицательной линией клеток (см. таблицу 41). См. также фигуры 23 и 24. В другом эксперименте индукция апоптоза составляла до 40% в c-Met-экспрессирующих линиях клеток OMM1.3 и Mel202, но не в OCM3 при обработке с помощью 10 нМ METxMET-ADC в течение 48 часов (данные не показаны). Посредством конъюгации c-Met-специфического антитела с цитотоксическим соединением можно избирательно нацеливаться на клетки увеальной меланомы для обеспечения апоптоза.
Пример 31. ADC на основе биспецифического антитела к MET x MET изменяет клеточный цикл клеток увеальной меланомы
[369] Клетки увеальной меланомы OMM1.3 и Mel202, которые экспрессируют c-Met, а также линию c-Met-отрицательных клеток OCM3 высевали на ночь в планшеты объемом 60 мм3 в количестве 800000 клеток на планшет в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2. Клетки либо не обрабатывали, либо обрабатывали с помощью 10 нМ конъюгата H4H14639D-майтанзиноид B в течение 1, 3, 6, 24 и 48 часов. Затем клетки собирали с помощью трипсина, промывали с помощью PBS, фиксировали холодным 70% этанолом в течение ночи при -20°C, инкубировали с антителом к MPM2 от Millipore в течение 2 часов, промывали с помощью PBS, инкубировали с антителом к мышиному IgG от Invitrogen, конъюгированным с Alexa Fluor 488 (Invitrogen), и снова промывали с помощью PBS. Затем клетки окрашивали с помощью 500 мкг/мл йодида пропидия и инкубировали в течение ночи при 4°C. Затем клетки пропускали через сито для клеток перед анализом на проточном цитометре BD Bioscience LSR II. Данные анализировали с применением программного обеспечения FCS Express 6 от De Novo software.
[370] Биспецифическое антитело к c-Met, конъюгированное с нагрузкой, представляющей собой майтанзиноид, конъюгат H4H14639D-майтанзиноид B, в значительной степени индуцировал остановку митоза в клетках OMM1.3 и Mel202 (фигуры 25 и 26 соответственно) через 6-24 часа после обработки, но не индуцировал остановку митоза в клетках OCM3 (фигура 27). Наблюдали увеличение популяции SubG1 среди клеток, экспрессирующих c-Met, обработанных конъюгатом H4H14639D-майтанзиноид B между 24-48 часами, что указывало на индукцию апоптоза, но увеличения популяции SubG1 среди c-Met-отрицательных клеток не наблюдали. См. таблицы 42-44. Анализ клеточного цикла подтвердил, что введение нагрузки, представляющей собой майтанзиноид, индуцировало остановку митоза и, следовательно, апоптоз только в экспрессирующих c-Met линиях клеток OMM1.3 и Mel202, но не в c-Met-отрицательной линии клеток OCM3.
Пример 32: экспрессия c-Met в линиях клеток увеальной меланомы
[371] Анализы посредством вестерн-блоттинга проводили для оценки различий в уровнях экспрессии белка c-Met в нескольких линиях клеток увеальной меланомы, а также в линии клеток карциномы желудка и линии клеток карциномы легкого.
[372] Линии клеток с различными уровнями экспрессии c-Met, включая SNU-5, линию клеток карциномы желудка A549, линию клеток карциномы легкого, а также линии клеток увеальной меланомы Mel290, 92.1, OMM1.3, OMM1, Mel285, Mel202, Mel270, OCM1A, OCM3, MP41, MP65, MP46 и UM004 высевали в планшеты объемом 60 мм3 в количестве 1000000 клеток на планшет в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2 в течение 24 часов. Затем клетки собирали с помощью трипсина, промывали с помощью PBS и лизировали с помощью буфера RIPA. Белковые лизаты анализировали на 20-луночных 4-12% миди-гелях Novex (Invitrogen), затем переносили на PVDF-мембрану. Затем мембрану блокировали в 5% растворе обезжиренного сухого молока, инкубировали с первичными антителами к c-Met (Cell Signaling) и тубулину (Cell Signaling) в течение ночи на встряхивателе при 4°C, промывали с помощью TBST, инкубировали с соответствующими вторичными антителами (GE Healthcare), конъюгированными с HRP, и промывали с помощью TBST. На мембрану добавляли субстрат ECL HRP и получали флуоресцентное изображение с применением камеры Fujifilm XA-2.
Результаты
[373] В линиях клеток увеальной меланомы обычно обнаруживают мутации в G-белках, таких как GNAQ или GNA11, но они также демонстрируют дифференциальную экспрессию c-Met. Как показано на фигуре 28, каждая из линий клеток увеальной меланомы экспрессирует рецептор c-Met на определенном уровне, за исключением линий клеток OCM1A и OCM3, которые являются мутантными клетками BRAFV600E-. SNU-5 представляет собой используемую в качестве положительного контроля линию клеток карциномы желудка, известную высокой экспрессией c-Met, в то время как A549 представляет собой линию клеток карциномы легкого, которая также экспрессирует c-Met.
Пример 33. ADC на основе биспецифического антитела к MET x MET индуцирует расщепление PARP и фосфорилирование гистона H3
[374] Анализы посредством вестерн-блоттинга проводили для оценки уровней белка c-Met, расщепления PARP и фосфорилирования гистона H3 в нескольких линиях клеток увеальной меланомы после обработки конъюгатом H4H14639D-майтанзиноид B.
[375] Клетки увеальной меланомы OMM1.3 и Mel202, которые экспрессируют c-Met, а также линию c-Met-отрицательных клеток OCM3 высевали на ночь в планшеты объемом 60 мм3 в количестве 800000 клеток на планшет в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2. Клетки либо не обрабатывали, либо обрабатывали возрастающими дозами конъюгата REGN1945-майтанзиноид B, H4H14639D и конъюгата H4H14639D-майтанзиноид B от 0,5 до 10 нМ в течение 24 часов. Затем клетки собирали с помощью трипсина, промывали с помощью PBS и лизировали с помощью буфера RIPA. Белковые лизаты анализировали на 20-луночных 4-12% миди-гелях Novex (Invitrogen), затем переносили на PVDF-мембрану. Затем мембрану блокировали в 5% растворе обезжиренного сухого молока, инкубировали с первичными антителами к PARP (Cell Signaling), фосфорилированному гистону H3 (Cell Signaling) и тубулину (Cell Signaling) в течение ночи на встряхивателе при 4°C, промывали с помощью TBST, инкубировали с соответствующими вторичными антителами (GE Healthcare), конъюгированными с HRP, и промывали с помощью TBST. На мембрану добавляли субстрат ECL HRP и получали флуоресцентное изображение с применением камеры Fujifilm XA-2.
[376] В другом эксперименте клетки увеальной меланомы OMM1.3, которые экспрессируют c-Met, а также линию c-Met-отрицательных клеток OCM3 высевали на ночь в планшеты объемом 60 мм3 в количестве 800000 клеток на планшет в RPMI с 10% FBS и инкубировали при 37°C с 5% CO2. Однако в данном эксперименте клетки либо не обрабатывали, либо обрабатывали с помощью 10 нМ конъюгата REGN1945-майтанзиноид B, H4H14639D и конъюгата H4H14639D-майтанзиноид B в течение более длительных периодов времени, составляющих 24, 48 и 72 часа. Затем клетки собирали с помощью трипсина, промывали с помощью PBS и лизировали с помощью буфера RIPA. Белковые лизаты анализировали на 20-луночных 4-12% миди-гелях Novex (Invitrogen), затем переносили на PVDF-мембрану. Затем мембрану блокировали в 5% растворе обезжиренного сухого молока, инкубировали с первичными антителами к c-Met (Cell Signaling), PARP (Cell Signaling), фосфорилированному гистону H3 (Cell Signaling) и тубулину (Cell Signaling) в течение ночи на встряхивателе при 4°C, промывали с помощью TBST, инкубировали с соответствующими вторичными антителами (GE Healthcare), конъюгированными с HRP, и промывали с помощью TBST. На мембрану добавляли субстрат ECL HRP и получали флуоресцентное изображение с применением камеры Fujifilm XA-2.
Результаты
[377] Фигура 29 представляет собой изображение результатов вестерн-блоттинга, демонстрирующее, что конъюгат H4H14639D-майтанзиноид B индуцирует расщепление PARP (маркер апоптоза) в клетках OMM1.3 и клетках Mel202 через 24 часа обработки. Ни конъюгат REGN1945-майтанзиноид B, ни H4H14639D не индуцировали расщепление PARP. В отличие от c-Met-положительных линий клеток, клетки OCM3 не демонстрировали расщепления PARP после обработки конъюгатом H4H14639D-майтанзиноид B. На фигуре 29 также продемонстрировано значительное повышение фосфорилирования гистона H3 в клетках OMM1.3 и Mel202, обработанных конъюгатом H4H14639D-майтанзиноид B, по сравнению с конъюгатом REGN1945-майтанзиноид B и H4H14639D, но не в клетках OCM3. Фосфорилирование гистона H3 индуцируется в ходе митоза и свидетельствует об остановке митоза в клетке, индуцированной майтанзиноидом. На фигуре 29 фосфорилирование гистона H3 наблюдается только в клетках, экспрессирующих c-Met (OMM1.3 и Mel202), но не в OCM3, и это является доказательством того, что майтанзиноид транспортируется в клетку с помощью антитела к c-Met. Эти данные дополнительно демонстрируют специфичность и эффективность ADC в отношении c-Met.
[378] Фигура 30 представляет собой изображение результатов вестерн-блоттинга, демонстрирующее зависящую от времени индукцию расщепления PARP в клетках OMM1.3, обработанных конъюгатом H4H14639D-майтанзиноид B, но не в клетках OMM1.3, обработанных конъюгатом REGN1945-майтанзиноид B или H4H14639D. В клетках OCM3 обработка конъюгатом H4H14639D-майтанзиноид B не влияла на белок PARP. Кроме того, общая экспрессия белка Met снижается при обработке с помощью H4H14639D и H4H14639D-M114 по сравнению с отсутствием обработки и обработкой с помощью REGN1945-M114, что указывает на интернализацию рецептора после обработки антителом или ADC. Наконец, наблюдали значительное повышение фосфорилирования гистона H3 в клетках OMM1.3, обработанных конъюгатом H4H14639D-майтанзиноид B (по сравнению с обработкой конъюгатом REGN1945-майтанзиноид B или H4H14639D), но, опять же, такого повышения не наблюдали в клетках OCM3.
[379] В заключение, иллюстративное биспецифическое антитело к c-Met, антитело H4H14639D, специфически нацеливается на c-Met в клетках, экспрессирующих данный рецептор. Посредством конъюгации данного антитела с майтанзиноидом (конъюгат H4H14639D-майтанзиноид B) можно специфически и эффективно индуцировать апоптоз в линиях клеток увеальной меланомы, которые экспрессируют c-Met.
Пример 34. ADC на основе биспецифического антитела к MET x MET подавляет инвазию клеток увеальной меланомы, экспрессирующих c-Met
[380] Клетки увеальной меланомы OMM1.3, которые экспрессируют c-Met, высевали на ночь во вставки с матригелем, помещенные в 24-луночный планшет, в количестве 120000 клеток на вставку, в среду RPMI с 0,1% FBS с последующими обработками: необработанный контроль, 125, 250 и 500 пМ R1945, конъюгата R1945-майтанзиноид B, H4H14639D и конъюгата H4H14639D-майтанзиноид B. RPMI с 10% FBS и 50 нг/мл HGF человека помещали в лунку в качестве хемоаттрактанта. Примерно через 24 часа матригель со стороны вставки очищали от немигрировавших клеток. Мигрировавшие клетки фиксировали метанолом в течение 2 минут и окрашивали 1% толуидином в течение 2 минут, а затем два раза промывали с помощью ddH2O. Высушенные матригели затем помещали на предметные стекла микроскопа и заключали в среду Cytoseal 60. Изображения получали с применением микроскопа Nikon TE-2000-U.
Результаты
[381] Конъюгат биспецифического антитела к c-Met H4H14639D-майтанзиноид B в значительной степени подавлял инвазию клеток увеальной меланомы OMM1.3, которые экспрессируют белок c-Met, по сравнению с контрольными обработками (R1945 и конъюгат R1945-майтанзиноид B), начиная с 250 пМ. Также наблюдали значительное подавление клеточной инвазии для клеток, обработанных с помощью H4H14639D, начиная с 250 пМ. Однако на жизнеспособность клеток не влияет нагрузка, представляющая собой конъюгированный майтанзиноид, в конъюгате H4H14639D-майтанзиноид B при данной дозе. См. фигуру 32.
[382] Объем настоящего изобретения не ограничен конкретными вариантами осуществления, описанными в данном документе. Действительно, различные модификации настоящего изобретения, кроме описанных в данном документе, будут очевидны специалистам в данной области техники из вышеизложенного описания и сопутствующих фигур. Предполагается, что такие модификации охватываются объемом прилагаемой формулы изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Regeneron Pharmaceuticals, Inc.
Schwartz, Gary
Surriga, Oliver
<120> СПОСОБЫ ЛЕЧЕНИЯ РАКА ГЛАЗА С ПРИМЕНЕНИЕМ АНТИТЕЛ К МЕТ И БИСПЕЦИФИЧЕСКИХ АНТИГЕНСВЯЗЫВАЮЩИХ МОЛЕКУЛ, КОТОРЫЕ СВЯЗЫВАЮТ МЕТ
<130> 10548WO01
<140> TBD
<141> 2020-02-20
<150> 62/808,839
<151> 2019-02-21
<150> 62/823,788
<151> 2019-03-26
<160> 158
<170> Версия PatentIn 3.5
<210> 1
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 1
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggagac cctgtccctc 60
acctgcactg tctctggtga ctccatcagt agttactatt ggacctggat ccggcagccc 120
ccagggaagg gactggagtg gattgggtat atcttttaca gggggggcac cacctacaac 180
ccctccctca agagtcgagt caccatatca gtagacacgt ccaagaacca gttctccctg 240
aagttgaggt ctgtgaccgc cgcagacacg gccgtgtatt actgtgcgag gggagacgat 300
cttttagtgg tgacaagtgt ctactggtac atcgatctct ggggccgtgg caccctggtc 360
accgtctcct ca 372
<210> 2
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 2
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Phe Tyr Arg Gly Gly Thr Thr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Asp Asp Leu Leu Val Val Thr Ser Val Tyr Trp Tyr Ile Asp
100 105 110
Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 3
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 3
ggtgactcca tcagtagtta ctat 24
<210> 4
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 4
Gly Asp Ser Ile Ser Ser Tyr Tyr
1 5
<210> 5
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 5
atcttttaca gggggggcac c 21
<210> 6
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 6
Ile Phe Tyr Arg Gly Gly Thr
1 5
<210> 7
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 7
gcgaggggag acgatctttt agtggtgaca agtgtctact ggtacatcga tctc 54
<210> 8
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 8
Ala Arg Gly Asp Asp Leu Leu Val Val Thr Ser Val Tyr Trp Tyr Ile
1 5 10 15
Asp Leu
<210> 9
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 9
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cgtccggatt caccttcagt ggctatggca tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg gatggcagtt atatggtatg atggaagtaa tgattactat 180
ccagactccg tgaagggccg attcaccatc tccagagaca attccaagaa cacgctgtat 240
ctgcaaatga acagcctgag agtcgaggac acggctgtgt attactgtgc gcgagatgcg 300
tgggacctac tacgttcctt tgactactgg ggccagggaa ccctggtcac cgtctcctca 360
<210> 10
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 10
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Asp Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Trp Asp Leu Leu Arg Ser Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 11
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 11
ggattcacct tcagtggcta tggc 24
<210> 12
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 12
Gly Phe Thr Phe Ser Gly Tyr Gly
1 5
<210> 13
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 13
atatggtatg atggaagtaa tgat 24
<210> 14
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 14
Ile Trp Tyr Asp Gly Ser Asn Asp
1 5
<210> 15
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 15
gcgcgagatg cgtgggacct actacgttcc tttgactac 39
<210> 16
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 16
Ala Arg Asp Ala Trp Asp Leu Leu Arg Ser Phe Asp Tyr
1 5 10
<210> 17
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 17
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagagtc 60
tcttgtgtag tgtctggatt caccttcagc agctttggca tgcattgggt ccgccaggct 120
ccagacaagg ggctggagtg ggtggcagtt atatggtatg atggaagtaa tgattactat 180
tcagactccg tgaagggccg attcaccatc tccagagaca attccaagaa cacgctgttt 240
ctacaaatga accgcctgag agccgaagac acggctgttt attactgtgc gcgagctaat 300
aactggaacc gttttgatgc ctttgatctc tggggccaag ggacaatggt caccgtctct 360
tca 363
<210> 18
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 18
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Val Ser Cys Val Val Ser Gly Phe Thr Phe Ser Ser Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Asp Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Asp Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Arg Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Asn Trp Asn Arg Phe Asp Ala Phe Asp Leu Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 19
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 19
ggattcacct tcagcagctt tggc 24
<210> 20
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 20
Gly Phe Thr Phe Ser Ser Phe Gly
1 5
<210> 21
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 21
atatggtatg atggaagtaa tgat 24
<210> 22
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 22
Ile Trp Tyr Asp Gly Ser Asn Asp
1 5
<210> 23
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 23
gcgcgagcta ataactggaa ccgttttgat gcctttgatc tc 42
<210> 24
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 24
Ala Arg Ala Asn Asn Trp Asn Arg Phe Asp Ala Phe Asp Leu
1 5 10
<210> 25
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 25
gaggtgcagc tggtggagtc tgggggaggc ttggttcagc ctggagggtc cctgagactc 60
tcctgtgcag cctctggatt catcttcagt aattatgaaa tgaactgggt ccgccaggct 120
ccagggaagg gactggaatg gatttcatac attactagta gtggtaatat gaaatattac 180
gcagactctg tgaagggccg attcaccatc tccagagaca acgacaagaa ttcactgtat 240
ctgcaaatga gtagtctgag agtcgaggac acggctgttt attattgtgt gagaggaggg 300
cgatttttgg agtggttgac ctactacgtt atggtcgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 26
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 26
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Ser Asn Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Thr Ser Ser Gly Asn Met Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asp Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Val Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Gly Gly Arg Phe Leu Glu Trp Leu Thr Tyr Tyr Val Met Val
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 27
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 27
ggattcatct tcagtaatta tgaa 24
<210> 28
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 28
Gly Phe Ile Phe Ser Asn Tyr Glu
1 5
<210> 29
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 29
attactagta gtggtaatat gaaa 24
<210> 30
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 30
Ile Thr Ser Ser Gly Asn Met Lys
1 5
<210> 31
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 31
gtgagaggag ggcgattttt ggagtggttg acctactacg ttatggtcgt c 51
<210> 32
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 32
Val Arg Gly Gly Arg Phe Leu Glu Trp Leu Thr Tyr Tyr Val Met Val
1 5 10 15
Val
<210> 33
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 33
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgcag tgtctggatt caccttcagt agctatggca tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg ggtggcaaat atttggtatg atggaactaa tgattactat 180
ccatactccg tgaagggccg attcaccatc tccagagaca attcccagaa cacactatat 240
ctgcaaatga acagcctgag agccgaggac acggctgtat attactgtgc gagagaggac 300
ttcattaact accggtcttt tgactattgg ggccagggaa ccctggtcac cgtctcctca 360
<210> 34
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 34
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Trp Tyr Asp Gly Thr Asn Asp Tyr Tyr Pro Tyr Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Gln Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Asp Phe Ile Asn Tyr Arg Ser Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 35
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 35
ggattcacct tcagtagcta tggc 24
<210> 36
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 36
Gly Phe Thr Phe Ser Ser Tyr Gly
1 5
<210> 37
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 37
atttggtatg atggaactaa tgat 24
<210> 38
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 38
Ile Trp Tyr Asp Gly Thr Asn Asp
1 5
<210> 39
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 39
gcgagagagg acttcattaa ctaccggtct tttgactat 39
<210> 40
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 40
Ala Arg Glu Asp Phe Ile Asn Tyr Arg Ser Phe Asp Tyr
1 5 10
<210> 41
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 41
caggtgcagc tggtggagtc tgggggaggc gtggtccagc cagggacgtc cctgagactc 60
tcctgtgtcg cgtctggatt caccttcaga aattttggaa tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg ggtggcaaat atatggtttg acggaagtaa tgagaactat 180
gtcgagtcca ttcagggccg attcaccatc tccagagaca attccaagaa cacactgaat 240
ctgcagatga acagcctgag agccgaggac tcggctgtct attactgtgt gagagaggga 300
atcctaggaa ctactaatcc ttatgatgct tttgatgtct ggggccaagg gacaatggtc 360
accgtctctt ca 372
<210> 42
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 42
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Thr
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Arg Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Trp Phe Asp Gly Ser Asn Glu Asn Tyr Val Glu Ser Ile
50 55 60
Gln Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Asn
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Val Arg Glu Gly Ile Leu Gly Thr Thr Asn Pro Tyr Asp Ala Phe Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 43
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 43
ggattcacct tcagaaattt tgga 24
<210> 44
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 44
Gly Phe Thr Phe Arg Asn Phe Gly
1 5
<210> 45
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 45
atatggtttg acggaagtaa tgag 24
<210> 46
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 46
Ile Trp Phe Asp Gly Ser Asn Glu
1 5
<210> 47
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 47
gtgagagagg gaatcctagg aactactaat ccttatgatg cttttgatgt c 51
<210> 48
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 48
Val Arg Glu Gly Ile Leu Gly Thr Thr Asn Pro Tyr Asp Ala Phe Asp
1 5 10 15
Val
<210> 49
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 49
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgcag cgtctggatt cacctttagt aactttggaa tgcactgggt ccgccaggcg 120
ccaggcaagg gactggagtg ggtggcaggt atatggtttg atggaagtaa taaaaactat 180
atagactccg tgaagggccg attcaccatc tcaagagaca attccaagaa cacgctgtat 240
ctgcaaatga acagcctgag agccgaggac acggctgtgt attactgtgc gagagagggc 300
tatgattcgg ggactgatta tatcccctat gatatttttg atatttgggg ccaagggaca 360
atggtcaccg tctcttca 378
<210> 50
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 50
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gly Ile Trp Phe Asp Gly Ser Asn Lys Asn Tyr Ile Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Asp Ser Gly Thr Asp Tyr Ile Pro Tyr Asp Ile
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 51
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 51
ggattcacct ttagtaactt tgga 24
<210> 52
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 52
Gly Phe Thr Phe Ser Asn Phe Gly
1 5
<210> 53
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 53
atatggtttg atggaagtaa taaa 24
<210> 54
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 54
Ile Trp Phe Asp Gly Ser Asn Lys
1 5
<210> 55
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 55
gcgagagagg gctatgattc ggggactgat tatatcccct atgatatttt tgatatt 57
<210> 56
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 56
Ala Arg Glu Gly Tyr Asp Ser Gly Thr Asp Tyr Ile Pro Tyr Asp Ile
1 5 10 15
Phe Asp Ile
<210> 57
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 57
gaagtgcagc tggtggagtc tgggggaggc ttggtacagc ctggcacgtc cctgagactc 60
tcctgtgcag cctctggatt cacctttgat gattatgcca tgcactgggt ccggcaagct 120
ccagggaagg gcctggagtg ggtctcaggt attacttgga atagttataa catagactat 180
gctgactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctccctgtat 240
ctgcaaatga acagtctgag agctgaggac acggccttgt attactgtgc aaaagatgat 300
gactacagta actacgttta ctttgactac tggggccagg gaaccctggt caccgtctcc 360
tca 363
<210> 58
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 58
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Thr
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Thr Trp Asn Ser Tyr Asn Ile Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Asp Asp Tyr Ser Asn Tyr Val Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 59
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 59
ggattcacct ttgatgatta tgcc 24
<210> 60
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 60
Gly Phe Thr Phe Asp Asp Tyr Ala
1 5
<210> 61
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 61
attacttgga atagttataa cata 24
<210> 62
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 62
Ile Thr Trp Asn Ser Tyr Asn Ile
1 5
<210> 63
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 63
gcaaaagatg atgactacag taactacgtt tactttgact ac 42
<210> 64
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 64
Ala Lys Asp Asp Asp Tyr Ser Asn Tyr Val Tyr Phe Asp Tyr
1 5 10
<210> 65
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 65
caggttcagc tggtgcagtc cggaactgag gtgaaggagc ctggggcctc agtgaaggtc 60
tcctgtaagg cctctggtta ctcctttacc acctatggta tcagctggct gcgacaggcc 120
cctggacaag gacttgagtg gatgggatgg atcagcactt acaatggtga cacaatctct 180
gcacagatgc tccaggacag agtcaccctg accgcagaca catccacgcg cacagcctac 240
atggaactga gaagcctgag atctgacgac acggccgtgt attactgtgc gagaggtcat 300
gagtatgata gtcttgttta ttcttactgg ggccagggaa ccctggtcac cgtctcctca 360
<210> 66
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 66
Gln Val Gln Leu Val Gln Ser Gly Thr Glu Val Lys Glu Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Thr Tyr
20 25 30
Gly Ile Ser Trp Leu Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Thr Tyr Asn Gly Asp Thr Ile Ser Ala Gln Met Leu
50 55 60
Gln Asp Arg Val Thr Leu Thr Ala Asp Thr Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly His Glu Tyr Asp Ser Leu Val Tyr Ser Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 67
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 67
ggttactcct ttaccaccta tggt 24
<210> 68
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 68
Gly Tyr Ser Phe Thr Thr Tyr Gly
1 5
<210> 69
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 69
atcagcactt acaatggtga caca 24
<210> 70
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 70
Ile Ser Thr Tyr Asn Gly Asp Thr
1 5
<210> 71
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 71
gcgagaggtc atgagtatga tagtcttgtt tattcttac 39
<210> 72
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 72
Ala Arg Gly His Glu Tyr Asp Ser Leu Val Tyr Ser Tyr
1 5 10
<210> 73
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 73
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgcag cgtctggatt caccttcagt agttatgcca tgcactgggt ccgccaggct 120
ccaggcaggg ggctggagtg ggtggcggtt atatggcatg atggagatgt tgaatactat 180
gtagactccg tgaaggaccg attcaccatc tccagagaca attccaagag cacgctgtat 240
ctgcaaatga acagcctgag agccgaagat acggctttat attattgtgc gagagaggcg 300
tgggacctac tacgtccctt tgactattgg ggccagggaa ccctggtcac cgtctcctca 360
<210> 74
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 74
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp His Asp Gly Asp Val Glu Tyr Tyr Val Asp Ser Val
50 55 60
Lys Asp Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Trp Asp Leu Leu Arg Pro Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 75
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 75
ggattcacct tcagtagtta tgcc 24
<210> 76
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 76
Gly Phe Thr Phe Ser Ser Tyr Ala
1 5
<210> 77
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 77
atatggcatg atggagatgt tgaa 24
<210> 78
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 78
Ile Trp His Asp Gly Asp Val Glu
1 5
<210> 79
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 79
gcgagagagg cgtgggacct actacgtccc tttgactat 39
<210> 80
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 80
Ala Arg Glu Ala Trp Asp Leu Leu Arg Pro Phe Asp Tyr
1 5 10
<210> 81
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 81
gaggtgcagc tggtggagtc tggaggaggc ttggtccagc ctggggggtc cctgagactc 60
tcctgtgcag cctctgggtt catcgtcacc accaactaca tgacctggct ccgccaggct 120
ccagggaagg ggctggagtg ggtctcactt atttatagca gtggtcacac atactacgca 180
gactccgtga agggccgatt caccatctcc agacacaatt ccaagaacac actgtatcta 240
caaatggaca gcctgagagc tgaggacacg gccgtgtatt actgtgcgag tgctttcgca 300
gcggatgttt ttgatatctg gggccaaggg acaatggtca ccgtctcttc a 351
<210> 82
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 82
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Val Thr Thr Asn
20 25 30
Tyr Met Thr Trp Leu Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Tyr Ser Ser Gly His Thr Tyr Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asp Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Ser Ala Phe Ala Ala Asp Val Phe Asp Ile Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser
115
<210> 83
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 83
gggttcatcg tcaccaccaa ctac 24
<210> 84
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 84
Gly Phe Ile Val Thr Thr Asn Tyr
1 5
<210> 85
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 85
atttatagca gtggtcacac a 21
<210> 86
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 86
Ile Tyr Ser Ser Gly His Thr
1 5
<210> 87
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 87
gcgagtgctt tcgcagcgga tgtttttgat atc 33
<210> 88
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 88
Ala Ser Ala Phe Ala Ala Asp Val Phe Asp Ile
1 5 10
<210> 89
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 89
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgttcag cgtctggatt ctccttcagt cactttggca tgcactgggt ccgccaggtt 120
ccaggcgggg gcctggagtg ggtgacaagt atatggtttg atggaagtaa tagatattat 180
gcagactcct tgaagggccg attcaccatc tccagagaca attccaagaa tactctgtat 240
ctggaaatga acagcctgag agccgaggac acggctgtgt attactgtgt gagagagggg 300
atactgggaa ctactaatcc ttatgatgtt tttgatgtct ggggtcaggg gacaatggtc 360
accgtctctt ca 372
<210> 90
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 90
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Ser Phe Ser His Phe
20 25 30
Gly Met His Trp Val Arg Gln Val Pro Gly Gly Gly Leu Glu Trp Val
35 40 45
Thr Ser Ile Trp Phe Asp Gly Ser Asn Arg Tyr Tyr Ala Asp Ser Leu
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Glu Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Glu Gly Ile Leu Gly Thr Thr Asn Pro Tyr Asp Val Phe Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 91
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 91
ggattctcct tcagtcactt tggc 24
<210> 92
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 92
Gly Phe Ser Phe Ser His Phe Gly
1 5
<210> 93
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 93
atatggtttg atggaagtaa taga 24
<210> 94
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 94
Ile Trp Phe Asp Gly Ser Asn Arg
1 5
<210> 95
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 95
gtgagagagg ggatactggg aactactaat ccttatgatg tttttgatgt c 51
<210> 96
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 96
Val Arg Glu Gly Ile Leu Gly Thr Thr Asn Pro Tyr Asp Val Phe Asp
1 5 10 15
Val
<210> 97
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 97
gaggtgcagc tggtggagtc tgggggaggc ttggtacagc cgggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttaga agctatgtca tgagctggtt ccgccaggct 120
ccagggaagg ggctggagtg ggtctcagga atgagtggga gtggtggaag cacatcctac 180
gcagactccg tgaagggccg gttcaccatc tccagagaca attcaaagaa tacgctgtat 240
ctgctaatga acagcctgag aaccgaggac acggccgtat attattgtgc gaaagaaaac 300
ggggctaact ggaactacgg ctactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 98
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 98
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Val Met Ser Trp Phe Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Met Ser Gly Ser Gly Gly Ser Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Leu Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Glu Asn Gly Ala Asn Trp Asn Tyr Gly Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 99
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 99
ggattcacct ttagaagcta tgtc 24
<210> 100
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 100
Gly Phe Thr Phe Arg Ser Tyr Val
1 5
<210> 101
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 101
atgagtggga gtggtggaag caca 24
<210> 102
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 102
Met Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 103
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 103
gcgaaagaaa acggggctaa ctggaactac ggctactacg gtatggacgt c 51
<210> 104
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 104
Ala Lys Glu Asn Gly Ala Asn Trp Asn Tyr Gly Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 105
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 105
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgtag cgtctggatt ctccttcagt aactttggca tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg ggtggcaatt atatggtatg atggaagtaa taaatactat 180
tcagactccg tgaagggccg cttcaccatc tccagagaca attccaagaa cacgctgtat 240
ctgcaaatga acagcctgag agtcgacgac acggctgtgt attactgtgc gagattcgat 300
cgctggaaat ttgacgcttt tgatatctgg ggccaaggga caatggtcac cgtctcttca 360
<210> 106
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 106
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Ser Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ile Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Asp Arg Trp Lys Phe Asp Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 107
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 107
ggattctcct tcagtaactt tggc 24
<210> 108
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 108
Gly Phe Ser Phe Ser Asn Phe Gly
1 5
<210> 109
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 109
atatggtatg atggaagtaa taaa 24
<210> 110
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 110
Ile Trp Tyr Asp Gly Ser Asn Lys
1 5
<210> 111
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 111
gcgagattcg atcgctggaa atttgacgct tttgatatc 39
<210> 112
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 112
Ala Arg Phe Asp Arg Trp Lys Phe Asp Ala Phe Asp Ile
1 5 10
<210> 113
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 113
caggtgcagc tggtggagtc tgggggaggc gtggtccagc ctgggaggtc cctgagactc 60
tcctgtgcag cgtctggatt caccttcagt agctttgcca tgcactgggt ccgccaggct 120
ccaggcaagg ggctggagtg ggtggcagtt atatggtatg atggaagtaa tgattactat 180
gcagcctccg tgaagggccg tttcaccatc tccagagaca attccaagaa cacgctgtat 240
ctggaaatga acagactgag agccgaggac acggctgtgt atcactgtgc gagagataac 300
tggaattact gggggggtat ggacgtctgg ggccaaggga ccacggtcac cgtctcctca 360
<210> 114
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 114
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Phe
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Asp Tyr Tyr Ala Ala Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Glu Met Asn Arg Leu Arg Ala Glu Asp Thr Ala Val Tyr His Cys
85 90 95
Ala Arg Asp Asn Trp Asn Tyr Trp Gly Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 115
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 115
ggattcacct tcagtagctt tgcc 24
<210> 116
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 116
Gly Phe Thr Phe Ser Ser Phe Ala
1 5
<210> 117
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 117
atatggtatg atggaagtaa tgat 24
<210> 118
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 118
Ile Trp Tyr Asp Gly Ser Asn Asp
1 5
<210> 119
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 119
gcgagagata actggaatta ctgggggggt atggacgtc 39
<210> 120
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 120
Ala Arg Asp Asn Trp Asn Tyr Trp Gly Gly Met Asp Val
1 5 10
<210> 121
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 121
gaggtgcagc tgttggagtc tgggggaggc tgggtgcagc cgggggggtc cctgagactc 60
tcctgtgcag cctctggatt cgcctttagt aattatgcca tgaactgggt ccgccagact 120
ccagggaagg ggctggagtg ggtctcagtt attagtagta gtggtggaaa cacatactac 180
gcagactccg tgaagggccg gttcgccatc tccagagaca attccaggga tacgctgcat 240
ctgcaaatga acagactgag agtcgaggac acggccgtct attactgtgc gaaagaaata 300
cgtccgtatt acgatctttc ctactattac ggtatggacg tctggggcca agggaccacg 360
gtcaccgtct cctca 375
<210> 122
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 122
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Trp Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ala Phe Ser Asn Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Ser Ser Gly Gly Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ser Arg Asp Thr Leu His
65 70 75 80
Leu Gln Met Asn Arg Leu Arg Val Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Glu Ile Arg Pro Tyr Tyr Asp Leu Ser Tyr Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 123
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 123
ggattcgcct ttagtaatta tgcc 24
<210> 124
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 124
Gly Phe Ala Phe Ser Asn Tyr Ala
1 5
<210> 125
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 125
attagtagta gtggtggaaa caca 24
<210> 126
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 126
Ile Ser Ser Ser Gly Gly Asn Thr
1 5
<210> 127
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 127
gcgaaagaaa tacgtccgta ttacgatctt tcctactatt acggtatgga cgtc 54
<210> 128
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 128
Ala Lys Glu Ile Arg Pro Tyr Tyr Asp Leu Ser Tyr Tyr Tyr Gly Met
1 5 10 15
Asp Val
<210> 129
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 129
caggtgcagc tgcaggagtc gggcccagga ctggtgaagt cttcggagac cctgtccctc 60
acctgcactg tctctggtgg ctccatcaga aatttctact ggagctggct ccggcagccc 120
ccagggaagg gactagagtg gattgggcac atcaattaca atgggggcac cgactacaac 180
ccctccctca agagtcgagt caccatatca gtagacacgt ccaagaatca gttctccctg 240
aatttgaact ctgtgaccgc cgcagacacg gccgtgtatt actgtgcgag acagagattc 300
tacggtatgg acgtctgggg tccagggacc acggtcaccg tctcctca 348
<210> 130
<211> 116
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 130
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Ser Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Arg Asn Phe
20 25 30
Tyr Trp Ser Trp Leu Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly His Ile Asn Tyr Asn Gly Gly Thr Asp Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gln Arg Phe Tyr Gly Met Asp Val Trp Gly Pro Gly Thr Thr Val
100 105 110
Thr Val Ser Ser
115
<210> 131
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 131
ggtggctcca tcagaaattt ctac 24
<210> 132
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 132
Gly Gly Ser Ile Arg Asn Phe Tyr
1 5
<210> 133
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 133
atcaattaca atgggggcac c 21
<210> 134
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 134
Ile Asn Tyr Asn Gly Gly Thr
1 5
<210> 135
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 135
gcgagacaga gattctacgg tatggacgtc 30
<210> 136
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 136
Ala Arg Gln Arg Phe Tyr Gly Met Asp Val
1 5 10
<210> 137
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 137
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccgtca 180
aggttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta cccctccgat caccttcggc 300
caagggacac gactggagat taaa 324
<210> 138
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 138
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 139
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 139
cagagcatta gcagctat 18
<210> 140
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 140
Gln Ser Ile Ser Ser Tyr
1 5
<210> 141
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 141
gctgcatcc 9
<210> 142
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 142
Ala Ala Ser
1
<210> 143
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 143
caacagagtt acagtacccc tccgatcacc 30
<210> 144
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 144
Gln Gln Ser Tyr Ser Thr Pro Pro Ile Thr
1 5 10
<210> 145
<211> 1408
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 145
Met Lys Ala Pro Ala Val Leu Ala Pro Gly Ile Leu Val Leu Leu Phe
1 5 10 15
Thr Leu Val Gln Arg Ser Asn Gly Glu Cys Lys Glu Ala Leu Ala Lys
20 25 30
Ser Glu Met Asn Val Asn Met Lys Tyr Gln Leu Pro Asn Phe Thr Ala
35 40 45
Glu Thr Pro Ile Gln Asn Val Ile Leu His Glu His His Ile Phe Leu
50 55 60
Gly Ala Thr Asn Tyr Ile Tyr Val Leu Asn Glu Glu Asp Leu Gln Lys
65 70 75 80
Val Ala Glu Tyr Lys Thr Gly Pro Val Leu Glu His Pro Asp Cys Phe
85 90 95
Pro Cys Gln Asp Cys Ser Ser Lys Ala Asn Leu Ser Gly Gly Val Trp
100 105 110
Lys Asp Asn Ile Asn Met Ala Leu Val Val Asp Thr Tyr Tyr Asp Asp
115 120 125
Gln Leu Ile Ser Cys Gly Ser Val Asn Arg Gly Thr Cys Gln Arg His
130 135 140
Val Phe Pro His Asn His Thr Ala Asp Ile Gln Ser Glu Val His Cys
145 150 155 160
Ile Phe Ser Pro Gln Ile Glu Glu Pro Ser Gln Cys Pro Asp Cys Val
165 170 175
Val Ser Ala Leu Gly Ala Lys Val Leu Ser Ser Val Lys Asp Arg Phe
180 185 190
Ile Asn Phe Phe Val Gly Asn Thr Ile Asn Ser Ser Tyr Phe Pro Asp
195 200 205
His Pro Leu His Ser Ile Ser Val Arg Arg Leu Lys Glu Thr Lys Asp
210 215 220
Gly Phe Met Phe Leu Thr Asp Gln Ser Tyr Ile Asp Val Leu Pro Glu
225 230 235 240
Phe Arg Asp Ser Tyr Pro Ile Lys Tyr Val His Ala Phe Glu Ser Asn
245 250 255
Asn Phe Ile Tyr Phe Leu Thr Val Gln Arg Glu Thr Leu Asp Ala Gln
260 265 270
Thr Phe His Thr Arg Ile Ile Arg Phe Cys Ser Ile Asn Ser Gly Leu
275 280 285
His Ser Tyr Met Glu Met Pro Leu Glu Cys Ile Leu Thr Glu Lys Arg
290 295 300
Lys Lys Arg Ser Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala
305 310 315 320
Tyr Val Ser Lys Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser
325 330 335
Leu Asn Asp Asp Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp
340 345 350
Ser Ala Glu Pro Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys
355 360 365
Tyr Val Asn Asp Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg
370 375 380
Cys Leu Gln His Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg
385 390 395 400
Thr Leu Leu Arg Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr
405 410 415
Arg Thr Glu Phe Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly
420 425 430
Gln Phe Ser Glu Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly
435 440 445
Asp Leu Thr Ile Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln
450 455 460
Val Val Val Ser Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu
465 470 475 480
Leu Asp Ser His Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu
485 490 495
Asn Gln Asn Gly Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys
500 505 510
Ile Pro Leu Asn Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln
515 520 525
Cys Leu Ser Ala Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys
530 535 540
Cys Val Arg Ser Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile
545 550 555 560
Cys Leu Pro Ala Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu
565 570 575
Gly Gly Thr Arg Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg
580 585 590
Asn Asn Lys Phe Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu
595 600 605
Ser Cys Thr Leu Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys
610 615 620
Thr Val Gly Pro Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile
625 630 635 640
Ser Asn Gly His Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp
645 650 655
Pro Val Ile Thr Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly
660 665 670
Thr Leu Leu Thr Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg
675 680 685
His Ile Ser Ile Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn
690 695 700
Ser Ile Leu Glu Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe
705 710 715 720
Ala Val Lys Leu Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe
725 730 735
Ser Tyr Arg Glu Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser
740 745 750
Phe Ile Ser Thr Trp Trp Lys Glu Pro Leu Asn Ile Val Ser Phe Leu
755 760 765
Phe Cys Phe Ala Ser Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn
770 775 780
Leu Asn Ser Val Ser Val Pro Arg Met Val Ile Asn Val His Glu Ala
785 790 795 800
Gly Arg Asn Phe Thr Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile
805 810 815
Ile Cys Cys Thr Thr Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro
820 825 830
Leu Lys Thr Lys Ala Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr
835 840 845
Phe Asp Leu Ile Tyr Val His Asn Pro Val Phe Lys Pro Phe Glu Lys
850 855 860
Pro Val Met Ile Ser Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly
865 870 875 880
Asn Asp Ile Asp Pro Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly
885 890 895
Asn Lys Ser Cys Glu Asn Ile His Leu His Ser Glu Ala Val Leu Cys
900 905 910
Thr Val Pro Asn Asp Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu
915 920 925
Trp Lys Gln Ala Ile Ser Ser Thr Val Leu Gly Lys Val Ile Val Gln
930 935 940
Pro Asp Gln Asn Phe Thr Gly Leu Ile Ala Gly Val Val Ser Ile Ser
945 950 955 960
Thr Ala Leu Leu Leu Leu Leu Gly Phe Phe Leu Trp Leu Lys Lys Arg
965 970 975
Lys Gln Ile Lys Asp Leu Gly Ser Glu Leu Val Arg Tyr Asp Ala Arg
980 985 990
Val His Thr Pro His Leu Asp Arg Leu Val Ser Ala Arg Ser Val Ser
995 1000 1005
Pro Thr Thr Glu Met Val Ser Asn Glu Ser Val Asp Tyr Arg Ala
1010 1015 1020
Thr Phe Pro Glu Asp Gln Phe Pro Asn Ser Ser Gln Asn Gly Ser
1025 1030 1035
Cys Arg Gln Val Gln Tyr Pro Leu Thr Asp Met Ser Pro Ile Leu
1040 1045 1050
Thr Ser Gly Asp Ser Asp Ile Ser Ser Pro Leu Leu Gln Asn Thr
1055 1060 1065
Val His Ile Asp Leu Ser Ala Leu Asn Pro Glu Leu Val Gln Ala
1070 1075 1080
Val Gln His Val Val Ile Gly Pro Ser Ser Leu Ile Val His Phe
1085 1090 1095
Asn Glu Val Ile Gly Arg Gly His Phe Gly Cys Val Tyr His Gly
1100 1105 1110
Thr Leu Leu Asp Asn Asp Gly Lys Lys Ile His Cys Ala Val Lys
1115 1120 1125
Ser Leu Asn Arg Ile Thr Asp Ile Gly Glu Val Ser Gln Phe Leu
1130 1135 1140
Thr Glu Gly Ile Ile Met Lys Asp Phe Ser His Pro Asn Val Leu
1145 1150 1155
Ser Leu Leu Gly Ile Cys Leu Arg Ser Glu Gly Ser Pro Leu Val
1160 1165 1170
Val Leu Pro Tyr Met Lys His Gly Asp Leu Arg Asn Phe Ile Arg
1175 1180 1185
Asn Glu Thr His Asn Pro Thr Val Lys Asp Leu Ile Gly Phe Gly
1190 1195 1200
Leu Gln Val Ala Lys Gly Met Lys Tyr Leu Ala Ser Lys Lys Phe
1205 1210 1215
Val His Arg Asp Leu Ala Ala Arg Asn Cys Met Leu Asp Glu Lys
1220 1225 1230
Phe Thr Val Lys Val Ala Asp Phe Gly Leu Ala Arg Asp Met Tyr
1235 1240 1245
Asp Lys Glu Tyr Tyr Ser Val His Asn Lys Thr Gly Ala Lys Leu
1250 1255 1260
Pro Val Lys Trp Met Ala Leu Glu Ser Leu Gln Thr Gln Lys Phe
1265 1270 1275
Thr Thr Lys Ser Asp Val Trp Ser Phe Gly Val Leu Leu Trp Glu
1280 1285 1290
Leu Met Thr Arg Gly Ala Pro Pro Tyr Pro Asp Val Asn Thr Phe
1295 1300 1305
Asp Ile Thr Val Tyr Leu Leu Gln Gly Arg Arg Leu Leu Gln Pro
1310 1315 1320
Glu Tyr Cys Pro Asp Pro Leu Tyr Glu Val Met Leu Lys Cys Trp
1325 1330 1335
His Pro Lys Ala Glu Met Arg Pro Ser Phe Ser Glu Leu Val Ser
1340 1345 1350
Arg Ile Ser Ala Ile Phe Ser Thr Phe Ile Gly Glu His Tyr Val
1355 1360 1365
His Val Asn Ala Thr Tyr Val Asn Val Lys Cys Val Ala Pro Tyr
1370 1375 1380
Pro Ser Leu Leu Ser Ser Glu Asp Asn Ala Asp Asp Glu Val Asp
1385 1390 1395
Thr Arg Pro Ala Ser Phe Trp Glu Thr Ser
1400 1405
<210> 146
<211> 1390
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 146
Met Lys Ala Pro Ala Val Leu Ala Pro Gly Ile Leu Val Leu Leu Phe
1 5 10 15
Thr Leu Val Gln Arg Ser Asn Gly Glu Cys Lys Glu Ala Leu Ala Lys
20 25 30
Ser Glu Met Asn Val Asn Met Lys Tyr Gln Leu Pro Asn Phe Thr Ala
35 40 45
Glu Thr Pro Ile Gln Asn Val Ile Leu His Glu His His Ile Phe Leu
50 55 60
Gly Ala Thr Asn Tyr Ile Tyr Val Leu Asn Glu Glu Asp Leu Gln Lys
65 70 75 80
Val Ala Glu Tyr Lys Thr Gly Pro Val Leu Glu His Pro Asp Cys Phe
85 90 95
Pro Cys Gln Asp Cys Ser Ser Lys Ala Asn Leu Ser Gly Gly Val Trp
100 105 110
Lys Asp Asn Ile Asn Met Ala Leu Val Val Asp Thr Tyr Tyr Asp Asp
115 120 125
Gln Leu Ile Ser Cys Gly Ser Val Asn Arg Gly Thr Cys Gln Arg His
130 135 140
Val Phe Pro His Asn His Thr Ala Asp Ile Gln Ser Glu Val His Cys
145 150 155 160
Ile Phe Ser Pro Gln Ile Glu Glu Pro Ser Gln Cys Pro Asp Cys Val
165 170 175
Val Ser Ala Leu Gly Ala Lys Val Leu Ser Ser Val Lys Asp Arg Phe
180 185 190
Ile Asn Phe Phe Val Gly Asn Thr Ile Asn Ser Ser Tyr Phe Pro Asp
195 200 205
His Pro Leu His Ser Ile Ser Val Arg Arg Leu Lys Glu Thr Lys Asp
210 215 220
Gly Phe Met Phe Leu Thr Asp Gln Ser Tyr Ile Asp Val Leu Pro Glu
225 230 235 240
Phe Arg Asp Ser Tyr Pro Ile Lys Tyr Val His Ala Phe Glu Ser Asn
245 250 255
Asn Phe Ile Tyr Phe Leu Thr Val Gln Arg Glu Thr Leu Asp Ala Gln
260 265 270
Thr Phe His Thr Arg Ile Ile Arg Phe Cys Ser Ile Asn Ser Gly Leu
275 280 285
His Ser Tyr Met Glu Met Pro Leu Glu Cys Ile Leu Thr Glu Lys Arg
290 295 300
Lys Lys Arg Ser Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala
305 310 315 320
Tyr Val Ser Lys Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser
325 330 335
Leu Asn Asp Asp Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp
340 345 350
Ser Ala Glu Pro Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys
355 360 365
Tyr Val Asn Asp Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg
370 375 380
Cys Leu Gln His Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg
385 390 395 400
Thr Leu Leu Arg Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr
405 410 415
Arg Thr Glu Phe Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly
420 425 430
Gln Phe Ser Glu Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly
435 440 445
Asp Leu Thr Ile Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln
450 455 460
Val Val Val Ser Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu
465 470 475 480
Leu Asp Ser His Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu
485 490 495
Asn Gln Asn Gly Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys
500 505 510
Ile Pro Leu Asn Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln
515 520 525
Cys Leu Ser Ala Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys
530 535 540
Cys Val Arg Ser Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile
545 550 555 560
Cys Leu Pro Ala Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu
565 570 575
Gly Gly Thr Arg Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg
580 585 590
Asn Asn Lys Phe Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu
595 600 605
Ser Cys Thr Leu Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys
610 615 620
Thr Val Gly Pro Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile
625 630 635 640
Ser Asn Gly His Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp
645 650 655
Pro Val Ile Thr Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly
660 665 670
Thr Leu Leu Thr Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg
675 680 685
His Ile Ser Ile Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn
690 695 700
Ser Ile Leu Glu Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe
705 710 715 720
Ala Val Lys Leu Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe
725 730 735
Ser Tyr Arg Glu Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser
740 745 750
Phe Ile Ser Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn
755 760 765
Ser Val Ser Val Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg
770 775 780
Asn Phe Thr Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys
785 790 795 800
Cys Thr Thr Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys
805 810 815
Thr Lys Ala Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp
820 825 830
Leu Ile Tyr Val His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val
835 840 845
Met Ile Ser Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp
850 855 860
Ile Asp Pro Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys
865 870 875 880
Ser Cys Glu Asn Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val
885 890 895
Pro Asn Asp Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Trp Lys
900 905 910
Gln Ala Ile Ser Ser Thr Val Leu Gly Lys Val Ile Val Gln Pro Asp
915 920 925
Gln Asn Phe Thr Gly Leu Ile Ala Gly Val Val Ser Ile Ser Thr Ala
930 935 940
Leu Leu Leu Leu Leu Gly Phe Phe Leu Trp Leu Lys Lys Arg Lys Gln
945 950 955 960
Ile Lys Asp Leu Gly Ser Glu Leu Val Arg Tyr Asp Ala Arg Val His
965 970 975
Thr Pro His Leu Asp Arg Leu Val Ser Ala Arg Ser Val Ser Pro Thr
980 985 990
Thr Glu Met Val Ser Asn Glu Ser Val Asp Tyr Arg Ala Thr Phe Pro
995 1000 1005
Glu Asp Gln Phe Pro Asn Ser Ser Gln Asn Gly Ser Cys Arg Gln
1010 1015 1020
Val Gln Tyr Pro Leu Thr Asp Met Ser Pro Ile Leu Thr Ser Gly
1025 1030 1035
Asp Ser Asp Ile Ser Ser Pro Leu Leu Gln Asn Thr Val His Ile
1040 1045 1050
Asp Leu Ser Ala Leu Asn Pro Glu Leu Val Gln Ala Val Gln His
1055 1060 1065
Val Val Ile Gly Pro Ser Ser Leu Ile Val His Phe Asn Glu Val
1070 1075 1080
Ile Gly Arg Gly His Phe Gly Cys Val Tyr His Gly Thr Leu Leu
1085 1090 1095
Asp Asn Asp Gly Lys Lys Ile His Cys Ala Val Lys Ser Leu Asn
1100 1105 1110
Arg Ile Thr Asp Ile Gly Glu Val Ser Gln Phe Leu Thr Glu Gly
1115 1120 1125
Ile Ile Met Lys Asp Phe Ser His Pro Asn Val Leu Ser Leu Leu
1130 1135 1140
Gly Ile Cys Leu Arg Ser Glu Gly Ser Pro Leu Val Val Leu Pro
1145 1150 1155
Tyr Met Lys His Gly Asp Leu Arg Asn Phe Ile Arg Asn Glu Thr
1160 1165 1170
His Asn Pro Thr Val Lys Asp Leu Ile Gly Phe Gly Leu Gln Val
1175 1180 1185
Ala Lys Gly Met Lys Tyr Leu Ala Ser Lys Lys Phe Val His Arg
1190 1195 1200
Asp Leu Ala Ala Arg Asn Cys Met Leu Asp Glu Lys Phe Thr Val
1205 1210 1215
Lys Val Ala Asp Phe Gly Leu Ala Arg Asp Met Tyr Asp Lys Glu
1220 1225 1230
Tyr Tyr Ser Val His Asn Lys Thr Gly Ala Lys Leu Pro Val Lys
1235 1240 1245
Trp Met Ala Leu Glu Ser Leu Gln Thr Gln Lys Phe Thr Thr Lys
1250 1255 1260
Ser Asp Val Trp Ser Phe Gly Val Leu Leu Trp Glu Leu Met Thr
1265 1270 1275
Arg Gly Ala Pro Pro Tyr Pro Asp Val Asn Thr Phe Asp Ile Thr
1280 1285 1290
Val Tyr Leu Leu Gln Gly Arg Arg Leu Leu Gln Pro Glu Tyr Cys
1295 1300 1305
Pro Asp Pro Leu Tyr Glu Val Met Leu Lys Cys Trp His Pro Lys
1310 1315 1320
Ala Glu Met Arg Pro Ser Phe Ser Glu Leu Val Ser Arg Ile Ser
1325 1330 1335
Ala Ile Phe Ser Thr Phe Ile Gly Glu His Tyr Val His Val Asn
1340 1345 1350
Ala Thr Tyr Val Asn Val Lys Cys Val Ala Pro Tyr Pro Ser Leu
1355 1360 1365
Leu Ser Ser Glu Asp Asn Ala Asp Asp Glu Val Asp Thr Arg Pro
1370 1375 1380
Ala Ser Phe Trp Glu Thr Ser
1385 1390
<210> 147
<211> 934
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 147
Met Lys Ala Pro Ala Val Leu Ala Pro Gly Ile Leu Val Leu Leu Phe
1 5 10 15
Thr Leu Val Gln Arg Ser Asn Gly Glu Cys Lys Glu Ala Leu Ala Lys
20 25 30
Ser Glu Met Asn Val Asn Met Lys Tyr Gln Leu Pro Asn Phe Thr Ala
35 40 45
Glu Thr Pro Ile Gln Asn Val Ile Leu His Glu His His Ile Phe Leu
50 55 60
Gly Ala Thr Asn Tyr Ile Tyr Val Leu Asn Glu Glu Asp Leu Gln Lys
65 70 75 80
Val Ala Glu Tyr Lys Thr Gly Pro Val Leu Glu His Pro Asp Cys Phe
85 90 95
Pro Cys Gln Asp Cys Ser Ser Lys Ala Asn Leu Ser Gly Gly Val Trp
100 105 110
Lys Asp Asn Ile Asn Met Ala Leu Val Val Asp Thr Tyr Tyr Asp Asp
115 120 125
Gln Leu Ile Ser Cys Gly Ser Val Asn Arg Gly Thr Cys Gln Arg His
130 135 140
Val Phe Pro His Asn His Thr Ala Asp Ile Gln Ser Glu Val His Cys
145 150 155 160
Ile Phe Ser Pro Gln Ile Glu Glu Pro Ser Gln Cys Pro Asp Cys Val
165 170 175
Val Ser Ala Leu Gly Ala Lys Val Leu Ser Ser Val Lys Asp Arg Phe
180 185 190
Ile Asn Phe Phe Val Gly Asn Thr Ile Asn Ser Ser Tyr Phe Pro Asp
195 200 205
His Pro Leu His Ser Ile Ser Val Arg Arg Leu Lys Glu Thr Lys Asp
210 215 220
Gly Phe Met Phe Leu Thr Asp Gln Ser Tyr Ile Asp Val Leu Pro Glu
225 230 235 240
Phe Arg Asp Ser Tyr Pro Ile Lys Tyr Val His Ala Phe Glu Ser Asn
245 250 255
Asn Phe Ile Tyr Phe Leu Thr Val Gln Arg Glu Thr Leu Asp Ala Gln
260 265 270
Thr Phe His Thr Arg Ile Ile Arg Phe Cys Ser Ile Asn Ser Gly Leu
275 280 285
His Ser Tyr Met Glu Met Pro Leu Glu Cys Ile Leu Thr Glu Lys Arg
290 295 300
Lys Lys Arg Ser Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala
305 310 315 320
Tyr Val Ser Lys Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser
325 330 335
Leu Asn Asp Asp Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp
340 345 350
Ser Ala Glu Pro Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys
355 360 365
Tyr Val Asn Asp Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg
370 375 380
Cys Leu Gln His Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg
385 390 395 400
Thr Leu Leu Arg Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr
405 410 415
Arg Thr Glu Phe Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly
420 425 430
Gln Phe Ser Glu Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly
435 440 445
Asp Leu Thr Ile Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln
450 455 460
Val Val Val Ser Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu
465 470 475 480
Leu Asp Ser His Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu
485 490 495
Asn Gln Asn Gly Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys
500 505 510
Ile Pro Leu Asn Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln
515 520 525
Cys Leu Ser Ala Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys
530 535 540
Cys Val Arg Ser Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile
545 550 555 560
Cys Leu Pro Ala Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu
565 570 575
Gly Gly Thr Arg Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg
580 585 590
Asn Asn Lys Phe Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu
595 600 605
Ser Cys Thr Leu Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys
610 615 620
Thr Val Gly Pro Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile
625 630 635 640
Ser Asn Gly His Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp
645 650 655
Pro Val Ile Thr Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly
660 665 670
Thr Leu Leu Thr Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg
675 680 685
His Ile Ser Ile Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn
690 695 700
Ser Ile Leu Glu Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe
705 710 715 720
Ala Val Lys Leu Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe
725 730 735
Ser Tyr Arg Glu Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser
740 745 750
Phe Ile Ser Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn
755 760 765
Ser Val Ser Val Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg
770 775 780
Asn Phe Thr Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys
785 790 795 800
Cys Thr Thr Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys
805 810 815
Thr Lys Ala Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp
820 825 830
Leu Ile Tyr Val His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val
835 840 845
Met Ile Ser Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp
850 855 860
Ile Asp Pro Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys
865 870 875 880
Ser Cys Glu Asn Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val
885 890 895
Pro Asn Asp Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Val Gly
900 905 910
Phe Leu His Ser Ser His Asp Val Asn Lys Glu Ala Ser Val Ile Met
915 920 925
Leu Phe Ser Gly Leu Lys
930
<210> 148
<211> 281
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 148
Lys Glu Ala Leu Ala Lys Ser Glu Met Asn Val Asn Met Lys Tyr Gln
1 5 10 15
Leu Pro Asn Phe Thr Ala Glu Thr Pro Ile Gln Asn Val Ile Leu His
20 25 30
Glu His His Ile Phe Leu Gly Ala Thr Asn Tyr Ile Tyr Val Leu Asn
35 40 45
Glu Glu Asp Leu Gln Lys Val Ala Glu Tyr Lys Thr Gly Pro Val Leu
50 55 60
Glu His Pro Asp Cys Phe Pro Cys Gln Asp Cys Ser Ser Lys Ala Asn
65 70 75 80
Leu Ser Gly Gly Val Trp Lys Asp Asn Ile Asn Met Ala Leu Val Val
85 90 95
Asp Thr Tyr Tyr Asp Asp Gln Leu Ile Ser Cys Gly Ser Val Asn Arg
100 105 110
Gly Thr Cys Gln Arg His Val Phe Pro His Asn His Thr Ala Asp Ile
115 120 125
Gln Ser Glu Val His Cys Ile Phe Ser Pro Gln Ile Glu Glu Pro Ser
130 135 140
Gln Cys Pro Asp Cys Val Val Ser Ala Leu Gly Ala Lys Val Leu Ser
145 150 155 160
Ser Val Lys Asp Arg Phe Ile Asn Phe Phe Val Gly Asn Thr Ile Asn
165 170 175
Ser Ser Tyr Phe Pro Asp His Pro Leu His Ser Ile Ser Val Arg Arg
180 185 190
Leu Lys Glu Thr Lys Asp Gly Phe Met Phe Leu Thr Asp Gln Ser Tyr
195 200 205
Ile Asp Val Leu Pro Glu Phe Arg Asp Ser Tyr Pro Ile Lys Tyr Val
210 215 220
His Ala Phe Glu Ser Asn Asn Phe Ile Tyr Phe Leu Thr Val Gln Arg
225 230 235 240
Glu Thr Leu Asp Ala Gln Thr Phe His Thr Arg Ile Ile Arg Phe Cys
245 250 255
Ser Ile Asn Ser Gly Leu His Ser Tyr Met Glu Met Pro Leu Glu Cys
260 265 270
Ile Leu Thr Glu Lys Arg Lys Lys Arg
275 280
<210> 149
<211> 1101
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 149
Ser Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser
1 5 10 15
Lys Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp
20 25 30
Asp Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu
35 40 45
Pro Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn
50 55 60
Asp Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln
65 70 75 80
His Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg Thr Leu Leu
85 90 95
Arg Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu
100 105 110
Phe Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser
115 120 125
Glu Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr
130 135 140
Ile Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln Val Val Val
145 150 155 160
Ser Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser
165 170 175
His Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu Asn Gln Asn
180 185 190
Gly Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu
195 200 205
Asn Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser
210 215 220
Ala Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg
225 230 235 240
Ser Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro
245 250 255
Ala Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr
260 265 270
Arg Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys
275 280 285
Phe Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr
290 295 300
Leu Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly
305 310 315 320
Pro Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly
325 330 335
His Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile
340 345 350
Thr Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu
355 360 365
Thr Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser
370 375 380
Ile Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu
385 390 395 400
Glu Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys
405 410 415
Leu Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg
420 425 430
Glu Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser
435 440 445
Thr Trp Trp Lys Glu Pro Leu Asn Ile Val Ser Phe Leu Phe Cys Phe
450 455 460
Ala Ser Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn Ser
465 470 475 480
Val Ser Val Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg Asn
485 490 495
Phe Thr Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys Cys
500 505 510
Thr Thr Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys Thr
515 520 525
Lys Ala Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp Leu
530 535 540
Ile Tyr Val His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val Met
545 550 555 560
Ile Ser Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp Ile
565 570 575
Asp Pro Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys Ser
580 585 590
Cys Glu Asn Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val Pro
595 600 605
Asn Asp Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Trp Lys Gln
610 615 620
Ala Ile Ser Ser Thr Val Leu Gly Lys Val Ile Val Gln Pro Asp Gln
625 630 635 640
Asn Phe Thr Gly Leu Ile Ala Gly Val Val Ser Ile Ser Thr Ala Leu
645 650 655
Leu Leu Leu Leu Gly Phe Phe Leu Trp Leu Lys Lys Arg Lys Gln Ile
660 665 670
Lys Asp Leu Gly Ser Glu Leu Val Arg Tyr Asp Ala Arg Val His Thr
675 680 685
Pro His Leu Asp Arg Leu Val Ser Ala Arg Ser Val Ser Pro Thr Thr
690 695 700
Glu Met Val Ser Asn Glu Ser Val Asp Tyr Arg Ala Thr Phe Pro Glu
705 710 715 720
Asp Gln Phe Pro Asn Ser Ser Gln Asn Gly Ser Cys Arg Gln Val Gln
725 730 735
Tyr Pro Leu Thr Asp Met Ser Pro Ile Leu Thr Ser Gly Asp Ser Asp
740 745 750
Ile Ser Ser Pro Leu Leu Gln Asn Thr Val His Ile Asp Leu Ser Ala
755 760 765
Leu Asn Pro Glu Leu Val Gln Ala Val Gln His Val Val Ile Gly Pro
770 775 780
Ser Ser Leu Ile Val His Phe Asn Glu Val Ile Gly Arg Gly His Phe
785 790 795 800
Gly Cys Val Tyr His Gly Thr Leu Leu Asp Asn Asp Gly Lys Lys Ile
805 810 815
His Cys Ala Val Lys Ser Leu Asn Arg Ile Thr Asp Ile Gly Glu Val
820 825 830
Ser Gln Phe Leu Thr Glu Gly Ile Ile Met Lys Asp Phe Ser His Pro
835 840 845
Asn Val Leu Ser Leu Leu Gly Ile Cys Leu Arg Ser Glu Gly Ser Pro
850 855 860
Leu Val Val Leu Pro Tyr Met Lys His Gly Asp Leu Arg Asn Phe Ile
865 870 875 880
Arg Asn Glu Thr His Asn Pro Thr Val Lys Asp Leu Ile Gly Phe Gly
885 890 895
Leu Gln Val Ala Lys Gly Met Lys Tyr Leu Ala Ser Lys Lys Phe Val
900 905 910
His Arg Asp Leu Ala Ala Arg Asn Cys Met Leu Asp Glu Lys Phe Thr
915 920 925
Val Lys Val Ala Asp Phe Gly Leu Ala Arg Asp Met Tyr Asp Lys Glu
930 935 940
Tyr Tyr Ser Val His Asn Lys Thr Gly Ala Lys Leu Pro Val Lys Trp
945 950 955 960
Met Ala Leu Glu Ser Leu Gln Thr Gln Lys Phe Thr Thr Lys Ser Asp
965 970 975
Val Trp Ser Phe Gly Val Leu Leu Trp Glu Leu Met Thr Arg Gly Ala
980 985 990
Pro Pro Tyr Pro Asp Val Asn Thr Phe Asp Ile Thr Val Tyr Leu Leu
995 1000 1005
Gln Gly Arg Arg Leu Leu Gln Pro Glu Tyr Cys Pro Asp Pro Leu
1010 1015 1020
Tyr Glu Val Met Leu Lys Cys Trp His Pro Lys Ala Glu Met Arg
1025 1030 1035
Pro Ser Phe Ser Glu Leu Val Ser Arg Ile Ser Ala Ile Phe Ser
1040 1045 1050
Thr Phe Ile Gly Glu His Tyr Val His Val Asn Ala Thr Tyr Val
1055 1060 1065
Asn Val Lys Cys Val Ala Pro Tyr Pro Ser Leu Leu Ser Ser Glu
1070 1075 1080
Asp Asn Ala Asp Asp Glu Val Asp Thr Arg Pro Ala Ser Phe Trp
1085 1090 1095
Glu Thr Ser
1100
<210> 150
<211> 1082
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 150
Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys
1 5 10 15
Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp
20 25 30
Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro
35 40 45
Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp
50 55 60
Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His
65 70 75 80
Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg
85 90 95
Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe
100 105 110
Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu
115 120 125
Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile
130 135 140
Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser
145 150 155 160
Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His
165 170 175
Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly
180 185 190
Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn
195 200 205
Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala
210 215 220
Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser
225 230 235 240
Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala
245 250 255
Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg
260 265 270
Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe
275 280 285
Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu
290 295 300
Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro
305 310 315 320
Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His
325 330 335
Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr
340 345 350
Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr
355 360 365
Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile
370 375 380
Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu
385 390 395 400
Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu
405 410 415
Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu
420 425 430
Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Gly
435 440 445
Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn Ser Val Ser Val
450 455 460
Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg Asn Phe Thr Val
465 470 475 480
Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr Thr Pro
485 490 495
Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys Ala Phe
500 505 510
Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile Tyr Val
515 520 525
His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val Met Ile Ser Met
530 535 540
Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp Ile Asp Pro Glu
545 550 555 560
Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys Ser Cys Glu Asn
565 570 575
Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val Pro Asn Asp Leu
580 585 590
Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala Ile Ser
595 600 605
Ser Thr Val Leu Gly Lys Val Ile Val Gln Pro Asp Gln Asn Phe Thr
610 615 620
Gly Leu Ile Ala Gly Val Val Ser Ile Ser Thr Ala Leu Leu Leu Leu
625 630 635 640
Leu Gly Phe Phe Leu Trp Leu Lys Lys Arg Lys Gln Ile Lys Asp Leu
645 650 655
Gly Ser Glu Leu Val Arg Tyr Asp Ala Arg Val His Thr Pro His Leu
660 665 670
Asp Arg Leu Val Ser Ala Arg Ser Val Ser Pro Thr Thr Glu Met Val
675 680 685
Ser Asn Glu Ser Val Asp Tyr Arg Ala Thr Phe Pro Glu Asp Gln Phe
690 695 700
Pro Asn Ser Ser Gln Asn Gly Ser Cys Arg Gln Val Gln Tyr Pro Leu
705 710 715 720
Thr Asp Met Ser Pro Ile Leu Thr Ser Gly Asp Ser Asp Ile Ser Ser
725 730 735
Pro Leu Leu Gln Asn Thr Val His Ile Asp Leu Ser Ala Leu Asn Pro
740 745 750
Glu Leu Val Gln Ala Val Gln His Val Val Ile Gly Pro Ser Ser Leu
755 760 765
Ile Val His Phe Asn Glu Val Ile Gly Arg Gly His Phe Gly Cys Val
770 775 780
Tyr His Gly Thr Leu Leu Asp Asn Asp Gly Lys Lys Ile His Cys Ala
785 790 795 800
Val Lys Ser Leu Asn Arg Ile Thr Asp Ile Gly Glu Val Ser Gln Phe
805 810 815
Leu Thr Glu Gly Ile Ile Met Lys Asp Phe Ser His Pro Asn Val Leu
820 825 830
Ser Leu Leu Gly Ile Cys Leu Arg Ser Glu Gly Ser Pro Leu Val Val
835 840 845
Leu Pro Tyr Met Lys His Gly Asp Leu Arg Asn Phe Ile Arg Asn Glu
850 855 860
Thr His Asn Pro Thr Val Lys Asp Leu Ile Gly Phe Gly Leu Gln Val
865 870 875 880
Ala Lys Gly Met Lys Tyr Leu Ala Ser Lys Lys Phe Val His Arg Asp
885 890 895
Leu Ala Ala Arg Asn Cys Met Leu Asp Glu Lys Phe Thr Val Lys Val
900 905 910
Ala Asp Phe Gly Leu Ala Arg Asp Met Tyr Asp Lys Glu Tyr Tyr Ser
915 920 925
Val His Asn Lys Thr Gly Ala Lys Leu Pro Val Lys Trp Met Ala Leu
930 935 940
Glu Ser Leu Gln Thr Gln Lys Phe Thr Thr Lys Ser Asp Val Trp Ser
945 950 955 960
Phe Gly Val Leu Leu Trp Glu Leu Met Thr Arg Gly Ala Pro Pro Tyr
965 970 975
Pro Asp Val Asn Thr Phe Asp Ile Thr Val Tyr Leu Leu Gln Gly Arg
980 985 990
Arg Leu Leu Gln Pro Glu Tyr Cys Pro Asp Pro Leu Tyr Glu Val Met
995 1000 1005
Leu Lys Cys Trp His Pro Lys Ala Glu Met Arg Pro Ser Phe Ser
1010 1015 1020
Glu Leu Val Ser Arg Ile Ser Ala Ile Phe Ser Thr Phe Ile Gly
1025 1030 1035
Glu His Tyr Val His Val Asn Ala Thr Tyr Val Asn Val Lys Cys
1040 1045 1050
Val Ala Pro Tyr Pro Ser Leu Leu Ser Ser Glu Asp Asn Ala Asp
1055 1060 1065
Asp Glu Val Asp Thr Arg Pro Ala Ser Phe Trp Glu Thr Ser
1070 1075 1080
<210> 151
<211> 626
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 151
Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys
1 5 10 15
Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp
20 25 30
Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro
35 40 45
Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp
50 55 60
Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His
65 70 75 80
Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg
85 90 95
Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe
100 105 110
Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu
115 120 125
Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile
130 135 140
Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser
145 150 155 160
Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His
165 170 175
Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly
180 185 190
Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn
195 200 205
Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala
210 215 220
Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser
225 230 235 240
Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala
245 250 255
Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg
260 265 270
Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe
275 280 285
Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu
290 295 300
Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro
305 310 315 320
Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His
325 330 335
Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr
340 345 350
Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr
355 360 365
Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile
370 375 380
Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu
385 390 395 400
Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu
405 410 415
Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu
420 425 430
Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Gly
435 440 445
Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn Ser Val Ser Val
450 455 460
Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg Asn Phe Thr Val
465 470 475 480
Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr Thr Pro
485 490 495
Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys Ala Phe
500 505 510
Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile Tyr Val
515 520 525
His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val Met Ile Ser Met
530 535 540
Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp Ile Asp Pro Glu
545 550 555 560
Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys Ser Cys Glu Asn
565 570 575
Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val Pro Asn Asp Leu
580 585 590
Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Val Gly Phe Leu His Ser
595 600 605
Ser His Asp Val Asn Lys Glu Ala Ser Val Ile Met Leu Phe Ser Gly
610 615 620
Leu Lys
625
<210> 152
<211> 650
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 152
Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys
1 5 10 15
Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp
20 25 30
Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro
35 40 45
Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp
50 55 60
Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His
65 70 75 80
Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg
85 90 95
Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe
100 105 110
Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu
115 120 125
Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile
130 135 140
Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser
145 150 155 160
Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His
165 170 175
Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly
180 185 190
Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn
195 200 205
Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala
210 215 220
Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser
225 230 235 240
Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala
245 250 255
Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg
260 265 270
Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe
275 280 285
Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu
290 295 300
Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro
305 310 315 320
Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His
325 330 335
Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr
340 345 350
Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr
355 360 365
Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile
370 375 380
Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu
385 390 395 400
Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu
405 410 415
Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu
420 425 430
Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Thr
435 440 445
Trp Trp Lys Glu Pro Leu Asn Ile Val Ser Phe Leu Phe Cys Phe Ala
450 455 460
Ser Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn Ser Val
465 470 475 480
Ser Val Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg Asn Phe
485 490 495
Thr Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr
500 505 510
Thr Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys
515 520 525
Ala Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile
530 535 540
Tyr Val His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val Met Ile
545 550 555 560
Ser Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp Ile Asp
565 570 575
Pro Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys Ser Cys
580 585 590
Glu Asn Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val Pro Asn
595 600 605
Asp Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala
610 615 620
Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Glu Gln Lys Leu Ile Ser
625 630 635 640
Glu Glu Asp Leu His His His His His His
645 650
<210> 153
<211> 838
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 153
Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys
1 5 10 15
Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp
20 25 30
Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro
35 40 45
Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp
50 55 60
Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His
65 70 75 80
Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg
85 90 95
Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe
100 105 110
Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu
115 120 125
Val Leu Leu Thr Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile
130 135 140
Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser
145 150 155 160
Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His
165 170 175
Pro Val Ser Pro Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly
180 185 190
Tyr Thr Leu Val Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn
195 200 205
Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala
210 215 220
Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser
225 230 235 240
Glu Glu Cys Leu Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala
245 250 255
Ile Tyr Lys Val Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg
260 265 270
Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe
275 280 285
Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu
290 295 300
Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro
305 310 315 320
Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His
325 330 335
Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr
340 345 350
Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr
355 360 365
Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile
370 375 380
Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu
385 390 395 400
Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu
405 410 415
Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu
420 425 430
Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Thr
435 440 445
Trp Trp Lys Glu Pro Leu Asn Ile Val Ser Phe Leu Phe Cys Phe Ala
450 455 460
Ser Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu Asn Ser Val
465 470 475 480
Ser Val Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg Asn Phe
485 490 495
Thr Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr
500 505 510
Thr Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys
515 520 525
Ala Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile
530 535 540
Tyr Val His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val Met Ile
545 550 555 560
Ser Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp Ile Asp
565 570 575
Pro Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys Ser Cys
580 585 590
Glu Asn Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val Pro Asn
595 600 605
Asp Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala
610 615 620
Met Glu Val Ser Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Val
625 630 635 640
Leu Thr Ile Thr Leu Thr Pro Lys Val Thr Cys Val Val Val Asp Ile
645 650 655
Ser Lys Asp Asp Pro Glu Val Gln Phe Ser Trp Phe Val Asp Asp Val
660 665 670
Glu Val His Thr Ala Gln Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser
675 680 685
Thr Phe Arg Ser Val Ser Glu Leu Pro Ile Met His Gln Asp Trp Leu
690 695 700
Asn Gly Lys Glu Phe Lys Cys Arg Val Asn Ser Ala Ala Phe Pro Ala
705 710 715 720
Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro
725 730 735
Gln Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met Ala Lys Asp Lys
740 745 750
Val Ser Leu Thr Cys Met Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr
755 760 765
Val Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr
770 775 780
Gln Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu
785 790 795 800
Asn Val Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser
805 810 815
Val Leu His Glu Gly Leu His Asn His His Thr Glu Lys Ser Leu Ser
820 825 830
His Ser Pro Gly Lys Glu
835
<210> 154
<211> 1100
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 154
Ser Thr Lys Lys Glu Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser
1 5 10 15
Lys Pro Gly Ala Gln Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp
20 25 30
Asp Ile Leu Phe Gly Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu
35 40 45
Pro Met Asp Arg Ser Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn
50 55 60
Asp Phe Phe Asn Lys Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln
65 70 75 80
His Phe Tyr Gly Pro Asn His Glu His Cys Phe Asn Arg Thr Leu Leu
85 90 95
Arg Asn Ser Ser Gly Cys Glu Ala Arg Arg Asp Glu Tyr Arg Ala Glu
100 105 110
Phe Thr Thr Ala Leu Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser
115 120 125
Glu Val Leu Leu Thr Ser Ile Ser Thr Phe Val Lys Gly Asp Leu Thr
130 135 140
Ile Ala Asn Leu Gly Thr Ser Glu Gly Arg Phe Met Gln Val Val Val
145 150 155 160
Ser Arg Ser Gly Pro Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser
165 170 175
His Pro Val Ser Pro Glu Val Ile Val Glu His Pro Leu Asn Gln Asn
180 185 190
Gly Tyr Thr Leu Val Val Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu
195 200 205
Asn Gly Leu Gly Cys Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser
210 215 220
Ala Pro Pro Phe Val Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg
225 230 235 240
Ser Glu Glu Cys Pro Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro
245 250 255
Ala Ile Tyr Lys Val Phe Pro Thr Ser Ala Pro Leu Glu Gly Gly Thr
260 265 270
Arg Leu Thr Ile Cys Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys
275 280 285
Phe Asp Leu Lys Lys Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr
290 295 300
Leu Thr Leu Ser Glu Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly
305 310 315 320
Pro Ala Met Asn Lys His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly
325 330 335
His Gly Thr Thr Gln Tyr Ser Thr Phe Ser Tyr Val Asp Pro Ile Ile
340 345 350
Thr Ser Ile Ser Pro Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu
355 360 365
Thr Leu Thr Gly Asn Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser
370 375 380
Ile Gly Gly Lys Thr Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu
385 390 395 400
Glu Cys Tyr Thr Pro Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys
405 410 415
Leu Lys Ile Asp Leu Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg
420 425 430
Glu Asp Pro Ile Val Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser
435 440 445
Gly Gly Ser Thr Ile Thr Gly Val Gly Lys Asn Leu His Ser Val Ser
450 455 460
Val Pro Arg Met Val Ile Asn Val His Glu Ala Gly Arg Asn Phe Thr
465 470 475 480
Val Ala Cys Gln His Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr Thr
485 490 495
Pro Ser Leu Gln Gln Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys Ala
500 505 510
Phe Phe Met Leu Asp Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile Tyr
515 520 525
Val His Asn Pro Val Phe Lys Pro Phe Glu Lys Pro Val Met Ile Ser
530 535 540
Met Gly Asn Glu Asn Val Leu Glu Ile Lys Gly Asn Asp Ile Asp Pro
545 550 555 560
Glu Ala Val Lys Gly Glu Val Leu Lys Val Gly Asn Lys Ser Cys Glu
565 570 575
Asn Ile His Leu His Ser Glu Ala Val Leu Cys Thr Val Pro Asn Asp
580 585 590
Leu Leu Lys Leu Asn Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala Ile
595 600 605
Ser Ser Thr Val Leu Gly Lys Val Ile Val Gln Pro Asp Gln Asn Phe
610 615 620
Thr Gly Leu Ile Ala Gly Val Val Ser Ile Ser Ile Ala Leu Leu Leu
625 630 635 640
Leu Leu Gly Leu Phe Leu Trp Leu Lys Lys Arg Lys Gln Ile Lys Asp
645 650 655
Leu Gly Ser Glu Leu Val Arg Tyr Asp Ala Arg Val His Thr Pro His
660 665 670
Leu Asp Arg Leu Val Ser Ala Arg Ser Val Ser Pro Thr Thr Glu Met
675 680 685
Val Ser Asn Glu Ser Val Asp Tyr Arg Ala Thr Phe Pro Glu Asp Gln
690 695 700
Phe Pro Asn Ser Ser Gln Asn Gly Ser Cys Arg Gln Val Gln Tyr Pro
705 710 715 720
Leu Thr Asp Met Ser Pro Ile Leu Thr Ser Gly Asp Ser Asp Ile Ser
725 730 735
Ser Pro Leu Leu Gln Asn Thr Val His Ile Asp Leu Ser Ala Leu Asn
740 745 750
Pro Glu Leu Val Gln Ala Val Gln His Val Val Ile Gly Pro Ser Ser
755 760 765
Leu Ile Val His Phe Asn Glu Val Ile Gly Arg Gly His Phe Gly Cys
770 775 780
Val Tyr His Gly Thr Leu Leu Asp Asn Asp Gly Lys Lys Ile His Cys
785 790 795 800
Ala Val Lys Ser Leu Asn Arg Ile Thr Asp Ile Gly Glu Val Ser Gln
805 810 815
Phe Leu Thr Glu Gly Ile Ile Met Lys Asp Phe Ser His Pro Asn Val
820 825 830
Leu Ser Leu Leu Gly Ile Cys Leu Arg Ser Glu Gly Ser Pro Leu Val
835 840 845
Val Leu Pro Tyr Met Lys His Gly Asp Leu Arg Asn Phe Ile Arg Asn
850 855 860
Glu Thr His Asn Pro Thr Val Lys Asp Leu Ile Gly Phe Gly Leu Gln
865 870 875 880
Val Ala Lys Gly Met Lys Tyr Leu Ala Ser Lys Lys Phe Val His Arg
885 890 895
Asp Leu Ala Ala Arg Asn Cys Met Leu Asp Glu Lys Phe Thr Val Lys
900 905 910
Val Ala Asp Phe Gly Leu Ala Arg Asp Met Tyr Asp Lys Glu Tyr Tyr
915 920 925
Ser Val His Asn Lys Thr Gly Ala Lys Leu Pro Val Lys Trp Met Ala
930 935 940
Leu Glu Ser Leu Gln Thr Gln Lys Phe Thr Thr Lys Ser Asp Val Trp
945 950 955 960
Ser Phe Gly Val Leu Leu Trp Glu Leu Met Thr Arg Gly Ala Pro Pro
965 970 975
Tyr Pro Asp Val Asn Thr Phe Asp Ile Thr Val Tyr Leu Leu Gln Gly
980 985 990
Arg Arg Leu Leu Gln Pro Glu Tyr Cys Pro Asp Pro Leu Tyr Glu Val
995 1000 1005
Met Leu Lys Cys Trp His Pro Lys Ala Glu Met Arg Pro Ser Phe
1010 1015 1020
Ser Glu Leu Val Ser Arg Ile Ser Ala Ile Phe Ser Thr Phe Ile
1025 1030 1035
Gly Glu His Tyr Val His Val Asn Ala Thr Tyr Val Asn Val Lys
1040 1045 1050
Cys Val Ala Pro Tyr Pro Ser Leu Leu Ser Ser Glu Asp Asn Ala
1055 1060 1065
Asp Asp Glu Val Asp Thr Glu Gln Lys Leu Ile Ser Glu Glu Asp
1070 1075 1080
Leu Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu His His His His
1085 1090 1095
His His
1100
<210> 155
<211> 936
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 155
Glu Cys Lys Glu Ala Leu Ala Lys Ser Glu Met Asn Val Asn Met Lys
1 5 10 15
Tyr Gln Leu Pro Asn Phe Thr Ala Glu Thr Pro Ile Gln Asn Val Ile
20 25 30
Leu His Glu His His Ile Phe Leu Gly Ala Thr Asn Tyr Ile Tyr Val
35 40 45
Leu Asn Glu Glu Asp Leu Gln Lys Val Ala Glu Tyr Lys Thr Gly Pro
50 55 60
Val Leu Glu His Pro Asp Cys Phe Pro Cys Gln Asp Cys Ser Ser Lys
65 70 75 80
Ala Asn Leu Ser Gly Gly Val Trp Lys Asp Asn Ile Asn Met Ala Leu
85 90 95
Val Val Asp Thr Tyr Tyr Asp Asp Gln Leu Ile Ser Cys Gly Ser Val
100 105 110
Asn Arg Gly Thr Cys Gln Arg His Val Phe Pro His Asn His Thr Ala
115 120 125
Asp Ile Gln Ser Glu Val His Cys Ile Phe Ser Pro Gln Ile Glu Glu
130 135 140
Pro Ser Gln Cys Pro Asp Cys Val Val Ser Ala Leu Gly Ala Lys Val
145 150 155 160
Leu Ser Ser Val Lys Asp Arg Phe Ile Asn Phe Phe Val Gly Asn Thr
165 170 175
Ile Asn Ser Ser Tyr Phe Pro Asp His Pro Leu His Ser Ile Ser Val
180 185 190
Arg Arg Leu Lys Glu Thr Lys Asp Gly Phe Met Phe Leu Thr Asp Gln
195 200 205
Ser Tyr Ile Asp Val Leu Pro Glu Phe Arg Asp Ser Tyr Pro Ile Lys
210 215 220
Tyr Val His Ala Phe Glu Ser Asn Asn Phe Ile Tyr Phe Leu Thr Val
225 230 235 240
Gln Arg Glu Thr Leu Asp Ala Gln Thr Phe His Thr Arg Ile Ile Arg
245 250 255
Phe Cys Ser Ile Asn Ser Gly Leu His Ser Tyr Met Glu Met Pro Leu
260 265 270
Glu Cys Ile Leu Thr Glu Lys Arg Lys Lys Arg Ser Thr Lys Lys Glu
275 280 285
Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys Pro Gly Ala Gln
290 295 300
Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp Ile Leu Phe Gly
305 310 315 320
Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro Met Asp Arg Ser
325 330 335
Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp Phe Phe Asn Lys
340 345 350
Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His Phe Tyr Gly Pro
355 360 365
Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg Asn Ser Ser Gly
370 375 380
Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe Thr Thr Ala Leu
385 390 395 400
Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu Val Leu Leu Thr
405 410 415
Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile Ala Asn Leu Gly
420 425 430
Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser Arg Ser Gly Pro
435 440 445
Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His Pro Val Ser Pro
450 455 460
Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly Tyr Thr Leu Val
465 470 475 480
Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn Gly Leu Gly Cys
485 490 495
Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala Pro Pro Phe Val
500 505 510
Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser Glu Glu Cys Leu
515 520 525
Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala Ile Tyr Lys Val
530 535 540
Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg Leu Thr Ile Cys
545 550 555 560
Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe Asp Leu Lys Lys
565 570 575
Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu Thr Leu Ser Glu
580 585 590
Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro Ala Met Asn Lys
595 600 605
His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His Gly Thr Thr Gln
610 615 620
Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr Ser Ile Ser Pro
625 630 635 640
Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr Leu Thr Gly Asn
645 650 655
Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile Gly Gly Lys Thr
660 665 670
Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu Cys Tyr Thr Pro
675 680 685
Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu Lys Ile Asp Leu
690 695 700
Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu Asp Pro Ile Val
705 710 715 720
Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Gly Gly Ser Thr Ile
725 730 735
Thr Gly Val Gly Lys Asn Leu Asn Ser Val Ser Val Pro Arg Met Val
740 745 750
Ile Asn Val His Glu Ala Gly Arg Asn Phe Thr Val Ala Cys Gln His
755 760 765
Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr Thr Pro Ser Leu Gln Gln
770 775 780
Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys Ala Phe Phe Met Leu Asp
785 790 795 800
Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile Tyr Val His Asn Pro Val
805 810 815
Phe Lys Pro Phe Glu Lys Pro Val Met Ile Ser Met Gly Asn Glu Asn
820 825 830
Val Leu Glu Ile Lys Gly Asn Asp Ile Asp Pro Glu Ala Val Lys Gly
835 840 845
Glu Val Leu Lys Val Gly Asn Lys Ser Cys Glu Asn Ile His Leu His
850 855 860
Ser Glu Ala Val Leu Cys Thr Val Pro Asn Asp Leu Leu Lys Leu Asn
865 870 875 880
Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala Ile Ser Ser Thr Val Leu
885 890 895
Gly Lys Val Ile Val Gln Pro Asp Gln Asn Phe Thr Glu Gln Lys Leu
900 905 910
Ile Ser Glu Glu Asp Leu Gly Gly Glu Gln Lys Leu Ile Ser Glu Glu
915 920 925
Asp Leu His His His His His His
930 935
<210> 156
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 156
Val Arg Arg Leu Lys Glu Thr Lys Asp Gly Phe Met Phe
1 5 10
<210> 157
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 157
Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp
1 5 10
<210> 158
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 158
Phe Ile Lys Gly Asp Leu Thr Ile Ala Asn Leu Gly Thr Ser Glu Gly
1 5 10 15
Arg Phe Met Gln Val Val Val Ser Arg Ser Gly Pro Ser Thr Pro His
20 25 30
Val Asn Phe
35
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2837821C1 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2808030C2 |
| ИММУНОАКТИВИРУЮЩАЯ АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА | 2015 |
|
RU2722788C2 |
| АНТИ-МЕТ АНТИТЕЛА И ИХ ИСПОЛЬЗОВАНИЕ | 2017 |
|
RU2765267C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С GPRC5D | 2020 |
|
RU2841523C2 |
| АНТИ-ROR1/АНТИ-CD3 БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2020 |
|
RU2831608C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, СПЕЦИФИЧЕСКИ СВЯЗЫВАЮЩИЕСЯ С PD1 И LAG3 | 2018 |
|
RU2778805C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СОДЕРЖАЩИЕ АНТИ-FAP КЛОН 212 | 2019 |
|
RU2799429C2 |
| УЛУЧШЕННЫЕ АНТИ-FLT3 АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ | 2019 |
|
RU2830982C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С GPRC5D | 2019 |
|
RU2797268C2 |

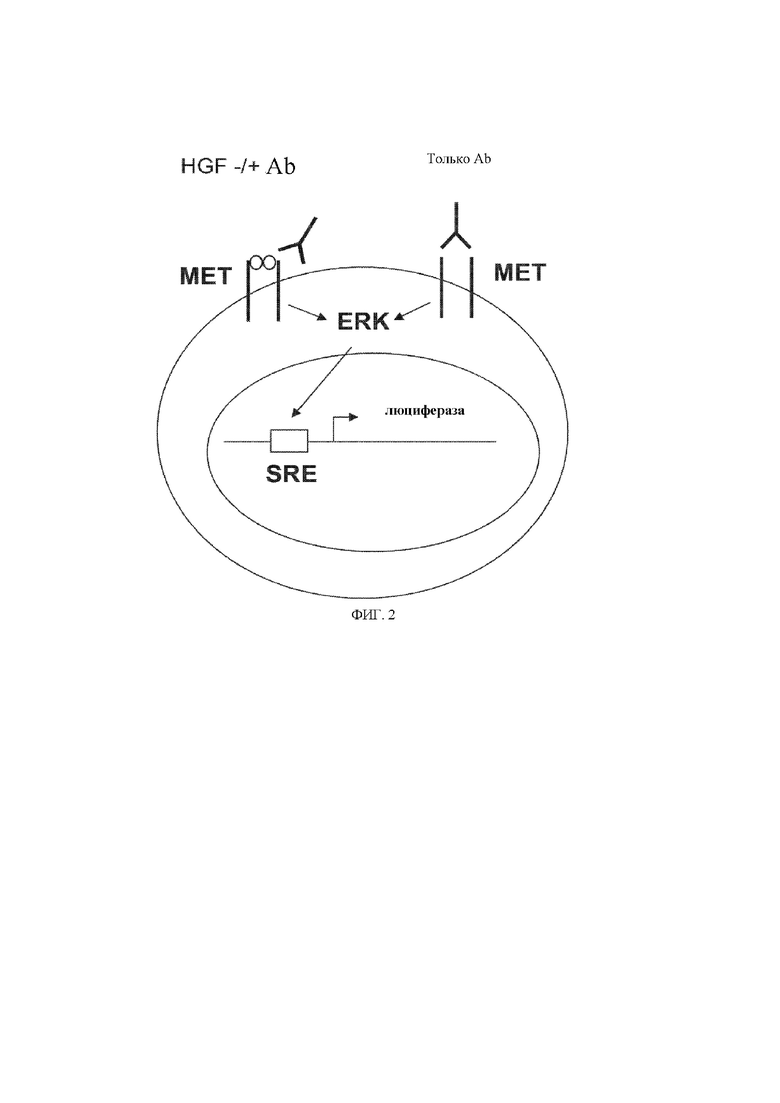
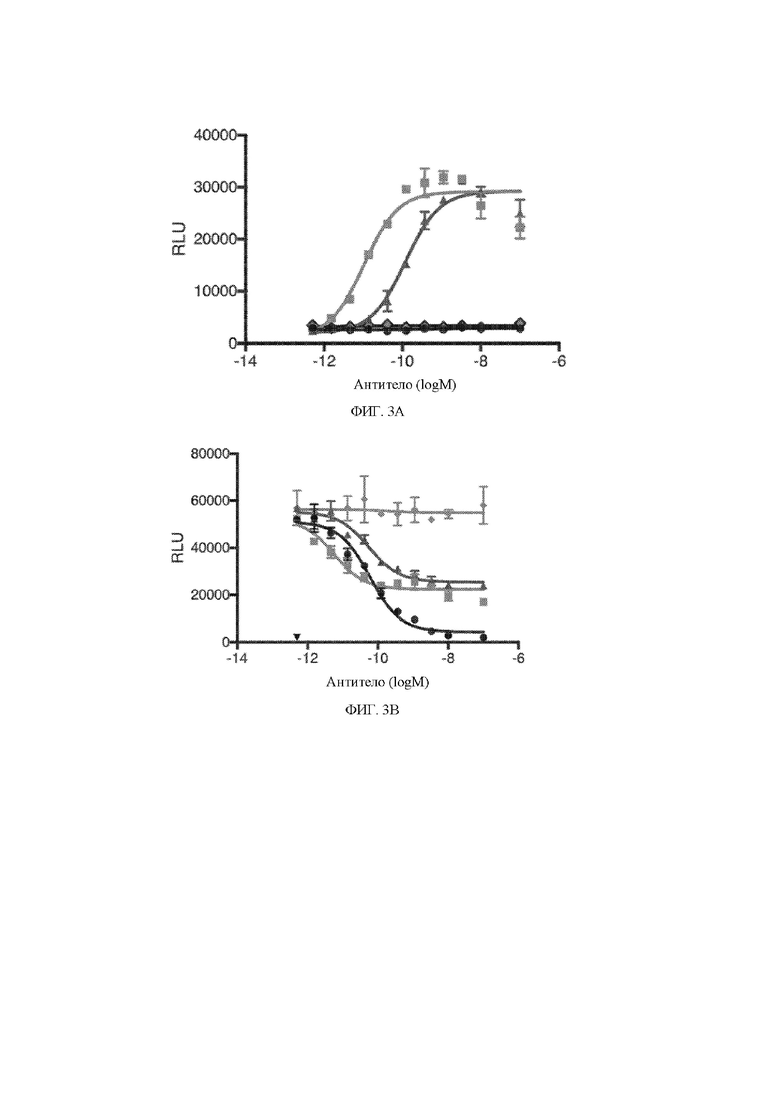
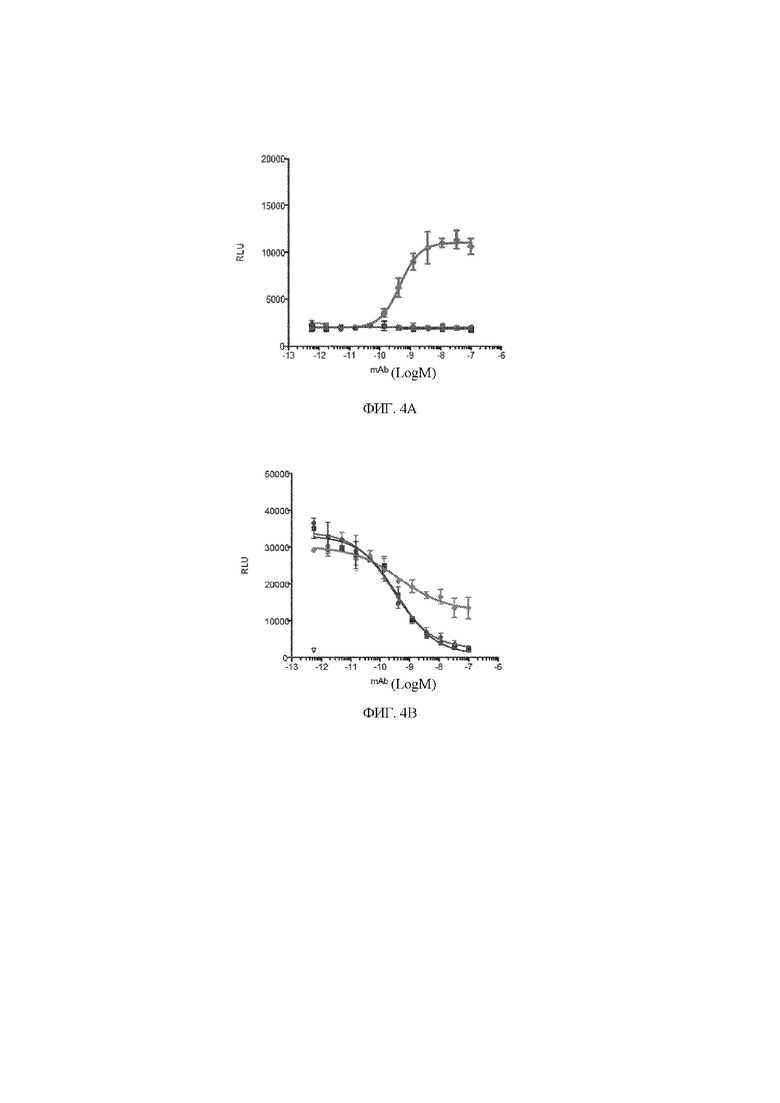
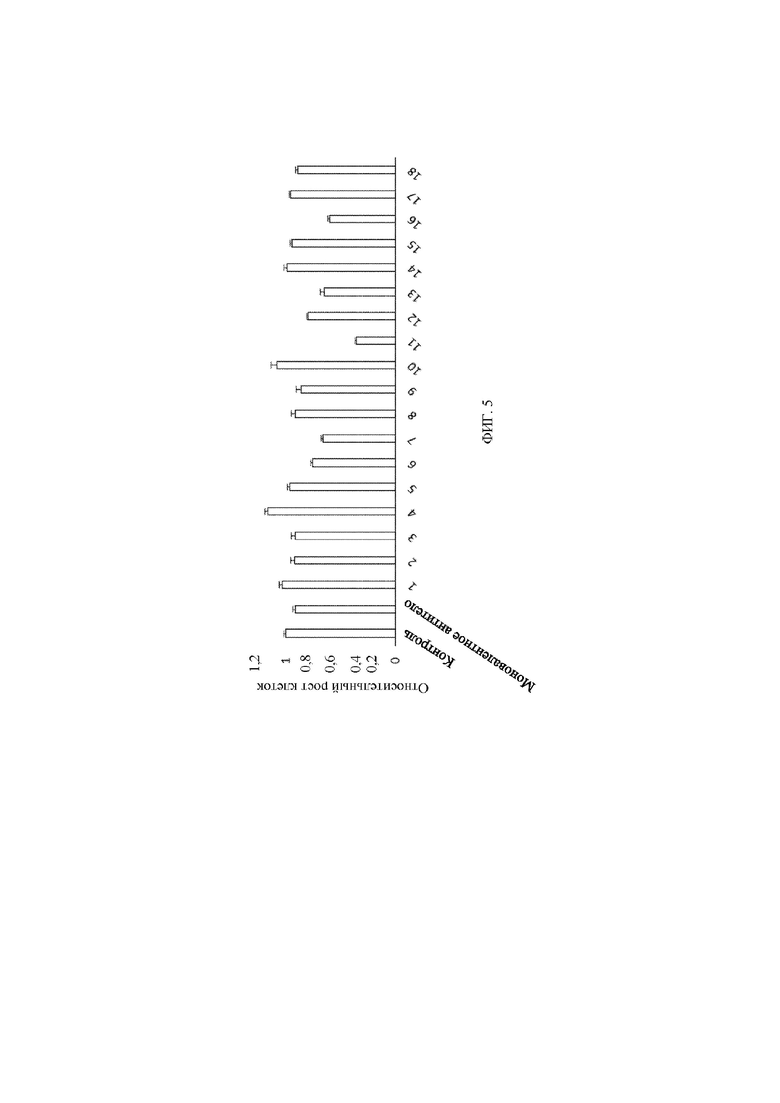
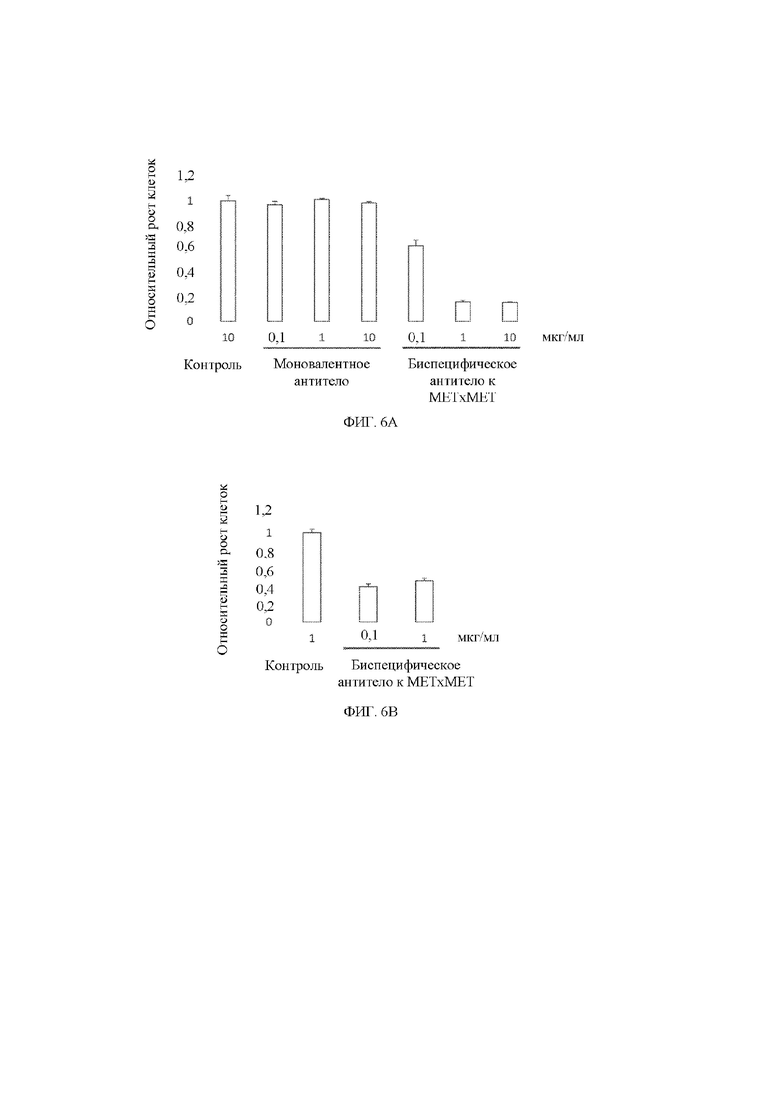
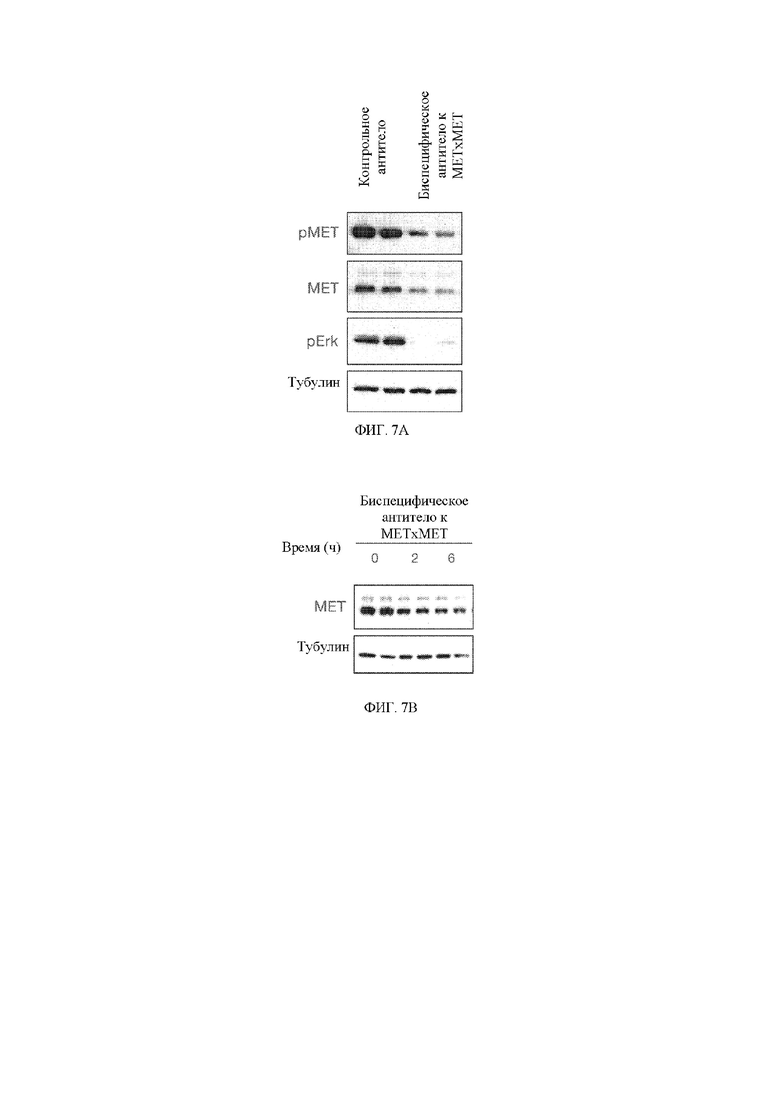

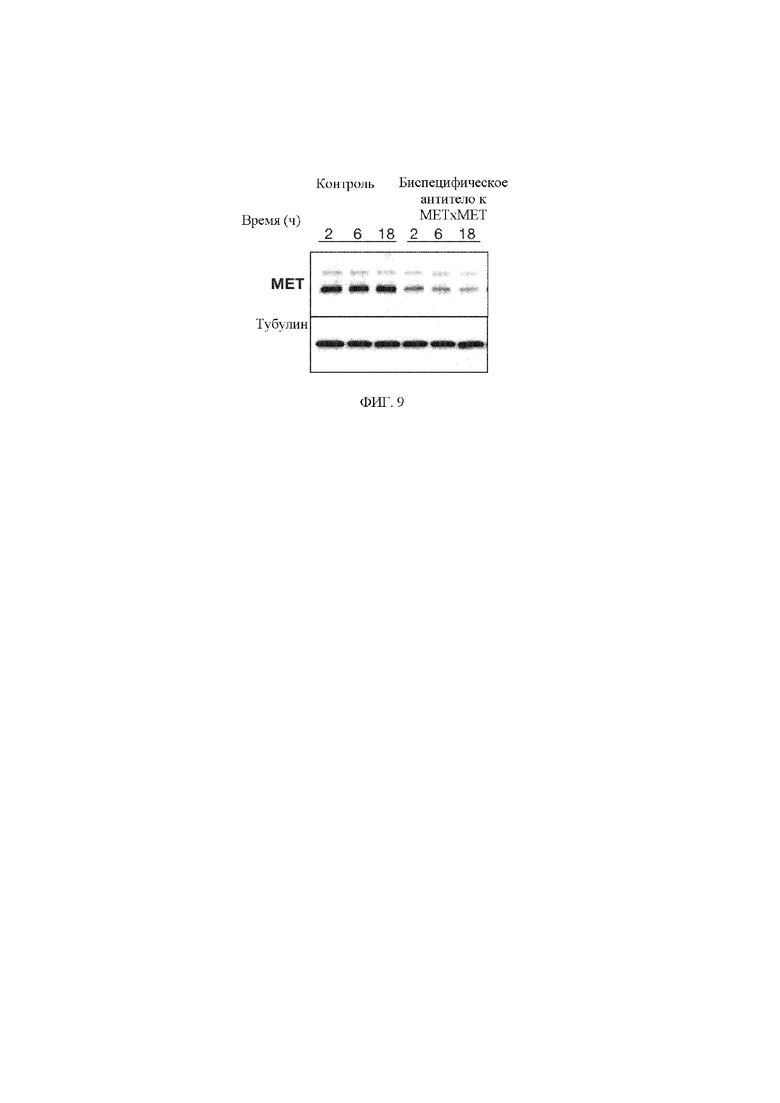
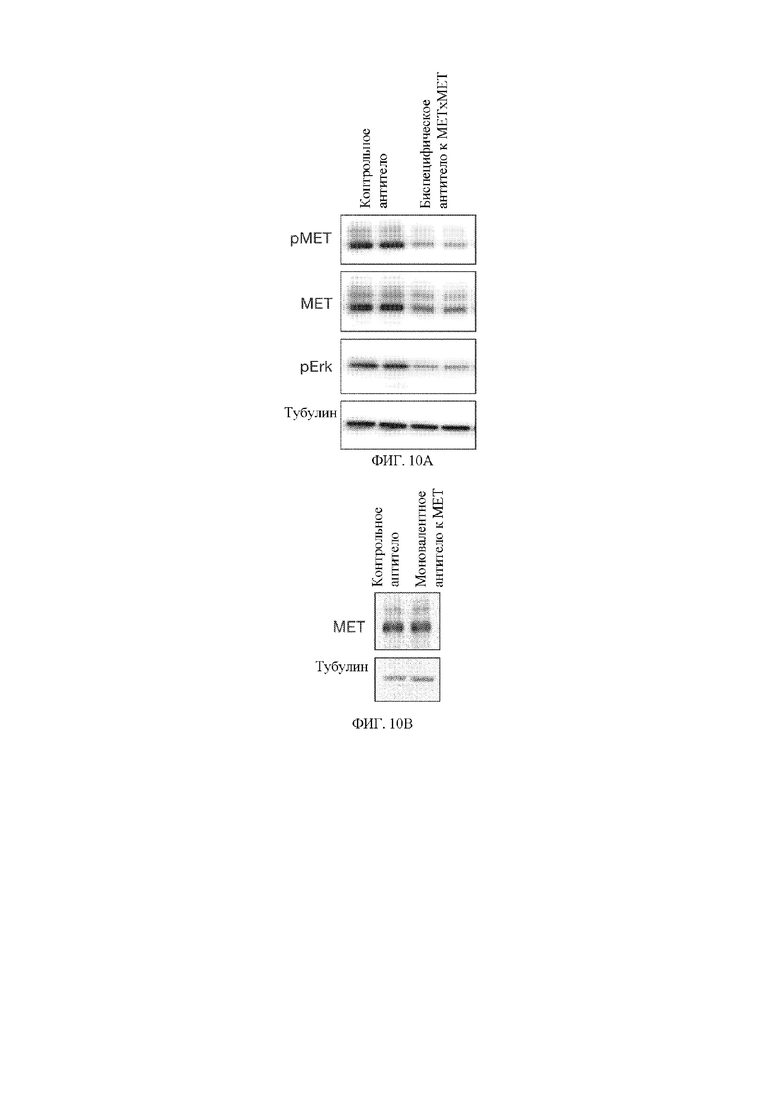

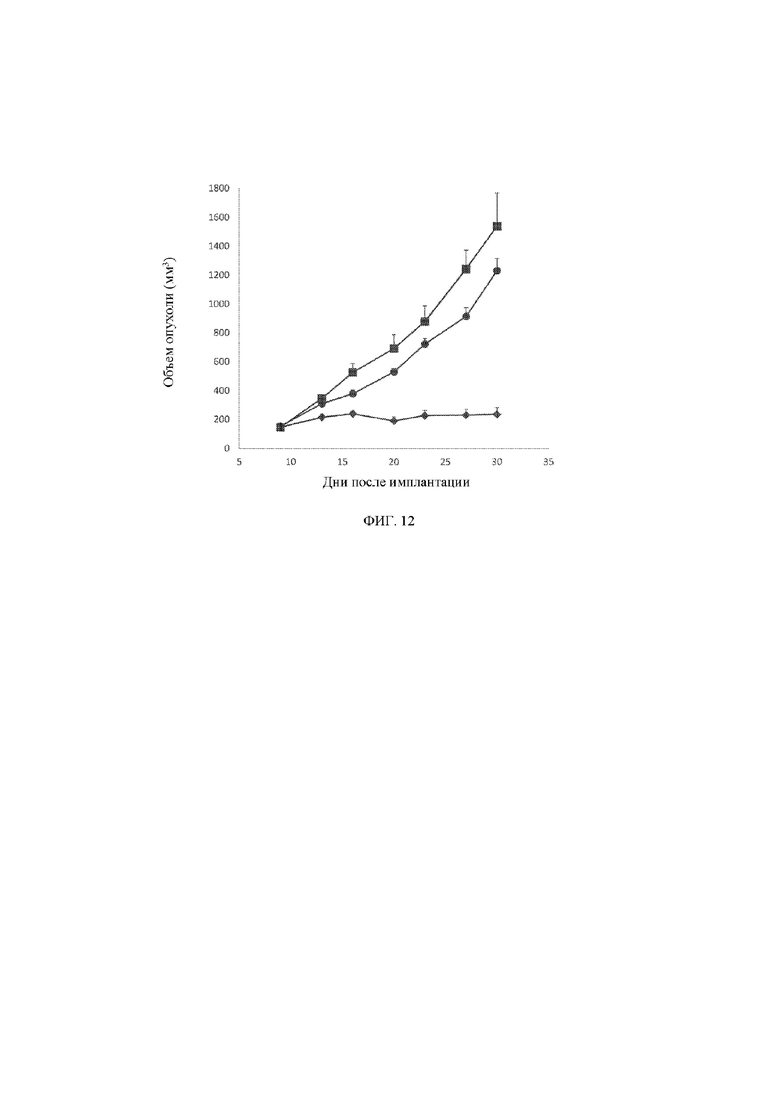
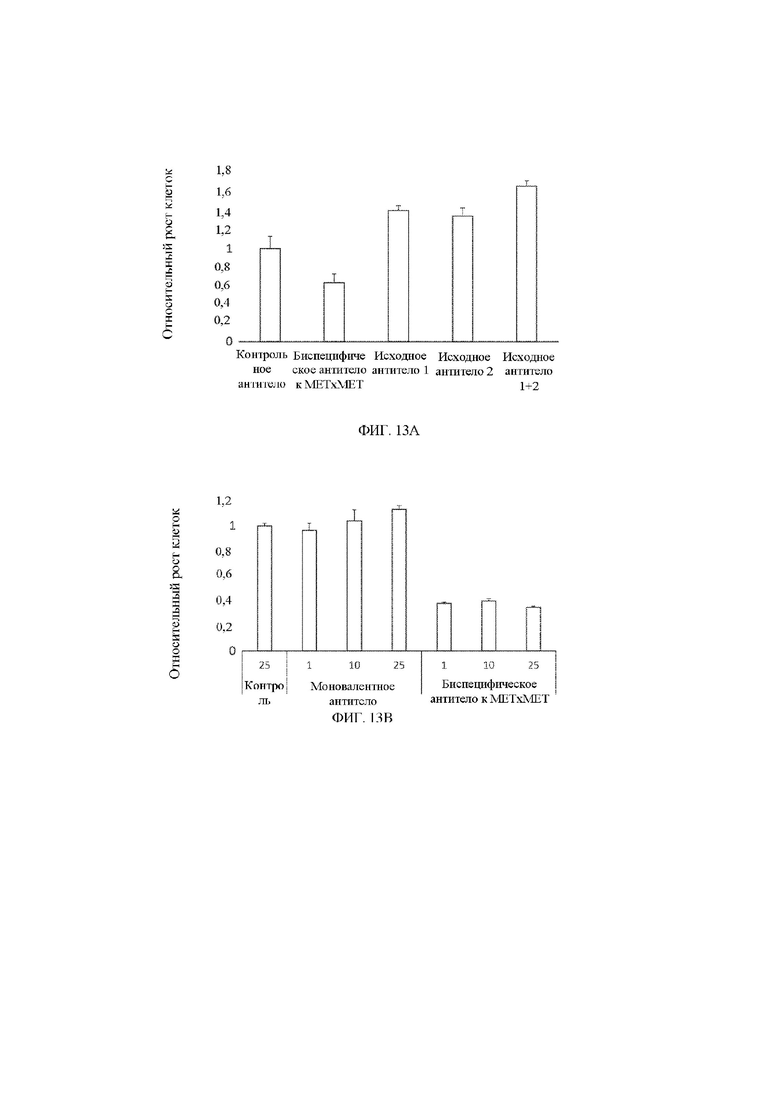

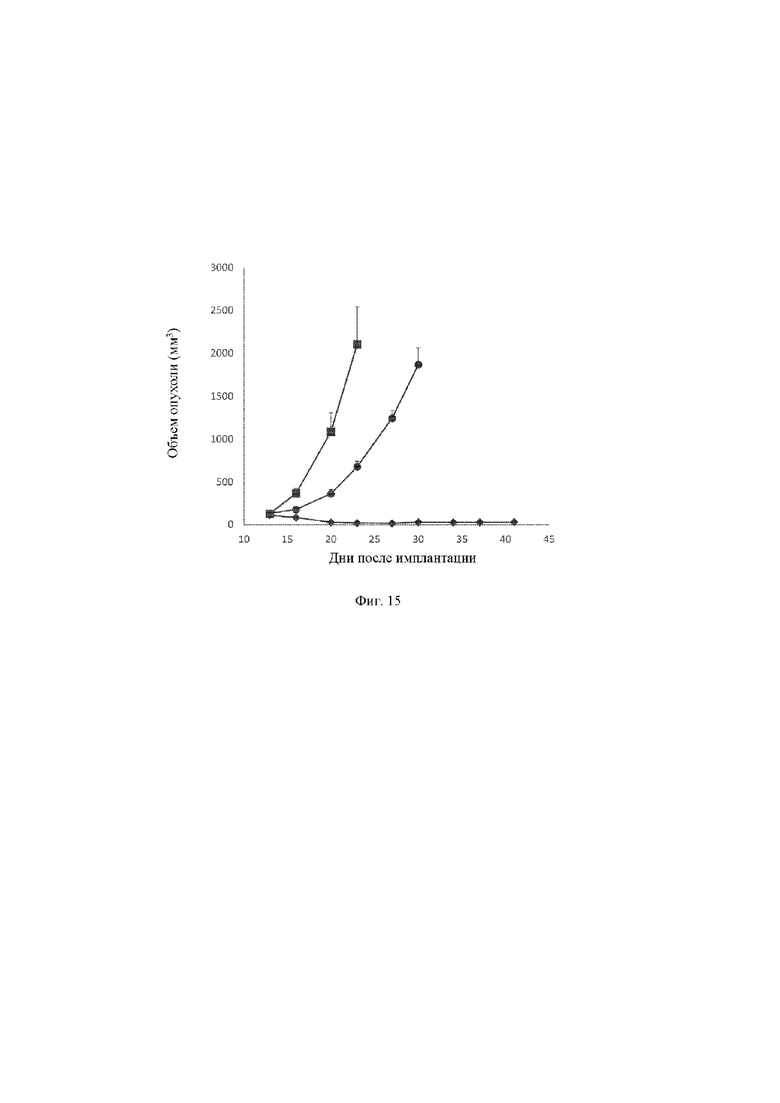
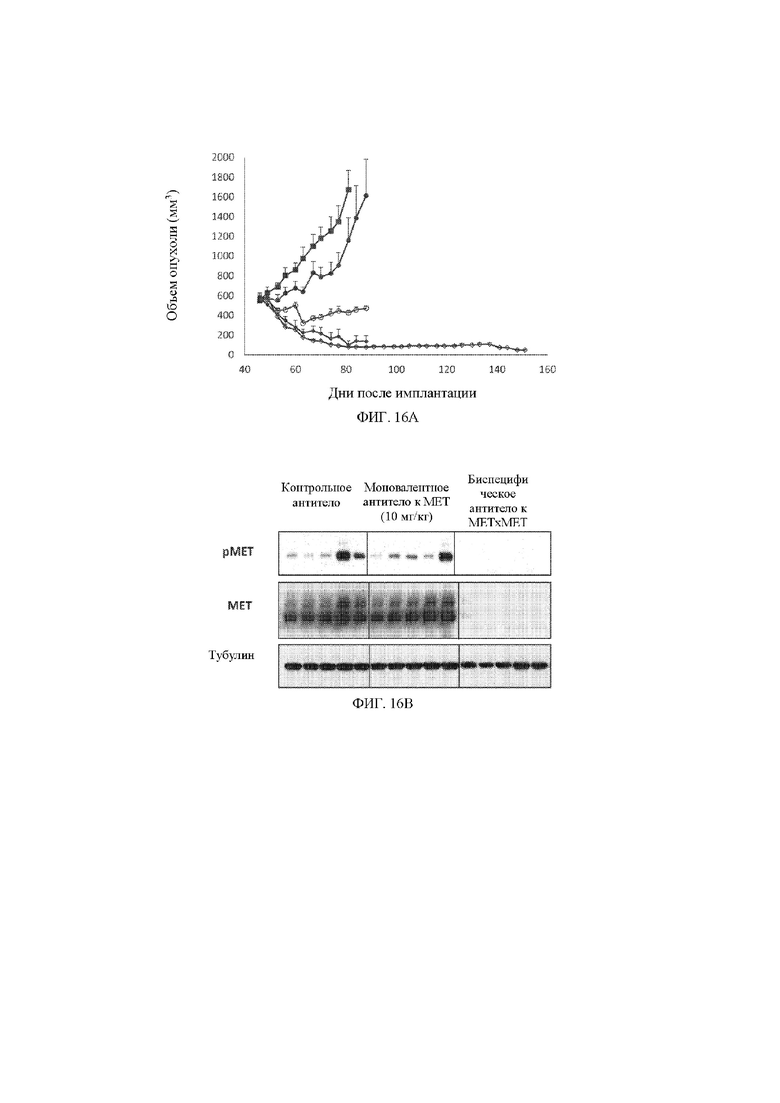
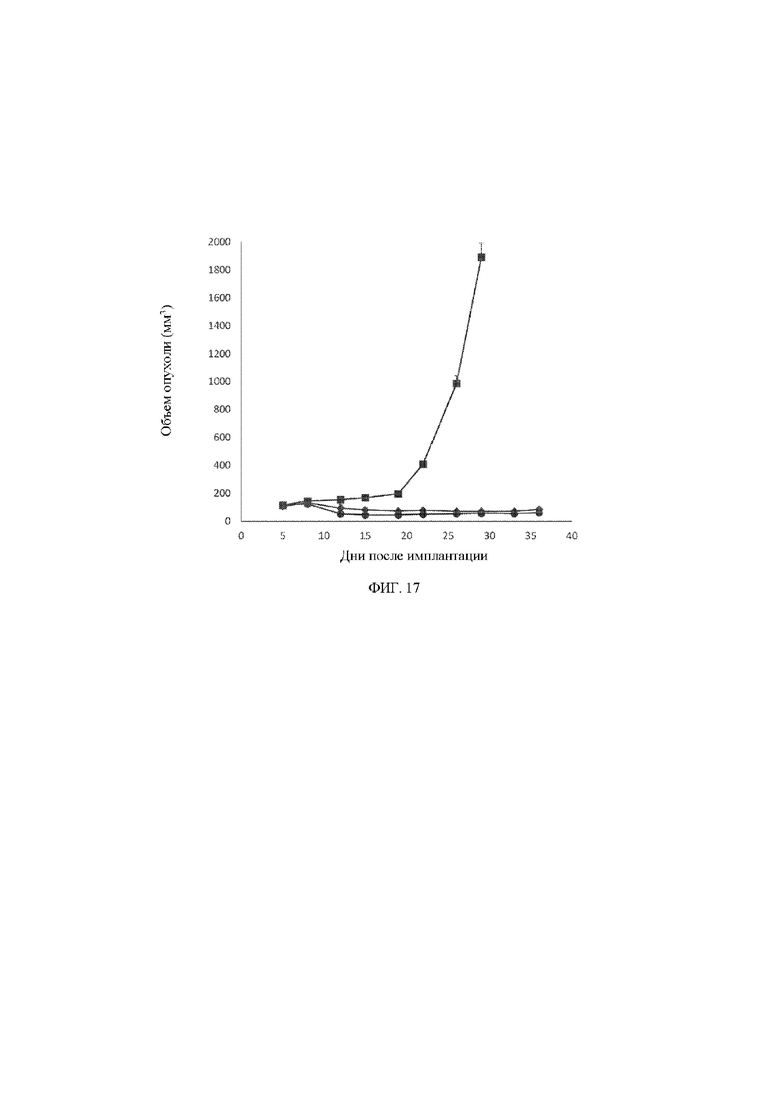
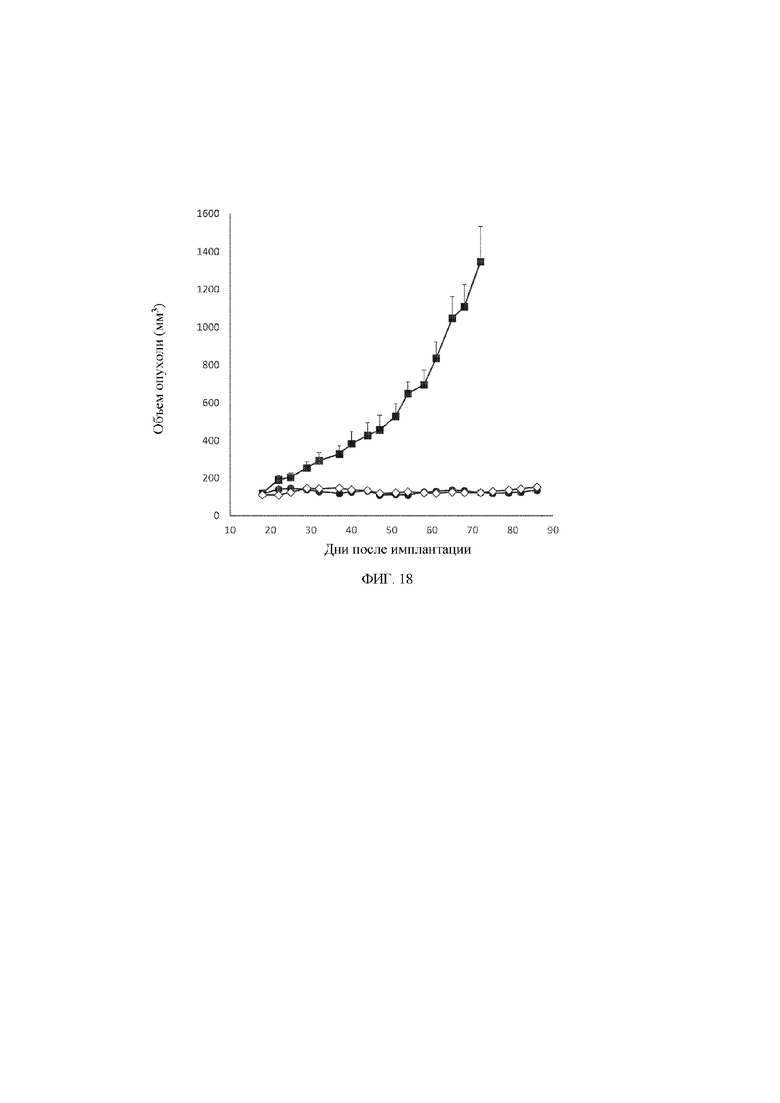
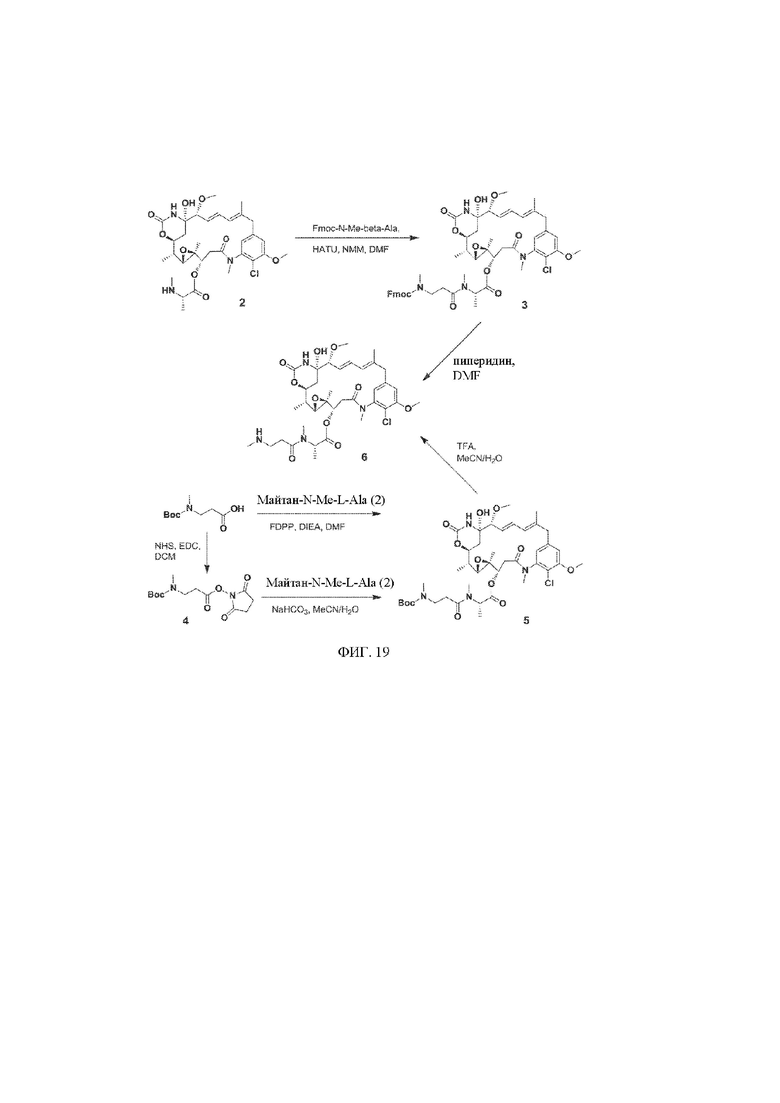
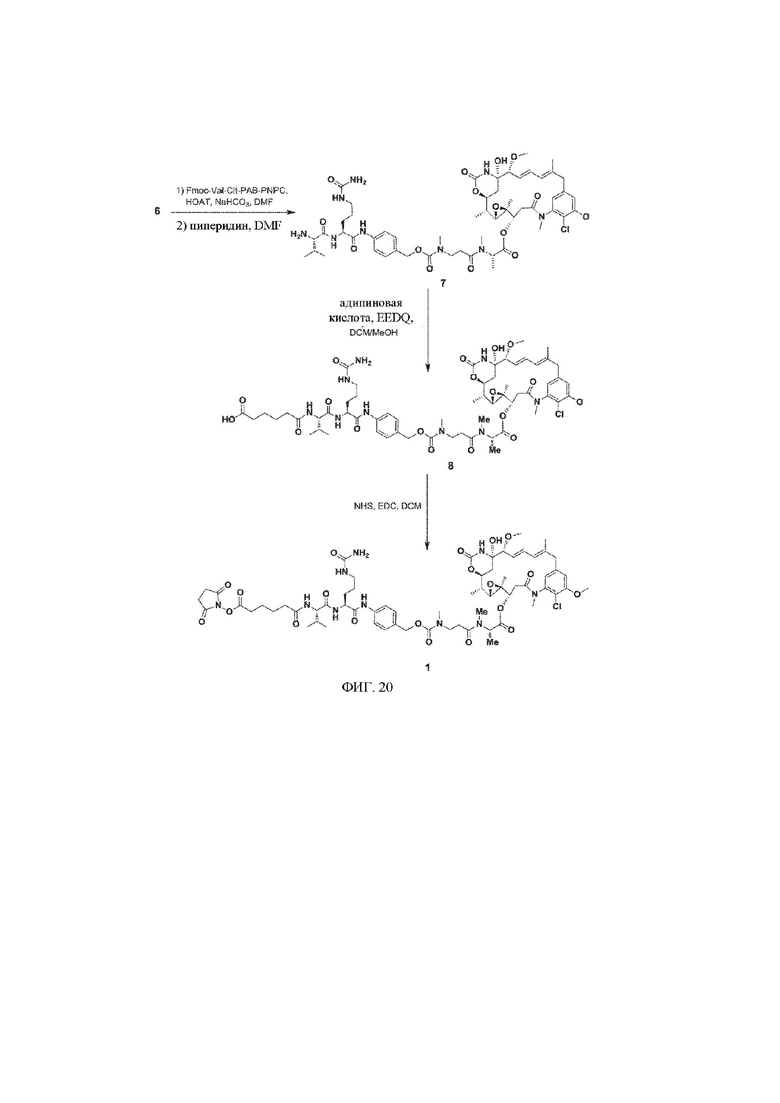
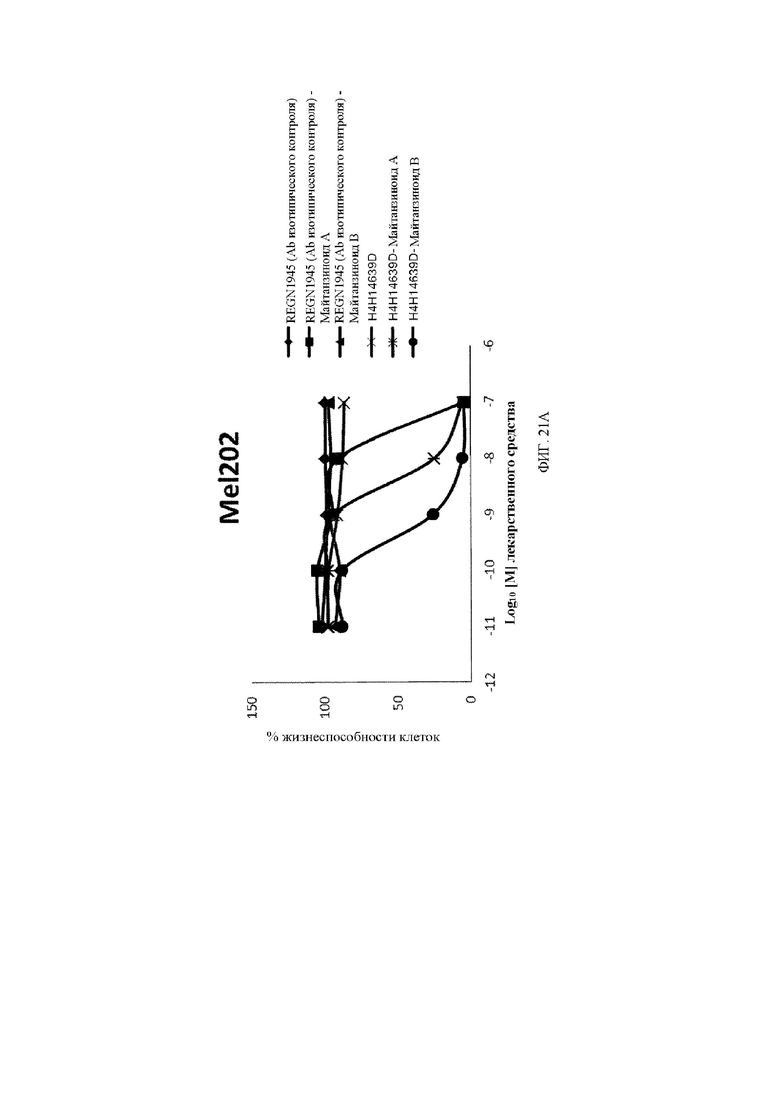
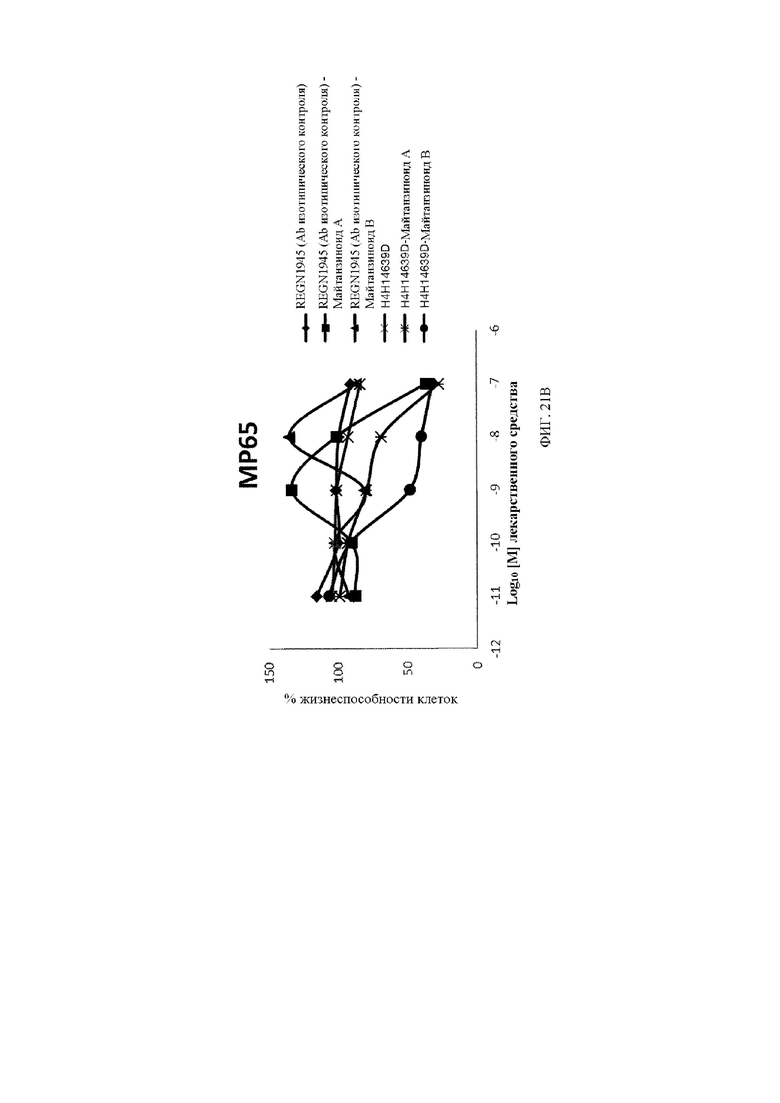
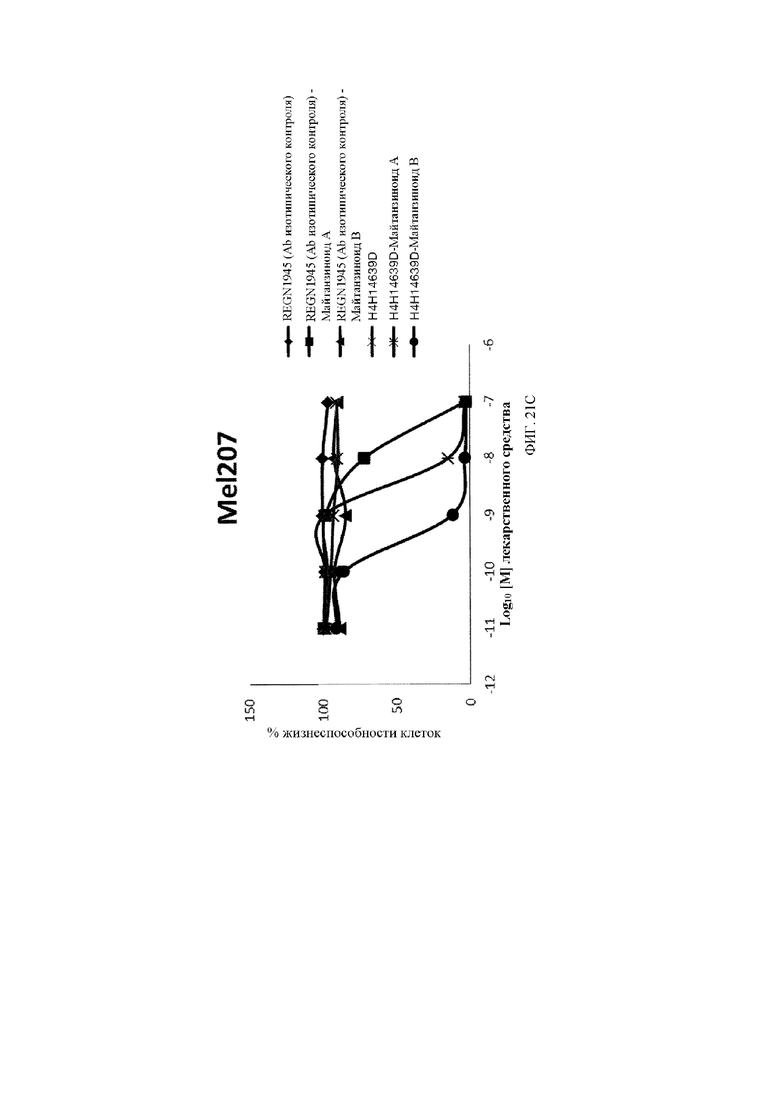
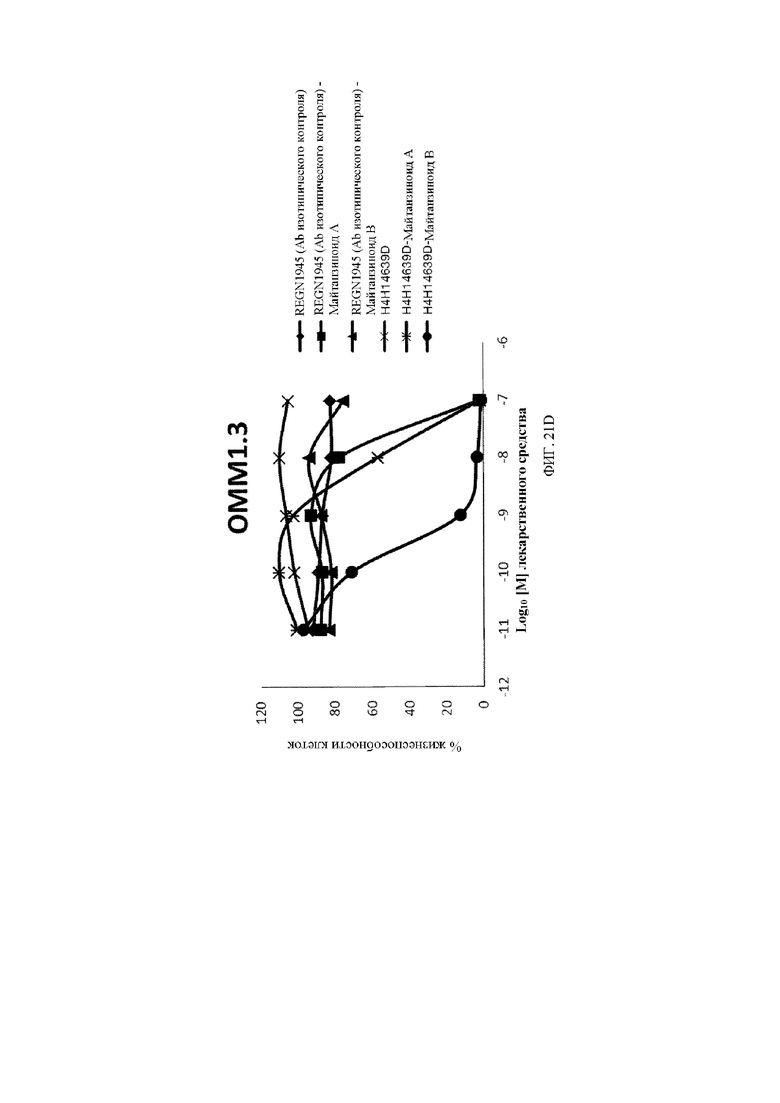
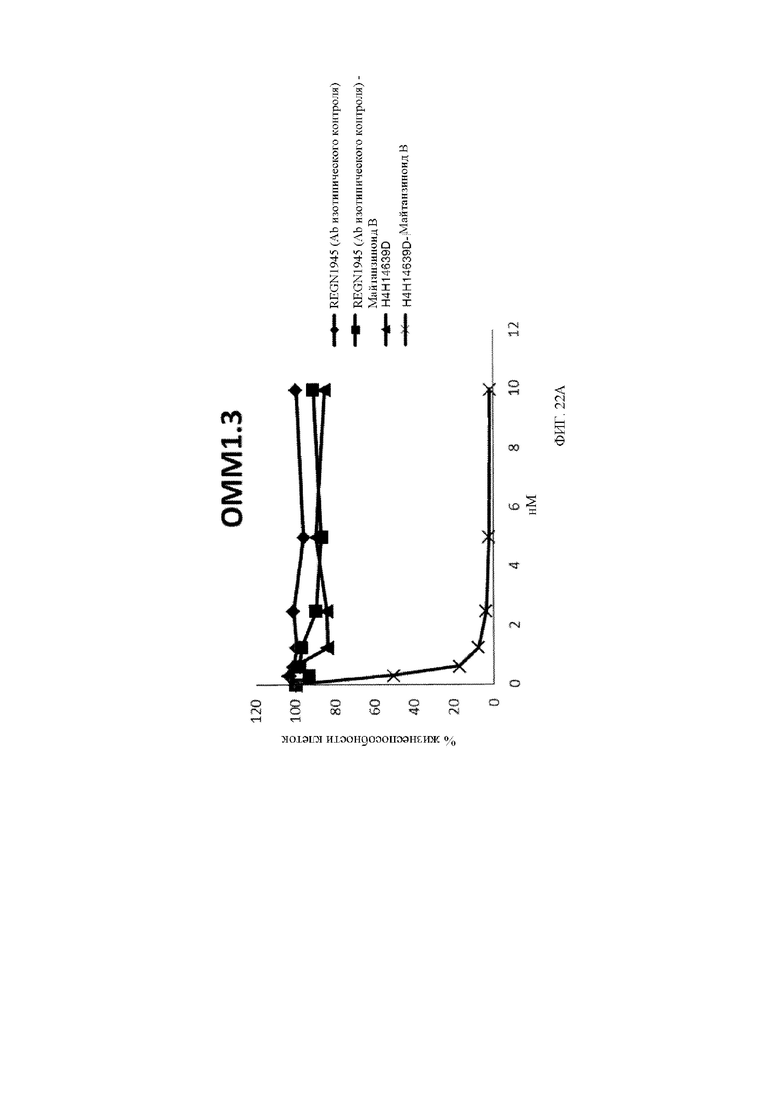
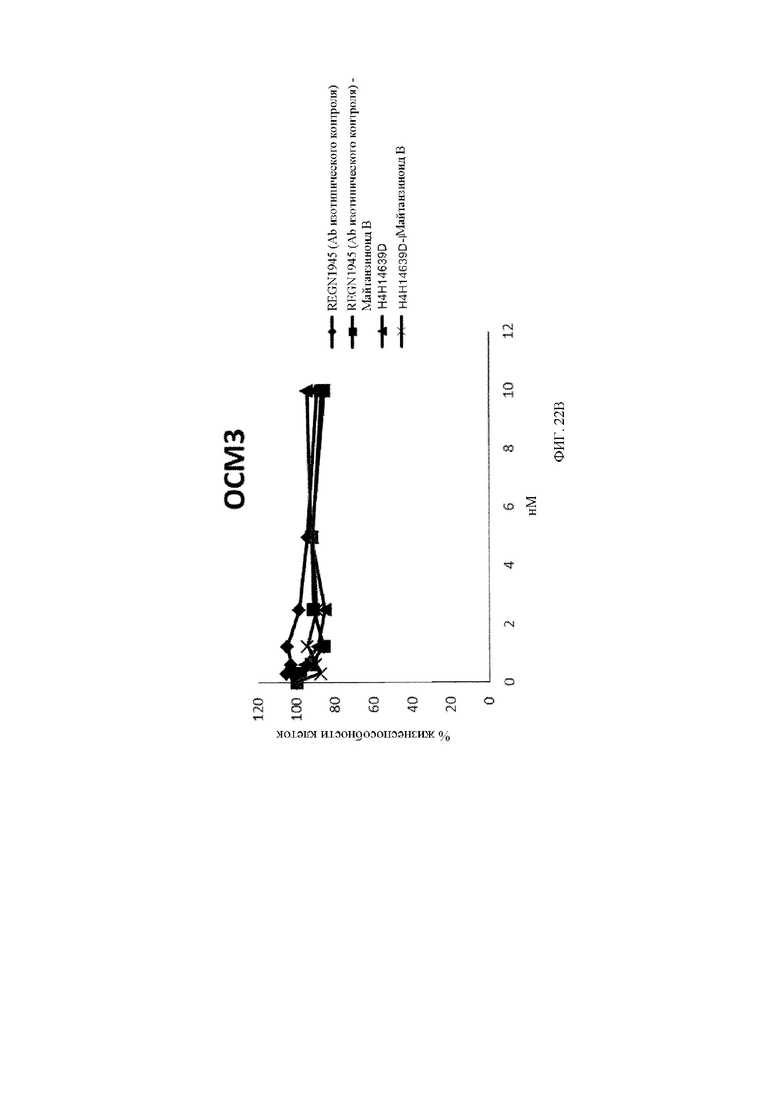
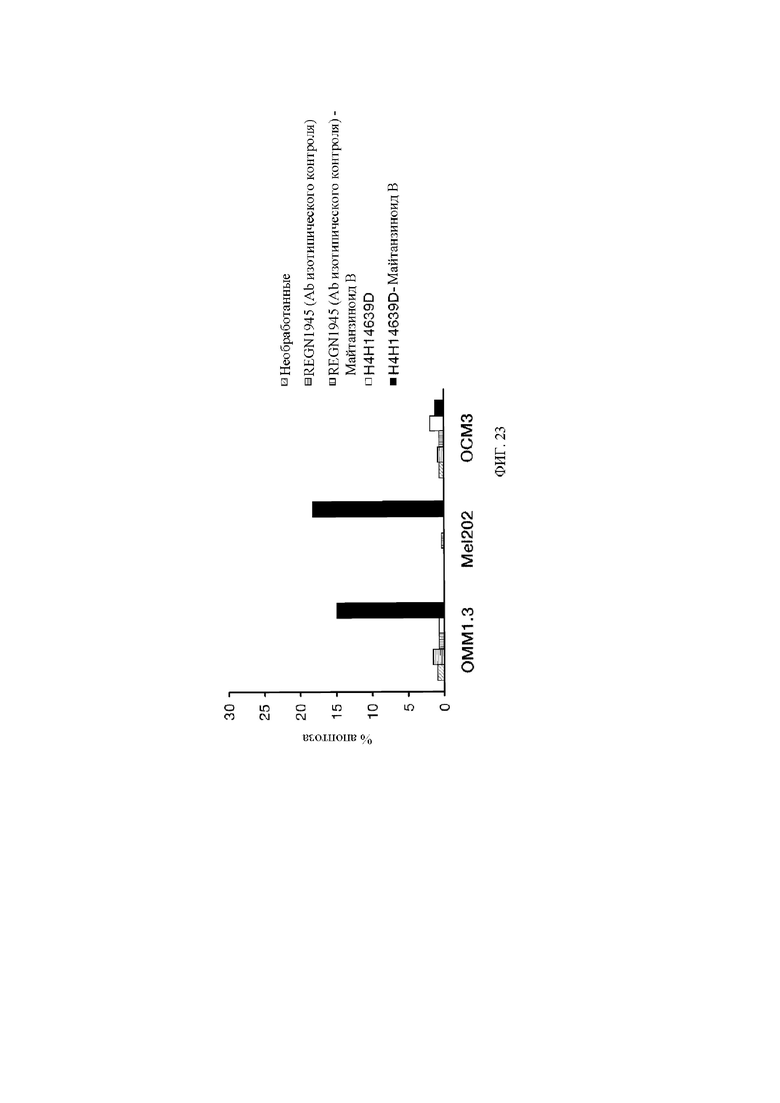



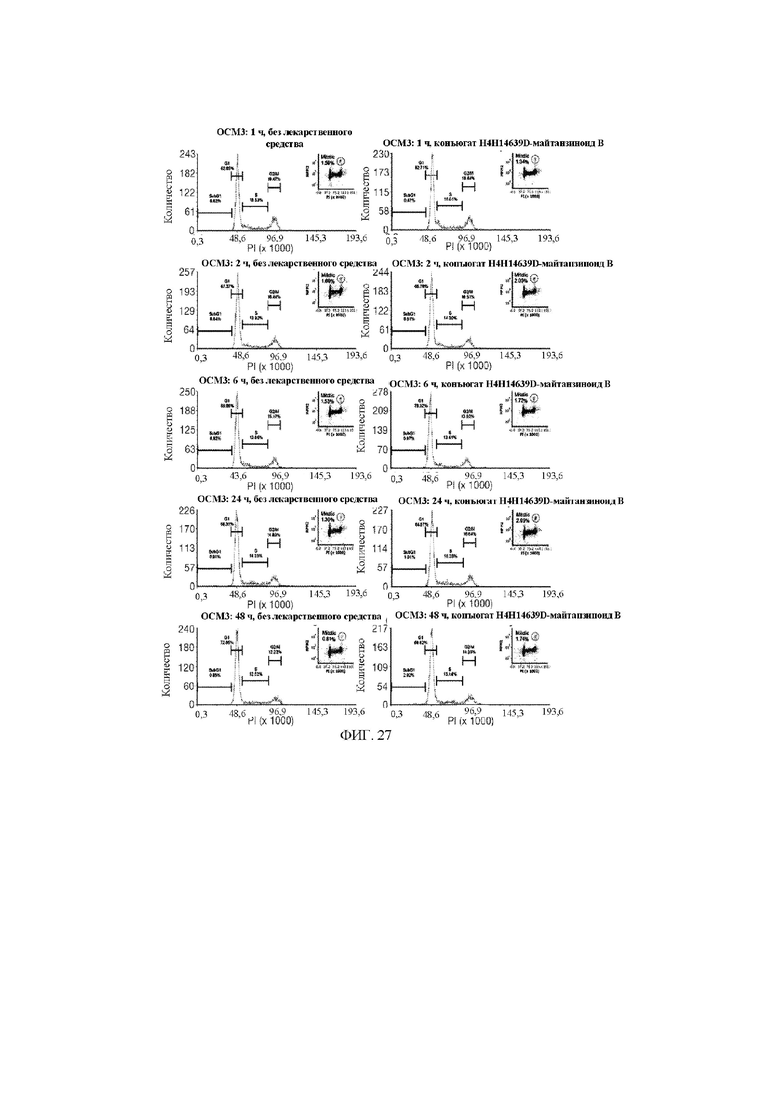



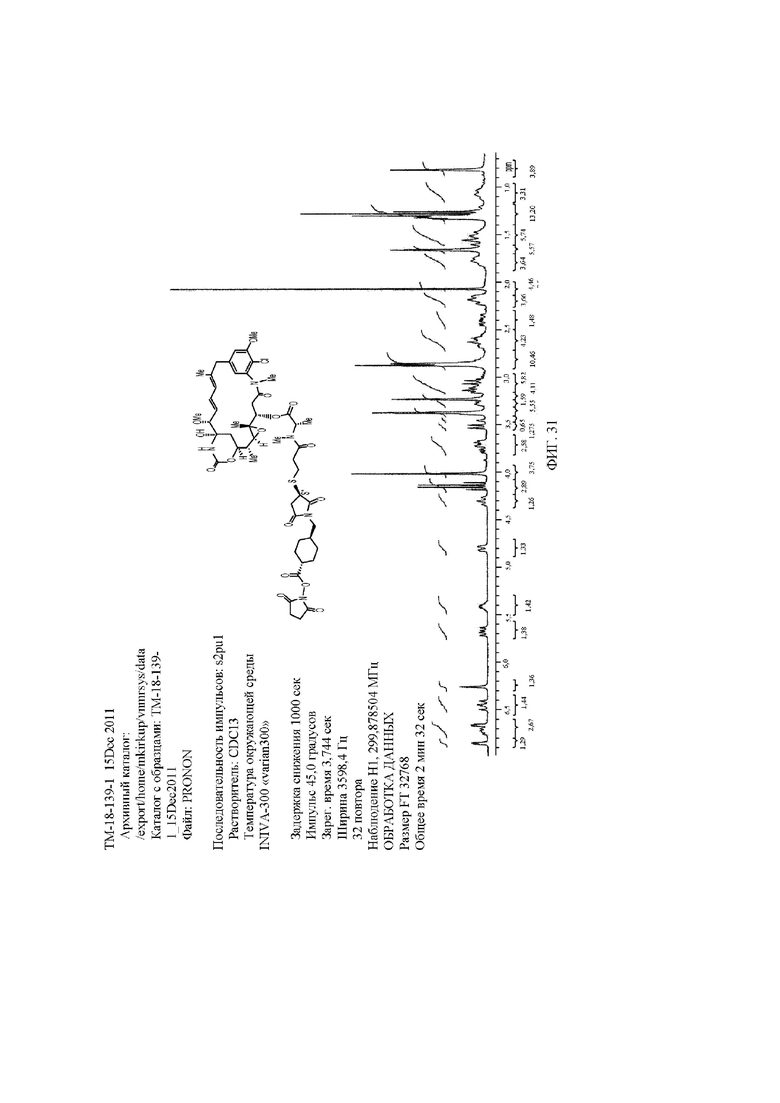
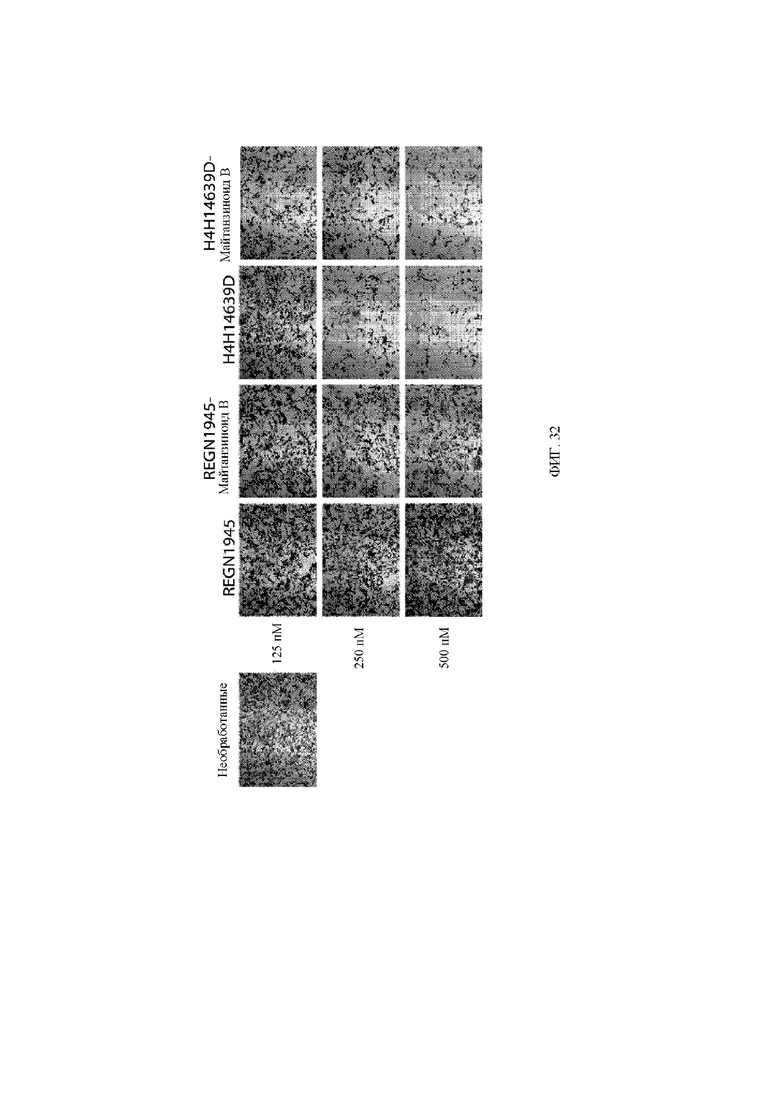
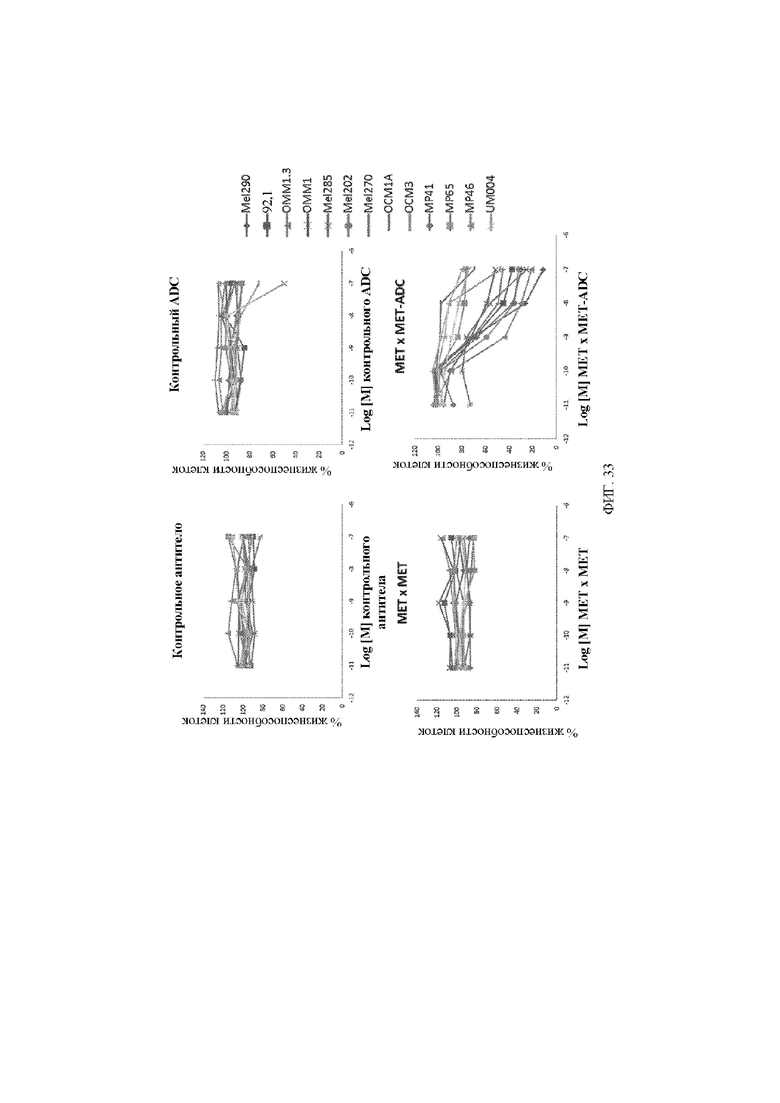
Изобретение относится к области биотехнологии, в частности к применению композиции для лечения увеальной меланомы, снижения роста опухоли при увеальной меланоме и/или инициации регресса увеальной меланомы. Указанная композиция содержит конъюгат антитело-лекарственное средство (ADC), содержащий биспецифическую антигенсвязывающую молекулу и майтанзиноид. Указанная биспецифическая антигенсвязывающая молекула включает первый антигенсвязывающий домен (D1), содержащий HCDR1-HCDR3 с последовательностями SEQ ID NO: 60, 62, 64 и LCDR1-LCDR3 с последовательностями SEQ ID NO: 140, 142, 144, а также второй антигенсвязывающий домен (D2), (D1), содержащий HCDR1-HCDR3 с последовательностями SEQ ID NO: 84, 86, 88 и LCDR1-LCDR3 с последовательностями SEQ ID NO: 140, 142, 144. Изобретение обеспечивает уничтожение c-Met экспрессирующих клеток увеальной меланомы. 16 з.п. ф-лы, 33 ил., 44 табл., 34 пр.
1. Применение композиции, содержащей конъюгат антитело-лекарственное средство (ADC), содержащий биспецифическую антигенсвязывающую молекулу и цитотоксин для лечения увеальной меланомы, снижения роста опухоли при увеальной меланоме и/или инициации регресса увеальной меланомы у субъекта, включающее введение композиции субъекту, нуждающемуся в этом, где биспецифическая антиген связывающая молекула содержит:
первый антигенсвязывающий домен (D1) и
второй антигенсвязывающий домен (D2),
где D1 специфически связывает первый эпитоп МЕТ человека, и
где D2 специфически связывает второй эпитоп МЕТ человека; и
где D1 содержит три определяющие комплементарность области тяжелой цепи, содержащие: HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 60; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 62; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 64; и три определяющие комплементарность области легкой цепи, содержащие: LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 140; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 142; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 144; и
где D2 содержит три определяющие комплементарность области тяжелой цепи, содержащие: HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 84; HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 86; HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 88; и три определяющие комплементарность области легкой цепи, содержащие: LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 140; LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 142; и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 144;
где цитотоксин представляет собой майтанзиноид; и
где введение ADC субъекту приводит к уничтожению c-Met экспрессирующих клеток увеальной меланомы.
2. Применение по п. 1, где D1 содержит вариабельную область тяжелой цепи (HCVR), содержащую аминокислотную последовательность под SEQ ID NO: 58, и вариабельную область легкой цепи (LCVR), содержащую аминокислотную последовательность под SEQ ID NO: 138.
3. Применение по п. 1, где D2 содержит вариабельную область тяжелой цепи (HCVR), содержащую аминокислотную последовательность под SEQ ID NO: 82, и вариабельную область легкой цепи (LCVR), содержащую аминокислотную последовательность под SEQ ID NO: 138.
4. Применение по п. 1, где биспецифическая антигенсвязывающая молекула содержит аминокислотную последовательность D1-HCVR под SEQ ID NO: 58 и аминокислотную последовательность D2-HCVR под SEQ ID NO: 82.
5. Применение по п. 1, где первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO: 155.
6. Применение по п. 1, где второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO: 155.
7. Применение по п. 1, где первый эпитоп МЕТ человека содержит аминокислоты 192-204 из SEQ ID NO: 155 и где второй эпитоп МЕТ человека содержит аминокислоты 305-315 и 421-455 из SEQ ID NO: 155.
8. Применение по п. 1, где цитотоксин конъюгирован с биспецифической антигенсвязывающей молекулой посредством линкера и где цитотоксин представляет собой:
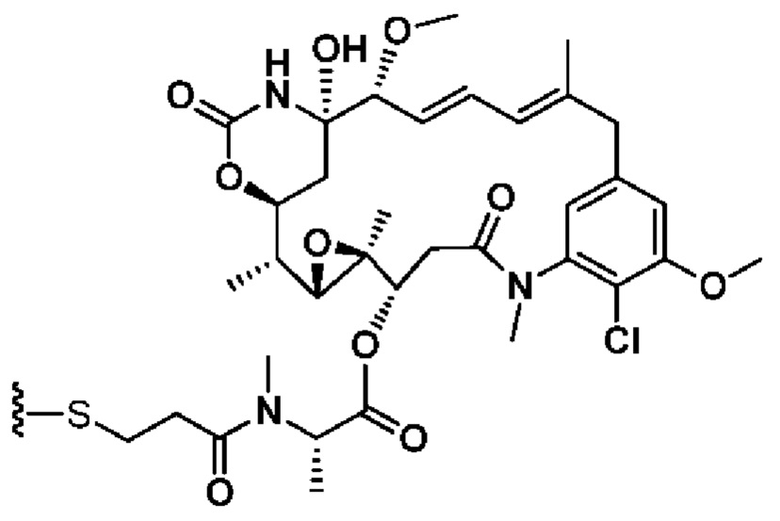 ,
,
где 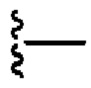 представляет собой связь с линкером.
представляет собой связь с линкером.
9. Применение по п. 8, где линкер представляет собой:
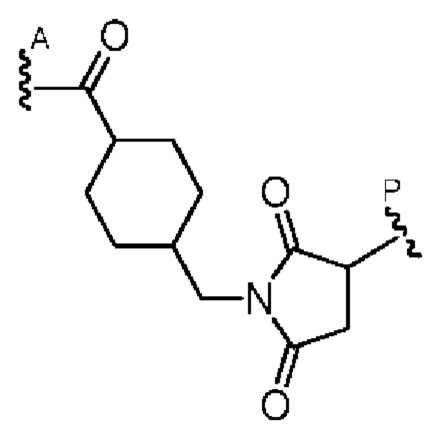 ,
,
где связь, отмеченная с помощью  , представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью
, представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью  , представляет собой связь с цитотоксином.
, представляет собой связь с цитотоксином.
10. Применение по п. 1, где цитотоксин конъюгирован с биспецифической антигенсвязывающей молекулой посредством линкера и где цитотоксин представляет собой:
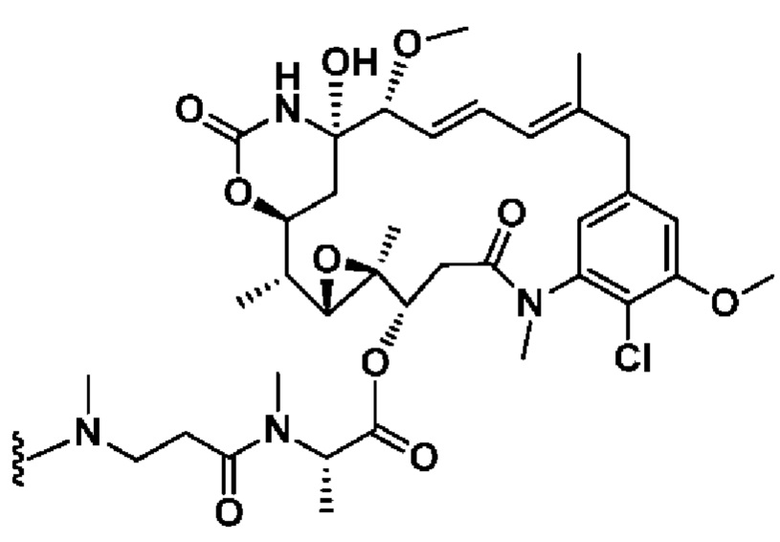 ,
,
где 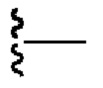 представляет собой связь с линкером.
представляет собой связь с линкером.
11. Применение по п. 10, где линкер представляет собой:
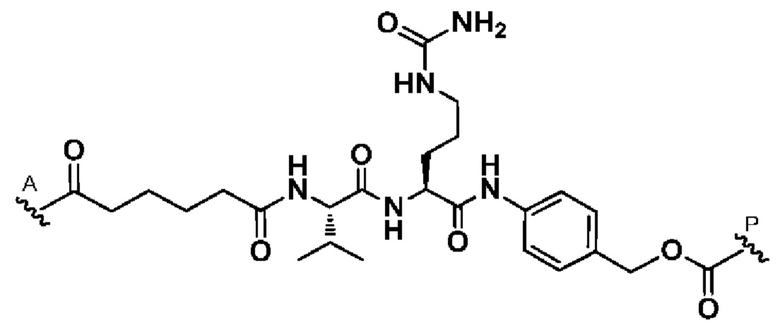 ,
,
где связь, отмеченная с помощью 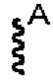 , представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью
, представляет собой связь с биспецифической антигенсвязывающей молекулой, а связь, отмеченная с помощью  , представляет собой связь с цитотоксином.
, представляет собой связь с цитотоксином.
12. Применение по п. 1, где композиция подавляет пролиферацию, подавляет инвазию, инициирует апоптоз и/или снижает жизнеспособность клетки увеальной меланомы.
13. Применение по п. 1, где композиция индуцирует остановку митоза клетки увеальной меланомы.
14. Применение по п. 1, где композиция подавляет метастазирование у субъекта, страдающего опухолью, экспрессирующей c-Met.
15. Применение по п. 1, дополнительно в комбинации со вторым противораковым терапевтическим средством.
16. Применение по п. 14, где D1 и D2 не конкурируют друг с другом за связывание с МЕТ человека.
17. Применение по п. 1, где D1 и D2 не конкурируют друг с другом за связывание с МЕТ человека.
| WO 2016149265 A1, 22.09.2016 | |||
| WO 2018093866 A1, 24.05.2018 | |||
| CHEN H | |||
| et al., Tubulin Inhibitor-Based Antibody-Drug Conjugates for Cancer Therapy, Molecules, 2017, Vol | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| OLIVER SURRIGA et al., Crizotinib, a c-Met Inhibitor, Prevents Metastasis in a Metastatic Uveal Melanoma Model, Molecular Cancer Therapeutics, 2013, Vol | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
2024-11-18—Публикация
2020-02-20—Подача