ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ПРИЛОЖЕНИЯ
[0001] По настоящей заявке испрашивается приоритет предварительной заявки на патент США № 62/880,650, поданной 30 июля 2019 г., предварительной заявки на патент США № 62/968,970, поданной 31 января 2020 г., и предварительной заявки на патент США № 63/030,123, поданной 26 мая 2020, каждая из которых полностью включена в настоящее описание посредством ссылки для любых целей.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Настоящее изобретение относится к выделенным антителам к парвовирусу псовых, например, с улучшенным рекомбинантным получением и нейтрализующим связыванием парвовируса псовых и/или парвовируса кошачьих, и к способам их применения, например, для формирования пассивного иммунитета к заражению парвовирусом псовых или кошачьих и/или для лечения парвовирусной инфекции у домашних животных, таких как собаки и кошки.
УРОВЕНЬ ТЕХНИКИ
[0003] Парвовирус псовых (CPV) является наиболее важным кишечным вирусом, поражающим собак во всем мире. Вирион CPV представляет собой безоболочечный ДНК-содержащий вирус. Существует несколько вариантов оригинального CPV, включая CPV-2a, CPV-2b и CPV-2c. Варианты CPV-2 отличаются друг от друга всего несколькими аминокислотами. Достаточно стойкий во внешней среде, CPV может оставаться инфекционным в течение нескольких месяцев. CPV распространяется через прямой и непрямой контакт. При контакте со слизистой оболочкой полости рта CPV начинает размножаться в местных лимфатических сосудах и распространяется системно. С инкубационным периодом от 4 до 14 дней CPV нацелен на быстро делящиеся клетки организма, включая костный мозг, лимфоциты и эпителиальные клетки кишечных крипт.
[0004] Клинически заболевание проявляется в виде лихорадки и депрессии, за которыми следуют рвота, диарея (профузная и кровавая), лимфопения, обезвоживание и довольно часто вторичная септицемия, и смерть. Смертность у щенков может превышать 70%. Инфекция чаще всего встречается у щенков после отъема, когда материнские антитела начинают ослабевать. Вакцины легко доступны и эффективно защищают от всех вариантов CPV-2.
[0005] Несмотря на то, что своевременно проведенные вакцинации обеспечивают защиту, парвовирусная инфекция остается проблемой. Первичная популяция восприимчивых собак включает щенков в период уязвимости, когда уровень антител материнского происхождения уже снижен до уровня, не обеспечивающего защиту, а вакцинация еще не проведена (см. фиг.1). Щенки в возрасте до 24 недель подвергаются наибольшему риску заболевания CPV. Кроме того, еще одной уязвимой популяцией являются щенки с отсутствием пассивной передачи материнских антител. Вспышки продолжают происходить и в наивных популяциях питомников и приютов.
[0006] Вплоть до этого момента лечение инфекции CPV было в значительной степени поддерживающим. Лечение обычно включает внутривенное вводимые жидкости, противорвотные средства и антибиотики широкого спектра действия для защиты от септицемии. Безуспешно были опробованы и различные другие методы лечения, включая противовирусные препараты и гипериммунную плазму. Обычно рекомендуется госпитализация, которая может быть непомерно дорогостоящей для многих владельцев и может привести к решению об эвтаназии. Госпитализация собак с инфекцией CPV требует соблюдения строгих протоколов изоляции. Для ветеринарных учреждений и персонала это может оказаться затруднительным с точки зрения логистики. Таким образом, существует неудовлетворенная медицинская потребность в профилактике и терапевтическом лечении.
[0007] В настоящее время отсутствуют утвержденные USDA или FDA методы лечения, специально предназначенные для CPV. Моноклональное антитело к парвовирусу, представленное в настоящем описании, можно вводить в качестве терапевтического воздействия на собак с активной инфекцией CPV для снижения тяжести или устранения заболеваемости и смертности, связанных с CPV. Кроме того, моноклональное антитело к парвовирусу, представленное в настоящем описании, может быть использовано в качестве профилактического средства для собак, подвергшихся контакту с инфицированными CPV собаками для предотвращения развития инфекции CPV.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Вариант осуществления 1. Выделенное антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, причем указанное антитело содержит: (a) (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4, (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5, (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6, и (iv) последовательность HC-FR1 SEQ ID NO: 7 или SEQ ID NO: 8; или (b) (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 42, (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 43, (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 44, и (iv) последовательность HC-FR1 SEQ ID NO: 45 или SEQ ID NO: 46.
Вариант осуществления 2. Выделенное антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где указанное антитело содержит: (a) (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13, (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14, (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15, и (iv) последовательность LC-FR1 SEQ ID NO: 16; или (b) (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 52, (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 53, (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 54, и (iv) последовательность LC-FR1 SEQ ID NO: 55 или SEQ ID NO: 56.
Вариант осуществления 3. Выделенное антитело по варианту осуществления 1, где антитело по пункту (а) содержит последовательность HC-FR4 SEQ ID NO: 12.
Вариант осуществления 4. Выделенное антитело по варианту осуществления 1, где антитело по пункту (b) содержит последовательность HC-FR2 SEQ ID NO: 48.
Вариант осуществления 5. Выделенное антитело по варианту осуществления 1 или варианту осуществления 4, где антитело по пункту (b) содержит последовательность HC-FR3 SEQ ID NO: 50.
Вариант осуществления 6. Выделенное антитело по варианту осуществления 2, где антитело по пункту (b) содержит последовательность HC-FR3 SEQ ID NO: 59.
Вариант осуществления 7. Выделенное антитело по варианту осуществления 2 или варианту осуществления 6, где антитело по пункту (b) содержит последовательность HC-F4 SEQ ID NO: 61.
Вариант осуществления 8. Выделенное антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где антитело представляет собой канинизированное или фелинизированное антитело, содержащее: а) тяжелую цепь, содержащую (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6, или b) тяжелую цепь, содержащую (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 42; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 43; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 44.
Вариант осуществления 9. Выделенное антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где антитело представляет собой канинизированное или фелинизированное антитело, содержащее: а) легкую цепь, содержащую (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15, или b) легкую цепь, содержащую (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 52; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 53; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 54.
Вариант осуществления 10. Выделенное антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где антитело представляет собой канинизированное или фелинизированное антитело, содержащее: а) тяжелую цепь, содержащую (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6, и b) легкую цепь, содержащую (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15.
Вариант осуществления 11. Выделенное антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где антитело представляет собой канинизированное или фелинизированное антитело, содержащее: а) тяжелую цепь, содержащую (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 42; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 43; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 44, и b) легкую цепь, содержащую (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 52; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 53; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 54.
Вариант осуществления 12. Антитело по любому из предшествующих вариантов осуществления, где антитело представляет собой химерное антитело.
Вариант осуществления 13. Антитело по любому из предшествующих вариантов осуществления, где указанное антитело содержит собачью или кошачью константную область тяжелой цепи или собачью или кошачью константную область легкой цепи.
Вариант осуществления 14. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит:
(a) собачью константную область тяжелой цепи, выбранную из константной области IgG-A, IgG-B, IgG-C и IgG D; или
(b) кошачью константную область тяжелой цепи, выбранную из константной области IgG1, IgG2a и IgG2b.
Вариант осуществления 15. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит Fc IgG дикого типа или его вариант, обладающий активностью связывания комплемента.
Вариант осуществления 16. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит Fc IgG дикого типа или его вариант, обладающий активностью антителозависимой клеточной цитотоксичности (ADCC).
Вариант осуществления 17. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит Fc IgG дикого типа или его вариант, обладающий активностью антителозависимого клеточного фагоцитоза (ADCP).
Вариант осуществления 18. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит: а) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 10 SEQ ID NO: 91; b) аспарагиновую кислоту или глутаминовую кислоту в положении 10 SEQ ID NO: 91; c) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 103 SEQ ID NO: 91; d) аспарагиновую кислоту или глутаминовую кислоту в положении 103 SEQ ID NO: 91; e) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 10 и/или положению 103 SEQ ID NO: 91; f) аспарагиновую кислоту или глутаминовую кислоту в положении 10 и/или положении 103 SEQ ID NO: 91; или g) аминокислотную последовательность SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 96, SEQ ID NO: 97, SEQ ID NO: 98 или SEQ ID NO: 99.
Вариант осуществления 19. Антитело по любому из предшествующих вариантов осуществления, где указанное антитело содержит собачью константную область легкой цепи κ или кошачью константную область легкой цепи κ.
Вариант осуществления 20. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит константную область легкой цепи κ кошачьих без одного или более сайтов N-гликозилирования.
Вариант осуществления 21. Антитело по любому из предшествующих вариантов осуществления, где антитело связывается с эпитопом, содержащим аминокислотную последовательность SEQ ID NO: 1, SEQ ID NO: 2 и/или SEQ ID NO: 3.
Вариант осуществления 22. Антитело по любому из предшествующих вариантов осуществления, где антитело связывается с парвовирусом псовых или парвовирусом кошачьих с константой диссоциации (Kd) менее 5×10-6 М, менее 1×10-6 М, менее 5×10-7 М, менее 1×10-7 М, менее 5×10-8 М, менее 1×10-8 М, менее 5×10-9 М, менее 1×10-9 М, менее 5×10-10 М, менее 1×10-10 М, менее 5×10-11 М, менее 1×10-11 М, менее 5×10-12 М, менее 1×10-12 М, менее 5×10-13 М или менее 1×10-13 М, измеренной методом биослойной интерферометрии.
Вариант осуществления 23. Антитело по любому из предшествующих вариантов осуществления, где антитело связывается с парвовирусом псовых или парвовирусом кошачьих, как определено с помощью иммуноблот-анализа и/или биослойной интерферометрии.
Вариант осуществления 24. Антитело по любому из предшествующих вариантов осуществления, где антитело в концентрации 200 мкг/мл имеет значение ингибирования гемагглютинации не менее 8000, не менее 16000, не менее 32000.
Вариант осуществления 25. Антитело по любому из предшествующих вариантов осуществления, где антитело представляет собой моноклональное антитело.
Вариант осуществления 26. Антитело по любому из предшествующих вариантов осуществления, содержащее одно или более из: (а) последовательности (HC-FR1) SEQ ID NO: 7, 8, 45 или 46; (b) последовательности HC-FR2 SEQ ID NO: 9, 47 или 48; (c) последовательности HC-FR3 SEQ ID NO: 10, 49 или 50; (d) последовательности HC-FR4 SEQ ID NO: 11, 12 или 51; (e) последовательности каркасного участка 1 вариабельной области легкой цепи (LC-FR1) SEQ ID NO: 16, 55 или 56; (f) последовательность LC-FR2 SEQ ID NO: 17 или 57; (g) последовательность LC-FR3 SEQ ID NO: 18, 58 или 59; или (h) последовательность LC-FR4 SEQ ID NO: 19, 60 или 61.
Вариант осуществления 27. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит: (a) последовательность вариабельной тяжелой цепи SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 85, SEQ ID NO: 86, SEQ ID NO: 40, SEQ ID NO: 62, SEQ ID NO: 63 или SEQ ID NO: 88; и/или (b) последовательность вариабельной легкой цепи SEQ ID NO: 22, SEQ ID NO: 87, SEQ ID NO: 41, SEQ ID NO: 64, SEQ ID NO: 65 или SEQ ID NO: 89.
Вариант осуществления 28. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит: (a) последовательность вариабельной тяжелой цепи SEQ ID NO: 20 и последовательность вариабельной легкой цепи SEQ ID NO: 22; (b) последовательность вариабельной тяжелой цепи SEQ ID NO: 21 и последовательность вариабельной легкой цепи SEQ ID NO: 22; (c) последовательность вариабельной тяжелой цепи SEQ ID NO: 85 и последовательность вариабельной легкой цепи SEQ ID NO: 87; (d) последовательность вариабельной тяжелой цепи SEQ ID NO: 86 и последовательность вариабельной легкой цепи SEQ ID NO: 87; (e) последовательность вариабельной тяжелой цепи SEQ ID NO: 40 и последовательность вариабельной легкой цепи SEQ ID NO: 41; (f) последовательность вариабельной тяжелой цепи SEQ ID NO: 62 и последовательность вариабельной легкой цепи SEQ ID NO: 64 или SEQ ID NO: 65; (g) последовательность вариабельной тяжелой цепи SEQ ID NO: 63 и последовательность вариабельной легкой цепи SEQ ID NO: 64 или SEQ ID NO: 65; или (h) последовательность вариабельной тяжелой цепи SEQ ID NO: 88 и последовательность вариабельной легкой цепи SEQ ID NO: 89.
Вариант осуществления 29. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит: (a) (i) последовательность тяжелой цепи SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 37, SEQ ID NO: 38, SEQ ID NO: 66, SEQ ID NO: 67 или SEQ ID NO: 79; и/или (ii) последовательность легкой цепи SEQ ID NO: 25, SEQ ID NO: 39, SEQ ID NO: 68, SEQ ID NO: 69 или SEQ ID NO: 80; или (b) (i) последовательность тяжелой цепи SEQ ID NO: 31, SEQ ID NO: 40 или SEQ ID NO: 74; и/или (ii) последовательность легкой цепи SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 41, SEQ ID NO: 75 или SEQ ID NO: 76.
Вариант осуществления 30. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит: (a) последовательность тяжелой цепи SEQ ID NO: 23 или SEQ ID NO: 24 и последовательность легкой цепи SEQ ID NO: 25; (b) последовательность тяжелой цепи SEQ ID NO: 31 и последовательность легкой цепи SEQ ID NO: 32 или SEQ ID NO: 33; (c) последовательность тяжелой цепи SEQ ID NO: 37 или SEQ ID NO: 38 и последовательность легкой цепи SEQ ID NO: 39; (d) последовательность тяжелой цепи SEQ ID NO: 66 или SEQ ID NO: 67 и последовательность легкой цепи SEQ ID NO: 68 или SEQ ID NO: 69; (e) последовательность тяжелой цепи SEQ ID NO: 66 и последовательность легкой цепи SEQ ID NO: 68; (f) последовательность тяжелой цепи SEQ ID NO: 67 и последовательность легкой цепи SEQ ID NO: 69; (g) последовательность тяжелой цепи SEQ ID NO: 74 и последовательность легкой цепи SEQ ID NO: 75 или SEQ ID NO: 76; или (h) последовательность тяжелой цепи SEQ ID NO: 79 и последовательность легкой цепи SEQ ID NO: 80.
Вариант осуществления 31. Антитело по любому из предшествующих вариантов осуществления, где антитело содержит последовательность тяжелой цепи SEQ ID NO: 24 и последовательность легкой цепи SEQ ID NO: 25.
Вариант осуществления 32. Выделенная нуклеиновая кислота, кодирующая антитело по любому из предшествующих вариантов осуществления.
Вариант осуществления 33. Клетка-хозяин, содержащая нуклеиновую кислоту по варианту осуществления 31.
Вариант осуществления 34. Способ получения антитела, включающий культивирование клетки-хозяина по варианту осуществления 32 и выделение антитела.
Вариант осуществления 35. Фармацевтическая композиция, содержащая антитело по любому одному или более вариантам осуществления 1-31 и фармацевтически приемлемый носитель.
Вариант осуществления 36. Фармацевтическая композиция по варианту осуществления 35, где фармацевтически приемлемый носитель представляет собой забуференный фосфатом физиологический раствор.
Вариант осуществления 37. Способ обеспечения пассивного иммунитета у субъекта к заражению парвовирусом псовых или кошачьих, включающий введение субъекту терапевтически эффективного количества моноклонального антитела, которое связывается с парвовирусом псовых или кошачьих.
Вариант осуществления 38. Способ по варианту осуществления 37, где моноклональное антитело вводят перед воздействием парвовируса псовых или кошачьих.
Вариант осуществления 39. Способ по варианту осуществления 37 или варианту осуществления 38, где моноклональное антитело вводят после воздействия парвовируса псовых или кошачьих.
Вариант осуществления 40. Способ по любому из вариантов осуществления 37-39, где моноклональное антитело вводят после инфицирования парвовирусом псовых или кошачьих.
Вариант осуществления 41. Способ по любому из вариантов осуществления 37-40, где моноклональное антитело вводят после того, как у субъекта проявился по меньшей мере один симптом, выбранный из лихорадки, рвоты, диареи, лимфопении и септицемии.
Вариант осуществления 42. Способ по любому из вариантов осуществления 37-41, где моноклональное антитело вводят после того, как парвовирус псовых или кошачьих был обнаружен в фекалиях, например, по результатам положительного теста SNAP в условиях содержания в клетке.
Вариант осуществления 43. Способ по любому из вариантов осуществления 37-42, где субъекту ранее вводили вакцину от парвовируса.
Вариант осуществления 44. Способ по любому из вариантов осуществления 37-42, где субъекту ранее не вводили вакцину от парвовируса.
Вариант осуществления 45. Способ по любому из вариантов осуществления 37-44, где у субъекта при рождении отсутствует защита из-за отсутствия материнских антител к парвовирусу псовых или кошачьих или из-за неудачи пассивного переноса антител к парвовирусу псовых или кошачьих.
Вариант осуществления 46. Способ по любому из вариантов осуществления 37-45, где субъект выращен вручную, мать субъекта не производит молока, или субъект не может вырабатывать антитела к парвовирусу.
Вариант осуществления 47. Способ по любому из вариантов осуществления 37-46, где субъект живет в среде, зараженной парвовирусом псовых или кошачьих.
Вариант осуществления 48. Способ лечения парвовирусной инфекции псовых или кошачьих у субъекта, включающий введение субъекту терапевтически эффективного количества моноклонального антитела, которое связывается с парвовирусом псовых или кошачьих.
Вариант осуществления 49. Способ по варианту осуществления 48, где моноклональное антитело вводят после того, как у субъекта проявился по меньшей мере один симптом, выбранный из лихорадки, рвоты, диареи, лимфопении и септицемии.
Вариант осуществления 50. Способ по варианту осуществления 48 или варианту осуществления 49, где моноклональное антитело вводят после обнаружения парвовируса псовых или кошачьих в фекалиях, например, при положительном результате теста SNAP в условиях содержания в клетке.
Вариант осуществления 51. Способ по любому из вариантов осуществления 48-50, где субъекту ранее вводили парвовирусную вакцину.
Вариант осуществления 52. Способ по любому из вариантов осуществления 48-50, где субъекту ранее не вводили парвовирусную вакцину.
Вариант осуществления 53. Способ по любому из вариантов осуществления 48-52, где субъект живет в среде, зараженной парвовирусом псовых или кошачьих.
Вариант осуществления 54. Способ по любому из вариантов осуществления 48-53, где субъектом является представитель псовых или кошачьих.
Вариант осуществления 55. Способ по любому из вариантов осуществления 48-53, где субъектом является человек.
Вариант осуществления 56. Способ по любому из вариантов осуществления 37-55, где указанный способ включает введение субъекту терапевтически эффективного количества моноклонального антитела, которое связывается с эпитопом, содержащим аминокислотную последовательность SEQ ID NO: 1, SEQ ID NO: 2 и/или SEQ ID NO: 3.
Вариант осуществления 57. Способ по любому из вариантов осуществления 37-56, где указанный способ включает введение субъекту терапевтически эффективного количества моноклонального антитела, содержащего: (a) тяжелую цепь, содержащую (i) CDR-H1, содержащую аминокислоту последовательность SEQ ID NO: 42; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 43; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 44, и (b) легкую цепь, содержащую (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 52; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 53; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 54.
Вариант осуществления 58. Способ по любому из вариантов осуществления 37-57, включающий введение субъекту терапевтически эффективного количества антитела по любому из вариантов осуществления 1-31 или фармацевтической композиции по варианту осуществления 35 или варианту осуществления 36.
Вариант осуществления 59. Способ по любому из вариантов осуществления 37-58, где антитело или фармацевтическую композицию вводят парентерально.
Вариант осуществления 60. Способ по любому из вариантов осуществления 37-59, где антитело или фармацевтическую композицию вводят внутримышечно, внутрибрюшинно, интрацереброспинально, подкожно, внутриартериально, интрасиновиально, интратекально, внутривенно или путем ингаляции.
Вариант осуществления 61. Способ по любому из вариантов осуществления 37-60, где антитело или фармацевтическую композицию вводят внутривенно.
Вариант осуществления 62. Способ по любому из вариантов осуществления 37-60, где антитело или фармацевтическую композицию вводят подкожно.
Вариант осуществления 63. Способ по любому из вариантов осуществления 37-62, где субъект находится в возрасте менее 1 недели, менее 2 недель, менее 3 недель, менее 4 недель, менее 5 недель, менее 6 недель, менее 6 недель, менее 7 недель, менее 8 недель, менее 9 недель, менее 10 недель, менее 11 недель, менее 12 недель, менее 6 месяцев, от 0 до 12 недель, от 0 до 10 недель, от 0 до 8 недель, от 0 до 6 недель, от 0 до 4 недель, от 0 до 2 недель, от 4 до 12 недель, от 6 до 12 недель, от 10 до 12 недель, от 4 недель до 6 месяцев, от 2 месяцев до 6 месяцев, от 4 месяцев до 6 месяцев, от 6 месяцев до 1 года, старше 13 недель или старше 1 года.
Вариант осуществления 64. Способ по любому из вариантов осуществления 37-63, где возраст субъекта составляет 13 недель или старше.
Вариант осуществления 65. Способ по любому из вариантов осуществления 37-64, где антитело вводят в количестве от 0,01 мг/кг массы тела до 100 мг/кг массы тела на дозу.
Вариант осуществления 66. Способ по любому из вариантов осуществления 37-65, где антитело вводят в количестве 5 мг/кг массы тела на дозу.
Вариант осуществления 67. Способ по любому из вариантов осуществления 37-66, где антитело или фармацевтическую композицию вводят в виде однократной дозы.
Вариант осуществления 68. Способ по любому из вариантов осуществления 37-67, где антитело или фармацевтическую композицию вводят несколько раз, например, один раз в неделю в течение по меньшей мере двух или трех недель подряд.
Вариант осуществления 69. Способ по любому из вариантов осуществления 37-68, включающий введение субъекту терапевтически эффективного количества двух или более разных антител по любому из вариантов осуществления 1-31, при этом два или более разных антитела вводят одновременно или последовательно, причем необязательно введение двух или более разных антител разделено одним или более днями.
Вариант осуществления 70. Способ по любому из вариантов осуществления 37-69, где субъект имеет титр ингибирования гемагглютинации менее 20, определенный с помощью анализа ингибирования гемагглютинации до введения антитела или фармацевтической композиции.
Вариант осуществления 71. Способ по любому из вариантов осуществления 37-70, где субъект имеет отрицательный титр парвовируса, определенный с помощью анализа ингибирования гемагглютинации до введения антитела или фармацевтической композиции.
Вариант осуществления 72. Способ по любому из вариантов осуществления 37-71, где субъект выживает при заражении парвовирусом псовых или кошачьих после введения антитела или фармацевтической композиции.
Вариант осуществления 73. Способ снижения инфицирования клетки парвовирусной инфекцией, включающий воздействие на клетку антителом по любому из вариантов осуществления 1-31 или фармацевтической композицией по варианту осуществления 35 или варианту осуществления 36 в условиях, допускающих связывание антитела с парвовирусом.
Вариант осуществления 74. Способ по варианту осуществления 73, где клетку подвергают воздействию антитела или фармацевтической композиции in vitro.
Вариант осуществления 75. Способ по варианту осуществления 73 или варианту осуществления 74, где клетка представляет собой клетку млекопитающего, человеческую клетку, собачью клетку или кошачью клетку.
Вариант осуществления 76. Способ детектирования парвовирусной инфекции в образце, взятом у субъекта, включающий приведение образца в контакт с антителом по любому из вариантов осуществления 1-31 или фармацевтической композицией по варианту осуществления 35 или варианту осуществления 36 в условиях, допускающих связывание антитела с парвовирусом и детектирование образования комплекса между антителом и парвовирусом в образце.
Вариант осуществления 77. Способ по варианту осуществления 76, где образец представляет собой биологический образец, полученный от представителя псовых, кошачьих или человека.
Вариант осуществления 78. Вариант полипептида Fc IgG, содержащий: а) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 10 SEQ ID NO: 91; b) аспарагиновую кислоту или глутаминовую кислоту в положении 10 SEQ ID NO: 91; c) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 103 SEQ ID NO: 91; d) аспарагиновую кислоту или глутаминовую кислоту в положении 103 SEQ ID NO: 91; e) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 10 и/или положению 103 SEQ ID NO: 91; или f) аспарагиновую кислоту или глутаминовую кислоту в положении 10 и/или положении 103 SEQ ID NO: 91.
Вариант осуществления 79. Полипептид, содержащий вариант полипептида IgG Fc по варианту осуществления 78.
Вариант осуществления 80. Полипептид, содержащий аминокислотную последовательность SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 96, SEQ ID NO: 97, SEQ ID NO: 98 или SEQ ID NO: 99.
Вариант осуществления 81. Выделенная нуклеиновая кислота, кодирующая полипептид по любому из вариантов осуществления 78-80.
Вариант осуществления 82. Клетка-хозяин, содержащая нуклеиновую кислоту по варианту осуществления 81.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0008] Фиг. 1 представляет собой схему окна восприимчивости к CPV.
[0009] На фиг. 2 показано связывание Mab A v2 и Mab B v2 с VP2.
[0010] На фиг. 3А показаны титры анализа HI для группы Mab A.
[0011] На фиг. 3B показаны титры анализа HI для группы Mab B.
[0012] На фиг. 3C показаны титры анализа HI для обеих групп Mab A и Mab B.
[0013] На фиг. 4А показана кинетика двухфазного распада Mab A v2.
[0014] На фиг. 4В показана кинетика двухфазного распада Mab B v2.
[0015] На фиг. 5 показаны структурные модели вариантов полипептидных последовательностей Fc собачьего IgG-B из примера 15 и собачьего CD16.
ОПИСАНИЕ НЕКОТОРЫХ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0016] В таблице 1 представлен список некоторых последовательностей, упомянутых в настоящем описании.
[0017] Таблица 1.
Q13A
S11A
(Mab A HC)
HC-FR1 Q13A
HC-FR4 S11A
(Mab A HC v2)
(Mab A LC)
(химерная A HC IgG-B)
HC-FR1 Q13A
HC-FR4 S11A
(химерная A HC v2 IgG-B)
(химерная A LC κ)
(химерная A HC IgG-B с лидерной последовательностью)
HC-FR1 Q13A
HC-FR4 S11A
(химерная A HC v2 IgG-B с лидерной последовательностью)
(химерная A LC κ с лидерной последовательностью)
(химерная A HC IgG-1)
(химерная A LC κ)
(Агликозилированная химерная A LC κ)
(канинизированная A HC v3 IgG-B с лидерной последовательностью)
(канинизированная A HC v4 IgG-B с лидерной последовательностью)
(канинизированная A LC κ с лидерной последовательностью)
(канинизированная A HC v3 IgG-B)
(канинизированная A HC v4 IgG-B)
(канинизированная A LC κ)
(фелинизированная A HC)
(фелинизированная A LC)
Q16E
I13M
H2N
R8K
S15T
L21F
M34I
F36Y
V3Q
T7S
S9P
L10V
N22S
S3P
L8I
(Mab B HC)
HC-FR1 Q16E
HC-FR2 I13M
HC-FR3 H2N
HC-FR3 R8K
HC-FR3 S15T
HC-FR3 L21F
HC-FR3 M34I
HC-FR3 F36Y
(Mab B HC v2)
(Mab B LC)
LC-FR1 V3Q
LC-FR1 T7S
LC-FR1 S9P
LC-FR1 L10V
LC-FR1 N22S
LC-FR3 S3P
LC-FR4 L8I
(Mab B LC v2)
(химерная B HC IgG-B)
HC-FR1 Q16E
HC-FR2 I13M
HC-FR3 H2N
HC-FR3 R8K
HC-FR3 S15T
HC-FR3 L21F
HC-FR3 M34I
HC-FR3 F36Y
(химерная B HC v2 IgG-B)
(химерная B LC κ)
LC-FR1 V3Q
LC-FR1 T7S
LC-FR1 S9P
LC-FR1 L10V
LC-FR1 N22S
LC-FR3 S3P
LC-FR4 L8I
(химерная B LC v2 κ)
(собачья химерная B HC с лидерной последовательностью)
HC-FR1 Q16E
HC-FR2 I13M
HC-FR3 H2N
HC-FR3 R8K
HC-FR3 S15T
HC-FR3 L21F
HC-FR3 M34I
HC-FR3 F36Y
(собачья химерная B HC v2 IgG-B с лидерной последовательностью)
(собачья химерная B LC κ с лидерной последовательностью)
LC-FR1 V3Q
LC-FR1 T7S
LC-FR1 S9P
LC-FR1 L10V
LC-FR1 N22S
LC-FR3 S3P
LC-FR4 L8I
(собачья химерная B LC v2 κ с лидерной последовательностью)
(кошачья химерная B HC IgG-1)
(кошачья химерная B LC κ)
(агликозилированная кошачья химерная B LC κ)
(канинизированная B HC v3 IgG-B с лидерной последовательностью)
(канинизированная B LC κ с лидерной последовательностью)
(канинизированная B HC v3 IgG-B)
(канинизированная B LC v3 κ)
Мутант с усиленным связыванием CD16
S10D
Мутант с усиленным связыванием CD16
S10E
Мутант с усиленным связыванием CD16
I103D
Мутант с усиленным связыванием CD16
I103E
Мутант с усиленным связыванием CD16
S10D
I103D
Мутант с усиленным связыванием CD16
S10D
I103E
Мутант с усиленным связыванием CD16
S10E
I103D
Мутант с усиленным связыванием CD16
S10E
I103E
ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0018] Предложены антитела, которые связываются с парвовирусом псовых и/или парвовирусом кошачьих. Также предложены тяжелые цепи и легкие цепи антител, которые способны образовывать антитела, связывающие парвовирус псовых и/или парвовирус кошачьих. Кроме того, предложены антитела, тяжелые цепи и легкие цепи, содержащие одну или более конкретных определяющих комплементарность областей (CDR). Предложены полинуклеотиды, кодирующие антитела к парвовирусу псовых и/или парвовирусу кошачьих. Также предложены способы получения или очистки антител к парвовирусу псовых и/или парвовирусу кошачьих. Предложены способы обеспечения пассивного иммунитета к заражению парвовирусом псовых или кошачьих и/или лечения парвовирусной инфекции с помощью антител к парвовирусу псовых и/или парвовирусу кошачьих.
[0019] Для удобства читателя ниже представлены определения терминов, используемых в настоящем описании.
[0020] Используемые в настоящем описании числовые значения, такие как Kd, рассчитываются на основе научных измерений и, таким образом, подвержены соответствующей погрешности измерения. В некоторых случаях числовой термин может включать числовые значения, округленные до ближайшего значащего числа.
[0021] В контексте настоящего описания единственное число означает «по меньшей мере один» или «один или более», если не указано иное. В контексте настоящего описания термин «или» означает «и/или», если не указано иное. В контексте множественных зависимых пунктов формулы изобретения «или» при обратной ссылке на другие пункты формулы изобретения относится только к этим пунктам формулы в качестве альтернативы.
Иллюстративные антитела к парвовирусу
[0022] Предложены новые антитела, направленные против парвовируса, например антитела, которые связываются с парвовирусом псовых и/или парвовирусом кошачьих. Представленные в настоящем описании антитела к парвовирусу включают, без ограничения, моноклональные антитела, химерные антитела, канинизированные антитела и фелинизированные антитела.
[0023] Также в настоящем описании представлены аминокислотные последовательности моноклональных антител к парвовирусу. Например, представлены CDR вариабельной тяжелой цепи (SEQ ID NO: 4-6), CDR вариабельной легкой цепи (SEQ ID NO: 13-15), каркасные последовательности вариабельной тяжелой цепи (SEQ ID NO: 7 и 8-11) и каркасные последовательности вариабельной легкой цепи (SEQ ID NO: 16-19) Mab A. Также представлены CDR вариабельной тяжелой цепи (SEQ ID NO: 42-44), CDR вариабельной легкой цепи (SEQ ID NO: 52-54), каркасные последовательности вариабельной тяжелой цепи (SEQ ID NO: 45, 47, 49 и 51) и каркасные последовательности вариабельной легкой цепи (SEQ ID NO: 55, 57, 58 и 60) Mab B. Представлены аминокислотные последовательности вариабельной тяжелой цепи и вариабельной легкой цепи Mab A (SEQ ID NO: 20 и 22, соответственно). Представлены аминокислотные последовательности вариабельной тяжелой цепи и вариабельной легкой цепи Mab B (SEQ ID NO: 62 и 64, соответственно).
[0024] Кроме того, представлены аминокислотные последовательности CDR, каркасные последовательности, вариабельные тяжелые и легкие цепи вариантов антител Mab A и Mab B. Представлены CDR вариабельной тяжелой цепи (SEQ ID NO: 4-6), каркасные участки вариабельной тяжелой цепи (SEQ ID NO: 8-10 и 12), вариабельная тяжелая цепь (SEQ ID NO: 21), CDR вариабельной легкой цепи (SEQ ID NO: 13-15), каркасные участки вариабельной легкой цепи (SEQ ID NO: 16-19) и вариабельная легкая цепь (SEQ ID NO: 22) Mab A варианта 2 (v2). Представлены CDR вариабельной тяжелой цепи (SEQ ID NO: 42-44), каркасные участки вариабельной тяжелой цепи (SEQ ID NO: 46, 48, 50 и 51), вариабельная тяжелая цепь (SEQ ID NO: 63), CDR вариабельной легкой цепи (SEQ ID NO: 52-54), каркасные участки вариабельной легкой цепи (SEQ ID NO: 56, 57, 59 и 61) и вариабельная легкая цепь (SEQ ID NO: 65) Mab B варианта 2 (v2).
[0025] В настоящем описании также представлены химерные собачьи, химерные кошачьи, канинизированные и фелинизированные антитела, полученные из Mab A, Mab B, Mab A v2 и Mab B v2. В некоторых вариантах осуществления представлены аминокислотные последовательности канинизированных и фелинизированных Mab A, Mab B, Mab A v2 и Mab B v2, такие как SEQ ID NO: 34-41, 88, 77-80, 88 и 89. В некоторых вариантах осуществления представлены аминокислотные последовательности химерных антител, полученные из Mab A, Mab B, Mab A v2 и Mab B v2, такие как SEQ ID NO: 23-25, 28-33 и 66-76.
[0026] В контексте настоящего описания термин «антитело» используется в самом широком смысле и охватывает различные структуры антител, включая, помимо прочего, моноклональные антитела, поликлональные антитела, полиспецифические антитела (например, биспецифические (такие как би-специфические вовлекающие Т-клетки) и триспецифические антитела) и фрагменты антител (такие как Fab, F(ab')2, ScFv, минитело, диатело, триантитело и тетратело) при условии, что они проявляют желаемую антигенсвязывающую активность. Виды псовых, кошачьих и лошадиных имеют разные разновидности (классы) антител, которые являются общими для многих млекопитающих.
[0027] Термин антитело включает, без ограничения, фрагменты, которые способны связываться с антигеном, такие как Fv, одноцепочечный Fv (scFv), Fab, Fab', dis-scFv, sdAb (однодоменное антитело) и (Fab')2 (включая химически связанный F(ab')2). Расщепление антител папаином дает два идентичных антигенсвязывающих фрагмента, называемых Fab-фрагментами, каждый из которых имеет один антигенсвязывающий участок, и остаточный Fc-фрагмент, название которого отражает его способность легко кристаллизоваться. Обработка пепсином дает фрагмент F(ab’)2, который имеет два антигенсвязывающих участка и все еще способен связывать антиген. Термин «антитело» также включает, без ограничения, химерные антитела, гуманизированные антитела и антитела различных видов, таких как мышиные, человеческие, антитело яванского макака, антитела псовых, кошачьих, лошадиных и т.д. Кроме того, для всех представленных в настоящем описании конструкций антител также предложены варианты, имеющие последовательности из других организмов. Таким образом, если описана мышиная версия антитела, специалисту в данной области известно, как трансформировать антитело на основе мышиной последовательности в последовательность кошки, собаки, лошади и т.д. Фрагменты антител также включают любую ориентацию одноцепочечных scFv, тандемных ди-scFv, диател, тандемных три-sdcFv, минител и т.д. Фрагменты антител также включают нанотела (sdAb, антитело, имеющее один мономерный домен, такой как пара вариабельных доменов тяжелых цепей, без легкой цепи). В некоторых вариантах осуществления фрагмент антитела может относиться к определенному виду (например, мышиный scFv или собачий scFv). Это означает последовательности по меньшей мере части областей, отличных от CDR, а не источник конструкции. В некоторых вариантах осуществления антитела содержат метку или конъюгированы со вторым фрагментом.
[0028] Термины «метка» и «детектируемая метка» означают фрагмент, присоединенный к антителу или его аналиту, что позволяет сделать реакцию (например, связывание) между членами пары специфического связывания детектируемой. Меченый член пары специфического связывания называется «детектируемо меченым». Таким образом, термин «меченый связывающий белок» относится к белку с включенной меткой, которая обеспечивает идентификацию связывающего белка. В некоторых вариантах осуществления метка представляет собой детектируемый маркер, который может генерировать сигнал, детектируемый с помощью визуальных или инструментальных средств, например, включение меченой радиоактивной меткой аминокислоты или прикрепление к полипептиду биотинильных фрагментов, которые можно детектировать с помощью меченого авидина (например, стрептавидина, содержащего флуоресцентный маркер или ферментативную активность, которую можно обнаружить оптическими или колориметрическими методами). Примеры меток для полипептидов включают, без ограничения, следующие: радиоизотопы или радионуклиды (например, 3H, 14C, 35S, 90Y, 99Tc, 111In, 125I, 131I, 177Lu, 166Ho или 153Sm); хромогены, флуоресцентные метки (например, FITS, родамин, лантанидные люминофоры), ферментативные метки (например, пероксидазу хрена, люциферазу, щелочную фосфатазу); хемилюминесцентные маркеры; биотинильные группы; предопределенные полипептидные эпитопы, распознаваемые вторичным репортером (например, парные последовательности лейциновой молнии, сайты связывания вторичных антител, металл-связывающие домены, эпитопные метки); и магнитные агенты, такие как хелаты гадолиния. Репрезентативные примеры меток, обычно используемых для иммунологических анализов, включают фрагменты, которые продуцируют свет, например соединения акридиния, и фрагменты, которые продуцируют флуоресценцию, например флуоресцеин. В этом отношении сам фрагмент может не быть детектируемо меченным, но может стать детектируемым в результате реакции с еще одним фрагментом.
[0029] Термин «моноклональное антитело» относится к антителу из по существу однородной популяции антител, т.е. отдельные антитела, составляющие популяцию, являются идентичными за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела обладают высокой специфичностью и направлены против одного антигенного сайта. Более того, в отличие от препаратов поликлональных антител, которые обычно включают разные антитела, направленные против разных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты антигена. Таким образом, образец моноклонального антитела может связываться с одним и тем же эпитопом на антигене. Модификатор «моноклональный» указывает на то, что антитело получено из по существу однородной популяции антител, и его не следует толковать как требующий получения антитела каким-либо конкретным способом. Например, моноклональные антитела могут быть получены методом гибридомы, впервые описанным Kohler and Milstein, 1975, Nature 256:495, или могут быть получены методами рекомбинантной ДНК, такими как описанные в патенте США № 4,816,567. Моноклональные антитела также могут быть выделены из фаговых библиотек, созданных методами, описанными, например, в McCafferty et al., 1990, Nature 348:552-554.
[0030] В некоторых вариантах осуществления моноклональное антитело представляет собой Mab A, Mab A v2, Mab B или Mab B v2.
[0031] «Аминокислотная последовательность» означает последовательность аминокислотных остатков в пептиде или белке. Термины «полипептид» и «белок» используются взаимозаменяемо для обозначения полимера из аминокислотных остатков и не ограничены минимальной длиной. Такие полимеры аминокислотных остатков могут содержать природные или неприродные аминокислотные остатки и включают, без ограничения, пептиды, олигопептиды, димеры, тримеры и мультимеры аминокислотных остатков. Под это определение попадают как полноразмерные белки, так и их фрагменты. Термины также включают пост-экспрессионные модификации полипептида, например, гликозилирование, сиалирование, ацетилирование, фосфорилирование и т.п. Кроме того, для целей настоящего изобретения «полипептид» относится к белку, который включает модификации, такие как делеции, добавления и замены (обычно консервативные по своей природе), в нативной последовательности с сохранением белком желаемой активности. Эти модификации могут быть преднамеренными, например, в результате направленного мутагенеза, или могут быть случайными, например, в результате мутаций хозяев, которые продуцируют белки, или ошибок из-за амплификации ПЦР.
[0032] «Парвовирус», используемый в настоящем описании, относится к любому встречающемуся в природе парвовирусу или варианту парвовируса и включает парвовирус псовых (CPV), такой как CPV-2a, CPV-2b и CPV-2c, и парвовирус кошачьих (вирус панлейкопении).
[0033] В контексте настоящего описания термин «эпитоп» относится к участку молекулы-мишени (например, антигена, такого как белок, нуклеиновая кислота, углевод или липид), к которому присоединяется антигенсвязывающая молекула (например, антитело, фрагмент антитела или каркасный белок, содержащий участки связывания антитела). Эпитопы часто включают химически активную поверхностную группу молекул, таких как аминокислоты, полипептиды или боковые цепи сахаров, и имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. Эпитопы могут быть образованы как из непрерывных, так и из смежных не являющихся непрерывными остатков (например, аминокислот, нуклеотидов, сахаров, липидного фрагмента) молекулы-мишени. Эпитопы, образованные из непрерывных остатков (например, аминокислот, нуклеотидов, сахаров, липидного фрагмента), обычно сохраняются при воздействии денатурирующих растворителей, тогда как эпитопы, образованные в результате третичной укладки, обычно теряются при обработке денатурирующими растворителями. Эпитоп может включать по меньшей мере 3, по меньшей мере 5 или 8-10 остатков (например, аминокислот или нуклеотидов), без ограничения. В некоторых примерах эпитоп имеет в длину менее 20 остатков (например, аминокислот или нуклеотидов), менее 15 остатков или менее 12 остатков. Два антитела могут связываться с одним и тем же эпитопом внутри антигена, если они демонстрируют конкурентное связывание с антигеном. В некоторых вариантах осуществления эпитоп можно идентифицировать по определенному минимальному расстоянию до остатка CDR на антигенсвязывающей молекуле. В некоторых вариантах осуществления эпитоп можно идентифицировать по указанному выше расстоянию и, кроме того, он может быть ограничен остатками, участвующими в связи (например, водородной связи) между остатком антитела и остатком антигена. Эпитоп также может быть идентифицирован с помощью различных сканирований, например, аланиновое или аргининовое сканирование может указывать на один или более остатков, с которыми может взаимодействовать антигенсвязывающая молекула. Если не указано иное, набор остатков в качестве эпитопа не исключает другие остатки, являющиеся частью эпитопа для конкретного антитела. Скорее наличие такого набора обозначает минимальную серию (или набор видов) эпитопов. Таким образом, в некоторых вариантах осуществления набор остатков, идентифицированный как эпитоп, обозначает минимальный эпитоп, релевантный для антигена, а не исключительный список остатков эпитопа на антигене.
[0034] В некоторых вариантах осуществления эпитоп содержит аминокислотную последовательность SEQ ID NO: 1, SEQ ID NO: 2 и/или SEQ ID NO: 3.
[0035] Термин «CDR» означает определяющую комплементарность область, которую специалист в данной области может определить с помощью по меньшей мере одного способа идентификации. В некоторых вариантах осуществления CDR могут быть определены в соответствии с любой из схем нумерации: по Чотиа (Chothia), по Кабат (Kabat), комбинацией Кабат и Чотиа, определением AbM, определением контакта или комбинацией Кабат, Чотиа, определения AbM или контакта. Различные CDR в антителе могут быть обозначены соответствующим номером и типом цепи, включая, помимо прочего, CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3. В контексте настоящего описания термин «CDR» также используется для обозначения «гипервариабельной области» или HVR, включая гипервариабельные петли.
[0036] В некоторых вариантах осуществления антитело к парвовирусу содержит тяжелую цепь, содержащую (а) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4; (b) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5; или (c) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6. В некоторых вариантах осуществления антитело к парвовирусу содержит легкую цепь, содержащую (a) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13; (b) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14; или (c) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15.
[0037] В некоторых вариантах осуществления антитело к парвовирусу содержит тяжелую цепь, содержащую (а) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 42; (b) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 43; или (c) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 44. В некоторых вариантах осуществления антитело к парвовирусу содержит легкую цепь, содержащую (a) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 52; (b) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 53; или (c) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 54.
[0038] В некоторых вариантах осуществления антитело к парвовирусу содержит тяжелую цепь, содержащую (а) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-H1 заменены другой аминокислотой; (b) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-H2 заменены другой аминокислотой; и/или (c) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-H3 заменены другой аминокислотой. В некоторых вариантах осуществления антитело к парвовирусу содержит легкую цепь, содержащую (а) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-L1 заменены другой аминокислотой; (b) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-L2 заменены другой аминокислотой; и/или (c) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-L3 заменены другой аминокислотой.
[0039] В некоторых вариантах осуществления антитело к парвовирусу содержит тяжелую цепь, содержащую (а) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 42, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-H1 заменены другой аминокислотой; (b) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 43, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-H2 заменены другой аминокислотой; и/или (c) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 44, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-H3 заменены другой аминокислотой. В некоторых вариантах осуществления антитело к парвовирусу содержит легкую цепь, содержащую (а) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 52, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-L1 заменены другой аминокислотой; (b) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 53, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-L2 заменены другой аминокислотой; и/или (c) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 54, или ее вариант, в котором 1, 2 или 3 аминокислоты CDR-L3 заменены другой аминокислотой.
[0040] В контексте настоящего описания термин «вариабельная область» относится к области, содержащей по меньшей мере три CDR. В некоторых вариантах осуществления вариабельная область включает три CDR и по меньшей мере один каркасный участок («FR»). Термины «вариабельная область тяжелой цепи» или «вариабельная тяжелая цепь» используются взаимозаменяемо для обозначения области, содержащей по меньшей мере три CDR тяжелой цепи. Термины «вариабельная область легкой цепи» или «вариабельная легкая цепь» используются взаимозаменяемо для обозначения области, содержащей по меньшей мере три CDR легкой цепи. В некоторых вариантах осуществления вариабельная тяжелая цепь или вариабельная легкая цепь содержат по меньшей мере один каркасный участок. В некоторых вариантах осуществления антитело содержит по меньшей мере один каркасный участок тяжелой цепи, выбранный из HC-FR1, HC-FR2, HC-FR3 и HC-FR4. В некоторых вариантах осуществления антитело содержит по меньшей мере один каркасный участок легкой цепи, выбранный из LC-FR1, LC-FR2, LC-FR3 и LC-FR4. Каркасные участки могут быть расположены смежно между CDR легкой цепи или между CDR тяжелой цепи. Например, антитело может содержать вариабельную тяжелую цепь, имеющую следующую структуру: (HC-FR1)-(CDR-H1)-(HC-FR2)-(CDR-H2)-(HC-FR3)-(CDR-H3)-(HC-FR4). Антитело может содержать вариабельную тяжелую цепь, имеющую следующую структуру: (CDR-H1)-(HC-FR2)-(CDR-H2)-(HC-FR3)-(CDR-H3). Антитело также может содержать вариабельную легкую цепь, имеющую следующую структуру: (LC-FR1)-(CDR-L1)-(LC-FR2)-(CDR-L2)-(LC-FR3)-(CDR-L3)-(LC-FR4). Антитело также может содержать вариабельную легкую цепь, имеющую следующую структуру: (CDR-L1)-(LC-FR2)-(CDR-L2)-(LC-FR3)-(CDR-L3).
[0041] В некоторых вариантах осуществления антитело к парвовирусу содержит одно или более из: (а) последовательности каркасного участка 1 вариабельной области тяжелой цепи (HC FR1) SEQ ID NO: 7 или SEQ ID NO: 8, (b) последовательности HC-FR2 SEQ ID NO: 9, (c) последовательности HC-FR3 SEQ ID NO: 10, (d) последовательности HC-FR4 SEQ ID NO: 11 или SEQ ID NO: 12, (e) последовательности каркасного участка 1 вариабельной области легкой цепи (LC-FR1) SEQ ID NO: 16, (f) последовательности LC-FR2 SEQ ID NO: 17, (g) последовательности LC-FR3 SEQ ID NO: 18, или (h) последовательности LC-FR4 SEQ ID NO: 19.
[0042] В некоторых вариантах осуществления антитело к парвовирусу содержит одно или более из: (а) последовательности каркасного участка 1 вариабельной области тяжелой цепи (HC FR1) SEQ ID NO: 45 или SEQ ID NO: 46, (b) последовательности HC-FR2 SEQ ID NO: 47 или SEQ ID NO: 48, (c) последовательности HC-FR3 SEQ ID NO: 49 или SEQ ID NO: 50, (d) последовательности HC-FR4 SEQ ID NO: 51, (e) последовательности каркасного участка 1 вариабельной области легкой цепи (LC-FR1) SEQ ID NO: 55 или SEQ ID NO: 56, (f) последовательности LC-FR2 SEQ ID NO: 57, (g) последовательности LC-FR3 SEQ ID NO: 58 или SEQ ID NO: 59, или (h) последовательности LC-FR4 SEQ ID NO: 60.
[0043] В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной легкой цепи SEQ ID NO: 22, SEQ ID NO: 87, SEQ ID NO: 41, SEQ ID NO: 64, SEQ ID NO: 65, SEQ ID NO: 89, SEQ ID NO: 82 или SEQ ID NO: 84. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 85, SEQ ID NO: 86, SEQ ID NO: 40, SEQ ID NO: 62, SEQ ID NO: 63, SEQ ID NO: 88, SQ ID NO: 81 или SEQ ID NO: 83.
[0044] В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 20 и последовательность вариабельной легкой цепи SEQ ID NO: 22. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 21 и последовательность вариабельной легкой цепи SEQ ID NO: 22. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 85 и последовательность вариабельной легкой цепи SEQ ID NO: 87. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 86 и последовательность вариабельной легкой цепи SEQ ID NO: 87. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 40 и последовательность вариабельной легкой цепи SEQ ID NO: 41. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 62 и последовательность вариабельной легкой цепи SEQ ID NO: 64 или SEQ ID NO: 65. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 63 и последовательность вариабельной легкой цепи SEQ ID NO: 64 или SEQ ID NO: 65. В некоторых вариантах осуществления антитело к парвовирусу содержит последовательность вариабельной тяжелой цепи SEQ ID NO: 88, и последовательность вариабельной легкой цепи SEQ ID NO: 89.
[0045] Термин «константная область», используемый в настоящем описании, относится к области, содержащей по меньшей мере три константных домена. Термины «константная область тяжелой цепи» или «константная тяжелая цепь» используются взаимозаменяемо для обозначения области, содержащей по меньшей мере три константных домена тяжелой цепи, СН1, СН2 и СН3. Неограничивающие примеры константных областей тяжелой цепи включают γ, δ, α, ε и μ. Каждая константная область тяжелой цепи соответствует изотипу антитела. Например, антитело, содержащее константную область γ, представляет собой антитело IgG, антитело, содержащее константную область δ, представляет собой антитело IgD, антитело, содержащее константную область α, представляет собой антитело IgA, антитело, содержащее константную область μ, представляет собой антитело IgM, и антитело, содержащее константную область ε, представляет собой антитело IgE. Некоторые изотипы могут быть дополнительно подразделены на подклассы. Например, антитела IgG включают, без ограничения, антитела IgG1 (содержащие константную область γ1), IgG2 (содержащие константную область γ2), IgG3 (содержащие константную область γ3) и IgG4 (содержащие константную область γ4); антитела IgA включают, без ограничения, антитела IgA1 (содержащие константную область α1) и IgA2 (содержащие константную область α2); и антитела IgM включают, без ограничения, IgM1 и IgM2. Термины «константная область легкой цепи» или «константная легкая цепь» используются взаимозаменяемо для обозначения области, содержащей константный домен легкой цепи, CL. Неограничивающие типичные константные области легкой цепи включают λ и κ. Делеции и замены в пределах доменов, не изменяющие функцию, входят в объем термина «константная область», если не указано иное. У представителей псовых и кошачьих имеются классы антител, такие как IgG, IgA, IgD, IgE и IgM. В класс антител IgG псовых входят IgG-A, IgG-B, IgG C и IgG-D. В класс антител IgG кошачьих входят IgG1, IgG2a и IgG2b.
[0046] Термин «химерное антитело» или «химерный» относится к антителу, в котором часть тяжелой цепи или легкой цепи получена из конкретного источника или вида, в то время как по меньшей мере часть остатка тяжелой цепи или легкой цепи происходит из другого источника или вида. В некоторых вариантах осуществления химерное антитело относится к антителу, содержащему по меньшей мере одну вариабельную область от первого вида (например, мыши, крысы, яванского макака и т.д.) и по меньшей мере одну константную область от второго вида (например, человека, собаки, кошки, лошади и др.). В некоторых вариантах осуществления химерное антитело содержит по меньшей мере одну мышиную вариабельную область и по меньшей мере одну собачью константную область. В некоторых вариантах осуществления химерное антитело содержит по меньшей мере одну мышиную вариабельную область и по меньшей мере одну кошачью константную область. В некоторых вариантах осуществления все вариабельные области химерного антитела относятся к первому виду, а все константные области химерного антитела относятся ко второму виду. В некоторых вариантах осуществления химерное антитело содержит константную область тяжелой цепи или константную область легкой цепи от животного-компаньона. В некоторых вариантах осуществления химерное антитело содержит мышиные вариабельные тяжелые и легкие цепи и константные тяжелые и легкие цепи животного-компаньона. Например, химерное антитело может содержать мышиные вариабельные тяжелые и легкие цепи и собачьи константные тяжелые и легкие цепи; химерное антитело может содержать мышиные вариабельные тяжелые и легкие цепи и кошачьи константные тяжелые и легкие цепи; или химерное антитело может содержать мышиные вариабельные тяжелые и легкие цепи и лошадиные константные тяжелые и легкие цепи.
[0047] В некоторых вариантах осуществления антитело к парвовирусу содержит химерное антитело, содержащее: (a) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 23; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 25; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); (b) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 24; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 25; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); (c) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 31; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 32; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); (d) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 31; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 33; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); (e) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 66; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 68; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); (f) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 67; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 69; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); (g) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 74; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 75; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii); или (h) (i) аминокислотную последовательность тяжелой цепи SEQ ID NO: 74; (ii) аминокислотную последовательность легкой цепи SEQ ID NO: 75; или (iii) аминокислотную последовательность тяжелой цепи, как определено в (i), и последовательность легкой цепи, как определено в (ii).
[0048] «Собачье химерное», «химерное собачье» или «собачье химерное антитело» относятся к химерным антителам, имеющим по меньшей мере часть тяжелой цепи или часть легкой цепи, полученную от собаки. «Кошачье химерное», «химерное кошачье» или «кошачье химерное антитело» относятся к химерному антителу, имеющему по меньшей мере часть тяжелой цепи или часть легкой цепи, полученную от кошки. В некоторых вариантах осуществления собачье химерное антитело содержит мышиные или крысиные вариабельные тяжелые и легкие цепи и собачьи константные тяжелые и легкие цепи. В некоторых вариантах осуществления кошачье химерное антитело содержит мышиные или крысиные вариабельные тяжелые и легкие цепи и кошачьи константные тяжелые и легкие цепи.
[0049] В некоторых вариантах осуществления антитело к парвовирусу содержит собачью константную область тяжелой цепи, выбранную из константной области IgG-A, IgG-B, IgG-C и IgG-D.
[0050] В некоторых вариантах осуществления антитело к парвовирусу содержит кошачью константную область тяжелой цепи, выбранную из константной области IgG1, IgG2a и IgG2b.
[0051] «Канинизированное антитело» означает антитело, в котором по меньшей мере одна аминокислота в части вариабельной области, не относящейся к собачьей (несобачьей), заменена соответствующей аминокислотой из собачьей вариабельной области. В некоторых вариантах осуществления канинизированное антитело содержит по меньшей мере одну собачью константную область (например, константную область γ, константную область α, константную область δ, константную область ε, константную область μ и т.д.) или ее фрагмент. В некоторых вариантах осуществления канинизированное антитело представляет собой фрагмент антитела, такой как Fab, scFv, (Fab')2 и т.д. Термин «канинизированный» также означает формы несобачьих (например, мышиных) антител, которые представляют собой химерные иммуноглобулины, иммуноглобулиновые цепи или их фрагменты (такие как Fv, Fab, Fab', F(ab')2 или другие антигенсвязывающие последовательности антител), которые содержат минимальную последовательность несобачьего иммуноглобулина. Канинизированные антитела могут включать собачьи иммуноглобулины (реципиентное антитело), в которых остатки из CDR реципиента заменены остатками из CDR видов, не относящихся к собачьим (донорское антитело), таких как мышь, крыса или кролик, с желаемой специфичностью, сродством и емкостью. В некоторых случаях остатки каркасного участка Fv (FR) собачьего иммуноглобулина заменены соответствующими остатками, не относящимися к собачьим. Кроме того, канинизированное антитело может содержать остатки, которые не обнаруживаются ни в антителе-реципиенте, ни в импортированных CDR или каркасных последовательностях, но включены для дальнейшего уточнения и оптимизации характеристик антитела.
[0052] В некоторых вариантах осуществления по меньшей мере один аминокислотный остаток в части крысиной или мышиной вариабельной области тяжелой цепи или крысиной или мышиной вариабельной области легкой цепи заменены соответствующей аминокислотой из собачьей вариабельной области. В некоторых вариантах осуществления модифицированная цепь слита с собачьей константной тяжелой цепью или собачьей константной легкой цепью.
[0053] «Фелинизированное антитело» означает антитело, в котором по меньшей мере одна аминокислота в части вариабельной области, не относящейся к кошачьей (некошачьей), заменена соответствующей аминокислотой из кошачьей вариабельной области. В некоторых вариантах осуществления кошачье антитело содержит по меньшей мере одну кошачью константную область (например, константную область γ, константную область α, константную область δ, константную область ε, константную область μ и т.д.) или ее фрагмент. В некоторых вариантах осуществления фелинизированное антитело представляет собой фрагмент антитела, такой как Fab, scFv, (Fab')2 и т.д. Термин «фелинизированный» также означает формы некошачьих (например, мышиных) антител, которые представляют собой химерные иммуноглобулины, иммуноглобулиновые цепи или их фрагменты (такие как Fv, Fab, Fab', F(ab')2 или другие антигенсвязывающие последовательности антител), которые содержат минимальную последовательность некошачьего иммуноглобулина. Фелинизированные антитела могут включать кошачьи иммуноглобулины (реципиентное антитело), в которых остатки из CDR реципиента заменены остатками из CDR вида, не относящегося к кошачьим (донорное антитело), такого как мышь, крыса или кролик, с желаемой специфичностью, сродством и емкостью. В некоторых случаях остатки каркасного участка Fv (FR) кошачьего иммуноглобулина заменены соответствующими остатками, не относящимися к кошачьим. Кроме того, фелинизированное антитело может содержать остатки, которые не обнаружены ни в реципиентном антителе, ни в импортированных CDR или каркасных последовательностях, но включены для дальнейшего уточнения и оптимизации характеристик антитела.
[0054] В некоторых вариантах осуществления по меньшей мере один аминокислотный остаток в части мышиной вариабельной тяжелой цепи или мышиной вариабельной легкой цепи заменен соответствующей аминокислотой из кошачьей вариабельной области. В некоторых вариантах осуществления модифицированная цепь слита с кошачьей константной тяжелой цепью или собачьей константной легкой цепью.
[0055] «Фрагмент кристаллизующегося полипептида» или «полипептид Fc» представляет собой часть молекулы антитела, которая взаимодействует с эффекторными молекулами и клетками. Он содержит С-концевые участки тяжелых цепей иммуноглобулина. Используемый в настоящем описании полипептид Fc включает фрагменты Fc-домена, обладающие одной или более биологическими активностями целого полипептида Fc. «Эффекторная функция» полипептида Fc представляет собой действие или активность, осуществляемую полностью или частично любым антителом в ответ на раздражитель, и может включать фиксацию комплемента и/или индукцию ADCC (антителозависимой клеточной цитотоксичности) и/или ADCP (антителозависимого клеточного фагоцитоза).
[0056] В некоторых вариантах осуществления биологическая активность полипептида Fc представляет собой способность связывать FcRn. В некоторых вариантах осуществления биологическая активность полипептида Fc представляет собой способность связывать C1q. В некоторых вариантах осуществления биологическая активность полипептида Fc представляет собой способность связывать CD16. В некоторых вариантах осуществления биологическая активность полипептида Fc представляет собой способность связывать белок А.
[0057] Термин «Fc IgX» означает, что Fc-область получена из определенного изотипа антитела (например, IgG, IgA, IgD, IgE, IgM и т. д.), где «X» обозначает изотип антитела. Так, «Fc IgG» обозначает Fc-область γ-цепи, «Fc IgA» обозначает Fc-область α-цепи, «Fc IgD» обозначает Fc-область δ-цепи, «Fc IgE» обозначает Fc-область ε-цепи, «Fc IgM» обозначает Fc-область μ-цепи и т.д. В некоторых вариантах осуществления Fc-область IgG содержит CH1, шарнир, CH2, CH3 и CL1. «IgX-N-Fc» означает, что Fc-область получена из определенного подкласса изотипа антитела (например, собачьего IgG подкласса A, B, C или D; или кошачьего IgG подкласса 1, 2a или 2b), где «N» обозначает подкласс. В некоторых вариантах осуществления Fc-области IgX или IgX-N-Fc происходят от домашнего животного, такого как собака или кошка. В некоторых вариантах осуществления Fc-области IgG выделяют из собачьих тяжелых цепей γ, таких как IgG-A, IgG-B, IgG-C или IgG-D. В некоторых случаях Fc-области IgG выделяют из кошачьих тяжелых цепей γ, таких как IgG1, IgG2a или IgG2b. Антитела, содержащие Fc-область IgG-A, IgG-B, IgG-C или IgG-D, могут обеспечивать более высокие уровни экспрессии в системах рекомбинантного продуцирования.
[0058] Термины «Fc IgX» и «полипептид Fc IgX» включают полипептиды Fc IgX дикого типа и варианты полипептидов Fc IgX, если не указано иное.
[0059] В некоторых вариантах осуществления вариант полипептида Fc IgG содержит вариант полипептида Fc IgG видов животных-компаньонов. В некоторых вариантах осуществления вариант полипептида Fc IgG содержит вариант полипептида Fc собачьего IgG или полипептид Fc кошачьего IgG. В некоторых вариантах осуществления вариант полипептида Fc IgG (например, вариант полипептида Fc собачьего IgG-A, вариант полипептида Fc собачьего IgG-C или вариант полипептида Fc собачьего IgG-D, вариант полипептида Fc кошачьего IgG1a, вариант Fc кошачьего IgG1b полипептид или вариант полипептида Fc кошачьего IgG2) обладает активностью, которая по существу отсутствует у эталонного полипептида (например, дикого типа).
[0060] Антитело может быть модифицировано для увеличения или уменьшения периода его полувыведения. В некоторых вариантах осуществления, включающих более высокую дозу антитела, для интенсивного лечения может быть желателен более короткий период полувыведения. В некоторых вариантах осуществления, включающих более низкую дозу антитела, для продолжительного лечения может быть желателен более длительный период полувыведения. Например, как обсуждается ниже, в Fc IgG могут быть введены мутации, которые влияют на взаимодействие с FcRn.
[0061] В некоторых вариантах осуществления антитело к парвовирусу содержит Fc IgG дикого типа или вариант, обладающий активностью связывания комплемента (или комплементзависимой цитотоксичностью (CDC)). В некоторых вариантах осуществления антитело к парвовирусу содержит Fc IgG дикого типа или вариант, обладающий активностью антителозависимой клеточной цитотоксичности (ADCC). В некоторых вариантах осуществления антитело к парвовирусу содержит Fc IgG дикого типа или вариант, обладающий активностью антителозависимого клеточного фагоцитоза (ADCP). В некоторых вариантах осуществления антитело к парвовирусу содержит Fc IgG дикого типа или вариант, обладающий активностью связывания комплемента, и/или активностью ADCC, и/или активностью ADCP. Полипептиды Fc IgG могут быть модифицированы для осуществления эффекторной функции или для усиления эффекторной функции.
[0062] В некоторых вариантах осуществления антитело к парвовирусу содержит Fc IgG дикого типа или вариант, который связывается с собачьим FcRn при низком pH. В некоторых вариантах осуществления парвовирус содержит Fc IgG дикого типа или вариант, который связывается с C1q. В некоторых вариантах осуществления парвовирус содержит Fc IgG дикого типа или вариант, который связывается с CD16. В некоторых вариантах осуществления парвовирус содержит вариант Fc IgG, содержащий один или более афукозилированных гликанов.
[0063] В некоторых вариантах осуществления вариант Fc IgG (например, вариант полипептида Fc собачьего IgG или вариант полипептида Fc кошачьего IgG) имеет модифицированное сродство связывания с FcRn по сравнению с эталонным полипептидом. В некоторых вариантах осуществления вариант Fc IgG имеет повышенное сродство связывания с FcRn при кислом рН (например, при рН в диапазоне от примерно 5,0 до примерно 6,5, например, при рН примерно 5,0, рН примерно 5,5, рН примерно 6,0 или рН примерно 6,5) по сравнению с эталонным полипептидом. Примеры вариантов полипептидов Fc IgG, обладающих повышенным сродством связывания с FcRn, раскрыты в WO 2020/082048, которая полностью включена в настоящее описание посредством ссылки.
[0064] В некоторых вариантах осуществления вариант Fc IgG (например, вариант полипептида Fc собачьего IgG или вариант полипептида Fc кошачьего IgG) имеет модифицированное сродство связывания с C1q по сравнению с эталонным полипептидом. В некоторых вариантах осуществления вариант IgG Fc обладает повышенным сродством связывания с C1q по сравнению с эталонным полипептидом. Примеры вариантов полипептидов Fc IgG, обладающих повышенным сродством связывания с C1q, раскрыты в WO 2020/139984 (например, пример 2), которая полностью включена в настоящее описание посредством ссылки.
[0065] В некоторых вариантах осуществления вариант Fc IgG (например, вариант полипептида Fc собачьего IgG или вариант полипептида Fc кошачьего IgG) имеет модифицированное сродство связывания с CD16 по сравнению с эталонным полипептидом. В некоторых вариантах осуществления вариант Fc IgG обладает повышенным сродством связывания с CD16 по сравнению с эталонным полипептидом. Примеры вариантов полипептидов Fc IgG, обладающих повышенным сродством связывания с CD16, раскрыты в WO 2020/139984 (например, пример 2), которая полностью включена в настоящее описание посредством ссылки.
[0066] В некоторых вариантах осуществления вариант Fc собачьего IgG обладает повышенным сродством связывания с CD16 по сравнению с эталонным полипептидом. В некоторых вариантах осуществления вариант Fc IgG содержит а) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 10 SEQ ID NO: 91; b) аспарагиновую кислоту или глутаминовую кислоту в положении 10 SEQ ID NO: 91; c) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 103 SEQ ID NO: 91; d) аспарагиновую кислоту или глутаминовую кислоту в положении 103 SEQ ID NO: 91; e) аспарагиновую кислоту или глутаминовую кислоту в положении, соответствующем положению 10 и/или положению 103 SEQ ID NO: 91; f) аспарагиновую кислоту или глутаминовую кислоту в положении 10 и/или положении 103 SEQ ID NO: 91. В некоторых вариантах осуществления вариант Fc IgG содержит аминокислотную последовательность SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 96, SEQ ID NO: 97, SEQ ID NO: 98 или SEQ ID NO: 99.
[0067] В некоторых вариантах осуществления вариант Fc IgG (например, вариант полипептида Fc собачьего IgG или вариант полипептида Fc кошачьего IgG) имеет модифицированное сродство связывания с белком А по сравнению с эталонным полипептидом. В некоторых вариантах осуществления вариант Fc IgG обладает повышенным сродством связывания с белком А по сравнению с эталонным полипептидом. Примеры вариантов полипептидов Fc IgG, обладающих повышенным сродством связывания с белком А, раскрыты в WO 2020/139984 (например, пример 2), которая полностью включена в настоящее описание посредством ссылки.
[0068] Термин «сродство» означает суммарную силу нековалентных взаимодействий между одним связывающим участком молекулы (например, антитела) и ее партнером по связыванию (например, антигеном). Сродство молекулы X к ее партнеру Y обычно может быть представлено константой диссоциации (KD). Сродство можно измерить обычными способами, известными в данной области, такими как, например, иммуноблоттинг, ELISA KD, KinEx A, биослойная интерферометрия (BLI), или с помощью устройств поверхностного плазмонного резонанса.
[0069] Термины «KD», «Kd», «Kd» или «значение Kd», используемые взаимозаменяемо, относятся к равновесной константе диссоциации взаимодействия антитело-антиген. В некоторых вариантах осуществления Kd антитела измеряют методом биослойной интерферометрии с помощью биосенсора, такого как система Octet® (Pall ForteBio LLC, Фримонт, Калифорния), в соответствии с инструкциями поставщика. Вкратце, биотинилированный антиген связывают с наконечником сенсора, и ассоциацию антител отслеживают в течение девяноста секунд, а диссоциацию отслеживают в течение 600 секунд. Буфер для разведения и связывания представляет собой 20 мМ фосфат, 150 мМ NaCl, рН 7,2. Вычитают пустую кривую, содержащую только буфер, чтобы скорректировать любой дрейф. Данные подгоняют к модели связывания 2:1 с помощью программного обеспечения для анализа данных ForteBio для определения константы скорости ассоциации (kon), константы скорости диссоциации (koff) и Kd. Константу равновесной диссоциации (Kd) вычисляют в виде отношение koff/kon. Термин «kon» относится к константе скорости ассоциации антитела с антигеном, а термин «koff» относится к константе скорости диссоциации антитела из комплекса антитело/антиген.
[0070] Термин «связывается» с антигеном или эпитопом является термином, который хорошо известен в данной области, и способы определения такого связывания также хорошо известны в данной области. Говорят, что молекула демонстрирует «связывание», если она реагирует, связывается или имеет сродство к конкретной клетке или веществу, и эта реакция, ассоциация или сродство выявляются одним или более методами, известными в данной области, такими как, например, иммуноблот, ELISA KD, KinEx A, биослойная интерферометрия (BLI), устройства поверхностного плазмонного резонанса и т.д.
[0071] «Поверхностный плазмонный резонанс» означает оптическое явление, которое позволяет выполнять анализ биоспецифических взаимодействий в реальном времени путем детектирования изменений концентрации белка в матрице биосенсора, например, с помощью системы BIAcoreТМ (BIAcore International AB, компания GE Healthcare, Уппсала, Швеция и Пискатауэй, Нью-Джерси). Дополнительные описания см. в Jonsson et al. (1993) Ann. Biol. Clin. 51:19-26.
[0072] «Биослойная интерферометрия» относится к оптическому аналитическому методу, который позволяет анализировать интерференционную картину света, отраженного от слоя иммобилизованного белка на наконечнике биосенсора и внутреннем эталонном слое. Изменения в количестве молекул, связанных с наконечником биосенсора, вызывают сдвиги в интерференционной картине, которые можно измерить в режиме реального времени. Неограничивающим типичным устройством для биослойной интерферометрии является система Octet® (Pall ForteBio LLC). См., например, Abdiche et al., 2008, Anal. Биохим. 377:209-277.
[0073] В некоторых вариантах осуществления антитело к парвовирусу связывается с парвовирусом псовых или парвовирусом кошачьих с константой диссоциации (Kd) менее 5×10-6 М, менее 1×10-6 М, менее 5×10-7 М, менее 1×10-7 М, менее 5×10-8 М, менее 1×10-8 М, менее 5×10-9 М, менее 1×10-9 М, менее 5×10-10 М, менее 1×10-10 М, менее 5×10-11 М, менее 1×10-11 М, менее 5×10-12 М или менее 1×10-12 M, измеренной методом биослойной интерферометрии. В некоторых вариантах осуществления антитело к парвовирусу связывается с парвовирусом псовых или парвовирусом кошачьих с Kd от 5×10-6 М до 1×10-6 М, от 5×10-6 М до 5×10-7 М, от 5×10-6 М до 1×10-7 М, от 5×10-6 М до 5×10-8 М, от 5×10-6 М до 1×10-8 М, от 5×10-6 М до 5×10-9 М, от 5×10-6 М до 1×10-9 М, от 5×10-6 М до 5×10-10 М, от 5×10-6 М до 1×10-10 М, от 5×10-6 М до 5×10-11 М, от 5×10-6 М до 1×10-11 М, от 5×10-6 М до 5×10-12 М, от 5×10-6 М до 1×10-12 М, от 1×10-6 М до 5×10-7 М, от 1×10-6 М до 1×10-7 М, от 1×10-6 M до 5×10-8 M, от 1×10-6 M до 1×10-8 M, от 1×10-6 M до 5×10-9 M, от 1×10-6 M до 1×10-9 М, от 1×10-6 М до 5×10-10 М, от 1×10-6 М до 1×10-10 М, от 1×10-6 М до 5×10-11 М, от 1×10-6 М до 1×10-11 М, от 1×10-6 М до 5×10-12 М, от 1×10-6 М до 1×10-12 М, от 5×10-7 M до 1×10-7 M, от 5×10-7 M до 5×10-8 M, от 5×10-7 M до 1×10-8 M, от 5×10-7 M до 5×10-9 М, от 5×10-7 М до 1×10-9 М, от 5 ×10-7 М до 5×10-10 М, от 5×10-7 М до 1×10-10 М, от 5×10-7 М до 5×10-11 М, от 5×10-7 М до 1×10-11 М, от 5×10-7 М до 5×10-12 М, от 5×10-7 М до 1×10-12 М, от 1×10-7 М до 5×10-8 М, 1×10-7 М до 1×10-8 М, от 1×10-7 М до 5×10-9 М, от 1×10-7 М до 1×10-9 М, от 1×10-7 М до 5×10-10 М, от 1×10-7 М до 1×10-10 М, от 1×10-7 М до 5×10-11 М, от 1×10-7 М до 1 ×10-11 М, от 1×10-7 М до 5×10-12 М, от 1×10-7 М до 1×10-12 М, от 5×10-8 М до 1×10-8 М, от 5×10-8 М до 5×10-9 М, от 5×10-8 М до 1×10-9 М, от 5×10-8 М до 5×10-10 М, от 5×10-8 М до 1×10-10 М, от 5×10-8 М до 5×10-11 М, от 5×10-8 М до 1×10-11 М, от 5×10-8 М до 5×10-12 М, от 5×10-8 М до 1×10-12 М, от 1×10-8 М до 5×10-9 М, от 1×10-8 М до 1×10-9 М, от 1×10-8 М до 5×10-10 М, от 1×10-8 М до 1×10-10 М, от 1×10-8 М до 5×10-11 М, от 1×10-8 М до 1×10-11 М, от 1×10-8 М до 5×10-12 М, от 1×10-8 М до 1×10-12 М, от 5×10-9 М до 1×10-9 М, от 5×10-9 M до 5×10-10 M, от 5×10-9 M до 1×10-10 M, от 5×10-9 M до 5×10-11 M, от 5×10-9 M до 1×10-11 М, от 5×10-9 М до 5×10-12 М, от 5×10-9 М до 1×10-12 М, от 1×10-9 М до 5×10-10 М, от 1×10-9 М до 1×10-10 М, от 1×10-9 М до 5×10-11 М, от 1×10-9 М до 1×10-11 М, от 1×10-9 M до 5×10-12 M, от 1×10-9 M до 1×10-12 M, от 5×10-10 M до 1×10-10 M, от 5×10-10 M до 5×10-11 М, от 1×10-10 М до 5 ×10-11 М, от 1×10-10 М до 1×10-11 М, от 1×10-10 М до 5 ×10-12 М, от 1×10-10 М до 1×10-12 М, от 5×10-11 М до 1×10-12 М, от 5×10-11 М до 5×10-12 М, от 5×10-11 М до 1 ×10-12 М, от 1×10-11 М до 5×10-12 М, или от 1×10-11 М до 1×10-12 М, измеренной методом биослойной интерферометрии. В некоторых вариантах осуществления антитело к парвовирусу связывается с парвовирусом псовых или парвовирусом кошачьих, что определяют анализом методом иммуноблота.
[0074] «Дикий тип» относится к немутированной версии полипептида, встречающегося в природе, или к его фрагменту. Полипептид дикого типа может быть получен рекомбинантным путем.
[0075] «Вариант» означает биологически активный полипептид, имеющий аминокислотную последовательность, на по меньшей мере примерно 50% идентичную полипептиду с нативной последовательностью после выравнивания последовательностей и введения гэпов, при необходимости, для достижения максимальной процентной идентичности последовательности и без учета каких-либо консервативных замен как части идентичности последовательности. Такие варианты включают, например, полипептиды, в которых один или более аминокислотных остатков добавлены или удалены на N- или С-конце полипептида.
[0076] В некоторых вариантах осуществления вариант имеет по меньшей мере 1, 2, 3, 4 или 5 аминокислот, замененных другой аминокислотой.
[0077] В некоторых вариантах осуществления вариант имеет последовательность, на по меньшей мере примерно 50% идентичную эталонной молекуле нуклеиновой кислоты или полипептиду после выравнивания последовательностей и введения гэпов, при необходимости, для достижения максимальной процентной идентичности последовательности и без учета каких-либо консервативных замен как части идентичности последовательности. Такие варианты включают, например, полипептиды, в которых один или более аминокислотных остатков добавлены или удалены на N- или С-конце полипептида. В некоторых вариантах осуществления вариант имеет последовательность, на по меньшей мере примерно 50%, по меньшей мере примерно 60%, по меньшей мере примерно 65%, по меньшей мере примерно 70%, по меньшей мере примерно 75%, по меньшей мере примерно 80%, по меньшей мере примерно 85%, по меньшей мере примерно 90%, по меньшей мере примерно 95%, по меньшей мере примерно 97%, по меньшей мере примерно 98% или по меньшей мере примерно 99% идентичную последовательности эталонной нуклеиновой кислоты или полипептида.
[0078] Используемый в настоящем описании термин «положение, соответствующее положению n», где n представляет собой любое число, относится к положению аминокислоты рассматриваемого полипептида, которое выровнено по положению n эталонного полипептида после выравнивания аминокислотных последовательностей субъекта и эталонных полипептидов и введения гэпов. Выравнивание с целью определения, соответствует ли положение рассматриваемого полипептида положению n эталонного полипептида, может быть достигнуто различными способами, известными специалистам в данной области, например, с помощью общедоступного компьютерного программного обеспечения, такого как BLAST, BLAST-2, CLUSTAL OMEGA, ALIGN или MEGALIGNТМ (DNASTAR). Специалисты в данной области техники могут определить подходящие параметры для выравнивания, включая любые параметры, необходимые для достижения максимального выравнивания по всей длине двух сравниваемых последовательностей. В некоторых вариантах осуществления рассматриваемый полипептид и эталонный полипептид имеют разную длину.
[0079] «Точечная мутация» представляет собой мутацию, которая затрагивает один аминокислотный остаток. Мутация может представлять собой потерю аминокислоты, замену одного аминокислотного остатка другим или вставку дополнительного аминокислотного остатка.
[0080] «Аминокислотная замена» относится к замене одной аминокислоты в полипептиде другой аминокислотой. В некоторых вариантах осуществления аминокислотная замена представляет собой консервативную замену. Неограничивающие примеры консервативных аминокислотных замен показаны в таблице 2. Аминокислотные замены могут быть введены в представляющую интерес молекулу, и продукты могут быть подвергнуты скринингу на желаемую активность, например сохранение/улучшение связывания антигена, снижение иммуногенности или улучшение ADCC или CDC или усиленную фармакокинетику.
[0081] Таблица 2.
[0082] Аминокислоты могут быть сгруппированы в соответствии с общими свойствами боковой цепи:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, влияющие на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
[0083] Неконсервативные замены влекут за собой замену члена одного из этих классов на другой класс.
[0084] Термин «вектор» используется для описания полинуклеотида, который можно сконструировать таким образом, чтобы он содержал клонированный полинуклеотид или полинуклеотиды, которые могут быть размножены в клетке-хозяине. Вектор может включать один или более из следующих элементов: точку начала репликации, одну или более регуляторных последовательностей (таких как, например, промоторы или энхансеры), которые регулируют экспрессию представляющего интерес полипептида, или один или более селектируемых маркерных генов (таких как, например, гены устойчивости к антибиотикам и гены, которые можно использовать в колориметрических анализах, например, β-галактозидаза). Термин «вектор экспрессии» относится к вектору, который используется для экспрессии представляющего интерес полипептида в клетке-хозяине.
[0085] «Клетка-хозяин» относится к клетке, которая может быть или была реципиентом вектора или выделенного полинуклеотида. Клетки-хозяева могут представлять собой прокариотические клетки или эукариотические клетки. Примеры эукариотических клеток включают клетки млекопитающих, такие как клетки приматов или животных, не являющихся приматами; клетки грибов, таких как дрожжи; растительные клетки; и клетки насекомых. Неограничивающие примеры клеток млекопитающих включают, без ограничения, клетки NS0, клетки PER.C6® (Crucell), клетки 293 и клетки CHO и их производные, такие как клетки 293-6E, DG44, CHO-S и CHO-К. Клетки-хозяева включают потомство одной клетки-хозяина, и это потомство не обязательно может быть полностью идентичным (по морфологии или комплементу геномной ДНК) исходной родительской клетке по причине естественной, случайной или преднамеренной мутации. Клетка-хозяин включает клетки, трансфицированные in vivo полинуклеотидом(-ами), кодирующим(-и) аминокислотную(-ые) последовательность(-и), представленную(-ые) в настоящем описании.
[0086] В контексте настоящего описания термин «выделенный» относится к молекуле, которая была отделена по меньшей мере от некоторых компонентов, с которыми она обычно встречается в природе или продуцируется. Например, полипептид называется «выделенным», когда он отделен от по меньшей мере некоторых компонентов клетки, в которой был продуцирован. Когда полипептид секретируется клеткой после экспрессии, физическое отделение супернатанта, содержащего полипептид, от клетки, которая его продуцировала, считается «выделением» полипептида. Точно так же полинуклеотид называется «выделенным», если он не является частью более крупного полинуклеотида (например, геномной ДНК или митохондриальной ДНК, в случае ДНК-полинуклеотида), в котором он обычно встречается в природе, или отделен от по меньшей мере некоторых компонентов клетки, в которой он был получен, например, в случае РНК-полинуклеотида. Таким образом, ДНК-полинуклеотид, содержащийся в векторе внутри клетки-хозяина, можно назвать «выделенным». В некоторых вариантах осуществления антитело к парвовирусу очищают с помощью хроматографии, такой как эксклюзионная хроматография, ионообменная хроматография, колоночная хроматография с белком А, хроматография гидрофобных взаимодействий и хроматография CHT.
[0087] «Уменьшать» или «ингибировать» означает снижать, уменьшать или блокировать активность, функцию или количество по сравнению с эталоном. В некоторых вариантах осуществления под «снижением» или «ингибированием» подразумевается способность вызывать общее уменьшение на 20% или более. В некоторых вариантах осуществления под «снижением» или «ингибированием» подразумевается способность вызывать общее уменьшение на 50% или более. В некоторых вариантах осуществления под «снижением» или «ингибированием» подразумевается способность вызывать общее уменьшение на 75%, 85%, 90%, 95% или более. В некоторых вариантах осуществления количество, указанное выше, ингибируется или уменьшается в течение определенного периода времени по сравнению с контрольной дозой (такой как плацебо) в течение того же периода времени. В контексте настоящего описания термин «эталон» относится к любому образцу, стандарту или уровню, используемому для целей сравнения. Эталон может быть получен из здорового или не затронутого заболеванием образца. В некоторых примерах эталон получают из образца здорового или не получавшего лечение животного-компаньона. В некоторых примерах эталон получают от одного или более здоровых животных определенного вида, которые не подлежат тестированию или лечению.
[0088] Термин «существенно уменьшенный», используемый в настоящем описании, обозначает достаточно высокую степень уменьшения числового значения относительно эталонного числового значения, чтобы специалист в данной области смог признать разницу между двумя значениями как статистически значимую в контексте биологической характеристики, измеряемой указанными значениями. В некоторых вариантах осуществления существенно уменьшенные числовые значения уменьшены более чем на любое из следующих значений: 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100% по сравнению с эталонным значением.
[0089] В некоторых вариантах осуществления антитело к парвовирусу может снижать титры парвовируса у представителя псовых или кошачьих на по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или 100% по сравнению с титрами парвовируса в отсутствие антитела, по данным анализа ингибирования гемагглютинации (HI) или анализа нейтрализации вируса (VN). В некоторых вариантах осуществления снижение титра парвовируса находится в пределах от 10% до 15%, от 10% до 20%, от 10% до 25%, от 10% до 30%, от 10% до 35%, от 10% до 40%, от 10% до 45%, от 10% до 50%, от 10% до 60%, от 10% до 70%, от 10% до 80%, от 10% до 90%, от 10% до 100%, от 15% до 20%, от 15% до 25%, от 15% до 30%, от 15% до 35%, от 15% до 40%, от 15% до 45%, от 15% до 50%, от 15% до 60%, от 15% до 70%, от 15% до 80%, от 15% до 90%, от 15% до 100%, от 20% до 25%, от 20% до 30%, от 20% до 35%, от 20% до 40%, от 20% до 45%, от 20% до 50%, от 20% до 60%, от 20% до 70%, от 20% до 80%, от 20% до 90%, от 20% до 100%, от 25% до 30%, от 25% до 35%, от 25% до 40%, от 25% до 45%, от 25% до 50%, от 25% до 60%, от 25% до 70%, от 25% до 80%, от 25% до 90%, от 25% до 100%, от 30% до 35%, от 30% до 40%, от 30% до 45%, от 30% до 50%, от 30% до 60%, от 30% до 70%, от 30% до 80%, от 30% до 90%, от 30% до 100%, от 35% до 40%, от 35% до 45%, от 35% до 50%, от 35% до 60%, от 35% до 70%, от 35% до 80%, от 35% до 90%, от 35% до 100%, от 40% до 45%, от 40% до 50%, от 40% до 60%, от 40% до 70%, от 40% до 80%, от 40% до 90%, от 40% до 100%, от 45% до 50%, от 45% до 60%, от 45% до 70%, от 45% до 80%, от 45% до 90%, от 45% до 100%, от 50% до 60%, от 50% до 70%, от 50% до 80%, от 50% до 90%, от 50% до 100%, от 60% до 70%, от 60% до 80%, от 60% до 90%, от 60% до 100%, от 70% до 80%, от 70% до 90%, от 70% до 100%, от 80% до 90%, от 80% до 100% или от 90% до 100%.
Примеры фармацевтических композиций
[0090] Термины «фармацевтический состав» и «фармацевтическая композиция» относятся к препарату, который находится в такой форме, которая обеспечивает эффективность биологической активности активного ингредиента(-ов) и который не содержит дополнительных компонентов, являющихся неприемлемо токсичными для субъекта, которому будет вводиться состав.
[0091] «Фармацевтически приемлемый носитель» относится к нетоксичному твердому, полутвердому или жидкому наполнителю, разбавителю, инкапсулирующему материалу, вспомогательному веществу, используемому для приготовления состава, или носителю, общепринятому в данной области техники для применения с терапевтическим средством, которые вместе составляют «фармацевтическую композицию» для введения субъекту. Фармацевтически приемлемый носитель нетоксичен для реципиентов в используемых дозировках и концентрациях и совместим с другими ингредиентами препарата. Фармацевтически приемлемый носитель подходит для используемой композиции. Примеры фармацевтически приемлемых носителей включают оксид алюминия; стеарат алюминия; лецитин; сывороточные белки, такие как человеческий сывороточный альбумин, собачий или другой животный альбумин; буферы, такие как фосфатный, цитратный, трометаминовый или HEPES буферы; глицин; сорбиновую кислоту; сорбат калия; смеси неполных глицеридов насыщенных растительных жирных кислот; воду; соли или электролиты, такие как сульфат протамина, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный кремнезем или трисиликат магния; поливинилпирролидон, вещества на основе целлюлозы; полиэтиленгликоль; сахарозу; маннит; или аминокислоты, включая, без ограничения, аргинин.
[0092] Фармацевтическая композиция может храниться в лиофилизированной форме. Таким образом, в некоторых вариантах осуществления процесс приготовления включает стадию лиофилизации. Затем лиофилизированную композицию можно восстановить, как правило, в виде водной композиции, подходящей для парентерального введения, перед введением собаке, кошке или лошади. В других вариантах осуществления, в частности, когда антитело обладает высокой стабильностью к термической и окислительной денатурации, фармацевтическую композицию можно хранить в виде жидкости, т.е. в виде водной композиции, которую можно вводить непосредственно или при соответствующем разведении собаке, кошке или лошади. Лиофилизированную композицию можно восстанавливать стерильной водой для инъекций (WFI). Могут быть включены антибактериальные агенты (например, бактериостатические реагенты, такие как бензиловый спирт). Таким образом, изобретение относится к фармацевтическим композициям в твердой или жидкой форме.
[0093] рН фармацевтических композиций при введении может находиться в диапазоне от примерно рН 5 до примерно рН 8. Композиции по изобретению являются стерильными, если они предназначены для использования в терапевтических целях. Стерильность может быть достигнута любым из нескольких способов, известных в данной области, включая фильтрацию через стерильные фильтрационные мембраны (например, 0,2-микронные мембраны). Стерильность можно поддерживать с помощью антибактериальных средств или без них.
[0094] В некоторых вариантах осуществления фармацевтически приемлемый носитель или фармацевтическая композиция имеет рН в диапазоне от 5,0 до 6,2, от 5,0 до 6,0 или от 5,3 до 5,7. В некоторых вариантах осуществления фармацевтический носитель представляет собой забуференный фосфатом солевой раствор, рН 7,2. В некоторых вариантах осуществления фармацевтический носитель представляет собой 50 мМ цитрата натрия, рН 7, 150 мМ NaCl.
[0095] В некоторых вариантах осуществления фармацевтически приемлемый носитель или фармацевтическая композиция содержит антибактериальный агент.
Примеры применения антител и фармацевтических композиций
[0096] Антитела или фармацевтические композиции, содержащие антитела по изобретению, могут быть полезны для формирования пассивного иммунитета к инфекции парвовирусом и/или для лечения парвовирусной инфекции. В контексте настоящего описания термин «парвовирусная инфекция» означает состояние, связанное с парвовирусной инфекцией, вызываемое парвовирусной инфекцией или характерное для парвовирусной инфекции. Такие состояния включают, без ограничения, инфекции, подтвержденные тестами ELISA в условиях содержания в клетке, анализом гемагглютинации (HA), гистопатологией, выделением вируса или титрами вируса или ПЦР. Инфекции, вызванные парвовирусом, часто включают лихорадку, рвоту, диарею, лимфопению, обезвоживание и/или вторичный сепсис.
[0097] В контексте настоящего описания термин «лечение» представляет собой подход для получения полезных или желаемых клинических результатов. В контексте настоящего описания «лечение» охватывает любое введение или применение терапевтического средства для лечения заболевания у субъекта, такого как млекопитающее, включая человека и домашнее животное (например, представителя псовых или кошачьих). Для целей настоящего изобретения благоприятные или желаемые клинические результаты включают, помимо прочего, любой один или более из следующих факторов: облегчение одного или более симптомов, предотвращение смертности, уменьшение степени и тяжести заболевания, предотвращение или замедление распространения заболевания, устранение или сокращение продолжительности выделения вируса, предотвращение или отсрочку рецидива заболевания, предотвращение или уменьшение цитопатических эффектов вируса, задержку или замедление прогрессирования заболевания, облегчение болезненного состояния, ингибирование заболевания или его прогрессирования, исчезновение клинических признаков заболевания, ингибирование или замедление заболевания или его прогрессирования, купирование развития заболевания и ремиссию (частичную или полную). Под «лечением» также понимают уменьшение патологических последствий пролиферативного заболевания. Предложенные в настоящем описании способы предусматривают любой один или более из этих аспектов лечения. В соответствии с вышеизложенным термин «лечение» не требует стопроцентного устранения всех аспектов расстройства.
[0098] В некоторых вариантах осуществления антитело к парвовирусу или содержащие его фармацевтические композиции можно использовать в соответствии с представленными в настоящем описании способами для обеспечения пассивного иммунитета к парвовирусной инфекции и/или для лечения парвовирусных инфекций. В некоторых вариантах осуществления антитело к парвовирусу или фармацевтические композиции вводят субъекту, такому как домашнее животное (например, представитель псовых или кошачьих) или человеку, для формирования пассивного иммунитета к заражению парвовирусом и/или для лечения парвовирусной инфекции.
[0099] «Терапевтически эффективное количество» вещества/молекулы, агониста или антагониста может варьировать в зависимости от таких факторов, как тип заболевания, подлежащего лечению, болезненное состояние, иммунный статус отдельного субъекта, встречающаяся вирулентная вирусная нагрузка, тяжесть и степень виремии, тяжесть и течение заболевания, тип терапевтической цели, любая предыдущая терапия, история болезни, ответ на предшествующее лечение, статус пассивного переноса материнских антител, предыдущий статус иммунизации отдельного животного, усмотрение лечащего ветеринара, возраст, пол и вес субъекта, а также способность вещества/молекулы, агониста или антагониста вызывать желаемую реакцию у субъекта. Терапевтически эффективное количество также представляет собой такое количество, при котором терапевтически полезные эффекты превосходят любые токсические или вредные эффекты вещества/молекулы, агониста или антагониста. Терапевтически эффективное количество может быть доставлено за одно или несколько введений. Терапевтически эффективное количество относится к количеству, эффективному в дозах и в течение периодов времени, необходимых для достижения желаемого терапевтического или профилактического результата.
[00100] В некоторых вариантах осуществления антитело к парвовирусу или фармацевтическую композицию, содержащую антитело к парвовирусу, вводят парентерально, путем подкожного введения, внутривенной инфузии или внутримышечной инъекции. В некоторых вариантах осуществления антитело к парвовирусу или фармацевтическую композицию, содержащую антитело к парвовирусу, вводят в виде однократной или многократной болюсной инъекции. В некоторых вариантах осуществления антитело к парвовирусу или фармацевтическую композицию, содержащую антитело к парвовирусу, вводят внутримышечно, внутривенно, внутрибрюшинно, интрацереброспинально, подкожно, внутриартериально, интрасиновиально, подоболочечно или путем ингаляции.
[00101] Антитела к парвовирусу, представленные в настоящем описании, можно вводить в количестве от 0,01 мг/кг массы тела до 100 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела к парвовирусу можно вводить в количестве от 0,5 мг/кг массы тела до 50 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела к парвовирусу можно вводить в количестве от 0,1 мг/кг массы тела до 10 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела к парвовирусу можно вводить в количестве от 0,1 мг/кг массы тела до 100 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела к парвовирусу можно вводить в количестве от 1 мг/кг массы тела до 10 мг/кг массы тела на дозу. В некоторых вариантах осуществления антитела к парвовирусу можно вводить в количестве от 0,5 мг/кг массы тела до 100 мг/кг массы тела, от 1 мг/кг массы тела до 100 мг/кг массы тела, от 5 мг/кг массы тела до 100 мг/кг массы тела, от 10 мг/кг массы тела до 100 мг/кг массы тела, от 20 мг/кг массы тела до 100 мг/кг массы тела, от 50 мг/кг массы тела до 100 мг/кг массы тела, от 1 мг/кг массы тела до 10 мг/кг массы тела, от 5 мг/кг массы тела до 10 мг/кг массы тела, от 0,5 мг/кг массы тела до 10 мг/кг массы тела, от 0,01 мг/кг массы тела до 0,5 мг/кг массы тела, от 0,01 мг/кг массы тела массы тела до 0,1 мг/кг массы тела или в диапазоне от 5 мг/кг массы тела до 50 мг/кг массы тела. В некоторых вариантах осуществления антитела к парвовирусу можно вводить в количестве 0,5 мг/кг массы тела.
[00102] Антитело к парвовирусу или фармацевтическую композицию, содержащую антитело к парвовирусу, можно вводить субъекту, такому как человек или животное-компаньон (например, представителю псовых или кошачьих), в виде разовой дозы, за один раз или в течение нескольких курсов лечения. Например, антитело к парвовирусу или фармацевтическую композицию, содержащую антитело к парвовирусу, можно вводить по меньшей мере один раз, более одного раза, по меньшей мере два раза, по меньшей мере три раза, по меньшей мере четыре раза или по меньшей мере пять раз.
[00103] В некоторых вариантах осуществления дозу вводят один раз в неделю в течение по меньшей мере двух или трех последовательных недель, и в некоторых вариантах осуществления этот цикл лечения повторяют два или более раз, необязательно чередуя с одной или более неделями без лечения. В других вариантах осуществления терапевтически эффективную дозу вводят один раз в сутки в течение двух-пяти дней подряд, и в некоторых вариантах осуществления этот цикл лечения повторяют два или более раз, необязательно чередуя с одним или более днями или неделями без лечения.
[00104] В некоторых вариантах осуществления дозу вводят субъекту, такому как человек или животное-компаньон (например, представителю псовых или кошачьих) в возрасте менее 1 недели, менее 2 недель, менее 3 недель, менее 4 недель, менее 5 недель, менее 6 недель, менее 6 недель, менее 7 недель, менее 8 недель, менее 9 недель, менее 10 недель, менее 11 недель, менее 12 недель, менее 6 месяцев, от 0 до 12 недель, от 0 до 10 недель, от 0 до 8 недель, от 0 до 6 недель, от 0 до 4 недель, от 0 до 2 недель, от 4 до 12 недель, от 6 до 12 недель, от 10 до 12 недель, от 4 недель до 6 месяцев, от 2 месяцев до 6 месяцев, от 4 месяцев до 6 месяцев, от 6 месяцев до 1 года, старше 13 недель или старше 1 года.
[00105] Может оказаться выгодным доставлять антитело к парвовирусу или нуклеиновую кислоту, кодирующую антитело к парвовирусу, младенцу в пренатальном и/или постнатальном периоде для обеспечения пассивного иммунитета к парвовирусной инфекции. В некоторых вариантах осуществления антитело к парвовирусу вводят беременной или кормящей материнской особи, например человеку или животному-компаньону (например, представителю псовых или кошачьих). В некоторых вариантах осуществления антитело к парвовирусу вводят в плаценту беременной женской особи.
[00106] В некоторых вариантах осуществления способ обеспечения пассивного иммунитета у младенца к инфекции собачьим или кошачьим парвовирусом включает введение беременной или кормящей материнской особи терапевтически эффективного количества моноклонального антитела, которое связывается с парвовирусом псовых или кошачьих. В некоторых вариантах осуществления антитело к парвовирусу вводят в плаценту беременной женской особи. В некоторых вариантах осуществления антитело к парвовирусу вводят субъекту в период грудного вскармливания.
[00107] В настоящем описании предложены способы применения антител к парвовирусу, полипептидов и полинуклеотидов для выявления, диагностики и мониторинга парвовирусной инфекции. В настоящем описании представлены способы определения того, будет ли субъект реагировать на терапию антителами к парвовирусу. В некоторых вариантах осуществления способ включает нейтрализацию вирусной сыворотки. В некоторых вариантах осуществления способ включает определение наличия у субъекта клеток, которые экспрессируют парвовирус, с использованием антитела к парвовирусу. В некоторых вариантах осуществления способ детектирования включает приведение образца в контакт с антителом, полипептидом или полинуклеотидом и определение того, отличается ли уровень связывания от уровня связывания эталонного или сравнительного образца (такого как контроль). В некоторых вариантах осуществления способ может быть полезен для определения того, являются ли антитела или полипептиды, представленные в настоящем описании, подходящим средством для лечения субъекта.
[00108] В некоторых вариантах осуществления образец представляет собой биологический образец. Термин «биологический образец» означает некоторое количество вещества, полученного от живого или бывшего ранее живым существа. В некоторых вариантах осуществления биологический образец представляет собой мазок, содержащий клеточный дебрис, клетки или клеточный/тканевой лизат. В некоторых вариантах осуществления биологический образец включает, без ограничения, кровь (например, цельную кровь), плазму, сыворотку, мочу, синовиальную жидкость, лимфатическую ткань и эпителиальные клетки.
[00109] В некоторых вариантах осуществления клетки или клеточный/тканевой лизат приводят в контакт с антителом к парвовирусу и определяют связывание между антителом и клеткой. Когда тестируемые клетки демонстрируют связывающую активность относительно эталонной клетки того же типа ткани, это может указывать на то, что субъекту будет полезно лечение антителом к парвовирусу. В некоторых вариантах осуществления тестируемые клетки получают из ткани субъекта, такого как человек или животное-компаньон (например, представитель псовых или кошачьих).
[00110] Для детектирования специфического связывания антитело-антиген можно использовать различные способы, известные в данной области. Типичные иммуноанализы, которые можно проводить, включают флуоресцентный поляризационный иммуноанализ (FPIA), флуоресцентный иммуноанализ (FIA), иммуноферментный анализ (EIA), нефелометрический иммуноферментный анализ (NIA), твердофазный иммуноферментный анализ (ELISA) и радиоиммуноанализ (RIA). Индикаторная часть или группа метки может быть присоединена к рассматриваемым антителам, и ее выбирают таким образом, чтобы она удовлетворяла потребности различных применений способа, которые часто диктуются наличием оборудования для анализа и совместимых процедур иммуноанализа. Соответствующие метки включают, помимо прочего, радионуклиды (например, 125I, 131I, 35S, 3H или 32P), ферменты (например, щелочную фосфатазу, пероксидазу хрена, люциферазу или b-галактозидазу), флуоресцентные фрагменты или белки (например, флуоресцеин, родамин, фикоэритрин, GFP или BFP) или люминесцентные фрагменты (например, наночастицы QdotТМ, поставляемые Quantum Dot Corporation, Пало-Альто, Калифорния). Общие методы, используемые при проведении различных иммунологических анализов, упомянутых выше, известны специалистам в данной области.
[00111] В целях диагностики полипептид, содержащий антитела, может быть помечен детектируемым фрагментом, включая, помимо прочего, радиоизотопы, флуоресцентные метки и различные фермент-субстратные метки, известные в данной области. Способы конъюгации метки с антителом известны в данной области. В некоторых вариантах осуществления антитела к парвовирусу не нужно метить, и их присутствие можно обнаружить с помощью второго меченого антитела, которое связывается с первым антителом к парвовирусу. В некоторых вариантах осуществления антитело к парвовирусу можно использовать в любом известном методе анализа, таком как анализы конкурентного связывания, прямые и непрямые сэндвич-анализы и анализы иммунопреципитации. Zola, Monoclonal Antibodies: A Manual of Techniques, рр. 147-158 (CRC Press, Inc., 1987). Антитела к парвовирусу и полипептиды также можно использовать для диагностических анализов in vivo, таких как визуализация in vivo. Как правило, антитело или полипептид метят радионуклидом (таким как 111In, 99Tc, 14C, 131I, 125I, 3H или любой другой радионуклидной меткой, включая раскрытые в настоящем описании), что позволяет локализовать представляющие интерес клетки или ткань с помощью иммуносцинтиографии. Антитело также можно использовать в качестве окрашивающего реагента при патологии с помощью методов, хорошо известных в данной области.
[00112] В некоторых вариантах осуществления первое антитело используется для диагностики, а второе антитело используется в качестве терапевтического средства. В некоторых вариантах осуществления первое и второе антитела различаются. В некоторых вариантах осуществления первое и второе антитела могут одновременно связываться с антигеном, связываясь при этом с отдельными эпитопами.
[00113] Приведенные ниже примеры иллюстрируют отдельные аспекты изобретения и никоим образом не предназначены для его ограничения.
ПРИМЕРЫ
Пример 1
Получение химерных собачьих антител Mab A и Mab B
[00114] Структурный анализ парвовируса псовых и парвовируса кошачьих в комплексе с фрагментами антител из восьми различных нейтрализующих моноклональных антител описан в Hafenstein S., et al., J Virol. 2009 Jun, 83(11):5556-66. Неполная информация об аминокислотной последовательности предоставлена для крысиных Mab E и Fab-фрагментов Mab F, которые продемонстрировали нейтрализацию парвовируса псовых в анализе in vitro. Неполные аминокислотные последовательности вариабельной тяжелой цепи и вариабельной легкой цепи Mab E представлены в SEQ ID NO. 81 и 82, соответственно. Неполные аминокислотные последовательности вариабельной тяжелой цепи и вариабельной легкой цепи Mab F представлены в SEQ ID NO. 83 и 84, соответственно.
[00115] Для создания реконструированного первого каркасного участка как для тяжелой, так и для легкой цепей Mab E и Mab F выполняли трехмерный анализ структуры белка. Аминокислотные последовательности тяжелой и легкой цепей модифицированных моноклональных антител, обозначенных Mab A и Mab B, приведены в SEQ ID NO: 20 (тяжелая цепь Mab A), SEQ ID NO: 22 (легкая цепь Mab A), SEQ ID NO: 62 (тяжелая цепь Mab B) и SEQ ID NO: 64 (легкая цепь Mab B цепь).
[00116] Последовательности ДНК, кодирующие химерное антитело, создавали для слияния VH Mab A (SEQ ID NO: 20) и VH Mab B (SEQ ID NO: 62) с константной тяжелой цепью собачьего IgG-B и VL Mab A (SEQ ID NO: 22) и LC Mab B (SEQ ID NO: 64) с собачьей константной областью легкой цепи κ с получением SEQ ID NO: 23 (химерной A HC IgG-B), SEQ ID NO: 66 (химерной B HC IgG-B), SEQ ID NO: 25 (химерной A LC κ) и SEQ ID NO: 68 (химерной B LC κ). Нуклеотидные последовательности тяжелой и легкой цепей синтезировали химически и встраивали в вектор экспрессии, пригодный для трансфекции в клетку-хозяина млекопитающего. После трансфекции пар векторов тяжелой и легкой цепей в клетки и культивирования антитела подвергали аффинной очистке из культуральной среды с использованием аффинной смолы CaptivA® Protein A Affinity Resin (Repligen). Очищенные химерные собачьи антитела Mab A и Mab B подтверждали анализом SDS-PAGE (данные не показаны).
[00117] Химерные антитела также могут быть сконструированы и получены на основе слияний VH Mab A (SEQ ID NO: 20) и VH Mab B (SEQ ID NO: 62) с константными тяжелыми цепями собачьих IgG-A, IgG-C и IgG-D.
Пример 2
Активность химерных собачьих антител Mab A и Mab B
[00118] Очищенные химерные собачьи Mab A и Mab B (приготовленные в PBS, pH 7,2 при 200 мкг/мл) использовали для оценки активности, направленной против парвовируса псовых, с помощью анализа ингибирования гемагглютинации (HI). Анализ выполняли в лаборатории службы вакцинации и иммунодиагностики животных-компаньонов Университета Висконсина, по существу, как описано Carmichael, et al., Am J of Vet Res. 1980 May, 41(5):784-91. Готовили серийные разведения образцов химерных собачьих Mab A и химерных собачьих Mab B, инкубированных с CPV. Затем добавляли свиные эритроциты. Парвовирус псовых вызывает агглютинацию эритроцитов свиньи. Как химерные собачьи Mab A, так и химерные собачьи Mab B предотвращали агглютинацию. Оба антитела имели HI для CPV-2b, равное 40960, в то время как нерелевантный собачий IgG давал HI<20. Считается, что большинство вакцинированных собак имеют антитела на уровне HI примерно 1280.
[00119] Кроме того, с помощью анализа нейтрализации вирусной сыворотки анализировали активность антител по предотвращению инфицирования и разрушения клеток живым CPV.
Пример 3
Варианты последовательностей VH и VL для усиленной экспрессии химерных собачьих Mab A и Mab B
[00120] Химерное собачье Mab A и химерное собачье Mab B одинаково плохо экспрессируются в транзиторных клетках CHOS или стабильных клетках CHOK1. Для повышения уровня экспрессии выполняли трехмерный анализ структуры белка для идентификации аминокислотных остатков VH и VL, подходящих для модификации. Создавали многочисленные конструкции с разными мутациями в VH и VL. Тестировали уровень экспрессии антител, содержащих комбинации собачьего IgG-B с вариантами VH и VL.
[00121] Варианты с повышенной экспрессией анализировали на их специфическую активность с помощью HI анализа парвовируса псовых. В этих экспериментах каждый из протестированных вариантов антитела готовили в PBS, pH 7,2, в концентрации 200 мкг/мл. Как химерное собачье Mab A (SEQ ID NO: 23 и 25), так и химерное собачье Mab B (SEQ ID NO: 66 и 68) продемонстрировали значение HI для CPV-2b, равное 10240. Варианты с повышенной экспрессией, химерное собачье Mab A v2 (SEQ ID NO: 24 и 25) и химерное собачье Mab B v2 (SEQ ID NO: 67 и 69), показали такое же значение HI, равное 10240, в то время как другие варианты показали более низкую специфическую активность.
Пример 4
Анализ активности парвовирусной инфекции (SVN)
[00122] Для определения способности химерного собачьего Mab A v2 (SEQ ID NO: 24 и 25) и химерного собачьего Mab B v2 (SEQ ID NO: 67 и 69) предотвращать инфицирование и разрушение клеток живым парвовирусом, выполняли анализ нейтрализации вируса в сыворотке (SVN). В этом анализе выращивали клетки Madin Darby Canine Kidney (MDCK). Серийные разведения антител смешивали с фиксированным титром парвовируса. Затем смесь инкубировали с клетками. После инкубации клетки исследовали под микроскопом для выявления цитопатического эффекта вируса (CPE). Считывание представляет собой конечное разведение образца антитела, при котором он достиг предела по предотвращению цитопатического эффекта, вызванного парвовирусом.
[00123] Как химерные собачьи Mab A v2 (1), хранившихся при 4°C, так и (2), подвергнутые 7 циклам замораживания-оттаивания при 200 мкг/мл, имели одинаковую активность: значение SVN для CPV-2b составило 32000 и значение SVN для CPV2c составило 8000.
Пример 5
Стабильность химерных собачьих Mab A v2 и Mab B v2
[00124] Тестировали стабильность химерного собачьего Mab A v2 (SEQ ID NO: 24 и 25) при 25 мг/мл и химерного собачьего Mab B v2 (SEQ ID NO: 67 и 69) при 20,5 мг/мл. Химерное собачье Mab A v2 и химерное собачье Mab B v2 имеют аналогичную специфическую активность, согласно анализу HI, при концентрации примерно 25 мг/мл и примерно 20,5 мг/мл, соответственно.
[00125] Оба, химерное собачье Mab A v2 и химерное собачье Mab B v2, полученные и очищенные из стабильного пула CHOK1, можно легко концентрировать до 25 мг/мл в PBS, pH 7,2, что свидетельствует о том, что растворимость обоих антител не вызывает проблем.
[00126] Химерное собачье Mab A v2 и химерное собачье Mab B v2 являются мономерными (>99%) при нейтральном pH и после хранения в течение 10 часов при pH 4,1, согласно результатам анализа методом эксклюзионной высокоэффективной жидкостной хроматографии (ВЭЖХ). В этом анализе мономер и агрегаты антител разделяли с помощью ВЭЖХ-ЭХ, используя систему Agilent 1100, колонку Shodex KW803 (8 мм x 300 мм) с предколонкой KW-G и буфер для подвижной фазы 2X PBS, pH 7,2 (270 мМ NaCl, 5,4 мМ KCl, 8,6 мМ Na2HPO4, 2,8 мМ KPO4) при постоянной скорости потока 0,5 мл/мин. Колонку калибровали с использованием маркеров Bio Rad (номер по каталогу 151-1901), состоящих из тиреоглобулина, γ-глобулина, овальбумина, миоглобина и витамина B12.
[00127] Стабильность химерного собачьего Mab A v2 оценивали в режиме реального времени в (1) PBS, pH 7,2 при 25 мг/мл и (2) 50 мМ Na-цитрат, pH 7, 150 мМ NaCl при 25 мг/мл при различных температурах. Результаты ВЭЖХ-ЭХ через десять месяцев обобщены в таблице 3.
[00128] Таблица 3.
[00129] Также тестировали стабильность, подвергая антитела трем циклам замораживания-оттаивания с замораживанием при -70°C и оттаиванием при комнатной температуре. Ни у одного из антител не наблюдали потерю активности, судя по значениям как HI для CPV-2b, так и HI для CPV-2c.
[00130] Стабильность дополнительно тестировали, подвергая антитела семи циклам замораживания-оттаивания с замораживанием при -20°C и оттаиванием при комнатной температуре. Оба антитела полностью сохранили активность, измеренную с помощью анализа HI.
[00131] Термостабильность двух антител в разных составах и в диапазоне pH анализировали методом дифференциальной сканирующей флуоресценции (DSF). Измеряли температуру плавления (Tm) каждого антитела в различных условиях. Буфер и 12 мкг антитела смешивали с красителем 1X Protein thermoshift (Applied Biosystem, № по каталогу 4461146). Кривую плавления получали с помощью системы ПЦР в реальном времени StepOne (Applied Biosystem, № по каталогу 4376357). Температуру повышали с 25°C до 99°C со скоростью линейного изменения 1% в соответствии с инструкциями производителя. Данные анализировали с помощью программного обеспечения Protein Thermal ShiftTM v1.0 (Applied Biosystem, № по каталогу 4466038) для определения Tm, которую вычисляли как наибольшее значение, полученное из первой производной кривой плавления белка. В каждом из протестированных составов, включая PBS, pH 7,2, химерное собачье Mab A v2 было значительно более стабильным, чем химерное собачье Mab B v2.
Пример 6
Связывание VLP химерных собачьих антител Mab A v2 и Mab B v2
[00132] Измеряли кажущееся сродство химерного собачьего Mab A v2 (SEQ ID NO: 24 и 25) и химерного собачьего Mab B v2 (SEQ ID NO: 67 и 69) с VLP парвовируса. Сначала биотинилированные химерные собачьи Mab A v2 и химерные собачьи Mab B v2 связывали с покрытыми стрептавидином наконечниками сенсора. Затем оценивали связывание рекомбинантного капсида собачьего парвовируса CPV2b (Advanced ImmunoChemical Inc Cat #8-CPV) с наконечником сенсора, связанным с Mab.
[00133] Каждое из химерного собачьего Mab A v2 и химерного собачьего Mab B v2 показало сродство связывания с собачьим VLP CPV 2b с кинетикой, потенциально достаточной для терапевтической активности. Анализ связывания выполняли с помощью биосенсора Octet следующим образом. Вкратце, химерное собачье Mab A v2 (SEQ ID NO: 24 и 25) и химерное собачье Mab B v2 (SEQ ID NO: 67 и 69) биотинилировали с помощью аминовой химии. Свободный непрореагировавший биотин удаляли экстенсивным диализом. Биотинилированные химерные собачьи Mab A v2 и химерные собачьи Mab B v2 захватывали покрытыми стрептавидином наконечниками сенсоров. Ассоциацию либо Mab A v2, либо Mab B v2 с VLP CPV 2b псовых (40 мкг/мл) отслеживали в течение 300 секунд. Диссоциацию контролировали в течение 300 секунд. Биотинилированный нерелевантный собачий IgG-B использовали в качестве отрицательного контроля. Данные подгоняли к модели связывания 1:1 с помощью программного обеспечения для анализа данных ForteBioТМ для определения kon, koff и Kd. Буфер для разведений и всех стадий связывания представлял собой 20 мМ фосфат, 150 мМ NaCl, рН 7,2. Kd для химерного собачьего Mab A v2 и VLP2b составляла 9,78×10-11 М, а для химерного собачьего Mab B v2 и VLP2b составляла 9,38×10-12 М (см. фиг. 2).
Пример 7
Канинизация Mab A v2 и Mab B v2
[00134] Для снижения потенциальной иммуногенности, особенно там, где необходимо повторное введение антител A или B, выполняли канинизацию VH и VL из Mab A v2 и B v2. Создавали несколько канинизированных VH и VL, осуществляли их экспрессию и очистку. Хороших экспрессоров отбирали по специфической активности с помощью анализа HI для CPV2b. Канинизированная A HC v3 IgG-B (SEQ ID NO: 37) плюс канинизированная A LC κ (SEQ ID NO: 39) и канинизированная A HC v4 IgG-B (SEQ ID NO: 38) плюс канинизированная A LC κ (SEQ ID NO: 39) сохраняли полную активность относительно химерной A HC IgG-B (SEQ ID NO: 23) плюс химерная A LC κ (SEQ ID NO: 25) и относительно химерной A HC v2 IgG-B (SEQ ID NO: 24) плюс химерная A LC κ (SEQ ID NO: 25). Канинизированная B HC v3 IgG-B (SEQ ID NO: 79) плюс канинизированная B LC v3 κ (SEQ ID NO: 80) сохраняли полную активность относительно химерной B HC IgG-B (SEQ ID NO: 66) плюс химерная B LC κ (SEQ ID NO: 68) и относительно химерной B HC v2 IgG-B (SEQ ID NO: 67) плюс химерная B LC v2 κ (SEQ ID NO: 69).
Пример 8
Кошачьи химерные Mab A и Mab B
[00135] Химерное собачье Mab A v2 (SEQ ID NO: 24 и 25) и химерное собачье Mab B v2 (SEQ ID NO: 67 и 69) показали активность в анализе HI парвовируса кошачьих. Химерное собачье Mab A v2 в концентрации 200 мкг/мл имело значение HI для парвовируса кошачьих, равное 262144, тогда как химерное собачье Mab B v2 в концентрации 200 мкг/мл показало значение HI для парвовируса кошачьих, равное 131072.
[00136] Таким образом, Mab A и Mab B можно использовать для профилактики или лечения парвовируса кошачьих (вируса панлейкопении). Кроме того, для спаривания с химерной вариабельной легкой цепью кошачьего Mab A и кошачьей цепи каппа (SEQ ID NO: 31 и 32) создавали вариабельную тяжелую цепь химерного кошачьего Mab A и кошачьего IgG-1. Для устранения потенциальной гетерогенности можно ввести мутацию, которая удаляет сайт гликозилирования, чтобы получить химерное кошачье Mab A-IgG1, связанное с агликозилированной цепью каппа (например, SEQ ID NO: 31 и 33).
[00137] Кроме того, для спаривания с вариабельной легкой цепью химерного кошачьего Mab B и кошачьей цепью каппа (SEQ ID NO: 74 и 75) создавали вариабельную тяжелую цепь химерного кошачьего Mab B и кошачьего IgG-1. Для получения химерного кошачьего Mab A-IgG1, связанного с агликозилированной цепью каппа (например, SEQ ID NO: 74 и 76), может быть введена мутация, которая удаляет сайт гликозилирования.
Пример 9
Безопасность и фармакодинамика у щенков
[00138] Исследование in vivo выполняли с использованием моноклональных химерных собачьих антител Mab A (SEQ ID NO: 23 и 25) и химерных собачьих антител Mab B (SEQ ID NO: 66 и 68). Цели этого исследования заключались в оценке безопасности, оценке влияния химерного собачьего Mab A и химерного собачьего Mab B на титры собачьего павовируса-2 (CPV-2), оценки нейтрализации вируса и реакции на моновалентную модифицированную живую вакцину после лечения двумя антителами у специально выведенных непривитых здоровых щенков. См. краткое описание дизайна исследования в таблице 4 ниже.
[00139] Таблица 4.
химерное собачье Mab A (SEQ ID NO: 23 и 25) и химерное собачье Mab B (SEQ ID NOs: 66 и 68)
• Не-GLP
• Однодозовым лабораторным исследованием для оценки фармакодинамики и безопасности для невакцинированных здоровых биглей с отрицательным титром CPV 2
• Щенков рандомизировали в одну из двух равных групп лечения (по 3 для Mab A:3 для Mab B).
• Распределение осуществляли с помощью списка рандомизации, предоставленного Спонсором.
• На этапе акклиматизации вводили сопутствующие препараты для профилактики кокцидий и гельминтозов.
• В возрасте 10-12 недель
• Весом по меньшей мере 1,5 кг
• Полученные с фермы Ridglan Farms, Висконсин
Введение TA: 28 января 2019 г.
Окончание исследования: 9 мая 2019 г.
[00140] После рандомизации, когда щенков распределили на две группы (3 Mab A (идентификаторы собак: BDW-8, DEW-8 и DFW-8):3 Mab B (идентификаторы собак: CTW-8, CWW-8 и DHW-8)) щенкам вводили соответствующее антитело однократно внутривенно (5 мг/кг) через клипированную и препарированную головную вену в день исследования 0. Моновалентную вакцину к CPV, Nobivac 1-Pv (Merck Animal Health, Кенилворт, Нью-Джерси) первоначально вводили щенкам при титрах 80 или ниже. Вторую дозу вводили через 21 день после первой дозы. Третью дозу вводили, если у щенка не наблюдалась сероконверсия примерно через 21 день после второй дозы.
[00141] За щенками наблюдали, используя анализ ингибирования гемагглютинации (HI) и нейтрализации вируса (VN) в течение всего периода, составившего 100 дней. HI используют для определения количества антител в образце сыворотки, и VN используют для определения способности антител предотвращать заражение и разрушение клеток живым вирусом. За щенками также наблюдали с целью определения, произошла ли у них сероконверсия после вакцинации CPV.
[00142] Всех щенков проверяли, чтобы их титры HI были <20 в день 0 перед внутривенным введением антител Mab A или B. Титры HI в день 1 после введения Mab A или B составляли от 2560 до 5120. Титры отслеживали в течение 100 дней, чтобы документировать деградацию антител и оценить время полувыведения из сыворотки.
[00143] На 37-й день, когда титры у отдельных щенков начали падать до 1:40, начали проводить вакцинацию для оценки нейтрализации вакцины CPV-2. Документально подтверждали, что антитела Mab A или B блокируют иммунизацию у щенков на различных уровнях. Щенкам вводили последующие дозы вакцины по графику, и устанавливали достоверность реакции. Сероконверсия вакцины в конечном итоге произошла у 5 из 6 щенков. Титры анализа HI для обеих групп животных отражены в таблице 5 ниже и на фиг. 3A (группа Mab A), фиг. 3B (группа Mab B) и фиг. 3C (обе группы объединены).
[00144] Для получения быстрого распределения и медленной фазы распада использовали кинетику двухфазного распада, используя HI как функцию времени. Период полувыведения химерного собачьего Mab A составлял 10,1 дня (фиг. 4A), тогда как период полувыведения химерного собачьего Mab B составлял 8,6 дня (фиг. 4B). Анализы VN в сыворотке отражали титры HI (см. таблицу 6 ниже). Период полувыведения примерно соответствует периоду полувыведения материнского антитела. (Carmichael, LE, Joubert, JC and Pollock, RVH; «A Modified Live Canine Parvovirus Vaccine. II. Immune Response», Cornell Vet, Volume 73, рр. 13-29; 1983).
[00145] Это первоначальное фармакодинамическое исследование показало, что внутривенное введение химерного собачьего Mab A (SEQ ID NO: 23 и 25) и химерного собачьего Mab B (SEQ ID NO: 66 и 68) приводит к первоначальным титрам антител, составляющим от 2560 до 5120, в пределах 24 часов после введения. Кроме того, данные VN очень хорошо согласуются с титрами HI. Приблизительный период полураспада антител составляет от 7 до 10 дней. Продолжительность иммунитета (т.е. отрезок времени, в течение которого титр HI поддерживается на уровне 80 или выше) колебалась от 30 до 42 дней после введения одной дозы химерного собачьего Mab A или химерного собачьего Mab B. Интерференция с вакцинацией вероятно происходит до тех пор, пока деградация антитела не достигнет достаточной степени, при которой оно теряет способность нейтрализовать вакцину CPV-2. Как химерное собачье Mab A, так и химерное собачье Mab B давали высокие титры, хорошо переносились, и в участке инъекции не были зарегистрированы побочные эффекты или реакции.
[00146] Первоначальная вакцинация CPV не привела к сероконверсии у 5 из 6 щенков, возможно, из-за остаточных химерных собачьих антител Mab A или B, нейтрализующих вакцину. Между блокированием репликации вакцинного вируса как собачьим Mab A, так и химерным собачьим Mab B наблюдалась in vivo корреляция первого порядка с данными о нейтрализации in vitro. Впоследствии у трех щенков произошла сероконверсия после второй вакцинации, и у одного щенка - после третьей вакцинации.
[00147] Что касается щенка CWW-8, сероконверсия на 56-й день не коррелировала со сроками вакцинации, проведенной на 37-й день. Предполагается, что выделение вакцинного вируса от других щенков в исследовании оказало воздействие на CWW-8 и вызвало сероконверсию после того, как титры достигли уровня <20.
[00148] Таблица 5
1 Введена 1-я моновалентная вакцина от парвовируса
2 Введена 2-я моновалентная вакцина от парвовируса
3 Сероконверсия вакцины
4 Введена 3-я моновалентная вакцина от парвовируса
[00149] Таблица 6
Подчеркнуто=введена 1-я моновалентная вакцина от парвовируса
Курсив=введена 2-я моновалентная вакцина от парвовируса.
Пример 10
Профилактика и лечение
[00150] В этом in vivo исследовании использовали антитело MabA v2. Цель этого исследования состояла в подтверждении корректности дозы живого CPV-2, которая будет использоваться для заражения собак в будущем опорном исследовании MabA v2, и в проверке обоснованности концепции для MabA v2 по двум показаниям, как в качестве профилактического лечения для предотвращения CPV-2 инфекции, так и в качестве терапевтического лечения собак, инфицированных CPV-2. См. краткое описание дизайна исследования в Таблице 7 ниже.
[00151] Таблица 7.
Химерное собачье Mab A v2 (SEQ ID NO: 24 и 25)
• Не GLP
• Однодозовым лабораторным исследованием для оценки PD и безопасности для невакцинированных здоровых биглей с отрицательным титром CPV 2
• Щенков рандомизировали в одну из шести равных групп лечения.
• Равное количество мужских и женских особей
• 11-недельный возраст
• Вес не менее 1,5 кг
• Получены с фермы Ridglan Farms, Висконсин
Введение CPV-2: 25 июня 2019 г.
Окончание исследования: 7 июля 2019 г.
[00152] Двенадцать собак рандомизировали и распределяли в одну из 6 групп, каждая группа включала одну мужскую особь и одну женскую особь. Группы 1-3 должны были получать только контрольную пробу с живым CPV-2 для подтверждения корректности дозы, необходимой для получения требуемого уровня заболеваемости и смертности при трех разных логарифмах вирусной нагрузки. Собаки в группах 4 и 5 получали Mab A v2 в качестве профилактического лечения перед инокуляцией живым CPV-2b. Собаки в группе 6 получали Mab A v2 после контрольного заражения и подтверждения развития инфекции CPV-2 с помощью теста ELISA SNAP в условиях содержания в клетке. См. таблицу 8 (ниже) для графика заражения инокуляцией CPV 2.
[00153] Таблица 8
** Группе 6 вводили Mab после подтверждения CPV-2 инфекции путем детектирования вируса в фекалиях (с помощью CPV-2 ELISA в условиях содержания в клетке) в соответствии с таблицей 10.
[00154] Группам 4 и 5 вводили MabA v2 в день исследования 1 в соответствии с таблицей 9 ниже.
[00155] Таблица 9.
[00156] Группе 6 давали Mab A v2 на 7-й день исследования после получения у каждого щенка положительного результата теста CPV-2 ELISA в условиях содержания в клетке, подтверждающего CPV-2 в фекалиях, что свидетельствовало о наличии парвовирусной инфекции. См. таблицу 10 ниже.
[00157] Таблица 10.
[00158] Это исследование предоставило первые фармакодинамические данные о MabA v2, вводимом подкожно. Внутривенно введенная доза собакам группы 4 обеспечила мгновенное повышение титров HI, как и предполагалось. Подкожно введенная доза у собак группы 5 вызывала сопоставимые титры в течение 24-часового периода. В приведенной ниже таблице 11 видна временная разница достижения пиковых титров MabA v2 HI после введения внутривенных и подкожных доз.
[00159] Как показано в таблице 12 ниже, введение MabA v2 вызывало титры циркулирующих антител у собак в течение 24 часов (в/в) и 48 часов (п/к) после введения. Защитные пассивные титры антител сохранялись в течение 16 дней несмотря на заражение с высокой вирусной нагрузкой.
[00160] Таблица 11
[00161] Таблица 12
NA - Не применимо
[00162] В День 1 группам 4 и 5 вводили MabA v2 внутривенно или подкожно, соответственно. На 4-й день всем 12 собакам во всех 6 группах вводили интраназально вирулентный CPV-2 в дозе прививки, указанной в таблице 8. Собак наблюдали в течение 14 дней, в течение которых каждые 6 часов регистрировали общее состояние здоровья (GHO), каждые 12 часов регистрировали клинические показатели (с помощью проверенной системы, Mohr et al, 2003) и посредством частых заборов крови для гематологии, HI и VN, а также анализа гемагглютинации в фекальных массах (HA). Кроме того, для всех собак выполняли тест ELISA на CPV 2 каждый день после инокуляции до получения положительного результата для оценки наличия парвовирусной инфекции. В таблице 13 обобщены клинические признаки CPV-2, наблюдаемые во время исследования.
[00163] Таблица 13.
[00164] Собаки в группах 3 и 6 (те, которые были заражены 106 живыми CPV-2 и не получали предварительно MabA v2) показали положительные тесты ELISA на CPV-2 в условиях содержания в клетке на третий или четвертый день после инокуляции. У обеих собак в группе 3 (фактически контрольной группе) развились выраженные классические клинические признаки парвовирусной инфекции, включая депрессию, рвоту, кровавый понос, прогрессирующее обезвоживание, они умерли и были подвергнуты эвтаназии через 7 дней после инокуляции. Обе собаки в группе 6 дали положительный результат в тесте ELISA на CPV-2 в условиях содержания в клетке через 3 дня после инокуляции живым CPV-2. После получения положительного теста ELISA на CPV-2 в условиях содержания в клетке собакам впоследствии были введены Mab A v2 внутривенно в дозе 5 мг/мл. Они не получали дополнительную вспомогательную или поддерживающую терапию.
[00165] В то время как собаки в группе 3 продолжали заболевать и в конечном итоге стали умирать и были гуманно усыплены, собаки в группе 6 выжили и достигли полного клинического выздоровления в течение периода исследования. Собаки группы 6 также снова показали отрицательный тест ELISA на CPV 2 в условиях содержания в клетке, что указывало на то, что они больше не выделяли вирусных частиц.
[00166] Все собаки в группах 4 и 5, получавшие Mab A v2 в качестве профилактического лечения, не только выжили, но и остались здоровыми (например, у них ни разу не был получен положительный результат ELISA на CPV-2 в условиях содержания в клетке и не было зарегистрировано ни одного клинического признака парвовирусной инфекции).
[00167] Анатомическую гистопатологию групп 3-6 проводили после гуманной эвтаназии при запланированном завершении исследования, за исключением случаев, когда эвтаназия проводилась раньше из гуманных соображений. В 4-й и 5-й группах значимых патологических изменений выявлено не было. Группа 6 показала лимфоидное истощение тимуса, но другие исследованные органы оставались в норме. Группа 3 показала лимфоидное истощение всех лимфоидных органов, атрофию/некроз ворсинок тонкой кишки от умеренной до тяжелой степени с некрозом крипт от легкой до тяжелой степени, что указывает на инфекцию CPV-2.
[00168] Это пилотное исследование для подтверждения концепции продемонстрировало, что Mab A v2 является многообещающим в качестве профилактического и терапевтического вмешательства. Ни одна из собак в профилактических группах (n=4) не заболела парвовирусной инфекцией, и все собаки оставались клинически нормальными. Все собаки в терапевтической группе (n=2), у которых было подтверждено инфицирование парвовирусом, выжили и достигли полного клинического выздоровления после введения Mab A v2 без какого-либо другого дополнительного или поддерживающего лечения. Это исследование также подтвердило, что подкожное введение Mab A v2 для профилактики является приемлемым вариантом. Наконец, продукт хорошо переносился, не вызывал побочных явлений или реакций в месте инъекции. В этом исследовании для подтверждения концепции профилактическое введение Mab A v2 перед контрольным заражением обеспечивало 100% защиту щенков от инфекции CPV-2. Кроме того, 100% щенков, получивших терапевтическое введение Mab A v2 после подтвержденной инфекции CPV, выжили и выздоровели.
Пример 11
Опорное исследование эффективности терапевтического лечения
[00169] В этом опорном исследовании оценивается эффективность Mab A v2 в качестве средства для лечения парвовирусной (CPV) болезни у псовых. Удовлетворительное завершение этого исследования и демонстрация эффективности могут служить в качестве подтверждения заявление на этикетке, в котором говорится: «Этот продукт продемонстрировал свою эффективность при лечении собак в возрасте 13 недель и старше от парвовируса псовых (CPV)».
[00170] Это GCP, рандомизированное, слепое, плацебо-контролируемое исследование длится 14 дней после по меньшей мере 7-дневного периода акклиматизации. В общей сложности 28 ранее не получавших лечение собак с отрицательным титром CPV-2 (в возрасте ≤13 недель в день 0, любого пола и весом ≥1,5 кг) рандомизируют для исследования в соотношении 3:1 в две группы (n=21 собака в группе 1 и n=7 в группе 2), как показано в таблице 14.
[00171] Во время акклиматизации собак приучают к процедурам кормления, содержания и ухода, при этом им вводят антигельминтные и антибиотические препараты для устранения распространенных гельминтозов и кокцидий.
[00172] День заражения CPV-2b считается днем 0. В день 0 всем собакам в группах 1 и 2 вводят вирулентный CPV-2b в дозе приблизительно 1×106 TCID50 интраназально (IN) (в объеме, равном приблизительно 1 мл; приблизительно 0,5 мл на ноздрю). В день обнаружения CPV в фекалиях (по положительному результату теста CPV SNAP в условиях содержания в клетке), каждой собаке вводят Mab A v2 или контрольный продукт (CP; фосфатно-солевой буфер (PBS)) путем внутривенной (IV) инъекции посредством катетера в доступную вену (например, цефалическую) с помощью шприца с люэровским замком. Mab A v2 вводят однократно в дозе 5 мг/кг в расчете на массу тела. CP имеет рН 7,2±0,2. Дозу Mab A v2 и CP рассчитывают следующим образом:
{(Масса тела в кг) x (5 мг/кг)} ÷ {25 мг/мл}=объем в мл для инъекции
[00173] В течение 14 дней в запланированные моменты времени, указанные в таблице 15, отслеживают состояние здоровья каждой собаки путем физикального обследования (PE), обследования общего состояния здоровья (GHO), измерения ректальной температуры (RT), проведения теста CPV SNP в условиях содержания в клетке, анализов HI в сыворотке, гемагглютинации (HA) в фекальных массах, биохимии сыворотки и гематологии.
[00174] Первичной переменной эффективности является предотвращение смертности от инфекции CPV у собак группы 1 по сравнению с собаками группы 2.
[00175] См. группы лечения в таблице 14 ниже.
[00176] Таблица 14.
(мг/мл)
[00177] Рандомизация. Это исследование может потребовать двухэтапной рандомизации. Первый этап заключается в определении, какие 28 собак будут участвовать в исследовании. Затем собак рандомизируют блоками размером 4 на основе помета, если это возможно, с соотношением 3:1 в группы 1 и 2, соответственно. Рандомизация основана на случайных числах, сгенерированных процедурой PLAN в SAS (версия 9.4 или более поздняя, SAS Institute, Cary NC) с помощью метода рандомизированного выбора с начальным числом.
По прибытии в испытательный центр собак размещают в клетках в 2-х комнатах в соответствии с порядком прибытия, и собаки из одного помета/блока по возможности остаются в той же комнате. Собаки могут быть подвергнуты вторичному воздействию вируса, передаваемого от инфицированных собак. Чтобы сохранить одинаковый уровень вторичного воздействия вируса в обеих группах лечения и обеспечить слепое исследование для персонала испытательного центра, в каждой комнате содержат обе группы лечения. После отбора 28 собак их клетки последовательно нумеруют от 1 до 28. Собаки из одного помета имеют соседние номера клеток, а в пометах из 4 собак - более ранние номера (например, 1-4, 5-8 и т.д.) на комнату. В одной комнате должны быть клетки с номерами 1-12, а в другой комнате - клетки с номерами 13-28. Собак регистрируют в порядке номеров клеток в списке рандомизации.
[00178] Слепой режим исследования. Исследователь и весь другой персонал испытательного центра (за исключением раздатчика и одного назначенного лица, которое удерживает собак во время введения дозы) не знают о фактическом назначении группы лечения в День 0. Только раздатчик и лицо, назначенное для удержания собак во время введения дозы, в испытательном центре имеют доступ к фактическому назначению группы лечения (Mab A v2 или CP) для каждой собаки. Раздатчик и лицо, удерживающее/держащее собак, не выполняют никаких исследований.
[00179] Технические характеристики. В общей сложности приобретают не менее 30 специально выведенных, невакцинированных, серонегативных по CPV-2 (HI <20), здоровых собак породы бигль. На момент прибытия собак в испытательный центр подтверждают отсутствие у них CPV с помощью теста CPV SNAP. Несмотря на то, что в исследование включено 28 собак, приобретают две дополнительные собаки, чтобы обеспечить соблюдение количества собак после скрининга и акклиматизации. В идеале 30 собак состоят из 7 пометов, по 4 собаки в каждом, плюс 2 собаки из другого помета (неполный помет).
[00180] Определение базовой активности. Серия, определяющая базовую эффективность, задает активность последующих серий, относящихся к одному выпуску, каждая серия должна быть на уровне или превышать активность серии, определяющей базовую эффективность, при сравнении при определении активности, чтобы считаться удовлетворительной для выпуска. Для установления основного эталона при определении активности, серию, определяющую базовую эффективность, тестируют с помощью анализа(ов) референсного мониторинга. Тестирование выполняют в день 0±7 дней после введения первой эффективной дозы, введенной исследуемым собакам.
[00181] Наблюдения
[00182] Физикальное обследование (РЕ). Ветеринар испытательного центра проводит физикальное обследование всех собак по меньшей мере в дни -7, -1, в день введения дозы Mab A v2/CP, в день 13 и, при необходимости, внепланово. Физикальное обследование включает всестороннюю оценку всех систем организма, включая статус гидратации и массу тела, и их регистрацию.
[00183] Потребление пищи. Один раз в сутки проводят качественную оценку потребления пищи в сочетании с обследованием общего состояния здоровья (GHO). Все наблюдаемые отклонения в потреблении пищи фиксируют.
[00184] Обследование общего состояния здоровья (GHO) и измерение ректальной температуры (RT). GHO выполняет ветеринарный врач испытательного центра или уполномоченное им лицо не реже одного раза в сутки во время периода акклиматизации с -7 по день -1. GHO проводят каждые 12 часов (±1 час), начиная с 0-го дня по 12-й день. Начиная с 0-го дня, в сочетании с каждым GHO также измеряют RT с помощью калиброванного термометра по шкале Фаренгейта.
[00185] Конкретную информацию по GHO собирают на основе этих четырех параметров:
• Отношение к окружающей среде - регистрируется как нормальное, легкая или умеренная депрессия, тяжелая депрессия, коллапс или агональное состояние.
• Аппетит - регистрируется как нормальный, добровольно ест небольшими порциями, не проявляет интереса к еде или отсутствие аппетита.
• Рвота - регистрируется как отсутствие, легкая (1 раз в 12 часов), умеренная (2-5 раз в 12 часов) или сильная (≥ 6 раз в 12 часов).
• Кал - регистрируется как хорошо сформированный или отсутствующий, мягкий или пастообразный кал, водянистый бескровный понос или водянистый, кровавый понос.
GHO также могут включать другие наблюдения в дополнение к этим четырем параметрам. Эти параметры документируют для каждой собаки в каждый период наблюдения.
[00186] Тест CPV SNAP в условиях содержания в клетке. Тесты ELISA на CPV в условиях содержания в клетке выполняют с помощью теста IDEXX CPV SNAP в соответствии с инструкциями производителя. Предварительные тесты CPV SNAP проводят на всех собаках по прибытии от поставщика в День -7, чтобы подтвердить, что у собак нет активной инфекции CPV. Последующие тесты CPV SNAP выполняют в одно и то же время утром, начиная с дня -1 и заканчивая в момент завершения исследования. В маловероятном случае, когда у собаки нет положительного результата теста CPV SNAP и, следовательно, она не получает Mab A v2/CP, она исключается из анализа эффективности.
[00187] Тестирование гемагглютинации (HI) CPV-2 в сыворотке. Образцы цельной крови собирают (приблизительно 1,5 мл) у всех собак через яремную, головную или латеральную подкожную вену в пробирки для сепарации сыворотки и перерабатывают в сыворотку в дни -7, 0, 3, 4, 6, 8, 10 и 13, причем образец в день 0 отбирают до заражения вирулентным CPV-2b. Образцы также собирают перед незапланированной эвтаназией. Образцы инвентаризируют и отправляют на сухом льду исследователю в лабораторию при первой же возможности. Образцы хранят в условиях заморозки (≤-60°C) до отправки. Данные записывают.
[00188] Анализ гемагглютинации CPV-2 (HA) в фекальных массах. Общий образец фекалий собирают у каждой собаки, начиная в День 0 до окончания исследования. Фекальную массу собирают у каждой собаки в пробирку объемом 50 мл, индивидуально замораживают и хранят для тестирования HA в фекальной массе для проверки результатов теста CPV SNAP и на соответствие одному из четырех критериев инфекции CPV-2b. Образцы фекалий гомогенизируют перед тестированием HA, чтобы максимизировать точность результатов и размер выборки. Процедуры сбора, хранения и транспортировки фекалий выполняют в соответствии с инструкциями исследователя лаборатории. Данные записывают.
[00189] Критерии инфицирования CPV-2b. Критерии CPV инфекции соответствуют 9 CFR §113.317, (c), (3), (i). Эти правила определяют четыре критерия активной инфекции CPV. Валидное заражение CPV-2b должно давать три из четырех критериев или приводить к летальному исходу по меньшей мере четырех из семи собак с CP. Согласно определению 9 CFR §113.317, четыре критерия наличия парвовируса являются следующими:
• Температура тела ≥103,4°F (39,7ºC)
• Лимфопения ≥50% от нормы до заражения
• Диарея, слизь и/или кровь в кале
• Вирусные гемагглютинины на уровне ≥1:64 при разведении кала 1:5 (или тест равной чувствительности)
Эти четыре критерия контролируют ежедневно у всех собак с помощью q12-часовых GHO, включая ректальную температуру (RT), гематологию через определенные промежутки времени для контроля количества лимфоцитов и тесты CPV SNAP, которые проводят ежедневно, а результаты подтверждают с помощью HA в фекальных массах. После заражения собаки из любой группы, которые умирают из-за инфекции CPV, считаются умершими от инфекции CPV. Собаки, которые считаются умирающими и должны быть подвергнуты эвтаназии в соответствии с пунктом о спасении, также считаются умершими от инфекции CPV.
[00190] Клиническая патология (гематология и клиническая биохимия). В День -7 оценивают исходный общий анализ крови (CBC) и биохимический профиль, чтобы убедиться, что собаки здоровы и не имеют ранее возникших болезненных состояний. В дни -1, 0, 3, 4, 5, 6, 7, 8, 10 и 13 кровь собирают для общего анализа крови для контроля количества лимфоцитов в крови. Образцы собирают в одно и то же время каждое утро и регистрируют. Приблизительно 0,5 мл крови берут для гематологического исследования, и приблизительно 1 мл крови берут для клинической биохимии через любую доступную вену (например, яремную, головную или латеральную подкожную вену). Все образцы анализируют для оценки данных CBC в режиме реального времени, чтобы определить, имела ли место лимфопения, которая является одним из четырех клинических признаков, соответствующих активному CPV в соответствии с 9 CFR 113.317.
[00191] Результаты эффективности
[00192] Первичный результат. Первичной переменной эффективности является смертность, вызванная CPV. Смертность рассчитывают в группах Mab A v2 и CP. Предотвращенную долю заболеваемости (PF) и нижний 95% доверительный интервал вычисляют для сравнения группы Mab A v2 с группой CP в одной комнате в качестве стратифицированной переменной с помощью метода Кохрана-Мантеля-Хензеля (Cochran-Mantel-Haenszel) (процедура FREQ в SAS, SAS Institute, Cary NC, версия 9.4 или более поздняя). В случае, если PF не может быть сгенерирован из-за отсутствия данных (например, 100% выживаемость Mab A v2), и результаты по комнатам являются однородными, выполняют тот же анализ без учета комнаты в качестве стратифицированной переменной. Первичная конечная точка эффективности достигается, если нижний 95% доверительный интервал PF>0, а уровень смертности в группе CP выше, чем в группе Mab A v2. Смертность у собак с Mab A v2/CP определяют как количество смертей от инфекции CPV или количество собак, которые считаются умирающими и должны быть подвергнуты эвтаназии в соответствии с пунктом о спасении. В маловероятном случае, когда у собаки нет положительного результата теста CPV SNAP и, следовательно, она не получает Mab A v2/CP, она исключается из анализа эффективности.
[00193] Пункт о спасении. Если ветеринарный врач испытательного центра сочтет отдельную собаку умирающей, он может исключить собаку из исследования согласно пункту о спасении и выбрать эвтаназию. Собаки, исключенные из исследования по гуманным соображениям, включаются в оценку эффективности как «смертность», за исключением случаев, когда причина эвтаназии не связана с CPV.
[00194] График событий представлен в таблице 15 ниже.
[00195] Таблица 15
12
12
12
12
12
12
12
12
12
12
12
12
12
2PE и BW также выполняют в тот же день, что и дозирование IVP/CP.
3Дозу IVP/CP вводят при обнаружении CPV-2 в фекалиях отдельных собак с помощью теста CPV SNAP.
4HA в фекальных массах выполняют для подтверждения заражения парвовирусом и проверки корректности результатов теста CPV SNAP.
[00196] Ниже представлена процедура заражения парвовирусом псовых:
1. Убрать пищу за ~12 часов до введения инфицирующего материала. Вода остается в свободном доступе.
2. Достать инфицирующий материал из сверхнизкотемпературной (-80°C) морозильной камеры и дать ему оттаять при комнатной температуре примерно за 1 час до использования.
3. Разморозить пять дополнительных аликвот, чтобы иметь запасные дозы на случай ошибки при обработке.
4. До момента использования хранить инфицирующий материал на жидком льду.
5. Набрать шприцем аликвоту инфицирующего материала объемом 1 мл по одной дозе за раз.
6. Использовать шприц (без иглы) с назальной канюлей для введения 0,5 мл препарата в каждую ноздрю.
7. Удерживать [животное] вручную; седация не требуется.
8. Помощник держит голову собаки приподнятой, слегка приподняв нос во время дозирования.
9. Подождать несколько секунд между введениями в каждую ноздрю, чтобы собака сглотнула и почувствовала себя комфортно.
10. Ожидать, что некоторое количество инфицирующего материала может вытечь из ноздрей.
11. Записать идентификационный номер собаки, дату и время в протоколе заражения животных после завершения дозирования.
12. Вернуть корм всем собакам сразу после дозирования.
13. Вернуть неиспользованный инфицирующий материал в морозильную камеру при температуре -80°C, пометить как «аликвота остатка, дата».
14. Хранить аликвоту до окончания исследования и вернуть исследователю лаборатории.
[00197] Ниже представлена процедура массового сбора фекалий:
1. Выбрать отдельную фекальную кучу (или ее часть), которая кажется наиболее ненормальной.
2. Используя отдельный деревянный шпатель для языка, собрать несколько граммов фекалий от каждой отдельной собаки - один сбор на собаку в сутки. Фекалии, вызывающие сильную диарею, возможно, потребуется собрать с помощью шприца.
3. Поместить фекалии в коническую пластиковую центрифужную пробирку объемом 50 мл. Тюбик должен быть заполнен не более чем наполовину.
4. Использовать этикетку с указанием ID собаки и даты.
5. Хранить в пластиковых пакетах для заморозки, сгруппированных по дате и группе лечения.
6. Заморозить при температуре -80°C до отправки исследователю лаборатории.
7. В конце периода сбора отправить все собранные фекалии на сухом льду для доставки исследователю лаборатории в течение ночи.
Пример 12
Исследование для определения профилактической базовой эффективности
[00198] Целью этого опорного исследования является оценка эффективности Mab A v2 в качестве профилактической терапии для предотвращения клинических признаков инфекции парвовируса (CPV) псовых.
[00199] Удовлетворительное завершение этого исследования и демонстрация эффективности могут служить подтверждением заявления на этикетке, в котором говорится: «Этот продукт продемонстрировал свою эффективность в отношении обеспечения пассивного иммунитета у здоровых собак в возрасте 13 недель и старше к парвовирусной болезни псовых (CPV)».
[00200] Это GCP, рандомизированное, слепое, плацебо-контролируемое исследование длится 14 дней после по меньшей мере 7-дневного периода акклиматизации. В общей сложности 25 ранее не получавших лечение CPV-2 серонегативных собак (титр ингибирования гемагглютинации CPV (HI) <20) рандомизируют в две группы (n=20 собак в группе 1 и n=5 в группе 2) в соответствии с таблицей 16. В день 0 собаки находятся в возрасте ≤13 недель, любого пола, по прибытии имеют вес ≥1,5 кг, находятся в хорошем состоянии и не имеют каких-либо клинических признаков заболевания на момент начала исследования.
[00201] Во время акклиматизации собак приучают к процедурам кормления, содержания и ухода, при этом им вводят антигельминтные и антибиотические препараты для устранения распространенных гельминтозов и кокцидий.
[00202] В день 0 всем собакам вводят назначенные им Mab A v2 (группа 1) или контрольный продукт [CP; Группа 2; фосфатно-солевой буфер (PBS)] путем подкожной (SC) инъекции. Mab A v2 вводят однократно в дозе 5 мг/кг в расчете на массу тела. CP имеет pH 7,2±0,2 и вводится в объеме, равном объему в группе 1. Дозу для Mab A v2 и CP рассчитывают следующим образом:
{(Масса тела в кг) x (5 мг/кг)} ÷ {25 мг/мл}=объем в мл для инъекции
[00203] Данные по локальной и системной безопасности собирают с 0-го дня (после лечения) до 2-го дня. На 3-й день всем собакам из обеих групп 1 и 2 интраназально вводят вирулентный CPV-2b в дозе приблизительно 1×106 TCID50/мл (IN) (объем, равный примерно 0,5 мл на ноздрю).
[00204] В течение 14 дней в запланированное время, указанное в таблице 17, проводят тщательный мониторинг здоровья каждой собаки путем физикального обследования (PE), измерения ректальной температуры (RT), проведения теста IDEXX SNAP CPV-2 ELISA в условиях содержания в клетке (тест CPV SNAP), анализов ингибирования гемагглютинации (HI) в сыворотке, гемагглютинации (HA) в фекальных массах и гематологии.
[00205] Первичной переменной эффективности является профилактика инфекции CPV у собак группы 1, которую определяют согласно критериям 9 CFR §113.317, (c), (3), (i):
• Температура тела ≥103,4°F (39,7ºC)
• Лимфопения ≥50% от контрольной дозы до CPV-2b в норме
• Диарея, слизь и/или кровь в кале
• Вирусные гемагглютинины на уровне ≥1:64 при разведении кала 1:5 (или тест равной чувствительности)
[00206] Эффективность считается продемонстрированной, если по меньшей мере 80% собак группы 2 (CP) имеют по меньшей мере три из четырех критериев, изложенных в 9 CFR §113.317, (c), (3), (i), и если по меньшей мере 19 собак, получавших Mab v2, остаются живыми и имеют ≤1 из четырех возможных клинических признаков.
[00207] См. группы лечения в таблице 16 ниже.
[00208] Таблица 16.
[00209] Рандомизация. В этом исследовании может потребоваться двухэтапная рандомизация. На первом этапе определяют, какие 25 собак будут участвовать в исследовании. Затем собак распределяют случайным образом блоками размером 5 с соотношением 4:1 в группы 1 и 2, соответственно. Рандомизация основана на случайных числах, сгенерированных процедурой PLAN в SAS (версия 9.4 или более поздняя, SAS Institute, Cary NC) с помощью метода рандомизированного выбора с начальным числом.
По прибытии в испытательный центр собак размещают в клетках в 2-х комнатах в соответствии с порядком прибытия, и собаки из одного помета/блока по возможности остаются в той же комнате. Собаки могут быть подвергнуты вторичному воздействию вируса, передаваемого от инфицированных собак. Чтобы сохранить одинаковый уровень вторичного воздействия вируса в обеих группах лечения и обеспечить слепое исследование для персонала испытательного центра, в каждой комнате содержат обе группы лечения. После отбора 25 собак их клетки последовательно нумеруют от 1 до 25. Собаки из одного помета имеют соседние номера клеток, при этом в пометах из 5 собак используются более ранние номера (например, 1-5, 6-10 и т. д.) на комнату. В одной комнате должны быть клетки с номерами 1-10, а в другой комнате - клетки с номерами 11-25. Собак регистрируют в порядке номеров клеток в списке рандомизации.
[00210] Маскировка исследования. Исследователь и весь другой персонал испытательного центра (за исключением раздатчика и одного назначенного лица, которое удерживает собак во время введения дозы) не знают о фактическом назначении группы лечения в День 0. Только раздатчик и лицо, назначенное для удержания собак во время введения дозы, в испытательном центре имеют доступ к фактическому назначению групп лечения (Mab A v2 или CP) для каждой собаки. Раздатчик и лицо, удерживающее/держащее собак, не выполняют никаких исследований.
[00211] Технические характеристики. В общей сложности приобретают не менее 27 специально выведенных, невакцинированных, серонегативных по CPV-2 (HI <20), здоровых собак породы бигль. На момент прибытия собак в испытательный центр подтверждают отсутствие у них CPV с помощью теста CPV SNAP. Несмотря на то, что в исследование включено 25 собак, приобретают две дополнительные собаки, чтобы обеспечить соблюдение количества собак после скрининга и акклиматизации. В идеале 27 собак состоят из 5 пометов, по 5 собак в каждом, плюс 2 собаки из другого помета (неполный помет).
[00212] Наблюдение
[00213] Физикальное обследование (PE). Ветеринар испытательного центра проводит физикальное обследование всех собак в дни -7, 0, 3, 13 и, при необходимости, внепланово. Физикальное обследование включает всестороннюю оценку всех систем организма, включая статус гидратации и массу тела.
[00214] Потребление пищи. Один раз в день проводят качественную оценку потребления пищи в сочетании с обследованием общего состояния здоровья (GHO). Все наблюдаемые отклонения в потреблении пищи фиксируют.
[00215] Осмотр места инъекции (ISO). ISO проводят через 4 часа ± 1 час после введения Mab A v2/CP для выявления клинических признаков местного воспаления (например, эритемы, жара или припухлости) один раз в сутки в день 1 и день 2. Регистрируют величину любых реакций. Все наблюдаемые отклонения фиксируют.
[00216] Обследование общего состояния здоровья (GHO) и измерение ректальной температуры (RT). GHO выполняет ветеринарный врач испытательного центра или уполномоченное им лицо не реже одного раза в сутки в течение периода акклиматизации с -7 по день -1. GHO проводят каждые 12 часов (±1 час), начиная с 0-го дня по 12-й день или внепланово. Начиная с 0-го дня, в сочетании с каждым GHO также измеряют ректальную температуру (RT) с помощью калиброванного термометра по шкале Фаренгейта. Обследование общего состояния здоровья включает, без ограничения, обследование общего внешнего вида, регистрацию отклонений в потреблении пищи или воды и/или появления рвоты или диареи. Состояние всех собак, в том числе без аномальных признаков, документируют.
[00217] ELISA на CPV в условиях содержания в клетке (тест CPV SNAP). Тесты ELISA на CPV в условиях содержания в клетке выполняют с помощью теста IDEXX CPV SNAP в соответствии с инструкциями производителя. Предварительные тесты CPV SNAP проводят на всех собаках по прибытии от поставщика в День -7, чтобы подтвердить, что у собак нет активной инфекции CPV. Последующие тесты CPV SNAP выполняют в одно и то же время утром в День 0, День 3 (до инокуляции вирулентным CPV-2b), а затем один раз в сутки до окончания исследования. Данные теста CPV SNAP записывают.
[00218] Тестирование гемагглютинации (HI) CPV-2 в сыворотке. Образцы цельной крови собирают (~1,5 мл) у всех собак через яремную, головную или латеральную подкожную вену в пробирки для сепарации сыворотки и перерабатывают в сыворотку в одно и то же время утром в дни -7, 0, 2, 3, 4, 6, 8, 10 и 13, причем образец в день 3 отбирают перед инокуляцией вирулентным CPV-2b. Образцы также собирают перед незапланированной эвтаназией. Образцы инвентаризируют и отправляют на сухом льду исследователю лаборатории при первой же возможности. Образцы хранят в условиях заморозки (≤-60°C) до отправки. Данные записывают.
[00219] Анализ гемагглютинации CPV-2 (HA) в фекальных массах. Общий образец фекалий берут у каждой собаки в День 0 и День 3 и до завершения исследования в одно и то же время утром. Фекальную массу собирают у каждой собаки в пробирку объемом 50 мл, индивидуально замораживают и хранят для тестирования HA в фекальной массе для проверки результатов теста CPV SNAP и на соответствие одному из четырех критериев инфекции CPV-2b. Образцы фекалий гомогенизируют перед тестированием HA, чтобы максимизировать точность результатов и размер выборки. Процедуры сбора, хранения и транспортировки фекалий выполняют в соответствии с инструкциями исследователя лаборатории. Данные записывают.
[00220] Критерии инфицирования CPV-2b. Критерии CPV инфекции соответствуют 9 CFR §113.317, (c), (3), (i). Эти правила определяют четыре критерия активной инфекции CPV. Валидное заражение CPV-2b должно давать три из четырех критериев по меньшей мере у 80% контрольных собак. Согласно определению 9 CFR §113.317, четыре критерия наличия парвовируса являются следующими:
• Температура тела ≥103,4°F (39,7ºC)
• Лимфопения ≥50% от нормы до заражения
• Диарея, слизь и/или кровь в кале
• Вирусные гемагглютинины на уровне ≥1:64 при разведении кала 1:5 (или тест равной чувствительности)
[00221] Эти четыре критерия контролируют ежедневно у всех собак с помощью q12-часовых GHO, включая ректальную температуру (RT), гематологию через определенные промежутки времени для контроля количества лимфоцитов и тесты CPV SNAP, которые проводят ежедневно, а результаты подтверждают с помощью HA в фекальных массах.
[00222] Клиническая патология (гематология и клиническая биохимия). В День -7 оценивают исходный общий анализ крови (CBC) и биохимический профиль, чтобы убедиться, что собаки здоровы и не имеют ранее возникших болезненных состояний. В дни 0, 3, 5, 6, 7, 8, 9, 10 и 13 собирают кровь для общего анализа крови для контроля количества лимфоцитов в крови. Образцы собирают в одно и то же время каждое утро и регистрируют. Приблизительно 0,5 мл крови берут для гематологического исследования, и приблизительно 1 мл крови берут для клинической биохимии через любую доступную вену (например, яремную, головную или латеральную подкожную вену). Все образцы анализируют для оценки данных CBC в режиме реального времени, чтобы определить, имела ли место лимфопения, которая является одним из четырех клинических признаков, соответствующих активному CPV в соответствии с 9 CFR 113.317.
[00223] Результаты эффективности
[00224] Первичный результат. Первичной переменной эффективности является предотвращение инфекции CPV, определяемой в соответствии с критериями 9 CFR §113.317, (c), (3), (i):
• Температура тела ≥103,4°F (39,7ºC)
• Лимфопения ≥50% от нормы до CPV-2b (среднее значение в дни -7, 0 и 3 до заражения)
• Диарея, слизь и/или кровь в кале
• Вирусные гемагглютинины на уровне ≥1:64 при разведении кала 1:5 (или тест равной чувствительности)
Эффективность считается установленной, если 80% контрольных собак имеют три из четырех критериев, изложенных в 9 CFR 113.317, и, если по меньшей мере 19 собак, получавших Mab A v2, остаются живыми и имеют ≤1 из четырех возможных клинических признаков.
[00225] Вторичные результаты. Могут быть оценены вторичные результаты, такие как результаты теста CPV SNAP, титры HI в сыворотке или другие параметры.
[00226] Результаты оценки безопасности. Собак из этого опорного исследования относят к необходимому количеству собак, получающих лечение в опорном полевом исследовании по оценке безопасности Mab A v2. Оценка безопасности проводится путем сопоставления всех местных и системных нежелательных явлений (НЯ) с 0-го дня (после лечения) по 3-й день. В частности, собак наблюдают на развитие реакций в месте инъекции, таких как эритема, жар и отек (через ежедневный ISO), и системных реакций, включая анафилаксию после введения Mab A v2. Данные по НЯ не подвергаются статистическому анализу, а обобщаются и сводятся в таблицы для окончательного отчета.
[00227] Серьезное НЯ. Серьезным НЯ является любое НЯ, которое приводит к смерти, является опасным для жизни, приводит к стойкой или значительной инвалидности/нетрудоспособности, врожденной аномалии или врожденному дефекту. Исследователь уведомляет руководителя разработки клинического исследования в течение 24 часов о возникновении любого серьезного НЯ.
[00228] График событий представлен в Таблице 17 ниже.
[00229] Таблица 17
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
12
GHO=обследование общего состояния здоровья
PE=физикальное обследование
CPV-2=парвовирус псовых тип 2
HI=Анализ ингибирования гемагглютинина
HA=Анализ гемагглютинина
IVP=Исследуемый ветеринарный продукт
ISO=Наблюдение за местом инъекции
1GHO выполняют каждые 24 часа во время акклиматизации. После введения IVP/CP в день 0 количество GHO увеличивают до каждых 12 часов. Наблюдение за общим состоянием здоровья включают, без ограничения, наблюдения за общим внешним видом, отклонения в потреблении пищи или воды и/или появление рвоты или диареи.
2Тест CPV-2 SNAP также может быть выполнен, если у собаки наблюдается лихорадка, вялость, рвота или диарея или другие признаки, которые, по мнению исследователя или ветеринара испытательного центра, могут указывать на парвовирусную инфекцию.
3HA в фекальных массах выполняют для подтверждения заражения парвовирусом и проверки корректности результатов теста CPV-2 SNAP.
[00230] Ниже представлена процедура заражения парвовирусом псовых:
1. Убрать пищу за ~12 часов до введения инфицирующего материала. Вода остается в свободном доступе.
2. Достать инфицирующий материал из сверхнизкотемпературной (-80°C) морозильной камеры и дать ему оттаять при комнатной температуре примерно за 1 час до использования.
3. Разморозить пять дополнительных аликвот, чтобы иметь запасные дозы на случай ошибки при обработке.
4. До момента использования хранить инфицирующий материал на жидком льду.
5. Набрать шприцем аликвоту инфицирующего материала объемом 1 мл по одной дозе за раз.
6. Использовать шприц (без иглы) с назальной канюлей для введения 0,5 мл препарата в каждую ноздрю.
7. Удерживать [животное] вручную; седация не требуется.
8. Помощник держит голову собаки приподнятой, слегка приподняв нос во время дозирования.
9. Подождать несколько секунд между введениями в каждую ноздрю, чтобы собака сглотнула и почувствовала себя комфортно.
10. Ожидать, что некоторое количество инфицирующего материала может вытечь из ноздрей.
11. Записать идентификационный номер собаки, дату и время в протоколе заражения животных после завершения дозирования.
12. Вернуть корм всем собакам сразу после дозирования.
13. Вернуть неиспользованный инфицирующий материал в морозильную камеру при температуре -80°C, пометить как «аликвота остатка, дата».
14. Хранить аликвоту до окончания исследования и вернуть исследователю лаборатории.
[00231] Ниже представлена процедура массового сбора фекалий:
1. Выбрать отдельную фекальную кучу (или ее часть), которая кажется наиболее ненормальной.
2. Используя отдельный деревянный шпатель для языка, собрать до нескольких граммов фекалий от каждой отдельной собаки - один сбор на собаку в сутки. Фекалии, вызывающие сильную диарею, возможно, потребуется собрать с помощью шприца.
3. Поместить фекалии в коническую пластиковую центрифужную пробирку объемом 50 мл. Тюбик должен быть заполнен не более чем наполовину.
4. Использовать этикетку с указанием ID собаки и даты.
5. Хранить в пластиковых пакетах для заморозки, сгруппированных по дате и группе лечения.
6. Заморозить при температуре -80°C до отправки исследователю лаборатории.
7. В конце периода сбора отправить все собранные фекалии на сухом льду для доставки исследователю лаборатории в течение ночи.
Пример 13
Период полураспада и отсутствие интерференции антител
[00232] В этом in vivo исследовании отслеживают деградацию Mab A v2 in vivo и оценивают продолжительность сохранения титра в анализе ингибирования гемагглютинации (HI) на уровне, достаточном для нейтрализации вакцинных штаммов CPV. Решаются следующие задачи:
• Характеристика периода полураспада Mab A v2 после подкожного (п/к) введения.
• Определение временного диапазона после введения, в течение которого Mab A v2 больше не будет подавлять активную иммунизацию против парвовируса (отсутствие интерференции антител или LOAI).
[00233] Серологический мониторинг титров HI после введения Mab A v2 может характеризовать период полураспада. LOAI определяют по активному иммунному ответу против парвовируса после введения вакцины у не менее чем 80% собак в каждой группе. Активный ответ определяют как четырехкратное увеличение титра по сравнению с исходным уровнем (сероконверсия) с достижением титров антител, равных или превышающих разведение 1:80, определенных HI. Этот уровень ответа антител обеспечивает иммунитет против парвовируса псовых, как показано в исследованиях иммунитета (Pollock and Carmichael, JAVMA 1982 Jan 1; 180(1):37-42).
[00234] Во-вторых, данные по безопасности собирают после лечения и до иммунизации CPV, которые могут быть использованы для достижения общего количества собак, необходимого для соблюдения требования USDA-CVB относительно минимального количества собак, равного 300, для выполнения Меморандума ветеринарных служб (VSM) No. 800.204.
[00235] Удовлетворительное завершение этого исследования и демонстрация того, когда произошла LOAI на иммунизацию против CPV, могут служить в качестве подтверждения двух заявлений на этикетке, в которых говорится:
• «Показано, что этот продукт обеспечивает пассивную иммунизацию здоровых собак в возрасте 13 недель и старше для предотвращения парвовирусной (CPV) болезни у псовых».
• «Показано, что этот продукт является эффективным для лечения парвовирусной инфекции псовых (CPV) у собак в возрасте 13 недель и старше».
[00236] В приведенном выше примере 9, описывающем предшествующее исследование KB-030-PK-301, Mab A v2 приводил к нейтрализации вакцинного CPV во многом так же, как антитело материнского происхождения. Настоящее исследование может предоставить информацию о сроках вакцинации CPV после введения Mab A v2 в качестве профилактической терапии.
[00237] Это исследование является рандомизированным неслепым открытым исследованием GCP, проведенным на здоровых серонегативных по CPV собаках породы бигль. Исследование длится до 113 дней с 7-дневным периодом акклиматизации. Во время акклиматизации собаки привыкают к процедурам кормления, содержания и обращения; и получают антигельминтные и антибиотические препараты для устранения распространенных гельминтозов и кокцидий.
[00238] В день 0 подкожно вводят 5 мг/кг Mab A v2 в межлопаточную область группам 1 и 2. Группы 3 и 4 не получают Mab A v2. Со дня 0 по день 41 в различные моменты времени собирают результаты обследования общего состояния здоровья (GHO), физикального обследования (PE) и осмотра места инъекции (ISO) для мониторинга собак на предмет любых локальных и системных реакций на Mab A v2.
[00239] На 42-й день одну предварительно назначенную моновалентную вакцину против CPV вводят группам 1 и 3, а другую предварительно назначенную моновалентную вакцину против CPV вводят группам 2 и 4. Каждой собаке на 42-й день после сбора сыворотки для определения титров HI вводят предварительно назначенную моновалентную вакцину против CPV (либо вакцину 1, либо вакцину 2). Если сероконверсия вакцины не документирована после предыдущей вакцинации, через 3 недели после первой вакцинации, на 63-й день, проводится ревакцинация («2-я CPV вакцина»). Если сероконверсия вакцины не документирована после второй CPV вакцины, на 84-й день осуществляют третью повторную вакцинацию предварительно назначенной моновалентной CPV вакциной («третья бустерная вакцина»). Выход из исследования отдельных собака происходит после получения результатов HI, подтверждающих сероконверсию. В случае, если у некоторых собак не развился иммунный ответ на вакцинацию после титров HI на 91-й день, на 105-й день вводят четвертую и последнюю моновалентную бустерную CPV вакцину («4-й бустерная вакцина»). Титры ингибирования гемагглютинации в сыворотке измеряют в различные моменты времени для мониторинга деградации Mab A v2 и определения момента, когда произошла LOAI на вакцинацию против CPV.
[00240] Со дня 43 до окончания исследования собирают GHO и PE в различные моменты времени для мониторинга общего состояния здоровья собак.
[00241] Две моновалентные CPV вакцины, предварительно назначенные и вводимые в исследовании, представляют собой:
Вакцина 2
[00242] См. группы лечения в Таблице 18 ниже.
[00243] Таблица 18.
Вакцина 1=Nobivac Canine 1-PV® (Merck); Вакцина 2=Рекомбитек® (Merial)
[00244] Рандомизация. Собак (в возрасте ≤13 недель в день 0, любого пола и весом ≥1,5 кг) рандомизируют в соотношении 2:2:1:1 в группы с 1 по 4 в день 0 или ранее с помощью списка рандомизации, предоставленного участвующим в исследовании программистом спонсора. Лечение назначают случайным образом в каждом блоке из 6 собак. Рандомизация основана на случайных числах, сгенерированных процедурой PLAN в SAS (SAS Institute, Cary NC, версия 9.4 или более поздняя) с помощью метода рандомизированного отбора с начальным числом.
[00245] Наблюдение
[00246] Физикальное обследование (PE). PE проводят во все из дней: в дни 7, 0, день выхода из исследования и внепланово, когда это необходимо. Физикальное обследование включает всестороннюю оценку всех систем организма, включая состояние гидратации и массу тела (МТ).
[00247] Осмотр места инъекции (ISO). В День -3 в месте инъекции удаляют шерсть для подготовки к дозированию в День 0. Перед введением дозы место инъекции с удаленной шерстью оценивают и регистрируют на отсутствие какого-либо воспаления или ожога машинкой для стрижки. Начиная с 0-го дня, место инъекции оценивают один раз в сутки до 14-го дня на наличие местных реакций в месте инъекции, включая, помимо прочего, эритему, жар и отек (например, узелок). Величину любых реакций записывает. Любую наблюдаемую реакцию в месте инъекции документируют в форме Осмотр места инъекции и регистрируют как нежелательное явление (НЯ).
[00248] Обследование общего состояния здоровья (GHO). GHO выполняет исследователь или уполномоченное им лицо один раз в сутки с -7 дня до окончания исследования. Обследование общего состояния здоровья включает, без ограничения, обследование общего внешнего вида, регистрацию отклонений в потреблении пищи или воды и/или появления рвоты или диареи. Состояние всех собак, в том числе без аномальных признаков, документируют в форме Обследование общего состояния здоровья для каждой собаки в каждый период наблюдения. В дни -7, 0 и день выхода из исследования, когда проводятся PE, PE заменяет GHO.
[00249] Тестирование гемагглютинации (HI) CPV-2 в сыворотке. Образцы цельной крови собирают (приблизительно 1,5 мл) у всех собак через яремную, головную или латеральную подкожную вену, помещают в пробирки для сепарации сыворотки и перерабатывают в сыворотку в дни -7, 0, 1, 7, 14, 21, 28, 35, 42, 49, 56, 63, 70, 77, 84, 91, 98, 105, 112. Если сероконверсия документирована на HI, последующий запланированный отбор проб прекращают, и отдельная собака выбывает из исследования. Образцы хранят в условиях заморозки (от 60 до -80°C) до тех пор, пока они не будут доставлены в аналитическую лабораторию при первой же возможности.
[00250] Клиническая патология. В день -7 выполняют исходный полный анализ крови (CBC) и оценивают биохимический профиль, чтобы убедиться, что собаки здоровы и не имеют ранее возникших болезненных состояний. Приблизительно 0,5 мл крови берут для гематологического исследования, и приблизительно 1 мл берут для клинической биохимии из яремной, головной или латеральной подкожной вены.
[00251] Нежелательные явления (НЯ). НЯ определяют как любое наблюдаемое событие у собаки, которое является неблагоприятным, неожиданным и непреднамеренным, возникшее после использования ветеринарного препарата, независимо от того, считается ли оно связанным с продуктом. После начала экспериментального лечения (день 0, когда вводят Mab A v2) любое аномальное событие из GHO, PE или ISO считается НЯ.
[00252] Первичная конечная точка. Первичной конечной точкой для каждой группы является количество дней с 0-го дня до момента времени, когда ≥80% собак в группе продемонстрировали сероконверсию CPV согласно титрам HI в сыворотке к вакцинации моновалентной вакциной против CPV. Сероконверсия определяется как четырехкратное увеличение титра антител по сравнению с исходным уровнем с достижением титров антител, равных или превышающих разведение 1:80, определенное по титрам HI в сыворотке. Количество собак в группе, которые продемонстрировали иммунный ответ на вакцины, и день исследования, когда это произошло, не анализируют статистически, а суммируют и заносят в таблицу для окончательного отчета.
[00253] См. график событий в Таблице 19 ниже.
[00254] Таблица 19.
сульфадиметоксин
1 Рандомизацию осуществляют в День 0 или ранее.
2 Осмотр места инъекции на наличие клинических признаков непереносимости (например, эритемы, жара, припухлости) выполняют ежедневно, начиная с 0-го дня, до введения дозы и после нее до 14-го дня. Все отклонения от нормы характеризуются (например, размер припухлости) и документируются в CRF Осмотр места инъекции
3 2-ю, 3-ю и 4-ю вакцины против парвовируса вводят только тем собакам, у которых не произошла сероконверсия после введения предыдущей вакцины.
Пример 14
Многоцентровое ключевое исследование по оценке безопасности на здоровых собаках
[00255] В этом полевом исследовании по оценке безопасности in vivo оценивают локальную и системную переносимость MabA v2. Отдельных собак наблюдают на наличие воспаления в месте инъекции (включая, помимо прочего, эритему, жар и/или отек) и системных реакций (например, анафилаксии).
[00256] Минимум 300 собакам вводят Mab A v2 либо подкожно (SC) (n=150), либо внутривенно (IV) (n=150). Данные по безопасности, собранные в ходе этого исследования, должны соответствовать основному требованию по безопасности Центра ветеринарных биологических препаратов Министерства сельского хозяйства США (USDA-CVB), согласно которому количетво протестированных собак должно составлять не менее 300 собак.
[00257] Удовлетворительное завершение этого исследования и демонстрация безопасности могут служить в качестве подтверждения двух заявлений на этикетке, в которых говорится:
• «Показано, что этот продукт обеспечивает пассивную иммунизацию здоровых собак в возрасте 13 недель и старше для предотвращения парвовирусной (CPV) болезни у псовых».
• «Показано, что этот продукт является эффективным для лечения парвовирусной инфекции псовых (CPV) у собак в возрасте 13 недель и старше».
[00258] Это исследование является рандомизированным, немаскированным, полевым исследованием по оценке безопасности GCP, проведенном на молодых, здоровых, специально выведенных собаках. Это исследование длится 16 дней в каждом исследовательском центре. В исследование включают не менее 100 собак минимального возраста (возраст ≤10 недель) любого пола и не менее 200 собак старше минимального возраста (возраст >10 недель) любого пола.
[00259] Критерии исключения. Собака:
• В настоящее время участвует в другом исследовании.
• Была включена в другое исследование в течение предыдущих 30 дней.
• Получала химерные биологические препараты за ≤90 дней до Дня -2.
• Не сотрудничает в учебных процедурах.
• Нет разумных оснований ожидать, что она переживет продолжительность исследования.
• Имеет какие-либо ранее существовавшие кожные заболевания, которые могут сбить с толку ISO.
• Имеет текущий медицинский анамнез, предполагающий серьезные сопутствующие заболевания (например, полиурию, полидипсию, полифагию, рвоту или диарею, необъяснимую потерю веса и т.д.).
[00260] Собаки минимального возраста находятся в одном месте (ферма Ridglan (Mount Horeb, Висконсин)), тогда как остальные собаки распределены по испытательным центрам в трех географических регионах. Для максимально возможного разнообразия генетики используются как минимум три испытательных центра, расположенных в трех отдельных географических регионах, и уникальные племенные колонии. На каждом участке собак рандомизируют в соотношении 1:1:1:1 в группы 1, 2, 3 и 4 в соответствии с таблицей 20.
[00261] В день 0 всем собакам вводят Mab A v2 либо подкожно, либо внутривенно. В этом исследовании вводят две разные предварительно лицензионные серии (PLS) Mab A v2. В каждой возрастной группе и группе метода лечения примерно половина собак случайным образом получает PLS № 1, а другая половина получает случайным образом PLS № 2.
[00262] Объем дозы рассчитывают в мл по системе EDC на основе массы тела в день 0 (МТ). Доза рассчитывается системой EDC следующим образом:
{(масса тела в кг) x (5 мг/кг)} ÷ {TBD мг/мл}=объем в мл для инъекции
[00263] Подкожные дозы вводят в подкожный слой межлопаточной области. Внутривенные дозы повторно вводят в головную вену.
[00264] В запланированное время, указанное в таблице 20, осуществляют тщательный мониторинг состояния здоровья отдельной собаки путем физического обследования (PE), осмотра места инъекции (ISO) и обследования общего состояния здоровья (GHO).
[00265] Оценку безопасности выполняют путем сопоставления всех нежелательных явлений (НЯ). В частности, осуществляют мониторинг собак на предмет реакций в месте инъекции, таких как эритема, жар или отек (через ежедневный ISO), а также на предмет системных реакций, включая анафилаксию, после введения Mab A v2. Данные по НЯ не подвергают статистическому анализу, а суммируют и заносят в таблицу.
[00266] См. группы лечения в таблице 20 ниже.
[00267] Таблица 20.
(≤10 недель)
(>10 недель)
[00268] Рандомизация. Из-за проблем с поиском испытательных центров с собаками соответствующего возраста примерно 100 собак минимального возраста поставлены из одного места. Приблизительно 200 остальных собак распределены между испытательными центрами как минимум в трех географических регионах и распределены между испытательными центрами настолько равномерно, насколько это возможно. Рандомизацию осуществляют в испытательном центре по блокам, содержащим четыре собаки. На каждом участке собак рандомизируют в соотношении 1:1:1:1 в группы 1 (PLS № 1, SC), 2 (PLS № 2, SC), 3 (PLS № 1, IV) и 4 (PLS № 2, IV). Рандомизация основана на случайных числах, сгенерированных процедурой PLAN в SAS (SAS Institute, Cary NC, версия 9.4 или более поздняя) с помощью метода рандомизированного отбора с начальным числом.
[00269] Акклиматизация. Это исследование проводится в испытательных центрах, где собаки предварительно акклиматизированы к диете, условиям содержания, процедурам обращения и т.д. Таким образом, проводится только 2-дневная фаза акклиматизации, чтобы убедиться, что собаки соответствуют критериям регистрации, и удалить шерсть с места инъекций на второй день.
[00270] Физикальное обследование (РЕ). РЕ выполняет ветеринар на месте на 2-й, 0-й (до введения дозы), 7-й и 14-й дни. РЕ включает субъективную оценку общего внешнего вида и состояния, состояния слуха, глаз, полости рта, слизистых оболочек, органов дыхания, сердечно-сосудистой системы, желудочно-кишечного тракта, неврологической, опорно-двигательной, покровной и мочеполовой систем. Для описания конкретных аномалий РЕ используется терминология низкого уровня VeDDRA. Аномалии (за исключением ранее существовавших состояний и ухудшения аномалий), зарегистрированные после 0-го дня, считаются нежелательными явлениями.
[00271] Осмотр места инъекции (ISO). В День -2 место инъекции очищают от шерсти для подготовки к дозированию в День 0. Перед лечением место инъекции с удаленной шерстью оценивают и регистрируют на отсутствие какого-либо воспаления или ожога машинкой для стрижки. Начиная с 0-го дня по 14-й день, место инъекции оценивают один раз в сутки на предмет локальных реакций в месте инъекции, включая, помимо прочего, эритему, жар, отек (например, узелок). Величину любых реакций записывают. Любую наблюдаемую реакцию в месте инъекции регистрируют как НЯ.
[00272] Обследование общего состояния здоровья (GHO). GHO повторяют один раз в сутки, начиная с акклиматизации и заканчивая исследованием, за одним исключением: в дни -2, 0, 7 и 14, когда выполняются PE, PE заменяет GHO. Обследование общего состояния здоровья включают, без ограничения, обследование общего внешнего вида, регистрацию отклонений в потреблении пищи или воды и/или появления рвоты или диареи. Для описания конкретных наблюдений используется терминология низкого уровня VeDDRA. Состояние всех собак, в том числе без аномальных признаков, документируют.
[00273] Масса тела. В День 0 измеряют МТ (записывают в килограммах (кг)) с помощью откалиброванных весов и регистрируют. Собак можно взвешивать после еды или натощак. Массу тела документируют.
[00274] Группа для оценки безопасности. Популяция для оценки безопасности состоит из всех собак, получающих Mab A v2.
[00275] Результаты по оценке безопасности. Оценку безопасности проводят путем сопоставления всех нежелательных явлений. В частности, собак наблюдают на предмет реакций в месте инъекции, таких как эритема, жар или отек (через ежедневный ISO), и системных реакций, включая анафилаксию после введения Mab A v2. Данные по НЯ не подвергаются статистическому анализу, а суммируются и заносятся в таблицу.
[00276] Нежелательные явления (НЯ). НЯ определяют как любое наблюдаемое событие у собаки, которое является неблагоприятным, неожиданным и непреднамеренным, возникшее после использования ветеринарного препарата, независимо от того, считается ли оно связанным с продуктом. Все нежелательные явления документируют и записывают с помощью терминов низкого уровня VEDDRA.
[00277] Серьезное НЯ. НЯ, которое является смертельным или опасным для жизни или требует профессионального вмешательства (например, состояние здоровья собаки таково, что исследователь решает, что собаку следует либо подвергнуть эвтаназии, либо предоставить ей медицинскую помощь).
[00278] Несерьезное НЯ. НЯ, недостаточно серьезное, чтобы требовать профессионального вмешательства или удаления собаки из исследования.
[00279] См. график событий в таблице 21 ниже.
[00280] Таблица 21.
-2
1-6
8-13
* GHO включает, без ограничения, обследование общего внешнего вида, отклонения в потреблении пищи или воды и/или появление рвоты или диареи.
* Место инъекции оценивают один раз в сутки с 0 по 14 день на наличие клинических признаков локального воспаления (включая, помимо прочего, эритему, жар, отек, узелки). Величину реакции записывают.
Пример 15
Идентификация вариантов полипептидов Fc собачьего IgG-B для повышения активности ADCC
[00281] Структурные модели собачьего CD16 и Fc собачьего IgG-B получали, используя в качестве матрицы структурные координаты комплекса Fc человеческого IgG1/CD16 (1e4k1.pdb). См. Sondermann P., «3.2-A Crystal Structure of the Human IgG1 Fc Fragment-Fc gammaRIII complex», Nature 406(6793):267-73 (2000). Были идентифицированы аминокислотные остатки, которые, по-видимому, участвуют во взаимодействии между Fc собачьего IgG B (SEQ ID NO: 91) и собачьим CD16 (SEQ ID NO: 90). Как Ser10, так и Ile103 в Fc собачьего IgG-B SEQ ID NO: 91 находятся в непосредственной близости от Lys148 собачьего CD16 SEQ ID NO: 90. Для получения электростатического взаимодействия Ser10 и/или Ile103 Fc собачьего IgG-B SEQ ID NO: 90 может быть заменен кислыми аминокислотами Asp или Glu для введения солевого мостика в K148 собачьего CD16 SEQ ID NO: 90. Расстояние между Ser10Asp и Lys148; между Ser10Glu и Lys148; между Ile103Asp и Lys148; а между Ile103Glu и Lys148 меньше 4 Å (фиг. 5). Типичные варианты полипептидных последовательностей Fc собачьего IgG-B с повышенной активностью ADCC включают SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 96, SEQ ID NO: 97, SEQ ID NO: 98 и SEQ ID NO: 99. Такие вариантные полипептиды Fc собачьего IgG-B могут быть использованы вместо Fc собачьего IgG-B дикого типа для усиления уничтожения инфицированных парвовирусом клеток.
Использованная литература:
[0282] 1. S. Nandi, Manoj Kumar. Canine Parvovirus: Current Perspective. Indian J. Virol. 2010; 21(1):31-44.
[0283] 2. Carla Miranda, Gertrude Thompson. Canine parvovirus: the worldwide occurrence of antigenic variants. Journal of General Virology. 2016; 97, 2043-2057.
[0284] 3. Melissa Kennedy, Adesola Odunayo. Canine Parvovirus. Clinician’s Brief. 2017.
[00285] 4. Brindhalakshmi B, Mukhopadhyay HK, Antony PX, Thanislass J, Vijayalakshmi P, Mangadevi N. Isolation and molecular characterization of canine and feline parvovirus strains - an updated review. Journal of Dairy, Veterinary & Animal Research. 2016; 3(5):164-169.
[0286] 5. Emilee Venn, Karolina Preisner, Pedro Boscan, David Twedt, Lauren A. Sullivan. Evaluation of an outpatient protocol in the treatment of canine parvoviral enteritis. Journal of Veterinary Emergency and Critical Care. 2017; 27(1):52-65.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> КИНДРЕД БАЙОСАЙЕНСИЗ, ИНК.
<120> АНТИТЕЛА К ПАРВОВИРУСУ ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ
<130> 01157-0020-00PCT
<150> US 62/880,650
<151> 2019-07-30
<150> US 62/968,970
<151> 2020-01-31
<150> US 63/030,123
<151> 2020-05-26
<160> 99
<170> PatentIn version 3.5
<210> 1
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Эпитоп 1
<400> 1
Glu Ser Glu Asn Tyr Arg Arg Val Val Val Asn Asn Met Asp Lys Thr
1 5 10 15
Ala Val Asn Gly Asn Met Ala Leu Asp Asp Ile His Ala Glu Ile Val
20 25 30
Thr Pro Trp Ser Leu Val
35
<210> 2
<211> 44
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Эпитоп 2
<400> 2
Thr Pro Trp Arg Tyr Tyr Phe Gln Trp Asp Arg Thr Leu Ile Pro Ser
1 5 10 15
His Thr Gly Thr Ser Gly Thr Pro Thr Asn Ile Tyr His Gly Thr Asp
20 25 30
Pro Asp Asp Val Gln Phe Tyr Thr Ile Glu Asn Ser
35 40
<210> 3
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Минимальный Эпитоп 2
<400> 3
Thr Pro Trp Arg Tyr Tyr Phe Gln Trp Asp Arg Thr Leu Ile Pro Ser
1 5 10 15
His Thr Gly Thr Ser Gly Thr Pro
20
<210> 4
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRH1 вариабельной тяжелой цепи Mab A
<400> 4
Gly Phe Ser Leu Ser Ser Tyr His Val His
1 5 10
<210> 5
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRH2 вариабельной тяжелой цепи Mab A
<400> 5
Val Met Trp Asn Asp Gly Asp Thr Ser
1 5
<210> 6
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRH3 вариабельной тяжелой цепи Mab A
<400> 6
Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr
1 5 10
<210> 7
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR1 каркасный участок вариабельной тяжелой цепи
Mab A
<400> 7
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 8
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR1 каркасный участок вариабельной тяжелой цепи
Mab A варианта 2 (v2), Q13A
<400> 8
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 9
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR2 каркасный участок вариабельной тяжелой цепи
Mab A
<400> 9
Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu Gly
1 5 10
<210> 10
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR3 каркасный участок вариабельной тяжелой цепи
Mab A
<400> 10
Tyr Asn Leu Ala Leu Asn Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser
1 5 10 15
Lys Ser Gln Val Phe Phe Lys Met Ser Ser Leu Gln Thr Glu Asp Thr
20 25 30
Ala Thr Tyr Tyr Cys Ala Arg
35
<210> 11
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR4 каркасный участок вариабельной тяжелой цепи
Mab A
<400> 11
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 12
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR4 каркасный участок вариабельной тяжелой цепи
Mab A варианта 2 (v2), S11A
<400> 12
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 13
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRL1 вариабельной легкой цепи Mab A
<400> 13
Lys Ala Ser Gln Asn Val Asp Ser Asn Val Asp
1 5 10
<210> 14
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRL2 вариабельной легкой цепи Mab A
<400> 14
Lys Ala Ser Asn Arg Asn Thr
1 5
<210> 15
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRL3 вариабельной легкой цепи Mab A
<400> 15
Met Gln Ser Thr Ser Tyr Pro Leu Thr Phe
1 5 10
<210> 16
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR1 каркасный участок вариабельной легкой цепи
Mab A
<400> 16
Asp Ile Val Met Thr Gln Thr Pro Ala Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys
20
<210> 17
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR2 каркасный участок вариабельной легкой цепи
Mab A
<400> 17
Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Asn Leu Leu Ile Tyr
1 5 10 15
<210> 18
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR3 каркасный участок вариабельной легкой цепи
Mab A
<400> 18
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Ser Asn Met Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys
20 25 30
<210> 19
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR4 каркасный участок вариабельной легкой цепи
Mab A
<400> 19
Gly Ser Gly Thr Lys Leu Glu Ile Lys
1 5
<210> 20
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная тяжелая цепь Mab A, (Mab A HC)
<400> 20
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Leu Asn
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 21
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная тяжелая цепь Mab A варианта 2, HC-FR1
Q13A, HC-FR4 S11A, (Mab A HC v2)
<400> 21
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Leu Asn
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 22
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная легкая цепь Mab A, (Mab A LC)
<400> 22
Asp Ile Val Met Thr Gln Thr Pro Ala Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Asn Met Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 23
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab A и
собачий IgG-B, (Химерная A HC IgG-B)
<400> 23
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Leu Asn
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu
210 215 220
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
275 280 285
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
290 295 300
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
340 345 350
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
355 360 365
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
370 375 380
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
405 410 415
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
420 425 430
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 24
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab A v2 и
собачий IgG-B, HC-FR1 Q13A, HC-FR4 S11A, (Химерная A HC v2 IgG-B)
<400> 24
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Leu Asn
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu
210 215 220
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
275 280 285
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
290 295 300
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
340 345 350
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
355 360 365
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
370 375 380
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
405 410 415
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
420 425 430
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 25
<211> 217
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab A и
собачья константная область легкой цепи каппа,
(Химерная A LC каппа)
<400> 25
Asp Ile Val Met Thr Gln Thr Pro Ala Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Asn Met Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg Asn Asp Ala Gln
100 105 110
Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly
115 120 125
Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 26
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Лидерная последовательность тяжелой цепи
<400> 26
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser
<210> 27
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Лидерная последовательность легкой цепи
<400> 27
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 28
<211> 476
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab A и
собачий IgG-B с лидерной последовательностью,
(Химерная A HC IgG-B с лидерной последовательностью)
<400> 28
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln
20 25 30
Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Ser Ser Tyr His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Leu Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu
65 70 75 80
Ala Leu Asn Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln
85 90 95
Val Phe Phe Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr
100 105 110
Tyr Cys Ala Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe
115 120 125
Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Thr Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser
145 150 155 160
Gly Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Met Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys
210 215 220
Asn Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro
225 230 235 240
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
245 250 255
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
290 295 300
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
305 310 315 320
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
325 330 335
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
340 345 350
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
355 360 365
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
370 375 380
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
385 390 395 400
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
405 410 415
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
420 425 430
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
435 440 445
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 29
<211> 476
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab A v2 и
собачий IgG-B с лидерной последовательностью, HC-FR1 Q13A,
HC-FR4 S11A, (Химерная A HC v2 IgG-B с лидерной
последовательностью)
<400> 29
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala
20 25 30
Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Ser Ser Tyr His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Leu Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu
65 70 75 80
Ala Leu Asn Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln
85 90 95
Val Phe Phe Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr
100 105 110
Tyr Cys Ala Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe
115 120 125
Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr
130 135 140
Thr Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser
145 150 155 160
Gly Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Met Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys
210 215 220
Asn Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro
225 230 235 240
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
245 250 255
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
290 295 300
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
305 310 315 320
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
325 330 335
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
340 345 350
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
355 360 365
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
370 375 380
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
385 390 395 400
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
405 410 415
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
420 425 430
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
435 440 445
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 30
<211> 237
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab A и
собачья константная область легкой цепи каппа с лидерной
последовательностью, (Химерная A LC каппа с лидерной
последовательностью)
<400> 30
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Val Met Thr Gln Thr Pro Ala Ser Met Ser
20 25 30
Ile Ser Val Gly Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn
35 40 45
Val Asp Ser Asn Val Asp Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro
50 55 60
Asn Leu Leu Ile Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Asp
65 70 75 80
Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser
85 90 95
Asn Met Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Met Gln Ser Thr
100 105 110
Ser Tyr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Asn Asp Ala Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln
130 135 140
Leu His Thr Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr
145 150 155 160
Pro Lys Asp Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp
165 170 175
Thr Gly Ile Gln Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr
180 185 190
Ser Leu Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His
195 200 205
Glu Leu Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu
210 215 220
Ile Lys Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
225 230 235
<210> 31
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab A и
кошачий IgG-1, (Химерная A HC IgG-1)
<400> 31
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Leu Asn
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Ser Ser Leu Gln Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Thr Thr Ser Gly Ala Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Leu Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ala Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Leu Ser Asp Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Pro Ser Asn Thr Lys Val Asp Lys Thr Val Arg Lys Thr Asp
210 215 220
His Pro Pro Gly Pro Lys Pro Cys Asp Cys Pro Lys Cys Pro Pro Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Ile Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Ser Ile Ser Arg Thr Pro Glu Val Thr Cys Leu Val Val
260 265 270
Asp Leu Gly Pro Asp Asp Ser Asp Val Gln Ile Thr Trp Phe Val Asp
275 280 285
Asn Thr Gln Val Tyr Thr Ala Lys Thr Ser Pro Arg Glu Glu Gln Phe
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Pro Ile Leu His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Glu Phe Lys Cys Lys Val Asn Ser Lys Ser Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Lys Gly Gln Pro His
340 345 350
Glu Pro Gln Val Tyr Val Leu Pro Pro Ala Gln Glu Glu Leu Ser Arg
355 360 365
Asn Lys Val Ser Val Thr Cys Leu Ile Lys Ser Phe His Pro Pro Asp
370 375 380
Ile Ala Val Glu Trp Glu Ile Thr Gly Gln Pro Glu Pro Glu Asn Asn
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Ser Asp Gly Thr Tyr Phe Val
405 410 415
Tyr Ser Lys Leu Ser Val Asp Arg Ser His Trp Gln Arg Gly Asn Thr
420 425 430
Tyr Thr Cys Ser Val Ser His Glu Ala Leu His Ser His His Thr Gln
435 440 445
Lys Ser Leu Thr Gln Ser Pro Gly Lys
450 455
<210> 32
<211> 217
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab A и
кошачья константная область легкой цепи каппа,
(Химерная A LC каппа)
<400> 32
Asp Ile Val Met Thr Gln Thr Pro Ala Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Asn Met Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Ala Gln
100 105 110
Pro Ser Val Phe Leu Phe Gln Pro Ser Leu Asp Glu Leu His Thr Gly
115 120 125
Ser Ala Ser Ile Val Cys Ile Leu Asn Asp Phe Tyr Pro Lys Glu Val
130 135 140
Asn Val Lys Trp Lys Val Asp Gly Val Val Gln Asn Lys Gly Ile Gln
145 150 155 160
Glu Ser Thr Thr Glu Gln Asn Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Gln Ser His Glu Lys Phe
180 185 190
Ser Cys Glu Val Thr His Lys Ser Leu Ala Ser Thr Leu Val Lys Ser
195 200 205
Phe Asn Arg Ser Glu Cys Gln Arg Glu
210 215
<210> 33
<211> 217
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab A и
кошачья константная область легкой цепи каппа без N-концевого
сайта гликозилирования, (Агликозилированная химерная A LC каппа)
<400> 33
Asp Ile Val Met Thr Gln Thr Pro Ala Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Asn Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Asn Met Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Ala Gln
100 105 110
Pro Ser Val Phe Leu Phe Gln Pro Ser Leu Asp Glu Leu His Thr Gly
115 120 125
Ser Ala Ser Ile Val Cys Ile Leu Asn Asp Phe Tyr Pro Lys Glu Val
130 135 140
Asn Val Lys Trp Lys Val Asp Gly Val Val Gln Asn Lys Gly Ile Gln
145 150 155 160
Glu Ser Thr Thr Glu Gln Asn Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Gln Ser His Glu Lys Phe
180 185 190
Ser Cys Glu Val Thr His Lys Ser Leu Ala Ser Thr Leu Val Lys Ser
195 200 205
Phe Gln Arg Ser Glu Cys Gln Arg Glu
210 215
<210> 34
<211> 476
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab A v3
и собачий IgG-B с лидерной последовательностью,
(Химерная A HC v3 IgG-B с лидерной последовательностью)
<400> 34
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys
20 25 30
Pro Gly Gly Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Ser Ser Tyr His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Val Ala Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu
65 70 75 80
Ala Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
85 90 95
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
100 105 110
Tyr Cys Ala Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe
115 120 125
Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Thr Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser
145 150 155 160
Gly Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Met Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys
210 215 220
Asn Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro
225 230 235 240
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
245 250 255
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
290 295 300
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
305 310 315 320
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
325 330 335
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
340 345 350
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
355 360 365
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
370 375 380
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
385 390 395 400
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
405 410 415
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
420 425 430
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
435 440 445
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 35
<211> 476
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab A v4
и собачий IgG-B с лидерной последовательностью,
(Канинизированная A HC v4 IgG-B с лидерной последовательностью)
<400> 35
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys
20 25 30
Pro Gly Gly Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Ser Ser Tyr His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Leu Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu
65 70 75 80
Ala Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr
85 90 95
Leu Tyr Phe Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr Tyr
100 105 110
Tyr Cys Ala Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe
115 120 125
Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Thr Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser
145 150 155 160
Gly Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Met Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys
210 215 220
Asn Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro
225 230 235 240
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
245 250 255
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
290 295 300
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
305 310 315 320
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
325 330 335
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
340 345 350
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
355 360 365
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
370 375 380
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
385 390 395 400
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
405 410 415
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
420 425 430
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
435 440 445
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 36
<211> 237
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная легкая цепь Mab A и
собачья константная область легкой цепи каппа с лидерной
последовательностью,
(Канинизированная A LC каппа с лидерной последовательностью)
<400> 36
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Glu Ile Val Met Thr Gln Ser Pro Ala Ser Leu Ser
20 25 30
Leu Ser Gln Glu Glu Lys Val Thr Ile Thr Cys Lys Ala Ser Gln Asn
35 40 45
Val Asp Ser Asn Val Asp Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
50 55 60
Lys Leu Leu Ile Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Phe Thr Ile Ser
85 90 95
Ser Leu Glu Pro Glu Asp Val Ala Val Tyr Tyr Cys Met Gln Ser Thr
100 105 110
Ser Tyr Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Asn Asp Ala Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln
130 135 140
Leu His Thr Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr
145 150 155 160
Pro Lys Asp Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp
165 170 175
Thr Gly Ile Gln Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr
180 185 190
Ser Leu Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His
195 200 205
Glu Leu Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu
210 215 220
Ile Lys Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
225 230 235
<210> 37
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab A v3
и собачий IgG-B, (Канинизированная A HC v3 IgG-B)
<400> 37
Gln Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu
210 215 220
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
275 280 285
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
290 295 300
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
340 345 350
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
355 360 365
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
370 375 380
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
405 410 415
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
420 425 430
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 38
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab A v4
и собачий IgG-B, (Канинизированная A HC v4 IgG-B)
<400> 38
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Phe
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu
210 215 220
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
275 280 285
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
290 295 300
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
340 345 350
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
355 360 365
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
370 375 380
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
405 410 415
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
420 425 430
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 39
<211> 217
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная легкая цепь Mab A и
собачья константная область легкой цепи каппа,
(Канинизированная A LC каппа)
<400> 39
Glu Ile Val Met Thr Gln Ser Pro Ala Ser Leu Ser Leu Ser Gln Glu
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Ser Phe Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Asn Asp Ala Gln
100 105 110
Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly
115 120 125
Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 40
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Фелинизированная вариабельная тяжелая цепь Mab A,
(Фелинизированная A HC)
<400> 40
Gln Leu Thr Leu Arg Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Ile Arg Gln Arg Pro Gly Arg Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Ala Phe Gln Gly Arg
50 55 60
Ile Ser Ile Thr Ala Asp Thr Ala Gln Asn Gln Phe Ser Leu Gln Leu
65 70 75 80
Ser Ser Met Thr Thr Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Pro
85 90 95
Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp Gly Gln
100 105 110
Gly Ala Leu Val Thr Val Ser
115
<210> 41
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Фелинизированная вариабельная легкая цепь Mab A,
(Фелинизированная A LC)
<400> 41
Ala Ile Thr Met Thr Gln Ser Pro Gly Ser Leu Ala Gly Ser Pro Gly
1 5 10 15
Gln Gln Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Pro Gly Gln His Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Ser Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 42
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRH1 вариабельной тяжелой цепи Mab B
<400> 42
Gly Phe Ser Leu Thr Ser Tyr Gly Val Ser
1 5 10
<210> 43
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRH2 вариабельной тяжелой цепи Mab B
<400> 43
Thr Met Trp Asn Asp Gly Asp Thr Asp
1 5
<210> 44
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRH3 вариабельной тяжелой цепи Mab B
<400> 44
Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr
1 5 10
<210> 45
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR1 каркасный участок вариабельной тяжелой цепи
Mab B
<400> 45
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 46
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR1 каркасный участок вариабельной тяжелой цепи
Mab B варианта 2 (v2), Q16E
<400> 46
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser
20 25
<210> 47
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR2 каркасный участок вариабельной тяжелой цепи
Mab B
<400> 47
Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
1 5 10
<210> 48
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR2 каркасный участок вариабельной тяжелой цепи
Mab B варианта 2 (v2), I13M
<400> 48
Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met Gly
1 5 10
<210> 49
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR3 каркасный участок вариабельной тяжелой цепи
Mab B
<400> 49
Tyr His Ser Ala Leu Arg Ser Arg Leu Ser Ile Ser Arg Asp Ser Ser
1 5 10 15
Lys Ser Gln Val Leu Leu Lys Met Asn Ser Leu Gln Thr Glu Asp Thr
20 25 30
Ala Met Tyr Phe Cys Ala Arg
35
<210> 50
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR3 каркасный участок вариабельной тяжелой цепи
Mab B варианта 2 (v2), H2N, R8K, S15T, L21F, M34I, F36Y
<400> 50
Tyr Asn Ser Ala Leu Arg Ser Lys Leu Ser Ile Ser Arg Asp Thr Ser
1 5 10 15
Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln Thr Glu Asp Thr
20 25 30
Ala Ile Tyr Tyr Cys Ala Arg
35
<210> 51
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: HC-FR4 каркасный участок вариабельной тяжелой цепи
Mab B
<400> 51
Trp Gly Gln Gly Thr Leu Val Ile Val Ser
1 5 10
<210> 52
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRL1 вариабельной легкой цепи Mab B
<400> 52
Lys Ala Ser His Asn Ile Asn Lys Asn Leu Glu
1 5 10
<210> 53
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRL2 вариабельной легкой цепи Mab B
<400> 53
Tyr Ala Asn Asn Leu Gln Thr
1 5
<210> 54
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: CDRL3 вариабельной легкой цепи Mab B
<400> 54
Tyr Gln Tyr Asn Ser Gly His Thr Phe
1 5
<210> 55
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR1 каркасный участок вариабельной легкой цепи
Mab B
<400> 55
Asp Ile Val Met Thr Gln Thr Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys
20
<210> 56
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR1 каркасный участок вариабельной легкой цепи
Mab B варианта 2 (v2), V3Q, T7S, S9P, L10V, N22S
<400> 56
Asp Ile Gln Met Thr Gln Ser Pro Pro Val Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Ser Cys
20
<210> 57
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR2 каркасный участок вариабельной легкой цепи
Mab B
<400> 57
Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile Tyr
1 5 10 15
<210> 58
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR3 каркасный участок вариабельной легкой цепи
Mab B
<400> 58
Gly Ile Ser Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys
20 25 30
<210> 59
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR3 каркасный участок вариабельной легкой цепи
Mab B варианта 2 (v2), S3P
<400> 59
Gly Ile Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys
20 25 30
<210> 60
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR4 каркасный участок вариабельной легкой цепи
Mab B
<400> 60
Gly Ala Gly Thr Lys Leu Glu Leu Lys
1 5
<210> 61
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: LC-FR4 каркасный участок вариабельной легкой цепи
Mab B варианта 2 (v2), L8I
<400> 61
Gly Ala Gly Thr Lys Leu Glu Ile Lys
1 5
<210> 62
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная тяжелая цепь Mab B, (Mab B HC)
<400> 62
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser Ala Leu Arg
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Ser Ser Lys Ser Gln Val Leu Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Met Tyr Phe Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Ile Val Ser
115 120
<210> 63
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная тяжелая цепь Mab B варианта 2,
HC-FR1 Q16E, HC-FR2 I13M, HC-FR3 H2N, HC-FR3 R8K, HC-FR3 S15T,
HC-FR3 L21F, HC-FR3 M34I, HC-FR3 F36Y, (Mab B HC v2),
<400> 63
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr Asn Ser Ala Leu Arg
50 55 60
Ser Lys Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Ile Val Ser
115 120
<210> 64
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная легкая цепь Mab B, (Mab B LC)
<400> 64
Asp Ile Val Met Thr Gln Thr Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Ser Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 65
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Вариабельная легкая цепь Mab B варианта 2,
LC-FR1 V3Q, LC-FR1 T7S, LC-FR1 S9P, LC-FR1 L10V, LC-FR1 N22S,
LC-FR3 S3P, LC-FR4 L8I, (Mab B LC v2),
<400> 65
Asp Ile Gln Met Thr Gln Ser Pro Pro Val Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Ser Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 66
<211> 456
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab B и
собачий IgG-B, (Химерная B HC IgG-B)
<400> 66
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser Ala Leu Arg
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Ser Ser Lys Ser Gln Val Leu Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Met Tyr Phe Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Ile Val Ser Ala Ser Thr Thr Ala Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val
130 135 140
Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val
180 185 190
Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His
195 200 205
Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn
210 215 220
Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu
225 230 235 240
Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly
275 280 285
Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Asn
290 295 300
Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp
305 310 315 320
Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro
325 330 335
Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln
340 345 350
Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn
355 360 365
Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile
370 375 380
Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr
385 390 395 400
Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr
405 410 415
Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe
420 425 430
Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu
435 440 445
Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 67
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab B v2 и
собачий IgG-B, HC-FR1 Q16E, HC-FR2 I13M, HC-FR3 H2N, HC-FR3 R8K,
HC-FR3 S15T, HC-FR3 L21F, HC-FR3 M34I, HC-FR3 F36Y,
(Химерная B HC v2 IgG-B)
<400> 67
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr Asn Ser Ala Leu Arg
50 55 60
Ser Lys Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Ile Val Ser Ala Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu
210 215 220
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
275 280 285
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
290 295 300
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
340 345 350
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
355 360 365
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
370 375 380
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
405 410 415
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
420 425 430
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 68
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab B и
собачья константная область легкой цепи каппа,
(Химерная B LC каппа)
<400> 68
Asp Ile Val Met Thr Gln Thr Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Ser Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr
165 170 175
Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser Cys
180 185 190
Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe Gln
195 200 205
Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 69
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab B v2 и
собачья константная область легкой цепи каппа, LC-FR1 V3Q,
LC-FR1 T7S, LC-FR1 S9P, LC-FR1 L10V, LC-FR1 N22S , LC-FR3 S3P,
LC-FR4 L8I, (Химерная B LC v2 каппа)
<400> 69
Asp Ile Gln Met Thr Gln Ser Pro Pro Val Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Ser Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr
165 170 175
Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser Cys
180 185 190
Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe Gln
195 200 205
Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 70
<211> 475
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab B и
собачий IgG-B с лидерной последовательностью,
(Собачья химерная B HC с лидерной последовательностью)
<400> 70
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln
20 25 30
Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Thr Ser Tyr Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Ile Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser
65 70 75 80
Ala Leu Arg Ser Arg Leu Ser Ile Ser Arg Asp Ser Ser Lys Ser Gln
85 90 95
Val Leu Leu Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Met Tyr
100 105 110
Phe Cys Ala Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe
115 120 125
Val Tyr Trp Gly Gln Gly Thr Leu Val Ile Val Ser Ala Ser Thr Thr
130 135 140
Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly
145 150 155 160
Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro
165 170 175
Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr
180 185 190
Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met
195 200 205
Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn
210 215 220
Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys
225 230 235 240
Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro
245 250 255
Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys
260 265 270
Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val
275 280 285
Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe
290 295 300
Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu
305 310 315 320
Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His
325 330 335
Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys
340 345 350
Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln
355 360 365
Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu
370 375 380
Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro
385 390 395 400
Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu
405 410 415
Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr
420 425 430
Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly
435 440 445
Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr
450 455 460
Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 71
<211> 476
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab B v2 и
собачий IgG-B с лидерной последовательностью, HC-FR1 Q16E,
HC-FR2 I13M, HC-FR3 H2N, HC-FR3 R8K, HC-FR3 S15T, HC-FR3 L21F,
HC-FR3 M34I, HC-FR3 F36Y,
(Собачья химерная B HC v2 IgG-B с лидерной последовательностью),
<400> 71
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln
20 25 30
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Thr Ser Tyr Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Met Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr Asn Ser
65 70 75 80
Ala Leu Arg Ser Lys Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln
85 90 95
Val Phe Leu Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Ile Tyr
100 105 110
Tyr Cys Ala Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe
115 120 125
Val Tyr Trp Gly Gln Gly Thr Leu Val Ile Val Ser Ala Ala Ser Thr
130 135 140
Thr Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser
145 150 155 160
Gly Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Met Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys
210 215 220
Asn Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro
225 230 235 240
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
245 250 255
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
290 295 300
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
305 310 315 320
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
325 330 335
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
340 345 350
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
355 360 365
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
370 375 380
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
385 390 395 400
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
405 410 415
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
420 425 430
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
435 440 445
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 72
<211> 236
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab B и
собачья константная область легкой цепи каппа с лидерной
последовательностью, (Собачья химерная B LC каппа с
лидерной последовательностью)
<400> 72
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Val Met Thr Gln Thr Pro Ser Leu Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Leu Asn Cys Lys Ala Ser His Asn
35 40 45
Ile Asn Lys Asn Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro
50 55 60
Lys Leu Leu Ile Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Ser Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn
100 105 110
Ser Gly His Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Asn
115 120 125
Asp Ala Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu
130 135 140
His Thr Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro
145 150 155 160
Lys Asp Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr
165 170 175
Gly Ile Gln Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser
180 185 190
Leu Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu
195 200 205
Leu Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile
210 215 220
Lys Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
225 230 235
<210> 73
<211> 236
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab B v2 и
собачья константная область легкой цепи каппа с лидерной
последовательностью, LC-FR1 V3Q, LC-FR1 T7S, LC-FR1 S9P,
LC-FR1 L10V, LC-FR1 N22S, LC-FR3 S3P, LC-FR4 L8I,
(Собачья химерная B LC v2 каппа с лидерной последовательностью)
<400> 73
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Gln Met Thr Gln Ser Pro Pro Val Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Leu Ser Cys Lys Ala Ser His Asn
35 40 45
Ile Asn Lys Asn Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro
50 55 60
Lys Leu Leu Ile Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn
100 105 110
Ser Gly His Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Asn
115 120 125
Asp Ala Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu
130 135 140
His Thr Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro
145 150 155 160
Lys Asp Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr
165 170 175
Gly Ile Gln Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser
180 185 190
Leu Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu
195 200 205
Leu Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile
210 215 220
Lys Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
225 230 235
<210> 74
<211> 456
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная тяжелая цепь Mab B и
кошачья IgG-1, (Кошачья химерная B HC IgG-1)
<400> 74
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser Ala Leu Arg
50 55 60
Ser Arg Leu Ser Ile Ser Arg Asp Ser Ser Lys Ser Gln Val Leu Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Met Tyr Phe Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Ile Val Ser Ala Ser Thr Thr Ala Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Cys Gly Thr Thr Ser Gly Ala Thr Val
130 135 140
Ala Leu Ala Cys Leu Val Leu Gly Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ala Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val
180 185 190
Pro Ser Ser Arg Trp Leu Ser Asp Thr Phe Thr Cys Asn Val Ala His
195 200 205
Pro Pro Ser Asn Thr Lys Val Asp Lys Thr Val Arg Lys Thr Asp His
210 215 220
Pro Pro Gly Pro Lys Pro Cys Asp Cys Pro Lys Cys Pro Pro Pro Glu
225 230 235 240
Met Leu Gly Gly Pro Ser Ile Phe Ile Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Ser Ile Ser Arg Thr Pro Glu Val Thr Cys Leu Val Val Asp
260 265 270
Leu Gly Pro Asp Asp Ser Asp Val Gln Ile Thr Trp Phe Val Asp Asn
275 280 285
Thr Gln Val Tyr Thr Ala Lys Thr Ser Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Pro Ile Leu His Gln Asp Trp
305 310 315 320
Leu Lys Gly Lys Glu Phe Lys Cys Lys Val Asn Ser Lys Ser Leu Pro
325 330 335
Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Lys Gly Gln Pro His Glu
340 345 350
Pro Gln Val Tyr Val Leu Pro Pro Ala Gln Glu Glu Leu Ser Arg Asn
355 360 365
Lys Val Ser Val Thr Cys Leu Ile Lys Ser Phe His Pro Pro Asp Ile
370 375 380
Ala Val Glu Trp Glu Ile Thr Gly Gln Pro Glu Pro Glu Asn Asn Tyr
385 390 395 400
Arg Thr Thr Pro Pro Gln Leu Asp Ser Asp Gly Thr Tyr Phe Val Tyr
405 410 415
Ser Lys Leu Ser Val Asp Arg Ser His Trp Gln Arg Gly Asn Thr Tyr
420 425 430
Thr Cys Ser Val Ser His Glu Ala Leu His Ser His His Thr Gln Lys
435 440 445
Ser Leu Thr Gln Ser Pro Gly Lys
450 455
<210> 75
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab B и
кошачья константная область легкой цепи каппа,
(Кошачья химерная B LC каппа)
<400> 75
Asp Ile Val Met Thr Gln Thr Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Ser Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Ser Asp Ala Gln Pro
100 105 110
Ser Val Phe Leu Phe Gln Pro Ser Leu Asp Glu Leu His Thr Gly Ser
115 120 125
Ala Ser Ile Val Cys Ile Leu Asn Asp Phe Tyr Pro Lys Glu Val Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Val Gln Asn Lys Gly Ile Gln Glu
145 150 155 160
Ser Thr Thr Glu Gln Asn Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Gln Ser His Glu Lys Phe Ser
180 185 190
Cys Glu Val Thr His Lys Ser Leu Ala Ser Thr Leu Val Lys Ser Phe
195 200 205
Asn Arg Ser Glu Cys Gln Arg Glu
210 215
<210> 76
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Химерная вариабельная легкая цепь Mab B и
кошачья константная область легкой цепи каппа без
N-концевого сайта гликозилирования,
(Агликозилированная кошачья химерная B LC каппа)
<400> 76
Asp Ile Val Met Thr Gln Thr Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Ile Ser Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Ser Asp Ala Gln Pro
100 105 110
Ser Val Phe Leu Phe Gln Pro Ser Leu Asp Glu Leu His Thr Gly Ser
115 120 125
Ala Ser Ile Val Cys Ile Leu Asn Asp Phe Tyr Pro Lys Glu Val Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Val Gln Asn Lys Gly Ile Gln Glu
145 150 155 160
Ser Thr Thr Glu Gln Asn Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Gln Ser His Glu Lys Phe Ser
180 185 190
Cys Glu Val Thr His Lys Ser Leu Ala Ser Thr Leu Val Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Glu
210 215
<210> 77
<211> 476
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab B v3
и собачий IgG-B с лидерной последовательностью,
(Канинизированная B HC v3 IgG-B с лидерной последовательностью)
<400> 77
Met Ala Val Leu Gly Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys
20 25 30
Pro Gly Gly Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Thr Ser Tyr Gly Val Ser Trp Val Arg Gln Ser Pro Gly Lys Gly Leu
50 55 60
Glu Trp Ile Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser
65 70 75 80
Ala Val Lys Gly Gln Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln
85 90 95
Val Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Met Tyr
100 105 110
Tyr Cys Ala Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe
115 120 125
Val Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Thr Ala Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser
145 150 155 160
Gly Ser Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Met Val Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys
210 215 220
Asn Val Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro
225 230 235 240
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
245 250 255
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
290 295 300
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
305 310 315 320
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
325 330 335
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
340 345 350
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
355 360 365
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
370 375 380
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
385 390 395 400
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
405 410 415
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
420 425 430
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
435 440 445
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
450 455 460
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
465 470 475
<210> 78
<211> 236
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная легкая цепь Mab B v3
и собачья константная область легкой цепи каппа с лидерной
последовательностью, (Канинизированная B LC каппа с лидерной
последовательностью)
<400> 78
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Glu Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala
20 25 30
Val Ser Leu Gly Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser His Asn
35 40 45
Ile Asn Lys Asn Leu Glu Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
50 55 60
Lys Leu Leu Ile Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ala
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Asn Ile His
85 90 95
Pro Met Glu Glu Asp Asp Thr Ala Met Tyr Tyr Cys Tyr Gln Tyr Asn
100 105 110
Ser Gly His Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Asn
115 120 125
Asp Ala Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu
130 135 140
His Thr Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro
145 150 155 160
Lys Asp Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr
165 170 175
Gly Ile Gln Glu Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser
180 185 190
Leu Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu
195 200 205
Leu Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile
210 215 220
Lys Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
225 230 235
<210> 79
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab B v3
и собачий IgG-B, (Канинизированная B HC v3 IgG-B)
<400> 79
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser Ala Val Lys
50 55 60
Gly Gln Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr
130 135 140
Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr
180 185 190
Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala
195 200 205
His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu
210 215 220
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
225 230 235 240
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
275 280 285
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
290 295 300
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
305 310 315 320
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
325 330 335
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
340 345 350
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
355 360 365
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
370 375 380
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
385 390 395 400
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
405 410 415
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
420 425 430
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 80
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная легкая цепь Mab B v3
и собачья константная область легкой цепи каппа,
(Канинизированная B LC v3 каппа)
<400> 80
Glu Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Asn Ile His Pro Met Glu Glu
65 70 75 80
Asp Asp Thr Ala Met Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr
165 170 175
Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser Cys
180 185 190
Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe Gln
195 200 205
Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 81
<211> 114
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: вариабельная HC Mab E
<400> 81
Gly Pro Gly Leu Val Gln Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr
1 5 10 15
Val Ser Gly Phe Ser Leu Ser Ser Tyr His Val His Trp Val Arg Gln
20 25 30
Pro Pro Gly Lys Gly Leu Glu Trp Leu Gly Val Met Trp Asn Asp Gly
35 40 45
Asp Thr Ser Tyr Asn Leu Ala Leu Asn Ser Arg Leu Ser Ile Ser Arg
50 55 60
Asp Thr Ser Lys Ser Gln Val Phe Phe Lys Met Ser Ser Leu Gln Thr
65 70 75 80
Glu Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Pro Glu Leu Pro Gly Leu
85 90 95
Thr Tyr Gly Val Trp Phe Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser
<210> 82
<211> 101
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: вариабельная LC Mab E
<400> 82
Ala Ser Met Ser Ile Ser Val Gly Asp Arg Val Thr Met Asn Cys Lys
1 5 10 15
Ala Ser Gln Asn Val Asp Ser Asn Val Asp Trp Tyr Gln Gln Lys Thr
20 25 30
Gly Gln Ser Pro Asn Leu Leu Ile Tyr Lys Ala Ser Asn Arg Asn Thr
35 40 45
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
50 55 60
Phe Thr Ile Ser Asn Met Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys
65 70 75 80
Met Gln Ser Thr Ser Tyr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu
85 90 95
Glu Ile Lys Arg Ala
100
<210> 83
<211> 114
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: вариабельная HC Mab F
<400> 83
Gly Pro Gly Leu Val Gln Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr
1 5 10 15
Val Ser Gly Phe Ser Leu Thr Ser Tyr Gly Val Ser Trp Val Arg Gln
20 25 30
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Thr Met Trp Asn Asp Gly
35 40 45
Asp Thr Asp Tyr His Ser Ala Leu Arg Ser Arg Leu Ser Ile Ser Arg
50 55 60
Asp Ser Ser Lys Ser Gln Val Leu Leu Lys Met Asn Ser Leu Gln Thr
65 70 75 80
Glu Asp Thr Ala Met Tyr Phe Cys Ala Arg Ser Gln Leu Pro Gly Tyr
85 90 95
Asn Leu Arg Gly Trp Phe Val Tyr Trp Gly Gln Gly Thr Leu Val Ile
100 105 110
Val Ser
<210> 84
<211> 100
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: вариабельная LC Mab F
<400> 84
Ser Leu Leu Ser Ala Ser Val Gly Asp Arg Val Thr Leu Asn Cys Lys
1 5 10 15
Ala Ser His Asn Ile Asn Lys Asn Leu Glu Trp Tyr Gln Gln Lys Leu
20 25 30
Gly Glu Ala Pro Lys Leu Leu Ile Tyr Tyr Ala Asn Asn Leu Gln Thr
35 40 45
Gly Ile Ser Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
50 55 60
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys
65 70 75 80
Tyr Gln Tyr Asn Ser Gly His Thr Phe Gly Ala Gly Thr Lys Leu Glu
85 90 95
Leu Lys Arg Ala
100
<210> 85
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab A v3
<400> 85
Gln Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 86
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab A v4
<400> 86
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
His Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Met Trp Asn Asp Gly Asp Thr Ser Tyr Asn Leu Ala Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr Phe
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Pro Glu Leu Pro Gly Leu Thr Tyr Gly Val Trp Phe Pro Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 87
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная легкая цепь Mab A
<400> 87
Glu Ile Val Met Thr Gln Ser Pro Ala Ser Leu Ser Leu Ser Gln Glu
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Asp Ser Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Arg Asn Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Ser Phe Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Met Gln Ser Thr Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 88
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная тяжелая цепь Mab B v3
<400> 88
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Lys Pro Gly Gly
1 5 10 15
Thr Leu Arg Leu Ser Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Ser Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Met Trp Asn Asp Gly Asp Thr Asp Tyr His Ser Ala Val Lys
50 55 60
Gly Gln Leu Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Ser Gln Leu Pro Gly Tyr Asn Leu Arg Gly Trp Phe Val Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 89
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Канинизированная вариабельная легкая цепь Mab B v3
<400> 89
Glu Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser His Asn Ile Asn Lys Asn
20 25 30
Leu Glu Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Asn Leu Gln Thr Gly Val Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Asn Ile His Pro Met Glu Glu
65 70 75 80
Asp Asp Thr Ala Met Tyr Tyr Cys Tyr Gln Tyr Asn Ser Gly His Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 90
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный собачий CD16 с линкером и поли-His
<400> 90
Met Trp Gln Leu Val Ser Ser Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
Gly Thr Gln Ala Ala Asp Val Pro Lys Ala Val Val Val Leu Glu Pro
20 25 30
Lys Trp Asn Arg Val Leu Thr Met Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
Gly Asp His Leu Leu Arg Asp Asn Tyr Thr Trp Leu His Asn Gly Arg
50 55 60
Pro Ile Ser Asn Gln Ile Ser Thr Tyr Ile Ile Lys Asn Ala Ser Ile
65 70 75 80
Lys Asn Ser Gly Glu Tyr Arg Cys Gln Thr Asp Gln Ser Lys Leu Ser
85 90 95
Asp Pro Val Gln Leu Glu Val His Thr Gly Trp Leu Leu Leu Gln Val
100 105 110
Pro Arg Leu Val Phe Gln Glu Gly Glu Leu Ile Gln Leu Lys Cys His
115 120 125
Ser Trp Lys Asn Thr Pro Val Arg Asn Val Gln Tyr Phe Gln Asn Gly
130 135 140
Arg Gly Lys Lys Phe Phe Tyr Asn Asn Ser Glu Tyr His Ile Pro Ala
145 150 155 160
Ala Thr Ser Glu His Asn Gly Ser Tyr Phe Cys Arg Gly Ile Ile Gly
165 170 175
Lys Lys Asn Glu Ser Ser Glu Ala Val Asn Ile Ile Ile Gln Gly Ser
180 185 190
Ser Leu Pro Ser Thr Ser Leu Leu Leu Ser His Trp Pro Gln Gly Ser
195 200 205
Gly Ser His His His His His His
210 215
<210> 91
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный Fc собачьего IgG-B дикого типа
<400> 91
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 92
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, S10D
<400> 92
Pro Ala Pro Glu Met Leu Gly Gly Pro Asp Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 93
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, S10E
<400> 93
Pro Ala Pro Glu Met Leu Gly Gly Pro Glu Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 94
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, I103D
<400> 94
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Asp Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 95
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, I103E
<400> 95
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Glu Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 96
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, S10D, I103D
<400> 96
Pro Ala Pro Glu Met Leu Gly Gly Pro Asp Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Asp Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 97
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, S10D, I103E
<400> 97
Pro Ala Pro Glu Met Leu Gly Gly Pro Asp Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Glu Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 98
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, S10E, I103D
<400> 98
Pro Ala Pro Glu Met Leu Gly Gly Pro Glu Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Asp Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<210> 99
<211> 220
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая: Иллюстративный вариант Fc собачьего IgG-B,
мутант с усиленным связыванием CD16, S10E, I103E
<400> 99
Pro Ala Pro Glu Met Leu Gly Gly Pro Glu Val Phe Ile Phe Pro Pro
1 5 10 15
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
20 25 30
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
35 40 45
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
50 55 60
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
65 70 75 80
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
85 90 95
Lys Ala Leu Pro Ser Pro Glu Glu Arg Thr Ile Ser Lys Ala Arg Gly
100 105 110
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
115 120 125
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
130 135 140
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
145 150 155 160
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
165 170 175
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
180 185 190
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
195 200 205
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
210 215 220
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА К МЕЗОТЕЛИНУ | 2019 |
|
RU2837574C2 |
| Терапевтические антитела к CD47 | 2016 |
|
RU2748401C2 |
| ВАРИАНТНЫЕ СВЯЗЫВАЮЩИЕ CD3 ДОМЕНЫ И ИХ ПРИМЕНЕНИЕ В КОМБИНИРОВАННОЙ ТЕРАПИИ ПРИ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2810222C2 |
| АНТИТЕЛА ПРОТИВ SARS-COV-2 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2021 |
|
RU2832025C1 |
| СПОСОБ ОЧИСТКИ ДЛЯ УДАЛЕНИЯ ВАРИАНТОВ АНТИТЕЛ С СУЛЬФАТИРОВАНИЕМ ТИРОЗИНА; ОЧИЩЕННЫЕ КОМПОЗИЦИИ | 2017 |
|
RU2793400C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ ADAM9, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783619C2 |
| АНТИТЕЛА К CD38 И СОСТАВЫ | 2020 |
|
RU2826957C2 |
| АНТИТЕЛА, ПОДХОДЯЩИЕ ДЛЯ ПАССИВНОЙ ИММУНИЗАЦИИ ПРОТИВ ГРИППА, И ИХ КОМПОЗИЦИИ, КОМБИНАЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ | 2015 |
|
RU2720282C1 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ МЕЗОТЕЛИН И CD137 | 2019 |
|
RU2815066C2 |
| АНТИ-PCSK9 АНТИТЕЛО, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2739208C2 |
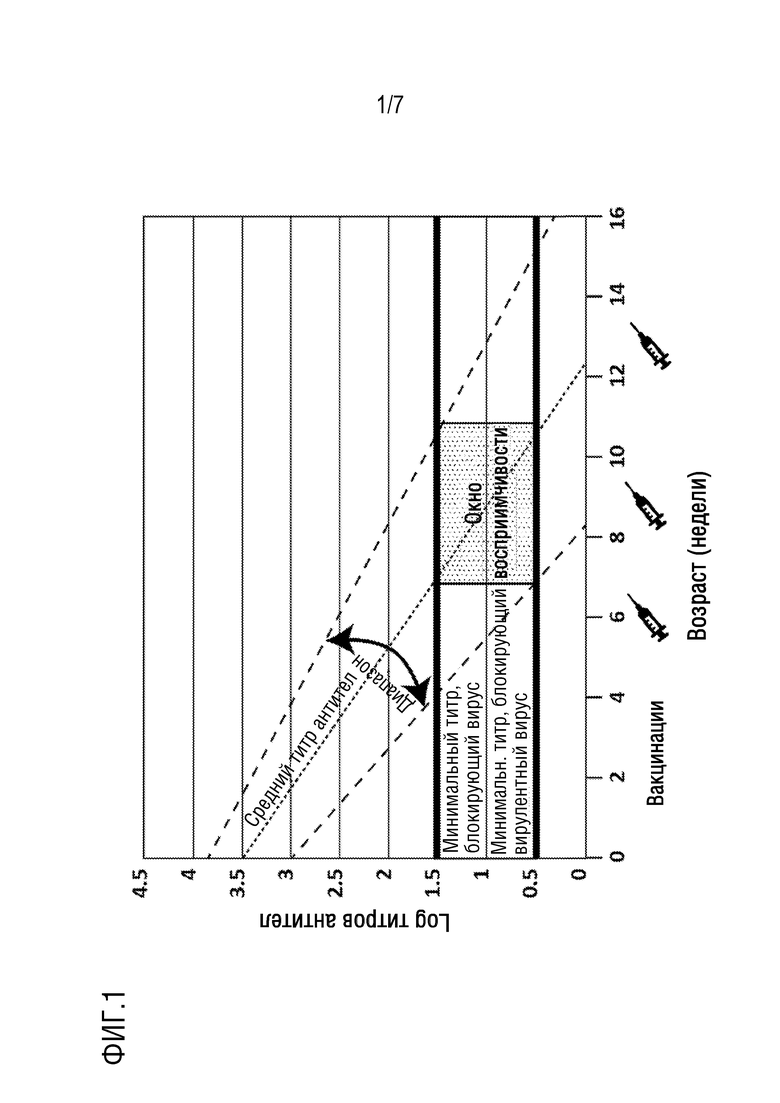
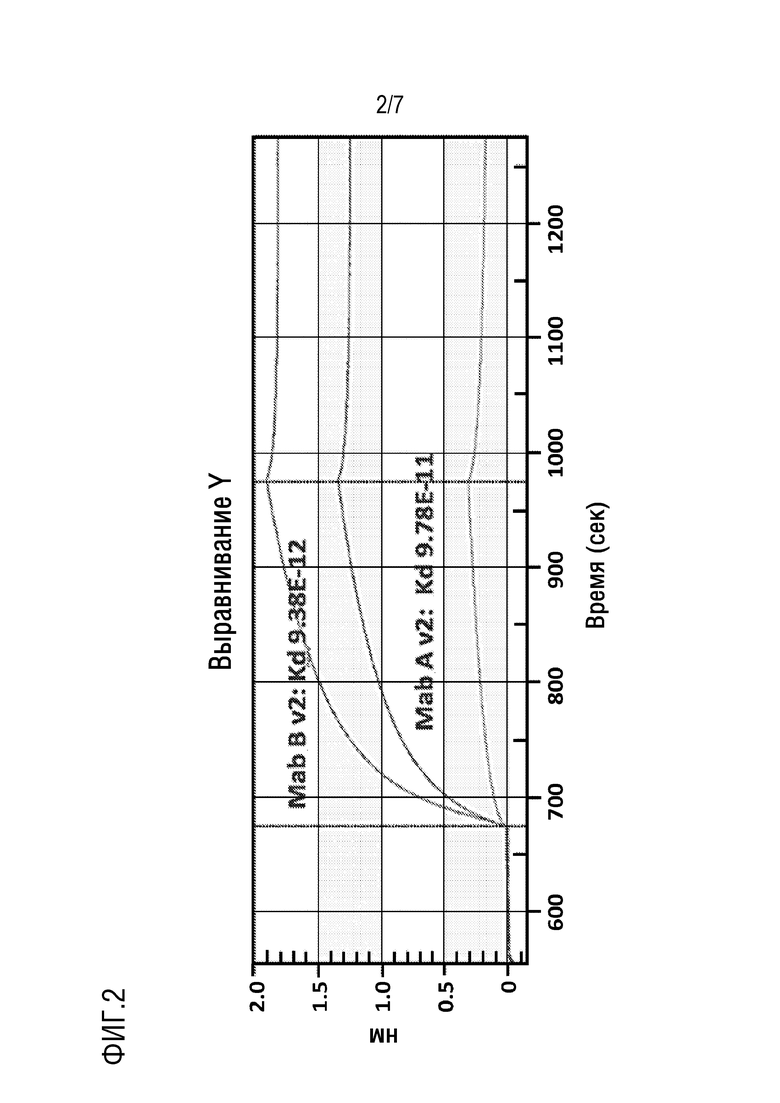
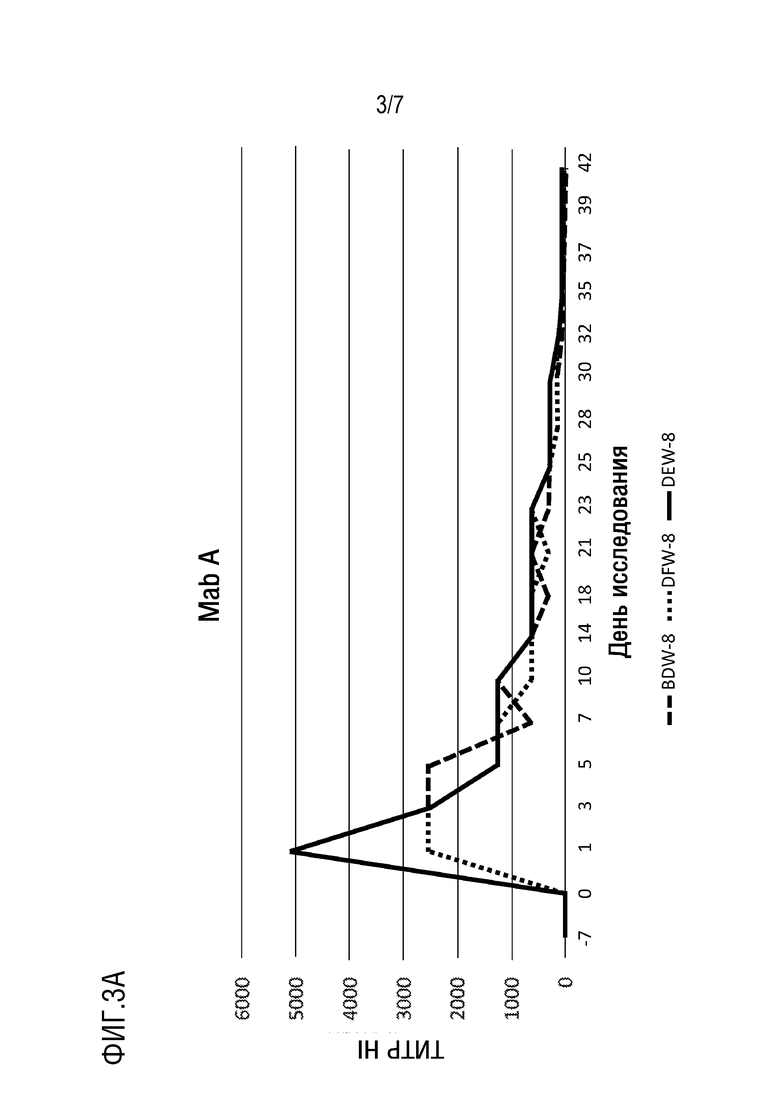
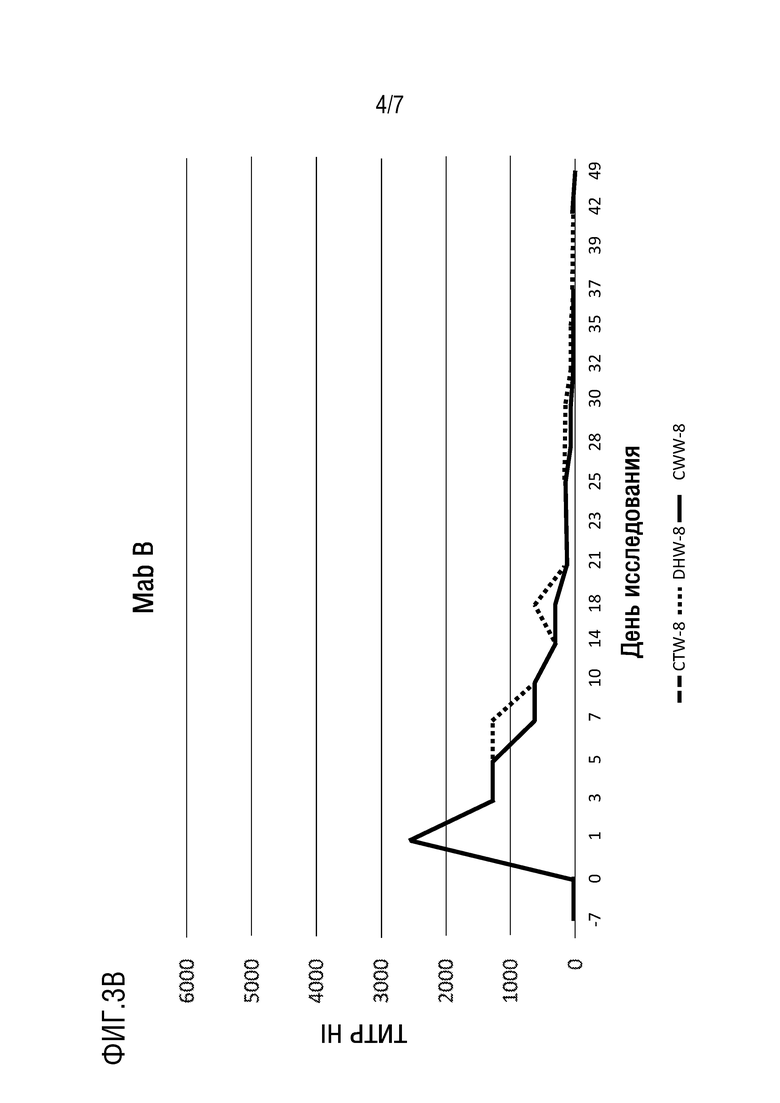
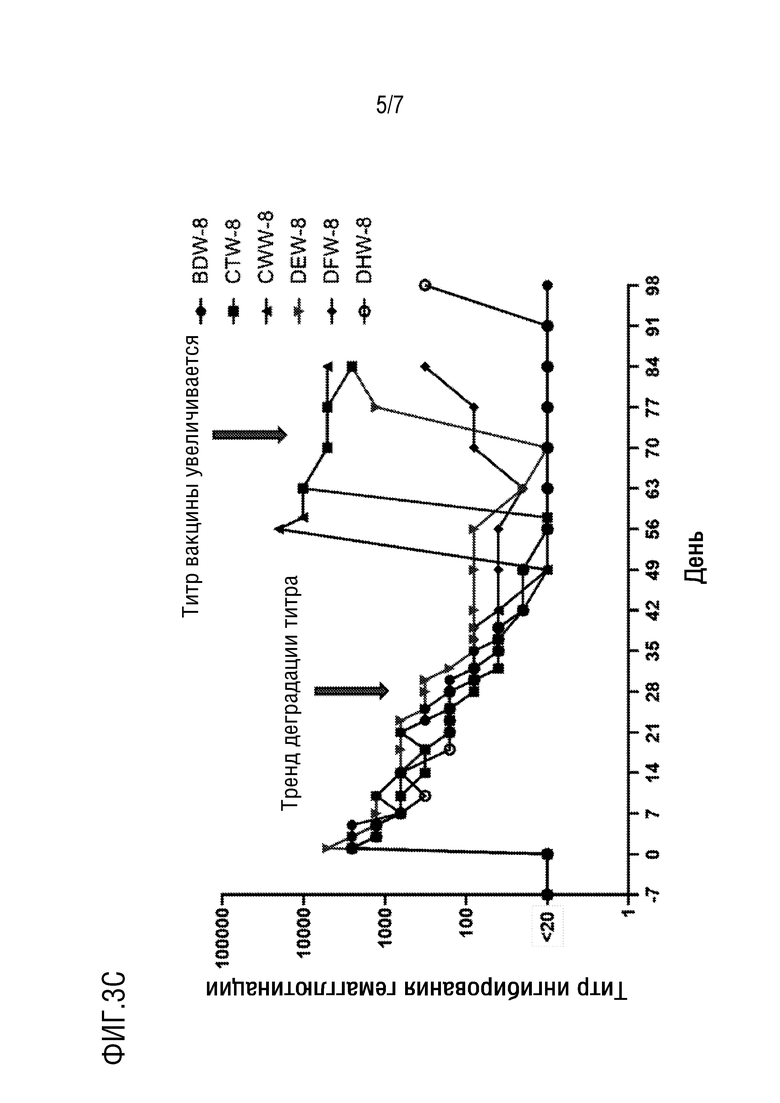
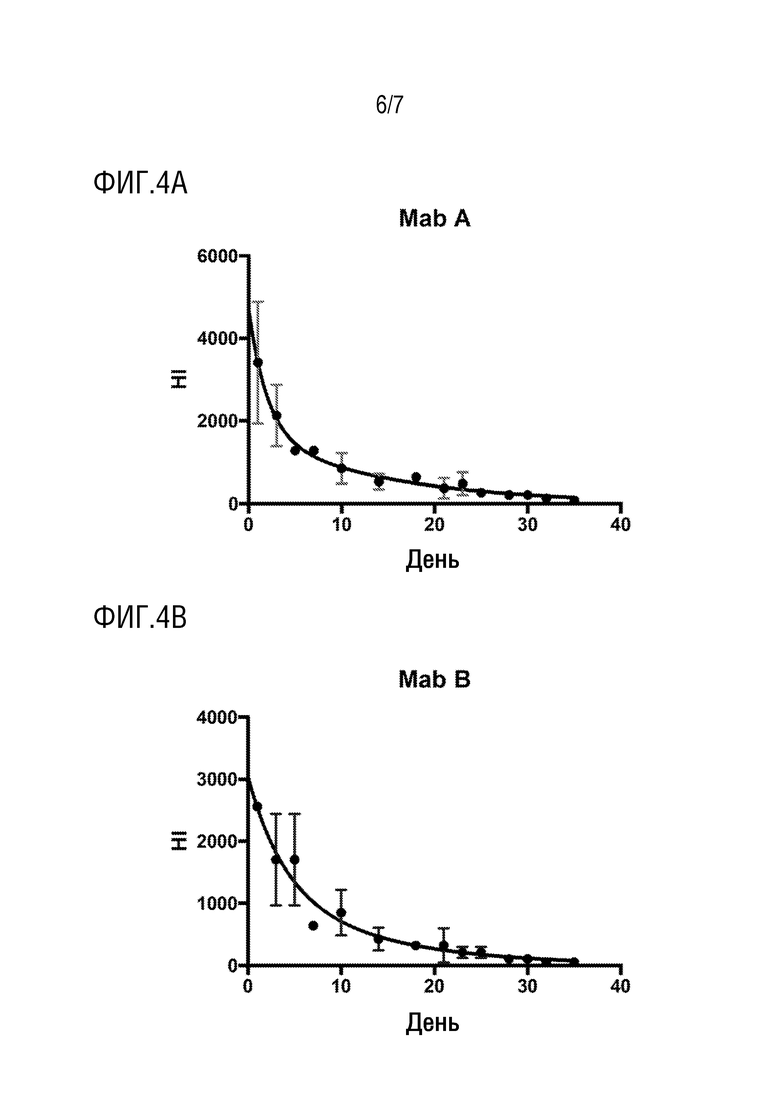
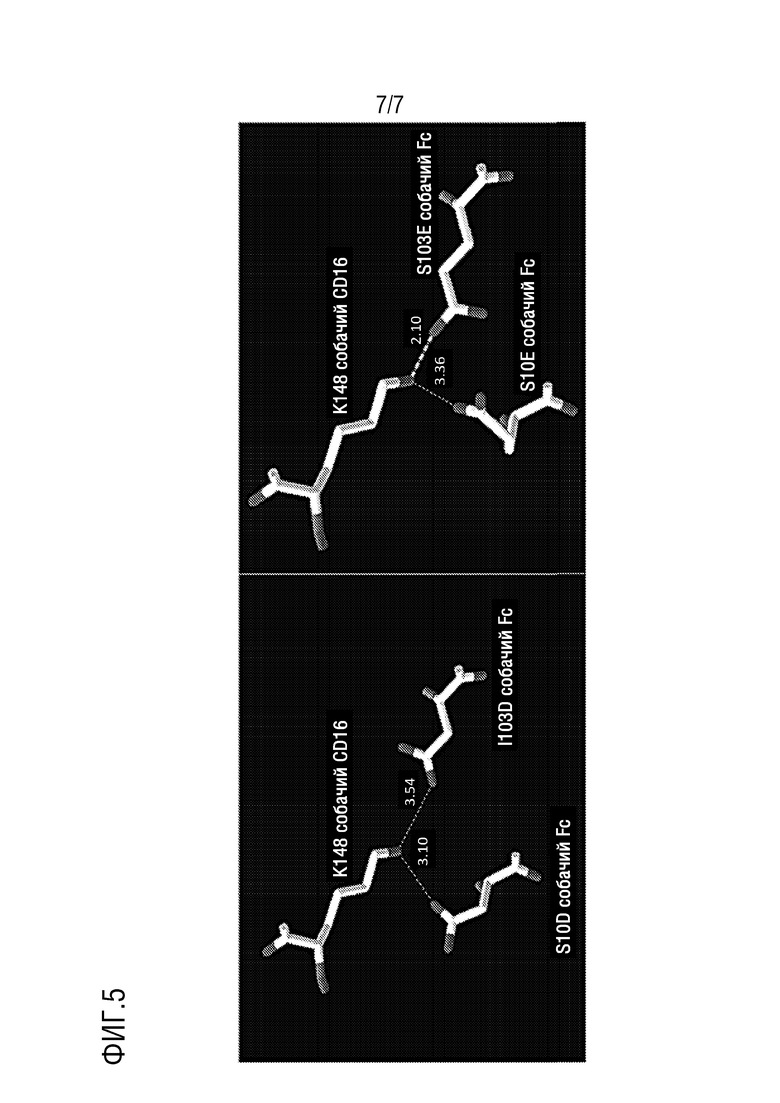
Изобретение относится к области биотехнологии. Предложены антитела, которые связываются с парвовирусом псовых и/или кошачьих, кодирующие их нуклеиновые кислоты, клетки-хозяева для получения указанных антител. Также изобретение относится к фармацевтическим композициям и способам пассивной иммунизации субъекта против заражения парвовирусом псовых или кошачьих, обнаружения и лечения парвовирусной инфекции. Полученные антитела обладают улучшенными характеристиками экспрессии. 13 н. и 13 з.п. ф-лы, 8 ил., 21 табл., 15 пр.
1. Антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где антитело содержит:
а) тяжелую цепь, содержащую (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6, и
b) легкую цепь, содержащую (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15; и
где последовательность тяжелой цепи по меньшей мере на 95% идентична SEQ ID NO: 24, и последовательность легкой цепи по меньшей мере на 95% идентична SEQ ID NO: 25.
2. Антитело по п. 1, где последовательность тяжелой цепи по меньшей мере на 98% идентична SEQ ID NO: 24 и/или последовательность легкой цепи по меньшей мере на 98% идентична SEQ ID NO: 25.
3. Антитело по п. 1 или 2, где последовательность тяжелой цепи по меньшей мере на 98% идентична SEQ ID NO: 24, и последовательность легкой цепи по меньшей мере на 98 % идентична SEQ ID NO: 25.
4. Антитело по любому из пп. 1-3, где последовательность тяжелой цепи по меньшей мере на 99% идентична SEQ ID NO: 24 и/или последовательность легкой цепи по меньшей мере на 99% идентична SEQ ID NO: 25.
5. Антитело по любому из пп. 1-4, где последовательность тяжелой цепи идентична SEQ ID NO: 24 и/или последовательность легкой цепи идентична SEQ ID NO: 25.
6. Антитело, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, где антитело содержит:
(a) (i) CDR-H1, содержащую аминокислотную последовательность SEQ ID NO: 4; (ii) CDR-H2, содержащую аминокислотную последовательность SEQ ID NO: 5; и (iii) CDR-H3, содержащую аминокислотную последовательность SEQ ID NO: 6; и
(b) (i) CDR-L1, содержащую аминокислотную последовательность SEQ ID NO: 13; (ii) CDR-L2, содержащую аминокислотную последовательность SEQ ID NO: 14; и (iii) CDR-L3, содержащую аминокислотную последовательность SEQ ID NO: 15; и
где последовательность тяжелой цепи содержит SEQ ID NO: 24 с необязательно 1, 2, 3, 4 или 5 аминокислотными заменами, и последовательность легкой цепи содержит SEQ ID NO: 25 с необязательно 1, 2, 3, 4 или 5 аминокислотными заменами.
7. Антитело по п. 6, где последовательность тяжелой цепи содержит SEQ ID NO: 24 с необязательно 1, 2 или 3 аминокислотными заменами и/или последовательность легкой цепи содержит SEQ ID NO: 25 с необязательно 1, 2 или 3 аминокислотными заменами.
8. Антитело по п. 6 или 7, где последовательность тяжелой цепи содержит SEQ ID NO: 24 с необязательно 1 или 2 аминокислотными заменами, и/или последовательность легкой цепи содержит SEQ ID NO: 25 с необязательно 1 или 2 аминокислотными заменами.
9. Антитело по любому из пп. 6-8, где последовательность тяжелой цепи содержит SEQ ID NO: 24 с необязательно 1 аминокислотной заменой, и/или последовательность легкой цепи содержит SEQ ID NO: 25 с необязательно 1 аминокислотной заменой.
10. Антитело по любому из пп. 6-9, где указанные аминокислотные замены являются консервативными заменами.
11. Антитело по любому из предшествующих пунктов, где антитело представляет собой химерное антитело и/или моноклональное антитело.
12. Антитело по любому из предшествующих пунктов, где
(a) антитело связывается с эпитопом, содержащим аминокислотную последовательность SEQ ID NO: 1, SEQ ID NO: 2 и/или SEQ ID NO: 3;
(b) антитело связывается с парвовирусом псовых или парвовирусом кошачьих с константой диссоциации (Kd) менее 5×10-6 М, менее 1×10-6 М, менее 5×10-7 М, менее 1×10-7 М, менее 5×10-8 М, менее 1×10-8 М, менее 5×10-9 М, менее 1×10-9 М, менее 5×10-10 М, менее 1×10-10 М, менее 5×10-11 М, менее 1×10-11 М, менее 5×10-12 М, менее 1×10-12 М, менее 5×10-13 М или менее 1×10-13 М, измеренной методом биослойной интерферометрии;
(c) антитело связывается с парвовирусом псовых или парвовирусом кошачьих, как определено анализом методом иммуноблота и/или биослойной интерферометрии; и/или
(d) антитело в концентрации 200 мкг/мл имеет значение ингибирования гемагглютинации, равное по меньшей мере 8000, по меньшей мере 16000, по меньшей мере 32000.
13. Антитело по любому из предшествующих пунктов, где антитело представляет собой выделенное антитело.
14. Нуклеиновая кислота, кодирующая антитело по любому из предшествующих пунктов.
15. Клетка-хозяин для получения антитела, которое связывается с парвовирусом псовых и/или парвовирусом кошачьих, содержащая нуклеиновую кислоту по п. 14.
16. Способ получения антитела, включающий культивирование клетки-хозяина по п. 15 и выделение антитела.
17. Фармацевтическая композиция для пассивной иммунизации субъекта против заражения парвовирусом псовых или кошачьих, содержащая антитело по любому из пп. 1-13 и фармацевтически приемлемый носитель, необязательно, где фармацевтически приемлемый носитель представляет собой забуференный фосфатом физиологический раствор.
18. Композиция, содержащая антитело по любому из пп. 1-13 или фармацевтическую композицию по п. 17, для применения в способе обеспечения пассивного иммунитета у субъекта к инфекции парвовирусом псовых или кошачьих, включающем введение субъекту терапевтически эффективного количества моноклонального антитела или фармацевтической композиции.
19. Композиция для применения по п. 16, где:
(a) способ включает введение антитела или фармацевтической композиции (i) перед воздействием парвовируса псовых или кошачьих или после воздействия парвовируса псовых или кошачьих;
(b) способ включает введение антитела или фармацевтической композиции после инфицирования парвовирусом псовых или кошачьих;
(c) способ включает введение антитела или фармацевтической композиции после того, как у субъекта проявился по меньшей мере один симптом, выбранный из лихорадки, рвоты, диареи, лимфопении и септицемии;
(d) способ включает введение антитела или фармацевтической композиции после того, как парвовирус псовых или кошачьих был обнаружен в фекалиях, например, при положительном результате теста SNAP в условиях содержания в клетке;
(e) субъекту (i) ранее вводили парвовирусную вакцину или (ii) ранее не вводили парвовирусную вакцину;
(f) у субъекта при рождении отсутствует защита из-за отсутствия материнских антител к парвовирусу псовых или кошачьих, или из-за неудачи пассивного переноса антител к парвовирусу псовых или кошачьих;
(g) субъект выращен вручную, мать субъекта не производит молока, или субъект не может вырабатывать антитела к парвовирусу; и/или
(h) субъект живет в среде, зараженной собачьим или кошачьим парвовирусом.
20. Фармацевтическая композиция для лечения парвовирусной инфекции псовых или кошачьих у субъекта, содержащая моноклональное антитело по одному или нескольким из пп. 1-13 и и фармацевтически приемлемый носитель, необязательно, где фармацевтически приемлемый носитель представляет собой забуференный фосфатом физиологический раствор.
21. Композиция, содержащая антитело по любому из пп. 1-13 или фармацевтическую композицию по п. 20, для применения в способе лечения парвовирусной инфекции псовых или кошачьих у субъекта, включающем введение субъекту терапевтически эффективного количества антитела или фармацевтической композиции.
22. Композиция для применения по п. 21, где:
(a) способ включает введение антитела или фармацевтической композиции после того, как у субъекта проявился по меньшей мере один симптом, выбранный из лихорадки, рвоты, диареи, лимфопении и септицемии;
(b) способ включает введение антитела или фармацевтической композиции после обнаружения парвовируса псовых или кошачьих в фекалиях, например, при положительном результате теста SNAP в условиях содержания в клетке;
(c) субъекту (i) ранее вводили парвовирусную вакцину или (ii) ранее не вводили парвовирусную вакцину; и/или
(d) субъект живет в среде, зараженной парвовирусом псовых или кошачьих;
(e) субъектом является представитель псовых или кошачьих, или человек;
(f) способ включает введение антитела или фармацевтической композиции парентерально;
(g) способ включает введение антитела или фармацевтической композиции внутримышечно, внутрибрюшинно, интрацереброспинально, подкожно, внутриартериально, интрасиновиально, интратекально, внутривено или путем ингаляции;
(h) способ включает введение антитела или фармацевтической композиции внутривенно;
(i) способ включает введение антитела или фармацевтической композиции подкожно;
(j) субъект находится в возрасте менее 1 недели, менее 2 недель, менее 3 недель, менее 4 недель, менее 5 недель, менее 6 недель, менее 6 недель, менее 7 недель, менее 8 недель, менее 9 недель, менее 10 недель, менее 11 недель, менее 12 недель, менее 6 месяцев, от 0 до 12 недель, от 0 до 10 недель, от 0 до 8 недель, от 0 до 6 недель, от 0 до 4 недель, от 0 до 2 недель, от 4 до 12 недель, от 6 до 12 недель, от 10 до 12 недель, от 4 недель до 6 месяцев, от 2 месяцев до 6 месяцев, от 4 месяцев до 6 месяцев, от 6 месяцев до 1 года, старше 13 недель или старше 1 года;
(k) возраст субъекта составляет 13 недель или старше;
(l) способ включает введение антитела в количестве от 0,01 мг/кг массы тела до 100 мг/кг массы тела на дозу;
(m) способ включает введение антитела в количестве 5 мг/кг массы тела на дозу;
(n) способ включает введение антитела или фармацевтической композиции (i) в виде однократной дозы или (ii) в виде нескольких доз, например, один раз в неделю в течение по меньшей мере двух или трех недель подряд;
(o) субъект имеет титр ингибирования гемагглютинации менее 20, определенный с помощью анализа ингибирования гемагглютинации до введения антитела или фармацевтической композиции;
(p) субъект имеет отрицательный титр парвовируса, определенный с помощью анализа ингибирования гемагглютинации до введения антитела или фармацевтической композиции; и/или
(r) способ включает введение субъекту терапевтически эффективного количества двух или более разных антител по любому из пп. 1-7, при этом два или более разных антитела вводят одновременно или последовательно, причем необязательно введение двух или более разных антител разделено одним или более днями.
23. Фармацевтическая композиция для снижения парвовирусной инфекции клетки, содержащая антитело по любому из пп. 1-13 и фармацевтически приемлемый носитель, необязательно, где фармацевтически приемлемый носитель представляет собой забуференный фосфатом физиологический раствор.
24. Способ снижения инфицирования клетки парвовирусной инфекцией, включающий воздействие на клетку антителом по любому из пп. 1-13 или фармацевтической композицией по п. 23 в условиях, допускающих связывание антитела с парвовирусом, необязательно где
(a) клетку подвергают воздействию антитела или фармацевтической композиции in vitro, и/или
(b) клетка представляет собой клетку млекопитающего, человеческую клетку, собачью клетку или кошачью клетку.
25. Фармацевтическая композиция для обнаружения парвовирусной инфекции в образце от субъекта, причем композиция содержит антитело по любому из пп. 1-13 и фармацевтически приемлемый носитель, необязательно, где фармацевтически приемлемый носитель представляет собой забуференный фосфатом физиологический раствор.
26. Способ детектирования парвовирусной инфекции в образце, взятом у субъекта, включающий приведение образца в контакт с антителом по любому из пп. 1-13 или фармацевтической композицией по п. 25 в условиях, допускающих связывание антитела с парвовирусом, и детектирование образования комплекса между антителом и парвовирусом в образце, необязательно, где образец получен от псовых, кошачьих или человека.
| WO 2012164372 A1, 06.12.2012 | |||
| WO 2013016460 A1, 31.01.2013 | |||
| WIKOFF W.R | |||
| et al | |||
| The structure of a neutralized virus: canine parvovirus complexed with neutralizing antibody fragment, Structure, 1994, Vol.2, No.7, pp.595-607 | |||
| GERLACH M | |||
| et al | |||
| Efficacy of feline anti-parvovirus antibodies in the treatment of canine parvovirus infection, Journal of |
Авторы
Даты
2024-11-19—Публикация
2020-07-30—Подача