Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает приоритет на основании предварительных заявок на патент США №62/195779, поданной 22 июля 2015 года, №62/236847, поданной 2 октября 2015 года, и №62/331960, поданной 4 мая 2016 года, содержание каждой из которых включено в настоящую заявку во всей полноте посредством ссылки.
Уровень техники
Олигонуклеотиды подходят для применения в терапевтических, диагностических, исследовательских целях и в качестве наноматериалов. Использование природных нуклеиновых кислот (например, немодифицированных ДНК или РНК) в терапевтических целях может быть ограничено, например, из-за их неустойчивости к действию вне- и внутриклеточных нуклеаз и/или недостаточной способности проникать в клетки и распределяться в них. Существует потребность в новых и улучшенных олигонуклеотидах и композициях олигонуклеотидов, таких как, например, новые антисмысловые олигонуклеотиды и олигонуклеотиды миРНК и композиции олигонуклеотидов.
Краткое описание
Среди прочего, настоящее раскрытие охватывает признание того факта, что такие структурные элементы олигонуклеотидов, как последовательность оснований, химические модификации (например, модификации сахара, основания и/или межнуклеотидных линкерных групп и их профилей) и/или стереохимия (например, стереохимия хиральных центров остова (хиральные межнуклеотидные линкерные группы) и/или их профили) могут оказывать значительное влияние на свойства, например, активности, олигонуклеотидов. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что композиции олигонуклеотидов, содержащие олигонуклеотиды с контролируемыми структурными элементами, например, контролируемыми химическими модификациями и/или контролируемыми стереохимическими профилями остова, обеспечивают неожиданные свойства, включающие, без ограничения, описанные в настоящем документе. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что комбинации химических модификаций и стереохимии могут обеспечить неожиданные, значительно улучшенные свойства (например, биоактивность, селективность и т.д.). Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов, содержащую определенную последовательность оснований и/или профиль модификаций сахара (например, 2'-ОМе, 2'-F, 2'-МОЕ и т.д.), и/или профиль модификаций оснований (например, 5-метилцитозин), и/или профиль модификаций остова (фосфат или фосфоротиоат), и/или профиль стереохимии модификаций остова (например, каждый фосфоротиоат представляет собой Sp или Rp).
Согласно некоторым вариантам осуществления модификации межнуклеотидных линкерных групп могут превращать атомы фосфора в модифицированных линкерных группах в хиральные центры. Например, при модификации фосфоротиоата (PS) один из немостиковых атомов кислорода (О), связанных с атомом фосфора (Р), заменяют атомом серы (S). Последствием использования модификации PS в синтезе олигонуклеотидов является то, что он создает хиральный центр у фосфора, который может характеризоваться конфигурацией «Sp» или «Rp». Например, обычная стереослучайная PS-модифицированная композиция олигонуклеотидов, составляющая в длину 19 PS-линкерных групп (например, содержащая 20 нуклеотидов в длину, 19 PS-модификаций, каждая из которых характеризуется двумя возможными стереохимиями (Sp или Rp) в каждой модификации PS], представляет собой случайную смесь из более чем 500000 (219) стереоизомеров, каждый из которых характеризуется одинаковой нуклеотидной последовательностью (например, последовательностью оснований), но отличающийся стереохимией вдоль своих остовов; такая композиция представляет собой «стереослучайную» композицию олигонуклеотидов. Согласно некоторым вариантам осуществления, в отличие от стереослучайных композиций, композиция олигонуклеотидов с контролируемой хиральностью представляет собой по существу чистый препарат единственного олигонуклеотида, так как предопределенный уровень олигонуклеотидов в композиции характеризуется одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления некоторые композиции олигонуклеотидов являются стереочистыми (то есть композиция олигонуклеотидов с контролируемой хиральностью), причем стереохимия в каждом PS определена (Sp или Rp). Согласно некоторым вариантам осуществления в стереослучайных композициях олигонуклеотидов различные олигонуклеотиды могут характеризоваться одной и той же последовательностью оснований, одним и тем же профилем модификаций сахара (например, 2'-ОМе, 2'-F, 2'-ОМЕ и т.д.), одним и тем же профилем модификаций оснований (например, 5-метилцитозин) и одним и тем же профилем модификаций остова (фосфат или PS), но разные профили хиральных центров остова и их уровни являются случайными из не стереоконтролируемого синтеза (не определенного заранее, как посредством стереоконтролируемого синтеза, как некоторые способы, приведенные в настоящем документе в качестве примера, с использованием хирального вспомогательного агента). Композицию олигонуклеотидов с контролируемой хиральностью можно выбрать так, чтобы она имела большую желательную биологическую активность (например, большую активность, эффективность интерференции РНК или опосредованных РНКазой Н путей и т.д.) и сниженную нежелательную активность (например, нежелательную иммуногенность, токсичность и т.д.), чем стереослучайный препарат олигонуклеотидов с той же последовательностью оснований. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью лучше способна различать мутантную (mu) последовательность НТТ и последовательность НТТ дикого типа (с различием в одном нуклеотиде).
Помимо всего прочего, настоящее раскрытие включает признание того, что стереослучайные олигонуклеотидные препараты содержат множество отдельных химических объектов, которые отличаются друг от друга, например, стереохимической структурой отдельных хиральных центров остова в олигонуклеотидной цепи. Без контроля стереохимии хиральных центров остова стереослучайные олигонуклеотидные препараты обеспечивают неконтролируемые композиции, содержащие неопределенные уровни олигонуклеотидных стереоизомеров. Несмотря на то, что эти стереоизомеры могут иметь одну и ту же последовательность оснований, они представляют собой различные химические объекты, по меньшей мере из-за их различной стереохимии остова, и они могут характеризоваться, как показано в настоящем документе, различными свойствами, например, биоактивностью. Среди прочего, настоящее раскрытие относится к новым композициям, которые представляют собой конкретные стереоизомеры представляющих интерес олигонуклеотидов или содержат их. Согласно некоторым вариантам осуществления конкретный стереоизомер может быть определен, например, по его последовательности оснований, его длине, его профилю линкерных групп остова, а также по его профилю хиральных центров остова. Как понятно в данной области техники, согласно некоторым вариантам осуществления последовательность оснований может относиться к статусу идентичности и/или модификации нуклеозидных остатков (например, компонентов сахара и/или оснований по отношению к стандартным встречающимся в природе нуклеотидам, таким как аденин, цитозин, гуанозин, тимин и урацил) в олигонуклеотиде, и/или к характеру гибридизации (т.е. способности гибридизоваться с конкретными комплементарными остатками) таких остатков.
В настоящем раскрытии, среди прочего, показано, что отдельные стереоизомеры конкретного олигонуклеотида могут показывать устойчивость и/или активность (например, функциональные свойства или свойства токсичности), отличающуюся от других. Более того, в настоящем раскрытии показано, что повышения устойчивости и/или активности, достигаемые за счет включения и/или расположения определенных хиральных структур в олигонуклеотиде, могут быть сопоставимы или быть даже лучше, чем те, которые достигаются посредством использования конкретных линкерных групп остова, модификаций остатков и т.д. (например, путем использования определенных типов модифицированных фосфатов (например, фосфоротиоата, замещенного фосфоротиоата и т.д.), модификаций сахара (например, 2'-модификаций и т.д.) и/или модификаций оснований (например, метилирования и т.д.)).
Помимо всего прочего, настоящее раскрытие предусматривает, что согласно некоторым вариантам осуществления свойства (например, стабильность и/или активности) олигонуклеотида могут регулироваться путем оптимизации его профиля хиральных центров остова, необязательно в сочетании с регулированием/оптимизацией одной или более других характеристик (например, профиля линкерных групп, профиля модификаций нуклеозидов и т.д.) олигонуклеотида.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены композиции олигонуклеотидов, причем олигонуклеотиды обладают одинаковым профилем хиральных центров остова, который неожиданно сильно повышает устойчивость и/или биологическую активность олигонуклеотидов. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает повышенную устойчивость. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает неожиданно повышенную активность. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает повышенную устойчивость и активность. Согласно некоторым вариантам осуществления, если олигонуклеотид используют для расщепления полимера нуклеиновой кислоты, то профиль хиральных центров остова, что удивительно само по себе, изменяет профиль расщепления полимера-мишени нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова эффективно предупреждает расщепление по вторичным сайтам. Согласно некоторым вариантам осуществления профиль хиральных центров остова создает новые сайты расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова минимизирует число сайтов расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова минимизирует число сайтов расщепления так, что целевой полимер нуклеиновой кислоты расщепляется только по одному сайту в последовательности полимера-мишени нуклеиновой кислоты, которая является комплементарной олигонуклеотиду. Согласно некоторым вариантам осуществления профиль хиральных центров остова усиливает эффективность расщепления в сайте расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова олигонуклеотида улучшает расщепление полимера-мишени нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова усиливает селективность. Согласно некоторым вариантам осуществления профиль хиральных центров остова минимизирует нецелевой эффект. Согласно некоторым вариантам осуществления профиль хиральных центров остова усиливает селективность, например, селективность расщепления в отношении двух целевых последовательностей, отличающихся только однонуклеотидным полиморфизмом (SNP). Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m или содержит один или более их повторов. В некоторых описанных в настоящем документе вариантах реализации m равно 1-50 и n равно 1-10, и t равно 1-50. Согласно некоторым вариантам осуществления профиль хиральных центров остова содержит или представляет собой (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления профиль хиральных центров остова содержит или представляет собой (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где m>2. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, содержащую по меньшей мере 5, 6, 7, 8, 9 или 10 или более последовательных (Sp) положений. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, содержащую по меньшей мере 5 последовательных (Sp) положений. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, содержащую по меньшей мере 8 последовательных (Sp) положений. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, содержащую по меньшей мере 10 последовательных (Sp) положений. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp). Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp) в положении SNP или рядом с ним. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце составляет в длину 1-9 нуклеотидов, сердцевина составляет в длину 1-15 нуклеотидов, а крыло на 3'-конце составляет в длину 1-9 нуклеотидов. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце составляет в длину 5 нуклеотидов, сердцевина составляет в длину 1-15 нуклеотидов, а крыло на 3'-конце составляет в длину 5 нуклеотидов. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце составляет в длину 1-9 нуклеотидов, сердцевина составляет в длину 10 нуклеотидов, а крыло на 3'-конце составляет в длину 1-9 нуклеотидов. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце составляет в длину 5 нуклеотидов, сердцевина составляет в длину 10 нуклеотидов, а крыло на 3'-конце составляет в длину 5 нуклеотидов. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце составляет в длину 5 нуклеотидов, сердцевина составляет в длину 10 нуклеотидов, а крыло на 3'-конце составляет в длину 5 нуклеотидов и по меньшей мере одно крыло содержит нуклеотид с модификацией 2'-ОМе. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем каждое крыло содержит по меньшей мере один нуклеотид с модификацией 2'-ОМе. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем каждый нуклеотид в обоих крыльях характеризуется модификацией 2'-ОМе. Согласно некоторым вариантам осуществления профиль хиральных центров остова представляет собой последовательность, состоящую из всех (Sp) с единственным (Rp), причем молекула имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце составляет в длину 5 нуклеотидов, сердцевина составляет в длину 10 нуклеотидов, а крыло на 3'-конце составляет в длину 5 нуклеотидов, а каждый нуклеотид в каждом крыле характеризуется модификацией 2'-ОМЕ. Согласно некоторым вариантам осуществления олигонуклеотид представляет собой одноцепочечный и имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце молекулы содержит от 4 до 8 нуклеотидов, каждый из которых характеризуется модификацией 2'-ОМе и причем нуклеотид на 5'-конце молекулы содержит фосфоротиоат в Sp-конформации; сердцевина содержит от 8 до 12 нуклеотидов, каждый из которых представляет собой ДНК (2'-Н), причем каждый имеет фосфоротиоат в положении Sp, за исключением одного нуклеотида, который содержит фосфоротиоат в положении Rp; и причем крыло на 3'-конце молекулы содержит от 4 до 8 нуклеотидов, каждый из которых характеризуется модификацией 2'-ОМе, и причем нуклеотид на 3'-конце молекулы содержит фосфоротиоат в Sp-конформации. Согласно некоторым вариантам осуществления олигонуклеотид является одноцепочечным и имеет формат крыло-сердцевина-крыло, причем крыло на 5'-конце молекулы содержит 6 нуклеотидов, каждый из которых характеризуется модификацией 2'-ОМе, и причем нуклеотид на 5'-конце молекулы содержит фосфоротиоат в Sp-конформации; сердцевина содержит 10 нуклеотидов, каждый из которых представляет собой ДНК (2'-Н), причем каждый содержит фосфоротиоат в положении Sp, за исключением одного нуклеотида, который содержит фосфоротиоат в положении Rp; и причем крыло на 3'-конце молекулы содержит 6 нуклеотидов, каждый из которых характеризуется модификацией 2'-ОМе, и причем нуклеотид на 3'-конце молекулы содержит фосфоротиоат в Sp-конформации.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрено, что такие химические модификации, как модификации нуклеозидов и межнуклеотидных линкерных групп, могут обеспечить улучшенные свойства. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что комбинации химических модификаций и стереохимии могут обеспечить неожиданные, значительно улучшенные свойства (например, биоактивность, селективность и т.д.). Согласно некоторым вариантам осуществления химические комбинации, такие как модификации сахаров, оснований и/или межнуклеотидных линкерных групп, объединяют с профилями стереохимии, например, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, для получения олигонуклеотидов и их композиций с неожиданно улучшенными свойствами. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов характеризуется контролируемой хиральностью и содержит комбинацию 2'-модификации одного или более фрагментов сахара, одной или более природных фосфатных линкерных групп, одной или более фосфоротиоатных линкерных групп и профиль стереохимии (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где m>2.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды, определяемые наличием:
1) одинаковой последовательности оснований и длины;
2) одинакового профиля линкерных групп остова, а также
3) одинакового профиля хиральных центров остова, причем композиция представляет собой по существу чистый препарат единственного олигонуклеотида в том отношении, что предопределенный уровень олигонуклеотидов в композиции характеризуется одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова,
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательность оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова, причем композиция представляет собой по существу чистый препарат одного олигонуклеотида, в котором по меньшей мере примерно 10% олигонуклеотидов в композиции характеризуется одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова.
Помимо всего прочего, в настоящем раскрытии предусмотрено, что комбинации структурных элементов олигонуклеотидов (например, профили химических модификаций, линкерных групп остова, хиральных центров остова и/или модификаций фосфора остова) могут обеспечить удивительно улучшенные свойства, такие как биоактивность. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов, содержащая предопределенный уровень олигонуклеотидов, которые содержат одну или более областей крыла и общую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и необязательно содержит одну или более хиральных межнуклеотидных линкерных групп;
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп, а общая область сердцевины характеризуется:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления в олигонуклеотиде, содержащем формат крыло-сердцевина-крыло, «крыло» представляет собой часть олигонуклеотида на 5'- или 3'-конце сердцевины с «сердцевиной» (альтернативно обозначенной как «пропуск») между двумя крыльями. Согласно некоторым вариантам осуществления олигонуклеотид может содержать единственное крыло и единственную сердцевину; в таких случаях крыло находится на 5' или 3' конце олигонуклеотида. Крыло и сердцевина могут быть определены любым из нескольких структурных элементов (например, модификаций или профилями модификаций сахара, основания, остова или стереохимии остова и т.д.). Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями нуклеозидов, причем крыло содержит нуклеозидную модификацию, которая не содержит области сердцевины. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях характеризуются структурой крыло-сердцевина с нуклеозидной модификацией. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях характеризуются структурой сердцевина-крыло с нуклеозидной модификацией. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях характеризуются структурой крыло-сердцевина-крыло с нуклеозидной модификацией. Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями фрагментов сахаров. Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями фрагментов оснований. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется такой же 2'-модификацией, которая не находится в области сердцевины. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется такой же 2'-модификацией, которая отличается от любых модификаций сахара в области сердцевины. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла содержит одинаковую 2'-модификацию, а область сердцевины не содержит 2'-модификаций. Согласно некоторым вариантам осуществления, когда присутствуют два или более крыла, каждый фрагмент сахара в области крыла содержит одинаковую 2'-модификацию, но общая 2'-модификация в области первого крыла может быть либо такой же, как общая 2'-модификация во второй области крыла, либо отличной от нее.
Согласно некоторым вариантам осуществления каждое крыло содержит по меньшей мере одну хиральную межнуклеотидную линкерную группу и по меньшей мере одну природную фосфатную линкерную группу. Согласно некоторым вариантам осуществления каждое крыло содержит по меньшей мере один модифицированный фрагмент сахара. Согласно некоторым вариантам осуществления фрагмент сахара каждого крыла модифицирован. Согласно некоторым вариантам осуществления фрагмент сахара крыла модифицируется посредством модификации, отсутствующей в области сердцевины. Согласно некоторым вариантам осуществления только область крыла содержит модифицированные межнуклеотидные линкерные группы на одном или обоих своих концах. Согласно некоторым вариантам осуществления только область крыла содержит модифицированную межнуклеотидную линкерную группу на своем 5'-конце. Согласно некоторым вариантам осуществления только область крыла содержит модифицированную межнуклеотидную линкерную группу на своем 3'-конце. Согласно некоторым вариантам осуществления только область крыла содержит модифицированные межнуклеотидные линкерные группы на своих 5'- и 3'-концах. Согласно некоторым вариантам осуществления крыло находится на 5'-конце сердцевины, и крыло содержит только модифицированную межнуклеотидную линкерную группу на своем 5'-конце. Согласно некоторым вариантам осуществления крыло находится на 5'-конце сердцевины, и крыло содержит только модифицированную межнуклеотидную линкерную группу на своем 3'-конце. Согласно некоторым вариантам осуществления крыло находится на 5'-конце сердцевины, и крыло содержит только модифицированные межнуклеотидные линкерные группы как на своем 5'-, так и на 3'-конце. Согласно некоторым вариантам осуществления крыло находится на 3'-конце сердцевины, и крыло содержит только модифицированную межнуклеотидную линкерную группу на своем 5'-конце. Согласно некоторым вариантам осуществления крыло находится на 3'-конце сердцевины, и только крыло содержит модифицированную межнуклеотидную линкерную группу на своем 3'-конце. Согласно некоторым вариантам осуществления крыло находится на 3'-конце сердцевины, и содержит только модифицированные межнуклеотидные линкерные группы как на своем 5'-, так и на 3'-конце. Согласно некоторым вариантам осуществления модификация(и) фрагмента сахара или межнуклеотидной линкерной группы или другие модификации в одном крыле могут отличаться от таковых в другом крыле.
Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа внутри области сердцевины модифицируется. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа в области сердцевины является хиральной. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где m>2. Помимо всего прочего, настоящее раскрытие демонстрирует, что согласно некоторым вариантам осуществления такие профили могут обеспечивать или улучшать контролируемое расщепление целевой последовательности, например, последовательности РНК.
Согласно некоторым вариантам осуществления олигонуклеотиды в предусмотренных композициях характеризуются одинаковым профилем фосфорных модификаций остова. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов, которая характеризуется контролируемой хиральностью в том отношении, что композиция содержит предопределенный уровень олигонуклеотидов отдельного типа олигонуклеотида, причем тип олигонуклеотида определяется:
1) последовательностью оснований;
2) профилем линкерных групп остова;
3) профилем хиральных центров остова, а также
4) профилем фосфорных модификаций остова.
Как отмечено выше и понятно в данной области техники, согласно некоторым вариантам осуществления последовательность оснований олигонуклеотида может относиться к статусу идентичности и/или модификации нуклеозидных остатков (например, компонентов сахаров и/или оснований по отношению к стандартным встречающимся в природе нуклеотидам, таким как аденин, цитозин, гуанозин, тимин и урацил) в олигонуклеотиде и/или характере гибридизации (т.е. способности гибридизоваться с конкретными дополнительными остатками) таких остатков.
Согласно некоторым вариантам осуществления определенный тип олигонуклеотида может быть определен посредством
1А) идентичности оснований;
1B) профиля модификации оснований;
1C) профиля модификации сахара;
2) профиля линкерных групп остова;
3) профиля хиральных центров остова, а также
4) профиля фосфорных модификаций остова.
Таким образом, согласно некоторым вариантам осуществления олигонуклеотиды определенного типа могут совместно характеризоваться наличием одинаковых оснований, но отличаться по своему профилю модификаций оснований и/или модификаций сахара. Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа могут характеризоваться наличием одинаковых оснований и профиля модификаций оснований (включая, например, отсутствие модификации оснований), но различаться по профилю модификаций сахаров.
Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа химически идентичны в том плане, что они характеризуются одной и той же последовательностью оснований (включая длину), одним и тем же профилем химических модификаций фрагментов сахаров и оснований, одним и тем же профилем линкерных групп остова (например, профилем природных фосфатных линкерных групп, фосфоротиоатных линкерных групп, фосфоротиоатных триэфирных линкерных групп и их комбинаций), одним и тем же профилем хиральных центров остова (например, профилем стереохимии (Rp/Sp) хиральных межнуклеотидных линкерных групп) и одним и тем же профилем фосфорных модификаций остова (например, профилем модификаций на межнуклеотидном атоме фосфора, таком как -S- и -L-R1 формулы I).
Согласно некоторым вариантам осуществления последовательность олигонуклеотида содержит последовательность любого описанного в настоящем документе олигонуклеотида или состоит из нее. Согласно некоторым вариантам осуществления последовательность, олигонуклеотида содержит или состоит из последовательности любого олигонуклеотида, выбранного из таблиц N1, N2, N3, N4 и 8. Согласно некоторым вариантам осуществления последовательность олигонуклеотида содержит или состоит из последовательности любого выбранного олигонуклеотида из таблиц N1A, N2A, N3A, N4A и 8. Согласно некоторым вариантам осуществления последовательность олигонуклеотида стереочистой (с контролируемой хиральностью) композиции олигонуклеотидов содержит или состоит из последовательности WV-1092, WVE120101, WV-2603 или WV-2595. Согласно некоторым вариантам осуществления последовательность олигонуклеотида включает любую одну или более из следующего: последовательность оснований (включая длину); профиль химических модификаций фрагментов сахара и оснований; профиль линкерных групп остова; профиль природных фосфатных линкерных групп, фосфоротиоатных линкерных групп, фосфоротиоатных триэфирных линкерных групп и их комбинации; профиль хиральных центров остова; профиль стереохимии (Rp/Sp) хиральных межнуклеотидных линкерных групп; профиль фосфорных модификаций остова; профиль модификаций на межнуклеотидном атоме фосфора, таком как -S- и -L-R1 формулы I.
Помимо всего прочего, в настоящем раскрытии предусмотрена сложная задача стереоселективного (а не стереослучайного или рацемического) получения олигонуклеотидов. Среди прочего, в настоящем раскрытии предусмотрены способы и реагенты для стереоселективного получения олигонуклеотидов, содержащих множественные (например, более 5, 6, 7, 8, 9 или 10) межнуклеотидные линкерные группы и, в частности, олигонуклеотидов, содержащих множество (например, более чем 5, 6, 7, 8, 9 или 10) хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления в стереослучайном или рацемическом препарате олигонуклеотидов по меньшей мере одна хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью менее чем 90:10, 95:5, 96:4, 97:3 или 98:2. Согласно некоторым вариантам осуществления для стереоселективного препарата олигонуклеотидов или препарата олигонуклеотидов с контролируемой хиральностью каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 90:10, 95:5, 96:4, 97:3 или 98:2. Согласно некоторым вариантам осуществления для стереоселективного препарата олигонуклеотидов или препарата олигонуклеотидов с контролируемой хиральностью каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 95:5. Согласно некоторым вариантам осуществления для стереоселективного препарата олигонуклеотидов или препарата олигонуклеотидов с контролируемой хиральностью каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 96:4. Согласно некоторым вариантам осуществления для стереоселективного препарата олигонуклеотидов или препарата олигонуклеотидов с контролируемой хиральностью каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 97:3. Согласно некоторым вариантам осуществления для стереоселективного препарата олигонуклеотидов или препарата олигонуклеотидов с контролируемой хиральностью каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 98:2. Согласно некоторым вариантам осуществления для стереоселективного препарата олигонуклеотидов или препарата олигонуклеотидов с контролируемой хиральностью каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 99:1. Согласно некоторым вариантам осуществления диастереоселективность хиральной межнуклеотидной линкерной группы в олигонуклеотиде может быть измерена посредством модельной реакции, например, образования димера при практически одинаковых или сопоставимых условиях, причем димер содержит такую же межнуклеотидную линкерную группу, как и хиральная межнуклеотидная линкерная группа, 5'-нуклеозид димера является таким же, как нуклеозид на 5'-конце хиральной межнуклеотидной линкерной группы, и 3'-нуклеозид димера является таким же, как нуклеозид на 3'-конце хиральной межнуклеотидной линкерной группы.
Помимо всего прочего, неожиданно было обнаружено, что некоторые предусмотренные композиции олигонуклеотидов достигают беспрецедентного контроля над расщеплением целевых последовательностей, например, расщеплением РНКазой Н целевой РНК. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что точный контроль химических и стереохимических признаков олигонуклеотидов обеспечивает улучшенную активность олигонуклеотидных препаратов по сравнению с другими аналогичными препаратами, для которых стереохимические признаки не контролируются. Среди прочего, настоящее раскрытие конкретно демонстрирует улучшенную скорость, степень и/или специфичность расщепления целевых нуклеиновых кислот, с которыми гибридизуются предусмотренные олигонуклеотиды.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены различные применения композиций олигонуклеотидов. Среди прочего, настоящее раскрытие демонстрирует, что, контролируя структурные элементы олигонуклеотидов, такие как последовательность оснований, химические модификации, стереохимия и т.д., свойства олигонуклеотидов могут быть значительно улучшены. Например, согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены способы высокоселективного подавления транскриптов целевой последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены способы лечения субъекта путем подавления транскриптов из вызывающей заболевание копии (например, вызывающего заболевание аллеля). Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены способы разработки и получения композиций олигонуклеотидов с удивительно усиленной активностью и/или селективностью при подавлении транскрипта целевой последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены способы разработки и/или получения композиций олигонуклеотидов, которые обеспечивают аллель-специфическое подавление транскрипта из целевой последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ контролируемого расщепления полимера нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования полимера нуклеиновой кислоты, нуклеотидная последовательность которого содержит целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой последовательность, которая комплементарна целевой последовательности, найденной в полимере нуклеиновой кислоты, или содержит ее;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся определенной последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ изменения профиля расщепления, наблюдаемого, когда полимер нуклеиновой кислоты, нуклеотидная последовательность которого включает целевую последовательность, контактирует с эталонной композицией олигонуклеотидов, которая содержит олигонуклеотиды, характеризующиеся определенной последовательностью оснований и длиной, конкретная последовательность оснований которых представляет собой последовательность, которая комплементарна целевой последовательности или содержит ее, причем способ предусматривает:
контактирование полимера нуклеиновой кислоты с композицией олигонуклеотидов с контролируемой хиральностью олигонуклеотидов, характеризующихся конкретной последовательностью оснований и длиной, причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся конкретной последовательностью оснований и длиной, олигонуклеотидами единственного типа олигонуклеотида, характеризующегося:
1) определенной последовательностью оснований и длиной;
2) определенным профилем линкерных групп остова, а также
3) определенным профилем хиральных центров остова.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновой кислоты в популяции, каждая из мишеней и аналогичных последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной, а также
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевой последовательности нуклеиновой кислоты, так и аналогичных последовательностей нуклеиновой кислоты, транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для аналогичной последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой в популяции существует одна или более аналогичных последовательностей нуклеиновых кислот, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность среди аналогичных последовательностей, причем способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной; а также
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевой последовательности нуклеиновой кислоты, так и аналогичные последовательности нуклеиновой кислоты, транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для аналогичной последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для любой из аналогичных последовательностей нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфическое подавление транскрипта из целевой последовательности нуклеиновой кислоты, для которой в популяции существует множество аллелей, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной; а также
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же последовательности нуклеиновой кислоты, транскрипты конкретного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова,
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же последовательности нуклеиновой кислоты, транскрипты конкретного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, по меньшей мере в 2 раза превышающей степень подавления, наблюдаемую для другого аллеля того же самого гена.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова,
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, по меньшей мере в 2 раза превышающей степень подавления, наблюдаемую для другого аллеля того же самого гена.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова,
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, по меньшей мере в 2 раза превышающей степень подавления, наблюдаемую для другого аллеля того же самого гена.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты; или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова,
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты; или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический характеристический элемент нуклеотидной последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды конкретного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ аллель-специфического подавления транскрипта из целевого гена, для которого в популяции существует множество аллелей, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель среди других аллелей того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной,
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления нуклеотидная характеристическая последовательность содержит мутацию, которая определяет целевую последовательность по сравнению с другими подобными последовательностями. Согласно некоторым вариантам осуществления нуклеотидная характеристическая последовательность содержит точечную мутацию, которая определяет целевую последовательность относительно других аналогичных последовательностей. Согласно некоторым вариантам осуществления нуклеотидная характеристическая последовательность содержит SNP, который определяет целевую последовательность относительно других подобных последовательностей.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ получения композиции олигонуклеотидов, содержащей олигонуклеотиды определенной последовательности, причем композиция обеспечивает избирательное подавление транскрипта целевой последовательности, предусматривающий предоставление композиции олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований, которая совпадает с конкретной последовательностью;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова, профиль которых содержит (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где:
m равно 1-50;
n равно 1-10;
t равно 1-50; а также
каждый Np представляет собой независимо Rp или Sp.
В общем, активности описанных в настоящем документе композиций олигонуклеотидов могут быть оценены с использованием любого подходящего анализа. Относительные активности для разных композиций (например, стереоконтролируемых против не стереоконтролируемых и/или разных стереоконтролируемых композиций), как правило, желательно определять в одном и том же анализе, согласно некоторым вариантам осуществления, по существу, одновременно и согласно некоторым вариантам осуществления со ссылкой на предыдущие результаты.
Специалистам в данной области техники будет известно и/или им будет легко разработать соответствующие анализы для конкретных композиций олигонуклеотидов. В настоящем раскрытии предусмотрены описания некоторых конкретных анализов, например, которые могут быть применимы при оценке одной или более характеристик поведения композиции олигонуклеотидов по отношению к расщеплению РНКазой Н целевой последовательности.
Например, некоторые анализы, которые могут быть применимы при оценке одной или более характеристик (например, скорости, степени и/или селективности расщепления) расщепления РНКазой Н, могут включать анализ, как описано в любом анализе, описанном и/или представленном в настоящем документе (например, в одном или более примерах 4, 9-10, 12, 14, 17-20 и т.д.).
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрено, что последовательность оснований может влиять на свойства олигонуклеотидов. Настоящее раскрытие демонстрирует, что химические и стереохимические модификации в сочетании с разработанными последовательностями оснований могут обеспечивать композиции олигонуклеотидов с неожиданно улучшенными свойствами (например, неожиданно более высокой активностью и/или селективностью и т.д.). Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований, комплементарной характеристическому элементу последовательности целевой последовательности нуклеиновой кислоты, обеспечивают лучшую активность по сравнению с другой одинаковой последовательностью оснований, комплементарной характеристическому элементу последовательности целевой последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований, комплементарной характеристическому элементу последовательности целевой последовательности нуклеиновой кислоты, обеспечивают лучшую селективность по сравнению с другой одинаковой последовательностью оснований, комплементарной характеристическому элементу последовательности целевой последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов, характеризующаяся одинаковой последовательностью оснований, комплементарной характеристическому элементу последовательности целевой последовательности нуклеиновой кислоты, по сравнению с другой композицией олигонуклеотидов, характеризующейся другой одинаковой последовательностью оснований, комплементарной характеристическому элементу последовательности целевой последовательности нуклеиновой кислоты, обеспечивает более высокую скорость расщепления транс крипта из целевой последовательности нуклеиновой кислоты и/или профиль расщепления, который имеет только один основной сайт расщепления, а основной сайт расщепления находится в пределах или вблизи характеристической последовательности нуклеотидов. Согласно некоторым вариантам осуществления композиция олигонуклеотидов, характеризующихся комплементарной одинаковой последовательностью оснований, по сравнению с другой композицией олигонуклеотидов, характеризующихся другой комплементарной одинаковой последовательностью оснований, обеспечивает более высокую скорость расщепления транскрипта из целевой последовательности нуклеиновой кислоты и профиль расщепления, который имеет только один основной сайт расщепления, а основной сайт расщепления находится в пределах или вблизи характеристической последовательности нуклеотидов. Согласно некоторым вариантам осуществления более 50%, 60%, 70%, 80% или 90% расщепления происходит в одном основном сайте расщепления, например, при измерении с помощью подходящего способа, например, анализа посредством РНКазы Н. Согласно некоторым вариантам осуществления композиция олигонуклеотидов, характеризующихся комплементарной одинаковой последовательностью оснований, по сравнению с другой композицией олигонуклеотидов, характеризующихся другой комплементарной одинаковой последовательностью оснований, обеспечивает более высокую скорость расщепления транскрипта из целевой последовательности нуклеиновой кислоты и профиль расщепления, который имеет только один основной сайт расщепления, а основной сайт расщепления находится внутри или вблизи мутации или SNP, который определяет целевую последовательность относительно других подобных последовательностей. Согласно некоторым вариантам осуществления мутация представляет собой точечную мутацию. Согласно некоторым вариантам осуществления основной сайт расщепления находится рядом с мутацией или SNP, который определяет целевую последовательность относительно других подобных последовательностей. Согласно некоторым вариантам осуществления каждая общая последовательность оснований на 100% комплементарна элементу характеристической последовательности целевой последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления основной сайт расщепления находится в пределах менее 5, 4, 3 или 1 межнуклеотидной линкер ной группы от мутации или SNP, который определяет целевую последовательность относительно других подобных последовательностей. Согласно некоторым вариантам осуществления основной сайт расщепления находится в пределах менее 5, 4, 3 или 1 межнуклеотидной линкерной группы от мутации или SNP, который определяет целевую последовательность относительно других подобных последовательностей и находится в пределах менее 5, 4, 3, или 1 межнуклеотидной линкерной группы от сайта расщепления, когда используется стереослучайная композиция олигонуклеотидов, характеризующихся одной и той же одинаковой последовательностью, и/или композиция олигонуклеотидов ДНК, характеризующихся одной и той же общей последовательностью. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт расщепления, когда используется стереослучайная композиция олигонуклеотидов, характеризующихся одной и той же одинаковой последовательностью. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой основной сайт расщепления, когда используется стереослучайная композиция олигонуклеотидов, характеризующихся одной и той же одинаковой последовательностью. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт расщепления, когда используется композиция олигонуклеотидов ДНК, характеризующихся одной и той же одинаковой последовательностью. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой основной сайт расщепления, когда используется композиция олигонуклеотидов ДНК, характеризующихся одной и той же одинаковой последовательностью.
Согласно некоторым вариантам осуществления при сравнении эффектов первой и второй одинаковых последовательностей оснований стереослучайная композиция олигонуклеотидов, характеризующихся первой одинаковой последовательностью оснований, может быть сравнена со стереослучайной композицией олигонуклеотидов, характеризующихся второй одинаковой последовательностью оснований. Согласно некоторым вариантам осуществления стереослучайная композиция представляет собой композицию олигонуклеотидов, характеризующихся одинаковой последовательностью оснований, одинаковым профилем нуклеозидных модификаций и одинаковым профилем линкерных групп остова. Согласно некоторым вариантам осуществления стереослучайная композиция представляет собой композицию олигонуклеотидов, характеризующихся одинаковой последовательностью оснований, одинаковым профилем модификаций нуклеозидов, причем каждая межнуклеотидная линкерная группа представляет собой фосфоротиоат. Согласно некоторым вариантам осуществления при сравнении эффектов первой и второй одинаковых последовательностей оснований композиция олигонуклеотидов с контролируемой хиральностью из олигонуклеотидов, характеризующихся первой одинаковой последовательностью оснований, может быть сравнена с композицией олигонуклеотидов с контролируемой хиральностью из олигонуклеотидов, характеризующихся второй одинаковой последовательностью оснований. Согласно некоторым вариантам осуществления олигонуклеотиды в композиции олигонуклеотидов с контролируемой хиральностью характеризуются одинаковой последовательностью оснований, одинаковым профилем нуклеозидных модификаций, одинаковым профилем линкерных групп остова, одинаковым профилем хиральных центров остова и одинаковым профилем модификаций фосфора остова. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа представляет собой фосфоротиоат.
Согласно некоторым вариантам осуществления описанные в настоящем документе композиции олигонуклеотидов и технологии особенно применимы для лечения болезни Хантингтона. Например, согласно некоторым вариантам осуществления настоящее раскрытие описывает стереохимически контролируемые композиции олигонуклеотидов, которые направляют расщепление (например, опосредованное РНКазой Н расщепление) нуклеиновых кислот, связанных с болезнью Хантингтона. Согласно некоторым вариантам осуществления такие композиции направляют преимущественное расщепление связанного с болезнью Хантингтона аллеля конкретной целевой последовательности, относительно одного или более (например, всех не связанных с болезнью Хантингтона) других аллелей последовательности.
Болезнь Хантингтона представляет собой наследственное заболевание, которое может вызывать прогрессирующую дегенерацию нервных клеток в головном мозге и влиять на двигательные и когнитивные способности субъекта. Согласно некоторым вариантам осуществления болезнь Хантингтона представляет собой аутосомно-доминантное расстройство. Согласно некоторым вариантам осуществления она вызвана мутациями в гене хантингтина. Нормальный ген НТТ содержит от 10 до 35 трехнуклеотидных повторов CAG. У людей с 40 или более повторами часто развивается расстройство. Согласно некоторым вариантам осуществления удлиненный сегмент CAG на первом экзоне гена НТТ приводит к получению аномально длинной версии белка хантингтина (удлиненный полиглютаминовый тракт), который разрезается на более мелкие токсичные фрагменты, которые связываются вместе и накапливаются в нейронах, нарушая нормальные функции этих клеток. Авторы Warby et al. (Am J Hum Genet., 2009, 84 (3), 351-366) сообщили о многих SNP, которые связаны с хромосомами заболевания и имеют более сильные ассоциации линкерных групп с удлинением CAG, чем те, о которых сообщалось ранее. Многие SNP, сильно связанные с удлинением CAG, не разделяются независимо друг от друга и находятся в состоянии равновесия между собой. Среди прочего, настоящее раскрытие признает, что сильная связь между конкретными SNP и хромосомами с удлиненным фрагментом CAG обеспечивает привлекательную терапевтическую возможность для лечения болезни Хантингтона, например, с помощью антисмысловой терапии. Кроме того, ассоциация специфических SNP в сочетании с высокими показателями гетерозиготности у пациентов с HD обеспечивает подходящие мишени для аллель-специфического нокдауна продукта мутантного гена. Например, в качестве ссылки смотрите Liu et al. Journal of Huntington's Disease 2, 2013, 491-500; Aronin, Neil and Pfister, Edith WO 2010/118263 A1; Pfister et al. Current Biology 2009, 19, 774-778.
Согласно некоторым вариантам осуществления целевой SNP настоящего раскрытия характеризуется высокой частотой гетерозиготности при HD и имеет конкретный вариант, связанный с мутантным НТТ-аллелем. Согласно некоторым вариантам осуществления SNP представляет собой rs362307. Согласно некоторым вариантам осуществления SNP представляет собой rs7685686. Согласно некоторым вариантам осуществления SNP может не связываться, но может характеризоваться высокой гетерозиготной частотой. Согласно некоторым вариантам осуществления SNP представляет собой rs362268 (область 3'-UTR). Согласно некоторым вариантам осуществления SNP представляет собой rs362306 (область 3'-UTR). Согласно некоторым вариантам осуществления SNP представляет собой rs2530595. Согласно некоторым вариантам осуществления SNP представляет собой rs362331.
Согласно некоторым вариантам осуществления предусмотрен способ лечения или профилактики болезни Хантингтона у субъекта, предусматривающий введение субъекту композиций олигонуклеотидов. Согласно некоторым вариантам осуществления предусмотрен способ лечения или профилактики болезни Хантингтона у субъекта, предусматривающий введение субъекту композиции олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательность оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида.
Согласно некоторым вариантам осуществления предусмотренный способ смягчает симптом болезни Хантингтона. Согласно некоторым вариантам осуществления предусмотренный способ замедляет начало болезни Хантингтона. Согласно некоторым вариантам осуществления предусмотренный способ замедляет прогрессирование болезни Хантингтона.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены способы идентификации пациентов для данной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены способы стратификации пациентов. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию мутации и/или SNP, связанных с вызывающим заболевание аллелем. Например, согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с удлиненными повторами CAG, которые связаны с болезнью Хантингтона или вызывают ее.
Согласно некоторым вариантам осуществления субъект содержит SNP в гене хантингтина субъекта. Согласно некоторым вариантам осуществления субъект содержит SNP, причем один аллель представляет собой мутантный хантингтин, связанный с удлиненными повторами CAG. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs362307, rs7685686, rs362268, rs2530595, rs362331 или rs362306. Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции содержат последовательность, комплементарную последовательности, содержащей SNP из вызывающего заболевание аллеля (мутантного), и композиция избирательно подавляет экспрессию из вызывающего заболевание аллеля.
Согласно некоторым вариантам осуществления последовательность олигонуклеотидов в предусмотренных технологиях (соединениях, композициях, способах и т.д.) содержит, состоит из или представляет собой последовательность любого описанного в настоящем документе олигонуклеотида. Согласно некоторым вариантам осуществления последовательность выбирается из таблиц N1A, N2A, N3A, N4A или 8; или WV-1092, WVE120101, WV-2603 или WV-2595. Согласно некоторым вариантам осуществления последовательность выбирается из последовательности WV-1092, WVE120101, WV-2603 или WV-2595. Согласно некоторым вариантам осуществления олигонуклеотиды характеризуются типом, определенным посредством WV-1092, WVE120101, WV-2603 или WV-2595. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды характеризуются типом, определенным посредством WV-1092. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды характеризуются типом, определенным посредством WVE120101. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды характеризуются типом, определенным посредством WV-2603. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды характеризуются типом, определенным посредством WV-2595.
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов содержат липид и олигонуклеотид. Согласно некоторым вариантам осуществления липид конъюгирован с олигонуклеотидом.
Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из списка: лауриновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, линолевая кислота, альфа-линоленовая кислота, гамма-линоленовая кислота, докозагексаеновая кислота (цис-DHA), турбинаровая кислота, арахидоновая кислота и дилинолеил. Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из списка: лауриновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, линолевая кислота, альфа-линоленовая кислота, гамма-линоленовая кислота, докозагексаеновая кислота (цис-DHA), турбинаровая кислота и дилинолеил.
Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из:








Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид,
причем липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов содержит множество олигонуклеотидов, которые совместно характеризуются:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем модификаций фосфора остова;
причем один или более олигонуклеотидов из множества отдельно конъюгированы с липидом.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит множество олигонуклеотидов, которые совместно характеризуются:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем модификаций фосфора остова;
причем:
композиция характеризуется контролируемой хиральностью в том отношении, что множество олигонуклеотидов имеют одну и ту же стереохимию в одной или более хиральных межнуклеотидных связях;
один или более олигонуклеотидов из множества отдельно конъюгированы с липидом; а также
один или более олигонуклеотидов из множества необязательно и отдельно конъюгированы с целевым соединением или фрагментом.
Согласно некоторым вариантам осуществления способ доставки олигонуклеотида в клетку или ткань у человека предусматривает:
(a) предоставление композиции любого из описанных в настоящем документе вариантов реализации, а также
(b) введение композиции субъекту-человеку таким образом, что олигонуклеотид доставляется в клетку или ткань у субъекта.
Согласно некоторым вариантам осуществления способ доставки олигонуклеотида в клетку или ткань предусматривает получение композиции в соответствии с любым из описанных в настоящем документе вариантов осуществления и контактирование клетки или ткани с композицией.
Согласно некоторым вариантам осуществления способ модуляции уровня транскрипта или продукта гена в клетке предусматривает стадию контактирования клетки с композицией в соответствии с любым из описанных в настоящем документе вариантов реализации, причем олигонуклеотид способен модулировать уровень транскрипта или продукта гена.
Согласно некоторым вариантам осуществления способ ингибирования экспрессии гена в клетке или ткани предусматривает получение композиции в соответствии с любым из описанных в настоящем документе вариантов осуществления и воздействие на клетку или ткань композицией.
Согласно некоторым вариантам осуществления способ ингибирования экспрессии гена в клетке или ткани у млекопитающего предусматривает получение композиции по любому из описанных в настоящем документе вариантов реализации и введение композиции млекопитающему.
Согласно некоторым вариантам осуществления способ лечения заболевания, вызванного чрезмерной экспрессией одного или более белков в клетке или ткани у субъекта, предусматривает введение субъекту композиции в соответствии с любым из описанных в настоящем документе вариантов реализации.
Согласно некоторым вариантам осуществления способ лечения заболевания, вызванного уменьшенной, подавленной или отсутствующей экспрессией одного или более белков у субъекта, предусматривает введение субъекту композиции в соответствии с любым из описанных в настоящем документе вариантов реализации.
Согласно некоторым вариантам осуществления способ получения иммунного ответа у субъекта предусматривает введение субъекту композиции в соответствии с любым из описанных в настоящем документе вариантов реализации, причем биологически активное соединение представляет собой иммуномодулирующую нуклеиновую кислоту.
Согласно некоторым вариантам осуществления способ лечения признака и/или симптома заболевания Хантингтона заключается в предоставлении композиции любого из описанных в настоящем документе вариантов реализации и введении композиции субъекту.
Согласно некоторым вариантам осуществления способ модуляции количества опосредованного РНКазой Н расщепления в клетке предусматривает стадию контактирования клетки с композицией в соответствии с любым из описанных в настоящем документе вариантов реализации, причем олигонуклеотид способен к модулированию количества опосредованного РНКазой Н расщепления.
Согласно некоторым вариантам осуществления способ введения олигонуклеотида нуждающемуся в этом субъекту предусматривает стадии предоставления композиции, содержащей агент и липид, и введения композиции субъекту, причем агент представляет собой любой раскрытый в настоящем документе агент и причем липид представляет собой любой раскрытый в настоящем документе липид.
Согласно некоторым вариантам осуществления способ лечения заболевания у субъекта предусматривает стадии предоставления композиции, содержащей агент и липид, и введения терапевтически эффективного количества композиции субъекту, причем агент представляет собой любой раскрытый в настоящем документе агент и причем липид представляет собой любой раскрытый в настоящем документе липид, и причем заболевание представляет собой любое раскрытое в настоящем документе заболевание.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более алифатическими группами С1-4.
Согласно некоторым вариантам осуществления липид содержит незамещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит не более одной необязательно замещенной С10-С40 линейной, насыщенной или частично ненасыщенной алифатической цепи.
Согласно некоторым вариантам осуществления липид содержит две или более необязательно замещенных С10-С40 линейных, насыщенных или частично ненасыщенных алифатических цепей.
Согласно некоторым вариантам осуществления липид не содержит трициклического или полициклического фрагмента.
Согласно некоторым вариантам осуществления липид характеризуется структурой R1-COOH, где R1 представляет собой необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
Композиция или способ по п. 16, причем липид конъюгирован через его карбоксильную группу.
Композиция или способ согласно любому из вариантов осуществления, описанных в настоящем документе, где липид выбран из:







Согласно некоторым вариантам осуществления липид конъюгирован с олигонуклеотидом.
Согласно некоторым вариантам осуществления липид непосредственно конъюгирован с олигонуклеотидом.
Согласно некоторым вариантам осуществления липид конъюгируют с олигонуклеотидом через линкерную группу.
Согласно некоторым вариантам осуществления линкерную группу выбирают из: незаряженной линкерной группы; заряженной линкерной группы; содержащей алкил линкерной группы; содержащей фосфат линкерной группы; разветвленной линкерной группы; неразветвленной линкерной группы; линкерной группы, содержащей по меньшей мере одну группу расщепления; линкерной группы, содержащей по меньшей мере одну группу редокс-расщепления; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе фосфата; линкерной группы, содержащей по меньшей мере одну группу расщепления кислотой; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе сложного эфира, и линкерной группы, содержащей по меньшей мере одну группу расщепления на основе пептидов.
Согласно некоторым вариантам осуществления каждый олигонуклеотид из множества отдельно конъюгирован с одним и тем же липидом в одном и том же месте.
Согласно некоторым вариантам осуществления липид конъюгируют с олигонуклеотидом через линкерную группу.
Согласно некоторым вариантам осуществления один или более олигонуклеотидов из множества независимо конъюгированы с целевым соединением или фрагментом.
Согласно некоторым вариантам осуществления один или более олигонуклеотидов из множества независимо конъюгированы с липидом и целевым соединением или фрагментом.
Согласно некоторым вариантам осуществления один или более олигонуклеотидов из множества независимо конъюгированы с липидом на одном конце и целевым соединением или фрагментом на другом.
Согласно некоторым вариантам осуществления олигонуклеотиды из множества характеризуются одними и теми же профилями химической модификации.
Согласно некоторым вариантам осуществления олигонуклеотиды из множества характеризуются одними и теми же профилями химических модификаций, содержащими одну или более модификаций оснований.
Согласно некоторым вариантам осуществления олигонуклеотиды из множества характеризуются одними и теми же профилями химических модификаций, содержащими одну или более модификаций сахара.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований способна гибридизоваться с транскриптом в клетке, причем транскрипт содержит мутацию, связанную с болезнью Хантингтона, или уровень, активность и/или распределение которой связаны с болезнью Хантингтона.
Согласно некоторым вариантам осуществления олигонуклеотид представляет собой нуклеиновую кислоту.
Согласно некоторым вариантам осуществления олигонуклеотид представляет собой олигонуклеотид.
Согласно некоторым вариантам осуществления олигонуклеотид представляет собой олигонуклеотид, который участвует в опосредуемом РНКазой Н расщеплении мРНК гена хантингтина млекопитающих.
Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой заболевание Хантингтона.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую группу, где одно или более метиленовых звеньев необязательно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена,  , C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О- -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная независима, как определено и описано в настоящем документе.
, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О- -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная независима, как определено и описано в настоящем документе.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную C10-C80 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид сдержит необязательно замещенную C10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид включает необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую группу, в которой одно или более метиленовых звеньев необязательно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена,  , C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная независима, как определено и описано в настоящем документе.
, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная независима, как определено и описано в настоящем документе.
Согласно некоторым вариантам осуществления липид включает необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид включает необязательно замещенную С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид включает необязательно замещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид включает необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую группу, в которой одно или более метиленовых звеньев необязательно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена,  ; C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная независима, как определено и описано в настоящем документе.
; C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная независима, как определено и описано в настоящем документе.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления композиция дополнительно содержит один или более дополнительных компонентов, выбранных из: полинуклеотида, ингибитора карбоангидразы, красителя, интеркалирующего агента, акридина, сшивающего агента, псоралена, митомицина С, порфирина, ТРРС4, тексафирина, сапфирина, полициклического ароматического углеводорода феназина, дигидрофеназина, искусственной эндонуклеазы, хелатирующего агента, ЭДТА, алкилирующего агента, фосфата, амино, меркапто, ПЭГ, ПЭГ-40К, MPEG, [MPEG]2, полиамино, алкила, замещенного алкила, меченого радиоактивным изотопом маркера, фермента, гаптен-биотина, облегчающего перенос/абсорбцию агента, аспирина, витамина Е, фолиевой кислоты, синтетической рибонуклеазы, белка, гликопротеина, пептида, молекулы имеющей специфическое сродство к со-лиганду, антитела, гормона, гормонального рецептора, соединений непептидной природы, липида, лектина, углевода, витамина, кофактора, агента избирательности или лекарственного агента. Согласно некоторым вариантам осуществления композиция дополнительно содержит один или более дополнительных компонентов, выбранных из: полинуклеотида, ингибитора карбоангидразы, красителя, интеркалирующего агента, акридина, сшивающего агента, псоралена, митомицина С, порфирина, ТРРС4, тексафирина, сапфирина, полициклического ароматического углеводорода феназина, дигидрофеназина, искусственной эндонуклеазы, хелатирующего агента, ЭДТА, алкилирующего агента, фосфата, амино, меркапто, ПЭГ, ПЭГ-40К, MPEG, [MPEG]2, полиамино, алкила, замещенного алкила, меченого радиоактивным изотопом маркера, фермента, гаптен-биотина, облегчающего перенос/абсорбцию агента, аспирина, витамина Е, фолиевой кислоты, синтетической рибонуклеазы, белка, гликопротеина, пептида, молекулы, имеющей специфическое сродство к со-лиганду, антитела, гормона, гормонального рецептора, соединений непептидной природы, липида, лектина, углевода, витамина, кофактора или лекарственного агента.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен олигонуклеотид, конъюгированный с агентом селективности. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция, содержащая олигонуклеотид или тип олигонуклеотида, содержащий агент селективности. Согласно некоторым вариантам осуществления агент селективности специфически связывается с одним или более транспортерами нейромедиаторов, выбранными из группы, состоящей из транспортера дофамина (DAT), транспортера серотонина (SERT) и транспортера норадреналина (NET). Согласно некоторым вариантам осуществления агент селективности выбирают из группы, состоящей из ингибитора обратного захвата дофамина (DRI), селективного ингибитора обратного захвата серотонина (SSRI), ингибитора обратного захвата норадреналина (NRI), ингибитора обратного захвата норэпинефрина и дофамина (NDRI) и ингибитора обратного захвата серотонина-норэпинефрина-дофамина (SNDRI). Согласно некоторым вариантам осуществления агент селективности выбирают из группы, состоящей из тройного ингибитора обратного захвата, двойного ингибитора обратного захвата норадреналина-дофамина, одинарного ингибитора обратного захвата серотонина, одинарного ингибитора обратного захвата норадреналина и одинарного ингибитора обратного захвата дофамина. Согласно некоторым вариантам осуществления агент селективности выбирают из группы, состоящей из ингибитора обратного захвата дофамина (DRI), ингибитора обратного захвата норэпинефрина-дофамина (NDRI) и ингибитора обратного захвата серотонина-норэпинефрина-дофамина (SNDRI). Согласно некоторым вариантам осуществления агента селективности выбирают из агентов селективности, которые описаны в патентах США №9084825 и 9193969 и публикациях международных заявок WO 2011131693, WO 2014064258.
Согласно некоторым вариантам осуществления липид содержит С10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления композиция дополнительно содержит линкерную группу, связывающую олигонуклеотид и липид, причем линкерную группу выбирают из: незаряженной линкерной группы; заряженной линкерной группы; содержащей алкил линкерной группы; содержащей фосфат линкерной группы; разветвленной линкерной группы; неразветвленной линкерной группы; линкерной группы, содержащей по меньшей мере одну группу расщепления; линкерной группы, содержащей по меньшей мере одну группу редокс-расщепления; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе фосфата; линкерной группы, содержащей по меньшей мере одну группу расщепления кислотой; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе сложного эфира, и линкерной группы, содержащей по меньшей мере одну группу расщепления на основе пептидов.
Согласно некоторым вариантам осуществления олигонуклеотид содержит или состоит из или представляет собой олигонуклеотид или композицию олигонуклеотидов или композицию олигонуклеотидов с контролируемой хиральностью.
Согласно некоторым вариантам осуществления олигонуклеотид содержит или состоит из или представляет собой композицию олигонуклеотидов или композицию олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности любого описанного в настоящем документе олигонуклеотида.
Согласно некоторым вариантам осуществления олигонуклеотид содержит или состоит из или представляет собой композицию олигонуклеотидов или композицию олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности любого олигонуклеотида, перечисленного в таблице 4.
Согласно некоторым вариантам осуществления олигонуклеотид содержит или состоит из или представляет собой композицию олигонуклеотидов или композицию олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности олигонуклеотида, обеспечивающего переключение сплайсинга.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем олигонуклеотид представляет собой композицию олигонуклеотидов с контролируемой хиральностью.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем заболевание или нарушение представляет собой болезнь Хантингтона.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении мРНК мутантного гена хантингтина.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем олигонуклеотид содержит, состоит из или представляет собой последовательность любого описанного в настоящем документе олигонуклеотида.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем олигонуклеотид способен различать аллель дикого типа и мутантный аллель Хантингтин.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении мРНК мутантного гена хантингтина.
Композиция или способ по любому из описанных в настоящем документе вариантов реализации, причем олигонуклеотид содержит, состоит из или представляет собой последовательность любого олигонуклеотида, раскрытого в таблице 4.
Согласно некоторым вариантам осуществления олигонуклеотид содержит или состоит из или представляет собой олигонуклеотид или композицию олигонуклеотидов, или композицию олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности любого из: WV-1092, WV-2595 или WV-2603.
Согласно некоторым вариантам осуществления последовательность олигонуклеотида включает любую одну или более из: последовательности оснований (включая длину); профиля химических модификаций фрагментов сахара и оснований; профиля линкерных групп остова; профиля природных фосфатных линкерных групп, фосфоротиоатных линкерных групп, фосфоротиоатных триэфирных линкерных групп и их комбинации; профиля хиральных центров остова; профиля стереохимии (Rp/Sp) хиральных межнуклеотидных линкерных групп; профиля фосфорных модификаций остова; профиля модификаций на межнуклеотидном атоме фосфора, таком как -S- и -L-R1 формулы I.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) общей последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся одной и той же последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида, причем олигонуклеотиды нацелены на мутантный ген хантингтина, и длина составляет от примерно 10 до примерно 50 нуклеотидов, причем линкерные группы остова содержат по меньшей мере один фосфоротиоат и причем профиль хиральных центров остова содержит по меньшей мере один хиральный центр в конформации Rp и по меньшей мере один хиральный центр в конформации Sp.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ расщепления нуклеиновой кислоты, характеризующейся последовательностью оснований, содержащей целевую последовательность, причем способ предусматривает стадии:
(а) контактирования нуклеиновой кислоты,. характеризующейся последовательностью оснований, содержащей целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности в нуклеиновой кислоте;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся конкретной последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида, причем олигонуклеотид нацелен на мутантный ген хантингтина, а длина составляет от примерно 10 до примерно 50 нуклеотидов, причем линкерные группы остова содержат по меньшей мере один фосфоротиоат и причем профиль хиральных центров остова содержит по меньшей мере один хиральный центр в конформации Rp и по меньшей мере один хиральный центр в конформации Sp.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрен способ расщепления нуклеиновой кислоты, характеризующейся последовательностью оснований, содержащей целевую последовательность, причем способ предусматривает стадии:
(а) контактирования нуклеиновой кислоты, характеризующейся последовательностью оснований, содержащей целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности в нуклеиновой кислоте;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся конкретной последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида, причем олигонуклеотид нацелен на мутантный ген хантингтина, а длина составляет от примерно 10 до примерно 50 нуклеотидов, причем линкерные группы остова содержат по меньшей мере один фосфоротиоат и причем профиль хиральных центров остова содержит по меньшей мере один хиральный центр в конформации Rp и по меньшей мере один хиральный центр в конформации Sp; а также
(b) расщепления нуклеиновой кислоты, опосредуемого механизмом интерференции РНКазы или РНК.
Согласно некоторым вариантам осуществления предусмотренная композиция дополнительно содержит агент селективности, выбранный из группы соединений, которые специфически связываются с одним или более транспортерами нейромедиаторов, выбранными из группы, состоящей из транспортера дофамина (DAT), транспортера серотонина (SERT) и транспортера норадреналина (NET), группы, состоящей из ингибитора обратного захвата дофамина (DRI), селективного ингибитора обратного захвата серотонина (SSRI), ингибитора обратного захвата норадреналина (NRI), ингибитора обратного захвата норэпинефрина и дофамина (NDRI) и ингибитора обратного захвата серотонина-норэпинефрина-дофамина (SNDRI), группы, состоящей из тройного ингибитора обратного захвата, двойного ингибитора обратного захвата норадреналина-дофамина, одинарного ингибитора обратного захвата серотонина, одинарного ингибитора обратного захвата норадреналина и одинарного ингибитора обратного захвата дофамина, группы, состоящей из ингибитора обратного захвата дофамина (DRI), ингибитора обратного захвата норэпинефрина-дофамина (NDRI) и ингибитора обратного захвата серотонина-норэпинефрина-дофамина (SNDRI).
Согласно некоторым вариантам осуществления предусмотренная композиция содержит олигонуклеотиды, причем последовательность оснований, профиль линкерных групп остова и/или профиль хиральных центров остова олигонуклеотидов содержит или состоит из последовательности оснований, профиля линкерных групп остова и/или профиля хиральных центров остова любого из олигонуклеотида, выбранного из таблиц N1A, N2A, N3A, N4A и 8; и публикаций международных заявок WV-1092, WV-2595 и WV-2603.
Согласно некоторым вариантам осуществления предложенная композиция содержит олигонуклеотиды, в которых последовательность оснований, профиль линкерных групп остова и/или профиль хиральных центров остова олигонуклеотидов содержит или состоит из последовательности оснований, профиля линкерных групп остова и/или профиля хиральных центров остова любого из олигонуклеотида, выбранного из таблиц N1A, N2A, N3A, N4A и 8; и публикаций международных заявок WV-1092, WV-2595 и WV-2603.
Согласно некоторым вариантам осуществления предложенная композиция содержит олигонуклеотиды, в которых последовательность оснований, профиль линкерных групп остова и/или профиль хиральных центров остова олигонуклеотидов содержит или состоит из последовательности оснований, профиля линкерных групп остова и/или профиля хиральных центров остова любого из олигонуклеотида, выбранного из таблиц N1A, N2A, N3A, N4A и 8; и публикаций международных заявок WV-1092, WV-2595 и WV-2603.
Описания
Алифатический: Термин «алифатический» или «алифатическая группа», используемый в настоящем описании, обозначает линейную (т.е. неразветвленную) или разветвленную замещенную или незамещенную углеводородную цепь, которая является полностью насыщенной или содержит один или более ненасыщенных участков, или моноциклический углеводород или бициклический или полициклический углеводород, который является полностью насыщенным или содержит один или более ненасыщенных участков, но не является ароматическим (его также называют в настоящем описании «карбоцикл», «циклоалифатический» или «циклоалкил»), и имеет одну точку присоединения к остатку молекулы. Согласно некоторым вариантам осуществления алифатические группы содержат 1-50 алифатических атомов углерода. Если не указано иное, алифатические группы содержат 1-10 алифатических атомов углерода. Согласно некоторым вариантам осуществления алифатические группы содержат 1-6 алифатических атомов углерода. Согласно некоторым вариантам осуществления алифатические группы содержат 1-5 алифатических атомов углерода. В других вариантах реализации алифатические группы содержат 1-4 алифатических атомов углерода. В других вариантах реализации алифатические группы содержат 1-3 алифатических атомов углерода, а в других вариантах реализации алифатические группы содержат 1-2 алифатических атомов углерода. Согласно некоторым вариантам осуществления «циклоалифатический» (или «карбоцикл» или «циклоалкил») относится к моноциклическому или бициклическому С3-С10 углеводороду, который является полностью насыщенным или содержит один или более ненасыщенных участков, но не является ароматическим, и имеет одну точку присоединения к остатку молекулы. Согласно некоторым вариантам осуществления «циклоалифатический» (или «карбоцикл» или «циклоалкил») относится к моноциклическому С3-С6 углеводороду, который является полностью насыщенным или содержит один или более ненасыщенных участков, но не является ароматическим, и имеет одну точку присоединения к остатку молекулы. Подходящие алифатические группы включают, но не ограничиваются ими, линейные или разветвленные замещенные или незамещенные алкильные, алкенильные, алкинильные группы и их гибриды, такие как (циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил.
Алкилен: Термин «алкилен» относится к двухвалентной алкильной группе. «Алкиленовая цепь» представляет собой полиметиленовую группу, т.е. -(СН2)n-, где n представляет собой положительное целое число предпочтительно от 1 до 6, от 1 до 4, от 1 до 3, от 1 до 2 или от 2 до 3. Замещенная алкиленовая цепь представляет собой полиметиленовую группу, в которой один или более метиленовых атомов водорода заменены на заместитель. Подходящие заместители включают те, что описаны далее для замещенной алифатической группы.
Алкенилен: Термин «алкенилен» относится к двухвалентной алкенильной группе. Замещенная алкениленовая цепь представляет собой полиметиленовую группу, содержащую по меньшей мере одну двойную связь, в которой один или более атомов водорода заменены на заместитель. Подходящие заместители включают те, что описаны далее для замещенной алифатической группы.
Животное: При использовании в настоящем описании термин «животное» относится к любому представителю царства животных. Согласно некоторым вариантам осуществления «животное» относится к человеку на любой стадии развития. Согласно некоторым вариантам осуществления «животное» относится к животным, отличным от человека, на любой стадии развития. В определенных вариантах реализации животное, отличное от человека, представляет собой млекопитающее (например, грызуна, мышь, крысу, кролика, обезьяну, собаку, кошку, овцу, крупный рогатый скот, примата и/или свинью). Согласно некоторым вариантам осуществления животные включают, но не ограничиваются ими, млекопитающих, птиц, рептилий, амфибий, рыб и/или червей. Согласно некоторым вариантам осуществления животное может представлять собой трансгенное животное, животное, выращенное методами генной инженерии, и/или клон.
Примерно: Предполагается, что в настоящем описании термины «примерно» или «примерно», используемые в отношении числового значения, включают числовые значения, которые не выходят за рамки 5%, 10%, 15% или 20% диапазона в обе стороны (более или менее) от указанного числового значения, если не указанное иное, или если из контекста не очевидно иное (за исключением тех случаев, когда указанное числовое значение будет составлять менее 0% или более 100% от возможного значения). Согласно некоторым вариантам осуществления использование термина «примерно» в отношении дозировок обозначает ± 5 мг/кг/день.
Арил: Термин «арил», используемый отдельно или в составе более крупного фрагмента, такого как «аралкил», «аралкокси» или «арилоксиалкил», относится к моноциклическим и бициклическим системам колец, содержащим всего от пяти до четырнадцати членов в кольце, где по меньшей мере одно кольцо в системе является ароматическим, и каждое кольцо в системе содержит от трех до семи членов в кольце. Термин «арил» можно использовать взаимозаменяемо с термином «арильное кольцо». В определенных вариантах реализации настоящего раскрытия «арил» относится к ароматической системе колец, включая, но не ограничиваясь ими, фенил, бифенил, нафтил, антрацил и т.д., которая может содержать один или более заместителей. Также в объем термина «арил», используемого в настоящем описании, включена группа, в которой ароматическое кольцо конденсировано с одним или более неароматическими кольцами, такая как инданил, фталимидил, нафтимидил, фенантридинил или тетрагидронафтил и т.д.
Характеристический фрагмент: При использовании в настоящем описании фраза «характеристический фрагмент» белка или полипептида представляет собой фрагмент, содержащий непрерывную последовательность аминокислот или набор непрерывных последовательностей аминокислот, которые вместе характеризуют белок или полипептид. Каждая непрерывная последовательность, в целом, содержит по меньшей мере две аминокислоты. Кроме того, специалистам в данной области техники должно быть понятно, что для определения характеристик белка, как правило, требуется по меньшей мере 5, 10, 15, 20 или более аминокислот. В целом, характеристический фрагмент представляет собой фрагмент, который помимо идентичной последовательности, указанной выше, наделяет важный неизмененный белок по меньшей мере одной функциональной характеристикой.
Характеристическая последовательность: «Характеристическая последовательность» представляет собой последовательность, которая содержится во всех членах семейства полипептидов или нуклеиновых кислот, и при помощи которой специалисты в данной области техники могут определять члены семейства.
Характеристический структурный элемент: Термин «характеристический структурный элемент» относится к отличительному структурному фрагменту (например, к структуре ядра, набору присоединенных фрагментов, элементу последовательности и т.д.), содержащемуся во всех членах семейства полипептидов, небольших молекул или нуклеиновых кислот, при помощи которого специалисты в данной области техники могут определять члены семейства.
Сравнимый: Термин «сравнимый» используют в настоящей заявке для описания двух (или более) наборов состояний или условий, которые достаточно похожи друг на друга, что позволяет проводить сравнение полученных результатов или наблюдаемых явлений. Согласно некоторым вариантам осуществления сравнимые наборы состояний или условий характеризуются совокупностью по существу одинаковых отличительных признаков и одним отличающимся отличительным признаком или незначительным количеством отличительных признаков. Специалистам в данной области техники должно быть понятно, что набор состояний сравним с другим набором, если характеризуется достаточным количеством и типом по существу одинаковых отличительных признаков, что позволяет сделать обоснованный вывод о том, что различия полученных результатов или наблюдаемых явлений для различных наборов состояний или условия вызваны или определены различиями отличающихся отличительных признаков.
Схема дозирования: При использовании в настоящем описании «схема дозирования» или «схема лечения» относятся к набору стандартных доз (как правило, более одной дозы), которые вводят по отдельности субъекту, как правило, с временными интервалами. Согласно некоторым вариантам осуществления данный терапевтический агент имеет рекомендуемую схему дозирования, в которую включены одна или более доз. Согласно некоторым вариантам осуществления схема дозирования включает совокупность доз, которые вводят отдельно друг от друга с одинаковыми временными интервалами; согласно некоторым вариантам осуществления схема дозирования включает совокупность доз и по меньшей мере два различных временных интервала между введением отдельных доз. Согласно некоторым вариантам осуществления все дозы, вводимые согласно схеме дозирования, содержат одинаковое стандартное дозируемое количество. Согласно некоторым вариантам осуществления различные дозы, вводимые согласно схеме дозирования, содержат различные количества. Согласно некоторым вариантам осуществления схема дозирования включает первую дозу, содержащую первое дозируемое количество, и одну или более дополнительных доз, содержащих второе дозируемое количество, отличающееся от первого дозируемого количества. Согласно некоторым вариантам осуществления схема дозирования включает первую дозу, содержащую первое дозируемое количество, а затем одну или более дополнительных доз, содержащих второе дозируемое количество, равное первому дозируемому количеству.
Эквивалентные агенты: Специалистам в данной области техники после изучения настоящего описанию будет понятно, что объем подходящих агентов в контексте настоящего раскрытия не ограничен теми, что конкретно указаны или предложены в настоящем описании. В частности специалистам в данной области техники должно быть понятно, что активные агенты, как правило, имеют структуру, состоящую из ядра и присоединенных фрагментов, кроме того, должно быть понятно, что небольшие изменения указанного ядра и/или присоединенных фрагментов существенно не изменяют активность агента. Например, согласно некоторым вариантам осуществления замещение одного или более присоединенных фрагментов на группы со сравнимой трехмерной структурой и/или химическими характеристиками, может приводить к получению замещенного соединения или фрагмента, эквивалентного исходному соединению или фрагменту сравнения. Согласно некоторым вариантам осуществления добавление или удаление одного или более присоединенных фрагментов может приводить к получению замещенного соединения, эквивалентного исходному соединению сравнения. Согласно некоторым вариантам осуществления изменение структуры ядра, например, путем добавления или удаления небольшого числа линкерных групп (как правило, не более чем 5, 4, 3, 2 или 1 связи, а часто только одной простой связи) может приводить к получению замещенного соединения, эквивалентного исходному соединению сравнения. Во многих вариантах реализации эквивалентные соединения можно получать при помощи способов, проиллюстрированных на общих схемах реакций, например таких как те, что приведены далее, или при помощи их модификаций с использованием легкодоступных исходных веществ, реагентов и традиционных или предложенных способов синтеза. В указанных взаимодействиях также можно использовать варианты, которые известны, как таковые, но не указаны в настоящем описании.
Эквивалентная дозировка: Термин «эквивалентная дозировка» используют в настоящем описании для сравнения дозировок различных фармацевтически активных агентов, которые приводят к одинаковому биологическому результату. Согласно настоящему раскрытию дозировки двух различных агентов считают «эквивалентными» друг другу, если после их введения достигают сравнимого уровня или степени биологического результата. Согласно некоторым вариантам осуществления эквивалентные дозировки различных фармацевтических агентов для применения согласно настоящему раскрытию определяют при помощи исследований in vitro и/или in vivo, описанных в настоящей заявке. Согласно некоторым вариантам осуществления один или более агентов, активирующих лизосомы, для применения согласно настоящему раскрытию используют в дозе, эквивалентной дозе агента сравнения, активирующего лизосомы; в некоторых из указанных вариантов реализации агент сравнения, активирующий лизосомы, подходящий для указанных задач, выбран из группы, состоящей из аллостерических активаторов, состоящих из небольших молекул (например, пиразолпиримидинов), иммуносахаров (например, изофагомина), антиоксидантов (например, н-ацетилцистеина) и регуляторов миграции клеток (например, полипептида Rab1a).
Гетероалифатический: Термин «гетероалифатический» относится к алифатической группе, где одно или более звеньев, выбранных из С, СН, СН2 или CH3, независимо заменены на гетероатом. Согласно некоторым вариантам осуществления гетероалифатическая группа представляет собой гетероалкил. Согласно некоторым вариантам осуществления гетероалифатическая группа представляет собой гетероалкенил.
Гетероарил: Термины «гетероарил» и «гетероар-», используемые по отдельности или в составе более крупного фрагмента, например, «гетероаралкил» или «гетероаралкокси», относятся к группам, содержащим от 5 до 10 атомов в кольце, предпочтительно 5, 6 или 9 атомов в кольце; содержащим 6, 10 или 14 π-электронов, распределенных по циклической матрице; и содержащим помимо атомов углерода от одного до пяти гетероатомов. Термин «гетероатом» относится к азоту, кислороду или сере и включает любую окисленную форму азота или серы и любую четвертичную форму основного атома азота. Гетероарильные группы включают без ограничений тиенил, фуранил, пирролил, имидазолил, пиразолил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиазолил, изотиазолил, тиадиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, индолизинил, пуринил, нафтиридинил и птеридинил. Термины «гетероарил» и «гетероар-», используемые в настоящем описании, также включают группы, в которых гетероароматическое кольцо конденсировано с одним или более арильными, циклоалифатическими и гетероциклильными кольцами, где радикал или место присоединения находится при гетероароматическом кольце. Неограничивающие примеры включают индолил, изоиндолил, бензотиенил, бензофуранил, дибензофуранил, индазолил, бензимидазолил, бензтиазолил, хинолил, изохинолил, циннолинил, фталазинил, хиназолинил, хиноксалинил, 4H-хинолизинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил, тетрагидрохинолинил, тетрагидроизохинолинил и пиридо[2,3-b]-1,4-оксазин-3(4Н)-он. Гетероарильная группа может быть моно- или бициклической. Термин «гетероарил» можно использовать взаимозаменяемо с терминами «гетероарильное кольцо», «гетероарильная группа» или «гетероароматический», любой из указанных терминов включает необязательно замещенные кольца. Термин «гетероаралкил» относится к алкильной группе, замещенной гетероарилом, где алкильный и гетероарильный фрагменты независимо необязательно замещены.
Гетероатом: Термин «гетероатом» обозначает один или более атомов, выбранных из кислорода, серы, азота, фосфора или кремния (включая любую окисленную форму азота, серы, фосфора или кремния; четвертичную форму любого основного атома азота; или атом азота гетероциклического кольца, который может иметь заместители, например, N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или NR+ (как в N-замещенном пирролидиниле)).
Гетероцикл: Используемые в настоящем описании термины «гетероцикл», «гетероциклил», «гетероциклический радикал» и «гетероциклическое кольцо», которые используют взаимозаменяемо, относятся к 3-7-членному моноциклическому или 7-10-членному бициклическому гетероциклическому фрагменту, который является насыщенным или частично ненасыщенным, и содержит помимо атомов углерода один или более, предпочтительно от одного до четырех гетероатомов, таких как определено выше. При использовании для описания атома кольца в гетероцикле термин «азот» включает замещенный атом азота. Например, в насыщенном или частично ненасыщенном кольце, содержащем 0-3 гетероатомов, выбранных из кислорода, серы или азота, атом азота может представлять собой N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или +NR (как в N-замещенном пирролидиниле).
Гетероциклическое кольцо может быть присоединено к соседней группе через любой гетероатом или атом углерода, что приводит к образованию стабильной структуры, любой из атомов в кольце может быть необязательно замещен. Примеры указанных насыщенных или частично ненасыщенных гетероциклических радикалов включают без ограничений тетрагидрофуранил, тетрагидротиофенил, пирролидинил, пиперидинил, пирролинил, тетрагидрохинолинил, тетрагидроизохинолинил, декагидрохинолинил, оксазолидинил, пиперазинил, диоксанил, диоксоланил, диазепинил, оксазепинил, тиазепинил, морфолинил и хинуклидинил. Термины «гетероцикл», «гетероциклил», «гетероциклильное кольцо», «гетероциклическая группа», «гетероциклический фрагмент» и «гетероциклический радикал», которые используют в настоящем описании взаимозаменяемо, также включают группы, в которых гетероциклическое кольцо конденсировано с одним или более арильными, гетероарильными или циклоалифатическими кольцами, такие как индолинил, 3H-индолил, хроманил, фенантридинил или тетрагидрохинолинил, где радикал или место присоединения находится при гетероциклильном кольце. Гетероциклильная группа может быть моно- или бициклической. Термин «гетероциклилалкил» относится к алкильной группе, замещенной гетероциклилом, где алкильный и гетероциклильный фрагменты независимо необязательно замещены.
Интраперитонеальный: Фразы «интраперитонеальное введение» и «вводимый интраперитонеально», используемые в настоящем описании, имеют общепринятое в данной области техники значение и относятся к введению соединения или композиции в брюшную полость субъекта.
In vitro: Используемый в настоящем описании термин «in vitro» относится к явлениям, происходящим в искусственной среде, например, в пробирке для исследований или в реакционном сосуде, в клеточной культуре и т.д., но не в организме (например, животного, растения и/или микроорганизма).
In vivo: Используемый в настоящем описании термин «in vivo» относится к явлениям, происходящим в организме (например, животного, растения и/или микроорганизма).
Низший алкил: Термин «низший алкил» относится к С1-4 линейной или разветвленной алкильной группе. Примерами низших алкильных групп являются метил, этил, пропил, изопропил, бутил, изобутил и трет-бутил.
Низший галогеналкил: Термин «низший галогеналкил» относится к С1-4 линейной или разветвленной алкильной группе, замещенной одним или более атомами галогенов.
Необязательно замещенный: Согласно настоящему описанию соединения согласно настоящему раскрытию могут содержать «необязательно замещенные» фрагменты. В целом, термин «замещенный», используемый совместно с предшествующим термином «возможно» или без него, означает, что один или более атомов водорода в указанном фрагменте заменены на подходящий заместитель. Если не указано иное, «необязательно замещенная» группа может содержать подходящий заместитель при каждом положении группы, которое может иметь заместители, и если в какой-либо данной структуре более одного положения могут быть замещены более чем одним заместителем, выбранным из указанных групп, то заместители при каждом положении могут быть одинаковыми или различными. Комбинации заместителей, подразумеваемые в настоящем раскрытии, предпочтительно представляют собой такие комбинации, которые приводят к образованию стабильных или химически разрешенных соединений. Термин «стабильный», используемый в настоящем описании, относится к соединениям, которые по существу не изменяются после воздействия в условиях получения, детектирования, а в определенных вариантах реализации выделения, очистки и использования для одной или более задач, предложенных в настоящем описании.
Подходящие одновалентные заместители при атоме углерода, который может иметь заместители, в «необязательно замещенной» группе независимо представляют собой галоген; -(CH2)0-4R°; -(CH2)0-4OR°; -O(CH2)0-4R°, -O-(CH2)0-4C(O)OR°; -(CH2)0-4CH(OR°)2; -(CH2)0-4SR°; -(CH2)0-4Ph, который может быть замещен R°; -(СН2)0-4О(СН2)0-1Ph, который может быть замещен R°; -CH=CHPh, который может быть замещен R°; -(СН2)0-4O(СН2)0-1-пиридил, который может быть замещен R°; -NO2; -CN; -N3; -(CH2)0-4N(R°)2; -(CH2)0-4N(R°)C(O)R°; -N(R°)C(S)R°; -(СН2)0-4N(R°)C(O)NR°2; -N(R°)C(S)NR°2; -(CH2)0-4N(R°)C(O)OR°; -N(R°)N(R°)C(O)R°; -N(R°)N(R°)C(O)NR°2; -N(R°)N(R°)C(O)OR°; -(CH2)0-4C(O)R°; -C(S)R°; -(CH2)0-4C(O)OR°; -(CH2)0-4C(O)SR°; -(CH2)0-4C(O)OSiR°3; -(CH2)0-4OC(O)R°; -OC(O)(CH2)0-4SR-, SC(S)SR°; -(CH2)0-4SC(O)R°; -(CH2)0-4C(O)NR°2; -C(S)NR°2; -C(S)SR°; -SC(S)SR°, -(CH2)0-4OC(O)NR°2; -C(O)N(OR°)R°; -C(O)C(O)R°; -C(O)CH2C(O)R°; -C(NOR°)R°; -(CH2)0-4SSR°; -(CH2)0-4S(O)2R°; -(CH2)0-4S(O)2OR°; -(CH2)0-4OS(O)2R°; -S(O)2NR°2; -(CH2)0-4S(O)R°; -N(R°)S(O)2NR°2; -N(R°)S(O)2R°; -N(OR°)R°; -C(NH)NR°2; -P(O)2R°; -P(O)R°2; -OP(O)R°2; -OP(O)(OR°)2; -SiR°3; -(C1-4 линейный или разветвленный алкилен)O-N(R°)2; или -(С1-4 линейный или разветвленный алкилен)С(O)O-N(R°)2, где каждый R° может быть замещен, как определено ниже, и независимо представляет собой водород, С1-6 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph, -СН2-(5-6-членное гетероарильное кольцо) или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы, или, несмотря на приведенное выше определение, два независимых R° совместно с соседним(и) атомом(ами) образуют 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы, которое может быть замещено, как определено ниже.
Подходящие одновалентные заместители при R° (или при кольце, полученном в результате объединения двух независимых R° совместно с соседними атомами) независимо представляют собой галоген, -(CH2)0-2R•, -(галоген-R•), -(СН2)0-2ОН, -(СН2)0-2OR•, -(CH2)0-2CH(OR•)2; -O(галоген-R•), -CN, -N3, -(CH2)0-2C(O)R•, -(СН2)0-2С(O)ОН, -(CH2)0-2C(O)OR•, -(CH2)0-2SR•, -(CH2)0-2SH, -(CH2)0-2NH2, -(CH2)0-2NHR•, -(CH2)0-2NR•2, -NO2, -SiR•3, -OSiR•3, -C(O)SR•, -(С1-4 линейный или разветвленный алкилен)С(O)OR• или -SSR•, где каждый R• является незамещенным, или если используется с предшествующим определением «галоген-», замещен только одним или более атомами галогенов, и независимо выбран из С1-4 алифатической группы, -CH2Ph, -O(CH2)0-1Ph или 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Подходящие двухвалентные заместители при насыщенном атоме углерода в R° включают =O и =S.
Подходящие двухвалентные заместители при насыщенном атоме углерода в «необязательно замещенной» группе включают следующие: =O, =S, =NNR*2, =NNHC(O)R*, =NNHC(O)OR*, =NNHS(O)2R*, =NR*, =NOR*, -O(C(R*2))2-3O- или -S(C(R*2))2-3S-, где в каждом независимом случае R* выбран из водорода, C1-6 алифатической группы, которая может быть замещена, как определено ниже, или незамещенного 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Подходящие двухвалентные заместители, связанные с вицинальными атомами углерода, которые могут иметь заместители, в «необязательно замещенной» группе включают: -O(CR*2)2-3O-, где в каждом независимом случае R* выбран из водорода, C1-6 алифатической группы, которая может быть замещена, как определено ниже, или незамещенного 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы.
Подходящие заместители при алифатической группе в R* включают галоген, -R•, -(галоген-R•), -ОН, -OR•-, -O(галоген-R•), -CN, -С(O)ОН, -C(O)OR•, -NH2, -NHR•, -NR•2 или -NO2, где каждый R• является незамещенным, или если ему предшествует определение «галоген», замещен только одним или более атомами галогенов, и независимо представляет собой С1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы.
Подходящие заместители при атоме азота, который может иметь заместители, в «необязательно замещенной» группе включают 
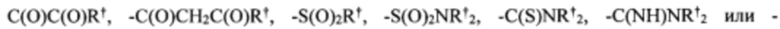
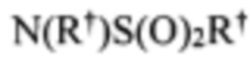 ; где каждый
; где каждый 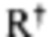 независимо представляет собой водород, C1-6 алифатическую группу, которая может быть замещена, как определено ниже, незамещенный -OPh или незамещенное 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы, или, несмотря на приведенное выше определение, два независимых
независимо представляет собой водород, C1-6 алифатическую группу, которая может быть замещена, как определено ниже, незамещенный -OPh или незамещенное 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы, или, несмотря на приведенное выше определение, два независимых 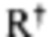 совместно с соседним(и) атомом(ами) образуют незамещенное 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы.
совместно с соседним(и) атомом(ами) образуют незамещенное 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы.
Подходящие заместители при алифатической группе в 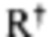 независимо представляют собой галоген, -R•, -(галоген-R•), -ОН, -OR•, -О(галоген-R•), -CN, -С(O)ОН, -C(O)OR•, -NH2, -NHR•, -NR•2 или -NO2, где каждый R• является незамещенным или, если ему предшествует определение «галоген», замещен только одним или более атомами галогенов, и независимо представляет собой С1-4 алифатическую группу, CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы.
независимо представляют собой галоген, -R•, -(галоген-R•), -ОН, -OR•, -О(галоген-R•), -CN, -С(O)ОН, -C(O)OR•, -NH2, -NHR•, -NR•2 или -NO2, где каждый R• является незамещенным или, если ему предшествует определение «галоген», замещен только одним или более атомами галогенов, и независимо представляет собой С1-4 алифатическую группу, CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатомов, независимо выбранных из азота, кислорода или серы.
Пероральный: Фразы «пероральное введение» или «вводимый перорально», используемые в настоящем описании, имеют общепринятое в данной области техники определение и относятся к введению соединения или композиции через рот.
Парентеральный: Фразы «парентеральное введение» и «вводимый парентерально», используемые в настоящем описании, имеют общепринятое в данной области техники значение и относятся к способам введения, отличным от энтерального и местного введения, которые, как правило, проводят путем инъекции, и включают без ограничений внутривенную, внутримышечную, внутриартериальную, интратекальную, внутрикапсульную, интраорбитальную, внутрисердечную, интрадермальную, интраперитонеальную, транстрахеальную, подкожную, внутрикожную, внутрисуставную, субкапсулярную, субарахноидальную, спинномозговую и интрастернальную инъекцию и инфузию.
Частично ненасыщенный: Используемый в настоящем описании термин «частично ненасыщенный» относится к кольцевому фрагменту, содержащему по меньшей мере одну двойную или тройную связь. Предполагается, что термин «частично ненасыщенный» охватывает кольца, содержащие несколько ненасыщенных участков, но не включает арильные или гетероарильные фрагменты, такие как определено в настоящем описании.
Фармацевтическая композиция: Используемый в настоящем описании термин «фармацевтическая композиция» относится к активному агенту, введенному в состав совместно с одним или более фармацевтически приемлемыми носителями. Согласно некоторым вариантам осуществления активный агент присутствует в стандартном дозируемом количестве, подходящем для введения согласно схеме лечения, при котором существует статистически значимая вероятность достижения предварительно определенного терапевтического действия после введения целевой популяции. Согласно некоторым вариантам осуществления фармацевтические композиции могут быть специально предназначены для введения в твердой или жидкой форме, включая формы, предназначенные: для перорального введения, например, жидкие лекарственные формы для перорального введения (водные или неводные растворы или суспензии), таблетки, например, предназначенные для трансбуккального, подъязычного и системного всасывания, болюсы, порошки, гранулы, пасты для нанесения на язык; для парентерального введения, например, путем подкожной, внутримышечной, внутривенной или эпидуральной инъекции, например, в виде стерильного раствора или суспензии или состава с замедленным высвобождением; для местного введения, например, в виде крема, мази или пластыря с контролируемым высвобождением или спрея, наносимого на кожу, в легкие или полость рта; для внутривагинального или ректального введения, например, в виде суппозитория, крема или пены; для подъязычного введения; введения в глаза; чрескожного введения; или введения в нос, легкие и через другие слизистые поверхности.
Фармацевтически приемлемый: Используемая в настоящем описании фраза «фармацевтически приемлемый» относится к соединениям, веществам, композициям и/или лекарственным формам, которые по результатам тщательного медицинского обследования подходят для применения в контакте с тканями человека и животных, не вызывая избыточную токсичность, раздражение, аллергический ответ или иную проблему или осложнение, и имеют приемлемое отношение польза/риск.
Фармацевтически приемлемый носитель: Используемый в настоящем описании термин «фармацевтически приемлемый носитель» обозначает фармацевтически приемлемое вещество, композицию или носитель, такое как жидкий или твердый наполнитель, разбавитель, вспомогательное вещество или вещество для инкапсулирования растворителя, участвующее в переносе или транспортировке целевого соединения из одного органа или фрагмента организма в другой орган или фрагмент организма. Каждый носитель должен быть «приемлемым» с точки зрения совместимости с другими ингредиентами состава и безвредности для пациента. Некоторые примеры веществ, которые можно применять в качестве фармацевтически приемлемых носителей, включают: сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошковую трагакантовую камедь; солод; желатин; тальк; вспомогательные вещества, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль; полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные агенты, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический солевой раствор; раствор Рингера; этиловый спирт; рН-буферные растворы; сложные полиэфиры, поликарбонаты и/или полиангидриды; и другие нетоксичные совместимые вещества, применяемые в фармацевтических составах.
Фармацевтически приемлемая соль: Термин «фармацевтически приемлемая соль», используемый в настоящем описании, относится к солям указанных соединений, подходящим для применения в области фармацевтики, т.е. к солям, которые по результатам тщательного медицинского обследования подходят для применения в контакте с тканями человека и низших животных, не вызывая нежелательную токсичность, раздражение, аллергический ответ и т.д., и имеют приемлемое отношение польза/риск. Фармацевтически приемлемые соли хорошо известны в данной области техники. Например, фармацевтически приемлемые соли подробно описаны в S.М. Berge, et al., J. Pharmaceutical Sciences, 66: 1-19 (1977). Согласно некоторым вариантам осуществления фармацевтически приемлемые соли включают, но не ограничиваются ими, соли присоединения нетоксичной кислоты, которые представляют собой соли аминогруппы, полученные с использованием неорганических кислот, таких как хлороводородная кислота, бромоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или органических кислот, таких как уксусная кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или при помощи других способов, используемых в данной области техники, таких как ионообмен. Согласно некоторым вариантам осуществления фармацевтически приемлемые соли включают, но не ограничиваются ими, адипат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептаноат, гексаноат, гидроиодид, 2-гидроксиэтансульфонат, лактобионат, лактат, лаурат, лаурилсульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, n-толуолсульфонат, ундеканоат, валератную соль и т.д. Типовые соли щелочных или щелочноземельных металлов включают соли натрия, лития, калия, кальция, магния и т.д. Согласно некоторым вариантам осуществления фармацевтически приемлемые соли содержат, если это возможно, нетоксичные катионы аммония, четвертичного аммония и аминов, полученные с использованием противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, алкил, содержащий от 1 до 6 атомов углерода, сульфонат и арилсульфонат.
Пролекарство: В целом, «пролекарство» при использовании в настоящем описании имеет значение, общепринятое в данной области техники, и представляет собой фрагмент, который после введения в организм подвергается метаболизму в организме для доставки указанного активного (например, терапевтического или диагностического) агента. Как правило, указанный метаболизм включает удаление по меньшей мере одного «фрагмента пролекарства», в результате чего образуется активный агент. В данной области техники известны различные формы «пролекарств». Примеры указанных фрагментов пролекарств см. в:
a) Design of Prodrugs, под ред. Н. Bundgaard, (Elsevier, 1985) и Methods in Enzymology, 42:309-396, под ред. K. Widder, et al. (Academic Press, 1985);
b) Prodrugs and Targeted Delivery, под ред. J. Rautio (Wiley, 2011);
c) Prodrugs and Targeted Delivery, под ред. J. Rautio (Wiley, 2011);
d) A Textbook of Drug Design and Development, под ред. Krogsgaard-Larsen;
e) Bundgaard, Глава 5 "Design and Application of Prodrugs", H. Bundgaard, p. 113-191 (1991);
f) Bundgaard, Advanced Drug Delivery Reviews, 8:1-38 (1992);
g) Bundgaard, et al., Journal of Pharmaceutical Sciences, 77:285 (1988); и
h) Kakeya, et al., Chem. Pharm. Bull., 32:692 (1984).
Как и в случае других соединений, описанных в настоящей заявке, пролекарства могут быть обеспечены в любой из ряда форм, например, в кристаллической форме, форме соли и т.д. Согласно некоторым вариантам осуществления пролекарства обеспечены в виде фармацевтически приемлемых солей.
Защитная группа: Термин «защитная группа», используемый в настоящем описании, хорошо известен в данной области техники и включает группы, подробно описанные в Protecting Groups in Organic Synthesis, Т.W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999, содержание которой включено в настоящую заявку во всей полноте посредством ссылки. Также включены защитные группы, специально предназначенные для химии нуклеозидов и нуклеотидов, описанные в Current Protocols in Nucleic Acid Chemistry, под ред. Serge L. Beaucage et al. 06/2012, где содержание Главы 2 включено в настоящую заявку во всей полноте посредством ссылки. Подходящие аминозащитные группы включают метилкарбамат, этилкарбамат, 9-флуоренилметилкарбамат (Fmoc), 9-(2-сульфо)флуоренилметилкарбамат, 9-(2,7-дибром)флуоренилметилкарбамат, 2,7-ди-трет-бутил-[9-(10,10-диоксо-10,10,10,10-тетрагидротиоксантил)]метилкарбамат (DBD-Tmoc), 4-метоксифенацилкарбамат (Phenoc), 2,2,2-трихлорэтилкарбамат (Troc), 2-триметилсилилэтилкарбамат (Теос), 2-фенилэтилкарбамат (hZ), 1-(1-адамантил)-1-метилэтилкарбамат (Adpoc), 1,1-диметил-2-галогенэтилкарбамат, 1,1-диметил-2,2-дибромэтилкарбамат (DB-t-BOC), 1,1-диметил-2,2,2-трихлорэтилкарбамат (ТСВОС), 1-метил-1-(4-бифенил)этилкарбамат (Врос), 1-(3,5-ди-трет-бутилфенил)-1-метилэтилкарбамат (t-Bumeoc), 2-(2'- и 4'-пиридил)этилкарбамат (Руос), 2-(N,N-дициклогексилкарбоксамидо)этилкарбамат, трет-бутилкарбамат (ВОС), 1-адамантилкарбамат (Adoc), винилкарбамат (Voc), аллилкарбамат (Alloc), 1-изопропилаллилкарбамат (Ipaoc), циннамилкарбамат (Сос), 4-нитроциннамилкарбамат (Noc), 8-хинолилкарбамат, N-гидроксипиперидинилкарбамат, алкилдитиокарбамат, бензилкарбамат (Cbz), n-метоксибензилкарбамат (Moz), n-нитробензилкарбамат, n-бромбензилкарбамат, n-хлорбензилкарбамат, 2,4-дихлорбензилкарбамат, 4-метилсульфинилбензилкарбамат (Msz), 9-антрилметилкарбамат, дифенилметилкарбамат, 2-метилтиоэтилкарбамат, 2-метилсульфонилэтилкарбамат, 2-(n-толуолсульфонил)этилкарбамат, [2-(1,3-дитианил)]метилкарбамат (Dmoc), 4-метилтиофенилкарбамат (Mtpc), 2,4-диметилтиофенилкарбамат (Bmpc), 2-фосфониоэтилкарбамат (Реос), 2-трифенилфосфониоизопропилкарбамат (Ррос), 1,1-диметил-2-цианоэтилкарбамат, м-хлор-n-ацилоксибензилкарбамат, n-(дигидроксиборил)бензилкарбамат, 5-бензизоксазолилметилкарбамат, 2-(трифторметил)-6-хромонилметилкарбамат (Tcroc), м-нитрофенилкарбамат, 3,5-диметоксибензилкарбамат, о-нитробензилкарбамат, 3,4-диметокси-6-нитробензилкарбамат, фенил(о-нитрофенил)метилкарбамат, производное фенотиазинил-(10)-карбонила, производное N'-n-толуолсульфониламинокарбонила, производное N'-фениламинотиокарбонила, трет-амилкарбамат, S-бензилтиокарбамат, n-цианобензилкарбамат, циклобутилкарбамат, циклогексилкарбамат, циклопентилкарбамат, циклопропилметилкарбамат, n-децилоксибензилкарбамат, 2,2-диметоксикарбонилвинилкарбамат, o-(N,N-диметилкарбоксамидо)бензилкарбамат, 1,1-диметил-3-(N,N-диметилкарбоксамидо)пропилкарбамат, 1,1-диметилпропинилкарбамат, ди(2-пиридил)метилкарбамат, 2-фуранилметилкарбамат, 2-йодэтилкарбамат, изоборнилкарбамат, изобутилкарбамат, изоникотинилкарбамат, n-(n'-метоксифенилазо)бензилкарбамат, 1-метилциклобутилкарбамат, 1-метилциклогексилкарбамат, 1-метил-1-циклопропилметилкарбамат, 1-метил-1-(3,5-диметоксифенил)этилкарбамат, 1-метил-1-(n-фенилазофенил)этилкарбамат, 1-метил-1-фенилэтилкарбамат, 1-метил-1-(4-пиридил)этилкарбамат, фенилкарбамат, n-(фенилазо)бензилкарбамат, 2,4,6-три-трет-бутилфенилкарбамат, 4-(триметиламмоний)бензилкарбамат, 2,4,6-триметилбензилкарбамат, формамид, ацетамид, хлорацетамид, трихлорацетамид, трифторацетамид, фенилацетамид, 3-фенилпропанамид, пиколинамид, 3-пиридилкарбоксамид, производное N-бензоилфенилаланина, бензамид, n-фенилбензамид, о-нитрофенилацетамид, о-нитрофеноксиацетамид, ацетоацетамид, (N'-дитиобензилоксикарбониламино)ацетамид, 3-(n-гидроксифенил)пропанамид, 3-(о-нитрофенил)пропанамид, 2-метил-2-(о-нитрофенокси)пропанамид, 2-метил-2-(о-фенилазофенокси)пропанамид, 4-хлорбутанамид, 3-метил-3-нитробутанамид, о-нитроциннамид, производное N-ацетилметионина, о-нитробензамид, о-(бензоилоксиметил)бензамид, 4,5-дифенил-3-оксазолин-2-он, N-фталимид, N-дитиасукцинимид (Dts), N,2,3-дифенилмалеимид, N-2,5-диметилпиррол, аддукт N-1,1,4,4-тетраметилдисилилазациклопентана (STABASE), 5-замещенный 1,3-диметил-1,3,5-триазациклогексан-2-он, 5-замещенный 1,3-дибензил-1,3,5-триазациклогексан-2-он, 1-замещенный 3,5-динитро-4-пиридон, N-метиламин, N-аллиламин, N-[2-(триметилсилил)этокси]метиламин (SEM), N-3-ацетоксипропиламин, N-(1-изопропил-4-нитро-2-оксо-3-пирролин-3-ил)амин, четвертичные аммонийные соли, N-бензиламин, N-ди-(4-метоксифенил)метиламин, N-5-дибензосубериламин, N-трифенилметиламин (Tr), N-[(4-метоксифенил)дифенилметил]амин (MMTr), N-9-фенилфлуорениламин (PhF), N-2,7-дихлор-9-флуоренилметиленамин, N-ферроценилметиламино (Fcm), N'-оксид N-2-пиколиламина, N-1,1-диметилтиометиленамин, N-бензилиденамин, N-n-метоксибензилиденамин, N-дифенилметиленамин, N-[(2-пиридил)мезитил]метиленамин, N-(N',N'-диметиламинометилен)амин, N,N'-изопропилиденамин, N-n-нитробензилиденамин, N-салицилиденамин, N-5-хлорсалицилиденамин, N-(5-хлор-2-гидроксифенил)фенилметиленамин, N-циклогексилиденамин, N-(5,5-диметил-3-оксо-1-циклогексенил)амин, производное N-борана, производное N-дифенилбориновой кислоты, N-[фенил(пентакарбонилхром- или вольфрам)карбонил]амин, хелат N-меди, хелат N-цинка, N-нитроамин, N-нитрозамин, N-оксид амина, дифенилфосфинамид (Dpp), диметилтиофосфинамид (Mpt), дифенилтиофосфинамид (Ppt), диалкилфосфорамидаты, дибензилфосфорамидат, дифенилфосфорамидат, бензолсульфенамид, о-нитробензолсульфенамид (Nps), 2,4-динитробензолсульфенамид, пентахлорбензосульфенамид, 2-нитро-4-метоксибензолсульфенамид, трифенилметилсульфенамид, 3-нитропиридинсульфенамид (Npys), n-толуолсульфонамид (Ts), бензолсульфонамид, 2,3,6-триметил-4-метоксибензолсульфонамид (Mtr), 2,4,6-триметоксибензолсульфонамид (Mtb), 2,6-диметил-4-метоксибензолсульфонамид (Pme), 2,3,5,6-тетраметил-4-метоксибензолсульфонамид (Mte), 4-метоксибензолсульфонамид (Mbs), 2,4,6-триметилбензолсульфонамид (Mts), 2,6-диметокси-4-метилбензолсульфонамид (iMds), 2,2,5,7,8-пентаметилхроман-6-сульфонамид (Pmc) метансульфонамид (Ms), β-триметилсилилэтансульфонамид (SES), 9-антраценсульфонамид, 4-(4',8'-диметоксинафтилметил)бензолсульфонамид (DNMBS), бензилсульфонамид, трифторметилсульфонамид и фенацилсульфонамид.
Подходящие защищенные карбоновые кислоты дополнительно включают, но не ограничиваются ими, силил-, алкил-, алкенил-, арил- и арилалкил-защищенные карбоновые кислоты. Примеры подходящих силильных групп включают триметилсилил, триэтилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, триизопропилсилил и т.д. Примеры подходящих алкильных групп включают метил, бензил, п-метоксибензил, 3,4-диметоксибензил, тритил, трет-бутил, тетрагидропиран-2-ил. Примеры подходящих алкенильных групп включают аллил. Примеры подходящих арильных групп включают необязательно замещенный фенил, бифенил или нафтил. Примеры подходящих аралкильных групп включают необязательно замещенный бензил (например, п-метоксибензил (МРМ), 3,4-диметоксибензил, О-нитробензил, п-нитробензил, п-галогенбензил, 2,6-дихлорбензил, п-цианобензил) и 2- и 4-пиколил.
Подходящие гидроксил-защитные группы включают метил, метоксиметил (MOM), метилтиометил (МТМ), трет-бутилтиометил, (фенилдиметилсилил)метоксиметил (SMOM), бензилоксиметил (ВОМ), n-метоксибензилоксиметил (РМВМ), (4-метоксифенокси)метил (р-АОМ), гваяколметил (GUM), трет-бутоксиметил, 4-пентенилоксиметил (РОМ), силоксиметил, 2-метоксиэтоксиметил (MEM), 2,2,2-трихлорэтоксиметил, бис(2-хлорэтокси)метил, 2-(триметилсилил)этоксиметил (SEMOR), тетрагидропиранил (ТНР), 3-бромтетрагидропиранил, тетрагидротиопиранил, 1-метоксициклогексил, 4-метокситетрагидропиранил (МТНР), 4-метокситетрагидротиопиранил, S,S-диоксид 4-метокситетрагидротиопиранила, 1-[(2-хлор-4-метил)фенил]-4-метоксипиридин-4-ил (СТМР), 1,4-диоксан-2-ил, тетрагидрофуранил, тетрагидротиофуранил, 2,3,3а,4,5,6,7,7а-октагидро-7,8,8-триметил-4,7-метанобензофуран-2-ил, 1-этоксиэтил, 1-(2-хлорэтокси)этил, 1-метил-1-метоксиэтил, 1-метил-1-бензилоксиэтил, 1-метил-1-бензилокси-2-фторэтил, 2,2,2-трихлорэтил, 2-триметилсилилэтил, 2-(фенилселенил)этил, трет-бутил, аллил, n-хлорфенил, n-метоксифенил, 2,4-динитрофенил, бензил, n-метоксибензил, 3,4-диметоксибензил, о-нитробензил, n-нитробензил, n-галогенбензил, 2,6-дихлорбензил, n-цианобензил, n-фенилбензил, 2-пиколил, 4-пиколил, N-оксид 3-метил-2-пиколила, дифенилметил, n,n'-динитробензгидрил, 5-дибензосуберил, трифенилметил, α-нафтилдифенилметил, n-метоксифенилдифенилметил, ди(n-метоксифенил)фенилметил, три(n-метоксифенил)метил, 4-(4'-бромфенацилоксифенил)дифенилметил, 4,4',4''-трис(4,5-дихлорфталимидофенил)метил, 4,4',4''-трис(левулиноилоксифенил)метил, 4,4',4''-трис(бензоилоксифенил)метил, 3-(имидазол-1-ил)-бис(4',4''-диметоксифенил)метил, 1,1-бис(4-метоксифенил)-1'-пиренилметил, 9-антрил, 9-(9-фенил)ксантенил, 9-(9-фенил-10-оксо)антрил, 1,3-бензодитиолан-2-ил, S,S-диоксид бензиодиазолила, триметилсилил (TMS), триэтилсилил (TES), триизопропилсилил (TIPS), диметилизопропилсилил (IPDMS), диэтилизопропилсилил (DEIPS), диметилгексилсилил, трет-бутилдиметилсилил (TBDMS), трет-бутилдифенилсилил (TBDPS), трибензилсилил, три-n-ксилилсилил, трифенилсилил, дифенилметилсилил (DPMS), трет-бутилметоксифенилсилил (TBMPS), формиат, бензоилформиат, ацетат, хлорацетат, дихлорацетат, трихлорацетат, трифторацетат, метоксиацетат, трифенилметоксиацетат, феноксиацетат, n-хлорфеноксиацетат, 3-фенил пропионат, 4-оксопентаноат (левулинат), 4,4-(этилендитио)пентаноат (левулиноилдитиоацеталь), пивалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, n-фенилбензоат, 2,4,6-триметилбензоат (мезитоат), алкилметилкарбонат, 9-флуоренилметилкарбонат (Fmoc), алкилэтилкарбонат, алкил-2,2,2-трихлорэтилкарбонат (Troc), 2-(триметилсилил)этилкарбонат (TMSEC), 2-(фенилсульфонил)этилкарбонат (Psec), 2-(трифенилфосфонио)этилкарбонат (Реос), алкилизобутилкарбонат, алкилвинилкарбонат, алкилаллилкарбонат, алкил-n-нитрофенилкарбонат, алкилбензилкарбонат, алкил-n-метоксибензилкарбонат, алкил-3,4-диметоксибензилкарбонат, алкил-о-нитробензилкарбонат, алкил-n-нитробензилкарбонат, алкил-S-бензилтиокарбонат, 4-этокси-1-нафтилкарбонат, метилдитиокарбонат, 2-йодбензоат, 4-азидобутират, 4-нитро-4-метилпентаноат, о-(дибромметил)бензоат, 2-формилбензолсульфонат, 2-(метилтиометокси)этил, 4-(метилтиометокси)бутират, 2-(метилтиометоксиметил)бензоат, 2,6-дихлор-4-метилфеноксиацетат, 2,6-дихлор-4-(1,1,3,3-тетраметилбутил)феноксиацетат, 2,4-бис(1,1-диметилпропил)феноксиацетат, хлордифенилацетат, изобутират, моносукцинат, (E)-2-метил-2-бутеноат, о-(метоксикарбонил)бензоат, α-нафтоат, нитрат, алкил-N,N,N',N'-тетраметилфосфордиамидат, алкил-N-фенилкарбамат, борат, диметилфосфинотиоил, алкил-2,4-динитрофенилсульфенат, сульфат, метансульфонат (мезилат), бензилсульфонат и тозилат (Ts). Защитные группы для защиты 1,2- или 1,3-диолов включают метиленацеталь, этилиденацеталь, 1-трет-бутилэтилиденкеталь, 1-фенилэтилиденкеталь, (4-метоксифенил)этилиденацеталь, 2,2,2-трихлорэтилиденацеталь, ацетонид, циклопентилиденкеталь, циклогексилиденкеталь, циклогептилиденкеталь, бензилиденацеталь, n-метоксибензилиденацеталь, 2,4-диметоксибензилиденкеталь, 3,4-диметоксибензилиденацеталь, 2-нитробензилиденацеталь, метоксиметиленацеталь, этоксиметиленацеталь, сложный ортоэфир диметоксиметилена, сложный ортоэфир 1-метоксиэтилидена, сложный ортоэфир 1-этоксиэтилидена, сложный ортоэфир 1,2-диметоксиэтилидена, сложный ортоэфир α-метоксибензилидена, производное 1-(N,N-диметиламино)этилидена, производное α-(N,N'-диметиламино)бензилидена, сложный ортоэфир 2-оксациклопентилидена, ди-трет-бутилсилиленовую группу (DTBS), производное 1,3-(1,1,3,3-тетраизопропилдисилоксанилидена) (TIPDS), производное тетра-трет-бутоксидисилоксан-1,3-диилидена (TBDS), циклические карбонаты, циклические боронаты, этилборонат и фенилборонат.
Согласно некоторым вариантам осуществления гидроксилзащитная группа представляет собой ацетил, трет-бутил, трет-бутоксиметил, метоксиметил, тетрагидропиранил, 1-этоксиэтил, 1-(2-хлорэтокси)этил, 2-триметилсилилэтил, п-хлорфенил, 2,4-динитрофенил, бензил, бензоил, п-фенилбензоил, 2,6-дихлорбензил, дифенилметил, п-нитробензил, трифенилметил (тритил), 4,4'-диметокситритил, триметилсилил, триэтилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, трифенилсилил, триизопропилсилил, бензоилформиат, хлорацетил, трихлорацетил, трифторацетил, пивалоил, 9-флуоренилметилкарбонат, мезилат, тозилат, трифлат, тритил, монометокситритил (MMTr), 4,4'-диметокситритил (DMTr) и 4,4',4''-триметокситритил (TMTr), 2-цианоэтил (СЕ или Cne), 2-(триметилсилил)этил (TSE), 2-(2-нитрофенил)этил, 2-(4-цианофенил)этил, 2-(4-нитрофенил)этил (NPE), 2-(4-нитрофенилсульфонил)этил, 3,5-дихлорфенил, 2,4-диметилфенил, 2-нитрофенил, 4-нитрофенил, 2,4,6-триметилфенил, 2-(2-нитрофенил)этил, бутилтиокарбонил, 4,4',4''-трис(бензоилокси)тритил, дифенилкарбамоил, левулинил, 2-(дибромметил)бензоил (Dbmb), 2-(изопропилтиометоксиметил)бензоил (Ptmt), 9-фенилксантен-9-ил (пиксил) или 9-(п-метоксифенил)ксантин-9-ил (МОХ). Согласно некоторым вариантам осуществления каждая из гидроксил-защитных групп независимо выбрана из ацетила, бензила, трет-бутилдиметилсилила, трет-бутилдифенилсилила и 4,4'-диметокситритила. Согласно некоторым вариантам осуществления гидроксил-защитная группа выбрана из группы, состоящей из тритила, монометокситритила и 4,4'-диметокситритильной группы.
Согласно некоторым вариантам осуществления фосфор-защитная группа представляет собой группу, присоединенную к межнуклеотидной фосфорсодержащей линкерной группе во время синтеза олигонуклеотида. Согласно некоторым вариантам осуществления фосфор-защитная группа присоединена к атому серы межнуклеотидной фосфоротиоатной линкерной группы. Согласно некоторым вариантам осуществления фосфор-защитная группа присоединена к атому кислорода межнуклеотидной фосфоротиоатной линкерной группы. Согласно некоторым вариантам осуществления фосфор-защитная группа присоединена к атому кислорода межнуклеотидной фосфатной линкерной группы. Согласно некоторым вариантам осуществления фосфор-защитная группа представляет собой 2-цианоэтил (СЕ или Cne), 2-триметилсилилэтил, 2-нитроэтил, 2-сульфонилэтил, метил, бензил, о-нитробензил, 2-(n-нитрофенил)этил (NPE или Npe), 2-фенилэтил, 3-(трет-бутилкарбоксамидо)-1-пропил, 4-оксопентил, 4-метилтио-l-бутил, 2-циано-1,1-диметилэтил, 4-N-метиламинобутил, 3-(2-пиридил)-1-пропил, 2-[N-метил-N-(2-пиридил)]аминоэтил, 2-(N-формил,N-метил)аминоэтил, 4-[N-метил-N-(2,2,2-трифторацетил)амино]бутил.
Белок: Используемый в настоящем описании термин «белок» относится к полипептиду (т.е. к последовательности по меньшей мере двух аминокислот, связанных друг с другом пептидными связями). Согласно некоторым вариантам осуществления белки включают только природные аминокислоты. Согласно некоторым вариантам осуществления белки включают одну или более аминокислот, не содержащихся в природе (например, фрагментов, образующих одну или более пептидных линкерных групп с соседними аминокислотами). Согласно некоторым вариантам осуществления один или более остатков в белковой цепи содержит фрагмент, отличный от аминокислоты (например, гликан и т.д.). Согласно некоторым вариантам осуществления белок содержит более одной полипептидной цепи, например, связанных при помощи одной или более дисульфидных линкерных групп или ассоциированных другим образом. Согласно некоторым вариантам осуществления белки содержат L-аминокислоты, D-аминокислоты или оба вида аминокислот; согласно некоторым вариантам осуществления белки содержат одну или более модификаций или аналогов аминокислот, известных в данной области техники. Подходящие модификации включают, например, ацетилирование, амидирование, метилирование терминальной группы и т.д. Термин «пептид», в целом, используют для описания полипептида, имеющего длину менее чем примерно 100 аминокислот, менее чем примерно 50 аминокислот, менее 20 аминокислот или менее 10 аминокислот. Согласно некоторым вариантам осуществления белки представляют собой антитела, фрагменты антител, биологически активные фрагменты антител и/или характеристические фрагменты антител.
Образец: Используемый в настоящем описании термин «образец» представляет собой специфический организм или полученный из него материал. Согласно некоторым вариантам осуществления образец представляет собой биологический образец, полученный или выделенный из исследуемого источника, описанного в настоящей заявке. Согласно некоторым вариантам осуществления исследуемый источник включает организм, такой как животное или человек. Согласно некоторым вариантам осуществления биологический образец содержит биологическую ткань или жидкую среду. Согласно некоторым вариантам осуществления биологический образец представляет собой или содержит одно или более из следующего: костный мозг; кровь; кровяные клетки; асциты; образцы ткани или тонкоигольной биопсии; биологические жидкости, содержащие клетки; свободные нуклеиновые кислоты; мокроту; слюну; мочу; спинномозговую жидкость, перитонеальную жидкость; плевральную жидкость; кал; лимфу; гинекологические жидкости; мазки с кожи; вагинальные мазки; мазки из полости рта; мазки из носа; промывки или лаважи, такие как дуктальный лаваж или бронхоальвеолярный лаваж; пунктаты; соскобы; образцы костного мозга; образцы биопсии тканей; хирургические образцы; кал, другие биологические жидкости, секреты и/или выделения; и/или содержащиеся в них клетки и т.д. Согласно некоторым вариантам осуществления биологический образец представляет собой или содержит клетки, полученные у индивидуума. Согласно некоторым вариантам осуществления образец представляет собой «первичный образец», полученный непосредственно из исследуемого источника при помощи подходящего способа. Например, согласно некоторым вариантам осуществления первичный биологический образец получают при помощи способов, выбранных из группы, состоящей из биопсии (например, тонкоигольной аспирационной биопсии или биопсии ткани), хирургии, отбора биологической жидкости (например, крови, лимфы, кала и т.д.) и т.д. Согласно некоторым вариантам осуществления, что будет очевидно из контекста, термин «образец» относится к препарату, полученному путем обработки (например, путем удаления одного или более компонентов и/или путем добавления одного или более агентов) первичного образца. Например, используют фильтрование через полупроницаемую мембрану. Указанный «обработанный образец» может содержать, например, нуклеиновые кислоты или белки, экстрагированные из образца, или полученные путем обработки первичного образца при помощи способов, таких как амплификация или обратная транскрипция мРНК, выделение и/или очистка определенных компонентов и т.д. Согласно некоторым вариантам осуществления образец представляет собой организм. Согласно некоторым вариантам осуществления образец представляет собой растение. Согласно некоторым вариантам осуществления образец представляет собой животное. Согласно некоторым вариантам осуществления образец представляет собой человека. Согласно некоторым вариантам осуществления образец представляет собой отличный от человеческого организм.
Стереохимически изомерные формы: Фраза «стереохимически изомерные формы», используемая в настоящем описании, относится к различным соединениям, полученным из одинаковых атомов, связанных при помощи одной последовательности линкерных групп, но имеющих различные трехмерные структуры, которые не являются взаимозаменяемыми. Согласно некоторым вариантам осуществления раскрытия предложенные химические композиции могут представлять собой или содержать чистые препараты отдельных стереохимически изомерных форм соединения; согласно некоторым вариантам осуществления предложенные химические композиции могут представлять собой или содержать смеси двух или более стереохимически изомерных форм соединения. В определенных вариантах реализации указанные смеси содержат равные количества различных стереохимически изомерных форм; в определенных вариантах реализации указанные смеси содержат различные количества по меньшей мере двух различных стереохимически изомерных форм. Согласно некоторым вариантам осуществления химическая композиция может содержать все диастереомеры и/или энантиомеры соединения. Согласно некоторым вариантам осуществления химическая композиция может содержать не все диастереомеры и/или энантиомеры соединения. Согласно некоторым вариантам осуществления, если конкретный энантиомер соединения согласно настоящему раскрытию является желательным, его можно получать, например, при помощи асимметрического синтеза, или путем превращения с использованием хирального вспомогательного вещества, где разделяют полученную диастереомерную смесь и проводят отщепление вспомогательной группы с получением чистых целевых энантиомеров. В качестве альтернативы, если молекула содержит основную функциональную группу, такую как аминогруппа, получают диастереомерные соли с использованием подходящей оптически-активной кислоты и проводят разделение, например, путем фракционной кристаллизации.
Субъект: Используемый в настоящем описании термин «субъект» или «исследуемый субъект» относится к любому организму, которому вводят предложенное соединение или композицию согласно настоящему раскрытию, например, в экспериментальных, диагностических, профилактических и/или терапевтических целях. Типовые субъекты включают животных (например, млекопитающих, таких как мыши, крысы, кролики, приматы, отличные от человека, и человек; насекомых; червей и т.д.) и растения. Согласно некоторым вариантам осуществления субъект может страдать и/или быть подверженным заболеванию, нарушению и/или состоянию.
По существу: Используемый в настоящем описании термин «по существу» относится к качественному описанию, заключающемуся в проявлении полного или практически полного уровня или степени рассматриваемой характеристики или свойства. Специалистам в области биологии будет понятно, что биологические и химические явления редко, если это вообще когда-либо происходит, проходят до конца и/или протекают полностью или обеспечивают абсолютный результат или его полное отсутствие. Термин «по существу», таким образом, используют в настоящем описании для учета возможной незавершенности, присущей многим биологическим и/или химическим явлениям.
Страдающий от: У индивидуума, который «страдает от» заболевания, нарушения и/или состояния, были диагностированы и/или проявились один или более симптомов заболевания, нарушения и/или состояния.
Подверженный: Индивидуум, который «подвержен» заболеванию, нарушению и/или состоянию, представляет собой индивидуума, у которого существует повышенный риск развития заболевания, нарушения и/или состояния по сравнению с обычным членом общества. Согласно некоторым вариантам осуществления у индивидуума, который подвержен заболеванию, нарушению и/или состоянию, заболевание, нарушение и/или состояние может быть и не диагностировано. Согласно некоторым вариантам осуществления у индивидуума, который подвержен заболеванию, нарушению и/или состоянию, могут проявляться симптомы заболевания, нарушения и/или состояния. Согласно некоторым вариантам осуществления у индивидуума, который подвержен заболеванию, нарушению и/или состоянию, могут отсутствовать симптомы заболевания, нарушения и/или состояния. Согласно некоторым вариантам осуществления у индивидуума, который подвержен заболеванию, нарушению и/или состоянию, развивается заболевание, нарушение и/или состояние. Согласно некоторым вариантам осуществления у индивидуума, который подвержен заболеванию, нарушению и/или состоянию, не развивается заболевание, нарушение и/или состояние.
Системный: Фразы «системное введение», «вводимый системно», «периферическое введение» и «вводимый периферически», используемые в настоящем описании, имеют общепринятое значение и относятся к введению соединения или композиции, при котором они попадают в организм потребителя.
Таутомерные формы: Фразу «таутомерные формы» согласно настоящей заявке используют для описания различных изомерных форм органических соединений, которые могут легко превращаться друг в друга. Таутомеры могут быть охарактеризованы формальной миграцией атома водорода или протона, сопровождающейся смещением простой связи и соседней двойной связи. Согласно некоторым вариантам осуществления таутомеры могут возникать в результате прототропной таутомерии (т.е. перемещения протона). Согласно некоторым вариантам осуществления таутомеры могут возникать в результате валентной таутомерии (т.е. быстрого перераспределения связывающих электронов). Предполагается, что все указанные таутомерные формы включены в объем настоящего раскрытия. Согласно некоторым вариантам осуществления таутомерные формы соединения существуют в мольном равновесии друг с другом, и поэтому попытки получения отдельных веществ приводят к образованию смеси. Согласно некоторым вариантам осуществления таутомерные формы соединения представляют собой соединения, которые можно разделять и выделять. Согласно некоторым вариантам осуществления раскрытия можно обеспечивать химические композиции, которые представляют собой или содержат чистые препараты отдельной таутомерной формы соединения. Согласно некоторым вариантам осуществления раскрытия можно обеспечивать химические композиции в виде смесей двух или более таутомерных форм соединения. В определенных вариантах реализации указанные смеси содержат равные количества различных таутомерных форм; в определенных вариантах реализации указанные смеси содержат разные количества по меньшей мере двух различных таутомерных форм соединения. Согласно некоторым вариантам осуществления раскрытия химические композиции могут содержать все таутомерные формы соединения. Согласно некоторым вариантам осуществления изобретения химические композиции могут содержать не все таутомерные формы соединения. Согласно некоторым вариантам осуществления изобретения химические композиции могут содержать одну или более таутомерных форм соединения в количествах, различающихся в разные моменты времени из-за взаимного превращения. Согласно некоторым вариантам осуществления раскрытия таутомерия представляет собой кето-енольную таутомерию. Специалистам в области химии должно быть понятно, что кето-енольный таутомер можно «захватывать» (т.е. химически модифицировать таким образом, чтобы он оставался в «енольной» форме) при помощи любого подходящего реагента, известного в области химии, для обеспечения енольного производного, которое впоследствии можно выделять при помощи одного или более подходящих способов, известных в данной области техники. Если не указано иное, настоящее раскрытие охватывает все таутомерные формы важных соединений, как в чистом виде, так и в виде смесей друг с другом.
Терапевтический агент: Используемая в настоящем описании фраза «терапевтический агент» относится к любому агенту, который после введения субъекту, оказывает терапевтическое действие и/или обеспечивает желаемое биологическое и/или фармакологическое действие. Согласно некоторым вариантам осуществления терапевтический агент представляет собой любое вещество, которое можно применять для облегчения, ослабления, снижения, подавления, предотвращения, задержки проявления, снижения степени тяжести и/или уменьшения проявления одного или более симптомов или отличительных признаков заболевания, нарушения и/или состояния.
Терапевтически эффективное количество: Используемый в настоящем описании термин «терапевтически эффективное количество» обозначает количество вещества (например, терапевтического агента, композиции и/или состава), обеспечивающее желаемый биологический ответ после введения согласно схеме лечения. Согласно некоторым вариантам осуществления терапевтически эффективное количество вещества представляет собой количество, которое после введения субъекту, страдающему или подверженному заболеванию, нарушению и/или состоянию, является достаточным для лечения, диагностики, предотвращения и/или задержки проявления заболевания, нарушения и/или состояния. Специалистам в данной области техники должно быть понятно, что эффективное количество вещества может быть различным в зависимости от таких факторов, как желаемый биологический конечный результат, доставляемое вещество, целевая клетка или ткань и т.д. Например, количество соединения в составе, которое является эффективным для лечения заболевания, нарушения и/или состояния, представляет собой количество, которое облегчает, ослабляет, снижает, подавляет, предотвращает, задерживает проявление, снижает тяжесть и/или снижает частоту проявления одного или более симптомов или отличительных признаков заболевания, нарушения и/или состояния. Согласно некоторым вариантам осуществления терапевтически эффективное количество вводят в виде одной дозы; согласно некоторым вариантам осуществления для доставки терапевтически эффективного количества требуется несколько стандартных доз.
Лечение: Используемый в настоящем описании термин «лечить», «лечение» или «излечить» относится к способу, используемому для частичного или полного облегчения, ослабления, снижения, подавления, предотвращения, задержки проявления, снижения степени тяжести и/или уменьшения частоты проявления одного или более симптомов или отличительных признаков заболевания, нарушения и/или состояния. Лечение можно проводить субъекту, у которого отсутствуют признаки заболевания, нарушения и/или состояния. Согласно некоторым вариантам осуществления лечение можно проводить субъекту, у которого присутствуют только ранние признаки заболевания, нарушения и/или состояния, например, для уменьшения риска развития патологии, связанной с заболеванием, нарушением и/или состоянием.
Ненасыщенный: Термин «ненасыщенный», используемый в настоящем описании, означает, что фрагмент содержит один или более ненасыщенных участков.
Стандартная доза: Выражение «стандартная доза», используемое в настоящем описании, относится к количеству, вводимому в виде одной дозы, и/или к физически дискретной частице, содержащей фармацевтическую композицию. Во многих вариантах реализации стандартная доза содержит предварительно определенное количество активного агента. Согласно некоторым вариантам осуществления стандартная доза содержит полную дозу агента. Согласно некоторым вариантам осуществления для обеспечения полной дозы вводят более чем одну стандартную дозу. Согласно некоторым вариантам осуществления для достижения предполагаемого действия требуется или предполагается введение нескольких стандартных доз. Стандартная доза, например, может содержаться в объеме жидкости (например, приемлемого носителя), содержащем предварительно определенное количество одного или более терапевтических агентов, предварительно определенное количество одного или более терапевтических агентов в твердом виде, состав с замедленным высвобождением или устройство доставки лекарственного агента, содержащее предварительно определенное количество одного или более терапевтических агентов, и т.д. Следует понимать, что стандартная доза может содержаться в составе, содержащем ряд компонентов помимо терапевтического(их) агента(ов). Например, согласно приведенному ниже описанию могут содержаться приемлемые носители (например, фармацевтически приемлемые носители), разбавители, стабилизаторы, буферы, консерванты и т.д. Специалистам в данной области техники должно быть понятно, что во многих вариантах реализации общая подходящая дневная дозировка конкретного терапевтического агента может содержать часть или совокупность стандартных доз и может определяться, например, лечащим врачом, по результатам тщательного медицинского обследования. Согласно некоторым вариантам осуществления конкретная эффективная дозировка для любого конкретного субъекта или организма может зависеть от ряда факторов, включая нарушение, подвергающееся лечению, и тяжесть нарушения; активность конкретного используемого активного соединения; конкретную используемую композицию; возраст, массу тела, общее состояние здоровья, пол и рацион субъекта; время введения и скорость выведения конкретного используемого активного соединения; продолжительность лечения; лекарственные агенты и/или дополнительные способы лечения, используемые в комбинации или совместно с конкретным(и) используемым(и) соединением(ями), и схожие факторы, хорошо известные в области медицины.
Дикий тип: Используемый в настоящем описании термин «дикий тип» имеет общепринятое значение и относится к элементу, имеющему структуру и/или активность такую же, что существует в природе в «нормальном» (в противоположность мутантному, подверженному болезни, измененному и т.д.) состоянии или контексте. Специалистам в данной области техники должно быть понятно, что гены и полипептиды дикого типа часто существуют во множестве различных форм (например, аллелей).
Нуклеиновая кислота: Термин «нуклеиновая кислота» включает любые нуклеотиды, их модифицированные варианты, их аналоги и полимеры. Термин «полинуклеотид», используемый в настоящем описании, относится к полимерной форме нуклеотидов любой длины, как к рибонуклеотидам (РНК), так и к дезоксирибонуклеотидам (ДНК) их модифицированным вариантам или аналогам. Указанные термины относятся к первичной структуре молекул и, таким образом, включают двух- и одноцепочечные ДНК и двух- и одноцепочечные РНК. Указанные термины включают в качестве эквивалентов аналоги РНК или ДНК, полученные из аналогов нуклеотидов и модифицированных полинуклеотидов, включая, но не ограничиваясь ими, метилированные, защищенные и/или кэппированные нуклеотиды или полинуклеотиды. Термины охватывают поли- или олигорибонуклеотиды (РНК) или поли- или олигодезоксирибонуклеотиды (ДНК); РНК или ДНК, полученные из N-гликозидов или С-гликозидов нуклеиновых оснований и/или модифицированных нуклеиновых оснований; нуклеиновые кислоты, полученные из сахаров и/или модифицированных сахаров; и нуклеиновые кислоты, полученные из фосфатных мостиковых групп и/или модифицированных мостиковых групп с атомом фосфора (также называемых в настоящем описании «межнуклеотидные линкерные группы»). Термин охватывает нуклеиновые кислоты, содержащие любые комбинации нуклеиновых оснований, модифицированных нуклеиновых оснований, сахаров, модифицированных сахаров, фосфатных мостиковых групп или мостиковых групп с модифицированным атомом фосфора. Примеры включают, но не ограничиваются ими, нуклеиновые кислоты, содержащие фрагменты рибозы, нуклеиновые кислоты, содержащие фрагменты дезоксирибозы, нуклеиновые кислоты, содержащие фрагменты рибозы и дезоксирибозы, нуклеиновые кислоты, содержащие фрагменты рибозы и модифицированной рибозы. Префикс поли- относится к нуклеиновой кислоте, содержащей от 2 до примерно 10000 мономерных нуклеотидных звеньев, а префикс олиго- относится к нуклеиновой кислоте, содержащей от 2 до примерно 200 мономерных нуклеотидных звеньев.
Нуклеотид: Термин «нуклеотид», используемый в настоящем описании, относится к мономерному звену полинуклеотида, которое состоит из гетероциклического основания, саха ра и одной или более фосфатных групп или фосфорсодержащих межнуклеотидных линкерных групп. Природные основания (гуанин (G), аденин (А), цитозин (С), тимин (Т) и урацил (U)) являются производными пурина или пиримидина, несмотря на это, следует понимать, что включены природные и не существующие в природе аналоги оснований. Природными сахарами являются пентоза (пятичленный сахар), дезоксирибоза (из которой образуется ДНК) или рибоза (из которой образуется РНК), несмотря на это, следует понимать, что включены природные и не существующие в природе аналоги сахаров. Нуклеотиды связаны посредством межнуклеотидных линкерных групп с образованием нуклеиновых кислот или полинуклеотидов. В данной области техники известно множество межнуклеотидных линкерных групп (включая, но не ограничиваясь ими, фосфаты, фосфоротиоаты, боранофосфаты и т.д.). Искусственные нуклеиновые кислоты включают ПНК (пептидонуклеиновые кислоты), фосфотриэфиры, фосфоротионаты, H-фосфонаты, фосфорамидаты, боранофосфаты, метилфосфонаты, фосфоноацетаты, тиофосфоноацетаты и другие варианты фосфатного остова естественных нуклеиновых кислот, таких как те, что описаны в настоящей заявке. Другие аналоги (например, искусственные нуклеиновые кислоты или компоненты, которые могут быть включены в нуклеиновую кислоту или искусственную нуклеиновую кислоту) включают: боранофосфатную РНК, FANA, запертые нуклеиновые кислоты (LNA), морфолинозы, пептидные нуклеиновые кислоты (PNA), треозо-нуклеиновую кислоту (TNA) и гликольнуклеиновую кислоту (GNA). Специалистам в данной области известно множество модифицированных нуклеотидов или нуклеотидных аналогов, включая, например, те, которые описаны в любом из: Gryaznov, S; Chen, J.-K. J. Am. Chem. Soc. 1994, 116, 3143; Hendrix etal. 1997 Chem. Eur. J. 3: 110; Hyrup et al. 1996 Bioorg. Med. Chem. 4: 5; Jepsen et al. 2004 Oligo. 14: 130-146; Jones et al. J. Org. Chem. 1993, 58, 2983; Koizumi et al. 2003 Nuc. Acids Res. 12: 3267-3273; Koshkin et al. 1998 Tetrahedron 54: 3607-3630; Kumar et al. 1998 Bioo. Med. Chem. Let. 8: 2219-2222; Lauritsen et al. 2002 Chem. Comm. 5: 530-531; Lauritsen et al. 2003 Bioo. Med. Chem. Lett. 13: 253-256; Mesmaeker et al. Angew. Chem., Int. Ed. Engl. 1994, 33, 226; Morita et al. 2001 Nucl. Acids Res. Supp.1: 241-242; Morita et al. 2002 Bioo. Med. Chem. Lett. 12: 73-76; Morita et al. 2003 Bioo. Med. Chem. Lett. 2211-2226; Nielsen et al. 1997 Chem. Soc. Rev. 73; Nielsen et al. 1997 J. Chem. Soc. Perkins Transl. 1: 3423-3433; Obika et al. 1997 Tetrahedron Lett. 38 (50): 8735-8; Obika et al. 1998 Tetrahedron Lett. 39: 5401-5404; Pallan et al. 2012 Chem. Comm. 48: 8195-8197; Petersen et al. 2003 TRENDS Biotech. 21: 74-81; Rajwanshi et al. 1999 Chem. Commun. 1395-1396; Schultz et al. 1996 Nucleic Acids Res. 24: 2966; Seth et al. 2009 J. Med. Chem. 52: 10-13; Seth et al. 2010 J. Med. Chem. 53: 8309-8318; Seth et al. 2010 J. Org. Chem. 75: 1569-1581; Seth et al. 2012 Bioo. Med. Chem. Lett. 22: 296-299; Seth et al. 2012 Mol. Ther-Nuc. Acids. 1, e47; Seth, Punit P; Siwkowski, Andrew; Allerson, Charles R; Vasquez, Guillermo; Lee, Sam; Prakash, Thazha P; Kinberger, Garth; Migawa, Michael T; Gaus, Hans; Bhat, Balkrishen; et al. From Nucleic Acids Symposium Series (2008), 52(1), 553-554; Singh et al. 1998 Chem. Comm. 1247-1248; Singh et al. 1998 J. Org. Chem. 63: 10035-39; Singh et al. 1998 J. Org. Chem. 63: 6078-6079; Sorensen 2003 Chem. Comm. 2130-2131; Ts'o et al. Ann. N. Y. Acad. Sci. 1988, 507, 220; Van Aerschot et al. 1995 Angew. Chem. Int. Ed. Engl. 34: 1338; Vasseur et al. J. Am. Chem. Soc. 1992, 114, 4006; публикациях международных заявок WO 20070900071; WO 20070900071 или WO 2016/079181.
Нуклеозид: Термин «нуклеозид» относится к фрагменту, где нуклеиновое основание или модифицированное нуклеиновое основание ковалентно связано с сахаром или модифицированным сахаром.
Сахар: Термин «сахар» относится к моносахариду в закрытой и/или открытой форме. Сахара включают, но не ограничиваются ими, рибозу, дезоксирибозу, пентофуранозу, пентопиранозу и гексопиранозу. Используемый в настоящем описании термин также охватывает структурные аналоги, используемые вместо традиционных фрагментов сахаров, такие как гликоль, полимер которого образует остов аналога нуклеиновой кислоты, гликольнуклеиновую кислоту (ГлНК).
Модифицированный сахар: Термин «модифицированный сахар» относится к фрагменту, который может заменять сахар. В модифицированном сахаре имитируются пространственное расположение, электронные свойства или некоторые другие физико-химические свойства сахара.
Нуклеиновое основание: Термин «нуклеиновое основание» относится к фрагментам нуклеиновых кислот, участвующим в образовании водородных линкерных групп, которые связывают одну последовательность нуклеиновых кислот с другой комплементарной последовательностью последовательно-специфическим образом. Наиболее распространенными природными нуклеиновыми основаниями являются аденин (А), гуанин (G), урацил (U), цитозин (С) и тимин (Т). Согласно некоторым вариантам осуществления природные нуклеиновые основания представляют собой модифицированный аденин, гуанин, урацил, цитозин или тимин. Согласно некоторым вариантам осуществления природные нуклеиновые основания представляют собой метилированный аденин, гуанин, урацил, цитозин или тимин. Согласно некоторым вариантам осуществления нуклеиновое основание нуклеиновое основание представляет собой «модифицированное нуклеиновое основание», например, нуклеиновое основание, отличающееся от аденина (А), гуанина (G), урацила (U), цитозина (С) и тимина (Т). Согласно некоторым вариантам осуществления модифицированные нуклеиновые основания представляют собой метилированный аденин, гуанин, урацил, цитозин или тимин. Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание имитирует пространственное расположение, электронные свойства или некоторые другие физико-химические свойства нуклеиновых оснований и сохраняет свойство образования водородных линкерных групп, которые соединяют одну последовательность нуклеиновых кислот с другой последовательно-специфическим образом. Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание может образовывать пару со всеми пятью природными основаниями (урацилом, тимином, аденином, цитозином или гуанином), по существу не влияя на характеристики плавления, распознавание внутриклеточными ферментами или активность дуплекса олигонуклеотидов.
Хиралъный лиганд: Термин «хиральный лиганд» или «хиральное вспомогательное вещество» относится к фрагменту, который является хиральным и который можно использовать для взаимодействия, в результате чего взаимодействие можно проводить с определенной стереоселективностью.
Агент конденсации: При реакции конденсации термин «агент конденсации» относится к реагенту, который активирует менее активный участок и делает его более чувствительным к воздействию другого реагента. Согласно некоторым вариантам осуществления указанный другой реагент представляет собой нуклеофил.
Блокирующая группа: Термин «блокирующая группа» относится к группе, которая маскирует активность функциональной группы. Впоследствии можно удалять маскировку функциональной группы путем удаления блокирующей группы. Согласно некоторым вариантам осуществления блокирующая группа представляет собой защитную группу.
Фрагмент: Термин «фрагмент» относится к специфичному сегменту или функциональной группе молекулы. Химические фрагменты часто представляют собой известные химические частицы, встроенные или присоединенные к молекуле.
Твердая подложка: Термин «твердая подложка» относится к любой подложке, которая позволяет проводить синтез нуклеиновых кислот. Согласно некоторым вариантам осуществления термин относится к стеклу или полимеру, которые не растворимы в среде, используемой на стадиях взаимодействия, проводимых для синтеза нуклеиновых кислот, и которые модифицированы таким образом, что содержат реакционно-способные группы. Согласно некоторым вариантам осуществления твердая подложка представляет собой полистирол с высокой степенью перекрестной сшивки (НСР) или стекло с контролируемым размером пор (CPG). Согласно некоторым вариантам осуществления твердая подложка представляет собой стекло с контролируемым размером пор (CPG). Согласно некоторым вариантам осуществления твердая подложка представляет собой гибридную подложку, состоящую из стекла с контролируемым размером пор (CPG) и полистирола с высокой степенью перекрестной сшивки (НСР).
Линкерный фрагмент: Термин «линкерный фрагмент» относится к любому фрагменту, необязательно расположенному между терминальным нуклеозидом и твердой подложкой или между терминальным нуклеозидом и другим нуклеозидом, нуклеотидом или нуклеиновой кислотой.
Молекула ДНК: «Молекула ДНК» относится к полимерной форме дезоксирибонуклеотидов (аденина, гуанина, тимина или цитозина) в виде одной нити или двухцепочечной спирали. Указанный термин относится только к первичной и вторичной структуре молекулы и не ограничивает их любыми конкретными третичными формами. Таким образом, указанный термин включает двухцепочечную ДНК, содержащуюся помимо прочего в линейных молекулах ДНК (например, в рестрикционных фрагментах), вирусах, плазмидах и хромосомах. При обсуждении структуры конкретных молекул двухцепочечных ДНК последовательности можно описывать в настоящей заявке согласно общепринятым правилам, где приведена только последовательность в направлении от 5' до 3' вдоль нетранскрибируемой цепи ДНК (т.е. цепи, имеющей последовательность, гомологичную мРНК).
Кодирующая последовательность: «Кодирующая последовательность» или «кодирующая область» ДНК представляет собой последовательность двухцепочечной ДНК, которая транскрибируется и транслируется в полипептид in vivo после воздействия соответствующих последовательностей, контролирующих экспрессию. Границы кодирующей последовательности («открытая рамка считывания» или «ОРС») определяются стартовым кодоном при 5'- (амино)-конце и стоп-кодоном трансляции при 3'- (карбоксильном) конце. Кодирующая последовательность может включать, но не ограничивается ими, прокариотические последовательности, кДНК эукариотической мРНК, геномные последовательности ДНК из ДНК эукариотов (например, млекопитающих) и синтетические последовательности ДНК. Сигнал полиаденилирования и последовательность терминации транскрипции, как правило, расположены в положении 3' кодирующей последовательности. Термин «некодирующая последовательность» или «некодирующая область» относится к областям последовательностей полинуклеотидов, которые не транслируются в аминокислоты (например, 5' и 3' нетранслируемые области).
Рамка считывания: Термин «рамка считывания» относится к одной из шести возможных рамок считывания, где в каждом направлении молекулы двухцепочечной ДНК расположены по три рамки. Используемая рамка считывания определяет кодоны, которые используются для кодирования аминокислот в кодирующей последовательности молекулы ДНК.
Антисмысловой: При использовании в настоящем описании молекула «антисмысловой» нуклеиновой кислоты содержит последовательность нуклеотидов, которая является комплементарной со «смысловой» нуклеиновой кислотой, кодирующей белок, например, комплементарной с кодирующей цепью молекулы двухцепочечной ДНК, комплементарной с последовательностью мРНК или комплементарной с кодирующей цепью гена. Соответственно, молекула антисмысловой нуклеиновой кислоты может быть ассоциирована посредством водородных линкерных групп с молекулой смысловой нуклеиновой кислоты. Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид представляет собой олигонуклеотид, который участвует в опосредованном РНКазой Н расщеплении; например, антисмысловый олигонуклеотид гибридизуется специфичным в отношении последовательности образом с частью целевой мРНК, таким образом, нацеливаясь на мРНК для расщепления с помощью РНКазы Н.
Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид способен различать аллель дикого типа и мутантный аллель мишени. Согласно некоторым вариантам осуществления антисмысловый олигонуклеотид в значительной степени участвует в опосредованном РНКазой Н расщеплении мутантного аллеля, но участвует в опосредованном РНКазой Н расщеплении аллеля дикого типа в гораздо меньшей степени (например, не существенно участвует в опосредованном РНКазой Н расщеплении аллеля дикого типа мишени).
Положение качелей: Используемое в настоящем описании «положение качелей» относится к третьему положению кодона. Мутации молекулы ДНК в положении качелей кодона согласно некоторым вариантам осуществления приводят к молчащим или консервативным мутациям уровня аминокислот. Например, существуют четыре кодона, кодирующих глицин, т.е. GGU, GGC, GGA и GGG, таким образом, мутация в положении качелей нуклеотида с заменой на любой другой нуклеотид, выбранный из A, U, С и G, не приводит к изменению уровня аминокислот кодируемого белка и, таким образом, является молчащим замещением.
Молчащее замещение: «Молчащее замещение» или «молчащая мутация» представляют собой мутацию, при которой происходит модификация нуклеотида в кодоне, но это не приводит к изменению остатка аминокислот, кодируемого кодоном. Примеры включают мутации в третьем положении кодона, а также в первом положении определенных кодонов, таких как кодон «CGG», который в результате мутации в AGG все равно кодирует Arg.
Ген: Термины «ген», «рекомбинантный ген» и «генетический конструкт», используемые в настоящем описании, относятся к молекуле ДНК или фрагменту молекулы ДНК, который кодирует белок или его фрагмент. Молекула ДНК может содержать открытую рамку считывания, кодирующую белок (последовательности экзонов), и может дополнительно содержать последовательности интронов. Термин «интрон», используемый в настоящем описании, относится к последовательности ДНК, присутствующей в данном гене, которая не транслируется в белок, и расположена в некоторых, но не во всех случаях, между экзонами. Ген желательно может быть функционально связан (или может содержать) с одним или более промоторами, усилителями, репрессорами и/или другими регуляторными последовательностями для модуляции активности или экспрессии гена, что хорошо известно в данной области техники.
Комплементарная ДНК: Используемая в настоящем описании «комплементарная ДНК» или «кДНК» включает рекомбинантные полинуклеотиды, синтезируемые в результате обратной транскрипции мРНК, из которых удалены промежуточные последовательности (интроны).
Гомология: «Гомология» или «идентичность» или «сходство» относятся к сходству последовательностей двух молекул нуклеиновых кислот. Гомологию и идентичность можно определять путем сравнения положений в каждой последовательности, которые можно согласованно выравнивать для сравнения. Если эквивалентные положения в сравниваемых последовательностях заняты одинаковым основанием, то молекулы являются идентичными по этому положению; если эквивалентные участки заняты одинаковыми или схожими остатками нуклеиновых кислот (например, имеющими схожую стерическую и/или электронную природу), то молекулы можно называть гомологичными (схожими) по этому положению. Выражение гомологии/сходства или идентичности в процентах относится к зависимости числа идентичных или схожих нуклеиновых кислот в общих положениях сравниваемых последовательностей. Последовательность, которая является «неродственной» или «негомологичной», является менее чем на 40% идентичной, менее чем на 35% идентичной, менее чем на 30% идентичной или менее чем на 25% идентичной с последовательностью, описанной в настоящей заявке. При сравнении двух последовательностей отсутствие остатков (аминокислот или нуклеиновых кислот) или наличие дополнительных остатков также уменьшает идентичность или гомологию/сходство.
Согласно некоторым вариантам осуществления термин «гомология» описывает полученный математически результат сравнения сходства последовательностей, который используют для выявления генов со схожими функциями или мотивами. Последовательности нуклеиновых кислот, описанные в настоящей заявке, можно использовать в качестве «искомой последовательности» для проведения исследования для сравнения с общими базами данных, например, для выявления других членов семейства, родственных последовательностей или гомологов. Согласно некоторым вариантам осуществления указанные исследования можно проводить при помощи программного обеспечения NBLAST и XBLAST (версия 2.0), Altschul, et al. (1990) J. Mol. Biol. 215: 403-10. Согласно некоторым вариантам осуществления исследования нуклеотидов BLAST можно проводить при помощи программы NBLAST, показатель (score) = 100, длина слова = 12, для получения последовательностей нуклеотидов, гомологичных молекулам нуклеиновых кислот согласно настоящему раскрытию. Согласно некоторым вариантам осуществления для получения выравнивания с пробелами для сравнения можно использовать Gapped BLAST согласно описанию Altschul et al., (1997) Nucleic Acids Res. 25(17): 3389-3402. При использовании программ BLAST и Gapped BLAST можно использовать базовые параметры соответствующих программ (например, XBLAST и BLAST) (см. www.ncbi.nlm.nih.gov).
Идентичность: Используемый в настоящем описании термин «идентичность» обозначает долю идентичных остатков нуклеотидов в процентах в соответствующих положениях двух или более последовательностей при выравнивании последовательностей для максимального совпадения последовательностей, т.е. с учетом пробелом и вставок. Идентичность можно легко рассчитывать при помощи известных способов, включая, но не ограничиваясь ими, способы, описанные в (Computational Molecular Biology, Lesk, A.M., ed., Oxford University Press, New York, 1988; Biocomputing: Informatics and Genome Projects, Smith, D.W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part I, Griffin, A.M., and Griffin, H.G., eds., Humana Press, New Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987; и Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991; и Carillo, H., and Lipman, D., SIAM J. Applied Math., 48: 1073 (1988)). Способы определения идентичности разработаны для определения максимального соответствия между исследуемыми последовательностями. Кроме того, способы определения идентичности систематизированы в компьютерных программах, имеющих открытый доступ. Способы определения идентичности между двумя последовательностями при помощи компьютерных программ включают, но не ограничиваются ими, пакет программного обеспечения GCG (Devereux, J., et al., Nucleic Acids Research 12(1): 387 (1984)), BLASTP, BLASTN и FASTA (Altschul, S. F. et al., J. Molec. Biol. 215: 403-410 (1990) и Altschul et al. Nuc. Acids Res. 25: 3389-3402 (1997)). Программа BLAST X, доступная в NCBI и в других источниках (BLAST Manual, Altschul, S., et al., NCBI NLM NIH Bethesda, Md. 20894; Altschul, S., et al., J. Mol. Biol. 215: 403-410 (1990), находится в открытом доступе. Для определения идентичности также можно использовать хорошо известный алгоритм Смита-Ватермана.
Гетерологичный: «Гетерологичная» область последовательности ДНК представляет собой распознаваемый сегмент ДНК в составе более крупной последовательности ДНК, который обычно не связан с более крупной последовательностью. Таким образом, если гетерологичная область кодирует ген млекопитающего, то ген обычно может содержать фланкирующую ДНК, которая отсутствует в геномной ДНК млекопитающего из генома исходного организма. Другим примером гетерологичной кодирующей последовательности является последовательность, где кодирующая последовательность, как таковая, отсутствует в естественных условиях (например, кДНК, где геномная кодирующая последовательность содержит интроны или синтетические последовательности, содержащие кодоны или мотивы, отличающиеся от немодифицированного гена). Изменения аллелей или естественные мутационные события не приводят к образованию гетерологичных областей ДНК, таких как определено в настоящем описании.
Транзиционная мутация: Термин «транзиционные мутации» относится к изменениям оснований в последовательности ДНК, при которых пиримидин (в цитидине (С) или тимидине (Т)) заменен на другой пиримидин, или пурин (в аденозине (А) или гуанозине (G)) заменен на другой пурин.
Трансверсионная мутация: Термин «трансверсионные мутации» относится к изменениям оснований в последовательности ДНК, при которых пиримидин (в цитидине (С) или тимидине (Т)) заменен на пурин, или пурин (в аденозине (А) или гуанозине (G)) заменен на пиримидин.
Олигонуклеотид: Термин «олигонуклеотид» относится к полимеру или олигомеру, состоящему из мономерных нуклеотидов, содержащему любую комбинацию нуклеиновых оснований, модифицированных нуклеиновых оснований, сахаров, модифицированных сахаров, фосфатных мостиковых групп или мостиковых групп с модифицированным атомом фосфора (также называемых в настоящем описании «межнуклеотидные линкерные группы», которые дополнительно определены в настоящем описании).
Олигонуклеотиды могут быть одноцепочечными или двухцепочечными. Используемый в настоящем описании термин «цепь олигонуклеотида» охватывает одноцепочечный олигонуклеотид. Одноцепочечный олигонуклеотид может содержать двухцепочечные области, а двухцепочечный олигонуклеотид может содержать одноцепочечные области. Примеры олигонуклеотидов включают, но не ограничиваются ими, структурные гены, гены, содержащие контрольные и терминальные области, самовоспроизводящиеся системы, такие как вирусная или плазмидная ДНК, одноцепочечные и двухцепочечные миРНК и другие агенты РНК-интерференции (агенты РНКи или агенты иРНК), кшРНК, антисмысловые олигонуклеотиды, рибозимы, микроРНК, имитаторы микроРНК, супермиры, аптамеры, антимиры, антагомиры, адаптеры UI, триплекс-образующие олигонуклеотиды, G-квадруплексные олигонуклеотиды, активаторы РНК, иммуностимулирующие олигонуклеотиды и олигонуклеотиды- «ловушки».
Двухцепочечные и одноцепочечные олигонуклеотиды, которые являются эффективными для инициирования РНК-интерференции, также называют в настоящем описании миРНК, агент РНКи или агент иРНК. Согласно некоторым вариантам осуществления указанные олигонуклеотиды, вызывающие РНК-интерференцию, ассоциированы с цитоплазматическим мультибелковым комплексом, известным как индуцируемый РНКи комплекс сайленсинга (RISC). Во многих вариантах реализации одноцепочечные и двухцепочечные агенты РНКи имеют достаточно длинные цепи, и они могут отщепляться под действием эндогенной молекулы, например, дайсера, с получением небольших олигонуклеотидов, которые могут быть задействованы в механизме RISC и участвуют в RISC-опосредованном расщеплении целевой последовательности, например, целевой мРНК.
Олигонуклеотиды согласно настоящему раскрытию могут иметь различную длину. В конкретных вариантах реализации длина олигонуклеотидов может находиться в диапазоне от примерно 2 до примерно 200 нуклеотидов. В различных схожих вариантах реализации одноцепочечные, двухцепочечные и трехцепочечные олигонуклеотиды могут иметь длину в диапазоне от примерно 4 до примерно 10 нуклеотидов, от примерно 10 до примерно 50 нуклеотидов, от примерно 20 до примерно 50 нуклеотидов, от примерно 15 до примерно 30 нуклеотидов, от примерно 20 до примерно 30 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет от примерно 9 до примерно 39 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 4 нуклеотида. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 5 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 6 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 7 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 8 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 9 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 10 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 11 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 12 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 15 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 20 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 25 нуклеотидов. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 30 нуклеотидов. Согласно некоторым вариантам осуществления олигонуклеотид представляет собой дуплекс комплементарных цепей, имеющих длину по меньшей мере 18 нуклеотидов. Согласно некоторым вариантам осуществления олигонуклеотид представляет собой дуплекс комплементарных цепей, имеющих длину по меньшей мере 21 нуклеотидов.
Межнуклеотидная линкерная группа: Используемая в настоящем описании фраза «межнуклеотидная линкерная группа», в целом, относится к фосфорсодержащей линкерной группе между нуклеотидными звеньями в олигонуклеотиде, и его используют взаимозаменяемо с терминами «межсахарная линкерная группа» и «мостиковая группа с атомом фосфора», используемыми выше в настоящем описании. Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа представляет собой фосфодиэфирную линкерную группу, содержащуюся в природных молекулах ДНК и РНК. Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа представляет собой «модифицированную межнуклеотидную линкерную группу», где каждый атом кислорода в фосфодиэфирной линкерной группе возможно и независимо заменен на органический или неорганический фрагмент. Согласно некоторым вариантам осуществления указанный органический или неорганический фрагмент выбран из =S, =Se, =NR', -SR', -SeR', -N(R')2, В(R')3, -S-, -Se- и -N(R')-, где каждый R' независимо является таким, как определено и описано далее, но не ограничивается ими. Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа представляет собой фосфотриэфирную линкерную группу, фосфоротиоатную сложную диэфирную линкерную группу (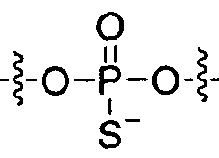 ) или модифицированную фосфоротиоатную сложную триэфирную линкерную группу. Специалистам в данной области техники должно быть понятно, что межнуклеотидная линкерная группа может существовать в виде аниона или катиона при данном рН за счет наличия кислотных или основных фрагментов в линкерной группе.
) или модифицированную фосфоротиоатную сложную триэфирную линкерную группу. Специалистам в данной области техники должно быть понятно, что межнуклеотидная линкерная группа может существовать в виде аниона или катиона при данном рН за счет наличия кислотных или основных фрагментов в линкерной группе.
Если не указано иное, при использовании в последовательности олигонуклеотида каждый из s, s1, s2, s3, s4, s5, s6 и s7 независимо представляет собой модифицированную межнуклеотидную линкерную группу, проиллюстрированную ниже в таблице 1.
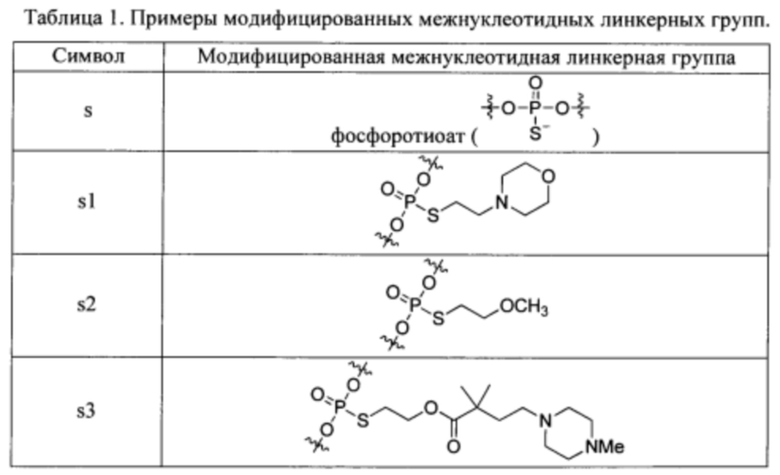
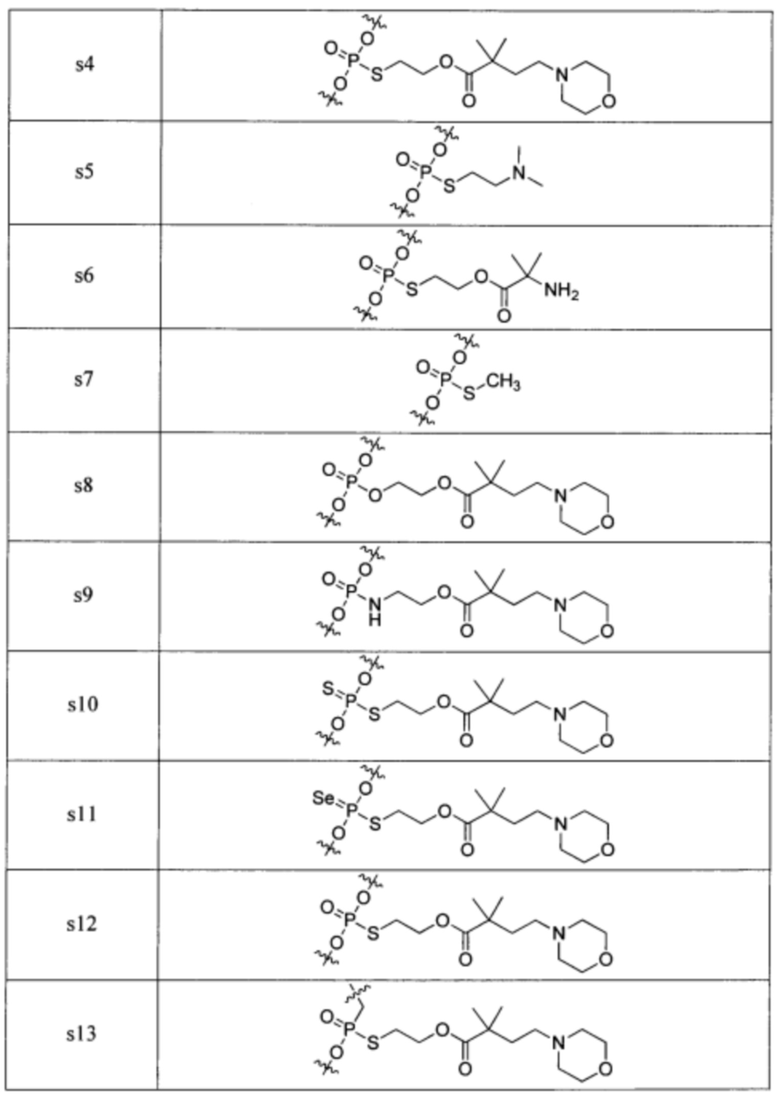
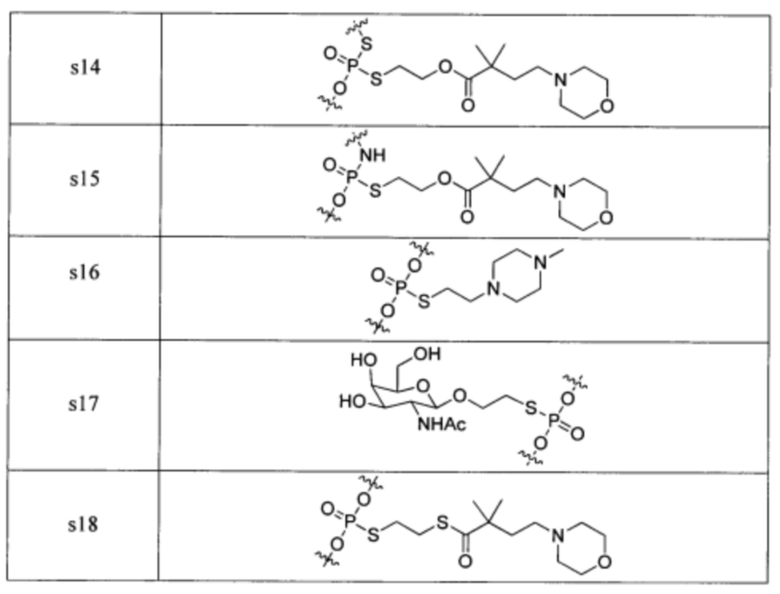
Например, (Rp,Sp)-ATsCs1GA содержит 1) фосфоротиоатную межнуклеотидную линкерную группу ( ) между Т и С; и 2) фосфоротиоатную сложную триэфирную межнуклеотидную линкерную группу, имеющую структуру
) между Т и С; и 2) фосфоротиоатную сложную триэфирную межнуклеотидную линкерную группу, имеющую структуру 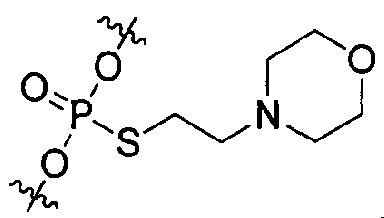 , между С и G. Если не указано иное, то обозначения Rp/Sp, указанные перед последовательностью олигонуклеотида, описывают конфигурации хиральных атомов фосфора линкерной группы в межнуклеотидных линкерных группах в направлении от положения 5' до 3' в последовательности олигонуклеотидов. Например, в (Rp,Sp)-ATsCs1GA атом фосфора в «s»-линкерной группе между Т и С имеет Rp-конфигурацию, а атом фосфора в «s1» линкерной группу между С и G имеет Sp-конфигурацию. Согласно некоторым вариантам осуществления «полностью-(Rp)» или «полностью-(Sp)» используют для указания того, что все хиральные атомы фосфора в линкерных группах олигонуклеотида имеют одинаковую Rp- или Sp-конфигурацию, соответственно. Например, полностью-(Rp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC означает, что все хиральные атомы фосфора в линкерной группе олигонуклеотида имеют Rp-конфигурацию; полностью-(Sp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC означает, что все хиральные атомы фосфора в линкерной группе олигонуклеотида имеют Sp-конфигурацию.
, между С и G. Если не указано иное, то обозначения Rp/Sp, указанные перед последовательностью олигонуклеотида, описывают конфигурации хиральных атомов фосфора линкерной группы в межнуклеотидных линкерных группах в направлении от положения 5' до 3' в последовательности олигонуклеотидов. Например, в (Rp,Sp)-ATsCs1GA атом фосфора в «s»-линкерной группе между Т и С имеет Rp-конфигурацию, а атом фосфора в «s1» линкерной группу между С и G имеет Sp-конфигурацию. Согласно некоторым вариантам осуществления «полностью-(Rp)» или «полностью-(Sp)» используют для указания того, что все хиральные атомы фосфора в линкерных группах олигонуклеотида имеют одинаковую Rp- или Sp-конфигурацию, соответственно. Например, полностью-(Rp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC означает, что все хиральные атомы фосфора в линкерной группе олигонуклеотида имеют Rp-конфигурацию; полностью-(Sp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC означает, что все хиральные атомы фосфора в линкерной группе олигонуклеотида имеют Sp-конфигурацию.
Тип олигонуклеотида: Согласно настоящему описанию фразу «тип олигонуклеотида» используют для определения олигонуклеотида, который имеет определенную последовательность оснований, профиль линкерных групп остова (т.е. профиль типов межнуклеотидных линкерных групп, например, фосфата, фосфоротиоата и т.д.), профиль хиральных центров остова (т.е. профиль стереохимии атомов фосфора линкерной группы (Rp/Sp)) и профиль модификаций атомов фосфора в остове (например, профиль групп «-XLR1» в формуле I). Олигонуклеотиды обозначенного единого «типа» имеют идентичную структуру друг с другом.
Специалистам в данной области техники должно быть понятно, что способы синтеза согласно настоящему раскрытию обеспечивают уровень контроля во время синтеза цепи олигонуклеотида, при котором каждое нуклеотидное звено, входящее в состав цепи олигонуклеотида, может быть разработано и/или выбрано заранее таким образом, чтобы оно имело конкретную стереохимию атома фосфора линкерной группы и/или конкретную модификацию атома фосфора линкерной группы и/или содержало конкретное основание и/или конкретный сахар. Согласно некоторым вариантам осуществления цепь олигонуклеотида подбирают и/или выбирают заранее таким образом, чтобы она имела конкретную комбинацию атомов фосфора в линкерных группах, которые являются стереоцентрами. Согласно некоторым вариантам осуществления цепь олигонуклеотида подбирают и/или выбирают таким образом, чтобы она имела определенную комбинацию модификаций атомов фосфора линкерной группы. Согласно некоторым вариантам осуществления цепь олигонуклеотида подбирают и/или выбирают таким образом, чтобы она содержала определенную комбинацию оснований. Согласно некоторым вариантам осуществления цепь олигонуклеотида подбирают и/или выбирают таким образом, чтобы она имела конкретную комбинацию одной или более приведенных выше структурных характеристик. В настоящем раскрытии предложены композиции, содержащие или состоящие из совокупности молекул олигонуклеотидов (например, композиции олигонуклеотидов с контролируемой хиральностью). Согласно некоторым вариантам осуществления все указанные молекулы принадлежат к одному типу (т.е. имеют идентичную структуру друг с другом). Во многих вариантах реализации, тем не менее, предложенные композиции содержат совокупность олигонуклеотидов различных типов, как правило, в предварительно определенных относительных количествах.
Хиральный контроль: Используемый в настоящем описании «хиральный контроль» относится к способности контролировать стереохимию каждого хирального атома фосфора линкерной группы в цепи олигонуклеотида. Фраза «олигонуклеотид с контролируемой хиральностью» относится к олигонуклеотиду, который существует в единственной диастереомерной форме, если рассматривать хиральные атомы фосфора линкерной группы. Олигонуклеотиды с контролируемой хиральностью получают из олигонуклеотидного синтеза с контролируемой хиральностью.
Композиция олигонуклеотидов с контролируемой хиральностью: Используемая в настоящем описании фраза «композиция олигонуклеотидов с контролируемой хиральностью» относится к композиции олигонуклеотидов, которая содержит предварительно определенное количество отдельных типов олигонуклеотидов. Например, согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит один тип олигонуклеотидов. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит более одного типа олигонуклеотида. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит смесь нескольких типов олигонуклеотидов. Примеры композиций олигонуклеотидов с контролируемой хиральностью дополнительно описаны в настоящей заявке.
Хирально-чистый: Согласно настоящему описанию фразу «хирально-чистый» используют для описания композиции олигонуклеотидов с контролируемой хиральностью, в которой все олигонуклеотиды существуют в единственной диастереомерной форме, если рассматривать атомы фосфора линкерной группы.
Хирально-однородный: Согласно настоящему описанию фразу «хирально-однородный» используют для описания молекулы или типа олигонуклеотида, в которых все нуклеотидные звенья имеют одинаковую стереохимию атомов фосфора линкерной группы. Например, олигонуклеотид, в котором все нуклеотидные звенья имеют Rp-стереохимию атомов фосфора линкерной группы, является хирально-однородным. Аналогично, олигонуклеотид, в котором все нуклеотидные звенья имеют Sp-стереохимию атомов фосфора линкерной группы, является хирально-однородным.
Предварительно определенный: Предварительно определенный понимают как целенаправленно выбранный, например, в противоположность случайным образом происходящему или достигаемому. Специалистам в данной области техники после изучения настоящего описания должно быть понятно, что в настоящем раскрытии предложены новые и неожиданные технологии, которые позволяют выбирать определенные типы олигонуклеотидов для получения и/или введения в предложенные композиции, а также позволяют получать контролируемым образом точно выбранные конкретные типы необязательно в выбранных определенных относительных количествах, и, таким образом, получают предложенные композиции. Указанные предложенные композиции являются «предварительно определенными» согласно настоящему описанию. Композиции, которые могут содержать определенные отдельные типы олигонуклеотидов, которые необходимо получать при помощи способа, в котором нельзя контролировать получение конкретного типа олигонуклеотида, не являются «предварительно определенными» композициями. Согласно некоторым вариантам осуществления предварительно определенная композиция представляет собой композицию, которую можно целенаправленно получать повторно (например, при помощи повторяемого контролируемого способа).
Атом фосфора линкерной группы: Согласно определению, приведенному в настоящем описании, фразу «атом фосфора линкерной группы» используют для указания на то, что конкретный указанный атом фосфора представляет собой атом фосфора, содержащийся в межнуклеотидной линкерной группе, где атом фосфора соответствует атому фосфора фосфодиэфира межнуклеотидной линкерной группы, которая присутствует в природных ДНК и РНК. Согласно некоторым вариантам осуществления атом фосфора линкерной группы содержится в модифицированной межнуклеотидной линкерной группе, где каждый атом кислорода фосфодиэфирной линкерной группы возможно и независимо заменен на органический или неорганический фрагмент. Согласно некоторым вариантам осуществления атом фосфора линкерной группы представляет собой Р* в формуле I. Согласно некоторым вариантам осуществления атом фосфора линкерной группы является хиральным. Согласно некоторым вариантам осуществления хиральный атом фосфора линкерной группы представляет собой Р* в формуле I.
Модификация Р: При использовании в настоящем описании термин «модификация Р» относится к любой модификации атома фосфора линкерной группы, отличной от стереохимической модификации. Согласно некоторым вариантам осуществления модификация Р включает присоединение, замещение или удаление присоединенного фрагмента, ковалентным образом связанного с атомом фосфора линкерной группы. Согласно некоторым вариантам осуществления «модификация Р» представляет собой -X-L-R1, где каждый из X, L и R1 независимо является таким, как определено и описано далее в настоящем описании.
Блокмер: Термин «блокмер», используемый в настоящем описании, относится к цепи олигонуклеотида, в которой профиль структурных признаков, характеризующий каждое отдельное нуклеотидное звено, характеризуется наличием по меньшей мере двух расположенных последовательно нуклеотидных звеньев, имеющих общий структурный признак атома фосфора межнуклеотидной линкерной группы. Под общим структурным признаком понимают одинаковую стереохимию атомов фосфора или одинаковую модификацию атомов фосфора линкерной группы. Согласно некоторым вариантам осуществления по меньшей мере два расположенных последовательно нуклеотидных звена, имеющих общий структурный признак атома фосфора межнуклеотидной линкерной группы, называют «блоком».
Согласно некоторым вариантам осуществления блокмер представляет собой «стереоблокмер», например, по меньшей мере два расположенных последовательно нуклеотидных звена имеют одинаковую стереохимию атомов фосфора линкерной группы. Указанные по меньшей мере два расположенных последовательно нуклеотидных звена образуют «стереоблок». Например, (Sp,Sp)-ATsCs1GA представляет собой стереоблокмер, так как два расположенных последовательно нуклеотидных звена, Ts и Cs1, имеют одинаковую стереохимию атомов фосфора линкерных групп (Sp в обоих случаях). В том же олигонуклеотиде (Sp,Sp)-ATsCs1GA TsCs1 образует блок, который представляет собой стереоблок.
Согласно некоторым вариантам осуществления блокмер представляет собой «блокмер с модификацией Р», например, по меньшей мере два расположенных последовательно нуклеотидных звена имеют одинаковую модификацию атомов фосфора линкерных групп. Указанные по меньшей мере два расположенных последовательно нуклеотидных звена образуют «блок с модификацией Р». Например, (Rp,Sp)-ATsCsGA представляет собой блокмер с модификацией Р, так как по меньшей мере два расположенных последовательно нуклеотидных звена, Ts и Cs, имеют одинаковую модификацию Р (т.е. оба атома присутствуют в виде фосфоротиоатного сложного диэфира). В том же олигонуклеотиде (Rp,Sp)-ATsCsGA TsCs образует блок, который представляет собой блок с модификацией Р.
Согласно некоторым вариантам осуществления блокмер представляет собой «блокмер с одинаковыми линкерными группами», например, по меньшей мере два расположенных последовательно нуклеотидных звена имеют одинаковую стереохимию и модификации атомов фосфора линкерных групп. По меньшей мере два расположенных последовательно нуклеотидных звена образуют «блок с одинаковыми линкерными группами». Например, (Rp,Rp)-ATsCsGA представляет собой блокмер с одинаковыми линкерными группами, так как по меньшей мере два расположенных последовательно нуклеотидных звена, Ts и Cs, имеют одинаковую стереохимию (Rp в обоих случаях) и модификацию Р (фосфоротиоат в обоих случаях). В том же олигонуклеотиде (Rp,Rp)-ATsCsGATsCs образует блок, который представляет собой блок с одинаковыми линкерными группами.
Согласно некоторым вариантам осуществления блокмер содержит один или более блоков, независимо выбранных из стереоблока, блока с модификацией Р и блока с одинаковыми линкерными группами. Согласно некоторым вариантам осуществления блокмер представляет собой стереоблокмер, если рассматривать один блок, и/или блокмер с модификацией Р, если рассматривать другой блок, и/или блокмер с одинаковыми линкерными группами, если рассматривать еще один блок. Например, (Rp,Rp,Rp,Rp,Rp,Sp,Sp,Sp)-AAsTsCsGsAs1Ts1Cs1Gs1ATCG представляет собой стереоблокмер, если рассматривать стереоблок AsTsCsGsAs1 (все атомы фосфора линкерных групп имеют Rp-конфигурацию) или Ts1Cs1Gs1 (все атомы фосфора линкерных групп имеют Sp-конфигурацию), блокмер с модификацией Р, если рассматривать блок с модификацией Р AsTsCsGs (все линкерные группы s) или As1Ts1Cs1Gs1 (все линкерные группы s1) или блокмер с одинаковыми линкерными группами, если рассматривать блок с одинаковыми линкерными группами AsTsCsGs (все атомы фосфора линкерных групп имеют Rp-конфигурацию и все линкерные группы s) или Ts1Cs1Gs1 (все атомы фосфора линкерных групп имеют Sp-конфигурацию и все линкерные группы s1).
Альтмер: Термин «альтмер», используемый в настоящем описании, относится к цепи олигонуклеотида, в которой профиль структурных признаков, характеризующий каждое отдельное нуклеотидное звено, характеризуется тем, что никакие два расположенные последовательно нуклеотидные звена в цепи олигонуклеотидов не имеют общий конкретный структурный признак атомов фосфора межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления альтмер составлен таким образом, что имеет повторяющийся профиль. Согласно некоторым вариантам осуществления альтмер составлен таким образом, что не имеет повторяющийся профиль.
Согласно некоторым вариантам осуществления альтмер представляет собой «стереоальтмер», например, никакие два расположенные последовательно нуклеотидные звена не имеют одинаковую стереохимию атомов фосфора линкерных групп. Например, (Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC.
Согласно некоторым вариантам осуществления альтмер представляет собой «альтмер с модификацией Р», например, никакие два расположенные последовательно нуклеотидные звена не имеют одинаковую модификацию атомов фосфора линкерных групп. Например, полностью-(Sp)-CAs1GsT, где каждый атом фосфора линкерных групп имеет отличающуюся модификацию Р по сравнению с другими атомами фосфора.
Согласно некоторым вариантам осуществления альтмер представляет собой «альтмер с различными чередующимися линкерными группами», например, никакие два расположенные последовательно нуклеотидные звена не имеют одинаковую стереохимию или модификацию атомов фосфора линкерных групп. Например, (Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp)-GsCs1CsTs1CsAs1GsTs1CsTs1GsCs1TsTs2CsGs3CsAs4CsC.
Унимер: Термин «унимер», используемый в настоящем описании, относится к цепи олигонуклеотида, в которой профиль структурных признаков, характеризующий каждое отдельное нуклеотидное звено, является таким, что все нуклеотидные звенья в цепи имеют по меньшей мере один общий структурный признак атома фосфора межнуклеотидной линкерной группы. Под общим структурным признаком понимают одинаковую стереохимию атомов фосфора линкерных групп или одинаковую модификацию атомов фосфора линкерных групп.
Согласно некоторым вариантам осуществления унимер представляет собой «стереоунимер», например, все нуклеотидные звенья имеют одинаковую стереохимию атомов фосфора линкерных групп. Например, полностью-(Sp)-CsAs1GsT, где все линкерные группы содержат атом фосфора в Sp-конфигурации.
Согласно некоторым вариантам осуществления унимер представляет собой «унимер с модификацией Р», например, все нуклеотидные звенья имеют одинаковую модификацию атомов фосфора линкерной группы. Например, (Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp,Rp,Sp, Rp,Sp,Rp,Sp,Rp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC, где все межнуклеотидные линкерные группы представляют собой фосфоротиоатные сложные диэфиры.
Согласно некоторым вариантам осуществления унимер представляет собой «унимер с одинаковыми линкерными группами», например, все нуклеотидные звенья имеют одинаковую стереохимию и одинаковые модификации атомов фосфора линкерных групп. Например, полностью-(Sp)-GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGsCsAsCsC, где все межнуклеотидные линкерные группы представляют собой фосфоротиоатный сложный диэфир, содержащий атом фосфора в Sp-конфигурации.
Гэпмер: Используемый в настоящем описании термин «гэпмер» относится к цепи олигонуклеотида, характеризующейся тем, что по меньшей мере одна межнуклеотидная фосфорсодержащая линкерная группа в цепи олигонуклеотида представляет собой фосфатную сложную диэфирную линкерную группу, например, такую как содержится в природных ДНК или РНК. Согласно некоторым вариантам осуществления более чем одна межнуклеотидная фосфорсодержащая линкерная группа цепи олигонуклеотида представляет собой фосфатную сложную диэфирную линкерную группу, такую как содержится в природных ДНК или РНК. Например, полностью-(Sp)-CAs1GsT, где межнуклеотидная линкерная группа между С и А представляет собой фосфатную сложную диэфирную линкерную группу.
Скипмер: Используемый в настоящем описании термин «скипмер» относится к типу гэпмера, в котором каждая вторая межнуклеотидная фосфорсодержащая линкерная группа в цепи олигонуклеотида представляет собой фосфатную сложную диэфирную линкерную группу, например, такую как содержится в природных ДНК или РНК, и каждая вторая межнуклеотидная фосфорсодержащая линкерная группа в цепи олигонуклеотида представляет собой модифицированную межнуклеотидную линкерную группу. Например, полностью (Sp)-AsTCs1GAs2TCs3G.
Для задач настоящего раскрытия химические элементы указаны в соответствии с Периодической таблицей элементов, версия CAS, Handbook of Chemistry and Physics, 67th Ed., 1986-87, форзац.
Способы и структуры, описанные в настоящей заявке, относящиеся к соединениям и композициям согласно настоящему раскрытию, также применимы к фармацевтически приемлемым солям присоединения кислоты или основания, а также ко всем стереоизомерным формам указанных соединений и композиций.
Краткое описание чертежей
Фигура 1. Обращенно-фазовая ВЭЖХ после инкубации с гомогенатом печени крыс. Измеряли общие количества олигонуклеотидов, оставшихся при инкубации с гомогенатом всей крысиной печени при 37°С в разные дни. Было обнаружено, что метаболическая стабильность in vitro ONT-154 была похожей на ONT-87, который содержит 2'-МОЕ крылья, в то время как оба имеют гораздо большую стабильность, чем 2'-МОЕ гэпмер, который является стереослучайным (ONT-41, мипомерсен). Измеряли количество оставшегося полноразмерного олигомера с помощью обращено-фазовой ВЭЖХ, где площадь представляющего интерес пика нормализовали с внутренним стандартом.
Фигура 2. Деградация различных хирально чистых аналогов мипомерсена (ONT-41) в гомогенате всей крысиной печени. Измеряли общие количества олигонуклеотида, остающегося при инкубации с гомогенатом всей крысиной печени при 37°С в разные дни. Было обнаружено, что метаболическая стабильность in vitro хирально чистых диастереомеров последовательности АроВ человека ONT-41 (мипомерсен) возрастала с увеличением межнуклеотидных линкерных групп в Sp-конфигурации. Измеряли количество оставшегося полноразмерного олигомера с помощью обращено-фазовой ВЭЖХ, где площадь представляющего интерес пика нормализовали с внутренним стандартом. Используемые композиции включают: ONT-41, ONT-75, ONT-77, ONT-80, ONT-81, ONT-87, ONT-88 и ONT-89.
Фигура 3. Деградация различных хирально чистых аналогов мышиной последовательности АроВ (ISIS 147764, ONT-83) в гомогенате всей крысиной печени. Измеряли общие количества олигонуклеотида, остающегося при инкубации с гомогенатом всей крысиной печени при 37°С в разные дни. Было обнаружено, что метаболическая стабильность in vitro хирально чистых диастереомеров мышиной последовательности АроВ (ISIS 147764, ONT-83) возрастала с увеличением межнуклеотидных линкерных групп в Sp-конфигурации. Измеряли количество оставшегося полноразмерного олигомера с помощью обращено-фазовой ВЭЖХ, где площадь представляющего интерес пика нормализовали с внутренним стандартом. Используемые композиции включают: ONT-82-ONT-86.
Фигура 4. Деградация аналога мипомерсена ONT-75 в гомогенате всей крысиной печени в течение 24 часов. На этой фигуре показана стабильность ONT-75 в гомогенате всей крысиной печени.
Фигура 5. Деградация аналога мипомерсена ONT-81 в гомогенате всей крысиной печени в течение 24 часов. На этой фигуре показана стабильность ONT-81 в гомогенате всей крысиной печени.
Фигура 6. Продолжительности нокдауна для ONT-87, ONT-88 и ONT-89. Стереоизомеры могут обладать существенно разными продолжительностями нокдауна. ONT-87 приводит по существу к более прочному подавлению, чем другие стереоизомеры. Наблюдалось увеличение продолжительности действия ONT-87 в нескольких исследованиях in vivo. ONT-88 показал сходный профиль эффективности и восстановления, что и ONT-41 (мипомерсен) в определенных исследованиях in vivo. Трансгенным мышам Hu АроВ, n=4, вводили IP болюс 10 мг/кг массы тела 2 раза в неделю в течение трех недель. Мышей рандомизировали в исследуемые группы и вводили внутрибрюшинно (IP) дозу 10 мг/кг в дни 1, 4, 8, 11, 15, 18 и 22 в зависимости от индивидуальной массы тела мыши, измеренной перед дозированным введением в каждый день введения. Кровь собирали в дни 0, 17, 24, 31, 38, 45 и 52 посредством подчелюстного (щечного) кровотечения и после умерщвления на 52 день с помощью пункции сердца, а затем получали из нее сыворотку. АроВ измеряли с помощью ELISA. Подчеркнутое: нокдаун 72% против 35%, поддерживаемый в течение 3 недель после введения дозы.
Фигура 7. Профили ВЭЖХ, показывающие разницу в метаболической стабильности, определенной в сыворотке крови человека, для дуплексов миРНК с несколькими конфигурациями Rp, Sp или стереослучайными фосфоротиоатными линкерными группами. Используемые композиции включают: ОНТ-114, ОНТ-116, ОНТ-109, ОНТ-107, ОНТ-108 и ОНТ-106.
Фигура 8. Влияние стереохимии на активности РНКазы H. Олигонуклеотиды гибридизовали с РНК, а затем инкубировали с РНКазой Н при 37°С в присутствии 1-кратного буфера РНКазы Н. Сверху вниз в 120 мин: ONT-89, ONT-77, ONT-81, ONT-80, ONT-75, ONT-41, ONT-88, ONT-154, ONT-87, с ONT-77/154 очень близко друг к другу.
Фигура 9. Анализ расщепления человеческой РНКазой H1 РНК 20-мер при гибридизации с различными препаратами стереоизомеров фосфоротиоатных олигонуклеотидов, нацеленных на ту же область мРНК АроВ человека. Конкретные участки расщепления находятся под сильным влиянием различных стереохимии. Стрелки обозначают положение расщепления (сайты расщепления). Продукты анализировали посредством ВЭЖХ/МС. Длина стрелки указывает на количество продуктов, присутствующих в реакционной смеси, которая была определена из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента (чем больше стрелка, тем больше обнаруженных продуктов расщепления). (А): Легенда для карт расщепления. (В) и (С): карты расщепления олигонуклеотидов. На фигурах:  указывает на то, что оба фрагмента расщепления РНКазой H1 (5'-фосфатной природы, а также 5'-ОН 3'-ОН природы) были идентифицированы в реакционных смесях.
указывает на то, что оба фрагмента расщепления РНКазой H1 (5'-фосфатной природы, а также 5'-ОН 3'-ОН природы) были идентифицированы в реакционных смесях.  указывает на то, что был обнаружен только компонент 5'-фосфатной природы и
указывает на то, что был обнаружен только компонент 5'-фосфатной природы и  указывает на то, что был обнаружен компонент 5'-ОН 3'-ОН в масс-спектрометрическом анализе. Используемые композиции включают: ONT-41, ONT-75, ONT-77, ONT-80, ONT-81, ONT-87, ONT-88, ONT-88 и ONT-154.
указывает на то, что был обнаружен компонент 5'-ОН 3'-ОН в масс-спектрометрическом анализе. Используемые композиции включают: ONT-41, ONT-75, ONT-77, ONT-80, ONT-81, ONT-87, ONT-88, ONT-88 и ONT-154.
Фигура 10. Карты расщепления различных композиций олигонуклеотидов ((А)-(С)). Эти три последовательности направлены на различные области в мРНК FOXO1. Каждую последовательность изучали посредством пяти различных химических анализов. Карты расщепления получают из реакционных смесей, полученных после 30 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера PBS при 37°С. Длина стрелки указывает на количество продуктов, присутствующих в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента (чем больше стрелка, тем больше обнаруженных продуктов расщепления). Только в тех случаях, когда 5'-ОН 3'-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки. Скорости расщепления определяли путем измерения количества полноразмерной РНК, остающейся в реакционных смесях, с помощью обратно-фазовой ВЭЖХ. Реакции останавливали в фиксированные точки времени с помощью 30 мМ Na2EDTA. Используемые композиции включают: ONT-316, ONT-355, ONT-361, ONT-367, ONT-373, ONT-302, ONT-352, ONT-358, ONT-364, ONT-370, ONT-315, ONT-354, ОНТ-360, ОНТ-366 и ОНТ-372.
Фигура 11. Карты расщепления композиций олигонуклеотидов, имеющих различные общие последовательности оснований и длину ((А) - (В)). На картах показано сравнение стереослучайных композиций ДНК (верхняя панель) с тремя различными и стереохимически чистыми композициями олигонуклеотидов. Данные представляют собой сравнение результатов композиций олигонуклеотидов с контролируемой хиральностью с двумя стереослучайными фосфоротиоатными композициями олигонуклеотидов (ONT-366 и ONT-367), направленно воздействующими на различные области в мРНК FOXO1. Каждая панель показывает сравнение стереослучайной ДНК (верхняя панель) с тремя различными и стереохимически чистыми олигонуклеотидными препаратами. Карты расщепления получали из реакционных смесей, полученных после 30 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера PBS при 37°С. Стрелки указывают на сайты расщепления. Длина стрелки указывает на количество продуктов, присутствующих в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента (чем больше стрелка, тем больше обнаруженных продуктов расщепления). Только в тех случаях, когда 5'-ОН 3'-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки. Используемые композиции включают: ONT-366, ONT-389, ONT-390, ONT-391, ONT-367, ONT-392, ONT-393 и ONT-394.
Фигура 12. Влияние стереохимии на активность РНКазы Н. В двух независимых экспериментах антисмысловые олигонуклеотиды, направленные на идентичную область мРНК FOXO1, гибридизовали с РНК, а затем инкубировали с РНКазой Н при 37°С в присутствии 1-кратного буфера РНКазы Н. Исчезновение полноразмерной РНК измеряли из площади пика при 254 нм с использованием обратно-фазовой ВЭЖХ. (А): сверху вниз в 60 мин: ONT-355, ONT-316, ONT-367, ONT-392, ONT-393 и ONT-394 (ONT-393 и ONT-394 примерно одинаковые в 60 мин; ONT-393 имели более высокий % РНК-субстрата, остающегося через 5 мин). (В): сверху вниз в 60 мин: ONT-315, ONT-354, ONT-366, ONT-391, ONT-389 и ONT-390. Скорости расщепления определяли путем измерения количества полноразмерной РНК, остающейся в реакционных смесях, с помощью обратно-фазовой ВЭЖХ. Реакции останавливали в фиксированные точки времени с помощью 30 мМ Na2EDTA.
Фигура 13. Оборот антисмысловых олигонуклеотидов. Дуплексы получали с каждой концентрацией ДНК-цепи, равной 6 мкМ, и РНК, составляющей 100 мкМ. Эти дуплексы инкубировали с 0,02 мкМ фермента РНКазы Н, и исчезновение полноразмерной РНК измеряли из площади ее пика при 254 нм с использованием ОФ-ВЭЖХ. Скорости расщепления определяли путем измерения количества полноразмерной РНК, остающейся в реакционных смесях, с помощью обратно-фазовой ВЭЖХ. Реакции останавливали в фиксированные точки времени с помощью 30 мМ Na2EDTA. Сверху вниз на 40 мин: ONT-316, ONT-367 и ONT-392.
Фигура 14. Карта расщепления, сравнивающая стереослучайный фосфоротиоатный олигонуклеотид с шестью различными и стереохимически чистыми олигонуклеотидными препаратами, направленными на одну и ту же область мРНК FOXO1. Используемые композиции включают: ONT-367, ONT-392, ONT-393, ONT-394, ONT-400, ONT-401 и ONT-406.
Фигура 15. Влияние стереохимии на активность РНКазы Н. Антисмысловые олигонуклеотиды гибридизировали с РНК, а затем инкубировали с РНКазой Н при 37°С в присутствии 1-кратного буфера РНКазы Н. Наблюдалась зависимость стереохимии от активности РНКазы Н. Также очевидна при сравнении ONT-367 (стереослучайная ДНК) и ONT-316 (5-10-5 2'-МОЕ гэпмер) сильная зависимость композиционной химии от активности РНКазы Н. Сверху вниз в 40 мин: ONT-316, ONT-421, ONT-367, ONT-392, ONT-394, ONT-415 и ONT-422 (ONT-394/415/422 характеризуются аналогичными уровнями в 40 мин; в 5 мин, ONT-422> ONT-394> ONT-415 в % РНК, оставшейся в ДНК/РНК-дуплексе).
Фигура 16. Влияние стереохимии на активность РНКазы Н. Антисмысловые олигонуклеотиды, направленные на идентичную область мРНК FOXO1, гибридизовали с РНК, а затем инкубировали с РНКазой Н при 37°С в присутствии 1-кратного буфера РНКазы Н. Наблюдалась зависимость стереохимии от активности РНКазы Н. Сверху вниз в 40 мин: ONT-396, ONT-409, ONT-414, ONT-408 (ONT-3 96/409/414/408 имеют аналогичные уровни в 40 мин), ONT-404, ONT-410, ONT-402 (ONT-404/410/408 имеют аналогичные уровни в 40 мин), ONT-403, ONT-407, ONT-405, ONT-401, ONT-406 и ONT-400 (ONT-401/405/406/400 имеют аналогичные уровни в 40 мин).
Фигура 17. Влияние стереохимии на активность РНКазы Н. Антисмысловые олигонуклеотиды, направленные на идентичную область мРНК FOXO1, гибридизовали с РНК, а затем инкубировали с РНКазой Н при 37°С в присутствии 1-кратного буфера РНКазы Н. Наблюдалась зависимость стереохимии от активности РНКазы Н. Наблюдалось, что ONT-406 вызывает расщепление образовавшей дуплекс РНК со скоростью, слегка превышающей таковую фосфодиэфирного олигонуклеотида ONT-415. Сверху вниз в 40 мин: ONT-396, ONT-421, ONT-392, ONT-394, ONT-415, ONT-406 и ONT-422 (ONT-394/415/406 имеют аналогичные уровни в 40 мин; в 5 мин, ONT-394> ONT-415> ONT-406 в % РНК оставшихся в ДНК/РНК-дуплексе).
Фигура 18. Иллюстративные УФ хроматограммы продуктов расщепления РНК, полученных при образовании дуплекса РНК (ONT-388) со стереослучайной ДНК, ONT-367 (вверху) и стереочистой ДНК с повторным триплетным мотивом-3'-SSR-5', ONT-394 (внизу). 2,35 мин: 7-мер; 3,16 мин: 8-мер и p-6-мер; 4,48 мин: Р-7-мер; 5,83 мин: Р-8-мер; 6,88 мин: 12-мер; 9,32 мин: 13-мер; 10,13 мин: Р-11-мер; 11,0 мин: Р-12-мер и 14-мер; 11,93 мин: Р-13-мер; 13,13 мин: Р-14-мер. ONT-394 (внизу)распределение пика: 4,55 мин: Р-7-мер; 4,97 мин: 10-мер; 9,53 мин: 13-мер.
Фигура 19. Спектр ионизации электрораспылением продуктов расщепления РНК. Фрагменты РНК, полученные из дуплекса ONT-387, РНК/ONT-354, (7-6-7, ДНК-2'-ОМе- ДНК) вверху и ONT-387, РНК/ONT-315, (5-10-5,2'-МОЕ гэпмер) внизу, когда эти дуплексы инкубировали с РНКазой Н в течение 30 минут в присутствии 1-кратного буфера РНКазы Н.
Фигура 20. УФ-хроматограмма и общая ионная хроматограмма (TIC) дуплекса ONT-406 и ONT-388 после 30 минут инкубации с РНКазой Н.
Фигура 21. Пример предложенного расщепления. Предложенные композиции олигонуклеотидов с контролируемой хиральностью способны расщеплять мишени, как показано.
Фигура 22. Иллюстративное аллельспецифическое расщепление направленной мутантной мРНК хантингтина. (А) и (В): иллюстративные олигонуклеотиды. (С)-(Е): карты расщепления. (F)-(H): расщепление РНК. Получали стереослучайные композиции олигонуклеотидов и композиции олигонуклеотидов с контролируемой хиральностью для направленного воздействия на однонуклеотидные полиморфизмы для аллельселективного подавления мутантного хантингтина. ONT-450 (стереослучайный), направленный на ONT-453 (мутантный НТТ) и ONT-454 (НТТ дикого типа), показал предельную дифференциацию в расщеплении РНК и их картах расщепления. Хирально контролируемый ONT-451 с селективным размещением мотива 3'-SSR-5' в сайте распознавания РНКазы Н, направленной на ONT-453 (мутантный НТТ) и ONT-454 (НТТ дикого типа), показал большую дифференциацию в скорости расщепления РНК. Из карты расщепления следует отметить, что мотив 3'-SSR-5' расположен таким образом, чтобы направить расщепление между положениями 8 и 9, который находится после ошибочно спаренных оснований, если считывать с 5'-конца РНК. ONT-452 с селективным размещением мотива 3'-SSR-5' в сайте распознавания РНКазы Н, направляющей ONT-453 (мутантный НТТ) и ONT-454 (НТТ дикого типа), показал умеренную дифференциацию скорости расщепления РНК. Мотив 3'-SSR-5' помещали таким образом, чтобы направить расщепление в положениях 7 и 8, которые находятся перед несоответствием, если считывать с 5'-конца РНК. Иллюстративные данные демонстрируют значимость положения в размещении мотива 3'-SSR-5' для достижения повышенной дискриминации для аллель специфического расщепления. Все карты расщепления получают из реакционных смесей, полученных через 5 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера PBS при 37°С. Стрелки указывают на сайты расщепления. Длина стрелки указывает на количество продуктов, присутствующих в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента (чем больше стрелка, тем больше обнаруженных продуктов расщепления). Только в тех случаях, когда компонент 5'-ОН 3'-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки. Используемые композиции включали: от ONT-450 до ONT-454.
Фигура 23. (А)-(С): пример аллельспецифического расщепления, направленного на мРНК FOXO1.
Фигура 24. Сайленсинг «доза-эффект» in vitro мРНК АроВ после лечения с олигонуклеотидами АроВ. Стереохимически чистые диастереомеры с крыльями 2'-МОЕ и без них показывают аналогичную эффективность, что и ONT-41 (мипомерсен). Используемые композиции включают: ONT-87, ONT-41 и ONT-154.
Фигура 25. Сравнение карт расщепления РНКазы H (А) и скорости расщепления РНК (В) для стереослучайной композиции (ONT-367) и композиций олигонуклеотидов с контролируемой хиральностью (ONT-421, полностью-Sp-конфигурация, и ONT-455, полностью-Rp-конфигурация) и ДНК (ONT-415). Эти последовательности направлены на ту же область в мРНК FOXO1. Карты расщепления получали из реакционных смесей, полученных через 5 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера PBS при 37°С. Стрелки указывают на сайты расщепления. Длина стрелки указывает на количество продуктов, присутствующих в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента (чем больше стрелка, тем больше обнаруженных продуктов расщепления). Только в тех случаях, когда компонент 5'-ОН 3'-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки. Скорости расщепления определяли путем измерения количества полноразмерной РНК, остающейся в реакционных смесях, с помощью обратно-фазовой ВЭЖХ. Реакции останавливали в фиксированные точки времени с помощью 30 мМ Na2EDTA.
Фигура 26. Сравнение карт расщепления последовательностей, содержащих одну Rp-конфигурацию с изменением положения, начиная с 3'-конца ДНК. Используемые композиции включают: ONT-396 - ONT-414. Эти последовательности направлены на ту же область в мРНК foxo1. Карты расщепления получали из реакционных смесей, полученных через 5 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера с РНКазой Н при 37°С. Стрелки указывают на сайты расщепления. Длина стрелки указывает на количество продуктов, присутствующих в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента (чем больше стрелка, тем больше обнаруженных продуктов расщепления). Только в тех случаях, когда компонент 5’-ОН 3’-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки.
Фигура 27. (А) Сравнение скоростей расщепления РНКазой Н стереочистых олигонуклеотидов (ONT-406), (ONT-401), (ONT-404) и (ONT-408). Все четыре последовательности представляют собой стереочистые фосфоротиоаты с одной линкерной группой в Rp-конфигурации. Эти последовательности направлены на ту же область в мРНК FOXO1. Все дуплексы инкубировали с РНКазой H1C в присутствии 1-кратного буфера РНКазы Н при 37°С. Реакции останавливали в фиксированные точки времени посредством 30 мМ Na2EDTA. Скорости расщепления определяли путем измерения количества полноразмерной РНК, остающейся в реакционных смесях, с помощью обратно-фазовой ВЭЖХ. Было обнаружено, что ONT-406 и ONT-401 характеризовались лучшими скоростями расщепления. (В) Соотношение между % РНК, расщепленного в анализе РНКазы Н (10 мкМ олигонуклеотида), и % нокдауна мРНК в анализе т vitro (20 нМ олигонуклеотида). Все последовательности направлены на ту же область в мРНК FOXO1. Количество остающейся РНК определяли по площади УФ пика для РНК при нормировании к ДНК в той же реакционной смеси. Все вышеперечисленные карты получают из реакционной смеси, полученной через 5 минут инкубации соответствующих дуплексов с РНКазой Н1С в присутствии 1-кратного буфера РНКазы Н при 37°С. Все последовательности от ONT-396 до ONT-414 имеют один фосфоротиоат в Rp-конфигурации и они варьируют в положении Rp. Фосфоротиоат ONT-421 (полностью-Sp) был неактивным в анализе т vitro. Это относится к низкой скорости расщепления РНК в анализе с РНКазой Н, когда ONT-421 образовывал дуплекс с комплементарной РНК.
Фигура 28. Анализ сывороточной устойчивости ДНК с единственным PS walk в конфигурации Rp (ONT-396-ONT-414), ДНК со стереослучайным PS (ONT-367), ДНК с PS в полностью-Sp-конфигурации (ONT-421) и ДНК с PS в полностью-Rp-конфигурации (ONT-455) в сыворотке крови крыс в течение 2-х дней. Используемые композиции включают: ONT-396 - ONT-414, ONT-367, ONT-421 и ONT-455.
Фигура 29. Иллюстративные олигонуклеотиды, включая гемимеры. (А): карты расщепления. (В): анализ расщепления РНК. (С): нокдаун мРНК FOXO1. Использовали ONT-440, ONT-441 и ONT-367. Согласно некоторым вариантам осуществления введение 2'-модификации на 5'-конце последовательностей увеличивает стабильность связывания с целевой РНК при сохранении активности РНКазы Н. ONT-367 (ДНК со стереослучайными фосфоротиоатами) и ONT-440 (5-15, 2'-F-ДНК) имеют одинаковые карты расщепления и аналогичную скорость расщепления РНК в анализе с РНКазой Н (10 мкМ олигонуклеотида). Согласно некоторым вариантам осуществления последовательность ONT-440 (5-11, 2''-F-ДНК) может иметь лучшие свойства проникновения в клетки. Согласно некоторым вариантам осуществления асимметричные 2'-модификации обеспечивают преимущество Tm при сохранении активности РНКазы Н. Введение мотивов RSS может еще больше повысить эффективность РНКазы Н в гемимерах. Карты расщепления получали из реакционных смесей, полученных через 5 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера РНКазы Н при 37°С. Стрелки указывают на сайты расщепления,  указывает на то, что в масс-спектрометрическом анализе в реакционных смесях были идентифицированы оба фрагмента, 5'-фосфатной природы, а также 5’-ОН 3’-ОН природы.
указывает на то, что в масс-спектрометрическом анализе в реакционных смесях были идентифицированы оба фрагмента, 5'-фосфатной природы, а также 5’-ОН 3’-ОН природы. 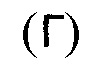 указывает на то, что был обнаружен только компонент 5'-фосфатной природы и
указывает на то, что был обнаружен только компонент 5'-фосфатной природы и 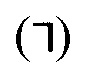 указывает на то, что был обнаружен компонент 5’-ОН 3’-ОН. Длина стрелки указывает на количество метаболита, присутствующего в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента. Только в тех случаях, когда компонент 5’-ОН 3’-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки.
указывает на то, что был обнаружен компонент 5’-ОН 3’-ОН. Длина стрелки указывает на количество метаболита, присутствующего в реакционной смеси, которое было определено из отношения площади пика УФ к теоретическому коэффициенту экстинкции этого фрагмента. Только в тех случаях, когда компонент 5’-ОН 3’-ОН не был обнаружен в реакционной смеси, пик 5'-фосфатной природы использовали для количественной оценки.
Фигура 30. Иллюстративные данные масс-спектрометрического анализа расщепления. Вверху: данные для ONT-367: 2,35 мин: 7-мер; 3,16 мин: 8-мер и Р-6-мер; 4,58 мин: Р-7-мер; 5,91 мин: Р-8-мер; 7,19 мин: 12-мер; 9,55 мин: 13-мер; 10,13 мин: Р-11-мер; 11,14 мин: Р-12-мер и 14-мер; 12,11 мин: Р-13-мер; 13,29 мин: Р-14-мер; 14,80 мин: полноразмерная РНК (ONT-388) и 18,33 мин: стереослучайная ДНК (ONT-367). Внизу: данные для ONT-406: 4,72 мин: п-rArUrGrGrCrUrA, 5'-фосфорилированная РНК из 7-мер; 9,46 мин: 5'-rGrUrGrArGrCrArGrCrUrGrCrA (SEQ ID NO: 8), 5’-ОН 3’-ОН РНК из 13-мер; 16,45 мин: полноразмерная РНК (ONT-388); 19,48 и 19,49 мин: стереочистая ДНК (ONT-406).
Фигура 31. Пример скорости расщепления РНК. Дуплексы инкубировали с РНКазой Н1С в присутствии 1-кратного буфера с РНКазой Н при 37°С. Реакции гасили в фиксированные моменты времени путем добавления 30 мМ Na2EDTA. Скорости расщепления определяли путем измерения количества полноразмерной РНК, оставшейся в реакционных смесях. Используемые композиции включают: WV-944, WV-945, WV-936, WV-904, WV-937, WV-905, WV-938, WV-906, WV-939, WV-907, WV-940, WV-908, WV-941 и WV-909.
Фигура 32. A-N: скорости расщепления РНК в анализе с РНКазой Н для определенных композиций, нацеленных на rs362307. Некоторые из этих композиций являются стереослучайными, а некоторые - с контролируемой хиральностью. Используемые композиции включают: WV-1085, WV-1086, WV-1087, WV-1088, WV-1089, WV-1090, WV-1091, WV-1092, WV-905, WV-944, WV-945, WV-911, WV-917, WV-931, WV-937 и WV-1497.
Фигура 33. А: Примеры карт расщепления. Карты расщепления получали из реакционных смесей, полученных после 5 минут инкубации соответствующих дуплексов с РНКазой Н1С в присутствии 1-кратного буфера с РНКазой Н при 37°С. В: Легенда. Стрелки указывают на места расщепления,  указывает, что были идентифицированы как фрагменты 5'-фосфатной природы, так и 3'-ОН природы.
указывает, что были идентифицированы как фрагменты 5'-фосфатной природы, так и 3'-ОН природы. 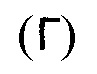 указывает на то, что были обнаружены только фрагменты 5’-ОН 3’-ОН природы и
указывает на то, что были обнаружены только фрагменты 5’-ОН 3’-ОН природы и 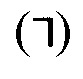 указывает, что был обнаружен 5'-фосфатный компонент. Длина стрелки означает количество фрагмента, присутствующего в реакционной смеси, которое было определено из отношения площади УФ-пика к теоретическому коэффициенту экстинкции этого фрагмента. Только в тех случаях, когда в реакционной смеси не обнаруживались фрагменты 5’-ОН 3’-ОН, для количественной оценки использовали пик 5'-фосфатной природы. Используемые композиции включают: WV-944, WV-945, WV-904, WV-905, WV-906, WV-907, WV-908 и WV-909.
указывает, что был обнаружен 5'-фосфатный компонент. Длина стрелки означает количество фрагмента, присутствующего в реакционной смеси, которое было определено из отношения площади УФ-пика к теоретическому коэффициенту экстинкции этого фрагмента. Только в тех случаях, когда в реакционной смеси не обнаруживались фрагменты 5’-ОН 3’-ОН, для количественной оценки использовали пик 5'-фосфатной природы. Используемые композиции включают: WV-944, WV-945, WV-904, WV-905, WV-906, WV-907, WV-908 и WV-909.
Фигура 34. Примеры карт расщепления. Карты расщепления получали из реакционных смесей, полученных после 30 минут инкубации соответствующих дуплексов с РНКазой H1C в присутствии 1-кратного буфера с РНКазой Н при 37°С. Для легенды смотрите фиг.33. Используемые композиции включают: WV-944, WV-945, WV-936, WV-937, WV-938, WV-939, WV-940, WV-941, WV-1085, WV-1086, WV-1087, WV-1088, WV-1089, WV-1090, WV-1091 и WV-1092.
Фигура 35. Примеры карт расщепления. Для легенды смотрите фиг.33. Используемые композиции включают: WV-944, WV-945, WV-905, WV-911, WV-917, WV-931 HWV-937.
Фигура 36. Общая ионообменная хроматограмма реакции расщепления РНКазой H для WV-937 при образовании дуплексов с РНК НТТ WT (WV-944, верхняя панель) или РНК мутантного НТТ (WV-945, нижняя панель). После гашения ферментативной реакции с динатрием ЭДТА через 30 минут продукты расщепления РНКазой Н хроматографически разрешали и анализировали с использованием Agilent 1290 СВЭЖХ в сочетании с масс-спектрометром Agilent 6230 MS-TOF. Спектры МС с высокой степенью точности с высоким разрешением для каждого идентифицированного пика экстрагировали и деконволюировали. Идентификацию метаболитов, которые приводили к определению положения расщепления, проводили путем сравнения деконволюционных средних масс с массами предсказанных метаболитов РНК.
Фигура 37. Иллюстрация основанного на люциферазном репортере скрининга.
Фигуры 38A-38I. На фиг. 38A-38I и 39A-39G показана активность различных НТТ-олигонуклеотидов. Кривые зависимости от дозы для сайленсинга НТТ в основанном на репортере анализе в клетках COS7 после трансфекции ASO, нацеленных на SNP rs362331_T или rs2530595_T. Специфичность ASO увеличивается без существенной потери мощности путем добавления стереочистого дизайна (указаны рассчитанные IC50). Данные представляют собой 2 независимых эксперимента. Линии показывают кривые по экспериментальным точкам, усы указывают на стандартные отклонения. На фигурах указано местоположение SNP. Композиции, исследуемые на фиг.38, включают: WV-2067, WV-2416, WV-2069, WV-2417, WV-2072, WV-2418, WV-2076, WV-2419, WV-2605, WV-2589, WV-2606, WV-2590, WV-2607, WV-2591, WV-2608, WV-2592, WV-2609, WV-2593, WV-2610, WV-2594, WV-2611, WV-2595, WV-2612, WV -2596, WV-2611, WV-2595, WV-2671, WV-2672, WV-2673, WV-2675, WV-2674, WV-2613, WV-2597, WV-2614, WV-2598, WV-2615, WV-2599, WV-2616, WV-2600, WV-2617, WV-2601, WV-2618, WV-2602, WV-2619, WV-2603, WV-2620 и WV-2604.
Фигуры 39A-39G. Кривые зависимости от дозы для сайленсинга НТТ в репортерном анализе в клетках COS7 после трансфекции ASO. Исследуемые композиции включают: WVE120101, WV-1092, WV-1497, WV-2619, WV-2603, WV-2611 и WV-2595. Также показаны данные IC50.
Фигуры 40A-40D. На фиг. 40A-40D показаны данные жидкостного хроматографа и масс-спектры для олигонуклеотидов: WV1092.22 (WV-1092), WV2595.01 (WV-2595) и WV2603.01 (WV-2603). Используемые в настоящем описании значения (01), (02),.01,.02,.22 и т.д. указывают номера партий.
Фигура 41. На фиг. 41 показаны данные жидкостного хроматографа и масс-спектров для олигонуклеотидов: WV-1510, WV-2378 и WV-2380.
Подробное описание определенных вариантов реализации
Синтетические олигонуклеотиды обеспечивают подходящие молекулярные инструменты для широкого ряда применений. Например, олигонуклеотиды подходят для терапевтических, диагностических, исследовательских применений и в качестве новых наноматериалов. Использование природных нуклеиновых кислот (например, немодифицированной ДНК или РНК) ограничено, например, их чувствительностью к действию эндо- и экзонуклеаз. Таким образом, для устранения указанных недостатков были разработаны различные синтетические аналоги. Они включают синтетические олигонуклеотиды, содержащие модификации остова, которые делают указанные молекулы менее чувствительными к разложению. С точки зрения структуры указанные модификации межнуклеотидных фосфатных линкерных групп делают указанные группы хиральными. Стало очевидно, что на определенные свойства олигонуклеотидов могут влиять конфигурации атомов фосфора, которые образуют остов олигонуклеотидов. Например, в исследованиях in vitro было показано, что на свойства антисмысловых нуклеотидов, такие как аффинность связывания, последовательно-специфическое связывание с комплементарной РНК, стабильность к действию нуклеаз, может влиять помимо прочего хиральность остова (например, конфигурации атомов фосфора).
Помимо всего прочего, настоящее раскрытие охватывает признание того факта, что структурные элементы олигонуклеотидов, такие как последовательность оснований, химические модификации (например, модификации сахара, основания и/или межнуклеотидных линкерных групп и их профили) и/или стереохимия (например, стереохимия хиральных центров остова (хиральных межнуклеотидных линкерных групп) и/или их профилей) могут оказывать значительное влияние на свойства, например, активности, олигонуклеотидов. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что композиции олигонуклеотидов, содержащие олигонуклеотиды с контролируемыми структурными элементами, например, профилями контролируемой химической модификации и/или контролируемой стереохимии цепи, обеспечивают неожиданные свойства, включая, но не ограничиваясь ими, описанные в настоящем документе. Согласно некоторым вариантам осуществления в настоящем описании предусмотрена композиция олигонуклеотидов, содержащая предопределенный уровень олигонуклеотидов отдельного типа олигонуклеотида, которые химически идентичны, например, они содержат одну и ту же последовательность оснований, один и тот же профиль модификаций нуклеозидов (модификаций фрагментов сахара и оснований, если таковые имеются), один и тот же профиль хиральных центров остова и один и тот же профиль модификаций фосфора остова.
Кроме всего прочего, настоящее изобретение охватывает признание того, что препараты стереослучайных олигонуклеотидов содержат множество различных химических объектов, которые отличаются друг от друга, например, по стереохимической структуре отдельных хиральных центров остова в олигонуклеотидной цепи. Без контроля стереохимии хиральных центров остова препараты стереослучайных олигонуклеотидов обеспечивают неконтролируемые композиции, содержащие неопределенные уровни олигонуклеотидных стереоизомеров. Несмотря на то, что эти стереоизомеры могут характеризоваться одной и той же последовательностью оснований, они представляют собой различные химические объекты по меньшей мере из-за их различной стереохимии остова, и они могут характеризоваться, как показано в настоящем документе, различными свойствами, например, биоактивностью. Стереочистая (или «с контролируемой хиральностью») композиция или препарат олигонуклеотида может характеризоваться улучшенной биологической активностью по сравнению со стереослучайным олигонуклеотидным препаратом, который в остальном идентичен (например, как чистые с точки зрения стереоизомерии, так и стереослучайные версии характеризуются одинаковой последовательностью оснований, профилем модификаций оснований и сахара и т.д.). Например, стереослучайная композиция олигонуклеотидов WV-1497 и стереочистая композиция олигонуклеотида WV-1092 характеризуются одинаковой последовательностью оснований и идентичными профилями модификаций сахара и линкерных групп остова, отличающихся только стереохимией. Однако при более высоких концентрациях наблюдалось заметное различие в способности стереочистой композиции WV-1092 и стереослучайной композиции WV-1497 различать мутантный НТТ и НТТ дикого типа (которые отличаются только одним нуклеотидом). При высокой концентрации оба нокаутировали мутантный НТТ в значительной степени, что желательно; но стереочистый WV-1092 показал лишь небольшой нокдаун НТТ дикого типа, в то время как WV-1497 показал значительно больший нокдаун НТТ дикого типа, что в некоторых случаях менее желательно.
Композиции олигонуклеотидов с контролируемой хиральностью как WVE120101, так и WV-1092 способны различать мутантные версии SNP rs362307, и версии дикого типа, которые отличаются одним нуклеотидом; как WVE120101, так и WV-1092 значительно нокаутировали мутантный аллель, но не дикого типа, тогда как стереослучайная версия, WV-1497, не была в состоянии значительно различать мутантные аллели и дикого типа (смотрите фиг. 39D). Модифицированные последовательности WVE120101 и WV-1092 являются идентичными.
Композиция олигонуклеотидов с контролируемой хиральностью WV-2595 была способна различать аллели С и Т в SNP rs2530595, которые также отличаются только одним нуклеотидом. Стереочистая композиция WV-2595 подвергала значительному нокдауну аллель Т, но не аллель С, в отличие от стереослучайной композиции олигонуклеотидов WV-2611, которая не могла значительно различать аллели (смотрите фиг. 39F). Последовательность WV-2595 представляет собой 5'-mG*mGmGmUmC*C*T*C*C*C*C*A*C*A*G*mAmGmGmG*mA-3' или 5'-mG*SmGmGmUmC*SC*ST*SC*SC*SC*SC*SA*SC*RA*SG*SmAmGmGmG*SmA -3' с определенной информацией о стереохимии.
Стереочистая композиция олигонуклеотидов WV-2603 была способна различать аллели С и Т в SNP rs362331, которые также отличаются только одним нуклеотидом. Стереочистая композиция WV-2603 подвергала значительному нокдауну аллель Т, но не аллель С, в отличие от стереослучайной композиции олигонуклеотидов WV-2619, которая не могла существенно различать аллели (смотрите фиг. 39А, 39В, 39С и 39Е). Последовательность WV-2603 представляет собой 5'-mG*mUmGmCmA*C*A*C*A*G*T*A*G*A*T*mGmAmGmG*mG-3' или 5'-mG*SmUmGmCmA*SC*SA*SC*SA*SG*ST*SA*SG*RA*ST*SmGmAmGmG*SmG-3' с определенной информацией о стереохимии.
Согласно некоторым вариантам осуществления последовательность олигонуклеотида в стереочистой (с контролируемой хиральностью) композиции олигонуклеотидов содержит или состоит из последовательности любого описанного в настоящем документе олигонуклеотида. Согласно некоторым вариантам осуществления последовательность олигонуклеотида в стереочистой (с контролируемой хиральностью) композиции олигонуклеотидов содержит или состоит из последовательности любого олигонуклеотида, выбранного из таблиц N1, N2, N3, N4 и 8. Согласно некоторым вариантам осуществления последовательность олигонуклеотида в стереочистой (с контролируемой хиральностью) композиции олигонуклеотидов содержит или состоит из последовательности любого олигонуклеотида, выбранного из таблиц N1A, N2A, N3A, N4A и 8. Согласно некоторым вариантам осуществления последовательность олигонуклеотида в стереочистой (с контролируемой хиральностью) композиции олигонуклеотидов содержит или состоит из последовательности WV-1092, WVE120101, WV-2603 или WV-2595.
Каждый описанный в настоящем документе олигонуклеотид, содержащий последовательность НТТ, представляет собой олигонуклеотид НТТ, который разрабатывали, конструировали и исследовали в различных анализах, согласно некоторым вариантам осуществления в одном или более анализах in vitro. Каждый олигонуклеотид НТТ, перечисленный в любой из таблиц N1A, N2A, N3A, N4A и 8 или описанный в настоящем описании в другом месте, разрабатывали, конструировали и исследовали в различных анализах, согласно некоторым вариантам осуществления в одном или более анализах in vitro. Например, описанные в настоящем документе олигонуклеотиды НТТ исследовали в репортерном анализе с двойной люциферазой. Согласно некоторым вариантам осуществления олигонуклеотиды НТТ исследовали в одном или более других анализах, описанных в этом документе и/или в данной области техники в соответствии с настоящим раскрытием. Согласно некоторым вариантам осуществления олигонуклеотиды НТТ, которые были признаны особенно эффективными в анализе с двойной люциферазой, исследовали в других анализах in vitro и in vivo в соответствии с настоящим раскрытием.
Согласно некоторым вариантам осуществления последовательность олигонуклеотида в стереочистой (с контролируемой хиральностью) композиции олигонуклеотидов включает любое одно или более из следующего: последовательность оснований (включая длину); профиль химических модификаций фрагментов сахара и оснований; профиль линкерных групп остова; профиль природных фосфатных линкерных групп, фосфоротиоатные линкерные группы, фосфоротиоатные триэфирные линкерные группы и их комбинации; профиль хиральных центров остова; профиль стереохимии (Rp/Sp) хиральных межнуклеотидных линкерных групп; профиль фосфорных модификаций остова; профиль модификаций на межнуклеотидном атоме фосфора, например, -S- и -L-R1 формулы I.
Помимо всего прочего, настоящее изобретение предусматривает новые композиции, которые представляют собой или содержат конкретные стереоизомеры представляющих интерес олигонуклеотидов. Согласно некоторым вариантам осуществления конкретный стереоизомер может быть определен, например, посредством его последовательности оснований, его длины, профиля линкерных групп остова и профиля хиральных центров остова. Как понятно в данной области техники, согласно некоторым вариантам осуществления последовательность оснований может относиться к статусу идентичности и/или модификации нуклеозидных остатков (например, компонентов сахара и/или оснований по отношению к стандартным природным нуклеотидам, таким как аденин, цитозин, гуанозин, тимин и урацил) в олигонуклеотиде и/или характеру гибридизации (т.е. способности гибридизоваться с конкретными комплементарными остатками) таких остатков. Согласно некоторым вариантам осуществления олигонуклеотиды в предусмотренных композициях содержат модификации сахара, например, 2'-модификации, например, в области крыла. Согласно некоторым вариантам осуществления олигонуклеотиды в предусмотренных композициях содержат область в середине, например, области сердцевины, которая не содержит модификаций сахара.
Настоящее раскрытие демонстрирует, среди прочего, что отдельные стереоизомеры конкретного олигонуклеотида могут демонстрировать различную стабильность и/или активность (например, функциональные и/или токсические свойства) друг от друга. Более того, настоящее раскрытие демонстрирует, что улучшения стабильности и/или активности, достигаемые посредством включения и/или локализации конкретных хиральных структур в олигонуклеотиде, могут быть сопоставимы или даже лучше, чем те, которые достигаются посредством использования конкретных линкерных групп остова, модификаций остатков и т.д. (например, путем использования определенных типов модифицированных фосфатов (например, фосфоротиоата, замещенного фосфоротиоата и т.д.), модификаций сахара (например, 2'-модификаций и т.д.) и/или модификаций оснований (например, метилирования и т.д.)).
Среди прочего, настоящее раскрытие признает тот факт, что согласно некоторым вариантам осуществления свойства (например, стабильность и/или активности) олигонуклеотида могут быть скорректированы путем оптимизации его профиля хиральных центров остова, необязательно в сочетании с корректировкой/оптимизацией одного или более других признаков (например, линкерного профиля, профиля модификаций нуклеозидов и т.д.) олигонуклеотида. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены композиции олигонуклеотидов, причем олигонуклеотиды содержат модификации нуклеозидов, хиральные межнуклеотидные линкерные группы и природные фосфатные линкерные группы. Например, WV-1092 содержит модификации 2'-ОМе, фосфатные линкерные группы в его областях 5'- и 3'-крыльев и фосфоротиоатные линкерные группы в его областях сердцевины.
Согласно некоторым вариантам осуществления настоящее изобретение демонстрирует, что повышение стабильности, достигаемое за счет включения и/или положения определенных хиральных структур в пределах олигонуклеотида, может быть сравнимо с тем, которое достигается за счет использования модифицированных линкерных групп, оснований и/или сахаров остова (например, путем использования определенных типов модифицированных фосфатов, 2'-модификаций, модификаций оснований и т.д.) или даже быть лучше. Настоящее раскрытие, согласно некоторым вариантам осуществления, также свидетельствует о том, что повышение активности, достигаемое за счет включения и/или положения определенных хиральных структур в пределах олигонуклеотида, может быть сравнимо с тем, которое достигается за счет использования модифицированных линкерных групп, оснований и/или сахаров остова (например, путем использования определенных типов модифицированных фосфатов, 2'-модификаций, модификаций оснований и т.д.) или даже быть лучше.
Согласно некоторым вариантам осуществления включение и/или положение конкретных хиральных линкерных групп внутри олигонуклеотида, может неожиданно изменить профиль расщепления полимера нуклеиновой кислоты, когда такой олигонуклеотид используется для расщепления указанного полимера нуклеиновой кислоты. Например, согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает неожиданно высокую эффективность расщепления целевого полимера нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает новые сайты расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает меньшее количество сайтов расщепления, например, путем блокирования некоторых существующих сайтов расщепления. Еще более неожиданно, согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает расщепление только в одном сайте целевого полимера нуклеиновой кислоты в последовательности, которая комплементарна олигонуклеотиду, используемому для расщепления. Согласно некоторым вариантам осуществления более высокая эффективность расщепления достигается за счет выбора профиля хиральных центров остова, чтобы свести к минимуму количество сайтов расщепления.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены композиции олигонуклеотидов, причем олигонуклеотиды характеризуются одинаковым профилем хиральных центров остова, что неожиданно значительно повышает стабильность и/или биологическую активность олигонуклеотидов. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает повышенную стабильность. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает неожиданно повышенную активность. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает повышенную стабильность и активность. Согласно некоторым вариантам осуществления, когда олигонуклеотид используется для расщепления полимера нуклеиновой кислоты, профиль хиральных центров остова, что неожиданно само по себе, изменяет профиль расщепления целевого полимера нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова эффективно предотвращает расщепление во вторичных сайтах. Согласно некоторым вариантам осуществления профиль хиральных центров остова создает новые сайты расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова сводит к минимуму количество сайтов расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова сводит к минимуму количество сайтов расщепления, так что целевой полимер нуклеиновой кислоты расщепляется только в одном сайте в последовательности целевого полимера нуклеиновой кислоты, который комплементарен олигонуклеотиду (например, расщепление в других сайтах не может быть легко обнаружено определенным способом, согласно некоторым вариантам осуществления происходит расщепление более 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% в таком сайте). Согласно некоторым вариантам осуществления профиль хиральных центров остова повышает эффективность расщепления в сайте расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова олигонуклеотида улучшает расщепление целевого полимера нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова увеличивает селективность. Согласно некоторым вариантам осуществления профиль хиральных центров остова сводит к минимуму эффект нецелевого воздействия. Согласно некоторым вариантам осуществления профиль хиральных центров остова увеличивает селективность, например, селективность расщепления между двумя целевыми последовательностями, отличающимися только однонуклеотидным полиморфизмом (SNP). Согласно некоторым вариантам осуществления профиль хиральных центров остова увеличивает расщепление в сайте расщепления стереослучайной или ДНК-олигонуклеотидной композиции. Согласно некоторым вариантам осуществления профиль хиральных центров остова увеличивает расщепление в основном сайте расщепления стереослучайной или ДНК-олигонуклеотидной композиции. Согласно некоторым вариантам осуществления такой сайт представляет собой основной сайт расщепления олигонуклеотидов, характеризующихся профилем хиральных центров остова. Согласно некоторым вариантам осуществления сайт считается основным сайтом, если он представляет собой сайт, имеющий наибольшее или второе, третье, четвертое или пятое наибольшее расщепление, или сайт, где происходит более 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% расщеплений. Согласно некоторым вариантам осуществления профиль хиральных центров остова содержит или представляет собой (Sp)m(Sp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления профиль хиральных центров остова содержит или представляет собой (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где m>2. Согласно некоторым вариантам осуществления профиль хиральных центров остова содержит или представляет собой (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где n равно 1, t>1 и m>2. Согласно некоторым вариантам осуществления m>3. Согласно некоторым вариантам осуществления m>4.
Согласно некоторым вариантам осуществления настоящее раскрытие признает тот факт, что такие химические модификации, как модификации нуклеозидов и межнуклеотидных линкерных групп, могут обеспечить улучшенные свойства. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что комбинации химических модификаций и стереохимии могут обеспечить неожиданные, значительно улучшенные свойства (например, биоактивность, селективность и т.д.). Согласно некоторым вариантам осуществления химические комбинации, такие как модификации сахаров, оснований и/или межнуклеотидных линкерных групп, объединены с профилями стереохимии, например, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, для получения олигонуклеотидов и их композиций с удивительно улучшенными свойствами. Согласно некоторым вариантам осуществления предусмотренная композиция олигонуклеотидов представляет собой композицию с контролируемой хиральностью и содержит комбинацию 2'-модификации одного или более фрагментов сахара, одной или более природных фосфатных линкерных групп, одной или более фосфоротиоатных линкерных групп и профиля стереохимии (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где m>2. Согласно некоторым вариантам осуществления n равно 1, t>1 и m>2. Согласно некоторым вариантам осуществления m>3. Согласно некоторым вариантам осуществления m>4.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды, определяемые наличием:
1) одинаковой последовательности оснований и длины;
2) одинакового профиля линкерных групп остова, а также
3) одинакового профиля хиральных центров остова, причем композиция представляет собой по существу чистый препарат одного олигонуклеотида в том плане, что предопределенный уровень олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований и длина могут упоминаться как одинаковая последовательность оснований. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований, могут иметь одинаковый профиль модификаций нуклеозидов, например, модификации сахара, модификации оснований и т.д. Согласно некоторым вариантам осуществления профиль нуклеозидных модификаций может быть представлен комбинацией местоположений и модификаций. Например, для WV-1092 профиль модификаций нуклеозидов представляет собой 5 x 2'-ОМе (модификация 2'-ОМе на фрагментах сахара)-ДНК (нет 2'-модификаций сахарного фрагмента)-5 x 2'-ОМе от 5'-конца к 3'-концу. Согласно некоторым вариантам осуществления профиль линкерных групп остова содержит местоположения и типы (например, фосфат, фосфоротиоат, замещенный фосфоротиоат и т.д.) каждой межнуклеотидной линкер ной группы. Согласно некоторым вариантам осуществления олигонуклеотид может характеризоваться заданным профилем линкерных групп остова. Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова nPS-nPO-nPS-nPO-nPS, где РО представляет собой фосфат (фосфодиэфир), PS представляет собой фосфоротиоат, а n равно 1-15, и каждое значение n может быть одинаковым или разным. Согласно некоторым вариантам осуществления по меньшей мере одно значение n больше чем 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20. Согласно некоторым вариантам осуществления по меньшей мере одно значение n для PS больше чем 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20. Согласно некоторым вариантам осуществления значение n для PS между двумя РО больше чем 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20. Согласно некоторым вариантам осуществления n больше чем 5. Согласно некоторым вариантам осуществления n больше чем 6. Согласно некоторым вариантам осуществления n больше чем 7. Согласно некоторым вариантам осуществления n больше чем 8. Согласно некоторым вариантам осуществления n больше чем 9. Согласно некоторым вариантам осуществления n больше чем 10. Согласно некоторым вариантам осуществления n больше чем 11. Согласно некоторым вариантам осуществления n больше чем 12. Согласно некоторым вариантам осуществления n больше чем 13. Согласно некоторым вариантам осуществления n больше чем 14. Согласно некоторым вариантам осуществления n больше чем 15. Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова 1-5PS-1-7РО-5-15PS-1-7РО-1-5PS (что означает от 1 до 5 фосфоротиоатов, от 1 до 7 фосфатов, от 5 до 15 фосфоротиоатов, от 1 до 7 фосфатов и от 1 до 5 фосфоротиоатов). Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова от 5' к 3' в виде 1PS-3PO-11PS-3PO-1PS (что означает 1 фосфоротиоат, 3 фосфата, 11 фосфоротиоатов, 3 фосфата и 1 фосфоротиоат, и который может альтернативно быть представлен в виде PS1 PO3 PS11 PO3 PS1). Например, для WV-1092 профиль линкерных групп остова представляет собой 1PS-3PO-11PS-3PO-1PS от 5'-конца к 3'-концу. Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова 1-5PS-1-7РО-5-15PS-1-7РО-1-5PS, где каждый PS представляет собой Sp, за исключением одного Rp.Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова 1-5PS-1-7РО-5-15PS-1-7РО-1-5PS, где каждый PS представляет собой Sp, за исключением одного PS в любом положении от 5 до 15 PS, который представляет собой Rp.Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова 1-5PS-1-7РО-5-15PS-1-7РО-1-5PS, причем каждый PS представляет собой Sp, за исключением того, что 10-й PS по счету от 5'-конца, представляет собой Rp. Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова 1-5PS-1-7РО-5-15PS-1-7PO-1-5PS, причем каждый PS представляет собой Sp, за исключением того, что 9-й по счету от 5'-конца PS представляет собой Rp. Согласно некоторым вариантам осуществления олигонуклеотид характеризуется профилем линкерных групп остова 1-5PS-1-7РО-5-15PS-1-7РО-1-5PS, причем каждый PS представляет собой Sp, за исключением того, что 11-й по счету от 5'-конца PS представляет собой Rp. Профиль хиральных центров остова олигонуклеотида может быть обозначен с помощью комбинации стереохимии фосфоров линкерных групп (Rp/Sp) от 5' к 3'. Например, WV-1092 имеет профиль 1S-3PO (фосфат)-8S-1R-2S-3PO-1S, a WV-937 имеет профиль 12S-1R-6S. Согласно некоторым вариантам осуществления все нехиральные линкерные группы (например, РО) могут быть опущены при описании профиля хиральных центров остова. Как проиллюстрировано выше, местоположения нехиральных линкерных групп могут быть получены, например, из профиля линкерных групп остова. Любая раскрытая в настоящем документе последовательность может быть объединена с любыми профилями хиральных центров остова и/или любыми профилями хиральных центров остова, описанными в настоящем документе. Последовательности оснований, профили хиральных центров остова, профили стереохимии (например, Rp или Sp), профили модификаций оснований, профили хиральных центров остова и т.д. представлены в направлении от 5' к 3', если не указано иное.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композицию олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она является обогащенной по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида.
Примером, по существу, рацемического получения олигонуклеотидов является получение фосфоротиоатных олигонуклеотидов посредством сульфирования фосфитных триэфиров из обычно используемого фосфорамидитного олигонуклеотидного синтеза либо с тетраэтилтиурамдисульфидом или (TETD), либо 3Н-1,2-бензодитиол-3-он-1,1-диоксидом (BDTD), хорошо известным в данной области техники. Согласно некоторым вариантам осуществления, по существу, рацемическое получение олигонуклеотидов обеспечивает по существу рацемические композиции олигонуклеотидов (или композиции олигонуклеотидов с контролируемой хиральностью).
Как понятно специалисту в данной области техники, стереослучайный или рацемический препарат олигонуклеотидов получают путем не стереоселективного и/или низкостероселективного связывания нуклеотидных мономеров, как правило, без использования каких-либо хиральных вспомогательных веществ, реагентов хиральной модификации и/или хиральных катализаторов. Согласно некоторым вариантам осуществления при по существу рацемическом (или хирально неконтролируемом) получении олигонуклеотидов, все или большинство стадий связывания не регулируются с помощью хирального контроля, так как стадии связывания проводятся без специального контроля хиральности для обеспечения повышенной стереоселективности. Примером по существу рацемического получения олигонуклеотидов является получение фосфоротиоатных олигонуклеотидов посредством сульфирования фосфитных триэфиров из обычно используемого фосфорамидитного олигонуклеотидного синтеза либо с тетраэтилтиурамдисульфидом или (TETD), либо 3Н-1,2-бензодитиол-3-он-1,1-диоксидом (BDTD), хорошо известным в данной области техники. Согласно некоторым вариантам осуществления по существу рацемическое получение олигонуклеотидов обеспечивает по существу рацемические композиции олигонуклеотидов (или композиции олигонуклеотидов с контролируемой хиральностью). Согласно некоторым вариантам осуществления по меньшей мере одно связывание нуклеотидного мономера имеет диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере два связывания нуклеотидного мономера имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере три связывания нуклеотидного мономера имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере четыре связывания нуклеотидного мономера имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере пять связываний нуклеотидного мономера имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления в стереочистых или рацемических препаратах по меньшей мере одна межнуклеотидная линкерная группа имеет диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере две межнуклеотидные линкерные группы имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере три межнуклеотидные линкерные группы имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере четыре межнуклеотидные линкерные группы имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления по меньшей мере пять межнуклеотидных линкерных групп имеют диастереоселективность ниже чем примерно 60:40, 70:30, 80:20, 85:15, 90:10, 91:9, 92:8, 97:3, 98:2 или 99:1. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 60:40. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 70:30. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 80:20. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 91:9. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 92:8. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 93:7. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 94:6. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 95:5. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 96:4. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 97:3. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 98:2. Согласно некоторым вариантам осуществления диастереоселективность ниже чем примерно 99:1. Согласно некоторым вариантам осуществления по меньшей мере одна связь имеет диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере две связи имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере три связи имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере четыре связи имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере пять связей имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере одна межнуклеотидная линкерная группа имеет диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере две межнуклеотидные линкерные группы имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере три межнуклеотидные линкерные группы имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере четыре межнуклеотидные линкерные группы имеют диастереоселективность ниже чем примерно 90:10. Согласно некоторым вариантам осуществления по меньшей мере пять межнуклеотидных линкерных групп имеют диастереоселективность ниже чем примерно 90:10.
Как понятно специалисту в данной области техники, согласно некоторым вариантам осуществления диастереоселективность связи или линкерной группы может быть оценена посредством диастереоселективности образования димера в тех же или сопоставимых условиях, где димер имеет те же самые 5'- и 3'-нуклеозиды и межнуклеотидные линкерные группы. Например, диастереоселективность подчеркнутой связи или линкерной группы в WV-1092 mG*SmGmCmAmC*SA*SA*SG*SG*SG*SC*SA*SC*RA*SG*SmAmCmUmU*SmC можно оценить из связи двух G-фрагментов в таких же или сопоставимых условиях, например, мономеры, хиральные вспомогательные вещества, растворители, активаторы, температуры и т.д.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрены композиции олигонуклеотидов с контролируемой хиральностью (и/или стереохимически чистые), содержащие олигонуклеотиды, определяемые наличием:
1) одинаковой последовательности оснований и длины;
2) одинакового профиля линкерных групп остова, а также
3) одинакового профиля хиральных центров остова, причем эта композиция представляет собой по существу чистый препарат одного олигонуклеотида в том отношении, что по меньшей мере примерно 10% олигонуклеотидов в композиции имеют одинаковую последовательность основания и длину, одинаковый профиль линкерных групп остова и одинаковый профиль хиральных центров остова.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью олигонуклеотидов в том отношении, что композиция обогащена по сравнению с по существу рацемическим препаратом тех же олигонуклеотидов, олигонуклеотидами одного типа олигонуклеотида. Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью олигонуклеотидов в том отношении, что композиция обогащена по сравнению с по существу рацемическим препаратом тех же олигонуклеотидов, олигонуклеотидами одного типа олигонуклеотида, которые совместно характеризуются:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова,
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида.
Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций фосфора остова и одинаковый профиль модификаций оснований. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций нуклеозидов. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют идентичные структуры.
Согласно некоторым вариантам осуществления олигонуклеотиды типа олигонуклеотида характеризуются одинаковым профилем модификаций фосфора и одинаковым профилем модификаций сахара остова. Согласно некоторым вариантам осуществления олигонуклеотиды типа олигонуклеотида характеризуются одинаковым профилем модификаций фосфора и одинаковым профилем модификаций оснований остова. Согласно некоторым вариантам осуществления олигонуклеотиды типа олигонуклеотида характеризуются одинаковым профилем модификаций фосфора и одинаковым профилем модификаций нуклеозидов остова. В некоторых вариантах олигонуклеотиды типа олигонуклеотида являются идентичными.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой по существу чистый препарат типа олигонуклеотида в том отношении, что олигонуклеотиды в композиции, которые не являются типа олигонуклеотида, представляют собой загрязненную форму процесса подготовки указанного типа олигонуклеотида, в некоторых случаях, после определенных процедур очистки.
Согласно некоторым вариантам осуществления по меньшей мере примерно 20% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 25% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 30% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 35% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 40% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 45% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 50% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 55% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 60% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 65% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 70% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 75% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 80% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 85% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 90% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 92% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 94% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 95% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления по меньшей мере примерно 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления более чем примерно 99% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова. Согласно некоторым вариантам осуществления чистота композиции олигонуклеотидов с контролируемой хиральностью олигонуклеотида может быть выражена как процент олигонуклеотидов в композиции, которые характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций фосфора остова. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций фосфора остова и одинаковый профиль модификаций нуклеозидов. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций фосфора остова и одинаковый профиль модификаций сахара. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций фосфора остова и одинаковый профиль модификаций оснований. Согласно некоторым вариантам осуществления олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, имеют одинаковый профиль модификаций фосфора остова и одинаковый профиль модификаций нуклеозидов. В некоторых вариантах олигонуклеотиды, характеризующиеся одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова, идентичны.
Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях характеризуются одинаковым профилем модификаций фосфора остова. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований типа олигонуклеотида. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов, которая характеризуется контролируемой хиральностью в том отношении, что композиция содержит предопределенный уровень олигонуклеотидов отдельного типа олигонуклеотида, причем тип олигонуклеотидов определяется:
1) последовательностью оснований;
2) профилем линкерных групп остова;
3) профилем хиральных центров остова; а также
4) профилем модификаций фосфора остова.
Как отмечено выше и понятно в данной области техники, согласно некоторым вариантам осуществления последовательность оснований олигонуклеотида может относиться к статусу идентичности и/или модификации нуклеозидных остатков (например, компонентов сахара и/или оснований относительно стандартных природных нуклеотидов, таких как аденин, цитозин, гуанозин, тимин и урацил) в олигонуклеотиде и/или к характеру гибридизации (т.е. способности гибридизоваться с конкретными комплементарными остатками) таких остатков.
Согласно некоторым вариантам осуществления определенный тип олигонуклеотида может быть определен посредством
1A) идентичности оснований;
1B) профиля модификации оснований;
1C) профиля модификации сахара;
2) профиля линкерных групп остова;
3) профиля хиральных центров остова; а также
4) профиля модификаций фосфора остова.
Таким образом, согласно некоторым вариантам осуществления олигонуклеотиды определенного типа могут характеризоваться идентичными основаниями, но отличаться по своему профилю модификаций оснований и/или модификаций сахаров. Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа могут характеризоваться идентичными основаниями и профилем модификаций оснований (включая, например, отсутствие модификации оснований), но различаться по профилю модификаций сахаров.
В некоторых вариантах олигонуклеотиды определенного типа идентичны в том отношении, что они имеют одну и ту же последовательность оснований (включая длину), один и тот же профиль химических модификаций фрагментов сахара и оснований, один и тот же профиль линкерных групп остова (например, профиль природных фосфатных линкерных групп, фосфоротиоатных линкерных групп, фосфоротиоатных триэфирных линкерных групп и их комбинации), один и тот же профиль хиральных центров остова (например, профиль стереохимии (Rp/Sp) хиральных межнуклеотидных линкерных групп) и один и тот же профиль модификаций фосфора остова (например, профиль модификаций на межнуклеотидном атоме фосфора, такой как -S- и -L-R1 формулы I).
Согласно некоторым вариантам осуществления чистота композиции олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида выражается как процент олигонуклеотидов в композиции, которые относятся к типу олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 10% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотида. Согласно некоторым вариантам осуществления по меньшей мере примерно 20% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 30% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 40% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 50% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 60% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 70% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 80% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 90% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 92% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 94% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 95% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 96% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 97% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 98% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов. Согласно некоторым вариантам осуществления по меньшей мере примерно 99% олигонуклеотидов в композиции олигонуклеотидов с контролируемой хиральностью представляют собой одинаковый тип олигонуклеотидов.
Согласно некоторым вариантам осуществления чистоту композиции олигонуклеотидов с контролируемой хиральностью можно задавать с помощью стереоселективности каждой стадии связывания в процессе ее получения. Согласно некоторым вариантам осуществления стадия связывания характеризуется стереоселективностью (например, диастереоселективностью), составляющей 60% (60% новой межнуклеотидной линкерной группы, образованной на стадии связывания, характеризуется предполагаемой стереохимией). После такой стадии связывания новая образованная межнуклеотидная линкерная группа может характеризоваться чистотой 60%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 60%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 70%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 80%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 85%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 90%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 91%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 92%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 93%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 94%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 95%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 96%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 97%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 98%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 99%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей по меньшей мере 99,5%. Согласно некоторым вариантам осуществления каждая стадия связывания характеризуется стереоселективностью, составляющей практически 100%. Согласно некоторым вариантам осуществления стадия связывания характеризуется стереоселективностью, составляющей практически 100%, в том отношении, что весь обнаруживаемый продукт после стадии связывания аналитическим способом (например, ЯМР, ВЭЖХ и т.д.), характеризуется предполагаемой стереоселективностью.
Помимо всего прочего, настоящее раскрытие признает тот факт, что комбинации структурных элементов олигонуклеотидов (например, профилей химических модификаций, линкерных групп остова, хиральных центров остова и/или модификаций фосфора остова) могут обеспечить удивительно улучшенные свойства, такие как биоактивность.
Согласно некоторым вариантам осуществления в настоящем раскрытии предусмотрена композиция олигонуклеотидов, содержащая предварительно определенный уровень олигонуклеотидов, которые содержат одну или более областей крыла и одинаковую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и необязательно содержит одну или более хиральных межнуклеотидных линкерных групп;
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп, а одинаковая область сердцевины характеризуется:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления область крыла содержит структурную особенность, которая не находится в области сердцевины. Согласно некоторым вариантам осуществления крыло и сердцевина могут быть определены любыми структурными элементами, например, модификациями оснований (например, метилированные/неметилированные, метилирование в положении 1/метилирование в положении 2 и т.д.), модификациями сахара (например, модифицированный/немодифицированный, 2'-модификация/другой тип модификации, один тип 2'-модификации/другой тип 2'-модификации и т.д.), типами линкерных групп остова (например, фосфат/фосфоротиоат, фосфоротиоат/замещенный фосфоротиоат и т.д.), стереохимией хирального центра остова (например, все Sp/все Rp, (SpRp) повторы/все Rp и т.д.), типами модификаций фосфора остова (например, s1/s2, s1/s3 и т.д.) и т.д.
Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями нуклеозидов, причем крыло содержит модификацию нуклеозидов, которую не содержит область сердцевины. Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями сахара, причем крыло содержит модификацию сахара, которую не содержит область сердцевины. Согласно некоторым вариантам осуществления модификация сахара представляет собой 2'-модификацию. Согласно некоторым вариантам осуществления модификация сахара представляет собой 2'-OR1. Согласно некоторым вариантам осуществления модификация сахара представляет собой 2'-МОЕ. Согласно некоторым вариантам осуществления модификация сахара представляет собой 2'-ОМе. Дополнительно примеры модификаций сахара описаны в настоящем описании.
Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях содержат структуру крыло-сердцевина (гемимер). Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях содержат структуру крыло-сердцевина модификаций нуклеозидов. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях содержат структуру сердцевина-крыло (другой тип гемимера). Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях содержат структуру сердцевина-крыло нуклеозидных модификаций. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях имеют структуру крыло-сердцевина крыло (гэпмер). Согласно некоторым вариантам осуществления олигонуклеотиды в предложенных композициях имеют структуру крыло-сердцевина-крыло нуклеозидных модификаций. Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями сахарных фрагментов. Согласно некоторым вариантам осуществления крыло и сердцевина определяются модификациями фрагментов оснований. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется одинаковой 2'-модификацией, которая не находится в области сердцевины. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется одинаковой 2'-модификацией, которая отличается от любых модификаций сахара в области сердцевины. Согласно некоторым вариантам осуществления область сердцевины не содержит модификации сахара. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется одинаковой 2'-модификацией, а область сердцевины не содержит 2'-модификаций. Согласно некоторым вариантам осуществления, когда присутствуют два или более крыльев, каждое крыло определяется его собственными модификациями. Согласно некоторым вариантам осуществления каждое крыло содержит свою собственную характерную модификацию сахара. Согласно некоторым вариантам осуществления каждое крыло содержит одинаковую характерную модификацию сахара, отличающую его от сердцевины. Согласно некоторым вариантам осуществления каждый фрагмент сахара крыла характеризуется одинаковой модификацией. Согласно некоторым вариантам осуществления каждый фрагмент сахара крыла характеризуется одинаковой 2'-модификацией. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется одинаковой 2'-модификацией, но одинаковая 2'-модификация в первой области крыла может быть либо такой же, либо отличной от одинаковой 2'-модификации во второй области крыла. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется одинаковой 2'-модификацией, а одинаковая 2'-модификация в первой области крыла такая же, как и одинаковая 2'-модификация во второй области крыла. Согласно некоторым вариантам осуществления каждый фрагмент сахара в области крыла характеризуется одинаковой 2'-модификацией, а одинаковая 2'-модификация в первой области крыла отличается от одинаковой 2'-модификации во второй области крыла.
Согласно некоторым вариантам осуществления предусмотренные препараты с контролируемой хиральностью (и/или стереохимически чистые) представляют собой антисмысловые олигонуклеотиды (например, chiromersen). Согласно некоторым вариантам осуществления предусмотренные препараты с контролируемой хиральностью (и/или стереохимически чистые) представляют собой олигонуклеотиды-миРНК. Согласно некоторым вариантам осуществления предусмотренная композиция олигонуклеотидов с контролируемой хиральностью представляет собой композицию из олигонуклеотидов, которые могут представлять собой антисмысловой олигонуклеотид, антагомир, микроРНК, пре-микроРНК, антимир, супермир, рибозим, Ul адаптор, активатор РНК, агент РНК-интерференции, олигонуклеотид-«ловушка», образующий триплекс олигонуклеотид, аптамер или адъювант. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой антисмысловые олигонуклеотиды. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-антагомир. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-микроРНК. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-микроРНК. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды антимир. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды супермир. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-рибозимы. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды Ul адаптеры. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-активаторы РНК. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-агенты РНК-интерференции. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-«ловушки». Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой образующие триплекс олигонуклеотиды. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой олигонуклеотиды-аптамеры. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой адъювантные олигонуклеотиды.
Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) представляют собой олигонуклеотиды, которые включают одну или более модифицированных линкерных групп, оснований и/или сахаров остова.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит две или более хиральные линкерные группы с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит три или более хиральные линкерные группы с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит четыре или более хиральные линкерные группы с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит пять или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 5 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 6 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 7 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 8 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 9 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 10 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 11 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 12 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 13 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 14 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 15 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 16 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 17 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 18 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 19 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 20 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 21 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 22 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 23 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 24 или более хиральных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида содержит 25 или более хиральных линкерных групп с модифицированными фосфатами.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% хиральных линкерных групп с модифицированными фосфатами. Примеры таких хиральных линкерных групп с модифицированными фосфатами описаны выше и в настоящем документе. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% хиральных линкерных групп с модифицированными фосфатами в конфигурации Sp.
Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 80%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 85%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 90%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 91%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 92%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 93%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 94%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 95%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 96%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 97%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 98%. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) характеризуются стереохимической чистотой, составляющей более чем примерно 99%.
Согласно некоторым вариантам осуществления хиральная линкерная группа с модифицированными фосфатами представляет собой хиральную фосфоротиоатную линкерную группу, т.е. фосфоротиоатную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% хиральных фосфоротиоатных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления все хиральные линкерные группы с модифицированными фосфатами представляют собой хиральные фосфоротиоатные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления по меньшей мере примерно 10, 20, 30, 40, 50, 60, 70, 80 или 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 10% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 20% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 30% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 40% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 50% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 60% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 70% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 80% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 95% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Sp. Согласно некоторым вариантам осуществления по меньшей мере примерно 10, 20, 30, 40, 50, 60, 70, 80 или 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 10% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 20% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 30% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 40% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 50% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 60% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 70% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 80% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления по меньшей мере примерно 95% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 10, 20, 30, 40, 50, 60, 70, 80, или 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 10% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 20% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 30% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 40% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 50% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 60% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 70% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 80% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления менее чем примерно 95% хиральных фосфоротиоатных межнуклеотидных линкерных групп предложенного олигонуклеотида характеризуются конформацией Rp. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит только одну хиральную фосфоротиоатную межнуклеотидную линкерную группу в конформации Rp. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит только одну хиральную фосфоротиоатную межнуклеотидную линкерную группу в конформации Rp, причем все межнуклеотидные линкерные группы представляют собой хиральные фосфоротиоатные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления хиральная фосфоротиоатная межнуклеотидная линкерная группа представляет собой хиральную фосфоротиоатную диэфирную линкерную группу. Согласно некоторым вариантам осуществления каждая хиральная фосфоротиоатная межнуклеотидная линкерная группа независимо представляет собой хиральную фосфоротиоатную диэфирную линкерную группу. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа независимо представляет собой хиральную фосфоротиоатную диэфирную линкерную группу. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа независимо представляет собой хиральную фосфоротиоатную диэфирную линкерную группу и только одна характеризуется Rp-конфигурацией.
Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, которые содержат одно или более модифицированных оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, которые не содержат модифицированных оснований. Примеры таких модифицированных оснований описаны выше и в настоящем документе.
Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или 10 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предлагаемых композиций содержат по меньшей мере одну линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере две линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере три линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере четыре линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере пять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере шесть природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере семь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере восемь природных фоосфатных линкерных групп. В некоторых вариантах олигонуклеотиды предложенных композиций содержат по меньшей мере девять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере десять природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат 2, 3, 4, 5, 6, 7, 8, 9 или 10 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат одну линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат две линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат три линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат четыре линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат пять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат шесть природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат семь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат восемь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат девять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат десять природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или 10 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере две последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере три последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере четыре последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере пять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере шесть последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере семь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере восемь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере девять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат по меньшей мере десять последовательных природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат 2, 3, 4, 5, 6, 7, 8, 9 или 10 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат две последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат три последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат четыре последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат пять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат шесть последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат семь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат восемь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат девять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций содержат десять последовательных природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 8 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 9 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 10 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 11 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 12 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 13 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 14 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 15 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 16 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 17 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 18 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 19 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 20 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 21 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 22 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 23 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 24 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 25 оснований. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) состоят из олигонуклеотидов, имеющих одинаковую последовательность оснований по меньшей мере из 30, 35, 40, 45, 50, 55, 60, 65, 70 или 75 оснований.
Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) содержат олигонуклеотиды, содержащие один или более остатков, которые модифицированы в фрагменте сахара. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) содержат олигонуклеотиды, содержащие один или более остатков, которые модифицированы в положении 2' фрагмента сахара (модификация, называемая в настоящем документе как «2'-модификация»). Примеры таких модификаций описаны выше и в настоящем документе и включают, но не ограничиваются ими, 2'-ОМе, 2'-МОЕ, 2'-LNA, 2'-F, FRNA, FANA, S-cEt и т.д. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) содержат олигонуклеотиды, содержащие один или более остатков, которые представляют собой 2'-модифицированные. Например, согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат один или более остатков, которые представляют собой 2'-O-метоксиэтил-(2'-МО)-модифицированные остатки. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) содержат олигонуклеотиды, которые не содержат никаких 2'-модификаций. Согласно некоторым вариантам осуществления предложенные препараты с контролируемой хиральностью (и/или стереохимически чистые) содержат олигонуклеотиды, которые не содержат какие-либо остатки 2'-МОЕ. То есть согласно некоторым вариантам осуществления предложенные олигонуклеотиды не являются МОЕ-модифицированными. Дополнительные примеры модификации сахара описаны в настоящем описании.
Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат общий мотив крыло-сердцевина или сердцевина-крыло (гемимер, также представленный в настоящем документе в общем виде как X-Y- или Y-X, соответственно. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат общий мотив крыло-сердцевина-крыло (гэпмер, также представленный в настоящем документе в общем виде как X-Y-X). Согласно некоторым вариантам осуществления каждое крыло независимо содержит один или более остатков, имеющих определенную модификацию, причем такая модификация отсутствует в сердцевинной части «Y». Согласно некоторым вариантам осуществления каждое крыло независимо содержит один или более остатков, имеющих конкретную нуклеозидную модификацию, причем эта модификация отсутствует в сердцевинной части «Y». Согласно некоторым вариантам осуществления каждое крыло независимо содержит один или более остатков, имеющих конкретную модификацию оснований, причем эта модификация отсутствует в сердцевинной части «Y». Согласно некоторым вариантам осуществления каждое крыло независимо содержит один или более остатков, имеющих конкретную модификацию сахара, причем эта модификация отсутствует в сердцевинной части «Y». Примеры модификаций сахара широко известны в данной области техники. Согласно некоторым вариантам осуществления модификация сахара представляет собой модификацию, выбранную из тех модификаций, которые описаны в US 9006198, причем модификации сахара включены в настоящее описание посредством ссылок. Дополнительные примеры модификаций сахара описаны в настоящем описании. Согласно некоторым вариантам осуществления каждое крыло содержит один или более остатков, имеющих 2'-модификацию, которая не присутствует в сердцевинной части. Согласно некоторым вариантам осуществления 2'-модификация представляет собой 2'-OR1, где R1 является таким, как определено и описано в настоящем раскрытии.
Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина, представленный как X-Y, или мотив сердцевина-крыло, представленный как Y-X, в котором остатки в части «X» представляют собой остатки с модифицированным сахаром определенного типа и остатки в сердцевинной части «Y» не представляют собой остатки с модифицированным сахаром такого же определенного типа. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина-крыло, представленный как X-Y-X, в котором остатки в каждой части «X» представляют собой остатки с модифицированным сахаром определенного типа и остатки в сердцевинной части «Y» не представляют собой остатки с модифицированным сахаром такого же типа. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина, представленный как X-Y, или мотив сердцевина-крыло, представленный как Y-X, в котором остатки в части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» не представляют собой 2'-модифицированные остатки такого же определенного типа. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина, представленный как X-Y, в котором остатки в части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» не представляют собой 2'-модифицированные остатки того же определенного типа. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив сердцевина-крыло, представленный как Y-X, в котором остатки в части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» не представляют собой 2'-модифицированные остатки того же определенного типа. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина-крыло, представленный как X-Y-X, в котором остатки в каждой части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» не представляют собой 2'-модифицированные остатки такого же определенного типа. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина, представленный как X-Y, в котором остатки в части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» представляют собой 2'-дезоксирибонуклеозид. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив сердцевина-крыло, представленный как Y-X, в котором остатки в части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» представляют собой 2'-дезоксирибонуклеозид. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина-крыло, представленный как X-Y-X, в котором остатки в каждой части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» представляют собой 2'-дезоксирибонуклеозид. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина-крыло, представленный как X-Y-X, в котором остатки в каждой части «X» представляют собой 2'-модифицированные остатки определенного типа и остатки в сердцевинной части «Y» представляют собой 2'-дезоксирибонуклеозид. Например, согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина-крыло, представленный в виде X-Y-X, в котором остатки в каждой части «X» представляют собой 2'-МОЕ-модифицированные остатки и остатки в сердцевинной части «Y» не представляют собой 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат мотив крыло-сердцевина-крыло, представленный как X-Y-X, в котором остатки в каждой части «X» представляют собой 2'-МОЕ-модифицированные остатки и остатки в сердцевинной части «Y» представляют собой 2'-дезоксирибонуклеозид. Специалисту в соответствующих областях техники будет понятно, что все такие описанные выше и в данном описании 2'-модификации рассматриваются в контексте таких мотивов X-Y, Y-X и/или X-Y-X.
Согласно некоторым вариантам осуществления крыло составляет в длину одно или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину два или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину три или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину четыре или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину пять или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину шесть или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину семь или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину восемь или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину девять или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину десять или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 11 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 12 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 13 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 14 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 15 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 16 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 17 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 18 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 19 или более оснований. Согласно некоторым вариантам осуществления крыло составляет в длину десять или более оснований.
Согласно некоторым вариантам осуществления крыло составляет в длину одно основание. Согласно некоторым вариантам осуществления крыло составляет в длину два основания. Согласно некоторым вариантам осуществления крыло составляет в длину три основания. Согласно некоторым вариантам осуществления крыло составляет в длину четыре основания. В некоторых вариантах крыло составляет в длину пять оснований. Согласно некоторым вариантам осуществления крыло составляет в длину шесть оснований. Согласно некоторым вариантам осуществления крыло составляет в длину семь оснований. Согласно некоторым вариантам осуществления крыло составляет в длину восемь оснований. Согласно некоторым вариантам осуществления крыло составляет в длину девять оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 10 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 11 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 12 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 13 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 14 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 15 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 16 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 17 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 18 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину 19 оснований. Согласно некоторым вариантам осуществления крыло составляет в длину десять оснований.
В некоторых вариантах крыло содержит одну или более хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит одну или более хиральных межнуклеотидных линкерных групп и одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит одну или более хиральных межнуклеотидных линкерных групп и две или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит одну или более хиральных межнуклеотидных линкерных групп и две или более природных фоосфатных линкерных групп, причем две или более линкерные группы с природными фосфатами являются последовательными. Согласно некоторым вариантам осуществления крыло не содержит хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждая линкерная группа крыла представляет собой линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления крыло не содержит линкерных групп с фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо представляет собой хиральную межнуклеотидную линкерную группу.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну или более хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну или более хиральных межнуклеотидных линкерных групп и одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну или более хиральных межнуклеотидных линкерных групп и две или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну или более хиральных межнуклеотидных линкерных групп и две или более природных фоосфатных линкерных групп, причем две или более природных фоосфатных линкерных групп являются последовательными.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере две хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере три хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере четыре хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере пять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере шесть хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере семь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере восемь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере девять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере десять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 11 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 12 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 13 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 14 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 15 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 16 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 17 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 18 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 19 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 20 хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления каждое крыло независимо содержит две хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит три хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит четыре хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит пять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит шесть хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит семь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит восемь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит девять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит десять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 11 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 12 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 13 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 14 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 15 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 16 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 17 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 18 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 19 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 20 хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере одну последовательную линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере две последовательные хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере три последовательные хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере четыре последовательные хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере пять последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере шесть последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере семь последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере восемь последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере девять последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере десять последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 11 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 12 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 13 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 14 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 15 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 16 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 17 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 18 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 19 последовательных хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 20 последовательных хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну последовательную линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления каждое крыло независимо содержит две последовательные хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит три последовательные хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит четыре последовательные хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждое крыло независимо содержит пять последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит шесть последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит семь последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит восемь последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит девять последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит десять последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 11 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 12 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 13 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 14 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 15 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 16 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 17 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 18 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 19 последовательных хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 20 последовательных хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере одну линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере две линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере три линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере четыре линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере пять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере шесть природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере семь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере восемь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере девять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере десять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 11 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 12 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 13 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 14 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 15 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 16 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 17 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 18 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 19 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 20 природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления каждое крыло независимо содержит две линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит три линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит четыре линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит пять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит шесть природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит семь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит восемь природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит девять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит десять природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 11 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 12 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 13 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 14 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 15 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 16 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 17 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 18 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 19 природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 20 природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере одну последовательную линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере две последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере три последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере четыре последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере пять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере шесть последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере семь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере восемь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере девять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере десять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 11 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 12 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 13 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 14 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 15 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 16 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 17 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 18 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 19 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит по меньшей мере 20 последовательных природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления каждое крыло независимо содержит одну последовательную линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления каждое крыло независимо содержит две последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит три последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит четыре последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления каждое крыло независимо содержит пять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит шесть последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит семь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит восемь последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит девять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит десять последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 11 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 12 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 13 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 14 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 15 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 16 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 17 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 18 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 19 последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления каждое крыло независимо содержит 20 последовательных природных фоосфатных линкерных групп.
Согласно некоторым вариантам осуществления крыло содержит только одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 5'-конце крыла. Согласно некоторым вариантам осуществления крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 5'-конце крыла, а хиральная межнуклеотидная линкерная группа представляет собой Rp. Согласно некоторым вариантам осуществления крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 5'-конце крыла, а хиральная межнуклеотидная линкерная группа представляет собой Sp. Согласно некоторым вариантам осуществления крыло 3'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 3'-конце крыла. Согласно некоторым вариантам осуществления крыло 3'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 3'-конце крыла, а хиральная межнуклеотидная линкерная группа представляет собой Rp. Согласно некоторым вариантам осуществления крыло 3'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 3'-конце крыла, а хиральная межнуклеотидная линкерная группа представляет собой Sp.
Согласно некоторым вариантам осуществления крыло содержит две или более природных фосфатных линкерных групп. Согласно некоторым вариантам осуществления все фосфатные линкерные группы внутри крыла являются последовательными, и нет никаких нефосфатных линкерных групп между любыми двумя фосфатными линкерными группами внутри крыла.
Согласно некоторым вариантам осуществления линкерная группа, соединяющая крыло и сердцевину, рассматривается как часть сердцевины при описании линкерных групп, например, химии линкерных групп, стереохимии линкерных групп и т.д. Например, в WV-1092 mG*SmGmCmAmC*SA*SA*SG*SG*SG*SC*SA*SC*RA*SG*SmAmCmUmU*SmC, подчеркнутые линкерные группы могут рассматриваться как часть сердцевины (жирные), его 5'-крыло (содержащее 2'-ОМе на остатках сахара) имеет одну единственную фосфоротиоатную линкерную группу Sp на своем 5'-конце, его 3'-крыло (содержащее 2'-ОМе на остатках сахара) имеет одну фосфоротиоатную линкерную группу Sp на своем 3'-конце, и его сердцевина не содержит 2'-модификаций на сахаре).
Согласно некоторым вариантам осуществления 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой модифицированную линкерную группу. Согласно некоторым вариантам осуществления 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой линкерную группу, характеризующуюся структурой формулы I. Согласно некоторым вариантам осуществления 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации представляет собой фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой замещенную фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную триэфирную линкерную группу. Согласно некоторым вариантам осуществления каждая 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой модифицированную линкерную группу. Согласно некоторым вариантам осуществления каждая 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой линкерную группу, характеризующуюся структурой формулы I. Согласно некоторым вариантам осуществления каждая 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления каждая 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой замещенную фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления каждая 5'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную триэфирную линкерную группу.
Согласно некоторым вариантам осуществления 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой модифицированную линкерную группу. Согласно некоторым вариантам осуществления 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой линкерную группу, характеризующуюся структурой формулы I. Согласно некоторым вариантам осуществления 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой замещенную фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную триэфирную линкерную группу. Согласно некоторым вариантам осуществления каждая 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой модифицированную линкерную группу. Согласно некоторым вариантам осуществления каждая 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой линкерную группу, характеризующуюся структурой формулы I. Согласно некоторым вариантам осуществления каждая 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления каждая 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой замещенную фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления каждая 3'-межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную триэфирную линкерную группу.
Согласно некоторым вариантам осуществления обе межнуклеотидные линкерные группы, связанные с фрагментом сахара без 2'-модификации, представляют собой модифицированные линкерные группы. Согласно некоторым вариантам осуществления обе межнуклеотидные линкерные группы, связанные с фрагментом сахара без 2'-модификации, представляют собой линкерные группы, характеризующиеся структурой формулы I. Согласно некоторым вариантам осуществления обе межнуклеотидные линкерные группы, связанные с фрагментом сахара без 2'-модификации, представляют собой фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления обе межнуклеотидные линкерные группы, связанные с фрагментом сахара без 2'-модификации, представляют собой замещенные фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления обе межнуклеотидные линкерные группы, связанные с фрагментом сахара без 2'-модификации, представляют собой фосфоротиоатные триэфирные линкерные группы. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой модифицированную линкерную группу. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой линкерную группу, характеризующуюся структурой формулы I. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой замещенную фосфоротиоатную линкерную группу. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа, связанная с фрагментом сахара без 2'-модификации, представляет собой фосфоротиоатную триэфирную линкерную группу.
Согласно некоторым вариантам осуществления фрагмент сахара без 2'-модификации представляет собой фрагмент сахара, обнаруженный в природном нуклеозиде ДНК.
Согласно некоторым вариантам осуществления для структуры крыло-сердцевина-крыло крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления для структуры крыло-сердцевина-крыло крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 5'-конце крыла. Согласно некоторым вариантам осуществления для структуры крыло-сердцевина-крыло крыло 3'-конца содержит только одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления для структуры крыло-сердцевина-крыло крыло 3'-конца содержит только одну хиральную межнуклеотидную линкерную группу на 3'-конце крыла. Согласно некоторым вариантам осуществления для структуры крыло-сердцевина-крыло каждое крыло содержит только одну хиральную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления для структуры крыло-сердцевина-крыло каждое крыло содержит только одну хиральную межнуклеотидную линкерную группу, в которой крыло 5'-конца содержит только одну хиральную межнуклеотидную линкерную группу на своем 5'-конце; и крыло 3'-конца содержит только одну хиральную межнуклеотидную линкерную группу на своем 3'-конце. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа в 5'-крыле представляет собой Rp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа в 5'-крыле представляет собой Sp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа в 3'-крыле представляет собой Rp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа в 3'-крыле представляет собой Sp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа как в 5'-, так и в 3'-крыльях представляет собой Sp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа как в 5'-, так и в 3'-крыльях представляет собой Rp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа в 5'-крыле представляет собой Sp, и единственная хиральная межнуклеотидная линкерная группа в 3'-крыле представляет собой Rp. Согласно некоторым вариантам осуществления единственная хиральная межнуклеотидная линкерная группа в 5'-крыле представляет собой Rp, и единственная хиральная межнуклеотидная линкерная группа в 3'-крыле представляет собой Sp.
Согласно некоторым вариантам осуществления крыло содержит две хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления крыло содержит только две хиральные межнуклеотидные линкерные группы и одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит только две хиральные межнуклеотидные линкерные группы и две или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит только две хиральные межнуклеотидные линкерные группы и две или более последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления крыло содержит только две хиральные межнуклеотидные линкерные группы и две последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления крыло содержит только две хиральные межнуклеотидные линкерные группы и три последовательные линкерные группы с природными фосфатами. Согласно некоторым вариантам осуществления 5'-крыло (к сердцевине) содержит только две хиральные межнуклеотидные линкерные группы, одну на своем 5'-конце, а другую на своем 3'-конце, с одной или более линкерными группами с природными фосфатами между ними. Согласно некоторым вариантам осуществления 5'-крыло (к сердцевине) содержит только две хиральные межнуклеотидные линкерные группы, одну на своем 5'-конце, а другую на своем 3'-конце, с двумя или более линкерными группами с природными фосфатами между ними. Согласно некоторым вариантам осуществления 3'-крыло (к сердцевине) содержит только две хиральные межнуклеотидные линкерные группы, одну на своем 3'-конце, а другую на своем 3'-конце, с одной или более линкерными группами с природными фосфатами между ними. Согласно некоторым вариантам осуществления 3'-крыло (к сердцевине) содержит только две хиральные межнуклеотидные линкерные группы, одну на своем 3'-конце, а другую на своем 3'-конце, с двумя или более линкерными группами с природными фосфатами между ними.
Согласно некоторым вариантам осуществления 5'-крыло содержит только две хиральные межнуклеотидные линкерные группы, одну на своем 5'-конце, а другую на своем 3'-конце, с одной или более линкерными группами с природными фосфатами между ними, и 3'-крыло содержит только одну межнуклеотидную линкерную группу на своем 3'-конце. Согласно некоторым вариантам осуществления 5'-крыло (к сердцевине) содержит только две хиральные межнуклеотидные линкерные группы, одну на своем 5'-конце, а другую на своем 3'-конце, с двумя или более линкерными группами с природными фосфатами между ними, и 3'-крыло содержит только одну межнуклеотидную линкерную группу на своем 3'-конце. Согласно некоторым вариантам осуществления каждая хиральная межнуклеотидная линкерная группа независимо имеет свою собственную стереохимию. Согласно некоторым вариантам осуществления обе хиральные межнуклеотидные линкерные группы в 5'-крыле имеют одинаковую стереохимию. Согласно некоторым вариантам осуществления обе хиральные межнуклеотидные линкерные группы в 5'-крыле имеют разную стереохимию. Согласно некоторым вариантам осуществления обе хиральные межнуклеотидные линкерные группы в 5'-крыле представляют собой Rp. Согласно некоторым вариантам осуществления обе хиральные межнуклеотидные линкерные группы в 5'-крыле представляют собой Sp. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы в 5'- и 3'-крыльях имеют одинаковую стереохимию. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы в 5'- и 3'-крыльях представляют собой Rp. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы в 5'- и 3'-крыльях представляют собой Sp. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы в 5'- и 3'-крыльях имеют различную стереохимию.
Согласно некоторым вариантам осуществления область сердцевины составляет в длину одно или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину одно или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину два или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину три или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину четыре или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину пять или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину шесть или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину семь или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину восемь или более оснований. В некоторых вариантах область сердцевины составляет в длину девять или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину десять или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 11 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 12 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 13 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 14 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 15 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 16 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 17 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 18 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 19 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 20 или более оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину более 20 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 2 основания. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 3 основания. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 4 основания. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 5 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 6 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 7 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 8 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 9 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 10 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 11 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 12 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 13 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 14 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 15 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 16 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 17 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 18 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 19 оснований. Согласно некоторым вариантам осуществления область сердцевины составляет в длину 20 оснований.
Согласно некоторым вариантам осуществления сердцевина содержит одну или более хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления сердцевина независимо содержит одну или более хиральных межнуклеотидных линкерных групп и одну или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления сердцевина не содержит линкерных групп с фосфатами. Согласно некоторым вариантам осуществления каждая линкерная группа сердцевины представляет собой хиральную межнуклеотидную линкерную группу.
Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере одну линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере две хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере три хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере четыре хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере пять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере шесть хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере семь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере восемь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере девять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере десять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 11 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 12 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 13 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 14 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 15 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 16 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 17 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 18 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 19 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит по меньшей мере 20 хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления сердцевина содержит одну линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления сердцевина содержит две хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления сердцевина содержит три хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления сердцевина содержит четыре хиральные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления сердцевина содержит пять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит шесть хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит семь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит восемь хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит девять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит десять хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 11 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 12 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 13 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 14 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 15 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 16 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 17 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 18 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 19 хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления сердцевина содержит 20 хиральных межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где каждый из m, n, t и Np независимо является таким, как определено и описано в настоящем раскрытии. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)m(Rp)n. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)m(Rp)n, где m>2 и n равно 1. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Rp)n(Sp)m. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Rp)n(Sp)m, где m>2 и n равно 1. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Np)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Np)t(Rp)n(Sp)m, где m>2 и n равно 1. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Np)t(Rp)n(Sp)m, где t>2, m>2 и n равно 1. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)t(Rp)n(Sp)m, где m>2 и n равно 1. Согласно некоторым вариантам осуществления область сердцевины характеризуется профилем хиральных центров остова, содержащим (Sp)t(Rp)n(Sp)m, где t>2, m>2 и n равно 1. Среди прочего, настоящее раскрытие демонстрирует, что согласно некоторым вариантам осуществления такие профили могут обеспечивать и/или усиливать контролируемое расщепление, улучшенную скорость расщепления, селективность и т.д. целевой последовательности, например, последовательности РНК. Примеры профилей хиральных центров остова описаны в настоящем раскрытии.
Согласно некоторым вариантам осуществления по меньшей мере 60% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 65% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 66% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 67% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 70% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 75% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 80% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 85% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 90% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере 95% хиральных межнуклеотидных линкерных групп в области сердцевины представляют собой Sp.
Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло (т.е. X-Y-X) представлен в цифровой форме как, например, 5-10-4, что означает, что крыло к 5'-концу сердцевины составляет 5 оснований в длину, область сердцевины составляет 10 оснований в длину, а область крыла к 3'-концу сердцевины составляет 4 основания в длину. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой любой из, например, 2-16-2, 3-14-3, 4-12-4, 5-10-5, 2-9-6, 3-9-3, 3-9-4, 3-9-5, 4- 7-4, 4-9-3, 4-9-4, 4-9-5, 4-10-5, 4-11-4, 4-11-5, 5-7-5, 5-8- 6, 8-7-5, 7-7-6, 5-9-3, 5-9-5, 5-10-4, 5-10-5, 6-7-6, 6-8-5 и 6-9-2 и т.д. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой 5-10-5. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой 7-7-6. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой 8-7-5.
Согласно некоторым вариантам осуществления мотив крыло-сердцевина представляет собой 5-15, 6-14, 7-13, 8-12, 9-12 и т.д. Согласно некоторым вариантам осуществления мотив сердцевина-крыло представляет собой 5-15, 6 -14, 7-13, 8-12, 9-12 и т.д.
Согласно некоторым вариантам осуществления все межнуклеотидные линкерные группы предложенных олигонуклеотидов таких мотивов крыло-сердцевина-крыло (т.е. X-Y-X) являются хиральными линкерными группами с модифицированными фосфатами. Согласно некоторым вариантам осуществления все межнуклеотидные линкерные группы предложенных олигонуклеотидов таких мотивов крыло-сердцевина-крыло (т.е. X-Y-X) являются хиральными фосфоротиоатными межнуклеотидными линкерными группами. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы предложенных олигонуклеотидов таких мотивов крыло-сердцевина-крыло составляют по меньшей мере примерно 10, 20, 30, 40, 50, 50, 70, 80 или 90% хиральных межнуклеотидных линкерных групп с модифицированными фосфатами. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы предложенных олигонуклеотидов таких мотивов крыло-сердцевина-крыло составляют по меньшей мере примерно 10, 20, 30, 40, 50, 60, 70, 80 или 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления хиральные межнуклеотидные линкерные группы предложенных олигонуклеотидов таких мотивов крыло-сердцевина-крыло составляют по меньшей мере примерно 10, 20, 30, 40, 50, 50, 70, 80 или 90% хиральных фосфоротиоатных межнуклеотидных линкерных групп конформации Sp.
Согласно некоторым вариантам осуществления каждая область крыла мотива крыло-сердцевина-крыло необязательно содержит хиральные межнуклеотидные линкерные группы с модифицированными фосфатами. Согласно некоторым вариантам осуществления каждая область крыла мотива крыло-сердцевина-крыло необязательно содержит хиральные фосфоротиоатные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления каждая область крыла мотива крыло-сердцевина-крыло содержит хиральные фосфоротиоатные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления две области крыла мотива крыло-сердцевина-крыло характеризуются одинаковой стереохимией межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления настоящего изобретения две области крыла мотива крыло-сердцевина-крыло характеризуются разной стереохимией межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления каждая межнуклеотидная линкерная группа в крыльях независимо представляет собой хиральную межнуклеотидную линкерную группу.
Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло необязательно содержит хиральные межнуклеотидные линкерные группы с модифицированными фосфатами. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло необязательно содержит хиральные фосфоротиоатные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой (Sp)mRp или Rp(Sp)m, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой (Sp)mRp или Rp(Sp)m, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой (Sp)mRp, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой Rp(Sp)m, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой (Sp)mRp или Rp(Sp)m, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой (Sp)mRp, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой Rp(Sp)m, где m представляет собой 1-50. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой мотив, содержащий по меньшей мере 33% межнуклеотидных линкерных групп в конформации S. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой мотив, содержащий по меньшей мере 50% межнуклеотидных линкерных групп в конформации S. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой мотив, содержащий по меньшей мере 66% межнуклеотидных линкерных групп в конформации S. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой повторяющийся триплетный мотив, выбранный из RpRpSp и SpSpRp. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой повторяющийся RpRpSp. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит повторяющийся профиль стереохимии межнуклеотидных линкерных групп, причем повторяющийся профиль представляет собой повторяющийся SpSpRp.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)mRp или Rp(Sp)m. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит Rp(Sp)m. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)mRp. Согласно некоторым вариантам осуществления m равно 2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит Rp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Rp)2Rp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит RpSpRp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит SpRpRp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)2Rp.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)mRp или Rp(Sp)m предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит Rp(Sp)m. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)mRp. Согласно некоторым вариантам осуществления m равно 2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит Rp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Rp)2Rp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит RpSpRp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит SpRpRp(Sp)2. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)2Rp.
Как определено в данном описании m равно 1-50. Согласно некоторым вариантам осуществления m равно 1. Согласно некоторым вариантам осуществления m равно 2-50. Согласно некоторым вариантам осуществления m равно 2, 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления m равно 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления m равно 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления m равно 5, 6, 7 или 8. Согласно некоторым вариантам осуществления m равно 6, 7 или 8. Согласно некоторым вариантам осуществления m равно 7 или 8. Согласно некоторым вариантам осуществления m равно 2. Согласно некоторым вариантам осуществления m равно 3. Согласно некоторым вариантам осуществления m равно 4. Согласно некоторым вариантам осуществления m равно 5. Согласно некоторым вариантам осуществления m равно 6. Согласно некоторым вариантам осуществления m равно 7. Согласно некоторым вариантам осуществления m равно 8. Согласно некоторым вариантам осуществления m равно 9. Согласно некоторым вариантам осуществления m равно 10. Согласно некоторым вариантам осуществления m равно 11. Согласно некоторым вариантам осуществления m равно 12. Согласно некоторым вариантам осуществления m равно 13. Согласно некоторым вариантам осуществления m равно 14. Согласно некоторым вариантам осуществления m равно 15. Согласно некоторым вариантам осуществления m равно 16. Согласно некоторым вариантам осуществления m равно 17. Согласно некоторым вариантам осуществления m равно 18. Согласно некоторым вариантам осуществления m равно 19. Согласно некоторым вариантам осуществления m равно 20. Согласно некоторым вариантам осуществления, m равно 21. Согласно некоторым вариантам осуществления m равно 22. Согласно некоторым вариантам осуществления m равно 23. Согласно некоторым вариантам осуществления m равно 24. Согласно некоторым вариантам осуществления m равно 25. Согласно некоторым вариантам осуществления m больше чем 25. Согласно некоторым вариантам осуществления повторяющийся профиль представляет собой (Sp)m(Rp)n, причем n представляет собой независимо 1-10 и m составляет независимо, как это определено выше и описано в данном описании. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)m(Rp)n
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)m(Rp)n. Согласно некоторым вариантам осуществления повторяющийся профиль представляет собой (Rp)n(Sp)m, где n равно 1-10, и m составляет независимо, как определено выше и описано в настоящем документе. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Rp)n(Sp)m. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Rp)n(Sp)m. Согласно некоторым вариантам осуществления (Rp)n(Sp)m представляет собой (Rp)(Sp)2. Согласно некоторым вариантам осуществления (Sp)n(Rp)m представляет собой (Sp)2(Rp). Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)m(Rp)n(Sp)t.
Согласно некоторым вариантам осуществления повторяющийся профиль представляет собой (Sp)m(Rp)n(Sp)t, где n равно 1-10, t равно 1-50 и m является таким, как определено выше и описано в настоящем документе. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)m(Rp)n(Sp)t. Согласно некоторым вариантам осуществления повторяющийся профиль представляет собой (Sp)t(Rp)n(Sp)m, где n равно 1-10, t равно 1-50, a m является таким, как определено выше и описано в настоящем документе. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Sp)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Sp)t(Rp)n(Sp)m.
Согласно некоторым вариантам осуществления повторяющийся профиль представляет собой (Np)t(Rp)n(Sp)m, где n равно 1-10, t равно 1-50, Np независимо представляет собой Rp или Sp, a m является таким, как определено выше и описано в настоящем документе. Согласно некоторым вариантам осуществления настоящее раскрытие представляет собой композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Np)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Np)t(Rp)n(Sp)m. Согласно некоторым вариантам осуществления повторяющийся профиль представляет собой (Np)m(Rp)n(Sp)t, где n равно 1-10, t равно 1-50, Np независимо представляет собой Rp или Sp, a m является таким, как определено выше и описано в настоящем документе. Согласно некоторым вариантам осуществления настоящее раскрытие представляет собой композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова содержит (Np)m(Rp)n(Sp)t. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, чей профиль хиральных центров остова в области сердцевины содержит (Np)m(Rp)n(Sp)t. Согласно некоторым вариантам осуществления Np представляет собой Rp. Согласно некоторым вариантам осуществления Np представляет собой Sp. Согласно некоторым вариантам осуществления все Np одинаковы. Согласно некоторым вариантам осуществления все Np представляют собой Sp. Согласно некоторым вариантам осуществления по меньшей мере один Np отличается от другого Np. Согласно некоторым вариантам осуществления t равно 2.
Как определено в данном описании, n равно 1-10. Согласно некоторым вариантам осуществления n равно 1, 2, 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления n равно 1. Согласно некоторым вариантам осуществления n равно 2, 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления n равно 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления n равно 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления n равно 5, 6, 7 или 8. Согласно некоторым вариантам осуществления n 6, 7 или 8. Согласно некоторым вариантам осуществления n 7 или 8. Согласно некоторым вариантам осуществления n равно 1. Согласно некоторым вариантам осуществления n равно 2. Согласно некоторым вариантам осуществления n равно 3. Согласно некоторым вариантам осуществления n равно 4. Согласно некоторым вариантам осуществления n равно 5. Согласно некоторым вариантам осуществления n равно 6. Согласно некоторым вариантам осуществления n 7. Согласно некоторым вариантам осуществления n равно 8. Согласно некоторым вариантам осуществления n равно 9.
Согласно некоторым вариантам осуществления n равно 10. Как определено в данном описании, t равно 1-50. Согласно некоторым вариантам осуществления t равно 1. Согласно некоторым вариантам осуществления t равно 2-50. Согласно некоторым вариантам осуществления t равно 2, 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления t равно 3, 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления t равно 4, 5, 6, 7 или 8. Согласно некоторым вариантам осуществления t равно 5, 6, 7 или 8. Согласно некоторым вариантам осуществления t равно 6, 7 или 8. Согласно некоторым вариантам осуществления t равно 7 или 8. Согласно некоторым вариантам осуществления t равно 2. Согласно некоторым вариантам осуществления t равно 3. Согласно некоторым вариантам осуществления t равно 4. Согласно некоторым вариантам осуществления t равно 5. Согласно некоторым вариантам осуществления t равно 6. Согласно некоторым вариантам осуществления t равно 7. Согласно некоторым вариантам осуществления t равно 8. Согласно некоторым вариантам осуществления, t равно 9. Согласно некоторым вариантам осуществления t равно 10. Согласно некоторым вариантам осуществления t равно 11. Согласно некоторым вариантам осуществления t равно 12. Согласно некоторым вариантам осуществления t равно 13. Согласно некоторым вариантам осуществления t равно 14. Согласно некоторым вариантам осуществления t является 15. Согласно некоторым вариантам осуществления t равно 16. Согласно некоторым вариантам осуществления t равно 17. Согласно некоторым вариантам осуществления t равно 18. Согласно некоторым вариантам осуществления t равно 19. Согласно некоторым вариантам осуществления t равно 20. Согласно некоторым вариантам осуществления t равно 21. Согласно некоторым вариантам осуществления t равно 22. Согласно некоторым вариантам осуществления t равно 23. Согласно некоторым вариантам осуществления t равно 24. Согласно некоторым вариантам осуществления t равно 25. Согласно некоторым вариантам осуществления t больше чем 25.
Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 2. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 3. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 4. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 5. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 6. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 7. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 8. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 9. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 10. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 11. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 12. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 13. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 14. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 15. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 16. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 17. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 18. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 19. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 20. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 21. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 22. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 23. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 24. Согласно некоторым вариантам осуществления по меньшей мере один из m и t больше чем 25.
Согласно некоторым вариантам осуществления каждый из m и t больше чем 2. Согласно некоторым вариантам осуществления каждый из m и t больше чем 3. Согласно некоторым вариантам осуществления каждый из m и t больше чем 4. Согласно некоторым вариантам осуществления каждый из m и t больше чем 5. Согласно некоторым вариантам осуществления каждый из m и t больше чем 6. Согласно некоторым вариантам осуществления каждый из m и t больше чем 7. Согласно некоторым вариантам осуществления, каждый из m и t больше чем 8. Согласно некоторым вариантам осуществления каждый из m и t больше чем 9. Согласно некоторым вариантам осуществления каждый из m и t больше чем 10. Согласно некоторым вариантам осуществления каждый из m и t больше чем 11. Согласно некоторым вариантам осуществления каждый из m и t больше чем 12. Согласно некоторым вариантам осуществления каждый из m и t больше чем 13. Согласно некоторым вариантам осуществления каждый из m и t больше чем 14. Согласно некоторым вариантам осуществления каждый из m и t больше чем 15. Согласно некоторым вариантам осуществления каждый из m и t больше чем 16. Согласно некоторым вариантам осуществления каждый из m и t больше чем 17. Согласно некоторым вариантам осуществления каждый из m и t больше чем 18. Согласно некоторым вариантам осуществления каждый из m и t больше чем 19. Согласно некоторым вариантам осуществления каждый из m и t больше чем 20.
Согласно некоторым вариантам осуществления сумма m и t больше чем 3. Согласно некоторым вариантам осуществления сумма m и t больше чем 4. Согласно некоторым вариантам осуществления сумма m и t больше чем 5. Согласно некоторым вариантам осуществления сумма m и t больше чем 6. Согласно некоторым вариантам осуществления сумма m и t больше чем 7. Согласно некоторым вариантам осуществления сумма m и t больше чем 8. Согласно некоторым вариантам осуществления сумма m и t больше чем 9. Согласно некоторым вариантам осуществления сумма m и t больше чем 10. Согласно некоторым вариантам осуществления сумма m и t больше чем 11. Согласно некоторым вариантам осуществления сумма m и t больше чем 12. Согласно некоторым вариантам осуществления сумма m и t больше чем 13. Согласно некоторым вариантам осуществления сумма m и t больше чем 14. Согласно некоторым вариантам осуществления сумма m и t больше чем 15. Согласно некоторым вариантам осуществления сумма m и t больше чем 16. Согласно некоторым вариантам осуществления сумма m и t больше чем 17. Согласно некоторым вариантам осуществления сумма m и t больше чем 18. Согласно некоторым вариантам осуществления сумма m и t больше чем 19. Согласно некоторым вариантам осуществления сумма m и t больше чем 20. Согласно некоторым вариантам осуществления сумма m и t больше чем 21. Согласно некоторым вариантам осуществления сумма m и t больше чем 22. Согласно некоторым вариантам осуществления сумма m и t больше чем 23. Согласно некоторым вариантам осуществления сумма m и t больше чем 24. Согласно некоторым вариантам осуществления сумма m и t больше чем 25.
Согласно некоторым вариантам осуществления n равно 1 и по меньшей мере один из m и t больше чем 1. Согласно некоторым вариантам осуществления n равно 1 и каждый из m и t независимо больше чем 1. Согласно некоторым вариантам осуществления m>n и t>n. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой SpRp(Sp)2. Согласно некоторым вариантам осуществления (Np)t(Rp)n(Sp)m представляет собой (Np)tRp(Sp)m. Согласно некоторым вариантам осуществления (Np)t(Rp)n(Sp)m представляет собой (Np)2Rp(Sp)m. Согласно некоторым вариантам осуществления (Np)t(Rp)n(Sp)m представляет собой (Rp)2Rp(Sp)m. Согласно некоторым вариантам осуществления (Np)t(Rp)n(Sp)m представляет собой (Sp)2Rp(Sp)m. Согласно некоторым вариантам осуществления (Np)t(Rp)n(Sp)m представляет собой RpSpRp(Sp)m. Согласно некоторым вариантам осуществления (Np)t(Rp)n(Sp)m представляет собой SpRpRp(Sp)m.
Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой SpRpSpSp. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)3Rp(Sp)3. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)4Rp(Sp)4. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)tRp(Sp)5. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой SpRp(Sp)5. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)2Rp(Sp)5. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)3Rp(Sp)5. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)4Rp(Sp)5. Согласно некоторым вариантам осуществления (Sp)t(Rp)n(Sp)m представляет собой (Sp)5Rp(Sp)5.
Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)3Rp(Sp)3. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)4Rp(Sp)4. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)mRp(Sp)5. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)2Rp(Sp)5. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)3Rp(Sp)5. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)4Rp(Sp)5. Согласно некоторым вариантам осуществления (Sp)m(Rp)n(Sp)t представляет собой (Sp)5Rp(Sp)5.
Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере одну межнуклеотидную линкерную группу Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере одну межнуклеотидную линкерную группу Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере одну фосфоротиоатную межнуклеотидную линкерную группу Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере одну фосфоротиоатную межнуклеотидную линкерную группу Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит только одну фосфоротиоатную межнуклеотидную линкерную группу Rp-конфигурации. Согласно некоторым вариантам осуществления мотив области сердцевины содержит по меньшей мере две межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере две межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере две фосфоротиоатные межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере три межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере три межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере три фосфоротиоатные межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере три фосфоротиоатные межнуклеотидные линкерные группы Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере 4, 5, 6, 7, 8, 9 или 10 межнуклеотидных линкерных групп Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины мотива крыло-сердцевина-крыло содержит по меньшей мере 4, 5, 6, 7, 8, 9 или 10 межнуклеотидных линкерных групп Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере 4, 5, 6, 7, 8, 9 или 10 фосфоротиоатных межнуклеотидных линкерных групп Rp-конфигурации. Согласно некоторым вариантам осуществления область сердцевины содержит по меньшей мере 4, 5, 6, 7, 8, 9 или 10 Rp фосфоротиоатных межнуклеотидных линкерных групп Rp-конфигурации.
Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляют собой 2'-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляют собой 2'-OR1-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляют собой 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляют собой 2'-ОМе-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в области сердцевины представляют собой остатки 2'-дезоксирибонуклеозида. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором все межнуклеозидные линкерные группы представляют собой фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором все межнуклеотидные линкерные группы представляют собой хиральные фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляет собой 2'-модифицированные остатки, остатки в области сердцевины представляют собой 2'-дезоксирибонуклеозидные остатки и все межнуклеотидные линкерные группы в области сердцевины представляет собой хиральные фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляет собой 2'-OR1-модифицированные остатки, остатки в области сердцевины представляют собой 2'-дезоксирибонуклеозидные остатки и все межнуклеотидные линкерные группы в области сердцевины представляют собой хиральные фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляют собой 2'-МОЕ-модифицированные остатки, остатки в области сердцевины представляют собой 2'-дезоксирибонуклеозидные остатки и все межнуклеотидные линкерные группы в области сердцевины представляют собой хиральные фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла представляет собой 2'-ОМе-модифицированные остатки, остатки в области сердцевины представляют собой 2'-дезоксирибонуклеозидные остатки и все межнуклеотидные линкерные группы в области сердцевины представляют собой хиральные фосфоротиоатные линкерные группы.
Согласно некоторым вариантам осуществления остатки в области крыла «X» не представляют собой 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина представляет собой мотив, в котором остатки в области крыла «X» не представляют собой 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления мотив сердцевина-крыло представляет собой мотив, в котором остатки в области крыла «X» не представляют собой 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив, в котором остатки в каждой области крыла «X» не представляют собой 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла «X» представляют собой не 2'-МОЕ-модифицированные остатки. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области сердцевины «Y» представляют собой остатки 2'-дезоксирибонуклеозида. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором все межнуклеозидные линкерные группы представляют собой фосфоротиоатные межнуклеозидные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором все межнуклеозидные линкерные группы представляют собой хиральные фосфоротиоатные межнуклеозидные линкерные группы. Согласно некоторым вариантам осуществления мотив крыло-сердцевина-крыло представляет собой мотив 5-10-5, в котором остатки в каждой области крыла «X» представляют собой не 2'-МОЕ-модифицированные остатки, остатки в каждой области сердцевины «Y» представляют собой остатки 2'-дезоксирибонуклеозида и все межнуклеозидные линкерные группы представляют собой хиральные фосфоротиоатные межнуклеозидные линкерные группы.
Как понятно специалисту в данной области техники предусмотренные олигонуклеотиды и композиции, среди прочего, могут нацеливаться на большое количество полимеров нуклеиновых кислот. Например, согласно некоторым вариантам осуществления предложенные олигонуклеотиды и композиции могут нацеливаться на транскрипт последовательности нуклеиновой кислоты, причем общая последовательность оснований олигонуклеотидов (например, последовательность оснований типа олигонуклеотида) содержит или представляет собой последовательность, комплементарную последовательности транскрипта. Согласно некоторым вариантам осуществления общая последовательность оснований содержит последовательность, комплементарную последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований представляет собой последовательность, комплементарную последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований содержит последовательность, которая на 100% комплементарна последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований представляет собой последовательность, которая на 100% комплементарна последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований в сердцевине содержит или представляет собой последовательность, комплементарную последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований в сердцевине содержит последовательность, комплементарную последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований в сердцевине представляет собой последовательность, которая на 100% комплементарна последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований в сердцевине содержит или представляет собой последовательность, которая на 100% комплементарна последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований в сердцевине содержит последовательность, которая на 100% комплементарна последовательности мишени. Согласно некоторым вариантам осуществления общая последовательность оснований в сердцевине содержит последовательность, которая на 100% комплементарна последовательности мишени.
Согласно некоторым вариантам осуществления, как описано в настоящем описании предложенные олигонуклеотиды и композиции могут обеспечивать новые профили расщепления, более высокую скорость расщепления, более высокую степень расщепления, более высокую селективность селекции и т.д. Согласно некоторым вариантам осуществления предложенные композиции могут избирательно подавлять (например, расщеплять) транскрипт из целевой последовательности нуклеиновой кислоты, которая имеет одну или более подобных последовательностей, существующую внутри субъекта или популяции, каждая из мишеней и аналогичных последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность по отношению к аналогичным последовательностям. Согласно некоторым вариантам осуществления, например, целевая последовательность представляет собой аллель дикого типа или копию гена, и аналогичная последовательность представляет собой последовательность, имеющую очень сходную последовательность оснований, например, последовательность с SNP, мутациями и т.д.; согласно некоторым вариантам осуществления характеристический элемент последовательности определяет эту целевую последовательность относительно аналогичной последовательности: например, когда целевая последовательность представляет собой связанный с болезнью Хантингтона аллель с Т в rs362307 (U в соответствующей РНК, С для не связанного с заболеванием аллеля), характеристическая последовательность содержит этот SNP.
Согласно некоторым вариантам осуществления аналогичная последовательность характеризуется гомологией последовательности, составляющей более чем 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% по отношению к целевой последовательностью. Согласно некоторым вариантам осуществления целевая последовательность представляет собой вызывающую заболевание копию последовательности нуклеиновой кислоты, содержащую одну или более мутаций и/или SNP, и аналогичная последовательность представляет собой копию, не вызывающую заболевания (дикого типа). Согласно некоторым вариантам осуществления целевая последовательность содержит мутацию, причем аналогичная последовательность представляет собой соответствующую последовательности дикого типа. Согласно некоторым вариантам осуществления целевая последовательность представляет собой мутантный аллель, тогда как аналогичная последовательность представляет собой аллель дикого типа. Согласно некоторым вариантам осуществления целевая последовательность содержит SNP, который связан с вызывающим заболевание аллелем, тогда как аналогичная последовательность содержит тот же SNP, который не связан с вызывающим заболевание аллелем. Согласно некоторым вариантам осуществления область целевой последовательности, которая комплементарна одинаковой последовательности оснований предложенной композиции олигонуклеотидов, характеризуется гомологией, составляющей более чем 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% по отношению к соответствующей области аналогичной последовательности. Согласно некоторым вариантам осуществления область целевой последовательности, которая комплементарна одинаковой последовательности оснований предложенной композиции олигонуклеотидов, отличается от соответствующей области аналогичной последовательности менее чем на 5, менее чем на 4, менее чем на 3, менее чем на 2 или только на 1 пару оснований. Согласно некоторым вариантам осуществления область целевой последовательности, которая комплементарна одинаковой последовательности оснований предложенной композиции олигонуклеотидов, отличается от соответствующей области аналогичной последовательности только в сайте мутации или сайте SNP. Согласно некоторым вариантам осуществления область целевой последовательности, которая комплементарна одинаковой последовательности оснований предложенной композиции олигонуклеотидов, отличается от соответствующей области аналогичной последовательности только в сайте мутации. Согласно некоторым вариантам осуществления область целевой последовательности, которая комплементарна одинаковой последовательности оснований предложенной композиции олигонуклеотидов, отличается от соответствующей области аналогичной последовательности только в сайте SNP.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, комплементарную характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность, комплементарную характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, которая на 100% комплементарна характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине содержит или представляет собой последовательность, комплементарную характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине содержит последовательность, комплементарную характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине представляет собой последовательность, комплементарную характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине содержит или представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине содержит последовательность, которая на 100% комплементарна характеристическому элементу последовательности. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности.
Согласно некоторым вариантам осуществления характеристический элемент последовательности содержит или представляет собой мутацию. Согласно некоторым вариантам осуществления характеристический элемент последовательности содержит мутацию. Согласно некоторым вариантам осуществления характеристический элемент последовательности представляет собой мутацию. Согласно некоторым вариантам осуществления характеристический элемент последовательности содержит или представляет собой точечную мутацию. Согласно некоторым вариантам осуществления характеристический элемент последовательности содержит точечную мутацию. Согласно некоторым вариантам осуществления характеристический элемент последовательности представляет собой точечную мутацию. Согласно некоторым вариантам осуществления характеристический элемент последовательности содержит или представляет собой SNP. Согласно некоторым вариантам осуществления характеристический элемент последовательности содержит SNP. Согласно некоторым вариантам осуществления характеристический элемент последовательности представляет собой SNP.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований на 100% соответствует целевой последовательности, которая не на 100% соответствует аналогичной последовательности целевой последовательности. Например, согласно некоторым вариантам осуществления одинаковая последовательность оснований соответствует мутации в вызывающей заболевание копии или аллеле целевой последовательности нуклеиновой кислоты, но не соответствует не вызывающей заболевание копии или аллелю в сайте мутации; в некоторых других вариантах реализации одинаковая последовательность оснований соответствует SNP в вызывающем заболевание аллеле целевой последовательности нуклеиновой кислоты, но не соответствует не вызывающему заболеванию аллелю в соответствующем сайте. Согласно некоторым вариантам осуществления одинаковая последовательность оснований в сердцевине на 100% соответствует целевой последовательности, которая не на 100% соответствует аналогичной последовательности целевой последовательности. Например, в WV-1092 его одинаковая последовательность оснований (и его одинаковая последовательность оснований в его сердцевине) соответствует связанному с заболеванием U, но не несвязанному с заболеванием (дикого типа) С в rs362307.
Помимо прочего, настоящее раскрытие признает тот факт, что последовательность оснований может оказывать влияние на свойства олигонуклеотидов. Согласно некоторым вариантам осуществления последовательность оснований может оказывать влияние на профиль расщепления мишени, когда олигонуклеотиды, имеющие последовательность оснований, используются для подавления мишени, например, через путь, включающий РНКазу Н: например, на фиг. 33 показано, что структурно подобные (все фосфоротиоатные линкерные группы, все стереослучайные) олигонуклеотиды имеют разные последовательности, могут иметь разные профили расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований нестереослучайных композиций олигонуклеотидов (например, определенных композиций олигонуклеотидов, представленных в настоящем описании) представляет собой последовательность оснований, которая при применении к композиции олигонуклеотидов ДНК (например, ONT-415) или стереослучайной композиции олигонуклеотидов со всеми фосфоротиоатными линкерными группами (например, WV-905), профиль расщепления ДНК (профиль расщепления ДНК) и/или стереослучайная композиция со всеми фосфоротиоатными линкерными группами (стереослучайный профиль расщепленная) имеет сайт расщепления внутри или вблизи характеристического элемента последовательности. Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи находится в последовательности, комплементарной области сердцевины одинаковой последовательности. Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи находится в последовательности, которая на 100% комплементарна области сердцевины одинаковой последовательности.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления внутри или вблизи характеристического элемента последовательности в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления внутри характеристического элемента последовательности в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи характеристического элемента последовательности в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации или SNP характеристического элемента последовательности в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи SNP в своем профиле расщепления ДНК.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления внутри или вблизи характеристического элемента последовательности в своем стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления в пределах характеристического элемента последовательности в своем стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи характеристического элемента последовательности в своем стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации или SNP характеристического элемента последовательности в своем стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации в своем стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи SNP в своем стереослучайном профиле расщепления.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации характеристического элемента последовательности в своей ДНК и/или стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации в своей ДНК и/или стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи мутации в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления сайт расщепления вблизи мутации находится в мутации, то есть сайт расщепления находится в межнуклеотидной линкерной группе мутированного нуклеотида (например, если мутация находится в А в целевой последовательности GGGACGTCTT, расщепление происходит между А и С). Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 межнуклеотидных линкерных группах от мутации, где 0 означает расщепление в сайте мутации (например, если мутация находится в точке А в целевой последовательности GGGACGTCTT, расщепление происходит между А и С для 0 межнуклеотидных линкерных групп, сайта расщепления в 1 линкерной группе от мутации находится между G и А к 5'-концу от мутации или между С и G к 3'-концу от мутации). Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3 или 4 межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3 или 4 межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3 или 4 межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2 или 3 межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2 или 3 межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2 или 3 межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1 или 2 межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1 или 2 межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1 или 2 межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 или 1 межнуклеотидной линкерной группе от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 или 1 межнуклеотидной линкерной группе к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 или 1 межнуклеотидной линкерной группе к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 линкерных групп от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в одной межнуклеотидной линкерной группе от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в одной межнуклеотидной линкерной группе к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в одной межнуклеотидной линкерной группе к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в двух межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в двух межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в двух межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в трех межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в трех межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в трех межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в четырех межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в четырех межнуклеотидных линкерных группах к 5'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в четырех межнуклеотидных линкерных группах к 3'-концу от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в пяти межнуклеотидных линкерных группах от мутации. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в пяти межнуклеотидных линкерных группах к 5'-концу от мутации.
Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в пяти межнуклеотидных линкерных группах к 3'-концу от мутации.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи SNP характеристического элемента последовательности в своей ДНК и/или стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи SNP в своей ДНК и/или стереослучайном профиле расщепления. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность оснований, которая содержит сайт расщепления вблизи SNP в своем профиле расщепления ДНК. Согласно некоторым вариантам осуществления сайт расщепления вблизи SNP находится в SNP, то есть сайт расщепления находится в межнуклеотидной линкерной группы нуклеотида в SNP (например, для мишени WV-905, G*G*C*A*C*A*A*G*G*G*C*A*C*A*G*A*C*T*T*C, который содержит rUrUrUrGrGrArArGrUrCrUrGrUrGrCrCrCrUrUrGrUrGrCrCrC (rs362307 выделен жирным шрифтом), расщепление находится между выделенным жирным шрифтом rU и подчеркнутым rG сразу после него). Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 межнуклеотидных линкерных группах от SNP, где 0 означает расщепление в SNP (например, для мишени WV-905, G*G*C*A*C*A*A*G*G*G*C*A*C*A*G*A*C*T*T*C, который содержит rUrUrUrGrGrArArGrUrCrUrGrUrGrCrCrCrUrUrGrUrGrCrCrC (rs362307 выделен жирным шрифтом), расщепление находится между выделенным жирным rU и подчеркнутым rG сразу после него для 0 межнуклеотидных линкерных групп, сайт расщепления в 1 межнуклеотидной линкерной группе от SNP находится между rG и rU к 5'-концу от SNP (подчеркнуто: rUrUrUrGrGrArArGrUrCrUrGrUrGrCrCrCrUrUrGrUrGrCrCrC) или между rG и rC к 3'-концу SNP (подчеркнуто: rUrUrUrGrGrArArGrUrCrUrGrUrGrCrCrCrUrUrGrUrGrCrCrC)). Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от SNP.
Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3 или 4 межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3 или 4 межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления 0, 1, 2, 3 или 4 межнуклеотидных линкерных групп к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2 или 3 межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2 или 3 межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2 или 3 межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1 или 2 межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1 или 2 межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1 или 2 межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 или 1 межнуклеотидной линкерной группе от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 или 1 межнуклеотидной линкерной группе к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0 или 1 межнуклеотидной линкерной группе к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в О межнуклеотидных линкерных групп от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в одной межнуклеотидной линкерной группе от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в одной межнуклеотидной линкерной группе к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в одной межнуклеотидной линкерной группе к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в двух межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в двух межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в двух межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в трех межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в трех межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в трех межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в четырех межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в четырех межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в четырех межнуклеотидных линкерных группах к 3'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в пяти межнуклеотидных линкерных группах от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в пяти межнуклеотидных линкерных группах к 5'-концу от SNP. Согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в пяти межнуклеотидных линкерных группах к 3'-концу от SNP. Например, на фиг. 33 показано, что стереослучайный профиль расщепления последовательности WV-905 содержит сайты расщепления в SNP (между CUGU и GCCC), в двух межнуклеотидных линкерных группах (между GUCU и GUGC и между GUGC и CCUU), в трех межнуклеотидных линкерных группах (между UGCC и CUUG); в четырех межнуклеотидных линкерных группах (между GCCC и UUGU и AAGU и CUGU) и пяти межнуклеотидных линкерных группах (между CCCU и UGUG).
Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи характеристического элемента последовательности, например, вблизи мутации, SNP и т.д., представляет собой основной сайт расщепления ДНК и/или стереослучайного профиля расщепления. Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой основной сайт расщепления профиля расщепления ДНК. Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой основной сайт расщепления стереослучайного профиля расщепления. Согласно некоторым вариантам осуществления сайт расщепления вблизи мутации представляет собой основной сайт расщепления профиля расщепления ДНК. Согласно некоторым вариантам осуществления сайт расщепления вблизи мутации представляет собой основной сайт расщепления стереослучайного профиля расщепления. Согласно некоторым вариантам осуществления сайт расщепления вблизи SNP представляет собой основной сайт расщепления профиля расщепления ДНК. Согласно некоторым вариантам осуществления сайт расщепления вблизи SNP представляет собой основной сайт расщепления стереослучайного профиля расщепления. Согласно некоторым вариантам осуществления основной сайт расщепления находится в последовательности, комплементарной области сердцевины одинаковой последовательности. Согласно некоторым вариантам осуществления основной сайт расщепления находится в последовательности, которая на 100% комплементарна области сердцевины одинаковой последовательности.
Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий наибольшее или второе, третье, четвертое или пятое наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий наибольшее или второе, третье или четвертое наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий наибольшее или второе или третье наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий наибольшее или второе наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий второе наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий третье наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий четвертое наибольшее расщепление. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, содержащий пятое наибольшее расщепление.
Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55% 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 5% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 10% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 15% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 20% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 25% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 30% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 35% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 40% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 45% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 50% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 55% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 60% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 65% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 70% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 75% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 80% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 85% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 90% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 91% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 92% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 93% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 94% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 95% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 96% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 97% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 98% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит более 99% расщеплений. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором происходит 100% расщеплений.
Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55% 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 5% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 10% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 15% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 20% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 25% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 30% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 35% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 40% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 45% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 50% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 55% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 60% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 65% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 70% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 75% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 80% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 85% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 90% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 91% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 92% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 93% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 94% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 95% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 96% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 97% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 98% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется более чем 99% мишени. Согласно некоторым вариантам осуществления основной сайт расщепления представляет собой сайт, в котором расщепляется 100% мишени. Согласно некоторым вариантам осуществления профиль расщепления может не иметь основного сайта расщепления, так как ни один сайт не достигает абсолютного порогового уровня расщепления.
Как понятно специалисту в данной области техники, могут быть применимы различные способы для создания профилей расщепления и/или идентификации сайтов расщепления, включая основной сайт расщепления. Согласно некоторым вариантам осуществления пример такого анализа представляет собой анализ расщепления РНКазой, как описано в настоящем документе; например, результатах, смотрите фиг. 33, фиг. 34 и т.д.
Согласно некоторым вариантам осуществления настоящее раскрытие распознает эффекты местоположения мотива последовательности, комплементарного характеристическому элементу последовательности. Согласно некоторым вариантам осуществления настоящее раскрытие распознает эффекты местоположения мотива последовательности, комплементарного мутации. Согласно некоторым вариантам осуществления настоящее раскрытие распознает эффекты местоположения мотива последовательности, комплементарного SNP.
Согласно некоторым вариантам осуществления положение 11, 12 или 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 11 последовательности, отсчитываемое от ее 5'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 12 последовательности, отсчитываемое от ее 5'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 8, 9 или 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 8 последовательности, отсчитываемое от ее 3'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 9 последовательности, отсчитываемое от ее 3'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 6, 7 или 8 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 6 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 7 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 8 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 3, 4 или 5 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 3 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 4 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с характеристическим элементом последовательности. Согласно некоторым вариантам осуществления положение 5 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с характеристическим элементом последовательности.
Согласно некоторым вариантам осуществления положение 11, 12 или 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 11 последовательности, отсчитываемое от ее 5'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 12 последовательности, отсчитываемое от ее 5'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 8, 9 или 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 8 последовательности, отсчитываемое от ее 3'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 9 последовательности, отсчитываемое от ее 3'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 6, 7 или 8 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 6 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 7 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 8 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 3, 4 или 5 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 3 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 4 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с мутацией. Согласно некоторым вариантам осуществления положение 5 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с мутацией.
Согласно некоторым вариантам осуществления положение 11, 12 или 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 11 последовательности, отсчитываемое от ее 5'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 12 последовательности, отсчитываемое от ее 5'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 8, 9 или 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 8 последовательности, отсчитываемое от ее 3'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 9 последовательности, отсчитываемое от ее 3'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 6, 7 или 8 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 6 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 7 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 8 области сердцевины, отсчитываемое от 5'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 3, 4 или 5 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 3 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 4 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с SNP. Согласно некоторым вариантам осуществления положение 5 области сердцевины, отсчитываемое от 3'-конца области сердцевины, выравнивается с SNP.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную вызывающей заболевание последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна вызывающей заболевание последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную характеристическому элементу последовательности вызывающей заболевание последовательности нуклеиновой кислоты, причем характеристические последовательности отличают вызывающую заболевание последовательность нуклеиновой кислоты от не вызывающей заболевание последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности вызывающей заболевание последовательности нуклеиновой кислоты, причем характеристические последовательности отличают вызывающую заболевание последовательность нуклеиновой кислоты от не вызывающей заболевание последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную связанной с заболеванием последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100%, комплементарна связанной с заболеванием последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную характеристическому элементу последовательности связанной с заболеванием последовательности нуклеиновой кислоты, причем характеристические последовательности отличают связанную с заболеванием последовательность нуклеиновой кислоты от не связанной с заболеванием последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности связанной с заболеванием последовательности нуклеиновой кислоты, причем характеристические последовательности отличают связанную с заболеванием последовательность нуклеиновой кислоты от не связанной с заболеванием последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную гену. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна гену. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную характеристическому элементу последовательности гена, причем характеристические последовательности отличают ген от аналогичной последовательности, характеризующейся общей гомологией с геном. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности гена, характеристические последовательности отличают ген от аналогичной последовательности, характеризующейся общей гомологией с геном. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную характеристическому элементу последовательности целевого гена, причем характеристические последовательности содержат мутацию, которая не обнаружена в других копиях гена, например, копии гена дикого типа, другой мутантной копии гена и т.д. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, которая на 100% комплементарна характеристическому элементу последовательности целевого гена, причем характеристические последовательности содержат мутацию, которая не обнаружена в других копиях этого гена, например, копии гена дикого типа, другой мутантной копии гена и т.д.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную последовательности, содержащей SNP. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит или представляет собой последовательность, комплементарную последовательности, содержащей SNP, и одинаковая последовательность оснований на 100% комплементарна SNP, который связан с заболеванием. Например, согласно некоторым вариантам осуществления одинаковая последовательность оснований на 100% комплементарна SNP, связанному со связанным с болезнью Хантингтона (или вызывающим ее) аллелем. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность WV-1092, которая на 100% комплементарна связанному с заболеванием аллелю, у многих пациентов с болезнью Хантингтона в rs362307. Согласно некоторым вариантам осуществления SNP представляет собой rs362307. Согласно некоторым вариантам осуществления SNP представляет собой rs7685686. Согласно некоторым вариантам осуществления SNP представляет собой rs362268. Согласно некоторым вариантам осуществления SNP представляет собой rs362306. Согласно некоторым вариантам осуществления SNP представляет собой rs362331. Согласно некоторым вариантам осуществления SNP представляет собой rs2530595. Согласно некоторым вариантам осуществления другим примером сайта SNP может быть любой из сайтов хантингтин, раскрытых в настоящем раскрытии.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GCCTCAGTCTGCTTCGCACC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GCCTCAGTCTGCTTCGCACC, причем последовательность, обнаруженная в GCCTCAGTCTGCTTCGCACC, содержит по меньшей мере 15 нуклеотидов. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GCCTCAGTCTGCTTCGCACC.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GAGCAGCTGCAACCTGGCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GAGCAGCTGCAACCTGGCAA, причем последовательность, обнаруженная в GAGCAGCTGCAACCTGGCAA, содержит по меньшей мере 15 нуклеотидов. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GAGCAGCTGCAACCTGGCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GGGCACAAGGGCACAGACTT. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GAGCAGCTGCAACCTGGCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GCACAAGGGCACAGACTTCC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой CACAAGGGCACAGACTTCCA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой ACAAGGGCACAGACTTCCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой CAAGGGCACAGACTTCCAAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GAGCAGCTGCAACCTGGCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GAGCAGCTGCAACCTGGCAA, причем последовательность, обнаруженная в GAGCAGCTGCAACCTGGCAA, содержит по меньшей мере 15 нуклеотидов. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GAGCAGCTGCAACCTGGCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GAGCAGCTGCAACCTGGCAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой AGCAGCTGCAACCTGGCAAC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GCAGCTGCAACCTGGCAACA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой CAGCTGCAACCTGGCAACAA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой AGCTGCAACCTGGCAACAAC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GCTGCAACCTGGCAACAACC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, содержащуюся в GGGCCAACAGCCAGCCTGCA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в GGGCCAACAGCCAGCCTGCA, причем последовательность, обнаруженная в GGGCCAACAGCCAGCCTGCA, содержит по меньшей мере 15 нуклеотидов. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GGGCCAACAGCCAGCCTGCA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GGGCCAACAGCCAGCCTGCA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GGCCAACAGCCAGCCTGCAG. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой GCCAACAGCCAGCCTGCAGG. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой CCAACAGCCAGCCTGCAGGA. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой CAACAGCCAGCCTGCAGGAG. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой AACAGCCAGCCTGCAGGAGG. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в ATTAATAAATTGTCATCACC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований содержит последовательность, обнаруженную в ATTAATAAATTGTCATCACC, причем последовательность, обнаруженная в ATTAATAAATTGTCATCACC, содержит по меньшей мере 15 нуклеотидов. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой ATTAATAAATTGTCATCACC. Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой ATTAATAAATTGTCATCACC.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает стереохимические параметры структуры для олигонуклеотидов. То есть, помимо всего прочего, настоящее изобретение демонстрирует влияние стереохимической структуры в разных положениях вдоль олигонуклеотидной цепи, например, на стабильность и/или активность олигонуклеотида, например, на взаимодействие олигонуклеотида с родственным лигандом и/или с ферментом для обработки. Настоящее раскрытие конкретно предусматривает олигонуклеотиды, структура которых включает или отражает параметры дизайна. Такие олигонуклеотиды представляют собой новые химические объекты по отношению к стереослучайным препаратам, имеющим ту же самую последовательность оснований и длину.
Согласно некоторым вариантам осуществления настоящее изобретение предусматривает стереохимические параметры дизайна для антисмысловых олигонуклеотидов. Согласно некоторым вариантам осуществления настоящее изобретение конкретно предусматривает параметры дизайна для олигонуклеотидов, которые могут связываться с и/или расщепляться РНКазой Н. Согласно некоторым вариантам осуществления настоящее изобретение предусматривает стереохимические параметры дизайна для олигонуклеотидов-миРНК. Согласно некоторым вариантам осуществления настоящее изобретение конкретно предусматривает параметры дизайна для олигонуклеотидов, которые могут быть связаны и/или расщеплены посредством, например, дайсер, белками аргонавт (например, аргонавт-1 и аргонавт-2) и т.д.
Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляет собой хиральную. Согласно некоторым вариантам осуществления по меньшей мере две из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере три из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере четыре из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере пять из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере шесть из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере семь из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере восемь из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере девять из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления одна первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляет собой хиральную. Согласно некоторым вариантам осуществления две из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления три из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления четыре из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления пять из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления шесть из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления семь из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляют собой хиральные. Согласно некоторым вариантам осуществления восемь из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления девять из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные.
Согласно некоторым вариантам осуществления десять из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные.
Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляет собой хиральную. Согласно некоторым вариантам осуществления по меньшей мере две из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере три из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере четыре из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере пять из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере шесть из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления по меньшей мере семь из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления одна из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляет собой хиральную. Согласно некоторым вариантам осуществления две из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления три из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления четыре из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления пять из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления шесть из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления семь из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные. Согласно некоторым вариантам осуществления восемь из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляют собой хиральные.
Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляет собой хиральную и по меньшей мере одна межнуклеотидная линкерная группа представляет собой ахиральную. Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляет собой хиральную и по меньшей мере одна межнуклеотидная линкерная группа представляет собой ахиральную. Согласно некоторым вариантам осуществления по меньшей мере две межнуклеотидные линкерные группы представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере три межнуклеотидные линкерные группы представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере четыре межнуклеотидные линкерные группы представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере пять межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере шесть межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере семь межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере восемь межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере девять межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 10 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 11 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 12 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 13 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 14 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 15 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 16 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 17 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 18 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 19 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 20 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления одна межнуклеотидная линкерная группа представляет собой ахиральную. Согласно некоторым вариантам осуществления две межнуклеотидные линкерные группы представляют собой ахиральные. Согласно некоторым вариантам осуществления три межнуклеотидные линкерные группы представляют собой ахиральные. Согласно некоторым вариантам осуществления четыре межнуклеотидные линкерные группы представляют собой ахиральные. Согласно некоторым вариантам осуществления пять межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления шесть межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления семь межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления восемь межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления девять межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 10 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 11 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 12 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 13 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 14 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 15 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 16 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 17 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 18 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 19 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления 20 межнуклеотидных линкерных групп представляют собой ахиральные. Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой все межнуклеотидные линкерные группы, за исключением по меньшей мере одной из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп, которая представляет собой хиральную, являются ахиральными.
Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляет собой хиральную и по меньшей мере одна межнуклеотидная линкерная группа представляет собой фосфат.
Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп представляет собой хиральную и по меньшей мере одна межнуклеотидная линкерная группа представляет собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере две межнуклеотидные линкерные группы представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере три межнуклеотидные линкерные группы представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере четыре межнуклеотидные линкерные группы представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере пять межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере шесть межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере семь межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере восемь межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере девять межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 10 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 11 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 12 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 13 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 14 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 15 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 16 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 17 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 18 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 19 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления по меньшей мере 20 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления одна межнуклеотидная линкерная группа представляет собой фосфат. Согласно некоторым вариантам осуществления две межнуклеотидные линкерные группы представляют собой фосфат. Согласно некоторым вариантам осуществления три межнуклеотидные линкерные группы представляют собой фосфат. Согласно некоторым вариантам осуществления четыре межнуклеотидные линкерные группы представляют собой фосфат. Согласно некоторым вариантам осуществления пять межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления шесть межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления семь межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления восемь межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления девять межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 10 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 11 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 12 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 13 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 14 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 15 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 16 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 17 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 18 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 19 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления 20 межнуклеотидных линкерных групп представляют собой фосфат. Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой все межнуклеотидные линкерные группы, за исключением по меньшей мере одной из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидных линкерных групп, которая представляет собой хиральную, представляют собой фосфат.
Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восьмой, девятой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидной линкерной группы представляет собой хиральную и по меньшей мере 10% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления один олигонуклеотид предложенной композиции содержит область, в которой по меньшей мере одна из первой, второй, третьей, пятой, седьмой, восемнадцатой, девятнадцатой и двадцатой межнуклеотидными линкерными группами представляет собой хиральную и по меньшей мере 10% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 20% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 30% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 40% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 50% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 60% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 70% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 80% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 90% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления по меньшей мере 50% всех межнуклеотидных линкерных групп в области представляют собой ахиральные. Согласно некоторым вариантам осуществления ахиральная межнуклеотидная линкерная группа представляет собой фосфатную линкерную группу. Согласно некоторым вариантам осуществления каждая ахиральная межнуклеотидная линкерная группа представляет собой фосфатную линкерную группу.
Согласно некоторым вариантам осуществления первая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления первая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления вторая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления вторая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления третья межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления третья межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления пятая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления пятая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления седьмая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления седьмая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления восьмая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления восьмая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления девятая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления девятая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления восемнадцатая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления восемнадцатая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления девятнадцатая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления девятнадцатая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации. Согласно некоторым вариантам осуществления двадцатая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Sp-конфигурации. Согласно некоторым вариантам осуществления двадцатая межнуклеотидная линкерная группа области представляет собой модифицированную межнуклеотидную линкерную группу в Rp-конфигурации.
Согласно некоторым вариантам осуществления область характеризуется длиной по меньшей мере 21 основание. Согласно некоторым вариантам осуществления область характеризуется длиной 21 основание. Согласно некоторым вариантам осуществления один олигонуклеотид в предложенной композиции характеризуется длиной по меньшей мере 21 основание. Согласно некоторым вариантам осуществления один олигонуклеотид в предложенной композиции характеризуется длиной 21 основание.
Согласно некоторым вариантам осуществления хиральная межнуклеотидная линкерная группа характеризуется структурой формулы I. Согласно некоторым вариантам осуществления хиральная межнуклеотидная линкерная группа является фосфоротиоатной. Согласно некоторым вариантам осуществления каждая хиральная межнуклеотидная линкерная группа в одном олигонуклеотиде предложенной композиции независимо характеризуется структурой формулы I. Согласно некоторым вариантам осуществления каждая хиральная межнуклеотидная линкерная группа в одном олигонуклеотиде предложенной композиции является фосфоротиоатной.
Согласно некоторым вариантам осуществления олигонуклеотиды по настоящему раскрытию содержат один или более модифицированных фрагментов сахара. Согласно некоторым вариантам осуществления олигонуклеотиды по настоящему раскрытию содержат один или более модифицированных фрагментов оснований. Как известно специалисту в данной области техники и описано в раскрытии, могут быть введены различные модификации в сахар и/или фрагмент. Например, согласно некоторым вариантам осуществления модификация представляет собой модификацию, описанную в US 9006198 и публикации международной заявки WO 2014/012081, модификации сахара и основания, каждая из которых включена в настоящее описание посредством ссылки.
Согласно некоторым вариантам осуществления модификация сахара представляет собой 2'-модификацию. Как правило, используемые 2'-модификации включают, но не ограничиваются ими, 2'-OR1, где R1 представляет собой не водород. Согласно некоторым вариантам осуществления модификация представляет собой 2'-OR, где R представляет собой необязательно замещенную алифатическую группу. Согласно некоторым вариантам осуществления модификация представляет собой 2'-ОМе. Согласно некоторым вариантам осуществления модификация представляет собой 2'-МОЕ. Согласно некоторым вариантам осуществления настоящее изобретение демонстрирует, что включение и/или положение конкретных хирально чистых межнуклеотидных линкерных групп может обеспечивать повышение стабильности, сравнимое с тем, которое достигается за счет использования модифицированных линкерных групп, оснований и/или сахаров остова, или быть лучше него. Согласно некоторым вариантам осуществления предложенный единственный олигонуклеотид предложенной композиции не имеет модификаций на сахарах. Согласно некоторым вариантам осуществления предложенный единственный олигонуклеотид предложенной композиции не имеет модификаций на 2'-положениях сахаров (т.е. две группы в 2'-положении представляют собой либо -Н/-Н, либо -Н/-ОН). Согласно некоторым вариантам осуществления предложенный единственный олигонуклеотид предложенной композиции не имеет каких-либо модификаций 2'-МОЕ.
Согласно некоторым вариантам осуществления 2'-модификация представляет собой -O-L- или -L-, который соединяет 2'-углерод фрагмента сахара с другим углеродом фрагмента сахара. Согласно некоторым вариантам осуществления 2'-модификация представляет собой -O-L- или -L-, который соединяет 2'-углерод фрагмента сахара с 4'-углеродом фрагмента сахара. Согласно некоторым вариантам осуществления 2'-модификация представляет собой S-cEt. Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой фрагмент LNA.
Согласно некоторым вариантам осуществления 2'-модификация представляет собой -F. Согласно некоторым вариантам осуществления 2'-модификация представляет собой FANA. Согласно некоторым вариантам осуществления 2'-модификация представляет собой FRNA.
Согласно некоторым вариантам осуществления модификация сахара представляет собой 5'-модификацию, например, R-5'-Ме, S-5'-Me и т.д.
Согласно некоторым вариантам осуществления модификация сахара изменяет размер сахарного кольца. Согласно некоторым вариантам осуществления модификация сахара представляет собой фрагмент сахара в ФГНК.
Согласно некоторым вариантам осуществления единственный олигонуклеотид предложенной композиции является лучшим субстратом для белков аргонавтов (например, hAgo-1 и hAgo-2) по сравнению со стереослучайными композициями олигонуклеотидов. Выбор и/или положение хирально чистых линкерных групп, как описано в настоящем описании, представляют собой полезные параметры дизайна для олигонуклеотидов, которые взаимодействуют с такими белками, как миРНК.
Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 25% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 30% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 35% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 40% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления один олигонуклеотид в представленной композиции, имеет, по меньшей мере примерно 45% его межнуклеотидных линкерных групп в конфигурации Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 50% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 55% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 60% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 65% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 70% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 75% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 80% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 85% межнуклеотидных линкерных групп характеризуются конфигурацией Sp. Согласно некоторым вариантам осуществления у единственного олигонуклеотида в предложенной композиции по меньшей мере примерно 90% межнуклеотидных линкерных групп характеризуются конфигурацией Sp.
Согласно некоторым вариантам осуществления олигонуклеотиды в представленной композиции не представляет собой олигонуклеотид, выбранный из: TkTkmCkAGTmCATGAmCTkTmCkmCk, где каждый нуклеозид, после которого следует нижний индекс 'k' обозначает (S)-cEt модификацию, R представляет собой фосфоротиоатную линкерную группу в конфигурации Rp, S представляет собой фосфоротиоатную линкерную группу в конфигурации Sp, каждый mC представляет собой 5-метилцитозин-модифицированный нуклеозид и все межнуклеозидные линкерные группы представляют собой фосфоротиоаты (PS) с профилями стереохимии выбранными из RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSSR, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRRSR, RRRRSSSSRS, SRRSRRRRRR, RSSRSSRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRRSRR, RSRRSRSSSR, RRSSRSRRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR, SSSSRRRRSR, RRRRRRRRRR и SSSSSSSSSS.
Согласно некоторым вариантам осуществления единственный олигонуклеотид в представленной композиции не представляет собой олигонуклеотид, выбранный из: TkTkmCkAGTmCATGAmCTTkmCkmCk, где каждый нуклеозид, после которого следует нижний индекс 'k' обозначает (S)-cEt модификацию, R представляет собой фосфоротиоатную линкерную группу в конфигурации Rp, S представляет собой фосфоротиоатную линкерную группу в конфигурации Sp, каждый mC представляет собой 5-метилцитозин-модифицированный нуклеозид и все межнуклеозидные линкерные группы сердцевины представляют собой фосфоротиоаты (PS) с профилями стереохимии выбранными из: RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSSR, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRRSR, RRRRSSSSRS, SRRSRRRRRR, RSSRSSRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRRSRR, RSRRSRSSSR, RRSSRSRRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR, SSSSRRRRSR, RRRRRRRRRR и SSSSSSSSSS.
Олигонуклеотиды с контролируемой хиральностью и композиции олигонуклеотидов с контролируемой хиральностью
В настоящем раскрытии предложены олигонуклеотиды с контролируемой хиральностью и композиции олигонуклеотидов с контролируемой хиральностью, которые имеют высокую чистоту и высокую диастереомерную чистоту. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды с контролируемой хиральностью и композиции олигонуклеотидов с контролируемой хиральностью, имеющие высокую чистоту. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды с контролируемой хиральностью и композиции олигонуклеотидов с контролируемой хиральностью, имеющие высокую диастереомерную чистоту.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой по существу чистый препарат типа олигонуклеотида в том отношении, что олигонуклеотиды в композиции, которые не представляют собой тип олигонуклеотидов, являются примесными формами процесса подготовки указанного типа олигонуклеотида, в некоторых случаях, после определенных процедур очистки.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды, содержащие одну или более диастереомерно чистых межнуклеотидных линкерных групп, если рассматривать хиральные атомы фосфора линкерных групп. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды, содержащие одну или более диастереомерно чистых межнуклеотидных линкерных групп, имеющих структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды, содержащие одну или более диастереомерно чистых межнуклеотидных линкерных групп, если рассматривать хиральные атомы фосфора, и одну или более фосфатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды, содержащие одну или более диастереомерно чистых межнуклеотидных линкерных групп, имеющих структуру формулы I, и одну или более фосфатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды, содержащие одну или более диастереомерно чистых межнуклеотидных линкерных групп, имеющих структуру формулы I-c, и одну или более фосфатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления указанные олигонуклеотиды получают при помощи стереоселективного способа синтеза олигонуклеотидов, описанного в настоящей заявке, для образования предварительно выбранных диастереомерно чистых межнуклеотидных линкерных групп, если рассматривать хиральные атомы фосфора линкерной группы. Например, в одном примере олигонуклеотида (Rp/Sp,Rp/Sp,Rp/Sp,Rp,Rp,Sp,Sp,Sp,Sp,SpSp,Sp,Sp,Sp,Rp,Rp,Rp,Rp,Rp)-d[GsCsCsTsCsAsGsTsCsTsGsCsTsTsCsGs1Cs1As1CsC] первые три межнуклеотидные линкерные группы получены при помощи традиционного способа синтеза олигонуклеотидов, а диастереомерно чистые межнуклеотидные линкерные группы получены при помощи стереохимического контроля согласно описанию настоящей заявки. Примеры межнуклеотидных линкерных групп, включая те, что имеют структуру формулы I, дополнительно описаны далее.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, причем по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различную стереохимию и/или различные модификации Р по сравнению друг с другом. В определенных вариантах реализации в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, причем по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различные модификации Р по сравнению друг с другом. В определенных вариантах реализации в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, причем по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различные модификации Р по сравнению друг с другом и причем олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу. В определенных вариантах реализации в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, причем по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различные модификации Р по сравнению друг с другом, и причем олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере одну фосфоротиоатную сложную диэфирную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления настоящее раскрытие представляет собой олигонуклеотид с контролируемой хиральностью, причем по меньшей мере две из отдельных межнуклеотидных линкерных групп внутри олигонуклеотида имеют разные модификации Р относительно друг друга и причем олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфоротиоатную сложную триэфирную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления настоящее раскрытие представляет собой олигонуклеотид с контролируемой хиральностью, причем по меньшей мере две из отдельных межнуклеотидных линкерных групп внутри олигонуклеотида имеют разные модификации Р относительно друг друга и причем олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере одну фосфоротиоатную сложную триэфирную межнуклеотидную линкерную группу.
В определенных вариантах реализации модифицированные межнуклеотидные линкерные группы независимо имеют структуру формулы I:
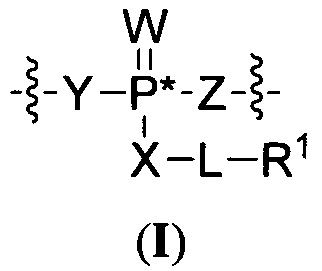
где каждая переменная такая, как определено и описано далее. Согласно некоторым вариантам осуществления линкерная группа формулы I представляет собой хиральную. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий одну или более модифицированных межнуклеотидных линкерных групп формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий одну или более модифицированных межнуклеотидных линкерных групп формулы I, и где отдельные межнуклеотидные линкерные группы формулы I в олигонуклеотиде содержат различные модификации Р по сравнению друг с другом. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий одну или более модифицированных межнуклеотидных линкерных групп формулы I, и где отдельные межнуклеотидные линкерные группы формулы I в олигонуклеотиде содержат различные группы X-L-R1 относительно друг друга. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий одну или более модифицированных межнуклеотидных линкерных групп формулы I, и где отдельные межнуклеотидные линкерные группы формулы I в олигонуклеотиде содержат различные X относительно друг друга. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий одну или более модифицированных межнуклеотидных линкерных групп формулы I, и где отдельные межнуклеотидные линкерные группы формулы I в олигонуклеотиде содержат различные -L-R1 относительно друг друга. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой олигонуклеотид в предложенной композиции, которая относится к определенному типу олигонуклеотида. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой олигонуклеотид в предложенной композиции, которая характеризуется одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления в настоящем изобретении предложен олигонуклеотид с контролируемой хиральностью, где по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различную стереохимию и/или различные модификации Р по сравнению друг с другом. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, где по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различную стереохимию по сравнению друг с другом, и по меньшей мере фрагмент структуры олигонуклеотида с контролируемой хиральностью характеризуется повторяющимся профилем групп с чередующейся стереохимией.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, где по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различные модификации Р по сравнению друг с другом за счет того, что они содержат различные атомы X во фрагментах -XLR1, и/или они содержат различные группы L во фрагментах -XLR1, и/или они содержат различные атомы R1 во фрагментах -XLR1.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, где по меньшей мере две отдельные межнуклеотидные линкерные группы в олигонуклеотиде имеют различную стереохимию и/или различные модификации Р по сравнению друг с другом, и олигонуклеотид имеет структуру, представленную следующей формулой:
[SBn1RBn2SBn3RBn4…SBnxRBny]
где:
каждый RB независимо представляет собой блок нуклеотидных звеньев, имеющих R-конфигурацию атомов фосфора линкерной группы;
каждый SB независимо представляет собой блок нуклеотидных звеньев, имеющих S-конфигурацию атомов фосфора линкерной группы;
каждый из n1-ny равен нулю или представляет собой целое число при условии, что по меньшей мере один нечетный n и по меньшей мере один четный n должен быть отличным от нуля, то есть олигонуклеотид содержит по меньшей мере две отдельные межнуклеотидные линкерные группы с различной стереохимией по сравнению друг с другом; и
где сумма n1-ny составляет от 2 до 200, а согласно некоторым вариантам осуществления находится в диапазоне от нижнего предела, выбранного из группы, состоящей из 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 или более, до верхнего предела, выбранного из группы, состоящей из 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190 и 200, где верхний предел выше нижнего предела.
В некоторых из указанных вариантов реализации все n имеют одинаковые значения; согласно некоторым вариантам осуществления каждый четный n имеет такое же значение, что и другие четные n; согласно некоторым вариантам осуществления каждый нечетный n имеет такое же значение, что и другие нечетные n; согласно некоторым вариантам осуществления по меньшей мере два четных n имеют значения, отличающиеся друг от друга; согласно некоторым вариантам осуществления по меньшей мере два нечетных n имеют значения, отличающиеся друг от друга.
Согласно некоторым вариантам осуществления по меньшей мере два соседние n равны друг другу, то есть предложенный олигонуклеотид содержит соседние блоки с S-стереохимией линкерных групп и R-стереохимией линкерных групп равной длины. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат повторяющиеся блоки с S- и R-стереохимией линкерных групп равной длины. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат повторяющиеся блоки с S- и R-стереохимией линкерных групп, где по меньшей мере два указанных блока имеют длины, отличающиеся друг от друга; в некоторых из указанных вариантов реализации каждый блок с S-стереохимией имеет одинаковую длину, которая отличается от каждого блока с R-стереохимией, которые необязательно могут иметь одинаковую длину друг с другом.
Согласно некоторым вариантам осуществления по меньшей мере два n, отделенные друг от друга, равны друг другу, то есть предложенный олигонуклеотид содержит по меньшей мере два блока линкерных групп с первой стереохимией, имеющие равную длину друг с другом и разделенные блоком линкерных групп с другой стереохимией, где разделительный блок может иметь одинаковую длину или различную длину с блоками, имеющими первую стереохимию.
Согласно некоторым вариантам осуществления n блоков линкерных групп, расположенных на концах предложенного олигонуклеотида, имеют одинаковые значения. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат терминальные блоки с одинаковой стереохимией линкерных групп. В некоторых из указанных вариантов реализации терминальные блоки отделены друг от друга центральным блоком, имеющим другую стереохимию линкерных групп.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой стереоблокмер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой стереоскипмер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой стереоальтмер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой гэпмер.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] имеет любой из описанных выше профилей и дополнительно имеет профиль модификации Р. Например, согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой стереоскипмер и скипмер с модификацией Р. Согласно некоторым вариантам осуществления предложены олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой стереоблокмер и альтмер с модификацией Р. Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой стереоальтмер и блокмер с модификацией Р.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид формулы [SBn1RBn2SBn3RBn4…SBnxRBny] представляет собой олигонуклеотид с контролируемой хиральностью, содержащий одну или более модифицированных межнуклеотидных линкерных групп, независимо имеющих структуру формулы I:
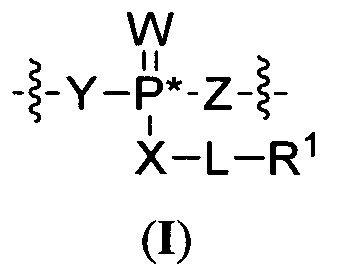
где:
Р* представляет собой асимметрический атом фосфора и имеет Rp или Sp-конфигурацию;
W представляет собой О, S или Se;
каждый из X, Y и Z независимо представляет собой -О-, -S-, -N(-L-R1)- или L;
L представляет собой ковалентную связь или необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенную группу, выбранную из C1-С6 алкилена, C1-С6 алкенилена, -С≡С- C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
R1 представляет собой галоген, R или необязательно замещенную С1-С50 алифатическую группу, где одно или более метиленовых звеньев возможно и необязательно заменены на необязательно замещенную группу, выбранную из C1-С6 алкилена, C1-С6 алкенилена, -С≡С-; C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
каждый R' независимо представляет собой -R, -C(O)R, -CO2R или -SO2R, или:
два R' взятые вместе со своими промежуточными атомами для образования необязательно замещенного арила, карбоциклического, гетероциклического или гетероарильного кольца;
-Су- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из фенилена, карбоциклилена, арилена, гетероарилена или гетероциклилена;
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из C1-С6 алифатической группы, карбоциклила, арила, гетероарила или гетеро циклила; и
каждый  независимо представляет собой место присоединения к нуклеозиду.
независимо представляет собой место присоединения к нуклеозиду.
Согласно некоторым вариантам осуществления L представляет собой ковалентную связь или необязательно замещенный линейный или разветвленный C1-C10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
R1 представляет собой галоген, R или необязательно замещенную C1-C50 алифатическую группу, где одно или более метиленовых звеньев возможно и необязательно заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
каждый R' независимо представляет собой -R, -C(O)R, -CO2R или -SO2R, или:
два R' при одном атоме азота объединены с соседними атомами с образованием необязательно замещенного гетероциклического или гетероарильного кольца, или
два R' при одном атоме углерода объединены с соседними атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца;
-Су- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из фенилена, карбоциклилена, арилена, гетероарилена или гетероциклилена;
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из C1-С6 алифатической группы, фенила, карбоциклила, арила, гетероарила или гетероциклила; и
каждый  независимо представляет собой место присоединения к нуклеозиду.
независимо представляет собой место присоединения к нуклеозиду.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит одну или более межнуклеотидных линкерных групп с модифицированным атомом фосфора. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит, например, фосфоротиоатную или фосфоротиоатную сложную триэфирную линкерную группу. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит фосфоротиоатную сложную триэфирную линкерную группу. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере две фосфоротиоатные сложные триэфирные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере три фосфоротиоатные сложные триэфирные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере четыре фосфоротиоатные сложные триэфирные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере пять фосфоротиоатных сложных триэфирных линкерных групп. Примеры таких модифицированных межнуклеотидных фосфорсодержащих линкерных групп дополнительно описаны в настоящей заявке.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит различные межнуклеотидные фосфорсодержащие линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере одну модифицированную межнуклеотидную линкерную группу. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере одну фосфоротиоатную сложную триэфирную линкерную группу. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере две фосфоротиоатные сложные триэфирные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере три фосфоротиоатные сложные триэфирные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере четыре фосфоротиоатные сложные триэфирные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере пять фосфоротиоатных сложных триэфирных линкерных групп. Примеры таких модифицированных межнуклеотидных фосфорсодержащих линкерных групп дополнительно описаны в настоящей заявке.
Согласно некоторым вариантам осуществления фосфоротиоатная сложная триэфирная линкерная группа содержит хиральное вспомогательное вещество, которое, например, используют для контроля стереоселективности взаимодействия. Согласно некоторым вариантам осуществления фосфоротиоатная сложная триэфирная линкерная группа не содержит хиральное вспомогательное вещество. Согласно некоторым вариантам осуществления фосфоротиоатную сложную триэфирную линкерную группу намеренно сохраняют до и/или во время введения субъекту.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью связан с твердой подложкой. Согласно некоторым вариантам осуществления проводят отщепление олигонуклеотида с контролируемой хиральностью от твердой подложки.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере две расположенные последовательно модифицированные межнуклеотидные линкерные группы. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью содержит по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере две расположенные последовательно фосфоротиоатные сложные триэфирные межнуклеотидные линкерные группы.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой блокмер. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой стереоблокмер. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой блокмер с модификацией Р. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой блокмер с одинаковыми линкерными группами.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой альтмер. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой стереоальтмер. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой альтмер с модификацией Р. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой альтмер с различными чередующимися линкерными группами.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой унимер. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой стереоунимер. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой унимер с модификацией Р. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой унимер с одинаковыми линкерными группами.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой гэпмер.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью представляет собой скипмер.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложены олигонуклеотиды, содержащие одну или более модифицированных межнуклеотидных линкерных групп, независимо имеющих структуру формулы I:
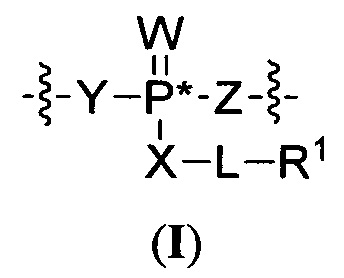
где:
Р* представляет собой асимметрический атом фосфора и имеет Rp- или Sp-конфигурацию;
W представляет собой О, S или Se;
каждый из X, Y и Z независимо представляет собой -О-, -S-, -NC-L-R1)- или L;
L представляет собой ковалентную связь или необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенную группу, выбранную из C1-С6 алкилена, C1-С6 алкенилена, -С≡С-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(O)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
R1 представляет собой галоген, R или необязательно замещенную С1-С50 алифатическую группу, где одно или более метиленовых звеньев возможно и необязательно заменены на необязательно замещенную группу, выбранную из C1-С6 алкилена, C1-С6 алкенилена, -С≡С, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
каждый R' независимо представляет собой -R, -C(O)R, -CO2R или -SO2R, или:
два R' взятые вместе со своими промежуточными атомами для образования необязательно замещенного арила, карбоциклического, гетероциклического или гетероарильного кольца;
-Су- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из фенилена, карбоциклилена, арилена, гетероарилена или гетероциклилена;
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из C1-С6 алифатической группы, карбоциклила, арила, гетероарила или гетероциклила; и
каждый  независимо представляет собой место присоединения к нуклеозиду.
независимо представляет собой место присоединения к нуклеозиду.
Согласно некоторым вариантам осуществления L представляет собой ковалентную связь или необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
R1 представляет собой галоген, R или необязательно замещенную C1-C50 алифатическую группу, где одно или более метиленовых звеньев возможно и необязательно заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R'), -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-;
каждый R' независимо представляет собой -R, -C(O)R, -CO2R или -SO2R, или:
два R' при одном атоме азота объединены с соседними атомами с образованием необязательно замещенного гетероциклического или гетероарильного кольца, или
два R' при одном атоме углерода объединены с соседними атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца;
-Су- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из фенилена, карбоциклилена, арилена, гетероарилена или гетероциклилена;
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из C1-С6 алифатической группы, фенила, карбоциклила, арила, гетероарила или гетероциклила; и
каждый  независимо представляет собой место присоединения к нуклеозиду.
независимо представляет собой место присоединения к нуклеозиду.
Согласно некоторым вариантам осуществления Р* представляет собой асимметрический атом фосфора и имеет Rp- или Sp-конфигурацию. Согласно некоторым вариантам осуществления Р* представляет собой Rp. В других вариантах реализации Р* представляет собой Sp. Согласно некоторым вариантам осуществления олигонуклеотид содержит одну или более межнуклеотидных линкерных групп формулы I, где каждый Р* независимо имеет Rp- или Sp-конфигурацию. Согласно некоторым вариантам осуществления олигонуклеотид содержит одну или более межнуклеотидных линкерных групп формулы I, где каждый Р* независимо представляет собой Rp. Согласно некоторым вариантам осуществления олигонуклеотид содержит одну или более межнуклеотидных линкерных групп формулы I, где каждый Р* независимо представляет собой Sp. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где Р* представляет собой Rp. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где Р* представляет собой Sp. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где Р* представляет собой Rp, и по меньшей мере одну межнуклеотидную линкерную группу формулы I, где Р* представляет собой Sp.
Согласно некоторым вариантам осуществления W представляет собой О, S или Se. Согласно некоторым вариантам осуществления W представляет собой О. Согласно некоторым вариантам осуществления W представляет собой S. Согласно некоторым вариантам осуществления W представляет собой Se. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где W представляет собой О. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где W представляет собой S. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где W представляет собой Se.
Согласно некоторым вариантам осуществления каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из C1-С6 алифатической группы, фенила, карбоциклила, арила, гетероарила или гетероциклила.
Согласно некоторым вариантам осуществления R представляет собой водород. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенную группу, выбранную из C1-С6 алифатической группы, фенила, карбоциклила, арила, гетероарила или гетероциклила.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенную C1-С6 алифатическую группу. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный C1-С6 алкил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный линейный или разветвленный гексил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный линейный или разветвленный пентил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный линейный или разветвленный бутил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный линейный или разветвленный пропил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный этил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный метил.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления R представляет собой замещенный фенил. Согласно некоторым вариантам осуществления R представляет собой фенил.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный карбоциклил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный С3-С10 карбоциклил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный моноциклический карбоциклил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный циклогептил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный циклогексил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный циклопентил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный циклобутил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный циклопропил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный бициклический карбоциклил.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный арил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное бициклическое арильное кольцо.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный гетероарил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 5-6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, серы или кислорода. Согласно некоторым вариантам осуществления R представляет собой замещенное 5-6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой незамещенное 5-6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, серы или кислорода.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 5-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, кислорода или серы.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 5-членное моноциклическое гетероарильное кольцо, содержащее 1 гетероатом, выбранный из азота, кислорода или серы. Согласно некоторым вариантам осуществления R выбран из пирролила, фуранила или тиенила.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 5-членное гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R представляет собой необязательно замещенное 5-членное гетероарильное кольцо, содержащее 1 атом азота и дополнительный гетероатом, выбранный из серы или кислорода. Примеры групп R включают необязательно замещенный пиразолил, имидазолил, тиазолил, изотиазолил, оксазолил и изоксазолил.
Согласно некоторым вариантам осуществления R представляет собой 6-членное гетероарильное кольцо, содержащее 1-3 атомов азота. В других вариантах реализации R представляет собой необязательно замещенное 6-членное гетероарильное кольцо, содержащее 1-2 атомов азота. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 6-членное гетероарильное кольцо, содержащее 2 атома азота. В определенных вариантах реализации R представляет собой необязательно замещенное 6-членное гетероарильное кольцо, содержащее 1 атом азота. Примеры групп R включают необязательно замещенный пиридинил, пиримидинил, пиразинил, пиридазинил, триазинил или тетразинил.
В определенных вариантах реализации R представляет собой необязательно замещенное 8-10-членное бициклическое гетероарильное кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. В других вариантах реализации R представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 1 гетероатом, независимо выбранный из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный индолил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный азабицикло[3.2.1]октанил. В определенных вариантах реализации R представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный азаиндолил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный бензимидазолил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный бензотиазолил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный бензоксазолил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный индазолил. В определенных вариантах реализации R представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 3 гетероатома, независимо выбранных из азота, кислорода или серы.
В определенных вариантах реализации R представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В других вариантах реализации R представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 1 гетероатом, независимо выбранный из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный хинолинил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный изохинолинил. Согласно одному из аспектов R представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой хиназолин или хиноксалин.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный гетероциклил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой замещенное 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой незамещенное 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный гетероциклил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 6-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 6-членное частично ненасыщенное гетероциклическое кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 6-членное частично ненасыщенное гетероциклическое кольцо, содержащее 2 атома кислорода.
В определенных вариантах реализации R представляет собой 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R представляет собой оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, оксепанил, азиридинил, азетидинил, пирролидинил, пиперидинил, азепанил, тииранил, тиетанил, тетрагидротиофенил, тетрагидротиопиранил, тиепанил, диоксоланил, оксатиоланил, оксазолидинил, имидазолидинил, тиазолидинил, дитиоланил, диоксанил, морфолинил, оксатианил, пиперазинил, тиоморфолинил, дитианил, диоксепанил, оксазепанил, оксатиепанил, дитиепанил, диазепанил, дигидрофуранонил, тетрагидропиранонил, оксепанонил, пирролидинонил, пиперидинонил, азепанонил, дигидротиофенонил, тетрагидротиопиранонил, тиепанонил, оксазолидинонил, оксазинанонил, оксазепанонил, диоксоланонил, диоксанонил, диоксепанонил, оксатиолинонил, оксатианонил, оксатиепанонил, тиазолидинонил, тиазинанонил, тиазепанонил, имидазолидинонил, тетрагидропиримидинонил, диазепанонил, имидазолидиндионил, оксазолидиндионил, тиазолидиндионил, диоксоландионил, оксатиоландионил, пиперазиндионил, морфолиндионил, тиоморфолиндионил, тетрагидропиранил, тетрагидрофуранил, морфолинил, тиоморфолинил, пиперидинил, пиперазинил, пирролидинил, тетрагидротиофенил или тетрагидротиопиранил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 5-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы.
В определенных вариантах реализации R представляет собой необязательно замещенное 5-6-членное частично ненасыщенное моноциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R представляет собой необязательно замещенный тетрагидропиридинил, дигидротиазолил, дигидрооксазолил или оксазолинильную группу.
Согласно некоторым вариантам осуществления R представляет собой необязательно замещенное 8-10-членное бициклическое насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный индолинил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный изоиндолинил. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный 1,2,3,4-тетрагидрохинолин. Согласно некоторым вариантам осуществления R представляет собой необязательно замещенный 1,2,3,4-тетрагидроизохинолин.
Согласно некоторым вариантам осуществления каждый R' независимо представляет собой -R, -C(O)R, -CO2R или -SO2R, или:
два R' при одном атоме азота объединены с соседними атомами с образованием необязательно замещенного гетероциклического или гетероарильного кольца, или
два R' при одном атоме углерода объединены с соседними атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца.
Согласно некоторым вариантам осуществления R' представляет собой -R, -C(O)R, -CO2R или -SO2R, где R такой, как определено и описано выше.
Согласно некоторым вариантам осуществления R' представляет собой -R, где R такой, как определено и описано выше. Согласно некоторым вариантам осуществления R' представляет собой водород.
Согласно некоторым вариантам осуществления R' представляет собой -C(O)R, где R такой, как определено и описано выше. Согласно некоторым вариантам осуществления R' представляет собой -CO2R, где R такой, как определено и описано выше. Согласно некоторым вариантам осуществления R' представляет собой -SO2R, где R такой, как определено и описано выше.
Согласно некоторым вариантам осуществления два R' при одном атоме азота объединены с соседними атомами с образованием необязательно замещенного гетероциклического или гетероарильного кольца. Согласно некоторым вариантам осуществления два R' при одном атоме углерода объединены с соседними атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца.
Согласно некоторым вариантам осуществления -Су- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из фенилена, карбоциклилена, арилена, гетероарилена или гетероциклилена.
Согласно некоторым вариантам осуществления -Су- представляет собой необязательно замещенный фенилен. Согласно некоторым вариантам осуществления -Су- представляет собой необязательно замещенный карбоциклилен. Согласно некоторым вариантам осуществления -Су- представляет собой необязательно замещенный арилен. Согласно некоторым вариантам осуществления -Су- представляет собой необязательно замещенный гетероарилен. Согласно некоторым вариантам осуществления -Су- представляет собой необязательно замещенный гетероциклилен.
Согласно некоторым вариантам осуществления каждый из X, Y и Z независимо представляет собой -О-, -S-, -N(-L-R1)- или L, где каждый из L и R1 независимо является таким, как определено выше и описано далее.
Согласно некоторым вариантам осуществления X представляет собой -О-. Согласно некоторым вариантам осуществления X представляет собой -S-. Согласно некоторым вариантам осуществления X представляет собой -О- или -S-. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где X представляет собой -О-. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где X представляет собой -S-. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где X представляет собой -О-, и по меньшей мере одну межнуклеотидную линкерную группу формулы I, где X представляет собой -S-. Согласно некоторым вариантам осуществления олигонуклеотид содержит по меньшей мере одну межнуклеотидную линкерную группу формулы I, где X представляет собой -О-, и по меньшей мере одну межнуклеотидную линкерную группу формулы I, где X представляет собой -S-, и по меньшей мере одну межнуклеотидную линкерную группу формулы I, где L представляет собой необязательно замещенный линейный или разветвленный C1-С10 алкилен, причем одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -C≡C-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R'), -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-.
Согласно некоторым вариантам осуществления X представляет собой -N(-L-R1)-. Согласно некоторым вариантам осуществления X представляет собой -N(R1)-. Согласно некоторым вариантам осуществления X представляет собой -N(R')-. Согласно некоторым вариантам осуществления X представляет собой -N(R)-. Согласно некоторым вариантам осуществления X представляет собой -NH-.
Согласно некоторым вариантам осуществления X представляет собой L. Согласно некоторым вариантам осуществления X представляет собой ковалентную связь. Согласно некоторым вариантам осуществления X представляет собой необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, - С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-. Согласно некоторым вариантам осуществления X представляет собой необязательно замещенный C1-C10 алкилен или C1-С10 алкенилен. Согласно некоторым вариантам осуществления X представляет собой метилен.
Согласно некоторым вариантам осуществления Y представляет собой -О-. Согласно некоторым вариантам осуществления Y представляет собой -S-.
Согласно некоторым вариантам осуществления Y представляет собой -N(-L-R1)-. Согласно некоторым вариантам осуществления Y представляет собой -N(R1)-. Согласно некоторым вариантам осуществления Y представляет собой -N(R')-. Согласно некоторым вариантам осуществления Y представляет собой -N(R)-. Согласно некоторым вариантам осуществления Y представляет собой -NH-.
Согласно некоторым вариантам осуществления Y представляет собой L. Согласно некоторым вариантам осуществления Y представляет собой ковалентную связь. Согласно некоторым вариантам осуществления Y представляет собой необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, - С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-. Согласно некоторым вариантам осуществления Y представляет собой необязательно замещенный C1-C10 алкилен или C1-С10 алкенилен. Согласно некоторым вариантам осуществления Y представляет собой метилен.
Согласно некоторым вариантам осуществления Z представляет собой -О-. Согласно некоторым вариантам осуществления Z представляет собой -S-.
Согласно некоторым вариантам осуществления Z представляет собой -N(-L-R1)-. Согласно некоторым вариантам осуществления Z представляет собой -N(R1)-. Согласно некоторым вариантам осуществления Z представляет собой -N(R')-. Согласно некоторым вариантам осуществления Z представляет собой -N(R)-. Согласно некоторым вариантам осуществления Z представляет собой -NH-.
Согласно некоторым вариантам осуществления Z представляет собой L. Согласно некоторым вариантам осуществления Z представляет собой ковалентную связь. Согласно некоторым вариантам осуществления Z представляет собой необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-. Согласно некоторым вариантам осуществления Z представляет собой необязательно замещенный C1-С10 алкилен или C1-С10 алкенилен. Согласно некоторым вариантам осуществления Z представляет собой метилен.
Согласно некоторым вариантам осуществления L представляет собой ковалентную связь или необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-.
Согласно некоторым вариантам осуществления L представляет собой ковалентную связь. Согласно некоторым вариантам осуществления L представляет собой необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-C6 алкилен, C1-C6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-.
Согласно некоторым вариантам осуществления L имеет структуру -L1-V-, где:
L1 представляет собой необязательно замещенную группу, выбранную из 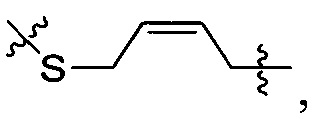
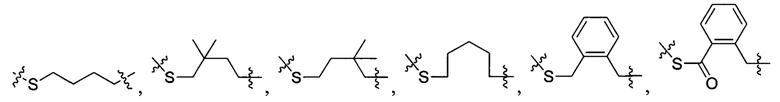
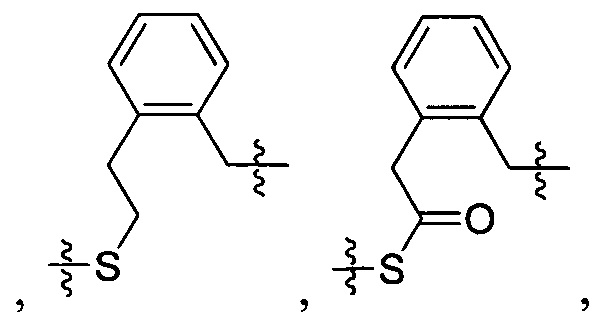 C1-С6 алкилена, C1-С6 алкенилена, карбоциклилена, арилена, C1-С6 гетероалкилена, гетероциклилена и гетероарилена;
C1-С6 алкилена, C1-С6 алкенилена, карбоциклилена, арилена, C1-С6 гетероалкилена, гетероциклилена и гетероарилена;
V выбран из -О-, -S-, -NR'-, C(R')2, -S-S-, -B-S-S-C-, 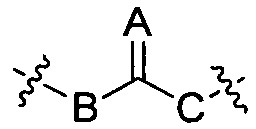 или необязательно замещенной группы, выбранной из C1-С6 алкилена, арилена, C1-С6 гетероалкилена, гетероциклилена и гетероарилена;
или необязательно замещенной группы, выбранной из C1-С6 алкилена, арилена, C1-С6 гетероалкилена, гетероциклилена и гетероарилена;
А представляет собой =O, =S, =NR' или =C(R')2;
каждый из В и С независимо представляет собой -O-, -S-, -NR'-, -C(R')2- или необязательно замещенную группу, выбранную из C1-С6 алкилена, карбоциклилена, арилена, гетероциклилена или гетероарилена; и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L1 представляет собой 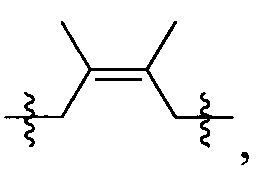

Согласно некоторым вариантам осуществления L1 представляет собой 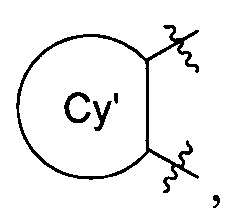 где кольцо Су' представляет собой необязательно замещенный арилен, карбоциклилен, гетероарилен или гетероциклилен. Согласно некоторым вариантам осуществления L1 представляет собой необязательно замещенный
где кольцо Су' представляет собой необязательно замещенный арилен, карбоциклилен, гетероарилен или гетероциклилен. Согласно некоторым вариантам осуществления L1 представляет собой необязательно замещенный 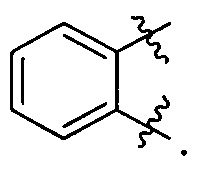 Согласно некоторым вариантам осуществления L1 представляет собой
Согласно некоторым вариантам осуществления L1 представляет собой 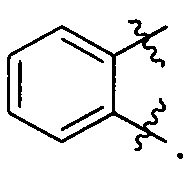
Согласно некоторым вариантам осуществления L1 соединен с X. Согласно некоторым вариантам осуществления L1 представляет собой необязательно замещенную группу, выбранную из 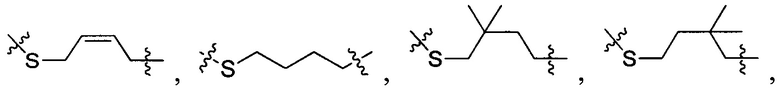
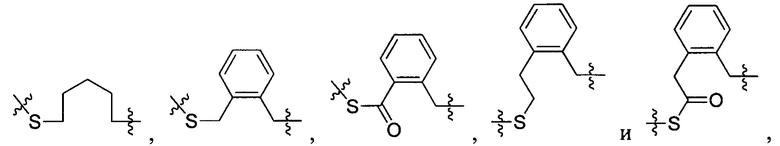 а атом серы соединен с V. Согласно некоторым вариантам осуществления L1 представляет собой необязательно замещенную группу, выбранную из
а атом серы соединен с V. Согласно некоторым вариантам осуществления L1 представляет собой необязательно замещенную группу, выбранную из 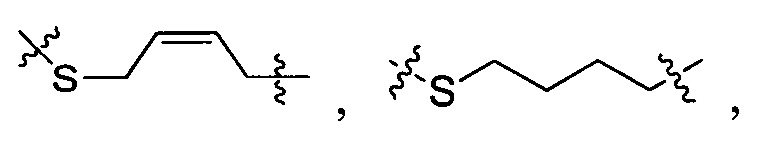
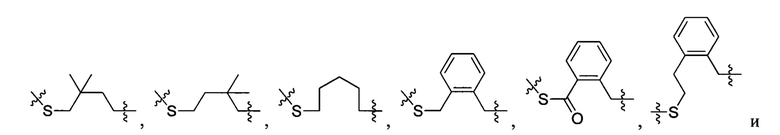
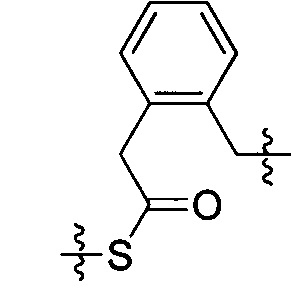 , а атом углерода соединен с X.
, а атом углерода соединен с X.
Согласно некоторым вариантам осуществления L имеет структуру:
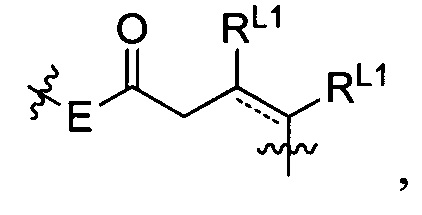
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
 представляет собой простую или двойную связь;
представляет собой простую или двойную связь;
два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, карбоциклического, гетероарильного или гетероциклического кольца; и каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
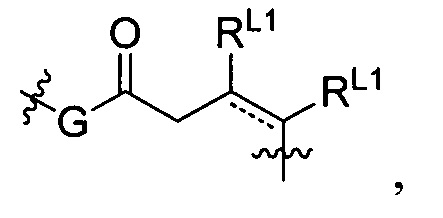
где:
G представляет собой -О-, -S- или -NR';
 представляет собой простую или двойную связь; и
представляет собой простую или двойную связь; и
два RL1 совместно с двумя атомами углерода, с которыми они связаны, образуют необязательно замещенное арильное, С3-С10 карбоциклическое, гетероарильное или гетероциклическое кольцо.
Согласно некоторым вариантам осуществления L имеет структуру:
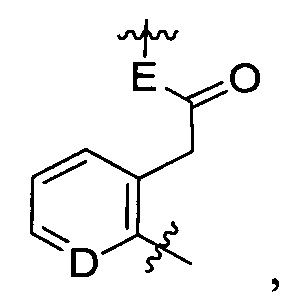
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =С(СО2-(С1-С6 алифатическая группа))- или =С(CF3)-; и
каждый R' является независимо таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
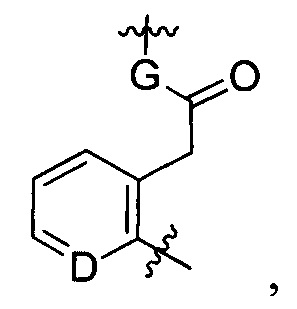
где:
G представляет собой -О-, -S- или -NR';
D представляет собой =N-, =C(F)-, =С(Cl)-, -C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =С(СО2-(C1-С6 алифатическая группа))- или =С(CF3)-.
Согласно некоторым вариантам осуществления L имеет структуру:
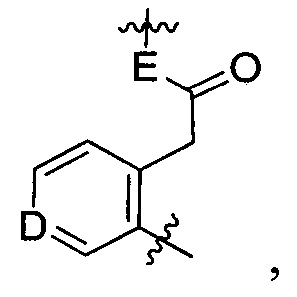
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
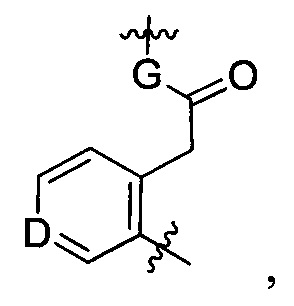
где:
G представляет собой -О-, -S- или -NR';
D представляет собой =N-, =C(F)-, =С(Cl)-, =С(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-.
Согласно некоторым вариантам осуществления L имеет структуру:
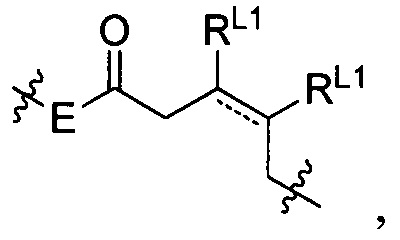
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
 представляет собой простую или двойную связь;
представляет собой простую или двойную связь;
два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца;
и каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
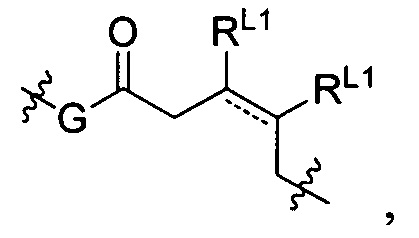
где:
G представляет собой -О-, -S- или -NR';
 представляет собой простую или двойную связь;
представляет собой простую или двойную связь;
два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца;
и каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
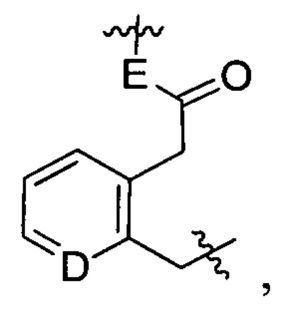
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
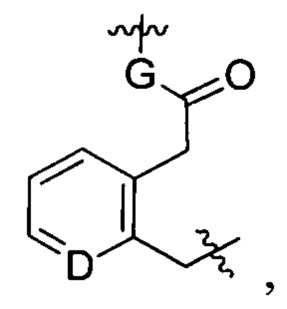
где:
G представляет собой -О-, -S- или -NR';
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =С(СО2-(С1-С6 алифатическая группа))- или =С(CF3)- и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
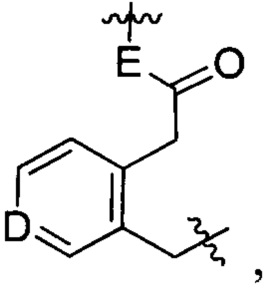 где:
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
D представляет собой =N-, =C(F)-, =C(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
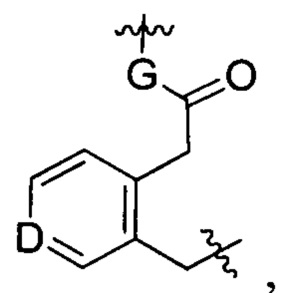
где:
G представляет собой -О-, -S- или -NR';
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
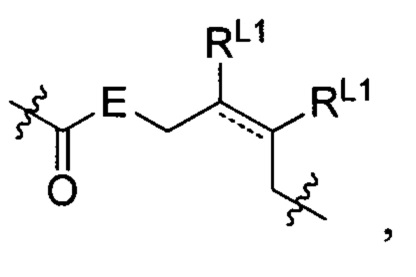
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
 представляет собой простую или двойную связь; два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца; и каждый R' независимо является таким, как определено выше в настоящем описании.
представляет собой простую или двойную связь; два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца; и каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
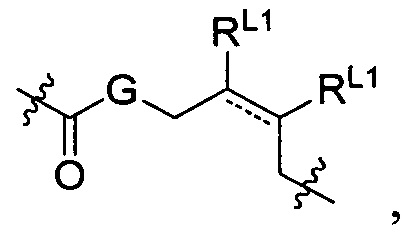
где:
G представляет собой -О-, -S- или -NR';
 представляет собой простую или двойную связь;
представляет собой простую или двойную связь;
два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца; и каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
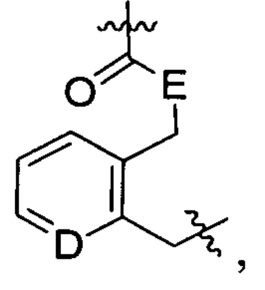
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-С6 алифатическая группа))- или =С(CF3)-; и
каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L имеет структуру:
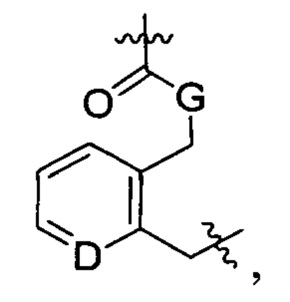
где:
G представляет собой -О-, -S- или -NR';
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
R' является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
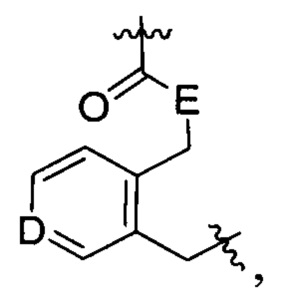
где:
Е представляет собой -О-, -S-, -NR'- или -C(R')2-;
D представляет собой =N-, =C(F)-, =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
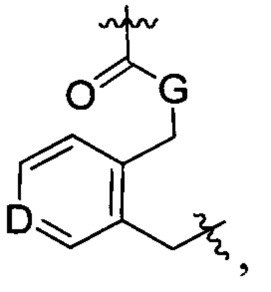
где:
G представляет собой -О-, -S- или -NR';
D представляет собой =N-, =C(F), =С(Cl)-, =C(Br)-, =C(I)-, =C(CN)-, =C(NO2)-, =C(CO2-(C1-C6 алифатическая группа))- или =С(CF3)-; и
R' является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L имеет структуру:
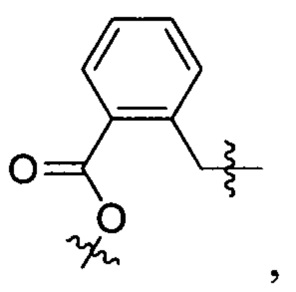
где фенильное кольцо является необязательно замещенным. Согласно некоторым вариантам осуществления фенильное кольцо является незамещенным. Согласно некоторым вариантам осуществления фенильное кольцо является замещенным.
Согласно некоторым вариантам осуществления L имеет структуру:
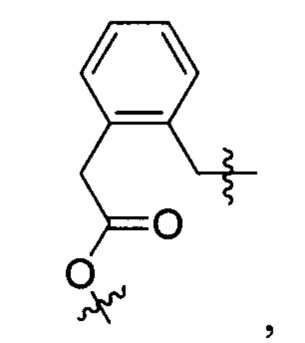
где фенильное кольцо является необязательно замещенным. Согласно некоторым вариантам осуществления фенильное кольцо является незамещенным. Согласно некоторым вариантам осуществления фенильное кольцо является замещенным.
Согласно некоторым вариантам осуществления L имеет структуру:
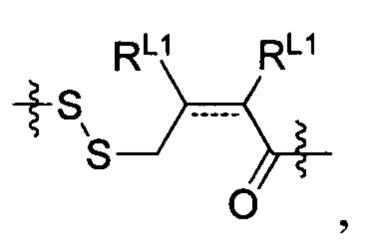
где:
 представляет собой простую или двойную связь; и
представляет собой простую или двойную связь; и
два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца.
Согласно некоторым вариантам осуществления L имеет структуру:
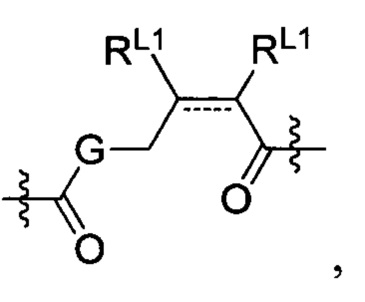
где:
G представляет собой -О-, -S- или -NR';
 представляет собой простую или двойную связь; и
представляет собой простую или двойную связь; и
два RL1 объединены с двумя атомами углерода, с которыми они связаны, с образованием необязательно замещенного арильного, С3-С10 карбоциклического, гетероарильного или гетероциклического кольца.
Согласно некоторым вариантам осуществления Е представляет собой -О-, -S-, -NR'-или -C(R')2-, где каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления Е представляет собой -О-, -S-или -NR'-. Согласно некоторым вариантам осуществления Е представляет собой -О-, -S-или -NH-. Согласно некоторым вариантам осуществления Е представляет собой -О-. Согласно некоторым вариантам осуществления Е представляет собой -S-. Согласно некоторым вариантам осуществления Е представляет собой -NH-.
Согласно некоторым вариантам осуществления G представляет собой -О-, -S- или -NR', где каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления G представляет собой -О-, -S-или -NH-. Согласно некоторым вариантам осуществления G представляет собой -О-. Согласно некоторым вариантам осуществления G представляет собой -S-. Согласно некоторым вариантам осуществления G представляет собой -NH-.
Согласно некоторым вариантам осуществления L представляет собой -L3-G-, где:
L3 представляет собой необязательно замещенный С1-С5 алкилен или алкенилен, причем одно или более метиленовых звеньев возможно и независимо заменены на -О-, -S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -S(O)-, -S(O)2- или  и
и
каждый из G, R' и кольца Су' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L представляет собой -L3-S-, где L3 является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой -L3-O-, где L3 является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой -L3-N(R')-, где каждый из L3 и R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой -L3-NH-, где каждый из L3 и R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L3 представляет собой необязательно замещенный С5 алкилен или алкенилен, где одно или более метиленовых звеньев возможно и независимо заменены на -О-, -S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -S(O)-, -S(O)2- или  а каждый из R' и кольца Су' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L3 представляет собой необязательно замещенный С5 алкилен. Согласно некоторым вариантам осуществления -L3-G- представляет собой
а каждый из R' и кольца Су' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L3 представляет собой необязательно замещенный С5 алкилен. Согласно некоторым вариантам осуществления -L3-G- представляет собой 
Согласно некоторым вариантам осуществления L3 представляет собой необязательно замещенный С4 алкилен или алкенилен, где одно или более метиленовых звеньев возможно и независимо заменены на -О-, -S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -S(O)-, -S(O)2- или  , а каждый из R' и Су' независимо является таким, как определено выше в настоящем описании.
, а каждый из R' и Су' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L3-G- представляет собой 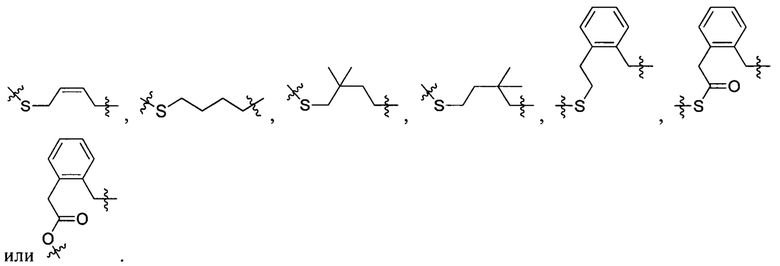 .
.
Согласно некоторым вариантам осуществления L3 представляет собой необязательно замещенный С3 алкилен или алкенилен, где одно или более метиленовых звеньев возможно и независимо заменены на -О-, -S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -S(O)-, -S(O)2- или 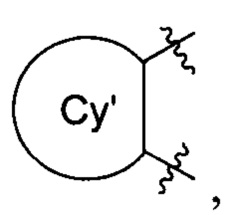 и каждый из R' и Су' независимо является таким, как определено выше в настоящем описании.
и каждый из R' и Су' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L3-G- представляет собой 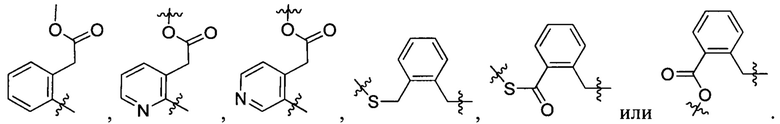
Согласно некоторым вариантам осуществления L представляет собой 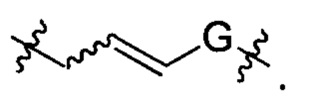
Согласно некоторым вариантам осуществления L представляет собой 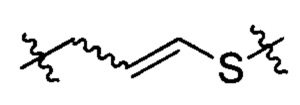 или
или 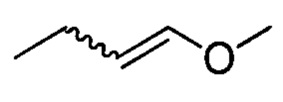 . Согласно некоторым вариантам осуществления L представляет собой
. Согласно некоторым вариантам осуществления L представляет собой 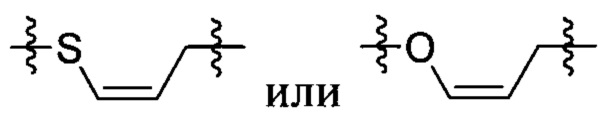 .
.
Согласно некоторым вариантам осуществления L3 представляет собой необязательно замещенный С2 алкилен или алкенилен, где одно или более метиленовых звеньев возможно и независимо заменены на -О-, -S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -S(O)-, -S(O)2- или 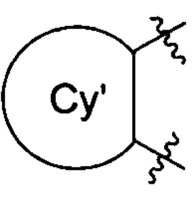 , и каждый из R' и Су' независимо является таким, как определено выше в настоящем описании.
, и каждый из R' и Су' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L3-G- представляет собой 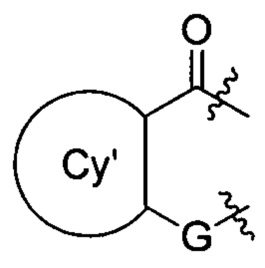 , где каждый из G и Су' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой
, где каждый из G и Су' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой 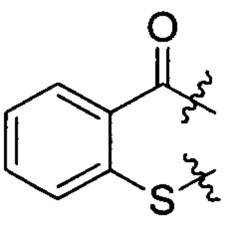 .
.
Согласно некоторым вариантам осуществления L представляет собой -L4-G-, где L4 представляет собой необязательно замещенный С1-С2 алкилен; и G является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой -L4-G-, где L4 представляет собой необязательно замещенный С1-С2 алкилен; G является таким, как определено выше в настоящем описании; и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой -L4-G-, где L4 представляет собой необязательно замещенный метилен; G является таким, как определено выше в настоящем описании; и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой -L4-G-, где L4 представляет собой метилен; G является таким, как определено выше в настоящем описании; и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой -L4-G-, где L4 представляет собой необязательно замещенный -(СН2)2-; G является таким, как определено выше в настоящем описании; и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой -L4-G-, где L4 представляет собой -(СН2)2-; G является таким, как определено выше в настоящем описании; и G соединен с R1.
Согласно некоторым вариантам осуществления L представляет собой 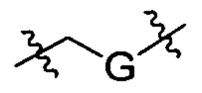 или
или 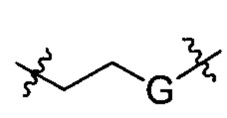 , где G является таким, как определено выше в настоящем описании, и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой
, где G является таким, как определено выше в настоящем описании, и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой 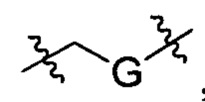 , где G является таким, как определено выше в настоящем описании, и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой
, где G является таким, как определено выше в настоящем описании, и G соединен с R1. Согласно некоторым вариантам осуществления L представляет собой 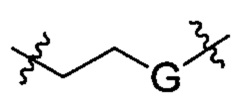 , где G является таким, как определено выше в настоящем описании, и G соединен с R1.
, где G является таким, как определено выше в настоящем описании, и G соединен с R1.
Согласно некоторым вариантам осуществления L представляет собой 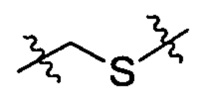 или
или 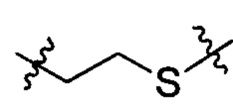 , где атом серы соединен с R1. Согласно некоторым вариантам осуществления L представляет собой
, где атом серы соединен с R1. Согласно некоторым вариантам осуществления L представляет собой 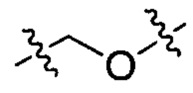 или
или 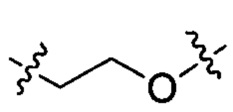 , где атом кислорода соединен с R1.
, где атом кислорода соединен с R1.
Согласно некоторым вариантам осуществления L представляет собой 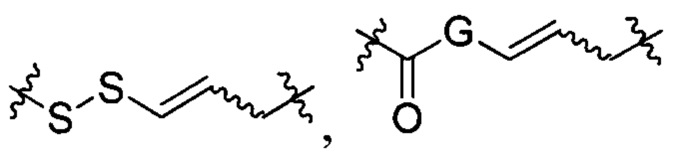 или
или 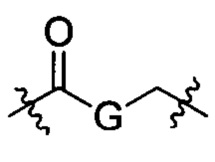 , где G является таким, как определено выше в настоящем описании.
, где G является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления L представляет собой -S-RL3_ или -S-C(O)-RL3_, где RL3_ представляет собой необязательно замещенный линейный или разветвленный С1-С9 алкилен, причем одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -C≡C-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, где каждый из R' и -Су- независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления L представляет собой -S-RL3_ или -S-C(O)-RL3_, где RL3_ представляет собой необязательно замещенный C1-С6 алкилен. Согласно некоторым вариантам осуществления L представляет собой -S-RL3_ или -S-C(O)-RL3_, где RL3_ представляет собой необязательно замещенный C1-С6 алкенилен. Согласно некоторым вариантам осуществления L представляет собой -S-RL3_ или -S-C(O)-RL3_, где RL3_ представляет собой необязательно замещенный C1-С6 алкилен, причем одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкенилен, арилен или гетероарилен. Согласно некоторым вариантам осуществления RL3_ представляет собой необязательно замещенный -S-(C1-C6 алкенилен)-, -S-(C1-C6 алкилен)-, -S-(C1-C6 алкилен)-арилен-(С1-С6 алкилен)-, -S-СО-арилен-(С1-С6 алкилен)- или -S-CO-(C1-C6 алкилен)-арилен-(С1-С6 алкилен)-.
Согласно некоторым вариантам осуществления L представляет собой 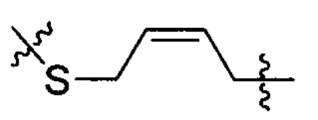
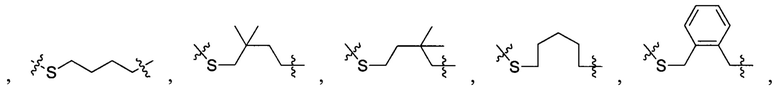
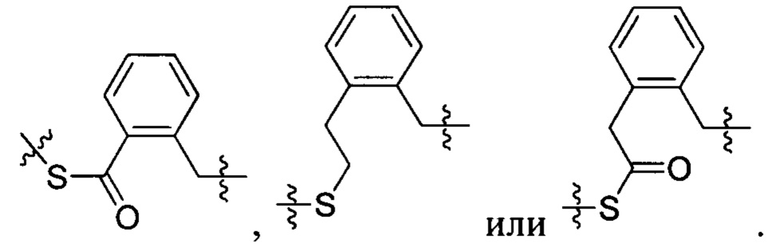
Согласно некоторым вариантам осуществления L представляет собой 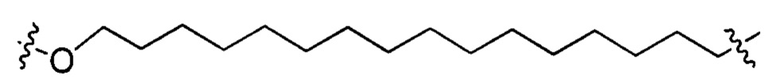 . Согласно некоторым вариантам осуществления L представляет собой
. Согласно некоторым вариантам осуществления L представляет собой 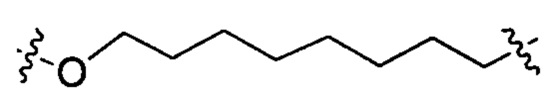 . Согласно некоторым вариантам осуществления
. Согласно некоторым вариантам осуществления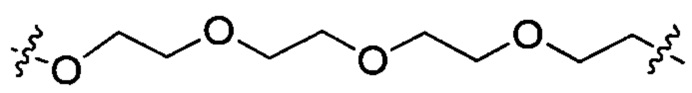 .
.
Согласно некоторым вариантам осуществления атом серы в вариантах реализации L, описанных выше в настоящей заявке, соединен с X. Согласно некоторым вариантам осуществления атом серы в вариантах реализации L, описанных выше в настоящей заявке, соединен с R1.
Согласно некоторым вариантам осуществления R1 представляет собой галоген, R или необязательно замещенную С1-С50 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, где каждая переменная независимо является такой, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой галоген, R или необязательно замещенную C1-С10 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-C6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления R1 представляет собой водород. Согласно некоторым вариантам осуществления R1 представляет собой галоген. Согласно некоторым вариантам осуществления R1 представляет собой -F. Согласно некоторым вариантам осуществления R1 представляет собой -Cl. Согласно некоторым вариантам осуществления R1 представляет собой -Br. Согласно некоторым вариантам осуществления R1 представляет собой -I.
Согласно некоторым вариантам осуществления R1 представляет собой R, где R такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления R1 представляет собой водород. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную группу, выбранную из C1-C50 алифатической группы, фенила, карбоциклила, арила, гетероарила или гетероциклила.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную С1-С50 алифатическую группу. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную C1-C10 алифатическую группу. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную C1-С6 алифатическую группу. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный C1-С6 алкил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный линейный или разветвленный гексил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный линейный или разветвленный пентил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный линейный или разветвленный бутил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный линейный или разветвленный пропил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный этил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный метил.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления R1 представляет собой замещенный фенил. Согласно некоторым вариантам осуществления R1 представляет собой фенил.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный карбоциклил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный С3-С10 карбоциклил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный моноциклический карбоциклил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный циклогептил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный циклогексил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный циклопентил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный циклобутил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный циклопропил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный бициклический карбоциклил.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный С1-С50 полициклический углеводород. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный С1-С50 полициклический углеводород, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, причем каждая переменная независимо является такой, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный 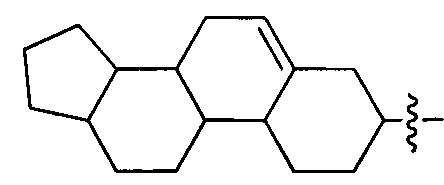 . Согласно некоторым вариантам осуществления R1 представляет собой
. Согласно некоторым вариантам осуществления R1 представляет собой 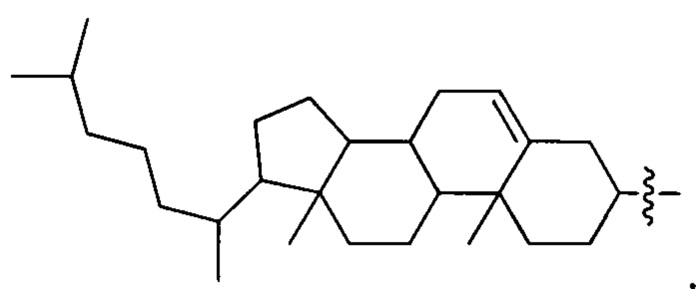 . Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный
. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный 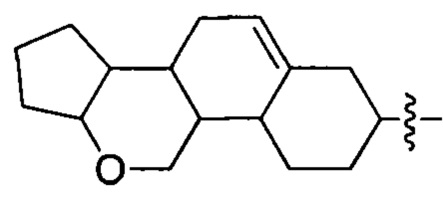 .
.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную С1-С50 алифатическую группу, содержащую один или более необязательно замещенных фрагментов полициклических углеводородов. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную C1-C50 алифатическую группу, содержащую один или более необязательно замещенных фрагментов полициклических углеводородов, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-C6 алкенилен, -С≡C-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, причем каждая переменная независимо является такой, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную С1-С50 алифатическую группу, содержащую один или более необязательно замещенных 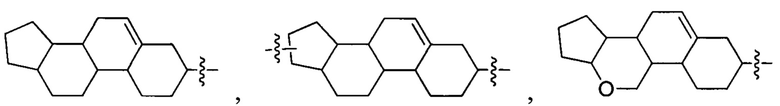 или
или 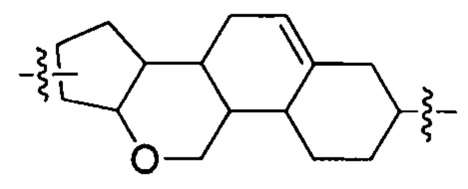 . Согласно некоторым вариантам осуществления R1 представляет собой
. Согласно некоторым вариантам осуществления R1 представляет собой 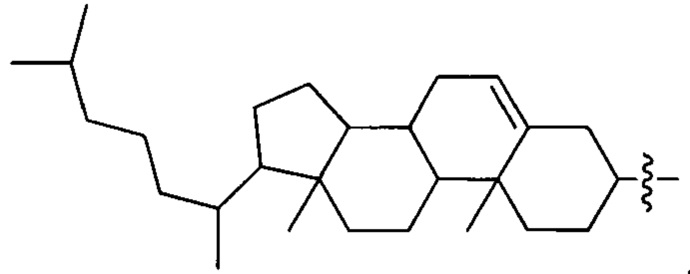 . Согласно некоторым вариантам осуществления R1 представляет собой
. Согласно некоторым вариантам осуществления R1 представляет собой  . Согласно некоторым вариантам осуществления R1 представляет собой
. Согласно некоторым вариантам осуществления R1 представляет собой  . Согласно некоторым вариантам осуществления R1 представляет собой
. Согласно некоторым вариантам осуществления R1 представляет собой  . Согласно некоторым вариантам осуществления R1 представляет собой
. Согласно некоторым вариантам осуществления R1 представляет собой  .
.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный арил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное бициклическое арильное кольцо.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный гетероарил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 5-6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, серы или кислорода. Согласно некоторым вариантам осуществления R1 представляет собой замещенное 5-6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой незамещенное 5-6-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, серы или кислорода.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 5-членное моноциклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 6-членное моно циклическое гетероарильное кольцо, содержащее 1-3 гетероатомов, независимо выбранных из азота, кислорода или серы.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 5-членное моноциклическое гетероарильное кольцо, содержащее 1 гетероатом, выбранный из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 выбран из пирролила, фуранила или тиенила.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 5-членное гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R1 представляет собой необязательно замещенное 5-членное гетероарильное кольцо, содержащее 1 атом азота и дополнительный гетероатом, выбранный из серы или кислорода. Примеры групп R1 включают необязательно замещенный пиразолил, имидазолил, тиазолил, изотиазолил, оксазолил и изоксазолил.
Согласно некоторым вариантам осуществления R1 представляет собой 6-членное гетероарильное кольцо, содержащее 1-3 атомов азота. В других вариантах реализации R1 представляет собой необязательно замещенное 6-членное гетероарильное кольцо, содержащее 1-2 атомов азота. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 6-членное гетероарильное кольцо, содержащее 2 атома азота. В определенных вариантах реализации R1 представляет собой необязательно замещенное 6-членное гетероарильное кольцо, содержащее 1 атом азота. Примеры групп R1 включают необязательно замещенный пиридинил, пиримидинил, пиразинил, пиридазинил, триазинил или тетразинил.
В определенных вариантах реализации R1 представляет собой необязательно замещенное 8-10-членное бициклическое гетероарильное кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. В других вариантах реализации R1 представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R1 представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 1 гетероатом, независимо выбранный из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный индолил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный азабицикло[3.2.1]октанил. В определенных вариантах реализации R1 представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный азаиндолил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный бензимидазолил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный бензотиазолил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный бензоксазолил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный индазолил. В определенных вариантах реализации R1 представляет собой необязательно замещенное 5,6-конденсированное гетероарильное кольцо, содержащее 3 гетероатома, независимо выбранных из азота, кислорода или серы.
В определенных вариантах реализации R1 представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В других вариантах реализации R1 представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 1 гетероатом, независимо выбранный из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный хинолинил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный изохинолинил. Согласно одному из аспектов R1 представляет собой необязательно замещенное 6,6-конденсированное гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой хиназолин или хиноксалин.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный гетероциклил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой замещенное 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой незамещенное 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный гетероциклил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 6-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 6-членное частично ненасыщенное гетероциклическое кольцо, содержащее 2 гетероатома, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 6-членное частично ненасыщенное гетероциклическое кольцо, содержащее 2 атома кислорода.
В определенных вариантах реализации R1 представляет собой 3-7-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R1 представляет собой оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, оксепанил, азиридинил, азетидинил, пирролидинил, пиперидинил, азепанил, тииранил, тиетанил, тетрагидротиофенил, тетрагидротиопиранил, тиепанил, диоксоланил, оксатиоланил, оксазолидинил, имидазолидинил, тиазолидинил, дитиоланил, диоксанил, морфолинил, оксатианил, пиперазинил, тиоморфолинил, дитианил, диоксепанил, оксазепанил, оксатиепанил, дитиепанил, диазепанил, дигидрофуранонил, тетрагидропиранонил, оксепанонил, пирролидинонил, пиперидинонил, азепанонил, дигидротиофенонил, тетрагидротиопиранонил, тиепанонил, оксазолидинонил, оксазинанонил, оксазепанонил, диоксоланонил, диоксанонил, диоксепанонил, оксатиолинонил, оксатианонил, оксатиепанонил, тиазолидинонил, тиазинанонил, тиазепанонил, имидазолидинонил, тетрагидропиримидинонил, диазепанонил, имидазолидиндионил, оксазолидиндионил, тиазолидиндионил, диоксоландионил, оксатиоландионил, пиперазиндионил, морфолиндионил, тиоморфолиндионил, тетрагидропиранил, тетрагидрофуранил, морфолинил, тиоморфолинил, пиперидинил, пиперазинил, пирролидинил, тетрагидротиофенил или тетрагидротиопиранил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 5-членное насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы.
В определенных вариантах реализации R1 представляет собой необязательно замещенное 5-6-членное частично ненасыщенное моноциклическое кольцо, содержащее 1-2 гетероатомов, независимо выбранных из азота, кислорода или серы. В определенных вариантах реализации R1 представляет собой необязательно замещенный тетрагидропиридинил, дигидротиазолил, дигидрооксазолил или оксазолинильную группу.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенное 8-10-членное бициклическое насыщенное или частично ненасыщенное гетероциклическое кольцо, содержащее 1-4 гетероатомов, независимо выбранных из азота, кислорода или серы. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный индолинил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный изоиндолинил. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный 1,2,3,4-тетрагидрохинолин. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный 1,2,3,4-тетрагидроизохинолин.
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную C1-C10 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-C6 алкилен, C1-C6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, причем каждая переменная независимо является такой, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную C1-C10 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -OC(O)- или -C(O)O-, причем каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную C1-С10 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -ОС(О)- или -С(O)O-, причем каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления R1 представляет собой 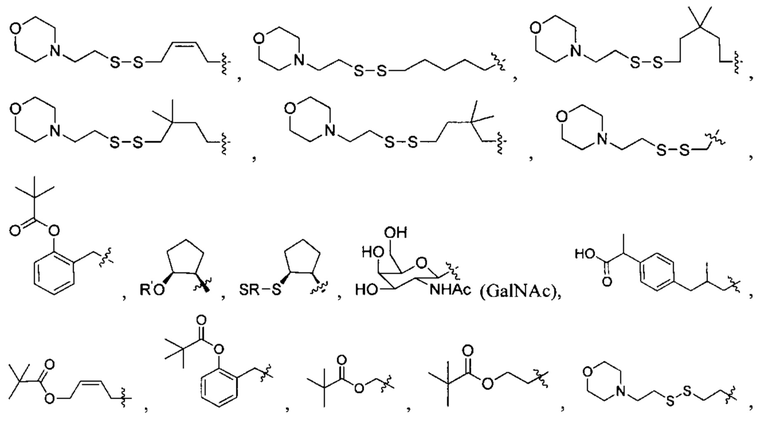
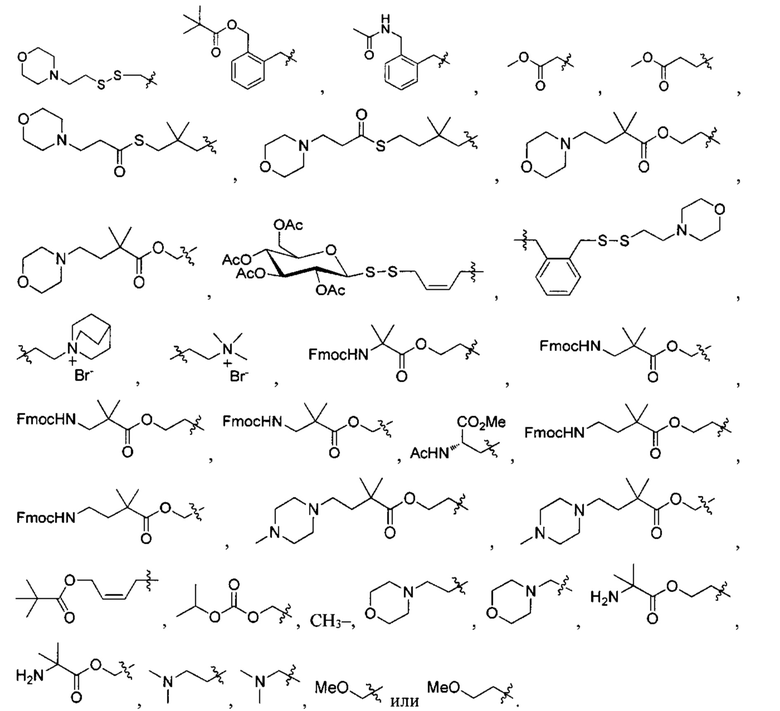
Согласно некоторым вариантам осуществления R1 представляет собой CH3-, 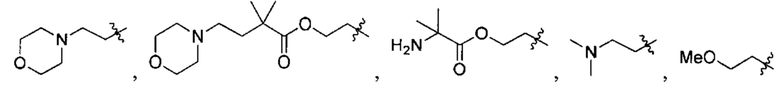 или
или 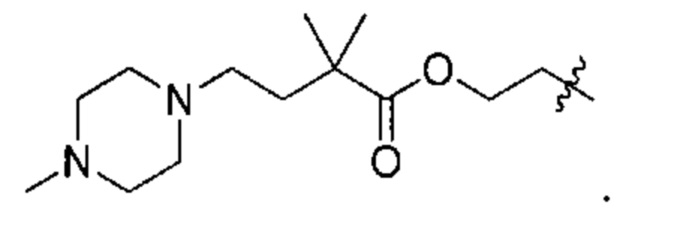
Согласно некоторым вариантам осуществления R1 содержит терминальный необязательно замещенный фрагмент -(СН2)2-, соединенный с L. Примеры таких групп R1 изображены ниже:
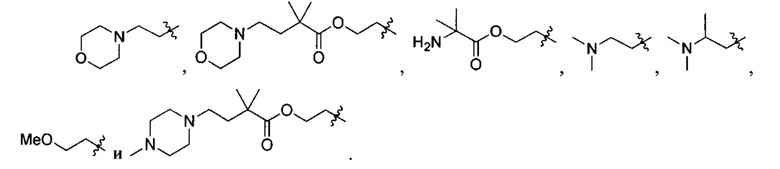
Согласно некоторым вариантам осуществления R1 содержит терминальный необязательно замещенный фрагмент -(CH2)-, соединенный с L. Примеры таких групп R1 изображены ниже:
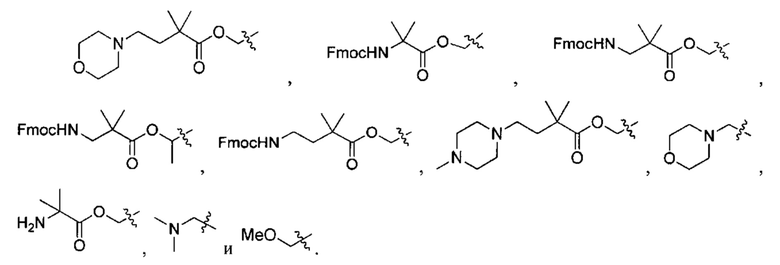
Согласно некоторым вариантам осуществления R1 представляет собой -S-RL2, где RL2 представляет собой необязательно замещенную С1-С9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, а каждый из R' и -Су- независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой -S-RL2, где атом серы соединен с атомом серы в группе L.
Согласно некоторым вариантам осуществления R1 представляет собой -C(O)-RL2, где RL2 представляет собой необязательно замещенную С1-С9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-C6 алкилен, C1-С6 алкенилен, -С≡C-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, а каждый из R' и -Су- независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления R1 представляет собой -C(O)-RL2, где карбонильная группа соединена с G в группе L. Согласно некоторым вариантам осуществления R1 представляет собой -C(O)-RL2, где карбонильная группа соединена с атомом серы в группе L.
Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную С1-С9 алифатическую группу. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенный C1-C9 алкил. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенный C1-C9 алкенил. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенный C1-C9 алкинил. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на -Су- или -С(О)-. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где одном или более метиленовых звеньев возможно и независимо заменены на -Су-. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный гетероциклилен. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный арилен. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный гетероарилен. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный С3-С10 карбоциклилен. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где два метиленовых звена возможно и независимо заменены на -Су- или -С(О)-. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, где два метиленовых звена возможно и независимо заменены на -Су- или -С(О)-. Примеры групп RL2 изображены ниже:
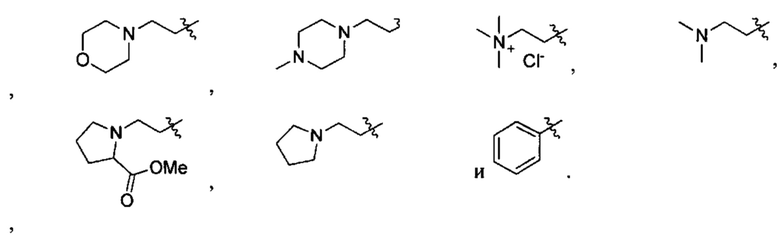
Согласно некоторым вариантам осуществления R1 представляет собой водород или необязательно замещенную группу, выбранную из 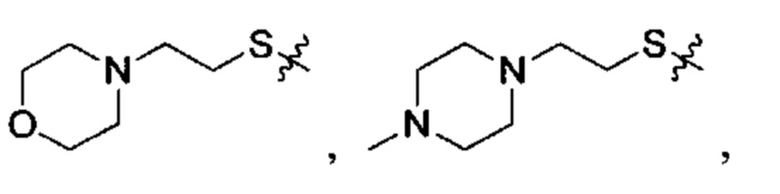
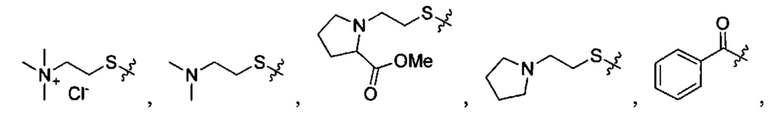 -S-(С1-С10 алифатическая группа), C1-С10 алифатической группы, арила, C1-С6 гетероалкила, гетероарила и гетероциклила. Согласно некоторым вариантам осуществления R1 представляет собой
-S-(С1-С10 алифатическая группа), C1-С10 алифатической группы, арила, C1-С6 гетероалкила, гетероарила и гетероциклила. Согласно некоторым вариантам осуществления R1 представляет собой 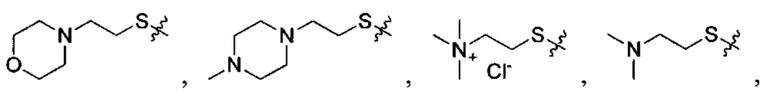
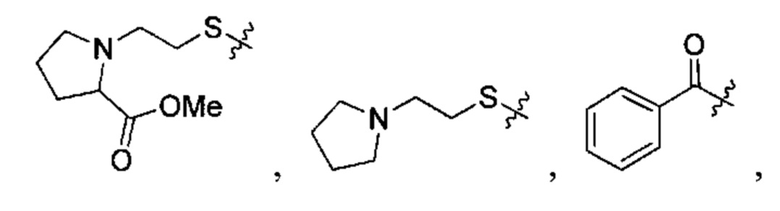 или -S-(C1-C10 алифатическая группа). Согласно некоторым вариантам осуществления R1 представляет собой
или -S-(C1-C10 алифатическая группа). Согласно некоторым вариантам осуществления R1 представляет собой 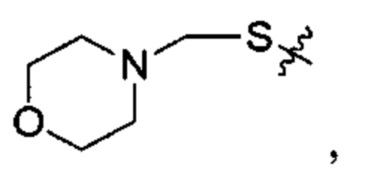
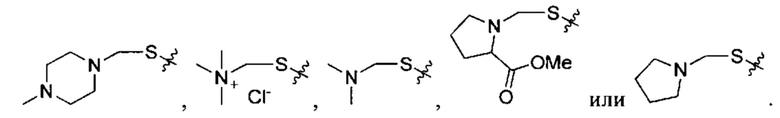
Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенную группу, выбранную из -S-(C1-C6 алифатическая группа), C1-C10 алифатической группы, C1-C6 гетероалифатической группы арила, гетероциклила и гетероарила.
Согласно некоторым вариантам осуществления R1 представляет собой 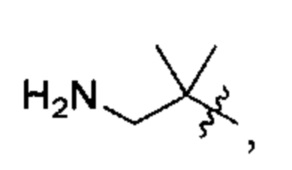
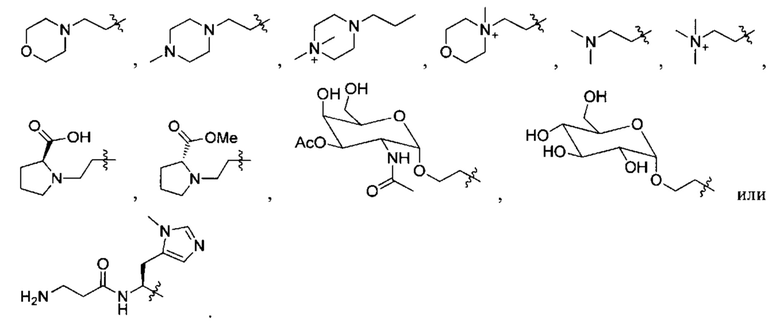
Согласно некоторым вариантам осуществления атом серы в вариантах реализации R1, описанных выше в настоящей заявке, соединен с атомом серы, фрагментом G, Е или -С(О)- в вариантах реализации L, описанных выше в настоящей заявке. Согласно некоторым вариантам осуществления фрагмент -С(О)- в вариантах реализации R1, описанных выше в настоящей заявке, соединен с атомом серы, фрагментом G, Е или -С(О)- в вариантах реализации L, описанных выше в настоящей заявке.
Согласно некоторым вариантам осуществления -L-R1 представляет собой любую комбинацию вариантов реализации L и вариантов реализации R1, определенных выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой –L3-G-R1, где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой -L4-G-R1, где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой -L3-G-S-RL2, где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой -L3-G-C(O)-RL2, где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой 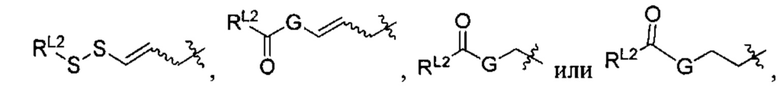 где RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-C6 алкилен, C1-C6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, а каждый G независимо является таким, как определено выше в настоящем описании.
где RL2 представляет собой необязательно замещенную C1-C9 алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-C6 алкилен, C1-C6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-, а каждый G независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой -RL3-S-S-RL2, где каждая переменная независимо является такой, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления -L-R1 представляет собой –RL13-C(O)-S-S-RL2, где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
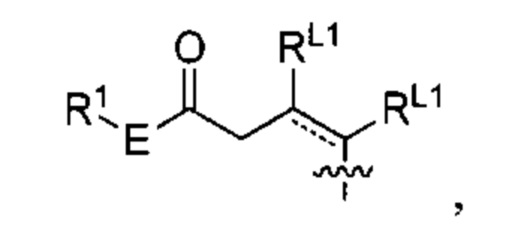
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
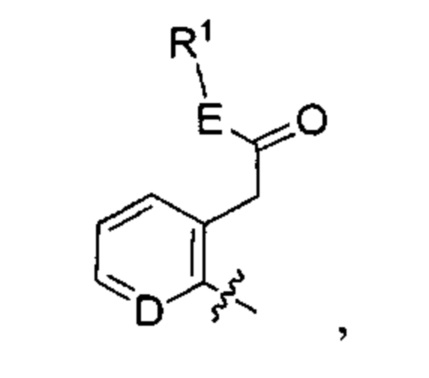
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
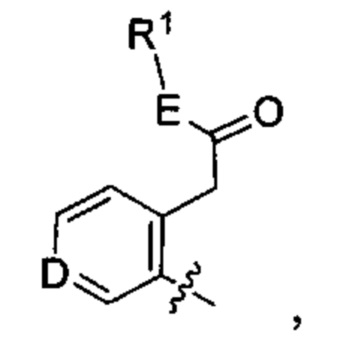
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
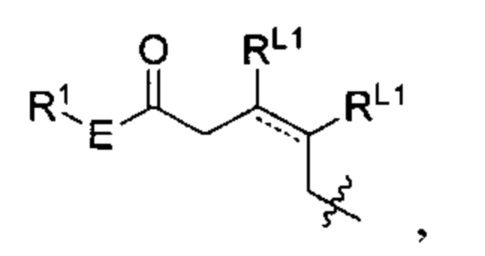
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
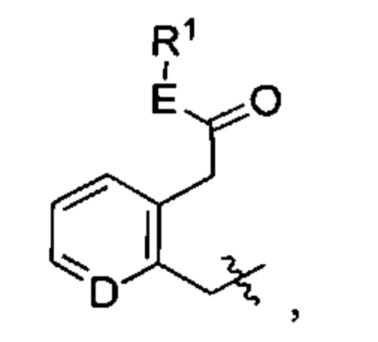
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
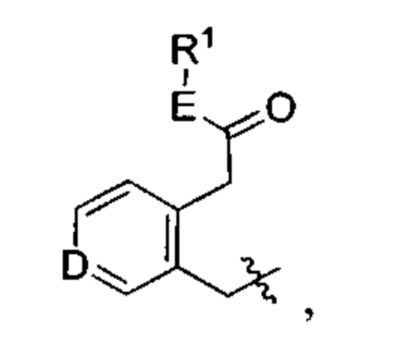
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
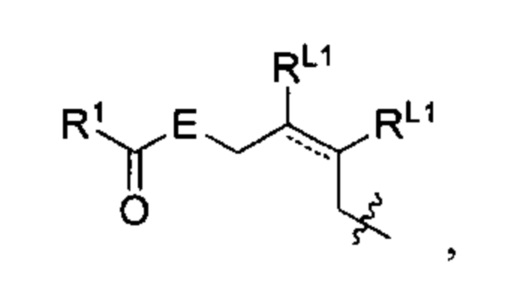
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
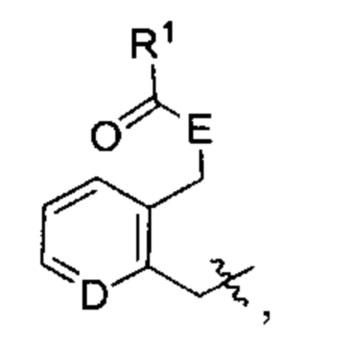
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
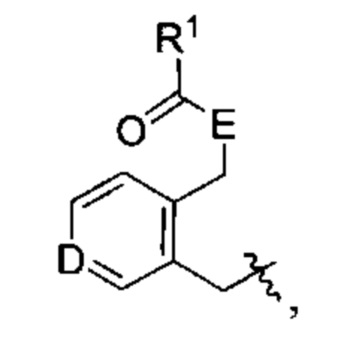
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
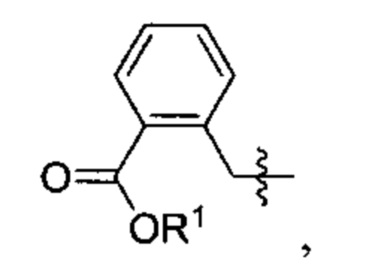
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
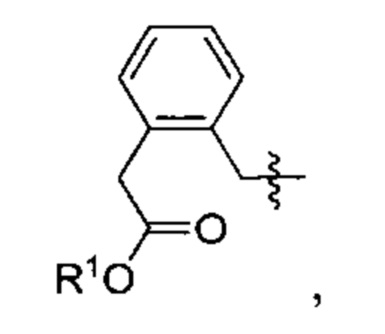
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
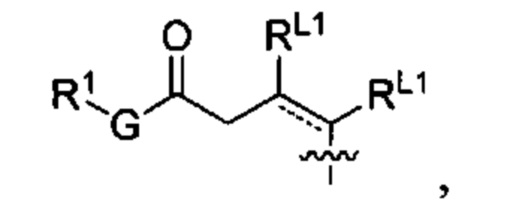
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
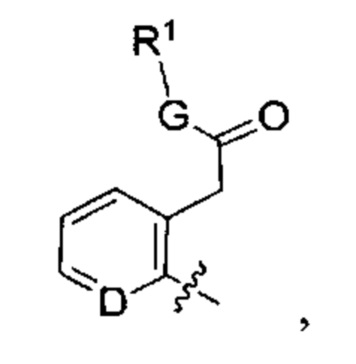
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
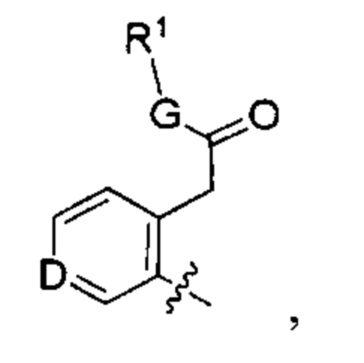
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
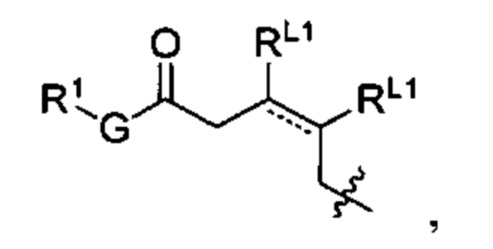
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
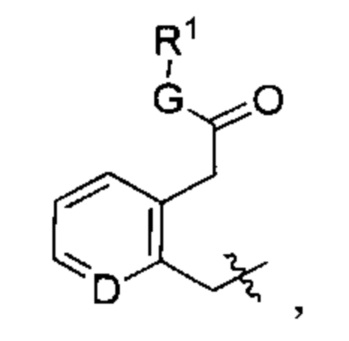
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
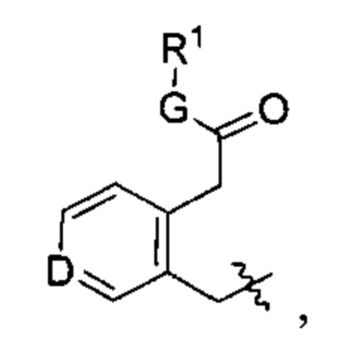
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
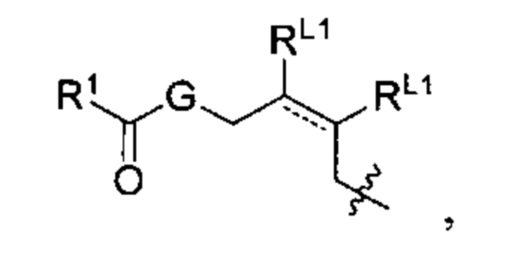
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
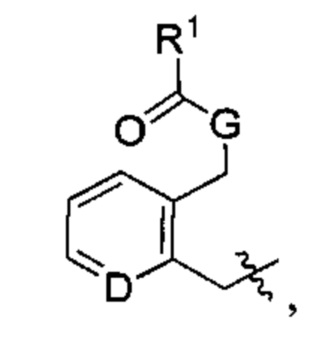
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
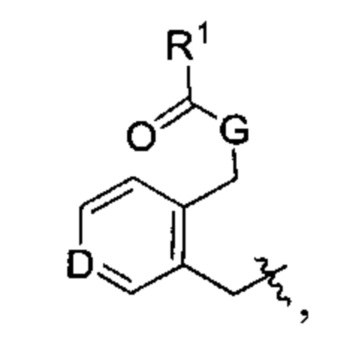
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
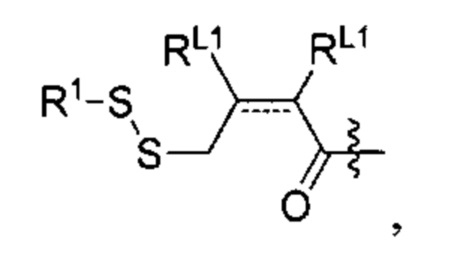
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
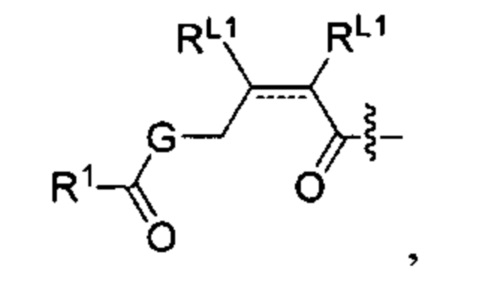
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 имеет структуру:
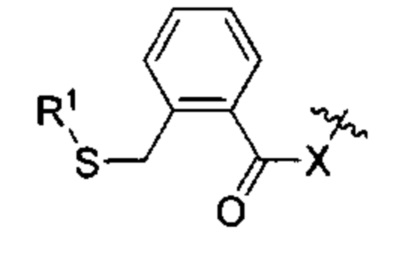
где:
фенильное кольцо является необязательно замещенным, и
каждый из R1 и X независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления -L-R1 представляет собой 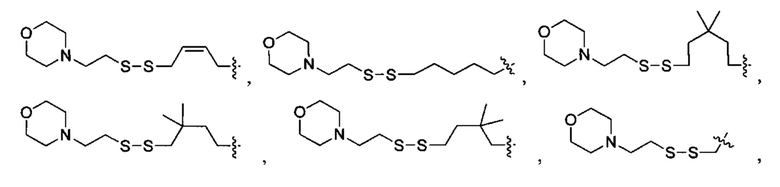
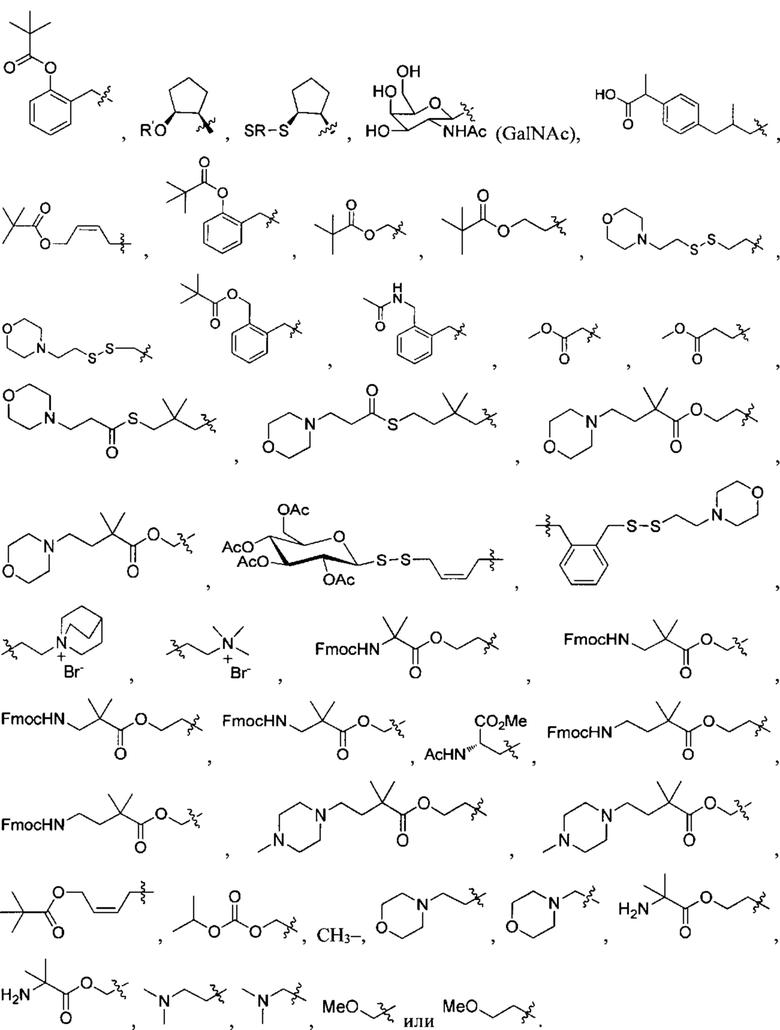
Согласно некоторым вариантам осуществления -L-R1 представляет собой:
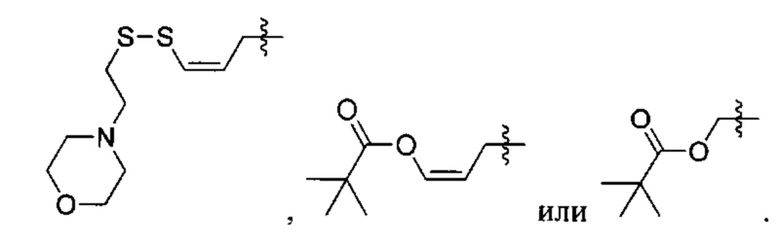
Согласно некоторым вариантам осуществления -L-R1 представляет собой: CH3-, 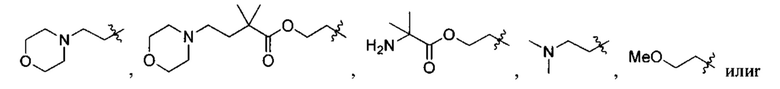
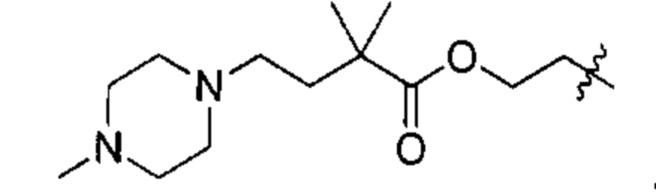 Согласно некоторым вариантам осуществления -L-R1 представляет собой:
Согласно некоторым вариантам осуществления -L-R1 представляет собой: 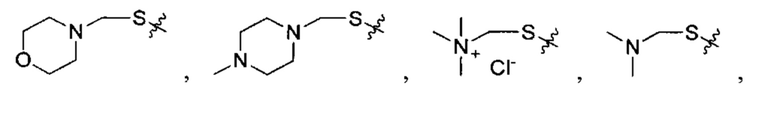
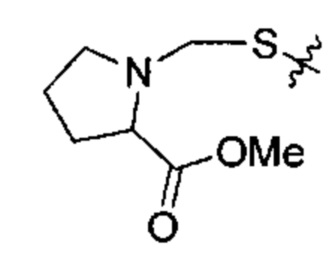 или
или 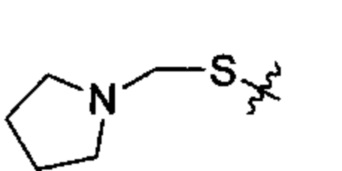 .
.
Согласно некоторым вариантам осуществления -L-R1 содержит терминальный необязательно замещенный фрагмент -(CH2)2-, соединенный с X. Согласно некоторым вариантам осуществления -L-R1 содержит терминальный фрагмент -(CH2)2-, соединенный с X. Примеры таких фрагментов -L-R1 изображены ниже:
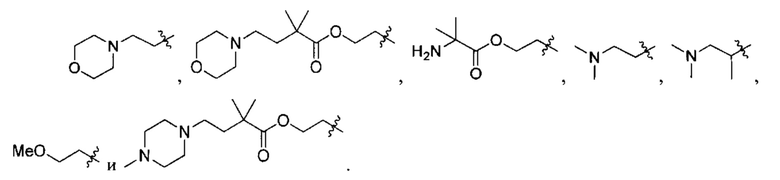
Согласно некоторым вариантам осуществления -L-R1 содержит терминальный необязательно замещенный фрагмент -(CH2)-, соединенный с X. Согласно некоторым вариантам осуществления -L-R1 содержит терминальный фрагмент -(CH2)-, соединенный с X. Примеры таких фрагментов -L-R1 изображены ниже:
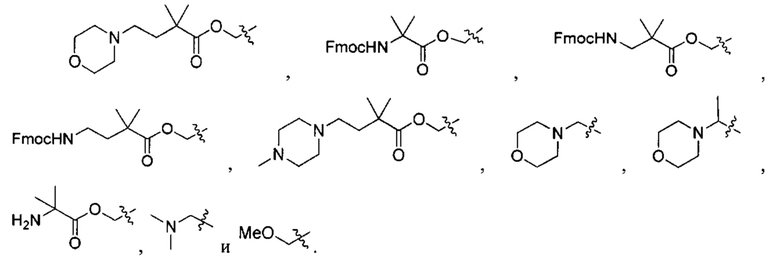
Согласно некоторым вариантам осуществления -L-R1 представляет собой 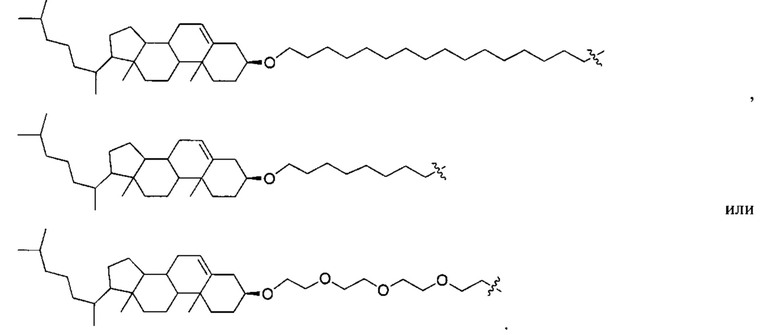
Согласно некоторым вариантам осуществления -L-R1 представляет собой СН3-, 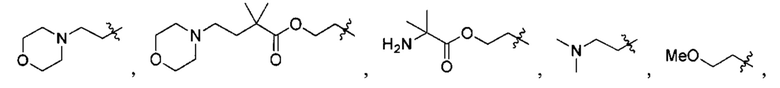
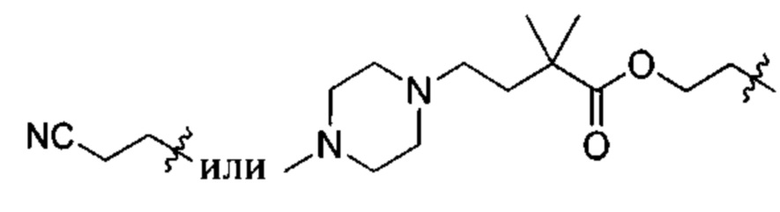 ; а X представляет собой -S-.
; а X представляет собой -S-.
Согласно некоторым вариантам осуществления -L-R1 представляет собой СН3-,
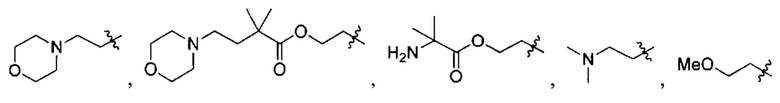 или
или 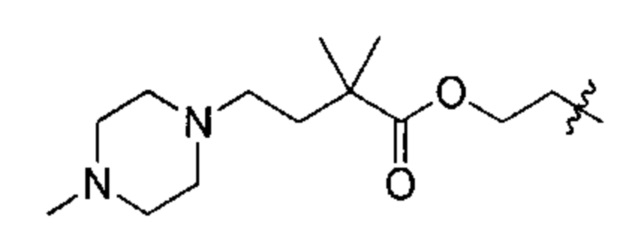 , X представляет собой -S-, W представляет собой О, Y представляет собой -О-, и Z представляет собой -О-.
, X представляет собой -S-, W представляет собой О, Y представляет собой -О-, и Z представляет собой -О-.
Согласно некоторым вариантам осуществления R1 представляет собой 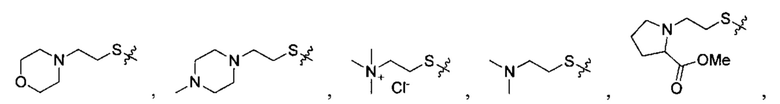
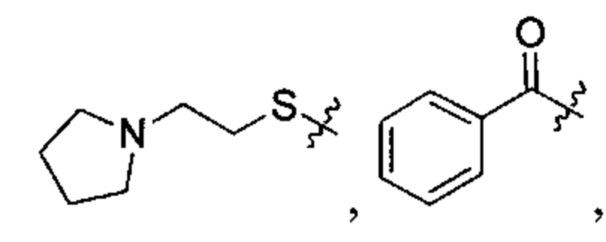 или -S-(C1-C10 алифатическая группа). Согласно некоторым вариантам осуществления R1 представляет собой
или -S-(C1-C10 алифатическая группа). Согласно некоторым вариантам осуществления R1 представляет собой 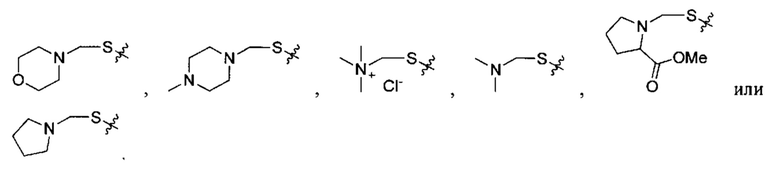
Согласно некоторым вариантам осуществления X представляет собой -О- или -S-, а R1 представляет собой 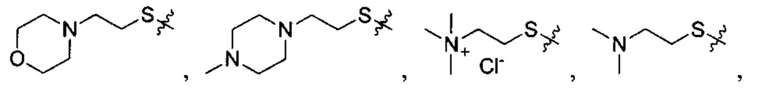
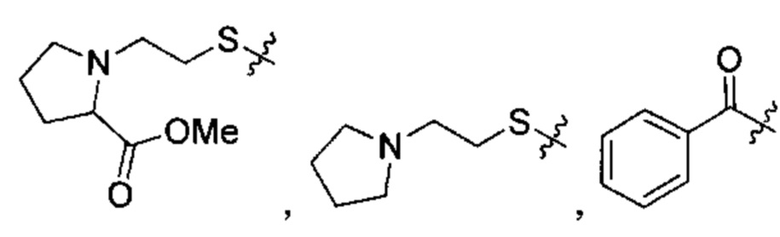 или -S-(C1-C10 алифатическая группа). Согласно некоторым вариантам осуществления X представляет собой -О- или -S-, а R1 представляет собой
или -S-(C1-C10 алифатическая группа). Согласно некоторым вариантам осуществления X представляет собой -О- или -S-, а R1 представляет собой 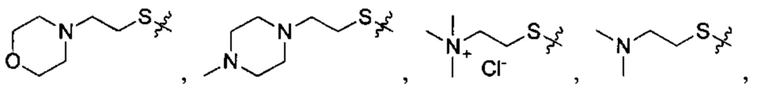
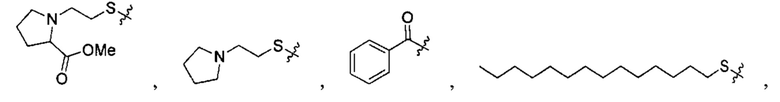
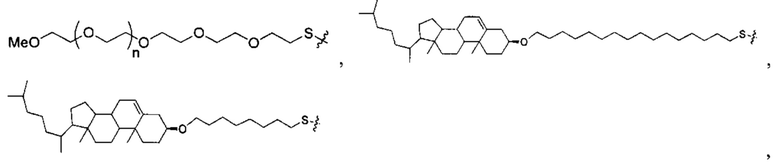
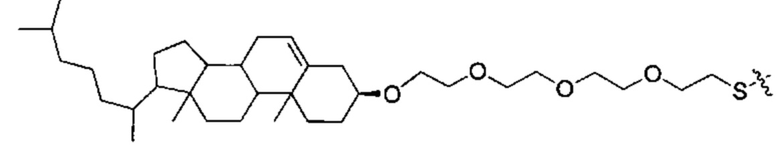 , -S-(C1-C10 алифатическая группа) или -S-(C1-C50 алифатическая группа).
, -S-(C1-C10 алифатическая группа) или -S-(C1-C50 алифатическая группа).
Согласно некоторым вариантам осуществления L представляет собой ковалентную связь, и -L-R1 представляет собой R1.
Согласно некоторым вариантам осуществления -L-R1 не является водородом.
Согласно некоторым вариантам осуществления -X-L-R1 представляет собой R1, который представляет собой 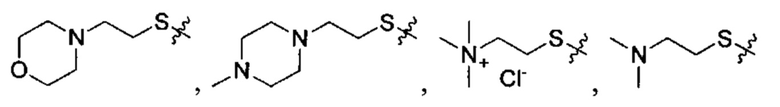
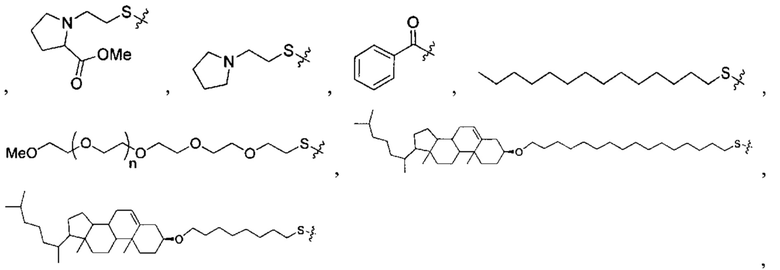
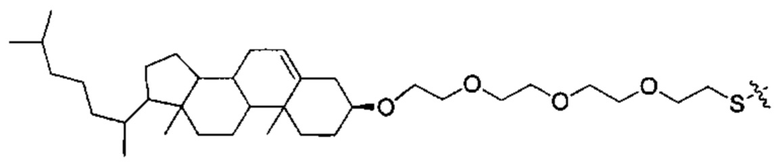 , -S-(C1-C10 алифатическая группа) или -S-(C1-C50 алифатическая группа).
, -S-(C1-C10 алифатическая группа) или -S-(C1-C50 алифатическая группа).
Согласно некоторым вариантам осуществления -X-L-R1 имеет структуру 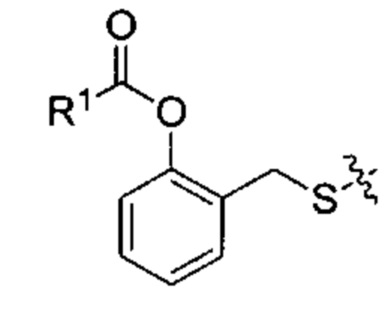 , где фрагмент
, где фрагмент 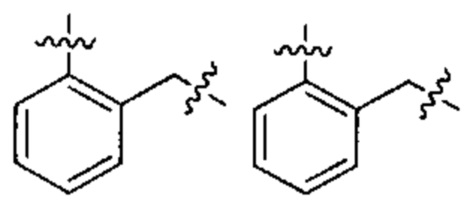 является необязательно замещенным. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
является необязательно замещенным. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 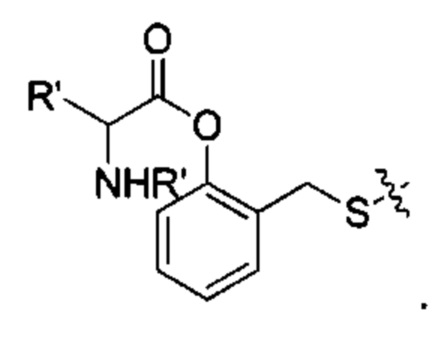 Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 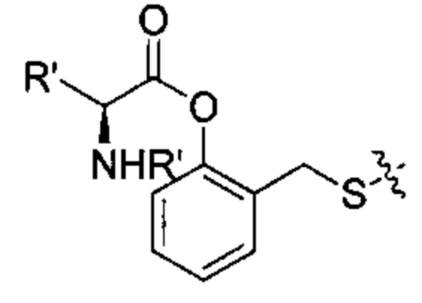 . Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 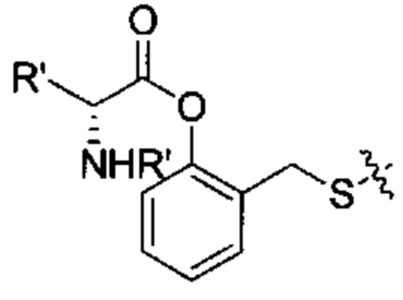 . Согласно некоторым вариантам осуществления -X-L-R1 имеет структуру
. Согласно некоторым вариантам осуществления -X-L-R1 имеет структуру 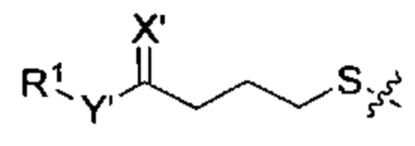 , где X' представляет собой О или S, Y' представляет собой -О-, -S- или -NR'-, а фрагмент
, где X' представляет собой О или S, Y' представляет собой -О-, -S- или -NR'-, а фрагмент 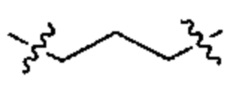 является необязательно замещенным. Согласно некоторым вариантам осуществления Y' представляет собой -О-, -S- или -NH-. Согласно некоторым вариантам осуществления
является необязательно замещенным. Согласно некоторым вариантам осуществления Y' представляет собой -О-, -S- или -NH-. Согласно некоторым вариантам осуществления 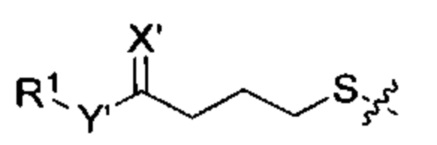 представляет собой
представляет собой 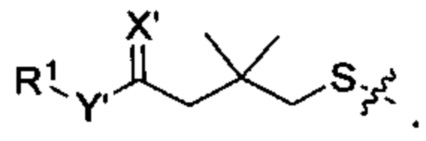 Согласно некоторым вариантам осуществления
Согласно некоторым вариантам осуществления 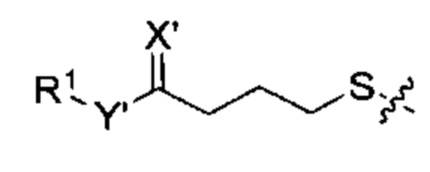 представляет собой
представляет собой 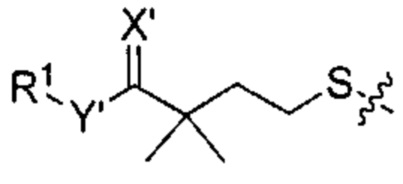 . Согласно некоторым вариантам осуществления
. Согласно некоторым вариантам осуществления 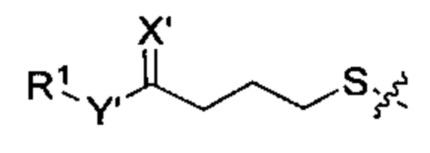 представляет собой
представляет собой 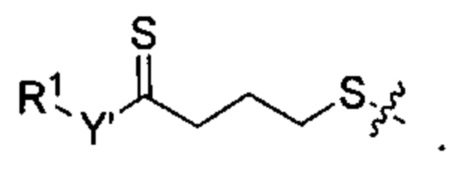 Согласно некоторым вариантам осуществления -X-L-R1 имеет структуру
Согласно некоторым вариантам осуществления -X-L-R1 имеет структуру 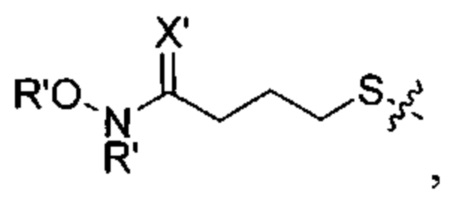 где X' представляет собой О или S, а фрагмент
где X' представляет собой О или S, а фрагмент 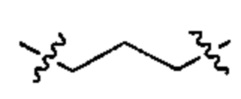 является необязательно замещенным. Согласно некоторым вариантам осуществления
является необязательно замещенным. Согласно некоторым вариантам осуществления 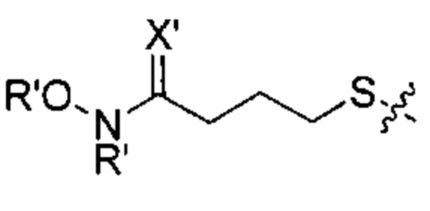 представляет собой
представляет собой 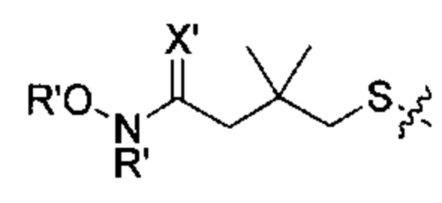 . Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 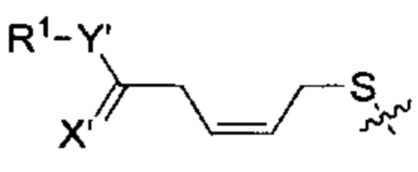 , где
, где 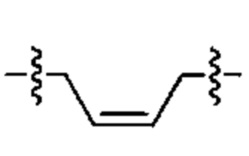 является необязательно замещенным. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
является необязательно замещенным. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 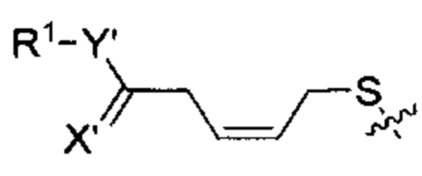 , где
, где 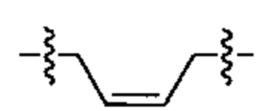 является замещенным. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
является замещенным. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 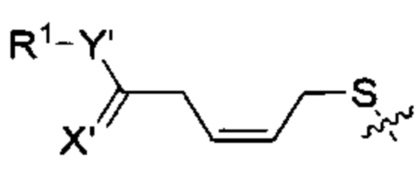 , где
, где  является незамещенным.
является незамещенным.
Согласно некоторым вариантам осуществления -X-L-R1 представляет собой R1-C(O)-S-Lx-S-, где Lx представляет собой необязательно замещенную группу, выбранную из  и
и  . Согласно некоторым вариантам осуществления Lx представляет собой
. Согласно некоторым вариантам осуществления Lx представляет собой  и
и 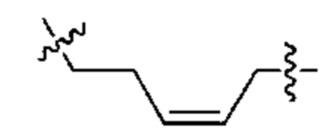 . Согласно некоторым вариантам осуществления -X-L-R1 представляет собой (CH3)3C-S-S-Lx-S-. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой R1-C(=X')-Y'-C(R)2-S-Lx-S-. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой R-C(=X')-Y'-CH2-S-Lx-S-. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой
. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой (CH3)3C-S-S-Lx-S-. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой R1-C(=X')-Y'-C(R)2-S-Lx-S-. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой R-C(=X')-Y'-CH2-S-Lx-S-. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой 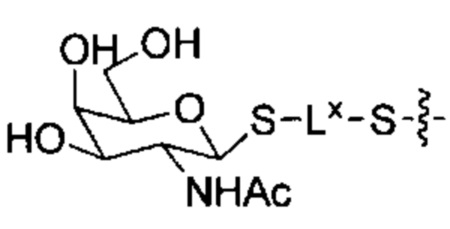 .
.
Специалистам в данной области техники должно быть понятно, что многие группы -X-L-R1, описанные в настоящей заявке, можно отщеплять и превращать в –X- после введения субъекту. Согласно некоторым вариантам осуществления -X-L-R1 является отщепляемой. Согласно некоторым вариантам осуществления -X-L-R1 представляет собой -S-L-R1 и превращается в –S- после введения субъекту. Согласно некоторым вариантам осуществления конверсия промотируется ферментом субъекта. Специалистам в данной области техники должно быть понятно, что способы определения возможного превращения группы -S-L-R1 в –S- после введения хорошо известны и широко применяются в данной области техники, включая те, что используют для исследования метаболизма и фармакокинетики лекарственных агентов.
Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа, имеющая структуру формулы I, представляет собой 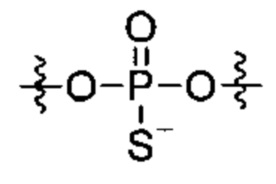 ,
, 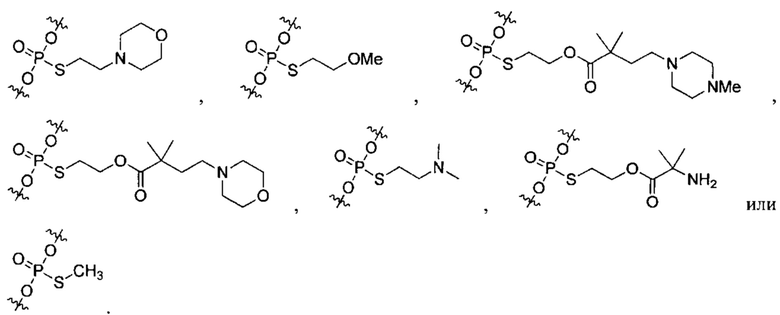
Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа формулы I имеет структуру формулы I-а:
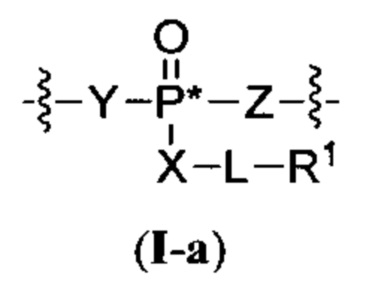
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа формулы I имеет структуру формулы I-b:
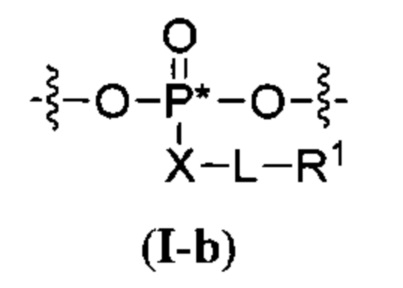
где каждая переменная независимо является такой, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа формулы I представляет собой фосфоротиоатную сложную триэфирную линкерную группу, имеющую структуру формулы I-c:
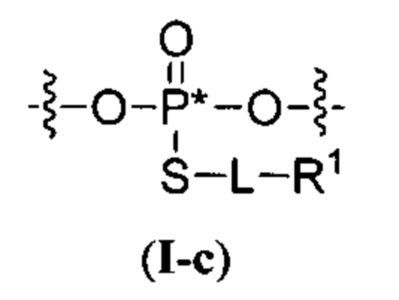
где:
Р* представляет собой асимметрический атом фосфора и имеет Rp- или Sp-конфигурацию;
L представляет собой ковалентную связь или необязательно замещенный линейный или разветвленный C1-С10 алкилен, где одно или более метиленовых звеньев в L возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R'), -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-;
R1 представляет собой галоген, R или необязательно замещенную С1-С50 алифатическую группу, где одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкилен, C1-С6 алкенилен, -С≡С-, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- или -C(O)O-;
каждый R' независимо представляет собой -R, -C(O)R, -CO2R или -SO2R, или:
два R' при одном атоме азота объединены с соседними атомами с образованием необязательно замещенного гетероциклического или гетероарильного кольца, или
два R' при одном атоме углерода объединены с соседними атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца;
-Су- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из фенилена, карбоциклилена, арилена, гетероарилена или гетероциклилена;
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из C1-С6 алифатической группы, фенила, карбоциклила, арила, гетероарила или гетероциклила;
каждый  независимо представляет собой место присоединения к нуклеозиду; и
независимо представляет собой место присоединения к нуклеозиду; и
R1 не является -Н, если L представляет собой ковалентную связь.
Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа, имеющая структуру формулы I, представляет собой 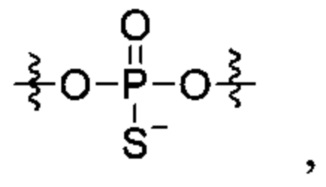
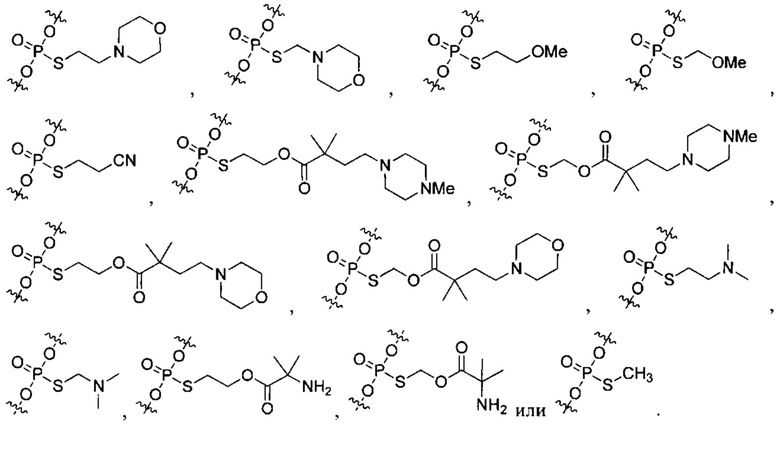
Согласно некоторым вариантам осуществления межнуклеотидная линкерная группа, имеющая структуру формулы I-c, представляет собой 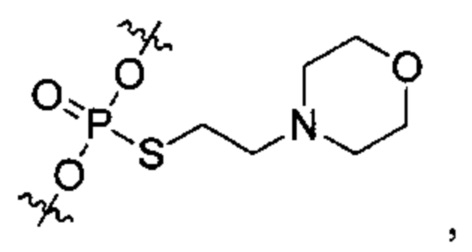
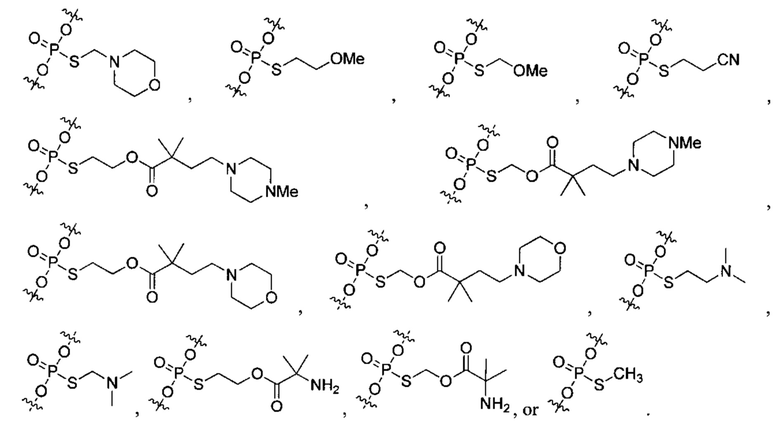
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий одну или более фосфатных сложных диэфирных линкерных групп и одну или более модифицированных межнуклеотидных линкерных групп, имеющих формулу I-a, I-b или I-c.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере одну фосфоротиоатную сложную триэфирную линкерную группу, имеющую структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере две фосфоротиоатные сложные триэфирные линкерные группы, имеющие структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере три фосфоротиоатные сложные триэфирные линкерные группы, имеющие структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере четыре фосфоротиоатные сложные триэфирные линкерные группы, имеющие структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий по меньшей мере одну фосфатную сложную диэфирную межнуклеотидную линкерную группу и по меньшей мере пять фосфоротиоатных сложных триэфирных линкерных групп, имеющих структуру формулы I-c.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, приведенную в GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где указанная последовательность более чем на 50% идентична с GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где указанная последовательность более чем на 60% идентична с GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где указанная последовательность более чем на 70% идентична с GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где указанная последовательность более чем на 80% идентична с GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где указанная последовательность более чем на 90% идентична с GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где указанная последовательность более чем на 95% идентична с GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа содержит хиральный атом фосфора линкерной группы. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 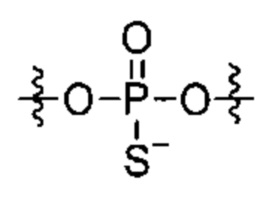 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, присутствующую в GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой 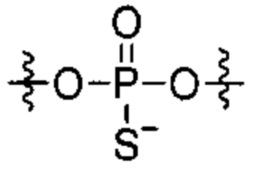 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 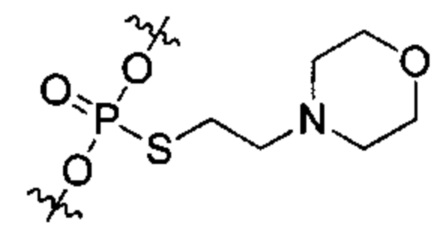 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой 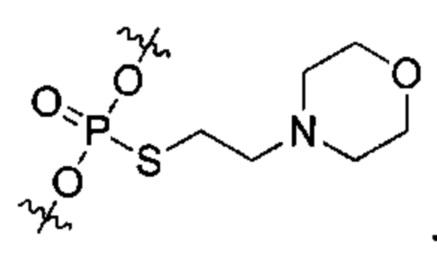
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа содержит хиральный атом фосфора линкерной группы. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 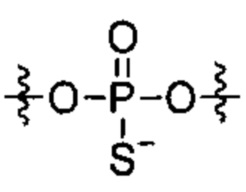 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой 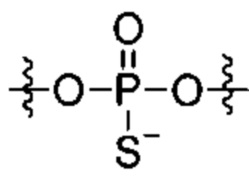 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 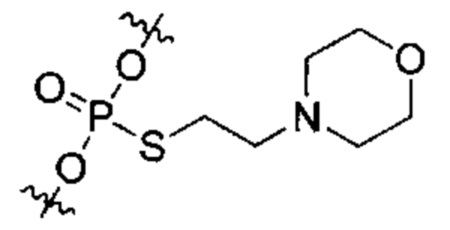 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой 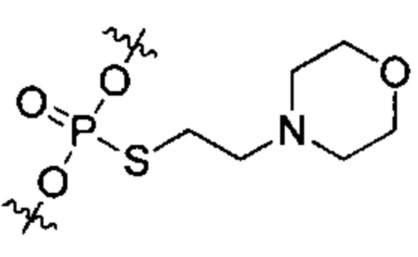 .
.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа содержит хиральный атом фосфора линкерной группы. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 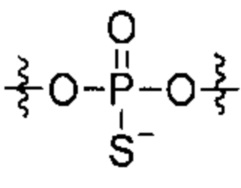 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой 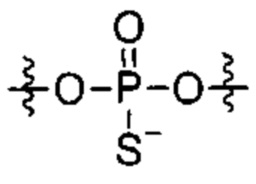 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 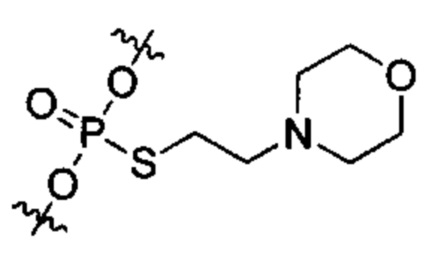 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждая межнуклеотидная линкерная группа представляет собой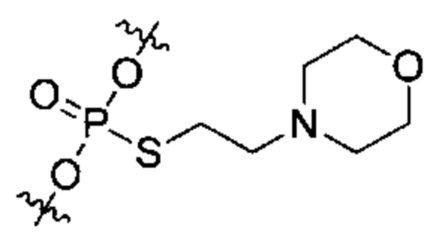 .
.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере один атом фосфора линкерной группы имеет Rp-конфигурацию. Специалистам в данной области техники должно быть понятно, что в определенных вариантах реализации, где олигонуклеотид с контролируемой хиральностью содержит последовательность РНК, каждый Т независимо и возможно заменен на U. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждый атом фосфора линкерной группы имеет Rp-конфигурацию. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере один атом фосфора линкерной группы имеет Sp-конфигурацию. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждый атом фосфора линкерной группы имеет Sp-конфигурацию Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой блокмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой стереоблокмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой блокмер с модификацией Р. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой блокмер с одинаковыми линкерными группами. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой альтмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой стереоальтмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой альтмер с модификацией Р. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой альтмер с различными чередующимися линкерными группами. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой унимер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой стереоунимер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой унимер с модификацией Р. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой унимер с одинаковыми линкерными группами. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой гэпмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где олигонуклеотид представляет собой скипмер.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждый цитозин возможно и независимо заменен на 5-метилцитозин. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где по меньшей мере один цитозин возможно и независимо заменен на 5-метилцитозин. Согласно некоторым вариантам осуществления в настоящем изобретении предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность GGCACAAGGGCACAGACTTC, где каждый цитозин возможно и независимо заменен 5-метилцитозином.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью подобран таким образом, что один или более нуклеотидов содержит модификацию фосфора, подверженную «самовысвобождению» при определенных условиях. То есть, конкретная модификация фосфора выполнена таким образом, что в определенных условиях происходит ее самоотщепление от олигонуклеотида с обеспечением, например, фосфатного сложного диэфира, такого как присутствует в природной ДНК или РНК. Согласно некоторым вариантам осуществления указанная модификация фосфора имеет структуру -О-L-R1, где каждый из L и R1 независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления самовысвобождаемая группа содержит морфолиногруппу. Согласно некоторым вариантам осуществления самовысвобождаемая группа характеризуется способностью доставлять агент к межнуклеотидной фосфорсодержащей линкерной группе, где агент способствует дополнительной модификации атома фосфора, такой как, например, десульфуризация. Согласно некоторым вариантам осуществления агент представляет собой воду, а дополнительная модификация представляет собой гидролиз с образованием фосфатного сложного диэфира, такого как содержится в природной ДНК или РНК.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую описанную в настоящем документе последовательность (включающую в качестве неограничивающих примеров любую последовательность, раскрытую в любой таблице). Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, которая более чем на 50% идентична любой описанной в настоящем документе последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, которая более чем на 60% идентична любой описанной в настоящем документе последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, которая более чем на 70% идентична любой описанной в настоящем документе последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, которая более чем на 80% идентична любой описанной в настоящем документе последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, которая более чем на 90% идентична любой описанной в настоящем документе последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий последовательность, которая более чем на 95% идентична любой описанной в настоящем документе последовательности. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую описанную в настоящем документе последовательность. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую описанную в настоящем документе последовательность.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа содержит хиральный атом фосфора линкер ной группы. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 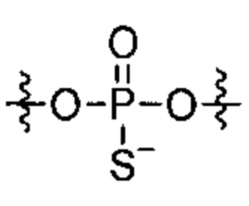 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой 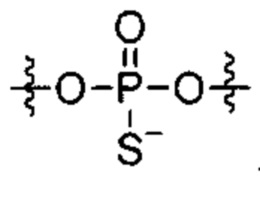 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 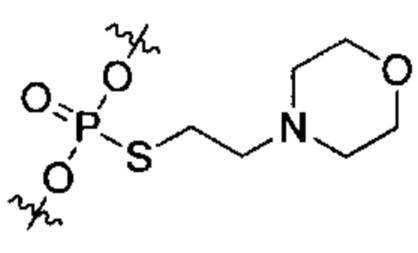 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой 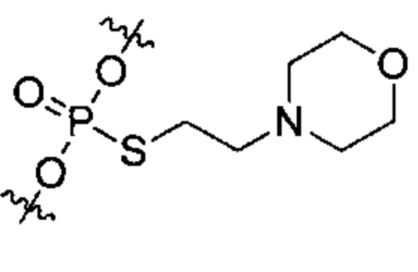 .
.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа содержит хиральный атом фосфора линкерной группы. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 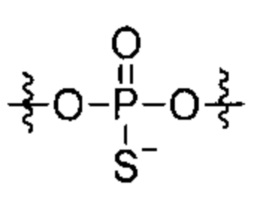 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой 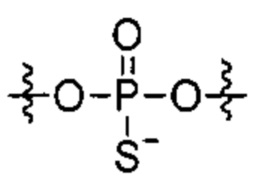 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 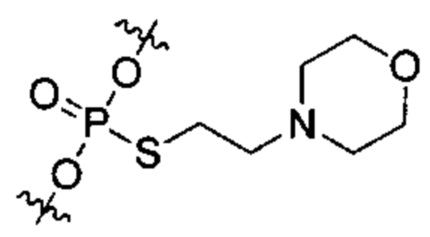 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, содержащий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой 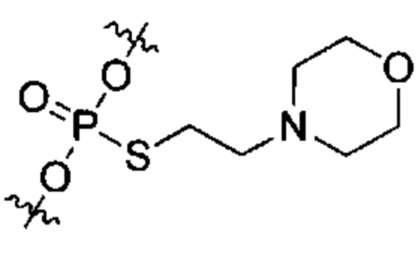 .
.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа содержит хиральный атом фосфора линкерной группы. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа имеет структуру формулы I. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа имеет структуру формулы I-c. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 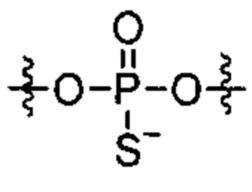 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой 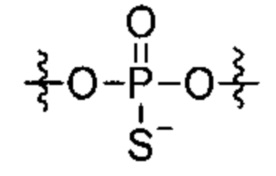 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере одна межнуклеотидная линкерная группа представляет собой 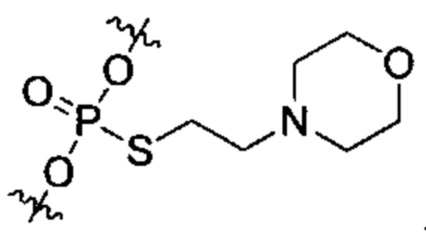 . Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой
. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждая межнуклеотидная линкерная группа представляет собой 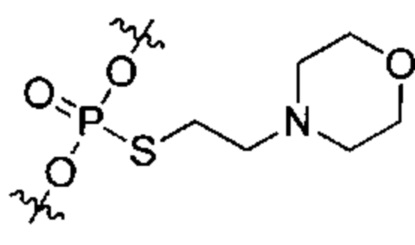 .
.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере один атом фосфора линкерной группы имеет Rp-конфигурацию. Специалистам в данной области техники должно быть понятно, что в определенных вариантах реализации, где олигонуклеотид с контролируемой хиральностью содержит последовательность РНК, каждый Т независимо и возможно заменен на U. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждый атом фосфора линкерной группы имеет Rp-конфигурацию. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере один атом фосфора линкерной группы имеет Sp-конфигурацию. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждый атом фосфора линкерной группы имеет Sp-конфигурацию Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой блокмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой стереоблокмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой блокмер с модификацией Р. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой блокмер с одинаковыми линкерными группами. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой альтмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой стереоальтмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой альтмер с модификацией Р. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой альтмер с различными чередующимися линкерными группами. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой унимер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой стереоунимер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой унимер с модификацией Р. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой унимер с одинаковыми линкерными группами. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой гэпмер. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где олигонуклеотид представляет собой скипмер.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждый цитозин возможно и независимо заменен на 5-метилцитозин. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где по меньшей мере один цитозин возможно и независимо заменен на 5-метилцитозин. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий любую раскрытую в настоящем документе последовательность, где каждый цитозин возможно и независимо заменен на 5-метилцитозин.
В различных вариантах реализации любая раскрытая в настоящем документе последовательность может быть объединена с одним или более из следующего, как описано в настоящем документе или известно в данной области техники: профиль линкерных групп остова; профиль хиральных центров остова и профиль модификаций Р остова; профиль модификации оснований; профиль модификации сахара; профиль линкерных групп остова; профиль хиральных центров остова и профиль модификаций Р остова.
Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью подобран таким образом, что конечные фармацевтические свойства улучшены за счет одной или более конкретных модификаций атома фосфора. В данной области техники существуют убедительные доказательства того, что определенные олигонуклеотиды быстро разлагаются под действием нуклеаз и слабо подвержены клеточному захвату через цитоплазматическую мембрану клетки [Poijarvi-Virta et al, Curr. Med. Chem. (2006), 13(28); 3441-65; Wagner et al, Med. Res. Rev. (2000), 20(6):417-51; Peyrottes et al, Mini Rev. Med. Chem. (2004), 4(4):395-408; Gosselin et al, (1996), 43(1):196-208; Bologna et al., (2002), Antisense & Nucleic Acid Drug Development 12:33-41]. Например, в Vives et al, Nucleic Acids Research (1999), 27(20):4071-76 обнаружили, что трет-бутил-SATE-проолигонуклеотиды имели значительно увеличенную клеточную проницаемость по сравнению с исходным олигонуклеотидом.
Согласно некоторым вариантам осуществления модификация атома фосфора линкерной группы характеризуется способностью превращаться в фосфатный сложный диэфир, такой как содержится в природных ДНК или РНК, под действием одного или более ферментов, выбранных из эстераз, нуклеаз и/или цитохрома Р450, включая, но не ограничиваясь ими, те, что приведены ниже в таблице 1А.

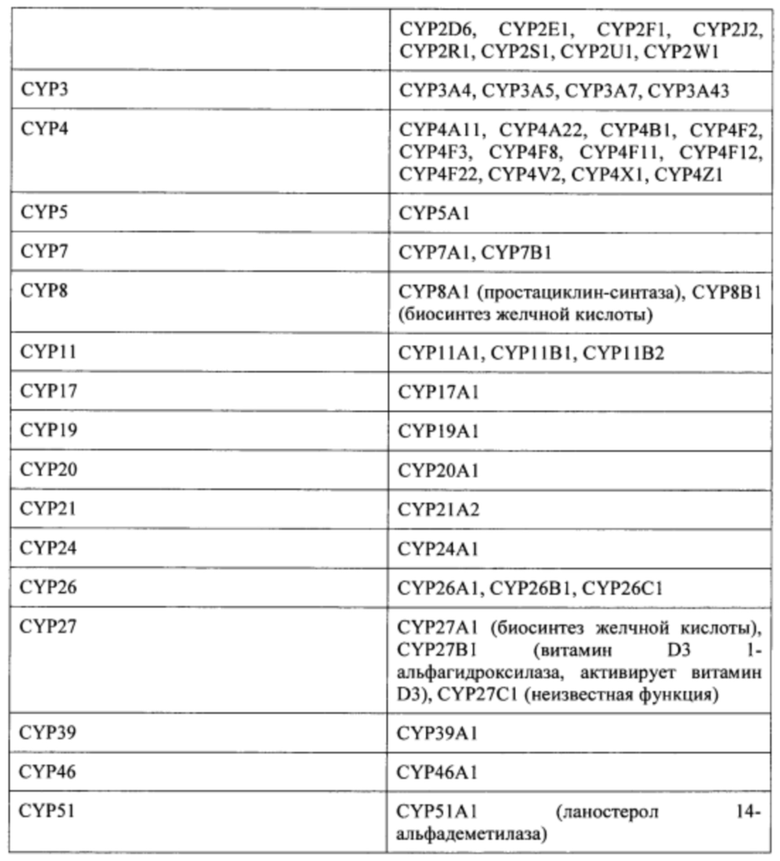
Согласно некоторым вариантам осуществления модификация атома фосфора приводит к тому, что фрагмент с модификацией Р характеризуется тем, что он выступает в качестве пролекарства, например, фрагмент с модификацией Р до своего удаления способствует доставке олигонуклеотида к желаемому участку. Например, согласно некоторым вариантам осуществления фрагмент с модификацией Р образуется в результате пегилирования атома фосфора линкерной группы. Специалистам в данной области техники должно быть понятно, что подходят ПЭГ с различной длиной цепи, и выбор длины цепи отчасти обусловлен результатом, который предположительно должно обеспечивать пегилирование. Например, согласно некоторым вариантам осуществления пегилирование проводят для уменьшения захвата RES и увеличения продолжительности циркуляции олигонуклеотида in vivo.
Согласно некоторым вариантам осуществления пегилирующий агент для применения согласно настоящему раскрытию имеет молекулярную массу от примерно 300 г/моль до примерно 100000 г/моль. Согласно некоторым вариантам осуществления пегилирующий агент имеет молекулярную массу от примерно 300 г/моль до примерно 10000 г/моль. Согласно некоторым вариантам осуществления пегилирующий агент имеет молекулярную массу от примерно 300 г/моль до примерно 5000 г/моль. Согласно некоторым вариантам осуществления пегилирующий агент имеет молекулярную массу примерно 500 г/моль. Согласно некоторым вариантам осуществления пегилирующий агент имеет молекулярную массу примерно 1000 г/моль. Согласно некоторым вариантам осуществления пегилирующий агент имеет молекулярную массу примерно 3000 г/моль. Согласно некоторым вариантам осуществления пегилирующий агент имеет молекулярную массу примерно 5000 г/моль.
Согласно некоторым вариантам осуществления пегилирующий агент представляет собой ПЭГ500. В определенных вариантах реализации пегилирующий агент представляет собой ПЭГ1000. В определенных вариантах реализации пегилирующий агент представляет собой ПЭГ3000. В определенных вариантах реализации пегилирующий агент представляет собой ПЭГ5000.
Согласно некоторым вариантам осуществления фрагмент с модификацией Р характеризуется тем, что он выступает в качестве усилителя ФК (фармакокинетики), например, липидов, пегилированных липидов и т.д.
Согласно некоторым вариантам осуществления фрагмент с модификацией Р характеризуется тем, что он выступает в качестве агента, промотирующего поступление в клетки и/или уклонение от эндосомы, такого как мембраноразрушающий липид или пептид.
Согласно некоторым вариантам осуществления фрагмент с модификацией Р характеризуется тем, что он действует в качестве агента направленного действия. Согласно некоторым вариантам осуществления фрагмент с модификацией Р представляет собой или содержит агент направленного действия. Фраза «агент направленного действия», используемая в настоящем описании, представляет собой группу, которая связывается с указанным полезным агентом (например, с олигонуклеотидом или композицией олигонуклеотидов), а также взаимодействует с указанной мишенью, в результате чего указанный полезный агент, ассоциированный с агентом направленного действия, при прочих сравнимых условиях доставляется к указанной мишени в существенно более высокой степени по сравнению тем случаем, когда указанный полезный агент не ассоциирован с агентом направленного действия. Агент направленного действия может представлять собой или содержать любой из различных химических фрагментов, включая, например, фрагменты небольших молекул, нуклеиновые кислоты, полипептиды, углеводы и т.д. Агенты направленного действия дополнительно описаны в Adarsh et al., "Organelle Specific Targeted Drug Delivery - A Review," International Journal of Research in Pharmaceutical and Biomedical Sciences, 2011, p. 895.
Примеры таких агентов направленного действия включают, но не ограничиваются ими, белки (например, трансферрин), олигопептиды (например, циклические и ациклические RGD-содержащие олигопептиды), антитела (моноклональные и поликлональные антитела, например, антитела IgG, IgA, IgM, IgD, IgE), сахара/углеводы (например, моносахариды и/или олигосахариды (маннозу, манноза-6-фосфат, галактозу и т.д.)), витамины (например, фолат) или другие небольшие биомолекулы. Согласно некоторым вариантам осуществления фрагмент направленного действия представляет собой молекулу стероида (например, желчных кислот, включая холевую кислоту, дезоксихолевую кислоту, дегидрохолевую кислоту; кортизон; дигоксигенин; тестостерон; холестерин; катионные стероиды, такие как кортизон, содержащий триметиламинометилгидразидную группу, присоединенную посредством двойной связи к положению 3 кольца кортизона и т.д.). Согласно некоторым вариантам осуществления фрагмент направленного действия представляет собой липофильную молекулу (например, алициклические углеводороды, насыщенные и ненасыщенные жирные кислоты, воски, терпены и полиалициклические углеводороды, такие как адамантин и бакминстерфуллерены). Согласно некоторым вариантам осуществления липофильная молекула представляет собой терпеноид, такой как витамин А, ретиноевую кислоту, ретиналь или дегидроретиналь. Согласно некоторым вариантам осуществления фрагмент направленного действия представляет собой пептид.
Согласно некоторым вариантам осуществления фрагмент с модификацией Р представляет собой агент направленного действия формулы -X-L-R1, где каждый из X, L и R1 является таким, как определено выше для формулы I.
Согласно некоторым вариантам осуществления фрагмент с модификацией Р характеризуется тем, что он способствует специфической доставке в клетки.
Согласно некоторым вариантам осуществления фрагмент с модификацией Р характеризуется тем, что он попадает в одну или более описанных выше категорий. Например, согласно некоторым вариантам осуществления фрагмент с модификацией Р выступает в качестве усилителя ФК и лиганда направленного действия. Согласно некоторым вариантам осуществления фрагмент с модификацией Р выступает в качестве пролекарства и агента уклонения от эндосомы. Специалистам в данной области техники должно быть понятно, что возможны различные другие указанные комбинации, и они охвачены настоящим раскрытием.
Нуклеиновые основания
Согласно некоторым вариантам осуществления нуклеиновое основание, содержащееся в предложенном олигонуклеотиде, представляет собой природное нуклеиновое основание или модифицированное нуклеиновое основание, полученное из природного нуклеинового основания. Примеры включают, но не ограничиваются ими, урацил, тимин, аденин, цитозин и гуанин, где соответствующие аминогруппы защищены ацилзащитными группами, 2-фторурацил, 2-фторцитозин, 5-бромурацил, 5-йодурацил, 2,6-диаминопурин, азацитозин, аналоги пиримидина, такие как псевдоизоцитозин и псевдоурацил, и другие модифицированные нуклеиновые основания, такие как 8-замещенные пурины, ксантин или гипоксантин (два последние являются природными продуктами разложения). Примеры модифицированных нуклеиновых оснований предложены в Chiu and Rana, RNA, 2003, 9, 1034-1048, Limbach et al. Nucleic Acids Research, 1994, 22, 2183-2196, и Revankar and Rao, Comprehensive Natural Products Chemistry, vol. 7, 313.
Соединения, приведенные на следующих общих формулах, также рассматривают как модифицированные нуклеиновые основания:
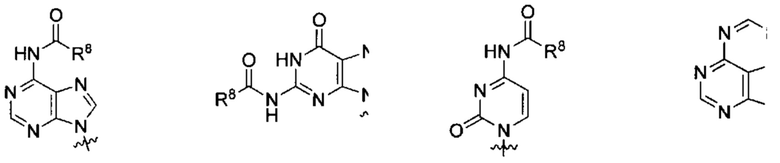
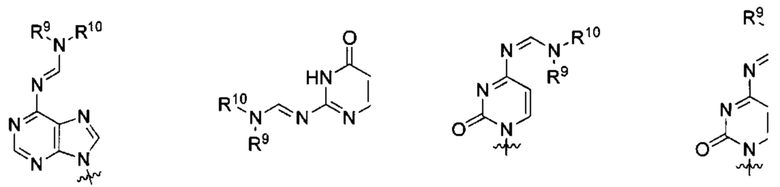
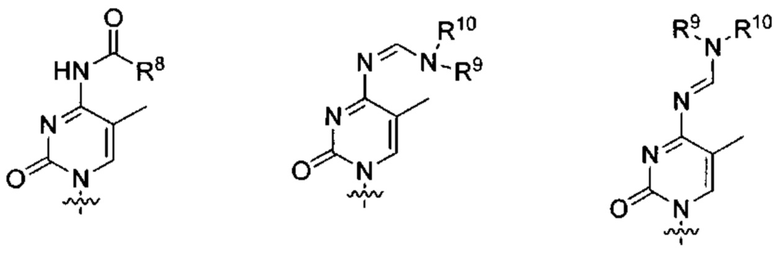
где R8 представляет собой необязательно замещенную линейную или разветвленную группу, выбранную из алифатической группы, арила, аралкила, арилоксиалкила, карбоциклила, гетероциклила или гетероарильной группы, содержащую от 1 до 15 атомов углерода, включая исключительно в качестве примеров метил, изопропил, фенил, бензил или феноксиметильную группу; а каждый из R9 и R10 независимо представляет собой необязательно замещенную группу, выбранную из линейной или разветвленной алифатической группы, карбоциклила, арила, гетероциклила и гетероарила.
Модифицированные нуклеиновые основания также включают увеличенные нуклеиновые основания, в которых добавлены одно или более арильных колец, таких как фенильные кольца. Замены нуклеиновых оснований, описанные в каталоге Glen Research (www.glenresearch.com); Krueger AT et al, Acc. Chem. Res., 2007, 40, 141-150; Kool, ET, Acc. Chem. Res., 2002, 35, 936-943; Benner S.A., et al., Nat. Rev. Genet, 2005, 6, 553-543; Romesberg, F.E., et al., Curr. Opin. Chem. Biol., 2003, 7, 723-733; Hirao, I., Curr. Opin. Chem. Biol., 2006, 10, 622-627, рассматривают как подходящие для синтеза нуклеиновых кислот, описанных в настоящей заявке. Некоторые примеры указанных увеличенных нуклеиновых оснований показаны ниже:
В настоящем описании модифицированные нуклеиновые основания также охватывают структуры, которые не являются общепринятыми нуклеиновыми основаниями, но представляют собой другие фрагменты, включая, но не ограничиваясь ими, кольцевые производные коррина или порфирина. Заменители оснований, представляющие собой производные порфирина, описаны в Morales-Rojas, Н and Kool, ET, Org. Lett., 2002, 4, 4377-4380. Ниже показан пример кольцевого производного порфирина, которое можно использовать в качестве заменителя основания:
Согласно некоторым вариантам осуществления модифицированные нуклеиновые основания имеют любую из следующих необязательно замещенных структур:
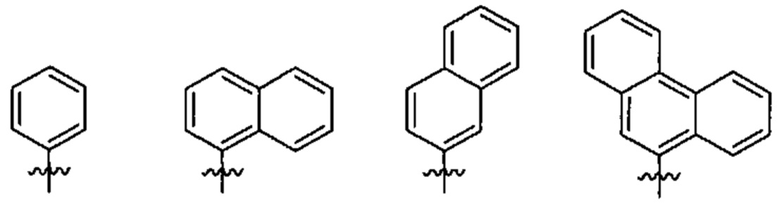
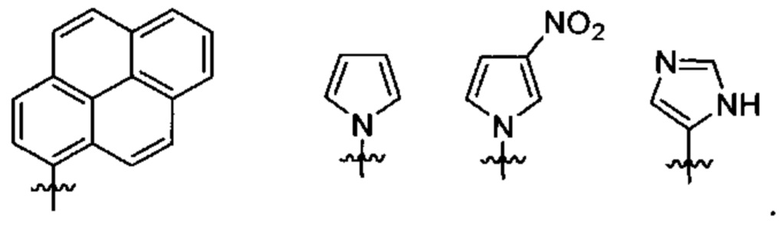
Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание является флуоресцентным. Примеры таких флуоресцентных модифицированных нуклеиновых оснований включают фенантрен, пирен, стильбен, изоксантин, изозантоптерин, терфенил, тертиофен, бензотертиофен, кумарин, лумазин, связанный стильбен, бензоурацил и нафтоурацил, как показано ниже:
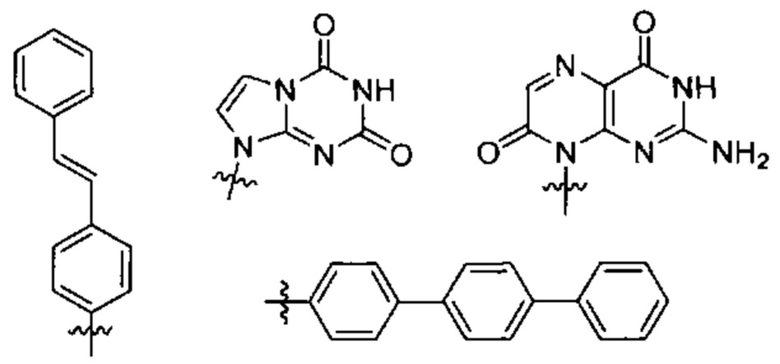
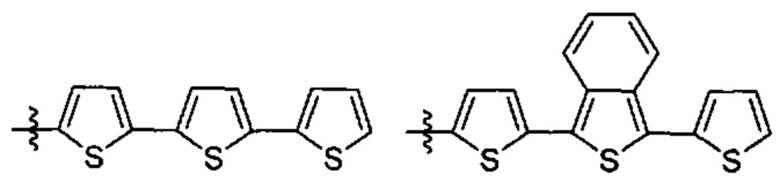
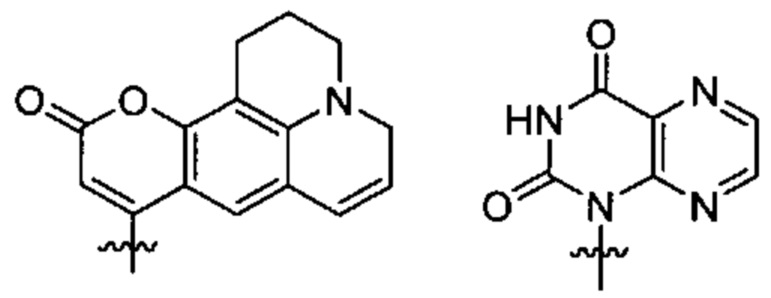
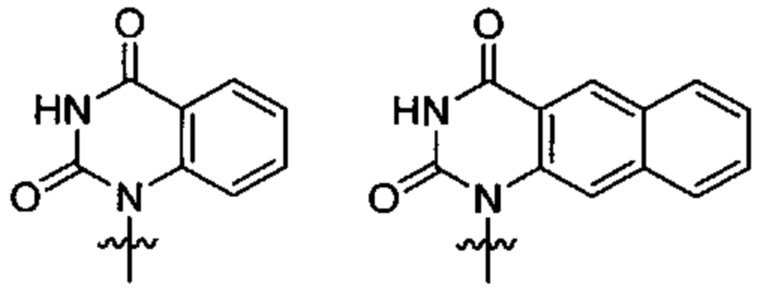
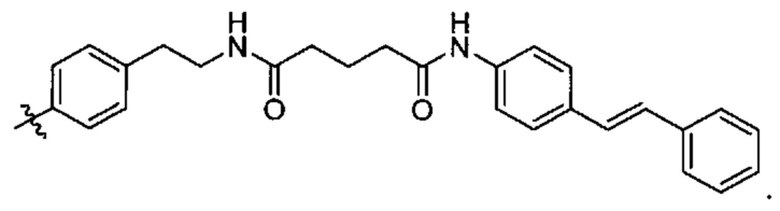
Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание является незамещенным. Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание является замещенным. Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание является замещенным, то есть оно содержит, например, гетероатомы, алкильные группы или линкерные фрагменты, присоединенные к флуоресцентным фрагментам, фрагментам биотина или авидина, или к другому белку или пептиду. Согласно некоторым вариантам осуществления модифицированное нуклеиновое основание представляет собой «универсальное основание», которое не является нуклеиновым основанием в его общепринятом значении, но имеет функции, схожие с нуклеиновым основанием. Одним из типовых примеров указанного универсального основания является 3-нитропиррол.
Согласно некоторым вариантам осуществления в способе, предложенном в настоящем описании, также можно применять другие нуклеозиды, включая нуклеозиды, содержащие модифицированные нуклеиновые основания или нуклеиновые основания, ковалентно связанные с модифицированными сахарами. Некоторые примеры нуклеозидов, содержащих модифицированные нуклеиновые основания, включают 4-ацетилцитидин; 5-(карбоксигидроксилметил)уридин; 2'-O-метилцитидин; 5-карбоксиметиламинометил-2-тиоуридин; 5-карбоксиметиламинометилуридин; дигидроуридин; 2'-О-метилпсевдоуридин; бета,D-галактозилквеуозин; 2'-O-метилгуанозин; N6-изопентиладенозин; 1-метиладенозин; 1-метилпсевдоуридин; 1-метилгуанозин; 1-метилинозин; 2,2-диметилгуанозин; 2-метиладенозин; 2-метилгуанозин; N7-метилгуанозин; 3-метилцитидин; 5-метилцитидин; 5-гидроксиметилцитидин; 5-формилцитозин; 5-карбоксилцитозин; N6-метиладенозин; 7-метилгуанозин; 5-метиламиноэтилуридин; 5-метоксиаминометил-2-тиоуридин; бета,D-маннозилквеуозин; 5-метоксикарбонилметилуридин; 5-метоксиуридин; 2-метилтио-N6-изопентениладенозин; N-((9-бета,D-рибофуранозил-2-метилтиопурин-6-ил)карбамоил)треонин; N-((9-бета,D-рибофуранозилпурин-6-ил)-N-метилкарбамоил)треонин; метиловый эфир уридин-5-оксиуксусной кислоты; уридин-5-оксиуксусную кислоту (v); псевдоуридин; квеуозин; 2-тиоцтидин; 5-метил-2-тиоуридин; 2-тиоуридин; 4-тиоуридин; 5-метилуридин; 2'-O-метил-5-метилуридин; и 2'-O-метилуридин.
Согласно некоторым вариантам осуществления нуклеозиды включают 6'-модифицированные бициклические аналоги нуклеозидов, которые имеют (R)- или (S)-конфигурацию положения 6', и включают аналоги, описанные в патенте США №7399845. В других вариантах реализации нуклеозиды включают 5'-модифицированные аналоги нуклеозидов, которые имеют (R)- или (S-конфигурацию положения 5', и включают аналоги, описанные в опубликованной заявке на патент США №20070287831.
Согласно некоторым вариантам осуществления нуклеиновое основание или модифицированное нуклеиновое основание содержит один или более фрагментов, связывающихся с биомолекулами, таких как, например, антитела, фрагменты антител, биотин, авидин, стрептавидин, лиганды рецепторов или хелатообразующие фрагменты. В других вариантах реализации нуклеиновое основание или модифицированное нуклеиновое основание представляет собой 5-бромурацил, 5-йодурацил или 2,6-диаминопурин. Согласно некоторым вариантам осуществления нуклеиновое основание или модифицированное нуклеиновое основание модифицируют путем замещения флуоресцентным фрагментом или фрагментом, связывающимся в биомолекулами. Согласно некоторым вариантам осуществления заместитель нуклеинового основания или модифицированного нуклеинового основания представляет собой флуоресцентный фрагмент. Согласно некоторым вариантам осуществления заместитель нуклеинового основания или модифицированного нуклеинового основания представляет собой биотин или авидин.
Типовые патенты США, в которых предложено получение определенных модифицированных нуклеиновых оснований из числа тех, что указаны выше, а также других модифицированных нуклеиновых оснований, включают, но не ограничиваются ими, указанный выше патент США №3687808, а также патенты США №4845205; 513030; 5134066; 5175273; 5367066; 5432272; 5457187; 5457191; 5459255; 5484908; 5502177; 5525711; 5552540; 5587469; 5594121, 5596091; 5614617; 5681941; 5750692; 6015886; 6147200; 6166197; 6222025; 6235887; 6380368; 6528640; 6639062; 6617438; 7045610; 7427672; и 7495088, содержание каждого из которых включено в настоящую заявку во всей полноте посредством ссылки.
Согласно некоторым вариантам осуществления основание необязательно замещено А, Т, С, G или U, где один или более -NH2 независимо и необязательно замещены -C(-L-R1)3, один или более -NH- независимо и необязательно замещены -C(-L-R1)2-, один или более =N- независимо и необязательно замещены -C(-L-R1)-, один или более =СН- независимо и необязательно замещены =N- и один или более =O независимо и необязательно замещены =S, =N(-L-R1) или =C(-L-R1)2, где два или более -L-R1 возможно взяты вместе с их промежуточными атомами с образованием 3-30-членного бициклического или полициклического кольца, имеющего 0-10 гетероатомных кольцевых атомов. Согласно некоторым вариантам осуществления модифицированное основание представляет собой необязательно замещенное А, Т, С, G или U, где один или более -NH2 независимо и необязательно замещены -C(-L-R1)3, один или более -NH- независимо и необязательно замещены -С(-L-R1)2-, один или более =N- независимо и необязательно замещены -C(-L-R1)-, один или более =СН- независимо и необязательно замещены =N- и один или более =O независимо и необязательно замещены =S, =N(-L-R1) или =C(-L-R1)2, где два или более -L-R1 возможно взяты вместе с их промежуточными атомами с образованием 3-30-членного бициклического или полициклического кольца, имеющего 0-10 гетероатомных кольцевых атомов, причем модифицированное основание отличается от природного А, Т, С, G и U. Согласно некоторым вариантам осуществления основание необязательно замещено А, Т, С, G или U. Согласно некоторым вариантам осуществления модифицированное основание замещено А, Т, С, G или U, где модифицированное основание отличается от природного А, Т, С, G и U.
Согласно некоторым вариантам осуществления модифицированный нуклеотид или нуклеотидный аналог представляет собой любой модифицированный нуклеотид или нуклеотидный аналог, описанный в любом из: Gryaznov, S; Chen, J.-K. J. Am. Chem. Soc. 1994, 116, 3143; Hendrix et al. 1997 Chem. Eur. J. 3: 110; Hyrup et al. 1996 Bioorg. Med. Chem. 4: 5; Jepsen et al. 2004 Oligo. 14: 130-146; Jones et al. J. Org. Chem. 1993, 58, 2983; Koizumi et al. 2003 Nuc. Acids Res. 12: 3267-3273; Koshkin et al. 1998 Tetrahedron 54: 3607-3630; Kumar et al. 1998 Bioo. Med. Chem. Let. 8: 2219-2222; Lauritsen et al. 2002 Chem. Comm. 5: 530-531; Lauritsen et al. 2003 Bioo. Med. Chem. Lett. 13: 253-256; Mesmaeker et al. Angew. Chem., Int. Ed. Engl. 1994, 33, 226; Morita et al. 2001 Nucl. Acids Res. Supp.1: 241-242; Morita et al. 2002 Bioo. Med. Chem. Lett. 12: 73-76; Morita et al. 2003 Bioo. Med. Chem. Lett. 2211-2226; Nielsen et al. 1997 Chem. Soc. Rev. 73; Nielsen et al. 1997 J. Chem. Soc. Perkins Transl. 1: 3423-3433; Obika et al. 1997 Tetrahedron Lett. 38 (50): 8735-8; Obika et al. 1998 Tetrahedron Lett. 39: 5401-5404; Pallan et al. 2012 Chem. Comm. 48: 8195-8197; Petersen et al. 2003 TRENDS Biotech. 21: 74-81; Rajwanshi et al. 1999 Chem. Commun. 1395-1396; Schultz et al. 1996 Nucleic Acids Res. 24: 2966; Seth et al. 2009 J. Med. Chem. 52: 10-13; Seth et al. 2010 J. Med. Chem. 53: 8309-8318; Seth et al. 2010 J. Org. Chem. 75: 1569-1581; Seth et al. 2012 Bioo. Med. Chem. Lett. 22: 296-299; Seth et al. 2012 Mol. Ther-Nuc. Acids. 1, e47; Seth, Punit P; Siwkowski, Andrew; Allerson, Charles R; Vasquez, Guillermo; Lee, Sam; Prakash, Thazha P; Kinberger, Garth; Migawa, Michael T; Gaus, Hans; Bhat, Balkrishen; et al. From Nucleic Acids Symposium Series (2008), 52(1), 553-554; Singh et al. 1998 Chem. Comm. 1247-1248; Singh et al. 1998 J. Org. Chem. 63: 10035-39; Singh et al. 1998 J. Org. Chem. 63: 6078-6079; Sorensen 2003 Chem. Comm. 2130-2131; Ts'o et al. Ann. N.Y. Acad. Sci. 1988, 507, 220; Van Aerschot et al. 1995 Angew. Chem. Int. Ed. Engl. 34: 1338; Vasseur et al. J. Am. Chem. Soc. 1992, 114, 4006; публикациях международных заявок WO 20070900071; WO 20070900071 или WO 2016/079181.
Сахара
Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат один или более модифицированных фрагментов сахара, расположенных вблизи природных фрагментов сахара.
Наиболее распространенные природные нуклеотиды состоят из сахаров группы рибоз, связанных с нуклеиновыми основаниями аденозином (А), цитозином (С), гуанином (G) и тимином (Т) или урацилом (U). Также предложены модифицированные нуклеотиды, где фосфатная группа или атом фосфора линкерной группы в нуклеотидах могут быть присоединены к различным положениям сахара или модифицированного сахара. В качестве неограничивающих примеров фосфатная группа или атом фосфора линкерной группы может быть присоединен к 2', 3', 4' или 5'-гидроксильному фрагменту сахара или модифицированного сахара. Нуклеотиды, содержащие модифицированные нуклеиновые основания, такие как описано в настоящей заявке, также предполагаются в контексте настоящего описания. Согласно некоторым вариантам осуществления нуклеотиды или модифицированные нуклеотиды, содержащие незащищенный фрагмент -ОН, применяют согласно способам согласно настоящему раскрытию.
В состав предложенного олигонуклеотида могут входить и другие модифицированные сахара. Согласно некоторым вариантам осуществления модифицированный сахар содержит один или более заместителей при положении 2', включая любой из следующих: -F; -CF3, -CN, -N3, -NO, -NO2, -OR', -SR' или -N(R')2, где каждый R' независимо является таким, как определено выше в настоящем описании; -О-(C1-С10 алкил), -S-(C1-С10 o алкил), -NH-(C1-С10 алкил) или -N(C1-С10 алкил)2; -O-(С2-С10 алкенил), -S-(C2-C10 алкенил), -NH-(C2-C10 алкенил) или -N(C2-C10 алкенил)г; -O-(С2-С10 алкинил), -S-(C2-C10 алкинил), -NH-(C2-C10 алкинил) или -N(C2-C10 алкинил)2; или -O-(C1-С10 алкилен)-O-(С1-С10 алкил), -O-(C1-C10 алкилен)-МН-(С1-С10 алкил) или -O-(C1-C10 алкилен)-NH(С1-С10 алкил)г, -NH-(C1-C10 алкилен)-O-(С1-С10 алкил) или -N(C1-C10 алкил)-(С1-С10 алкилен)-O-(С1-С10 алкил), где алкил, алкилен, алкенил и алкинил могут быть замещенными или незамещенными. Примеры заместителей включают, но не ограничиваются ими, -O(СН2)nOCH3 и -O(CH2)nNH2, где n равен от 1 до примерно 10, МОЕ, DMAOE, DMAEOE. Также в настоящем описании предложены модифицированные сахара, описанные в международной заявке на патент WO2001/088198; и Martin et al, Helv. Chim. Acta, 1995, 78, 486-504. Согласно некоторым вариантам осуществления модифицированный сахар содержит одну или более групп, выбранных из замещенной силильной группы, РНК-отщепляющей группы, репортерной группы, флуоресцентной метки, интеркалятора, группы, улучшающей фармакодинамические свойства нуклеиновой кислоты, или других заместителей, имеющих схожие свойства. Согласно некоторым вариантам осуществления модификации проводят по одному или более положениям, выбранным из положений 2', 3', 4', 5' или 6' сахара или модифицированного сахара, включая положение 3' сахара при 3'-терминальном нуклеотиде или положение 5' при 5'-терминальном нуклеотиде.
Согласно некоторым вариантам осуществления 2'-ОН рибозы заменена на заместитель, включая любой из следующих: -Н, -F; -CF3, -CN, -N3, -NO, -NO2, -OR', -SR' или -N(R')2, где каждый R' независимо является таким, как определено выше в настоящей заявке; -O-(C1-С10 алкил), -S-(C1-С10 алкил), -NH-(C1-С10 алкил) или -N(C1-С10 алкил)2; -О-(С2-С10 алкенил), -S-(C2-C10 алкенил), -NH-(C2-C10 алкенил) или -N(C2-C10 алкенил)2; -О-(С2-С10 алкинил), -S-(C2-C10 алкинил), -NH-(C2-C10 алкинил) или -N(C2-C10 алкинил)2; или -O-(C1-C10 алкилен)-O-(С1-С10 алкил), -O-(C1-C10 алкилен)-NH-(С1-С10 алкил) или -O-(C1-С10 алкилен)-NH(С1-С10 алкил)2, -NH-(C1-C10 алкилен)-O-(С1-С10 алкил) или -N(C1-C10 алкил)-(C1-C10 алкилен)-O-(С1-С10 алкил), где алкил, алкилен, алкенил и алкинил могут быть замещенными или незамещенными. Согласно некоторым вариантам осуществления 2'-ОН заменен на -Н (дезоксирибоза). Согласно некоторым вариантам осуществления 2'-ОН заменен на -F. Согласно некоторым вариантам осуществления 2'-ОН заменен на -OR'. Согласно некоторым вариантам осуществления 2'-ОН заменен на -ОМе. Согласно некоторым вариантам осуществления 2'-ОН заменен на -ОСН2СН2ОМе.
Модифицированные сахара также включают закрытые нуклеиновые кислоты (ЗНК). Согласно некоторым вариантам осуществления два заместителя на атомах углерода сахара, взятые вместе, образуют двухвалентный фрагмент. Согласно некоторым вариантам осуществления два заместителя находятся на двух разных атомах углерода сахара. Согласно некоторым вариантам осуществления образуемый двухвалентный фрагмент имеет структуру -L-, как определено в настоящем описании. Согласно некоторым вариантам осуществления -L- представляет собой -О-СН2-, где -СН2- представляет собой необязательно замещенный. Согласно некоторым вариантам осуществления -L-представляет собой -О-СН2-. Согласно некоторым вариантам осуществления -L-представляет собой -O-CH(Et)-. Согласно некоторым вариантам осуществления -L-находится между С2 и С4 фрагмента сахара. Согласно некоторым вариантам осуществления закрытая нуклеиновая кислота имеет структуру, указанную ниже. Ниже указана структуру закрытой нуклеиновой кислоты, где Ва представляет собой нуклеиновое основание или модифицированное нуклеиновое основание, такое как описано в настоящей заявке, a R2s представляет собой -ОСН2С4'-.

Согласно некоторым вариантам осуществления модифицированный сахар представляет собой ЭНК, такие как те, что описаны, например, в Seth et al., J Am Chem Soc. 2010 October 27; 132(42): 14942-14950. Согласно некоторым вариантам осуществления модифицированный сахар представляет собой любой сахар, присутствующий в КНК (ксенонуклеиновой кислоте), например, арабинозу, ангидрогексит, треозу, 2'-фторарабинозу или циклогексен.
Модифицированные сахара включают имитаторы сахаров, такие как циклобутильные или циклопентильные фрагменты, содержащиеся вместо пентофуранозильного фрагмента сахара. Типовые патенты США, в которых предложено получение сахаров с указанными модифицированными структурами, включают, но не ограничиваются ими, патенты США №4981957; 5118800; 5319080; и 5359044. Некоторые предложенные модифицированные сахара включают сахара, где атом кислорода в рибозном кольце заменен на атомы азота, серы, селена или углерода. Согласно некоторым вариантам осуществления модифицированный сахар представляет собой модифицированную рибозу, где атом кислорода в рибозном кольце заменен на атом азота, а атом азота необязательно замещен алкильной группой (например, метилом, этилом, изопропилом и т.д.).
Неограничивающие примеры модифицированных сахаров включают глицерин, из которого получают аналоги глицериннуклеиновых кислот (ГНК). Один из примеров аналогов ГНК показан ниже и описан в Zhang, R et al., J. Am. Chem. Soc., 2008, 130, 5846-5847; Zhang L, et al, J. Am. Chem. Soc, 2005, 127, 4174-4175 и Tsai CH et al., PNAS, 2007, 14598-14603 (X=O-):
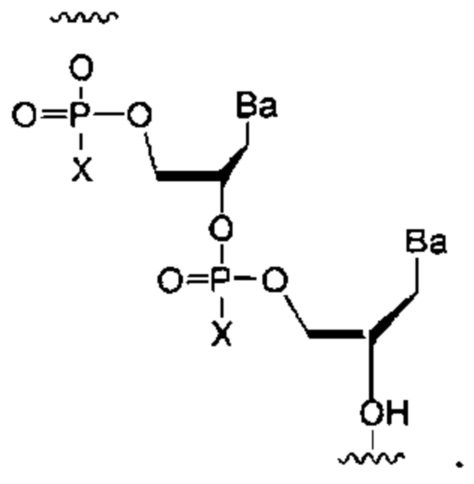
Другой пример аналога производного ГНК, пластичной нуклеиновой кислоты (flexible nucleic acid, FNA), основанный на смеси ацетальаминаля формилглицерина, описан в Joyce GF et al., PNAS, 1987, 84, 4398-4402 и Heuberger BD and Switzer C, J. Am. Chem. Soc., 2008, 130, 412-413, и показан ниже:
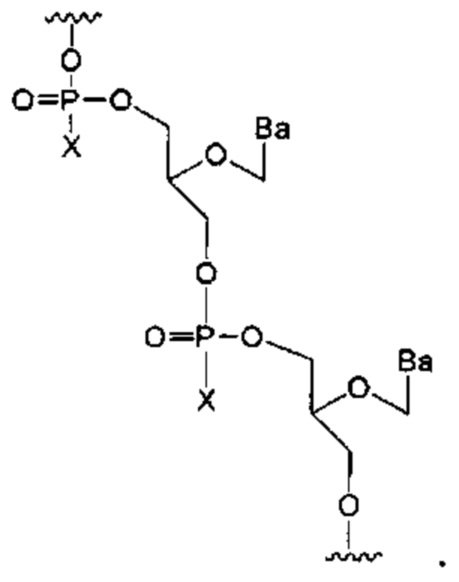
Дополнительные неограничивающие примеры модифицированных сахаров включают гексопиранозильные (от 6' до 4'), пентопиранозильные (от 4' до 2'), пентопиранозильные (от 4' до 3') или тетрофуранозильные (от 3' до 2') сахара. Согласно некоторым вариантам осуществления гексопиранозильный (от 6' до 4') сахар имеет любую из следующих формул:
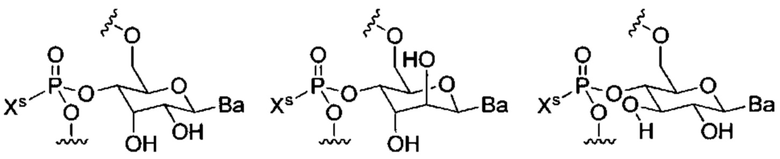
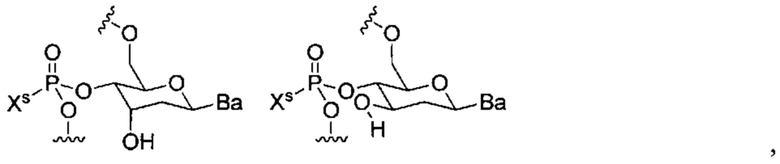
где Xs соответствует группе с модификацией Р «-XLR1», описанной в настоящей заявке, а Ва такой, как определено в настоящем описании.
Согласно некоторым вариантам осуществления пентопиранозильный (от 4' до 2') сахар имеет любую из следующих формул:
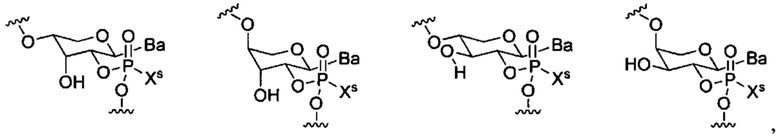
где Xs соответствует группе с модификацией Р «-XLR1», описанной в настоящей заявке, а Ва такой, как определено в настоящем описании.
Согласно некоторым вариантам осуществления пентопиранозильный (от 4' до 3') сахар имеет любую из следующих формул:
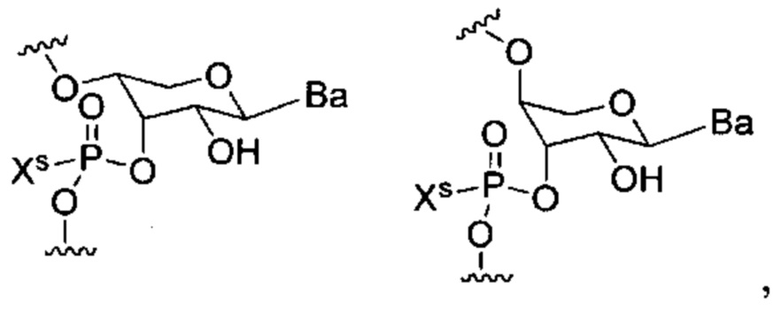
где Xs соответствует группе с модификацией Р «-XLR1», описанной в настоящей заявке, а Ва такой, как определено в настоящем описании.
Согласно некоторым вариантам осуществления тетрофуранозильный (от 3' до 2') сахар имеет любую из следующих формул:
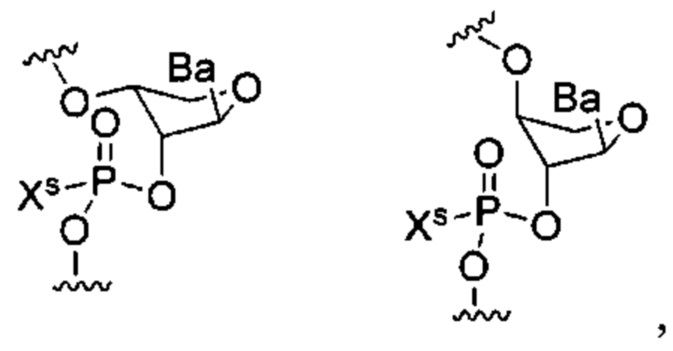
где Xs соответствует группе с модификацией Р «-XLR1», описанной в настоящей заявке, а Ва такой, как определено в настоящем описании.
Согласно некоторым вариантам осуществления модифицированный сахар имеет любую из следующих формул:
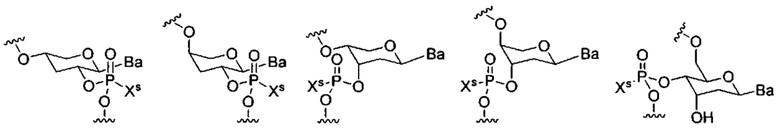
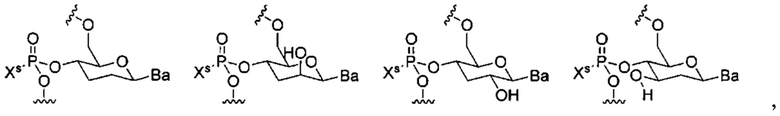
где Xs соответствует группе с модификацией Р «-XLR1», описанной в настоящей заявке, а Ва такой, как определено в настоящем описании.
Согласно некоторым вариантам осуществления одна или более гидроксильных групп во фрагменте сахара возможно и независимо заменена на галоген, R', -N(R')2, -OR' или -SR', где каждый R' независимо является таким, как определено выше в настоящем описании.
Согласно некоторым вариантам осуществления имитатор сахара является таким, как проиллюстрировано далее; где Xs соответствует группе с модификацией Р «-XLR1», описанной в настоящей заявке, Ва такой, как определено в настоящем описании, а X1 выбран из -S-, -Se-, -СН2-, -NMe-, -NEt- или -NiPr-.
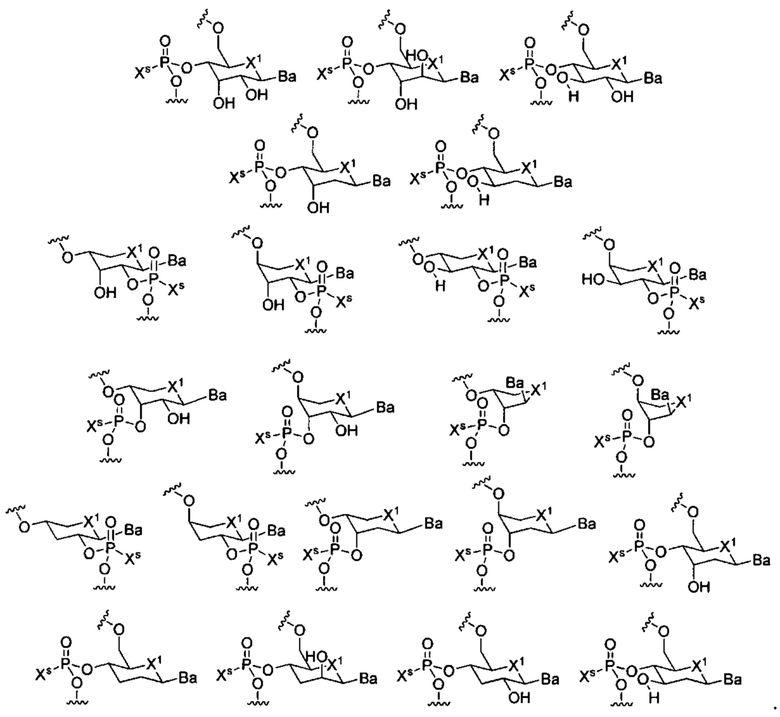
Согласно некоторым вариантам осуществления по меньшей мере 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50% или более (например, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или более) сахаров в композиции олигонуклеотидов с контролируемой хиральностью, включительно, являются модифицированными. Согласно некоторым вариантам осуществления только пуриновые остатки являются модифицированными (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50% или более [например, 55%, 60%, 65%, 70%, 75%, 80%), 85%, 90%, 95% или более] пуриновых остатков являются модифицированными). Согласно некоторым вариантам осуществления только пиримидиновые остатки являются модифицированными (например, примерно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50% или более [например, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или более] пиримидиновых остатков являются модифицированными). Согласно некоторым вариантам осуществления модифицированными являются и пуриновые и пиримидиновые остатки.
Модифицированные сахара и имитаторы сахаров можно получать при помощи способов, известных в данной области техники, включая, но не ограничиваясь ими: А. Eschenmoser, Science (1999), 284:2118; М. Bohringer et al, Helv. Chim. Acta (1992), 75:1416-1477; M. Egli et al, J. Am. Chem. Soc. (2006), 128(33):10847-56; A. Eschenmoser в Chemical Synthesis: Gnosis to Prognosis, C. Chatgilialoglu and V. Sniekus, Ed., (Kluwer Academic, Netherlands, 1996), p. 293; K.-U. Schoning et al, Science (2000), 290:1347-1351; A. Eschenmoser et al, Helv. Chim. Acta (1992), 75:218; J. Hunziker et al, Helv. Chim. Acta (1993), 76:259; G. Otting et al, Helv. Chim. Acta (1993), 76:2701; K. Groebke et al, Helv. Chim. Acta (1998), 81:375; и A. Eschenmoser, Science (1999), 284:2118. Модификации положения 2' можно найти в Verma, S. et al. Annu. Rev. Biochem. 1998, 67, 99-134 и по ссылкам, указанным в данном документе. Конкретные модификации рибозы можно найти по следующим ссылкам: 2'-фтор- (Kawasaki et. al., J. Med. Chem., 1993, 36, 831-841), 2'-MOE (Martin, P. Helv. Chim. Acta 1996, 79, 1930-1938), «ЗНК» (Wengel, J. Acc. Chem. Res. 1999, 32, 301-310). Согласно некоторым вариантам осуществления модифицированный сахар представляет собой любой из тех, что описаны в опубликованной международной заявке на патент РСТ WO2012/030683, содержание которой включено в настоящую заявку посредством ссылки, и изображены на фигурах 26-30 настоящей заявки. Согласно некоторым вариантам осуществления модифицированный сахар представляет собой любой модифицированный сахар, описанный любой из следующих публикаций: Gryaznov, S; Chen, J.-K. J. Am. Chem. Soc. 1994, 116, 3143; Hendrix et al. 1997 Chem. Eur. J. 3: 110; Hyrup et al. 1996 Bioorg. Med. Chem. 4: 5; Jepsen et al. 2004 Oligo. 14: 130-146; Jones et al. J. Org. Chem. 1993, 58, 2983; Koizumi et al. 2003 Nuc. Acids Res. 12: 3267-3273; Koshkin et al. 1998 Tetrahedron 54: 3607-3630; Kumar et al. 1998 Bioo. Med. Chem. Let. 8: 2219-2222; Lauritsen et al. 2002 Chem. Comm. 5: 530-531; Lauritsen et al. 2003 Bioo. Med. Chem. Lett. 13: 253-256; Mesmaeker et al. Angew. Chem., Int. Ed. Engl. 1994, 33, 226; Morita et al. 2001 Nucl. Acids Res. Supp.1: 241-242; Morita et al. 2002 Bioo. Med. Chem. Lett. 12: 73-76; Morita et al. 2003 Bioo. Med. Chem. Lett. 2211-2226; Nielsen et al. 1997 Chem. Soc. Rev. 73; Nielsen et al. 1997 J. Chem. Soc. Perkins Transl. 1: 3423-3433; Obika et al. 1997 Tetrahedron Lett. 38 (50): 8735-8; Obika et al. 1998 Tetrahedron Lett. 39: 5401-5404; Pallan et al. 2012 Chem. Comm. 48: 8195-8197; Petersen et al. 2003 TRENDS Biotech. 21: 74-81; Rajwanshi et al. 1999 Chem. Commun. 1395-1396; Schultz et al. 1996 Nucleic Acids Res. 24: 2966; Seth et al. 2009 J. Med. Chem. 52: 10-13; Seth et al. 2010 J. Med. Chem. 53: 8309-8318; Seth et al. 2010 J. Org. Chem. 75: 1569-1581; Seth et al. 2012 Bioo. Med. Chem. Lett. 22: 296-299; Seth et al. 2012 Mol. Ther-Nuc. Acids. 1, e47; Seth, Punit P; Siwkowski, Andrew; Allerson, Charles R; Vasquez, Guillermo; Lee, Sam; Prakash, Thazha P; Kinberger, Garth; Migawa, Michael T; Gaus, Hans; Bhat, Balkrishen; et al. From Nucleic Acids Symposium Series (2008), 52(1), 553-554; Singh et al. 1998 Chem. Comm. 1247-1248; Singh et al. 1998 J. Org. Chem. 63: 10035-39; Singh et al. 1998 J. Org. Chem. 63: 6078-6079; Sorensen 2003 Chem. Comm. 2130-2131; Ts'o et al. Ann. N. Y. Acad. Sci. 1988, 507, 220; Van Aerschot et al. 1995 Angew. Chem. Int. Ed. Engl. 34: 1338; Vasseur et al. J. Am. Chem. Soc. 1992, 114, 4006; публикациях международных заявкок WO 20070900071; WO 20070900071 или WO 2016/079181.
Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой необязательно замещенный фрагмент пентозы или гексозы. Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой необязательно замещенный фрагмент пентозы. Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой необязательно замещенный фрагмент гексозы. Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой необязательно замещенный фрагмент рибозы или гексита. Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой необязательно замещенный фрагмент рибозы. Согласно некоторым вариантам осуществления модифицированный фрагмент сахара представляет собой необязательно замещенный фрагмент гексита.
Согласно некоторым вариантам осуществления пример модифицированной межнуклеотидной линкерной группы и/или сахара выбран из:
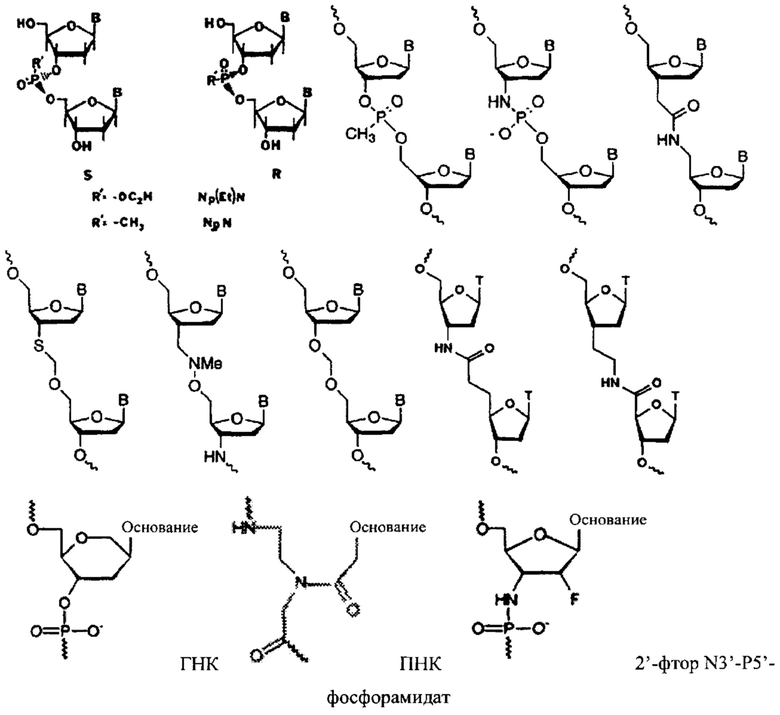
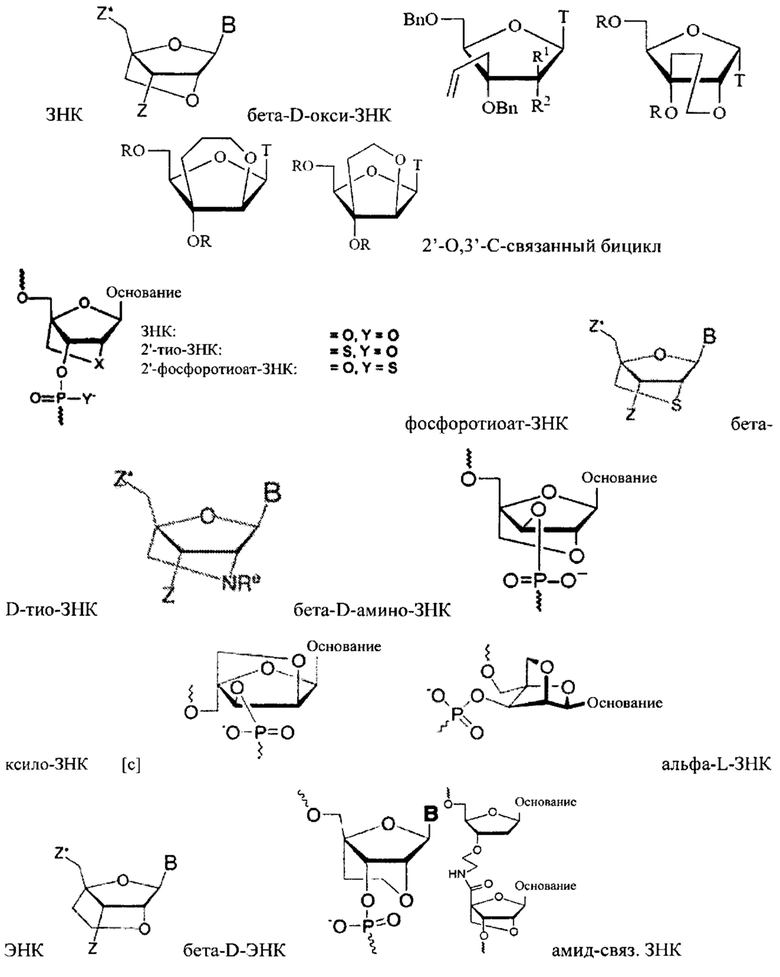
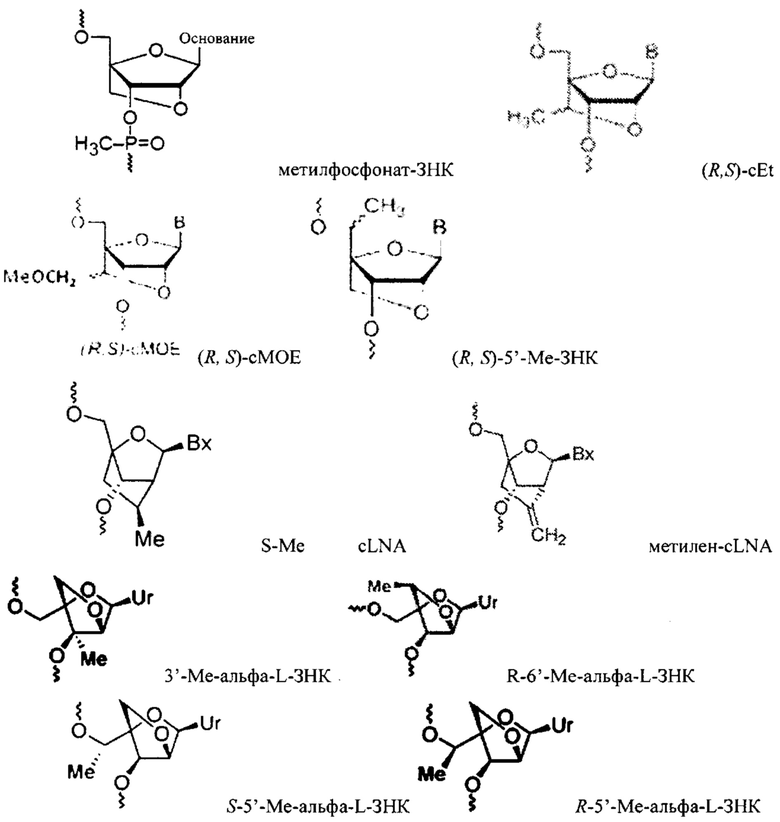
Согласно некоторым вариантам осуществления R1 представляет собой R, как определено и описано. Согласно некоторым вариантам осуществления R2 представляет собой R. Согласно некоторым вариантам осуществления Re представляет R. Согласно некоторым вариантам осуществления Re представляет собой Н, СН3, Bn, COCF3, бензоил, бензил, пирен-1-илкарбонил, пирен-1-илметил, 2-аминоэтил. Согласно некоторым вариантам осуществления пример модифицированной межнуклеотидной линкерной группы и/или сахара выбирают из примеров, описанных в Ts'o et al. Ann. N. Y. Acad. Sci. 1988, 507, 220; Gryaznov, S.; Chen, J.-K. J. Am. Chem. Soc. 1994, 116, 3143; Mesmaeker et al. Angew. Chem., Int. Ed. Engl. 1994, 33, 226; Jones et al. J. Org. Chem. 1993, 58, 2983; Vasseur et al. J. Am. Chem. Soc. 1992, 114, 4006; Van Aerschot et al. 1995 Angew. Chem. Int. Ed. Engl. 34: 1338; Hendrix et al. 1997 Chem. Eur. J. 3: 110; Koshkin et al. 1998 Tetrahedron 54: 3607-3630; Hyrup et al. 1996 Bioorg. Med. Chem. 4: 5; Nielsen et al. 1997 Chem. Soc. Rev. 73; Schultz et al. 1996 Nucleic Acids Res. 24: 2966; Obika et al. 1997 Tetrahedron Lett. 38 (50): 8735-8; Obika et al. 1998 Tetrahedron Lett. 39: 5401-5404; Singh et al. 1998 Chem. Comm. 1247-1248; Kumar et al. 1998 Bioo. Med. Chem. Let. 8: 2219-2222; Nielsen et al. 1997 J. Chem. Soc. Perkins Transl. 1: 3423-3433; Singh et al. 1998 J. Org. Chem. 63: 6078-6079; Seth et al. 2010 J. Org. Chem. 75: 1569-1581; Singh et al. 1998 J. Org. Chem. 63: 10035-39; Sorensen 2003 Chem. Comm. 2130-2131; Petersen et al. 2003 TRENDS Biotech. 21: 74-81; Rajwanshi et al. 1999 Chem. Commun. 1395-1396; Jepsen et al. 2004 Oligo. 14: 130-146; Morita et al. 2001 Nucl. Acids Res. Supp. 1: 241-242; Morita et al. 2002 Bioo. Med. Chem. Lett. 12: 73-76; Morita et al. 2003 Bioo. Med. Chem. Lett. 2211-2226; Koizumi et al. 2003 Nuc. Acids Res. 12: 3267-3273; Lauritsen et al. 2002 Chem. Comm. 5: 530-531; Lauritsen et al. 2003 Bioo. Med. Chem. Lett. 13: 253-256; WO 20070900071; Seth et al., Nucleic Acids Symposium Series (2008), 52(1), 553-554; Seth et al. 2009 J. Med. Chem. 52: 10-13; Seth et al. 2012 Mol. Ther-Nuc. Acids. 1, e47; Pallan et al. 2012 Chem. Comm. 48: 8195-8197; Seth et al. 2010 J. Med. Chem. 53: 8309-8318; Seth et al. 2012 Bioo. Med. Chem. Lett. 22: 296-299; публикации международной завки WO 2016/079181; патентах США US 6326199; US 6066500 и US 6,440,739, модификации оснований и сахаров каждого включены в настоящее описание посредством ссылки.
Олигонуклеотиды
Согласно некоторым вариантам осуществления в настоящем изобретении предложены олигонуклеотиды с контролируемой хиральностью и композиции олигонуклеотидов. Например, согласно некоторым вариантам осуществления предложенная композиция содержит предварительно определенное количество одного или более нуклеотидов отдельного типа, где тип олигонуклеотида определяется: 1) последовательностью оснований; 2) профилем линкерных групп остова; 3) профилем хиральных центров остова; и 4) профилем Р-модификаций остова. Согласно некоторым вариантам осуществления определенный тип олигонуклеотидов может быть определен с помощью 1А) идентификации оснований; 1 В) профиля модификации оснований; 1С) профиля модификации сахара; 2) профиля линкерных групп остова; 3) профиля хиральных центров остова и 4) профиля модификаций Р остова. Согласно некоторым вариантам осуществления олигонуклеотиды того же типа олигонуклеотида являются идентичными.
Как описано в настоящем документе, настоящее раскрытие предусматривает различные олигонуклеотиды. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды, содержащие последовательность, которая характеризуется общей идентичностью, составляющей более чем 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% по отношению к последовательности, найденной в представленных иллюстративных олигонуклеотидах, например, перечисленных в различных таблицах. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой WV-1092. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой WV-2595. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой WV-2603. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды, содержащие или состоящие из последовательности, найденной в представленном иллюстративном олигонуклеотиде. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды, содержащие или состоящие из последовательности, найденной в WV-1092. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды, содержащие или состоящие из последовательности, найденной в WV-2595. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды, содержащие или состоящие из последовательности, найденной в WV-2603. Согласно некоторым вариантам осуществления предложенный олигонуклеотид дополнительно содержит одну или более природных фоосфатных линкерных групп и одну или более модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит две или более природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит две или более последовательных природных фоосфатных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит две или более модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит две или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 5 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 5 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 6 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 7 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 8 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 9 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит 10 или более последовательных модифицированных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления по меньшей мере одна из модифицированных межнуклеотидных линкерных групп представляет собой межнуклеотидную линкерную группу с контролируемой хиральностью в том отношении, что олигонуклеотиды, имеющие одну и ту же последовательность и химические модификации внутри композиции, имеют одну и ту же конфигурацию, либо Rp, либо Sp, при хиральном атоме фосфора модифицированной межнуклеотидной линкерной группы. Согласно некоторым вариантам осуществления по меньшей мере две модифицированные межнуклеотидные линкерные группы характеризуются контролируемой хиральностью. Согласно некоторым вариантам осуществления по меньшей мере одна модифицированная межнуклеотидная линкерная группа в области последовательных модифицированных межнуклеотидных линкерных групп характеризуются контролируемой хиральностью. Согласно некоторым вариантам осуществления по меньшей мере две модифицированные межнуклеотидные линкерные группы в области последовательных модифицированных межнуклеотидных линкерных групп характеризуются контролируемой хиральностью. Согласно некоторым вариантам осуществления каждая модифицированная межнуклеотидная линкерная группа в области последовательных модифицированных межнуклеотидных линкерных групп характеризуются контролируемой хиральностью. Согласно некоторым вариантам осуществления каждая модифицированная межнуклеотидная линкерная группа характеризуются контролируемой хиральностью. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит профиль (Sp)xRp(Sp)y, где каждый из х и у независимо равен от 1 до 20, а сумма х и у равна от 1 до 50. Согласно некоторым вариантам осуществления каждый из х и у независимо равен от 2 до 20. Согласно некоторым вариантам осуществления по меньшей мере один из х и у больше чем 5, 6, 7, 8, 9 или 10. Согласно некоторым вариантам осуществления сумма х и у больше чем 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более химических модификаций, представленных в предложенном иллюстративном олигонуклеотиде. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более модификаций оснований, представленных в предложенном иллюстративном олигонуклеотиде. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более модификаций сахара, представленных в предложенном иллюстративном олигонуклеотиде. Согласно некоторым вариантам осуществления модификация сахара представляет собой 2'-модификацию. Согласно некоторым вариантам осуществления модификация сахара представляет собой ЗНК. Согласно некоторым вариантам осуществления модификация сахара представляет собой ЭНК. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой олигонуклеотид с контролируемой хиральностью. В некоторых вариантах настоящее раскрытие относится к композиции олигонуклеотидов, содержащей олигонуклеотид. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов представляет собой композицию олигонуклеотидов с контролируемой хиральностью.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой унимер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой унимер с модификацией Р. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой стереоунимер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой стереоунимер с Rp-конфигурацией. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой стереоунимер с Sp-конфигурацией.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой альтмер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой альтмер с модификацией Р. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой стереоальтмер.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой блокмер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой блокмер с модификацией Р. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой стереоблокмер.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой гэпмер.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой скипмер.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой гемимер. Согласно некоторым вариантам осуществления гемимер представляет собой олигонуклеотид, в котором 5'-конец или 3'-конец имеет последовательность, которая обладает особенностью структуры, которой нет у остальной части олигонуклеотида. Согласно некоторым вариантам осуществления 5'-конец или 3'-конец имеет или содержит от 2 до 20 нуклеотидов. Согласно некоторым вариантам осуществления структурной особенностью является модификация оснований. Согласно некоторым вариантам осуществления структурной особенностью является модификация сахаров. Согласно некоторым вариантам осуществления структурной особенностью является Р-модификации. Согласно некоторым вариантам осуществления структурной особенностью является стереохимия хиральной межнуклеотидной линкерной группы. Согласно некоторым вариантам осуществления структурной особенностью является или она содержит модификацию оснований, модификацию сахаров, Р-модификацию или стереохимию хиральной межнуклеотидной линкерной группы или их комбинации. Согласно некоторым вариантам осуществления гемимер представляет собой олигонуклеотид, в котором каждый фрагмент сахара 5'-концевой последовательности имеет одинаковую модификацию. Согласно некоторым вариантам осуществления гемимер представляет собой олигонуклеотид, в котором каждый фрагмент сахара 3'-концевой последовательности имеет одинаковую модификацию. Согласно некоторым вариантам осуществления общая модификация сахара 5'- или 3'-концевой последовательности не разделяется другими остатками сахара в олигонуклеотиде. Согласно некоторым вариантам осуществления иллюстративный гемимер представляет собой олигонуклеотид, содержащий последовательность замещенных или незамещенных нуклеозидов с модифицированным 2'-O-алкилом сахара, нуклеозидов с модифицированным бициклическим сахаром, бета-D-рибонуклеозиды или бета-D-дезоксирибонуклеозиды (например, 2'-МОЕ-модифицированные нуклеозиды и нуклеозиды с модифицированным бициклическим сахаром LNA™ и ENA™) на одном конце, и последовательность нуклеозидов с отличным фрагментом сахара (например, замещенных или незамещенных нуклеозидов с модифицированным 2'-O-алкилом сахара, нуклеозидов с модифицированным бициклическим сахаром или природного нуклеозида) на другом конце. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой комбинацию одного или более из унимера, альтмеров, блокмера, гэпмера, гемимера и скипмера. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой комбинацию одной или более разновидностей, выбранных из унимера, альтмера, блокмера, гэпмера и скипмера. Например, согласно некоторым вариантам осуществления предложенный олигонуклеотид является альтмером и гэпмером. Согласно некоторым вариантам осуществления предложенный нуклеотид является гэпмером и скипмером. Специалистам в области химии и химического синтеза будет понятно, что доступны различные другие комбинации профилей, и они ограничены только коммерческой доступностью и/или возможностью использования в синтезе различных составляющих, требуемых для синтеза предложенного олигонуклеотида согласно способам согласно настоящему раскрытию. Согласно некоторым вариантам осуществления структура гемимера обеспечивает выгодные преимущества, как проиллюстрировано на фиг. 29. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды представляют собой 5'-гемимеры, которые содержат модифицированные сахарные фрагменты в 5'-концевой последовательности. Согласно некоторым вариантам осуществления структура гемимера обеспечивает выгодные преимущества, как проиллюстрировано на фиг. 29. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды представляют собой 5'-гемимеры, которые содержат модифицированные 2'-сахарные фрагменты в 5'-концевой последовательности.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более необязательно замещенных нуклеотидов. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более модифицированных нуклеотидов. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более необязательно замещенных нуклеозидов. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более модифицированных нуклеозидов. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных ЗНК.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одно или более необязательно замещенных нуклеиновых оснований. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одно или более необязательно замещенных природных нуклеиновых оснований. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одно или более необязательно замещенных модифицированных нуклеиновых оснований. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более 5-метилцитидинов; 5-гидроксиметилцитидинов, 5-формилцитозинов или 5-карбоксилцитозинов. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более 5-метилцитидинов.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более необязательно замещенных сахаров. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более необязательно замещенных сахаров, присутствующих в природных ДНК или РНК. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных рибоз или дезоксирибоз. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных рибоз или дезоксирибоз, где одна или более гидроксильных групп во фрагменте рибозы или дезоксирибозы возможно и независимо заменены на галоген, R', -N(R')2, -OR' или -SR', где каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' дезоксирибозы возможно и независимо замещено галогеном, R', -N(R')2, -OR' или -SR', причем каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' дезоксирибозы возможно и независимо замещено галогеном. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' дезоксирибозы возможно и независимо замещено одним или более -F. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' в дезоксирибозе возможно и независимо замещено -OR', причем каждый R' независимо является таким, как определено выше в настоящем описании. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' в дезоксирибозе возможно и независимо замещено -OR', причем каждый R' независимо представляет собой необязательно замещенную C1-С6 алифатическую группу. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' в дезоксирибозе возможно и независимо замещено -OR', причем каждый R' независимо представляет собой необязательно замещенный C1-С6 алкил. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' в дезоксирибозе возможно и независимо замещено -ОМе. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит одну или более необязательно замещенных дезоксирибоз, где положение 2' в дезоксирибозе возможно и независимо замещено -О-метоксиэтилом.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой одноцепочечный олигонуклеотид.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой гибридизованную цепь олигонуклеотида. В определенных вариантах реализации предложенный олигонуклеотид представляет собой частично гибридизованную цепь олигонуклеотида. В определенных вариантах реализации предложенный олигонуклеотид представляет собой полностью гибридизованную цепь олигонуклеотида. В определенных вариантах реализации предложенный олигонуклеотид представляет собой двухцепочечный олигонуклеотид. В определенных вариантах реализации предложенный олигонуклеотид представляет собой трехцепочечный олигонуклеотид (например, триплекс).
Согласно некоторым вариантам осуществления предложенный олигонуклеотид является химерным. Например, согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой химеру ДНК-РНК, химеру ДНК-ЗНК и т.д.
Согласно некоторым вариантам осуществления любую и структур, содержащих нуклеотид, приведенный в WO 2012/030683, можно модифицировать в соответствии со способами согласно настоящему раскрытию для обеспечения их хирально-контролируемых вариантов. Например, согласно некоторым вариантам осуществления хирально-контролируемые варианты содержат стереохимическую модификацию любого одного или более атомов фосфора линкерных групп и/или модификацию Р любого одного или более атомов фосфора линкерных групп. Например, согласно некоторым вариантам осуществления предварительно выбирают нуклеотидное звено олигонуклеотида, предложенного в WO 2012/030683, для проведения стереохимической модификации атома фосфора линкерной группы указанного нуклеотидного звена и/или для модификации Р атома фосфора линкерной группы указанного нуклеотидного звена. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью имеет любую из структур, изображенных на фигурах 26-30. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью является вариантом (например, модифицированным вариантом) любой из структур, изображенных на фигурах 26-30. Описание заявки WO 2012/030683 включено в настоящую заявку во всей полноте посредством ссылки.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой терапевтический агент.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой антисмысловой олигонуклеотид.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой антигенный олигонуклеотид.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой олигонуклеотид-«ловушку».
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой часть ДНК-вакцины.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой иммуномодулирующий олигонуклеотид, например, иммуностимулирующий олигонуклеотид и иммуноподавляющий олигонуклеотид.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид является адъювантом.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой аптамер.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой рибозим.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой дезоксирибозим (ДНК-зимы или ферменты ДНК).
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой миРНК.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой микроРНК или мкРНК.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой нкРНК (некодирующую РНК), включая длинноцепочечные некодирующие РНК (дл.-нкRNA) и короткоцепочечные некодирующие РНК, такие как пиви-взаимодействующие РНК (пиРНК).
Согласно некоторым вариантам осуществления предложенный олигонуклеотид является комплементарным структурной РНК, например, тРНК.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой аналог нуклеиновой кислоты, например, ГНК, ЗНК, ПНК, ТНК, ГНК, АНК, ФАНК, цГНК, ГНК, ННК, ЦНК или морфолино.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой пролекарство с модификацией Р.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой праймер. Согласно некоторым вариантам осуществления праймеры предназначены для применения в полимеразных цепных реакциях (т.е. ПНР) для амплификации нуклеиновых кислот. Согласно некоторым вариантам осуществления праймер предназначен для применения в любых известных вариантах ПЦР, таких как ПЦР с обратной транскрипцией (ОТ-ПЦР) и ПЦР в реальном времени (РВ-ПЦР).
Согласно некоторым вариантам осуществления предложенный олигонуклеотид характеризуется способностью модулировать активацию РНКазы Н. Например, согласно некоторым вариантам осуществления активация РНКазы Н модулируется за счет наличия стереоконтролируемых фосфоротиоатных аналогов нуклеиновых кислот, где природные ДНК/РНК являются в равной или более высокой степени чувствительными по сравнению с Rp-стереоизомером, который в свою очередь является более чувствительным по сравнению с соответствующим Sp-стереоизомером.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид характеризуется способностью косвенным образом или напрямую увеличивать или уменьшать активность белка или ингибировать или промотировать экспрессию белка. Согласно некоторым вариантам осуществления предложенный олигонуклеотид характеризуется тем, что он подходит для контролирования пролиферации клеток, репликации вируса и/или других клеточных сигнальных процессов.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 200 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 180 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 160 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 140 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 120 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 100 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 90 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 80 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 70 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 60 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 50 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 40 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 30 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 29 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 28 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 27 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 26 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 25 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 24 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 23 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 22 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 21 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 2 до примерно 20 нуклеотидных звеньев.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 200 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 180 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 160 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 140 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 120 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 100 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 90 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 80 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 70 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 60 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 50 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 40 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 30 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 29 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 28 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 27 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 26 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 25 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 24 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 23 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 22 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 21 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 4 до примерно 20 нуклеотидных звеньев.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 5 до примерно 10 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 10 до примерно 30 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину от примерно 15 до примерно 25 нуклеотидных звеньев. Согласно некоторым вариантам осуществления предложенный олигонуклеотид имеет длину более чем примерно 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 нуклеотидных звеньев.
Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 2 нуклеотидных звена. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 3 нуклеотидных звена. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 4 нуклеотидных звена. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 5 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 6 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 7 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 8 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 9 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 10 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 11 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 12 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 13 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 14 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 15 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 16 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 17 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 18 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 19 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 20 нуклеотидных звеньев. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 21 нуклеотидное звено. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 22 нуклеотидных звена. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 23 нуклеотидных звена. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 24 нуклеотидных звена. Согласно некоторым вариантам осуществления длина олигонуклеотида составляет по меньшей мере 25 нуклеотидных звеньев. В некоторых других вариантах реализации длина олигонуклеотида составляет по меньшей мере 30 нуклеотидных звеньев. В некоторых других вариантах реализации олигонуклеотид представляет собой дуплекс комплементарных цепей, длина которых составляет по меньшей мере 18 нуклеотидных звеньев. В некоторых других вариантах реализации олигонуклеотид представляет собой дуплекс комплементарных цепей, длина которых составляет по меньшей мере 21 нуклеотидное звено.
Согласно некоторым вариантам осуществления 5'-конец и/или 3'-конец предложенного олигонуклеотида является модифицированным. Согласно некоторым вариантам осуществления 5'-конец и/или 3'-конец предложенного олигонуклеотида модифицирован терминальным концевым фрагментом. Указанные типовые модификации, включая терминальные концевые фрагменты, подробно описаны в настоящей заявке и в уровне техники, включая, например, модификации, описанные в опубликованной заявке на патент США №2009/0023675А1.
Согласно некоторым вариантам осуществления олигонуклеотиды типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также 3) одинаковым профилем хиральных центров остова,
имеют одинаковую химическую структуру. Например, они имеют ту же последовательность оснований, такой же профиль нуклеозидных модификаций, такой же профиль линкерных групп остова (т.е. профиль типов межнуклеотидных линкерных групп, например, фосфатные, фосфоротиоатные и т.д.), такой же профиль хиральных центров остова (т.е. профиль стереохимии фосфора линкерной группы (Rp/Sp)) и такой же профиль модификаций фосфора остова (например, профиль групп "-XLR1" в формуле I).
Иллюстративные олигонуклеотиды и композиции
Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью содержит последовательность или часть последовательности мипомерсена. Мипомерсен основан на следующей последовательности оснований GCCT/UCAGT/UCT/UGCT/UT/UCGCACC. Согласно некоторым вариантам осуществления один или более нуклеотидов или линкерных групп могут быть модифицированы согласно настоящему раскрытию. Согласно некоторым вариантам осуществления в настоящем раскрытии предложен олигонуклеотид с контролируемой хиральностью, имеющий последовательность G*-C*-C*-U*-C*-dA-dG-dT-dC-dT-dG-dmC-dT-dT-dmC-G*-C*-A*-C*-C* [d=2'-дезокси, *=2'-O-(2-метоксиэтил)] и 3'→5' фосфоротиоатные линкерные группы. Иллюстративные модифицированные последовательности мипомерсена описаны в настоящей заявке и включают, но не ограничиваются ими, тем, что приведены в таблице 2.
В определенных вариантах реализации предложенный олигонуклеотид представляет собой унимер мипомерсена. В определенных вариантах реализации предложенный олигонуклеотид представляет собой унимер мипомерсена с Rp-конфигурацией. В определенных вариантах реализации предложенный олигонуклеотид представляет собой унимер мипомерсена с Sp-конфигурацией.
Типовые олигонуклеотиды с контролируемой хиральностью, содержащие последовательность или часть последовательности мипомерсена, изображены ниже в таблице 2.

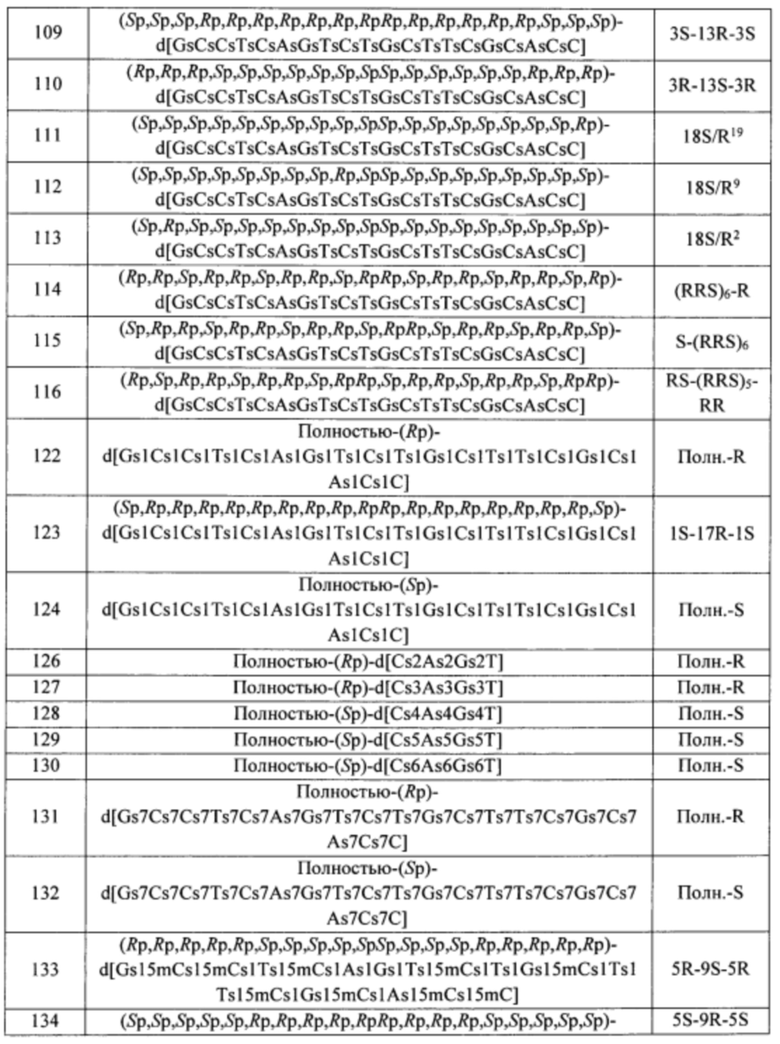
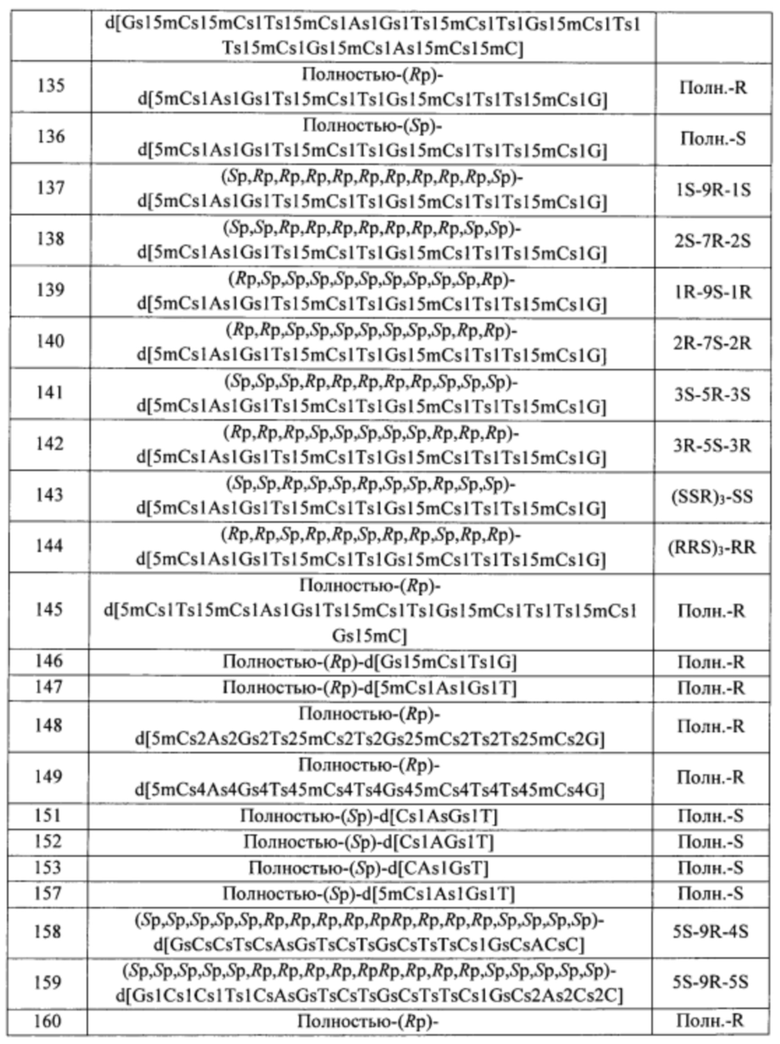
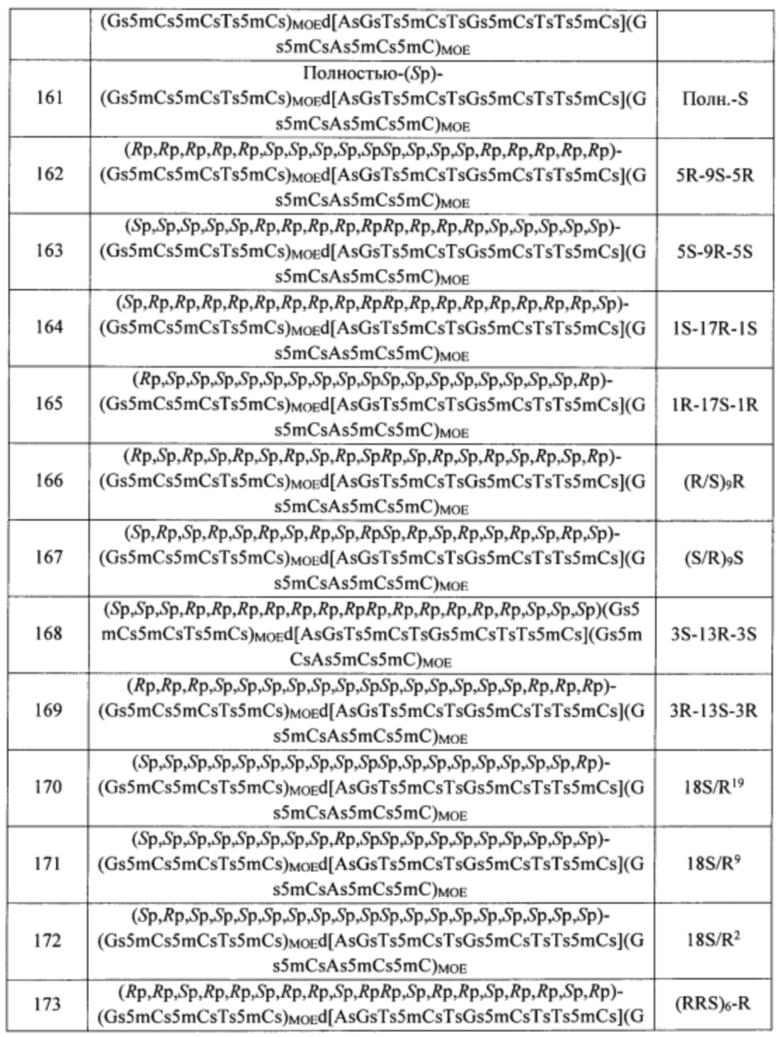
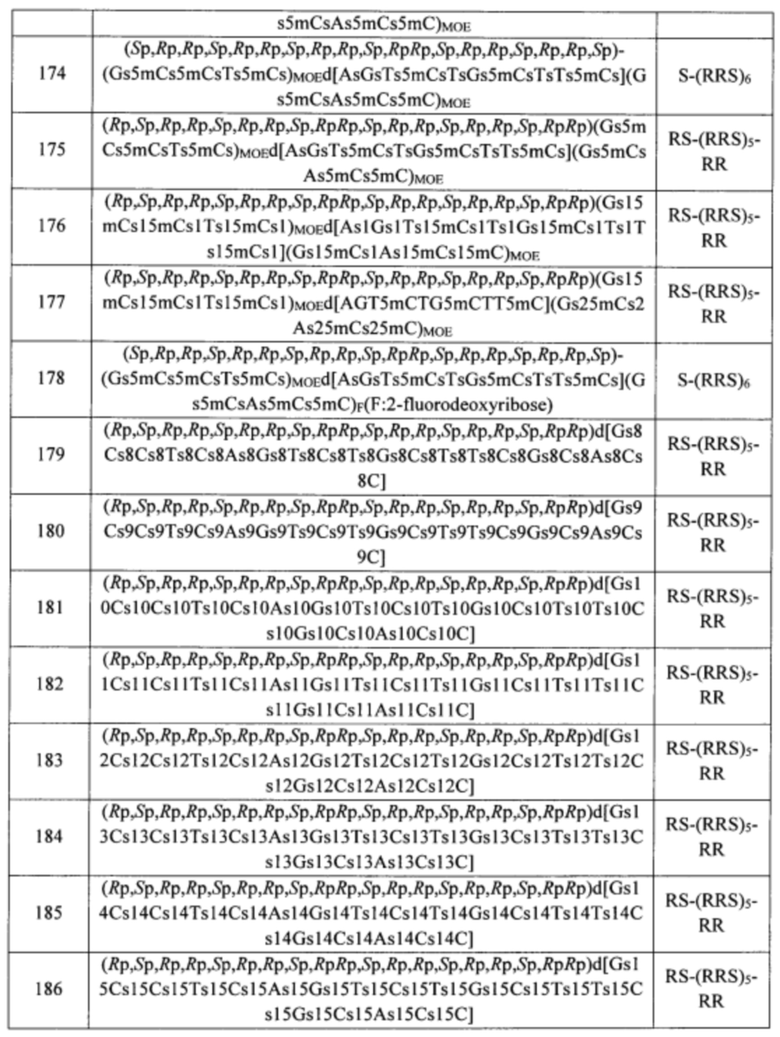
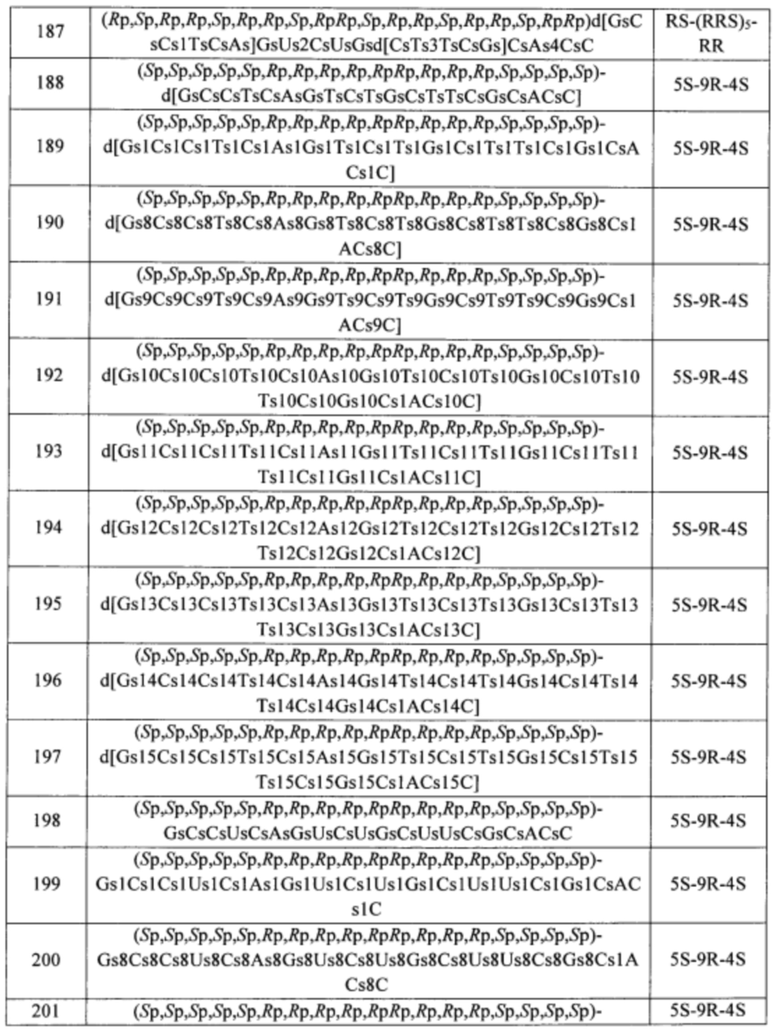

Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды и/или композиции олигонуклеотидов, которые применимы для лечения болезни Хантингтона, например, выбранные из:
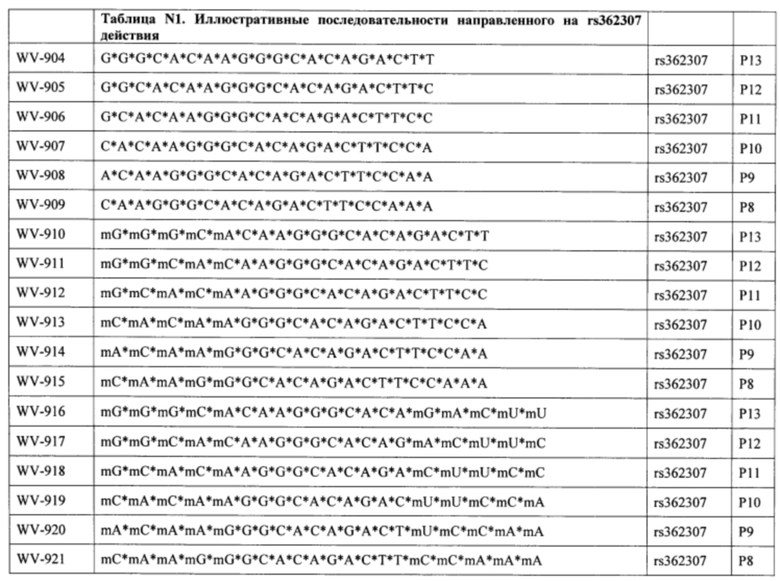

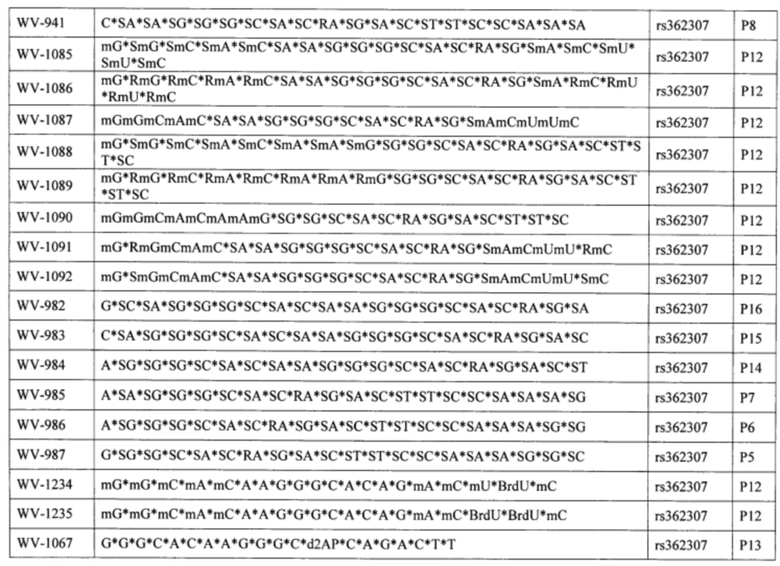
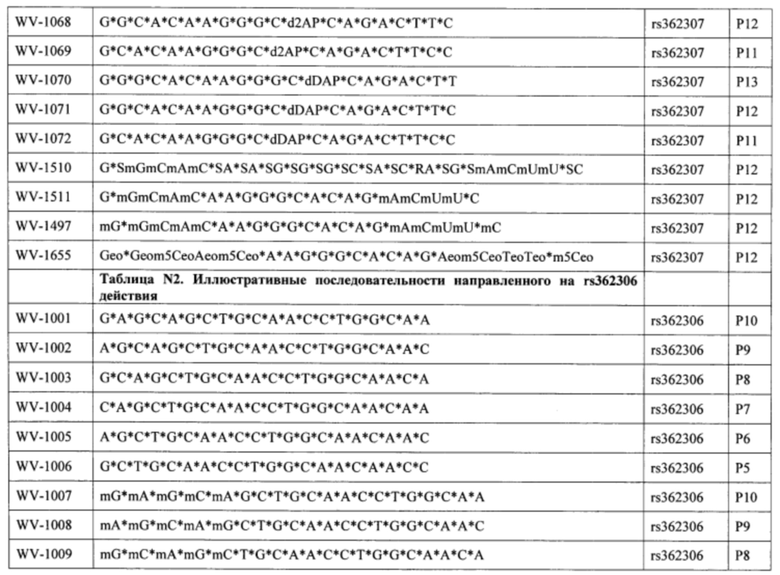

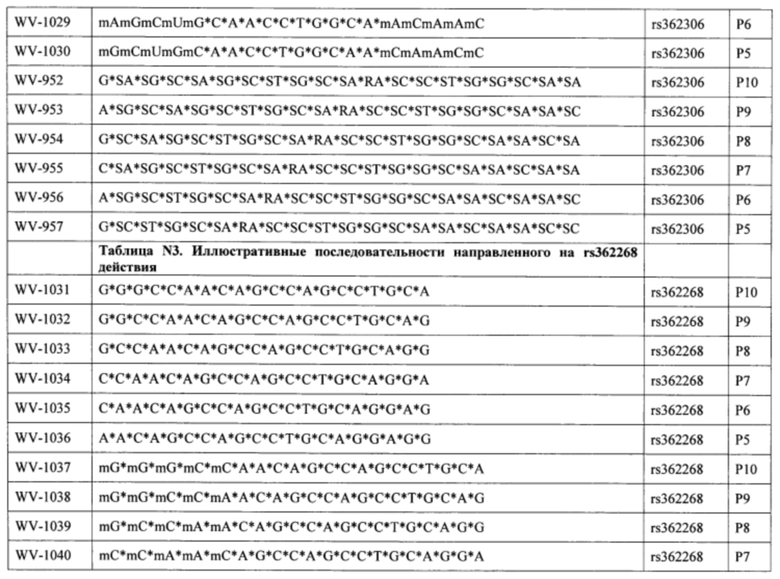







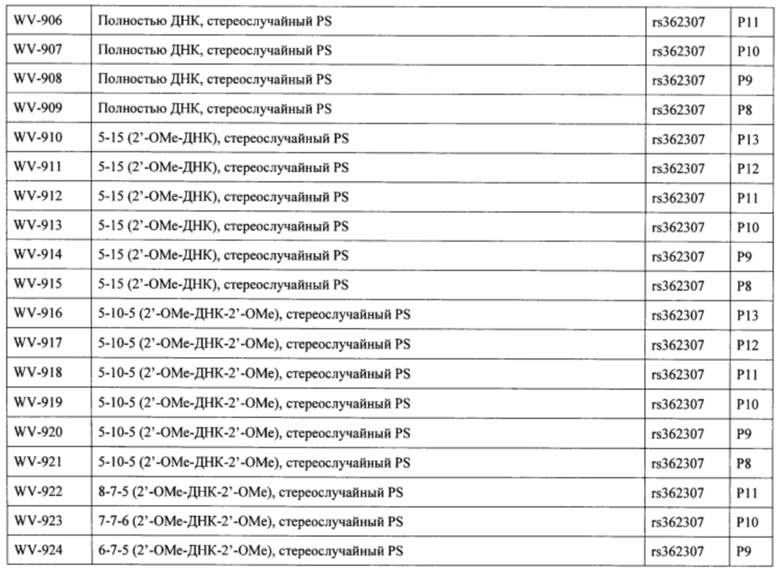
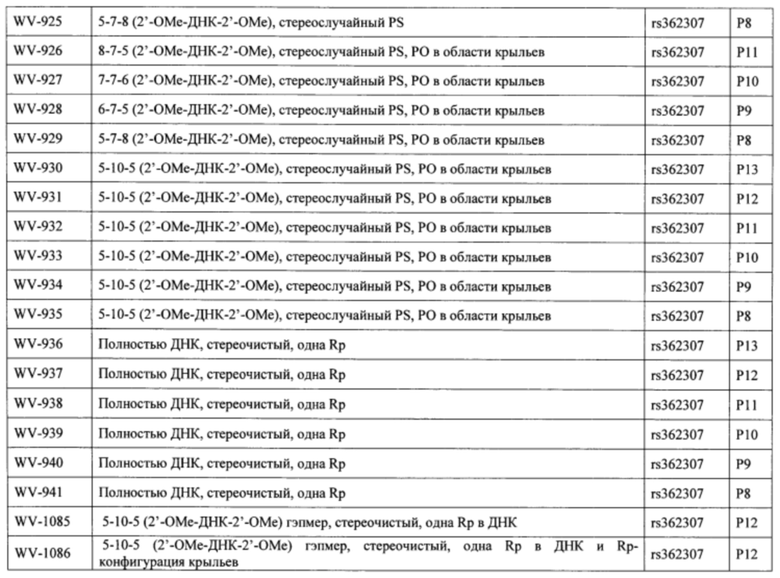
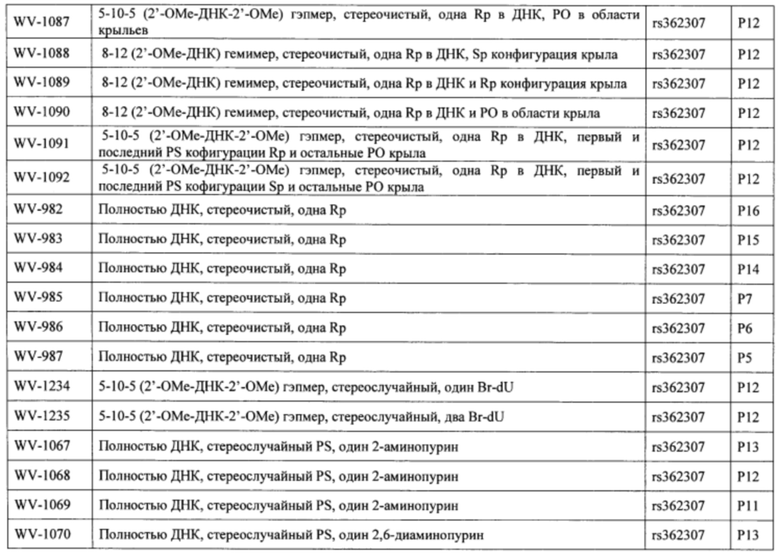
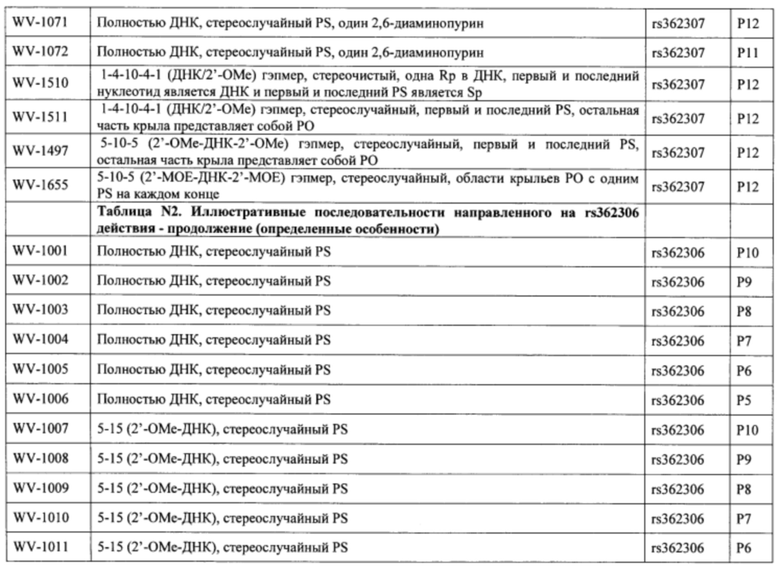

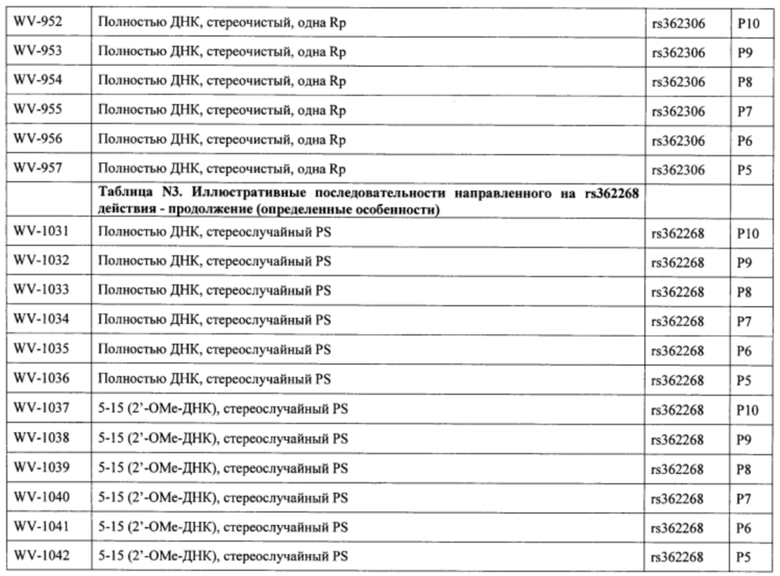

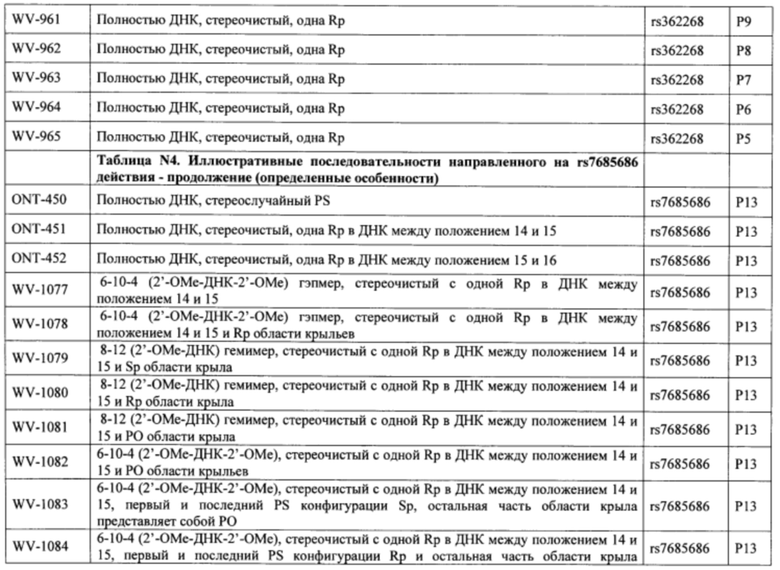

В таблице N1-N4 * представляет собой только стереослучайную фосфоротиоатную линкерную группу; *S представляет собой фосфоротиоатную линкерную группу Sp-конфигурации, *R представляет собой фосфоротиоатную линкерную группу Rp-конфигурации, вся немеченная линкерная группа представляет собой линкерную группу с природным фосфатом, m, предшествующая основанию, представляет собой 2'-ОМе, d2AP представляет собой 2-аминопурин и dDAP представляет собой 2,6-диаминопурин.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает олигонуклеотиды и/или композиции олигонуклеотидов, которые применимы для лечения болезни Хантингтона, например, выбранные из:
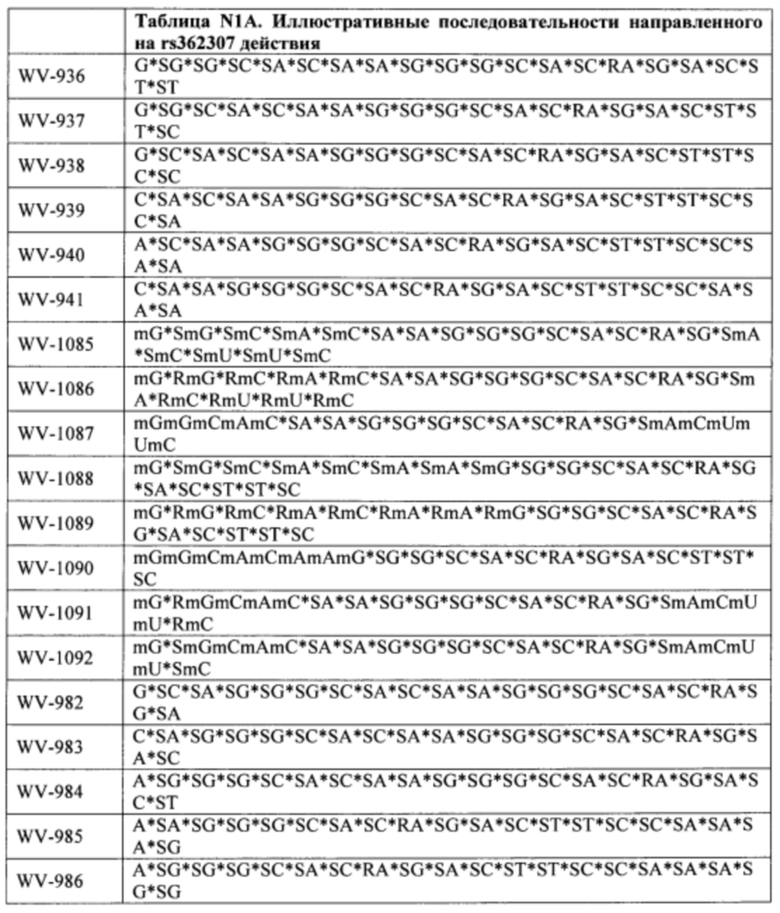
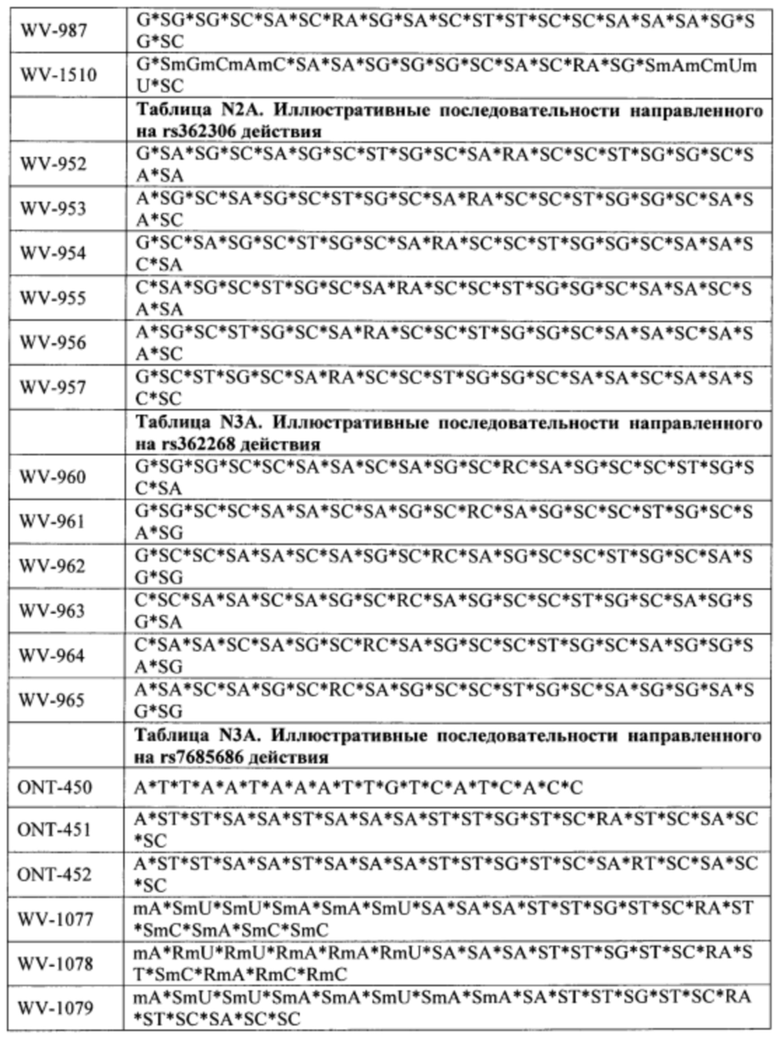

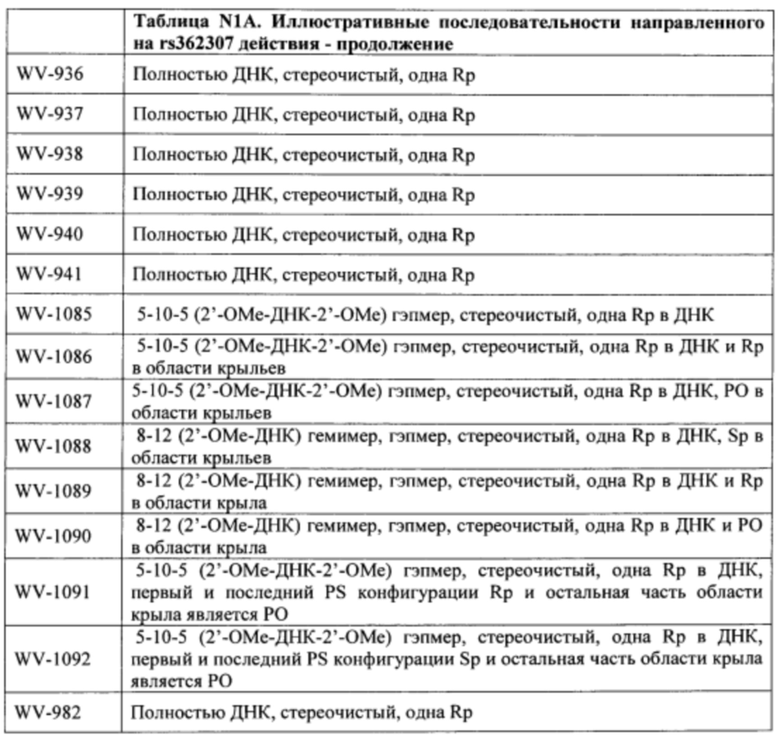
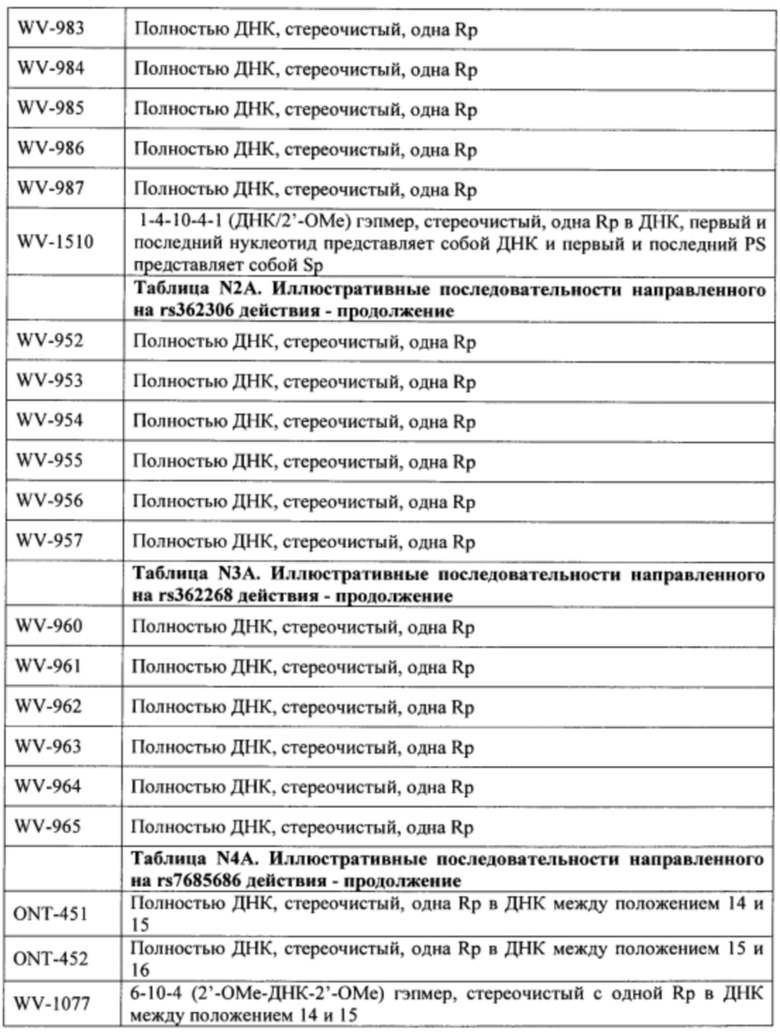

В таблице N1A-N4A * представляет собой только стереослучайную фосфоротиоатную линкерную группу; *S представляет собой фосфоротиоатную линкерную группу Sp-конфигурации, *R представляет собой фосфоротиоатную линкерную группу Rp-конфигурации, вся немеченная линкерная группа представляет собой линкерную группу с природным фосфатом, m, предшествующая основанию, представляет собой 2'-ОМе, d2AP представляет собой 2-аминопурин и dDAP представляет собой 2,6-диаминопурин.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов представляет собой композицию олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, представленного в таблице N1A, таблице N2A, таблице N3A и таблице N4A. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-1092. Каждый описанный в настоящем документе олигонуклеотид, содержащий последовательность НТТ, представляет собой олигонуклеотид НТТ, который был разработан, сконструирован и испытан в различных анализах, например, в анализах in vitro в соответствии с настоящим раскрытием. Например, каждый олигонуклеотид НТТ, указанный в любой из таблиц N1A, N2A, N3A, N4A и 8, или описанный в настоящем документе в другом месте, был разработан, сконструирован и испытан in vitro в соответствии с настоящим изобретением. Среди прочего, каждый олигонуклеотид НТТ, описанный в настоящем документе, был испытан в анализе репортерного гена с двойной люциферазой. Согласно некоторым вариантам осуществления олигонуклеотиды НТТ, которые были признаны особенно эффективными в двойном анализе с люциферазой, испытывали в дальнейшем in vitro и in vivo. Согласно некоторым вариантам осуществления предложенную композицию выбирают из: WVE120101; WV-2603; WV-2595; WV-1510; WV-2378 и WV-2380; каждый из которых оказался высокоэффективным, например, как показано in vitro в двойном репортерном анализе с люциферазой в соответствии с настоящим изобретением. Согласно некоторым вариантам осуществления предлагаемая композиция выбирается из: WV-1092; WV-1497; WV-1085; WV-1086; ОНТ-905; и WV-2623; каждый из которых оказался высокоэффективным, например, как показано in vitro в анализе репортерного гена с двойной люциферазой в соответствии с настоящим изобретением. Было также показано, что различные дополнительные олигонуклеотиды НТТ являются особенно эффективными. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-1092. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-1497. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-1085. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-1086. Согласно некоторым вариантам осуществления предложенная композиция представляет собой ОНТ-905. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-2623.
В настоящем раскрытии предложены композиции, содержащие или состоящие из совокупности предложенных олигонуклеотидов (например, композиции олигонуклеотидов с контролируемой хиральностью). Согласно некоторым вариантам осуществления все указанные предложенные олигонуклеотиды имеют один тип, т.е. имеют одинаковую последовательность оснований, профиль линкерных групп остова (т.е. профиль межнуклеотидных линкерных групп, например, фосфатов, фосфоротиоатов и т.д.), профиль хиральных центров остова (т.е. профиль стереохимии атомов фосфора линкерных групп (Rp/Sp)) и профиль модификаций атомов фосфора остова (например, профиль групп «-XLR1» формулы I). Согласно некоторым вариантам осуществления все олигонуклеотиды одного и того же типа являются идентичными. Во многих вариантах реализации, тем не менее, предложенные композиции содержат совокупность типов олигонуклеотидов, как правило, в предварительно определенных относительных количествах.
Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень олигонуклеотида, выбранного из таблицы. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень олигонуклеотида, выбранного из таблиц N1-N4. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень WV-1092. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень WV-2595. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень WV-2603. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень mG*SmGmCmAmC*SA*SA*SG*SG*SG*SC*SA*SC*RA*SG*SmAmCmUmU*SmC, где олигонуклеотид имеет свободный 5'-ОН и 3'-ОН, m, предшествующее основанию, представляет собой модификацию 2'-ОМе в нуклеозиде, содержащем основание, *S представляет собой фосфоротиоатную линкерную группу Sp-конфигурации, *R представляет собой фосфоротиоатную линкерную группу Rp-конфигурации, и вся немеченная линкерная группа представляет собой линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень mG*SmGmGmUmC*SC*ST*SC*SC*SC*SC*SA*SC*RA*SG*SmAmGmGmG*S mA, где олигонуклеотид имеет свободный 5'-ОН и 3'-ОН, m, предшествующее основанию, представляет собой модификацию 2'-ОМе в нуклеозиде, содержащем основание, *S представляет собой фосфоротиоатную линкерную группу Sp-конфигурации, *R представляет собой фосфоротиоатную линкерную группу Rp-конфигурации, и вся немеченная линкерная группа представляет собой линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления предложенная композиция содержит предопределенный уровень mG*SmUmGmCmA*SC*SA*SC*SA*SG*ST*SA*SG*RA*ST*SmGmAmGmG*S mG, где олигонуклеотид имеет свободный 5'-ОН и 3'-ОН, m, предшествующее основанию, представляет собой модификацию 2'-ОМе в нуклеозиде, содержащем основание, *S представляет собой фосфоротиоатную линкерную группу Sp-конфигурации, *R представляет собой фосфоротиоатную линкерную группу Rp-конфигурации, и вся немеченная линкерная группа представляет собой линкерную группу с природным фосфатом.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью представляет собой хирально-чистую композицию мипомерсена. То есть, согласно некоторым вариантам осуществления в предложенной композиции олигонуклеотидов с контролируемой хиральностью обеспечен мипомерсен в виде единственного диастереомера, если рассматривать конфигурацию атомов фосфора линкерных групп. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью представляет собой хирально-однородную композицию мипомерсена. То есть, согласно некоторым вариантам осуществления каждый атом фосфора линкерной группы в мипомерсене имеет Rp-конфигурацию, или каждый атом фосфора линкерной группы в мипомерсене имеет Sp-конфигурацию.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию одного или более предложенных типов олигонуклеотидов. Специалистам в области химии и медицины будет понятно, что выбор и количество каждого из одного или более типов предложенных нуклеотидов в предложенной композиции зависит от предполагаемого применения указанной композиции. То есть, специалисты в данной области техники смогут подбирать предложенную хирально-контролируемую композицию олигонуклеотидов таким образом, чтобы количества и типы предложенных олигонуклеотидов, содержащихся в указанной композиции, образовывали композицию, которая в целом обладала бы определенными желаемыми характеристиками (например, желаемыми с точки зрения биологии, лечения и т.д.).
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию двух или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию трех или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию четырех или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию пяти или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию шести или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию семи или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию восьми или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию девяти или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию десяти или более предложенных типов олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит комбинацию пятнадцати или более предложенных типов олигонуклеотидов.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью представляет собой комбинацию количества хирально-однородного мипомерсена с Rp-конфигурацией и количества хирально-однородного мипомерсена Sp-конфигурацией.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью представляет собой комбинацию количества хирально-однородного мипомерсена с Rp-конфигурацией, количества хирально-однородного мипомерсена с Sp-конфигурацией и количества одной или более хирально-чистых диастереомерных форм мипомерсена.
Согласно некоторым вариантам осуществления предложенный тип олигонуклеотида выбирают из тех, которые описаны в PCT/US2013/050407, который включен в настоящее описание посредством ссылки. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью содержит олигонуклеотиды типа олигонуклеотида, выбранного из описанных в PCT/US2013/050407.
Иллюстративные способы получения олигонуклеотидов и их композиций
В настоящем раскрытии предложены способы получения олигонуклеотидов с контролируемой хиральностью и композиций с контролируемой хиральностью, содержащих один или более конкретных типов нуклеотидов. Согласно некоторым вариантам осуществления фраза «тип олигонуклеотида», используемая в настоящем описании, определяет олигонуклеотид, который имеет определенную последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и профиль модификаций атомов фосфора остова (например, групп «-XLR1»). Олигонуклеотиды одного общего указанного «типа» имеют идентичную структуру друг с другом, если рассматривать последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и профиль модификаций атомов фосфора остова. Согласно некоторым вариантам осуществления олигонуклеотиды типа олигонуклеотида являются идентичными.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью согласно настоящему раскрытию имеет свойства, отличные от соответствующей стереослучайной смеси олигонуклеотидов. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью имеет липофильность, отличающуюся от стереослучайной смеси олигонуклеотидов. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью имеет отличающееся время удерживания ВЭЖХ. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью может иметь пик времени удерживания, значительно отличающийся от соответствующей стереослучайной смеси олигонуклеотидов. Во время очистки олигонуклеотидов путем ВЭЖХ, традиционно используемой в уровне техники, происходит потеря большей части, если не всех, определенных олигонуклеотидов с контролируемой хиральностью. Во время очистки олигонуклеотидов путем ВЭЖХ, традиционно используемой в уровне техники, происходит потеря большей части, если не всех, определенных олигонуклеотидов с контролируемой хиральностью. Одним из последствий является то, что определенные диастереомеры, входящие в состав стереослучайной смеси олигонуклеотидов (определенные олигонуклеотиды с контролируемой хиральностью), невозможно испытывать в исследованиях. Другим следствием является то, что в зависимости от партии из-за неизбежных инструментальных и субъективных погрешностей предполагаемый «чистый» стереослучайный олигонуклеотид будет иметь состав, отличающийся от состава диастереомеров в композиции, и их относительные и абсолютные количества будут различаться в зависимости от партии. В олигонуклеотидах с контролируемой хиральностью и хирально-контролируемых композициях олигонуклеотидов, предложенных в настоящем раскрытии, эта проблема решена, так как олигонуклеотид с контролируемой хиральностью синтезируют при помощи хирально-контролируемого способа в виде единственного диастереомера, а композиция олигонуклеотидов с контролируемой хиральностью содержит предварительно определенные количества одного или более отдельных типов олигонуклеотидов.
Специалистам в данной области техники должно быть понятно, что способы синтеза согласно настоящему раскрытию обеспечивают уровень контроля во время синтеза предложенного олигонуклеотида, при котором каждое нуклеотидное звено олигонуклеотида может быть разработано и/или выбрано заранее таким образом, чтобы оно имело конкретную стереохимию атома фосфора линкерной группы и/или конкретную модификацию атома фосфора линкерной группы и/или содержало конкретное основание и/или конкретный сахар. Согласно некоторым вариантам осуществления предложенный олигонуклеотид разработан и/или выбран заранее таким образом, чтобы он имел определенную комбинацию атомов фосфора линкерных группы, которые являются стереоцентрами межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид, полученный при помощи способов согласно настоящему раскрытию, разработан и/или выбран таким образом, чтобы он имел определенную комбинацию модификаций атомов фосфора линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид, полученный при помощи способов согласно настоящему раскрытию, разработан и/или выбран таким образом, чтобы он имел определенную комбинацию оснований. Согласно некоторым вариантам осуществления предложенный олигонуклеотид, полученный при помощи способов согласно настоящему раскрытию, разработан и/или выбран таким образом, чтобы он имел определенную комбинацию Сахаров. Согласно некоторым вариантам осуществления предложенный олигонуклеотид, полученный при помощи способов согласно настоящему раскрытию, разработан и/или выбран таким образом, чтобы он имел определенную комбинацию одной или более приведенных выше структурных характеристик.
Способы согласно настоящему раскрытию обеспечивают высокую степень хирального контроля. Например, способы согласно настоящему раскрытию способствуют контролированию стереохимической конфигурации каждого отдельного атома фосфора линкерных групп в предложенном олигонуклеотиде. Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают олигонуклеотид, содержащий одну или более модифицированных межнуклеотидных линкерных групп, независимо имеющих структуру формулы I.
Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают олигонуклеотид, который является унимером мипомерсена. Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают олигонуклеотид, который является унимером мипомерсена с. Rp-конфигурацией. Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают олигонуклеотид, который является унимером мипомерсена с Sp-конфигурацией.
Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают хирально-контролируемую композицию олигонуклеотидов, т.е. композицию олигонуклеотидов, содержащую предварительно определенные количества отдельных типов олигонуклеотидов. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит один тип олигонуклеотидов. Согласно некоторым вариантам осуществления хирально-контролируемая композиция содержит более одного типа олигонуклеотида. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит совокупность типов олигонуклеотидов. Примеры композиций олигонуклеотидов с контролируемой хиральностью, полученные согласно настоящему раскрытию, описаны в настоящей заявке.
Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают хирально-чистые композиции мипомерсена, если рассматривать конфигурацию атомов фосфора линкерных групп. То есть, согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают композиции мипомерсена, где мипомерсен присутствует в композиции в виде единственного диастереомера, если рассматривать конфигурацию атомов фосфора линкерных групп.
Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают хирально-однородные композиции мипомерсена, если рассматривать конфигурацию атомов фосфора линкерных групп. То есть, согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают композиции мипомерсена, в которых все нуклеотидные звенья имеют одинаковую стереохимию, если рассматривать конфигурацию атомов фосфора линкерных групп, например, все нуклеотидные звенья имеют Rp-конфигурацию атомов фосфора линкерных групп, или все нуклеотидные звенья имеют Sp-конфигурацию атомов фосфора линкерных групп.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более 50%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 55%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 60%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 65%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 70%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 75%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 80%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 85%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 90%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 91%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 92%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 93%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 94%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 95%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 96%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 97%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 98%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 99%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 99,5%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 99,6%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 99,7%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 99,8%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту более чем примерно 99,9%. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью имеет чистоту по меньшей мере примерно 99%.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью разработана таким образом, чтобы она содержала один тип олигонуклеотидов. В определенных вариантах реализации имеют диастереомерную чистоту примерно 50%. Согласно некоторым вариантам осуществления указанные композицию имеют диастереомерную чистоту примерно 50%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 50%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 55%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 60%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 65%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 70%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 75%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 80%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 85%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 90%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 91%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 92%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 93%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 94%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 95%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 96%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 97%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 98%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 99%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 99,5%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 99,6%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 99,7%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 99,8%. Согласно некоторым вариантам осуществления указанные композиции имеют диастереомерную чистоту примерно 99,9%. Согласно некоторым вариантам осуществления указанные композицию имеют диастереомерную чистоту по меньшей мере примерно 99%.
Среди прочего, настоящее раскрытие признает проблему стереоселективного (а не стереослучайного или рацемического) получения олигонуклеотидов. Среди прочего, настоящее раскрытие предусматривает способы и реагенты для стереоселективного получения олигонуклеотидов, содержащих множество (например, более 5, 6, 7, 8, 9 или 10) межнуклеотидных линкерных групп и, в частности, для олигонуклеотидов, содержащих множество (например, более чем 5, 6, 7, 8, 9 или 10) хиральных межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления при стереослучайном или рацемическом получении олигонуклеотидов образуется по меньшей мере одна хиральная межнуклеотидная линкерная группа с диастереоселективностью менее чем 90:10, 95:5, 96:4, 97:3 или 98:2. Согласно некоторым вариантам осуществления при стереоселективном или хирально-контролируемом получении олигонуклеотидов каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 90:10, 95:5, 96:4, 97:3 или 98:2. Согласно некоторым вариантам осуществления при стереоселективном или хирально-контролируемом получении олигонуклеотидов каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 95:5. Согласно некоторым вариантам осуществления при стереоселективном или хирально-контролируемом получении олигонуклеотидов каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 96:4. Согласно некоторым вариантам осуществления при стереоселективном или хирально-контролируемом получении олигонуклеотидов каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 97:3. Согласно некоторым вариантам осуществления при стереоселективном или хирально-контролируемом получении олигонуклеотидов каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 98:2. Согласно некоторым вариантам осуществления при стереоселективном или хирально-контролируемом получении олигонуклеотидов каждая хиральная межнуклеотидная линкерная группа образуется с диастереоселективностью более чем 99:1. Согласно некоторым вариантам осуществления диастереоселективность хиральной межнуклеотидной линкерной группы в олигонуклеотиде может быть измерена посредством модельной реакции, например, образования димера при практически одинаковых или сопоставимых условиях, в которых димер имеет одинаковую межнуклеотидную линкерную группу как хиральную межнуклеотидную линкерную группу, 5'-нуклеозид димера является таким же, как нуклеозид к 5'-концу хиральной межнуклеотидной линкерной группы, и 3'-нуклеозид димера является таким же, как нуклеозид к 3'-концу хиральной межнуклеотидной линкерной группы.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью представляет собой композицию, разработанную таким образом, чтобы она содержала несколько типов олигонуклеотидов. Согласно некоторым вариантам осуществления способы согласно настоящему раскрытию обеспечивают получение библиотеки олигонуклеотидов с контролируемой хиральностью, то есть предварительно выбранное количество любых одного или более типов олигонуклеотидов с контролируемой хиральностью можно смешивать с любыми одним или более типами олигонуклеотидов с контролируемой хиральностью для получения композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления предварительно выбранное количество типа олигонуклеотида представляет собой композицию, имеющую любое из описанных выше значений диастереомерной чистоты.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложены способы получения олигонуклеотида с контролируемой хиральностью, включающие стадии:
(1) сочетания;
(2) введения блокирующей группы;
(3) модификации;
(4) удаления блокирующей группы; и
(5) повторения стадий (1) - (4) до достижения желаемой длины.
При описании предложенных способов слово «цикл» имеет общепринятое значение, известное специалистам в данной области техники. Согласно некоторым вариантам осуществления одну последовательность стадий (1)-(4) называют циклом.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложены способы получения композиций олигонуклеотидов с контролируемой хиральностью, включающие стадии:
(a) обеспечения количества первого олигонуклеотида с контролируемой хиральностью; и
(b) необязательно обеспечения количества одного или более дополнительных олигонуклеотидов с контролируемой хиральностью.
Согласно некоторым вариантам осуществления первый олигонуклеотид с контролируемой хиральностью представляет собой олигонуклеотид, имеющий тип, такой как описано в настоящей заявке. Согласно некоторым вариантам осуществления один или более дополнительных олигонуклеотидов с контролируемой хиральностью представляют собой один или более олигонуклеотидов, имеющих типы, такие как описано в настоящей заявке.
Специалистам в соответствующих областях химии и синтеза должна быть понятна степень универсальности и контролирования структурных изменений и стереохимической конфигурации предложенного олигонуклеотида, синтезированного при помощи способов согласно настоящему раскрытию. Например, после завершения первого цикла можно проводить последующий цикл с применением нуклеотидного звена, отдельно выбранного для указанного последующего цикла, которое согласно некоторым вариантам осуществления содержит нуклеиновое основание и/или сахар, отличающиеся от нуклеинового основания и/или сахара, применяемого в первом цикле. Аналогично, хиральное вспомогательное вещество, применяемое на стадии сочетания в последующем цикле, может отличаться от хирального вспомогательного вещества, применяемого в первом цикле, то есть второй цикл обеспечивает получение фосфорсодержащей линкерной группы, имеющей отличающуюся стереохимическую конфигурацию. Согласно некоторым вариантам осуществления стереохимию атомов фосфора линкерных групп новой межнуклеотидной линкерной группы контролируют путем применения стереохимически чистых фосфорамидитов. Кроме того, агент модификации, применяемый на стадии модификации в последующем цикле, может отличаться от агента модификации, применяемого в первом или предшествующем цикле. Суммарное действие от указанного подхода с многократным встраиванием звеньев заключается в том, что в каждом компоненте предложенного олигонуклеотида можно с высокой степенью настраивать структуру и конфигурацию. Дополнительным преимуществом этого подхода является то, что стадия введения блокирующей группы минимизирует образование примесей «n-1», которые в иных случаях значительно затрудняют выделение предложенного олигонуклеотида, в частности олигонуклеотидов, имеющих большую длину.
Согласно некоторым вариантам осуществления иллюстративный цикл способа получения олигонуклеотидов с контролируемой хиральностью проиллюстрирован в иллюстративных схемах, описанных в настоящем раскрытии. Согласно некоторым вариантам осуществления цикл способа получения олигонуклеотидов с контролируемой хиральностью проиллюстрирован на схеме I. Согласно некоторым вариантам осуществления  представляет собой твердую подложку, и необязательно фрагмент растущего олигонуклеотида с контролируемой хиральностью присоединен к твердой подложке. Предложенное хиральное вспомогательное вещество имеет структуру формулы 3-I:
представляет собой твердую подложку, и необязательно фрагмент растущего олигонуклеотида с контролируемой хиральностью присоединен к твердой подложке. Предложенное хиральное вспомогательное вещество имеет структуру формулы 3-I:
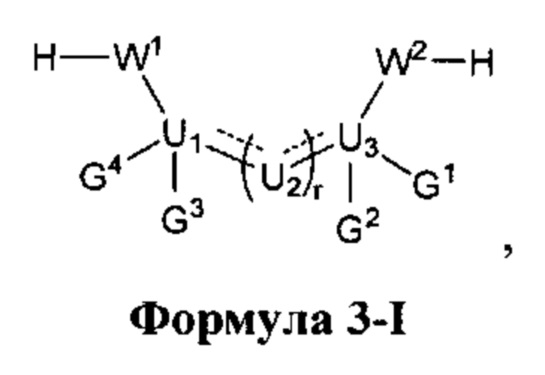
которая дополнительно описана ниже. «Сар» представляет собой любой химический фрагмент, присоединенный к атому азота на стадии введения блокирующей группы, а согласно некоторым вариантам осуществления представляет собой аминозащитную группу. Специалисты в данной области техники понимают, что в после начала первого цикла к твердой подложке может быть присоединен только один нуклеозид, и цикл необязательно можно завершать до удаления блокирующей группы. Специалистам в данной области техники должно быть понятно, что BPRO представляет собой защищенное основание, применяемое в синтезе олигонуклеотида. Каждая стадия цикла, изображенного на схеме I, дополнительно описана далее.
Схема I. Синтез олигонуклеотида с контролируемой хиральностью.
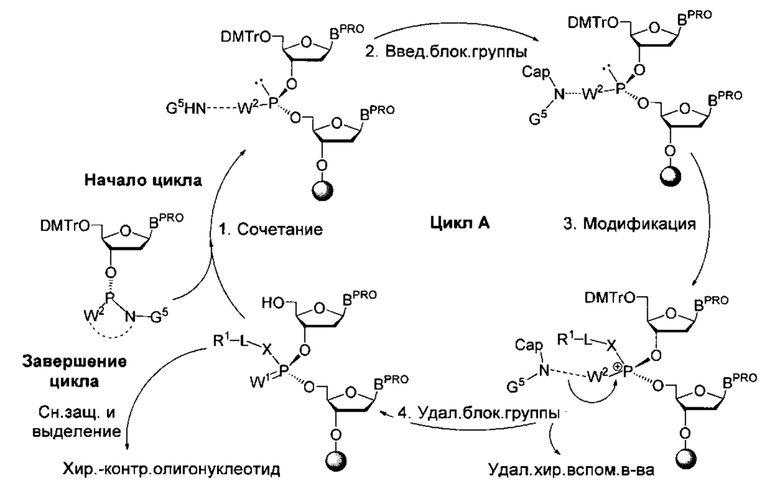
Синтез на твердой подложке
Согласно некоторым вариантам осуществления синтез предложенного олигонуклеотида проводят на твердой фазе. Согласно некоторым вариантам осуществления реакционно-способные группы, присутствующие в твердой подложке, защищены. Согласно некоторым вариантам осуществления реакционно-способные группы, присутствующие в твердой подложке, являются незащищенными. Во время синтеза олигонуклеотида твердую подложку обрабатывают различными реагентами в нескольких циклах синтеза для обеспечения постепенного увеличения растущей цепи олигонуклеотида за счет отдельных нуклеотидных звеньев. Нуклеозидное звено, расположенное в конце цепи, которое непосредственно связано с твердой подложкой, называют в настоящем описании «первым нуклеозидом». Первый нуклеозид связан с твердой подложкой посредством линкерного фрагмента, т.е. бирадикала, содержащего ковалентные связи между CPG, полимером или другой твердой подложкой и нуклеозидом. Линкерная группа не вступает во взаимодействия во время циклов синтеза, проводимых для построения цепи олигонуклеотида, и ее отщепляют после построения цепи для отделения олигонуклеотида от подложки.
Твердые подложки для твердофазного синтеза нуклеиновых кислот включают подложки, описанные, например, в патентах США №4659774, 5141813, 4458066; в патентах США №4415732, 4458066, 4500707, 4668777, 4973679 и 5132418 (автор Карутерс (Caruthers)); в патентах США №5047524, 5262530 (авторы Андрус (Andrus) с соавторами); и в патенте США №4725677 (замененный RE34069) (автор Костер (Koster)). Согласно некоторым вариантам осуществления твердая фаза представляет собой подложку органического полимера. Согласно некоторым вариантам осуществления твердая фаза представляет собой подложку неорганического полимера. Согласно некоторым вариантам осуществления подложка органического полимера представляет собой полистирол, аминометилполистирол, привитой сополимер полиэтиленгликоля-полистирола, полиакриламид, полиметакрилат, поливиниловый спирт, полимер с высокой степенью перекрестной сшивки (НРС) или другие синтетические полимеры, углеводы, такие как целлюлоза и крахмал или другие полимерные углеводы, или другие органические полимеры и сополимеры, композиционные материалы или комбинация приведенных выше неорганических или органических веществ. Согласно некоторым вариантам осуществления подложка неорганического полимера представляет собой оксид кремния, оксид алюминия, полимерное стекло с контролируемым размером пор (англ. controlled polyglass, CPG), которое представляет собой подложку силикагеля или аминопропил-CPG. Другие подходящие твердые подложки включают фтористые твердые подложки (см., например, международную заявку на патент WO/2005/070859), твердые подложки стекла с контролируемым размером пор (CPG), содержащего длинноцепочечный алкиламин (LCAA) (см., например, S.P. Adams, K.S. Kavka, Е.J. Wykes, S.В. Holder and G.R. Galluppi, J. Am. Chem. Soc., 1983, 105, 661-663; G.R. Gough, M.J. Bruden and P.T. Gilham, Tetrahedron Lett., 1981, 22, 4177-4180). Мембранные подложки и полимерные мембраны (см., например, Innovation and Perspectives in Solid Phase Synthesis, Peptides, Proteins and Nucleic Acids, ch 21 pp 157-162, 1994, Ed. Roger Epton и патент США №4923901) также подходят для синтеза нуклеиновых кислот. В полученную мембрану можно вводить химические функциональные группы для применения в синтезе нуклеиновых кислот. Помимо присоединения функциональной группы к мембране согласно некоторым вариантам осуществления также применяют линкерную или разделительную группу, присоединенную к мембране, для минимизации стерических затруднений между мембраной и синтезируемой цепью.
Другие подходящие твердые подложки включают те, что хорошо известны в данной области техники и подходят для применения в твердофазных методиках, включая, например, стекло, реализуемое как подложка PrimerTM 200, стекло с контролируемым размером пор (CPG), оксалилсодержащее стекло с контролируемым размером пор (см., например, Alul, et al., Nucleic Acids Research, 1991, 19, 1527), подложка TentaGel - подложка-производное аминополиэтиленгликоля (см., например, Wright, et al., Tetrahedron Lett., 1993, 34, 3373), и Poros - сополимер полистирола/дивинилбензола.
Было продемонстрировано применение поверхностно-активированных полимеров для использования в синтезе природных и модифицированных нуклеиновых кислот и белков на некоторых твердых подложках. Вещество твердой подложки может представлять собой любой полимер, имеющий подходящую однородную пористость, достаточное содержание аминогрупп и подходящую универсальность для возможности проведения любых операцию присоединения без потери целостности. Примеры подходящих выбранных веществ включают нейлон, полипропилен, сложный полиэфир, политетрафторэтилен, полистирол, поликарбонат и нитроцеллюлозу. В качестве твердой подложки в зависимости от решения изобретателя можно использовать и другие вещества. Если рассматривать некоторые решения, то можно выбирать металл с покрытием, в частности золото или платину (см., например, опубликованную заявку на патент США №20010055761). В одном из вариантов реализации синтеза олигонуклеотида, например, нуклеозид прикрепляют к твердой подложке, функционализированной гидроксильными или амино-остатками. В качестве альтернативы проводят превращение твердой подложки для обеспечения лабильной к действию кислот триалкокситритильной группы, такой как триметокситритильная группа (ТМТ). Не желая быть связанными теорией, ожидают, что наличие триалкокситритильной защитной группы позволяет проводить начальное детритилирование в условиях, обычно используемых в ДНК-синтезаторах. Для ускоренного высвобождения олигонуклеотидного материала в раствор водного аммиака в подложку необязательно вводят дигликолатную линкерную группу.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид в качестве альтернативы синтезируют в направлении от 5' до 3'. Согласно некоторым вариантам осуществления нуклеиновую кислоту присоединяют к твердой подложке через 5'-конец растущей нуклеиновой кислоты, т.е. с использованием 5'-нуклеозидфосфорамидатов или ферментной реакции (например, лигирования и полимеризации с использованием нуклеозид-5'-трифосфатов), таким образом, для взаимодействия предоставлена 3'-группа. Если рассматривать синтез в направлении от 5' до 3', то многократно повторяющиеся стадии согласно настоящему раскрытию остаются неизменными (т.е. введение блокирующих групп и модификация хиральных атомов фосфора).
Линкерный фрагмент
Линкерный фрагмент или линкерную группу необязательно используют для связывания твердой подложки с соединением, содержащим свободный нуклеофильный фрагмент. Известны подходящие линкерные группы, такие как короткоцепочечные молекулы, которые используют для соединения твердой подложки с функциональными группами (например, с гидроксильными группами) молекул исходных нуклеозидов в способах твердофазного синтеза. Согласно некоторым вариантам осуществления линкерный фрагмент представляет собой линкерную группу моноамида янтарной кислоты или сукцинатную линкерную группу (-СО-CH2-CH2-СО-) или оксалиловую линкерную группу (-СО-СО-). Согласно некоторым вариантам осуществления линкерный фрагмент и нуклеозид связаны друг с другом посредством сложноэфирной связи. Согласно некоторым вариантам осуществления линкерный фрагмент и нуклеозид связаны друг с другом посредством амидной связи. Согласно некоторым вариантам осуществления линкерный фрагмент связывает нуклеозид с другим нуклеотидом или нуклеиновой кислотой. Подходящие линкерные группы предложены, например, в Oligonucleotides And Analogues A Practical Approach, Ekstein, F. Ed., IRL Press, N.Y., 1991, Chapter 1 и в Solid-Phase Supports for Oligonucleotide Synthesis, Pon, R. Т., Curr. Prot. Nucleic Acid Chem., 2000, 3.1.1-3.1.28.
Линкерный фрагмент используют для связывания соединения, содержащего свободный нуклеофильный фрагмент, с другим нуклеозидом, нуклеотидом или нуклеиновой кислотой. Согласно некоторым вариантам осуществления линкерный фрагмент представляет собой фосфодиэфирную линкерную группу. Согласно некоторым вариантам осуществления линкерный фрагмент представляет собой H-фосфонатный фрагмент. Согласно некоторым вариантам осуществления линкерный фрагмент представляет собой модифицированную фосфорсодержащую линкерную группу, такую как описано в настоящей заявке. Согласно некоторым вариантам осуществления для присоединения олигонуклеотида к твердой подложке применяют универсальную линкерную группу (UnyLinker) (Ravikumar et al., Org. Process Res. Dev., 2008, 12 (3), 399-410). Согласно некоторым вариантам осуществления применяют другие универсальные линкерные группы (Pon, R. Т., Curr. Prot. Nucleic Acid Chem., 2000, 3.1.1-3.1.28). Согласно некоторым вариантам осуществления применяют различные ортогональные линкерные группы (такие как дисульфидные линкерные группы) (Pon, R. Т., Curr. Prot. Nucleic Acid Chem.,2000, 3.1.1-3.1.28).
Помимо всего прочего, настоящее раскрытие признает, что линкерная группа может быть выбрана или разработана так, чтобы быть совместимой с набором условий реакции, используемых для синтеза олигонуклеотидов. Согласно некоторым вариантам осуществления во избежание деградации олигонуклеотидов и во избежание десульфуризации вспомогательные группы избирательно удаляются перед удалением защитной группы. Согласно некоторым вариантам осуществления группа DPSE может избирательно удаляться ионами F-. Согласно некоторым вариантам осуществления настоящее раскрытие обеспечивает линкерные группы, которые стабильны в условиях удаления защитной группы DPSE, например 0,1 М TBAF в MeCN, 0,5 М HF-Et3N в ТГФ или MeCN и т.д. Согласно некоторым вариантам осуществления предложенная линкерная группа представляет собой линкерную группу SP. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что линкерная группа SP стабильна в условиях удаления защитной группы DPSE, например 0,1 М TBAF в MeCN, 0,5 М HF-Et3N в ТГФ или MeCN и т.д.; они также стабильны, например, в безводных основных условиях, таких как 1М DBU в MeCN.
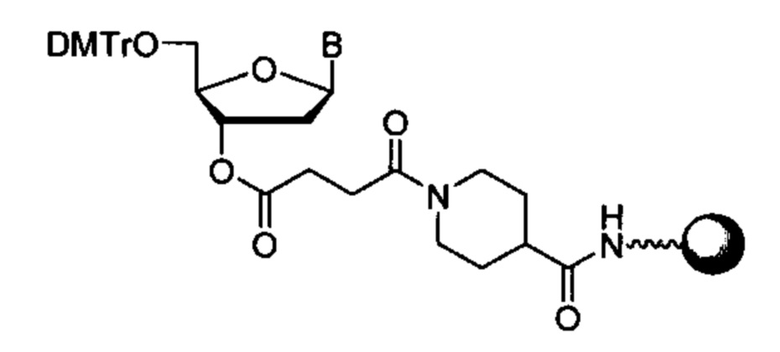
Сукцинил-пиперидиновая (SP) линкерная группа
Согласно некоторым вариантам осуществления иллюстративный линкер представляет собой:
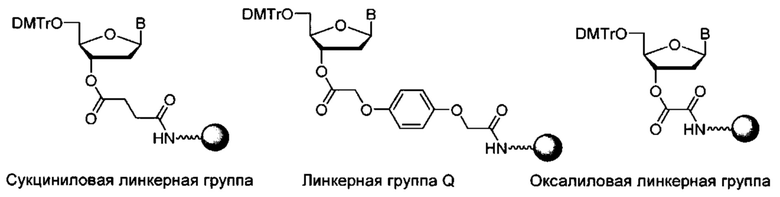
Согласно некоторым вариантам осуществления сукциниловая линкерная группа, линкерная группа Q или оксалиловая линкерная группа нестабильна в отношении одного или нескольких условий удаления защитной группы DPSE с использованием F-.
Общие условия - растворители для синтеза
Синтез предложенных олигонуклеотидов, в целом, проводят в апротонных органических растворителях. Согласно некоторым вариантам осуществления растворитель представляет собой нитрилсодержащий растворитель, такой как, например, ацетонитрил. Согласно некоторым вариантам осуществления растворитель представляет собой основный аминосодержащий растворитель, такой как, например, пиридин. Согласно некоторым вариантам осуществления растворитель представляет собой эфирный растворитель, такой как, например, тетрагидрофуран. Согласно некоторым вариантам осуществления растворитель представляет собой галогенированный углеводород, такой как, например, дихлорметан. Согласно некоторым вариантам осуществления применяют смесь растворителей. В определенных вариантах реализации растворитель представляет собой смесь любого одного или более описанных выше классов растворителей.
Согласно некоторым вариантам осуществления, если апротонный органический растворитель не является основным, то на стадии взаимодействия используют основание. Согласно некоторым вариантам осуществления, если присутствует основание, то оно представляет собой основный амин, такой как, например, пиридин, хинолин или N,N-диметиланилин. Примеры других основных аминов включают пирролидин, пиперидин, N-метилпирролидин, пиридин, хинолин, N,N-диметиламинопиридин (DMAP) или N,N-диметиланилин.
Согласно некоторым вариантам осуществления основание отличается от основного амина.
Согласно некоторым вариантам осуществления апротонный органический растворитель является безводным. Согласно некоторым вариантам осуществления безводный апротонный органический растворитель является свежеперегнанным. Согласно некоторым вариантам осуществления свежеперегнанный безводный апротонный растворитель представляет собой основный аминосодержащий растворитель, такой как, например, пиридин. Согласно некоторым вариантам осуществления свежеперегнанный безводный апротонный органический растворитель представляет собой эфирный растворитель, такой как, например, тетрагидрофуран. Согласно некоторым вариантам осуществления свежеперегнанный безводный апротонный органический растворитель представляет собой нитрилсодержащий растворитель, такой как, например, ацетонитрил.
Хиральный реагент/хиральное вспомогательное вещество
Согласно некоторым вариантам осуществления хиральные реагенты используются для обеспечения стереоселективности при производстве олигонуклеотидов с контролируемой хиральностью. Многие различные хиральные реагенты, также упомянутые специалистами в данной области техники и в настоящем документе как хиральные вспомогательные вещества, могут быть использованы в соответствии со способами настоящего раскрытия. Примеры таких хиральных реагентов описаны в настоящем документе и в Wada I, II и III, указанных выше. Согласно некоторым вариантам осуществления хиральный реагент представляет собой таковой, как описан так, как описано Wada I. Согласно некоторым вариантам осуществления хиральный реагент для использования в соответствии со способами настоящего изобретения относится к формуле 3-I ниже:
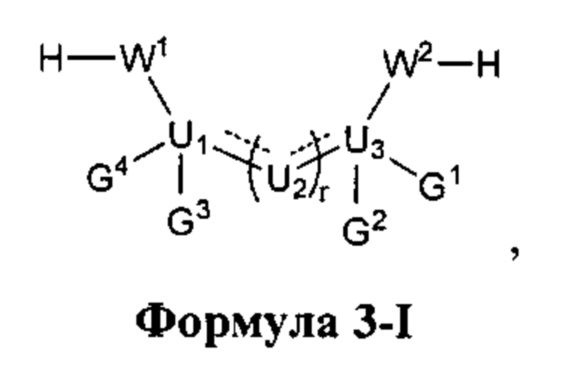
где W1 и W2 представляют собой любые из -О-, -S- или -NG5-, U1 и U3, представляют собой атомы углерода, которые связаны с U2, если они присутствуют, или друг с другом, если r равно 0, посредством одной, двойной или тройной связи. U2 представляет собой -С-, -CG8-, -CG8G8-, -NG8-, -N-, -О- или -S-, где r представляет собой целое число от 0 до 5 и не более двух гетероатомов являются смежными. Когда любой из U2 представляет собой С, тройная связь должна быть образована между вторым U2, который представляет собой С, или одним из U1 или U3. Аналогичным образом, когда любой из U2 представляет собой CG8, образуется двойная связь между вторым U2, который представляет собой -CG8- или -N-, или одним из U1 или U3.
Согласно некоторым вариантам осуществления -U1(G3G4)-(U2)r-U3(G1G2) представляет собой -CG3G4-CG1G2-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет собой -CG3=CG1-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет собой -С≡С-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет собой -CG3=CG8-CG1G2-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет -CG3G4-O-CG1G2-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет -CG3G4-NG8-CG1G2-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет -CG3G4-N-CG2-. Согласно некоторым вариантам осуществления -U1-(U2)r-U3- представляет -CG3G4-N=CG8-CG1G2-.
Как определено в настоящем документе, G1, G2, G3, G4, G5 и G8 независимо представляют собой водород или необязательно замещенную группу, выбранную из алкила, аралкила, циклоалкила, циклоалкилалкила, гетероциклила, гетероарила и арила; или два из G1, G2, G3, G4 и G5 представляют собой G6 (взятые вместе с образованием необязательно замещенного, насыщенного, частично ненасыщенного или ненасыщенного карбоциклического или гетероатомсодержащего кольца до примерно 20 кольцевых атомов, которое представляет собой моноциклическое или полициклическое, и представляет собой конденсированное или неконденсированное). Согласно некоторым вариантам осуществления образованное таким образом кольцо замещено фрагментами оксо, тиоксо, алкила, алкенила, алкинила, гетероарила или арила. Согласно некоторым вариантам осуществления, когда кольцо, образованное путем взятия двух G6 вместе, замещено, оно замещено фрагментом, который является достаточно объемным для обеспечения стереоселективности во время реакции.
Согласно некоторым вариантам осуществления кольцо, образованное путем взятия двух из G6 вместе, представляет собой необязательно замещенный циклопентил, пирролил, циклопропил, циклогексенил, циклопентенил, тетрагидропиранил или пиперазинил. Согласно некоторым вариантам осуществления кольцо, образованное путем взятия двух из G6 вместе, представляет собой необязательно замещенный циклопентил, пирролил, циклопропил, циклогексенил, циклопентенил, тетрагидропиранил, пирролидинил или пиперазинил.
Согласно некоторым вариантам осуществления G1 представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления G1 представляет собой фенил. Согласно некоторым вариантам осуществления G2 представляет собой метил или водород. Согласно некоторым вариантам осуществления G1 представляет собой необязательно замещенный фенил и G2 представляет собой метил. Согласно некоторым вариантам осуществления G1 представляет собой фенил и G2 представляет собой метил.
Согласно некоторым вариантам осуществления г равно 0.
Согласно некоторым вариантам осуществления W1 представляет собой -NG5-. Согласно некоторым вариантам осуществления один из G3 и G4 взят вместе с G5 с образованием необязательно замещенного пирролидинилового кольца. Согласно некоторым вариантам осуществления один из G3 и G4 взят вместе с G5 с образованием пирролидинилового кольца.
Согласно некоторым вариантам осуществления W2 представляет собой -О-.
Согласно некоторым вариантам осуществления хиральный реагент представляет собой соединение формулы 3-АА:
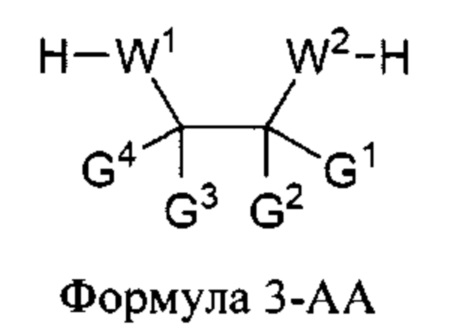
где каждая переменная представляет собой независимо таковую, как определено выше и описано в настоящем документе.
Согласно некоторым вариантам осуществления формулы 3АА W1 и W2 независимо представляют собой -NG5-, -О- или -S-; G1, G2, G3, G4 и G5 независимо представляют собой водород или необязательно замещенную группу, выбранную из алкила, аралкила, циклоалкила, циклоалкилалкила, гетероциклила, гетероарила или арила; или два из G1, G2, G3, G4 и G5 представляют собой G6 (взятые вместе с образованием необязательно замещенного насыщенного, частично ненасыщенного или ненасыщенного карбоциклического или гетероатомсодержащего кольца до примерно 20 атомов в кольце, которое представляет собой моноциклическое или полициклическое, и представляет собой конденсированное или неконденсированное), и не более четырех из G1, G2, G3, G4 и G5 представляют собой G6. Аналогично соединениям формулы 3-I любой из G1, G2, G3, G4 или G5 необязательно замещен фрагментами оксо, тиоксо, алкила, алкенила, алкинила, гетероарила или арила. Согласно некоторым вариантам осуществления такая замена индуцирует стереоселективность в производстве олигонуклеотида с контролируемой хиральностью.
Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 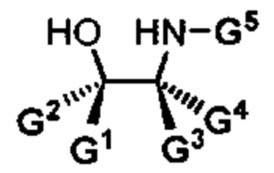 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 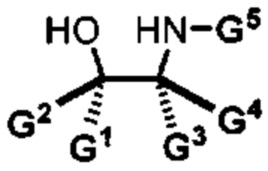 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 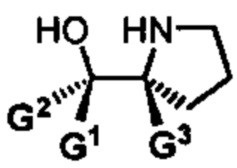 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 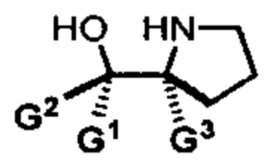 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 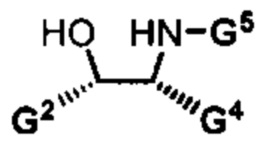 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 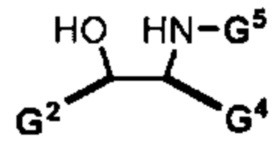 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 
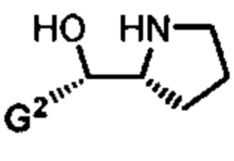 . Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 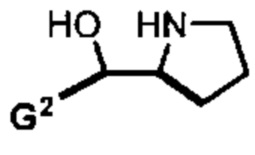 .
.
Согласно некоторым вариантам осуществления W1 представляет собой -NG5, W2 представляет собой О, каждый из G1 и G3 независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного С1-10, G2 представляет собой -C(R)2Si(R)3, a G4 и G5 взятые вместе с образованием необязательно замещенного насыщенного, частично ненасыщенного или ненасыщенного гетероатомсодержащего кольца до примерно 20 кольцевых атомов, которое является моноциклическим или полициклическим, конденсированным или не конденсированным. Согласно некоторым вариантам осуществления каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, карбоциклильного, арильного, гетероарильного и гетероциклильного C1-С6. Согласно некоторым вариантам осуществления G2 представляет собой -C(R)2Si(R)3, где -C(R)2- представляет собой необязательно замещенный -СН2-, и каждый R в -Si(R)3 независимо представляет собой необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного С1-10. Согласно некоторым вариантам осуществления по меньшей мере один R-Si(R)3 независимо представляет собой необязательно замещенный С1-10 алкил. Согласно некоторым вариантам осуществления по меньшей мере один R-Si(R)3 независимо представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления один R-Si(R)3 независимо представляет собой необязательно замещенный фенил, и каждый из двух других R независимо представляет собой необязательно замещенный C1-10 алкил. Согласно некоторым вариантам осуществления один R-Si(R)3 независимо представляет собой необязательно замещенный C1-10 алкил, и каждый из двух других R независимо представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления G2 необязательно замещен -CH2Si(Ph)(Me)2. Согласно некоторым вариантам осуществления G2 необязательно замещен -CH2Si(Me)(Ph)2. Согласно некоторым вариантам осуществления G2 представляет собой -CH2Si(Me)(Ph)2. Согласно некоторым вариантам осуществления G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-6-членного кольца, содержащего один атом азота (к которому присоединен G5). Согласно некоторым вариантам осуществления G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота. Согласно некоторым вариантам осуществления G1 представляет собой водород. Согласно некоторым вариантам осуществления G3 представляет собой водород. Согласно некоторым вариантам осуществления как G1, так и G3 представляют собой водород.
Согласно некоторым вариантам осуществления хиральный реагент имеет одну из следующих формул:
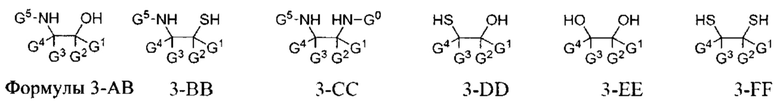
Согласно некоторым вариантам осуществления хиральный реагент представляет собой аминоспирт. Согласно некоторым вариантам осуществления хиральный реагент представляет собой аминотиол. Согласно некоторым вариантам осуществления хиральный реагент представляет собой аминофенол. В некоторых вариантах хиральный реагент представляет собой (S)- и (R)-2-метиламино-1-фенилэтанол, (1R, 2S)-эфедрин или (1R, 2S)-2-метиламино-1,2-дифенилэтанол.
Согласно некоторым вариантам осуществления настоящего раскрытия хиральный реагент представляет собой соединение одной из следующих формул:
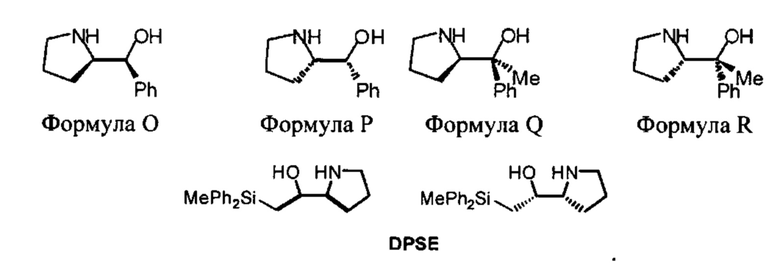
Как показано в настоящем документе, при использовании для получения хиральной межнуклеотидной линкерной группы, чтобы получить стереоселективность, как правило, используют стереохимически чистые хиральные реагенты. Среди прочего, настоящее раскрытие предусматривает стереохимически чистые хиральные реагенты, включая те, которые имеют описанные структуры.
Выбор хирального реагента, например изомера, представленного формулой Q, или его стереоизомера, формулы R, позволяет осуществлять специфический контроль хиральности при атоме фосфора линкерной группы. Таким образом, в каждом синтетическом цикле может быть выбрана конфигурация Rp или Sp, позволяющая контролировать общую трехмерную структуру олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью имеет все стереоцентры Rp.Согласно некоторым вариантам осуществления настоящего раскрытия олигонуклеотид с контролируемой хиральностью имеет все стереоцентры Sp.Согласно некоторым вариантам осуществления настоящего раскрытия каждый атом фосфора линкерной группы в олигонуклеотиде с контролируемой хиральностью независимо представляет собой Rp или Sp.Согласно некоторым вариантам осуществления настоящего раскрытия каждый атом фосфора линкерной группы в олигонуклеотиде с контролируемой хиральностью независимо представляет собой Rp или Sp, и по меньшей мере один представляет собой Rp и по меньшей мере один представляет собой Sp. Согласно некоторым вариантам осуществления выбор центров Rp и Sp производится для придания конкретной трехмерной суперструктуры олигонуклеотиду с контролируемой хиральностью. Примеры таких выборок описаны в настоящем документе более подробно.
Согласно некоторым вариантам осуществления хиральный реагент для использования в соответствии с настоящим раскрытием выбирается для его способности к удалению на конкретной стадии вышеописанного цикла. Например, согласно некоторым вариантам осуществления желательно удалить хиральный реагент на этапе модификации атома фосфора линкерной группы. Согласно некоторым вариантам осуществления желательно удалить хиральный реагент перед стадией модификации атома фосфора линкерной группы. Согласно некоторым вариантам осуществления желательно удалить хиральный реагент после стадии модификации атома фосфора линкерной группы. Согласно некоторым вариантам осуществления желательно удалить хиральный реагент после первой стадии связывания, но до того, как произошла вторая стадия связывания, так что хиральный реагент отсутствует на растущем олигонуклеотиде во время второго связывания (а также для дополнительных последующих стадий связывания). Согласно некоторым вариантам осуществления хиральный реагент удаляется во время реакции «деблокирования», которая возникает после модификации атома фосфора линкерной группы, но до начала последующего цикла. Примеры способов и реагентов для удаления описаны в настоящем документе.
Согласно некоторым вариантам осуществления удаление хирального вспомогательного вещества достигается при выполнении стадии модификации и/или удаления блокирующей группы, как показано на схеме I. Может быть полезно сочетать удаление хирального вспомогательного вещества вместе с другими преобразованиями, такими как модификация и удаление блокирующей группы. Специалисту в данной области техники было бы понятно, что сохраненные стадии/трансформация могут улучшить общую эффективность синтеза, например, в отношении выхода и чистоты продукта, особенно для более длинных олигонуклеотидов. Один пример, в котором хиральное вспомогательное вещество удаляется во время модификации и/или удаления блокирующей группы, проиллюстрирован на схеме I.
Согласно некоторым вариантам осуществления хиральный реагент для использования в соответствии со способами настоящего раскрытия отличается тем, что он является удаляемым при определенных условиях. Например, согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться в кислых условиях. Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться в слабокислых условиях. Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться посредством реакции элиминации Е1 (например, удаление происходит посредством образования промежуточного катиона на хиральном реагенте в кислых условиях, заставляя хиральный реагент отщепляться от олигонуклеотида). Согласно некоторым вариантам осуществления хиральный реагент характеризуется тем, что он имеет структуру, которая признана способной обеспечивать или облегчать реакцию элиминации Е1. Специалисты в соответствующих областях техники оценят, какие структуры будут рассматриваться как подверженные таким реакциям ликвидации.
Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться нуклеофилом. Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться аминовым нуклеофилом. Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться нуклеофилом, отличным от амина.
Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться основанием. Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться амином. Согласно некоторым вариантам осуществления хиральный реагент выбирают по его способности удаляться основанием, отличным от амина.
Дополнительные хиральные вспомогательные вещества и их использование можно найти, например, в Wada I (JP 4348077; WO 2005/014609; WO 2005/092909), Wada II (WO 2010/064146), Wada III (WO 2012/039448), Chiral Control (WO 2010/064146), etc.
Активация
Ахиральный H-фосфонатный фрагмент обрабатывают первым активирующим реагентом с образованием первого промежуточного вещества. В одном из вариантов реализации первый активирующий реагент добавляют в реакционную смесь на стадии конденсации. Применение первого активирующего реагента зависит от условий взаимодействия, таких как растворители, используемые для взаимодействия. Примерами первого активирующего реагента являются фосген, трихлорметилхлорформиат, бис(трихлорметил)карбонат (ВТС), оксалилхлорид, Ph3PCl2, (PhO)3PCl2, N,N'-бис(2-оксо-3-оксазолидинил)фосфинхлорид (BopCl), гексафторфосфат 1,3-диметил-2-(3-нитро-1,2,4-триазол-1-ил)-2-пирролидин-1-ил-1,3,2-диазафосфолидиния (MNTP) или гексафторфосфат 3-нитро-1,2,4-триазол-1-ил-трис(пирролидин-1-ил)фосфония (PyNTP).
Примером ахирального H-фосфонатного фрагмента является соединение, показанное на приведенной выше схеме. DBU представляет собой 1,8-диазабицикло[5.4.0]ундец-7-ен. H+DBU может представлять собой, например, ион аммония, ион алкиламмония, ион гетероароматического иминия или ион гетероциклического иминия, каждый из которых может быть первичным, вторичным, третичным или четвертичным, или одновалентный ион металла.
Взаимодействие с хиральным реагентом
После первой стадии активации активированные ахиральный H-фосфонатный фрагмент подвергают взаимодействию с хиральным реагентом, представленным формулой (Z-I) или (Z-I') с образованием хирального промежуточного вещества формулы (Z-Va), (Z-Vb), (Z-Va') или (Z-Vb').
Стадия стереоспецифической конденсации
Хиральное промежуточное вещество формулы (Z-Va), (Z-Vb), (Z-Va') или (Z-Vb') обрабатывают вторым активирующим реагентом и нуклеозидом с образованием промежуточного вещества конденсации. Нуклеозид может быть обеспечен на твердой подложке. Примерами второго активирующего реагента являются 4,5-дицианоимидазол (DCI), 4,5-дихлоримидазол, трифлат 1-фенилимидазолия (PhIMT), трифлат бензимидазолия (BIT), бензтриазол, 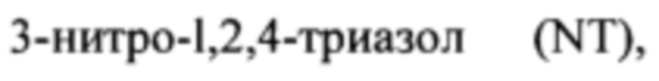 тетразол, 5-этилтиотетразол (ЕТТ), 5-бензилтиотетразол (ВТТ), 5-(4-нитрофенил)тетразол, трифлат N-цианометилпирролидиния (СМРТ), трифлат N-цианометилпиперидиния, трифлат N-цианометилдиметиламмония Хиральное промежуточное вещество формулы Z-Va ((Z-Vb), (Z-Va') или (Z-Vb')) можно выделять в качестве мономера. Как правило, хиральное промежуточное вещество Z-Va ((Z-Vb), (Z-Va') или (Z-Vb')) не выделяют и используют для взаимодействия с нуклеозидом или модифицированным нуклеозидом в том же сосуде для обеспечения хирального фосфитного соединения, промежуточного вещества конденсации. В других вариантах реализации, если способ проводят как твердофазный синтез, твердую подложку, содержащую соединение, отфильтровывают от побочных продуктов, примесей и/или реагентов.
тетразол, 5-этилтиотетразол (ЕТТ), 5-бензилтиотетразол (ВТТ), 5-(4-нитрофенил)тетразол, трифлат N-цианометилпирролидиния (СМРТ), трифлат N-цианометилпиперидиния, трифлат N-цианометилдиметиламмония Хиральное промежуточное вещество формулы Z-Va ((Z-Vb), (Z-Va') или (Z-Vb')) можно выделять в качестве мономера. Как правило, хиральное промежуточное вещество Z-Va ((Z-Vb), (Z-Va') или (Z-Vb')) не выделяют и используют для взаимодействия с нуклеозидом или модифицированным нуклеозидом в том же сосуде для обеспечения хирального фосфитного соединения, промежуточного вещества конденсации. В других вариантах реализации, если способ проводят как твердофазный синтез, твердую подложку, содержащую соединение, отфильтровывают от побочных продуктов, примесей и/или реагентов.
Стадия введения блокирующей группы
Если конечная нуклеиновая кислота имеет размер крупнее димера, то в непрореагировавший фрагмент -ОН вводят блокирующую группу, и хиральную вспомогательную группу в соединении также можно маскировать блокирующей группой с образованием промежуточного вещества конденсации с блокирующими группами. Если конечная нуклеиновая кислота представляет собой димер, то стадия введения блокирующей группы является необязательной.
Стадия модификации
Соединение модифицируют путем взаимодействия с электрофилом. Промежуточное вещество конденсации с блокирующими группами можно обрабатывать на стадии модификации. Согласно некоторым вариантам осуществления стадию модификации проводят с применением серосодержащего электрофила, селеносодержащего электрофила или борирующего агента. Примерами стадий модификации являются стадии окисления и сульфуризации.
Согласно некоторым вариантам осуществления способа серосодержащий электрофил представляет собой соединение, имеющее одну из следующих формул:
S8 (формула Z-B), Zz1-S-S-Zz2 или Zz1-S-Vz-Zz2;
где Zz1 и Zz2 независимо представляют собой алкил, аминоалкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси, гетероарилокси, ацил, амид, имид или тиокарбонил, или Zz1 и Zz2 объединены с образованием 3-8-членного алициклического или гетероциклического кольца, которое может быть замещенным или незамещенным; Vz представляет собой SO2, О или NRf; a Rf представляет собой водород, алкил, алкенил, алкинил или арил.
Согласно некоторым вариантам осуществления способа серосодержащий электрофил представляет собой соединение следующих формул Z-A, Z-B, Z-C, Z-D, Z-E или Z-F:
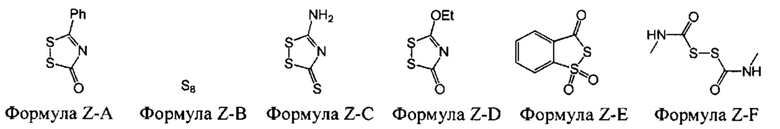
Согласно некоторым вариантам осуществления реагент сульфурирования представляет собой 3-фенил-1,2,4-дитиазолин-5-он.
Согласно некоторым вариантам осуществления селеносодержащий электрофил представляет собой соединение, имеющее одну из следующих формул:
Se (формула Z-G), Zz3-Se-Se-Zz4 или Zz3-Se-Vz-Zz4;
где Zz3 и Zz4 независимо представляют собой алкил, аминоалкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси, гетероарилокси, ацил, амид, имид или тиокарбонил, или Zz3 и Zz4 объединены с образованием 3-8-членного алициклического или гетероциклического кольца, которое может быть замещенным или незамещенным; Vz представляет собой SO2, S, О или NRf; а Rf представляет собой водород, алкил, алкенил, алкинил или арил.
Согласно некоторым вариантам осуществления селеносодержащий электрофил представляет собой соединение формулы Z-G, Z-H, Z-I, Z-J, Z-K или Z-L.
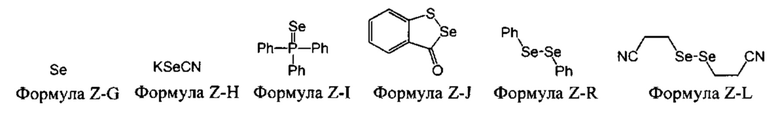
Согласно некоторым вариантам осуществления борирующий агент представляет собой боран-N,N-диизопропилэтиламин (ВН3-DIPEA), боран-пиридин (ВН3-Ру), боран-2-хлорпиридин (ВН3-СРу), боран-анилин (ВН3-An), боран-тетрагидрофуран (ВН3-ТГФ) или боран диметилсульфид (ВН3-Me2S).
Согласно некоторым вариантам осуществления после стадии модификации хиральная вспомогательная группа отпадает от растущей олигонуклеотидной цепи. Согласно некоторым вариантам осуществления после стадии модификации хиральная вспомогательная группа остается связанной с межнуклеотидным атомом фосфора.
Согласно некоторым вариантам осуществления способа стадия модификации представляет собой стадию окисления. Согласно некоторым вариантам осуществления способа стадия модификации представляет собой стадию окисления, при котором используют условия, схожие с теми, что описаны выше в настоящей заявке. Согласно некоторым вариантам осуществления стадия окисления является такой, как описано, например, в заявке на патент Японии 2010-265304 А и международной заявке на патент WO 2010/064146.
Цикл роста цепи и стадия снятия защиты
Для удаления блокирующей группы при 5'-конце растущей цепи нуклеиновой кислоты и обеспечения соединения проводят «деблокировку» промежуточного вещества конденсации с блокирующими группами. Соединение необязательно повторно используют в цикле роста цепи для получения промежуточного вещества конденсации, промежуточного вещества конденсации с блокирующими группами, модифицированного промежуточного вещества конденсации с блокирующими группами и модифицированного промежуточного вещества с блокирующими группами и удаленной защитной группой в положении 5'. После проведения одного цикла роста цепи проводят дополнительное удаление блокирующих групп в модифицированном промежуточном веществе с блокирующими группами и удаленной защитной группой в положении 5' путем удаления хирального вспомогательного лиганда и других защитных групп, например, защитных групп нуклеинового основания, модифицированного нуклеинового основания, сахара и модифицированного сахара, для обеспечения нуклеиновой кислоты. В других вариантах реализации нуклеозид, содержащий фрагмент 5'-ОН, представляет собой промежуточное вещество, полученное в предшествующем цикле роста цепи, как описано в настоящей заявке. В других вариантах реализации нуклеозид, содержащий фрагмент 5'-ОН, представляет собой промежуточное вещество, полученное при помощи другого известного способа синтеза нуклеиновой кислоты. В тех вариантах реализации, где применяют твердую подложку, затем проводят отщепление нуклеиновой кислоты с модифицированным атомом фосфора от твердой подложки. В определенных вариантах реализации нуклеиновые кислоты остаются присоединенными к твердой подложке для проведения очистки, а после очистки их отщепляют от твердой подложки.
В других вариантах реализации нуклеозид, содержащий фрагмент 5'-ОН, представляет собой промежуточное вещество, полученное при помощи другого известного способа синтеза нуклеиновой кислоты. В других вариантах реализации нуклеозид, содержащий фрагмент 5'-ОН, представляет собой промежуточное вещество, полученное при помощи другого известного способа нуклеиновой кислоты, такого как описано в настоящей заявке. В других вариантах реализации нуклеозид, содержащий фрагмент 5'-ОН, представляет собой промежуточное вещество, полученное при помощи другого известного способа синтеза нуклеиновой кислоты, включающего один или более циклов, проиллюстрированных на схеме I. В других вариантах реализации нуклеозид, содержащий фрагмент 5'-ОН, представляет собой промежуточное вещество, полученное при помощи другого известного способа синтеза нуклеиновой кислоты, включающего один или более циклов, проиллюстрированных на схеме I-b, I-е или I-d.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложены способы синтеза олигонуклеотидов, в которых применяют стабильные и коммерчески доступные вещества в качестве исходных веществ. Согласно некоторым вариантам осуществления в настоящем раскрытии предложены способы синтеза олигонуклеотидов для получения стереоконтролируемых производных олигонуклеотидов с модифицированным атомом фосфора с применением ахирального исходного вещества.
Согласно некоторым вариантам осуществления способ согласно настоящему раскрытию не приводит к разложению на стадиях удаления защитных групп. Кроме того, способ не требует применения специальных блокирующих агентов для получения производных олигонуклеотидов с модифицированным атомом фосфора.
Реагент конденсации
Реагенты конденсации (CR), подходящие в соответствии со способами согласно настоящему изобретению, имеют любую из следующих общих формул:
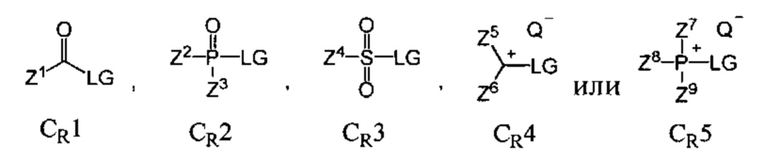
где Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8 и Z9 независимо представляют собой необязательно замещенную группу, выбранную из алкила, аминоалкила, циклоалкила, гетероцикла, циклоалкилалкила, гетероциклоалкила, арила, гетероарила, алкилокси, арилокси или гетероарилокси, или любые из Z2 и Z3, Z5 и Z6, Z7 и Z8, Z8 и Z9, Z9 и Z7 или Z7 и Z8 и Z9 объединены с образованием 3-20-членного алициклического или гетероциклического кольца; Q- представляет собой анион; a LG представляет собой уходящую группу.
Согласно некоторым вариантам осуществления противоион в реагенте конденсации CR представляет собой Cl-, Br-, BF4-, PF6-, TfO-, Tf2N-, AsF6- ClO4- или SbF6-, где Tf представляет собой CF3SO2. Согласно некоторым вариантам осуществления уходящая группа в реагенте конденсации CR представляет собой F, Cl, Br, I, 3-нитро-1,2,4-триазол, имидазол, алкилтриазол, тетразол, пентафторбензол или 1-гидроксибензотриазол.
Примеры реагентов конденсации, применяемых в соответствии со способами согласно настоящему раскрытию включают, но не ограничиваются ими, пентафторбензоилхлорид, карбонилдиимидазол (CDI), 1-мезитиленсульфонил-3-нитротриазол (MSNT), гидрохлорид 1-этил-3-(3'-диметиламинопропил)карбодиимида (EDCI-HCl), гексафторфосфат бензотриазол-1-илокси-трис(диметиламино)фосфония (РуВОР), хлорид N,N'-бис(2-оксо-3-оксазолидин)фосфина (BopCl), гексафторфосфат 2-(1H-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония (HATU) и гексафторфосфат О-бензотриазол-N,N,N',N'-тетраметилурония (HBTU), DIPCDI; бромид N,N'-бис(2-оксо-3-оксазолидинил)фосфина (BopBr), гексафторфосфат 1,3-диметил-2-(3-нитро-1,2,4-триазол-1-ил)-2-пирролидин-1-ил-1,3,2-диазафосфолидиния (MNTP), гексафторфосфат 3-нитро-1,2,4-триазол-1-ил-трис(пирролидин-1-ил)фосфония (PyNTP), гексафторфосфат бромтрипирролидинофосфония (PyBrOP); тетрафторборат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (TBTU); и гексафторфосфат тетраметилфторформамидиния (TFFH). В определенных вариантах реализации противоион в реагенте конденсации CR представляет собой Cl-, Br-, BF4-, PF6-, TfO-, Tf2N-, AsF6-, ClO4- или SbF6-, где Tf представляет собой CF3SO2.
Согласно некоторым вариантам осуществления реагент конденсации представляет собой 1-(2,4,6-триизопропилбензолсульфонил)-5-(пиридин-2-ил)тетразолид, пивалоилхлорид, гексафторфосфат бромтриспирролидинофосфония, хлорид N,N'-бис(2-оксо-3-оксазолидинил)фосфина (BopCl) или 2-хлор-5,5-диметил-2-оксо-1,3,2-диоксафосфинат. Согласно некоторым вариантам осуществления реагент конденсации представляет собой хлорид N,N'-бис(2-оксо-3-оксазолидинил)фосфина (BopCl). Согласно некоторым вариантам осуществления реагент конденсации выбран из тех, что описаны в международной заявке на патент WO/2006/066260).
Согласно некоторым вариантам осуществления реагент конденсации представляет собой гексафторфосфат 1,3-диметил-2-(3-нитро-1,2,4-триазол-1-ил)-2-пирролидин-1-ил-1,3,2-диазафосфолидиния (MNTP) или гексафторфосфат 3-нитро-1,2,4-триазол-1-ил-трис(пирролидин-1-ил)фосфония (PyNTP):
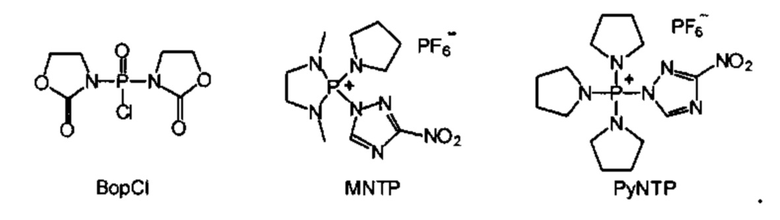
Выбор основания и сахара для нуклеозидного партнера по реакции сочетания
Согласно настоящему описанию нуклеозидные партнеры по реакции сочетания для применения в соответствии со способами согласно настоящему раскрытию могут быть одинаковыми или могут отличаться друг от друга. Согласно некоторым вариантам осуществления нуклеозидные партнеры по реакции сочетания для применения в синтезе предложенного олигонуклеотида имеют одинаковую структуру и/или стереохимическую конфигурацию друг с другом. Согласно некоторым вариантам осуществления каждый нуклеозидный партнер по реакции сочетания для применения в синтезе предложенного олигонуклеотида имеет структуру и/или стереохимическую конфигурацию, отличающуюся от определенных других нуклеозидных партнеров по реакции сочетания в олигонуклеотиде. Примеры нуклеиновых оснований и Сахаров для применения в соответствии со способами согласно настоящему раскрытию описаны в настоящей заявке. Специалистам в родственных областях химии и синтеза будет понятно, что любая комбинация нуклеиновых оснований и Сахаров, описанных в настоящей заявке, предложена для применения в соответствии со способами согласно настоящему раскрытию.
Стадия сочетания:
Примеры способов сочетания и хиральные реагенты и реагенты конденсации для применения согласно настоящему изобретению приведены, помимо прочего, в Wada I (патент Японии 4348077; международные заявки на патент WO 2005/014609; WO 2005/092909), Wada II (WO 2010/064146), Wada III (WO 2012/039448) и хиральный контроль (международная заявка на патент WO 2010/064146). Хиральные нуклеозидные партнеры по реакции сочетания для применения согласно настоящему раскрытию также называют в настоящем описании «амидиты Wada». Согласно некоторым вариантам осуществления партнер по реакции сочетания имеет структуру 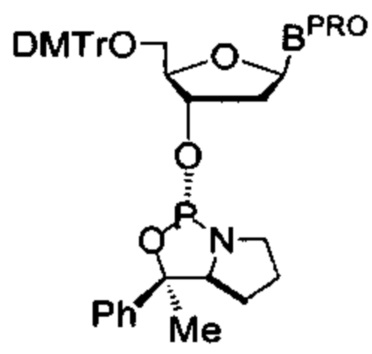 , где BPRO представляет собой защищенное нуклеиновое основание. Согласно некоторым вариантам осуществления партнер по реакции сочетания имеет структуру
, где BPRO представляет собой защищенное нуклеиновое основание. Согласно некоторым вариантам осуществления партнер по реакции сочетания имеет структуру 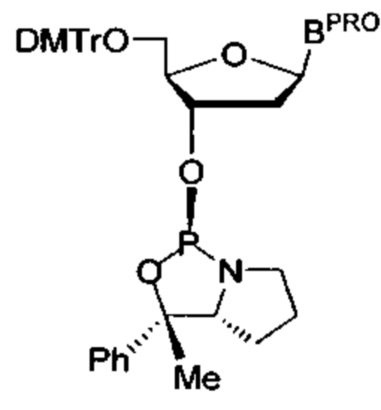 , где BPRO представляет собой защищенное нуклеиновое основание. Согласно некоторым вариантам осуществления партнер по по реакции сочетания имеет структуру
, где BPRO представляет собой защищенное нуклеиновое основание. Согласно некоторым вариантам осуществления партнер по по реакции сочетания имеет структуру 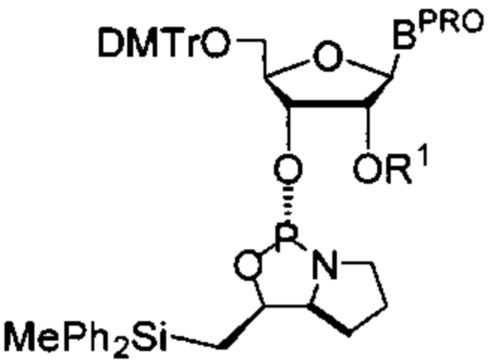 , где BPRO представляет собой защищенное нуклеиновое основание, и R1 такой, как определено и описано в настоящем документе. Согласно некоторым вариантам осуществления партнер по реакции сочетания имеет структуру
, где BPRO представляет собой защищенное нуклеиновое основание, и R1 такой, как определено и описано в настоящем документе. Согласно некоторым вариантам осуществления партнер по реакции сочетания имеет структуру 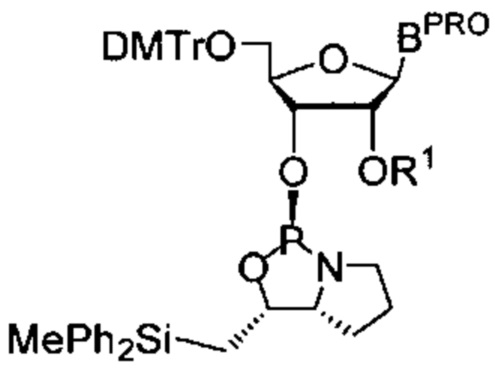 , где BPRO представляет собой защищенное нуклеиновое основание, и R1 такой, как определено и описано в настоящем документе. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный C1-6 алкил. Согласно некоторым вариантам осуществления R1 представляет собой Me.
, где BPRO представляет собой защищенное нуклеиновое основание, и R1 такой, как определено и описано в настоящем документе. Согласно некоторым вариантам осуществления R1 представляет собой необязательно замещенный C1-6 алкил. Согласно некоторым вариантам осуществления R1 представляет собой Me.
Пример хиральных фосфорамидитов в качестве партнера по реакции сочетания изображен ниже:
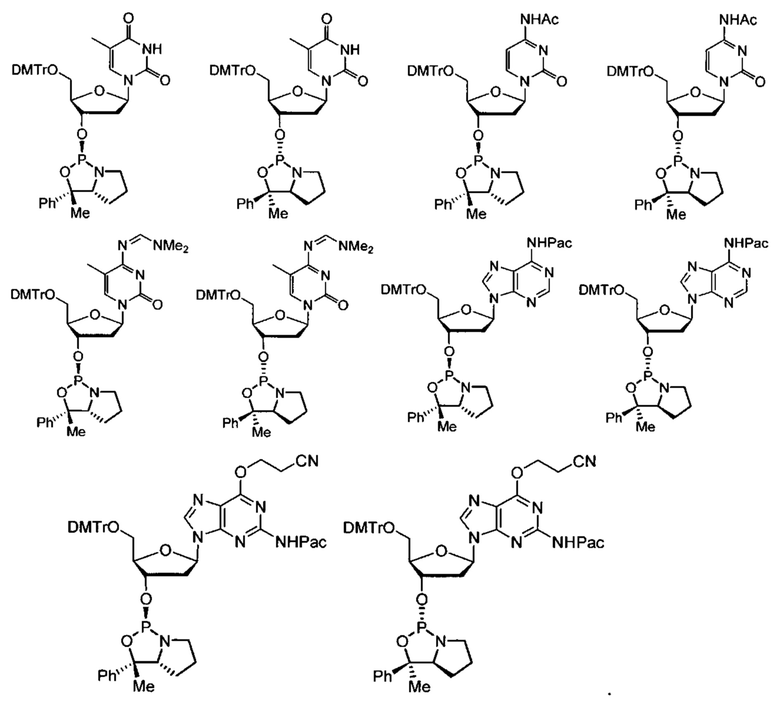
Дополнительные примеры описаны в Хиральном контроле (международная заявка на патент WO 2010/064146).
Один из способов, применяемых для синтеза партнера по реакции сочетания, изображен ниже на схеме II.
Схема II. Пример способа синтеза партнера по реакции сочетания.
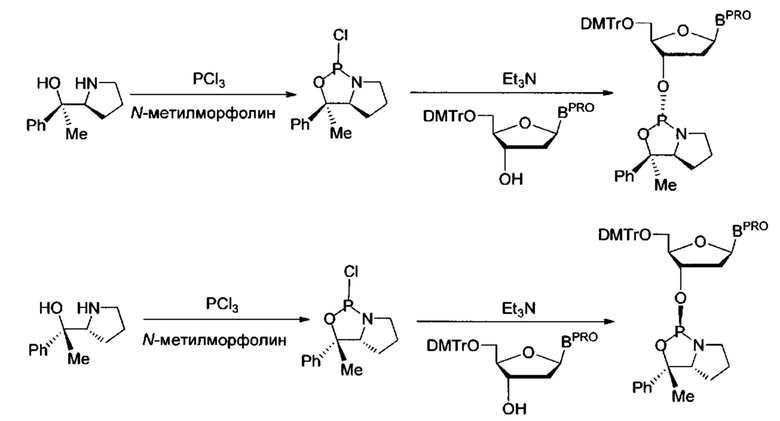
Согласно некоторым вариантам осуществления стадия сочетания включает взаимодействие свободной гидроксильной группы нуклеотидного звена олигонуклеотида с нуклеозидным партнером по реакции сочетания в условиях, подходящих для протекания сочетания. Согласно некоторым вариантам осуществления стадии сочетания предшествует стадия удаления блокирующей группы. Например, согласно некоторым вариантам осуществления 5'-гидрокс ильная группа растущего олигонуклеотида заблокирована (т.е. является защищенной), и для последующего взаимодействия с нуклеозидным партнером по реакции сочетания необходимо удаление блокирующей группы.
После удаления блокирующей группы соответствующей гидроксильной группы растущего олигонуклеотида подложку промывают и сушат для последующей доставки раствора, содержащего хиральный реагент, и раствора, содержащего активатор. Согласно некоторым вариантам осуществления хиральный реагент и активатор доставляют одновременно. Согласно некоторым вариантам осуществления совместная доставка включает доставку количества хирального реагента в растворе (например, в растворе фосфорамидита) и количества активатора в растворе (например, в растворе СМРТ) в полярном апротонном растворителе, таком как нитрилсодержащий растворитель (например, ацетонитрил).
Согласно некоторым вариантам осуществления стадия сочетания обеспечивает композицию неочищенного продукта, в которой хиральный фосфитный продукт содержится в диастереомерном избытке >95%. Согласно некоторым вариантам осуществления хиральный фосфитный продукт содержится в диастереомерном избытке >96%. Согласно некоторым вариантам осуществления хиральный фосфитный продукт содержится в диастереомерном избытке >97%. Согласно некоторым вариантам осуществления хиральный фосфитный продукт содержится в диастереомерном избытке >98%. Согласно некоторым вариантам осуществления хиральный фосфитный продукт содержится в диастереомерном избытке >99%.
Стадия введения блокирующей группы:
Предложенные способы получения олигонуклеотидов с контролируемой хиральностью включают стадию введения блокирующей группы. Согласно некоторым вариантам осуществления стадия введения блокирующей группы включает единственную стадию. Согласно некоторым вариантам осуществления стадия введения блокирующей группы включает две стадии. Согласно некоторым вариантам осуществления стадия введения блокирующей группы включает более двух стадий.
Согласно некоторым вариантам осуществления стадия введения блокирующей группы включает стадии введения блокирующей группы к свободному амину хирального вспомогательного вещества и введения блокирующей группы к любым оставшимся непрореагировавшим 5'-гидроксильным группам. Согласно некоторым вариантам осуществления свободный амин хирального вспомогательного вещества и непрореагировавшие 5'-гидроксильные группы защищают при помощи одинаковых блокирующих групп. Согласно некоторым вариантам осуществления свободный амин хирального вспомогательного вещества и непрореагировавшие 5'-гидроксильные группы защищают при помощи различных блокирующих групп. В определенных вариантах реализации введение различных блокирующих групп обеспечивает селективное удаление одной блокирующей группы, но не другой, во время синтеза олигонуклеотида. Согласно некоторым вариантам осуществления введение обеих блокирующих групп проводят одновременно. Согласно некоторым вариантам осуществления введение обеих блокирующих групп проводят последовательно.
В определенных вариантах реализации введение блокирующей группы, которое проводят последовательно, включает первую стадию введения блокирующей группы свободного амина и последующую вторую стадию введения блокирующей группы свободной 5'-гидроксильной группы, где блокировку свободного амина и 5'-гидроксильной группы проводят с использованием одинаковых блокирующих групп. Например, согласно некоторым вариантам осуществления блокировку свободного амина хирального вспомогательного вещества проводят с использованием ангидрида (например, ангидрида феноксиуксусной кислоты, т.е. Pac2O), а затем при помощи того же ангидрида проводят блокировку 5'-гидроксильной группы. В определенных вариантах реализации блокировку 5'-гидроксильной группы проводят с использованием того же ангидрида, но в отличающихся условиях (например, в присутствии одного или более дополнительных реагентов). Согласно некоторым вариантам осуществления введение блокирующей группы 5'-гидроксильной группы проводят в присутствии основного амина в эфирном растворителе (например, NMI (N-метилимидазол) в ТГФ). Фразу «блокирующая группа» используют в настоящем описании взаимозаменяемо с фразами «защитная группа» и «группа блокировки».
Согласно некоторым вариантам осуществления блокирующая группа амина характеризуется тем, что она эффективно блокирует амин и, таким образом, предотвращает перегруппировку и/или разложение промежуточных фосфитных частиц. Согласно некоторым вариантам осуществления блокирующую группу выбирают с учетом возможности защиты амина хирального вспомогательного вещества для предотвращения внутримолекулярного отщепления межнуклеотидной линкерной группы по атому фосфора.
Согласно некоторым вариантам осуществления блокирующая группа 5'-гидроксильной группы характеризуется тем, что она эффективно блокирует гидроксильную группу и, таким образом, предотвращает получение «шортмеров» (англ. «shortmer»), например, примесей «n-m» (m и n представляют собой целые числа, причем m<n; n представляет собой количество оснований в целевом олигонуклеотиде), образующихся в результате взаимодействия с участием цепи олигонуклеотида, которая не вступает во взаимодействие во время первого цикла, но вступает во взаимодействие в одном или более последующих циклах. Наличие указанных шортмеров, в частности «n-1» отрицательно влияет на чистоту неочищенного олигонуклеотида и делает трудоемкой и в целом низкоэффективной конечную очистку олигонуклеотида.
Согласно некоторым вариантам осуществления конкретную блокирующую группу выбирают с учетом способности опосредовать взаимодействия определенного типа в определенных условиях. Например, согласно некоторым вариантам осуществления блокирующую группу выбирают с учетом способности опосредовать реакцию элиминирования Е1, где происходит отщепление блокирующей группы и/или вспомогательного вещества от растущего олигонуклеотида. Согласно некоторым вариантам осуществления блокирующую группу выбирают с учетом способности опосредовать реакцию элиминирования Е2, где происходит отщепление блокирующей группы и/или вспомогательного вещества от растущего олигонуклеотида. Согласно некоторым вариантам осуществления блокирующую группу выбирают с учетом способности опосредовать реакцию β-элиминирования, где происходит отщепление блокирующей группы и/или вспомогательного вещества от растущего олигонуклеотида.
Стадия модификации:
Согласно настоящему описанию фразы «стадия модификации», «модифицирующая стадия» и «стадия модификации Р», которые используют взаимозаменяемо, относятся в целом к любой одной или более стадиям, применяемым для встраивания модифицированной межнуклеотидной линкерной группы. Согласно некоторым вариантам осуществления модифицированная межнуклеотидная линкерная группа имеет структуру формулы I. Стадию модификации Р согласно настоящему раскрытию проводят во время получения предложенного олигонуклеотида, но не после завершения получения предложенного олигонуклеотида. Таким образом, можно модифицировать атом фосфора линкерной группы каждого нуклеотидного звена предложенного олигонуклеотида по отдельности во время цикла встраивания нуклеотидного звена.
Согласно некоторым вариантам осуществления подходящий реагент модификации Р представляет собой серосодержащий электрофил, селеносодержащий электрофил, кислородсодержащий электрофил, борирующий реагент или азидный реагент.
Например, согласно некоторым вариантам осуществления селеносодержащий реагент представляет собой элементный селен, соль селена или замещенный диселенид.
Согласно некоторым вариантам осуществления кислородсодержащий электрофил представляет собой элементный кислород, пероксид или замещенный пероксид. Согласно некоторым вариантам осуществления борирующий агент представляет собой боран-амин (например, N,N-диизопропилэтиламин (BH3⋅DIPEA), боран-пиридин (ВН3⋅Ру), боран-2-хлорпиридин (ВН3⋅СРу), боран-анилин (ВН3⋅An)), реагент боран-простой эфир (например, боран-тетрагидрофуран (ВН3⋅ТГФ)), реагент боран-диалкилсульфид (например, BH3⋅Me2S), анилин-цианоборан или трифенилфосфин-карбоалкоксиборан. Согласно некоторым вариантам осуществления азидный реагент содержит азидную группу, которую впоследствии можно восстанавливать до аминогруппы.
Согласно некоторым вариантам осуществления реагент модификации Р представляет собой реагент сульфуризации, такой как описано в настоящей заявке. Согласно некоторым вариантам осуществления стадия модификации включает сульфуризацию атома фосфора для обеспечения фосфоротиоатной линкерной группы или фосфоротиоатной сложной триэфирной линкерной группы. Согласно некоторым вариантам осуществления стадия модификации обеспечивает олигонуклеотид, содержащий межнуклеотидные линкерные группы формулы I.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложены реагенты сульфуризации и способы их получения и применения.
Согласно некоторым вариантам осуществления указанные реагенты сульфуризации представляют собой тиосульфонатные реагенты. Согласно некоторым вариантам осуществления тиосульфонатный реагент имеет структуру формулы S-I:
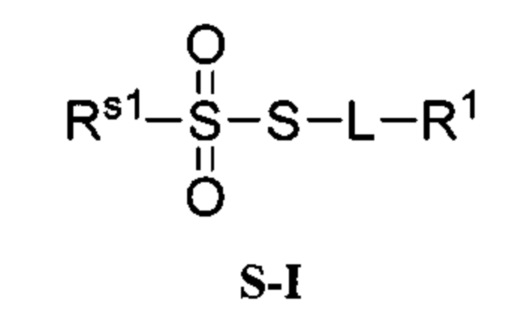
где:
Rs1 представляет собой R и
каждый из R, L и R1 независимо является таким, как определено и описано выше в настоящей заявке.
Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой бис(тиосульфонатный) реагент. Согласно некоторым вариантам осуществления бис(тиосульфонатный) реагент имеет структуру формулы S-II:
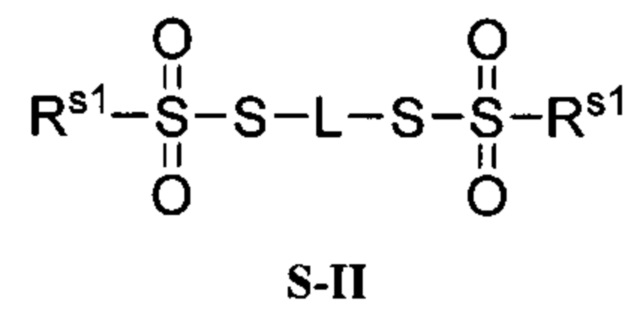
где каждый из Rs1 и L независимо является таким, как определено и описано выше в настоящей заявке.
Согласно приведенному выше общему определению Rs1 представляет собой R, где R является таким, как определено и описано выше в настоящей заявке. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенную алифатическую группу, арил, гетероциклил или гетероарил. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенный ал кил. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенный алкил. Согласно некоторым вариантам осуществления Rs1 представляет собой метил. Согласно некоторым вариантам осуществления Rs1 представляет собой цианометил. Согласно некоторым вариантам осуществления Rs1 представляет собой нитрометил. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенный арил. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления Rs1 представляет собой фенил. Согласно некоторым вариантам осуществления Rs1 представляет собой n-нитрофенил. Согласно некоторым вариантам осуществления Rs1 представляет собой n-метилфенил. Согласно некоторым вариантам осуществления Rs1 представляет собой n-хлорфенил. Согласно некоторым вариантам осуществления Rs1 представляет собой о-хлорфенил. Согласно некоторым вариантам осуществления Rs1 представляет собой 2,4,6-трихлорфенил. Согласно некоторым вариантам осуществления Rs1 представляет собой пентафторфенил. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенный гетероциклил. Согласно некоторым вариантам осуществления Rs1 представляет собой необязательно замещенный гетероарил.
Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 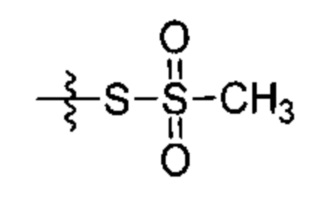 (MTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S-представляет собой
(MTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S-представляет собой 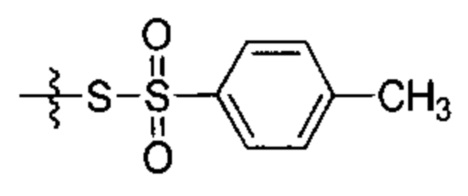 (TTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(TTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 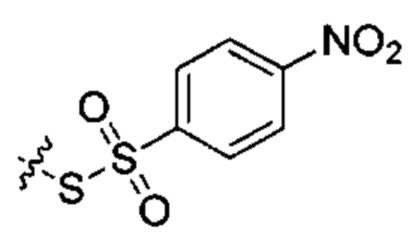 (NO2PheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(NO2PheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 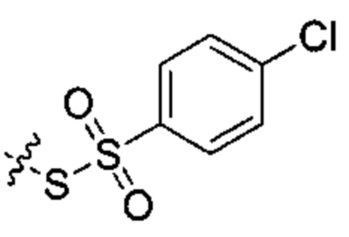 (р-ClPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(р-ClPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 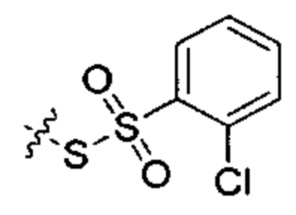 (o-ClPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(o-ClPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 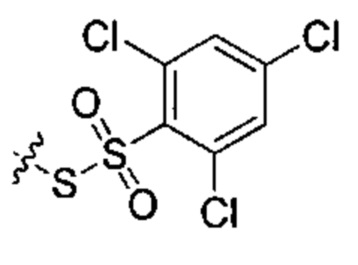 (2,4,6-TriClPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(2,4,6-TriClPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 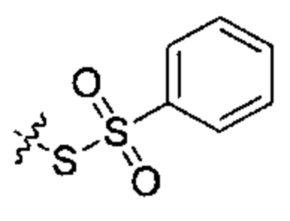 (PFPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(PFPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 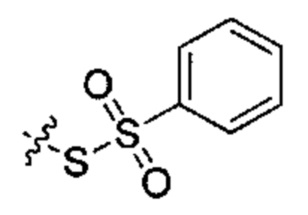 (PFPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(PFPheTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 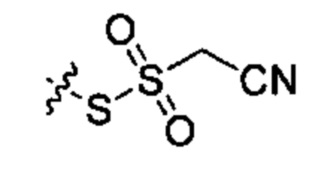 (a-CNMTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(a-CNMTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 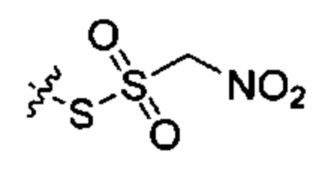 (a-NO2MTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(a-NO2MTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 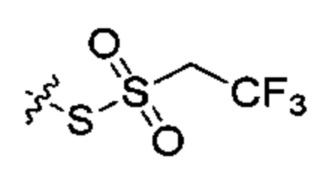 (a-CF3MTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(a-CF3MTS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 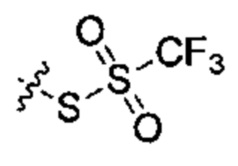 (а-CF3TS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(а-CF3TS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 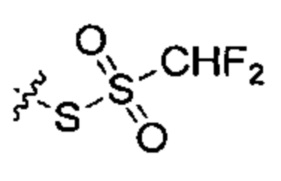 (a-CHF2TS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой
(a-CHF2TS). Согласно некоторым вариантам осуществления Rs1-S(O)2S- представляет собой 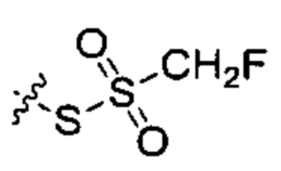 (a-CH2FTS).
(a-CH2FTS).
Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где L представляет собой -S-RL3- или -S-C(O)-RL3-. Согласно некоторым вариантам осуществления L представляет собой -S-RL3- или -S-C(O)-RL3-, где RL3 представляет собой необязательно замещенный C1-С6 алкилен. Согласно некоторым вариантам осуществления L представляет собой -S-RL3- или -S-C(O)-RL3-, где RL3 представляет собой необязательно замещенный C1-С6 алкенилен. Согласно некоторым вариантам осуществления L представляет собой -S-RL3- или -S-C(O)-RL3-, где RL3 представляет собой необязательно замещенный C1-С6 алкилен, причем одно или более метиленовых звеньев возможно и независимо заменены на необязательно замещенный C1-С6 алкенилен, арилен или гетероарилен. Согласно некоторым вариантам осуществления RL3 представляет собой необязательно замещенный -S-(C1-C6 алкенилен)-, -S-(C1-C6 алкинилен)-, -S-(C1-C6 алкилен)-арилен-(С1-С6 алкилен)-, -S-CO-арилен-(C1-С6 алкилен)- или -S-CO-(C1-C6 алкилен)-арилен-(С1-С6 алкилен)-. Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где L представляет собой -S-RL3- или -S-C(O)-RL3-, а атом серы присоединен к R1.
Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где L представляет собой алкилен, алкенилен, арилен или гетероарилен.
Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где L представляет собой 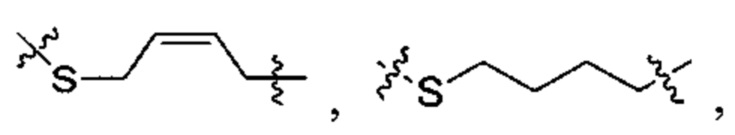
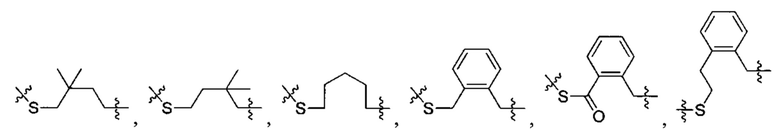 или
или 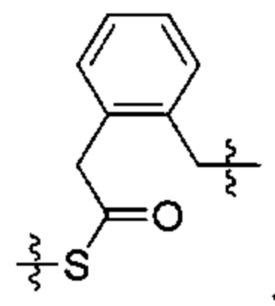 . Согласно некоторым вариантам осуществления L представляет собой
. Согласно некоторым вариантам осуществления L представляет собой 
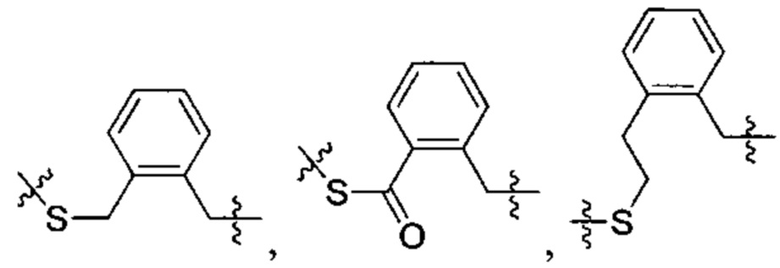 , или
, или 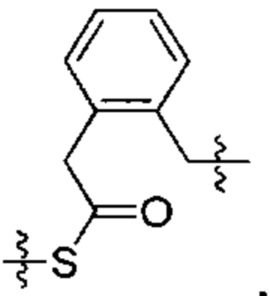 , где атом серы соединен с R1.
, где атом серы соединен с R1.
Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где R1 представляет собой 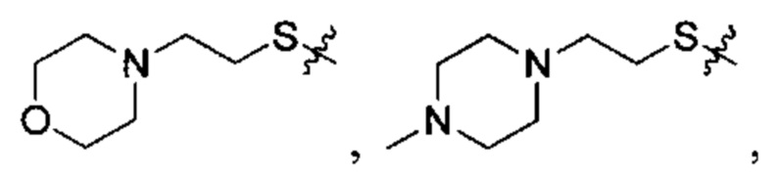
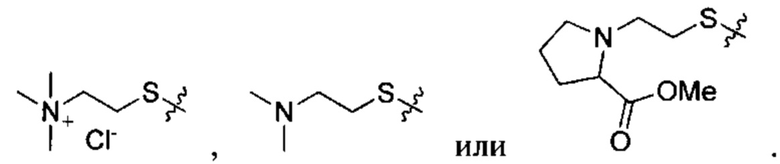 Согласно некоторым вариантам осуществления R1 представляет собой
Согласно некоторым вариантам осуществления R1 представляет собой 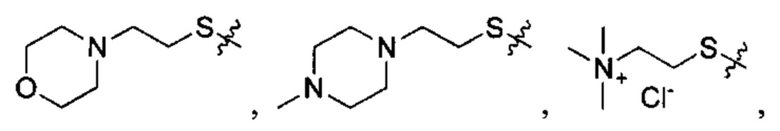
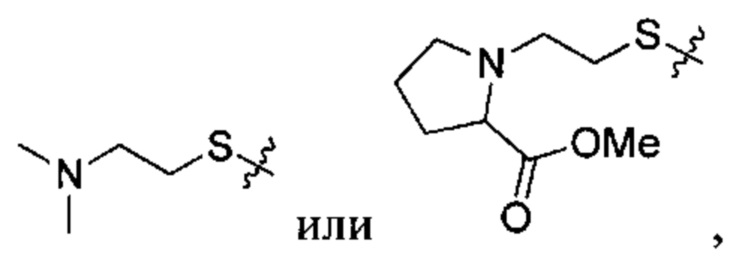 где атом серы соединен с L.
где атом серы соединен с L.
Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где L представляет собой 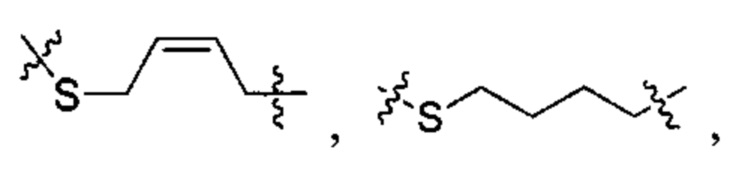
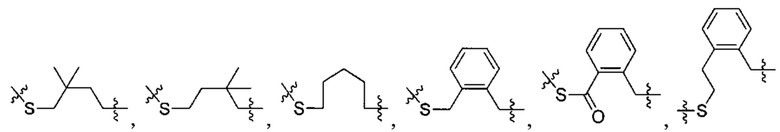 или
или 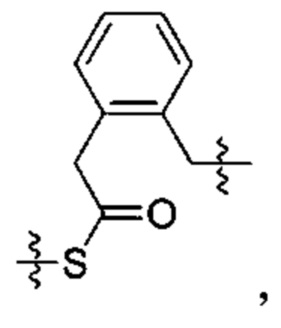 причем атом серы соединен с R1; a R1 представляет собой
причем атом серы соединен с R1; a R1 представляет собой 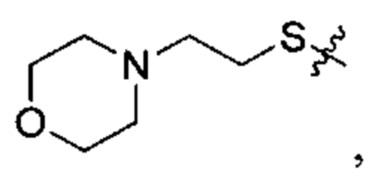
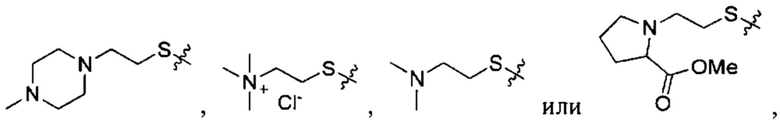 причем атом серы соединен с L.
причем атом серы соединен с L.
Согласно некоторым вариантам осуществления реагент сульфуризации имеет структуру S-I или S-II, где R1 представляет собой -S-RL2, причем RL2 является таким, как определено выше и описано в настоящей заявке. Согласно некоторым вариантам осуществления RL2 представляет собой необязательно замещенную группу, выбранную из -S-(C1-C6 алкилен)-гетероциклила, -S-(C1-C6 алкенилен)-гетероциклила, -S-(C1-C6 алкилен)-N(R')2, -S-(C1-C6 алкилен)-N(R')3, где каждый R' является таким, как определено выше и описано в настоящей заявке.
Согласно некоторым вариантам осуществления -L-R1 представляет собой -RL3-S-S-RL2, где каждая переменная независимо является такой, как определено выше и описано в настоящей заявке. Согласно некоторым вариантам осуществления -L-R1 представляет собой -RL3-C(O)-S-S-RL2, где каждая переменная независимо является такой, как определено выше и описано в настоящей заявке.
Примеры бис(тиосульфонатных) реагентов формулы S-II изображены ниже:
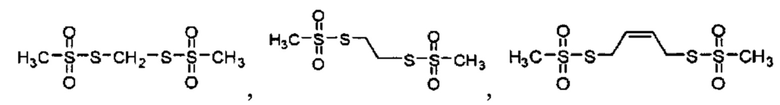
Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой соединение, имеющее одну из следующих формул:
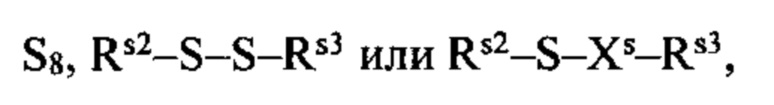
где:
каждый из Rs2 и Rs3 независимо представляет собой необязательно замещенную группу, выбранную из алифатической группы, аминоалкила, карбоциклила, гетероциклила, гетероциклоалкила, арила, гетероарила, алкилокси, арилокси, гетероарилокси, ацила, амида, имида или тиокарбонила; или
Rs2 и Rs3 объединены с атомами, к которым они присоединены, с образованием необязательно замещенного гетероциклического или гетероарильного кольца;
Xs представляет собой -S(O)2-, -О- или -N(R')- и
R' является таким, как определено и описано выше в настоящей заявке.
Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой 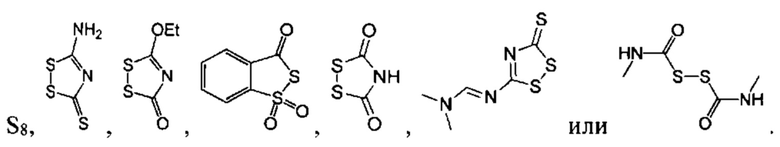 Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой
Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой 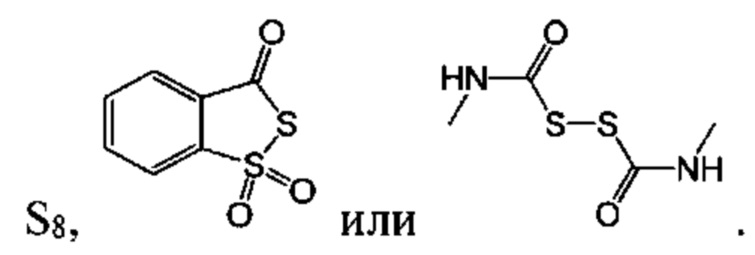 Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой
Согласно некоторым вариантам осуществления реагент сульфуризации представляет собой 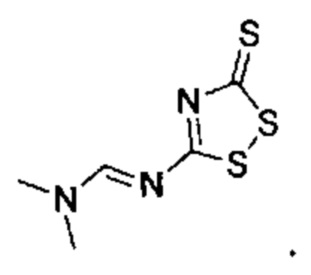
Примеры реагентов сульфуризации изображены ниже в таблице 5.
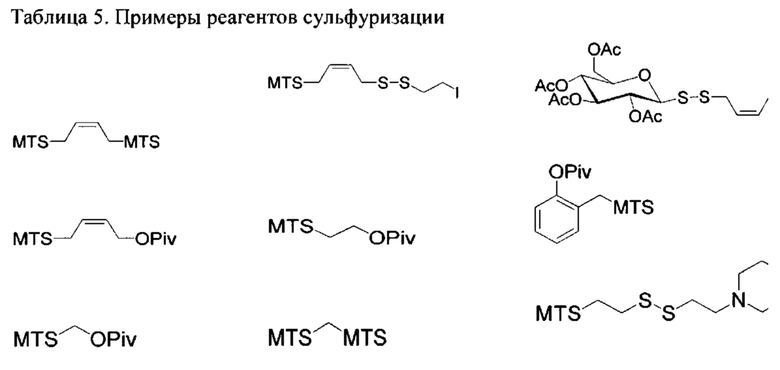
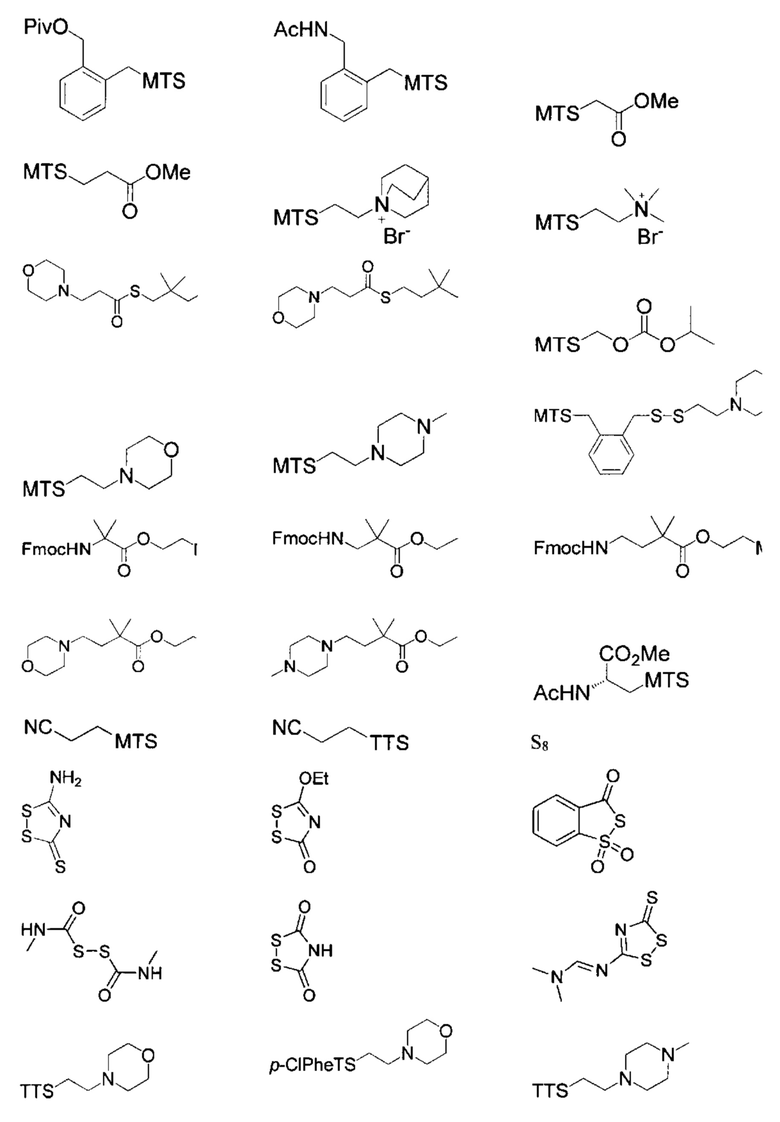
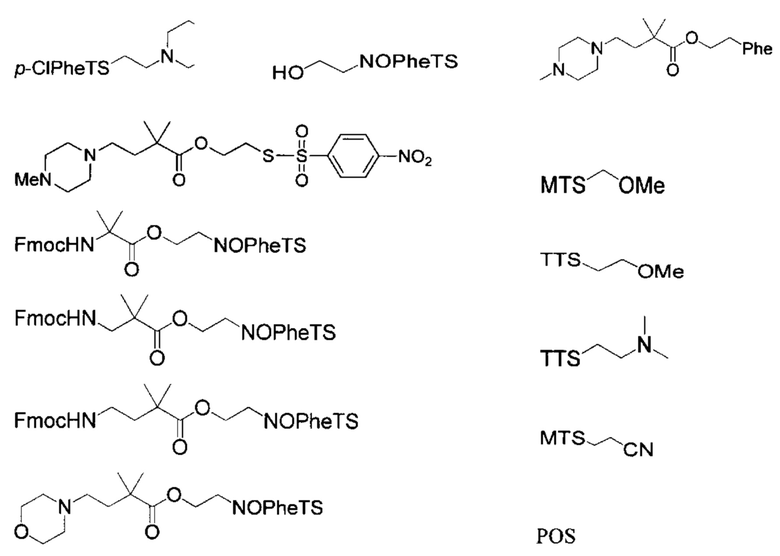
Согласно некоторым вариантам осуществления предложенный реагент сульфуризации применяют для модификации Н-фосфоната. Например, согласно некоторым вариантам осуществления Н-фосфонатный олигонуклеотид синтезируют, например, при помощи способов, описанных в Wada I или Wada II, и модифицируют с применением реагента сульфуризации формулы S-I или S-II:
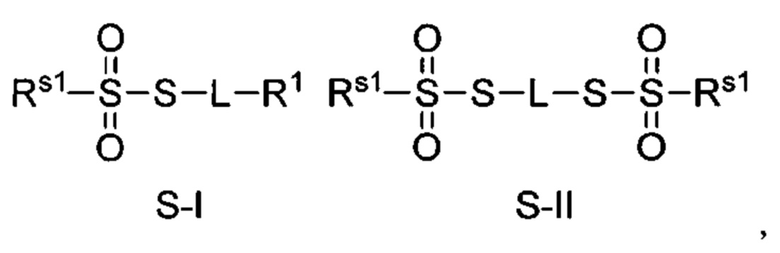
где каждый из Rs1, L и R1 являются такими, как описано и определено выше в настоящей заявке.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложен способ синтеза фосфоротиоатного сложного триэфира, включающий стадии:
i) взаимодействия Н-фосфоната со структурой:
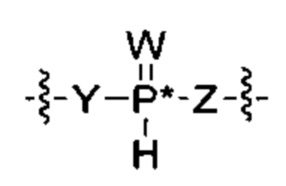
где каждый из W, Y и Z является таким, как описано и определено выше в настоящей заявке, с силилирующим агентом для обеспечения силилоксифосфоната; и
ii) взаимодействия силилоксифосфоната с реагентом сульфуризации со структурой S-I или S-II:
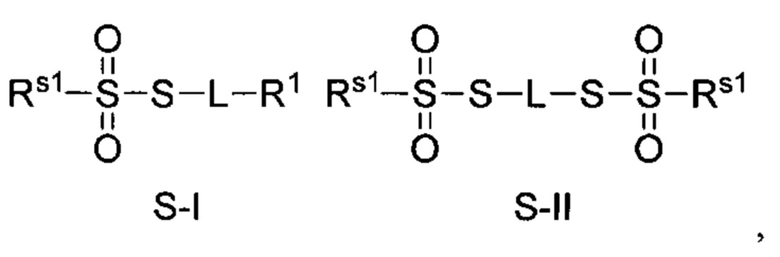
для обеспечения фосфоротиоатного сложного триэфира.
Согласно некоторым вариантам осуществления для модификации межнуклеотидной линкерной группы применяют селеносодержащий электрофил вместо реагента сульфуризации. Согласно некоторым вариантам осуществления селеносодержащий электрофил представляет собой соединение, имеющее одну из следующих формул:
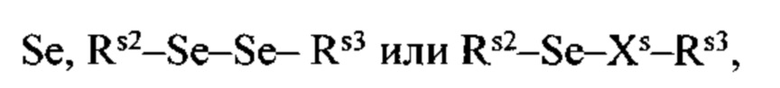
где:
каждый из Rs2 и Rs3 независимо представляет собой необязательно замещенную группу, выбранную из алифатической группы, аминоалкила, карбоциклила, гетероциклила, гетероциклоалкила, арила, гетероарила, алкилокси, арилокси, гетероарилокси, ацила, амида, имида или тиокарбонила; или
Rs2 и Rs3 объединены с атомами, к которым они присоединены, с образованием необязательно замещенного гетероциклического или гетероарильного кольца;
Xs представляет собой -S(O)2-, -О- или -N(R')-; и
R' является таким, как определено и описано выше в настоящей заявке.
В других вариантах реализации селеносодержащий электрофил представляет собой соединение, выбранное из Se, KSeCN, 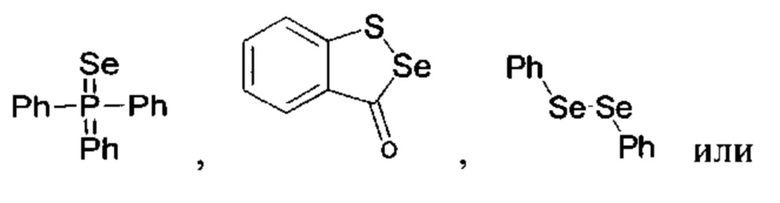
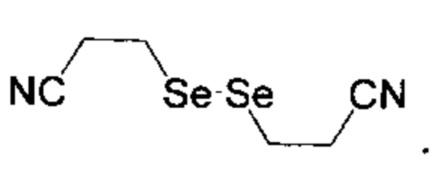 Согласно некоторым вариантам осуществления селеносодержащий электрофил представляет собой Se или
Согласно некоторым вариантам осуществления селеносодержащий электрофил представляет собой Se или 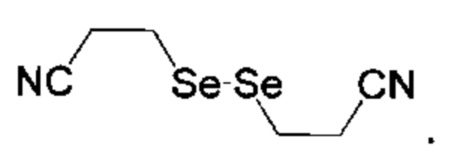
Согласно некоторым вариантам осуществления реагент сульфуризации для применения согласно настоящему раскрытию характеризуется тем, что фрагмент, переносимый на атом фосфора во время сульфуризации, представляет собой замещенный атом серы (например, -SR), но не просто атом серы (например, -S- или =S).
Согласно некоторым вариантам осуществления реагент сульфуризации для применения согласно настоящему раскрытию характеризуется тем, что активность реагента можно регулировать путем модификации реагента определенными электроноакцепторными или донорными группами.
Согласно некоторым вариантам осуществления реагент сульфуризации для применения согласно настоящему раскрытию характеризуется тем, что он является кристаллическим. Согласно некоторым вариантам осуществления реагент сульфуризации для применения согласно настоящему раскрытию характеризуется тем, что он имеет высокую степень кристалличности. В определенных вариантах реализации реагент сульфуризации для применения согласно настоящему раскрытию характеризуется простотой очистки реагента, например, путем кристаллизации. В определенных вариантах реализации реагент сульфуризации для применения согласно настоящему раскрытию характеризуется тем, что он по существу не содержит серосодержащие примеси. Согласно некоторым вариантам осуществления реагенты сульфуризации, которые по существу не содержат серосодержащие примеси, имеют увеличенную эффективность.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью содержит одну или более фосфатных сложных диэфирных линкерных групп. Для синтеза указанных олигонуклеотидов с контролируемой хиральностью одну или более стадий модификации необязательно заменяют на стадию окисления для встраивания соответствующих фосфатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления стадию окисления проводят аналогично традиционным способам синтеза олигонуклеотидов. Согласно некоторым вариантам осуществления стадия окисления включает применение I2. Согласно некоторым вариантам осуществления стадия окисления включает применение I2 и пиридина. Согласно некоторым вариантам осуществления стадия окисления включает применение 0,02М I2 в системе сорастворителей ТГФ/пиридин/вода (70:20:10 (об./об./об.)). Пример цикла изображен на схеме I-c.
Согласно некоторым вариантам осуществления фосфоротиоат непосредственно образуется путем сульфуризации с помощью реагентов для сульфуризации, например, 3-фенил-1,2,4-дитиазолин-5-она. Согласно некоторым вариантам осуществления после непосредственной вставки фосфоротиоата, хиральная вспомогательная группа остается присоединенной к межнуклеотидному атому фосфора. Согласно некоторым вариантам осуществления требуется дополнительная стадия удаления защитной группы для удаления хирального вспомогательного вещества (например, для хирального вспомогательного агента типа DPSE, с использованием TBAF, HF-Et3N и т.д.).
Согласно некоторым вариантам осуществления предшественник фосфоротиоата применяют для синтеза олигонуклеотидов с контролируемой хиральностью, содержащих фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления указанный предшественник фосфоротиоата представляет собой 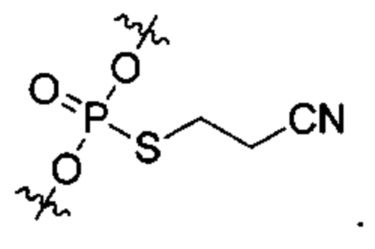 Согласно некоторым вариантам осуществления
Согласно некоторым вариантам осуществления 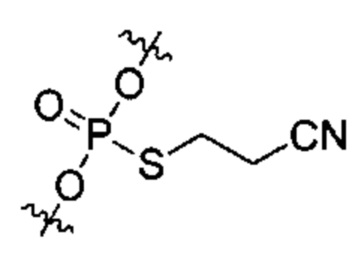 превращают в фосфоротиоатные сложные диэфирные линкерные группы при помощи стандартных способов удаления защитных групп/высвобождения после завершения цикла. Примеры дополнительно изображены ниже.
превращают в фосфоротиоатные сложные диэфирные линкерные группы при помощи стандартных способов удаления защитных групп/высвобождения после завершения цикла. Примеры дополнительно изображены ниже.
Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью содержит одну или более фосфатных сложных диэфирных линкерных групп и одну или более фосфоротиоатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления предложенный олигонуклеотид с контролируемой хиральностью содержит одну или более фосфатных сложных диэфирных линкерных групп и одну или более фосфоротиоатных сложных диэфирных линкерных групп, где по меньшей мере одну фосфатную сложную диэфирную линкерную группу встраивают после всех фосфоротиоатных сложных диэфирных линкерных групп при способе синтеза в направлении от 3' до 5'. Для синтеза указанных олигонуклеотидов с контролируемой хиральностью согласно некоторым вариантам осуществления одну или более стадий модификации необязательно заменяют на стадию окисления для встраивания соответствующих фосфатных сложных диэфирных линкерных групп, а на место каждой будущей фосфоротиоатной сложной диэфирной линкерной группы встраивают предшественник фосфоротиоата. Согласно некоторым вариантам осуществления предшественник фосфоротиоата превращают в фосфоротиоатную сложную диэфирную линкерную группу после достижения желаемой длины олигонуклеотида. Согласно некоторым вариантам осуществления на стадии удаления защитной группы/высвобождения, проводимой в рамках цикла или после его завершения, происходит превращение предшественников фосфоротиоатов в фосфоротиоатные сложные диэфирные линкерные группы. Согласно некоторым вариантам осуществления предшественник фосфоротиоата характеризуется тем, что его можно удалять по пути бета-отщепления. Согласно некоторым вариантам осуществления предшественник фосфоротиоата представляет собой 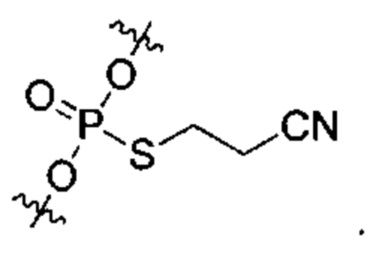 Специалистам в данной области техники понятно, что одним из преимуществ применения предшественника фосфоротиоата, например,
Специалистам в данной области техники понятно, что одним из преимуществ применения предшественника фосфоротиоата, например, 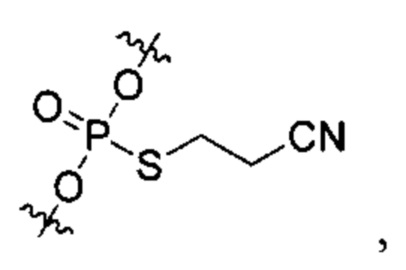 в способе синтеза является то, что
в способе синтеза является то, что 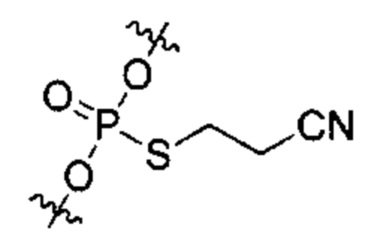 является более стабильным по сравнению с фосфоротиоатом в определенных условиях.
является более стабильным по сравнению с фосфоротиоатом в определенных условиях.
Согласно некоторым вариантам осуществления предшественник фосфоротиоата представляет собой фосфорзащитную группу, такую как описано в настоящей заявке, например, 2-цианоэтил (СЕ или Cne), 2-триметилсилилэтил, 2-нитроэтил, 2-сульфонилэтил, метил, бензил, о-нитробензил, 2-(n-нитрофенил)этил (NPE или Npe), 2-фенилэтил, 3-(N-трет-бутилкарбоксамидо)-1-пропил, 4-оксопентил, 4-метилтио-1-бутил, 2-циано-1,1-диметилэтил, 4-N-метиламинобутил, 3-(2-пиридил)-1-пропил, 2-[N-метил-N-(2-пиридил)]аминоэтил, 2-(N-формил,N-метил)аминоэтил, 4-[N-метил-N-(2,2,2-трифторацетил)амино]бутил. Примеры дополнительно приведены ниже.
Способы синтеза целевых реагентов сульфуризации описаны в настоящей заявке и в разделе примеров.
Как отмечалось выше, согласно некоторым вариантам осуществления сульфуризацию проводят в условиях, при которых происходит отщепление хирального реагента от растущего олигонуклеотида. Согласно некоторым вариантам осуществления сульфуризацию проводят в условиях, при которых не происходит отщепление хирального реагента от растущего олигонуклеотида.
Согласно некоторым вариантам осуществления реагент сульфуризации растворяют в подходящем растворителе и доставляют в колонку. В определенных вариантах реализации растворитель представляет собой полярный апротонный растворитель, такой как нитрилсодержащий растворитель. Согласно некоторым вариантам осуществления растворитель представляет собой ацетонитрил. Согласно некоторым вариантам осуществления раствор реагента сульфуризации получают путем смешения реагента сульфуризации (например, тиосульфонатного производного, такого как описано в настоящей заявке) и BSTFA (N,O-бис-триметилсилилтрифторацетамида) в нитрилсодержащем растворителе (например, в ацетонитриле). Согласно некоторым вариантам осуществления BSTFA не включают в состав смеси. Например, авторы настоящего изобретения обнаружили, что реагенты сульфуризации общей формулы Rs2-S-S(O)2-Rs3, имеющие относительно более высокую реакционную способность, часто можно эффективно использовать в реакциях сульфуризации без использования BSTFA. Исключительно в качестве примера авторы настоящего изобретения продемонстрировали, что если Rs2 представляет собой n-нитрофенил, a Rs3 представляет собой метил, то BSTFA не требуется. С учетом настоящего описания специалисты в данной области техники с легкостью смогут определять другие ситуации и/или реагенты сульфуризации, для которых не требуется BSTFA.
Согласно некоторым вариантам осуществления стадию сульфуризации проводят при комнатной температуре. Согласно некоторым вариантам осуществления стадию сульфуризации проводят при более низких температурах, таких как примерно 0°С, примерно 5°С, примерно 10°С или примерно 15°С. Согласно некоторым вариантам осуществления стадию сульфуризации проводят при повышенных температурах, составляющих более чем примерно 20°С.
Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 120 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 90 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 60 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 30 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 25 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 20 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 15 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 1 минуты до примерно 10 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение периода времени от примерно 5 минут до примерно 60 минут.
Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 5 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 10 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 15 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 20 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 25 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 30 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 35 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 40 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 45 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 50 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 55 минут. Согласно некоторым вариантам осуществления реакцию сульфуризации проводят в течение примерно 60 минут.
Неожиданно было обнаружено, что определенные продукты, модифицированные путем сульфуризации, полученные в соответствии со способами согласно настоящему раскрытию, обладают неожиданной стабильностью. Согласно некоторым вариантам осуществления продукты с неожиданной стабильностью представляют собой фосфоротиоатные сложные триэфиры. Согласно некоторым вариантам осуществления продукты с неожиданной стабильностью представляют собой олигонуклеотиды с контролируемой хиральностью, содержащие одну или более межнуклеотидных линкерных групп, имеющих структуру формулы I-c.
Специалистам в родственных областях техники должно быть понятно, что способы сульфуризации, описанные в настоящей заявке, и реагенты сульфуризации, описанные в настоящей заявке, также подходят с точки зрения модификации Н-фосфонатных олигонуклеотидов, таких как те, что описаны в заявке Wada II (WO 2010/064146).
Согласно некоторым вариантам осуществления реакция сульфуризации на каждой стадии имеет эффективность сульфуризации по меньшей мере примерно 80%, 85%, 90%, 95%, 96%, 97% или 98%. Согласно некоторым вариантам осуществления реакция сульфуризации обеспечивает неочищенную композицию динуклеотидного продукта, имеющую чистоту по меньшей мере 98%. В некоторых варианта реализации реакция сульфуризации обеспечивает композицию неочищенного тетрануклеотидного продукта, имеющего чистоту по меньшей мере 90%. Согласно некоторым вариантам осуществления реакция сульфуризация обеспечивает композицию неочищенного додекануклеотидного продукта, имеющего чистоту по меньшей мере 70%. Согласно некоторым вариантам осуществления реакция сульфуризации обеспечивает композицию неочищенного икозануклеотидного продукта, имеющего чистоту по меньшей мере 50%.
После завершения стадии модификации атома фосфора линкерной группы олигонуклеотид подвергают обработке на другой стадии удаления блокирующей группы перед введением в повторный цикл. Согласно некоторым вариантам осуществления хиральное вспомогательное вещество остается в неизменном виде после сульфуризации, а удаление блокирующей группы проводят на последующей стадии удаления блокирующей группы, которую обязательно проводят перед повторным введением в цикл. Способ удаления блокирующей группы, сочетания, введения блокирующей группы и модификации используют повторно до достижения желаемой длины растущего олигонуклеотида, после чего олигонуклеотид можно немедленно отщеплять от твердой подложки или оставлять на подложке для очистки, а после этого отщеплять. Согласно некоторым вариантам осуществления при одном или более нуклеотидных основаниях содержатся одна или более защитных групп, а отщепление олигонуклеотида от подложки и удаление защитных групп в основаниях проводят на одной стадии. Согласно некоторым вариантам осуществления при одном или более нуклеотидных основаниях содержатся одна или более защитных групп, а отщепление олигонуклеотида от подложки и удаление защитных групп в основаниях проводят более чем за одну стадию. Согласно некоторым вариантам осуществления удаление защитных групп и отщепление от подложки проводят в основных условиях с использованием, например, одного или более основных аминов. В определенных вариантах реализации один или более основных аминов содержат пропиламин. В определенных вариантах реализации один или более основных аминов содержат пиридин.
Согласно некоторым вариантам осуществления отщепление от подложки и/или удаление защитных групп проводят при повышенной температуре от примерно 30°С до примерно 90°С. Согласно некоторым вариантам осуществления отщепление от подложки и/или удаление защитных групп проводят при повышенной температуре от примерно 40°С до примерно 80°С. Согласно некоторым вариантам осуществления отщепление от подложки и/или удаление защитных групп проводят при повышенной температуре от примерно 50°С до примерно 70°С. Согласно некоторым вариантам осуществления отщепление от подложки и/или удаление защитных групп проводят при повышенной температуре, составляющей примерно 60°С. Согласно некоторым вариантам осуществления отщепление от подложки и/или удаление защитных групп проводят при температуре окружающей среды.
Примеры способов очистки описаны в настоящей заявке и/или известны в родственных областях техники.
Следует отметить, что удаление хирального вспомогательного вещества от растущего олигонуклеотида во время каждого цикла является эффективным по меньшей мере по следующим причинам: (1) отсутствует необходимость удаления вспомогательного вещества на отдельной стадии по завершении синтеза олигонуклеотидов, когда к атому фосфора прикрепляют возможно чувствительные функциональные группы; и (2) предотвращается получение нестабильных промежуточных веществ, содержащих фосфор и вспомогательную группу, подверженных протеканию побочных реакций и/или отрицательно влияющих на химизм последующих процессов. Таким образом, удаление хирального вспомогательного вещества во время каждого цикла увеличивает эффективность синтеза в целом.
Несмотря на то, что выше описана стадия удаления блокирующей группы в рамках цикла, дополнительные общие способы приведены ниже.
Стадия удаления блокирующих групп
Согласно некоторым вариантам осуществления стадии сочетания предшествует стадия удаления блокирующей группы. Например, согласно некоторым вариантам осуществления 5'-гидроксильная группа растущего олигонуклеотида является заблокированной (т.е. защищенной), и для проведения последующего взаимодействия с нуклеозидным партнером по реакции сочетания необходимо удалять блокирующую группу.
Согласно некоторым вариантам осуществления для удаления блокирующей группы используют подкисление. Согласно некоторым вариантам осуществления кислота представляет собой кислоту Бренстеда или кислоту Льюиса. Подходящими кислотами Бренстеда являются карбоновые кислоты, алкилсульфокислоты, арилсульфокислоты, фосфорную кислоту и ее производные, фосфоновую кислоту и ее производные, алкилфосфоновые кислоты и их производные, арилфосфоновые кислоты и их производные, фосфиновую кислоту, диалкилфосфиновые кислоты и диарилфосфиновые кислоты, которые имеют значение pKa (при 25°С в воде) от -0,6 (трифторуксусная кислота) до 4,76 (уксусная кислота) в органическом растворителе или воде (в случае 80% уксусной кислоты). Концентрация кислоты (от 1 до 80%), применяемой на стадии подкисления, зависит от кислотности кислоты. Необходимо учитывать силу кислоту, так как сильнокислотные условия приводят к депуринизации/депиримидинации, при которых происходит отщепление пуринильных или пиримидинильных оснований от кольца рибозы или кольца другого сахара. Согласно некоторым вариантам осуществления кислота выбрана из Ra1COOH, Ra1SO3H, Ra3SO3H, 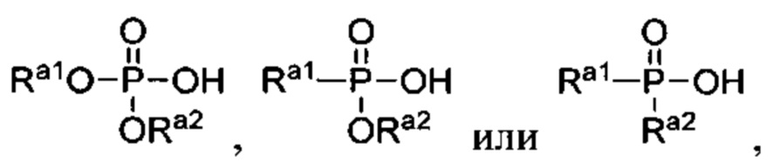 где каждый из Ra1 и Ra2 независимо представляет собой водород или необязательно замещенный алкил или арил, a Ra3 представляет собой необязательно замещенный алкил или арил.
где каждый из Ra1 и Ra2 независимо представляет собой водород или необязательно замещенный алкил или арил, a Ra3 представляет собой необязательно замещенный алкил или арил.
Согласно некоторым вариантам осуществления подкисление проводят с использованием кислоты Льюиса в органическом растворителе. Примеры таких подходящих кислот Льюиса представляют собой Zn(Xa)2, где Ха представляет собой Cl, Br, I или CF3SO3.
Согласно некоторым вариантам осуществления стадия подкисления включает добавление количества кислоты Бренстеда или кислоты Льюиса, которое является эффективным для удаления блокирующей группы, но не удаления пуриновых фрагментов в промежуточном веществе конденсации.
Кислоты, подходящие для стадии подкисления, также включают, но не ограничиваются ими, 10% фосфорную кислоту в органическом растворителе, 10% хлороводородную кислоту в органическом растворителе, 1% трифторуксусную кислоту в органическом растворителе, 3% дихлоруксусную кислоту или трихлоруксусную кислоту в органическом растворителе или 80% уксусную кислоту в воде. Концентрацию любой кислоты Бренстеда или Льюиса, используемой на указанной стадии, выбирают таким образом, чтобы концентрация кислоты не превышала концентрацию, обеспечивающую отщепление нуклеинового основания от фрагмента сахара.
Согласно некоторым вариантам осуществления подкисление включает добавление 1% трифторуксусной кислоты в органическом растворителе. Согласно некоторым вариантам осуществления подкисление включает добавление трифторуксусной кислоты с концентрацией от примерно 0,1% до примерно 8% в органическом растворителе. Согласно некоторым вариантам осуществления подкисление включает добавление 3% дихлоруксусной кислоты или трихлоруксусной кислоты в органическом растворителе. Согласно некоторым вариантам осуществления подкисление включает добавление дихлоруксусной или трихлоруксусной кислоты в концентрации от примерно 0,1% до примерно 10% в органическом растворителе. Согласно некоторым вариантам осуществления подкисление включает добавление 3% трихлоруксусной кислоты в органическом растворителе. Согласно некоторым вариантам осуществления подкисление включает добавление трихлоруксусной кислоты в концентрации от примерно 0,1% до примерно 10% в органическом растворителе. Согласно некоторым вариантам осуществления подкисление включает добавление 80% уксусной кислоты в воде. Согласно некоторым вариантам осуществления подкисление включает добавление уксусной кислоты в концентрации от примерно 50% до примерно 90% или от примерно 50% до примерно 80%, от примерно 50% до примерно 70%, от примерно 50% до примерно 60%, от примерно 70% до примерно 90% в воде. Согласно некоторым вариантам осуществления подкисление включает дополнительное добавление катионных очистителей в кислотный растворитель. В определенных вариантах реализации катионные очистители могут представлять собой триэтилсилан или триизопропилсилан. Согласно некоторым вариантам осуществления блокирующую группу удаляют путем подкисления, включающего добавление 1% трифторуксусной кислоты в органическом растворителе. Согласно некоторым вариантам осуществления блокирующую группу удаляют путем подкисления, включающего добавление 3% дихлоруксусной кислоты в органическом растворителе. Согласно некоторым вариантам осуществления блокирующую группу удаляют путем подкисления, включающего добавление 3% трихлоруксусной кислоты в органическом растворителе. Согласно некоторым вариантам осуществления блокирующую группу удаляют путем подкисления, включающего добавление 3% трихлоруксусной кислоты в дихлорметане.
В определенных вариантах реализации способы согласно настоящему раскрытию проводят в синтезаторе, а стадия удаления блокирующей группы гидроксильной группы растущего олигонуклеотида включает доставку количества растворителя в колонку синтезатора, где колонка содержит твердую подложку, к которой присоединен олигонуклеотид. Согласно некоторым вариантам осуществления растворитель представляет собой галогенированный растворитель (например, дихлорметан). В определенных вариантах реализации растворитель содержит количество кислоты. Согласно некоторым вариантам осуществления растворитель содержит количество органической кислоты, такой как, например, трихлоруксусная кислота. В определенных вариантах реализации кислота содержится в количестве от примерно 1% до примерно 20% (масс./об.). В определенных вариантах реализации кислота содержится в количестве от примерно 1% до примерно 10% (масс./об.). В определенных вариантах реализации кислота содержится в количестве от примерно 1% до примерно 5% (масс./об.). В определенных вариантах реализации кислота содержится в количестве от примерно 1 до примерно 3% (масс./об.). В определенных вариантах реализации кислота содержится в количестве примерно 3% (масс./об.). Способы удаления блокирующей группы гидроксильной группы дополнительно описаны в настоящей заявке. Согласно некоторым вариантам осуществления кислота содержится в дихлорметане в концентрации 3% (масс./об.).
Согласно некоторым вариантам осуществления хиральное вспомогательное вещество удаляют перед проведением стадии удаления блокирующей группы. Согласно некоторым вариантам осуществления хиральное вспомогательное вещество удаляют на стадии удаления блокирующей группы.
Согласно некоторым вариантам осуществления цикл завершают до проведения стадии удаления блокирующей группы. Согласно некоторым вариантам осуществления цикл завершают после стадии удаления блокирующей группы.
Общие условия удаления блокирующей группы/защитной группы
Функциональные группы, такие как гидроксильные или амино-фрагменты, расположенные при нуклеиновых основаниях или фрагментах сахаров, традиционно защищают во время синтеза с использованием блокирующих (защитных) групп (фрагментов), а затем удаляют блокирующих группы. В целом, блокирующая группа делает химическую функциональную группу молекулы инертной к определенным условиям взаимодействия, и впоследствии ее можно удалять от указанной функциональной группы, не нанося существенных повреждений остатку молекулы (см., например, Green and Wuts, Protective Groups in Organic Synthesis, 2nd Ed., John Wiley & Sons, New York, 1991). Например, аминогруппы можно блокировать с использованием групп, блокирующих азот, таких как фталимидо, 9-флуоренилметоксикарбонил (FMOC), трифенилметилсульфенил, t-ВОС, 4,4'-диметокситритил (DMTr), 4-метокситритил (MMTr), 9-фенилксантин-9-ил (пиксил), тритил (Tr) или 9-(n-метоксифенил)ксантин-9-ил (МОХ). Карбоксильные группы можно защищать в виде ацетильных групп. Гидроксигруппы можно защищать с использованием групп, таких как тетрагидропиранил (ТНР), трет-бутилдиметилсилил (TBDMS), 1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-ил (Ctmp), 1-(2-фторфенил)-4-метоксипиперидин-4-ил (Fpmp), 1-(2-хлорэтокси)этил, 3-метокси-1,5-дикарбометоксипентан-3-ил (MDP), бис(2-ацетоксиэтокси)метил (АСЕ), триизопропилсилилоксиметил (ТОМ), 1-(2-цианоэтокси)этил (СЕЕ), 2-цианоэтоксиметил (СЕМ), [4-(N-дихлорацетил-N-метиламино)бензилокси]метил, 2-цианоэтил (CN), пивалоилоксиметил (PivOM), левунилоксиметил (ALE). Существует описание и других типовых гидроксил-блокирующих групп (см., например, Beaucage et al., Tetrahedron, 1992, 46, 2223). Согласно некоторым вариантам осуществления гидроксил-блокирующие группы представляют собой группы, лабильные к действию кислот, такие как тритил, монометокситритил, диметокситритил, триметокситритил, 9-фенилксантин-9-ил (пиксил) и 9-(п-метоксифенил)ксантин-9-ил (МОХ). Химические функциональные группы также можно блокировать за счет введения их в виде предшественников. Таким образом, азидогруппу можно рассматривать как блокированную форму амина, так как азидогруппа легко превращается в амин. Известны и другие типовые защитные группы, применяемые при синтезе нуклеиновых кислот (см., например, Agrawal et al., Protocols for Oligonucleotide Conjugates, Eds., Humana Press, New Jersey, 1994, Vol. 26, pp. 1-72).
Известно применение различных способов для удаления блокирующих групп нуклеиновых кислот. Согласно некоторым вариантам осуществления удаляют все блокирующие группы. Согласно некоторым вариантам осуществления удаляют часть блокирующих групп. Согласно некоторым вариантам осуществления условия взаимодействия регулируют для селективного удаления определенных блокирующих групп.
Согласно некоторым вариантам осуществления блокирующие группы нуклеиновых оснований, если они присутствуют, можно отщеплять с использованием кислотного реагента после получения предложенного олигонуклеотида. Согласно некоторым вариантам осуществления блокирующие группы нуклеиновых оснований, если они присутствуют, можно отщеплять в условиях, которые не являются ни кислотными, ни основными, например, их можно отщеплять с использованием фторидных солей или комплексов фтороводородной кислоты. Согласно некоторым вариантам осуществления блокирующие группы нуклеиновых оснований, если они присутствуют, можно отщеплять в присутствии основания или основного растворителя после получения предложенного олигонуклеотида. В определенных вариантах реализации одна или более блокирующих групп нуклеинового основания характеризуются тем, что их можно отщеплять в присутствии основания или основного растворителя после получения предложенного олигомера, но они являются стабильными в определенных условиях на одной или более стадиях удаления защитных групп, проводимых ранее при получении предложенного олигонуклеотида.
Согласно некоторым вариантам осуществления блокирующие группы нуклеиновых оснований не требуются. Согласно некоторым вариантам осуществления блокирующие группы нуклеиновых оснований требуются. Согласно некоторым вариантам осуществления для определенных нуклеиновых оснований требуются одна или более блокирующих групп, тогда как для других нуклеиновых оснований одна или более блокирующих групп не требуются.
Согласно некоторым вариантам осуществления олигонуклеотид отщепляют от твердой подложки после синтеза. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение пропиламина. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение пропиламина в пиридине. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение 20% пропиламина в пиридине. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение пропиламина в безводном пиридине. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение 20% пропиламина в безводном пиридине. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение полярного апротонного растворителя, такого как ацетонитрил, NMP, ДМСО, сульфон и/или лутидин. Согласно некоторым вариантам осуществления отщепление от твердой подложки включает применение растворителя, например, полярного апротонного растворителя, и одного или более первичных аминов (например, С1-10 амина) и/или одного или более соединений, выбранных из метоксиламина, гидразина и чистого безводного аммиака.
Согласно некоторым вариантам осуществления удаление защитных групп олигонуклеотида включает применение пропиламина. Согласно некоторым вариантам осуществления удаление защитных групп олигонуклеотида включает применение пропиламина в пиридине. Согласно некоторым вариантам осуществления удаление защитных групп олигонуклеотида включает применение 20% пропиламина в пиридине. Согласно некоторым вариантам осуществления удаление защитных групп олигонуклеотида включает применение пропиламина в безводном пиридине. Согласно некоторым вариантам осуществления удаление защитных групп олигонуклеотида включает применение 20% пропиламина в безводном пиридине.
Согласно некоторым вариантам осуществления удаление защитных групп олигонуклеотида проводят во время отщепления.
Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят примерно при комнатной температуре. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при повышенной температуре. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при температуре более чем примерно 30°С, 40°С, 50°С, 60°С, 70°С, 80°С, 90°С или 100°С. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при температуре примерно 30°С, 40°С, 50°С, 60°С, 70°С, 80°С, 90°С или 100°С. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при температуре примерно 40-80°С. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при температуре примерно 50-70°С. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят примерно при 60°С.
Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение более чем 0,1 часа, 1 часа, 2 часов, 5 часов, 10 часов, 15 часов, 20 часов, 24 часов, 30 часов или 40 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 0,1-5 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 3-10 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 5-15 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 10-20 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 15-25 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 20-40 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 2 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 5 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 10 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 15 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 18 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят в течение примерно 24 часов.
Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при комнатной температуре в течение более чем 0,1 часа, 1 часа, 2 часов, 5 часов, 10 часов, 15 часов, 20 часов, 24 часов, 30 часов или 40 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при комнатной температуре в течение 5-48 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при комнатной температуре в течение примерно 10-24 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при комнатной температуре в течение 18 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при повышенной температуре в течение более чем 0,1 часа, 1 часа, 2 часов, 5 часов, 10 часов, 15 часов, 20 часов, 24 часов, 30 часов или 40 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят при повышенной температуре в течение 0,5-5 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят примерно при 60°С в течение примерно 0,5-5 часов. Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида проводят примерно при 60°С в течение примерно 2 часов.
Согласно некоторым вариантам осуществления отщепление олигонуклеотида от твердой подложки или удаление защитных групп олигонуклеотида включает применение пропиламина, и его проводят при комнатной температуре или при повышенной температуре в течение более чем 0,1 часа, 1 часа, 2 часов, 5 часов, 10 часов, 15 часов, 20 часов, 24 часов, 30 часов или 40 часов. Примерами условий являются 20% пропиламин в пиридине при комнатной температуре в течение примерно 18 часов и 20% пропиламин в пиридине при 60°С в течение примерно 18 часов.
Согласно некоторым вариантам осуществления перед отщеплением от твердой подложки проводят стадию удаления хиральной вспомогательной группы, если она все еще присоединена к межнуклеотидному атому фосфора. Согласно некоторым вариантам осуществления, например, одна или более хиральных вспомогательных групп типа DPSE остаются присоединенными к межнуклеотидным атомам фосфора в течение цикла синтеза олигонуклеотидов. Подходящие условия для удаления оставшихся хиральных вспомогательных групп широко известны в данной области техники, например, описаны в Wada I, Wada II, Wada III, Хиральном контроле и т.д. Согласно некоторым вариантам осуществления условием для удаления хирального вспомогательного вещества типа DPSE является TBAF или HF-Et3N, например, 0,1 М TBAF в MeCN, 0,5 М HF-Et3N в ТГФ или MeCN и т.д. Согласно некоторым вариантам осуществления настоящее раскрытие признает, что линкерная группа может быть отщеплена во время процесса удаления хиральной вспомогательной группы. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает линкерные группы, такие как линкерная группа SP, которая обеспечивает лучшую стабильность при удалении хиральной вспомогательной группы. Среди прочего, некоторые линкерные группы, предложенные настоящим раскрытием, обеспечивают улучшенный выход и/или чистоту.
Согласно некоторым вариантам осуществления активатор представляет собой активатор «Wada», т.е. активатор представляет собой любой активатор, описанный в документах Wada I, II или III, приведенных выше.
Примеры активирующих групп изображены далее:
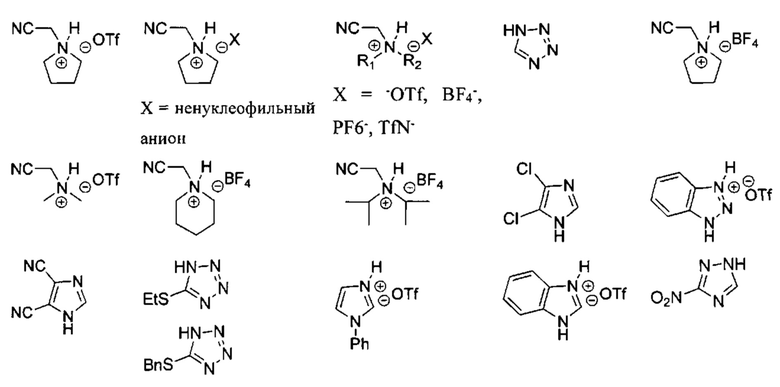
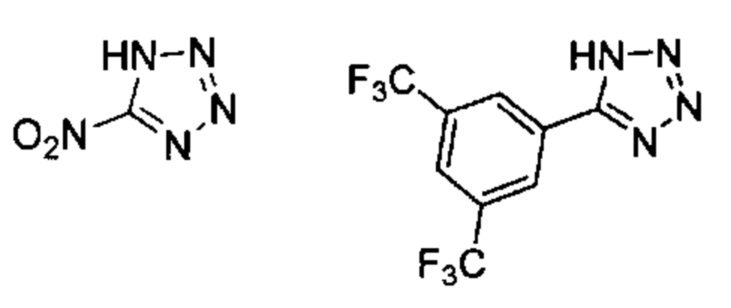
Согласно некоторым вариантам осуществления активирующие группы выбирают из
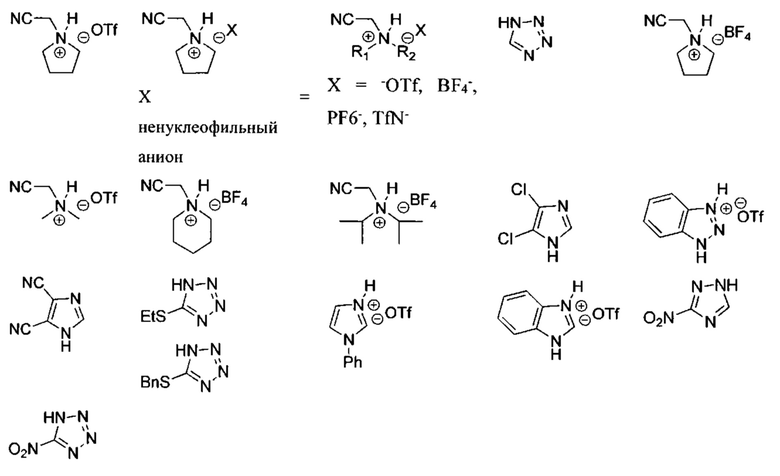
Согласно некоторым вариантам осуществления пример цикла изображен на схеме I-b.
Схема I-b. Встраивание фосфоротиоатных линкерных групп.
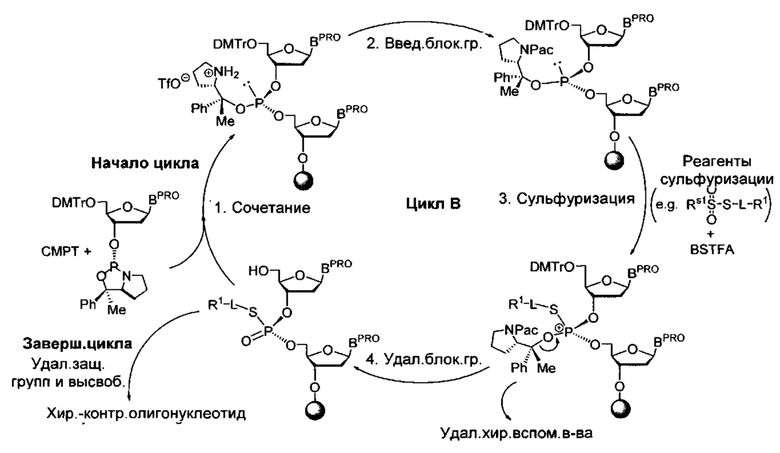
Согласно некоторым вариантам осуществления пример цикла проиллюстрирован на схеме I-c.
Схема I-c. Встраивание фосфатных сложных диэфирных и модифицированных межнуклеотидных линкерных групп в олигонуклеотид с контролируемой хиральностью.
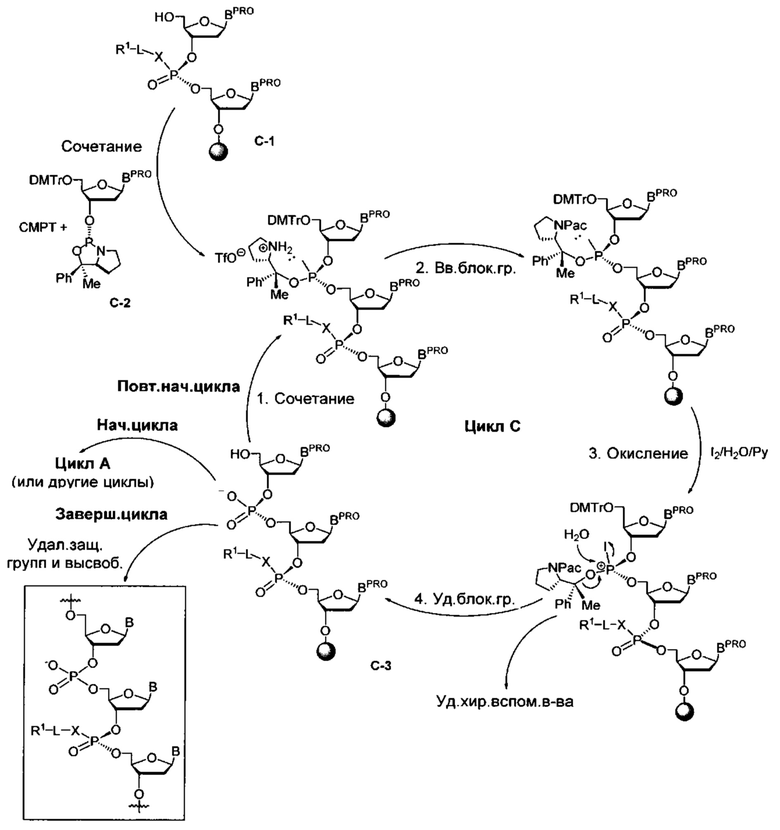
На схеме I-c олигонуклеотид (или нуклеотид или олигонуклеотид с модифицированными межнуклеотидными линкерными группами) на твердой подложке (С-1) подвергают сочетанию с фосфорамидитом С-2. После сочетания и введения блокирующей группы проводят стадию окисления. После удаления блокирующей группы получают фосфатную сложную диэфирную линкерную группу. Продукт цикла С-3 можно повторно использовать в цикле С для введения дополнительных фосфатных сложных диэфирных линкерных групп или в других циклах для встраивания других типов межнуклеотидных линкерных групп, или можно завершать цикл.
Согласно некоторым вариантам осуществления вместо С-2 на схеме I-c можно использовать фосфорамидит, который не является хирально-чистым. Согласно некоторым вариантам осуществления применяют β-цианоэтилфосфорамидиты, защищенные DMTr. Согласно некоторым вариантам осуществления применяемый фосфорамидит имеет структуру
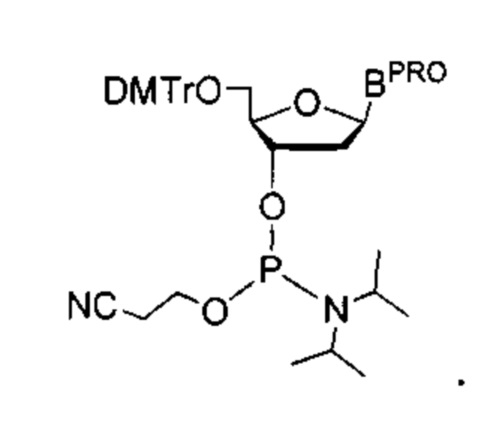
Согласно некоторым вариантам осуществления применение предшественника фосфоротиоатного сложного диэфира увеличивает стабильность олигонуклеотида во время синтеза. Согласно некоторым вариантам осуществления применение предшественника фосфоротиоатного сложного диэфира увеличивает эффективность синтеза олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления применение предшественника фосфоротиоатного сложного диэфира увеличивает выход синтеза олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления применение предшественника фосфоротиоатного сложного диэфира увеличивает чистоту продукта синтеза олигонуклеотида с контролируемой хиральностью.
Согласно некоторым вариантам осуществления предшественник фосфоротиоатного сложного диэфира, применяемый в указанных выше способах, представляет собой 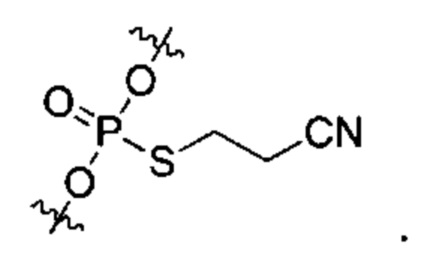 Согласно некоторым вариантам осуществления
Согласно некоторым вариантам осуществления 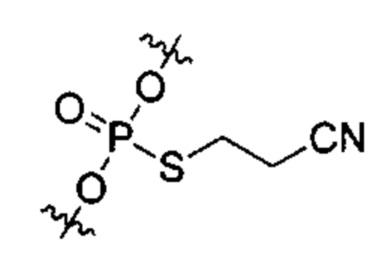 превращают в фосфоротиоатную сложную диэфирную линкерную группу во время удаления защитных групп/высвобождения. Согласно некоторым вариантам осуществления пример цикла изображен на схеме I-d. Дополнительные примеры изображены ниже.
превращают в фосфоротиоатную сложную диэфирную линкерную группу во время удаления защитных групп/высвобождения. Согласно некоторым вариантам осуществления пример цикла изображен на схеме I-d. Дополнительные примеры изображены ниже.
Схема I-d. Предшественник фосфоротиоатного сложного диэфира в синтезе олигонуклеотида с контролируемой хиральностью.
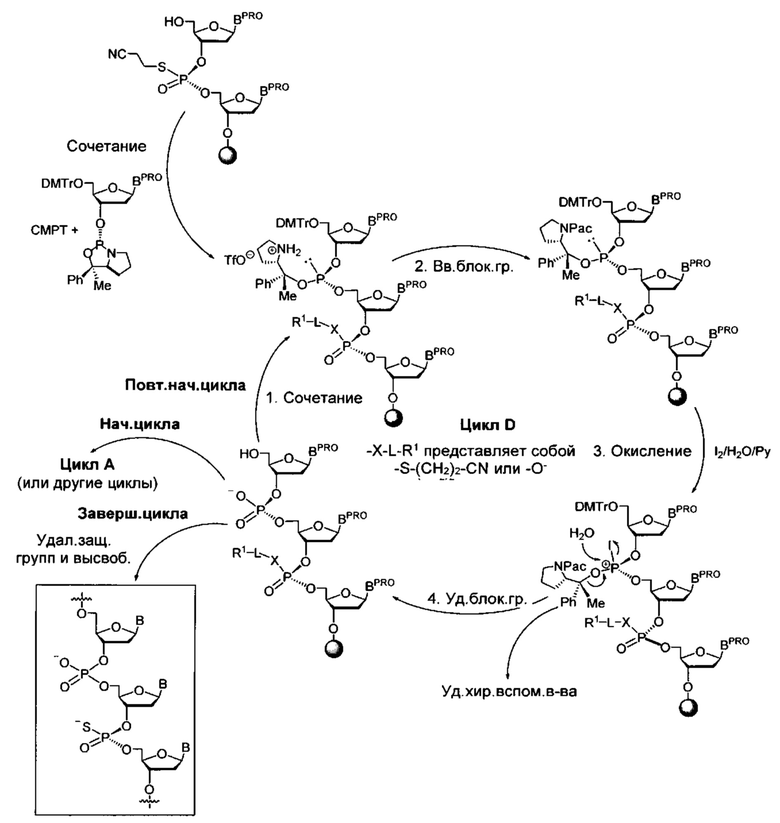
Как проиллюстрировано на схеме I-d, фосфоротиоатные и фосфатные сложные диэфирные линкерные группы можно вводить в один олигонуклеотид с контролируемой хиральностью. Специалистам в данной области техники должно быть понятно, что предложенные способы не требуют последовательного расположения фосфоротиоатного сложного диэфира и фосфатного сложного диэфира - между ними можно встраивать и другие межнуклеотидные линкерные группы с использованием цикла, такого как описано выше. На схеме I-d предшественники фосфоротиоатных сложных диэфиров, 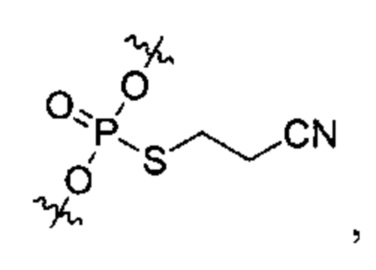 встраивают вместо фосфоротиоатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления указанная замена обеспечивала увеличенную эффективность синтеза на определенных стадиях, например, на стадии окисления. Согласно некоторым вариантам осуществления применение предшественников фосфоротиоатных сложных диэфиров, в целом, увеличивает стабильность олигонуклеотидов с контролируемой хиральностью во время синтеза и/или при хранении. После завершения цикла во время удаления защитных групп/высвобождения предшественник фосфоротиоатного сложного диэфира превращают в фосфоротиоатную сложную диэфирную линкерную группу. Согласно некоторым вариантам осуществления эффективным является применение предшественника фосфоротиоатного сложного диэфира, даже если в олигонуклеотиде с контролируемой хиральностью отсутствуют фосфатные сложные диэфирные линкерные группы, или во время синтеза не требуется стадия окисления.
встраивают вместо фосфоротиоатных сложных диэфирных линкерных групп. Согласно некоторым вариантам осуществления указанная замена обеспечивала увеличенную эффективность синтеза на определенных стадиях, например, на стадии окисления. Согласно некоторым вариантам осуществления применение предшественников фосфоротиоатных сложных диэфиров, в целом, увеличивает стабильность олигонуклеотидов с контролируемой хиральностью во время синтеза и/или при хранении. После завершения цикла во время удаления защитных групп/высвобождения предшественник фосфоротиоатного сложного диэфира превращают в фосфоротиоатную сложную диэфирную линкерную группу. Согласно некоторым вариантам осуществления эффективным является применение предшественника фосфоротиоатного сложного диэфира, даже если в олигонуклеотиде с контролируемой хиральностью отсутствуют фосфатные сложные диэфирные линкерные группы, или во время синтеза не требуется стадия окисления.
Как и на схеме I-c, согласно некоторым вариантам осуществления фосфорамидит, который не является хирально-чистым, можно применять в циклах, включающих стадии окисления. Согласно некоторым вариантам осуществления применяют β-цианоэтилфосфорамидиты, защищенные DMTr. Согласно некоторым вариантам осуществления применяемый фосфорамидит имеет структуру 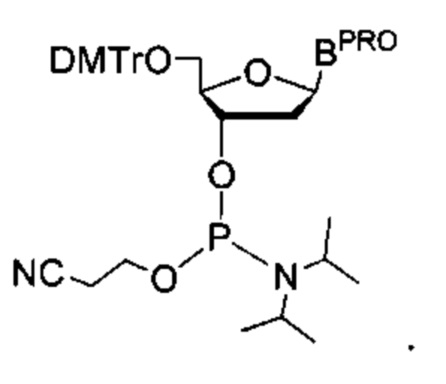
Согласно некоторым вариантам осуществления способы согласно настоящему изобретению обеспечивают композиции олигонуклеотидов с контролируемой хиральностью, обогащенные олигонуклеотидом определенного типа.
Согласно некоторым вариантам осуществления по меньшей мере примерно 10% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 20% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 30% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 40% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 50% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 60% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 70% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 80% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 90% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 95% предложенной неочищенной композиции представляют собой олигонуклеотид определенного типа.
Согласно некоторым вариантам осуществления по меньшей мере примерно 1% предложенной композиции представляет собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 2% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 3% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 4% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 5% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 10% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 20% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 30% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 40% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 50% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 60% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 70% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 80% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 90% предложенной композиции представляют собой олигонуклеотид определенного типа. Согласно некоторым вариантам осуществления по меньшей мере примерно 95% предложенной композиции представляют собой олигонуклеотид определенного типа.
Согласно некоторым вариантам осуществления пример цикла изображен на схеме I-е ниже.
Схема I-е. Пример цикла с использованием хирального вспомогательного вещества PhMe.

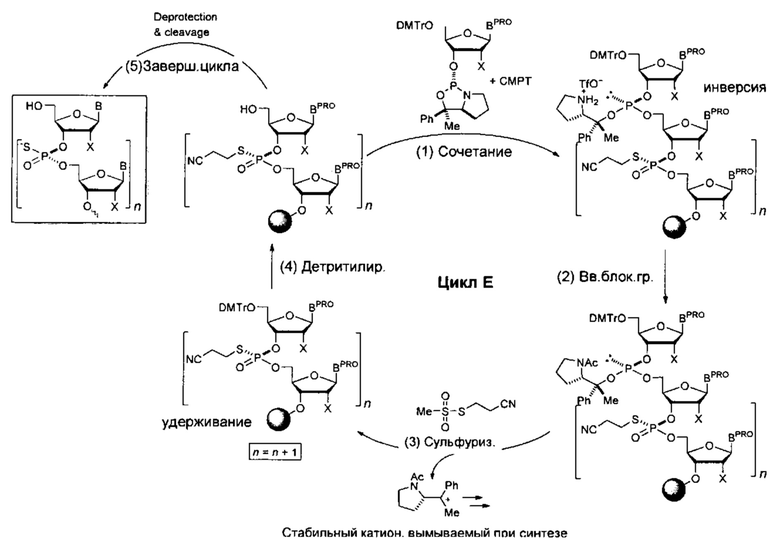
Согласно некоторым вариантам осуществления X представляет собой Н или 2'-модификацию. Согласно некоторым вариантам осуществления X представляет собой Н или -OR1, где R1 не представляет собой водород. Согласно некоторым вариантам осуществления X представляет собой Н или -OR1, где R1 представляет собой необязательно замещенный C1-6 алкил. Согласно некоторым вариантам осуществления X представляет собой Н. Согласно некоторым вариантам осуществления X представляет собой -ОМе. Согласно некоторым вариантам осуществления X представляет собой -ОСН2СН2ОСН3. Согласно некоторым вариантам осуществления X представляет собой -F.
Согласно некоторым вариантам осуществления пример цикла изображен на схеме I-f.
Схема I-е. Пример цикла с использованием хирального вспомогательного вещества DPSE.
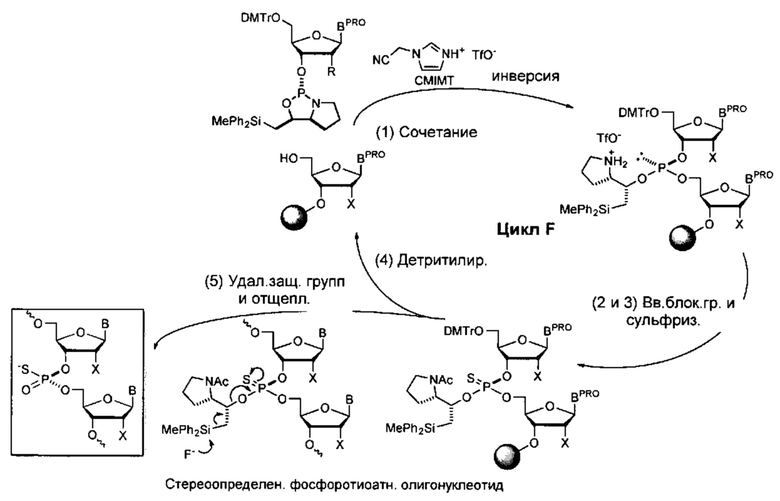
Согласно некоторым вариантам осуществления X представляет собой Н или 2'-модификацию. Согласно некоторым вариантам осуществления X представляет собой Н или -OR1, где R1 не представляет собой водород. Согласно некоторым вариантам осуществления X представляет собой Н или -OR1, где R1 представляет собой необязательно замещенный C1-6 алкил. Согласно некоторым вариантам осуществления X представляет собой Н. Согласно некоторым вариантам осуществления X представляет собой -ОМе. Согласно некоторым вариантам осуществления X представляет собой -ОСН2СН2ОСН3. Согласно некоторым вариантам осуществления X представляет собой -F.
Специалисту в данной области техники понятно, что различные типы циклов могут быть объединены для обеспечения полного контроля за химическими модификациями и стереохимией олигонуклеотидов. Согласно некоторым вариантам осуществления, например, способ синтеза олигонуклеотидов может содержать один или более циклов A-F. Согласно некоторым вариантам осуществления предложенный способ содержит по меньшей мере один цикл с использованием хирального вспомогательного вещества типа DPSE.
Согласно некоторым вариантам осуществления настоящее раскрытие содержит способы получения предложенных олигонуклеотидов и композиций олигонуклеотидов. Согласно некоторым вариантам осуществления предложены способы, предусматривающие предоставление предложенного хирального реагента, имеющего структуру 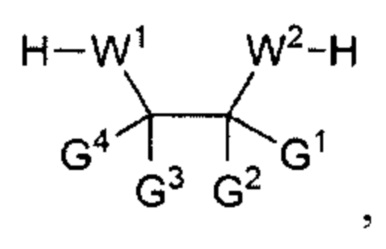 где W1 представляет собой -NG5, W2 представляет собой О, каждый из G1 и G3 независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного C1-10, G2 представляет собой -C(R)2Si(R)3 и G4 и G5, взятые вместе, образуют необязательно замещенное насыщенное, частично ненасыщенное или ненасыщенное гетероатомсодержащее кольцо до примерно 20 кольцевых атомов, которое является моноциклическим или полициклическим, конденсированным или неконденсированным, где каждый R независимо представляет собой водород или необязательно замещенную группу выбранную из алифатического, карбоциклильного, арильного, гетероарильного и гетероциклильного C1-С6. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру
где W1 представляет собой -NG5, W2 представляет собой О, каждый из G1 и G3 независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного C1-10, G2 представляет собой -C(R)2Si(R)3 и G4 и G5, взятые вместе, образуют необязательно замещенное насыщенное, частично ненасыщенное или ненасыщенное гетероатомсодержащее кольцо до примерно 20 кольцевых атомов, которое является моноциклическим или полициклическим, конденсированным или неконденсированным, где каждый R независимо представляет собой водород или необязательно замещенную группу выбранную из алифатического, карбоциклильного, арильного, гетероарильного и гетероциклильного C1-С6. Согласно некоторым вариантам осуществления предложенный хиральный реагент имеет структуру 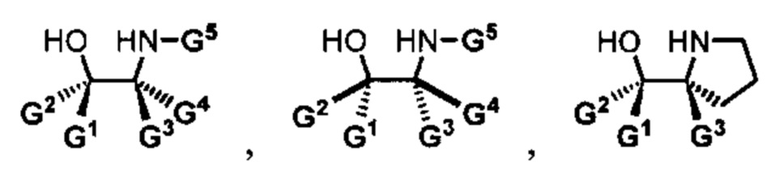 или
или 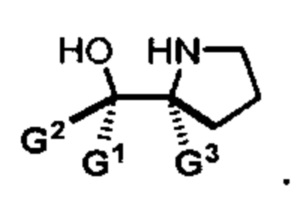 Согласно некоторым вариантам осуществления предложенные способы предусматривают получение фосфорамидита, содержащего фрагмент из хирального реагента, имеющего структуру
Согласно некоторым вариантам осуществления предложенные способы предусматривают получение фосфорамидита, содержащего фрагмент из хирального реагента, имеющего структуру 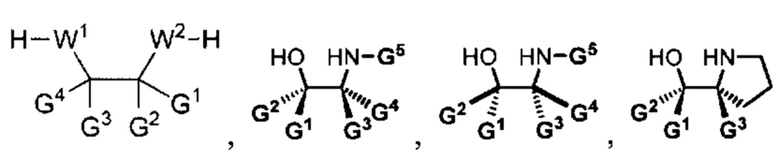 или
или 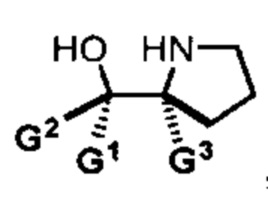 , где -W1H и -W2H, или гидроксильные и аминогруппы, образуют связи с атомом фосфора фосфорамидита. Согласно некоторым вариантам осуществления -W1H и -W2H или гидроксильные и аминогруппы образуют связи с атомом фосфора фосфорамидита, например, в
, где -W1H и -W2H, или гидроксильные и аминогруппы, образуют связи с атомом фосфора фосфорамидита. Согласно некоторым вариантам осуществления -W1H и -W2H или гидроксильные и аминогруппы образуют связи с атомом фосфора фосфорамидита, например, в 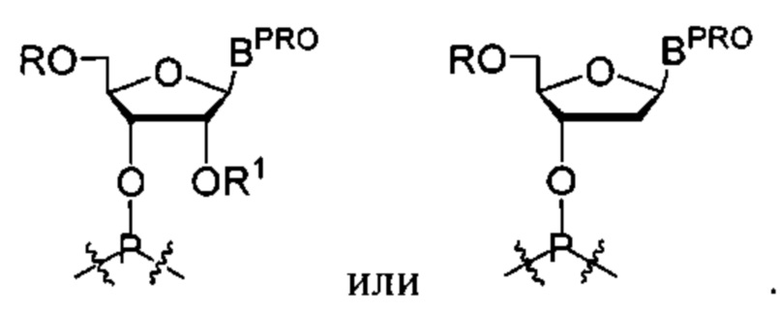 Согласно некоторым вариантам осуществления фосфорамидит имеет структуру
Согласно некоторым вариантам осуществления фосфорамидит имеет структуру 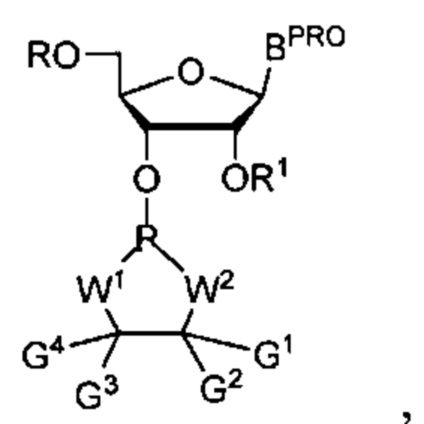
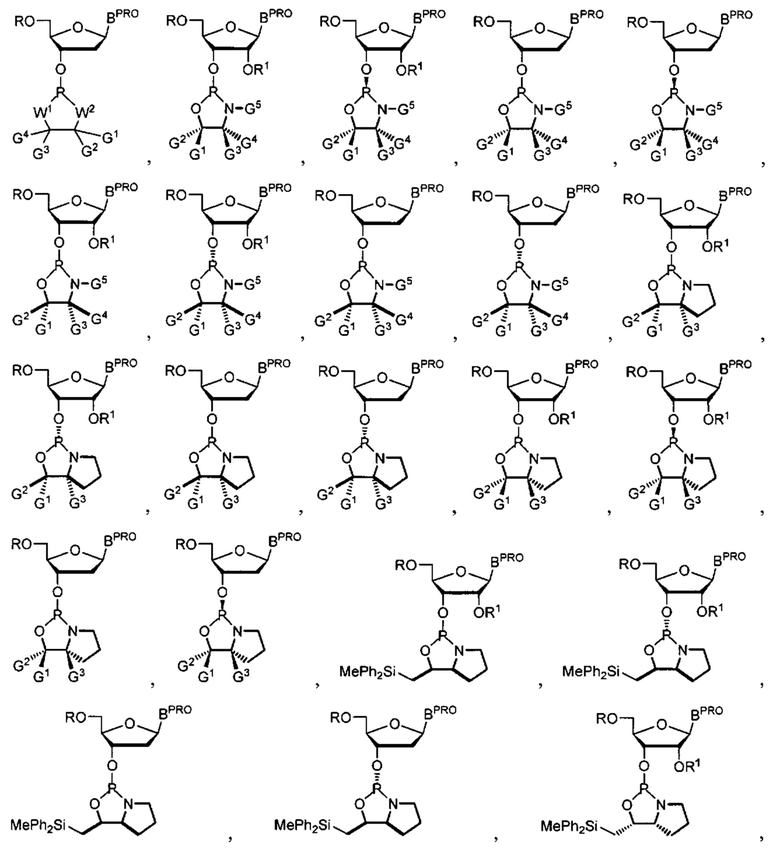
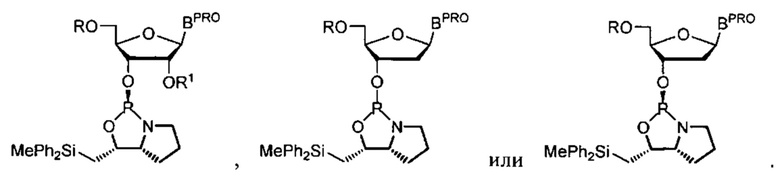 Согласно некоторым вариантам осуществления R представляет собой группу защиты. Согласно некоторым вариантам осуществления R представляет собой DMTr. Согласно некоторым вариантам осуществления G2 представляет собой -C(R)2Si(R)3, где -C(R)2 представляет собой необязательно замещенный -СН2-, и каждый R в -Si(R)3 независимо представляет собой необязательно замещенную группу, выбранную из алифатического С1-10, гетероциклила, гетероарила и арила. Согласно некоторым вариантам осуществления по меньшей мере один R-Si(R)3 независимо представляет собой необязательно замещенный С1-10 алкил. Согласно некоторым вариантам осуществления по меньшей мере один R-Si(R)3 независимо представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления один R-Si(R)3 независимо представляет собой необязательно замещенный фенил, и каждый из двух других R независимо представляет собой необязательно замещенный С1-10 алкил. Согласно некоторым вариантам осуществления один R-Si(R)3 независимо представляет собой необязательно замещенный С1-10 алкил, и каждый из двух других R независимо представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления G2 представляет собой необязательно замещенный -CH2Si(Ph)(Me)2. Согласно некоторым вариантам осуществления G2 представляет собой необязательно замещенный -CH2Si(Me)(Ph)2. Согласно некоторым вариантам осуществления G2 представляет собой -CH2Si(Me)(Ph)2. Согласно некоторым вариантам осуществления G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-6-членного кольца, содержащего один атом азота (к которому присоединен G5). Согласно некоторым вариантам осуществления G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота. Согласно некоторым вариантам осуществления G1 представляет собой водород. Согласно некоторым вариантам осуществления G3 представляет собой водород. Согласно некоторым вариантам осуществления как G1, так и G3 представляют собой водород. Согласно некоторым вариантам осуществления как G1, так и G3 представляют собой водород, G2 представляет собой -C(R)2Si(R)3, где -C(R)2 представляет собой необязательно замещенный -СН2-, и каждый R-Si(R)3 представляет собой независимо, необязательно замещенную группу, выбранную из алифатического C1-10, гетероциклила, гетероарила и арила, и G4 и G5, взятые вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота. Согласно некоторым вариантам осуществления предложенный способ дополнительно предусматривает обеспечение фторсодержащего реагента. Согласно некоторым вариантам осуществления предложенный фторсодержащий реагент удаляет хиральный реагент или продукт, образованный из хирального реагента, из олигонуклеотидов после синтеза. В соответствии с настоящим изобретением могут использоваться различные известные фторсодержащие реагенты, включая источники F-, для удаления групп -SiR3, например, TBAF, HF3-Et3N и т.д. Согласно некоторым вариантам осуществления фторсодержащий реагент обеспечивает лучшие результаты, например, более короткое время обработки, более низкую температуру, меньшее десульфурирование и т.д. по сравнению с традиционными способами, такими как концентрированный аммиак. Согласно некоторым вариантам осуществления для определенного фторсодержащего реагента настоящее раскрытие обеспечивает линкерные группы для улучшения результатов, например, меньшего отщепление олигонуклеотидов от подложки во время удаления хирального реагента (или продукта, образовавшегося из него во время синтеза олигонуклеотидов). Согласно некоторым вариантам осуществления предложенная линкерная группа представляет собой линкерную группу SP. Согласно некоторым вариантам осуществления настоящее раскрытие показало, что может быть использован комплекс HF-основания, такой как HF-NR3, для контроля отщепления во время удаления хирального реагента (или продукта, образованного из него во время синтеза олигонуклеотидов). Согласно некоторым вариантам осуществления HF-NR3 представляет собой HF-NEt3. Согласно некоторым вариантам осуществления HF-NR3 позволяет использовать традиционные линкерные группы, например, сукцинильную линкерную группу.
Согласно некоторым вариантам осуществления R представляет собой группу защиты. Согласно некоторым вариантам осуществления R представляет собой DMTr. Согласно некоторым вариантам осуществления G2 представляет собой -C(R)2Si(R)3, где -C(R)2 представляет собой необязательно замещенный -СН2-, и каждый R в -Si(R)3 независимо представляет собой необязательно замещенную группу, выбранную из алифатического С1-10, гетероциклила, гетероарила и арила. Согласно некоторым вариантам осуществления по меньшей мере один R-Si(R)3 независимо представляет собой необязательно замещенный С1-10 алкил. Согласно некоторым вариантам осуществления по меньшей мере один R-Si(R)3 независимо представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления один R-Si(R)3 независимо представляет собой необязательно замещенный фенил, и каждый из двух других R независимо представляет собой необязательно замещенный С1-10 алкил. Согласно некоторым вариантам осуществления один R-Si(R)3 независимо представляет собой необязательно замещенный С1-10 алкил, и каждый из двух других R независимо представляет собой необязательно замещенный фенил. Согласно некоторым вариантам осуществления G2 представляет собой необязательно замещенный -CH2Si(Ph)(Me)2. Согласно некоторым вариантам осуществления G2 представляет собой необязательно замещенный -CH2Si(Me)(Ph)2. Согласно некоторым вариантам осуществления G2 представляет собой -CH2Si(Me)(Ph)2. Согласно некоторым вариантам осуществления G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-6-членного кольца, содержащего один атом азота (к которому присоединен G5). Согласно некоторым вариантам осуществления G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота. Согласно некоторым вариантам осуществления G1 представляет собой водород. Согласно некоторым вариантам осуществления G3 представляет собой водород. Согласно некоторым вариантам осуществления как G1, так и G3 представляют собой водород. Согласно некоторым вариантам осуществления как G1, так и G3 представляют собой водород, G2 представляет собой -C(R)2Si(R)3, где -C(R)2 представляет собой необязательно замещенный -СН2-, и каждый R-Si(R)3 представляет собой независимо, необязательно замещенную группу, выбранную из алифатического C1-10, гетероциклила, гетероарила и арила, и G4 и G5, взятые вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота. Согласно некоторым вариантам осуществления предложенный способ дополнительно предусматривает обеспечение фторсодержащего реагента. Согласно некоторым вариантам осуществления предложенный фторсодержащий реагент удаляет хиральный реагент или продукт, образованный из хирального реагента, из олигонуклеотидов после синтеза. В соответствии с настоящим изобретением могут использоваться различные известные фторсодержащие реагенты, включая источники F-, для удаления групп -SiR3, например, TBAF, HF3-Et3N и т.д. Согласно некоторым вариантам осуществления фторсодержащий реагент обеспечивает лучшие результаты, например, более короткое время обработки, более низкую температуру, меньшее десульфурирование и т.д. по сравнению с традиционными способами, такими как концентрированный аммиак. Согласно некоторым вариантам осуществления для определенного фторсодержащего реагента настоящее раскрытие обеспечивает линкерные группы для улучшения результатов, например, меньшего отщепление олигонуклеотидов от подложки во время удаления хирального реагента (или продукта, образовавшегося из него во время синтеза олигонуклеотидов). Согласно некоторым вариантам осуществления предложенная линкерная группа представляет собой линкерную группу SP. Согласно некоторым вариантам осуществления настоящее раскрытие показало, что может быть использован комплекс HF-основания, такой как HF-NR3, для контроля отщепления во время удаления хирального реагента (или продукта, образованного из него во время синтеза олигонуклеотидов). Согласно некоторым вариантам осуществления HF-NR3 представляет собой HF-NEt3. Согласно некоторым вариантам осуществления HF-NR3 позволяет использовать традиционные линкерные группы, например, сукцинильную линкерную группу.
Биологические применения и пример использования
Кроме всего прочего настоящее раскрытие признает, что свойства и активность олигонуклеотида можно регулировать путем оптимизации профиля хиральных центров остова за счет использования предложенных композиций олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композиции олигонуклеотидов с контролируемой хиральностью, в которой олигонуклеотиды имеют одинаковый профиль хиральных центров остова, который повышает их стабильность и/или биологическую активность. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает неожиданно повышенную стабильность. Согласно некоторым вариантам осуществления профиль хиральных центров остова неожиданно обеспечивает значительно повышенную активность. Согласно некоторым вариантам осуществления профиль хиральных центров остова обеспечивает, как повышенную стабильность, так и активность. Согласно некоторым вариантам осуществления, когда используется олигонуклеотид, чтобы расщепить полимер нуклеиновой кислоты, профиль хиральных центров остова олигонуклеотида, что удивительно само по себе, изменяет профиль расщепления полимера-мишени нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова эффективно предотвращает расщепление во вторичных сайтах. Согласно некоторым вариантам осуществления профиль хиральных центров остова создает новые сайты расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова минимизирует количество сайтов расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова минимизирует число сайтов расщепления таким образом, что целевой полимер нуклеиновой кислоты расщепляется только в одном сайте в пределах последовательности полимера-мишени нуклеиновой кислоты, которая является комплементарной олигонуклеотиду. Согласно некоторым вариантам осуществления профиль хиральных центров остова повышает эффективность расщепления в сайте расщепления. Согласно некоторым вариантам осуществления профиль хиральных центров остова олигонуклеотида улучшает расщепление полимера-мишени нуклеиновой кислоты. Согласно некоторым вариантам осуществления профиль хиральных центров остова повышает селективность. Согласно некоторым вариантам осуществления профиль хиральных центров остова сводит к минимуму побочный эффект. Согласно некоторым вариантам осуществления профиль хиральных центров остова повышает селективность, например, селективность расщепления среди последовательностей-мишеней, отличающихся точечными мутациями или однонуклеотидными полиморфизмами (SNP). Согласно некоторым вариантам осуществления профиль хиральных центров остова повышает селективность, например, селективность расщепления среди последовательностей-мишеней, отличающихся только одной точечной мутацией или однонуклеотидным полиморфизмом (SNP).
В частности, неожиданно было обнаружено, что некоторые предложенные композиции олигонуклеотидов достигают беспрецедентного контроля отщепления целевых последовательностей, например, отщепления целевой РНК посредством РНКазы Н. Согласно некоторым вариантам осуществления настоящее раскрытие демонстрирует, что точный контроль химических и стереохимических признаков олигонуклеотидов обеспечивает улучшенную активность олигонуклеотидных препаратов по сравнению с другими аналогичными препаратами, для которых стереохимические признаки не контролируются. Среди прочего, настоящее раскрытие конкретно демонстрирует улучшенную скорость, степень и/или специфичность отщепления целевых нуклеиновых кислот, с которыми гибридизуются олигонуклеотиды.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает различные применения композиций олигонуклеотидов. Среди прочего, настоящее раскрытие демонстрирует, что, контролируя структурные элементы олигонуклеотидов, такие как последовательность оснований, химические модификации, стереохимия и т.д., свойства олигонуклеотидов могут быть значительно улучшены. Например, согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы высокоселективного подавления транскриптов целевой последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы лечения субъекта путем подавления транскриптов из вызывающей заболевание копии (например, вызывающего заболевание аллеля). Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы разработки и получения композиций олигонуклеотидов с удивительно усиленной активностью и/или селективностью при подавлении транскрипта целевой последовательности. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы разработки и/или получения композиций олигонуклеотидов, которые обеспечивают аллель-специфическое подавление транскрипта из последовательности целевой нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ контролируемого расщепления полимера нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования полимера нуклеиновой кислоты, нуклеотидная последовательность которого содержит целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, найденной в полимере нуклеиновой кислоты;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова;
причем эта композиция представляет собой хирально контролируемую, поскольку она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ изменения профиля расщепления, наблюдаемый, когда полимер нуклеиновой кислоты, нуклеотидная последовательность которого включает целевую последовательность, контактирует с эталонной композицией олигонуклеотидов, которая содержит олигонуклеотиды, имеющие определенную последовательность основания и длину, причем определенная последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, причем способ предусматривает:
контактирование полимера нуклеиновой кислоты с композицией олигонуклеотидов с контролируемой хиральностью олигонуклеотидов, имеющих определенную последовательность оснований и длину, причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами одного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ контролируемого расщепления полимера нуклеиновой кислоты, предусматривающий обеспечение композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна последовательности, обнаруженной в полимере нуклеиновой кислоты;
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова, причем указанная композиция представляет собой по существу чистый препарат единственного олигонуклеотида в том отношении, что по меньшей мере примерно 10% олигонуклеотидов в композиции имеют одинаковую последовательность оснований и длину, одинаковый профиль линкерных групп остова и одинаковый профиль хиральных центров остова; а также
причем полимер нуклеиновой кислоты расщепляется в профиле расщепления, который отличается от профиля расщепления, когда предусмотрена композиция олигонуклеотида с неконтролируемой хиральностью.
В данном описании профиль расщепления полимера нуклеиновой кислоты определяется числом сайтов расщепления, положением сайтов расщепления и процентом расщепления в каждом сайте. Согласно некоторым вариантам осуществления профиль расщепления имеет несколько сайтов расщепления, а процент расщепления в каждом сайте различен. Согласно некоторым вариантам осуществления профиль расщепления имеет несколько сайтов расщепления, а процент расщепления в каждом сайте такой же. Согласно некоторым вариантам осуществления профиль расщепление имеет только один сайт расщепления. Согласно некоторым вариантам осуществления профили расщепления отличаются друг от друга тем, что они имеют разное количество сайтов расщепления. Согласно некоторым вариантам осуществления профили расщепления отличаются друг от друга тем, что по меньшей мере одно положение расщепления отличается. Согласно некоторым вариантам осуществления профили расщепления отличаются друг от друга тем, что процент расщепления по меньшей мере одного общего сайта расщепления различен. Согласно некоторым вариантам осуществления профили расщепления отличаются друг от друга тем, что они имеют разное количество сайтов расщепления, и/или тем, что отличаются по меньшей мере в одном положении расщепления, и/или тем, что отличается процент расщепления по меньшей мере в одном общем сайте расщепления.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ контролируемого расщепления полимера нуклеиновой кислоты, причем указанный способ предусматривает следующие стадии:
контактирование полимера нуклеиновой кислоты, нуклеотидная последовательность которого содержит целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, обнаруженной в полимере нуклеиновой кислоты;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида, при этом контактирование выполняется в условиях, в которых происходит расщепление полимера нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ изменения первого профиля расщепления полимера нуклеиновой кислоты в результате использования первой композиции олигонуклеотидов, предусматривающий обеспечение второй композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды, определенные как имеющие:
1) одинаковую последовательность оснований и длину, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, обнаруженной в полимере нуклеиновой кислоты;
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова, причем указанная композиция представляет собой по существу чистый препарат единственного олигонуклеотида в том отношении, что по меньшей мере примерно 10% олигонуклеотидов в композиции имеют одинаковую последовательность оснований и длину, одинаковый профиль линкерных групп остова и одинаковый профиль хиральных центров остова; а также
причем полимер нуклеиновой кислоты расщепляется в профиле расщепления, который отличается от первого профиля расщепления.
Согласно некоторым вариантам осуществления настоящее изобретение предусматривает способ изменения профиля расщепления, наблюдаемого тогда, когда полимер нуклеиновой кислоты, нуклеотидная последовательность которого включает целевую последовательность, контактирует с эталонной композицией олигонуклеотидов, которая содержит олигонуклеотиды, имеющие определенную последовательность оснований и длину, причем определенная последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, причем указанный способ предусматривает:
контактирование полимера нуклеиновой кислоты с композицией олигонуклеотидов с контролируемой хиральностью олигонуклеотидов, имеющих определенную последовательность оснований и длину, композиция которых представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами единственного типа олигонуклеотида, характеризующегося:
1) определенной последовательностью оснований и длиной;
2) определенным профилем линкерных групп остова; а также
3) определенным профилем хиральных центров остова,
контактирование выполняется в условиях, в которых происходит расщепление полимера нуклеиновой кислоты.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью уменьшает количество сайтов расщепления в пределах целевой последовательности. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью обеспечивает односайтовое расщепление в пределах целевой последовательности. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает повышенную скорость расщепления в сайте расщепления в пределах целевой последовательности. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает повышенную эффективность в сайте расщепления в пределах целевой последовательности. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает повышенный оборот в расщеплении целевого полимера нуклеиновой кислоты. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью увеличивает процент расщепления в сайте внутри или вблизи характеристического элемента последовательности. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью увеличивает процент расщепления в сайте вблизи мутации. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью увеличивает процент расщепления в сайте вблизи SNP. Иллюстративные варианты реализации сайта внутри или вблизи характеристического элемента последовательности, вблизи мутации, вблизи SNP, описаны в настоящем раскрытии. Например, согласно некоторым вариантам осуществления сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от мутации; в некоторых других вариантах реализации сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от SNP.
Согласно некоторым вариантам осуществления расщепление происходит с профилем расщепления, отличающимся от эталонного профиля расщепления. Согласно некоторым вариантам осуществления эталонный профиль расщепления представляет собой тот, который наблюдается, когда полимер нуклеиновой кислоты вводят в контакт в сравнимых условиях с эталонной композицией олигонуклеотидов. Согласно некоторым вариантам осуществления эталонная композиция олигонуклеотидов представляет собой композицию олигонуклеотидов с неконтролируемой хиральностью (например, стереослучайную) олигонуклеотидов, которые характеризуются одинаковой последовательностью оснований и длиной композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления эталонная композиция олигонуклеотидов представляет собой по существу рацемический препарат олигонуклеотидов, которые характеризуются одинаковой последовательностью и длиной.
Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты представляет собой РНК. Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты представляет собой олигонуклеотид. Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты представляет собой олигонуклеотид-РНК. Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты представляет собой транскрипт. Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции олигонуклеотидов с контролируемой хиральностью образуют дуплексы с полимером нуклеиновой кислоты для расщепления.
Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты расщепляется ферментом. Согласно некоторым вариантам осуществления фермент расщепляет дуплекс, образованный полимером нуклеиновой кислоты. Согласно некоторым вариантам осуществления фермент представляет собой РНКазу Н. Согласно некоторым вариантам осуществления фермент представляет собой дайсер. Согласно некоторым вариантам осуществления фермент представляет собой белок аргонавт. Согласно некоторым вариантам осуществления фермент представляет собой Ago2. Согласно некоторым вариантам осуществления фермент находится в пределах белкового комплекса. Пример белкового комплекса представляет собой индуцированный РНК комплекс сайленсинга (RISC).
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды с одинаковым профилем хиральных центров остова, обеспечивает неожиданно такую высокую селективность, что полимеры нуклеиновых кислот, у которых имеются только небольшие вариации последовательности в пределах области-мишени, могут подвергаться селективному направленному воздействию. Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты представляет собой транскрипт из аллеля. Согласно некоторым вариантам осуществления на транскрипты из различных аллелей могут быть селективно направлены предложенные композиции олигонуклеотидов с контролируемой хиральностью.
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью и способы их применения позволяют точно контролировать сайты расщепления в пределах целевой последовательности. Согласно некоторым вариантам осуществления сайт расщепления находится вокруг последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится выше против хода транскрипции и вблизи последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 5 пар оснований выше против хода транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 4 пар оснований выше против хода транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 3 пар оснований выше против хода транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 2 пар оснований выше против хода транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 1 пары оснований выше против хода транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится ниже по ходу транскрипции и вблизи последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 5 пар оснований ниже по ходу транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 4 пар оснований ниже по ходу транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 3 пар оснований ниже по ходу транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 2 пар оснований ниже по ходу транскрипции от последовательности хиральных центров остова RpSpSp. Согласно некоторым вариантам осуществления сайт расщепления находится в пределах 1 пары оснований ниже по ходу транскрипции от последовательности хиральных центров остова RpSpSp. Помимо всего прочего, настоящее раскрытие, таким образом, обеспечивает контроль над сайтами расщепления в пределах целевой последовательности. Согласно некоторым вариантам осуществления иллюстративное расщепление изображено на фиг. 21. Согласно некоторым вариантам осуществления расщепление, изображенное на фиг. 21, обозначается как расщепление в сайте в двух парах оснований ниже по ходу транскрипции от последовательности хиральных центров остова RpSpSp. Как подробно описано в настоящем описании, последовательность хиральных центров остова RpSpSp можно обнаружить в единственном или повторяющихся звеньях (Np)m(Rp)n(Sp)t, (Np)t(Rp)n(Sp)m, (Sp)m(Rp)n(Sp)t, (Sp)t(Rp)n(Sp)m, (Rp)n(Sp)m, (Rp)m(Sp)n, (Sp)mRp и/или Rp(Sp)m, каждый из которых независимо является таким, как определено выше и описано в данном документе. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью создает новый сайт расщепления в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени (например, фиг. 21), причем указанный новый сайт расщепления не существует, если используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов (не может быть обнаружена). Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте расщепления в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени (например, фиг. 21), причем расщепление в таком сайте происходит с более высоким процентом, чем если используется эталонная (например, без контролируемой хиральности) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления расщепление в таком сайте с помощью предложенной композиции олигонуклеотидов с контролируемой хиральностью превышает по меньшей мере в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 500 или 1000 раз расщепление, осуществляемой с помощью эталонной композиции олигонуклеотидов (например, при измерении по проценту расщепления в сайте). Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью обеспечивает ускоренное расщепление в сайте расщепления в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени (например, фиг. 21), чем если используется эталонная (например, без контролируемой хиральности) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления расщепление в таком сайте с помощью предложенной композиции олигонуклеотидов с контролируемой хиральностью происходит по меньшей мере в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 500 или 1000 раз быстрее, чем расщепление, осуществляемое с помощью эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления сайт расщепления предложенной композиции олигонуклеотидов с контролируемой хиральностью в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени (например, смотрите фиг. 21) представляет собой сайт расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления сайт расщепления предложенной композиции олигонуклеотидов с контролируемой хиральностью в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени (например, смотрите фиг. 21) находится в пределах одной пары оснований от сайта расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления сайт расщепления предложенной композиции олигонуклеотидов с контролируемой хиральностью в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени (например, смотрите фиг. 21) находится в пределах двух пар оснований от сайта расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления он находится в пределах 3 пар оснований. Согласно некоторым вариантам осуществления он находится в пределах 4 пар оснований. Согласно некоторым вариантам осуществления он находится в пределах 5 пар оснований. Согласно некоторым вариантам осуществления сайт расщепления предложенной композиции олигонуклеотидов с контролируемой хиральностью в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени является одним из основных сайтов расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления такой сайт является сайтом расщепления с наибольшим процентом расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления сайт расщепления предложенной композиции олигонуклеотидов с контролируемой хиральностью в 2 парах оснований ниже по ходу транскрипции от хиральных центров остова RpSpSp в молекуле-мишени является одним из сайтов расщепления с более высокой скоростью расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов. Согласно некоторым вариантам осуществления такой сайт является сайтом расщепления с самой высокой скоростью расщепления, когда используется эталонная (например, с неконтролируемой хиральностью) композиция олигонуклеотидов.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в одном или более сайтах, например, по отношению к эталонной (например, с неконтролируемой хиральностью/стереослучайной) композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в единственном сайте относительно эталонной (например, с неконтролируемой хиральностью/стереослучайной) композиции. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте, обеспечивая более высокую скорость расщепления. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте, обеспечивая более высокий процент расщепления в указанном сайте. Процент расщепления в сайте может быть определен различными способами, широко известными и практикуемыми в данной области техники. Согласно некоторым вариантам осуществления процент расщепления в сайте определяется с помощью анализа продуктов расщепления, например, с помощью ВЭЖХ-МС, как показано на фиг. 18, фиг. 19 и фиг. 30; смотрите также иллюстративные карты отщепления, такие как фиг. 9, фиг. 10, фиг. 11, фиг. 14, фиг. 22, фиг. 25 и 26. Согласно некоторым вариантам осуществления усиление представляет собой усиление относительно эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления усиление представляет собой усиление относительно другого сайта расщепления. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте, который является предпочтительным сайтом расщепления эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предпочтительный сайт расщепления или группа предпочтительных сайтов расщепления является сайтом или сайтами, которые имеют относительно высокий процент расщепления по сравнению с одним или несколькими другими сайтами расщепления. Согласно некоторым вариантам осуществления предпочтительные сайты расщепления могут указывать на предпочтение в ферменте. Например, для РНКазы Н, когда используют олигонуклеотид ДНК, полученные в результате сайты расщепления могут указывать на предпочтение РНКазы Н. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте, который является предпочтительным сайтом расщепления ферментом. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте, который не является предпочтительным сайтом расщепления эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте, который не является предпочтительным сайтом расщепления эталонной композиции олигонуклеотидов, эффективно создавая новый сайт расщепления, который не существует, когда используется эталонная композиция олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте в пределах 5 пар оснований от нацеленной мутации или SNP, тем самым увеличивая селективное расщепление нежелательного олигонуклеотида-мишени. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте в пределах 4 пар оснований от нацеленной мутации или SNP, тем самым увеличивая селективное расщепление нежелательного олигонуклеотида-мишени. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте в пределах 3 пар оснований от нацеленной мутации или SNP, тем самым увеличивая селективное расщепление нежелательного олигонуклеотида-мишени. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте в пределах 2 пар оснований от нацеленной мутации или SNP, тем самым увеличивая селективное расщепление нежелательного олигонуклеотида-мишени. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление в сайте непосредственно выше против хода транскрипции или ниже по ходу транскрипции нацеленной мутации или SNP, тем самым увеличивая селективное расщепление нежелательного олигонуклеотида-мишени (например, фиг. 22, Панель D, мутанта. РНК).
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в одном или нескольких сайтах, например, по отношению к эталонной (например, с неконтролируемой хиральностью/стереослучайной) композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в единственном сайте относительно эталонной (например, с неконтролируемой хиральностью/стереослучайной) композиции. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в сайте, обеспечивая более низкую скорость расщепления. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в сайте, обеспечивая более низкий процент расщепления в указанном сайте. Согласно некоторым вариантам осуществления подавление представляет собой подавление относительно эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления подавление представляет собой подавление относительно другого сайта расщепления. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в сайте, который является предпочтительным сайтом расщепления эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предпочтительный сайт расщепления или группа предпочтительных сайтов расщепления является сайтом или сайтами, которые имеют относительно высокий процент расщепления по сравнению с одним или несколькими другими сайтами расщепления. Согласно некоторым вариантам осуществления предпочтительные сайты расщепления могут указывать на предпочтение в ферменте. Например, для РНКазы Н, когда используют олигонуклеотид ДНК, полученные в результате сайты расщепления могут указывать на предпочтение РНКазы Н. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в сайте, который является предпочтительным сайтом расщепления ферментом. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью подавляет расщепление в сайте, который не является предпочтительным сайтом расщепления эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью подавляет все сайты расщепления эталонной композиции олигонуклеотидов. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью в целом улучшает расщепление олигонуклеотидов-мишеней. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью, как правило, подавляет расщепление олигонуклеотидов-не мишеней. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью усиливает расщепление олигонуклеотидов-мишеней и подавляет расщепление олигонуклеотидов-не мишеней. Используя фиг. 22, панель D, в качестве примера, целевой олигонуклеотид для расщепления представляет собой мутантную РНК, в то время как нецелевой олигонуклеотид представляет собой РНК дикого типа. У субъекта, содержащего патологическую ткань с мутацией или SNP, целевой олигонуклеотид для расщепления может представлять собой транскрипты с мутацией или SNP, в то время как нецелевой олигонуклеотид может представлять собой нормальные транскрипты без мутации или SNP, такие как те, которые экспрессируются в здоровых тканях.
Согласно некоторым вариантам осуществления эталонная композиция олигонуклеотидов представляет собой стереослучайную композицию олигонуклеотидов. Согласно некоторым вариантам осуществления эталонная композиция олигонуклеотидов представляет собой стереослучайную композицию олигонуклеотидов, из которых все межнуклеотидные линкерные группы являются фосфоротиоатом. Согласно некоторым вариантам осуществления эталонная композиция олигонуклеотидов представляет собой композицию олигонуклеотидов ДНК со всеми фосфатными линкерными группами.
Согласно некоторым вариантам осуществления, помимо профилей хиральных центров остова, описанных в настоящем документе, предложенные олигонуклеотиды необязательно содержат модифицированные основания, модифицированные сахара, модифицированные линкерные группы остова и любые их комбинации. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой унимер, альтмер, блокмер, гэпмер, гемимер и скипмер. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит один или более фрагментов унимера, альтмера, блокмера, гэпмера, гемимера и скипмера или любые их комбинации. Согласно некоторым вариантам осуществления, помимо профилей хиральных центров остова в данном описании, предложенный олигонуклеотид представляет собой гемимер. Согласно некоторым вариантам осуществления, помимо профилей хиральных центров остова в данном описании, предложенный олигонуклеотид представляет собой 5'-гемимер с модифицированными фрагментами сахара. Согласно некоторым вариантам осуществления предложенный олигонуклеотид представляет собой 5'-гемимер с 2'-модифицированными фрагментами сахара. Подходящие модификации широко известны в данной области техники, например, те, которые описаны в настоящей заявке. Согласно некоторым вариантам осуществления модификация представляет собой 2'-F. Согласно некоторым вариантам осуществления модификация представляет собой 2'-МОЕ. Согласно некоторым вариантам осуществления модификация представляет собой s-cEt.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевой последовательности нуклеиновой кислоты, так и аналогичной последовательности нуклеиновой кислоты, транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для аналогичной последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевой последовательности нуклеиновой кислоты, так и аналогичной последовательности нуклеиновой кислоты, транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для аналогичной последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой или содержит последовательность, которая на 100% комплементарна характеристическим элементам последовательности. Согласно некоторым вариантам осуществления подавление можно оценить с помощью различных подходящих анализов, известных специалисту в данной области техники. Согласно некоторым вариантам осуществления анализ представляет собой анализ с помощью РНКазы Н, как описано в настоящем описании, который может оценивать подавление путем оценки расщепления последовательности, обнаруженной в транскрипте целевой последовательности нуклеиновой кислоты, содержащей характеристический элемент последовательности, и расщепления последовательности, обнаруженной в транскрипт аналогичной последовательности. Согласно некоторым вариантам осуществления транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для любой аналогичной последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления иллюстративная целевая и аналогичная последовательности описаны в настоящем раскрытии.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель относительно других аллелей одной и той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет определенный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же самой последовательности нуклеиновой кислоты, транскрипты определенного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же самой последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями той же целевой последовательности нуклеиновой кислоты, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же последовательности нуклеиновой кислоты, транскрипты конкретного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями той же целевой последовательности нуклеиновой кислоты, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, при этом композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же последовательности нуклеиновой кислоты, транскрипты конкретного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты,
контактирование осуществляется в условиях, определенных как позволяющие композиции подавлять транскрипты определенного аллеля.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями той же целевой последовательности нуклеиновой кислоты, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что, когда она контактирует с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она показывает подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
с) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями той же целевой последовательности нуклеиновой кислоты, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, при этом композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она проявляет подавление транскриптов определенного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями той же целевой последовательности нуклеиновой кислоты, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, при этом композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она проявляет подавление транскриптов определенного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
с) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты,
контактирование осуществляется в условиях, определенных как позволяющие композиции подавлять транскрипты конкретного аллеля.
Согласно некоторым вариантам осуществления транскрипт подавляется путем расщепления указанного транскрипта. Согласно некоторым вариантам осуществления специфический нуклеотидный характеристический элемент последовательности находится в интроне. Согласно некоторым вариантам осуществления специфический нуклеотидный характеристический элемент последовательности находится в экзоне. Согласно некоторым вариантам осуществления специфический нуклеотидный характеристический элемент последовательности находится частично в экзоне и частично в интроне. Согласно некоторым вариантам осуществления специфический нуклеотидный характеристический элемент последовательности содержит мутацию, которая дифференцирует аллель от других аллелей. Согласно некоторым вариантам осуществления мутация представляет собой делецию. Согласно некоторым вариантам осуществления мутация представляет собой вставку. Согласно некоторым вариантам осуществления мутация представляет собой точечную мутацию. Согласно некоторым вариантам осуществления специфический нуклеотидный характеристический элемент последовательности содержит по меньшей мере один однонуклеотидный полиморфизм (SNP), который отличает аллель от других аллелей.
Согласно некоторым вариантам осуществления целевая последовательность нуклеиновой кислоты представляет собой целевой ген.
Согласно некоторым вариантам осуществления настоящее изобретение предусматривает способ аллель-специфического подавления гена, последовательность которого содержит по меньшей мере один однонуклеотидный полиморфизм (SNP), предусматривающий обеспечение композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды, определенные как имеющие:
1) одинаковую последовательность оснований и длину, причем общая последовательность оснований представляет собой или содержит последовательность, которая полностью комплементарна последовательности, обнаруженной в транскрипте от первого аллеля, но не соответствующей последовательности, обнаруженной в транскрипте от второго аллеля, причем последовательность, обнаруженная в транскриптах, содержит сайт SNP;
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова; причем композиция представляет собой по существу чистый препарат единственного олигонуклеотида в том отношении, что по меньшей мере примерно 10% олигонуклеотидов в композиции имеют одинаковую последовательность оснований и длину, одинаковый профиль линкерных групп остова и одинаковый профиль хиральных центров остова;
причем транскрипт от первого аллеля подавляется по меньшей мере в пять раз сильнее, чем от второго аллеля.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями одного и того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину;
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля, подавляются в степени по меньшей мере в 2 раза превышающей степень подавления, наблюдаемую для другого аллеля того же самого гена.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевого гена, для которого существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями того же целевого гена, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты, как целевого аллеля, так и другого аллеля того же самого гена, транскрипты конкретного аллеля подавляются по меньшей мере в 2 раза сильнее, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевого гена, для которого существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями того же целевого гена, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем указанная композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты, как целевого аллеля, так и другого аллеля того же самого гена, транскрипты конкретного аллеля подавляются по меньшей мере в 2 раза сильнее, чем степень подавления, наблюдаемая для другого аллеля того же гена,
контактирование осуществляется в условиях, определенных как позволяющие композиции подавлять транскрипты конкретного аллеля.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевого гена, для которого существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями того же целевого гена, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, при этом композиция характеризуется тем, что, когда она вступает в контакт с системой, содержащей транскрипты, как целевого аллеля, так и другого аллеля того же самого гена, транскрипты конкретного аллеля подавляются по меньшей мере в 2 раза сильнее, чем степень подавления, наблюдаемая для другого аллеля того же гена,
контактирование осуществляется в условиях, определенных как позволяющие композиции подавлять транскрипты конкретного аллеля.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями одного и того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину;
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
а) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта от целевого гена, для которого существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями того же целевого гена, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что, когда она вступает в контакт с системой, экспрессирующей транскрипты целевого гена, она показывает подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта от целевого гена, для которого существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями того же целевого гена, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, при этом композиция характеризуется тем, что, когда она вступает в контакт с системой, экспрессирующей транскрипты целевого гена, она показывает подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена,
контактирование осуществляется в условиях, определенных как позволяющие композиции подавлять транс крипты конкретного аллеля.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ аллель-специфического подавления транскрипта целевого гена, для которого существует множество аллелей в пределах популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по сравнению с другими аллелями того же целевого гена, причем указанный способ предусматривает следующие стадии:
контактирование образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция представляет собой композицию с контролируемой хиральностью в том отношении, что она обогащена по отношению к по существу рацемическому препарату олигонуклеотидов, имеющих ту же самую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что, когда она вступает в контакт с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена,
контактирование осуществляется в условиях, определенных как позволяющие композиции подавлять транскрипты конкретного аллеля.
Как описано в настоящем документе, согласно некоторым вариантам осуществления в предусмотренном способе контактирование осуществляют в условиях, определенных для того, чтобы позволить композиции подавлять транскрипты конкретного аллеля. Согласно некоторым вариантам осуществления контактирование осуществляют в условиях, определенных для того, чтобы позволить композиции подавлять экспрессию определенного аллеля.
Согласно некоторым вариантам осуществления подавление транскриптов конкретного аллеля происходит в степени, которая больше, чем когда композиция отсутствует. Согласно некоторым вариантам осуществления подавление транскриптов конкретного аллеля происходит в степени, которая по меньшей мере в 1,1 раза больше по отношению к тому, когда композиция отсутствует, в том отношении, что транскрипты от конкретных аллелей обнаруживаются в количествах, которые по меньшей мере в 1,1 раза меньше, когда композиция присутствует по отношению к тому, когда она отсутствует. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,2 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,3 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,4 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,5 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,6 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,7 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,8 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,9 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 2 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 3 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 4 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 5 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 6 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 7 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 8 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 9 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 10 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 11 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 12 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 13 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 14 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 15 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 20 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 30 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 40 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 50 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 75 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 100 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 150 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 200 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 300 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 400 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 500 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 750 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1000 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 5000 раз больше.
Согласно некоторым вариантам осуществления подавление транскриптов конкретного аллеля происходит в степени, которая больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления подавление транскриптов конкретного аллеля происходит в степени, которая по меньшей мере в 1,1 раза больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,2 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,3 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,4 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,5 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,6 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,7 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,8 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1,9 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 2 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 3 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 4 раза больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 5 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 6 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 7 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 8 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 9 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 10 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 11 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 12 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 13 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 14 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 15 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 20 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 30 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 40 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 50 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 75 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 100 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 150 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 200 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 300 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 400 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 500 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 750 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 1000 раз больше. Согласно некоторым вариантам осуществления степень по меньшей мере в 5000 раз больше.
Согласно некоторым вариантам осуществления подавление транскриптов конкретного аллеля происходит в такой степени, которая больше, чем когда композиция отсутствует, в степени, которая превышает степень подавления, наблюдаемую для другого аллеля той же последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления подавление транскриптов конкретного аллеля происходит в степени, которая по меньшей мере в 1,1 раза больше по сравнению с тем, когда композиция отсутствует, и по меньшей мере 1,1 раза больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления каждая кратность независимо является такой, как описано выше.
Согласно некоторым вариантам осуществления система представляет собой композицию, содержащую транскрипт. Согласно некоторым вариантам осуществления система представляет собой композицию, содержащую транскрипты от различных аллелей. Согласно некоторым вариантам осуществления система может быть in vivo или in vitro, и в любом случае может содержать одну или более клеток, тканей, органов или организмов. Согласно некоторым вариантам осуществления система содержит одну или более клеток. Согласно некоторым вариантам осуществления система содержит одну или более тканей. Согласно некоторым вариантам осуществления система содержит один или более органов. Согласно некоторым вариантам осуществления система содержит один или более организмов. Согласно некоторым вариантам осуществления система является субъектом.
Согласно некоторым вариантам осуществления подавление транскрипта или подавление экспрессии аллеля, из которого транскрибируется транскрипт, можно измерить в анализе in vitro. Согласно некоторым вариантам осуществления последовательность от транскрипта и содержащая специфический нуклеотидный характеристический элемент последовательности используется в анализах вместо полноразмерного транскрипта. Согласно некоторым вариантам осуществления анализ представляет собой биохимический анализ. Согласно некоторым вариантам осуществления анализ представляет собой биохимический анализ, причем полимер нуклеиновой кислоты, например, транскрипт или последовательность от транскрипта и содержащий специфический нуклеотидный характерной элемент последовательности исследуют на наличие расщепления ферментом в присутствии композиции олигонуклеотидов с контролируемой хиральностью.
Согласно некоторым вариантам осуществления предложенную композицию олигонуклеотидов с контролируемой хиральностью вводят субъекту. Согласно некоторым вариантам осуществления субъект представляет собой животное. Согласно некоторым вариантам осуществления субъект представляет собой растение. Согласно некоторым вариантам осуществления субъектом является человек.
Согласно некоторым вариантам осуществления для аллель-специфического подавления транскриптов от конкретного аллеля, транскрипты расщепляют в сайте вблизи различия последовательностей, например, мутации, в пределах специфического нуклеотидного характеристического элемента последовательности, причем различие последовательностей дифференцирует транскрипты от конкретного аллеля от транскриптов от других аллелей. Согласно некоторым вариантам осуществления транскрипты селективно расщепляются в сайте вблизи такого различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются с более высоким процентом в сайте вблизи такого различия последовательностей, чем когда используется композиция олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются только в сайте различия последовательностей внутри специфического нуклеотидного характеристического элемента последовательности. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 5 пар оснований ниже по ходу транскрипции или выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 4 пар оснований ниже по ходу транскрипции или выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 3 пар оснований ниже по ходу транскрипции или выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 2 пар оснований ниже по ходу транскрипции или выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 1 пары оснований ниже по ходу транскрипции или выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 5 пар оснований ниже по ходу транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 4 пар оснований ниже по ходу транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 3 пар оснований ниже по ходу транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 2 пар оснований ниже по ходу транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 1 пары оснований ниже по ходу транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 5 пар оснований выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 4 пар оснований выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 3 пар оснований выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах 2 пар оснований выше против хода транскрипции от различия последовательностей. Согласно некоторым вариантам осуществления транскрипты расщепляются в сайте в пределах в пределах 1 пары оснований выше против хода транскрипции от различия последовательностей. Такой точный контроль профилей расщепления и полученное в результате высоко избирательное подавление транскриптов от определенного аллеля не было бы возможно без композиций олигонуклеотидов с контролируемой хиральностью и способов их применения, предоставленных заявителем в данном описании.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы лечения субъекта или профилактики заболевания у субъекта путем специфического подавления транскриптов от конкретного аллеля, например, аллеля, который вызывает или может вызвать заболевание. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы лечения субъекта, страдающего от заболевания, предусматривающие введение субъекту фармацевтической композиции, содержащей композицию олигонуклеотидов с контролируемой хиральностью, причем транскрипты от аллеля, который вызывает или способствует заболеванию, избирательно подавляются. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы лечения субъекта, страдающего от заболевания, предусматривающие введение субъекту фармацевтической композиции, содержащей композицию олигонуклеотидов с контролируемой хиральностью, причем транскрипты от аллеля, который вызывает заболевание, избирательно подавляются. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы лечения субъекта, страдающего от заболевания, предусматривающие введение субъекту фармацевтической композиции, содержащей композицию олигонуклеотидов с контролируемой хиральностью, причем транскрипты от аллеля, который способствует заболеванию, избирательно подавляются. Согласно некоторым вариантам осуществления настоящее раскрытие относится к способам лечения страдающего от заболевания субъекта, предусматривающим введение субъекту фармацевтической композиции, содержащей композицию олигонуклеотидов с контролируемой хиральностью, причем транскрипты от аллеля, который связан с заболеванием, избирательно подавляются. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы профилактики заболевания у субъекта, путем специфического подавления транскриптов от конкретного аллеля, который может вызвать заболевание. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы профилактики заболевания у субъекта путем специфического подавления транскриптов от конкретного аллеля, который повышает риск заболевания у субъекта. Согласно некоторым вариантам осуществления предложенный способ предусматривает введение субъекту фармацевтической композиции, содержащей композицию олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления фармацевтическая композиция дополнительно содержит фармацевтически приемлемый носитель.
Согласно некоторым вариантам осуществления нуклеотидная характеристическая последовательность содержит мутацию, которая определяет целевую последовательность относительно других аналогичных последовательностей. Согласно некоторым вариантам осуществления нуклеотидная характеристическая последовательность содержит точечную мутацию, которая определяет целевую последовательность относительно других аналогичных последовательностей. Согласно некоторым вариантам осуществления нуклеотидная характеристическая последовательность содержит SNP, который определяет целевую последовательность относительно других аналогичных последовательностей.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ получения композиции олигонуклеотидов для избирательного подавления транскрипта целевой последовательности нуклеиновой кислоты, предусматривающий предоставление композиции олигонуклеотидов, содержащей предопределенный уровень олигонуклеотидов определенного типа олигонуклеотида, характеризующийся:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова, профиль которых содержит (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где каждый из m, n, t, Np независимо является таким, как определено и описано в настоящем документе;
причем целевая последовательность нуклеиновой кислоты содержит характеристический элемент последовательности, который определяет целевую последовательность нуклеиновой кислоты относительно аналогичной последовательности нуклеиновой кислоты;
причем одинаковая последовательность оснований представляет собой последовательность, чей профиль расщепления ДНК и/или стереослучайный профиль расщепления содержит сайт расщепления внутри или вблизи характеристического элемента последовательности.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ получения композиции олигонуклеотидов для избирательного подавления транскрипта целевой последовательности нуклеиновой кислоты, предусматривающий предоставление композиции олигонуклеотидов, содержащей предопределенный уровень олигонуклеотидов определенного типа олигонуклеотида, характеризующийся:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова, профиль которых содержит (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где каждый из m, n, t, Np независимо является таким, как определено и описано в настоящем документе;
причем целевая последовательность нуклеиновой кислоты содержит характеристический элемент последовательности, который определяет целевую последовательность нуклеиновой кислоты относительно аналогичной последовательности нуклеиновой кислоты;
причем одинаковая последовательность оснований представляет собой последовательность, чей профиль расщепления ДНК и/или стереослучайный профиль расщепления содержит сайт расщепления внутри или вблизи характеристического элемента последовательности.
Согласно некоторым вариантам осуществления одинаковый профиль хиральных центров остова содержит (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, как описано выше. Согласно некоторым вариантам осуществления одинаковый профиль хиральных центров остова содержит (Sp)m(Rp)n, как описано выше. Согласно некоторым вариантам осуществления одинаковый профиль хиральных центров остова содержит (Rp)n(Sp)m, как описано выше. Согласно некоторым вариантам осуществления одинаковый профиль хиральных центров остова содержит (Np)t(Rp)n(Sp)m, как описано выше. Согласно некоторым вариантам осуществления одинаковый профиль хиральных центров остова содержит (Sp)t(Rp)n(Sp)m, как описано выше. Согласно некоторым вариантам осуществления n равно 1. Согласно некоторым вариантам осуществления m>2. Согласно некоторым вариантам осуществления n равно 1 и m>2. Согласно некоторым вариантам осуществления t>2. Согласно некоторым вариантам осуществления n равно 1, m>2 и t>2.
Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа олигонуклеотида характеризуются структурой крыло-сердцевина. Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа олигонуклеотида характеризуются структурой сердцевины. Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа олигонуклеотида характеризуются структурой крыло-сердцевина. Согласно некоторым вариантам осуществления каждый фрагмент сахара в областях крыла содержит модификацию сахара. В некоторых вариантах каждый фрагмент сахара в областях крыла содержит 2'-модификацию. Согласно некоторым вариантам осуществления каждый фрагмент сахара в областях крыла содержит 2'-модификацию, причем 2'-модификация представляет собой 2'-OR1, где R1 представляет собой необязательно замещенный C1-6 алкил. В некоторых вариантах каждый фрагмент сахара в областях крыла содержит 2'-ОМе. Согласно некоторым вариантам осуществления каждое крыло независимо содержит хиральную межнуклеотидную линкерную группу и линкерную группу с природным фосфатом. Согласно некоторым вариантам осуществления хиральная межнуклеотидная линкерная группа представляет собой фосфоротиоат. Согласно некоторым вариантам осуществления для структуры крыло-сердцевина, как и в WV-1092, 5'-крыло содержит межнуклеотидную линкерную группу Sp на каждом из своих 5'- и 3'-концов и фосфатные линкерные группы между ними, а 3'-крыло содержит межнуклеотидную линкерную группу Sp на своем 3'-конце, а остальные ее межнуклеотидные линкерные группы представляют собой фосфат. Дополнительные варианты реализации для крыла и/или сердцевины, например, модификация сахара, стереохимия и т.д., описаны в настоящем описании.
Обычные последовательности оснований, которые представляют собой последовательности, у которых профили расщепления ДНК и/или стереослучайные профили расщепления имеют сайты расщепления внутри или вблизи целевой последовательности нуклеиновой кислоты, подробно описаны в настоящем раскрытии. Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи целевой последовательности нуклеиновой кислоты представляет собой сайт расщепления вблизи мутации, которая определяет целевую последовательность от ее аналогичных последовательностей. Согласно некоторым вариантам осуществления сайт расщепления внутри или вблизи целевой последовательности нуклеиновой кислоты представляет собой сайт расщепления вблизи SNP, который определяет целевую последовательность от ее аналогичных последовательностей. Согласно некоторым вариантам осуществления, как описано выше, вблизи мутации или SNP представляет собой в 0, 1, 2, 3, 4, 5 межнуклеотидных линкерных группах от мутации или SNP. Дополнительные варианты осуществления описаны выше в настоящем раскрытии.
Согласно некоторым вариантам осуществления одинаковая последовательность оснований представляет собой последовательность, у которой профиль расщепления ДНК и/или стереослучайный профиль расщепления имеет основной сайт расщепления внутри или вблизи целевой последовательности нуклеиновой кислоты. Согласно некоторым вариантам осуществления основной сайт расщепления определяется абсолютным расщеплением в этом сайте (% расщепления в этом сайте по всей целевой последовательности). Дополнительные примеры вариантов осуществления основного сайта расщепления описаны в настоящем описании. Согласно некоторым вариантам осуществления, как проиллюстрировано на фиг. 33, одинаковая последовательность оснований (P12) может быть идентифицирована путем сравнения карт расщепления различных последовательностей, комплементарных характеристическому элементу последовательности.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способ получения композиции олигонуклеотидов, содержащей олигонуклеотиды определенной последовательности, причем эта композиция обеспечивает избирательное подавление транскрипта целевой последовательности, предусматривающий предоставление композиции олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований, которая является такой же, как определенная последовательность;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова, профиль которых содержит (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где:
каждый n и t независимо представляет собой 1, 2, 3, 4, 5, 6, 7 или 8;
m равно 2, 3, 4, 5, 6, 7 или 8 и
каждый Np представляет собой независимо Rp или Sp.
Заболевания, который включают вызывающие заболевания аллели, широко известны в данной области техники, включая, но без ограничения ими, описанные в Hohjoh, Pharmaceuticals 2013, 6, 522-535; публикации заявки на патент США US 2013/0197061; ∅stergaard et al., Nucleic Acids Research 2013, 41(21), 9634-9650 и Jiang et al., Science 2013, 342, 111-114. Согласно некоторым вариантам осуществления заболевание представляет собой болезнь Хантингтона. Согласно некоторым вариантам осуществления заболевание представляет собой гипертрофическую кардиомиопатию человека (ГКМ). Согласно некоторым вариантам осуществления заболевание представляет собой дилатационную кардиомиопатию. Согласно некоторым вариантам осуществления вызывающий заболевание аллель представляет собой аллель тяжелых цепей миозина (МНС). Согласно некоторым вариантам осуществления иллюстративное заболевание выбирают из:

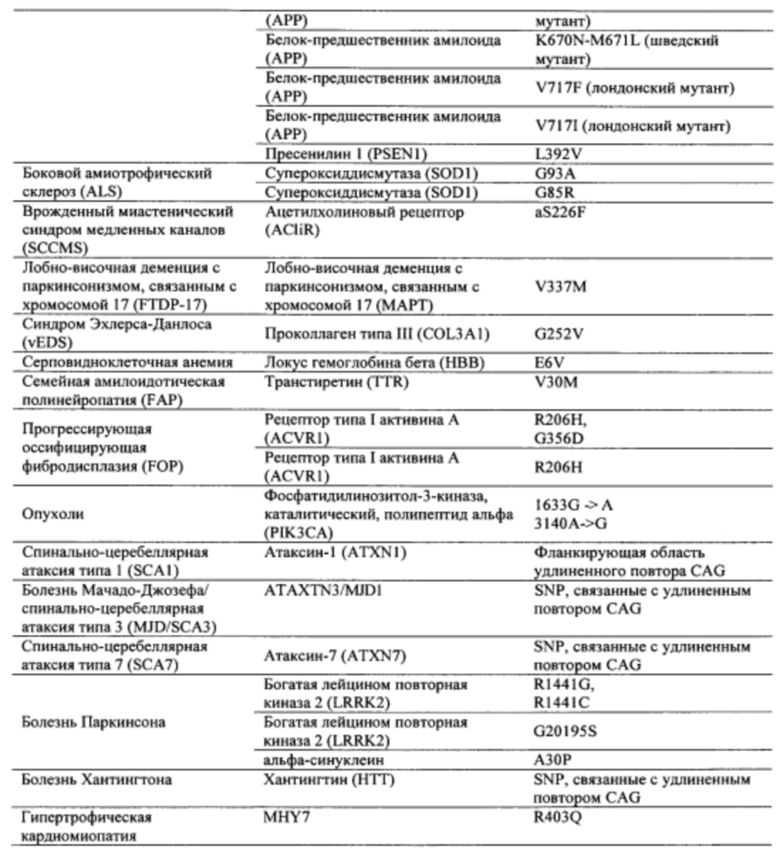
Согласно некоторым вариантам осуществления иллюстративные мишени и заболевания, которые можно лечить с помощью предложенных композиций олигонуклеотидов с контролируемой хиральностью, включают:

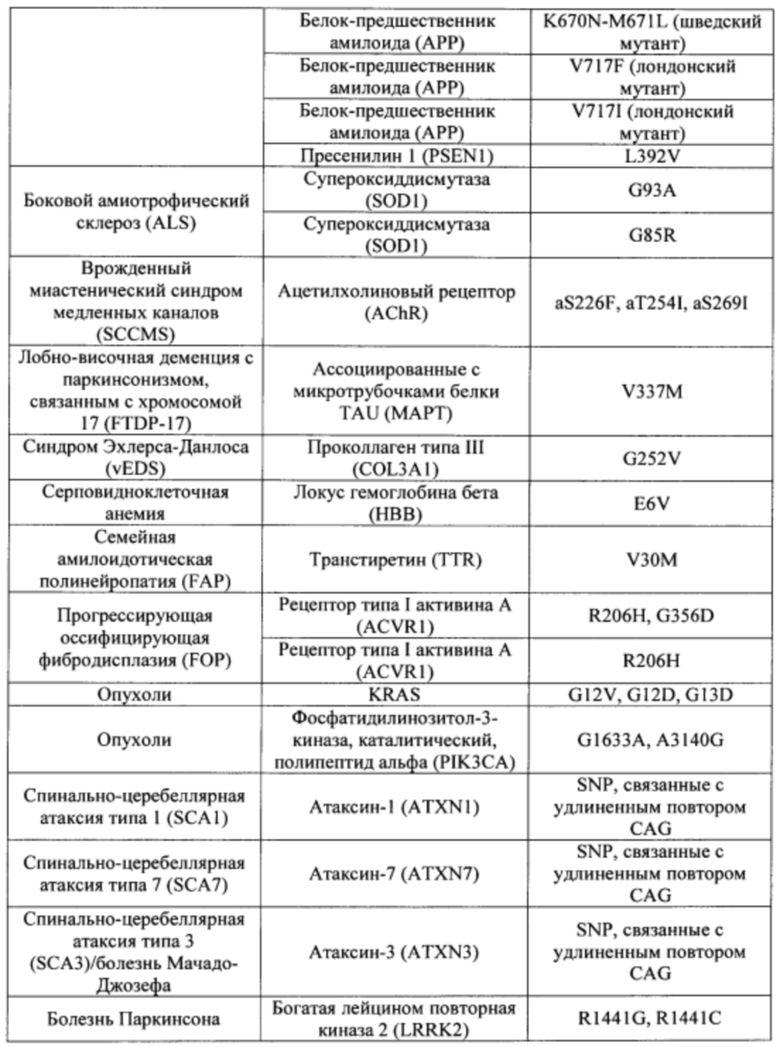
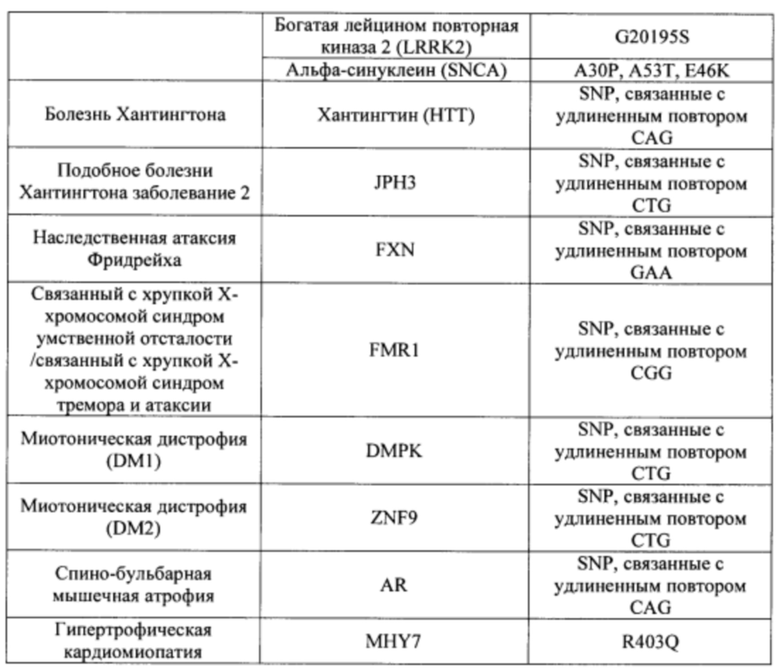
Согласно некоторым вариантам осуществления композиции олигонуклеотидов и технологии, описанные в настоящем документе, особенно применимы для лечения болезни Хантингтона. Например, согласно некоторым вариантам осуществления настоящее описание определяет стереохимически контролируемые композиции олигонуклеотидов, которые направляют расщепление (например, опосредованное РНКазой Н расщепление) нуклеиновых кислот, связанных с болезнью Хантингтона. Согласно некоторым вариантам осуществления такие композиции обеспечивают прямое преимущественное расщепление связанного с болезнью Хантингтона аллеля определенной целевой последовательности, относительно одного или более (например, всех не связанных с болезнью Хантингтона) других аллелей последовательности.
Согласно некоторым вариантам осуществления предусмотрен способ лечения или профилактики болезни Хантингтона у субъекта, предусматривающий введение субъекту композиции олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида. Согласно некоторым вариантам осуществления олигонуклеотиды определенного типа олигонуклеотида являются идентичными. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью.
SNP, связанные с болезнью Хантингтона, широко известны в данной области техники. Согласно некоторым вариантам осуществления одинаковая последовательность оснований комплементарна последовательности нуклеиновой кислоты, содержащей SNP, связанный с болезнью Хантингтона. Согласно некоторым вариантам осуществления предложенная композиция избирательно подавляет транскрипты из вызывающего заболевание аллеля. Согласно некоторым вариантам осуществления предложенная композиция избирательно расщепляет транскрипты из вызывающего заболевание аллеля. Примеры SNP, которые могут быть нацелены на предложенную композицию (целевые сайты Хантингтона), описаны в настоящем документе.
Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из rs9993542_C, rs362310_C, rs362303_C, rs10488840_G, rs363125_C, rs363072_A, rs7694687_C, rs363064_C, rs363099_C, rs363088_A, rs34315806_C, rs2298967_T, rs362272_G, rs362275_C, rs362306_G, rs3775061_A, rs1006798_A, rs16843804_C, rs3121419_C, rs362271_G, rs362273_A, rs7659144_C, rs3129322_T, rs3121417_G, rs3095074_G, rs362296_C, rs108850_C, rs2024115_A, rs916171_C, rs7685686_A, rs6844859_T, rs4690073_G, rs2285086_A, rs362331_T, rs363092_C, rs3856973_G, rs4690072_T, rs7691627_G, rs2298969_A, rs2857936_C, rs6446723_T, rs762855_A, rs1263309_T, rs2798296_G, rs363096_T, rs10015979_G, rs11731237_T, rs363080_C, rs2798235_G и rs362307_T. Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из rs34315806_C, rs362273_A, rs362331_T, rs363099_C, rs7685686_A, rs362306_G, rs363064_C, rs363075_G, rs2276881_G, rs362271_G, rs362303_C, rs362322_A, rs363088_A, rs6844859_T, rs3025838_C, rs363081_G, rs3025849_A, rs3121419_C, rs2298967_T, rs2298969_A, rs16843804_C, rs4690072_T, rs362310_C, rs3856973_G, rs2530595_C, rs2530595_T и rs2285086_A. Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из rs34315806_C, rs362273_A, rs362331_T, rs363099_C, rs7685686_A, rs362306_G, rs363064_C, rs363075_G, rs2276881_G, rs362271_G, rs362303_C, rs362322_A, rs363088_A, rs6844859_T, rs3025838_C, rs363081_G, rs3025849_A, rs3121419_C, rs2298967_T, rs2298969_A, rs16843804_C, rs4690072_T, rs362310_C, rs3856973_G и rs2285086_A. Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из rs362331_T, rs7685686_A, rs6844859_T, rs2298969_A, rs4690072_T, rs2024115_A, rs3856973_G, rs2285086_A, rs363092_C, rs7691627_G, rs10015979_G, rs916171_C, rs6446723_T, rs11731237_T, rs362272_G, rs4690073_G и rs363096_T. Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из rs362267, rs6844859, rs1065746, rs7685686, rs362331, rs362336, rs2024115, rs362275, rs362273, rs362272, rs3025805, rs3025806, rs35892913, rs363125, rs17781557, rs4690072, rs4690074, rs1557210, rs363088, rs362268, rs362308, rs362307, rs362306, rs362305, rs362304, rs362303, rs362302, rs363075 rs2530595 и rs2298969. Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из rs362267, rs6844859, rs1065746, rs7685686, rs362331, rs362336, rs2024115, rs362275, rs362273, rs362272, rs3025805, rs3025806, rs35892913, rs363125, rs17781557, rs4690072, rs4690074, rs1557210, rs363088, rs362268, rs362308, rs362307, rs362306, rs362305, rs362304, rs362303, rs362302, rs363075 and rs2298969 и rs2298969. Согласно некоторым вариантам осуществления целевой сайт Хантингтона выбирают из:

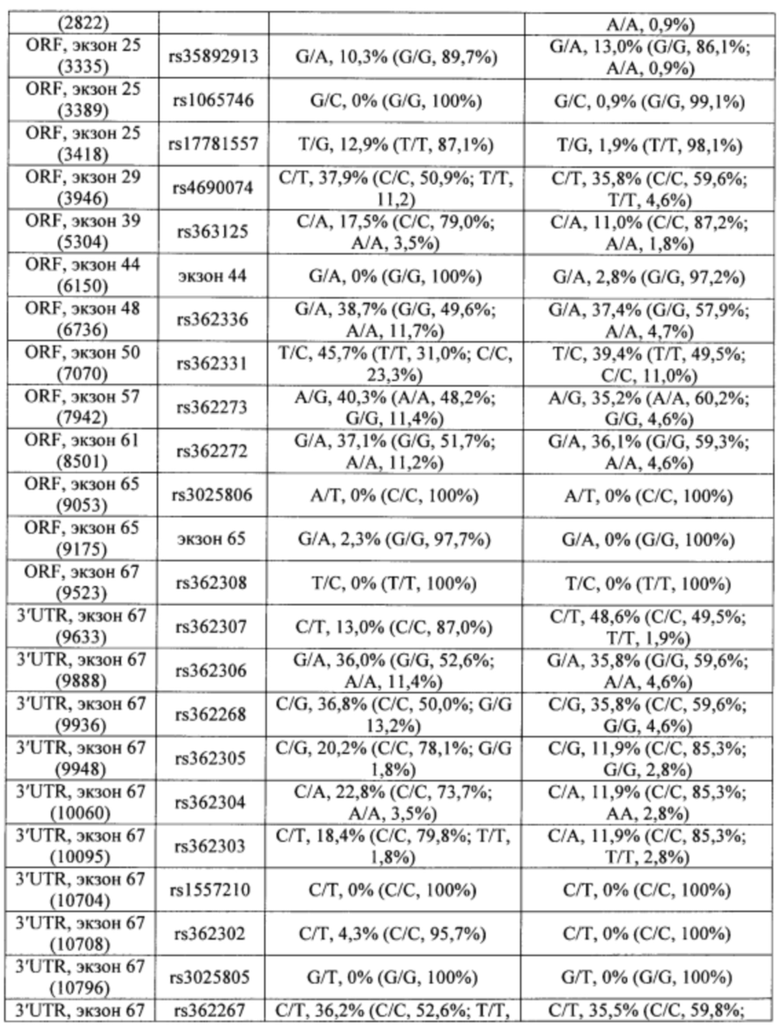
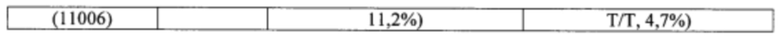
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью направленно воздействует на два или более сайтов. Согласно некоторым вариантам осуществления два или более сайтов для направленного воздействия выбирают из перечисленных в данном описании. Согласно некоторым вариантам осуществления целевой SNP представляет собой rs362307, rs7685686, rs362268, rs2530595, rs362331 или rs362306. Согласно некоторым вариантам осуществления целевой SNP представляет собой rs362307, rs7685686, rs362268 или rs362306. Согласно некоторым вариантам осуществления целевой SNP представляет собой rs362307. Согласно некоторым вариантам осуществления целевой SNP представляет собой rs7685686. Согласно некоторым вариантам осуществления целевой SNP не представляет собой rs7685686. Согласно некоторым вариантам осуществления целевой SNP представляет собой rs362268. Согласно некоторым вариантам осуществления целевой SNP представляет собой rs362306.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью способна различать два аллеля определенного SNP.
Композиции олигонуклеотидов с контролируемой хиральностью как WVE120101, так и WV-1092 были способны различать версии дикого типа и мутантные версии SNP rs362307, которые отличаются одним нуклеотидом; как WVE120101, так и WV-1092 композиции олигонуклеотидов с контролируемой хиральностью подвергали значительному нокдауну мутантный аллель, но не дикого типа, в то время как стереослучайная композиция олигонуклеотидов WV-1497 не могла значительно различать аллели дикого типа и мутантные аллели (см. фиг. 39D).
Композиция олигонуклеотидов с контролируемой хиральностью WV-2595 также была способна различать аллели С и Т в SNP rs2530595, которые также отличаются только одним нуклеотидом. Композиция олигонуклеотидов WV-2595 с контролируемой хиральностью подвергала значительному нокдауну аллель Т, но не аллель С, в отличие от стереослучайной композиции олигонуклеотидов WV-2611, которая не могла значительно различать аллели (см. фиг. 39F).
Композиция олигонуклеотидов с контролируемой хиральностью WV-2603 была способна различать аллели С и Т в SNP rs362331, которые также отличаются только одним нуклеотидом. Композиция олигонуклеотидов с контролируемой хиральностью WV-2603 подвергала значительному нокдауну аллель Т, но не аллель С, в отличие от стереослучайной композиции олигонуклеотидов WV-2619, которая не могла существенно различать аллели (см. фиг. 39А, 39В, 39С и 39Е).
Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблиц N1, N2, N3 или N4. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N1. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N2. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N3. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N4. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблиц N1A, N2A, N3A или N4A. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N1A. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N2A. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N3A. Согласно некоторым вариантам осуществления предложенная композиция для лечения болезни Хантингтона выбрана из таблицы N4A. Согласно некоторым вариантам осуществления предложенная композиция представляет собой WV-1092. Согласно некоторым вариантам осуществления предложенную композицию выбирают из: олигонуклеотида, имеющего последовательность WVE120101; WV-2603; WV-2595; WV-1510; WV-2378 и WV-2380; каждый из них был сконструирован и оказался очень эффективным, например, как показано in vitro в анализе репортерного гена двойной люциферазы. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WVE120101, WV-2603, WV-2595, WV-1510, WV-2378 или WV-2380. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-937. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-1087. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-1090. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-1091. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-1092. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-1510. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-2378. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-2380. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-2595. Согласно некоторым вариантам осуществления предложенная композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью WV-2603. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль химических модификаций (например, модификаций основания, модификаций сахара и т.д.) любого олигонуклеотида, описанного в настоящем документе.
Согласно некоторым вариантам осуществления предложенная композиция не представляет собой композицию ONT-451, ONT-452 или ONT-450. Согласно некоторым вариантам осуществления предложенная композиция не представляет собой композицию ONT-451. Согласно некоторым вариантам осуществления предложенная композиция не представляет собой композицию ONT-452. Согласно некоторым вариантам осуществления предложенная композиция не представляет собой композицию ONT-450. Согласно некоторым вариантам осуществления композиция не содержит предопределенный уровень ONT-451 или ONT-452. Согласно некоторым вариантам осуществления композиция не содержит предопределенный уровень ONT-451. Согласно некоторым вариантам осуществления композиция не содержит предопределенный уровень ONT-452. Согласно некоторым вариантам осуществления тип олигонуклеотида не представляет собой ONT-451 или ONT-452. Согласно некоторым вариантам осуществления тип олигонуклеотида не представляет собой ONT-451. Согласно некоторым вариантам осуществления тип олигонуклеотида не представляет собой ONT-452. Согласно некоторым вариантам осуществления композиция не представляет собой композицию олигонуклеотидов с контролируемой хиральностью ONT-451 или ONT-452. Согласно некоторым вариантам осуществления композиция не представляет собой композицию олигонуклеотидов с контролируемой хиральностью ONT-451. Согласно некоторым вариантам осуществления композиция не представляет собой композицию олигонуклеотидов с контролируемой хиральностью ONT-452.
Согласно некоторым вариантам осуществления предложенный способ уменьшает симптом болезни Хантингтона. Согласно некоторым вариантам осуществления предложенный способ замедляет начало болезни Хантингтона. Согласно некоторым вариантам осуществления предложенный способ замедляет прогрессирование болезни Хантингтона. Согласно некоторым вариантам осуществления предложенный способ останавливает прогрессирование болезни Хантингтона. Согласно некоторым вариантам осуществления предложенный способ излечивает болезнь Хантингтона в соответствии с клиническим стандартом.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы идентификации пациентов для данной композицию олигонуклеотидов. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает способы стратификации пациентов. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию мутации и/или SNP, связанных с вызывающим заболевание аллелем. Например, согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с удлиненными повторами CAG, которые связаны с болезнью Хантингтона или вызывают ее. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с более чем 35 повторами CAG в хантингтине. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с более чем 36 повторами CAG в хантингтине. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с более чем 37 повторами CAG в хантингтине. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с более чем 38 повторами CAG в хантингтине. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с более чем 39 повторами CAG в хантингтине. Согласно некоторым вариантам осуществления предложенный способ предусматривает идентификацию у субъекта SNP, связанного с более чем 40 повторами CAG в хантингтине.
Согласно некоторым вариантам осуществления субъект содержит SNP в гене хантингтина субъекта. Согласно некоторым вариантам осуществления субъект содержит SNP, причем один аллель представляет собой мутантный хантингтин, связанный с удлиненными повторами CAG. Согласно некоторым вариантам осуществления субъект содержит SNP, как описано в настоящем документе. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs362307, rs7685686, rs362268, rs2530595, rs362331 или rs362306. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs362307, rs7685686, rs362268 или rs362306. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs362307. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs7685686. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs362268. Согласно некоторым вариантам осуществления субъект содержит SNP, выбранный из rs362306.
Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции имеют последовательность, комплементарную последовательности, содержащей SNP из вызывающего заболевание аллеля (мутанта), и композиция избирательно подавляет экспрессию из вызывающего заболевание аллеля. Согласно некоторым вариантам осуществления SNP представляет собой rs362307, rs7685686, rs362268, rs2530595, rs362331 или rs362306. Согласно некоторым вариантам осуществления SNP представляет собой rs362307, rs7685686, rs362268 или rs362306. Согласно некоторым вариантам осуществления SNP представляет собой rs362307. Согласно некоторым вариантам осуществления SNP представляет собой rs7685686. Согласно некоторым вариантам осуществления SNP представляет собой rs362268. Согласно некоторым вариантам осуществления SNP представляет собой rs362306. Согласно некоторым вариантам осуществления SNP представляет собой rs2530595. Согласно некоторым вариантам осуществления SNP представляет собой rs362331.
Как понятно специалисту в данной области техники, различные способы могут использоваться для контроля процесса воздействия. Согласно некоторым вариантам осуществления мутантный НТТ (mHTT) может быть оценен из спинномозговой жидкости (Wild et al., Quantification of mutant Huntingtin protein in cerebrospinal fluid from Huntington's disease patients, J Clin Invest. 2015; 125 (5): 1979-86) и может использоваться для контроля лечения. Согласно некоторым вариантам осуществления этот подход может использоваться для определения и/или оптимизации схемы лечения, контроля фармакодинамических конечных точек и/или определения дозировки и частоты для введения и т.д.
Специалисту в данной области техники понятно, что предложенные способы применимы к любым подобным мишеням, содержащих несоответствие. Согласно некоторым вариантам осуществления несоответствие наблюдается между материнским и отцовским геном. Дополнительные иллюстративные мишени для подавления и/или нокдауна, в том числе аллель-специфического подавления и/или нокдауна, могут представлять собой любые генетические аномалии, например, мутации, связанные с каким-либо заболеваниям. Согласно некоторым вариантам осуществления мишени или наборы мишеней выбирают из генетических детерминант заболеваний, например, как раскрыто в Xiong, et al., The human splicing code reveals new insights into the genetic determinants of disease. Science Vol. 347 no. 6218 DOI: 10.1126/science.1254806. Согласно некоторым вариантам осуществления несоответствие наблюдается между мутантом и диким типом.
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью и способы их применения используются для селективного подавления олигонуклеотидов с мутацией при заболевании. Согласно некоторым вариантам осуществления это заболевание представляет собой злокачественную опухоль. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью и способы их применения используются для селективного подавления транскриптов с мутациями при злокачественной опухоли. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью и способы их применения используются для подавления транскриптов KRAS. Иллюстративные сайты-мишени KRAS содержат G12V=GGU->GUU положение 227 G->U, G12D=GGU->GAU положение 227 G->A и G13D=GGC->GAC положение 230 G->A.
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью и способы их применения обеспечивают аллель-специфическое подавление транскрипта в организме. Согласно некоторым вариантам осуществления организм содержит целевой ген, для которого существуют два или более аллеля. Например, субъект имеет ген дикого типа в нормальных тканях, в то время как тот же самый ген мутирует в пораженных тканях, таких, как в опухоли. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композиции олигонуклеотидов с контролируемой хиральностью и способы их применения, которые избирательно подавляют один аллель, например, аллель с мутацией или SNP. Согласно некоторым вариантам осуществления настоящее раскрытие обеспечивает лечение с более высокой эффективностью и/или низкой токсичностью, и/или другими преимуществами, как описано в данной заявке.
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью содержат олигонуклеотиды одного типа олигонуклеотида. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью содержат олигонуклеотиды только одного типа олигонуклеотида. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов с контролируемой хиральностью имеют олигонуклеотиды только одного типа олигонуклеотида. Согласно некоторым вариантам осуществления композиции олигонуклеотидов с контролируемой хиральностью содержат олигонуклеотиды двух или более типов олигонуклеотида. Согласно некоторым вариантам осуществления с использованием таких композиций предложенные способы могут предназначаться для более чем одной мишени. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью, содержащая два или более типа олигонуклеотида, направленно воздействует на две или более мишени. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью, содержащая два или более типа олигонуклеотида, направленно воздействует на два или более несовпадения. Согласно некоторым вариантам осуществления единственный тип олигонуклеотида направленно воздействует на две или более мишени, например, мутации. Согласно некоторым вариантам осуществления целевая область олигонуклеотидов одного типа олигонуклеотида содержит два или более «целевых сайтов», таких как две мутации или SNP.
Согласно некоторым вариантам осуществления олигонуклеотиды в предложенной композиции олигонуклеотидов с контролируемой хиральностью необязательно содержат модифицированные основания или сахара. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью не содержит модифицированные основания или сахара. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью не содержит каких-либо модифицированных оснований. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенной композиции олигонуклеотидов с контролируемой хиральностью содержат модифицированные основания и сахара. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенной композиции олигонуклеотидов с контролируемой хиральностью содержат модифицированное основание. Согласно некоторым вариантам осуществления олигонуклеотиды в предложенной композиции олигонуклеотидов с контролируемой хиральностью содержат модифицированный сахар. Модифицированные основания и сахара для олигонуклеотидов широко известны в данной области техники, включая без ограничения те, которые описаны в настоящем документе. Согласно некоторым вариантам осуществления модифицированное основание представляет собой 5-mC. Согласно некоторым вариантам осуществления модифицированный сахар представляет собой 2'-модифицированный сахар. Подходящие 2'-модификации олигонуклеотидных сахаров широко известны специалисту в данной области техники. Согласно некоторым вариантам осуществления 2'-модификации включают без ограничения 2'-OR1, где R1 представляет собой не водород. Согласно некоторым вариантам осуществления 2'-модификация представляет собой 2'-OR1, где R1 представляет собой необязательно замещенную C1-6 алифатическую группу. Согласно некоторым вариантам осуществления 2'-модификация представляет собой 2'-МОЕ. Согласно некоторым вариантам осуществления модификация представляет собой 2'-галоген. Согласно некоторым вариантам осуществления модификация представляет собой 2'-F. Согласно некоторым вариантам осуществления модифицированные основания или сахара могут дополнительно повышать активность, стабильность и/или селективность композиции олигонуклеотидов с контролируемой хиральностью, чей общий профиль хиральных центров остова обеспечивает неожиданную активность, стабильность и/или селективность.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью не содержит модифицированных сахаров. Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью не содержит каких-либо 2'-модифицированных сахаров. Согласно некоторым вариантам осуществления в настоящем раскрытии неожиданно было обнаружено, что при использовании композиций олигонуклеотидов с контролируемой хиральностью модифицированные сахара не нужны для стабильности, активности и/или контроля профилей расщепления. Кроме того, согласно некоторым вариантам осуществления в настоящем раскрытии неожиданно было обнаружено, что композиции олигонуклеотидов с контролируемой хиральностью без модифицированных сахаров обеспечивают лучшие свойства с точки зрения стабильности, активности, оборота и/или контроля профилей расщепления. Например, согласно некоторым вариантам осуществления неожиданно было обнаружено, что композиции олигонуклеотидов с контролируемой хиральностью олигонуклеотидов, не имеющих модифицированные сахара, диссоциируют гораздо быстрее из продуктов расщепления и обеспечивают значительно ускоренный оборот, чем композиции олигонуклеотидов с модифицированными сахарами.
Согласно некоторым вариантам осуществления олигонуклеотиды предложенных композиций олигонуклеотидов с контролируемой хиральностью, применимых для предложенных способов, содержат структуры, которые подробно описаны в настоящем документе. Согласно некоторым вариантам осуществления олигонуклеотид имеет структуру крыло-сердцевина-крыло, как это описано. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)mRp согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)2Rp. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)m(Rp)n согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Rp)n(Sp)m согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит Rp(Sp)m согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит Rp(Sp)2. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)m(Rp)n(Sp)t согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)mRp(Sp)t согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)t(Rp)n(Sp)m согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)tRp(Sp)m согласно описанию. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит SpRpSpSp. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)2Rp(Sp)2. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)3Rp(Sp)3. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)4Rp(Sp)4. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)tRp(Sp)5. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит SpRp(Sp)5. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)2Rp(Sp)5. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)3Rp(Sp)5. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)4Rp(Sp)5. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предусмотренной композиции олигонуклеотидов с контролируемой хиральностью содержит (Sp)5Rp(Sp)5. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова имеет только одну конфигурацию Rp и каждая из других межнуклеотидных линкерных групп находится в Sp-конфигурации. Согласно некоторым вариантам осуществления одинаковая длина составляет больше, чем 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 32, 35, 40, 45 или 50 оснований, как описано в настоящем раскрытии. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 10 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 11 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 12 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 13 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 14 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 15 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 16 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 17 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 18 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 19 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 20 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 21 основание. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 22 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 23 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 24 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 25 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 26 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 27 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 28 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 29 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 30 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 31 основания. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 32 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 33 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 34 оснований. Согласно некоторым вариантам осуществления одинаковая длина составляет больше 35 оснований.
Согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов с контролируемой хиральностью обеспечивает высокий оборот. Согласно некоторым вариантам осуществления продукты расщепления полимера нуклеиновой кислоты диссоциируют из олигонуклеотидов предложенной композиции олигонуклеотидов с контролируемой хиральностью с более высокой скоростью, чем из олигонуклеотидов эталонной композиции олигонуклеотидов, например, композиции олигонуклеотидов с неконтролируемой хиральностью. Согласно некоторым вариантам осуществления предложенную композицию олигонуклеотидов с контролируемой хиральностью можно вводить в более низкой стандартной дозированной форме и/или общей дозе, и/или меньшей дозе, чем композицию олигонуклеотидов с неконтролируемой хиральностью.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает меньшее количество сайтов расщепления в последовательности полимера нуклеиновой кислоты, которая является комплементарной к общей последовательности оснований или последовательности в пределах общей последовательности оснований по сравнению с эталонной композицией олигонуклеотидов. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает меньшее количество сайтов расщепления в последовательности полимера нуклеиновой кислоты, которая является комплементарной к общей последовательности оснований. Согласно некоторым вариантам осуществления полимер нуклеиновой кислоты селективно расщепляется в единственном сайте в пределах последовательности, которая комплементарна общей последовательности оснований или последовательности в пределах общей последовательности оснований композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает более высокий процент расщепления в сайте расщепления в пределах последовательности, которая комплементарна общей последовательности оснований или последовательности в пределах общей последовательности оснований композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает более высокий процент расщепления в сайте расщепления в последовательности, которая комплементарна общей последовательности оснований композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления сайт, имеющий более высокий процент расщепления, представляет собой сайт расщепления, когда используется эталонная композиция олигонуклеотидов. Согласно некоторым вариантам осуществления сайт, имеющий более высокий процент расщепления, представляет собой сайт расщепления, который не присутствует, когда используется эталонная композиция олигонуклеотидов.
Неожиданно было обнаружено, что с уменьшением числа сайтов расщепления в комплементарной последовательности, скорость расщепления может быть неожиданно увеличена и/или может быть достигнут более высокий процент расщепления. Как показано в примерах данного описания, предложенные композиции олигонуклеотидов с контролируемой хиральностью, которые производят меньшее количество сайтов расщепления, особенно те, которые обеспечивают расщепление в единственном сайте, в пределах комплементарных последовательностей полимеров-мишеней нуклеиновых кислот, обеспечивают гораздо более высокие скорости расщепления и значительно более низкие уровни остающихся нерасщепленных полимеров нуклеиновых кислот. Такие результаты находятся в резком контрасте с общими исследованиями в настоящей области техники, в которых большее количество сайтов расщепления было подано с целью увеличения скорости расщепления.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью увеличивает скорость расщепления в 1,5 раза по сравнению с эталонной композицией олигонуклеотидов. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 2 раза. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 3 раза. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 4 раза. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 5 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 6 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 7 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 8 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 9 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 10 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 11 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 12 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 13 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 14 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 15 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 20 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 30 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 40 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 50 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 60 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 70 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 80 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 90 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 100 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 200 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 300 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 400 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере в 500 раз. Согласно некоторым вариантам осуществления скорость расщепления увеличивается по меньшей мере более чем в 500 раз.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью обеспечивает более низкое содержание оставшегося нерасщепленного полимера-мишени нуклеиновой кислоты по сравнению с эталонной композицией олигонуклеотидов. Согласно некоторым вариантам осуществления оно в 1,5 раза ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 2 раза ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 3 раза ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 4 раза ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 5 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 6 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 7 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 8 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 9 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 10 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 11 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 12 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 13 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 14 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 15 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 20 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 30 раз ниже. Согласно некоторым вариантам осуществления по меньшей мере в 40 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 50 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 60 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 70 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 80 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 90 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 100 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 200 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 300 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 400 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 500 раз ниже. Согласно некоторым вариантам осуществления оно по меньшей мере в 1000 раз ниже.
Как подробно обсуждается в настоящем раскрытии, в настоящем изобретении помимо прочего предложена композиция олигонуклеотидов с контролируемой хиральностью, это обозначает, что композиция содержит совокупность олигонуклеотидов по меньшей мере одного типа. Каждая молекула олигонуклеотида определенного «типа» состоит из предварительно выбранных (например, предварительно определенных) структурных элементов, включая: (1) последовательность оснований; (2) профиль линкерных групп остова; (3) профиль хиральных центров остова; и (4) профиль фрагментов остова с модификацией Р. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов содержат олигонуклеотиды, полученные при помощи единственного способа синтеза. Согласно некоторым вариантам осуществления предложенные композиции содержат олигонуклеотиды, имеющие более одной хиральной конфигурации в одной молекуле олигонуклеотида (например, если различные остатки олигонуклеотида имеют различную стереохимию); в некоторых указанных вариантах реализации указанные олигонуклеотиды можно получать при помощи единственного способа синтеза, и для получения отдельных молекул олигонуклеотидов, имеющих более одной хиральной конфигурации, не требуются вторичные стадии конъюгации.
Композиции олигонуклеотидов, предложенные в настоящем описании, можно применять в качестве агентов для модуляции различных клеточных процессов и механизмов, включая, но не ограничиваясь ими, транскрипцию, трансляцию, иммунные ответы, эпигенетику и т.д. Кроме того, композиции олигонуклеотидов, предложенные в настоящем описании, можно применять в качестве реагентов для исследовательских и/или диагностических задач. Специалистам в данной области техники будет очевидно, что описание настоящего изобретения не ограничено конкретным применением, но изобретение можно применять в любых ситуациях, где желательно применение синтетических олигонуклеотидов. Помимо прочего предложенные композиции подходят для различных терапевтических, диагностических, сельскохозяйственных и/или исследовательских применений.
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов содержат олигонуклеотиды и/или их остатки, содержащие одну или более структурных модификаций, таких как подробно описано в настоящей заявке. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов содержат олигонуклеотиды, содержащие один или более аналогов нуклеиновых кислот. Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов содержат олигонуклеотиды, содержащие одну или более искусственных нуклеиновых кислот или их остатков (например, нуклеотидный аналог), включая, но не ограничиваясь ими: пептидонуклеиновую кислоту (ПНК), закрытую нуклеиновую кислоту (ЗНК), морфолино, треозо-нуклеиновую кислоту (ТНК), гликоль-нуклеиновую кислоту (ГНК), арабино-нуклеиновую кислоту (АНК), 2'-флюороарабино-нуклеиновую кислоту (ФАНК), циклогексен-нуклеиновую кислоту (цГНК), ангидрогекситоловую нуклеиновую кислоту (АНК) и/или незапертую нуклеиновую кислоту (ННК), треозо-нуклеиновую кислоту (ТНК), и/или ксенонуклеиновые кислоты (КНК) и любую их комбинацию.
В любых вариантах реализации настоящее раскрытие подходит для модуляции экспрессии генов, иммунного ответа на основе олигонуклеотидов и т.д. Соответственно, вместо традиционных стереослучайных или не являющихся хирально-чистыми олигонуклеотидов можно применять стереоопределенные композиции олигонуклеотидов согласно настоящему раскрытию, которые содержат олигонуклеотиды предварительно определенного типа (т.е. которые являются хирально-контролируемыми и необязательно хирально-чистыми). Согласно некоторым вариантам осуществления предложенные композиции обладают улучшенным предполагаемым действием и/или пониженными нежелательными побочными эффектами. Определенные варианты реализации биологических и клинических/терапевтических применений согласно настоящему раскрытию подробно обсуждают ниже.
Для введения предложенных композиций олигонуклеотидов с контролируемой хиральностью можно применять различные схемы дозирования. Согласно некоторым вариантам осуществления вводят несколько стандартных доз, разделенных периодами времени. Согласно некоторым вариантам осуществления данная композиция имеет рекомендованную схему дозирования, которая может включать одну или более доз. Согласно некоторым вариантам осуществления схема дозирования включает совокупность доз, введение каждой из которых отделено от введения другой дозы периодами времени одинаковой продолжительности; согласно некоторым вариантам осуществления схема дозирования включает совокупность доз, а введение отдельных доз разделяют по меньшей мере два различных периода времени. Согласно некоторым вариантам осуществления все дозы, входящие в схему дозирования, содержат одинаковое дозируемое количество. Согласно некоторым вариантам осуществления различные дозы, входящие в схему дозирования, содержат различные количества. Согласно некоторым вариантам осуществления схема дозирования включает первую дозу, содержащую первое дозируемое количество, а затем одну или более дополнительных доз, содержащих второе дозируемое количество, отличающееся от первого дозируемого количества. Согласно некоторым вариантам осуществления схема дозирования включает первую дозу, содержащую первое дозируемое количество, а затем одну или более дополнительных доз, содержащих второе (или последующее) дозируемое количество, которое является одинаковым или отличается от первого дозируемого (или предшествующего дозируемого) количества. Согласно некоторым вариантам осуществления схема дозирования включает введение по меньшей мере одной стандартной дозы в течение по меньшей мере одного дня. Согласно некоторым вариантам осуществления схема дозирования включает введение более чем одной дозы в течение периода времени, составляющего по меньшей мере один день, а иногда более одного дня. Согласно некоторым вариантам осуществления схема дозирования включает введение нескольких доз в течение периода времени, составляющего по меньшей мере неделю. Согласно некоторым вариантам осуществления период времени составляет по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40 или более (например, примерно 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более) недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в неделю в течение более чем одной недели. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в неделю в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40 или более (например, примерно 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более) недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы каждые две недели в течение более чем двух недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы каждые две недели в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40 или более (например, примерно 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более) недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в месяц в течение одного месяца. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в месяц в течение более чем одного месяца. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в месяц в течение 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более месяцев. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в неделю в течение примерно 10 недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в неделю в течение примерно 20 недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в неделю в течение примерно 30 недель. Согласно некоторым вариантам осуществления схема дозирования включает введение одной дозы в неделю в течение 26 недель. Согласно некоторым вариантам осуществления хирально-контролируемую композицию олигонуклеотида вводят согласно схеме дозирования, отличающейся от схемы, в которой применяют хирально-неконтролируемую (например, стереослучайную) композицию олигонуклеотидов, имеющих такие же последовательности, и/или другую хирально-контролируемую композицию олигонуклеотидов, имеющих такие же последовательности. Согласно некоторым вариантам осуществления хирально-контролируемую композицию олигонуклеотидов вводят согласно схеме дозирования, которая сокращена по сравнению со схемой, в которой применяют хирально-неконтролируемую (например, стереослучайную) композицию олигонуклеотидов, имеющих такие же последовательности, то есть она обеспечивает пониженный уровень общего воздействия в данный промежуток времени, включает использование одной или более уменьшенных стандартных доз и/или включает уменьшение количества доз, вводимых за данный промежуток времени. Согласно некоторым вариантам осуществления хирально-контролируемую композицию олигонуклеотидов вводят согласно схеме дозирования, которая является более продолжительной по сравнению со схемой, в которой применяют хирально-неконтролируемую (например, стереослучайную) композицию олигонуклеотидов, имеющих такие же последовательности. Не желая быть ограниченными теорией, авторы настоящего изобретения отмечают, что согласно некоторым вариантам осуществления сокращение схемы дозирования и/или увеличение интервалов между введением доз могут быть обусловлены улучшенной стабильностью, биодоступностью и/или эффективностью композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью имеет более продолжительную схему дозирования по сравнению с соответствующей хирально-неконтролируемой композицией олигонуклеотидов. Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью имеет уменьшенные интервалы между введением по меньшей мере двух доз по сравнению с соответствующей хирально-неконтролируемой композицией олигонуклеотидов. Не желая быть ограниченными теорией, авторы настоящего изобретения отмечают, что согласно некоторым вариантам осуществления увеличение продолжительности схемы дозирования и/или сокращение интервалов между введением доз могут быть обусловлены улучшенной безопасностью композиции олигонуклеотидов с контролируемой хиральностью.
Однократная дозировка может содержать различные количества олигонуклеотида с контролируемой хиральностью, подходящие согласно настоящей заявке. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 1, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250, 260, 270, 280, 290, 300 или более (например, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000 или более) мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 1 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 5 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 10 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 15 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 20 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 50 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 100 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 150 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 200 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 250 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления однократная дозировка содержит примерно 300 мг олигонуклеотида с контролируемой хиральностью. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью вводят с использованием более низких количеств, содержащихся в одной дозе, и/или более низкой общей дозировки по сравнению с хирально-неконтролируемым олигонуклеотидом. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью вводят с использованием более низких количеств, содержащихся в одной дозе, и/или более низкой общей дозировки по сравнению с хирально-неконтролируемым олигонуклеотидом благодаря улучшенной эффективности. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью вводят с использованием более высоких количеств, содержащихся в одной дозе, и/или более высокой общей дозировки по сравнению с хирально-неконтролируемым олигонуклеотидом. Согласно некоторым вариантам осуществления олигонуклеотид с контролируемой хиральностью вводят с использованием более высоких количеств, содержащихся в одной дозе, и/или более высокой общей дозировки по сравнению с хирально-неконтролируемым олигонуклеотидом благодаря улучшенной безопасности.
Биологически активные олигонуклеотиды
Предложенная композиция олигонуклеотидов, применяемая согласно настоящему описанию, может содержать одноцепочечные олигонуклеотиды и/или олигонуклеотиды, состоящие из нескольких цепей. Согласно некоторым вариантам осуществления одноцепочечные олигонуклеотиды содержат самокомплементарные фрагменты, которые могут гибридизоваться в соответствующих условиях, то есть при использовании даже одноцепочечные олигонуклеотиды могут иметь по меньшей мере отчасти характеристики двойной цепи. Согласно некоторым вариантам осуществления олигонуклеотид, содержащийся в предложенной композиции, является одноцепочечным, двухцепочечным или трехцепочечным. Согласно некоторым вариантам осуществления олигонуклеотид, содержащийся в предложенной композиции, содержит одноцепочечный фрагмент и фрагмент, содержащий несколько цепей олигонуклеотида. Согласно некоторым вариантам осуществления, как отмечалось выше, отдельные одноцепочечные олигонуклеотиды могут содержать двухцепочечные фрагменты и одноцепочечные фрагменты.
Согласно некоторым вариантам осуществления предложенные композиции содержат один или более олигонуклеотидов, которые являются полностью или частично комплементарными с цепями: структурных генов, генов, содержащих контрольные и терминальные области, и/или самовоспроизводящихся систем, таких как вирусная или плазмидная ДНК. Согласно некоторым вариантам осуществления предложенные композиции содержат один или более олигонуклеотидов, представляющих собой или действующих как миРНК и другие агенты РНК-интерференции (агенты РНКи или агенты иРНК), кшРНК, антисмысловые олигонуклеотиды, самоотщепляемые РНК, рибозимы, их фрагменты и/или варианты (такие как пептидилтрансфераза 23S рРНК, РНКаза Р, интроны группы I и группы II, разветвленные рибозимы GIR1, лидзим, рибозимы со шпилечными структурами, рибозимы со структурой «головка молотка», рибозимы HDV, рибозим млекопитающих СРЕВ3, рибозимы VS, рибозимы glmS, рибозим СоТС и т.д.), микроРНК, имитаторы микроРНК, супермиры, аптамеры, антимиры, антагомиры, адапторы UI, триплекс-образующие олигонуклеотиды, активаторы РНК, длинноцепочечные некодирующие РНК, короткоцепочечные некодирующие РНК (например, пиРНК), иммуномодулирующие олигонуклеотиды (такие как иммуностимулирующие олигонуклеотиды, иммуноподавляющие олигонуклеотиды), ГНК, ЗНК, ЭНК, ПНК, ТНК, ГНК, ТНК, КНК, HeNA цГНК, морфолино, G-квадруплексы (РНК и ДНК), противовирусные олигонуклеотиды и олигонуклеотиды-«ловушки».
Согласно некоторым вариантам осуществления предложенные композиции содержат один или более гибридных (например, химерных) олигонуклеотидов. В контексте настоящего описания термин «гибрид» в целом относится к смешанным структурным компонентам олигонуклеотидов. Гибридные олигонуклеотиды могут относиться, например, к (1) молекуле олигонуклеотида, содержащей нуклеотиды смешанных классов, например, части ДНК и части РНК в одной молекуле (например, ДНК-РНК); (2) комплементарным парам нуклеиновых кислот различных классов, то есть происходит внутримолекулярное или межмолекулярное спаривание оснований ДНК:РНК; или к обоим указанным типам; или (3) олигонуклеотиду, содержащему два или более видов остовов или межнуклеотидных линкерных групп.
Согласно некоторым вариантам осуществления предложенные композиции содержат один или более олигонуклеотидов, содержащих более одного класса остатков нуклеиновых кислот в одной молекуле. Например, в любом из вариантов реализации, описанных в настоящей заявке, олигонуклеотид может содержать фрагмент ДНК и фрагмент РНК. Согласно некоторым вариантам осуществления олигонуклеотид может содержать немодифицированный фрагмент и модифицированный фрагмент.
Предложенные композиции олигонуклеотидов могут содержать олигонуклеотиды, содержащие любую из различных модификаций, например, таких как описано в настоящей заявке. Согласно некоторым вариантам осуществления конкретные модификации выбирают, например, с учетом предполагаемого применения. Согласно некоторым вариантам осуществления желательно модифицировать одну или обе цепи двухцепочечного олигонуклеотида (или двухцепочечного фрагмента одноцепочечного олигонуклеотида). Согласно некоторым вариантам осуществления две цепи (или фрагмента) содержат различные модификации. Согласно некоторым вариантам осуществления две цепи содержат одинаковые модификации. Специалистам в данной области техники будет понятно, что уровень и тип модификаций, обеспечиваемые при помощи способов согласно настоящему раскрытию, позволяют проводить разнообразные перестановки модификаций. Примеры таких модификаций описаны в настоящей заявке и не являются ограничивающими.
Фраза «антисмысловая цепь», используемая в настоящем описании, относится к олигонуклеотиду, который является по существу или на 100% комплементарным данной целевой последовательности. Фраза «антисмысловая цепь» включает антисмысловой фрагмент обоих олигонуклеотидов, полученных из двух отдельных цепей, а также одномолекулярные олигонуклеотиды, в которых могут образовываться шпилечные структуры или структуры типа «гантель». Термины «антисмысловая цепь» и «направляющая цепь» используют в настоящем описании взаимозаменяемо.
Фраза «смысловая цепь» относится к олигонуклеотиду, имеющему последовательность нуклеозидов, которая является полностью или частично одинаковой с целевой последовательностью, такому как информационная РНК или последовательность ДНК. Термины «смысловая цепь» и «сопровождающая цепь» используют в настоящем описании взаимозаменяемо.
Под «целевой последовательностью» понимают любую последовательность нуклеиновой кислоты, экспрессию или активность которой необходимо модулировать. Целевая нуклеиновая кислота может представлять собой ДНК или РНК, такую как эндогенная ДНК или РНК, вирусная ДНК или РНК или другие РНК, кодируемые геном, вирусом, бактерией, грибком, млекопитающим или растением. Согласно некоторым вариантам осуществления целевая последовательность связана с заболеванием или нарушением. Согласно некоторым вариантам осуществления целевая последовательность представляет собой или содержит часть гена хантингтина. Согласно некоторым вариантам осуществления целевая последовательность представляет собой или содержит часть гена хантингтина, содержащего SNP.
Под «специфической гибридизацией» или «комплементарностью» подразумевают, что нуклеиновая кислота может образовывать водородную(ые) связь(и) с другой последовательностью нуклеиновой кислоты по традиционной модели Уотсона-Крика или другому нетрадиционному механизму. Если рассматривать молекулы нуклеиновых кислот согласно настоящему раскрытию, то свободная энергия связывания молекулы нуклеиновой кислоты с комплементарной последовательностью является достаточной для осуществления важной функции нуклеиновой кислоты, например, активности РНКи. Определение свободной энергии связывания для молекул нуклеиновых кислот хорошо известно в данной области техники (см., например, Turner et al, 1987, CSH Symp. Quant. Biol. LIT pp. 123-133; Frier et al., 1986, Proc. Nat. Acad. Sci. USA 83:9373-9377; Turner et al., 1987, /. Ain. Chem. Soc. 109:3783-3785).
Комплементарность в процентах указывает на содержание в процентах сопряженных остатков в молекулы нуклеиновой кислоты, которые могут образовывать водородные связи (например, пары оснований Уотсона-Крика) с последовательностью второй нуклеиновой кислоты (например, 5, 6, 7, 8, 9, 10 из 10 соответствуют 50%, 60%, 70%, 80%, 90% и 100% комплементарности). «Полная комплементарность» или «100% комплементарность» обозначают, что все сопряженные остатки последовательности нуклеиновой кислоты образуют водородные связи с таким же числом сопряженных остатков последовательности второй нуклеиновой кислоты. Неполная комплементарность относится к ситуации, при которой некоторые, но не все нуклеозидные звенья двух цепей могут образовывать водородные связи друг с другом. «Существенная комплементарность» относится к цепям полинуклеотидов, имеющих комплементарность 90% или более, за исключением фрагментов цепей полинуклеотидов, таких как «липкие» концы, которые специально выбирают таким образом, чтобы они были некомплементарными. Специфическое связывание требует значительной степени комплементарности для предотвращения неспецифического связывания олигомерного соединения с последовательностями, не являющимися целевыми, в условиях, при которых желательно специфическое связывание, например, в физиологических условиях в случае исследований in vivo или терапевтического лечения, а в случае исследований in vitro в условиях, при которых проводят исследование. Согласно некоторым вариантам осуществления последовательности, не являющиеся целевыми, отличаются от соответствующих целевых последовательностей по меньшей мере на 5 нуклеотидов.
При использовании в качестве терапевтического агента предложенный олигонуклеотид вводят в виде фармацевтической композиции. Согласно некоторым вариантам осуществления фармацевтическая композиция содержит терапевтически эффективное количество предложенного олигонуклеотида или его фармацевтически приемлемой соли и по меньшей мере один фармацевтически приемлемый неактивный ингредиент, выбранный из фармацевтически приемлемых разбавителей, фармацевтически приемлемых вспомогательных веществ и фармацевтически приемлемых носителей. В другом варианте реализации фармацевтическая композиция предназначена для внутривенной инъекции, перорального введения, трансбуккального введения, ингаляции, интраназального введения, местного введения, введения в глаза, интратекального введения или введения уши. В другом варианте реализации фармацевтическая композиция составлена для внутривенной инъекции, перорального введения, буккального введения, ингаляции, введения в нос, местного введения, введения в глаза или введения в уши. В других вариантах реализации фармацевтическая композиция представляет собой таблетку, пилюлю, капсулу, жидкость, ингалируемый препарат, раствор для назального спрея, суппозиторий, суспензию, гель, коллоид, дисперсию, суспензию, раствор, эмульсию, мазь, лосьон, глазные капли, ушные капли или препарат, содержащий искусственную спинномозговую жидкость. В других вариантах реализации фармацевтическая композиция представляет собой таблетку, пилюлю, капсулу, жидкость, ингалируемый препарат, раствор для назального спрея, суппозиторий, суспензию, гель, коллоид, дисперсию, суспензию, раствор, эмульсию, мазь, лосьон, глазные капли или ушные капли. Согласно некоторым вариантам осуществления фармацевтическая композиция содержит спинномозговую жидкость. Согласно некоторым вариантам осуществления фармацевтическая композиция содержит искусственную спинномозговую жидкость. Согласно некоторым вариантам осуществления фармацевтическая композиция содержит олигонуклеотид, причем последовательность олигонуклеотида содержит последовательность, которая нацелена на часть гена хантингтина. Согласно некоторым вариантам осуществления последовательность нацелена на часть гена хантингтина, содержащего SNP. Согласно некоторым вариантам осуществления последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль модификаций сахара олигонуклеотида представляет собой или содержит последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль модификаций сахара любого олигонуклеотида, описанного в настоящем документе, и олигонуклеотид содержится в фармацевтической композиции, содержащей любой компонент описанной в настоящем документе фармацевтической композиции. Согласно некоторым вариантам осуществления олигонуклеотид нацелен на ген хантингтин (в качестве неограничивающего примера, SNP в гене хантингтина), и последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль модификаций сахара олигонуклеотида представляет собой или содержит последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль модификаций сахара любого описанного в настоящем документе олигонуклеотида, и олигонуклеотид содержится в фармацевтической композиции, содержащей искусственную спинномозговую жидкость, и фармацевтическую композицию вводят посредством интратекального введения.
Фармацевтические композиции
При использовании в качестве терапевтического агента предложенный олигонуклеотид или композицию олигонуклеотидов, описанную в настоящей заявке, вводят в виде фармацевтической композиции. Согласно некоторым вариантам осуществления фармацевтическая композиция содержит терапевтически эффективное количество предложенных олигонуклеотидов или их фармацевтически приемлемых солей и по меньшей мере один фармацевтически приемлемый неактивный ингредиент, выбранный из фармацевтически приемлемых разбавителей, фармацевтически приемлемых вспомогательных веществ и фармацевтически приемлемых носителей. Согласно некоторым вариантам осуществления фармацевтическая композиция предназначена для внутривенной инъекции, перорального введения, трансбуккального введения, ингаляции, интраназального введения, местного введения, введения в глаза, интратекального введения или в уши. Согласно некоторым вариантам осуществления фармацевтическая композиция составлена для внутривенной инъекции, перорального введения, буккального введения, ингаляции, интраназального введения, местного введения, введения в глаза или введения в уши. Согласно некоторым вариантам осуществления фармацевтическая композиция представляет собой таблетку, пилюлю, капсулу, жидкость, ингалируемый препарат, раствор для распыления в нос, суппозиторий, суспензию, гель, коллоид, дисперсию, суспензию, раствор, эмульсию, мазь, лосьон, глазные капли, ушные капли или препарат, содержащий искусственную спинномозговую жидкость. Согласно некоторым вариантам осуществления фармацевтическая композиция представляет собой таблетку, пилюлю, капсулу, жидкость, ингалируемый препарат, раствор для назального спрея, суппозиторий, суспензию, гель, коллоид, дисперсию, суспензию, раствор, эмульсию, мазь, лосьон, глазные капли или ушные капли. Согласно некоторым вариантам осуществления предложенная композиция содержит спинномозговую жидкость. Согласно некоторым вариантам осуществления предложенная композиция содержит искусственную спинномозговую жидкость.
Согласно некоторым вариантам осуществления в настоящем раскрытии предложена фармацевтическая композиция, содержащая олигонуклеотид с контролируемой хиральностью или содержащую его композицию в смеси с фармацевтически приемлемым вспомогательным веществом. Специалистам в данной области техники должно быть понятно, что фармацевтические композиции содержат фармацевтически приемлемые соли олигонуклеотида с контролируемой хиральностью или содержащую его композицию, описанную выше.
Для доставки нуклеиновых кислот можно применять различные супрамолекулярные наноносители. Примеры наноносителей включают, но не ограничиваются ими, липосомы, комплексы катионных полимеров и различные полимеры. Образование комплексов нуклеиновых кислот с различными поликатионами является другим подходом для внутриклеточной доставки; этот подход включает использованием пегилированных поликатионов, комплексов полиэтиленимина (ПЭИ), катионные блоксополимеры и дендримеры. Некоторые катионные наноносители, включая ПЭИ и полиамидоамин-дендримеры, способствуют высвобождению содержимого из эндосом. Другие подходы включают использование полимерных наночастиц, полимерных мицелл, квантовых точек и липоплексов.
Помимо иллюстративных стратегий доставки, описанных в настоящей заявке, известны дополнительные стратегии доставки нуклеиновых кислот.
Для терапевтических и/или диагностических применений соединения согласно настоящему раскрытию соединения могут быть введены в составы, подходящие для различных способов введения, включая системное и местное или локализованное введение. Способы и составы, в целом, можно найти в Remington, The Science and Practice of Pharmacy, (20th ed. 2000).
Предложенные олигонуклеотиды и содержащие их композиции являются эффективными в широком диапазоне дозировок. Например, при лечении взрослого человека примерами дозировок, которые можно применять, являются дозировки от примерно 0,01 до примерно 1000 мг, от примерно 0,5 до примерно 100 мг, от примерно 1 до примерно 50 мг в день и от примерно 5 до примерно 100 мг в день. Точная дозировка зависит от способа введения, формы, в которой вводят соединение, субъекта, подвергающегося лечению, массы тела субъекта, подвергающегося лечению, и предпочтения и опыта лечащего врача.
Фармацевтически приемлемые соли, в целом, хорошо известны специалистам в данной области техники и могут включать в качестве примера, но не ограничения, ацетат, бензолсульфонат, безилат, бензоат, бикарбонат, битартрат, бромид, эдетат кальция, камзилат, карбонат, цитрат, эдетат, эдизилат, эстолат, эзилат, фумарат, глюцептат, глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изетионат, лактат, лактобионат, малат, малеат, манделат, мезилат, мукат, нафзилат, нитрат, памоат (эмбонат), пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, субацетат, сукцинат, сульфат, таннат, тартрат или теоклат. Другие фармацевтически приемлемые соли можно найти, например, в Remington, The Science and Practice of Pharmacy (20th ed. 2000). Предпочтительные фармацевтически приемлемые соли включают, например, ацетат, бензоат, бромид, карбонат, цитрат, глюконат, гидробромид, гидрохлорид, малеат, мезилат, нафзилат, памоат (эмбонат), фосфат, салицилат, сукцинат, сульфат или тартрат.
В зависимости от конкретных состояний, подвергающихся лечению, указанные агенты можно вводить в состав жидких или твердых лекарственных форм и вводить системно или местно. Агенты можно доставлять, например, в форме с регулируемым по времени или замедленным высвобождением, что известно специалистам в данной области техники. Способы получения составов и введения можно найти в Remington, The Science and Practice of Pharmacy (20th ed. 2000). Подходящие способы введения могут включать пероральное, трансбуккальное, введение путем ингалируемого спрея, подъязычное, ректальное, трансдермальное, внутривагинальное, чресслизистое, интраназальное или энтеральное введение; парентеральную доставку, включая внутримышечные, подкожные, внутрикостные инъекции, а также интратекальные, прямые внутрижелудочковые, внутривенные, внутрисуставные, интрастернальные, интрасиновиальные, внутрипеченочные, внутриочаговые, интракраниальные, интраперитонеальные, интраназальные или внутриглазные инъекции или другие способы доставки.
Согласно некоторым вариантам осуществления способа или композиции по настоящему раскрытию композицию, содержащую олигонуклеотид, вводят путем интратекального введения. Согласно некоторым вариантам осуществления способа или композиции по настоящему раскрытию композиция, содержащая олигонуклеотид, содержит искусственную спинномозговую жидкость и вводится путем интратекального введения. Согласно некоторым вариантам осуществления способа или композиции по настоящему раскрытию композиция, содержащая олигонуклеотид, содержит один или более компонентов искусственной спинномозговой жидкости (например, NaCl, NaHCO3, KCl, NaH2PO4, MgCl2 и глюкозу) и вводится путем интратекального введения. Согласно некоторым вариантам осуществления способа или композиции по настоящему раскрытию композиция, содержащая олигонуклеотид, содержит один или более компонентов искусственной спинномозговой жидкости (например, NaCl, NaHCO3, KCl, NaH2PO4, MgCl2 и глюкоза) и вводится путем интратекального введения, причем последовательность олигонуклеотида содержит последовательность, которая нацелена на часть гена хантингтина. Согласно некоторым вариантам осуществления способа или композиции по настоящему раскрытию композиция, содержащая олигонуклеотид, содержит два или более компонентов искусственной спинномозговой жидкости (например, NaCl, NaHCO3, KCl, NaH2PO4, MgCl2 и глюкоза) и вводится путем интратекального введения, причем последовательность олигонуклеотида содержит последовательность, которая нацелена на часть гена хантингтина. Согласно некоторым вариантам осуществления способа или композиции по настоящему раскрытию композиция, содержащая олигонуклеотид, содержит три или более компонентов искусственной спинномозговой жидкости (например, NaCl, NaHCO3, KCl, NaH2PO4, MgCl2 и глюкоза) и вводится путем интратекального введения, причем последовательность олигонуклеотида содержит последовательность, которая нацелена на часть гена хантингтина. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль химических модификаций (например, модификаций основания, модификаций сахара и т.д.) любого описанного в настоящем документе олигонуклеотида. Согласно некоторым вариантам осуществления последовательность нацелена на часть гена хантингтина, содержащего SNP.
В случае инъекций агенты согласно настоящему раскрытию можно вводить в состав и разбавлять в водных растворах, таких как физиологически совместимые буферы, такие как раствор Хэнка, раствор Рингера или физиологический солевой буфер. В случае чресслизистого введения в составе используют агенты, увеличивающие проницаемость через барьер, через который необходимо проникать. Указанные агенты, увеличивающие проницаемость, в целом известны в данной области техники.
Применение фармацевтически приемлемых инертных носителей для получения составов, содержащих соединения, предложенные в настоящем раскрытии для реализации настоящего раскрытия, в дозировках, подходящих для системного введения, включено в объем изобретения. При надлежащем выборе носителя и подходящего способа получения композиции согласно настоящему раскрытию, в частности те, что получены в виде растворов, можно вводить парентерально, например, путем внутривенной инъекции.
Соединения можно легко вводить в составы с использованием фармацевтически приемлемых носителей, хорошо известных в данной области техники, в дозировках, подходящих для перорального введения. Указанные носители позволяет вводить соединения согласно настоящему раскрытию в состав таблеток, пилюль, капсул, жидкостей, гелей, сиропов, взвесей, суспензий и т.д., которые субъект (например, пациент), подвергающийся лечению, принимает внутрь при помощи перорального способа.
В случае интраназальной доставки или доставки путем ингаляции агенты согласно настоящему раскрытию также можно вводить в составы при помощи способов, известных специалистам в данной области техники, включая, но не ограничиваясь ими, например, использование веществ, увеличивающих растворимость, разбавляющих или диспергирующих веществ, таких как солевой раствор, консервантов, таких как бензиловый спирт, усилителей всасываемости и фторуглеродов.
Согласно некоторым вариантам осуществления олигонуклеотиды и композиции доставляют в ЦНС. Согласно некоторым вариантам осуществления олигонуклеотиды и композиции доставляют в спинномозговую жидкость. Согласно некоторым вариантам осуществления олигонуклеотиды и композиции вводят в паренхиму головного мозга. Согласно некоторым вариантам осуществления олигонуклеотиды и композиции доставляют животному/субъекту путем интратекального введения или интрацеребровентрикулярного введения. Широкое распространение описанных в настоящем документе олигонуклеотидов и композиций в центральной нервной системе может быть достигнуто с помощью интрапаренхиматозного введения, интратекального введения или интрацеребровентрикулярного введения.
Согласно некоторым вариантам осуществления парентеральное введение осуществляют путем инъекции, например, с помощью шприца, насоса и т.д. Согласно некоторым вариантам осуществления инъекция представляет собой болюсную инъекцию. Согласно некоторым вариантам осуществления инъекцию вводят непосредственно в ткань, такую как стриатум, каудат, кора, гиппокамп и мозжечок.
Согласно некоторым вариантам осуществления способы специфической локализации фармацевтического агента, такие как болюсная инъекция, снижают среднюю эффективную концентрацию (ЕС50) в 20, 25, 30, 35, 40, 45 или 50. Согласно некоторым вариантам осуществления фармацевтический агент в антисмысловом соединении является таковым, как описано далее. В определенных вариантах реализации целевая ткань представляет собой ткань головного мозга. Согласно некоторым вариантам осуществления целевая ткань представляет собой стриарную ткань. Согласно некоторым вариантам осуществления желательно уменьшение ЕС50, поскольку оно уменьшает дозу, необходимую для достижения фармакологического результата у нуждающегося в этом пациента.
Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид вводят посредством инъекции или инфузии один раз в месяц, каждые два месяца, каждые 90 дней, каждые 3 месяца, каждые 6 месяцев, два раза в год или один раз в год.
Фармацевтические композиции, подходящие для применения согласно настоящему раскрытию, включают композиции, где активные ингредиенты содержатся в количестве, которое является эффективным для достижения предполагаемой цели. Определение эффективных количеств, в частности с учетом приведенного подробного описания находится в рамках компетенции специалистов в данной области техники.
Помимо активных ингредиентов указанные фармацевтические композиции могут содержать подходящие фармацевтически приемлемые носители, включая вспомогательные вещества и добавки, которые способствуют введению активных соединений в препараты, которые можно применять в области фармацевтики. Препараты, предназначенные для перорального введения, могут быть в виде таблеток, драже, капсул или растворов.
Фармацевтические препараты для перорального применения можно получать путем объединения активных соединений и твердых вспомогательных веществ, необязательно измельчения полученной смеси и обработки смеси гранул после добавления подходящих добавок, если это желательно, с получением таблеток или ядер драже. Подходящими вспомогательными веществами в частности являются наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; препараты целлюлозы, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза (КМЦ) натрия и/или поливинилпирролидон (PVP; повидон). При желании можно добавлять разрыхлители, такие как перекрестно-сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
Ядра драже обеспечены подходящими оболочками. Для этого можно использовать концентрированные растворы сахаров, которые необязательно могут содержать аравийскую камедь, тальк, поливинилпирролидон, гель карбопол, полиэтиленгликоль (ПЭГ) и/или диоксид титана, растворы лаков и подходящие органические растворители или смеси растворителей. Для распознавания или определения различных комбинаций доз активного соединения в таблетки или оболочки драже можно добавлять красители или пигменты.
Фармацевтические препараты, которые можно использовать перорально, включают твердые капсулы, полученные из желатина, а также мягкие закрытые капсулы, полученные из желатина и пластификатора, такого как глицерин или сорбит. Твердые капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связывающими веществами, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния, и, необязательно, со стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкие полиэтиленгликоли (ПЭГ). Кроме того, можно добавлять стабилизаторы.
В зависимости от конкретного состояния или болезненного состояния, подвергающегося лечению или предотвращению, совместно с олигонуклеотидами согласно настоящему раскрытию можно вводить дополнительные терапевтические агенты, которые обычно вводят для лечения или предотвращения указанного состояния. Например, для лечения пролиферативных заболеваний и рака химиотерапевтические агенты или другие антипролиферативные агенты можно объединять с олигонуклеотидами согласно настоящему раскрытию. Примеры известных химиотерапевтических агентов включают, но не ограничиваются ими, адриамицин, дексаметазон, винкристин, циклофосфамид, фторурацил, топотекан, таксол, интерфероны и производные платины.
Функция и преимущество указанных и других вариантов реализации настоящего раскрытия будут понятны в более полной мере после изучения примеров, описанных ниже. Предполагается, что следующие примеры иллюстрируют преимущества настоящего раскрытия, но не определяют полный объем раскрытия.
Липиды
Согласно некоторым вариантам осуществления предложенные композиции олигонуклеотидов дополнительно содержат один или более липидов. Согласно некоторым вариантам осуществления липиды конъюгируют с предложенными олигонуклеотидами в композициях. Согласно некоторым вариантам осуществления два или более одинаковых или разных липидов могут быть конъюгированы с одним олигонуклеотидом посредством одинаковой или разной химии и/или положения. Согласно некоторым вариантам осуществления композиция может содержать описанный в настоящем документе олигонуклеотид (в качестве неограничивающих примеров, композицию олигонуклеотидов с контролируемой хиральностью или композицию олигонуклеотидов с контролируемой хиральностью, в которой последовательность олигонуклеотида содержит, состоит из или представляет собой последовательность любого описанного в настоящем документе олигонуклеотида, или композицию олигонуклеотидов с контролируемой хиральностью, в которой последовательность олигонуклеотида содержит, состоит из или представляет собой последовательность любого олигонуклеотида, описанного в таблице 8 или любой другой таблице в настоящем документе и т.д.) и липид. Согласно некоторым вариантам осуществления предложенный олигонуклеотид содержит последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль химических модификаций (например, модификаций основания, модификаций сахара и т.д.) любого описанного в настоящем документе олигонуклеотида и конъюгирован к липиду. Согласно некоторым вариантам осуществления предложенная композиция содержит описанный в настоящем документе олигонуклеотид и липид, причем липид конъюгирован с олигонуклеотидом.
Согласно некоторым вариантам осуществления настоящее раскрытие относится к композиции, содержащей олигонуклеотид и липид. Многие липиды могут быть использованы в предусмотренных технологиях в соответствии с настоящим раскрытием.
Согласно некоторым вариантам осуществления липид содержит группу RLD, причем RLD представляет собой необязательно замещенную C10-C80 насыщенную или частично ненасыщенную алифатическую группу, в которой одно или более метиленовых звеньев возможно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Cy-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)-, и -C(O)O-, где: каждый R' независимо представляет собой -R, C(O)R, CO2R или -SO2R, или:
два R' берутся вместе с их промежуточными атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца;
-Cy- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из карбоциклилена, арилена, гетероарилена и гетероциклилена; а также
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, фенильного, карбоциклильного, арильного, гетероарильного или гетероциклильного C1-С6.
Согласно некоторым вариантам осуществления липид содержит группу RLD, причем RLD представляет собой необязательно замещенную C10-С60 насыщенную или частично ненасыщенную алифатическую группу, в которой одно или более метиленовых звеньев возможно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Cy-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где: каждый R' независимо представляет собой -R, C(O)R, CO2R или -SO2R, или:
два R' берутся вместе с их промежуточными атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца;
-Cy- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из карбоциклилена, арилена, гетероарилена и гетероциклилена; а также
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, фенильного, карбоциклильного, арильного, гетероарильного или гетероциклильного C1-С6.
Согласно некоторым вариантам осуществления липид содержит группу RLD, причем RLD представляет собой необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую группу, в которой одно или более метиленовых звеньев возможно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Cy-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R')-, -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где: каждый R' независимо представляет собой -R, C(O)R, CO2R или -SO2R, или:
два R' берутся вместе с их промежуточными атомами с образованием необязательно замещенного арильного, карбоциклического, гетероциклического или гетероарильного кольца;
-Cy- представляет собой необязательно замещенное двухвалентное кольцо, выбранное из карбоциклилена, арилена, гетероарилена и гетероциклилена; а также
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, фенильного, карбоциклильного, арильного, гетероарильного или гетероциклильного C1-С6.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную C10-C80 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2- и -Cy-. Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2- и -Cy-. Согласно некоторым вариантам осуществления RLD представляет собой углеводородную группу, состоящую из атомов углерода и водорода.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2- и -Cy-. Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2- и -Cy-. Согласно некоторым вариантам осуществления RLD представляет собой углеводородную группу, состоящую из атомов углерода и водорода.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2- и -Cy-. Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо замещены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -C≡C-, C1-С6 гетероалифатического фрагмента, -C(R')2- и -Cy-. Согласно некоторым вариантам осуществления RLD представляет собой углеводородную группу, состоящую из атомов углерода и водорода.
Алифатическая группа RLD может характеризоваться разной подходящей длиной. Согласно некоторым вариантам осуществления она представляет собой C10-C80. Согласно некоторым вариантам осуществления она представляет собой С10-С75. Согласно некоторым вариантам осуществления она представляет собой С10-С70. Согласно некоторым вариантам осуществления она представляет собой С10-Сб5. Согласно некоторым вариантам осуществления она представляет собой С10-С60. Согласно некоторым вариантам осуществления она представляет собой С10-С50. Согласно некоторым вариантам осуществления она представляет собой С10-С40. Согласно некоторым вариантам осуществления она представляет собой C10-С35. Согласно некоторым вариантам осуществления она представляет собой С10-С30. Согласно некоторым вариантам осуществления она представляет собой С10-С25. Согласно некоторым вариантам осуществления она представляет собой С10-С24. Согласно некоторым вариантам осуществления она представляет собой С10-С23. Согласно некоторым вариантам осуществления она представляет собой C10-С22. Согласно некоторым вариантам осуществления она представляет собой С10-С21. Согласно некоторым вариантам осуществления она представляет собой С12-С22. Согласно некоторым вариантам осуществления она представляет собой С13-С22. Согласно некоторым вариантам осуществления она представляет собой С14-С22. Согласно некоторым вариантам осуществления она представляет собой С15-С22. Согласно некоторым вариантам осуществления она представляет собой С16-С22. Согласно некоторым вариантам осуществления она представляет собой С17-С22. Согласно некоторым вариантам осуществления она представляет собой С18-С22. Согласно некоторым вариантам осуществления она представляет собой С10-С20. Согласно некоторым вариантам осуществления нижний конец диапазона представляет собой С10, С11, С12, С13, С14, С15, C16, С17 или C18. Согласно некоторым вариантам осуществления высший конец диапазона представляет собой C18, С19, С20, С21, С22, С23, С24, С25, С26, С27, С28, С29, С30, С35, С40, С45, С50, С55 или С60. Согласно некоторым вариантам осуществления он представляет собой С10. Согласно некоторым вариантам осуществления он представляет собой С11. Согласно некоторым вариантам осуществления он представляет собой С12. Согласно некоторым вариантам осуществления он представляет собой C13. Согласно некоторым вариантам осуществления он представляет собой С14. Согласно некоторым вариантам осуществления он представляет собой С15. Согласно некоторым вариантам осуществления он представляет собой C16. Согласно некоторым вариантам осуществления он представляет собой C17. Согласно некоторым вариантам осуществления он представляет собой C18. Согласно некоторым вариантам осуществления он представляет собой С19. Согласно некоторым вариантам осуществления он представляет собой С20. Согласно некоторым вариантам осуществления он представляет собой С21. Согласно некоторым вариантам осуществления он представляет собой С22. Согласно некоторым вариантам осуществления он представляет собой С23. Согласно некоторым вариантам осуществления он представляет собой С24. Согласно некоторым вариантам осуществления он представляет собой С25. Согласно некоторым вариантам осуществления он представляет собой С30. Согласно некоторым вариантам осуществления он представляет собой С35. Согласно некоторым вариантам осуществления он представляет собой С40. Согласно некоторым вариантам осуществления он представляет собой С45. Согласно некоторым вариантам осуществления он представляет собой C50. Согласно некоторым вариантам осуществления он представляет собой С55. Согласно некоторым вариантам осуществления он представляет собой C60.
Согласно некоторым вариантам осуществления липид содержит не более одной группы RLD. Согласно некоторым вариантам осуществления липид содержит две или более группы RLD.
Согласно некоторым вариантам осуществления липид конъюгирован с биологически активным агентом, возможно через линкерную группу, в виде фрагмента, содержащего группу RLD. Согласно некоторым вариантам осуществления липид конъюгирован с биологически активным агентом, возможно через линкерную группу, в виде фрагмента, содержащего не более одной группы RLD. Согласно некоторым вариантам осуществления липид конъюгирован с биологически активным агентом, возможно через линкерную группу, в качестве группы RLD. Согласно некоторым вариантам осуществления липид конъюгирован с биологически активным агентом, возможно через линкерную группу, в виде фрагмента, содержащего две или более группы RLD.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит необязательно замещенную C10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления RLD представляет собой С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более C1-4 алифатическими группами. Согласно некоторым вариантам осуществления липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более C1-4 алифатическими группами. Согласно некоторым вариантам осуществления RLD представляет собой С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-2 алифатическими группами. Согласно некоторым вариантам осуществления липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-2 алифатическими группами. Согласно некоторым вариантам осуществления RLD представляет собой C10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более метальными группами. Согласно некоторым вариантам осуществления липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более метальными группами.
Согласно некоторым вариантам осуществления RLD представляет собой незамещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит незамещенную линейную, насыщенную или частично ненасыщенную алифатическую цепь С10-С40.
Согласно некоторым вариантам осуществления липид содержит не более одной необязательно замещенной C10-С40 линейной, насыщенной или частично ненасыщенной алифатической цепи. Согласно некоторым вариантам осуществления липид содержит две или более необязательно замещенных C10-С40 линейных, насыщенных или частично ненасыщенных алифатических цепей.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления RLD представляет собой С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами. Согласно некоторым вариантам осуществления липид содержит С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами. Согласно некоторым вариантам осуществления RLD представляет собой С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-2 алифатическими группами. Согласно некоторым вариантам осуществления липид содержит С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-2 алифатическими группами. Согласно некоторым вариантам осуществления RLD представляет собой С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более метальными группами. Согласно некоторым вариантам осуществления липид содержит С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более метальными группами.
Согласно некоторым вариантам осуществления RLD представляет собой незамещенную C10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит незамещенную С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит не более одной необязательно замещенной С10-С60 линейной, насыщенной или частично ненасыщенной алифатической цепи. Согласно некоторым вариантам осуществления липид содержит две или более необязательно замещенных С10-С60 линейных, насыщенных или частично ненасыщенных алифатических цепей.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления RLD представляет собой необязательно замещенную С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит необязательно замещенную C10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления RLD представляет собой C10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами. Согласно некоторым вариантам осуществления липид содержит С10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более C1-4 алифатическими группами. Согласно некоторым вариантам осуществления RLD представляет собой С10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-2 алифатическими группами. Согласно некоторым вариантам осуществления липид содержит C10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-2 алифатическими группами. Согласно некоторым вариантам осуществления RLD представляет собой С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более метильными группами. Согласно некоторым вариантам осуществления липид содержит С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более метальными группами.
Согласно некоторым вариантам осуществления RLD представляет собой незамещенную С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь. Согласно некоторым вариантам осуществления липид содержит незамещенную С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
Согласно некоторым вариантам осуществления липид содержит не более одной необязательно замещенной С10-C80 линейной, насыщенной или частично ненасыщенной алифатической цепи. Согласно некоторым вариантам осуществления липид содержит две или более необязательно замещенных C10-C80 линейных, насыщенных или частично ненасыщенных алифатических цепей.
Согласно некоторым вариантам осуществления RLD представляет собой или содержит С10 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С10 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С11 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С11 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С12 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С12 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C13 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C13 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С14 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С14 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С15 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C15 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C16 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C16 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C17 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С17 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит C18 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С18 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С19 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С19 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С20 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С20 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С21 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С21 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С22 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С22 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С23 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С23 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С24 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С24 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С25 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С25 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С26 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С26 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С27 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С27 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С28 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С28 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С29 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С29 частично ненасыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С30 насыщенную линейную алифатическую цепь. Согласно некоторым вариантам осуществления RLD представляет собой или содержит С30 частично ненасыщенную линейную алифатическую цепь.
Согласно некоторым вариантам осуществления липид имеет структуру RLD-OH. Согласно некоторым вариантам осуществления липид имеет структуру RLD-C(O)OH. Согласно некоторым вариантам осуществления RLD представляет собой







Согласно некоторым вариантам осуществления липид представляет собой лауриновую кислоту, миристиновую кислоту, пальмитиновую кислоту, стеариновую кислоту, олеиновую кислоту, линолевую кислоту, альфа-линоленовую кислоту, гамма-линоленовую кислоту, докозагексаеновую кислоту (DHA или цис-DHA), турбинаровую кислоту, арахидоновую кислоту и дилинолеил. Согласно некоторым вариантам осуществления липид представляет собой лауриновую кислоту, миристиновую кислоту, пальмитиновую кислоту, стеариновую кислоту, олеиновую кислоту, линолевую кислоту, альфа-линоленовую кислоту, гамма-линоленовую кислоту, докозагексаеновую кислоту (DHA или цис-DHA). Согласно некоторым вариантам осуществления липид имеет структуру: 






Согласно некоторым вариантам осуществления липид содержит или состоит из любой из: по меньшей мере частично гидрофобной или амфифильной молекулы, фосфолипида, триглицерида, диглицерида, моноглицерида, жирорастворимого витамина, стерола, жира и воска. Согласно некоторым вариантам осуществления липид представляет собой любой из: жирной кислоты, глицеролипида, глицерофосфолипида, сфинголипида, стеринового липида, пренолового липида, сахаролипида, поликетида и другой молекулы.
Липиды могут быть включены в предусмотренные технологии посредством многих типов способов в соответствии с настоящим раскрытием. Согласно некоторым вариантам осуществления липиды физически смешиваются с предложенными олигонуклеотидами для образования предложенных композиций. Согласно некоторым вариантам осуществления липиды химически конъюгируют с олигонуклеотидами.
Согласно некоторым вариантам осуществления предложенные композиции содержат два или более липидов. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат два или более конъюгированных липидов. Согласно некоторым вариантам осуществления два или более конъюгированных липидов являются одинаковыми. Согласно некоторым вариантам осуществления два или более конъюгированных липидов являются различными. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат не более одного липида. Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции содержат различные типы конъюгированных липидов. Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции содержат липиды того же типа.
Липиды могут быть конъюгированы с олигонуклеотидами возможно через линкерные группы. В соответствии с настоящим раскрытием могут использоваться различные типы линкерных групп в данной области техники. Согласно некоторым вариантам осуществления линкерная группа содержит фосфатную группу, которая может, например, использоваться для конъюгирования липидов с помощью химии, аналогичной той, которая используется для синтеза олигонуклеотидов. Согласно некоторым вариантам осуществления линкерная группа содержит амид, сложный эфир или эфирную группу. Согласно некоторым вариантам осуществления линкерная группа имеет структуру -L-. Согласно некоторым вариантам осуществления после конъюгации с олигонуклеотидами липид образует фрагмент, имеющий структуру -L-RLD, причем каждый из L и RLD независимо является таким, как определено и описано в настоящем документе.
Согласно некоторым вариантам осуществления -L- содержит двухвалентную алифатическую цепь. Согласно некоторым вариантам осуществления -L- содержит фосфатную группу. Согласно некоторым вариантам осуществления -L- содержит фосфоротиоатную группу. Согласно некоторым вариантам осуществления -L- имеет структуру -C(O)NH-(CH2)6-OP(=O)(S-)-.
Липиды, возможно через линкерные группы, могут быть конъюгированы с олигонуклеотидами в различных подходящих местах. Согласно некоторым вариантам осуществления липиды конъюгируют через группу 5'-ОН. Согласно некоторым вариантам осуществления липиды конъюгируют через группу 3'-ОН. Согласно некоторым вариантам осуществления липиды конъюгируют через один или более фрагментов сахара. Согласно некоторым вариантам осуществления липиды конъюгируют через одно или более оснований. Согласно некоторым вариантам осуществления липиды включены через одну или более межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотид может содержать несколько конъюгированных липидов, которые независимо конъюгированы через его 5'-ОН, 3'-ОН, сахарные фрагменты, фрагменты оснований и/или межнуклеотидные линкерные группы.
Согласно некоторым вариантам осуществления липид конъюгируют с олигонуклеотидом возможно через фрагмент линкерной группы. Специалисту в данной области техники будет понятно, что могут быть использованы различные технологии для конъюгации липидов с олигонуклеотидом в соответствии с настоящим раскрытием. Например, для липидов, содержащих карбоксильные группы, такие липиды могут быть конъюгированы через карбоксильные группы. Согласно некоторым вариантам осуществления липид конъюгируют через линкерную группу, имеющую структуру -L-, где L является такой, как определено и описано в формуле I. Согласно некоторым вариантам осуществления L содержит сложный диэфир фосфата или модифицированный сложный диэфир фосфата. Согласно некоторым вариантам осуществления соединение, образованное липидной конъюгацией, имеет структуру (RLD-L-)x-(олигонуклеотид), где x равно 1 или целому числу, превышающему 1, и каждый из RLD и L независимо является таким, как определено и описано в настоящем документе. Согласно некоторым вариантам осуществления x равен 1. Согласно некоторым вариантам осуществления x больше 1. Согласно некоторым вариантам осуществления олигонуклеотид представляет собой олигонуклеотид. Например, согласно некоторым вариантам осуществления конъюгат имеет следующие структуры:
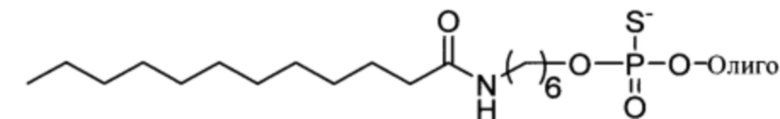
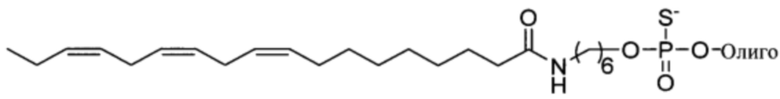
Согласно некоторым вариантам осуществления линкерную группу выбирают из: незаряженной линкерной группы; заряженной линкерной группы; линкерной группы, содержащей алкил; линкерной группы, содержащей фосфат; разветвленной линкерной группы; неразветвленной линкерной группы; линкерной группы, содержащей по меньшей мере одну группу расщепления; линкерной группы, содержащей по меньшей мере одну группу редокс-расщепления; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе фосфата; линкерной группы, содержащей по меньшей мере одну группу расщепления кислотой; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе сложного эфира, и линкерной группы, содержащей по меньшей мере одну группу расщепления на основе пептидов.
Согласно некоторым вариантам осуществления липид не конъюгирован с олигонуклеотидом.
Согласно некоторым вариантам осуществления настоящее раскрытие относится к композициям и способам, относящимся к композиции, содержащей олигонуклеотид и липид, содержащий С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, причем липид конъюгирован с биологически активным агентом. Согласно некоторым вариантам осуществления настоящее раскрытие относится к композициям и способам, относящимся к композиции, содержащей олигонуклеотид и липид, содержащий С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами, причем липид конъюгирован с биологически активным агентом.
Согласно некоторым вариантам осуществления настоящее раскрытие относится к композициям и способам, относящимся к композиции, содержащей олигонуклеотид и липид, содержащий С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, причем липид не конъюгирован с биологически активным агентом. Согласно некоторым вариантам осуществления настоящее раскрытие относится к композициям и способам, относящимся к композиции, содержащей олигонуклеотид и липид, содержащий С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами, причем липид не конъюгирован с биологически активным агентом.
Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты, арахидоновой кислоты и дилинолеила, причем липид не конъюгирован с биологически активным агентом. Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты и дилинолеила, причем липид не конъюгирован с биологически активным агентом.
Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты, арахидоновой кислоты и дилинолеила, причем липид конъюгирован с биологически активным агентом. Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты и дилинолеила, причем липид конъюгирован с биологически активным агентом.
Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты, арахидоновой кислоты и дилинолеила, причем липид непосредственно конъюгирован с биологически активным агентом (без линкерной группы, расположенной между липидом и биологически активным агентом). Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты и дилинолеила, где липид непосредственно конъюгирован с биологически активным агентом (без линкерной группы, расположенной между липидом и биологически активным агентом).
Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты, арахидоновой кислоты и дилинолеила, причем липид опосредованно конъюгирован с биологически активным агентом (с линкерной группой, расположенной между липидом и биологически активным агентом). Согласно некоторым вариантам осуществления композиция содержит олигонуклеотид и липид, выбранный из: лауриновой кислоты, миристиновой кислоты, пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, линолевой кислоты, альфа-линоленовой кислоты, гамма-линоленовой кислоты, докозагексаеновой кислоты (цис-DHA), турбинаровой кислоты и дилинолеила, причем липид опосредованно конъюгирован с биологически активным агентом (с линкерной группой, расположенной между липидом и биологически активным агентом).
Линкерная группа представляет собой фрагмент, который соединяет две части композиции; в качестве неограничивающего примера, линкерная группа физически связывает олигонуклеотид с липидом.
Неограничивающие примеры подходящих линкерных групп включают: незаряженную линкерную группу; заряженную линкерную группу; содержащую алкил линкерную группу; содержащую фосфат линкерную группу; разветвленную линкерную группу; неразветвленную линкерную группу; линкерную группу, содержащую по меньшей мере одну группу расщепления; линкерную группу, содержащую по меньшей мере одну группу редокс-расщепления; линкерную группу, содержащую по меньшей мере одну группу расщепления на основе фосфата; линкерную группу, содержащую по меньшей мере одну группу расщепления кислотой; линкерную группу, содержащую по меньшей мере одну группу расщепления на основе сложного эфира, и линкерную группу, содержащую по меньшей мере одну группу расщепления на основе пептидов.
Согласно некоторым вариантам осуществления линкерная группа содержит незаряженную линкерную группу или заряженную линкерную группу.
Согласно некоторым вариантам осуществления линкерная группа содержит алкил.
Согласно некоторым вариантам осуществления линкерная группа содержит фосфат. В различных вариантах реализации фосфат также может быть модифицирован путем замены мостикового кислорода (то есть кислорода, который связывает фосфат с нуклеозидом) на азот (мостиковые фосфорамидаты), серу (мостиковые фосфоротиоаты) и углерод (мостиковые метиленфосфонаты). Замена может происходить либо в любом связующем кислороде, либо в обоих связующих кислородах. Когда мостиковый кислород представляет собой 3'-кислород нуклеозида, может быть сделана замена углеродом. Когда мостиковый кислород представляет собой 5'-кислород нуклеозида, может быть сделана замена азотом. В различных вариантах реализации линкерная группа, содержащая фосфат, содержит любой один или более из: фосфородитиоата, фосфорамидата, боранофосфоната или соединения формулы (I): 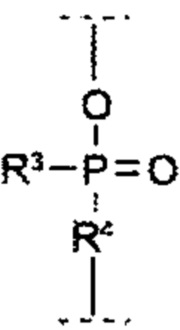 (I), где R3 выбран из ОН, SH, NH2, ВН3, СН3, С1-6 алкила, С6-10 арила, C1-6 алкокси и С6-10 арилокси, где C1-6 алкил и С6-10 арил являются незамещенными или возможно независимо замещены 1-3 группами, независимо выбранными из галогена, гидроксила и NH2; и R4 выбран из О, S, NH или СН2.
(I), где R3 выбран из ОН, SH, NH2, ВН3, СН3, С1-6 алкила, С6-10 арила, C1-6 алкокси и С6-10 арилокси, где C1-6 алкил и С6-10 арил являются незамещенными или возможно независимо замещены 1-3 группами, независимо выбранными из галогена, гидроксила и NH2; и R4 выбран из О, S, NH или СН2.
Согласно некоторым вариантам осуществления линкерная группа содержит прямую связь или атом, такой как кислород или серу, звено, такое как NR1, С(О), C(O)NH, SO, SO2, SO2NH, или цепь атомов, например, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, арилалкил, арилалкенил, арилалкинил, гетероарилалкил, гетероарилалкенил, гетероарилалкинил, гетероциклилалкил, гетероциклилалкенил, гетероциклилалкинил, арил, гетероарил, гетероциклил, циклоалкил, циклоалкенил, алкиларилалкил, алкиларилалкенил, арилалкилалкинил, алкениларилалкил, алкениларилалкенил, алкениларилалкинил, алкиниларилалкил, алкиниларилалкенил, алкиниларилалкинил, алкилгетероарилалкил, алкилгетероарилалкенил, алкилгетероарилалкинил, алкенилгетероарилалкил, алкенилгетероарилалкенил, алкенилгетероарилалкинил, алкинилгетероарилалкил, алкинилгетероарилалкенил, алкинилгетероарилалкинил, алкилгетероцилилалкил, алкилгетероцилклилалкенил, алкилгетероцилклилалкинил, алкенилгетероциклилалкил, алкенилгетероциклилалкенил, алкенилгетероциклилалкинил, алкинилгетероциклилалкил, алкинилгетероциклилалкенил, алкинилгетероциклилалкинил, алкиларил, алкениларил, алкиниларил, алкилгетероарил, алкенилгетероарил, алкинилгероарил, где один или более метиленов могут прерываться или заканчиваться О, S, S(O), SO2, N(R1)2, С(О), расщепляемой связывающей группой, замещенным или незамещенным арилом, замещенным или незамещенным гетероарилом, замещенной или незамещенной гетероциклической группой; где R1 представляет собой водород, ацил, алифатическую или замещенную алифатическую группу.
Согласно некоторым вариантам осуществления линкерная группа представляет собой разветвленную линкерную группу. Согласно некоторым вариантам осуществления точка разветвления разветвленной линкерной группы может быть по меньшей мере трехвалентной, но может представлять собой четырехвалентный, пятивалентный или шестивалентный атом или группу, представляющую такую множественную валентность. Согласно некоторым вариантам осуществления точка разветвления представляет собой --N, --N(Q)-C, --O--С, --S--C, --SS--C, --C(O)N(Q)-C, --OC(O)N(Q)-C, --N(Q)C(O)--C или --N(Q)C(O)O--C; где Q независимо представляет собой для каждого случая Н или необязательно замещенный алкил. В другом варианте реализации точка разветвления представляет собой глицерин или производное глицерина.
В одном варианте реализации линкерная группа содержит по меньшей мере одну отщепляемую связывающую группу.
В качестве неограничивающего примера отщепляемая связывающая группа может быть достаточно стабильной вне клетки, но после входа в целевую клетку расщепляться для высвобождения двух частей, которые линкерная группа удерживает вместе. В качестве неограничивающего примера отщепляемая связывающая группа расщепляется по меньшей мере в 10 раз или более, по меньшей мере в 100 раз быстрее в клетке-мишени или при первом эталонном условии (которое может быть выбрано, например, для имитации или представления внутриклеточных состояний), чем в крови субъекта, или при втором эталонном условии (которое может, например, быть выбрано для имитации или представления условий, обнаруженных в крови или сыворотке). Отщепляемые связывающие группы чувствительны к агентам отщепления, например, pH, окислительно-восстановительному потенциалу или наличию деградирующих молекул. Как правило, отщепляющие агенты более распространены или их содержание или активность внутри клеток выше, чем в сыворотке или крови. Примеры таких деградирующих агентов включают: окислительно-восстановительные агенты, которые выбраны для конкретных субстратов или которые не имеют субстратной специфичности, включая, например, окислительные или восстановительные ферменты или восстановительные агенты, такие как меркаптаны, присутствующие в клетках, которые могут разрушать редокс-расщепляемую связывающую группу посредством восстановления; эстеразы; эндосомы или агенты, которые могут образовывать кислотную среду, например, те, которые приводят к pH 5 или ниже; ферменты, которые могут гидролизовать или деградировать связывающую кислоту связывающую группу, действуя как общая кислота, пептидазы (которые могут быть субстратными) и фосфатазы.
В качестве неограничивающего примера отщепляемая связывающая группа, такая как дисульфидная связь, может быть восприимчива к pH. pH сыворотки человека составляет 7,4, тогда как среднее внутриклеточное значение pH несколько ниже, в пределах от примерно 7,1-7,3. Эндосомы имеют более кислое значение pH в диапазоне 5,5-6,0, а лизосомы имеют еще более кислое значение pH примерно 5,0. Некоторые линкерные группы будут иметь отщепляемую связывающую группу, которая отщепляется при желаемом значении pH, тем самым высвобождая катионный липид из лиганда внутри клетки или в желаемый компартмент клетки.
В качестве неограничивающего примера линкерная группа может включать отщепляемую связывающую группу, которая расщепляется конкретным ферментом. Тип отщепляемой связывающей группы, включенной в линкерную группу, может зависеть от целевой клетки. Например, лиганды, нацеленно воздействующие на печень, могут быть связаны с катионными липидами через линкерную группу, которая включает сложноэфирную группу. Клетки печени богаты эстеразами, поэтому линкерная группа будет расщепляться более эффективно в клетках печени, чем в типах клеток, которые не богаты эстеразой. Другие типы клеток, богатые эстеразами, включают клетки легкого, почечную кору и яички.
В качестве неограничивающего примера линкерная группа может содержать пептидную связь, которая может быть использована при нацеливании на типы клеток, богатые пептидазами, такие как клетки печени и синовиоциты.
В качестве неограничивающего примера пригодность потенциальной отщепляемой связывающей группы может быть оценена путем тестирования способности деградирующего агента (или условия) расщеплять потенциальную связывающую группу. Также желательно проверить потенциальную отщепляемую связывающую группу на способности противостоять расщеплению в крови или при контакте с другой нецелевой тканью. Таким образом, можно определить относительную восприимчивость к расщеплению между первым и вторым условиями, где первое выбрано, чтобы указывать на расщепление в клетке-мишени, а второе выбрано, чтобы указывать на расщепление в других тканях или биологических жидкостях, например, крови или сыворотке. Оценки могут проводиться в бесклеточных системах, в клетках, в культуре клеток, в культуре органов или тканей или у всех животных. Может быть полезно сделать первоначальные оценки в условиях отсутствия клеток или культуры и подтвердить путем дальнейших оценок у всех животных. В качестве неограничивающего примера полезные соединения-кандидаты расщепляются по меньшей мере в 2, 4, 10 или 100 раз быстрее в клетке (или в условиях in vitro, выбранных для имитации внутриклеточных состояний) по сравнению с кровью или сывороткой (или в условиях in vitro, выбранных для имитации внеклеточных состояний).
Согласно некоторым вариантам осуществления линкерная группа содержит окислительно-восстановительную отщепляемую связывающую группу. В качестве неограничивающего примера один класс отщепляемых связывающих групп представляет собой окислительно-восстановительные отщепляемые связывающие группы, которые расщепляются при восстановлении или окислении. Неограничивающим примером восстановительно отщепляемой связывающей группы является дисульфидная связывающая группа (--S--S--). Чтобы определить, является ли потенциальная отщепляемая связывающая группа подходящей «восстановительной отщепляемой связывающей группой» или, например, пригодна для использования с конкретным фрагментом iRNA и конкретным агентом нацеливания, можно рассмотреть способы, описанные в настоящем документе. В качестве неограничивающего примера кандидат может быть оценен путем инкубации с дитиотреитолом (DTT) или другим восстановителем с использованием реагентов, известных в данной области техники, которые имитируют скорость расщепления, которая будет наблюдаться в клетке, например, целевой клетке. Кандидаты также могут быть оценены в условиях, выбранных для имитации условий крови или сыворотки. В качестве неограничивающего примера соединения-кандидаты расщепляются не более чем на 10% в крови. В качестве неограничивающего примера применимые потенциальные соединения деградируют по меньшей мере в 2, 4, 10 или 100 раз быстрее в клетке (или в условиях in vitro, выбранных для имитации внутриклеточных состояний) по сравнению с кровью (или в условиях in vitro, выбранных для имитации внеклеточных условий). Скорость расщепления потенциальных соединений может быть определена с использованием стандартных анализов кинетики ферментов в условиях, выбранных для имитации внутриклеточных сред, и по сравнению с условиями, выбранными для имитации внеклеточных сред.
Согласно некоторым вариантам осуществления линкерная группа, содержащая отщепляемые связывающие группы на основе фосфата, расщепляется агентами, которые деградируют или гидролизуют фосфатную группу. Примером агента, который расщепляет фосфатные группы в клетках, являются ферменты, такие как фосфатазы в клетках. Примерами связующих групп на основе фосфата являются --O--P(O)(ORk)-O--, --О--P(S)(ORk)-O--, --O--P(S)(SRk)-O--, --S--P(O)(ORk)-O--, --O--P(O)(ORk)-S--, --S--P(O)(ORk)-S--, --O--P(S)(ORk)-S--, --S--P(S)(ORk)-O--, --O--P(O)(Rk)-O--, --O--P(S)(Rk)-O--, --S--P(O)(Rk)-O--, --S--P(S)(Rk)-O--, --S--P(O)(Rk)-S--, --O--P(S)(Rk)-S--. Дополнительными нелимитирующими примерами являются --O--Р(O)(ОН)--O--, --O--P(S)(OH)--O--, --О--P(S)(SH)--O--, -S-P(O)(OH)--O--, --O--P(O)(OH)--S--, --S-P(O)(OH)--S--, --O--P(S)(OH)--S--, --S--P(S)(OH)--O--, --O--P(O)(H)--O--, --O--P(S)(H)--O--, --S--P(O)(H)--O--, --S--P(S)(H)--O--, --S--P(O)(H)--S--, --O-P(S)(H)--S--. Дополнительными нелимитирующими примерами являются --O--Р(O)(ОН)--O--.
Согласно некоторым вариантам осуществления линкерная группа содержит кислотные отщепляемые связывающие группы, которые являются связывающими группами, расщепляемыми в кислых условиях. В качестве неограничивающего примера кислотные расщепляемые связывающие группы расщепляются в кислой среде с pH примерно 6,5 или ниже (например, примерно 6,0, 5,5, 5,0 или ниже) или такими агентами, как ферменты, которые могут действовать как общая кислота. В клетке специфические органеллы с низким pH, такие как эндосомы и лизосомы, могут обеспечить среду расщепления для кислотных отщепляемых связывающих групп. Примеры кислотных отщепляемых связывающих групп включают, но не ограничиваются ими, гидразоны, сложные эфиры и сложные эфиры аминокислот. Кислотные отщепляемые группы могут иметь общую формулу --C=NN--, С(O)O или --ОС(О). В дополнительном неограничивающем примере, когда углерод, присоединенный к кислороду сложного эфира (алкоксигруппа), представляет собой арильную группу, замещенную алкильную группу или третичную алкильную группу, такую как диметилпентил или трет-бутил.
Согласно некоторым вариантам осуществления линкерная группа содержит связывающие группы на основе сложного эфира. В качестве неограничивающего примера отщепляемые связывающие группы на основе сложного эфира расщепляются ферментами, такими как эстеразы и амидазы в клетках. Примеры отщепляемых связывающих групп на основе сложного эфира включают, но не ограничиваются ими, сложные эфиры алкиленовых, алкениленовых и алкиниленовых групп. Сложноэфирные отщепляемые связывающие группы имеют общую формулу --С(O)O-- или --ОС(О)--. Эти кандидаты могут быть оценены с использованием способов, аналогичных описанным выше.
Согласно некоторым вариантам осуществления линкерная группа содержит отщепляемую группу на основе пептида. Отщепляемые связывающие группы на основе пептида расщепляются ферментами, такими как пептидазы и протеазы в клетках. Отщепляемые связывающие группы на основе пептидов представляют собой пептидные связи, образованные между аминокислотами с получением олигопептидов (например, дипептидов, трипептидов и т.д.) и полипептидов. В качестве неограничивающего примера, отщепляемые группы на основе пептидов не включают амидную группу (--C(O)NH--). Амидная группа может быть образована между любым алкиленом, алкениленом или алкиниленом. Пептидная связь представляет собой особый тип амидной связи, образованной между аминокислотами с образованием пептидов и белков. В качестве неограничивающего примера отщепляемая группа на основе пептида может быть ограничена пептидной связью (то есть амидной связью), образованной между аминокислотами, дающими пептиды и белки, и не включает всю амидную функциональную группу. В качестве неограничивающего примера, отщепляемые связывающие группы на основе пептидов могут иметь общую формулу -NHCHRAC(O)NHCHRBC(O)--, где RA и RB представляют собой R-группы двух соседних аминокислот. Эти кандидаты могут быть оценены с использованием способов, аналогичных описанным выше.
Может быть использована любая линкерная группа, описанная в данной области техники, в том числе в качестве неограничивающих примеров, описанных в заявке на патент США №20150265708.
Неограничивающий пример способа конъюгирования липида и олигонуклеотида представлен в примере 1.
Неограничивающим примером линкерной группы является линкерная группа С6-амино.
Целевые компоненты
Согласно некоторым вариантам осуществления предложенная композиция дополнительно содержит целевой компонент (целевое соединение или фрагмент). Целевой компонент может быть либо конъюгирован, либо не конъюгирован с липидом или биологически активным агентом. Согласно некоторым вариантам осуществления целевой компонент конъюгирован с биологически активным агентом. Согласно некоторым вариантам осуществления биологически активный агент конъюгирован как с липидом, так и с целевым компонентом. Как описано в настоящем документе, согласно некоторым вариантам осуществления биологически активный агент представляет собой предложенный олигонуклеотид. Таким образом, согласно некоторым вариантам осуществления предложенная композиция олигонуклеотидов дополнительно содержит помимо липидов и олигонуклеотидов, целевые элементы. В соответствии с настоящим раскрытием могут использоваться различные целевые компоненты, например, липиды, антитела, пептиды, углеводы и т.д.
Целевые компоненты могут быть включены в предусмотренные технологии посредством многих типов способов в соответствии с настоящим раскрытием. Согласно некоторым вариантам осуществления целевые компоненты физически смешивают с предложенными олигонуклеотидами для образования предложенных композиций. Согласно некоторым вариантам осуществления целевые компоненты химически конъюгируют с олигонуклеотидами.
Согласно некоторым вариантам осуществления предложенные композиции содержат два или более целевых компонента. Согласно некоторым вариантам осуществления олигонуклеотиды содержат два или более конъюгированных целевых компонента. Согласно некоторым вариантам осуществления два или более конъюгированных целевых компонентов являются одинаковыми. Согласно некоторым вариантам осуществления два или более конъюгированных целевых компонентов различны. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат не более одного целевого компонента. Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции содержат различные типы конъюгированных целевых компонентов. Согласно некоторым вариантам осуществления олигонуклеотиды предложенной композиции содержат целевые компоненты того же типа.
Целевые компоненты могут быть конъюгированы с олигонуклеотидами возможно через линкерные группы. В соответствии с настоящим раскрытием могут использоваться различные типы линкерных групп в данной области техники. Согласно некоторым вариантам осуществления линкерная группа содержит фосфатную группу, которая может, например, использоваться для конъюгации целевых компонентов посредством химии, аналогичной той, которая используется для синтеза олигонуклеотидов. Согласно некоторым вариантам осуществления линкерная группа содержит амидную, сложноэфирную или эфирную группу. Согласно некоторым вариантам осуществления линкерная группа имеет структуру -L-. Целевые компоненты могут быть конъюгированы с помощью одной или более линкерных групп по сравнению с липидами.
Целевые компоненты, возможно через линкерные группы, могут быть конъюгированы с олигонуклеотидами в различных подходящих местоположениях. Согласно некоторым вариантам осуществления целевые компоненты конъюгируют через 5'-OH-группу. Согласно некоторым вариантам осуществления целевые компоненты конъюгируют через 3'-OH-группу. Согласно некоторым вариантам осуществления целевые компоненты конъюгируют через один или более фрагментов сахара. Согласно некоторым вариантам осуществления целевые компоненты конъюгируют через одно или более оснований. Согласно некоторым вариантам осуществления целевые компоненты включают через одну или более межнуклеотидных линкерных групп. Согласно некоторым вариантам осуществления олигонуклеотид может содержать многочисленные конъюгированные целевые компоненты, которые независимо конъюгированы через его 5'-ОН, 3'-ОН, фрагменты сахара, фрагменты оснований и/или межнуклеотидные линкерные группы. Целевые компоненты и липиды могут быть конъюгированы либо в том же, соседнем и/или отделенном местоположениях. Согласно некоторым вариантам осуществления целевой компонент конъюгирует на одном конце олигонуклеотида. а липид конъюгирует на другом конце.
Согласно некоторым вариантам осуществления олигонуклеотид или олигонуклеотиды в композиции олигонуклеотидов с контролируемой хиральностью является антисмысловым олигонуклеотидом или являются антисмысловыми олигонуклеотидами. Согласно некоторым вариантам осуществления последовательность олигонуклеотида(ов) содержит или состоит из последовательности любого олигонуклеотида, описанного в настоящем документе. Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль химических модификаций (например, модификации оснований, модификации сахара и т.д.) любого олигонуклеотида, описанного в настоящем документе. Согласно некоторым вариантам осуществления последовательность олигонуклеотида(ов) содержит или состоит из последовательности любого олигонуклеотида, раскрытого в таблице 8.
Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид представляет собой олигонуклеотид, который участвует в опосредованном РНКазой Н расщеплении; например, антисмысловой олигонуклеотид гибридизуется специфичным к последовательности образом с частью целевой мРНК, таким образом, нацеливаясь на мРНК для расщепления с помощью РНКазы Н. Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид способен различать различные аллели одного и того же гена или мишени. Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид способен различать аллель дикого типа и мутантный аллель мишени. Согласно некоторым вариантам осуществления антисмысловый олигонуклеотид в значительной степени участвует в опосредованном РНКазой Н расщеплении мутантного аллеля, но участвует в опосредованном РНКазой Н расщеплении аллеля дикого типа в гораздо меньшей степени (например, не участвует в опосредованном РНКазой Н расщеплении аллеля дикого типа мишени). Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию. Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид нацелен на мутантный аллель. Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид нацелен на мутантный аллель гена хантингтина.
Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид способен различать аллель дикого типа и мутантный аллель мишени в гене хантингтина.
Согласно некоторым вариантам осуществления настоящее раскрытие относится к:
способу ингибирования экспрессии мутантного гена хантингтина у млекопитающего, предусматривающему получение композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и введение композиции млекопитающему;
способу лечения заболевания, вызванного чрезмерной экспрессией мутантного гена хантингтина у субъекта, причем указанный способ предусматривает введение композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина);
способу лечения болезни Хантингтона, предусматривающему введение композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина);
способу лечения признака и/или симптома болезни Хантингтона у субъекта путем обеспечения композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и введения терапевтически эффективного количества композиции субъекту;
способу введения олигонуклеотида нуждающемуся в этом субъекту, предусматривающему стадии получения композиции, содержащей олигонуклеотид и липид, и введения композиции субъекту, причем биологически активное соединение представляет собой олигонуклеотид (в виде неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу лечения заболевания у субъекта, предусматривающему стадии получения композиции, содержащей олигонуклеотид и липид, и введения терапевтически эффективного количества композиции субъекту, причем биологически активное соединение представляет собой олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем заболевание представляет собой любое заболевание, раскрытое в настоящем документе;
способу ингибирования экспрессии мутантного гена хантингтина у млекопитающего, предусматривающему стадии получения композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и введение композиции млекопитающему;
способу введения биологически активного агента нуждающемуся в этом субъекту, предусматривающему стадии получения композиции, содержащей биологически активный агент и липид, и введения композиции субъекту, причем биологически активное соединение представляет собой олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу лечения болезни Хантингтона у субъекта, предусматривающему стадии получения композиции, содержащей биологически активный агент и липид, и введения терапевтически эффективного количества композиции субъекту, причем биологически активное соединение представляет собой олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу опосредования опосредованного РНКазой Н расщепления нуклеиновой кислоты, содержащей мутантный ген хантингтина, у млекопитающего, причем способ предусматривает стадии получения композиции, содержащей липид и антисмысловый олигонуклеотид, и введения композиции млекопитающему;
способу лечения заболевания, вызванного мутацией в гене хантингтина, причем указанный способ предусматривает введение композиции, содержащей липид и антисмысловой олигонуклеотид, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию;
способу лечения признака и/или симптома болезни Хантингтона у субъекта путем обеспечения композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и введения терапевтически эффективного количества композиции субъекту;
способу введения олигонуклеотида нуждающемуся в этом субъекту, предусматривающему стадии получения композиции, содержащей олигонуклеотид и липид, и введения композиции субъекту, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу лечения болезни Хантингтона у субъекта, причем заболевание или нарушение связано с мутацией в гене, причем способ предусматривает стадии обеспечения композиции, содержащей олигонуклеотид и липид, и введения терапевтически эффективного количества композиции субъекту, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу опосредования опосредованного РНКазой Н расщепления нуклеиновой кислоты, содержащей мутантный ген хантингтина, у млекопитающего, причем способ предусматривает стадии получения композиции, содержащей липид и антисмысловой олигонуклеотид, и введения композиции млекопитающему;
способу лечения заболевания, связанного с мутацией в гене хантингтина, причем указанный способ предусматривает введение композиции, содержащей липид и антисмысловой олигонуклеотид, причем антисмысловой олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию;
способу лечения заболевания, вызванного мутацией в гене Хантингтин, причем указанный способ предусматривает введение композиции, содержащей липид и олигонуклеотид, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты кислота, содержащей мутацию;
способу лечения признака и/или симптома болезни Хантингтона у субъекта путем обеспечения композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и введения терапевтически эффективного количества композиции субъекту;
способу введения олигонуклеотида нуждающемуся в этом субъекту, предусматривающему стадии получения композиции, содержащей олигонуклеотид и липид, и введения композиции субъекту, причем олигонуклеотид способен участвовать в опосредованном РНКазой расщеплении нуклеиновой кислоты, содержащей мутацию, и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу лечения болезни Хантингтона у субъекта, причем болезнь Хантингтона связана с мутацией в гене хантингтина, причем способ предусматривает стадии получения композиции, содержащей олигонуклеотид и липид, и введения терапевтически эффективного количества композиции субъекту, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, и причем липид представляет собой любой липид, раскрытый в настоящем документе;
способу опосредования опосредованного РНКазой Н расщепления нуклеиновой кислоты, содержащей мутантный ген хантингтина у млекопитающего, причем способ предусматривает стадии получения композиции, содержащей липид и антисмысловой олигонуклеотид, и введения композиции млекопитающему, причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем последовательность антисмыслового олигонуклеотида содержит или состоит из последовательности любого антисмыслового олигонуклеотида, описанного в настоящем документе (например, в таблице 8). Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль химических модификаций (например, модификаций оснований, модификаций сахара и т.д.) любого олигонуклеотида, описанного в настоящем документе (например, в таблице 8);
способу лечения заболевания, связанного с мутацией в гене хантингтина, указанный способ предусматривает введение композиции, содержащей липид и антисмысловой олигонуклеотид, причем антисмысловый олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем последовательность антисмыслового олигонуклеотида содержит или состоит из последовательности любого антисмыслового олигонуклеотида, описанного в настоящем документе (например, в таблице 8);
способу лечения заболевания, вызванного мутацией в гене хантингтина, причем указанный способ предусматривает введение композиции, содержащей липид и олигонуклеотид, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем олигонуклеотид содержит или состоит из последовательности любого антисмыслового олигонуклеотида, описанного в настоящем документе (например, в таблице 8);
способу лечения признака и/или симптома болезни Хантингтона у субъекта путем обеспечения композиции, содержащей липид и олигонуклеотид (в качестве неограничивающего примера, антисмысловой олигонуклеотид, который нацелен на мутантный аллель гена хантингтина), и введения терапевтически эффективного количества композиции субъекту, причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем последовательность олигонуклеотида содержит или состоит из последовательности любого антисмыслового олигонуклеотида, описанного в настоящем документе (например, в таблице 8);
способу введения олигонуклеотида нуждающемуся в этом субъекту, предусматривающему стадии получения композиции, содержащей олигонуклеотид и липид, и введения композиции субъекту, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, и причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем последовательность олигонуклеотида содержит или состоит из последовательности любого антисмыслового олигонуклеотида, описанного в настоящем документе (например, в таблице 8);
способу лечения болезни Хантингтона у субъекта, причем болезнь Хантингтона связана с мутацией в гене хантингтина, причем способ предусматривает стадии получения композиции, содержащей олигонуклеотид и липид, и введения терапевтически эффективного количества композиции субъекту, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении нуклеиновой кислоты, содержащей мутацию, и причем липид представляет собой любой липид, раскрытый в настоящем документе, и причем олигонуклеотид содержит или состоит из последовательности любого антисмыслового олигонуклеотида, раскрытого в настоящем документе (например, в таблице 8).
Согласно некоторым вариантам осуществления предложенные олигонуклеотиды содержат последовательность оснований, профиль линкерных групп остова, профиль хиральных центров остова и/или профиль химических модификаций (например, модификаций оснований, модификаций сахара и т.д.) любого олигонуклеотида, описанного в настоящем документе.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов содержит множество олигонуклеотидов, которые характеризуются:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем модификаций фосфора остова;
причем один или более олигонуклеотидов из множества индивидуально конъюгированы с липидом.
Согласно некоторым вариантам осуществления композиция олигонуклеотидов с контролируемой хиральностью содержит множество олигонуклеотидов, которые характеризуются:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем модификаций фосфора остова; причем:
композиция характеризуется контролируемой хиральностью в том плане, что множество олигонуклеотидов имеют одну и ту же стереохимию при одной или более хиральных межнуклеотидных линкерных группах;
один или более олигонуклеотидов из множества индивидуально конъюгированы с липидом; а также
один или более олигонуклеотидов из множества возможно и индивидуально конъюгированы с целевым соединением или фрагментом.
Согласно некоторым вариантам осуществления антисмысловой олигонуклеотид находится в композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления олигонуклеотид находится в композиции олигонуклеотидов с контролируемой хиральностью.
Различные олигонуклеотиды перечислены в таблице 8. Многие из них способны участвовать в опосредованном РНКазой Н расщеплении гена хантингтина человека, как показано в данных, представленных в заявке на патент США №62/195779, поданной 7/22/15, и заявке на патент США №62/331,960, поданной 5/4/16, которые включены посредством ссылки в полном объеме; и в приведенных в настоящем документе данных.
Различные олигонуклеотиды, особенно способные участвовать в опосредованном РНКазой Н расщеплении целевого гена хантингтина человека или его мутантного варианта, включают: WV-1092, WVE120101, WV-2603 или WV-2595 или любую другую нуклеиновую кислоту, описанную в настоящем документе (включая, но не ограничиваясь ими, те, которые перечислены в таблице 8).
Любой олигонуклеотид или композиция олигонуклеотидов с контролируемой хиральностью может использоваться в комбинации с любым способом или композицией (например, любой фармацевтической композицией, модификацией и/или способом использования и/или производства), раскрытой в настоящем документе.
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает следующие варианты реализации:
1. Композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды, определяемые наличием:
1) одинаковой последовательности оснований и длины;
2) одинакового профиля линкерных групп остова; а также
3) одинакового профиля хиральных центров остова, причем композиция представляет собой по существу чистый препарат единственного олигонуклеотида в том отношении, что предопределенное количество олигонуклеотидов в композиции имеют одинаковую последовательность оснований и длину, одинаковый профиль линкерных групп остова и одинаковый профиль хиральных центров остова.
2. Композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова,
причем эта композиция характеризуется контролируемой хиральностью, поскольку она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида.
2а. Композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова,
причем эта композиция характеризуется контролируемой хиральностью, поскольку она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида, причем олигонуклеотиды нацелены на мутантный ген хантингтина, а длина составляет от примерно 10 до примерно 50 нуклеотидов, причем линкерные группы остова содержат по меньшей мере один фосфоротиоат и причем профиль хиральных центров остова содержит по меньшей мере один хиральный центр в конформации Rp и по меньшей мере один хиральный центр в конформации Sp.
3. Композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова, причем эта композиция представляет собой по существу чистый препарат одного олигонуклеотида, в котором по меньшей мере примерно 10% олигонуклеотидов в композиции имеют одинаковую последовательность оснований и длину, одинаковый профиль линкерных групп остова и одинаковый профиль хиральных центров остова.
4. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды содержат одну или более областей крыла и общую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и возможно содержит одну или более хиральных межнуклеотидных линкерных групп; а также
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп.
5. Композиция олигонуклеотидов, содержащая предопределенный уровень олигонуклеотидов, которые содержат одну или более областей крыла и общую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и возможно содержит одну или более хиральных межнуклеотидных линкерных групп;
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп, а общая область сердцевины имеет:
1) одинаковую последовательность оснований и длину;
2) одинаковый профиль линкерных групп остова; а также
3) одинаковый профиль хиральных центров остова.
6. Композиция олигонуклеотидов, содержащая предопределенный уровень олигонуклеотидов, которые содержат одну или более областей крыла и общую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и возможно содержит одну или более хиральных межнуклеотидных линкерных групп;
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп, а общая область сердцевины имеет:
1) одинаковую последовательность оснований;
2) одинаковый профиль линкерных групп остова; а также
3) одинаковый профиль хиральных центров остова; а также
4) одинаковый профиль модификаций фосфора остова.
6а. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды типа олигонуклеотида содержат по меньшей мере одну область крыла и область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и возможно содержит одну или более хиральных межнуклеотидных линкерных групп;
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп, и
причем по меньшей мере один нуклеотид в области крыла отличается от по меньшей мере одного нуклеотида области сердцевины, причем отличие заключается в одном или более из следующего:
1) линкерная группа остова;
2) профиль хиральных центров остова;
3) модификация сахара.
7. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды определяются по наличию одинакового профиля модификаций фосфора остова.
8. Композиция по любому из предшествующих вариантов реализации, в которой композиция содержит предопределенный уровень олигонуклеотидов отдельного типа олигонуклеотида, причем тип олигонуклеотида определяется:
1) последовательностью оснований;
2) профилем линкерных групп остова;
3) профилем хиральных центров остова; а также
4) профилем модификаций фосфора остова.
9. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды, имеющие одинаковую последовательность оснований, представляют собой олигонуклеотиды одного и того же типа олигонуклеотида, характеризующегося последовательностью основания, профилем линкерных групп остова, профилем хиральных центров остова и профилем модификаций фосфора остова.
10. Композиция по любому из предшествующих вариантов реализации, в которой композиция содержит предопределенные уровни олигонуклеотидов двух или более отдельных типов олигонуклеотида, причем тип олигонуклеотида определяется:
1) последовательностью оснований;
2) профилем линкерных групп остова;
3) профилем хиральных центров остова; а также
4) профилем модификаций фосфора остова.
11. Композиция олигонуклеотидов, которая характеризуется контролируемой хиральностью в том отношении, что композиция содержит предопределенный уровень олигонуклеотидов отдельного типа олигонуклеотида, причем тип олигонуклеотида определяется я:
1) последовательностью оснований;
2) профилем линкерных групп остова;
3) профилем хиральных центров остова; а также
4) профилем модификаций фосфора остова.
12. Композиция по любому из предшествующих вариантов реализации, причем композиция содержит два или более отдельных типа олигонуклеотида.
13. Композиция по любому из предшествующих вариантов реализации, в которой тип олигонуклеотида определяется идентичностью оснований, профилем модификации оснований, профилем модификации сахара, профилем линкерных групп остова, профилем хиральных центров остова и профилем модификаций фосфора остова.
14. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды, имеющие одинаковую последовательность, имеют идентичную структуру.
15. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды одного и того же типа олигонуклеотида имеют идентичную структуру.
16. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды имеют одно крыло.
17. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды представляют собой гемимеры, имеющие структуру крыло-сердцевина.
18. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды представляют собой гемимеры, имеющие структуру сердцевина-крыло.
19. Композиция по любому из вариантов реализации 1-15, в которой олигонуклеотиды имеют два крыла.
20. Композиция по любому из вариантов реализации 1-15, в которой олигонуклеотиды представляют собой гэпмеры, имеющие структуру крыло-сердцевина-крыло.
21. Композиция по любому из предшествующих вариантов реализации, в которой крыло содержит хиральную межнуклеотидную линкерную группу.
22. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо содержит хиральную межнуклеотидную линкерную группу.
23. Композиция по любому из вариантов реализации 1-17 и 19-22, в которой крыло к 5'-концу сердцевины содержит хиральную межнуклеотидную линкерную группу на 5'-конце крыла.
24. Композиция по любому из вариантов реализации 1-16 и 18-22, в которой крыло к 3'-концу сердцевины содержит хиральную межнуклеотидную линкерную группу на 3'-конце крыла.
25. Композиция по любому из предшествующих вариантов реализации, в которой крыло имеет только одну хиральную межнуклеотидную линкерную группу, и каждая из других межнуклеотидных линкерных групп крыла представляет собой природную фоосфатную линкерную группу(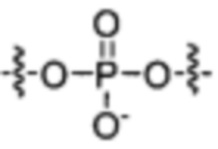 ).
).
26. Композиция по любому из предшествующих вариантов реализации, в которой хиральная межнуклеотидная линкерная группа имеет структуру формулы I.
27. Композиция по любому из предшествующих вариантов реализации, в которой хиральная межнуклеотидная линкерная группа имеет структуру формулы I и где X представляет собой S, a Y и Z представляют собой О.
28. Композиция по любому из предшествующих вариантов реализации, в которой хиральная межнуклеотидная линкерная группа представляет собой фосфоротиоатную линкерную группу.
29. Композиция по любому из предшествующих вариантов реализации, в которой хиральная межнуклеотидная линкерная группа характеризуется конфигурацией Sp.
30. Композиция по любому из предшествующих вариантов реализации, в которой каждая хиральная межнуклеотидная линкерная группа характеризуется конфигурацией Sp.
31. Композиция по любому из вариантов реализации 1-29, в которой хиральная межнуклеотидная линкерная группа характеризуется конфигурацией Rp.
32. Композиция по любому из вариантов реализации 1-28, в которой каждая хиральная межнуклеотидная линкерная группа характеризуется конфигурацией Rp.
33. Композиция по любому из вариантов реализации 1-31, в которой крыло содержит фосфоротиоатную линкерную группу конфигурации Sp.
34. Композиция по любому из вариантов реализации 1-31, в которой каждое крыло независимо содержит фосфоротиоатную линкерную группу конфигурации Sp.
35. Композиция по любому из вариантов реализации 1-17, 19-31 и 33-34, в которой крыло относится к 5'-концу сердцевины и крыло содержит фосфоротиоатную линкерную группу конфигурации Sp.
36. Композиция по любому из вариантов реализации 1-17, 19-31 и 33-35, в которой крыло относится к 5'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Sp на 5'-конце крыла.
37. Композиция по любому из вариантов реализации 1-17, 19-31 и 33-36, в которой крыло находится на 5'-конце сердцевины, крыло содержит фосфоротиоатную линкерную группу конфигурации Sp на 5'-конце крыла, и каждая из других межнуклеотидных линкерных групп крыла представляет собой природную фоосфатную линкерную группу 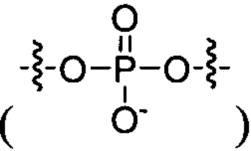 .
.
38. Композиция по любому из вариантов реализации 1-16, 18-31 и 33-34, в которой крыло относится к 3'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Sp на 3'-конце крыла.
39. Композиция по любому из вариантов реализации 1-16, 18-31, 33-34 и 38, в которой крыло относится к 3'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Sp на 3'- конец крыла.
40. Композиция по любому из вариантов 1-16, 18-31, 33-34 и 38-39, в которой одно крыло относится к 3'-концу общей сердцевины, крыло содержит фосфоротиоатную линкерную группу конфигурации Sp на 3'-конце крыла, и каждая из других межнуклеотидных линкерных групп крыла представляет собой природную фоосфатную линкерную группу  .
.
41. Композиция по любому из вариантов реализации 1-29 и 31-40, в которой крыло содержит фосфоротиоатную линкерную группу конфигурации Rp.
42. Композиция по любому из вариантов реализации 1-29 и 31-40, в которой каждое крыло независимо содержит фосфоротиоатную линкерную группу конфигурации Rp.
43. Композиция по любому из вариантов реализации 1-17, 19-29 и 31-42, в которой крыло относится к 5'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Rp.
44. Композиция по любому из вариантов реализации 1-17, 19-29 и 31-43, в которой крыло относится к 5'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Rp на 5'-конце крыла.
45. Композиция по любому из вариантов реализации 1-17, 19-29 и 31-44, в которой крыло относится к 5'-концу сердцевины, крыло содержит фосфоротиоатную линкерную группу конфигурации Rp на 5'-конце крыла и каждая из других межнуклеотидных линкерных групп крыла представляет собой природную фоосфатную линкерную группу  .
.
46. Композиция по любому из вариантов реализации 1-16, 18-29 и 31-42, в которой крыло относится к 3'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Rp.
47. Композиция по любому из вариантов реализации 1-16, 18-29 и 31-42, в которой крыло относится к 3'-концу сердцевины, и крыло содержит фосфоротиоатную линкерную группу конфигурации Rp на 3'-конце крыла.
48. Композиция по любому из вариантов реализации 1-16, 18-29 и 31-42, в которой одно крыло относится к 3'-концу общей сердцевины, крыло содержит фосфоротиоатную линкерную группу конфигурации Rp на 3'-конце крыла и каждая из других межнуклеотидных линкерных групп крыла представляет собой природную фоосфатную линкерную группу  .
.
49. Композиция по любому из вариантов реализации 1-28, в которой крыло относится к 5'-концу сердцевины, а его 5'-концевая межнуклеотидная линкерная группа представляет собой хиральную межнуклеотидную линкерную группу.
50. Композиция по любому из вариантов реализации 1-28, в которой крыло относится к 5'-концу сердцевины, а его 5'-концевая межнуклеотидная линкерная группа представляет собой хиральную межнуклеотидную линкерную группу конфигурации Sp.
51. Композиция по любому из вариантов реализации 1-28, в которой крыло относится к 5'-концу сердцевины, а его 5'-концевая межнуклеотидная линкерная группа представляет собой хиральную межнуклеотидную линкерную группу конфигурации Rp.
52. Композиция по любому из вариантов реализации 1-28 и 49-51, в которой крыло относится к 3'-концу сердцевины, а его 3'-концевая межнуклеотидная линкерная группа представляет собой хиральную межнуклеотидную линкерную группу.
53. Композиция по любому из вариантов реализации 1-28 и 49-51, в которой крыло относится к 3'-концу сердцевины, а его 3'-концевая межнуклеотидная линкерная группа представляет собой хиральную межнуклеотидную линкерную группу конфигурации Sp.
54. Композиция по любому из вариантов реализации 1-28 и 49-51, в которой крыло относится к 3'-концу сердцевины, а его 3'-концевая межнуклеотидная линкерная группа представляет собой хиральную межнуклеотидную линкерную группу конфигурации Rp.
55. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо содержит природную фоосфатную линкерную группу  .
.
56. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо содержит две или более природных фоосфатных линкерных групп  .
.
57. Композиция по любому из предшествующих вариантов реализации, в которой каждая область крыла независимо содержит две или более природных фоосфатных линкерных групп, и все линкерные группы с природными фосфатами являются последовательными.
58. Композиция по любому из предшествующих вариантов реализации, в которой крыло составляет в длину три или более оснований.
59. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину четыре или более оснований.
60. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину 5 или более оснований.
61. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину шесть или более оснований.
62. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину 7 или более оснований.
63. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину восемь или более оснований.
64. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину девять или более оснований.
65. Композиция по любому из предшествующих вариантов реализации, в которой одно крыло составляет в длину десять или более оснований.
66. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину три или более оснований.
67. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину четыре или более оснований.
68. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину пять или более оснований.
69. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину шесть или более оснований.
70. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину семь или более оснований.
71. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину восемь или более оснований.
72. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину девять или более оснований.
73. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо составляет в длину десять или более оснований.
74. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину два основания.
75. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину три основания.
76. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину четыре основания.
77. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину пять оснований.
78. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину шесть оснований.
79. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину семь оснований.
80. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину восемь оснований.
81. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину девять оснований.
82. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину десять оснований.
83. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину 11 оснований.
84. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину 12 оснований.
85. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину 13 оснований.
86. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину 14 оснований.
87. Композиция по любому из вариантов реализации 1-57, в которой крыло составляет в длину 15 оснований.
88. Композиция по любому из вариантов реализации 1-11 и 15-76, в которой каждое крыло имеет одинаковую длину.
89. Композиция по любому из предшествующих вариантов реализации, в которой крыло определено модификациями сахара относительно сердцевины.
90. Композиция по любому из предшествующих вариантов реализации, в которой каждое крыло независимо содержит модифицированный фрагмент сахара.
91. Композиция по любому из предшествующих вариантов реализации, в которой каждый фрагмент сахара крыла представляет собой независимо модифицированный фрагмент сахара.
92. Композиция по любому из предшествующих вариантов реализации, в которой модифицированный фрагмент сахара содержит высокоаффинную модификацию сахара.
93. Композиция по любому из предшествующих вариантов реализации, в которой модифицированный фрагмент сахара имеет 2'-модификацию.
94. Композиция по любому из предшествующих вариантов реализации, в которой модифицированный фрагмент сахара содержит бициклическую модификацию сахара.
95. Композиция по любому из предшествующих вариантов реализации, в которой модифицированный фрагмент сахара содержит бициклическую модификацию сахара, имеющую мостик -L- или -O-L-, соединяющий два кольцевых атома углерода.
96. Композиция по любому из предшествующих вариантов реализации, в которой модифицированный фрагмент сахара содержит бициклическую модификацию сахара, имеющую мостик 4'-СН(СН3)-O-2'.
97. Композиция по любому из вариантов реализации 1-93, в которой модифицированный фрагмент сахара содержит 2'-модификацию, в которой 2'-модификация представляет собой 2'-OR1.
98. Композиция по любому из вариантов реализации 1-93, в которой модифицированный фрагмент сахара содержит 2'-модификацию, в которой 2'-модификация представляет собой 2'-OR1, где R1 представляет собой необязательно замещенный C1-6 алкил.
99. Композиция по любому из вариантов реализации 1-93, в которой модифицированный фрагмент сахара содержит 2'-модификацию, где 2'-модификация представляет собой 2'-МОЕ.
100. Композиция по любому из вариантов реализации 1-93, в которой модифицированный фрагмент сахара содержит 2'-модификацию, где 2'-модификация представляет собой 2'-ОМе.
101. Композиция по любому из вариантов реализации 1-96, в которой модифицированный фрагмент сахара содержит 2'-модификацию, где 2'-модификация представляет собой S-cEt.
102. Композиция по любому из вариантов реализации 1-93, в которой модифицированный фрагмент сахара содержит 2'-модификацию, где 2'-модификация представляет собой FANA.
103. Композиция по любому из вариантов реализации 1-93, в которой модифицированный фрагмент сахара содержит 2'-модификацию, где 2'-модификация представляет собой FRNA.
104. Композиция по любому из вариантов реализации 1-92, в которой модифицированный фрагмент сахара имеет 5'-модификацию.
105. Композиция по любому из вариантов реализации 1-92, в которой модифицированный фрагмент сахара представляет собой R-5'-Ме-ДНК.
106. Композиция по любому из вариантов реализации 1-92, в которой модифицированный фрагмент сахара представляет собой S-5'-Ме-ДНК.
107. Композиция по любому из вариантов реализации 1-92, в которой модифицированный фрагмент сахара представляет собой ФГНК.
108. Композиция по любому из предшествующих вариантов реализации, в которой каждый фрагмент сахара крыла модифицирован.
109. Композиция по любому из предшествующих вариантов реализации, в которой все модифицированные фрагменты сахара крыла внутри крыла имеют одинаковую модификацию.
110. Композиция по любому из предшествующих вариантов реализации, в которой все модифицированные фрагменты сахара крыла имеют одинаковую модификацию.
111. Композиция по любому из вариантов реализации 1-108, в которой по меньшей мере один модифицированный фрагмент сахара крыла отличается от другого модифицированного фрагмента сахара крыла.
112. Композиция по любому из предшествующих вариантов реализации, в которой крыло содержит модифицированное основание.
113. Композиция по любому из предшествующих вариантов реализации, в которой крыло содержит 2S-dT.
114. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину пять или более оснований.
115. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину шесть или более оснований.
116. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину семь или более оснований.
117. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину восемь или более оснований.
118. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину девять или более оснований.
119. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину десять или более оснований.
120. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину 11 или более оснований.
121. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину 12 или более оснований.
122. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину 13 или более оснований.
123. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину 14 или более оснований.
124. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины составляет в длину 15 или более оснований.
125. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину пять оснований.
126. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину шесть оснований.
127. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину семь оснований.
128. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину восемь оснований.
129. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину девять оснований.
130. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину десять оснований.
131. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину 11 оснований.
132. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину 12 оснований.
133. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину 13 оснований.
134. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину 14 оснований.
135. Композиция по любому из вариантов реализации 1-113, в которой область сердцевины составляет в длину 15 оснований.
136. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины не имеет 2'-модификации.
137. Композиция по любому из предшествующих вариантов реализации, в которой каждый фрагмент сахара сердцевины не модифицирован.
138. Композиция по любому из предшествующих вариантов реализации, в которой каждый фрагмент сахара области сердцевины представляет собой природный фрагмент сахара ДНК.
139. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины содержит хиральную межнуклеотидную линкерную группу.
140. Композиция по любому из предшествующих вариантов реализации, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой хиральную межнуклеотидную линкерную группу.
141. Композиция по любому из предшествующих вариантов реализации, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой хиральную межнуклеотидную линкерную группу, имеющую структуру формулы I.
142. Композиция по любому из предшествующих вариантов реализации, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой хиральную межнуклеотидную линкерную группу, имеющую структуру формулы I, и где Х представляет собой S, a Y и Z представляют собой О.
143. Композиция по любому из предшествующих вариантов реализации, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой хиральную межнуклеотидную линкерную группу, имеющую структуру формулы I, и где один -L-R1 не представляет собой -Н.
144. Композиция по любому из вариантов реализации 1-142, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой фосфоротиоатную линкерную группу.
145. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины характеризуется профилем хирального центра остова, который содержит (Sp)m(Rp)n, где m равно 1-50, а n равно 1-10.
146. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины характеризуется профилем хирального центра остова, который содержит (Sp)m(Rp)n, где m равно 1-50, n равно 1-10 и m>n,
147. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины характеризуется профилем хирального центра остова, который содержит (Sp)m(Rp)n, где m равно 2, 3, 4, 5, 6, 7 или 8, и n равно 1.
148. Композиция по любому из вариантов реализации 1-144, в которой область сердцевины характеризуется профилем хиральных центров остова, содержащих (Rp)n(Sp)m, где m равно 1-50, а n равно 1-10.
149. Композиция по любому из вариантов реализации 1-144 и 148, в которой область сердцевины характеризуется профилем хиральных центров остова, содержащих Rp(Sp)m, где m равно 2, 3, 4, 5, 6, 7 или 8.
150. Композиция по любому из вариантов реализации 1-144 и 148-149, в которой область сердцевины характеризуется профилем хиральных центров остова, содержащих Rp(Sp)2.
151. Композиция по любому из вариантов реализации 1-144, в которой область сердцевины характеризуется профилем хиральных центров остова, содержащих (Np)t(Rp)n(Sp)m, где t равно 1-10, n равно 1-10, m равно 1-50, и каждый Np независимо представляет собой Rp или Sp.
152. Композиция по любому из вариантов реализации 1-144 и 151, в которой область сердцевины характеризуется профилем хиральных центров остова, содержащих (Sp)t(Rp)n(Sp)m, где t равно 1-10, n равно 1-10, m равно 1-50.
153. Композиция по любому из вариантов реализации 1-144 и 151-152, где n равно 1.
154. Композиция по любому из вариантов реализации 1-144 и 151-153, где t равно 2, 3, 4, 5, 6, 7 или 8.
155. Композиция по любому из вариантов реализации 1-144 и 151-154, где m равно 2, 3, 4, 5, 6, 7 или 8.
156. Композиция по любому из вариантов реализации 1-144 и 151-155, в которой по меньшей мере один из t и m больше 5.
157. Композиция по любому из предшествующих вариантов реализации, в которой область сердцевины характеризуется профилем хиральных центров остова, содержащих SpSpRpSpSp.
158. Композиция по любому из предшествующих вариантов реализации, в которой 50% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
159. Композиция по любому из предшествующих вариантов реализации, в которой 60% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
160. Композиция по любому из предшествующих вариантов реализации, в которой 70% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
161. Композиция по любому из предшествующих вариантов реализации, в которой 80% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
162. Композиция по любому из предшествующих вариантов реализации, в которой 90% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
163. Композиция по любому из предшествующих вариантов реализации, в которой каждая межнуклеотидная линкерная группа в области сердцевины является хиральной, область сердцевины имеет только одну конфигурацию Rp и каждая из других межнуклеотидных линкерных групп в области сердцевины представляет собой конфигурацию Sp.
164. Композиция по любому из предшествующих вариантов реализации, в которой каждый фрагмент основания в сердцевине не модифицирован.
165. Композиция по любому из вариантов реализации 1-163, в которой область сердцевины содержит модифицированное основание.
166. Композиция по любому из вариантов реализации 1-163, в которой область сердцевины содержит модифицированное основание, причем модифицированное основание представляет собой замещенные А, Т, С или G.
167. Композиция по любому из вариантов реализации 1-164, в которой каждый фрагмент основания в области сердцевины независимо выбран из А, Т, С и G.
168. Композиция по любому из вариантов реализации 1-163, в которой область сердцевины представляет собой последовательность ДНК, фосфатные линкерные группы которой независимо заменены фосфоротиоатными линкерными группами.
169. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды являются одноцепочечными.
170. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды представляют собой антисмысловой олигонуклеотид, антагомир, микроРНК, пре-микроРНК, антимир, супермир, рибозим, U1 адаптер, активатор РНК, агент РНК-интерференции, олигонуклеотид-«ловушка», образующий триплекс олигонуклеотид, аптамер или адъювант.
171. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды являются антисмысловыми олигонуклеотидами.
172. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 10 оснований.
173. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 11 оснований.
174. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 12 оснований.
175. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 13 оснований.
176. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 14 оснований.
177. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 15 оснований.
178. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 16 оснований.
179. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 17 оснований.
180. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 18 оснований.
181. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 19 оснований.
182. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 20 оснований.
183. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 21 основание.
184. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 22 основания.
185. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 23 основания.
186. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 24 основания.
187. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину более чем 25 оснований.
188. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды составляют в длину менее чем примерно 200 оснований.
189. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды составляют в длину менее чем примерно 150 оснований.
190. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды составляют в длину менее чем примерно 100 оснований.
191. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды составляют в длину менее чем примерно 50 оснований.
192. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды составляют в длину менее чем примерно 40 оснований.
193. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды составляют в длину менее чем примерно 30 оснований.
194. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 10 оснований.
195. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 11 оснований.
196. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 12 оснований.
197. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 13 оснований.
198. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 14 оснований.
199. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 15 оснований.
200. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 16 оснований.
201. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 17 оснований.
202. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 18 оснований.
203. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 19 оснований.
204. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 20 оснований.
205. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 21 основание.
206. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 22 основания.
207. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 23 основания.
208. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 24 основания.
209. Композиция по любому из вариантов реализации 1-171, в которой олигонуклеотиды составляют в длину 25 оснований.
210. Композиция по любому из предшествующих вариантов реализации, в которой тип олигонуклеотида представляет собой не (Sp, Sp, Rp, Sp, Sp, Rp, Sp, Sp, Rp, Sp, Sp)-d[5mCs1As1Gs1Ts15mCs1Ts1Gs15mCs1Ts1Ts15mCs1G] или (Rp, Rp, Rp, Rp, Rp, Sp, Sp, Rp, Sp, Sp, Rp, Sp, Sp, Rp, Rp, Rp, Rp, Rp, Rp)-Gs5mCs5mCsTs5mCsAsGsTs5mCsTsGs5mCsTsTs5mCsGs5mCsAs5mCs5mC (5R-(SSR)3-5R), где подчеркнутые нуклеотиды являются 2'-МОЕ модифицированными.
211. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотид представляет собой не олигонуклеотид, выбранный из: (Sp, Sp, Rp, Sp, Sp, Rp, Sp, Sp, Rp, Sp, Sp)-d[5mCs1As1Gs1Ts15mCs1Ts1Gs15mCs1Ts1Ts15mCs1G] или (Rp, Rp, Rp, Rp, Rp, Sp, Sp, Rp, Sp, Sp, Rp, Sp, Sp, Rp, Rp, Rp, Rp, Rp, Rp)-Gs5mCs5mCsTs5mCsAsGsTs5mCsTsGs5mCsTsTs5mCsGs5mCsAs5mCs5mC (5R-(SSR)3-5R), где подчеркнутые нуклеотиды являются 2'-МОЕ модифицированными.
212. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотид представляет собой не олигонуклеотид, выбранный из:

где строчные буквы представляют собой остатки 2'-ОМе РНК; заглавные буквы представляют собой остатки 2'-ОН РНК и "s" обозначает фосфоротиоатный фрагмент; а также

где строчные буквы представляют собой остатки 2'-ОМе РНК; заглавные буквы представляют собой остатки РНК, d = остатки 2'-дезокси и "s" обозначает фосфоротиоатный фрагмент; а также

где строчные буквы представляют собой остатки 2'-ОМе РНК; заглавные буквы представляют собой остатки РНК, d = остатки 2'-дезокси и "s" обозначает фосфоротиоатный фрагмент; а также

где строчные буквы представляют собой остатки 2'-ОМе РНК; заглавные буквы представляют собой остатки 2'-F РНК, d = остатки 2'-дезокси и "s" обозначает фосфоротиоатный фрагмент; а также

213. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотид не представляет собой олигонуклеотид, выбранный из: d[ARCSARCSARCSARCSARC], d[CSCSCSCRCRCSCSCSCSC], d[CSCSCSCSCSCSCRCRCSC] и d[CSCSCSCSCSCRCRCSCSC], где R представляет собой фосфоротиоатную линкерную группу в конфигурации Rp и S представляет собой фосфоротиоатную линкерную группу в конфигурации Sp.
214. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотид не представляет собой олигонуклеотид, выбранный из: GGARTSGRTSTRmCSTCGA, GGARTRGSTSTRmCRTCGA, GGASTSGRTRTSmCSTCGA, где R представляет собой фосфоротиоатную линкерную группу в конфигурации Rp и S представляет собой фосфоротиоатную линкерную группу в конфигурации Sp, все остальные линкерные группы представляют собой РО и каждая mC представляет собой 5-метилцитозин-модифицированный нуклеозид.
215. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотид не представляет собой олигонуклеотид, выбранный из: TkTkmCkAGTmCATGAmCTkTmCkmCk, где каждый нуклеозид с последующим нижним индексом 'k' указывает на (S)-cEt модификацию, R представляет собой фосфоротиоатную линкерную группу в конфигурации Rp и S представляет собой фосфоротиоатную линкерную группу в конфигурации Sp, каждая mC представляет собой 5-метилцитозин-модифицированный нуклеозид и все межнуклеотидные линкерные группы являются фосфоротиоатными (PS) с профилями стереохимии, выбранными из RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSSR, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRRSR, RRRRSSSSRS, SRRSRRRRRR, RSSRSSRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRRSRR, RSRRSRSSSR, RRSSRSRRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR, SSSSRRRRSR, RRRRRRRRRR и SSSSSSSSSS.
215а. Композиция по любому из предшествующих вариантов реализации, в которой одинаковый профиль хиральных центров остова содержит SSR, RSS, SSRSS, SSRSSR, RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSSR, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRSRSR, RRRRSSSSRS, SRRSRRRRRR, RSSRSSRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRSRRR, RSRRSRSSSR, RRSRRSRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR или SSSSRRRRSR.
215b. Композиция по любому из предшествующих вариантов реализации, в которой одинаковый профиль хиральных центров остова содержит SSRSS, SSRSSR, RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSSR, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRSRSR, RRRRSSSSRS, SRRSRRRRR, RSSRSSRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRRSRR, RSRRSRSSSR, RRSSRSRRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR или SSSSRRRRSR.
215с. Композиция по любому из предшествующих вариантов реализации, в которой одинаковый профиль хиральных центров остова содержит RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSS, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRSRSR, RRRRSSSSRS, SRRSRRRRRR, RRRRRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRSRSRR, RSRRSRSSSR, RRSSRSRRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRSRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR или SSSSRRRRSR.
216. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотид не представляет собой олигонуклеотид, выбранный из: TkTkmCkAGTmCATGAmCTTkmCkmCk, где каждый нуклеозид с последующим нижним индексом 'k' указывает на (S)-cEt модификацию, R представляет собой фосфоротиоатную линкерную группу в конфигурации Rp и S представляет собой фосфоротиоатную линкерную группу в конфигурации Sp, каждая mC представляет собой 5-метилцитозин-модифицированный нуклеозид и все межнуклеотидные линкерные группы в подчеркнутой сердцевине являются фосфоротиоатными (PS) с профилями стереохимии, выбранными из RSSSRSRRRS, RSSSSSSSSS, SRRSRSSSSR, SRSRSSRSSR, RRRSSSRSSS, RRRSRSSRSR, RRSSSRSRSR, SRSSSRSSSS, SSRRSSRSRS, SSSSSSRRSS, RRRSSRRRSR, RRRRSSSSRS, SRRSRRRRRR, RSSRSSRRRR, RSRRSRRSRR, RRSRSSRSRS, SSRRRRRSRR, RSRRSRSSSR, RRSSRSRRRR, RRSRSRRSSS, RRSRSSSRRR, RSRRRRSRSR, SSRSSSRRRS, RSSRSRSRSR, RSRSRSSRSS, RRRSSRRSRS, SRRSSRRSRS, RRRRSRSRRR, SSSSRRRRSR, RRRRRRRRRR и SSSSSSSSSS.
217. Композиция по варианту реализации 215 или 216, в которой каждый фосфоротиоатный фрагмент каждого нуклеотида, содержащий модификацию (S)-cEt, является стереометрическим.
218. Композиция по любому из предшествующих вариантов реализации, в которой последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, причем при контакте с полимером нуклеиновой кислоты, содержащим целевую последовательность, композиция обеспечивает измененный профиль расщепления по отношению к эталонному профилю расщепления эталонной композиции олигонуклеотидов.
219. Композиция по любому из предшествующих вариантов реализации, в которой полимер нуклеиновой кислоты представляет собой РНК, а эталонная композиция олигонуклеотидов представляет собой по существу рацемический препарат олигонуклеотидов, которые имеют одинаковую последовательность и длину.
220. Композиция по любому из предшествующих вариантов реализации, в которой полимер нуклеиновой кислоты представляет собой РНК, а эталонная композиция олигонуклеотидов представляет собой композицию олигонуклеотидов с неконтролируемой хиральностью олигонуклеотидов, которые имеют одинаковую последовательность и длину.
221. Композиция по любому из предшествующих вариантов реализации, в которой измененный профиль расщепления имеет меньше сайтов расщепления, чем эталонный профиль расщепления.
222. Композиция по любому из предшествующих вариантов реализации, в которой измененный профиль расщепления содержит только один сайт расщепления в целевой последовательности, а эталонный профиль расщепления имеет два или более сайтов расщепления в целевой последовательности.
223. Композиция по любому из предшествующих вариантов реализации, в которой последовательность оснований для олигонуклеотидов представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель целевого гена относительно других аллелей одного и того же целевого гена, которые существуют в популяции, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 2 раза превышает степень подавления, наблюдаемую для другого аллеля того же самого гена.
224. Композиция по любому из предшествующих вариантов реализации, в которой последовательность оснований для олигонуклеотидов представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель целевого гена относительно других аллелей одного и того же целевого гена которые существуют в популяции, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она демонстрирует подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
225. Композиция по любому из предшествующих вариантов реализации, в которой последовательность оснований содержит последовательность, которая комплементарна характеристическому элементу последовательности мишени, причем характеристический элемент последовательности определяет эту целевую последовательность относительно аналогичной последовательности.
226. Композиция по любому из предшествующих вариантов реализации, в которой последовательность оснований области сердцевины содержит последовательность, которая комплементарна характеристическому элементу последовательности мишени, причем характеристический элемент последовательности определяет эту целевую последовательность относительно аналогичной последовательности.
227. Композиция по любому из предшествующих вариантов реализации, в которой целевая последовательность представляет собой последовательность, содержащую мутацию, а аналогичная последовательность представляет собой последовательность дикого типа.
228. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности определяет конкретный аллель целевой последовательности относительно других аллелей одной и той же целевой последовательности.
229. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности определяет конкретный аллель целевого гена относительно других аллелей одного и того же целевого гена.
230. Композиция по любому из предшествующих вариантов реализации, в которой последовательность на 100% комплементарна характеристическому элементу последовательности.
231. Композиция по любому из предшествующих вариантов реализации, в которой положение 11, 12 или 13 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
232. Композиция по любому из вариантов реализации 1-230, в которой положение 11 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
233. Композиция по любому из вариантов реализации 1-230, в которой положение 12 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
234. Композиция по любому из вариантов реализации 1-230, в которой положение 13 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
235. Композиция по любому из вариантов реализации 1-230, в которой положение 8, 9 или 10 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
236. Композиция по любому из вариантов реализации 1-230, в которой положение 8 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
237. Композиция по любому из вариантов реализации 1-230, в которой положение 9 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
238. Композиция по любому из вариантов реализации 1-230, в которой положение 10 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
239. Композиция по любому из вариантов реализации 1-230, в которой положение 6, 7 или 8 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
240. Композиция по любому из вариантов реализации 1-230, в которой положение 6 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
241. Композиция по любому из вариантов реализации 1-230, в которой положение 7 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
242. Композиция по любому из вариантов реализации 1-230, в которой положение 8 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
243. Композиция по любому из вариантов реализации 1-230, в которой положение 3, 4 или 5 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
244. Композиция по любому из вариантов реализации 1-230, в которой положение 3 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
245. Композиция по любому из вариантов реализации 1-230, в которой положение 4 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
246. Композиция по любому из вариантов реализации 1-230, в которой положение 5 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
247. Композиция по любому из предшествующих вариантов реализации, в которой одинаковая последовательность оснований или последовательность оснований типа олигонуклеотида представляет собой последовательность, у которой профиль расщепления ДНК содержит сайт расщепления внутри или вблизи характеристического элемента последовательности целевой последовательности нуклеиновой кислоты.
248. Композиция по любому из предшествующих вариантов реализации, в которой профиль расщепления ДНК представляет собой профиль расщепления композиции олигонуклеотидов ДНК, имеющих последовательность, причем каждый олигонуклеотид в композиции имеет одинаковую структуру.
249. Композиция по любому из предшествующих вариантов реализации, в которой одинаковая последовательность оснований или последовательность оснований типа олигонуклеотида представляет собой последовательность, стереослучайный профиль расщепления которой содержит сайт расщепления внутри или вблизи характеристического элемента последовательности целевой последовательности нуклеиновой кислоты.
250. Композиция по любому из предшествующих вариантов реализации, в которой стереослучайный профиль расщепления представляет собой профиль расщепления стереослучайной композиции олигонуклеотидов, имеющих последовательность, в которой каждая межнуклеотидная линкерная группа представляет собой фосфоротиоат.
251. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления с или рядом с характеристическим элементом последовательности целевой последовательности нуклеиновой кислоты находится в области сердцевины.
252. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления находится вблизи характеристического элемента последовательности целевой последовательности нуклеиновой кислоты.
253. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 0, 1, 2, 3, 4 или 5 межнуклеотидных линкерных группах от характеристического элемента последовательности.
254. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 0 межнуклеотидных линкерных группах от характеристического элемента последовательности.
255. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 1 межнуклеотидной линкерной группе от характеристического элемента последовательности.
256. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 2 межнуклеотидных линкерных группах от характеристического элемента последовательности.
257. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 3 межнуклеотидных линкерных группах от характеристического элемента последовательности.
258. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 4 межнуклеотидных линкерных группах от характеристического элемента последовательности.
259. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления в 5 межнуклеотидных линкерных группах от характеристического элемента последовательности.
260. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления, расположенный к 5'-концу от сайта расщепления.
261. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления вблизи представляет собой сайт расщепления, расположенный к 3'-концу от сайта расщепления.
261 а. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой основной сайт расщепления.
262. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления.
263. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 40% всех расщеплений.
264. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 50% всех расщеплений.
265. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 60% всех расщеплений.
266. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 70% всех расщеплений.
267. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 80% всех расщеплений.
268. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 90% всех расщеплений.
269. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 95% всех расщеплений.
270. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой относительный основной сайт расщепления, причем в сайте происходит более чем 100% всех расщеплений.
271. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 5% всех мишеней.
272. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 10% всех мишеней.
273. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 15% всех мишеней.
274. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 20% всех мишеней.
275. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 25% всех мишеней.
276. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 30% всех мишеней.
277. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 35% всех мишеней.
278. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 40% всех мишеней.
279. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 45% всех мишеней.
280. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 50% всех мишеней.
281. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 60% всех мишеней.
282. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 70% всех мишеней.
283. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 80% всех мишеней.
284. Композиция по любому из предшествующих вариантов реализации, в которой сайт расщепления внутри или вблизи характеристического элемента последовательности представляет собой абсолютный основной сайт расщепления, причем в сайте расщепляется более чем 90% всех мишеней.
285. Композиция по любому из предшествующих вариантов реализации, в которой относительный или абсолютный основной сайт расщепления определяют посредством анализа с помощью РНКазы Н.
286. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности содержит однонуклеотидный полиморфизм (SNP) или мутацию.
287. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности содержит однонуклеотидный полиморфизм.
288. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности представляет собой однонуклеотидный полиморфизм.
289. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой связанный с болезнью Хантингтона однонуклеотидный полиморфизм.
290. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой однонуклеотидный полиморфизм, обнаруженный в гене хантингтина.
291. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм выбран из rs362307, rs7685686, rs362268, rs2530595, rs362331 или rs362306.
291a. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм выбран из rs362307, rs7685686, rs362268 или rs362306.
292. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой rs362307.
293. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой rs7685686.
294. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой rs362268.
295. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой rs362306.
295а. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой rs2530595.
295b. Композиция по любому из предшествующих вариантов реализации, в которой однонуклеотидный полиморфизм представляет собой rs362331.
296. Композиция по любому из вариантов реализации 1-290, в которой однонуклеотидный полиморфизм находится в экзоне.
297. Композиция по любому из вариантов реализации 1-290, в которой однонуклеотидный полиморфизм находится в интроне.
298. Композиция по любому из вариантов реализации 1-290, причем композицию выбирают из таблиц N1, N2, N3, N4 и 8.
298А. Композиция по любому из вариантов реализации 1-290, причем композицию выбирают из таблиц N1, N2, N3 и N4.
299. Композиция по любому из вариантов реализации 1-290, причем композицию выбирают из таблиц N1A, N2A, N3A, N4A и 8; и WV-1092, WVE120101, WV-2603 и WV-2595.
299а. Композиция по любому из вариантов реализации 1-290, причем композицию выбирают из таблиц N1A, N2A, N3A и E191-E233N4A.
300. Композиция по любому из вариантов реализации 1-290, причем композиция представляет собой WV-1092.
300а. Композиция по любому из вариантов реализации 1-290, причем композиция представляет собой WVE 120101.
300b. Композиция по любому из вариантов реализации 1-290, причем композиция представляет собой WV-2603.
300с. Композиция по любому из вариантов реализации 1-290, причем композиция представляет собой WV-2595.
301. Композиция по любому из вариантов реализации 1-290, причем композиция не представляет собой ONT-450, ONT-451 или ONT-452.
302. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности содержит мутацию.
303. Композиция по любому из предшествующих вариантов реализации, в которой характеристический элемент последовательности представляет собой мутацию.
304. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды по меньшей мере на 95% комплементарны мутантному аллелю.
305. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды на 100% комплементарны мутантному аллелю.
306. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды по меньшей мере на 95% комплементарны целевой последовательности, содержащей SNP, причем SNP связан с заболеванием.
307. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды на 100% комплементарны целевой последовательности, содержащей SNP, причем SNP связан с заболеванием.
307а. Композиция по любому из предшествующих вариантов реализации, в которой олигонуклеотиды избирательно снижают уровень РНК мутантного аллеля.
308. Фармацевтическая композиция, содержащая композицию по любому из предшествующих вариантов реализации и фармацевтический носитель.
308а. Композиция по любому из предшествующих вариантов реализации, дополнительно содержащая спинномозговую жидкость.
309. Композиция по любому из предшествующих вариантов реализации, дополнительно содержащая искусственную спинномозговую жидкость.
310. Способ контролируемого расщепления полимера нуклеиновой кислоты, предусматривающий стадии:
контактирования полимера нуклеиновой кислоты, нуклеотидная последовательность которого содержит целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, обнаруженной в полимере нуклеиновой кислоты;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, характеризующихся конкретной последовательностью оснований и длиной, олигонуклеотидами определенного типа олигонуклеотида.
310а. Способ расщепления нуклеиновой кислоты, имеющей последовательность оснований, содержащую целевую последовательность, причем способ предусматривает стадии:
(а) контактирования нуклеиновой кислоты, имеющей последовательность оснований, содержащую целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности в нуклеиновой кислоте;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида, причем олигонуклеотид нацелен на мутантный ген хантингтина, а длина составляет от примерно 10 до примерно 50 нуклеотидов, причем линкерные группы остова содержат по меньшей мере один фосфоротиоат и причем профиль хиральных центров остова содержит по меньшей мере один хиральный центр в конформации Rp и по меньшей мере один хиральный центр в конформации Sp.
310b. Способ расщепления нуклеиновой кислоты, имеющей последовательность оснований, содержащую целевую последовательность, причем способ предусматривает стадии:
(а) контактирования нуклеиновой кислоты, имеющей последовательность оснований, содержащую целевую последовательность, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности в нуклеиновой кислоте;
2) одинаковым профилем линкерных групп остова, а также
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида, причем олигонуклеотид нацелен на мутантный ген хантингтина, а длина составляет от примерно 10 до примерно 50 нуклеотидов, причем линкерные группы остова содержат по меньшей мере один фосфоротиоат и причем профиль хиральных центров остова содержит по меньшей мере один хиральный центр в конформации Rp и по меньшей мере один хиральный центр в конформации Sp; а также
(b) расщепления нуклеиновой кислоты, опосредуемое механизмом интерференции РНКазы или РНК.
311. Способ по варианту реализации 310, при котором контактирование выполняется в условиях, при которых происходит расщепление полимера нуклеиновой кислоты.
312. Способ по любому из вариантов реализации 310-311, при котором расщепление происходит с профилем расщепления, который отличается от эталонного профиля расщепления, наблюдаемого при контакте полимера нуклеиновой кислоты в сопоставимых условиях с эталонной композицией олигонуклеотидов.
313. Способ изменения профиля расщепления, наблюдаемый, когда полимер нуклеиновой кислоты, нуклеотидная последовательность которого включает целевую последовательность, контактирует с эталонной композицией олигонуклеотидов, которая содержит олигонуклеотиды, имеющие определенную последовательность оснований и длину, причем эта определенная последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности, причем способ предусматривает:
контактирование полимера нуклеиновой кислоты с композицией олигонуклеотидов с контролируемой хиральностью олигонуклеотидов, имеющих определенную последовательность оснований и длину, причем эта композиция характеризуется контролируемой хиральностью, поскольку она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих определенную последовательность оснований и длину, олигонуклеотидами единственного типа олигонуклеотида, характеризующегося:
1) определенной последовательностью оснований и длиной;
2) определенным профилем линкерных групп остова; а также
3) определенным профилем хиральных центров остова.
314. Способ по варианту реализации 313, при котором контактирование выполняется в условиях, в которых происходит расщепление полимера нуклеиновой кислоты.
315. Способ по любому из вариантов реализации 312-314, при котором эталонная композиция олигонуклеотидов представляет собой по существу рацемический препарат олигонуклеотидов, которые имеют одинаковую последовательность и длину.
316. Способ по любому из вариантов реализации 312-314, при котором эталонная композиция олигонуклеотидов представляет собой композицию олигонуклеотидов с неконтролируемой хиральностью олигонуклеотидов, которые имеют одинаковую последовательность и длину.
317. Способ по любому из вариантов реализации 312-316, при котором профиль расщепления, обеспечиваемый композицией олигонуклеотидов с контролируемой хиральностью, отличается от эталонного расщепления тем, что он имеет меньше сайтов расщепления в пределах целевой последовательности, обнаруженной в полимере нуклеиновой кислоты, чем эталонный профиль расщепления.
318. Способ по варианту реализации 317, при котором профиль расщепления, обеспечиваемый композицией олигонуклеотидов с контролируемой хиральностью, имеет единственный сайт расщепления в пределах целевой последовательности, обнаруженной в полимере нуклеиновой кислоты, чем эталонный профиль расщепления.
319. Способ по варианту реализации 318, при котором единственный сайт расщепления представляет собой сайт расщепления в эталонном профиле расщепления.
320. Способ по варианту реализации 318, при котором единственный сайт расщепления представляет собой сайт расщепления не в эталонном профиле расщеплении.
321. Способ по любому из вариантов реализации 312-316, при котором профиль расщепления, обеспечиваемый композицией олигонуклеотидов с контролируемой хиральностью, отличается от эталонного профиля расщепления тем, что увеличивает процент расщепления в сайте расщепления.
322. Способ по варианту реализации 321, при котором сайт расщепления с увеличенным процентом расщепления представляет собой сайт расщепления в эталонном профиле расщепления.
323. Способ по варианту реализации 321, при котором сайт расщепления с увеличенным процентом расщепления представляет собой сайт расщепления не в эталонном профиле расщепления.
324. Способ по любому из вариантов реализации 310-323, при котором композиция олигонуклеотидов с контролируемой хиральностью обеспечивает более высокую скорость расщепления целевого полимера нуклеиновой кислоты, чем эталонная композиция олигонуклеотидов.
325. Способ по любому из вариантов реализации 310-324, при котором скорость расщепления по меньшей мере в 5 раз выше.
326. Способ по любому из вариантов реализации 310-325, при котором композиция олигонуклеотидов с контролируемой хиральностью обеспечивает более низкий уровень оставшегося нерастворенного целевого полимера нуклеиновой кислоты, чем эталонная композиция олигонуклеотидов.
327. Способ по любому из вариантов реализации 310-326, при котором оставшийся нерасщепленный целевой полимер нуклеиновой кислоты по меньшей мере в 5 раз ниже.
328. Способы по любому из вариантов реализации 310-327, при которых продукты расщепления из полимера нуклеиновой кислоты диссоциируют из олигонуклеотидов определенного типа олигонуклеотида в композиции олигонуклеотидов с контролируемой хиральностью с более высокой скоростью, чем из олигонуклеотидов эталонной композиции олигонуклеотидов.
329. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой в популяции существует одна или более аналогичных последовательностей нуклеиновых кислот, каждая из целевой и аналогичной последовательностей содержит специфический характеристический элемент нуклеотидной последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевой последовательности нуклеиновой кислоты, так и аналогичных последовательностей нуклеиновой кислоты, транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для аналогичной последовательности нуклеиновой кислоты.
330. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевой последовательности нуклеиновой кислоты, так и аналогичной последовательности нуклеиновой кислоты, транскрипты целевой последовательности нуклеиновой кислоты подавляются в большей степени, чем степень подавления, наблюдаемая для аналогичной последовательности нуклеиновой кислоты.
331. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретную целевую последовательность относительно аналогичных последовательностей, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 2 раза превышает степень подавления, наблюдаемую для другого аллеля того же самого гена.
332. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретную целевую последовательность относительно аналогичных последовательностей, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 2 раза превышает степень подавления, наблюдаемую для другого аллеля того же самого гена.
333. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину;
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретную целевую последовательность относительно аналогичных последовательностей, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретной целевой последовательности в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для аналогичной последовательности, или
с) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для аналогичной последовательности.
334. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевой и аналогичной последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину;
2) одинаковый профиль линкерных групп остова;
3) одинаковый профиль хиральных центров остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретную целевую последовательность относительно аналогичных последовательностей, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретной целевой последовательности в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для аналогичной последовательности, или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для аналогичной последовательности.
335. Способ подавления транскрипта из последовательности целевой нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевых и аналогичных последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность по отношению к аналогичной последовательности, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретную целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что, когда она вступает в контакт с системой, экспрессирующей транскрипты целевой последовательности нуклеиновой кислоты, она показывает подавление экспрессии транскриптов конкретной целевой последовательности нуклеиновой кислоты в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретной целевой последовательности нуклеиновой кислоты обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для аналогичной последовательности; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретной целевой последовательности нуклеиновой кислоты обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для аналогичной последовательности.
336. Способ подавления транскрипта из последовательности целевой нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевых и аналогичных последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность по отношению к аналогичной последовательности, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретную целевую последовательность нуклеиновой кислоты, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевой последовательности нуклеиновой кислоты, она показывает подавление экспрессии транскриптов конкретной целевой последовательности нуклеиновой кислоты в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретной целевой последовательности нуклеиновой кислоты обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для аналогичной последовательности; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретной целевой последовательности нуклеиновой кислоты обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для аналогичной последовательности.
337. Способ по любому из предшествующих вариантов реализации, при котором целевая последовательность представляет собой последовательность, содержащую мутацию, а аналогичная последовательность представляет собой последовательность дикого типа.
338. Способ по любому из предыдущих вариантов реализации, при котором характеристический элемент последовательности определяет конкретный аллель целевой последовательности относительно других аллелей одной и той же целевой последовательности.
339. Способ по любому из предыдущих вариантов реализации, при котором характеристический элемент последовательности определяет конкретный аллель целевого гена относительно других аллелей одного и того же целевого гена.
340. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательностью оснований и длину;
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же последовательности нуклеиновой кислоты, транскрипты конкретного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
341. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля той же последовательности нуклеиновой кислоты, транскрипты конкретного аллеля подавляются в большей степени, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
342. Способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательностью оснований и длину;
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля, подавляются в степени, которая по меньшей мере в 2 раза превышает степень подавления, наблюдаемую для другого аллеля того же самого гена.
343. Способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям одного и того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля, подавляются в степени, которая по меньшей мере в 2 раза превышает степень подавления, наблюдаемую для другого аллеля того же самого гена.
344. Способ по варианту реализации 340 или 342, при котором контактирование осуществляется в условиях, определенных для того, чтобы позволить композиции подавлять транскрипты конкретного аллеля.
345. Способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям одного и того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля, подавляются в степени, которая по меньшей мере в 2 раза превышает степень подавления, наблюдаемую для другого аллеля того же самого гена.
346. Способ по варианту реализации 345, при котором контактирование выполняется в условиях, определенных для того, чтобы позволить композиции подавлять экспрессию конкретного аллеля.
347. Способ по любому из вариантов реализации 340-346, при котором транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 5, 10, 20, 50, 100, 200 или 500 раз больше, чем степень подавления, наблюдаемая для другого аллеля одного и того же гена.
348. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям одной и той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину;
2) одинаковый профиль линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
349. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждая из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова; причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
350. Способ контролируемого расщепления полимера нуклеиновой кислоты, предусматривающий контактирование полимера нуклеиновой кислоты, нуклеотидная последовательность которого содержит целевую последовательность, с олигонуклеотидом или композицией олигонуклеотидов по любому из вариантов реализации 540-574.
351. Способ подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует одна или более аналогичных последовательностей нуклеиновых кислот в популяции, каждая из целевых и аналогичных последовательностей содержит специфический нуклеотидный характеристический элемент последовательности, который определяет целевую последовательность относительно аналогичных последовательностей, причем способ предусматривает контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с олигонуклеотидом или композицией олигонуклеотидов по любому из вариантов реализации 540-574, причем последовательность оснований олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты.
352. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель относительно других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с олигонуклеотидом или композицией олигонуклеотидов любого из вариантов реализации 540-574, причем последовательность оснований олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет целевую последовательность нуклеиновой кислоты.
353. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель относительно других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с олигонуклеотидом или композицией олигонуклеотидов по любому из вариантов реализации 540-574, причем последовательность оснований олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем олигонуклеотид или композиция олигонуклеотидов характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 2 раза выше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
354. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель относительно других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с олигонуклеотидом или композицией олигонуклеотидов по любому из вариантов реализации 540-574, причем последовательность оснований олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем олигонуклеотид или композиция олигонуклеотидов характеризуется тем, что при контакте с системой, содержащей транскрипты как целевого аллеля, так и другого аллеля того же гена, транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 2 раза выше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
355. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель относительно других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с олигонуклеотидом или композицией олигонуклеотидов по любому из вариантов реализации 540-574, причем последовательность оснований олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем олигонуклеотид или композиция олигонуклеотидов характеризуется тем, что при контакте с системой, содержащей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
с) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
356. Способ аллель-специфического подавления транскрипта из целевой последовательности нуклеиновой кислоты, для которой существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель относительно других аллелей той же целевой последовательности нуклеиновой кислоты, причем способ предусматривает контактирование образца, содержащего транскрипты целевой последовательности нуклеиновой кислоты, с олигонуклеотидом или композицией олигонуклеотидов по любому из вариантов реализации 540-574, причем последовательность оснований олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем олигонуклеотид или композиция олигонуклеотида характеризуется тем, что при контакте с системой, экспрессирующей транскрипты той же целевой последовательности нуклеиновой кислоты, она демонстрирует подавление транскриптов конкретного аллеля в степени, которая:
a) больше, чем когда композиция отсутствует;
b) больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты, или
c) как больше, чем когда композиция отсутствует, так и больше, чем степень подавления, наблюдаемая для другого аллеля той же последовательности нуклеиновой кислоты.
357. Способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям одного и того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов, содержащей олигонуклеотиды, характеризующиеся:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она показывает подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
358. Способ аллель-специфического подавления транскрипта из целевого гена, для которого существует множество аллелей в популяции, каждый из которых содержит специфический нуклеотидный характеристический элемент последовательности, который определяет аллель по отношению к другим аллелям одного и того же целевого гена, причем способ предусматривает стадии:
контактирования образца, содержащего транскрипты целевого гена, с композицией олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова;
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одинаковую последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида;
причем одинаковая последовательность оснований для олигонуклеотидов определенного типа олигонуклеотида представляет собой или содержит последовательность, которая комплементарна характеристическому элементу последовательности, который определяет конкретный аллель, причем композиция характеризуется тем, что при контакте с системой, экспрессирующей транскрипты целевого гена, она показывает подавление экспрессии транскриптов конкретного аллеля в степени, которая:
a) по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует;
b) по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена; или
c) как по меньшей мере в 2 раза больше в том отношении, что транскрипты от конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, по отношению к тому, когда она отсутствует, так и по меньшей мере в 2 раза больше, чем степень подавления, наблюдаемая для другого аллеля того же гена.
359. Способ по любому из предшествующих вариантов реализации, при котором транскрипты из конкретного аллеля обнаруживаются в количествах, которые при отсутствии композиции в 2 раза или более превышают те, которые наблюдаются при ее наличии.
360. Способ по любому из предшествующих вариантов реализации, при котором уровень транскриптов другого аллеля одного и того же гена по меньшей мере в 2 раза превышает уровень транскриптов конкретного аллеля.
361. Способ по любому из предыдущих вариантов реализации, при котором транскрипты из конкретного аллеля обнаруживаются в количествах, которые при отсутствии композиции в 2 раза или более превышают те, которые наблюдаются при ее наличии, и уровень транскриптов другого аллеля того же гена по меньшей мере в 2 раза больше, чем уровень транскриптов конкретного аллеля.
362. Способ по любому из предшествующих вариантов реализации, при котором контактирование осуществляется в условиях, определенных для того, чтобы позволить композиции подавлять транскрипты конкретного аллеля.
363. Способ по любому из предыдущих вариантов реализации, при котором контактирование осуществляется в условиях, определенных для того, чтобы позволить композиции подавлять экспрессию конкретного аллеля.
364. Способ по любому из предшествующих вариантов реализации, при котором транскрипты конкретного аллеля подавляются в степени, которая представляет собой по меньшей мере 5-, 10-, 20-, 50-, 100-, 200- или 500-кратную в том отношении, что транскрипты из конкретного аллеля обнаруживаются в количествах, которые в 2 раза ниже, когда композиция присутствует, относительно того, когда она отсутствует.
365. Способ по любому из предшествующих вариантов реализации, при котором транскрипты конкретного аллеля подавляются в степени, которая по меньшей мере в 5, 10, 20, 50, 100, 200 или 500 раз больше, чем степень подавления, наблюдаемая для другого аллеля одного и того же гена.
366. Способ по любому из предыдущих вариантов реализации, при котором система представляет собой систему in vitro или in vivo.
366а. Способ по любому из предшествующих вариантов реализации, при котором способ осуществляют in vitro или in vivo.
367. Способ по любому из предшествующих вариантов реализации, при котором система содержит одну или более клеток, тканей или органов.
368. Способ по любому из предшествующих вариантов реализации, при котором система содержит один или более организмов.
369. Способ по любому из предшествующих вариантов реализации, при котором система содержит один или более субъектов.
370. Способ по любому из предшествующих вариантов реализации, при котором транскрипты конкретного аллеля расщепляются.
371. Способ по любому из предшествующих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности присутствует внутри интрона целевой последовательности нуклеиновой кислоты или гена.
372. Способ по любому из предыдущих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности присутствует в экзоне целевой последовательности нуклеиновой кислоты или гена.
373. Способ по любому из предшествующих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности охватывает экзон и интрон целевой последовательности нуклеиновой кислоты или гена.
374. Способ по любому из предшествующих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности содержит мутацию.
375. Способ по любому из предшествующих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности представляет собой мутацию.
376. Способ по любому из предшествующих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности содержит SNP.
377. Способ по любому из предшествующих вариантов реализации, при котором специфический нуклеотидный характеристический элемент последовательности представляет собой SNP.
378. Способ по любому из предшествующих вариантов реализации, при котором композицию олигонуклеотидов вводят субъекту.
379. Способ по любому из предшествующих вариантов реализации, при котором целевой полимер нуклеиновой кислоты или транскрипты являются олигонуклеотидами.
380. Способ по любому из предшествующих вариантов реализации, при котором целевой полимер нуклеиновой кислоты или транскрипты являются РНК.
381. Способ по любому из предшествующих вариантов реализации, при котором целевой полимер нуклеиновой кислоты или транскрипты являются вновь транскрибируемой РНК.
382. Способ по любому из предшествующих вариантов реализации, при котором олигонуклеотиды определенного типа олигонуклеотида в композиции олигонуклеотидов с контролируемой хиральностью образуют дуплексы с полимером нуклеиновой кислоты или транскриптами.
383. Способ по любому из предшествующих вариантов реализации, при котором полимер нуклеиновой кислоты или транскрипты расщепляются ферментом.
384. Способ по любому из предшествующих вариантов реализации, при котором фермент представляет собой РНКазу Н.
385. Способ по любому из предыдущих вариантов реализации, при котором SNP представляет собой связанный с болезнью Хантингтона SNP.
386. Способ по любому из предшествующих вариантов реализации, при котором SNP представляет собой обнаруженный в гене Хантингтин SNP.
387. Способ по любому из предшествующих вариантов реализации, при котором SNP выбирают из rs362307, rs7685686, rs362268 или rs362306.
388. Способ по вариантам реализации 310-387, при котором SNP представляет собой rs362307.
389. Способ по вариантам реализации 310-387, при котором однонуклеотидный полиморфизм представляет собой rs7685686.
390. Способ по вариантам реализации 310-387, при котором однонуклеотидный полиморфизм представляет собой rs362268.
391. Способ по вариантам реализации 310-387, при котором однонуклеотидный полиморфизм представляет собой rs362306.
392. Способ по вариантам реализации 310-391, при котором положение 11 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
393. Способ по вариантам реализации 310-391, при котором положение 12 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
394. Способ по вариантам реализации 310-391, при котором положение 13 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
395. Способ по вариантам реализации 310-391, при котором положение 8 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
396. Способ по вариантам реализации 310-391, при котором положение 9 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
397. Способ по вариантам реализации 310-391, при котором положение 10 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
398. Способ по любому из предыдущих вариантов реализации, при котором олигонуклеотиды содержат одну или более областей крыла и общую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и возможно содержит одну или более хиральных межнуклеотидных линкерных групп; а также
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп.
399. Способ по любому из вариантов реализации 310-398, при котором положение 6 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
400. Способ по любому из вариантов реализации 310-398, при котором положение 7 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
401. Способ по любому из вариантов реализации 310-398, при котором положение 8 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
402. Способ по любому из вариантов реализации 310-398, при котором положение 3 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
403. Способ по любому из вариантов реализации 310-398, при котором положение 4 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
404. Способ по любому из вариантов реализации 310-398, при котором положение 5 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
405. Способ по любому из предыдущих вариантов реализации, при котором:
каждая область крыла независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп и одну или более природных фосфатных линкерных групп; а также
область сердцевины независимо составляет в длину два или более оснований, причем каждая межнуклеотидная линкерная группа в области сердцевины является хиральной, только одна межнуклеотидная линкерная группа в области сердцевины характеризуется конфигурацией Rp, а каждая из других межнуклеотидных линкерных групп в области сердцевины представляет собой конфигурацию Sp.
406. Способ по любому из предшествующих вариантов реализации, при котором олигонуклеотиды представляют собой гемимеры, имеющие структуру крыло-сердцевина.
407. Способ по любому из вариантов реализации 310-405, при котором олигонуклеотиды представляют собой гемимеры, имеющие структуру сердцевина-крыло.
408. Способ по любому из вариантов реализации 310-405, при котором олигонуклеотиды представляют собой гэпмеры, имеющие структуру крыло-сердцевина-крыло.
409. Способ по любому из предыдущих вариантов реализации, при котором уровень транскриптов от вызывающего заболевание аллеля избирательно подавляется.
410. Способ по любому из предшествующих вариантов реализации, при котором уровень белка, транслированного из транскриптов от вызывающего заболевание аллеля, подавляется.
411. Способ лечения или профилактики болезни Хантингтона у субъекта, предусматривающий введение субъекту композиции олигонуклеотидов, содержащей олигонуклеотиды, имеющие:
1) одинаковую последовательность оснований и длину; а также
2) одинаковый профиль линкерных групп остова.
412. Способ лечения или профилактики болезни Хантингтона у субъекта, предусматривающий введение субъекту композиции олигонуклеотидов с контролируемой хиральностью, содержащей олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова;
причем эта композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида.
413. Способ по варианту реализации 411 или 412, при котором олигонуклеотиды содержат одну или более областей крыла и общую область сердцевины, причем:
каждая область крыла независимо составляет в длину два или более оснований и независимо и возможно содержит одну или более хиральных межнуклеотидных линкерных групп; а также
область сердцевины независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп.
414. Способ по любому из вариантов реализации 411-4113, при котором:
каждая область крыла независимо составляет в длину два или более оснований и независимо содержит одну или более хиральных межнуклеотидных линкерных групп и одну или более природных фосфатных линкерных групп; а также
область сердцевины независимо составляет в длину два или более оснований, причем каждая межнуклеотидная линкерная группа в области сердцевины является хиральной, только одна из межнуклеотидных линкерных групп в области сердцевины характеризуется конформацией Rp, а каждая из других межнуклеотидных линкерных групп в области сердцевины представляет собой конформацию Sp.
415. Способ по любому из вариантов реализации 411-414, при котором олигонуклеотиды представляют собой гемимеры, имеющие структуру крыло-сердцевина.
416. Способ по любому из вариантов реализации 411-414, при котором олигонуклеотиды представляют собой гемимеры, имеющие структуру сердцевина-крыло.
417. Способ по любому из вариантов реализации 411-414, при котором олигонуклеотиды представляют собой гэпмеры, имеющие структуру крыло-сердцевина-крыло.
418. Способ по вариантам реализации 411-417, при котором положение 11 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
419. Способ по вариантам реализации 411-417, при котором положение 12 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
420. Способ по вариантам реализации 411-417, при котором положение 13 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
421. Способ по вариантам реализации 411-417, при котором положение 8 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
422. Способ по вариантам реализации 411-417, при котором положение 9 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
423. Способ по вариантам реализации 411-417, при котором положение 10 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с однонуклеотидным полиморфизмом.
424. Способ по любому из вариантов реализации 411-417, при котором положение 6 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
425. Способ по любому из вариантов реализации 411-417, при котором положение 7 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
426. Способ по любому из вариантов реализации 411-417, при котором положение 8 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
427. Способ по любому из вариантов реализации 411-417, при котором положение 3 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
428. Способ по любому из вариантов реализации 411-417, при котором положение 4 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
429. Способ по любому из вариантов реализации 411-417, при котором положение 5 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с однонуклеотидным полиморфизмом.
430. Способ по любому из вариантов реализации 411-429, при котором способ облегчает симптом болезни Хантингтона.
431. Способ по любому из вариантов реализации 411-429, при котором способ замедляет начало болезни Хантингтона.
432. Способ по любому из вариантов реализации 411-429, при котором способ замедляет прогрессирование болезни Хантингтона.
433. Способ по любому из вариантов реализации 411-432, при котором субъект имеет SNP, связанный с болезнью Хантингтона.
434. Способ по любому из вариантов реализации 411-433, при котором субъект имеет SNP в гене хантингтина субъекта.
435. Способ по любому из вариантов реализации 411-434, при котором субъект имеет SNP, причем один аллель представляет собой мутантный хантингтин, связанный с удлиненными повторами CAG.
436. Способ по любому из вариантов реализации 411-435, при котором субъект имеет SNP, выбранный из rs362307, rs7685686, rs362268, rs2530595, rs362331 или rs362306.
436a. Способ по любому из вариантов реализации 411-435, при котором субъект имеет SNP, выбранный из rs362307, rs7685686, rs362268 или rs362306.
437. Способ по любому из вариантов реализации 411-436, при котором субъект имеет SNP rs362307.
438. Способ по любому из вариантов реализации 411-436, при котором субъект имеет SNP rs7685686.
439. Способ по любому из вариантов реализации 411-436, при котором субъект имеет SNP rs362268.
440. Способ по любому из вариантов реализации 411-436, при котором субъект имеет SNP rs362306.
440а. Способ по любому из вариантов реализации 411-436, при котором субъект имеет SNP rs2530595.
440b. Способ по любому из вариантов реализации 411-436, при котором субъект имеет SNP rs362331.
441. Композиция по любому из вариантов реализации 1-309, в которой по существу рацемический препарат олигонуклеотидов получают посредством нестереоселективного получения.
442. Композиция по любому из вариантов реализации 1-309 и 441, в которой по существу рацемический препарат олигонуклеотидов получают посредством нестереоселективного получения причем хиральный вспомогательный компонент не используется для образования хиральной межнуклеотидной линкерной группы.
443. Композиция по любому из вариантов реализации 1-309 и 441-442, в которой по существу рацемический препарат олигонуклеотидов получают посредством нестереоселективного получения, причем по меньшей мере одна хиральная межнуклеотидная линкерная группа образуется с диастереомерной селективностью менее 80:20.
444. Композиция по любому из вариантов реализации 1-309 и 441-443, в которой по существу рацемический препарат олигонуклеотидов получают посредством нестереоселективного получения, причем по меньшей мере одна хиральная межнуклеотидная линкерная группа образуется с диастереомерной селективностью менее 90:10.
445. Композиция по любому из вариантов реализации 1-309 и 441-444, в которой по существу рацемический препарат олигонуклеотидов получают посредством нестереоселективного получения, причем по меньшей мере одна хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью менее 95:5.
446. Композиция по любому из вариантов реализации 1-309 и 441-445, в которой по существу рацемический препарат олигонуклеотидов получают посредством нестереоселективного получения, причем по меньшей мере одна хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью менее чем 97:3.
447. Композиция по любому из вариантов реализации 1-309, в которой каждая хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью более чем 90:10.
448. Композиция по любому из вариантов реализации 1-309, в которой каждая хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью более чем 95:5.
449. Композиция по любому из вариантов реализации 1-309, в которой каждая хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью более чем 96:4.
450. Композиция по любому из вариантов реализации 1-309, в которой каждая хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью более чем 97:3.
451. Композиция по любому из вариантов 1-309, в которой каждая хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью более чем 98:2.
452. Композиция по любому из вариантов реализации 1-309, в которой каждая хиральная межнуклеотидная линкерная группа образована с диастереомерной селективностью более чем 98:2.
453. Композиция по любому из вариантов реализации 443-452, в которой диастереомерная селективность для образования хиральной межнуклеотидной линкерной группы измеряется путем образования димерного олигонуклеотида, содержащего хиральную межнуклеотидную линкерную группу и нуклеозиды с обеих сторон хиральной межнуклеотидной линкерной группы в тех же или сравнимых условиях реакции.
454. Способ получения композиции олигонуклеотидов для избирательного подавления транскрипта целевой последовательности нуклеиновой кислоты, предусматривающий предоставление композиции олигонуклеотидов, содержащей предопределенный уровень олигонуклеотидов определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем хиральных центров остова, профиль которых содержит (Sp)m(Rp)n, (Rp)n(Sp)m, (Np)t(Rp)n(Sp)m или (Sp)t(Rp)n(Sp)m, где:
m равно 1-50;
n равно 1-10;
t равно 1-50;
каждый Np представляет собой независимо Rp или Sp;
причем целевая последовательность нуклеиновой кислоты содержит характеристический элемент последовательность, который определяет целевую последовательность нуклеиновой кислоты от аналогичной последовательности нуклеиновой кислоты;
причем одинаковая последовательность оснований представляет собой последовательность, чей профиль расщепления ДНК и/или стереослучайный профиль расщепления имеет сайт расщепления в пределах или вблизи целевой последовательности нуклеиновой кислоты.
455. Способ по варианту реализации 454, при котором профиль содержит (Sp)m(Rp)n.
456. Способ по варианту реализации 454, при котором профиль содержит (Rp)n(Sp)m.
457. Способ по варианту реализации 454, при котором профиль содержит (Np)t(Rp)n(Sp)m.
458. Способ по варианту реализации 454, при котором профиль содержит (Sp)t(Rp)n(Sp)m.
459. Способ по варианту реализации 454, при котором профиль представляет собой профиль в любом из вариантов реализации 145-157.
460. Способ по любому из вариантов реализации 454-458, при котором сайт расщепления находится в любом из вариантов реализации 247-285.
461. Способ по любому из предшествующих вариантов реализации, при котором композиция олигонуклеотидов представляет собой композицию любого из вариантов реализации 1-309 и 441-453.
462. Композиция или способ по любому из предшествующих вариантов реализации, причем последовательность олигонуклеотида в композиции олигонуклеотидов с контролируемой хиральностью содержит, состоит из или представляет собой последовательность любого описанного в настоящем документе олигонуклеотида или выбирается из таблиц N1A, N2A, N3A, N4A или 8; или WV-1092, WVE120101, WV-2603 или WV-2595.
463. Композиция, содержащая липид и олигонуклеотид.
463а. Композиция по любому из предшествующих вариантов реализации, причем композиция содержит один или более липидов, конъюгированных с одним или более олигонуклеотидами в композиции.
464. Композиция, содержащая олигонуклеотид и липид, выбранный из перечня: лауриновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, линолевая кислота, альфа-линоленовая кислота, гамма-линоленовая кислота, докозагексаеновая кислота (цис-DHA), турбинаровая кислота, арахидоновая кислота и дилинолеил.
464а. Композиция, содержащая олигонуклеотид и липид, выбранный из перечня: лауриновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, линолевая кислота, альфа-линоленовая кислота, гамма-линоленовая кислота, докозагексаеновая кислота (цис-DHA), турбинаровая кислота и дилинолеил.
465. Композиция, содержащая олигонуклеотид и липид, выбранный из:
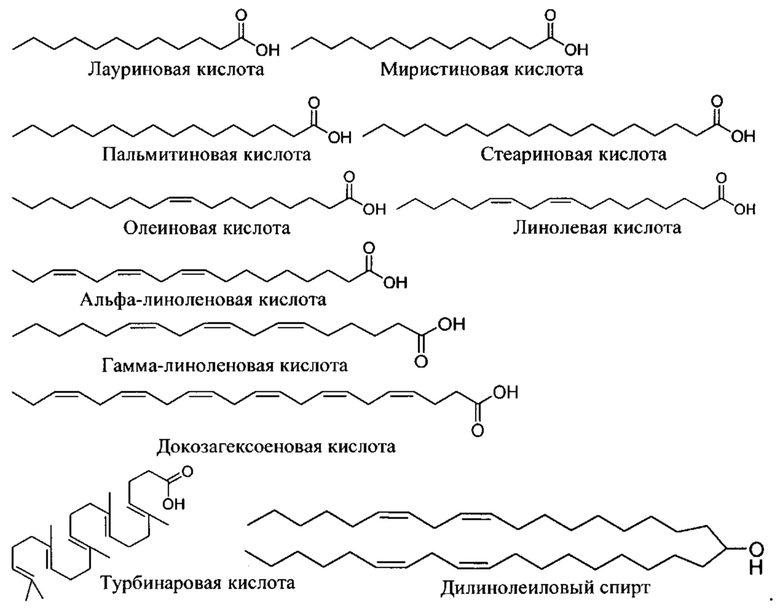
466. Композиция, содержащая олигонуклеотид и липид,
причем липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами.
467. Композиция олигонуклеотидов, содержащая множество олигонуклеотидов, которые характеризуются:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем модификаций фосфора остова;
причем один или более олигонуклеотидов из множества отдельно конъюгированы с липидом.
468. Композиция олигонуклеотидов с контролируемой хиральностью, содержащая множество олигонуклеотидов, которые характеризуются:
1) одинаковой последовательностью оснований;
2) одинаковым профилем линкерных групп остова; а также
3) одинаковым профилем модификаций фосфора остова; причем:
композиция характеризуется контролируемой хиральностью в том отношении, что множество олигонуклеотидов имеют одну и ту же стереохимию при одной или более хиральных межнуклеотидных линкерных группах;
один или более олигонуклеотидов из множества отдельно конъюгированы с липидом; а также
один или более олигонуклеотидов из множества возможно и отдельно конъюгированы с целевым соединением или фрагментом.
469. Способ доставки олигонуклеотида в клетку или ткань субъекта-человека, предусматривающий:
(a) обеспечение композиции любого из предыдущих вариантов реализации; а также
(b) введение композиции субъекту-человеку таким образом, что олигонуклеотид доставляется в клетку или ткань субъекта.
470. Способ доставки олигонуклеотида в клетку или ткань, предусматривающий получение композиции по любому из предыдущих вариантов реализации и обработку [контактирование] клетки или ткани композицией.
471. Способ модуляции уровня транскрипта или генного продукта гена в клетке, причем способ предусматривает стадию контактирования клетки с композицией в соответствии с любым из предыдущих вариантов реализации, причем олигонуклеотид способен модулировать уровень транскрипта или генного продукта.
472. Способ ингибирования экспрессии гена в клетке или ткани, предусматривающий получение композиции в соответствии с любым из предшествующих вариантов реализации и обработку клетки или ткани композицией.
473. Способ ингибирования экспрессии гена в клетке или ткани у млекопитающего, предусматривающий получение композиции в соответствии с любым из предшествующих вариантов реализации и введение композиции млекопитающему.
474. Способ лечения заболевания, вызванный избыточной экспрессией одного или более белков в клетке или ткани у субъекта, причем указанный способ предусматривает введение композиции в соответствии с любым из предшествующих вариантов реализации субъекту.
475. Способ лечения заболевания, который вызван уменьшенной, подавленной или отсутствующей экспрессией одного или более белков у субъекта, причем указанный способ предусматривает введение композиции в соответствии с любым из предшествующих вариантов реализации субъекту.
476. Способ получения иммунного ответа у субъекта, причем указанный способ предусматривает введение композиции в соответствии с любым из предыдущих вариантов реализации субъекту, причем биологически активное соединение представляет собой иммуномодулирующую нуклеиновую кислоту.
477. Способ лечения признака и/или симптома болезни Хантингтона путем обеспечения композиции согласно любому из предшествующих вариантов реализации и введения композиции субъекту.
478. Способ модуляции количества опосредованного РНКазой Н расщепления в клетке, причем способ предусматривает стадию контактирования клетки с композицией в соответствии с любым из предшествующих вариантов реализации, причем олигонуклеотид способен модулировать количество опосредованного РНКазой Н расщепления.
479. Способ введения олигонуклеотида нуждающемуся в этом субъекту, предусматривающий стадии обеспечения композиции, содержащей агент и липид, и введения композиции субъекту, причем агент представляет собой любой раскрытый в настоящем документе агент и причем липид представляет собой любой раскрытый в настоящем документе липид.
480. Способ лечения заболевания у субъекта, причем способ предусматривает стадии предоставления композиции, содержащей агент и липид, и введения терапевтически эффективного количества композиции субъекту, причем агент представляет собой любой раскрытый в настоящем документе агент и причем липид представляет собой любой раскрытый в настоящем документе липид, и причем заболевание представляет собой любое раскрытое в настоящем документе заболевание.
481. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
482. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
483. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь, необязательно замещенную одной или более С1-4 алифатическими группами.
484. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит незамещенную C10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
485. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит не более одной необязательно замещенной С10-С40 линейной, насыщенной или частично ненасыщенной алифатической цепи.
486. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит две или более необязательно замещенных С10-С40 линейных, насыщенных или частично ненасыщенных алифатических цепей.
487. Композиция или способ по любому из предшествующих вариантов реализации, причем липид не содержит трициклического или полициклического фрагмента.
488. Композиция или способ по любому из предшествующих вариантов реализации, причем липид имеет структуру R'-COOH, где R1 представляет собой необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
489. Композиция или способ по любому из вариантов реализации 16, причем липид конъюгирован через свою карбоксильную группу.
490. Композиция или способ по любому из предшествующих вариантов реализации, причем липид выбран из:
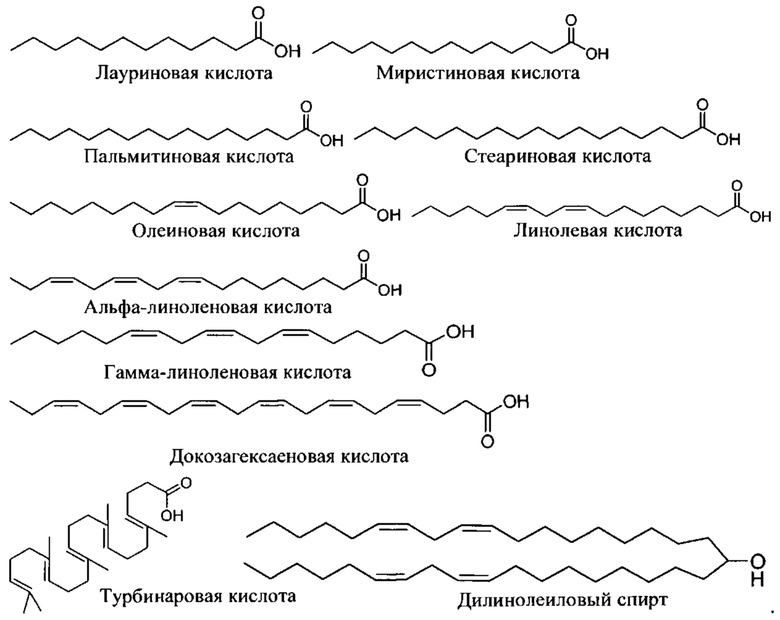
491. Композиция или способ по любому из предшествующих вариантов реализации, причем липид конъюгирован с олигонуклеотидом.
492. Композиция или способ по любому из предшествующих вариантов реализации, причем липид непосредственно конъюгирован с олигонуклеотидом.
493. Композиция или способ по любому из предшествующих вариантов реализации, причем липид конъюгирован с олигонуклеотидом через линкерную группу.
494. Композиция или способ по любому из предшествующих вариантов реализации, причем линкерная группа выбрана из: незаряженной линкерной группы; заряженной линкерной группы; содержащей алкил линкерной группы; содержащей фосфат линкерной группы; разветвленной линкерной группы; неразветвленной линкерной группы; содержащей по меньшей мере одну группу расщепления линкерной группы; содержащей по меньшей мере одну группу редокс-расщепления линкерной группы; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе фосфата; линкерной группы, содержащей по меньшей мере одну группу расщепления кислотой; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе сложного эфира; и линкерной группы, содержащей по меньшей мере одну группу расщепления на основе пептидов.
495. Композиция или способ по любому из предшествующих вариантов реализации, причем каждый олигонуклеотид из множества отдельно конъюгирован с одним и тем же липидом в одном и том же месте.
496. Композиция или способ по любому из предшествующих вариантов реализации, причем липид конъюгирован с олигонуклеотидом через линкерную группу.
497. Композиция или способ по любому из предшествующих вариантов реализации, причем один или более олигонуклеотидов из множества независимо конъюгированы с целевым соединением или фрагментом.
498. Композиция или способ по любому из предшествующих вариантов реализации, причем один или более олигонуклеотидов из множества независимо конъюгированы с липидом и целевым соединением или фрагментом.
499. Композиция или способ по любому из предшествующих вариантов реализации, причем один или более олигонуклеотидов из множества независимо конъюгированы с липидом на одном конце и целевым соединением или фрагментом на другом.
500. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотиды из множества характеризуются одними и теми же профилями химической модификации.
501. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотиды из множества характеризуются одними и теми же профилями химической модификации, содержащими одну или более модификаций основания.
502. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотиды из множества характеризуются одними и теми же профилями химической модификации, содержащими одну или более модификаций сахара.
503. Композиция или способ по любому из предшествующих вариантов реализации, причем одинаковая последовательность оснований способна гибридизоваться с транскриптом в клетке, причем этот транскрипт содержит мутацию, которая связана с заболеванием мышц, или чье содержание, активность и/или распределение связано с заболеванием мышц.
504. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид представляет собой нуклеиновую кислоту.
505. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид представляет собой олигонуклеотид.
506. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид представляет собой олигонуклеотид, который опосредует перепрыгивание экзона.
507. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид представляет собой стереоопределенный олигонуклеотид, который опосредует перепрыгивание экзона.
508. Композиция или способ по любому из предшествующих вариантов реализации, причем заболевание или нарушение представляет собой связанное с мышцами заболевание или нарушение.
509. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -с≡с-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R'), -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная является независимо таковой, как определено и описано в настоящем документе.
510. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С80 насыщенную или частично ненасыщенную алифатическую цепь.
511. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
512. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую цепь.
513. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
514. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную C10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
515. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную C10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
516. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С60 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -c≡c-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R'), -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная является независимо таковой, как определено и описано в настоящем документе.
517. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-C80 насыщенную или частично ненасыщенную алифатическую цепь.
518. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С60 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
519. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
520. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную С10-С40 насыщенную или частично ненасыщенную алифатическую группу, причем одно или более метиленовых звеньев возможно и независимо заменены необязательно замещенной группой, выбранной из C1-С6 алкилена, C1-С6 алкенилена, -c≡c-, C1-С6 гетероалифатического фрагмента, -C(R')2-, -Су-, -О-, -S-, -S-S-, -N(R')-, -С(О)-, -C(S)-, -C(NR')-, -C(O)N(R')-, -N(R')C(O)N(R'), -N(R')C(O)-, -N(R')C(O)O-, -OC(O)N(R')-, -S(O)-, -S(O)2-, -S(O)2N(R')-, -N(R')S(O)2-, -SC(O)-, -C(O)S-, -OC(O)- и -C(O)O-, где каждая переменная является независимо таковой, как определено и описано в настоящем документе.
521. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную C10-С40 насыщенную или частично ненасыщенную алифатическую цепь.
522. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит необязательно замещенную C10-С40 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
523. Композиция или способ по любому из предшествующих вариантов реализации, причем композиция дополнительно содержит один или более дополнительных компонентов, выбранных из: полинуклеотида, ингибитора карбоангидразы, красителя, интеркалирующего агента, акридина, сшивающего агента, псоралена, митомицина С, порфирина, ТРРС4, тексафирина, сапфирина, полициклического ароматического углеводорода феназина, дигидрофеназина, искусственной эндонуклеазы, хелатирующего агента, ЭДТА, алкилирующего агента, фосфата, амино, меркапто, ПЭГ, PEG-40K, MPEG, [MPEG]2, полиамино, алкила, замещенного алкила, меченного радиоактивным изотопом маркера, фермента, гаптен-биотина, облегчающего транспорт/абсорбцию вещества, аспирина, витамина Е, фолиевой кислоты, синтетической рибонуклеазы, гликопротеина, пептида, молекулы, имеющей специфическое сродство к со-лиганду, антитела, гормона, гормонального рецептора, непептидного вида, липида, лектина, углевода, витамина, кофактора или лекарственного агента.
524. Композиция или способ по любому из предшествующих вариантов реализации, причем липид содержит C10-C80 линейную, насыщенную или частично ненасыщенную алифатическую цепь.
525. Композиция или способ по любому из предшествующих вариантов реализации, причем композиция дополнительно содержит линкерную группу, связывающий олигонуклеотид и липид, причем линкерная группа выбрана из: незаряженной линкерной группы; заряженной линкерной группы; содержащей алкил линкерной группы; содержащей фосфат линкерной группы; разветвленной линкерной группы; неразветвленной линкерной группы; содержащей по меньшей мере одну группу расщепления линкерной группы; содержащей по меньшей мере одну группу редокс-расщепления линкерной группы; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе фосфата; линкерной группы, содержащей по меньшей мере одну группу расщепления кислотой; линкерной группы, содержащей по меньшей мере одну группу расщепления на основе сложного эфира; и линкерной группы, содержащей по меньшей мере одну группу расщепления на основе пептидов.
526. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит или состоит из олигонуклеотида или композиции олигонуклеотидов или композиции олигонуклеотидов с контролируемой хиральностью.
527. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит или состоит из олигонуклеотида или композиции олигонуклеотидов, или композиции олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности любого описанного в данном описании олигонуклеотида.
528. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит или состоит из олигонуклеотида или композиции олигонуклеотидов, или композиции олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности любого олигонуклеотида, перечисленного в Таблице 4.
529. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит или состоит из олигонуклеотида или композиции олигонуклеотидов, или композиции олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности переключения сплайсинга олигонуклеотида.
530. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит или состоит из олигонуклеотида или композиции олигонуклеотидов, или композиции олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности олигонуклеотида, способного к перепрыгиванию или опосредованию перепрыгивания экзона в гене дистрофии.
531. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид представляет собой композицию олигонуклеотидов с контролируемой хиральностью.
532. Композиция или способ по любому из предшествующих вариантов реализации, причем заболевание или нарушение представляет собой болезнь Хантингтона.
533. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении мРНК гена хантингтина млекопитающих.
534. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит, состоит из или представляет собой последовательность любого описанного в настоящем документе олигонуклеотида.
535. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид способен различать аллель хантингтин дикого типа и мутантный.
536. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид способен участвовать в опосредованном РНКазой Н расщеплении мРНК мутантного гена хантингтина.
537. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит, состоит из или представляет собой последовательность любого олигонуклеотида, раскрытого в таблице 4.
538. Композиция или способ по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит или состоит из олигонуклеотида или композиции олигонуклеотидов, или композиции олигонуклеотидов с контролируемой хиральностью, причем последовательность олигонуклеотида содержит или состоит из последовательности любого из: WV-1092, WV-2595 или WV-2603.
539. Композиция или способ по любому из предшествующих вариантов реализации, причем последовательность олигонуклеотида включает любую одну или более из следующего: последовательность оснований (включая длину); профиль химических модификаций фрагментов сахара и оснований; профиль линкерных групп остова; профиль природных фосфатных линкерных групп, фосфоротиоатных линкерных групп, фосфоротиоатных триэфирных линкерных групп и их комбинации; профиль хиральных центров остова; профиль стереохимии (Rp/Sp) хиральных межнуклеотидных линкерных групп; профиль модификаций фосфора остова; профиль модификаций на межнуклеотидном атоме фосфора, таком как -S- и -L-R1 формулы I.
540. Олигонуклеотид, содержащий последовательность, которая характеризуется идентичностью, составляющей более чем примерно 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, по отношению к последовательности, найденной в представленном примере олигонуклеотида.
540а. Олигонуклеотид по варианту реализации 540, причем последовательность олигонуклеотида представляет собой последовательность предоставленного примера олигонуклеотида.
540b. Олигонуклеотид по варианту реализации 540 или 540а, причем представленный пример олигонуклеотида представляет собой олигонуклеотид, выбранный из таблицы N1A, N2A, N3A, N4A или 8.
541. Олигонуклеотид по варианту реализации 540, причем предложенный иллюстративный олигонуклеотид представляет собой WV-1092.
542. Олигонуклеотид по варианту реализации 540, причем предложенный иллюстративный олигонуклеотид представляет собой WV-2595.
543. Олигонуклеотид по варианту реализации 540, причем представленный предложенный иллюстративный олигонуклеотид представляет собой WV-2603
544. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит последовательность, представленную в предложенном иллюстративном олигонуклеотиде.
545. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид состоит из последовательности, найденной в предложенном иллюстративном олигонуклеотиде.
546. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит одну или более природных фоосфатных линкерных групп и одну или более модифицированных межнуклеотидных линкерных групп.
547. Олигонуклеотид по варианту реализации 546, причем олигонуклеотид представляет собой олигонуклеотид по любому из вариантов реализации 540-545.
548. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит 2, 3, 4, 5, 6, 7, 8, 9, 10 или более природных фоосфатных линкерных групп.
549. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит одну или более модифицированных межнуклеотидных линкерных групп.
550. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит две или более модифицированных межнуклеотидных линкерных групп.
551. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более модифицированных межнуклеотидных линкерных групп.
552. Олигонуклеотид по любому из предшествующих вариантов реализации, в причем олигонуклеотид содержит 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более модифицированных межнуклеотидных линкерных групп.
553. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид содержит 10 или более модифицированных межнуклеотидных линкерных групп.
554. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором по меньшей мере одна из модифицированных межнуклеотидных линкерных групп представляет собой межнуклеотидную линкерную группу с контролируемой хиральностью, причем олигонуклеотиды, имеющие одну и ту же последовательность и химические модификации внутри композиции, имеют одну и ту же конфигурацию, либо Rp, либо Sp, при атоме хирального фосфора модифицированной межнуклеотидной линкерной группы.
555. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором по меньшей мере две модифицированные межнуклеотидные линкерные группы характеризуются контролируемой хиральностью.
556. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 модифицированных межнуклеотидных линкерных групп характеризуются контролируемой хиральностью.
557. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором по меньшей мере одна модифицированная межнуклеотидная линкерная группа в последовательной модифицированной области межнуклеотидной линкерной группы характеризуются контролируемой хиральностью.
558. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором по меньшей мере две модифицированные межнуклеотидные линкерные группы в последовательной модифицированной области межнуклеотидной линкерной группы характеризуются контролируемой хиральностью.
559. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 модифицированных межнуклеотидных линкерных групп в последовательной модифицированной области межнуклеотидной линкерной группы характеризуются контролируемой хиральностью.
560. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором каждая модифицированная межнуклеотидная линкерная группа в последовательной модифицированной области межнуклеотидной линкерной группы характеризуются контролируемой хиральностью.
561. Олигонуклеотид по любому из предшествующих вариантов реализации, в котором каждая модифицированная межнуклеотидная линкерная группа характеризуются контролируемой хиральностью.
562. Олигонуклеотид по любому из предшествующих вариантов реализации, причем предложенный олигонуклеотид содержит профиль (Sp)xRp(Sp)y, где каждый из х и у независимо равен 1-20, а сумма х и у равна 1-50.
563. Олигонуклеотид по любому из предшествующих вариантов реализации, где каждый из х и у независимо представляет собой 2-20.
564. Олигонуклеотид по любому из предшествующих вариантов реализации, где по меньшей мере один из х и у больше чем 5, 6, 7, 8, 9 или 10.
565. Олигонуклеотид по любому из предшествующих вариантов реализации, где сумма х и у больше чем 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20.
566. Олигонуклеотид по любому из предшествующих вариантов реализации, причем предложенный олигонуклеотид содержит одну или более химических модификаций.
567. Олигонуклеотид по любому из предшествующих вариантов реализации, причем предложенный олигонуклеотид содержит одну или более модификаций основания.
568. Олигонуклеотид по любому из предшествующих вариантов реализации, причем предложенный олигонуклеотид содержит одну или более модификаций сахара.
569. Олигонуклеотид по любому из предшествующих вариантов реализации, причем модификация сахара представляет собой 2'-модификацию.
570. Олигонуклеотид по любому из предшествующих вариантов реализации, причем модификация сахара представляет собой LNA.
571. Олигонуклеотид по любому из предшествующих вариантов реализации, причем предложенный олигонуклеотид представляет собой олигонуклеотид с контролируемой хиральностью.
572. Олигонуклеотид по любому из предшествующих вариантов реализации, причем олигонуклеотид конъюгирован с нацеливающим компонентом.
573. Композиция олигонуклеотидов, содержащая олигонуклеотид по любому из предшествующих вариантов реализации.
573а. Композиция по варианту реализации 573, причем композиция представляет собой композицию олигонуклеотидов с контролируемой хиральностью, содержащую предопределенный уровень олигонуклеотида.
574. Композиция по любому из предшествующих вариантов реализации или композиция в способе по любому из предшествующих вариантов реализации, дополнительно содержащая селективный агент, выбранный из группы соединений, которые специфически связываются с одним или более транспортерами нейромедиаторов, выбранными из группы, состоящей из транспортера дофамина (DAT), транспортера серотонина (SERT) и транспортера норадреналина (NET); группы, состоящей из ингибитора обратного захвата дофамина (DRI), селективного ингибитора обратного захвата серотонина (SSRI), ингибитора обратного захвата норадреналина (NRI), ингибитора обратного захвата норэпинефрина и дофамина (NDRI) и ингибитора обратного захвата серотонина-норэпинефрина-дофамина (SNDRI); группы, состоящей из тройного ингибитора обратного захвата, двойного ингибитора обратного захвата норадреналина-дофамина, одинарного ингибитора обратного захвата серотонина, одинарного ингибитора обратного захвата норадреналина и одинарного ингибитора обратного захвата дофамина; и группы, состоящей из ингибитора обратного захвата дофамина (DRI), ингибитора обратного захвата норэпинефрина-дофамина (NDRI) и ингибитора обратного захвата серотонина-норэпинефрина-дофамина (SNDRI).
575. Способ лечения или профилактики болезни Хантингтона у субъекта, предусматривающий введение субъекту олигонуклеотида или композиции по любому из предшествующих вариантов реализации.
575а. Способ по любому из предшествующих вариантов реализации, при котором олигонуклеотид или композицию вводят путем интратекального введения.
576. Способ получения олигонуклеотида, предусматривающий предоставление хирального реагента, имеющего структуру формулы 3-АА.
577. Способ получения олигонуклеотида, предусматривающий предоставление хирального реагента, имеющего структуру 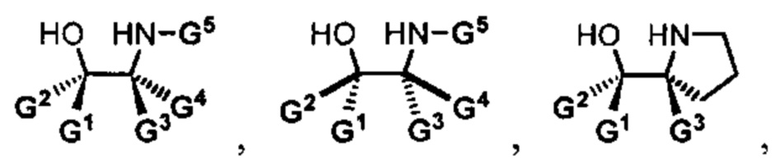
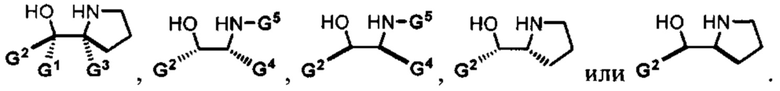
578. Способ по любому из предшествующих вариантов реализации, при котором хиральный реагент является хирально чистым.
579. Способ получения олигонуклеотида, предусматривающий предоставление соединения, содержащего фрагмент из хирального реагента, имеющего структуру по любому из предыдущих вариантов реализации, где -W1H и -W2H или гидроксильные и аминогруппы образуют связи с атомом фосфора фосфорамидита.
580. Способ по варианту реализации 579, при котором соединение имеет структуру
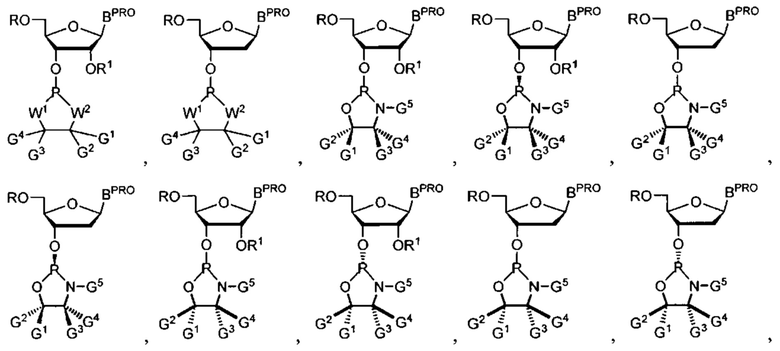
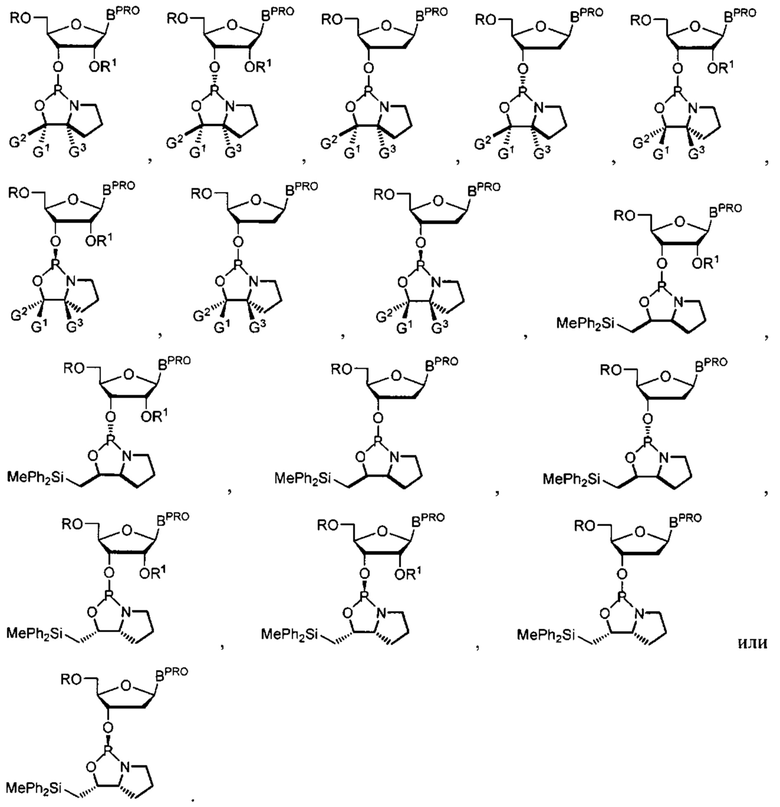
581. Способ по варианту реализации 580, при котором R, связанный с 5'-O, представляет собой гидроксильную защитную группу.
582. Способ по варианту реализации 581, при котором гидроксильная защитная группа представляет собой DMTr.
583. Способ по варианту реализации 582, при котором BPRO представляет собой защищенное нуклеотидное основание.
584. Способ по варианту реализации 583, при котором нуклеотидное основание представляет собой необязательно замещенное нуклеотидное основание, выбранное из А, Т, С и G.
585. Способ по любому из предшествующих вариантов реализации, при котором W1 представляет собой -NG5, W2 представляет собой О.
586. Способ по любому из предшествующих вариантов реализации, при котором каждый из G1 и G3 независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного С1-10, G2 представляет собой -C(R)2Si(R)3, a G4 и G5 берут вместе для образования необязательно замещенного насыщенного, частично ненасыщенного или ненасыщенного гетероатомсодержащего кольца, содержащего вплоть до 20 атомов в кольце, которое является моноциклическим или полициклическим, конденсированным или неконденсированным.
587. Способ по любому из предшествующих вариантов реализации, при котором каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, карбоциклильного, арильного, гетероарильного и гетероциклильного C1-С6.
588. Способ по любому из предшествующих вариантов реализации, при котором G1 представляет собой водород.
589. Способ по любому из предшествующих вариантов реализации, при котором G2 представляет собой -C(R)2Si(R)3, где -C(R)2 представляет собой необязательно замещенную группу -СН2-, и каждый R из -Si(R)3 независимо представляет собой необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного С1-10.
590. Способ по любому из предшествующих вариантов реализации, при котором по меньшей мере один R в -Si(R)3 представляет собой независимо необязательно замещенный С1-10 алкил.
591. Способ по любому из предшествующих вариантов реализации, при котором по меньшей мере один R в -Si(R)3 независимо представляет собой необязательно замещенный фенил.
592. Способ по любому из предшествующих вариантов реализации, при котором один R в -Si(R)3 независимо представляет собой необязательно замещенный C1-10 алкил, и каждый из двух других R независимо представляет собой необязательно замещенный фенил.
593. Способ по любому из предшествующих вариантов реализации, при котором G2 представляет собой необязательно замещенный -CH2Si(Me)(Ph)2.
594. Способ по любому из предшествующих вариантов реализации, при котором G2 представляет собой -CH2Si(Me)(Ph)2.
595. Способ по любому из предшествующих вариантов реализации, при котором G3 представляет собой водород.
596. Способ по любому из предшествующих вариантов реализации, при котором G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-6-членного кольца, содержащего один атом азота.
597. Способ по любому из предшествующих вариантов реализации, при котором G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота.
598. Способ по любому из предшествующих вариантов реализации, при котором хиральный реагент представляет собой 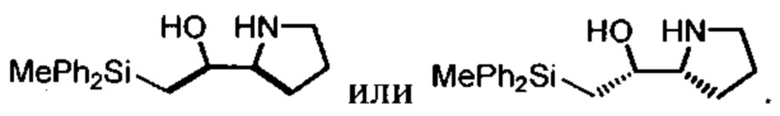
599. Способ по любому из предшествующих вариантов реализации, предусматривающий предоставление фторсодержащего реагента.
600. Способ по любому из предшествующих вариантов реализации, при котором фторсодержащий реагент представляет собой TBAF.
601. Способ по любому из предшествующих вариантов реализации, предусматривающий использование линкерной группы, которая стабильна по отношению к условию TBAF для удаления хирального реагента.
602. Способ по любому из предшествующих вариантов реализации, при котором линкерная группа представляет собой линкерную группу SP.
603. Способ по любому из вариантов реализации 576-599, при котором фторсодержащий реагент представляет собой HF-NR3.
604. Способ по варианту реализации 603, при котором фторсодержащий реагент представляет собой HF-NEt3.
605. Способ по варианту реализации 603 или 604, предусматривающий использование линкерной группы, которая стабильна по отношению к условию HF-NR3 для удаления хирального реагента.
606. Способ по любому из вариантов реализации 603-605, при котором линкерная группа представляет собой сукцинильную линкерную группу.
ПРИМЕРЫ
Выше было приведено описание определенных неограничивающих вариантов реализации раскрытия. Соответственно, следует понимать, что варианты реализации раскрытия, описанные в настоящей заявке, исключительно иллюстрируют применение принципов раскрытия. Подразумевается, что подробное описание проиллюстрированных вариантов реализации не ограничивает объем формулы изобретения.
Пример 1. Метаболическая стабильность in vitro chiromersens человека в преинкубированных гомогенатах всей крысиной печени
В настоящем примере описано сравнение стабильности in vitro гомогената всей печени крысы мипомерсена (стереохимическая смесь) с композицией олигонуклеотидов с контролируемой хиральностью мипомерсена («chiromersens»). Способ, в частности, применим в скрининге соединений для прогнозирования периода полураспада in vivo.
Как известно специалистам в данной области техники, мипомерсен (ранее ISIS 301012, продаваемый под торговым названием Кинамро) представляет собой 20-мерный олигонуклеотид, последовательность оснований которого является антисмысловой по отношению к части гена аполипопротеина В. Мипомерсен ингибирует экспрессию гена аполипопротеина В, предположительно посредством направленного воздействия на мРНК. Мипомерсен характеризуется следующей структурой:
G*-C*-C*-U*-C*-dA-dG-dT-dC-dT-dG-dmC-dT-dT-dmC-G*-C*-A*-C*-C*
[d=2'-дезокси, *=2'-O-(2-метоксиэтил)]
с 3'→5' фосфоротиоатными линкерными группами. Таким образом, мипомерсен содержит 2'-O-метоксиэтил-модифицированные остатки рибозы на обоих концах и остатки дезоксирибозы в середине.
Исследуемые стереохимически чистые аналоги мипомерсена, описанные в этом примере, включали 3'→5' фосфоротиоатные линкерные группы. Согласно некоторым вариантам осуществления исследуемые аналоги включают один или более 2'-O-(2-метоксиэтил)-модифицированных остатков; согласно некоторым вариантам осуществления исследуемые аналоги включают только остатки 2'-дезокси. Определенные исследуемые аналоги имели структуры, представленные ниже в таблицах 3 и 4.
Протокол: Авторы настоящего изобретения использовали протокол, предложенный Geary et al. (Oligonucleotides, Volume 20, Number 6, 2010), с некоторыми изменениями.
Тест-системы: Шесть самцов крыс Спрег-Доули (Rattus norvegicus) были предоставлены компанией Charles River Laboratories, Inc., (Hollister, CA) и были получены в SNBL США.
Коллекция тканей: Животных акклиматизировали к лаборатории в течение двух дней до начала сбора тканей. В момент сбора тканей животных анестезировали посредством внутрибрюшинной (IP) инъекции пентобарбитала натрия. Перфузию печени проводили с использованием 500 мл на животное охлажденного физиологического раствора, вводимого через воротную вену печени. После перфузии печень иссекали и поддерживали на льду. Печень измельчали на мелкие кусочки, а затем взвешивали.
Получение гомогената печени: Измельченные кусочки тканей печени переносили в тарированные центрифужные пробирки объемом 50 мл и взвешивали. Охлажденный буфер для гомогенизации (100 мМ Трис, рН 8,0, 1 мМ ацетат магния, с антибиотиком и противогрибковым средством) добавляли в каждую пробирку, таким образом, что пробирка(и) содержала 5 мл буфера на грамм ткани. С использованием гомогенизатора тканей QIAGEN TissueRuptor смесь печени/буфера гомогенизировали при поддержании пробирку на льду. Концентрацию белка в объеме гомогената печени определяли с использованием анализа белка Pierce ВСА. Гомогенаты печени разделяли на аликвоты по 5 мл, переносили в меченые криопробирки соответствующего размера и хранили при -60°С.
Условия инкубации: Аликвоты замороженного гомогената печени объемом 5 мл (концентрация белка = 22,48 мг/мл) размораживали и инкубировали при 37°С в течение 24 часов. Для каждого олигомера в таблице 1 брали шесть эппендорф (2 мл) и добавляли в каждую пробирку 450 мкл гомогената. В каждую пробирку добавляли 50 мкл ASO (200 мкМ). Сразу же после смешивания 125 мкл (5-кратного) стоп-буфера (2,5% IGEPAL, 0,5 М NaCl, 5 мМ ЭДТА, 50 мМ Трис, рН=8,0) и 12,5 мкл протеиназы К в концентрации 20 мг/мл (Амбион, # АМ2546) добавляли в одну пробирку для временной точки 0 часов. Остальные реакционные смеси инкубировали при 37°С при встряхивании со скоростью 400 оборотов в минуту на инкубационном микропланшетном шейкере VWR. После инкубации в течение определенного периода (1, 2, 3, 4 и 5 дней) каждую смесь обрабатывали посредством 125 мкл (5-кратного) стоп-буфера (2,5% IGEPAL, 0,5 М NaCl, 5 мМ ЭДТА, 50 мМ Трис, рН=8,0) и 12,5 мкл протеиназы К в концентрации 20 мг/мл (Амбион, # АМ2546).
Исследование и биоанализ: ISIS 355868 (5'-GCGTTTGCTCTTCTTCTTGCGTTTTTT-3'), 27-мерный олигонуклеотид (подчеркнутые основания представляют собой МОЕ-модифицированные) использовали в качестве внутреннего стандарта для количественного измерения chiromersens. 50 мкл внутреннего стандарта (200 мкМ) добавляли в каждую пробирку, а затем добавляли 250 мкл 30%-ного раствора гидроксида аммония, 800 мкл смеси фенол:хлороформ:изоамиловый спирт (25:24:1). После перемешивания и центрифугирования при 600 оборотов в минуту водный слой упаривали на speed vac до 100 мкл и загружали в колонку Sep Рак (С18, 1G, ВАТ 036905). Все водные смывы (2×20 мл) колонки Sep Рак исследовали посредством быстрого ионообменного метода, чтобы гарантировать, что ни один продукт не был там найден. 50% ACN (3,5 мл) использовали для элюирования олигонуклеотида и метаболитов, и колонку дополнительно промывали 70% CAN (3,5), чтобы гарантировать, что ничего не осталось на колонке. Для каждой последовательности собирали пять фракций: water wash 1, 2, 3, ACN1 и 2 с использованием системы Visiprep (Sigma, номер детали: 57031-U).
Ионообменный метод

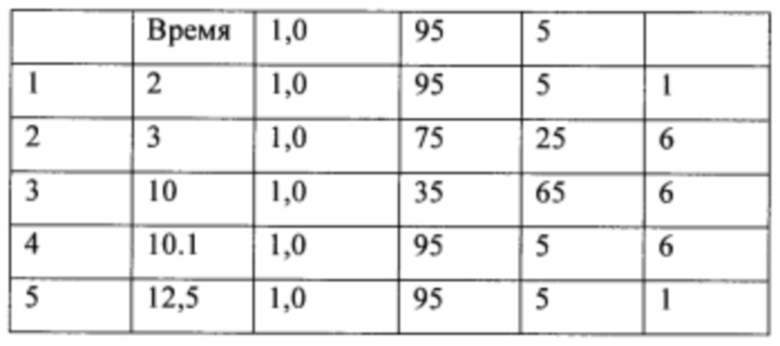
Буфер А=10 мМ Трис-НС1, 50% ACN, рН 8,0
Буфер В=А+800 мМ NaClO4
Колонка = DNA рас 100
Температура колонки 60°С
Способ отмывки использовали после каждого пропускания (описано в М9-Ехр21) с использованием тех же буферов, как описано выше, и в соотношении 50:50 (метанол:вода) в буферной линии С.
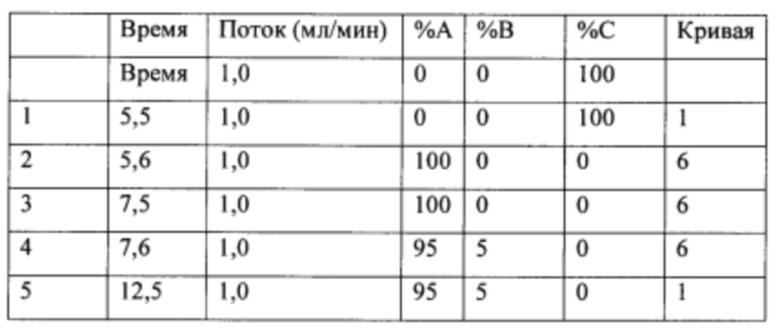
Элюат ацетонитрила концентрировали досуха и растворяли в 100 мкл воды, чтобы проанализировать посредством RPHPIPC.
Элюент А=10 мМ ацетат трибутиламмония, рН=7,0
Элюент В=ACN (ВЭЖХ, B&J)
Колонка: Xterra MS С18, 3,5 мкм, 4,6×50 мм, номер по каталогу: 186000432
Предколонка от Phenomenex, номер по каталогу: KJ0-4282
Температура колонки = 60°С
Градиент ВЭЖХ:
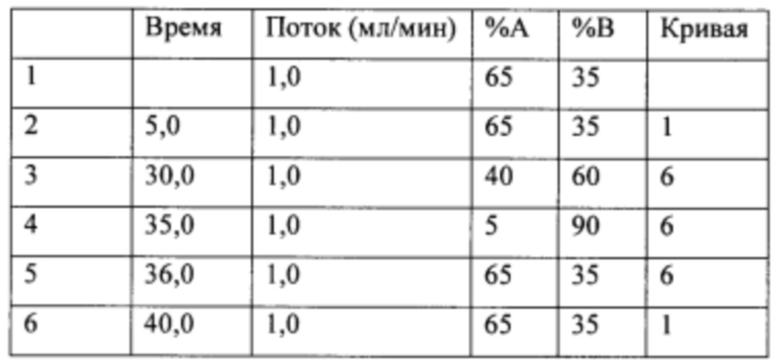
Для аналитической ОФ ВЭЖХ 10 мкл этого исходного раствора добавляли к 40 мкл воды и впрыскивали 40 мкл.

Обсуждение: 2' модификации в антисмысловых и миРНК прогнозируются как стабилизирующие эти молекулы и повышающие их устойчивость в плазме крови и тканях по сравнению с ДНК и миРНК дикого типа.
Структура 2'-МОЕ крыло-сердцевина-крыло в мипомерсене. Антисмысловые олигонуклеотиды первого поколения, применяемые в первых антисмысловых клинических испытаниях, содержали 2'-дезоксирибонуклеотидные остатки и фосфоротиоатные межнуклеозидные линкерные группы. Впоследствии были разработаны антисмысловые олигонуклеотиды второго поколения, которые представляют собой, как правило, то, что называется в настоящем документе «дизайн 5-10-5 2'-МОЕ крыло-сердцевина-крыло», в том отношении, что пять (5) остатков на каждом конце представляют собой 2'-O-метоксиэтил (2'-МОЕ)-модифицированные остатки и десять (10) остатков в середине представляют собой 2'-дезоксирибонуклеотиды; межнуклеотидные линкерные группы таких олигонуклеотидов представляют собой фосфоротиоатные. Такие олигонуклеотиды "5-10-5 2'-МОЕ крыло-сердцевина-крыло" проявляли заметное улучшение эффективности по сравнению с первым поколением (PCT/US 2005/033837). Подобные мотивы крыло-сердцевина-крыло, в виде 2-16-2, 3-14-3, 4-12-4 или 5-10-5, были разработаны, чтобы улучшить стабильность олигонуклеотидов к нуклеазам при этом сохраняя достаточную структуру ДНК для активности РНКазы.
Хирально-чистые олигонуклеотиды. Настоящее раскрытие предусматривает хирально-чистые олигонуклеотиды и демонстрирует, среди прочего, что выбор стереохимии само по себе может улучшить стабильность олигонуклеотида (т.е. не зависит от модификации остатков, таких как модификация 2'МОЕ). Действительно, данное раскрытие демонстрирует, что хирально-чистые фосфоротиоатные олигонуклеотиды могут обеспечить такую же или более высокую стабильность, чем соответствующие 2'-модифицированные стереослучайные фосфоротиоатные соединения.
Согласно некоторым вариантам осуществления исследуемые хирально-чистые олигонуклеотиды характеризуются общей структурой X-Y-X относительно стереохимии в том отношении, что они содержат области крыла «X» (как правило, примерно 1-10 остатков в длину), где все остатки имеют такую же стереохимию, фланкирующие область сердцевины «Y», в которой стереохимия варьирует. Во многих вариантах реализации примерно 20-50% нуклеотидных аналогов в таких исследуемых олигонуклеотидах не являются субстратами для РНКазы Н. Способность контролировать стереохимию фосфоротиоатов в ДНК позволяет защитить олигомеры от деградации нуклеазами при сохранении активных сайтов РНКазы. Одна из таких структур представляет собой ONT-154, где крылья олигонуклеотида были стабилизированы фосфоротиоатной химией конфигурации Sp с сохранением нескольких фосфоротиоатов в конфигурации Rp, которые являются лучшими субстратами для РНКазы Н (Molecular Cell, 2007). Кристаллическая структура человеческой РНКазы Н в виде комплекса с ДНК/РНК-дуплексом показывает, что фосфат-связывающий карман фермента контактирует с четырьмя смежными фосфатами ДНК. Первые три контакта кажутся сильнее, чем четвертый и они предпочитают атомы кислорода Pro-R/Pro-R/Pro-S каждого из этих трех фосфатов. Комбинируя преимущества стабильности благодаря стереохимии Sp с активными сайтами РНКазы Н, могут быть разработаны несколько последовательностей, чтобы конкурировать с/или улучшать 2'-модификации. Из эксперимента стабильности гомогената всей печени крысы, сравнивающего мипомерсен (ONT-41) с правильным (хирально-контролируемым) дизайном с 2'-модификациями и без них (ONT-87 и ONT-154) (таблица 1 и фиг. 1), очевидно, что посредством удаления 2'-модификаций и тщательного контроля хиральности с фосфоротиоатами в конфигурации Rp и Sp, авторы настоящего изобретения могут улучшать стабильность этих олигонуклеотидов, которые впоследствии влияют на эффективность in vivo.



Пример 2. Иллюстративные молекулы миРНК с контролируемой хиральностью 
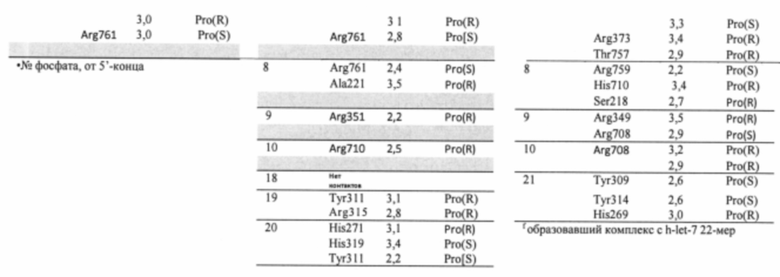
Настоящее раскрытие, несмотря на учения в данной области техники, напротив, признает, что стереохимия межнуклеотидных линкерных групп может быть использована для повышения стабильности и активности олигонуклеотидов посредством композиций олигонуклеотидов с контролируемой хиральностью. Такие композиции олигонуклеотидов с контролируемой хиральностью могут обеспечить гораздо лучшие результаты, чем композиции олигонуклеотидов с неконтролируемой хиральностью, как показано в данном раскрытии.
Сообщалось о двух кристаллических структурах РНК в комплексе с человеческим белком Аргонавт-2 (hAgo2): The Crystal Structure of Human Argonaute-2, Science, 2012 (PDB-4ei3) и The Structure of Human Argonaute-2 in Complex with miR-20a, Cell, 2012 PDB-4f3t). Кроме того, существует одна кристаллическая структура РНК Let-7 в комплексе с человеческим белком Аргонавт-1 (Hago-1): The Making of a Sheer: Activation of Human Argonaut©-1, Cell Rep.2013 (PDB-4krf).
На основании информации, содержащейся в этих публикациях, предполагалось, что могут быть сделаны некоторые суждения о выгодных преимуществах стереохимии в межнуклеотидной фосфатной линкерной группе, если фосфодиэфирные связи должны были быть заменены фосфоротиоатными связями. Эти преимущества могут быть связаны со значительным улучшением эффективности, стабильности и других фармакологических свойств. Имея это в виду, компьютерная программа Pymol использовалась для обнаружения всех полярных взаимодействий между белком и межнуклеотидной фосфодиэфирной линкерной группой кристаллизованной РНК для всех трех структур. Полярные взаимодействия на расстоянии более 3,5 А были проигнорированы.
Результаты этого анализа представлены в таблице 1. Конкретный атом фосфора фосфодиэфирного остова на РНК находится в конфигурации Pro(R) или Pro(S), на основании предположения о том, что в фосфоротиоатном диэфирном аналоге очень похожая связь находилась бы между полярной группой по аминокислотному остатку и атомом кислорода фосфата. Замещение серой вместо не-мостикового кислорода, поэтому, будет придавать уникальную стереохимию (абсолютную конфигурацию либо (Sp), либо (Rp)) на атоме фосфора в пределах этого мотива.
Следует особо отметить чрезвычайно хорошее согласие между двумя структурами hAgo-2 в комплексе с РНК. Кроме того, существует отличное совпадение между структурами hAgo-1 и hAgo-2 в комплексе с РНК, что указывает на то, что конформация, которую принимает молекула РНК, высоко консервативна между этими двумя белками. Любые выводы или правила, которые формируются на основании результатов этого анализа, вероятно, поэтому, будут справедливы для обеих белковых молекул.
Как можно видеть, существует, как правило, более одного полярного взаимодействия в любой фосфодиэфирной группе, за исключением тех, которые расположены между фосфодиэфирами в фосфатных положениях 9 и 10 и hAgo-2 (Cell 2012), которые принимают исключительно предпочтение Pro(Rp) путем связывания с Arg351 и Arg710, соответственно.
Тем не менее, более короткие расстояния (которые соответствуют более сильным взаимодействиям), а также количество связей на кислороде может вызывать преобладающее взаимодействие для кислородов Pro(Rp) или Pro(Sp): следовательно, приводя в результате к нескольким взаимодействиям, которые являются в основном одного стереохимического типа или другого. В рамках этой группы находятся взаимодействия между фосфодиэфирами в фосфатных положениях 2 (Sp), 3 (Rp), 4 (Rp), 6 (Rp), 8 (Sp), 19 (Rp), 20 (Sp) и 21 (Sp).
Из остальных взаимодействий, кажется, нет предпочтения в одной конкретной стереохимии над другой, так что предпочтительная стереохимия может быть либо (Sp), либо (Rp).
В этой категории существуют взаимодействия, образованные между фосфодиэфирами в фосфатных положениях 5 (Rp или Sp) и 7 (Rp или Sp).
Для взаимодействий в другом фосфатном остове, нет никакой информации о кристаллической структуре, поэтому стереохимия в этих положениях может аналогичным образом быть либо (Rp), либо (Sp), пока эмпирические данные не покажут иное.
С этой целью таблица 6 содержит несколько неограничивающих примеров общих конструкций миРНК, которые могут быть задуманы, чтобы воспользоваться преимуществом этого предпочтения стереохимии в отдельных фосфоротиоатных диэфирных мотивах.
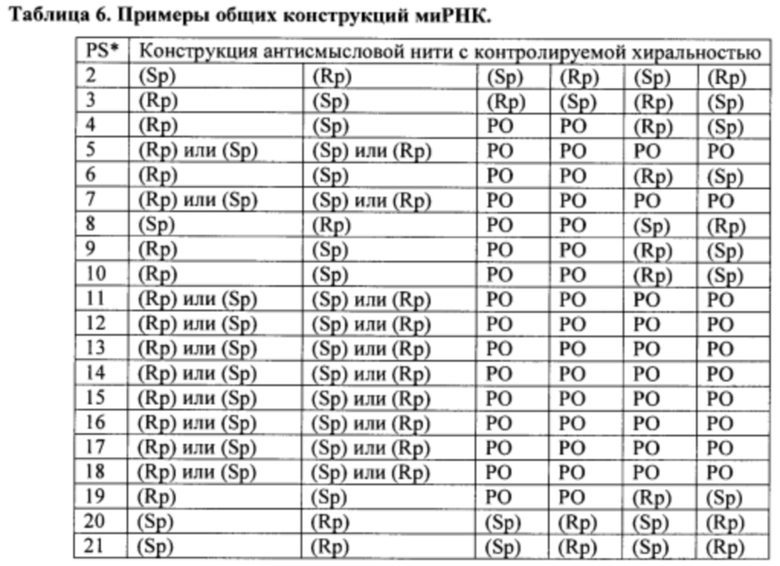
*Число указывает на положение фосфата от 5'-конца антисмысловой нити миРНК, (например, #2 расположен между нуклеотидами 1 и 2 и #21 расположен между нуклеотидами 20 и 21). (Sp) и (Rp) обозначают стереохимию атома фосфора на фосфоротиоатной (PS) диэфирной межнуклеотидной линкерной группе в указанном положении. РО обозначает фосфодиэфирную межнуклеотидную линкерную группу в указанном положении.
Примеры миРНК включают, но не ограничиваются ими, миРНК, имеющие конфигурацию Sp для хирального фосфоротиоата на 3'-конце и на 5'-конце антисмысловой цепи дуплекса миРНК, которая придает беспрецедентно повышенную стабильность в сыворотке крови или биологической жидкости человека. Та же конфигурация Sp для хирального фосфоротиоата на 3'-конце и на 5'-конце антисмысловой цепи дуплекса миРНК придает беспрецедентно повышенную биологическую активность, вызванную повышенной аффинностью к белку Ago2, что приводит к увеличению активности в рамках комплекса сайленсинга РНК-интерференции RISC.
В одном варианте реализации единственный хиральный фосфоротиоатный мотив вводится независимо в каждом положении вдоль антисмысловой или смысловой цепи молекулы миРНК. Для 21-мер это обеспечивает 80 уникальных последовательностей, либо с (Sp), либо с (Rp) фосфоротиоатной группой с контролируемой хиральностью. Когда образуют дуплексы независимо, готовят 1600 уникальных комбинаций миРНК.
Трансфекция миРНК хиральных молекул миРНК
Клетки Нер3В или HeLa обратно трансфицируют при плотности 2,0×104 клеток/лунку в 96-луночные планшеты. Трансфекция миРНК осуществляется с липофектамином RNAiMax (Life Technologies, номер в каталоге 13778-150) с использованием протокола изготовителя, за исключением того, что вносят уменьшенное количество липофектамина RNAiMax 0,2 мкл на лунку. Создают двенадцать разведений дуплексов миРНК 1:3, начиная с 1 мкМ. 10 мкл 10-кратного дуплекса миРНК затем подвергают действию липоплекса с подготовленной смесью 9,8 мкл безсывороточной среды и 0,2 мкл липофектамина RNAiMax на лунку. После 10-15-минутной инкубации добавляют 2,0×104 клеток в 80 мкл среды для клеточного роста ЕМЕМ (АТСС, 30-2003), чтобы довести конечный объем до 100 мкл на лунку. Для каждой дозы выполняют два отдельных события трансфекции.
Через 24 часа после трансфекции клетки Нер3В или HeLa лизируют и мРНК, против которых нацелена миРНК, очищают с использованием набора для выделения всей РНК MagMAX™-96 (Life Technologies, AM 1830); 15 мкл кДНК синтезируют посредством набора для обратной транскрипции кДНК с высокой пропускной способностью с ингибитором РНКазы (Life Technologies, 4374967). Экспрессию генов оценивают с помощью ПЦР в реальном времени на Lightcycler 480 (Roche) с использованием зондов Master Mix (Roche, 04 707 494 001) в соответствии с протоколом производителя.
IC50 и анализ данных
Метод два дельта Ct используется для расчета значений. Образцы нормируют к hGAPDH и калибруют, чтобы имитировать трансфицированные и необработанные образцы. Стереослучайную молекулу используют в качестве контроля. Данные представлены в виде среднего из 2-х биологических повторов с использованием GraphPad Prism. Четырехпараметровую линейную регрессионную кривую подгоняют к данным, а низ и верх ограничивают константами 0 и 100, соответственно, чтобы вычислить относительную IC50.
В настоящем примере показано успешное ингибирование экспрессии целевого гена с использованием агентов миРНК, состоящих из олигонуклеотидов с контролируемой хиральностью, как описано в настоящем документе. В частности, этот пример описывает гибридизацию отдельных олигонуклеотидных нитей, полученных с помощью синтеза с контролируемой хиральностью, как описано в настоящем документе, так что предоставляются двухцепочечные композиции олигонуклеотидов миРНК с контролируемой хиральностью. Этот пример дополнительно демонстрирует успешную трансфекцию клеток с такими агентами, и, кроме того, успешное ингибирование экспрессии целевого гена.
Метаболические стабильности In Vitro дуплексов миРНК PCSK9 человека, содержащих стереоконтролируемые фосфоротиоатные диэфирные линкерные группы в сыворотке крови человека.
10 мкМ дуплексов миРНК инкубировали в 90% сыворотки человека (50 мкл, Sigma, Н4522) при температуре 37°С в течение 24 часов. Получали временную точку 0 мин (50 мкл), а также временную точку инкубации контроля PBS (50 мкл), где 10 мкМ дуплекса миРНК инкубировали в 90% 1-кратного PBS (50 мкл при 37°С в течение 24 ч). После завершения инкубации в каждую временную точку добавляли 10 мкл стоп-раствора (0,5 М NaCl, 50 мМ Трис, 5 мМ ЭДТА, 2,5% IGEPAL), а затем 3,2 мкл протеиназы К (20 мг/мл, Амбион). Образцы инкубировали при 60°С в течение 20 мин, а затем центрифугировали при 2000 оборотах в минуту в течение 15 мин. Конечные реакционные смеси непосредственно анализировали в денатурирующей ионообменной ВЭЖХ (вводимый объем 50 мкл). Отношение интегрированной области в 24 ч и 0 мин использовали для определения % деградации для каждой миРНК.
Было обнаружено, что конфигурация стереохимии единственного фосфоротиоата в положении 21 (3'-конец) как антисмысловой цепи, так и смысловой цепи миРНК имело решающее влияние на стабильность дуплекса при инкубации в сыворотке крови человека (фиг. 1). Как показано на фиг. 1 и как определено следующим соотношением интеграции профиля деградации, дуплекс миРНК (Rp, Rp) проявлял значительную деградацию 55,0% через 24 ч. Стереослучайная смесь фосфоротиоатов в стереослучайной миРНК показала деградацию 25,2% через 24 ч. миРНК (Sp/Sp) показала лишь незначительную деградацию 7,3% через 24 ч. Это иллюстрирует сильный эффект, который фосфоротиоатная стереохимия оказывает на терапевтические миРНК. Дополнительные иллюстративные данные были представлены на фиг. 2, фиг. 3, фиг. 4 и фиг. 5.
Следует отметить, что каждая из стереочистых конструкций показывает различную эффективность (значения IC50) в зависимости от положения фосфоротиоатного мотива вдоль остова. Также наблюдается, что получают различные значения IC50 в зависимости от того, находится ли фосфоротиоатный мотив в каком-либо одном положении (Sp) или (Rp). Воздействие стереохимии на стабильность подобным образом понятно и различие устанавливается с использованием либо описанной выше сыворотки человека, либо экстракта цитозоля печени человека или фосфодиэстеразы змеиного яда, либо выделенной эндонуклеазы или выделенной экзонуклеазы.
Определенные правила структуры могут быть составлены на основании данных, полученных в приведенном выше примере. Эта информация по структуре может быть применена для введения нескольких хиральных фосфоротиоатных линкерных групп в антисмысловую и/или смысловую цепь миРНК, примеры которых приведены ниже. Настоящее раскрытие признает, что увеличенное количество хирального фосфоротиоата в антисмысловой и/или смысловой цепи миРНК, введенного в правильных положениях и имеющего правильную конфигурацию стереохимии, приводит к значительному улучшению конструкций миРНК с точки зрения эффективности и метаболической стабильности in vitro - транслируя в значительно фармакологически улучшенные терапевтические миРНК.
Примеры олигонуклеотидов с контролируемой хиральностью миРНК направленного действия на PCSK9
Пропротеинконвертаза субтилизин/кексин типа 9 (PCSK9) представляет собой фермент, задействованный в метаболизме холестерина. PCSK9 связывается с рецептором липопротеинов низкой плотности (ЛПНП), вызывая его разрушение. Несмотря на то, что ЛПНП, ассоциированные с рецептором, также уничтожаются при разрушении рецептора, суммарный эффект от связывания PCSK9 фактически приводит к увеличению уровня ЛПНП, так как рецептор в ином случае циклически возвращается на поверхность клетки и удаляет дополнительное количество холестерина.
Несколько компаний занимаются разработкой терапевтических агентов направленного действия на PCSK9. В контексте настоящего изобретения особенно важно, что каждая из компаний Isis Pharmaceuticals, Santaris Pharma и Alnylam Pharmaceuticals разрабатывает нуклеиновую кислоту, представляющую собой агент, ингибирующий PCSK9. Было показано, что продукт Isis Pharmaceuticals, антисмысловой олигонуклеотид, увеличивает экспрессию ЛПНП-Р и уменьшает общий уровень циркуляции холестерина у мышей (Graham et al "Antisense inhibition of proprotein convertase subtilisin/kexin type 9 reduces serum LDL in hyperlipidemic mice". J. Lipid Res. 48 (4): 763-7, April 2007). В первых клинических испытаниях продукта Alnylam Pharmaceuticals, ALN-PCS, было показано, что РНК-интерференция обеспечивает эффективный механизм ингибирования PCSK9 (Frank-Kamenetsky et al "Therapeutic RNAi targeting PCSK9 acutely lowers plasma cholesterol in rodents and LDL cholesterol in nonhuman primates". Proc. Natl. Acad. Sci. U.S.A. 105 (33): 11915-20, August 2008).
Согласно некоторым вариантам осуществления, несмотря на известные результаты, свидетельствующие об обратном, настоящее раскрытие признает, что фосфоротиоатные мотивы одной или другой стереохимической конформации могут быть рационально разработаны, чтобы воспользоваться преимуществами повышенной эффективности, стабильности и другими фармакологическими свойствами с помощью композиций олигонуклеотидов с контролируемой хиральностью. Чтобы усилить эту концепцию, таблица 3 содержит примеры стереохимически чистых конструкций, основанных на последовательности миРНК, которая направленно действует на матричную РНК PCSK9.
В этом иллюстративном варианте реализации единственный хиральный фосфоротиоатный мотив независимо вводят в каждое положение вдоль антисмысловой или смысловой цепи молекулы миРНК. Для 21-мер это обеспечивает 80 уникальных последовательностей с хирально контролируемой фосфоротиоатной группой в конфигурации либо (Sp), либо (Rp). Когда дуплексы образуются независимо, получают 1600 уникальных комбинаций миРНК.
В других примерах вариантов реализации единственный хиральный фосфоротиоатный мотив вводится независимо в каждое положение вдоль антисмысловой или смысловой цепи молекулы миРНК, в то время как фосфоротиоатная линкерная группа в конфигурации 3'-(Sp) сохраняется. Для 21-мер это обеспечивает еще дополнительные 80 уникальных последовательностей с хирально контролируемой фосфоротиоатной группой в конфигурации либо (Sp), либо (Rp). Когда дуплексы образуются независимо, получают 1600 уникальных комбинаций миРНК.
В других примерах вариантов реализации несколько хиральных фосфоротиоатных мотивов вводят независимо в нескольких положениях вдоль антисмысловой или смысловой цепи молекулы миРНК, после кодов, описанных в таблице 7, в то время как фосфоротиоатная линкерная группа в конфигурации 3'-(Sp) сохраняется. 
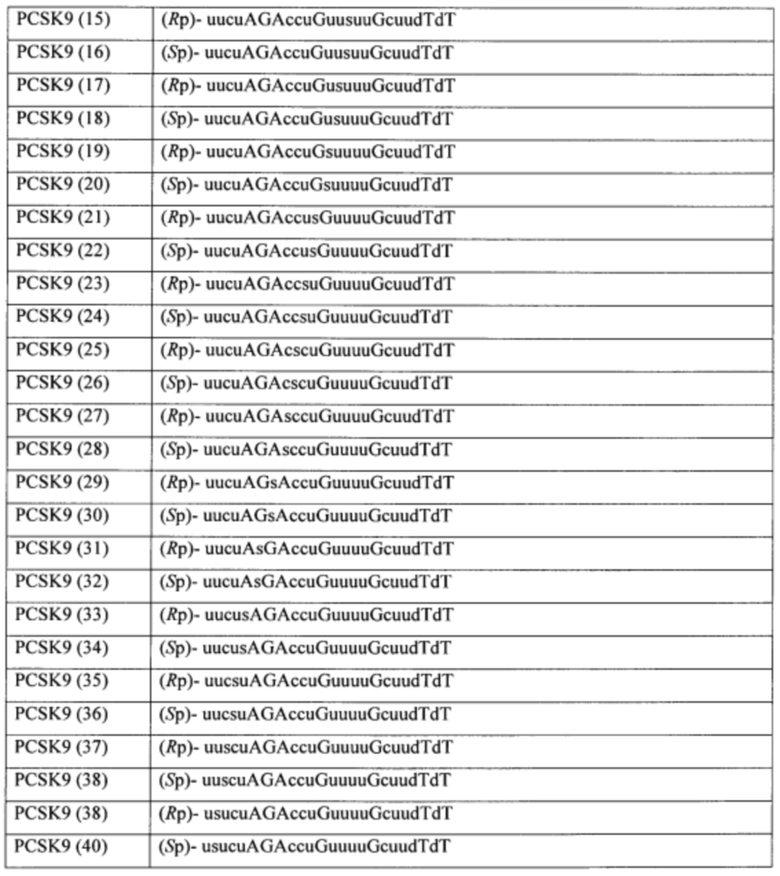
Примечание: строчные буквы представляют собой остатки 2'-ОМе РНК; заглавные буквы представляют собой остатки РНК; d = остатки 2'-дезокси и "s" обозначает фосфоротиоатный фрагмент.
Примеры синтеза антисмысловых цепей миРНК PCSK9 человека с несколькими хиральными фосфоротиоатными межнуклеотидными линкерными группами и с полностью хиральными фосфоротиоатными межнуклеотидными линкерными группами. 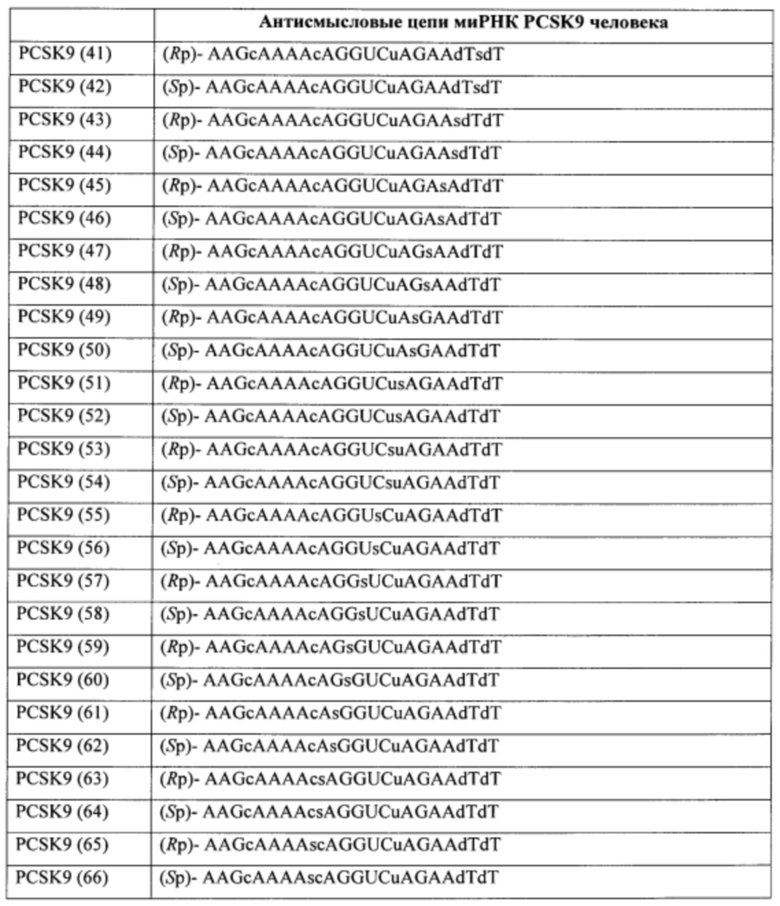
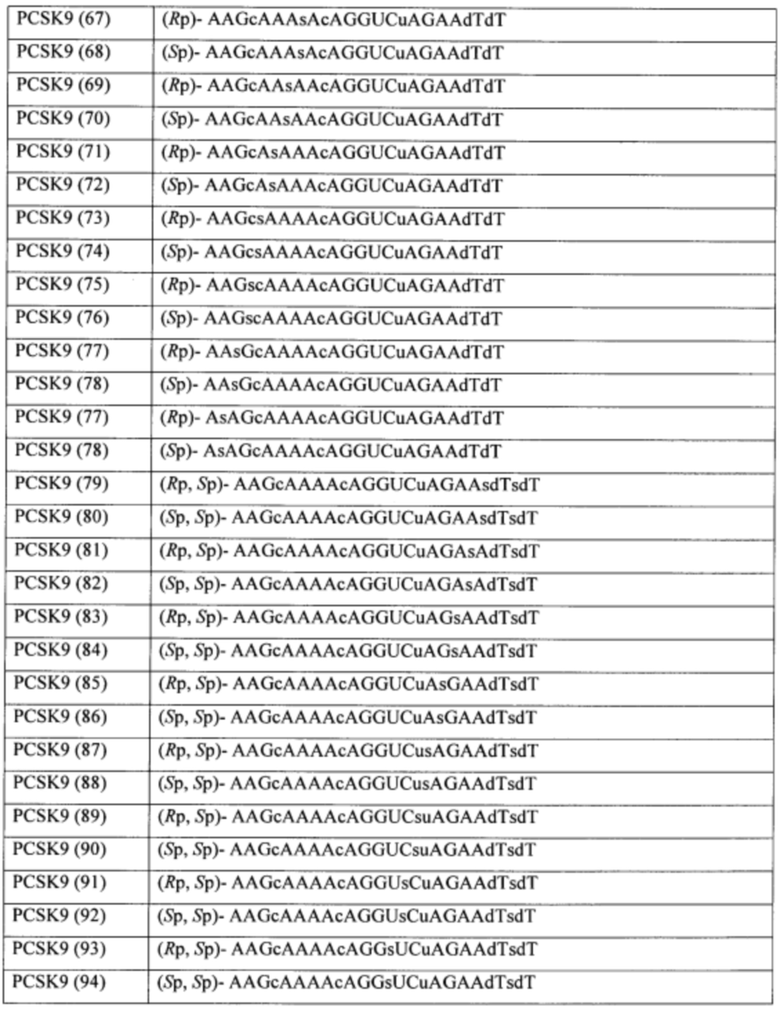
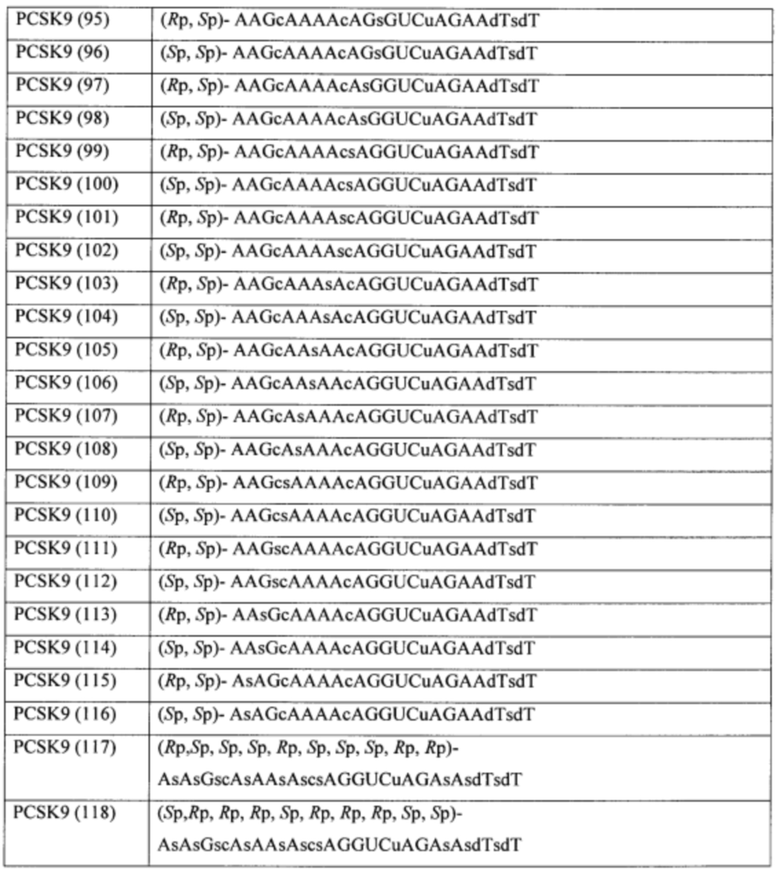
Примечание: строчные буквы представляют собой остатки 2'-ОМе РНК; заглавные буквы представляют собой остатки РНК; d = остатки 2'-дезокси и "s" обозначает фосфоротиоатный фрагмент.
Пример 3. Стереочистые антисмысловые аналоги FOXO-1.
Рациональный дизайн - антисмысловые композиции олигонуклеотидов с контролируемой хиральностью
Беспрецедентная нуклеазная стабильность, определенная in vivo и на модели гомогената целой печени крысы, хиральной фосфоротиоатной межнуклеотидной линкерной группы в конфигурации Sp применяется в новом дизайне новых типов субстратных гэпмеров РНКазы Н, в результате чего внешние боковые поверхности состоят из немодифицированной ДНК и внутреннее ядро с зазором модифицируется посредством 2' химических модификаций (2'ОМе, 2'МОЕ, 2'LNA, 2'F и т.д.). В конечном счете этот дизайн распространяется на терапевтические олигонуклеотиды с полностью немодифицированной ДНК, причем тщательный хиральный контроль фосфоротиоатного остова придает желаемые фармакологические свойства терапевтическому олигонуклеотиду РНКазе Н.
Также было использовано применение триплет-фосфатного повторяющегося мотива, разработанного после изучения кристаллической структуры человеческой РНКазы Н. Кристаллическая структура РНКазы Н была ранее опубликована (Structure of Human RNase H1 Complexed with an RNA/DNA Hybrid: Insight into HIV Reverse Transcription, Nowotny et al., Molecular Cell, Volume 28, Issue 2, 264-276, 2007, файл pdf: 2 qkb). Помимо всего прочего, настоящее изобретение признает важность стереохимии межнуклеотидных линкерных групп олигонуклеотидов, например, в установках согласно настоящему раскрытию. При выполнении анализа in silico с этой структурой с использованием программы Pymol, заявитель обнаружил, что фосфат-связывающий карман РНКазы HI человека образует полярные контакты с тремя смежными фосфатами образовавшей комплекс ДНК и взаимодействует преимущественно с Pro-R/Pro-R/Pro-S (или с Pro-S/Pro-S/Pro-R) соответствующими атомами кислорода каждого из этих трех фосфатов. На основании этого наблюдения авторы настоящего изобретения разработали две хиральные архитектуры с повторяющимися триплетными фосфоротиоатными (RRS) и (SSR) мотивами в виде субстратов РНКазы Н. Заявитель также разработал другие стереохимические профили межнуклеотидных линкерных групп. Как показывают предложенные в данном описании иллюстративные результаты, предложенные композиции олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида, которые содержат некоторые профили межнуклеотидных линкерных групп остова (профили хиральных центров остова), обеспечивают значительно повышенную активность и/или кинетику. Среди прочего, последовательность хиральных центров остова 5'-RSS-3' представляет собой особенно применимую и обеспечивает неожиданные результаты, как описано в настоящем раскрытии.
Сочетание остова с повышенной Sp хиральностью (для ферментативной стабильности и других фармакологически выгодных свойств) и (RRS) или (SSR) повторяющихся триплетных хиральных мотивов остова (для усиления свойства в качестве субстрата РНКазы Н) также используется в новых дизайнах; "S" представляет собой фосфоротиоатную линкерную группу в конфигурации Sp и "R" представляет собой фосфоротиоатную линкерную группу в конфигурации Rp.
Еще один альтернативный дизайн основан на увеличенном количестве хирального фосфоротиоатного остова в Sp-конфигурации в расширенных повторяющихся мотивах, таких как:
(SSSR)n, SR(SSSR)n, SSR(SSSR)n, SSR(SSSR)n;
(SSSSR)n, SR(SSSSR)n, SSR(SSSSR)n, SSR(SSSSR)n, SSSR(SSSSR)n;
(SSSSSR)n; SR(SSSSSR)n, SSR(SSSSSR)n, SSR(SSSSSR)n, SSSR(SSSSSR)n, SSSSR(SSSSSR)n и т.д., где n=0-50, в зависимости от количества соответствующих межнуклеотидных линкерных групп; "S" представляет собой фосфоротиоатную линкерную группу в конфигурации Sp и "R" представляет собой фосфоротиоатную линкерную группу в конфигурации Rp. Согласно некоторым вариантам осуществления n равно 0. Согласно некоторым вариантам осуществления R составляет 1-50. Согласно некоторым вариантам осуществления R равно 1. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предложенной композиции олигонуклеотидов с контролируемой хиральностью содержит описанный в настоящем документе мотив. Согласно некоторым вариантам осуществления мотив находится в области сердцевины. Согласно некоторым вариантам осуществления n равно 0. Согласно некоторым вариантам осуществления R составляет 1-50. Согласно некоторым вариантам осуществления R равно 1. Согласно некоторым вариантам осуществления n равно 2. Согласно некоторым вариантам осуществления n равно 3. Согласно некоторым вариантам осуществления n равно 4. Согласно некоторым вариантам осуществления n равно 5.
Еще один альтернативный дизайн основан на "инвертированном" архитектурном дизайне стерео остова («стереоинвертные-меры»). Они являются результатом позиционирования стереохимии хирального фосфоротиоата инвертированным способом, воздействуя на некоторые Sp-богатые мотивы на 5' и 3'-конце олигонуклеотида, а также на среднюю часть олигонуклеотида, и имеют повторяющиеся мотивы стереохимии, расположенные инвертированным способом с обеих сторон, такие как:
SS(SSR)n(SSS)(RSS)nSS;
SS(SSR)n(SRS)(RSS)nSS;
SS(SSR)n(SSR)(RSS)nSS;
SS(SSR)n(RSS)(RSS)nSS;
SS(RSS)n(SSS)(SSR)nSS;
SS(RSS)n(SRS)(SSR)nSS;
SS(RSS)n(SSR)(SSR)nSS;
SS(RSS)n(RSS)(SSR)nSS и т.д.,
где n=0-50, в зависимости от количества соответствующих межнуклеотидных линкерных групп; "S" представляет собой фосфоротиоатную линкерную группу в конфигурации Sp и "R" представляет собой фосфоротиоатную линкерную группу в конфигурации Rp. Согласно некоторым вариантам осуществления общий профиль хиральных центров остова предложенной композиции олигонуклеотидов с контролируемой хиральностью содержит описанный в настоящем документе мотив. Согласно некоторым вариантам осуществления мотив находится в области сердцевины. Согласно некоторым вариантам осуществления n равно 0. Согласно некоторым вариантам осуществления n равно 1. Согласно некоторым вариантам осуществления n составляет 1-50. Согласно некоторым вариантам осуществления n равно 2. Согласно некоторым вариантам осуществления n равно 3. Согласно некоторым вариантам осуществления n равно 4. Согласно некоторым вариантам осуществления n равно 5.
Начальный скрининг

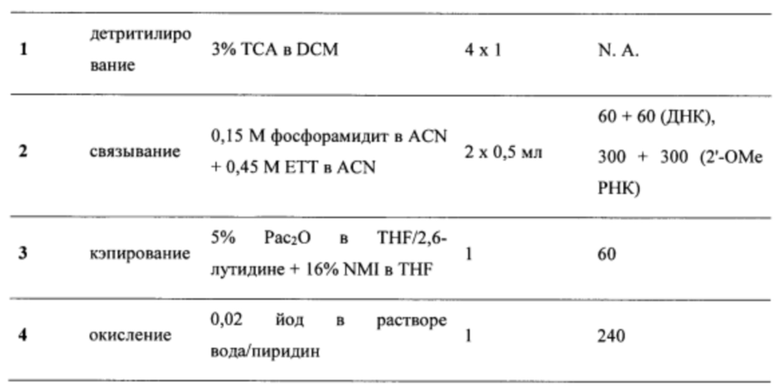
Стереослучайные олигонуклеотиды PS, характеризующиеся дизайном ДНК-2'-ОМе-ДНК (7-6-7)


Биологические данные in vitro в клетках HepG2 для начального дизайна ДНК-2'-ОМе-ДНК (7-6-7): (заглавная буква d) = ДНК; строчные буквы = 2'-ОМе; s = Фосфоротиоат

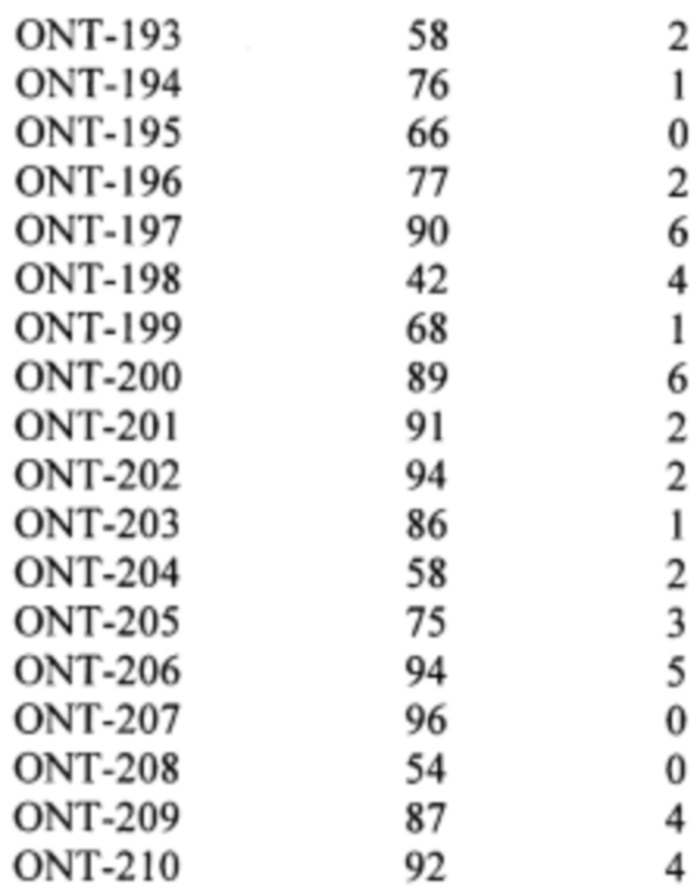


Стереослучайные олигонуклеотиды PS, характеризующиеся дизайном 2'-ОМе-ДНК-2'-ОМе (3-14-3): (заглавная буква d) = ДНК; строчные буквы - 2'-ОМе; s = фосфоротиоат


Биологические данные in vitro в клетках HepG2 для дизайна 2'-ОМе-ДНК-2'-ОМе (3-14-3)

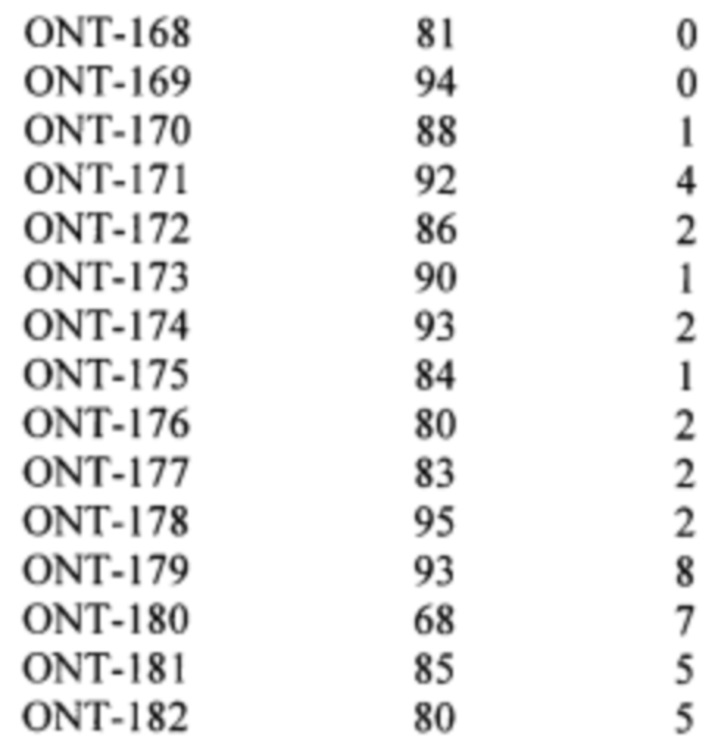


Выделение попаданий:

Вторичный скрининг. Химический и стереохимический скрининг
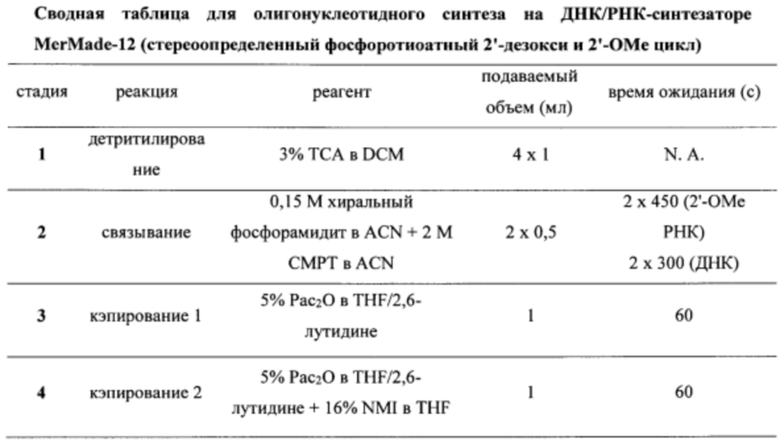
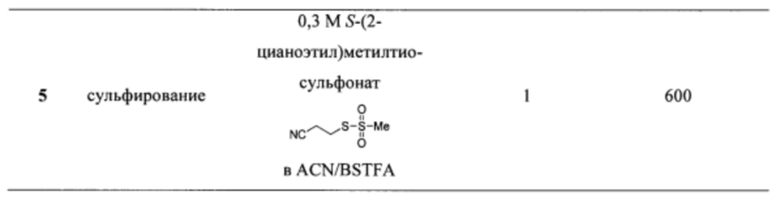
Примеры, применяемые на последовательностях попаданий FOXO1
Примеры включают, но не ограничиваются этим:


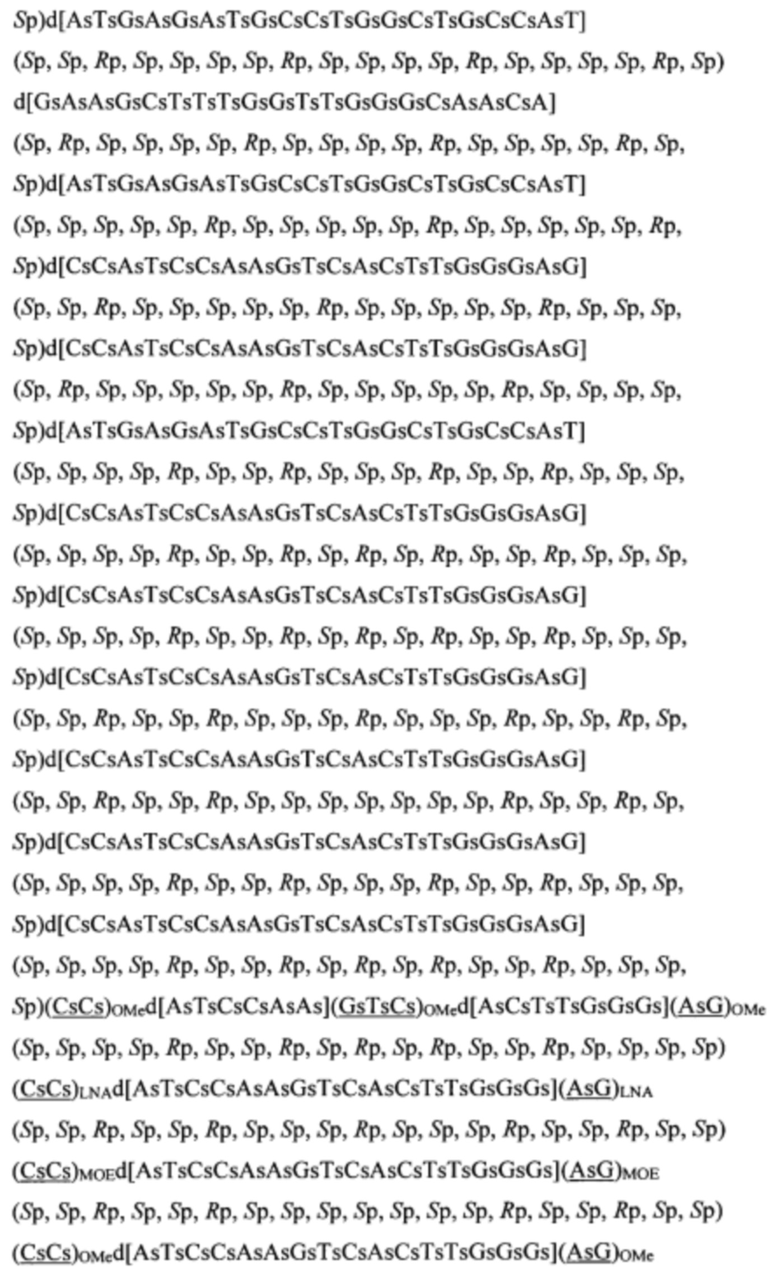
Пример 4. Подавление полимера нуклеиновой кислоты
Кроме всего прочего, настоящее раскрытие предусматривает композиции олигонуклеотидов с контролируемой хиральностью и способы их применения, которые обеспечивают неожиданные результаты, когда, например, используются для подавления полимеров нуклеиновых кислот путем, в некоторых случаях, расщепления таких полимеров нуклеиновых кислот. Примеры включают, но не ограничиваются ими, представленные в настоящем документе.
Анализ РНКазы Н
Скорость расщепления полимеров нуклеиновых кислот с помощью нуклеаз, например, РНК с помощью РНКазы Н, имеет важное значение в отношении использования олигонуклеотидов в терапевтических технологиях, таких как антисмысловая технология. С помощью своего анализа авторы настоящего изобретения исследовали скорости расщепления и анализировали метаболиты для композиций олигонуклеотидов с контролируемой хиральностью определенных типов олигонуклеотида (P-диастереомеры), когда олигонуклеотиды определенных типов олигонуклеотида связаны с комплементарной РНК. Результаты ниже также иллюстрируют важность профилей расщепления, распознаваемых в соответствии с настоящим раскрытием.
РНКаза Н, используемая в настоящем документе, представляет собой повсеместно экспрессируемую эндонуклеазу, которая гидролизует цепь РНК гибрида РНК/ДНК. Она играет важную роль в механизме действия антисмысловых олигонуклеотидов. Согласно некоторым вариантам осуществления скорость расщепления РНКазы Н значительно снижается, когда субстрат РНК структурирован (Lima, W.F., Venkatraman, М., Crooke, S.T. The Influence of Antisense Oligonucleotide-induced RNA Structure on Escherichia coli RNase H1 Activity The Journal Of Biological Chemistry 272, No. 29, 18191-18199, (1997)). Кроме того, дизайны 2'-MOE гэпмера (5-10-5) предлагают более высокие аффинности к РНК-мишеням, ведущие к минимальному обороту антисмысловой цепи. Наличие 2'-МОЕ модификаций в крыльях также уменьшает количество сайтов расщепления РНКазы Н.
Для изучения скорости расщепления РНК, настоящее раскрытие предусматривает простой анализ, чтобы количественно определить длину РНК, остающейся после инкубации с РНКазой Н. Предложенный способ, помимо всего прочего, предусматривает относительные скорости расщепления РНКазой Н стереослучайных 2'-модифицированных гэпмеров, стереослучайных композиций олигонуклеотидов ДНК и хирально-чистых Р-диастереомеров (композиции олигонуклеотидов с контролируемой хиральностью соответствующего типа олигонуклеотида) для различных олигомеров для различных мишеней. Изменение стереохимии в 2'-модифицированных областях и сердцевине ДНК содержит информацию относительно того, как стереохимия в этих областях влияет на взаимодействие РНКазы Н со своими субстратам. Реакционные смеси РНКазы Н в различные моменты времени анализировали с помощью ЖХ-МС, чтобы определить профиль расщепления. Настоящее раскрытие, кроме всего прочего, предусматривает полимер нуклеиновой кислоты, например, РНК, скорости расщепления и профили расщепления (карты), которые имеют решающее значение для разработки стереохимических архитектур нуклеиновых кислот для оптимальной активности, например, антисмысловой активности.
Оборудование:
ВЭЖХ Альянс, 2489 - TUV, 2695Е - оснащенный автосамплером
Кэри 100 (Agilent Technologies)
Способы:
Получение дуплексов ДНК/РНК: Концентрации олигонуклеотидов определяли путем измерения оптической плотности в воде при 260 нм. Дуплексы ДНК/РНК получали смешиванием эквимолярных растворов олигонуклеотидов с каждой концентрацией цепей 10 мкМ. Смеси нагревали при 90°С в течение 2 минут на водяной бане и медленно охлаждали в течение нескольких часов.
Экспрессия и очистка белка РНКазы Н человека: Клон РНКазы НС человека получали из лаборатории профессора Вэй Янга в NIH Bethesda. Протокол для получения этой РНКазы НС человека (остатки 136-286) был описан (Nowotny, М. et al. Structure of Human RNase H1 Complexed with an RNA/DNA Hybrid: Insight into HIV Reverse Transcription. Molecular Cell 28, 264-276, (2007). Экспрессию белка выполняли по следующему опубликованному протоколу, за тем исключением, что полученный белок имел N-концевой тег His6. Клетки BL21(DE3) E.coli в среде LB использовали для экспрессии белка. Клетки выращивали при температуре 37°С до тех пор, пока OD600 достигала примерно 0,7. Культуры затем охлаждали и добавляли 0,4 мМ IPTG, чтобы индуцировать экспрессию белка в течение ночи при 16°С. Экстракт E.coli готовили путем обработки ультразвуком в буфере А (40 мМ NaH2PO4 (рН 7,0), 1 М NaCl, 5% глицерина, 2,8 мМ β-меркаптоэтанола и 10 мМ имидазола) с добавлением ингибиторов протеазы (Sigma-Aldrich). Экстракт очищали с помощью Ni-аффинной колонки с использованием буфера А плюс 60 мМ имидазола. Белок элюировали с линейным градиентом от 60 до 300 мМ имидазола. Пик белка собирали и дополнительно очищали на колонке Mono S (GE Healthcare) с градиентом NaCl 100 мМ - 500 мМ в буфере В. Фракции, содержащие РНКазу НС, концентрировали до 0,3 мг/мл в буфере для хранения (20 мМ HEPES (рН 7,0), 100 мМ NaCl, 5% глицерина, 0,5 мМ ЭДТА, 2 мМ ДТТ) и хранили при -20°С. Концентрация фермента 0,3 мг/мл соответствует 17,4 мкМ на основании его коэффициента экстинкции (32095 см-1М-1) и MW (18963,3 единиц Да).
Анализ РНКазы Н: В 96-луночный планшет к 25 мкл дуплекса ДНК/РНК (10 мкМ) добавляли 5 мкл 10-кратного буфера РНКазы Н, а затем 15 мкл воды. Смесь инкубировали при 37°С в течение нескольких минут, а затем 5 мкл 0,1 мкМ исходного раствора фермента добавляли, чтобы получить общий объем 50 мкл с конечной концентрацией субстрата/фермента 5 мкМ/0,01 мкМ (500:1) и дополнительно инкубировали при 37°С. Были изучены различные соотношения дуплекса ДНК/РНК: белка РНКазы Н с использованием этих условий, чтобы найти оптимальное соотношение для изучения кинетики. Реакции останавливали в различные моменты времени с использованием 10 мкл раствора динатрия ЭДТА в воде с концентрацией 500 мМ. В момент времени ноль мин ЭДТА добавляли к реакционной смеси перед добавлением фермента. Контроль проводили для того, чтобы ЭДТА смог успешно ингибировать активность фермента полностью. После того, как все реакции останавливали, 10 мкл каждой реакционной смеси вводили в аналитическую колонку ВЭЖХ (XBridge С18, 3,5 мкм, 4,6×150 мм, Waters Part # 186003034). Kcat/Km может быть измерена с помощью ряда способов, таких как анализ зависимой РНКазы Н посредством FRET (способ резонансного переноса энергии флуоресценции) с использованием двойной меченой РНК и контроля с помощью SpectraMax.
Протокол твердофазной экстракция для подготовки проб для жидкостной хроматомасс-спектрометрии: 96-луночный планшет (Waters, номер в каталоге 186002321) использовали для очистки реакционной смеси РНКазы Н перед запуском жидкостной хроматомасс-спектрометрии. 500 мкл ацетонитрила, а затем воду использовали для уравновешивания планшета при умеренном вакууме с помощью коллектора (Millipore, номер в каталоге МСВ MHTS00). Была принята предосторожность, чтобы не позволить планшету высохнуть. 50-100 мкл реакционной смеси РНКазы Н загружали в каждую лунку с последующим добавлением водных отмываний (2 мл) при умеренном вакууме. 2×500 мкл 70% ACN/воды использовали для восстановления образца. Восстановленные образцы переносили в центрифужные пробирки объемом 2 мл и концентрировали до сухого состояния в speed vac. Каждый сухой образец восстанавливали в 100 мкл воды и 10 мкл вносили на Acquity UPLC@OCT C18 1,7 мкм, 2,1×50 мм (номер в каталоге 186003949) для анализа посредством жидкостной хроматомасс-спектрометрии.
Для масс-спектрометрического анализа реакционные смеси после гашения очищали с использованием 96-луночного планшета C18 (Waters). Олигомеры элюировали в 70% смеси ацетонитрила/воды. Ацетонитрил выпаривали с помощью speedvac и полученный остаток восстанавливали в воде для инъекций.
Элюент А=50 мМ триэтилацетат аммония
Элюент В = Ацетонитрил
Температура колонки = 60°С
УФ регистрировали при 254 нм и 280 нм
Градиентный метод ОФ-ВЭЖХ
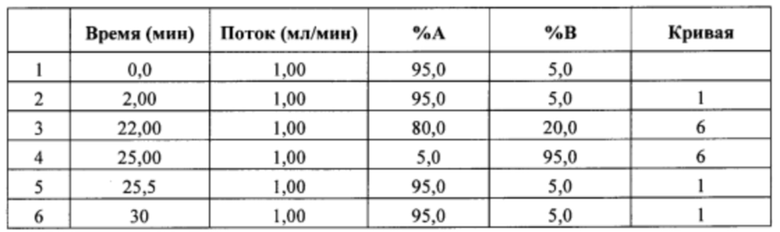
На хроматограммах ВЭЖХ площади пиков, соответствующие полноразмерному олигомеру РНК (ONT-28), объединяли, нормировали с использованием пика ДНК и наносили на график в зависимости от времени (фиг. 8). ONT-87 продемонстрировал превосходное расщепление для комплементарной РНК, когда находится в дуплексной форме, по сравнению с другими продуктами-кандидатами и мипомерсеном. Так как все диастереоизомеры в этой панели имеют 2'-МОЕ модифицированные крылья, которые не активируют фермент РНКазу Н, без намерения ограничиваться теорией заявитель отмечает, что активность, вероятно, продиктована стереохимией в сердцевине ДНК. Гетеродуплексы с ONT-77 до ONT-81, включая мипомерсен в антисмысловой цепи, показывают очень схожие показатели расщепления РНК. ONT-89 с чередующейся стереохимией Sp/Rp показал наименьшую активность в исследуемые сроки при исследуемых условиях. Среди исследованных олигонуклеотидов с модификациями МОЕ, единицы ONT-87 и ONT-88 в антисмысловой цепи показали увеличенную активность по сравнению с остальными гетеродуплексами. В частности, ONT-87 показал неожиданно высокую скорость расщепления и неожиданно низкое содержание оставшейся РНК-мишени. Дополнительные иллюстративные данные были показаны на фиг. 6 и фиг. 24.
Анализ олигонуклеотидной трансфекции In Vitro: Анализы трансфекции широко известны и практикуются специалистами в данной области техники. Пример протокола описан в данном документе. Нер3В клетки обратно трансфицируют с липофектамином 2000 (Life Technologies, номер в каталоге 11668-019) при плотности 18×103 клеток/лунку в 96-луночных планшетах с использованием протокола производителя. Для получения кривых зависимости эффекта от дозы используют восемь 1/3 серийных разведений, начиная от 60-100 нМ. 25 мкл 6-кратной концентрации олигонуклеотида смешивают с приготовленной смесью 0,4 мкл липофектамина 2000 с 25 мкл безсывороточной среды OPTI-MEM (Gibco, номер в каталоге 31985-062) на лунку. После 20-минутной инкубации 100 мкл 180×103 клеток/мл, суспендированных в 10% FBS в среде для культивирования клеток DMEM (Gibco, № в каталоге 11965-092), добавляют, чтобы довести конечный объем до 150 мкл на лунку. Через 24-48 часов после трансфекции клетки Нер3В лизируют путем добавления 75 мкл лизирующей смеси с 0,5 мг/мл протеиназы К с использованием набора обработки образцов QuantiGene для культивированных клеток (Affymetrix, №в каталоге QS0103). Уровни экспрессии мРНК-мишени и мРНК GAPDH в лизатах клеток измеряют с использованием набора для анализа Affymetrix QuantiGene 2.0 (№ в каталоге QS0011) в соответствии с протоколом производителя. Экспрессию мРНК-мишени нормировали к экспрессии мРНК GAPDH из того же образца; и относительные уровни мишени/GAPDH сравнивают с трансфекциями с использованием только липофектамина 2000 (без олигонуклеотида) в качестве контроля. Кривые зависимости от дозы получают с помощью GraphPad Prism 6 с использованием логарифма нелинейной регрессии (ингибитора) по сравнению с кривой отклика, установленной с переменным наклоном (4 параметра). Для примеров результатов смотрите фиг. 24, фиг. 27 и фиг. 29.
Пример 5. Предусмотренные композиции и способы обеспечивают контроль профилей расщепления
В настоящем раскрытии неожиданно обнаружили, что профиль стереохимии межнуклеотидных линкерных групп оказывает неожиданное воздействие на профили расщепления полимеров нуклеиновых кислот. Изменяя общие профили хиральных центров остова композиций олигонуклеотидов с контролируемой хиральностью, количества сайтов расщепления, процент расщепления в сайте расщепления и/или положения сайтов расщепления могут быть, на удивление, изменены, как самостоятельно, так и в комбинации. Как описано в примере в данном описании предложенные композиции и способы могут обеспечить контроль над профилями расщепления полимеров нуклеиновых кислот.
Используя аналогичные условия анализа исследовали различные композиции олигонуклеотидов с контролируемой хиральностью различных типов олигонуклеотида. Примеры профилей расщепления последовательности РНК-мишени представлены на фиг. 9. Определенный профиль хиральных центров остова, таких как в ONT-87 и ONT-154, на удивление производит только один сайт расщепления в целевой последовательности. Более того, неожиданно обнаружено, что олигонуклеотиды с едиными сайтом расщепления, например, ONT-87 и ONT-154, обеспечивают неожиданно высокую скорость расщепления и низкое содержание оставшегося полимера-мишени нуклеиновой кислоты. Смотрите также фиг. 8, фиг. 10 и фиг. 11.
Пример 6. Пример расщепления мРНК FOXO1
Композиции олигонуклеотидов, направленные на разные области мРНК FOX01, исследовали в анализах расщепления, как это описано выше. В каждом случае, было показано, что композиции олигонуклеотидов с контролируемой хиральностью способны обеспечить измененный профиль расщепления по отношению к эталонным профилям расщепления, в отличие от композиций олигонуклеотидов с неконтролируемой хиральностью, характеризующихся той же одинаковой последовательностью оснований и длиной. Для примера результатов смотрите фиг. 10 и фиг. 11. Как показано на фиг. 12, иллюстративные композиции олигонуклеотидов с контролируемой хиральностью обеспечивают как значительно большую скорость расщепления, так и неожиданно низкое содержание остальных субстратов по сравнению с эталонными композициями олигонуклеотидов с неконтролируемой хиральностью. Согласно некоторым вариантам осуществления, как показано на фиг. 11, сайты расщепления связаны с последовательностью хирального центра остова RpSpSp. Согласно некоторым вариантам осуществления сайты расщепления представляют собой две пары оснований выше против хода транскрипции от RpSpSp.
Примеры композиций олигонуклеотидов перечислены ниже.
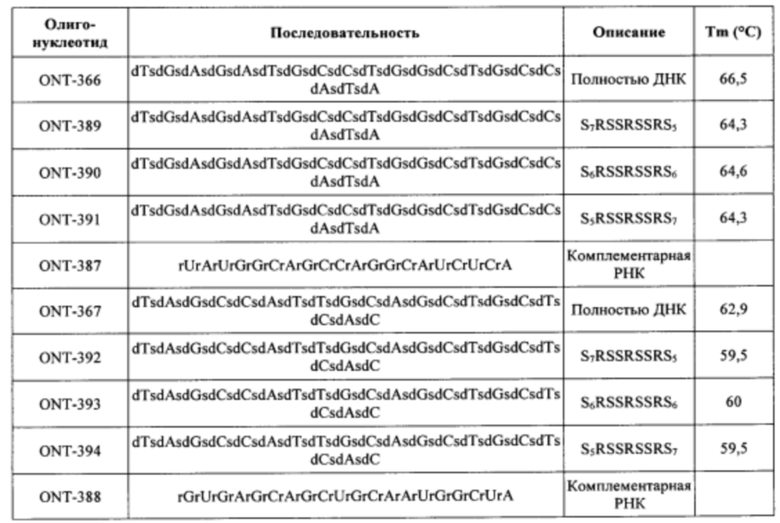
Пример 7. Примеры композиций олигонуклеотидов с контролируемой хиральностью обеспечивают более высокий оборот
В тех случаях, когда Tm расщепленных фрагментов полимеров нуклеиновых кислот, например, фрагментов РНК, до олигонуклеотидов больше физиологической температуры, диссоциация продукта может быть ингибирована и олигонуклеотиды могут быть не в состоянии диссоциировать и находить другие нити-мишени для образования дуплексов и вызывания расщепления нитей-мишеней. Tm ONT-316 (5-10-5 2'-МОЕ гэпмер) до комплементарной РНК составляет 76°С. После разреза или нескольких разрезов в последовательности РНК, комплементарной олигонуклеотидам, фрагменты 2'-МОЕ могут оставаться связанными с РНК и, следовательно, не могут вызывать расщепление других молекул-мишеней. Термические температуры плавления нитей ДНК, как правило, гораздо ниже дуплексной РНК, например, ONT-367 (63°С) и ONT-392 60°С). Кроме того, термическая стабильность в последовательностях ДНК часто относительно равномерно распределена по сравнению с 2'-МОЕ модифицированными олигонуклеотидами. Согласно некоторым вариантам осуществления олигонуклеотиды в предусмотренных композициях олигонуклеотидов с контролируемой хиральностью не содержат 2'-модификации, такие как 2'-МОЕ. Согласно некоторым вариантам осуществления олигонуклеотиды в предусмотренных композициях олигонуклеотидов с контролируемой хиральностью, которые не содержат 2'-модификации, такие как 2'-МОЕ, более легко диссоциируют из фрагментов расщепления полимеров нуклеиновых кислот и имеют более высокий оборот, чем олигонуклеотиды, имеющие 2'-модификации, такие как 2'-МОЕ. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает все дизайны ДНК, в которых олигонуклеотиды не имеют 2'-модификации. Согласно некоторым вариантам осуществления предусмотрены композиции олигонуклеотидов с контролируемой хиральностью, в которых олигонуклеотиды, не имеющие 2'-модификации, обеспечивают более высокий оборот нуклеазы, такой как РНКаза Н. Согласно некоторым вариантам осуществления после расщепления РНКаза Н диссоциирует более легко из дуплекса, образованного РНК и олигонуклеотидами предложенных композиций олигонуклеотидов с контролируемой хиральностью. Используя аналогичные протоколы, как описано выше, две иллюстративные композиции олигонуклеотидов с контролируемой хиральностью типа олигонуклеотида ONT-367 и ONT-392 действительно показали более высокий оборот, чем скорость оборота эталонных композиций олигонуклеотидов с неконтролируемой хиральностью (фиг. 13).
Пример 8. Пример расщепления мРНК FOXO1
Как проиллюстрировано на фиг. 14, композиции олигонуклеотидов с контролируемой хиральностью и способы их получения в настоящем описании могут обеспечить контролируемое расщепление полимеров нуклеиновых кислот. Согласно некоторым вариантам осуществления композиции олигонуклеотидов с контролируемой хиральностью согласно настоящему раскрытию производят измененный профиль расщепления с точки зрения числа сайтов расщепления, локализации сайтов расщепления и/или относительного процента сайтов расщепления. Согласно некоторым вариантам осуществления, как на примере ONT-401 и ONT-406, композиции олигонуклеотидов с контролируемой хиральностью обеспечивают единственный сайт расщепления.
Согласно некоторым вариантам осуществления был обнаружен только один компонент из расщепления РНК. Без намерения ограничиваться теорией заявитель отмечает, что такое наблюдение может быть связано с процессивной природой фермента РНКаза Н, который мог бы сделать несколько разрезов на том же дуплексе, что приводит к гораздо более коротким фрагментам 5'-ОН 3'-ОН.
Дополнительно исследовали дополнительные композиции олигонуклеотидов с контролируемой хиральностью. Как было описано выше, предложенные композиции олигонуклеотидов с контролируемой хиральностью обеспечивает неожиданные результаты, например, с точки зрения скорости расщепления и % РНК, остающейся в дуплексе ДНК/РНК. Смотрите фиг.15-17. Типовые аналитические данные представлены на фиг.18-20. Без намерения ограничиваться теорией заявитель отмечает, что согласно некоторым вариантам осуществления расщепление может происходить, как показано на фиг. 21. Следует отметить, что на фиг. 17 наблюдалось, что ONT-406 вызывает расщепление образовавшей дуплекс РНК со скоростью, немного превышающей таковую природного олигонуклеотида ДНК ONT-415, имеющего ту же самую последовательность оснований и длину. Заявитель отмечает, что композиции олигонуклеотидов с контролируемой хиральностью ONT-40 и другие композиции олигонуклеотидов с контролируемой хиральностью, предложенные в данном описании, имеют другие предпочтительные свойства, которые композиция ONT-415 не имеет, например, лучшие профили стабильности in vitro и/или in vivo. Дополнительные иллюстративные данные были представлены на фиг. 25. Кроме того, как будет понятно специалистам в данной области техники, иллюстративные данные, показанные на фиг. 26 и на фиг. 27, подтверждают, что предусмотренные иллюстративные композиции олигонуклеотидов с контролируемой хиральностью, особенно когда они разработаны таким образом, чтобы контролировать профили расщепления посредством профилей хиральных центров остова, приводили к гораздо лучшим результатам, чем эталонные композиции олигонуклеотидов, например, стереослучайная композиция олигонуклеотидов. Как проиллюстрировано на фиг. 26, контролируемые профили хиральных центров остова, среди прочего, могут избирательно увеличивать и/или уменьшать расщепление в существующем сайте расщепления при использовании олигонуклеотида ДНК или создавать совершенно новые сайты расщепления, которые не существуют, когда используется олигонуклеотид ДНК (смотрите фиг. 25, ONT-415). Согласно некоторым вариантам осуществления сайты расщепления из олигонуклеотида ДНК указывают на эндогенное предпочтение расщепления РНКазой Н. Как было подтверждено на фиг. 27, предложенные композиции олигонуклеотидов с контролируемой хиральностью способны модулировать скорость расщепления мишени. Согласно некоторым вариантам осуществления примерно 75% вариации в клеточной активности объясняется различиями в скорости расщепления, которые можно контролировать посредством профилей хиральных центров остова. Как предусмотрено в данной заявке, дополнительные структурные особенности, такие как модификации оснований и их профили, модификации Сахаров и их профили, модификации межнуклеотидных линкерных групп и их профили и/или любые их комбинации, могут быть объединены с профилями хиральных центров остова, чтобы обеспечить желаемые олигонуклеотидные свойства.
Пример 9. Пример аллельспецифического подавления mHTT
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает композиции олигонуклеотидов с контролируемой хиральностью и способы их применения для аллельспецифического подавления транскриптов от одного конкретного аллеля с селективностью над другими. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает аллельспецифическое подавление mHTT.
На фиг. 22 показаны примеры композиций олигонуклеотидов с контролируемой хиральностью, которые специфически подавляют транскрипты от одного аллеля, но не другие. Олигонуклеотиды 451 и 452 исследовали с транскриптами, полученными от обоих аллелей, примеры которых приведены, с использованием описанных выше биохимических анализов. Аллельспецифическое подавление также исследовали в клетках и на животных моделях с использованием аналогичных процедур, как описано в Hohjoh, Pharmaceuticals 2013, 6, 522-535; публикация заявки на патент США US 2013/0197061 и ∅stergaard et al., Nucleic Acids Research, 2013, 41(21), 9634-9650. Во всех случаях транскрипты от целевого аллеля селективно подавляются по сравнению с другими от других аллелей. Как будет понятно специалистам в данной области техники, иллюстративные данные, изображенные на фиг. 22, подтверждают, что предусмотренные иллюстративные композиции олигонуклеотидов с контролируемой хиральностью, особенно, когда разработаны таким образом, чтобы контролировать профили расщепления через стереохимию, производили гораздо лучшие результаты, чем эталонные композиции олигонуклеотидов, в данном случае, стереослучайная композиция олигонуклеотидов. Как было подтверждено на фиг. 22, профили хиральных центров остова могут резко изменять профили расщепления (фиг. 22 С-Е), а также профили стереохимии могут быть использованы для размещения сайта расщепления в сайте ошибочно спаренных оснований (фиг. 22 С-Е), и/или могут значительно повышать селективность между мутантом и диким типом (фиг. 22 G-H). Согласно некоторым вариантам осуществления композиции олигонуклеотидов с контролируемой хиральностью инкубируют с РНК дикого типа и мутантной РНК мишени и оба дуплекса инкубировали с РНКазой Н.
Аллель хантингтина Tm

Пример 10. Иллюстративное аллельспецифическое подавление FOXO1
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает аллельспецифическое подавление FOXO1.
На фиг. 23 показаны иллюстративные композиции олигонуклеотидов с контролируемой хиральностью, которые специфически подавляют транскрипты от одного аллеля, но не другие. Олигонуклеотиды ONT-400, ONT-402 и ONT-406 исследовали с транскриптами от обоих представленных в качестве примеров аллелей с использованием описанных выше биохимических анализов. Аллельспецифическое подавление также исследуется в клетках и на животных моделях с использованием аналогичных процедур, как описано в Hohjoh, Pharmaceuticals 2013, 6, 522-535; публикация заявки на патент США US 2013/0197061; ∅stergaard et al., Nucleic Acids Research 2013, 47(21), 9634-9650 и Jiang et al., Science 2013, 342, 111-114. Транскрипты целевого аллеля подавляются избирательно, по сравнению с теми, которые от других аллелей. В некоторых случаях синтезируются две РНК с ошибочно спаренными основаниями ONT-442 (A/G, положение 7) и ONT-443 (A/G, положение 13) из ONT-388 и образуют дуплексы с ONT-396 до ONT-414. Для получения скорости расщепления и карт расщепления проводят анализ РНКазы Н.
Пример 11. Определенные примеры олигонуклеотидов и композиций олигонуклеотидов
Стереослучайные олигонуклеотиды с различными 2'-заменами, направленными на три отдельные области мРНК FOXO1, с температурами плавления при образовании дуплексов с комплементарной РНК. Концентрация каждой нити составляла 1 мкМ в 1-кратном буфере PBS.

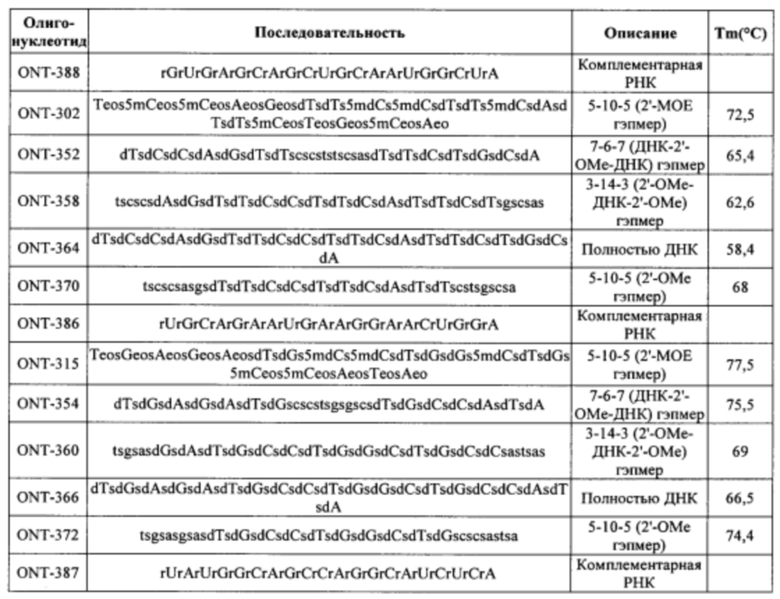
Дополнительные примеры стереослучайных композиций олигонуклеотидов представлены ниже.


Иллюстративные олигонуклеотиды РНК и ДНК представлены ниже.
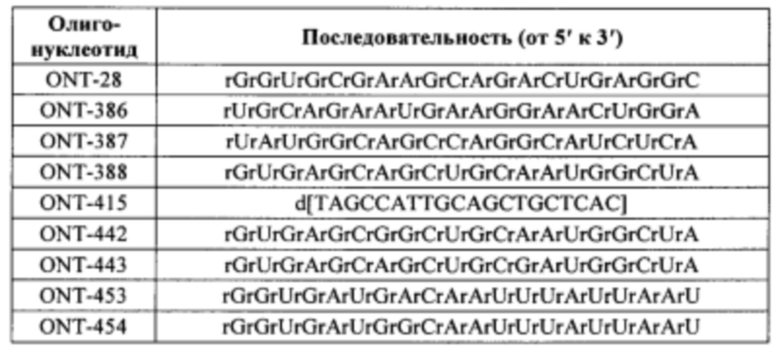
Примеры хирально-чистых олигонуклеотидов представлены ниже. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает соответствующие композиции олигонуклеотидов с контролируемой хиральностью каждого из следующих примеров олигонуклеотидов.

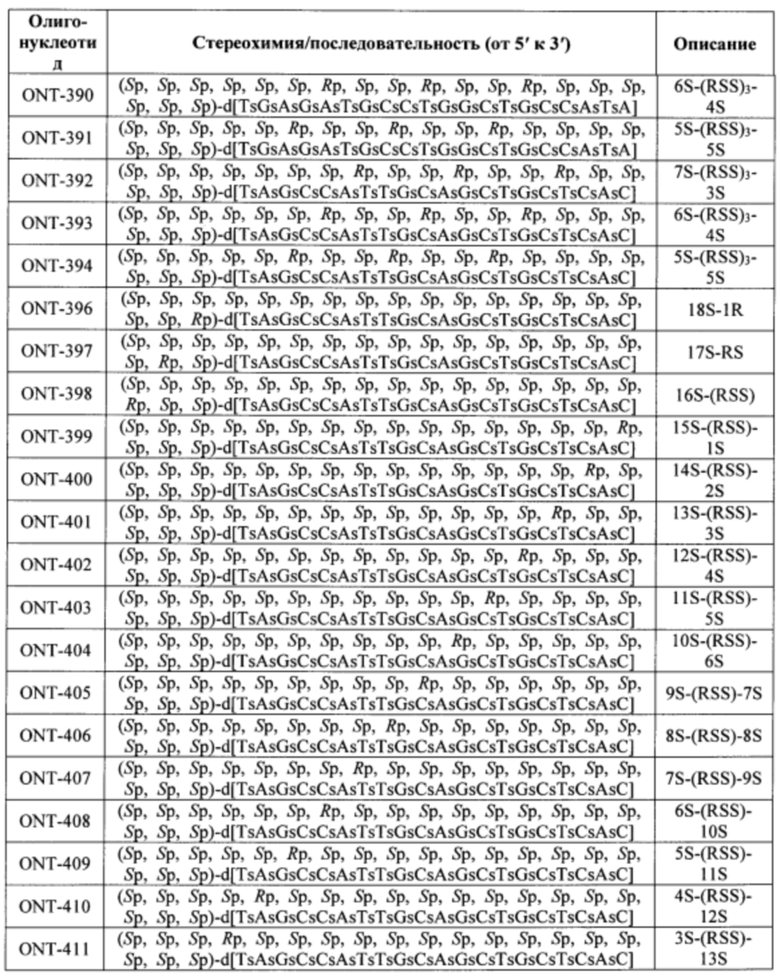
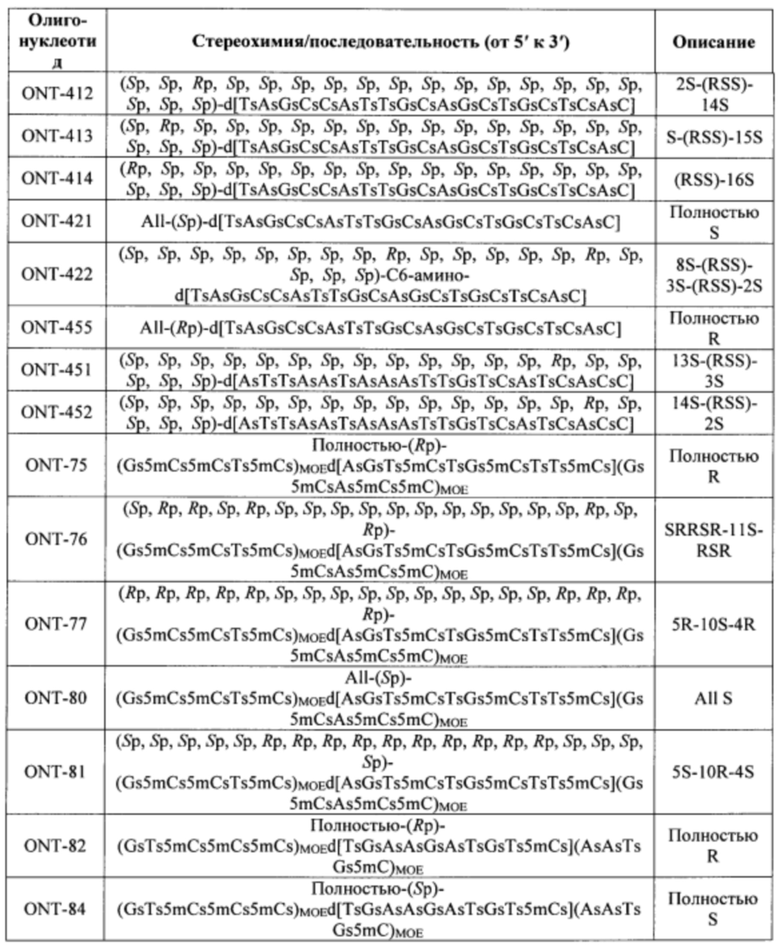
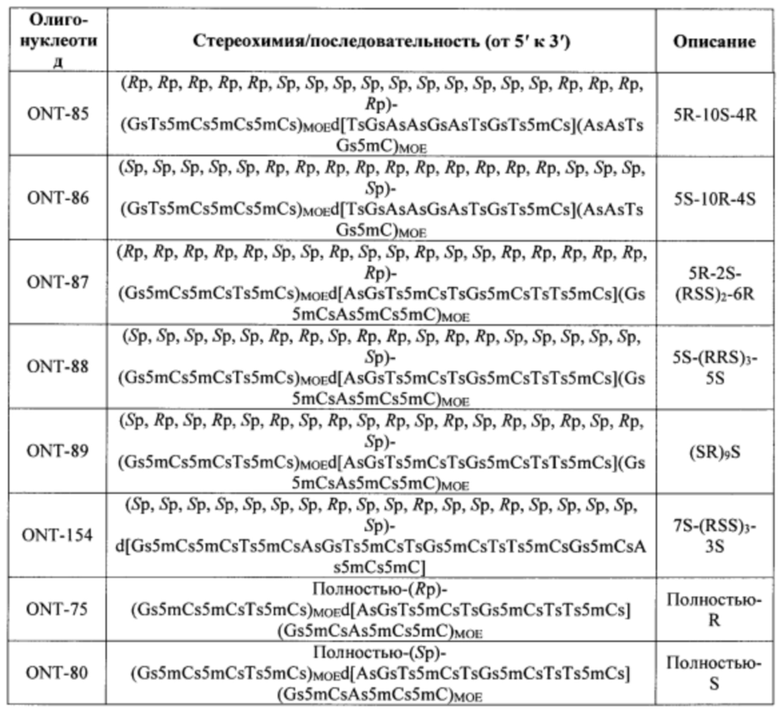
Дополнительные иллюстративные олигонуклеотиды, направленно воздействующие на FOXO1 с Tm, представлены ниже. Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает соответствующие композиции олигонуклеотидов с контролируемой хиральностью каждого из следующих иллюстративных олигонуклеотидов.


Пример 12. Пример дополнительного контролируемого расщепления предложенных композиций олигонуклеотидов с контролируемой хиральностью
Как будет понятно специалистам в данной области техники, иллюстративные данные, представленные на фиг. 26, подтверждают, что предусмотренные композиции олигонуклеотидов с контролируемой хиральностью и способы их применения обеспечивают неожиданные результаты по сравнению с эталонными композициями, такими как стереослучайные композиции олигонуклеотидов. Помимо всего прочего, композиции олигонуклеотидов с контролируемой хиральностью могут производить контролируемые профили расщепления, в том числе, но не ограничиваясь ими, контроль положений сайтов расщепления, количество сайтов расщепления и относительный процент расщепления сайтов расщепления. Смотрите также иллюстративные данные, представленные на фиг. 27.
Пример 13. Стабильность композиций олигонуклеотидов с контролируемой хиральностью
Как будет понятно специалистам в данной области техники, иллюстративные данные, показанные на фиг. 26, подтверждают, что стабильность композиций олигонуклеотидов с контролируемой хиральностью можно регулировать путем варьирования профилей хиральных центров остова. Для иллюстративных данных смотрите фиг. 7 и фиг. 28. Пример протокола для проведения эксперимента стабильности в сыворотке описан ниже.
Протокол: ДНК с Р-стереохимически чистыми PS (ONT-396-ONT-414 (единственная конфигурация Rp от 3'-конца к 5'-концу)), ДНК со стереослучайными PS (ONT-367), ДНК с PS в конфигурации полностью-Sp (ОНТ-421) и ДНК с PS в конфигурации полностью-Rp (ONT-455) инкубировали в крысиной сыворотке (Sigma, R9759) (0 ч и 48 ч) и анализировали с помощью ионообменной-ВЭЖХ.
Способ инкубации: 5 мкл 250 мкМ каждого из растворов ДНК и 45 мкл крысиной сыворотки смешивали и инкубировали при 37°С для каждой временной точки (0 и 48 часов). В каждую временную точку реакцию останавливали добавлением 25 мкл 150 мМ раствора ЭДТА, 30 мкл буфера для лизиса (erpicentre, MTC096H) и 3 мкл раствора протеиназы К (20 мг/мл). Смесь инкубировали при 60°С в течение 20 мин, а затем вносили 20 мкл смеси для ионообменной-ВЭЖХ и анализировали.
Инкубация контрольного образца: Готовили смесь из 5 мкл 250 мкМ каждого из растворов ДНК и 103 мкл 1-кратного PBS буфера и 20 мкл смеси анализировали с помощью ионообменной-ВЭЖХ в качестве контроля для проверки абсолютной количественной оценки.
Пример аналитического способа:
Ионообменная-ВЭЖХ
А: 10 мМ Трис НС1, 50% ACN (рН 8,0)
В: 10 мМ Трис НС1, 800 мМ NaCl, 50% ACN (рН 8,0)
С: Вода-ACN (1: 1, об/об)
Температура: 60°С
Колонка: DIONEX DNAPac PA-100, 250×4 мм
Градиент:
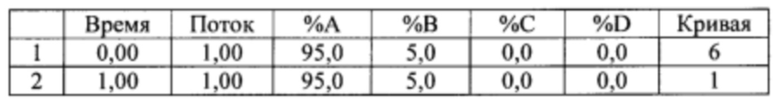
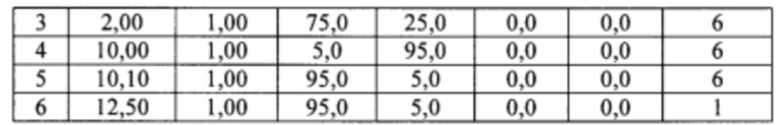
Отмывание:
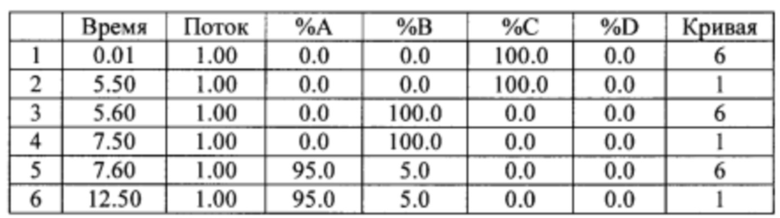
Температура колонки: 60°С
Промывание производили каждый раз после пробега образца.
Процент оставшейся ДНК PS рассчитывали путем анализа соотношения от 0 ч до 48 ч с использованием области интеграции ВЭЖХ-хроматограммы.
Пример 14. Примеры аналитических результатов (фиг. 19)
Распределение пиков на фиг. 19 (верхняя панель, M12-Exp11 B10, ONT-354, 30 мин.
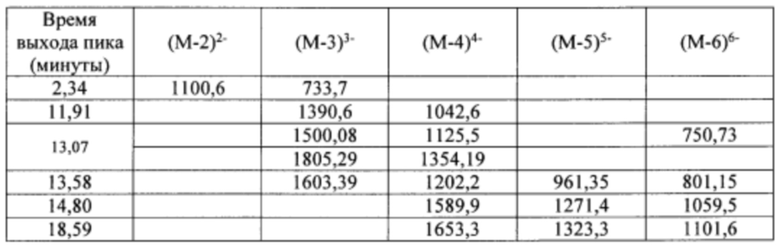
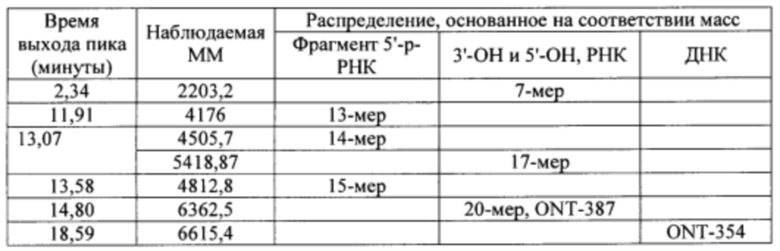
Распределение пиков на фиг. 19 (нижняя панель, М12-Ехр11 А10, ONT-315, 30 мин.
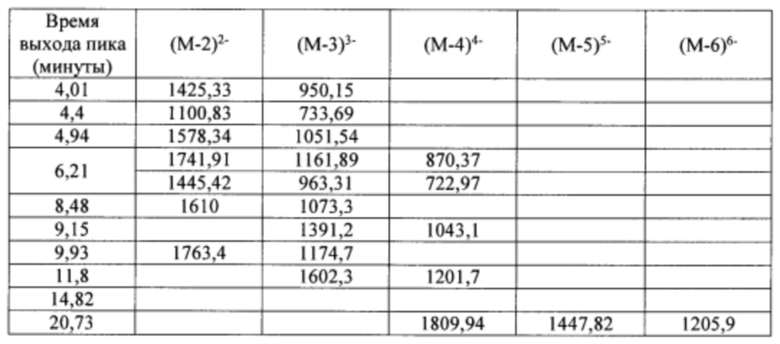
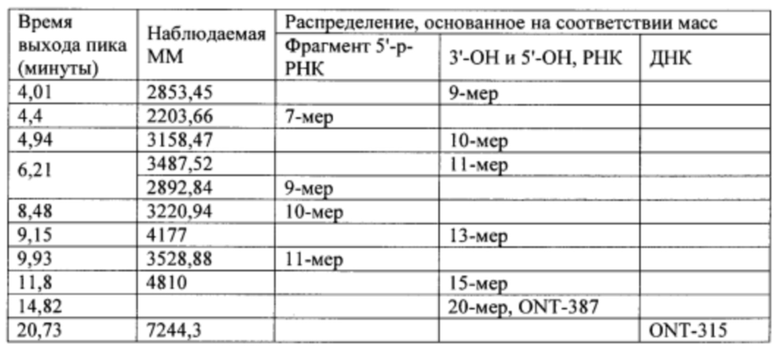
Пример 15. Иллюстративные аналитические результаты (фиг. 30)
Распределение пиков на фиг. 30 (верхняя панель, М12-Ехр11 D2, ONT-367, 30 мин.
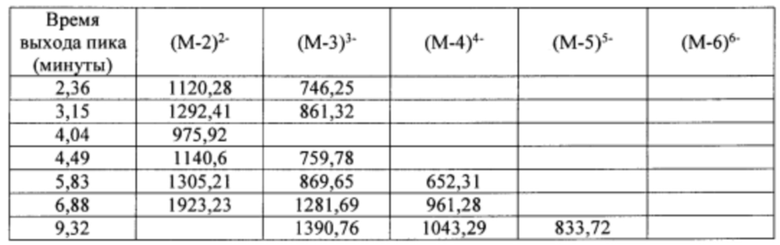
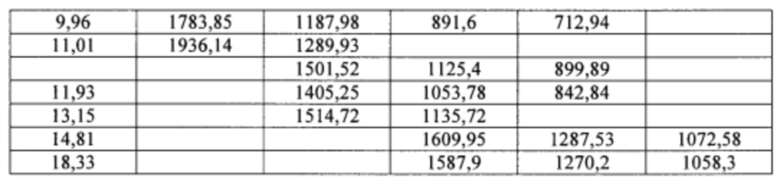
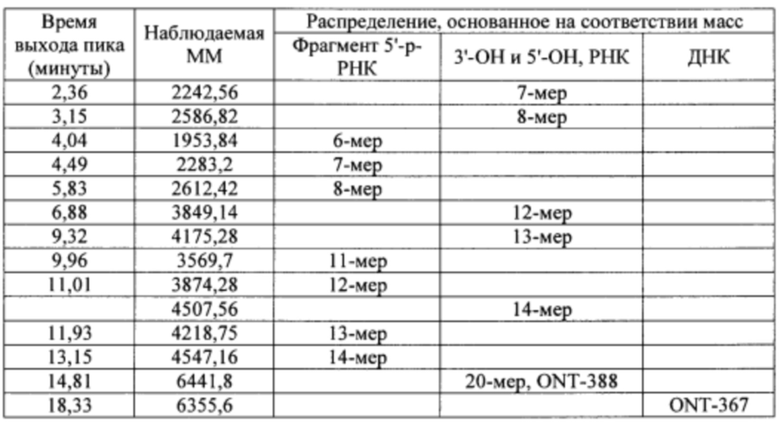
Распределение пиков на фиг. 30 (нижняя панель, M12-Exp11 NM планшет 1 (пул) F11, ONT-406, 30 мин.
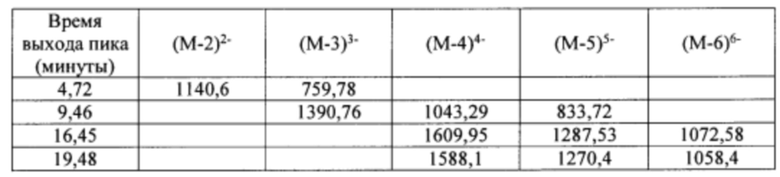


Пример 16. Пример получения линкерных групп
Согласно некоторым вариантам осуществления линкерную группу SP получали по следующей схеме:
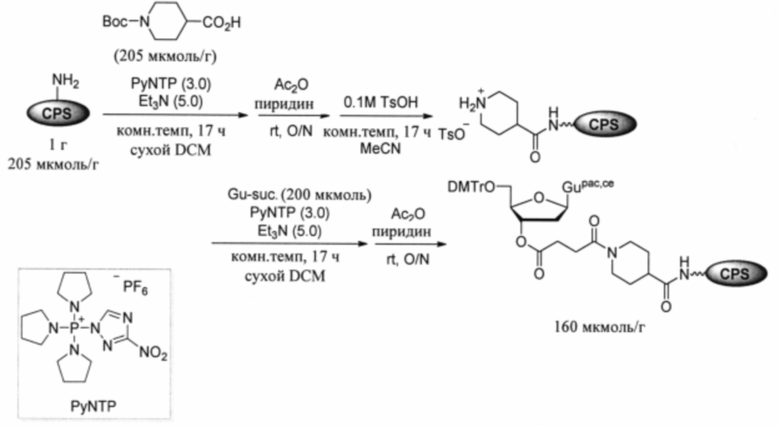
Пример 17. Иллюстративный дизайн последовательности оснований
Как описано в настоящем описании, настоящее раскрытие признает важность последовательности оснований, например, для предложенной композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления настоящее раскрытие, как проиллюстрировано в настоящем документе, предусматривает способы для разработки последовательности оснований для олигонуклеотидов, таких как антисмысловые олигонуклеотиды.
Согласно некоторым вариантам осуществления, среди прочего, биоинформатика используется для конструирования последовательности для мишени, например, связанного с болезнью Хантингтона мутантного аллеля. В настоящем примере описаны примеры стадий, которые могут быть использованы для дизайнов антисмысловых олигонуклеотидов для, например, rs362268, rs362306, rs2530595, rs362331, rs362307 и т.д. Согласно некоторым вариантам осуществления предложенные способы предусматривают стадию изучения признаков последовательности на нецелевое сродство связывания с мишенью, смежные G и палиандромные фрагменты. Согласно некоторым вариантам осуществления предложенные способы предусматривают стадию изучения нецелевых эффектов в присутствии ошибочно спаренных оснований. Согласно некоторым вариантам осуществления последовательность, найденная в мишени, содержащая характеристический элемент последовательности, например, мутацию, SNP и т.д., и имеющая длину примерно 10-1000, например, примерно 10, примерно 20, примерно 30, примерно 40, примерно 50, примерно 60, примерно 70, примерно 80, примерно 90, примерно 100, примерно 110, примерно 120, примерно 130, примерно 140, примерно 150, примерно 200, примерно 250, примерно 300, примерно 400, примерно 500, примерно 600, примерно 700, примерно 800, примерно 900, примерно 1000, примерно 2000, примерно 3000, примерно 4000, примерно 5000 и т.д. нуклеотидов, используются в анализах, например, анализе с РНКазой Н, репортерном анализе и т.д. Согласно некоторым вариантам осуществления, как в настоящем примере, использовали фланкирующие последовательности 40 п. н. для SNP, например, rs362268, rs362306, rs2530595, rs362331, rs362307 и т.д. Ряд таких последовательностей, например от 6 до 12, может быть легко оценен с помощью предложенных способов. Примеры испытанных последовательностей перечислены ниже: 
Как описано в настоящем описании и понятно специалисту в данной области техники, согласно некоторым вариантам осуществления анализы, например, анализ расщепления РНКазой, описанный в настоящем документе, применимы при оценке одного или более признаков (например, скорости, степени и/или селективности расщепления). Согласно некоторым вариантам осуществления анализ расщепления РНКазой обеспечивает профиль расщепления композиции олигонуклеотидов. Согласно некоторым вариантам осуществления используется композиция олигонуклеотидов ДНК, имеющих одну и ту же последовательность, анализ с РНКазой Н может обеспечить профиль расщепления ДНК последовательности. Согласно некоторым вариантам осуществления для получения профиля расщепления ДНК все олигонуклеотиды ДНК в композиции идентичны. Согласно некоторым вариантам осуществления, когда используется стереослучайная композиция олигонуклеотидов из фосфоротиоатов, имеющих одну и ту же последовательность, анализ с РНКазой Н может обеспечить стереослучайный профиль расщепления последовательности. Согласно некоторым вариантам осуществления для получения стереослучайного профиля расщепления все олигонуклеотиды в стереослучайной композиции идентичны. Согласно некоторым вариантам осуществления, когда используется композиция олигонуклеотидов с контролируемой хиральностью, анализ с РНКазой Н может обеспечивать стереослучайный профиль расщепления композиции олигонуклеотидов с контролируемой хиральностью. Согласно некоторым вариантам осуществления для получения профиля расщепления композиции олигонуклеотидов с контролируемой хиральностью все олигонуклеотиды в композиции олигонуклеотидов с контролируемой хиральностью идентичны. Согласно некоторым вариантам осуществления анализ с РНКазой Н обеспечивает информацию о скорости расщепления. Согласно некоторым вариантам осуществления анализ с РНКазой Н обеспечивает относительную степень расщепления, например, (расщепление в сайте)/(все расщепления). Согласно некоторым вариантам осуществления анализ с РНКазой Н обеспечивает абсолютную степень расщепления (расщепленная мишень в сайте)/(все мишени, как расщепленные, так и нерасщепленные). Согласно некоторым вариантам осуществления анализ с РНКазой Н обеспечивает избирательность. Согласно некоторым вариантам осуществления анализ с РНКазой Н обеспечивает информацию об уровне подавления.
Согласно некоторым вариантам осуществления, как проиллюстрировано в настоящем документе, анализ с РНКазой Н обеспечивает скорости расщепления. Например, результаты, смотрите фиг. 31. Р представляет собой положение несоответствия в олигонуклеотидах от 5'-конца.
Проводили анализ расщепления с РНКазой HI человека 25-мерной РНК при гибридизации с различными фосфоротиоатными олигонуклеотидами, нацеленными на SNP rs362307. WV-944 и WV-945 представляют собой 25-мерные РНК, которые включают вариант дикого типа и мутантный вариант rs362307, соответственно. WV-936-WV-941 представляют собой стереочистые ДНК, тогда как WV-904-WV-909 являются стереослучайными ДНК. Все дуплексы инкубировали с РНКазой H1C в присутствии 1-кратного буфера с РНКазой Н при 37°С. Реакции гасили в фиксированные моменты времени с помощью 30 мМ Na2EDTA. Одну десятую этой реакционной смеси вносили в обращеннофазовую ВЭЖХ и измеряли площади пиков для полноразмерной РНК, оставшейся в реакционных смесях в разные моменты времени. Скорости расщепления определяли путем построения этих площадей пиков с соответствующими временными точками. Согласно некоторым вариантам осуществления наблюдали отличие между скоростями расщепления РНК дикого типа против мутантной РНК.
Согласно некоторым вариантам осуществления, как показано на фиг. 31, когда положение 11, 12 или 13 последовательности, отсчитываемое от ее 5'-конца, выравнивается с SNP, или положение 8, 9 или 10 последовательности, отсчитываемое от ее 3'-конца, выравнивается с SNP, наблюдалась лучшая селективность расщепления.
Пример 18. Пример дизайнов крыла, сердцевины, крыла-сердцевины и крыла-сердцевины-крыла
Помимо прочего, настоящее раскрытие предусматривает различные варианты реализации структур крыла, сердцевины, крыла-сердцевины, сердцевины-крыла и крыла-сердцевины-крыла. Согласно некоторым вариантам осуществления было неожиданно обнаружено, что олигонуклеотиды с крыльями, содержащими фосфатные линкерные группы, и сердцевинами, содержащими фосфоротиоатные линкерные группы, обеспечивают неожиданно увеличенную эффективность и селективность расщепления. Например, смотрите фиг. 32 С, F, G, Н и т.д.
Анализ расщепления РНКазой HI человека 25-мерной РНК при гибридизации с различными композициями олигонуклеотидов с контролируемой хиральностью нацеленными на SNP rs362307. WV-944 и WV-945 представляют собой 25-мерные РНК, которые включают вариант дикого типа и мутантный вариант rs362307, соответственно. WV-1085-WV-1092 представляют собой стереочистые 2'-ОМе/ДНК со смешанным остовом PO/PS. Все дуплексы инкубировали с РНКазой H1C в присутствии 1-кратного буфера РНКазы при 37°С. Реакции гасили в фиксированные моменты времени с помощью 30 мМ Na2EDTA. Одну десятую этой реакционной смеси вносили в обращеннофазовую ВЭЖХ и измеряли площади пиков для полноразмерной РНК, оставшейся в реакционных смесях в разные моменты времени. Скорость расщепления определяли путем построения этих площадей пиков с соответствующими временными точками.
Согласно некоторым вариантам осуществления крылья с 2'-ОМе-модификациями фосфатов изменяют скорость расщепления и/или селективность. Согласно некоторым вариантам осуществления крылья с 2'-ОМе-модификациями фосфатов изменяют скорость расщепления и селективность. Согласно некоторым вариантам осуществления крылья с 2'-ОМе-модификациями фосфатов изменяют скорость расщепления или селективность. Согласно некоторым вариантам осуществления крыло с 2'-ОМе-модификациями фосфатов изменяет скорость расщепления. Согласно некоторым вариантам осуществления крыло с 2'-ОМе-модификациями фосфатов изменяет скорости расщепления как мутантного аллеля, так и аллеля дикого типа. Согласно некоторым вариантам осуществления крыло с 2'-ОМе-модификациями фосфатов изменяет селективность расщепления. Согласно некоторым вариантам осуществления крыло с 2'-ОМе-модификациями фосфатов изменяет профиль расщепления.
Согласно некоторым вариантам осуществления включение фосфатной межнуклеотидной линкерной группы неожиданно улучшает скорость расщепления и/или селективность. Согласно некоторым вариантам осуществления включение фосфатной межнуклеотидной линкерной группы неожиданно улучшает скорость расщепления и селективность. Согласно некоторым вариантам осуществления включение фосфатной межнуклеотидной линкерной группы неожиданно улучшает скорость расщепления или селективность. Согласно некоторым вариантам осуществления включение фосфатной межнуклеотидной линкерной группы неожиданно улучшает скорость расщепления. Согласно некоторым вариантам осуществления фосфатная межнуклеотидная линкерная группа улучшает скорость расщепления как мутантного аллеля, так и аллеля дикого типа, но в более высокой степени для мутантного аллеля, чем для аллеля дикого типа. Согласно некоторым вариантам осуществления включение фосфатной межнуклеотидной линкерной группы неожиданно улучшает селективность расщепления.
Согласно некоторым вариантам осуществления, как показано в примерах, представленных в настоящем документе, стереочистые композиции олигонуклеотидов обеспечивают неожиданно высокую скорость и/или селективность расщепления по сравнению с соответствующими стереослучайными композициями; например, смотрите стереочистый WV-1497/стереослучайный WV-1092, 905/937, 931/1087 и т.д.
Пример 19. Пример карт расщепления
Как описано в настоящем документе, согласно некоторым вариантам осуществления анализ, такой как анализ с РНКазой Н, обеспечивает карты расщепления для стереослучайных композиций олигонуклеотидов или композиций олигонуклеотидов с контролируемой хиральностью. Примеры карт расщепления приведены на фиг. 33, которые иллюстрируют стереослучайные профили расщепления множественных последовательностей оснований. Дополнительные карты расщепления представлены на фиг. 35, которые иллюстрируют, среди прочего, стереослучайные профили расщепления последовательности оснований без нуклеозидных модификаций (WV-905), а также последовательности оснований, имеющей нуклеозидные модификации.
Пример профилей расщепления стереочистых композиций олигонуклеотидов с контролируемой хиральностью представлены на фиг. 34. Как описано в настоящем раскрытии, основные сайты расщепления могут быть идентифицированы с помощью анализов, таких как анализ с РНКазой Н, из профилей расщепления. Например, для WV-937 относительный основной сайт расщепления, оцененный (расщепление в сайте/полное расщепление) и отраженный длинами стрелок, находится между GCGC и CCUU для дикого типа (2 межнуклеотидные линкерные группы от SNP), а также между CUGU и GCCC для мутанта (в сайте SNP в 0 межнуклеотидных линкерных групп от SNP). Согласно некоторым вариантам осуществления относительный основной сайт расщепления возможно представляет собой абсолютный основной сайт расщепления, который требует, чтобы определенный процент от всех мишеней, в данном случае РНК, расщеплялся в сайте. Например, согласно некоторым вариантам осуществления сайт между GCGC и CCUU для WV-937/дикого типа не представляет собой основной сайт расщепления, если более 20% всех мишеней необходимо расщепить в сайте, чтобы квалифицировать сайт как основной сайт расщепления (см. фиг. 32, М); сайт между CUGU и GCCC для WV-937/мутант остается основным сайтом расщеплений, если порог для основного сайта составляет 20% от всех мишеней, расщепляемых в этом сайте.
Согласно некоторым вариантам осуществления различные композиции олигонуклеотидов имеют разные скорости расщепления. Согласно некоторым вариантам осуществления карты расщепления получают в разные моменты времени. Например, для композиции олигонуклеотидов, имеющей более высокую скорость расщепления, ее карта расщепления может быть получена в более ранний момент времени (например, 5 минут, 10 минут, 15 минут и т.д.), чем для композиции олигонуклеотидов, имеющей более медленную скорость расщепления (например, 30 минут, 45 минут, 60 минут и т.д.).
Согласно некоторым вариантам осуществления, когда продукты расщепления только в одном сайте могут быть идентифицированы с помощью аналитических способов, например, ВЭЖХ, ВЭЖХ-МС и т.д., считается, что соответствующий профиль расщепления имеет единственный сайт расщепления. Согласно некоторым вариантам осуществления, когда более чем примерно 90%, более чем примерно 91%, более чем примерно 92%, более чем примерно 93%, более чем примерно 94%, более чем примерно 95%, более чем примерно 96%, более чем примерно 97%, более чем 98%, более чем 99% или более чем 99,5% общего расщепления происходит в сайте, соответствующий профиль расщепления может рассматриваться как единый сайт расщепления. Согласно некоторым вариантам осуществления, как понятно специалисту в данной области техники, селективность, например, в клетках, тканях, органах, субъектах и т.д., может быть выше, чем наблюдаемая в анализе с РНКазой Н. Согласно некоторым вариантам осуществления сайт, имеющий более чем примерно 90%, более чем примерно 91%, более чем примерно 92%, более чем примерно 93%, более чем примерно 94%, более чем примерно 95%, более чем примерно 96%, более чем примерно 97%, более чем примерно 98%, более чем примерно 99% или более чем примерно 99,5% общего расщепления в анализе с РНКазой H, может иметь более высокую селективность в клетках, тканях, органах или субъектах. Согласно некоторым вариантам осуществления сайт, имеющий более чем примерно 90% общего расщепления в анализе с РНКазой Н, может представлять собой единственный сайт расщепления (например, более чем примерно 99%, более чем примерно 99,5%, 100% и т.д.) в клетках, тканях, органах или субъектах.
Согласно некоторым вариантам осуществления селективность может быть оценена путем сравнения абсолютных значений оставшихся транскриптов (или их репрезентативных последовательностей, таких как последовательности РНК, используемые в примерах, описанных в настоящем документе) целевой последовательности и аналогичной последовательности, например, РНК, или репрезентативных синтетических последовательностей, мутантного аллеля в качестве мишени и аллеля дикого типа в качестве аналогичной последовательности. Согласно некоторым вариантам осуществления селективность может быть оценена путем сравнения абсолютных количеств оставшихся транскриптов (или их репрезентативных последовательностей, таких как последовательности РНК, используемые в примерах, описанных в настоящем документе) целевой последовательности и аналогичной последовательности, когда исходные количества являются одинаковыми. Согласно некоторым вариантам осуществления селективность может быть оценена по процентам расщепления транскриптов (или их репрезентативных последовательностей, таких как последовательности РНК, используемые в примерах, описанных в настоящем документе) целевой последовательности и аналогичной последовательности. Согласно некоторым вариантам осуществления селективность может быть оценена путем сравнения соотношений расщепленных и нерасщепленных транскриптов (или их репрезентативных последовательностей, таких как последовательности РНК, используемые в примерах, описанных в настоящем документе).
Согласно некоторым вариантам осуществления селективность может быть оценена с помощью одного или более анализов, представленных в настоящем документе. Согласно некоторым вариантам осуществления селективность может быть измерена с помощью анализа расщепления РНКазой Н. Например, селективное расщепление мишени (например, РНК из мутантного аллеля) может быть измерено с помощью биохимического анализа расщепления РНКазой Н, где расщепление мутантной целевой последовательности сравнивается с расщеплением последовательности РНК дикого типа, и селективность может быть представлена либо скоростью расщепления, отношением расщепленной мутантной РНК и РНК дикого типа в определенный момент времени, либо соотношением оставшейся мутантной РНК и РНК дикого типа в определенный момент времени, или их комбинациями. Согласно некоторым вариантам осуществления момент времени составляет 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60 или более минут. Согласно некоторым вариантам осуществления момент времени составляет 10 минут. Согласно некоторым вариантам осуществления момент времени составляет 15 минут. Согласно некоторым вариантам осуществления момент времени составляет 20 минут. Согласно некоторым вариантам осуществления момент времени составляет 25 минут. Согласно некоторым вариантам осуществления момент времени составляет 30 минут. Согласно некоторым вариантам осуществления момент времени составляет 35 минут. Согласно некоторым вариантам осуществления момент времени составляет 40 минут. Согласно некоторым вариантам осуществления момент времени составляет 45 минут. Согласно некоторым вариантам осуществления момент времени составляет 50 минут. Согласно некоторым вариантам осуществления момент времени составляет 55 минут. Согласно некоторым вариантам осуществления момент времени составляет 60 минут. Согласно некоторым вариантам осуществления момент времени составляет 60 или более минут. Специалист в данной области техники понимает, как выбрать момент времени, например, для расщепления, показанного на фиг. 32, можно выбрать один или более моментов времени из 5, 10, 15, 20, 20, 45 и 60 минут для оценки селективности. Согласно некоторым вариантам осуществления селективность может быть измерена соотношениями IC50 для целевых (например, мутантных) и нецелевых (например, дикого типа) последовательностей, например, из клеточных анализов или животных моделей.
Примеры трасс ВЭЖХ-МС представлены на фиг. 36. Согласно некоторым вариантам осуществления иллюстративные условия анализа с РНКазой Н описаны ниже.
Получение дуплекса ДНК/РНК. Концентрации олигонуклеотидов определяли путем измерения абсорбции в воде при 260 нм. Дуплексы ДНК/РНК готовили смешиванием эквимолярных растворов олигонуклеотидов с концентрацией каждой нити 20 мкМ. Смеси нагревали при 90°С в течение 2 минут на водяной бане и медленно охлаждали в течение нескольких часов.
Экспрессия и очистка белка РНКазы Н человека: клон РНКазы НС человека получали из лаборатории профессора Вэй Яна в NIH Bethesda. Был описан протокол для получения этой человеческой РНКазы НС (остатки 136-286) (Nowotny, M. et al. Structure of Human RNase H1 Complexed with an RNA/DNA Hybrid: Insight into HIV Reverse Transcription. Molecular Cell 28, 264-276, (2007)). Экспрессию белка проводили по следующему протоколу, за исключением того, что полученный белок имел N-концевую His6-метку. Клетки BL21(DE3) E.coli в среде LB использовали для экспрессии белка. Клетки выращивали при 37°С до OD600 нм, достигавшего около 0,7. Культуры затем охлаждали и добавляли 0,4 мМ IPTG для индуцирования экспрессии белка в течение ночи при 16°С. Экстракт E.coli получали ультразвуком в буфере А (40 мМ NaH2PO4 (pH 7,0), 1 M NaCl, 5% глицерина, 2,8 мМ β-меркаптоэтанола и 10 мМ имидазола) с добавлением ингибиторов протеазы (Sigma-Aldrich). Экстракт очищали посредством аффинной колонки с использованием буфера А плюс 60 мМ имидазола. Белок элюировали линейным градиентом от 60 до 300 мМ имидазола. Пик белка собирали и дополнительно очищали на колонке Mono S (GE Healthcare) с градиентом NaCl 100 мМ - 500 мМ в буфере В. Фракции, содержащие РНКазу НС, концентрировали до 0,3 мг/мл в буфере для хранения (20 мМ HEPES (pH 7,0), 100 мМ NaCl, 5% глицерина, 0,5 мМ ЭДТА, 2 мМ DTT) и хранили при -20°С. Концентрация фермента 0,3 мг/мл соответствует 17,4 мкМ в зависимости от зарегистрированного коэффициента экстинкции (32095 см-1М-1) и молекулярной массы (18963,3 Да).
В 96-луночном планшете к 50 мкл дуплекса ДНК/РНК (20 мкМ) добавляли 10 мкл 10-кратного буфера РНКазы Н, а затем 30 мкл воды. Смесь инкубировали при 37°С в течение нескольких минут и затем добавляли 10 мкл исходного раствора фермента в концентрации 0,2 мкМ с получением общего объема 100 мкл с конечной концентрацией субстрата/фермента 10 мкМ/0,02 мкМ (500:1) и далее инкубировали при 37°С. Различные соотношения дуплекса ДНК/РНК с белком РНКазы Н предварительно изучали с использованием этих условий, чтобы найти это оптимальное соотношение (500:1) для изучения кинетики. Реакции гасили в разные моменты времени, используя 7 мкл раствора динатрия ЭДТА в концентрации 500 мМ в воде. В момент времени нуль минут ЭДТА добавляли к реакционной смеси перед добавлением фермента. Контроли прогоняли, чтобы убедиться, что ЭДТА может полностью ингибировать активность фермента. После того, как все реакции гасили, 10 мкл или 20 мкл каждой реакционной смеси вносили в LCMS-TOF с использованием аналитической колонки (Agilent Poroshell 120 ЕС-С18 2,7 микрон, 2,1×150 мм, часть №699775-902). Отношение площади пика оставшейся полноразмерной РНК к ДНК в каждой реакционной смеси нормировали против этого отношения в нулевой точечной реакции, чтобы получить % оставшейся полноразмерной РНК.
Согласно некоторым вариантам осуществления пример условия ВЭЖХ представляет собой:
Элюант А = 8 мМ TEA, 200 мМ HFIP в воде
Элюант В = 50:50 (Элюант А: метанол)
Температура колонки = 50°С
Температура автодозатора = 4°С
УФ регистрировали при 254 нм и 280 нм
Способ градиента LC
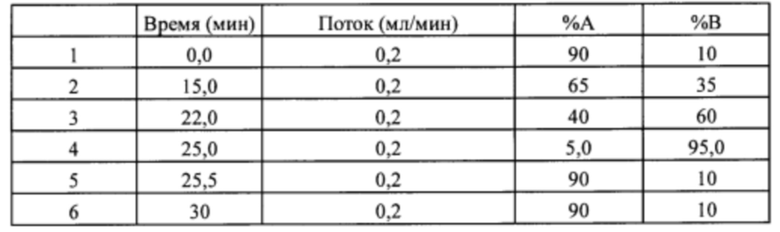
Пример 20. Примеры анализов для оценки олигонуклеотидов
Согласно некоторым вариантам осуществления настоящее раскрытие предусматривает репортерные анализы для оценки свойств предложенных олигонуклеотидов и композиций. Согласно некоторым вариантам осуществления предложенный репортерный анализ представляет собой анализ двойной люциферазы, например, как описано ниже.
Определение ингибирования мРНК олигонуклеотидами с использованием системы Dual Glo Luciferase: векторная система psiCheck2 из Promega представляет собой коммерчески доступный вектор, который кодирует гены люцифераз как Photinus pyralis, так и Renilla Reniformis на одной плазмиде с множественным сайтом клонирования в 3' UTR люциферазы Renilla для вставки олигонуклеотидов, кодирующих целевые сайты миРНК (или другие клонированные регуляторные последовательности, такие как целевые 3'UTR). Фрагмент 250 пар оснований, содержащий представляющую интерес целевую область и его обратный комплемент и имеющий соответствующие выступающие основания, соответствующие рестрикционному ферменту(ам), используемому для расщепления вектора psiCheck, клонировали в вектор psiCHECK-2 (Promega, C8021) между сайтами рестрикционных ферментов NotI и XhoI. Вектор, содержащий вставку, секвенировали, чтобы подтвердить правильную ориентацию вставки, удлиненную и очищенную. Несколько векторов получали с использованием вышеуказанного дизайна для представляющих интерес SNP. В типичном эксперименте по совместной трансфекции после того, как клетки находились с правильной плотностью (с 30 до 40% слияния), олигонуклеотиды и вектор подвергали обратной трансфекции с использованием Lipofectamine 2000 (Life Technologies). Эффекты олигонуклеотидов на целевую мРНК можно увидеть уже через 24 ч после трансфекции и они все еще присутствуют через 48 часов. Через 24 часа или через 48 часов после трансфекции векторов psiCheck клетки анализировали на активность люциферазы. Вкратце, клетки промывали PBS, лизировали в пассивном буфере для лизиса, добавляли люцифериновые реагенты и образцы считывали на приборе Spectramax M5 (Molecular Devices). Измерения проводили при концентрациях вектора 20 нг на лунку 96-луночного планшета. Эксперименты проводили при различных концентрациях олигонуклеотидов (30, 10 и 3,3 нМ) и двух временных точках (24 и 48 часов). Относительные уровни люциферазы Renilla против Firefly измеряли для необработанных клеток и клеток, которые были обработаны олигонуклеотидами, нацеленными на Renilla (WV-975) для измерения максимального нокдауна Renilla. Контрольные олигонуклеотиды (например, WV-437, WV-993 и т.д.) выбирали для нормализации уровней R/F. Согласно некоторым вариантам осуществления репортерный анализ двойной люциферазы использовали для оценки олигонуклеотидов в клеточной линии Cos7. Согласно некоторым вариантам осуществления клеточную линию подвергали котрансфекции в течение 24 часов с олигонуклеотидами и любой из плазмид psiCHECK.2, включая rs362307 (Т) или rs362307 (С) SNP. Согласно некоторым вариантам осуществления rs362307 (Т) и rs362307 (С) упоминаются как mu и wt.
Различные композиции олигонуклеотидов с контролируемой хиральностью и стереослучайные исследовали при 30 нМ с использованием анализа двойной люциферазы. Для олигонуклеотидов с несовпадением в одном и том же положении (например, положениях 8, 9, 10, 11, 12 и 13 относительно 5'-конца) композиции с контролируемой хиральностью поддерживали высокие уровни измерений широкого типа.
Согласно некоторым вариантам осуществления при исследовании при 30 нМ WV-1092 селективно подавлял экспрессию мутантной последовательности через 24 и/или 48 часов, как показано с помощью репортерного анализа гена двойной люциферазы. Согласно некоторым вариантам осуществления наблюдаемая селективность для WV-1092 при 30 нМ в течение 24 часов и/или 48 часов была в несколько раз больше, чем для других композиций олигонуклеотидов, например, WV-917, WV-1497, некоторых стереочистых олигонуклеотидов Р12 и т.д. Согласно некоторым вариантам осуществления при 30 нМ через 48 часов WV-1092 поддерживали более 90% дикого типа и уменьшали мутант примерно до 30%, тогда как WV-917 уменьшал дикий тип до примерно 60% и мутант примерно до 30%. Олигонуклеотиды исследовали в нескольких условиях (например, концентрациях, временных точках и т.д.) и показали улучшенные свойства, например, активность, селективность и т.д.
Как понятно специалисту в данной области техники, свойства олигонуклеотидов, например, активность, селективность и т.д., могут быть оценены с помощью многих других анализов, таких как анализы на основе клеток, модели животных и т.д. Согласно некоторым вариантам осуществления аллель-специфическое подавление может быть исследовано в клетках и на животных моделях, используя аналогичные процедуры, как описанные в Hohjoh, Pharmaceuticals 2013, 6, 522-535; публикации патентной заявки США US 2013/0197061; ∅stergaard et al.. Nucleic Acids Research 2013, 41 (21), 9634-9650; Jiang et al.. Science 2013, 342, 111-114 и US 9006198. Согласно некоторым вариантам осуществления селективность может быть оценена по значениям IC50 для аллеля дикого типа и мутантного аллеля. Предложенные композиции, в том числе нацеленные на связанные с болезнью Хантингтона SNP, селективно подавляют связанный с заболеванием аллель, по сравнению с аллелями дикого типа.
Пример 21. Примеры способов получения олигонуклеотидов и композиций
Сокращения
АМА: конц. NH3 - 40% MeNH2 в H2O (1:1, об/об)
CMIMT: трифлат N-цианометилимидазолия
DBU: 1,8-диазабицикло[5.4.0]ундец-7-ен
DCA: дихлоруксусная кислота
ДСМ: дихлорметан, CH2Cl2
DMTr: 4,4'-диметокситритил
DVB: дивинилбензол
НСР: сильно сшитый полистирол (содержит 50% DVB, ненабухающий полистирол)
MeIm: N-метилимидазол
MQ: вода, полученная из «Milli-Q Reference»
PhIMT: N-фенилимидазол трифлат
POS: 3-фенил-1,2,4-дитиазолин-5-он
PS200: поддержка праймера 200, коммерчески доступная от GE Healthcare
PS5G: поддержка праймера 5G, коммерчески доступная от GE Healthcare
TBAF: фторид тетрабутиламмония
ТБХФ: +-бутилгидропероксид
ТЕАА: триэтиламмоний ацетат
Твердая подложка: исследовали различные типы твердой подложки (различная загрузка нуклеозидов). Согласно некоторым вариантам осуществления НСР> PS5G ≈ PS200 ≥ CPG. Согласно некоторым вариантам осуществления твердая подложка представляет собой НСР. Согласно некоторым вариантам осуществления твердая подложка представляет собой PS5G. Согласно некоторым вариантам осуществления твердая подложка представляет собой PS200. Согласно некоторым вариантам осуществления твердая подложка представляет собой CPG. Для загрузки нуклеозидов исследовали различный диапазон (30-300 мкмоль/г). Согласно некоторым вариантам осуществления осуществляли загрузку 70~80 мкмоль/г, в отличие от других. Согласно некоторым вариантам осуществления загрузка нуклеозидов составляет 70~80 мкмоль/г. CPG приобретали у различных поставщиков (GlenReseach, LinkTechnologies, ChemGenes, PrimeSynthesis и 3-Prime).
Различные линкерные группы были исследованы и могут быть использованы. Согласно некоторым вариантам осуществления при получении композиций олигонуклеотидов с контролируемой хиральностью с использованием химии типа DPSE использовали SP-линкерную группу.
Различные активаторы получали и/или приобретали и оценивали. Согласно некоторым вариантам осуществления для химии типа DPSE использовали CMIMT.
Пример аналитических условий:
1) ОФ-СВЭЖХ-МС
- Система: Waters, Aquity СВЭЖХ I-Class, Xevo G2-Tof
- Колонка: Waters, ВЕН С18, 1,7 мкм, 2,1×150 мм
- Темп. и скорость потока: 55°С, 0,3 мл/мин
- Буфер: А: 0,1 М TEA; В: MeCN
- Градиент: % В: 1-30%/30 мин.
2) Анионообменная-ВЭЖХ
- Система: Waters, Alliance e2695
- Колонка: Thermo, DNAPac PA-200, 4×250 мм
- Темп. и скорость потока: 50°С, 1 мл/мин
- Буфер: А: 20 мМ NaOH; В: А + 1М NaClO4
- Градиент: % В: 10-50%/30 мин.
Пример процедуры синтеза хиральных олигонуклеотидов (масштаб 1 мкмоль):
Автоматический твердофазный синтез хиральных олигонуклеотидов проводили в соответствии с примерами циклов, показанных в настоящем документе. После циклов синтеза смолу обрабатывали 0,1 М TBAF в MeCN (1 мл) в течение 2 ч (как правило, достаточно 30 мин) при комнатной температуре, промывали MeCN, высушивали и добавляли АМА (1 мл) в течение 30 мин при 45°С. Смесь охлаждали до комнатной температуры и смолу удаляли посредством мембранной фильтрации. Фильтрат концентрировали при пониженном давлении до примерно 1 мл. Остаток разбавляли 1 мл H2O и анализировали с помощью анионообменной-ВЭЖХ и ОФ-СВЭЖХ-МС (пример условий: смотрите аналитические условия).

Как описано, обработка TBAF может обеспечить лучшие результаты, например, меньшее десульфирование. Согласно некоторым вариантам осуществления линкерная группа SP обеспечивала лучшие выходы и/или чистоту, без намерения ограничиваться теорией, лучшую стабильность при удалении хирального вспомогательного агента, как описано. Согласно некоторым вариантам осуществления фторсодержащие реагенты, такие как HF-NR3 (например, HF-TEA (триэтиламин)), обеспечивали лучшие выходы и/или чистоту, когда использовалась сукцинил-линкерная группа, без намерения быть ограниченным теорией, уменьшая расщепление при удалении хирального вспомогательного вещества. Согласно некоторым вариантам осуществления после синтеза смолу обрабатывали 1М TEA-HF в DMF-H2O (3:1, об./об., 1 мл) в течение 2 ч при 50°С. PS5G промывали MeCN, H2O и добавляли АМА (концентрация NH3 - 40% MeNH2 (1:1, об./об.)) (1 мл) в течение 45 мин при 50°С. Смесь охлаждали до комнатной температуры и смолу удаляли посредством мембранной фильтрации (промывали H2O в течение 2 мл). Фильтрат концентрировали при пониженном давлении до тех пор, пока он не достигал примерно 1 мл. Остаток разбавляли 1 мл H2O и анализировали с помощью анионообменной-ВЭЖХ и ОФ-СВЭЖХ-МС (условия: смотрите раздел аналитических условий).
Пример процедуры очистки хиральных олигонуклеотидов (шкала 1 мкмоль): согласно некоторым вариантам осуществления неочищенные олигонуклеотиды очищали AEX-MPLC в соответствии со следующими иллюстративными условиями:
- Система: АКТА Purifier-10
- Колонка: TOHSOH, DNA STAT, 4,6×100 мм
- Темп. и скорость потока: 60°С, 0,5 мл/мин
- Буфер: А: 20 мМ Трис-HCl (рН 9,0) + 20% MeCN, В: А + 1,5 М NaCl
- Градиент: % В: 20-70%/25CV (2%/CV)
Все фракции анализировали с помощью аналитической анионообменной-ВЭЖХ, а фракции, содержащие хиральные олигонуклеотиды более 80% чистоты, корректировали и обессоливали с помощью Sep-Pak Plus tC18 (WAT036800), используя иллюстративные условия ниже:
1. Кондиционирование Sep-Pak Plus с 15 мл MeCN.
2. Промывка картриджа с 15 мл 50% MeCN/MQ.
3. Уравнивание картриджа с 30 мл MQ.
4. Загрузка образца и промывка с 40 мл MQ.
5. Элюирование хиральных олигонуклеотидов с 10 мл 50% MeCN/MQ.
Элюированный образец испаряли при пониженном давлении для удаления MeCN и лиофилизировали. Продукт растворяли в MQ (1 мл), фильтровали с помощью фильтра шприца с диаметром 0,2 мкм и анализировали. После расчета выхода по УФ-поглощению препарат снова лиофилизировали.
Иллюстративные способы, условия и реагенты были описаны, например, в JP 2002-33436, публикациях международных заявок WO 2005/092909, WO 2010/064146, WO 2012/039448, WO 2011/108682, WO 2014/010250, WO 2014/010780, WO 201401081 и т.д., и могут быть применимы для получения предложенных олигонуклеотидов и/или композиций.
Дополнительный пример олигонуклеотидов приведен ниже. Согласно некоторым вариантам осуществления один или более олигонуклеотидов, приведенных ниже, используются в качестве контролей. Согласно некоторым вариантам осуществления один или более олигонуклеотидов ниже представляют собой последовательности РНК в качестве мишеней расщепления в одном или более анализах.
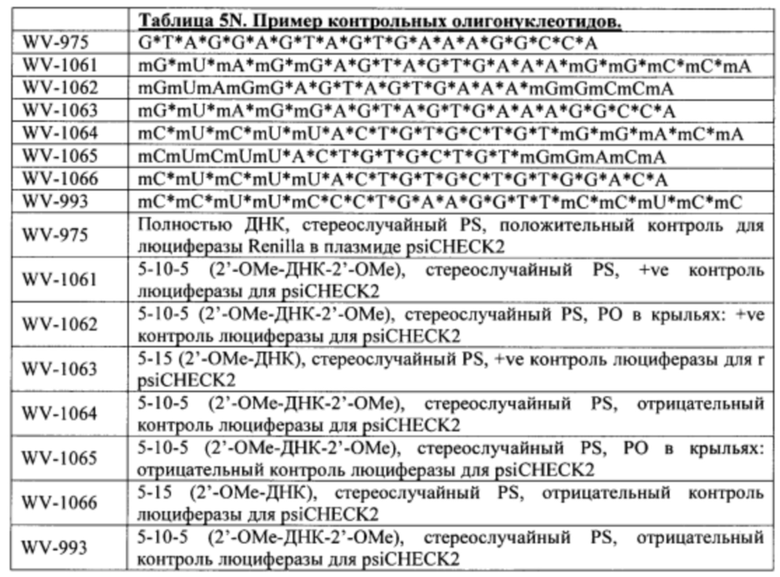
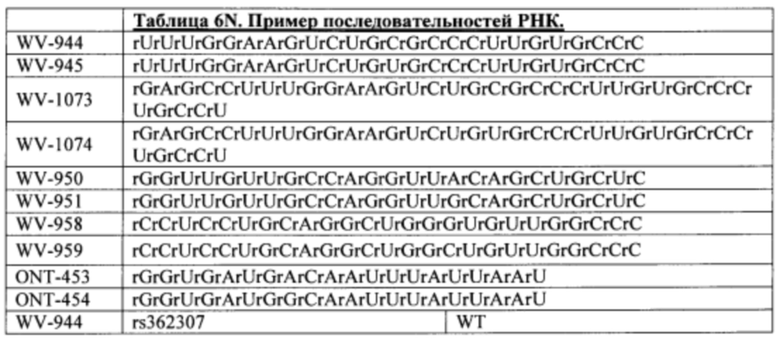
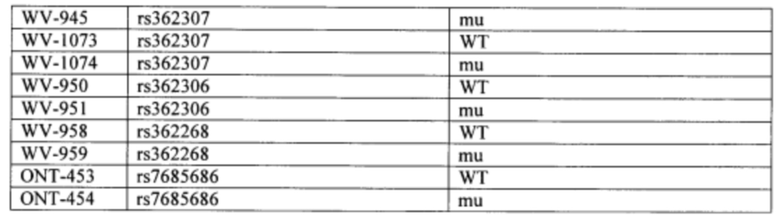
Пример 22. Пример олигонуклеотидов.
Дополнительные иллюстративные олигонуклеотиды перечислены ниже в таблице 8.
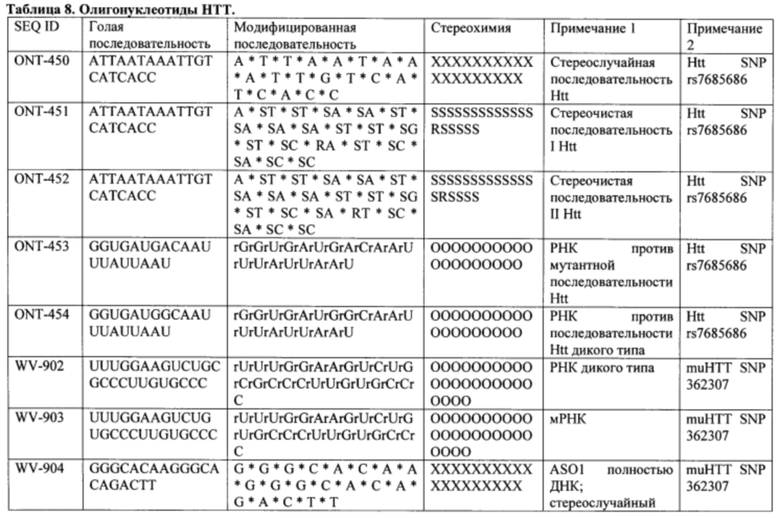
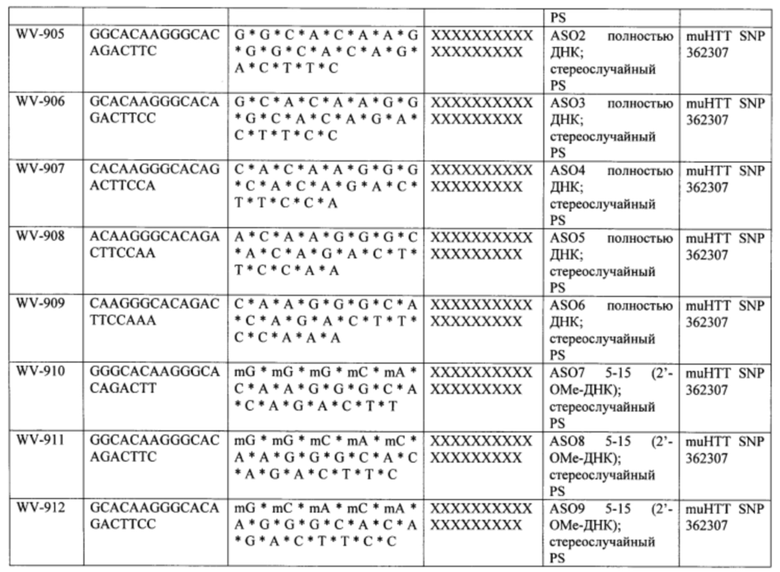
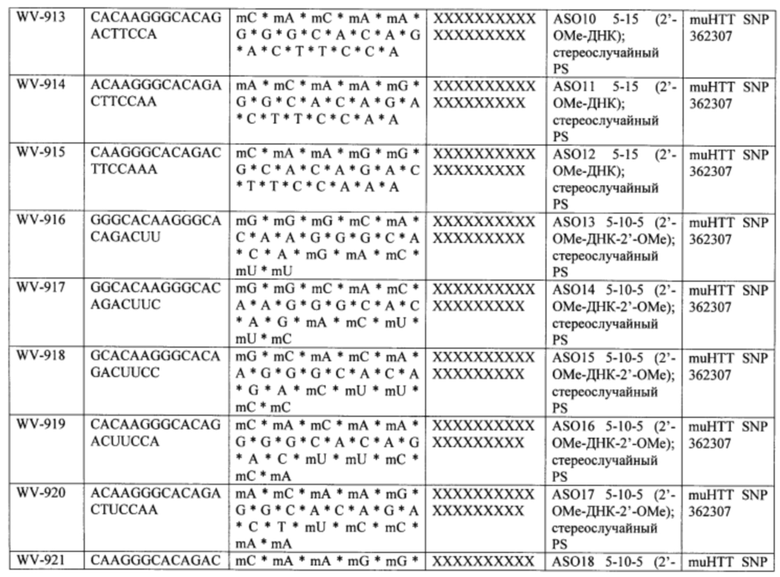
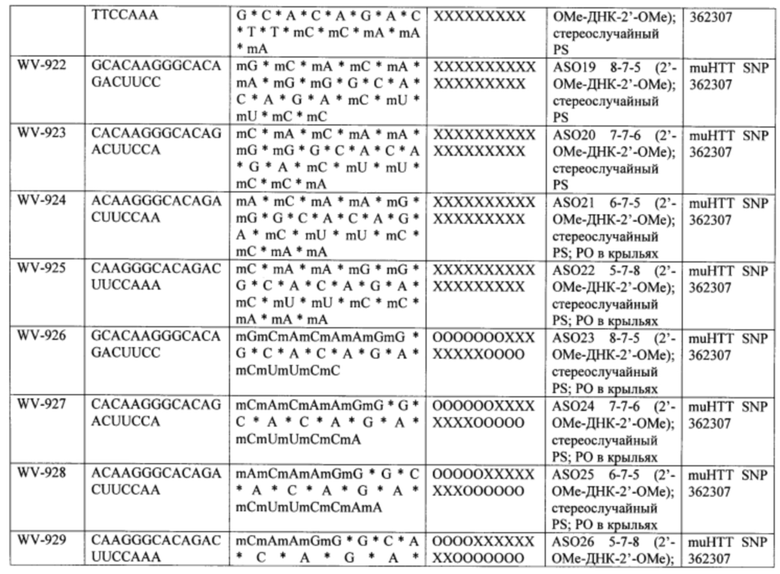
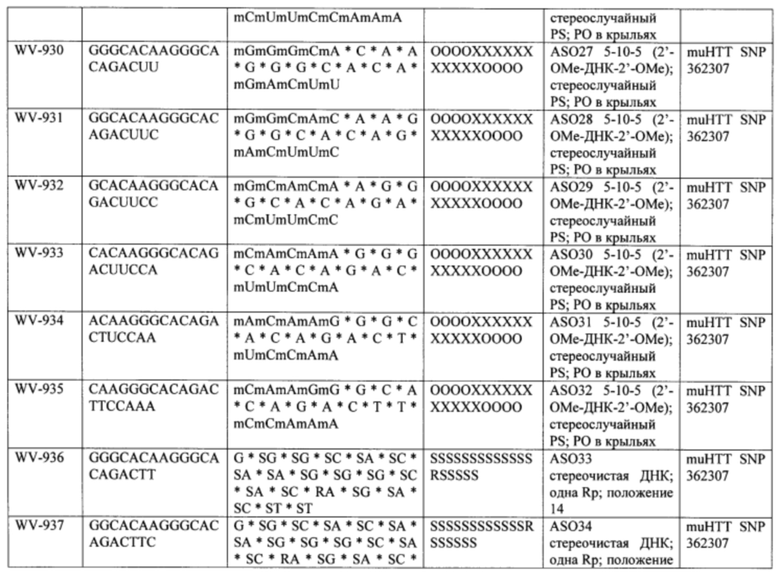
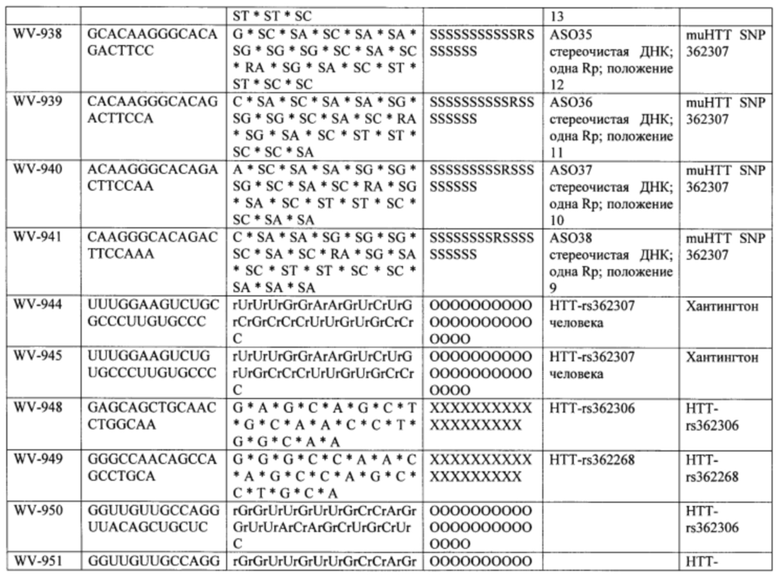
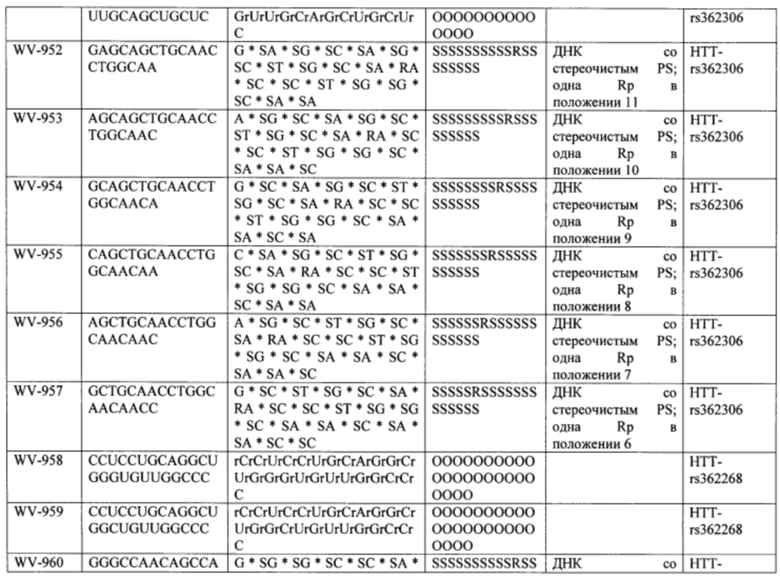
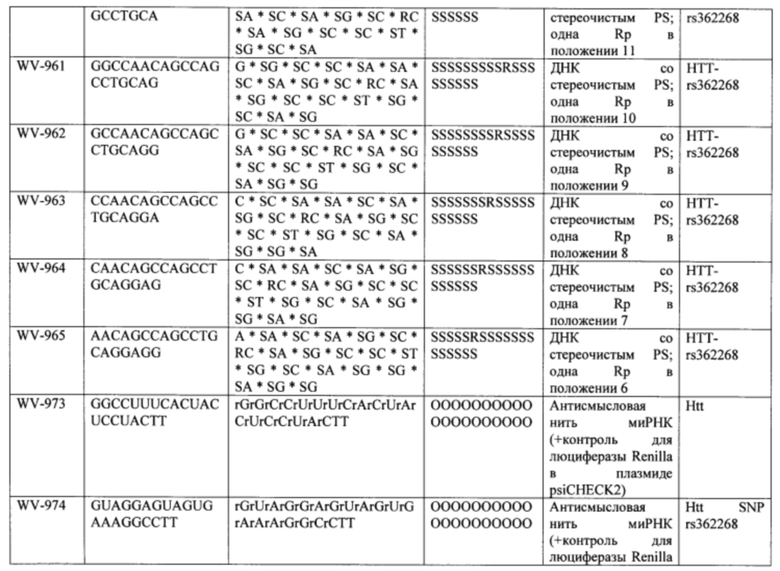
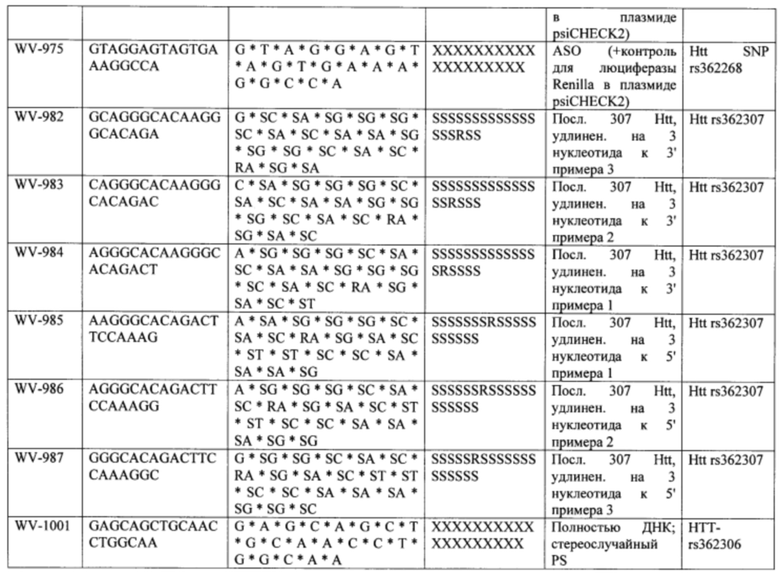
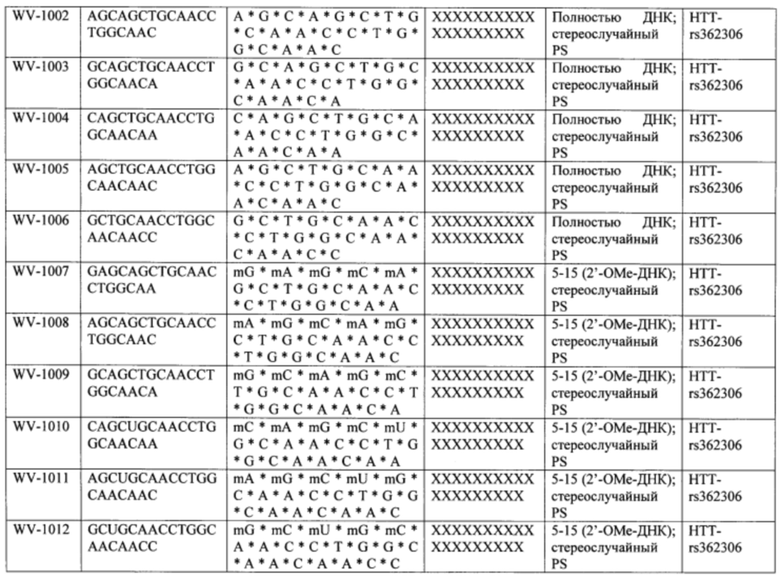
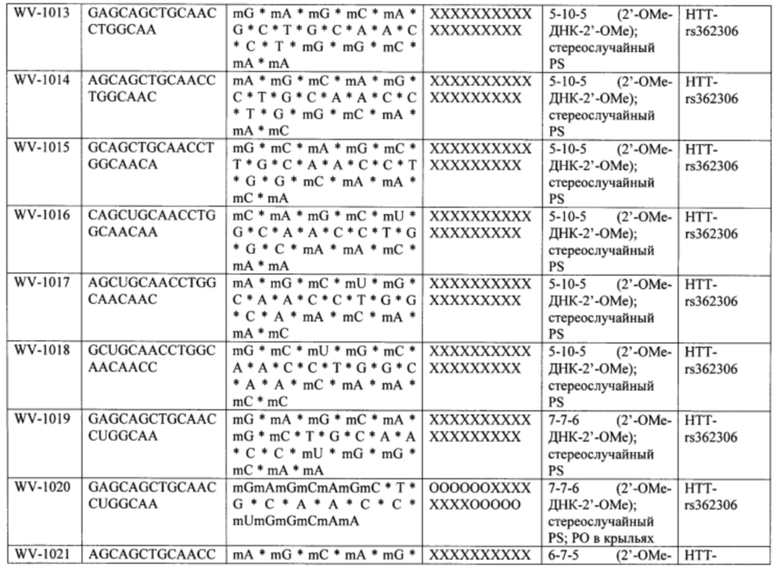
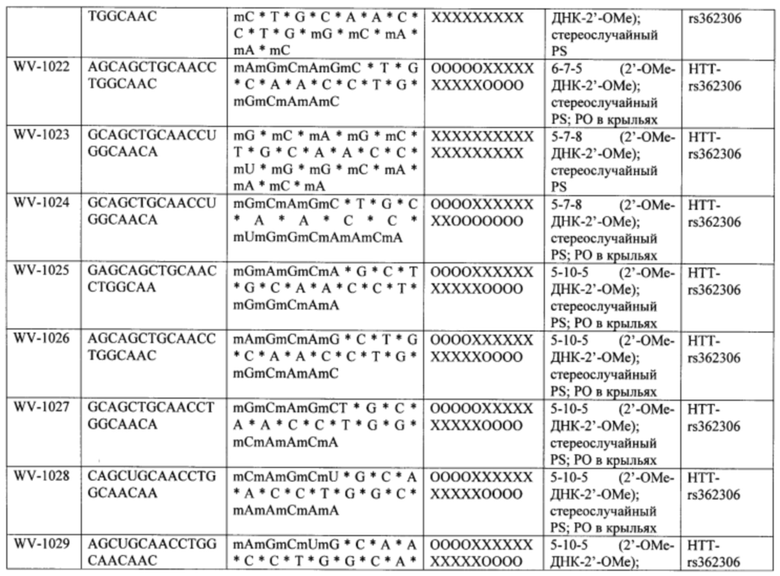
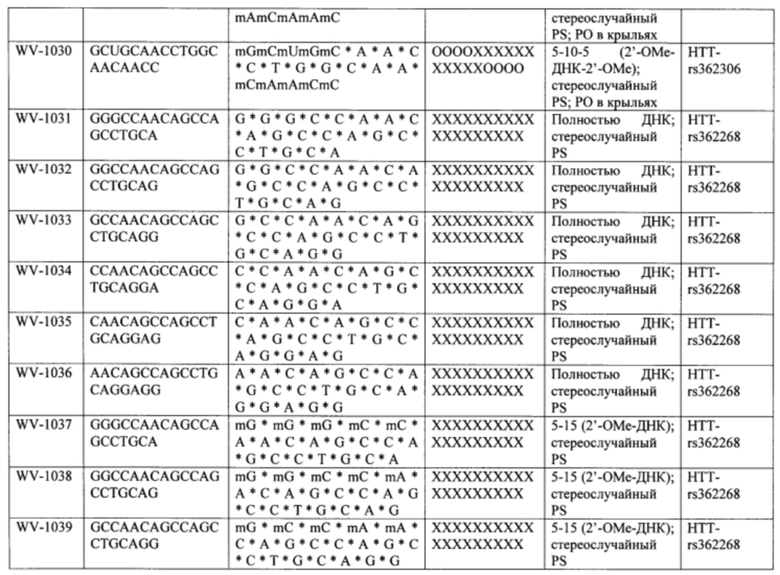
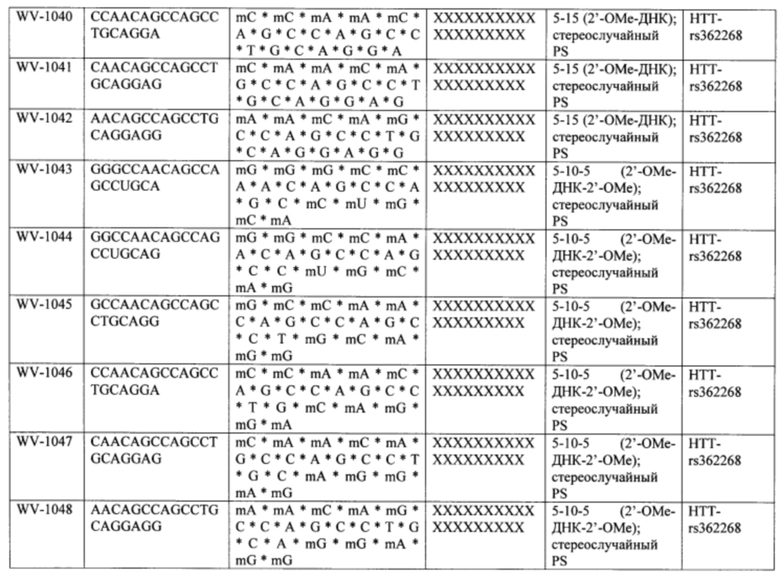
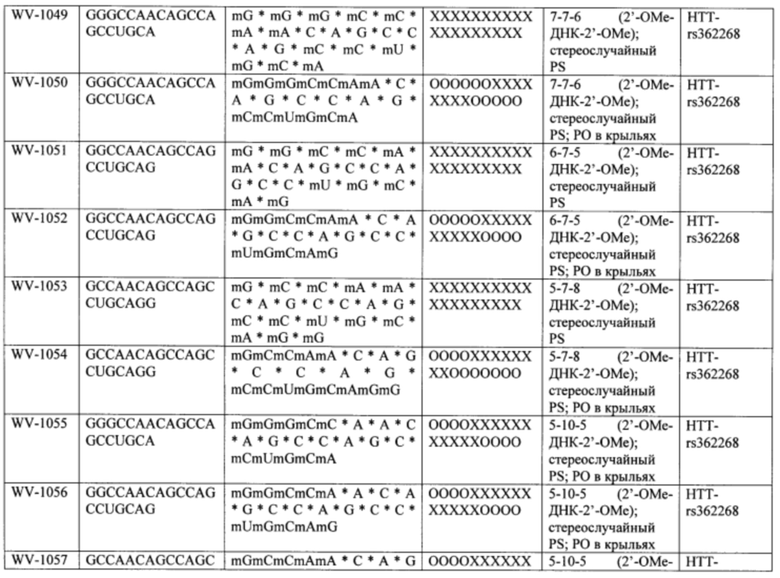
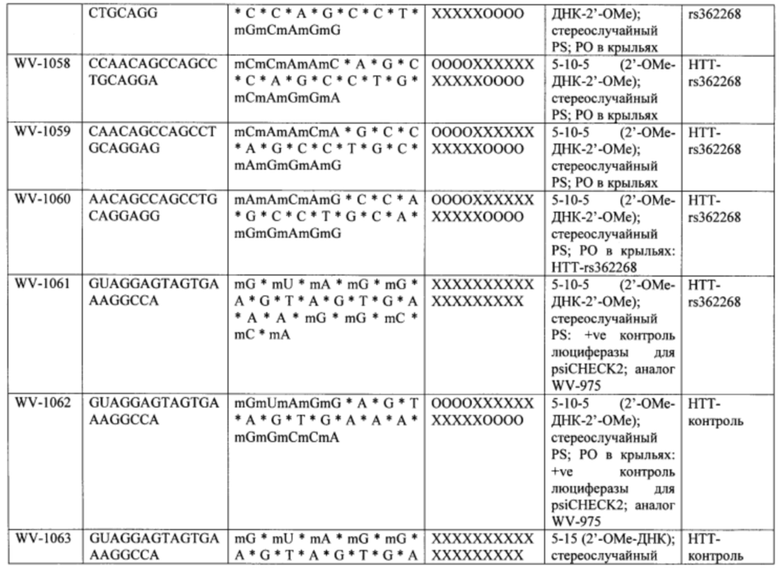
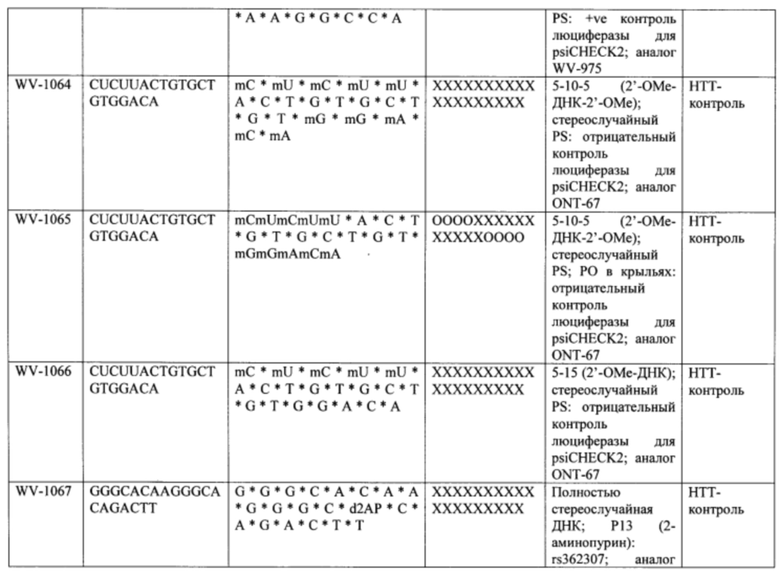

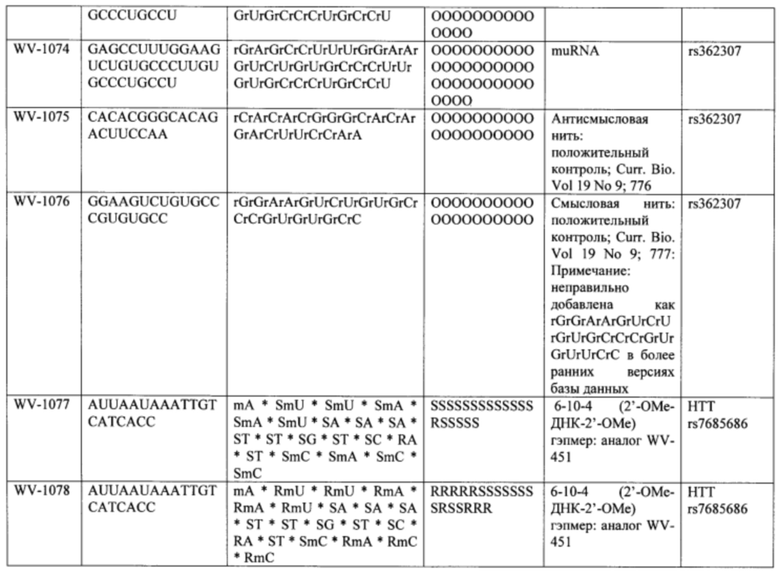
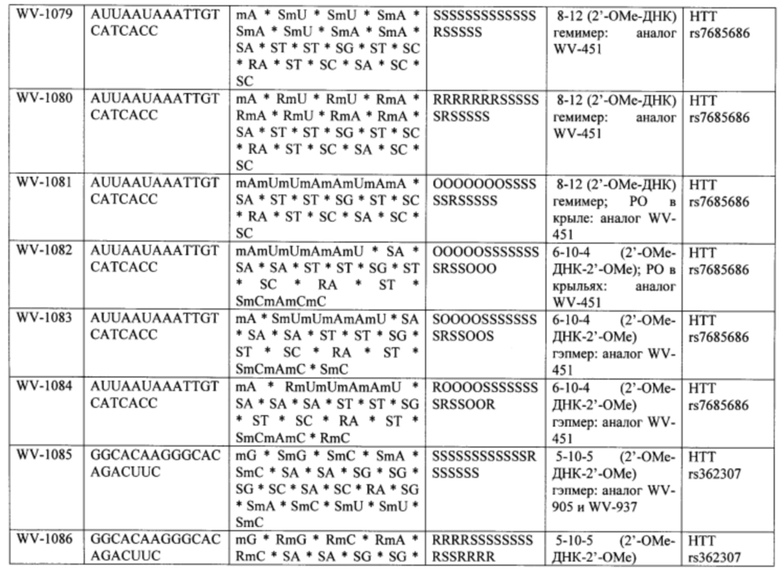
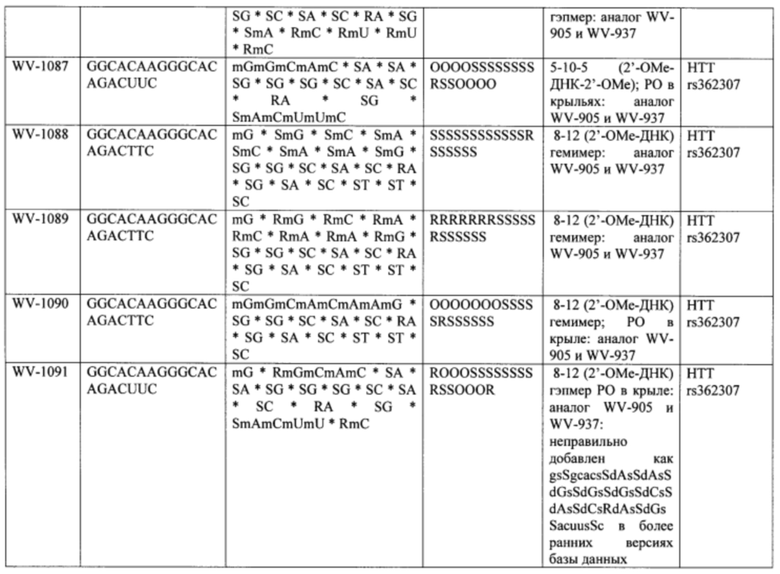
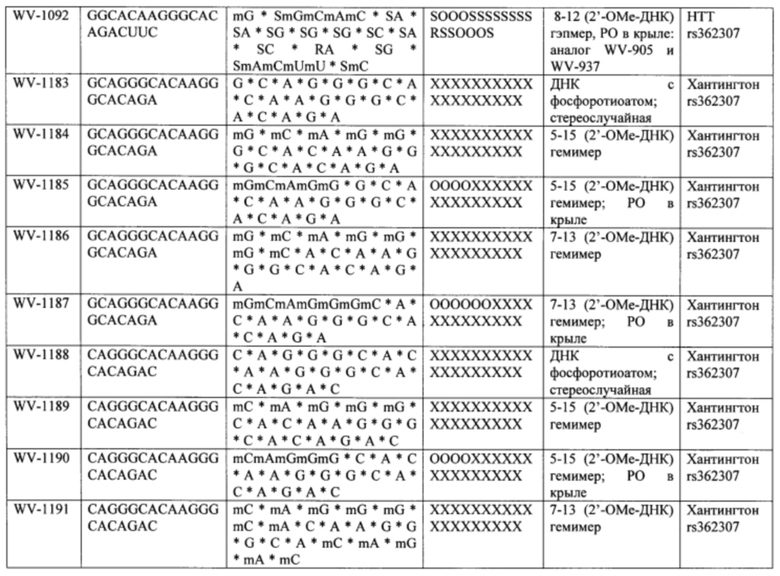
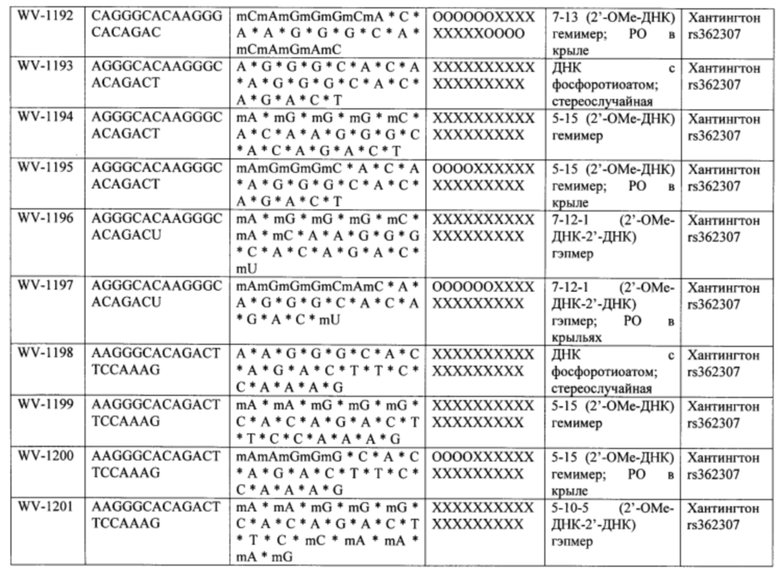
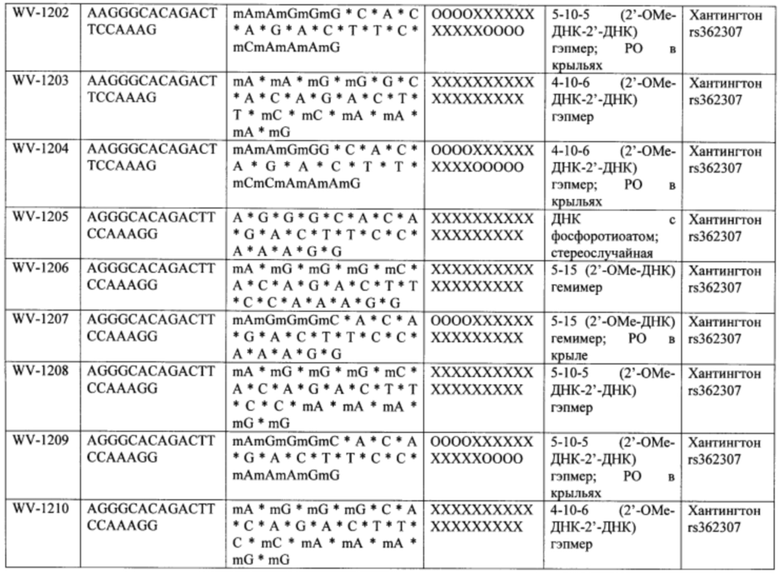
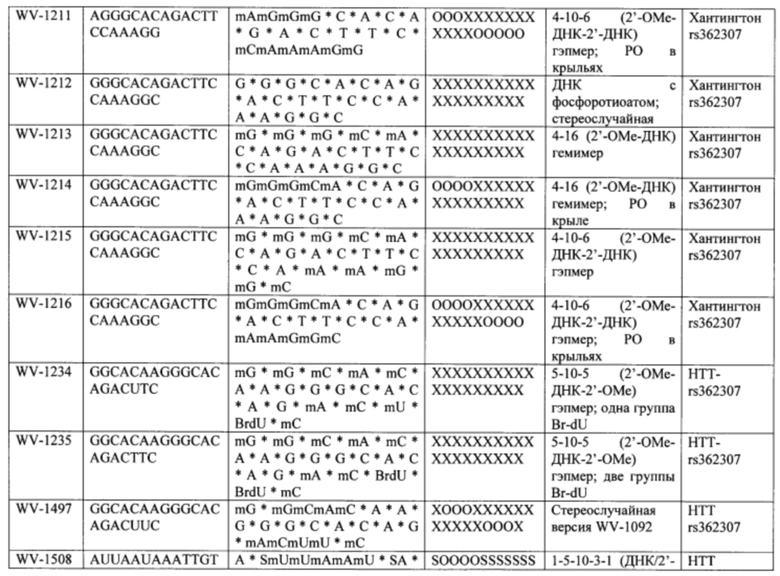
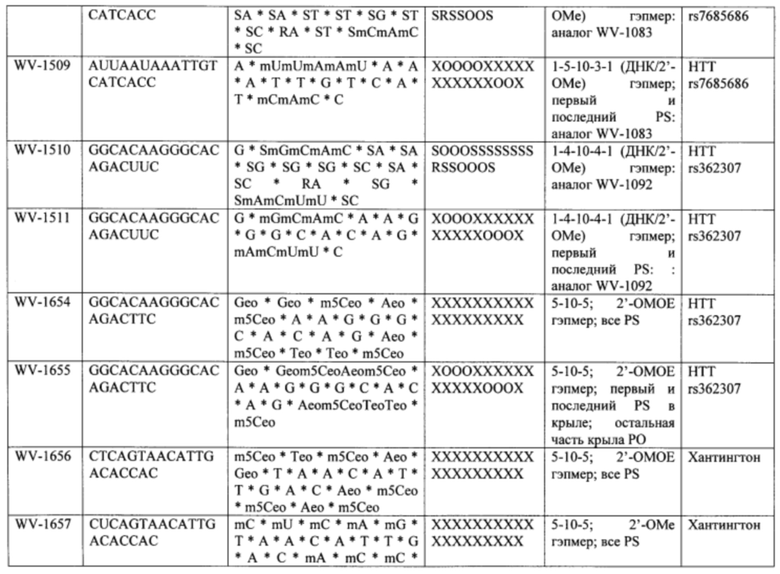
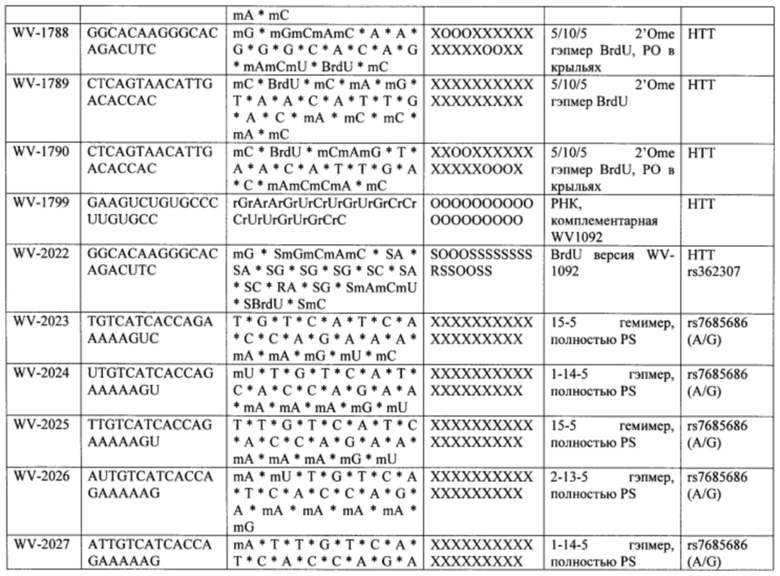
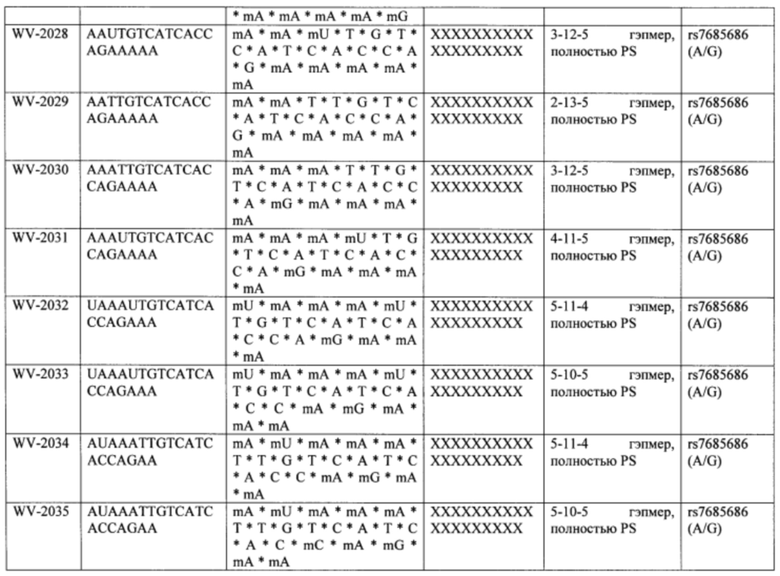
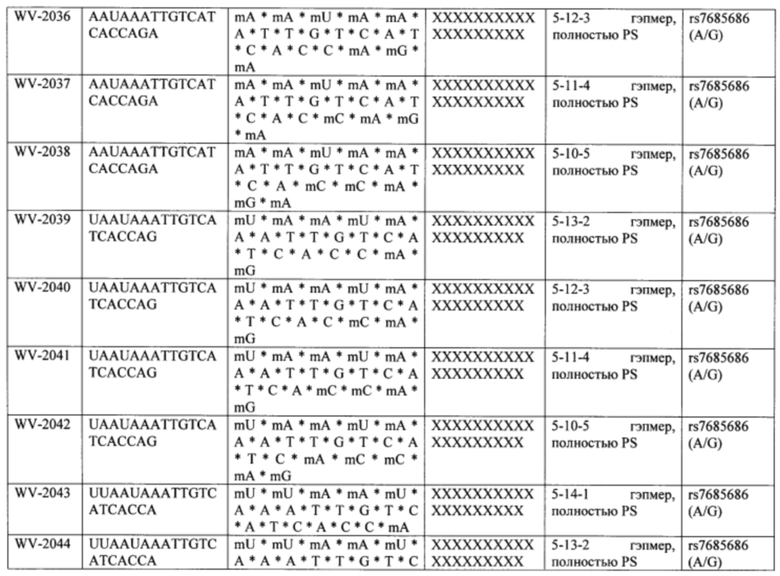
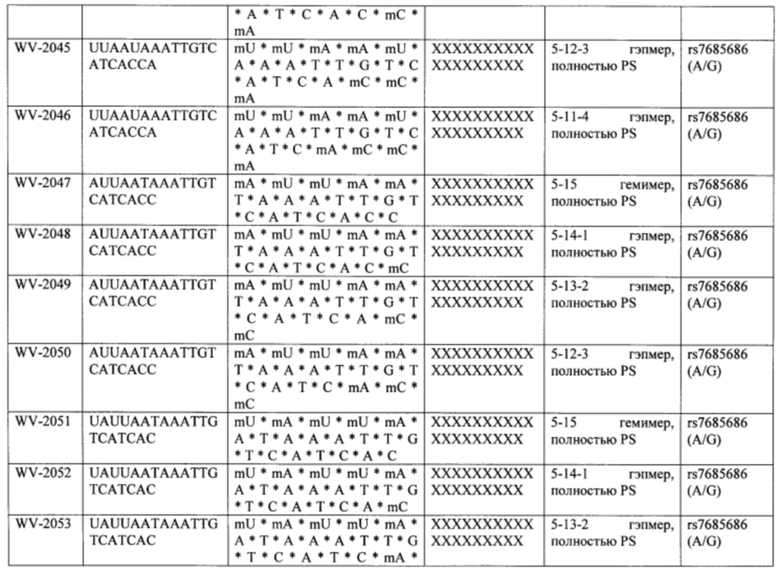
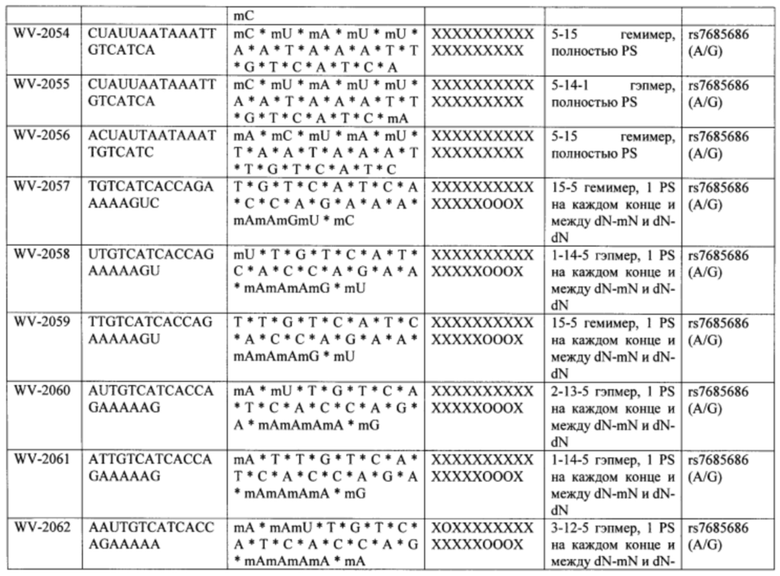
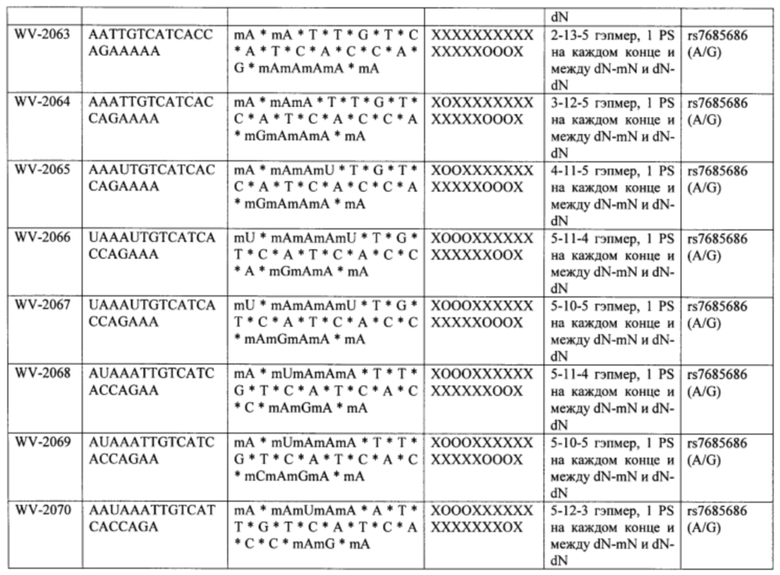
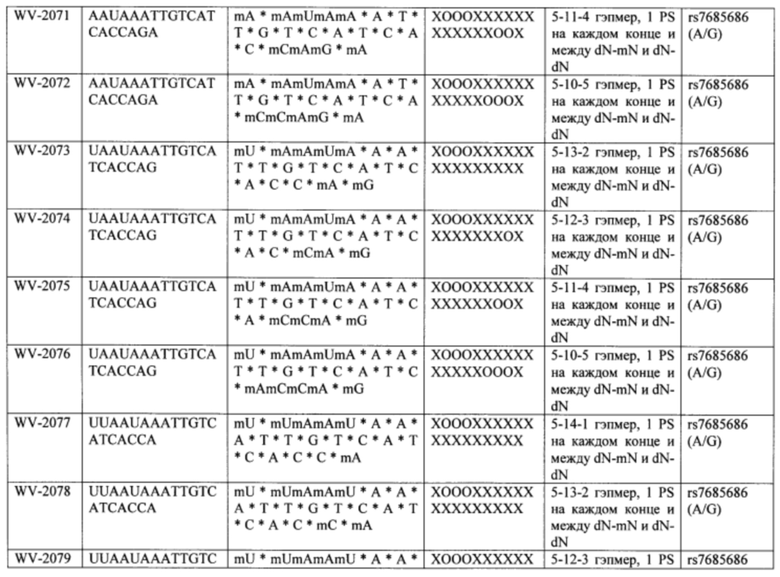
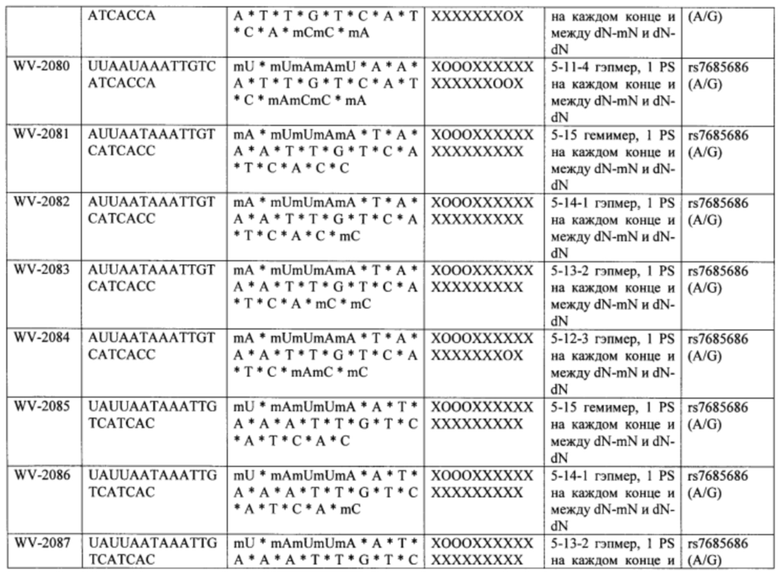
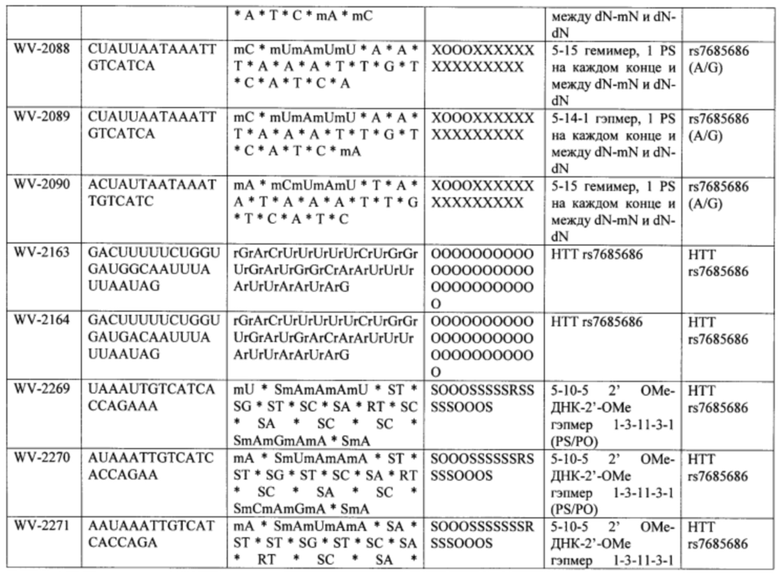
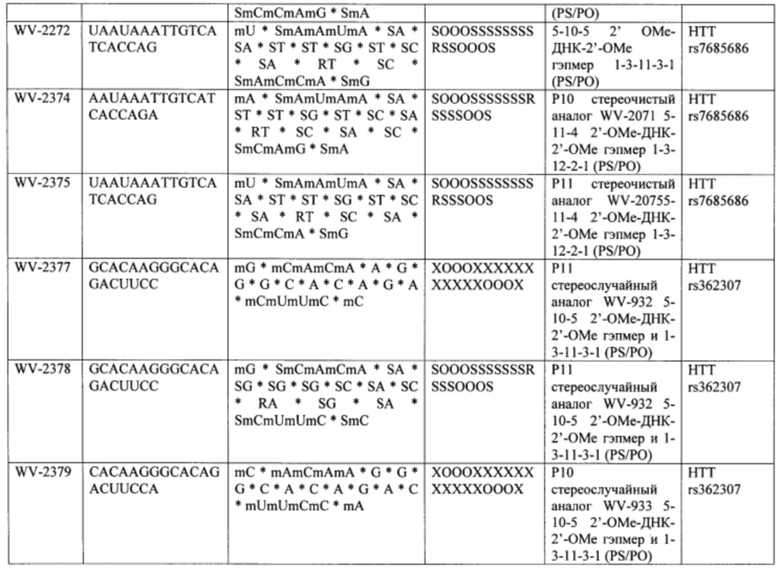
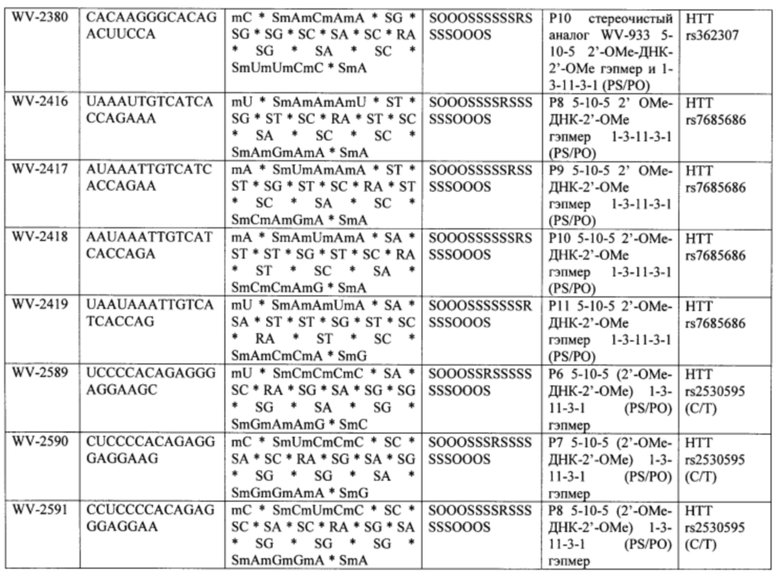
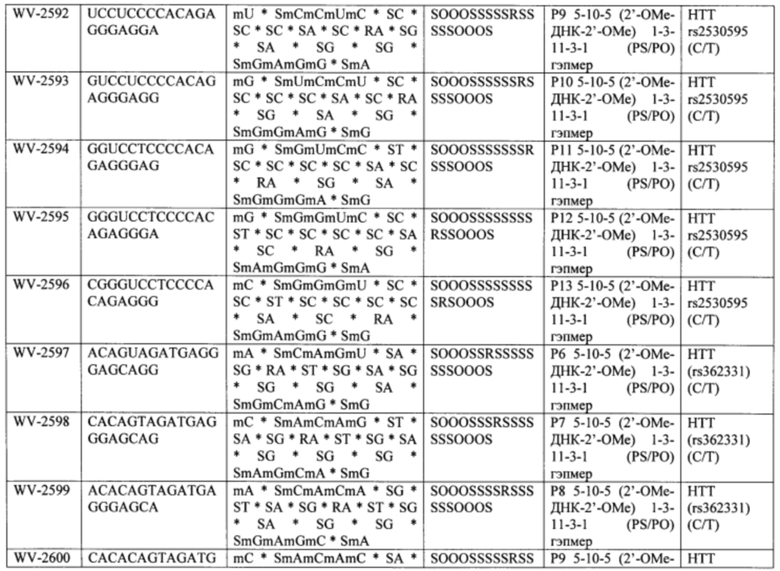
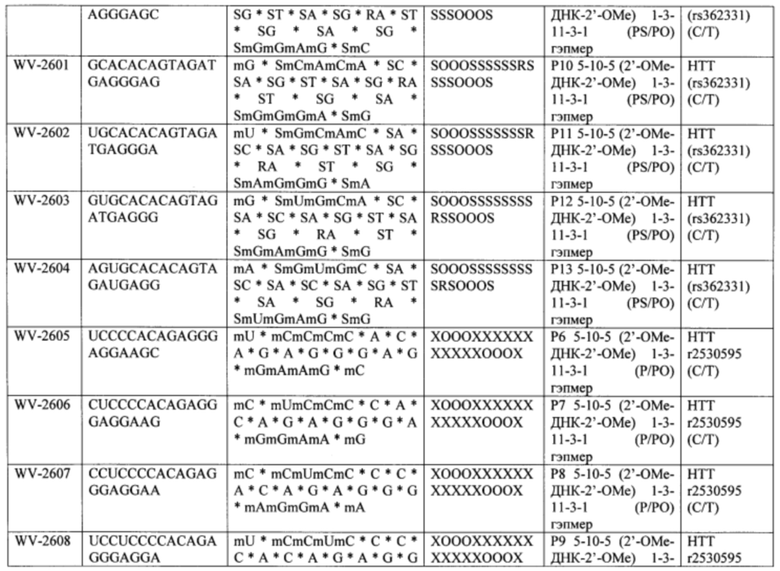
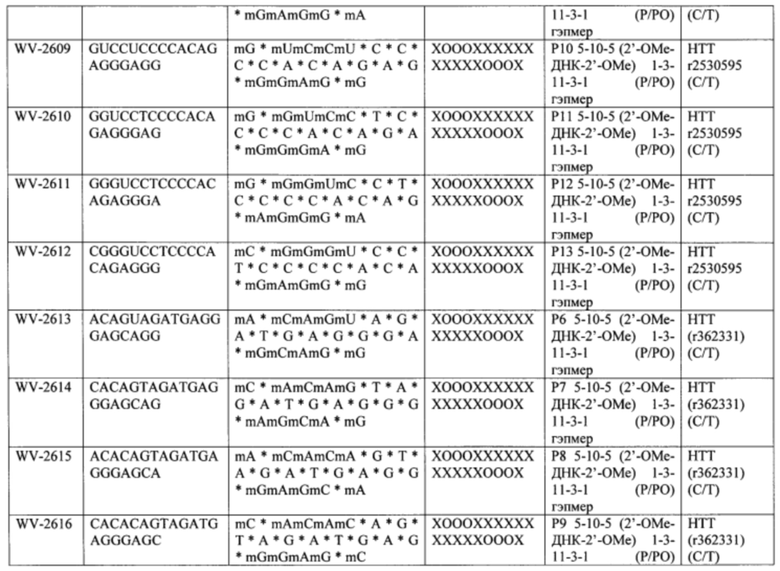
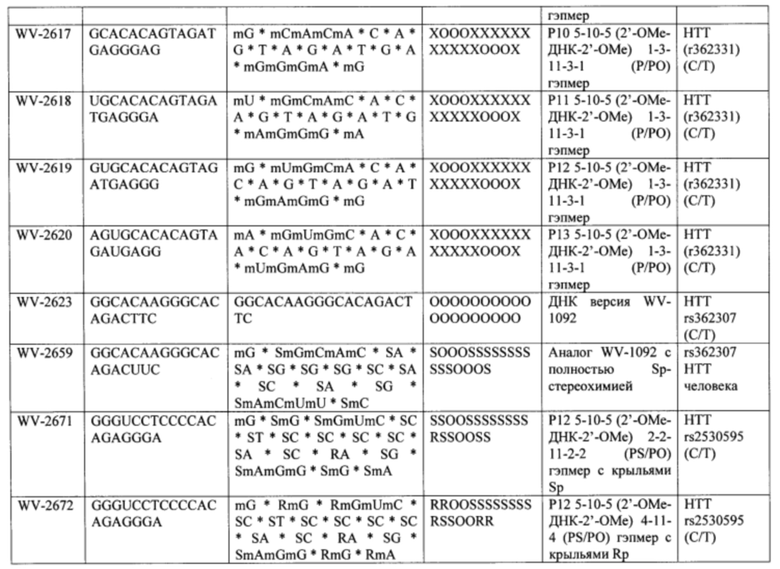
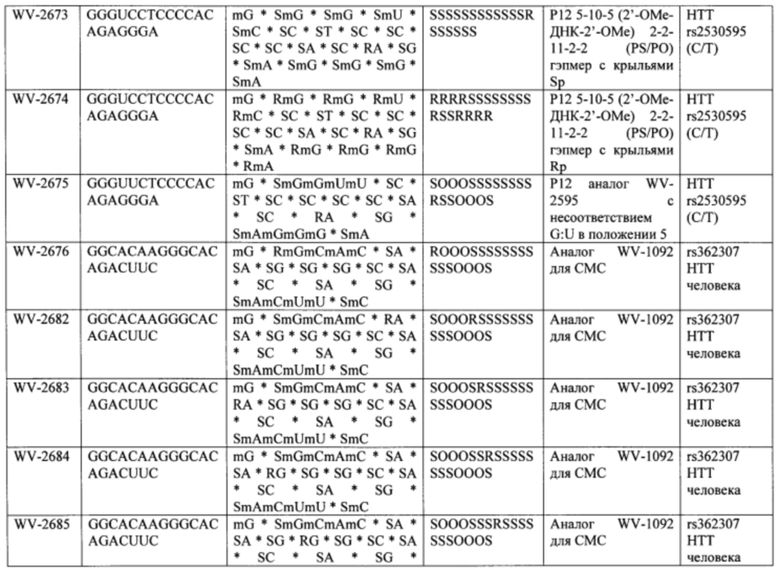
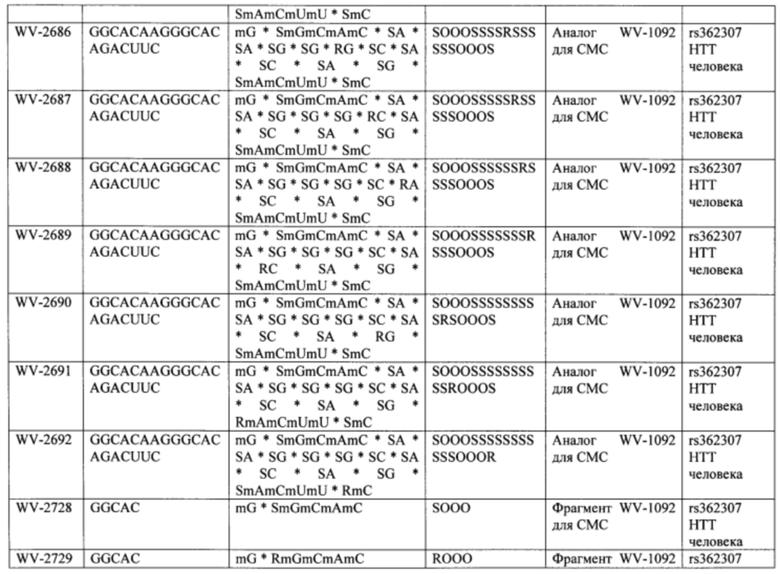
Сокращения:
2\': 2'
3\': 3'
5z': 5'
307: SNP rs362307
C6: С6-амино-линкерная группа
F, f: 2'-F
Htt, HTT: ген Хантингтин или болезнь Хантингтона
Lauric, Myristic, Palmitic, Stearic, Oleic, Linoleic, alpha-Linoleic, gamma-Linoleic, DHA, Turbinaric, Dilinoleic: лауриновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, линолевая кислота, альфа-линоленовая кислота, гамма-линоленовая кислота, докозагексаеновая кислота, турбинаровая кислота, дилинолеиновая кислота, соответственно.
muHtt или muHTT: мутантный ген хантингтина или генный продукт
ОМе: 2'-ОМе
О, РО: фосфодиэфир (фосфат)
*, PS: фосфоротиоат
R, Rp: фосфоротиоат в конформации Rp
S, Sp: фосфоротиоат в конформации Sp
WV: WV-
WV-: WV
X: фосфоротиоат, стереослучайный
Эквиваленты
Специалистам в данной области техники должно быть понятно, что приведенное выше описание некоторых иллюстративных вариантов реализации раскрытия является исключительно иллюстративным и не ограничивающим и предложено исключительно в качестве примера. Специалисты в данной области техники могут предложить многочисленные модификации и другие иллюстративные варианты реализации, которые включены в объем настоящего раскрытия. В частности, несмотря на то, что многие примеры, приведенные в настоящем описании, включают конкретные комбинации стадий способов или элементов систем, следует понимать, что указанные стадии и элементы можно объединять другим образом для решения указанных задач. Предполагается, что стадии, элементы и отличительные признаки, обсуждаемые только для одного варианта реализации, не исключены из других вариантов реализации, где они выполняют схожую роль. Кроме того, в случае одного или более ограничений «средство плюс функция», приведенных в последующей формуле изобретения, предполагается, что средства не ограничены средствами, предложенными в настоящем описании для осуществления указанной функции, но охватывают диапазон любых средств, которые известны на данный момент или будут разработаны впоследствии, для осуществления указанной функции.
Использование традиционных терминов, таких как «первый», «второй», «третий» и т.д. в формуле изобретения для модификации заявленного элемента само по себе не подразумевает какой-либо приоритет, предпочтение или расположение одного заявленного элемента по сравнению с другим или последовательность проведения стадий способа во времени, но указанные термины используют исключительно в качестве пояснений, используемых для проведения различий между одним заявленным элементом, имеющим определенное название, и другим элементом, имеющим такое же название (за исключением использования традиционных терминов). Аналогично, использование а), b) и т.д. или i), ii) и т.д. само по себе не подразумевает какой-либо приоритет, предпочтение или порядок стадий в формуле изобретения. Аналогично, использование указанных терминов в описании само по себе не подразумевает какой-либо требуемый приоритет, предпочтение или порядок.
Приведенное выше напечатанное описание рассматривают как достаточное для того, чтобы специалисты в данной области техники смогли реализовать раскрытие. Настоящее раскрытие не ограничено объемом предложенных примеров, так как примеры предложены исключительно в качестве иллюстрации одного из аспектов раскрытия, и другие функционально-эквивалентные варианты реализации включены в объем раскрытия. Различные модификации раскрытия, помимо тех, что показаны и описаны в настоящей заявке, будут очевидны специалистам в данной области техники после изучения приведенного выше описания и включены в объем прилагаемой формулы раскрытия. Преимущества и задачи настоящего раскрытия необязательно охвачены каждым вариантом реализации раскрытия.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> WAVE LIFE SCIENCES LTD.
<120> OLIGONUCLEOTIDE COMPOSITIONS AND METHODS THEREOF
<130> 2010581-0228
<140> PCT/US2016/043542
<141> 2016-07-22
<150> 62/331,960
<151> 2016-05-04
<150> 62/236,847
<151> 2015-10-02
<150> 62/195,779
<151> 2015-07-22
<160> 1565
<170> PatentIn version 3.5
<210> 1
<211> 105
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polynucleotide
<220>
<221> misc_feature
<222> (1)..(105)
<223> This sequence may encompass 10-35 "cag" repeating units,
wherein
some positions may be absent
<400> 1
cagcagcagc agcagcagca gcagcagcag cagcagcagc agcagcagca gcagcagcag
60
cagcagcagc agcagcagca gcagcagcag cagcagcagc agcag
105
<210> 2
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 2
gcctcagtct gcttcgcacc
20
<210> 3
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 3
gcctcagtct gcttcgcacc
20
<210> 4
<211> 13
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 4
aatcgatcga tcg
13
<210> 5
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 5
gcctcagtct gcttcgcacc
20
<210> 6
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 6
gcctcagtct gcttcgcacc
20
<210> 7
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 7
gcctcagtct gcttcgcacc
20
<210> 8
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 8
gcctcagtct gcttcgcacc
20
<210> 9
<211> 13
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 9
gugagcagcu gca
13
<210> 10
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 10
gggucctccc cacagaggga
20
<210> 11
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 11
gggucctccc cacagaggga
20
<210> 12
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 12
gugcacacag tagatgaggg
20
<210> 13
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 13
gugcacacag tagatgaggg
20
<210> 14
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 14
ggcacaaggg cacagacuuc
20
<210> 15
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 15
ggcacaaggg cacagacuuc
20
<210> 16
<211> 10
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 16
gggacgtctt
10
<210> 17
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 17
ggcacaaggg cacagacttc
20
<210> 18
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 18
uuuggaaguc ugugcccuug ugccc
25
<210> 19
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 19
gcctcagtct gcttcgcacc
20
<210> 20
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 20
gagcagctgc aacctggcaa
20
<210> 21
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 21
gggcacaagg gcacagactt
20
<210> 22
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 22
gcacaagggc acagacttcc
20
<210> 23
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 23
cacaagggca cagacttcca
20
<210> 24
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 24
acaagggcac agacttccaa
20
<210> 25
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 25
caagggcaca gacttccaaa
20
<210> 26
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 26
agcagctgca acctggcaac
20
<210> 27
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 27
gcagctgcaa cctggcaaca
20
<210> 28
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 28
cagctgcaac ctggcaacaa
20
<210> 29
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 29
agctgcaacc tggcaacaac
20
<210> 30
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 30
gctgcaacct ggcaacaacc
20
<210> 31
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 31
gggccaacag ccagcctgca
20
<210> 32
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 32
ggccaacagc cagcctgcag
20
<210> 33
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 33
gccaacagcc agcctgcagg
20
<210> 34
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 34
ccaacagcca gcctgcagga
20
<210> 35
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 35
caacagccag cctgcaggag
20
<210> 36
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 36
aacagccagc ctgcaggagg
20
<210> 37
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 37
attaataaat tgtcatcacc
20
<210> 38
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 38
ttcagtcatg acttcc
16
<210> 39
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 39
ttcagtcatg acttcc
16
<210> 40
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 40
gcctcagtct gcttcgcacc
20
<210> 41
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 41
ggcacaaggg cacagacttc
20
<210> 42
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<220>
<221> modified_base
<222> (4)..(4)
<223> t or u
<220>
<221> modified_base
<222> (8)..(8)
<223> t or u
<220>
<221> modified_base
<222> (10)..(10)
<223> t or u
<220>
<221> modified_base
<222> (13)..(14)
<223> t or u
<400> 42
gccncagncn gcnncgcacc
20
<210> 43
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 43
gccucagtct gcttcgcacc
20
<210> 44
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 44
gcctcagtct gcttcgcacc
20
<210> 45
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 45
gcctcagtct gcttcgcacc
20
<210> 46
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 46
gcctcagtct gcttcgcacc
20
<210> 47
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 47
gcctcagtct gcttcgcacc
20
<210> 48
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 48
gcctcagtct gcttcgcacc
20
<210> 49
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 49
gcctcagtct gcttcgcacc
20
<210> 50
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 50
gcctcagtct gcttcgcacc
20
<210> 51
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 51
gcctcagtct gcttcgcacc
20
<210> 52
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 52
gcctcagtct gcttcgcacc
20
<210> 53
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 53
gcctcagtct gcttcgcacc
20
<210> 54
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 54
gcctcagtct gcttcgcacc
20
<210> 55
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 55
gcctcagtct gcttcgcacc
20
<210> 56
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 56
gcctcagtct gcttcgcacc
20
<210> 57
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 57
gcctcagtct gcttcgcacc
20
<210> 58
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 58
gcctcagtct gcttcgcacc
20
<210> 59
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 59
gcctcagtct gcttcgcacc
20
<210> 60
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 60
gcctcagtct gcttcgcacc
20
<210> 61
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 61
gcctcagtct gcttcgcacc
20
<210> 62
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 62
gcctcagtct gcttcgcacc
20
<210> 63
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 63
gcctcagtct gcttcgcacc
20
<210> 64
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 64
gcctcagtct gcttcgcacc
20
<210> 65
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 65
gcctcagtct gcttcgcacc
20
<210> 66
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 66
gcctcagtct gcttcgcacc
20
<210> 67
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 67
cagtctgctt cg
12
<210> 68
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 68
cagtctgctt cg
12
<210> 69
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 69
cagtctgctt cg
12
<210> 70
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 70
cagtctgctt cg
12
<210> 71
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 71
cagtctgctt cg
12
<210> 72
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 72
cagtctgctt cg
12
<210> 73
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 73
cagtctgctt cg
12
<210> 74
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 74
cagtctgctt cg
12
<210> 75
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 75
cagtctgctt cg
12
<210> 76
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 76
cagtctgctt cg
12
<210> 77
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 77
ctcagtctgc ttcgc
15
<210> 78
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 78
cagtctgctt cg
12
<210> 79
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 79
cagtctgctt cg
12
<210> 80
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 80
gcctcagtct gcttcgcacc
20
<210> 81
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 81
gcctcagtct gcttcgcacc
20
<210> 82
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 82
gcctcagtct gcttcgcacc
20
<210> 83
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 83
gcctcagtct gcttcgcacc
20
<210> 84
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 84
gcctcagtct gcttcgcacc
20
<210> 85
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 85
gcctcagtct gcttcgcacc
20
<210> 86
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 86
gcctcagtct gcttcgcacc
20
<210> 87
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 87
gcctcagtct gcttcgcacc
20
<210> 88
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 88
gcctcagtct gcttcgcacc
20
<210> 89
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 89
gcctcagtct gcttcgcacc
20
<210> 90
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 90
gcctcagtct gcttcgcacc
20
<210> 91
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 91
gcctcagtct gcttcgcacc
20
<210> 92
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 92
gcctcagtct gcttcgcacc
20
<210> 93
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 93
gcctcagtct gcttcgcacc
20
<210> 94
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 94
gcctcagtct gcttcgcacc
20
<210> 95
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 95
gcctcagtct gcttcgcacc
20
<210> 96
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 96
gcctcagtct gcttcgcacc
20
<210> 97
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 97
gcctcagtct gcttcgcacc
20
<210> 98
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 98
gcctcagtct gcttcgcacc
20
<210> 99
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 99
gcctcagtct gcttcgcacc
20
<210> 100
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 100
gcctcagtct gcttcgcacc
20
<210> 101
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 101
gcctcagtct gcttcgcacc
20
<210> 102
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 102
gcctcagtct gcttcgcacc
20
<210> 103
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 103
gcctcagtct gcttcgcacc
20
<210> 104
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 104
gcctcagtct gcttcgcacc
20
<210> 105
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 105
gcctcagtct gcttcgcacc
20
<210> 106
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 106
gcctcagtct gcttcgcacc
20
<210> 107
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 107
gcctcagtct gcttcgcacc
20
<210> 108
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 108
gcctcagtct gcttcgcacc
20
<210> 109
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 109
gcctcagucu gcttcgcacc
20
<210> 110
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 110
gcctcagtct gcttcgcacc
20
<210> 111
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 111
gcctcagtct gcttcgcacc
20
<210> 112
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 112
gcctcagtct gcttcgcacc
20
<210> 113
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 113
gcctcagtct gcttcgcacc
20
<210> 114
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 114
gcctcagtct gcttcgcacc
20
<210> 115
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 115
gcctcagtct gcttcgcacc
20
<210> 116
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 116
gcctcagtct gcttcgcacc
20
<210> 117
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 117
gcctcagtct gcttcgcacc
20
<210> 118
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 118
gcctcagtct gcttcgcacc
20
<210> 119
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 119
gcctcagtct gcttcgcacc
20
<210> 120
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 120
gccucagucu gcuucgcacc
20
<210> 121
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 121
gccucagucu gcuucgcacc
20
<210> 122
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 122
gccucagucu gcuucgcacc
20
<210> 123
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 123
gccucagucu gcuucgcacc
20
<210> 124
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 124
gccucagucu gcuucgcacc
20
<210> 125
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 125
gccucagucu gcuucgcacc
20
<210> 126
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 126
gccucagucu gcuucgcacc
20
<210> 127
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 127
gccucagucu gcuucgcacc
20
<210> 128
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 128
gccucagucu gcuucgcacc
20
<210> 129
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 129
gccucagucu gcuucgcacc
20
<210> 130
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 130
gggcacaagg gcacagactt
20
<210> 131
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 131
ggcacaaggg cacagacttc
20
<210> 132
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 132
gcacaagggc acagacttcc
20
<210> 133
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 133
cacaagggca cagacttcca
20
<210> 134
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 134
acaagggcac agacttccaa
20
<210> 135
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 135
caagggcaca gacttccaaa
20
<210> 136
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 136
gggcacaagg gcacagactt
20
<210> 137
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 137
ggcacaaggg cacagacttc
20
<210> 138
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 138
gcacaagggc acagacttcc
20
<210> 139
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 139
cacaagggca cagacttcca
20
<210> 140
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 140
acaagggcac agacttccaa
20
<210> 141
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 141
caagggcaca gacttccaaa
20
<210> 142
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 142
gggcacaagg gcacagacuu
20
<210> 143
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 143
ggcacaaggg cacagacuuc
20
<210> 144
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 144
gcacaagggc acagacuucc
20
<210> 145
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 145
cacaagggca cagacuucca
20
<210> 146
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 146
acaagggcac agactuccaa
20
<210> 147
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 147
caagggcaca gacttccaaa
20
<210> 148
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 148
gcacaagggc acagacuucc
20
<210> 149
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 149
cacaagggca cagacuucca
20
<210> 150
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 150
acaagggcac agacuuccaa
20
<210> 151
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 151
caagggcaca gacuuccaaa
20
<210> 152
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 152
gcacaagggc acagacuucc
20
<210> 153
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 153
cacaagggca cagacuucca
20
<210> 154
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 154
acaagggcac agacuuccaa
20
<210> 155
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 155
caagggcaca gacuuccaaa
20
<210> 156
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 156
gggcacaagg gcacagacuu
20
<210> 157
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 157
ggcacaaggg cacagacuuc
20
<210> 158
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 158
gcacaagggc acagacuucc
20
<210> 159
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 159
cacaagggca cagacuucca
20
<210> 160
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 160
acaagggcac agactuccaa
20
<210> 161
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 161
caagggcaca gacttccaaa
20
<210> 162
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 162
gggcacaagg gcacagactt
20
<210> 163
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 163
ggcacaaggg cacagacttc
20
<210> 164
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 164
gcacaagggc acagacttcc
20
<210> 165
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 165
cacaagggca cagacttcca
20
<210> 166
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 166
acaagggcac agacttccaa
20
<210> 167
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 167
caagggcaca gacttccaaa
20
<210> 168
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 168
ggcacaaggg cacagacuuc
20
<210> 169
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 169
ggcacaaggg cacagacuuc
20
<210> 170
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 170
ggcacaaggg cacagacuuc
20
<210> 171
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 171
ggcacaaggg cacagacttc
20
<210> 172
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 172
ggcacaaggg cacagacttc
20
<210> 173
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 173
ggcacaaggg cacagacttc
20
<210> 174
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 174
ggcacaaggg cacagacuuc
20
<210> 175
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 175
ggcacaaggg cacagacuuc
20
<210> 176
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 176
gcagggcaca agggcacaga
20
<210> 177
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 177
cagggcacaa gggcacagac
20
<210> 178
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 178
agggcacaag ggcacagact
20
<210> 179
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 179
aagggcacag acttccaaag
20
<210> 180
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 180
agggcacaga cttccaaagg
20
<210> 181
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 181
gggcacagac ttccaaaggc
20
<210> 182
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 182
ggcacaaggg cacagacuuc
20
<210> 183
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 183
ggcacaaggg cacagacuuc
20
<210> 184
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 184
gggcacaagg gcacagactt
20
<210> 185
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 185
ggcacaaggg cacagacttc
20
<210> 186
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 186
gcacaagggc acagacttcc
20
<210> 187
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 187
gggcacaagg gcacagactt
20
<210> 188
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 188
ggcacaaggg cacagacttc
20
<210> 189
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 189
gcacaagggc acagacttcc
20
<210> 190
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 190
ggcacaaggg cacagacuuc
20
<210> 191
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 191
ggcacaaggg cacagacuuc
20
<210> 192
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 192
ggcacaaggg cacagacuuc
20
<210> 193
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 193
ggcacaaggg cacagacttc
20
<210> 194
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 194
gagcagctgc aacctggcaa
20
<210> 195
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 195
agcagctgca acctggcaac
20
<210> 196
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 196
gcagctgcaa cctggcaaca
20
<210> 197
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 197
cagctgcaac ctggcaacaa
20
<210> 198
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 198
agctgcaacc tggcaacaac
20
<210> 199
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 199
gctgcaacct ggcaacaacc
20
<210> 200
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 200
gagcagctgc aacctggcaa
20
<210> 201
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 201
agcagctgca acctggcaac
20
<210> 202
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 202
gcagctgcaa cctggcaaca
20
<210> 203
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 203
cagcugcaac ctggcaacaa
20
<210> 204
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 204
agcugcaacc tggcaacaac
20
<210> 205
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 205
gcugcaacct ggcaacaacc
20
<210> 206
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 206
gagcagctgc aacctggcaa
20
<210> 207
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 207
agcagctgca acctggcaac
20
<210> 208
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 208
gcagctgcaa cctggcaaca
20
<210> 209
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 209
cagcugcaac ctggcaacaa
20
<210> 210
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 210
agcugcaacc tggcaacaac
20
<210> 211
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 211
gcugcaacct ggcaacaacc
20
<210> 212
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 212
gagcagctgc aaccuggcaa
20
<210> 213
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 213
gagcagctgc aaccuggcaa
20
<210> 214
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 214
agcagctgca acctggcaac
20
<210> 215
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 215
agcagctgca acctggcaac
20
<210> 216
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 216
gcagctgcaa ccuggcaaca
20
<210> 217
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 217
gcagctgcaa ccuggcaaca
20
<210> 218
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 218
gagcagctgc aacctggcaa
20
<210> 219
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 219
agcagctgca acctggcaac
20
<210> 220
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 220
gcagctgcaa cctggcaaca
20
<210> 221
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 221
cagcugcaac ctggcaacaa
20
<210> 222
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 222
agcugcaacc tggcaacaac
20
<210> 223
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 223
gcugcaacct ggcaacaacc
20
<210> 224
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 224
gagcagctgc aacctggcaa
20
<210> 225
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 225
agcagctgca acctggcaac
20
<210> 226
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 226
gcagctgcaa cctggcaaca
20
<210> 227
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 227
cagctgcaac ctggcaacaa
20
<210> 228
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 228
agctgcaacc tggcaacaac
20
<210> 229
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 229
gctgcaacct ggcaacaacc
20
<210> 230
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 230
gggccaacag ccagcctgca
20
<210> 231
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 231
ggccaacagc cagcctgcag
20
<210> 232
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 232
gccaacagcc agcctgcagg
20
<210> 233
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 233
ccaacagcca gcctgcagga
20
<210> 234
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 234
caacagccag cctgcaggag
20
<210> 235
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 235
aacagccagc ctgcaggagg
20
<210> 236
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 236
gggccaacag ccagcctgca
20
<210> 237
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 237
ggccaacagc cagcctgcag
20
<210> 238
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 238
gccaacagcc agcctgcagg
20
<210> 239
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 239
ccaacagcca gcctgcagga
20
<210> 240
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 240
caacagccag cctgcaggag
20
<210> 241
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 241
aacagccagc ctgcaggagg
20
<210> 242
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 242
gggccaacag ccagccugca
20
<210> 243
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 243
ggccaacagc cagccugcag
20
<210> 244
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 244
gccaacagcc agcctgcagg
20
<210> 245
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 245
ccaacagcca gcctgcagga
20
<210> 246
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 246
caacagccag cctgcaggag
20
<210> 247
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 247
aacagccagc ctgcaggagg
20
<210> 248
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 248
gggccaacag ccagccugca
20
<210> 249
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 249
gggccaacag ccagccugca
20
<210> 250
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 250
ggccaacagc cagccugcag
20
<210> 251
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 251
ggccaacagc cagccugcag
20
<210> 252
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 252
gccaacagcc agccugcagg
20
<210> 253
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 253
gccaacagcc agccugcagg
20
<210> 254
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 254
gggccaacag ccagccugca
20
<210> 255
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 255
ggccaacagc cagccugcag
20
<210> 256
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 256
gccaacagcc agcctgcagg
20
<210> 257
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 257
ccaacagcca gcctgcagga
20
<210> 258
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 258
caacagccag cctgcaggag
20
<210> 259
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 259
aacagccagc ctgcaggagg
20
<210> 260
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 260
gggccaacag ccagcctgca
20
<210> 261
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 261
ggccaacagc cagcctgcag
20
<210> 262
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 262
gccaacagcc agcctgcagg
20
<210> 263
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 263
ccaacagcca gcctgcagga
20
<210> 264
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 264
caacagccag cctgcaggag
20
<210> 265
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 265
aacagccagc ctgcaggagg
20
<210> 266
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 266
attaataaat tgtcatcacc
20
<210> 267
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 267
attaataaat tgtcatcacc
20
<210> 268
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 268
attaataaat tgtcatcacc
20
<210> 269
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 269
auuaauaaat tgtcatcacc
20
<210> 270
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 270
auuaauaaat tgtcatcacc
20
<210> 271
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 271
auuaauaaat tgtcatcacc
20
<210> 272
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 272
auuaauaaat tgtcatcacc
20
<210> 273
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 273
auuaauaaat tgtcatcacc
20
<210> 274
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 274
auuaauaaat tgtcatcacc
20
<210> 275
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 275
auuaauaaat tgtcatcacc
20
<210> 276
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 276
auuaauaaat tgtcatcacc
20
<210> 277
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 277
auuaauaaat tgtcatcacc
20
<210> 278
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 278
auuaauaaat tgtcatcacc
20
<210> 279
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 279
tgtcatcacc agaaaaaguc
20
<210> 280
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 280
utgtcatcac cagaaaaagu
20
<210> 281
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 281
ttgtcatcac cagaaaaagu
20
<210> 282
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 282
autgtcatca ccagaaaaag
20
<210> 283
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 283
attgtcatca ccagaaaaag
20
<210> 284
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 284
aautgtcatc accagaaaaa
20
<210> 285
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 285
aattgtcatc accagaaaaa
20
<210> 286
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 286
aaattgtcat caccagaaaa
20
<210> 287
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 287
aaautgtcat caccagaaaa
20
<210> 288
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 288
uaaautgtca tcaccagaaa
20
<210> 289
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 289
uaaautgtca tcaccagaaa
20
<210> 290
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 290
auaaattgtc atcaccagaa
20
<210> 291
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 291
auaaattgtc atcaccagaa
20
<210> 292
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 292
aauaaattgt catcaccaga
20
<210> 293
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 293
aauaaattgt catcaccaga
20
<210> 294
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 294
aauaaattgt catcaccaga
20
<210> 295
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 295
uaauaaattg tcatcaccag
20
<210> 296
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 296
uaauaaattg tcatcaccag
20
<210> 297
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 297
uaauaaattg tcatcaccag
20
<210> 298
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 298
uaauaaattg tcatcaccag
20
<210> 299
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 299
uuaauaaatt gtcatcacca
20
<210> 300
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 300
uuaauaaatt gtcatcacca
20
<210> 301
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 301
uuaauaaatt gtcatcacca
20
<210> 302
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 302
uuaauaaatt gtcatcacca
20
<210> 303
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 303
auuaataaat tgtcatcacc
20
<210> 304
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 304
auuaataaat tgtcatcacc
20
<210> 305
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 305
auuaataaat tgtcatcacc
20
<210> 306
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 306
auuaataaat tgtcatcacc
20
<210> 307
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 307
uauuaataaa ttgtcatcac
20
<210> 308
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 308
uauuaataaa ttgtcatcac
20
<210> 309
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 309
uauuaataaa ttgtcatcac
20
<210> 310
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 310
cuauuaataa attgtcatca
20
<210> 311
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 311
cuauuaataa attgtcatca
20
<210> 312
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 312
acuautaata aattgtcatc
20
<210> 313
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 313
tgtcatcacc agaaaaaguc
20
<210> 314
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 314
utgtcatcac cagaaaaagu
20
<210> 315
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 315
ttgtcatcac cagaaaaagu
20
<210> 316
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 316
autgtcatca ccagaaaaag
20
<210> 317
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 317
attgtcatca ccagaaaaag
20
<210> 318
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 318
aautgtcatc accagaaaaa
20
<210> 319
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 319
aattgtcatc accagaaaaa
20
<210> 320
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 320
aaattgtcat caccagaaaa
20
<210> 321
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 321
aaautgtcat caccagaaaa
20
<210> 322
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 322
uaaautgtca tcaccagaaa
20
<210> 323
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 323
uaaautgtca tcaccagaaa
20
<210> 324
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 324
auaaattgtc atcaccagaa
20
<210> 325
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 325
auaaattgtc atcaccagaa
20
<210> 326
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 326
aauaaattgt catcaccaga
20
<210> 327
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 327
aauaaattgt catcaccaga
20
<210> 328
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 328
aauaaattgt catcaccaga
20
<210> 329
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 329
uaauaaattg tcatcaccag
20
<210> 330
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 330
uaauaaattg tcatcaccag
20
<210> 331
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 331
uaauaaattg tcatcaccag
20
<210> 332
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 332
uaauaaattg tcatcaccag
20
<210> 333
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 333
uuaauaaatt gtcatcacca
20
<210> 334
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 334
uuaauaaatt gtcatcacca
20
<210> 335
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 335
uuaauaaatt gtcatcacca
20
<210> 336
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 336
uuaauaaatt gtcatcacca
20
<210> 337
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 337
auuaataaat tgtcatcacc
20
<210> 338
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 338
auuaataaat tgtcatcacc
20
<210> 339
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 339
auuaataaat tgtcatcacc
20
<210> 340
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 340
auuaataaat tgtcatcacc
20
<210> 341
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 341
uauuaataaa ttgtcatcac
20
<210> 342
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 342
uauuaataaa ttgtcatcac
20
<210> 343
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 343
uauuaataaa ttgtcatcac
20
<210> 344
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 344
cuauuaataa attgtcatca
20
<210> 345
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 345
cuauuaataa attgtcatca
20
<210> 346
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 346
acuautaata aattgtcatc
20
<210> 347
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 347
gggcacaagg gcacagactt
20
<210> 348
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 348
ggcacaaggg cacagacttc
20
<210> 349
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 349
gcacaagggc acagacttcc
20
<210> 350
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 350
cacaagggca cagacttcca
20
<210> 351
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 351
acaagggcac agacttccaa
20
<210> 352
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 352
caagggcaca gacttccaaa
20
<210> 353
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 353
ggcacaaggg cacagacuuc
20
<210> 354
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 354
ggcacaaggg cacagacuuc
20
<210> 355
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 355
ggcacaaggg cacagacuuc
20
<210> 356
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 356
ggcacaaggg cacagacttc
20
<210> 357
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 357
ggcacaaggg cacagacttc
20
<210> 358
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 358
ggcacaaggg cacagacttc
20
<210> 359
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 359
ggcacaaggg cacagacuuc
20
<210> 360
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 360
ggcacaaggg cacagacuuc
20
<210> 361
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 361
gcagggcaca agggcacaga
20
<210> 362
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 362
cagggcacaa gggcacagac
20
<210> 363
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 363
agggcacaag ggcacagact
20
<210> 364
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 364
aagggcacag acttccaaag
20
<210> 365
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 365
agggcacaga cttccaaagg
20
<210> 366
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 366
gggcacagac ttccaaaggc
20
<210> 367
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 367
ggcacaaggg cacagacuuc
20
<210> 368
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 368
gagcagctgc aacctggcaa
20
<210> 369
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 369
agcagctgca acctggcaac
20
<210> 370
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 370
gcagctgcaa cctggcaaca
20
<210> 371
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 371
cagctgcaac ctggcaacaa
20
<210> 372
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 372
agctgcaacc tggcaacaac
20
<210> 373
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 373
gctgcaacct ggcaacaacc
20
<210> 374
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 374
gggccaacag ccagcctgca
20
<210> 375
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 375
ggccaacagc cagcctgcag
20
<210> 376
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 376
gccaacagcc agcctgcagg
20
<210> 377
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 377
ccaacagcca gcctgcagga
20
<210> 378
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 378
caacagccag cctgcaggag
20
<210> 379
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 379
aacagccagc ctgcaggagg
20
<210> 380
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 380
attaataaat tgtcatcacc
20
<210> 381
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 381
attaataaat tgtcatcacc
20
<210> 382
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 382
attaataaat tgtcatcacc
20
<210> 383
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 383
auuaauaaat tgtcatcacc
20
<210> 384
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 384
auuaauaaat tgtcatcacc
20
<210> 385
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 385
auuaauaaat tgtcatcacc
20
<210> 386
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 386
auuaauaaat tgtcatcacc
20
<210> 387
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 387
auuaauaaat tgtcatcacc
20
<210> 388
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 388
auuaauaaat tgtcatcacc
20
<210> 389
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 389
auuaauaaat tgtcatcacc
20
<210> 390
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 390
auuaauaaat tgtcatcacc
20
<210> 391
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 391
auuaauaaat tgtcatcacc
20
<210> 392
<211> 27
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 392
gcgtttgctc ttcttcttgc gtttttt
27
<210> 393
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 393
gcctcagtct gcttcgcacc
20
<210> 394
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 394
gcctcagtct gcttcgcacc
20
<210> 395
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 395
gcctcagtct gcttcgcacc
20
<210> 396
<211> 27
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 396
gcgtttgctc ttcttcttgc gtttttt
27
<210> 397
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 397
gcctcagtct gcttcgcacc
20
<210> 398
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 398
gcctcagtct gcttcgcacc
20
<210> 399
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 399
gcctcagtct gcttcgcacc
20
<210> 400
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 400
gcctcagtct gcttcgcacc
20
<210> 401
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 401
gcctcagtct gcttcgcacc
20
<210> 402
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 402
gcctcagtct gcttcgcacc
20
<210> 403
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 403
gcctcagtct gcttcgcacc
20
<210> 404
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 404
gcctcagtct gcttcgcacc
20
<210> 405
<211> 27
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 405
gcgtttgctc ttcttcttgc gtttttt
27
<210> 406
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 406
gtccctgaag atgtcaatgc
20
<210> 407
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 407
gtccctgaag atgtcaatgc
20
<210> 408
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 408
gtccctgaag atgtcaatgc
20
<210> 409
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 409
gtccctgaag atgtcaatgc
20
<210> 410
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 410
gtccctgaag atgtcaatgc
20
<210> 411
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 411
uucuagaccu guuuugcuut t
21
<210> 412
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 412
uucuagaccu guuuugcuut t
21
<210> 413
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 413
uucuagaccu guuuugcuut t
21
<210> 414
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 414
uucuagaccu guuuugcuut t
21
<210> 415
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 415
uucuagaccu guuuugcuut t
21
<210> 416
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 416
uucuagaccu guuuugcuut t
21
<210> 417
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 417
uucuagaccu guuuugcuut t
21
<210> 418
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 418
uucuagaccu guuuugcuut t
21
<210> 419
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 419
uucuagaccu guuuugcuut t
21
<210> 420
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 420
uucuagaccu guuuugcuut t
21
<210> 421
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 421
uucuagaccu guuuugcuut t
21
<210> 422
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 422
uucuagaccu guuuugcuut t
21
<210> 423
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 423
uucuagaccu guuuugcuut t
21
<210> 424
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 424
uucuagaccu guuuugcuut t
21
<210> 425
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 425
uucuagaccu guuuugcuut t
21
<210> 426
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 426
uucuagaccu guuuugcuut t
21
<210> 427
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 427
uucuagaccu guuuugcuut t
21
<210> 428
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 428
uucuagaccu guuuugcuut t
21
<210> 429
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 429
uucuagaccu guuuugcuut t
21
<210> 430
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 430
uucuagaccu guuuugcuut t
21
<210> 431
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 431
uucuagaccu guuuugcuut t
21
<210> 432
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 432
uucuagaccu guuuugcuut t
21
<210> 433
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 433
uucuagaccu guuuugcuut t
21
<210> 434
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 434
uucuagaccu guuuugcuut t
21
<210> 435
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 435
uucuagaccu guuuugcuut t
21
<210> 436
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 436
uucuagaccu guuuugcuut t
21
<210> 437
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 437
uucuagaccu guuuugcuut t
21
<210> 438
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 438
uucuagaccu guuuugcuut t
21
<210> 439
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 439
uucuagaccu guuuugcuut t
21
<210> 440
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 440
uucuagaccu guuuugcuut t
21
<210> 441
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 441
uucuagaccu guuuugcuut t
21
<210> 442
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 442
uucuagaccu guuuugcuut t
21
<210> 443
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 443
uucuagaccu guuuugcuut t
21
<210> 444
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 444
uucuagaccu guuuugcuut t
21
<210> 445
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 445
uucuagaccu guuuugcuut t
21
<210> 446
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 446
uucuagaccu guuuugcuut t
21
<210> 447
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 447
uucuagaccu guuuugcuut t
21
<210> 448
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 448
uucuagaccu guuuugcuut t
21
<210> 449
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 449
uucuagaccu guuuugcuut t
21
<210> 450
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 450
uucuagaccu guuuugcuut t
21
<210> 451
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 451
aagcaaaaca ggucuagaat t
21
<210> 452
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 452
aagcaaaaca ggucuagaat t
21
<210> 453
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 453
aagcaaaaca ggucuagaat t
21
<210> 454
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 454
aagcaaaaca ggucuagaat t
21
<210> 455
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 455
aagcaaaaca ggucuagaat t
21
<210> 456
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 456
aagcaaaaca ggucuagaat t
21
<210> 457
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 457
aagcaaaaca ggucuagaat t
21
<210> 458
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 458
aagcaaaaca ggucuagaat t
21
<210> 459
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 459
aagcaaaaca ggucuagaat t
21
<210> 460
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 460
aagcaaaaca ggucuagaat t
21
<210> 461
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 461
aagcaaaaca ggucuagaat t
21
<210> 462
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 462
aagcaaaaca ggucuagaat t
21
<210> 463
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 463
aagcaaaaca ggucuagaat t
21
<210> 464
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 464
aagcaaaaca ggucuagaat t
21
<210> 465
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 465
aagcaaaaca ggucuagaat t
21
<210> 466
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 466
aagcaaaaca ggucuagaat t
21
<210> 467
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 467
aagcaaaaca ggucuagaat t
21
<210> 468
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 468
aagcaaaaca ggucuagaat t
21
<210> 469
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 469
aagcaaaaca ggucuagaat t
21
<210> 470
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 470
aagcaaaaca ggucuagaat t
21
<210> 471
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 471
aagcaaaaca ggucuagaat t
21
<210> 472
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 472
aagcaaaaca ggucuagaat t
21
<210> 473
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 473
aagcaaaaca ggucuagaat t
21
<210> 474
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 474
aagcaaaaca ggucuagaat t
21
<210> 475
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 475
aagcaaaaca ggucuagaat t
21
<210> 476
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 476
aagcaaaaca ggucuagaat t
21
<210> 477
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 477
aagcaaaaca ggucuagaat t
21
<210> 478
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 478
aagcaaaaca ggucuagaat t
21
<210> 479
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 479
aagcaaaaca ggucuagaat t
21
<210> 480
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 480
aagcaaaaca ggucuagaat t
21
<210> 481
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 481
aagcaaaaca ggucuagaat t
21
<210> 482
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 482
aagcaaaaca ggucuagaat t
21
<210> 483
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 483
aagcaaaaca ggucuagaat t
21
<210> 484
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 484
aagcaaaaca ggucuagaat t
21
<210> 485
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 485
aagcaaaaca ggucuagaat t
21
<210> 486
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 486
aagcaaaaca ggucuagaat t
21
<210> 487
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 487
aagcaaaaca ggucuagaat t
21
<210> 488
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 488
aagcaaaaca ggucuagaat t
21
<210> 489
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 489
aagcaaaaca ggucuagaat t
21
<210> 490
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 490
aagcaaaaca ggucuagaat t
21
<210> 491
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 491
aagcaaaaca ggucuagaat t
21
<210> 492
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 492
aagcaaaaca ggucuagaat t
21
<210> 493
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 493
aagcaaaaca ggucuagaat t
21
<210> 494
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 494
aagcaaaaca ggucuagaat t
21
<210> 495
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 495
aagcaaaaca ggucuagaat t
21
<210> 496
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 496
aagcaaaaca ggucuagaat t
21
<210> 497
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 497
aagcaaaaca ggucuagaat t
21
<210> 498
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 498
aagcaaaaca ggucuagaat t
21
<210> 499
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 499
aagcaaaaca ggucuagaat t
21
<210> 500
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 500
aagcaaaaca ggucuagaat t
21
<210> 501
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 501
aagcaaaaca ggucuagaat t
21
<210> 502
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 502
aagcaaaaca ggucuagaat t
21
<210> 503
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 503
aagcaaaaca ggucuagaat t
21
<210> 504
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 504
aagcaaaaca ggucuagaat t
21
<210> 505
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 505
aagcaaaaca ggucuagaat t
21
<210> 506
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 506
aagcaaaaca ggucuagaat t
21
<210> 507
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 507
aagcaaaaca ggucuagaat t
21
<210> 508
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 508
aagcaaaaca ggucuagaat t
21
<210> 509
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 509
aagcaaaaca ggucuagaat t
21
<210> 510
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 510
aagcaaaaca ggucuagaat t
21
<210> 511
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 511
aagcaaaaca ggucuagaat t
21
<210> 512
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 512
aagcaaaaca ggucuagaat t
21
<210> 513
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 513
aagcaaaaca ggucuagaat t
21
<210> 514
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 514
aagcaaaaca ggucuagaat t
21
<210> 515
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 515
aagcaaaaca ggucuagaat t
21
<210> 516
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 516
aagcaaaaca ggucuagaat t
21
<210> 517
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 517
aagcaaaaca ggucuagaat t
21
<210> 518
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 518
aagcaaaaca ggucuagaat t
21
<210> 519
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 519
aagcaaaaca ggucuagaat t
21
<210> 520
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 520
aagcaaaaca ggucuagaat t
21
<210> 521
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 521
aagcaaaaca ggucuagaat t
21
<210> 522
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 522
aagcaaaaca ggucuagaat t
21
<210> 523
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 523
aagcaaaaca ggucuagaat t
21
<210> 524
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 524
aagcaaaaca ggucuagaat t
21
<210> 525
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 525
aagcaaaaca ggucuagaat t
21
<210> 526
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 526
aagcaaaaca ggucuagaat t
21
<210> 527
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 527
aagcaaaaca ggucuagaat t
21
<210> 528
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 528
aagcaaaaca ggucuagaat t
21
<210> 529
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 529
aagcaaaaca ggucuagaat t
21
<210> 530
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 530
aagcaaaaca ggucuagaat t
21
<210> 531
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 531
ccctctggat tgagcatcca
20
<210> 532
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 532
aagctttggt tgggcaacac
20
<210> 533
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 533
agtcacttgg gagcttctcc
20
<210> 534
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 534
cacttgggag cttctcctgg
20
<210> 535
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 535
atagccattg cagctgctca
20
<210> 536
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 536
tggattgagc atccaccaag
20
<210> 537
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 537
ccatagccat tgcagctgct
20
<210> 538
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 538
gtcacttggg agcttctcct
20
<210> 539
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 539
ccagggcact catctgcatg
20
<210> 540
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 540
gccatccaag tcacttggga
20
<210> 541
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 541
gaagctttgg ttgggcaaca
20
<210> 542
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 542
ctggattgag catccaccaa
20
<210> 543
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 543
caagtcactt gggagcttct
20
<210> 544
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 544
atgccatcca agtcacttgg
20
<210> 545
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 545
atgagatgcc tggctgccat
20
<210> 546
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 546
ttgggagctt ctcctggtgg
20
<210> 547
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 547
tgggagcttc tcctggtgga
20
<210> 548
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 548
ttatgagatg cctggctgcc
20
<210> 549
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 549
gttatgagat gcctggctgc
20
<210> 550
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 550
ccaagtcact tgggagcttc
20
<210> 551
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 551
agctttggtt gggcaacaca
20
<210> 552
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 552
tatgagatgc ctggctgcca
20
<210> 553
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 553
tgttatgaga tgcctggctg
20
<210> 554
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 554
atccaagtca cttgggagct
20
<210> 555
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 555
gggaagcttt ggttgggcaa
20
<210> 556
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 556
ctccatccat gaggtcattc
20
<210> 557
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 557
aagtcacttg ggagcttctc
20
<210> 558
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 558
ccatccaagt cacttgggag
20
<210> 559
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 559
tccaagtcac ttgggagctt
20
<210> 560
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 560
cctctggatt gagcatccac
20
<210> 561
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 561
acttgggagc ttctcctggt
20
<210> 562
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 562
cttgggagct tctcctggtg
20
<210> 563
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 563
catgccatcc aagtcacttg
20
<210> 564
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 564
tgccatccaa gtcacttggg
20
<210> 565
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 565
tccatccatg aggtcattcc
20
<210> 566
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 566
agggcactca tctgcatggg
20
<210> 567
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 567
ccagttcctt cattctgcac
20
<210> 568
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 568
catagccatt gcagctgctc
20
<210> 569
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 569
tctggattga gcatccacca
20
<210> 570
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 570
ggattgagca tccaccaaga
20
<210> 571
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 571
ccctctggat tgagcatcca
20
<210> 572
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 572
aagctttggt tgggcaacac
20
<210> 573
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 573
agtcacttgg gagcttctcc
20
<210> 574
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 574
cacttgggag cttctcctgg
20
<210> 575
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 575
atagccattg cagctgctca
20
<210> 576
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 576
tggattgagc atccaccaag
20
<210> 577
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 577
ccatagccat tgcagctgct
20
<210> 578
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 578
gtcacttggg agcttctcct
20
<210> 579
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 579
ccagggcact catctgcatg
20
<210> 580
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 580
gccatccaag tcacttggga
20
<210> 581
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 581
gaagctttgg ttgggcaaca
20
<210> 582
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 582
ctggattgag catccaccaa
20
<210> 583
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 583
caagtcactt gggagcttct
20
<210> 584
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 584
atgccatcca agtcacttgg
20
<210> 585
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 585
atgagatgcc tggctgccat
20
<210> 586
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 586
ttgggagctt ctcctggtgg
20
<210> 587
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 587
tgggagcttc tcctggtgga
20
<210> 588
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 588
ttatgagatg cctggctgcc
20
<210> 589
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 589
gttatgagat gcctggctgc
20
<210> 590
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 590
ccaagtcact tgggagcttc
20
<210> 591
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 591
agctttggtt gggcaacaca
20
<210> 592
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 592
tatgagatgc ctggctgcca
20
<210> 593
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 593
tgttatgaga tgcctggctg
20
<210> 594
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 594
atccaagtca cttgggagct
20
<210> 595
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 595
gggaagcttt ggttgggcaa
20
<210> 596
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 596
ctccatccat gaggtcattc
20
<210> 597
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 597
aagtcacttg ggagcttctc
20
<210> 598
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 598
ccatccaagt cacttgggag
20
<210> 599
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 599
tccaagtcac ttgggagctt
20
<210> 600
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 600
cctctggatt gagcatccac
20
<210> 601
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 601
acttgggagc ttctcctggt
20
<210> 602
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 602
cttgggagct tctcctggtg
20
<210> 603
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 603
catgccatcc aagtcacttg
20
<210> 604
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 604
tgccatccaa gtcacttggg
20
<210> 605
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 605
tccatccatg aggtcattcc
20
<210> 606
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 606
agggcactca tctgcatggg
20
<210> 607
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 607
ccagttcctt cattctgcac
20
<210> 608
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 608
catagccatt gcagctgctc
20
<210> 609
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 609
tctggattga gcatccacca
20
<210> 610
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 610
ggattgagca tccaccaaga
20
<210> 611
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 611
gaagctttgg ttgggcaaca
20
<210> 612
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 612
ccatccaagt cacttgggag
20
<210> 613
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 613
atgagatgcc tggctgccat
20
<210> 614
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 614
aagctttggt tgggcaacac
20
<210> 615
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 615
atagccattg cagctgctca
20
<210> 616
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 616
tatgagatgc ctggctgcca
20
<210> 617
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 617
ttatgagatg cctggctgcc
20
<210> 618
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 618
ccatccaagt cacttgggag
20
<210> 619
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 619
ccatccaagt cacttgggag
20
<210> 620
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 620
gaagctttgg ttgggcaaca
20
<210> 621
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 621
ccatccaagt cacttgggag
20
<210> 622
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 622
ccatccaagt cacttgggag
20
<210> 623
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 623
gaagctttgg ttgggcaaca
20
<210> 624
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 624
atgagatgcc tggctgccat
20
<210> 625
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 625
atgagatgcc tggctgccat
20
<210> 626
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 626
atgagatgcc tggctgccat
20
<210> 627
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 627
atgagatgcc tggctgccat
20
<210> 628
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 628
gaagctttgg ttgggcaaca
20
<210> 629
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 629
ccatccaagt cacttgggag
20
<210> 630
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 630
atgagatgcc tggctgccat
20
<210> 631
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 631
ccatccaagt cacttgggag
20
<210> 632
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 632
atgagatgcc tggctgccat
20
<210> 633
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 633
ccatccaagt cacttgggag
20
<210> 634
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 634
atgagatgcc tggctgccat
20
<210> 635
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 635
ccatccaagt cacttgggag
20
<210> 636
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 636
atgagatgcc tggctgccat
20
<210> 637
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 637
ccatccaagt cacttgggag
20
<210> 638
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 638
atgagatgcc tggctgccat
20
<210> 639
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 639
ccatccaagt cacttgggag
20
<210> 640
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 640
atgagatgcc tggctgccat
20
<210> 641
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 641
gaagctttgg ttgggcaaca
20
<210> 642
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 642
atgagatgcc tggctgccat
20
<210> 643
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 643
ccatccaagt cacttgggag
20
<210> 644
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 644
atgagatgcc tggctgccat
20
<210> 645
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 645
gaagctttgg ttgggcaaca
20
<210> 646
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 646
atgagatgcc tggctgccat
20
<210> 647
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 647
ccatccaagt cacttgggag
20
<210> 648
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 648
ccatccaagt cacttgggag
20
<210> 649
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 649
atgagatgcc tggctgccat
20
<210> 650
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 650
ccatccaagt cacttgggag
20
<210> 651
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 651
ccatccaagt cacttgggag
20
<210> 652
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 652
ccatccaagt cacttgggag
20
<210> 653
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 653
ccatccaagt cacttgggag
20
<210> 654
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 654
ccatccaagt cacttgggag
20
<210> 655
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 655
ccatccaagt cacttgggag
20
<210> 656
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 656
ccatccaagt cacttgggag
20
<210> 657
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 657
ccatccaagt cacttgggag
20
<210> 658
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 658
ccatccaagt cacttgggag
20
<210> 659
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 659
ccatccaagt cacttgggag
20
<210> 660
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 660
tgagatgcct ggctgccata
20
<210> 661
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 661
tgagatgcct ggctgccata
20
<210> 662
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 662
tgagatgcct ggctgccata
20
<210> 663
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 663
tgagatgcct ggctgccata
20
<210> 664
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 664
uauggcagcc aggcaucuca
20
<210> 665
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 665
tagccattgc agctgctcac
20
<210> 666
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 666
tagccattgc agctgctcac
20
<210> 667
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 667
tagccattgc agctgctcac
20
<210> 668
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 668
tagccattgc agctgctcac
20
<210> 669
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 669
gugagcagcu gcaauggcua
20
<210> 670
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 670
tagccattgc agctgctcac
20
<210> 671
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 671
tagccattgc agctgctcac
20
<210> 672
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 672
tagccattgc agctgctcac
20
<210> 673
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 673
tagccattgc agctgctcac
20
<210> 674
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 674
tagccattgc agctgctcac
20
<210> 675
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 675
gugagcagcu gcaauggcua
20
<210> 676
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 676
tccagttcct tcattctgca
20
<210> 677
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 677
tccagttcct tcattctgca
20
<210> 678
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 678
tccagttcct tcattctgca
20
<210> 679
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 679
tccagttcct tcattctgca
20
<210> 680
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 680
tccagttcct tcattctgca
20
<210> 681
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 681
ugcagaauga aggaacugga
20
<210> 682
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 682
tgagatgcct ggctgccata
20
<210> 683
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 683
tgagatgcct ggctgccata
20
<210> 684
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 684
tgagatgcct ggctgccata
20
<210> 685
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 685
tgagatgcct ggctgccata
20
<210> 686
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 686
tgagatgcct ggctgccata
20
<210> 687
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 687
uauggcagcc aggcaucuca
20
<210> 688
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 688
gcctcagtct gcttcgcacc
20
<210> 689
<211> 27
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 689
gcgtttgctc ttcttcttgc gtttttt
27
<210> 690
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 690
gtccctgaag atgtcaatgc
20
<210> 691
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 691
tccagttcct tcattctgca
20
<210> 692
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 692
tgagatgcct ggctgccata
20
<210> 693
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 693
tagccattgc agctgctcac
20
<210> 694
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 694
tccagttcct tcattctgca
20
<210> 695
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 695
tgagatgcct ggctgccata
20
<210> 696
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 696
tagccattgc agctgctcac
20
<210> 697
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 697
tccagttcct tcattctgca
20
<210> 698
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 698
tgagatgcct ggctgccata
20
<210> 699
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 699
tagccattgc agctgctcac
20
<210> 700
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 700
tccagttcct tcattctgca
20
<210> 701
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 701
tgagatgcct ggctgccata
20
<210> 702
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 702
tagccattgc agctgctcac
20
<210> 703
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 703
tccagttcct tcattctgca
20
<210> 704
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 704
tgagatgcct ggctgccata
20
<210> 705
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 705
tagccattgc agctgctcac
20
<210> 706
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 706
uagccattgc agctgctcac
20
<210> 707
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 707
uagccattgc agctgc
16
<210> 708
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 708
tagccattgc agctgctcac
20
<210> 709
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 709
attaataaat tgtcatcacc
20
<210> 710
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 710
ggugcgaagc agacugaggc
20
<210> 711
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 711
ugcagaauga aggaacugga
20
<210> 712
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 712
uauggcagcc aggcaucuca
20
<210> 713
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 713
gugagcagcu gcaauggcua
20
<210> 714
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 714
tagccattgc agctgctcac
20
<210> 715
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 715
gugagcggcu gcaauggcua
20
<210> 716
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 716
gugagcagcu gcgauggcua
20
<210> 717
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 717
ggugaugaca auuuauuaau
20
<210> 718
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 718
ggugauggca auuuauuaau
20
<210> 719
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 719
tgagatgcct ggctgccata
20
<210> 720
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 720
tgagatgcct ggctgccata
20
<210> 721
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 721
tgagatgcct ggctgccata
20
<210> 722
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 722
tagccattgc agctgctcac
20
<210> 723
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 723
tagccattgc agctgctcac
20
<210> 724
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 724
tagccattgc agctgctcac
20
<210> 725
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 725
tagccattgc agctgctcac
20
<210> 726
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 726
tagccattgc agctgctcac
20
<210> 727
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 727
tagccattgc agctgctcac
20
<210> 728
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 728
tagccattgc agctgctcac
20
<210> 729
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 729
tagccattgc agctgctcac
20
<210> 730
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 730
tagccattgc agctgctcac
20
<210> 731
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 731
tagccattgc agctgctcac
20
<210> 732
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 732
tagccattgc agctgctcac
20
<210> 733
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 733
tagccattgc agctgctcac
20
<210> 734
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 734
tagccattgc agctgctcac
20
<210> 735
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 735
tagccattgc agctgctcac
20
<210> 736
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 736
tagccattgc agctgctcac
20
<210> 737
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 737
tagccattgc agctgctcac
20
<210> 738
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 738
tagccattgc agctgctcac
20
<210> 739
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 739
tagccattgc agctgctcac
20
<210> 740
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 740
tagccattgc agctgctcac
20
<210> 741
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 741
tagccattgc agctgctcac
20
<210> 742
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 742
tagccattgc agctgctcac
20
<210> 743
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 743
tagccattgc agctgctcac
20
<210> 744
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 744
tagccattgc agctgctcac
20
<210> 745
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 745
tagccattgc agctgctcac
20
<210> 746
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 746
tagccattgc agctgctcac
20
<210> 747
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 747
attaataaat tgtcatcacc
20
<210> 748
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 748
attaataaat tgtcatcacc
20
<210> 749
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 749
gcctcagtct gcttcgcacc
20
<210> 750
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 750
gcctcagtct gcttcgcacc
20
<210> 751
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 751
gcctcagtct gcttcgcacc
20
<210> 752
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 752
gcctcagtct gcttcgcacc
20
<210> 753
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 753
gcctcagtct gcttcgcacc
20
<210> 754
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 754
gtccctgaag atgtcaatgc
20
<210> 755
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 755
gtccctgaag atgtcaatgc
20
<210> 756
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 756
gtccctgaag atgtcaatgc
20
<210> 757
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 757
gtccctgaag atgtcaatgc
20
<210> 758
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 758
gcctcagtct gcttcgcacc
20
<210> 759
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 759
gcctcagtct gcttcgcacc
20
<210> 760
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 760
gcctcagtct gcttcgcacc
20
<210> 761
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 761
gcctcagtct gcttcgcacc
20
<210> 762
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 762
gcctcagtct gcttcgcacc
20
<210> 763
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 763
gcctcagtct gcttcgcacc
20
<210> 764
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 764
uagccattgc agctgctcac
20
<210> 765
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 765
uagccattgc agctgctcac
20
<210> 766
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 766
uagccattgc agctgc
16
<210> 767
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 767
tagccattgc agctgctcac
20
<210> 768
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 768
tagccattgc agctgctcac
20
<210> 769
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 769
tagccattgc agctgctcac
20
<210> 770
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 770
tagccattgc agctgctcac
20
<210> 771
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 771
tagccattgc agctgctcac
20
<210> 772
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 772
tagccattgc agctgctcac
20
<210> 773
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 773
tagccattgc agctgctcac
20
<210> 774
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 774
tagccattgc agctgctcac
20
<210> 775
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 775
uuuggaaguc ugcgcccuug ugccc
25
<210> 776
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 776
uuuggaaguc ugugcccuug ugccc
25
<210> 777
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 777
gggcacaagg gcacagactt
20
<210> 778
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 778
ggcacaaggg cacagacttc
20
<210> 779
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 779
gcacaagggc acagacttcc
20
<210> 780
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 780
cacaagggca cagacttcca
20
<210> 781
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 781
acaagggcac agacttccaa
20
<210> 782
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 782
caagggcaca gacttccaaa
20
<210> 783
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 783
gtaggagtag tgaaaggcca
20
<210> 784
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 784
guaggagtag tgaaaggcca
20
<210> 785
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 785
guaggagtag tgaaaggcca
20
<210> 786
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 786
guaggagtag tgaaaggcca
20
<210> 787
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 787
cucuuactgt gctgtggaca
20
<210> 788
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 788
cucuuactgt gctgtggaca
20
<210> 789
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 789
cucuuactgt gctgtggaca
20
<210> 790
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 790
ccuuccctga aggttccucc
20
<210> 791
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 791
uuuggaaguc ugcgcccuug ugccc
25
<210> 792
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 792
uuuggaaguc ugugcccuug ugccc
25
<210> 793
<211> 35
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 793
gagccuuugg aagucugcgc ccuugugccc ugccu
35
<210> 794
<211> 35
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 794
gagccuuugg aagucugugc ccuugugccc ugccu
35
<210> 795
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 795
gguuguugcc agguuacagc ugcuc
25
<210> 796
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 796
gguuguugcc agguugcagc ugcuc
25
<210> 797
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 797
ccuccugcag gcuggguguu ggccc
25
<210> 798
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 798
ccuccugcag gcuggcuguu ggccc
25
<210> 799
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 799
ggugaugaca auuuauuaau
20
<210> 800
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 800
ggugauggca auuuauuaau
20
<210> 801
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 801
attaataaat tgtcatcacc
20
<210> 802
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 802
attaataaat tgtcatcacc
20
<210> 803
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 803
attaataaat tgtcatcacc
20
<210> 804
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 804
ggugaugaca auuuauuaau
20
<210> 805
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 805
ggugauggca auuuauuaau
20
<210> 806
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 806
uuuggaaguc ugcgcccuug ugccc
25
<210> 807
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 807
uuuggaaguc ugugcccuug ugccc
25
<210> 808
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 808
gggcacaagg gcacagactt
20
<210> 809
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 809
ggcacaaggg cacagacttc
20
<210> 810
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 810
gcacaagggc acagacttcc
20
<210> 811
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 811
cacaagggca cagacttcca
20
<210> 812
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 812
acaagggcac agacttccaa
20
<210> 813
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 813
caagggcaca gacttccaaa
20
<210> 814
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 814
gggcacaagg gcacagactt
20
<210> 815
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 815
ggcacaaggg cacagacttc
20
<210> 816
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 816
gcacaagggc acagacttcc
20
<210> 817
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 817
cacaagggca cagacttcca
20
<210> 818
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 818
acaagggcac agacttccaa
20
<210> 819
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 819
caagggcaca gacttccaaa
20
<210> 820
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 820
gggcacaagg gcacagacuu
20
<210> 821
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 821
ggcacaaggg cacagacuuc
20
<210> 822
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 822
gcacaagggc acagacuucc
20
<210> 823
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 823
cacaagggca cagacuucca
20
<210> 824
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 824
acaagggcac agactuccaa
20
<210> 825
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 825
caagggcaca gacttccaaa
20
<210> 826
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 826
gcacaagggc acagacuucc
20
<210> 827
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 827
cacaagggca cagacuucca
20
<210> 828
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 828
acaagggcac agacuuccaa
20
<210> 829
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 829
caagggcaca gacuuccaaa
20
<210> 830
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 830
gcacaagggc acagacuucc
20
<210> 831
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 831
cacaagggca cagacuucca
20
<210> 832
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 832
acaagggcac agacuuccaa
20
<210> 833
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 833
caagggcaca gacuuccaaa
20
<210> 834
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 834
gggcacaagg gcacagacuu
20
<210> 835
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 835
ggcacaaggg cacagacuuc
20
<210> 836
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 836
gcacaagggc acagacuucc
20
<210> 837
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 837
cacaagggca cagacuucca
20
<210> 838
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 838
acaagggcac agactuccaa
20
<210> 839
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 839
caagggcaca gacttccaaa
20
<210> 840
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 840
gggcacaagg gcacagactt
20
<210> 841
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 841
ggcacaaggg cacagacttc
20
<210> 842
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 842
gcacaagggc acagacttcc
20
<210> 843
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 843
cacaagggca cagacttcca
20
<210> 844
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 844
acaagggcac agacttccaa
20
<210> 845
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 845
caagggcaca gacttccaaa
20
<210> 846
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 846
uuuggaaguc ugcgcccuug ugccc
25
<210> 847
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 847
uuuggaaguc ugugcccuug ugccc
25
<210> 848
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 848
gagcagctgc aacctggcaa
20
<210> 849
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 849
gggccaacag ccagcctgca
20
<210> 850
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 850
gguuguugcc agguuacagc ugcuc
25
<210> 851
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 851
gguuguugcc agguugcagc ugcuc
25
<210> 852
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 852
gagcagctgc aacctggcaa
20
<210> 853
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 853
agcagctgca acctggcaac
20
<210> 854
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 854
gcagctgcaa cctggcaaca
20
<210> 855
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 855
cagctgcaac ctggcaacaa
20
<210> 856
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 856
agctgcaacc tggcaacaac
20
<210> 857
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 857
gctgcaacct ggcaacaacc
20
<210> 858
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 858
ccuccugcag gcuggguguu ggccc
25
<210> 859
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 859
ccuccugcag gcuggcuguu ggccc
25
<210> 860
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 860
gggccaacag ccagcctgca
20
<210> 861
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 861
ggccaacagc cagcctgcag
20
<210> 862
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 862
gccaacagcc agcctgcagg
20
<210> 863
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 863
ccaacagcca gcctgcagga
20
<210> 864
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 864
caacagccag cctgcaggag
20
<210> 865
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 865
aacagccagc ctgcaggagg
20
<210> 866
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 866
ggccuuucac uacuccuact t
21
<210> 867
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 867
guaggaguag ugaaaggcct t
21
<210> 868
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 868
gtaggagtag tgaaaggcca
20
<210> 869
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 869
gcagggcaca agggcacaga
20
<210> 870
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 870
cagggcacaa gggcacagac
20
<210> 871
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 871
agggcacaag ggcacagact
20
<210> 872
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 872
aagggcacag acttccaaag
20
<210> 873
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 873
agggcacaga cttccaaagg
20
<210> 874
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 874
gggcacagac ttccaaaggc
20
<210> 875
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 875
gagcagctgc aacctggcaa
20
<210> 876
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 876
agcagctgca acctggcaac
20
<210> 877
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 877
gcagctgcaa cctggcaaca
20
<210> 878
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 878
cagctgcaac ctggcaacaa
20
<210> 879
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 879
agctgcaacc tggcaacaac
20
<210> 880
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 880
gctgcaacct ggcaacaacc
20
<210> 881
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 881
gagcagctgc aacctggcaa
20
<210> 882
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 882
agcagctgca acctggcaac
20
<210> 883
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 883
gcagctgcaa cctggcaaca
20
<210> 884
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 884
cagcugcaac ctggcaacaa
20
<210> 885
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 885
agcugcaacc tggcaacaac
20
<210> 886
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 886
gcugcaacct ggcaacaacc
20
<210> 887
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 887
gagcagctgc aacctggcaa
20
<210> 888
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 888
agcagctgca acctggcaac
20
<210> 889
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 889
gcagctgcaa cctggcaaca
20
<210> 890
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 890
cagcugcaac ctggcaacaa
20
<210> 891
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 891
agcugcaacc tggcaacaac
20
<210> 892
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 892
gcugcaacct ggcaacaacc
20
<210> 893
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 893
gagcagctgc aaccuggcaa
20
<210> 894
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 894
gagcagctgc aaccuggcaa
20
<210> 895
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 895
agcagctgca acctggcaac
20
<210> 896
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 896
agcagctgca acctggcaac
20
<210> 897
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 897
gcagctgcaa ccuggcaaca
20
<210> 898
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 898
gcagctgcaa ccuggcaaca
20
<210> 899
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 899
gagcagctgc aacctggcaa
20
<210> 900
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 900
agcagctgca acctggcaac
20
<210> 901
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 901
gcagctgcaa cctggcaaca
20
<210> 902
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 902
cagcugcaac ctggcaacaa
20
<210> 903
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 903
agcugcaacc tggcaacaac
20
<210> 904
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 904
gcugcaacct ggcaacaacc
20
<210> 905
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 905
gggccaacag ccagcctgca
20
<210> 906
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 906
ggccaacagc cagcctgcag
20
<210> 907
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 907
gccaacagcc agcctgcagg
20
<210> 908
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 908
ccaacagcca gcctgcagga
20
<210> 909
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 909
caacagccag cctgcaggag
20
<210> 910
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 910
aacagccagc ctgcaggagg
20
<210> 911
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 911
gggccaacag ccagcctgca
20
<210> 912
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 912
ggccaacagc cagcctgcag
20
<210> 913
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 913
gccaacagcc agcctgcagg
20
<210> 914
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 914
ccaacagcca gcctgcagga
20
<210> 915
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 915
caacagccag cctgcaggag
20
<210> 916
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 916
aacagccagc ctgcaggagg
20
<210> 917
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 917
gggccaacag ccagccugca
20
<210> 918
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 918
ggccaacagc cagccugcag
20
<210> 919
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 919
gccaacagcc agcctgcagg
20
<210> 920
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 920
ccaacagcca gcctgcagga
20
<210> 921
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 921
caacagccag cctgcaggag
20
<210> 922
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 922
aacagccagc ctgcaggagg
20
<210> 923
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 923
gggccaacag ccagccugca
20
<210> 924
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 924
gggccaacag ccagccugca
20
<210> 925
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 925
ggccaacagc cagccugcag
20
<210> 926
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 926
ggccaacagc cagccugcag
20
<210> 927
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 927
gccaacagcc agccugcagg
20
<210> 928
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 928
gccaacagcc agccugcagg
20
<210> 929
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 929
gggccaacag ccagccugca
20
<210> 930
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 930
ggccaacagc cagccugcag
20
<210> 931
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 931
gccaacagcc agcctgcagg
20
<210> 932
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 932
ccaacagcca gcctgcagga
20
<210> 933
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 933
caacagccag cctgcaggag
20
<210> 934
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 934
aacagccagc ctgcaggagg
20
<210> 935
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 935
guaggagtag tgaaaggcca
20
<210> 936
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 936
guaggagtag tgaaaggcca
20
<210> 937
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 937
guaggagtag tgaaaggcca
20
<210> 938
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 938
cucuuactgt gctgtggaca
20
<210> 939
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 939
cucuuactgt gctgtggaca
20
<210> 940
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 940
cucuuactgt gctgtggaca
20
<210> 941
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 941
gggcacaagg gcacagactt
20
<210> 942
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 942
ggcacaaggg cacagacttc
20
<210> 943
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 943
gcacaagggc acagacttcc
20
<210> 944
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 944
gggcacaagg gcacagactt
20
<210> 945
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 945
ggcacaaggg cacagacttc
20
<210> 946
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 946
gcacaagggc acagacttcc
20
<210> 947
<211> 35
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 947
gagccuuugg aagucugcgc ccuugugccc ugccu
35
<210> 948
<211> 35
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 948
gagccuuugg aagucugugc ccuugugccc ugccu
35
<210> 949
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 949
cacacgggca cagacuucca a
21
<210> 950
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 950
ggaagucugu gcccgugugc c
21
<210> 951
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 951
auuaauaaat tgtcatcacc
20
<210> 952
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 952
auuaauaaat tgtcatcacc
20
<210> 953
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 953
auuaauaaat tgtcatcacc
20
<210> 954
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 954
auuaauaaat tgtcatcacc
20
<210> 955
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 955
auuaauaaat tgtcatcacc
20
<210> 956
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 956
auuaauaaat tgtcatcacc
20
<210> 957
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 957
auuaauaaat tgtcatcacc
20
<210> 958
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 958
auuaauaaat tgtcatcacc
20
<210> 959
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 959
ggcacaaggg cacagacuuc
20
<210> 960
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 960
ggcacaaggg cacagacuuc
20
<210> 961
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 961
ggcacaaggg cacagacuuc
20
<210> 962
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 962
ggcacaaggg cacagacttc
20
<210> 963
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 963
ggcacaaggg cacagacttc
20
<210> 964
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 964
ggcacaaggg cacagacttc
20
<210> 965
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 965
ggcacaaggg cacagacuuc
20
<210> 966
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 966
ggcacaaggg cacagacuuc
20
<210> 967
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 967
gcagggcaca agggcacaga
20
<210> 968
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 968
gcagggcaca agggcacaga
20
<210> 969
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 969
gcagggcaca agggcacaga
20
<210> 970
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 970
gcagggcaca agggcacaga
20
<210> 971
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 971
gcagggcaca agggcacaga
20
<210> 972
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 972
cagggcacaa gggcacagac
20
<210> 973
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 973
cagggcacaa gggcacagac
20
<210> 974
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 974
cagggcacaa gggcacagac
20
<210> 975
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 975
cagggcacaa gggcacagac
20
<210> 976
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 976
cagggcacaa gggcacagac
20
<210> 977
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 977
agggcacaag ggcacagact
20
<210> 978
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 978
agggcacaag ggcacagact
20
<210> 979
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 979
agggcacaag ggcacagact
20
<210> 980
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 980
agggcacaag ggcacagacu
20
<210> 981
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 981
agggcacaag ggcacagacu
20
<210> 982
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 982
aagggcacag acttccaaag
20
<210> 983
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 983
aagggcacag acttccaaag
20
<210> 984
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 984
aagggcacag acttccaaag
20
<210> 985
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 985
aagggcacag acttccaaag
20
<210> 986
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 986
aagggcacag acttccaaag
20
<210> 987
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 987
aagggcacag acttccaaag
20
<210> 988
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 988
aagggcacag acttccaaag
20
<210> 989
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 989
agggcacaga cttccaaagg
20
<210> 990
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 990
agggcacaga cttccaaagg
20
<210> 991
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 991
agggcacaga cttccaaagg
20
<210> 992
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 992
agggcacaga cttccaaagg
20
<210> 993
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 993
agggcacaga cttccaaagg
20
<210> 994
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 994
agggcacaga cttccaaagg
20
<210> 995
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 995
agggcacaga cttccaaagg
20
<210> 996
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 996
gggcacagac ttccaaaggc
20
<210> 997
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 997
gggcacagac ttccaaaggc
20
<210> 998
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 998
gggcacagac ttccaaaggc
20
<210> 999
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 999
gggcacagac ttccaaaggc
20
<210> 1000
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1000
gggcacagac ttccaaaggc
20
<210> 1001
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1001
ggcacaaggg cacagacutc
20
<210> 1002
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1002
ggcacaaggg cacagacttc
20
<210> 1003
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1003
ggcacaaggg cacagacuuc
20
<210> 1004
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1004
auuaauaaat tgtcatcacc
20
<210> 1005
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1005
auuaauaaat tgtcatcacc
20
<210> 1006
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1006
ggcacaaggg cacagacuuc
20
<210> 1007
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1007
ggcacaaggg cacagacuuc
20
<210> 1008
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1008
ggcacaaggg cacagacttc
20
<210> 1009
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1009
ggcacaaggg cacagacttc
20
<210> 1010
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1010
ctcagtaaca ttgacaccac
20
<210> 1011
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1011
cucagtaaca ttgacaccac
20
<210> 1012
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1012
ggcacaaggg cacagacutc
20
<210> 1013
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1013
ctcagtaaca ttgacaccac
20
<210> 1014
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1014
ctcagtaaca ttgacaccac
20
<210> 1015
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1015
gaagucugug cccuugugcc
20
<210> 1016
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1016
ggcacaaggg cacagacutc
20
<210> 1017
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1017
tgtcatcacc agaaaaaguc
20
<210> 1018
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1018
utgtcatcac cagaaaaagu
20
<210> 1019
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1019
ttgtcatcac cagaaaaagu
20
<210> 1020
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1020
autgtcatca ccagaaaaag
20
<210> 1021
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1021
attgtcatca ccagaaaaag
20
<210> 1022
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1022
aautgtcatc accagaaaaa
20
<210> 1023
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1023
aattgtcatc accagaaaaa
20
<210> 1024
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1024
aaattgtcat caccagaaaa
20
<210> 1025
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1025
aaautgtcat caccagaaaa
20
<210> 1026
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1026
uaaautgtca tcaccagaaa
20
<210> 1027
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1027
uaaautgtca tcaccagaaa
20
<210> 1028
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1028
auaaattgtc atcaccagaa
20
<210> 1029
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1029
auaaattgtc atcaccagaa
20
<210> 1030
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1030
aauaaattgt catcaccaga
20
<210> 1031
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1031
aauaaattgt catcaccaga
20
<210> 1032
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1032
aauaaattgt catcaccaga
20
<210> 1033
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1033
uaauaaattg tcatcaccag
20
<210> 1034
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1034
uaauaaattg tcatcaccag
20
<210> 1035
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1035
uaauaaattg tcatcaccag
20
<210> 1036
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1036
uaauaaattg tcatcaccag
20
<210> 1037
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1037
uuaauaaatt gtcatcacca
20
<210> 1038
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1038
uuaauaaatt gtcatcacca
20
<210> 1039
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1039
uuaauaaatt gtcatcacca
20
<210> 1040
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1040
uuaauaaatt gtcatcacca
20
<210> 1041
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1041
auuaataaat tgtcatcacc
20
<210> 1042
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1042
auuaataaat tgtcatcacc
20
<210> 1043
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1043
auuaataaat tgtcatcacc
20
<210> 1044
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1044
auuaataaat tgtcatcacc
20
<210> 1045
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1045
uauuaataaa ttgtcatcac
20
<210> 1046
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1046
uauuaataaa ttgtcatcac
20
<210> 1047
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1047
uauuaataaa ttgtcatcac
20
<210> 1048
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1048
cuauuaataa attgtcatca
20
<210> 1049
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1049
cuauuaataa attgtcatca
20
<210> 1050
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1050
acuautaata aattgtcatc
20
<210> 1051
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1051
tgtcatcacc agaaaaaguc
20
<210> 1052
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1052
utgtcatcac cagaaaaagu
20
<210> 1053
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1053
ttgtcatcac cagaaaaagu
20
<210> 1054
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1054
autgtcatca ccagaaaaag
20
<210> 1055
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1055
attgtcatca ccagaaaaag
20
<210> 1056
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1056
aautgtcatc accagaaaaa
20
<210> 1057
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1057
aattgtcatc accagaaaaa
20
<210> 1058
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1058
aaattgtcat caccagaaaa
20
<210> 1059
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1059
aaautgtcat caccagaaaa
20
<210> 1060
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1060
uaaautgtca tcaccagaaa
20
<210> 1061
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1061
uaaautgtca tcaccagaaa
20
<210> 1062
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1062
auaaattgtc atcaccagaa
20
<210> 1063
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1063
auaaattgtc atcaccagaa
20
<210> 1064
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1064
aauaaattgt catcaccaga
20
<210> 1065
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1065
aauaaattgt catcaccaga
20
<210> 1066
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1066
aauaaattgt catcaccaga
20
<210> 1067
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1067
uaauaaattg tcatcaccag
20
<210> 1068
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1068
uaauaaattg tcatcaccag
20
<210> 1069
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1069
uaauaaattg tcatcaccag
20
<210> 1070
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1070
uaauaaattg tcatcaccag
20
<210> 1071
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1071
uuaauaaatt gtcatcacca
20
<210> 1072
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1072
uuaauaaatt gtcatcacca
20
<210> 1073
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1073
uuaauaaatt gtcatcacca
20
<210> 1074
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1074
uuaauaaatt gtcatcacca
20
<210> 1075
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1075
auuaataaat tgtcatcacc
20
<210> 1076
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1076
auuaataaat tgtcatcacc
20
<210> 1077
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1077
auuaataaat tgtcatcacc
20
<210> 1078
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1078
auuaataaat tgtcatcacc
20
<210> 1079
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1079
uauuaataaa ttgtcatcac
20
<210> 1080
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1080
uauuaataaa ttgtcatcac
20
<210> 1081
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1081
uauuaataaa ttgtcatcac
20
<210> 1082
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1082
cuauuaataa attgtcatca
20
<210> 1083
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1083
cuauuaataa attgtcatca
20
<210> 1084
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1084
acuautaata aattgtcatc
20
<210> 1085
<211> 32
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1085
gacuuuuucu ggugauggca auuuauuaau ag
32
<210> 1086
<211> 32
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1086
gacuuuuucu ggugaugaca auuuauuaau ag
32
<210> 1087
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1087
uaaautgtca tcaccagaaa
20
<210> 1088
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1088
auaaattgtc atcaccagaa
20
<210> 1089
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1089
aauaaattgt catcaccaga
20
<210> 1090
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1090
uaauaaattg tcatcaccag
20
<210> 1091
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1091
aauaaattgt catcaccaga
20
<210> 1092
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1092
uaauaaattg tcatcaccag
20
<210> 1093
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1093
gcacaagggc acagacuucc
20
<210> 1094
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1094
gcacaagggc acagacuucc
20
<210> 1095
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1095
cacaagggca cagacuucca
20
<210> 1096
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1096
cacaagggca cagacuucca
20
<210> 1097
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1097
uaaautgtca tcaccagaaa
20
<210> 1098
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1098
auaaattgtc atcaccagaa
20
<210> 1099
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1099
aauaaattgt catcaccaga
20
<210> 1100
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1100
uaauaaattg tcatcaccag
20
<210> 1101
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1101
uccccacaga gggaggaagc
20
<210> 1102
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1102
cuccccacag agggaggaag
20
<210> 1103
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1103
ccuccccaca gagggaggaa
20
<210> 1104
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1104
uccuccccac agagggagga
20
<210> 1105
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1105
guccucccca cagagggagg
20
<210> 1106
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1106
ggucctcccc acagagggag
20
<210> 1107
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1107
gggucctccc cacagaggga
20
<210> 1108
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1108
cgggucctcc ccacagaggg
20
<210> 1109
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1109
acaguagatg agggagcagg
20
<210> 1110
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1110
cacagtagat gagggagcag
20
<210> 1111
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1111
acacagtaga tgagggagca
20
<210> 1112
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1112
cacacagtag atgagggagc
20
<210> 1113
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1113
gcacacagta gatgagggag
20
<210> 1114
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1114
ugcacacagt agatgaggga
20
<210> 1115
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1115
gugcacacag tagatgaggg
20
<210> 1116
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1116
agugcacaca gtagaugagg
20
<210> 1117
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1117
uccccacaga gggaggaagc
20
<210> 1118
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1118
cuccccacag agggaggaag
20
<210> 1119
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1119
ccuccccaca gagggaggaa
20
<210> 1120
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1120
uccuccccac agagggagga
20
<210> 1121
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1121
guccucccca cagagggagg
20
<210> 1122
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1122
ggucctcccc acagagggag
20
<210> 1123
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1123
gggucctccc cacagaggga
20
<210> 1124
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1124
cgggucctcc ccacagaggg
20
<210> 1125
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1125
acaguagatg agggagcagg
20
<210> 1126
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1126
cacagtagat gagggagcag
20
<210> 1127
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1127
acacagtaga tgagggagca
20
<210> 1128
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1128
cacacagtag atgagggagc
20
<210> 1129
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1129
gcacacagta gatgagggag
20
<210> 1130
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1130
ugcacacagt agatgaggga
20
<210> 1131
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1131
gugcacacag tagatgaggg
20
<210> 1132
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1132
agugcacaca gtagaugagg
20
<210> 1133
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1133
ggcacaaggg cacagacttc
20
<210> 1134
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1134
ggcacaaggg cacagacuuc
20
<210> 1135
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1135
gggucctccc cacagaggga
20
<210> 1136
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1136
gggucctccc cacagaggga
20
<210> 1137
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1137
gggucctccc cacagaggga
20
<210> 1138
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1138
gggucctccc cacagaggga
20
<210> 1139
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1139
ggguuctccc cacagaggga
20
<210> 1140
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1140
ggcacaaggg cacagacuuc
20
<210> 1141
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1141
ggcacaaggg cacagacuuc
20
<210> 1142
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1142
ggcacaaggg cacagacuuc
20
<210> 1143
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1143
ggcacaaggg cacagacuuc
20
<210> 1144
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1144
ggcacaaggg cacagacuuc
20
<210> 1145
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1145
ggcacaaggg cacagacuuc
20
<210> 1146
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1146
ggcacaaggg cacagacuuc
20
<210> 1147
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1147
ggcacaaggg cacagacuuc
20
<210> 1148
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1148
ggcacaaggg cacagacuuc
20
<210> 1149
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1149
ggcacaaggg cacagacuuc
20
<210> 1150
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1150
ggcacaaggg cacagacuuc
20
<210> 1151
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1151
ggcacaaggg cacagacuuc
20
<210> 1152
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1152
ggcacaaggg cacagacuuc
20
<210> 1153
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1153
attaataaat tgtcatcacc
20
<210> 1154
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1154
attaataaat tgtcatcacc
20
<210> 1155
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1155
attaataaat tgtcatcacc
20
<210> 1156
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1156
ggugaugaca auuuauuaau
20
<210> 1157
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1157
ggugauggca auuuauuaau
20
<210> 1158
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1158
uuuggaaguc ugcgcccuug ugccc
25
<210> 1159
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1159
uuuggaaguc ugugcccuug ugccc
25
<210> 1160
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1160
gggcacaagg gcacagactt
20
<210> 1161
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1161
ggcacaaggg cacagacttc
20
<210> 1162
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1162
gcacaagggc acagacttcc
20
<210> 1163
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1163
cacaagggca cagacttcca
20
<210> 1164
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1164
acaagggcac agacttccaa
20
<210> 1165
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1165
caagggcaca gacttccaaa
20
<210> 1166
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1166
gggcacaagg gcacagactt
20
<210> 1167
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1167
ggcacaaggg cacagacttc
20
<210> 1168
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1168
gcacaagggc acagacttcc
20
<210> 1169
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1169
cacaagggca cagacttcca
20
<210> 1170
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1170
acaagggcac agacttccaa
20
<210> 1171
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1171
caagggcaca gacttccaaa
20
<210> 1172
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1172
gggcacaagg gcacagacuu
20
<210> 1173
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1173
ggcacaaggg cacagacuuc
20
<210> 1174
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1174
gcacaagggc acagacuucc
20
<210> 1175
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1175
cacaagggca cagacuucca
20
<210> 1176
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1176
acaagggcac agactuccaa
20
<210> 1177
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1177
caagggcaca gacttccaaa
20
<210> 1178
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1178
gcacaagggc acagacuucc
20
<210> 1179
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1179
cacaagggca cagacuucca
20
<210> 1180
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1180
acaagggcac agacuuccaa
20
<210> 1181
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1181
caagggcaca gacuuccaaa
20
<210> 1182
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1182
gcacaagggc acagacuucc
20
<210> 1183
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1183
cacaagggca cagacuucca
20
<210> 1184
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1184
acaagggcac agacuuccaa
20
<210> 1185
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1185
caagggcaca gacuuccaaa
20
<210> 1186
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1186
gggcacaagg gcacagacuu
20
<210> 1187
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1187
ggcacaaggg cacagacuuc
20
<210> 1188
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1188
gcacaagggc acagacuucc
20
<210> 1189
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1189
cacaagggca cagacuucca
20
<210> 1190
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1190
acaagggcac agactuccaa
20
<210> 1191
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1191
caagggcaca gacttccaaa
20
<210> 1192
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1192
gggcacaagg gcacagactt
20
<210> 1193
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1193
ggcacaaggg cacagacttc
20
<210> 1194
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1194
gcacaagggc acagacttcc
20
<210> 1195
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1195
cacaagggca cagacttcca
20
<210> 1196
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1196
acaagggcac agacttccaa
20
<210> 1197
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1197
caagggcaca gacttccaaa
20
<210> 1198
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1198
uuuggaaguc ugcgcccuug ugccc
25
<210> 1199
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1199
uuuggaaguc ugugcccuug ugccc
25
<210> 1200
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1200
gagcagctgc aacctggcaa
20
<210> 1201
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1201
gggccaacag ccagcctgca
20
<210> 1202
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1202
gguuguugcc agguuacagc ugcuc
25
<210> 1203
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1203
gguuguugcc agguugcagc ugcuc
25
<210> 1204
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1204
gagcagctgc aacctggcaa
20
<210> 1205
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1205
agcagctgca acctggcaac
20
<210> 1206
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1206
gcagctgcaa cctggcaaca
20
<210> 1207
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1207
cagctgcaac ctggcaacaa
20
<210> 1208
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1208
agctgcaacc tggcaacaac
20
<210> 1209
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1209
gctgcaacct ggcaacaacc
20
<210> 1210
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1210
ccuccugcag gcuggguguu ggccc
25
<210> 1211
<211> 25
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1211
ccuccugcag gcuggcuguu ggccc
25
<210> 1212
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1212
gggccaacag ccagcctgca
20
<210> 1213
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1213
ggccaacagc cagcctgcag
20
<210> 1214
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1214
gccaacagcc agcctgcagg
20
<210> 1215
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1215
ccaacagcca gcctgcagga
20
<210> 1216
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1216
caacagccag cctgcaggag
20
<210> 1217
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1217
aacagccagc ctgcaggagg
20
<210> 1218
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1218
ggccuuucac uacuccuact t
21
<210> 1219
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1219
guaggaguag ugaaaggcct t
21
<210> 1220
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1220
gtaggagtag tgaaaggcca
20
<210> 1221
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1221
gcagggcaca agggcacaga
20
<210> 1222
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1222
cagggcacaa gggcacagac
20
<210> 1223
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1223
agggcacaag ggcacagact
20
<210> 1224
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1224
aagggcacag acttccaaag
20
<210> 1225
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1225
agggcacaga cttccaaagg
20
<210> 1226
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1226
gggcacagac ttccaaaggc
20
<210> 1227
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1227
gagcagctgc aacctggcaa
20
<210> 1228
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1228
agcagctgca acctggcaac
20
<210> 1229
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1229
gcagctgcaa cctggcaaca
20
<210> 1230
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1230
cagctgcaac ctggcaacaa
20
<210> 1231
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1231
agctgcaacc tggcaacaac
20
<210> 1232
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1232
gctgcaacct ggcaacaacc
20
<210> 1233
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1233
gagcagctgc aacctggcaa
20
<210> 1234
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1234
agcagctgca acctggcaac
20
<210> 1235
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1235
gcagctgcaa cctggcaaca
20
<210> 1236
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1236
cagcugcaac ctggcaacaa
20
<210> 1237
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1237
agcugcaacc tggcaacaac
20
<210> 1238
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1238
gcugcaacct ggcaacaacc
20
<210> 1239
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1239
gagcagctgc aacctggcaa
20
<210> 1240
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1240
agcagctgca acctggcaac
20
<210> 1241
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1241
gcagctgcaa cctggcaaca
20
<210> 1242
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1242
cagcugcaac ctggcaacaa
20
<210> 1243
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1243
agcugcaacc tggcaacaac
20
<210> 1244
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1244
gcugcaacct ggcaacaacc
20
<210> 1245
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1245
gagcagctgc aaccuggcaa
20
<210> 1246
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1246
gagcagctgc aaccuggcaa
20
<210> 1247
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1247
agcagctgca acctggcaac
20
<210> 1248
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1248
agcagctgca acctggcaac
20
<210> 1249
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1249
gcagctgcaa ccuggcaaca
20
<210> 1250
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1250
gcagctgcaa ccuggcaaca
20
<210> 1251
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1251
gagcagctgc aacctggcaa
20
<210> 1252
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1252
agcagctgca acctggcaac
20
<210> 1253
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1253
gcagctgcaa cctggcaaca
20
<210> 1254
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1254
cagcugcaac ctggcaacaa
20
<210> 1255
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1255
agcugcaacc tggcaacaac
20
<210> 1256
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1256
gcugcaacct ggcaacaacc
20
<210> 1257
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1257
gggccaacag ccagcctgca
20
<210> 1258
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1258
ggccaacagc cagcctgcag
20
<210> 1259
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1259
gccaacagcc agcctgcagg
20
<210> 1260
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1260
ccaacagcca gcctgcagga
20
<210> 1261
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1261
caacagccag cctgcaggag
20
<210> 1262
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1262
aacagccagc ctgcaggagg
20
<210> 1263
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1263
gggccaacag ccagcctgca
20
<210> 1264
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1264
ggccaacagc cagcctgcag
20
<210> 1265
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1265
gccaacagcc agcctgcagg
20
<210> 1266
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1266
ccaacagcca gcctgcagga
20
<210> 1267
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1267
caacagccag cctgcaggag
20
<210> 1268
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1268
aacagccagc ctgcaggagg
20
<210> 1269
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1269
gggccaacag ccagccugca
20
<210> 1270
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1270
ggccaacagc cagccugcag
20
<210> 1271
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1271
gccaacagcc agcctgcagg
20
<210> 1272
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1272
ccaacagcca gcctgcagga
20
<210> 1273
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1273
caacagccag cctgcaggag
20
<210> 1274
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1274
aacagccagc ctgcaggagg
20
<210> 1275
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1275
gggccaacag ccagccugca
20
<210> 1276
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1276
gggccaacag ccagccugca
20
<210> 1277
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1277
ggccaacagc cagccugcag
20
<210> 1278
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1278
ggccaacagc cagccugcag
20
<210> 1279
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1279
gccaacagcc agccugcagg
20
<210> 1280
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1280
gccaacagcc agccugcagg
20
<210> 1281
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1281
gggccaacag ccagccugca
20
<210> 1282
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1282
ggccaacagc cagccugcag
20
<210> 1283
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1283
gccaacagcc agcctgcagg
20
<210> 1284
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1284
ccaacagcca gcctgcagga
20
<210> 1285
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1285
caacagccag cctgcaggag
20
<210> 1286
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1286
aacagccagc ctgcaggagg
20
<210> 1287
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1287
guaggagtag tgaaaggcca
20
<210> 1288
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1288
guaggagtag tgaaaggcca
20
<210> 1289
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1289
guaggagtag tgaaaggcca
20
<210> 1290
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1290
cucuuactgt gctgtggaca
20
<210> 1291
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1291
cucuuactgt gctgtggaca
20
<210> 1292
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1292
cucuuactgt gctgtggaca
20
<210> 1293
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1293
gggcacaagg gcacagactt
20
<210> 1294
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1294
ggcacaaggg cacagacttc
20
<210> 1295
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1295
gcacaagggc acagacttcc
20
<210> 1296
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1296
gggcacaagg gcacagactt
20
<210> 1297
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1297
ggcacaaggg cacagacttc
20
<210> 1298
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1298
gcacaagggc acagacttcc
20
<210> 1299
<211> 35
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1299
gagccuuugg aagucugcgc ccuugugccc ugccu
35
<210> 1300
<211> 35
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1300
gagccuuugg aagucugugc ccuugugccc ugccu
35
<210> 1301
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1301
cacacgggca cagacuucca a
21
<210> 1302
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1302
ggaagucugu gcccgugugc c
21
<210> 1303
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1303
auuaauaaat tgtcatcacc
20
<210> 1304
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1304
auuaauaaat tgtcatcacc
20
<210> 1305
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1305
auuaauaaat tgtcatcacc
20
<210> 1306
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1306
auuaauaaat tgtcatcacc
20
<210> 1307
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1307
auuaauaaat tgtcatcacc
20
<210> 1308
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1308
auuaauaaat tgtcatcacc
20
<210> 1309
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1309
auuaauaaat tgtcatcacc
20
<210> 1310
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1310
auuaauaaat tgtcatcacc
20
<210> 1311
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1311
ggcacaaggg cacagacuuc
20
<210> 1312
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1312
ggcacaaggg cacagacuuc
20
<210> 1313
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1313
ggcacaaggg cacagacuuc
20
<210> 1314
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1314
ggcacaaggg cacagacttc
20
<210> 1315
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1315
ggcacaaggg cacagacttc
20
<210> 1316
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1316
ggcacaaggg cacagacttc
20
<210> 1317
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1317
ggcacaaggg cacagacuuc
20
<210> 1318
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1318
ggcacaaggg cacagacuuc
20
<210> 1319
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1319
gcagggcaca agggcacaga
20
<210> 1320
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1320
gcagggcaca agggcacaga
20
<210> 1321
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1321
gcagggcaca agggcacaga
20
<210> 1322
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1322
gcagggcaca agggcacaga
20
<210> 1323
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1323
gcagggcaca agggcacaga
20
<210> 1324
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1324
cagggcacaa gggcacagac
20
<210> 1325
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1325
cagggcacaa gggcacagac
20
<210> 1326
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1326
cagggcacaa gggcacagac
20
<210> 1327
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1327
cagggcacaa gggcacagac
20
<210> 1328
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1328
cagggcacaa gggcacagac
20
<210> 1329
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1329
agggcacaag ggcacagact
20
<210> 1330
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1330
agggcacaag ggcacagact
20
<210> 1331
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1331
agggcacaag ggcacagact
20
<210> 1332
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1332
agggcacaag ggcacagacu
20
<210> 1333
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1333
agggcacaag ggcacagacu
20
<210> 1334
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1334
aagggcacag acttccaaag
20
<210> 1335
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1335
aagggcacag acttccaaag
20
<210> 1336
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1336
aagggcacag acttccaaag
20
<210> 1337
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1337
aagggcacag acttccaaag
20
<210> 1338
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1338
aagggcacag acttccaaag
20
<210> 1339
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1339
aagggcacag acttccaaag
20
<210> 1340
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1340
aagggcacag acttccaaag
20
<210> 1341
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1341
agggcacaga cttccaaagg
20
<210> 1342
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1342
agggcacaga cttccaaagg
20
<210> 1343
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1343
agggcacaga cttccaaagg
20
<210> 1344
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1344
agggcacaga cttccaaagg
20
<210> 1345
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1345
agggcacaga cttccaaagg
20
<210> 1346
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1346
agggcacaga cttccaaagg
20
<210> 1347
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1347
agggcacaga cttccaaagg
20
<210> 1348
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1348
gggcacagac ttccaaaggc
20
<210> 1349
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1349
gggcacagac ttccaaaggc
20
<210> 1350
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1350
gggcacagac ttccaaaggc
20
<210> 1351
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1351
gggcacagac ttccaaaggc
20
<210> 1352
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1352
gggcacagac ttccaaaggc
20
<210> 1353
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1353
ggcacaaggg cacagacuuc
20
<210> 1354
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1354
ggcacaaggg cacagacuuc
20
<210> 1355
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1355
ggcacaaggg cacagacuuc
20
<210> 1356
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1356
auuaauaaat tgtcatcacc
20
<210> 1357
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1357
auuaauaaat tgtcatcacc
20
<210> 1358
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1358
ggcacaaggg cacagacuuc
20
<210> 1359
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1359
ggcacaaggg cacagacuuc
20
<210> 1360
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1360
ggcacaaggg cacagacttc
20
<210> 1361
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1361
ggcacaaggg cacagacttc
20
<210> 1362
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1362
ctcagtaaca ttgacaccac
20
<210> 1363
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1363
cucagtaaca ttgacaccac
20
<210> 1364
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1364
ggcacaaggg cacagacuuc
20
<210> 1365
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1365
cucagtaaca ttgacaccac
20
<210> 1366
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1366
cucagtaaca ttgacaccac
20
<210> 1367
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1367
gaagucugug cccuugugcc
20
<210> 1368
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1368
ggcacaaggg cacagacuuc
20
<210> 1369
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1369
tgtcatcacc agaaaaaguc
20
<210> 1370
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1370
utgtcatcac cagaaaaagu
20
<210> 1371
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1371
ttgtcatcac cagaaaaagu
20
<210> 1372
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1372
autgtcatca ccagaaaaag
20
<210> 1373
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1373
attgtcatca ccagaaaaag
20
<210> 1374
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1374
aautgtcatc accagaaaaa
20
<210> 1375
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1375
aattgtcatc accagaaaaa
20
<210> 1376
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1376
aaattgtcat caccagaaaa
20
<210> 1377
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1377
aaautgtcat caccagaaaa
20
<210> 1378
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1378
uaaautgtca tcaccagaaa
20
<210> 1379
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1379
uaaautgtca tcaccagaaa
20
<210> 1380
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1380
auaaattgtc atcaccagaa
20
<210> 1381
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1381
auaaattgtc atcaccagaa
20
<210> 1382
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1382
aauaaattgt catcaccaga
20
<210> 1383
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1383
aauaaattgt catcaccaga
20
<210> 1384
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1384
aauaaattgt catcaccaga
20
<210> 1385
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1385
uaauaaattg tcatcaccag
20
<210> 1386
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1386
uaauaaattg tcatcaccag
20
<210> 1387
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1387
uaauaaattg tcatcaccag
20
<210> 1388
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1388
uaauaaattg tcatcaccag
20
<210> 1389
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1389
uuaauaaatt gtcatcacca
20
<210> 1390
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1390
uuaauaaatt gtcatcacca
20
<210> 1391
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1391
uuaauaaatt gtcatcacca
20
<210> 1392
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1392
uuaauaaatt gtcatcacca
20
<210> 1393
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1393
auuaataaat tgtcatcacc
20
<210> 1394
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1394
auuaataaat tgtcatcacc
20
<210> 1395
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1395
auuaataaat tgtcatcacc
20
<210> 1396
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1396
auuaataaat tgtcatcacc
20
<210> 1397
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1397
uauuaataaa ttgtcatcac
20
<210> 1398
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1398
uauuaataaa ttgtcatcac
20
<210> 1399
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1399
uauuaataaa ttgtcatcac
20
<210> 1400
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1400
cuauuaataa attgtcatca
20
<210> 1401
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1401
cuauuaataa attgtcatca
20
<210> 1402
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1402
acuautaata aattgtcatc
20
<210> 1403
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1403
tgtcatcacc agaaaaaguc
20
<210> 1404
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1404
utgtcatcac cagaaaaagu
20
<210> 1405
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1405
ttgtcatcac cagaaaaagu
20
<210> 1406
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1406
autgtcatca ccagaaaaag
20
<210> 1407
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1407
attgtcatca ccagaaaaag
20
<210> 1408
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1408
aautgtcatc accagaaaaa
20
<210> 1409
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1409
aattgtcatc accagaaaaa
20
<210> 1410
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1410
aaattgtcat caccagaaaa
20
<210> 1411
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1411
aaautgtcat caccagaaaa
20
<210> 1412
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1412
uaaautgtca tcaccagaaa
20
<210> 1413
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1413
uaaautgtca tcaccagaaa
20
<210> 1414
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1414
auaaattgtc atcaccagaa
20
<210> 1415
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1415
auaaattgtc atcaccagaa
20
<210> 1416
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1416
aauaaattgt catcaccaga
20
<210> 1417
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1417
aauaaattgt catcaccaga
20
<210> 1418
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1418
aauaaattgt catcaccaga
20
<210> 1419
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1419
uaauaaattg tcatcaccag
20
<210> 1420
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1420
uaauaaattg tcatcaccag
20
<210> 1421
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1421
uaauaaattg tcatcaccag
20
<210> 1422
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1422
uaauaaattg tcatcaccag
20
<210> 1423
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1423
uuaauaaatt gtcatcacca
20
<210> 1424
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1424
uuaauaaatt gtcatcacca
20
<210> 1425
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1425
uuaauaaatt gtcatcacca
20
<210> 1426
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1426
uuaauaaatt gtcatcacca
20
<210> 1427
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1427
auuaataaat tgtcatcacc
20
<210> 1428
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1428
auuaataaat tgtcatcacc
20
<210> 1429
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1429
auuaataaat tgtcatcacc
20
<210> 1430
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1430
auuaataaat tgtcatcacc
20
<210> 1431
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1431
uauuaataaa ttgtcatcac
20
<210> 1432
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1432
uauuaataaa ttgtcatcac
20
<210> 1433
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1433
uauuaataaa ttgtcatcac
20
<210> 1434
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1434
cuauuaataa attgtcatca
20
<210> 1435
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1435
cuauuaataa attgtcatca
20
<210> 1436
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1436
acuautaata aattgtcatc
20
<210> 1437
<211> 32
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1437
gacuuuuucu ggugauggca auuuauuaau ag
32
<210> 1438
<211> 32
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1438
gacuuuuucu ggugaugaca auuuauuaau ag
32
<210> 1439
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1439
uaaautgtca tcaccagaaa
20
<210> 1440
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1440
auaaattgtc atcaccagaa
20
<210> 1441
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1441
aauaaattgt catcaccaga
20
<210> 1442
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1442
uaauaaattg tcatcaccag
20
<210> 1443
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1443
aauaaattgt catcaccaga
20
<210> 1444
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1444
uaauaaattg tcatcaccag
20
<210> 1445
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1445
gcacaagggc acagacuucc
20
<210> 1446
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1446
gcacaagggc acagacuucc
20
<210> 1447
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1447
cacaagggca cagacuucca
20
<210> 1448
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1448
cacaagggca cagacuucca
20
<210> 1449
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1449
uaaautgtca tcaccagaaa
20
<210> 1450
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1450
auaaattgtc atcaccagaa
20
<210> 1451
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1451
aauaaattgt catcaccaga
20
<210> 1452
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1452
uaauaaattg tcatcaccag
20
<210> 1453
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1453
uccccacaga gggaggaagc
20
<210> 1454
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1454
cuccccacag agggaggaag
20
<210> 1455
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1455
ccuccccaca gagggaggaa
20
<210> 1456
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1456
uccuccccac agagggagga
20
<210> 1457
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1457
guccucccca cagagggagg
20
<210> 1458
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1458
ggucctcccc acagagggag
20
<210> 1459
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1459
gggucctccc cacagaggga
20
<210> 1460
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1460
cgggucctcc ccacagaggg
20
<210> 1461
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1461
acaguagatg agggagcagg
20
<210> 1462
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1462
cacagtagat gagggagcag
20
<210> 1463
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1463
acacagtaga tgagggagca
20
<210> 1464
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1464
cacacagtag atgagggagc
20
<210> 1465
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1465
gcacacagta gatgagggag
20
<210> 1466
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1466
ugcacacagt agatgaggga
20
<210> 1467
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1467
gugcacacag tagatgaggg
20
<210> 1468
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1468
agugcacaca gtagaugagg
20
<210> 1469
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1469
uccccacaga gggaggaagc
20
<210> 1470
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1470
cuccccacag agggaggaag
20
<210> 1471
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1471
ccuccccaca gagggaggaa
20
<210> 1472
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1472
uccuccccac agagggagga
20
<210> 1473
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1473
guccucccca cagagggagg
20
<210> 1474
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1474
ggucctcccc acagagggag
20
<210> 1475
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1475
gggucctccc cacagaggga
20
<210> 1476
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1476
cgggucctcc ccacagaggg
20
<210> 1477
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1477
acaguagatg agggagcagg
20
<210> 1478
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1478
cacagtagat gagggagcag
20
<210> 1479
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1479
acacagtaga tgagggagca
20
<210> 1480
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1480
cacacagtag atgagggagc
20
<210> 1481
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1481
gcacacagta gatgagggag
20
<210> 1482
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1482
ugcacacagt agatgaggga
20
<210> 1483
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1483
gugcacacag tagatgaggg
20
<210> 1484
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1484
agugcacaca gtagaugagg
20
<210> 1485
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1485
ggcacaaggg cacagacttc
20
<210> 1486
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1486
ggcacaaggg cacagacuuc
20
<210> 1487
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1487
gggucctccc cacagaggga
20
<210> 1488
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1488
gggucctccc cacagaggga
20
<210> 1489
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1489
gggucctccc cacagaggga
20
<210> 1490
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1490
gggucctccc cacagaggga
20
<210> 1491
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1491
ggguuctccc cacagaggga
20
<210> 1492
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1492
ggcacaaggg cacagacuuc
20
<210> 1493
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1493
ggcacaaggg cacagacuuc
20
<210> 1494
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1494
ggcacaaggg cacagacuuc
20
<210> 1495
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1495
ggcacaaggg cacagacuuc
20
<210> 1496
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1496
ggcacaaggg cacagacuuc
20
<210> 1497
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1497
ggcacaaggg cacagacuuc
20
<210> 1498
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1498
ggcacaaggg cacagacuuc
20
<210> 1499
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1499
ggcacaaggg cacagacuuc
20
<210> 1500
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1500
ggcacaaggg cacagacuuc
20
<210> 1501
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1501
ggcacaaggg cacagacuuc
20
<210> 1502
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1502
ggcacaaggg cacagacuuc
20
<210> 1503
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1503
ggcacaaggg cacagacuuc
20
<210> 1504
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1504
ggcacaaggg cacagacuuc
20
<210> 1505
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1505
cagtctgctt cg
12
<210> 1506
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1506
gcctcagtct gcttcgcacc
20
<210> 1507
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1507
uucuagaccu guuuugcuut t
21
<210> 1508
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1508
uucuagaccu guuuugcuut t
21
<210> 1509
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1509
aagcaaaaca ggucuagaat t
21
<210> 1510
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1510
aagcaaaaca ggucuagaat t
21
<210> 1511
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1511
aagcaaaaca ggucuagaat t
21
<210> 1512
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1512
agcaaaacag gucuagaatt
20
<210> 1513
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1513
agcaaaacag gucuagaatt
20
<210> 1514
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1514
agcaaaacag gucuagaatt
20
<210> 1515
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1515
uucuagaccu guuuugcuut t
21
<210> 1516
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1516
uucuagaccu guuuugcuut t
21
<210> 1517
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1517
uucuagaccu guuuugcuut t
21
<210> 1518
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1518
uucuagaccu guuuugcuut t
21
<210> 1519
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1519
uucuagaccu guuuugcuut t
21
<210> 1520
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1520
uucuagaccu guuuugcuut t
21
<210> 1521
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1521
aagcaaaaca ggucuagaat t
21
<210> 1522
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1522
aagcaaaaca ggucuagaat t
21
<210> 1523
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1523
aagcaaaaca ggucuagaat t
21
<210> 1524
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1524
aagcaaaaca ggucuagaat t
21
<210> 1525
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1525
aagcaaaaca ggucuagaat t
21
<210> 1526
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1526
aagcaaaaca ggucuagaat t
21
<210> 1527
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1527
aagcaaaaca ggucuagaat t
21
<210> 1528
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1528
aagcaaaaca ggucuagaat t
21
<210> 1529
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1529
aagcaaaaca ggucuagaat t
21
<210> 1530
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1530
aagcaaaaca ggucuagaat t
21
<210> 1531
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1531
aagcaaaaca ggucuagaat t
21
<210> 1532
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1532
aagcaaaaca ggucuagaat t
21
<210> 1533
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1533
uucuagaccu guuuugcuut t
21
<210> 1534
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1534
uucuagaccu guuuugcuut t
21
<210> 1535
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1535
uucuagaccu guuuugcuut t
21
<210> 1536
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1536
uucuagaccu guuuugcuut t
21
<210> 1537
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1537
uucuagaccu guuuugcuut t
21
<210> 1538
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1538
uucuagaccu guuuugcuut t
21
<210> 1539
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1539
aagcaaaaca ggucuagaat t
21
<210> 1540
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1540
aagcaaaaca ggucuagaat t
21
<210> 1541
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1541
aagcaaaaca ggucuagaat t
21
<210> 1542
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1542
aagcaaaaca ggucuagaat t
21
<210> 1543
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1543
aagcaaaaca ggucuagaat t
21
<210> 1544
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1544
aagcaaaaca ggucuagaat t
21
<210> 1545
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1545
aagcaaaaca ggucuagaat t
21
<210> 1546
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<220>
<223> Description of Combined DNA/RNA Molecule: Synthetic
oligonucleotide
<400> 1546
aagcaaaaca ggucuagaat t
21
<210> 1547
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1547
ggatgttctc ga
12
<210> 1548
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1548
ggatgttctc ga
12
<210> 1549
<211> 12
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1549
ggatgttctc ga
12
<210> 1550
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1550
ttcagtcatg acttcc
16
<210> 1551
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1551
ttcagtcatg acttcc
16
<210> 1552
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
6xHis tag
<400> 1552
His His His His His His
1 5
<210> 1553
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1553
ggaagucugu gcccguguuc c
21
<210> 1554
<211> 20
<212> RNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1554
ggcacaaggg cacagacuuc
20
<210> 1555
<211> 10
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1555
acacacacac
10
<210> 1556
<211> 10
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1556
cccccccccc
10
<210> 1557
<211> 10
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1557
cccccccccc
10
<210> 1558
<211> 10
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1558
cccccccccc
10
<210> 1559
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1559
gcctcagtct gcttcgcacc
20
<210> 1560
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1560
tagccattgc agctgctcac
20
<210> 1561
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1561
tccagttcct tcattctgca
20
<210> 1562
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1562
tgagatgcct ggctgccata
20
<210> 1563
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1563
attaataaat tgtcatcacc
20
<210> 1564
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1564
attaataaat tgacatcacc
20
<210> 1565
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
oligonucleotide
<400> 1565
attaataaat tggcatcacc
20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ДНК-СОДЕРЖАЩИЕ ПОЛИНУКЛЕОТИДЫ И РУКОВОДЯЩИЕ ПОСЛЕДОВАТЕЛЬНОСТИ ДЛЯ СИСТЕМ CRISPR ТИПА V И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2832314C1 |
| КОМПОНЕНТЫ СИСТЕМЫ CRISPR-CAS, СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ МАНИПУЛЯЦИИ С ПОСЛЕДОВАТЕЛЬНОСТЯМИ | 2013 |
|
RU2796549C2 |
| ДОСТАВКА, КОНСТРУИРОВАНИЕ И ОПТИМИЗАЦИЯ СИСТЕМ, СПОСОБОВ И КОМПОЗИЦИЙ ДЛЯ МАНИПУЛЯЦИИ С ПОСЛЕДОВАТЕЛЬНОСТЯМИ И ПРИМЕНЕНИЯ В ТЕРАПИИ | 2013 |
|
RU2721275C2 |
| КОНСТРУИРОВАНИЕ СИСТЕМ, СПОСОБЫ И ОПТИМИЗИРОВАННЫЕ НАПРАВЛЯЮЩИЕ КОМПОЗИЦИИ ДЛЯ МАНИПУЛЯЦИИ С ПОСЛЕДОВАТЕЛЬНОСТЯМИ | 2013 |
|
RU2796017C2 |
| СИСТЕМЫ CRISPR-CAS И СПОСОБЫ ИЗМЕНЕНИЯ ЭКСПРЕССИИ ПРОДУКТОВ ГЕНОВ | 2013 |
|
RU2796273C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ КОНСТРУКЦИИ ПРОТИВ HER2 | 2014 |
|
RU2737882C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ К АЛЬФА-СИНУКЛЕИНУ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2773197C2 |
| НОВЫЕ ФЕРМЕНТЫ И СИСТЕМЫ CRISPR | 2016 |
|
RU2777988C2 |
| НОВЫЕ ФЕРМЕНТЫ CRISPR И СИСТЕМЫ | 2016 |
|
RU2771826C2 |
| ПОЛУЧЕНИЕ ПЛЮРИПОТЕНТНЫХ КЛЕТОК DE NOVO | 2013 |
|
RU2696071C2 |
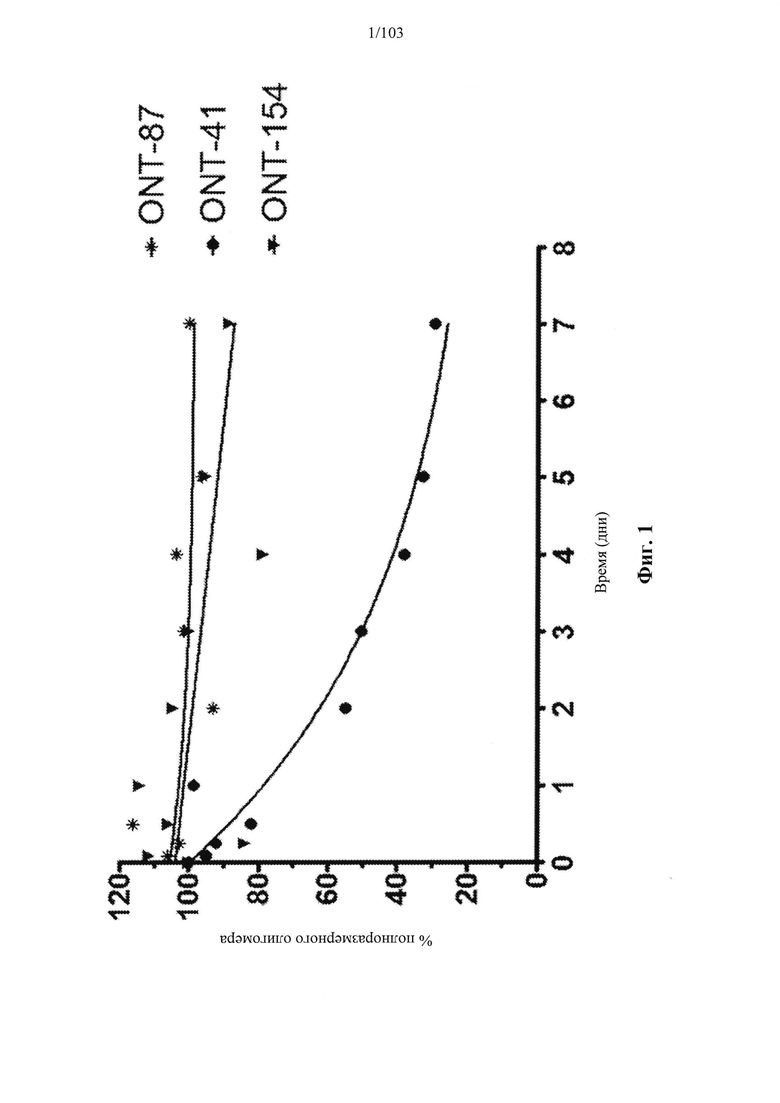
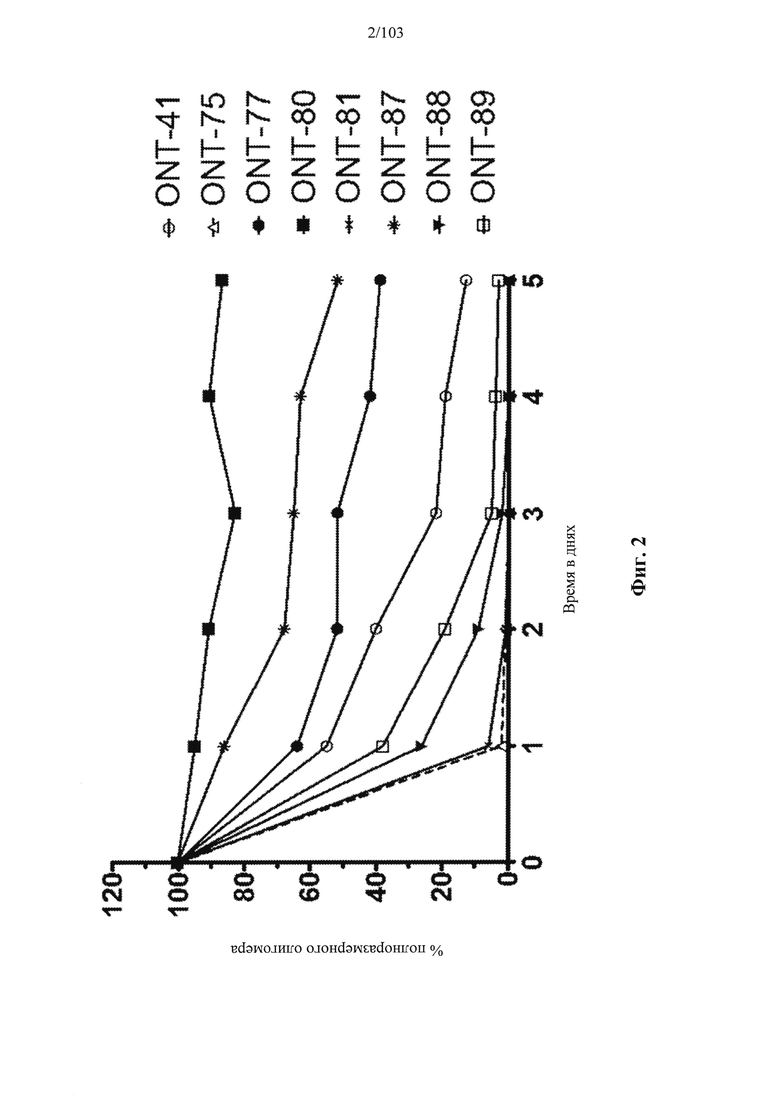
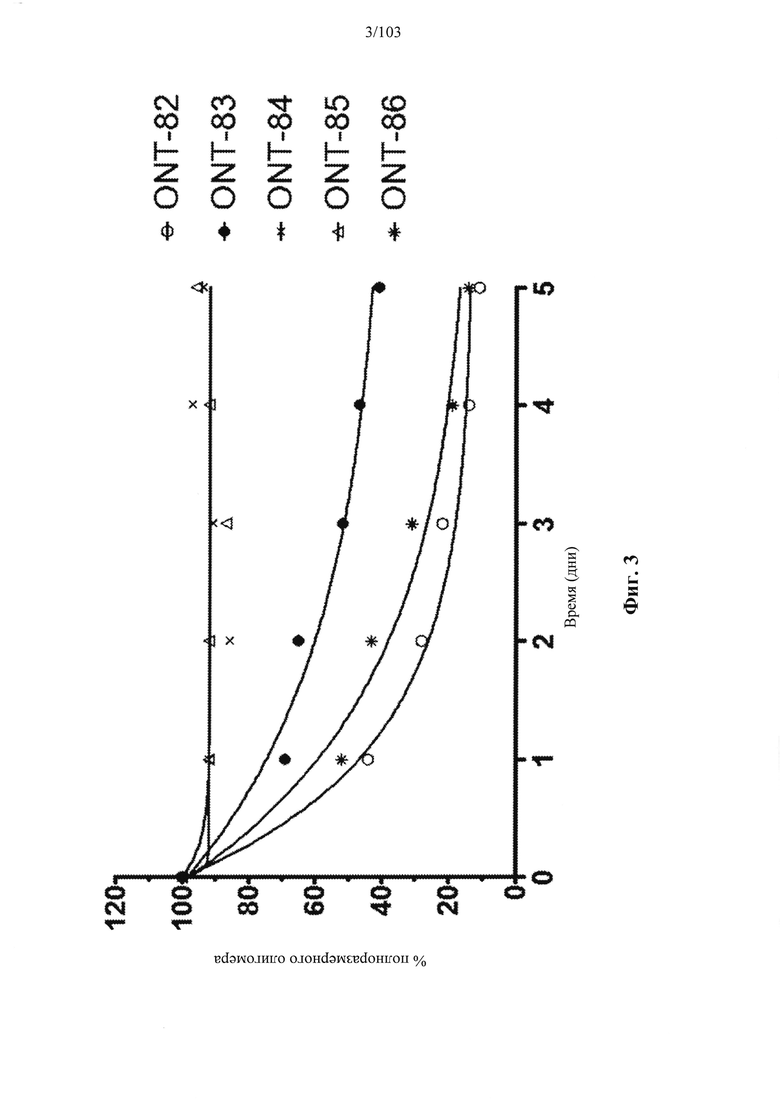
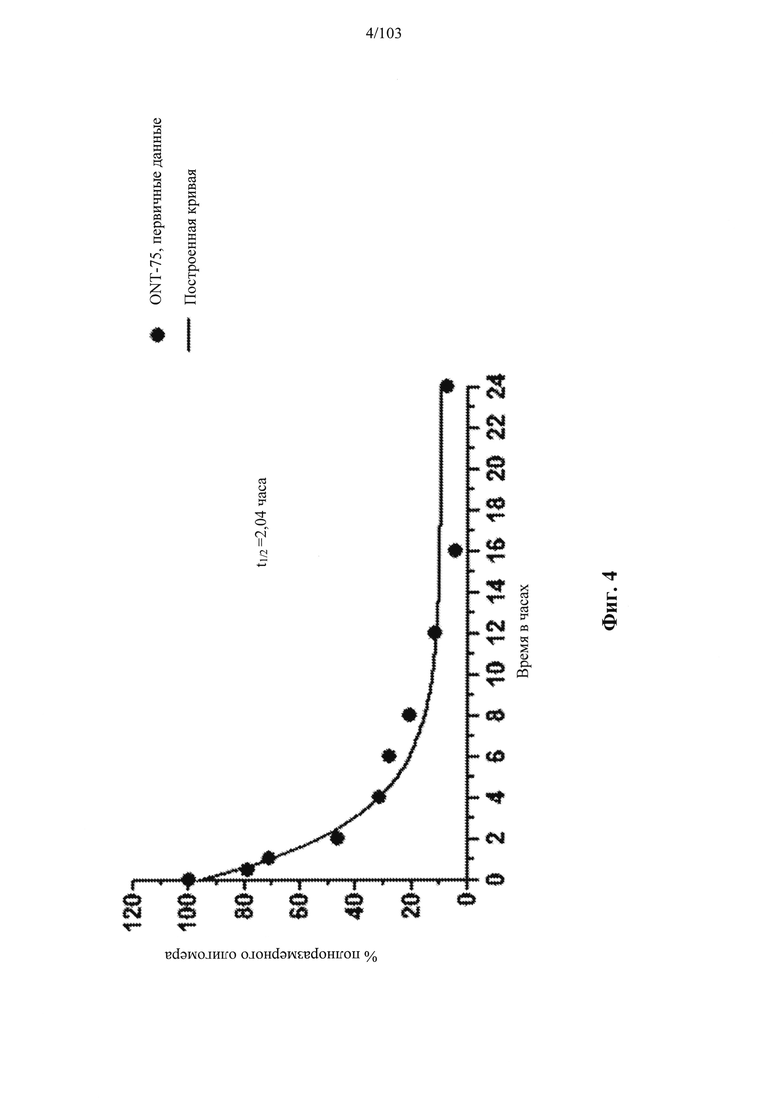
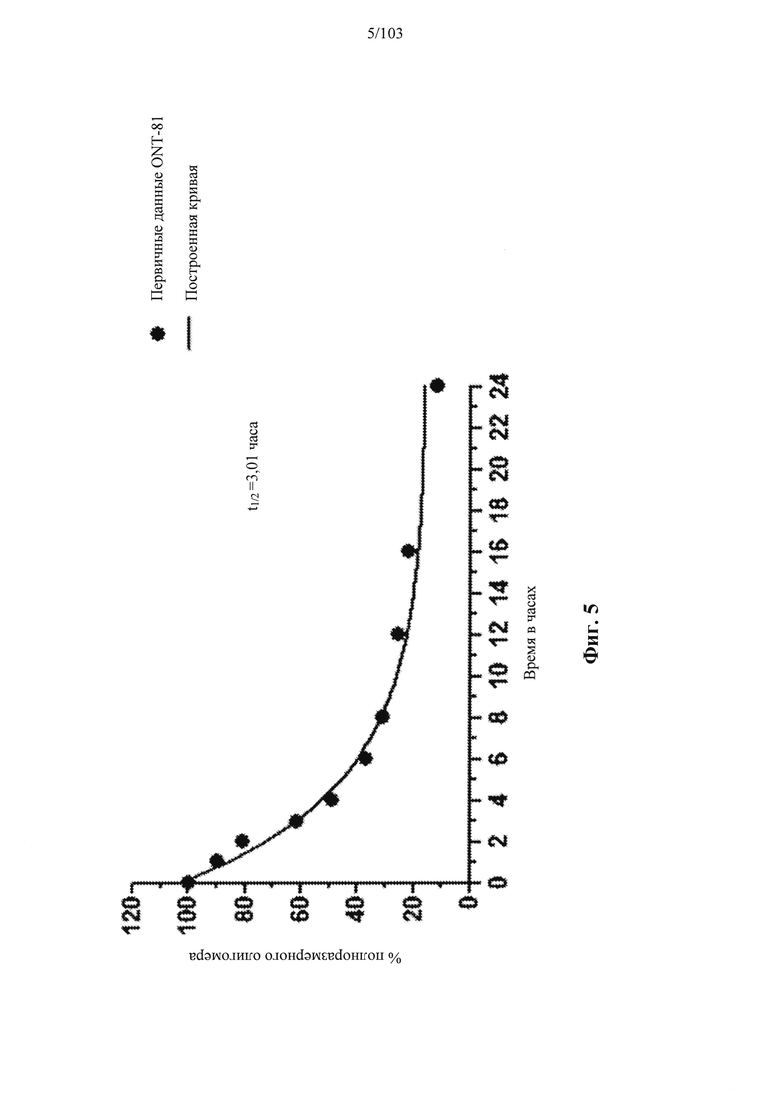
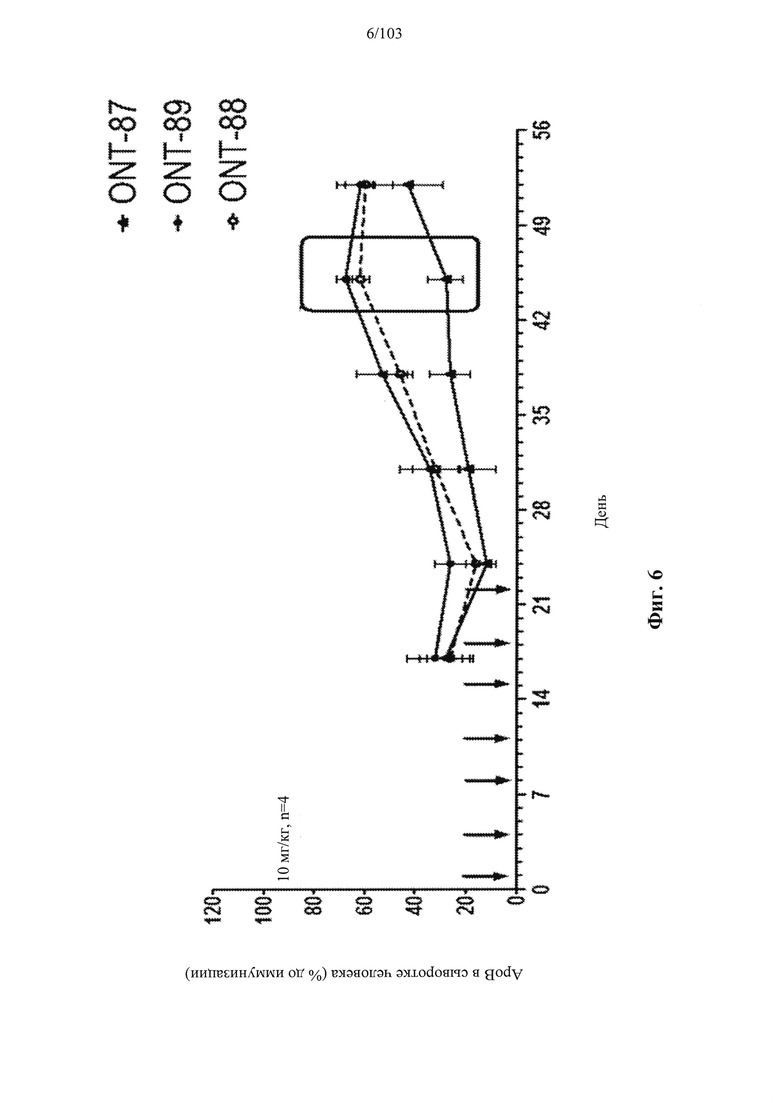
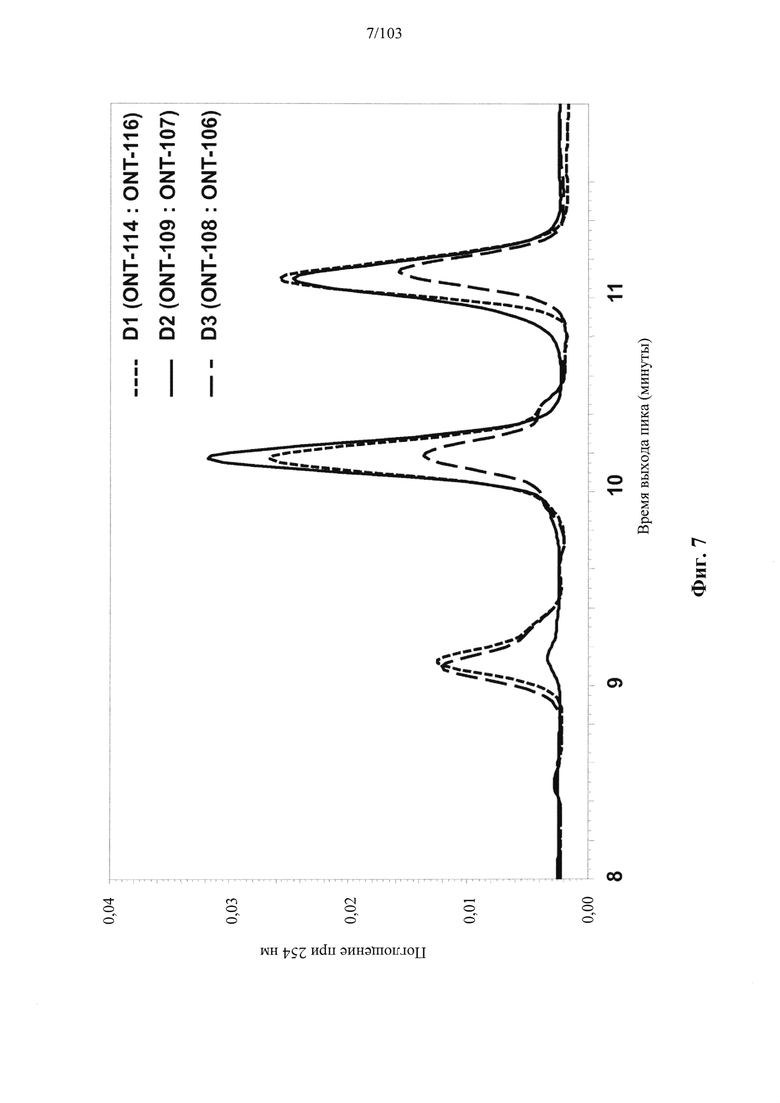
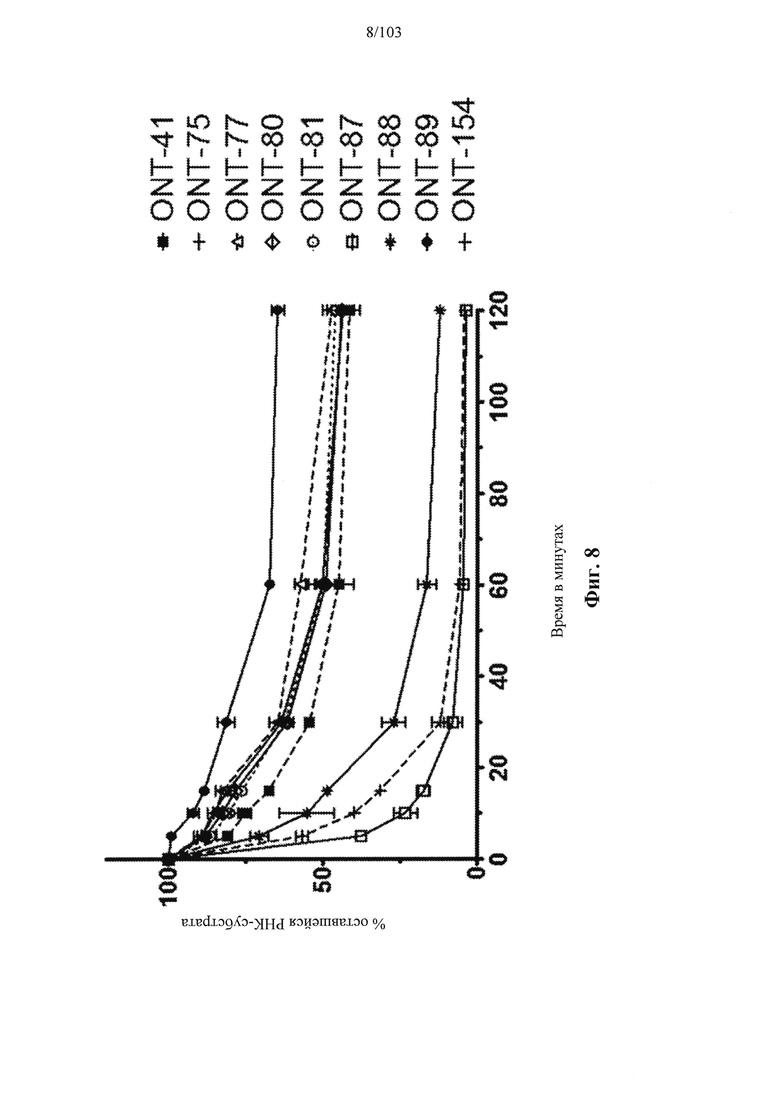
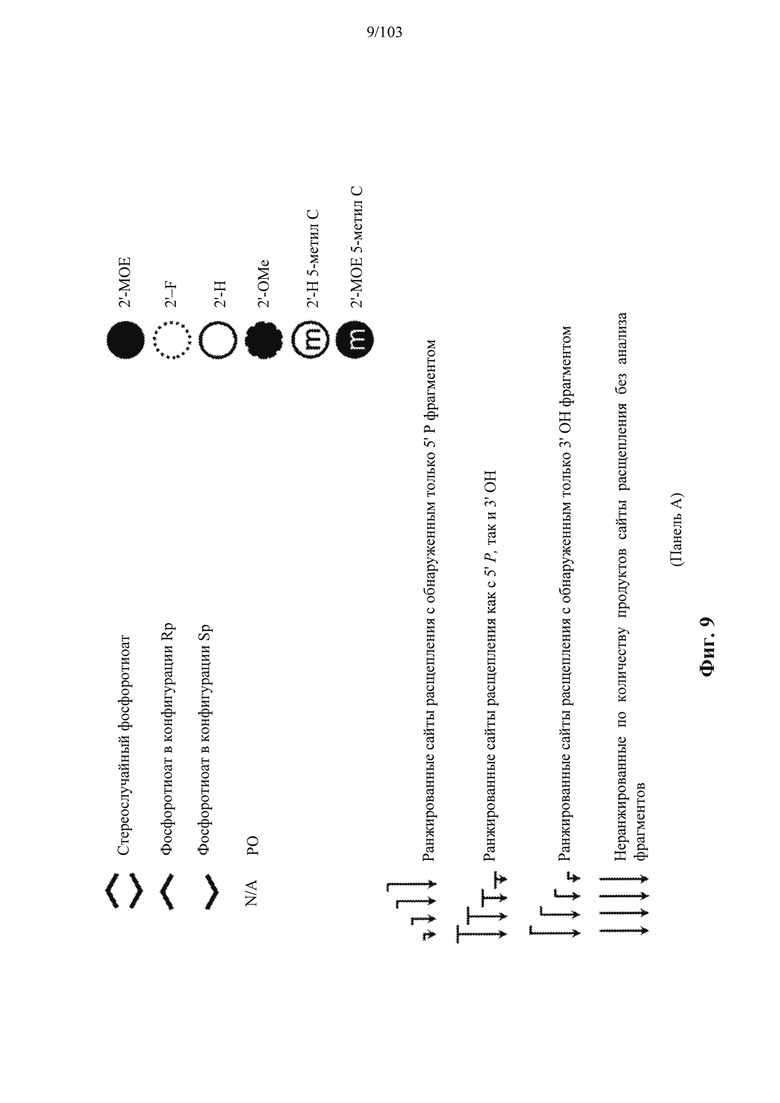
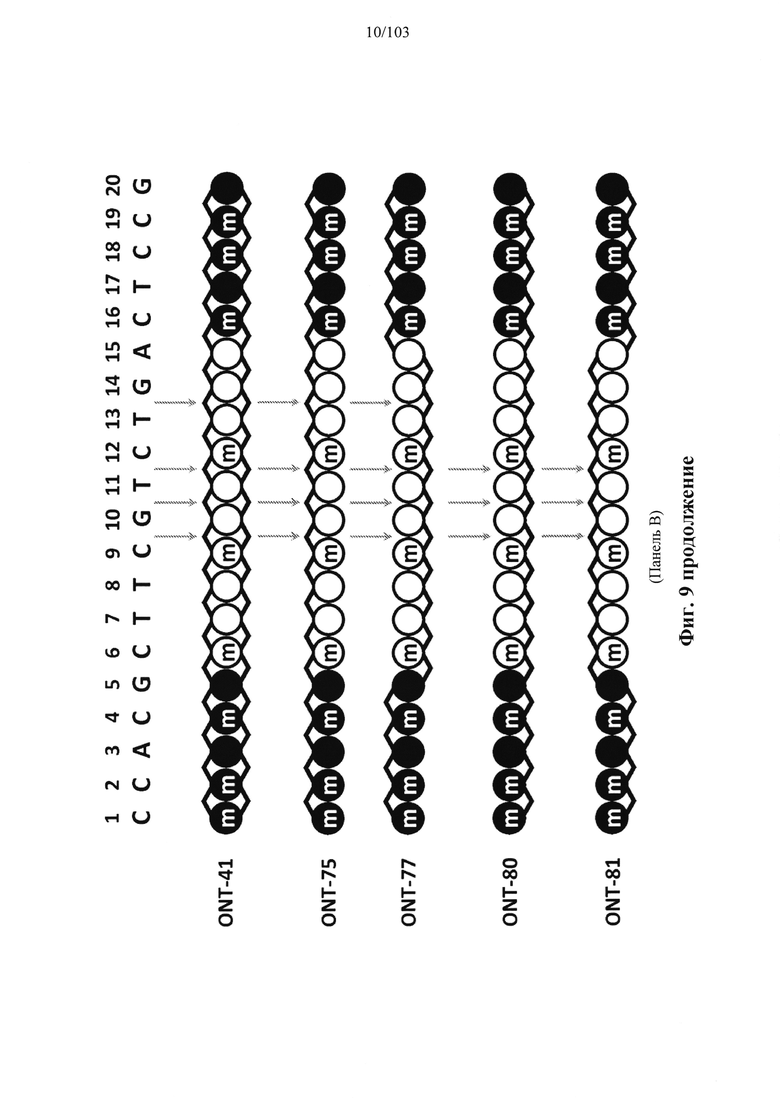
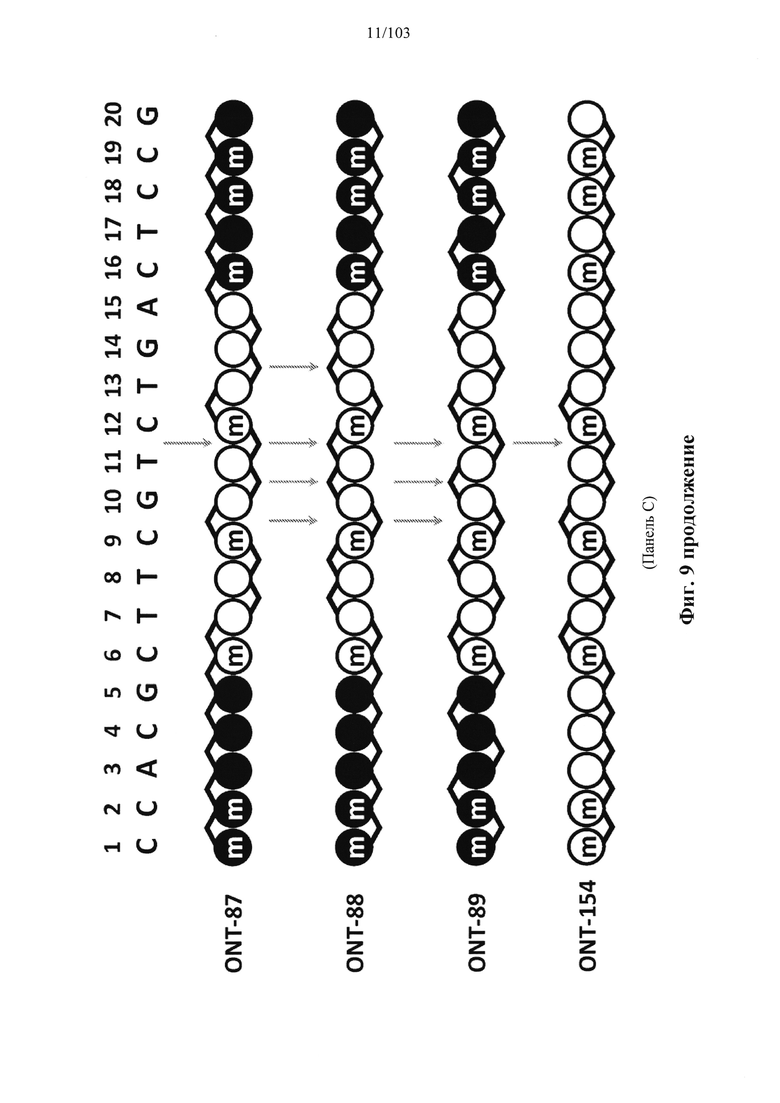
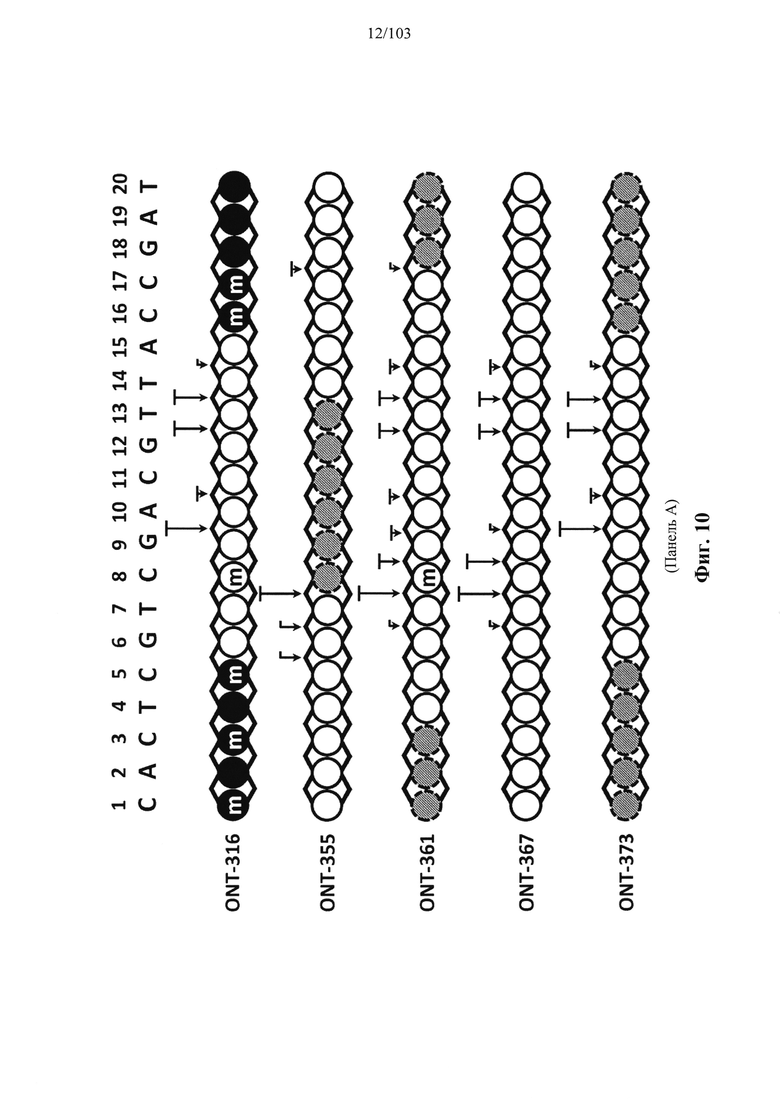
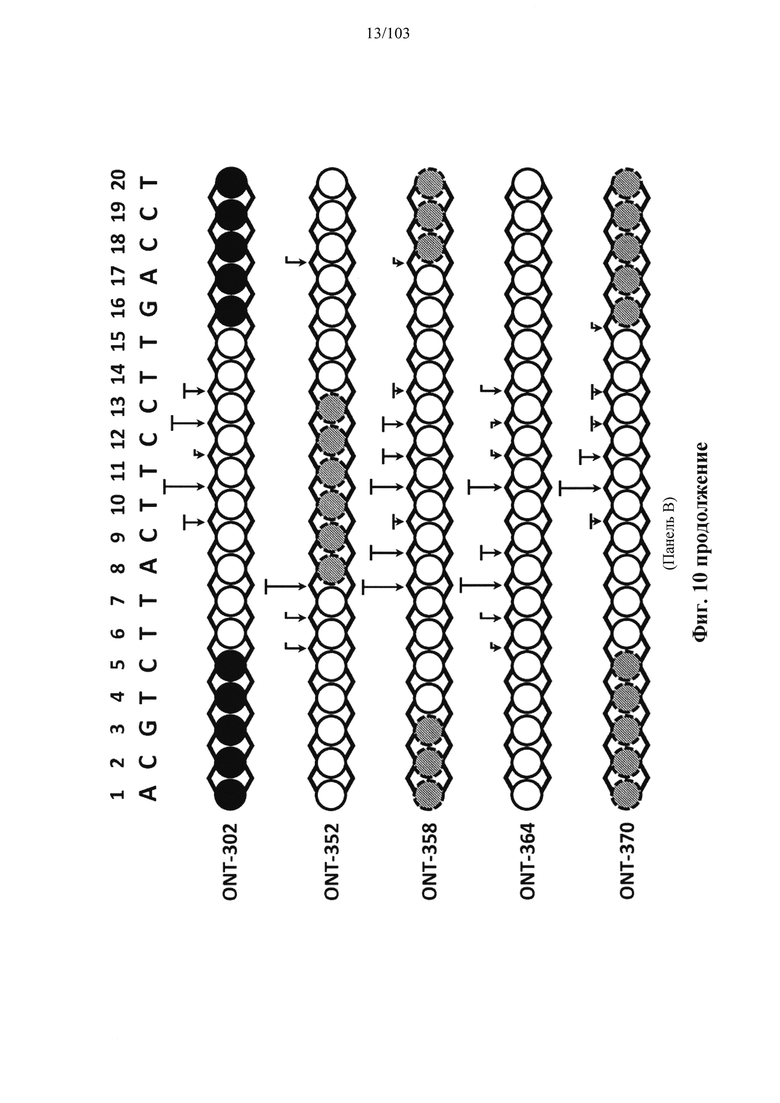
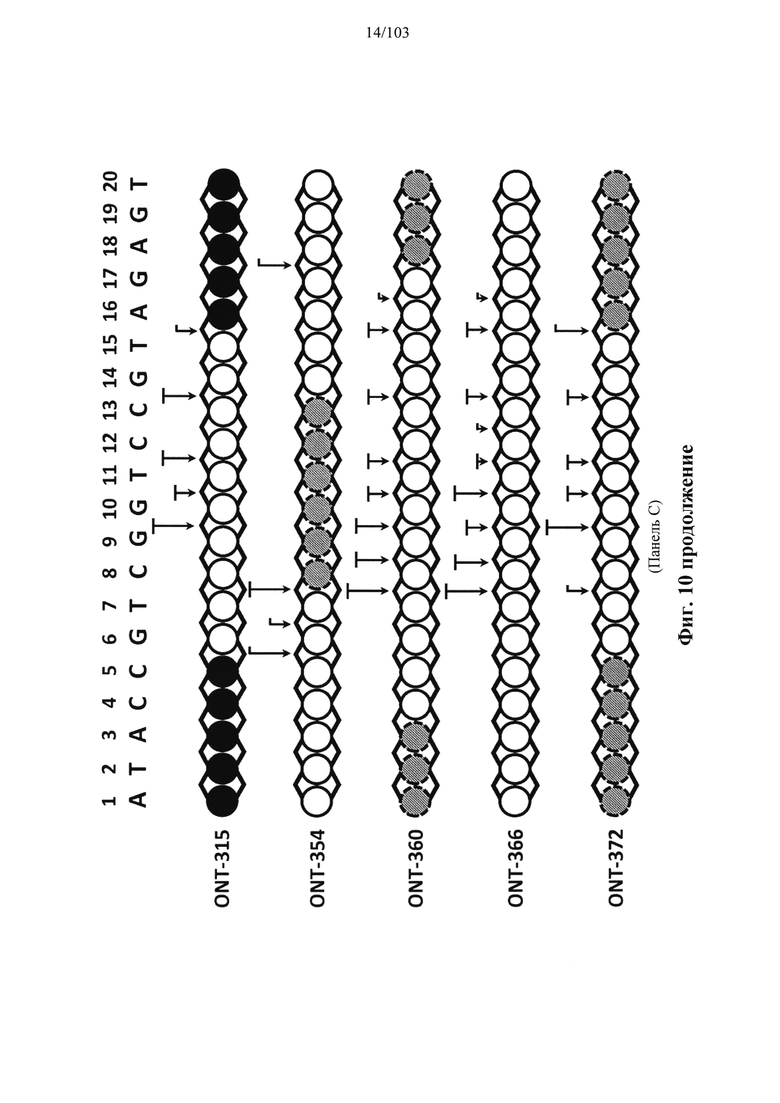
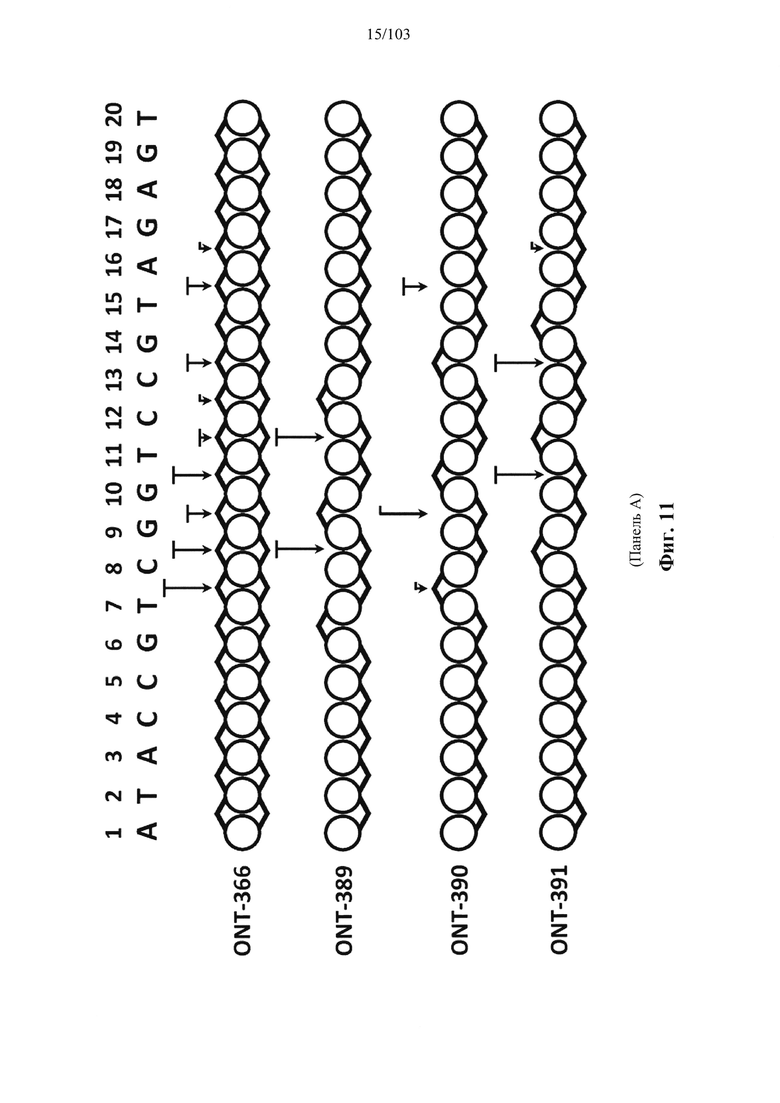
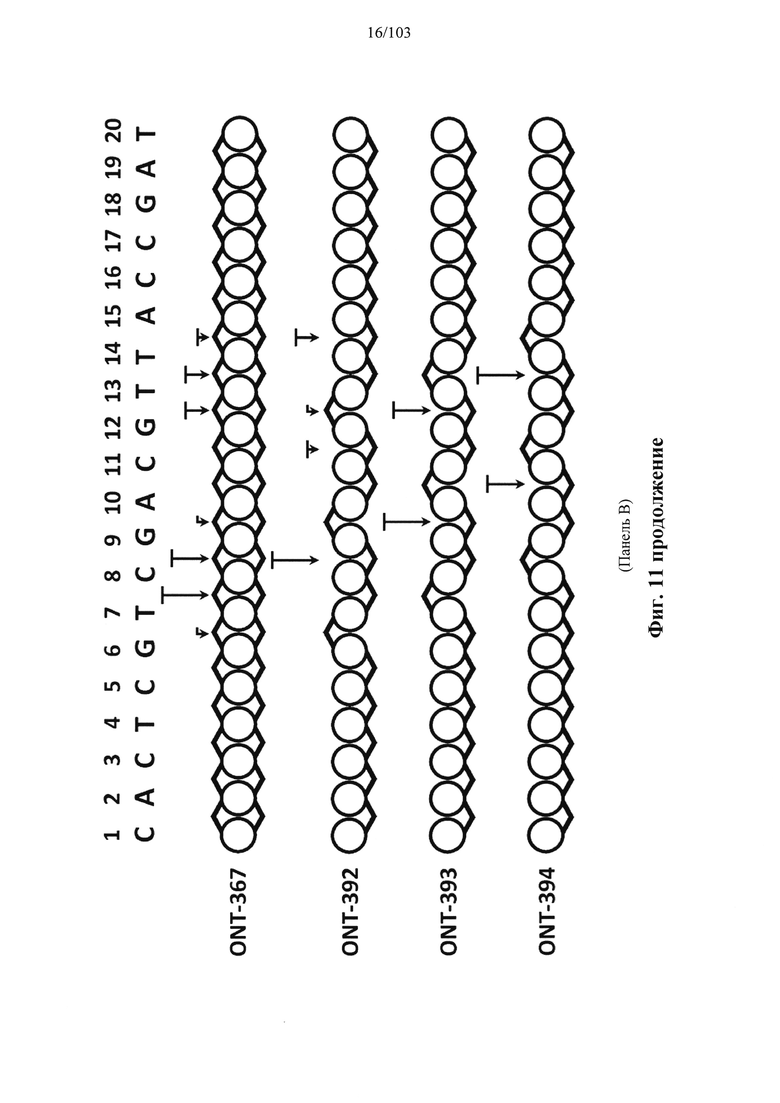
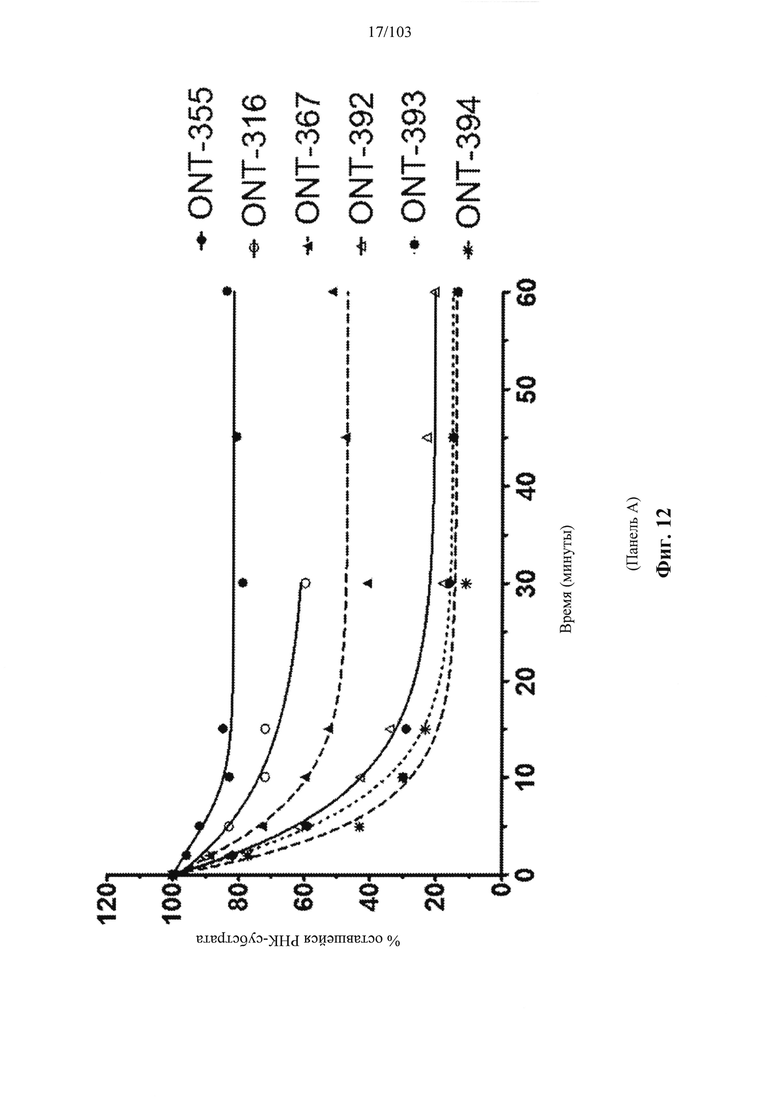
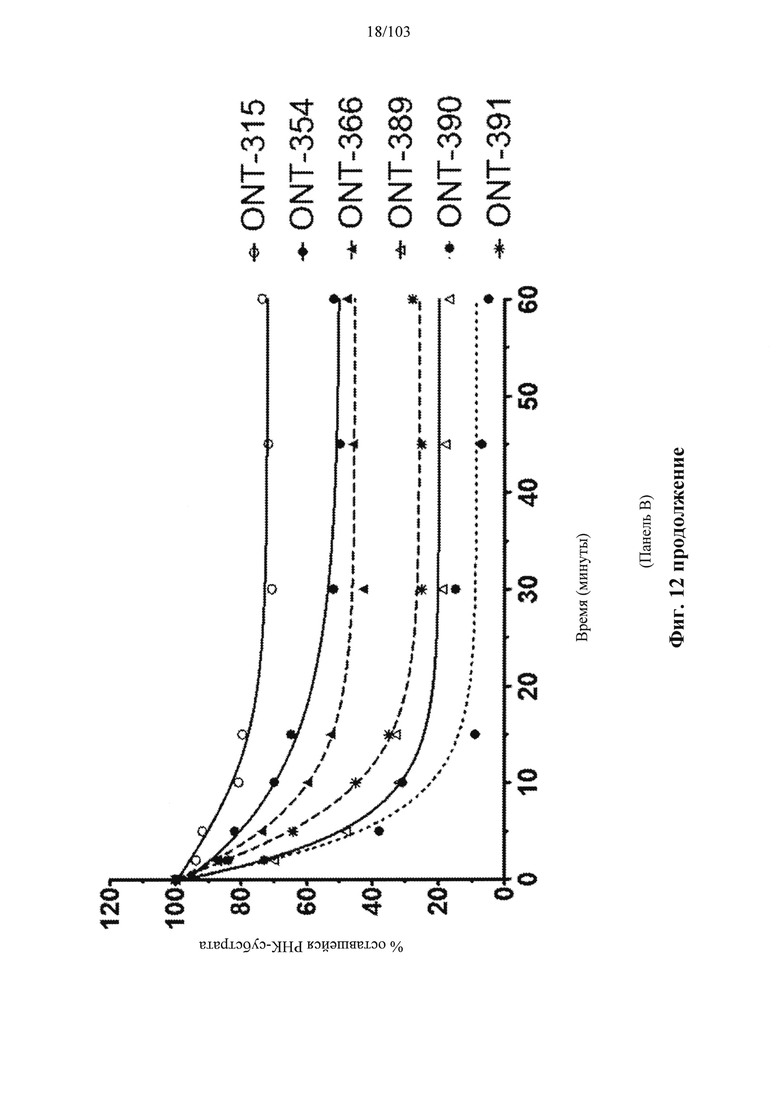
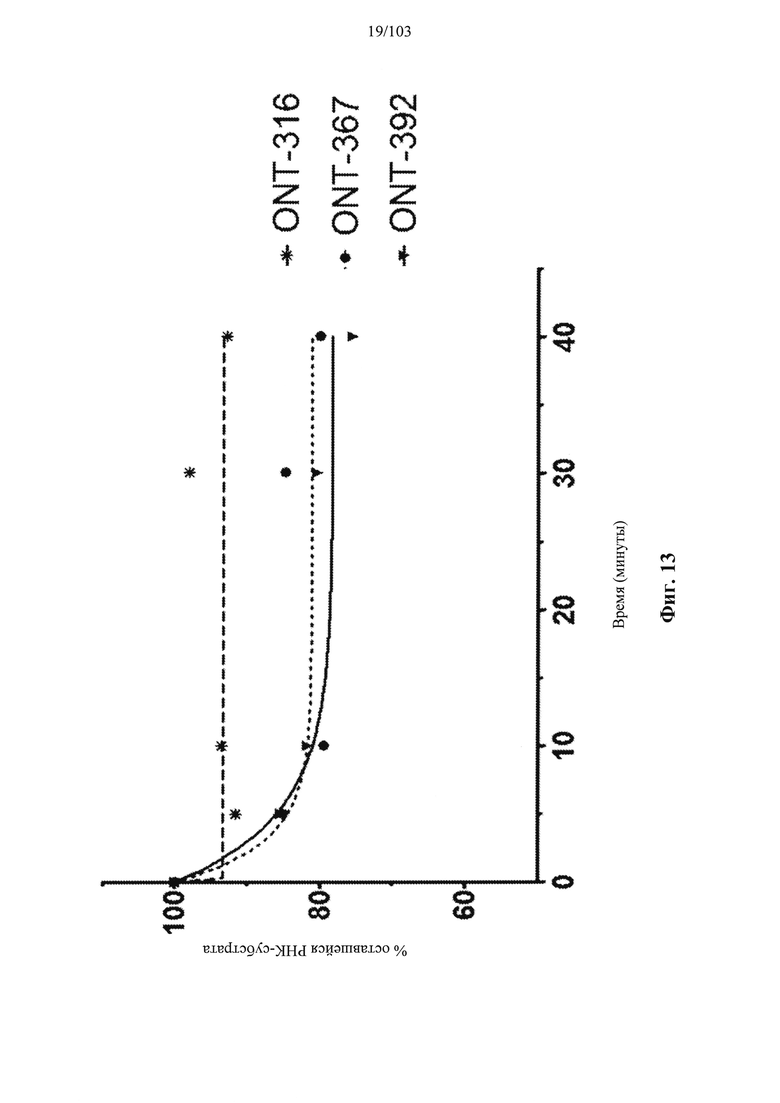
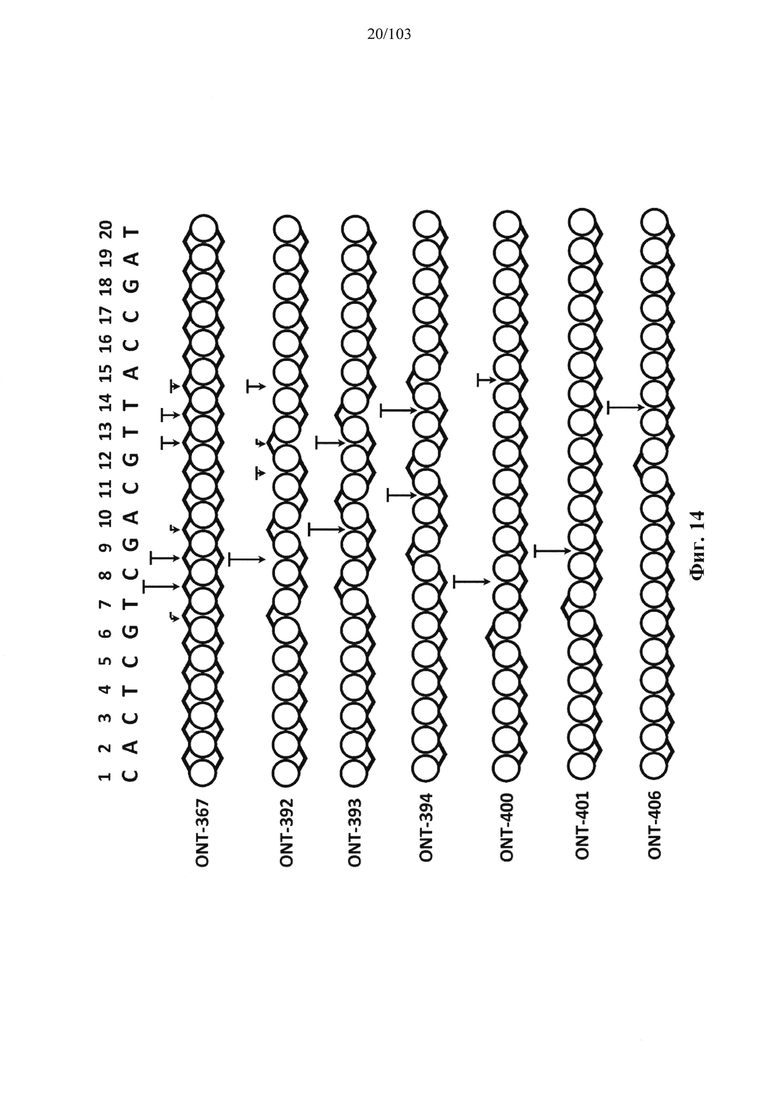
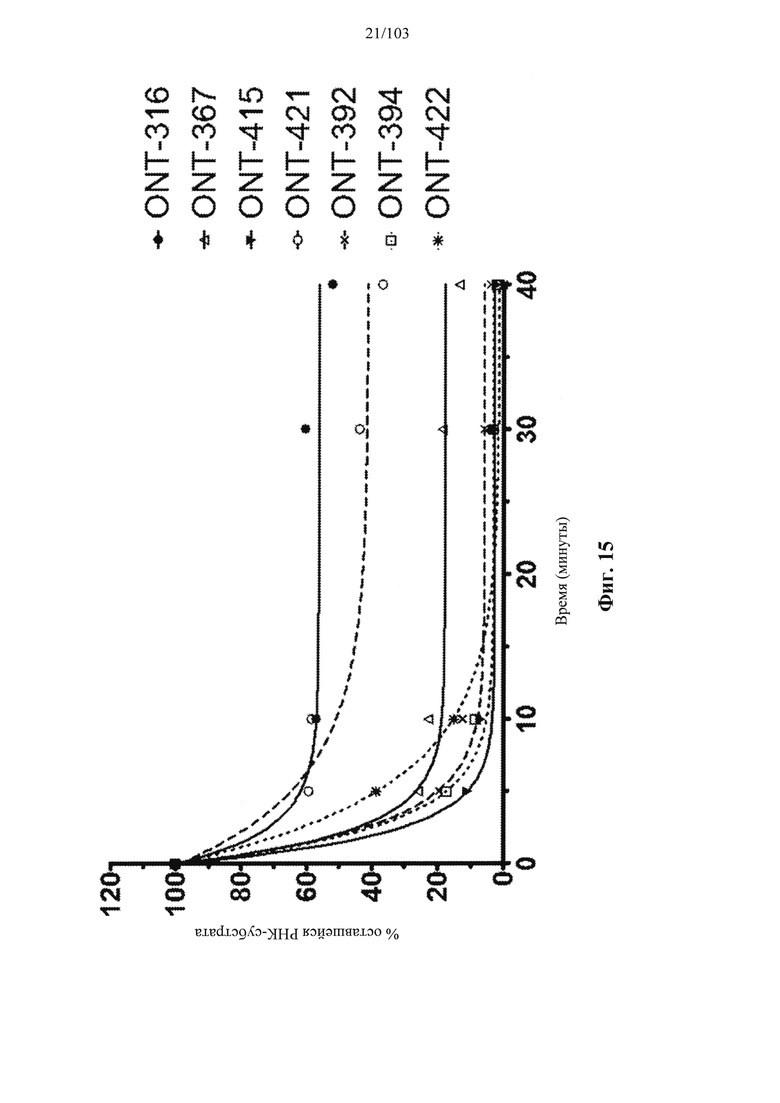
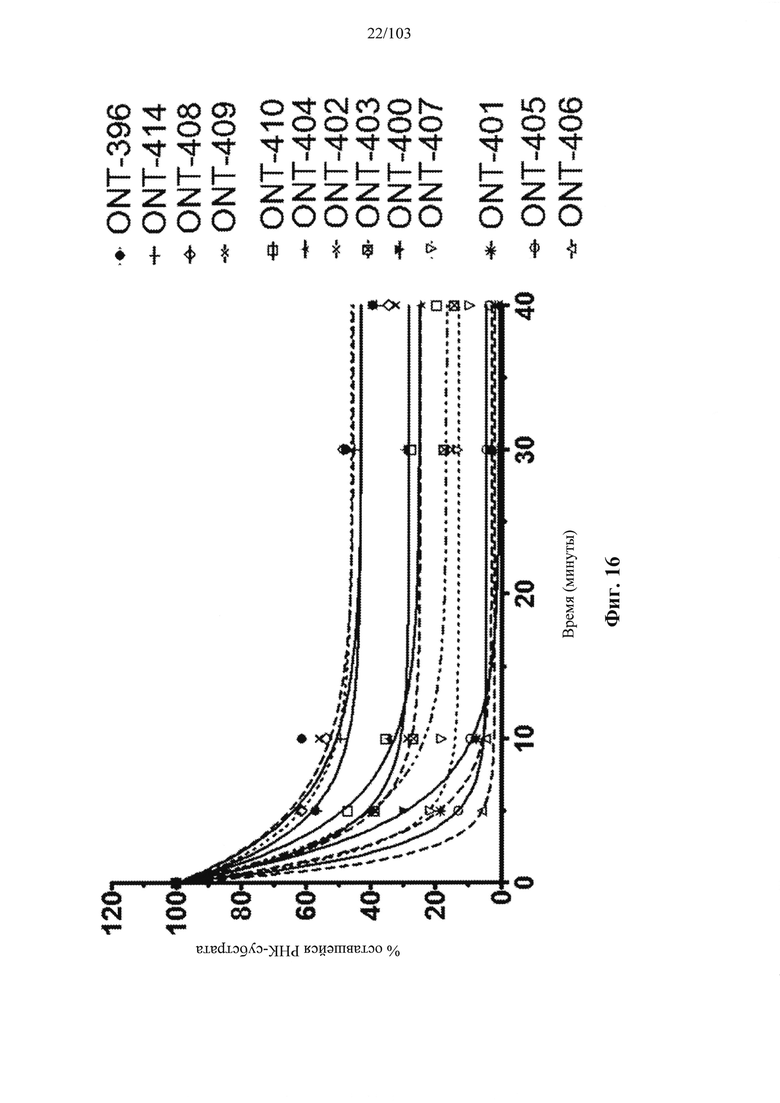
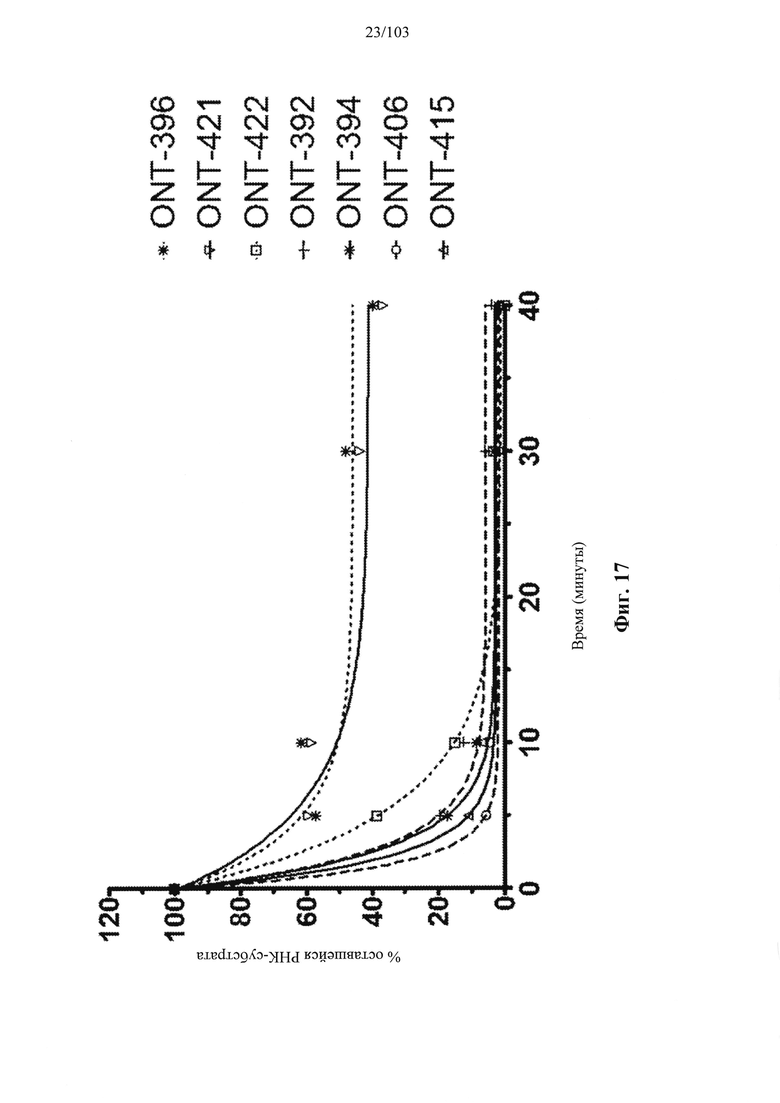
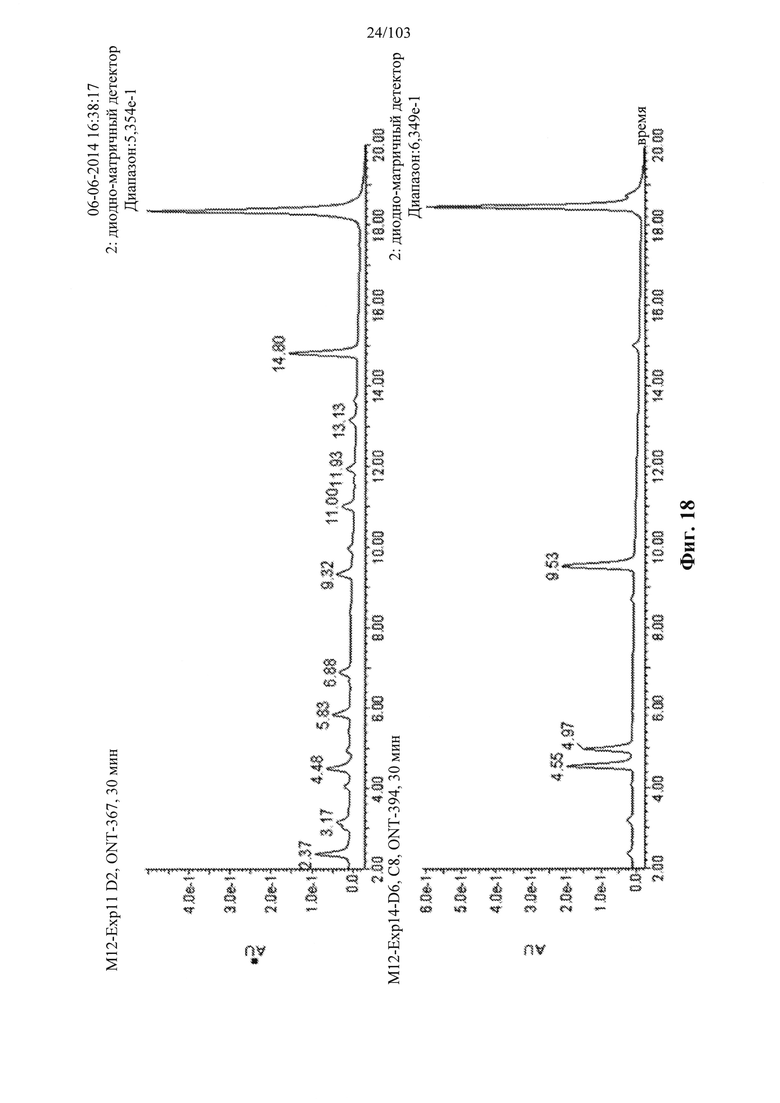
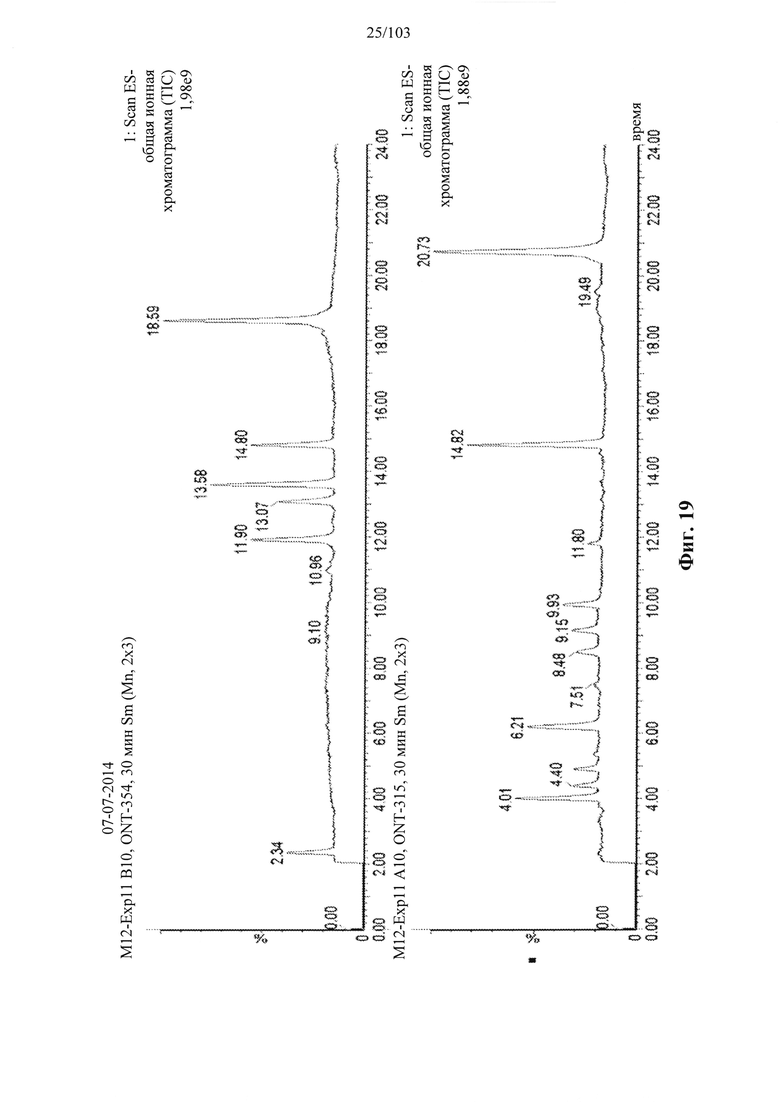
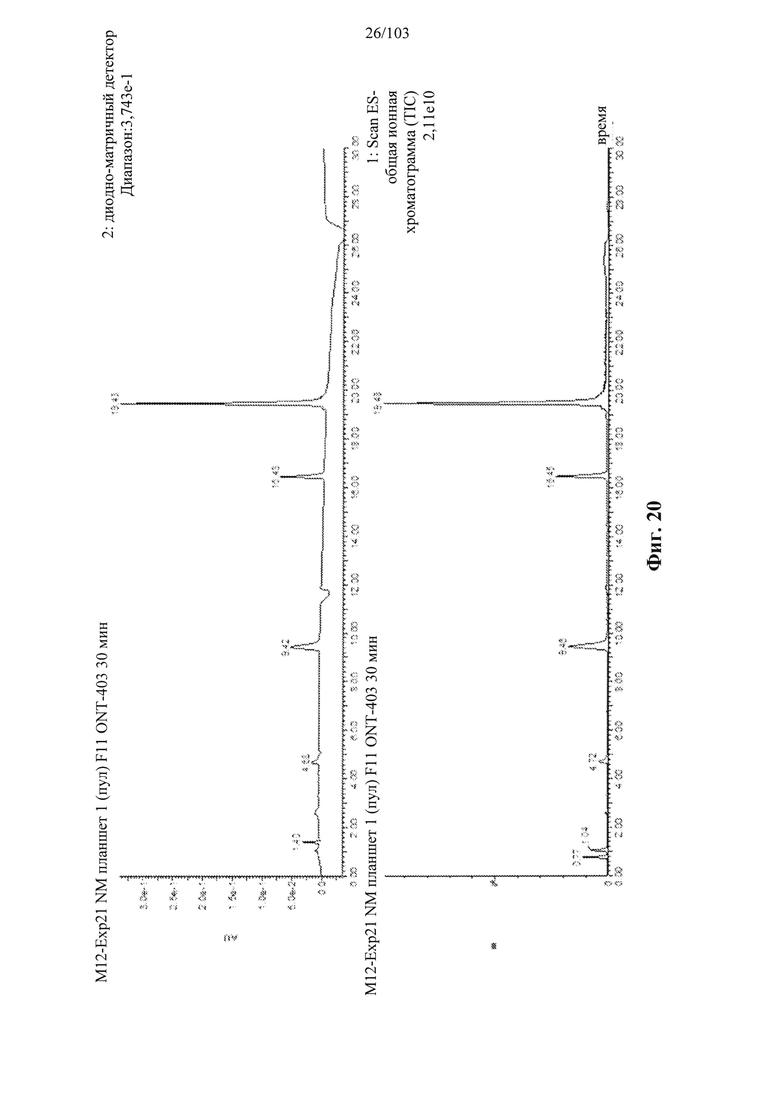
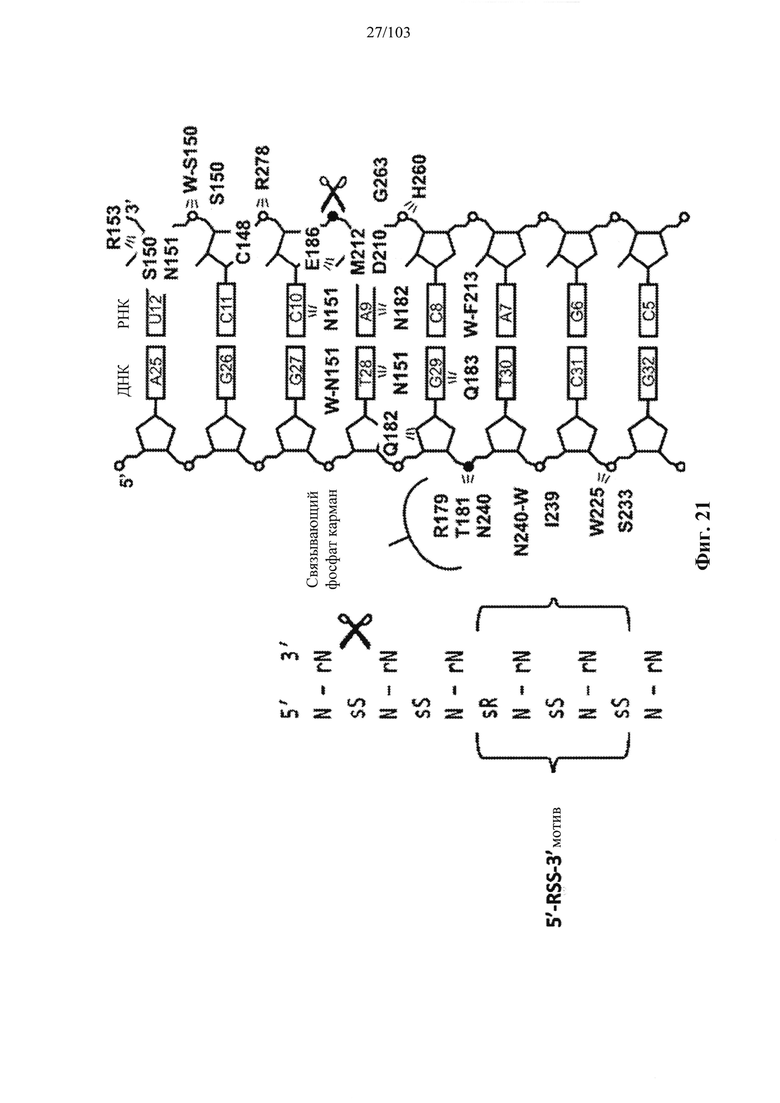
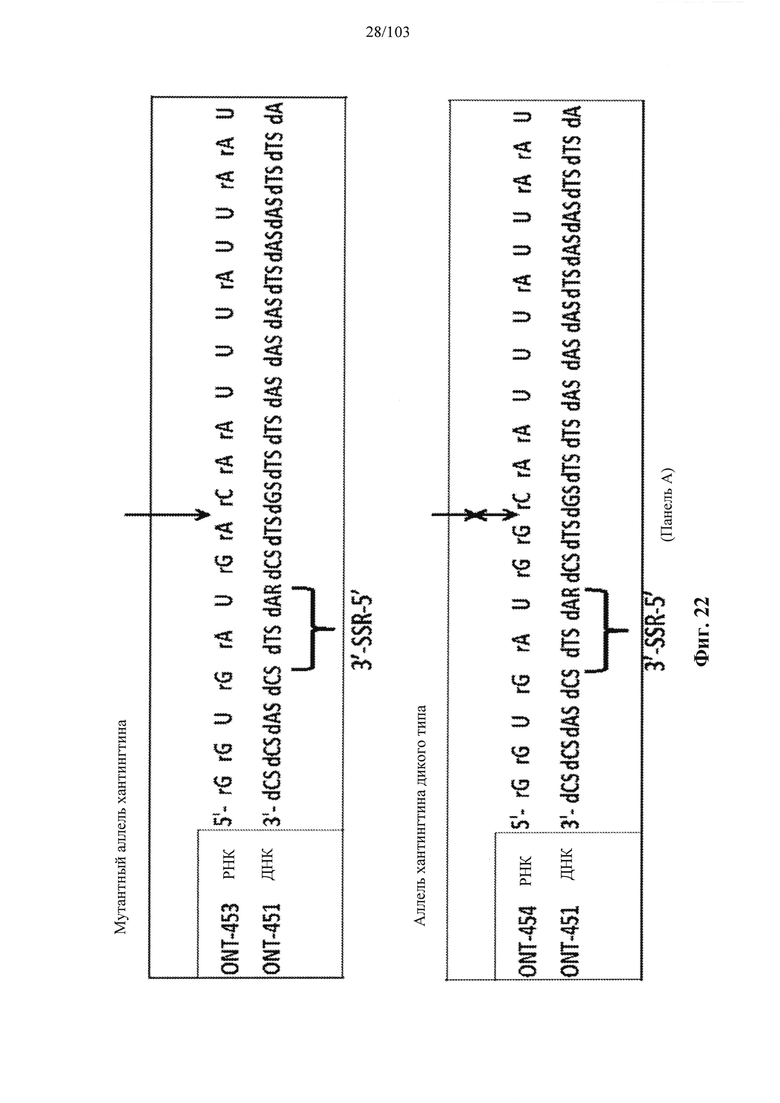
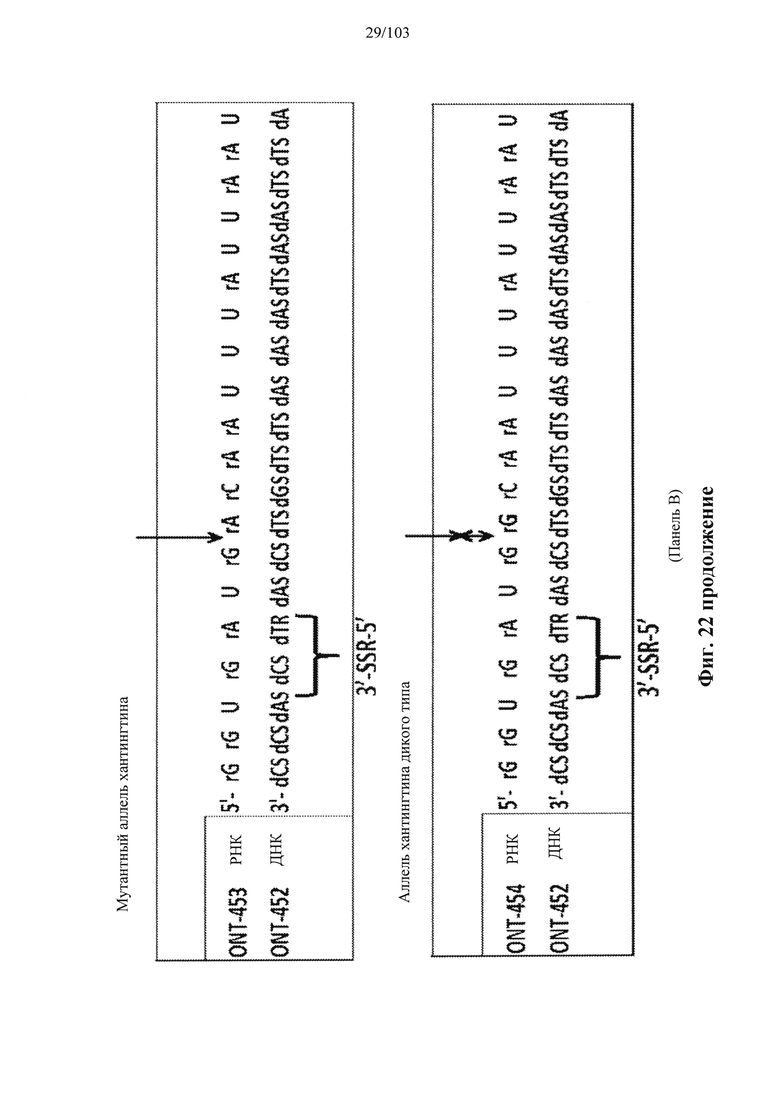
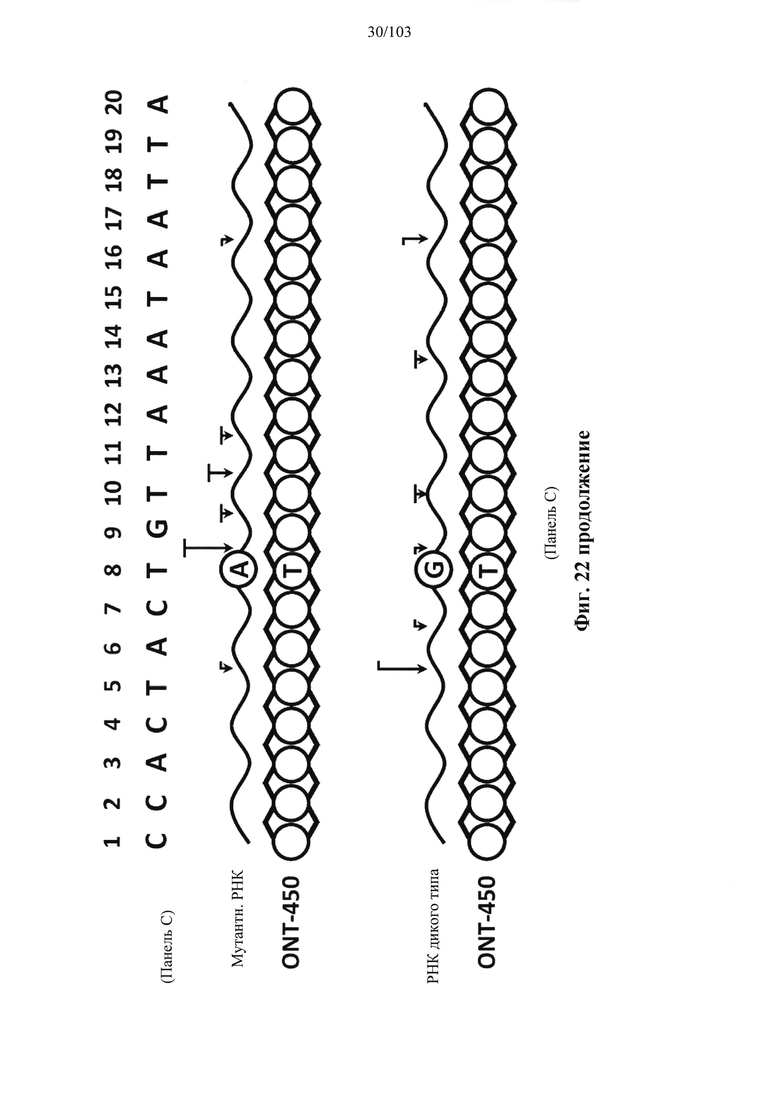
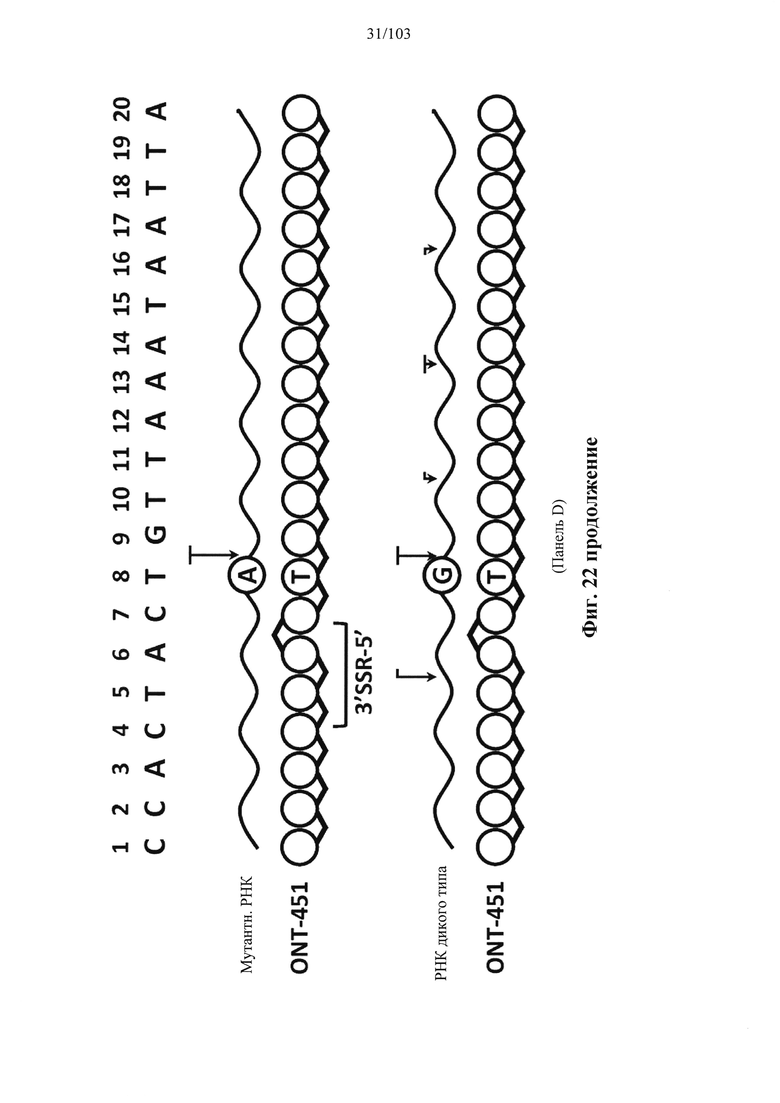
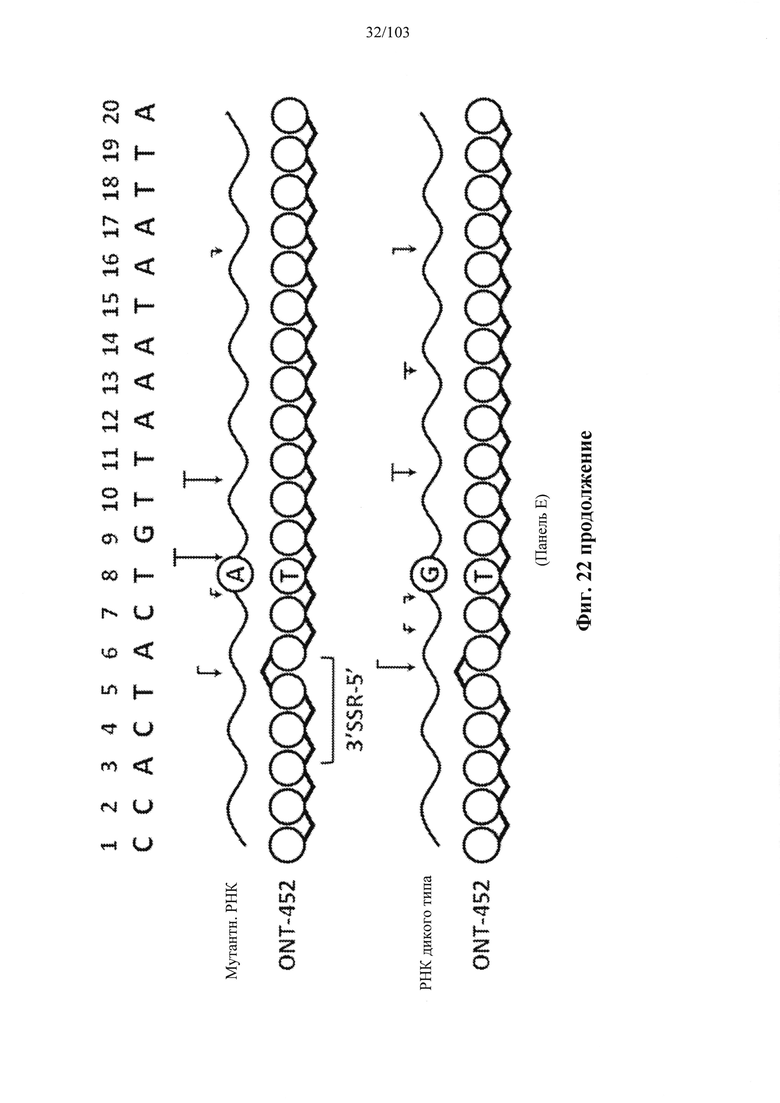
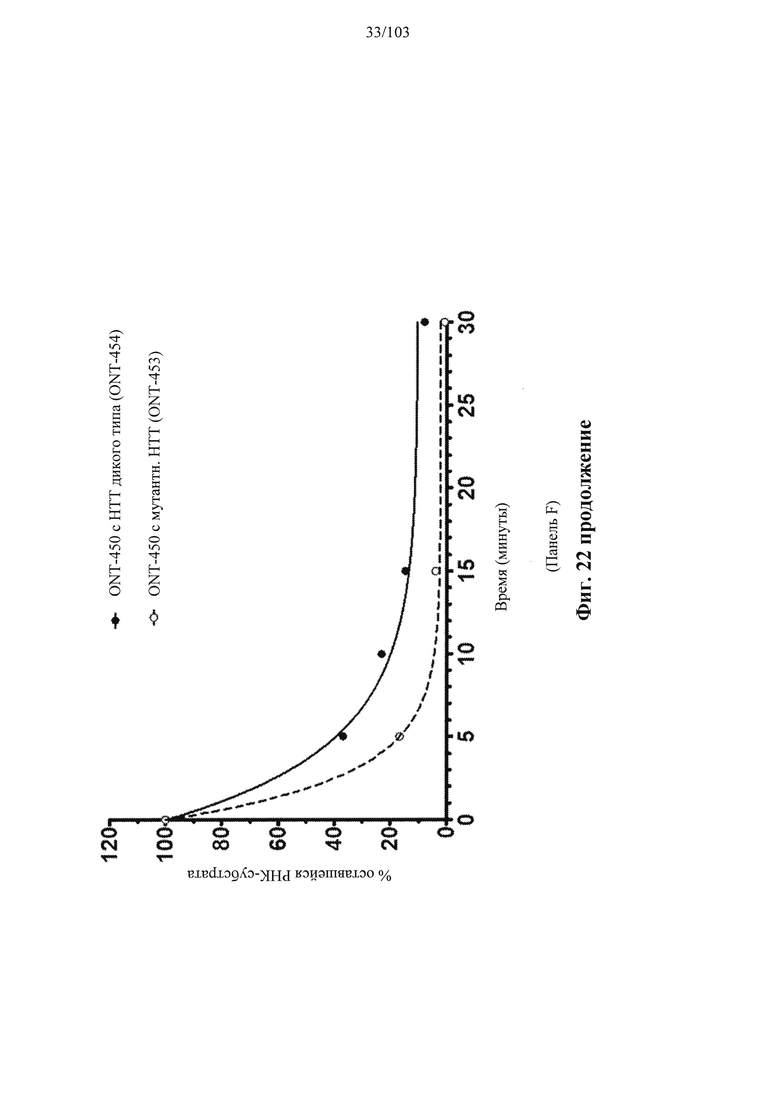
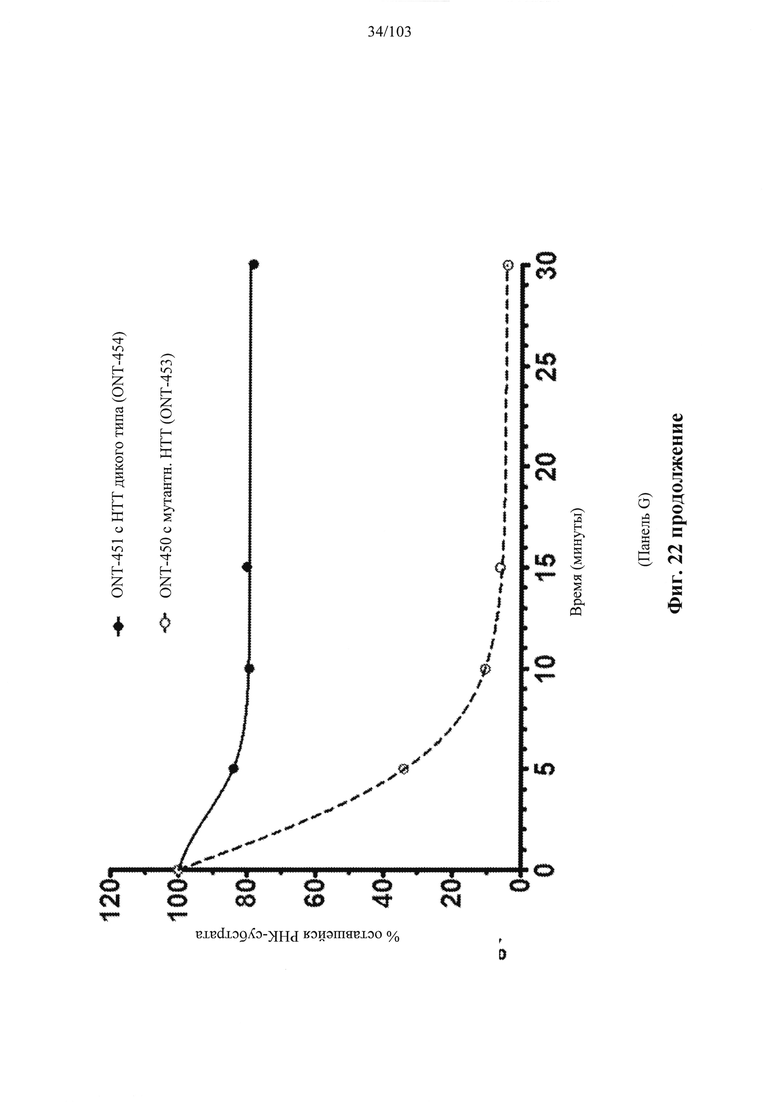
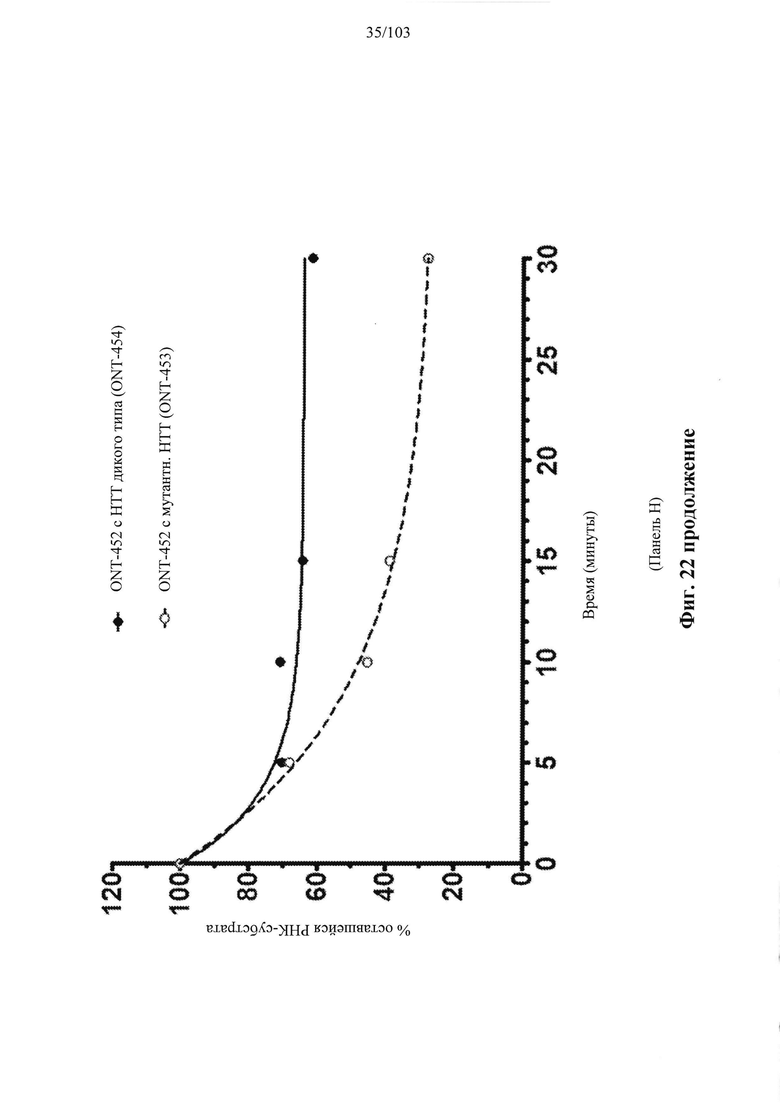
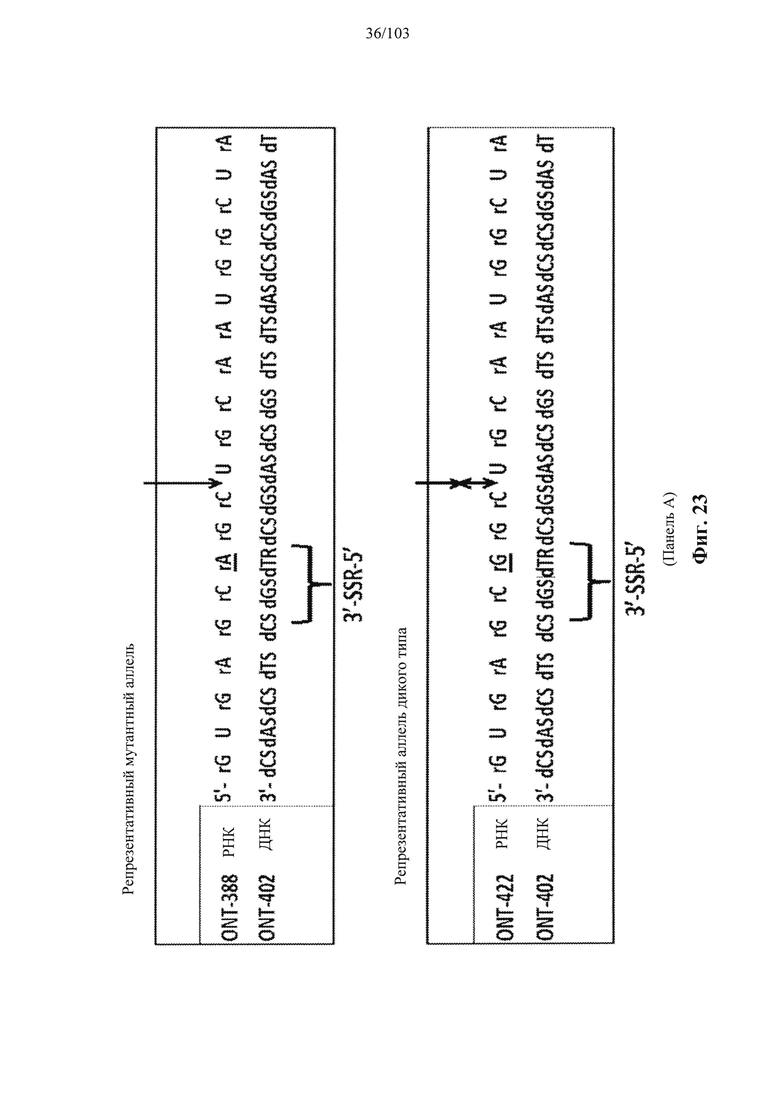
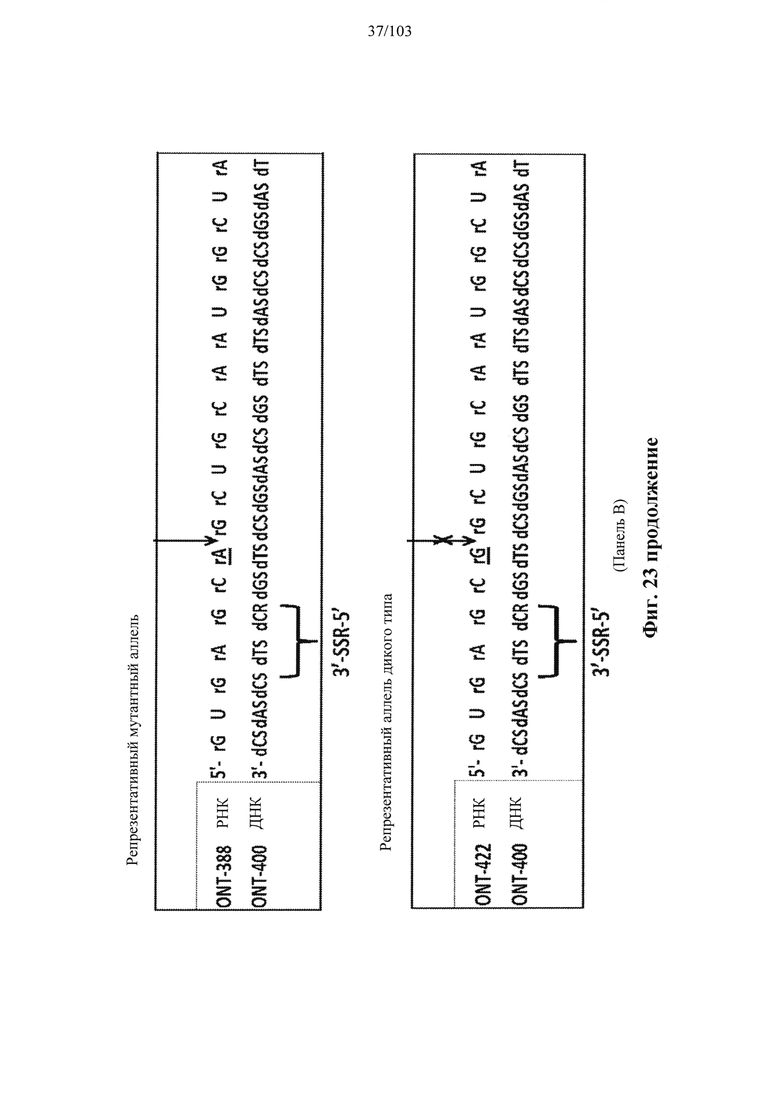
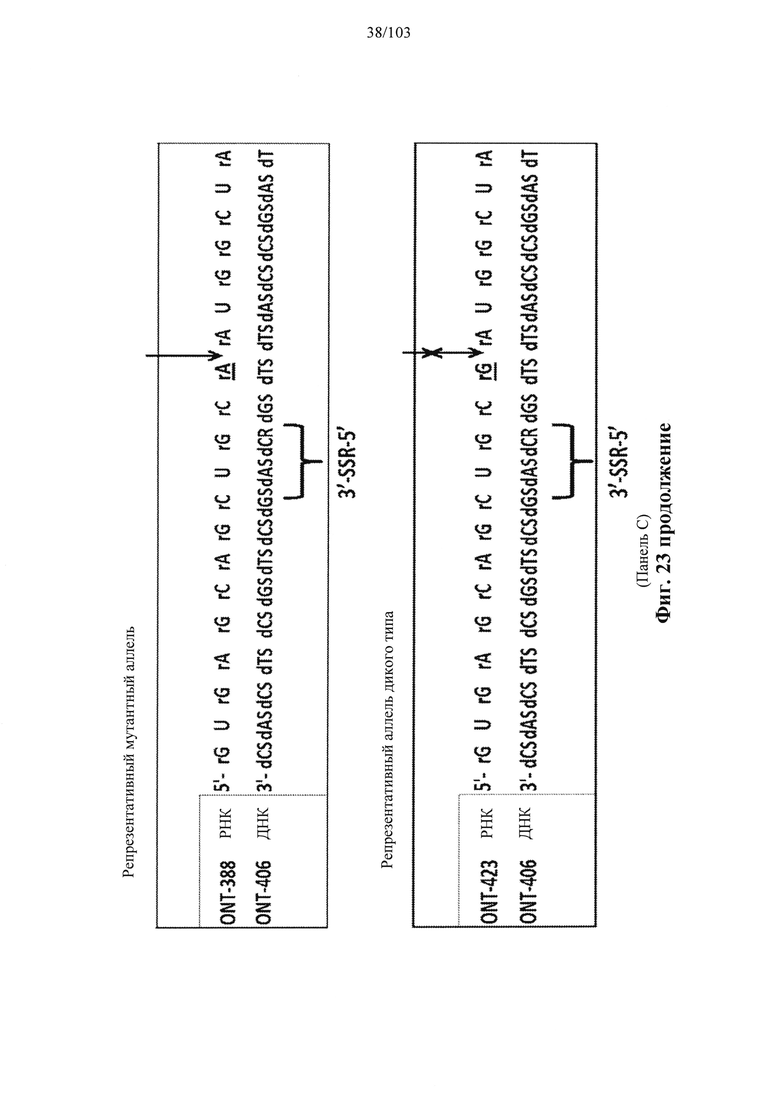
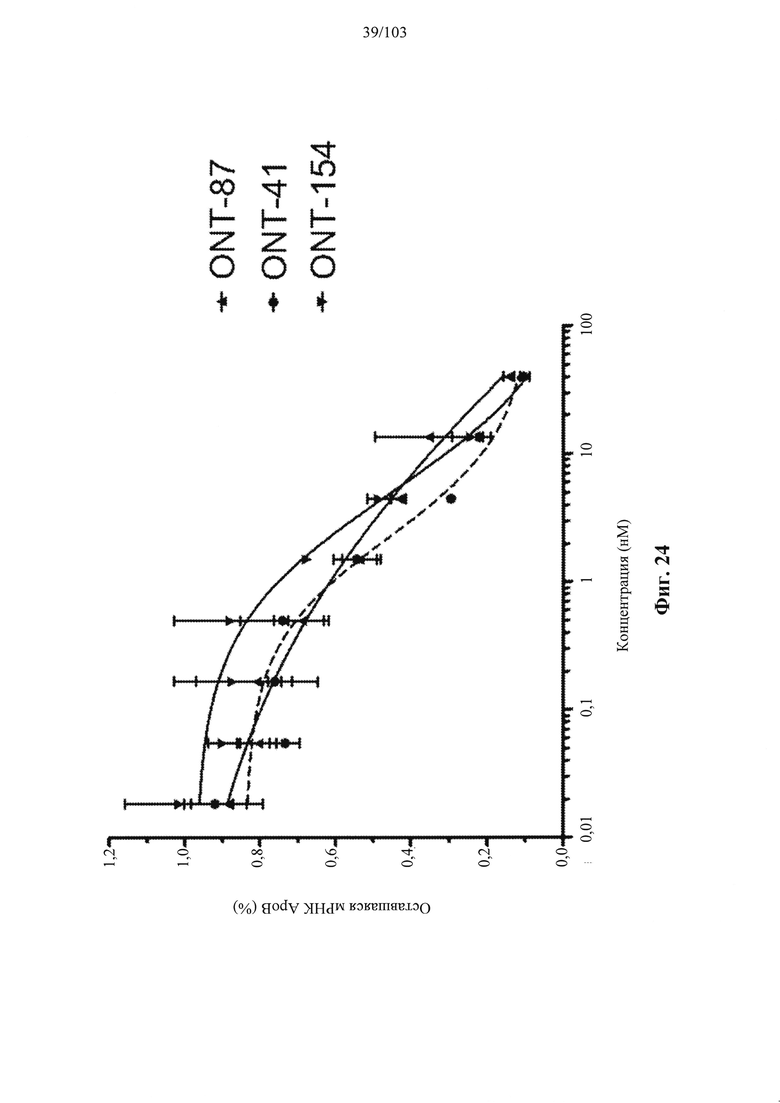
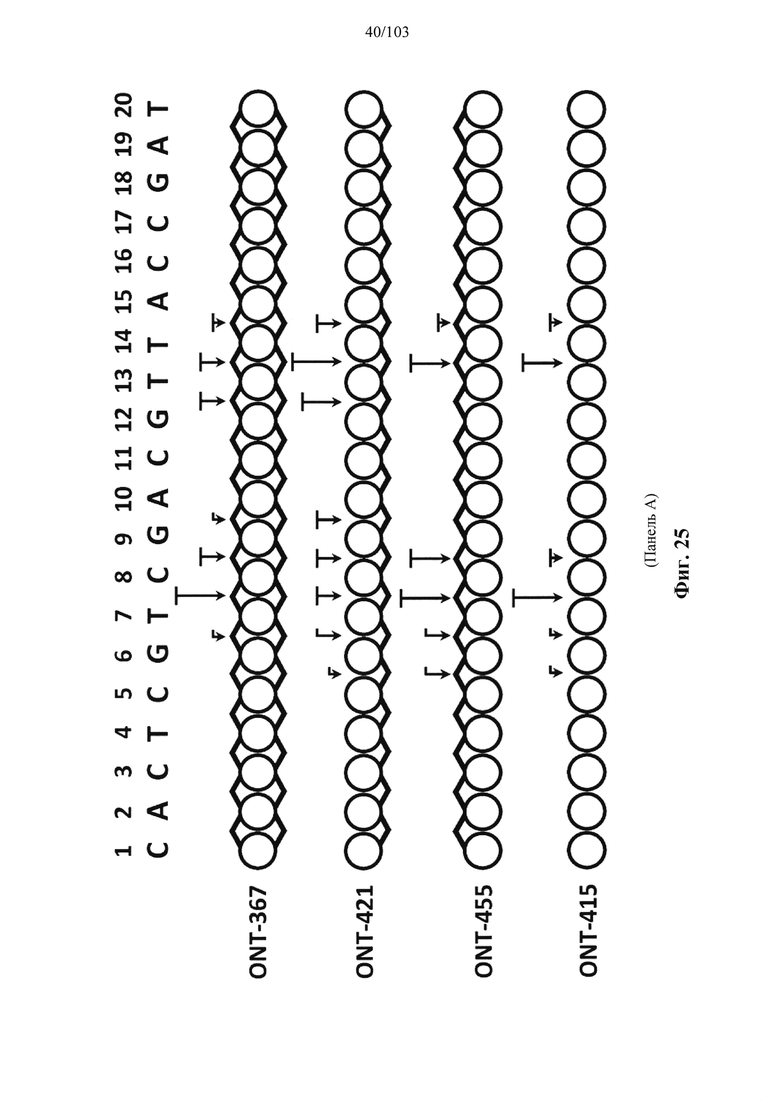
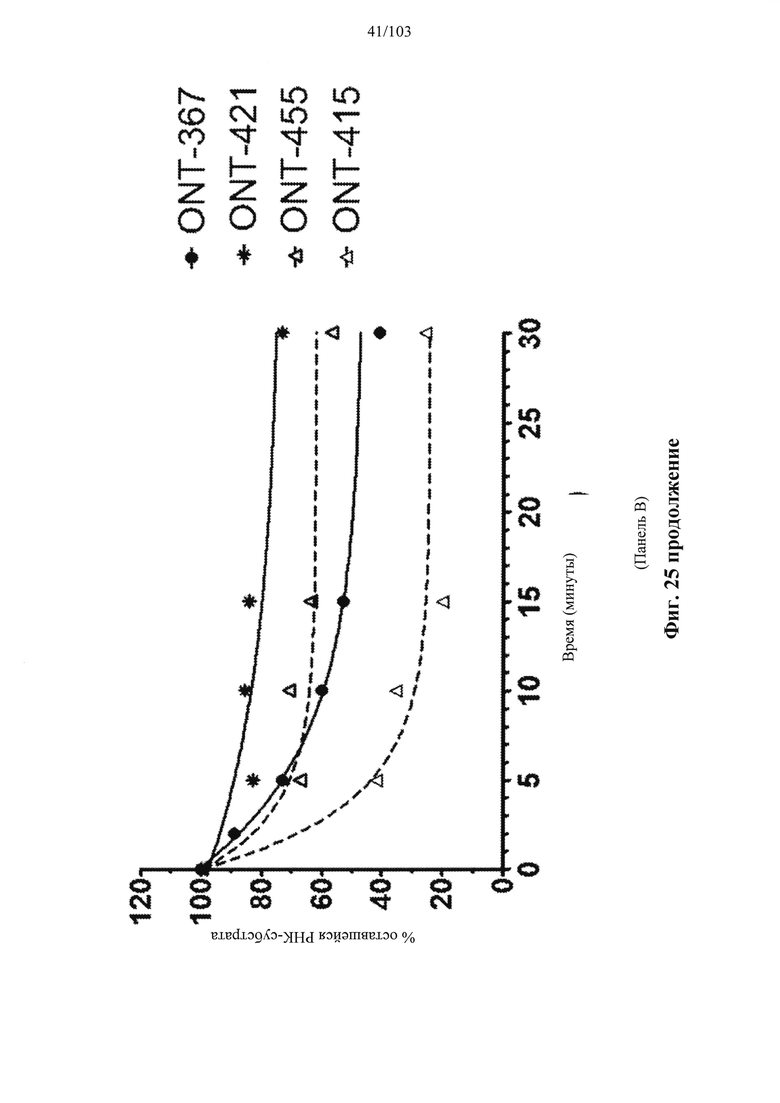
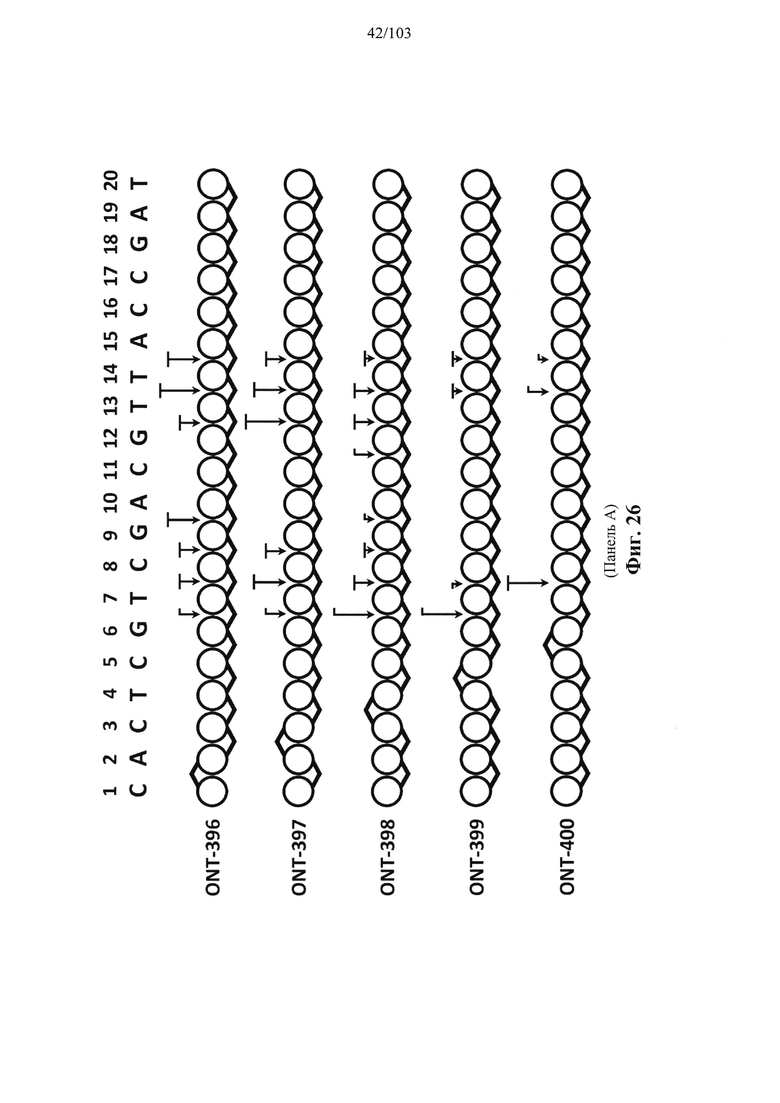
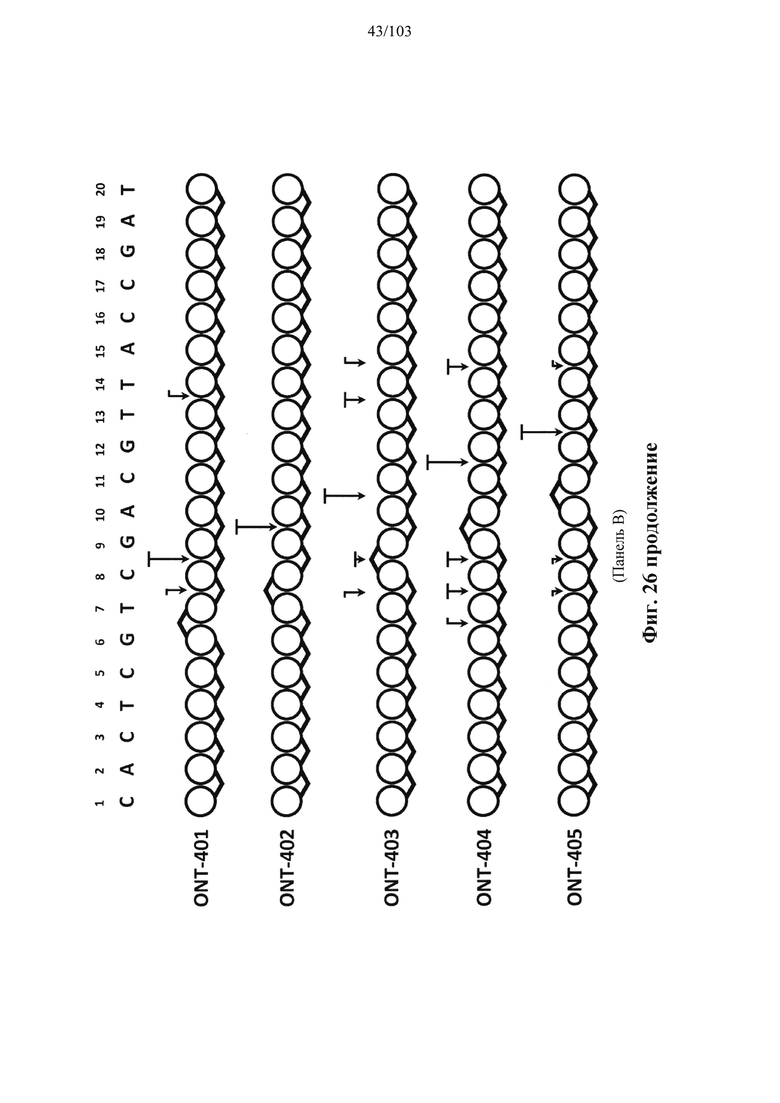
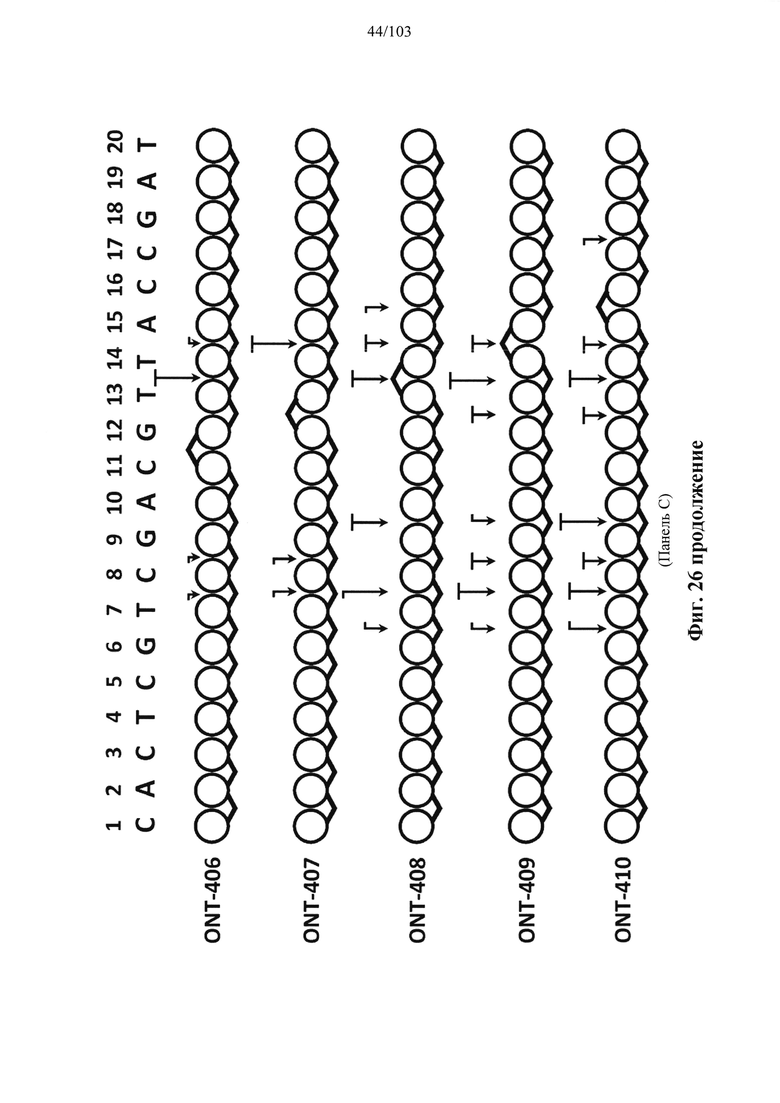
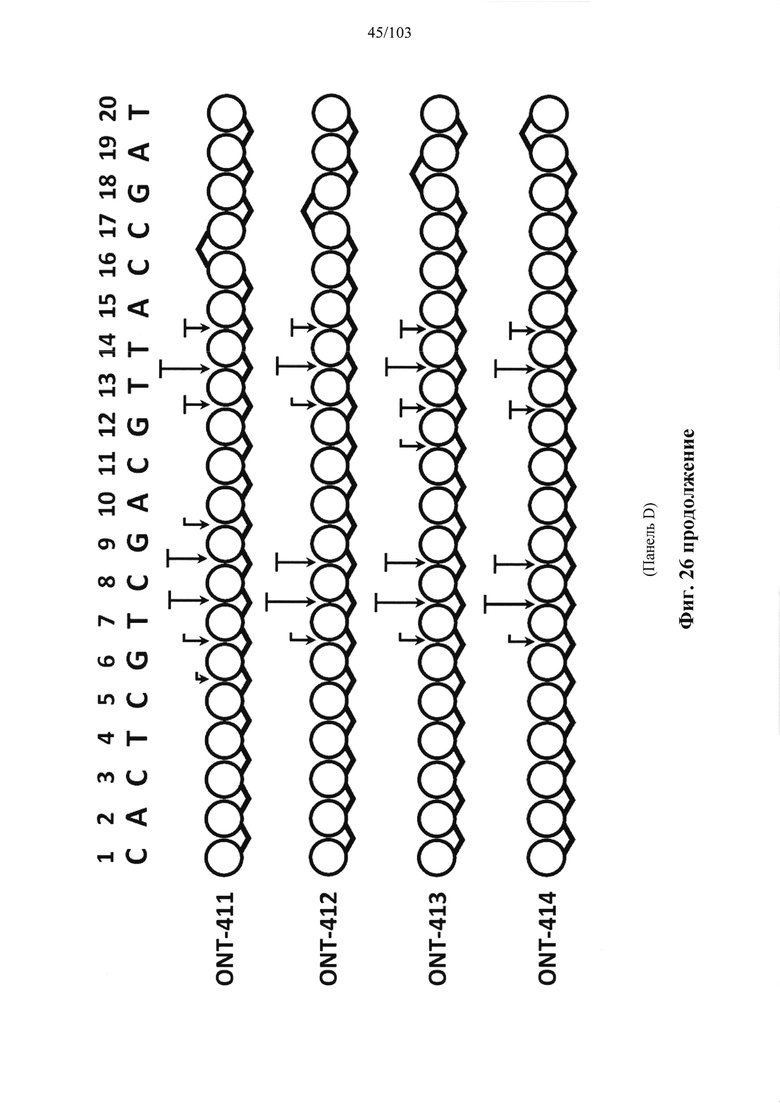
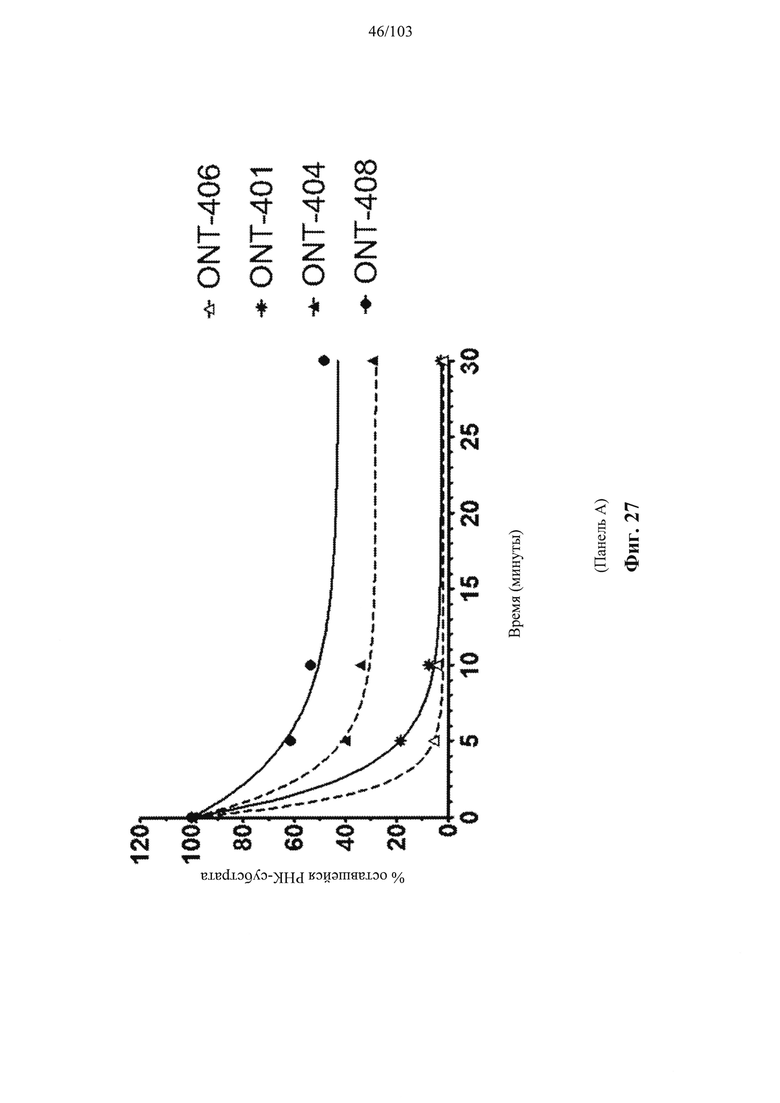
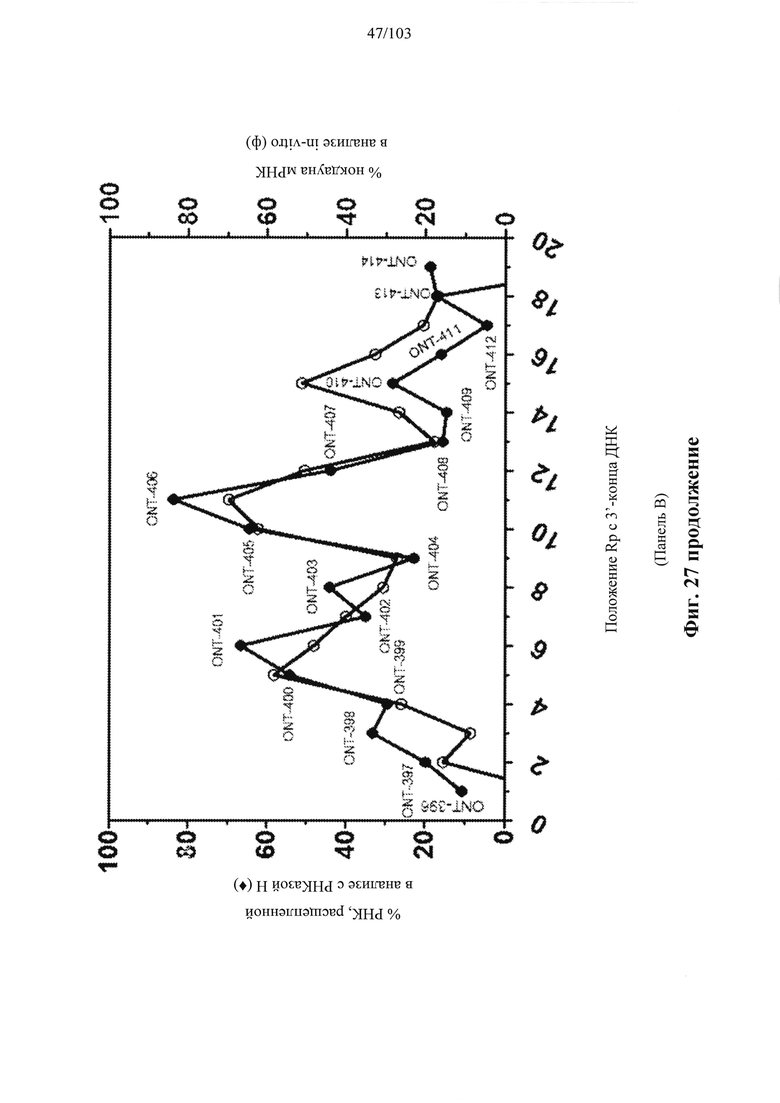
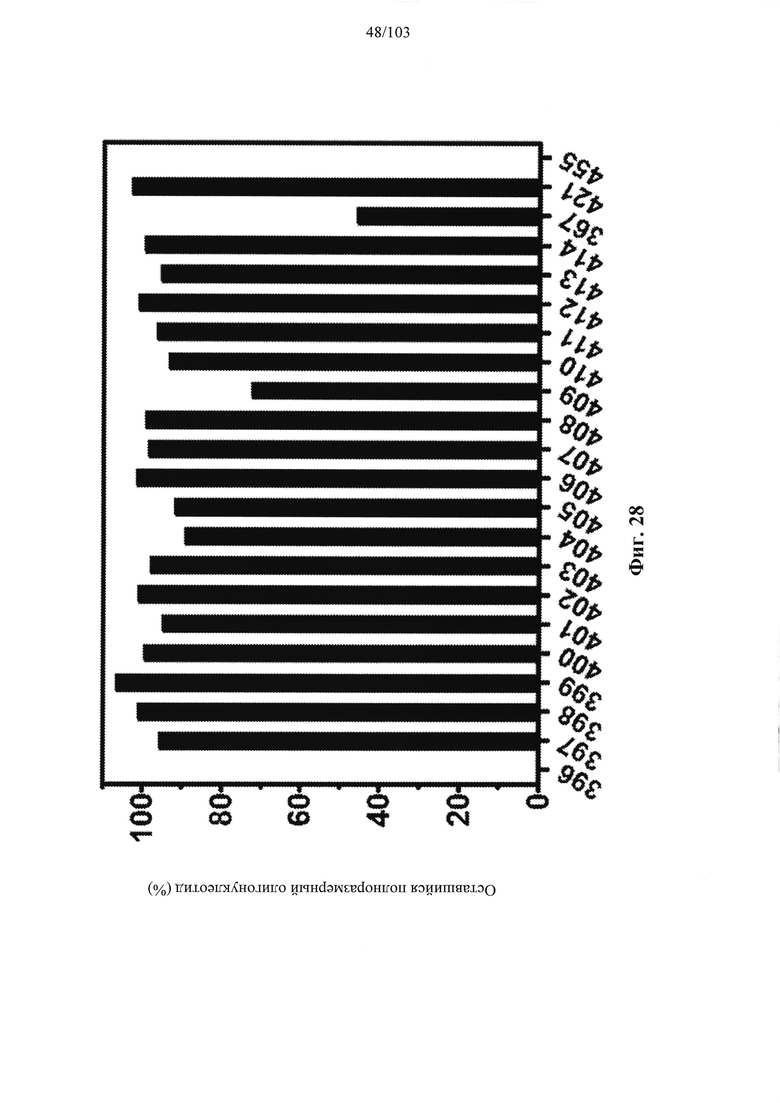
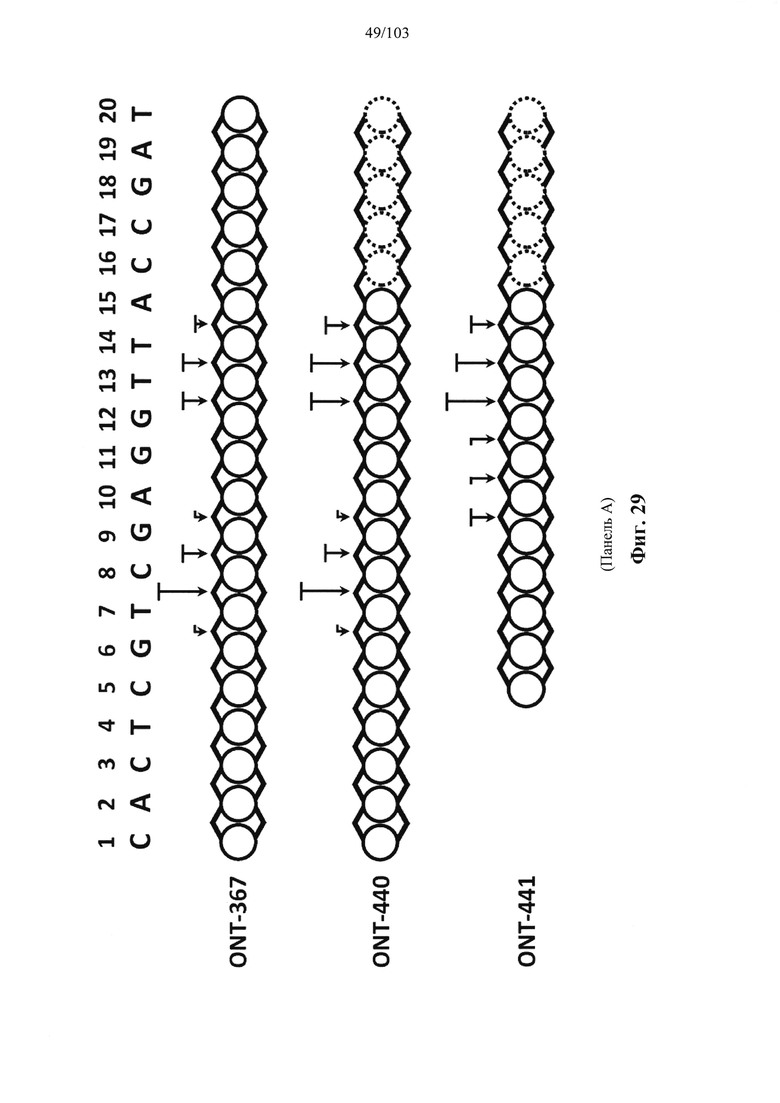
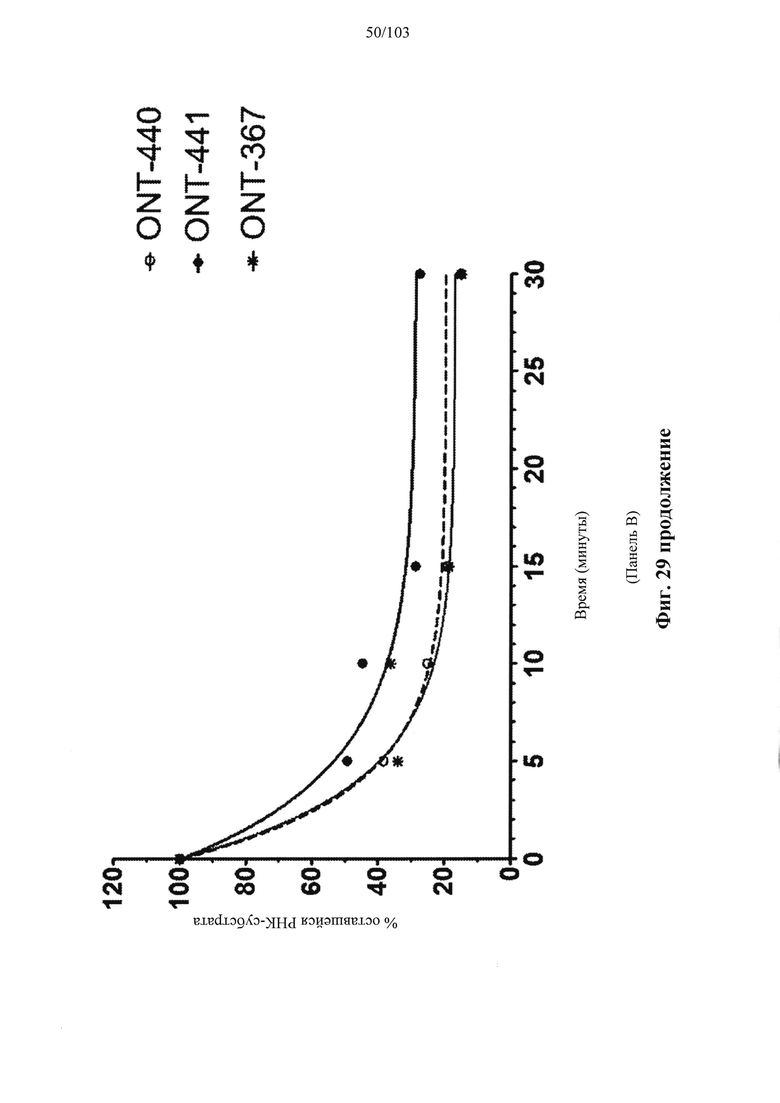
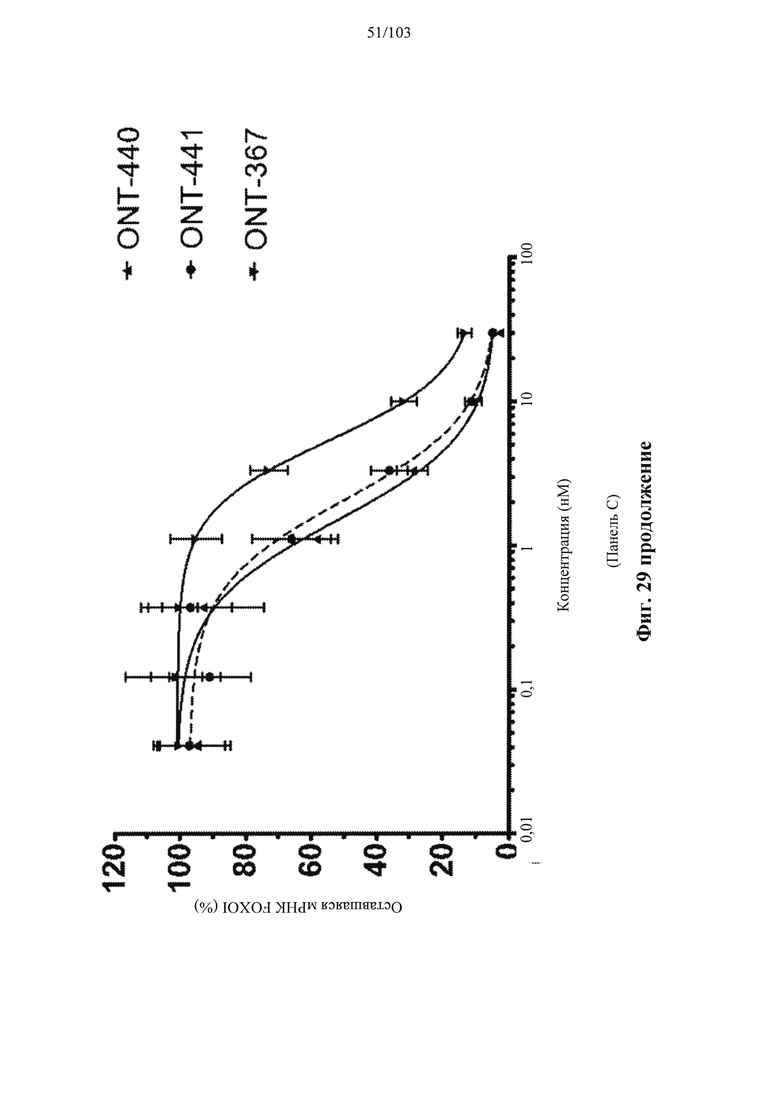
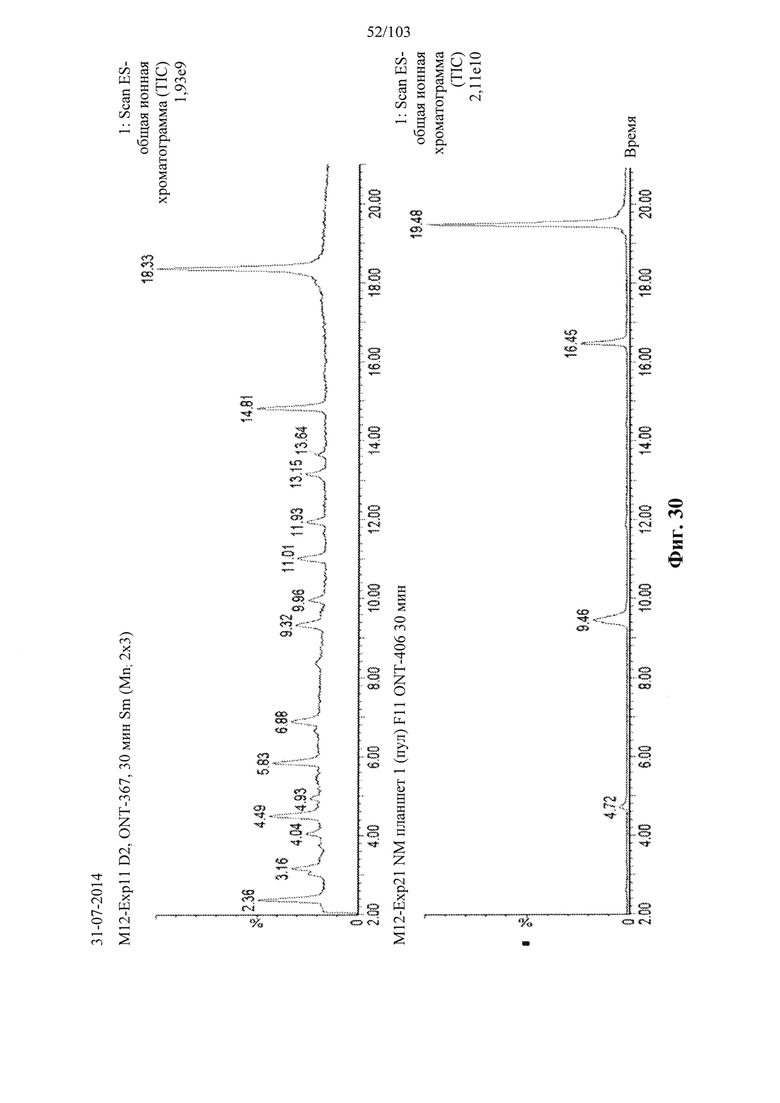
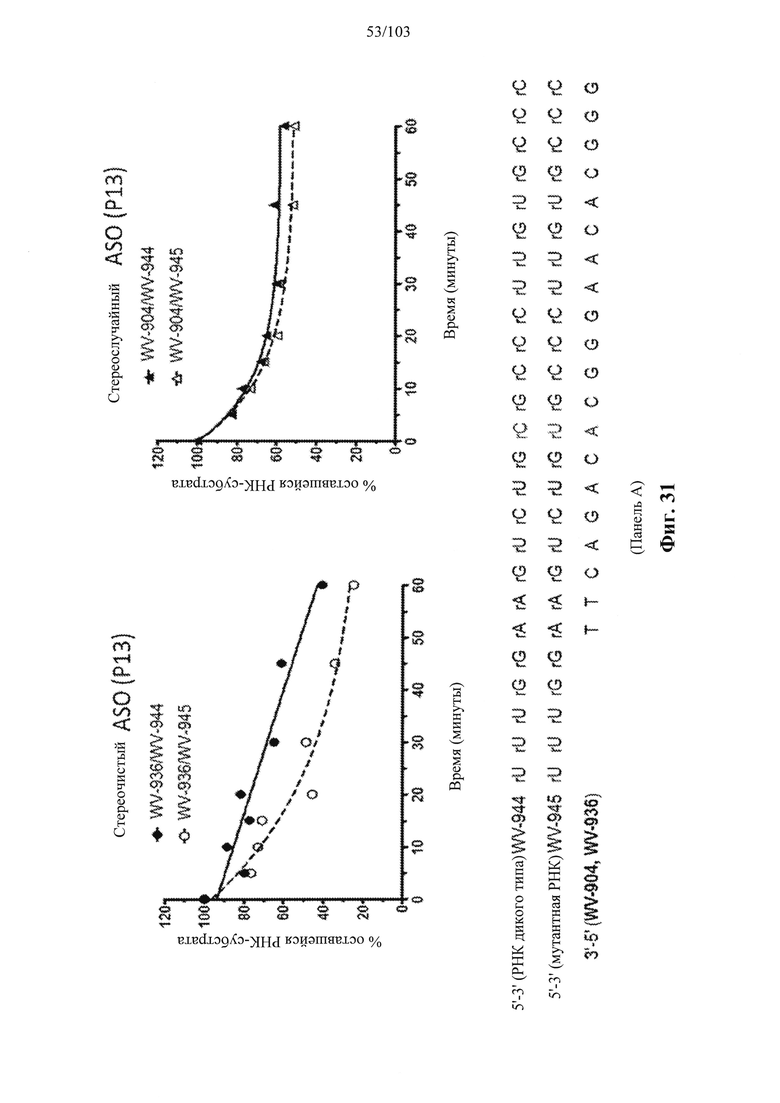
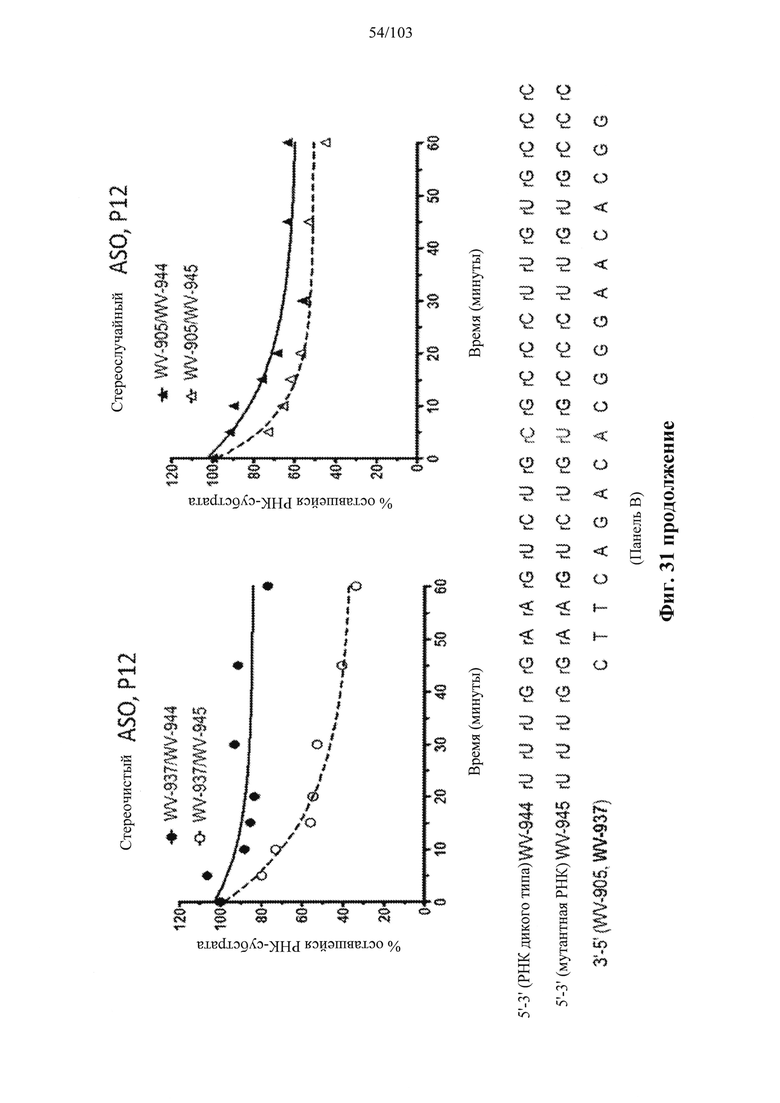
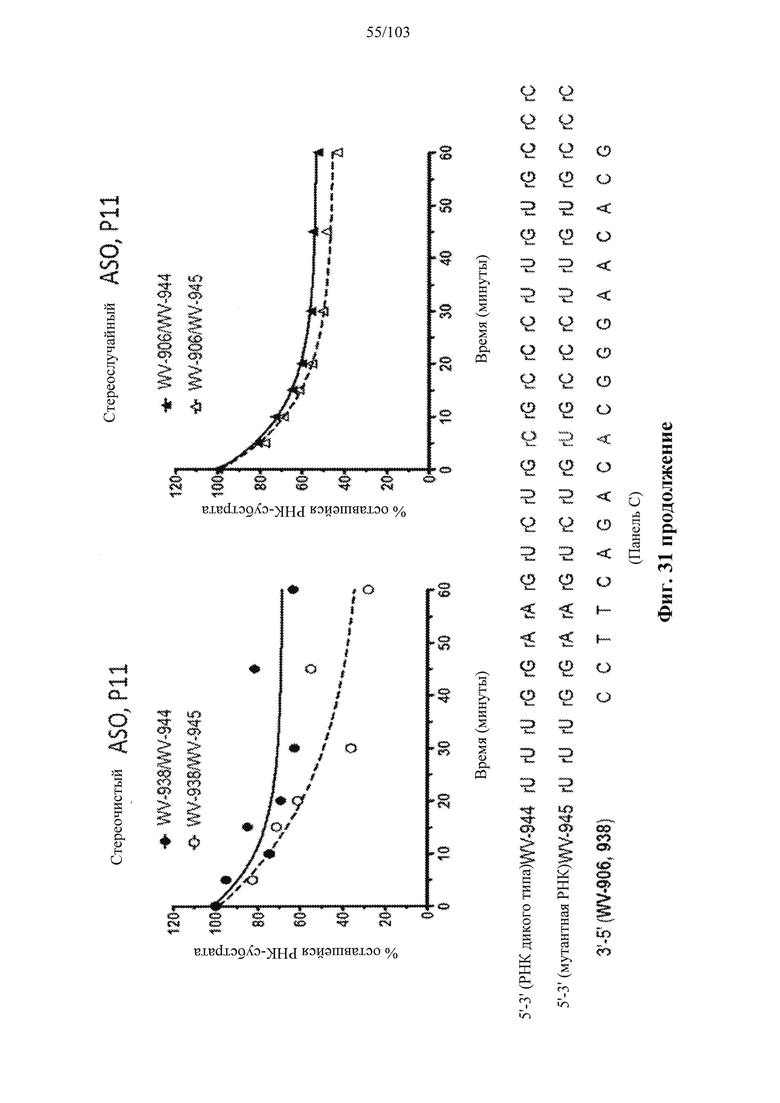
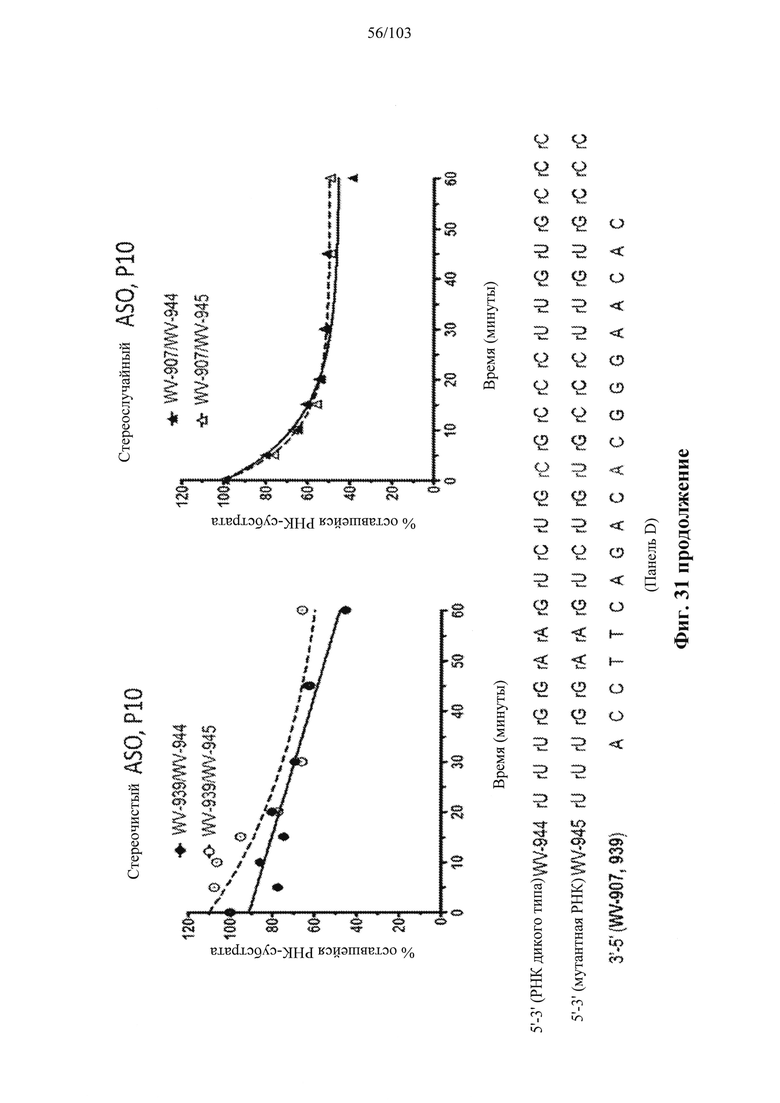
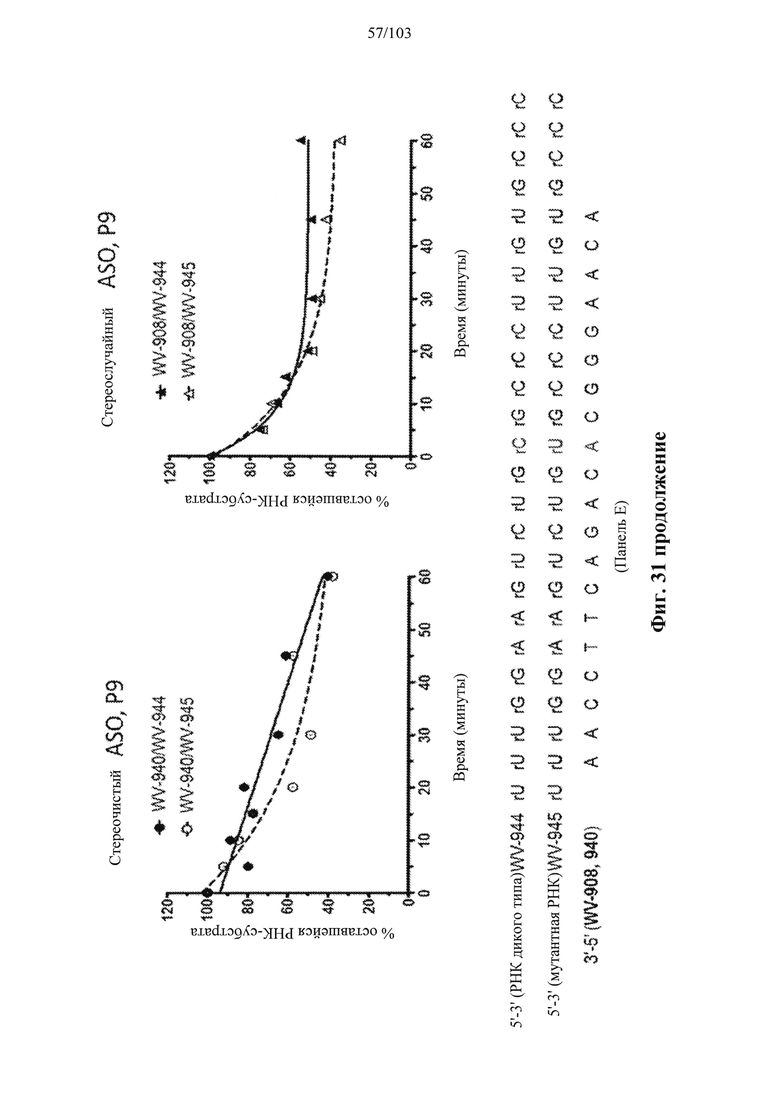
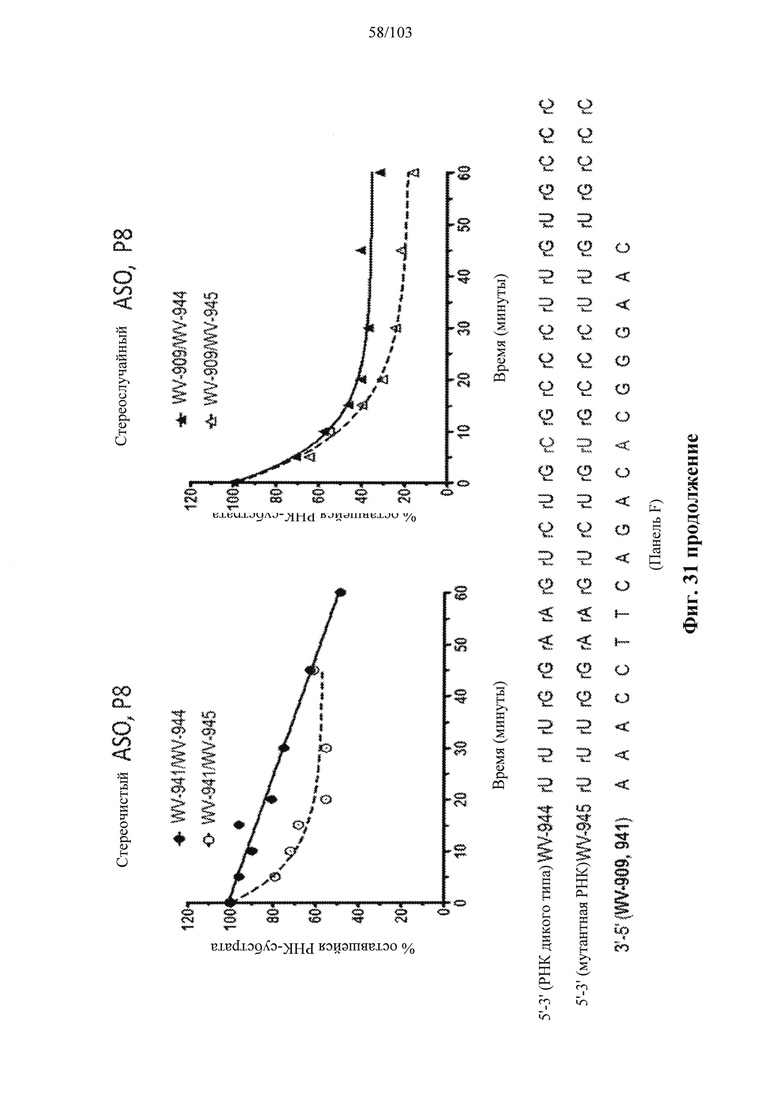
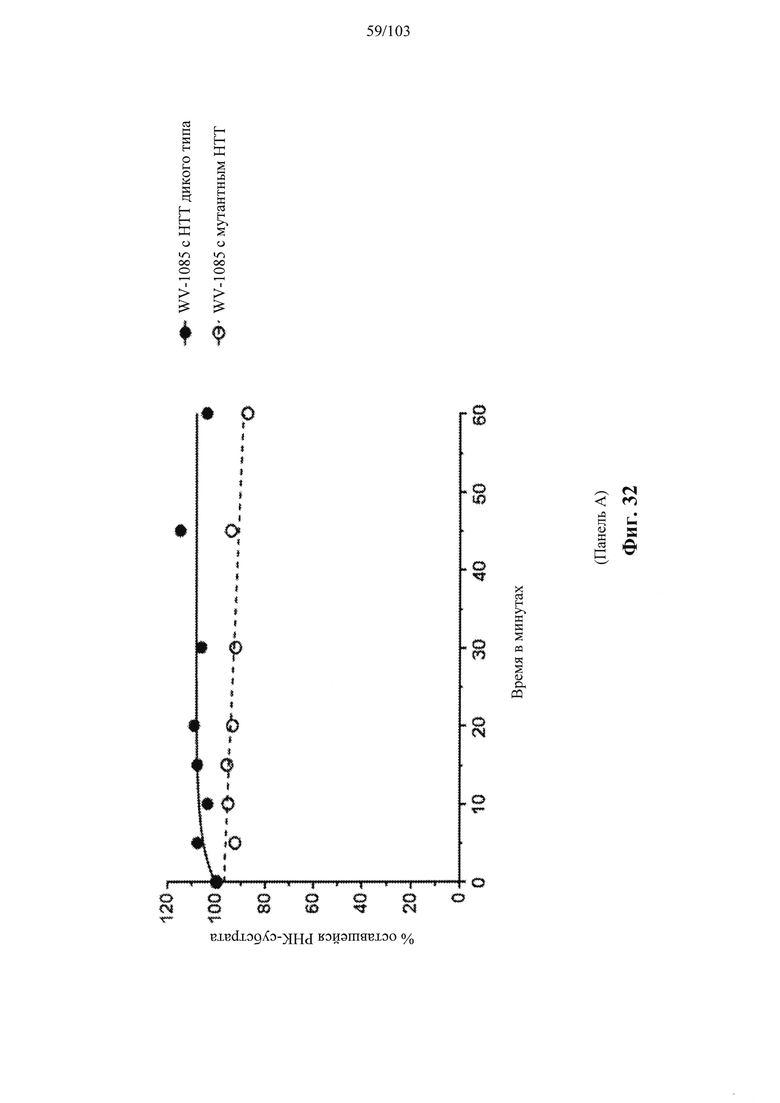
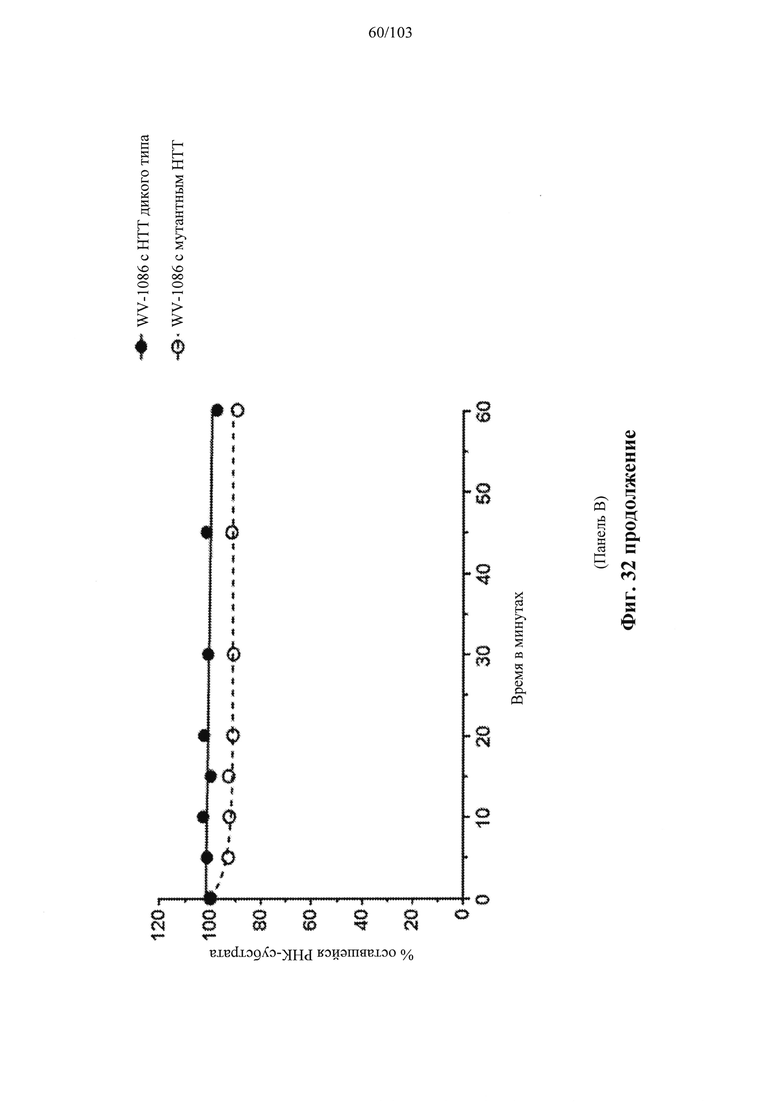
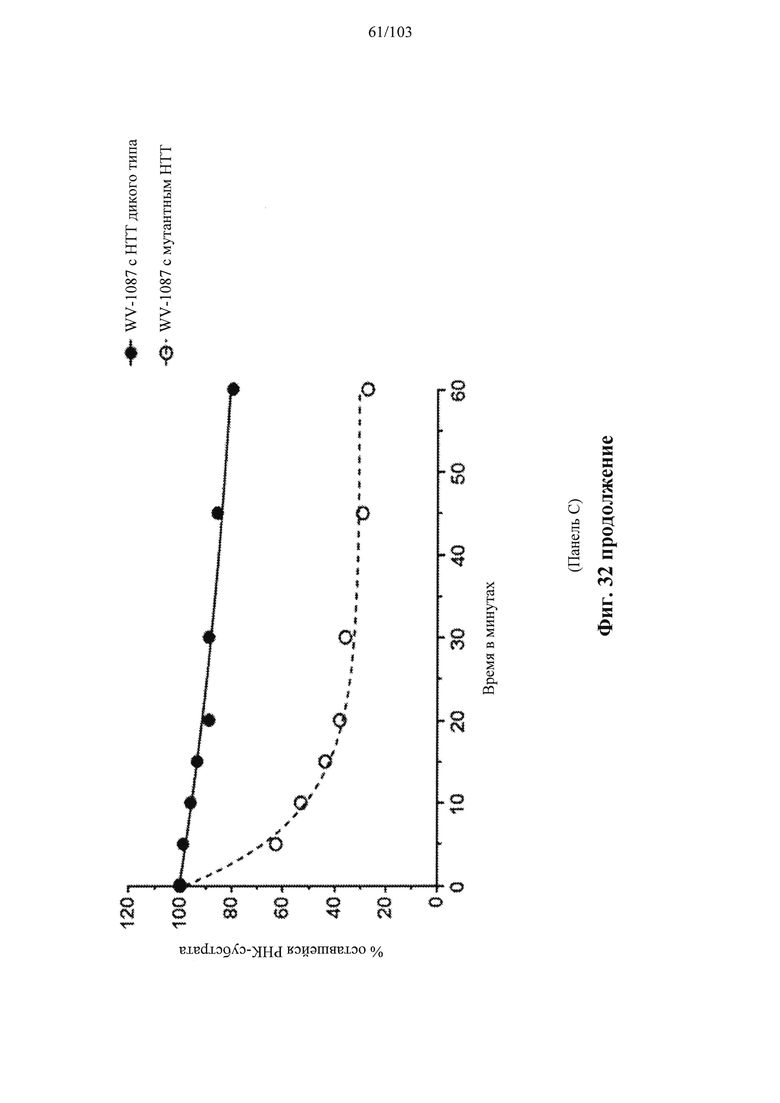
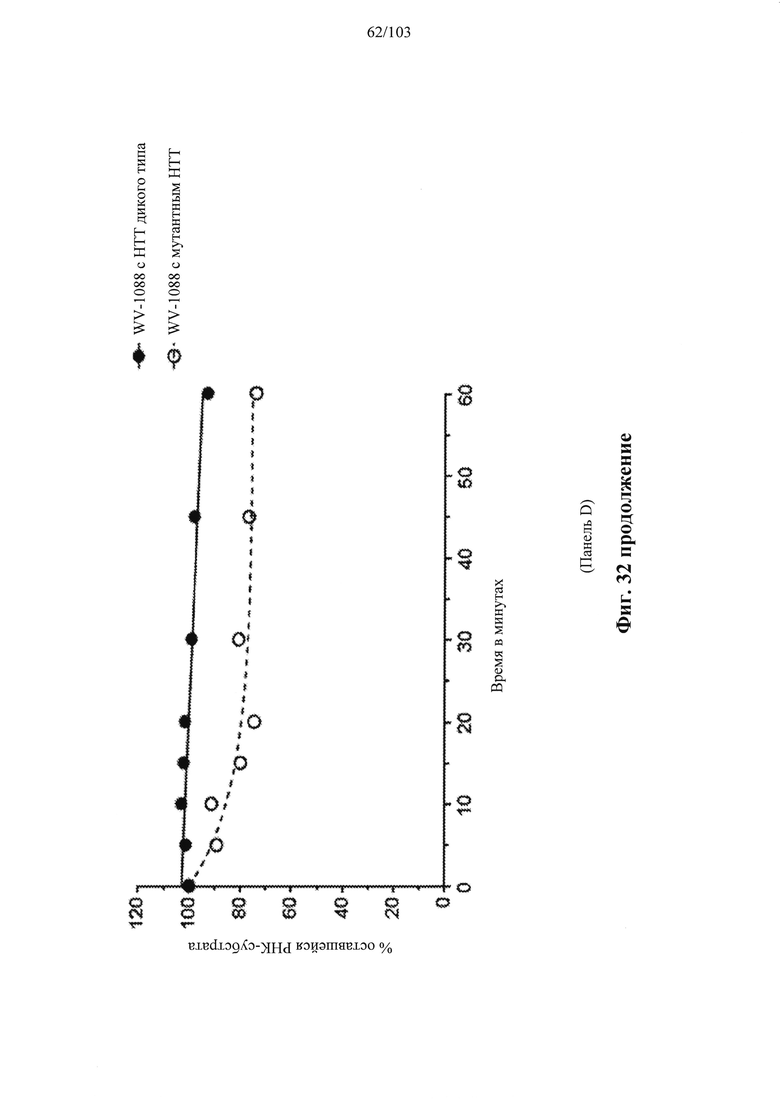
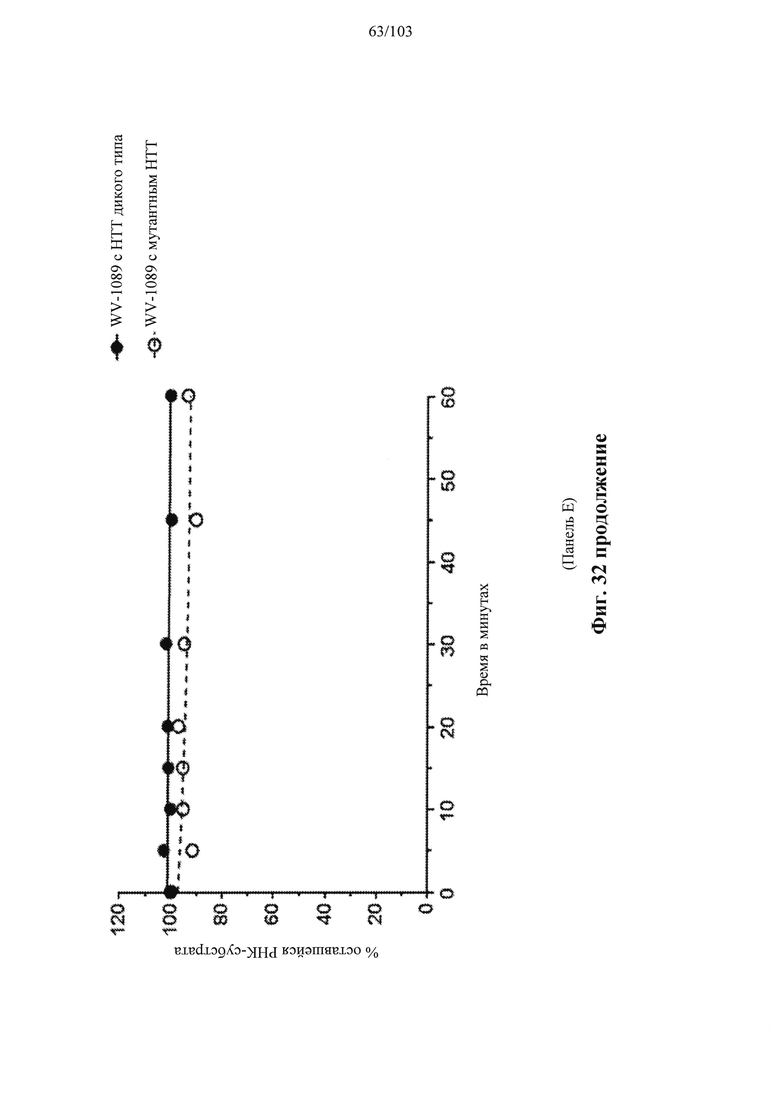
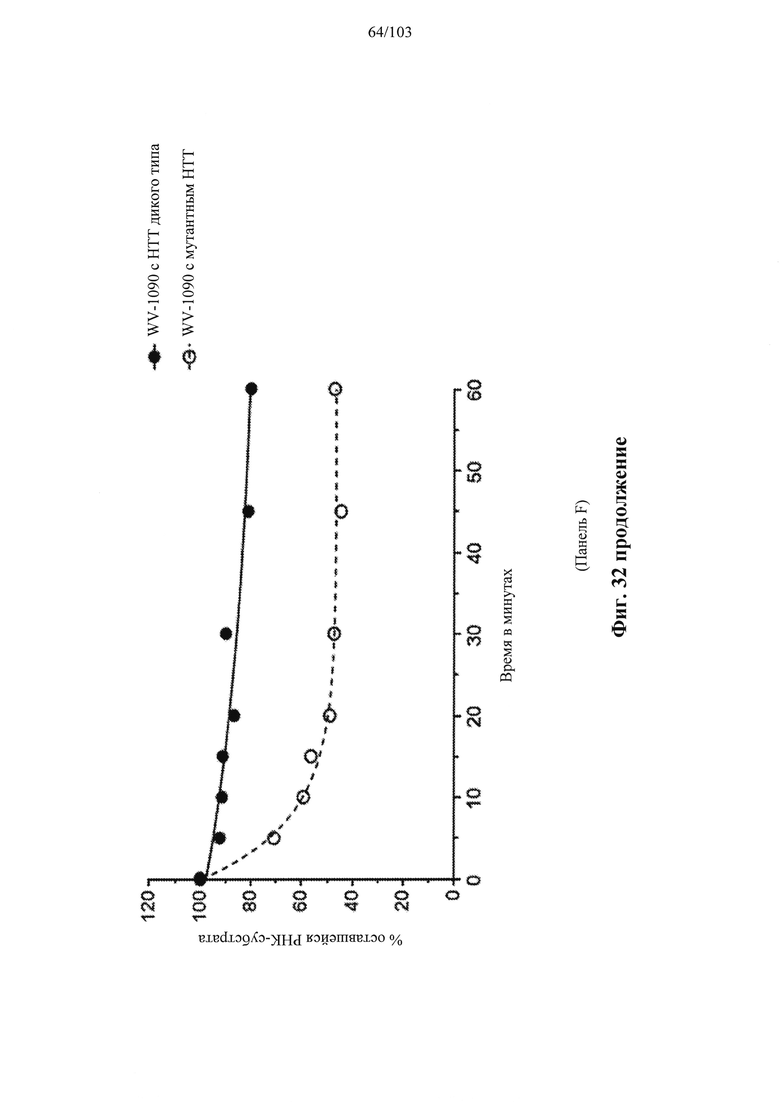
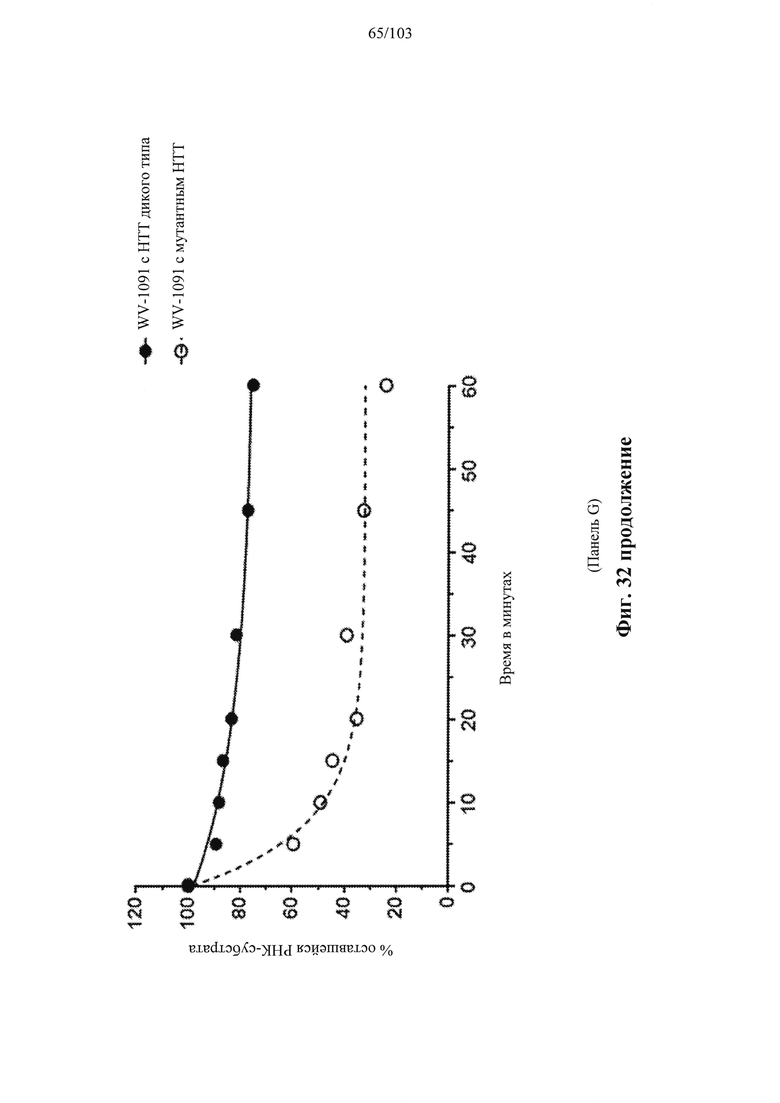
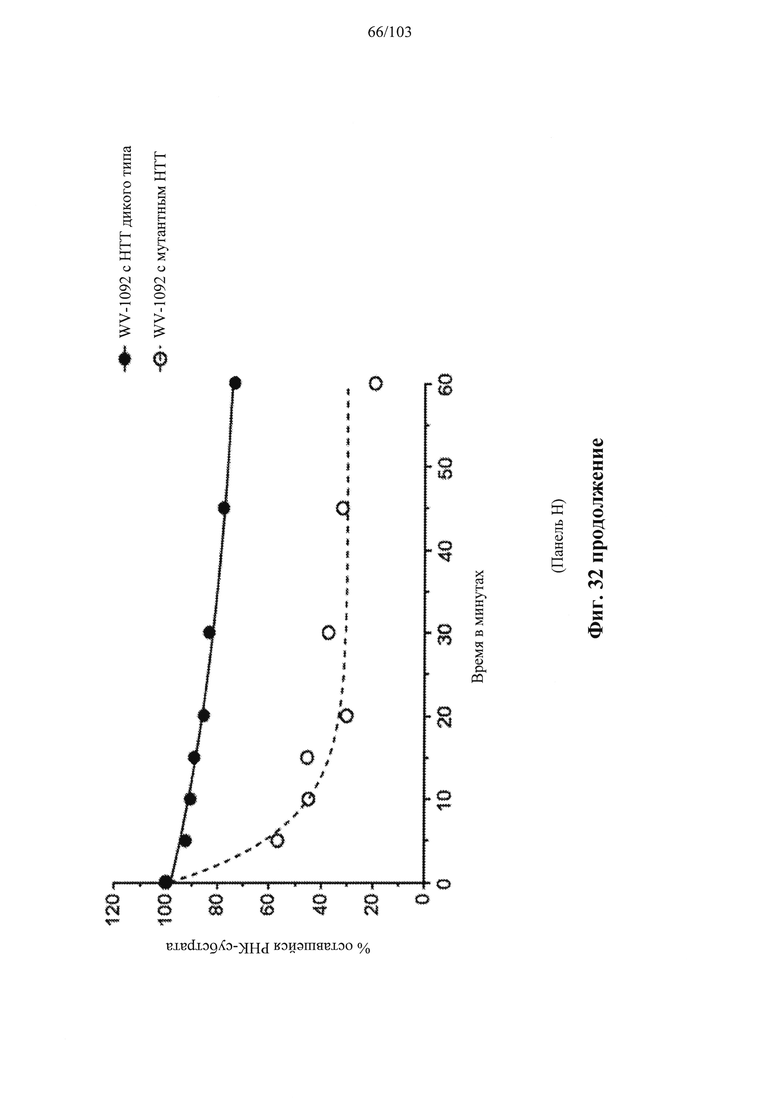
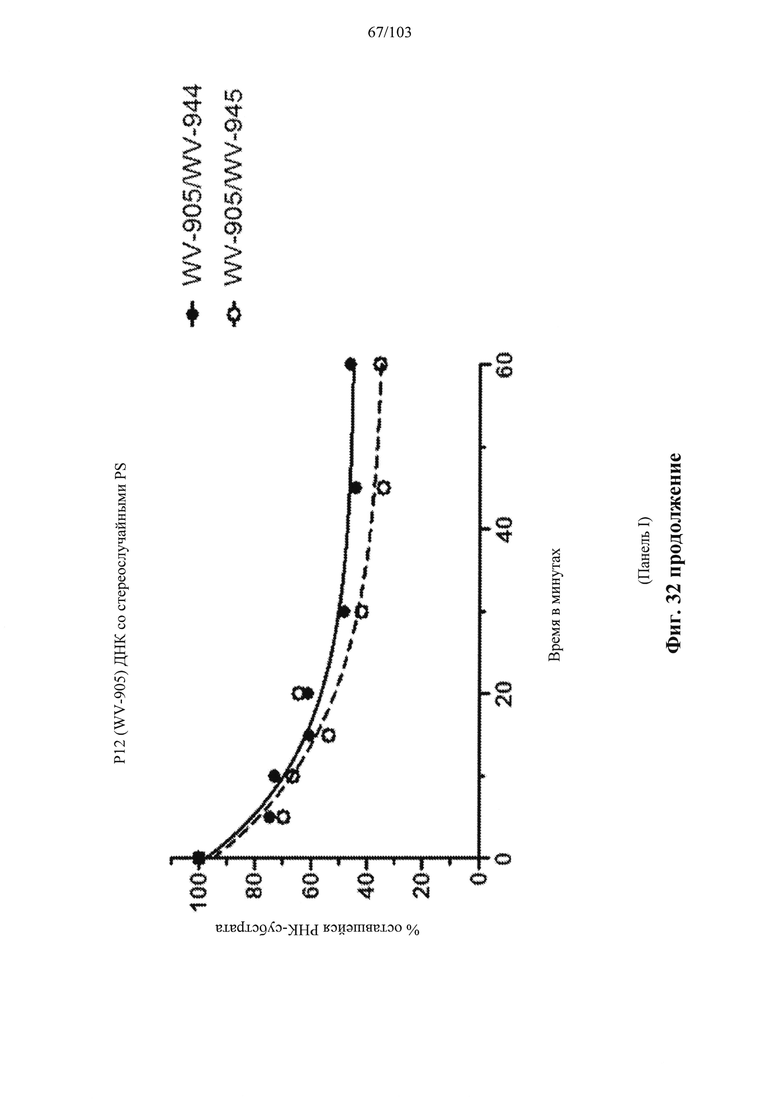
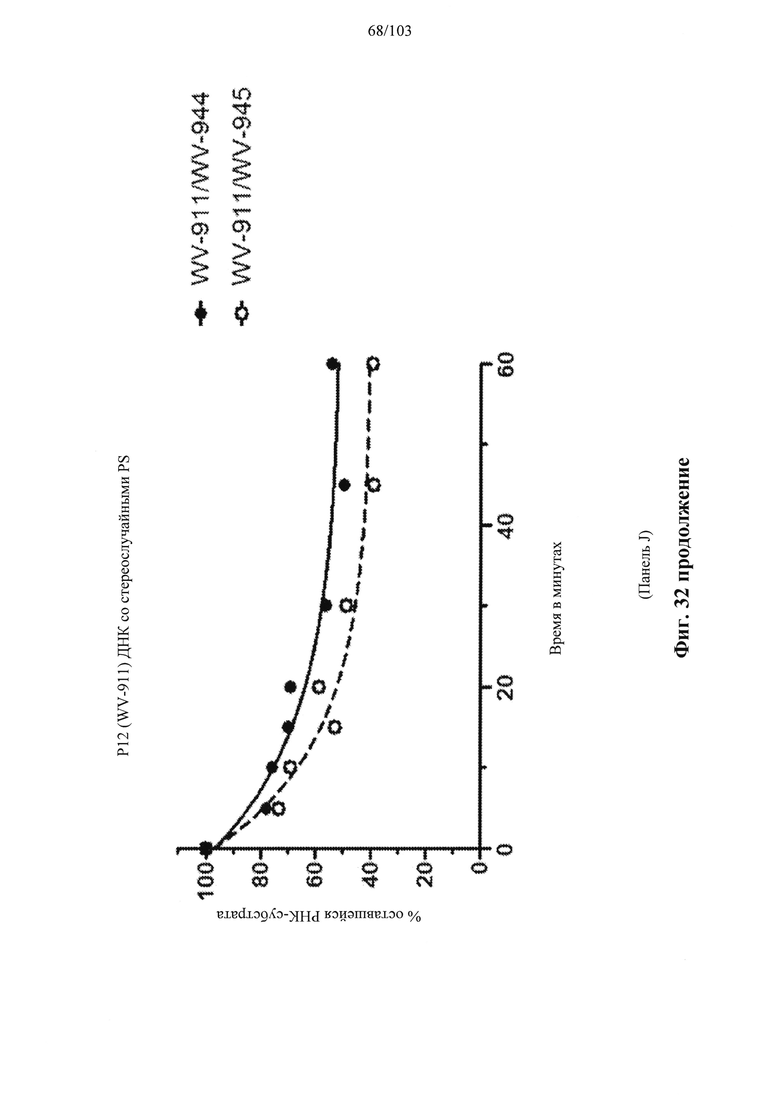
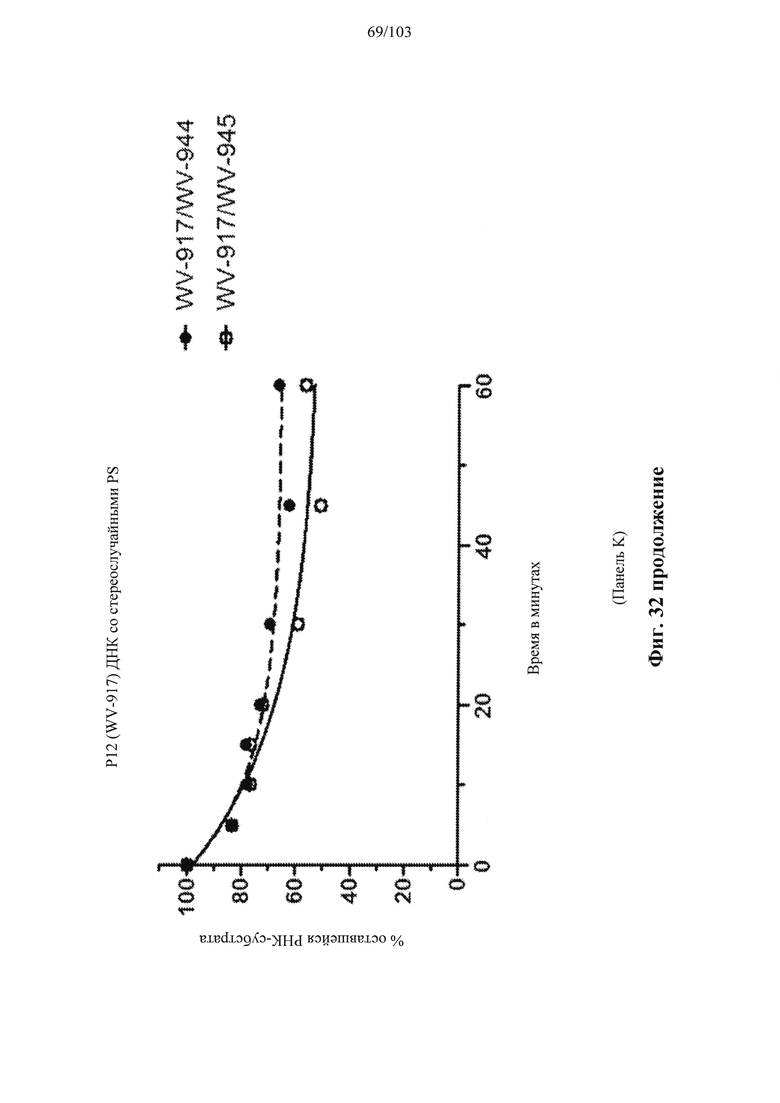
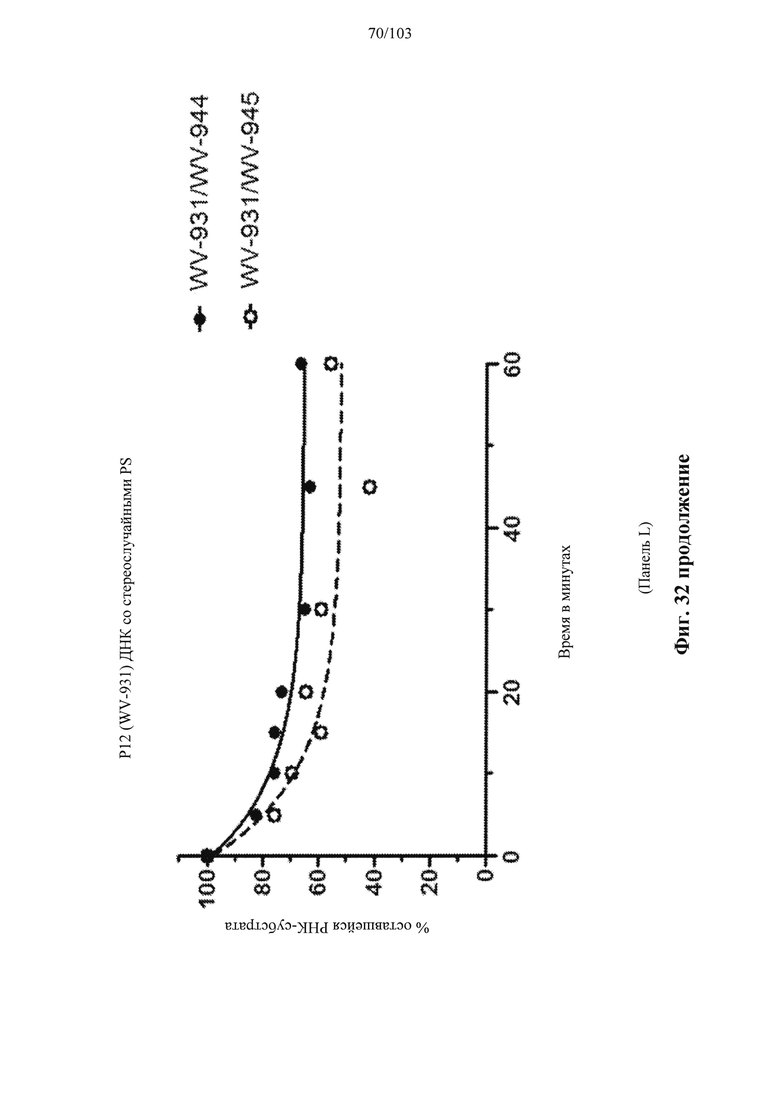
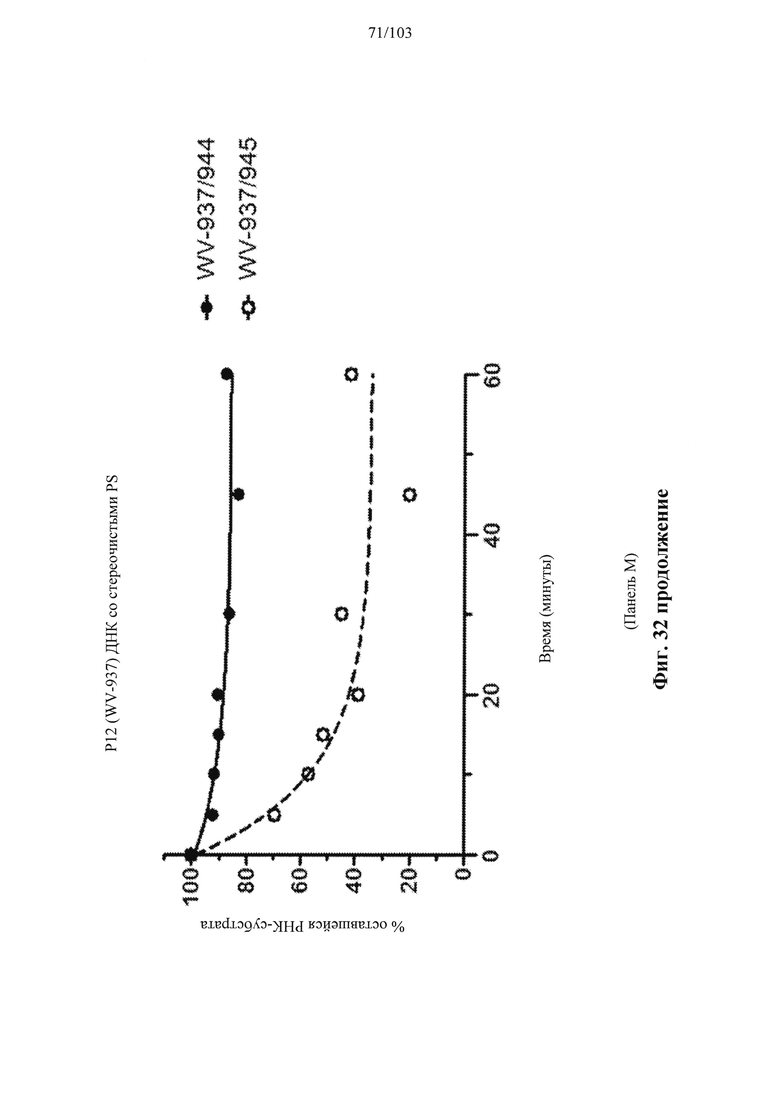
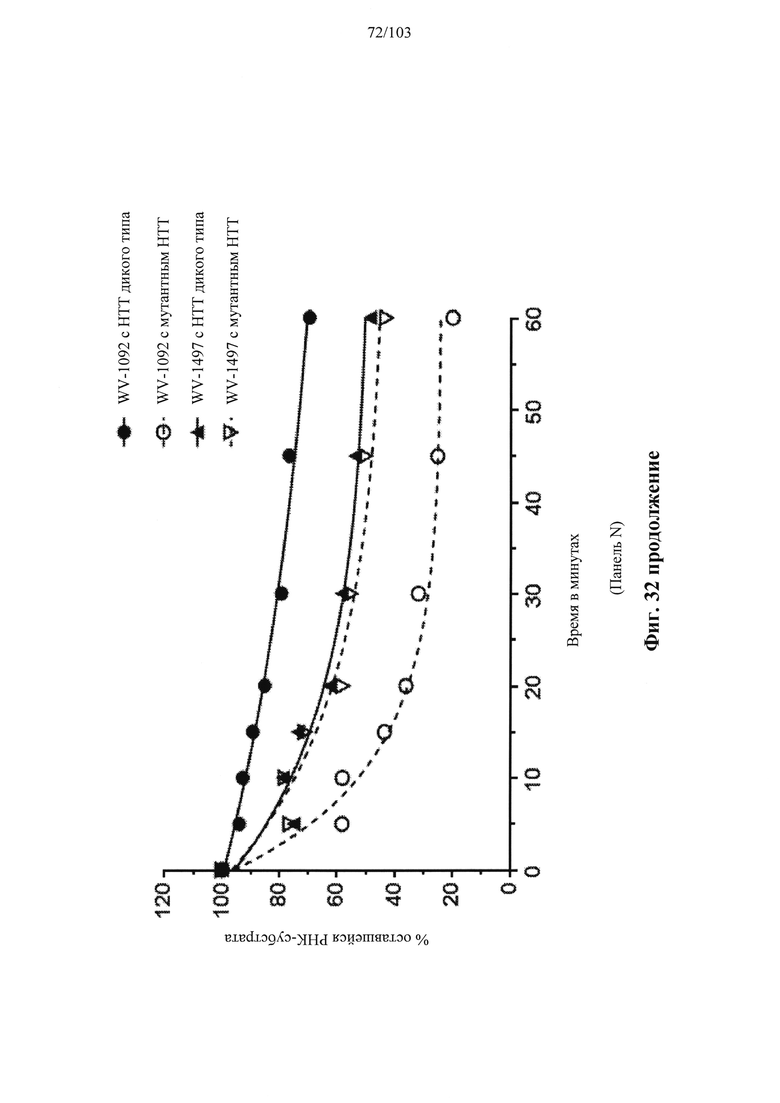




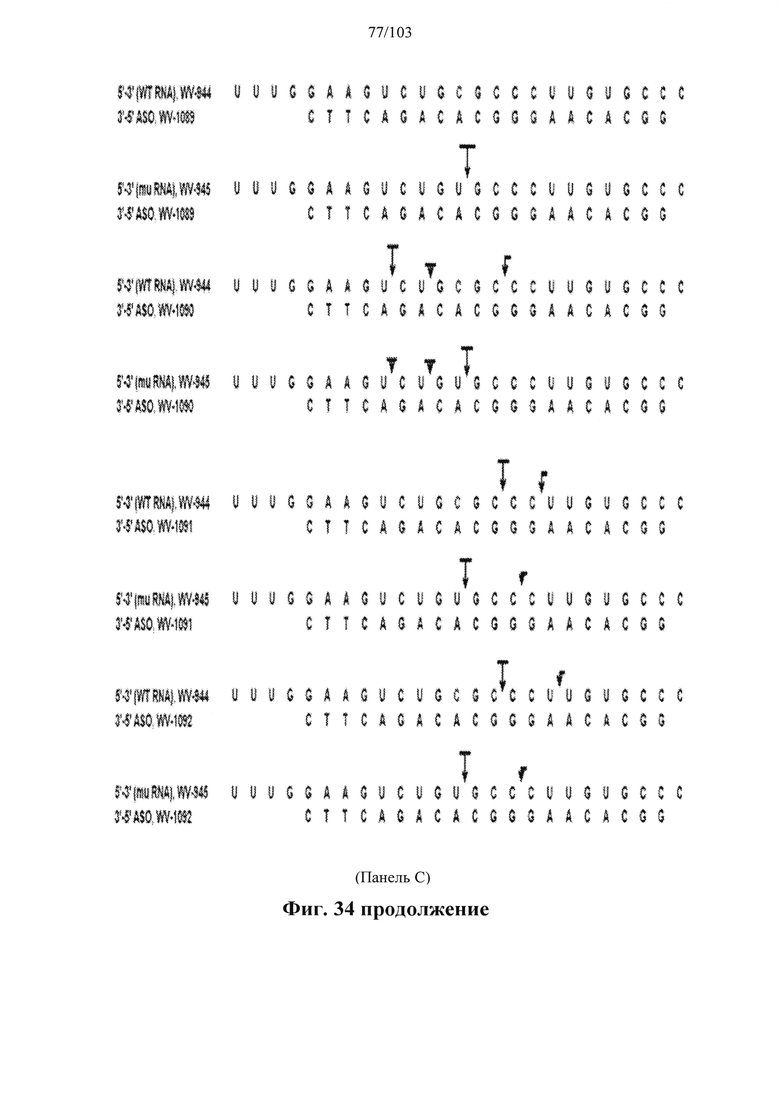
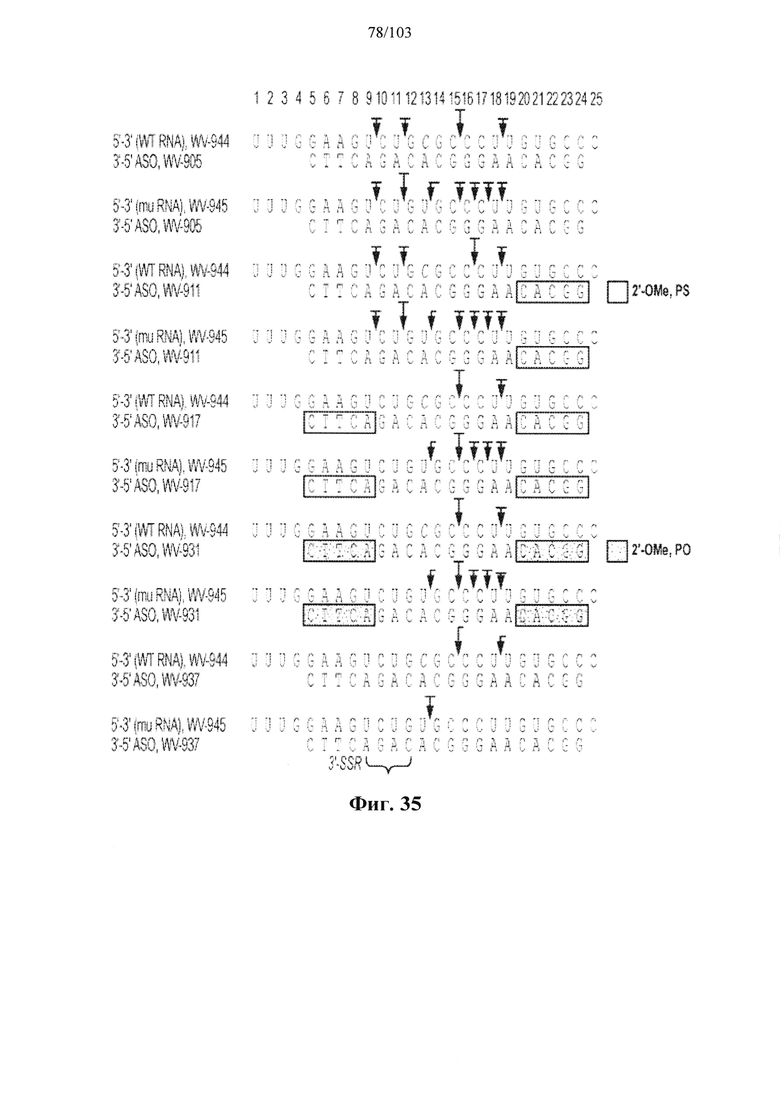
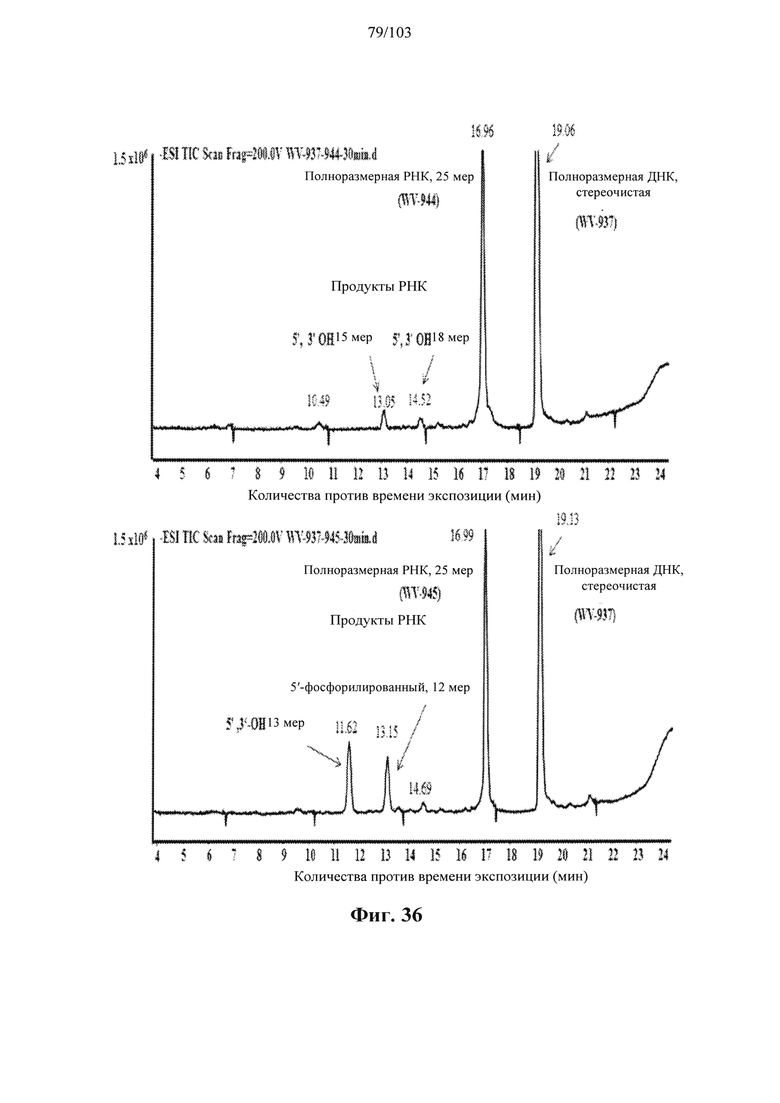
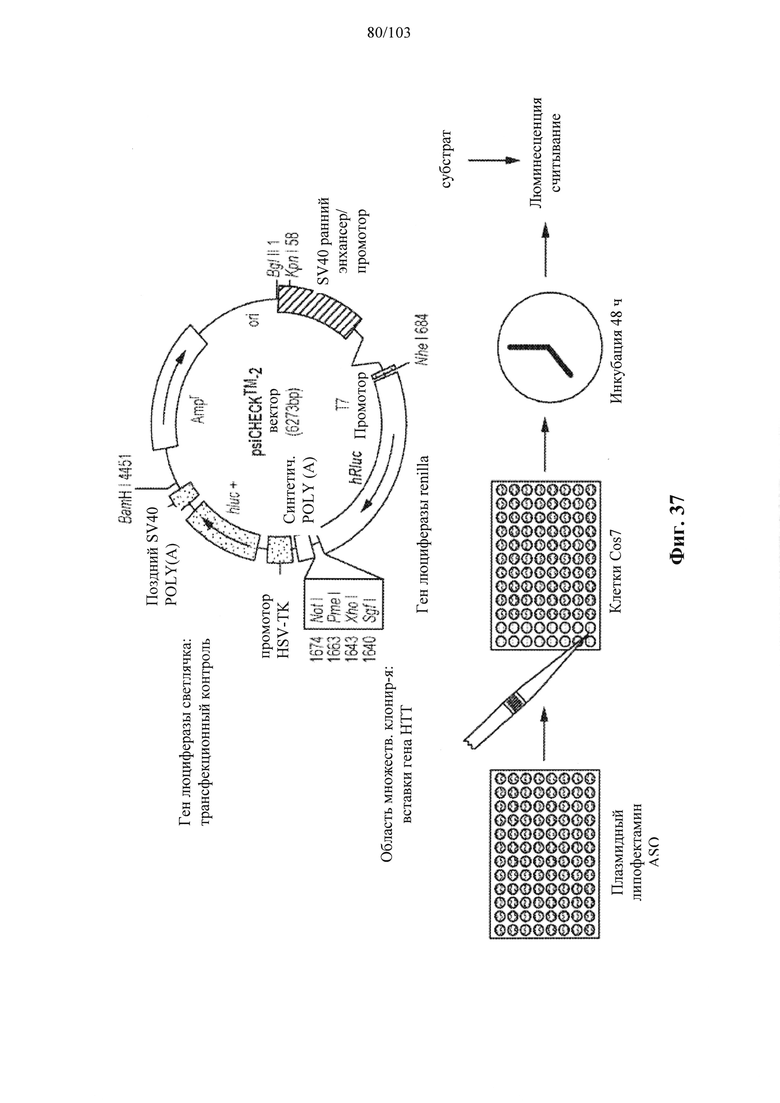
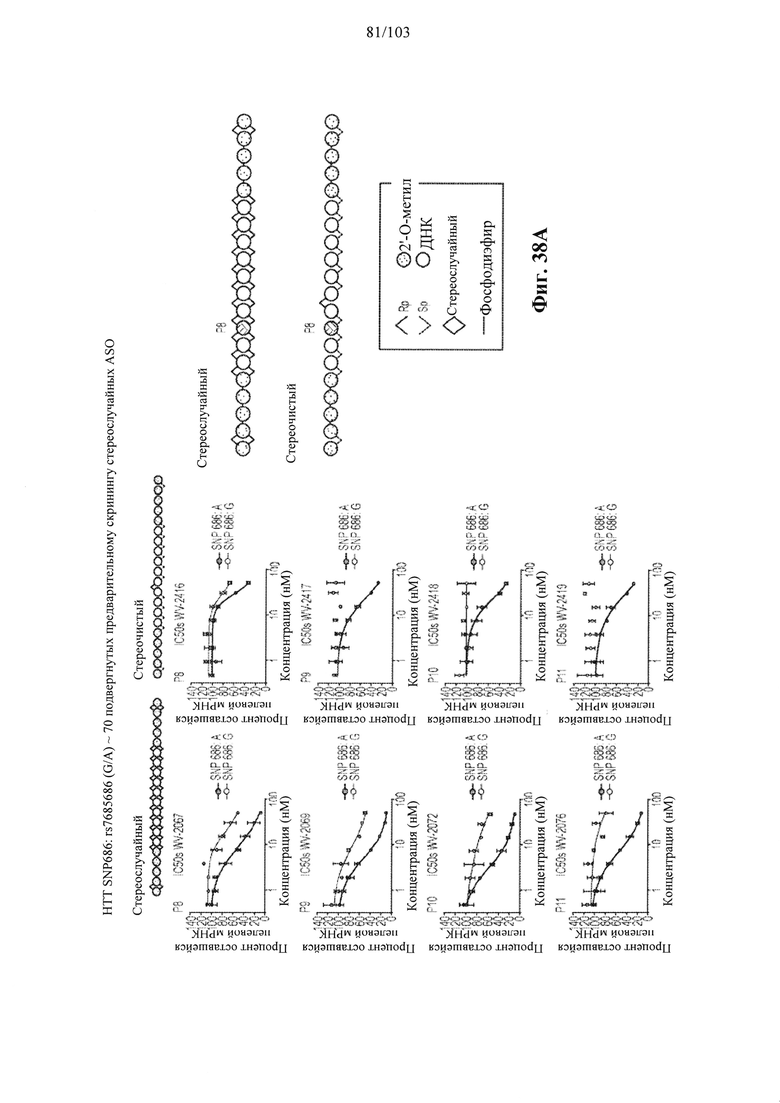

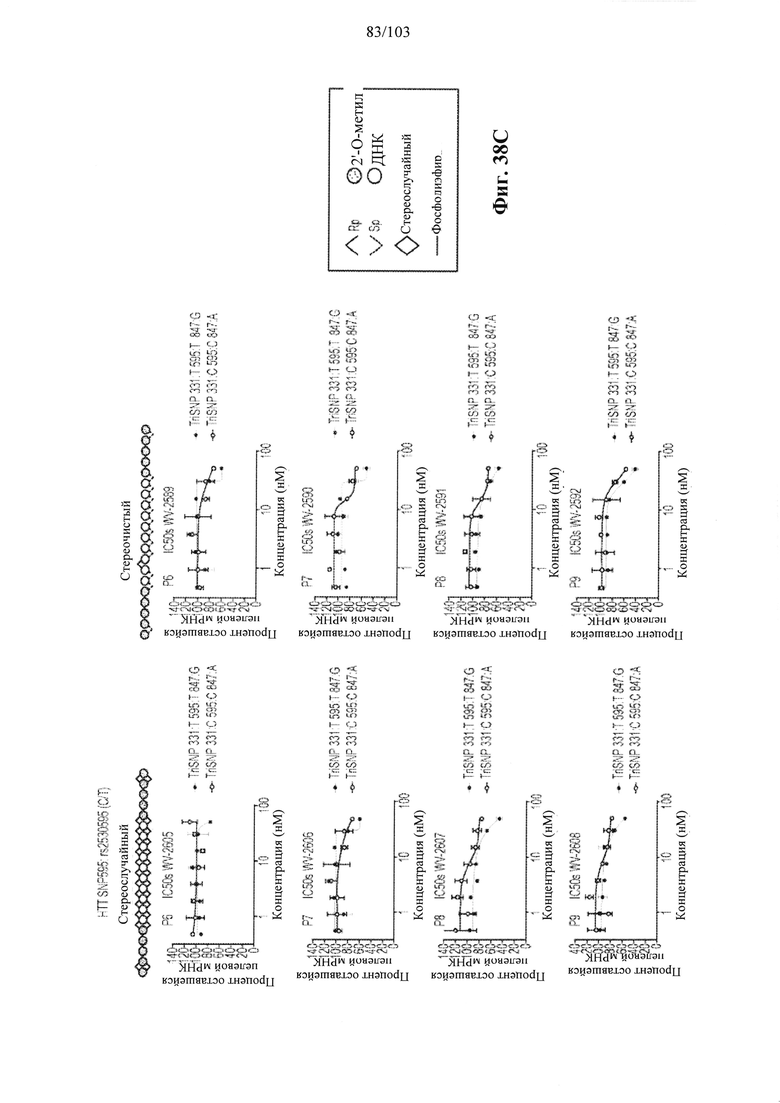
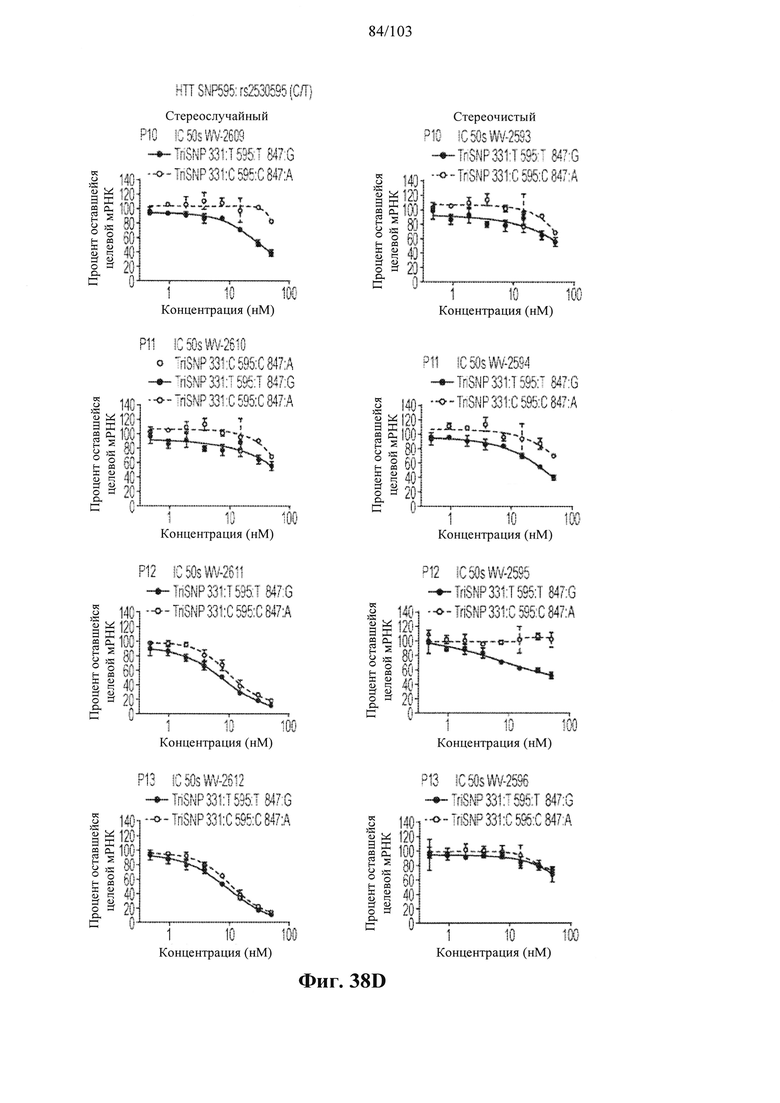
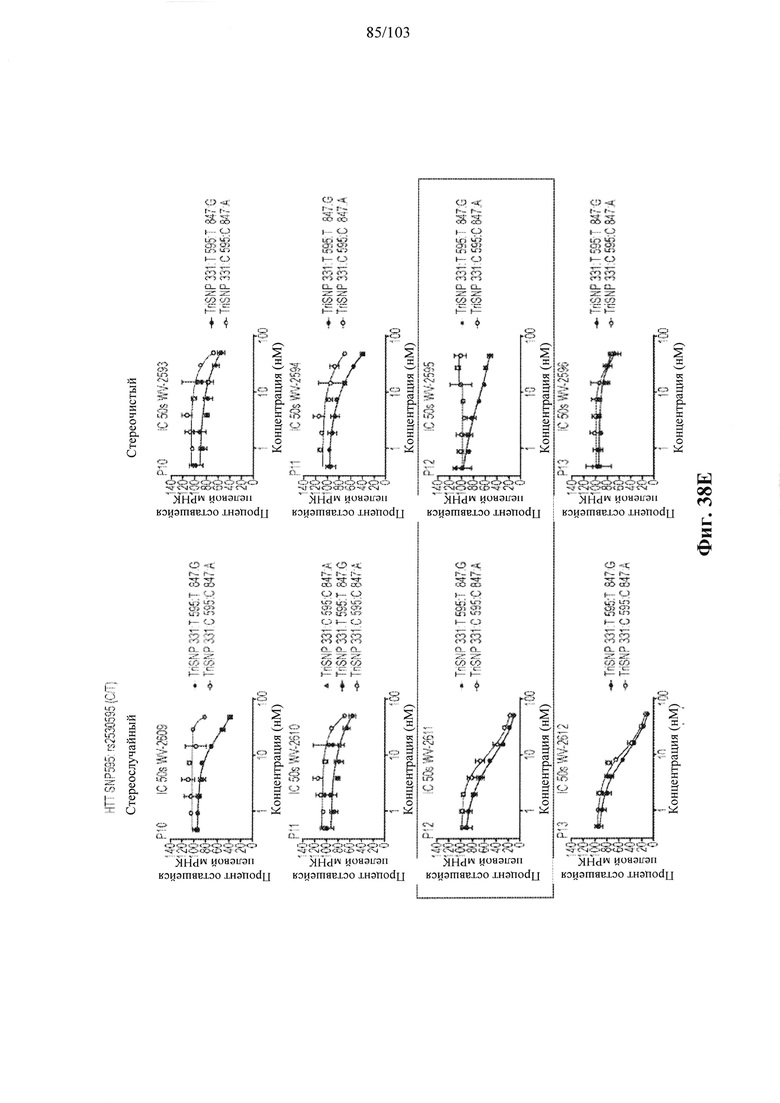
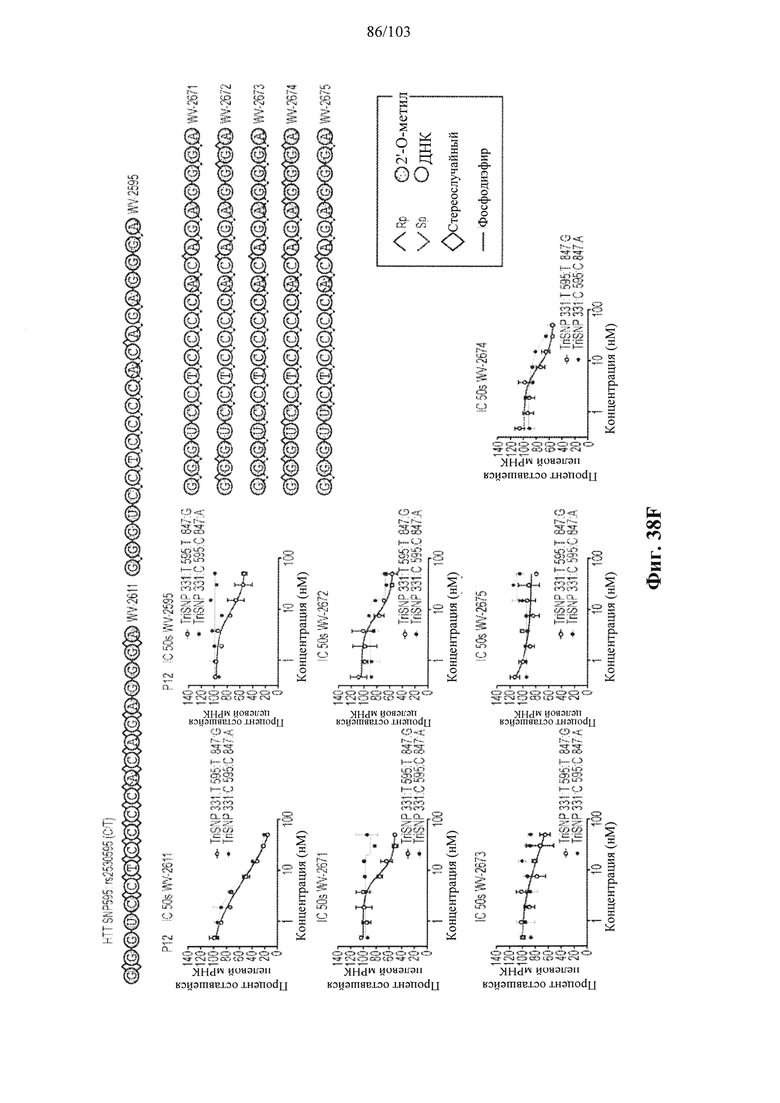
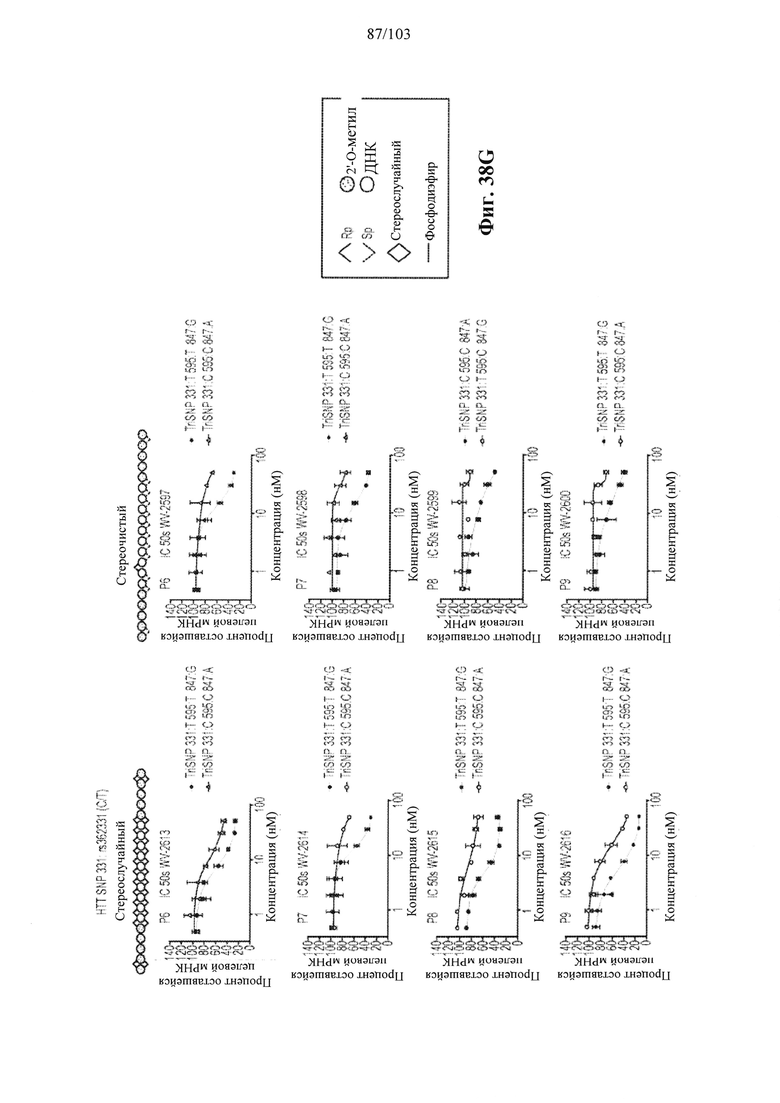

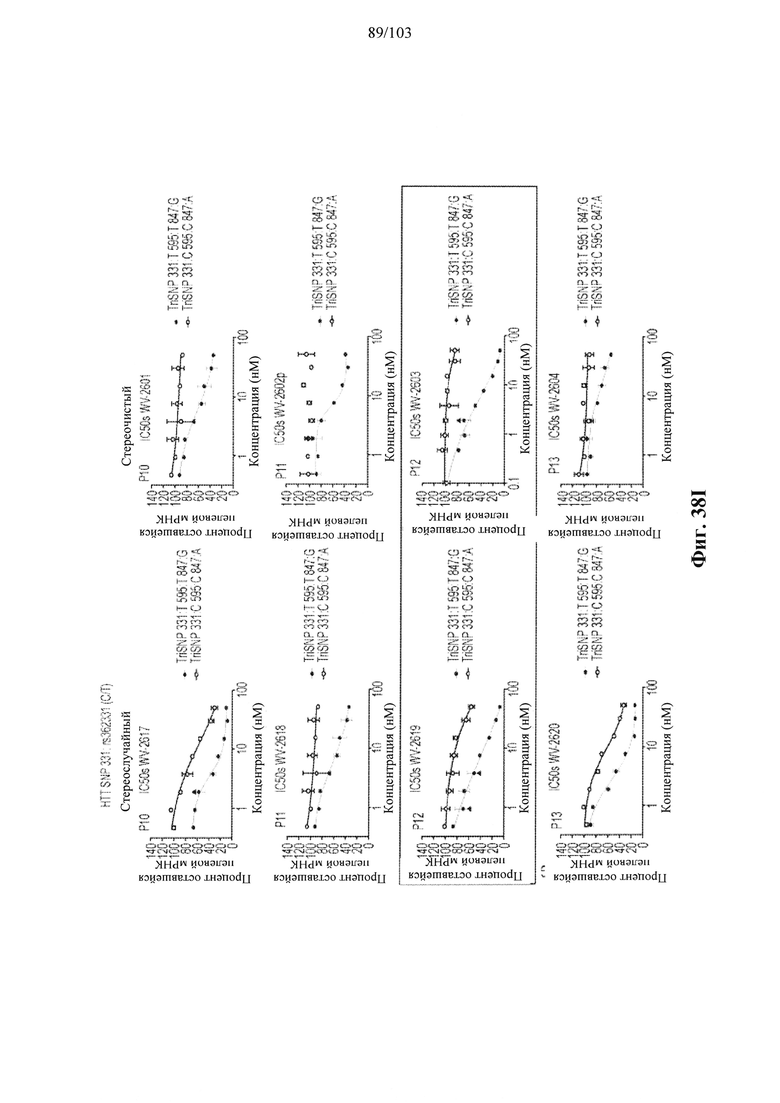
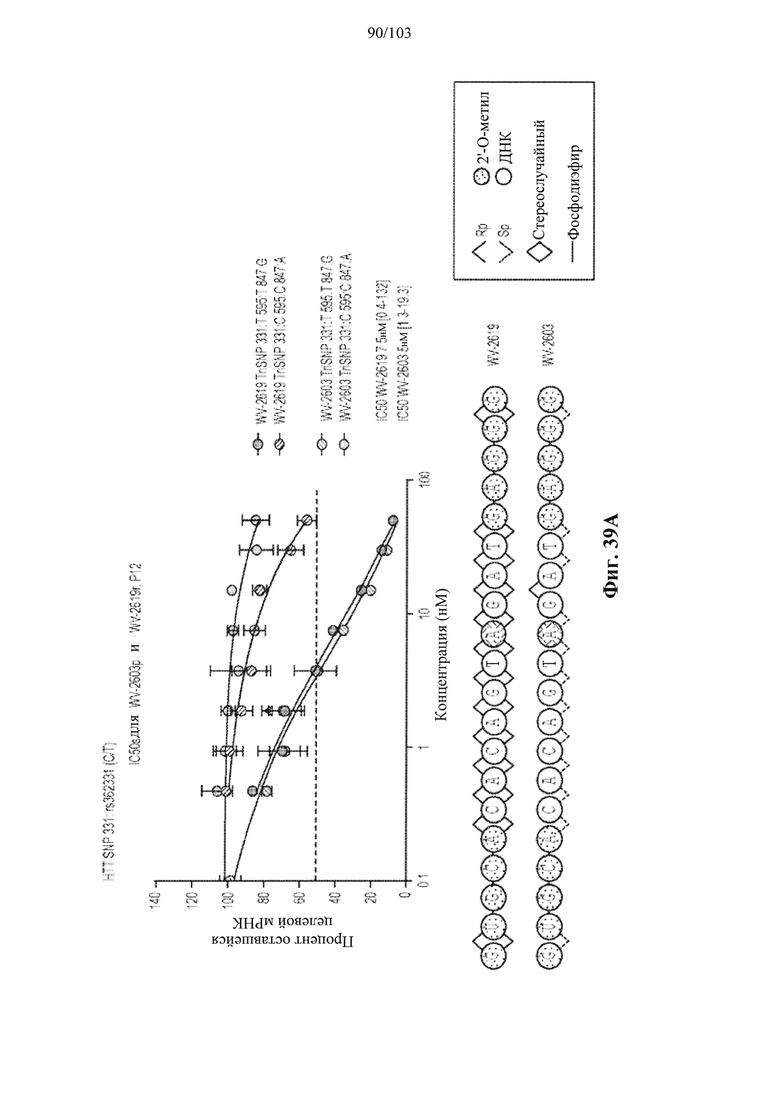
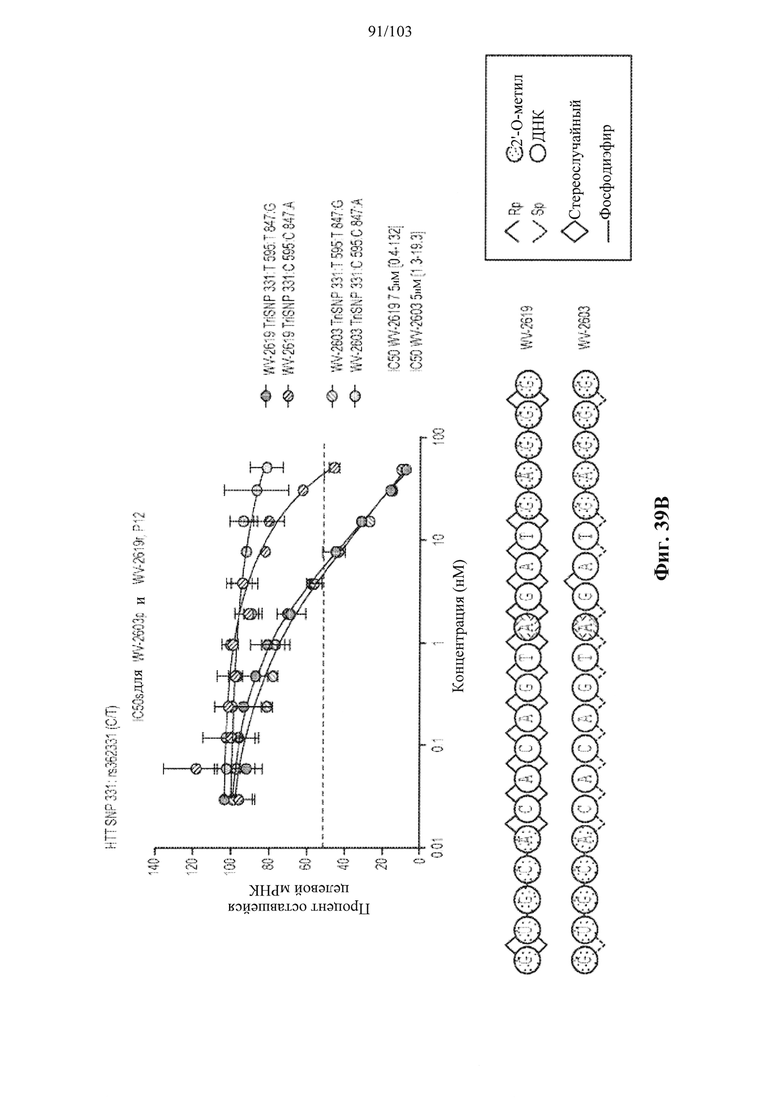
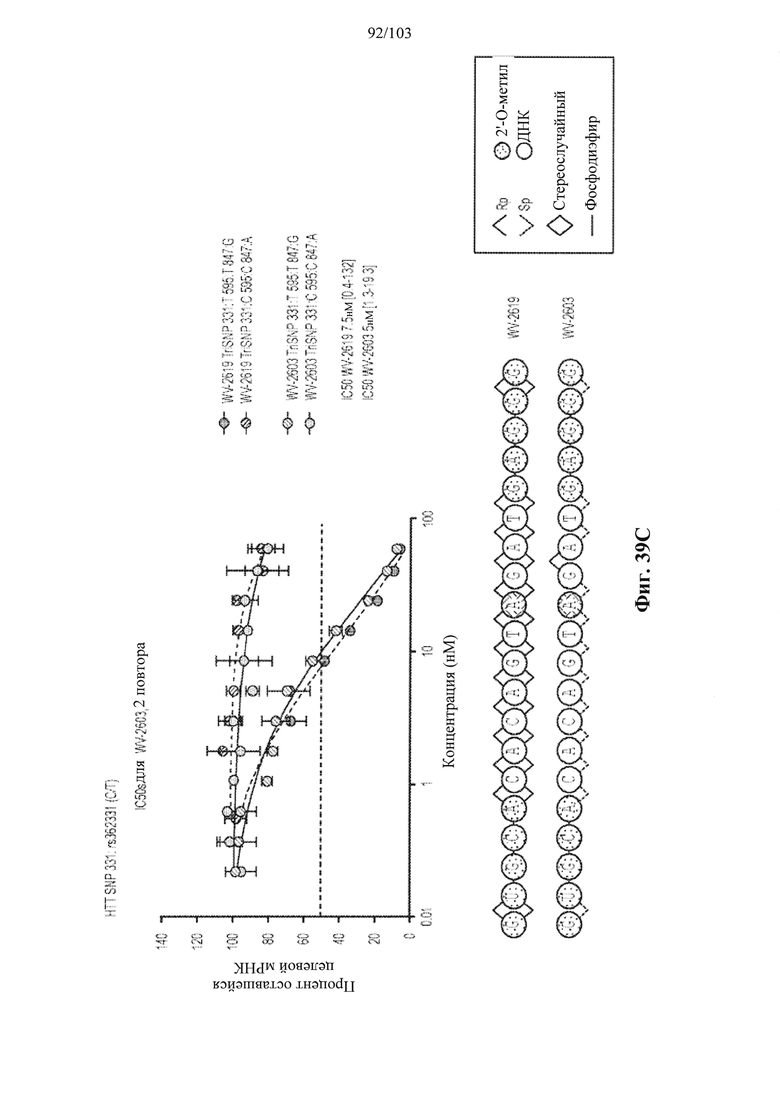
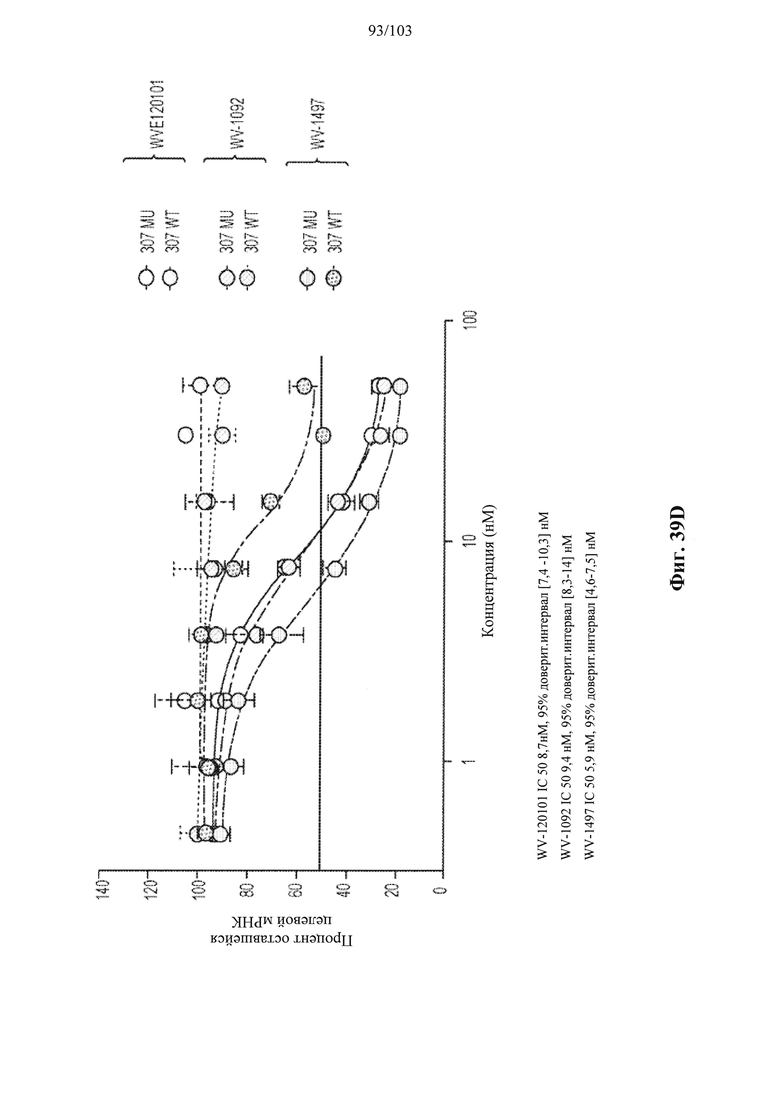
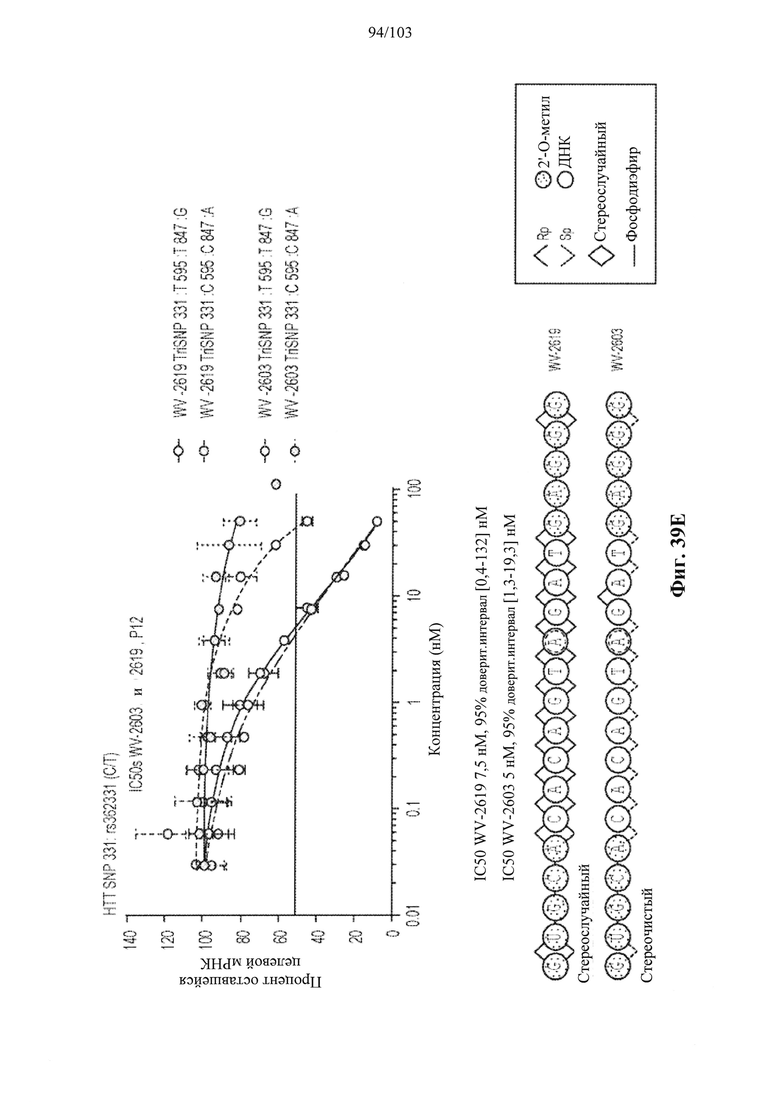
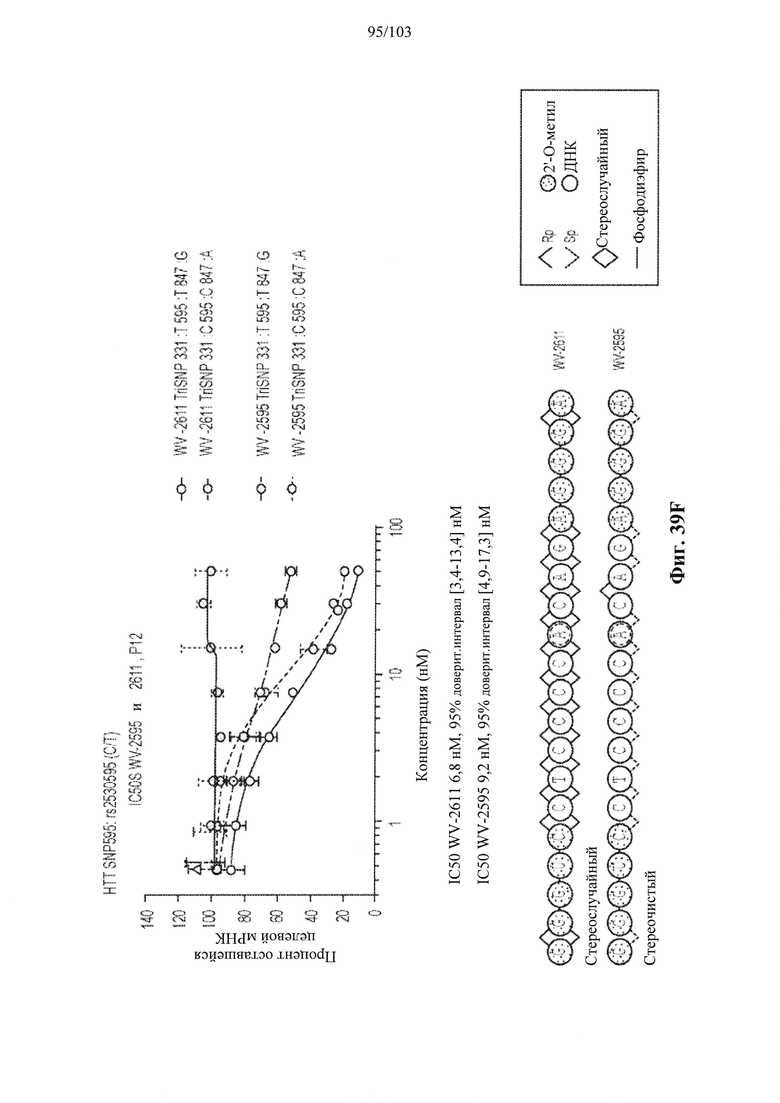
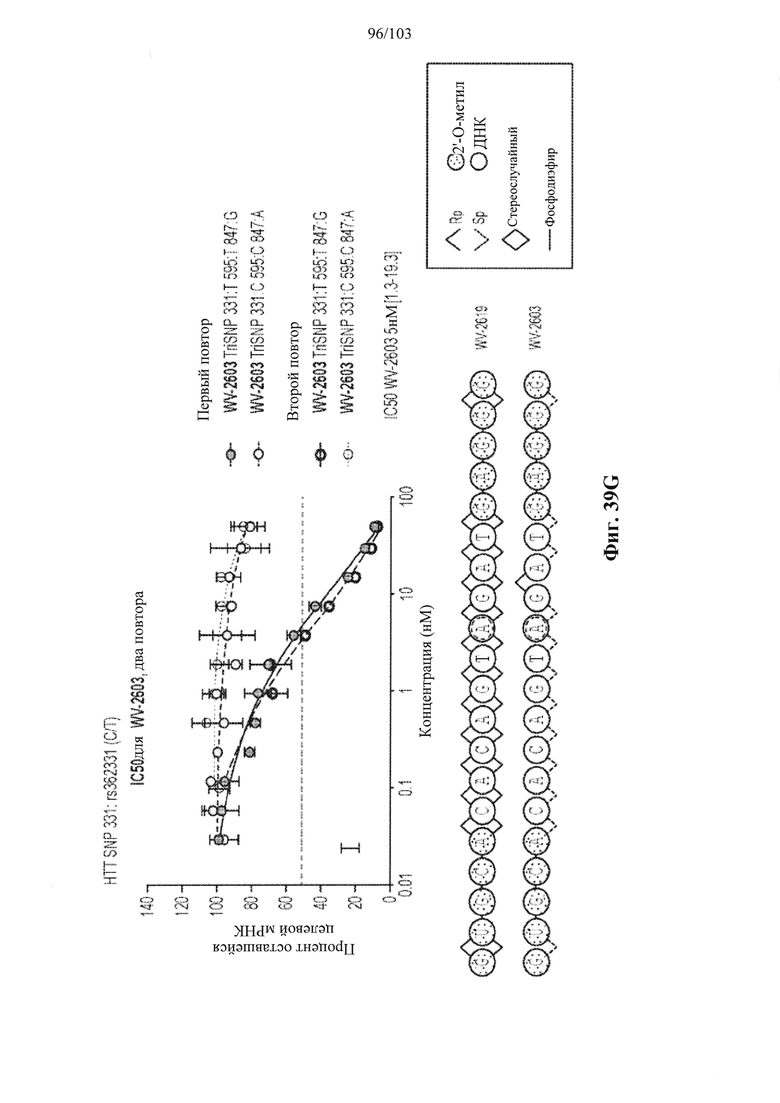
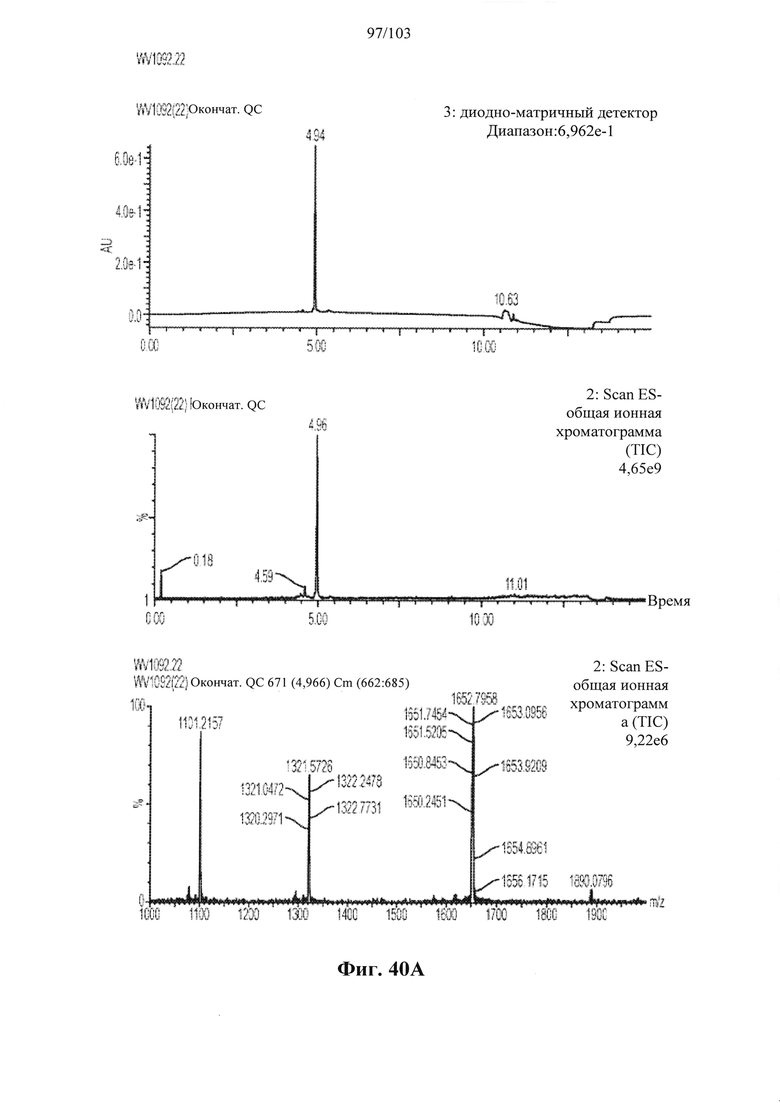
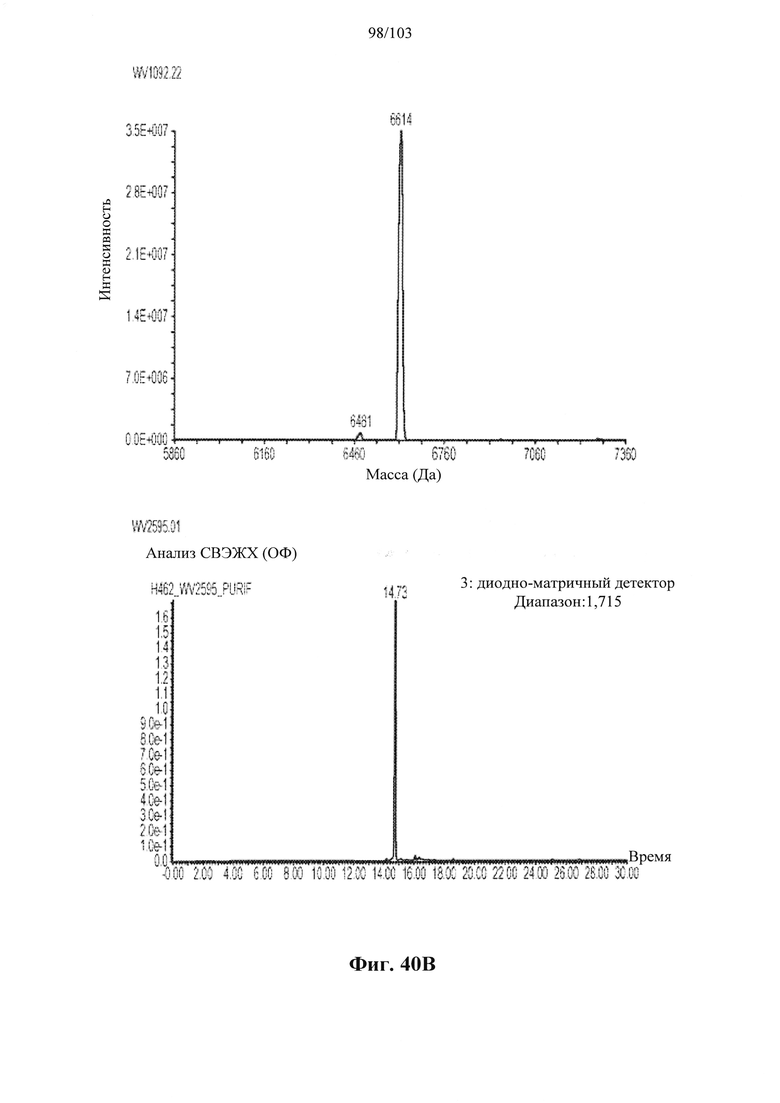
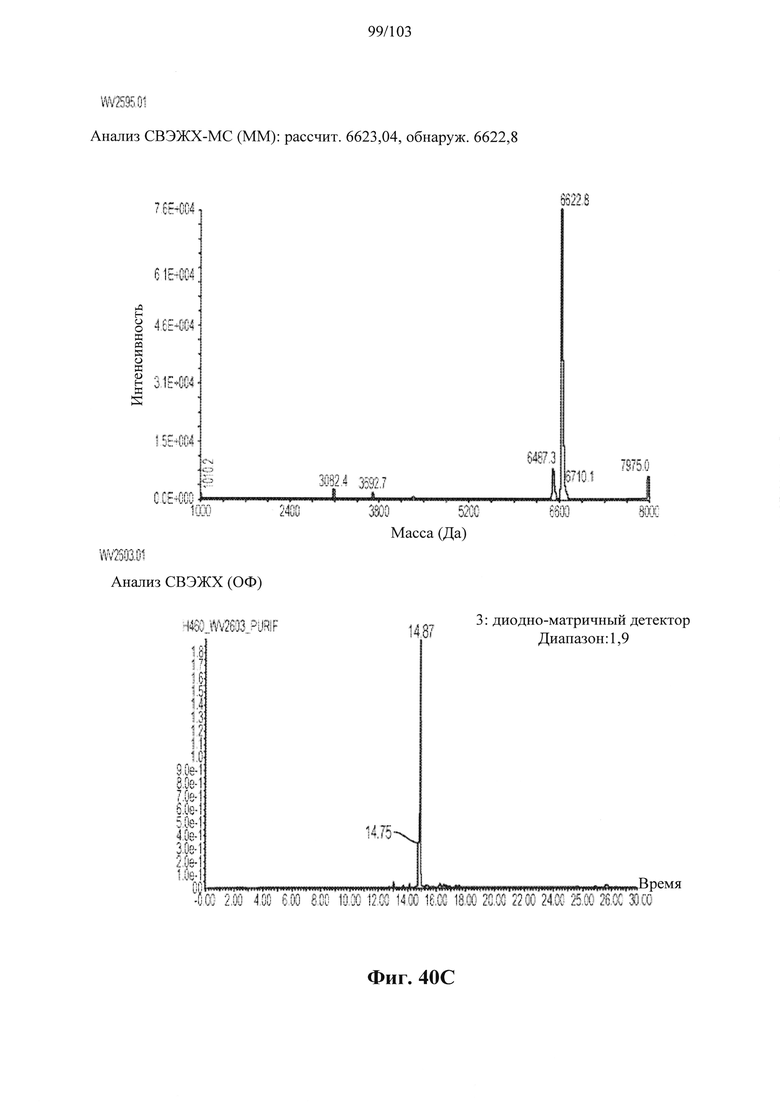
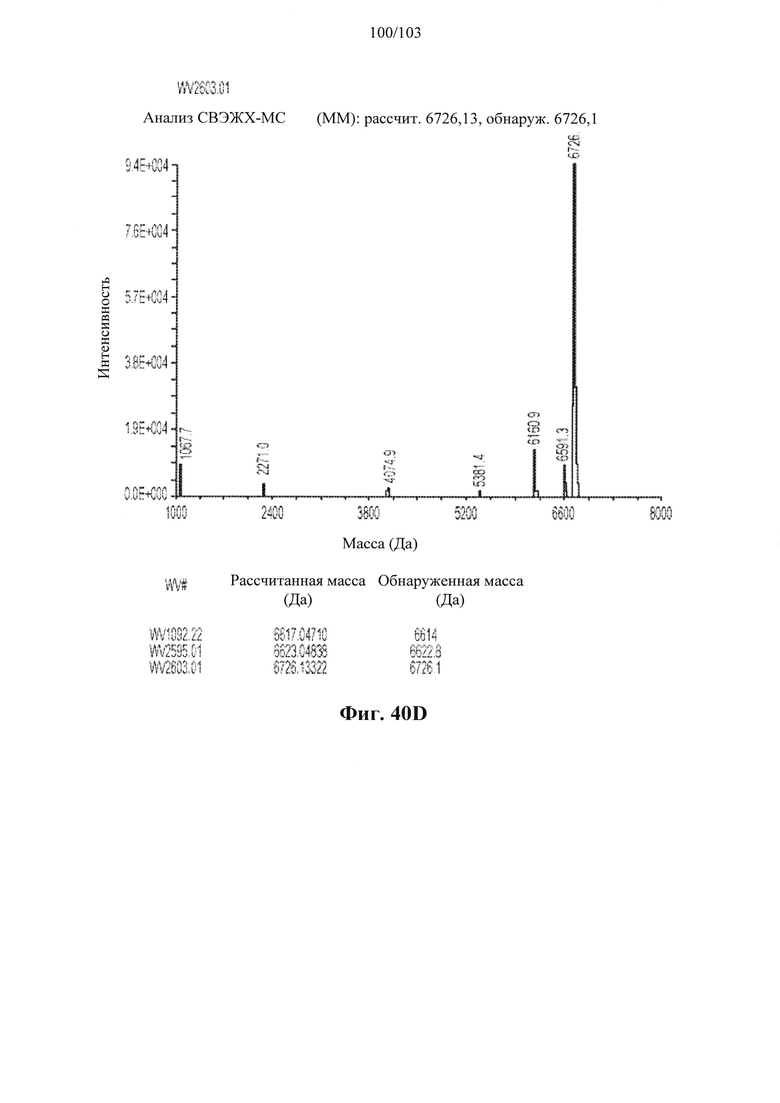
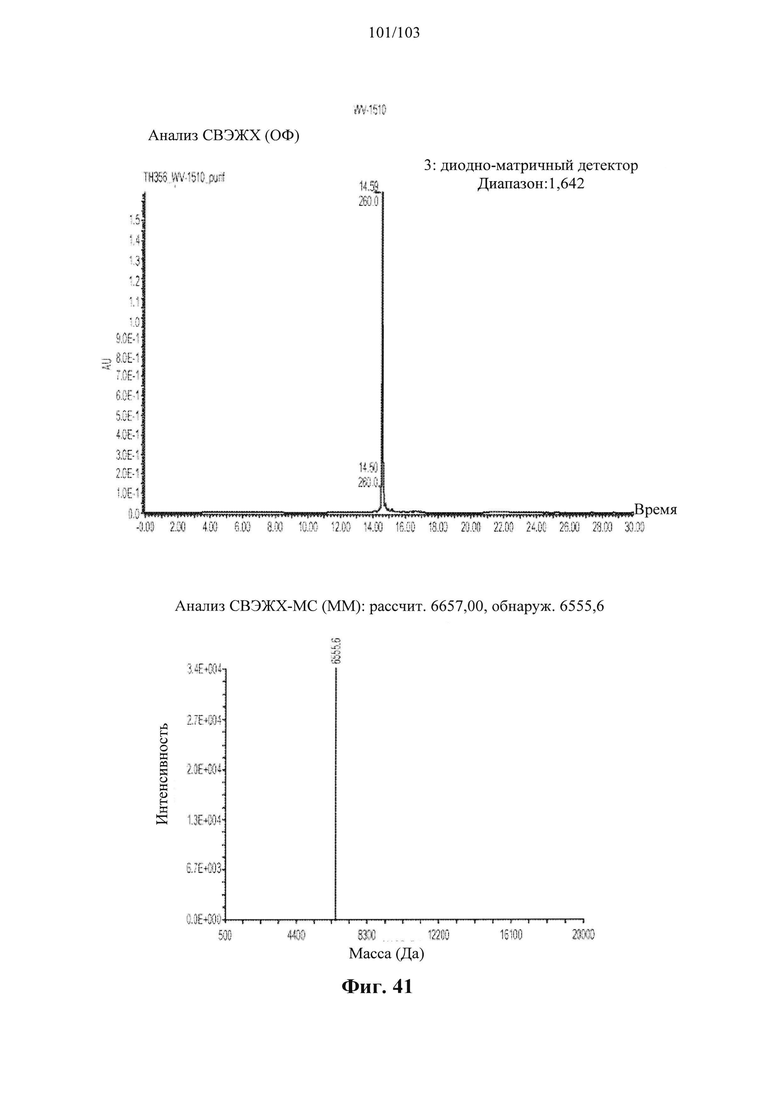
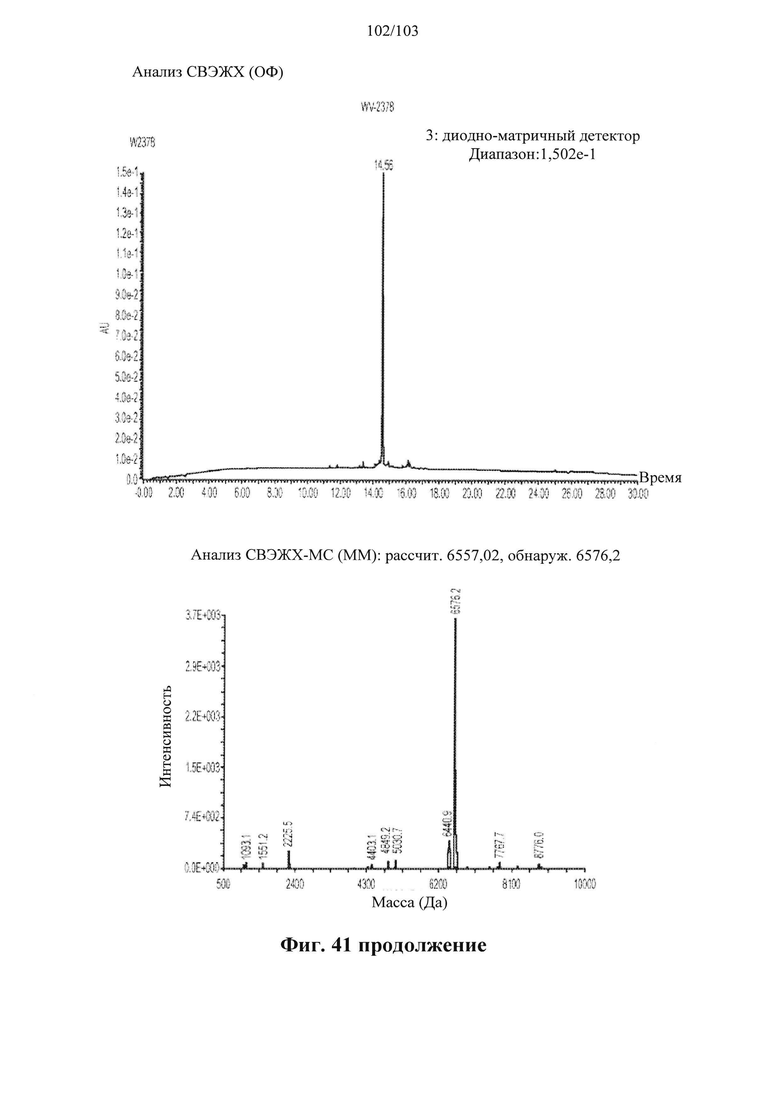
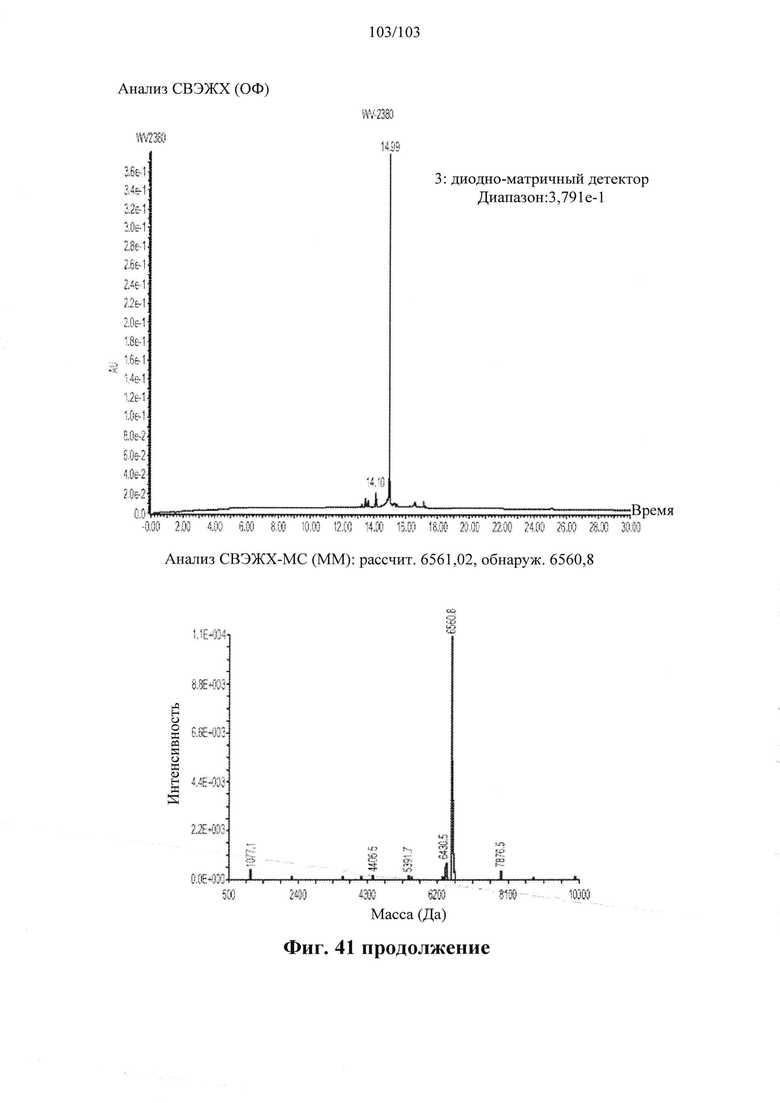
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая композицию олигонуклеотидов с контролируемой хиральностью, способную избирательно подавлять транскрипты целевой последовательности нуклеиновой кислоты, фармацевтическую композицию для лечения болезни Хантингтона, способ расщепления нуклеиновой кислоты, применение композиции олигонуклеотидов с контролируемой хиральностью в способе лечения и/или профилактики болезни Хантингтона и способ получения композиции олигонуклеотидов с контролируемой хиральностью. В одном варианте реализации композиция с контролируемой хиральностью содержит в себе олигонуклеотиды с одинаковой последовательностью оснований и длиной, профилем линкерных групп остова и профилем хиральных центров остова. Изобретение расширяет арсенал средств для избирательного подавления транскрипта целевой последовательности нуклеиновой кислоты. 5 н. и 54 з.п. ф-лы, 41 ил., 44 табл., 22 пр.
1. Композиция олигонуклеотидов с контролируемой хиральностью, содержащая олигонуклеотиды определенного типа олигонуклеотида, характеризующегося:
1) одинаковой последовательностью оснований и длиной;
2) одинаковым профилем линкерных групп остова; и
3) одинаковым профилем хиральных центров остова;
причем композиция характеризуется контролируемой хиральностью в том отношении, что она обогащена относительно по существу рацемического препарата олигонуклеотидов, имеющих одну и ту же последовательность оснований и длину, олигонуклеотидами определенного типа олигонуклеотида, где:
олигонуклеотиды определенного типа олигонуклеотида каждый содержит структуру крыло-сердцевина-крыло;
каждая область крыла независимо составляет в длину два или более основания, при этом по меньшей мере одно крыло содержит одну или несколько природных фосфатных линкерных групп и каждая независимо и необязательно содержит одну или несколько хиральных межнуклеотидных линкерных групп;
область сердцевины имеет профиль хиральных центров остова, содержащий Rp(Sp)2; и
причем композиция способна избирательно подавлять транскрипты целевой последовательности нуклеиновой кислоты.
2. Композиция по п. 1, в которой олигонуклеотиды нацелены на мутантный ген хантингтина и их длина составляет от примерно 10 до примерно 50 нуклеотидов.
3. Композиция по любому из пп. 1, 2,
в которой по меньшей мере один нуклеотид в области крыла отличается от по меньшей мере одного нуклеотида в области сердцевины, причем различие заключается в одном или более из:
1) линкерная группа остова;
2) профиль хиральных центров остова;
3) модификация сахара.
4. Композиция по любому из предшествующих пунктов, в которой олигонуклеотиды одного и того же типа характеризуются идентичной структурой.
5. Композиция по любому из предшествующих пунктов, в которой олигонуклеотиды содержат одну или более природных фосфатных линкерных групп (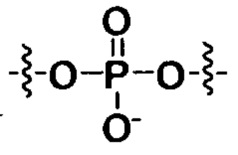 ) и одну или более фосфоротиоатных линкерных групп.
) и одну или более фосфоротиоатных линкерных групп.
6. Композиция по любому из предшествующих пунктов, в которой сердцевина содержит одну или более фосфоротиоатных линкерных групп.
7. Композиция по любому из предшествующих пунктов, отличающаяся тем, что область сердцевины имеет профиль хиральных центров остова, содержащий Rp(Sp)2, и где каждая межнуклеотидная связь Rp(Sp)2 независимо представляет собой фосфоротиоатную связь.
8. Композиция по любому из предшествующих пунктов, в которой каждое крыло независимо содержит модифицированный фрагмент сахара.
9. Композиция по п. 8, в которой модифицированный фрагмент сахара имеет 2'-модификацию.
10. Композиция по п. 8, в которой модифицированный фрагмент сахара содержит модификацию бициклического сахара.
11. Композиция по п. 8, в которой модифицированный фрагмент сахара содержит 2'-модификацию, причем 2'-модификация представляет собой 2'-OR1, где R1 представляет собой необязательно замещенный C1-6 алкил.
12. Композиция по п. 8, в которой модифицированный фрагмент сахара содержит 2'-модификацию, причем 2'-модификация представляет собой 2'-МОЕ.
13. Композиция по п. 8, в которой модифицированный фрагмент сахара содержит 2'-модификацию, причем 2'-модификация представляет собой 2'-ОМе.
14. Композиция по любому из предшествующих пунктов, в которой каждый фрагмент сахара крыла модифицирован модификацией, отсутствующей в области сердцевины.
15. Композиция по любому из предшествующих пунктов, в котором каждый фрагмент сахара области сердцевины представляет собой природный фрагмент сахара ДНК.
16. Композиция по любому из предшествующих пунктов, в которой крыло относится к 5'-концу сердцевины и содержит хиральную межнуклеотидную линкерную группу на 5'-конце крыла.
17. Композиция по п. 16, в которой крыло относится к 5'-концу сердцевины и содержит фосфоротиоатную межнуклеотидную линкерную группу конфигурации Sp на 5'-конце крыла.
18. Композиция по любому из предшествующих пунктов, в которой крыло на 3'-конце сердцевины содержит хиральную межнуклеотидную линкерную группу на 3'-конце крыла.
19. Композиция по п. 18, в которой крыло относится к 3'-концу сердцевины и содержит фосфоротиоатную межнуклеотидную линкерную группу конфигурации Sp на 3'-конце крыла.
20. Композиция по любому из предшествующих пунктов, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой хиральную межнуклеотидную линкерную группу.
21. Композиция по любому из предшествующих пунктов, в которой область сердцевины характеризуется профилем хирального центра остова, который содержит (Sp)t(Rp)n(Sp)m, где t равно 1-10, n равно 1 и m составляет 2-50.
22. Композиция по любому из предшествующих пунктов, в которой область сердцевины характеризуется профилем хирального центра остова, который содержит (Np)t(Rp)n(Sp)m, где каждый Np независимо представляет собой Rp или Sp, t равно 1-10, n равно 1 и m равно 2-50.
23. Композиция по любому из пп. 21, 22, в которой каждый Rp и Sp независимо представляет собой фосфоротиоатную линкерную группу.
24. Композиция по любому из пп. 21-23, в которой по меньшей мере одно из значений t и m больше 5.
25. Композиция по любому из пп. 21-24, в которой t больше 5.
26. Композиция по любому из предшествующих пунктов, в которой 50% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
27. Композиция по любому из предшествующих пунктов, в которой 60% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
28. Композиция по любому из предшествующих пунктов, в которой 70% или более хиральных межнуклеотидных линкерных групп в области сердцевины имеют конфигурацию Sp.
29. Композиция по любому из предшествующих пунктов, в которой каждая межнуклеотидная линкерная группа в области сердцевины является хиральной, и область сердцевины имеет только одну межнуклеотидную связь Rp, и каждая из других межнуклеотидных линкерных групп в области сердцевины представляет собой Sp.
30. Композиция по любому из предшествующих пунктов, в которой каждая межнуклеотидная линкерная группа области сердцевины представляет собой фосфоротиоатную связь.
31. Композиция по любому из предшествующих пунктов, в которой олигонуклеотиды определенного типа составляют в длину более чем 15 оснований.
32. Композиция по п. 22, в которой олигонуклеотиды определенного типа составляют в длину менее чем 50 оснований.
33. Композиция по п. 22, в которой олигонуклеотиды определенного типа составляют в длину 19, 20 или 21 основание.
34. Композиция по любому из предшествующих пунктов, в которой по меньшей мере примерно 50% олигонуклеотидов в композиции характеризуются одинаковой последовательностью оснований и длиной, одинаковым профилем линкерных групп остова и одинаковым профилем хиральных центров остова.
35. Композиция по любому из предшествующих пунктов, в которой одинаковая последовательность оснований содержит последовательность, которая на 100% комплементарна характеристическому элементу последовательности целевой последовательности, при этом характеристический элемент последовательности определяет эту целевую последовательность относительно аналогичной последовательности.
36. Композиция по любому из предшествующих пунктов, в которой последовательность оснований области сердцевины содержит последовательность, которая на 100% комплементарна характеристическому элементу последовательности целевой последовательности, при этом характеристический элемент последовательности определяет эту целевую последовательность относительно аналогичной последовательности.
37. Композиция по любому из предшествующих пунктов, в которой положение 11, 12 или 13 олигонуклеотидов при отсчете от 5'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
38. Композиция по любому из предшествующих пунктов, в которой положение 8, 9 или 10 олигонуклеотидов при отсчете от 3'-конца олигонуклеотидов выравнивается с характеристическим элементом последовательности.
39. Композиция по любому из предшествующих пунктов, в которой положение 6, 7 или 8 области сердцевины при отсчете от 5'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
40. Композиция по любому из предшествующих пунктов, в которой положение 3, 4 или 5 области сердцевины при отсчете от 3'-конца области сердцевины выравнивается с характеристическим элементом последовательности.
41. Композиция по любому из предшествующих пунктов, в которой целевая последовательность представляет собой последовательность, содержащую характеристический элемент последовательности, который представляет собой мутацию, и аналогичная последовательность представляет собой последовательность дикого типа.
42. Композиция по любому из предшествующих пунктов, в которой характеристический элемент последовательности определяет конкретный аллель целевого гена по отношению к другим аллелям одного и того же целевого гена.
43. Композиция по любому из предшествующих пунктов, в которой характеристический элемент последовательности представляет собой однонуклеотидный полиморфизм (SNP), связанный с заболеванием.
44. Композиция по п. 42, в которой SNP связан с болезнью Хантингтона.
45. Композиция по п. 42, в которой SNP выбран из rs362307, rs7685686, rs362268 или rs362306.
46. Фармацевтическая композиция, содержащая композицию по любому из пп. 1-45 и по меньшей мере один фармацевтически приемлемый неактивный ингредиент, выбранный из фармацевтически приемлемых разбавителей, фармацевтически приемлемых вспомогательных веществ и фармацевтически приемлемых носителей, причем фармацевтическая композиция предназначена для лечения болезни Хантингтона.
47. Композиция по любому из предшествующих пунктов, дополнительно содержащая искусственную спинномозговую жидкость.
48. Способ расщепления нуклеиновой кислоты, имеющей последовательность оснований, содержащую целевую последовательность, причем способ предусматривает
контактирование нуклеиновой кислоты, имеющей последовательность оснований, содержащую целевую последовательность, с композицией олигонуклеотидов по любому из пп. 1-45, причем одинаковая последовательность оснований представляет собой или содержит последовательность, которая комплементарна целевой последовательности в нуклеиновой кислоте.
49. Применение композиции по любому из пп. 1-47 в способе профилактики и/или лечения болезни Хантингтона у субъекта.
50. Применение по п. 49, в которой экспрессия аллеля, вызывающего заболевание, избирательно подавляется.
51. Способ получения композиции олигонуклеотидов по любому из пп. 1-47, включающий:
1) получение фосфорамидита, который содержит фрагмент хирального реагента, имеющего структуру
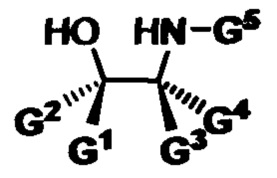 ,
,
где гидроксильные и аминогруппы образуют связи с атомом фосфора фосфорамидита и где:
каждый из G1 и G3 независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного C1-10,
G2 представляет собой -C(R)2Si(R)3 и G4 и G5, взятые вместе, образуют необязательно замещенное насыщенное, частично ненасыщенное или ненасыщенное гетероатомсодержащее кольцо до примерно 20 кольцевых атомов, которое является моноциклическим или полициклическим, конденсированным или неконденсированным, и
каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, карбоциклильного, арильного, гетероарильного и гетероциклильного C1-С6; и
2) удаление фрагмента из хирального реагента с использованием фторсодержащего реагента.
52. Способ по п. 51, в котором G2 представляет собой -C(R)2Si(R)3, где -C(R)2-необязательно замещен -СН2- и каждый R из -Si(R)3 представляет собой независимо, необязательно замещенную группу, выбранную из алифатического, гетероциклильного, гетероарильного и арильного C1-10.
53. Способ по п. 51 или 52, где G2 представляет собой -CH2Si(Me)(Ph)2.
54. Способ по любому из пп. 51-53, в котором G4 и G5 берут вместе с образованием необязательно замещенного насыщенного 5-членного кольца, содержащего один атом азота (к которому присоединен G5).
55. Способ по любому из пп. 51-54, в котором G1 представляет собой водород.
56. Способ по любому из пп. 51-55, в котором G3 представляет собой водород.
57. Способ по любому из пп. 51-56, в котором хиральный реагент представляет собой 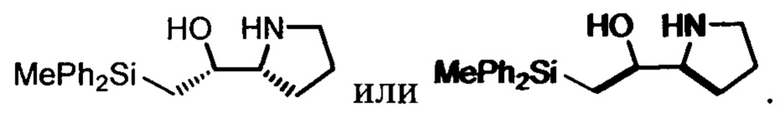
58. Способ по любому из пп. 51-57, в котором фторсодержащий реагент представляет собой HF-NR3 и каждый R независимо представляет собой водород или необязательно замещенную группу, выбранную из алифатического, фенильного, карбоциклильного, арильного, гетероарильного или гетероциклильного C1-С6.
59. Способ по любому из пп. 51-58, в котором фторсодержащий реагент представляет собой HF-NEt3.
| WO 2014012081 A2, 16.01.2014 | |||
| WO 2011005761 A1, 13.01.2011 | |||
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С СУБСТРАТОМ РЕЦЕПТОРА ИНСУЛИНА 2 (IRS2), ПУТЕМ ИНГИБИРОВАНИЯ ПРИРОДНОГО АНТИСМЫСЛОВОГО ТРАНСКРИПТА К IRS2 | 2010 |
|
RU2616283C2 |
| Natsuhisa Oka, Takeshi Wada "Stereocontrolled synthesis of oligonucleotide analogs containing chiral internucleotidic phosphorus atoms", Chem | |||
| Soc | |||
| Rev | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Pfister E.L | |||
| et al | |||
| "Five siRNAs targeting three SNPs may provide therapy for | |||
Авторы
Даты
2024-11-22—Публикация
2016-07-22—Подача