ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По этой заявке испрашиваются преимущества китайской патентной заявки 202110049777.7, поданной 14 января 2021 г., содержание которой целиком включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к области биологических фармацевтических препаратов, в частности к препарату стабильной вакцины из вирусоподобных частиц папилломавируса человека.
УРОВЕНЬ ТЕХНИКИ
[0003] Рак шейки матки является одной из наиболее распространенных злокачественных опухолей у женщин, с примерно 500000 новых пациентов во всем мире каждый год, и уровень заболеваемости является вторым среди опухолей у женщин. Более 95% случаев рака шейки матки связаны с папилломавирусом человека (ПВЧ). Помимо непосредственной причины рака шейки матки, ПВЧ также сильно связан с бронхогенным раком, раком прямой кишки, раком полости рта и раком кожи. Кроме того, ПВЧ также является основным патогенным фактором, вызывающим бородавки на коже и слизистых оболочках.
[0004] В настоящее время обнаружено более 100 типов ПВЧ, и разные типы ПВЧ могут вызывать разные заболевания. По своей тесной связи с раком шейки матки ПВЧ можно разделить на тип высокого риска, тип с подозрением на канцерогенность и тип низкого риска. Тип высокого риска и тип с подозрением на канцерогенность могут вызывать рак, такой как рак шейки матки; к типам высокого риска относятся типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59. К типам с подозрением на канцерогенность относятся типы 26, 53, 66, 68, 73 и 82. Типы низкого риска в основном связаны с генитальными бородавками, остроконечными кондиломами и другими заболеваниями и включают типы 6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81 и 89. Типы ПВЧ 6, 11 и 16 были подтипами с самой высокой частотой выявления у пациентов с генитальными поражениями.
[0005] Вакцина против ПВЧ представляет собой эффективный способ остановки инфекции папилломавируса. Вакцина на основе вирусоподобных частиц (ВПЧ) является наиболее предпочтительной формой вакцины среди многих форм вакцин. Однако вакцина против ПВЧ на основе ВПЧ является типоспецифичной, т. е. она демонстрирует сильную защиту только против типов ПВЧ, присутствующих в вакцине ВПЧ. Для обеспечения широкой защиты необходима разработка мультивалентных вакцин против ПВЧ.
[0006] Однако перед введением состав вакцины против вируса папилломы человека подвергается процессу хранения и транспортировки, во время которого антиген подвергается физической и химической деградации, и эти нестабильности могут снизить иммуногенность и/или безопасность антигена и, таким образом, существует необходимость в стабильном составе для обеспечения того, чтобы антиген по-прежнему сохранял иммуногенность и безопасность непосредственно перед введением, удовлетворяя при этом профилактическим целям.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0007] В одном аспекте настоящее изобретение обеспечивает стабильный состав поливалентной вакцины из вирусоподобных частиц папилломавируса человека для профилактики заболеваний или инфекций, связанных с ПВЧ, содержащий множество вирусоподобных частиц папилломавируса, адсорбированных на адъюванте; а также физиологически приемлемые концентрации буфера, регулятора осмотического давления и необязательно поверхностно-активного вещества.
[0008] При этом вирусоподобные частицы папилломавируса человека выбирают из вирусоподобных частиц ПВЧ, собранных белками L1 типов ПВЧ 6, 11, 16, 18, 31, 33, 45, 52 и 58, соответственно; и одну или несколько вирусоподобных частиц ПВЧ, собранных из белков L1 других патогенных типов ПВЧ.
[0009] В одном из вариантов осуществления,
буфер выбирают из одного или нескольких из буфера с лимонной кислотой, буфера с уксусной кислотой или гистидинового буфера;
регулятор осмотического давления выбирают из одного или нескольких из хлорида натрия, фосфата натрия или сульфата натрия;
поверхностно-активное вещество представляет собой полиэтоксиэфир, предпочтительно полисорбат 80;
адъювант выбирают из одного или нескольких из гидроксифосфата алюминия (AlPO4), аморфного сульфата гидроксифосфата алюминия (AAHS) или гидроксида алюминия (Al(OH)3), предпочтительно гидроксифосфата алюминия (AlPO4).
[0010] В одном из вариантов осуществления,
(a) общая концентрация вирусоподобных частиц папилломавирусов всех типов составляет от 40 мкг/мл до 740 мкг/мл;
(б) концентрация буфера составляет от 10 мМ до 26 мМ, предпочтительно 10 мМ, 18 мМ или 26 мМ;
(в) концентрация регулятора осмотического давления составляет от 150 мМ до 320 мМ, предпочтительно 150 мМ или 320 мМ;
(г) концентрация поверхностно-активного вещества составляет от 0 до 0,02% по весу;
(д) концентрация адъюванта составляет около 1,0 мг/мл;
(е) pH состава составляет 5,9-6,5, предпочтительно 5,9, 6,2 или 6,5.
[0011] В одном из вариантов осуществления, концентрация любого отдельного типа вирусоподобных частиц папилломавируса, входящих в состав поливалентных вирусоподобных частиц папилломавируса, составляет от 40 мкг/мл до 120 мкг/мл.
[0012] В одном из вариантов осуществления, препарат содержит в общей сложности 0,74 мг/мл вирусоподобных частиц папилломавирусов всех типов, 1,0 мг/мл адъюванта фосфата алюминия, 18 мМ гистидинового буфера, 320 мМ хлорида натрия, рН раствора препарата 6,2; необязательно полисорбат 80 в концентрации не более 0,3 мг/мл.
[0013] В одном из вариантов осуществления, один или несколько других патогенных типов ПВЧ выбраны из типов ПВЧ 35, 39, 51, 56 и 59.
[0014] В одном из вариантов осуществления, по меньшей мере одна из вирусоподобных частиц ВПЧ представляет собой химерную вирусоподобную частицу ВПЧ, содержащую химерный белок L1 ПВЧ; при этом указанный химерный белок L1 ПВЧ содержит от его N-конца до его C-конца:
a. N-концевой фрагмент, полученный из белка L1 папилломавируса первого типа, причём этот N-концевой фрагмент сохраняет иммуногенность белка L1 этого типа, при этом папилломавирус первого типа выбран из ПВЧ типов 6, 11, 16, 18, 31, 33, 45, 52 и 58, и одного или нескольких других патогенных типов ПВЧ; и
б. С-концевой фрагмент, полученный из белка L1 папилломавируса второго типа, обладающий лучшими характеристиками экспрессии и растворимости по сравнению с белками L1 других типов,
при этом такой химерный белок L1 ПВЧ обладает иммуногенностью белка L1 папилломавируса первого типа.
[0015] В одном из вариантов осуществления, указанный N-концевой фрагмент представляет собой фрагмент, полученный укорочением С-конца природной последовательности указанного белка L1 папилломавируса первого типа в любом положении аминокислоты в пределах его области α5, и фрагмент, имеющий по меньшей мере 98% идентичности с ним; а указанный С-концевой фрагмент представляет собой фрагмент, полученный укорочением N-конца природной последовательности указанного белка L1 папилломавируса второго типа в любом положении аминокислоты в пределах его области α5 и функциональных вариантов, возникающих в результате дальнейших мутаций, делеций и/или дополнения к этому фрагменту.
[0016] В одном из вариантов осуществления, С-концевой фрагмент содержит одну или несколько последовательностей ядерной локализации.
[0017] В одном из вариантов осуществления, при этом белок L1 папилломавируса первого типа выбран из ПВЧ типов 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56 или 58; предпочтительно, его природная последовательность представляет собой аминокислотную последовательность, кодируемую кодирующим геном, приведённую в SEQ ID No: 30, SEQ ID No: 31, SEQ ID No: 32, SEQ ID No: 33, SEQ ID No: 34, SEQ ID No: 35, SEQ ID No: 36, SEQ ID No: 37, SEQ ID No: 38, SEQ ID No: 39, SEQ ID No: 40, или SEQ ID No: 41, соответственно;
белок L1 папилломавируса второго типа выбран из белка L1 ВПЧ типов 16, 28, 33, 59 или 68;
более предпочтительно, белок L1 папилломавируса второго типа выбран из белка L1 ПВЧ типа 33 или ПВР типа 59.
[0018] В одном из вариантов осуществления, указанный С-концевой фрагмент представляет собой SEQ ID No: 1; или его фрагмент, имеющий длину m1 аминокислот, предпочтительно фрагмент, охватывающий аминокислоты 1-m1 SEQ ID No:1; где m1 представляет собой целое число от 8 до 26; или указанный С-концевой фрагмент представляет собой SEQ ID No: 2; или его фрагмент, имеющий длину m2 аминокислот, предпочтительно фрагмент, охватывающий аминокислоты 1-m2 SEQ ID No:2; где m2 представляет собой целое число от 13 до 31.
[0019] В одном из вариантов осуществления, указанный С-концевой фрагмент представляет собой SEQ ID No: 3; или его фрагмент, имеющий длину n аминокислот, предпочтительно фрагмент, охватывающий аминокислоты 1-n SEQ ID No:3; где n представляет собой целое число от 16 до 38.
[0020] В одном из вариантов осуществления, указанный N-концевой фрагмент белка L1 ПВЧ типа 6 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No: 4, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 11 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:5, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 16 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:6, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 18 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:7, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 31 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:8, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 35 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:9, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 39 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No: 10, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 45 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:11, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 51 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:12, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 52 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:13, в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 56 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:14, в любом положении аминокислоты в пределах его области α5; и
указанный N-концевой фрагмент белка L1 ПВЧ типа 58 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путём укорочения C-конца последовательности, представленной в SEQ ID No:15, в любом положении аминокислоты в пределах его области α5.
[0021] В одном из вариантов осуществления, С-конец N-концевого фрагмента соединён непосредственно с N-концом С-концевого фрагмента или соединен посредством линкера.
[0022] В одном из вариантов осуществления, когда С-конец указанного N-концевого фрагмента соединён с N-концом указанного С-концевого фрагмента, непрерывная аминокислотная последовательность RKFL присутствует в диапазоне плюс-минус 4 аминокислотных положения сайта сплайсинга,
предпочтительно непрерывная аминокислотная последовательность LGRKFL присутствует в диапазоне плюс-минус 6 аминокислотных положений сайта сплайсинга.
[0023] В одном из вариантов осуществления, химерные белки L1 ПВЧ типов 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56 и 58 имеют 98%, 98,5%, 99%, 99,5% или 100% идентичность с SEQ ID No:16, SEQ ID No:17, SEQ ID No:18, SEQ ID No:19, SEQ ID No:20, SEQ ID No:21, SEQ ID No:22, SEQ ID No:23, SEQ ID No:24, SEQ ID No:25, SEQ ID No:26 и SEQ ID No: 27, соответственно; а белок L1 ПВЧ типа 33 и белок L1 ПВЧ типа 59 имеют 98%, 98,5%, 99%, 99,5% или 100% идентичность с SEQ ID No:28 и SEQ ID No:29, соответственно.
[0024] В одном из вариантов осуществления, указанный препарат содержит химерные белки L1 ПВЧ типов 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56 и 58, имеющие последовательности аминокислот, показанные в SEQ ID No:16, SEQ ID No:17, SEQ ID No:18, SEQ ID No:19, SEQ ID No:20, SEQ ID No:21, SEQ ID No:22, SEQ ID No:23, SEQ ID No:24, SEQ ID No:25, SEQ ID No:26 и SEQ ID No: 27, соответственно; и
а белок L1 ПВЧ типа 33 и белок L1 ПВЧ типа 59 имеют последовательности аминокислот, показанные в SEQ ID No:28 и SEQ ID No: 29, соответственно.
[0025] В одном из аспектов, настоящее изобретение относится к способу профилактики заболевания или инфекции, связанной с ПВЧ, включающему введение субъекту стабильного препарата поливалентной вакцины из вирусоподобных частиц папилломавируса человека. Профилактику можно рассматривать как лечение и эти два термина используются взаимозаменяемо. В одном варианте осуществления субъектом является человек.
[0026] В одном из аспектов, препарат стабилен при температуре от 2 до 8 °C не менее 24 месяцев и при 25 °C не менее 16 недель.
[0027] В одном из аспектов, настоящее изобретение обеспечивает применение препарата вакцины из вирусоподобных частиц папилломавируса человека для приготовления вакцины для профилактики заболеваний или инфекций, связанных с ПВЧ.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0028] На Фиг. 1 показаны результаты теста на степень адсорбции каждого образца препарата в Примере 1.
[0029] На Фиг. 2 показан результат анализа содержания антигена в каждом образце препарата в Примере 1. T0:37 °C, неделя 0; 37 °C_1W: 37 °C, неделя 1; 37 °C_2 W: 37 °C, неделя 2; 37 °C_4 W: 37 °C неделя 4.
[0030] На Фиг. 3 показаны результаты теста на степень адсорбции каждого образца препарата в Примере 2.
[0031] На Фиг. 4 показан результат анализа содержания антигена в каждом образце препарата в Примере 2. T0:37 °C, неделя 0; 37 °C_1W: 37 °C, неделя 1; 37 °C_2 W: 37 °C, неделя 2; 37 °C_4 W: 37 °C неделя 4.
[0032] На Фиг. 5 показаны результаты теста на степень адсорбции каждого образца препарата в Примере 3.
[0033] На Фиг. 6 показан результат анализа содержания антигена в каждом образце препарата в Примере 3. T0:37 °C, неделя 0; 37 °C_1W: 37 °C, неделя 1; 37 °C_2 W: 37 °C, неделя 2; 37 °C_4 W: 37 °C неделя 4.
[0034] На Фиг. 7 показаны результаты теста на степень адсорбции каждого образца препарата в Примере 4.
[0035] На Фиг. 8 показан результат анализа содержания антигена в каждом образце препарата в Примере 4. T0:37 °C, неделя 0; 37 °C_1W: 37 °C, неделя 1; 37 °C_2 W: 37 °C, неделя 2; 37 °C_4 W: 37 °C неделя 4.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0036] Настоящее изобретение обеспечивает стабильный препарат вакцины против папилломавируса человека, решает проблему стабильности антител в процессах хранения и транспортировки и гарантирует, что предварительно дозированный антиген по-прежнему обладает иммуногенностью и безопасностью, которые удовлетворяют целям профилактики.
[0037] Термин «препарат» относится к композиции, которая поддерживает биологическую активность активного компонента эффективным образом и не содержит других компонентов, неприемлемо токсичных для субъекта. Такие препараты стерильны. Термин «стерильный» относится к отсутствию живых бактерий или отсутствию или отсутствию по существу всех живых микроорганизмов и их спор.
[0038] Используемый в настоящем документе термин «стабильный» в отношении препарата относится к препарату, в котором активный ингредиент по существу сохраняет свою физическую и/или химическую стабильность и/или биологическую активность после хранения. Предпочтительно препарат по существу сохраняет свою физическую и химическую стабильность, а также свою биологическую активность после хранения.
[0039] Термины «пациент» или «субъект» используются взаимозаменяемо и относятся к любому млекопитающему, страдающему от состояния или заболевания в соответствии с настоящим изобретением. Предпочтительно, это человек.
[0040] Используемый в настоящем документе термин «физиологически приемлемый» означает концентрацию или ионную силу буфера, эксципиента или соли, делающие препарат биологически совместимым с иммунизированным хозяином-мишенью, например, человеком.
[0041] Стабильный препарат согласно настоящему изобретению содержит вирусоподобные частицы папилломавируса человека, буфер, регулятор осмотического давления и адъювант на основе алюминия.
[0042] Термин «содержащий» означает, что в дополнение к упомянутым компонентам могут быть включены дополнительные компоненты.
[0043] Используемые в настоящем описании и в прилагаемой формуле изобретения формы единственного числа «указанный» также включают формы во множественном числе, если из контекста явно не следует иное.
[0044] Используемый в настоящем документе термин «буфер» относится к буферному раствору, который противостоит изменению pH под действием его сопряженной пары кислотно-основных веществ. В одном варианте осуществления настоящего изобретения используют гистидиновый буфер, а рН раствора препарата предпочтительно составляет примерно от 5,9 до 6,5, более предпочтительно 6,2.
[0045] Используемый в настоящем документе термин «сурфактант» относится к поверхностно-активному агенту, и в одном варианте осуществления поверхностно-активное вещество в данном документе представляет собой полисорбат 80.
[0046] Термин «регулятор осмотического давления» означает фармацевтически приемлемый регулятор осмотического давления. Подходящие регуляторы осмотического давления включают соли, но не ограничиваются ими, и в одном варианте осуществления настоящего изобретения представляют собой хлорид натрия (NaCl) с концентрацией примерно от 150 мМ до 320 мМ.
[0047] Термин «адъювант» относится к соединению или смеси, которые усиливают иммунный ответ. В частности, вакцина согласно настоящему изобретению может содержать адъювант. Адъюванты, используемые в настоящем изобретении, выбирают из одного или нескольких из гидроксифосфата алюминия (AlPO4), аморфного сульфата гидроксифосфата алюминия (AAHS) или гидроксида алюминия (Al(OH)3), предпочтительно гидроксифосфата алюминия (AlPO4).
[0048] «Стабильность» белка после хранения при выбранной температуре в течение выбранного периода времени можно оценить качественно и/или количественно несколькими различными способами. В варианте осуществления настоящего изобретения твёрдофазный иммуноферментный анализ (ИФА) использовали для измерения содержания активного антигена, связывающегося с рекомбинантным антителом, нейтрализующим вирус папилломы человека, и отношение содержания активного антигена в каждый момент времени к T0 использовали для сравнения стабильности соответствующего препарата; с помощью иммуноферментного анализа (ИФА) определяли содержание антигена, не адсорбировавшегося на алюмофосфатном адъюванте, после центрифугирования и затем рассчитывали степень абсорбции; определяли EC50 препарата вакцины против папилломавируса человека и положительного контроля к рекомбинантному антителу, нейтрализующему папилломавирус человека, соответственно, рассчитывали отношение EC50 препарата вакцины к положительному контролю, тем самым определяли относительную активность вакцины in vitro.
[0049] Термин «иммуногенность» относится к способности вещества, такого как белок или полипептид, стимулировать иммунный ответ, т.е. стимулировать выработку антител, в частности ответы, которые вызывают гуморальные или стимулированные клеточно-опосредованные ответы.
[0050] Термин «ПВЧ» или «вирус ПВЧ» относится к папилломавирусам семейства Papillomaviridae, который представляет собой непокрытый ДНК-вирус, имеющий двухцепочечный ДНК-геном с замкнутой петлей размером около 8 т.п.н., который обычно можно разделить на три области: ① ранняя область (E), содержащая шесть открытых рамок считывания, кодирующих неструктурные белки, родственные E1, белки репликации, транскрипции и трансформации вирусов Е2, Е4-Е7, а также открытые рамки считывания Е3 и Е8; ② поздняя область (L) содержит рамку считывания, кодирующую основной капсидный белок L1 и минорный капсидный белок L2; ③ длинная регуляторная область (LCR) не кодирует какой-либо белок, но имеет точку начала репликации и множество сайтов связывания факторов транскрипции.
[0051] Термины «белок L1 ПВЧ» и «белок L2 ПВЧ» относятся к белкам, кодируемым поздней областью (L) генома ПВЧ и синтезируемых в среднем и позднем периоде инфекционного цикла ПВЧ. Белок L1 является основным белком капсида и имеет молекулярную массу 55-60 кДа. Белок L2 является минорным капсидным белком. Семьдесят два пентамера L1 образуют оболочку икосаэдрических частиц вируса ПВЧ, обертывая замкнутую двухцепочечную ДНК-микрохромосому. Белок L2 локализован на внутренней оболочке белка L1.
[0052] Термин «вирусоподобные частицы» представляет собой полую частицу, содержащую один или несколько структурных белков вируса без вирусной нуклеиновой кислоты.
[0053] Термин «концентрация вирусоподобных частиц папилломавируса любого отдельного типа» относится к содержанию вирусоподобных частиц папилломавируса любого отдельного типа в препарате, а термин «общая концентрация вирусоподобных частиц папилломавируса всех типов» представляет собой сумму концентраций вирусоподобных частиц папилломавируса каждого отдельного типа, включённых в препарат.
[0054] В одном варианте осуществления настоящего изобретения используют поливалентную иммуногенную композицию папилломавируса человека, описанную в патентной заявке PCT/CN2020/102601, поданной 17 июля 2020 г., при этом заявка PCT/CN2020/102601 целиком включена посредством ссылки в настоящее описание и формулу изобретения.
[0055] В наиболее предпочтительном варианте осуществления настоящего изобретения препарат содержит 0,74 мг/мл вирусоподобных частиц папилломавируса, 1,0 мг/мл адъюванта фосфата алюминия, 18 мМ гистидинового буфера, 320 мМ хлорида натрия и рН 6,2. При этом вакцина содержит полисорбат 80 в концентрации не более 0,3 мг/мл за счёт остатков, образованных при приготовлении. Препарат обладает хорошей стабильностью и может стабильно храниться при температуре от 2 до 8 °C не менее 24 месяцев и при 25 °C не менее 16 недель.
[0056] Препараты согласно настоящему изобретению могут быть предоставлены в жидкой форме или могут быть предоставлены в лиофилизированной форме. Лиофилизированный препарат может быть восстановлен перед введением.
ПРИМЕРЫ
[0057] Настоящее изобретение будет более полно понято со ссылкой на следующие примеры. Однако их не следует рассматривать как ограничивающие объём настоящего изобретения. Все процитированные документы, патенты и патентные заявки целиком включены в настоящий документ посредством ссылки.
[0058] В приведенных ниже примерах приготовление, характеристика и идентификация эффективности различных типов используемых вирусоподобных частиц папилломавируса описаны в патентной заявке PCT/CN2020/102601, поданной 17 июля 2020 г.
[0059] В следующих примерах использовали следующий метод детектирования:
[0060] 1) Анализ содержания антигена (иммуноферментный анализ (ИФА)
[0061] Положительный контроль (вирусоподобная частица папилломавируса человека, стандарт, источник: SinoCellTech Ltd., химерные ПВЧ типов 6, 16, 18, 31, 35, 30, 45, 51, 52 и 56, химерный белок L1 ПВЧ и белок L1 ПВЧ типа 33 и белок L1 ПВЧ типа 59, соответствующие последовательностям аминокислот SEQ ID NO:16-29, соответственно, такие же, как и ниже), и анализируемый образец полностью растворяли с использованием буфера для десорбции, служащего в качестве положительного контроля, и анализируемого образца.
[0062] Рекомбинантное антитело, нейтрализующее папилломавирус человека (источник: Sino Biological, Inc., как указано ниже), объединяли с твёрдофазным носителем с образованием твёрдофазного антитела. Разводили положительный контроль и детектируемый образец разбавителем образца, а затем объединяли с твёрдофазным антителом с образованием твёрдофазного комплекса антиген-антитело; затем добавляли антитело, меченное ферментом, и субстрат для проявления, и окрашивание продукта считывали при длине волны 450 нм. Строили линейную регрессию для концентрации ряда положительных контролей и соответствующего поглощения, подставляли значения поглощения анализируемого образца в уравнение линейной регрессии и получали содержание антигена в детектируемом образце (M. Shank-Retzlaff, F. Wang, T. Morley и др. Correlation between Mouse Potency and In Vitro Relative Potency for Human Papillomavirus Type 16 Virus-Like Particles and Gardasil Vaccine Samples. Human Vaccines, 1:5, 191-197).
[0063] 2) Анализ степени адсорбции (иммуноферментный анализ (ИФА)
[0064] Рекомбинантное антитело, нейтрализующее папилломавирус человека, объединяли с твёрдофазным носителем с образованием твёрдофазного антитела. Центрифугировали образец для обнаружения и брали супернатант в качестве анализируемого образца. Разбавляли положительный контроль и анализируемый образец соответственно разбавителем образца, а затем объединяли с твёрдофазным антителом с образованием твёрдофазного комплекса антиген-антитело; затем добавляли антитело, меченное ферментом, и субстрат для проявления, и окрашивание продукта считывали при длине волны 450 нм. Строили линейную регрессию для концентрации ряда положительных контролей и соответствующего поглощения, подставляли значения поглощения, измеренного с анализируемым образцом, в уравнение линейной регрессии для получения концентрации антигена в супернатанте и рассчитывали степени адсорбции образца для обнаружения в соответствии со следующим уравнением (Michael J. Caulfield, Li Shi, Su Wang и др. Effect of Alternative Aluminum Adjuvants on the Absorption and Immunogenicity of HPV16 L1 VLPs in Mice. Human Vaccines 3:4, 139-146).
[0065] Степень адсорбции (%) = (1 - концентрация антигена в супернатанте / концентрация антигена в анализируемом образце) %.
[0066] 3) Определение относительной активности in vitro, IVRP (IVRP)
[0067] Положительный контроль (14-валентная вакцина против папилломавируса человека (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59) контрольный продукт, полученный от SinoCellTech Ltd., с последовательностью, такой же, как последовательность белка в тестируемом образце), и анализируемый образец полностью растворяли с использованием буфера для десорбции и использовали в качестве положительного контроля и анализируемого образца. Рекомбинантное антитело, нейтрализующее вирус папилломы человека, разбавляли до конечной концентрации 2 мкг/мл, добавляли в 96-луночные планшеты по 100 мкл/лунку, планшеты постукивали для смешивания образцов, и образцы покрывали в течение ночи при 4 °C; планшеты однократно промывали промывочным раствором в дозе 200 мкл/лунку и сушили ИФА-планшет. Затем планшет для ИФА блокировали раствором для блокирования в количестве 300 мкл на лунку в течение одного часа при комнатной температуре. Образцы дважды промывали промывочным раствором из расчёта 300 мкл на лунку, и в каждую лунку добавляли по 100 мкл обработанного контроля (буферного раствора, соответствующего анализируемому образцу), положительного контроля и анализируемого образца и инкубировали в течение 1 часа при комнатной температуре. После того, как планшеты трижды промывали промывочным раствором в количестве 200 мкл на лунку, добавляли разбавленное рекомбинантное антитело, нейтрализующее папилломавирус человека, меченное ферментом, в количестве 100 мкл на лунку. После инкубации при комнатной температуре в течение 1 ч планшеты промывали промывочным раствором по 200 мкл на лунку три раза, добавляли проявляющий раствор по 200 мкл на лунку и помещали при комнатной температуре на 20±5 мин. Реакцию останавливали добавлением стоп-раствора в количестве 50 мкл/лунку; поглощение при 450 нм определяли устройством для считывания микропланшетов. Данные обрабатывали с использованием компьютерной программы Origin или метода подгонки с четырьмя параметрами, принимая концентрацию положительного контроля или анализируемого образца за ось абсцисс и среднее поглощение за ординату для получения EC50 анализируемого образца и положительного контроля, и делили EC50 анализируемого образца на EC50 положительного контроля для получения относительной активности анализируемого образца in vitro (M. Shank-Retzlaff, F. Wang, T. Morley и др. Correlation between Mouse Potency and In Vitro Relative Potency for Human Papillomavirus Type 16 Virus-Like Particles and Gardasil Vaccine Samples. Human Vaccines, 1:5, 191-197).
[0068] Пример 1: Скрининговое исследование концентрации сурфактанта
[0069] Состав препарата вакцины вирусоподобных частиц папилломавируса согласно настоящему Примеру указан в следующей таблице:
[0070] Способ приготовления препарата вакцины вирусоподобных частиц папилломавируса:
[0071] Брали определённое количество вирусоподобных частиц ПВЧ типа 18, соответствующих препарату, а затем смешивали его с адъювантом на основе фосфата алюминия и адсорбировали в течение ночи при 4 °C, так чтобы pH, соответствующие концентрации вирусоподобных частиц папилломавируса, адъювант фосфата алюминия, гистидина, хлорида натрия и полисорбата 80 в составе препарата вакцины с вирусоподобными частицами папилломавируса, соответственно, соответствовали требованиям Таблицы 1, и дозировали его в аликвотах. Маркировали его соответствующими номерами, помещали образцы в инкубатор при 37 °С и доставали для анализа степени адсорбции и содержания антигена на 0-й неделе, а также для анализа содержания антигена на 1-й, 2-й и 4-й неделях.
[0072] Аналитический метод исследования:
[0073] Анализ степени адсорбции: принцип обнаружения заключается в том, что антигены, не адсорбированные на адъюванте на основе фосфата алюминия, отделяют центрифугированием, а их содержание анализируют для расчёта степени адсорбции.
[0074] Анализ содержания антигена: принцип обнаружения заключается в том, что содержание активного антигена, способного связываться с рекомбинантным антителом, нейтрализующим папилломавирус человека, измеряют с помощью ИФА, и сравнивают стабильность каждого препарата путём сравнения соотношения содержания активного антигена в каждый момент времени с моментом T0. Чем выше соотношение, тем выше содержание активного антигена в препарате и тем лучше сохраняется его активность.
[0075] Результаты испытаний приведены в Таблицах 2-3 и на Фиг. 1-2.
[0076] Результаты испытаний показали, что степень адсорбции обоих вакцинных препаратов вирусоподобных частиц папилломавируса была выше 99%, и не было существенной разницы в изменениях содержания антигена между F1 и F2, то есть стабильности F1 и F2 были сопоставимыми.
[0077] Пример 2: Скрининговое исследование рН
[0078] Состав препарата вакцины вирусоподобных частиц папилломавируса согласно настоящему примеру приведен в следующей Таблице:
[0079] Способ приготовления препарата вакцины вирусоподобных частиц папилломавируса:
[0080] Брали определённое количество вирусоподобных частиц ПВЧ 18, соответствующих препарату, а затем смешивали его с адъювантом фосфата алюминия и адсорбировали в течение ночи при 4 °С, так чтобы рН, соответствующие концентрации вирусоподобных частиц папилломавируса, адъювант фосфата алюминия, гистидина, хлорида натрия и полисорбата 80 в препарате вакцины с вирусоподобными частицами против папилломавируса соответствовали требованиям Таблицы 4, дозировали его в аликвотах. Маркировали его соответствующими номерами, помещали образцы в инкубатор при 37 °С и доставали для анализа степени адсорбции и содержания антигена на 0-й неделе, а также для анализа содержания антигена на 1-й, 2-й и 4-й неделях.
[0081] Аналитический метод исследования:
[0082] Анализ степени адсорбции: принцип обнаружения заключается в том, что антигены, не адсорбированные на адъюванте фосфата алюминия, получают центрифугированием и анализируют их содержание для расчёта степени адсорбции.
[0083] Анализ содержания антигена: принцип обнаружения заключается в том, что содержание активного антигена, способного связываться с рекомбинантным антителом, нейтрализующим папилломавирус человека, измеряют с помощью ИФА, и сравнивают стабильность каждого препарата путём сравнения соотношения содержания активного антигена в каждом момент времени с моментом T0. Чем выше соотношение, тем выше содержание активного антигена в препарате и тем лучше сохраняется активность.
[0084] Результаты испытаний приведены в Таблицах 5-6 и на Фиг. 3-4.
[0085] Результаты испытаний показали, что степень адсорбции трёх вакцинных препаратов вирусоподобных частиц папилломавируса была выше 99%, а тенденции изменения содержания антигена вакцин вирусоподобных частиц папилломавируса в F1 и F2 были лучше, чем у препарата F3, что то есть стабильность F1 и F2 была лучше, чем у F3.
[0086] Пример 3: Скрининговое исследование концентрации регулятора осмотического давления
[0087] Состав вакцинного препарата вирусоподобных частиц папилломавируса согласно настоящему примеру приведен в следующей Таблице:
[0088] Способ приготовления препарата вакцины вирусоподобных частиц папилломавируса:
[0089] Брали определённое количество вирусоподобных частиц ПВЧ 18, соответствующих препарату, а затем смешивали его с адъювантом фосфата алюминия и адсорбировали в течение ночи при 4 °C, так чтобы рН, соответствующие концентрации вирусоподобных частиц папилломавируса, адъювант фосфата алюминия, гистидина, хлорида натрия и полисорбата 80 в препарате вакцины с вирусоподобными частицами против папилломавируса, соответствовали требованиям Таблицы 7, дозировали его в аликвотах. Маркировали его соответствующими номерами, помещали образцы в инкубатор при 37 °С и доставали для анализа степени адсорбции и содержания антигена на 0-й неделе, а также для анализа содержания антигена на 1-й, 2-й и 4-й неделях.
[0090] Аналитический метод исследования:
[0091] Анализ степени адсорбции: принцип обнаружения заключается в том, что антигены, не адсорбированные на адъюванте фосфата алюминия, отделяют центрифугированием и анализируют их содержание для расчёта степени адсорбции.
[0092] Анализ содержания антигена: принцип обнаружения заключается в том, что содержание активного антигена, способного связываться с рекомбинантным антителом, нейтрализующим папилломавирус человека, измеряют с помощью ИФА, и стабильность каждого препарата сравнивают путём сравнения соотношения содержания активного антигена в каждый момент времени с моментом T0. Чем выше соотношение, тем выше содержание активного антигена в препарате и тем лучше сохраняется активность.
[0093] Результаты испытаний приведены в Таблицах 8-9 и на Фиг. 5-6.
[0094] Результаты испытаний показали, что степень адсорбции двух препаратов вакцины вирусоподобных частиц папилломавируса превышала 99%. Не было существенной разницы в изменении содержания активного антигена в препаратах F1 и F2 через 4 недели при 37 °C, то есть стабильность F1 и F2 была сопоставима.
[0095] Пример 4: скрининговое исследование концентрации буфера
[0096] Состав препарата вакцины вирусоподобных частиц папилломавируса согласно настоящему примеру приведён в следующей Таблице.:
[0097] Способ приготовления препарата вакцины вирусоподобных частиц папилломавируса:
[0098] Брали определённое количество вирусоподобных частиц ПВЧ 18, соответствующих препарату, а затем смешивали его с адъювантом фосфата алюминия и адсорбировали в течение ночи при 4 °C, так чтобы рН, соответствующие концентрации вирусоподобных частиц папилломавируса, адъюванта фосфата алюминия, гистидина, хлорида натрия и полисорбата 80 в препарат вакцины вирусоподобных частиц против папилломавируса соответствовали требованиям Таблицы 10, дозировали его в аликвотах. Маркировали его соответствующими номерами, помещали образцы в инкубатор при 37 °С и доставали для анализа степени адсорбции и содержания антигена на 0-й неделе, а также для анализа содержания антигена на 1-й, 2-й и 4-й неделях.
[0099] Аналитический метод исследования:
[00100] Анализ степени адсорбции: принцип обнаружения заключается в том, что антигены, не адсорбированные на адъюванте фосфата алюминия, отделяют центрифугированием, и их содержание анализируют для расчёта степени адсорбции.
[00101] Анализ содержания антигена: принцип обнаружения заключается в том, что содержание активного антигена, способного связываться с рекомбинантным антителом, нейтрализующим папилломавирус человека, измеряют с помощью ИФА, и сравнивают стабильность каждого препарата путём сравнения соотношения содержания активного антигена в каждый момент времени с моментом T0. Чем выше соотношение, тем выше содержание активного антигена в препарате и тем лучше сохраняется активность.
[00102] Результаты испытаний приведены в Таблицах 11-12 и на Фиг. 7-8.
[00103] Результаты испытаний показали, что степень адсорбции трёх вакцинных препаратов вирусоподобных частиц папилломавируса была выше 99%, а тенденции изменения содержания антигена в вакцинах вирусоподобных частиц папилломавируса в F1 и F2 были лучше, чем у препарата F3, что то есть стабильность F1 и F2 была лучше, чем у F3.
[00104] Пример 5: Исследование для подтверждения состава каждого отдельного типа (тип 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) вирусоподобных частиц вакцины против папилломавируса
[00105] Каждый отдельный тип (тип 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59) вакцинных препаратов вирусоподобных частиц папилломавируса (препарат: 0,74 мг/мл вирусоподобных частиц папилломавируса +1,0 мг/мл адъюванта фосфата алюминия +18 мМ гистидиновый буфер +320 мМ хлорид натрия при рН 6,2) подвергали мониторингу стабильности при 2-8 °С, соответственно. При этом вакцина содержала полисорбат 80 в концентрации не более 0,3мг/мл за счёт остатков, образовавшихся в процессе получения препарата. Точки времени мониторинга составляли 3 м (3 месяца), 6 м (6 месяцев), 9 м (9 месяцев) и 12 м (12 месяцев), при этом контролировали степень адсорбции и относительную активность in vitro.
[00106] Аналитический метод исследования:
[00107] Анализ степени адсорбции: принцип обнаружения заключается в том, что антигены, не адсорбированные на адъюванте фосфата алюминия, отделяют центрифугированием, и их содержание анализируют для расчёта степени адсорбции.
[00108] Относительная активность in vitro: принцип обнаружения этого метода заключается в определении ЕС50 анализируемого образца и положительного контроля с помощью рекомбинантного антитела, нейтрализующего папилломавирус человека, соответственно, а затем в расчёте его процентного отношения ЕС50. Чем выше значение, тем выше относительная эффективность in vitro и выше качество тестируемого образца.
[00109] Результаты экспериментов показаны в Таблица 13.
[00110] Экспериментальные результаты демонстрируют, что каждый отдельный тип препаратов вакцины вирусоподобных частиц папилломавируса, раскрытых в настоящем изобретении, обладает хорошей стабильностью и может стабильно храниться в течение по меньшей мере 12 месяцев при температуре 2-8 °C.
Таблица 13. Данные стабильности всех 14 отдельных типов (6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59) вирусоподобных частиц папилломавируса в жидкой композиции с адсорбцией на адъюванте.
in vitro, %
[00111] Пример 6. Получение и подтверждение состава 14-валентной вакцины против папилломавируса человека (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59)
[00112] Способ получения 14-валентной вакцины против папилломавируса человека (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59):
[00113] Каждый отдельный тип (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59) препарата вакцины вирусоподобной частицы папилломавируса (состав: 0,74 мг/мл вирусоподобной частицы папилломавируса + 1,0 мг/мл адъюванта фосфата алюминия + 18мМ гистидиновый буфер + 320мМ хлорид натрия, значение рН: 6,2), соответственно, брали и смешивали в определённом объёмном соотношении (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 = 1,5:2:3:2:1:1:1:1:1:1:1:1:1:1) для получения полуфабриката 14-валентной вакцины против папилломавируса человека (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) с соответствующими концентрациями 0,06 мг/мл, 0,08 мг/мл, 0,12 мг/мл, 0,08 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл, 0,04 мг/мл каждого типа вирусоподобных частиц, соответственно; затем разливали во флаконы с пенициллином, которые затем закупоривали, закрывали крышкой и маркировали для приготовления рекомбинантной 14-валентной вакцины против вируса папилломы человека (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59), при этом вакцина содержала полисорбат 80 в концентрации не более 0,3 мг/мл за счет, полученных в процессе получения препарата. Затем проводили мониторинг стабильности при 2-8 °C (моменты времени 3, 6, 9, 12, 18 и 24 месяца) и 25±2 °C (моменты времени 2 недели, 4 недели, 8 недель и 16 недель), и контролировали относительную эффективность и степень адсорбции in vitro.
[00114] Аналитический метод исследования:
[00115] Анализ степени адсорбции: принцип обнаружения заключается в том, что антигены, не адсорбированные на адъюванте фосфата алюминия, отделяют центрифугированием, и их содержание анализируют для расчёта степени адсорбции.
[00116] Анализ содержания антигена: принцип обнаружения заключается в том, что содержание активного антигена, способного связываться с рекомбинантным антителом, нейтрализующим папилломавирус человека, измеряют с помощью ИФА, и сравнивают стабильность каждого препарата путём сравнения соотношения содержания активного антигена в каждый момент времени с моментом T0. Чем выше соотношение, тем выше содержание активного антигена в препарате и тем лучше сохраняется активность.
[00117] Результаты эксперимента приведены в Таблицах 14-17.
[00118]
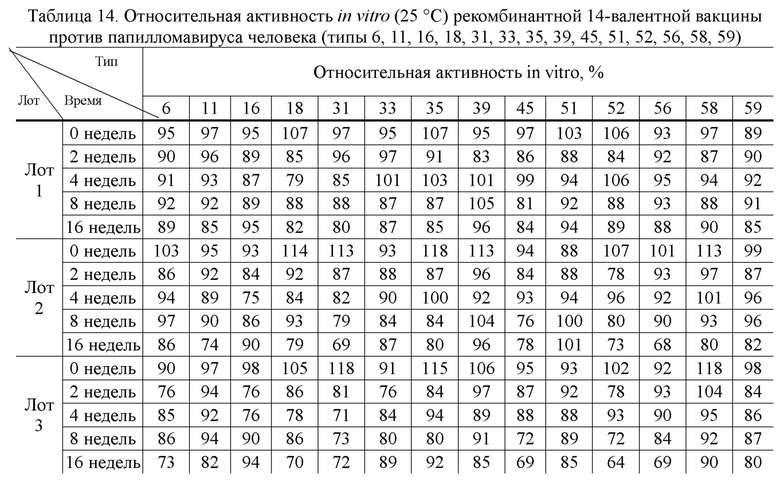
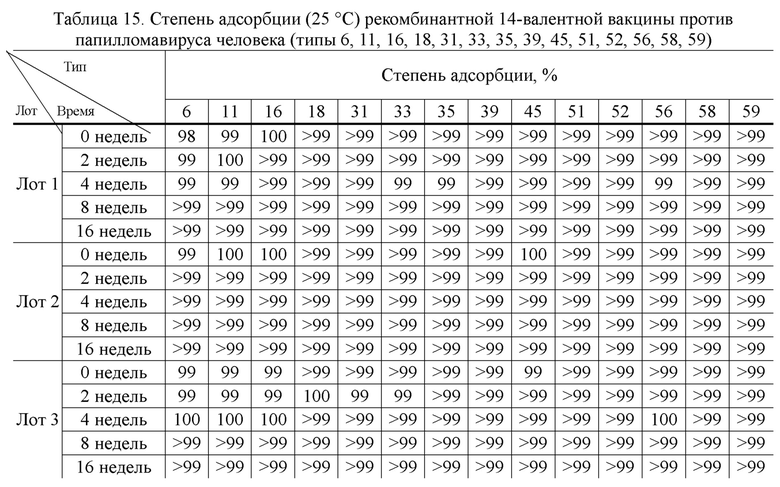
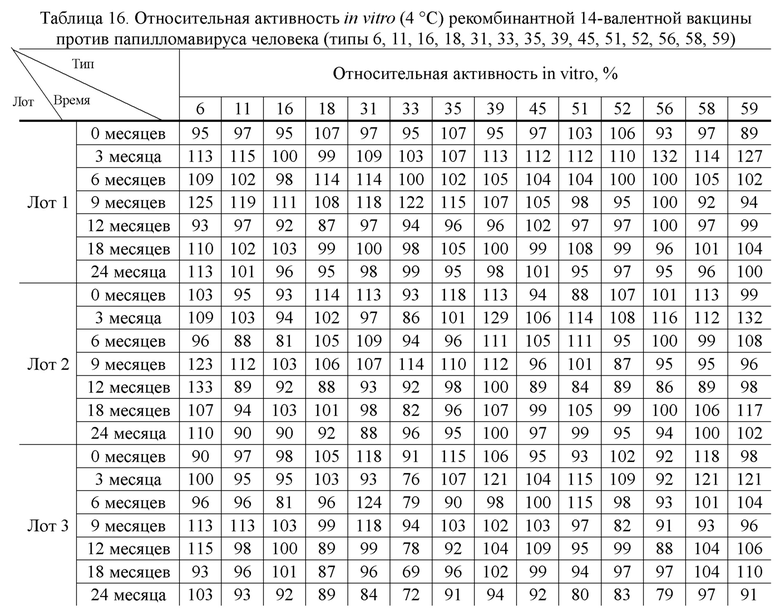
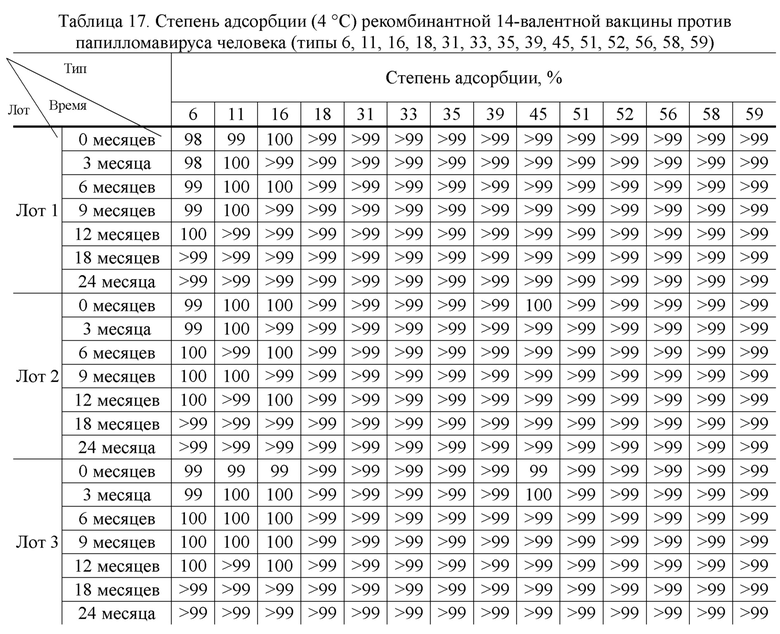
[00119] Результаты эксперимента показывают, что 14-валентная вакцина против папилломавируса человека (типы 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59), раскрытая в настоящем изобретении, обладает хорошей стабильностью и может стабильно храниться не менее 24 месяцев при температуре 2 - 8 °С и не менее 16 недель при температуре 25 °С.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SINOCELLTECH
<120> СТАБИЛЬНЫЙ ПРЕПАРАТ ВАКЦИНЫ ИЗ ВИРУСОПОДОБНЫХ ЧАСТИЦ ПАПИЛЛОМАВИРУСА
ЧЕЛОВЕКА
<130> PCT74213SXB
<160> 41
<170> PatentIn version 3.3
<210> 1
<211> 26
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 1
Lys Ala Lys Pro Lys Leu Lys Arg Ala Ala Pro Thr Ser Thr Arg Thr
1 5 10 15
Ser Ser Ala Lys Arg Lys Lys Val Lys Lys
20 25
<210> 2
<211> 31
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 2
Leu Gln Ala Gly Leu Lys Ala Lys Pro Lys Leu Lys Arg Ala Ala Pro
1 5 10 15
Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys Val Lys Lys
20 25 30
<210> 3
<211> 38
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 3
Leu Gln Leu Gly Ala Arg Pro Lys Pro Thr Ile Gly Pro Arg Lys Arg
1 5 10 15
Ala Ala Pro Ala Pro Thr Ser Thr Pro Ser Pro Lys Arg Val Lys Arg
20 25 30
Arg Lys Ser Ser Arg Lys
35
<210> 4
<211> 469
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 4
Met Trp Arg Pro Ser Asp Ser Thr Val Tyr Val Pro Pro Pro Asn Pro
1 5 10 15
Val Ser Lys Val Val Ala Thr Asp Ala Tyr Val Thr Arg Thr Asn Ile
20 25 30
Phe Tyr His Ala Ser Ser Ser Arg Leu Leu Ala Val Gly His Pro Tyr
35 40 45
Phe Ser Ile Lys Arg Ala Asn Lys Thr Val Val Pro Lys Val Ser Gly
50 55 60
Tyr Gln Tyr Arg Val Phe Lys Val Val Leu Pro Asp Pro Asn Lys Phe
65 70 75 80
Ala Leu Pro Asp Ser Ser Leu Phe Asp Pro Thr Thr Gln Arg Leu Val
85 90 95
Trp Ala Cys Thr Gly Leu Glu Val Gly Arg Gly Gln Pro Leu Gly Val
100 105 110
Gly Val Ser Gly His Pro Phe Leu Asn Lys Tyr Asp Asp Val Glu Asn
115 120 125
Ser Gly Ser Gly Gly Asn Pro Gly Gln Asp Asn Arg Val Asn Val Gly
130 135 140
Met Asp Tyr Lys Gln Thr Gln Leu Cys Met Val Gly Cys Ala Pro Pro
145 150 155 160
Leu Gly Glu His Trp Gly Lys Gly Lys Gln Cys Thr Asn Thr Pro Val
165 170 175
Gln Ala Gly Asp Cys Pro Pro Leu Glu Leu Ile Thr Ser Val Ile Gln
180 185 190
Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met Asn Phe Ala Asp
195 200 205
Leu Gln Thr Asn Lys Ser Asp Val Pro Ile Asp Ile Cys Gly Thr Thr
210 215 220
Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ala Ala Asp Pro Tyr Gly Asp
225 230 235 240
Arg Leu Phe Phe Phe Leu Arg Lys Glu Gln Met Phe Ala Arg His Phe
245 250 255
Phe Asn Arg Ala Gly Glu Val Gly Glu Pro Val Pro Asp Thr Leu Ile
260 265 270
Ile Lys Gly Ser Gly Asn Arg Thr Ser Val Gly Ser Ser Ile Tyr Val
275 280 285
Asn Thr Pro Ser Gly Ser Leu Val Ser Ser Glu Ala Gln Leu Phe Asn
290 295 300
Lys Pro Tyr Trp Leu Gln Lys Ala Gln Gly His Asn Asn Gly Ile Cys
305 310 315 320
Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr Thr Arg Ser Thr
325 330 335
Asn Met Thr Leu Cys Ala Ser Val Thr Thr Ser Ser Thr Tyr Thr Asn
340 345 350
Ser Asp Tyr Lys Glu Tyr Met Arg His Val Glu Glu Tyr Asp Leu Gln
355 360 365
Phe Ile Phe Gln Leu Cys Ser Ile Thr Leu Ser Ala Glu Val Met Ala
370 375 380
Tyr Ile His Thr Met Asn Pro Ser Val Leu Glu Asp Trp Asn Phe Gly
385 390 395 400
Leu Ser Pro Pro Pro Asn Gly Thr Leu Glu Asp Thr Tyr Arg Tyr Val
405 410 415
Gln Ser Gln Ala Ile Thr Cys Gln Lys Pro Thr Pro Glu Lys Glu Lys
420 425 430
Pro Asp Pro Tyr Lys Asn Leu Ser Phe Trp Glu Val Asn Leu Lys Glu
435 440 445
Lys Phe Ser Ser Glu Leu Asp Gln Tyr Pro Leu Gly Arg Lys Phe Leu
450 455 460
Leu Gln Ser Gly Tyr
465
<210> 5
<211> 470
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 5
Met Trp Arg Pro Ser Asp Ser Thr Val Tyr Val Pro Pro Pro Asn Pro
1 5 10 15
Val Ser Lys Val Val Ala Thr Asp Ala Tyr Val Lys Arg Thr Asn Ile
20 25 30
Phe Tyr His Ala Ser Ser Ser Arg Leu Leu Ala Val Gly His Pro Tyr
35 40 45
Tyr Ser Ile Lys Lys Val Asn Lys Thr Val Val Pro Lys Val Ser Gly
50 55 60
Tyr Gln Tyr Arg Val Phe Lys Val Val Leu Pro Asp Pro Asn Lys Phe
65 70 75 80
Ala Leu Pro Asp Ser Ser Leu Phe Asp Pro Thr Thr Gln Arg Leu Val
85 90 95
Trp Ala Cys Thr Gly Leu Glu Val Gly Arg Gly Gln Pro Leu Gly Val
100 105 110
Gly Val Ser Gly His Pro Leu Leu Asn Lys Tyr Asp Asp Val Glu Asn
115 120 125
Ser Gly Gly Tyr Gly Gly Asn Pro Gly Gln Asp Asn Arg Val Asn Val
130 135 140
Gly Met Asp Tyr Lys Gln Thr Gln Leu Cys Met Val Gly Cys Ala Pro
145 150 155 160
Pro Leu Gly Glu His Trp Gly Lys Gly Thr Gln Cys Ser Asn Thr Ser
165 170 175
Val Gln Asn Gly Asp Cys Pro Pro Leu Glu Leu Ile Thr Ser Val Ile
180 185 190
Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met Asn Phe Ala
195 200 205
Asp Leu Gln Thr Asn Lys Ser Asp Val Pro Leu Asp Ile Cys Gly Thr
210 215 220
Val Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ala Ala Asp Pro Tyr Gly
225 230 235 240
Asp Arg Leu Phe Phe Tyr Leu Arg Lys Glu Gln Met Phe Ala Arg His
245 250 255
Phe Phe Asn Arg Ala Gly Thr Val Gly Glu Pro Val Pro Asp Asp Leu
260 265 270
Leu Val Lys Gly Gly Asn Asn Arg Ser Ser Val Ala Ser Ser Ile Tyr
275 280 285
Val His Thr Pro Ser Gly Ser Leu Val Ser Ser Glu Ala Gln Leu Phe
290 295 300
Asn Lys Pro Tyr Trp Leu Gln Lys Ala Gln Gly His Asn Asn Gly Ile
305 310 315 320
Cys Trp Gly Asn His Leu Phe Val Thr Val Val Asp Thr Thr Arg Ser
325 330 335
Thr Asn Met Thr Leu Cys Ala Ser Val Ser Lys Ser Ala Thr Tyr Thr
340 345 350
Asn Ser Asp Tyr Lys Glu Tyr Met Arg His Val Glu Glu Phe Asp Leu
355 360 365
Gln Phe Ile Phe Gln Leu Cys Ser Ile Thr Leu Ser Ala Glu Val Met
370 375 380
Ala Tyr Ile His Thr Met Asn Pro Ser Val Leu Glu Asp Trp Asn Phe
385 390 395 400
Gly Leu Ser Pro Pro Pro Asn Gly Thr Leu Glu Asp Thr Tyr Arg Tyr
405 410 415
Val Gln Ser Gln Ala Ile Thr Cys Gln Lys Pro Thr Pro Glu Lys Glu
420 425 430
Lys Gln Asp Pro Tyr Lys Asp Met Ser Phe Trp Glu Val Asn Leu Lys
435 440 445
Glu Lys Phe Ser Ser Glu Leu Asp Gln Phe Pro Leu Gly Arg Lys Phe
450 455 460
Leu Leu Gln Ser Gly Tyr
465 470
<210> 6
<211> 474
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 6
Met Ser Leu Trp Leu Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ala Arg Thr Asn
20 25 30
Ile Tyr Tyr His Ala Gly Thr Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Phe Pro Ile Lys Lys Pro Asn Asn Asn Lys Ile Leu Val Pro Lys
50 55 60
Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Ile His Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Asp Thr Gln
85 90 95
Arg Leu Val Trp Ala Cys Val Gly Val Glu Val Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Leu Asp Asp
115 120 125
Thr Glu Asn Ala Ser Ala Tyr Ala Ala Asn Ala Gly Val Asp Asn Arg
130 135 140
Glu Cys Ile Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Ile Gly
145 150 155 160
Cys Lys Pro Pro Ile Gly Glu His Trp Gly Lys Gly Ser Pro Cys Thr
165 170 175
Asn Val Ala Val Asn Pro Gly Asp Cys Pro Pro Leu Glu Leu Ile Asn
180 185 190
Thr Val Ile Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met
195 200 205
Asp Phe Thr Thr Leu Gln Ala Asn Lys Ser Glu Val Pro Leu Asp Ile
210 215 220
Cys Thr Ser Ile Cys Lys Tyr Pro Asp Tyr Ile Lys Met Val Ser Glu
225 230 235 240
Pro Tyr Gly Asp Ser Leu Phe Phe Tyr Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Leu Phe Asn Arg Ala Gly Ala Val Gly Glu Asn Val Pro
260 265 270
Asp Asp Leu Tyr Ile Lys Gly Ser Gly Ser Thr Ala Asn Leu Ala Ser
275 280 285
Ser Asn Tyr Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Asp Ala
290 295 300
Gln Ile Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Met Ser Leu Cys Ala Ala Ile Ser Thr Ser Glu
340 345 350
Thr Thr Tyr Lys Asn Thr Asn Phe Lys Glu Tyr Leu Arg His Gly Glu
355 360 365
Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu Thr
370 375 380
Ala Asp Val Met Thr Tyr Ile His Ser Met Asn Ser Thr Ile Leu Glu
385 390 395 400
Asp Trp Asn Phe Gly Leu Gln Pro Pro Pro Gly Gly Thr Leu Glu Asp
405 410 415
Thr Tyr Arg Phe Val Thr Ser Gln Ala Ile Ala Cys Gln Lys His Thr
420 425 430
Pro Pro Ala Pro Lys Glu Asp Pro Leu Lys Lys Tyr Thr Phe Trp Glu
435 440 445
Val Asn Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu
450 455 460
Gly Arg Lys Phe Leu Leu Gln Ala Gly Leu
465 470
<210> 7
<211> 470
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 7
Met Ala Leu Trp Arg Pro Ser Asp Asn Thr Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Arg Val Val Asn Thr Asp Asp Tyr Val Thr Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Thr Val Gly Asn Pro
35 40 45
Tyr Phe Arg Val Pro Ala Gly Gly Gly Asn Lys Gln Asp Ile Pro Lys
50 55 60
Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Gln Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Leu Pro Asp Thr Ser Ile Tyr Asn Pro Glu Thr Gln
85 90 95
Arg Leu Val Trp Ala Cys Ala Gly Val Glu Ile Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Leu Ser Gly His Pro Phe Tyr Asn Lys Leu Asp Asp
115 120 125
Thr Glu Ser Ser His Ala Ala Thr Ser Asn Val Ser Glu Asp Val Arg
130 135 140
Asp Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Leu Gly
145 150 155 160
Cys Ala Pro Ala Ile Gly Glu His Trp Ala Lys Gly Thr Ala Cys Lys
165 170 175
Ser Arg Pro Leu Ser Gln Gly Asp Cys Pro Pro Leu Glu Leu Lys Asn
180 185 190
Thr Val Leu Glu Asp Gly Asp Met Val Asp Thr Gly Tyr Gly Ala Met
195 200 205
Asp Phe Ser Thr Leu Gln Asp Thr Lys Cys Glu Val Pro Leu Asp Ile
210 215 220
Cys Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala Asp
225 230 235 240
Pro Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Leu Phe
245 250 255
Ala Arg His Phe Trp Asn Arg Ala Gly Thr Met Gly Asp Thr Val Pro
260 265 270
Gln Ser Leu Tyr Ile Lys Gly Thr Gly Met Arg Ala Ser Pro Gly Ser
275 280 285
Cys Val Tyr Ser Pro Ser Pro Ser Gly Ser Ile Val Thr Ser Asp Ser
290 295 300
Gln Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln Gly His Asn
305 310 315 320
Asn Gly Val Cys Trp His Asn Gln Leu Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Leu Thr Ile Cys Ala Ser Thr Gln Ser Pro Val
340 345 350
Pro Gly Gln Tyr Asp Ala Thr Lys Phe Lys Gln Tyr Ser Arg His Val
355 360 365
Glu Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Thr Ile Thr Leu
370 375 380
Thr Ala Asp Val Met Ser Tyr Ile His Ser Met Asn Ser Ser Ile Leu
385 390 395 400
Glu Asp Trp Asn Phe Gly Val Pro Pro Pro Pro Thr Thr Ser Leu Val
405 410 415
Asp Thr Tyr Arg Phe Val Gln Ser Val Ala Ile Thr Cys Gln Lys Asp
420 425 430
Ala Ala Pro Ala Glu Asn Lys Asp Pro Tyr Asp Lys Leu Lys Phe Trp
435 440 445
Asn Val Asp Leu Lys Glu Lys Phe Ser Leu Asp Leu Asp Gln Tyr Pro
450 455 460
Leu Gly Arg Lys Phe Leu
465 470
<210> 8
<211> 475
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 8
Met Ser Leu Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Thr Arg Thr Asn
20 25 30
Ile Tyr Tyr His Ala Gly Ser Ala Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Tyr Ser Ile Pro Lys Ser Asp Asn Pro Lys Lys Ile Val Val Pro
50 55 60
Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Glu Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Leu Glu Val Gly Arg Gly Gln
100 105 110
Pro Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Phe Asp
115 120 125
Asp Thr Glu Asn Ser Asn Arg Tyr Ala Gly Gly Pro Gly Thr Asp Asn
130 135 140
Arg Glu Cys Ile Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Leu
145 150 155 160
Gly Cys Lys Pro Pro Ile Gly Glu His Trp Gly Lys Gly Ser Pro Cys
165 170 175
Ser Asn Asn Ala Ile Thr Pro Gly Asp Cys Pro Pro Leu Glu Leu Lys
180 185 190
Asn Ser Val Ile Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala
195 200 205
Met Asp Phe Thr Ala Leu Gln Asp Thr Lys Ser Asn Val Pro Leu Asp
210 215 220
Ile Cys Asn Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Lys Met Val Ala
225 230 235 240
Glu Pro Tyr Gly Asp Thr Leu Phe Phe Tyr Leu Arg Arg Glu Gln Met
245 250 255
Phe Val Arg His Phe Phe Asn Arg Ser Gly Thr Val Gly Glu Ser Val
260 265 270
Pro Thr Asp Leu Tyr Ile Lys Gly Ser Gly Ser Thr Ala Thr Leu Ala
275 280 285
Asn Ser Thr Tyr Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Asp
290 295 300
Ala Gln Ile Phe Asn Lys Pro Tyr Trp Met Gln Arg Ala Gln Gly His
305 310 315 320
Asn Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp
325 330 335
Thr Thr Arg Ser Thr Asn Met Ser Val Cys Ala Ala Ile Ala Asn Ser
340 345 350
Asp Thr Thr Phe Lys Ser Ser Asn Phe Lys Glu Tyr Leu Arg His Gly
355 360 365
Glu Glu Phe Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu
370 375 380
Ser Ala Asp Ile Met Thr Tyr Ile His Ser Met Asn Pro Ala Ile Leu
385 390 395 400
Glu Asp Trp Asn Phe Gly Leu Thr Thr Pro Pro Ser Gly Ser Leu Glu
405 410 415
Asp Thr Tyr Arg Phe Val Thr Ser Gln Ala Ile Thr Cys Gln Lys Ser
420 425 430
Ala Pro Gln Lys Pro Lys Glu Asp Pro Phe Lys Asp Tyr Val Phe Trp
435 440 445
Glu Val Asn Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro
450 455 460
Leu Gly Arg Lys Phe Leu Leu Gln Ala Gly Tyr
465 470 475
<210> 9
<211> 472
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 9
Met Ser Leu Trp Arg Ser Asn Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Ser Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Thr Arg Thr Asn
20 25 30
Ile Tyr Tyr His Ala Gly Ser Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Tyr Ala Ile Lys Lys Gln Asp Ser Asn Lys Ile Ala Val Pro Lys
50 55 60
Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Lys Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asp Pro Ala Ser Gln
85 90 95
Arg Leu Val Trp Ala Cys Thr Gly Val Glu Val Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Leu Asp Asp
115 120 125
Thr Glu Asn Ser Asn Lys Tyr Val Gly Asn Ser Gly Thr Asp Asn Arg
130 135 140
Glu Cys Ile Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Ile Gly
145 150 155 160
Cys Arg Pro Pro Ile Gly Glu His Trp Gly Lys Gly Thr Pro Cys Asn
165 170 175
Ala Asn Gln Val Lys Ala Gly Glu Cys Pro Pro Leu Glu Leu Leu Asn
180 185 190
Thr Val Leu Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met
195 200 205
Asp Phe Thr Thr Leu Gln Ala Asn Lys Ser Asp Val Pro Leu Asp Ile
210 215 220
Cys Ser Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Lys Met Val Ser Glu
225 230 235 240
Pro Tyr Gly Asp Met Leu Phe Phe Tyr Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Leu Phe Asn Arg Ala Gly Thr Val Gly Glu Thr Val Pro
260 265 270
Ala Asp Leu Tyr Ile Lys Gly Thr Thr Gly Thr Leu Pro Ser Thr Ser
275 280 285
Tyr Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Asp Ala Gln Ile
290 295 300
Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn Asn Gly
305 310 315 320
Ile Cys Trp Ser Asn Gln Leu Phe Val Thr Val Val Asp Thr Thr Arg
325 330 335
Ser Thr Asn Met Ser Val Cys Ser Ala Val Ser Ser Ser Asp Ser Thr
340 345 350
Tyr Lys Asn Asp Asn Phe Lys Glu Tyr Leu Arg His Gly Glu Glu Tyr
355 360 365
Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu Thr Ala Asp
370 375 380
Val Met Thr Tyr Ile His Ser Met Asn Pro Ser Ile Leu Glu Asp Trp
385 390 395 400
Asn Phe Gly Leu Thr Pro Pro Pro Ser Gly Thr Leu Glu Asp Thr Tyr
405 410 415
Arg Tyr Val Thr Ser Gln Ala Val Thr Cys Gln Lys Pro Ser Ala Pro
420 425 430
Lys Pro Lys Asp Asp Pro Leu Lys Asn Tyr Thr Phe Trp Glu Val Asp
435 440 445
Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu Gly Arg
450 455 460
Lys Phe Leu Leu Gln Ala Gly Leu
465 470
<210> 10
<211> 469
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 10
Met Ala Met Trp Arg Ser Ser Asp Ser Met Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Lys Val Val Asn Thr Asp Asp Tyr Val Thr Arg Thr Gly
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Phe Lys Val Gly Met Asn Gly Gly Arg Lys Gln Asp Ile Pro Lys
50 55 60
Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Thr Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Ser Ile Pro Asp Ala Ser Leu Tyr Asn Pro Glu Thr Gln
85 90 95
Arg Leu Val Trp Ala Cys Val Gly Val Glu Val Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Ile Ser Gly His Pro Leu Tyr Asn Arg Gln Asp Asp
115 120 125
Thr Glu Asn Ser Pro Phe Ser Ser Thr Thr Asn Lys Asp Ser Arg Asp
130 135 140
Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Ile Gly Cys
145 150 155 160
Val Pro Ala Ile Gly Glu His Trp Gly Lys Gly Lys Ala Cys Lys Pro
165 170 175
Asn Asn Val Ser Thr Gly Asp Cys Pro Pro Leu Glu Leu Val Asn Thr
180 185 190
Pro Ile Glu Asp Gly Asp Met Ile Asp Thr Gly Tyr Gly Ala Met Asp
195 200 205
Phe Gly Ala Leu Gln Glu Thr Lys Ser Glu Val Pro Leu Asp Ile Cys
210 215 220
Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala Asp Val
225 230 235 240
Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Leu Phe Ala
245 250 255
Arg His Phe Trp Asn Arg Gly Gly Met Val Gly Asp Ala Ile Pro Ala
260 265 270
Gln Leu Tyr Ile Lys Gly Thr Asp Ile Arg Ala Asn Pro Gly Ser Ser
275 280 285
Val Tyr Cys Pro Ser Pro Ser Gly Ser Met Val Thr Ser Asp Ser Gln
290 295 300
Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln Gly His Asn Asn
305 310 315 320
Gly Ile Cys Trp His Asn Gln Leu Phe Leu Thr Val Val Asp Thr Thr
325 330 335
Arg Ser Thr Asn Phe Thr Leu Ser Thr Ser Ile Glu Ser Ser Ile Pro
340 345 350
Ser Thr Tyr Asp Pro Ser Lys Phe Lys Glu Tyr Thr Arg His Val Glu
355 360 365
Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Thr Val Thr Leu Thr
370 375 380
Thr Asp Val Met Ser Tyr Ile His Thr Met Asn Ser Ser Ile Leu Asp
385 390 395 400
Asn Trp Asn Phe Ala Val Ala Pro Pro Pro Ser Ala Ser Leu Val Asp
405 410 415
Thr Tyr Arg Tyr Leu Gln Ser Ala Ala Ile Thr Cys Gln Lys Asp Ala
420 425 430
Pro Ala Pro Glu Lys Lys Asp Pro Tyr Asp Gly Leu Lys Phe Trp Asn
435 440 445
Val Asp Leu Arg Glu Lys Phe Ser Leu Glu Leu Asp Gln Phe Pro Leu
450 455 460
Gly Arg Lys Phe Leu
465
<210> 11
<211> 478
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 11
Met Ala Leu Trp Arg Pro Ser Asp Ser Thr Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Arg Val Val Asn Thr Asp Asp Tyr Val Ser Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Thr Val Gly Asn Pro
35 40 45
Tyr Phe Arg Val Val Pro Ser Gly Ala Gly Asn Lys Gln Ala Val Pro
50 55 60
Lys Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Ala Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Leu Pro Asp Ser Thr Ile Tyr Asn Pro Glu Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Met Glu Ile Gly Arg Gly Gln
100 105 110
Pro Leu Gly Ile Gly Leu Ser Gly His Pro Phe Tyr Asn Lys Leu Asp
115 120 125
Asp Thr Glu Ser Ala His Ala Ala Thr Ala Val Ile Thr Gln Asp Val
130 135 140
Arg Asp Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Leu
145 150 155 160
Gly Cys Val Pro Ala Ile Gly Glu His Trp Ala Lys Gly Thr Leu Cys
165 170 175
Lys Pro Ala Gln Leu Gln Pro Gly Asp Cys Pro Pro Leu Glu Leu Lys
180 185 190
Asn Thr Ile Ile Glu Asp Gly Asp Met Val Asp Thr Gly Tyr Gly Ala
195 200 205
Met Asp Phe Ser Thr Leu Gln Asp Thr Lys Cys Glu Val Pro Leu Asp
210 215 220
Ile Cys Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala
225 230 235 240
Asp Pro Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Leu
245 250 255
Phe Ala Arg His Phe Trp Asn Arg Ala Gly Val Met Gly Asp Thr Val
260 265 270
Pro Thr Asp Leu Tyr Ile Lys Gly Thr Ser Ala Asn Met Arg Glu Thr
275 280 285
Pro Gly Ser Cys Val Tyr Ser Pro Ser Pro Ser Gly Ser Ile Thr Thr
290 295 300
Ser Asp Ser Gln Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln
305 310 315 320
Gly His Asn Asn Gly Ile Cys Trp His Asn Gln Leu Phe Val Thr Val
325 330 335
Val Asp Thr Thr Arg Ser Thr Asn Leu Thr Leu Cys Ala Ser Thr Gln
340 345 350
Asn Pro Val Pro Asn Thr Tyr Asp Pro Thr Lys Phe Lys His Tyr Ser
355 360 365
Arg His Val Glu Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Thr
370 375 380
Ile Thr Leu Thr Ala Glu Val Met Ser Tyr Ile His Ser Met Asn Ser
385 390 395 400
Ser Ile Leu Glu Asn Trp Asn Phe Gly Val Pro Pro Pro Pro Thr Thr
405 410 415
Ser Leu Val Asp Thr Tyr Arg Phe Val Gln Ser Val Ala Val Thr Cys
420 425 430
Gln Lys Asp Thr Thr Pro Pro Glu Lys Gln Asp Pro Tyr Asp Lys Leu
435 440 445
Lys Phe Trp Thr Val Asp Leu Lys Glu Lys Phe Ser Ser Asp Leu Asp
450 455 460
Gln Tyr Pro Leu Gly Arg Lys Phe Leu Val Gln Ala Gly Leu
465 470 475
<210> 12
<211> 474
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 12
Met Ala Leu Trp Arg Thr Asn Asp Ser Lys Val Tyr Leu Pro Pro Ala
1 5 10 15
Pro Val Ser Arg Ile Val Asn Thr Glu Glu Tyr Ile Thr Arg Thr Gly
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Ile Thr Leu Gly His Pro
35 40 45
Tyr Phe Pro Ile Pro Lys Thr Ser Thr Arg Ala Ala Ile Pro Lys Val
50 55 60
Ser Ala Phe Gln Tyr Arg Val Phe Arg Val Gln Leu Pro Asp Pro Asn
65 70 75 80
Lys Phe Gly Leu Pro Asp Pro Asn Leu Tyr Asn Pro Asp Thr Asp Arg
85 90 95
Leu Val Trp Gly Cys Val Gly Val Glu Val Gly Arg Gly Gln Pro Leu
100 105 110
Gly Val Gly Leu Ser Gly His Pro Leu Phe Asn Lys Tyr Asp Asp Thr
115 120 125
Glu Asn Ser Arg Ile Ala Asn Gly Asn Ala Gln Gln Asp Val Arg Asp
130 135 140
Asn Thr Ser Val Asp Asn Lys Gln Thr Gln Leu Cys Ile Ile Gly Cys
145 150 155 160
Ala Pro Pro Ile Gly Glu His Trp Gly Ile Gly Thr Thr Cys Lys Asn
165 170 175
Thr Pro Val Pro Pro Gly Asp Cys Pro Pro Leu Glu Leu Val Ser Ser
180 185 190
Val Ile Gln Asp Gly Asp Met Ile Asp Thr Gly Phe Gly Ala Met Asp
195 200 205
Phe Ala Ala Leu Gln Ala Thr Lys Ser Asp Val Pro Leu Asp Ile Ser
210 215 220
Gln Ser Val Cys Lys Tyr Pro Asp Tyr Leu Lys Met Ser Ala Asp Thr
225 230 235 240
Tyr Gly Asn Ser Met Phe Phe His Leu Arg Arg Glu Gln Ile Phe Ala
245 250 255
Arg His Tyr Tyr Asn Lys Leu Val Gly Val Gly Glu Asp Ile Pro Asn
260 265 270
Asp Tyr Tyr Ile Lys Gly Ser Gly Asn Gly Arg Asp Pro Ile Glu Ser
275 280 285
Tyr Ile Tyr Ser Ala Thr Pro Ser Gly Ser Met Ile Thr Ser Asp Ser
290 295 300
Gln Ile Phe Asn Lys Pro Tyr Trp Leu His Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Asn Asn Gln Leu Phe Ile Thr Cys Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Leu Thr Ile Ser Thr Ala Thr Ala Ala Val Ser
340 345 350
Pro Thr Phe Thr Pro Ser Asn Phe Lys Gln Tyr Ile Arg His Gly Glu
355 360 365
Glu Tyr Glu Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu Thr
370 375 380
Thr Glu Val Met Ala Tyr Leu His Thr Met Asp Pro Thr Ile Leu Glu
385 390 395 400
Gln Trp Asn Phe Gly Leu Thr Leu Pro Pro Ser Ala Ser Leu Glu Asp
405 410 415
Ala Tyr Arg Phe Val Arg Asn Ala Ala Thr Ser Cys Gln Lys Asp Thr
420 425 430
Pro Pro Gln Ala Lys Pro Asp Pro Leu Ala Lys Tyr Lys Phe Trp Asp
435 440 445
Val Asp Leu Lys Glu Arg Phe Ser Leu Asp Leu Asp Gln Phe Ala Leu
450 455 460
Gly Arg Lys Phe Leu Leu Gln Val Gly Val
465 470
<210> 13
<211> 478
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 13
Met Ser Val Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ser Arg Thr Ser
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Phe Ser Ile Lys Asn Thr Ser Ser Gly Asn Gly Lys Lys Val Leu
50 55 60
Val Pro Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Ile Lys Leu
65 70 75 80
Pro Asp Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro
85 90 95
Glu Thr Gln Arg Leu Val Trp Ala Cys Thr Gly Leu Glu Ile Gly Arg
100 105 110
Gly Gln Pro Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys
115 120 125
Phe Asp Asp Thr Glu Thr Ser Asn Lys Tyr Ala Gly Lys Pro Gly Ile
130 135 140
Asp Asn Arg Glu Cys Leu Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys
145 150 155 160
Ile Leu Gly Cys Lys Pro Pro Ile Gly Glu His Trp Gly Lys Gly Thr
165 170 175
Pro Cys Asn Asn Asn Ser Gly Asn Pro Gly Asp Cys Pro Pro Leu Gln
180 185 190
Leu Ile Asn Ser Val Ile Gln Asp Gly Asp Met Val Asp Thr Gly Phe
195 200 205
Gly Cys Met Asp Phe Asn Thr Leu Gln Ala Ser Lys Ser Asp Val Pro
210 215 220
Ile Asp Ile Cys Ser Ser Val Cys Lys Tyr Pro Asp Tyr Leu Gln Met
225 230 235 240
Ala Ser Glu Pro Tyr Gly Asp Ser Leu Phe Phe Phe Leu Arg Arg Glu
245 250 255
Gln Met Phe Val Arg His Phe Phe Asn Arg Ala Gly Thr Leu Gly Asp
260 265 270
Pro Val Pro Gly Asp Leu Tyr Ile Gln Gly Ser Asn Ser Gly Asn Thr
275 280 285
Ala Thr Val Gln Ser Ser Ala Phe Phe Pro Thr Pro Ser Gly Ser Met
290 295 300
Val Thr Ser Glu Ser Gln Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg
305 310 315 320
Ala Gln Gly His Asn Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val
325 330 335
Thr Val Val Asp Thr Thr Arg Ser Thr Asn Met Thr Leu Cys Ala Glu
340 345 350
Val Lys Lys Glu Ser Thr Tyr Lys Asn Glu Asn Phe Lys Glu Tyr Leu
355 360 365
Arg His Gly Glu Glu Phe Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys
370 375 380
Ile Thr Leu Thr Ala Asp Val Met Thr Tyr Ile His Lys Met Asp Ala
385 390 395 400
Thr Ile Leu Glu Asp Trp Gln Phe Gly Leu Thr Pro Pro Pro Ser Ala
405 410 415
Ser Leu Glu Asp Thr Tyr Arg Phe Val Thr Ser Thr Ala Ile Thr Cys
420 425 430
Gln Lys Asn Thr Pro Pro Lys Gly Lys Glu Asp Pro Leu Lys Asp Tyr
435 440 445
Met Phe Trp Glu Val Asp Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp
450 455 460
Gln Phe Pro Leu Gly Arg Lys Phe Leu Leu Gln Ala Gly Leu
465 470 475
<210> 14
<211> 467
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 14
Met Ala Thr Trp Arg Pro Ser Glu Asn Lys Val Tyr Leu Pro Pro Thr
1 5 10 15
Pro Val Ser Lys Val Val Ala Thr Asp Ser Tyr Val Lys Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Tyr Ser Val Thr Lys Asp Asn Thr Lys Thr Asn Ile Pro Lys Val
50 55 60
Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp Pro Asn
65 70 75 80
Lys Phe Gly Leu Pro Asp Thr Asn Ile Tyr Asn Pro Asp Gln Glu Arg
85 90 95
Leu Val Trp Ala Cys Val Gly Leu Glu Val Gly Arg Gly Gln Pro Leu
100 105 110
Gly Ala Gly Leu Ser Gly His Pro Leu Phe Asn Arg Leu Asp Asp Thr
115 120 125
Glu Ser Ser Asn Leu Ala Asn Asn Asn Val Ile Glu Asp Ser Arg Asp
130 135 140
Asn Ile Ser Val Asp Gly Lys Gln Thr Gln Leu Cys Ile Val Gly Cys
145 150 155 160
Thr Pro Ala Met Gly Glu His Trp Thr Lys Gly Ala Val Cys Lys Ser
165 170 175
Thr Gln Val Thr Thr Gly Asp Cys Pro Pro Leu Ala Leu Ile Asn Thr
180 185 190
Pro Ile Glu Asp Gly Asp Met Ile Asp Thr Gly Phe Gly Ala Met Asp
195 200 205
Phe Lys Val Leu Gln Glu Ser Lys Ala Glu Val Pro Leu Asp Ile Val
210 215 220
Gln Ser Thr Cys Lys Tyr Pro Asp Tyr Leu Lys Met Ser Ala Asp Ala
225 230 235 240
Tyr Gly Asp Ser Met Trp Phe Tyr Leu Arg Arg Glu Gln Leu Phe Ala
245 250 255
Arg His Tyr Phe Asn Arg Ala Gly Lys Val Gly Glu Thr Ile Pro Ala
260 265 270
Glu Leu Tyr Leu Lys Gly Ser Asn Gly Arg Glu Pro Pro Pro Ser Ser
275 280 285
Val Tyr Val Ala Thr Pro Ser Gly Ser Met Ile Thr Ser Glu Ala Gln
290 295 300
Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn Asn
305 310 315 320
Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr Thr
325 330 335
Arg Ser Thr Asn Met Thr Ile Ser Thr Ala Thr Glu Gln Leu Ser Lys
340 345 350
Tyr Asp Ala Arg Lys Ile Asn Gln Tyr Leu Arg His Val Glu Glu Tyr
355 360 365
Glu Leu Gln Phe Val Phe Gln Leu Cys Lys Ile Thr Leu Ser Ala Glu
370 375 380
Val Met Ala Tyr Leu His Asn Met Asn Ala Asn Leu Leu Glu Asp Trp
385 390 395 400
Asn Ile Gly Leu Ser Pro Pro Val Ala Thr Ser Leu Glu Asp Lys Tyr
405 410 415
Arg Tyr Val Arg Ser Thr Ala Ile Thr Cys Gln Arg Glu Gln Pro Pro
420 425 430
Thr Glu Lys Gln Asp Pro Leu Ala Lys Tyr Lys Phe Trp Asp Val Asn
435 440 445
Leu Gln Asp Ser Phe Ser Thr Asp Leu Asp Gln Phe Pro Leu Gly Arg
450 455 460
Lys Phe Leu
465
<210> 15
<211> 473
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 15
Met Ser Val Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ser Arg Thr Ser
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Ala Val Gly Asn Pro
35 40 45
Tyr Phe Ser Ile Lys Ser Pro Asn Asn Asn Lys Lys Val Leu Val Pro
50 55 60
Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Asp Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Leu Glu Ile Gly Arg Gly Gln
100 105 110
Pro Leu Gly Val Gly Val Ser Gly His Pro Tyr Leu Asn Lys Phe Asp
115 120 125
Asp Thr Glu Thr Ser Asn Arg Tyr Pro Ala Gln Pro Gly Ser Asp Asn
130 135 140
Arg Glu Cys Leu Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Ile
145 150 155 160
Gly Cys Lys Pro Pro Thr Gly Glu His Trp Gly Lys Gly Val Ala Cys
165 170 175
Asn Asn Asn Ala Ala Ala Thr Asp Cys Pro Pro Leu Glu Leu Phe Asn
180 185 190
Ser Ile Ile Glu Asp Gly Asp Met Val Asp Thr Gly Phe Gly Cys Met
195 200 205
Asp Phe Gly Thr Leu Gln Ala Asn Lys Ser Asp Val Pro Ile Asp Ile
210 215 220
Cys Asn Ser Thr Cys Lys Tyr Pro Asp Tyr Leu Lys Met Ala Ser Glu
225 230 235 240
Pro Tyr Gly Asp Ser Leu Phe Phe Phe Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Phe Phe Asn Arg Ala Gly Lys Leu Gly Glu Ala Val Pro
260 265 270
Asp Asp Leu Tyr Ile Lys Gly Ser Gly Asn Thr Ala Val Ile Gln Ser
275 280 285
Ser Ala Phe Phe Pro Thr Pro Ser Gly Ser Ile Val Thr Ser Glu Ser
290 295 300
Gln Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Met Thr Leu Cys Thr Glu Val Thr Lys Glu Gly
340 345 350
Thr Tyr Lys Asn Asp Asn Phe Lys Glu Tyr Val Arg His Val Glu Glu
355 360 365
Tyr Asp Leu Gln Phe Val Phe Gln Leu Cys Lys Ile Thr Leu Thr Ala
370 375 380
Glu Ile Met Thr Tyr Ile His Thr Met Asp Ser Asn Ile Leu Glu Asp
385 390 395 400
Trp Gln Phe Gly Leu Thr Pro Pro Pro Ser Ala Ser Leu Gln Asp Thr
405 410 415
Tyr Arg Phe Val Thr Ser Gln Ala Ile Thr Cys Gln Lys Thr Ala Pro
420 425 430
Pro Lys Glu Lys Glu Asp Pro Leu Asn Lys Tyr Thr Phe Trp Glu Val
435 440 445
Asn Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu Gly
450 455 460
Arg Lys Phe Leu Leu Gln Ser Gly Leu
465 470
<210> 16
<211> 495
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 16
Met Trp Arg Pro Ser Asp Ser Thr Val Tyr Val Pro Pro Pro Asn Pro
1 5 10 15
Val Ser Lys Val Val Ala Thr Asp Ala Tyr Val Thr Arg Thr Asn Ile
20 25 30
Phe Tyr His Ala Ser Ser Ser Arg Leu Leu Ala Val Gly His Pro Tyr
35 40 45
Phe Ser Ile Lys Arg Ala Asn Lys Thr Val Val Pro Lys Val Ser Gly
50 55 60
Tyr Gln Tyr Arg Val Phe Lys Val Val Leu Pro Asp Pro Asn Lys Phe
65 70 75 80
Ala Leu Pro Asp Ser Ser Leu Phe Asp Pro Thr Thr Gln Arg Leu Val
85 90 95
Trp Ala Cys Thr Gly Leu Glu Val Gly Arg Gly Gln Pro Leu Gly Val
100 105 110
Gly Val Ser Gly His Pro Phe Leu Asn Lys Tyr Asp Asp Val Glu Asn
115 120 125
Ser Gly Ser Gly Gly Asn Pro Gly Gln Asp Asn Arg Val Asn Val Gly
130 135 140
Met Asp Tyr Lys Gln Thr Gln Leu Cys Met Val Gly Cys Ala Pro Pro
145 150 155 160
Leu Gly Glu His Trp Gly Lys Gly Lys Gln Cys Thr Asn Thr Pro Val
165 170 175
Gln Ala Gly Asp Cys Pro Pro Leu Glu Leu Ile Thr Ser Val Ile Gln
180 185 190
Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met Asn Phe Ala Asp
195 200 205
Leu Gln Thr Asn Lys Ser Asp Val Pro Ile Asp Ile Cys Gly Thr Thr
210 215 220
Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ala Ala Asp Pro Tyr Gly Asp
225 230 235 240
Arg Leu Phe Phe Phe Leu Arg Lys Glu Gln Met Phe Ala Arg His Phe
245 250 255
Phe Asn Arg Ala Gly Glu Val Gly Glu Pro Val Pro Asp Thr Leu Ile
260 265 270
Ile Lys Gly Ser Gly Asn Arg Thr Ser Val Gly Ser Ser Ile Tyr Val
275 280 285
Asn Thr Pro Ser Gly Ser Leu Val Ser Ser Glu Ala Gln Leu Phe Asn
290 295 300
Lys Pro Tyr Trp Leu Gln Lys Ala Gln Gly His Asn Asn Gly Ile Cys
305 310 315 320
Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr Thr Arg Ser Thr
325 330 335
Asn Met Thr Leu Cys Ala Ser Val Thr Thr Ser Ser Thr Tyr Thr Asn
340 345 350
Ser Asp Tyr Lys Glu Tyr Met Arg His Val Glu Glu Tyr Asp Leu Gln
355 360 365
Phe Ile Phe Gln Leu Cys Ser Ile Thr Leu Ser Ala Glu Val Met Ala
370 375 380
Tyr Ile His Thr Met Asn Pro Ser Val Leu Glu Asp Trp Asn Phe Gly
385 390 395 400
Leu Ser Pro Pro Pro Asn Gly Thr Leu Glu Asp Thr Tyr Arg Tyr Val
405 410 415
Gln Ser Gln Ala Ile Thr Cys Gln Lys Pro Thr Pro Glu Lys Glu Lys
420 425 430
Pro Asp Pro Tyr Lys Asn Leu Ser Phe Trp Glu Val Asn Leu Lys Glu
435 440 445
Lys Phe Ser Ser Glu Leu Asp Gln Tyr Pro Leu Gly Arg Lys Phe Leu
450 455 460
Leu Gln Ser Gly Tyr Lys Ala Lys Pro Lys Leu Lys Arg Ala Ala Pro
465 470 475 480
Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys Val Lys Lys
485 490 495
<210> 17
<211> 496
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 17
Met Trp Arg Pro Ser Asp Ser Thr Val Tyr Val Pro Pro Pro Asn Pro
1 5 10 15
Val Ser Lys Val Val Ala Thr Asp Ala Tyr Val Lys Arg Thr Asn Ile
20 25 30
Phe Tyr His Ala Ser Ser Ser Arg Leu Leu Ala Val Gly His Pro Tyr
35 40 45
Tyr Ser Ile Lys Lys Val Asn Lys Thr Val Val Pro Lys Val Ser Gly
50 55 60
Tyr Gln Tyr Arg Val Phe Lys Val Val Leu Pro Asp Pro Asn Lys Phe
65 70 75 80
Ala Leu Pro Asp Ser Ser Leu Phe Asp Pro Thr Thr Gln Arg Leu Val
85 90 95
Trp Ala Cys Thr Gly Leu Glu Val Gly Arg Gly Gln Pro Leu Gly Val
100 105 110
Gly Val Ser Gly His Pro Leu Leu Asn Lys Tyr Asp Asp Val Glu Asn
115 120 125
Ser Gly Gly Tyr Gly Gly Asn Pro Gly Gln Asp Asn Arg Val Asn Val
130 135 140
Gly Met Asp Tyr Lys Gln Thr Gln Leu Cys Met Val Gly Cys Ala Pro
145 150 155 160
Pro Leu Gly Glu His Trp Gly Lys Gly Thr Gln Cys Ser Asn Thr Ser
165 170 175
Val Gln Asn Gly Asp Cys Pro Pro Leu Glu Leu Ile Thr Ser Val Ile
180 185 190
Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met Asn Phe Ala
195 200 205
Asp Leu Gln Thr Asn Lys Ser Asp Val Pro Leu Asp Ile Cys Gly Thr
210 215 220
Val Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ala Ala Asp Pro Tyr Gly
225 230 235 240
Asp Arg Leu Phe Phe Tyr Leu Arg Lys Glu Gln Met Phe Ala Arg His
245 250 255
Phe Phe Asn Arg Ala Gly Thr Val Gly Glu Pro Val Pro Asp Asp Leu
260 265 270
Leu Val Lys Gly Gly Asn Asn Arg Ser Ser Val Ala Ser Ser Ile Tyr
275 280 285
Val His Thr Pro Ser Gly Ser Leu Val Ser Ser Glu Ala Gln Leu Phe
290 295 300
Asn Lys Pro Tyr Trp Leu Gln Lys Ala Gln Gly His Asn Asn Gly Ile
305 310 315 320
Cys Trp Gly Asn His Leu Phe Val Thr Val Val Asp Thr Thr Arg Ser
325 330 335
Thr Asn Met Thr Leu Cys Ala Ser Val Ser Lys Ser Ala Thr Tyr Thr
340 345 350
Asn Ser Asp Tyr Lys Glu Tyr Met Arg His Val Glu Glu Phe Asp Leu
355 360 365
Gln Phe Ile Phe Gln Leu Cys Ser Ile Thr Leu Ser Ala Glu Val Met
370 375 380
Ala Tyr Ile His Thr Met Asn Pro Ser Val Leu Glu Asp Trp Asn Phe
385 390 395 400
Gly Leu Ser Pro Pro Pro Asn Gly Thr Leu Glu Asp Thr Tyr Arg Tyr
405 410 415
Val Gln Ser Gln Ala Ile Thr Cys Gln Lys Pro Thr Pro Glu Lys Glu
420 425 430
Lys Gln Asp Pro Tyr Lys Asp Met Ser Phe Trp Glu Val Asn Leu Lys
435 440 445
Glu Lys Phe Ser Ser Glu Leu Asp Gln Phe Pro Leu Gly Arg Lys Phe
450 455 460
Leu Leu Gln Ser Gly Tyr Lys Ala Lys Pro Lys Leu Lys Arg Ala Ala
465 470 475 480
Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys Val Lys Lys
485 490 495
<210> 18
<211> 500
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 18
Met Ser Leu Trp Leu Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ala Arg Thr Asn
20 25 30
Ile Tyr Tyr His Ala Gly Thr Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Phe Pro Ile Lys Lys Pro Asn Asn Asn Lys Ile Leu Val Pro Lys
50 55 60
Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Ile His Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Asp Thr Gln
85 90 95
Arg Leu Val Trp Ala Cys Val Gly Val Glu Val Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Leu Asp Asp
115 120 125
Thr Glu Asn Ala Ser Ala Tyr Ala Ala Asn Ala Gly Val Asp Asn Arg
130 135 140
Glu Cys Ile Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Ile Gly
145 150 155 160
Cys Lys Pro Pro Ile Gly Glu His Trp Gly Lys Gly Ser Pro Cys Thr
165 170 175
Asn Val Ala Val Asn Pro Gly Asp Cys Pro Pro Leu Glu Leu Ile Asn
180 185 190
Thr Val Ile Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met
195 200 205
Asp Phe Thr Thr Leu Gln Ala Asn Lys Ser Glu Val Pro Leu Asp Ile
210 215 220
Cys Thr Ser Ile Cys Lys Tyr Pro Asp Tyr Ile Lys Met Val Ser Glu
225 230 235 240
Pro Tyr Gly Asp Ser Leu Phe Phe Tyr Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Leu Phe Asn Arg Ala Gly Ala Val Gly Glu Asn Val Pro
260 265 270
Asp Asp Leu Tyr Ile Lys Gly Ser Gly Ser Thr Ala Asn Leu Ala Ser
275 280 285
Ser Asn Tyr Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Asp Ala
290 295 300
Gln Ile Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Met Ser Leu Cys Ala Ala Ile Ser Thr Ser Glu
340 345 350
Thr Thr Tyr Lys Asn Thr Asn Phe Lys Glu Tyr Leu Arg His Gly Glu
355 360 365
Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu Thr
370 375 380
Ala Asp Val Met Thr Tyr Ile His Ser Met Asn Ser Thr Ile Leu Glu
385 390 395 400
Asp Trp Asn Phe Gly Leu Gln Pro Pro Pro Gly Gly Thr Leu Glu Asp
405 410 415
Thr Tyr Arg Phe Val Thr Ser Gln Ala Ile Ala Cys Gln Lys His Thr
420 425 430
Pro Pro Ala Pro Lys Glu Asp Pro Leu Lys Lys Tyr Thr Phe Trp Glu
435 440 445
Val Asn Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu
450 455 460
Gly Arg Lys Phe Leu Leu Gln Ala Gly Leu Lys Ala Lys Pro Lys Leu
465 470 475 480
Lys Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys
485 490 495
Lys Val Lys Lys
500
<210> 19
<211> 496
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 19
Met Ala Leu Trp Arg Pro Ser Asp Asn Thr Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Arg Val Val Asn Thr Asp Asp Tyr Val Thr Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Thr Val Gly Asn Pro
35 40 45
Tyr Phe Arg Val Pro Ala Gly Gly Gly Asn Lys Gln Asp Ile Pro Lys
50 55 60
Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Gln Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Leu Pro Asp Thr Ser Ile Tyr Asn Pro Glu Thr Gln
85 90 95
Arg Leu Val Trp Ala Cys Ala Gly Val Glu Ile Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Leu Ser Gly His Pro Phe Tyr Asn Lys Leu Asp Asp
115 120 125
Thr Glu Ser Ser His Ala Ala Thr Ser Asn Val Ser Glu Asp Val Arg
130 135 140
Asp Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Leu Gly
145 150 155 160
Cys Ala Pro Ala Ile Gly Glu His Trp Ala Lys Gly Thr Ala Cys Lys
165 170 175
Ser Arg Pro Leu Ser Gln Gly Asp Cys Pro Pro Leu Glu Leu Lys Asn
180 185 190
Thr Val Leu Glu Asp Gly Asp Met Val Asp Thr Gly Tyr Gly Ala Met
195 200 205
Asp Phe Ser Thr Leu Gln Asp Thr Lys Cys Glu Val Pro Leu Asp Ile
210 215 220
Cys Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala Asp
225 230 235 240
Pro Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Leu Phe
245 250 255
Ala Arg His Phe Trp Asn Arg Ala Gly Thr Met Gly Asp Thr Val Pro
260 265 270
Gln Ser Leu Tyr Ile Lys Gly Thr Gly Met Arg Ala Ser Pro Gly Ser
275 280 285
Cys Val Tyr Ser Pro Ser Pro Ser Gly Ser Ile Val Thr Ser Asp Ser
290 295 300
Gln Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln Gly His Asn
305 310 315 320
Asn Gly Val Cys Trp His Asn Gln Leu Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Leu Thr Ile Cys Ala Ser Thr Gln Ser Pro Val
340 345 350
Pro Gly Gln Tyr Asp Ala Thr Lys Phe Lys Gln Tyr Ser Arg His Val
355 360 365
Glu Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Thr Ile Thr Leu
370 375 380
Thr Ala Asp Val Met Ser Tyr Ile His Ser Met Asn Ser Ser Ile Leu
385 390 395 400
Glu Asp Trp Asn Phe Gly Val Pro Pro Pro Pro Thr Thr Ser Leu Val
405 410 415
Asp Thr Tyr Arg Phe Val Gln Ser Val Ala Ile Thr Cys Gln Lys Asp
420 425 430
Ala Ala Pro Ala Glu Asn Lys Asp Pro Tyr Asp Lys Leu Lys Phe Trp
435 440 445
Asn Val Asp Leu Lys Glu Lys Phe Ser Leu Asp Leu Asp Gln Tyr Pro
450 455 460
Leu Gly Arg Lys Phe Leu Lys Ala Lys Pro Lys Leu Lys Arg Ala Ala
465 470 475 480
Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys Val Lys Lys
485 490 495
<210> 20
<211> 501
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 20
Met Ser Leu Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Thr Arg Thr Asn
20 25 30
Ile Tyr Tyr His Ala Gly Ser Ala Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Tyr Ser Ile Pro Lys Ser Asp Asn Pro Lys Lys Ile Val Val Pro
50 55 60
Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Glu Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Leu Glu Val Gly Arg Gly Gln
100 105 110
Pro Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Phe Asp
115 120 125
Asp Thr Glu Asn Ser Asn Arg Tyr Ala Gly Gly Pro Gly Thr Asp Asn
130 135 140
Arg Glu Cys Ile Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Leu
145 150 155 160
Gly Cys Lys Pro Pro Ile Gly Glu His Trp Gly Lys Gly Ser Pro Cys
165 170 175
Ser Asn Asn Ala Ile Thr Pro Gly Asp Cys Pro Pro Leu Glu Leu Lys
180 185 190
Asn Ser Val Ile Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala
195 200 205
Met Asp Phe Thr Ala Leu Gln Asp Thr Lys Ser Asn Val Pro Leu Asp
210 215 220
Ile Cys Asn Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Lys Met Val Ala
225 230 235 240
Glu Pro Tyr Gly Asp Thr Leu Phe Phe Tyr Leu Arg Arg Glu Gln Met
245 250 255
Phe Val Arg His Phe Phe Asn Arg Ser Gly Thr Val Gly Glu Ser Val
260 265 270
Pro Thr Asp Leu Tyr Ile Lys Gly Ser Gly Ser Thr Ala Thr Leu Ala
275 280 285
Asn Ser Thr Tyr Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Asp
290 295 300
Ala Gln Ile Phe Asn Lys Pro Tyr Trp Met Gln Arg Ala Gln Gly His
305 310 315 320
Asn Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp
325 330 335
Thr Thr Arg Ser Thr Asn Met Ser Val Cys Ala Ala Ile Ala Asn Ser
340 345 350
Asp Thr Thr Phe Lys Ser Ser Asn Phe Lys Glu Tyr Leu Arg His Gly
355 360 365
Glu Glu Phe Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu
370 375 380
Ser Ala Asp Ile Met Thr Tyr Ile His Ser Met Asn Pro Ala Ile Leu
385 390 395 400
Glu Asp Trp Asn Phe Gly Leu Thr Thr Pro Pro Ser Gly Ser Leu Glu
405 410 415
Asp Thr Tyr Arg Phe Val Thr Ser Gln Ala Ile Thr Cys Gln Lys Ser
420 425 430
Ala Pro Gln Lys Pro Lys Glu Asp Pro Phe Lys Asp Tyr Val Phe Trp
435 440 445
Glu Val Asn Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro
450 455 460
Leu Gly Arg Lys Phe Leu Leu Gln Ala Gly Tyr Lys Ala Lys Pro Lys
465 470 475 480
Leu Lys Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg
485 490 495
Lys Lys Val Lys Lys
500
<210> 21
<211> 498
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 21
Met Ser Leu Trp Arg Ser Asn Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Ser Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Thr Arg Thr Asn
20 25 30
Ile Tyr Tyr His Ala Gly Ser Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Tyr Ala Ile Lys Lys Gln Asp Ser Asn Lys Ile Ala Val Pro Lys
50 55 60
Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Lys Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asp Pro Ala Ser Gln
85 90 95
Arg Leu Val Trp Ala Cys Thr Gly Val Glu Val Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Leu Asp Asp
115 120 125
Thr Glu Asn Ser Asn Lys Tyr Val Gly Asn Ser Gly Thr Asp Asn Arg
130 135 140
Glu Cys Ile Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Ile Gly
145 150 155 160
Cys Arg Pro Pro Ile Gly Glu His Trp Gly Lys Gly Thr Pro Cys Asn
165 170 175
Ala Asn Gln Val Lys Ala Gly Glu Cys Pro Pro Leu Glu Leu Leu Asn
180 185 190
Thr Val Leu Gln Asp Gly Asp Met Val Asp Thr Gly Phe Gly Ala Met
195 200 205
Asp Phe Thr Thr Leu Gln Ala Asn Lys Ser Asp Val Pro Leu Asp Ile
210 215 220
Cys Ser Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Lys Met Val Ser Glu
225 230 235 240
Pro Tyr Gly Asp Met Leu Phe Phe Tyr Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Leu Phe Asn Arg Ala Gly Thr Val Gly Glu Thr Val Pro
260 265 270
Ala Asp Leu Tyr Ile Lys Gly Thr Thr Gly Thr Leu Pro Ser Thr Ser
275 280 285
Tyr Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Asp Ala Gln Ile
290 295 300
Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn Asn Gly
305 310 315 320
Ile Cys Trp Ser Asn Gln Leu Phe Val Thr Val Val Asp Thr Thr Arg
325 330 335
Ser Thr Asn Met Ser Val Cys Ser Ala Val Ser Ser Ser Asp Ser Thr
340 345 350
Tyr Lys Asn Asp Asn Phe Lys Glu Tyr Leu Arg His Gly Glu Glu Tyr
355 360 365
Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu Thr Ala Asp
370 375 380
Val Met Thr Tyr Ile His Ser Met Asn Pro Ser Ile Leu Glu Asp Trp
385 390 395 400
Asn Phe Gly Leu Thr Pro Pro Pro Ser Gly Thr Leu Glu Asp Thr Tyr
405 410 415
Arg Tyr Val Thr Ser Gln Ala Val Thr Cys Gln Lys Pro Ser Ala Pro
420 425 430
Lys Pro Lys Asp Asp Pro Leu Lys Asn Tyr Thr Phe Trp Glu Val Asp
435 440 445
Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu Gly Arg
450 455 460
Lys Phe Leu Leu Gln Ala Gly Leu Lys Ala Lys Pro Lys Leu Lys Arg
465 470 475 480
Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys Val
485 490 495
Lys Lys
<210> 22
<211> 507
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 22
Met Ala Met Trp Arg Ser Ser Asp Ser Met Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Lys Val Val Asn Thr Asp Asp Tyr Val Thr Arg Thr Gly
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Phe Lys Val Gly Met Asn Gly Gly Arg Lys Gln Asp Ile Pro Lys
50 55 60
Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Thr Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Ser Ile Pro Asp Ala Ser Leu Tyr Asn Pro Glu Thr Gln
85 90 95
Arg Leu Val Trp Ala Cys Val Gly Val Glu Val Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Ile Ser Gly His Pro Leu Tyr Asn Arg Gln Asp Asp
115 120 125
Thr Glu Asn Ser Pro Phe Ser Ser Thr Thr Asn Lys Asp Ser Arg Asp
130 135 140
Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Ile Gly Cys
145 150 155 160
Val Pro Ala Ile Gly Glu His Trp Gly Lys Gly Lys Ala Cys Lys Pro
165 170 175
Asn Asn Val Ser Thr Gly Asp Cys Pro Pro Leu Glu Leu Val Asn Thr
180 185 190
Pro Ile Glu Asp Gly Asp Met Ile Asp Thr Gly Tyr Gly Ala Met Asp
195 200 205
Phe Gly Ala Leu Gln Glu Thr Lys Ser Glu Val Pro Leu Asp Ile Cys
210 215 220
Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala Asp Val
225 230 235 240
Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Leu Phe Ala
245 250 255
Arg His Phe Trp Asn Arg Gly Gly Met Val Gly Asp Ala Ile Pro Ala
260 265 270
Gln Leu Tyr Ile Lys Gly Thr Asp Ile Arg Ala Asn Pro Gly Ser Ser
275 280 285
Val Tyr Cys Pro Ser Pro Ser Gly Ser Met Val Thr Ser Asp Ser Gln
290 295 300
Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln Gly His Asn Asn
305 310 315 320
Gly Ile Cys Trp His Asn Gln Leu Phe Leu Thr Val Val Asp Thr Thr
325 330 335
Arg Ser Thr Asn Phe Thr Leu Ser Thr Ser Ile Glu Ser Ser Ile Pro
340 345 350
Ser Thr Tyr Asp Pro Ser Lys Phe Lys Glu Tyr Thr Arg His Val Glu
355 360 365
Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Thr Val Thr Leu Thr
370 375 380
Thr Asp Val Met Ser Tyr Ile His Thr Met Asn Ser Ser Ile Leu Asp
385 390 395 400
Asn Trp Asn Phe Ala Val Ala Pro Pro Pro Ser Ala Ser Leu Val Asp
405 410 415
Thr Tyr Arg Tyr Leu Gln Ser Ala Ala Ile Thr Cys Gln Lys Asp Ala
420 425 430
Pro Ala Pro Glu Lys Lys Asp Pro Tyr Asp Gly Leu Lys Phe Trp Asn
435 440 445
Val Asp Leu Arg Glu Lys Phe Ser Leu Glu Leu Asp Gln Phe Pro Leu
450 455 460
Gly Arg Lys Phe Leu Leu Gln Leu Gly Ala Arg Pro Lys Pro Thr Ile
465 470 475 480
Gly Pro Arg Lys Arg Ala Ala Pro Ala Pro Thr Ser Thr Pro Ser Pro
485 490 495
Lys Arg Val Lys Arg Arg Lys Ser Ser Arg Lys
500 505
<210> 23
<211> 504
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 23
Met Ala Leu Trp Arg Pro Ser Asp Ser Thr Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Arg Val Val Asn Thr Asp Asp Tyr Val Ser Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Thr Val Gly Asn Pro
35 40 45
Tyr Phe Arg Val Val Pro Ser Gly Ala Gly Asn Lys Gln Ala Val Pro
50 55 60
Lys Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Ala Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Leu Pro Asp Ser Thr Ile Tyr Asn Pro Glu Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Met Glu Ile Gly Arg Gly Gln
100 105 110
Pro Leu Gly Ile Gly Leu Ser Gly His Pro Phe Tyr Asn Lys Leu Asp
115 120 125
Asp Thr Glu Ser Ala His Ala Ala Thr Ala Val Ile Thr Gln Asp Val
130 135 140
Arg Asp Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Leu
145 150 155 160
Gly Cys Val Pro Ala Ile Gly Glu His Trp Ala Lys Gly Thr Leu Cys
165 170 175
Lys Pro Ala Gln Leu Gln Pro Gly Asp Cys Pro Pro Leu Glu Leu Lys
180 185 190
Asn Thr Ile Ile Glu Asp Gly Asp Met Val Asp Thr Gly Tyr Gly Ala
195 200 205
Met Asp Phe Ser Thr Leu Gln Asp Thr Lys Cys Glu Val Pro Leu Asp
210 215 220
Ile Cys Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala
225 230 235 240
Asp Pro Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Leu
245 250 255
Phe Ala Arg His Phe Trp Asn Arg Ala Gly Val Met Gly Asp Thr Val
260 265 270
Pro Thr Asp Leu Tyr Ile Lys Gly Thr Ser Ala Asn Met Arg Glu Thr
275 280 285
Pro Gly Ser Cys Val Tyr Ser Pro Ser Pro Ser Gly Ser Ile Thr Thr
290 295 300
Ser Asp Ser Gln Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln
305 310 315 320
Gly His Asn Asn Gly Ile Cys Trp His Asn Gln Leu Phe Val Thr Val
325 330 335
Val Asp Thr Thr Arg Ser Thr Asn Leu Thr Leu Cys Ala Ser Thr Gln
340 345 350
Asn Pro Val Pro Asn Thr Tyr Asp Pro Thr Lys Phe Lys His Tyr Ser
355 360 365
Arg His Val Glu Glu Tyr Asp Leu Gln Phe Ile Phe Gln Leu Cys Thr
370 375 380
Ile Thr Leu Thr Ala Glu Val Met Ser Tyr Ile His Ser Met Asn Ser
385 390 395 400
Ser Ile Leu Glu Asn Trp Asn Phe Gly Val Pro Pro Pro Pro Thr Thr
405 410 415
Ser Leu Val Asp Thr Tyr Arg Phe Val Gln Ser Val Ala Val Thr Cys
420 425 430
Gln Lys Asp Thr Thr Pro Pro Glu Lys Gln Asp Pro Tyr Asp Lys Leu
435 440 445
Lys Phe Trp Thr Val Asp Leu Lys Glu Lys Phe Ser Ser Asp Leu Asp
450 455 460
Gln Tyr Pro Leu Gly Arg Lys Phe Leu Val Gln Ala Gly Leu Lys Ala
465 470 475 480
Lys Pro Lys Leu Lys Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser
485 490 495
Ala Lys Arg Lys Lys Val Lys Lys
500
<210> 24
<211> 500
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 24
Met Ala Leu Trp Arg Thr Asn Asp Ser Lys Val Tyr Leu Pro Pro Ala
1 5 10 15
Pro Val Ser Arg Ile Val Asn Thr Glu Glu Tyr Ile Thr Arg Thr Gly
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Ile Thr Leu Gly His Pro
35 40 45
Tyr Phe Pro Ile Pro Lys Thr Ser Thr Arg Ala Ala Ile Pro Lys Val
50 55 60
Ser Ala Phe Gln Tyr Arg Val Phe Arg Val Gln Leu Pro Asp Pro Asn
65 70 75 80
Lys Phe Gly Leu Pro Asp Pro Asn Leu Tyr Asn Pro Asp Thr Asp Arg
85 90 95
Leu Val Trp Gly Cys Val Gly Val Glu Val Gly Arg Gly Gln Pro Leu
100 105 110
Gly Val Gly Leu Ser Gly His Pro Leu Phe Asn Lys Tyr Asp Asp Thr
115 120 125
Glu Asn Ser Arg Ile Ala Asn Gly Asn Ala Gln Gln Asp Val Arg Asp
130 135 140
Asn Thr Ser Val Asp Asn Lys Gln Thr Gln Leu Cys Ile Ile Gly Cys
145 150 155 160
Ala Pro Pro Ile Gly Glu His Trp Gly Ile Gly Thr Thr Cys Lys Asn
165 170 175
Thr Pro Val Pro Pro Gly Asp Cys Pro Pro Leu Glu Leu Val Ser Ser
180 185 190
Val Ile Gln Asp Gly Asp Met Ile Asp Thr Gly Phe Gly Ala Met Asp
195 200 205
Phe Ala Ala Leu Gln Ala Thr Lys Ser Asp Val Pro Leu Asp Ile Ser
210 215 220
Gln Ser Val Cys Lys Tyr Pro Asp Tyr Leu Lys Met Ser Ala Asp Thr
225 230 235 240
Tyr Gly Asn Ser Met Phe Phe His Leu Arg Arg Glu Gln Ile Phe Ala
245 250 255
Arg His Tyr Tyr Asn Lys Leu Val Gly Val Gly Glu Asp Ile Pro Asn
260 265 270
Asp Tyr Tyr Ile Lys Gly Ser Gly Asn Gly Arg Asp Pro Ile Glu Ser
275 280 285
Tyr Ile Tyr Ser Ala Thr Pro Ser Gly Ser Met Ile Thr Ser Asp Ser
290 295 300
Gln Ile Phe Asn Lys Pro Tyr Trp Leu His Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Asn Asn Gln Leu Phe Ile Thr Cys Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Leu Thr Ile Ser Thr Ala Thr Ala Ala Val Ser
340 345 350
Pro Thr Phe Thr Pro Ser Asn Phe Lys Gln Tyr Ile Arg His Gly Glu
355 360 365
Glu Tyr Glu Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu Thr
370 375 380
Thr Glu Val Met Ala Tyr Leu His Thr Met Asp Pro Thr Ile Leu Glu
385 390 395 400
Gln Trp Asn Phe Gly Leu Thr Leu Pro Pro Ser Ala Ser Leu Glu Asp
405 410 415
Ala Tyr Arg Phe Val Arg Asn Ala Ala Thr Ser Cys Gln Lys Asp Thr
420 425 430
Pro Pro Gln Ala Lys Pro Asp Pro Leu Ala Lys Tyr Lys Phe Trp Asp
435 440 445
Val Asp Leu Lys Glu Arg Phe Ser Leu Asp Leu Asp Gln Phe Ala Leu
450 455 460
Gly Arg Lys Phe Leu Leu Gln Val Gly Val Lys Ala Lys Pro Lys Leu
465 470 475 480
Lys Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys
485 490 495
Lys Val Lys Lys
500
<210> 25
<211> 504
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 25
Met Ser Val Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ser Arg Thr Ser
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Phe Ser Ile Lys Asn Thr Ser Ser Gly Asn Gly Lys Lys Val Leu
50 55 60
Val Pro Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Ile Lys Leu
65 70 75 80
Pro Asp Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro
85 90 95
Glu Thr Gln Arg Leu Val Trp Ala Cys Thr Gly Leu Glu Ile Gly Arg
100 105 110
Gly Gln Pro Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys
115 120 125
Phe Asp Asp Thr Glu Thr Ser Asn Lys Tyr Ala Gly Lys Pro Gly Ile
130 135 140
Asp Asn Arg Glu Cys Leu Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys
145 150 155 160
Ile Leu Gly Cys Lys Pro Pro Ile Gly Glu His Trp Gly Lys Gly Thr
165 170 175
Pro Cys Asn Asn Asn Ser Gly Asn Pro Gly Asp Cys Pro Pro Leu Gln
180 185 190
Leu Ile Asn Ser Val Ile Gln Asp Gly Asp Met Val Asp Thr Gly Phe
195 200 205
Gly Cys Met Asp Phe Asn Thr Leu Gln Ala Ser Lys Ser Asp Val Pro
210 215 220
Ile Asp Ile Cys Ser Ser Val Cys Lys Tyr Pro Asp Tyr Leu Gln Met
225 230 235 240
Ala Ser Glu Pro Tyr Gly Asp Ser Leu Phe Phe Phe Leu Arg Arg Glu
245 250 255
Gln Met Phe Val Arg His Phe Phe Asn Arg Ala Gly Thr Leu Gly Asp
260 265 270
Pro Val Pro Gly Asp Leu Tyr Ile Gln Gly Ser Asn Ser Gly Asn Thr
275 280 285
Ala Thr Val Gln Ser Ser Ala Phe Phe Pro Thr Pro Ser Gly Ser Met
290 295 300
Val Thr Ser Glu Ser Gln Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg
305 310 315 320
Ala Gln Gly His Asn Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val
325 330 335
Thr Val Val Asp Thr Thr Arg Ser Thr Asn Met Thr Leu Cys Ala Glu
340 345 350
Val Lys Lys Glu Ser Thr Tyr Lys Asn Glu Asn Phe Lys Glu Tyr Leu
355 360 365
Arg His Gly Glu Glu Phe Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys
370 375 380
Ile Thr Leu Thr Ala Asp Val Met Thr Tyr Ile His Lys Met Asp Ala
385 390 395 400
Thr Ile Leu Glu Asp Trp Gln Phe Gly Leu Thr Pro Pro Pro Ser Ala
405 410 415
Ser Leu Glu Asp Thr Tyr Arg Phe Val Thr Ser Thr Ala Ile Thr Cys
420 425 430
Gln Lys Asn Thr Pro Pro Lys Gly Lys Glu Asp Pro Leu Lys Asp Tyr
435 440 445
Met Phe Trp Glu Val Asp Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp
450 455 460
Gln Phe Pro Leu Gly Arg Lys Phe Leu Leu Gln Ala Gly Leu Lys Ala
465 470 475 480
Lys Pro Lys Leu Lys Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser
485 490 495
Ala Lys Arg Lys Lys Val Lys Lys
500
<210> 26
<211> 498
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 26
Met Ala Thr Trp Arg Pro Ser Glu Asn Lys Val Tyr Leu Pro Pro Thr
1 5 10 15
Pro Val Ser Lys Val Val Ala Thr Asp Ser Tyr Val Lys Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Tyr Ser Val Thr Lys Asp Asn Thr Lys Thr Asn Ile Pro Lys Val
50 55 60
Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp Pro Asn
65 70 75 80
Lys Phe Gly Leu Pro Asp Thr Asn Ile Tyr Asn Pro Asp Gln Glu Arg
85 90 95
Leu Val Trp Ala Cys Val Gly Leu Glu Val Gly Arg Gly Gln Pro Leu
100 105 110
Gly Ala Gly Leu Ser Gly His Pro Leu Phe Asn Arg Leu Asp Asp Thr
115 120 125
Glu Ser Ser Asn Leu Ala Asn Asn Asn Val Ile Glu Asp Ser Arg Asp
130 135 140
Asn Ile Ser Val Asp Gly Lys Gln Thr Gln Leu Cys Ile Val Gly Cys
145 150 155 160
Thr Pro Ala Met Gly Glu His Trp Thr Lys Gly Ala Val Cys Lys Ser
165 170 175
Thr Gln Val Thr Thr Gly Asp Cys Pro Pro Leu Ala Leu Ile Asn Thr
180 185 190
Pro Ile Glu Asp Gly Asp Met Ile Asp Thr Gly Phe Gly Ala Met Asp
195 200 205
Phe Lys Val Leu Gln Glu Ser Lys Ala Glu Val Pro Leu Asp Ile Val
210 215 220
Gln Ser Thr Cys Lys Tyr Pro Asp Tyr Leu Lys Met Ser Ala Asp Ala
225 230 235 240
Tyr Gly Asp Ser Met Trp Phe Tyr Leu Arg Arg Glu Gln Leu Phe Ala
245 250 255
Arg His Tyr Phe Asn Arg Ala Gly Lys Val Gly Glu Thr Ile Pro Ala
260 265 270
Glu Leu Tyr Leu Lys Gly Ser Asn Gly Arg Glu Pro Pro Pro Ser Ser
275 280 285
Val Tyr Val Ala Thr Pro Ser Gly Ser Met Ile Thr Ser Glu Ala Gln
290 295 300
Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn Asn
305 310 315 320
Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr Thr
325 330 335
Arg Ser Thr Asn Met Thr Ile Ser Thr Ala Thr Glu Gln Leu Ser Lys
340 345 350
Tyr Asp Ala Arg Lys Ile Asn Gln Tyr Leu Arg His Val Glu Glu Tyr
355 360 365
Glu Leu Gln Phe Val Phe Gln Leu Cys Lys Ile Thr Leu Ser Ala Glu
370 375 380
Val Met Ala Tyr Leu His Asn Met Asn Ala Asn Leu Leu Glu Asp Trp
385 390 395 400
Asn Ile Gly Leu Ser Pro Pro Val Ala Thr Ser Leu Glu Asp Lys Tyr
405 410 415
Arg Tyr Val Arg Ser Thr Ala Ile Thr Cys Gln Arg Glu Gln Pro Pro
420 425 430
Thr Glu Lys Gln Asp Pro Leu Ala Lys Tyr Lys Phe Trp Asp Val Asn
435 440 445
Leu Gln Asp Ser Phe Ser Thr Asp Leu Asp Gln Phe Pro Leu Gly Arg
450 455 460
Lys Phe Leu Leu Gln Ala Gly Leu Lys Ala Lys Pro Lys Leu Lys Arg
465 470 475 480
Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys Val
485 490 495
Lys Lys
<210> 27
<211> 499
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 27
Met Ser Val Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ser Arg Thr Ser
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Ala Val Gly Asn Pro
35 40 45
Tyr Phe Ser Ile Lys Ser Pro Asn Asn Asn Lys Lys Val Leu Val Pro
50 55 60
Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Asp Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Leu Glu Ile Gly Arg Gly Gln
100 105 110
Pro Leu Gly Val Gly Val Ser Gly His Pro Tyr Leu Asn Lys Phe Asp
115 120 125
Asp Thr Glu Thr Ser Asn Arg Tyr Pro Ala Gln Pro Gly Ser Asp Asn
130 135 140
Arg Glu Cys Leu Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Ile
145 150 155 160
Gly Cys Lys Pro Pro Thr Gly Glu His Trp Gly Lys Gly Val Ala Cys
165 170 175
Asn Asn Asn Ala Ala Ala Thr Asp Cys Pro Pro Leu Glu Leu Phe Asn
180 185 190
Ser Ile Ile Glu Asp Gly Asp Met Val Asp Thr Gly Phe Gly Cys Met
195 200 205
Asp Phe Gly Thr Leu Gln Ala Asn Lys Ser Asp Val Pro Ile Asp Ile
210 215 220
Cys Asn Ser Thr Cys Lys Tyr Pro Asp Tyr Leu Lys Met Ala Ser Glu
225 230 235 240
Pro Tyr Gly Asp Ser Leu Phe Phe Phe Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Phe Phe Asn Arg Ala Gly Lys Leu Gly Glu Ala Val Pro
260 265 270
Asp Asp Leu Tyr Ile Lys Gly Ser Gly Asn Thr Ala Val Ile Gln Ser
275 280 285
Ser Ala Phe Phe Pro Thr Pro Ser Gly Ser Ile Val Thr Ser Glu Ser
290 295 300
Gln Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Gly Asn Gln Leu Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Met Thr Leu Cys Thr Glu Val Thr Lys Glu Gly
340 345 350
Thr Tyr Lys Asn Asp Asn Phe Lys Glu Tyr Val Arg His Val Glu Glu
355 360 365
Tyr Asp Leu Gln Phe Val Phe Gln Leu Cys Lys Ile Thr Leu Thr Ala
370 375 380
Glu Ile Met Thr Tyr Ile His Thr Met Asp Ser Asn Ile Leu Glu Asp
385 390 395 400
Trp Gln Phe Gly Leu Thr Pro Pro Pro Ser Ala Ser Leu Gln Asp Thr
405 410 415
Tyr Arg Phe Val Thr Ser Gln Ala Ile Thr Cys Gln Lys Thr Ala Pro
420 425 430
Pro Lys Glu Lys Glu Asp Pro Leu Asn Lys Tyr Thr Phe Trp Glu Val
435 440 445
Asn Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu Gly
450 455 460
Arg Lys Phe Leu Leu Gln Ser Gly Leu Lys Ala Lys Pro Lys Leu Lys
465 470 475 480
Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys
485 490 495
Val Lys Lys
<210> 28
<211> 499
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 28
Met Ser Val Trp Arg Pro Ser Glu Ala Thr Val Tyr Leu Pro Pro Val
1 5 10 15
Pro Val Ser Lys Val Val Ser Thr Asp Glu Tyr Val Ser Arg Thr Ser
20 25 30
Ile Tyr Tyr Tyr Ala Gly Ser Ser Arg Leu Leu Ala Val Gly His Pro
35 40 45
Tyr Phe Ser Ile Lys Asn Pro Thr Asn Ala Lys Lys Leu Leu Val Pro
50 55 60
Lys Val Ser Gly Leu Gln Tyr Arg Val Phe Arg Val Arg Leu Pro Asp
65 70 75 80
Pro Asn Lys Phe Gly Phe Pro Asp Thr Ser Phe Tyr Asn Pro Asp Thr
85 90 95
Gln Arg Leu Val Trp Ala Cys Val Gly Leu Glu Ile Gly Arg Gly Gln
100 105 110
Pro Leu Gly Val Gly Ile Ser Gly His Pro Leu Leu Asn Lys Phe Asp
115 120 125
Asp Thr Glu Thr Gly Asn Lys Tyr Pro Gly Gln Pro Gly Ala Asp Asn
130 135 140
Arg Glu Cys Leu Ser Met Asp Tyr Lys Gln Thr Gln Leu Cys Leu Leu
145 150 155 160
Gly Cys Lys Pro Pro Thr Gly Glu His Trp Gly Lys Gly Val Ala Cys
165 170 175
Thr Asn Ala Ala Pro Ala Asn Asp Cys Pro Pro Leu Glu Leu Ile Asn
180 185 190
Thr Ile Ile Glu Asp Gly Asp Met Val Asp Thr Gly Phe Gly Cys Met
195 200 205
Asp Phe Lys Thr Leu Gln Ala Asn Lys Ser Asp Val Pro Ile Asp Ile
210 215 220
Cys Gly Ser Thr Cys Lys Tyr Pro Asp Tyr Leu Lys Met Thr Ser Glu
225 230 235 240
Pro Tyr Gly Asp Ser Leu Phe Phe Phe Leu Arg Arg Glu Gln Met Phe
245 250 255
Val Arg His Phe Phe Asn Arg Ala Gly Thr Leu Gly Glu Ala Val Pro
260 265 270
Asp Asp Leu Tyr Ile Lys Gly Ser Gly Thr Thr Ala Ser Ile Gln Ser
275 280 285
Ser Ala Phe Phe Pro Thr Pro Ser Gly Ser Met Val Thr Ser Glu Ser
290 295 300
Gln Leu Phe Asn Lys Pro Tyr Trp Leu Gln Arg Ala Gln Gly His Asn
305 310 315 320
Asn Gly Ile Cys Trp Gly Asn Gln Val Phe Val Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Met Thr Leu Cys Thr Gln Val Thr Ser Asp Ser
340 345 350
Thr Tyr Lys Asn Glu Asn Phe Lys Glu Tyr Ile Arg His Val Glu Glu
355 360 365
Tyr Asp Leu Gln Phe Val Phe Gln Leu Cys Lys Val Thr Leu Thr Ala
370 375 380
Glu Val Met Thr Tyr Ile His Ala Met Asn Pro Asp Ile Leu Glu Asp
385 390 395 400
Trp Gln Phe Gly Leu Thr Pro Pro Pro Ser Ala Ser Leu Gln Asp Thr
405 410 415
Tyr Arg Phe Val Thr Ser Gln Ala Ile Thr Cys Gln Lys Thr Val Pro
420 425 430
Pro Lys Glu Lys Glu Asp Pro Leu Gly Lys Tyr Thr Phe Trp Glu Val
435 440 445
Asp Leu Lys Glu Lys Phe Ser Ala Asp Leu Asp Gln Phe Pro Leu Gly
450 455 460
Arg Lys Phe Leu Leu Gln Ala Gly Leu Lys Ala Lys Pro Lys Leu Lys
465 470 475 480
Arg Ala Ala Pro Thr Ser Thr Arg Thr Ser Ser Ala Lys Arg Lys Lys
485 490 495
Val Lys Lys
<210> 29
<211> 508
<212> PRT
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 29
Met Ala Leu Trp Arg Ser Ser Asp Asn Lys Val Tyr Leu Pro Pro Pro
1 5 10 15
Ser Val Ala Lys Val Val Ser Thr Asp Glu Tyr Val Thr Arg Thr Ser
20 25 30
Ile Phe Tyr His Ala Gly Ser Ser Arg Leu Leu Thr Val Gly His Pro
35 40 45
Tyr Phe Lys Val Pro Lys Gly Gly Asn Gly Arg Gln Asp Val Pro Lys
50 55 60
Val Ser Ala Tyr Gln Tyr Arg Val Phe Arg Val Lys Leu Pro Asp Pro
65 70 75 80
Asn Lys Phe Gly Leu Pro Asp Asn Thr Val Tyr Asp Pro Asn Ser Gln
85 90 95
Arg Leu Val Trp Ala Cys Val Gly Val Glu Ile Gly Arg Gly Gln Pro
100 105 110
Leu Gly Val Gly Leu Ser Gly His Pro Leu Tyr Asn Lys Leu Asp Asp
115 120 125
Thr Glu Asn Ser His Val Ala Ser Ala Val Asp Thr Lys Asp Thr Arg
130 135 140
Asp Asn Val Ser Val Asp Tyr Lys Gln Thr Gln Leu Cys Ile Ile Gly
145 150 155 160
Cys Val Pro Ala Ile Gly Glu His Trp Thr Lys Gly Thr Ala Cys Lys
165 170 175
Pro Thr Thr Val Val Gln Gly Asp Cys Pro Pro Leu Glu Leu Ile Asn
180 185 190
Thr Pro Ile Glu Asp Gly Asp Met Val Asp Thr Gly Tyr Gly Ala Met
195 200 205
Asp Phe Lys Leu Leu Gln Asp Asn Lys Ser Glu Val Pro Leu Asp Ile
210 215 220
Cys Gln Ser Ile Cys Lys Tyr Pro Asp Tyr Leu Gln Met Ser Ala Asp
225 230 235 240
Ala Tyr Gly Asp Ser Met Phe Phe Cys Leu Arg Arg Glu Gln Val Phe
245 250 255
Ala Arg His Phe Trp Asn Arg Ser Gly Thr Met Gly Asp Gln Leu Pro
260 265 270
Glu Ser Leu Tyr Ile Lys Gly Thr Asp Ile Arg Ala Asn Pro Gly Ser
275 280 285
Tyr Leu Tyr Ser Pro Ser Pro Ser Gly Ser Val Val Thr Ser Asp Ser
290 295 300
Gln Leu Phe Asn Lys Pro Tyr Trp Leu His Lys Ala Gln Gly Leu Asn
305 310 315 320
Asn Gly Ile Cys Trp His Asn Gln Leu Phe Leu Thr Val Val Asp Thr
325 330 335
Thr Arg Ser Thr Asn Leu Ser Val Cys Ala Ser Thr Thr Ser Ser Ile
340 345 350
Pro Asn Val Tyr Thr Pro Thr Ser Phe Lys Glu Tyr Ala Arg His Val
355 360 365
Glu Glu Phe Asp Leu Gln Phe Ile Phe Gln Leu Cys Lys Ile Thr Leu
370 375 380
Thr Thr Glu Val Met Ser Tyr Ile His Asn Met Asn Thr Thr Ile Leu
385 390 395 400
Glu Asp Trp Asn Phe Gly Val Thr Pro Pro Pro Thr Ala Ser Leu Val
405 410 415
Asp Thr Tyr Arg Phe Val Gln Ser Ala Ala Val Thr Cys Gln Lys Asp
420 425 430
Thr Ala Pro Pro Val Lys Gln Asp Pro Tyr Asp Lys Leu Lys Phe Trp
435 440 445
Pro Val Asp Leu Lys Glu Arg Phe Ser Ala Asp Leu Asp Gln Phe Pro
450 455 460
Leu Gly Arg Lys Phe Leu Leu Gln Leu Gly Ala Arg Pro Lys Pro Thr
465 470 475 480
Ile Gly Pro Arg Lys Arg Ala Ala Pro Ala Pro Thr Ser Thr Pro Ser
485 490 495
Pro Lys Arg Val Lys Arg Arg Lys Ser Ser Arg Lys
500 505
<210> 30
<211> 1522
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 30
ctgggtacca tgtggagacc atctgacagc acagtctatg tgcctcctcc aaaccctgtg 60
agcaaggtgg tggctacaga tgcctatgtg accaggacca acatcttcta ccatgcctcc 120
tccagcagac tgctggctgt gggacaccca tacttcagca tcaagagggc taacaagaca 180
gtggtgccaa aggtgtctgg ctaccaatac agggtgttca aggtggtgct gcctgaccca 240
aacaagtttg ccctgcctga ctcctccctg tttgacccaa ccacccagag actggtgtgg 300
gcttgtactg gattggaggt gggcagggga caaccactgg gagtgggagt gtctggacac 360
ccattcctga acaaatatga tgatgtggag aactctggct ctggaggcaa ccctggacaa 420
gacaacaggg tgaatgtggg gatggactac aagcagaccc aactttgtat ggtgggctgt 480
gcccctccac tgggagaaca ctggggcaag ggcaagcagt gtaccaacac acctgtccag 540
gctggagact gtcctccatt ggaactgatt acctctgtga ttcaggatgg agatatggtg 600
gacacaggct ttggagctat gaactttgct gacctccaaa ccaacaagtc tgatgtgcca 660
attgacatct gtggcaccac ttgtaaatac cctgactacc tccaaatggc tgctgaccca 720
tatggagaca gactgttctt cttcctgagg aaggaacaga tgtttgccag acacttcttc 780
aacagggctg gagaggtggg agaacctgtg cctgacaccc tgattatcaa gggctctggc 840
aacaggacct ctgtgggctc cagcatctat gtgaacacac catctggctc cctggtgtcc 900
tctgaggctc aacttttcaa caagccatac tggctccaaa aggctcaagg acacaacaat 960
ggcatctgtt ggggcaacca actttttgtg acagtggtgg acaccaccag gagcaccaat 1020
atgaccctgt gtgcctctgt gaccacctcc agcacctaca ccaactctga ctacaaggaa 1080
tatatgaggc atgtggagga atatgacctc caattcatct tccaactttg tagcatcacc 1140
ctgtctgctg aggtgatggc ttacatccac acaatgaacc catctgtgtt ggaggactgg 1200
aactttggac tgagccctcc tccaaatggc accttggagg acacctacag atatgtccag 1260
agccaggcta tcacttgtca gaagccaaca cctgagaagg agaagcctga cccatacaag 1320
aacctgtcct tctgggaggt gaacctgaaa gagaagttct cctctgaact ggaccaatac 1380
ccactgggca ggaagttcct gctccaatct ggctacaggg gcaggtccag catcaggaca 1440
ggagtgaaga gacctgctgt gagcaaggca tctgctgccc caaagaggaa gagggctaag 1500
accaagaggt aaactcgagc tc 1522
<210> 31
<211> 1525
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 31
ctgggtacca tgtggagacc atctgacagc acagtctatg tgcctcctcc aaaccctgtg 60
agcaaggtgg tggctacaga tgcctatgtg aagaggacca acatcttcta ccatgcctcc 120
tccagcagac tgctggctgt gggacaccca tactacagca tcaagaaggt gaacaagaca 180
gtggtgccaa aggtgtctgg ctaccaatac agggtgttca aggtggtgct gcctgaccca 240
aacaagtttg ccctgcctga ctcctccctg tttgacccaa ccacccagag actggtgtgg 300
gcttgtactg gattggaggt gggcagggga caaccactgg gagtgggagt gtctggacac 360
ccactgctga acaaatatga tgatgtggag aactctggag gctatggagg caaccctgga 420
caagacaaca gggtgaatgt ggggatggac tacaagcaga cccaactttg tatggtgggc 480
tgtgcccctc cactgggaga acactggggc aagggcaccc agtgtagcaa cacctctgtc 540
cagaatggag actgtcctcc attggaactg attacctctg tgattcagga tggagatatg 600
gtggacacag gctttggagc tatgaacttt gctgacctcc aaaccaacaa gtctgatgtg 660
ccactggaca tctgtggcac agtgtgtaaa taccctgact acctccaaat ggctgctgac 720
ccatatggag acagactgtt cttctacctg aggaaggaac agatgtttgc cagacacttc 780
ttcaacaggg ctggcacagt gggagaacct gtgcctgatg acctgctggt gaagggaggc 840
aacaacaggt cctctgtggc atccagcatc tatgtgcata caccatctgg ctccctggtg 900
tcctctgagg ctcaactttt caacaagcca tactggctcc aaaaggctca aggacacaac 960
aatggcatct gttggggcaa ccacctgttt gtgacagtgg tggacaccac caggagcacc 1020
aatatgaccc tgtgtgcctc tgtgagcaag tctgccacct acaccaactc tgactacaag 1080
gaatatatga ggcatgtgga ggagtttgac ctccaattca tcttccaact ttgtagcatc 1140
accctgtctg ctgaggtgat ggcttacatc cacacaatga acccatctgt gttggaggac 1200
tggaactttg gactgagccc tcctccaaat ggcaccttgg aggacaccta cagatatgtc 1260
cagagccagg ctatcacttg tcagaagcca acacctgaga aggagaagca ggacccatac 1320
aaggatatga gtttctggga ggtgaacctg aaagagaagt tctcctctga actggaccag 1380
tttccactgg gcaggaagtt cctgctccaa tctggctaca ggggcaggac ctctgccagg 1440
acaggcatca agagacctgc tgtgagcaag ccaagcacag ccccaaagag gaagaggacc 1500
aagaccaaga agtaaactcg agctc 1525
<210> 32
<211> 1537
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 32
ctgggtacca tgagtctgtg gctgccatct gaggctacag tctacctgcc tcctgtgcct 60
gtgagcaagg tggtgagcac agatgaatat gtggcaagga ccaacatcta ctaccatgct 120
ggcaccagca gactgctggc tgtgggacac ccatactttc caatcaagaa gccaaacaac 180
aacaagattc tggtgccaaa ggtgtctgga ctccaataca gggtgttcag gattcacctg 240
cctgacccaa acaagtttgg ctttcctgac acctccttct acaaccctga cacccagaga 300
ctggtgtggg cttgtgtggg agtggaggtg ggcaggggac aaccactggg agtgggcatc 360
tctggacacc cactgctgaa caaactggat gacacagaga atgcctctgc ctatgctgcc 420
aatgctggag tggacaacag ggagtgtatc agtatggact acaagcagac ccaactttgt 480
ctgattggct gtaagcctcc aattggagaa cactggggca agggcagccc atgtaccaat 540
gtggctgtga accctggaga ctgtcctcca ttggaactga taaacacagt gattcaggat 600
ggagatatgg tggacacagg ctttggagct atggacttca ccaccctcca agccaacaag 660
tctgaggtgc cactggacat ctgtaccagc atctgtaaat accctgacta catcaagatg 720
gtgtctgaac catatggaga ctccctgttc ttctacctga ggagggaaca gatgtttgtg 780
agacacctgt tcaacagggc tggagcagtg ggagagaatg tgcctgatga cctctacatc 840
aagggctctg gcagcacagc caacctggca tccagcaact actttccaac accatctggc 900
agtatggtga cctctgatgc ccagattttc aacaagccat actggctcca aagggctcaa 960
ggacacaaca atggcatctg ttggggcaac caactttttg tgacagtggt ggacaccacc 1020
aggagcacca atatgagtct gtgtgctgcc atcagcacct ctgagaccac ctacaagaac 1080
accaacttca aggaatacct gagacatgga gaggaatatg acctccaatt catcttccaa 1140
ctttgtaaga ttaccctgac agcagatgtg atgacctaca tccacagtat gaacagcacc 1200
atcttggagg actggaactt tggactccaa cctcctcctg gaggcacctt ggaggacacc 1260
tacaggtttg tgaccagcca ggctattgcc tgtcagaaac acacacctcc tgccccaaag 1320
gaggacccac tgaaaaaata caccttctgg gaggtgaacc tgaaagagaa gttctctgct 1380
gacctggacc agtttccact gggcaggaag ttcctgctcc aagcaggact gaaagccaag 1440
ccaaagttca ccctgggcaa gaggaaggct acaccaacca cctccagcac cagcaccaca 1500
gccaagagga agaagaggaa actgtaaact cgagctc 1537
<210> 33
<211> 1543
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 33
ctgggtacca tggccctctg gagaccatcc gataacacag tgtacttgcc cccacccagc 60
gtcgcccggg tggtgaacac agacgactac gtcaccagaa cctcaatctt ctaccacgcc 120
gggtccagcc ggctgctgac cgtgggcaac ccctacttcc gcgtgcccgc cggcggcgga 180
aacaaacaag acatccccaa agtcagcgcc tatcagtacc gggtgttccg cgtccaactg 240
cccgatccca acaagttcgg cctgcccgac acctccatct acaaccccga gacccagagg 300
ctggtctggg cttgcgccgg cgtcgagatc gggaggggcc aacccctggg cgtggggttg 360
tccggccacc ccttctacaa caagctggac gataccgagt ccagccacgc agcaaccagc 420
aacgtctccg aagatgtgcg cgataacgtc agcgtggact acaaacaaac ccaactgtgc 480
atcctgggat gcgcacccgc catcggcgag cattgggcca aggggaccgc ctgcaagagc 540
aggcccctga gccaagggga ctgtccaccc ctggagttga agaataccgt gctcgaggac 600
ggcgacatgg tggacaccgg ctacggcgct atggatttct ccaccctcca ggacaccaag 660
tgcgaagtgc ccctcgacat ctgccaaagc atctgcaagt accccgacta cctccagatg 720
agcgccgacc cctacggcga cagcatgttc ttctgtctca gaagggaaca attgttcgcc 780
cgccacttct ggaaccgggc cggcacaatg ggagatacag tcccccagag cctgtacatc 840
aaggggaccg gaatgagggc cagccccggg tcctgcgtct acagcccaag cccctccggg 900
agcatcgtca caagcgatag ccaactcttc aacaagccct actggctcca caaagcccaa 960
ggccacaata acggggtgtg ttggcacaac cagctgttcg tgaccgtcgt ggacacaacc 1020
aggtccacaa acctgaccat ctgcgccagc acccaaagcc ccgtgcccgg ccagtacgac 1080
gccacaaagt tcaaacaata ctctcggcac gtggaagagt acgacctcca attcatcttc 1140
caactctgca ccatcaccct caccgccgac gtgatgagct acatccactc catgaactcc 1200
tccatcctgg aagactggaa tttcggcgtg ccaccacccc ctaccacctc cctcgtcgac 1260
acctacagat tcgtgcagag cgtggccatc acatgccaga aagacgccgc ccccgccgag 1320
aacaaagacc catacgacaa actgaaattc tggaacgtcg acctgaaaga gaaattcagc 1380
ctggatctgg accagtaccc attgggcagg aagttcctcg tgcaagccgg cctcaggaga 1440
aaaccaacaa tcgggcccag gaagaggagc gcccccagcg caaccaccag cagcaagccc 1500
gcaaaaaggg tcagagtgag ggcacgcaaa taaactcgag ctc 1543
<210> 34
<211> 1534
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 34
ctgggtacca tgagcctgtg gaggcccagc gaggccaccg tgtacctgcc ccccgtgccc 60
gtgagcaagg tggtgagcac cgacgagtac gtgaccagga ccaacatcta ctaccacgcc 120
ggcagcgcca ggctgctgac cgtgggccac ccctactaca gcatccccaa gagcgacaac 180
cccaagaaga tcgtggtgcc caaggtgagc ggcctgcagt acagggtgtt cagggtgagg 240
ctgcccgacc ccaacaagtt cggcttcccc gacaccagct tctacaaccc cgagacccag 300
aggctggtgt gggcctgcgt gggcctggag gtgggcaggg gccagcccct gggcgtgggc 360
atcagcggcc accccctgct gaacaagttc gacgacaccg agaacagcaa caggtacgcc 420
ggcggccccg gcaccgacaa cagggagtgc atcagcatgg actacaagca gacccagctg 480
tgcctgctgg gctgcaagcc ccccatcggc gagcactggg gcaagggcag cccctgcagc 540
aacaacgcca tcacccccgg cgactgcccc cccctggagc tgaagaacag cgtgatccag 600
gacggcgaca tggtggacac cggcttcggc gccatggact tcaccgccct gcaggacacc 660
aagagcaacg tgcccctgga catctgcaac agcatctgca agtaccccga ctacctgaag 720
atggtggccg agccctacgg cgacaccctg ttcttctacc tgaggaggga gcagatgttc 780
gtgaggcact tcttcaacag gagcggcacc gtgggcgaga gcgtgcccac cgacctgtac 840
atcaagggca gcggcagcac cgccaccctg gccaacagca cctacttccc cacccccagc 900
ggcagcatgg tgaccagcga cgcccagatc ttcaacaagc cctactggat gcagagggcc 960
cagggccaca acaacggcat ctgctggggc aaccagctgt tcgtgaccgt ggtggacacc 1020
accaggagca ccaacatgag cgtgtgcgcc gccatcgcca acagcgacac caccttcaag 1080
agcagcaact tcaaggagta cctgaggcac ggcgaggagt tcgacctgca gttcatcttc 1140
cagctgtgca agatcaccct gagcgccgac atcatgacct acatccacag catgaacccc 1200
gccatcctgg aggactggaa cttcggcctg accacccccc ccagcggcag cctggaggac 1260
acctacaggt tcgtgaccag ccaggccatc acctgccaga agtccgcccc ccagaagccc 1320
aaggaggacc ccttcaagga ctacgtgttc tgggaggtga acctgaagga gaagttcagc 1380
gccgacctgg accagttccc cctgggcagg aagttcctgc tgcaggccgg ctacagggcc 1440
aggcccaagt tcaaggccgg caagaggagc gcccccagcg ccagcaccac cacccccgcc 1500
aagaggaaga agaccaagaa gtaaactcga gctc 1534
<210> 35
<211> 1528
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 35
ctgggtacca tgagtctgtg gaggagcaat gaggctacag tctacctgcc tcctgtgtct 60
gtgagcaagg tggtgagcac agatgaatat gtgaccagga ccaacatcta ctaccatgct 120
ggctccagca gactgctggc tgtgggacac ccatactatg ccatcaagaa gcaggacagc 180
aacaagattg ctgtgccaaa ggtgtctgga ctccaataca gggtgttcag ggtgaaactg 240
cctgacccaa acaagtttgg ctttcctgac acctccttct atgaccctgc cagccagaga 300
ctggtgtggg cttgtactgg agtggaggtg ggcaggggac aaccactggg agtgggcatc 360
tctggacacc cactgctgaa caaactggat gacacagaga acagcaacaa atatgtgggc 420
aactctggca cagacaacag ggagtgtatc agtatggact acaagcagac ccaactttgt 480
ctgattggct gtagacctcc aattggagaa cactggggca agggcacacc atgtaatgcc 540
aaccaggtga aggctggaga gtgtcctcca ttggaactgc tgaacacagt gctccaagat 600
ggagatatgg tggacacagg ctttggagct atggacttca ccaccctcca agccaacaag 660
tctgatgtgc cactggacat ctgttccagc atctgtaaat accctgacta cctgaaaatg 720
gtgtctgaac catatggaga tatgctgttc ttctacctga ggagggaaca gatgtttgtg 780
agacacctgt tcaacagggc tggcacagtg ggagagacag tgcctgctga cctctacatc 840
aagggcacca caggcaccct gccaagcacc tcctactttc caacaccatc tggcagtatg 900
gtgacctctg atgcccagat tttcaacaag ccatactggc tccaaagggc tcaaggacac 960
aacaatggca tctgttggag caaccaactt tttgtgacag tggtggacac caccaggagc 1020
accaatatga gtgtgtgttc tgctgtgtcc tcctctgaca gcacctacaa gaatgacaac 1080
ttcaaggaat acctgagaca tggagaggaa tatgacctcc aattcatctt ccaactttgt 1140
aagattaccc tgacagcaga tgtgatgacc tacatccaca gtatgaaccc aagcatcttg 1200
gaggactgga actttggact gacacctcct ccatctggca ccttggagga cacctacaga 1260
tatgtgacca gccaggctgt gacttgtcag aagccatctg ccccaaagcc aaaggatgac 1320
ccactgaaaa actacacctt ctgggaggtg gacctgaaag agaagttctc tgctgacctg 1380
gaccagtttc cactgggcag gaagttcctg ctccaagcag gactgaaagc cagaccaaac 1440
ttcagactgg gcaagagggc tgcccctgcc agcaccagca agaagtccag caccaagagg 1500
aggaaggtga agagctaaac tcgagctc 1528
<210> 36
<211> 1537
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 36
ctgggtacca tggctatgtg gaggtcctct gacagtatgg tctacctgcc tcctccatct 60
gtggctaagg tggtgaacac agatgactat gtgaccagga caggcatcta ctactatgct 120
ggctccagca gactgctgac agtgggacac ccatacttca aggtggggat gaatggaggc 180
aggaagcagg acatcccaaa ggtgtctgcc taccaataca gggtgttcag ggtgaccctg 240
cctgacccaa acaagttcag catccctgat gcctccctct acaaccctga gacccagaga 300
ctggtgtggg cttgtgtggg agtggaggtg ggcaggggac aaccactggg agtgggcatc 360
tctggacacc cactctacaa cagacaggat gacacagaga acagcccatt ctccagcacc 420
accaacaagg acagcaggga caatgtgtct gtggactaca agcagaccca actttgtatc 480
attggctgtg tgcctgccat tggagaacac tggggcaagg gcaaggcttg taagccaaac 540
aatgtgagca caggagactg tcctccattg gaactggtga acacaccaat tgaggatgga 600
gatatgattg acacaggcta tggagctatg gactttggag ccctccaaga gaccaagtct 660
gaggtgccac tggacatctg tcagagcatc tgtaaatacc ctgactacct ccaaatgagt 720
gctgatgtct atggagacag tatgttcttc tgtctgagga gggaacaact ttttgccaga 780
cacttctgga acaggggagg gatggtggga gatgccatcc ctgcccaact ctacatcaag 840
ggcacagaca tcagggctaa ccctggctcc tctgtctact gtccaagccc atctggcagt 900
atggtgacct ctgacagcca acttttcaac aagccatact ggctgcacaa ggctcaagga 960
cacaacaatg gcatctgttg gcacaaccaa cttttcctga cagtggtgga caccaccagg 1020
agcaccaact tcaccctgag caccagcatt gagtccagca tcccaagcac ctatgaccca 1080
agcaagttca aggaatacac caggcatgtg gaggaatatg acctccaatt catcttccaa 1140
ctttgtactg tgaccctgac cacagatgtg atgagttaca tccacacaat gaactccagc 1200
atcctggaca actggaactt tgctgtggct cctcctccat ctgcctccct ggtggacacc 1260
tacagatacc tccaatctgc tgccatcact tgtcagaagg atgcccctgc ccctgagaag 1320
aaggacccat atgatggact gaagttctgg aatgtggacc tgagggagaa gttctccttg 1380
gaactggacc agtttccact gggcaggaag ttcctgctcc aagccagggt gaggaggaga 1440
ccaaccattg gaccaaggaa gagacctgct gccagcacct cctcctcctc tgccaccaaa 1500
cacaagagga agagggtgag caagtaaact cgagctc 1537
<210> 37
<211> 1543
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 37
ctgggtacca tggctctgtg gagaccatct gacagcacag tctacctgcc tcctccatct 60
gtggcaaggg tggtgaacac agatgactat gtgagcagga ccagcatctt ctaccatgct 120
ggctccagca gactgctgac agtgggcaac ccatacttca gggtggtgcc aagtggagca 180
ggcaacaagc aggctgtgcc aaaggtgtct gcctaccaat acagggtgtt cagggtggct 240
ctgcctgacc caaacaagtt tggactgcct gacagcacca tctacaaccc tgagacccag 300
agactggtgt gggcttgtgt ggggatggag attggcaggg gacaaccact gggcattgga 360
ctgtctggac acccattcta caacaaactg gatgacacag agtctgccca tgctgccaca 420
gcagtgatta cccaggatgt gagggacaat gtgtctgtgg actacaagca gacccaactt 480
tgtatcctgg gctgtgtgcc tgccattgga gaacactggg ctaagggcac cctgtgtaag 540
cctgcccaac tccaacctgg agactgtcct ccattggaac tgaaaaacac catcattgag 600
gatggagata tggtggacac aggctatgga gctatggact tcagcaccct ccaagacacc 660
aagtgtgagg tgccactgga catctgtcag agcatctgta aataccctga ctacctccaa 720
atgagtgctg acccatatgg agacagtatg ttcttctgtc tgaggaggga acaacttttt 780
gccagacact tctggaacag ggctggagtg atgggagaca cagtgccaac agacctctac 840
atcaagggca cctctgccaa tatgagggag acacctggct cctgtgtcta cagcccaagc 900
ccatctggca gcatcaccac ctctgacagc caacttttca acaagccata ctggctgcac 960
aaggctcaag gacacaacaa tggcatctgt tggcacaacc aactttttgt gacagtggtg 1020
gacaccacca ggagcaccaa cctgaccctg tgtgccagca cccagaaccc tgtgccaaac 1080
acctatgacc caaccaagtt caagcactac agcaggcatg tggaggaata tgacctccaa 1140
ttcatcttcc aactttgtac catcaccctg acagcagagg tgatgagtta catccacagt 1200
atgaactcca gcatcttgga gaactggaac tttggagtgc ctcctcctcc aaccacctcc 1260
ctggtggaca cctacaggtt tgtccagtct gtggctgtga cttgtcagaa ggacaccaca 1320
cctcctgaga agcaggaccc atatgacaaa ctgaagttct ggacagtgga cctgaaagag 1380
aagttctcct ctgacctgga ccaataccca ctgggcagga agttcctggt ccaggctgga 1440
ctgaggagga gaccaaccat tggaccaagg aagagacctg ctgccagcac cagcacagcc 1500
agcagacctg ccaagagggt gaggattagg agcaagaagt aaa 1543
<210> 38
<211> 1534
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 38
ctgggtacca tggctctgtg gaggaccaat gacagcaagg tctacctgcc tcctgcccct 60
gtgagcagga ttgtgaacac agaggaatac atcaccagga caggcatcta ctactatgct 120
ggctccagca gactgattac cctgggacac ccatactttc caatcccaaa gaccagcacc 180
agggctgcca tcccaaaggt gtctgccttc caatacaggg tgttcagggt ccaacttcct 240
gacccaaaca agtttggact gcctgaccca aacctctaca accctgacac agacagactg 300
gtgtggggct gtgtgggagt ggaggtgggc aggggacaac cactgggagt gggactgtct 360
ggacacccac tgttcaacaa atatgatgac acagagaaca gcaggattgc caatggcaat 420
gcccaacagg atgtgaggga caacacctct gtggacaaca agcagaccca actttgtatc 480
attggctgtg cccctccaat tggagaacac tggggcattg gcaccacttg taagaacaca 540
cctgtgcctc ctggagactg tcctccattg gaactggtgt cctctgtgat tcaggatgga 600
gatatgattg acacaggctt tggagctatg gactttgctg ccctccaagc caccaagtct 660
gatgtgccac tggacatcag ccagtctgtg tgtaaatacc ctgactacct gaaaatgagt 720
gctgacacct atggcaacag tatgttcttc cacctgagga gggaacagat ttttgccaga 780
cactactaca acaaactggt gggagtggga gaggacatcc caaatgacta ctacatcaag 840
ggctctggca atggcaggga cccaattgag tcctacatct actctgccac accatctggc 900
agtatgatta cctctgacag ccagattttc aacaagccat actggctgca cagggctcaa 960
ggacacaaca atggcatctg ttggaacaac caacttttca tcacttgtgt ggacaccacc 1020
aggagcacca acctgaccat cagcacagcc acagcagcag tgagcccaac cttcacacca 1080
agcaacttca agcaatacat cagacatgga gaggaatatg aactccaatt catcttccaa 1140
ctttgtaaga ttaccctgac cacagaggtg atggcttacc tgcacacaat ggacccaacc 1200
atcttggaac agtggaactt tggactgacc ctgcctccat ctgcctcctt ggaggatgcc 1260
tacaggtttg tgaggaatgc tgccacctcc tgtcagaagg acacacctcc acaggctaag 1320
cctgacccac tggctaaata caagttctgg gatgtggacc tgaaagagag gttctccctg 1380
gacctggacc agtttgccct gggcaggaag ttcctgctcc aagtgggagt ccagaggaag 1440
ccaagacctg gactgaaaag acctgcctcc tctgcctcct cctcctcctc ctcctctgcc 1500
aagaggaaga gggtgaagaa gtaaactcga gctc 1534
<210> 39
<211> 1531
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 39
ctgggtacca tgagcgtgtg gaggcccagc gaggccaccg tgtacctgcc ccccgtgccc 60
gtgagcaagg tggtgagcac cgacgagtac gtgagcagga ccagcatcta ctactacgcc 120
ggcagcagca ggctgctgac cgtgggccac ccctacttca gcatcaagaa caccagcagc 180
ggcaacggca agaaggtgct ggtgcccaag gtgagcggcc tgcagtacag ggtgttcagg 240
atcaagctgc ccgaccccaa caagttcggc ttccccgaca ccagcttcta caaccccgag 300
acccagaggc tggtgtgggc ctgcaccggc ctggagatcg gcaggggcca gcccctgggc 360
gtgggcatca gcggccaccc cctgctgaac aagttcgacg acaccgagac cagcaacaag 420
tacgccggca agcccggcat cgacaacagg gagtgcctga gcatggacta caagcagacc 480
cagctgtgca tcctgggctg caagcccccc atcggcgagc actggggcaa gggcaccccc 540
tgcaacaaca acagcggcaa ccccggcgac tgcccccccc tgcagctgat caacagcgtg 600
atccaggacg gcgacatggt ggacaccggc ttcggctgca tggacttcaa caccctgcag 660
gccagcaaga gcgacgtgcc catcgacatc tgcagcagcg tgtgcaagta ccccgactac 720
ctgcagatgg ccagcgagcc ctacggcgac agcctgttct tcttcctgag gagggagcag 780
atgttcgtga ggcacttctt caacagggcc ggcaccctgg gcgaccccgt gcccggcgac 840
ctgtacatcc agggcagcaa cagcggcaac accgccaccg tgcagagcag cgccttcttc 900
cccaccccca gcggcagcat ggtgaccagc gagagccagc tgttcaacaa gccctactgg 960
ctgcagaggg cccagggcca caacaacggc atctgctggg gcaaccagct gttcgtgacc 1020
gtggtggaca ccaccaggag caccaacatg accctgtgcg ccgaggtgaa gaaggagagc 1080
acctacaaga acgagaactt caaggagtac ctgaggcacg gcgaggagtt cgacctgcag 1140
ttcatcttcc agctgtgcaa gatcaccctg accgccgacg tgatgaccta catccacaag 1200
atggacgcca ccatcctgga ggactggcag ttcggcctga cccccccccc cagcgccagc 1260
ctggaggaca cctacaggtt cgtgaccagc accgccatca cctgccagaa gaacaccccc 1320
cccaagggca aggaggaccc cctgaaggac tacatgttct gggaggtgga cctgaaggag 1380
aagttcagcg ccgacctgga ccagttcccc ctgggcagga agttcctgct gcaggccggc 1440
ctgcaggcca ggcccaagct gaagaggccc gccagcagcg cccccaggac cagcaccaag 1500
aagaagaagg tgaagaggta aactcgagct c 1531
<210> 40
<211> 1519
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 40
ctgggtacca tggctacctg gagaccatct gagaacaagg tctacctgcc tccaacacct 60
gtgagcaagg tggtggctac agactcctat gtgaagagga ccagcatctt ctaccatgct 120
ggctccagca gactgctggc tgtgggacac ccatactact ctgtgaccaa ggacaacacc 180
aagaccaaca tcccaaaggt gtctgcctac caatacaggg tgttcagggt gagactgcct 240
gacccaaaca agtttggact gcctgacacc aacatctaca accctgacca ggagagactg 300
gtgtgggctt gtgtgggatt ggaggtgggc aggggacaac cactgggagc aggactgtct 360
ggacacccac tgttcaacag actggatgac acagagtcca gcaacctggc taacaacaat 420
gtgattgagg acagcaggga caacatctct gtggatggca agcagaccca actttgtatt 480
gtgggctgta ctcctgctat gggagaacac tggaccaagg gagcagtgtg taagagcacc 540
caggtgacca caggagactg tcctccactg gctctgataa acacaccaat tgaggatgga 600
gatatgattg acacaggctt tggagctatg gacttcaagg tgctccaaga gagcaaggct 660
gaggtgccac tggacattgt ccagagcact tgtaaatacc ctgactacct gaaaatgagt 720
gctgatgcct atggagacag tatgtggttc tacctgagga gggaacaact ttttgccaga 780
cactacttca acagggctgg caaggtggga gagaccatcc ctgctgaact ctacctgaaa 840
ggcagcaatg gcagggaacc tcctccatcc tctgtctatg tggctacacc atctggcagt 900
atgattacct ctgaggctca acttttcaac aagccatact ggctccaaag ggctcaagga 960
cacaacaatg gcatctgttg gggcaaccaa ctttttgtga cagtggtgga caccaccagg 1020
agcaccaata tgaccatcag cacagccaca gaacaactta gcaaatatga tgccaggaag 1080
ataaaccaat acctgaggca tgtggaggaa tatgaactcc aatttgtgtt ccaactttgt 1140
aagattaccc tgtctgctga ggtgatggct tacctgcaca atatgaatgc caacctgttg 1200
gaggactgga acattggact gagccctcct gtggctacct ccttggagga caaatacaga 1260
tatgtgagga gcacagccat cacttgtcag agggaacaac ctccaacaga gaagcaggac 1320
ccactggcta aatacaagtt ctgggatgtg aacctccaag actccttcag cacagacctg 1380
gaccagtttc cactgggcag gaagttcctg atgcaacttg gcaccaggag caagcctgct 1440
gtggctacca gcaagaagag gtctgcccca accagcacca gcacacctgc caagaggaag 1500
aggaggtaaa ctcgagctc 1519
<210> 41
<211> 1507
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность является искусственно синтезированной
<400> 41
ctgggtacca tgagcgtgtg gaggcccagc gaggccaccg tgtacctgcc ccccgtgccc 60
gtgagcaagg tggtgagcac cgacgagtac gtgagcagga ccagcatcta ctactacgcc 120
ggcagcagca ggctgctggc cgtgggcaac ccctacttca gcatcaagag ccccaacaac 180
aacaagaagg tgctggtgcc caaggtgagc ggcctgcagt acagggtgtt cagggtgagg 240
ctgcccgacc ccaacaagtt cggcttcccc gacaccagct tctacaaccc cgacacccag 300
aggctggtgt gggcctgcgt gggcctggag atcggcaggg gccagcccct gggcgtgggc 360
gtgagcggcc acccctacct gaacaagttc gacgacaccg agaccagcaa caggtacccc 420
gcccagcccg gcagcgacaa cagggagtgc ctgagcatgg actacaagca gacccagctg 480
tgcctgatcg gctgcaagcc ccccaccggc gagcactggg gcaagggcgt ggcctgcaac 540
aacaacgccg ccgccaccga ctgccccccc ctggagctgt tcaacagcat catcgaggac 600
ggcgacatgg tggacaccgg cttcggctgc atggacttcg gcaccctgca ggccaacaag 660
agcgacgtgc ccatcgacat ctgcaacagc acctgcaagt accccgacta cctgaagatg 720
gccagcgagc cctacggcga cagcctgttc ttcttcctga ggagggagca gatgttcgtg 780
aggcacttct tcaacagggc cggcaagctg ggcgaggccg tgcccgacga cctgtacatc 840
aagggcagcg gcaacaccgc cgtgatccag agcagcgcct tcttccccac ccccagcggc 900
agcatcgtga ccagcgagag ccagctgttc aacaagccct actggctgca gagggcccag 960
ggccacaaca acggcatctg ctggggcaac cagctgttcg tgaccgtggt ggacaccacc 1020
aggagcacca acatgaccct gtgcaccgag gtgaccaagg agggcaccta caagaacgac 1080
aacttcaagg agtacgtgag gcacgtggag gagtacgacc tgcagttcgt gttccagctg 1140
tgcaagatca ccctgaccgc cgagatcatg acctacatcc acaccatgga cagcaacatc 1200
ctggaggact ggcagttcgg cctgaccccc ccccccagcg ccagcctgca ggacacctac 1260
aggttcgtga ccagccaggc catcacctgc cagaagaccg ccccccccaa ggagaaggag 1320
gaccccctga acaagtacac cttctgggag gtgaacctga aggagaagtt cagcgccgac 1380
ctggaccagt tccccctggg caggaagttc ctgctgcaga gcggcctgaa ggccaagccc 1440
aggctgaaga ggagcgcccc caccaccagg gcccccagca ccaagaggaa gaaggtgaag 1500
aagtaaa 1507
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЙ БЕЛОК L1 ПАПИЛЛОМАВИРУСА | 2020 |
|
RU2808002C2 |
| ПОЛИВАЛЕНТНАЯ ИММУНОГЕННАЯ КОМПОЗИЦИЯ ПРОТИВ ПАПИЛЛОМАВИРУСА ЧЕЛОВЕКА | 2020 |
|
RU2806424C2 |
| РЕКОМБИНАНТНЫЕ ВАКЦИНЫ ОТ FMDV И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2745373C2 |
| УЛУЧШЕНИЕ ИММУНОГЕННОСТИ ПЕПТИДА L2 ВПЧ | 2017 |
|
RU2743016C2 |
| ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ С ВЫСОКОПЛОТНЫМ ПОКРЫТИЕМ ДЛЯ ИНДУКЦИИ ЭКСПРЕССИИ АНТИТЕЛ | 2017 |
|
RU2813282C2 |
| СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ БЕЛКОВОГО/ПЕПТИДНОГО АНТИГЕНА | 2021 |
|
RU2830627C1 |
| МУТАНТЫ ГЕМАГГЛЮТИНИНА ВИРУСА ГРИППА | 2019 |
|
RU2801708C2 |
| МУТАНТЫ ГЕМАГГЛЮТИНИНА ВИРУСА ГРИППА | 2019 |
|
RU2809237C2 |
| АНТАГОНИСТЫ NGF ДЛЯ МЕДИЦИНСКОГО ИСПОЛЬЗОВАНИЯ | 2020 |
|
RU2829812C2 |
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
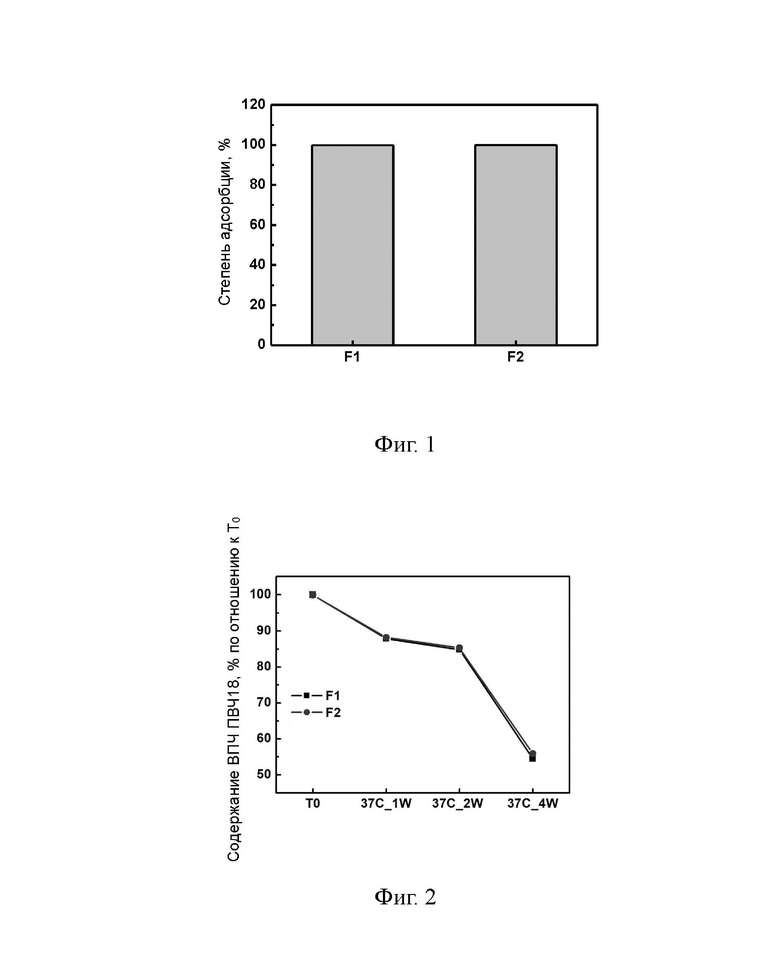
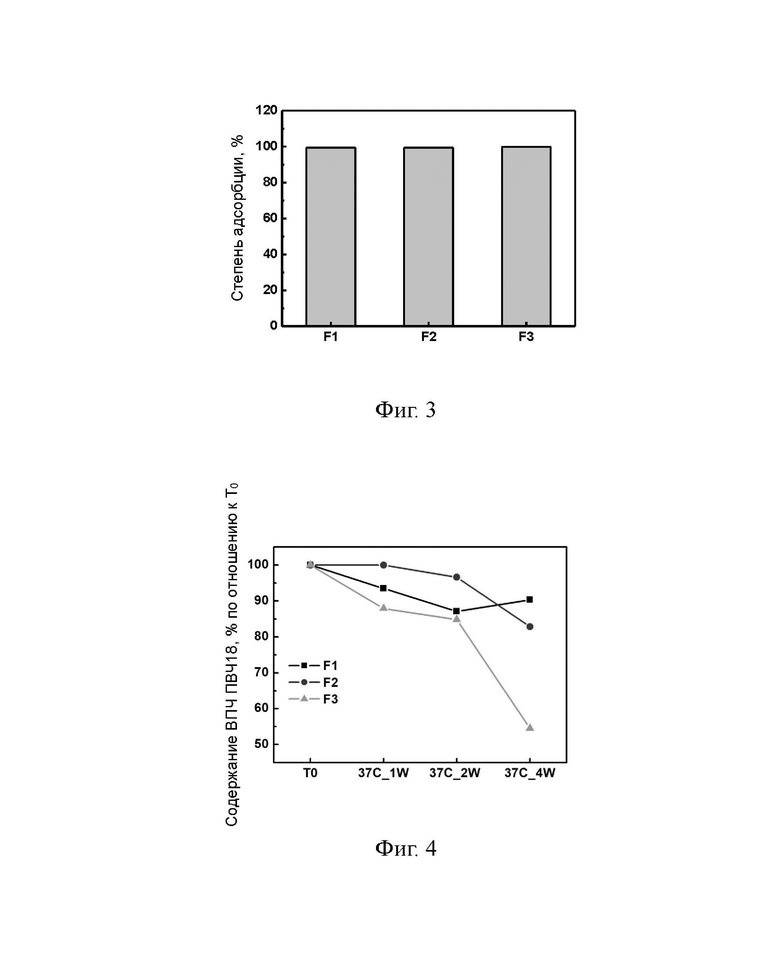
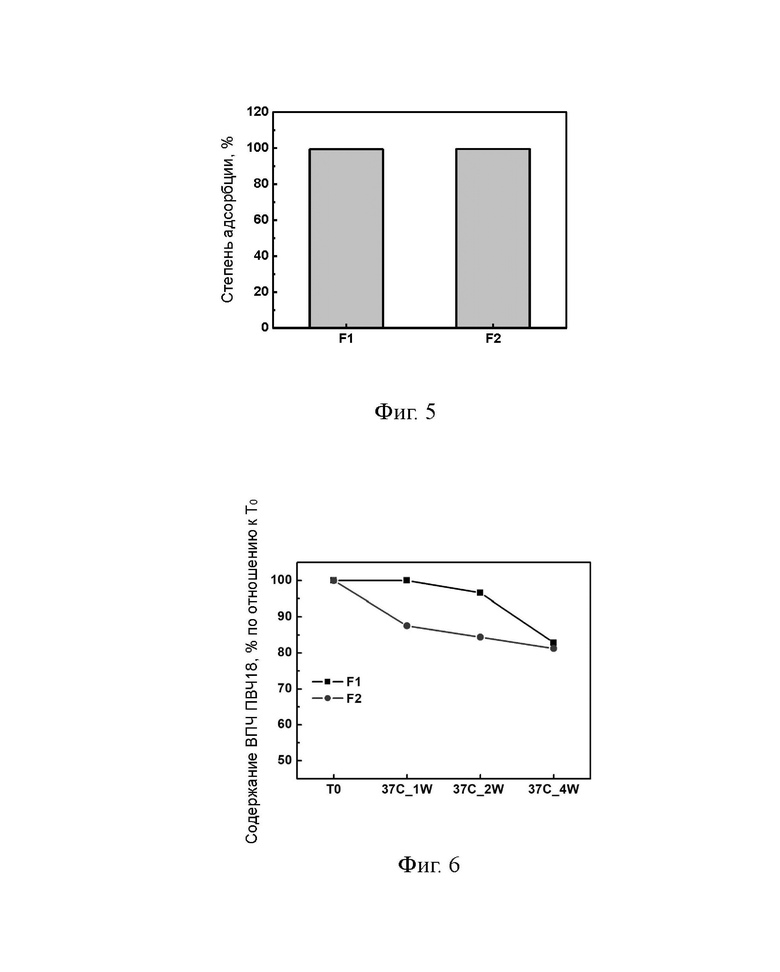
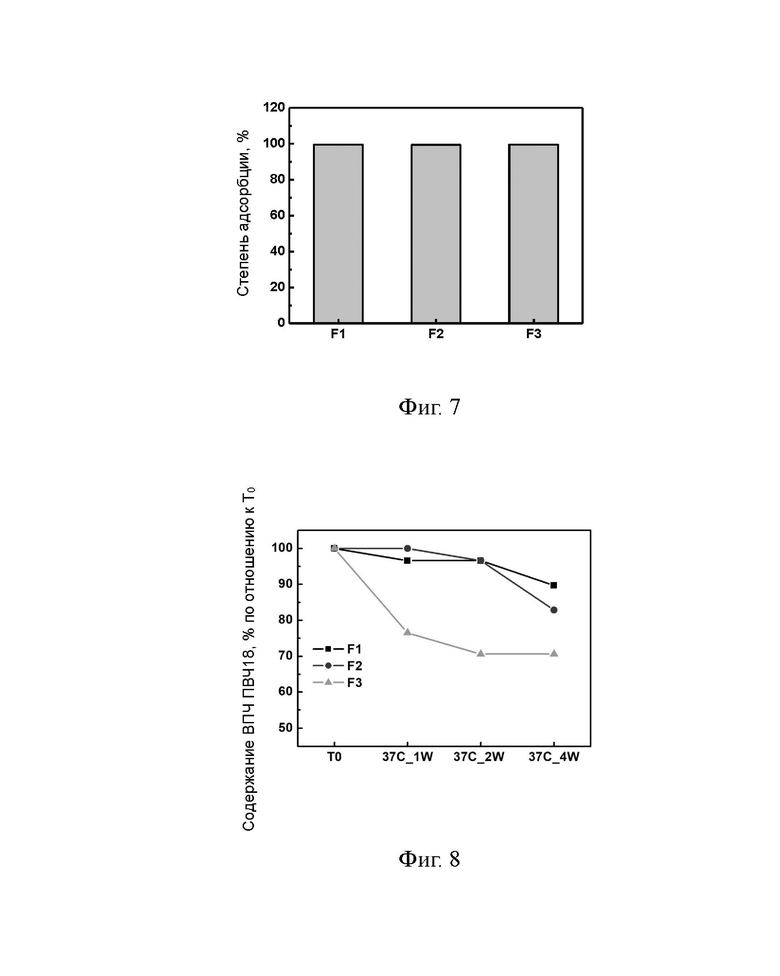
Изобретение относится к медицинской биотехнологии. Предложен стабильный препарат поливалентной вакцины из вирусоподобных частиц папилломавируса человека для профилактики заболеваний или инфекций, связанных с ПВЧ. Стабильный препарат содержит: (а) множество вирусоподобных частиц папилломавируса человека, где концентрация вирусоподобных частиц папилломавируса любого отдельного типа, входящих в состав поливалентных вирусоподобных частиц папилломавируса, составляет от 40 до 120 мкг/мл; (б) адъювант, представляющий собой фосфат алюминия; (в) гистидиновый буфер концентрации от 10 до 26 мМ; (г) регулятор осмотического давления, представляющий собой хлорид натрия концентрации от 150 до 320 мМ; и, необязательно, (д) сурфактант, представляющий собой полисорбат 80 концентрации не более 0,3 мг/мл, при этом указанные вирусоподобные частицы папилломавируса человека выбраны из вирусоподобных частиц ПВЧ, образованных белками L1 ПВЧ типов 6, 11, 16, 18, 31, 33, 45, 52 и 58; и одних или более вирусоподобных частиц ПВЧ, образованных белками L1 других патогенных типов ПВЧ, выбранных из типов ПВЧ 35, 39, 51, 56 и 59, при этом указанные вирусоподобные частицы папилломавируса человека адсорбированы на адъюванте. Предложен способ профилактики связанного с ПВЧ заболевания или инфекции, включающий введение субъекту указанного препарата поливалентной вакцины из вирусоподобных частиц папилломавируса человека, а также применение указанного препарата для получения вакцины для профилактики связанного с ПВЧ заболевания или инфекции. Препарат способен повышать стабильность вакцины и продлевать срок действия вакцины в водном препарате. 3 н. и 14 з.п. ф-лы, 17 табл., 8 ил., 6 пр.
1. Стабильный препарат поливалентной вакцины из вирусоподобных частиц папилломавируса человека (ПВЧ) для профилактики заболеваний или инфекций, связанных с ПВЧ, содержащий:
(а) множество вирусоподобных частиц папилломавируса человека, где концентрация вирусоподобных частиц папилломавируса любого отдельного типа, входящих в состав поливалентных вирусоподобных частиц папилломавируса, составляет от 40 до 120 мкг/мл;
(б) адъювант, представляющий собой фосфат алюминия;
(в) гистидиновый буфер концентрации от 10 до 26 мМ;
(г) регулятор осмотического давления, представляющий собой хлорид натрия концентрации от 150 до 320 мМ; и, необязательно,
(д) сурфактант, представляющий собой полисорбат 80 концентрации не более 0,3 мг/мл,
при этом указанные вирусоподобные частицы папилломавируса человека выбраны из вирусоподобных частиц ПВЧ, образованных белками L1 ПВЧ типов 6, 11, 16, 18, 31, 33, 45, 52 и 58; и
одних или более вирусоподобных частиц ПВЧ, образованных белками L1 других патогенных типов ПВЧ, выбранных из типов ПВЧ 35, 39, 51, 56 и 59,
при этом указанные вирусоподобные частицы папилломавируса человека адсорбированы на адъюванте.
2. Препарат по п. 1, отличающийся тем, что
адъювантом, представляющим собой фосфат алюминия, является гидроксифосфат алюминия (AlPO4).
3. Препарат по п. 1 или 2, отличающийся тем, что:
(a) общая концентрация вирусоподобных частиц папилломавирусов всех типов составляет от 80 до 740 мкг/мл;
(б) концентрация буфера составляет 10 мМ, 18 мМ или 26 мМ;
(в) концентрация регулятора осмотического давления составляет 150 мМ или 320 мМ;
(г) концентрация сурфактанта составляет от 0 до 0,02 вес.%;
(д) концентрация адъюванта составляет 1,0 мг/мл;
(е) pH препарата находится в диапазоне от 5,9 до 6,5, предпочтительно 5,9, 6,2 или 6,5.
4. Препарат по любому из пп. 1-3, содержащий 0,74 мг/мл всех вирусоподобных частиц папилломавирусов всех типов, 1,0 мг/мл адъюванта фосфата алюминия, 18 мМ гистидинового буфера, 320 мМ хлорида натрия, рН 6,2; и, необязательно, полисорбат 80 в концентрации не более 0,3 мг/мл.
5. Препарат по п. 4, отличающийся тем, что по меньшей мере одна из вирусоподобных частиц ПВЧ представляет собой химерную вирусоподобную частицу ПВЧ, содержащую химерный белок L1 ПВЧ; при этом указанный химерный белок ПВЧ L1 содержит от его N-конца до его C-конца:
a) N-концевой фрагмент, полученный из белка L1 вируса папилломы первого типа, при этом указанный N-концевой фрагмент сохраняет иммуногенность белка L1 папилломавируса первого типа и указанный белок L1 папилломавируса первого типа выбран из ПВЧ типов 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56, 58 и одного или нескольких других патогенных типов ПВЧ,
при этом белок L1 папилломавируса первого типа выбран из белка L1 ПВЧ типа 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56 или 58; предпочтительно, чтобы его природная последовательность представляла собой последовательность аминокислот, кодируемую кодирующим геном, приведенную в SEQ ID No: 30, SEQ ID No: 31, SEQ ID No: 32, SEQ ID No: 33, SEQ ID No: 34, SEQ ID No: 35, SEQ ID No: 36, SEQ ID No: 37, SEQ ID No: 38, SEQ ID No: 39, SEQ ID No: 40 или SEQ ID No: 41 соответственно; и
б) С-концевой фрагмент, полученный из белка L1 папилломавируса второго типа, при этом белок L1 второго типа папилломавируса имеет лучший уровень экспрессии и растворимости по сравнению с белками L1 других типов,
при этом белок L1 папилломавируса второго типа выбран из белка L1 ПВЧ типа 16, 28, 33, 59 или 68, предпочтительно белок L1 папилломавируса второго типа выбран из группы, состоящей из белков L1 ПВЧ типа 33 или 59;
при этом указанный химерный белок обладает иммуногенностью белка L1 первого типа папилломавируса.
6. Препарат по п. 5, отличающийся тем, что
указанный N-концевой фрагмент представляет собой фрагмент, полученный путем укорочения С-конца природной последовательности указанного белка L1 папилломавируса первого типа в любом положении аминокислоты в пределах его области α5, или фрагмент, имеющий по меньшей мере 98% идентичность с ним; и
указанный С-концевой фрагмент представляет собой фрагмент, полученный путем укорочения N-конца природной последовательности указанного белка L1 папилломавируса второго типа в любом положении аминокислоты в пределах его области α5, или функциональный вариант, полученный в результате дополнительных мутаций, делеций и/или дополнений к указанному фрагменту.
7. Препарат по п. 6, отличающийся тем, что указанный С-концевой фрагмент содержит одну или несколько последовательностей ядерной локализации.
8. Препарат по п. 5, отличающийся тем, что указанный С-концевой фрагмент представляет собой SEQ ID No: 1; или его фрагмент, имеющий длину m1 аминокислот, предпочтительно фрагмент, содержащий аминокислоты 1-m1 SEQ ID No: 1, где m1 - целое число от 8 до 26; или этот С-концевой фрагмент представляет собой SEQ ID No: 2, или его фрагменты, имеющие длину m2 аминокислот,
предпочтительно фрагмент, содержащий аминокислоты 1-m2 SEQ ID No: 2, где m2 - целое число от 13 до 31.
9. Препарат по п. 5, отличающийся тем, что указанный С-концевой фрагмент представляет собой SEQ ID No: 3; или его фрагмент, имеющий длину n аминокислот, предпочтительно фрагмент, содержащий аминокислоты 1-n SEQ ID No: 3; где n - целое число от 16 до 38.
10. Препарат по п. 5, отличающийся тем, что
указанный N-концевой фрагмент белка L1 ПВЧ типа 6 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 4 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 11 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 5 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 16 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 6 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 18 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 7 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 31 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 8 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 35 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 9 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 39 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 10 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 45 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 11 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 51 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 12 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 52 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 13 в любом положении аминокислоты в пределах его области α5;
указанный N-концевой фрагмент белка L1 ПВЧ типа 56 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 14 в любом положении аминокислоты в пределах его области α5; и
указанный N-концевой фрагмент белка L1 ПВЧ типа 58 имеет 98%, 98,5%, 99%, 99,5%, 99% или 100% идентичность с фрагментом, полученным путем укорочения C-конца последовательности, представленной в SEQ ID No: 15 в любом положении аминокислоты в пределах его области α5.
11. Препарат по п. 5, отличающийся тем, что С-конец N-концевого фрагмента соединен непосредственно с N-концом С-концевого фрагмента или соединен с ним посредством линкера.
12. Препарат по п. 5, отличающийся тем, что, когда С-конец указанного N-концевого фрагмента соединен с N-концом указанного С-концевого фрагмента, непрерывная последовательность аминокислот RKFL присутствует в диапазоне плюс-минус 4 положений аминокислот от сайта сплайсинга,
предпочтительно непрерывная последовательность аминокислот LGRKFL присутствует в диапазоне плюс-минус 6 положений аминокислот от сайта сплайсинга.
13. Препарат по п. 5, отличающийся тем, что
химерные белки L1 ПВЧ типа 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56 и 58 имеют 98%, 98,5%, 99%, 99,5% или 100% идентичность с SEQ ID No: 16, SEQ ID No: 17, SEQ ID No: 18, SEQ ID No: 19, SEQ ID No: 20, SEQ ID No: 21, SEQ ID No: 22, SEQ ID No: 23, SEQ ID No: 24, SEQ ID No: 25, SEQ ID No: 26 и SEQ ID No: 27 соответственно; и
белок L1 ПВЧ типа 33 и белок L1 ПВЧ типа 59 имеет 98%, 98,5%, 99%, 99,5% или 100% идентичность с SEQ ID No: 28 и SEQ ID No: 29 соответственно.
14. Препарат по п. 13, содержащий
химерные белки L1 ПВЧ типа 6, 11, 16, 18, 31, 35, 39, 45, 51, 52, 56 и 58, имеющие последовательности аминокислот, показанные в SEQ ID No: 16, SEQ ID No: 17, SEQ ID No: 18, SEQ ID No: 19, SEQ ID No: 20, SEQ ID No: 21, SEQ ID No: 22, SEQ ID No: 23, SEQ ID No: 24, SEQ ID No: 25, SEQ ID No: 26 и SEQ ID No: 27 соответственно; и
белок L1 ПВЧ типа 33 и белок L1 ПВЧ типа 59, имеющие последовательности аминокислот, показанные в SEQ ID No: 28 и SEQ ID No: 29 соответственно.
15. Препарат вакцины против папилломавируса по пп. 1-14, отличающийся тем, что может стабильно храниться при температуре от 2 до 8°С не менее 24 месяцев и при 25°С не менее 16 недель.
16. Способ профилактики связанного с ПВЧ заболевания или инфекции, включающий введение субъекту препарата по любому из пп. 1-15.
17. Применение препарата по любому из пп. 1-15 для получения вакцины для профилактики связанного с ПВЧ заболевания или инфекции.
| CN 102349996 A, 15.02.2012 | |||
| N | |||
| D | |||
| Christensen et al., Hybrid papillomavirus LI molecules assemble into virus-like particles that reconstitute conformational epitopes and induce neutralizing antibodies to distinct HPV types, Virology 291, Issue 2, 20 December 2001,324-334 (2001), doi:10.1006/viro.2001.1220, см | |||
| с | |||
| Водяной двигатель | 1921 |
|
SU325A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Г.Н | |||
| МИНКИНА, | |||
Авторы
Даты
2024-11-26—Публикация
2022-01-13—Подача