Изобретение относится к порошковой металлургии, в частности, к способам электролитического получения порошков силицидов циркония для изготовления функциональных материалов различного назначения.
В настоящее время существует устойчивый спрос на керамические и композиционные материалы, обладающие повышенной устойчивостью к химическому, термическому, механическому воздействию и другим видам нагрузок. Например, керамические и композиционные материалы с добавками карбидов, боридов и силицидов циркония привлекают большое внимание как сверхвысокотемпературные конструкционные материалы для возможного применения в аэрокосмических аппаратах, реактивных двигателях или сверхзвуковых аппаратах в экстремальных условиях. Благодаря низкому сечению поглощения нейтронов и слабой чувствительности к повреждениям, вышеперечисленные материалы могут выступать в качестве инертного матричного материала в энергетических реакторах.
Силициды циркония обладают устойчивостью к окислению в агрессивных средах и при высоких температурах, высокой стойкостью к термоударам, высокой тепло- и электропроводностью. Все это обуславливает высокий спрос на данные материалы в различных областях применения. Однако на сегодняшний день способы физического получения силицидов циркония представляются крайне дорогими, ввиду необходимости предварительного получения чистых циркония и кремния. Кроме того, для повышения эффективности использования в керамических и композиционных материалах силициды циркония должны быть представлены субмикронными и наноразмерными частицами, что не всегда может быть достигнуто физическими методами в условиях высоких давлений (до 50 МПа) и температур (до 1900°С), приводящих к их спеканию и агломерации в более крупные частицы.
Из способов получения силицидов циркония, осуществляемых при относительно низкой температуре и давлении, можно отметить способы металлотермического и твердофазного синтеза.
Известен способ получения порошков силицидов циркония, включающий механохимическое смешение порошков магния и хлорида натрия со средним размером частиц 40-50 мкм с порошками ZrSiO4 (размер частиц 150 мкм) или с порошками ZrO2 (размер частиц 1 мкм) и SiO2 (размер частиц 45 мкм) с последующей выдержкой смеси в реакторе с избыточным давлением 2,5 МПа [1]. Способ является относительно простым в исполнении, при этом характеризуется такими недостатками как необходимость предварительного получения чистых порошков, в частности магния, относительно высокими и неконтролируемыми температурами в зоне реакции, а также наличием в продуктах синтеза трудноудаляемых соединений состава Mg-Zr-O. Аналогичными недостатками характеризуются способы получения порошков силицидов циркония при использовании алюминия и лития вместо магния в качестве восстановителя.
Например, известен способ получения силицидов циркония, включающий смешение порошка высокочистого циркония со средним размером частиц от 1 до 5 мкм с порошком высокочистого карбида кремния со средним размером частиц около 0,5 мкм, изотермическую выдержку полученной смеси при температуре от 800 до 1000°С в инертной атмосфере в течение 2-6 часов [2]. Способ является наиболее простым в исполнении, но предполагает использование высокочистых микронных и субмикронных исходных порошков, получение и хранение которых представляется дорогостоящим. Более того в результате синтеза образуются лишь смеси силицидов циркония с непрореагировавшими исходными порошками, что указывает на низкую эффективность процесса и невозможность осуществления способа с использованием более крупных порошков исходных реагентов.
Силициды циркония могут быть получены электролитическими методами в расплавленных солях при существенно меньшей температуре и при меньших энергозатратах. На это указывают многочисленные способы получения индивидуальных кремния и циркония.
Известен способ электролитического получения циркония в расплавленных солях, включающий электролиз галогенидно-оксидного расплава CaCl2-NaCl эвтектического состава в корундовом реакторе в атмосфере аргона при температуре 850°С и постоянном напряжении 3,1 В между анодом и катодом [3]. В известном способе при электролизе в качестве анода используют графитовый стержень, а в качестве катода - предварительно спрессованные таблетки ZrSiO4/C на проволоке из никеля. Известным способом могут быть получены смеси ZrSi, ZrC и SiC со средним размером частиц около 50 нм. Недостатками способа являются необходимость предварительного прессования таблеток ZrSiO4/C, относительно сложная конструкция реактора, низкая скорость процесса, отсутствие возможности получения силицидов циркония без карбидов, высокая вероятность получения целевых продуктов с наличием трудноотделяемых примесей, содержащих CaO, соединения Ca-Si-O, Ca-Zr-O, а также Ca-Al-O вследствие использования корундового (Al2O3) реактора.
Известен способ электролитического получения циркония в расплавленных солях, включающий электролиз галогенидно-оксидного расплава CaCl2-NaCl эвтектического состава в корундовом реакторе в атмосфере аргона при температуре 850°С и постоянном напряжении 2,8 В между анодом и катодом [4]. При электролизе в качестве анода используют графитовый стержень, а в качестве катода - предварительно спрессованные таблетки ZrSiO4/C на стальном токоподводе. Способ позволяет получить порошки с размером частиц от 50 нм до 2 мкм, а также волокна диаметром от 100 до 400 нм, представленные смесью ZrSi, ZrC и SiC с промежуточными продуктами электролиза Ca-Si-O и Ca-Zr-O. Способ характеризуется аналогичными недостатками, при этом помимо алюминия в продукте также появляется примесь железа.
Наиболее близком к заявленному является способ электролитического получения порошков силицидов циркония в расплавленных солях, включающий электролиз расплавленного электролита KCl-KF с добавками K2SiF6 и K2ZrF6 в атмосфере аргона при температуре от 700 до 750°С [5]. Электролиз с использованием графитового катода ведут при катодной плотности тока 0,8-1,5 А/см2 в области величин потенциала на 0,3-0,5 В положительнее потенциала электровосстановления ионов кремния. Описанным способом были получены порошки силицидов циркония (ZrSi, ZrSi2) со средним размером частиц от 0,5 до 10 мкм. Преимуществами известного способа являются относительно низкая температура и возможность получения чистых порошков силицидов циркония без дополнительного включения исходных реагентов и промежуточных продуктов. В то же время, присутствие в расплаве значительного количества KF приводит, во-первых, к необходимости проведения предварительных энергоемких операций по очистке соли от влаги, и, во-вторых, к повышенной коррозии конструкционных материалов реактора и появлению примесей в расплавленном электролите и катодном продукте. Также не рассмотрена возможность использования в качестве источников циркония и кремния оксидных реагентов, что позволило бы исключить необходимость периодической корректировки состава электролита и операции предварительного получения фторцирконата и фторсиликата калия из оксидов.
Технической проблемой, на решение которой направлено изобретение, является разработка способа электролитического получения порошков силицидов циркония с минимизацией энергетических затрат и возможностью использования оксидных реагентов в качестве источников циркония и кремния.
Технический результат заключается в упрощении и снижении энергетических затрат за счет исключения химически агрессивного компонента из состава электролита и необходимости его предварительной очистки, а также в обеспечении возможности получения силицидов циркония непосредственно из наиболее дешевого и доступного оксидного сырья.
Для решения проблемы предлагается способ электролитического получения порошков силицидов циркония в расплавленных солях, который, как и прототип, включает электролиз расплавленного электролита при температуре с использованием графитового катода с контролем катодной плотности тока и потенциала катода. Заявленный способ отличается тем, что в качестве расплавленного электролита используют смесь KCl-K2SiF6, электролиз расплавленного электролита c температурой 780-800°С ведут при катодной плотности тока до 20 мА/см2 и потенциале от 0,1 до -0,3 В относительно потенциала кремния в данном электролите, а в качестве источников кремния и циркония используют оксиды кремния и циркония SiO2, ZrO2 и ZrSiO4.
Сущность способа заключается в следующем. Расплавленные электролиты KCl-K2SiF6 за счет частичного термического разложения K2SiF6 содержат в своем составе свободные ионы фтора (KF), обеспечивающие по предварительным эмпирическим наблюдениям и результатам растворение оксидов кремния и циркония в электролите с образованием электроактивных ионов кремния и циркония. Согласно работам [6, 7], растворение оксидов SiO2, ZrO2 и ZrSiO4 в расплавленных электролитах KF-KCl-K2SiF6 может сопровождаться образованием электроактивных ионов SiF73-, SiO3F3-, SiO2F22-, ZrF62, ZrFnClm(4-n-m)-, а также ионов SiO44-, электроактивность которых также отмечена в ряде работ при электроосаждении кремния из расплавов CaCl2-CaO-SiO2. Аналогичная ситуация должна наблюдаться и при растворении SiO2, ZrO2 и ZrSiO4 в электролите KCl-K2SiF6, за исключением того, что растворимость оксидов при снижении доли свободных ионов фтора будет меньше.
При электролизе расплавленных электролитов KCl-K2SiF6 с добавками SiO2, ZrO2 и ZrSiO4 на катоде из углеродного материала могут протекать следующие вероятные суммарные реакции:
Zr4+ + 4e- = Zr
Si4+ + 4e- = Si
Zr4+ + 4e- + C = ZrC
Si4+ + 4e- + C = SiC
ySi4+ + yZr4+ + (x+y)4e- = ZrySix
где y и x - стехиометрические коэффициенты.
Ввиду относительно низкой температуры электровосстановление ионов циркония и кремния до соответствующих карбидов является маловероятным, тем не менее их возможность не исключается полностью.
Для определения параметров электроосаждения кремния и циркония из расплавленных электролитов KCl-K2SiF6 с добавками SiO2, ZrO2 и ZrSiO4 при температуре 790°С методом циклической вольтамперометрии была изучена кинетика катодного процесса на стеклоуглероде. По количеству пиков в катодной области полученных вольтамперограмм показано протекание 3-4 реакций в области потенциалов от 0,1 до -0,3 В относительно потенциала кремниевого квазиэлектрода сравнения, связанных с электровосстановлением ионов кремния и циркония до силицидов циркония, а также кремния и циркония. При потенциалах отрицательнее -0,4 В начинается разряд ионов калия. Из квазистационарных поляризационных зависимостей была определена максимальная катодная плотность тока процессов в диапазоне потенциалов от 0,1 до -0,3 В относительно кремниевого квазиэлектрода сравнения. Из общеизвестных представлений можно отметить, что состав и соотношение фаз в катодном продукте будет зависеть от катодной плотности тока и потенциала катода, при этом в случае необходимости получения катодного продукта с преобладанием доли силицида циркония конкретной стехиометрии, потребуется ведение электролиза в условиях контроля потенциала катода и концентрации элекроактивных ионов в электролите. Для снижения вероятности включения в катодный осадок исходных оксидных реагентов, содержание последних в электролите должно быть меньше предела насыщения или растворимости.
Для полноценной реализации способа наряду с электроосаждением целевых продуктов требуется протекание анодного процесса, обеспечивающего сохранение состава расплавленного электролита. Для этого ионы кислорода, введенные с добавками SiO2, ZrO2 и ZrSiO4 в электролит, должны разряжаться на аноде до кислорода или CO/CO2 и удаляться из электролита с продуваемым через реактор аргоном.
Изобретение иллюстрируется Фигурами, где на Фигуре 1 приведены микрофотографии типового катодного осадка, полученного при электролизе расплавленного электролита KCl-K2SiF6 с добавкой 0,3 мас.% ZrO2 при температуре 790°С и катодной плотности тока 15 мА/см2, а на Фигуре 2 - спектры энергодисперсионного анализа осадка и атомные проценты кремния и циркония в осадке.
Для экспериментального подтверждения работоспособности заявленного способа наряду с изучением кинетики катодного процесса была выполнена серия экспериментов по электролизу расплавленных электролитов KCl-K2SiF6 с добавками SiO2, ZrO2 и ZrSiO4 при температуре 790°С. Эксперименты выполняли в лабораторном электролизере из графита, размещенном в герметичной реторте из жаропрочной стали марки AISI 304. В крышке реторты были предусмотрены штуцера для термопары, квазиэлектрода сравнения, противоэлектрода, загрузочной трубки, а также шлюз для замены рабочего электрода. В графитовый тигель реактора на дне стальной реторты загружали предварительно приготовленный из солей квалификации «х.ч.» и «осч» (Реахим, Россия) электролит KCl-K2SiF6 с добавками SiO2, ZrO2 и ZrSiO4 квалификации «х.ч.» (Реахим, Россия). После этого в крышке реторты размещали электроды и вспомогательные устройства, и плотно закрывали реторту. Реторту размещали в печи сопротивления и поэтапно нагревали до температуры 500°С в условиях вакуумирования, после чего нагревали до рабочей температуры в потоке высокочистого аргона (99,9996%, УралКриоГаз-Трейд, Россия). Температуру в печи сопротивления задавали и поддерживали в пределах ±2°С при помощи терморегулятора «Варта ТП 703». Температуру расплава контролировали периодическим погружением в расплав термопары S-типа, которая подключена к компьютеру при помощи модуля USB-TC01 (National Instruments, США). После достижения рабочей температуры в расплав погружали электроды и вели электролиз.
В качестве рабочего электрода использовали стеклоуглеродные (СУ-2000) и графитовые (МПГ-6) стержни цилиндрической формы, а квазиэлектродом сравнения выступал кремний марки КР-00. В качестве противоэлектрода были применены бруски кремния (КР-00) и графита (МПГ-6). Электролиз в потенциостатическом и гальваностатическом режиме с контролем тока и потенциала, соответственно, вели при помощи потенциостата/гальваностата AutoLab 302N (Metrohm, Нидерланды) c программным обеспечением (Nova 2.1.5). После окончания электролиза рабочий электрод извлекали из электролита, охлаждали до комнатной температуры и многократно промывали в слабокислом растворе HF. В серии экспериментов варьировали катодную плотность тока или потенциал катода с целью определения влияния параметров электролиза на морфологию, фазовый и элементный состав катодного продукта.
Анализ морфологии и состава полученных осадков осуществляли методами сканирующей электронной микроскопии и энергодисперсионного анализа с использованием сканирующего электронного микроскопа Tescan Vega 4 (Tescan, Чехия) и системы EDS Oxford Xplore 30 (Oxford, Великобритания).
Результаты экспериментальной апробации приведены на Фигурах 1-3. На Фигуре 1 приведена морфология типового катодного осадка, полученного при электролизе расплавленного электролита KCl-K2SiF6 с добавкой 0,3 мас.% ZrO2 при температуре 790°С и катодной плотности тока 15 мА/см2. Полученный осадок представлен порошком с размером частиц от 1 до 8 мкм, причем в продукте имеются также дендриты большего размера. По данным энергодисперсионного анализа, представленным на Фигуре 2, осадок был представлен на 53,1 ат.% кремнием и на 46,9 ат.% цирконием, что соответствует получению в осадке преимущественно интерметаллидного соединения ZrSi с элементарным цирконием.
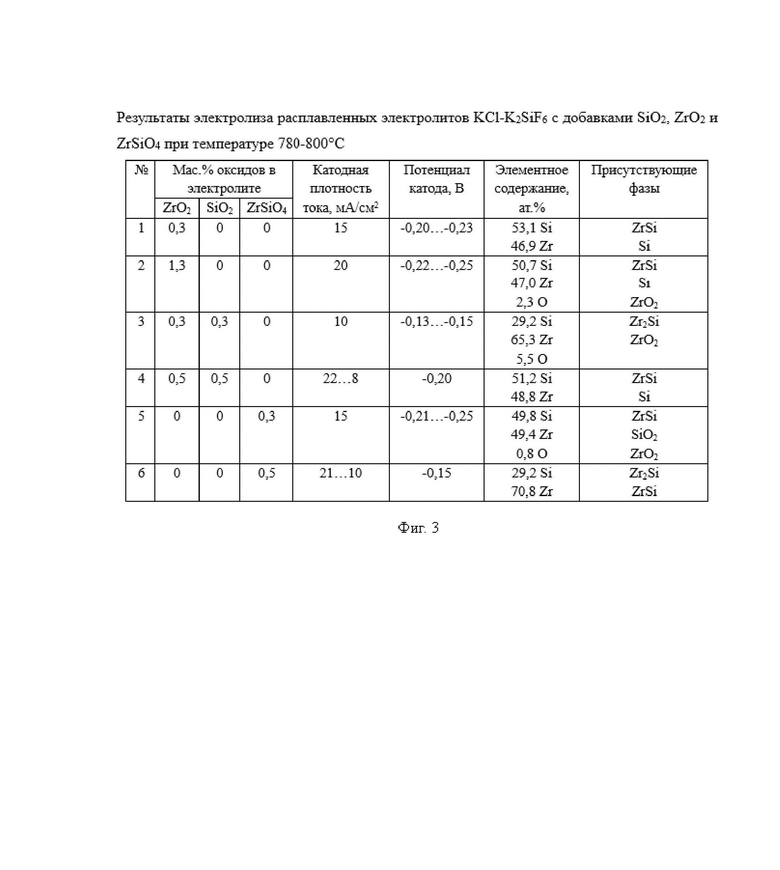
Подобные результаты были получены при варьировании параметров электролиза, о чем свидетельствуют результаты на Фигуре 3. В большинстве случаев в результате электролиза были получены осадки, представленные более чем на 95 % порошками силицидов циркония с размерами частиц от 0,5 до 10 мкм с содержанием оксидных примесей, которые могли появиться на развитой поверхности осадков при контакте с атмосферой воздуха.
Полученные результаты в целом указывают на принципиальную возможность электролитического получения силицидов циркония заявленным способом с возможностью регулирования составом катодных продуктов.
Более того, совокупность признаков способа позволяет исключить предварительные энергоемкие операции по приготовлению фторида, фторсиликата и фторцирконата калия, и использовать в качестве источников циркония и кремния наиболее дешевые и доступные оксидные реагенты.
Источники
1. Cho I., Park K., Lee S., Nersisyan H.H., Kim Y., Lee J. Rapid and cost-effective method for synthesizing zirconium silicides // Chemical Engineering Journal, 2010, Vol. 165, pp. 728-734.
2. Chen Y., Wu Sh., Ma Sh., Zhao X., Cao B. Preparation of zirconium carbide-zirconium silicide composite powders by solid reaction of Zr and SiC powders // Materials Science, 2020, Vol. 26, pp. 348-351.
3. Liu H., Cai Y., Xu Q., Liu H., Song Q., Qi Y. In situ nano-sized ZrC/ZrSi composite powder fabricated by a one-pot electrochemical process in molten salts // RSC Advances, 2017, Vol. 7, № 2301.
4. Liu H., Song W., Xu Q., Ma W., Bai Y. Direct fabrication of ZrC/ZrSi composite fibers from ZrSiO4/C precursors in molten chlorides by electrochemical method // Ceramics International, 2020, Vol. 46, pp. 8015-8020.
5. Malyshev V.V., Uskova N.N., Shapoval V.I. Electrochemical synthesis of molybdenum, tungsten, titanium, and zirconium silicides in a dispersed state // Powder Metallurgy and Metal Ceramics, 1997, Vol. 36, pp. 289-292.
6. Трифонов К.И., Постнов И.И., Глазырина Л.Н. Влияние глубины разложения циркона смесями хлорида и кремнефторида калия на характер изменения физико-химических свойств образующихся расплавов // Расплавы, 1996, №1, с. 87-92.
7. Zaykov Yu.P., Isakov A.V., Zakiryanova I.D., Reznitskikh O.G., Chemezov O.V., Redkin A.A. Interaction between SiO2 and a KF-KCl-K2SiF6 Melt // Journal of Physical Chemistry B, 2014, Vol. 118, pp. 1584-1588.
| название | год | авторы | номер документа |
|---|---|---|---|
| Электролитический способ получения кремния из расплавленных солей | 2021 |
|
RU2775862C1 |
| Способ электроосаждения сплошных осадков кремния из расплавленных солей | 2022 |
|
RU2795477C1 |
| СПОСОБ ЭЛЕКТРОЛИТИЧЕСКОГО СИНТЕЗА ОСАДКОВ КРЕМНИЯ С РАЗВИТОЙ ПОВЕРХНОСТЬЮ ИЗ РАСПЛАВЛЕННЫХ СОЛЕЙ | 2024 |
|
RU2840651C1 |
| Электролитический способ получения наноразмерных осадков кремния в расплавленных солях | 2021 |
|
RU2770846C1 |
| Способ электролитического получения микроразмерных пленок кремния из расплавленных солей | 2022 |
|
RU2797969C1 |
| Способ электролитического получения кремния из расплавленных солей | 2020 |
|
RU2751201C1 |
| Способ электролитического получения кремния из расплавленных солей | 2021 |
|
RU2760027C1 |
| СПОСОБ УТИЛИЗАЦИИ ХЛОРА, ФТОРА ИЗ АНОДНОГО ГАЗА И ОТРАБОТАННОГО ЭЛЕКТРОЛИТА, ОБРАЗУЮЩИХСЯ В ПРОЦЕССЕ ЭЛЕКТРОЛИТИЧЕСКОГО ПОЛУЧЕНИЯ ЦИРКОНИЯ | 1997 |
|
RU2140465C1 |
| Электролитический способ получения наноразмерного кремния из иодидно-фторидного расплава | 2022 |
|
RU2778989C1 |
| Способ изготовления литий-ионного источника тока с анодом на основе кремния | 2023 |
|
RU2828331C1 |

Изобретение относится к порошковой металлургии, в частности к способам электролитического получения порошков силицидов циркония для изготовления функциональных материалов различного назначения. Способ включает электролиз расплавленного электролита с использованием графитового катода с контролем катодной плотности тока и потенциала катода, при этом в качестве расплавленного электролита используют смесь KCl-K2SiF6, электролиз расплавленного электролита c температурой 780-800°C ведут при катодной плотности тока от 8 до 20 мА/см2 и потенциале от 0,1 до -0,3 В относительно потенциала кремния в данном электролите, а в качестве источников кремния и циркония используют оксиды кремния и циркония. Технический результат - упрощение получения порошков силицида циркония и снижение энергетических затрат. 3 ил.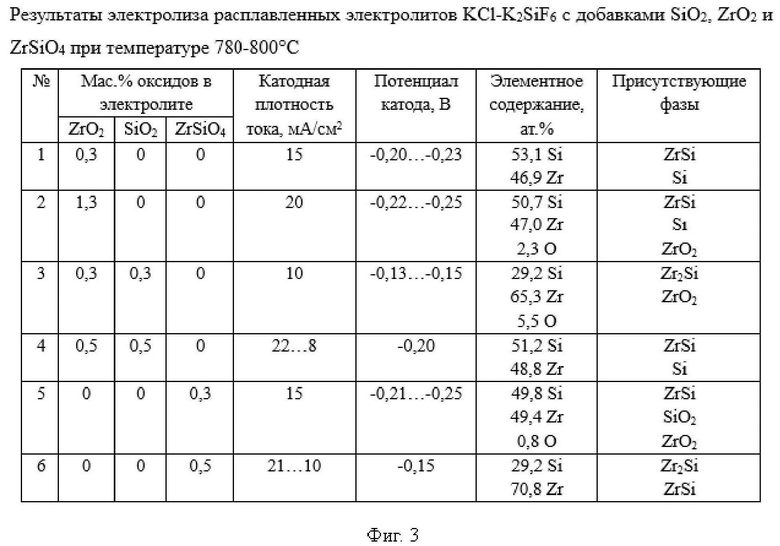
Способ электролитического получения порошков силицидов циркония в расплавленных солях, включающий электролиз расплавленного электролита с использованием графитового катода с контролем катодной плотности тока и потенциала катода, отличающийся тем, что в качестве расплавленного электролита используют смесь KCl-K2SiF6, электролиз расплавленного электролита c температурой 780-800°С ведут при катодной плотности тока от 8 до 20 мА/см2 и потенциале от 0,1 до -0,3 В относительно потенциала кремния в данном электролите, а в качестве источников кремния и циркония используют оксиды кремния и циркония.
| Malyshev V.V | |||
| и др | |||
| Electrochemical synthesis of molybdenum, tungsten, titanium, and zirconium silicides in a dispersed state, Powder Metallurgy and Metal Ceramics, Vol 36, pp | |||
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
| Zaykov Yu.P | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор для массовой выработки лекал | 1921 |
|
SU118A1 |
| Устройство для охлаждения цилиндровых крышек двигателей внутреннего горения большой мощности | 1924 |
|
SU1584A1 |
| Способ электрохимического получения наноразмерного порошка силицида металла | 2018 |
|
RU2718022C1 |
Авторы
Даты
2024-12-03—Публикация
2023-12-18—Подача