Область техники
Группа изобретений относится к области биотехнологии и иммунологии, а именно к способам анализа с помощью проточной цитометрии.
Уровень техники
Фагоцитоз – процесс, при котором клетки захватывают и переваривают твёрдые частицы, – широко распространён среди животных, начиная от простейших и заканчивая многоклеточными организмами. Фагоцитирующие клетки многоклеточных млекопитающих: моноциты и макрофаги, нейтрофилы, дендритные клетки, – представители врожденного иммунитета, первая линия защиты против разнообразных патогенов, попадающих в организм из окружающей среды и способных вызвать инфекцию. Фагоцитоз необходим также при элиминации апоптотических клеток. Таким образом, фагоцитоз является необходимым процессом поддержания гомеостаза у многоклеточных животных [Lancaster C.E. et al. Phagocytosis: what’s on the menu? // Biochemistry and Cell Biology. – 2019. – Т. 97. – №. 1. – С. 21-29]. Снижение способности клеток к фагоцитозу связано с рядом заболеваний, в том числе с иммунодефицитными состояниями при инфекционных заболеваниях. Например, сниженный фагоцитоз обнаруживается при пародонтозе [Carneiro V.M.A. et al. Decreased phagocytic function in neutrophils and monocytes from peripheral blood in periodontal disease // Journal of Applied Oral Science. – 2012. – Т. 20. – С. 503-509], синдроме бактериальной колонизации нижних дыхательных путей [Singh R. et al. Defective monocyte-derived macrophage phagocytosis is associated with exacerbation frequency in COPD //Respiratory Research. – 2021. – Т. 22. – №. 1. – С. 1-11] и других состояниях, приводящих к опасным патологиям [Nakahashi-Oda C. et al. CD300a blockade enhances efferocytosis by infiltrating myeloid cells and ameliorates neuronal deficit after ischemic stroke // Sci. Immunol. – 2021. – Т. 6. – №. 64. – С. eabe7915; Kelley S.M., Ravichandran K.S. Putting the brakes on phagocytosis:“don't‐eat‐me” signaling in physiology and disease // EMBO reports. – 2021. – Т. 22. – №. 6. – С. e52564].
При вторжении в организм чужеродного агента «профессиональные» фагоциты распознают его паттерны разнообразными толл-подобными рецепторами (TLR, toll-like receptors), находящимися на поверхности фагоцитов. TLR распознают, например, компоненты клеточной стенки бактерий, a Fc рецепторы распознают опсонизированные антителами антигены патогенов [Tang Z. et al. Inflammatory macrophages exploit unconventional pro-phagocytic integrins for phagocytosis and anti-tumor immunity // Cell Reports. - 2021. - T. 37. - №. 11]. Инициация воспаления через альтернативные механизмы также в первую очередь активирует фагоцитоз. Фагоцитоз незаменимый, базовый механизм, способствующий элиминации патогена или подавлению его распространения. Именно поэтому многие инфекционные агенты в процессе эволюции выработали пути блокировки фагоцитоза в качестве основных механизмов, защищающих их от иммунитета хозяина [Uribe-Querol Е., Rosales С.Control of phagocytosis by microbial pathogens // Frontiers in immunology. 2017. T. 8. C. 1368; Gagnon E. et al. Endoplasmic reticulum-mediated phagocytosis is a mechanism of entry into macrophages // Cell. 2002. T. 110. №. 1. C. 119-131]. Блокировка фагоцитоза является также одним из основных механизмов ухода опухолей от иммунного распознавания и элиминации [Dempsey L.A. Inhibiting phagocytosis // Nature Immunology. - 2019. - Т. 20. - №. 9. - С. 1089-1089].
Фагоцитоз является важным звеном между врожденным и адаптивным иммунитетом: фагоцитоз патогенов оканчивается представлением коротких пептидных последовательностей чужеродного микроорганизма после процессинга антигенов. Короткие последовательности представляются на поверхности фагоцитов в связи с комплексом гистосовместимости класса II (МНС II), что инициирует пролиферацию Т-лимфоцитов, запуская адаптивный иммунный ответ [Cruz F.М., Chan A., Rock K.L. Pathways of МНС I cross-presentation of exogenous antigens // Seminars in Immunology. -Academic Press, 2023. - T. 66. - C. 101729]. Таким образом, анализ эффективности фагоцитоза исключительно важен для выявления и лечения патологий иммунитета, исследования механизмов развития опасных заболеваний, а также проверки влияния лекарственных препаратов на фагоцитарную активность.
Анализ фагоцитарной активности лейкоцитов стандартно проводят с помощью специальных фагоцитарных тестов [Porpodis K. et al. Roflumilast, a phosphodiesterase-4 inhibitor, induces phagocytic activity in Greek COPD patients // International journal of chronic obstructive pulmonary disease. - 2015. C. 1123-1128; Morais Т.C. et al. Melatonin action on the activity of phagocytes from the colostrum of obese women // Medicina. - 2019. - T. 55. - №. 10. - C. 625]. Существует множество вариаций этого анализа с использованием различных объектов фагоцитоза, одним из которых является кишечная палочка Escherichia coli. В состав клеточной стенки этих бактерий входит липополисахарид (ЛПС), который распознается толл-подобным рецептором 4 (TLR4, CD284) на поверхности фагоцита [Garcia-Seyda N. et al. Human neutrophils swim and phagocytise bacteria // Biology of the Cell. - 2021. - T. 113. -№. 1. - C. 28-38].
Важным количественным параметром фагоцитоза является фагоцитарное число -количество поглощаемых одним фагоцитом бактерий в течение времени проведения эксперимента. Интегральные показатели фагоцитоза, такие как фагоцитарное число, не учитывают пространственное положение бактерии относительно клеточной мембраны фагоцита, теряя таким образом сведения о кинетике поглощения и завышая показатели фагоцитоза. Для рутинной оценки фагоцитарного числа необходимы высокопроизводительные методы, обеспечивающих подсчет адгезированных на поверхности и действительно фагоцитированных, то есть находящихся внутри фагоцита, бактерий, что позволит более точно оценивать фагоцитарную активность и учитывать кинетику процесса.
Применяемая для оценки фагоцитарного числа микроскопия требует больших затрат времени, что приводит к низкой производительности метода и, как следствие, ограничениям для статистической валидации. Проточная цитометрия высокопроизводительный и один из наиболее простых и доступных методов оценки данных фагоцитарного теста, особенно с появлением визуализирующих проточных цитометров, объединяющих в себе преимущества проточной цитометрии и микроскопии. Проточный цитометр с визуализацией представляет из себя прибор, позволяющий анализировать фотографические образы клеток и с определенным разрешением идентифицировать микроскопические детали объектов с высокой скоростью до 2000 образов в секунду. Кроме того, он способен анализировать флуоресценцию от окрашенных клеток в нескольких спектральных диапазонах, возбуждаемых лазерами (см., например, описание проточного цитометра с визуализацией Amnis® FlowSight® компании Cytek® Biosciences Inc., США: https://www.medicalexpo.ru/prod/cytek-biosciences-inc/product-128128-1113438.html, дата обращения 16.11.2023). Однако в любом проточном цитометре с визуализацией фотофиксация клетки делается в одной проекции. Это сильно снижает точность определения местоположения бактерий: снаружи или внутри, - при оценке встроенной в прибор программой.
Известен способ анализа Aβ-FAM-фагоцитоза с помощью проточного цитометра Amnis FlowSight Imaging (Luminex Corporation, Остин, Техас, США), оснащенного двумя лазерами, работающими на 488 и 642 нм, двумя камерами и двенадцатью стандартными каналами обнаружения, которые объединяют проточную цитометрию и микроскопию высокого разрешения. Аппарат одновременно создает изображения с боковым рассеянием (темное поле), одно или два изображения в проходящем свете (светлое поле) и до десяти каналов флуоресцентных изображений каждой клетки. FlowSight, использующий систему Inspire™, регистрирует 2000 клеток в секунду и работает с размером пикселя 1 мкм (~20-кратное увеличение), позволяя визуализировать флуоресценцию мембраны, цитоплазмы или ядра. Программное обеспечение IDEAS для анализа изображений позволяет количественно оценивать клеточную морфологию и флуоресценцию при различных локализациях клеток путем определения конкретных клеточных областей (масок) и математических выражений, использующих пиксельные данные изображения или маски (свойства). Фагоцитоз оценивали путем анализа признака интернализации с использованием маски, представляющей всю клетку, определенной по изображению brightfield (BF), и внутренней маски, определенной путем разрушения маски всей клетки для устранения флуоресцентного сигнала, поступающего от Aβ42-FAM, прикрепленного к поверхности клетки, таким образом, измеряя только интернализованную часть. Функция интернализации была впервые использована для вычисления отношения интенсивности FAM (сигнала Аβ42) внутри ячейки к общей интенсивности FAM вне ячейки. Более высокие показатели интернализации (IS) указывают на большую концентрацию Аβ42 FAM внутри клетки». [La Rosa F., et al. TREM2 Expression and Amyloid-Beta Phagocytosis in Alzheimer's Disease // International Journal of Molecular Sciences. - 2023. - T. 24. - №10. - C. 8626].
Применение современных проточных цитометров с визуализацией ограничено глубиной фокуса и одной проекцией, в которой делаются снимки. Поэтому применение масок, с помощью которых обрабатываются полученные изображения, дает существенную ошибку локализации. Даже с применением более продвинутых проточных цитометров с визуализацией определение внутриклеточной локализации бактерий или других частиц сопряжено с существенными ошибками. Разделение по интенсивности флуоресценции интернализуемых объектов описывает усредненные характеристики, но не позволяет с высокой точностью определить количественно локализацию объектов фагоцитоза индивидуально для каждой клетки.
Из статьи Павловой с соавторами известен способ анализа фагоцитарной активности человеческих макрофагов, заключающийся в том, что объекты фагоцитоза, конъюгированные с IgG из сыворотки человека, добавляют непосредственно в культуральную среду при соотношении клеток к частицам примерно 1:100, которую добавляют к культуре макрофагов и инкубируют в течение 3 или 6 часов в СО2-инкубаторе, после чего останавливают фагоцитоз, помещая чашки с клетками на лед. Затем клетки открепляют от стекла, переводят в суспензию, фиксируют в формальдегиде и ресуспендируют. Суспензию клеток анализируют с помощью проточного цитометра с визуализацией Amnis® ImageStreamX Mk II (Amnis-Luminex, США), анализ данных проводят с помощью IDEAS 6.2 (Amnis, EMD Millipore), как рекомендовано для анализа фагоцитоза производителем проточного цитометра с визуализацией. [Pavlova Е., et al. Quantitative Analysis of Latex Beads Phagocytosis by Human Macrophages Using Imaging Flow Cytometry with Extended Depth of Field (EDF) // Methods Mol Biol. 2023. T. 2635. C. 203-215]. Авторы анализировали в качестве объекта фагоцитоза флуоресцентные монодисперсные полистироловые микросферы Fluoresbrite® ВВ размером 1,00 мкм, используя проточный цитометр с визуализацией. Описанный способ не позволяет отличить фагоцитированные микросферы от адгезированных на клеточной поверхности микросфер, находящихся в центре образа клеток.
Во многих исследованиях для анализа фагоцитоза используются различные объекты, в частности, Е. coli, меченные рН-зависимыми красителями. Однако использование этих реагентов требует постоянного контроля и применение специального буфера, пагубно влияющего на жизнеспособность клеток [Yang F. et al. Establishment of the reference intervals of whole blood neutrophil phagocytosis by flow cytometry // Journal of Clinical Laboratory Analysis. 2021. T. 35. - №. 8. - С. e23884].
Из работы Смирнова с соавторами известен способ оценки фагоцитирующей активности нейтрофилов [Smirnov A., et al. Using Imaging Flow Cytometry to Quantify Neutrophil Phagocytosis // Methods Mol Biol. - 2020. - T. 2087. - C. 127-140], при котором в качестве объектов фагоцитоза используют бактерии Neisseria gonorrhoeae, маркированные флуоресцентным красителем Tag-it Violet™ (TIV) (Biolegend), для анализа эффективности фагоцитоза культуру нейтрофилов инкубируют в суспензии упомянутых бактерии, затем фагоцитоз останавливают, культуру нейтрофилов промывают и окрашивают козьими антителами против Neisseria gonorrhoeae (Biosource), конъюгированными с флуоресцентным красителем DyLight™ 650 (DL650) в соответствии с протоколом производителя (Thermo). Полученную суспензию нейтрофилов анализируют на проточном цитометре с визуализацией ImageStreamX Mk II с использованием программного обеспечения INSPIRE® и IDEAS® v. 6.2 (Amnis Luminex Corporation). Способ позволяет отдельно анализировать и сортировать бактерии внутри нейтрофилов, которые не могут быть окрашены антителами после фагоцитоза, и бактерии, адгезированные к нейтрофилам и доступные для окрашивания антителами. Такое двойное окрашивание обеспечивает увеличение точности при анализе на проточном питометре с визуализацией в потоке. Однако такое окрашивание более трудоемко, чем биотинилирование, применимо только данного вида бактерий и не может применяться для других объектов фагоцитоза.
Технической задачей, на решение которой направлено настоящее изобретение, является решение как минимум одной из вышеуказанных в уровне техники проблем.
Сущность изобретения
Технической решением является использование описанного признаками в пунктах формулы изобретения.
Одной из возможных технических задач, на решение которой направлено настоящее изобретение, являлось создание способа анализа эффективности фагоцитоза, позволяющего оценить количество действительно фагоцитированных объектов и количество адгезированных объектов. Техническим результатом является увеличение точности определения локализации объектов фагоцитоза внутри клетки.
Задача может решаться тем, что предлагается способ анализа эффективности фагоцитоза при помощи проточного цитометра с визуализацией, заключающийся в том, что
i) проводят фагоцитоз, используя объекты фагоцитоза, предварительно конъюгированные с флуоресцентной меткой и биотином, и образец клеток, способных к фагоцитозу,
ii) после остановки фагоцитоза образец фагоцитировавших клеток окрашивают стрептавидином, конъюгированным с флуоресцентной меткой,
iii) затем при помощи проточного цитометра с визуализацией анализируют в образце количество и пространственное расположение упомянутых объектов фагоцитоза, где количество объектов фагоцитоза и их расположение внутри или снаружи клетки является одним или более измерениями флуоресценции, которые группируют с помощью гейтирования интенсивности флуоресценции;
при этом спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки, конъюгированной со стрептавидином, и оба спектра находятся в диапазоне детекции упомянутого проточного цитометра с визуализацией.
В одном из вариантов осуществления изобретения для получения конъюгированных объектов фагоцитоза суспензию объектов фагоцитоза фиксируют 2% параформальдегидом, после чего отмывают и последовательно конъюгируют с изотиоцианатом флуоресцеина (FITC) и биотином.
В другом варианте осуществления изобретения конъюгированные объекты фагоцитоза хранят в присутствии 10% глицерина при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней.
В одном из вариантов осуществления изобретения конъюгированные объекты фагоцитоза высушивают в вакуумной установке и хранят в плотно закрытых сухих пробирках при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней.
В одном из вариантов осуществления изобретения в качестве образца образца клеток, способных к фагоцитозу, используют цельную кровь, в частном случае при этом в качестве объекта фагоцитоза используют клетки бактерий при соотношении клеток бактерий относительно лейкоцитов крови 20:1. При этом на этапе ii) образец может быть дополнительно окрашен антителами против CD45 человека. Дополнительно в образце могут проводить лизирование эритроцитов после этапа ii).
В одном из вариантов осуществления изобретения перед этапом iii) образец фиксируют 2% формальдегидом или его аналогами и хранят до 7 дней при 4°С.
В другом варианте осуществления предлагается применение упомянутого способа анализа эффективности фагоцитоза для оценки влияния биологически активного соединения или их комбинации на скорость и эффективность фагоцитоза.
В еще одном варианте осуществления предлагается применение упомянутого способа анализа эффективности фагоцитоза для оценки влияния терапевтического антитела на скорость и эффективность антителозависимого фагоцитоза опухолевых клеток.
Также в настоящей группе изобретений предлагается способ сортировки фагоцитирующих клеток при помощи проточного цитометра с визуализацией и возможностью сортировки, заключающийся в том, что
i) проводят фагоцитоз, используя объекты фагоцитоза, предварительно конъюгированные с флуоресцентной меткой и биотином, и образец клеток, способных к фагоцитозу,
ii) после остановки фагоцитоза образец фагоцитировавших клеток окрашивают стрептавидином, конъюгированным с флуоресцентной меткой,
iii) затем при помощи проточного цитометра с визуализацией и возможностью сортировки проводят сортировку клеток в образце по количеству и пространственному расположению упомянутых объектов фагоцитоза, где количество объектов фагоцитоза и их расположение внутри или снаружи клетки является одним или более измерениями флуоресценции, которые группируют с помощью гейтирования интенсивности флуоресценции;
при этом спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки, конъюгированной со стрептавидином, и оба спектра находятся в диапазоне детекции упомянутого проточного цитометра с визуализацией.
В одном из вариантов осуществления изобретения для получения конъюгированных объектов фагоцитоза, суспензию объектов фагоцитоза фиксируют 2% параформальдегидом, после чего отмывают и последовательно конъюгируют с изотиоцианатом флуоресцеина (FITC) и биотином.
В другом варианте осуществления изобретения конъюгированные объекты фагоцитоза хранят в присутствии 10% глицерина при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней до замораживания.
В одном из вариантов осуществления изобретения конъюгированные объекты фагоцитоза высушивают в вакуумной установке и хранят в плотно закрытых сухих пробирках при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней до замораживания.
18. Способ по любому из пп. 13-17, характеризующийся тем, что в качестве образца клеток, способных к фагоцитозу, используют цельную кровь, в частном случае при этом в качестве объекта фагоцитоза используют клетки бактерий при соотношении клеток бактерий относительно лейкоцитов цельной крови 20:1. При этом на этапе ii) образец дополнительно окрашивают антителами против CD45 человека. Дополнительно в образце могут проводить лизирование эритроцитов после этапа ii).
В одном из вариантов осуществления изобретения перед этапом iii) образец фиксируют 2% формальдегидом или его аналогами и хранят до 7 дней при 4°С.
Применение двойного мечения объекта фагоцитоза, используемое в настоящем способе, позволяет определить локализацию объекта фагоцитоза по окрашиванию одним или двумя флуорохромами в зависимости от того, внутри или снаружи клетки объект находится. Заявленный способ можно использовать независимо или в сочетании с существующими методами анализа на проточных цитометрах с визуализацией.
Заявленный способ может быть применен практически к любому объекту фагоцитоза, который возможно конъюгировать с флуоресцентным красителем и биотином.
Изобретение иллюстрируются следующими графическими материалами:
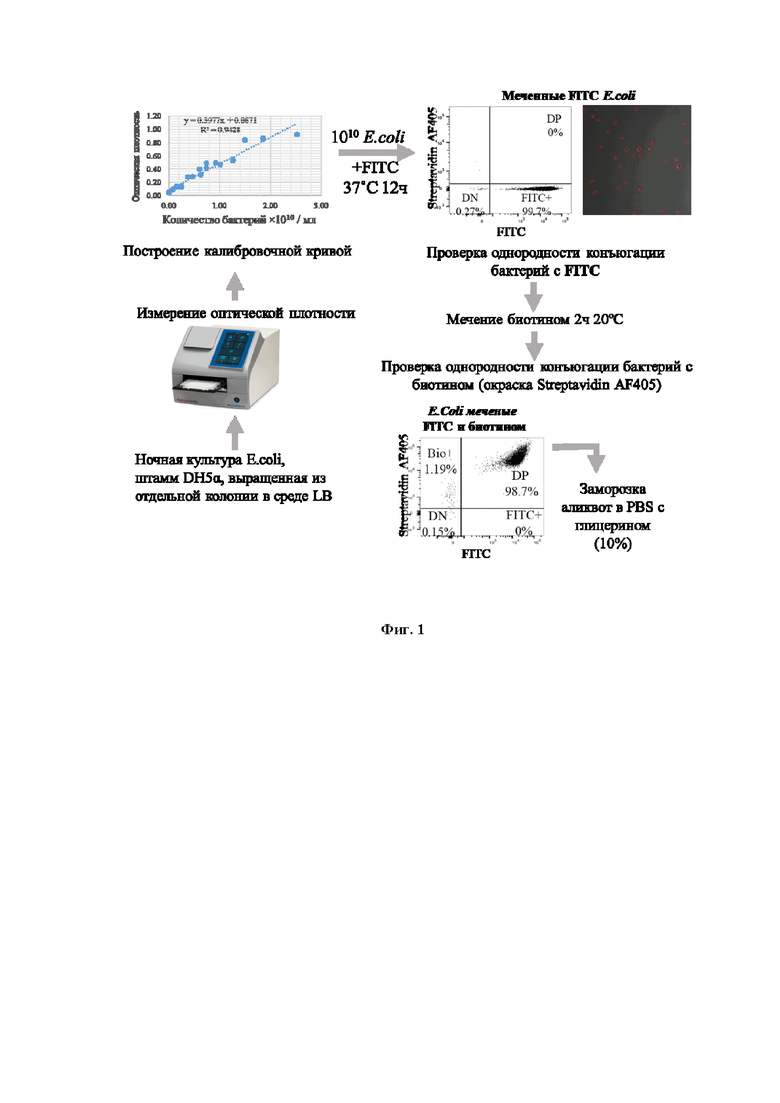
На Фиг. 1 представлена схема мечения бактерий. E.coli конъюгировали с FITC, а затем с биотином для того, чтобы различать бактерии внутри и снаружи фагоцитирующих клеток. Показана последовательность проведения конъюгаций и контроль качества препарата Е. coli. Верхний ряд слева: калибровочная кривая, построенная для оценки количества бактерий по оптической плотности. Верхний ряд, средний график: контрольная проточная цитометрия меченных FITC Е. coli - 99,7% конъюгированы с FITC. Верхний ряд, справа: пример подсчета бактерий по изображению в дифференциальном интерференционном контрасте (DIC, Differential Interference Contrast) и флуоресценции в заданном объеме. Нижний график слева: контрольная проточная цитометрия меченных FITC и биотином Е. coli - 98,7% конъюгированы с двумя красителями. Условные обозначения:
DN - двойная негативная популяция – клетки, интенсивность флуоресценции которых находится на уровне автофлуоресценции неокрашенных клеток;
Dim клетки, интенсивность которых не более чем на декаду выше, чем DN;
Mid клетки с умеренной интенсивностью флуоресценции (в пределах декады выше, чем Dim);
DP – двойная позитивная популяция по FITC и AF405;
DPhi – наиболее яркая субпопуляция клеток DP (интенсивность флуоресценции выше 105 в канале FITC);
DPlow менее яркая, по сравнению с DPhi субпопуляция клеток DP (интенсивность флуоресценции 104-105 в канале FITC); SSC - боковое светорассеяние;
FSC прямое светорассеяние;
CD45+ лейкоциты, определенные как позитивная популяция по маркеру CD45;
GR – гранулоциты;
LY – лимфоциты;
МО – моноциты.
На Фиг. 2 представлена стратегия гейтирования для проточного цитометра с визуализацией Amnis FlowSight и обобщенное представление результатов визуализации. Цифрами обозначены процент клеток в популяции и количество бактерий внутри (IN), и снаружи (OUT) клеток. Для отдельных популяций было проанализировано до 352 клеток (Фиг. 3). Число независимых экспериментов n=3. Условные обозначения как на Фиг. 1.
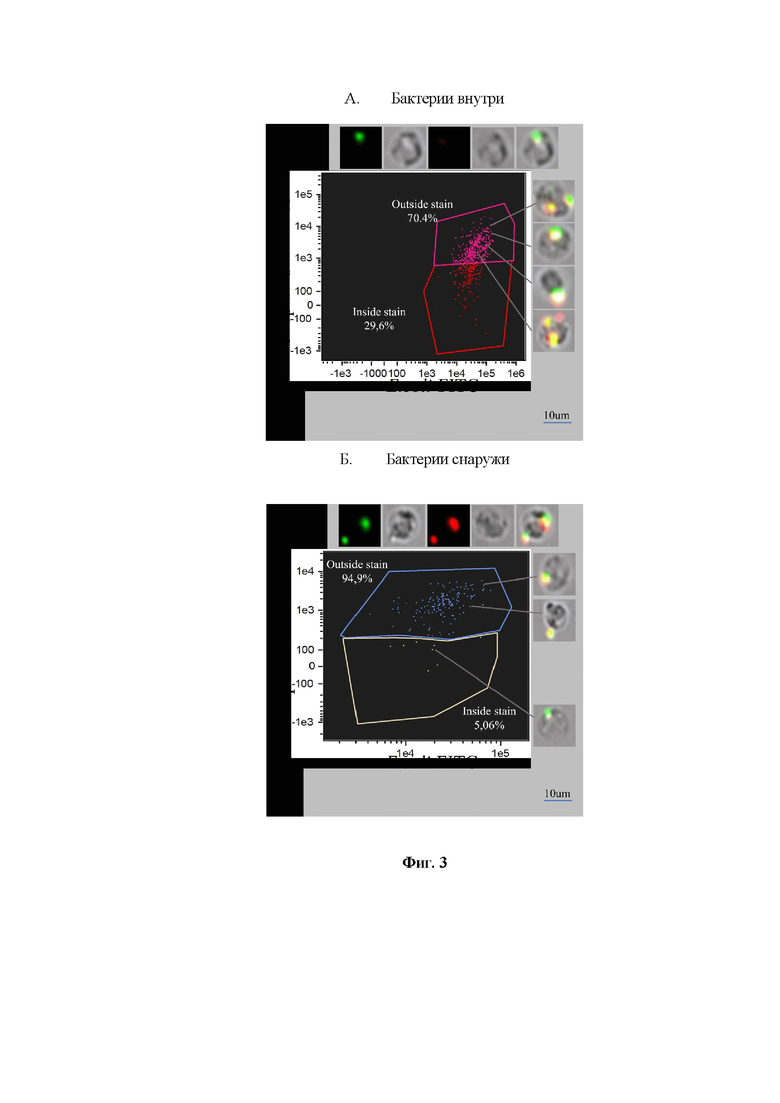
На Фиг. 3А показаны бактерии, детектируемые программой для оценки фагоцитарной активности и встроенной в приложение IDEAS, как находящиеся внутри клеток. Гейты были выставлены на основе флуоресцентного минус один контроля. На Фиг. ЗБ показаны бактерии, детектируемые программой как находящиеся снаружи клеток. Верхние панели иллюстрируют (слева-направо) каналы: FITC (Е. coli), Brightfield 1, AF405 (biotin-streptavidin, Е. coli), Brightfield 2 и наложение всех каналов. Правые панели визуализируют клетки, показанные в виде точек на графиках проточной цитометрии. Синей линией дана масштабная метка 10 мкм для изображений клеток.
Детальное описание изобретения
Если не указано иначе, предполагается, что все термины, обозначения и другие научные термины, используемые в данной заявке, имеют значения, которые обычно понимают специалисты в области, к которой относится настоящее изобретение. В некоторых случаях определения терминов с общепринятыми значениями приведены в данной заявке для ясности и/или для быстрой справки и понимания, и включение таких определений в настоящее описание не должно истолковываться как наличие существенного отличия значения термина от обычно подразумеваемого в данной области.
Кроме того, если по контексту не требуется иное, термины в единственном числе включают в себя термины во множественном числе, и термины во множественном числе включают в себя термины в единственном числе. Как правило, используемая классификация и методы культивирования клеток, молекулярной биологии, иммунологии, микробиологии, генетики, аналитической химии, химии органического синтеза, медицинской и фармацевтической химии, а также гибридизации и химии белка и нуклеиновых кислот, описанные в настоящем документе, хорошо известны специалистам и широко применяются в данной области. Ферментативные реакции и способы очистки осуществляют в соответствии с инструкциями производителя, как это обычно осуществляется в данной области, или как описано в настоящем документе.
Одной из возможных технических задач, на решение которой направлено настоящее изобретение, являлось создание способа анализа эффективности фагоцитоза, позволяющего оценить количество действительно фагоцитированных объектов и количество адгезированных объектов. Техническим результатом является увеличение точности определения локализации объектов фагоцитоза внутри клетки.
Термин «объект фагоцитоза» относится к частицам, в том числе к микросферам, прокариотическим клеткам (например, бактериям) и их компонентам, эукариотическим клеткам и любым другим объектам, которые могут быть подвергнуты фагоцитозу.
Термин «фагоцитирующая клетка» или «фагоцит» относится к клеткам, способным к фагоцитозу, в частности, к клеткам цельной крови, адгезионным и суспензионным клеточным культурам, клеткам простейших и другим.
Термин «фагоцитировавшая клетка» относится к клетке, осуществившей фагоцитоз, то есть в которой с помощью применяемых методов анализа может быть детектирован объект фагоцитоза или его компоненты.
В одном из вариантов осуществления настоящего изобретения предлагается способ анализа эффективности фагоцитоза при помощи проточного цитометра с визуализацией, заключающийся в том, что
i) проводят фагоцитоз, используя объекты фагоцитоза, предварительно конъюгированные с флуоресцентной меткой и биотином, и образец клеток, способных к фагоцитозу,
ii) после остановки фагоцитоза образец фагоцитировавших клеток окрашивают стрептавидином, конъюгированным с флуоресцентной меткой,
iii) затем при помощи проточного цитометра с визуализацией анализируют в образце количество и пространственное расположение упомянутых объектов фагоцитоза, где количество объектов фагоцитоза и их расположение внутри или снаружи клетки является одним или более измерениями флуоресценции, которые группируют с помощью гейтирования интенсивности флуоресценции;
при этом спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки, конъюгированной со стрептавидином, и оба спектра находятся в диапазоне детекции упомянутого проточного цитометра с визуализацией.
Под «эффективностью фагоцитоза» мы понимаем количество клеток и объектов фагоцитоза совокупность параметров фагоцитоза: фагоцитарный индекс, то есть процент взаимодействующих с бактериями клеток; фагоцитарное число; количественное соотношение между двойной позитивной популяцией клеток (удерживающей бактерий на своей поверхности) и фагоцитировавших клеток; скорость интернализации бактерий и скорость их переваривания. Заявленный способ позволяет подсчитать количество объектов фагоцитоза внутри и снаружи клеток, а также количество фагоцитировавших клеток, на основании этих данных могут быть рассчитаны все параметры фагоцитоза, определяющие его эффективность.
Термин «фагоцитарное число» количественно отражает фагоцитоз отдельной клетки, то есть количество фагоцитированных объектов фагоцитоза на одну клетку. Термин «фагоцитарный индекс» относится к проценту взаимодействующих с бактериями клеток. Термин «скорость интернализации бактерий» относится к временной характеристике фагоцитоза, которая отражает способность клеток фагоцитировать бактерий через определенные временные интервалы. Термин «скорость переваривания бактерий» оценивается как исчезновение флуоресценции отдельных объектов фагоцитоза и ее распределение по цитоплазме.
При осуществлении этого способа может быть использован любой известный из уровня техники проточный цитометра с визуализацией, например, Amnis ImageStreamX Mark II (Luminex), Amnis knageStream XMk II Imaging Cell Sorter / Counter Lab (Luminex), Amnis FlowSight (Cytek) или аналогичные приборы.
Объекты фагоцитоза могут быть конъюгированы с флуоресцентной меткой любым известным из уровня техники способом, например, активированным флуоресцентным эфиром по аминогруппам, с использованием клик-технологии, с помощью пептидных меток и другими описанными способами [Selective chemical labeling of proteins – Organic & Biomolecular Chemistry (RSC Publishing) doi:10.1039/С6ОВ00126В]. В том числе можно использовать коммерчески доступные конъюгированные объекты фагоцитоза, такие как, например, конъюгированные с флуоресцентными красителями бактерии и дрожжи [https://www.thermofisher.com/ru/ru/home/references/molecular-probes-the-handbook/tables/molecular-probes-selection-of-bioparticles-fluorescent-bacteria-and-yeast.html, дата обращения 23.11.2023].
Объекты фагоцитоза могут быть конъюгированы с биотином любым доступным из уровня техники способом, например, с сукцинимид иловым эфиром биотина, активированным тиолом биотина и другими методами [https://www.aatbio.com/resources/application-notes/biotin-labeling-molecules-and-their-biological-applications#sec_21, дата обращения 08.12.2023]. В том числе можно использовать коммерчески доступные наборы для конъюгирования белков на поверхности объектов фагоцитоза [https://www.dojindo.com/EUROPE/products/B592/, дата обращения 08.12.2023; https://www.gerbu.de/Biotin-Labeling-Kit-NH2 2/, дата обращения 08.12.2023; https://www.thermofisher.com/order/catalog/product/A10235/, дата обращения 08.12.2023; https://www.cytivalifesciences.com/en/us/shop/protein-analysis/ blotting-and-detection/blotting-standards-and-reagents/amersham-quickstain-protein-labeling-kit-p-06258, дата обращения 08.12.2023].
Условия проведения фагоцитоза не являются существенным признаком заявленного способа, поскольку назначением способа является анализ эффективности фагоцитоза, при этом упомянутая эффективность может варьировать в зависимости от объектов фагоцитоза, фагоцитирующих клеток, условий проведения фагоцитоза, наличия активных веществ, влияющих на фагоцитарную активность и пр. Фагоцитоз обычно проводят при 37°С и 5% СО2, такие условия считаются оптимальными для культивирования клеток и поддерживаются большинством инкубаторов для культивирования клеток. Отклонения от этих условий, не влияющие на жизнеспособность и функциональную активность клеток, не влияют на достижение технического результата. Наши экспериментальные данные подтверждают, что условия фагоцитоза не влияют на достижение технического результата изобретения, и могут варьировать, в том числе, заявленное изобретение может быть использовано для определения и исследования оптимальных условий проведения фагоцитоза, поскольку изобретение позволяет с большой точностью показать эффективность фагоцитоза.
Примеры осуществления изобретения показали, что уже через 15 минут фагоцитоз может произойти и клетки будут доступны для анализа его эффективности. Наши эксперименты показали, что время фагоцитоза не влияет на технический результат изобретения, более того, анализ эффективности фагоцитоза может проводиться в одном и том же образце фагоцитирующих клеток в динамике, в этом случае из образца фагоцитирующих клеток через определенные промежутки времени можно брать аликвоты, останавливать в них фагоцитоз и проводить дальнейшее окрашивание стрептавидином с последующим анализом с помощью проточного цитометра с визуализацией. В приведенных примерах фагоцитоз проводили вплоть до 180 минут, но это не должно ограничивать объем прав настоящего изобретения, поскольку максимальное время фагоцитоза не влияет на технический результат изобретения.
Для того, чтобы остановить процесс фагоцитоза, можно использовать известные из уровня техники способы, например, можно добавить химический ингибитор, или ледяной PBS, или поместить на лед. Способы остановки фагоцитоза известны из уровня техники [см., например https://www.bdbiosciences.com/en-eu/products/reagents/flow-cytometry-reagents/research-reagents/single-color-antibodies-ruo/protein-transport-inhibitor-containing-monensin.554724, дата обращения 08.12.2023; https://www.bangslabs.com/pha2 gocytosis, дата обращения 08.12.2023; https://assets.thermofisher.com/TFS-Assets/LSG/manuals/mp 10026.pdf, дата обращения 08.12.2023; Azuma Y, Wang PL, Shinohara M, Ohura K. Differentiation by in vitro treatment of lidocaine-epinephrine and prilocaine-felypressine in neutrophils. Immunol Lett. 2001; 77(3): 151-158. doi:10.1016/s0165-2478(01)00221-8], не являются существенными признаками заявленного способа и не влияют на технический результат.
Стрептавидин, конъюгированный с флуоресцентной меткой, можно получить известным из уровня техники способом, например, любыми подходами для мечения белков или взять коммерчески доступный, например [https://www.thermofisher.com/order/catalog/product/SA1001, дата обращения 08.12.2023; https://ru.lumiprobe.com/p/streptavidin-af-488?ysclid=lps4huy0oz939123787, дата обращения 08.12.2023; https://www.biolegend.com/fr-ch/products/alexa-fluor-647-streptavi-din-9305, дата обращения 08.12.2023; https://www.helicon.ru/catalog/reagenty/mikrosko-piya-kolorimetriya-spektrofotometriya-protochnaya-tsitometriya/vspomogatelnye-reaktivy/af-594-streptavidin/?ysclid=lps4jcoeo8844043908, дата обращения 08.12.2023].
Окрашивание стрептавидином проводят при оптимальных для конкретного препарата стрептавидина условий, известных из уровня техники или рекомендаций производителя, и подходящих для выбранного дизайна эксперимента, до достижения максимального окрашивания.
При создании настоящего изобретения была разработана стратегия гейтирования, позволяющая с одной стороны разделить субпопуляции клеток, а с другой стороны визуально идентифицировать расположение объектов по двойному окрашиванию в разных каналах флуоресценции (Фиг. 2). Для этого сначала выделяли популяцию Focus (клетки, при пролете попавшие в фокус объектива). Далее выделяли одиночное клетки (Singlets) от дуплетов и агрегатов клеток. Отделяли клетки от конгломератов бактерий по гранулярности и размеру - по показателям SSC, или бокового рассеяния.
В одном из вариантов осуществления изобретения дизайн эксперимента предполагал использование CD45 для улучшения отделения лейкоцитов, в данной гейтинг-стратегии было использовано гейтирование по CD45. После этого, из CD45+ клеток по показателям SSC, или бокового рассеяния, выделяли разные популяции лейкоцитов (лимфоциты, моноциты и гранулоциты) и определяли соотношение разных популяций фагоцитирующих клеток, что также представлено на Фиг. 2. Разные фагоцитирующие популяции также можно оценивать после гейтирования клеток по CD45+ без разделения на субпопуляции по SSC. Совмещенные снимки проточного цитометра с визуализацией и получившееся распределение клеток по интенсивности их флуоресценции в разных каналах представлены на Фиг. 2 (слева внизу).
При осуществлении настоящего изобретения спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки. Это позволяет различить, используя разные светофильтры, интенсивность флуоресценции объектов фагоцитоза в различных каналах флуоресценции выбранных меток и таким образом идентифицировать локализацию бактерий по количеству этих детектируемых меток (одноцветные меченые бактерии находятся внутри фагоцитов, двуцветные - снаружи).
После инкубирования любого образца фагоцитов, будь то клетки в культуре или кровь и ее производные, с объектами фагоцитоза, мы можем ресуспендировать клетки, отмыть от несвязавшихся бактерий и покрасить стрептавидином. После этого проанализировать в проточном цитометре с визуализацией, выбрав стратегию гейтирования: выделить популяции лейкоцитов, моноцитов и гранулоцитов по SSC. Если использовать образец клеток в культуре, на основании свойств этих клеток возможно применять другие подходящие антитела или же без дополнительного окрашивания гейтировать образец по гранулярности (SSC) и размеру (FSC) клеток. Оценка фагоцитированных и адгезированных бактерий также происходит в каналах связанного с бактерией флуорофора, например, FITC, и меченого стрептавидина и зависит от конъюгированного с ним флуорофора.
В одном из вариантов осуществления изобретения для получения конъюгированных объектов фагоцитоза суспензию объектов фагоцитоза фиксируют 2% параформальдегидом, после чего отмывают и последовательно конъюгируют с изотиоцианатом флуоресцеина (FITC) и биотином. Получают препарат фиксированных, то есть неспособных к размножению, бактерий, свыше 98% бактерий детектируемы в двух флуоресцентных каналах (канале FITC и втором флуоресцентном канале, соответствующем флуоресцентной метке используемого стрептавидина); контроль качества был выполнен на проточном цитометре BD LSR Fortessa.
В другом варианте осуществления изобретения конъюгированные объекты фагоцитоза хранят в присутствии 10% глицерина при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней до замораживания. Таким образом, обеспечивается сохранность объекта фагоцитоза: при повторном анализе эффективность мечения приближена к исходной и составляет выше 98%.
В одном из вариантов осуществления изобретения конъюгированные объекты фагоцитоза высушивают (лиофилизируют) в вакуумной установке и хранят в плотно закрытых сухих пробирках при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней до замораживания. Таким образом, обеспечивается сохранность объекта фагоцитоза: при повторном анализе эффективность мечения приближена к исходной и составляет выше 98%. Лиофилизация является одним из возможных способов длительного хранения препаратов бактерий, в том числе, при более широком интервале температур.
В одном из вариантов осуществления изобретения в качестве образца клеток, способных к фагоцитозу, используют цельную кровь, в частном случае при этом в качестве объекта фагоцитоза используют клетки бактерий при соотношении клеток бактерий относительно лейкоцитов крови 20:1. Использование цельной крови позволяет проводить фагоцитарный тест в условиях, максимально приближенных к физиологическим и, таким образом, получать данные, приближенные процессам, происходящим в живых системах; кроме того, использование цельной крови позволяет сократить время процедуры выделения фагоцитирующей популяции клеток при тестировании первичных культур клеток.
При этом на этапе ii) образец может быть дополнительно окрашен антителами против CD45 человека. Дополнительно в образце могут проводить лизирование эритроцитов. CD45 универсальный маркер лейкоцитов, который позволяет с большей уверенностью дифференцировать лейкоциты от нецелевых клеток (от фрагментов тромбоцитов, эритроцитов и/или плохо отмытых конгломератов бактерий).
В одном из вариантов осуществления изобретения перед этапом iii) образец фиксируют 2% формальдегидом или его аналогами и хранят до 7 дней при 4°С. Этот подход актуален для возможности разнесения эксперимента на несколько дней без замораживания бактерий.
В другом варианте осуществления предлагается применение упомянутого способа анализа эффективности фагоцитоза для оценки влияния биологически активного соединения или их комбинации на скорость и эффективность фагоцитоза. Так, например, в литературе описана способность смесей лидокаин-эпинефрин блокировать способность клеток к фагоцитозу [Azuma Y, Wang PL, Shinohara M, Ohura К. Differentiation by in vitro treatment of lidocaine-epinephrine and prilocaine-felypressine in neutrophils. Immunol Lett. 2001; 77(3): 151-158. doi:10.1016/s0165-2478(01)00221-8]; кроме этого, известен метод предобработки клеток с помощью LPS для активации рецепторов (TLR4), участвующих в фагоцитозе [Blanco GA, Escalada AM, Alvarez E, Hajos S. LPS-induced stimulation of phagocytosis in the sipunculan worm Themiste petricola: possible involvement of human CD14, CD11B and CD11C cross-reactive molecules. Dev Comp Immunol. 1997; 21(4): 349-362. doi:10.1016/s0145-305x(97)00007-4]. Кроме того, опсонизирующие объекты фагоцитоза антитела провоцируют стимуляцию антитело-зависимого фагоцитоза. Биологически активным соединением в данном случае выступают антитела - иммуноглобулины сыворотки крови. [Kamen L., Myneni S., Langsdorf С., et al. A novel method for determining antibody-dependent cellular phagocytosis. J Immunol Methods. 2019; 468:55-60. doi:10.1016/j.jim.2019.03.001]. Добавление сыворотки и инкубация бактерий с ними положительно влияет на эффективность фагоцитоза и степень этого влияния может быть измерена с использованием способа по настоящему изобретению.
В еще одном варианте осуществления предлагается применение упомянутого способа анализа эффективности фагоцитоза для оценки влияния терапевтического антитела на скорость и эффективность антителозависимого фагоцитоза опухолевых клеток. Опухоль таргетируется антителами, и, по аналогии с антителами сыворотки крови, которые опсонизируют бактерий, происходит антитело-зависимый фагоцитоз, его эффективность выше чем без таргетирования антителами. К тому же опухоль уходит от иммунного распознавания, а антитела помогают сделать ее «видимой» для фагоцитов [Gül N, van Egmond М. Antibody-Dependent Phagocytosis of Tumor Cells by Macrophages: A Potent Effector Mechanism of Monoclonal Antibody Therapy of Cancer. Cancer Res. 2015; 75(23): 5008-5013. doi:10.1158/0008-5472.CAN-15-1330]. Степень влияния терапевтического антитела на фагоцитоз опухолевых клеток также можно оценивать с помощью заявленного способа анализа эффективности фагоцитоза.
Также в настоящей группе изобретений предлагается способ сортировки фагоцитирующих клеток при помощи проточного цитометра с визуализацией и возможностью сортировки, заключающийся в том, что
i) проводят фагоцитоз, используя объекты фагоцитоза, предварительно конъюгированные с флуоресцентной меткой и биотином, и образец клеток, способных к фагоцитозу,
ii) после остановки фагоцитоза образец фагоцитировавших клеток окрашивают стрептавидином, конъюгированным с флуоресцентной меткой,
iii) затем при помощи проточного цитометра с визуализацией и возможностью сортировки проводят сортировку клеток в образце по количеству и пространственному расположению упомянутых объектов фагоцитоза, где количество объектов фагоцитоза и их расположение внутри или снаружи клетки является одним или более измерениями флуоресценции, которые группируют с помощью гейтирования интенсивности флуоресценции;
при этом спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки, конъюгированной со стрептавидином, и оба спектра находятся в диапазоне детекции упомянутого проточного цитометра с визуализацией и возможностью сортировки.
Заявленный способ позволяет анализировать и сортировать разные популяции клеток, в том числе клеток с разным фагоцитарным числом, клеток с бактериями, локализованными внутри и/или на их поверхности. Заявленный способ позволяет разделять клетки для проведения дальнейшего генетического и функционального анализа. Поскольку принцип действия проточного цитометра с визуализацией один и тот же для цитометров с возможностью сортировки и без такой возможности, заявленный способ будет работать как для анализа эффективности фагоцитоза, так и для разделения (сортировки) фагоцитирующих клеток по результатам этого анализа. Сортировка может проводиться на группы в зависимости от целей конкретного эксперимента: фагоцитировавшие клетки с определенным количеством объектов фагоцитоза, нефагоцитировавшие клетки, нефагоцитировавшие клетки с адгезированными объектами фагоцитоза, фагоцитировавшие клетки с адгезированными объектами фагоцитоза и пр.
В одном из вариантов осуществления изобретения для получения конъюгированных объектов фагоцитоза, суспензию объектов фагоцитоза фиксируют 2% параформальдегидом, после чего отмывают и последовательно конъюгируют с изотиоцианатом флуоресцеина (FITC) и биотином. Получают препарат фиксированных, то есть неспособных к размножению, бактерий, свыше 98% бактерий детектируемы в двух флуоресцентных каналах (канале FITC и втором флуоресцентном канале, соответствующем флуоресцентной метке используемого стрептавидина); контроль качества был выполнен на проточном цитометре BD LSR Fortessa.
В другом варианте осуществления изобретения конъюгированные объекты фагоцитоза хранят в присутствии 10% глицерина при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней до замораживания. Таким образом, обеспечивается сохранность объекта фагоцитоза: при повторном анализе эффективность мечения приближена к исходной и составляет выше 98%.
В одном из вариантов осуществления изобретения конъюгированные объекты фагоцитоза высушивают в вакуумной установке и хранят в плотно закрытых сухих пробирках при -20°С и ниже до этапа i). При этом конъюгированные объекты фагоцитоза могут транспортироваться при 4-10°С в течение 7-10 дней до замораживания. Таким образом, обеспечивается сохранность объекта фагоцитоза: при повторном анализе эффективность мечения приближена к исходной и составляет выше 98%. Лиофилизация является одним из возможных способов длительного хранения препаратов бактерий, в том числе, при более широком интервале температур.
В одном из вариантов осуществления изобретения в качестве образца клеток, способных к фагоцитозу, используют цельную кровь, в частном случае при этом в качестве объекта фагоцитоза используют клетки бактерий при соотношении клеток бактерий относительно лейкоцитов цельной крови 20:1. Использование цельной крови позволяет проводить фагоцитарный тест в условиях, максимально приближенных к физиологическим и, таким образом, получать данные, приближенные процессам, происходящим в живых системах; кроме того, использование цельной крови позволяет сократить время процедуры выделения фагоцитирующей популяции клеток при тестировании первичных культур клеток.
При этом на этапе ii) образец дополнительно окрашивают антителами против CD45 человека. Дополнительно в образце могут проводить лизирование эритроцитов. CD45 – универсальный маркер лейкоцитов, который позволяет с большей уверенностью дифференцировать лейкоциты от нецелевых клеток (от фрагментов тромбоцитов, эритроцитов и/или плохо отмытых конгломератов бактерий).
В одном из вариантов осуществления изобретения перед этапом iii) образец фиксируют 2% формальдегидом или его аналогами и хранят до 7 дней при 4°С. Этот подход актуален для возможности разнесения эксперимента на несколько дней без замораживания бактерий.
Способ анализа по настоящему изобретению позволяет оценить количество объектов фагоцитоза с одновременной оценкой адгезированных на поверхности и поглощенных фагоцитами объектов. Заявленный способ анализа позволяет выявить оставшиеся после фагоцитоза снаружи (адгезированные) объекты, поскольку конъюгированный с ними биотин специфически связывается со стрептавидином, конъюгированным с флуоресцентным красителем. Этого не происходит у фагоцитированных (интернализованных) объектов, поскольку стрептавидин не может проникнуть внутрь фагоцитов, т.е. интернализованные объекты не окрашиваются вторым флуоресцентным красителем. Таким образом, фагоциты с интернал изо ванными объектами, детектируются только в канале связанного с бактерией флуоресцентного красителя проточного цитометра, а фагоциты с адгезированными на поверхности бактериями образуют двойную позитивную популяцию по параметрам связанного с бактерией флуоресцентного красителя и связанного со стрептавидином флуоресцентного красителя. По интенсивности флуоресценции можно выделить несколько субпопуляций фагоцитов, соответствующих количеству интернализованных или адгезированных бактерий. Заявленный способ позволяет определить процент фагоцитов, способных к поглощению объектов, оценить количество объектов, находящихся как внутри, так и снаружи фагоцита, и оценить скорость поглощения объектов.
Кроме того, двойное мечение объекта фагоцитоза позволяет детектировать объекты внутри клеток с высокой точностью. Так, было показано, что при использовании проточной цитометрии с визуализацией без второй метки, 94,9% бактерий, обнаруженных на поверхности клеток, в действительности оказались на поверхности, однако всего лишь 29,6% бактерий, обнаруженных внутри клеток, в действительности оказались внутри. Заявленный способ выявил все 100% бактерий снаружи и внутри клеток, при этом точность определения объекта фагоцитоза внутри клетки значительно выше, чем при использовании проточной цитометрии с визуализацией без заявленного способа.
Сущность и промышленная применимость изобретения поясняются следующими примерами:
Пример 1.1. Приготовление бактерий, конъюгированных с FITC и биотином.
В качестве объектов фагоцитоза использовали бактерии Escherichia coli штамма DH5a. В 20 мл ночной культуры бактерий, выращенной из отдельной колонии в среде LB, добавляли стерильный глицерин до концентрации 10% и замораживали на 20°С в аликвотах по 50 мкл. За день до эксперимента, 50 мкл 10% глицериновой аликвоты Е. coli помещали в 10 мл среды LB и выращивали течение ночи. Оптическую плотность суспензии измеряли на спектрофотометре Multiskan SkyHigh Microplate Spectrophotometer (ThermoFisher) при 540 нм. Разводили до оптической плотности 0,6, что по заранее отработанной калибровочной кривой соответствовало концентрации 1,29⋅1010 бактерий/мл. Далее 500 мкл этой суспензии центрифугировали 1 минуту при 2350 g. Осадок бактерий ресуспендировали в 250 мкл фиксатора: 10% растворе формалина (ООО «Компания Элемент») в фосфатно-солевом буфере (ФБС, PBS), тщательно перемешивали пипетированием и на вортексе. Фиксировали 30 мин при комнатной температуре на ротационном перемешивателе (10 об/мин). Отмывку от фиксатора проводили в трех сменах по 500 мкл PBS, осаждая центрифугированием 2 мин при 2350 g. После последнего центрифугирования осадок ресуспендировали в 250 мкл PBS, добавляли 250 мкл боратного буфера (50 мМ, рН 9.0) и конъюгировали с FAM изотиоцианатом (FITC) (Lumiprobe, Россия) согласно инструкции производителя. Для этого сухой FITC растворяли в концентрации 20 мг/мл в диметилсульфоксиде, аликвотировали по 10 мкл и хранили при -80°С. К 500 мкл суспензии бактерий добавляли 1 мкл 20 мг/мл FITC и немедленно интенсивно перемешивали, далее инкубировали 16 часов в темноте при 37°С и постоянном перемешивании в термошейкере Biosan TS-100 (400 об/мин). По окончании инкубации бактерии отмывали в трех сменах по 500 мкл PBS, осаждая центрифугированием 2 мин при 2350 g. После последнего центрифугирования осадок ресуспендировали в 200 мкл PBS и хранили до использования при 4°С не более 24 часов. Эффективность конъюгации оценивали на проточном цитометре BD LSRFortessa по интенсивности флуоресценции в канале FITC (лазер 488 нм, фильтр 530/20 нм) в сравнении с контрольными не конъюгированными фиксированными образцами.
Далее бактерии конъюгировали с биотином, используя коммерческий набор FluoReporter Mini-biotin-XX Protein Labeling Kit (Thermo Fisher, кат. №F6347), согласно инструкции производителя. Для этого к 200 мкл бактериальной суспензии добавляли 20 мкл свежеприготовленного 1 М водного раствора бикарбоната натрия, рН 8.3 8.5, и добавляли 20 мкл водного раствора активного эфира биотина. Бактерии инкубировали с биотином 2 часа в темноте, при комнатной температуре и постоянном перемешивании в термошейкере Biosan TS-100 (400 об/мин), после чего дважды отмывали в PBS центрифугированием 2 мин при 2350 g и ресуспендированием в 200 мкл PBS, затем добавляли стерильный глицерин до концентрации 10%. Определяли концентрацию бактерий подсчетом в камере Горяева, доводили PBS до концентрации 1010 бактерий/мл, замораживали в аликвотах по 30 мкл, и хранили при -20°С. Все работы производили в стерильных условиях.
Для проверки эффективности конъюгации биотином к аликвоте Е. coli (300 мкл, 1×107 бактерий/мл) добавляли 1 мкл стрептавидина, конъюгированного с AF405 (Invitrogen, кат. №S32351), инкубировали 30 мин на льду, промывали, центрифугировали 2 мин при 2350 g, ресуспендировали в 200 мкл PBS и анализировали на проточном цитометре BD LSRFortessa, оценивая двойную позитивную популяцию в каналах FITC и AF405 (лазер 405 нм, фильтр 450/50 нм).
Пример 1.2. Фагоцитарный тест
Для отработки фагоцитоза использовали цельную кровь человека, неантропоидных приматов, мышей и летучих мышей. Периферическую кровь отбирали в пробирки с Na-гепарином (Химмедснаб). Концентрацию лейкоцитов в образце определяли на гематологическом анализаторе МЕК-7300K (Nihon Kohden). Рассчитывали количество добавляемых бактерий исходя из соотношения лейкоциты: бактерии = 1:20, в соответствии с ранее опубликованными исследованиями оптимального соотношения объектов фагоцитоза и фагоцитов [Robinson J.P., Carter W.О., Narayanan P. Functional assays by flow cytometry // Manual of clinical laboratory immunology. - 1997. - C. 245-254]. Для проведения теста отбирали 100 мкл цельной крови в полипропиленовую неадгезионную пробирку (Eppendorf, кат. номер 0030125150) стабилизировали температуру в СО2-инкубаторе (37°С, 5% СО2) 5 мин. Фагоцитоз проводили в суспензионной фракции клеток цельной крови без применения специальных процедур для адгезии к поверхности, как описано в [Garcia-Seyda N. et al. Human neutrophils swim and phagocytise bacteria // Biology of the Cell. - 2021. - T. 113. - №. 1. - C. 28-38]. К 100 мкл крови добавляли суспензии бактерий из расчета 20 бактерий на один лейкоцит, инкубировали 1 ч при 37°С и 5% СО2. Для остановки фагоцитоза, образцы помещали на лед как описано в [Serrander L. et al. Selective inhibition of IgG-mediated phagocytosis in gelsolin-deficient murine neutrophils // The Journal of Immunology. 2000. T. 165. №. 5. - C. 2451-2457].
Пример 1.3. Проточная цитометрия и сортировка клеток
К образцу крови на льду после проведения фагоцитоза добавляли антитела CD45 APC-eFluor780 (клон H130, eBioscience, кат. №47-0459-42; 1:100) для маркирования лейкоцитов, а также стрептавидин, конъюгированный с AF405 (Invitrogen, кат. №S32351; 1:100), для выявления бактерий, адгезированных на поверхности клеток. Образцы инкубировали 30 минут в темноте на льду, промывали в PBS с последующим центрифугированием в течение 5 мин при 330 g; супернатант удаляли и ресуспендировали осторожным пипетированием, после чего добавляли в образцы 9 объемов 1-кратного лизирующего буфера с фиксирующим агентом BD FACS Lysing Solution (BD, кат. №349202) и инкубировали 10 минут в темноте при комнатной температуре. Далее образцы центрифугировали 5 мин при 330 g, осадок ресуспендировали в 200 мкл PBS и до анализа хранили при 4°С.
Настройку компенсации проводили в автоматическом режиме в программном обеспечении соответствующего проточного цитометра или сортера по одноцветным контролям (могли быть использованы флуоресцентные частицы согласно рекомендациям производителя и с помощью одноцветных окрашиваний клеток крови теми маркерами, которые затем анализируем совместно в образцах с полным окрашиванием), приготовленным в соответствии с описанной выше методикой. Исключение составил контроль для AF405, который готовился путем окрашивания образца интактной крови антителами CD33 biotin (клон АС104.3ЕЗ, Miltenyi, кат. №130-113-347) в течение 30 мин на льду, с последующим выявлением биотина стрептавидином, конъюгированным с AF405 и дальнейшей обработкой, как описано выше.
Для высокопроизводительного анализа определения пространственного расположения и количества бактерий в фагоцитах и получения точных показателей фагоцитарных индексов методом визуализирующей проточной цитометрии применяли проточный питометр с визуализацией Amnis FlowSight (Cytek), оснащенный 3 лазерами (405, 488 и 642 нм), позволяющий фотографировать клетки в потоке со скоростью до нескольких тысяч в секунду и анализировать пространственное положение микробных частиц в фагоцитах. На Фиг. 2 показаны стратегия гейтирования при анализе на Amnis FlowSight и суммарное представление данных с визуализацией (Фиг. 2, нижний ряд, левый рисунок). Над графиком, иллюстрирующим полученные данные, представлена панель снимков клеток, сделанные питометром. Фотографии клеток разделены по каналам флуоресценции (канале FITC, которым окрашены все бактерии, BF и BF 2 -образы клеток в светлом поле, AF450 подсвечены бактерии на поверхности клеток и наложение каналов (Merge). Анализ изображений клеток позволяет заключить, что двойное окрашивание демонстрируют не поглощенные клеткой бактерии, а только находящиеся на ее поверхности, в то время как поглощенные клеткой бактерии детектируются только в канале FITC. По интенсивности сигнала флуоресценции возможно разделить 4 популяции клеток, различающихся количеством Е. coli внутри и снаружи клеток. Так, в популяции DPlow клетки содержат по 1-2 бактерии на своей поверхности, DPhi - 2-4 бактерии на поверхности, FITClow внутри фагоцитировавших клеток содержится по 1-2 бактерии, FITChi по 2-4 бактерии внутри фагоцитов.
Пример 1.4. Программное обеспечение
Обработку результатов проводили в Microsoft Excel 2019; анализ данных Amnis FlowSight в программе Amnis IDEAS 6.2.
Данное программное обеспечение позволяет проанализировать каждую клетку и с помощью визуального детектирования двойного окрашивания выставлять гейты, разделяющие клетки с бактериями снаружи (с двойным мечением) и внутри (с мечением одним флуорохромом), что позволило провести массовый анализ клеток и определить повышение точности детектирования бактерий, находящихся внутри фагоцитов, наблюдаемое при применении двойного окрашивания (фиг. 3А, красный гейт; фиг. 4). На Фиг. 3А показаны бактерии, детектируемые программой для оценки фагоцитарной активности и встроенной в приложение IDEAS, как находящиеся внутри клеток. Гейты были выставлены на основе флуоресцентного минус один контроля. Однако 70,4% из этих клеток были позитивны и по FITC, и по Streptavidin-AF 405. Таким образом, 70,4% бактерий, детектируемых проточным цитометром с визуализацией как интернализованные, по данным двойного мечения оказались адгезированными на поверхности клеток.
При этом при детектировании программой поверхностной локализации бактерий, применение двойного окрашивания значительно не увеличивает точность прибора (из 100% обнаруженных программой на поверхности, около 5% бактерий, согласно данным двойного окрашивания, были локализованы внутри клеток, фиг. 3Б, бежевый гейт). На Фиг. 3Б показаны бактерии, детектируемые программой как находящиеся снаружи клеток. 94,9% из этих клеток действительно были позитивны и по FITC, и по Streptavidin-AF 405. То есть данные двойного окрашивания с точностью 94,9% подтвердили локализацию бактерий на поверхности клеток.
Таким образом, способ по настоящему изобретению позволяет детектировать интернализованные клетками объекты фагоцитоза с высокой точностью: более чем в 3 раза выше, чем при использовании проточной цитометрии с визуализацией без заявленного способа.
Все публикации, патенты и заявки на патенты включены в настоящий документ посредством ссылки. Хотя в вышеприведенном описании это изобретение было описано в отношении некоторых предпочтительных вариантов его осуществления, и многие детали были изложены в целях иллюстрации, для специалистов в данной области техники будет очевидно, что изобретение допускает дополнительные варианты осуществления и что некоторые детали, описанные в данном документе, могут значительно изменяться без отклонения от сущности изобретения.
Использование терминов в единственном числе в контексте описания изобретения должно толковаться как охватывающее как единственное, так и множественное число, если иное не указано в данном документе или явно не противоречит контексту. Термины «состоящий из», «имеющий», «включающий» и «содержащий» следует толковать как неограничивающие термины, т.е. означающие «включая, но не ограничиваясь», если не указано иное. Перечисление диапазонов значений в данном документе просто предназначено для использования в качестве сокращенного способа индивидуальной ссылки на каждое отдельное значение, попадающее в этот диапазон, если здесь не указано иное, и каждое отдельное значение включено в спецификацию, как если бы оно было отдельно изложено в данном документе. Все способы, описанные в данном документе, могут выполняться в любом подходящем порядке, если иное не указано в данном документе или иным образом явно не противоречит контексту. Использование любых и всех примеров или иллюстративного языка (например, «такой как»), представленных в данном документе, предназначено просто для лучшего описания изобретения и не налагает ограничения на объем изобретения, если иное не заявлено. Никакие формулировки в описании не следует истолковывать как указывающие на какой-либо не заявленный элемент как существенный для практического применения изобретения.
Здесь описаны варианты осуществления этого изобретения, включая лучший из известных изобретателям способа осуществления изобретения. Разновидности этих вариантов осуществления могут стать очевидными для специалистов в данной области техники после прочтения предшествующего описания. Авторы ожидают, что квалифицированные специалисты будут использовать такие варианты в зависимости от обстоятельств, и авторы предполагают, что изобретение будет реализовано на практике иначе, чем конкретно описано в данном документе. Соответственно, это изобретение включает в себя все модификации и эквиваленты признаков, изложенных в прилагаемой формуле изобретения, как это разрешено действующим законодательством. Более того, любая комбинация вышеописанных признаков во всех их возможных вариациях охватывается изобретением, если иное не указано в данном документе или иным образом явно не противоречит контексту.
Заявитель просит рассмотреть представленные материалы заявки «Способ анализа эффективности фагоцитоза» на предмет выдачи патента на изобретение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ сортировки фагоцитирующих клеток | 2024 |
|
RU2835814C1 |
| СПОСОБ ОЦЕНКИ ФАГОЦИТАРНОЙ АКТИВНОСТИ НЕЙТРОФИЛОВ | 2023 |
|
RU2824345C1 |
| ИСПОЛЬЗОВАНИЕ ОКСИДА ГРАФЕНА ДЛЯ АКТИВАЦИИ ФАГОЦИТАРНОЙ ФУНКЦИИ МАКРОФАГОВ | 2022 |
|
RU2809372C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ЭКЗОСОМ ИЗ ПЛАЗМЫ КРОВИ | 2020 |
|
RU2741638C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И АНАЛИЗА ЭКЗОСОМ | 2022 |
|
RU2788198C1 |
| НОВАЯ АССОЦИИРОВАННАЯ С МЕТАСТАТИЧЕСКОЙ ОПУХОЛЬЮ ЧЕЛОВЕКА МОЛЕКУЛА, СПОСОБЫ ДЕТЕКЦИИ КАК АКТИВИРОВАННОГО ГЕНА, ТАК И БЕЛКА И ПРЕПЯТСТВОВАНИЯ ЭКСПРЕССИИ ГЕНОВ | 2009 |
|
RU2546000C2 |
| СПОСОБ ОЦЕНКИ ФАГОЦИТОЗА | 1985 |
|
SU1522923A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ФАГОЦИТОВ ПРИ АЛЛЕРГИИ | 2002 |
|
RU2225984C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ВЫДЕЛЕНИЯ, ОБНАРУЖЕНИЯ И АНАЛИЗА КЛЕТОК ПЛОДА | 2020 |
|
RU2834057C2 |
| Способ оценки прямой контактной токсичности частиц микропластика на модели выделенных моноядерных лейкоцитов периферической крови | 2024 |
|
RU2832331C1 |

Изобретение относится к области анализа биоматериалов с помощью проточной цитометрии и касается способа анализа эффективности фагоцитоза. Способ заключается в том, что проводят фагоцитоз, используя объекты фагоцитоза, предварительно конъюгированные с флуоресцентной меткой и биотином, и образец клеток, способных к фагоцитозу. После остановки фагоцитоза образец фагоцитировавших клеток окрашивают стрептавидином, конъюгированным с флуоресцентной меткой. Затем при помощи проточного цитометра с визуализацией анализируют количество и пространственное расположение объектов фагоцитоза, где количество объектов фагоцитоза и их расположение является одним или более измерениями флуоресценции, которые группируют с помощью гейтирования интенсивности флуоресценции. При этом спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки, конъюгированной со стрептавидином, и оба спектра находятся в диапазоне детекции проточного цитометра. Технический результат заключается в повышении точности определения локализации объектов фагоцитоза внутри клетки. 9 з.п. ф-лы, 3 ил.
1. Способ анализа эффективности фагоцитоза, заключающийся в том, что
i) проводят фагоцитоз, используя объекты фагоцитоза, предварительно конъюгированные с флуоресцентной меткой и биотином, и образец клеток, способных к фагоцитозу,
ii) после остановки фагоцитоза образец фагоцитировавших клеток окрашивают стрептавидином, конъюгированным с флуоресцентной меткой,
iii) затем при помощи проточного цитометра с визуализацией анализируют в образце количество и пространственное расположение упомянутых объектов фагоцитоза, где количество объектов фагоцитоза и их расположение внутри или снаружи клетки является одним или более измерениями флуоресценции, которые группируют с помощью гейтирования интенсивности флуоресценции;
при этом спектр эмиссии флуоресцентной метки, конъюгированной с объектом фагоцитоза, не перекрывается со спектром эмиссии флуоресцентной метки, конъюгированной со стрептавидином, и оба спектра находятся в диапазоне детекции упомянутого проточного цитометра с визуализацией.
2. Способ по п. 1, характеризующийся тем, что для получения конъюгированных объектов фагоцитоза суспензию объектов фагоцитоза фиксируют 2% параформальдегидом, после чего отмывают и последовательно конъюгируют с изотиоцианатом флуоресцеина (FITC) и биотином.
3. Способ по п. 2, характеризующийся тем, что конъюгированные объекты фагоцитоза хранят в присутствии 10% глицерина при –20°С и ниже до этапа i).
4. Способ по п. 2, характеризующийся тем, что конъюгированные объекты фагоцитоза высушивают в вакуумной установке и хранят в плотно закрытых сухих пробирках при –20°С и ниже до этапа i).
5. Способ по любому из пп. 3 или 4, характеризующийся тем, что конъюгированные объекты фагоцитоза транспортируют при 4–10°C в течение 7–10 дней.
6. Способ по любому из пп. 1–5, характеризующийся тем, что в качестве образца клеток, способных к фагоцитозу, используют цельную кровь.
7. Способ по п. 6, характеризующийся тем, что в качестве объекта фагоцитоза используют клетки бактерий при соотношении клеток бактерий относительно лейкоцитов крови 20:1.
8. Способ по любому из пп. 6 или 7, характеризующийся тем, что на этапе ii) образец дополнительно окрашивают антителами против CD45 человека.
9. Способ по любому из пп. 6–8, характеризующийся тем, что после этапа ii) в образце проводят лизирование эритроцитов.
10. Способ по любому из пп. 1–9, характеризующийся тем, что перед этапом iii) образец фиксируют 2% формальдегидом или его аналогами и хранят до 7 дней при 4°C.
| Smirnov A | |||
| и др | |||
| "Using Imaging Flow Cytometry to Quantify Neutrophil Phagocytosis", METHODS IN MOLECULAR BIOLOGY, т | |||
| Прибор для разгонки рельс | 1925 |
|
SU2087A1 |
| Способ получения морфия из опия | 1922 |
|
SU127A1 |
| Мазуров Д.В | |||
| и др | |||
| "Применение проточной цитометрии в иммунодиагностике", МЕДИЦИНСКАЯ ИММУНОЛОГОИЯ, т | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения олифы или массы для приготовления лаков | 1913 |
|
SU507A1 |
| WO 2012074882 A2, 07.06.2012 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ФАГОЦИТАРНОЙ АКТИВНОСТИ НЕЙТРОФИЛОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ЧЕЛОВЕКА ПО СТЕПЕНИ ГАШЕНИЯ БИОЛЮМИНЕСЦЕНЦИИ | 2005 |
|
RU2292553C1 |
Авторы
Даты
2024-12-03—Публикация
2023-12-14—Подача