Настоящее изобретение испрашивает приоритет на основании предшествующей заявки, имеющей номер заявки на патент 2020107908681, поданной в Национальное управление интеллектуальной собственности Китая 7 августа 2020 г., и предшествующей заявки, имеющей номер заявки на патент 2020111050353, поданной в Национальное управление интеллектуальной собственности Китая 15 октября 2020 г., а также приоритет на основании предшествующей заявки, имеющей номер заявки на патент 2020110930801, поданной в Национальное управление интеллектуальной собственности Китая 13 октября 2020 г., полное содержание которых включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к технической области генетической инженерии и микроорганизмов, и в частности, относится к штамму Corynebacterium с повышенной способностью к продукции L-аминокислот, а также к способу его конструирования и применению.
УРОВЕНЬ ТЕХНИКИ
Получение L-аминокислот в промышленных масштабах осуществляется путем ферментации с применением микроорганизмов, таких как бактерии, обладающие способностью продуцировать L-аминокислоты. В качестве таких микроорганизмов могут быть применены, например, штаммы, выделенные из природных источников, и их мутантные штаммы.
Улучшения в получении L-аминокислот путем ферментации могут включать такие методики ферментации, как перемешивание и подача кислорода; или состав питательной среды, например концентрация сахара в процессе ферментации; или обработку культуральной жидкости с получением подходящей формы продукта, например, путем сушки и гранулирования культуральной жидкости или путем ионообменной хроматографии; или могут включать неотъемлемые эксплуатационные характеристики соответствующего микроорганизма как такового. Способы улучшения эксплуатационных характеристик этих микроорганизмов включают мутагенез, селекцию и скрининг мутантов. Штаммы, полученные таким образом, устойчивы к действию антиметаболитов или являются ауксотрофными в отношении обладающих регуляторной значимостью метаболитов и продуцируют L-аминокислоты. Сохраняется потребность в разработке способов экономически более выгодного получения L-аминокислот с высоким выходом.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложен рекомбинантный штамм для получения L-аминокислот, рекомбинантный способ его конструирования и его применение для получения аминокислот путем ферментации.
В настоящем изобретении используют Corynebacterium glutamicum YP97158 в качестве исходной бактерии и вводят сайт-направленную мутацию в ее кодирующую область гена NCgl1089, и/или кодирующую область гена NCgl0761, и/или кодирующую область гена ptsS, и/или обеспечивают их улучшенную экспрессию, и полученный мутантный ген и рекомбинантный штамм, содержащий указанный ген, обладают способностью к эффективной продукции L-аминокислот, что значительно увеличивает продукцию L-аминокислот, а также полученный штамм является стабильным, что снижает производственные расходы при его применении в качестве штамма-продуцента L-аминокислот.
Таким образом, в настоящем изобретении предложены следующие технические решения:
В настоящем изобретении предложен принадлежащий к роду Corynebacterium микроорганизм, продуцирующий L-аминокислоты, который обладает улучшенной экспрессией полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 3, и/или SEQ ID NO: 35, и/или SEQ ID №: 63. Согласно настоящему изобретению улучшенная экспрессия представляет собой усиленную экспрессию полинуклеотида, или полинуклеотид, кодирующий аминокислотную последовательность, имеет точечную мутацию, или полинуклеотид, кодирующий аминокислотную последовательность, имеет точечную мутацию, и экспрессия является усиленной.
Первый аспект настоящего изобретения:
Аминокислотная последовательность SEQ ID NO: 3 представляет собой белок, кодируемый геном NCgl1089.
Полинуклеотид может кодировать аминокислотную последовательность, которая имеет составляющую примерно 90% или более, примерно 92% или более, примерно 95% или более, примерно 97% или более, примерно 98% или более, примерно 99% или более гомологию последовательностей с аминокислотной последовательностью SEQ ID NO: 3.
В одном из воплощений настоящего изобретения полинуклеотид может включать нуклеотидную последовательность SEQ ID NO: l.
В одном из воплощений настоящего изобретения полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 3, имеет точечную мутацию, которая приводит к замене глутаминовой кислоты в положении 170 аминокислотной последовательности SEQ ID NO: 3 на другие аминокислоты.
Согласно настоящему изобретению предпочтительно глутаминовая кислота в положении 170 заменена на лизин.
Согласно настоящему изобретению аминокислотная последовательность представлена SEQ ID NO: 3, при этом аминокислотная последовательность после замены глутаминовой кислоты (Е) в положении 170 на лизин (К) представлена SEQ ID NO: 4.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность с точечной мутацией образуется вследствие мутации основания в положении 508 полинуклеотидной последовательности, представленной SEQ ID NO: 1.
Согласно настоящему изобретению указанная мутация включает приводящую к замене гуанина (G) на аденин (А) мутацию основания в положении 508 полинуклеотидной последовательности, представленной SEQ ID NO: 1.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность с точечной мутацией включает полинуклеотидную последовательность, представленную SEQ ID NO: 2.
Согласно настоящему изобретению регулирующие экспрессию последовательности полинуклеотидов согласно настоящему изобретению могут быть модифицированы. Регулирующие экспрессию последовательности контролируют экспрессию полинуклеотида, с которым они функционально связаны. Регуляторные последовательности могут представлять собой, например, промоторы, терминаторы, энхансеры, сайленсеры и тому подобное.
В одном из воплощений настоящего изобретения промотор представляет собой промотор полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 3 (ген NCgl1089).
В настоящем изобретении дополнительно предложены полинуклеотидная последовательность, аминокислотная последовательность, кодируемая указанной полинуклеотидной последовательностью, рекомбинантный вектор, включающий указанную полинуклеотидную последовательность, и рекомбинантный штамм, содержащий указанную полинуклеотидную последовательность.
Согласно настоящему изобретению полинуклеотидная последовательность включает полинуклеотид, кодирующий аминокислотную последовательность, представленную SEQ ID NO: 3, в которой глутаминовая кислота в положении 170 заменена на другие аминокислоты.
Согласно настоящему изобретению предпочтительно глутаминовая кислота в положении 170 заменена на лизин.
Согласно настоящему изобретению аминокислотная последовательность представлена SEQ ID NO: 3, при этом аминокислотная последовательность после замены глутаминовой кислоты (Е) в положении 170 на лизин (К) представлена SEQ ID NO: 4.
Согласно настоящему изобретению предпочтительно полинуклеотидная последовательность, кодирующая аминокислотную последовательность, представленную SEQ ID NO: 3, содержит полинуклеотидную последовательность, представленную SEQ ID NO: 1.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность образуется вследствие мутации основания в положении 508 полинуклеотидной последовательности, представленной SEQ ID NO: 1.
Согласно настоящему изобретению указанная мутация включает приводящую к замене гуанина (G) на аденин (А) мутацию основания в положении 508 полинуклеотидной последовательности, представленной SEQ ID NO: 1.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность включает полинуклеотидную последовательность, представленную SEQ ID NO: 2.
Согласно настоящему изобретению аминокислотная последовательность включает аминокислотную последовательность, представленную SEQ ID NO: 4.
Согласно настоящему изобретению рекомбинантный вектор конструируют путем введения полинуклеотидной последовательности в плазмиду.
В одном из воплощений настоящего изобретения плазмида представляет собой плазмиду pK18mobsacB.
В другом воплощении настоящего изобретения плазмида представляет собой плазмиду pXMJ19.
В частности, полинуклеотидная последовательность и плазмида могут быть сконструированы с получением рекомбинантного вектора с помощью системы рекомбинации NEBuilder.
Согласно настоящему изобретению рекомбинантный штамм содержит полинуклеотидную последовательность.
В качестве одного из воплощений настоящего изобретения, исходной бактерией для рекомбинантного штамма является YP97158.
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма Corynebacterium.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
Полинуклеотидную последовательность NCgl1089 дикого типа, представленную SEQ ID NO: 1 в штамме-хозяине, подвергают трансформации, и основание в положении 508 подвергают мутации с получением рекомбинантного штамма Corynebacterium, включающего ген, кодирующий мутантный NCgl1089.
В соответствии со способом конструирования согласно настоящему изобретению трансформация включает по меньшей мере один из следующих подходов: мутагенез, сайт-направленный мутагенез посредством ПЦР и/или гомологичную рекомбинацию.
В соответствии со способом конструирования согласно настоящему изобретению указанная мутация относится к приводящей к замене гуанина (G) на аденин (А) мутации основания в положении 508 в SEQ ID NO: 1; в частности, полинуклеотидная последовательность, включающая ген, кодирующий мутантный NCgl1089, представлена SEQ ID NO: 2.
Помимо этого, указанный способ конструирования включает следующие стадии: (1) трансформация нуклеотидной последовательности гена NCgl1089 дикого типа, представленной SEQ ID NO: 1, вследствие чего основание в положении 508 подвергается мутации, с получением полинуклеотидной последовательности мутантного гена NCgl1089;
(2) обработка полученной мутантной полинуклеотидной последовательности и плазмиды с помощью системы рекомбинации NEBuilder с конструированием рекомбинантного вектора;
(3) введение полученного рекомбинантного вектора в штамм-хозяин с получением рекомбинантного штамма Corynebacterium, включающего ген, кодирующий мутантный NCgl1089.
В соответствии со способом конструирования согласно настоящему изобретению стадия (1) включает: конструирование гена NCgl1089 с точечной мутацией: синтез двух пар праймеров, Р1 и Р2, а также Р3 и Р4, в соответствии с последовательностью генома Corynebacterium glutamicum для амплификации фрагмента гена NCgl1089, введение точечной мутации в ген NCgl1089 дикого типа SEQ ID NO: 1 с помощью сайт-направленного мутагенеза посредством ПЦР с получением нуклеотидной последовательности гена NCgl1089 с точечной мутацией SEQ ID NO: 2, обозначенной как NCgl1089G508A.
В одном из воплощений настоящего изобретения геном Corynebacterium glutamicum может быть получен из штамма АТСС13032, и последовательность его генома может быть получена с помощью веб-сайта NCBI.
В одном из воплощений настоящего изобретения на стадии (1) праймеры представляют собой:
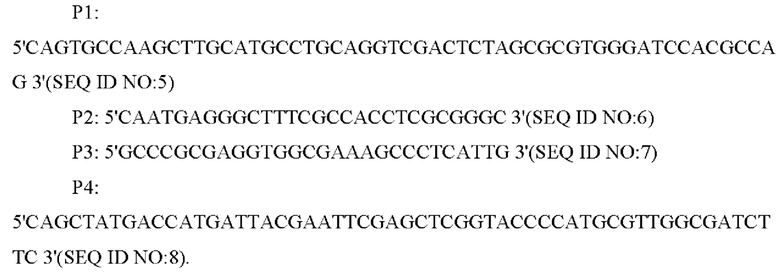
В одном из воплощений настоящего изобретения амплификацию методом ПЦР проводят следующим образом: денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, и элонгация при 72°С в течение 40 с (30 циклов).
В одном из воплощений настоящего изобретения амплификацию методом ПЦР с перекрывающимися праймерами проводят следующим образом: денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, и элонгация при 72°С в течение 90 с (30 циклов).
В соответствии со способом конструирования согласно настоящему изобретению стадия (2) включает конструирование рекомбинантной плазмиды, включающее: объединение выделенных и очищенных плазмид NCgl1089G508A и pK18mobsacB с помощью системы рекомбинации NEBuilder с получением рекомбинантной плазмиды pK18-NCgl1089G508A.
В соответствии со способом конструирования согласно настоящему изобретению стадия (3) включает конструирование рекомбинантного штамма, и штамм-хозяин трансформируют рекомбинантной плазмидой pK18-NCgl1089G508A с получением рекомбинантного штамма.
В одном из воплощений настоящего изобретения трансформацию на стадии (3) осуществляют методом электротрансформации.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения рекомбинацию осуществляют методом гомологичной рекомбинации.
В четвертом аспекте настоящего изобретения дополнительно предложен способ конструирования рекомбинантного штамма Corynebacterium.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
амплификацию вышележащего и нижележащего фрагментов гомологичного плеча гена NCgl1089, кодирующей области гена NCgl1089, кодирующей области гена NCgl1089G508A и промоторной последовательности гена, а также введение гена NCgl1089 или NCgl1089 G508A в геном штамма-хозяина путем гомологичной рекомбинации с обеспечением штамма, характеризующегося сверхэкспрессией гена NCgl1089 или NCgl1089G508A.
В одном из воплощений настоящего изобретения праймеры для амплификации вышележащего фрагмента гомологичного плеча представляют собой:
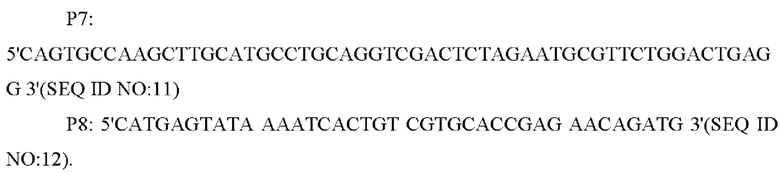
В одном из воплощений настоящего изобретения праймеры для амплификации нижележащих фрагментов гомологичного плеча представляют собой:
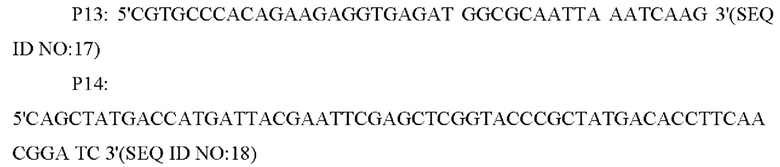
В одном из воплощений настоящего изобретения праймеры для амплификации последовательности промоторной области гена представляют собой:
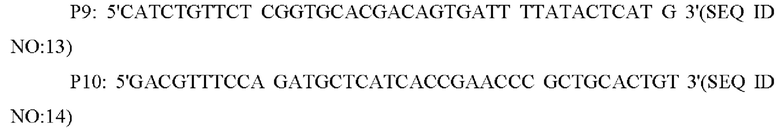
В одном из воплощений настоящего изобретения праймеры для амплификации кодирующей области гена NCgl1089 или кодирующей области гена NCgl1089G508A представляют собой:
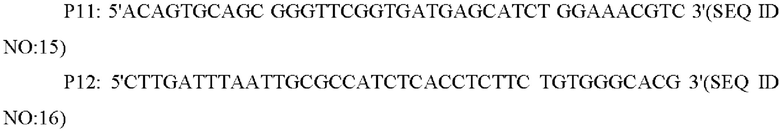
В одном из воплощений настоящего изобретения фрагмент NCgl1089 или NCgl1089G508A с его собственным промотором амплифицируют с применением указанных выше Р9/Р12 в качестве праймеров, а также фрагмента промотора гена NCgl1089 и NCgl1089 или NCgl1089G508A, полученных путем амплификации, в качестве матриц.
В одном из воплощений настоящего изобретения амплификацию проводят с применением указанных выше Р7/Р14 в качестве праймеров и трех фрагментов, включающих вышележащий гомологичный фрагмент, нижележащий гомологичный фрагмент HNCgl1089 или NCgl1089G508A с собственным промотором, полученным путем амплификации, в качестве матриц с получением интегрированных фрагментов гомологичного плеча.
В одном из воплощений настоящего изобретения применяют следующую систему для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения систему рекомбинации NEBuilder применяют для соединения челночной плазмиды PK18mobsacB и интегрируемого фрагмента гомологического плеча с получением интегрирующей плазмиды.
В одном из воплощений настоящего изобретения осуществляют трансфекцию интегрирующей плазмиды в штамм-хозяин, и ген NCgl1089 или NCgl1089G508A встраивается в геном штамма-хозяина посредством гомологичной рекомбинации.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой штамм, несущий полинуклеотидную последовательность, представленную SEQ ID NO: 2.
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма Corynebacterium.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
амплификацию последовательностей кодирующей области и промоторной области гена NCgl1089 или NCgl1089G508A, конструирование плазмидного вектора сверхэкспрессии и перенос указанного вектора в штамм-хозяин с обеспечением штамма, характеризующегося сверхэкспрессией генов NCgl1089 и NCgl1089G508A.
В одном из воплощений настоящего изобретения праймеры для амплификации фрагмента промотора NCgl1089 представляют собой:
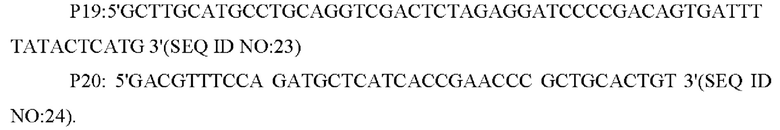
В одном из воплощений настоящего изобретения праймеры для амплификации гена NCgl1089 или NCgl1089G508A представляют собой:
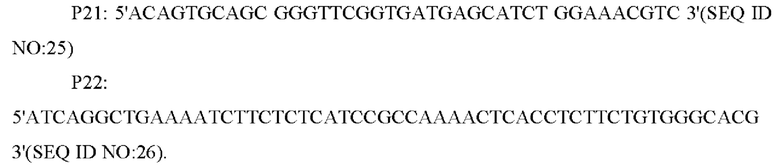
В одном из воплощений настоящего изобретения фрагмент NCgl1089 или NCgl1089G508A с его собственным промотором получают путем амплификации методом ПЦР с перекрывающимися праймерами с применением указанных выше Р19/Р22 в качестве праймеров, а также фрагмента промотора гена NCgl1089 и NCgl1089 или NCgl1089 G508A полученных путем амплификации, в качестве матриц.
В одном из воплощений настоящего изобретения система для ПЦР является следующей: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл; амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения систему рекомбинации NEBuilder применяют для соединения челночной плазмиды pXMJ19 и фрагмента NCgl1089 или NCgl1089G508A с его собственным промотором с получением плазмиды сверхэкспрессии.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой штамм, несущий полинуклеотидную последовательность, представленную SEQ ID NO: 2.
Рекомбинантный штамм, полученный в соответствии с настоящим изобретением, может быть применен для получения L-лизина путем ферментации отдельно, а также может быть смешан с другими продуцирующими L-лизин бактериями для получения L-лизина путем ферментации.
В настоящем изобретении дополнительно предложен способ получения L-лизина, включающий культивирование микроорганизма и получение L-лизина из культуры.
Второй аспект настоящего изобретения:
В настоящем изобретении предложены бактерии, продуцирующие L-аминокислоты, у которых улучшена экспрессия полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 35. В настоящем изобретении дополнительно предложен способ получения L-аминокислот с применением микроорганизма.
Аминокислотная последовательность SEQ ID NO: 35 представляет собой белок, кодируемый геном NCgl0761.
Полинуклеотид может кодировать аминокислотную последовательность, которая имеет составляющую примерно 90% или более, примерно 92% или более, примерно 95% или более, примерно 97% или более, примерно 98% или более, примерно 99% или более гомологию последовательностей с аминокислотной последовательностью SEQ ID NO: 35.
Указанные бактерии обладают повышенной способностью к продукции L-аминокислот по сравнению с немодифицированными штаммами.
В одном из воплощений настоящего изобретения полинуклеотид может включать нуклеотидную последовательность SEQ ID NO: 35.
В одном из воплощений настоящего изобретения полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 35, имеет точечную мутацию, которая приводит к замене лейцина в положении 31 аминокислотной последовательности SEQ ID NO: 35 на другие аминокислоты.
Согласно настоящему изобретению предпочтительно лейцин в положении 31 заменен на аргинин.
Согласно настоящему изобретению полинуклеотидная последовательность представлена SEQ ID NO: 35, при этом аминокислотная последовательность после замены лейцина в положении 31 на аргинин представлена SEQ ID NO: 36.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность с точечной мутацией образуется вследствие мутации основания в положении 92 полинуклеотидной последовательности, представленной SEQ ID NO: 33.
Согласно настоящему изобретению указанная мутация включает приводящую к замене тимина (Т) на гуанин (G) мутацию основания в положении 92 полинуклеотидной последовательности, представленной SEQ ID NO: 33.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность с точечной мутацией включает полинуклеотидную последовательность, представленную SEQ ID NO: 34.
Согласно настоящему изобретению регулирующие экспрессию последовательности полинуклеотидов могут быть модифицированы. Регулирующие экспрессию последовательности контролируют экспрессию полинуклеотидов, с которыми они функционально связаны, и могут включать, например, промоторы, терминаторы, энхансеры, сайленсеры и тому подобное. Полинуклеотиды могут иметь модификации в инициирующем кодоне.
В одном из воплощений настоящего изобретения промотор представляет собой промотор полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 35 (ген NCgl0761).
В одном из воплощений настоящего изобретения микроорганизм, принадлежащий к роду Corynebacterium, представляет собой Corynebacterium glutamicum АТСС13869.
В настоящем изобретении дополнительно предложены полинуклеотидная последовательность, аминокислотная последовательность, кодируемая указанной полинуклеотидной последовательностью, рекомбинантный вектор, включающий указанную полинуклеотидную последовательность, и рекомбинантный штамм, содержащий указанную полинуклеотидную последовательность.
Согласно настоящему изобретению полинуклеотидная последовательность включает полинуклеотид, кодирующий полипептид, включающий аминокислотную последовательность, представленную SEQ ID NO: 35, где лейцин в положении 31 заменен на другие аминокислоты.
Согласно настоящему изобретению предпочтительно лейцин в положении 31 заменен на аргинин.
Согласно настоящему изобретению полинуклеотидная последовательность представлена SEQ ID NO: 35, при этом аминокислотная последовательность после замены лейцина в положении 31 на аргинин представлена SEQ ID NO: 36.
Согласно настоящему изобретению предпочтительно полинуклеотидная последовательность, кодирующая аминокислотную последовательность, представленную SEQ ID NO: 35, содержит полинуклеотидную последовательность, представленную SEQ ID NO: 33.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность образуется вследствие мутации основания в положении 92 полинуклеотидной последовательности, представленной SEQ ID NO: 33.
Согласно настоящему изобретению указанная мутация включает приводящую к замене тимина (Т) на гуанин (G) мутацию основания в положении 92 полинуклеотидной последовательности, представленной SEQ ID NO: 33.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность включает полинуклеотидную последовательность, представленную SEQ ID NO: 34.
Согласно настоящему изобретению аминокислотная последовательность включает аминокислотную последовательность, представленную SEQ ID NO: 36.
Согласно настоящему изобретению рекомбинантный вектор конструируют путем введения полинуклеотидной последовательности в плазмиду.
В одном из воплощений настоящего изобретения плазмида представляет собой плазмиду pK18mobsacB.
В другом воплощении настоящего изобретения плазмида представляет собой плазмиду pXMJ19.
В частности, полинуклеотидная последовательность и плазмида могут быть сконструированы с получением рекомбинантного вектора с помощью системы рекомбинации NEBuilder.
Согласно настоящему изобретению рекомбинантный штамм содержит полинуклеотидную последовательность.
В качестве одного из воплощений настоящего изобретения, исходной бактерией для рекомбинантного штамма является YP97158.
В качестве одного из воплощений настоящего изобретения, исходной бактерией для рекомбинантного штамма является АТСС 13869
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма, продуцирующего L-аминокислоту.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
Полинуклеотидную последовательность NCgl0761 дикого типа, представленную SEQ ID NO: 33 в штамме-хозяине, подвергают трансформации, и основание в положении 92 подвергают мутации с получением рекомбинантного штамма, включающего ген, кодирующий мутантный NCgl0761.
В соответствии со способом конструирования согласно настоящему изобретению трансформация включает по меньшей мере один из следующих подходов: мутагенез, сайт-направленный мутагенез посредством ПЦР и/или гомологичную рекомбинацию.
В соответствии со способом конструирования согласно настоящему изобретению указанная мутация относится к приводящей к замене тимина (Т) на гуанин (G) мутации основания в положении 92 SEQ ID NO: 33; в частности, полинуклеотидная последовательность, включающая ген, кодирующий мутантный NCgl0761, представлена SEQ ID NO: 34.
Помимо этого, указанный способ конструирования включает следующие стадии:
(1) трансформация нуклеотидной последовательности гена NCgl0761 дикого типа, представленной SEQ ID NO: 33, вследствие чего основание в положении 92 подвергается мутации, с получением полинуклеотидной последовательности мутантного гена NCgl0761;
(2) соединение мутантной полинуклеотидной последовательности с плазмидой с конструированием рекомбинантного вектора;
(3) введение полученного рекомбинантного вектора в штамм-хозяин с получением рекомбинантного штамма, включающего ген, кодирующий мутантный NCgl0761.
В соответствии со способом конструирования согласно настоящему изобретению стадия (1) включает: конструирование гена NCgl0761 с точечной мутацией: синтез двух пар праймеров, Р1 и Р2, а также Р3 и Р4, в соответствии с последовательностью генома немодифицированного штамма для амплификации фрагмента гена NCgl10761, введение точечной мутации в ген NCgl0761 дикого типа SEQ ID NO: 33 с помощью сайт-направленного мутагенеза посредством ПЦР с получением нуклеотидной последовательности гена NCgl0761 с точечной мутацией SEQ ID NO: 34, обозначенной как NCgl0761L31R.
В одном из воплощений настоящего изобретения геном немодифицированного штамма может быть получен из штамма АТСС13032 или АТСС13869, и последовательность его генома может быть получена с помощью веб-сайта NCBI.
В одном из воплощений настоящего изобретения на стадии (1) праймеры представляют собой:
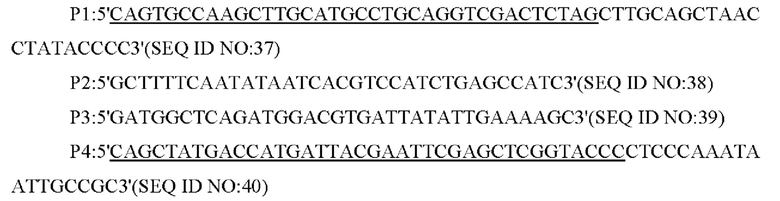
В одном из воплощений настоящего изобретения амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, и элонгация при 72°С в течение 40 с (30 циклов), финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения амплификацию методом ПЦР с перекрывающимися праймерами проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, и элонгация при 72°С в течение 60 с (30 циклов), финальная элонгация при 72°С в течение 10 мин.
В соответствии со способом конструирования согласно настоящему изобретению стадия (2) включает конструирование рекомбинантной плазмиды, включающее: объединение выделенных и очищенных плазмид NCgl0761L31R и pK18mobsacB с помощью системы рекомбинации NEBuilder с получением рекомбинантной плазмиды.
В соответствии со способом конструирования согласно настоящему изобретению стадия (3) включает конструирование рекомбинантного штамма, и штамм-хозяин трансформируют рекомбинантной плазмидой с получением рекомбинантного штамма.
В одном из воплощений настоящего изобретения трансформацию на стадии (3) осуществляют методом электротрансформации.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой АТСС 13869.
В одном из воплощений настоящего изобретения рекомбинацию осуществляют методом гомологичной рекомбинации.
В четвертом аспекте настоящего изобретения дополнительно предложен способ конструирования рекомбинантного штамма, продуцирующего L-аминокислоту.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
амплификацию вышележащего и нижележащего фрагментов гомологичного плеча гена NCgl0761, кодирующей области гена NCgl0761 и последовательности его промоторной области или кодирующей области гена NCgl0761L31R и последовательности его промоторной области, а также их введение в геном штамма-хозяина путем гомологичной рекомбинации генов NCgl0761 и NCgl0761L31R с обеспечением штамма, характеризующегося сверхэкспрессией генов NCgl0761 и NCgl0761L31R.
В одном из воплощений настоящего изобретения праймеры для амплификации вышележащего фрагмента гомологичного плеча представляют собой:
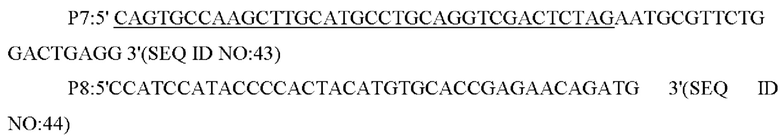
В одном из воплощений настоящего изобретения праймеры для амплификации нижележащих фрагментов гомологичного плеча представляют собой:

В одном из воплощений настоящего изобретения праймеры для амплификации последовательности кодирующей области гена и его промоторной области представляют собой:
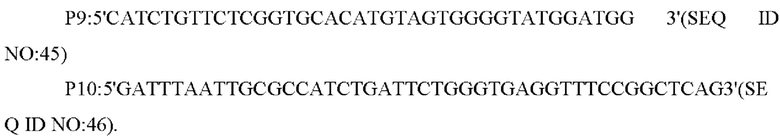
В одном из воплощений настоящего изобретения применяют следующую систему для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения систему рекомбинации NEBuilder применяют для соединения челночной плазмиды PK18mobsacB, вышележащего и нижележащего фрагментов гомологичного плеча, кодирующей области гена и фрагмента промоторной области с получением интегрирующей плазмиды.
В одном из воплощений настоящего изобретения осуществляют трансфекцию интегрирующей плазмиды в штамм-хозяин, и ген NCgl0761 или NCgl0761L31R встраивается в геном штамма-хозяина посредством гомологичной рекомбинации.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой АТСС 13869.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой штамм, несущий полинуклеотидную последовательность, представленную SEQ ID NO: 2.
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма для получения L-аминокислот.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
амплификацию кодирующей области и последовательности промоторной области гена NCgl0761 или кодирующей области и последовательности промоторной области гена NCgl0761L31R, конструирование плазмидного вектора сверхэкспрессии и перенос указанного вектора в штамм-хозяин с обеспечением штамма, характеризующегося сверхэкспрессией генов NCgl0761 и NCgl0761L31R.
В одном из воплощений настоящего изобретения праймеры для амплификации последовательности кодирующей области гена и его промоторной области представляют собой:

В одном из воплощений настоящего изобретения система для ПЦР является следующей: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения систему рекомбинации NEBuilder применяют для соединения челночной плазмиды pXMJ19 и фрагмента NCgl0761 или NCgl0761L31R с его собственным промотором с получением плазмиды сверхэкспрессии.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой АТСС 13869.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой штамм, несущий полинуклеотидную последовательность, представленную SEQ ID NO: 34.
Рекомбинантный штамм, полученный в соответствии с настоящим изобретением, может быть применен для получения L-аминокислоты путем ферментации отдельно, а также может быть смешан с другими продуцирующими L-аминокислоты бактериями для получения L-аминокислоты путем ферментации.
В настоящем изобретении дополнительно предложен способ получения L-аминокислоты, включающий культивирование бактерии и получение L-аминокислоты из культуры.
Третий аспект настоящего изобретения:
В настоящем изобретении предложена продуцирующая L-аминокислоту бактерия, которая обладает улучшенной экспрессией полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 63. Согласно настоящему изобретению улучшенная экспрессия представляет собой усиленную экспрессию полинуклеотида, или полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63, имеет точечную мутацию, или полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63, имеет точечную мутацию, и экспрессия является усиленной.
Аминокислотная последовательность SEQ ID NO: 63 представляет собой белок, кодируемый геном ptsS.
Бактерии обладают повышенной способностью к продукции L-аминокислот.
Бактерии, обладающие способностью продуцировать L-аминокислоты, могут представлять собой бактерии, способные накапливать целевую L-аминокислоту в среде в количестве предпочтительно 0,5 г/л или более, более предпочтительно 1,0 г/л или более.
Полинуклеотид может кодировать аминокислотную последовательность, которая имеет составляющую примерно 90% или более, примерно 92% или более, примерно 95% или более, примерно 97% или более, примерно 98% или более, примерно 99% или более гомологию последовательностей с аминокислотной последовательностью SEQ ID NO: 3.
В некоторых воплощениях настоящего изобретения применяемый вектор представляет собой плазмиду pK18mobsacB, плазмиду pXMJ19.
В конкретном воплощении настоящего изобретения полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63, может включать нуклеотидную последовательность SEQ ID NO: 61.
В одном из воплощений настоящего изобретения улучшение экспрессии означает, что полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63, имеет точечную мутацию, вследствие чего метионин в положении 162 аминокислотной последовательности SEQ ID NO: 63 заменен на другие аминокислоты.
Согласно настоящему изобретению предпочтительно метионин в положении 162 заменен на треонин.
Согласно настоящему изобретению аминокислотная последовательность представлена SEQ ID NO: 63, при этом аминокислотная последовательность после замены метионина в положении 162 на треонин представлена SEQ ID NO: 64.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность с точечной мутацией образуется вследствие мутации основания в положении 485 полинуклеотидной последовательности, представленной SEQ ID NO: 61.
Согласно настоящему изобретению указанная мутация включает приводящую к замене тимина (Т) на цитозин (С) мутацию основания в положении 485 полинуклеотидной последовательности, представленной SEQ ID NO: 61.
В одном из воплощений настоящего изобретения полинуклеотидная последовательность с точечной мутацией включает полинуклеотидную последовательность, представленную SEQ ID NO: 62.
Согласно настоящему изобретению полинуклеотидная последовательность функционально связана с регуляторной последовательностью.
В конкретном воплощении настоящего изобретения промотор представляет собой промотор полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 63 (ген ptsS).
В одном из воплощений настоящего изобретения микроорганизм, принадлежащий к роду Corynebacterium, представляет собой Corynebacterium glutamicum АТСС13869. Согласно настоящему изобретению бактерии также могут иметь другие улучшения, связанные с увеличением продукции L-аминокислот.
В настоящем изобретении дополнительно предложены полинуклеотидная последовательность, аминокислотная последовательность, кодируемая указанной полинуклеотидной последовательностью, рекомбинантный вектор, включающий указанную полинуклеотидную последовательность, и рекомбинантный штамм, содержащий указанную полинуклеотидную последовательность.
Согласно настоящему изобретению полинуклеотидная последовательность имеет улучшенную экспрессию, при этом улучшение включает точечную мутацию полинуклеотида, кодирующего полипептид, включающий аминокислотную последовательность, представленную SEQ ID NO: 63, вследствие чего метионин в положении 162 указанной аминокислотной последовательности заменен на другие аминокислоты.
Согласно настоящему изобретению предпочтительно метионин в положении 162 заменен на треонин.
Согласно настоящему изобретению аминокислотная последовательность представлена SEQ ID NO: 63, при этом аминокислотная последовательность после замены метионина в положении 162 на треонин представлена SEQ ID NO: 64.
Согласно настоящему изобретению полинуклеотидная последовательность, кодирующая аминокислотную последовательность, представленную SEQ ID NO: 63, содержит полинуклеотидную последовательность, представленную SEQ ID NO: 61.
В одном из воплощений настоящего изобретения мутантная полинуклеотидная последовательность, предложенная в настоящем изобретении, образуется вследствие мутации основания в положении 485 полинуклеотидной последовательности, представленной SEQ ID NO: 61.
Согласно настоящему изобретению указанная мутация включает приводящую к замене тимина (Т) на цитозин (С) мутацию основания в положении 485 полинуклеотидной последовательности, представленной SEQ ID NO: 61.
В одном из воплощений настоящего изобретения мутантная полинуклеотидная последовательность включает полинуклеотидную последовательность, представленную SEQ ID NO: 62.
Согласно настоящему изобретению содержащая замену аминокислотная последовательность включает аминокислотную последовательность, представленную SEQ ID NO: 64.
Согласно настоящему изобретению рекомбинантный вектор конструируют путем введения полинуклеотидной последовательности в плазмиду.
В одном из воплощений настоящего изобретения плазмида представляет собой плазмиду pK18mobsacB.
В другом воплощении настоящего изобретения плазмида представляет собой плазмиду pXMJ19.
В частности, полинуклеотидная последовательность и плазмида могут быть сконструированы с получением рекомбинантного вектора с помощью системы рекомбинации NEBuilder.
Согласно настоящему изобретению рекомбинантный штамм содержит полинуклеотидную последовательность.
В качестве одного из воплощений настоящего изобретения, исходной бактерией для рекомбинантного штамма является YP97158.
В качестве одного из воплощений настоящего изобретения, исходной бактерией для рекомбинантного штамма является АТСС 13869
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма, продуцирующего L-аминокислоту.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
трансформацию полинуклеотидной последовательности ptsS дикого типа, представленной SEQ ID NO: 61, в штамме-хозяине, а также обеспечение мутации основания в положении 485 с получением рекомбинантного штамма, включающего ген, кодирующий мутантный ptsS.
В соответствии со способом конструирования согласно настоящему изобретению трансформация включает по меньшей мере один из следующих подходов: мутагенез, сайт-направленный мутагенез посредством ПЦР и/или гомологичную рекомбинацию.
В соответствии со способом конструирования согласно настоящему изобретению указанная мутация относится к приводящей к замене тимина (Т) на цитозин (С) мутации основания в положении 485 SEQ ID NO: 61; в частности, полинуклеотидная последовательность, включающая ген, кодирующий мутантный ptsS, представлена SEQ ID NO: 62.
Помимо этого, указанный способ конструирования включает следующие стадии:
(1) трансформация нуклеотидной последовательности гена ptsS дикого типа, представленной SEQ ID NO: 61, вследствие чего основание в положении 485 подвергается мутации, с получением полинуклеотидной последовательности мутантного гена ptsS;
(2) соединение мутантной полинуклеотидной последовательности с плазмидой с конструированием рекомбинантного вектора;
(3) введение полученного рекомбинантного вектора в штамм-хозяин с получением рекомбинантного штамма, включающего ген, кодирующий мутантный ptsS.
В соответствии со способом конструирования согласно настоящему изобретению стадия (1) включает: конструирование гена ptsS с точечной мутацией: синтез двух пар праймеров, Р1 и Р2, а также Р3 и Р4, в соответствии с последовательностью генома немодифицированного штамма для амплификации фрагмента гена ptsS, точечную мутацию вводят в ген ptsS дикого типа SEQ ID NO: 61 с помощью сайт-направленного мутагенеза посредством ПЦР с получением нуклеотидной последовательности гена ptsS с точечной мутацией SEQ ID NO: 62, обозначенной как ptsS Т485С.
В одном из воплощений настоящего изобретения геном немодифицированного штамма может быть получен из штамма АТСС 13032, и последовательность его генома может быть получена с помощью веб-сайта NCBI.
В одном из воплощений настоящего изобретения на стадии (1) праймеры представляют собой:
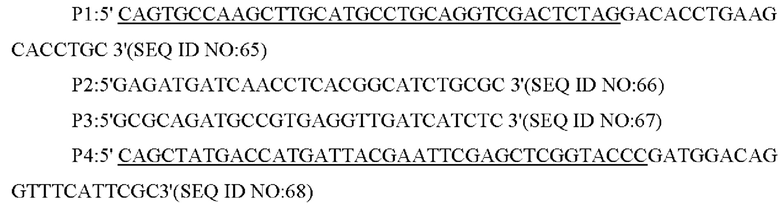
В одном из воплощений настоящего изобретения амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 40 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения амплификацию методом ПЦР с перекрывающимися праймерами проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, и элонгация при 72°С в течение 90 с (30 циклов), финальная элонгация при 72°С в течение 10 мин.
В соответствии со способом конструирования согласно настоящему изобретению стадия (2) включает конструирование рекомбинантной плазмиды, включающее: объединение выделенных и очищенных плазмид ptsSM162T и pK18mobsacB с помощью системы рекомбинации NEBuilder с получением рекомбинантной плазмиды.
В соответствии со способом конструирования согласно настоящему изобретению стадия (3) включает конструирование рекомбинантного штамма, и штамм-хозяин трансформируют рекомбинантной плазмидой с получением рекомбинантного штамма.
В одном из воплощений настоящего изобретения трансформацию на стадии (3) осуществляют методом электротрансформации.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения рекомбинацию осуществляют методом гомологичной рекомбинации.
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма, продуцирующего L-аминокислоту.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
Амплификацию вышележащего и нижележащего фрагментов гомологичного плеча гена ptsS, кодирующей области и последовательности промоторной области гена ptsS, или амплификацию кодирующей области и последовательности промоторной области гена ptsS или PtsSM162T; и полученный ген ptsS или PtsSМ162Т вводят в геном штамма-хозяина путем гомологичной рекомбинации с получением штамма, характеризующегося сверхэкспрессией гена PtsS или PtsSМ1б2Т.
В одном из воплощений настоящего изобретения праймеры для амплификации вышележащего фрагмента гомологичного плеча представляют собой:
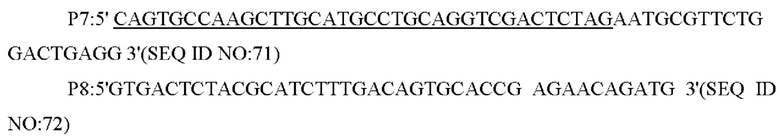
В одном из воплощений настоящего изобретения праймеры для амплификации нижележащих фрагментов гомологичного плеча представляют собой:
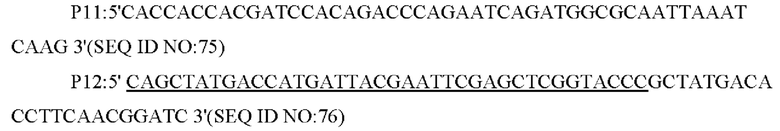
В одном из воплощений настоящего изобретения праймеры для амплификации последовательности кодирующей области гена и его промоторной области представляют собой:
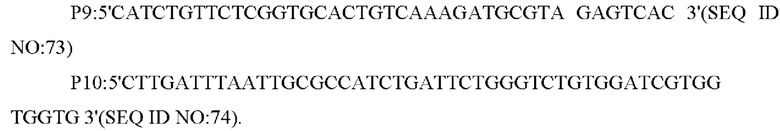
В одном из воплощений настоящего изобретения применяют указанные выше Р7-Р12 в качестве праймеров и три фрагмента, включающие вышележащий гомологичный фрагмент, нижележащий гомологичный фрагмент и PtsS или PtsSM162T с собственным промотором, полученным путем амплификации, в качестве матриц для амплификации с получением интегрированных фрагментов гомологичного плеча.
В одном из воплощений настоящего изобретения применяют следующую систему для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения систему рекомбинации NEBuilder применяют для соединения челночной плазмиды PK18mobsacB, вышележащего и нижележащего фрагментов гомологичного плеча, кодирующей области гена и фрагмента промоторной области с получением интегрирующей плазмиды.
В одном из воплощений настоящего изобретения осуществляют трансфекцию интегрирующей плазмиды в штамм-хозяин, и ген PtsS или PtsSM162T встраивается в геном штамма-хозяина посредством гомологичной рекомбинации.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158. В одном из воплощений настоящего изобретения штамм-хозяин представляет собой штамм, несущий полинуклеотидную последовательность, представленную SEQ ID NO: 62.
В настоящем изобретении дополнительно предложен способ конструирования рекомбинантного штамма для получения L-аминокислот.
Согласно настоящему изобретению указанный способ конструирования включает следующие стадии:
Амплификацию кодирующей области и последовательности промоторной области гена PtsS или кодирующей области и последовательности промоторной области гена PtsSM162T, конструирование плазмидного вектора сверхэкспрессии и перенос указанного вектора в штамм-хозяин с обеспечением штамма, характеризующегося сверхэкспрессией генов PtsS и PtsSM162T.
В одном из воплощений настоящего изобретения праймеры для амплификации последовательности кодирующей области гена и его промоторной области представляют собой:

В одном из воплощений настоящего изобретения применяют следующую систему для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводят следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
В одном из воплощений настоящего изобретения систему рекомбинации NEBuilder применяют для соединения челночной плазмиды pXMJ19 и фрагмента PtsS или PtsSM162T с его собственным промотором с получением плазмиды сверхэкспрессии.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой YP97158.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой АТСС 13869.
В одном из воплощений настоящего изобретения штамм-хозяин представляет собой штамм, несущий полинуклеотидную последовательность, представленную SEQ ID NO: 62.
Рекомбинантный штамм, полученный в соответствии с настоящим изобретением, может быть применен для получения L-аминокислоты путем ферментации отдельно, а также может быть смешан с другими продуцирующими L-аминокислоты бактериями для получения L-аминокислоты путем ферментации.
В настоящем изобретении дополнительно предложен способ получения L-аминокислоты, включающий культивирование бактерии и получение L-аминокислоты из культуры.
Настоящее изобретение подробно описано ниже.
Термин «бактерии, обладающие способностью продуцировать L-аминокислоты» относится к способности продуцировать и накапливать целевую L-аминокислоту в среде и/или клетках бактерий до такой степени, что L-аминокислоты могут быть собраны при культивировании бактерий в среде. Бактерии, обладающие способностью продуцировать L-аминокислоты, могут представлять собой бактерии, способные накапливать целевую L-аминокислоту в среде и/или клетках бактерий в большем количестве, чем количество, получаемое при применении немодифицированного штамма.
Термин «немодифицированный штамм» относится к контрольному штамму, который не был модифицирован таким образом, чтобы он имел характерные особенности. То есть примеры немодифицированных штаммов включают штаммы дикого типа и родительские штаммы.
Бактерии, обладающие способностью продуцировать L-аминокислоты, могут представлять собой бактерии, способные накапливать целевую L-аминокислоту в среде в количестве предпочтительно 0,5 г/л или более, более предпочтительно 1,0 г/л или более.
Примеры L-аминокислот включают основные аминокислоты, такие как L-лизин, L-орнитин, L-аргинин, L-гистидин и L-цитруллин; алифатические аминокислоты, такие как L-изолейцин, L-аланин, L-валин, L-лейцин и глицин; аминокислоты, которые представляют собой гидроксимоноаминокарбоновые кислоты, такие как L-треонин и L-серин; циклические аминокислоты, такие как L-пролин; ароматические аминокислоты, такие как L-фенилаланин, L-тирозин и L-триптофан; серосодержащие аминокислоты, такие как L-цистеин, L-цистин и L-метионин; кислые аминокислоты, такие как L-глутаминовая кислота и L-аспарагиновая кислота; и аминокислоты с амидной группой в боковой цепи, такие как L-глутамин и L-аспарагин.
Конкретные примеры L-аминокислот включают L-глутаминовую кислоту, L-лизин, L-треонин, L-аргинин, L-гистидин, L-изолейцин, L-валин, L-лейцин, L-фенилаланин, L-тирозин, L-триптофан и L-цистеин.
Более конкретные примеры L-аминокислот включают L-глутаминовую кислоту, L-лизин, L-треонин и L-триптофан. Более конкретные примеры L-аминокислот включают L-глутаминовую кислоту, L-лизин.
В настоящем изобретении, если не указано иное, термин «аминокислота» относится к L-аминокислотам. В настоящем изобретении, если не указано иное, термин «L-аминокислота» относится к L-аминокислоте в свободной форме, ее соли или их смеси.
Термин «гомология» относится к идентичности в процентах между двумя полинуклеотидами или двумя полипептидными модулями. Гомология последовательностей между одним модулем и другим может быть определена с применением способов, известных в данной области техники. Такая гомология последовательностей может быть определена, например, с помощью алгоритма BLAST.
В настоящем изобретении усиление экспрессии полинуклеотидов относится к: усилению экспрессии путем замены или мутации регулирующих экспрессию последовательностей, путем введения мутаций в последовательность полинуклеотида, путем увеличения числа копий полинуклеотида посредством хромосомной вставки или введения вектора, или комбинации указанного и тому подобному.
Согласно настоящему изобретению мутация относится к изменению основания/нуклеотида в указанном положении, и способ обеспечения мутации может быть выбран по меньшей мере из одного из методов мутагенеза, сайт-направленного мутагенеза посредством ПЦР и/или гомологичной рекомбинации. В настоящем изобретении предпочтительно применяют сайт-направленный мутагенез посредством ПЦР и/или гомологичную рекомбинацию.
Согласно настоящему изобретению регулирующие экспрессию последовательности полинуклеотидов могут быть модифицированы. Регулирующие экспрессию последовательности контролируют экспрессию полинуклеотидов, с которыми они функционально связаны, и могут включать, например, промоторы, терминаторы, энхансеры, сайленсеры и тому подобное. Полинуклеотиды могут иметь модификации в инициирующем кодоне. Полинуклеотиды могут быть встроены в конкретный участок хромосомы, вследствие чего увеличивается количество копий. В настоящем документе конкретный участок может включать, например, участок транспозона или межгенную область. Кроме того, полинуклеотиды могут быть встроены в вектор экспрессии, и полученный вектор экспрессии вводят в клетку-хозяина с обеспечением увеличения числа копий.
В одном из воплощений настоящего изобретения количество копий увеличивают путем встраивания полинуклеотида или полинуклеотида с точечной мутацией в конкретный участок хромосомы микроорганизма.
В одном из воплощений настоящего изобретения полинуклеотид с промоторной последовательностью или полинуклеотид с промоторной последовательностью с точечной мутацией встраивают в конкретный участок хромосомы микроорганизма с обеспечением сверхэкспрессии последовательности нуклеиновой кислоты.
В одном из воплощений настоящего изобретения полинуклеотид или полинуклеотид, имеющий точечную мутацию, встраивают в вектор экспрессии, и полученный вектор экспрессии вводят в клетку-хозяина с обеспечением увеличения числа копий.
В одном из воплощений настоящего изобретения полинуклеотид с промоторной последовательностью или полинуклеотид с промоторной последовательностью с точечной мутацией встраивают в вектор экспрессии, и полученный вектор экспрессии вводят в клетку-хозяина с обеспечением сверхэкспрессии последовательности нуклеиновой кислоты.
Термин «функционально связанный» относится к функциональной связи между регуляторной последовательностью и полинуклеотидной последовательностью, вследствие чего регуляторная последовательность контролирует транскрипцию и/или трансляцию полинуклеотидной последовательности. Регуляторная последовательность может представлять собой сильный промотор, способный повышать уровень экспрессии полинуклеотида. Регуляторные последовательности могут представлять собой промоторы, имеющие происхождение от микроорганизмов, принадлежащих к роду Corynebacterium, или могут представлять собой промоторы, имеющие происхождение от других микроорганизмов. Например, промотор может представлять собой промотор trc, промотор gap, промотор tac, промотор Т7, промотор lac, промотор trp, промотор araBAD или промотор cj7.
Термин «вектор» относится к полинуклеотидной конструкции, которая содержит регуляторную и кодирующую последовательности гена и выполнена с возможностью экспрессии гена-мишени в подходящей клетке-хозяине. В качестве альтернативы, вектор может, в свою очередь, относиться к полинуклеотидной конструкции, содержащей последовательности, пригодные для гомологичной рекомбинации, таким образом, вследствие введения вектора в клетку-хозяина регуляторные последовательности эндогенного гена в геноме клетки-хозяина могут быть изменены, или ген-мишень, который может экспрессироваться, может быть встроен в конкретный участок генома хозяина. В связи с этим вектор, применяемый в настоящем изобретении, может дополнительно включать селектируемый маркер для определения введения вектора в клетку-хозяина или встраивания вектора в хромосому клетки-хозяина. Селектируемые маркеры могут включать маркеры, которые обеспечивают селектируемый фенотип, такой как устойчивость к действию лекарственных средств, ауксотрофия, устойчивость к действию цитотоксических агентов или экспрессия поверхностных белков. В среде, обработанной соответствующими селектирующими агентами, могут быть отобраны трансформированные клетки, поскольку только клетки, экспрессирующие селектируемый маркер, способны к выживанию или проявлению различных фенотипических признаков.
В некоторых воплощениях настоящего изобретения применяемый вектор представляет собой плазмиду pK18mobsacB, плазмиду pXMJ19.
Термин «трансформация» относится к введению полинуклеотида в клетку-хозяина, вследствие чего полинуклеотид становится реплицируемым в качестве внегеномного элемента или встраивается в геном клетки-хозяина. Способ трансформации вектора, применяемый в настоящем изобретении, может включать способ введения нуклеиновой кислоты в клетки. Кроме того, согласно описанному в уровне техники, в зависимости от клетки-хозяина может быть осуществлен способ с применением электрических импульсов.
В настоящем изобретении микроорганизмы, принадлежащие к роду Corynebacterium, могут представлять собой Corynebacterium glutamicum, Brevibacterium flavum, Brevibacterium lactofermentum, Corynebacterium ammoniagenes и Corynebacterium pekinense.
В одном из воплощений настоящего изобретения микроорганизм, принадлежащий к роду Corynebacterium, представляет собой Corynebacterium glutamicum YP97158, номер депонирования: CGMCC No. 12856, дата депонирования: 16 августа 2016 г., депозитарий: China General Microbiological Culture Collection Center. No. 3, Yard 1, West Beichen Road, Chaoyang District, Beijing, Tel: 010-64807355, штамм зарегистрирован в китайской заявке на патент CN 106367432 А (дата подачи заявки 1 сентября 2016 г., дата публикации 1 февраля 2017 г.).
В настоящем изобретении бактерии также могут иметь другие улучшения, связанные с увеличением продукции L-аминокислот, например, активность ферментов, таких как глутаматдегидрогеназа, аконитатгидратаза, цитратсинтаза, метилцитратсинтаза, пируваткарбоксилаза, пируватдегидрогеназа, пируваткиназа, фосфоенолпируватсинтаза, фосфоглицератмутаза, фосфоглицераткиназа, глицеральдегид-3-фосфатдегидрогеназа, триозофосфатизомераза, фруктозобисфосфатальдолаза, глюкозофосфатизомераза, 6-фосфоглюконатдегидратаза, 2-кето-3-дезокси-6-фосфоглюконатальдолаза, глюкозодегидрогеназа, глюконаткиназа, аспартаткиназа III, аспартат-полуальдегиддегидрогеназа, гомосеринкиназа, треонинсинтаза, дигидродипиколинатсинтаза, дигидродипиколинатредуктаза, м-диаминопимелатдегидрогеназа, диаминопимелатдекарбоксилаза, или повышенную или сниженную экспрессию генов, или гены могут быть заменены на чужеродные гены.
Кроме того, микроорганизм также может иметь другие улучшения, связанные с повышенной продукцией L-лизина, например, повышенную или сниженную экспрессию генов, связанных с образованием NADPH (например, гена, кодирующего глюкозодегидрогеназу, гена, кодирующего глюконаткиназу, гена, кодирующего альдегид-3-фосфатдегидрогеназу, гена, кодирующего глюкозо-6-фосфатдегидрогеназу, или гена, кодирующего 6-фосфоглюконатдегидрогеназу) и/или других генов, связанных с биосинтезом или секрецией L-лизина (например, гена, кодирующего аспартатаминотрансферазу, гена, кодирующего аспартаткиназу, гена, кодирующего аспартат-полуальдегиддегидрогеназу, гена, кодирующего дигидродипиколинатсинтазу, гена, кодирующего дигидродипиколинатредуктазу, гена, кодирующего м-диаминопимелатдегидрогеназу, гена, кодирующего диаминопимелатдекарбоксилазу, lysE), или могут иметь гены, замененные на чужеродные гены.
В настоящем изобретении мутация относится к изменению основания/нуклеотида в указанном положении, и способ обеспечения мутации может быть выбран по меньшей мере из одного из таких методов, как мутагенез, сайт-направленный мутагенез посредством ПЦР и/или гомологичная рекомбинация. В настоящем изобретении предпочтительно применяют сайт-направленный мутагенез посредством ПЦР и/или гомологичную рекомбинацию.
В настоящем изобретении культивирование бактерий может быть выполнено в подходящей среде в условиях культивирования, известных в данной области техники. Среда может содержать: источники углерода, источники азота, микроэлементы и их комбинации. Во время культивирования можно регулировать рН культуры. Кроме того, культивирование может включать предупреждение образования пузырьков воздуха, например, путем применения противовспенивающего агента. Кроме того, культивирование может включать введение газа в культуру. Газ может включать любой газ, способный поддерживать аэробные условия культивирования. При культивировании температура культуры может составлять от 20 до 45°С. Полученные L-аминокислоты могут быть выделены из культуры путем обработки культуры серной кислотой или соляной кислотой, и так далее, с последующим применением комбинации методов, таких как анионообменная хроматография, концентрирование, кристаллизация и изоэлектрическое осаждение.
ПОЛЕЗНЫЙ ЭФФЕКТ
В настоящем изобретении в качестве исходной бактерии используют Corynebacterium glutamicum YP97158, обеспечивают ослабление экспрессии или нокаутирование гена NCgl1089, гена NCgl0761 и гена ptsS в ее фоновом генотипе и обнаруживают, что продукт, кодируемый указанным геном, оказывает влияние на способность к продукции L-аминокислоты. В кодирующую последовательность вводят точечную мутацию, или увеличивают количество копий гена, или получают рекомбинантный штамм путем сверхэкспрессии, и полученный штамм обладает существенной способностью к продукции L-аминокислот, что обеспечивает продукцию L-аминокислоты в высокой концентрации.
ПРЕДПОЧТИТЕЛЬНЫЙ СПОСОБ ВОПЛОЩЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Указанные выше и другие признаки и преимущества настоящего изобретения более подробно пояснены и проиллюстрированы ниже посредством описания воплощений настоящего изобретения. Следует понимать, что следующие воплощения предназначены для иллюстрации технических решений настоящего изобретения, но не предназначены для ограничения объема защиты настоящего изобретения, определенного формулой изобретения и ее эквивалентами.
Если не указано иное, все сырье и реагенты, применяемые в следующих примерах, являются коммерчески доступными продуктами или могут быть получены известными способами; выполняемые операции известны в данной области техники или выполняются в соответствии с руководствами пользователя коммерчески доступных продуктов.
Основная среда, применяемая для культивирования штаммов в следующих примерах, имеет идентичный указанному состав, и, соответственно, при необходимости сахарозу, канамицин или хлорамфеникол и тому подобное добавляют к этому составу основной среды, и состав основной среды является следующим:
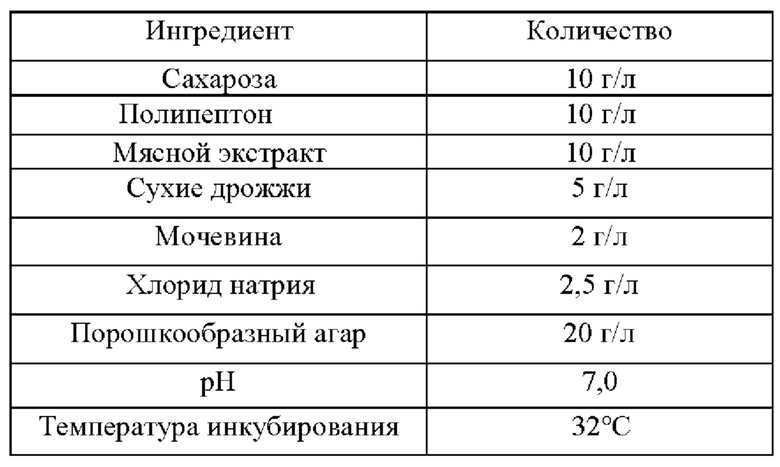
Приготовление компонентов и условия PAGE-электрофореза (электрофорез в полиакриламидном геле) для анализа SSCP (конформационный полиморфизм однонитевых фрагментов), описанные в следующих примерах, являются следующими:
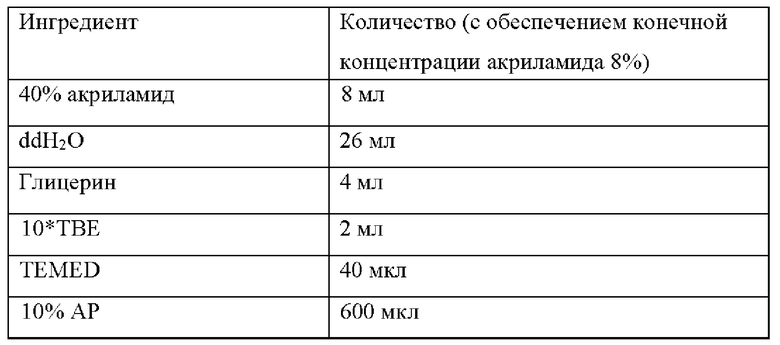

Пример 1
(1) Конструирование трансформирующего вектора pK18-NCgl1089G508A, содержащего кодирующую область гена NCgl1089 с точечной мутацией
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, были сконструированы и синтезированы две пары праймеров для амплификации последовательности кодирующей области гена NCgl1089, была введена точечная мутация в кодирующую область (SEQ ID NO: 1) гена NCgl1089 в фоновом генотипе штамма YP97158 (номер депонирования: CGMCC No. 12856, дата депонирования: 16 августа 2016 г., депозитарий: China General Microbiological Culture Collection Center. No. 3, Yard 1, West Beichen Road, Chaoyang District, Beijing, Tel: 010-64807355, штамм зарегистрирован в китайской заявке на патент CN 106367432 A (дата подачи заявки 1 сентября 2016 г., дата публ. 1 февраля 2017 г.)) путем аллельной замены, аминокислотная последовательность, соответствующая кодируемому белку, представляла собой SEQ ID NO: 3, основание в положении 508 нуклеотидной последовательности гена NCgl1089 было заменено с G на A (SEQ ID NO: 2: NCgl1089G508A), и аминокислота в положении 170 аминокислотной последовательности, соответствующей кодируемому белку, была заменена с глутаминовой кислоты на лизин (SEQ ID NO: 4: NCgl1089E170K).
Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):
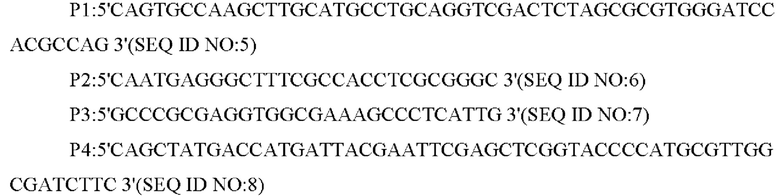
Способ конструирования: Corynebacterium glutamicum АТСС13032 использовали в качестве матрицы для проведения амплификации методом ПЦР с праймерами Р1 и Р2, Р3 и Р4, соответственно.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 40 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин, с получением двух фрагментов ДНК (NCgl1089Up и NCgl1089Down) размером 724 п. н. и 839 п. н., содержащих кодирующую область гена NCgl1089, соответственно.
После разделения и очистки указанных выше двух фрагментов ДНК с помощью электрофореза в агарозном геле амплифицировали фрагмент длиной примерно 1535 п. н. методом ПЦР с перекрывающимися праймерами с применением двух указанных выше фрагментов ДНК в качестве матриц и Р1 и Р4 в качестве праймеров.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Этот фрагмент ДНК (NCgl1089G508A) обусловливает замену гуанина (G) в положении 508 кодирующей области гена NCgl1089 YP97158 на аденин (А), и в итоге аминокислота в положении 170 кодируемого белка была заменена с глутаминовой кислоты (Е) на аминокислоту лизин (K).
После расщепления плазмиды pK18mobsacB (приобретенной у Addgene) под действием Xba I линеаризованную плазмиду pK18mobsacB и NCgl1089G508A разделяли и очищали методом электрофореза в агарозном геле, а затем объединяли с помощью системы рекомбинации NEBuilder с получением вектора pK18-NCgl1089G508A, который содержит маркер устойчивости к канамицину. Полученный вектор pK18-NCgl1089G508A отправляли в компанию, занимающуюся секвенированием, для идентификации путем секвенирования, и вектор pK18-NCgl1089G508A, содержащий надлежащую точечную мутацию (G-A), сохраняли для последующего применения.
(2) Конструирование генноинженерного штамма NCgl1089G508A, содержащего точечную мутацию
Способ конструирования: Плазмиду pK18-NCgl1089G508A для аллельной замены трансформировали в запатентованный штамм YP97158 продуцирующих L-лизин бактерий с помощью электрических импульсов (способ ее конструирования см. в источнике WO 2014121669 A1; секвенирование подтвердило, что кодирующая область гена NCgl1089 дикого типа в хромосоме этого штамма была сохранена), отдельную колонию, полученную при культивировании, идентифицировали с применением праймера Р1 и универсального праймера M13R, соответственно, и штамм, который мог обеспечивать амплификацию зоны размером 1542 п. н., представлял собой положительный штамм. Положительные штаммы культивировали на среде, содержащей 15% сахарозы, и отдельную колонию, полученную при культивировании, культивировали на среде, содержащей канамицин и не содержащей канамицина, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, дополнительно идентифицировали с помощью ПЦР с применением следующих праймеров (синтезированных компанией Shanghai Invitrogen):

Указанные выше продукты амплификации, полученные с помощью ПЦР, подвергали электрофорезу для анализа SSCP (в качестве положительного контроля использовали амплифицированный фрагмент плазмиды pK18-NCgl1089G508A, в качестве отрицательного контроля использовали амплифицированный фрагмент YP97158, и в качестве контроля фона использовали воду) после высокотемпературной денатурации и помещения на ледяную баню. Вследствие различий в структуре фрагментов и положения при электрофорезе штаммы, положения которых при электрофорезе не соответствовали положениям фрагмента отрицательного контроля и соответствовали фрагменту положительного контроля, представляли собой штаммы с успешной аллельной заменой. Целевой фрагмент штамма с успешной аллельной заменой повторно амплифицировали методом ПЦР с праймерами Р5 и Р6 и соединяли с вектором PMD19-T для секвенирования. Успешная аллельная замена штамма была подтверждена путем выравнивания последовательностей для мутантной последовательности оснований, и указанный штамм был назван YPL-4-017.
(3) Конструирование генно-инженерных штаммов, характеризующихся сверхэкспрессией гена NCgl1089 или NCgl1089G508A в геноме
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, были сконструированы и синтезированы четыре пары праймеров для амплификации последовательностей вышележащего и нижележащего фрагментов гомологичного плеча, кодирующей области гена NCgl1089, кодирующей области гена NCgl1089G508A и промоторной области указанного гена, и ген NCgl1089 или NCgl1089G508A вводили в штамм YP97158 путем гомологичной рекомбинации.
Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):

Способ конструирования: Corynebacterium glutamicum АТСС 13032 использовали в качестве матрицы для проведения амплификации методом ПЦР с праймерами Р7/Р8, Р9/Р10, Р13/Р14, соответственно, с получением вышележащего фрагмента гомологичного плеча размером 805 п. н., фрагмента промотора гена NCgl1089 размером 318 п. н. и нижележащего фрагмента гомологичного плеча размером 628 п.н.; затем в качестве матриц использовали Corynebacterium glutamicum АТСС 13032 и YPL-4-017, соответственно, а в качестве праймеров использовали Р11/Р12, и с помощью амплификации методом ПЦР получали фрагмент гена NCgl1089 или NCgl1089G508A размером 694 п.н.; затем в качестве праймеров использовали Р9/Р12, а в качестве матриц использовали фрагмент промотора гена NCgl1089 и NCgl1089 или NCgl1089G508A с получением фрагмента NCgl1089 или NCgl1089G508A размером 972 п.н. с собственным промотором; затем в качестве праймеров использовали Р7/Р14, а в качестве матриц для амплификации использовали смесь вышележащего фрагмента гомологичного плеча, нижележащего фрагмента гомологичного плеча и фрагментов NCgl1089 или NCgl1089G508A с собственными промоторами, и получали интегрированный фрагмент гомологичного плеча.
После реакции ПЦР амплифицированный продукт выделяли методом электрофореза, и необходимый фрагмент ДНК размером 2365 п. н. выделяли с помощью набора для выделения ДНК из геля на колонке (TIANGEN) и соединяли с челночной плазмидой PK18mobsacB, выделенной путем расщепления под действием Xba I, с помощью системы рекомбинации NEBuilder с получением интегрирующей плазмиды PK18mobsacB-NCgl1089 или PK18mobsacB-NCgl1089G508A Плазмида содержала маркер устойчивости к канамицину, и рекомбинантная плазмида, интегрированная в геном, может быть получена путем селекции с применением канамицина.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Две интегрирующие плазмиды подвергали электротрансформации в запатентованный штамм YP97158 продуцирующих L-лизин бактерий, соответственно, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР с применением праймеров Р15/Р16, и штамм, который мог обеспечивать амплификацию зоны размером 1332 п.н., представлял собой положительный штамм, а штаммы, которые не способны обеспечивать амплификацию указанных фрагментов, представляли собой исходные штаммы. Положительные штаммы подвергали скринингу на среде с 15% сахарозы и культивировали на содержащей канамицин и не содержащей канамицина среде, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, в дальнейшем идентифицировали методом ПЦР с применением праймеров Р17/Р18, и амплифицированные штаммы размером 1187 п. н. представляли собой штаммы, гены которых были интегрированы в геном YP97158, и были названы YPL-4-018 (без точечной мутации) и YPL-4-019 (с точечной мутацией), соответственно.
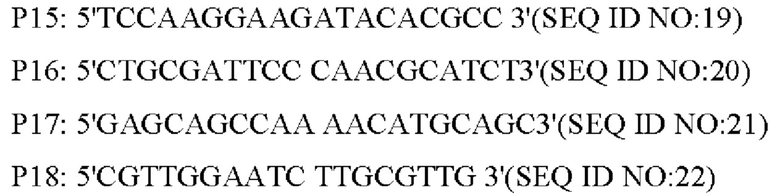
(4) Конструирование генноинженерных штаммов, характеризующихся сверхэкспрессией гена NCgl1089 или NCgl1089G508A в плазмиде
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, были сконструированы и синтезированы две пары праймеров для амплификации последовательности кодирующей области и промоторной области гена NCgl1089 или NCgl1089G508A. Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):
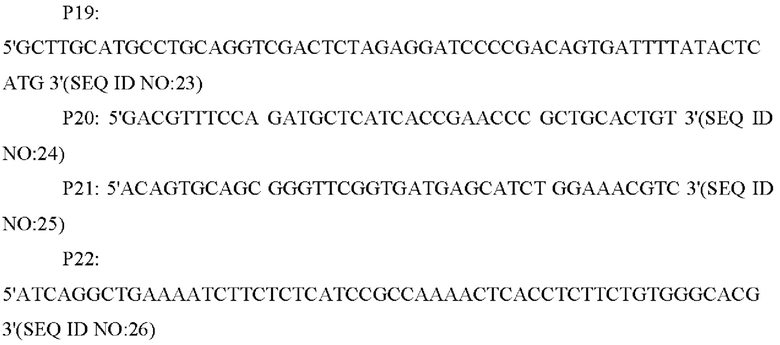
Способ конструирования: YPL-4-018 использовали в качестве матрицы и получали фрагмент промотора NCgl1089 размером 378 п.н. с помощью ПЦР с праймерами Р19/Р20; затем Corynebacterium glutamicum дикого типа АТСС 13032 и YPL-4-017 использовали в качестве матриц, соответственно, и получали фрагмент гена NCgl1089 или NCgl1089G508A размером 708 п.н. с помощью ПЦР с праймерами Р21/Р22; указанный выше промотор и фрагмент гена использовали в качестве матриц и получали фрагмент гена NCgl1089 или NCgl1089G508A размером 1066 п.н. с собственным промотором с помощью ПЦР с перекрывающимися праймерами с применением праймеров Р19/Р22. Амплифицированный продукт выделяли методом электрофореза, и необходимый фрагмент ДНК размером 1066 п.н. выделяли с помощью набора для выделения ДНК из геля на колонке и соединяли с челночной плазмидой pXMJ19, выделенной путем расщепления под действием EcoR I, с помощью системы рекомбинации NEBuilder с получением плазмиды сверхэкспрессии pXMJ19-NCgl1089 или pXMJ19-NCgl1089G508A. Плазмида содержала маркер устойчивости к хлорамфениколу, и указанная плазмида могла быть трансформирована в штамм путем скрининга с применением хлорамфеникола.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
pXMJ19-NCgl1089 или PXMJ19-NCgl1089G508A подвергали электротрансформации в запатентованный штамм YP97158 продуцирующих L-лизин бактерий, соответственно, и отдельную колонию, полученную при культивировании, идентифицировали с применением праймеров М13 (-48) и Р22. Фрагмент размером 1104 п.н. представлял собой трансформированный штамм, который был назван YPL-4-020 (без точечной мутации) или YPL-4-021 (с точечной мутацией), соответственно. Амплифицированный с помощью ПЦР фрагмент, содержащий фрагмент размером 1104 п.н., представлял собой трансформированный штамм, который был назван YPL-4-020 (без точечной мутации) или YPL-4-021 (содержащий точечную мутацию), соответственно.
(5) Конструирование генноинженерных штаммов, в геноме которых отсутствует ген NCgl1089
В соответствии с последовательностью генома Corynebacterium glutamicum АТСС13032, опубликованной NCBI, были синтезированы две пары праймеров для амплификации фрагментов с обоих концов кодирующей области гена NCgl1089 в виде вышележащего и нижележащего фрагментов гомологичного плеча. Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Yingjun):
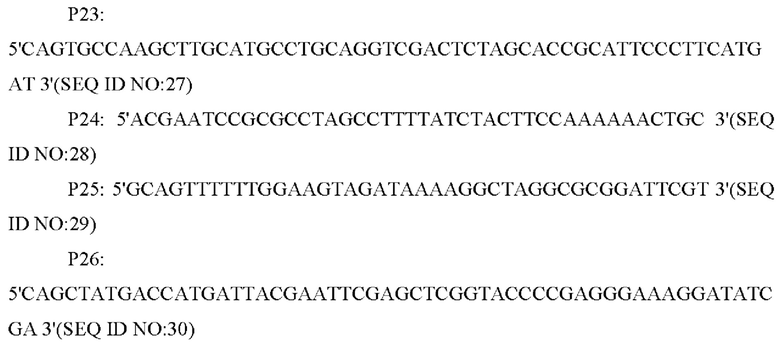
Corynebacterium glutamicum АТСС 13032 применяли в качестве матрицы, амплификацию методом ПЦР проводили с праймерами Р23/Р24 и Р25/Р26, соответственно, с получением вышележащего фрагмента гомологичного плеча размером 779 п.н. и нижележащего фрагмента гомологичного плеча размером 800 п.н., и затем получали полный фрагмент гомологичного плеча размером 1539 п.н. методом ПЦР с перекрывающимися праймерами с применением праймеров Р23/Р26. После реакции ПЦР амплифицированный продукт выделяли методом электрофореза, необходимый фрагмент ДНК размером 1539 п.н. выделяли с помощью набора для выделения ДНК из геля на колонке и соединяли с челночной плазмидой PK18mobsacB, выделенной путем расщепления под действием Xba I, с помощью системы рекомбинации NEBuilder с получением нокаутной плазмиды. Эта плазмида содержала маркер устойчивости к канамицину.
Нокаутную плазмиду подвергали электротрансформации в запатентованный штамм YP97158, продуцирующий лизин, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР со следующими праймерами (синтезированы компанией Shanghai Yingjun), соответственно:

Штаммы с зонами размером 1429 п.н. и 2401 п.н., амплифицированными с помощью описанной выше ПЦР, представляли собой положительные штаммы, а штамм с амплифицированной зоной размером 2401 п.н. представлял собой исходный штамм. Положительные штаммы подвергали скринингу на среде с 15% сахарозы и культивировали на среде, содержащей канамицин, и среде, не содержащей канамицина, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, в дальнейшем идентифицировали методом ПЦР с применением праймеров Р27/Р28, и амплифицированные штаммы размером 1429 п.н. представляли собой генноинженерные штаммы, в которых кодирующая область гена NCgl1089 была нокаутирована, и получили название YPL-4-022.
(6) Эксперимент с получением L-лизина путем ферментации Штаммы, сконструированные в примерах, и исходный штамм YP97158 подвергали экспериментам по ферментации в ферментере BLBIO-5GC-4-H (приобретенном у Shanghai Bailun Biotechnology Co., Ltd.) со средой, представленной в табл. 1, и процессом контроля, представленным в табл. 2. Эксперимент с каждым штаммом повторяли три раза, результаты представлены в табл. 3.

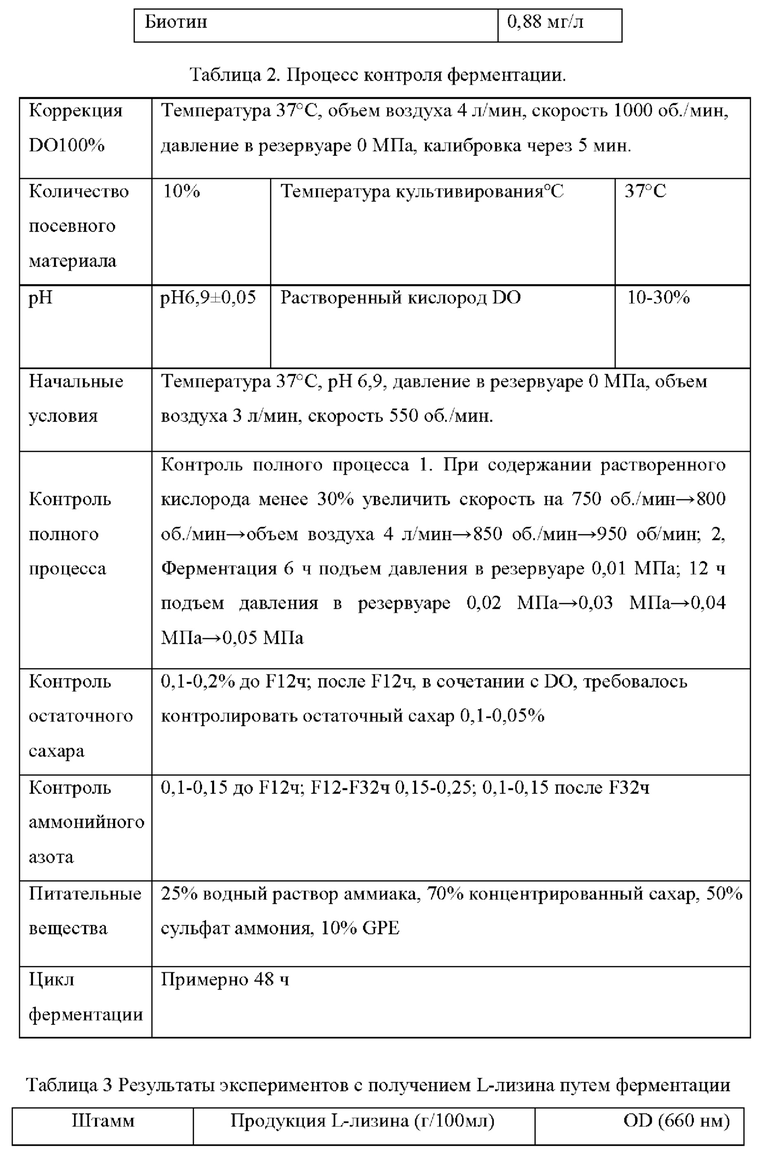
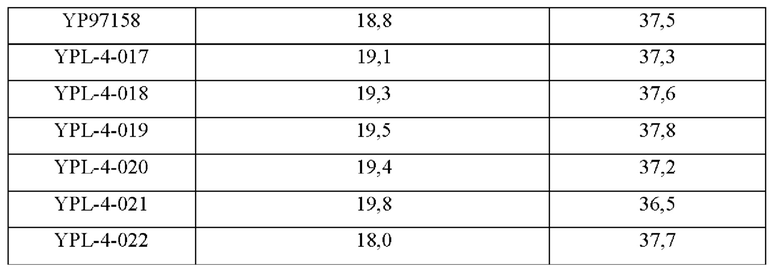
Результаты представлены в табл. 3. Сверхэкспрессия гена NCgl1089 или точечная мутация NCgl1089G508A и сверхэкспрессия кодирующей области гена NCgl1089 у Corynebacterium glutamicum способствовали улучшению продукции L-лизина, в то время как ослабление или нокаутирование гена не способствовало накоплению L-лизина.
Пример 2
(1) Конструирование трансформирующего вектора pK18-NCgl0761L31R, содержащего кодирующую область гена NCgl1089 с точечной мутацией
В соответствии с последовательностью генома Corynebacterium glutamicum АТСС13032, опубликованной NCBI, были сконструированы и синтезированы две пары праймеров для амплификации последовательности кодирующей области гена NCgl0761, была введена точечная мутация в кодирующую область (SEQ ID NO: 33) гена NCgl0761 в фоновом генотипе штамма YP97158 (номер депонирования: CGMCC No. 12856, дата депонирования: 16 августа 2016 г., депозитарий: China General Microbiological Culture Collection Center. No. 3, Yard 1, West Beichen Road, Chaoyang District, Beijing, Tel: 010-64807355, штамм зарегистрирован в китайской заявке на патент CN 106367432 A (дата подачи заявки 1 сентября 2016 г., дата публикации 1 февраля 2017 г.)) путем аллельной замены, аминокислотная последовательность, соответствующая кодируемому белку, представляла собой SEQ ID NO: 35, основание в положении 92 нуклеотидной последовательности гена NCgl0761 было заменено с Т на G (SEQ ID NO: 34), и аминокислота в положении 31 аминокислотной последовательности, соответствующей кодируемому белку, была заменена с лейцина на аргинин (SEQ ID NO: 36: NCgl0761L31R). Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):

Способ конструирования: Corynebacterium glutamicum АТСС 13032 использовали в качестве матрицы для проведения амплификации методом ПЦР с праймерами Р1 и Р2, РЗ и Р4, соответственно. Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ех Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 40 с, 30 циклов, и финальная элонгация при 72°С в течение 10 мин, с получением двух фрагментов ДНК (NCgl0761Up и NCgl0761Down) размером 636 п.н. и 681 п.н., содержащих кодирующую область гена NCgl0761, соответственно. После разделения и очистки указанных выше двух фрагментов ДНК с помощью электрофореза в агарозном геле амплифицировали фрагмент длиной примерно 1283 п. н. методом ПЦР с перекрывающимися праймерами с применением двух указанных выше фрагментов ДНК в качестве матриц и Р1 и Р4 в качестве праймеров.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с, 30 циклов, и финальная элонгация при 72°С в течение 10 мин.
Этот фрагмент ДНК обусловливает замену тимина (Т) в положении 92 кодирующей области гена NCgl0761 YP97158 на гуанин (G), и в итоге аминокислота в положении 31 кодируемого белка была заменена с лейцина (L) на аргинин (R). Указанный фрагмент ДНК очищали после электрофореза в агарозном геле, а затем лигировали с очищенной плазмидой pK18mobsacB (приобретенной в компании Addgene и дважды расщепленной Xbal I/BamH I, соответственно), дважды подвергнутой расщеплению, с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин. Отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с получением положительного вектора pK18-NCgl0761L31R, который содержал маркер устойчивости к канамицину на этой плазмиде. Надлежащим образом расщепленный вектор pK18-NCgl0761L31R отправляли в компанию, занимающуюся секвенированием, для идентификации путем секвенирования, и вектор pK18-NCgl0761L31R, содержащий надлежащую точечную мутацию (T-G), сохраняли для последующего применения.
(2) Конструирование генноинженерного штамма pK18-NCgl0761L31R, содержащего точечную мутацию
Способ конструирования: Плазмиду pK18-NCgl0761L31R для аллельной замены трансформировали в запатентованный штамм YP97158 продуцирующих L-лизин бактерий с помощью электрических импульсов (способ ее конструирования см. в источнике WO 2014121669 A1; секвенирование подтвердило, что кодирующая область гена NCgl0761 дикого типа в хромосоме этого штамма была сохранена), отдельную колонию, полученную при культивировании, идентифицировали с применением праймера Р1 и универсального праймера M13R, соответственно, и штамм, который мог обеспечивать амплификацию зоны размером 1369 п. н., представлял собой положительный штамм. Положительные штаммы культивировали на среде, содержащей 15% сахарозы, и отдельную колонию, полученную при культивировании, культивировали на среде, содержащей канамицин и не содержащей канамицина, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, дополнительно идентифицировали с помощью ПЦР с применением следующих праймеров (синтезированных компанией Shanghai Invitrogen):
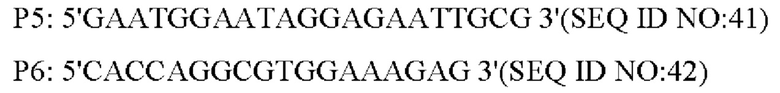
Указанный выше продукт амплификации размером 267 п. н., полученный с помощью ПЦР, подвергали электрофорезу для анализа SSCP (в качестве положительного контроля использовали амплифицированный фрагмент плазмиды pK18-NCgl0761L31R, в качестве отрицательного контроля использовали амплифицированный фрагмент YP97158, и в качестве контроля фона использовали воду) после высокотемпературной денатурации при 95°С в течение 10 мин и помещения на ледяную баню на 5 мин. Вследствие различий в структуре фрагментов и положения при электрофорезе штаммы, положения которых при электрофорезе не соответствовали положениям фрагмента отрицательного контроля и соответствовали фрагменту положительного контроля, представляли собой штаммы с успешной аллельной заменой. Фрагмент положительного штамма NCgl0761 повторно амплифицировали методом ПЦР с праймерами Р5 и Р6 и соединяли с вектором PMD19-Т для секвенирования. Согласно результатам выравнивания последовательностей штамм с мутацией (T-G) в последовательности оснований представлял собой положительный штамм с успешной аллельной заменой и был назван YPL-4-029.
(3) Конструирование генноинженерных штаммов, характеризующихся сверхэкспрессией гена NCgl0761 или NCgl0761L31R в геноме
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, были сконструированы и синтезированы три пары праймеров для амплификации последовательностей вышележащего и нижележащего фрагментов гомологичного плеча, кодирующей области гена NCgl0761 или NCgl0761L31R и промоторной области, и ген NCgl0761 или NCgl0761L31R вводили в штамм YP97158 путем гомологичной рекомбинации.
Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):

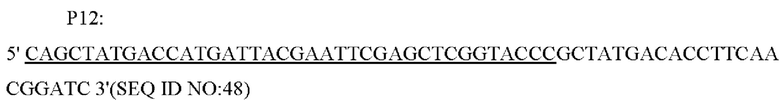
Способ конструирования: Corynebacterium glutamicum АТСС 13032 или YPL-4-029 использовали в качестве матрицы для проведения амплификации методом ПЦР с праймерами Р7/Р8, Р9/Р10, Р11/Р12, соответственно, с получением вышележащего фрагмента гомологичного плеча размером 802 п.н., гена NCgl0761 или NCgl0761L31R и его промоторного фрагмента размером 737 п.н., а также нижележащего фрагмента гомологичного плеча размером 647 п. н. После реакции ПЦР три амплифицированных фрагмента выделяли методом электрофореза с применением набора для выделения ДНК из геля на колонке (TIANGEN). Три выделенных фрагмента лигировали с очищенной плазмидой pK18mobsacB (приобретенной в компании Addgene и дважды расщепленной Xbal I/BamH I, соответственно), дважды подвергнутой расщеплению, с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин, и отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с праймером М13 с получением положительной интегрированной плазмиды pK18mobsacB-NCgl0761 и pK18mobsacB-NCgl0761L31R. Плазмида содержала маркер устойчивости к канамицину, и рекомбинантная плазмида, интегрированная в геном, может быть получена путем селекции с применением канамицина.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Две надлежащим образом секвенированные интегрирующие плазмиды подвергали электротрансформации в запатентованный штамм YP97158 продуцирующих L-лизин бактерий, соответственно, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР с применением праймеров Р13/Р14, и штамм, который мог обеспечивать амплификацию зоны размером 1325 п. н., представлял собой положительный штамм, а штаммы, которые не способны обеспечивать амплификацию указанных фрагментов, представляли собой исходные штаммы. Положительные штаммы культивировали на среде, содержащей 15% сахарозы, и отдельную колонию, полученную при культивировании, дополнительно идентифицировали с помощью ПЦР с применением праймеров Р15/Р16. Амплифицированные штаммы размером 1002 п. н. представляли собой положительные штаммы с геном NCgl0761 или NCgl0761L31R, интегрированным в геном YP97158, и были названы YPL-4-030 (без точечной мутации) и YPL-4-031 (с точечной мутацией).
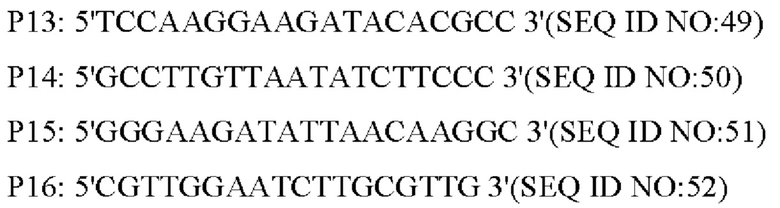
(4) Конструирование генно-инженерных штаммов, характеризующихся сверхэкспрессией гена NCgl0761 или NCgl0761L31R в плазмиде
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, была сконструирована и синтезирована одна пара праймеров для амплификации последовательности кодирующей области и промоторной области гена NCgl0761 или NCgl0761L31R. Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):
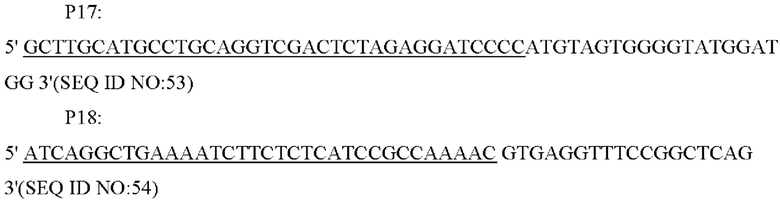
Способ конструирования: Corynebacterium glutamicum АТСС 13032 и YPL-4-029 использовали в качестве матриц для проведения амплификации методом ПЦР с праймерами Р17/Р18, соответственно, с получением reHaNCgl0761 или NCgl0761L31R и его промоторного фрагмента размером 737 п. н., и полученные продукты амплификации подвергали электрофорезу и очищали с помощью набора для выделения ДНК из геля на колонке. Выделенный фрагмент ДНК и челночную плазмиду pXMJ19, полученную с помощью расщепления EcoR I, лигировали с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин, и отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с праймером М13 с получением положительной плазмиды сверхэкспрессии pXMJ19-NCgl0761 и pXMJ19-NCgl0761L31R, и полученную плазмиду отправляли на секвенирование. Поскольку плазмида содержала маркер устойчивости к хлорамфениколу, она могла быть использована для скрининга того, была ли плазмида трансформирована в штамм, проводимого с применением хлорамфеникола.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Надлежащим образом секвенированные плазмиды pXMJ19-NCgl0761 и pXMJ19-NCgl0761 L31R подвергали электротрансформации в запатентованный штамм YP97158 продуцирующих L-лизин бактерий, соответственно, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР с праймерами М13/Р18. Амплифицированный с помощью ПЦР фрагмент, содержащий фрагмент размером 745 п. н., представлял собой положительный штамм, названный YPL-4-032 (без точечной мутации) и YPL-4-033 (с точечной мутацией).
(5) Конструирование генно-инженерных штаммов, в геноме которых отсутствует ген NCgl0761
В соответствии с последовательностью генома Corynebacterium glutamicum АТСС13032, опубликованной NCBI, были синтезированы две пары праймеров для амплификации фрагментов с обоих концов кодирующей области гена NCgl0761 в виде вышележащего и нижележащего фрагментов гомологичного плеча. Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Yingjun):
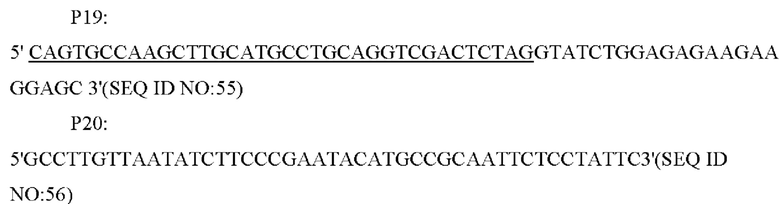
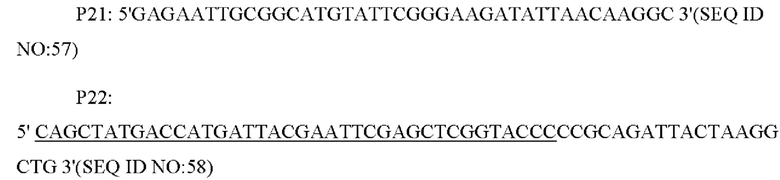
Способ конструирования: Corynebacterium glutamicum АТСС13032 применяли в качестве матрицы, амплификацию методом ПЦР проводили с праймерами Р19/Р20 и Р21/Р22, соответственно, с получением вышележащего фрагмента гомологичного плеча размером 658 п.н. и нижележащего фрагмента гомологичного плеча размером 716 п.н., и затем получали полный фрагмент гомологичного плеча размером 1335 п.н. методом ПЦР с перекрывающимися праймерами с применением праймеров Р19/Р22. Амплифицированный продукт подвергли электрофорезу и очистке с помощью набора для выделения ДНК из геля на колонке, и выделенный фрагмент ДНК лигировали с очищенной плазмидой pK18mobsacB (приобретенной в компании Addgene и дважды расщепленной Xbal I/BamH I, соответственно), дважды подвергнутой расщеплению, с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин, и отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с праймером М13 с получением положительного нокаутного вектора pK18-ΔNCgl0761, который отправляли на секвенирование. Эта плазмида содержала маркер устойчивости к канамицину в качестве селектируемого маркера.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Надлежащим образом секвенированную нокаутную плазмиду pK18-ΔNCgl0761 подвергали электротрансформации в запатентованный штамм YP97158, продуцирующий лизин, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР со следующими праймерами (синтезированы компанией Shanghai Yingjun):
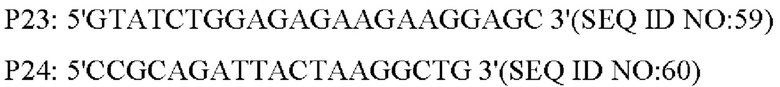
Штаммы с зонами размером 1374 п.н. и 1520 п.н., одновременно амплифицированными с помощью описанной выше ПЦР, представляли собой положительные штаммы, а штамм с амплифицированной зоной размером 1520 п. н. отдельно представлял собой исходный штамм. Положительные штаммы подвергали скринингу на среде с 15% сахарозы и культивировали на среде, содержащей канамицин, и среде, не содержащей канамицина, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, в дальнейшем идентифицировали методом ПЦР с применением праймеров Р23/Р24, и амплифицированные штаммы размером 1374 п. н. представляли собой положительный штамм, в котором кодирующая область гена NCgl0761 была нокаутирована. Фрагмент положительного штамма NCgl0761 повторно амплифицировали методом ПЦР с праймерами Р23/Р24 и лигировали с вектором PMD19-T для секвенирования. Штамм с надлежащими результатами секвенирования был назван YPL-4-034. (6) Эксперимент с получением L-лизина путем ферментации Штаммы, сконструированные в примерах, и исходный штамм YP97158 подвергали экспериментам по ферментации в ферментере BLBIO-5GC-4-H (приобретенном у Shanghai Bailun Biotechnology Co., Ltd.) со средой, представленной в табл. 4, и процессом контроля, представленным в табл. 5. Эксперимент с каждым штаммом повторяли три раза, результаты представлены в табл. 6.
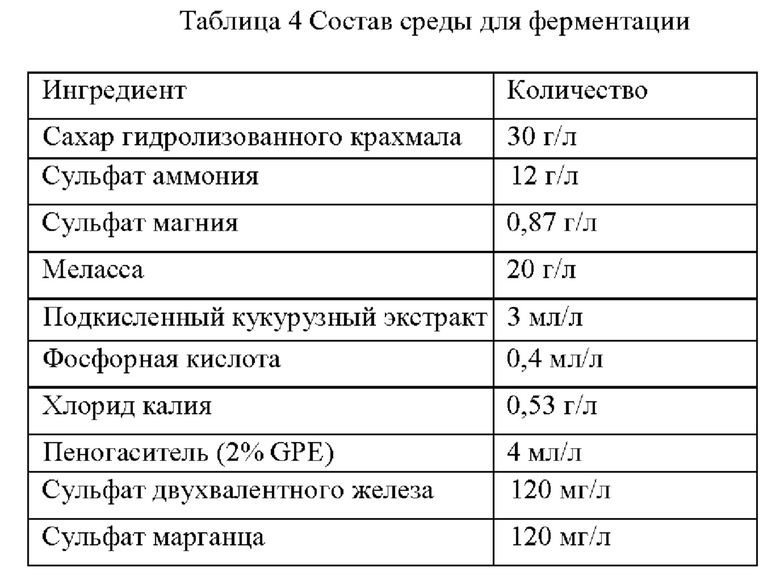
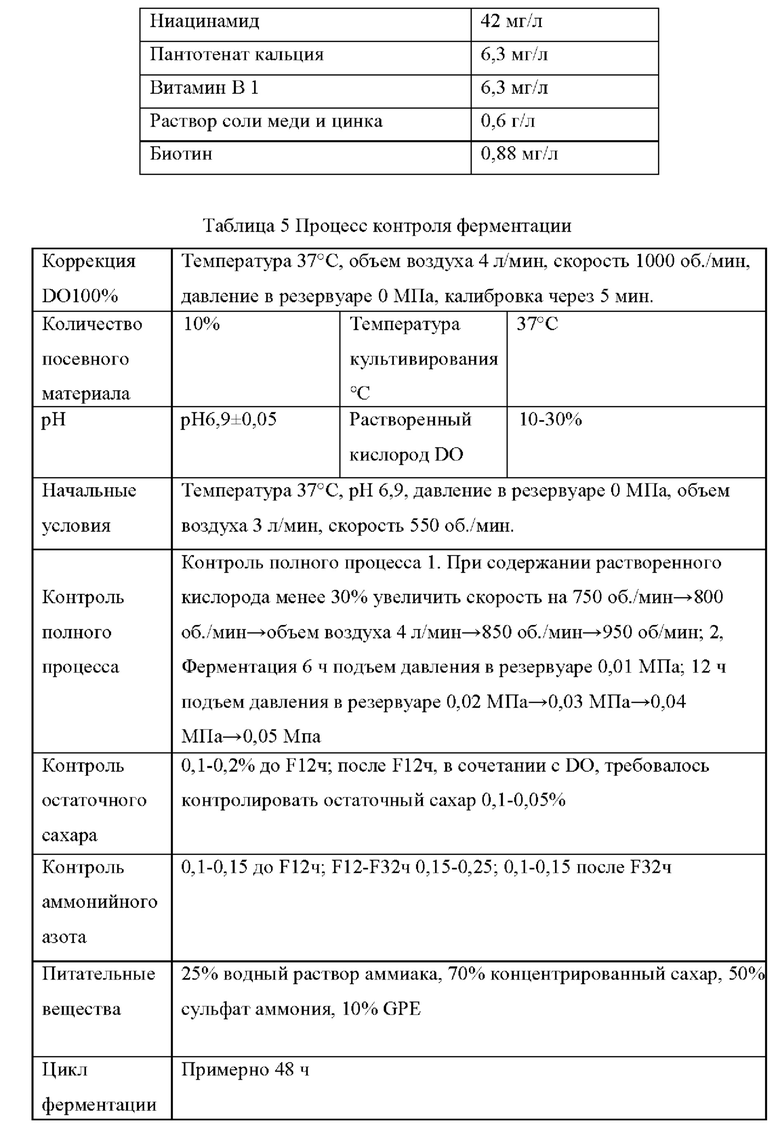
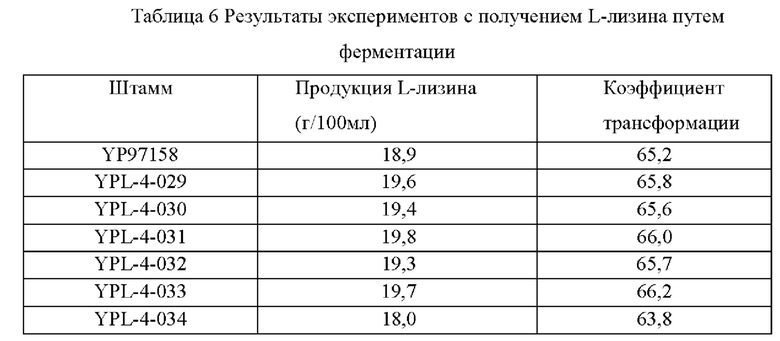
Результаты представлены в табл. 6. Сверхэкспрессия гена NCgl0761 или точечная мутация NCgl0761L31R и сверхэкспрессия кодирующей области гена NCgl0761 у Corynebacterium glutamicum способствовали улучшению продукции L-лизина и повышению коэффициента трансформации, в то время как ослабление или нокаутирование указанного гена не способствовало накоплению L-лизина, и в то же время снижало коэффициент трансформации.
(7) Ген NCgl0761 вводили в продуцирующий глутаминовую кислоту штамм и обеспечивали сверхэкспрессию, или кодирующую область гена NCgl0761 подвергали точечной мутации NCgl0761L31R и обеспечивали сверхэкспрессию, и проводили эксперименты по ферментации.
В соответствии со способом, описанным в примерах (1-5), использовали те же праймеры и экспериментальные условия, и Corynebacterium АТСС 13869 использовали в качестве исходной бактерии, а бактерию АТСС 13869 использовали в качестве бактерии экспрессии для получения продуцирующего глутаминовую кислоту генноинженерного штамма с pK18-NCgl0761L31R, содержащего точечную мутацию (YPG-001), продуцирующего глутаминовую кислоту генноинженерного штамма, характеризующегося сверхэкспрессией генов NCgl0761(YPG-002) или NCgl0761L31R(YPG-003) в геноме, и продуцирующего глутаминовую кислоту генноинженерного штамма, характеризующегося сверхэкспрессией генов NCgl0761 (YPG-004) или NCgl0761L31R(YPG-005) в плазмидах, а также продуцирующего глутаминовую кислоту генноинженерного штамма, в геноме которого отсутствует ген NCgl0761 (YPG-006).
Штаммы, сконструированные в примерах, и исходный штамм АТСС 13869 подвергали экспериментам по ферментации в ферментере BLBIO-5GC-4-H (приобретенном у Shanghai Bailun Biotechnology Co., Ltd.) со средой, представленной в табл. 7, и процессом контроля, представленным в табл. 8. Эксперимент с каждым штаммом повторяли три раза, результаты представлены в табл. 9.
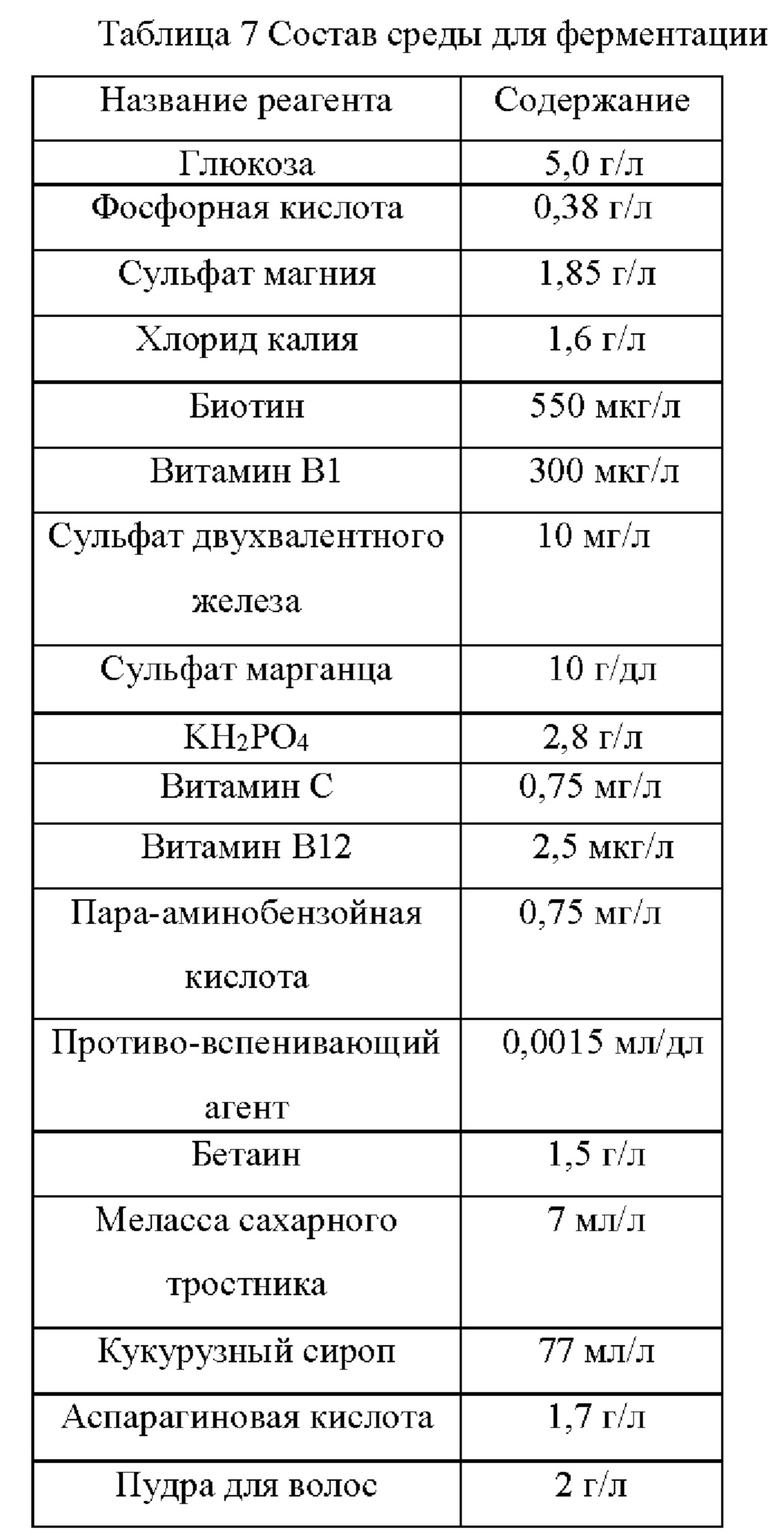
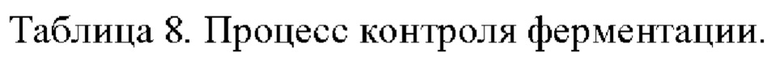
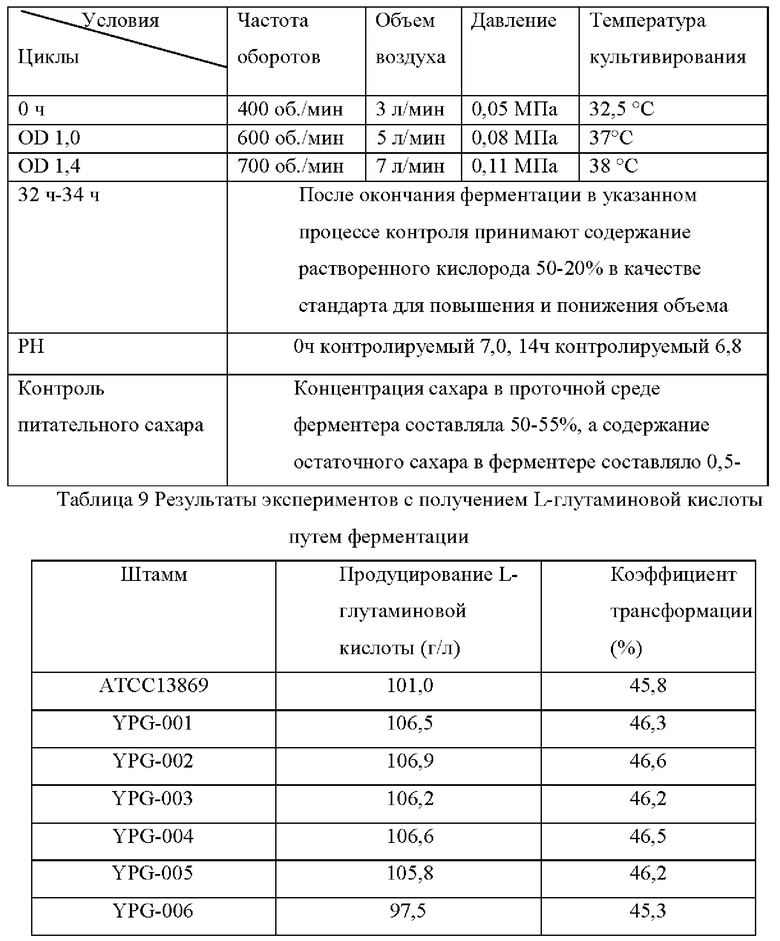
Результаты представлены в табл. 9. Сверхэкспрессия гена NCgl0761 или точечная мутация NCgl0761L31R и сверхэкспрессия кодирующей области гена NCgl0761 у Corynebacterium glutamicum способствовали улучшению продукции L-лизина и повышению коэффициента трансформации, в то время как ослабление или нокаутирование указанного гена не способствовало накоплению L-лизина, и в то же время снижало коэффициент трансформации.
Пример 3
(1) Конструирование трансформирующего вектора pK18-ptsSM162T, содержащего кодирующую область гена ptsS с точечной мутацией
В соответствии с последовательностью генома Corynebacterium glutamicum АТСС13032 дикого типа, опубликованной NCBI, были сконструированы и синтезированы две пары праймеров для амплификации последовательности кодирующей области гена ptsS, была введена точечная мутация в кодирующую область (SEQ ID NO: 61) гена ptsS в фоновом генотипе штамма YP97158 (номер депонирования: CGMCC No. 12856, дата депонирования: 16 августа 2016 г., депозитарий: China General Microbiological Culture Collection Center. No. 3, Yard 1, West Beichen Road, Chaoyang District, Beijing, Tel: 010-64807355, штамм зарегистрирован в китайской заявке на патент CN106367432A (дата подачи заявки 1 сентября 2016 г., дата публикации 1 февраля 2017 г. )) путем аллельной замены, аминокислотная последовательность, соответствующая кодируемому белку, представляла собой SEQ ID NO: 63, основание в положении 485 нуклеотидной последовательности гена ptsS было заменено с тимина Т на цитозин С (SEQ ID NO: 62), и аминокислота в положении 162 аминокислотной последовательности, соответствующей кодируемому белку, была заменена с метионина на треонин (SEQ ID NO: 64: ptsSM162T). Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):

Способ конструирования: Corynebacterium glutamicum АТСС 13032 использовали в качестве матрицы, амплификацию методом ПЦР проводили с праймерами Р1 и Р2, Р3 и Р4, соответственно. Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, (денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 40 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин, были получены два фрагмента ДНК (ptsS Up и ptsS Down), содержащие кодирующую область гена ptsS, размером 666 п. н. и 703 п.н., соответственно. После разделения и очистки указанных выше двух фрагментов ДНК с помощью электрофореза в агарозном геле указанные выше два фрагмента ДНК использовали в качестве матриц, а Р1 и Р4 использовали в качестве праймеров, и амплифицировали фрагмент длиной примерно 1341 п. н. методом ПЦР с перекрывающимися праймерами.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин (денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с, 30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Этот фрагмент ДНК обеспечивал замену тимина (Т) в положении 485 кодирующей области гена YP97158ptsS на цитозин (С) и в итоге обусловливал замену аминокислоты в положении 162 кодируемого белка с метионина (М) на треонин (Т). Этот фрагмент ДНК очищали путем электрофореза в агарозном геле и лигировали с плазмидой pK18mobsacB, очищенной после двойного расщепления (приобретенной у Addgene и подвергнутой двойному расщеплению под действием Xbal I/BamH I, соответственно), с помощью фермента NEBuilder при 50°С в течение 30 мин. После трансформации полученного продукта лигирования применяли метод моноклональной ПЦР для идентификации вектора pK18-ptsSM162T, содержащего маркер устойчивости к канамицину. Надлежащим образом расщепленный вектор pK18-ptsSM162T отправляли в компанию, занимающуюся секвенированием, для идентификации путем секвенирования, и вектор pK18-ptsSM162T, содержащий надлежащую точечную мутацию (Т-С), сохраняли для последующего применения.
(2) Конструирование генноинженерного штамма ptsSM162T, содержащего точечную мутацию
Способ конструирования: Плазмиду pK18-ptsSM162T для аллельной замены трансформировали в запатентованный штамм YP97158 продуцирующих L-лизин бактерий с помощью электрических импульсов (способ ее конструирования см. в источнике WO 2014121669 A1; секвенирование подтвердило, что кодирующая область гена ptsS дикого типа в хромосоме этого штамма была сохранена), отдельную колонию, полученную при культивировании, идентифицировали с применением праймера Р1 и универсального праймера M13R, соответственно, и штамм, который мог обеспечивать амплификацию зоны размером 1393 п. н., представлял собой положительный штамм. Положительные штаммы культивировали на среде, содержащей 15% сахарозы, и отдельную колонию, полученную при культивировании, культивировали на среде, содержащей канамицин и не содержащей канамицина, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, дополнительно идентифицировали с помощью ПЦР с применением следующих праймеров (синтезированных компанией Shanghai Invitrogen):
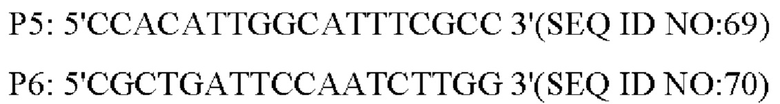
Указанный выше продукт амплификации размером 311 п. н., полученный с помощью ПЦР, подвергали электрофорезу для анализа sscp (в качестве положительного контроля использовали амплифицированный фрагмент плазмиды pK18-ptsSM162T, в качестве отрицательного контроля использовали амплифицированный фрагмент YP97158, и в качестве контроля фона использовали воду) после высокотемпературной денатурации при 95°С в течение 10 мин и помещения на ледяную баню на 5 мин. Вследствие различий в структуре фрагментов и положения при электрофорезе штаммы, положения которых при электрофорезе не соответствовали положениям фрагмента отрицательного контроля и соответствовали фрагменту положительного контроля, представляли собой штаммы с успешной аллельной заменой. Фрагмент положительного штамма ptsS повторно амплифицировали методом ПЦР с праймерами Р5 и Р6 и соединяли с вектором PMD19-T для секвенирования. Согласно результатам выравнивания последовательностей штамм с мутацией (A-G) в последовательности оснований представлял собой положительный штамм с успешной аллельной заменой и был назван YPL-4-035.
(3) Конструирование генно-инженерных штаммов, характеризующихся сверхэкспрессией гена PtsS или PtsSM162T в геноме
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, были сконструированы и синтезированы три пары праймеров для амплификации последовательностей вышележащего и нижележащего фрагментов гомологичного плеча, кодирующей области гена PtsS или PtsSM162T и промоторной области, и ген PtsS или PtsSM162T вводили в штамм YP97158 путем гомологичной рекомбинации.
Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):

Способ конструирования
Corynebacterium glutamicum АТСС 13032 или YPL-4-035 использовали в качестве матрицы для проведения амплификации методом ПЦР с праймерами Р7/Р8, Р9/Р10, Р11/Р12, соответственно, с получением вышележащего фрагмента гомологичного плеча размером 802 п.н., гена PtsS или PtsSM162T и его промоторного фрагмента размером 2354 п.н., а также нижележащего фрагмента гомологичного плеча размером 647 п.н. После реакции ПЦР три амплифицированных фрагмента выделяли методом электрофореза с применением набора для выделения ДНК из геля на колонке (TIANGEN). Три выделенных фрагмента лигировали с очищенной плазмидой pK18mobsacB (приобретенной в компании Addgene и дважды расщепленной Xbal I/BamH I, соответственно), дважды подвергнутой расщеплению, с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин. Отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с получением положительной интегрированной плазмиды и pK18mobsacB-PtsS или PtsSM162T и pK18mobsacB-PtsSM162T. Плазмида содержала маркер устойчивости к канамицину, и рекомбинантная плазмида, интегрированная в геном, может быть получена путем селекции с применением канамицина.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Две надлежащим образом секвенированные интегрирующие плазмиды подвергали электротрансформации в запатентованный штамм YP97158 продуцирующих L-лизин бактерий, соответственно, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР с применением праймеров Р13/Р14, и штамм, который мог обеспечивать амплификацию зоны размером 1298 п. н., представлял собой положительный штамм, а штаммы, которые не способны обеспечивать амплификацию указанных фрагментов, представляли собой исходные штаммы. Положительные штаммы культивировали на среде, содержащей 15% сахарозы, и отдельную колонию, полученную при культивировании, дополнительно идентифицировали с помощью ПЦР с применением праймеров Р15/Р16. Амплифицированные штаммы размером 1133 п.н. представляли собой положительные штаммы с геном PtsS или PtsSM162T, интегрированным в геном YP97158, и были названы YPL-4-036 (без точечной мутации) и YPL-4-037 (с точечной мутацией).
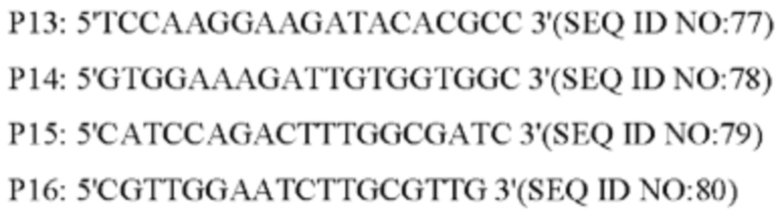
(4) Конструирование генноинженерных штаммов, характеризующихся сверхэкспрессией гена PtsS или PtsSM162T в плазмиде
В соответствии с последовательностью генома Corynebacterium glutamicum дикого типа АТСС 13032, опубликованной NCBI, была сконструирована и синтезирована одна пара праймеров для амплификации последовательности кодирующей области и промоторной области гена PtsS или PtsSM162T праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Invitrogen):

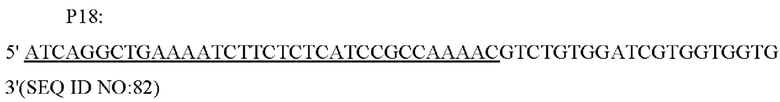
Способ конструирования: АТСС 13032 и YPL-4-035 использовали в качестве матриц для проведения амплификации методом ПЦР с праймерами Р17/Р18 с получением гена PtsS или PtsSM162T и его промоторного фрагмента размером 2354 п.н., и полученные продукты амплификации подвергали электрофорезу и очищали с помощью набора для выделения ДНК из геля на колонке. Выделенный фрагмент ДНК и челночную плазмиду pXMJ19, полученную с помощью расщепления EcoR I, лигировали с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин, и отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с праймером М13 с получением положительной плазмиды сверхэкспрессии pXMJ19-PtsS и pXMJ19-PtsSM162T, и полученную плазмиду отправляли на секвенирование. Поскольку плазмида содержала маркер устойчивости к хлорамфениколу, она могла быть использована для скрининга того, была ли плазмида трансформирована в штамм, проводимого с применением хлорамфеникола.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл.
Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 60 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Надлежащим образом секвенированные плазмиды pXMJ19-RsS и pXMJ19-PtsSM162T подвергали электротрансформации в запатентованный штамм YP97158 продуцирующих L-лизин бактерий, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР с праймерами М13/Р18. Амплифицированный с помощью ПЦР фрагмент, содержащий фрагмент размером 2362 п.н., представлял собой положительный штамм, названный YPL-4-038 (без точечной мутации) и YPL-4-039 (с точечной мутацией).
(5) Конструирование генноинженерных штаммов, в геноме которых отсутствует ген PtsS
В соответствии с последовательностью генома Corynebacterium glutamicum АТСС13032, опубликованной NCBI, были синтезированы две пары праймеров для амплификации фрагментов с обоих концов кодирующей области гена PtsS в виде вышележащего и нижележащего фрагментов гомологичного плеча. Праймеры были сконструированы следующим образом (синтезированы компанией Shanghai Yingjun):

Способ конструирования: Corynebacterium glutamicum АТСС 13032 применяли в качестве матрицы, амплификацию методом ПЦР проводили с праймерами Р19/Р20 и Р21/Р22, соответственно, с получением вышележащего фрагмента гомологичного плеча размером 794 п.н. и нижележащего фрагмента гомологичного плеча размером 703 п.н., и затем получали полный фрагмент гомологичного плеча размером 1459 п.н. методом ПЦР с перекрывающимися праймерами с применением праймеров Р19/Р22. Амплифицированный продукт подвергли электрофорезу и очистке с помощью набора для выделения ДНК из геля на колонке, и выделенный фрагмент ДНК лигировали с очищенной плазмидой pK18mobsacB (приобретенной в компании Addgene и дважды расщепленной Xbal I/BamH I, соответственно), дважды подвергнутой расщеплению, с применением фермента NEBuilder (приобретенного в компании NEB) при 50°С в течение 30 мин, и отдельный клон, выращенный после трансформации продукта лигирования, идентифицировали с помощью ПЦР с праймером М13 с получением положительного нокаутного вектора pK18-APtsS, который отправляли на секвенирование. Эта плазмида содержала маркер устойчивости к канамицину в качестве селектируемого маркера.
Система для ПЦР: 10×Ех Taq-буфер - 5 мкл, смесь dNTP (2,5 мМ каждого) - 4 мкл, Mg2+(25 мМ) - 4 мкл, праймеры (10 пМ) - 2 мкл каждого, Ex Taq (5 Ед/мкл) - 0,25 мкл, общий объем 50 мкл. Амплификацию методом ПЦР проводили следующим образом: предварительная денатурация при 94°С в течение 5 мин, денатурация при 94°С в течение 30 с, отжиг при 52°С в течение 30 с, элонгация при 72°С в течение 90 с (30 циклов), и финальная элонгация при 72°С в течение 10 мин.
Надлежащим образом секвенированную нокаутную плазмиду pK18-APtsS подвергали электротрансформации в запатентованный штамм YP97158, продуцирующий лизин, и отдельную колонию, полученную при культивировании, идентифицировали с помощью ПЦР со следующими праймерами (синтезированы компанией Shanghai Yingjun):
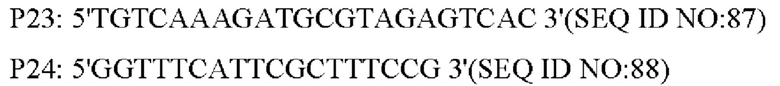
Штаммы с зонами размером 758 п. н. и 2249 п.н., одновременно амплифицированными с помощью описанной выше ПЦР, представляли собой положительные штаммы, а штамм с амплифицированной зоной размером 2249 п.н. отдельно представлял собой исходный штамм. Положительные штаммы подвергали скринингу на среде с 15% сахарозы и культивировали на среде, содержащей канамицин, и среде, не содержащей канамицина, соответственно. Штаммы, которые росли на среде без канамицина, но не росли на среде, содержащей канамицин, в дальнейшем идентифицировали методом ПЦР с применением праймеров Р23/Р24, и амплифицированные штаммы размером 758 п.н. представляли собой положительный штамм, в котором кодирующая область гена PtsS была нокаутирована. Фрагмент положительного штамма ptsS повторно амплифицировали методом ПЦР с праймерами Р23/Р24 и лигировали с вектором PMD19-T для секвенирования. Штамм с надлежащими результатами секвенирования был назван YPL-4-040. (6) Эксперимент с получением L-лизина путем ферментации Штаммы, сконструированные в примерах, и исходный штамм YP97158 подвергали экспериментам по ферментации в ферментере BLBIO-5GC-4-H (приобретенном у Shanghai Bailun Biotechnology Co., Ltd.) со средой, представленной в табл. 10, и процессом контроля, представленным в табл. 11. Эксперимент с каждым штаммом повторяли три раза, результаты представлены в табл. 12.

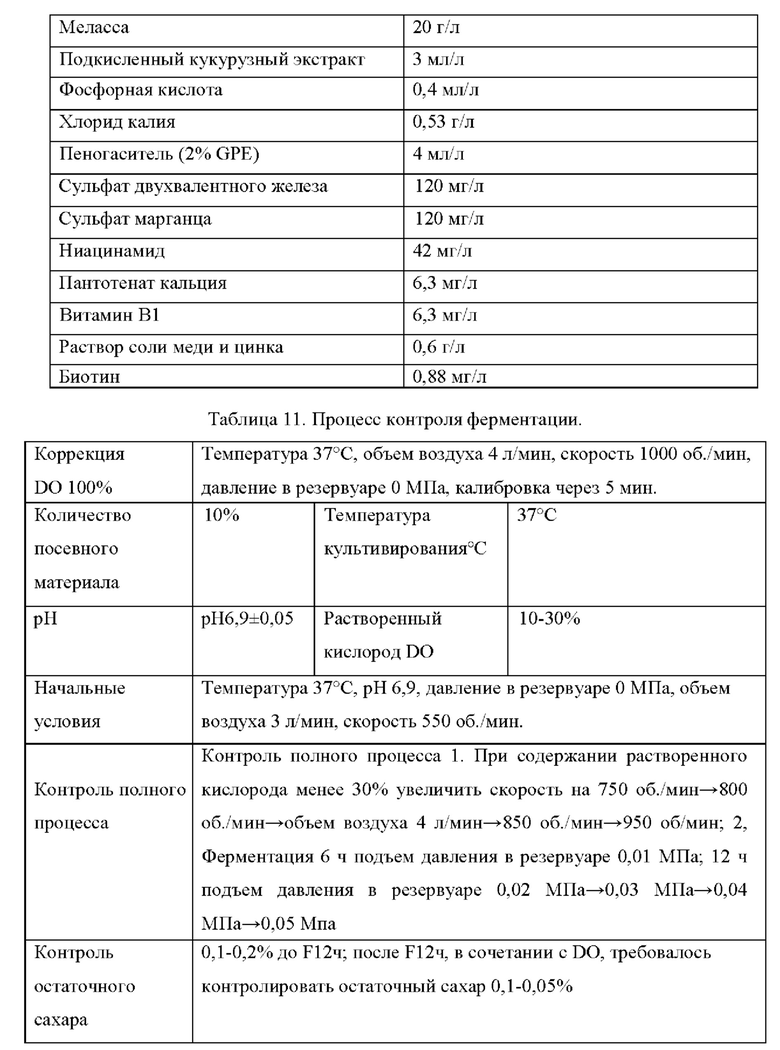
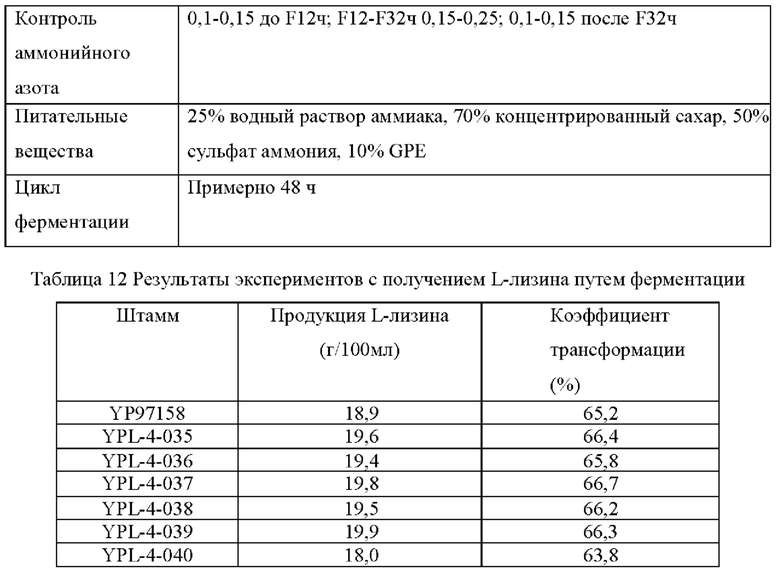
Результаты представлены в табл. 12. Точечная мутация PtsSM162T и сверхэкспрессия кодирующей области гена PtsS у Corynebacterium glutamicum способствовали улучшению продукции L-лизина и повышению коэффициента трансформации, в то время как ослабление или нокаутирование указанного гена не способствовало накоплению L-лизина и в то же время снижало коэффициент трансформации.
(7) Ген PtsS вводили в продуцирующий глутаминовую кислоту штамм и обеспечивали сверхэкспрессию, или кодирующую область гена PtsS подвергали точечной мутации ptsSM162T и обеспечивали сверхэкспрессию, и проводили эксперименты по ферментации.
В соответствии со способом, описанным в этих примерах (1-5), использовали те же праймеры и экспериментальные условия, и Corynebacterium АТСС 13869 использовали в качестве исходной бактерии, а бактерию АТСС 13869 использовали в качестве бактерии экспрессии для получения продуцирующего глутаминовую кислоту генноинженерного штамма с ptsSM162T, содержащим точечную мутацию, продуцирующего глутаминовую кислоту генноинженерного штамма, характеризующегося сверхэкспрессией генов ptsS и ptsS в геноме, и продуцирующего глутаминовую кислоту генноинженерного штамма, характеризующегося сверхэкспрессией генов ptsS и ptsSM162T в плазмидах, а также продуцирующего глутаминовую кислоту генноинженерного штамма, в геноме которого отсутствует ген ptsS.
Штаммы, сконструированные в примерах, и исходный штамм АТСС 13869 подвергали экспериментам по ферментации в ферментере BLBIO-5GC-4-H (приобретенном у Shanghai Bailun Biotechnology Co., Ltd.) со средой, представленной в табл. 13, и процессом контроля, представленным в табл. 14. Эксперимент с каждым штаммом повторяли три раза, результаты представлены в табл. 15.


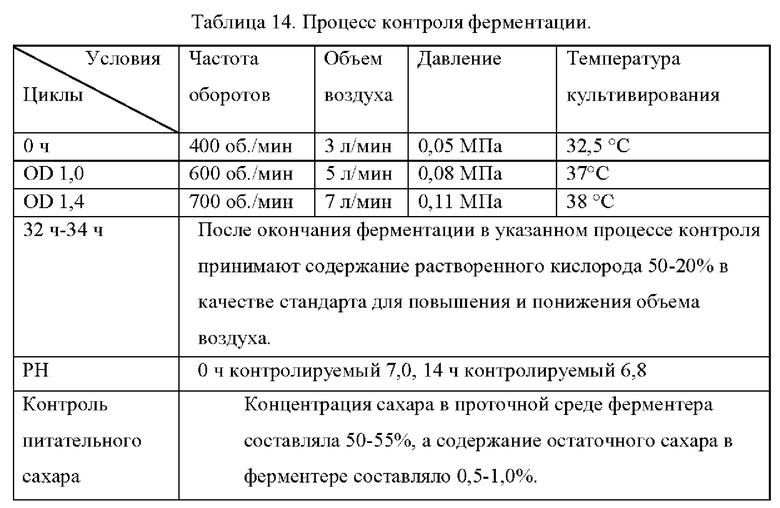
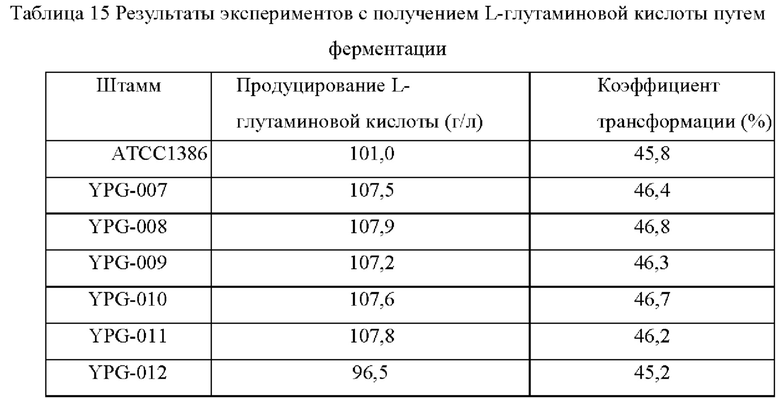
Результаты представлены в табл. 15. Точечная мутация PtsSM162T и/или сверхэкспрессия кодирующей области гена PtsS у Corynebacterium glutamicum способствовали улучшению продукции L-лизина и повышению коэффициента трансформации, в то время как ослабление или нокаутирование указанного гена не способствовало накоплению L-лизина и в то же время снижало коэффициент трансформации.
Воплощения настоящего изобретения описаны выше. Однако настоящее изобретение не ограничивается описанными выше воплощениями. Любая модификация, эквивалентная замена, усовершенствование и так далее, соответствующие сущности и принципу настоящего изобретения, должны быть включены в объем охраны настоящего изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NINGXIA EPPEN BIOTECH CO., LTD.
<120> Рекомбинантный штамм для получения L-аминокислоты, способ его
конструирования и применение
<130> CPWO20411700
<160> 88
<170> PatentIn, версия 3.5
<210> 1
<211> 654
<212> ДНК
<213> Corynebacterium glutamicum
<400> 1
atgagcatct ggaaacgtct gttagtgcag tacccgcgct tcgccgacac cctcacagcc 60
ggccaaccca tcacgctcga ggaattagca accccggaag tgatcttgga agctgttgcc 120
aaaggccaag aaattttcgg cattgagcag ccaaaacatg cagcacaact ctggtttcac 180
tccctgtgca ccgcaattgt cggccccgcc gtcaccgcca tggtggaatt cgatgtcatc 240
cccagcctcg acatacgtcg aggtcagctg cataacatcg acggttactg gttcggcttc 300
aggccggagg agatgcttgt cgacgcctcc ctccacctgt cgggcaccca attcggcgag 360
agtatccgcg tggtgattga tgcattatgc gctgccacgg atctgcgacc ggcacccctg 420
tgggcggttg cctcagatgc gttgggaatc gcagctagcg gcgcaggtgt cgaggccttt 480
gaagaagaac atgcccgcga ggtggcggaa gccctcattg aaggaatgaa tagtgtgaac 540
tcagttccat cgccgcggtt taacgacgac gattatttca ttcgagctgg atgctgcatg 600
attttccact caccacgagc tgatttttgc acgtcgtgcc cacagaagag gtga 654
<210> 2
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 2
atgagcatct ggaaacgtct gttagtgcag tacccgcgct tcgccgacac cctcacagcc 60
ggccaaccca tcacgctcga ggaattagca accccggaag tgatcttgga agctgttgcc 120
aaaggccaag aaattttcgg cattgagcag ccaaaacatg cagcacaact ctggtttcac 180
tccctgtgca ccgcaattgt cggccccgcc gtcaccgcca tggtggaatt cgatgtcatc 240
cccagcctcg acatacgtcg aggtcagctg cataacatcg acggttactg gttcggcttc 300
aggccggagg agatgcttgt cgacgcctcc ctccacctgt cgggcaccca attcggcgag 360
agtatccgcg tggtgattga tgcattatgc gctgccacgg atctgcgacc ggcacccctg 420
tgggcggttg cctcagatgc gttgggaatc gcagctagcg gcgcaggtgt cgaggccttt 480
gaagaagaac atgcccgcga ggtggcgaaa gccctcattg aaggaatgaa tagtgtgaac 540
tcagttccat cgccgcggtt taacgacgac gattatttca ttcgagctgg atgctgcatg 600
attttccact caccacgagc tgatttttgc acgtcgtgcc cacagaagag gtga 654
<210> 3
<211> 217
<212> БЕЛОК
<213> Corynebacterium glutamicum
<400> 3
Met Ser Ile Trp Lys Arg Leu Leu Val Gln Tyr Pro Arg Phe Ala Asp
1 5 10 15
Thr Leu Thr Ala Gly Gln Pro Ile Thr Leu Glu Glu Leu Ala Thr Pro
20 25 30
Glu Val Ile Leu Glu Ala Val Ala Lys Gly Gln Glu Ile Phe Gly Ile
35 40 45
Glu Gln Pro Lys His Ala Ala Gln Leu Trp Phe His Ser Leu Cys Thr
50 55 60
Ala Ile Val Gly Pro Ala Val Thr Ala Met Val Glu Phe Asp Val Ile
65 70 75 80
Pro Ser Leu Asp Ile Arg Arg Gly Gln Leu His Asn Ile Asp Gly Tyr
85 90 95
Trp Phe Gly Phe Arg Pro Glu Glu Met Leu Val Asp Ala Ser Leu His
100 105 110
Leu Ser Gly Thr Gln Phe Gly Glu Ser Ile Arg Val Val Ile Asp Ala
115 120 125
Leu Cys Ala Ala Thr Asp Leu Arg Pro Ala Pro Leu Trp Ala Val Ala
130 135 140
Ser Asp Ala Leu Gly Ile Ala Ala Ser Gly Ala Gly Val Glu Ala Phe
145 150 155 160
Glu Glu Glu His Ala Arg Glu Val Ala Glu Ala Leu Ile Glu Gly Met
165 170 175
Asn Ser Val Asn Ser Val Pro Ser Pro Arg Phe Asn Asp Asp Asp Tyr
180 185 190
Phe Ile Arg Ala Gly Cys Cys Met Ile Phe His Ser Pro Arg Ala Asp
195 200 205
Phe Cys Thr Ser Cys Pro Gln Lys Arg
210 215
<210> 4
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 4
Met Ser Ile Trp Lys Arg Leu Leu Val Gln Tyr Pro Arg Phe Ala Asp
1 5 10 15
Thr Leu Thr Ala Gly Gln Pro Ile Thr Leu Glu Glu Leu Ala Thr Pro
20 25 30
Glu Val Ile Leu Glu Ala Val Ala Lys Gly Gln Glu Ile Phe Gly Ile
35 40 45
Glu Gln Pro Lys His Ala Ala Gln Leu Trp Phe His Ser Leu Cys Thr
50 55 60
Ala Ile Val Gly Pro Ala Val Thr Ala Met Val Glu Phe Asp Val Ile
65 70 75 80
Pro Ser Leu Asp Ile Arg Arg Gly Gln Leu His Asn Ile Asp Gly Tyr
85 90 95
Trp Phe Gly Phe Arg Pro Glu Glu Met Leu Val Asp Ala Ser Leu His
100 105 110
Leu Ser Gly Thr Gln Phe Gly Glu Ser Ile Arg Val Val Ile Asp Ala
115 120 125
Leu Cys Ala Ala Thr Asp Leu Arg Pro Ala Pro Leu Trp Ala Val Ala
130 135 140
Ser Asp Ala Leu Gly Ile Ala Ala Ser Gly Ala Gly Val Glu Ala Phe
145 150 155 160
Glu Glu Glu His Ala Arg Glu Val Ala Lys Ala Leu Ile Glu Gly Met
165 170 175
Asn Ser Val Asn Ser Val Pro Ser Pro Arg Phe Asn Asp Asp Asp Tyr
180 185 190
Phe Ile Arg Ala Gly Cys Cys Met Ile Phe His Ser Pro Arg Ala Asp
195 200 205
Phe Cys Thr Ser Cys Pro Gln Lys Arg
210 215
<210> 5
<211> 55
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 5
cagtgccaag cttgcatgcc tgcaggtcga ctctagcgcg tgggatccac gccag 55
<210> 6
<211> 28
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 6
caatgagggc tttcgccacc tcgcgggc 28
<210> 7
<211> 28
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 7
gcccgcgagg tggcgaaagc cctcattg 28
<210> 8
<211> 56
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 8
cagctatgac catgattacg aattcgagct cggtacccca tgcgttggcg atcttc 56
<210> 9
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 9
ggtgattgat gcattatgcg c 21
<210> 10
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 10
cctagccttt cacctcttct gt 22
<210> 11
<211> 55
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 11
cagtgccaag cttgcatgcc tgcaggtcga ctctagaatg cgttctggac tgagg 55
<210> 12
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 12
catgagtata aaatcactgt cgtgcaccga gaacagatg 39
<210> 13
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 13
catctgttct cggtgcacga cagtgatttt atactcatg 39
<210> 14
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 14
gacgtttcca gatgctcatc accgaacccg ctgcactgt 39
<210> 15
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 15
acagtgcagc gggttcggtg atgagcatct ggaaacgtc 39
<210> 16
<211> 40
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 16
cttgatttaa ttgcgccatc tcacctcttc tgtgggcacg 40
<210> 17
<211> 40
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 17
cgtgcccaca gaagaggtga gatggcgcaa ttaaatcaag 40
<210> 18
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 18
cagctatgac catgattacg aattcgagct cggtacccgc tatgacacct tcaacggatc 60
<210> 19
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 19
tccaaggaag atacacgcc 19
<210> 20
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 20
ctgcgattcc caacgcatct 20
<210> 21
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 21
gagcagccaa aacatgcagc 20
<210> 22
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 22
cgttggaatc ttgcgttg 18
<210> 23
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 23
gcttgcatgc ctgcaggtcg actctagagg atccccgaca gtgattttat actcatg 57
<210> 24
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 24
gacgtttcca gatgctcatc accgaacccg ctgcactgt 39
<210> 25
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 25
acagtgcagc gggttcggtg atgagcatct ggaaacgtc 39
<210> 26
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 26
atcaggctga aaatcttctc tcatccgcca aaactcacct cttctgtggg cacg 54
<210> 27
<211> 56
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 27
cagtgccaag cttgcatgcc tgcaggtcga ctctagcacc gcattccctt catgat 56
<210> 28
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 28
acgaatccgc gcctagcctt ttatctactt ccaaaaaact gc 42
<210> 29
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 29
gcagtttttt ggaagtagat aaaaggctag gcgcggattc gt 42
<210> 30
<211> 56
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 30
cagctatgac catgattacg aattcgagct cggtaccccg agggaaagga tatcga 56
<210> 31
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 31
caccgcattc ccttcatgat 20
<210> 32
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 32
cgagggaaag gatatcga 18
<210> 33
<211> 432
<212> ДНК
<213> Corynebacterium glutamicum
<400> 33
atgtattccg acaagctgat tctcttgttc ctttctgagc aggattcaag ctatgaatgc 60
tgcgtaggtt tattagatgg ctcagatgga cttgattata ttgaaaagct tctgaagggt 120
aggaagctga agaaccattt tcttgaatgg gaagatatta acaaggctga tgttgctcgt 180
gaagaaatat ataaagggca attggtgcat ctggtgtttg tgacggctct ttccacgcct 240
ggtgaaattt cttttgtttt tccaggtcaa tctcttatga gtgcaacact cgaagaagac 300
tttgctgcgc ttgtgctcga agaggagcgc acatcattta gacctgaact gtctcacctg 360
tggtcactcc ccgtagggtg ggtagctccg gggcttgagg gtttcgtgga gcgtaattcc 420
gaggcagctt ga 432
<210> 34
<211> 432
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 34
atgtattccg acaagctgat tctcttgttc ctttctgagc aggattcaag ctatgaatgc 60
tgcgtaggtt tattagatgg ctcagatgga cgtgattata ttgaaaagct tctgaagggt 120
aggaagctga agaaccattt tcttgaatgg gaagatatta acaaggctga tgttgctcgt 180
gaagaaatat ataaagggca attggtgcat ctggtgtttg tgacggctct ttccacgcct 240
ggtgaaattt cttttgtttt tccaggtcaa tctcttatga gtgcaacact cgaagaagac 300
tttgctgcgc ttgtgctcga agaggagcgc acatcattta gacctgaact gtctcacctg 360
tggtcactcc ccgtagggtg ggtagctccg gggcttgagg gtttcgtgga gcgtaattcc 420
gaggcagctt ga 432
<210> 35
<211> 143
<212> БЕЛОК
<213> Corynebacterium glutamicum
<400> 35
Met Tyr Ser Asp Lys Leu Ile Leu Leu Phe Leu Ser Glu Gln Asp Ser
1 5 10 15
Ser Tyr Glu Cys Cys Val Gly Leu Leu Asp Gly Ser Asp Gly Leu Asp
20 25 30
Tyr Ile Glu Lys Leu Leu Lys Gly Arg Lys Leu Lys Asn His Phe Leu
35 40 45
Glu Trp Glu Asp Ile Asn Lys Ala Asp Val Ala Arg Glu Glu Ile Tyr
50 55 60
Lys Gly Gln Leu Val His Leu Val Phe Val Thr Ala Leu Ser Thr Pro
65 70 75 80
Gly Glu Ile Ser Phe Val Phe Pro Gly Gln Ser Leu Met Ser Ala Thr
85 90 95
Leu Glu Glu Asp Phe Ala Ala Leu Val Leu Glu Glu Glu Arg Thr Ser
100 105 110
Phe Arg Pro Glu Leu Ser His Leu Trp Ser Leu Pro Val Gly Trp Val
115 120 125
Ala Pro Gly Leu Glu Gly Phe Val Glu Arg Asn Ser Glu Ala Ala
130 135 140
<210> 36
<211> 143
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 36
Met Tyr Ser Asp Lys Leu Ile Leu Leu Phe Leu Ser Glu Gln Asp Ser
1 5 10 15
Ser Tyr Glu Cys Cys Val Gly Leu Leu Asp Gly Ser Asp Gly Arg Asp
20 25 30
Tyr Ile Glu Lys Leu Leu Lys Gly Arg Lys Leu Lys Asn His Phe Leu
35 40 45
Glu Trp Glu Asp Ile Asn Lys Ala Asp Val Ala Arg Glu Glu Ile Tyr
50 55 60
Lys Gly Gln Leu Val His Leu Val Phe Val Thr Ala Leu Ser Thr Pro
65 70 75 80
Gly Glu Ile Ser Phe Val Phe Pro Gly Gln Ser Leu Met Ser Ala Thr
85 90 95
Leu Glu Glu Asp Phe Ala Ala Leu Val Leu Glu Glu Glu Arg Thr Ser
100 105 110
Phe Arg Pro Glu Leu Ser His Leu Trp Ser Leu Pro Val Gly Trp Val
115 120 125
Ala Pro Gly Leu Glu Gly Phe Val Glu Arg Asn Ser Glu Ala Ala
130 135 140
<210> 37
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 37
cagtgccaag cttgcatgcc tgcaggtcga ctctagcttg cagctaacct atacccc 57
<210> 38
<211> 34
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 38
gcttttcaat ataatcacgt ccatctgagc catc 34
<210> 39
<211> 34
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 39
gatggctcag atggacgtga ttatattgaa aagc 34
<210> 40
<211> 56
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 40
cagctatgac catgattacg aattcgagct cggtacccct cccaaataat tgccgc 56
<210> 41
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 41
gaatggaata ggagaattgc g 21
<210> 42
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 42
caccaggcgt ggaaagag 18
<210> 43
<211> 55
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 43
cagtgccaag cttgcatgcc tgcaggtcga ctctagaatg cgttctggac tgagg 55
<210> 44
<211> 55
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 44
cagtgccaag cttgcatgcc tgcaggtcga ctctagaatg cgttctggac tgagg 55
<210> 45
<211> 38
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 45
catctgttct cggtgcacat gtagtggggt atggatgg 38
<210> 46
<211> 44
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 46
gatttaattg cgccatctga ttctgggtga ggtttccggc tcag 44
<210> 47
<211> 44
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 47
ctgagccgga aacctcaccc agaatcagat ggcgcaatta aatc 44
<210> 48
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 48
cagctatgac catgattacg aattcgagct cggtacccgc tatgacacct tcaacggatc 60
<210> 49
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 49
tccaaggaag atacacgcc 19
<210> 50
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 50
gccttgttaa tatcttccc 19
<210> 51
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 51
gggaagatat taacaaggc 19
<210> 52
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 52
cgttggaatc ttgcgttg 18
<210> 53
<211> 56
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 53
gcttgcatgc ctgcaggtcg actctagagg atccccatgt agtggggtat ggatgg 56
<210> 54
<211> 52
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 54
atcaggctga aaatcttctc tcatccgcca aaacgtgagg tttccggctc ag 52
<210> 55
<211> 58
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 55
cagtgccaag cttgcatgcc tgcaggtcga ctctaggtat ctggagagaa gaaggagc 58
<210> 56
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 56
gccttgttaa tatcttcccg aatacatgcc gcaattctcc tattc 45
<210> 57
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 57
gagaattgcg gcatgtattc gggaagatat taacaaggc 39
<210> 58
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 58
cagctatgac catgattacg aattcgagct cggtaccccc gcagattact aaggctg 57
<210> 59
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 59
gtatctggag agaagaagga gc 22
<210> 60
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая
<400> 60
ccgcagatta ctaaggctg 19
<210> 61
<211> 1986
<212> ДНК
<213> Corynebacterium glutamicum
<400> 61
atggaccata aggacctcgc gcaacgcatc ctgcgcgaca ttggcggcga agacaacatt 60
gtcgccgccg cacactgtgc aacgcgttta cgcctcgtgc tcaaagacac caaggatgtg 120
gatcgccaaa gtctggatga tgatccagat ctgaaaggca cgtttgaaac gggtggtatg 180
ttccagatca tcgtcgggcc aggcgatgtg gatcatgttt tcaaagaact cgatgacgca 240
acctccaaag acatcgctgt gtccacagag cagctcaaag atgttgtggc taacaacgcc 300
aactggttca gccgtgctgt gaaggtattg gcggacattt tcgtcccgct gattccaatc 360
ttggttggtg gcggtctgct catggctatc aacaatgtgt tggttgcgca ggatctgttc 420
ggtccgcaat cactggtgga gatgttccct cagatcagcg gtgttgctga gatgatcaac 480
ctcatggcat ctgcgccgtt cgcgttcttg ccagtgttgg ttggtttcac cgcaaccaag 540
cgtttcggcg gcaatgagtt cctgggcgcc ggtattggta tggcgatggt gttcccgagc 600
ttggtgaacg gctacgacgt ggccgccacc atggctgcgg gcgaaatgcc aatgtggtcc 660
ctgtttggtt tagatgttgc ccaagccggt taccagggca ccgtgcttcc tgtgctggtg 720
gtttcttgga ttctggcaac gatcgagaag ttcctgcaca agcgactcaa gggcactgca 780
gacttcctga tcactccagt gctgacgttg ctgctcaccg gattccttac attcatcgcc 840
attggcccag caatgcgctg ggtgggcgat gtgctggcac acggtctaca gggactttat 900
gatttcggtg gtccagtcgg cggtctgctc ttcggtctgg tctactcacc aatcgtcatc 960
actggtctgc accagtcctt cccgccaatt gagctggagc tgtttaacca gggtggatcc 1020
ttcatcttcg caacggcatc tatggctaat atcgcccagg gtgcggcatg tttggcagtg 1080
ttcttcctgg cgaagagtga aaagctcaag ggccttgcag gtgcttcagg tgtctccgct 1140
gttcttggta ttacggagcc tgcgatcttc ggtgtgaacc ttcgcctgcg ctggccgttc 1200
ttcatcggta tcggtaccgc agctatcggt ggcgctttga ttgcactctt taatatcaag 1260
gcagttgcgt tgggcgctgc aggtttcttg ggtgttgttt ctattgatgc tccagatatg 1320
gtcatgttct tggtgtgtgc agttgttacc ttcttcatcg cattcggcgc agcgattgct 1380
tatggccttt acttggttcg ccgcaacggc agcattgatc cagatgcaac cgctgctcca 1440
gtgcctgcag gaacgaccaa agccgaagca gaagcacccg cagaattttc aaacgattcc 1500
accatcatcc aggcaccttt gaccggtgaa gctattgcac tgagcagcgt cagcgatgcc 1560
atgtttgcca gcggaaagct tggctcgggc gttgccatcg tcccaaccaa ggggcagtta 1620
gtttctccgg tgagtggaaa gattgtggtg gcattcccat ctggccatgc tttcgcagtt 1680
cgcaccaagg ctgaggatgg ttccaatgtg gatatcttga tgcacattgg tttcgacaca 1740
gtaaacctca acggcacgca ctttaacccg ctgaagaagc agggcgatga agtcaaagca 1800
ggggagctgc tgtgtgaatt cgatattgat gccattaagg ctgcaggtta tgaggtaacc 1860
acgccgattg ttgtttcgaa ttacaagaaa accggacctg taaacactta cggtttgggc 1920
gaaattgaag cgggagccaa cctgctcaac gtcgcaaaga aagaagcggt gccagcaaca 1980
ccataa 1986
<210> 62
<211> 1986
<212> ДНК
<213> Искусственная последовательность
<400> 62
atggaccata aggacctcgc gcaacgcatc ctgcgcgaca ttggcggcga agacaacatt 60
gtcgccgccg cacactgtgc aacgcgttta cgcctcgtgc tcaaagacac caaggatgtg 120
gatcgccaaa gtctggatga tgatccagat ctgaaaggca cgtttgaaac gggtggtatg 180
ttccagatca tcgtcgggcc aggcgatgtg gatcatgttt tcaaagaact cgatgacgca 240
acctccaaag acatcgctgt gtccacagag cagctcaaag atgttgtggc taacaacgcc 300
aactggttca gccgtgctgt gaaggtattg gcggacattt tcgtcccgct gattccaatc 360
ttggttggtg gcggtctgct catggctatc aacaatgtgt tggttgcgca ggatctgttc 420
ggtccgcaat cactggtgga gatgttccct cagatcagcg gtgttgctga gatgatcaac 480
ctcacggcat ctgcgccgtt cgcgttcttg ccagtgttgg ttggtttcac cgcaaccaag 540
cgtttcggcg gcaatgagtt cctgggcgcc ggtattggta tggcgatggt gttcccgagc 600
ttggtgaacg gctacgacgt ggccgccacc atggctgcgg gcgaaatgcc aatgtggtcc 660
ctgtttggtt tagatgttgc ccaagccggt taccagggca ccgtgcttcc tgtgctggtg 720
gtttcttgga ttctggcaac gatcgagaag ttcctgcaca agcgactcaa gggcactgca 780
gacttcctga tcactccagt gctgacgttg ctgctcaccg gattccttac attcatcgcc 840
attggcccag caatgcgctg ggtgggcgat gtgctggcac acggtctaca gggactttat 900
gatttcggtg gtccagtcgg cggtctgctc ttcggtctgg tctactcacc aatcgtcatc 960
actggtctgc accagtcctt cccgccaatt gagctggagc tgtttaacca gggtggatcc 1020
ttcatcttcg caacggcatc tatggctaat atcgcccagg gtgcggcatg tttggcagtg 1080
ttcttcctgg cgaagagtga aaagctcaag ggccttgcag gtgcttcagg tgtctccgct 1140
gttcttggta ttacggagcc tgcgatcttc ggtgtgaacc ttcgcctgcg ctggccgttc 1200
ttcatcggta tcggtaccgc agctatcggt ggcgctttga ttgcactctt taatatcaag 1260
gcagttgcgt tgggcgctgc aggtttcttg ggtgttgttt ctattgatgc tccagatatg 1320
gtcatgttct tggtgtgtgc agttgttacc ttcttcatcg cattcggcgc agcgattgct 1380
tatggccttt acttggttcg ccgcaacggc agcattgatc cagatgcaac cgctgctcca 1440
gtgcctgcag gaacgaccaa agccgaagca gaagcacccg cagaattttc aaacgattcc 1500
accatcatcc aggcaccttt gaccggtgaa gctattgcac tgagcagcgt cagcgatgcc 1560
atgtttgcca gcggaaagct tggctcgggc gttgccatcg tcccaaccaa ggggcagtta 1620
gtttctccgg tgagtggaaa gattgtggtg gcattcccat ctggccatgc tttcgcagtt 1680
cgcaccaagg ctgaggatgg ttccaatgtg gatatcttga tgcacattgg tttcgacaca 1740
gtaaacctca acggcacgca ctttaacccg ctgaagaagc agggcgatga agtcaaagca 1800
ggggagctgc tgtgtgaatt cgatattgat gccattaagg ctgcaggtta tgaggtaacc 1860
acgccgattg ttgtttcgaa ttacaagaaa accggacctg taaacactta cggtttgggc 1920
gaaattgaag cgggagccaa cctgctcaac gtcgcaaaga aagaagcggt gccagcaaca 1980
ccataa 1986
<210> 63
<211> 661
<212> БЕЛОК
<213> Corynebacterium glutamicum
<400> 63
Met Asp His Lys Asp Leu Ala Gln Arg Ile Leu Arg Asp Ile Gly Gly
1 5 10 15
Glu Asp Asn Ile Val Ala Ala Ala His Cys Ala Thr Arg Leu Arg Leu
20 25 30
Val Leu Lys Asp Thr Lys Asp Val Asp Arg Gln Ser Leu Asp Asp Asp
35 40 45
Pro Asp Leu Lys Gly Thr Phe Glu Thr Gly Gly Met Phe Gln Ile Ile
50 55 60
Val Gly Pro Gly Asp Val Asp His Val Phe Lys Glu Leu Asp Asp Ala
65 70 75 80
Thr Ser Lys Asp Ile Ala Val Ser Thr Glu Gln Leu Lys Asp Val Val
85 90 95
Ala Asn Asn Ala Asn Trp Phe Ser Arg Ala Val Lys Val Leu Ala Asp
100 105 110
Ile Phe Val Pro Leu Ile Pro Ile Leu Val Gly Gly Gly Leu Leu Met
115 120 125
Ala Ile Asn Asn Val Leu Val Ala Gln Asp Leu Phe Gly Pro Gln Ser
130 135 140
Leu Val Glu Met Phe Pro Gln Ile Ser Gly Val Ala Glu Met Ile Asn
145 150 155 160
Leu Met Ala Ser Ala Pro Phe Ala Phe Leu Pro Val Leu Val Gly Phe
165 170 175
Thr Ala Thr Lys Arg Phe Gly Gly Asn Glu Phe Leu Gly Ala Gly Ile
180 185 190
Gly Met Ala Met Val Phe Pro Ser Leu Val Asn Gly Tyr Asp Val Ala
195 200 205
Ala Thr Met Ala Ala Gly Glu Met Pro Met Trp Ser Leu Phe Gly Leu
210 215 220
Asp Val Ala Gln Ala Gly Tyr Gln Gly Thr Val Leu Pro Val Leu Val
225 230 235 240
Val Ser Trp Ile Leu Ala Thr Ile Glu Lys Phe Leu His Lys Arg Leu
245 250 255
Lys Gly Thr Ala Asp Phe Leu Ile Thr Pro Val Leu Thr Leu Leu Leu
260 265 270
Thr Gly Phe Leu Thr Phe Ile Ala Ile Gly Pro Ala Met Arg Trp Val
275 280 285
Gly Asp Val Leu Ala His Gly Leu Gln Gly Leu Tyr Asp Phe Gly Gly
290 295 300
Pro Val Gly Gly Leu Leu Phe Gly Leu Val Tyr Ser Pro Ile Val Ile
305 310 315 320
Thr Gly Leu His Gln Ser Phe Pro Pro Ile Glu Leu Glu Leu Phe Asn
325 330 335
Gln Gly Gly Ser Phe Ile Phe Ala Thr Ala Ser Met Ala Asn Ile Ala
340 345 350
Gln Gly Ala Ala Cys Leu Ala Val Phe Phe Leu Ala Lys Ser Glu Lys
355 360 365
Leu Lys Gly Leu Ala Gly Ala Ser Gly Val Ser Ala Val Leu Gly Ile
370 375 380
Thr Glu Pro Ala Ile Phe Gly Val Asn Leu Arg Leu Arg Trp Pro Phe
385 390 395 400
Phe Ile Gly Ile Gly Thr Ala Ala Ile Gly Gly Ala Leu Ile Ala Leu
405 410 415
Phe Asn Ile Lys Ala Val Ala Leu Gly Ala Ala Gly Phe Leu Gly Val
420 425 430
Val Ser Ile Asp Ala Pro Asp Met Val Met Phe Leu Val Cys Ala Val
435 440 445
Val Thr Phe Phe Ile Ala Phe Gly Ala Ala Ile Ala Tyr Gly Leu Tyr
450 455 460
Leu Val Arg Arg Asn Gly Ser Ile Asp Pro Asp Ala Thr Ala Ala Pro
465 470 475 480
Val Pro Ala Gly Thr Thr Lys Ala Glu Ala Glu Ala Pro Ala Glu Phe
485 490 495
Ser Asn Asp Ser Thr Ile Ile Gln Ala Pro Leu Thr Gly Glu Ala Ile
500 505 510
Ala Leu Ser Ser Val Ser Asp Ala Met Phe Ala Ser Gly Lys Leu Gly
515 520 525
Ser Gly Val Ala Ile Val Pro Thr Lys Gly Gln Leu Val Ser Pro Val
530 535 540
Ser Gly Lys Ile Val Val Ala Phe Pro Ser Gly His Ala Phe Ala Val
545 550 555 560
Arg Thr Lys Ala Glu Asp Gly Ser Asn Val Asp Ile Leu Met His Ile
565 570 575
Gly Phe Asp Thr Val Asn Leu Asn Gly Thr His Phe Asn Pro Leu Lys
580 585 590
Lys Gln Gly Asp Glu Val Lys Ala Gly Glu Leu Leu Cys Glu Phe Asp
595 600 605
Ile Asp Ala Ile Lys Ala Ala Gly Tyr Glu Val Thr Thr Pro Ile Val
610 615 620
Val Ser Asn Tyr Lys Lys Thr Gly Pro Val Asn Thr Tyr Gly Leu Gly
625 630 635 640
Glu Ile Glu Ala Gly Ala Asn Leu Leu Asn Val Ala Lys Lys Glu Ala
645 650 655
Val Pro Ala Thr Pro
660
<210> 64
<211> 661
<212> БЕЛОК
<213> Искусственная последовательность
<400> 64
Met Asp His Lys Asp Leu Ala Gln Arg Ile Leu Arg Asp Ile Gly Gly
1 5 10 15
Glu Asp Asn Ile Val Ala Ala Ala His Cys Ala Thr Arg Leu Arg Leu
20 25 30
Val Leu Lys Asp Thr Lys Asp Val Asp Arg Gln Ser Leu Asp Asp Asp
35 40 45
Pro Asp Leu Lys Gly Thr Phe Glu Thr Gly Gly Met Phe Gln Ile Ile
50 55 60
Val Gly Pro Gly Asp Val Asp His Val Phe Lys Glu Leu Asp Asp Ala
65 70 75 80
Thr Ser Lys Asp Ile Ala Val Ser Thr Glu Gln Leu Lys Asp Val Val
85 90 95
Ala Asn Asn Ala Asn Trp Phe Ser Arg Ala Val Lys Val Leu Ala Asp
100 105 110
Ile Phe Val Pro Leu Ile Pro Ile Leu Val Gly Gly Gly Leu Leu Met
115 120 125
Ala Ile Asn Asn Val Leu Val Ala Gln Asp Leu Phe Gly Pro Gln Ser
130 135 140
Leu Val Glu Met Phe Pro Gln Ile Ser Gly Val Ala Glu Met Ile Asn
145 150 155 160
Leu Thr Ala Ser Ala Pro Phe Ala Phe Leu Pro Val Leu Val Gly Phe
165 170 175
Thr Ala Thr Lys Arg Phe Gly Gly Asn Glu Phe Leu Gly Ala Gly Ile
180 185 190
Gly Met Ala Met Val Phe Pro Ser Leu Val Asn Gly Tyr Asp Val Ala
195 200 205
Ala Thr Met Ala Ala Gly Glu Met Pro Met Trp Ser Leu Phe Gly Leu
210 215 220
Asp Val Ala Gln Ala Gly Tyr Gln Gly Thr Val Leu Pro Val Leu Val
225 230 235 240
Val Ser Trp Ile Leu Ala Thr Ile Glu Lys Phe Leu His Lys Arg Leu
245 250 255
Lys Gly Thr Ala Asp Phe Leu Ile Thr Pro Val Leu Thr Leu Leu Leu
260 265 270
Thr Gly Phe Leu Thr Phe Ile Ala Ile Gly Pro Ala Met Arg Trp Val
275 280 285
Gly Asp Val Leu Ala His Gly Leu Gln Gly Leu Tyr Asp Phe Gly Gly
290 295 300
Pro Val Gly Gly Leu Leu Phe Gly Leu Val Tyr Ser Pro Ile Val Ile
305 310 315 320
Thr Gly Leu His Gln Ser Phe Pro Pro Ile Glu Leu Glu Leu Phe Asn
325 330 335
Gln Gly Gly Ser Phe Ile Phe Ala Thr Ala Ser Met Ala Asn Ile Ala
340 345 350
Gln Gly Ala Ala Cys Leu Ala Val Phe Phe Leu Ala Lys Ser Glu Lys
355 360 365
Leu Lys Gly Leu Ala Gly Ala Ser Gly Val Ser Ala Val Leu Gly Ile
370 375 380
Thr Glu Pro Ala Ile Phe Gly Val Asn Leu Arg Leu Arg Trp Pro Phe
385 390 395 400
Phe Ile Gly Ile Gly Thr Ala Ala Ile Gly Gly Ala Leu Ile Ala Leu
405 410 415
Phe Asn Ile Lys Ala Val Ala Leu Gly Ala Ala Gly Phe Leu Gly Val
420 425 430
Val Ser Ile Asp Ala Pro Asp Met Val Met Phe Leu Val Cys Ala Val
435 440 445
Val Thr Phe Phe Ile Ala Phe Gly Ala Ala Ile Ala Tyr Gly Leu Tyr
450 455 460
Leu Val Arg Arg Asn Gly Ser Ile Asp Pro Asp Ala Thr Ala Ala Pro
465 470 475 480
Val Pro Ala Gly Thr Thr Lys Ala Glu Ala Glu Ala Pro Ala Glu Phe
485 490 495
Ser Asn Asp Ser Thr Ile Ile Gln Ala Pro Leu Thr Gly Glu Ala Ile
500 505 510
Ala Leu Ser Ser Val Ser Asp Ala Met Phe Ala Ser Gly Lys Leu Gly
515 520 525
Ser Gly Val Ala Ile Val Pro Thr Lys Gly Gln Leu Val Ser Pro Val
530 535 540
Ser Gly Lys Ile Val Val Ala Phe Pro Ser Gly His Ala Phe Ala Val
545 550 555 560
Arg Thr Lys Ala Glu Asp Gly Ser Asn Val Asp Ile Leu Met His Ile
565 570 575
Gly Phe Asp Thr Val Asn Leu Asn Gly Thr His Phe Asn Pro Leu Lys
580 585 590
Lys Gln Gly Asp Glu Val Lys Ala Gly Glu Leu Leu Cys Glu Phe Asp
595 600 605
Ile Asp Ala Ile Lys Ala Ala Gly Tyr Glu Val Thr Thr Pro Ile Val
610 615 620
Val Ser Asn Tyr Lys Lys Thr Gly Pro Val Asn Thr Tyr Gly Leu Gly
625 630 635 640
Glu Ile Glu Ala Gly Ala Asn Leu Leu Asn Val Ala Lys Lys Glu Ala
645 650 655
Val Pro Ala Thr Pro
660
<210> 65
<211> 54
<212> ДНК
<213> Искусственная последовательность
<400> 65
cagtgccaag cttgcatgcc tgcaggtcga ctctaggaca cctgaagcac ctgc 54
<210> 66
<211> 28
<212> ДНК
<213> Искусственная последовательность
<400> 66
gagatgatca acctcacggc atctgcgc 28
<210> 67
<211> 28
<212> ДНК
<213> Искусственная последовательность
<400> 67
gcgcagatgc cgtgaggttg atcatctc 28
<210> 68
<211> 58
<212> ДНК
<213> Искусственная последовательность
<400> 68
cagctatgac catgattacg aattcgagct cggtacccga tggacaggtt tcattcgc 58
<210> 69
<211> 18
<212> ДНК
<213> Искусственная последовательность
<400> 69
ccacattggc atttcgcc 18
<210> 70
<211> 18
<212> ДНК
<213> Искусственная последовательность
<400> 70
cgctgattcc aatcttgg 18
<210> 71
<211> 55
<212> ДНК
<213> Искусственная последовательность
<400> 71
cagtgccaag cttgcatgcc tgcaggtcga ctctagaatg cgttctggac tgagg 55
<210> 72
<211> 40
<212> ДНК
<213> Искусственная последовательность
<400> 72
gtgactctac gcatctttga cagtgcaccg agaacagatg 40
<210> 73
<211> 40
<212> ДНК
<213> Искусственная последовательность
<400> 73
catctgttct cggtgcactg tcaaagatgc gtagagtcac 40
<210> 74
<211> 49
<212> ДНК
<213> Искусственная последовательность
<400> 74
cttgatttaa ttgcgccatc tgattctggg tctgtggatc gtggtggtg 49
<210> 75
<211> 49
<212> ДНК
<213> Искусственная последовательность
<400> 75
caccaccacg atccacagac ccagaatcag atggcgcaat taaatcaag 49
<210> 76
<211> 60
<212> ДНК
<213> Искусственная последовательность
<400> 76
cagctatgac catgattacg aattcgagct cggtacccgc tatgacacct tcaacggatc 60
<210> 77
<211> 19
<212> ДНК
<213> Искусственная последовательность
<400> 77
tccaaggaag atacacgcc 19
<210> 78
<211> 19
<212> ДНК
<213> Искусственная последовательность
<400> 78
gtggaaagat tgtggtggc 19
<210> 79
<211> 19
<212> ДНК
<213> Искусственная последовательность
<400> 79
catccagact ttggcgatc 19
<210> 80
<211> 18
<212> ДНК
<213> Искусственная последовательность
<400> 80
cgttggaatc ttgcgttg 18
<210> 81
<211> 58
<212> ДНК
<213> Искусственная последовательность
<400> 81
gcttgcatgc ctgcaggtcg actctagagg atcccctgtc aaagatgcgt agagtcac 58
<210> 82
<211> 54
<212> ДНК
<213> Искусственная последовательность
<400> 82
atcaggctga aaatcttctc tcatccgcca aaacgtctgt ggatcgtggt ggtg 54
<210> 83
<211> 55
<212> ДНК
<213> Искусственная последовательность
<400> 83
cagtgccaag cttgcatgcc tgcaggtcga ctctaggccg ttatcaatca agcgc 55
<210> 84
<211> 38
<212> ДНК
<213> Искусственная последовательность
<400> 84
cgccaaagtc tggatgatgg tggaaagatt gtggtggc 38
<210> 85
<211> 42
<212> ДНК
<213> Искусственная последовательность
<400> 85
gccaccacaa tctttccacc atcatccaga ctttggcgat cc 42
<210> 86
<211> 58
<212> ДНК
<213> Искусственная последовательность
<400> 86
cagctatgac catgattacg aattcgagct cggtacccgc agtaaacggt tctgatgc 58
<210> 87
<211> 22
<212> ДНК
<213> Искусственная последовательность
<400> 87
tgtcaaagat gcgtagagtc ac 22
<210> 88
<211> 18
<212> ДНК
<213> Искусственная последовательность
<400> 88
ggtttcattc gctttccg 18
<---
Изобретение относится к биотехнологии. Предложен микроорганизм, продуцирующий L-лизин, отличающийся тем, что указанный микроорганизм имеет точечную мутацию полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 3, приводящую к замене глутаминовой кислоты в положении 170 аминокислотной последовательности SEQ ID NO: 3 на лизин, и/или полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 63, приводящую к замене метионина в положении 162 аминокислотной последовательности SEQ ID NO: 63 на треонин. Также предложены полинуклеотид, оказывающий влияние на способность указанного микроорганизма продуцировать L-лизин, белок, оказывающий влияние на способность указанного микроорганизма продуцировать L-лизин, рекомбинантный экспрессионный вектор, содержащий указанный полинуклеотид, рекомбинантный микроорганизм для получения L-лизина, содержащий указанный полинуклеотид, а также способ получения L-лизина. Изобретение обеспечивает высокую продукцию L-лизина. 6 н. и 6 з.п. ф-лы, 15 табл., 3 пр.
1. Микроорганизм, продуцирующий L-лизин, отличающийся тем, что указанный микроорганизм имеет точечную мутацию полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 3, приводящую к замене глутаминовой кислоты в положении 170 аминокислотной последовательности SEQ ID NO: 3 на лизин, и/или полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 63, приводящую к замене метионина в положении 162 аминокислотной последовательности SEQ ID NO: 63 на треонин.
2. Микроорганизм по п. 1, отличающийся тем, что указанный микроорганизм имеет усиленную экспрессию полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 3, или усиленную экспрессию полинуклеотида, кодирующего аминокислотную последовательность SEQ ID NO: 63, по сравнению с немодифицированным микроорганизмом.
3. Микроорганизм по любому из пп. 1, 2, отличающийся тем, что полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 3, содержит нуклеотидную последовательность SEQ ID NO: 1; полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63, содержит нуклеотидную последовательность SEQ ID NO: 61.
4. Микроорганизм по любому из пп. 1-3, отличающийся тем, что полинуклеотидная последовательность с точечной мутацией образована посредством мутации основания в положении 508 полинуклеотидной последовательности, представленной SEQ ID NO: 1, с гуанина (G) на аденин (A); предпочтительно полинуклеотидная последовательность с точечной мутацией содержит полинуклеотидную последовательность, представленную SEQ ID NO: 2; и/или полинуклеотид с точечной мутацией образован посредством мутации основания в положении 485 полинуклеотидной последовательности, представленной SEQ ID NO: 61, с тимина (T) на цитозин (C); предпочтительно полинуклеотидная последовательность с точечной мутацией содержит полинуклеотидную последовательность, представленную SEQ ID NO: 62.
5. Микроорганизм по любому из пп. 1-4, отличающийся тем, что указанный микроорганизм представляет собой бактерию, в частности Corynebacterium glutamicum; предпочтительно YP97158 или ATCC 13869.
6. Полинуклеотид, оказывающий влияние на способность микроорганизма по п. 1 продуцировать L-лизин, содержащий полинуклеотидную последовательность, кодирующую аминокислотную последовательность, представленную SEQ ID NO: 3, где глутаминовая кислота в положении 170 заменена на лизин;
или содержащий полинуклеотидную последовательность, кодирующую аминокислотную последовательность, представленную SEQ ID NO: 63, где метионин в положении 162 заменен на треонин.
7. Полинуклеотид по п. 6, содержащий полинуклеотидную последовательность, кодирующую аминокислотную последовательность, представленную SEQ ID NO: 4; предпочтительно, указанная полинуклеотидная последовательность образована посредством мутации основания в положении 508 полинуклеотидной последовательности, представленной SEQ ID NO: 1, с гуанина (G) на аденин (A); предпочтительно, указанная полинуклеотидная последовательность содержит полинуклеотидную последовательность, представленную SEQ ID NO: 2.
8. Полинуклеотид по п. 6, содержащий полинуклеотидную последовательность, кодирующую аминокислотную последовательность, представленную SEQ ID NO: 64; предпочтительно, указанная полинуклеотидная последовательность образована посредством мутации основания в положении 485 полинуклеотидной последовательности, представленной SEQ ID NO: 61, c тимина (T) на цитозин (C); предпочтительно, указанная полинуклеотидная последовательность содержит полинуклеотидную последовательность, представленную SEQ ID NO: 62.
9. Белок, оказывающий влияние на способность микроорганизма по п. 1 продуцировать L-лизин, имеющий аминокислотную последовательность, представленную SEQ ID NO: 4 или SEQ ID NO: 64.
10. Рекомбинантный экспрессионный вектор, содержащий полинуклеотид по п. 6.
11. Рекомбинантный микроорганизм для получения L-лизина, содержащий полинуклеотид по п. 6.
12. Способ получения L-лизина, включающий: культивирование микроорганизма по любому из пп. 1-5 или рекомбинантного микроорганизма по п. 11 и выделение L-лизина из культуры.
| US 2005003494 A1, 06.01.2005 | |||
| Устройство для электромагнитного управления электрическими двигателями | 1930 |
|
SU25533A1 |
| Станок для шлифования топоров, ножей и т.п. изделий | 1926 |
|
SU13032A1 |
| Устройство для электромагнитного управления электрическими двигателями | 1930 |
|
SU25533A1 |
| Предохранитель для рук при работе на штамповальных прессах | 1924 |
|
SU1320A1 |
| Спускная труба при плотине | 0 |
|
SU77A1 |
| Найдено онлайн: | |||
Авторы
Даты
2024-12-04—Публикация
2021-01-04—Подача