ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к производному соединения, содержащему 6-7 бициклическое кольцо, и его применению. Соединение по настоящему изобретению можно эффективно использовать для профилактики или лечения заболеваний, вызванных протеинаргининметилтрансферазами 5 (PRMT5), за счет его действия как ингибитора PRMT5.
УРОВЕНЬ ТЕХНИКИ
PRMT (протеинаргининметилтрансферазы) представляют собой ферменты, которые переносят метильные группы на аргинин в белках-мишенях с использованием кофактора SAM (S-аденозилметионина). На сегодняшний день известно всего 9 изоформ PRMT (PRMT1-9), и они в основном делятся на 3 типа. Известно, что PRMT1, 2, 3, 4, 6 и 8, которые относятся к PRMT типа I, вызывают монометилирование и асимметричное диметилирование аргинина, и PRMT5 и PRMT9, принадлежащие к PRMT типа II, вызывают монометилирование и симметричное диметилирование аргинина. Между тем, PRMT7, который является PRMT типа III, в основном вызывает монометилирование аргинина. PRMT индуцирует метилирование различных субстратов, присутствующих в ядре и цитоплазме, тем самым регулируя важные биологические процессы в клетках, такие как клеточная пролиферация, дифференцировка и сплайсинг.
PRMT5 представляет собой основной фермент переноса метильной группы аргинина среди PRMT типа II. Он образует функциональный комплекс с метилосомным белком 50 (MEP50), вызывая метилирование белка-мишени. PRMT5 участвует в формировании лейкоза, лимфомы, глиобластомы, рака легких и рака молочной железы путем метилирования белков-мишеней, включая гистоновый белок в ядре и не гистоновый белок, такой как p53, NFκB, PI3K/AKT и CRAF. В частности, хорошо известно, что образование рака с помощью PRMT5 происходит при способствовании пролиферации, дифференциации, инвазии и миграции опухолевых клеток. Кроме того, согласно нескольким сообщениям, известно, что чем выше экспрессия PRMT5, тем хуже прогноз у онкологических больных. Наоборот, было замечено, что когда экспрессия PRMT5 ингибируется, пролиферация опухолевых клеток может быть подавлена.
Между тем, недавно сообщалось, что другие заболевания, помимо рака, также могут быть опосредованы PRMT5.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ПРОБЛЕМА
Задачей настоящего изобретения является предоставление нового соединения на основе 6-7 бициклического кольца, проявляющего превосходный ингибирующий эффект в отношении PRMT5, или его оптического изомера, стереоизомера или изотопного варианта, или его фармацевтически приемлемой соли.
Другой целью настоящего изобретения является предоставление фармацевтической композиции, содержащей указанное выше новое соединение на основе 6-7 бициклического кольца или его оптический изомер, стереоизомер или изотопный вариант, или его фармацевтически приемлемую соль в качестве активного ингредиента.
РЕШЕНИЕ ПРОБЛЕМЫ
Для решения вышеуказанной задачи настоящее изобретение предоставляет соединение, представленное следующей Формулой 1, или его оптический изомер, стереоизомер или изотопный вариант, или его фармацевтически приемлемую соль:
[Формула 1]
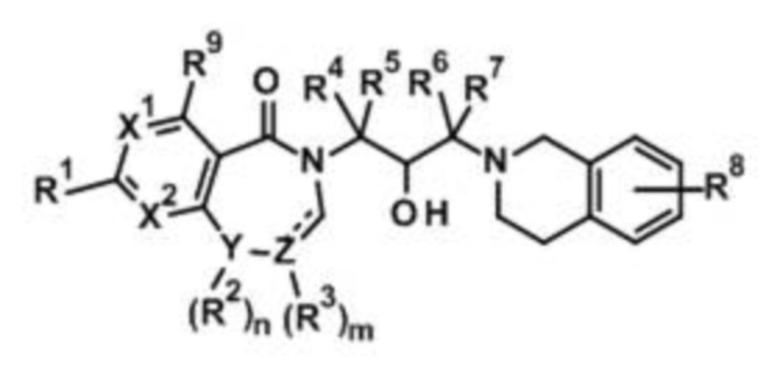
где
X1 и X2 каждый независимо представляет собой углерод или азот;
Y представляет собой углерод, кислород или азот;
Z представляет собой углерод;
n представляет собой целое число 0 или 1;
m представляет собой целое число 0-2;
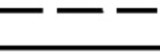 представляет собой одинарную связь или двойную связь;
представляет собой одинарную связь или двойную связь;
R1 представляет собой -D-R10; где D представляет собой прямую связь, -O-, -C(=O)-, -C≡C- или -CR11R12-; R10 представляет собой водород, галоген, гидрокси, циано, алкил, гидроксиалкил, галогеналкил, галогеналкилсульфонат, диалкиламино, алкиламиноалкил, диалкиламиноалкил, диалкиламинокарбонилалкил, насыщенный или ненасыщенный карбоциклил, насыщенный или ненасыщенный гетероциклил, насыщенный или ненасыщенный карбоциклил-алкил, или насыщенный или ненасыщенный гетероциклил-алкил; R11 и R12 каждый независимо представляет собой водород, гидрокси или алкил; карбоцикл или гетероцикл может быть замещен одним или несколькими заместителями, выбранными из гидрокси, галогена, оксо, формила (-CHO), нитрила, алкила, алкокси, гидроксиалкила, гидроксигалогеналкила, алкоксиалкила, галогеналкила, нитрилалкила, алкилкарбонила, алкилтиокарбонила, алкоксикарбонила, галогеналкилкарбонила, карбоциклила, карбоциклилкарбонила, (алкил)(галогеналкил)амино, (алкил)(гетероциклил)амино, гетероциклила и гетероциклил-алкила;
R2 представляет собой водород или алкил;
R3 представляет собой водород или алкил;
R4, R5, R6 и R7 каждый независимо представляет собой водород или алкил;
R8 представляет собой водород, галоген, алкил, алкокси или амино; и
R9 представляет собой водород, галоген или алкил.
Если не указано иное, термин «алкил», применяемый в настоящем документе, либо отдельно, либо в комбинации с дополнительными терминами (например, галогеналкил), относится к радикалу или насыщенной алифатической углеводородной группе, имеющей, например 1-7 атомов углерода в линейной или разветвленной цепи. Например, алкил может включать группы, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, 1-метилбутил, 2-метилбутил, 1-этилпропил и 1,2-диметилпропил, но не ограничен ими.
Если не указано иное, термин «алкокси», применяемый в настоящем документе, относится к алкилокси, имеющему, например 1-7 атомов углерода.
Если не указано иное, термин «галоген» применяемый в настоящем документе, либо отдельно, либо в комбинации с дополнительными терминами (например, галогеналкил), относится к радикалу фтора (F), хлора (Cl), брома (Br) или йода (I).
Если не указано иное, термин «галогеналкил» применяемый в настоящем документе относится к алкилу, такому, как определен выше, в котором один или несколько атомов водорода замещены одним или несколькими одинаковыми или разными атомами галогена. типовой галогеналкил может включать -CH2Cl, -CH2CF3, -CH2CCl3 или перфторалкил (например, -CF3).
Если не указано иное, термин «оксо» применяемый в настоящем документе относится к группе =O (то есть кислороду, имеющему двойную связь). Например, 1-оксо-этильная группа представляет собой ацетильную группу.
Если не указано иное, термин «гидроксиалкил» применяемый в настоящем документе относится к алкилу, в котором один или несколько атомов водорода замещены одной или несколькими гидрокси (-OH) группами. Например, он может включать атомы водорода, которые замещены 2 или 3 гидроксигруппами.
Если не указано иное, термин «насыщенный или ненасыщенный карбоциклил» применяемый в настоящем документе, относится к радикалу углеводорода, который не насыщен или частично или полностью насыщен, образуя одинарное или конденсированное циклическое кольцо, имеющее, например 3-24 атомов углерода. Более конкретно, карбоциклил может иметь 3-10 атомов углерода. Карбоцикл может включать мостиковую структуру или спиро структуру. Кроме того, ненасыщенный карбоцикл может включать ароматический углеводород, такой как арил.
Согласно одному варианту осуществления настоящего изобретения, карбоциклом может быть циклогексан, циклогексен, циклопропан, циклобутан или циклопентан, но не ограничен ими.
Если не указано иное, термин «насыщенный или ненасыщенный гетероциклил» применяемый в настоящем документе относится к 3-24-членному углеводороду, который не насыщен или частично или полностью насыщен, образуя одинарное или конденсированное циклическое кольцо, и имеет один или несколько гетероатомов, например 1-8 гетероатомов, выбранных из группы, состоящей из азота (N), кислорода (O) и серы (S). Более конкретно, гетероциклил может быть 4-10-членным углеводородом, имеющим 1-3 гетероатома. Гетероцикл может включать мостиковую структуру или сиро структуру. Кроме того, ненасыщенный гетероциклил может включать ароматический углеводород, такой как гетероарил.
Согласно одному варианту осуществления настоящего изобретения, гетероцикл может представлять собой тетрагидропиридин, дигидропиридин, пиперидин, дигидропиран, тетрагидропиран, пирролидин, 2-окса-6-азаспирогептан, азетидин, морфолин, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррол, пирролидин, оксазепан, 2-окса-5-азабицикло[2.2.1]гептан, пиридил, тетрагидрофуран, 8-азабицикло[3.2.1]октан, пиперазин, 2-азаспиро[3.3]гептан, 2-окса-7-азаспиро[3.4]октан, 2-азабицикло[2.2.1]гептан, 3-окса-8-азабицикло[3.2.1]октан, 3,4-дигидро-1H-пирроло[1,2-a]пиразин, 3,4,6,7,8,8a-гексагидро-1H-пирроло[1,2]-a]пиразин, пиримидин, пиразол, 2-окса-7-азаспиро[3.5]нонан или оксетан, но не ограничен ими.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, X1 и X2 каждый независимо представляет собой CH или N.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, Y представляет собой CH2, O или NH, если n равно 0; и Y представляет собой CH или N, если n равно 1.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, Z представляет собой CH2 или CH, если m равно 0; Z представляет собой CH или C, если m равно 1; и Z представляет собой C, если m равно 2.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, 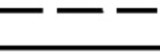 представляет собой одинарную связь или двойную связь.
представляет собой одинарную связь или двойную связь.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R1 представляет собой -D-R10; где D представляет собой прямую связь, -O-, -C(=O)-, -C≡C- или -CR11R12-.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R10 представляет собой водород, галоген, гидрокси, циано, C1-C7 алкил, гидрокси-C1-C7 алкил, галоген-C1-C7 алкил, галоген-C1-C7 алкилсульфонат, ди(C1-C7 алкил)амино, C1-C7 алкиламино-C1-C7 алкил, ди(C1-C7 алкил)амино-C1-C7 алкил, ди(C1-C7 алкил)аминокарбонил-C1-C7 алкил, насыщенный или ненасыщенный C3-C10 карбоциклил, насыщенный или ненасыщенный, 4-10-членный гетероциклил, насыщенный или ненасыщенный C3-C10 карбоциклил-C1-C7 алкил, или насыщенный или ненасыщенный, 4-10-членный гетероциклил-алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R11 и R12 каждый независимо представляет собой водород, гидрокси или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, оксо, формила, нитрила, C1-C7 алкила, C1-C7 алкокси, гидрокси-C1-C7 алкила, гидроксигалоген-C1-C7 алкила, C1-C7 алкокси-C1-C7 алкила, галоген-C1-C7 алкила, нитрил-C1-C7 алкила, C1-C7 алкилкарбонила, C1-C7 алкилтиокарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7 алкилкарбонила, насыщенного или ненасыщенного C3-C10 карбоциклила, насыщенного или ненасыщенного C3-C10 карбоциклилкарбонила, (C1-C7 алкил)(галоген-C1-C7 алкил)амино, (C1-C7 алкил)(насыщенный или ненасыщенный, 4-10-членным гетероциклил)амино, насыщенного или ненасыщенного, 4-10-членного гетероциклила и насыщенного или ненасыщенного, 4-10-членного гетероциклил-C1-C7 алкила.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R2 представляет собой водород или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R3 представляет собой водород или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R4, R5, R6 и R7 каждый независимо представляет собой водород или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R8 представляет собой водород, галоген, C1-C7 алкил, C1-C7 алкокси или амино.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R9 представляет собой водород, галоген или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, X1 и X2 каждый независимо представляет собой CH или N; Y представляет собой CH2, O или NH, если n равно 0; Y представляет собой CH или N, если n равно 1; Z представляет собой CH2 или CH, если m равно 0; Z представляет собой CH или C, если m равно 1; Z представляет собой C, если m равно 2; и 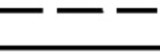 представляет собой одинарную связь или двойную связь.
представляет собой одинарную связь или двойную связь.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R1 представляет собой -D-R10; где D представляет собой прямую связь, -O-, -C(=O)-, -C≡C- или -CR11R12-; R10 представляет собой водород, галоген, гидрокси, циано, C1-C7 алкил, гидрокси-C1-C7 алкил, галоген-C1-C7 алкил, галоген-C1-C7 алкилсульфонат, ди(C1-C7 алкил)амино, C1-C7 алкиламино-C1-C7 алкил, ди(C1-C7 алкил)амино-C1-C7 алкил, ди(C1-C7 алкил)аминокарбонил-C1-C7 алкил, насыщенный или ненасыщенный C3-C10 карбоциклил, насыщенный или ненасыщенный, 4-10-членный гетероциклил, насыщенный или ненасыщенный C3-C10 карбоциклил-C1-C7 алкил, или насыщенный или ненасыщенный, 4-10-членный гетероциклил-алкил; и R11 и R12 каждый независимо представляет собой водород, гидрокси или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R10 представляет собой галоген, C1-C7 алкил, гидрокси-C1-C7 алкил, галоген-C1-C7 алкил, насыщенный или ненасыщенный C3-C10 карбоциклил, насыщенный или ненасыщенный, 4-10-членный гетероциклил, или насыщенный или ненасыщенный, 4-10-членный гетероциклил-алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, оксо, формила, нитрила, C1-C7 алкила, C1-C7 алкокси, гидрокси-C1-C7 алкила, гидроксигалоген-C1-C7 алкила, C1-C7 алкокси-C1-C7 алкила, галоген-C1-C7 алкила, нитрил-C1-C7 алкила, C1-C7 алкилкарбонила, C1-C7 алкилтиокарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7 алкилкарбонила, насыщенного или ненасыщенного C3-C10 карбоциклила, насыщенного или ненасыщенного C3-C10 карбоциклилкарбонила, (C1-C7 алкил)(галоген-C1-C7 алкил)амино, (C1-C7 алкил)(насыщенный или ненасыщенный, 4-10-членный гетероциклил)амино, насыщенный или ненасыщенный, 4-10-членного гетероциклила и насыщенного или ненасыщенного, 4-10-членного гетероциклил-C1-C7 алкила.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, формила, C1-C7 алкила, гидрокси-C1-C7 алкила, C1-C7 алкокси-C1-C7 алкила, галоген-C1-C7 алкила, C1-C7 алкилкарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7 алкилкарбонила, насыщенного или ненасыщенного C3-C10 карбоциклила, насыщенного или ненасыщенного C3-C10 карбоциклилкарбонила, (C1-C7 алкил)(галоген-C1-C7 алкил)амино, (C1-C7 алкил)(насыщенный или ненасыщенный, 4-10-членный гетероциклил)амино и насыщенного или ненасыщенного, 4-10-членного гетероциклил-C1-C7 алкила.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, гетероцикл может быть замещен 1 или 2 заместителями, выбранными из гидрокси, галогена, формила, C1-C7 алкила, гидрокси-C1-C7 алкила, C1-C7 алкокси-C1-C7 алкила, галоген-C1-C7 алкила, C1-C7 алкилкарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7 алкилкарбонила, насыщенного или ненасыщенного C3-C10 карбоциклила, насыщенного или ненасыщенного C3-C10 карбоциклилкарбонила и насыщенного или ненасыщенного, 4-10-членного гетероциклил-C1-C7 алкила.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, карбоцикл может быть замещен 1 или 2 заместителями, выбранными из галоген-C1-C7 алкила, (C1-C7 алкил)(галоген-C1-C7 алкил)амино и (C1-C7 алкил)(насыщенный или ненасыщенный, 4-10-членный гетероциклил)амино.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R1 представляет собой -D-R10; где D представляет собой прямую связь; R10 представляет собой водород, галоген, циано, C1-C7 алкил, галоген-C1-C7 алкил, ди(C1-C7 алкил)амино-C1-C7 алкил, насыщенный или ненасыщенный, 4-10-членный гетероциклил, насыщенный или ненасыщенный C3-C10 карбоциклил, или насыщенный или ненасыщенный, 4-10-членный гетероциклил-алкил; и гетероцикл может быть замещен 1 или 2 заместителями, выбранными из гидрокси, галоген, формила, C1-C7 алкила, C1-C7 алкокси, гидрокси-C1-C7 алкила, галоген-C1-C7 алкила, нитрил-C1-C7 алкила, C1-C7 алкилкарбонила, C1-C7 алкокси-C1-C7 алкила, C1-C7 алкоксикарбонила, галоген-C1-C7 алкилкарбонила, и насыщенного или ненасыщенного, 4-10-членного гетероциклила.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, R2 представляет собой водород или C1-C7 алкил; R3 представляет собой водород или C1-C7 алкил; R4, R5, R6 и R7 каждый независимо представляет собой водород или C1-C7 алкил; R8 представляет собой водород, галоген, C1-C7 алкил, C1-C7 алкокси или амино; и R9 представляет собой водород, галоген или C1-C7 алкил.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, 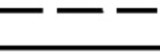 представляет собой одинарную связь.
представляет собой одинарную связь.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, гетероцикл представляет собой насыщенный или ненасыщенный, 4-8-членный углеводород, имеющий 1 или 2 гетероатома, выбранных из N и O.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, гетероцикл выбран из группы, состоящей из тетрагидропиридина, дигидропиридина, пиперидина, дигидропирана, тетрагидропирана, пирролидина, 2-окса-6-азаспирогептана, азетидина, морфолина, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррола, оксазепана, 2-окса-5-азабицикло[2.2.1]гептана, пиридила, тетрагидрофурана, 8-азабицикло[3.2.1]октана, пиперазина, 2-азаспиро[3.3]гептана, 2-окса-7-азаспиро[3.4]октана, 2-азабицикло[2.2.1]гептана, 3-окса-8-азабицикло[3.2.1]октана, 3,4-дигидро-1H-пирроло[1,2-a]пиразина, 3,4,6,7,8,8a-гексагидро-1H-пирроло[1,2]-a]пиразина, пиримидина, пиразола, 2-окса-7-азаспиро[3.5]нонана и оксетана.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, гетероцикл выбран из группы, состоящей из тетрагидропиридина, дигидропиридина, пиперидина, тетрагидропирана, пирролидина, 2-окса-6-азаспирогептана, азетидина, морфолина, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррола, пиридила, 8-азабицикло[3.2.1]октана, пиперазина, 2-азаспиро[3.3]гептана, пиразола и оксетана.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, карбоцикл выбран из группы, состоящей из циклогексана, циклогексена, циклопропана, циклобутана и циклопентана.
Согласно одному варианту осуществления настоящего изобретения, в указанной выше формуле 1, D представляет собой прямую связь, -O-, -C(=O)- или -C≡C-; R10 представляет собой галоген, C1-C7 алкил, гидрокси-C1-C7 алкил, галоген-C1-C7 алкил, насыщенный или ненасыщенный C3-C10 карбоциклил, насыщенный или ненасыщенный, 4-10-членный гетероциклил, или насыщенный или ненасыщенный, 4-10-членный гетероциклил-алкил; карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, формила, C1-C7 алкила, гидрокси-C1-C7 алкила, C1-C7 алкокси-C1-C7 алкила, галоген-C1-C7 алкила, C1-C7 алкилкарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7 алкилкарбонила, насыщенного или ненасыщенного C3-C10 карбоциклила, насыщенного или ненасыщенного C3-C10 карбоциклилкарбонила, (C1-C7 алкил)(галоген-C1-C7 алкил)амино, (C1-C7 алкил)(насыщенный или ненасыщенный, 4-10-членным гетероциклил)амино, и насыщенного или ненасыщенного, 4-10-членного гетероциклил-C1-C7 алкила; гетероцикл выбран из группы, состоящей из тетрагидропиридина, дигидропиридина, пиперидина, тетрагидропирана, пирролидина, 2-окса-6-азаспирогептана, азетидина, морфолина, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррола, пиридила, 8-азабицикло[3.2.1]октана, пиперазина, 2-азаспиро[3.3]гептана, пиразола и оксетана; и карбоцикл выбран из группы, состоящей из циклогексана, циклогексена и циклопропана.
Типовые примеры соединения формулы 1 в соответствии с настоящим изобретением могут включать соединения, показанные в таблице 1, н не ограничены ими.
[Таблица 1]
Поскольку соединения по настоящему изобретению могут иметь асимметричный углеродный центр и асимметричную ось или асимметричную плоскость, они могут существовать в виде по существу чистых энантиомеров, таких как R и S энантиомеры, а также во всех оптических и стереоизомерных формах, включая смеси рацематов, и все их изомеры и соединения входят в объем настоящего изобретения. В отношении чистого энантиомера, энантиомерный избыток такого энантиомера и его фармацевтически приемлемой соли, представленных формулой 1, может предпочтительно составлять 60% эи или более, более предпочтительно, 95% эи или более, и наиболее предпочтительно, 98% эи или более.
Термин «эи» относится к энантиомерному избытку. Например, один энантиомер в конкретном соединении присутствует в виде смеси энантиомеров в соединении в большем количестве, чем другие энантиомеры. Энантиомерно обогащенные формы могут включать энантиомерные соединения конкретного соединения, в которых концентрация отдельного энантиомера в энантиомерной смеси конкретного соединения составляет, по меньшей мере, 50%, чаще, по меньшей мере, 60%, 70%, 80% или 90% или более (например, >95%, >97%, >98%, >99%, >99,5%) по отношению к другим энантиомерам соединения.
В настоящем документе, если не указано иное, соединение, представленное формулой 1, используется в значении, включающем все соединения, представленные формулой 1, их оптический изомер, стереоизомер, изотопный вариант, и его фармацевтически приемлемую соль.
В настоящем документе термин «изотопный вариант» относится к соединению, которое содержит не существующие в природе пропорции изотопов в одном или нескольких атомах, составляющих такое соединение. Например, изотопный вариант соединения может быть радиомеченным; атом водорода может быть выбран из водорода, дейтерия и трития и могут содержать углерод-13 (13C), азот-15 (15N) или подобные.
Соединение формулы 1 или его оптический изомер, стереоизомер или изотопный вариант по настоящему изобретению может образовывать фармацевтически приемлемую соль. Фармацевтически приемлемые соли включают кислотно- или основно-аддитивные соли и формы их стереохимических изомеров. Соль может включать любую соль, которая поддерживает активность исходного соединения у субъекта, которому его вводят, и не вызывает нежелательного эффекта, но не ограничена ими. Соли включают неорганические соли и органические соли и могут быть кислотно-аддитивными солями, например, солями уксусной кислоты, азотной кислоты, аспарагиновой кислоты, сульфоновой кислоты, серной кислоты, малеиновой кислоты, глутаминовой кислоты, муравьиной кислоты, янтарной кислоты, фосфорной кислоты, фталевой кислоты, дубильной кислоты, винной кислоты, бромистоводородной кислоты, пропионовой кислоты, бензолсульфоновой кислоты, бензойной кислоты, стеариновой кислоты, этансульфоновой кислоты, молочной кислоты, бикарбоновой кислоты, бисерной кислоты, бивинной кислоты, щавелевой кислоты, бутиловой кислоты, эдатата кальция, камсиловой кислоты, карбоновой кислоты, хлорбензойной кислоты, лимонной кислоты, эдетовой кислоты, толуолсульфоновой кислоты, эдицилиновой кислоты, эцилиновой кислоты, фумаровой кислоты, глюцептовой кислоты, памовой кислоты, глюконовой кислоты, гликолларсаниловой кислоты, нитрата метила, полигалактуроновой кислоты, гексилизорциновой кислоты, малоновой кислоты, гидрабаминовой кислоты, хлористоводородной кислоты, йодистоводородной кислоты, гидроксинафтоловой кислоты, изетионовой кислоты, лактобионовой кислоты, миндальной кислоты, эстолиновой кислоты, слизевой кислоты, нафтеновой кислоты, муконовой кислоты, п-нитрометансульфоновой кислоты, гексаминовой кислоты, пантотеновой кислоты, моногидрофосфорной кислоты, дигидрофосфорной кислоты, салициловой кислоты, сульфаминовой кислоты, сульфаниловой кислоты, метансульфоновой кислоты или теоклиновой кислоты. Кроме того, примеры основных солей включают соли щелочных и щелочноземельных металлов, такие как соли аммония, соли лития, соли натрия, соли калия, соли магния и соли кальция, соли, содержащие органические основания, такие как бензатин, N-метил-D-глюкамин, и соли гидрабамина, и соли, содержащие аминокислоты, такие как аргинин и лизин. Кроме того, форма соли может быть преобразована в свободную форму путем обработки соответствующим основанием или кислотой. Используемый в настоящем документе термин «аддитивная соль» может включать сольваты, получаемые из любого соединения, представленного формулой 1, и его соли. Примерами этих сольватов являются гидраты или алкоголяты.
Термины и сокращения, используемые в настоящем описании, имеют свои первоначальные значения, если не указано иное.
Настоящее изобретение также относится к способу получения соединения формулы 1. Далее, способ получения соединения формулы 1 будет описан на основе типовой схемы реакции для лучшего понимания настоящего изобретения. Однако следует понимать, что специалисты в данной области техники могут получить соединение формулы 1 различными способами с использованием известных соединений, основанных на структуре формулы 1, или соединений, которые могут быть легко получены из нее, и следует понимать, что все способы могут быть включены в объем настоящего изобретения, то есть соединение формулы 1 может быть получено произвольным комбинированием нескольких способов синтеза, описанных в настоящем описании или описанных в известном уровне техники, и, таким образом, последующее описание, относящееся к способу получения соединения формулы 1, является только иллюстративным, и, при необходимости, порядок стандартных операций может быть выборочно изменен, и объем способа получения настоящего изобретения этим не ограничивается.
[Схема реакции 1]
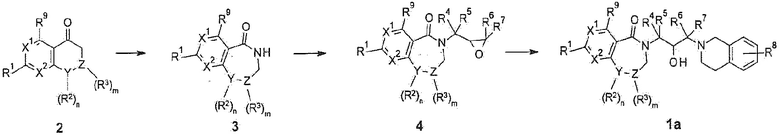
В общем способе синтеза, промежуточное соединение 3 может быть получено из исходного материала 2 по реакции Шмидта с использованием азида натрия в кислых условиях. Из этого соединения, промежуточное соединение 4, в которое введен оксиран, получают реакцией замещения, и конечное соединение 1а может быть получено реакцией присоединения тетрагидроизохинолина.
[Схема реакции 2]
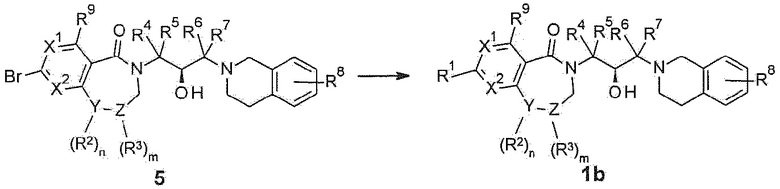
В качестве другого способа синтеза конечного соединения 1b, в котором алкильные и алкенильные группы замещены, может быть получено реакцией сочетания Сузуки в условиях палладия с использованием соединения 5 в качестве исходного материала.
[Схема реакции 3]
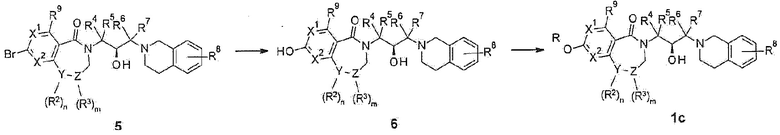
В еще одном способе синтеза, как на схеме 3, соединение 5 используют в качестве исходного материала, и получают промежуточное соединение 6, полученное путем замещения группы брома гидроксильной группой с использованием гидроксида калия в условиях палладия, и затем может быть получено конечное соединение 1c, в котором эфирная группа была замещена в реакции замещения.
В соответствии с другим аспектом настоящего изобретения представлена фармацевтическая композиция для профилактики или лечения заболевания, связанного с ингибированием PRMT5, содержащая терапевтически эффективное количество соединения или его оптического изомера, стереоизомера или изотопного варианта, или фармацевтически приемлемую соль, в качестве активного ингредиента, вместе с фармацевтически приемлемым носителем. Кроме того, пролекарства, имеющие различные формы, которые при желании превращаются в соединение формулы 1 in vivo, также входят в объем настоящего изобретения. Фармацевтическая композиция может дополнительно включать одну или несколько добавок, выбранных из группы, состоящей из фармацевтически приемлемого носителя, разбавителя и адъюванта.
Используемый в настоящем документе термин «лечение» относится к прерыванию, задержке или прекращению прогрессирования заболевания при применении у субъекта, имеющего симптом.
Используемый в настоящем документе термин «профилактика» относится к уменьшению возможности заболевания или устранению возможности заболевания.
Используемый в настоящем документе термин «фармацевтическая композиция» может включать другие химические компоненты, такие как носители, разбавители, эксципиенты и подобные, в дополнение к активным соединениям по настоящему изобретению. Соответственно, фармацевтическая композиция может включать фармацевтически приемлемый носитель, разбавитель, эксципиент или их комбинацию, если необходимо. Фармацевтическая композиция облегчает введение активного соединения в организм. Известно множество методов введения фармацевтических композиций, содержащих соединение, в которых методы включают пероральное, парентеральное и местное введение, но не ограничивается ими. Кроме того, фармацевтическая композиция может быть стерилизована, может дополнительно включать адъювант, такой как консервант, стабилизатор, ускоритель гидратации или эмульгирования, соль для регулирования осмотического давления и/или буфер, может дополнительно включать другие терапевтически полезные вещества, и может быть составлена в соответствии с обычными способами смешивания, гранулирования или нанесения покрытия.
Используемый в настоящем документе термин «носитель» относится к соединению, которое облегчает введение соединения в клетку или ткань. Например, диметилсульфоксид (ДМСО) является обычным носителем для легкого введения большого количества органических соединений в клетки или ткани организма.
Используемый в настоящем документе термин «разбавитель» относится к соединению, которое стабилизирует биологически активную форму представляющего интерес соединения, и разбавляется водой, которая растворяет соединение. Растворенная в буфере соль используется в качестве разбавителя в данной области техники. Обычно используемый буфер представляет собой фосфатно-солевой буфер, который имитирует солевую форму раствора человеческого организма. Поскольку буферная соль способна контролировать рН раствора при низких концентрациях, буферный разбавитель редко модифицируют биологическую активность соединения.
Используемый в настоящем документе термин «фармацевтически приемлемый» относится к свойству, не нарушающему биологическую активность и физические свойства соединения.
Кроме того, фармацевтическая композиция может представлять собой композицию для профилактики и/или лечения заболеваний, связанных с ингибированием PRMT5. Заболевания, связанные с ингибированием PRMT5, могут представлять собой, например, рак, заболевание крови, аутоиммунное заболевание, воспалительное заболевание или нейродегенеративное заболевание, и может включать любое заболевание, о котором известно, что оно связано с PRMT5.
Рак включает, но не ограничен ими, невриному слухового нерва, аденокарциному, рак надпочечников, рак анального канала, ангиосаркому, доброкачественную моноклональную гаммаглобулинопатию, холангиокарциному, рак мочевого пузыря, рак молочной железы, рак головного мозга, лимфому, множественную миелому, опухоль слезной железы, рак бронхов, рак шейки матки, краниофарингиома, колоректальный рак, эпителиальную карциному, эпителиально-клеточную опухоль, эндотелиальную саркому, рак эндометрия, рак пищевода, аденокарциному Барретта, саркому Юинга, рак глаза, рак желчного пузыря, рак желудка, гастроинтестинальную стромальную опухоль (GIST), рак головы и шеи, рак ротовой полости (плоскоклеточный рак ротовой полости, OSCC), рак горла, гемопоэтический рак, гемангиобластому, воспалительную миофибробластную опухоль, амилоидоз иммунных клеток, рак почки, рак печени, рак легкого, миелодиспластический синдром (MDS), мезотелиому, миелопролиферативное заболевание (MPD), хронический идиопатический миелофиброз, хронический миелогенный лейкоз (CML), хронический нейтрофильный лейкоз (CNL), нейробластому, нейрофиброму, нейроэндокринный рак, остеосаркому, рак яичников, папиллярную аденокарциному, рак поджелудочной железы, рак полового члена, рак предстательной железы, рак прямой кишки, рабдомиосаркому, рак слюнных желез, рак кожи, рак тонкой кишки, саркому мягких тканей, рак щитовидной железы, рак уретры, рак влагалища и рак вульвы. Рак головного мозга может включать, но не ограничен ими, менингиому, глиому, медуллобластому, глиобластому и рак с метастазами в головной мозг.
Заболевание крови может представлять собой гемоглобинемию или серповидноклеточную анемию, но не ограничен ими.
Аутоиммунное заболевание может включать, но не ограничено ими, ревматоидный артрит, артрит позвоночника, подагрический артрит, дегенеративное заболевание суставов, остеоартрит, системную красную волчанку, рассеянный склероз, псориатический артрит, ювенильный артрит, астму, атеросклероз, остеопороз, бронхит, тендинит, псориаз, экзему, ожоги, дерматит, зуд, энурез, эозинофильную болезнь, пептическую язву, локализованный энтерит, дивертикулит, желудочно-кишечное кровотечение, эозинофильный эзофагит, эозинофильный гастрит, эозинофильный гастроэнтерит и эозинофильный колит.
Воспалительное заболевание может включать, но не ограничено ими, воспаление, связанное с акне, апластическую анемию, гемолитическую аутоиммунную анемию, ринит, астму, полиартериит, височный артериит, узелковый периартериит, артериит Такаясу, кристаллический артрит, остеоартрит, псориатический артрит, подагрический артрит, реактивный артрит, ревматоидный артрит, боковой амиотрофический склероз, аутоиммунное заболевание, аллергию или аллергическую реакцию, атеросклероз, бронхит, бурсит, хронический простатит, конъюнктивит, хроническая обструктивная болезнь легких, дерматит, диабет I типа, диабет 2 типа, псориаз, экзему, реакцию гиперчувствительности к экземе, ожог, дерматит, зуд, эндометриоз, инфекцию, ишемическую болезнь сердца, гломерулонефрит, гингивит, чувствительность, мигрень, головную боль напряжения, послеоперационную непроходимость кишечника, непроходимость кишечника при сепсисе, идиопатическую тромбоцитопеническую пурпуру, болевой синдром в мочевом пузыре, пептическую язву, локализованный энтерит, дивертикулит, желудочное кровотечение, эозинофильный эзофагит, эозинофильный гастрит, эозинофильный гастроэнтерит, эозинофильный колит, гастрит, диарею, гастроэзофагеальную рефлюксную болезнь, болезнь Крона, язвенный колит, коллагенозный колит, лимфоцитарный колит, ишемический колит, колит при шунтировании, синдром Бехчета, неопределенный колит, синдром воспаленного кишечника (IBS), волчанку, экхимозы, миастению гравис и ишемию миокарда.
Нейродегенеративное заболевание может включать, но не ограничено ими, заболевание двигательных нейронов, болезнь Пика, болезнь Альцгеймера, деменцию, связанную со СПИД, болезнь Паркинсона, боковой амиотрофический склероз, пигментацию сетчатки, спинальную мышечную атрофию и дегенерацию мозжечка.
Фармацевтическая композиция может быть составлена в виде различных дозированных форм для перорального или парентерального введения. Например, фармацевтическая композиция может быть составлена в виде любой дозированной формы для перорального введения, такой как таблетки, пилюли, твердые/мягкие капсулы, растворы, суспензии, эмульгаторы, сиропы, гранулы или эликсиры. Состав для перорального введения может включать, например, фармацевтически приемлемый носитель, такой как разбавитель, такой как лактоза, декстроза, сахароза, маннит, сорбит, целлюлоза и/или глицин, или смазывающий агент, такой как диоксид кремния, тальк, стеариновая кислота, магниевая или кальциевая соль, и/или полиэтиленгликоль, в дополнение к активному ингредиенту, в соответствии с типовой конфигурацией каждого состава.
Кроме того, когда состав для перорального введения представляет собой таблетку, состав может включать связующий агент, такой как алюмосиликат магния, крахмальная паста, желатин, трагакант, метилцеллюлоза, карбоксиметилцеллюлоза натрия и/или поливинилпирролидин, и, необязательно, может включать разрыхлитель, такой как крахмал, агар, альгиновая кислота или ее натриевая соль, кипящая смесь и/или абсорбент, краситель, ароматизатор или подсластитель.
Когда фармацевтическую композицию составляют в виде парентеральной дозированной формы, фармацевтическую композицию можно вводить парентеральным способом введения, таким как подкожная инъекция, внутривенная инъекция, внутримышечная инъекция или интраторакальная инъекция. Фармацевтическая композиция может быть приготовлена в виде раствора или суспензии путем смешивания активного ингредиента, т. е. соединения формулы 1, или его оптического изомера, стереоизомера или изотопного варианта, или его фармацевтически приемлемой соли, со стабилизатором или буфером в воде, и раствор или суспензия может быть приготовлена в виде стандартной дозированной формы ампулы или флакона.
Кроме того, фармацевтическая композиция может быть стерилизована или дополнительно содержать адъюванты, такие как консерванты, стабилизаторы, гидратирующие агенты или ускорители эмульгирования, соли и/или буферы для контроля осмотического давления или другие терапевтически полезные агенты, и может быть составлена в соответствии с обычным способом смешивания, гранулирования или нанесения покрытия.
Активный ингредиент, т.е. соединение формулы 1 или его оптический изомер, стереоизомер или изотопный вариант, или его фармацевтически приемлемая соль, может быть включен в фармацевтическую композицию в эффективном количестве от 0,1 до 500 мг/кг ( массы тела), предпочтительно, от 0,5 до 100 мг/кг (массы тела) в сутки, в отношении млекопитающих, включая человека, и фармацевтическая композиция может быть разделена один или два раза в сутки и введена пероральным или парентеральным путем.
ПРЕИМУЩЕСТВА ИЗОБРЕТЕНИЯ
В соответствии с настоящим изобретением, представлены соединения на основе 6-7 бициклического кольца, которые оказывают превосходное ингибирующее действие на PRMT5, или их оптические изомеры, стереоизомеры или изотопные варианты, или их фармацевтически приемлемые соли. Следовательно, такие соединения или их оптические изомеры, стереоизомеры или изотопные варианты, или их фармацевтически приемлемые соли можно эффективно применять для профилактики или лечения заболеваний, связанных с ингибированием PRMT5, таких как рак, заболевания крови, аутоиммунные заболевания, воспалительные заболевания или нейродегенеративные заболевания.
Кроме того, соединения по настоящему изобретению, или их оптические изомеры, стереоизомеры или изотопные варианты, или их фармацевтически приемлемые соли могут обладать улучшенной проницаемостью гематоэнцефалического барьера, превосходной эффективностью или улучшенными фармакокинетическими свойствами.
ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение поясняется более подробно с помощью следующих примеров. Однако следует понимать, что объем охраны настоящего изобретения не ограничивается этими примерами.
Пример 1: Синтез 4-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-метокси-2,3-дигидро-1,4-бензоксазепин-5-она
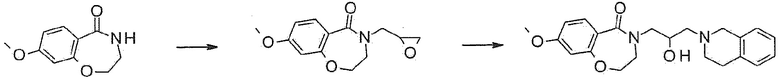
Пример 1-1: Синтез 8-метокси-4-(оксиран-2-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
8-Метокси-3,4-дигидро-2H-1,4-бензоксазепин-5-он (97 мг, 0,5 ммоль) растворяют в диметилформамиде, и туда добавляют 60% гидрид натрия (30 мг, 0,75 ммоль) на ледяной бане. После перемешивания реакционного раствора при 0°C в течение 30 минут, туда медленно добавляют эпибромгидрин (0,056 мл, 0,65 ммоль), и смесь перемешивают при комнатной температуре в течение 2 часов. Реакцию останавливает добавлением метанола. После добавления этилацетата, реакционную смесь промывают насыщенным водным раствором хлорида аммония, и насыщенным водным раствором хлорида натрия, и органический слой сушат над безводным сульфатом магния. Растворитель удаляют выпариванием при пониженном давлении, и полученное соединение используют в следующей реакции без дальнейшей очистки.
Пример 1-2: Синтез 4-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-метокси-2,3-дигидро-1,4-бензоксазепин-5-она
Исходный материал, полученный в примере 1-1 растворяют в 3 мл изопропанола, и туда добавляют тетрагидроизохинолин (0,06 мл, 0,5 ммоль) и перемешивают при 80°C в течение 12 часов. Температуру понижают до комнатной температуры, и маслянистую жидкость, полученную концентрированием растворителя очищают флэш-хроматографией с получением прозрачного и липкого твердого соединения. ЯМР данные для полученного указанного в заголовке соединения следующие:
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,20-7,00 (м, 4H), 6,75 (дд, J=8,8, 2,5 Гц, 1H), 6,58 (д, J=2,5 Гц, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,23 (кв, J=8,2, 6,4 Гц, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,84 (с, 3H), 3,81-3,68 (м, 4H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 2,97-2,85 (м, 4H), 2,69-2,60 (м, 2H).
Пример 2: Синтез 2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-метокси-4,5-дигидро-3H-2-бензазепин-1-она
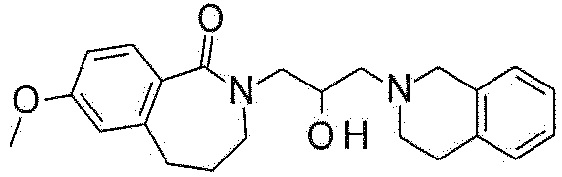
7-Метокси-2,3,4,5-тетрагидро-2-бензазепин-1-он используют в качестве исходного материала по методике примера 1 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,42 (д, J=8,5 Гц, 1H), 6,99 (дд, J=20,3, 3,4 Гц, 4H), 6,78 (дд, J=8,7, 2,6 Гц, 1H), 6,69 (д, J=2,5 Гц, 1H), 4,17-4,08 (м, 1H), 3,79 (дд, J=13,9, 3,8 Гц, 1H), 3,73 (с, 3H), 3,71 (с, 2H), 3,35-3,23 (м, 3H), 2,88-2,79 (м, 4H), 2,68 (т, J=7,1 Гц, 2H), 2,64-2,52 (м, 2H), 2,02 (п, J=7,0 Гц, 2H).
Пример 3: Синтез 2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-гидрокси-4,5-дигидро-3H-2-бензазепин-1-она
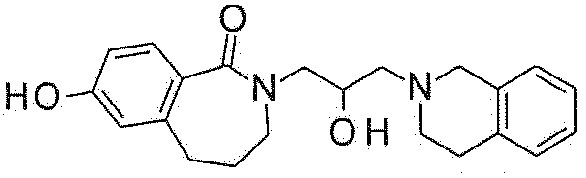
(1-Оксо-2,3,4,5-тетрагидро-2-бензазепин-7-ил) ацетат используют в качестве исходного материала по методике примера 1 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,56 (д, J=8,5 Гц, 1H), 7,15-7,02 (м, 4H), 6,97 (дд, J=9,0, 1,9 Гц, 1H), 6,90 (д, J=2,0 Гц, 1H), 4,32-4,22 (м, 1H), 4,14 (дд, J=9,9, 4,1 Гц, 1H), 4,05 (дд, J=9,8, 6,0 Гц, 1H), 3,78 (с, 2H), 3,07 (т, J=6,5 Гц, 2H), 2,98-2,86 (м, 4H), 2,86-2,78 (м, 3H), 2,73 (дд, J=13,1, 7,5 Гц, 1H), 2,09-1,97 (м, 2H).
Пример 4: Синтез 2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-(трифторметокси)-4,5-дигидро-3H-2-бензазепин-1-она
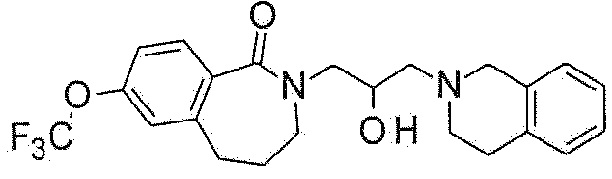
6-(Трифторметокси)тетралин-1-он используют в качестве исходного материала по методике примера 1 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,4 Гц, 1H), 7,21 (дд, J=8,5, 2,3 Гц, 1H), 7,13 (д, J=2,4 Гц, 1H), 7,10-6,96 (м, 4H), 4,23-4,13 (м, 1H), 3,88 (дд, J=13,8, 3,6 Гц, 1H), 3,70 (с, 2H), 3,41-3,29 (м, 2H), 3,30-3,20 (м, 1H), 2,92-2,84 (м, 2H), 2,84-2,73 (м, 4H), 2,64-2,52 (м, 2H), 2,15-2,04 (м, 2H).
Пример 5: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(трифторметил)-2,3-дигидро-1,4-бензоксазепин-5-она
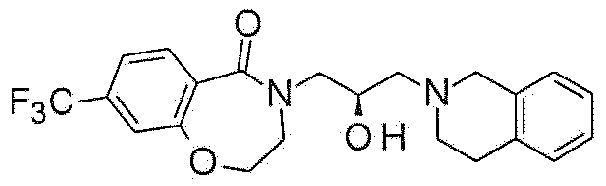
Указанное в заголовке соединение синтезируют по методике примера 1, за исключением того, что 7-(трифторметил)хроман-4-он используют в качестве исходного материала и (R)-(-)-глицидилнозилат используют вместо эпибромгидрина в Примере 1-1.
1H ЯМР (400 MГц, Метанол-d4) δ 7,90 (д, J=8,2 Гц, 1H), 7,48 (д, J=8,2 Гц, 1H), 7,36 (с, 1H), 7,16-7,03 (м, 4H), 4,56 (т, J=5,1 Гц, 2H), 4,25-4,22 (м, 1H), 4,02 (дд, J=13,9, 3,5 Гц, 1H), 3,76-3,74 (с, 4H), 3,47 (дд, J=14,0, 8,0 Гц, 1H), 2,99-2,83 (м, 4H), 2,73-2,60 (м, 2H).
Пример 6: Синтез 2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-(трифторметокси)-4,5-дигидро-3H-2-бензазепин-1-она
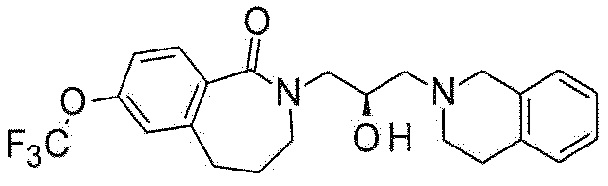
7-(Трифторметокси)-2,3,4,5-тетрагидро-2-бензазепин-1-он используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,5 Гц, 1H), 7,27 (д, J=8,6 Гц, 1H), 7,20 (д, J=2,3 Гц, 1H), 7,16-7,02 (м, 4H), 4,29-4,20 (м, 1H), 3,94 (дд, J=13,8, 3,6 Гц, 1H), 3,78 (с, 2H), 3,48-3,34 (м, 2H), 3,37 (д, J=6,7 Гц, 1H), 2,99-2,82 (м, 6H), 2,72-2,59 (м, 2H), 2,18 (кв, J=6,8 Гц, 2H).
Пример 7: Синтез 2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-этокси-4,5-дигидро-3H-2-бензазепин-1-она
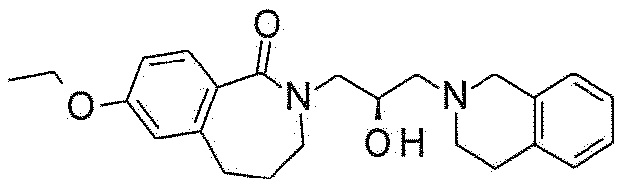
7-Этокси-2,3,4,5-тетрагидро-2-бензазепин-1-он используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,52 (д, J=8,5 Гц, 1H), 7,19-7,04 (м, 4H), 6,92-6,84 (м, 1H), 6,78 (с, 1H), 4,30-4,20 (м, 1H), 4,09 (кв, J=7,1 Гц, 2H), 3,91 (дд, J=13,8, 3,8 Гц, 1H), 3,82 (с, 2H), 3,40 (тд, J=13,6, 12,5, 7,2 Гц, 3H), 3,03-2,90 (м, 4H), 2,79 (т, J=7,1 Гц, 2H), 2,73-2,62 (м, 2H), 2,19-2,07 (м, 2H), 1,41 (т, J=7,0 Гц, 3H).
Пример 8: Синтез [2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-оксо-4,5-дигидро-3H-2-бензазепин-7-ил] трифторметансульфоната
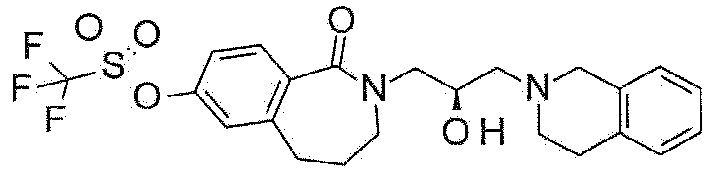
(1-Оксо-2,3,4,5-тетрагидро-2-бензазепин-7-ил) трифторметансульфонат используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,74 (д, J=8,2 Гц, 1H), 7,38 (дд, J=8,5, 2,4 Гц, 1H), 7,32 (д, J=2,3 Гц, 1H), 7,18-6,99 (м, 4H), 4,30-4,19 (м, 1H), 3,94 (дд, J=13,8, 3,6 Гц, 1H), 3,78 (с, 2H), 3,46-3,3,4 (м, 3H), 2,98-2,83 (м, 6H), 2,71-2,62 (м, 2H), 2,18 (п, J=6,8 Гц, 2H).
Пример 9: Синтез 2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-оксо-4,5-дигидро-3H-2-бензазепин-7-карбонитрила
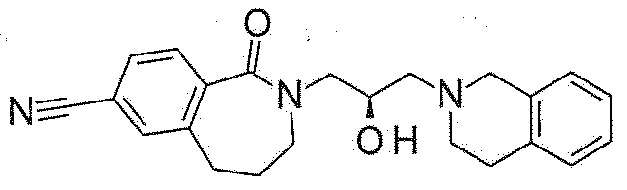
7-Циано-2,3,4,5-тетрагидро-2-бензазепин-1-он используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,73 (с, 2H), 7,66 (с, 1H), 7,21-7,02 (м, 4H), 4,31-4,17 (м, 1H), 3,94 (дд, J=13,9, 3,6 Гц, 1H), 3,77 (с, 2H), 3,57-3,34 (м, 3H), 3,01-2,81 (м, 6H), 2,70-2,61 (т, J=5,4 Гц, 2H), 2,17 (п, J=7,0 Гц, 2H).
Пример 10: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-метил-2,3-дигидро-1,4-бензоксазепин-5-она

Пример 10-1: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-3,4-дигидро-2H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
Пример 10-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-метил-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (96 мг, 0,22 ммоль), метилбороновую кислоту (27 мг, 0,45 ммоль), Pd(dppf)Cl2.CH2Cl2 (18 мг, 0,022 ммоль) и карбонат калия (91 мг, 0,66 мг) растворяют в 10 мл 1,4-диоксана:дистиллированной воды (=3:1) и перемешивают при 100°C. После подтверждения завершения реакции, реакционный раствор концентрируют при пониженном давлении и фильтруют с этилацетатом. Фильтрат концентрируют при пониженном давлении и очищают колоночной флэш-хроматографией с получением указанного в заголовке соединения (11 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,59 (д, J=7,9 Гц, 1H), 7,18-6,98 (м, 5H), 6,88 (с, 1H), 4,45 (т, J=5,2 Гц, 2H), 4,23 (п, J=3,3 Гц, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,76 (с, 2H), 3,69 (т, J=5,3 Гц, 2H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 2,98-2,83 (м, 4H), 2,71-2,59 (м, 2H), 2,36 (с, 3H).
Пример 11: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-пропил-2,3-дигидро-1,4-бензоксазепин-5-она
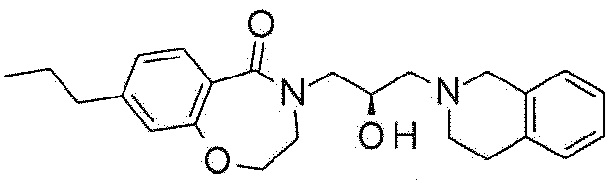
Указанное в заголовке соединение синтезируют по методике примера 10, за исключением того, что пропилбороновую кислоту используют вместо метилбороновой кислоты в примере 10-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=7,9 Гц, 1H), 7,16-6,99 (м, 5H), 6,88 (с, 1H), 4,46 (т, J=5,2 Гц, 2H), 4,25 (дд, J=8,3, 4,3 Гц, 1H), 3,98 (дд, J=13,9, 3,7 Гц, 1H), 3,78 (с, 2H), 3,70 (т, J=5,2 Гц, 2H), 3,45 (дд, J=13,9, 7,6 Гц, 1H), 2,97-2,88 (м, 4H), 2,73-2,65 (м, 2H), 2,62 (т, J=7,6 Гц, 2H), 1,67 (кв, J=7,5 Гц, 2H), 0,97 (т, J=7,3 Гц, 3H).
Пример 12: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-изобутил-2,3-дигидро-1,4-бензоксазепин-5-она
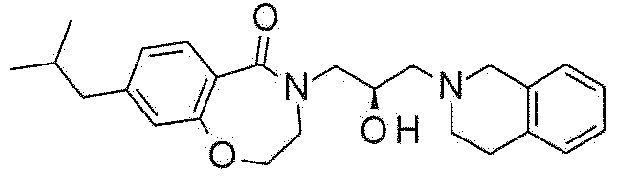
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 0,23 ммоль), изобутилбороновую кислоту (47 мг, 0,46 ммоль), Pd(dppf)Cl2 (17 мг, 0,023 ммоль) и карбонат калия (95 мг, 0,69 мг) растворяют в 2 мл толуола и перемешивают при 120°C в течение 2 часов. После подтверждения полного расхода бороновой кислоты, реакционный раствор концентрируют при пониженном давлении и фильтруют с этилацетатом. Фильтрат концентрируют при пониженном давлении и очищают колоночной флэш-хроматографией с получением указанного в заголовке соединения (11 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,0 Гц, 1H), 7,16-7,03 (м, 4H), 7,00 (дд, J=7,9, 1,6 Гц, 1H), 6,85 (д, J=1,6 Гц, 1H), 4,46 (т, J=5,1 Гц, 2H), 4,28-4,20 (м, 1H), 3,99 (дд, J=13,9, 3,6 Гц, 1H), 3,76 (с, 2H), 3,70 (т, J=5,2 Гц, 2H), 3,44 (дд, J=13,9, 7,6 Гц, 1H), 2,97-2,84 (м, 4H), 2,69-2,59 (м, 2H), 2,51 (д, J=7,2 Гц, 2H), 1,96-1,83 (м, 1H), 0,93 (д, J=6,6 Гц, 6H).
Пример 13: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,3,3-трифторпропил)-2,3-дигидро-1,4-бензоксазепин-5-она
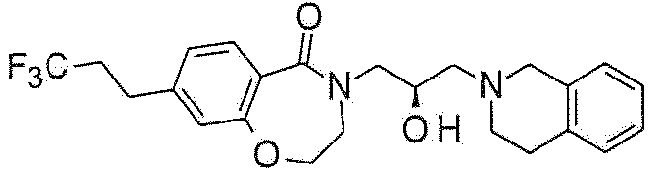
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 3,3,3-трифторпропилбороновую кислоту используют вместо изобутилбороновой кислоты при 100°C.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,0 Гц, 1H), 7,19-7,05 (м, 5H), 6,97 (с, 1H), 4,48 (т, J=5,1 Гц, 2H), 4,28-4,25 (м, 1H), 3,98 (дд, J=13,8, 3,7 Гц, 1H), 3,81 (с, 2H), 3,71 (т, J=5,3 Гц, 2H), 3,46 (дд, J=13,9, 7,6 Гц, 1H), 2,96-2,89 (м, 6H), 2,76-2,64 (м, 2H), 2,59-2,44 (м, 2H).
Пример 14: Синтез трет-бутил 4-[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]-3,6-дигидро-2H-пиридин-1-карбоксилата
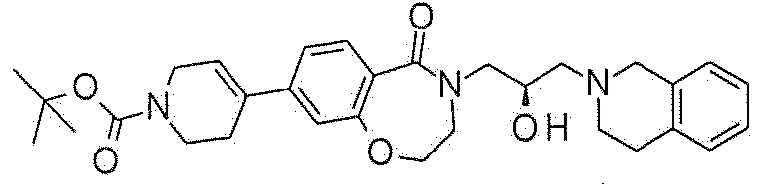
Указанное в заголовке соединение синтезируют по методике примера 10, за исключением того, что трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-3,6-дигидро-2H-пиридин-1-карбоксилат используют вместо метилбороновой кислоты в примере 10-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,3 Гц, 1H), 7,29 (д, J=8,2 Гц, 1H), 7,19-7,03 (м, 5H), 6,26 (с, 1H), 4,49 (т, J=5,2 Гц, 2H), 4,30-4,19 (м, 1H), 4,16-4,05 (м, 2H), 4,00 (дд, J=13,8, 3,8 Гц, 1H), 3,77 (с, 2H), 3,76-3,69 (м, 2H), 3,70-3,60 (м, 2H), 3,45 (дд, J=14,0, 7,7 Гц, 1H), 2,98-2,85 (м, 4H), 2,73-2,63 (м, 2H), 2,55 (с, 2H), 1,51 (с, 9H).
Пример 15: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,2,3,6-тетрагидропиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
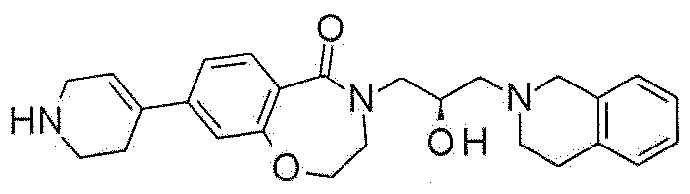
Трет-бутил 4-[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]-3,6-дигидро-2H-пиридин-1-карбоксилат, полученный в примере 14, растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Смесь перемешивают при комнатной температуре до завершения реакции, разбавляют этилдиэтиловым эфиром, и фильтруют с получением указанного в заголовке соединения в форме белого твердого вещества, дигидрохлорида. После добавления воды, указанное в заголовке соединение в форме дигидрохлорида промывают этилацетатом 3 раза. Полученный водный слой подщелачивают водным раствором гидроксида натрия до достижения рН 14, и этил ацетат снова добавляют для экстрагирования 3 раза. Объединенные органические слои сушат над безводным сульфатом натрия, фильтруют, и концентрируют при пониженном давлении с получением указанного в заголовке соединения без дополнительной очистки.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,2 Гц, 1H), 7,29 (д, J=8,3 Гц, 1H), 7,17-7,01 (м, 5H), 6,32 (с, 1H), 4,49 (т, J=5,1 Гц, 2H), 4,29-4,19 (м, 1H), 4,00 (дд, J=14,0, 3,6 Гц, 1H), 3,79-3,65 (м, 4H), 3,53 (д, J=3,2 Гц, 2H), 3,45 (дд, J=13,9, 7,7 Гц, 1H), 3,11 (т, J=5,8 Гц, 2H), 2,98-2,84 (м, 4H), 2,71-2,62 (м, 2H), 2,53 (шс, 2H).
Пример 16: Синтез 8-(1-ацетил-3,6-дигидро-2H-пиридин-4-ил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
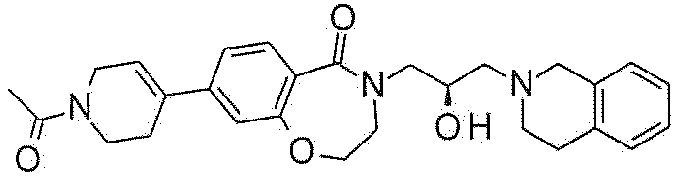
Дигидрохлорид 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,2,3,6-тетрагидропиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она, полученный в примере 15 (75 мг, 0,16 ммоль), и карбонат калия (66 мг, 0,48 ммоль) растворяют в 1,5 мл ацетона, и туда медленно добавляют уксусный ангидрид (0,03 мл, 0,32 ммоль) при комнатной температуре. Реакционный раствор перемешивают при комнатной температуре и фильтруют после подтверждения завершения реакции. Фильтрат концентрируют при пониженном давлении и очищают колоночной флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,2 Гц, 1H), 7,29 (д, J=8,2 Гц, 1H), 7,19-7,02 (м, 5H), 6,28 (с, 1H), 4,49 (т, J=5,1 Гц, 2H), 4,31-4,19 (м, 3H), 3,98 (дд, J=13,9, 3,7 Гц, 1H), 3,88-3,78 (м, 3H), 3,80-3,67 (м, 3H), 3,47 (дд, J=13,9, 7,5 Гц, 1H), 3,02-2,90 (м, 4H), 2,77-2,68 (м, 2H), 2,64 (шс, 1H), 2,56 (шс, 1H), 2,18 (д, J=15,1 Гц, 3H).
Пример 17: Синтез 8-(1-ацетил-4-пиперидил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он
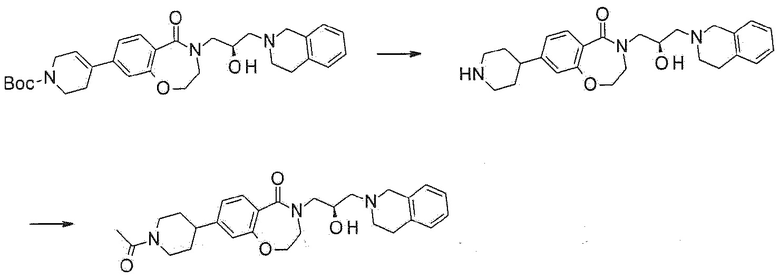
Пример 17-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидил)-2,3-дигидро-1,4-бензоксазепин-5-она
Трет-бутил 4-[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]-3,6-дигидро-2H-пиридин-1-карбоксилат, полученный в примере 14, растворяют в метаноле, и туда добавляют 5% палладий на угле в каталитическом количестве. Реакционный раствор перемешивают под баллоном водорода и фильтруют через целит. Фильтрат концентрируют при пониженном давлении, растворяют в незначительном количестве метанола, и затем туда добавляют 4 N хлористоводородную кислоту, растворенную в 1,4-диоксане, с последующим перемешиванием при комнатной температуре в течение 1 часа. После добавления дистиллированной воды, реакционный раствор промывают этилацетатом. Полученный водный слой подщелачивают водным раствором гидроксида натрия до достижения рН 14 и экстрагируют дихлорметаном 3 раза. Объединенные органические слои сушат над безводным сульфатом натрия, фильтруют, и концентрируют при пониженном давлении с получением указанного в заголовке соединения без дополнительной очистки.
Пример 17-2: Синтез 8-(1-ацетил-4-пиперидил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидил)-2,3-дигидро-1,4-бензоксазепин-5-он (50 мг, 0,11 ммоль), полученный в примере 17-1, и карбонат калия (46 мг, 0,33 мг) растворяют в дихлорметане, и туда медленно добавляют уксусный ангидрид (0,02 мл, 0,17 ммоль). Реакционный раствор перемешивают при комнатной температуре в течение одного дня, разбавляют дихлорметаном, фильтруют и концентрируют при пониженном давлении. Полученный концентрат очищают колоночной флэш-хроматографией с получением указанного в заголовке соединения (21 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,65 (д, J=8,0 Гц, 1H), 7,18-7,02 (м, 5H), 6,95 (с, 1H), 4,69 (д, J=13,4 Гц, 1H), 4,47 (т, J=5,2 Гц, 2H), 4,29-4,18 (м, 1H), 4,03 (дд, J=27,3, 14,3 Гц, 2H), 3,80-3,65 (м, 4H), 3,44 (дд, J=14,0, 7,7 Гц, 1H), 3,29-3,20 (м, 1H), 2,98-2,82 (м, 4H), 2,80-2,60 (м, 3H), 2,16 (с, 3H), 1,98-1,85 (м, 2H), 1,78-1,50 (м, 3H).
Пример 18: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-этил-3,6-дигидро-2H-пиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
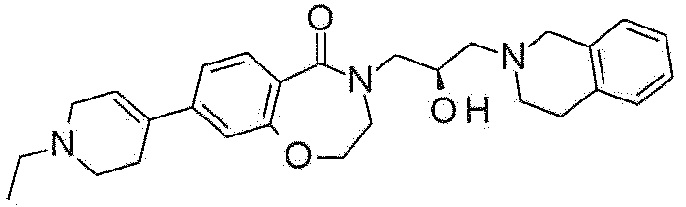
Дигидрохлорид 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,2,3,6-тетрагидропиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она, полученный в примере 15 (75 мг, 0,16 ммоль) растворяют в метаноле, и туда добавляют избыток ацетальдегида. Перемешивая реакционный раствор, добавляют избыток цианоборгидрида натрия, с последующим перемешиванием при комнатной температуре в течение одного дня. Реакцию останавливают добавлением насыщенного водного раствора хлорида аммония к реакционному раствору, и 1 N водный раствор гидроксида натрия добавляют для подщелачивания. Реакционную смесь экстрагируют этилацетатом 3 раза и сушат над безводным сульфатом натрия. Маслянистую жидкость, полученную удалением растворителя выпариванием при пониженном давлении, очищают колоночной флэш-хроматографией с получением указанного в заголовке соединения (10 мг) в виде белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,2 Гц, 1H), 7,30 (д, J=7,9 Гц, 1H), 7,09 (д, J=18,9 Гц, 5H), 6,30 (с, 1H), 4,49 (т, J=5,1 Гц, 2H), 4,29-4,18 (м, 1H), 4,00 (дд, J=13,7, 3,5 Гц, 1H), 3,77 (с, 2H), 3,73 (т, J=5,2 Гц, 2H), 3,45 (дд, J=13,8, 7,6 Гц, 1H), 3,27 (с, 2H), 2,99-2,85 (м, 4H), 2,83 (т, J=5,9 Гц, 2H), 2,71-2,59 (м, 6H), 1,21 (т, J=7,2 Гц, 3H).
Пример 19: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-изопропил-3,6-дигидро-2H-пиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
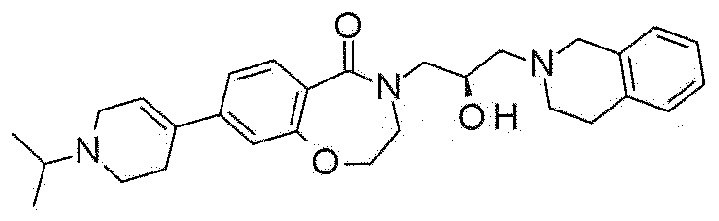
Указанное в заголовке соединение синтезируют по методике примера 18, за исключением того, что ацетон используют вместо ацетальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=8,2 Гц, 1H), 7,23 (д, J=8,2 Гц, 1H), 7,10-6,95 (м, 5H), 6,24 (с, 1H), 4,42 (т, J=5,2 Гц, 2H), 4,22-4,12 (м, 1H), 3,96-3,84 (м, 1H), 3,71 (с, 2H), 3,65 (т, J=5,2 Гц, 2H), 3,48-3,31 (м, 3H), 3,05-2,90 (м, 3H), 2,90-2,78 (м, 4H), 2,68-2,50 (м, 4H), 1,17 (д, J=6,5 Гц, 6H).
Пример 20: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,6-дигидро-2H-пиран-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
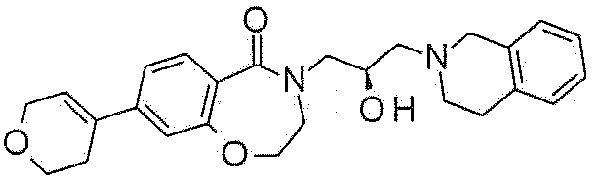
Указанное в заголовке соединение синтезируют по методике примера 10, за исключением того, что 2-(3,6-дигидро-2H-пиран-4-ил)-4,4,5,5-тетраметил-1,3,2-диоксабборолан используют вместо метилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,2 Гц, 1H), 7,30 (д, J=8,3 Гц, 1H), 7,20-6,98 (м, 5H), 6,34 (с, 1H), 4,49 (т, J=5,1 Гц, 2H), 4,32 (д, J=3,3 Гц, 2H), 4,29-4,19 (м, 1H), 4,00 (дд, J=13,8, 3,6 Гц, 1H), 3,94 (т, J=5,5 Гц, 2H), 3,81-3,68 (м, 4H), 3,48-3,40 (м, 1H), 2,99-2,84 (м, 4H), 2,69-2,60 (м, 2H), 2,53 (шс, 2H).
Пример 21: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-тетрагидропиран-4-ил-2,3-дигидро-1,4-бензоксазепин-5-она
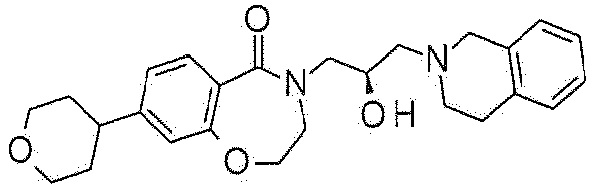
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,6-дигидро-2H-пиран-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-он, полученный в примере 20, растворяют в метаноле, и туда добавляют 5% палладий на угле в каталитическом количестве. Реакционный раствор перемешивают под баллоном водорода и фильтруют через целит. Фильтрат концентрируют при пониженном давлении и очищают флэш-хроматографией с получением указанного в заголовке соединения в виде прозрачного масла.
1H ЯМР (400 MГц, Метанол-d4) δ 7,65 (д, J=8,1 Гц, 1H), 7,17-7,02 (м, 5H), 6,95 (с, 1H), 4,48 (т, J=5,2 Гц, 2H), 4,29-4,17 (м, 1H), 4,08-3,95 (м, 3H), 3,76 (с, 2H), 3,71 (т, J=5,3 Гц, 2H), 3,63-3,52 (м, 2H), 3,44 (дд, J=13,9, 7,7 Гц, 1H), 2,98-2,80 (м, 5H), 2,69-2,59 (м, 2H), 1,84-1,72 (м, 4H).
Пример 22: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(морфолинометил)-2,3-дигидро-1,4-бензоксазепин-5-она
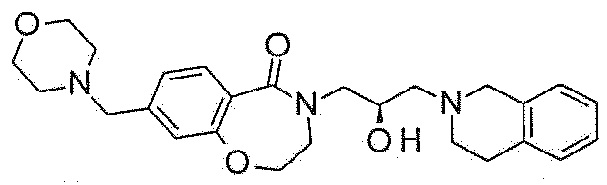
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (160 мг, 0,37 ммоль), (морфолин-4-ил)метилтрифторборат калия (85 мг, 0,41 мг), ацетат палладия (4 мг, 0,0185 ммоль), XPhos (18 мг, 0,037 ммоль) и карбонат цезия (362 мг, 1,11 ммоль) растворяют в 3 мл растворителя тетрагидрофуран:дистиллированная вода (=10:1), и загружают азот, с последующим перемешиванием при 80°C в течение 16 часов. Реакционный раствор охлаждают до комнатной температуры, разбавляют этилацетатом и фильтруют через целит. Полученный раствор концентрируют при пониженном давлении и очищают флэш-хроматографией с получением белого указанного в заголовке соединения (103 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,16-7,03 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,30-4,19 (м, 1H), 3,99 (дд, J=13,9, 3,6 Гц, 1H), 3,77 (с, 2H), 3,71 (т, J=4,8 Гц, 6H), 3,55 (с, 2H), 3,46 (дд, J=13,9, 7,6 Гц, 1H), 2,99-2,85 (м, 4H), 2,72-2,60 (м, 2H), 2,48 (т, J=4,7 Гц, 4H).
Пример 23: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-пиперидилметил)-2,3-дигидро-1,4-бензоксазепин-5-она
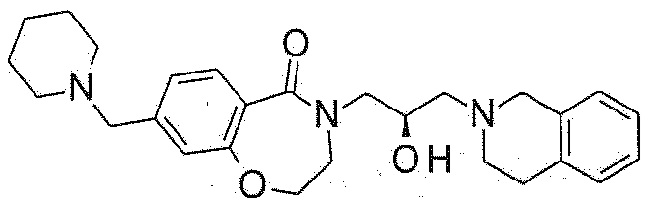
Указанное в заголовке соединение синтезируют по методике примера 22, за исключением того, что (пиперидин-1-ил)метилтрифторборат калия используют вместо (морфолин-4-ил)метилтрифторбората калия.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,17 (д, J=8,0 Гц, 1H), 7,15-7,02 (м, 5H), 4,49 (т, J=5,1 Гц, 2H), 4,29-4,20 (м, 1H), 4,00 (дд, J=13,8, 3,6 Гц, 1H), 3,76 (с, 2H), 3,72 (т, J=5,3 Гц, 2H), 3,53 (с, 2H), 3,45 (дд, J=13,8, 7,6 Гц, 1H), 2,96-2,86(м, 4H), 2,71-2,59 (м, 2H), 2,46 (шс, 4H), 1,62 (кв, J=5,6 Гц, 4H), 1,49 (шс, 2H).
Пример 24: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пирролидин-1-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
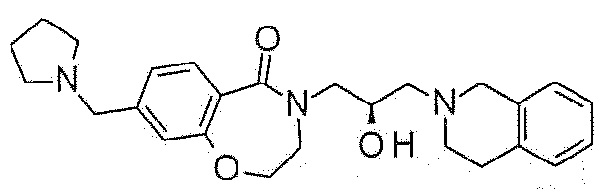
Указанное в заголовке соединение синтезируют по методике примера 22, за исключением того, что 1-трифторборатометилпирролидин калия используют вместо (морфолин-4-ил)метилтрифторбората калия.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,0 Гц, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,15-7,03 (м, 5H), 4,49 (т, J=5,1 Гц, 2H), 4,27-4,24 (м, 1H), 4,00 (дд, J=13,9, 3,6 Гц, 1H), 3,81-3,67 (м, 6H), 3,46 (дд, J=13,9, 7,7 Гц, 1H), 2,95-2,88 (м, 4H), 2,66 (шс, 6H), 1,87 (шс, 4H).
Пример 25: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(диметиламино)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
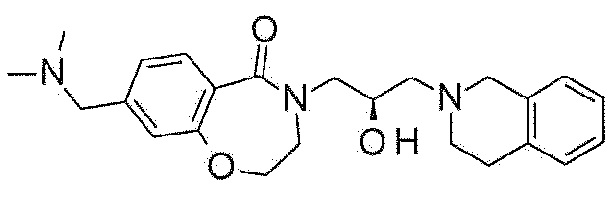
Указанное в заголовке соединение синтезируют по методике примера 22, за исключением того, что диметиламинометилтрифторборонат калия используют вместо (морфолин-4-ил)метилтрифторбората калия.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,75 (д, J=8,0 Гц, 1H), 7,18-7,07 (м, 4H), 7,06-6,95 (м, 2H), 4,51-4,39 (м, 2H), 4,17-4,06 (м, 2H), 3,93 (д, J=14,7 Гц, 1H), 3,83 (д, J=15,0 Гц, 1H), 3,74-3,66 (м, 2H), 3,63 (д, J=14,9 Гц, 1H), 3,56 (дд, J=14,2, 6,0 Гц, 1H), 3,42 (с, 2H), 3,00-2,87 (м, 3H), 2,77-2,70 (м, 1H), 2,69-2,63 (м, 1H), 2,56 (т, J=11,3 Гц, 1H), 2,25 (с, 6H).
Пример 26: Синтез 8-(диэтиламинометил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
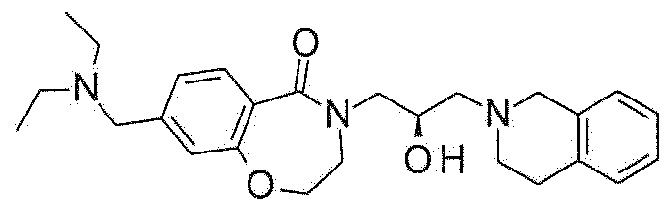
Указанное в заголовке соединение синтезируют по методике примера 22, за исключением того, что диэтиламинометилтрифторборонат калия используют вместо (морфолин-4-ил)метилтрифторбората калия.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,74 (д, J=7,9 Гц, 1H), 7,18-7,08 (м, 4H), 7,02 (шс, 2H), 4,45 (квт, J=10,8, 4,6 Гц, 2H), 4,16-4,06 (м, 1H), 3,93 (д, J=14,2 Гц, 1H), 3,83 (д, J=14,9 Гц, 1H), 3,75-3,66 (м, 2H), 3,63 (д, J=14,9 Гц, 1H), 3,57-3,54 (м, 3H), 3,00-2,87 (м, 3H), 2,74 (дд, J=10,7, 5,3 Гц, 1H), 2,67 (дд, J=12,5, 3,9 Гц, 1H), 2,61-2,47 (м, 5H), 1,04 (т, J=7,1 Гц, 6H).
Пример 27: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метил-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
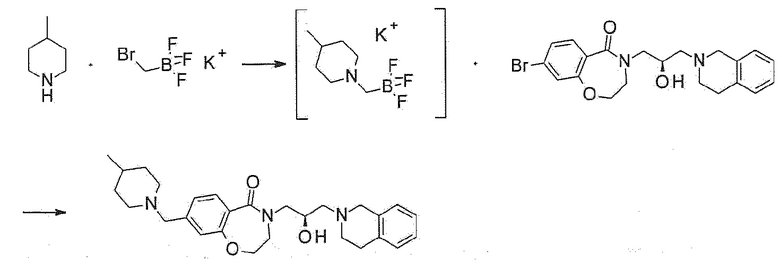
4-Метилпиперидин (0,054 мл, 0,46 ммоль) и (бромметил)трифторборат калия (92 мг, 0,46 ммоль) растворяют в 2 мл тетрагидрофурана, и перемешивают при 80°C в течение 12 часов. Реакционную смесь охлаждают до комнатной температуры, и туда добавляют 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 0,23 ммоль), ацетат палладия (3 мг, 0,011 ммоль), XPhos (11 мг, 0,023 ммоль), карбонат цезия (225 мг, 0,69 ммоль) и 2 мл тетрагидрофурана:дистиллированной воды (=10:1), с последующей загрузкой реакционного сосуда азотом. Реакционный раствор перемешивают при 80°C в течение 16 часов, разбавляют этилацетатом и фильтруют через целит. Полученный раствор концентрируют при пониженном давлении и очищают флэш-хроматографией с получением белого указанного в заголовке соединения (70 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,17 (д, J=8,0 Гц, 1H), 7,14-7,02 (м, 5H), 4,49 (т, J=5,1 Гц, 2H), 4,29-4,19 (м, 1H), 4,00 (дд, J=13,9, 3,6 Гц, 1H), 3,76 (с, 2H), 3,72 (т, J=5,2 Гц, 2H), 3,54 (с, 2H), 3,46 (дд, J=13,8, 7,7 Гц, 1H), 2,98-2,83 (м, 6H), 2,72-2,60 (м, 2H), 2,07 (д, J=11,6 Гц, 1H), 1,66 (д, J=13,0 Гц, 2H), 1,41 (шс, 1H), 1,34-1,19 (м, 2H), 0,96 (д, J=6,4 Гц, 3H).
Пример 28: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-окса-6-азаспиро[3,3]гептан-6-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
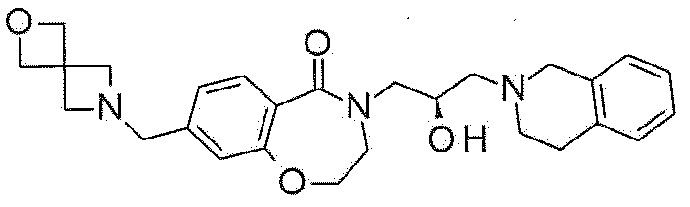
Указанное в заголовке соединение синтезируют по методике примера 27, за исключением того, что добавляют 4 эквивалента карбоната калия, и 2-окса-6-азаспиро[3,3]гептан оксалат используют вместо 4-метилпиперидина.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,18-7,03 (м, 5H), 6,98 (с, 1H), 4,75 (с, 4H), 4,48 (т, J=5,1 Гц, 2H), 4,30-4,19 (м, 1H), 3,99 (дд, J=14,0, 3,6 Гц, 1H), 3,78 (с, 2H), 3,71 (т, J=5,3 Гц, 2H), 3,62 (с, 2H), 3,47-3,43 (м, 5H), 2,95-2,89 (м, 4H), 2,74-2,61 (м, 2H).
Пример 29: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-метоксиазетидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
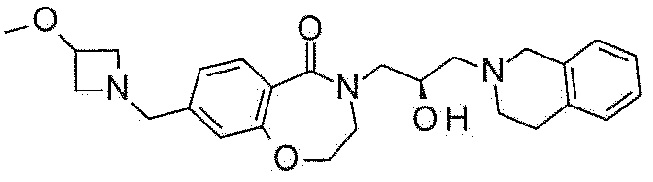
3-Метоксиазетидина гидрохлорид (57 мг, 0,46 ммоль), (бромметил)трифторборат калия (92 мг, 0,46 ммоль) и карбонат калия (127 мг, 0,92 ммоль) растворяют в тетрагидрофуране:дистиллированной воде (10:1), и перемешивают при 80°C в течение 12 часов. Реакционную смесь охлаждают до комнатной температуры, и туда добавляют 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 0,23 ммоль), ацетат палладия (3 мг, 0,011 ммоль), XPhos (11 мг, 0,023 ммоль), карбонат цезия (225 мг, 0,69 ммоль) и тетрагидрофуран:дистиллированную воду (=10:1), с последующей загрузкой реакционного сосуда азотом. Реакционный раствор перемешивают при 80°C в течение 16 часов, разбавляют этилацетатом и фильтруют через целит. Полученный раствор концентрируют при пониженном давлении и очищают флэш-хроматографией с получением белого указанного в заголовке соединения (16 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,16-7,04 (м, 5H), 7,00 (с, 1H), 4,48 (т, J=5,1 Гц, 2H), 4,28-4,19 (м, 1H), 4,11-4,04 (м, 1H), 3,99 (дд, J=13,9, 3,7 Гц, 1H), 3,77 (с, 2H), 3,74-3,67 (м, 3H), 3,61 (т, J=7,3 Гц, 2H), 3,45 (дд, J=14,0, 7,6 Гц, 1H), 3,27 (с, 3H), 3,08 (т, J=7,1 Гц, 2H), 3,00-2,84 (м, 4H), 2,71-2,61 (м, 2H).
Пример 30: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-метилморфолин-4-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
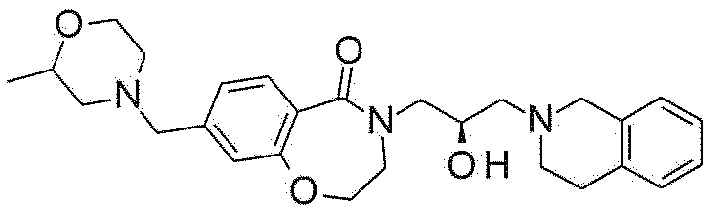
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 2-метилморфолин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,15-7,03 (м, 5H), 4,49 (т, J=5,1 Гц, 2H), 4,30-4,17 (м, 1H), 3,99 (дд, J=13,8, 3,7 Гц, 1H), 3,88-3,79 (м, 1H), 3,77 (с, 2H), 3,75-3,61 (м, 4H), 3,54 (с, 2H), 3,46 (дд, J=13,8, 7,6 Гц, 1H), 2,98-2,84 (м, 4H), 2,76 (д, J=11,4 Гц, 1H), 2,72-2,62 (м, 3H), 2,21-2,11 (м, 1H), 1,86 (т, J=10,6 Гц, 1H), 1,12 (д, J=6,3 Гц, 3H).
Пример 31: Синтез 8-[(4,4-дифтор-1-пиперидил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
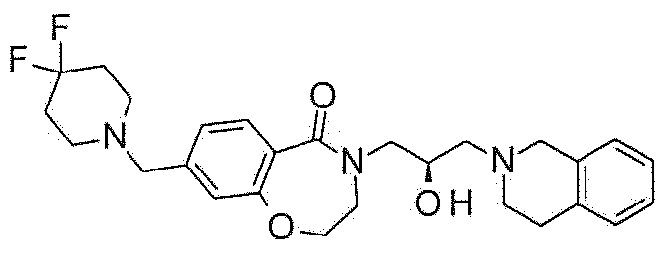
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 4,4-дифторпиперидин гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=7,9 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,15-7,03 (м, 4H), 4,49 (т, J=5,1 Гц, 2H), 4,29-4,19 (м, 1H), 4,00 (дд, J=13,8, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=5,2 Гц, 2H), 3,60 (с, 2H), 3,46 (дд, J=13,8, 7,6 Гц, 1H), 2,99-2,84 (м, 4H), 2,71-2,64 (м, 2H), 2,59 (т, J=5,8 Гц, 4H), 2,01 (ддт, J=19,4, 12,4, 5,6 Гц, 4H).
Пример 32: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-фтор-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
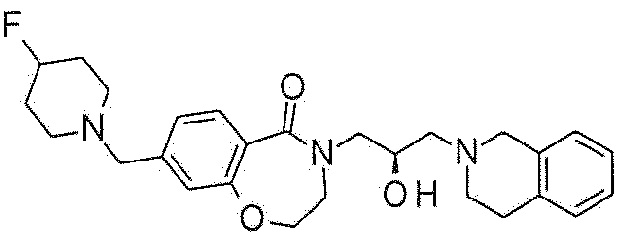
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 4-фторпиперидин гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,14-7,01 (м, 5H), 4,67 (д, J=48,8 Гц, 1H), 4,48 (т, J=5,1 Гц, 2H), 4,29-4,17 (м, 1H), 3,99 (дд, J=13,8, 3,6 Гц, 1H), 3,81-3,67 (м, 4H), 3,55 (с, 2H), 3,45 (дд, J=13,9, 7,7 Гц, 1H), 2,99-2,83 (м, 4H), 2,72-2,54 (м, 4H), 2,50-2,35 (м, 2H), 2,00-1,76 (м, 4H).
Пример 33: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3,5-диметил-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
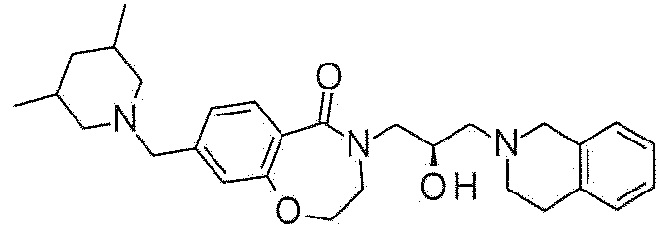
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3,5-диметилпиперидин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=7,9 Гц, 1H), 7,17 (д, J=8,0 Гц, 1H), 7,16-6,95 (м, 4H), 4,49 (т, J=5,2 Гц, 2H), 4,25 (с, 1H), 4,00 (дд, J=14,0, 3,6 Гц, 1H), 3,75 (д, J=16,5 Гц, 2H), 3,55 (с, 2H), 3,46 (дд, J=13,7, 7,7 Гц, 1H), 3,01-2,81 (м, 5H), 2,67 (д, J=5,2 Гц, 2H), 1,75 (д, J=13,2 Гц, 3H), 1,55 (т, J=11,0 Гц, 2H), 0,87 (д, J=6,3 Гц, 6H).
Пример 34: Синтез 8-(3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррол-2-илметил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
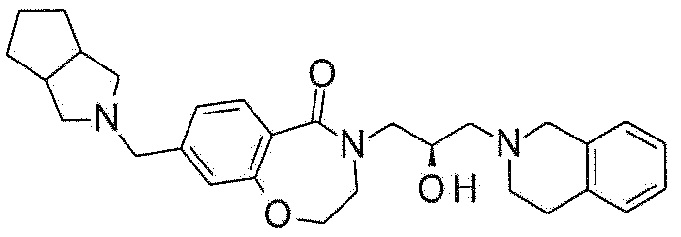
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 1,2,3,3a,4,5,6,6a-октагидроциклопента[c]пиррол гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,18 (с, 0H), 7,14-7,02 (м, 4H), 4,48 (т, J=5,1 Гц, 2H), 4,24 (с, 1H), 4,00 (дд, J=13,9, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=5,1 Гц, 2H), 3,60 (с, 2H), 3,46 (дт, J=13,8, 7,6 Гц, 1H), 2,94 (д, J=5,5 Гц, 2H), 2,89 (д, J=6,2 Гц, 3H), 2,76-2,59 (м, 4H), 2,08 (дд, J=9,4, 5,4 Гц, 2H), 1,62 (д, J=41,3 Гц, 4H), 1,47 (с, 2H).
Пример 35: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-гидроксипирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
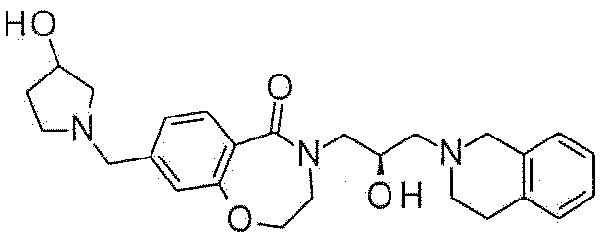
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что пирролидин-3-ол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,12 (д, J=4,2 Гц, 3H), 7,08 (с, 2H), 4,48 (т, J=5,2 Гц, 2H), 4,37 (с, 1H), 4,24 (с, 1H), 4,00 (дд, J=13,7, 3,6 Гц, 1H), 3,77 (с, 2H), 3,75-3,68 (м, 3H), 3,65 (д, J=13,0 Гц, 1H), 3,46 (дт, J=13,8, 7,4 Гц, 1H), 2,94 (д, J=5,6 Гц, 2H), 2,89 (д, J=5,4 Гц, 2H), 2,84-2,74 (м, 2H), 2,75-2,63 (м, 2H), 2,61-2,48 (м, 2H), 2,16 (дт, J=14,3, 7,0 Гц, 1H).
Пример 36: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2R)-2-метилпирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
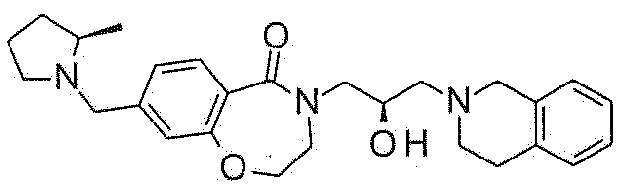
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что (2R)-2-метилпирролидин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,12 (д, J=4,3 Гц, 3H), 7,07 (с, 2H), 4,49 (т, J=5,2 Гц, 2H), 4,24 (с, 0H), 4,11-3,93 (м, 2H), 3,76 (с, 2H), 3,72 (т, J=5,3 Гц, 2H), 3,46 (дт, J=13,9, 7,7 Гц, 1H), 3,24 (д, J=12,9 Гц, 1H), 2,94 (д, J=5,7 Гц, 3H), 2,89 (д, J=5,7 Гц, 2H), 2,71-2,62 (м, 2H), 2,57-2,45 (м, 1H), 2,24 (д, J=9,2 Гц, 1H), 2,03 (дкв, J=14,6, 7,3 Гц, 1H), 1,74 (п, J=8,1 Гц, 2H), 1,49 (дт, J=17,6, 8,9 Гц, 1H), 1,21 (д, J=6,1 Гц, 3H).
Пример 37: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-(гидроксиметил)-1-пиперидил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
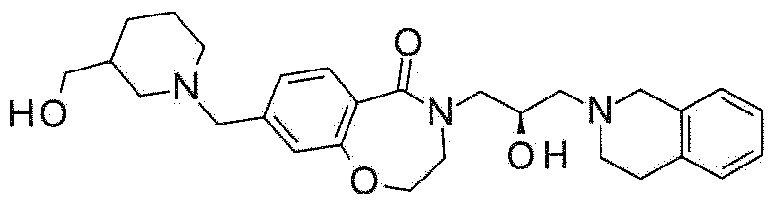
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3-пиперидилметанол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,12 (д, J=4,2 Гц, 3H), 7,06 (с, 2H), 4,49 (т, J=5,1 Гц, 2H), 4,24 (с, 1H), 3,99 (дд, J=14,0, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=5,0 Гц, 2H), 3,65-3,53 (м, 2H), 3,54-3,41 (м, 1H), 3,00 (д, J=7,1 Гц, 1H), 2,94 (д, J=5,4 Гц, 2H), 2,88 (т, J=10,9 Гц, 3H), 2,73-2,61 (м, 2H), 2,16-1,95 (м, 1H), 1,76 (д, J=18,7 Гц, 2H), 1,63 (д, J=12,4 Гц, 1H).
Пример 38: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метокси-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
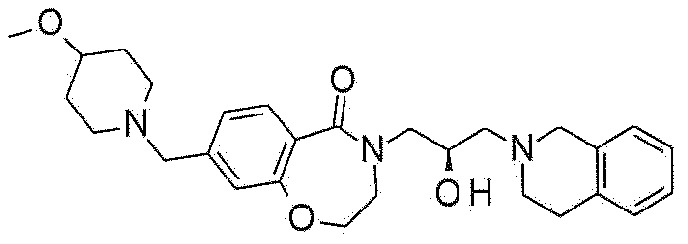
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 4-метоксипиперидин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,17 (д, J=8,0 Гц, 1H), 7,15-7,01 (м, 5H), 4,49 (т, J=5,2 Гц, 2H), 4,31-4,19 (м, 1H), 4,00 (дд, J=13,8, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=4,8 Гц, 2H), 3,55 (с, 2H), 3,46 (дд, J=13,8, 7,7 Гц, 1H), 3,34 (с, 3H), 3,31-3,24 (м, 1H), 2,98-2,85 (м, 4H), 2,76 (дд, J=11,1, 3,9 Гц, 2H), 2,71-2,62 (м, 2H), 2,25 (т, J=10,8 Гц, 2H), 1,99-1,87 (м, 2H), 1,67-1,52 (м, 2H).
Пример 39: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,4-оксазепан-4-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
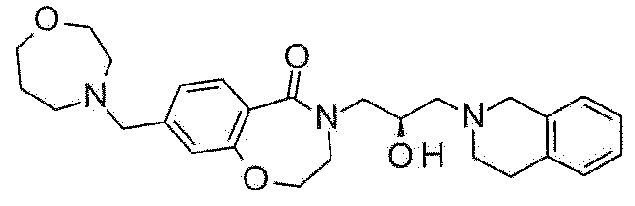
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 1,4-оксазепан гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,15-7,03 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,29-4,19 (м, 1H), 3,99 (дд, J=13,7, 3,6 Гц, 1H), 3,83 (т, J=6,1 Гц, 2H), 3,79-3,65 (м, 8H), 3,46 (дд, J=13,8, 7,6 Гц, 1H), 2,98-2,84 (м, 4H), 2,78-2,68 (м, 4H), 2,69-2,61 (м, 2H), 1,93 (п, J=5,8 Гц, 2H).
Пример 40: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-гидрокси-3-метил-пирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
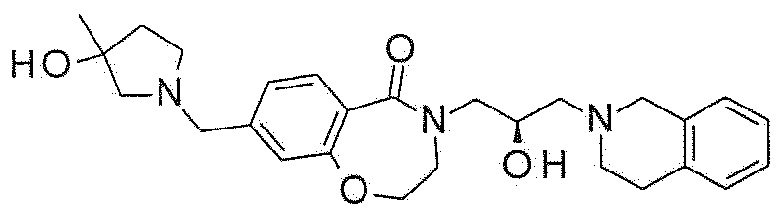
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3-метилпирролидин-3-ол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,16-7,01 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,30-4,19 (м, 1H), 4,00 (дд, J=14,0, 3,6 Гц, 1H), 3,77 (с, 2H), 3,75-3,61 (м, 4H), 3,46 (дд, J=13,9, 7,6 Гц, 1H), 2,94 (д, J=5,6 Гц, 2H), 2,92-2,80 (м, 4H), 2,73-2,60 (м, 4H), 2,55 (д, J=10,1 Гц, 1H), 1,95-1,85 (м, 2H), 1,36 (с, 3H).
Пример 41: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[2-(гидроксиметил)-1-пиперидил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
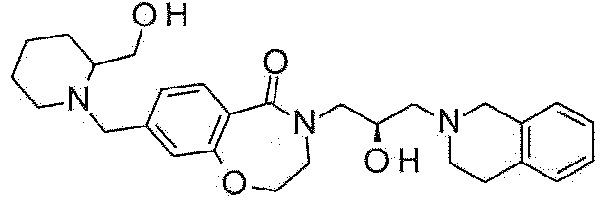
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что морфолин-3-илметанол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=7,9 Гц, 1H), 7,21 (д, J=8,1 Гц, 1H), 7,15-7,04 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,29-4,19 (м, 1H), 4,14 (д, J=13,3 Гц, 1H), 3,99 (дд, J=14,0, 3,5 Гц, 1H), 3,91-3,84 (м, 1H), 3,83-3,75 (м, 3H), 3,75-3,63 (м, 4H), 3,64-3,50 (м, 2H), 3,46 (дд, J=13,8, 7,6 Гц, 1H), 3,39 (д, J=13,9 Гц, 1H), 2,99-2,85 (м, 4H), 2,72-2,63 (м, 3H), 2,53 (с, 1H), 2,29 (д, J=9,3 Гц, 1H).
Пример 42: Синтез 8-[(3,3-дифтор-1-пиперидил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
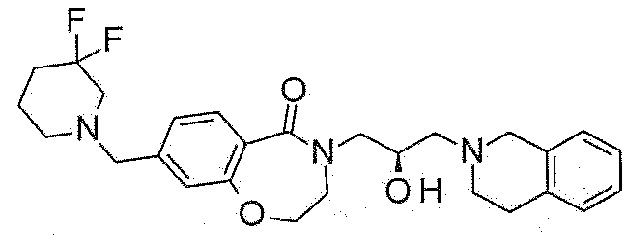
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3,3-дифторпиперидин гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=7,9 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,09 (дд, J=21,4, 4,6 Гц, 4H), 4,49 (т, J=5,2 Гц, 2H), 4,31-4,20 (м, 1H), 3,99 (дд, J=14,0, 3,6 Гц, 1H), 3,78 (с, 2H), 3,72 (т, J=5,3 Гц, 2H), 3,63 (с, 2H), 3,46 (дд, J=13,9, 7,9 Гц, 1H), 3,00-2,83 (м, 4H), 2,74-2,58 (м, 4H), 2,55-2,44 (м, 2H), 1,97-1,83 (м, 2H), 1,82-1,72 (м, 2H).
Пример 43: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
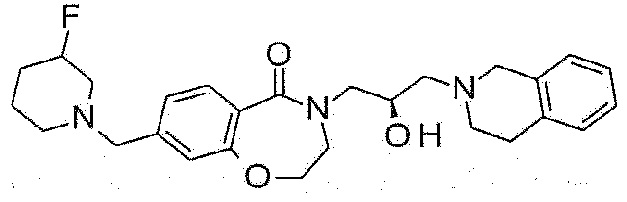
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3-фторпиперидин гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,15-7,02 (м, 5H), 4,63 (д, J=48,0 Гц, 1H), 4,49 (т, J=5,1 Гц, 2H), 4,30-4,19 (м, 1H), 4,00 (дд, J=14,0, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=5,3 Гц, 2H), 3,58 (с, 2H), 3,46 (дд, J=13,9, 7,7 Гц, 1H), 3,00-2,82 (м, 4H), 2,81-2,58 (м, 3H), 2,55-2,41 (м, 2H), 2,38 (т, J=9,9 Гц, 1H), 1,94-1,78 (м, 2H), 1,70-1,51 (м, 2H).
Пример 44: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-гидрокси-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
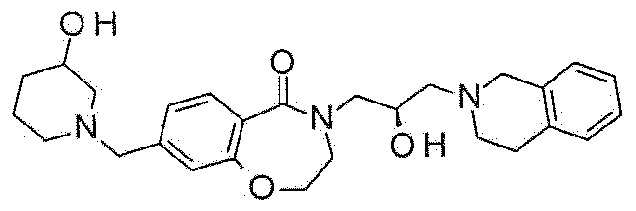
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что пиперидин-3-ол гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,16-7,01 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,30-4,19 (м, 1H), 3,99 (дд, J=13,7, 3,6 Гц, 1H), 3,78 (с, 2H), 3,75-3,63 (м, 3H), 3,63-3,50 (м, 2H), 3,46 (дд, J=13,9, 7,7 Гц, 1H), 3,00-2,82 (м, 5H), 2,77-2,61 (м, 3H), 2,12-2,04 (м, 1H), 1,99-1,88 (м, 2H), 1,82-1,70 (м, 1H), 1,65-1,50 (м, 1H).
Пример 45: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-гидрокси-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
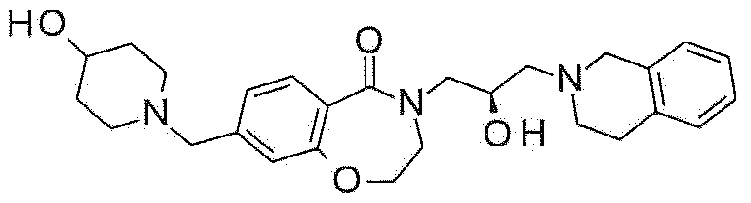
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что пиперидин-4-ол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,15-7,03 (м, 5H), 4,49 (т, J=5,0 Гц, 2H), 4,29-4,20 (м, 1H), 4,02-3,96 (м, 1H), 3,77 (с, 2H), 3,76-3,70 (м, 2H), 3,68-3,59 (м, 1H), 3,55 (с, 2H), 3,46 (дд, J=13,8, 7,5 Гц, 1H), 2,98-2,86 (м, 4H), 2,86-2,76 (м, 2H), 2,70-2,63 (м, 2H), 2,28-2,15 (м, 2H), 1,92-1,82 (м, 2H), 1,66-1,53 (м, 2H).
Пример 46: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2S)-2-(гидроксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
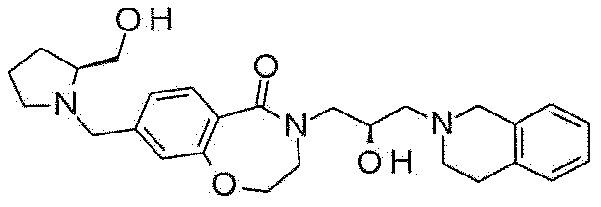
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что [(2S)-пирролидин-2-ил]метанол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=7,9 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,16-7,03 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,29-4,19 (м, 1H), 4,13 (д, J=12,8 Гц, 1H), 4,00 (дд, J=14,1, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=5,4 Гц, 2H), 3,60 (дд, J=11,1, 4,6 Гц, 1H), 3,56-3,41 (м, 3H), 3,02-2,85 (м, 5H), 2,79-2,62 (м, 3H), 2,39-2,25 (м, 1H), 2,03-1,93 (м, 1H), 1,82-1,66 (м, 3H).
Пример 47: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2R)-2-(гидроксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
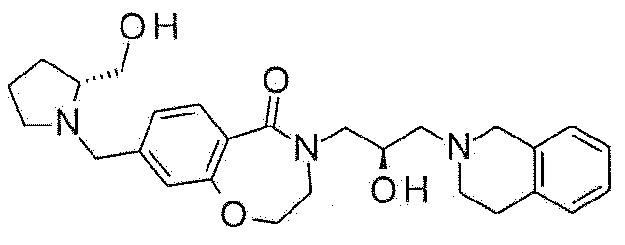
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что [(2R)-пирролидин-2-ил]метанол используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,0 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,17-7,02 (м, 5H), 4,48 (т, J=5,2 Гц, 2H), 4,24 (с, 1H), 4,14 (д, J=13,2 Гц, 1H), 3,99 (дд, J=13,8, 3,5 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=4,9 Гц, 2H), 3,60 (дд, J=11,0, 4,6 Гц, 1H), 3,57-3,41 (м, 3H), 3,02-2,84 (м, 5H), 2,79-2,68 (м, 1H), 2,69-2,61 (м, 2H), 2,38-2,27 (м, 1H), 2,05-1,92 (м, 1H), 1,83-1,66 (м, 3H).
Пример 48: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-этилпирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
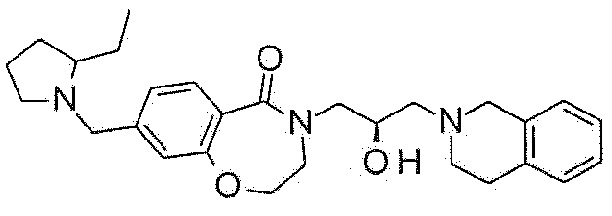
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 2-этилпирролидин гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,16-7,02 (м, 5H), 4,48 (т, J=5,2 Гц, 2H), 4,29-4,19 (м, 1H), 4,07 (д, J=13,2 Гц, 1H), 4,00 (дд, J=14,1, 3,5 Гц, 1H), 3,76 (с, 2H), 3,74-3,67 (м, 2H), 3,45 (дд, J=13,9, 7,7 Гц, 1H), 3,25 (д, J=12,9 Гц, 1H), 2,99-2,81 (м, 5H), 2,70-2,60 (м, 2H), 2,41-2,29 (м, 1H), 2,27-2,15 (м, 1H), 2,09-1,99 (м, 1H), 1,91-1,80 (м, 1H), 1,79-1,65 (м, 2H), 1,57-1,45 (м, 1H), 1,43-1,26 (м, 2H), 0,96 (т, J=7,5 Гц, 3H).
Пример 49: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2S)-2-(метоксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
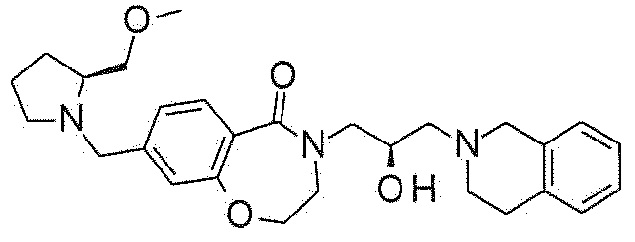
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что (2S)-2-(метоксиметил)пирролидин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=7,9 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,16-7,03 (м, 5H), 4,48 (т, J=5,3 Гц, 2H), 4,24 (дд, J=9,6, 5,5 Гц, 1H), 4,16 (д, J=13,1 Гц, 1H), 4,00 (д, J=11,2 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=6,2 Гц, 2H), 3,52-3,42 (м, 3H), 3,43-3,36 (м, 1H), 3,36 (с, 3H), 2,99-2,85 (м, 5H), 2,84-2,74 (м, 1H), 2,71-2,60 (м, 2H), 2,35-2,24 (м, 1H), 2,02-1,88 (м, 1H), 1,80-1,69 (м, 2H), 1,67-1,57 (м, 1H).
Пример 50: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2R)-2-(метоксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
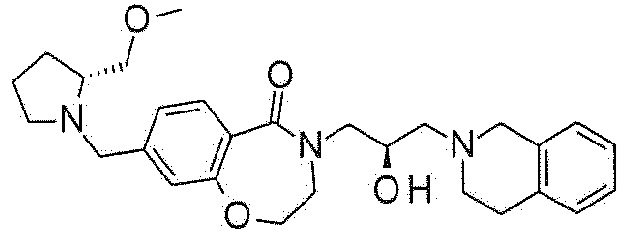
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что (2R)-2-(метоксиметил)пирролидин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=7,9 Гц, 1H), 7,19 (д, J=7,9 Гц, 1H), 7,15-7,02 (м, 5H), 4,48 (т, J=5,2 Гц, 2H), 4,30-4,19 (м, 1H), 4,15 (д, J=13,4 Гц, 1H), 4,00 (дд, J=13,9, 3,5 Гц, 1H), 3,76 (с, 2H), 3,72 (т, J=5,2 Гц, 2H), 3,51-3,41 (м, 3H), 3,41-3,37 (м, 1H), 3,36 (с, 3H), 2,98-2,84 (м, 5H), 2,83-2,74 (м, 1H), 2,71-2,60 (м, 2H), 2,35-2,22 (м, 1H), 2,02-1,89 (м, 1H), 1,80-1,68 (м, 2H), 1,68-1,54 (м, 1H).
Пример 51: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фторпирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
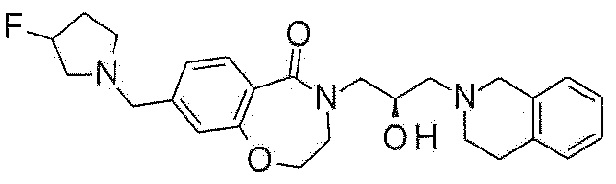
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3-фторпирролидин гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,0 Гц, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,16-7,04 (м, 5H), 5,30-5,22 (м, 1H), 5,16-5,08 (м, 1H), 4,49 (т, J=5,2 Гц, 2H), 4,30-4,19 (м, 1H), 4,00 (дд, J=13,7, 3,6 Гц, 1H), 3,77 (с, 2H), 3,74-3,62 (м, 4H), 3,46 (дд, J=13,9, 7,7 Гц, 1H), 2,98-2,89 (м, 4H), 2,71-2,62 (м, 2H), 2,47 (кв, J=8,0 Гц, 1H), 2,32-2,13 (м, 2H), 2,10-1,91 (м, 2H).
Пример 52: Синтез 8-[(3,3-дифторпирролидин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
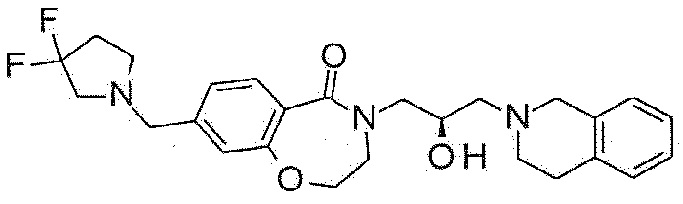
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 3,3-дифторпирролидин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=7,9 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,15-7,02 (м, 5H), 4,49 (т, J=5,0 Гц, 2H), 4,29-4,19 (м, 1H), 4,00 (дд, J=14,0, 3,6 Гц, 1H), 3,77 (с, 2H), 3,72 (т, J=4,9 Гц, 2H), 3,68 (с, 2H), 3,46 (дд, J=14,0, 7,7 Гц, 1H), 3,00-2,91 (м, 3H), 2,92-2,85 (м, 3H), 2,79 (т, J=7,0 Гц, 2H), 2,71-2,62 (м, 2H), 2,36-2,23 (м, 2H).
Пример 53: Синтез 8-[(4-ацетилпиперазин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
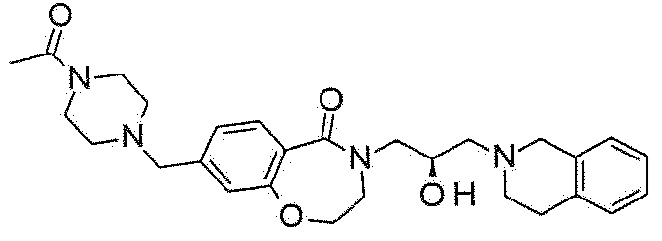
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 1-пиперазин-1-ил-этанон используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=7,9 Гц, 1H), 7,20 (д, J=8,0 Гц, 1H), 7,13 (д, J=4,4 Гц, 3H), 7,07 (с, 2H), 4,49 (т, J=5,1 Гц, 2H), 4,25 (с, 1H), 3,99 (дд, J=13,9, 3,7 Гц, 1H), 3,79 (с, 2H), 3,72 (т, J=5,3 Гц, 2H), 3,59 (дкв, J=10,4, 5,0 Гц, 7H), 3,47 (дд, J=13,9, 7,6 Гц, 1H), 2,93 (дд, J=14,0, 4,7 Гц, 4H), 2,74-2,63 (м, 2H), 2,48 (дт, J=19,1, 5,1 Гц, 5H), 2,11 (с, 3H).
Пример 54: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метилпиперазин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
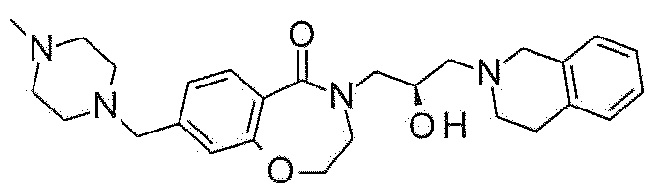
Пример 54-1: Синтез трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]метил]пиперазин-1-карбоксилата
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что трет-бутил пиперазин-1-карбоксилат используют вместо 3-метоксиазетидина гидрохлорида.
Пример 54-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пиперазин-1-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]метил]пиперазин-1-карбоксилат, полученный в примере 54-1, растворяют в метаноле, и туда медленно добавляют 4 M раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре, разбавляют диэтиловым эфиром, и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества.
Пример 54-3: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метилпиперазин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она
Полученный гидрохлорид растворяют в метаноле, и туда добавляют избыток параформальдегида и цианоборгидрид натрия, с последующим перемешиванием при комнатной температуре в течение 12 часов. Реакцию останавливают добавлением насыщенного водного раствора хлорида аммония к реакционному раствору, и 1 N водный раствор гидроксида натрия добавляют для подщелачивания. Смесь экстрагируют этилацетатом 3 раза и сушат над безводным сульфатом натрия. Бледно-желтую маслянистую жидкость, полученную удалением растворителя выпариванием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,9 Гц, 1H), 7,18 (д, J=8,0 Гц, 1H), 7,09 (дд, J=23,3, 5,1 Гц, 5H), 4,48 (т, J=5,3 Гц, 2H), 4,28-4,19 (м, 1H), 4,00 (д, J=13,6 Гц, 1H), 3,79-3,67 (м, 4H), 3,56 (с, 2H), 3,45 (дд, J=13,8, 7,6 Гц, 1H), 2,98-2,84 (м, 4H), 2,66 (д, J=6,5 Гц, 2H), 2,53 (шс, 6H), 2,31 (с, 3H).
Пример 55: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-окса-5-азабицикло[2,2,1]гептан-5-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
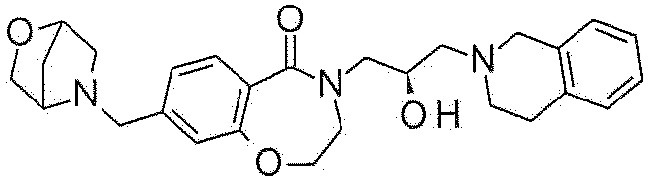
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 2-окса-5-азабицикло[2,2,1]гептан гидрохлорид используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,16-7,02 (м, 5H), 4,47 (дд, J=11,9, 6,9 Гц, 3H), 4,29-4,19 (м, 2H), 4,11 (д, J=7,8 Гц, 1H), 3,99 (дд, J=14,0, 3,6 Гц, 1H), 3,81 (д, J=6,1 Гц, 2H), 3,77 (с, 2H), 3,72 (т, J=5,3 Гц, 2H), 3,65 (д, J=7,9 Гц, 1H), 3,54 (с, 1H), 3,46 (дд, J=13,9, 7,6 Гц, 1H), 2,98-2,83 (м, 5H), 2,73-2,59 (м, 3H), 2,00-1,93 (м, 1H), 1,76 (д, J=10,2 Гц, 1H).
Пример 56: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиридилметокси)-2,3-дигидро-1,4-бензоксазепин-5-она

Пример 56-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (9,0 г, 21 ммоль), гидроксид калия (4,68 г, 83 ммоль), Pd(dba)2 (180 мг, 0,315 ммоль) и tBuXPhos (270 мг, 0,63 ммоль) растворяют в 80 мл 1,4-диоксана:дистиллированной воды (=1:1), и реакционный раствор загружают азотом. Реакционный раствор перемешивают при 100°C в течение 3 часов, и водный раствор хлористоводородной кислоты добавляют на ледяной бане для подкисления реакционного раствора до pH ~1. Водный слой промывают этилацетатом 3 раза, и добавляют водный раствор гидроксида натрия на ледяной бане для подщелачивания до pH 14, с последующим экстрагированием этилацетатом 3 раза. Объединенные органические слои сушат над безводным сульфатом магния и концентрируют при пониженном давлении с получением указанного в заголовке соединения в виде белого твердого вещества без дополнительной очистки.
Пример 56-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиридилметокси)-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 0,27 ммоль), полученный в примере 56-1, растворяют в диметилформамиде, и туда добавляют 60% гидрид натрия (33 мг, 0,81 ммоль) и 3-(хлорметил)пиридин гидрохлорид (66 мг, 0,41 ммоль) при комнатной температуре. Реакционный раствор перемешивают при комнатной температуре в течение 3 часов и экстрагируют добавлением этилацетата и дистиллированной воды. Маслянистую жидкость, полученную сушкой органического слоя над безводным сульфатом натрия и концентрированием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения (64 мг) в виде липкого белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 8,66 (с, 1H), 8,54 (д, J=4,9 Гц, 1H), 7,98 (д, J=8,0 Гц, 1H), 7,71 (д, J=8,8 Гц, 1H), 7,50 (т, J=6,6 Гц, 1H), 7,18-7,02 (м, 4H), 6,86 (д, J=8,8 Гц, 1H), 6,70 (д, J=2,9 Гц, 1H), 5,22 (с, 2H), 4,49 (т, J=5,0 Гц, 2H), 4,29-4,17 (м, 1H), 3,98 (дд, J=13,8, 3,2 Гц, 1H), 3,83-3,67 (м, 4H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 2,99-2,83 (м, 4H), 2,71-2,59 (м, 2H).
Пример 57: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиридилметокси)-2,3-дигидро-1,4-бензоксазепин-5-она
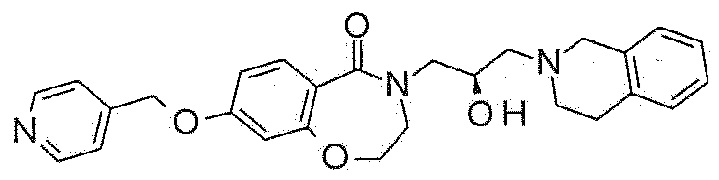
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что 4-(хлорметил)пиридин гидрохлорид используют вместо 3-(хлорметил)пиридина гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,60-8,51 (м, 2H), 7,71 (д, J=8,8 Гц, 1H), 7,54 (д, J=5,2 Гц, 2H), 7,18-7,00 (м, 4H), 6,86 (д, J=9,0 Гц, 1H), 6,68 (д, J=2,4 Гц, 1H), 5,25 (с, 2H), 4,48 (т, J=4,9 Гц, 2H), 4,27-4,18 (м, 1H), 3,98 (дд, J=14,0, 3,6 Гц, 1H), 3,81-3,67 (м, 4H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 2,99-2,83 (м, 4H), 2,71-2,60 (м, 2H).
Пример 58: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-фтор-4-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
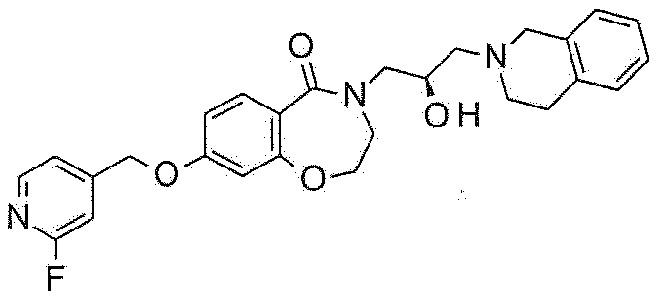
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что (2-фтор-4-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,22 (д, J=5,3 Гц, 1H), 7,71 (дд, J=8,8, 2,0 Гц, 1H), 7,40 (д, J=5,2 Гц, 1H), 7,18 (с, 1H), 7,12 (т, J=2,6 Гц, 3H), 7,06 (д, J=6,8 Гц, 1H), 6,87 (дд, J=8,9, 2,4 Гц, 1H), 6,69 (д, J=2,5 Гц, 1H), 5,27 (с, 2H), 4,49 (т, J=5,1 Гц, 2H), 4,24 (с, 1H), 3,97 (дд, J=13,7, 3,3 Гц, 1H), 3,79 (с, 2H), 3,74 (т, J=4,7 Гц, 2H), 3,44 (дд, J=13,9, 7,7 Гц, 1H), 2,93 (дд, J=11,6, 4,7 Гц, 4H), 2,68 (д, J=6,4 Гц, 2H).
Пример 59: Синтез 8-[(2,6-дихлор-4-пиридил)метокси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
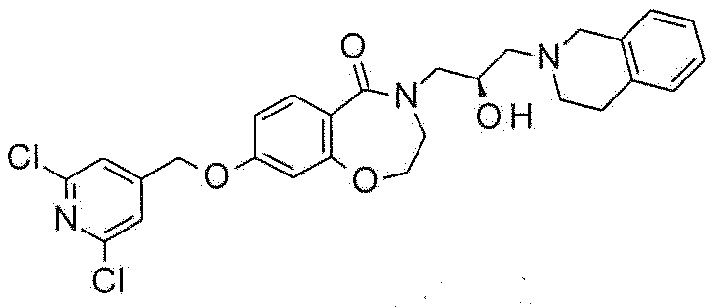
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что 2,6-дихлор-4-этилпиридин гидрохлорид используют вместо 3-(хлорметил)пиридин гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,72 (д, J=8,8 Гц, 1H), 7,53 (с, 2H), 7,23-7,06 (м, 2H), 7,06 (с, 1H), 6,86 (д, J=8,7 Гц, 1H), 6,69 (д, J=3,1 Гц, 1H), 5,23 (с, 2H), 4,64 (с, 2H), 4,50 (д, J=5,6 Гц, 2H), 4,23 (с, 1H), 4,00 (с, 1H), 3,75 (с, 4H), 3,55-3,37 (м, 1H), 2,93 (д, J=5,7 Гц, 2H), 2,88 (д, J=5,5 Гц, 2H), 2,64 (д, J=6,2 Гц, 2H).
Пример 60: Синтез 8-[(2,3-дифтор-4-пиридил)метокси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
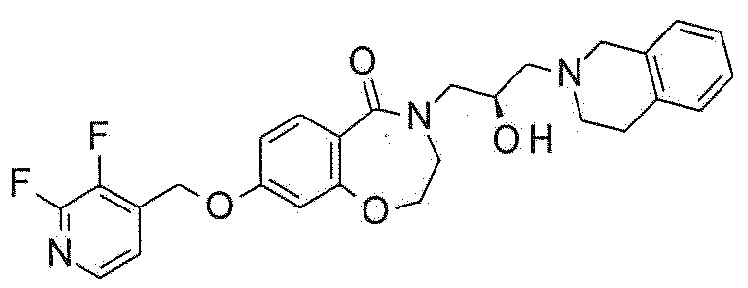
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что (2,3-дифтор-4-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,02 (д, J=5,0 Гц, 1H), 7,83-7,66 (м, 1H), 7,51 (д, J=5,3 Гц, 1H), 7,26-7,06 (м, 3H), 7,06 (д, J=6,5 Гц, 1H), 6,89-6,84 (м, 1H), 6,71 (д, J=2,9 Гц, 1H), 5,34 (с, 2H), 4,48 (д, J=5,4 Гц, 2H), 4,23 (д, J=7,0 Гц, 1H), 4,05-3,92 (м, 1H), 3,75 (д, J=10,7 Гц, 4H), 3,43 (дд, J=14,0, 7,7 Гц, 1H), 2,98-2,92 (м, 2H), 2,89 (д, J=5,3 Гц, 2H), 2,66 (д, J=6,1 Гц, 2H).
Пример 61: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(6-фтор-3-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
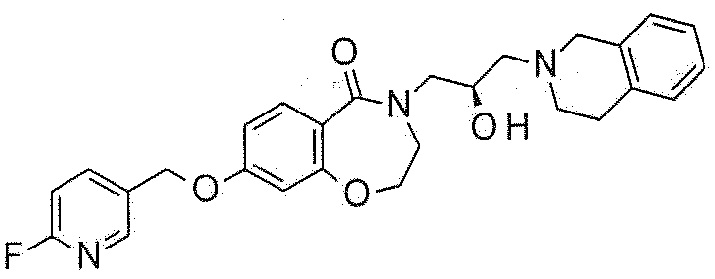
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что (6-фтор-3-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,32 (с, 1H), 8,07 (т, J=8,3 Гц, 1H), 7,70 (дд, J=8,8, 2,2 Гц, 1H), 7,20-7,03 (м, 5H), 6,85 (д, J=8,9 Гц, 1H), 6,69 (д, J=2,7 Гц, 1H), 5,18 (с, 2H), 4,48 (т, J=5,3 Гц, 2H), 4,23 (с, 1H), 3,98 (д, J=13,9 Гц, 1H), 3,75 (д, J=15,5 Гц, 4H), 3,43 (дд, J=14,0, 7,8 Гц, 1H), 3,03-2,82 (м, 4H), 2,66 (д, J=6,1 Гц, 2H).
Пример 62: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
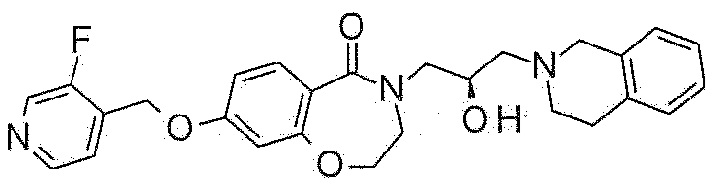
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что (3-фтор-4-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,50 (с, 1H), 8,44 (д, J=5,0 Гц, 1H), 7,72 (д, J=8,8 Гц, 1H), 7,65 (т, J=5,7 Гц, 1H), 7,16-7,02 (м, 4H), 6,87 (д, J=9,3 Гц, 1H), 6,70 (д, J=2,9 Гц, 1H), 5,32 (с, 2H), 4,49 (т, J=5,0 Гц, 2H), 4,27-4,18 (м, 1H), 3,98 (дд, J=13,7, 3,1 Гц, 1H), 3,79-3,67 (м, 4H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 2,97-2,83 (м, 4H), 2,69-2,59 (м, 2H).
Пример 63: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(5-фтор-2-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
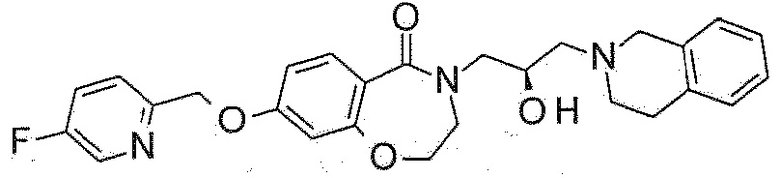
Указанное в заголовке соединение синтезируют по методике примера 56, за исключением того, что (5-фтор-2-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида в примере 56-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,49 (с, 1H), 7,68 (дд, J=15,0, 6,3 Гц, 3H), 7,16-7,03 (м, 4H), 6,85 (д, J=8,9 Гц, 1H), 6,67 (с, 1H), 5,22 (с, 2H), 4,48 (т, J=5,0 Гц, 2H), 4,28-4,16 (м, 1H), 3,98 (д, J=15,0 Гц, 1H), 3,78-3,69 (м, 4H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 3,00-2,83 (м, 4H), 2,70-2,61 (м, 2H).
Пример 64: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-тетрагидропиран-4-илокси-2,3-дигидро-1,4-бензоксазепин-5-она
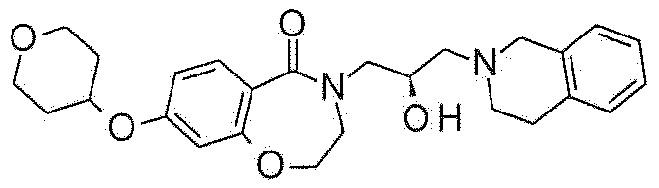
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 0,27 ммоль), полученный в примере 56-1, карбонат калия (112 мг, 0,81 ммоль) и 4-хлортетрагидропиран (0,12 мл, 0,81 ммоль) растворяют в диметилформамиде и перемешивают при 150°С в течение 12 часов или дольше. Реакционный раствор охлаждают до комнатной температуры, и туда добавляют дистиллированную воду, с последующим экстрагированием этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом натрия и концентрированием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения в виде липкого белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,7 Гц, 1H), 7,17-7,02 (м, 4H), 6,78 (д, J=8,9 Гц, 1H), 6,61 (с, 1H), 4,69-4,61 (м, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,27-4,19 (м, 1H), 4,02-3,91 (м, 3H), 3,78 (с, 2H), 3,77-3,70 (м, 2H), 3,62 (т, J=10,0 Гц, 2H), 3,43 (дд, J=13,5, 7,5 Гц, 1H), 2,99-2,82 (м, 4H), 2,72-2,60 (м, 2H), 2,11-2,01 (м, 2H), 1,79-1,67 (м, 2H).
Пример 65: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(тетрагидропиран-2-илметокси)-2,3-дигидро-1,4-бензоксазепин-5-она
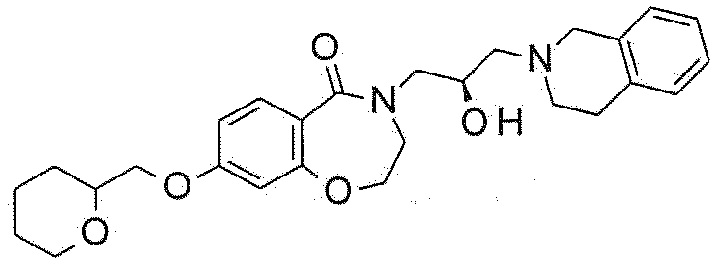
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что тетрагидропиран-2-илметил метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,65 (д, J=8,7 Гц, 1H), 7,12 (д, J=4,1 Гц, 3H), 7,06 (д, J=6,6 Гц, 1H), 6,73 (д, J=8,9 Гц, 1H), 6,55 (с, 1H), 4,47 (т, J=5,1 Гц, 2H), 4,23 (с, 1H), 4,05-3,94 (м, 1H), 3,89-3,67 (м, 7\6H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 2,92 (дд, J=17,2, 5,3 Гц, 4H), 2,66 (д, J=6,2 Гц, 2H), 1,89 (д, J=13,1 Гц, 2H), 1,84-1,66 (м, 4H), 1,49-1,19 (м, 4H), 1,11 (кв, J=12,1 Гц, 2H).
Пример 66: Синтез 8-(циклогексилметокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
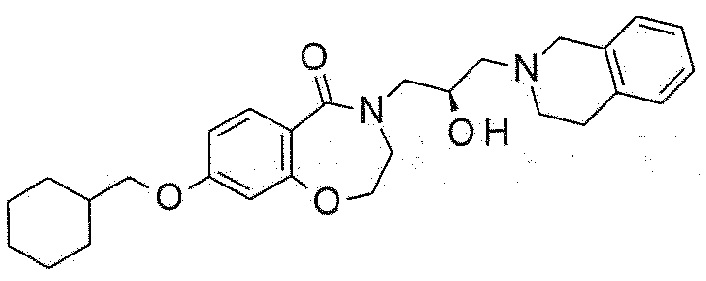
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что циклогексилметил метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,7 Гц, 1H), 7,13 (д, J=5,0 Гц, 4H), 7,06 (д, J=6,8 Гц, 1H), 6,76 (д, J=8,9 Гц, 1H), 6,59 (с, 1H), 4,46 (д, J=5,2 Гц, 2H), 4,28-4,17 (м, 1H), 3,99 (дд, J=14,1, 9,2 Гц, 4H), 3,88-3,66 (м, 6H), 3,53 (тд, J=10,8, 3,5 Гц, 1H), 3,43 (дд, J=14,0, 7,6 Гц, 1H), 2,94 (дд, J=9,6, 4,6 Гц, 4H), 2,74-2,57 (м, 2H), 1,92 (д, J=6,5 Гц, 1H), 1,69 (т, J=14,9 Гц, 1H), 1,61 (д, J=10,2 Гц, 3H), 1,51-1,41 (м, 1H).
Пример 67: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(тетрагидрофуран-2-илметокси)-2,3-дигидро-1,4-бензоксазепин-5-она
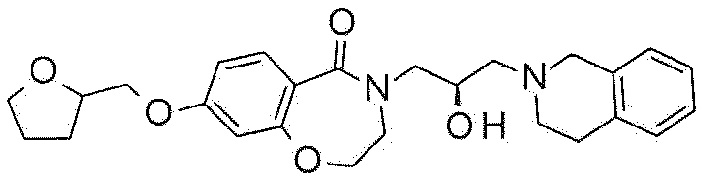
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что тетрагидрофуран-2-илметил метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,79 (д, J=8,7 Гц, 1H), 7,20-7,10 (м, 3H), 7,04 (д, J=6,7 Гц, 1H), 6,74 (д, J=8,8 Гц, 1H), 6,55 (с, 1H), 4,46 (кв, J=5,4 Гц, 2H), 4,30 (т, J=6,2 Гц, 1H), 4,13 (д, J=8,1 Гц, 1H), 4,06-3,90 (м, 4H), 3,86 (дд, J=15,1, 8,3 Гц, 2H), 3,77-3,60 (м, 3H), 3,53 (дд, J=14,1, 6,2 Гц, 1H), 3,02-2,87 (м, 4H), 2,84-2,51 (м, 3H), 2,31-2,05 (м, 1H), 1,98 (кв, J=6,9 Гц, 2H), 1,79 (дт, J=12,0, 7,2 Гц, 1H), 1,35-1,22 (м, 1H).
Пример 68: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
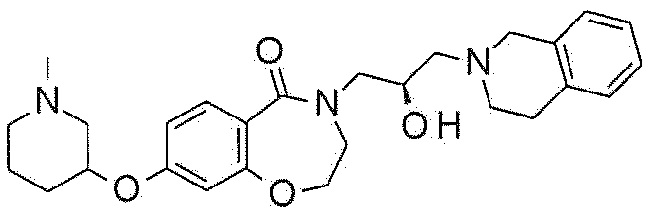
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что (1-метил-3-пиперидил) метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (дд, J=8,8, 1,9 Гц, 1H), 7,12 (д, J=2,9 Гц, 3H), 7,06 (д, J=6,6 Гц, 1H), 6,78 (д, J=8,7 Гц, 1H), 6,61 (д, J=2,9 Гц, 1H), 4,69-4,42 (м, 3H), 4,24 (с, 1H), 3,97 (дд, J=14,5, 3,4 Гц, 1H), 3,78 (с, 2H), 3,74 (д, J=5,5 Гц, 2H), 3,43 (дд, J=14,0, 7,6 Гц, 1H), 3,03-2,84 (м, 5H), 2,67 (д, J=6,6 Гц, 3H), 2,37 (д, J=2,0 Гц, 3H), 2,05 (д, J=9,8 Гц, 2H), 1,91 (д, J=16,4 Гц, 3H), 1,66 (д, J=20,3 Гц, 3H), 0,93 (кв, J=16,5, 10,6 Гц, 2H).
Пример 69: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
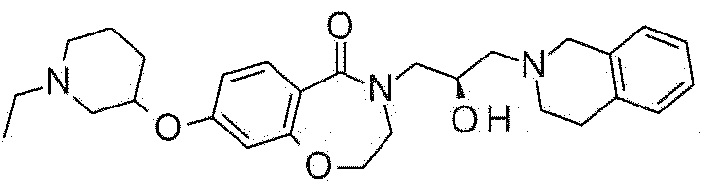
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что (1-этил-3-пиперидил) метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,17-7,02 (м, 4H), 6,78 (дд, J=8,5, 2,5 Гц, 1H), 6,61 (д, J=2,4 Гц, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,28-4,17 (м, 1H), 4,11-3,94 (м, 3H), 3,79-3,68 (м, 4H), 3,43 (дд, J=13,8, 7,6 Гц, 1H), 3,26 (шс, 1H), 3,18-3,09 (м, 1H), 3,04 (шс, 1H), 2,99-2,91 (м, 2H), 2,92-2,84 (м, 2H), 2,71-2,59 (м, 2H), 2,54 (шс, 1H), 2,44 (шс, 1H), 2,16-2,05 (м, 1H), 1,89 (дд, J=16,4, 8,7 Гц, 2H), 1,81-1,71 (м, 1H), 1,20 (т, J=7,3 Гц, 3H).
Пример 70: Синтез 8-[(1-ацетил-4-пиперидил)метокси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
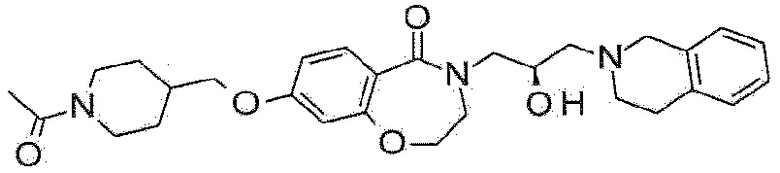
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что (1-ацетил-4-пиперидил)метил метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,8 Гц, 1H), 7,17-7,01 (м, 4H), 6,79-6,71 (м, 1H), 6,58 (с, 1H), 4,59 (д, J=13,3 Гц, 1H), 4,53-4,41 (м, 2H), 4,27-4,17 (м, 1H), 3,98 (д, J=13,6 Гц, 2H), 3,91 (д, J=6,3 Гц, 2H), 3,83-3,64 (м, 4H), 3,42 (дд, J=13,9, 7,6 Гц, 1H), 3,21-3,12 (м, 1H), 2,98-2,82 (м, 4H), 2,75-2,60 (м, 3H), 2,13 (с, 3H), 1,92 (дд, J=25,3, 14,0 Гц, 2H), 1,45-1,21 (м, 3H).
Пример 71: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2,2,2-трифторэтокси)-2,3-дигидро-1,4-бензоксазепин-5-она
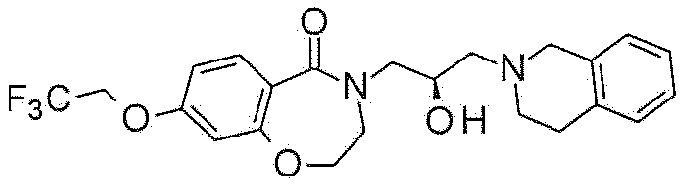
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что 2,2,2-трифторэтил метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,73 (д, J=8,8 Гц, 1H), 7,19-6,99 (м, 4H), 6,84 (д, J=9,0 Гц, 1H), 6,69 (с, 1H), 4,61 (кв, J=8,4 Гц, 2H), 4,50 (т, J=5,1 Гц, 2H), 4,27-4,17 (м, 1H), 3,99 (д, J=13,6 Гц, 1H), 3,81-3,67 (м, 4H), 3,43 (дд, J=13,9, 7,4 Гц, 1H), 3,00-2,82 (м, 4H), 2,65 (д, J=6,2 Гц, 2H).
Пример 72: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(диметиламино)этокси]-2,3-дигидро-1,4-бензоксазепин-5-она
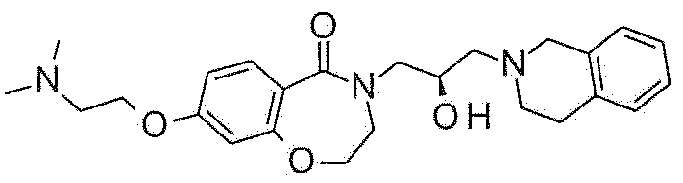
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что 2-хлор-N, N-диметилэтанамин гидрохлорид используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,6 Гц, 1H), 7,19-7,01 (м, 4H), 6,79 (д, J=9,0 Гц, 1H), 6,62 (с, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,28-4,19 (м, 1H), 4,16 (т, J=5,5 Гц, 2H), 3,98 (д, J=13,8 Гц, 1H), 3,82-3,69 (м, 4H), 3,43 (дд, J=13,8, 7,8 Гц, 1H), 2,99-2,85 (м, 4H), 2,86-2,77 (м, 2H), 2,69-2,60 (м, 2H), 2,38 (с, 6H).
Пример 73: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-морфолиноэтокси)-2,3-дигидро-1,4-бензоксазепин-5-она
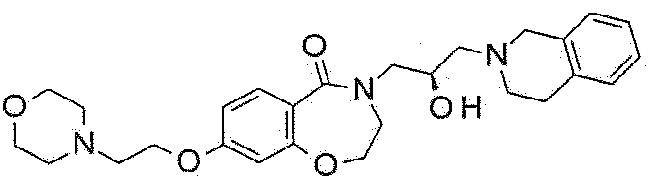
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что 4-(2-хлорэтил)морфолин гидрохлорид используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,78 (д, J=8,7 Гц, 1H), 7,13 (дд, J=9,7, 5,6 Гц, 3H), 7,01 (д, J=6,7 Гц, 1H), 6,69 (д, J=8,7 Гц, 1H), 6,50 (с, 1H), 4,45 (д, J=4,7 Гц, 2H), 4,12 (т, J=5,6 Гц, 3H), 3,93 (д, J=14,1 Гц, 1H), 3,83 (д, J=14,9 Гц, 1H), 3,73 (д, J=4,8 Гц, 6H), 3,63 (д, J=14,8 Гц, 1H), 3,51 (дд, J=14,1, 6,2 Гц, 1H), 2,93 (дкв, J=13,3, 5,5 Гц, 3H), 2,81 (т, J=5,7 Гц, 3H), 2,77-2,71 (м, 1H), 2,66 (дд, J=12,3, 4,0 Гц, 1H), 2,57 (кв, J=6,0, 5,3 Гц, 5H), 1,31-1,20 (м, 1H).
Пример 74: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(2-оксопирролидин-1-ил)этокси]-2,3-дигидро-1,4-бензоксазепин-5-она
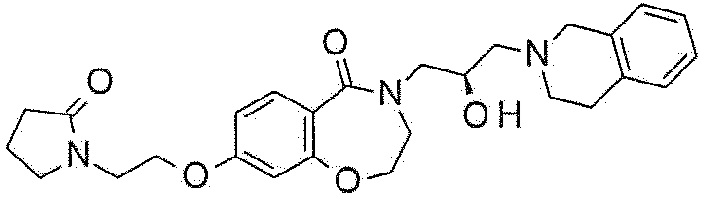
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что 2-(2-оксопирролидин-1-ил)этил метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,79 (д, J=8,7 Гц, 1H), 7,13 (д, J=9,0 Гц, 3H), 7,01 (д, J=7,0 Гц, 1H), 6,67 (д, J=8,9 Гц, 1H), 6,48 (с, 1H), 4,46 (д, J=4,8 Гц, 3H), 4,12 (д, J=5,3 Гц, 4H), 3,88 (дд, J=41,5, 14,5 Гц, 2H), 3,79-3,43 (м, 8H), 2,93 (д, J=16,8 Гц, 3H), 2,70 (дд, J=32,9, 9,3 Гц, 2H), 2,60-2,48 (м, 1H), 2,39 (т, J=8,1 Гц, 2H), 2,12-1,97 (м, 3H), 1,26 (с, 1H).
Пример 75: Синтез 2-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]-N, N-диэтилацетамида
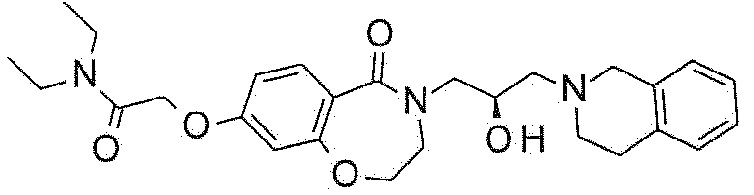
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что [2-(диэтиламино)-2-оксоэтил]метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,79 (д, J=8,7 Гц, 1H), 7,13 (д, J=8,9 Гц, 3H), 7,02 (д, J=6,8 Гц, 1H), 6,74 (д, J=8,9 Гц, 1H), 6,55 (с, 1H), 4,69 (с, 2H), 4,53-4,42 (м, 2H), 4,12 (д, J=7,8 Гц, 1H), 3,93 (д, J=14,1 Гц, 1H), 3,83 (д, J=14,9 Гц, 1H), 3,76-3,57 (м, 3H), 3,52 (дд, J=14,1, 6,1 Гц, 1H), 3,39 (дкв, J=14,6, 7,0 Гц, 4H), 2,93 (д, J=16,7 Гц, 3H), 2,74 (д, J=5,6 Гц, 1H), 2,66 (д, J=12,4 Гц, 1H), 2,55 (т, J=11,3 Гц, 1H), 2,05 (с, 1H), 1,30-1,20 (м, 3H), 1,15 (т, J=7,2 Гц, 3H).
Пример 76: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(6-оксо-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
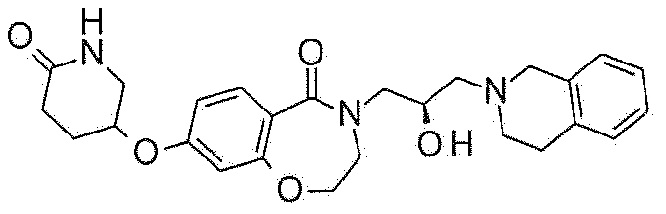
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что (6-оксо-3-пиперидил)метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,17-7,02 (м, 4H), 6,82-6,75 (м, 1H), 6,62 (с, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,28-4,17 (м, 1H), 4,13-4,02 (м, 2H), 4,02-3,92 (м, 2H), 3,79-3,67 (м, 4H), 3,42 (дд, J=13,8, 7,6 Гц, 1H), 2,98-2,84 (м, 4H), 2,70-2,59 (м, 2H), 2,54-2,43 (м, 1H), 2,38 (дд, J=17,1, 13,5 Гц, 2H), 2,08-1,97 (м, 1H).
Пример 77: Синтез трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]пиперидин-1-карбоксилата
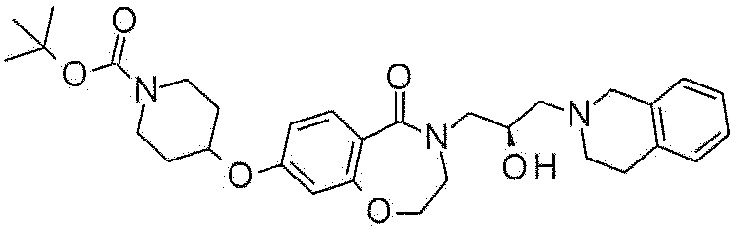
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что трет-бутил 4-метилсульфонилоксипиперидин-1-карбоксилат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,7 Гц, 1H), 7,09 (д, J=19,7 Гц, 4H), 6,79 (д, J=9,0 Гц, 1H), 6,62 (с, 1H), 4,70-4,60 (м, 1H), 4,51-4,44 (м, 2H), 4,27-4,19 (м, 1H), 3,98 (д, J=14,4 Гц, 1H), 3,85-3,64 (м, 6H), 3,45 (д, J=7,4 Гц, 1H), 2,98-2,92 (м, 2H), 2,93-2,86 (м, 2H), 2,71-2,62 (м, 2H), 2,04-1,89 (м, 3H), 1,76-1,60 (м, 2H), 1,49 (с, 9H).
Пример 78: Синтез 8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
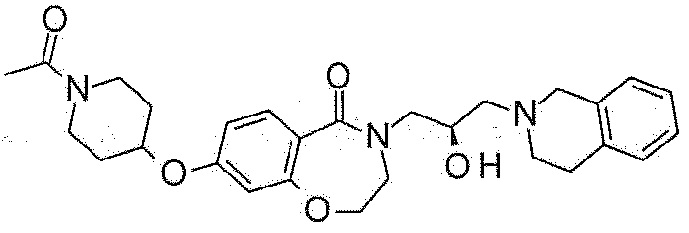
Пример 78-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]пиперидин-1-карбоксилат, полученный в примере 77, растворяют в метаноле, и туда медленно добавляют 4 M раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре, разбавляют диэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества.
Пример 78-2: Синтез 8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 78-1, растворяют в дихлорметане, и туда добавляют триметиламин и уксусный ангидрид, с последующим перемешиванием при комнатной температуре в течение 3 часов. В реакционную смесь добавляют насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом натрия и концентрированием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения в виде белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 7,58 (д, J=8,8 Гц, 1H), 7,27-7,05 (м, 4H), 6,70 (дд, J=9,0, 2,4 Гц, 1H), 6,54 (д, J=1,9 Гц, 1H), 4,65-4,49 (м, 2H), 4,47-4,28 (м, 4H), 3,81-3,57 (м, 7H), 3,48-3,33 (м, 3H), 3,33-3,23 (м, 2H), 3,12 (кв, J=7,4 Гц, 2H), 2,03 (с, 3H), 1,97-1,80 (м, 3H), 1,77-1,54 (м, 2H).
Пример 79: Синтез 8-[(1-ацетил-3-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
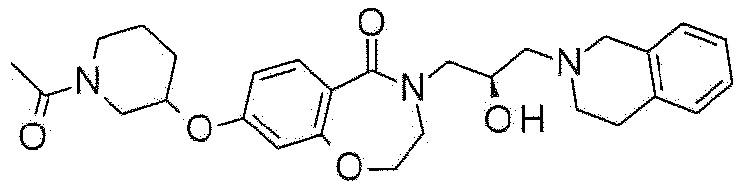
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что (1-ацетил-3-пиперидил)метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (диастереомерная смесь, 400 MГц, Метанол-d4) δ 7,72-7,65 (м, 2H), 7,17-7,02 (м, 8H), 6,83-6,74 (м, 2H), 6,61 (с, 2H), 4,68-4,59 (м, 1H), 4,48 (кв, J=4,6 Гц, 5H), 4,23 (с, 2H), 4,10-3,93 (м, 4H), 3,86 (дд, J=14,3, 4,8 Гц, 1H), 3,81-3,68 (м, 8H), 3,66-3,48 (м, 4H), 3,43 (дд, J=14,0, 7,7 Гц, 2H), 3,20 (т, J=11,3 Гц, 1H), 2,99-2,84 (м, 8H), 2,71-2,59 (м, 4H), 2,17-1,95 (м, 9H), 1,93-1,77 (м, 3H), 1,70-1,52 (м, 2H).
Пример 80: Синтез 8-(1-ацетилпирролидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
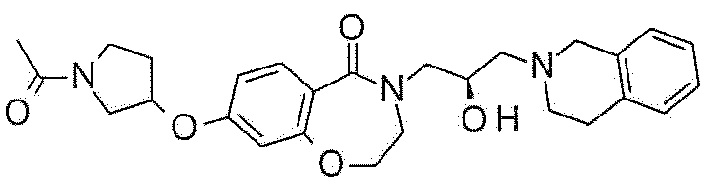
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что трет-бутил 4-метилсульфонилоксипирролидин-1-карбоксилат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (дд, J=8,8, 3,8 Гц, 1H), 7,18-7,00 (м, 4H), 6,77 (т, J=8,6 Гц, 1H), 6,60 (дд, J=5,8, 2,3 Гц, 1H), 5,19-5,04 (м, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,30-4,18 (м, 1H), 3,97 (дд, J=14,0, 3,5 Гц, 1H), 3,92-3,59 (м, 7H), 3,54-3,37 (м, 2H), 3,00-2,84 (м, 4H), 2,73-2,59 (м, 2H), 2,35-2,23 (м, 1H), 2,25-2,15 (м, 1H), 2,09 (д, J=15,8 Гц, 3H).
Пример 81: Синтез 8-[(3R)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
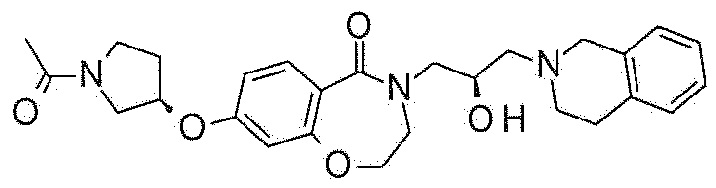
Указанное в заголовке соединение синтезируют по методике примера 80, за исключением того, что трет-бутил (3S)-3-метилсульфонилоксипирролидин-1-карбоксилат используют вместо трет-бутил 4-метилсульфонилоксипирролидин-1-карбоксилата.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (д, J=8,8 Гц, 1H), 7,09 (д, J=20,4 Гц, 4H), 6,81-6,72 (м, 1H), 6,61 (д, J=5,8 Гц, 1H), 5,13 (д, J=22,4 Гц, 1H), 4,52-4,44 (м, 2H), 4,29-4,18 (м, 1H), 3,98 (д, J=14,1 Гц, 1H), 3,83-3,62 (м, 8H), 3,43 (дд, J=14,2, 7,5 Гц, 1H), 2,99-2,81 (м, 4H), 2,70-2,59 (м, 2H), 2,36-2,27 (м, 1H), 2,27-2,16 (м, 1H), 2,09 (д, J=15,7 Гц, 3H).
Пример 82: Синтез 8-[(3S)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
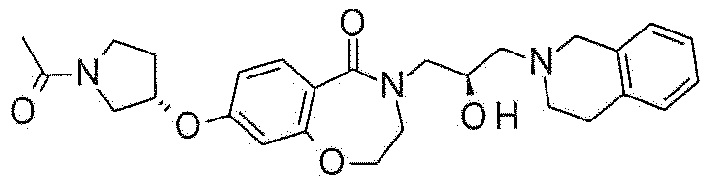
Указанное в заголовке соединение синтезируют по методике примера 80, за исключением того, что трет-бутил (3R)-3-метилсульфонилоксипирролидин-1-карбоксилат используют вместо трет-бутил 4-метилсульфонилоксипирролидин-1-карбоксилата.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,6 Гц, 1H), 7,17-7,02 (м, 4H), 6,77 (т, J=7,5 Гц, 1H), 6,61 (д, J=4,8 Гц, 1H), 5,13 (д, J=22,4 Гц, 1H), 4,53-4,43 (м, 2H), 4,22 (дд, J=12,1, 5,5 Гц, 1H), 3,98 (д, J=13,4 Гц, 1H), 3,91-3,61 (м, 8H), 3,43 (дд, J=13,9, 7,9 Гц, 1H), 2,99-2,82 (м, 4H), 2,70-2,58 (м, 2H), 2,37-2,26 (м, 1H), 2,26-2,16 (м, 1H), 2,09 (д, J=15,6 Гц, 3H).
Пример 83: Синтез 8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
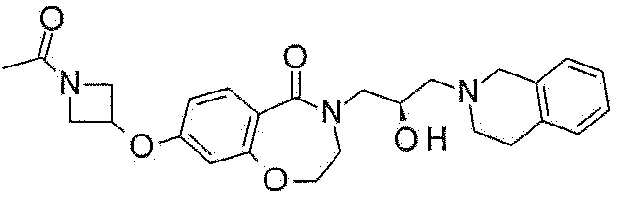
Пример 83-1: Синтез 8-(азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный заменой 4-хлортетрагидропирана на трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилат в примере 64, в качестве исходного материала, используют по методике примера 78-1 с получением указанного в заголовке соединения.
Пример 83-2: Синтез 8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
8-(Азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 83-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,71 (д, J=8,7 Гц, 1H), 7,19-7,00 (м, 4H), 6,69 (дд, J=8,7, 2,2 Гц, 1H), 6,49 (д, J=2,3 Гц, 1H), 5,09 (дт, J=12,0, 6,5 Гц, 1H), 4,69-4,61 (м, 1H), 4,49 (т, J=5,0 Гц, 2H), 4,42 (дд, J=11,0, 6,6 Гц, 1H), 4,29-4,18 (м, 2H), 4,04-3,91 (м, 2H), 3,82-3,67 (м, 4H), 3,43 (дд, J=13,7, 7,7 Гц, 1H), 3,00-2,83 (м, 4H), 2,72-2,58 (м, 2H), 1,93 (с, 3H).
Пример 84: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-пропаноилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она
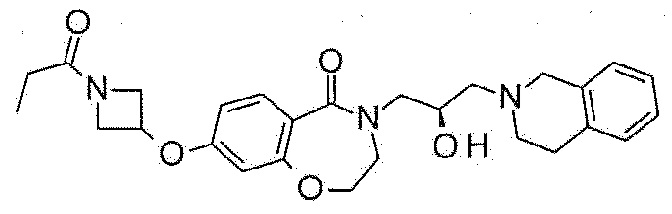
8-(Азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 83-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения, за исключением того, что пропаноил хлорид используют вместо уксусного ангидрида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,71 (д, J=8,7 Гц, 1H), 7,21-7,01 (м, 4H), 6,72-6,65 (м, 1H), 6,49 (д, J=2,4 Гц, 1H), 5,15-5,05 (м, 1H), 4,69-4,59 (м, 1H), 4,49 (т, J=5,0 Гц, 2H), 4,46-4,38 (м, 1H), 4,28-4,17 (м, 2H), 4,03-3,90 (м, 2H), 3,85-3,68 (м, 4H), 3,44 (дд, J=13,9, 7,7 Гц, 1H), 3,02-2,82 (м, 4H), 2,75-2,62 (м, 2H), 2,21 (кв, J=7,5 Гц, 2H), 1,12 (т, J=7,5 Гц, 3H).
Пример 85: Синтез 8-[1-(циклопропанкарбонил)азетидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
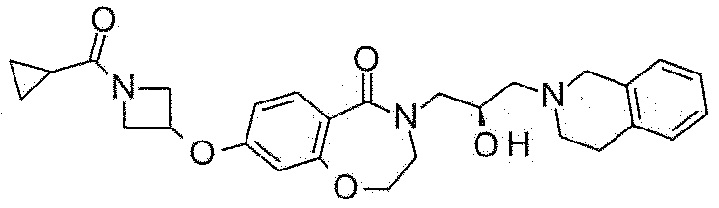
8-(Азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 83-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения, за исключением того, что циклопропанкарбонил хлорид используют вместо уксусного ангидрида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,71 (д, J=8,7 Гц, 1H), 7,20-7,02 (м, 4H), 6,71 (д, J=8,4 Гц, 1H), 6,50 (с, 1H), 5,19-5,08 (м, 1H), 4,82-4,74 (м, 1H), 4,49 (т, J=5,1 Гц, 2H), 4,45-4,37 (м, 1H), 4,33 (д, J=9,9 Гц, 1H), 4,29-4,16 (м, 1H), 3,97 (д, J=12,2 Гц, 2H), 3,84-3,68 (м, 4H), 3,44 (дд, J=13,9, 7,7 Гц, 1H), 3,00-2,84 (м, 4H), 2,74-2,61 (м, 2H), 1,67-1,56 (м, 1H), 0,93-0,78 (м, 4H).
Пример 86: Синтез метил 3-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]азетидин-1-карбоксилата
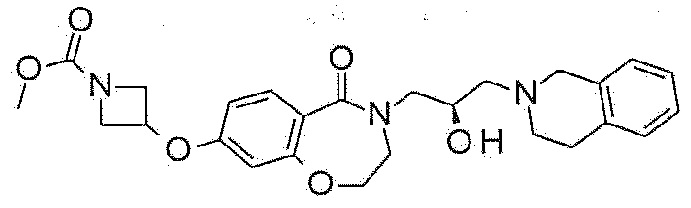
8-(Азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 83-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения, за исключением того, что метил хлорформиат используют вместо уксусного ангидрида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (д, J=8,8 Гц, 1H), 7,16-7,00 (м, 4H), 6,66 (д, J=8,7 Гц, 1H), 6,46 (с, 1H), 5,10-5,00 (м, 1H), 4,54-4,35 (м, 4H), 4,28-4,16 (м, 1H), 4,06-3,90 (м, 3H), 3,78-3,70 (м, 4H), 3,69 (с, 3H), 3,41 (дд, J=14,0, 7,7 Гц, 1H), 2,98-2,81 (м, 4H), 2,69-2,58 (м, 2H).
Пример 87: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
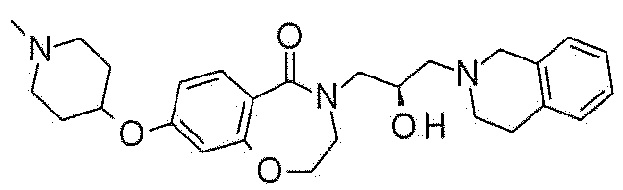
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид (100 мг, 0,19 ммоль), полученный в примере 78-1, растворяют в метаноле, и туда добавляют параформальдегид (57 мг, 1,9 ммоль) и цианоборгидрид натрия (36 мг, 0,57 ммоль). Реакционный раствор перемешивают при комнатной температуре до завершения реакции, и добавляют насыщенный водный раствор хлорида аммония, перемешивают в течение 30 минут, и затем 1 N водный раствор гидроксида натрия добавляют для подщелачивания. Смесь экстрагируют этилацетатом 3 раза и сушат над безводным сульфатом натрия. Бледно-желтую маслянистую жидкость, полученную удалением растворителя выпариванием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения в виде белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,8 Гц, 1H), 7,16-7,00 (м, 4H), 6,76 (дд, J=8,8, 2,4 Гц, 1H), 6,58 (д, J=2,4 Гц, 1H), 4,56-4,41 (м, 3H), 4,27-4,16 (м, 1H), 3,97 (дд, J=13,9, 3,5 Гц, 1H), 3,79-3,63 (м, 4H), 3,41 (дд, J=13,9, 7,7 Гц, 1H), 2,98-2,88 (м, 2H), 2,90-2,80 (м, 2H), 2,79-2,68 (м, 2H), 2,68-2,56 (м, 2H), 2,49-2,36 (м, 2H), 2,32 (с, 3H), 2,10-2,01 (м, 3H), 1,90-1,76 (м, 2H).
Пример 88: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
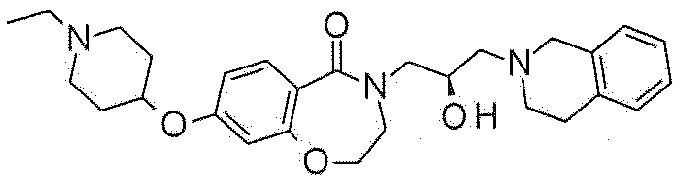
Указанное в заголовке соединение синтезируют по методике примера 87, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,7 Гц, 1H), 7,17-7,03 (м, 4H), 6,81-6,74 (м, 1H), 6,60 (с, 1H), 4,61-4,51 (м, 1H), 4,47 (т, J=5,0 Гц, 2H), 4,28-4,16 (м, 1H), 4,02-3,92 (м, 1H), 3,82-3,68 (м, 4H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 3,01-2,80 (м, 6H), 2,74-2,51 (м, 6H), 2,15-2,02 (м, 2H), 1,96-1,78 (м, 2H), 1,19 (т, J=7,2 Гц, 3H).
Пример 89: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-изопропил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
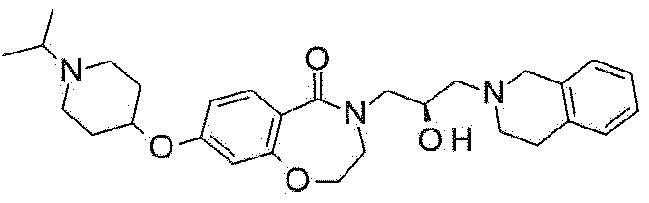
Указанное в заголовке соединение синтезируют по методике примера 87, за исключением того, что ацетон используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,7 Гц, 1H), 7,16-7,01 (м, 4H), 6,78 (д, J=8,8 Гц, 1H), 6,61 (с, 1H), 4,63-4,51 (м, 1H), 4,47 (т, J=4,9 Гц, 2H), 4,22 (дд, J=7,8, 4,4 Гц, 1H), 3,97 (д, J=13,9 Гц, 1H), 3,81-3,66 (м, 4H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 3,10-2,98 (м, 2H), 2,98-2,82 (м, 4H), 2,83-2,70 (м, 2H), 2,69-2,58 (м, 2H), 2,18-1,98 (м, 3H), 1,95-1,82 (м, 2H), 1,21 (д, J=6,5 Гц, 6H).
Пример 90: Синтез 8-[(1-циклопропил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
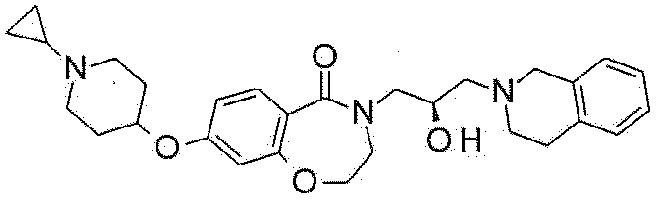
Указанное в заголовке соединение синтезируют по методике примера 87 при 60°C, за исключением того, что (1-этоксициклопропокси)триметилсилан используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=9,0 Гц, 1H), 7,18-7,02 (м, 4H), 6,76 (д, J=8,8 Гц, 1H), 6,59 (с, 1H), 4,58-4,41 (м, 3H), 4,28-4,17 (м, 1H), 3,97 (дд, J=14,0, 3,6 Гц, 1H), 3,83-3,66 (м, 4H), 3,42 (дд, J=14,0, 7,7 Гц, 1H), 3,01-2,78 (м, 6H), 2,73-2,51 (м, 4H), 2,10-1,96 (м, 2H), 1,86-1,66 (м, 3H), 0,59-0,39 (м, 4H).
Пример 91: Синтез 8-[(1-циклобутил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
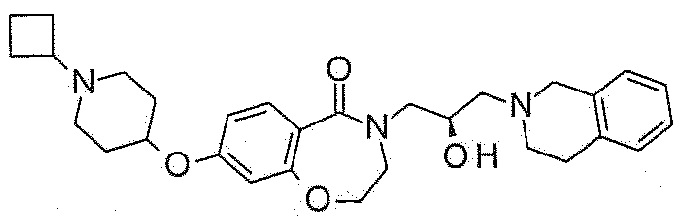
Указанное в заголовке соединение синтезируют по методике примера 87, за исключением того, что циклобутанон используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,10 (д, J=21,0 Гц, 4H), 6,77 (д, J=8,9 Гц, 1H), 6,60 (с, 1H), 4,63-4,50 (м, 2H), 4,47 (д, J=5,3 Гц, 2H), 4,29-4,18 (м, 1H), 3,97 (д, J=14,5 Гц, 1H), 3,80 (с, 2H), 3,77-3,67 (м, 2H), 3,44 (дд, J=14,0, 7,5 Гц, 1H), 3,05-2,88 (м, 5H), 2,86-2,74 (м, 2H), 2,71-2,63 (м, 2H), 2,56-2,35 (м, 3H), 2,22-2,11 (м, 2H), 2,11-1,93 (м, 4H), 1,92-1,74 (м, 4H).
Пример 92: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(оксетан-3-ил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
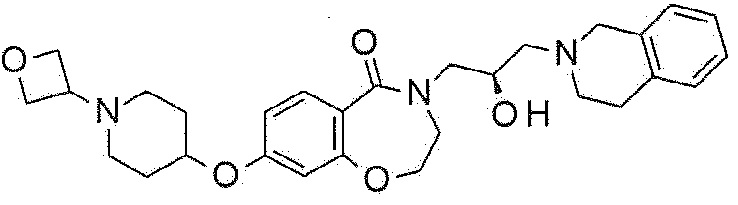
Указанное в заголовке соединение синтезируют по методике примера 87, за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,75-7,56 (м, 1H), 7,12 (д, J=3,1 Гц, 3H), 7,06 (д, J=6,7 Гц, 1H), 6,76 (д, J=8,8 Гц, 1H), 6,58 (д, J=2,1 Гц, 1H), 4,71 (т, J=6,7 Гц, 2H), 4,62 (т, J=6,3 Гц, 2H), 4,54-4,41 (м, 3H), 4,23 (с, 1H), 4,02-3,91 (м, 1H), 3,79 (с, 2H), 3,73 (с, 2H), 3,55 (т, J=6,5 Гц, 1H), 3,43 (дд, J=14,0, 7,6 Гц, H), 2,93 (дд, J=11,3, 4,6 Гц, 4H), 2,68 (д, J=6,6 Гц, 2H), 2,61 (с, 2H), 2,28 (т, J=10,0 Гц, 2H), 2,04 (д, J=10,2 Гц, 2H), 1,89 (д, J=36,1 Гц, 2H).
Пример 93: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-метилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она
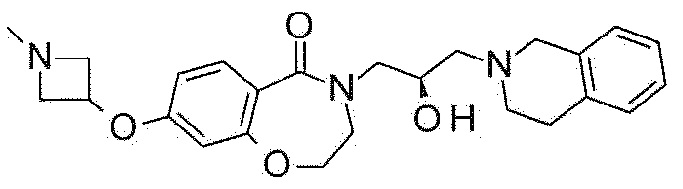
Продукт, полученный в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,5 Гц, 1H), 7,09 (д, J=19,7 Гц, 4H), 6,65 (д, J=8,9 Гц, 1H), 6,44 (с, 1H), 4,86 (т, J=5,6 Гц, 3H), 4,47 (т, J=5,2 Гц, 2H), 4,29-4,17 (м, 1H), 3,98 (дд, J=13,7, 2,5 Гц, 1H), 3,83 (т, J=7,5 Гц, 2H), 3,78-3,69 (м, 4H), 3,42 (дд, J=13,9, 7,8 Гц, 1H), 3,28 (дд, J=8,6, 5,1 Гц, 3H), 2,98-2,82 (м, 4H), 2,70-2,58 (м, 2H), 2,44 (с, 3H).
Пример 94: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-этилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она
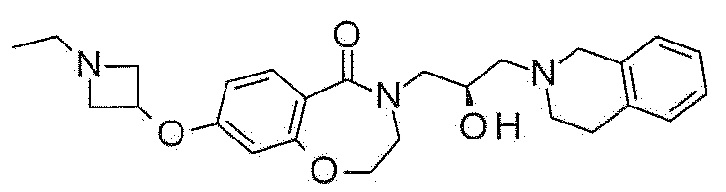
Продукт, полученный в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,57 (д, J=8,7 Гц, 1H), 7,05-6,91 (м, 4H), 6,55 (д, J=8,7 Гц, 1H), 6,34 (д, J=2,9 Гц, 1H), 4,36 (т, J=5,0 Гц, 2H), 4,15-4,04 (м, 1H), 3,90-3,80 (м, 1H), 3,73 (т, J=7,7 Гц, 2H), 3,66 (с, 2H), 3,61 (т, J=5,2 Гц, 2H), 3,31 (дд, J=13,9, 7,7 Гц, 1H), 3,17 (дд, J=8,8, 4,9 Гц, 4H), 2,87-2,73 (м, 4H), 2,60-2,47 (м, 4H), 1,96-1,85 (м, 3H), 0,92 (т, J=7,2 Гц, 3H).
Пример 95: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-изопропилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она
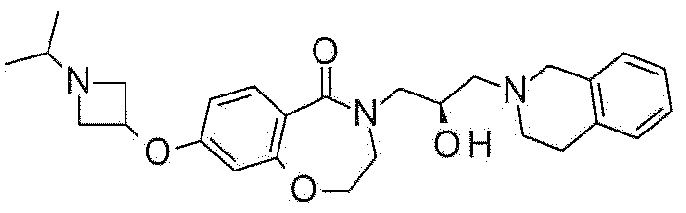
Продукт, полученный в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетон используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,7 Гц, 1H), 7,18-7,01 (м, 4H), 6,67 (д, J=8,9 Гц, 1H), 6,46 (с, 1H), 4,88-4,78 (м, 1H), 4,48 (т, J=5,2 Гц, 2H), 4,28-4,17 (м, 1H), 4,02-3,93 (м, 1H), 3,86-3,65 (м, 6H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 3,24 (т, J=7,0 Гц, 2H), 3,00-2,83 (м, 4H), 2,72-2,60 (м, 2H), 2,57-2,46 (м, 1H), 1,01 (д, J=6,2 Гц, 6H).
Пример 96: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(оксетан-3-илил)азетидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он
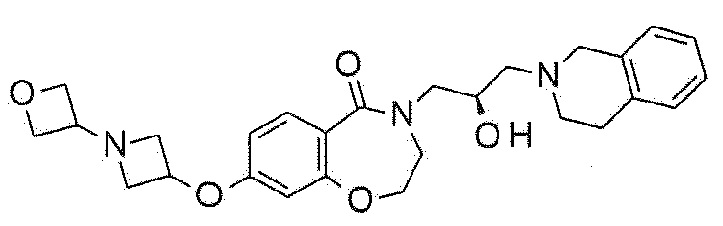
Продукт, полученный в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,7 Гц, 1H), 7,19-7,02 (м, 4H), 6,67 (д, J=8,7 Гц, 1H), 6,47 (с, 1H), 4,77 (т, J=6,9 Гц, 2H), 4,50 (дт, J=15,6, 5,6 Гц, 4H), 4,25 (д, J=6,3 Гц, 1H), 4,01-3,83 (м, 4H), 3,82 (с, 2H), 3,73 (д, J=5,0 Гц, 2H), 3,44 (дд, J=13,9, 7,5 Гц, 1H), 2,95 (с, 4H), 2,69 (д, J=6,7 Гц, 2H).
Пример 97: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этилазетидин-3-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
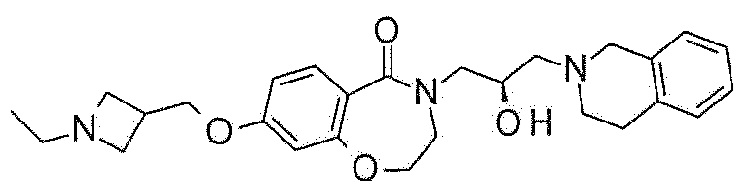
Продукт, полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 3-(метилсульфонилоксиметил)азетидин-1-карбоксилат, в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,7 Гц, 1H), 7,17-7,01 (м, 4H), 6,76 (д, J=8,8 Гц, 1H), 6,60 (с, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,27-4,17 (м, 1H), 4,14 (д, J=6,4 Гц, 2H), 3,98 (дд, J=13,7, 3,5 Гц, 1H), 3,80-3,67 (м, 4H), 3,53-3,37 (м, 3H), 3,15 (т, J=7,2 Гц, 2H), 3,01-2,89 (м, 3H), 2,90-2,80 (м, 2H), 2,70-2,61 (м, 2H), 2,57 (кв, J=7,4 Гц, 2H), 1,00 (т, J=7,2 Гц, 3H).
Пример 98: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-метилпирролидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она
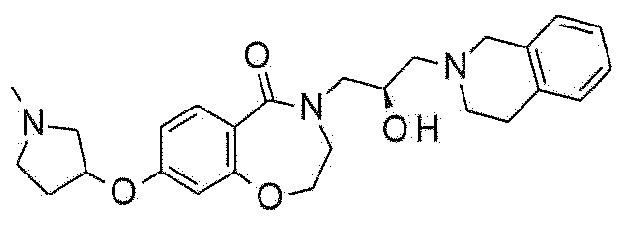
Продукт, полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 4-метилсульфонилоксипирролидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (дд, J=8,7, 2,0 Гц, 1H), 7,11 (д, J=3,3 Гц, 3H), 7,05 (д, J=6,7 Гц, 1H), 6,72 (дд, J=8,8, 2,4 Гц, 1H), 6,53 (д, J=2,4 Гц, 1H), 4,95 (д, J=6,9 Гц, 1H), 4,47 (т, J=5,3 Гц, 2H), 4,22 (д, J=6,3 Гц, 1H), 3,98 (дд, J=14,0, 3,4 Гц, 1H), 3,74 (д, J=9,3 Гц, 4H), 3,42 (дд, J=14,0, 7,7 Гц, 1H), 3,00-2,81 (м, 8H), 2,64 (д, J=6,2 Гц, 2H), 2,53-2,45 (м, 1H), 2,41 (с, 3H), 2,07-1,93 (м, 2H), 1,32 (д, J=6,0 Гц, 1H).
Пример 99: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-этилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
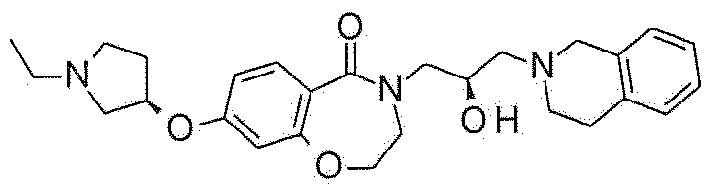
Продукт, полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил (3S)-3-метилсульфонилоксипирролидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=8,7 Гц, 1H), 7,10-6,95 (м, 4H), 6,66 (д, J=8,9 Гц, 1H), 6,48 (с, 1H), 4,94 (с, 1H), 4,41 (т, J=5,0 Гц, 2H), 4,21-4,11 (м, 1H), 3,90 (д, J=16,4 Гц, 1H), 3,72 (с, 2H), 3,66 (т, J=5,1 Гц, 2H), 3,37 (дд, J=14,0, 7,5 Гц, 1H), 3,03-2,77 (м, 7H), 2,72-2,53 (м, 5H), 2,40-2,29 (м, 1H), 1,98 (дд, J=10,0, 7,6 Гц, 2H), 1,13 (т, J=7,3 Гц, 3H).
Пример 100: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-пиридилокси)-2,3-дигидро-1,4-бензоксазепин-5-она
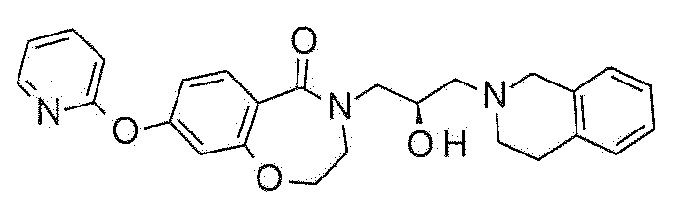
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что карбонат цезия используют вместо карбоната калия, и 2-фторпиридин используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Хлороформ-d) δ 8,26 (д, J=5,2 Гц, 1H), 7,75 (т, J=7,7 Гц, 1H), 7,38 (д, J=8,6 Гц, 1H), 7,22-6,94 (м, 7H), 6,73 (д, J=2,2 Гц, 1H), 6,56 (д, J=8,7 Гц, 1H), 4,16-4,01 (м, 1H), 3,91-3,77 (м, 1H), 3,69 (т, J=14,7 Гц, 2H), 3,52 (д, J=14,5 Гц, 1H), 3,06-2,87 (м, 3H), 2,80 (д, J=8,8 Гц, 1H), 2,68-2,53 (м, 2H), 2,05 (д, J=11,5 Гц, 1H), 1,63 (д, J=6,0 Гц, 1H), 1,01-0,73 (м, 1H).
Пример 101: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2S)-1-изопропилпирролидин-2-ил]метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
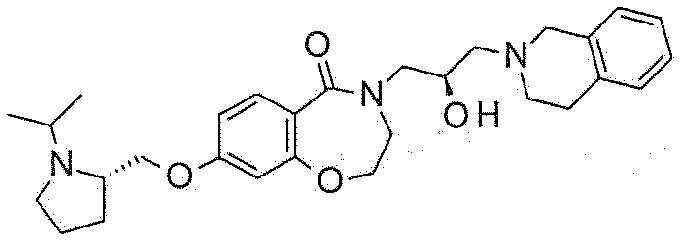
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил (2R)-2-(метилсульфонилоксиметил)пирролидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетон используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,7 Гц, 1H), 7,08-7,03 (м, 3H), 6,98 (д, J=6,7 Гц, 1H), 6,78-6,69 (м, 1H), 6,56 (д, J=2,4 Гц, 1H), 4,41 (т, J=5,1 Гц, 2H), 4,16 (с, 1H), 4,03 (д, J=5,7 Гц, 2H), 3,94-3,85 (м, 1H), 3,73-3,62 (м, 4H), 3,37 (дд, J=13,7, 7,6 Гц, 2H), 3,22-3,15 (м, 1H), 2,95 (д, J=9,3 Гц, 1H), 2,89-2,80 (м, 4H), 2,60 (д, J=6,4 Гц, 2H), 2,08 (т, J=9,4 Гц, 1H), 1,98-1,79 (м, 5H), 1,24 (д, J=6,7 Гц, 5H), 1,19 (д, J=6,5 Гц, 3H).
Пример 102: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-4-пиперидил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
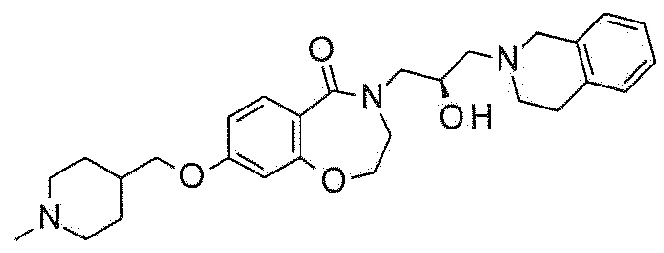
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 4-(метилсульфонилоксиметил)пиперидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,59 (д, J=8,7 Гц, 1H), 7,06 (д, J=5,1 Гц, 3H), 7,00 (д, J=7,0 Гц, 1H), 6,80-6,60 (м, 1H), 6,51 (д, J=2,6 Гц, 1H), 5,42 (д, J=1,7 Гц, 1H), 4,39 (т, J=5,2 Гц, 2H), 4,29-4,07 (м, 1H), 4,01-3,74 (м, 5H), 3,65 (т, J=5,0 Гц, 2H), 3,47 (д, J=7,2 Гц, 2H), 3,32 (д, J=12,1 Гц, 2H), 3,25 (п, J=1,7 Гц, 3H), 2,90 (с, 4H), 2,76 (т, J=12,5 Гц, 2H), 2,71-2,57 (м, 6H), 2,05-1,92 (м, 4H), 1,55 (д, J=12,9 Гц, 2H), 1,11 (т, J=7,0 Гц, 1H).
Пример 103: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
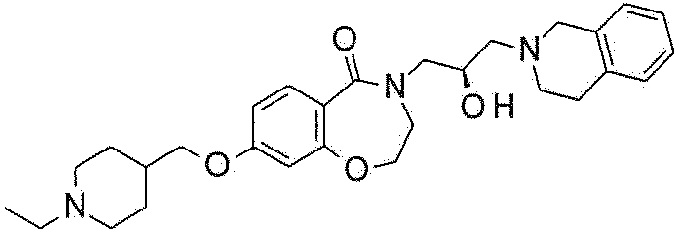
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 4-(метилсульфонилоксиметил)пиперидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,60 (д, J=8,8 Гц, 1H), 7,07 (д, J=4,4 Гц, 4H), 7,00 (д, J=6,0 Гц, 1H), 6,69 (д, J=8,9 Гц, 1H), 6,52 (д, J=2,5 Гц, 1H), 4,40 (т, J=5,1 Гц, 2H), 4,18 (с, 1H), 3,89 (д, J=5,2 Гц, 3H), 3,79 (с, 2H), 3,66 (т, J=5,1 Гц, 2H), 3,44 (ддт, J=21,3, 13,9, 6,9 Гц, 4H), 3,29 (с, 1H), 3,02 (кв, J=7,4 Гц, 2H), 2,91 (с, 4H), 2,81 (т, J=12,8 Гц, 2H), 2,66 (д, J=7,8 Гц, 2H), 2,03 (д, J=14,1 Гц, 4H), 1,59 (д, J=13,0 Гц, 1H), 1,26 (т, J=7,3 Гц, 5H)
Пример 104: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метилморфолин-2-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
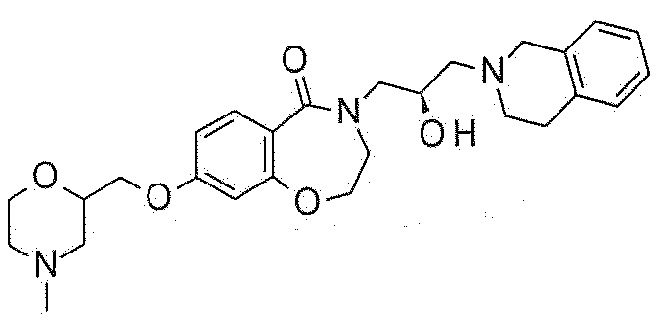
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 2-(метилсульфонилоксиметил)морфолин-4-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,12 (д, J=4,0 Гц, 3H), 7,06 (с, 1H), 6,77 (д, J=8,9 Гц, 1H), 6,60 (с, 1H), 4,48 (т, J=4,9 Гц, 2H), 4,23 (с, 1H), 4,12-3,86 (м, 5H), 3,80-3,66 (м, 5H), 3,56-3,35 (м, 1H), 2,91 (дд, J=20,1, 6,0 Гц, 5H), 2,74 (д, J=11,8 Гц, 1H), 2,67-2,56 (м, 2H), 2,35 (с, 3H), 2,26-2,16 (м, 1H), 2,07 (кв, J=9,9, 8,9 Гц, 2H).
Пример 105: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-этилморфолин-2-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
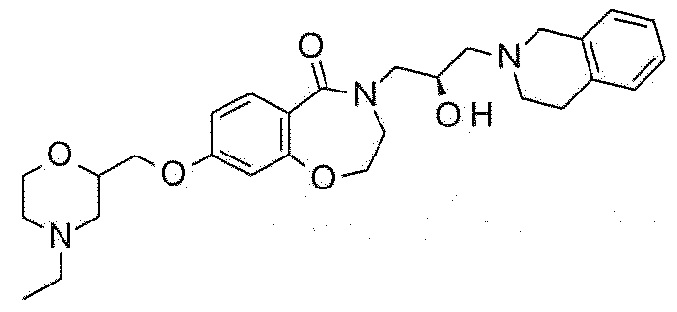
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 2-(метилсульфонилоксиметил)морфолин-4-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,12 (с, 3H), 7,07 (с, 1H), 6,77 (д, J=9,0 Гц, 1H), 6,60 (с, 1H), 4,48 (с, 2H), 4,24 (с, 1H), 4,13-3,86 (м, 5H), 3,75 (д, J=22,3 Гц, 5H), 3,51-3,37 (м, 2H), 2,93 (тд, J=30,3, 29,0, 11,6 Гц, 6H), 2,68 (с, 2H), 2,51 (кв, J=7,3 Гц, 2H), 2,20 (д, J=11,2 Гц, 2H), 2,05 (д, J=10,7 Гц, 4H), 1,30 (д, J=9,4 Гц, 4H), 1,15 (т, J=7,3 Гц, 3H).
Пример 106: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метилпирролидин-3-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
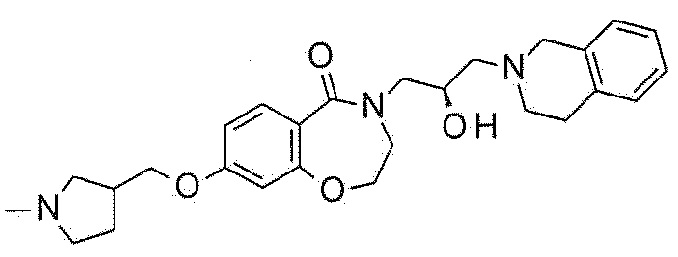
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 3-(метилсульфонилоксиметил)пирролидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,7 Гц, 1H), 7,11 (д, J=3,6 Гц, 3H), 7,06 (с, 1H), 6,75 (д, J=8,9 Гц, 1H), 6,58 (с, 1H), 4,47 (т, J=5,2 Гц, 2H), 4,23 (с, 1H), 3,97 (т, J=7,8 Гц, 3H), 3,74 (д, J=11,0 Гц, 4H), 3,42 (дд, J=14,0, 7,7 Гц, 1H), 2,93 (д, J=5,7 Гц, 2H), 2,89-2,82 (м, 3H), 2,74-2,62 (м, 4H), 2,54 (т, J=8,2 Гц, 1H), 2,43 (с, 3H), 2,12 (т, J=11,3 Гц, 1H), 2,05 (д, J=9,8 Гц, 1H), 1,69 (дд, J=13,2, 6,7 Гц, 1H).
Пример 107: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она
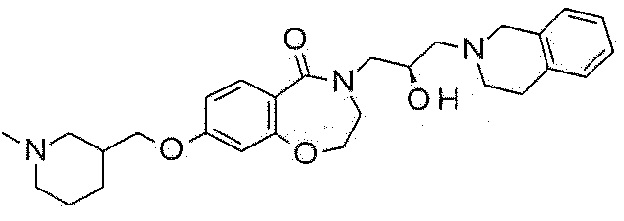
Продукт полученный заменой трет-бутил 3-метилсульфонилоксиазетидин-1-карбоксилата на трет-бутил 3-(метилсульфонилоксиметил)пиперидин-1-карбоксилат в примере 83-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,7 Гц, 1H), 7,16-7,09 (м, 3H), 7,05 (д, J=6,7 Гц, 1H), 6,75 (дд, J=8,8, 2,4 Гц, 1H), 6,57 (д, J=2,3 Гц, 1H), 4,47 (т, J=5,1 Гц, 2H), 4,22 (с, 1H), 3,96 (ддд, J=15,0, 11,6, 4,5 Гц, 3H), 3,86 (д, J=7,7 Гц, 1H), 3,76-3,69 (м, 4H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 3,04 (д, J=11,3 Гц, 1H), 2,93 (д, J=6,0 Гц, 3H), 2,87 (д, J=5,6 Гц, 3H), 2,68-2,59 (м, 2H), 2,31 (д, J=8,8 Гц, 4H), 2,02 (тд, J=11,9, 11,4, 6,9 Гц, 2H), 1,93-1,74 (м, 4H), 1,66 (д, J=13,3 Гц, 1H), 1,20-1,09 (м, 1H).
Пример 108: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-(морфолинометил)-2,3-дигидро-1,4-бензоксазепин-5-она
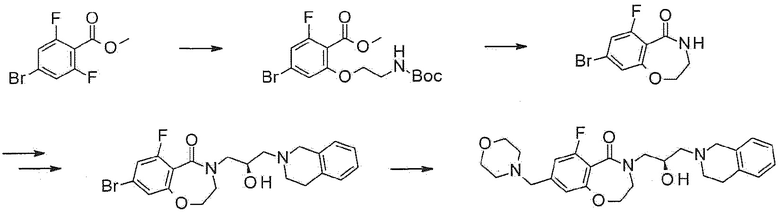
Пример 108-1: Синтез метил 4-бром-2-[2-(трет-бутоксикарбониламино)этокси]-6-фторбензоат
Метил 4-бром-2,6-дифторбензоат (5,0 г, 19,9 ммоль) растворяют в 50 мл тетрагидрофурана, и туда медленно добавляют 60% гидрид натрия (1,03 г, 25,8 ммоль) и трет-бутил N-(2-гидроксиэтил)карбамат (3,7 мл, 23,9 ммоль) при 0°С, с последующим перемешиванием при той же температуре. К реакционному раствору добавляют насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом магния и концентрацией, очищают флэш-хроматографией с получением указанного в заголовке соединения (5,07 г) в виде прозрачной жидкости.
Пример 108-2: Синтез 8-бром-6-фтор-3,4-дигидро-2H-1,4-бензоксазепин-5-она
Метил 4-бром-2-[2-(трет-бутоксикарбониламино)этокси]-6-фторбензоат (5,07 г, 12,9 ммоль), полученный в примере 108-1, растворяют в 20 мл метанола, и туда добавляют 4 M раствор хлористоводородной кислоты, растворенный в 1,4-диоксане (20 мл, 80 ммоль). Реакционный раствор перемешивают при комнатной температуре, и добавляют водный раствор гидроксида натрия на ледяной бане для подщелачивания, с последующим экстрагированием этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом магния и концентрацией при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке твердого соединения (870 мг).
Пример 108-3: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-6-фтор-3,4-дигидро-2H-1,4-бензоксазепин-5-он, полученный в примере 108-2, используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
Пример 108-4: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-(морфолинометил)-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-2,3-дигидро-1,4-бензоксазепин-5-он, полученный в примере 108-3, используют в качестве исходного материала по методике примера 22 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,12 (д, J=3,8 Гц, 3H), 7,06 (д, J=9,8 Гц, 2H), 6,95 (с, 1H), 4,43 (т, J=5,6 Гц, 2H), 4,29-4,20 (м, 1H), 4,03-3,94 (м, 1H), 3,85-3,76 (м, 2H), 3,76-3,65 (м, 6H), 3,54 (с, 2H), 3,52-3,44 (м, 1H), 3,02-2,86 (м, 4H), 2,74-2,63 (м, 2H), 2,54-2,42 (м, 4H).
Пример 109: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
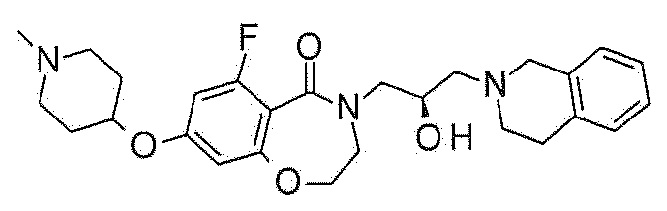
Пример 109-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-гидрокси-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-2,3-дигидро-1,4-бензоксазепин-5-он, полученный в примере 108-3, используют в качестве исходного материала по методике примера 56-1 с получением указанного в заголовке соединения.
Пример 109-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-гидрокси-2,3-дигидро-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примеров 77, 78-1 и 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,09 (д, J=19,1 Гц, 4H), 6,65 (д, J=12,2 Гц, 1H), 6,51 (с, 1H), 4,57-4,46 (м, 1H), 4,41 (т, J=5,7 Гц, 2H), 4,28-4,16 (м, 1H), 3,97 (д, J=12,0 Гц, 1H), 3,77 (с, 2H), 3,71 (т, J=5,6 Гц, 2H), 3,45 (дд, J=13,8, 7,6 Гц, 1H), 3,00-2,83 (м, 4H), 2,81-2,70 (м, 2H), 2,70-2,59 (м, 2H), 2,51-2,38 (м, 2H), 2,35 (с, 3H), 2,12-1,99 (м, 2H), 1,92-1,76 (м, 2H).
Пример 110: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-2,2-диметил-3H-1,4-бензоксазепин-5-она
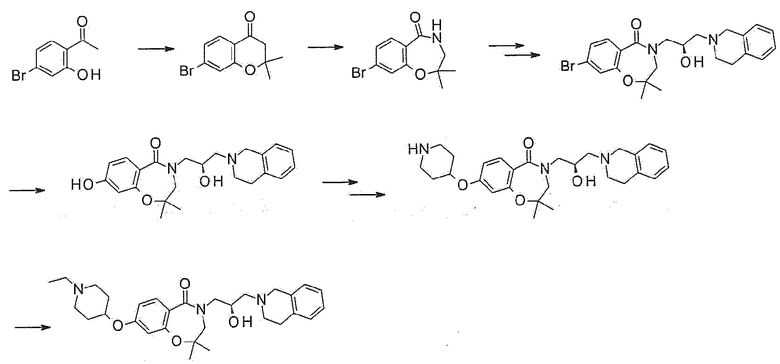
Пример 110-1: Синтез 7-бром-2,2-диметил-хроман-4-она
1-(4-Бром-2-гидроксифенил)этанон (5,0 г, 23,2 ммоль) растворяют в 20 мл метанола, и туда добавляют пирролидин (5 мл, 60,9 ммоль) и перемешивают в течение 30 минут на ледяной бане. К реакционному раствору добавляют ацетон (2,5 мл, 33,7 ммоль), нагревают до кипения с обратным холодильником в течение 4 часов, и воду добавляют для завершения реакции, с последующим экстрагированием этилацетатом 3 раза. Объединенные органические слои сушат над безводным сульфатом магния, концентрируют, растворяют в этилацетате, и фильтруют через небольшое количество диоксида кремния. Раствор концентрируют при пониженном давлении с получением указанного в заголовке соединения (4,7 г) в виде кристаллического твердого вещества без дополнительной очистки.
Пример 110-2: Синтез 8-бром-2,2-диметил-3,4-дигидро-1,4-бензоксазепин-5-она
7-Бром-2,2-диметил-хроман-4-он (4,7 г, 18,6 ммоль), полученный в примере 110-1, растворяют в 25 мл метансульфоновой кислоты, и туда медленно добавляют азид натрия (1,81 г, 27,9 ммоль) на ледяной бане. Реакционный раствор перемешивают при комнатной температуре в течение 5 часов, и 1 M водный раствор гидроксида натрия медленно добавляют при поддержании при 0°С на ледяной бане. После подщелачивания реакционного раствора до pH 10 или более, туда добавляют этилацетат и экстрагируют 3 раза. Объединенные органические слои сушат над безводным сульфатом магния, растворитель удаляют выпариванием при пониженном давлении, и затем перекристаллизовывают из дихлорметана и гексана с получением указанного в заголовке твердого соединения.
Пример 110-3: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она
8-Бром-2,2-диметил-3,4-дигидро-1,4-бензоксазепин-5-он, полученный в примере 110-2, используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
Пример 110-4: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2,2-диметил-3H-1,4-бензоксазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-он, полученный в примере 110-3, используют в качестве исходного материала по методике примера 56-1 с получением указанного в заголовке соединения.
Пример 110-5: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиперидилокси)-3H-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный в примере 110-4, используют в качестве исходного материала по методике примеров 77 и 78-1 с получением указанного в заголовке соединения.
Пример 110-6: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-2,2-диметил-3H-1,4-бензоксазепин-5-она
Продукт, полученный в примере 110-5, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,58 (д, J=8,0 Гц, 1H), 7,09 (д, J=19,8 Гц, 4H), 6,81 (д, J=8,9 Гц, 1H), 6,52 (с, 1H), 4,58-4,48 (м, 1H), 4,32-4,22 (м, 1H), 4,03 (д, J=13,7 Гц, 1H), 3,76 (с, 2H), 3,50 (с, 2H), 3,41 (дд, J=10,0, 3,2 Гц, 1H), 2,97-2,90 (м, 2H), 2,91-2,76 (м, 4H), 2,71-2,59 (м, 2H), 2,59-2,41 (м, 4H), 2,14-1,98 (м, 2H), 1,94-1,78 (м, 2H), 1,43 (с, 3H), 1,34 (с, 3H), 1,16 (т, J=7,2 Гц, 3H).
Пример 111: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(морфолинометил)-3H-1,4-бензоксазепин-5-она
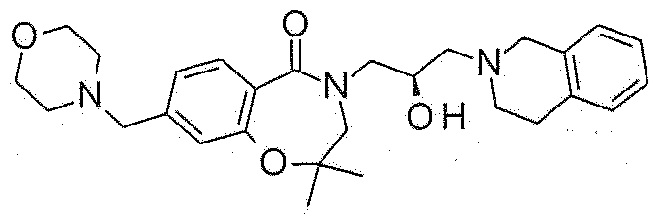
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примера 22 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=7,8 Гц, 1H), 7,22 (д, J=7,9 Гц, 1H), 7,17-7,02 (м, 4H), 7,00 (с, 1H), 4,34-4,24 (м, 1H), 4,06 (дд, J=13,7, 2,6 Гц, 1H), 3,78 (с, 2H), 3,71 (т, J=4,7 Гц, 4H), 3,56 (с, 2H), 3,53-3,38 (м, 3H), 2,99-2,81 (м, 4H), 2,72-2,58 (м, 2H), 2,48 (т, J=4,8 Гц, 4H), 1,43 (с, 3H), 1,33 (с, 3H).
Пример 112: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[(1-метил-4-пиперидил)окси]-3H-1,4-бензоксазепин-5-она
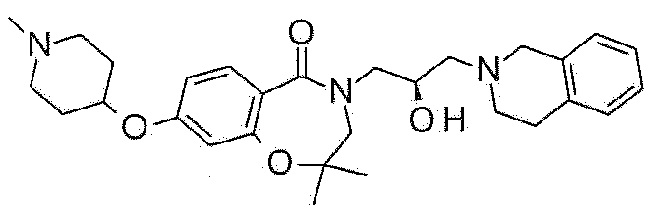
Продукт, полученный в примере 110-5, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,57 (д, J=8,6 Гц, 1H), 7,17-7,02 (м, 4H), 6,81 (д, J=8,7 Гц, 1H), 6,52 (с, 1H), 4,56-4,46 (м, 1H), 4,33-4,21 (м, 1H), 4,03 (д, J=13,3 Гц, 1H), 3,75 (с, 2H), 3,50 (с, 2H), 3,40 (дд, J=14,0, 8,1 Гц, 1H), 2,98-2,81 (м, 4H), 2,80-2,66 (м, 2H), 2,66-2,54 (м, 2H), 2,51-2,39 (м, 2H), 2,34 (с, 3H), 2,10-1,98 (м, 2H), 1,89-1,76 (м, 2H), 1,43 (с, 3H), 1,34 (с, 3H).
Пример 113: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиридилметокси)-3H-1,4-бензоксазепин-5-она
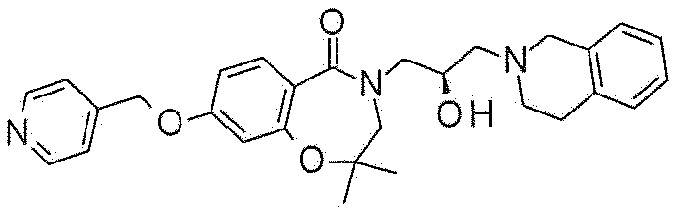
Продукт, полученный в примере 110-4, используют в качестве исходного материала по методике примера 56-2 с получением указанного в заголовке соединения, за исключением того, что 4-(хлорметил)пиридин гидрохлорид используют вместо 3-(хлорметил)пиридина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 8,56 (д, J=5,2 Гц, 2H), 7,61 (д, J=8,6 Гц, 1H), 7,54 (д, J=5,1 Гц, 2H), 7,17-7,00 (м, 4H), 6,90 (д, J=8,8 Гц, 1H), 6,62 (с, 1H), 5,25 (с, 2H), 4,32-4,22 (м, 1H), 4,03 (д, J=13,8 Гц, 1H), 3,76 (с, 2H), 3,50 (с, 2H), 3,41 (дд, J=13,9, 8,2 Гц, 1H), 2,97-2,82 (м, 4H), 2,66-2,57 (м, 2H), 1,42 (с, 3H), 1,32 (с, 3H).
Пример 114: Синтез 8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она
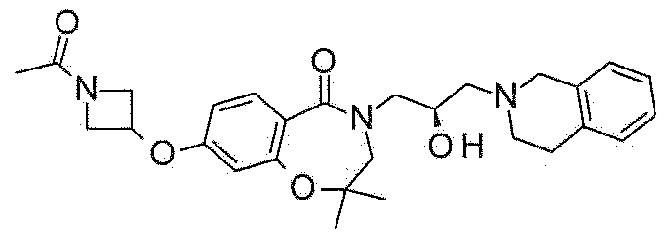
Продукт, полученный в примере 110-4, используют в качестве исходного материала по методике примера 83 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=8,6 Гц, 1H), 7,16-7,02 (м, 4H), 6,72 (д, J=8,1 Гц, 1H), 6,44 (с, 1H), 5,15-5,05 (м, 1H), 4,69-4,59 (м, 1H), 4,47-4,37 (м, 1H), 4,33-4,19 (м, 2H), 4,10-4,00 (м, 1H), 4,01-3,92 (м, 1H), 3,76 (с, 2H), 3,50 (с, 2H), 3,40-3,33 (м, 1H), 2,99-2,81 (м, 4H), 2,67-2,58 (м, 2H), 1,93 (с, 3H), 1,43 (с, 3H), 1,34 (с, 3H).
Пример 115: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(морфолинометил)-2,3-дигидро-1,4-бензодиазепин-5-она
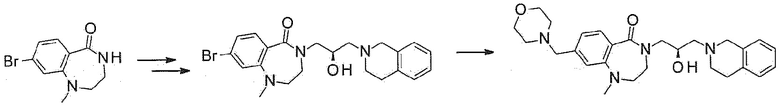
Пример 115-1: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
8-Бром-1-метил-3,4-дигидро-2H-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
Пример 115-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(морфолинометил)-2,3-дигидро-1,4-бензодиазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 22 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,49 (д, J=8,0 Гц, 1H), 7,15-7,08 (м, 2H), 7,09-7,03 (м, 1H), 7,01 (д, J=7,0 Гц, 2H), 4,29-4,20 (м, 1H), 3,94 (дд, J=14,0, 4,0 Гц, 1H), 3,78 (с, 2H), 3,72 (т, J=4,7 Гц, 4H), 3,65-3,57 (м, 2H), 3,55 (с, 2H), 3,50 (т, J=7,4 Гц, 1H), 3,48-3,36 (м, 3H), 3,00-2,88 (м, 4H), 2,86 (с, 3H), 2,69 (т, J=5,4 Гц, 2H), 2,49 (с, 4H).
Пример 116: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(3,3,3-трифторпропил)-2,3-дигидро-1,4-бензодиазепин-5-она
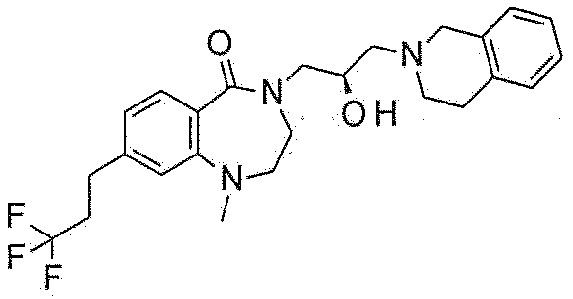
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 10 с получением указанного в заголовке соединения, за исключением того, что 3,3,3-трифторпропилбороновую кислоту используют вместо метилбороновой кислоты.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,59 (д, J=7,8 Гц, 1H), 7,14 (кв, J=5,6, 5,1 Гц, 3H), 7,09-6,91 (м, 1H), 6,82 (д, J=7,8 Гц, 1H), 6,67 (с, 1H), 4,11 (с, 1H), 3,98-3,76 (м, 2H), 3,73-3,48 (м, 4H), 3,41 (дт, J=11,8, 6,0 Гц, 1H), 3,30 (дт, J=10,8, 5,3 Гц, 1H), 2,94 (д, J=11,3 Гц, 2H), 2,87 (д, J=8,0 Гц, 5H), 2,84 (с, 1H), 2,75 (с,1H), 2,68 (дд, J=12,5, 4,2 Гц, 1H), 2,65-2,56 (м, 1H), 2,39 (дкв, J=20,0, 10,5 Гц, 2H), 1,00-0,78 (м, 2H).
Пример 117: Синтез 8-(циклогексилметил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
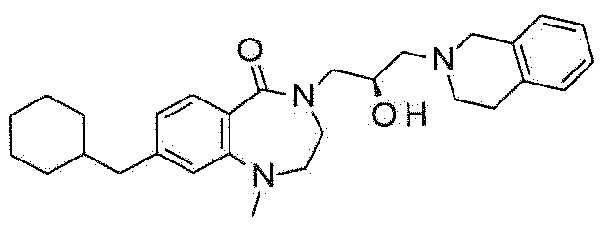
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 10 с получением указанного в заголовке соединения, за исключением того, что циклогексилметилбороновую кислоту используют вместо метилбороновой кислоты.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,53 (д, J=7,8 Гц, 1H), 7,24-7,04 (м, 3H), 7,02 (д, J=6,7 Гц, 1H), 6,78 (д, J=7,8 Гц, 1H), 6,61 (с, 1H), 4,12 (с, 1H), 3,85 (дд, J=17,6, 14,1 Гц, 2H), 3,74-3,52 (м, 4H), 3,39 (дт, J=11,7, 5,9 Гц, 1H), 3,33-3,21 (м, 1H), 2,95 (с, 1H), 2,82 (с, 2H), 2,77 (д, J=9,0 Гц, 1H), 2,71-2,59 (м, 2H), 2,46 (д, J=7,1 Гц, 2H), 1,68 (д, J=11,4 Гц, 5H), 1,32-1,13 (м, 5H), 0,93 (кв, J=13,8, 12,4 Гц, 3H).
Пример 118: Синтез 8-(циклогексен-1-ил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
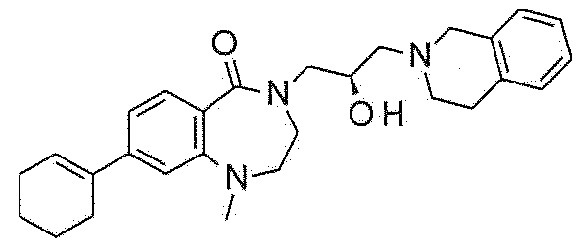
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 10 с получением указанного в заголовке соединения, за исключением того, что 2-(циклогексен-1-ил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан используют вместо метилбороновой кислоты.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,57 (д, J=8,0 Гц, 1H), 7,19-7,07 (м, 3H), 7,01 (т, J=6,2 Гц, 2H), 6,86 (с, 1H), 6,17 (с, 1H), 4,12 (д, J=7,3 Гц, 1H), 3,97-3,76 (м, 2H), 3,70-3,44 (м, 4H), 3,38 (дт, J=11,9, 6,1 Гц, 1H), 3,27 (дт, J=10,6, 5,2 Гц, 1H), 2,91 (д, J=5,3 Гц, 4H), 2,85 (с, 3H), 2,75 (т, J=7,8 Гц, 1H), 2,70-2,56 (м, 2H), 2,40 (с, 2H), 2,25-2,18 (м, 2H), 2,17 (с, 1H), 2,05 (с, 1H), 1,78 (кв, J=6,2, 5,3 Гц, 2H), 1,67 (т, J=5,8 Гц, 2H), 1,30-1,20 (м, 1H).
Пример 119: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[4-(трифторметил)циклогексен-1-ил]-2,3-дигидро-1,4-бензодиазепин-5-она
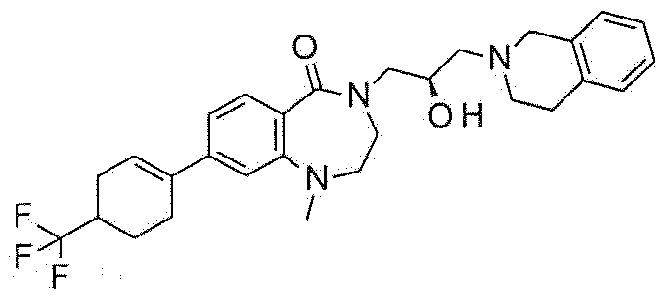
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 10 с получением указанного в заголовке соединения, за исключением того, что 4,4,5,5-тетраметил-2-[4-(трифторметил)циклогексен-1-ил]-1,3,2-диоксаборолан используют вместо метилбороновой кислоты.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,59 (д, J=7,9 Гц, 1H), 7,19-7,07 (м, 3H), 7,00 (дд, J=13,6, 7,3 Гц, 2H), 6,84 (с, 1H), 6,11 (д, J=5,1 Гц, 1H), 4,11 (т, J=7,1 Гц, 2H), 3,95-3,76 (м, 2H), 3,65 (с, 1H), 3,60 (дд, J=10,0, 4,6 Гц, 3H), 3,39 (дт, J=10,4, 5,1 Гц, 1H), 3,29 (дкв, J=10,4, 5,2 Гц, 1H), 2,92 (кв, J=8,0, 6,0 Гц, 4H), 2,85 (с, 3H), 2,75 (дд, J=10,8, 5,0 Гц, 1H), 2,69-2,58 (м, 2H), 2,57-2,43 (м, 2H), 2,42-2,24 (м, 1H), 2,23-2,14 (м, 1H), 2,05 (с, 1H), 1,69 (квд, J=11,9, 5,8 Гц, 1H), 1,43-1,18 (м, 1H).
Пример 120: Синтез трет-бутил 4-[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-5-оксо-2,3-дигидро-1,4-бензодиазепин-8-ил]-3,6-дигидро-2H-пиридин-1-карбоксилата
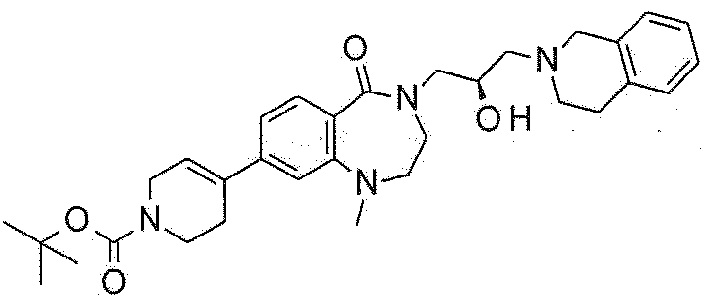
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 10 с получением указанного в заголовке соединения, за исключением того, что 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-3,6-дигидро-2H-пиридин-1-карбоксилат используют вместо метилбороновой кислоты.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,60 (д, J=8,0 Гц, 1H), 7,18-7,08 (м, 3H), 7,01 (т, J=8,8 Гц, 2H), 6,84 (с, 1H), 6,08 (с, 1H), 4,21-4,04 (м, 3H), 4,01-3,75 (м, 2H), 3,74-3,52 (м, 5H), 3,48-3,35 (м, 1H), 3,36-3,24 (м, 1H), 2,92 (с, 2H), 2,85 (с, 3H), 2,74 (с, 1H), 2,72-2,56 (м, 2H), 2,52 (с, 2H), 2,05 (с, 1H), 1,49 (с, 7H), 1,31-1,21 (м, 2H).
Пример 121: Синтез 8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
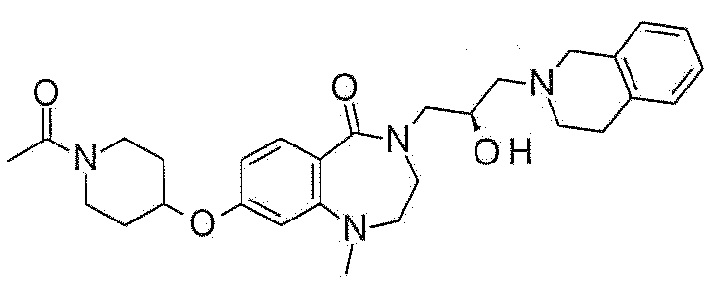
Пример 121-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-он используют в качестве исходного материала по методике примера 56-1 с получением указанного в заголовке соединения
Пример 121-2: Синтез 8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что (1-ацетил-4-пиперидил) метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,61 (д, J=8,5 Гц, 1H), 7,13 (д, J=8,2 Гц, 3H), 7,02 (д, J=6,7 Гц, 1H), 6,51 (д, J=8,6 Гц, 1H), 6,38 (с, 1H), 4,59 (с, 1H), 4,11 (т, J=7,1 Гц, 2H), 3,99-3,81 (м, 1H), 3,84-3,72 (м, 2H), 3,74-3,56 (м, 6H), 3,42 (дд, J=11,6, 5,8 Гц, 2H), 3,36-3,25 (м, 1H), 2,91 (д, J=8,7 Гц, 3H), 2,81 (с, 3H), 2,75 (с, 1H), 2,69-2,53 (м, 2H), 2,13 (д, J=1,5 Гц, 3H), 2,05 (д, J=1,5 Гц, 1H), 1,98-1,77 (м, 5H), 1,44-1,15 (м, 2H), 1,09-0,81 (м, 1H).
Пример 122: Синтез 8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
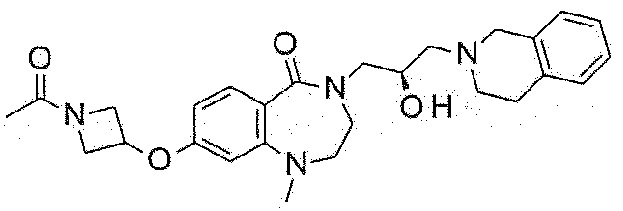
Продукт полученный в примере 121-1 используют в качестве исходного материала по методике примера 83 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Хлороформ-d) δ 7,61 (д, J=8,4 Гц, 1H), 7,19-7,07 (м, 3H), 7,02 (д, J=6,7 Гц, 1H), 6,44-6,16 (м, 2H), 4,97 (т, J=5,7 Гц, 1H), 4,49 (т, J=8,0 Гц, 1H), 4,39 (дд, J=10,9, 6,6 Гц, 1H), 4,28-3,99 (м, 4H), 3,95-3,72 (м, 2H), 3,75-3,50 (м, 4H), 3,52-3,26 (м, 2H), 2,93 (кв, J=9,0, 6,9 Гц, 3H), 2,81 (с, 3H), 2,78-2,54 (м, 3H), 2,05 (с, 1H), 1,92 (с, 3H), 1,26 (т, J=7,2 Гц, 1H).
Пример 123: Синтез 8-[(3R)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
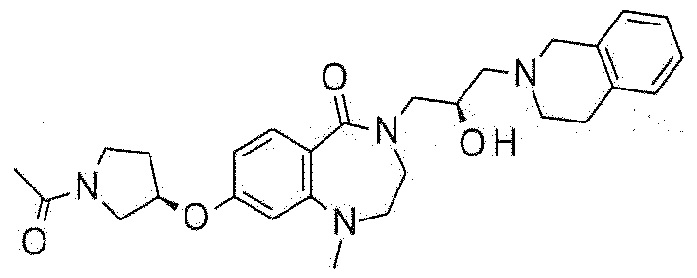
Продукт, полученный в примере 121-1, в качестве исходного материала и промежуточное соединение, полученное заменой 4-хлортетрагидропирана на трет-бутил (3S)-3-метилсульфонилоксипирролидин-1-карбоксилат в примере 64, используют по методике примера 78 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,51 (дд, J=8,7, 3,2 Гц, 1H), 7,29-7,03 (м, 4H), 6,68-6,34 (м, 2H), 5,15 (д, J=22,7 Гц, 1H), 4,27 (с, 1H), 3,99-3,84 (м, 3H), 3,79-3,57 (м, 6H), 3,55-3,39 (м, 2H), 3,01 (д, J=8,8 Гц, 4H), 2,81 (д, J=15,8 Гц, 5H), 2,40-2,14 (м, 2H), 2,16-1,90 (м, 5H), 1,31 (с, 3H).
Пример 124: Синтез 8-[(3S)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
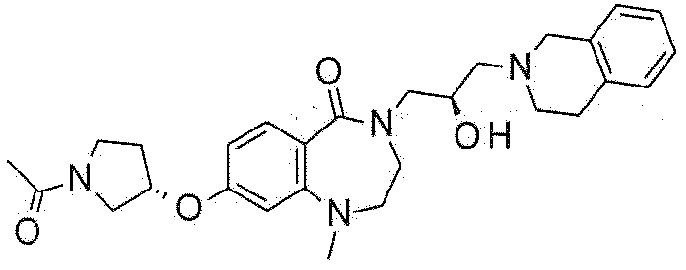
Продукт, полученный в примере 121-1, в качестве исходного материала и промежуточное соединение, полученное заменой 4-хлортетрагидропирана на трет-бутил (3R)-3-метилсульфонилоксипирролидин-1-карбоксилат в примере 64, используют по методике примера 78 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,57-7,45 (м, 1H), 7,15 (д, J=4,5 Гц, 3H), 7,09 (с, 1H), 6,60 (д, J=7,9 Гц, 1H), 6,48 (д, J=5,6 Гц, 1H), 5,15 (д, J=22,7 Гц, 1H), 4,27 (с, 1H), 3,90 (д, J=14,7 Гц, 3H), 3,79-3,58 (м, 5H), 3,59-3,41 (м, 2H), 2,99 (с, 4H), 2,80 (д, J=23,3 Гц, 5H), 2,31 (с, 1H), 2,23 (с, 1H), 2,18-1,98 (м, 4H), 1,96 (с, 1H), 1,28 (д, J=20,7 Гц, 2H).
Пример 125: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она
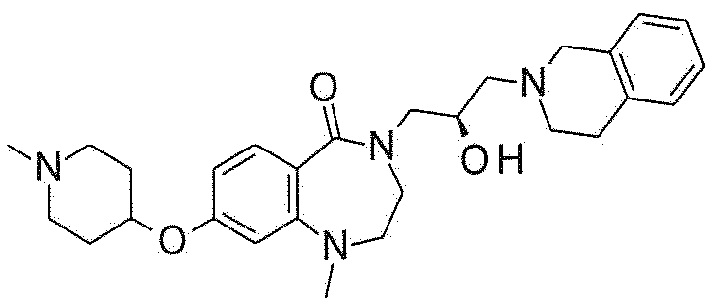
Пример 125-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензодиазепин-5-она дигидрохлорида
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примеров 77 и 78-1 с получением указанного в заголовке соединения.
Пример 125-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она
Продукт, полученный в примере 125-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,49 (д, J=8,4 Гц, 1H), 7,13 (д, J=4,4 Гц, 3H), 7,08 (с, 1H), 6,62 (д, J=8,7 Гц, 1H), 6,50 (с, 1H), 4,25 (с, 1H), 4,00-3,78 (м, 3H), 3,61 (д, J=5,7 Гц, 2H), 3,52-3,38 (м, 2H), 2,89 (д, J=52,2 Гц, 8H), 2,73 (с, 3H), 2,49 (с, 3H), 2,05 (д, J=11,4 Гц, 3H), 1,94 (с, 2H).
Пример 126: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
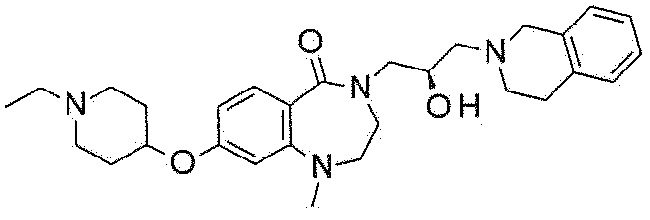
Продукт, полученный в примере 125-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,50 (д, J=8,6 Гц, 1H), 7,13 (д, J=3,0 Гц, 3H), 7,07 (д, J=6,9 Гц, 1H), 6,63 (д, J=8,8 Гц, 1H), 6,51 (с, 1H), 4,65 (д, J=9,6 Гц, 1H), 4,25 (с, 1H), 3,91 (дд, J=13,9, 3,9 Гц, 1H), 3,84 (с, 2H), 3,62 (т, J=5,8 Гц, 2H), 3,51-3,36 (м, 3H), 3,18-3,04 (м, 2H), 2,96 (с, 4H), 2,85 (д, J=12,9 Гц, 6H), 2,73 (т, J=5,5 Гц, 2H), 2,14 (с, 2H), 2,09-1,93 (м, 3H), 1,35-1,10 (м, 5H).
Пример 127: Синтез 8-[(1-циклобутил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
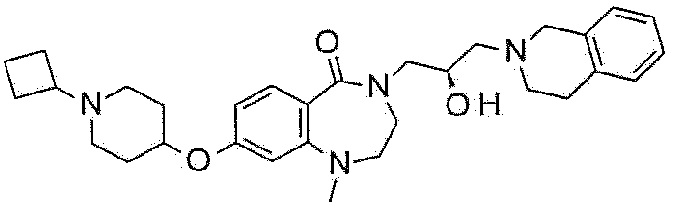
Продукт, полученный в примере 125-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что циклобутанон используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,41 (д, J=8,5 Гц, 1H), 7,05 (д, J=3,0 Гц, 3H), 6,99 (с, 1H), 6,53 (д, J=8,6 Гц, 1H), 6,41 (с, 1H), 4,47 (с, 1H), 4,15 (д, J=6,7 Гц, 1H), 3,85 (д, J=14,6 Гц, 1H), 3,71 (с, 2H), 3,54 (с, 2H), 3,37 (дт, J=11,7, 6,3 Гц, 2H), 2,92-2,81 (м, 4H), 2,75 (с, 3H), 2,68-2,54 (м, 4H), 2,32 (с, 2H), 2,06 (с, 2H), 1,97 (д, J=8,7 Гц, 4H), 1,88 (д, J=9,6 Гц, 1H), 1,79-1,62 (м, 4H).
Пример 128: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-тетрагидрофуран-3-ил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она
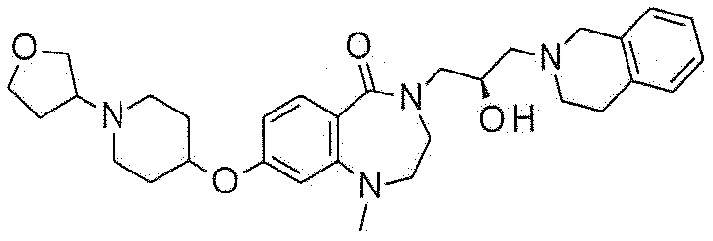
Продукт, полученный в примере 125-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что тетрагидрофуран-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,48 (д, J=8,6 Гц, 1H), 7,12 (д, J=4,2 Гц, 3H), 7,06 (с, 1H), 6,60 (д, J=8,6 Гц, 1H), 6,47 (с, 1H), 4,51 (д, J=7,7 Гц, 1H), 4,23 (т, J=5,9 Гц, 1H), 3,93 (тт, J=12,0, 4,8 Гц, 6H), 3,78 (с, 5H), 3,69-3,51 (м, 5H), 3,48-3,36 (м, 2H), 3,06 (т, J=7,3 Гц, 1H), 2,94 (д, J=5,3 Гц, 2H), 2,90 (д, J=4,6 Гц, 2H), 2,82 (с, 3H), 2,74-2,64 (м, 3H), 2,51 (т, J=10,1 Гц, 1H), 2,41 (т, J=9,8 Гц, 1H), 2,16 (дд, J=13,1, 6,9 Гц, 2H), 2,04 (д, J=9,5 Гц, 3H), 1,94-1,71 (м, 5H).
Пример 129: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[[1-(оксетан-3-ил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензодиазепин-5-она
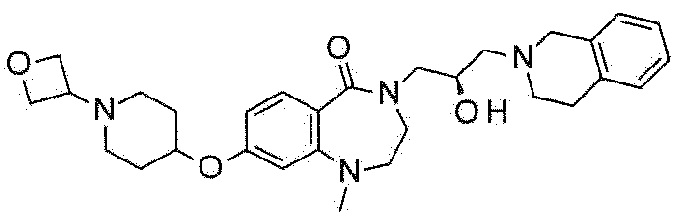
Продукт, полученный в примере 125-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,55-7,37 (м, 1H), 7,12 (д, J=5,1 Гц, 3H), 7,06 (д, J=6,8 Гц, 1H), 6,60 (д, J=8,6 Гц, 1H), 6,47 (с, 1H), 4,71 (т, J=6,7 Гц, 2H), 4,62 (т, J=6,2 Гц, 2H), 4,53 (с, 1H), 4,23 (с, 1H), 3,94 (с, 1H), 3,79 (с, 2H), 3,69 (д, J=4,9 Гц, 1H), 3,64-3,51 (м, 3H), 3,44 (дт, J=13,1, 6,7 Гц, 2H), 2,93 (дд, J=11,8, 4,7 Гц, 4H), 2,82 (с, 3H), 2,68 (д, J=7,8 Гц, 2H), 2,62 (д, J=12,0 Гц, 2H), 2,29 (т, J=9,8 Гц, 2H), 2,04 (д, J=10,2 Гц, 2H), 1,85 (с, 2H).
Пример 130: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она
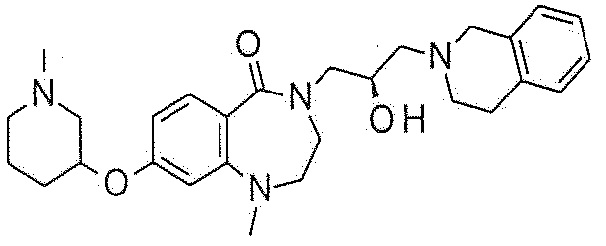
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примера 68 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,50 (дд, J=8,6, 1,7 Гц, 1H), 7,12 (т, J=2,5 Гц, 3H), 7,06 (д, J=6,6 Гц, 1H), 6,61 (дд, J=8,5, 2,5 Гц, 1H), 6,51 (д, J=2,4 Гц, 1H), 4,28-4,20 (м, 1H), 4,08 (д, J=5,3 Гц, 2H), 3,92 (дд, J=14,2, 3,9 Гц, 1H), 3,78 (с, 2H), 3,62 (дт, J=8,6, 4,5 Гц, 2H), 3,42 (ддд, J=21,1, 15,3, 6,7 Гц, 2H), 3,17 (дт, J=10,1, 4,3 Гц, 1H), 2,99-2,87 (м, 5H), 2,87-2,81 (м, 3H), 2,67 (т, J=4,7 Гц, 2H), 2,57 (д, J=1,8 Гц, 3H), 2,47 (кв, J=8,9 Гц, 1H), 2,14 (дд, J=12,4, 8,3 Гц, 1H), 2,05 (д, J=10,0 Гц, 2H), 1,93-1,73 (м, 4H), 1,31 (с, 3H).
Пример 131: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метилпирролидин-3-ил)метокси]-2,3-дигидро-1,4-бензодиазепин-5-она
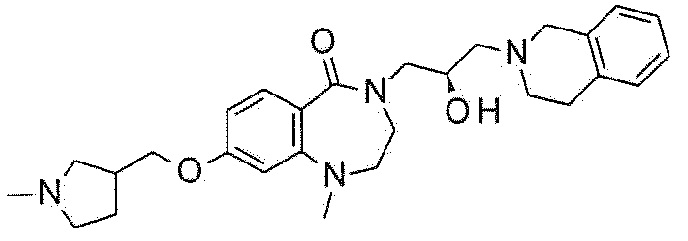
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примера 106 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,49 (д, J=8,5 Гц, 1H), 7,11 (с, 3H), 7,06 (с, 1H), 6,58 (д, J=8,7 Гц, 1H), 6,48 (с, 1H), 4,23 (с, 1H), 4,07-3,87 (м, 3H), 3,76 (с, 2H), 3,61 (с, 2H), 3,51-3,40 (м, 2H), 2,91 (дд, J=19,1, 5,4 Гц, 5H), 2,84 (с, 3H), 2,68 (д, J=8,9 Гц, 5H), 2,56 (д, J=8,0 Гц, 1H), 2,43 (д, J=2,1 Гц, 3H), 2,05 (д, J=9,6 Гц, 3H), 1,71 (д, J=7,2 Гц, 1H), 1,57 (с, 1H), 0,91 (с, 2H).
Пример 132: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(1-метилпирролидин-3-ил)окси-2,3-дигидро-1,4-бензодиазепин-5-она
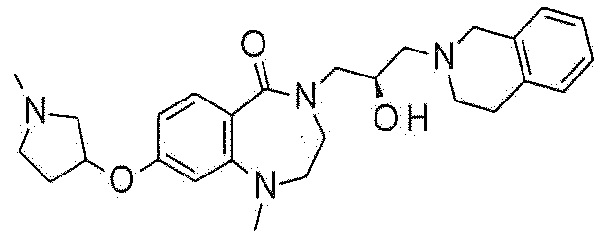
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примера 98 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,49 (д, J=8,5 Гц, 1H), 7,11 (с, 3H), 7,07 (с, 1H), 6,53 (д, J=8,6 Гц, 1H), 6,44 (с, 1H), 4,98 (с, 1H), 4,23 (с, 1H), 3,93 (д, J=13,8 Гц, 1H), 3,77 (с, 2H), 3,62 (с, 2H), 3,44 (дд, J=14,5, 7,2 Гц, 2H), 2,91 (дд, J=18,9, 6,2 Гц, 6H), 2,83 (с, 3H), 2,66 (д, J=7,7 Гц, 2H), 2,49 (д, J=8,0 Гц, 1H), 2,42 (с, 3H), 2,05 (д, J=10,2 Гц, 3H), 1,31 (с, 4H).
Пример 133: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-3-пиперидил)метокси]-2,3-дигидро-1,4-бензодиазепин-5-она
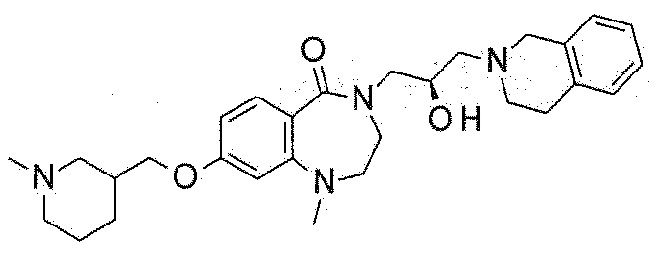
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примера 107 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,48 (д, J=8,5 Гц, 1H), 7,11 (д, J=4,7 Гц, 3H), 7,06 (с, 1H), 6,57 (д, J=8,6 Гц, 1H), 6,47 (с, 1H), 4,22 (с, 1H), 4,00-3,84 (м, 4H), 3,76 (с, 2H), 3,61 (д, J=5,4 Гц, 2H), 3,44 (дд, J=14,2, 7,8 Гц, 2H), 3,05 (д, J=12,9 Гц, 1H), 2,93 (д, J=6,0 Гц, 5H), 2,85 (д, J=16,2 Гц, 6H), 2,65 (д, J=7,2 Гц, 2H), 2,30 (дд, J=10,2, 1,7 Гц, 5H), 2,14 (с, 2H), 2,09-1,81 (м, 4H), 1,77 (с, 1H).
Пример 134: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиридил)метокси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
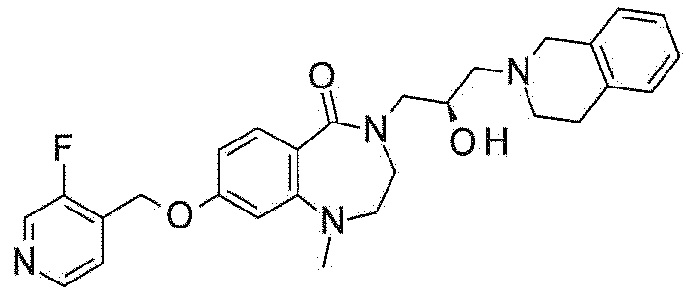
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примера 56-2 с получением указанного в заголовке соединения, за исключением того, что (3-фтор-4-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 8,50 (с, 1H), 8,44 (д, J=5,0 Гц, 1H), 7,67 (т, J=5,8 Гц, 1H), 7,52 (дд, J=8,7, 2,0 Гц, 1H), 7,20-7,00 (м, 4H), 6,68 (дд, J=8,7, 2,6 Гц, 1H), 6,60 (д, J=2,8 Гц, 1H), 5,33 (с, 2H), 4,23 (с, 1H), 3,95-3,87 (м, 1H), 3,77 (с, 2H), 3,62 (с, 2H), 3,49-3,37 (м, 3H), 2,92 (дд, J=15,9, 5,2 Гц, 4H), 2,84 (д, J=2,0 Гц, 3H), 2,74-2,62 (м, 2H), 1,31 (с, 1H).
Пример 135: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиперидил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она; дигидрохлорида
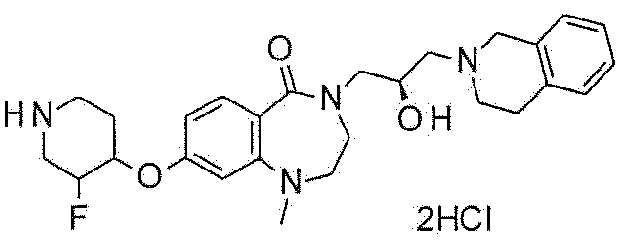
Промежуточное соединение, в котором Boc замещена, синтезируют с применением продукта, полученного в примере 121-1 в качестве исходного материала и заменяя 4-хлортетрагидропиран на трет-бутил 3-фтор-4-метилсульфонилоксипиперидин-1-карбоксилат в примере 64. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,5 Гц, 1H), 7,31 (кв, J=7,5 Гц, 3H), 7,24 (т, J=7,6 Гц, 1H), 6,94 (д, J=8,8 Гц, 1H), 6,89 (с, 1H), 5,06 (д, J=44,3 Гц, 2H), 4,74-4,58 (м, 1H), 4,49 (тд, J=15,4, 14,0, 7,3 Гц, 2H), 3,93-3,86 (м, 1H), 3,80 (д, J=9,6 Гц, 1H), 3,74-3,63 (м, 6H), 3,60 (с, 1H), 3,52 (д, J=15,3 Гц, 2H), 3,44-3,35 (м, 2H), 3,25-3,14 (м, 1H), 3,02 (с, 3H), 2,44-2,30 (м, 1H), 2,19 (д, J=15,7 Гц, 1H).
Пример 136: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-3-фтор-4-пиперидил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
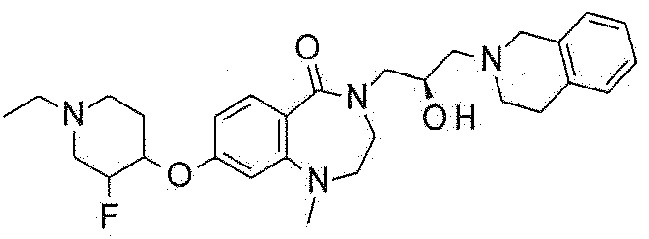
Продукт, полученный в примере 135, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,49 (дд, J=8,6, 1,9 Гц, 1H), 7,12 (д, J=3,1 Гц, 3H), 7,06 (д, J=6,7 Гц, 1H), 6,65 (д, J=8,6 Гц, 1H), 6,53 (д, J=2,6 Гц, 1H), 4,67 (д, J=48,8 Гц, 1H), 4,52 (с, 1H), 4,23 (с, 1H), 3,92 (дд, J=13,7, 3,8 Гц, 1H), 3,78 (с, 2H), 3,62 (с, 2H), 3,45 (дд, J=14,4, 7,6 Гц, 2H), 3,14-3,02 (м, 1H), 2,94 (д, J=5,2 Гц, 3H), 2,90 (д, J=4,6 Гц, 2H), 2,83 (д, J=1,8 Гц, 3H), 2,68 (т, J=5,4 Гц, 2H), 2,55 (д, J=7,2 Гц, 1H), 2,46 (д, J=8,2 Гц, 0H), 2,34 (т, J=10,8 Гц, 1H), 2,21 (с, 1H), 1,77 (дд, J=12,9, 8,8 Гц, 1H), 1,19-1,11 (м, 3H).
Пример 137: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(8-этил-8-азабицикло[3,2,1]октан-3-ил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
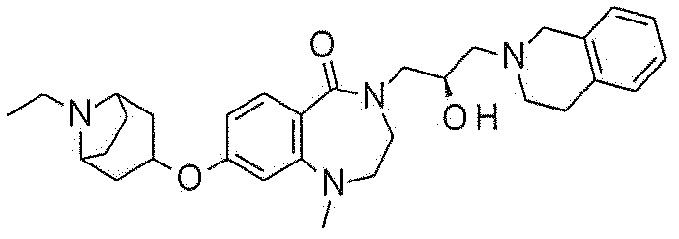
Пример 137-1: Синтез 8-(8-азабицикло[3,2,1]октан-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она дигидрохлорида
Промежуточное соединение, в котором Вос замещена, синтезируют с применением продукта, полученного в примере 121-1, в качестве исходного материала и заменяя 4-хлортетрагидропиран на трет-бутил 3-метилсульфонилокси-8-азабицикло [3,2,1]октан-8-карбоксилат в примере 64. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
Пример 137-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(8-этил-8-азабицикло[3,2,1]октан-3-ил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
Продукт, полученный в примере 137-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что ацетальдегид используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66-7,39 (м, 1H), 7,12 (д, J=4,9 Гц, 3H), 7,05 (д, J=6,7 Гц, 1H), 6,63 (д, J=8,6 Гц, 1H), 6,45 (д, J=2,4 Гц, 1H), 4,80 (дкв, J=10,7, 5,6, 4,9 Гц, 1H), 4,22 (д, J=8,0 Гц, 1H), 3,94-3,87 (м, 1H), 3,77 (с, 2H), 3,69 (с, 2H), 3,61 (дд, J=7,5, 3,6 Гц, 2H), 3,43 (дт, J=11,7, 6,2 Гц, 2H), 2,93 (д, J=5,5 Гц, 2H), 2,89 (д, J=5,3 Гц, 2H), 2,82 (с, 4H), 2,71-2,54 (м, 2H), 2,30-2,13 (м, 4H), 2,03 (д, J=1,6 Гц, 1H), 1,97-1,84 (м, 5H), 1,24 (т, J=7,1 Гц, 4H).
Пример 138: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(2-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она; дигидрохлорида
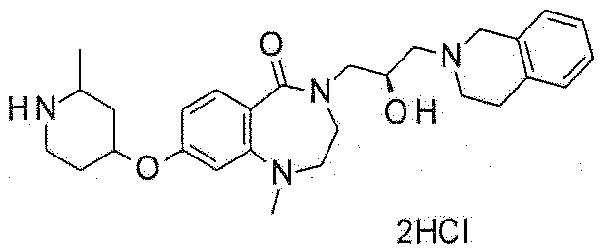
Промежуточное соединение, в котором Вос замещена, синтезируют с применением продукта, полученного в примере 121-1, в качестве исходного материала и заменяя 4-хлортетрагидропиран на трет-бутил 2-метил-4-метилсульфонилокси-пиперидин-1-карбоксилат в примере 64. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,60 (д, J=8,6 Гц, 1H), 7,32 (кв, J=7,7, 7,1 Гц, 3H), 7,23 (д, J=7,7 Гц, 1H), 6,87 (д, J=8,9 Гц, 1H), 6,76 (с, 1H), 4,75 (д, J=11,8 Гц, 1H), 4,74-4,62 (м, 1H), 4,49 (тд, J=15,2, 12,9, 6,6 Гц, 2H), 3,89 (с, 1H), 3,84-3,75 (м, 1H), 3,73-3,61 (м, 3H), 3,51 (т, J=17,0 Гц, 3H), 3,44-3,36 (м, 2H), 3,20 (кв, J=13,8 Гц, 2H), 3,00 (с, 3H), 2,42 (т, J=13,0 Гц, 1H), 1,80 (кв, J=11,8, 10,8 Гц, 1H), 1,68-1,57 (м, 1H), 1,42 (д, J=6,4 Гц, 2H), 1,37 (д, J=6,5 Гц, 1H).
Пример 139: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(5-фтор-2-пиридил)метокси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
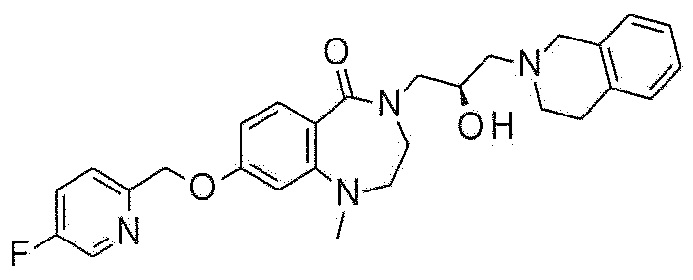
Продукт, полученный в примере 121-1, используют в качестве исходного материала по методике примера 56-2 с получением указанного в заголовке соединения, за исключением того, что (5-фтор-2-пиридил)метил метансульфонат используют вместо 3-(хлорметил)пиридина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 8,49 (с, 1H), 7,80-7,62 (м, 2H), 7,50 (д, J=8,5 Гц, 1H), 7,11 (д, J=3,6 Гц, 3H), 7,06 (с, 1H), 6,65 (д, J=8,7 Гц, 1H), 6,59 (с, 1H), 5,23 (с, 2H), 4,23 (с, 1H), 3,92 (д, J=13,8 Гц, 1H), 3,77 (с, 2H), 3,62 (д, J=5,4 Гц, 2H), 3,44 (дд, J=13,3, 6,9 Гц, 2H), 2,94 (д, J=5,5 Гц, 2H), 2,89 (д, J=5,2 Гц, 2H), 2,82 (с, 3H), 2,71-2,60 (м, 2H).
Пример 140: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
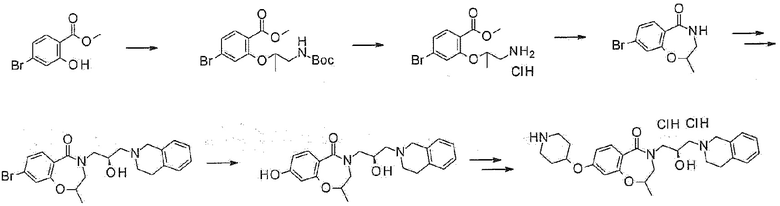
Пример 140-1: Синтез метил 4-бром-2-[2-(трет-бутоксикарбониламино)пропокси]бензоата
Метил 4-бром-2-гидроксибензоат (3 г, 12,98 ммоль), Cs2CO3 (12,7 г, 51,95 ммоль) и [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат (7 мл, 25,98 ммоль) растворяют в ацетонитриле, перемешивают в течение одного дня и нагревают до кипения с обратным холодильником. Реакционный раствор охлаждают до комнатной температуры, и туда добавляют дистиллированную воду, затем разбавляют этилацетатом. Объединенные органические слои сушат над безводным сульфатом магния, концентрируют и очищают флэш-хроматографией с получением указанного в заголовке соединения.
Пример 140-2: Синтез метил 2-(2-аминопропокси)-4-бромбензоата гидрохлорида
Продукт, полученный в примере 140-1, в качестве исходного материала растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты, растворенный в 1,4-диоксане, затем перемешивают при комнатной температуре. Реакционный раствор концентрируют при пониженном давлении с получением указанного в заголовке соединения без дополнительной очистки.
Пример 140-3: Синтез 8-бром-2-метил-3,4-дигидро-2H-1,4-бензоксазепин-5-она
Продукт (2,3 г, 8,01 ммоль), полученный в примере 140-2, растворяют в толуоле, и туда добавляют триэтиламин. Реакционный раствор перемешивают и нагревают до кипения с обратным холодильником. После подтверждения завершения реакции, реакционный раствор охлаждают до комнатной температуры, и растворитель удаляют при пониженном давлении. Концентрат очищают флэш-хроматографией с получением указанного в заголовке соединения.
Пример 140-4: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 140-3, используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
Пример 140-5: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 140-4, используют в качестве исходного материала по методике примера 56-1 с получением указанного в заголовке соединения.
Пример 140-6: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный в примере 140-5, используют в качестве исходного материала по методике примеров 77 и 78-1 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,5 Гц, 1H), 7,32 (д, J=8,4 Гц, 3H), 7,23 (с, 1H), 6,93-6,84 (м, 1H), 6,67 (с, 1H), 4,82 (с, 2H), 4,68 (д, J=16,0 Гц, 1H), 4,48 (д, J=10,0 Гц, 2H), 4,01-3,83 (м, 3H), 3,70 (д, J=15,8 Гц, 2H), 3,58-3,36 (м, 8H), 3,26 (д, J=13,3 Гц, 3H), 3,08 (д, J=26,7 Гц, 1H), 2,21 (с, 2H), 2,05 (д, J=14,1 Гц, 3H), 1,76 (с, 1H), 1,34 (дд, J=14,1, 6,4 Гц, 3H).
Пример 141: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
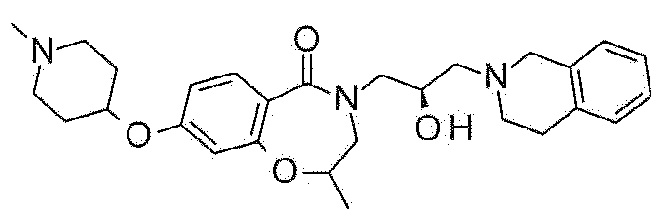
Продукт, полученный в примере 140, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,8 Гц, 1H), 7,10 (д, J=21,1 Гц, 3H), 6,80 (с, 1H), 6,57 (с, 1H), 4,55 (с, 1H), 4,25 (с, 1H), 4,15 (д, J=14,1 Гц, 1H), 3,79 (с, 2H), 3,63 (д, J=14,6 Гц, 1H), 3,49 (кв, J=7,6, 6,7 Гц, 1H), 3,27-3,15 (м, 1H), 2,93 (д, J=13,9 Гц, 3H), 2,84 (с, 2H), 2,71-2,61 (м, 2H), 2,56 (с, 2H), 2,42 (с, 2H), 2,06 (с, 2H), 1,88 (с, 2H), 1,31 (дд, J=16,5, 6,5 Гц, 3H).
Пример 142: Синтез (2R)-8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
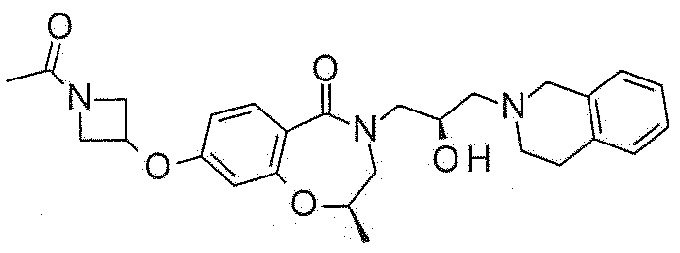
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 83 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,6 Гц, 1H), 7,19-7,02 (м, 4H), 6,70 (д, J=8,7 Гц, 1H), 6,47 (с, 1H), 5,10 (т, J=5,4 Гц, 1H), 4,80 (с, 1H), 4,65 (т, J=8,5 Гц, 1H), 4,42 (дд, J=11,1, 6,7 Гц, 1H), 4,23 (д, J=10,2 Гц, 2H), 4,14 (д, J=13,8 Гц, 1H), 3,97 (д, J=11,3 Гц, 1H), 3,81 (с, 2H), 3,64 (д, J=15,5 Гц, 1H), 3,50 (дд, J=15,9, 7,5 Гц, 1H), 3,29-3,20 (м, 1H), 2,95 (с, 4H), 2,68 (т, J=6,9 Гц, 2H), 1,93 (с, 3H), 1,34 (д, J=6,3 Гц, 4H).
Пример 143: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
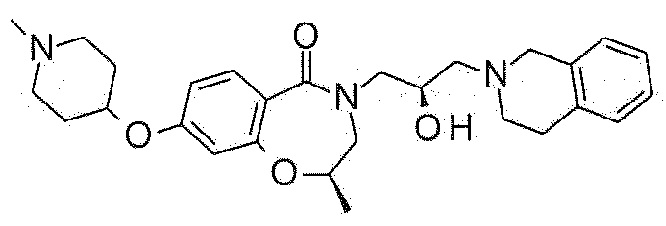
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 141 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,8 Гц, 1H), 7,17-7,02 (м, 4H), 6,79 (д, J=8,8 Гц, 1H), 6,57 (с, 1H), 4,79 (с, 1H), 4,56 (с, 1H), 4,24 (с, 1H), 4,14 (д, J=12,2 Гц, 1H), 3,79 (с, 2H), 3,69-3,59 (м, 1H), 3,50 (дд, J=15,6, 7,6 Гц, 1H), 3,24 (дд, J=13,8, 8,1 Гц, 1H), 2,98-2,80 (м, 6H), 2,63 (дт, J=24,4, 8,0 Гц, 4H), 2,05 (д, J=13,3 Гц, 2H), 1,92 (д, J=18,6 Гц, 2H), 1,33 (д, J=6,4 Гц, 3H).
Пример 144: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она
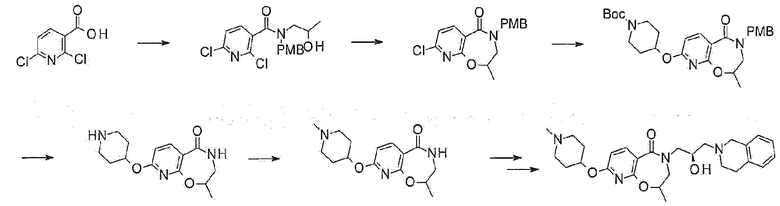
Пример 144-1: Синтез 2,6-дихлор-N-(2-гидроксипропил)-N-[(4-метоксифенил)метил]пиридин-3-карбоксамида
2,6-Дихлорпиридин-3-карбоновую кислоту (5,0 г, 26 ммоль) растворяют в дихлорметане, и туда добавляют оксалилхлорид (3,3 мл, 39 ммоль) и каталитическое количество диметилформамида. Реакционный раствор перемешивают при комнатной температуре и концентрируют при пониженном давлении с получением 2,6-дихлорпиридин-3-карбонилхлорида без дополнительной очистки. 1-[(4-Метоксифенил)метиламино]пропан-2-ол (1,3 г, 7,2 ммоль) и K2CO3 (2,2 г, 15,8 ммоль) растворяют в дихлорметане, и туда медленно добавляют 2,6-дихлорпиридин-3-карбонилхлорид (1,6 г, 7,6 ммоль), растворенный в дихлорметане на ледяной бане. Реакционный раствор перемешивают при той же температуре в течение 1 часа, и реакцию останавливают добавлением воды. Реакционный раствор экстрагируют дихлорметаном, сушат над безводным сульфатом магния и концентрируют при пониженном давлении с получением указанного в заголовке соединения (2,64 г) в виде липкой жидкости.
Пример 144-2: Синтез 8-хлор-4-[(4-метоксифенил)метил]-2-метил-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она
2,6-Дихлор-N-(2-гидроксипропил)-N-[(4-метоксифенил)метил]пиридин-3-карбоксамид (2,64 г), полученный в примере 144-1, растворяют в тетрагидрофуране, и туда медленно добавляют 60% гидрид натрия (630 мг, 15,8 ммоль) на ледяной бане. Реакционный раствор медленно нагревают до комнатной температуры, перемешивают до полного исчезновения исходного материала, и метанол добавляют для завершения реакции. В реакционную смесь добавляют насыщенный водный раствор хлорида натрия, экстрагируют этилацетатом, сушат над безводным сульфатом магния и концентрируют при пониженном давлении. Концентрат очищают флэш-хроматографией с получением указанного в заголовке соединения (1,35 г) в виде липкой жидкости.
Пример 144-3: Синтез трет-бутил 4-[[4-[(4-метоксифенил)метил]-2-метил-5-оксо-2,3-дигидропиридо[3,2-f][1,4]оксазепин-8-ил]окси]пиперидин-1-карбоксилата
Продукт (500 мг, 1,51 ммоль), полученный в примере 144-2, трет-бутил 4-гидроксипиперидин-1-карбоксилат (460 мг, 2,26 ммоль) и 60% гидрид натрия (180 мг, 4,5 ммоль) растворяют в 20 мл тетрагидрофурана и перемешивают при 60°C в течение одного дня. Реакционный раствор экстрагируют насыщенным водным раствором хлорида натрия и этилацетатом, и очищают флэш-хроматографией с получением указанного в заголовке соединения (540 мг).
Пример 144-4: Синтез 2-метил-8-(4-пиперидилокси)-3,4-дигидро-2H-пиридо[3,2-f][1,4]оксазепин-5-она
Продукт (540 мг), полученный в примере 144-3, растворяют в 4 мл трифторуксусной кислоты, и реакцию проводят с применением микроволн при 120°C в течение 30 минут. Реакционный раствор разбавляют этилацетатом на ледяной бане и подщелачивают водным раствором K2CO3. Реакционную смесь промывают этилацетатом 3 раза, и KOH добавляют в водный слой для подщелачивания pH до 9 или выше, с последующим экстрагированием этилацетатом. Экстрагированный органический слой сушат над безводным сульфатом натрия и концентрируют с получением указанного в заголовке соединения.
Пример 144-5: Синтез 2-метил-8-[(1-метил-4-пиперидил)окси]-3,4-дигидро-2H-пиридо[3,2-f][1,4]оксазепин-5-она
Продукт, полученный в примере 144-4, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
Пример 144-6: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она
Продукт, полученный в примере 144-5, используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) (диастереомерная смесь) δ 8,18 (т, J=7,4 Гц, 2H), 7,17-7,01 (м, 8H), 6,57 (дд, J=9,0, 3,9 Гц, 2H), 5,10 (с, 2H), 4,83 (д, J=7,4 Гц, 3H), 4,29-4,16 (м, 2H), 4,12 (д, J=14,1 Гц, 1H), 3,85 (д, J=14,1 Гц, 1H), 3,78-3,66 (м, 8H), 3,68-3,53 (м, 3H), 3,21 (дд, J=13,9, 8,7 Гц, 1H), 2,98-2,85 (м, 9H), 2,85-2,73 (м, 4H), 2,69-2,56 (м, 4H), 2,46 (с, 4H), 2,36 (с, 6H), 2,12-2,02 (м, 4H), 1,93-1,78 (м, 4H), 1,44 (т, J=6,7 Гц, 6H).
Пример 145: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[(1-метил-4-пиперидил)окси]-3H-пиридо[3,2-f][1,4]оксазепин-5-она
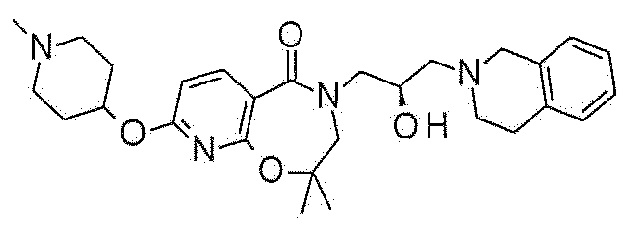
Указанное в заголовке соединение синтезируют по методике примера 144, за исключением того, что 1-[(4-метоксифенил)метиламино]-2-метил-пропан-2-ол используют вместо 1-[(4-метоксифенил)метиламино]пропан-2-ола.
1H ЯМР (400 MГц, Метанол-d4) δ 8,04 (д, J=8,0 Гц, 1H), 7,17-7,02 (м, 4H), 6,62 (д, J=8,3 Гц, 1H), 5,17-5,03 (м, 1H), 4,32-4,21 (м, 1H), 4,03 (д, J=14,1 Гц, 1H), 3,76 (с, 2H), 3,71-3,57 (м, 2H), 3,41 (дд, J=13,8, 8,1 Гц, 1H), 2,97-2,84 (м, 4H), 2,85-2,73 (м, 2H), 2,71-2,58 (м, 3H), 2,55-2,41 (м, 2H), 2,37 (с, 3H), 2,13-2,01 (м, 2H), 1,91-1,80 (м, 2H), 1,45 (д, J=18,4 Гц, 6H).
Пример 146: Синтез (2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
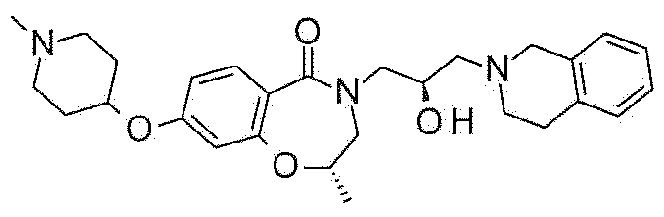
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1R)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140 используют в качестве исходного материала по методике примера 141 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,5 Гц, 1H), 7,18-7,04 (м, 4H), 6,81 (д, J=8,8 Гц, 1H), 6,58 (д, J=2,8 Гц, 1H), 4,83 (с, 1H), 4,57 (с, 1H), 4,32 (д, J=2,0 Гц, 3H), 4,25 (с, 1H), 3,79 (д, J=13,0 Гц, 3H), 3,68-3,58 (м, 2H), 3,47 (дд, J=15,6, 9,2 Гц, 1H), 2,92 (д, J=23,0 Гц, 5H), 2,70 (д, J=6,3 Гц, 2H), 2,63 (с, 2H), 2,46 (д, J=2,0 Гц, 3H), 2,08 (с, 2H), 1,95-1,87 (м, 2H), 1,29 (д, J=6,5 Гц, 3H).
Пример 147: Синтез 4-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
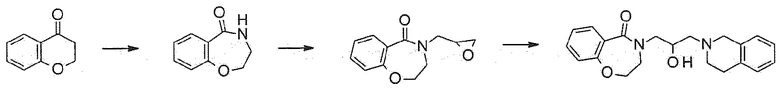
Пример 147-1: Синтез 3,4-дигидро-2H-1,4-бензоксазепин-5-она
Хроман-4-он (2,0 г, 14 ммоль) растворяют в 10 мл концентрированной серной кислоты, и туда медленно добавляют азид натрия (1,1 г, 18 ммоль) при 0°C. Реакционную смесь медленно нагревают до комнатной температуры и перемешивают в течение 12 часов. Реакционную смесь выдерживают при 0°C на ледяной бане, и туда медленно добавляют 1 M водный раствор гидроксида натрия. После подщелачивания реакционного раствора до pH 10 или более, добавляют этилацетат и экстрагируют 3 раза. Объединенные органические слои сушат над безводным сульфатом магния, растворитель удаляют выпариванием при пониженном давлении, и перекристаллизуют с дихлорметаном и гексаном с получением указанного в заголовке соединения в виде белого твердого вещества.
Пример 147-2: Синтез 4-(оксиран-2-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
3,4-Дигидро-2H-1,4-бензоксазепин-5-он (163 мг, 1 ммоль), полученный в примере 147-1, растворяют в диметилформамиде, и туда добавляют гидрид натрия (52 мг, 1,3 ммоль) на ледяной бане. Реакционный раствор перемешивают при 0°C в течение 30 минут, и туда медленно добавляют эпибромгидрин (0,1 мл, 1,2 ммоль) и перемешивают при комнатной температуре в течение 2 часов. Метанол добавляют в реакционную смесь для завершения реакции, и добавляют этилацетат, и промывают насыщенным водным раствором хлорида аммония и насыщенным водным раствором хлорида натрия. Органический слой сушат над безводным сульфатом магния. Растворитель удаляют выпариванием при пониженном давлении, и полученное указанное в заголовке соединение используют в следующей реакции без дальнейшей очистки.
Пример 147-3: Синтез 4-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
4-(Оксиран-2-илметил)-2,3-дигидро-1,4-бензоксазепин-5-он, полученный в примере 147-2, растворяют в изопропаноле, и туда добавляют тетрагидроизохинолин (0,13 мл, 1,0 ммоль) и перемешивают при 80°C в течение 12 часов. Температуру понижают до комнатной температуры, и маслянистую жидкость, полученную концентрированием растворителя очищают флэш-хроматографией с получением прозрачного и липкого твердого соединения. ЯМР данные для полученного указанного в заголовке соединения следующие.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (дд, J=7,9, 1,7 Гц, 1H), 7,48 (тд, J=7,8, 1,7 Гц, 1H), 7,20 (т, J=7,5 Гц, 1H), 7,15-6,99 (м, 5H), 4,46 (т, J=5,2 Гц, 2H), 4,29-4,18 (м, 1H), 3,99 (дд, J=13,9, 3,6 Гц, 1H), 3,68 (тд, J=5,1, 1,6 Гц, 2H), 3,44 (дд, J=13,8, 7,7 Гц, 1H), 2,92 (д, J=5,6 Гц, 2H), 2,86 (т, J=6,2 Гц, 2H), 2,70-2,59 (м, 2H).
Пример 148: Синтез 2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-4,5-дигидро-3H-2-бензазепин-1-она
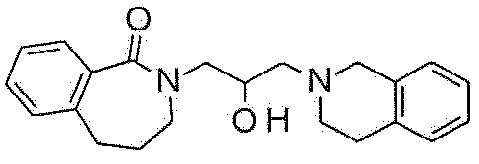
Тетралин-1-он (1,9 г, 14 ммоль) используют в качестве исходного материала по методике примера 147 с получением указанного в заголовке соединения, за исключением того, что 35% водный раствор хлористоводородной кислоты (30 мл) используют вместо концентрированной серной кислоты в примере 147-1.
1H ЯМР (400 MГц, Метанол-d4) δ 7,58 (д, J=7,9 Гц, 1H), 7,45 (т, J=7,4 Гц, 1H), 7,36 (т, J=7,5 Гц, 1H), 7,25 (д, J=7,4 Гц, 1H), 7,17-7,02 (м, 4H), 4,25 (дт, J=7,8, 3,7 Гц, 1H), 3,95 (дд, J=13,8, 3,7 Гц, 1H), 3,48-3,36 (м, 3H), 2,94 (д, J=5,5 Гц, 3H), 2,91-2,86 (м, 2H), 2,82 (т, J=7,1 Гц, 2H), 2,66 (h, J=7,6 Гц, 2H), 2,14 (п, J=6,8 Гц, 2H).
Пример 149: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
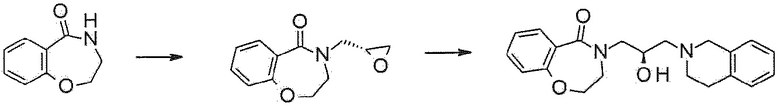
Пример 149-1: Синтез 4-[[(2R)-оксиран-2-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она
3,4-Дигидро-2H-1,4-бензоксазепин-5-он (163 мг, 1 ммоль), полученный в примере 147-1, растворяют в 5 мл диметилформамида, и туда добавляют гидрид натрия (48 мг, 1,2 ммоль) на ледяной бане. Реакционный раствор перемешивают при 0°C в течение 30 минут, и туда медленно добавляют (R)-(-)-глицидилнозилат (298 мг, 1,15 ммоль) и перемешивают при комнатной температуре в течение 2 часов. Метанол добавляют в реакционную смесь для завершения реакции, и этилацетат добавляют, и промывают насыщенным водным раствором хлорида аммония и насыщенным водным раствором хлорида натрия. Органический слой сушат над безводным сульфатом магния. Растворитель удаляют выпариванием при пониженном давлении, и полученное указанное в заголовке соединение используют в следующей реакции без дальнейшей очистки.
Пример 149-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[[(2R)-оксиран-2-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-он, полученный в примере 149-1, используют по методике примера 147-3 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (дд, J=7,9, 1,7 Гц, 1H), 7,48 (тд, J=7,8, 1,8 Гц, 1H), 7,20 (т, J=7,5 Гц, 1H), 7,15-7,02 (м, 5H), 4,46 (т, J=5,2 Гц, 2H), 4,29-4,19 (м, 1H), 3,99 (дд, J=13,9, 3,6 Гц, 1H), 3,75 (д, J=2,2 Гц, 2H), 3,74-3,63 (м, 2H), 3,44 (дд, J=13,9, 7,7 Гц, 1H), 2,97-2,90 (м, 2H), 2,91-2,83 (м, 2H), 2,70-2,60 (м, 2H).
Пример 150: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-фтор-2,3-дигидро-1,4-бензоксазепин-5-она
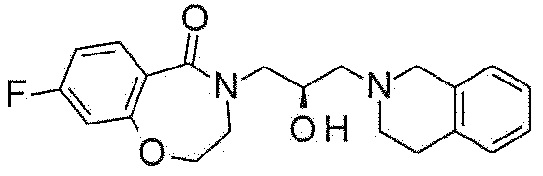
7-Фторхроман-4-он используют в качестве исходного материала по методике примеров 147-1 и 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,81-7,73 (м, 1H), 7,16-7,02 (м, 4H), 6,94 (тд, J=8,5, 2,6 Гц, 1H), 6,81 (дд, J=9,9, 2,6 Гц, 1H), 4,52 (т, J=5,0 Гц, 2H), 4,27-4,20 (м, 1H), 3,99 (дд, J=13,9, 3,6 Гц, 1H), 3,81-3,71 (м, 4H), 3,44 (дд, J=13,9, 7,8 Гц, 1H), 2,98-2,84 (м, 4H), 2,69-2,61 (м, 2H).
Пример 151: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
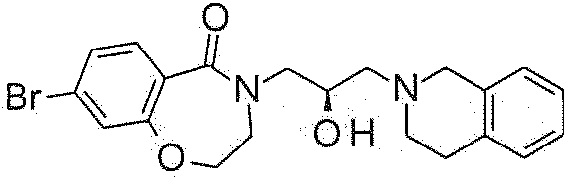
7-Бромхроман-4-он используют в качестве исходного материала по методике примеров 147-1 и 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,4 Гц, 1H), 7,35 (дд, J=8,4, 1,7 Гц, 1H), 7,26 (д, J=1,6 Гц, 1H), 7,16-7,01 (м, 4H), 4,51 (т, J=5,0 Гц, 2H), 4,27-4,17 (м, 1H), 3,99 (дд, J=13,7, 3,5 Гц, 1H), 3,74 (д, J=6,5 Гц, 4H), 3,44 (дд, J=13,9, 7,8 Гц, 1H), 2,97-2,83 (м, 4H), 2,69-2,59 (м, 2H).
Пример 152: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидропиридо[4,3-f][1,4]оксазепин-5-она
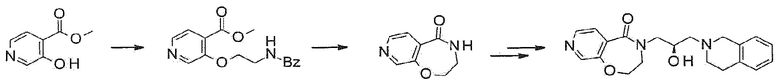
Пример 152-1: Синтез метил 3-[2-(бензилоксикарбониламино)этокси]пиридин-4-карбоксилата
Метил 3-гидроксипиридин-4-карбоксилат (1,0 г, 6,53 ммоль), бензил N-(2-гидроксиэтил)карбамат (1,53 г, 7,84 ммоль) и трифенилфосфин (2,06 г) растворяют в тетрагидрофуране, и туда медленно добавляют диизопропилазодикарбоксилат при 0°С. Реакционный раствор перемешивают при комнатной температуре в течение 12 часов, и растворитель удаляют при пониженном давлении. Концентрат очищают флэш-хроматографией в условиях растворителя гексана и этилацетата с получением указанного в заголовке соединения.
Пример 152-2: Синтез 3,4-дигидро-2H-пиридо[4,3-f][1,4]оксазепин-5-она
Метил 3-[2-(бензилоксикарбониламино)этокси]пиридин-4-карбоксилат, полученный в примере 152-1, растворяют в этаноле при комнатной температуре, и туда добавляют 5% палладий на угле, с последующим перемешиванием под баллоном водорода в течение 24 часов. Реакционный раствор фильтруют через целит и промывают этанолом. Полученный раствор концентрируют при пониженном давлении и очищают флэш-хроматографией с получением указанного в заголовке соединения (548 мг) в виде белого кристаллического твердого вещества.
Пример 152-3: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидропиридо[4,3-f][1,4]оксазепин-5-она
3,4-Дигидро-2H-пиридо[4,3-f][1,4]оксазепин-5-он, полученный в примере 152-2, используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,36 (с, 1H), 8,31 (д, J=5,1 Гц, 1H), 7,75 (д, J=5,1 Гц, 1H), 7,17-7,02 (м, 4H), 4,62 (т, J=4,7 Гц, 2H), 4,30-4,20 (м, 1H), 4,02 (дд, J=13,9, 3,5 Гц, 1H), 3,82 (т, J=4,6 Гц, 2H), 3,76 (с, 2H), 3,45 (дд, J=13,9, 8,0 Гц, 1H), 2,98-2,90 (м, 2H), 2,91-2,83 (м, 2H), 2,69-2,60 (м, 2H).
Пример 153: Синтез 8-хлор-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она
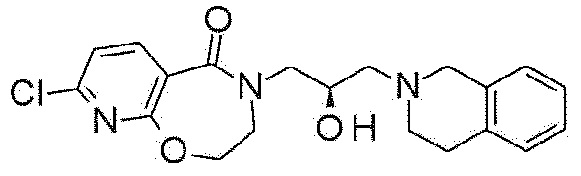
8-Хлор-3,4-дигидро-2H-пиридо[3,2-f][1,4]оксазепин-5-он используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,36 (дд, J=8,1, 1,4 Гц, 1H), 7,26 (дд, J=8,2, 1,4 Гц, 1H), 7,17-7,00 (м, 4H), 4,70-4,67 (м, 2H), 4,24 (кв, J=9,0, 8,0 Гц, 1H), 3,99 (дд, J=13,9, 3,5 Гц, 1H), 3,89 (т, J=4,3 Гц, 2H), 3,76 (с, 2H), 3,42 (дд, J=13,8, 8,1 Гц, 1H), 2,94-2,86 (дд, J=17,3, 5,4 Гц, 4H), 2,65 (д, J=6,3 Гц, 2H).
Пример 154: Синтез 7-хлор-2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-4,5-дигидро-3H-2-бензазепин-1-она
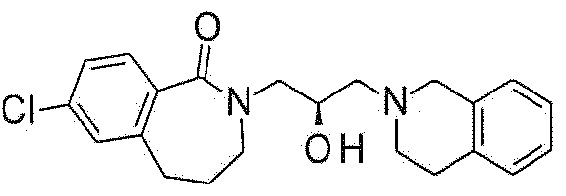
7-Хлор-2,3,4,5-тетрагидро-2-бензазепин-1-он используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,55 (д, J=8,2 Гц, 1H), 7,35 (дд, J=8,3, 1,9 Гц, 1H), 7,27 (д, J=2,1 Гц, 1H), 7,15-7,00 (м, 4H), 4,27-4,18 (м, 1H), 3,91 (дд, J=13,8, 3,6 Гц, 1H), 3,75 (с, 2H), 3,44-3,33 (м, 2H), 3,32-3,23 (м, 1H), 2,97-2,89 (м, 2H), 2,90-2,82 (м, 2H), 2,78 (т, J=7,1 Гц, 2H), 2,68-2,59 (м, 2H), 2,11 (п, J=6,8 Гц, 2H).
Пример 155: Синтез 7-бром-2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-4,5-дигидро-3H-2-бензазепин-1-она
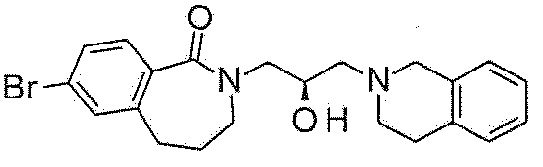
7-Бром-2,3,4,5-тетрагидро-2-бензазепин-1-он используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,55-7,51 (м, 1H), 7,51-7,45 (м, 2H), 7,16-7,01 (м, 4H), 4,29-4,19 (м, 1H), 3,92 (дд, J=13,8, 3,6 Гц, 1H), 3,78 (с, 2H), 3,47-3,38 (м, 2H), 3,36-3,34 (м, 1H), 2,99-2,91 (м, 2H), 2,93-2,85 (м, 2H), 2,80 (т, J=7,1 Гц, 2H), 2,71-2,61 (м, 2H), 2,14 (п, J=6,9 Гц, 2H).
Пример 156: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
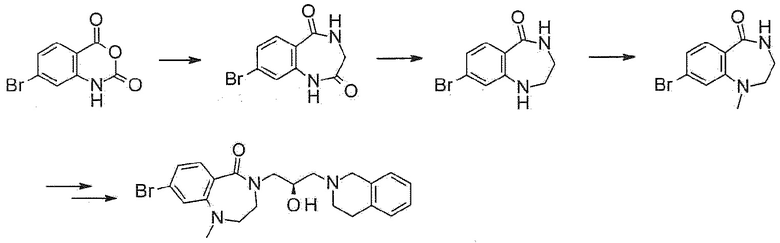
Пример 156-1: Синтез 8-бром-3,4-дигидро-1H-1,4-бензодиазепин-2,5-диона
7-Бром-1H-3,1-бензоксазин-2,4-дион (550 г, 2,27 моль) растворяют в 2,5 л дистиллированной воды, и туда добавляют триэтиламин (230 г, 2,27 моль) и глицин (239 г, 3,18 моль). Реакционный раствор перемешивают при комнатной температуре в течение 4 часов, концентрируют, снова растворяют в 3 л уксусной кислоты, и смесь перемешивают при 140°C в течение 8 часов. Реакционный раствор разбавляют петролейным эфиром и фильтруют с получением указанного в заголовке соединения (866 г, 74,7%) в виде белого твердого вещества.
Пример 156-2: Синтез 8-бром-1,2,3,4-тетрагидро-1,4-бензодиазепин-5-она
8-Бром-3,4-дигидро-1H-1,4-бензодиазепин-2,5-дион (200 г, 784 ммоль), полученный в примере 156-1, растворяют в 4 л тетрагидрофурана, и туда медленно добавляют LAH (50,6 г, 1,33 моль) при 0°C. Реакционный раствор перемешивают при 70°C в течение 3 часов, и после охлаждения, медленно добавляют 100 мл дистиллированной воды, 100 мл 15% водного раствора гидроксида натрия, и еще 100 мл дистиллированной воды для завершения реакции. Смешанный раствор сушат над безводным сульфатом натрия, фильтруют с горячим тетрагидрофураном, растворитель удаляют при пониженном давлении, и перекристаллизовывают добавлением 500 мл этилацетата с получением указанного в заголовке соединения (177 г, 46,8%) в виде белого твердого вещества.
Пример 156-3: Синтез 8-бром-1-метил-3,4-дигидро-2H-1,4-бензодиазепин-5-она
8-Бром-1,2,3,4-тетрагидро-1,4-бензодиазепин-5-он (177 г, 734 ммоль), полученный в примере 156-2, растворяют в 1,2 л метанола, и туда добавляют параформальдегид (200 г, 3,67 моль), растворенный в 1,2 л уксусной кислоты. Реакционный раствор перемешивают при 50°C в течение 1 часа. Цианоборгидрид натрия (231 г, 3,67 моль) добавляют к реакционному раствору, перемешивают при 50°C в течение 4 часов, и концентрируют удалением растворителя при пониженном давлении. Смесь разбавляют 4 л дистиллированной воды и экстрагируют дихлорметан 2 раза. Объединенные органические слои промывают насыщенным водным раствором хлорида натрия 2 раза, сушат над безводным сульфатом натрия, фильтруют, и концентрируют при пониженном давлении. Метанол добавляют в полученный концентрат и перекристаллизовывают с получением указанного в заголовке соединения (выход: 78%) в виде белого твердого вещества.
Пример 156-4: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она
8-Бром-1-метил-3,4-дигидро-2H-1,4-бензодиазепин-5-он, полученный в примере 156-3, используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,42 (д, J=7,7 Гц, 1H), 7,20-7,02 (м, 6H), 4,23 (м, 1H), 3,94 (дд, J=13,8, 3,9 Гц, 1H), 3,76 (с, 2H), 3,63 (кв, J=4,9 Гц, 2H), 3,52-3,37 (м, 3H), 2,93 (д, J=5,7 Гц, 2H), 2,92-2,80 (м, 5H), 2,73-2,59 (м, 2H).
Пример 157: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-этил-2,3-дигидро-1,4-бензодиазепин-5-она
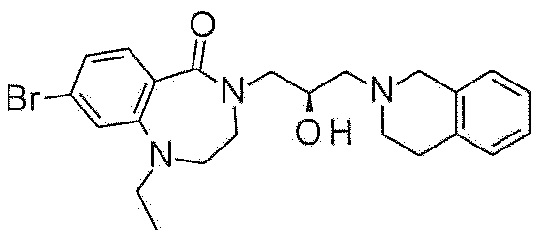
Пример 157-1: Синтез 8-бром-1-этил-3,4-дигидро-2H-1,4-бензодиазепин-5-она
8-Бром-1,2,3,4-тетрагидро-1,4-бензодиазепин-5-он (100 мг, 0,41 ммоль), полученный в примере 156-2, и карбонат калия (170 мг, 1,23 ммоль) растворяют в диметилформамиде, и туда добавляют йодэтан (0,07 мл, 0,82 ммоль). Реакционный раствор перемешивают при 60°С в течение одного дня. Реакционную смесь охлаждают до комнатной температуры, разбавляют дистиллированной водой и экстрагируют этилацетатом 3 раза. Объединенные органические слои промывают насыщенным водным раствором хлорида натрия 2 раза, сушат над безводным сульфатом магния, фильтруют, и концентрируют при пониженном давлении. Полученный концентрат очищают флэш-хроматографией с получением указанного в заголовке твердого соединения.
Пример 157-2: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-этил-2,3-дигидро-1,4-бензодиазепин-5-она
Продукт, полученный в примере 157-1, используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,42 (д, J=8,6 Гц, 1H), 7,17-7,09 (м, 5H), 7,06 (д, J=5,6 Гц, 1H), 4,23 (дт, J=12,4, 6,4 Гц, 1H), 3,90 (дд, J=13,8, 4,0 Гц, 1H), 3,79 (с, 2H), 3,61 (д, J=5,9 Гц, 2H), 3,49 (дд, J=14,4, 6,8 Гц, 2H), 3,41 (т, J=5,4 Гц, 2H), 3,22 (дт, J=11,9, 6,8 Гц, 2H), 2,95-2,88 (м, 4H), 2,76-2,63 (м, 2H), 1,20 (т, J=7,1 Гц, 3H).
Пример 158: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-этил-3H-1,4-бензодиазепин-2,5-диона
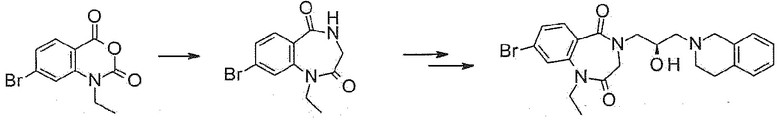
Пример 158-1: Синтез 8-бром-1-этил-3,4-дигидро-1,4-бензодиазепин-2,5-диона
7-Бром-1-этил-3,1-бензоксазин-2,4-дион (262 мг, 0,97 ммоль) и глицин (73 мг, 0,97 ммоль) растворяют в уксусной кислоте, и нагревают до кипения с обратным холодильником в течение 4 часов. Реакционную смесь охлаждают до комнатной температуры, разбавляют дистиллированной водой и фильтруют. Полученное твердое вещество промывают диэтиловым эфиром с получением указанного в заголовке твердого соединения (100 мг) без дополнительной очистки.
Пример 158-2: Синтез 8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-этил-3H-1,4-бензодиазепин-2,5-диона
Продукт, полученный в примере 158-1, используют в качестве исходного материала по методике примера 149 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,72-7,69 (м, 2H), 7,55 (д, J=8,5 Гц, 1H), 7,17-6,99 (м, 4H), 4,24 (п, J=7,4 Гц, 2H), 4,15 (дд, J=14,9, 6,0 Гц, 1H), 4,01-3,95 (м, 2H), 3,85-3,67 (м, 4H), 3,53-3,45 (м, 1H), 2,93-2,86 (м, 4H), 2,63 (д, J=7,0 Гц, 2H), 1,19-1,09 (м, 3H).
Пример 159: Синтез 2-[4-[[4-(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]-1-пиперидил]ацетонитрила
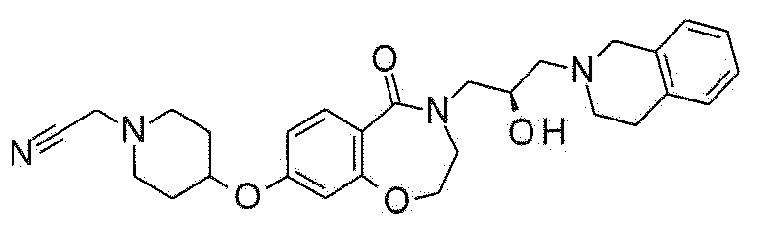
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 78-1, растворяют в ацетонитриле, туда добавляют карбонат калия и 2-бромацетонитрил, с последующим перемешиванием при 90°С в течение 1 часа. В реакционную смесь добавляют насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом натрия и концентрацией при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения в виде белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (дд, J=8,7, 2,2 Гц, 1H), 7,16-7,09 (м, 3H), 7,06 (д, J=6,6 Гц, 1H), 6,81 (дд, J=8,8, 2,7 Гц, 1H), 6,64 (д, J=2,6 Гц, 1H), 4,76 (дкв, J=7,2, 3,8 Гц, 1H), 4,47 (д, J=5,4 Гц, 2H), 4,23 (с, 1H), 4,17-4,07 (м, 1H), 3,97 (дт, J=13,8, 3,2 Гц, 1H), 3,86-3,65 (м, 6H), 3,61 (т, J=11,6 Гц, 1H), 3,43 (дд, J=14,2, 7,6 Гц, 1H), 2,97-2,86 (м, 4H), 2,67 (д, J=6,1 Гц, 2H), 2,04 (т, J=6,5 Гц, 3H), 1,87 (ддд, J=23,5, 11,9, 4,2 Гц, 2H), 1,26 (тд, J=7,4, 2,2 Гц, 1H).
Пример 160: Синтез 8-[[1-(2,2-дифторацетил)-4-пиперидил]окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
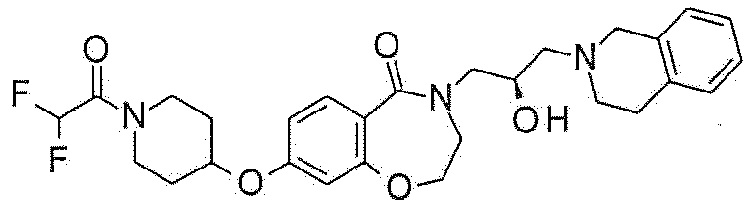
Указанное в заголовке соединение синтезируют по методике примера 78 за исключением того, что дифторуксусный ангидрид используют вместо уксусного ангидрида в примере 78-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (дд, J=8,8, 2,1 Гц, 1H), 7,14 (h, J=5,8 Гц, 3H), 7,07 (д, J=7,0 Гц, 1H), 6,77 (дд, J=8,8, 2,9 Гц, 1H), 6,60 (д, J=2,3 Гц, 1H), 4,52 (с, 1H), 4,47 (д, J=5,4 Гц, 2H), 4,26 (с, 1H), 3,95 (дд, J=13,9, 3,4 Гц, 1H), 3,86 (с, 2H), 3,77-3,65 (м, 4H), 3,46 (дд, J=14,0, 7,5 Гц, 1H), 2,98 (с, 3H), 2,88-2,67 (м, 4H), 2,58 (т, J=9,5 Гц, 2H), 2,08-2,00 (м, 2H), 1,86 (д, J=11,8 Гц, 2H).
Пример 161: Синтез 8-[[1-(2,2-дифторацетил)азетидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
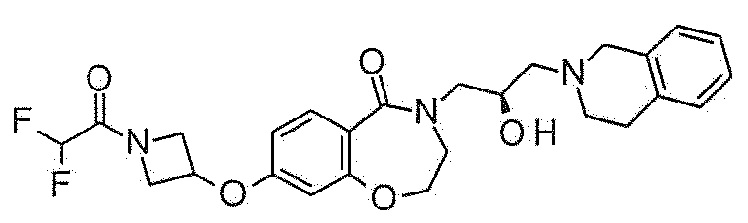
8-(Азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 83-1, используют в качестве исходного материала по методике примера 160 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,72 (дд, J=8,7, 2,0 Гц, 1H), 7,14 (д, J=5,7 Гц, 3H), 7,07 (д, J=6,9 Гц, 1H), 6,69 (д, J=8,6 Гц, 1H), 6,49 (д, J=2,3 Гц, 1H), 5,21-5,14 (м, 1H), 4,88-4,77 (м, 1H), 4,60-4,37 (м, 4H), 4,25 (д, J=7,2 Гц, 1H), 4,11 (тд, J=11,8, 10,3, 5,3 Гц, 2H), 3,96 (дд, J=13,9, 3,2 Гц, 1H), 3,85 (с, 2H), 3,72 (h, J=7,3, 6,4 Гц, 2H), 3,46 (дд, J=14,1, 7,6 Гц, 1H), 2,97 (с, 3H), 2,80-2,69 (м, 2H).
Пример 162: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
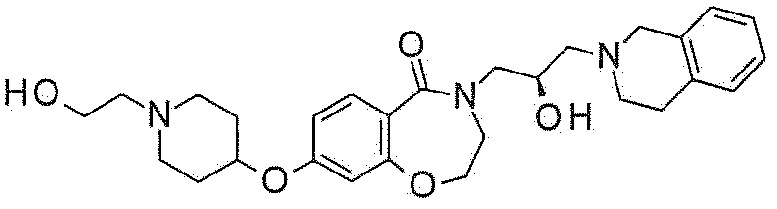
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид (100 мг, 0,19 ммоль), полученный в примере 78-1, карбонат калия (79 мг, 0,57 ммоль) и 2-йодэтанол (15 мкл, 0,19 ммоль) растворяют в ацетонитриле и перемешивают. После завершения реакции, реакционный раствор концентрируют и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,9 Гц, 1H), 7,11-7,03 (м, 4H), 6,76 (д, J=8,9 Гц, 1H), 6,59 (с, 1H), 4,51-4,46 (м, 3H), 4,18 (с, 1H), 3,98 (д, J=13,9 Гц, 1H), 3,76-3,71 (м, 6H), 3,42 (дд, J=14,0, 7,9 Гц, 1H), 3,02-2,79 (м, 6H), 2,71-2,58 (м, 4H), 2,58-2,43 (м, 2H), 2,04 (т, J=7,4 Гц, 2H), 1,91-1,75 (м, 2H).
Пример 163: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-фторэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
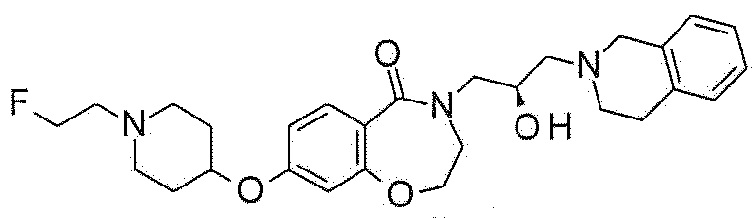
Указанное в заголовке соединение синтезируют по методике примера 162 за исключением того, что 2-фторэтил 4-метилбензолсульфонат используют вместо 2-йодэтанола при 90°C.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,7 Гц, 1H), 7,17-7,01 (м, 4H), 6,76 (д, J=8,9 Гц, 1H), 6,58 (с, 1H), 4,66 (т, J=5,0 Гц, 1H), 4,59-4,42 (м, 4H), 4,23 (с, 1H), 3,97 (д, J=13,4 Гц, 1H), 3,84-3,66 (м, 4H), 3,42 (дд, J=13,9, 7,6 Гц, 1H), 3,02-2,76 (м, 7H), 2,75-2,59 (м, 3H), 2,51 (т, J=10,2 Гц, 2H), 2,13-2,00 (м, 2H), 1,93-1,75 (м, 2H).
Пример 164: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-фторэтил)-4-пиперидил]окси]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она
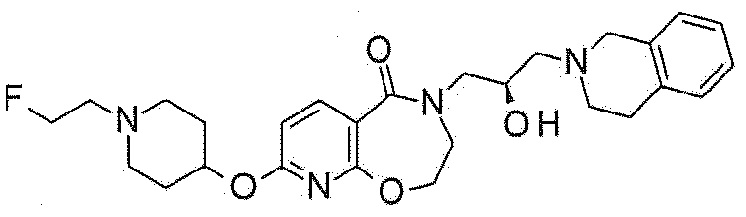
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-он дигидрохлорид используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,26 (д, J=8,5 Гц, 1H), 7,19-6,97 (м, 4H), 6,55 (д, J=8,5 Гц, 1H), 5,08 (с, 1H), 4,66 (с, 1H), 4,61 (с, 2H), 4,55 (с, 1H), 4,29-4,18 (м, 1H), 3,99 (д, J=13,9 Гц, 1H), 3,90-3,83 (м, 2H), 3,75 (с, 2H), 3,43-3,37 (м, 1H), 2,99-2,83 (м, 6H), 2,80 (с, 1H), 2,73 (с, 1H), 2,63 (д, J=6,2 Гц, 2H), 2,55-2,43 (м, 2H), 2,14-2,03 (м, 2H), 1,90-1,77 (м, 2H).
Пример 165: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-[(3-метилоксетан-3-ил)метил]-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
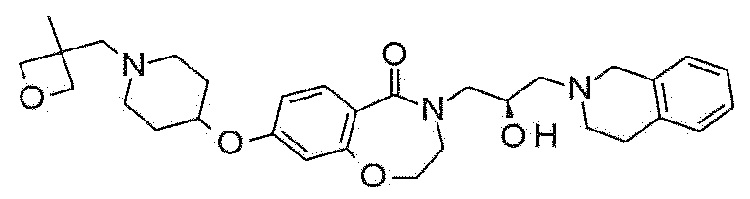
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он (200 мг, 0,443 ммоль), полученный в примере 78-1, карбонат цезия (288 мг, 0,886 ммоль) и 3-(бромметил)-3-метилоксетан (110 мг, 0,665 ммоль) растворяют в диметилформамиде, нагревают до 60°C и перемешивают. После завершения реакции, реакционный раствор экстрагируют насыщенным водным раствором хлорида натрия и этилацетатом, и очищают флэш-хроматографией с получением указанного в заголовке соединения (6 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,7 Гц, 1H), 7,12 (д, J=3,1 Гц, 3H), 7,06 (д, J=6,6 Гц, 1H), 6,75 (д, J=8,7 Гц, 1H), 6,57 (д, J=3,2 Гц, 1H), 4,56-4,46 (м, 4H), 4,45 (с, 2H), 4,33 (д, J=5,7 Гц, 2H), 4,23 (с, 1H), 4,01-3,92 (м, 1H), 3,80-3,69 (м, 4H), 3,42 (дд, J=14,0, 7,6 Гц, 1H), 2,97-2,85 (м, 4H), 2,66 (д, J=6,7 Гц, 2H), 2,61 (с, 3H), 2,31 (т, J=10,3 Гц, 2H), 2,06-1,98 (м, 2H), 1,79 (т, J=10,2 Гц, 2H), 1,43 (с, 3H).
Пример 166: Синтез 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоазепин-8-ил]окси]пиперидин-1-карбонитрил
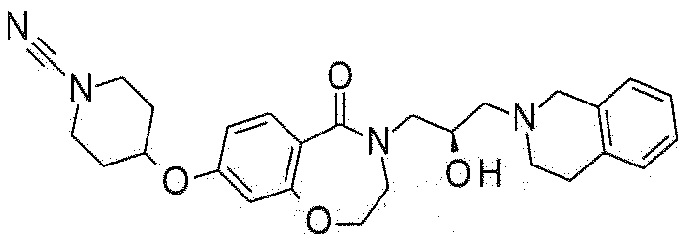
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он (200 мг, 0,443 ммоль), полученный в примере 78-1, цианогенбромид (94 мг, 0,886 ммоль) и карбонат цезия (433 мг, 1,329 ммоль) растворяют в диметилформамид, и реакцию проводят с применением микроволн при 70°C в течение 3 часов. После завершения реакции, реакционный раствор экстрагируют насыщенным водным раствором хлорида натрия и этилацетатом, и очищают флэш-хроматографией с получением указанного в заголовке соединения (14 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (дд, J=8,7, 2,1 Гц, 1H), 7,14-7,09 (м, 3H), 7,05 (д, J=6,7 Гц, 1H), 6,79 (дд, J=8,8, 2,3 Гц, 1H), 6,63 (д, J=2,4 Гц, 1H), 4,65 (дкв, J=7,1, 3,6 Гц, 1H), 4,51-4,43 (м, 2H), 4,23 (д, J=7,3 Гц, 1H), 3,97 (дт, J=14,1, 2,9 Гц, 1H), 3,82-3,69 (м, 4H), 3,55-3,37 (м, 3H), 3,26 (т, J=9,9 Гц, 2H), 2,93 (д, J=5,6 Гц, 2H), 2,91-2,84 (м, 2H), 2,65 (д, J=6,3 Гц, 2H), 2,09 (т, J=10,7 Гц, 2H), 1,94-1,81 (м, 2H).
Пример 167: Синтез 8-[(4-ацетилпиперазин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она
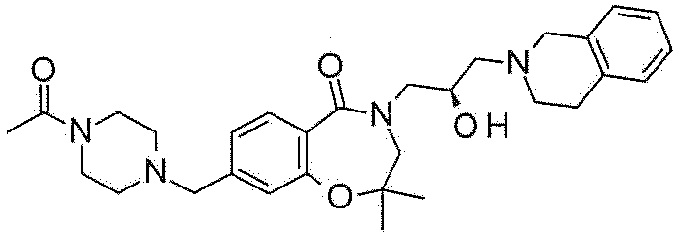
Пример 167-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(пиперазин-1-илметил)-3H-1,4-бензоксазепин-5-она; дигидрохлорида
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примеров 54-1 и 54-2 с получением указанного в заголовке соединения.
Пример 167-2: Синтез 8-[(4-ацетилпиперазин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она
Продукт, полученный в примере 167-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=7,8 Гц, 1H), 7,23 (д, J=8,0 Гц, 1H), 7,17-7,02 (м, 4H), 7,00 (с, 1H), 4,29 (с, 1H), 4,06 (д, J=13,6 Гц, 1H), 3,77 (с, 2H), 3,59 (т, J=10,1 Гц, 6H), 3,48 (с, 2H), 3,43 (дд, J=14,0, 8,0 Гц, 2H), 2,93 (с, 4H), 2,74-2,56 (м, 2H), 2,55-2,41 (м, 4H), 2,10 (с, 3H), 1,43 (с, 3H), 1,33 (с, 3H).
Пример 168: Синтез 3-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]окси]азетидин-1-карбальдегида
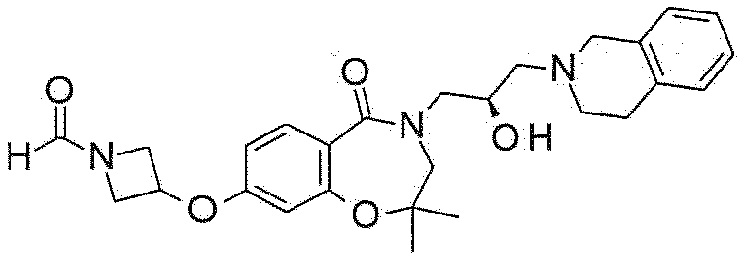
Пример 168-1: Синтез 8-(азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она дигидрохлорида
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2,2-диметил-3H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примера 83-1 с получением указанного в заголовке соединения.
Пример 168-2: Синтез 3-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]окси]азетидин-1-карбальдегида
Продукт (105 мг, 0,2 ммоль), полученный в примере 168-1, растворяют в 2 мл ацетонитрила, и туда добавляют муравьиную кислоту (38 мкл, 1,0 ммоль), триэтиламин (0,17 мл, 1,2 мл) и HATU(114 мг, 0,3 ммоль) и перемешивают при комнатной температуре.
После подтверждения завершения реакции, добавляют насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом 3 раза. Объединенные органические слои сушат над безводным сульфатом магния, концентрируют при пониженном давлении и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,03 (с, 1H), 7,62 (д, J=8,4 Гц, 1H), 7,21-7,03 (м, 4H), 6,72 (д, J=8,7 Гц, 1H), 6,45 (с, 1H), 5,19 (с, 1H), 4,68 (т, J=8,4 Гц, 1H), 4,52-4,42 (м, 1H), 4,35-4,18 (м, 2H), 4,02 (т, J=13,6 Гц, 2H), 3,79 (с, 2H), 3,51 (с, 2H), 3,43-3,37 (м, 1H), 2,93 (д, J=11,6 Гц, 4H), 2,73-2,59 (м, 2H), 1,44 (с, 3H), 1,35 (с, 3H).
Пример 169: Синтез 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]метил]пиперазин-1-карбальдегида
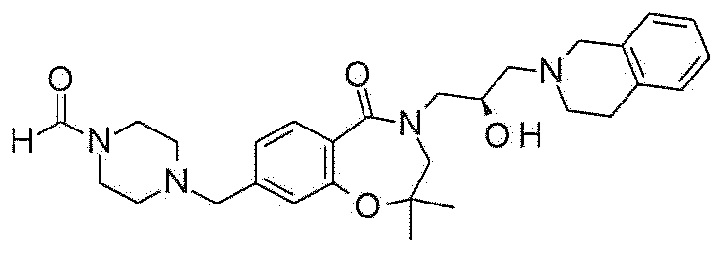
Продукт, полученный в примере 167-1, используют в качестве исходного материала по методике примера 168-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,03 (с, 1H), 7,61 (д, J=7,9 Гц, 1H), 7,23 (д, J=8,0 Гц, 1H), 7,19-7,03 (м, 4H), 7,01 (с, 1H), 4,30 (с, 1H), 4,06 (д, J=13,8 Гц, 1H), 3,79 (с, 2H), 3,61 (с, 2H), 3,56 (с, 2H), 3,52-3,38 (м, 5H), 2,93 (д, J=11,0 Гц, 4H), 2,75-2,60 (м, 2H), 2,49 (д, J=17,2 Гц, 4H), 1,44 (с, 3H), 1,34 (с, 3H).
Пример 170: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(2-окса-6-азаспиро[3,3]гептан-6-илметил)-3H-1,4-бензоксазепин-5-она
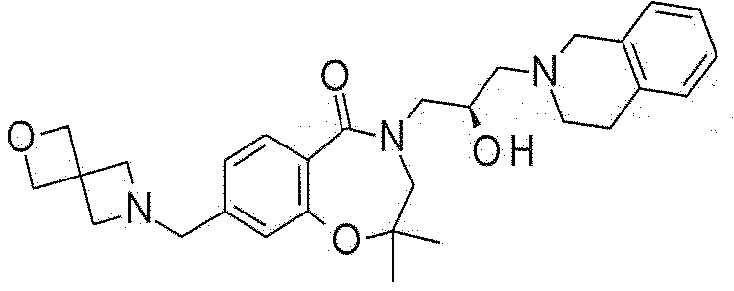
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примера 28 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,60 (д, J=7,8 Гц, 1H), 7,19-7,01 (м, 5H), 6,92 (с, 1H), 4,76 (с, 4H), 4,29 (с, 1H), 4,06 (д, J=13,8 Гц, 1H), 3,76 (с, 2H), 3,62 (с, 2H), 3,47 (с, 6H), 3,43-3,38 (м, 1H), 2,98-2,83 (м, 4H), 2,64 (с, 2H), 1,43 (с, 3H), 1,33 (с, 3H).
Пример 171: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(8-этил-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
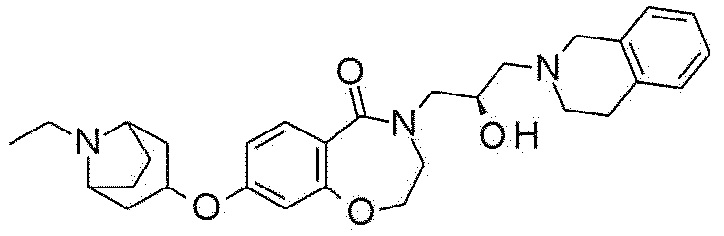
Пример 171-1: Синтез 8-[(8-азабицикло[3,2,1]октан-3-ил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение синтезируют заменой 4-хлортетрагидропирана на трет-бутил 3-метилсульфонилокси-8-азабицикло[3,2,1]октан-8-карбоксилат в примере 64. Полученное промежуточное соединение используют в качестве исходного материала по методике примера 78-1 с получением указанного в заголовке соединения.
Пример 171-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(8-этил-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 171-1, используют в качестве исходного материала по методике примера 88 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,60 (д, J=8,7 Гц, 1H), 7,09-6,92 (м, 4H), 6,61 (д, J=8,8 Гц, 1H), 6,42 (с, 1H), 4,56 (д, J=5,1 Гц, 1H), 4,38 (д, J=5,3 Гц, 2H), 4,13 (д, J=7,5 Гц, 1H), 4,00-3,87 (м, 1H), 3,65 (д, J=6,7 Гц, 4H), 3,42-3,27 (м, 3H), 2,96-2,71 (м, 4H), 2,53 (дд, J=14,6, 6,8 Гц, 4H), 2,09 (дд, J=29,8, 11,7 Гц, 4H), 2,01-1,78 (м, 4H), 1,09 (т, J=7,3 Гц, 3H).
Пример 172: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-этил-2-азаспиро[3,3]гептан-6-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
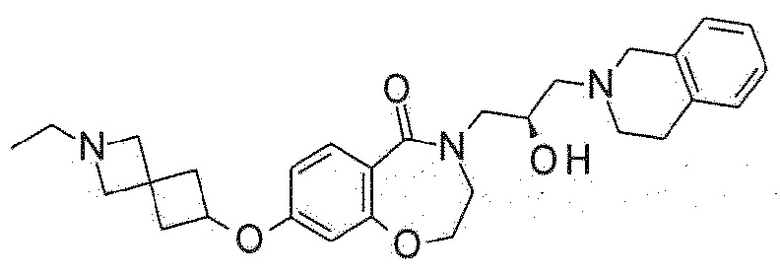
Пример 172-1: Синтез 8-(2-азаспиро[3,3]гептан-6-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение синтезируют заменой 4-хлортетрагидропирана на трет-бутил 6-метилсульфонилокси-2-азаспиро[3,3]гептан-2-карбоксилат в примере 64. Полученное промежуточное соединение используют в качестве исходного материала по методике примера 78-1 с получением указанного в заголовке соединения.
Пример 172-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-этил-2-азаспиро[3,3]гептан-6-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 172-1, используют в качестве исходного материала по методике примера 88 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,65 (дд, J=8,7, 2,1 Гц, 1H), 7,18-6,99 (м, 4H), 6,65 (д, J=8,5 Гц, 1H), 6,44 (д, J=3,0 Гц, 1H), 4,66 (т, J=6,8 Гц, 1H), 4,45 (д, J=5,1 Гц, 2H), 4,33-4,18 (м, 1H), 3,97 (дт, J=14,1, 2,9 Гц, 1H), 3,82-3,70 (м, 4H), 3,45-3,28 (м, 7H), 2,92 (д, J=5,8 Гц, 2H), 2,87 (д, J=6,0 Гц, 2H), 2,73 (ддд, J=11,3, 7,0, 3,6 Гц, 2H), 2,63 (д, J=6,3 Гц, 2H), 2,58-2,48 (м, 2H), 2,26 (ддд, J=13,1, 6,2, 2,4 Гц, 2H), 0,99 (тд, J=7,3, 2,0 Гц, 3H).
Пример 173: Синтез 8-[(8-ацетил-8-азабицикло[3,2,1]октан-3-ил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
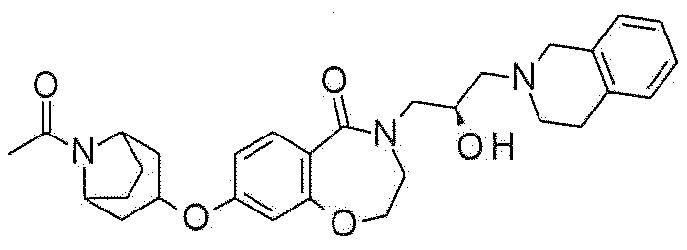
8-(8-Азабицикло[3,2,1]октан-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 171-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (дд, J=8,8, 2,0 Гц, 1H), 7,19-6,99 (м, 4H), 6,71 (дд, J=8,8, 2,6 Гц, 1H), 6,53 (д, J=2,5 Гц, 1H), 4,92 (с, 2H), 4,73 (д, J=4,9 Гц, 1H), 4,65-4,55 (м, 1H), 4,46 (д, J=5,1 Гц, 2H), 4,32-4,17 (м, 2H), 3,97 (дд, J=13,9, 3,4 Гц, 1H), 3,80-3,67 (м, 4H), 3,41 (дд, J=14,1, 7,6 Гц, 1H), 3,01-2,81 (м, 4H), 2,64 (д, J=6,2 Гц, 2H), 2,32-1,91 (м, 9H).
Пример 174: Синтез 8-[(2-ацетил-2-азаспиро[3,3]гептан-6-ил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
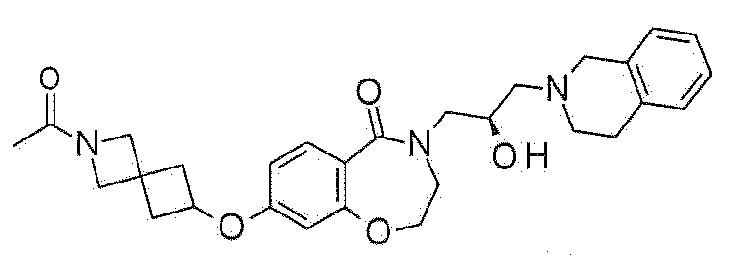
8-(2-Азаспиро[3,3]гептан-6-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 172-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,54 (дд, J=8,9, 2,3 Гц, 1H), 7,12-6,87 (м, 4H), 6,53 (дд, J=7,2, 4,3 Гц, 1H), 6,35 (д, J=2,7 Гц, 1H), 4,57 (кв, J=6,6 Гц, 1H), 4,33 (д, J=5,1 Гц, 2H), 4,23-4,04 (м, 3H), 3,93 (с, 1H), 3,84 (д, J=11,1 Гц, 2H), 3,75-3,51 (м, 4H), 3,36-3,26 (м, 1H), 2,89-2,72 (м, 4H), 2,67 (ддт, J=13,7, 6,7, 3,1 Гц, 2H), 2,61-2,46 (м, 2H), 2,22 (ддд, J=10,2, 6,6, 3,2 Гц, 2H), 1,74 (дд, J=6,7, 2,3 Гц, 3H).
Пример 175: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пирролидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она

Пример 175-1: Синтез метил 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксилата
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (1,0 эквив.), гексакарбонил молибдена (1,0 эквив.), транс-бис(ацетато)бис[о-(ди-о-толилфосфино)бензил]дипалладий (II) (0,1 эквив.), тетрафторборат три-трет-бутилфосфония (0,2 эквив.) и 1,8-диазабицикло[5,4,0]унлец-7-ен (1,5 эквив.) растворяют в метаноле:ацетонитриле (=1:1) и перемешивают при 150°C в течение 3 часов. Реакционный раствор охлаждают до комнатной температуры, разбавляют этилацетатом и фильтруют через целит. Фильтрат концентрируют при пониженном давлении, дистиллированную воду добавляют, и смесь экстрагируют этилацетатом 3 раза. Объединенные органические слои сушат над безводным сульфатом магния, концентрируют и очищают флэш-хроматографией с получением указанного в заголовке соединения.
Пример 175-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пирролидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
Метил 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксилат (1,0 эквив.), полученный в примере 175-1, пирролидин (5,0 эквив.) и 1,8-диазабицикло[5,4,0]ундец-7-ен (1 мл) смешивают и нагревают до 120°C в течение ночи. Реакционную смесь экстрагируют этилацетатом, сушат над сульфатом магния и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (дд, J=8,1, 2,2 Гц, 1H), 7,19 (д, J=8,0 Гц, 1H), 7,06 (с, 1H), 7,04-6,85 (м, 4H), 4,39 (т, J=5,2 Гц, 2H), 4,12 (дт, J=11,3, 4,9 Гц, 1H), 3,88 (дт, J=13,9, 3,1 Гц, 1H), 3,63 (д, J=11,4 Гц, 4H), 3,48 (т, J=7,1 Гц, 2H), 3,34 (кв, J=7,3 Гц, 3H), 2,90-2,65 (м, 4H), 2,54 (д, J=5,9 Гц, 2H), 1,84 (дп, J=33,2, 6,7 Гц, 4H).
Пример 176: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пиперидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
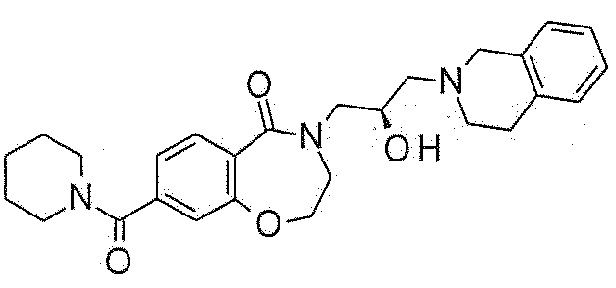
Указанное в заголовке соединение синтезируют по методике примера 175, за исключением того, что пиперидин используют вместо пирролидина в примере 175-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,07 (д, J=8,1 Гц, 1H), 6,97 (д, J=20,8 Гц, 5H), 4,41 (д, J=5,3 Гц, 2H), 4,13 (с, 1H), 3,88 (д, J=13,9 Гц, 1H), 3,74-3,53 (м, 6H), 3,35 (дд, J=14,0, 7,8 Гц, 1H), 2,79 (дд, J=18,3, 5,6 Гц, 4H), 2,54 (д, J=6,3 Гц, 2H), 1,75-1,49 (м, 5H).
Пример 177: Синтез 8-(3,3-дифторпирролидин-1-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
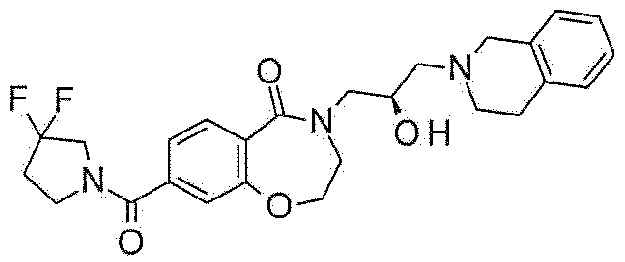
Указанное в заголовке соединение синтезируют по методике примера 175, за исключением того, что 3,3-дифторпирролидин используют вместо пирролидина в примере 175-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,80 (д, J=7,8 Гц, 1H), 7,22 (д, J=8,1 Гц, 1H), 7,12 (кв, J=11,5, 8,0 Гц, 5H), 4,54 (д, J=5,4 Гц, 2H), 4,27 (с, 1H), 4,05-3,95 (м, 1H), 3,89-3,72 (м, 5H), 3,64-3,39 (м, 4H), 2,96 (с, 4H), 2,72 (д, J=6,7 Гц, 2H), 2,56 (с, 2H), 2,44 (с, 2H), 2,35 (д, J=2,1 Гц, 3H).
Пример 178: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-метилпиперазин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
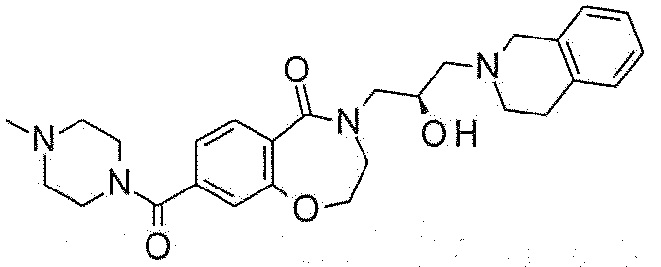
Указанное в заголовке соединение синтезируют по методике примера 175, за исключением того, что 1-метилпиперазин используют вместо пирролидина в примере 175-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (дд, J=8,0, 2,2 Гц, 1H), 7,22 (т, J=6,7 Гц, 1H), 7,10 (с, 1H), 7,08-6,88 (м, 4H), 4,40 (д, J=5,5 Гц, 2H), 4,13 (с, 1H), 3,95-3,70 (м, 4H), 3,63 (д, J=7,8 Гц, 5H), 3,35 (дд, J=14,1, 7,8 Гц, 1H), 2,81 (д, J=5,7 Гц, 2H), 2,76 (т, J=5,7 Гц, 2H), 2,54 (д, J=6,1 Гц, 2H), 2,45-2,25 (м, 2H).
Пример 179: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(пирролидин-1-илметил)-3H-1,4-бензоксазепин-5-она
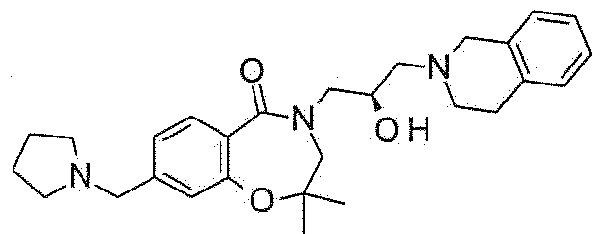
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примера 24 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=7,9 Гц, 1H), 7,23 (д, J=8,0 Гц, 1H), 7,17-7,03 (м, 4H), 7,01 (с, 1H), 4,29 (с, 1H), 4,06 (д, J=13,5 Гц, 1H), 3,76 (с, 2H), 3,72 (с, 2H), 3,49 (с, 2H), 3,43 (дд, J=13,7, 8,2 Гц, 1H), 2,98-2,83 (м, 4H), 2,64 (д, J=7,2 Гц, 6H), 1,86 (с, 4H), 1,44 (с, 3H), 1,34 (с, 3H).
Пример 180: Синтез 8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она
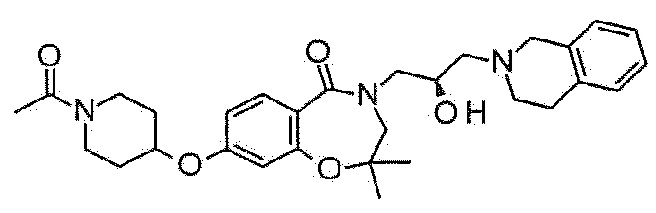
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиперидилокси)-3H-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 110-5, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,59 (дд, J=8,7, 2,5 Гц, 1H), 7,15-7,09 (м, 3H), 7,06 (д, J=6,4 Гц, 1H), 6,84 (д, J=8,8 Гц, 1H), 6,57 (с, 1H), 4,72 (дд, J=8,6, 4,9 Гц, 1H), 4,29 (с, 1H), 4,04 (д, J=13,8 Гц, 1H), 3,90-3,72 (м, 4H), 3,53 (д, J=17,0 Гц, 4H), 3,40 (дд, J=13,9, 8,3 Гц, 1H), 2,91 (дд, J=19,8, 5,2 Гц, 4H), 2,67-2,60 (м, 2H), 2,14 (д, J=2,4 Гц, 3H), 2,11-1,93 (м, 2H), 1,79 (д, J=31,6 Гц, 2H), 1,43 (с, 3H), 1,34 (д, J=2,4 Гц, 3H).
Пример 181: Синтез 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]окси]пиперидин-1-карбальдегида
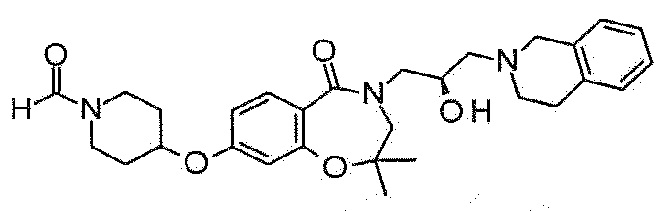
Продукт, полученный в примере 110-5, используют в качестве исходного материала по методике примера 78 с получением указанного в заголовке соединения, за исключением того, что f или mic acid используют вместо уксусный ангидрид в примере 78-2.
1H ЯМР (400 MГц, Метанол-d4) δ 8,06 (с, 1H), 7,63-7,56 (м, 1H), 7,12 (с, 3H), 7,07 (с, 1H), 6,85 (д, J=9,1 Гц, 1H), 6,58 (с, 1H), 4,77 (с, 1H), 4,28 (с, 1H), 4,04 (д, J=13,9 Гц, 1H), 3,73 (д, J=32,7 Гц, 5H), 3,57-3,37 (м, 6H), 2,89 (с, 2H), 2,64 (д, J=7,3 Гц, 2H), 2,03 (с, 2H), 1,77 (с, 2H), 1,43 (с, 3H), 1,33 (д, J=13,9 Гц, 3H).
Пример 182: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[[4-(оксетан-3-ил)пиперазин-1-ил]метил]-3H-1,4-бензоксазепин-5-она
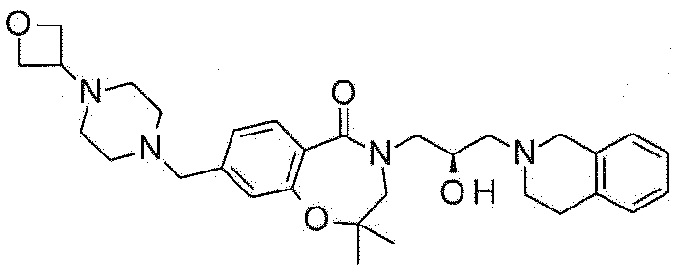
Продукт, полученный в примере 167-1, используют в качестве исходного материала по методике примера 92 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,60 (д, J=7,9 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,17-7,01 (м, 4H), 6,99 (с, 1H), 4,70 (т, J=6,8 Гц, 2H), 4,66-4,53 (м, 2H), 4,29 (с, 1H), 4,06 (д, J=13,9 Гц, 1H), 3,77 (с, 2H), 3,59 (с, 2H), 3,53 (т, J=7,0 Гц, 1H), 3,48 (с, 2H), 3,42 (дд, J=13,5, 8,3 Гц, 1H), 3,01-2,81 (м, 4H), 2,71-2,27 (м, 10H), 1,43 (с, 3H), 1,33 (с, 3H).
Пример 183: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(2-окса-7-азаспиро[3,4]октан-7-илметил)-3H-1,4-бензоксазепин-5-она
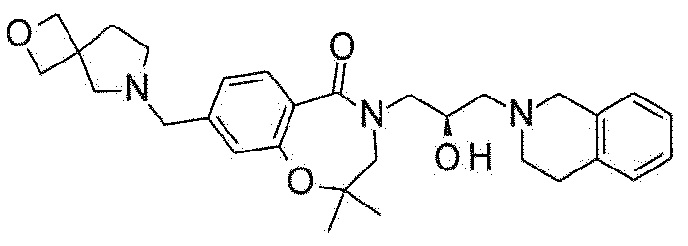
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-он используют в качестве исходного материала по методике примера 29 с получением указанного в заголовке соединения, за исключением того, что 2-окса-7-азаспиро[3,4]октан используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,49 (д, J=7,8 Гц, 1H), 7,08 (д, J=7,9 Гц, 1H), 7,04-6,90 (м, 4H), 6,86 (с, 1H), 4,51 (п, J=5,7, 5,2 Гц, 4H), 4,17 (с, 1H), 3,94 (д, J=13,6 Гц, 1H), 3,64 (с, 2H), 3,53 (с, 2H), 3,36 (с, 2H), 3,31 (дд, J=13,9, 8,2 Гц, 2H), 2,85-2,68 (м, 6H), 2,60-2,43 (м, 4H), 2,06 (т, J=7,3 Гц, 2H), 1,32 (с, 3H), 1,22 (с, 3H).
Пример 184: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-фторпиперидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
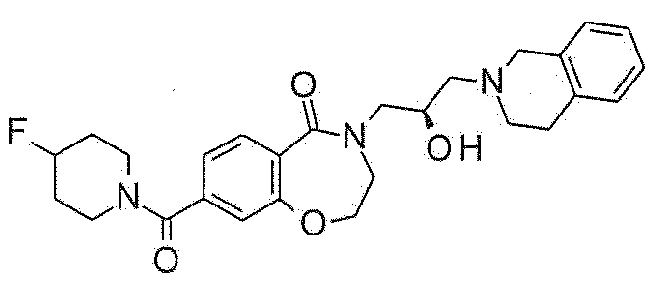
Указанное в заголовке соединение синтезируют по методике примера 175, за исключением того, что 4-фторпиперидин используют вместо пирролидина в примере 175-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,80 (дд, J=7,9, 2,2 Гц, 1H), 7,22 (д, J=8,0 Гц, 1H), 7,17-6,97 (м, 5H), 5,00-4,76 (м, 1H), 4,52 (д, J=5,2 Гц, 2H), 4,24 (д, J=7,1 Гц, 1H), 4,07-3,83 (м, 2H), 3,76 (д, J=6,6 Гц, 5H), 3,63-3,36 (м, 4H), 2,94 (д, J=5,6 Гц, 2H), 2,89 (д, J=5,4 Гц, 2H), 2,67 (д, J=6,0 Гц, 2H), 2,13 -1,70 (м, 3H).
Пример 185: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[3-(трифторметил)пиперидин-1-карбонил]-2,3-дигидро-1,4-бензоксазепин-5-она
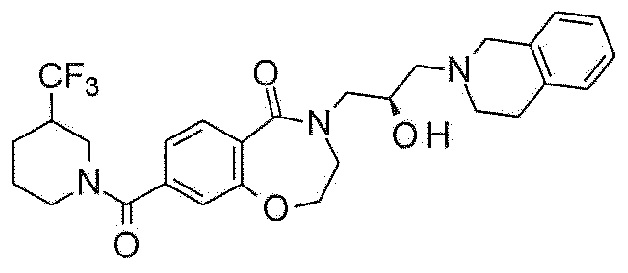
Указанное в заголовке соединение синтезируют по методике примера 175, за исключением того, что 3-трифторметилпиперидин используют вместо пирролидина в примере 175-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=7,9 Гц, 1H), 7,10 (д, J=8,1 Гц, 1H), 7,05-6,81 (м, 5H), 4,66-4,23 (м, 3H), 4,13 (кв, J=6,1, 5,4 Гц, 1H), 3,88 (дт, J=14,2, 2,9 Гц, 1H), 3,64 (д, J=6,5 Гц, 5H), 3,34 (дд, J=14,1, 7,8 Гц, 1H), 2,97 (дт, J=45,9, 12,8 Гц, 2H), 2,81 (д, J=5,6 Гц, 2H), 2,77 (д, J=5,4 Гц, 2H), 2,54 (д, J=6,3 Гц, 2H), 2,45-2,29 (м, 1H), 1,99 (д, J=12,2 Гц, 1H), 1,70-1,37 (м, 3H).
Пример 186: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-(трифторметил)пиперидин-1-карбонил]-2,3-дигидро-1,4-бензоксазепин-5-она
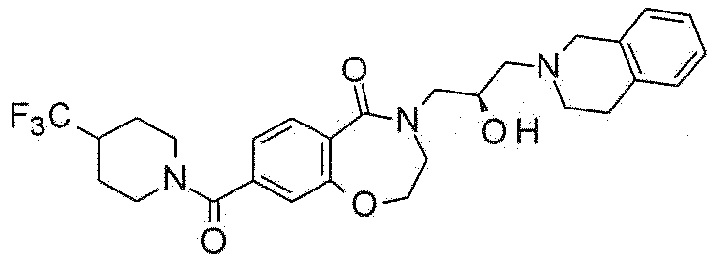
Указанное в заголовке соединение синтезируют по методике примера 175, за исключением того, что 4-трифторметилпиперидин используют вместо пирролидина в примере 175-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,75-7,61 (м, 1H), 7,09 (д, J=8,0 Гц, 1H), 7,05-6,83 (м, 5H), 4,62 (д, J=13,2 Гц, 1H), 4,41 (д, J=5,6 Гц, 2H), 4,13 (д, J=6,7 Гц, 1H), 3,88 (дт, J=14,0, 3,1 Гц, 1H), 3,63 (с, 5H), 3,34 (дд, J=14,0, 7,7 Гц, 1H), 3,05 (т, J=13,9 Гц, 1H), 2,88-2,67 (м, 5H), 2,53 (д, J=6,3 Гц, 2H), 2,47-2,30 (м, 1H), 2,01-1,83 (м, 1H), 1,75 (д, J=12,8 Гц, 1H), 1,43 (кв, J=13,5, 12,9 Гц, 2H).
Пример 187: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2,6-диметилморфолин-4-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
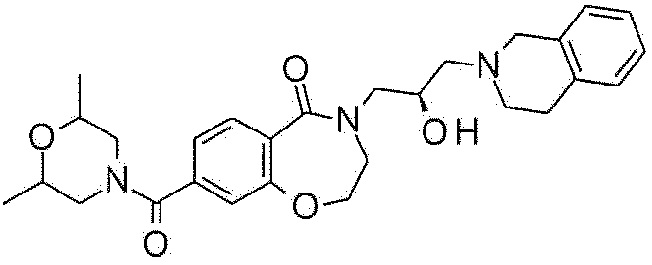
2,6-Диметилморфолин (33 мкл, 1,1 эквив.) растворяют в 1,4-диоксане (1 мл), и туда добавляют 2 M раствор триметилалюминия в толуоле (134 мкл, 1,1 эквив.) в условиях азота при 0°C. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа, и туда добавляют метил 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксилат (100 мг), растворенный в 1,4-диоксане. Реакционный раствор перемешивают при 110°C в течение 3 часов, и реакцию останавливают насыщенным водным раствором тартрата калия-натрия, с последующим экстрагированием этилацетатом. Объединенные органические слои сушат над безводным сульфатом магния, концентрируют и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,81 (д, J=7,8 Гц, 1H), 7,21 (д, J=8,1 Гц, 1H), 7,18-7,00 (м, 5H), 4,63-4,44 (м, 3H), 4,33-4,18 (м, 1H), 4,00 (дт, J=13,9, 2,8 Гц, 1H), 3,75 (д, J=7,6 Гц, 4H), 3,71-3,55 (м, 2H), 3,55-3,39 (м, 2H), 2,99-2,80 (м, 5H), 2,62 (дд, J=23,2, 9,1 Гц, 3H), 1,24 (д, J=6,5 Гц, 3H), 1,09 (дд, J=17,3, 6,2 Гц, 3H).
Пример 188: Синтез 8-(2-азабицикло[2,2,1]гептан-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
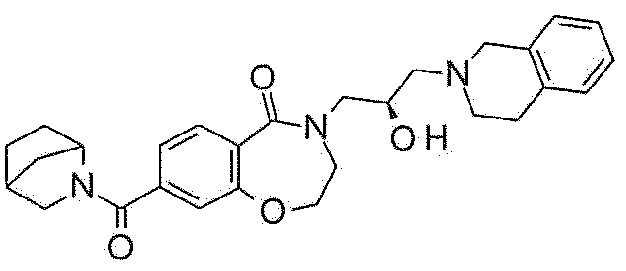
Указанное в заголовке соединение синтезируют по методике примера 187, за исключением того, что 2-азабицикло[2,2,1]гептан используют вместо 2,6-диметилморфолина.
1H ЯМР (400 MГц, Метанол-d4) δ 7,86-7,73 (м, 1H), 7,29 (д, J=8,1 Гц, 1H), 7,24-6,99 (м, 5H), 4,52 (кв, J=6,0 Гц, 2H), 4,24 (дд, J=10,3, 5,4 Гц, 1H), 4,12 (с, 1H), 4,00 (дт, J=14,1, 3,2 Гц, 1H), 3,75 (д, J=8,9 Гц, 4H), 3,60-3,38 (м, 2H), 3,12 (дд, J=63,7, 10,4 Гц, 1H), 2,99-2,84 (м, 4H), 2,76-2,56 (м, 3H), 1,89-1,66 (м, 4H), 1,59 (д, J=9,9 Гц, 1H), 1,52 (кв, J=10,4, 7,9 Гц, 1H).
Пример 189: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-окса-8-азабицикло[3,2,1]октан-8-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
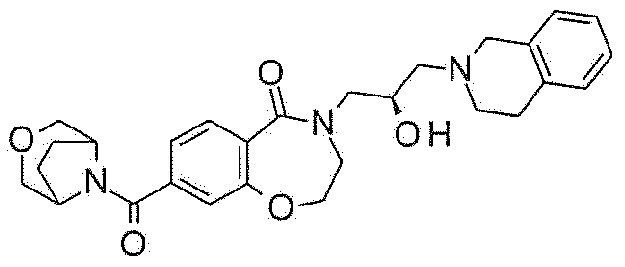
Указанное в заголовке соединение синтезируют по методике примера 187, за исключением того, что 3-окса-8-азабицикло[3,2,1]октан используют вместо 2,6-диметилморфолина.
1H ЯМР (400 MГц, Метанол-d4) δ 7,81 (д, J=7,8 Гц, 1H), 7,30 (д, J=8,0 Гц, 1H), 7,18 (с, 1H), 7,15-7,02 (м, 4H), 4,64 (с, 1H), 4,53 (д, J=5,3 Гц, 2H), 4,29-4,19 (м, 1H), 4,04-3,93 (м, 2H), 3,81 (д, J=11,5 Гц, 1H), 3,77-3,66 (м, 6H), 3,59 (д, J=11,1 Гц, 1H), 3,46 (дд, J=14,0, 7,8 Гц, 1H), 2,92 (д, J=5,7 Гц, 2H), 2,87 (д, J=5,8 Гц, 2H), 2,65 (д, J=6,2 Гц, 2H), 2,05 (дд, J=28,2, 10,9 Гц, 4H).
Пример 190: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-метилморфолин-4-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
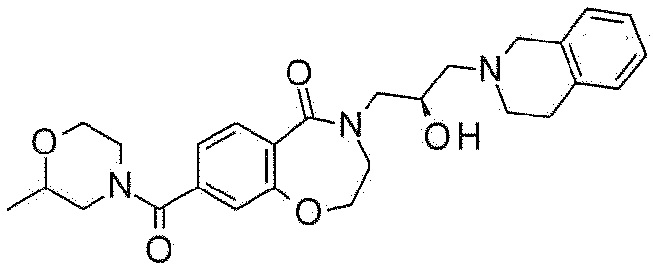
Указанное в заголовке соединение синтезируют по методике примера 187, за исключением того, что 2-метилморфолин используют вместо 2,6-диметилморфолина.
1H ЯМР (400 MГц, Метанол-d4) δ 7,81 (д, J=7,9 Гц, 1H), 7,21 (д, J=8,0 Гц, 1H), 7,17-6,92 (м, 5H), 4,62-4,35 (м, 3H), 4,24 (дкв, J=11,4, 6,7, 6,1 Гц, 1H), 4,08-3,68 (м, 6H), 3,65-3,18 (м, 5H), 2,92 (д, J=5,6 Гц, 2H), 2,87 (д, J=5,7 Гц, 2H), 2,66 (т, J=7,1 Гц, 2H), 1,23 (h, J=6,1, 5,0 Гц, 2H), 1,06 (д, J=6,2 Гц, 1H).
Пример 191: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-метилморфолин-4-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
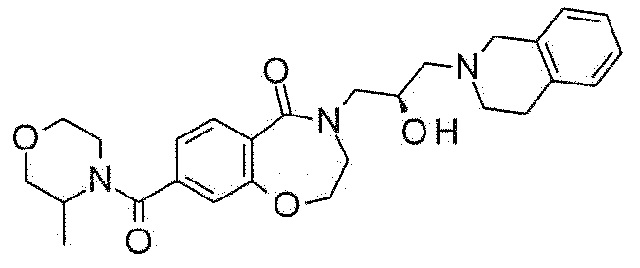
Указанное в заголовке соединение синтезируют по методике примера 187, за исключением того, что 3-метилморфолин используют вместо 2,6-диметилморфолина.
1H ЯМР (400 MГц, Метанол-d4) δ 7,81 (д, J=8,0 Гц, 1H), 7,28-6,97 (м, 6H), 4,51 (д, J=5,2 Гц, 2H), 4,24 (кв, J=7,3, 6,0 Гц, 1H), 3,99 (дд, J=13,8, 3,3 Гц, 1H), 3,95-3,62 (м, 7H), 3,59-3,39 (м, 3H), 3,06-2,72 (м, 4H), 2,67 (д, J=6,1 Гц, 2H), 1,37 (д, J=7,0 Гц, 3H).
Пример 192: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(морфолинометил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она
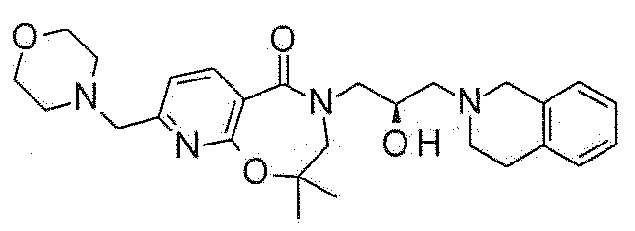
8-Хлор-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-он используют в качестве исходного материала по методике примера 22 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,14 (д, J=7,9 Гц, 1H), 7,43 (д, J=7,0 Гц, 1H), 7,19-7,01 (м, 4H), 4,35-4,21 (м, 1H), 4,05 (д, J=13,8 Гц, 1H), 3,77 (с, 2H), 3,73 (с, 4H), 3,62 (с, 4H), 3,45 (дд, J=14,0, 8,6 Гц, 1H), 2,92 (с, 2H), 2,89 (с, 2H), 2,66 (кв, J=5,7, 4,1 Гц, 2H), 1,50 (с, 3H), 1,43 (с, 3H).
Пример 193: Синтез 8-(3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррол-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она

Пример 193-1: Синтез калия;4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксилата
Метил 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксилат и триметилсиланоат калия растворяют в тетрагидрофуране и перемешивают при комнатной температуре в течение ночи. Реакционный раствор концентрируют при пониженном давлении и применяют в следующей реакции без дополнительной очистки.
Пример 193-2: Синтез 8-(3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррол-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
Исходный материал (100 мг, 1,0 эквив.), полученный в примере 193-1, октагидроциклопента[c]пиррол (1,5 эквив.), HATU (131 мг, 1,5 эквив.) и диизопропилэтиламин (120 мкл, 3 эквив.) растворяют в метиленхлориде и перемешивают при комнатной температуре в течение 2 часов. Реакционный раствор экстрагируют метиленхлоридом, сушат над сульфатом магния и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (дд, J=8,0, 2,1 Гц, 1H), 7,16 (д, J=8,0 Гц, 1H), 7,08-6,89 (м, 5H), 4,41 (кв, J=5,7 Гц, 2H), 4,13 (дд, J=9,8, 5,2 Гц, 1H), 3,88 (дт, J=14,2, 3,1 Гц, 1H), 3,75-3,60 (м, 5H), 3,55 (дд, J=11,4, 7,9 Гц, 1H), 3,43-3,34 (м, 2H), 3,21 (д, J=2,8 Гц, 2H), 3,18-3,07 (м, 1H), 2,89-2,73 (м, 4H), 2,73-2,46 (м, 4H), 1,73 (ддт, J=39,4, 20,0, 7,0 Гц, 3H), 1,49 (ддт, J=33,3, 12,5, 6,8 Гц, 2H), 1,28 (дт, J=11,8, 5,8 Гц, 1H).
Пример 194: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-фторпиперидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она
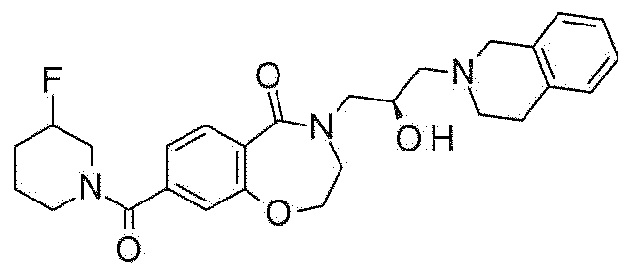
Указанное в заголовке соединение синтезируют по методике примера 193, за исключением того, что 3-фторпиперидин используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=7,8 Гц, 1H), 7,08 (д, J=8,0 Гц, 1H), 7,06-6,89 (м, 5H), 4,57 (д, J=48,2 Гц, 1H), 4,41 (т, J=5,1 Гц, 2H), 4,33-4,08 (м, 2H), 3,89 (дд, J=13,8, 3,2 Гц, 1H), 3,64 (д, J=7,0 Гц, 5H), 3,52-3,23 (м, 3H), 3,17-2,95 (м, 1H), 2,90-2,71 (м, 4H), 2,54 (д, J=6,2 Гц, 2H), 1,89-1,65 (м, 2H), 1,50 (д, J=50,2 Гц, 1H).
Пример 195: Синтез 8-(2,2-дифторморфолин-4-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
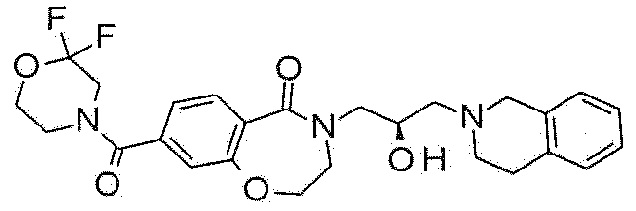
Указанное в заголовке соединение синтезируют по методике примера 193, за исключением того, что 2,2-дифторморфолин используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (д, J=7,6 Гц, 1H), 7,13 (д, J=8,0 Гц, 1H), 7,08-6,89 (м, 5H), 4,41 (д, J=5,3 Гц, 2H), 4,14 (д, J=6,5 Гц, 1H), 4,08-3,77 (м, 5H), 3,71-3,42 (м, 6H), 3,36 (дд, J=14,1, 7,7 Гц, 1H), 3,23 (д, J=16,0 Гц, 2H), 2,87-2,74 (м, 4H), 2,56 (д, J=6,1 Гц, 2H).
Пример 196: Синтез 8-(4,4-дифторпиперидин-1-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
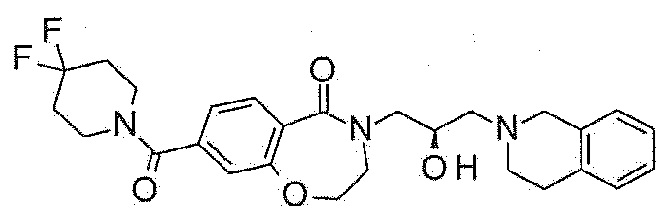
Указанное в заголовке соединение синтезируют по методике примера 193, за исключением того, что 4,4-дифторпиперидин используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (дд, J=8,0, 2,2 Гц, 1H), 7,13 (д, J=8,0 Гц, 1H), 7,06-6,91 (м, 5H), 4,46-4,34 (м, 2H), 4,14 (дд, J=7,2, 3,9 Гц, 1H), 3,85 (дт, J=14,0, 3,2 Гц, 1H), 3,75 (с, 1H), 3,70 (с, 2H), 3,62 (с, 2H), 3,42 (м, 3H), 2,93-2,78 (м, 4H), 2,59 (д, J=5,9 Гц, 2H), 2,12-1,78 (м, 4H).
Пример 197: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(1-пиперидилметил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она
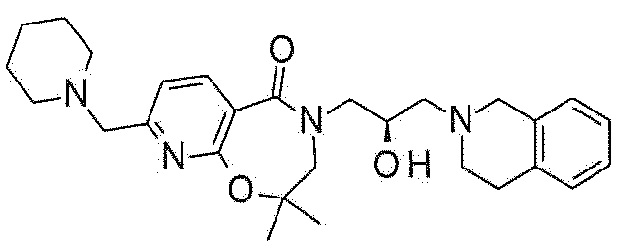
8-Хлор-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-он используют в качестве исходного материала по методике примера 23 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,13 (д, J=7,7 Гц, 1H), 7,42 (д, J=7,8 Гц, 1H), 7,19-7,01 (м, 4H), 4,29 (с, 1H), 4,06 (д, J=13,7 Гц, 1H), 3,75 (с, 2H), 3,69-3,54 (м, 4H), 3,45 (дд, J=13,7, 8,3 Гц, 1H), 3,00-2,80 (м, 4H), 2,72-2,57 (м, 2H), 2,50 (с, 4H), 1,70-1,58 (м, 4H), 1,50 (с, 5H), 1,44 (с, 3H).
Пример 198: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-[метил(оксетан-3-ил)амино]циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-она
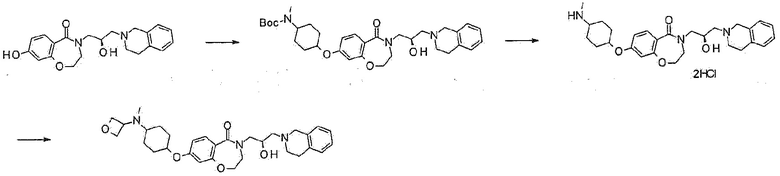
Пример 198-1: Синтез трет-бутил N-[4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]циклогексил]-N-метилкарбамата
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что [4-[трет-бутоксикарбонил(метил)амино]циклогексил]метансульфонат, карбонат цезия и ацетонитрил используют вместо 4-хлортетрагидропирана, карбоната калия и диметилформамида, соответственно.
Пример 198-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-(метиламино)циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Трет-бутил N-[4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]циклогексил]-N-метил-карбамат, полученный в примере 198-1, растворяют в метаноле, и туда медленно добавляют 4 M раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре, разбавляют диэтиловым эфиром и фильтруют с получением указанного в заголовке твердого соединения.
Пример 198-3: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-[метил(оксетан-3-ил)амино]циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-(метиламино)циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 198-2, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,7 Гц, 1H), 7,12 (д, J=3,8 Гц, 3H), 7,06 (д, J=6,5 Гц, 1H), 6,76 (д, J=8,8 Гц, 1H), 6,58 (с, 1H), 4,67 (д, J=7,1 Гц, 4H), 4,61 (с, 1H), 4,46 (д, J=5,5 Гц, 2H), 4,23 (д, J=7,3 Гц, 1H), 4,06 (кв, J=7,3 Гц, 1H), 3,97 (дд, J=14,0, 3,6 Гц, 1H), 3,78 (с, 2H), 3,73 (д, J=5,4 Гц, 2H), 3,43 (дд, J=14,0, 7,6 Гц, 1H), 2,97-2,86 (м, 4H), 2,67 (д, J=6,2 Гц, 2H), 2,47 (т, J=11,2 Гц, 1H), 2,24 (с, 3H), 2,12 (д, J=12,0 Гц, 2H), 1,64 (тт, J=23,8, 11,0 Гц, 6H).
Пример 199: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-[2-фторэтил(метил)амино]циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-она
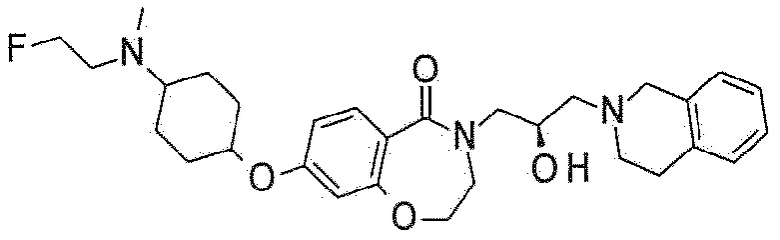
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-(метиламино)циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид (200 мг, 0,362 ммоль), полученный в примере 198-2, карбонат калия (150 мг, 1,086 ммоль) и 2-фторэтил 4-метилбензолсульфонат (93 мкл, 0,543 ммоль) растворяют в ацетонитриле и перемешивают при 100°C в течение одного дня. В реакционную смесь добавляют насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом натрия и концентрированием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения (45 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (дд, J=8,9, 2,5 Гц, 1H), 7,10 (д, J=3,5 Гц, 3H), 7,04 (д, J=6,6 Гц, 1H), 6,76 (д, J=8,6 Гц, 1H), 6,58 (с, 1H), 4,61 (кв, J=4,0 Гц, 2H), 4,47 (дкв, J=12,2, 4,3, 3,9 Гц, 3H), 4,22 (дкв, J=10,0, 5,8, 5,0 Гц, 1H), 3,97 (дд, J=13,9, 3,1 Гц, 1H), 3,72 (д, J=9,9 Гц, 4H), 3,45-3,35 (м, 1H), 2,86 (тд, J=23,1, 4,6 Гц, 6H), 2,69-2,50 (м, 3H), 2,37 (д, J=2,5 Гц, 3H), 2,12 (д, J=12,8 Гц, 2H), 1,75-1,56 (м, 6H).
Пример 200: Синтез (2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этантиол-4-пиперидил)окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
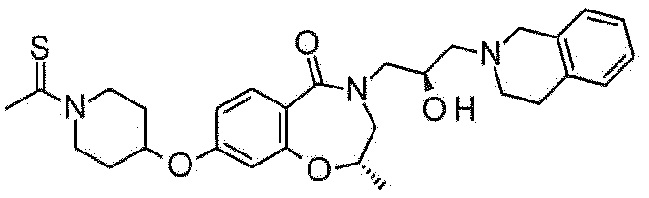
Пример 200-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат на [(1R)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 78-1 с получением указанного в заголовке соединения.
Пример 200-2: Синтез 8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 200-1, используют в качестве исходного материала по методике примера 78-2 с получением указанного в заголовке соединения
Пример 200-3: Синтез (2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этантиол-4-пиперидил)окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 200-2, в качестве исходного материала растворяют в тетрагидрофуране, и туда добавляют реагент Лавессона. Реакционную смесь перемешивают при 50°C до завершения реакции, реакционный раствор охлаждают до комнатной температуры, дистиллированную воду добавляют, и смесь экстрагируют этилацетатом. Объединенные органические слои сушат над безводным сульфатом магния, концентрируют и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,19-8,09 (м, 1H), 7,65-7,55 (м, 1H), 7,29 (д, J=9,3 Гц, 2H), 6,89 (дд, J=32,8, 8,6 Гц, 3H), 5,46 (с, 1H), 4,80 (с, 1H), 4,65 (с, 1H), 4,44 (с, 2H), 4,18-4,07 (м, 2H), 3,99 (с, 1H), 3,83 (д, J=2,4 Гц, 5H), 3,60-3,45 (м, 1H), 2,67 (с, 2H), 2,14-2,00 (м, 3H), 1,95-1,80 (м, 2H), 1,35-1,20 (м, 3H), 1,03 (д, J=6,3 Гц, 2H).
Пример 201: Синтез (2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-фторэтил)азетидин-3-ил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
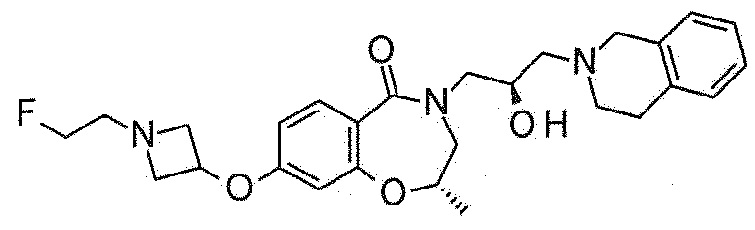
Пример 201-1: Синтез 8-(азетидин-3-илокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение, в котором Вос замещена, синтезируют с применением продукта, полученного по методике примеров 140-1-140-5 за исключением того, что [(1R)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат используют вместо [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната в качестве исходного материала, и способ по методике примера 64 за исключением того, что трет-бутил 3-гидроксиазетидин-1-карбоксилат используют вместо 4-хлортетрагидропирана. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
Пример 201-2: Синтез (2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-фторэтил)азетидин-3-ил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
Продукт, полученный в примере 201-1 в качестве исходного материала, 2-фторэтил пара-толуолсульфонат и карбонат калия растворяют в ацетонитриле, и реакционный раствор перемешивают при 60°C в течение одного дня. Реакционную смесь охлаждают до комнатной температуры, разбавляют дистиллированной водой, и экстрагируют этилацетатом 3 раза. Объединенные органические слои промывают дважды насыщенным водным раствором хлорида натрия, сушат над безводным сульфатом магния, фильтруют и концентрируют при пониженном давлении. Полученный концентрат очищают флэш-хроматографией с получением указанного в заголовке твердого соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (дд, J=8,7, 2,5 Гц, 1H), 7,12 (д, J=3,7 Гц, 3H), 7,06 (д, J=6,6 Гц, 1H), 6,68 (д, J=8,5 Гц, 1H), 6,43 (д, J=3,2 Гц, 1H), 4,82 (ддд, J=10,1, 6,6, 3,4 Гц, 1H), 4,55 (кв, J=3,9 Гц, 1H), 4,43 (кв, J=3,9 Гц, 1H), 4,25 (тд, J=6,8, 3,6 Гц, 1H), 3,90 (т, J=7,4 Гц, 2H), 3,80 (д, J=14,0 Гц, 3H), 3,62 (дт, J=15,2, 3,4 Гц, 2H), 3,46 (ддд, J=15,0, 9,8, 5,3 Гц, 1H), 2,90 (тдд, J=20,0, 9,1, 4,9 Гц, 7H), 2,68 (дд, J=6,4, 2,4 Гц, 2H), 1,38-1,25 (м, 4H).
Пример 202: Синтез (2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-фторэтил)-4-пиперидил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
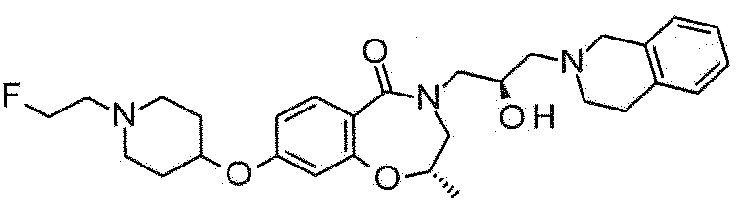
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1R)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (дд, J=8,6, 2,1 Гц, 1H), 7,12 (д, J=3,2 Гц, 3H), 7,06 (д, J=6,5 Гц, 1H), 6,79 (д, J=8,7 Гц, 1H), 6,55 (с, 1H), 4,67 (с, 1H), 4,58-4,49 (м, 2H), 4,24 (с, 1H), 3,78 (д, J=8,0 Гц, 2H), 3,67-3,58 (м, 2H), 3,47 (дд, J=15,6, 9,3 Гц, 1H), 2,93 (д, J=5,4 Гц, 2H), 2,91-2,81 (м, 4H), 2,80 (с, 1H), 2,73 (т, J=5,2 Гц, 1H), 2,66 (д, J=6,4 Гц, 2H), 2,52 (т, J=10,2 Гц, 2H), 2,05 (д, J=10,5 Гц, 2H), 1,85 (с, 2H), 1,31-1,26 (м, 3H).
Пример 203: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(3-окса-8-азабицикло[3,2,1]октан-8-карбонил)-3H-1,4-бензоксазепин-5-она
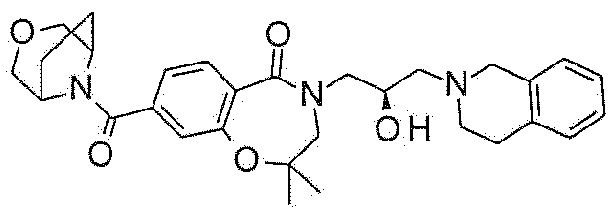
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-карбоксилат калия используют в качестве исходного материала по методике примера 193 с получением указанного в заголовке соединения, за исключением того, что 3-окса-8-азабицикло[3,2,1]октан используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=7,9 Гц, 1H), 7,28-7,15 (м, 1H), 7,06-6,88 (м, 5H), 4,53 (с, 1H), 4,26-4,08 (м, 1H), 3,98-3,92 (м, 1H), 3,84 (с, 1H), 3,70 (д, J=11,0 Гц, 1H), 3,61 (д, J=26,9 Гц, 4H), 3,48 (д, J=11,0 Гц, 1H), 3,39 (с, 2H), 3,32 (дд, J=13,7, 8,3 Гц, 1H), 2,84-2,72 (м, 4H), 2,58-2,48 (м, 2H), 1,33 (с, 3H), 1,23 (с, 3H).
Пример 204: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(2-окса-5-азабицикло[2,2,1]гептан-5-карбонил)-3H-1,4-бензоксазепин-5-она
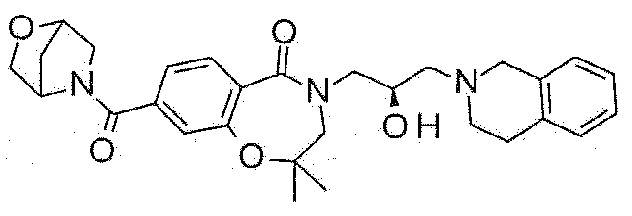
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-карбоксилат калия используют в качестве исходного материала по методике примера 193 с получением указанного в заголовке соединения, за исключением того, что 2-окса-5-азабицикло[2,2,1]гептан используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67-7,55 (м, 1H), 7,30-7,16 (м, 1H), 7,07-6,86 (м, 5H), 4,24-4,10 (м, 1H), 4,02-3,89 (м, 1H), 3,85 (дд, J=7,7, 3,4 Гц, 1H), 3,71 (ддд, J=31,5, 7,7, 1,6 Гц, 1H), 3,64 (с, 2H), 3,53-3,42 (м, 1H), 3,42-3,35 (м, 3H), 3,32 (тд, J=6,5, 4,9, 2,5 Гц, 1H), 2,84-2,69 (м, 4H), 2,58-2,45 (м, 2H), 1,95-1,72 (м, 2H), 1,40-1,27 (м, 3H), 1,27-1,17 (м, 3H).
Пример 205: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,5-диметилморфолин-4-карбонил)-2,2-диметил-3H-1,4-бензоксазепин-5-она
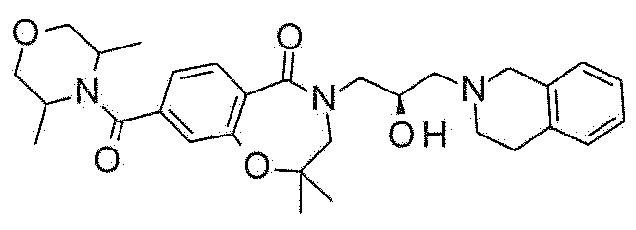
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-карбоксилат калия используют в качестве исходного материала по методике примера 193 с получением указанного в заголовке соединения, за исключением того, что 3,5-диметилморфолин используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,58 (д, J=7,8 Гц, 1H), 7,13 (дд, J=7,8, 1,6 Гц, 1H), 7,05-6,91 (м, 4H), 6,89 (д, J=1,6 Гц, 1H), 4,16 (кв, J=7,9, 6,8 Гц, 1H), 3,94 (дд, J=13,7, 3,7 Гц, 1H), 3,69-3,51 (м, 4H), 3,45-3,25 (м, 7H), 2,80 (д, J=5,7 Гц, 2H), 2,77-2,71 (м, 2H), 2,52 (дд, J=6,3, 3,8 Гц, 2H), 1,40 (с, 6H), 1,32 (с, 3H), 1,22 (с, 3H).
Пример 206: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
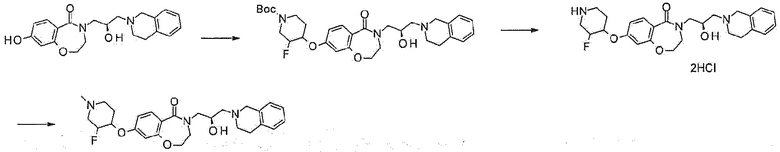
Пример 206-1: Синтез трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]-3-фтор-пиперидин-1-карбоксилата
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что трет-бутил 3-фтор-4-метилсульфонилоксипиперидин-1-карбоксилат, карбонат цезия и ацетонитрил используют вместо 4-хлортетрагидропирана, карбоната калия и диметилформамида, соответственно.
Пример 206-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]-3-фторпиперидин-1-карбоксилат, полученный в примере 206-1, растворяют в метаноле, и туда медленно добавляют 4 M раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре, разбавляют диэтиловым эфиром и фильтруют с получением указанного в заголовке твердого соединения.
Пример 206-3: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 206-2, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,18-7,06 (м, 3H), 7,06-7,01 (м, 1H), 6,82 (дд, J=8,8, 2,5 Гц, 1H), 6,65 (д, J=2,5 Гц, 1H), 4,79-4,43 (м, 4H), 4,29-4,18 (м, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,78-3,64 (м, 4H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 3,07-2,83 (м, 5H), 2,74-2,58 (м, 3H), 2,51 (кв, J=8,2, 7,7 Гц, 1H), 2,36 (с, 4H), 2,24-2,15 (м, 1H), 1,77 (дтд, J=13,1, 9,0, 3,7 Гц, 1H).
Пример 207: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-фтор-1-(2-фторэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
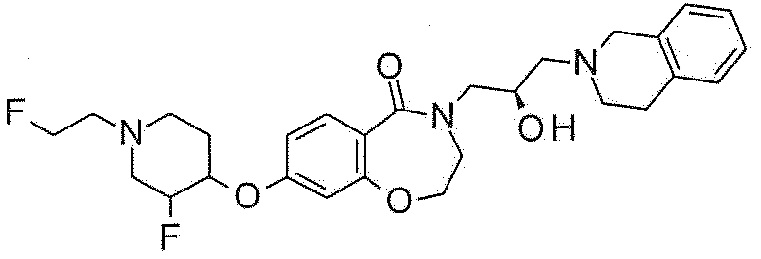
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 206-2, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,17-7,02 (м, 4H), 6,82 (дд, J=8,8, 2,5 Гц, 1H), 6,65 (д, J=2,5 Гц, 1H), 4,65 (дкв, J=5,6, 4,6 Гц, 2H), 4,56-4,45 (м, 4H), 4,27-4,17 (м, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,81-3,69 (м, 4H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 2,94 (д, J=5,4 Гц, 2H), 2,90-2,83 (м, 4H), 2,79 (дт, J=9,4, 5,0 Гц, 2H), 2,76-2,71 (м, 1H), 2,68-2,62 (м, 2H), 2,53 (дд, J=11,2, 7,5 Гц, 1H), 2,47-2,38 (м, 1H), 2,21 (дд, J=9,7, 4,6 Гц, 1H), 1,76 (дд, J=11,9, 7,8 Гц, 1H).
Пример 208: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
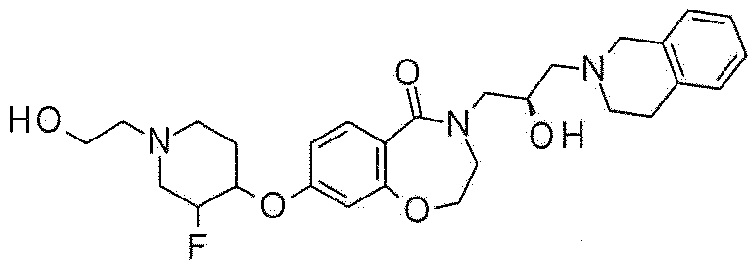
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 206-2, используют в качестве исходного материала по методике примера 162 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,17-7,00 (м, 4H), 6,81 (дд, J=8,8, 2,5 Гц, 1H), 6,65 (д, J=2,5 Гц, 1H), 4,67 (дтд, J=49,2, 8,2, 4,6 Гц, 1H), 4,48 (т, J=5,0 Гц, 3H), 4,23 (с, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,82-3,62 (м, 6H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 3,26-3,14 (м, 1H), 2,98-2,80 (м, 5H), 2,71-2,56 (м, 4H), 2,47 (кв, J=8,9, 8,3 Гц, 1H), 2,37 (т, J=10,4 Гц, 1H), 2,26-2,14 (м, 1H), 1,80-1,65 (м, 1H).
Пример 209: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,4-дигидро-1H-пирроло[1,2-a]пиразин-2-карбонил)-2,2-диметил-3H-1,4-бензоксазепин-5-она
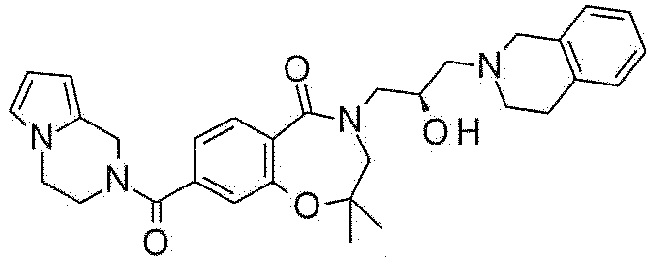
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-карбоксилат калия используют в качестве исходного материала по методике примера 193 с получением указанного в заголовке соединения, за исключением того, что 1,2,3,4-тетрагидропиррол[1,2-a]пиразин используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,75 (д, J=7,9 Гц, 1H), 7,31 (д, J=7,9 Гц, 1H), 7,21-6,96 (м, 5H), 6,65 (с, 1H), 6,08 (д, J=16,4 Гц, 1H), 5,85 (д, J=81,0 Гц, 1H), 4,87 (с, 1H), 4,62 (с, 1H), 4,32 (тт, J=8,5, 4,3 Гц, 1H), 4,20-3,96 (м, 4H), 3,79 (д, J=20,8 Гц, 3H), 3,56-3,40 (м, 3H), 2,95 (кв, J=5,0, 4,2 Гц, 4H), 2,70 (т, J=5,6 Гц, 2H), 1,45 (с, 3H), 1,36 (с, 3H).
Пример 210: Синтез 8-(3,4,6,7,8,8a-гексагидро-1H-пирроло[1,2-a]пиразин-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она
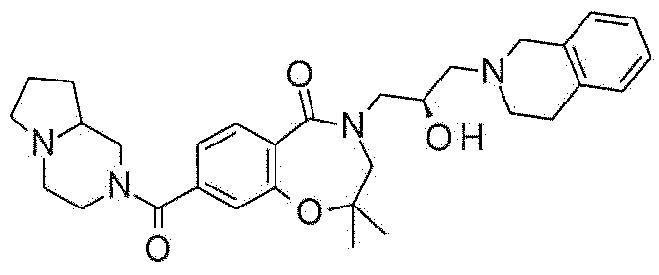
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-карбоксилат калия используют в качестве исходного материала по методике примера 193 с получением указанного в заголовке соединения, за исключением того, что 1,2,3,4,6,7,8,8a-октагидропиррол[1,2-a]пиразин используют вместо октагидроциклопента[c]пиррола в примере 193-2.
1H ЯМР (400 MГц, Метанол-d4 δ 7,73 (д, J=7,8 Гц, 1H), 7,26 (дд, J=7,8, 1,6 Гц, 1H), 7,18-6,96 (м, 5H), 4,70 (дд, J=50,1, 13,0 Гц, 1H), 4,30 (дд, J=7,5, 3,6 Гц, 1H), 4,07 (д, J=14,6 Гц, 1H), 3,79 (с, 3H), 3,52 (с, 2H), 3,44 (дд, J=13,8, 8,4 Гц, 1H), 3,33 (п, J=1,7 Гц, 4H), 3,23-3,05 (м, 2H), 2,98 (д, J=12,7 Гц, 1H), 2,75-2,63 (м, 2H), 2,25 (кв, J=12,1, 11,3 Гц, 2H), 2,13-1,98 (м, 2H), 1,88 (дд, J=48,6, 16,4 Гц, 4H), 1,62-1,51 (м, 1H), 1,45 (с, 3H), 1,35 (с, 3H).
Пример 211: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(5-фторпиримидин-2-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она
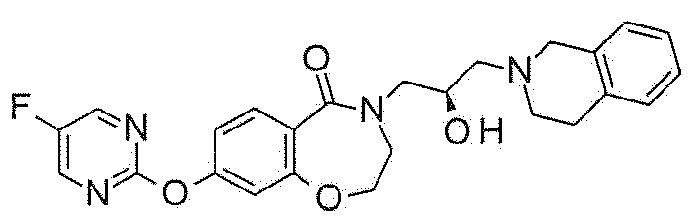
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2,3-дигидро-1,4-бензоксазепин-5-он (1,0 эквив.), 2-хлор-5-фторпиримидин (1,5 эквив.) и карбонат цезия (2 эквив.) растворяют в ацетонитриле и нагревают до кипения с обратным холодильником в течение ночи. Реакционный раствор экстрагируют этилацетатом. Отделенный органический слой сушат над сульфатом магния, концентрируют и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,46 (с, 2H), 7,67 (д, J=8,6 Гц, 1H), 7,08-6,92 (м, 4H), 6,89 (дд, J=8,6, 2,4 Гц, 1H), 6,77 (д, J=2,3 Гц, 1H), 4,39 (т, J=5,0 Гц, 2H), 4,14 (тт, J=7,6, 3,6 Гц, 1H), 3,87 (дд, J=13,9, 3,6 Гц, 1H), 3,70 (д, J=2,3 Гц, 2H), 3,65 (т, J=5,1 Гц, 2H), 3,35 (дд, J=13,9, 7,6 Гц, 1H), 2,87-2,75 (м, J=4,4, 3,8 Гц, 4H), 2,62-2,54 (м, 2H).
Пример 212: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксипропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
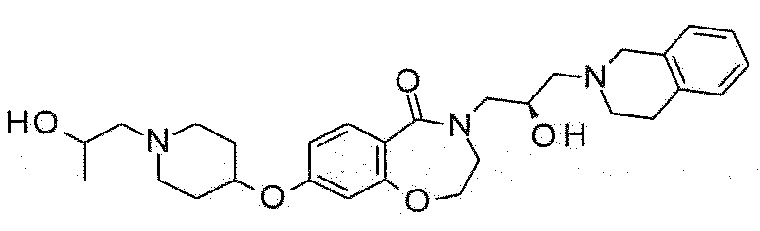
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 78-1, растворяют в смешанном растворе воды и ацетонитрила, и туда добавляют 2-метоксиран и гидроксид натрия и перемешивают при комнатной температуре в течение 1 часа. В реакционную смесь, добавляют воду и экстрагируют этилацетатом 3 раза. Маслянистую жидкость, полученную сушкой объединенных органических слоев над безводным сульфатом натрия и концентрированием при пониженном давлении, очищают флэш-хроматографией с получением указанного в заголовке соединения в виде белого твердого вещества.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,17-6,97 (м, 4H), 6,76 (дд, J=8,8, 2,5 Гц, 1H), 6,59 (д, J=2,5 Гц, 1H), 4,49 (дт, J=18,2, 4,4 Гц, 3H), 4,23 (т, J=5,4 Гц, 1H), 4,04-3,91 (м, 2H), 3,83-3,67 (м, 4H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 3,00-2,83 (м, 6H), 2,69-2,41 (м, 6H), 2,05 (д, J=14,9 Гц, 2H), 1,93-1,78 (м, 2H), 1,18 (д, J=6,2 Гц, 3H).
Пример 213: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
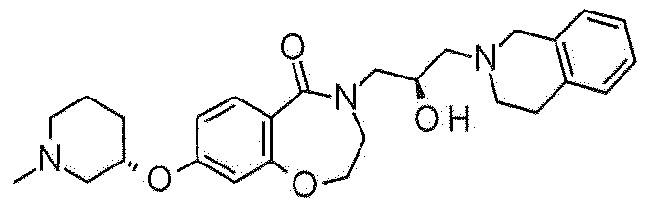
Пример 213-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Указанное в заголовке соединение синтезируют по методике примеров 64 и 78-1, за исключением того, что трет-бутил (S)-3-метилсульфонилоксипиперидин-1-карбоксилат используют вместо 4-хлортетрагидропирана в примере 64.
Пример 213-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 213-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,60 (д, J=8,8 Гц, 1H), 7,12-6,92 (м, 4H), 6,70 (дд, J=8,8, 2,5 Гц, 1H), 6,53 (д, J=2,5 Гц, 1H), 4,40 (т, J=5,0 Гц, 3H), 4,15 (кв, J=7,1, 5,2 Гц, 1H), 3,90 (дд, J=13,9, 3,6 Гц, 1H), 3,76-3,53 (м, 4H), 3,36 (дд, J=13,9, 7,6 Гц, 1H), 2,92-2,72 (м, 5H), 2,63-2,45 (м, 3H), 2,28 (с, 4H), 2,04-1,76 (м, 3H), 1,58 (д, J=20,6 Гц, 2H).
Пример 214: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-пропаноил-2,3-дигидро-1,4-бензоксазепин-5-она

Пример 214-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-N-метокси-N-метил-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксамида
Указанное в заголовке соединение синтезируют по методике примера 193-2, за исключением того, что N, O-диметилгидроксиамин гидрохлорид используют вместо октагидроциклопента[c]пиррола.
Пример 214-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-пропаноил-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-N-метокси-N-метил-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-карбоксамат (700 мг, 1 эквив.) растворяют в тетрагидрофуране, и туда добавляют 1 M бромид этилмагния (2 мл, раствор в тетрагидрофуране) при 0°C. Реакционный раствор перемешивают при комнатной температуре в течение 5 часов, экстрагируют этилацетатом, сушат над сульфатом магния и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,74-7,59 (м, 2H), 7,50 (д, J=1,6 Гц, 1H), 7,05-6,86 (м, 4H), 4,40 (т, J=5,1 Гц, 2H), 4,12 (тдд, J=7,5, 5,4, 3,6 Гц, 1H), 3,88 (дд, J=13,8, 3,6 Гц, 1H), 3,70-3,61 (м, 2H), 3,60 (дт, J=5,0, 2,5 Гц, 2H), 3,40-3,30 (м, 1H), 2,94 (кв, J=7,2 Гц, 2H), 2,89-2,69 (м, 4H), 2,58-2,52 (м, 2H), 1,07 (т, J=7,2 Гц, 3H).
Пример 215: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-2-фторэтил]-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
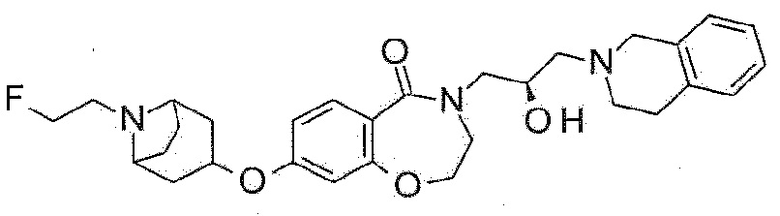
Пример 215-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение синтезируют заменой 4-хлортетрагидропирана на трет-бутил 3-метилсульфонилокси-8-азабицикло[3,2,1]октан-8-карбоксилат в примере 64. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Смесь перемешивают при комнатной температуре до завершения реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме двухвалентного дигидрохлорида.
Пример 215-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-2-фторэтил]-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 215-1, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,18-6,99 (м, 4H), 6,69 (дд, J=8,8, 2,5 Гц, 1H), 6,50 (д, J=2,4 Гц, 1H), 4,65 (дт, J=9,8, 5,0 Гц, 2H), 4,54 (т, J=5,0 Гц, 1H), 4,47 (т, J=5,0 Гц, 2H), 4,24 (д, J=5,7 Гц, 1H), 3,98 (дд, J=13,9, 3,7 Гц, 1H), 3,74 (дд, J=11,1, 6,0 Гц, 4H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 3,36 (с, 2H), 2,88 (ддд, J=26,4, 14,4, 5,1 Гц, 5H), 2,76 (т, J=5,0 Гц, 1H), 2,69-2,60 (м, 2H), 2,23 (д, J=15,2 Гц, 2H), 2,16-1,98 (м, 4H), 1,98-1,90 (м, 2H).
Пример 216: Синтез 8-(циклопропанкарбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
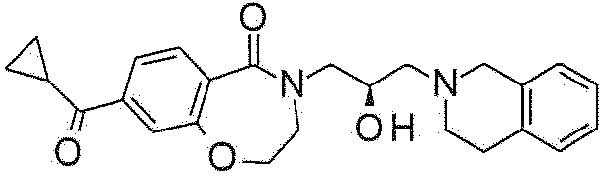
Указанное в заголовке соединение синтезируют по методике примера 241, за исключением того, что бромид циклопропилмагния используют вместо бромида этилмагния в примере 214-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (д, J=1,1 Гц, 2H), 7,54 (д, J=1,1 Гц, 1H), 7,07-6,80 (м, 4H), 4,39 (т, J=5,1 Гц, 2H), 4,17-4,06 (м, 1H), 3,87 (дд, J=13,8, 3,6 Гц, 1H), 3,69-3,51 (м, 4H), 3,33 (дд, J=13,8, 7,7 Гц, 1H), 2,80 (т, J=6,2 Гц, 2H), 2,73 (дд, J=8,8, 3,7 Гц, 2H), 2,71-2,66 (м, 1H), 2,59-2,45 (м, 2H), 1,07-0,92 (м, 4H).
Пример 217: Синтез 8-(циклопентанкарбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
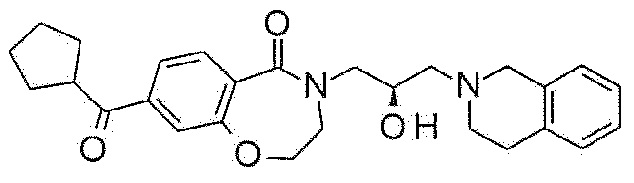
Указанное в заголовке соединение синтезируют по методике примера 241, за исключением того, что бромид циклопентилмагния используют вместо бромида этилмагния в примере 214-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,75-7,60 (м, 2H), 7,51 (д, J=1,5 Гц, 1H), 7,04-6,88 (м, 4H), 4,41 (т, J=5,1 Гц, 2H), 4,13 (тдд, J=7,5, 5,3, 3,5 Гц, 1H), 3,88 (дд, J=13,9, 3,6 Гц, 1H), 3,75-3,58 (м, 5H), 3,36 (дд, J=13,9, 7,7 Гц, 1H), 2,87-2,70 (м, 4H), 2,61-2,49 (м, 2H), 1,86 (дтдд, J=10,2, 7,6, 6,0, 2,9 Гц, 2H), 1,74 (дкв, J=13,3, 7,2 Гц, 2H), 1,66-1,51 (м, 4H).
Пример 218: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
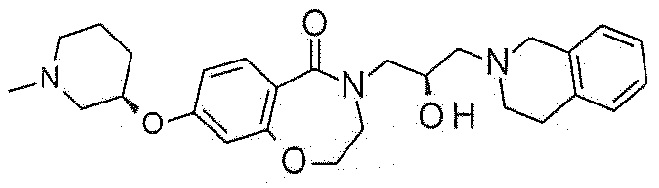
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что [rac-(3R)-1-метил-3-пиперидил]метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,18-7,00 (м, 4H), 6,77 (дд, J=8,8, 2,5 Гц, 1H), 6,60 (д, J=2,4 Гц, 1H), 4,49 (дт, J=14,9, 4,4 Гц, 3H), 4,27-4,18 (м, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,81-3,68 (м, 4H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 2,94 (т, J=6,2 Гц, 2H), 2,90-2,79 (м, 3H), 2,68-2,54 (м, 3H), 2,33 (с, 4H), 2,08-1,80 (м, 3H), 1,73-1,53 (м, 2H).
Пример 219: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
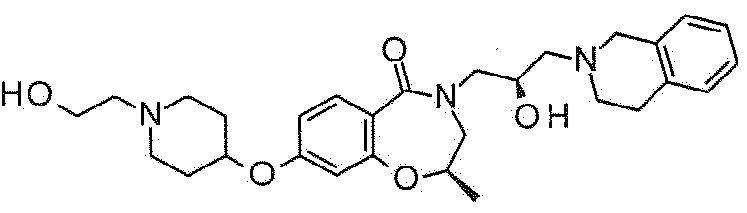
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 162 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,7 Гц, 1H), 7,18-7,02 (м, 4H), 6,80 (дд, J=8,7, 2,5 Гц, 1H), 6,58 (д, J=2,4 Гц, 1H), 4,79 (дт, J=7,2, 3,6 Гц, 1H), 4,56 (с, 1H), 4,30-4,20 (м, 1H), 4,15 (дд, J=13,7, 3,7 Гц, 1H), 3,84-3,70 (м, 3H), 3,64 (дд, J=15,5, 3,4 Гц, 1H), 3,50 (дд, J=15,5, 7,7 Гц, 1H), 3,26-3,18 (м, 2H), 2,93 (дд, J=15,1, 4,1 Гц, 5H), 2,79-2,58 (м, 5H), 2,08 (д, J=9,8 Гц, 2H), 1,89 (с, 2H), 1,32 (с, 3H).
Пример 220: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидрокси-2-метилпропил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
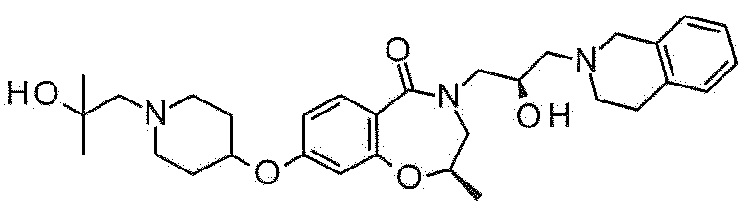
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140 используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения, за исключением того, что 2,2-диметилоксиран используют вместо 2-метоксирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=8,7 Гц, 1H), 7,17-7,02 (м, 4H), 6,77 (дд, J=8,8, 2,5 Гц, 1H), 6,54 (д, J=2,4 Гц, 1H), 4,84-4,74 (м, 1H), 4,44 (дт, J=8,0, 4,1 Гц, 1H), 4,29-4,19 (м, 1H), 4,15 (дд, J=13,7, 3,6 Гц, 1H), 3,78 (д, J=11,8 Гц, 2H), 3,63 (дд, J=15,6, 3,4 Гц, 1H), 3,49 (дд, J=15,6, 7,6 Гц, 1H), 3,23 (дд, J=13,8, 8,2 Гц, 1H), 2,91 (дт, J=19,8, 5,5 Гц, 6H), 2,68-2,50 (м, 4H), 2,38 (с, 2H), 2,08-1,97 (м, 2H), 1,85-1,75 (м, 2H), 1,32 (дд, J=7,0, 3,1 Гц, 2H), 1,21 (с, 6H).
Пример 221: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-морфолиноэтил)-2,3-дигидро-1,4-бензоксазепин-5-она
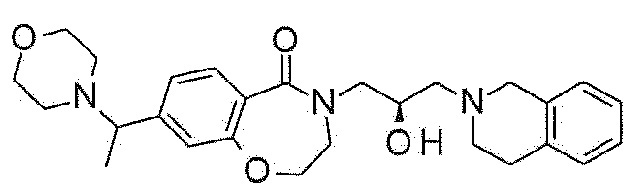
Пример 221-1: Синтез 8-ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
Указанное в заголовке соединение синтезируют по методике примера 214-2, за исключением того, что бромид метилмагния используют вместо бромида этилмагния.
Пример 221-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-морфолиноэтил)-2,3-дигидро-1,4-бензоксазепин-5-она
8-Ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 1 эквив.), морфолин (66 мкл, 3 эквив.), цианоборгидрид натрия (48 мг, 3 эквив.) и уксусную кислоту (1 капля) растворяют в 1 мл метанола и перемешивают при 80°С в течение 6 часов. Реакционную смесь экстрагируют этилацетатом, сушат над сульфатом магния и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,55 (д, J=8,0 Гц, 1H), 7,05 (дд, J=8,0, 1,5 Гц, 1H), 7,03-6,95 (м, 3H), 6,92 (д, J=7,2 Гц, 2H), 4,35 (т, J=5,1 Гц, 2H), 4,11 (дт, J=9,6, 3,5 Гц, 1H), 3,86 (дд, J=13,9, 3,6 Гц, 1H), 3,63 (с, 2H), 3,57 (дт, J=9,6, 4,8 Гц, 6H), 3,31 (дд, J=13,8, 7,6 Гц, 1H), 3,23 (с, 1H), 2,81 (т, J=6,1 Гц, 2H), 2,74 (т, J=5,7 Гц, 2H), 2,60-2,48 (м, 2H), 2,48-2,33 (м, 2H), 2,25 (дт, J=10,9, 4,7 Гц, 2H), 1,24 (д, J=6,6 Гц, 3H).
Пример 222: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-окса-6-азаспиро[3,3]гептан-6-ил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она
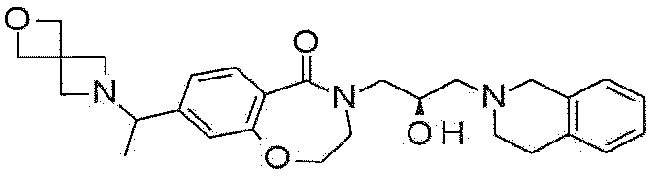
Указанное в заголовке соединение синтезируют по методике примера 221, за исключением того, что 2-окса-6-азаспиро[3,3]гептан используют вместо морфолина в примере 221-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,56 (д, J=8,0 Гц, 1H), 7,05-6,91 (м, 5H), 6,88 (д, J=1,6 Гц, 1H), 4,61 (с, 4H), 4,35 (т, J=5,1 Гц, 2H), 4,18-4,04 (м, 1H), 3,85 (дд, J=13,9, 3,6 Гц, 1H), 3,65 (д, J=2,0 Гц, 2H), 3,62-3,50 (м, 2H), 3,35-3,16 (м, 6H), 2,89-2,69 (м, 4H), 2,62-2,47 (м, 2H), 1,10 (д, J=6,5 Гц, 3H).
Пример 223: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-гидроксипро-1-пинил)-2,3-дигидро-1,4-бензоксазепин-5-она
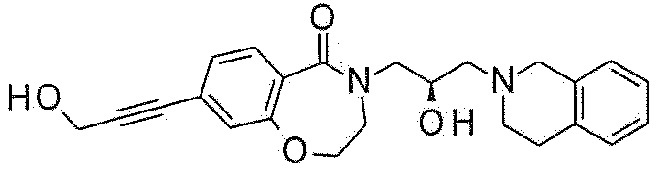
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 1,0 эквив.), проп-2-ин-1-ол (3 эквив.), дихлорид бис(трифенилфосфин)палладия (II) (8 мг, 0,05 эквив.), йодид меди(I) (5 мг, 0,1 эквив.) и триэтиламин (97 мкл, 3 эквив.) растворяют в N, N-диметилформамиде (1 мл) и перемешивают при 100°C в течение 4 часов. Реакционный раствор охлаждают до комнатной температуры, фильтруют через целит и экстрагируют насыщенным водным раствором хлорида аммония и этилацетатом. Объединенные органические слои промывают насыщенным водным раствором хлорида натрия и сушат над сульфатом магния. Полученный раствор концентрируют при пониженном давлении и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,1 Гц, 1H), 7,23 (дд, J=8,1, 1,6 Гц, 1H), 7,19-6,99 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,42 (с, 2H), 4,31-4,18 (м, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,82-3,76 (м, 2H), 3,76-3,68 (м, 2H), 3,45 (дд, J=13,9, 7,6 Гц, 1H), 3,01-2,82 (м, 4H), 2,73-2,62 (м, 2H).
Пример 224: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-метоксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
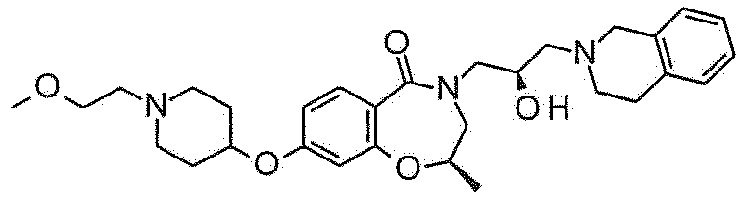
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения, за исключением того, что 1-бром-2-метоксиэтан используют вместо 2-фторэтил пара-толуолсульфоната.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,7 Гц, 1H), 7,17-7,02 (м, 4H), 6,78 (дд, J=8,7, 2,5 Гц, 1H), 6,55 (д, J=2,4 Гц, 1H), 4,79 (тд, J=7,0, 3,3 Гц, 1H), 4,50 (т, J=3,7 Гц, 1H), 4,23 (дт, J=8,6, 4,0 Гц, 1H), 4,15 (дд, J=13,8, 3,7 Гц, 1H), 3,77 (с, 2H), 3,68-3,45 (м, 4H), 3,37 (с, 2H), 3,23 (дд, J=13,8, 8,2 Гц, 1H), 2,94 (д, J=5,3 Гц, 2H), 2,88 (т, J=5,5 Гц, 4H), 2,66 (дт, J=13,4, 6,6 Гц, 4H), 2,50 (д, J=10,2 Гц, 2H), 2,10-2,00 (м, 2H), 1,88-1,80 (м, 2H), 1,35-1,30 (м, 3H).
Пример 225: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она
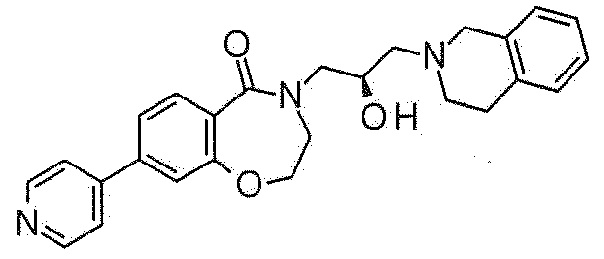
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 4-пиридилбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 8,70-8,56 (м, 2H), 7,87 (д, J=8,1 Гц, 1H), 7,81-7,69 (м, 2H), 7,60 (дд, J=8,2, 1,8 Гц, 1H), 7,48 (д, J=1,8 Гц, 1H), 7,17-7,04 (м, 4H), 4,56 (т, J=5,0 Гц, 2H), 4,27 (д, J=5,4 Гц, 1H), 4,03 (дд, J=13,9, 3,6 Гц, 1H), 3,79 (д, J=7,0 Гц, 4H), 3,48 (дд, J=13,9, 7,7 Гц, 1H), 2,95 (д, J=5,2 Гц, 2H), 2,89 (дд, J=8,9, 3,5 Гц, 2H), 2,68 (дд, J=6,2, 2,1 Гц, 2H).
Пример 226: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(4-пиридил)этинил]-2,3-дигидро-1,4-бензоксазепин-5-она
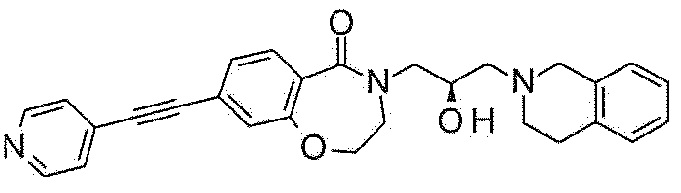
Указанное в заголовке соединение синтезируют по методике примера 223, за исключением того, что 4-этинилпиридин используют вместо проп-2-ин-1-ола.
1H ЯМР (400 MГц, Метанол-d4) δ 8,55-8,33 (м, 2H), 7,63 (д, J=8,0 Гц, 1H), 7,50-7,40 (м, 2H), 7,26 (дд, J=8,1, 1,6 Гц, 1H), 7,14 (д, J=1,6 Гц, 1H), 7,09-6,83 (м, 4H), 4,39 (т, J=5,1 Гц, 2H), 4,13 (дддд, J=9,0, 7,4, 4,6, 2,6 Гц, 1H), 3,87 (дд, J=13,9, 3,6 Гц, 1H), 3,70-3,52 (м, 4H), 3,35 (дд, J=13,8, 7,7 Гц, 1H), 2,88-2,69 (м, 4H), 2,65-2,48 (м, 2H).
Пример 227: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(3-пиридил)этинил]-2,3-дигидро-1,4-бензоксазепин-5-она
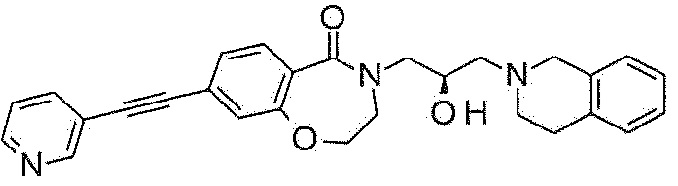
Указанное в заголовке соединение синтезируют по методике примера 223, за исключением того, что 3-этинилпиридин используют вместо проп-2-ин-1-ола.
1H ЯМР (400 MГц, Метанол-d4) δ 8,67-8,56 (м, 1H), 8,43 (дд, J=5,0, 1,6 Гц, 1H), 7,88 (дт, J=8,0, 1,9 Гц, 1H), 7,61 (д, J=8,0 Гц, 1H), 7,36 (ддд, J=8,0, 5,0, 0,9 Гц, 1H), 7,25 (дд, J=8,1, 1,6 Гц, 1H), 7,13 (д, J=1,5 Гц, 1H), 7,06-6,96 (м, 3H), 6,95-6,89 (м, 1H), 4,39 (т, J=5,1 Гц, 2H), 4,11 (ддд, J=7,4, 5,7, 3,4 Гц, 1H), 3,88 (дд, J=13,9, 3,5 Гц, 1H), 3,70-3,52 (м, 4H), 3,32 (дд, J=13,8, 7,8 Гц, 1H), 2,82 (т, J=6,2 Гц, 2H), 2,75 (т, J=5,5 Гц, 2H), 2,57-2,40 (м, 2H).
Пример 228: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-гидроксибу-1-тинил)-2,3-дигидро-1,4-бензоксазепин-5-она
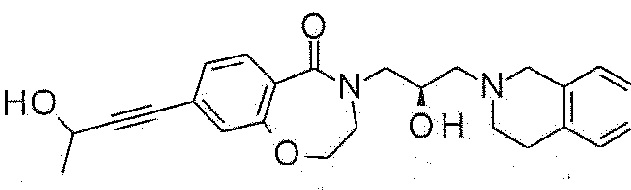
Указанное в заголовке соединение синтезируют по методике примера 223, за исключением того, что бут-3-ин-2-ол используют вместо проп-2-ин-1-ола.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,0 Гц, 1H), 7,21 (дд, J=8,1, 1,6 Гц, 1H), 7,16-6,94 (м, 5H), 4,70 (кв, J=6,6 Гц, 1H), 4,47 (т, J=5,1 Гц, 2H), 4,22 (дкв, J=10,1, 5,6, 4,5 Гц, 1H), 3,98 (дд, J=13,9, 3,5 Гц, 1H), 3,75 (с, 2H), 3,73-3,64 (м, 2H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 2,92 (д, J=5,6 Гц, 2H), 2,86 (т, J=5,6 Гц, 2H), 2,64 (д, J=6,5 Гц, 2H), 1,50 (д, J=6,6 Гц, 3H).
Пример 229: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[3-(метиламино)про-1-пинил]-2,3-дигидро-1,4-бензоксазепин-5-она
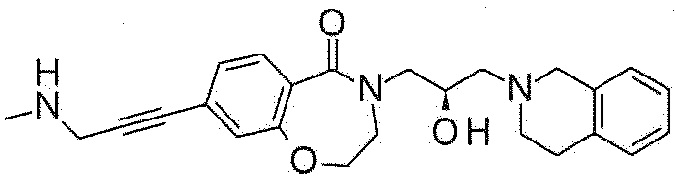
Указанное в заголовке соединение синтезируют по методике примера 223, за исключением того, что N-метилпроп-2-ин-1-амин используют вместо проп-2-ин-1-ола.
1H ЯМР (400 MГц, Метанол-d4) δ 7,55 (д, J=8,1 Гц, 1H), 7,11 (дд, J=8,1, 1,6 Гц, 1H), 7,06-6,89 (м, 5H), 4,36 (т, J=5,1 Гц, 2H), 4,18-4,05 (м, 1H), 3,86 (дд, J=13,9, 3,6 Гц, 1H), 3,68-3,63 (м, 2H), 3,59 (дт, J=5,0, 2,9 Гц, 2H), 3,52 (с, 2H), 3,33 (дд, J=13,9, 7,7 Гц, 1H), 2,81 (д, J=5,3 Гц, 2H), 2,75 (дд, J=8,9, 3,6 Гц, 2H), 2,57-2,50 (м, 2H), 2,39 (с, 3H).
Пример 230: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она
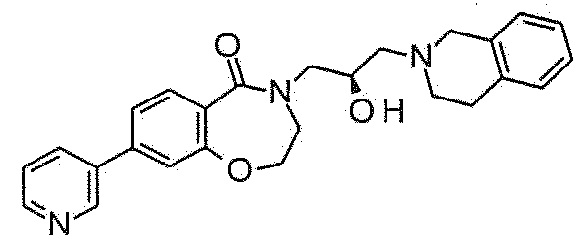
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 3-пиридилбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 8,94-8,83 (м, 1H), 8,64-8,53 (м, 1H), 8,21-8,09 (м, 1H), 7,85 (д, J=8,1 Гц, 1H), 7,64-7,46 (м, 2H), 7,40 (д, J=1,8 Гц, 1H), 7,18-6,92 (м, 4H), 4,56 (т, J=5,1 Гц, 2H), 4,31-4,23 (м, 1H), 4,03 (дд, J=13,8, 3,6 Гц, 1H), 3,84-3,75 (м, 4H), 3,49 (дд, J=13,9, 7,7 Гц, 1H), 3,00-2,87 (м, 4H), 2,70 (дд, J=6,3, 2,4 Гц, 2H).
Пример 231: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,3-диметилпиразол-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
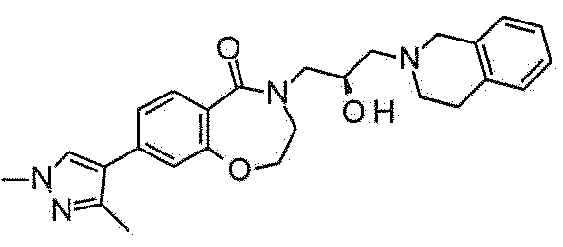
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 1,3-диметилпиразолбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 7,84 (с, 1H), 7,73 (д, J=8,1 Гц, 1H), 7,28 (дд, J=8,1, 1,8 Гц, 1H), 7,18-7,03 (м, 5H), 4,51 (т, J=5,1 Гц, 2H), 4,30-4,22 (м, 1H), 4,00 (дд, J=13,8, 3,6 Гц, 1H), 3,88 (с, 3H), 3,83-3,72 (м, 4H), 3,47 (дд, J=13,9, 7,6 Гц, 1H), 2,93 (ддд, J=11,9, 9,3, 4,3 Гц, 4H), 2,74-2,62 (м, 2H), 2,40 (с, 3H).
Пример 232: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-метилпиразол-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
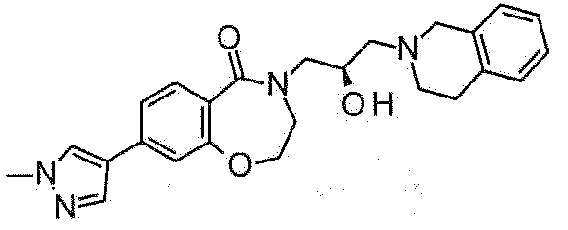
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 1-метилпиразолбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 8,06 (с, 1H), 7,93-7,81 (м, 1H), 7,74-7,66 (м, 1H), 7,39 (дд, J=8,1, 1,7 Гц, 1H), 7,25 (д, J=1,7 Гц, 1H), 7,16-7,02 (м, 4H), 4,50 (т, J=5,1 Гц, 2H), 4,31-4,21 (м, 1H), 4,03-3,89 (м, 4H), 3,81 (с, 2H), 3,78-3,71 (м, 2H), 3,47 (дд, J=13,9, 7,6 Гц, 1H), 2,94 (дд, J=9,5, 4,6 Гц, 4H), 2,72-2,66 (м, 2H).
Пример 233: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,5-диметилпиразол-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она
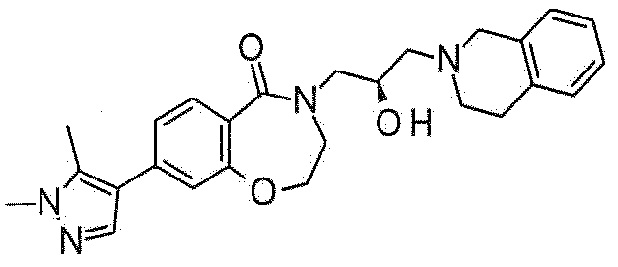
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 1,5-диметилпиразолбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 7,83-7,53 (м, 3H), 7,25 (дд, J=8,1, 1,7 Гц, 1H), 7,11 (ддд, J=14,4, 6,0, 2,5 Гц, 4H), 4,52 (т, J=5,1 Гц, 2H), 4,27 (д, J=9,2 Гц, 1H), 4,01 (дд, J=13,9, 3,7 Гц, 1H), 3,86 (с, 3H), 3,82-3,71 (м, 4H), 3,48 (дд, J=13,9, 7,6 Гц, 1H), 2,93 (дт, J=8,6, 4,9 Гц, 4H), 2,73-2,64 (м, 2H), 2,46 (с, 3H).
Пример 234: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она
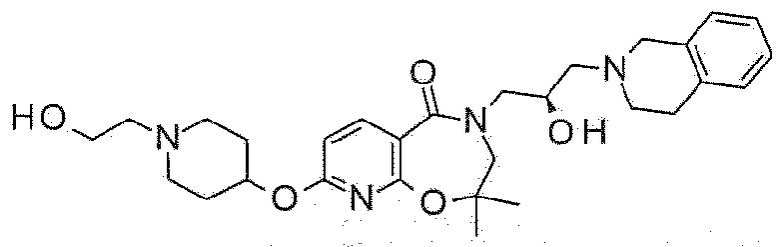
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиперидилокси)-3H-пиридо[3,2-f][1,4]оксазепин-5-он дигидрохлорид используют в качестве исходного материала по методике примера 162 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,04 (д, J=8,4 Гц, 1H), 7,16-7,00 (м, 4H), 6,61 (д, J=8,4 Гц, 1H), 5,14-5,00 (м, 1H), 4,27 (с, 1H), 4,04 (дд, J=13,8, 3,6 Гц, 1H), 3,78-3,57 (м, 6H), 3,40 (дд, J=13,7, 8,2 Гц, 1H), 2,97-2,79 (м, 6H), 2,66-2,53 (м, 4H), 2,48 (с, 2H), 2,12-2,02 (м, 2H), 1,89-1,76 (м, 2H), 1,48 (с, 3H), 1,43 (с, 3H).
Пример 235: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[[(3R)-1-метил-3-пиперидил]окси]-3H-пиридо[3,2-f][1,4]оксазепин-5-она
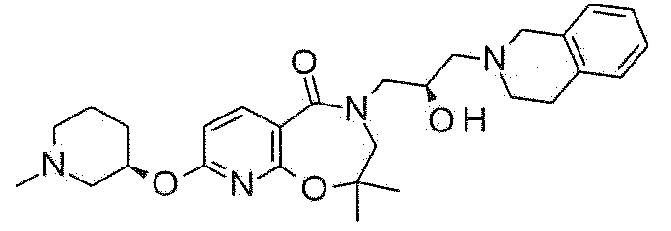
Указанное в заголовке соединение синтезируют по методике примеров 144-1 и 114-3-144-6, за исключением того, что 1-[(4-метоксифенил)метиламино]-2-метилпропан-2-ол используют вместо 1-[(4-метоксифенил)метиламино]пропан-2-ола в примере 144-1, и трет-бутил 3-гидроксипиперидин-1-карбоксилат используют вместо трет-бутил 4-гидроксипиперидин-1-карбоксилата в примере 144-3.
1H ЯМР (400 MГц, Метанол-d4) δ 8,04 (д, J=8,4 Гц, 1H), 7,17-7,02 (м, 4H), 6,63 (д, J=8,4 Гц, 1H), 5,18 (с, 1H), 4,27 (с, 1H), 4,04 (дд, J=13,8, 3,6 Гц, 1H), 3,76 (с, 2H), 3,71-3,56 (м, 2H), 3,39 (дд, J=13,8, 8,3 Гц, 1H), 2,99-2,81 (м, 5H), 2,64 (дд, J=6,3, 2,8 Гц, 2H), 2,60 (д, J=6,8 Гц, 1H), 2,52-2,35 (м, 2H), 2,33 (с, 3H), 2,02-1,84 (м, 2H), 1,75-1,58 (м, 2H), 1,47 (с, 3H), 1,42 (с, 3H).
Пример 236: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(1-(2-фторэтил)-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
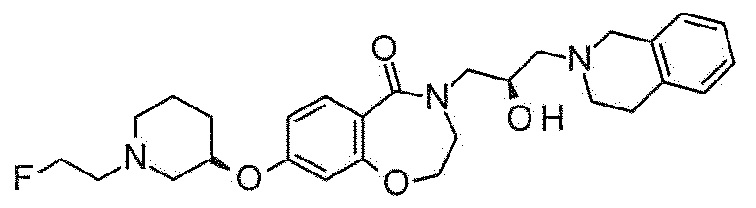
Пример 236-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-она; дигидрохлорида
Указанное в заголовке соединение синтезируют по методике примеров 77 и 78-1, за исключением того, что трет-бутил (R)-3-метилсульфонилоксипиперидин-1-карбоксилат используют вместо трет-бутил 4-метилсульфонилоксипиперидин-1-карбоксилата в примере 77.
Пример 236-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(1-(2-фторэтил)-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 236-1, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,19-6,98 (м, 4H), 6,77 (дд, J=8,8, 2,5 Гц, 1H), 6,60 (д, J=2,5 Гц, 1H), 4,66 (тд, J=5,0, 2,2 Гц, 1H), 4,57-4,41 (м, 4H), 4,23 (тдд, J=7,5, 5,4, 3,7 Гц, 1H), 3,97 (дд, J=13,9, 3,7 Гц, 1H), 3,80-3,68 (м, 4H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 3,06 (д, J=11,4 Гц, 1H), 2,98-2,85 (м, 4H), 2,85-2,71 (м, 3H), 2,70-2,61 (м, 2H), 2,36 (ддд, J=21,3, 11,4, 5,6 Гц, 2H), 2,04 (д, J=8,9 Гц, 1H), 1,86 (дт, J=8,4, 4,3 Гц, 1H), 1,76-1,62 (м, 1H), 1,59-1,48 (м, 1H).
Пример 237: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(1-(2-гидрокси)-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она
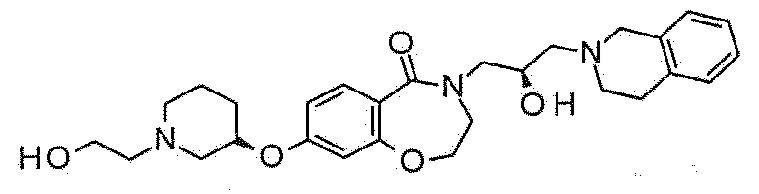
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он, дигидрохлорид, полученный в примере 236-1, используют в качестве исходного материала по методике примера 162 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,19-6,99 (м, 4H), 6,78 (дд, J=8,8, 2,5 Гц, 1H), 6,62 (д, J=2,4 Гц, 1H), 4,50 (дт, J=22,5, 4,6 Гц, 3H), 4,24 (тт, J=7,8, 4,1 Гц, 1H), 3,97 (дд, J=13,9, 3,7 Гц, 1H), 3,81 (с, 2H), 3,72 (кв, J=5,9 Гц, 4H), 3,44 (дд, J=13,9, 7,5 Гц, 1H), 3,14-3,04 (м, 1H), 2,94 (дт, J=9,5, 4,8 Гц, 4H), 2,82 (дд, J=10,8, 5,0 Гц, 1H), 2,67 (дт, J=17,1, 5,2 Гц, 3H), 2,49-2,32 (м, 2H), 2,05 (д, J=10,2 Гц, 2H), 1,87 (с, 1H), 1,70 (дт, J=9,5, 4,1 Гц, 1H), 1,64-1,51 (м, 1H).
Пример 238: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидрокси-2-метилпропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
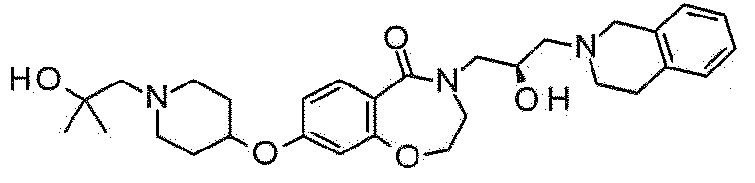
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 78-1, используют в качестве исходного материала по методике примера 220 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,7 Гц, 1H), 7,17-6,99 (м, 4H), 6,76 (дд, J=8,8, 2,4 Гц, 1H), 6,58 (д, J=2,4 Гц, 1H), 4,46 (кв, J=11,0, 8,0 Гц, 3H), 4,24 (с, 1H), 3,97 (дд, J=13,9, 3,7 Гц, 1H), 3,83-3,68 (м, 4H), 3,44 (дд, J=13,9, 7,6 Гц, 1H), 2,93 (дд, J=13,7, 4,6 Гц, 6H), 2,75-2,53 (м, 4H), 2,42 (д, J=7,6 Гц, 2H), 2,03 (с, 2H), 1,83 (д, J=9,5 Гц, 2H), 1,22 (с, 6H).
Пример 239: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(6-фтор-2-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она
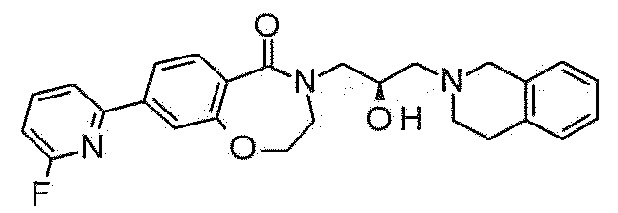
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 6-фтор-2-пиридилбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 8,03 (кв, J=8,1 Гц, 1H), 7,92-7,78 (м, 3H), 7,75 (д, J=1,7 Гц, 1H), 7,17-7,01 (м, 5H), 4,55 (т, J=5,1 Гц, 2H), 4,33-4,21 (м, 1H), 4,02 (дд, J=13,8, 3,6 Гц, 1H), 3,85-3,70 (м, 4H), 3,49 (дд, J=13,8, 7,7 Гц, 1H), 3,01-2,86 (м, 4H), 2,75-2,64 (м, 2H).
Пример 240: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-этоксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
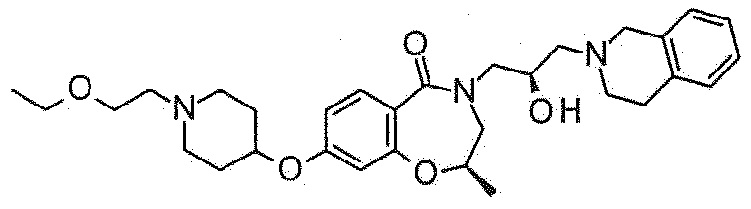
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения, за исключением того, что 1-бром-2-этоксиэтан используют вместо 2-фторэтил пара-толуолсульфоната.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,7 Гц, 1H), 7,16-6,99 (м, 4H), 6,79 (дд, J=8,7, 2,5 Гц, 1H), 6,57 (д, J=2,4 Гц, 1H), 4,79 (тд, J=6,9, 3,3 Гц, 1H), 4,53 (дп, J=7,7, 3,7 Гц, 1H), 4,29-4,19 (м, 1H), 4,14 (дд, J=13,9, 3,7 Гц, 1H), 3,79 (с, 2H), 3,68-3,58 (м, 3H), 3,58-3,43 (м, 3H), 3,24 (дд, J=13,8, 8,1 Гц, 1H), 2,93 (квд, J=9,2, 8,7, 4,5 Гц, 6H), 2,76 (т, J=5,6 Гц, 2H), 2,64 (дт, J=16,5, 7,0 Гц, 4H), 2,07 (ддд, J=16,6, 10,3, 6,3 Гц, 2H), 1,93-1,81 (м, 2H), 1,32 (д, J=6,4 Гц, 3H), 1,22 (т, J=7,0 Гц, 3H).
Пример 241: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-2-гидрокси]-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
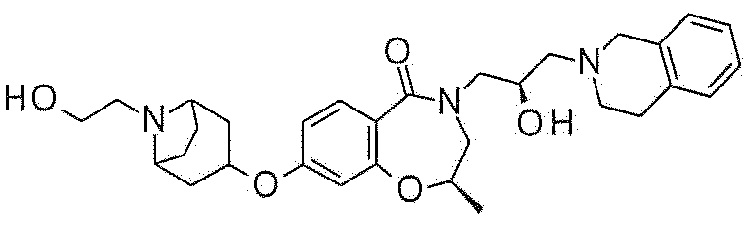
Пример 241-1: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение, в котором Вос замещена, синтезируют с применением продукта, полученного по методике примера 140 за исключением того, что [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат используют вместо [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната в качестве исходного материала и способом по методике примера 64 за исключением того, что трет-бутил 3-метилсульфонилокси-8-азабицикло[3,2,1]октан-8-карбоксилат применяют вместо 4-хлортетрагидропирана. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
Пример 241-2: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-2-гидрокси]-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[-8-азабицикло[3,2,1]октан-3-ил)окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 241-1, используют в качестве исходного материала по методике примера 162 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,8 Гц, 1H), 7,19-6,99 (м, 4H), 6,79 (дд, J=8,7, 2,5 Гц, 1H), 6,55 (д, J=2,4 Гц, 1H), 4,81-4,74 (м, 2H), 4,24 (д, J=5,4 Гц, 1H), 4,15 (дд, J=13,8, 3,6 Гц, 1H), 3,79-3,58 (м, 7H), 3,55-3,45 (м, 1H), 3,23 (д, J=5,5 Гц, 1H), 3,00-2,77 (м, 6H), 2,66 (г, J=5,2 Гц, 2H), 2,15 (с, 4H), 1,97-1,80 (м, 4H), 1,33 (д, J=6,4 Гц, 3H).
Пример 242: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-2-фторэтил]-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
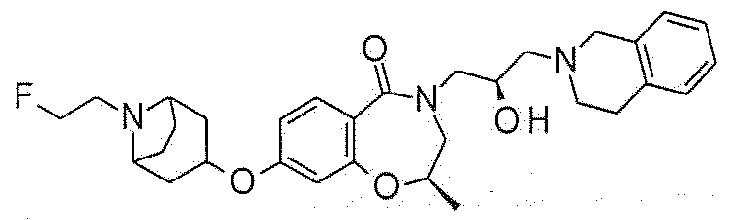
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 241-1, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,61 (д, J=8,7 Гц, 1H), 7,17-7,00 (м, 4H), 6,77 (дд, J=8,7, 2,5 Гц, 1H), 6,52 (д, J=2,4 Гц, 1H), 4,78 (тд, J=6,9, 3,3 Гц, 1H), 4,73-4,62 (м, 1H), 4,54 (т, J=5,0 Гц, 1H), 4,16 (ддд, J=23,5, 11,6, 8,0 Гц, 2H), 3,77 (д, J=9,9 Гц, 3H), 3,63 (дд, J=15,6, 3,4 Гц, 1H), 3,53-3,41 (м, 2H), 3,23 (дд, J=13,8, 8,2 Гц, 1H), 2,96-2,91 (м, 4H), 2,88 (тд, J=6,4, 5,7, 2,7 Гц, 3H), 2,81 (т, J=5,0 Гц, 1H), 2,70 (дд, J=12,9, 4,1 Гц, 1H), 2,62 (дт, J=13,0, 6,5 Гц, 2H), 2,12-2,00 (м, 3H), 1,89-1,77 (м, 3H), 1,33 (д, J=6,4 Гц, 3H).
Пример 243: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-метоксиэтил)-4-пиридил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
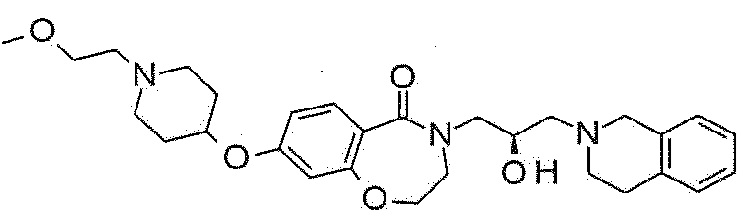
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 78-1, используют в качестве исходного материала по методике примера 224 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,20-7,01 (м, 4H), 6,77 (дд, J=8,8, 2,5 Гц, 1H), 6,59 (д, J=2,4 Гц, 1H), 4,50 (дт, J=25,8, 4,4 Гц, 3H), 4,30-4,19 (м, 1H), 3,97 (дд, J=13,9, 3,7 Гц, 1H), 3,84-3,67 (м, 4H), 3,60 (т, J=5,5 Гц, 2H), 3,45 (дд, J=13,9, 7,6 Гц, 1H), 3,38 (с, 3H), 2,93 (дт, J=11,0, 5,7 Гц, 6H), 2,76 (т, J=5,5 Гц, 2H), 2,72-2,54 (м, 4H), 2,06 (дд, J=18,1, 11,0 Гц, 2H), 1,93-1,82 (м, 2H).
Пример 244: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(6-метокси-2-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она
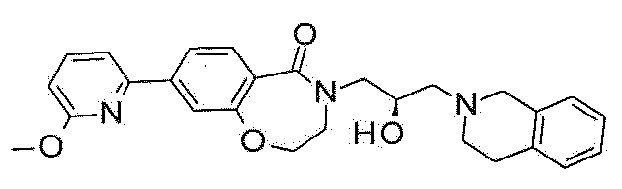
Указанное в заголовке соединение синтезируют по методике примера 12, за исключением того, что 6-метокси-2-пиридилбороновую кислоту используют вместо изобутилбороновой кислоты.
1H ЯМР (400 MГц, Метанол-d4) δ 7,90 (дд, J=8,3, 1,7 Гц, 1H), 7,84-7,69 (м, 3H), 7,52 (д, J=7,4 Гц, 1H), 7,18-7,01 (м, 4H), 6,78 (д, J=8,2 Гц, 1H), 4,54 (т, J=5,1 Гц, 2H), 4,33-4,21 (м, 1H), 4,03 (с, 4H), 3,82-3,71 (м, 4H), 3,49 (дд, J=13,9, 7,7 Гц, 1H), 3,00-2,82 (м, 4H), 2,74-2,62 (м, 2H).
Пример 245: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксипропил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
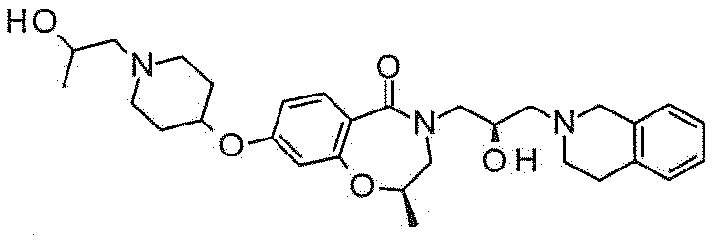
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,7 Гц, 1H), 7,17-7,00 (м, 4H), 6,79 (дд, J=8,7, 2,4 Гц, 1H), 6,57 (д, J=2,4 Гц, 1H), 4,82-4,77 (м, 1H), 4,56 (с, 1H), 4,24 (тт, J=8,3, 4,6 Гц, 1H), 4,13 (ддд, J=13,9, 7,8, 5,4 Гц, 1H), 4,00 (п, J=6,3 Гц, 1H), 3,79 (с, 2H), 3,64 (дд, J=15,6, 3,4 Гц, 1H), 3,50 (дд, J=15,6, 7,6 Гц, 1H), 3,27-3,21 (м, 1H), 3,10-2,87 (м, 6H), 2,80-2,62 (м, 4H), 2,57 (д, J=6,4 Гц, 2H), 2,17-2,04 (м, 2H), 1,94 (с, 2H), 1,33 (д, J=6,4 Гц, 3H), 1,19 (д, J=6,2 Гц, 3H).
Пример 246: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(1-морфолиноэтил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она
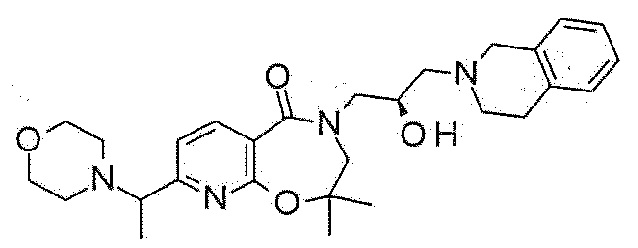
Пример 246-1: Синтез 8-ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она
8-Хлор-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-он (200 мг, 0,48 ммоль), трибутил (1-этоксивинил)олово (0,21 мл, 0,62 ммоль) и тетракис(трифенилфосфин)палладий (28 мг, 0,024 ммоль) растворяют в 4 мл толуола 4 мл, и реакцию проводят с применением микроволн при 120°C в течение 2 часов. К реакционному раствору добавляют водный раствор концентрированной хлористоводородной кислоты и 1,4-диоксан, с последующим перемешиванием при комнатной температуре в течение 10 минут. Реакционный раствор разбавляют этилацетатом и подщелачивают водным раствором гидроксида натрия. Смесь экстрагируют этилацетатом, сушат над сульфатом магния и очищают флэш-хроматографией с получением указанного в заголовке соединения.
Пример 246-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(1-морфолиноэтил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она
8-Ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-он, полученный в примере 246-1, используют в качестве исходного материала по методике примера 221-2 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,13 (д, J=7,8 Гц, 1H), 7,39 (дд, J=7,8, 1,2 Гц, 1H), 7,17-7,00 (м, 4H), 4,29 (с, 1H), 4,05 (ддд, J=13,7, 7,3, 3,8 Гц, 1H), 3,77 (с, 2H), 3,70 (т, J=4,7 Гц, 4H), 3,62 (д, J=2,4 Гц, 2H), 3,55-3,39 (м, 2H), 2,99-2,80 (м, 4H), 2,72-2,61 (м, 2H), 2,64-2,52 (м, 2H), 2,41 (дт, J=11,0, 4,6 Гц, 2H), 1,50 (д, J=2,3 Гц, 3H), 1,44 (д, J=2,2 Гц, 3H), 1,39 (д, J=6,8 Гц, 3H).
Пример 247: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[1-(2-окса-6-азаспиро[3,3]гептан-6-ил)этил]-3H-пиридо[3,2-f][1,4]оксазепин-5-она
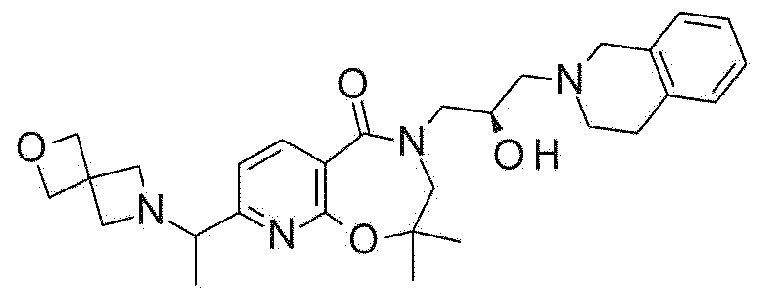
8-Ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-он, полученный в примере 246-1, используют в качестве исходного материала по методике примера 222 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,13 (д, J=7,8 Гц, 1H), 7,28 (д, J=7,8 Гц, 1H), 7,15-7,03 (м, 4H), 4,75 (с, 4H), 4,28 (с, 1H), 4,05 (ддд, J=12,9, 8,5, 3,8 Гц, 1H), 3,76 (с, 2H), 3,61 (д, J=2,1 Гц, 2H), 3,49-3,37 (м, 6H), 2,97-2,82 (м, 4H), 2,65 (дд, J=6,3, 3,8 Гц, 2H), 1,50 (д, J=2,8 Гц, 3H), 1,44 (д, J=2,8 Гц, 3H), 1,25 (д, J=6,6 Гц, 3H).
Пример 248: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксипропил)-4-пиперидил]окси]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она
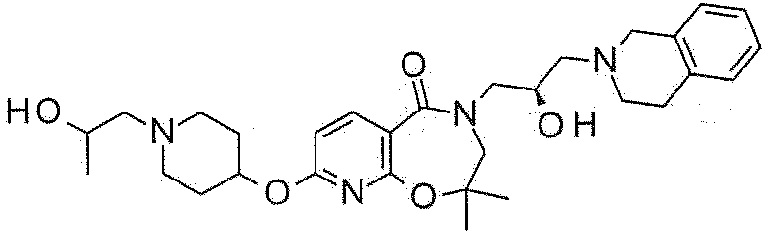
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиперидилокси)-3H-пиридо[3,2-f][1,4]оксазепин-5-он дигидрохлорид используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,04 (д, J=8,4 Гц, 1H), 7,15-7,02 (м, 4H), 6,60 (д, J=8,4 Гц, 1H), 5,07 (с, 1H), 4,26 (с, 1H), 4,03 (дд, J=13,6, 3,6 Гц, 1H), 3,96 (кв, J=6,0 Гц, 1H), 3,75 (с, 2H), 3,71-3,57 (м, 2H), 3,41 (дд, J=13,8, 8,2 Гц, 1H), 2,90 (дд, J=19,1, 5,4 Гц, 6H), 2,63 (дд, J=6,2, 3,0 Гц, 2H), 2,53 (с, 1H), 2,41 (д, J=8,6 Гц, 3H), 2,06 (с, 2H), 1,85 (с, 2H), 1,48 (с, 3H), 1,43 (с, 3H), 1,17 (д, J=6,2 Гц, 3H).
Пример 249: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,4-дигидро-1H-пирроло[1,2-a]пиразин-2-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
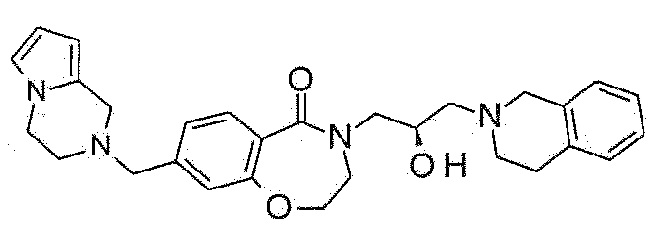
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 1,2,3,4-тетрагидропирроло[1,2-a]пиразин используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (д, J=8,0 Гц, 1H), 7,22 (дд, J=8,0, 1,6 Гц, 1H), 7,17-6,99 (м, 5H), 6,59-6,50 (м, 1H), 6,11-5,97 (м, 1H), 5,74 (дд, J=3,5, 1,6 Гц, 1H), 4,48 (т, J=5,1 Гц, 2H), 4,24 (тдд, J=7,3, 5,2, 3,5 Гц, 1H), 3,99 (ддд, J=9,5, 4,3, 2,6 Гц, 3H), 3,77 (д, J=2,3 Гц, 2H), 3,72 (д, J=7,3 Гц, 4H), 3,62 (с, 2H), 3,46 (дд, J=13,9, 7,6 Гц, 1H), 2,96-2,91 (м, 2H), 2,91-2,83 (м, 4H), 2,67 (дд, J=6,2, 2,2 Гц, 2H).
Пример 250: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(2-окса-6-азаспиро[3,3]гептан-6-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
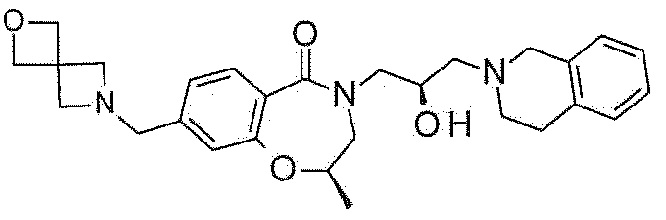
Указанное в заголовке соединение синтезируют по методике примера 28, за исключением того, что (2R)-8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-он используют в качестве исходного материала.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=7,9 Гц, 1H), 7,17-7,01 (м, 5H), 6,95 (д, J=1,6 Гц, 1H), 4,84-4,78 (м, 1H), 4,75 (с, 3H), 4,23 (тд, J=7,9, 4,2 Гц, 1H), 4,15 (дд, J=13,8, 3,7 Гц, 1H), 3,77 (с, 2H), 3,66-3,56 (м, 3H), 3,46 (с, 5H), 3,26 (дд, J=13,8, 8,1 Гц, 1H), 2,97-2,83 (м, 4H), 2,64 (г, J=7,6 Гц, 2H), 1,31 (д, J=6,3 Гц, 4H).
Пример 251: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-окса-7-азаспиро[3,5]нонан-7-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
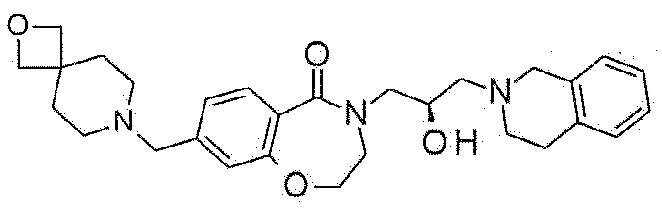
Указанное в заголовке соединение синтезируют по методике примера 29, за исключением того, что 2-окса-7-азаспиро[3,5]нонан оксалат используют вместо 3-метоксиазетидина гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,0 Гц, 1H), 7,19-6,97 (м, 6H), 4,47 (т, J=5,1 Гц, 2H), 4,42 (с, 4H), 4,28-4,19 (м, 1H), 3,99 (дд, J=13,9, 3,6 Гц, 1H), 3,78-3,67 (м, 4H), 3,51-3,40 (м, 3H), 2,93 (дд, J=9,0, 4,0 Гц, 2H), 2,86 (дд, J=8,9, 3,7 Гц, 2H), 2,67-2,60 (м, 2H), 2,37 (с, 4H), 1,89 (т, J=5,5 Гц, 4H).
Пример 252: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(2-окса-7-азаспиро[3,5]нонан-7-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она
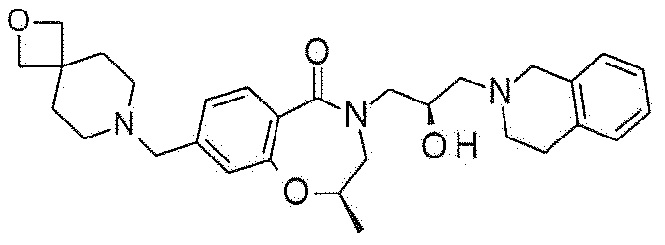
Указанное в заголовке соединение синтезируют по методике примера 251, за исключением того, что (2R)-8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-он используют в качестве исходного материала.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=7,9 Гц, 1H), 7,20-6,95 (м, 6H), 4,83-4,77 (м, 1H), 4,42 (с, 4H), 4,27-4,20 (м, 1H), 4,16 (дд, J=13,8, 3,7 Гц, 1H), 3,75 (д, J=5,4 Гц, 2H), 3,62 (дд, J=15,6, 3,6 Гц, 1H), 3,52-3,41 (м, 3H), 3,26 (дд, J=13,7, 8,1 Гц, 1H), 2,96-2,82 (м, 4H), 2,63 (г, J=7,5 Гц, 2H), 2,38 (с, 4H), 1,90 (т, J=5,6 Гц, 4H), 1,31 (д, J=6,4 Гц, 3H).
Пример 253: Синтез 4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
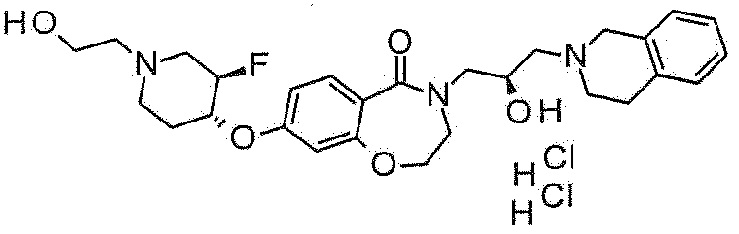
Пример 253-1: Синтез 4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)]-8-[[(3R,4R)-3-фтор-1-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение в котором Вос замещена, синтезируют по методике примера 140 за исключением того, что (S)-трет-бутил 3-фтор-4-метилсульфонилокси-пиперидин-1-карбоксилат используют вместо 4-хлортетрагидропирана. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
Пример 253-2: Синтез 4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный в примере 253-1, используют в качестве исходного материала по методике примера 162, и затем указанное в заголовке соединение получают образованием гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,76 (д, J=8,7 Гц, 1H), 7,40-7,19 (м, 4H), 6,94 (д, J=8,7 Гц, 1H), 6,80 (с, 1H), 5,13 (д, J=43,3 Гц, 1H), 4,97 (с, 1H), 4,67 (дд, J=15,4, 8,5 Гц, 1H), 4,57 (ддд, J=10,7, 7,0, 3,6 Гц, 1H), 4,53-4,42 (м, 3H), 4,05-3,83 (м, 5H), 3,77 (ддд, J=9,9, 8,1, 5,1 Гц, 5H), 3,65-3,57 (м, 2H), 3,54-3,36 (м, 6H), 3,29-3,07 (м, 2H), 2,53-2,18 (м, 2H).
Пример 254: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксипропил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она двухвалентного гидрохлорида
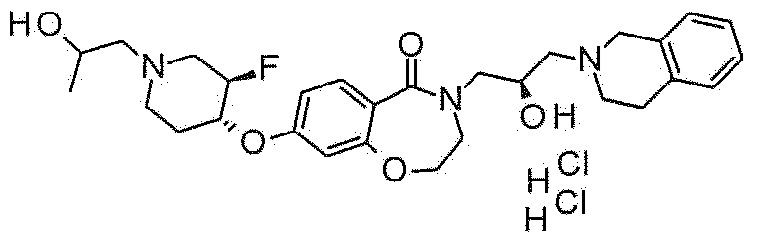
Продукт, полученный в примере 253-1, используют в качестве исходного материала по методике примера 212, и затем указанное в заголовке соединение получают образованием гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,76 (д, J=8,6 Гц, 1H), 7,32 (кв, J=7,5, 6,7 Гц, 3H), 7,23 (т, J=7,0 Гц, 1H), 6,93 (д, J=8,8 Гц, 1H), 6,79 (с, 1H), 5,23-5,01 (м, 1H), 4,96 (с, 1H), 4,67 (дд, J=15,4, 8,3 Гц, 1H), 4,56 (ддд, J=10,8, 7,0, 3,5 Гц, 1H), 4,52-4,41 (м, 3H), 4,26 (с, 1H), 3,98-3,70 (м, 7H), 3,63-3,35 (м, 7H), 3,29-3,06 (м, 4H), 2,60-2,18 (м, 2H), 1,29-1,25 (м, 3H).
Пример 255: Синтез (2R)-4-[(2R)-3-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
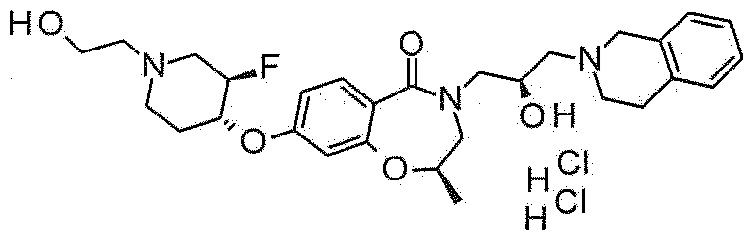
Пример 255-1: Синтез (2R)-4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)]-8-[[(3R,4R)-3-фтор-1-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение, в котором Вос замещена, синтезируют с применением продукта, полученного по методике примеров 140-1-140-5 за исключением того, что [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат используют вместо [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната в качестве исходного материала и способа по методике примера 64 за исключением того, что (S)-трет-бутил 3-фтор-4-метилсульфонилокси-пиперидин-1-карбоксилат используют вместо 4-хлортетрагидропирана. Полученное промежуточное соединение растворяют в метаноле, и туда добавляют 4 N раствор хлористоводородной кислоты растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре до остановки реакции, разбавляют этилдиэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества в форме дигидрохлорида.
Пример 255-2: Синтез (2R)-4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
(2R)-4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)]-8-[[(3R,4R)-3-фтор-1-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 255-1, используют в качестве исходного материала по методике примера 162, и затем указанное в заголовке соединение получают образованием гидрохлорида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,70 (дд, J=8,8, 3,7 Гц, 1H), 7,39-7,20 (м, 4H), 6,96 (д, J=8,9 Гц, 1H), 6,77 (с, 1H), 5,13 (д, J=43,3 Гц, 1H), 4,97 (с, 1H), 4,79 (с, 1H), 4,68 (дд, J=15,3, 7,4 Гц, 1H), 4,55-4,42 (м, 2H), 3,96 (дт, J=14,4, 4,3 Гц, 5H), 3,71 (д, J=14,7 Гц, 3H), 3,64-3,35 (м, 10H), 3,30-3,13 (м, 2H), 2,57-2,20 (м, 2H), 1,36 (д, J=6,3 Гц, 3H).
Пример 256: Синтез 8-[[3,3-дифтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она
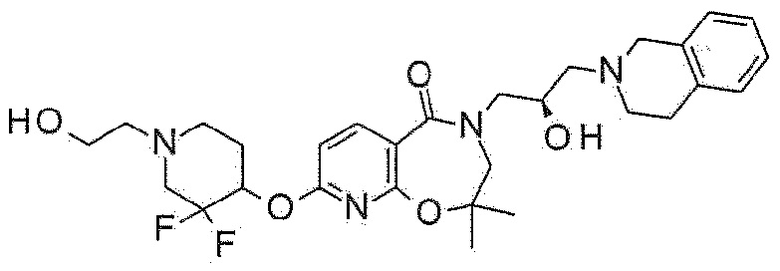
Пример 256-1: Синтез 8-[(3,3-дифтор-4-пиперидил)окси]-2,2-диметил-3,4-дигидропиридо[3,2-f][1,4]оксазепин-5-она
Продукт, полученный заменой 1-[(4-метоксифенил)метиламино]пропан-2-ола на 1-[(4-метоксифенил)метиламино]-2-метилпропан-2-ол в примере 144, используют в качестве исходного материала по методике примеров 144-1-144-4 с получением указанного в заголовке соединения, за исключением того, что трет-бутил 3,3-дифтор-4-гидроксипиперидин-1-карбоксилат используют вместо трет-бутил 4-гидроксипиперидин-1-карбоксилата в примере 144-3.
Пример 256-2: Синтез 8-[[3,3-дифтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2,2-диметил-3,4-дигидропиридо[3,2-f][1,4]оксазепин-5-она
8-[(3,3-Дифтор-4-пиперидил)окси]-2,2-диметил-3,4-дигидропиридо[3,2-f][1,4]оксазепин-5-он, полученный в примере 256-1, используют в качестве исходного материала по методике примера 163 с получением указанного в заголовке соединения, за исключением того, что 2-йодэтанол используют вместо 2-фторэтил пара-толуолсульфоната.
Пример 256-3: Синтез 8-[[3,3-дифтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она
8-[[3,3-Дифтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2,2-диметил-3,4-дигидропиридо[3,2-f][1,4]оксазепин-5-он, полученный в примере 256-2, используют в качестве исходного материала по методике примера 5 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,10 (д, J=8,4 Гц, 1H), 7,18-7,02 (м, 4H), 6,70 (д, J=8,4 Гц, 1H), 5,49-5,36 (м, 1H), 4,27 (с, 1H), 4,11-3,97 (м, 1H), 3,77 (с, 2H), 3,71 (т, J=5,8 Гц, 2H), 3,69-3,58 (м, 2H), 3,44 (дд, J=14,4, 8,9 Гц, 1H), 3,08 (с, 1H), 2,91 (дд, J=16,5, 5,2 Гц, 4H), 2,81 (с, 2H), 2,73-2,54 (м, 5H), 2,23-2,09 (м, 1H, 1,94 (с, 1H), 1,48 (д, J=1,5 Гц, 3H), 1,44 (д, J=1,7 Гц, 3H).
Пример 257: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она

Пример 257-1: Синтез 8-ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
8-Бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (200 мг, 0,464 ммоль), полученный в примере 10-1, трибутил(1-этоксивинил)олово (204 мкл, 0,603 ммоль), тетракис(трифенилфосфин)палладий(0) (27 мг, 0,023 ммоль) добавляют к 4 мл толуола и нагревают до кипения с обратным холодильником в течение одного дня, при перемешивании. После завершения реакции, добавляют 35% водный раствор хлористоводородной кислоты и перемешивают в течение 1 часа, затем подщелачивают водным раствором гидроксида натрия до достижения рН 14, с последующим экстрагированием этилацетатом. Органический слой сушат над безводным сульфатом магния, фильтруют, концентрируют при пониженном давлении и очищают флэш-хроматографией с получением указанного в заголовке соединения (80 мг).
Пример 257-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она
8-Ацетил-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (100 мг, 0,254 ммоль), полученный в примере 257-1, пиперидин (50 мкл, 0,508 ммоль) и изопропоксид титана(IV) (223 мкл, 0,762 ммоль) растворяют в тетрагидрофуране и нагревают до кипения с обратным холодильником в течение 4 часов. Затем, туда добавляют цианоборгидрид натрия (64 мг, 1,016 ммоль) и нагревают до 45°C и перемешивают в течение одного дня. После завершения реакции, реакционный раствор экстрагируют насыщенным водным раствором хлорида натрия и этилацетатом и очищают флэш-хроматографией с получением указанного в заголовке соединения (6 мг).
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,0 Гц, 1H), 7,21-7,00 (м, 6H), 4,49 (т, J=5,1 Гц, 2H), 4,23 (кв, J=7,3, 5,7 Гц, 1H), 3,99 (дд, J=13,9, 3,7 Гц, 1H), 3,81-3,68 (м, 4H), 3,55 (кв, J=6,8 Гц, 1H), 3,47 (дд, J=13,9, 7,6 Гц, 1H), 2,99-2,85 (м, 4H), 2,71-2,62 (м, 2H), 2,56 (с, 2H), 2,51-2,41 (м, 2H), 2,04 (д, J=9,5 Гц, 1H), 1,62 (кв, J=5,9, 5,3 Гц, 4H), 1,43 (д, J=6,8 Гц, 4H).
Пример 258: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(4-гидрокси-1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она
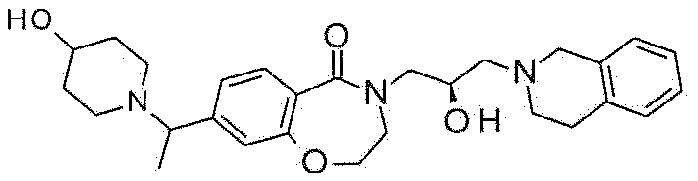
Указанное в заголовке соединение синтезируют по методике примера 257, за исключением того, что 4-гидроксипиперидин используют вместо пиперидина в примере 257-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,0 Гц, 1H), 7,22-7,00 (м, 6H), 4,49 (т, J=5,1 Гц, 2H), 4,25 (дт, J=7,7, 3,7 Гц, 1H), 3,98 (дд, J=13,9, 3,7 Гц, 1H), 3,81 (с, 2H), 3,73 (т, J=5,1 Гц, 2H), 3,64-3,53 (м, 2H), 3,48 (дд, J=13,9, 7,5 Гц, 1H), 2,94 (дп, J=8,9, 4,6, 3,7 Гц, 5H), 2,83-2,73 (м, 1H), 2,73-2,61 (м, 2H), 2,24 (т, J=10,7 Гц, 2H), 1,93-1,79 (м, 2H), 1,70-1,50 (м, 2H), 1,43 (д, J=6,7 Гц, 3H).
Пример 259: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(4-метокси-1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она
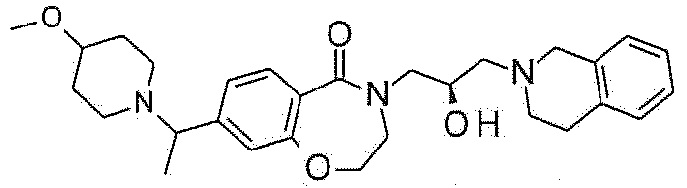
Указанное в заголовке соединение синтезируют по методике примера 257, за исключением того, что 4-метоксипиперидин используют вместо пиперидина в примере 257-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (д, J=8,0 Гц, 1H), 7,20-7,00 (м, 6H), 4,49 (т, J=5,1 Гц, 2H), 4,30-4,19 (м, 1H), 3,98 (дд, J=13,9, 3,7 Гц, 1H), 3,79 (д, J=2,2 Гц, 2H), 3,73 (кв, J=6,0, 5,1 Гц, 2H), 3,57-3,42 (м, 2H), 3,24 (тт, J=8,2, 3,9 Гц, 1H), 2,93 (дт, J=8,0, 4,2 Гц, 5H), 2,76-2,64 (м, 3H), 2,31-2,18 (м, 2H), 1,93 (д, J=11,5 Гц, 2H), 1,62-1,52 (м, 2H), 1,41 (д, J=6,8 Гц, 3H).
Пример 260: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(3-гидрокси-3-метил-пирролидин-1-ил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она
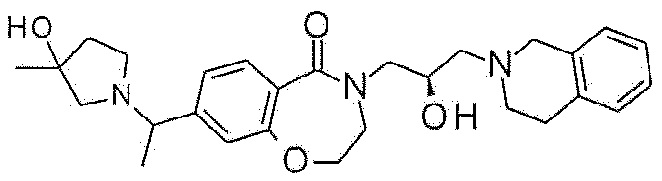
Указанное в заголовке соединение синтезируют по методике примера 257, за исключением того, что 3-метилпирролидин-3-ол используют вместо пиперидина в примере 257-2.
1H ЯМР (400 MГц, Метанол-d4) δ 7,69 (дд, J=8,0, 1,4 Гц, 1H), 7,21 (дд, J=8,1, 1,8 Гц, 1H), 7,16-6,96 (м, 5H), 4,49 (т, J=5,1 Гц, 2H), 4,25 (квд, J=7,6, 4,6 Гц, 1H), 3,98 (дд, J=13,9, 3,7 Гц, 1H), 3,80 (д, J=2,2 Гц, 2H), 3,73 (кв, J=6,5, 5,1 Гц, 2H), 3,52-3,42 (м, 2H), 2,93 (дт, J=10,1, 5,1 Гц, 4H), 2,82-2,49 (м, 6H), 1,89 (тд, J=7,4, 3,2 Гц, 2H), 1,42 (т, J=6,2 Гц, 3H), 1,35 (с, 3H).
Пример 261: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
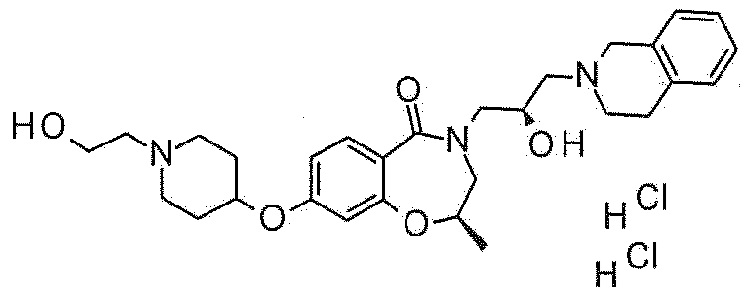
Указанное в заголовке соединение получают образованием гидрохлорида с (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-оном, полученным в примере 219.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (дт, J=9,1, 4,6 Гц, 1H), 7,40-7,18 (м, 4H), 6,95-6,80 (м, 1H), 6,68 (д, J=15,4 Гц, 1H), 4,81-4,62 (м, 4H), 4,47 (дд, J=15,3, 10,2 Гц, 2H), 4,12 (дд, J=10,9, 5,7 Гц, 1H), 4,04-3,80 (м, 5H), 3,78-3,36 (м, 9H), 3,31-3,01 (м, 4H), 2,40 (д, J=14,1 Гц, 1H), 2,23 (д, J=12,5 Гц, 2H), 2,07-1,94 (м, 1H), 1,36 (д, J=6,3 Гц, 3H).
Пример 262: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-метоксиэтил)-4-пиперидил]окси]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она
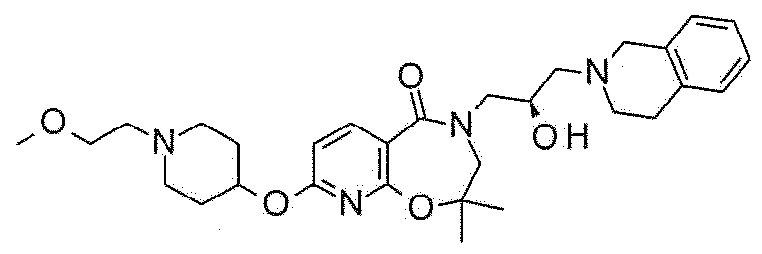
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиперидилокси)-3H-пиридо[3,2-f][1,4]оксазепин-5-он дигидрохлорид используют в качестве исходного материала по методике примера 224 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 8,04 (д, J=8,4 Гц, 1H), 7,16-7,01 (м, 4H), 6,60 (д, J=8,4 Гц, 1H), 5,07 (дт, J=8,3, 4,2 Гц, 1H), 4,32-4,20 (м, 1H), 4,03 (дд, J=13,8, 3,6 Гц, 1H), 3,75 (с, 2H), 3,71-3,60 (м, 2H), 3,57 (т, J=5,6 Гц, 2H), 3,41 (дд, J=13,8, 8,2 Гц, 3H), 3,36 (с, 4H), 2,93 (д, J=5,7 Гц, 2H), 2,91-2,78 (м, 4H), 2,64 (кв, J=5,2, 4,4 Гц, 4H), 2,47 (т, J=9,9 Гц, 2H), 2,12-2,01 (м, 2H), 1,83 (кв, J=16,6, 13,0 Гц, 2H), 1,48 (с, 3H), 1,43 (с, 3H).
Пример 263: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3S)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
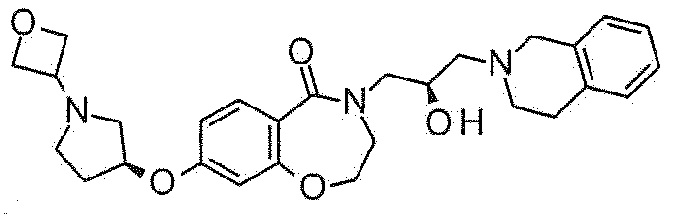
Пример 263-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3S)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный заменой 4-хлортетрагидропирана на (S)-1-(трет-бутоксикарбонил)-3-пирролидинол в примере 64, используют в качестве исходного материала по методике примера 78-1 с получением указанного в заголовке соединения.
Пример 263-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3S)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3S)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 263-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения, за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,19-7,00 (м, 4H), 6,73 (дд, J=8,8, 2,5 Гц, 1H), 6,54 (д, J=2,4 Гц, 1H), 5,02-4,94 (м, 1H), 4,75 (т, J=6,7 Гц, 2H), 4,64 (дт, J=11,8, 6,1 Гц, 2H), 4,48 (т, J=5,0 Гц, 2H), 4,23 (кв, J=7,2, 5,8 Гц, 1H), 3,97 (дд, J=13,9, 3,7 Гц, 1H), 3,82-3,65 (м, 5H), 3,43 (дд, J=13,9, 7,6 Гц, 1H), 3,00-2,87 (м, 5H), 2,87-2,79 (м, 2H), 2,70-2,62 (м, 2H), 2,56 (тд, J=8,5, 6,2 Гц, 1H), 2,38 (дкв, J=14,0, 7,1 Гц, 1H), 2,06-1,95 (м, 1H).
Пример 264: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3S)-1-метилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
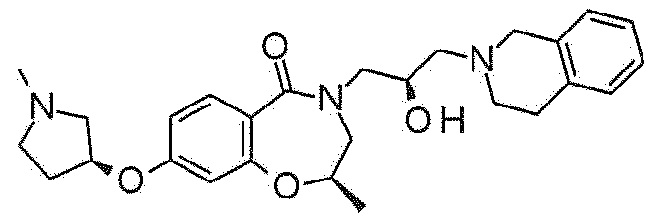
Пример 264-1: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
Указанное в заголовке соединение синтезируют по методике примеров 140-1-140-5, за исключением того, что [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат используют вместо [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната в примере 140-1.
Пример 264-2: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3S)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение синтезируют с применением (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она, полученного в примере 264-1, в качестве исходного материала по методике примера 64 за исключением того, что (S)-1-(трет-бутоксикарбонил)-3-пирролидинол применяют вместо 4-хлортетрагидропирана. Туда медленно добавляют 4 M раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре, разбавляют диэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества.
Пример 264-3: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3S)-1-метилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3S)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 264-2, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,56 (д, J=8,7 Гц, 1H), 7,11-6,92 (м, 4H), 6,67 (дд, J=8,7, 2,4 Гц, 1H), 6,45 (д, J=2,4 Гц, 1H), 4,93 (с, 1H), 4,72 (тд, J=7,2, 3,4 Гц, 1H), 4,23-4,11 (м, 1H), 4,07 (дд, J=13,9, 3,7 Гц, 1H), 3,73 (с, 2H), 3,56 (дд, J=15,6, 3,4 Гц, 1H), 3,42 (дд, J=15,6, 7,6 Гц, 1H), 3,17 (дд, J=13,8, 8,1 Гц, 1H), 3,02-2,79 (м, 7H), 2,68-2,49 (м, 3H), 2,42 (с, 4H), 1,96 (дт, J=14,8, 6,6 Гц, 1H), 1,26 (д, J=6,4 Гц, 3H).
Пример 265: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолинoн-2-ил)-2-гидроксипропил]-8-[(3R)-тетрагидрофуран-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
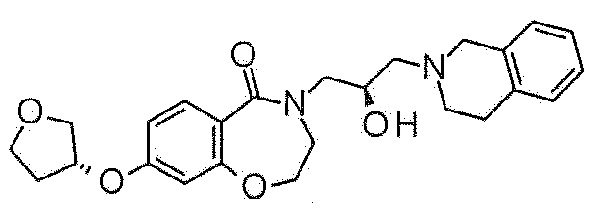
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что [(3S)-тетрагидрофуран-3-ил]метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,7 Гц, 1H), 7,21-6,98 (м, 4H), 6,74 (дд, J=8,8, 2,5 Гц, 1H), 6,56 (д, J=2,4 Гц, 1H), 5,07 (д, J=5,6 Гц, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,24 (с, 1H), 4,04-3,85 (м, 5H), 3,85-3,67 (м, 4H), 3,44 (дд, J=13,8, 7,6 Гц, 1H), 3,03-2,84 (м, 4H), 2,75-2,60 (м, 2H), 2,33-2,23 (м, 1H), 2,16-2,05 (м, 1H).
Пример 266: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолинoн-2-ил)-2-гидроксипропил]-8-[(3S)-тетрагидрофуран-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
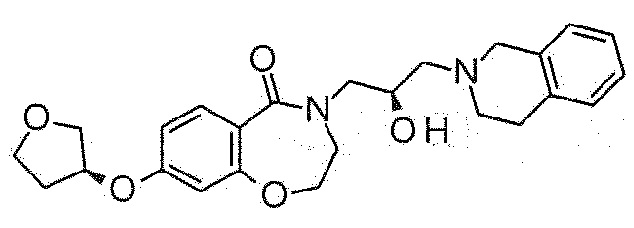
Указанное в заголовке соединение синтезируют по методике примера 64, за исключением того, что [(3R)-тетрагидрофуран-3-ил]метансульфонат используют вместо 4-хлортетрагидропирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,19-6,99 (м, 4H), 6,74 (дд, J=8,8, 2,5 Гц, 1H), 6,56 (д, J=2,4 Гц, 1H), 5,13-5,02 (м, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,23 (кв, J=7,5, 5,9 Гц, 1H), 4,02-3,84 (м, 5H), 3,82-3,69 (м, 4H), 3,44 (дд, J=13,9, 7,6 Гц, 1H), 3,00-2,82 (м, 4H), 2,67 (дд, J=6,2, 2,3 Гц, 2H), 2,36-2,21 (м, 1H), 2,12 (дт, J=12,7, 5,8 Гц, 1H).
Пример 267: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-[(2S)-2-гидроксипропил]-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
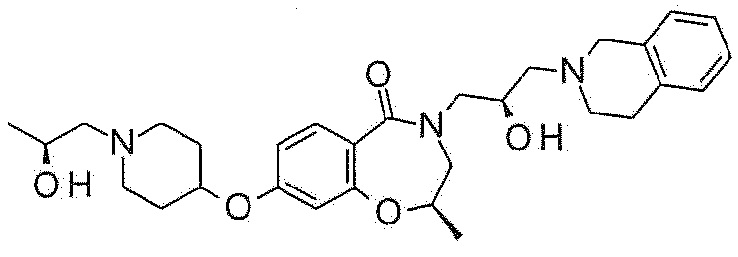
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения, за исключением того, что (S)-2-метоксиран используют вместо 2-метоксирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,7 Гц, 1H), 7,16-6,97 (м, 4H), 6,78 (дд, J=8,7, 2,5 Гц, 1H), 6,56 (д, J=2,4 Гц, 1H), 4,79 (тд, J=7,1, 3,3 Гц, 1H), 4,51 (с, 1H), 4,23 (кв, J=8,0, 5,8 Гц, 1H), 4,15 (дд, J=13,7, 3,7 Гц, 1H), 3,97 (дт, J=12,5, 6,2 Гц, 1H), 3,77 (с, 2H), 3,64 (дд, J=15,6, 3,4 Гц, 1H), 3,49 (дд, J=15,6, 7,5 Гц, 1H), 3,23 (дд, J=13,7, 8,2 Гц, 1H), 2,99-2,79 (м, 6H), 2,70-2,40 (м, 6H), 2,06 (с, 2H), 1,86 (с, 2H), 1,33 (д, J=6,4 Гц, 3H), 1,18 (д, J=6,3 Гц, 3H).
Пример 268: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-[(2R)-2-гидроксипропил]-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
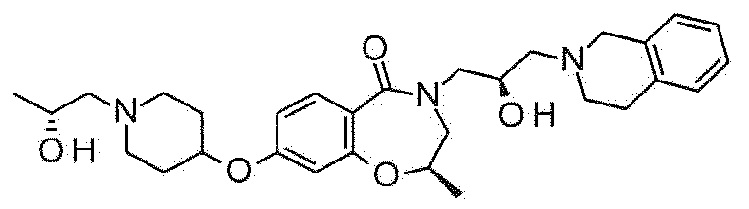
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения, за исключением того, что (R)-2-метоксиран используют вместо 2-метоксирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,7 Гц, 1H), 7,16-6,99 (м, 4H), 6,78 (дд, J=8,8, 2,5 Гц, 1H), 6,56 (д, J=2,4 Гц, 1H), 4,79 (тд, J=7,0, 3,3 Гц, 1H), 4,51 (с, 1H), 4,24 (дт, J=12,8, 6,1 Гц, 1H), 4,15 (дд, J=13,8, 3,6 Гц, 1H), 3,97 (h, J=6,2, 5,5 Гц, 1H), 3,77 (с, 2H), 3,63 (дд, J=15,6, 3,4 Гц, 1H), 3,49 (дд, J=15,6, 7,6 Гц, 1H), 3,23 (дд, J=13,8, 8,1 Гц, 1H), 2,99-2,80 (м, 6H), 2,69-2,40 (м, 6H), 2,05 (д, J=11,0 Гц, 2H), 1,93-1,80 (м, 2H), 1,33 (д, J=6,4 Гц, 3H), 1,18 (д, J=6,2 Гц, 3H).
Пример 269: Синтез 8-[циклопропил(гидрокси)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
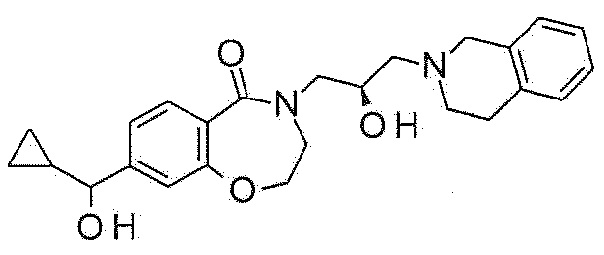
8-(Циклопропанкарбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он (1 эквив.), полученный в примере 216, растворяют в метаноле, и туда добавляют избыток боргидрида натрия. Реакционный раствор перемешивают при комнатной температуре в течение 10 минут и экстрагируют этилацетатом. Экстрагированный органический раствор концентрируют при пониженном давлении и очищают флэш-хроматографией с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,47 (д, J=8,0 Гц, 1H), 7,05 (дд, J=8,1, 1,6 Гц, 1H), 6,97-6,82 (м, 5H), 4,28 (т, J=5,2 Гц, 2H), 4,10-4,00 (м, 1H), 3,84-3,73 (м, 2H), 3,60 (с, 2H), 3,58-3,44 (м, 3H), 3,26 (дд, J=13,9, 7,6 Гц, 1H), 2,74 (дд, J=10,0, 4,5 Гц, 4H), 2,56-2,42 (м, 2H), 0,93 (тдд, J=8,0, 5,4, 3,0 Гц, 1H), 0,48-0,37 (м, 1H), 0,37-0,26 (м, 2H), 0,25-0,15 (м, 1H)
Пример 270: Синтез 8-[циклопентил(гидрокси)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она
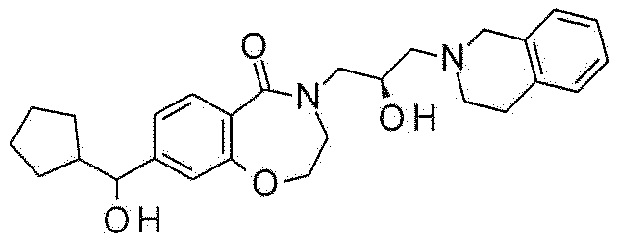
8-(Циклопентанкарбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-он, полученный в примере 217, используют в качестве исходного материала по методике примера 269 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,66 (д, J=8,0 Гц, 1H), 7,22-7,01 (м, 5H), 4,48 (т, J=5,1 Гц, 2H), 4,37 (д, J=8,2 Гц, 1H), 4,25 (с, 1H), 3,99 (дд, J=13,9, 3,7 Гц, 1H), 3,79 (с, 2H), 3,71 (т, J=5,3 Гц, 2H), 3,46 (дд, J=13,9, 7,7 Гц, 1H), 3,01-2,85 (м, 4H), 2,74-2,61 (м, 2H), 2,19 (кв, J=8,2 Гц, 1H), 1,90-1,80 (м, 1H), 1,74-1,46 (м, 6H), 1,44-1,34 (м, 1H), 1,30-1,16 (м, 1H).
Пример 271: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
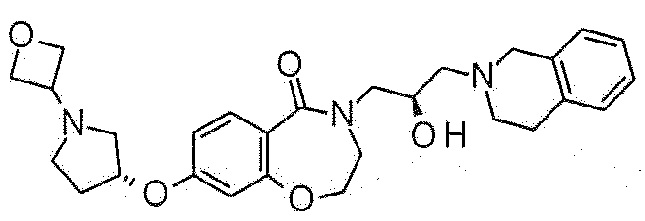
Пример 271-1: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Продукт, полученный заменой 4-хлортетрагидропирана на (R)-1-(трет-бутоксикарбонил)-3-пирролидинол в примере 64, используют в качестве исходного материала по методике примера 78-1 с получением указанного в заголовке соединения.
Пример 271-2: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 271-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,8 Гц, 1H), 7,16-7,02 (м, 4H), 6,73 (дд, J=8,8, 2,5 Гц, 1H), 6,54 (д, J=2,4 Гц, 1H), 4,98 (тд, J=6,1, 5,3, 2,8 Гц, 1H), 4,75 (т, J=6,7 Гц, 2H), 4,64 (дт, J=11,8, 6,1 Гц, 2H), 4,48 (т, J=4,9 Гц, 2H), 4,23 (квд, J=7,2, 3,7 Гц, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,80-3,71 (м, 5H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 2,98-2,80 (м, 7H), 2,69-2,62 (м, 2H), 2,56 (ддд, J=9,2, 7,8, 6,1 Гц, 1H), 2,38 (дкв, J=14,0, 7,1 Гц, 1H), 2,01 (дт, J=13,7, 4,4 Гц, 1H).
Пример 272: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(2-метоксиэтил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
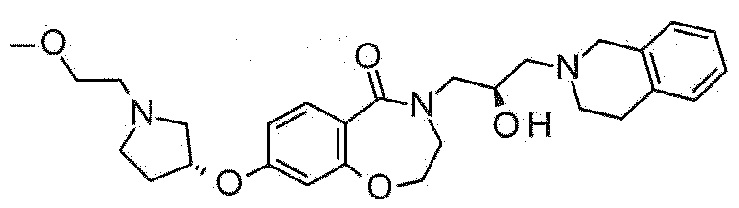
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 271-1, используют в качестве исходного материала по методике примера 224 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,68 (д, J=8,7 Гц, 1H), 7,18-7,00 (м, 4H), 6,71 (дд, J=8,8, 2,5 Гц, 1H), 6,53 (д, J=2,4 Гц, 1H), 4,95 (ддд, J=7,7, 5,7, 2,9 Гц, 1H), 4,48 (т, J=5,0 Гц, 2H), 4,23 (тдд, J=7,6, 6,3, 5,2, 3,7 Гц, 1H), 3,98 (дд, J=13,9, 3,6 Гц, 1H), 3,79-3,70 (м, 4H), 3,56 (т, J=5,6 Гц, 2H), 3,42 (дд, J=13,9, 7,7 Гц, 1H), 3,36 (с, 3H), 2,98-2,86 (м, 6H), 2,75 (ткв, J=12,7, 6,4, 5,4 Гц, 2H), 2,66-2,60 (м, 2H), 2,37 (дтд, J=13,6, 7,6, 5,9 Гц, 1H), 1,96 (дтд, J=13,2, 6,8, 6,4, 2,2 Гц, 1H).
Пример 273: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-1-метилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
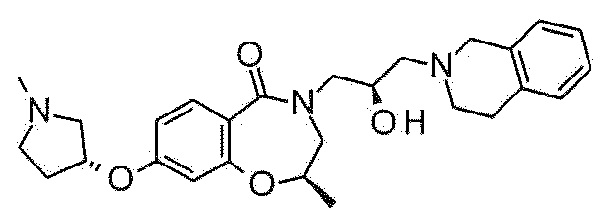
Пример 273-1: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида
Промежуточное соединение синтезируют с применением (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-гидрокси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она, полученного в примере 264-1, в качестве исходного материала по методике примера 64 за исключением того, что (R)-1-(трет-бутоксикарбонил)-3-пирролидинол используют вместо 4-хлортетрагидропирана. Туда медленно добавляют 4 M раствор хлористоводородной кислоты, растворенный в 1,4-диоксане. Реакционный раствор перемешивают при комнатной температуре, разбавляют диэтиловым эфиром и фильтруют с получением указанного в заголовке соединения в виде белого твердого вещества.
Пример 273-2: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-1-метилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 273-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,55 (д, J=8,7 Гц, 1H), 7,10-6,93 (м, 4H), 6,67 (дд, J=8,7, 2,5 Гц, 1H), 6,44 (д, J=2,5 Гц, 1H), 4,92 (д, J=6,9 Гц, 1H), 4,72 (тд, J=7,0, 3,3 Гц, 1H), 4,16 (дт, J=8,2, 4,1 Гц, 1H), 4,06 (дд, J=13,8, 3,6 Гц, 1H), 3,72 (с, 2H), 3,56 (дд, J=15,6, 3,4 Гц, 1H), 3,42 (дд, J=15,6, 7,6 Гц, 1H), 3,17 (дд, J=13,8, 8,1 Гц, 1H), 2,88 (ддд, J=19,7, 9,7, 6,8 Гц, 7H), 2,65-2,46 (м, 3H), 2,41 (с, 4H), 2,00-1,91 (м, 1H), 1,25 (д, J=6,4 Гц, 3H).
Пример 274: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(2-метоксиэтил)пирролидин-3-ил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она
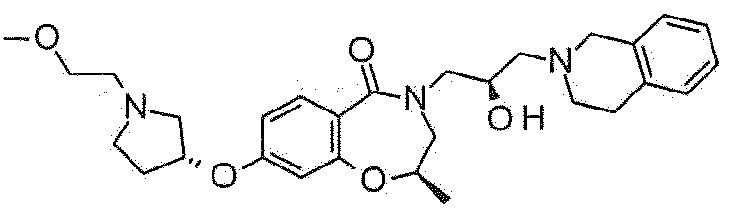
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 273-1, используют в качестве исходного материала по методике примера 224 с получением указанного в заголовке соединения.
1H ЯМР (400 MГц, Метанол-d4) δ 7,63 (д, J=8,7 Гц, 1H), 7,17-7,00 (м, 4H), 6,73 (дд, J=8,7, 2,5 Гц, 1H), 6,50 (д, J=2,4 Гц, 1H), 4,95 (ддт, J=7,7, 5,3, 2,5 Гц, 1H), 4,79 (тд, J=7,1, 3,3 Гц, 1H), 4,28-4,20 (м, 1H), 4,15 (дд, J=13,8, 3,6 Гц, 1H), 3,77 (с, 2H), 3,63 (дд, J=15,6, 3,4 Гц, 1H), 3,56 (т, J=5,6 Гц, 2H), 3,49 (дд, J=15,6, 7,5 Гц, 1H), 3,36 (с, 3H), 3,23 (дд, J=13,8, 8,2 Гц, 1H), 2,94 (дддд, J=21,2, 15,4, 9,2, 3,8 Гц, 7H), 2,84-2,70 (м, 2H), 2,68-2,55 (м, 3H), 2,37 (дтд, J=13,6, 7,6, 5,9 Гц, 1H), 1,97 (дкв, J=9,9, 7,4 Гц, 1H), 1,33 (д, J=6,4 Гц, 3H).
Пример 275: Синтез 4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-)-2-гидроксипропил]-8-[[1-(3,3,3-трифтор-2-гидроксипропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
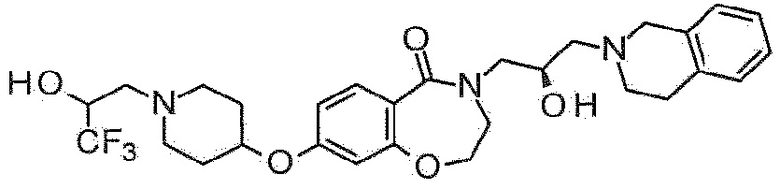
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 78-1, используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения, за исключением того, что 2-(трифторметил)оксиран используют вместо 2-метоксирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,67 (д, J=8,8 Гц, 1H), 7,17-7,02 (м, 4H), 6,76 (дд, J=8,8, 2,5 Гц, 1H), 6,58 (д, J=2,4 Гц, 1H), 4,48 (дт, J=9,9, 4,4 Гц, 3H), 4,27-4,14 (м, 2H), 3,97 (дд, J=13,9, 3,6 Гц, 1H), 3,78-3,70 (м, 4H), 3,43 (дд, J=13,9, 7,7 Гц, 1H), 2,93 (д, J=5,5 Гц, 2H), 2,91-2,81 (м, 4H), 2,70-2,59 (м, 4H), 2,52 (д, J=10,5 Гц, 2H), 2,03 (с, 2H), 1,84 (кв, J=9,9, 8,8 Гц, 2H).
Пример 276: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-)-2-гидроксипропил]-2-метил-8-[[1-(3,3,3-трифтор-2-гидроксипропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она
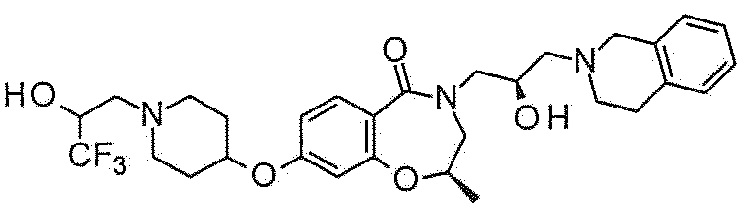
Продукт, полученный заменой [2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфоната на [(1S)-2-(трет-бутоксикарбониламино)-1-метилэтил]метансульфонат в примере 140, используют в качестве исходного материала по методике примера 212 с получением указанного в заголовке соединения, за исключением того, что 2-(трифторметил)оксиран используют вместо 2-метоксирана.
1H ЯМР (400 MГц, Метанол-d4) δ 7,62 (д, J=8,7 Гц, 1H), 7,20-6,98 (м, 4H), 6,78 (дд, J=8,8, 2,5 Гц, 1H), 6,55 (д, J=2,4 Гц, 1H), 4,78 (дд, J=6,8, 3,3 Гц, 1H), 4,53-4,44 (м, 1H), 4,28-4,09 (м, 3H), 3,78 (д, J=11,9 Гц, 2H), 3,63 (дд, J=15,7, 3,4 Гц, 1H), 3,49 (дд, J=15,5, 7,6 Гц, 1H), 3,24 (дд, J=13,7, 8,1 Гц, 1H), 3,00-2,80 (м, 6H), 2,64 (дт, J=7,7, 4,5 Гц, 4H), 2,52 (кв, J=10,3 Гц, 2H), 2,03 (с, 2H), 1,85 (д, J=10,5 Гц, 2H), 1,33 (д, J=6,4 Гц, 3H).
Пример 277: Синтез (2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она
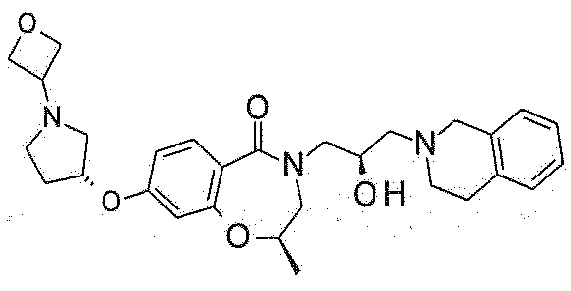
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-он дигидрохлорид, полученный в примере 273-1, используют в качестве исходного материала по методике примера 87 с получением указанного в заголовке соединения за исключением того, что оксетан-3-он используют вместо параформальдегида.
1H ЯМР (400 MГц, Метанол-d4) δ 7,64 (д, J=8,7 Гц, 1H), 7,15-7,01 (м, 4H), 6,73 (дд, J=8,7, 2,5 Гц, 1H), 6,51 (д, J=2,4 Гц, 1H), 4,96 (ддт, J=8,2, 5,4, 2,5 Гц, 1H), 4,76 (дт, J=23,0, 6,8 Гц, 3H), 4,63 (дт, J=11,8, 6,1 Гц, 2H), 4,23 (тд, J=7,9, 4,2 Гц, 1H), 4,14 (дд, J=13,8, 3,6 Гц, 1H), 3,79-3,69 (м, 3H), 3,62 (дд, J=15,6, 3,4 Гц, 1H), 3,48 (дд, J=15,6, 7,5 Гц, 1H), 3,21 (дд, J=13,8, 8,2 Гц, 1H), 2,98-2,76 (м, 7H), 2,66-2,59 (м, 2H), 2,54 (ддд, J=9,3, 7,8, 6,1 Гц, 1H), 2,36 (дкв, J=14,0, 7,1 Гц, 1H), 2,07-1,94 (м, 1H), 1,32 (д, J=6,4 Гц, 3H).
Экспериментальный пример
Способ для измерения ферментной активности
Анализ in vitro: ферментный комплекс PRMT5-MEP50, кофактор S-аденозилметионин (SAM) и пептид гистона H4 подвергают взаимодействию in vitro, и измеряют метилирование аргинина (H4R3), который является третьей аминокислотой гистона H4, для измерения активности фермента PRMT5.
Реагенты: ферментный комплекс PRMT5-MEP50 (каталожный № 51045), блокирующий буфер (52100-B), реакционный буфер гистонметилтрансферазы 2 (4х буфер для анализа HMT 2, каталожный № 52170) и первичное антитело (первичное антитело 4-3), каталожный № по каталогу 52150) приобретают у BPS Bioscience (USA). Пептид гистона Н4 (1-20 аминокислот) изготавливают на заказ компанией Komabiotech (Korea) и используют. S-аденозилметионин приобретают у NEB (New England Biolabs, USA, каталожный № B9003S). Планшеты для покрытия пептидом гистона H4, буфером для промывания и реагентом для проявления цвета приобретают у следующих поставщиков: планшет (Immobilizer™-Amino Plate, NUNC, Denmark, каталожный № 436023), карбонатно-бикарбонатный буфер (Sigma-Aldrich, USA, каталожный № C3041), буфер для промывания (10х TBST, Biosesang, Korea, каталожный № T2005), субстрат TMB ELISA (Abcam, UK, каталожный № ab210902), антитело, конъюгированное с пероксидазой хрена (HRP) (Abcam, UK, каталожный № ab6721).
Методика эксперимента: Пептид гистона Н4 разводят карбонатно-бикарбонатным буфером и доводят до концентрации 100 мкг/мл, затем распределяют в планшет по 100 мкл и подвергают реакции при 37°C в течение 1 часа. Ферментный комплекс PRMT5-MEP50 и S-аденозилметионин разводят реакционным буфером гистон-метилтрансферазы для получения 5 мкг/мл и 2 мкМ, соответственно, и затем 20 мкл ферментного комплекса PRMT5-MEP50 и 25 мкл S-аденозилметионина распределяют в подготовленный выше планшет. Туда добавляют 5 мкл соединения, разведенного 10% раствором диметилсульфоксида и подвергают реакции при комнатной температуре в течение 2 часов (конечный объем=50 мкл). Концентрацию соединения разводят 1:5 от 10 мкМ до самой низкой концентрации 0,128 нМ, и 8 точек применяют для тестирования. После приготовления первичных антител путем разведения 1:2000 блокирующим буфером, в планшет добавляют 100 мкл и подвергают реакции при комнатной температуре в течение 1 часа. После приготовления антител, конъюгированных с пероксидазой хрена, путем разведения 1:10000 блокирующим буфером, в планшет добавляют 100 мкл и подвергают реакции при комнатной температуре в течение 1 ч. Добавляют 100 мкл субстрата ТМВ и подвергают реакции в течение 3 минут при комнатной температуре, и затем добавляют 100 мкл 1 N серной кислоты для завершения реакции. Затем измеряют абсорбцию при 450 нм для расчета значения IC50 соединения. (+++: от 1 до 100 нМ, ++: от более чем 100 до 1000 нМ, +: от более чем 1000 до 10000 нМ).
[Таблица 2]
Тестирование in vivo активности ингибирования мишени
После подкожной имплантации опухолевых клеток U87MG голым мышам, перорально вводят ингибитор PRMT5 (25 или 50 мг/кг) 1-2 раза в сутки в течение одной недели, и затем измеряют степень снижения уровня SDMA в опухоли.
Реагенты: раствор Бредфорда (каталожный № 500-0006) приобретают у Bio-rad (USA), антитело SDMA (каталожный № 13222s) приобретают у Cell Signaling Technology (USA), антитело SmD3 (каталожный № ap12451a) приобретают от Abgent (USA), и вторичное антитело (каталожный № ab6721) и субстрат ТМВ (каталожный № ab210902) приобретают у Abcam (UK).
Методика эксперимента: Опухолевые ткани, трансплантированные мышам, иссекают, клетки лизируют, и затем количественно определяют с раствором Бредфорда. 5-10 мкг белка на образец разводят карбонатно-бикарбонатным буфером и распределяют в 96-луночный планшет и подвергают реакции при комнатной температуре в течение 2 часов. После промывания 3 раза фосфатно-солевым буфером (PBST), содержащим 0,05% Tween-20, добавляют 200 мкл PBST, содержащего 5% бычьего сывороточного альбумина (BSA-PBST), и подвергают реакции при комнатной температуре в течение 2 часов. После промывания 3 раза PBST, антитело SDMA и антитело SmD3 разводят в BSA-PBST, и 100 мкл каждого из них распределяют в планшет и подвергают реакции при 4°C в течение ночи. После промывания 3 раза PBST на следующий день, добавляют 100 мкл вторичного антитела, разведенного в BSA-PBST, и подвергают реакции при комнатной температуре в течение 1 часа. После промывания 3 раза PBST, добавляют 100 мкл субстрата ТМВ и подвергают реакции при комнатной температуре в течение 10-20 минут, и 100 мкл 1N раствор серной кислоты добавляют для прекращения реакции. Затем измеряют абсорбцию при 450 нм для расчета степени ингибирования SDMA соединением (+++: более 70%, ++: более 30% и 70% или менее, +: 30% или менее)
[Таблица 3]
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТА АДЕНОЗИНОВОГО РЕЦЕПТОРА A2a И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2022 |
|
RU2840068C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗО[1,2-A]ПИРИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2017 |
|
RU2725147C1 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОПИРИДИНА И ИХ ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2017 |
|
RU2722594C1 |
| ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ IRAK И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2743360C2 |
| НОВОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ | 2019 |
|
RU2792163C2 |
| СОЕДИНЕНИЯ, ЯВЛЯЮЩИЕСЯ АНТАГОНИСТАМИ А3-АДЕНОЗИНОВОГО РЕЦЕПТОРА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2737157C2 |
| ЗАМЕЩЕННЫЕ ХРОМАНЫ | 2015 |
|
RU2718060C2 |
| АНТАГОНИСТЫ ЕР4 | 2016 |
|
RU2761341C2 |
| ПРОИЗВОДНЫЕ БЕНЗОКСАЗЕПИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ И ИХ ПРИМЕНЕНИЕ | 2004 |
|
RU2337100C2 |
| СОЕДИНЕНИЕ, СОДЕРЖАЩЕЕ ОКСАДИАЗОЛ, И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2019 |
|
RU2789456C2 |
Изобретение относится к соединению, представленному Формулой 1, или его оптическому изомеру, или стереоизомеру, или его фармацевтически приемлемой соли, которые ингибируют протеинаргининметилтрансферазу 5 (PRMT5) и могут найти применение для профилактики или лечения заболевания, связанного с ингибированием PRMT5. В Формуле 1 X1 и X2 каждый независимо представляет собой СН или N; Y представляет собой CH2, O или NH, когда n равно 0; Y представляет собой CH или N, когда n равно 1; Z представляет собой CH2 или CH, когда m равно 0; Z представляет собой CH или C, когда m равно 1; Z представляет собой C, когда m равно 2; n представляет собой целое число 0 или 1; m представляет собой целое число 0-2;  представляет собой одинарную связь; R1 представляет собой -D-R10; где D представляет собой прямую связь, -O-, -C(=O)-, -C≡C- или -CR11R12-; R10 представляет собой водород, галоген, гидрокси, циано, C1-C7алкил, гидроксиC1-C7алкил, галогенC1-C7алкил, галогенC1-C7алкилсульфонат, ди(C1-C7)алкиламино, C1-C7алкиламиноC1-C7алкил, ди(C1-C7алкил)аминоC1-C7алкил, ди(C1-C7алкил)аминокарбонилC1-C7алкил, насыщенный или ненасыщенный C3-C10карбоциклил и т.д.; R11 и R12 каждый независимо представляет собой водород, гидрокси или C1-C7алкил; R2 представляет собой водород или C1-C7алкил; R3 представляет собой водород или C1-C7алкил; R4, R5, R6 и R7 каждый независимо представляет собой водород или C1-C7алкил; R8 представляет собой водород, C1-C7алкил или C1-C7алкокси и R9 представляет собой водород, галоген или C1-C7алкил. Изобретение относится также к фармацевтической композиции, содержащей указанное соединение. 2 н. и 16 з.п. ф-лы, 3 табл., 277 пр.
представляет собой одинарную связь; R1 представляет собой -D-R10; где D представляет собой прямую связь, -O-, -C(=O)-, -C≡C- или -CR11R12-; R10 представляет собой водород, галоген, гидрокси, циано, C1-C7алкил, гидроксиC1-C7алкил, галогенC1-C7алкил, галогенC1-C7алкилсульфонат, ди(C1-C7)алкиламино, C1-C7алкиламиноC1-C7алкил, ди(C1-C7алкил)аминоC1-C7алкил, ди(C1-C7алкил)аминокарбонилC1-C7алкил, насыщенный или ненасыщенный C3-C10карбоциклил и т.д.; R11 и R12 каждый независимо представляет собой водород, гидрокси или C1-C7алкил; R2 представляет собой водород или C1-C7алкил; R3 представляет собой водород или C1-C7алкил; R4, R5, R6 и R7 каждый независимо представляет собой водород или C1-C7алкил; R8 представляет собой водород, C1-C7алкил или C1-C7алкокси и R9 представляет собой водород, галоген или C1-C7алкил. Изобретение относится также к фармацевтической композиции, содержащей указанное соединение. 2 н. и 16 з.п. ф-лы, 3 табл., 277 пр.
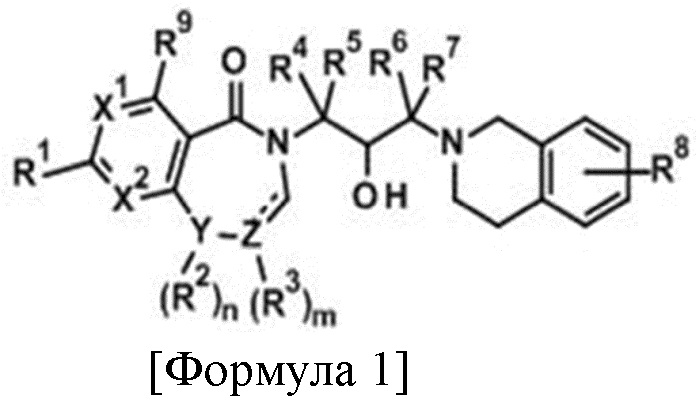
1. Соединение, представленное следующей Формулой 1, или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль:
[Формула 1]
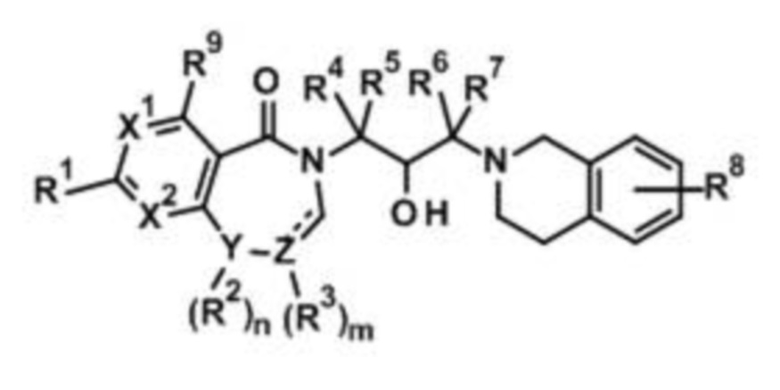 ,
,
где X1 и X2 каждый независимо представляет собой СН или N;
Y представляет собой CH2, O или NH, когда n равно 0; Y представляет собой CH или N, когда n равно 1;
Z представляет собой CH2 или CH, когда m равно 0; Z представляет собой CH или C, когда m равно 1; Z представляет собой C, когда m равно 2;
n представляет собой целое число 0 или 1;
m представляет собой целое число 0-2;
 представляет собой одинарную связь;
представляет собой одинарную связь;
R1 представляет собой -D-R10; где D представляет собой прямую связь, -O-, -C(=O)-, -C≡C- или -CR11R12-; R10 представляет собой водород, галоген, гидрокси, циано, C1-C7алкил, гидроксиC1-C7алкил, галогенC1-C7алкил, галогенC1-C7алкилсульфонат, ди(C1-C7)алкиламино, C1-C7алкиламиноC1-C7алкил, ди(C1-C7алкил)аминоC1-C7алкил, ди(C1-C7алкил)аминокарбонилC1-C7алкил, насыщенный или ненасыщенный C3-C10карбоциклил, насыщенный или ненасыщенный 4-10-членный гетероциклил, насыщенный или ненасыщенный C3-C10карбоциклилC1-C7алкил или насыщенный или ненасыщенный 4-10-членный гетероциклил-C1-C7алкил; R11 и R12 каждый независимо представляет собой водород, гидрокси или C1-C7алкил; карбоцикл или гетероцикл может быть замещен одним или несколькими заместителями, выбранными из гидрокси, галогена, оксо, формила (-CHO), нитрила, C1-C7алкила, C1-C7алкокси, гидроксиC1-C7алкила, гидроксигалогенC1-C7алкила, C1-C7алкоксиC1-C7алкила, галогенC1-C7алкила, нитрилC1-C7алкила, C1-C7алкилкарбонила, C1-C7алкилтиокарбонила, C1-C7алкоксикарбонила, галогенC1-C7алкилкарбонила, C3-C10карбоциклила, C3-C10карбоциклилкарбонила, (C1-C7алкил)(галогенC1-C7алкил)амино, (C1-C7алкил)(4-10-членный гетероциклил)амино, 4-10-членного гетероциклила и 4-10-членного гетероциклилC1-C7алкила;
R2 представляет собой водород или C1-C7алкил;
R3 представляет собой водород или C1-C7алкил;
R4, R5, R6 и R7 каждый независимо представляет собой водород или C1-C7алкил;
R8 представляет собой водород, C1-C7алкил или C1-C7алкокси и
R9 представляет собой водород, галоген или C1-C7алкил,
где гетероциклил имеет от 1 до 8 гетероатомов, выбранных из группы, состоящей из азота (N), кислорода (О) и серы (S).
2. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что R10 представляет собой галоген, C1-C7алкил, гидрокси-C1-C7алкил, галоген-C1-C7алкил, насыщенный или ненасыщенный C3-C10карбоциклил, насыщенный или ненасыщенный 4-10-членный гетероциклил или насыщенный или ненасыщенный 4-10-членный гетероциклил-алкил.
3. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, оксо, формила, нитрила, C1-C7алкила, C1-C7алкокси, гидрокси-C1-C7алкила, гидроксигалоген-C1-C7алкила, C1-C7алкокси-C1-C7алкила, галоген-C1-C7алкила, нитрил-C1-C7алкила, C1-C7алкилкарбонила, C1-C7алкилтиокарбонила, C1-C7алкоксикарбонила, галоген-C1-C7алкилкарбонила, насыщенного или ненасыщенного C3-C10карбоциклила, насыщенного или ненасыщенного C3-C10 карбоциклилкарбонила, (C1-C7 алкил)(галоген-C1-C7алкил)амино, (C1-C7алкил)(насыщенный или ненасыщенный 4-10-членный гетероциклил)амино, насыщенного или ненасыщенного 4-10-членного гетероциклила и насыщенного или ненасыщенного 4-10-членного гетероциклил-C1-C7алкила.
4. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 3, отличающееся тем, что карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, формила, C1-C7алкила, гидрокси-C1-C7алкила, C1-C7алкокси-C1-C7алкила, галоген-C1-C7алкила, C1-C7алкилкарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7алкилкарбонила, насыщенного или ненасыщенного C3-C10 карбоциклила, насыщенного или ненасыщенного C3-C10карбоциклилкарбонила, (C1-C7алкил)(галоген-C1-C7алкил)амино, (C1-C7алкил)(насыщенный или ненасыщенный 4-10-членный гетероциклил)амино и насыщенного или ненасыщенного 4-10-членного гетероциклил-C1-C7алкила.
5. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что гетероцикл может быть замещен 1 или 2 заместителями, выбранными из гидрокси, галогена, формила, C1-C7алкила, гидрокси-C1-C7алкила, C1-C7алкокси-C1-C7алкила, галоген-C1-C7алкила, C1-C7алкилкарбонила, C1-C7алкоксикарбонила, галоген-C1-C7алкилкарбонила, насыщенного или ненасыщенного C3-C10карбоциклила, насыщенного или ненасыщенного C3-C10карбоциклилкарбонила и насыщенного или ненасыщенного 4-10-членного гетероциклил-C1-C7алкила.
6. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что карбоцикл может быть замещен 1 или 2 заместителями, выбранными из галоген-C1-C7алкила, (C1-C7алкил)(галоген-C1-C7алкил)амино и (C1-C7алкил)(насыщенный или ненасыщенный 4-10-членный гетероциклил)амино.
7. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что R1 представляет собой -D-R10; отличающееся тем, что D представляет собой прямую связь; R10 представляет собой водород, галоген, циано, C1-C7алкил, галоген-C1-C7алкил, ди(C1-C7алкил)амино-C1-C7алкил, насыщенный или ненасыщенный 4-10-членный гетероциклил, насыщенный или ненасыщенный C3-C10карбоциклил или насыщенный или ненасыщенный 4-10-членный гетероциклил-алкил; и гетероцикл может быть замещен 1 или 2 заместителями, выбранными из гидрокси, галогена, формила, C1-C7алкила, C1-C7алкокси, гидрокси-C1-C7алкила, галоген-C1-C7алкила, нитрил-C1-C7алкила, C1-C7алкилкарбонила, C1-C7алкокси-C1-C7алкила, C1-C7алкоксикарбонила, галоген-C1-C7алкилкарбонила и насыщенного или ненасыщенного 4-10-членного гетероциклила.
8. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по любому из пп. 1-7, отличающееся тем, что гетероцикл представляет собой насыщенный или ненасыщенный 4-8-членный углеводород, имеющий 1 или 2 гетероатома, выбранных из N и O.
9. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по любому из пп. 1-7, отличающееся тем, что гетероцикл выбран из группы, состоящей из тетрагидропиридина, дигидропиридина, пиперидина, дигидропирана, тетрагидропирана, пирролидина, 2-окса-6-азаспирогептана, азетидина, морфолина, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррола, оксазепана, 2-окса-5-азабицикло[2,2,1]гептана, пиридила, тетрагидрофурана, 8-азабицикло[3,2,1]октана, пиперазина, 2-азаспиро[3,3]гептана, 2-окса-7-азаспиро[3,4]октана, 2-азабицикло[2,2,1]гептана, 3-окса-8-азабицикло[3,2,1]октана, 3,4-дигидро-1H-пирроло[1,2-a]пиразина, 3,4,6,7,8,8a-гексагидро-1H-пирроло[1,2-a]пиразина, пиримидина, пиразола, 2-окса-7-азаспиро[3,5]нонана и оксетана.
10. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 9, отличающееся тем, что гетероцикл выбран из группы, состоящей из тетрагидропиридина, дигидропиридина, пиперидина, тетрагидропирана, пирролидина, 2-окса-6-азаспирогептана, азетидина, морфолина, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррола, пиридила, 8-азабицикло[3,2,1]октана, пиперазина, 2-азаспиро[3,3]гептана, пиразола и оксетана.
11. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по любому из пп. 1-7, отличающееся тем, что карбоцикл выбран из группы, состоящей из циклогексана, циклогексена, циклопропана, циклобутана и циклопентана.
12. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что D представляет собой прямую связь, -O-, -C(=O)- или -C≡C-; R10 представляет собой галоген, C1-C7алкил, гидрокси-C1-C7алкил, галоген-C1-C7алкил, насыщенный или ненасыщенный C3-C10карбоциклил, насыщенный или ненасыщенный 4-10-членный гетероциклил или насыщенный или ненасыщенный 4-10-членный гетероциклил-алкил; карбоцикл или гетероцикл может быть замещен 1-5 заместителями, выбранными из гидрокси, галогена, формила, C1-C7алкила, гидрокси-C1-C7алкила, C1-C7алкокси-C1-C7алкила, галоген-C1-C7алкила, C1-C7алкилкарбонила, C1-C7 алкоксикарбонила, галоген-C1-C7алкилкарбонила, насыщенного или ненасыщенного C3-C10карбоциклила, насыщенного или ненасыщенного C3-C10карбоциклилкарбонила, (C1-C7алкил)(галоген-C1-C7алкил)амино, (C1-C7алкил)(насыщенный или ненасыщенный 4-10-членный гетероциклил)амино и насыщенного или ненасыщенного 4-10-членного гетероциклил-C1-C7алкила; гетероцикл выбран из группы, состоящей из тетрагидропиридина, дигидропиридина, пиперидина, тетрагидропирана, пирролидина, 2-окса-6-азаспирогептана, азетидина, морфолина, 3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррола, пиридила, 8-азабицикло[3,2,1]октана, пиперазина, 2-азаспиро[3,3]гептана, пиразола и оксетана и карбоцикл выбран из группы, состоящей из циклогексана, циклогексена и циклопропана.
13. Соединение или его оптический изомер, или стереоизомер, или его фармацевтически приемлемая соль по п. 1, отличающееся тем, что соединение выбрано из группы, состоящей из:
4-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-метокси-2,3-дигидро-1,4-бензоксазепин-5-она;
2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-метокси-4,5-дигидро-3H-2-бензазепин-1-она;
2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-гидрокси-4,5-дигидро-3H-2-бензазепин-1-она;
2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-(трифторметокси)-4,5-дигидро-3H-2-бензазепин-1-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(трифторметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-(трифторметокси)-4,5-дигидро-3H-2-бензазепин-1-она;
2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-7-этокси-4,5-дигидро-3H-2-бензазепин-1-она;
[2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-оксо-4,5-дигидро-3H-2-бензазепин-7-ил] трифторметансульфоната;
2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-оксо-4,5-дигидро-3H-2-бензазепин-7-карбонитрила;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-пропил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-изобутил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,3,3-трифторпропил)-2,3-дигидро-1,4-бензоксазепин-5-она;
трет-бутил 4-[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]-3,6-дигидро-2H-пиридин-1-карбоксилата;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,2,3,6-тетрагидропиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(1-ацетил-3,6-дигидро-2H-пиридин-4-ил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(1-ацетил-4-пиперидил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-этил-3,6-дигидро-2H-пиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-изопропил-3,6-дигидро-2H-пиридин-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,6-дигидро-2H-пиран-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-тетрагидропиран-4-ил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(морфолинометил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-пиперидилметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пирролидин-1-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(диметиламино)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(диэтиламинометил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метил-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-окса-6-азаспиро[3,3]гептан-6-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-метоксиазетидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-метилморфолин-4-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(4,4-дифтор-1-пиперидил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-фтор-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3,5-диметил-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррол-2-илметил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-гидроксипирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2R)-2-метилпирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-(гидроксиметил)-1-пиперидил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метокси-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,4-оксазепан-4-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-гидрокси-3-метил-пирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-(гидроксиметил)морфолин-4-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(3,3-дифтор-1-пиперидил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-гидрокси-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-гидрокси-1-пиперидил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2S)-2-(гидроксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2R)-2-(гидроксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-этилпирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2S)-2-(метоксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2R)-2-(метоксиметил)пирролидин-1-ил]метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фторпирролидин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(3,3-дифторпирролидин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(4-ацетилпиперазин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метилпиперазин-1-ил)метил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-окса-5-азабицикло[2,2,1]гептан-5-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиридилметокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиридилметокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-фтор-4-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(2,6-дихлор-4-пиридил)метокси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(2,3-дифтор-4-пиридил)метокси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(6-фтор-3-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(5-фтор-2-пиридил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-тетрагидропиран-4-илокси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(тетрагидропиран-2-илметокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(циклогексилметокси)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(тетрагидрофуран-2-илметокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(1-ацетил-4-пиперидил)метокси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2,2,2-трифторэтокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(диметиламино)этокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-морфолиноэтокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(2-оксопирролидин-1-ил)этокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-пиридилокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(6-оксо-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
трет-бутил 4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]пиперидин-1-карбоксилата;
8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(1-ацетил-3-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(1-ацетилпирролидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(3R)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(3S)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-пропаноилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[1-(циклопропанкарбонил)азетидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
метил 3-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоксазепин-8-ил]окси]азетидин-1-карбоксилата;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-изопропил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(1-циклопропил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(1-циклобутил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(оксетан-3-ил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-метилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-этилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-изопропилазетидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(оксетан-3-ил)азетидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этилазетидин-3-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-метилпирролидин-3-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-этилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-пиридилокси)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(2S)-1-изопропилпирролидин-2-ил]метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-4-пиперидил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-метилморфолин-2-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(4-этилморфолин-2-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метилпирролидин-3-ил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)метокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-(морфолинометил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-6-фтор-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-2,2-диметил-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(морфолинометил)-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[(1-метил-4-пиперидил)окси]-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(4-пиридилметокси)-3H-1,4-бензоксазепин-5-она;
8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(морфолинометил)-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(3,3,3-трифторпропил)-2,3-дигидро-1,4-бензодиазепин-5-она;
8-(циклогексилметил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
8-(циклогексен-1-ил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[4-(трифторметил)циклогексен-1-ил]-2,3-дигидро-1,4-бензодиазепин-5-она;
трет-бутил 4-[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-5-оксо-2,3-дигидро-1,4-бензодиазепин-8-ил]-3,6-дигидро-2H-пиридин-1-карбоксилата;
8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
8-[(3R)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
8-[(3S)-1-ацетилпирролидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-4-пиперидил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
8-[(1-циклобутил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-тетрагидрофуран-3-ил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[[1-(оксетан-3-ил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метилпирролидин-3-ил)метокси]-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-(1-метилпирролидин-3-ил)окси-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(1-метил-3-пиперидил)метокси]-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиридил)метокси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-4-пиперидил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она дигидрохлорида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этил-3-фтор-4-пиперидил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(8-этил-8-азабицикло[3,2,1]октан-3-ил)окси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-8-[(2-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензодиазепин-5-она дигидрохлорида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(5-фтор-2-пиридил)метокси]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(4-пиперидилокси)-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-8-(1-ацетилазетидин-3-ил)окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[(1-метил-4-пиперидил)окси]-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
(2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
2-[3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-4,5-дигидро-3H-2-бензазепин-1-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-фтор-2,3-дигидро-1,4-бензоксазепин-5-она;
8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-хлор-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она;
7-хлор-2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-4,5-дигидро-3H-2-бензазепин-1-она;
7-бром-2-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-4,5-дигидро-3H-2-бензазепин-1-она;
8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-метил-2,3-дигидро-1,4-бензодиазепин-5-она;
8-бром-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-1-этил-2,3-дигидро-1,4-бензодиазепин-5-она;
2-[4-[[4-(2R)-3-(3,4,-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3,-дигидро-1,4,-бензоксазепин-8-ил]-1-пиперидил]ацетонитрила;
8-[[1-(2,2-дифторацетил)-4-пиперидил]окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[[1-(2,2-дифторацетил)азетидин-3-ил]окси-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-фторэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-фторэтил)-4-пиперидил]окси]-2,3-дигидропиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-[(3-метилоксетан-3-ил)метил]-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-5-оксо-2,3-дигидро-1,4-бензоазепин-8-ил]окси]пиперидин-1-карбонитрила;
8-[(4-ацетилпиперазин-1-ил)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она;
3-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]окси]азетидин-1-карбальдегида;
4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]метил]пиперазин-1-карбальдегида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(2-окса-6-азаспиро[3,3]гептан-6-илметил)-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(8-этил-8-азабицикло[3,2,1]октан-3-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(2-этил-2-азаспиро[3,3]гептан-6-ил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(8-ацетил-8-азабицикло[3,2,1]октан-3-ил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[(2-ацетил-2-азаспиро[3,3]гептан-6-ил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пирролидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(пиперидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(3,3-дифторпирролидин-1-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-метилпиперазин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(пирролидин-1-илметил)-3H-1,4-бензоксазепин-5-она;
8-[(1-ацетил-4-пиперидил)окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она;
4-[[4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-5-оксо-3H-1,4-бензоксазепин-8-ил]окси]пиперидин-1-карбальдегида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[[4-(оксетан-3-ил)пиперазин-1-ил]метил]-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(2-окса-7-азаспиро[3,4]октан-7-илметил)-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-фторпиперидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[3-(трифторметил)пиперидин-1-карбонил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-(трифторметил)пиперидин-1-карбонил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2,6-диметилморфолин-4-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(2-азабицикло[2,2,1]гептан-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-окса-8-азабицикло[3,2,1]октан-8-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-метилморфолин-4-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-метилморфолин-4-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(морфолинометил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
8-(3,3a,4,5,6,6a-гексагидро-1H-циклопента[c]пиррол-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-фторпиперидин-1-карбонил)-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(2,2-дифторморфолин-4-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(4,4-дифторпиперидин-1-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(1-пиперидилметил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-[метил(оксетан-3-ил)амино]циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[4-[2-фторэтил(метил)амино]циклогексокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
(2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-этантиол-4-пиперидил)окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-фторэтил)азетидин-3-ил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2S)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-фторэтил)-4-пиперидил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(3-окса-8-азабицикло[3,2,1]октан-8-карбонил)-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(2-окса-5-азабицикло[2,2,1]гептан-5-карбонил)-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,5-диметилморфолин-4-карбонил)-2,2-диметил-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3-фтор-1-метил-4-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-фтор-1-(2-фторэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,4-дигидро-1H-пирроло[1,2-a]пиразин-2-карбонил)-2,2-диметил-3H-1,4-бензоксазепин-5-она;
8-(3,4,6,7,8,8a-гексагидро-1H-пирроло[1,2-a]пиразин-2-карбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(5-фторпиримидин-2-ил)окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксипропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-пропаноил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-2-фторэтил]-8-азабицикло[3,2,1]октан-3-илокси]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(циклопропанкарбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-(циклопентанкарбонил)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-метил-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидрокси-2-метил-пропил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-морфолиноэтил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(2-окса-6-азаспиро[3,3]гептан-6-ил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-гидроксипро-1-пинил)-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-метоксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(4-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(4-пиридил)этинил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[2-(3-пиридил)этинил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-гидроксибу-1-тинил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[3-(метиламино)про-1-пинил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,3-диметилпиразол-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1-метилпиразол-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(1,5-диметилпиразол-4-ил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[[(3R)-1-метил-3-пиперидил]окси]-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(1-(2-фторэтил)-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(1-(2-гидрокси)-3-пиперидил)окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидрокси-2-метил-пропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(6-фтор-2-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-этоксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-(2-гидрокси)-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[8-(2-фторэтил)-8-азабицикло[3,2,1]октан-3-ил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-метоксиэтил)-4-пиридил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(6-метокси-2-пиридил)-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксипропил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-(1-морфолиноэтил)-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-8-[1-(2-окса-6-азаспиро[3,3]гептан-6-ил)этил]-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксипропил)-4-пиперидил]окси]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(3,4-дигидро-1H-пирроло[1,2-a]пиразин-2-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(2-окса-6-азаспиро[3,3]гептан-6-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-(2-окса-7-азаспиро[3,5]нонан-7-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-(2-окса-7-азаспиро[3,5]нонан-7-илметил)-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксипропил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида;
(2R)-4-[(2R)-3-(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[(3R,4R)-3-фтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида;
8-[[3,3-дифтор-1-(2-гидроксиэтил)-4-пиперидил]окси]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(4-гидрокси-1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(4-метокси-1-пиперидил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[1-(3-гидрокси-3-метил-пирролидин-1-ил)этил]-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-гидроксиэтил)-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она дигидрохлорида;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-(2-метоксиэтил)-4-пиперидил]окси]-2,2-диметил-3H-пиридо[3,2-f][1,4]оксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3S)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3S)-1-метилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолинoн-2-ил)-2-гидроксипропил]-8-[(3R)-тетрагидрофуран-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолинoн-2-ил)-2-гидроксипропил]-8-[(3S)-тетрагидрофуран-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-[(2S)-2-гидроксипропил]-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[[1-[(2R)-2-гидроксипропил]-4-пиперидил]окси]-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[циклопропил(гидрокси)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
8-[циклопентил(гидрокси)метил]-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(2-метоксиэтил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-1-метилпирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-8-[(3R)-1-(2-метоксиэтил)пирролидин-3-ил]окси-2-метил-2,3-дигидро-1,4-бензоксазепин-5-она;
4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-)-2-гидроксипропил]-8-[[1-(3,3,3-трифтор-2-гидроксипропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она;
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-)-2-гидроксипропил]-2-метил-8-[[1-(3,3,3-трифтор-2-гидроксипропил)-4-пиперидил]окси]-2,3-дигидро-1,4-бензоксазепин-5-она и
(2R)-4-[(2R)-3-(3,4-дигидро-1H-изохинолин-2-ил)-2-гидроксипропил]-2-метил-8-[(3R)-1-(оксетан-3-ил)пирролидин-3-ил]окси-2,3-дигидро-1,4-бензоксазепин-5-она.
14. Фармацевтическая композиция для профилактики или лечения заболевания, связанного с ингибированием протеинаргининметилтрансферазы 5 (PRMT5), содержащая терапевтически эффективное количество соединения или его оптического изомера, или стереоизомера, или его фармацевтически приемлемой соли, как определено по любому из пп. 1-13, в качестве активного ингредиента вместе с фармацевтически приемлемым носителем.
15. Фармацевтическая композиция по п. 14, отличающаяся тем, что заболевание, связанное с ингибированием PRMT5, выбрано из рака, заболевания крови, аутоиммунного заболевания, воспалительного заболевания и нейродегенеративного заболевания.
16. Фармацевтическая композиция по п. 15, отличающаяся тем, что рак выбран из группы, состоящей из невриномы слухового нерва, аденокарциномы, рака надпочечников, рака анального канала, ангиосаркомы, доброкачественной моноклональной гаммаглобулинопатии, холангиокарциномы, рака мочевого пузыря, рака молочной железы, рака головного мозга, лимфомы, множественной миеломы, опухоли слезной железы, рака бронхов, рака шейки матки, краниофарингиомы, колоректального рака, эпителиальной карциномы, эпителиально-клеточной опухоли, эндотелиальной саркомы, рака эндометрия, рака пищевода, аденокарциномы Барретта, саркомы Юинга, рака глаза, рака желчного пузыря, рака желудка, гастроинтестинальной стромальной опухоли (GIST), рака головы и шеи, рака ротовой полости (плоскоклеточного рака ротовой полости, OSCC), рака горла, гемопоэтического рака, гемангиобластомы, воспалительной миофибробластной опухоли, амилоидоза иммунных клеток, рака почки, рака печени, рака легкого, миелодиспластического синдрома (MDS), мезотелиомы, миелопролиферативного заболевания (MPD), хронического идиопатического миелофиброза, хронического миелогенного лейкоза (CML), хронического нейтрофильного лейкоза (CNL), нейробластомы, нейрофибромы, нейроэндокринного рака, остеосаркомы, рака яичников, папиллярной аденокарциномы, рака поджелудочной железы, рака полового члена, рака предстательной железы, рака прямой кишки, рабдомиосаркомы, рака слюнных желез, рака кожи, рака тонкой кишки, саркомы мягких тканей, рака щитовидной железы, рака уретры, рака влагалища и рака вульвы.
17. Фармацевтическая композиция по п. 16, отличающаяся тем, что рак головного мозга выбран из группы, состоящей из менингиомы, глиомы, медуллобластомы, глиобластомы и рака с метастазами в головной мозг.
18. Фармацевтическая композиция по п. 15, отличающаяся тем, что заболевание крови представляет собой гемоглобинемию или серповидноклеточную анемию; аутоиммунное заболевание выбрано из группы, состоящей из ревматоидного артрита, артрита позвоночника, подагрического артрита, дегенеративного заболевания суставов, остеоартрита, системной красной волчанки, рассеянного склероза, псориатического артрита, ювенильного артрита, астмы, атеросклероза, остеопороза, бронхита, тендинита, псориаза, экземы, ожогов, дерматита, зуда, энуреза, эозинофильной болезни, пептической язвы, локализованного энтерита, дивертикулита, желудочно-кишечного кровотечения, эозинофильного эзофагита, эозинофильного гастрита, эозинофильного гастроэнтерита и эозинофильного колита; воспалительное заболевание выбрано из группы, состоящей из воспаления, связанного с акне, апластической анемии, гемолитической аутоиммунной анемии, ринита, астмы, полиартериита, височного артериита, узелкового периартериита, артериита Такаясу, кристаллического артрита, остеоартрита, псориатического артрита, подагрического артрита, реактивного артрита, ревматоидного артрита, бокового амиотрофического склероза, аутоиммунного заболевания, аллергии или аллергической реакции, атеросклероза, бронхита, бурсита, хронического простатита, конъюнктивита, хронической обструктивной болезни легких, дерматомиозита, диабета 1 типа, диабета 2 типа, псориаза, экземы, реакции гиперчувствительности к экземе, ожога, дерматита, зуда, эндометриоза, инфекции, ишемической болезни сердца, гломерулонефрита, гингивита, чувствительности, мигрени, головной боли напряжения, послеоперационной непроходимости кишечника, непроходимости кишечника при сепсисе, идиопатической тромбоцитопенической пурпуры, болевого синдрома в мочевом пузыре, пептической язвы, локализованного энтерита, дивертикулита, желудочного кровотечения, эозинофильного эзофагита, эозинофильного гастрита, эозинофильного гастроэнтерита, эозинофильного колита, гастрита, диареи, гастроэзофагеальной рефлюксной болезни, болезни Крона, язвенного колита, коллагенозного колита, лимфоцитарного колита, ишемического колита, колита при шунтировании, синдрома Бехчета, неопределенного колита, синдрома воспаленного кишечника (IBS), волчанки, экхимозов, миастении гравис и ишемии миокарда; и нейродегенеративное заболевание выбрано из группы, состоящей из заболевания двигательных нейронов, болезни Пика, болезни Альцгеймера, деменции, связанной со СПИД, болезни Паркинсона, бокового амиотрофического склероза, пигментации сетчатки, спинальной мышечной атрофии и дегенерации мозжечка.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Приспособление для впрыскивания горючего в двигателях внутреннего горения | 1930 |
|
SU27908A1 |
Авторы
Даты
2024-12-09—Публикация
2020-09-29—Подача