Изобретение относится к способу получения поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана (ПЭИ), являющегося одним из видов полиэфиримидов, и который имеет следующую структурную формулу:
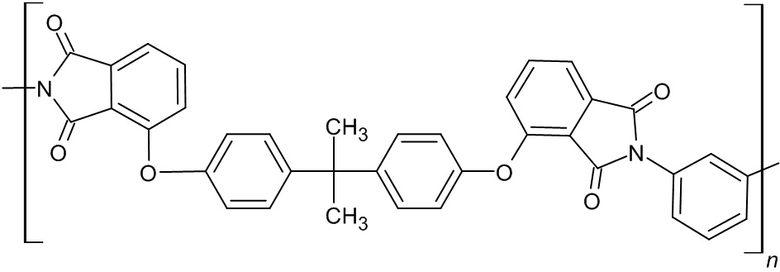
Благодаря наличию в повторяющемся элементарном звене сразу трех шарнирных групп, этот полимер легко перерабатывается из расплава и органических растворителей. Это прочный термопласт с высокой тепло- и термостойкостью, хорошими механическими, диэлектрическими свойствами.
Полимер имеет температуру длительного использования до + 170°С. Он огнестоек без антипиренов, имеет низкое дымовыделение при контакте с открытым пламенем, что делает его незаменимым для изготовления многих деталей в авиационной промышленности.
Изделия из ПЭИ находят применение в машиностроении и станкостроении: втулки перемещения суппорта, зубчатые колеса распредвала, венцы червячных редукторов РЧ-32, РЧ-37, маточные гайки поперечных суппортов, подвижные направляющие, шестерни коробки скоростей, червячные колеса редуктора привода, втулки, вкладыши в узлах трения (салазки, бабки, ползуны и т.п.), вкладыши шпинделя, салазки, втулки, шестерни, подшипники скольжения, звездочки 7-ми, 12-ти, 14-ти лучевые [Бородулин А.С., Калинников А.Н., Терешков А.Г., Музыка С.С Полиэфиримиды для создания теплостойких полимерных композиционных материалов с высокими физико-техническими свойствами // Вестник БГТУ им. В.Г. Шухова. 2019. № 11. С. 94-100. DOI:10.34031/2071-7318-2019-4-11-94-100].
Для химической промышленности из ПЭИ изготавливают такие изделия как: насосы (лопасти, крыльчатки, зубчатые колеса, подшипники скольжения и качения, манжеты сальников, корпуса роторов); фильтры (колеса и ступицы); сетчатые столы; дозаторы, сепараторы (вкладыши узлов трения, корпуса) [Бородулин А.С., Калинников А.Н., Терешков А.Г., Музыка С.С Полиэфиримиды для создания теплостойких полимерных композиционных материалов с высокими физико-техническими свойствами // Вестник БГТУ им. В.Г. Шухова. 2019. № 11. С. 94-100. DOI:10.34031/2071-7318-2019-4-11-94-100].
ПЭИ - это единственный пластик, имеющий сертификацию для работы с пищевыми продуктами.
Применение ПЭИ в 3D-печати позволяет создавать высокопрочные детали любого размера и любой геометрии для разных отраслей промышленности и науки.
Существуют два основных варианта синтеза ПЭИ: циклизацией полиамидокислоты, которую получают поликонденсацией диангидрида 2,2-бис-[4-(3,4-дикарбоксифенокси)фенил]пропана и м-фенилендиамина или реакцией полинитрозамещения.
Заявляемый способ относится к реакции полинитрозамещения бис(3-нитрофталимидо)бензола с динатриевой солью бисфенола А и поэтому в описании изобретения рассматриваются аналоги, относящиеся к процессам этого типа. Это означает, что признаками всех рассмотренных способов получения ПЭИ в описании, совпадающими с существенными признаками заявляемого изобретения, являются полинитрозамещение активированных ароматических нитрогрупп с динатриевыми солями бисфенола А с образованием макромолекул, содержащих фталимидные и дифенилолпропановые группы.
К числу публикаций в данном направлении относится патент США № 3838097, опубл. 24.09.1974, защитившая способ получения линейных термопластичных полиэфиримидов, реакцией динатриевой соли бисфенола А с 4,4′-бис(3-нитрофталимидо)дифенилметаном, 4,4′-бис(3-нитрофталимидо)дифениловым эфиром, 1,6-бис(3-нитрофталимидо)гексаном, 1,2-бис(3-нитрофталимидо)этаном, 4.4′-бис(3-нитрофталимидо)дифенилсульфоном, эфиром, 4,4′-бис(3-нитрофталимидо)дифениловым эфиром и 4,4′-бис(4-нитрофталимидо)дифениловым эфиром, 1,6-бис(3-нитрофталимидо)гексаном, 2,4-бис(3-нитрофталимидо)толуолом.
Условия поликонденсации и некоторые характеристики полиэфиримидов, приведенные в патенте США № 3838097, опубл. 24.09.1974, представлены в табл. 1.
Таблица 1. Условия поликонденсации и некоторые характеристики полиэфиримидов общей формулы

(CH2CI2)
(CH2CI2)
при 70°С - 0.5 ч.
при 70°С - 2 мин., затем 0.5 ч при комнатной температуре.
(CH2CI2)
(CH2CI2)
a [η] - характеристическая вязкость полимера; b Tg - температура стеклования; сТразл - температура разложения.
Описанные условия синтеза полиэфиримидов отличаются друг от друга, а именно использованием различных растворителей, температурой и продолжительности процесса. Это означает, что оптимальные условия получения полиэфиримидов конкретной структуры строго индивидуальны.
К недостаткам способа следует относится отсутствие примера с использованием бис(3-нитрофталимидо)бензола и м-фенилендиамина, хотя в число перечисленных диаминов м-фенилендиамин входит. Кроме того, к недостаткам данного способа следует отнести довольно низкие значения характеристической вязкости полимера от 0.13 до 0.28 дл/г, определенные в разных растворителях [хлористый метилен и диметилформамид (ДМФА)] и отсутствие прямых определений молекулярных масс полимера методами гель-проникающей хроматографии, светорассеяния и др.
В патентах США 3787364, опубл. 24.09.1974 г. и № 4024110, опубл. 17.05.1977 г. сообщается, что реакция полинитрозамещения бисимидов с динатриевой солью бисфенола А протекает в среде полярных апротонных растворителях [диметилсульфоксид (ДМСО), N-метилпиролидон, ДМФА]. Данный факт подтвержден результатами, приведенными в работе [Takekoshi T., J. E. Kochanowski J.E., Manello J.S., Webber M., NASA Contractor Report CR-145007. 1976].
Недостатками вышеуказанных способов получения полиэфиримидов являются отсутствие методики синтеза ПЭИ на основе бис(3-нитрофталимидо)бензола, отсутствие значений молекулярных масс или характеристической вязкости полимеров.
В работе Takekoshi T. [Takekoshi T. Synthesis of High Performance Aromatic Polymers via Nucleophilic Nitro Displacement Reaction // Polymer J. 1987. V. 19. N 1. P.191-202. DOI: 10.1295/polymj.19.191] показана возможность получения полиэфиримидов реакцией полинитрозамещения путем взаимодействия динатриевой соли бисфенола А с бис[3(4)-нитрофталимидами]ариленами.
Недостатком вышеуказанного способа получения полиэфиримидов является отсутствие подробной методики синтеза промежуточных и конечных продуктов.
Известен способ получения полиэфиримида, в том числе и ПЭИ, реакцией бис[4(3-фторфталимид)фенил]метана, бис[4(3-хлорфталимид)фенил]метана, бис[4(3-фторфталимид)фенил]оксида, 1,6-бис(3-фторфталимидо)гексана, бис[4(4-фторфталимид)фенил]метана с динатриевой солью бисфенола А [Патент СССР № 1151201, опубл. 15.04. 1985 г.]. Близкий к заявляемому изобретению пример из патента:
Смесь, состоящая из 1.659 частей (все части -весовые) 50%-ного раствора NaOH, 2.362 частей бисфенола А, 25 частей толуола и 15 частей ДМСО, нагревают с обратным холодильником, удаляя воду азеотропной перегонкой. После охлаждения реакционной смеси до 65°С добавляют 5 частей бис[4(3-фторфталимид)фенил]метана и 15 частей толуола и полученную смесь нагревают при температуре 70°С в течение 6 часов. Характеристическая вязкость полимера равна 0.277 дл/г. Реакция с участием бис[4(4-фторфталимид)фенил]метана проведена при температуре 80°С в течение 10 часов, характеристическая вязкость полимера составляла 0.23 дл/г. Сообщается, что реакция с участием бисфторфталимида идет значительно быстрее, чем с бисхлорфталимидом.
Недостатком данного способа является отсутствие значений выхода полимера во всех приведенных примерах в патенте, применение дорогостоящего фторсодержащего соединения, невысокие значения характеристической вязкости, а также отсутствие прямых определений молекулярных масс полимера методами гель-проникающей хроматографии, светорассеяния и др.
Известен способ получения бис[3(4)-хлорфталимидо]бензола реакцией м-фенилендиамина с 3(4)-хлорфталевым ангидридом в среде дифенилсульфона [Патент EP 3131950 B1, опубл. 15.01.2020 г.]. Процесс проводят при температуре 170-200°C в течение 3 ч. Реакция бис[3(4)-хлорфталимидо]бензола с динатриевой солью бисфенола А приводит к образованию ПЭИ путем замещения атомов хлора [Патент США № 3787364, опубл. 24.09.1974 г.; Патент EP № 3131950 B1, опубл. 15.01.2020 г.]. Недостатками этого способа являются высокая температура реакции и использование дорогостоящего дифенилсульфона.
Наиболее близкой к описываемому изобретению по технической сущности является способ получения ПЭИ [White D.M., Takekoshi T., Williams F.J., Relles H.F., Donahue P.E., Klopfer H.J., Loucks G.R., Manello J.S., Matthews R.O., Schlunz R.W. Polyetherimides via nitro-displacement polymerization: Monomer synthesis and 13C-NMR analysis of monomers and polymers // Journal of Polymer Science: Polymer Chemistry Edition. 1981. V. 19. N 7. P. 1635-1658. DOI:10.1002/pol.1981.170190705]. Указанный способ по существенным признакам наиболее близок к заявляемому способу, поэтому был выбран в качестве способа-прототипа.
Признаками способа-прототипа, совпадающими с существенными признаками заявляемого изобретения, являются полинитрозамещение активированных ароматических нитрогрупп с динатриевыми солями бисфенола А с образованием макромолекул, содержащих фталимидные и дифенилолпропановые группы.
Процесс получения ПЭИ в способе-прототипа осуществляется реакцией динатриевой соли бисфенола А с бис(3-нитрофталимидо)бензолом, однако описание методики получения бис(3-нитрофталимидо)бензола не приводится.
Близкий к заявляемому изобретению пример из патента: 0.01985 моль динатриевой соли бисфенола А растворяют в смеси ДМСО и толуола и добавляют 0.01985 моль бис(3-нитрофталимидо)бензола при тщательном перемешивании. Температура процесса 55°С. Через 5 ч в реакционную смесь вносят 4-метилфеноксида натрия (0.0046 моль) для удаления оставшихся нитрогрупп и через 15 мин добавляют 1 мл уксусной кислоты. Полимер осаждают метанолом и отфильтровывают. Выход полимера - 87%, Tg=227°С. Данные гель-проникающей хроматографии: Mw=21000; Мn=4130; Mw/Mn=5.09. Установлено, что на хроматограмме присутствуют два низкомолекулярных пика, которые авторы статьи относят циклическому мономеру (слабая интенсивность) и циклическому димеру (очень слабый).
Недостатками способа-прототипа являются отсутствие методики получения бис(3-нитрофталимидо)бензола, присутствие в ПЭИ примесей в виде циклического мономера и димера, низкий выход полимера (87%) и его небольшие значения молекулярных масс (Mw=21000, Мn=4130), использование опасного для здоровья человека 4-метилфеноксида натрия.
Технический результат изобретений заключается в способе получения ПЭИ, лишенных перечисленных недостатков, приведенных в способе- прототипа: разработана подробная методика синтеза бис(3)-нитрофталимидо]бензола с высоким выходом и методами ЯМР (1Н, 13С)- спектроскопии доказана его структура; отсутствие в ПЭИ примесей в виде циклического мономера и димера; замена опасного 4-метилфеноксида натрия на менее опасный фенолят натрия; более высокие значения молекулярных масс ПЭИ, определенные методом гель-проникающей хроматографии, по сравнению со способом-прототипа.
Технический результат изобретений достигается тем, что в способ получения поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана реакцией бис(3-нитрофталимидо)бензола с динатриевой солью бисфенола А, согласно изобретению, целевой продукт, полученный в смеси сухого ДМСО и сухого толуола при температуре 55°С в течение 18 ч, не содержит примесей циклического мономера и димера и имеет среднечисловое и средневесовое значение молекулярной массы, равное 215709 и 617697 соответственно, при этом бис(3-нитрофталимидо)бензол получен реакцией 3-нитрофталевого ангидрида с м-фенилендиамином с использованием N-метилпирролидона и толуола с одновременным удалением образующейся воды азеотропной перегонкой при помощи ловушки Дина-Старка, а динатриевая соль бисфенола А получена реакцией металлического натрия и бисфенола А в абсолютном метаноле и сухом толуоле с последующим упаривании образующегося раствора при 15 Торр, при этом выход целевого продукта составляет 91,1%.
Заявляемый способ получения ПЭИ обладает существенными преимуществами:
- высокой степенью чистоты полимера и высокими его выходами;
- высокими значениями средневесовой (Mw=411562-617697) и среднечисловой молекулярной массы (Мп=133905-215709) полимера;
- в процессе получения полимера используются недорогостоящие, доступные, отечественные крупнотоннажные исходные вещества;
- простотой получения полимера;
- получение отечественного полиэфиримида по данному способу имеет большие перспективы для промышленного его производства.
ИК-спектры регистрировали в таблетках с KBr на приборе ’’Vertex 70" фирмы "Bruker" в таблетках с KBr.
Спектры ЯМР снимали на спектрометре "Bruker DPX-400" в ДМСО-d6 на рабочих частотах 400 (1Н) и 100 (13С) МГц. В качестве внутреннего стандарта использовали гексаметилдисилокеан.
Элементный анализ выполняли на анализаторе "Flash ЕА 1112 CHNS-O/MAS 200" фирмы "Thermo Scientific".
Измерения гель-проникающей хроматографии проводили на высокоэффективном гель-проникающем хроматографе "Shimadzu LC-20 Prominence", включающем дифференциальный рефрактометрический детектор "Shimadzu RID-20A" и хроматографическую колонку "PolyPore" 7.5 × 300 мм ("Agilent") с соответствующей предколонкой. В качестве подвижной фазы использовали диметилформамид особой чистоты для высокоэффективной жидкостной хроматографии со скоростью пропускания потока 1 мл/мин. Для построения калибровочной кривой использовали набор полистирольных стандартов "Polystyrene High EasiVials" (PL2010-0201), состоящий из двенадцати образцов с М = = 162-(657 × 104). Растворение образцов проводили при 80°С в течение 12 ч с применением системы пробоподготовки "Varian PL-SP 260VS", совмещающей функции управляемого нагревания и перемешивания.
Определение температуры стеклования ПЭИ проводили методом дифференциальной сканирующей калориметрии с использованием прибора синхронного термического анализа STA 449 F1. Навески образцов нагревали от 40 до 800°С со скоростью 10°С/мин. Исследования проводили в инертной атмосфере (расход аргона 70 мл/мин, расход защитного газа 20 мл/мин) в корундовых тиглях для дифференциальной сканирующей калориметрии. В ходе эксперимента производили контроль качественного и количественного состава газовых продуктов термолиза с помощью квадрупольного масс-спектрометра QMS 403 C Aeolos. Энергия электронного удара 70 эВ.
Сущность изобретения иллюстрируется следующими примерами.
Пример 1. Синтез бис(3-нитрофталимидо)бензола.

В круглодонную трехгорловую колбу объемом 0.5 л, снабженную механической мешалкой, насадкой Дина-Старка и капельной воронкой помещают 97.57 г (0.5055 моль) 3-нитрофталевого ангидрида и 50 мл N-метилпирролидона и перемешивают до образования суспензии. м-Фенилендиамин в количестве 25.05 г (0.232 моль) растворяют в 30 мл N-метилпирролидона и добавляют полученный раствор маленькими порциями через капельную воронку к полученой суспензии при энергичном перемешивании. При взаимодействии м-фенилендиамина и 3-нитрофталевого ангидрида наблюдается повышение температуры реакционной смеси до 45°С, при этом содержимое колбы постепенно приобретает светло-серый цвет. Далее в реакционную массу добавляют 200 мл толуола и при перемешивании нагревают на масляной бане (температура бани 137°С, температура содержимого в колбе 117-118°С). Через 40 мин наблюдается выпадение осадка желтого цвета, при этом одновременно удаляют образующуюся воду азеотропной перегонкой при помощи ловушки Дина-Старка. Реакционную смесь нагревают в течение 18 ч. По истечении этого времени содержимое колбы охлаждают до комнатной температуры и реакционную смесь выливают в 600 мл метанола, перемешивают и оставляют при комнатной температуре до осаждения осадка. Образовавшийся осадок отфильтровывают на воронке Шотта и промывают осадок 400 мл метанола (пока фильтрат не стал бесцветным). Полученный осадок сушат на воздухе в течение 12 ч, а затем в сушильном шкафу при 50°С. Выход продукта - 97 %. Тпл. = 290-305°С.
Элементный анализ. C22H10N4O8. Молекулярная масса 458. Вычислено, %: C 57.52; Н 2.4; N 12.2. Найдено, %: C 56.42; H 2.32; N 11.505 %.
Структура 1,3-бис[N-(3-нитрофталимидо)]бензола доказана методами ИК и ЯМР (1Н и 13С) спектроскопии. В ИК-спектрах присутствуют полосы поглощения, характерные для карбоксильных групп имидного цикла в области 1780-1715 см-1 [Chopin S., Chaignon, F., Blart E., Odobel, F. Syntheses and properties of core-sustituted naphthalene bisimides with aryl ethynyl or cyano groups. Journal of Materials Chemistry. 2007. V. 17. N 39. P. 4139. DOI:10.1039/b704489e и для 1,3-замещенных бензола в области 810-750 см-1 [Беллами Л. Д.
и для 1,3-замещенных бензола в области 810-750 см-1 [Беллами Л. Д.
Инфракрасные спектры сложных молекул / Перевод с англ. В. М. Акимова [и др.] ; Под ред. канд. хим. наук Ю. А. Пентина. - [2-е изд., перераб. и расшир.]. - Москва : Изд-во иностр. лит., 1963. - 590 с. ].
Спектр ЯМР 1H (ДМСОd6), δ, м.д. 8.35 д [2Н, H(4), 3JHH5 = 8.1, 4JHH6=0.7 Hz)]; 8.27 д [2Н, H(6), 3JHH5 = 7.5, 4JHH4= 0.7 Hz)]; 8.14-8.11м [2 Н, H(5)]; 7.76-7.69 м [ 1Н, H(11)]; 7.62-7.56 м [3Н, C(12), H(10)].
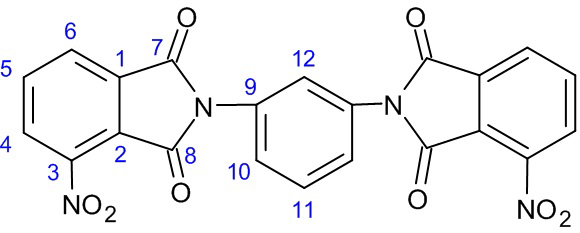
Спектр ЯМР 1H (ДМСОd6), δ, м.д. 8.35 д [2Н, H(4), 3JHH5 = 8.1, 4JHH6=0.7 Hz)]; 8.27 д [2Н, H(6), 3JHH5 = 7.5, 4JHH4= 0.7 Hz)]; 8.14-8.11м [2 Н, H(5)]; 7.76-7.69 м [ 1Н, H(11)]; 7.62-7.56 м [3Н, C(12), H(10)].
Спектр ЯМР 13С (100 MHz, ДМСОd6), δС, м. д.: C(7) -165.17; C(8) -162.62; C(3) -144.72; C(5) -136.59; C(9) -133.75; C(1) -132.10; C(11) -129.53; C(6) -128.57; C(4) -127.64; C(2) -127.25; C(10) -126.49; C(12) -123.11.
Пример 2. Приготовление динатриевой соли бисфенола А.

0.76 г (0.033 моль) металлического натрия растворяют в 100 мл абсолютного метанола. Затем добавляют 3.76 г (0.0165 моль) бисфенола А и после добавления 20 мл сухого толуола, раствор упаривают при 15 Торр. Образовавшееся твердое вещество дополнительно сушат в течение 1 ч при 3 Торр. Полученная динатриевая соль бисфенола А хранится в колбе, в которой в дальнейшем была проведена полимеризация.
ИК-спектр динатриевой соли бисфенола А содержит полосы поглощения при 1600-1500 см-1, характерные для валентных колебаний С=С ароматических колец, дублеты полос поглощения при 1600, 1100, 902, 828, 744 см-1, свойственные производным дифенила и полосу поглощения изопропильной группы при 1171 см-1 [Верховская З.Н. Дифенилолпропан / Под редакцией И.В. Калечица. - Москва : Изд-во Химия, 1971. С. 7; Беллами Л. Д. Инфракрасные спектры сложных молекул / Перевод с англ. В. М. Акимова [и др.] ; Под ред. канд. хим. наук Ю. А. Пентина. - [2-е изд., перераб. и расшир.]. Москва : Изд-во иностр. лит., 1963. - 590 с.].
Пример 3. Синтез поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана (ПЭИ).

Получение бис(3-нитрофталимидо)бензола и сухой динатриевой соли бисфенола А описано примерах 1 и 2 соответственно.
При добавлении к 4.493 г (0.0165 моль) динатриевой соли бисфенола А 30 мл сухого ДМСО и 39 мл сухого толуола образуется суспензия, которую при перемешивании нагревают до 55°С, затем в свежеприготовленную суспензию добавляют 7.4 г (0.016 моль) 1,3-бис(3-нитрофталимидо)бензола. Процесс проводят при 55°С и при энергичном перемешивании в течение 5 ч, по истечении этого времени добавляют 0.46 г (0.004 моль) фенолята натрия и продолжают нагревание в течение 30 минут. Далее в реакционную смесь добавляют 1 мл ледяной уксусной кислоты и перемешивают еще в течение 15 минут. После охлаждения реакционной смеси до комнатной температуры, полимер осаждают этиловым спиртом в химическом стакане при энергичном перемешивании. Образовавшийся полимер отфильтровывают, промывают этиловым спиртом и сушат до постоянной массы в вакуум-сушильном шкафу. Выход полимера 10.2 г (87 % от теоретического).
Элементный анализ. C37H24N2O6. Вычислено, %: С 74.98; H 4,05; N 4,73. Найдено, %: С 66.73; H 3.71,05; N 3.50.
Температура стеклования, определенная методом дифференциальной сканирующей калориметрии, равна 227°С. Данные гель-проникающей хроматографии: Mn = 19402, Mw = 21952, Mw /Mn = 1.13.
В ИК-спектрах ПЭИ присутствуют полосы поглощения, характерные для карбоксильных групп имидного цикла (1780-1720 см-1), дифенилолпропановых (1597, 1109, 902, 828, 743 см-1) и изопропильных групп (1171 см-1), а также деформационные колебания C-N в имидном цикле (729 см-1). В области 2925 см-1 наблюдаются слабоинтенсивные полосы поглощения, характерные для колебаний связи C-H метильного заместителя.
Спектр ЯМР 13С (ДМСО-d6): C(1) -134.30; C(2) - 118.56; С(3) - 154.45; С(4) - 127.58; С(5) - 137.47; С(6) - 115.25; С(7) - 166.69; С(8) -165.01; С(9) - 153.40; С(10) -119.51; С(11) - 128.81; С(12) 147.09; С(13) - 42.44; С(14) - 31.07; С(15) -132.74; С(16) - 124.34; С(17) 129.39; С(18) - 124.34.

Пример 4. Синтез поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана (ПЭИ).
Получение бис(3-нитрофталимидо)бензола и сухой динатриевой соли бисфенола А описано примерах 1 и 2 соответственно. Схема получения поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана приведена в примере 3.
При добавлении к 29.05 г (0.1068 моль) динатриевой соли бисфенола А 80 мл ДМСО и 54 мл толуола образуется суспензия, которую при перемешивании нагревают до 55°С, затем в свежеприготовленную суспензию добавляют раствор, полученный растворением 47.5 г (0.1037 моль) 1,3-бис[N-(3-нитрофталимидо)]бензола в смеси 120 мл сухого ДМСО и 200 мл сухого толуола. Содержимое колбы окрашивается в темно-вишневый цвет, который сохраняется на протяжении всей реакции. Через 5 ч в смесь вносят раствор фенолята натрия 3.00 г (0.0259 моль) в смеси растворителей (9.4 мл ДМСО и 6.3 мл толуола) и через 15 мин добавляют 3 мл ледяной уксусной кислоты. Затем содержимое колбы охлаждают до комнатной температуры и полимер осаждают метанолом в химическом стакане при перемешивании механической мешалкой. Образовавшийся полимер отфильтровывают, промывают и сушат до постоянной массы в вакуум-сушильном шкафу. Выход полимера 39.7 г (57.9 % от теоретического).
Элементный анализ. C37H24N2O6. Вычислено, %: С 74.98; H 4,05; N 4,73. Найдено, %: С 72.61; H 3.83,05; N 3.26.
Температура стеклования, определенная методом дифференциальной сканирующей калориметрии, равна 217°С. Данные гель-проникающей хроматографии: Mn = 146189, Mw = 552974, Mw /Mn = 3.78.
ИК-спектр и спектр ЯМР 13С полученного поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана аналогичны ИК-спектру и спектру 13С ЯМР ПЭИ, приведенному в примере 3.
Пример 5. Синтез поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана (ПЭИ).
Получение бис(3-нитрофталимидо)бензола и сухой динатриевой соли бисфенола А описано примерах 1 и 2 соответственно. Схема синтеза поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана приведена в примере 3.
При добавлении к 29.05 г (0.1068 моль) динатриевой соли бисфенола А 80 мл ДМСО и 54 мл толуола образуется суспензия, которую при перемешивании нагревают до 55°С, затем в свежеприготовленную суспензию добавляют раствор, полученный растворением 47.5 г (0.1037 моль) 1,3-бис[N-(3-нитрофталимидо)]бензола в смеси 120 мл сухого ДМСО и 200 мл сухого толуола. Содержимое колбы окрашивается в темно-вишневый цвет, который сохраняется на протяжении всей реакции. Через 18 ч в содержимое колбы вносят раствор, полученный растворением 3.00 г (0.0259 моль) фенолята натрия в 9.4 мл ДМСО и 6.3 мл толуола, и через 15 мин добавляют 3 мл ледяной уксусной кислоты. Реакционную смесь охлаждают до комнатной температуры и осаждают метанолом в химическом стакане при перемешивании механической мешалкой, образовавшийся осадок отфильтровывают, промывают и сушат до постоянной массы. Выход полимера 62.17 г. (90.7 % от теоретического).
Элементный анализ. C37H24N2O6. Вычислено, %: С 74.98; H 4,05; N 4,73. Найдено, %: С 67.14; H 4.54; N 4.44.
Температура стеклования, определенная методом дифференциальной сканирующей калориметрии, равна 217°С.
Данные гель-проникающей хроматографии: Mn = 133905, Mw = 411562, Mw /Mn = 3.07.
ИК-спектр и спектр ЯМР 13С полученного поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана аналогичны ИК-спектру и спектру 13С ЯМР ПЭИ, приведенному в примере 3.
Пример 6. Синтез поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана (ПЭИ).
Получение бис(3-нитрофталимидо)бензола и сухой динатриевой соли бисфенола А описано примерах 1 и 2 соответственно. Схема синтеза поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана приведена в примере 3.
При добавлении к 58.01 г (0.2136 моль) динатриевой соли бисфенола А 160 мл ДМСО и 100 мл толуола образуется суспензия, которую при перемешивании нагревают до 55°С, затем в свежеприготовленную суспензию добавляют раствор, полученный растворением 95 г (0.2074 моль) 1,3-бис[N-(3-нитрофталимидо)]бензола в смеси 240 мл сухого диметилсульфоксида и 400 мл сухого толуола. Содержимое колбы окрашивается в темно-вишневый цвет, который сохраняется на протяжении всей реакции. Через 18 ч в содержимое колбы вносят раствор, полученный 6.00 г (0.0517 моль) фенолята натрия в 8.6 мл диметилсульфоксида и 12.6 мл толуола, и через 15 мин добавляют 6 мл уксусной кислоты. Реакционную смесь охлаждают до комнатной температуры и осаждают метанолом в химическом стакане при перемешивании механической мешалкой. Образовавшийся осадок отфильтровывают, промывают и сушат сначала на воздухе в течение 12 ч, а затем при 50°С и остаточном давлении 0,09 МПа в вакуум-сушильном шкафу в течение 2 ч. Выход полимера 124.3 г (91.1 % от теоретического).
Элементный анализ. C37H24N2O6. Вычислено, %: С 74.98; H 4,05; N 4,73. Найдено, %: С 72.02; H 4.22; N 3.91.
Температура стеклования, определенная методом дифференциально-сканирующей калориметрии, равна 218°С.
Данные гель-проникающей хроматографии: Mn = 215709, Mw = 617697, Mw /Mn = 2.86.
ИК-спектр и спектр ЯМР 13С полученного поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана аналогичны спектру 13С ЯМР полимера, приведенному в примере 3.
Заявляемый способ получения поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана имеет хорошие перспективы для промышленного его производства благодаря высокой степени обеспеченности отечественным сырьем (3-нитрофталевый ангидрид, бисфенол А) и большому, постоянно растущему внутреннему рынку потребления. На сегодняшний день производство поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана в России отсутствует, и поэтому производство такого важного полимера позволит преодолеть технологическое отставание в промышленности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БИСИМИДА 2,2-БИС [4(3,4-ДИКАРБОКСИФЕНОКСИ)ФЕНИЛ]-ПРОПАНА | 1992 |
|
RU2036906C1 |
| Способ получения полиэфиримида | 1974 |
|
SU1151201A3 |
| ПОЛИКАРБОНАТЫ И СОПОЛИКАРБОНАТЫ С УЛУЧШЕННОЙ АДГЕЗИЕЙ К МЕТАЛЛУ | 2007 |
|
RU2451035C2 |
| Способ получения полиэфиримидов | 1974 |
|
SU674677A3 |
| Способ получения ароматических бис (эфироангидридов) | 1974 |
|
SU547175A3 |
| РЕАКТИВНЫЙ РАЗБАВИТЕЛЬ ФТАЛОНИТРИЛЬНЫХ СМОЛ И ТЕРМООТВЕРЖДАЕМАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2018 |
|
RU2712547C1 |
| Способ получения полиэфиромидов | 1974 |
|
SU541440A3 |
| Способ получения полиэфиримидов | 1974 |
|
SU1181553A3 |
| Бис-(аценафтенхинонокси)-арилены в качестве мономеров для теплостойких пленко- и волокнообразующих полихиноксалинов | 1976 |
|
SU653249A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2-БИС[4-(4-НИТРОФЕНОКСИ)ФЕНИЛ]ГЕКСАФТОРПРОПАНА ПОД ДЕЙСТВИЕМ УЛЬТРАЗВУКА | 2015 |
|
RU2577544C1 |
Изобретение относится к области технологии синтеза полимеров, конкретно к способу получения поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана (ПЭИ). Способ осуществляется реакцией бис(3-нитрофталимидо)бензола с динатриевой солью бисфенола А и характеризуется тем, что целевой продукт получают в смеси сухого ДМСО и сухого толуола в течение 18 ч при температуре 55°С. Бис(3-нитрофталимидо)бензол получают реакцией 3-нитрофталевого ангидрида с м-фенилендиамином с использованием N-метилпирролидона и толуола, с одновременным удалением образующейся воды азеотропной перегонкой. Динатриевую соль бисфенола А получают реакцией металлического натрия и бисфенола А в абсолютном метаноле и сухом толуоле с последующим упариванием образующегося раствора. Технический результат изобретения заключается в предоставлении метода получения целевого высокомолекулярного ПЭИ с отсутствием примесей циклического мономера и димера, а также высоким выходом продукта. 1 табл., 6 пр.
Способ получения поли-2,2-бис[4-(м-фениленфталимидо-3-окси)фенил]пропана реакцией бис(3-нитрофталимидо)бензола с динатриевой солью бисфенола А, отличающийся тем, что целевой продукт без примесей циклического мономера и димера, среднечисловой и средневесовой молекулярной массы, равной 215709 и 617697 соответственно, получают в смеси сухого ДМСО и сухого толуола при температуре 55°С в течение 18 ч, при этом бис(3-нитрофталимидо)бензол получают реакцией 3-нитрофталевого ангидрида с м-фенилендиамином с использованием N-метилпирролидона и толуола, с одновременным удалением образующейся воды азеотропной перегонкой при помощи ловушки Дина-Старка, а динатриевую соль бисфенола А получают реакцией металлического натрия и бисфенола А в абсолютном метаноле и сухом толуоле с последующим упариванием образующегося раствора при 15 Торр, при этом выход целевого продукта составляет 91,1%.
| White D.M | |||
| et al | |||
| Насос | 1917 |
|
SU13A1 |
| Journal of Polymer Science: Polymer Chemistry Edition, v | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Аэропланная лыжа удобообтекаемой формы | 1924 |
|
SU1635A1 |
| Кумыков Р.М | |||
| и др | |||
| РЕАКЦИИ СИНТЕЗА ПРОСТЫХ АРОМАТИЧЕСКИХ ПОЛИЭФИРОВ И ПОЛИЭФИРАРИЛЕНИМИДОВ С ИСПОЛЬЗОВАНИЕМ НИТРОСОДЕРЖАЩИХ | |||
Авторы
Даты
2024-12-23—Публикация
2024-02-15—Подача