наково взаимодействует и с белками глубоких слоев кожи так, что кожа, по лученная после такой обработки, имеет поверхность, испорченную бороздками и углублениями , Цель изобретения - получение фермента, обладающего более селективным действием, обеспечиващим более эффективную ферментативную эпиляцию, без порчи кожи„ Поставленная цель достигается тем что согласно способу получения нового протеолитического фермента из Strepto myces caligosus DS ItjSS штамм NRRL 8195, культивируют указанный продуцен в аэробных условиях на питательной среде, содержащей источники углерода, азота, минеральные соли и о случае не;обходимости фактор роста, при начальном рН ,8 и температуре 23 33С с последующим отделением куль туральной жидкости и выделением фермента „ Причем культивирование проводят обычно при аэрировании среды со скоростью аэрации 0,3-3 л воздуха на 1 л питательной среды в 1 мин„ Наиболее близким к Streptomyces caligosus DS является Streptomyces nobori toens is,так как последний производит мелаиновый пигмент на органических средах, развивает на большинстве питательных сред более или менее густую темно-(коричневую грибницу, в частности на картофеле, где он образует вегетативную грибницу весьма густого коричневого цвета и имеет спо ровую воздушную грибницу серого цвета Однако описываемый штамм следует отличать от известного, так как Strep tomyces noboritoensis не образует повторяющихся спиралей споровых цепочек не сжижает желатину или делает это слабо, не дает растворимого пигмента или дает только слаборастворимый коричневатый пигмент только на аспарагин-глюкозовом агаре, производит раст вориь«а1Й густой красно-коричневый пигмент на питательном агаре, тогда как Streptomyces caligosus DS lAi86 образует споровые цепочки, которые регулярно закручиваются в сжатые спирали, сжижает желатину, дает черный растворимый пигмент на глюкозо-аспарагиновом агаре и дает серовато-коричневый растворимый пигмент на пита тельном агаре; Streptomyces noboritoens is образует также на содержащем нитраты синтетическом агаре, на саха624розе неокрашенную вегетативную грибницу, тогда как Streptomyces caligosus DS на этой среде образует сjpOBaTO-коричневую толстую вегетативную грибницу; к тому.же Streptomyces noboritoensis не усваивает ни рамнозы, ни сахарозы, а усваивает ( и очень ограниченно) только арабинозу, инозит и ксилозу, тогда как Streptomyces caligosus DS усваивает очень хорошо все эти источники углерода. Стрептомициновый штамм, которьй является организмом-продуцентом нового протеолитического фермента, извлечен из образца земли, ему присвоен номер DS о Образец этого штамма находится на хранении в музее Nortern National Research laboratory US, (Сельскохозяйственный департамент в PEOPIA, Ш, США), где он зарегистрирован под номером NRRL 8195 Этот организм ввиду его новых качеств, которые не позволяют отождествить его с уже описанными видами, еледует рассматривать как новый вид с наименованием Streptomyces caligosus DS I4it86. Выделение осуществляется по общему методу, который состоит в суспендировании небольшого количества земли в дистиллированной стерильной воде, в разбавлении суспензии до различных концентраций, в растекании небольшого объема каждого разбавления по поверхности чашки Петри, содержащей питательный агаро После инкубации при 2б°С в течение нескольких дней, что позволяет микроорганизмам развиться, колонии, которые можно изолировать для проведения исследования, отбирают и пересаживают на питательный агар для того, чтобы получить более обильное разведение Streptomyces caligosus DS образует цилиндрические споры размером 0,8-1,0 мк/0,6-0,8 мк„ Он образует спороподобные гроздья; цепи спор могут насчитывать до нескольких десятков спор, они закручиваются в сжатые более или менее длинные спирали, образуя, в основном 2-3 кольца, но довольно часто и до 6-8 или доже до 12 колец По виду своего спорообразования Streptomyces caligosus DS размещается в Section Spira .по классификации Придама. Streptomyces caligosus DS хорошо развивается при 26°С, плохо при и совсем не развивается при Он имеет споровую воздушну грибницу серого цвета Окраска ее ве гетативной грибницы в зависимости от питательной среды меняется от более или менее густой коричневой до темно-коричневой. На органических средах, особенно на специальном тирозиновом агаре - дрожжевом экстракте Ваксмана ( меланинобразущей среде), он дает вещество а довольно большом количестве с меланиновой окраской, которая придает среде темный оттенок; на многих синтетических ре дах он способен производить в более или менее значительных количествах растворимый черноватый пигмент В питательных средах поддерживаемых при 26 С, фермент обладает следующими биологическими характе ристиками: Образование мела- Происходит Нина. Образование - и ТирозиназаОбразуется Разжижение жела- Происходит тины Усвоение целлю- - лозы Образование нит- Отсутствует на РИДОВ из нитра- питательном бу товльоне, содержа щем нитраты, происходит на синтетических средах. Происходит Гидролиз амидона Диспергировани Питательная среда без коагуляции на снятом молоке Результаты выращивания Streptomyces caligosus DS mtSS иа различных питательных средах приведены в табл Культивирование проводят около 3 недель при , кроме указанных и ключений. Эти характе ист ики наблюда ются на питательных агарах и бульонах обычно используемых для определения -морфологических характеристик штаммов Streptomyces, выращивание на ага ровых средах осуществляется на наклонных агарах. Ряд использованных сред для выращивания приготовлено по известным формулам, указанным, на пример , В случае З состав среды обозначен буквой WH номе ром, который приписан ему . Составляющие других питательных сред также известны L J Особенность Streptomyces caligosus DS 8() усваивать различные ис162 точники углерода или азота для обеспечения своего развития и степень раз вития, наблюдаемая на основной среде с замещением глюкозы различными, соответственно испытанными источниками углерода, либо различными, соответственно испытанными источниками азота ();) показан в табл. 2, Для получения нового протеолитического фермента выращивание Streptomyces caligosus DS IlifSS штамм NRRL 8195 можно осуществлять методом аэробного выращивания на по верхности или в глубине, последний спосо() особенно удобен ..С этой целью используют технику засевания и ферментации, а также различные типы аппаратов, которые обычно используются в ферментационной промышленностио Ферментационная среда в принципе является известной 7 и содержит источники усваиваемых углерода и азота, минеральные элементы и в случае необходимости факторы роста, все эти элементы могут быть внесеньг в виде отдельных веществ или в виде сложных смесей, которые находятся вобиологических продуктах различного прохождения о В качестве источника усваиваемого углерода можно использовать углеводы, такие как глюкоза, сахароза, мальтоза, декстрины, амидон или другие углеродсодержащие вещества, как глицерин или некоторые другие органические кислоты (молочная и лимонная кислоты) о Некоторые животные или растительные масла (свиное сало и соевое масло) могут выгодно заменять эти различные углеродсодержащие источники или могут быть добавлены к ним Подходящие источники усваиваемого азота чрезвычайно разнообразны. Они могут быть очень простыми химическими веществами, например неорганическими или органическими солями аммония, мочевиной, некоторыми аминосодержащими кислотами. Они могут быть также внесены сложными веществами, содержащими азот в белковой форме: казеином, лактальбумином, Тлотеном и их гидролизатами, соевой, арахисовой, рыбной мукой, мясными экстрактами, дрожжами, растворимыми дистилляторами и замоченным зерном, Среди добавляемых элементов некоторые могут иметь буферное или нейтрализующее действие, как, например, фосфаты щелочных или щелочно-земель71 . нмх элементов или карбонати кальция и магния о Другие приносят ионное рав новесие, необходимое для развития Streptomyces caligosus DS и дл переработки фермента, как, например, хлориды и сульфаты щелочных и щелочно-земельных элементов о Наконец, некоторые действуют более специфически как активаторы метаболических реакций Streptomyces cnl igosus DS это соли цинка, кобальта, ;(елеза, меди и мер ганца о факторы роста - это вещества типа витаминов, такие как рибофлавин, фолиевая кислота, пантотеновая кислота о . рН ферментационной среды при начале разведения должно находиться в пределах ,8, предпочтительно 6,2-7,0 Оптимальная температура ферментации находится в пределах 25-30 С но удовлетворительный рост получается при 23-33°С. Аэрация брожения может меняться в широких пределах. Однако найдено, что аэрация 0,3-3 л воздуха на 1 л бульона в 1 мин наиболее оптимальна. Максимальный выход фермента 2 199 RP получают после 2-8 дней развития, это время существенно зависит от используемой питательной ереДы. Фермент может быть выделен из сусла для брожения следующим образом Сусло для брожения можно фильтровать в случае необходимости в присут ствии фильтрующего агента при том рН , ко торое создается в среде в конце процесса получения. Полученный фильтрат концентрируют до 1 /5 первоначального объема, затем фермент осаждается добавление растворителя, например ацетона. Неочищенный продукт может быть очищен путем фракционного осаждения с помощью твердых неорганических солей или водных концентрированных растворов, например сульфата аммония и/или растворителя фермента, например ацетона Продукт может быть также очищен путем диализа через мембрану, предпочтительно через мембрану из регенерированной целлюлозы о Разведение Streptomyces caligosus NRPL 8195 в описанных условиях позволяет получить фермент 2 199 RP белкогеое вещество, имеющее вид порошка темно-коричневого цвета, достаточно хорошо растворимое в воде, очень слабо растворимое в концентрированном водном растворе нейтральных солей 628 (например сульфата аммония и в водноспиртовых или водно-ацетонивых смесях, практически нерастворимо с спиртах и в безводных кетонах; масса его молекулы равна 27000 и его изоэлектрическая точка лежит при 3j7 Протеолитическая активность нового протеолитического фермента проявляется на большом числе белковых субстратов таких, как казеин, гемоглобин, фибрин (лизис сгустков крови) J/lли молоко (коагуляция Активность на казеине определяетс способом, аналогичным способу Кунитца„ Пептиды, растворимые в трихлоруксусной кислоте, которые высвобождаются во время гидролиза, определяются либо спектрометрически при 280 нм (тогда выражаются в единицах Кунитца), либо колориметрически о Активность выражается в мг тирозина, образующегося за минуту в условиях проведения определения. Коагулирующая активность на молоке определяется согласно способу, предложенному Берриджем, и может быть выражена в единицах закваски (UP), on-, ределение которых таково: одна единица закваски - это количество фермента, которое способно вызвать свертывание 10 см молока за 100 с. Фибринолитическая активность определяется на сгустках стандартного фибрина, полученного действием тромбина на фибриноген, и может быть выражена в литических единицах, определение которых следующее: раствор в 100 литических единиц на см(100 UL/cM ) это раствор, который лизирует стандартный сгусток фибрина за 30 4иНо Следующие примеры показывают как изобретение может быть использовано на практике. Активность продукта выражается в единицах KUNIIZ (UK), определенных выше. Эта активность выражается в и К/см, когда речь идет о растворе, и UK/r, когда речь идет о твердом веществе Пример 1 о В ферментатор на 170 л помещают: Пептон, г1200 Дрожжевой экстракт, г 600 Агар-агар, Вода q,Srp, л105 рН среды 6 „55. Стерилизуют, блрботируя в течение 40 мин при 120 С. После охлаждения из-за конденсации паров во время стерилизации об-ьем бульона становится равным 115.л, его дополняют до 120 л путем доливания 5 л стерильного водного раствора, содержащего 1200 г моногидратной глю козы . рН среды 6,80. Засевают 205 см перемешиваемой культуры Streptomyces caligosus DS }kk86 штамм NRRL 8195. Культура развивается при в течение 23 ч с перемешиванием и аэрацией стерильным воздухом; тогда она становится пригодной для засевания для продуктивной разподки, Продуктивную разводку осуществляют в бродильном чане на ЗОО л, загруженном следующими веществами: Перегнанный растворитель, кг Сахароза, кг Соевое масло, л 0,08 Сульфат | арганца,кг 370 Вода, л рН среды подгоняют до 7,3 путем добавления 850 см соды, потом она стерилизуется барботированием пара с температурой 122° С в течение 40 I После охлаждения из-за конденсации паров во время стерилизации объем бульона становится равным 400 л, рН 6,60. Засевают ЦО л прививаемой культурь1 в бродильный чан на 170 л. Культу ра развивается при в течение 9 ч при перемешивании с помощью вра щающейся мешалки (205 об/мин) и при аэрации стерильного воздуха (20 тогда получается рН культуры 7,30 и объем сусла 400 л. Протеолитическая активность сусла при рН 7 и 37 С рав на 3,6 ик/см „ . Фильтруют 11 л сусла, полученного как описано выше, потом промывают ос док k л дистиллированной воды Фильт рат и промывку соединяют, затем концентрируют до 2 л при пониженном дав лении (5 мм рт.ст.), температура не ниже 30°С К охлажденному до концентрату быстро добавляют при пер мешивании 2, л ацетона, предварител но охлажденного до , Продолжают перемешивать в течение 2 мин, затем нерастворимую часть отделяют центрифугированием при и 5000( в теч ние 10 мин о Полученную нерастворимую часть последовательно экстрагируют 5Q см, потом 150 см воды при при -Ь4 С течение 2ч, отделяя в течение ч, отделяя каждый раз не растворенную часть центрифугирование при при 5000%- в течение 10 мин 10 2 Получают 800 см водного экстракта, рН которого 7 и 7,5. Этот экстракт поддерживают при н-+ С и добавляют при перемешивании г кристаллического сульфата аммония, перемешивание .продолжают еще 15 мин, после окончания добавления оставляют в покое на 1 ч, потом отделяют нерастворимую часть центрифугированием при 10000%- в течение 10 мин и при Нерастворившуюся часть растворяют 500 см помешиванием в течение 1 ч в воды, подгоняя рН до 6-7,5., и полученный раствор подвергаю диализу при +4°С в течение 17 ч в дистиллированной воде. Получают 920 см диализированного экстракта, в который быстро заливают и перемешивают 1,1 л ацетона, охлажденного до -10 С. Нерастворимый фермент отделяют центрифугированием при 5000 cj. в течение 10 мин при , потом высушивают при низком давлении при . в присутствии обезвоживающего агента (РуО , Окончательно получают 9,5 г фермента, ферментативная активность которого следующая: Протеазная активность, ик/г Коагулирующая активность, (J Р/г Фибринолитическая 920 активность, UL/r При м е р 2, ЗбО сусла, полученного по примеру 1 фильтруют на прессованном фильтре в пр исутствии 25 кг вещества, помогающего фильтрации, К 200 л полученного фильтрата добавляют АОО л метанола, охлажденного до -10 Со После охлаждения смеси до -10° С полученный осадок отделяют путем холодного центрифугирования и высушивают при низком давлении при , Отделяют 229 г фермента с активностью 290 и К/г о В табл. 3 собраны результаты, полученные на различных субстратах с предлагаемым ферментом. Активность фермента проявляется в широкой области рН: оптимальная величина рН для гидролиза казеина около 7,5, И фермент сохраняет по крайней мере 60 своей максимальной активности при рН 5-8,5. Максимальная активность фермента проявляется при температуре около 1110 , и активность очень быстро падает, когда температура превышает 50 С Специфичность фермента по отношению к кератину волос и кожи и к гликопротеинам волосяной луковицы и волос животных не может быть выведена из активности, полученной на обычных субстратах, представленных в приведен ных примерах, она может быть обнаружена только путем натурных испытаний удаления волос так, как они описаны ниже ферментативная эпиляция с использованием полученного фермента заключается в том, что обрабатываемую шкуру приводят в соприкосновение с ферментом в эпиляционном баке, в котором процент воды по отношению к шку рам составляет , предпочтительно 20-25 0 Операция продолжается ч, температура ванны находится в пределах 24-30°С и рН соответствует максимальной протеолитической актибности фермента, т„е находится между 7 и 8,5; рН удерживается постоянным во время операции путем использования буферных растворов, создаваемых обычно добавлением тринатрийфосфата или буры. Кроме того, можно считать, что 0, вес„ч, шкур является той областью .соотношений, в которой эффективность и себестоимость обработки оказываются наилучшими Практически способ обработки шкур состоит либо в погружении их в раствор, содержащий 10-30 г/л фермента, показатель активности которого около 290ик г, либо в применении опрыскивания из пистолета раствором, содержащим 1-10 г/л фермента, показатель которого около 290 U К/г (в случае овчины) и в случае овчины, и в случае шкур крупного рогатого скота используемая активность фермента опти чальна, когда его концентрация и его показатель находятся в указанных выше соотношенияхЁмкостью для эпиляции служит любой бак или барабан, которые используются при известных способах Для того, чтобы удаление волоса с кожи было полным, действие фермента должно сопровождаться или предшествовать механическому вытаскиванию . Это может быть просто трение одной шкуры о другую во время перемешивания, дополняемое в случае необходимости сгонкой волос во время короткого периода более интенсивного пере2мешиваниЯо Это может та1сже осуществляться пропусканием обрабатываемых кож через машину для сгона шерсти, ко торая позволяет получать неповрежденную и несваленную шерсть Предлагаемый способ может производиться и/или следовать за большим числом дополнительных операций Очистку шкур желательно производить до эпиляциио Она может состоять из мытья в воде в барабане или баркасе, предназначенном, в основном, для отмывки шкуры от солей, которыми она пропитывается при консервации Промывка может следовать за обезжириванием с помощью обычных ароматических или хлорированных растворителей или моющих водных растворов Эта операция позволяет убрать большое число органических загрязнений, таких как жиры и неорганические вещества, которые пачкают шкуру и закупоривают волосяные мешочки Обезжиривание было бы выгодно сопровождать новой промывкой водой таким образом, чтобы получить чистую шкуру ( насколько это возможно, лишенную загрязнений и очищающих веществ ;После эпиляции шкуры промывают и воде позволяют стечь Промывная вода содержит неповрежденную шерсть и фермент, которые быть разделены известными способами - декантацией, фильтрованием Затем шкуры вводят в чистый известковый зольник, который гидролизует,их. Этот зольник используется много раз, так как шкуры, которые туда помещаются, практически чисты и только слабо загрязняют его Отмечено, что после обработки в зольнике лицевой слой кокш не портится и прочно скреплен с дермой, тогда как шкура, эпилированная посредством ферментов типа алкалазы, имеет испорченныи лицевой слои, студенистый при прикосновении, с оторванной, местами дермой Во время операции эпилирования сброс загрязняющих продуктов значительно уменьшается Особенно заметно это по отношению к сульфидам и к раст воренной шерсти,которых теперь совершенно нет в сточных водах, тогда как они в изобилии имеются в отбросах, получаемых при эпиляции путем растворения шерсти После обработки шкур можно осущес гвить все обычные операции дубильного
производства: обезэоливание,пикеле- вание, хромовое дубление, спилка и подстрижка, повторное дубление, эмульсионна я жировка, сушка, тяжка и чистовая обработка кожи,$
Полученные таким образом кожи имеют очень тонкое зерно, высокое качеств во по сравнению с теми, которые получены известково-сульфидным способом, to в них отсутствуют прожилки и они имеют очень хорошую адгезию .лицевой поверхйИсти даже на вытянутых частях боков животных.
в тебя.. приведены сравнительные данные, полученные при эпиляции шкур крупного рогатого скота тремя следующими способами: эпиляция с использованием предлагаемого фермента (А); эпиляция с использованием протеолитического фермента из Вас, subttlfs (В) и эпиляция известным путем с растворением волоса в ванне, содержащей известь и сульфид натрия (с)о
Положительно










| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФИБРИНОЛИТИЧЕСКОГОФЕРМЕНТА | 1972 |
|
SU434662A3 |
| Способ получения антибактериального и антикокцидиозного вещества | 1975 |
|
SU673184A3 |
| ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS - ПРОДУЦЕНТ КЕРАТИНАЗЫ | 2000 |
|
RU2177994C2 |
| Штамм актиномицета SтRертомUсеS LaVeNDULae - продуцент протеолитических ферментов | 1989 |
|
SU1735364A1 |
| Способ получения антибиотика | 1965 |
|
SU556732A3 |
| Способ получения антибиотика 17.967 | 1969 |
|
SU544385A3 |
| ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS-ПРОДУЦЕНТ ЩЕЛОЧНОЙ ПРОТЕАЗЫ | 2005 |
|
RU2303066C1 |
| Способ получения метаболита "а 27 106 | 1974 |
|
SU539538A3 |
| ПИТАТЕЛЬНАЯ ДОБАВКА ДЛЯ СРЕДЫ СПИРТОВОГО БРОЖЕНИЯ | 2007 |
|
RU2495926C2 |
| Способ получения антибиотика | 1964 |
|
SU561520A3 |

D-Манитолл Положительно L-Тирозин
Положительно, но медленно
Положительно
II
II
Положительно
Отрицательно Положительно ...D-Сорби Инозито Салицин Показатели
Вид шерсти:
волосяные мешочки
поверхность
На ощупь
Гибкость
Отделка на машине
Сопротивление натяжению,
кг/мм
Удлинение при разрыве, %
Стрела прогиба при образовании складки, мм
Очень чистые Мало чистые Округлая Очень ровная
Слегка плот- Слегка плотная ная
Хорошая Средняя
1,5 66
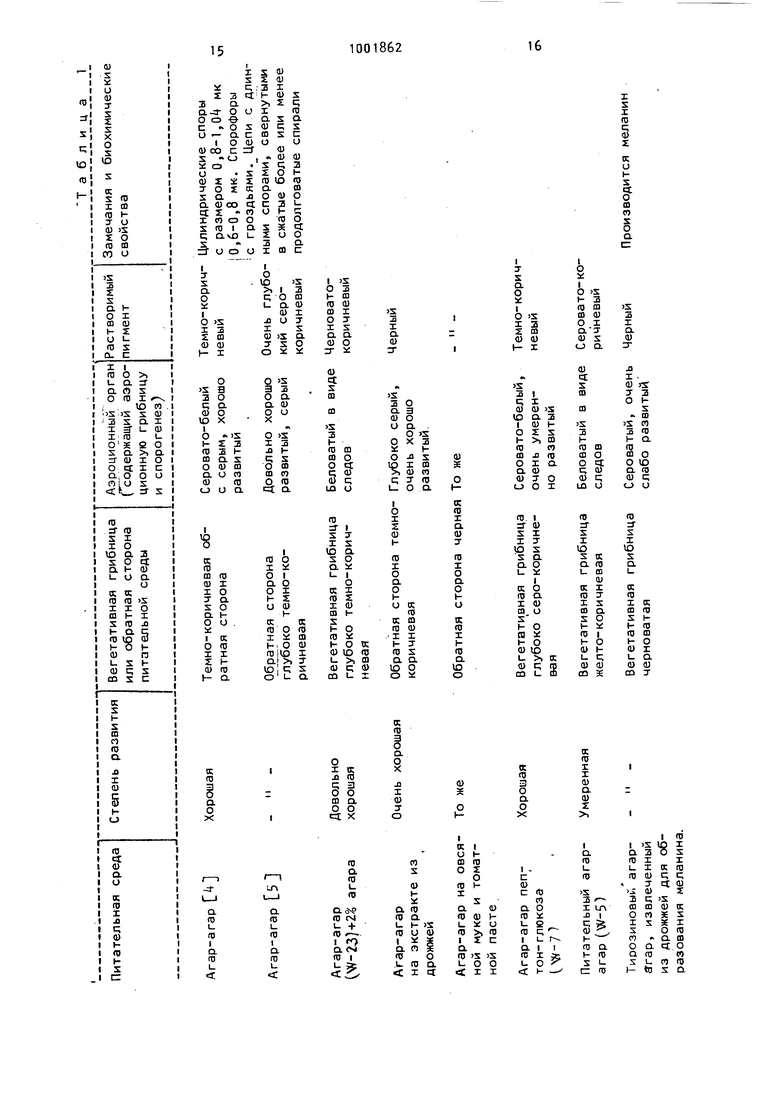
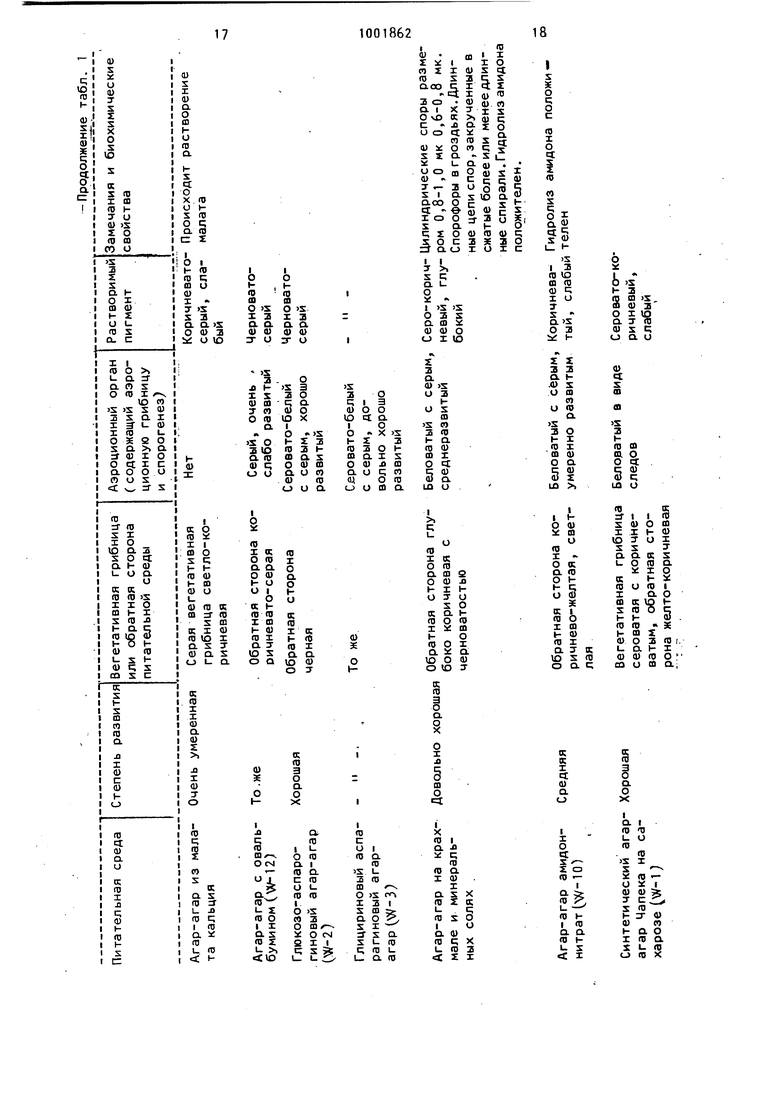
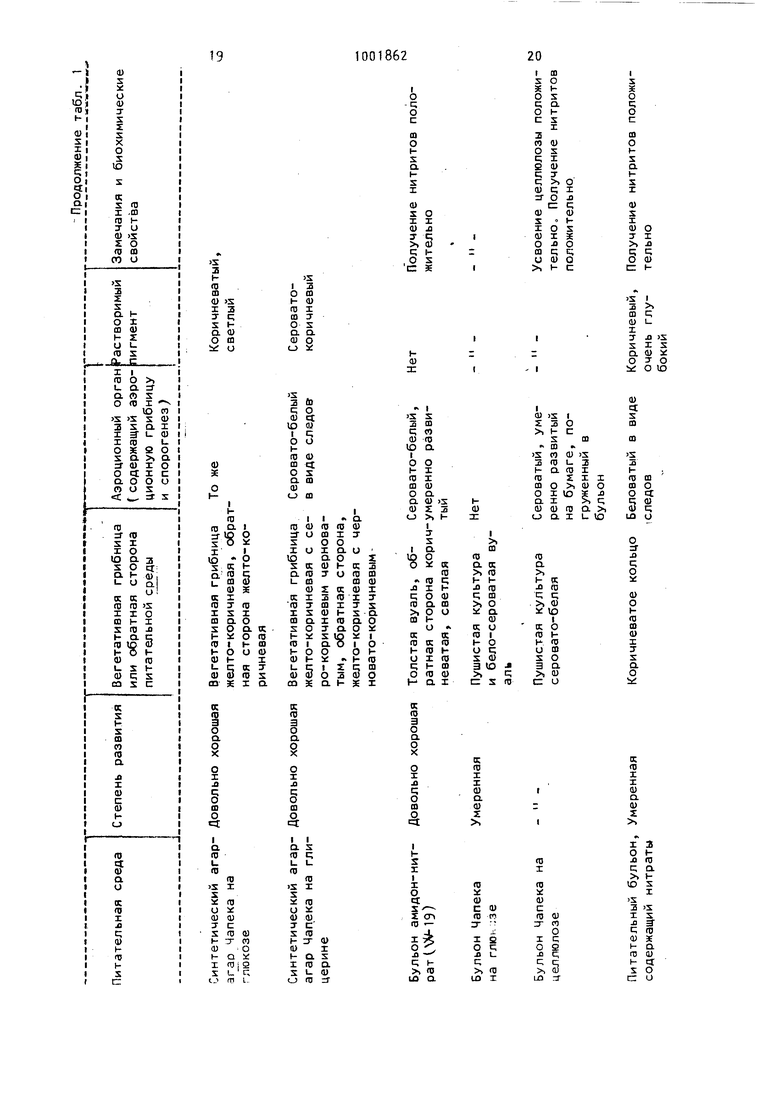
7,5 Г11 1L....L.J...1.:. - DL-Пролин и - и L-Хистидин, - Ограниченно L-Триптофан - и Субстрат I РеакцияАктивность Казеин Протеолиз Ик/г Молоко Свертывание Й500 UP/r Фибриоген Лизис сгуст- 4920 Ои/мг ков фибрина 1LО Реакция при рН 7,5 и при 37 С, концентрация субстрата 5 г/л. Реакция при рН 6,35 и при на восстановленном молоке Реакция лри рН 7,5 и при . .... .-/.L.i...l.......L.L....... Продолжение табл. 2 Бетаин Таблица 3 - Таблица А Способ эпиляции
27 100186228
формула изобретенияИсточники инфорМэции,
кого фермента из Streptonyces caligo-(f 66002, кл. А 22 В 5/08, .
SUS DS штамм NRRL 8195, о т л л-52„ Грачева И.М. Технология ферментчающийся тем, что осуществляютных препаратов М„, Пищевая промышкультивирование указанного продуценталенность, 1975, с, k7-,
в аэробных условиях на питательной3. Waksman S,A The Actinomyceсреде содержащей источники углерода,tes The Willfams and Wilkins Comазота, минеральные соли и в случае не-Юрапу, Baltimore, 19б1 , v.v J ,2-,
обходимости фактор роста, при началь-Ц, Pridham T.G. et col. Hickey and
ном рН 5,8-7,8 и температуре 23-33С гTresners Agar. - Antibiotics Annuc последующим отделенмем культуральнойal., 1956-950.
жидкости и выделением фермента.5. Waksman S.А. The Actinomyce2. Способ по п. 1, о т л и ч а ю- 15tes Sennets Agar, 19б1, v. 2, p.331.
ц и и с я тем, что культивирование6. H.D. Tresner et F. Yandaпроводят при аэрировании среды со ско- G. of Bacteriology, 1958, 76 239-2.
ростью аэрации 0,3-3 л воздуха на 1 л,J, Патент Великобритании № 1377105,
питательной среды в 1 мин;кл, С 12Т 13/10, опублик„ 197
принятые во внимание при экспертизе
Авторы
Даты
1983-02-28—Публикация
1977-08-24—Подача