соким коронарорасширяющим действием и проявляющих меньшую токсичность при действии на живой организм.
Указанная цель достигается новым химическим соединением - З-фенил- 2 - 2 -диэтиламиноэтокси)-5-хлорфенил -пропанола-1 гидрохлоридом вышеуказанной формулы (1), обладающим коронарорасширяющим и спазмолитичесКИМ действием.
. Описываемое соединение получают гидрированием исходного 3-фенил-1 2 (2 -диэтиламиноэтокси)-5 -хлорфёнил пропен-2-она-1, взятого в свободном виде или в виде гидрохлорида, в полярном органическом растворителе, таком как низший алифатический спирт или указанная кислота, в присутствии катализаторов гидрирования при атмосферном давлении и комнатной температуре. В качестве катализаторов гидрирования используются палладий, осажденный на карбонате кальция, угле, или сернокислом барие, или никель Ренея. Выход целевого продукта составляет 50-88%. Структура соединения доказана данными элементного анализа и спектральных исследований. Для Cj, Hj O-iNCl..
Найдено, %: С 63,88; Н 7,24j . N 4,00; С1 17,54.
Вычислено, %-. С 63,64; Н 6,87; N 3,53; С1 17,91.
ИК-спектр (таблетка КВг): 1675 см (); 2300-2700 ( NH); 3030,
4- .
1595j 1485 (ароматическое кольцо) 2980, 2940, 2915; 2870, 1463, 146р, 1470, 1385 см- ( СН); 1270 см
(c-o-q-).
ЯМР-спектр (СДСЦ, ГМДС, 100 мгц): (6,91-7,44 м.д. CeHs-, CfeH,, NH;
9-Н; мультиплет); 4,55 м.д. (-О-СН 2-Н; триплет); 2,82 - 3,35 м.д.
( 10-Н; мультиплет); 1,26 м.д. (-СНJ; 6-Н; триплет).
3-Фенил--1. - (2 -диэтиламиноэтокси -5-хлорфенил1-пропанон-1 гидрохло рид представляет собой белый мелкокристаллический порошок с т.пл. 129,5131 С, хорошо растворим в воде, низших спиртах, хлороформе. Нерастворим в ацетоне, эфире, этилацетате.
П р и м е р ы 1-6. Растворяют 7,9 г (0,02 моль) 3-фенил-1- 2-(2 диэтиламиноэтокси)-5 -хлорфенил }-пропен-2-она-1 гидрохлорида кристаллогидрата (в случае гидрирования с никелем Ренея в реакции используют основание) в 70 мл растворителя и добавляют катализатор гидрирования, гидрируют до поглощения расчетного количества водорода (500 мл), отфильтровывают катализатор, упаривают растворитель, К маслянистому остатку добавляют 10 мл холодного этилацетата, при этом выпадает белый кристаллический осадок (в случае гидрирования с никелем Ренея, этилацетатный раствор обрабатьшают этиловым спиртом, насьш;енным. хлористым водородом) Осадок отфильтровьшают, промьшают на фильтре 5 мл этилацетата и перекристаллизовывают из смеси этилового спирта и этилацетата. Условия получения и выходы целевого продукта приведены в табл. 1.
Фармакологическое действие 3-феmui-l- J2 -(2-диэтиламиноэтокси)-5 хлорфенил -пропанона-1 гидрохлорида изучают Следующим образом.
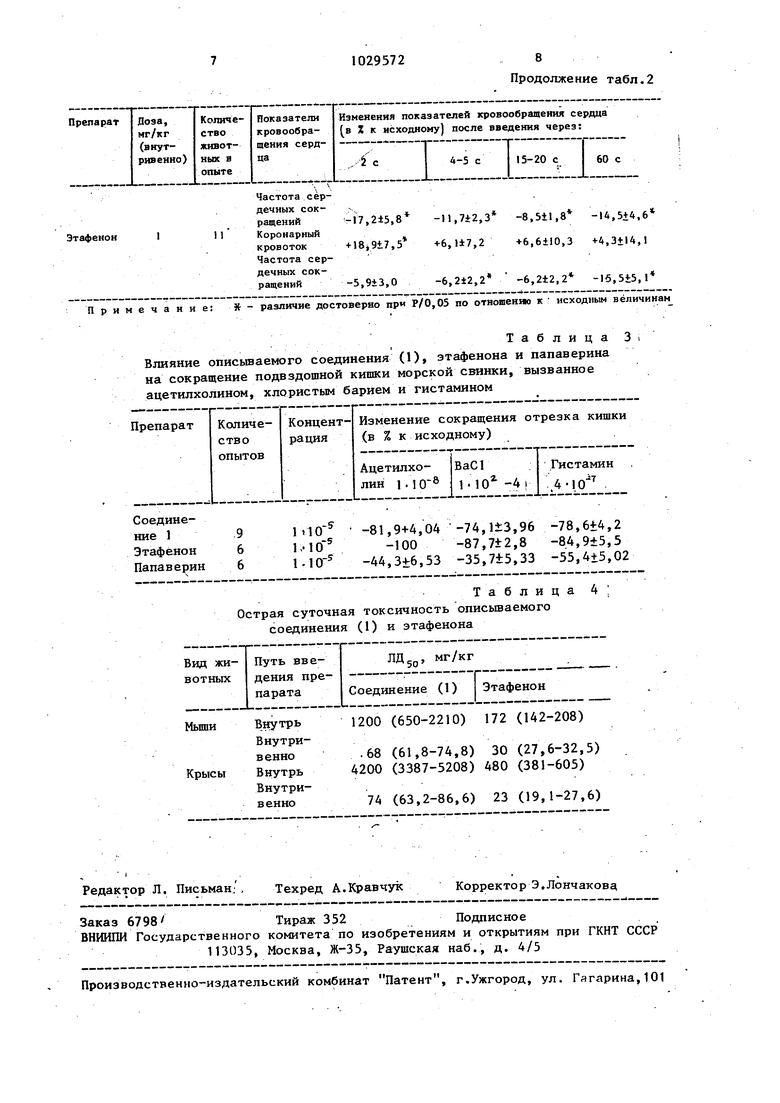
В острых опытах на кошках изучаютвлияние описываемого соединения (1) в сравнении с этафеноном на объемную скорость коронарного кровотока, частоту пульса, артериальное давление и вегетативно-сосудистые реакции, вызванные адреналином и норадреналином. В опытах in vitro исследуют влияние препарата на сокращение изолированного отрезка подвздошной кишки морской свинки, которое вызывают хлористым барием,.ацетилхолином и гистамином. Острую суточную токсичность (ЛД др) определяют на белых мьшгах и крысах.
,L ,
Результаты опытов, представленные в табл. 2, показьшают, что описьшаемре соединение (1) в дозе 1 мг/кг (внутривенно обладает выраженным
-, коронарорасширяющим действием. Так, через 2 мин после введения соединение (1) увеличивает объемную скорость коронарного кровотока на 124%. Коронарорасширяющий эффект препарата хотя и уменьшается со временем, но остается значимым в течение 1 ч. Коррнарорасширяющее действие этафенона значительно слабее: коронарный кровоток усиливается в течение 2 мин на 18,9%. Оба препарата в указанной доз вызывают брадикардию.
Соединение (1) и этафенон не оказьшают существенного влияния на артериальное давление и вегетативно-сосудистые реакции.
В оцытах in vitro было обнаружено что соединение (1), также как и эта- . фенон, в концентрации Ь уменьшает сокращение отрезка кишки, вызванное ацетилхолином, хлористым барием и гистамином. Оба препарата по спазмолитическому действию превосходят папаверин (табл. 3).
Определение острой суточной токсичности показывает, что соединение
(} на разных видах животных и при различных путях введения менее ток-
сично, чем этафенон-(табл. 4).
I . .
Таким образом, описываемый 3-фенил-1- 2 -{2 -дизтиламиноэтокси)-. 5-хлорфенил -пропанона-1 гидрохлорид проявляет более высокий коронарорасширяющий эффект, чем используемый в медицинской практике этафенон, и з обладает значительно меньшей токсиЧ ностью


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения О-(2-диэтиламиноэтокси)- @ -фенилпропиофенона гидрохлорида | 1981 |
|
SU1015598A1 |
| ГИДРОХЛОРИДЫ N-АЛЛИЛ- И N-[3-(3,4-ДИМЕТОКСИ)-ФЕНИЛ]-2-ПРОПЕНИЛИЗОХРОМАНИЛ-1-МЕТИЛАМИНОВ, ОБЛАДАЮЩИЕ КОРОНАРОРАСШИРЯЮЩЕЙ АКТИВНОСТЬЮ | 1983 |
|
SU1137734A1 |
| Производные 1-арил-2-метоксикарбонил-3-метил-1,4-дигидро-бензотиено(3,2- @ )-пиридин-9,9-диоксида,обладающие коронародилатирующей активностью | 1981 |
|
SU1018396A1 |
| 2-Оксо-4-(о-дифторметилтиофенил)-5-метоксикарбонил-6-метил-1,2,3,4-тетрагидропиримидин, обладающий коронарорасширяющим действием | 1985 |
|
SU1433958A1 |
| МОРФОЛИЛАМИД 5-N-МОРФОЛИНОМЕТИЛФУРАН-2-КАРБОНОВОЙ КИСЛОТЫ, ИЛИ ЕГО ГИДРОХЛОРИД, ИЛИ ЕГО ОКСАЛАТ, ИЛИ ЕГО ЦИТРАТ, ОБЛАДАЮЩИЕ КОРОНАРОРАСШИРЯЮЩИМ ДЕЙСТВИЕМ | 1979 |
|
SU841275A1 |
| МОРФОЛИЛАМИД 5-ХЛОРМЕТИЛФУРАН-2-КАРБОНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ КОРОНАРОРАСШИРЯЮЩЕЙ АКТИВНОСТЬЮ | 1979 |
|
SU770049A1 |
| ФУНКЦИОНАЛЬНО ЗАМЕЩЕННЫЕ 1-ФЕНИЛОЛИГООКСИЭТИЛАМИНЫ, ПРОЯВЛЯЮЩИЕ АНТИАРИТМИЧЕСКУЮ АКТИВНОСТЬ | 1997 |
|
RU2141941C1 |
| СПОСОБ ПОЛУЧЕНИЯ (1R,2R)-3-(3-ДИМЕТИЛАМИНО-1-ЭТИЛ-2-МЕТИЛ-ПРОПИЛ)-ФЕНОЛА | 2007 |
|
RU2466124C2 |
| Способ получения 1-(алкилгидроксифенил)-1-гидрокси-2-(алкиламино)-пропанов или их фармакологически активных солей | 1984 |
|
SU1319783A3 |
| @ -Бициклическое производное норпростановой кислоты, обладающее спазмолитической активностью | 1981 |
|
SU1028667A1 |
3-Фенил-Г- 2-
3-Фенил-1 - 2 (2 -диэтиламииоэтокси)-5 -хлорфенил -пропен-2-она-1 гидрохлорид
То же
11
3-Фенил-1- 2 (2 -диэтиламиноэтокси)-5 -хлорфешш -пропен-2он-1
Влияние описьтаемого соединения 1 -и этафенона- на объемную скорость коронарного кровотока и частоту сердечных сокрацений Коронарный Контроль кровоток Частота сердечных сокращений О Коронарный +12A,2t24, Соединение (I) кровоток
Таблица 1
Этиловый
спирт Уксусная
кислота Этиловый
спирт Метиловый
спирт Изопропиловый 0,67 cniipT
70
Никель Ренея Этиловый 1,0 спирт
Таблицаа -1.2±3,5 -5,4±3.7 -5,,3 -Г, ,1 . . . О -г,04-1,4 -0,,4 93,2±16,8 +51,0±14,5 +27,4iH,8 I 11 Этафенон Примечание: ftВлияние описьш на сокращение ацетилхолином,
Острая суточная токсичность описьшаемого соединения (1) и этафенона
Продолжение табл.2
Таблица 4 Частота сердечных сокращенийКоронарный кровоток +18j9t7,5 +6,147,2 +6,6+10,3 +4,3+14,1 Частота сердачных сокращений -5,9+3,0 -6,2±2,2 -6,2±2,2 -15,515,1 различие достоверно при Р/0,05 по отношению к исходным величинам емого соединения (1), этафенона и папаверина одвздошной кишки морской свинки, вызванное хлористым барием и гистамином -17,2±5,8 -n,7i2,3 -8,5±1,8 -14,5+4,6 Т а б л И Ц а 3 S
| H.J | |||
| Hapke, W | |||
| Sterne Pharmacplogische und toxicoloaische Untersuchungen zur Wirkungscharakterisierung von Etafenon, AfEneiroittelForschung, 1969, № 10, s | |||
| Штатив для микроскопа | 1924 |
|
SU1664A1 |
| W.K | |||
| Kukovetz Wirkung von o-(Die aihylaininoathoxy)-phenylpropiophenol | |||
| HCl (Ethafenoti) auf Dynamik, stoffwechsei, O j -Utilisation und CoronarodurchfluB des Herzens, Arzneimittel-Forschung, 1969, № 10, s | |||
| Автоматическое переключающее приспособление для паровозных инжекторов, работающих свежим и мятым паром | 1924 |
|
SU1672A1 |
Авторы
Даты
1989-09-15—Публикация
1981-06-29—Подача