1l Изобретение относится к химии семичленных циклических фосфонатов с атомом фосфора в цикле, э именно к усовершенствованному способу полумения 2-(2-хлоралкокси)-2-оксо-1 ,,2-ди оксафосфепанов общей формулы Cl-CH-CHOx в в Е5 Б 15 «7 R , R -и R - водород или где R , R метил; R и R - водород, алкил или фенил, которые могут быть использованы в качестве пластификаторов пластмасс с целью придания последним антипиренных свойств, в качестве мономеров для получения полимеров, а также в качестве селективных экстрагентов благородных и редких металлов. Известен способ получения 2-(2-хло алкокси)-2-оксо-1 ,1,2-диоксафосфорина нов взаимодействием 2-хлор-1,3,2-диоксафосфоланов с 1,3-диоксоланами в среде инертного органического растворителя при 0-150 С в присутствии ката лизатора - хлористого цинка Cl ; Наиболее близким к предлагаемому изобретению по технической сущности и достигаемому результату являTi72 ется способ получения 1,|,2-диокса- , фосфепанов, в частности 2-(2-хлорэтокси)-2-оксо-1 ,4,2-диоксафосЛепана, заключающийся в том, что 2-хлор-1,352-диоксафосфолан подвергают взаимодействию с 1,3-диоксаном при 80-100 С в присутствии катализатора - четыреххлористого олова с последующим выделением целевого продукта перегонкой Выход неочищенного продукта около 15° ПгТ . к недостаткам известного способа относится низкий выход целевого продукта, а также его загрязненность. Целью изобретения является повышение выхода целевых продуктов и расЬйрение их ассортимента. Поставленная цель достигается способом получения 2-(2-хлорал(окси)-2-оксо-1,,2-диоксафосфепанов общей формулы (|), закликающимся в том, цуо незамещенный или метилзамещенный 2-хлор-1,3,2-диоксафосфолан подвер ают взаимодействию с 1,3-Диоксаном при нагревании до бО-ЮО С в среде 1, -диоксана в присутствии катализатора - хлористого цинка, с последующим нейтральным гидролизом образующейся реакционной смеси при . нейтрализацией выделившейся кислоты раствором.щелочи и экстракцией целевого продукта. Процесс протекает по схеме:





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-( -хлоралкокси) -2-оксо-1,4,2-диоксафосфоринанов | 1979 |
|
SU777040A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ТИО-2-ПИРРОЛИДИДО-1,3,2- ДИОКСАФОСФОЛАНОВ ИЛИ ФОСФОРИНАНОВ | 1972 |
|
SU430102A1 |
| СПОСОБ ПОЛУЧЕНИЯ2-01{СО-2-ПИРРОЛИдаДО-1,3,2-ДИОКС АФОСФОЛАПОВ ИДИ ^ЮФОРИНАТОВ | 1972 |
|
SU433152A1 |
| Способ получения N-ацил-2-окси-1,3-диаминопропанов | 1978 |
|
SU910114A3 |
| Способ получения 0-(2-Хлоралкоксикарбонилфенил)фосфонитов | 1988 |
|
SU1583427A1 |
| Способ получения 2-хлорциклобутанонов или 2-хлорциклобутен2-онов | 1975 |
|
SU608468A3 |
| Способ получения эфиров алкилсульфоновых кислот 1,3,2оксазафосфациклических соединений | 1973 |
|
SU518137A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ |5-(р-ХЛОРАЛКОКСО)-винилфосфоновых кислот | 1971 |
|
SU302344A1 |
| ПРОИЗВОДНЫЕ 5,6-БИСАРИЛ-2-ПИРИДИНКАРБОКСАМИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В ТЕРАПИИ В КАЧЕСТВЕ АНТАГОНИСТОВ РЕЦЕПТОРОВ УРОТЕНЗИНА II | 2009 |
|
RU2497808C2 |
| 2-(1-Гидрокси-2,2,2-трихлорэтил)-2-оксо-4-хлорметил-1,3,2-диоксафосфолан, обладающий гербицидной активностью | 1986 |
|
SU1398362A1 |
СПОСОБ ПОЛУЧЕНИЯ 2-
Как видно из схемы, перегруппировка промежуточно образующегося пентаорганофосфорана может протекать в двух направлениях, - с раскрытием 1,3,2-диоксафосфоланового цикла (схема А) или с. его сохранением (схема Б).Экспериментально установлено, что во всех приведенных примерах имеет мест,о протекания перегруппировки по схеме Б (в большей или меньшей степени). Очистка целевых продуктов от побочных производится гидролизом при 720. При этом побочные (3 хлоралкокси)-алкил 3-2-оксо-1,3,2-диоксафосфоланы претерпевают полный гидролитический распад до кислоты, которая может быть оттитрована щелочью, 1,,2 Диоксафосфепаны в этих условиях оказываются гидролитически устойчивыми ц выделяют ся из гидролизата экстракциёй хлороформом. Взаимодействие алкиленфосфористых кислот с 1,3 диоксанами лучше всего . проводить при SO-IOO C в присутствии каталитических количеств безводного inClj (1 .г. ZnCl. на 1 моль реагентов) и трехкратного мольно.го избытка, 1 ,Адиоксана.в качестве растворителя. Выходы целевых 1 jt.Z-диоксафосфепанов колеблются от 22 до 8S,S% от теоретического. В целях увеличения выхода во всех случаях используют 3-5 часово нагревание реакционной массы. Способ прост в исполнении и базируется на доступных химических продуктах. Алкиленхлорфосфиты легко получаются из треххлористого фосфора -и гликолей с выходом более 90, Циклические 1,3-Диоксаны также доступные вещества, образующиеся при конденсации альдегидов и кетонов с 1,3 глико.лями, при винилировании 1,3-гликолей и при синтезе дивинила и изопрена по реакции Принса. Целевые 2-(2-xлapaлкoкcи)-2-oкco-1 ,,2-диоксафосфепаны - бесцветные вязкие жидкости, растворимые в спиртах, 1 ,|-диоксане, хлороформе и других органических растворителях за исключением предельных углеводородов В воде растворяются по-разному,. в за висимости от строения, радикалов Р - и R. Если ,H; Н, раство римость в воде хорошая. Если R и , , Н, -(} - раство римость в воде плохая. Общая методика получения и выделения 2-(2-хлоралкокСи)-2-оксо-1,t,2 диоксафосфепанов. .В стеклянный реактор, снабженный водяной термостатируемой рубашкой, термометром, капельной воронкой, мешалкой и обратным холодильником, помещают 1 моль 2-хлор-1,3,2-диоксафос фолана, 1 г безводного ZnP, 1 и 3,0 моль абсолютного 1 ,-диоксана. При температуре.раствора 80-100 С при пе ремешивании в реактор прибавляют 1 моль 1 ,.3-диоксана с такой скорость чтобы подъем температуры в реакторе не превышал трех градусов от заданной. По окончании прибавления реакци онную смесь перемешивают при этой же (80-ЮО С)температуре 3-5 ч и охлаж дают, заменив воду в рубашке на проточную холодную. К охлажденной реакционной смеси прибавляют 100 мл холо ной воды с растворенным индикатором (бромфеноловым синим) с такой скорос тью, чтобы температура не поднималас выше 20 С, а затем реакционную смесь при перемешивании нейтрализуют раствором щелочи до переходной окраски по индикатору. Полученный гидролизат переносят в делительную воронку, добавляют 300 мл воды и экстрагируют тремя порциями хлороформа (500:300 :300 мл). Объединенные вытяжки сушат безводным N а (3.504 отгоняют растворитель при пониженном давлении, аостаток перегоняют в вакууме. Получают чистые 1 ,, 2-дио.ксафосфепаны (табл.1 и 2). Выходы составляют 2285 от теоретического. Пример 1. Синтез2-(2-хлорэтокси)-2-оксо-1,,2-диоксафосфепана (1), В реактор помещают раствор 38 г (€,3 М) 2-ХЛОР-1,3,2-диоксафосфолана, 0,3 г ZnCli и 132 г (0,9 М) абсолютного 1 ,-диоксана. При и при перемешивании прибавляют 26,7 г (0,3 М) 1,3-диоксана. По окончании прибавления, реакционную смесь продолжают термостатировать () еще 5 ч, затем охлаж дают,. заменяя термостатированиё горячей водой на проточную с температурой-7-10 С, и при непрерывном перемешивании прибавляют tO мл воды с растворенным индикатором (бромфеноловый синий). Далее в этих же условиях прибавляют раствор КОН до переходной окраски по индикатору (расход КОН 39 мл), и по формуле „М. в. У N кон. 100 гидролиза - теоретическое количество фосфепана 100 где М.в. - молекулярный вес фосфепана; V - расход щелочи, мл; N - нормальность щелочи, находят % гидролиза, т.е. приблизительное содержание изомера с пятичленным циклом (23,21%). Гидролизат переносят-в делительную воронку, добавляют 100 мл холодной воды и экстрагируют трижды хлороформом (200:100: :100 мл). Объединенные хлороформенные вытяжки сушат безводным , удаляют растворители, а остаток фракционируют в вакууме. Получают 27 г (41,9) 2-(2-хлорэтокси)-2-оксо-1 i, 2-диокса фосфепана (|) (табл.1 и 2). Т.кип,С (мм. рт. ст.) 106-110 (2-10), . HR °Jf°2 «™ ,Ч2., Найдено, %: С 33,2; Н S,73; Р И,19; С1 16,66. . $10 Вычислено, I: С 33,58;Н 5,63; Р Й,|3; С1 16,52. . Прим ер 2. Синтез 2-f2-xnopэтокси)-2-рксо-3-метил-1,4,2-диоксафосфелана (1 1).. В реакторе к раствору 25 г (0,19б 2-хлор-1,3,2-диоксафосфолана, 0,2 г ZnClrj в 52 мл (0,588м) абсолютного 1,-диоксана при перемешивании и тем пературе 9бС прибавляют 20 г (0,19б 2-метил 1,3 диоксана. Реакционную смесь продолжают перемешивать еще 3 при и охлаждают, подключив к рубашке проточную воду. Прибавляют 50 мл воды с растворенным бромфеноло вым синим. При постоянном перемешива нии и температуре титруют 10 КОН до переходной окраски ( расход 22 мл) 228,621J 22 1,7857 20,14% ГИДР г,Ш -ТО Гидролизат переносят в делительную воронку, добавляют 100 мл воды и экстрагируют три раза хлороформом (100, 60, 60 мл) Объединенные вы тяжки сушат безводным Na Qi, удаляю растворители, а остаток перегоняют в вакууме. Получают 3,6 г (77,2%) чис того 2-(2-хлорэтокси)-2-оксо-3-метил -1,4,2-диоксафосфепана (11).Т. кип. (мм рт.ст.) 110-112(), 1,4824, dl 1,3122. 1).лилеА5.70, МКрЙЬ 50,Об. Найдено, I: С 36,4-3; Н 6,05; Р 13,57; С1 15,49. С7Н.404РС1 Вычислено, %: С 36,77; Н 6,17; р 13,55; С1 15.51. П р и м е-р 3. Синтез 2-(2-хлорэтокси)-2-оксо-3,7-Диметил-1,4,2-диоксафосфепана (I.V). В реакторе к раствору 39,34 г (о,зим) 2-хлор-1,3,2-диоксафосфолана 0,3 г ZnCl и 82 мл абсолютного 1,4диоксана при прибавляют 36,1 г (О,зим) 2,4-диметил-1 ,3-диоксана. Реакционную cMfecb перемешивают при этой температуре 3 ч, охлаждают до 8 С и приливают 20 мл воды с индикатором. При смесь титруют 10%ным КОН (расход 18 мл, процент гидро. лиза 10,33) до переходной окраски и переносят в делительную воронку с 200 мл воды. Экстрагируют трижды хлороформом (150:100:100. мл ). Объединенные вытяжки сушат , отгоняют 1 аст8Ормтель, а остаток перегоняют в вакууме. Получают 64,5 г (85,5%) . 7 2-(2-хлорэтокси)-2-оксо-3,7-Диметил-1 ,,2-диоксафосфепана, ft.кип., С (мм рт.ст.) 112-П(8-10); п| },k76(, d| 1,2593. Рт,„,Лд5А,, MRpBwM5.71. . Найдено, ; С 39,78; Н 6,71; Р 12,43; С1 Й,6«. Вычислено, %: С 39.60; Н б. Р |2,7б;.С1 U,61. Пример 4. Синтез 2-(2-хлорэтокси)-2-оксо-3 фенил-1 .i ,2-диоксафосфепана (VII). В реакторе при 80 С к раствору 38 г (0,ЗМ) 2-хлор-1,3,2-диоксафосфолана, 0,3 г ZnCl2. R 79 мл абсолютного 1,4-диоксана прибавляют раствор ,3г (0,ЗМ) -фенил-Т,3-диоксана в 18 мл абсолютного 1,4-диоксана. По окрнчании прибавления реакционную смесь прэдолЖают термост атировать при 80 С еще 4 ч, охлаждают проточной водой и приливают 50 мл воды с растворенным индикатором. Смесь титруют 10%-ным раствором КОН до переходной, окраски расход 30 мл, 17,85), переносят в делительную воронку с 100 мл воды и экстрагируют трижды хлороформом, а остаток перегоняют в вакууме. Получают 66 г (75,7) 2-(2-хлорзтокси)-2-оксо-З-фенил-1,4,2-диоксафосфепана. (Т.кип.,с (мм рт.ст.) 165(41П-3), h%i;5390, df b3100,:MR. 69.51, ko Ла Й- -РИаиД . PjBbW 69.02. Найдено, %: С Л9,12; Н 5,69; Р 10,31; С1 12.55. (, Вычислено, %:, С 49,58; Н 5,55; Р 10,65; С1 12,19. П Р и м е .р 5. Синтез 2-(2-хлорпропокси)-2-оксо-6,6-диметил-1,4,2диоксафосфепана (VII О. К раствору 42 г (0,3 М) 4-метил-2-хлор-1,3,2-диОксафосфолана, 0,3 г ZnClg. в 79 мл абсолютного 1,4-диоксана при и перемешивании прибавляют 34,8 г (0,3 м) -5,5-диметил-1,3диоксана. Реакционную смесь перемеши:вают при 98С 4 ч и охлаждают проточной водой. Приливают 50 мл воды с растворенным индикатором и титруют раствором. КОН до переходной окраски. Гидролизат переносят в делительную воронку со 150 мл воды и экстрагируют трижды хлороформом (150:100:100 мл). Вытяжки объединяют, Сушат , отгоняют растворитель, а остаток перегоняют в вакууме. Полуиают 3,2 г (kk,k%) 2-(2-хлорпропокси)-2-оксо-6,6-диметил-1 .t.Z-AMOKcaOocфепана (Vlfl). Т.кип. С (мм рт.ст.) 87-90 (310-«-), 1,t759, d5.°b23V3, %имА5 78, НРде1,,ч59,Зб. 5
Найдено, %: С ,13; Н 7,25; Р 11,89; С1 13,80.
CpH g04PC1
бымислёно, : С 2,11; Н 7,07; Р С1 13,81.10
П Р и-м е Р 6. Синтез 2-(1-метил-2-хлорпророкси)-2-оксо-3 пропил-1-,2-диоксафосфепана (iX).
В реакторе при и перемешивании к раствору 31)5 г (0,2 М) ,5-.ди- t5 метил-2-хлор-1,3,2- диоксафосфолана, 0,2 г ZriC1(2 в 53. мл а сол1отного 1,диоксана прибавляют 26 г (0,2 М) 2-пропил 1 3-Ди6ксана. Термостатируют реакционную смесь при перемешивании 20 3 ч и охлаждают до 8-}0°С, При этой температуре в реакционную смесь добавляют 0 мл воды с растворенным бромфеноловым и титруют 1.0%-ным КОН (расход 75 мл, что соответствует 25 67% гидролизе). ГиДролизат выливают в делительную воронку с 70 мл воды и
экстрагируют трижды хлороформом (100:50:50 мл). Вытяжки объединяют, сушат Ма ЗС и отгоняют растворитель. Перегонкой остатка в вакууме получают 15,7 г (27,6%) 2-(1-метил-2-хлорпропокси)-2-оксо-З-прорил-1 ,,2-диоксафосфепана (tX). Т.кйп., (мм рт.ст.) 136-138 (2-10-2-), 1,, d I 1.5151. Sмдйл 9, МВраыч68.б5. .
. Найдено, %: С. «5,93; Н 7, Р 10,22; С1 12,2.
1 2гОаРС1
Вычислено, i:C 6, Н 7,78; Р 10,88; С1 12,it5.
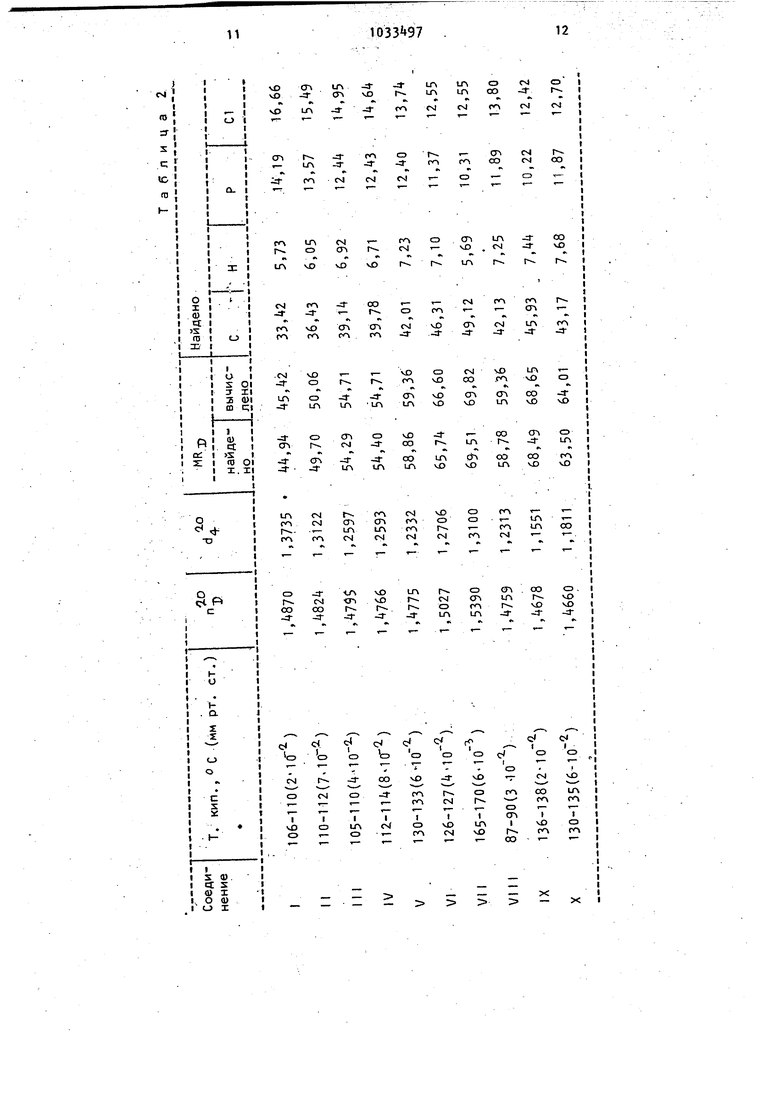
В табл.1 даны условия синтеза, исходные вещества, выходы и строение 2-(2-хлоралкокси}-2-оксо-1,,2-диоксафосфепанов, в табп.2 - их физико-химические константы..
IТаким образом, предлагаемый способ
получения 2-{2-хлоралкокси)-2-оксо-1 ,4,2-диоксафосфепанов позволяет повысить выход целевых продуктов до 22-85%, а также расширить ассортимент 1 ,4,2-диоксафосФепанов.
13
ЮЗЗ
. IJ
Таблица 2
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство для обеспечения безопасности следования поездов | 1926 |
|
SU9175A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Петров К.А | |||
| и др | |||
| Алкоксиметилирование диалкил-этилен- и дифенилхлорфосфитов диалкиформалями | |||
| - ЖОХ, 1980, 50, с.1021-1026 (прототип). | |||
Авторы
Даты
1983-08-07—Публикация
1982-04-29—Подача