() СПОСОБ ПОЛУЧЕНИЯ Ы-АЦИЛ-2-ОКСИ-1 ,3-ДИАМИНОПРОПАНОВ
Изобретение относится к способу получения новых М-ацил-2-окси-1,3-Диамкнопропанов, которые обладают биологической активностью и могут найти применение в медицине.
Известен способ получения N-ацил-2-окси-1,3 диаминопропанов взаимодействием соответствующих эпихлорRi-CONH-CHj,-СИв которой R - линейный или раз ветвленный алкильный радикал, содержащий от 1 до 20 атомов углерода, линейный или разветвленный алкенильный остаток, содержащий от 2 до 7 атомов углерода, 1,3-пентадиен-1-ильный остаток, циклоалкильный или циклоалкилметиленовый остаток С причем эти остатки содержат в некоторых случаях в качестве заместителя метил, циклоалкен- или циклоалкенмегидринов с замещенным анилином 1 .
Цель изобретения - получение новых соединений, обладающих ценным эффектом при лечении язв.
Указанная цель достигается тем, что в способе получения К-ацил-2. -окси-1,3 диаминопропанов общей формулы
Кз ОН
15 тиленовый остаток , который в случае необходимости может быть замещен метильным остатком, адамантиль- ный или адамантилметиленовый остаток, фенилметиленовый остаток, фенилэти20 леновый остаток 3 -диметоксифенилметиленовый остаток 3| диметоксифе-. нилэтиленовый остаток 3,4 метилендиоксифенильный остаток, З. Этилендиоксифенильный остаток, -фторфениль25 ный, 2-фторфенильный, 2-трифторметил39фенильный остаток, диметоксифенильный остаток, 2-пиридил-, 3 пиридил-, -пиридильный остаток, 2-фурил; R - водород, линейный или разветвленный С/( -алкильный остаток, остаток метоксиэтила; R, и R. - одинаковые или различные и означают водород, галоид, С.,алкил или Cj -алкоксил, за исключением того, что R означает 3 Аиметоксифенил, 2-фторфенил 2-трифторметилфенил, а Rn означает водород, метил или этил, один из R Il Rj означает -хлор, А-бром, 4-фтор, -метил, -метокси-остаток или R и R означают 3 -диметокси-остаток или R означает 2-фурил, Я2-метил, а один из RO, и хлор-остаток, соединение общей формулы R -CO-NH-CH2-Z I I где R имеет указанные выше значения f означает -СН (ОH)Cfi2 -галоген или - СН - СН NO /Вводят во взаимодействие с анилином общей формулы/: H-N-( I К где R,2, R о и R, имеют указанные вы ше значения, в присутствии растворителя при температуре от 15 до с последующим выделением целевого продукта в свободном виде или в виде соли. В том случае, когда Z имеет значе ние СН(ОН), процесс осущест вляют в присутствии кислотосвязующего агента, а именно карбоната калия, карбоната натрия, гидроокиси калия, гидроокиси натрия, П р и м е р 1о К раствору из 39,5:г 2-фенил-5-хлорметилоксазолиди на в 150 мл хлороформа и 16 мл пиридина прибавляют при перемешивании по каплям 15,7 г ацетилхлорида при -40 Раствору дают нагреться до комнатной температуры. Через Н ч к смеси прибавляют 100 мл концентрированной соляной кислоты После интенсивного перемешивания отделенную водную фазу разбавляют водой до двойного объе ма и насыщают хлористым натрием. Пу тем экстракции с помощью метиленхлорида получают после Ушки и удаления растворителя 19,7 г М-ацетил-2-окси -З-хлор-1-аминопропана в виде масла, которое без дополнительной очистки может обрабатываться далее IS г Н-ацетил-2-окси-3-хлор-1-аминопропана прибавляют к 6,1 г порошкообразной гидроокиси калия в 200 мл диоксана. После добавления ,7 г 4-хлоранилина раствор перемешивают при комнатной температуре в течение 1 ч, затем фильтруют и испаряют в вакууме растворитель. Маслянистый остаток растворяют в небольшом количестве этанола. После добавления эфира кристаллизуется 8 г Ц-aцeтил-N2-(А-хлорфенил)-2-окси-1,3-Диаминопропана, Топл. 123-124 С. Пример2. По примеру 1 1,7 г N-ацетил-2-окси-З-хлор-1-аминопропана с ,0 г 4-хлоранилина растворяют в 50 мл изопропанола и перемешивают с 10 мл 30%-ного водного раствора гидроокиси натрия при комнатной температуре в течение k ч. Реакционную смесь разбавляют толуолом, отделяют органичесую фазу, промывают ее водой и сушат над сульфатом натрия После фильтрования-и выпаривания растворителя в вакууме получают маслянистый остаток. Этот остаток обрабатывают эфиром, чтобы отделить не вступивший в реакцию 4-хлоранилин. Из смеси этанол/эфир кристаллизуется, как описано в примере 1, 3,0 г М -ацетил|-N - (it-хлорфенил)-2-окси-1,3 диаминопропана, т.пл. 123-12 0. ПримерЗ. 6,8г полученного согласно примеру 1 М -ацетил-М -(4-хлорфенил)-2 окси-1,3-Диаминопропана нагревают в 5 мл муравьиной кислоты с 27 мл 36%-ного водного раствора формалина в течение 3 ч на водяной бане. Для обработки выливают на лед. Доведенный до щелочной реакции с помощью разбавленного раствора гидроокиси натрия раствор экстрагируют хлороформом. Отделяют органическую фазу, промывают ее водой и сушат над сульфатом натрия. Послефильтрования и выпаривания растворителя в ваку-уме получают маслянистый остаток, который кристаллизуется из смеси этилацетат/эфир. Получают +,8 г N -ацетил-М2 -метил-М2-(-хлорфенил)-2-окси 1,3 диаминопропана, т.пл. 85-86С, Пример . 3,0г полученного согласно примеру 1 N -ацетил-М -(Ахлорфенил)-2-окси-1,3 диаминопропана перемешивают в 45 мл диоксана с 3,7 г бикарбоната натрия в 7,5 мл воды и if, мл диметилсульфата в течение 30 мин при . Смешивают с 10 мл 5 10%-ного раствора гидроокиси натрия и выдерживают температуру в течение дальнейших 10 мин. Затем удаляют рас воритель в вакууме и вещество обрабатывают хлороформом. После обработки получают 2,0 г Н-ацетил-М -метил-Н - ( -хлорфенил)-2-окси-1,3-Диаминопропана, т.пл. 85-86 с. П р и м е р 5. Если вводят во вза имодействие 19I8 г 2-фенил-5-хлорметилоксазолидина соответственно при меру 1 с Т, г циклогексилкарбонилхлорида в 8 мл пипиридина и 100 мл хлороформа, то получают после кристаллизации из смеси эфир/петролейный эфир ,Q г циклогексилкарбонил-2-окси-3-хлор-1-аминопропана, ТоПл.90 91 С. 4,4 г полученного таким образом амида вводят во взаимодействие соответственно примеру с 2,2 г анилина в 50 мл диоксана с добавкой 1,3 г гидроокиси калия. Получают 3,0 г М -циклогексилкарбонил-М -феНИЛ-2-ОКСИ-1,3-диаминопропана,. т.пл. I S-ISO G кристаллизованного из этанола. Пример 6. 1г N-метиланилина нагревают с 2,0 г N-циклогексилкарбонил-2-окси-З-хлор-1-аминопропанв течение 2 ч при , затем охлаж дают, растворяют в хлороформе и промывают разбавленным водным раствором гидроокиси натрия. После обработки, как указано в примере 1, получают не очищенное масло, которое очищают путем хроматографии на колонне на окиси алюминия стадии активности lie помощью толуолметиленхлорида. Из эти ацетата получают l,i г N -циклoгeкcилкapбoнил-N2 -мeтил-N2-фeнил-2-oкcи-1,3-диаминопропана, т.пл. 83-85 G. Примеру. 2,2 г N-циклогекси карбонил-2-окси-3-хлор-1-аминопропа7 на и 1 ,3-N-мeтилaнилинa вводят ео аз имодействие соответственно примеру 5 с 0,7 г гидроокиси калия в 50 мл. ди океана. Из смеси бензол/петролейный эфир получают 2,3 г N -циклогексйлкарбонил-Н2-метил-М2-фенил-2-окси-1,3 диаминопропана, т.пл. С. П р и м е р 8. Если вводят во вза имодействие N-циклогексилкарбонил-2-окси-3-хлор-1-аминопропан соответственно примеру 1 с З-хлор-2-метиланилином, то-получают Nyf-циклогeкcилкapбoнил-N2- (3-хлор-)2-метилфенил)-2-окси-1,3 Диаминопропан, т.пл. 123С. 146 П р и м е р 9. 6,0 г N-циклогексилкарбонил-2-окси-З-хлор-1-аминопропана перемешивают в 80 мл эфира с 1,8 порошкообразной гидроокиси калия в течение 18 ч при комнатной температуре. После добавления сульфата натрия раствор фильтруют и концентрируют в вакууме. При охлаждении выпадает в виде кристаллов ,5 г М-циклогексилкарбонил-2,3-эпокси-1 -аминопропана, т.пл. УЗ-ВО С. 2,5 г полученного таким образом эпоксида нагревают с 1,5 г N-метиланилина и 0,8 г ледяной уксусной кислоты в течени 5 ч при . Затем реакционную смесь растворяют в хлороформе, промывают водным раствором гидроокиси натрия. Из этилацетата получают 2,6 г N -циклогексилкарбонил-М -метил-Ы,-фенил-2-окси-1 ,3-Диаминопропана в виде кристаллов, т.пл.8385 С. .П р и м е р 10.- В отличие от примера 9 1.8 г М-циклогексилкарбонил-2,3-эпокси-1-аминопропана с 1,1 г N-мётиланилина нагревают при наличии флегны в 50 мл изопропанола в течение 6 ч. После удаления растворителя в вакууме получают соответственно примеру 1 6 г кристаллизованного из этилацетата N -циклoгekcилкapбoнил-N2-мeтил-N2-фeнил-2-oкcи-1,3-диаминопррпана, т.пл. 83-85С. Пример 11. Соответственно примеру 1 получают из 2-фенил-5-хлорметилоксазолина с 3, диметоксифенил-. ацетилхлоридом N-(3,4-диметоксифенилацетил)-З-хлор-2-окси-1-аминопропан, т.пл. 128-130С. Из негр соответственно примеру 9 получают в бензолтетраг идрофуране N- (3, -диметоксифе-. нилацетил)-2,3-эпокси-1-аминопропан, т,пл. . 5,2 г описанного выше эпоксидного соединения нагревают с 1 ,2. г уксусной кислоты и 2,3 г М-метил-4-хлоранилина в. течение 5 м при 60°С. После обработки, как указано в примере 9, получают масло, которое после взаимоействия с п-толуолсульфокислотой и после дигедрирования петролейным эфиром кристаллизуется в виде соли п-толуолсульфокислоты из ацетона. Поучают 6,0 г п-толуолсульфоната - (1,3-ДИметоксифенилацетил) -М/ -мегип- о- (А-хлорфенил)-2-окси-| 1,3 ДИминопропана, т.пл. 170-172 С. . 9 П р и м е р 12. Соответственно примеру 1 из 9,1 г М-фуроил-2-окси-3 хлор-1-аминопропана ( т.пл. 73 С) с 2,6 г гидроокиси калия в 130 мл тетрагидрофурана получают 7,0 N-фypoил-2,3-эпoкcи-1-aминoпpoпан, который без очистки в качестве масла далее вводят во взаимодействие с k,() г 3 фторанилина и 2,7 г ук сусной кислоты. После обработки получают ,6 г N,-фуроил-Мд-(З-фторанилин)-2-окси-1,3 диаминопропана в виде масла. Пример 13. N -фуроил N-2 - (3 фторанилин) -2-окси-1 ,3диаминопропана соответственно примеру 3 нагревают в 31 мл муравьиной кислоты с 15,5 мл Зб -ного водного раствора формалина в течение 3 м на водяной бане и обрабатывают. Получают 2,2 г М /фУРОил-М -метил-М - (З-фторфенил)-2-ОКСИ-1,3-Диаминопропана, т,пл.8688 С, в виде кристаллов из смеси изопропанол/эфир. Пример 1. К раствору 15,0 г 2-фенил-5-хлорметилоксазолидина в 200 мл хлороформа и 6 мл пиридина при С и при перемешивании прикапывают 15,2 г 3,-диметоксибензоилхл рида в 0 мл хлороформа. Раствор нагревают до комнатной температуры. По истечении It ч добавляют 20 мл концентрированной соляной кислоты, фазы хорошо перемешивают в течение 10 мин и разделяют. Отделенную водную фазу разбавляют в два раза водой и насыщают поваренной солью. Путем экстракции хлороформом получают после высушивания и удаления растворите ля 15,0 г Н-(3,-Диметоксибензоил)-3-хлор-2-окси-1-аминопропана в виде масла, который без дальнейшей очисткиможет вводиться во взаимодействие далее Кристаллизованное из смеси этанола с толуолом вещество плавится при . К 1,8 г тонко измельченного гидрата окиси калия в 160 мл диоксана добавляют 8,2 г полученного вещест. ва и 4,0 г 2-хлоранилина. После пере мешивания в течение 14 ч при комнатной температуре и фильтрования раствор вакуумируют, оставшийся остаток обрабатывают хлороформом и промывают водой. После высушивания и удаления растворителя получают 5,1 г (3,4 -диметоксибензоил) -N,- (2-хлорфенил) -2-окси-1,3 диаминопропана 0 виде маслянистого остатка, который кристаллизуется из ацетона, т.пл. 1141164. П р и /. е р 15. 3,5 г М-(3,4-диметоксибензоил)-2-окси-З-хлор-1-пропиламина в 250 мл бензола перемешивают с 0,8 г тонко измельченной гидроокиси калия в течение 16 ч при комнатной температуре. Раствор фильтруют и вакуумируюто После кристаллизации из толуола получают 2,5 г (3,4-диметоксибензоил)-2,3-эпокси- 1-аминопропана, т.пл. 108-111- С. Добавляют 4-бром-н-пропиланилин, растворенную затем в хлороформе реакционную смесь промывают водой, сушат над сульфатом натрия и фильтруют. После удаления растворителя получают 2,6 г маслянистого NJ-(3,4-диметоксибeнзoил)-N2.-пpoпил-N - (4-бромфенил)-2-ОКСИ-1,3-диаминопропана, кристаллизованного из смеси ацетона с петролейным эфиром, т.пл. 12б-128С. П р и м е р 1-6. 4,2 г М-(3-хлор-2-окрипропил)-3,4-диметоксибензамида в 75 мл диоксана перемешивают в течение 6 ч при 30-40°С с 3,0 г 2-бром- анилина и 1,0 г порошкообразной гидроокиси калия. Отфильтрованный раствор вакуумируют и оставшееся неочищенное масло фильтруют через окись алюминия стадии активности II с помощью смеси хлороформа с этилацетатом. 2,7 г (3,4-димeтoкcибeнзoил) - 2 -2-бромфенил-2-окси-1,3 диаминопропана кристаллизуется из смеси ацетона с петролейным эфиром, т.пл.114Пб С. При.мер 17о 4,1 г (3,4-диметоксибензоил)-М -фенил-2-окси-1 ,3-диаминопропана в 19 мл муравьиной кислоты и 10 мм Зб -ного водного раствора формалина нагревают в течение 3 ч на водяной бане., Смешанный затем со льдом реакционный раствор подщелачивают разбавленным раствором гидроокиси натрия и вещество выделяют из хлороформа. 3,3 г (3,4-диметоксибензоил)-N -мeтил-N--фeнил-2-окси-1,3-диаминопропана кристаллизуется из этр1Нацетата, т.пл.141142 С. П р и м е р 18. 3,4 г N.,-(3,4-диметоксибензоил)-М2-фенил-2-окси-1,3 диаминопропана растворяют в 60 мл диоксана, смешивают с 2,5 г бикарбоната натрия в 5 мл воды и после добавления 2,7 мл диметилсуль99
фата нагревают в течение 0,5 ч при 60-70 С. Затем раствор перемешивают с 60 мл 15 5-ного раствора гидроокиси натрия, удаляют растворитель в вакууме и выделяют вещество из хлороформа. Получают 2,0 г (3,-диметоксибензоил)-М2 -метил-Мд-фенил-2-ОКСИ-1,3 диаминопропана, т.пл..
П р и м е р 19. Согласно примеру I 5,6 г М-(3-хлор-2-оксипропил). диметоксибензамида вводят во взаимодействие .с 1,2 г гидроокиси калия и 2 г анилина в 350 мл бензола. 3,1 г выделенного (3, -диметоксибензоил)-N -фенил-2-окси-1,3-диаминопропана в виде неочищенного масла согласно примеру 15 в 30 мл диоксана вводят во взаимодействие с ,1 мл диэтилсульфата и 2,7 г бикарбоната натрия в 5,6 мл воды. Получают 1,3 г NJ-(З ,-диметoкcибeнзoил)-N -этил-N 2Фенил-2-окси-1,3 диаминопропана, который кристаллизуется из этилацетата, т.пл. .
Пример 20. 2,А г М-(2,3-эпоксипропил)- 31 -диметоксибензамида. и 1,2 г N-метиланилина в 30 мл толуола кипятят с обратным холодильником в течение 5 ч. Затем реакционный раствор концентрируют в вакууме досуха и оставшийся остаток фильтруют через окись алюминия стадии активности II с помощью смеси хлороформа с толуолом. Получают 2,2 г (3,ДИметоксибензоил)-М2-метил-Мл-фенил-2-окси-1,3 диаминопропана, кристаллизованного из смеси ацетона с петролейным эфиром, т.пл,
П р и м е р 21. Согласно примеру 15 1+,5 г N-(З,-метилендиоксибензоил)-2-окси-Зхлор-1-аминопропана с т.пл. 128- 130°С вводят во вза.имодействие с 3,5 г гидроокиси калия в 600 мл бензола. Реакционный раствор затем сушат над сульфатом натрия фильтруют и концентрируют в вакууме.
.Из концентрированного раствора получают 10,5 г М-(3,-метилендиоксибензоил)-2,3-эпокси-1-аминопропана, т.пл. 117-119С. 2,2 г полученного эпоксида вместе с 1,5 г -хлор-М-метиланилина и 1 мл ледяной уксусной кислоты нагревают в-течение 6 ч при . После обработки согласно приме ру 15 получают 2,0 г ,-метилендиоксибензоил)-Ы метил-Мс С -хлорk10
фенил)-2-окси-1,3 диаминопропана, т.пл. 1tO-1 3C, кристаллизобаиного из смеси хлористого метилена с эфиро
П р и м е р 22. Согласно примеру 15 из N-(2,3 эпоксипропил}-А-метилендиоксибензамида и 4-хлоранилина получают 3,+-метилендиоксибензоил ( -хлорфенил)-2-окси-1 ,3-диаминопррпана, т.пл. 158-1бОС.
П р и м е р 23. Согласно примеру 17 9,8 г, (3, -мeтилeндиoкcибeнзoил) (4-хлорфенил)-2-окси-1,3-диаминопропана превращают в 5 мл муравьиной кислоты и 27 мл Зб ;-ного формалина. Выделенное вещество кристаллизуется из смеси хлористого метилена с эфиром. Получают 1 г (3, -метилендиоксибензоил) -М,2 -метил- { -хлорфенил)-2-окси-1,3 Диаминопропан т.пл. l40-lit3C.
П р и м е р 2s. Согласно примерам 14-23 из М -диметоксибензоил-(3it-метилендиоксибензоил) или (3,4-этилендиоксибензоил)-3-хлор-2-окси-1-аминопропанов, получают соответствующие М-ацил-2-окси-М2 -фенил-1 ,3-диаминопропаны или -ацил-2-окси-Мл-алкил-М -фенилдиаминопропаны, причем при известных условиях названные первыми ацильные соединения можно алкилировать.
П р и м е р 25 Если 2-хлорметил-5-фенилоксазолидин согласно примеру вводят во взаимодействие с 2-фторбензоилхлоридом, то получают М-(3 -хлор-2-оксипропил)-2-фторбензамид т.пл. 77 78С„ 3,9 г полученного вещества согласно примеру 14 вводят во взаимодействие с 2,0 г N-пропиланилина и 1,0 г гидроокиси калия в 50 мл диоксана и обрабатывают. Получают 1,9 г N. - (2-фтopбeнзoил)-N2 Пpoпил-N,,-фенил-2-окси- 1,3-диаминопропана, ТоПЛ. 9б-97 С, кристаллизованного из смеси изопропанола с циклогексаном.
Пример 26. Согласно примеру 15 2,3 г N-(3-хлор-2-оксипропил)-2-фторбензамида вводят во взаимодействие с гидроокисью калия с получением N-(2,3-эпоксипропил)-2-фторбензамида. Полученное масло без очистки вместе с 1,1 г N-пропиланилина в 50 мл толуола кипятят с обратным холодильником в течение 6 ч. После удаления растворителя из изопропанола с циклогексаном кристаллизуется 1,6 г (2-фторбензоил)-М1-поопил М.2.феМ91нил-2-окси-З-окси-1,ЗДиаминопропана т пл. 9б-97С. Пример 27. Согласно примеру 25 при взаимодействии М-(3-хлор-2оксипропил)-2-фторбензамила с анилином получают (2-фтopбeнзoил)-N2-фенил-2-окси-1,3 диаминопропан в виде масла. Пример 28. 2,9г (2-фторбензоил) -М2.фенил-2-окси-1,3 диамино пропана в 15 мл диоксана с 3,0 г бикарбоната натрия в 6 мл воды и Ц, м диэтилсульфата нагревают в течение 30 мин при . После обработки согласно примеру 19 получают 1,5 г NJ - {2-фторбензоил) -М2-этил-М2 -фенил-2-ОКСИ-1 ,3 диаминопропана, т.пл. С, кристаллизованного из смеси изопропанола с циклогексаном. П р и м е р 29. Согласно примерам из соответствующих Ny-(2-фторбензоил) (-фторбензоил) или (2-трифторметилбензоил)-3-хяор-2-окси-1,3-диаминопропанов получают соответствующие N-ацилN 2-фенил-2-окси-1,3 диаминопропаны или М(-ацил-М2 -алкил-М2-фенил-2-окси-1,3-Диаминопропаны, причем первые при известных условиях могут алкилироваться. П р и м е р 30. Если 2-хлорметилфенилоксазолидин согласно примеру Н вводят во взаимодействие с хлорангидридом 2-фуранкарбоновой кислоты, то получают М-фуроил-3 хлор -2-окси-1-аминопропан, т.пл. С Согласно примеру 15 из 20,t г описан ного выше соединения в 300 мл тетрагидрофурана с 6,0 г гидроокиси калия получают 10 г амида М-(2,3-эпоксипропил)-фуран-2-карбоновой кислоты в виде масла. 8,2 г полученного вещества вводят во взаимодействие с 3,2 мл ледяной уксусной кислоты и 8,2 г 4-броманилина и обрабатывают согласно примеру 15. Из неочищенного масла при растирании с эфиром кристаллизуется 6,0 г N -фypoил-N2-( -бромфенил)-2-окси-1,3 диаминопропана из смеси этилацетата с петролейным эфиром , т„пл. 132-133С. Пример31.,8г N -фуроил-Ы -(4-бромфенил)-2-оксй-1,3-диаминопропанола в 27,0 мЛ муравьиной кис лоты и 13,5 мл Зб ного раствора фор малина нагревают в течение 3,5 ч на водяной бане. Вылитую на лед реакционную смесь обрабатывают согласно пр меру 17. Получают 3,3 г кристаллизованного из изопропанола N -фуроилметил-N - { -бромфенил) -2-окси-1,3-диаминопропана, т.пл. 10б-107 С. П р и м-е р 32. Согласно примерам 30 и 31 из Н-фуроил-3-хлор-2-окси-1,3 диаминопропанов получают соответствующие N; --фypoил-N2-aлкил-М2 -фенил-2-окси- 1,3-диаминопропаны или N -фypoил-N/ -фeнил-2-oкcи-1,3-диаминопропаны, причем первые при известных условиях могут алкилироваться. Температуры плавления полученных новых соединений приведены в табл.1-3. Новые соединения обладают ярко выраженной непосредственно подавляющей язвы активностью при хорошем терапевтическом спектре без влияния на .секрецию желудка. Их использование восстанавливает нарушенное заболеванием физиологическое равновесие в слизистой оболочке. Описание фармакологических методов исследования. Острая токсичность. Острая семидневная токсичность определяется после одноразового введения перорально натощак белой мыши NMPI, Расчет значений ЛД 5-0 осуществляется через EDV путем Probtt aHaлиза (Cavalli-Sforra L., Fischer Gustav-Verlag. Stuttgart, 1964, S.I 53). Испытание на вызванной индометационной язве у крысы. Ис.пытание проводят, модифицированно по U.Jahn и R.W.Adrian (Arzheim Forsh Drug-Res,,, 1969, 19, S 36). Испытуемое вещество вводят минимально 6 самцам крыс весом по 170200 г в объеме 0,5 мл суспензионной среды (100 г веса животного/перорально Животные контрольной группы получают соответствующий объем суспензионной среды . Спустя час после введения крысам вводят перорально 20 мг/кг индометацина в 0,5 мл суспензионной среды (ЮО г веса животного) для того,чтобы вызвать образование язвы. Животных умерщвляют спустя 2k ч после введения индоматацина. Оценку проводят видоизмененно по O.Munchow(Arzheim Forseh trug-Res. 195, , S. ). Рассчитывают среднее значение и стандартное отклонение числа язв и з&тем определяют подавляющее действие испытуемого и
1391
тандартного веществ в процентах о отношению к контролю.
Действие на желудочную секрецию аходящихся под наркозом крыс изерение рН)„
Для изучения.действия вещества на желудочную секрецию используется модифицированная методика испытания по M,N. Chosh и H.O.Shild.CBrlt.J.Phermacol, 1958, 13 5).Исследование проводят на находящихся под наркозом самцах крыс весом по 200-230 г. Для этого желудки крыс через кардинальный и пилорический катетер перфондируют 1 мл/мин н.+ООО раствора гидроокиси натрия. рН перфузата, который выходит из желудка через пилорический катетер, измеряют с помощью одностержневых измерительных цепей и непрерывно регистрируют. Для определения контрольного значения по истечении предварительных 20 мин осуществляют вв едение внутрибрюшиннс 10 мг/кг ацетилхолина. Контрольное значение устанавливается равным 100, После достижения снова исходной основы вводят интрадуоденально испытуемое вещество.Для оценки с помощью правила Симпсона определяют численное значение межгалловых поверхностей
Соединение
N -(2,3 Диметоксибензоил)-М -метил-Н2 -( -хлорфенил)-2-окси-1,3 диаминопропан
N - {2, -диметоксибензоил}-М2 -метил-Ы,-(-хлорфенил)-2-окси-1,3 диаминопропан
N - (3,5-Диметоксибензоил) -М -метил-М -(4-хлорфенил)-2-окси-1,3 диаминопропан
N - (3, -диметоксибензоил) -М -метил-Ы -(4-изопропилфенил)-2-окси-1,3-Диаминопро
N - (3, t-димeтoкcибeнзoил)-N2 -мeтил-N2-(3, -дихлорфенил)-2-окси-1,3 Аиаминопроп
Nyf - (3, «-диметоксибензоигг) -Nй -изoпpoпилфенил-2-окси-1,3-диаминопропан
(3, -этилендиоксибеноил)-Н -метил-(4-хлорфенил)-2-окси-1,3 диаминопропан
(2,6-диметоксибензоил)-М2 метил-(4-хлор)фенил)-2-окси-1,3, диаминопропан
Flachen-lntegral. Подавление секреции определяется из разниц между поверхностями до и после введения вещества. Например, исследуются следующие новые соединения по описанным методам: 1) (3,4-диметокси6ензойл)(2-хлорфенил-2-окси-1,3 диамино, пропан;
10 2) (3,-ДИмeтoкcибeнзoил-N„-мeтил H - (3 ,-Дихлорфенил) -2-ОКСИ-1 , 3-диаминопропан;З) (3, -ДИметоксибензоил)-М,-пропил-Ы2.-{ -хлорфенил)-2-окси-1,315 диаминопропан;
k) К -{2-фторбензоил)-М,-метил- Ni-(3, -ДИхлорфенил)-2-окси-1,3-ДИаминопропан;
5)Н -фуроил-М -метил-М -С -изопро20 пилфенил)-2-окси-1,3-диаминопроп эн, В качестве стандартных веществ используют
6)Атропинсульфат;
7)Sucus lignirital.
5 Результаты исследований приведены в табл,k,
Из полученных данных следует, что вещества, полученные по предлагаемому способу при отсутствующем подавле0 НИИ желудочной секреции обладают хорошим противоязвенным действием. Таблица 1
Т.пл., С
96-97 132-13 128-130 107-108 138-1А2 103-10 186-187 140-Й2
159101Й16 (3,Диметоксибензоил)-Ы2(2-метилфенил)-2-окси-1,3 диаминопропан (3, -Диметоксибензоил)-М2-(3 метилфенил)-2-окси-1,3-Диаминопропан N.(-(3,Динeтoкcибeнзoил)-N2.-(3xлop-2-метилфенил)-2-окси 1,3-диаминопропангидрохлорид(3,4-диметоксибензоил)-М2-(2,6-диметилфенил)-2-окси-1,3-Диаминопропан (3,-ДИметоксибензоил)-М,-метил-И2-(3фенил)-2-окси-1,3-диаминопропан
Соединение.1Т.пл., С
.. табл. 1 2
Таблица 2 122-125 96-100 158-163 99-101 155-159
17
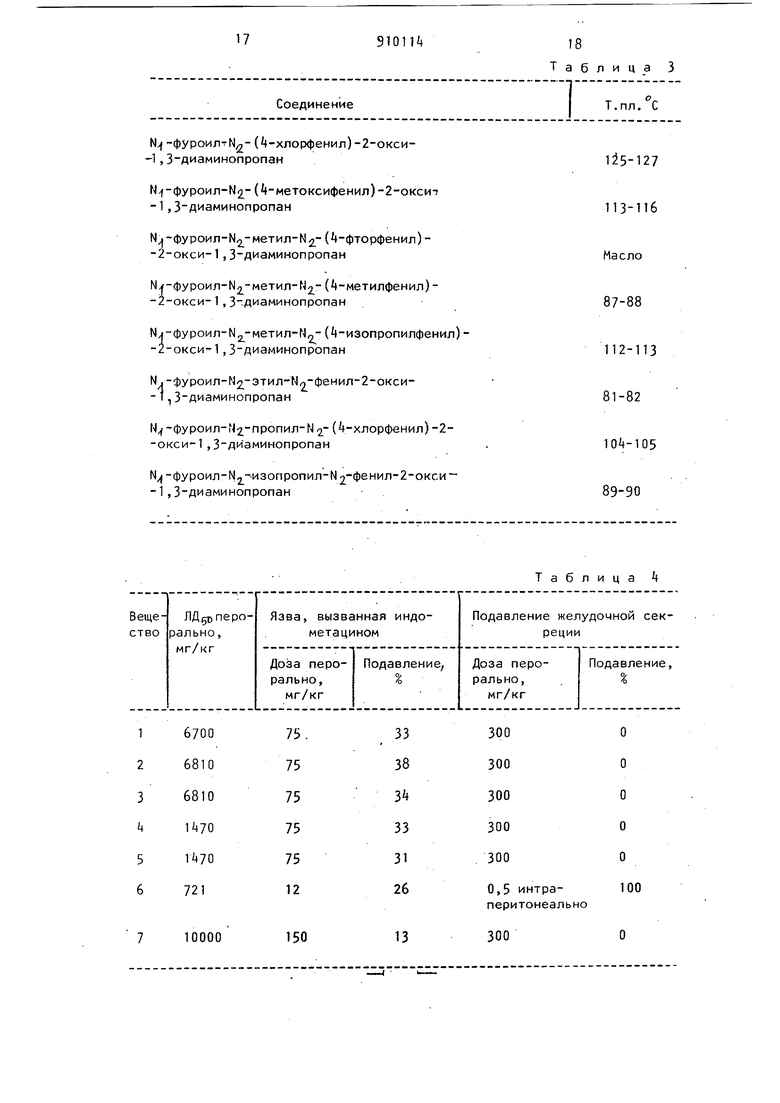
Соединение
N.f -фypoил N - (4-хлорфенил) -2-окси-1 ,3 диаминопропан
М -фуроил-Ы2 -(-метоксифенил)-2-окси-1,3 диаминопропан
Мх| ФУРОил-Ы -метил-Н2 (-фторфенил)-2-ОКСИ-1,3-Диаминопропан
М -фуроил-М2-метил- 42-( -метилфенил)
18 Таблица 3
Т.пл. С
1 5-127 113-116 Масло








| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения (1,2)-анеллированных 1,4-бензодиазепинов или их оптических изомеров или кислотно-аддитивных солей | 1982 |
|
SU1331431A3 |
| Способ получения 2-галоидметил1,4бензодиазепинов или их солей | 1976 |
|
SU727144A3 |
| Способ получения /1,2/-аннелированных 7-фенил-1,4-бензодиазепинов или их солей | 1979 |
|
SU904526A3 |
| Способ получения 2-замещенных 1,4-бензодиазепинов | 1976 |
|
SU1126209A3 |
| Способ получения 2-ациламинометил-1Н-2,3-дигидро-1,4-бензодиазепинов или их солей присоединения кислот | 1980 |
|
SU1253430A3 |
| Способ получения производных 2,9-диоксатрицикло (4,3,1,0 )декана или их солей | 1977 |
|
SU791242A3 |
| Способ получения 2-ациламинометил-1 @ -2,3-дигидро-1,4-бензодиазепиновых соединений,а также их оптических изомеров и их солей кислотного присоединения | 1982 |
|
SU1245259A3 |
| Способ получения 1-фенил-2-аминокарбонилиндольных соединений или их кислотно-аддитивных солей | 1983 |
|
SU1223843A3 |
| Способ получения карбаматов 4 -окси-2,9-диоксатрицикло-/4,3,1,0,3,7,/ -деканов | 1975 |
|
SU659086A3 |
| Способ получения @ -четвертичных производных 10-бромсандвицина и 10-бромизосандвицина | 1980 |
|
SU1012796A3 |

150
10000
Таблица
перитонеально
300 19 Формула изобретения 1. Способ получения М-ацил-2-окси-1,3-диаминопропанов общей формулы Rl-CONIt-CIli-CK-CHz N-/ II иЛч к . он RJ V в которой R - линейный или разветвленный алкильный радикал, содержащий от 1 до 20 атомов углерода, линейный или разветвленный алкенильный остаток, содержащий от 2 до 7 атомов углерода, 1,3 пeнтaдиeн-1-иль ный остаток, циклоалкильный или циклоалкилметиленовый остаток , при чем эти остатки содержат в некоторых случаях в качестве заместителя метил циклоалкен- или циклоалкенмет,иленовый остаток С , который в случае необходимости может быть замещен метильным остатком, адамантильный или адамантилметиленовый остаток, фенилметиленовый остаток, фенилэтиленовый остаток, 3,-ДИметоксифенилметиленовый остаток, 3,-ДИметоксифенилэтиле новмм остатрк, 3 мeтилeндиo Jcифeнил ный остаток, 3,« этилендиоксифенильный остаток, -фгорфенильный, 2-фтор фенильный, 2-трифторметилфенильный остаток, диметоксифенильный остаток, 2-пиридил-, 3 пиридил-, 4-пиридияьный остаток, 2-фурил; R2 -водород, линейный или разветвленный алкильный остаток, остаток метоксиэтила; Ro, и R4 одинаковые или различные и означают водород, галоид, С., алкил или C/t--, -алкоксил, за исклгэчением того, что R osHaчает 3, -диметоксифенил, 2-фторфенил 91 20 2-трифторметилфенил, а Rj означает водород, метил или этил, один из R3 и R4 означает -хлор, -бром, -фтор, -метил, -метокси- остаток или R и R означают 3,-диметокси-остаток, или R. означает 2-фурил, R -метил, а один из R- и R 4-хлор-остатокотличающийся тем, что соединение общей формулы 11 СО -NH-CH -Z, где R имеет указанные выше значения, Z - СН(ОН) или СН-СН9 вводят во взаимодействие с анилином общей формулы III где R2, R и R имеют указанные выше значения, в присутствии растворителя при Температуре от 15 до с последующим выделением целевого продукта в свободном виде или в виде соли, 2. Способ по По 1, о т л и ч а (-0щ и и с я тем, что, в том случае когда Z имеет значение t:CH(OH) , процесс осуществляют в присутствии кислотосвязующего агента, а именно карбоната калия, карбоната натрия, гидроокисикалия, гидроокиси натрия. Источники информации, принятые во внимание при экспертизе 1, Выложенная заявка ФРГ 2221558, кл. 12 р 10,01, 1973.
Авторы
Даты
1982-02-28—Публикация
1978-05-10—Подача