Изобретение относится к химии фос форорганических соединений с С-Р свя зью, а именно к усовершенствованному способу получения дигалогенангидриД08 2-алкоксиалкенилфосфонистых кис лот общей формулы . X2P-CH C{R)OR , (I) где X - хлор или бром; R - водород, или С -СА алкил; R - С2-Сц.-алкил, и могут найти применение в качестве полупродуктов фосфорорганимеского синтеза, а также в качестве мономеро для синтеза фосфорсодержащих полимеров. Известен способ получения дихлорангидридов 2-алкоксиалкенилфосфонистых кислот взаимодействием пятихлористого фосфора с винилалкиловыми - эфирами в среде органического раство рителя, с последующей обработкой об,разующегося комплекса раствором белого фосфора в сероуглероде в присутствии каталитических количеств иода. Процесс проводят при температуре (-10) - (-15)С, выход целевых продуктов составляет tl701 Ei3 Недостатками указанного способа являются многостадийность процесса и использование сероуглерода и белого фосфора в качестве реагентов, поскол ку известно, что эти вещества относятся к числу чрезвычайно ядовитых и самовоспламеняющихся. Наиболее близким к предлагаемому изобретению по технической сущности и достигаемому результату является способ получения дигалогенангидридов Z-алкоксиалкенилфосфонистых кислот, который заключается в том, что тригалогеНид фосфора подвергают взаимодействию с винилалкиловым Зфиром в эквимольном соотношении реагентов,, при температуре 0-40°С в атмосфере инертного газа в среде органического .растворителя, например, диэтилового эфира, с последующей обработкой полученного аддукта диа.лкиланилином при температуре от (-50) до (+20) С. Выход целевого продукта составляет 68-83%, -считая на прореагировавший трйгдлогенид фосфора, и , считая на взятый в реакцию тригалогенид фосфора 23 К недостаткам этого способа следу ет отнести двухстадийность процесса 82 и необходимость использования низких температур. Целью изобретения является упрощение процесса. Поставленная цель достигается способом получения дигалогенангидридов 2-алкоксиалкенилфосфонистых кислот общей формулы (i), который заключается в том, что тригалогенид фосфора подвергают взаимодействию с винилалкиловым эфиром и третичным амином при одновременном смешении всех реагентов в среде инертного органического растворителя в атмосфере инертного газа при температуре от (-20) до (+70)С. Тригалогенид фосфора, винилалкиловый эфир и третичный амин желательно использовать при мольном соотношении реагентов, равном 1:1-2:1-2. В качестве инертного органического растворителя предпочтительно использовать бензол или .петролейный эфир. Предлагаемый способ позволяет получать как дихлорангидриды, так и дибромангидРИДЫ 2-алкоксиалкенилфосфонистых кислот в одну стадию в более мягких условиях, чем по известному способу. По известному способу взаимодействие трехбромистого фосфора с винилалкиловыми эфирами осуществляется как двухстадийная реакция, включающая первоначальное присоединение трехбромистого фосфора по двойной связи винилалкилового эфира и последующее отщепление бромистого водорода, которое проходит либо самопроизвольно, либо под действием третичного амина (диалкиланилина). При самопроизвольном отщеплении бромистого водорода реакция трудно контролируется (происходит сильное разогревание) и осложняется побочными процессами полимеризации как исходного винилалкилового эфира, так и целевого продукта. Таким образом, использование третичного амина для отщепления бромистого водорода обусловлено необходимостью проведения процесса в кoнтpoлиpJfeмыx условиях для получения приемлемых выходов целевого продукта. Возможность осуществления реакции с треххлористым фосфором по предлагаемому способу обусловлена тем, что изменение порядка смешения реагентов приводит к изменению механизма превращения. Треххлористый фосфор не присоединяется к винилалкиловыи эфирам и, следовательно, по известному способу нельзя получить дихлорангидриды 2-алкоксиалкенилфосфонистых кис лот. Согласно предлагаемому способу образование связи фосфор-углерод осу ществляется в результате нового превращения - фосфорилирования винилалкиловых эфиров, включающего промежуточное образование фосфорсодержаще го карбокатионного интермедиата, ста билизирующегося путем отщепления про тона (облегчаемого присутствием третичного амина) с образованием целевы продуктов. Реакция протекает по следующей схеме: Jt5P-l-CH2 №) ((SlOBHR5T HX: где X, R И R имеют указанные значеR - алкил. Реакцию необходимо проводить в среде инертного органического раство рителя, в качестве которого удобно использовать бензол или петролейный эфир. Эти растворители имеют преимущество по сравнению с известным диэтиловым эфиром, так как образующаяс соль тре тичного амина в них не растворяется (в отличие от диэтилового эфира), что позволяет легче отделить ее от целевого продукта. Оптимальными для осуществления предлагаемого способа являются температуры от (-20) до (+70)С, так как при более низких температурах реакция проходит с меньшей скоростью а при температурах выше 70 С наблюдается сильное осмоление реакционной смеси, связанное с полимеризацией исходных и целевых продуктов. Целевые продукты представляют собой бесцветные тяжелые жидкости, устойчивы и не изменяются при хранении без доступа влаги и кислорода воздуха при 0-5 С. Данные элементног анализа, ИК- ПМР и спектров соответствуют приведенной формуле. Все операции проводят в ат(юсфере инертного газа, например аргона. Пример 1. К смеси 14, г (0,2 моль) винилэтилового эфира и 10,1 г (0,1 моль) триэтиламина в 50 мл абсолютного петролейного эфира(т.кип. i iO-60°C) при 20-25 С при перемешивании из капельной воронки прибавляют по каплям 13,7 г (0,1 моль) треххлористого фосфора. Реакционную смесь перемешивают при этой же температуре 6 течение 2Ц ч. Выпавший осадок гидрохлорида триэтиламина отделяют центрифугированием, промывают 50 мл абсолютного петролейного эфира, растворитель отгоняют в вакууме и после перегонки получают 12,3 г (71%) дихлорангидрида 2-этоксиэтенилфосфонистой кислоты, т.кип, (12 мм рт.ст.) п 1,5200, Литературные данные: т,кип. 78, (13 мм рт.ст,), п 1,5228. ИК-г.пектр содержит полосу поглощения Я)с С . Спектр ПМР, сГ.м.д.: 2,10 т и it,70 к () и дублет квартетов винильных протонов 6,kS (РСН) и 7,85 (СНО), J lit Гц, 6 Гц, Гц. Пример 2. К смеси 13,7 г (0,1 моль) треххлористого фосфора и 10,1 г (0,1 моль) триэтиламина в 50 мл абсолютного петролейного эфира при 20-25С и перемешивании прибавляют по каплям 20 г (0,2 моль) винилбутилового эфира. Реакционную смесь перемешивают при этой температуре в течение Зб ч. Выделившийся осадок гидрохлорида триэтиламина отделяют центрифугированием, промывают 100 мл абсолютного петролейного эфира, растворитель отгоняют в вакууме и после перегонки получают 18,8 г (85) дихлорангидрида 2-бутоксиэтенилфосфонистой кислоты, т.кип. 9б-97С (k мм рт.ст,), 1, . Литературные данные: т.кип. ЮОЧ (9 мм рт.ст.), п%° 1,5127. ИК-спектр содержит полосу поглощения Д)с-(-; 1бОО см . Спектр ПМР, сГ м.д. 1,35 т и 1,87 м, it,20 т (OCH,.CH,j,CH5) и дублет квартетов винильных протонов 6,05 и 7,15, j 1 Гц, .jp-H 6 Гц, 12 Гц. Спектр содержит сигнал трехкоординационного фосфора сГ 1б7 м,д. Пример З-К смеси 9,2 г (0,092 моль) 1-этилэтенилэтилового эфи ра и 9|3 г (0,092 моль) триэтиламина в 50 мл абсолютного бензола при перемешивании из капельной воронки при5Юбавляют по каплям 24,9 г (О,092 моль) трехбромистого фосфора в течение мин. Температура реакционной смеси самопроизвольно поднимается до 60 С. После охлаждения до 20С выпавший осадок гидр обромида триэтиламина центрифугируют, бензол отгоняют в вакууме, к остатку добавляют пентан до полного осаждения гидробромида триэтиламина.Осадок центрифугируют, пен тан отгоняют в вакууме и после перегонки получают 19,7 г (66%) дибромангидрида 2-этил-2-этрксиэтенил{ сфонистой кислоты, т.кип. 92-93 С (2 мм рт.ст.). Найдеяо, %: С 25,10; Н 3,85; CfcHnBr-iOP Р 10,50. ;: С г4,83; Н 3,79; Вычислено, Р 10,69. ИКтспектр содержит полосу поглощения с 1570 . Спектр ПМР, (Гм.д.: 1,33 т, и 3,95 к (ОСНаСНз), 1,15 т и 2,50 к (), 5,75 д (СН-), 5 Гц. Спектр ЯИР Р содержит сигнал трехкоординационного фосфора Г 158,7 м.д. Пример 4. К смеси 11,i г (0,1 моль) ct-изопропилвинилэтилового эфира и 5,1 г (0,05 моль) триэтиламина в 25 мл абсолютного бензола при .20-25 С при перемешивании прибавляют по капл;ям 6,9 г (0,05 моль) треххлористого фосфора. Реакционную смесь нагревают при 55 60С в течение 16-18 ч, затем добавляют 50 мл петролейного эфира (т.кип. ) и цент рифугируют осадок гидрохлорида.три этиламйна, осадок промывают 50 мл абсолютного петролейного эфира, ра воритель отгоняют в вакууме и посл перегонки получают 7,5 г (70) дих/юрангидрида 2-изопропил-2-этокси этенилфосфонистой кислоты, т.кип. 68-694 (3 мм рт.ст.). Найдено, %: С 39,42; Н 6,13; Р 14,66 С„Н СргОР Вычислено, : С 39,05; Н 6,05; Р 14,42. ИК-спектр содержит полосу погло щения .o, 15 70 см1. Спектр ПНР, СГм.д 1,4 т и 3,95 к (), 1,2 Я и 3,30 м, (изо-С Н) и 5,55 (СИ), 4 Гц. Спектр ЯМР Р содержит сигнал трехкоординационно фосфора, (Те 169,2 м.д. Пример 5. К смеси 11 ,-4 г (0,1 моль) с/-изопропилвинилэтиловвого эфира и 5,1 г (0,05 моль) триэтиламина в 25 мл абсолютного бензола при перемешивании из капельной воронки прибавляют по каплям 13,6 г (0,05 моль) трехбромистого фосфора в течение 20 мин. .Температура реакционной смеси самопроизвольно поднимается до 5С. После охлаждения до реакционную смесь центрифугируют, осадок гйдробромида триэтиламина промывают 100 мл петролейного эфира, растворитель отгоняют в вакууме и после перегонки получают 9,6 г (63,5) дибромангидрида 2-изопропил-2-этоксиэтенилфосфонистой кислоты, т.кип. 85-86С (1 мм рт.ст.). . Найдено, : С 28,00: Н Ц,20; Р 10,10. . Вычислено, I: С 27,63;.Н ,28; Р 10,20. ИК-спектр содержит полосу поглощения 1570 см-. Спектр ПМР, сГм.д.: l, т и 3,95 к (), 1,2 д и 3,30 м (изо-С,Н) и 5,70 д (CHi), 5 Гц. Спектр ЯМР содержит сигнал трехкоординационного фосфора сГ 159,1 м.д. Пример 6. К смеси 7,8 г (0,05 моль) о1-бутилвинилбутилового эфира и 10,1 г (0,1 моль) триэтиламина в 25 мл абсолютного петролейного эфира (т.кип. О-бО С) при перемешивании прибавляют по каплям при в течение 20 мин 13,6 г (0,05 яоль) трехбромистого фосфора. Реакционную смесь выдерживают при этой температуре, I ч, температуру поднимают до комнатной и центрифугируют. Осадок гидробромида триэтиламина промывают 100 мл петролейного эфира, растворитель отгоняют в вакууме и после перегонки получают 10,3 г (60%) дибромангидрида 2-бутил-2-бутоксиэтенилфосфонистой кислоты, т.кип. 105С (2 мм рт.ст.). Найдено, °4: С 35,00; Н 5,55; Р 9,25. C oH pBBiOP Вычислено,: С 34,68; Н 5,50; Р 9,25. ИК-спектр содержит полосу поглощения 570 см-Л Спектр ПМР сГм.д.: 1,15 м, 3,90 т (ОСфН). 1,05т и 1,70 м, 2,50 т (, 6,10 д (СНд), Тр-н 5 Гц. Спектр содержит сигнал трехкоординационного фосфора cf 157,6 м.д.
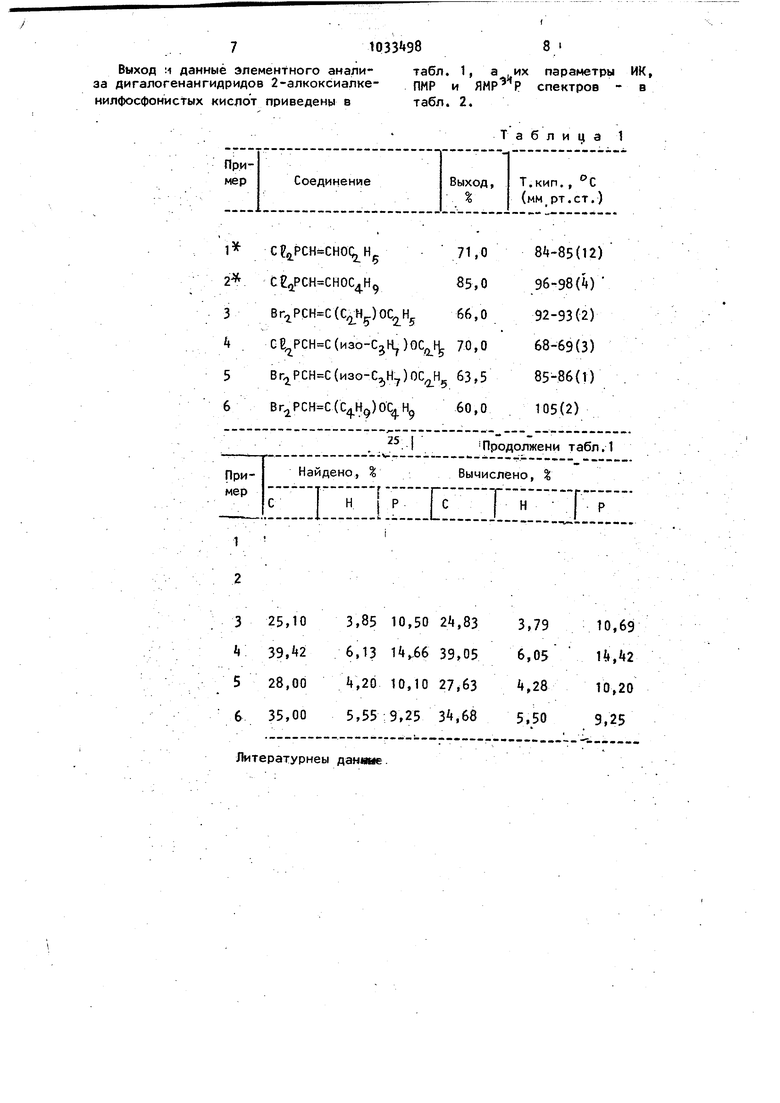
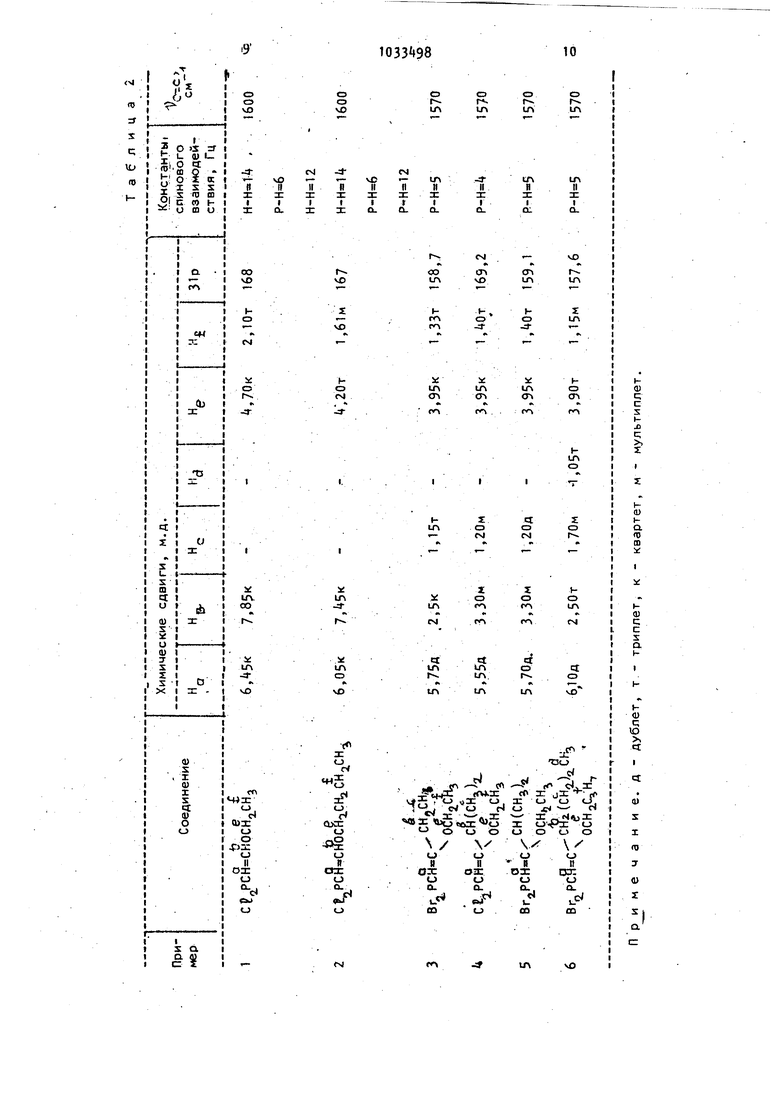
Выход :i данные элементного анализа дигалогенангидридов 2-алкоксиалкенилфосфонистых кислот приведены в
табл. 1, а .их параметры ИК, ПМР и ЯМР Р спектров - в табл. 2.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения дигалогенангидридов 1-алкил-2-алкоксиэтенилфосфонистых кислот | 1983 |
|
SU1154285A1 |
| Способ получения дигалогенангидридов 1-бром-2-алкоксиэтенилфосфонистых кислот | 1983 |
|
SU1142479A1 |
| Способ получения дигалоидангидридов -галоид- алкоксивинилфосфонистых кислот | 1976 |
|
SU598910A1 |
| Способ получения дибромангидридов -алкоксивинилфосфонистых кислот | 1977 |
|
SU643511A1 |
| Способ получения дигалогенангидридов 2-фенилэтинилфосфонистой кислоты | 1984 |
|
SU1235870A1 |
| Способ получения дигалоидангидридов @ -триметилсилил /гермил/- @ -галоид- @ -алкоксивинилфосфонистых кислот | 1980 |
|
SU899569A1 |
| Способ получения дигалоидангидридов тиофосфоновых кислот или их бисаналогов | 1969 |
|
SU653262A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИХЛОР- ИЛИ ДИВРОМАНГИДРИдШр^^^^^ ТИОФОСФОНОВЫХ кислот или их БИС-АИАЛОГОВ I ЬИ5]Г | 1972 |
|
SU332095A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДАНГИДРИДОВ ТИОФОСФОНОВЫХ кислот или их БИСАНАЛОГОВ | 1972 |
|
SU332094A1 |
| Способ получения дихлорангидридов хлорсодержащих 1,3-бутадиен-2-фосфоновых кислот | 1976 |
|
SU681066A1 |

Литературнеы дансюе.
1110 33 9812
Таким образом, предлагаемый спо- взаимодействие с винилапкиловыми соб получения дигалогенангидридовэфирами треххяористого фосфора. Спо 2-алкоксиаякенилфосфонистых кислотсоб получения прост и не требует сложпо сравнению с известным позволяеткого аппаратурного оформления. Полупроводить процесс в одну стадию, что 5ченные соединения могут найти примеисключает необходимость использова-нение в качестве мономеров для полуния низких температур, повысить выходчения фосфорсодержащих полимеров, обцелевого продукта в расчете на взятыйладающих повышенной термостойкостью, в реакцию тригалогенид фосфора до 60а также как промежуточные продукты 851 ( против в известном , и для синтеза неизвестных ранее прорёсшиРИТь ассортимент целевых продук-изводных трех- и четырехкоординационтов, что достигается за введенияногр фосфора.
Авторы
Даты
1983-08-07—Публикация
1982-04-23—Подача