Изобретение относится к (иикробио логи.и и касается способа определения скорости окисления органических .субстратов в микробных суспензиях, основанного на определение COj выделяемого при окислении органичес кого- субстрата, и может быть использовано в научных исследованиях при изучении биохимических особенно тей микроорганизмов, а также в промышленности, например в. очистных сооружениях нефтехимических и других производств при изучении биологической активности и эффективности работы ила. Известен способ определения скорости окисления органических субстратов в микробных суспензиях по измерению скорости продуцирования дву окиси углерода (СО методом, газовой хроматографии ij . Недостатком этого способа являет ся сложность используемой для анали за аппаратуры. Наиболее близким к предлагаемому по технической сущности и достигаемому эффекту является способ опре- деления скорости окисления органиче ких субстратов в микробных суспензиях, предусматривающий измерение скорости продуцирования двуокиси углерода микроорганизмами. Согласно способу измерение образования СО проводят манометрическим методом в сосудиках Варбурга Гз . Однако газообмен осуществляется в замкнутом пространстве, в результате поглощения кислорода изменяется газовый состав среды, результатом чего является возможное снижение скорости окисления субстрата во времени. Конструкция аппарата Варбурга такова, что не дает возможности одновременного изучения более 6 субстратов,, что ограничивает его возможности. Цель изобретения - упрощение. процесса.. Поставленная цель достигается тем, что согласно способу определения скорости окисления органических субстратов в микробных суспензиях, предусматривающему измерение скорос ти продуцирования двуокиси углерода микроорганизмами, перед измерением скорости продуцирования двуокиси углерода микробные суспензии помещают на полиуретановый носитель, подвещенный на стальной проволоке в стеклянном сосуде с 0,05 N раствором гидрата окиси бария, выдерживают в течение 5-6 ч, а измерение ско рости продуцирования двуокиси углер да проводят путем титрования O/OBN раствором соляной кислоты в присут. ствии фенолфталеина. На чертеже показан предлагаемый прибор. Прибор состоит из стеклянной цилиндрической колбочки 1. объемом 25 мм, в которую подвешивается нанизанная на ст альной проволоке 3 полоска полиуретановой губки 2 размером 3.0x8x8 мм. Стальная проволока 3 укрепляется в резиновой пробке 5 через которую проходят стеклянная трубка 4, наполненная натронной известью. Она предназначена для соединения газовой фазы колбочки с наруж-. ным воздухом. Натронная известь пропускает в колбочку кислород, но i поглощает углекислоту. Суспензия микроорганизмов объемом 0,1-0,2 мм впитывается в боковые грани полиуретановой губки, органический субстрат добавляется на верхнюю, горизонтальную грань губки. В колбочку наливается 2 мл раствора 0,05N Ва(ОН;2. Полоски полиуретана с суспензией микроорганизмов подвешиваются в колбочке и зкспонируется в термостате при 5-6 ч. При постановке опыта необходимо следить, чтобы пробка 5 плотно прилегала к горлу колбочки 1.. Определение выделившегося и поглощенного раствором гидрата окиси бария СО осуществляют методом тит- рования 0,05N раствором НС1 в присутствии фенолфталеина. Для определения СО-г., имеющегося в воздухе, ста1вят контрольную колбочку без суспен-зии микроорганизмов. Об окислении органического субстрата и окислительной активности микроорганизма судят по интенсивности продуцирования СО в присутствии данного субстрата. Определение окислительной активности проводят для двухсуточных культур микроорганизмов, выращенных на жидких или агаризованных органических или минеральных средах. Культуры отмываются три раза буфером со значениями рН, соответствующими физиологическим. особенностям данного микроорганизма, впитываются в полоску губки и экспонируются.в колбочках в присутствии BaCOHJj. Через 5-6 ч путем.титрования 0,05 NHC1 в присутствии фенолфталеина определяется количество выделившегося СО 2 по формуле -В 0 05-44, где А МЛО,05 N 3a(OHh, налитое в колбочку (2 В мл-0,05Н НС1, пошедшее на титрованиеJ 0,05 - нормальность раствора На(ОН); 44 - мг-эквивалент С02; п - вес биомассы, добавленной в губку; t - время экспозиции; АСБ - абсолютно сухая биомасса. Количество вьоделившегося СОд. представляют в мг на 1 мг сухой биомассы
за 1 ч. Абсолютно сухую биомассу можно выразить также содержанием, азота, в этом случае количество СО выражают в мг на 1 мл азота за 1 ч.Делением весового значения на 0,00195 можно получить объемные значения COj. в микролитрах (л).
Пример , 2-суточная куль.Tvoa дрожжей Candida guiiliermondii 916,.вь5ращенная на сусло-агаре,смывается с поверхности среды и отмываетс три раза фосфатным буфером рН 5,4. Полученную пасту разводят тем же буфером для получения суспензии с оптической плотностью D - 1,2-1,5 0,2 мл (1 мг) этой суспензии впитывается в полоски поролона, предварительно надетого на проволоку. На верхнюю часть полоски добавляются 0,02 мл н-гексадекана. В колбу добавляется 2 мл раствора 0,05N Ba{OHJ,. Резиновой Пробкой с проволокой и надетой на проволоку полоской .поролона плотно закрывают колбу таким образом, чтобы полоска поролона была полностью в колбочке,.нижний
конец полоски не должен соприкасаться с поверхностью раствора Ba(OH)j,. Одновременно с опытными колбами ставятся контрольные без микробной суспензии для учета углекислого газа воздуха в колбочке. Колбочки экспонируют в те1 1остате при 28ЗО С 5 ч. Колбочки в этот период ,иногда осторожно встряхивают. По . окончании времени экспозиции в колбочки добавляется капля фенолфталеина и избыток гидрата окиси бария титруется 0,p5N раствором соляной кислоты до обесцвечивания. По разнице между титрованием контроля и опыта определяется количество вьщелившегося углекислого газа микробной суспензией. Интенсивность продуцирования COg выражается в мг на 1 мг сухой биомассы за 5 ч.Ошибка определения --до 3-5%.
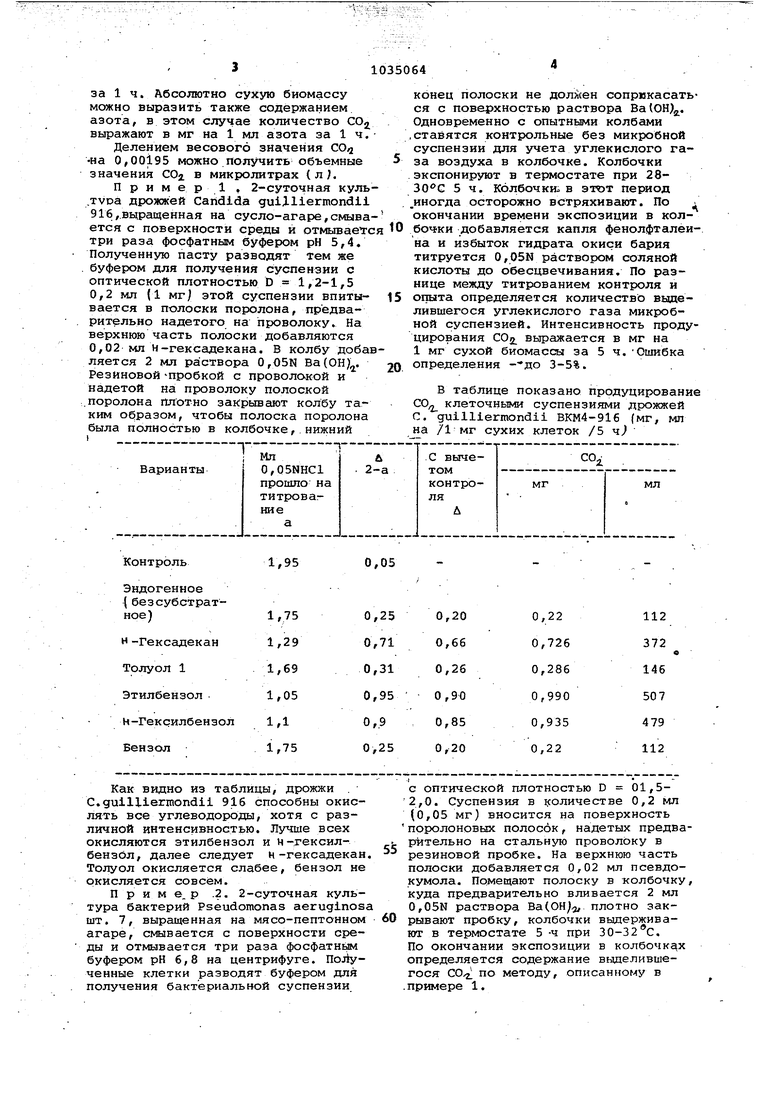
В таблице показано продуцирование СО клеточными суспензиями дрожжей С. guiiliermondii ВКМ4-916 (мг, мл на /1 мг сухих клеток /5 ч

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭФФЕКТИВНОСТИ БИОДЕГРАДАЦИИ УГЛЕВОДОРОДОВ НЕФТИ В НАТИВНЫХ И ЗАГРЯЗНЕННЫХ ПОЧВАХ | 2010 |
|
RU2477472C2 |
| СПОСОБ ПРОДУЦИРОВАНИЯ С2-ОКСИГЕНАТОВ ПУТЕМ ФЕРМЕНТАЦИИ С ИСПОЛЬЗОВАНИЕМ СЕРЫ С ВЫСОКОЙ СТЕПЕНЬЮ ОКИСЛЕНИЯ | 2013 |
|
RU2644239C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОССТАНОВЛЕННОГО КОФЕРМЕНТА Q И СПОСОБ ПОЛУЧЕНИЯ ОКИСЛЕННОГО КОФЕРМЕНТА Q | 2002 |
|
RU2298035C2 |
| Штамм Gordonia amicalis, способный к генерации непосредственно в нефтяном пласте нефтевытесняющего агента - биоПАВ и снижающий содержание сероорганических соединений нефти | 2018 |
|
RU2673747C1 |
| Способ определения биомассы микроорганизмов в почве | 1986 |
|
SU1388802A1 |
| БИОПРЕПАРАТ ДЛЯ БИОРЕМЕДИАЦИИ НЕФТЕЗАГРЯЗНЕННЫХ ПОЧВ ДЛЯ КЛИМАТИЧЕСКИХ УСЛОВИЙ КРАЙНЕГО СЕВЕРА | 2013 |
|
RU2565549C2 |
| СПОСОБ БИООКИСЛЕНИЯ МИНЕРАЛЬНОГО СЫРЬЯ | 1991 |
|
RU2099432C1 |
| СПОСОБ БИОТРАНСФОРМАЦИИ СОЕДИНЕНИЙ КОЛХИЦИНОИДОВ В СООТВЕТСТВУЮЩИЕ 3-ГЛИКОЗИЛПРОИЗВОДНЫЕ | 1997 |
|
RU2196826C2 |
| Способ определения количества микроорганизмов в почве | 1984 |
|
SU1298246A1 |
| МИКРОБНЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРАВАСТАТИНА | 2000 |
|
RU2252258C2 |
СПОСОБ ОПРЕДЕЛЕНИЯ СКОРОСТИ ОКИСЛЕНИЯ ОРГАНИЧЕСКИХ СУБСТРАТОВ В МИКРОБНЫХ СУСПЕНЗИЯХ, предусматривающий измерение скорости продуцирования двуокиси углерода, микроорганизмами, отличающийс я тем, что, с целью упрощения процесса, перед измерением скорости продуцирования двуокиси углерода микробные суспензии помещают на полиуретановый носитель, подвешенный на стальной проволоке в стеклянном сосуде с 0,05 N раствором гидрата окиси бария, ВЕадерживают в течение 5-6 ч,а измерение скорости продуцирования двуокиси углерода проводят путем титрования О ,-05 N раствором соляной g кислоты в присутствии фенолфталеина.
1,95
Контроль
Эндогенное (безсубстратКак видно из таблицы, дрожжи . С.guiiliermondii 916 способны окислять все углеводороды, хотя с различной интенсивностью. Лучше всех окисляются этилбензол и н-гексилбензбл, далее следует к-гексадекан Толуол окисляется слабее, бензол не окисляется совсем.
П р и м е р .2. 2-суточная культура бактерий Pseudomonas aeruginos шт. 7, выращенная на мясо-пептонном агаре, смывается с поверхности среды и отмывается три раза фосфатньм буфером рН 6,8 на центрифуге. nojiyченные клетки разводят буфером для получения бактериальной суспензии
0,05
с оптической плотностью D 01,52,0. Суспензия в количестве 0,2 мл
(0,05 мг) вносится на поверхность поролоновых полосок, надетых предварительно на стальную проволоку в резиновой пробке. На верхнюю часть полоски добавляется 0,02 мл псевдокумола. Помещают полоску в колбочку куда предварительно вливается 2 мл 0,05N раствора Ва( плотно закрывают пробку, колбочки вьщерживают в термостате 5 -ч при 30-32 С. По окончании экспозиции в колбочках определяется содержание выделившегося СО по методу, описанному в .примере 1.
Использование предлагаемого спо соба определения скорости окисления органических субстратов в микробных суспензиях обеспечивает по сравнению с известным способом еледующие преимущества: определение окисления органических субстратов значительно упрощается, так как предлагаемая конструкция прибора проста и доступна любой лаборатории создается возможность проведения анализа не только в лабораторых условиях, но и непосредственно в полевых условиях, в экспедиции; отпадает необходимость в приобретении сложного и дорогого оборудования; в аппарате Варбурга при наличии полного набора манометров возможно одновременное изучение окисления не более 6 органических субстратов. Приборов предлагаемой конструкции можно изготовить в количестве необходимом для изучения одновременно неограниченного количества субстратов, что значительно экономит; время, .
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Имшенецкий А. | |||
| А | |||
| ,Мурзаков Б.Г | |||
| Определение углекислоты, выделяемой из почвы при различной ее влажности.- Микробиология, 1978, 47, 6, с | |||
| РЕВЕРСИВНЫЙ КОЛОВРАТНЫЙ ДВИГАТЕЛЬ | 1921 |
|
SU1086A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Уибрейт В.В., Буррис Р.Х., .Штауффер Дж.Ф | |||
| Манометрические методы изучения тканевого обмена | |||
| М., Иностранная литература, 1951 (прототип ) | |||
| SU,,.; IQ35064 А 3 | |||
Авторы
Даты
1983-08-15—Публикация
1982-04-05—Подача