Изобретение относится к контрольНр-измерительной технике, предназначено для электрохимического определе, ния концентраций физиологически активных веществ аденозинтрифосфата (АТФ) при помощи ферментных реакций, и может быть использовано в медицине Известен способ определения аденозинтрифосфата, заключающийся.9 реакции окисления люциферина в присутс W 2.4вии аденозинтрифосфата и солей Мд , катализируемой люциферазой. Реакция сопровождается выделением света, интенсивность которого пропорциональна концентрации аденозинтрифосфата ft. Недостатком данного способа является ограниченное его применение, по скольку используемые при этом люциферии и люцифераза выделяются из насекомых, а хемилюминесцентная установка сложна, измерения проводятся лишь в периодическом режиме. Так, лирфилизованный экстракт из хвостиков светляков фирмы Серва растёоряется в 5 мл бидистилята в течение 1 мин и помещается в лед. Рабочий раствор готовитря, непосредственно перед проведением измерений. 0,1 мл исходного экстракта добавляется в 0,9 мл буферного раствораТЕПЭС 0,25 Н (рН 7,5), содержащего KgSO 10 мМ И проводится определение фона (0,3 мин). После введения образца АТФ определяется свечение в течение 1 мин. При каждом определении используются ноёые порции экстракта. Наиболее близким к изобретению является Способ определения концентрации физиологически активных веществ, заключающийей в электролизе исследуемого раствора в присутствии глюкозорксидазы, содержащейся в приэлектродНОм слое мембраны, измерении тока и определении концентрации по йзмемению тока 2. Способ позволяет опг редёлить концентрацию глюкозы. НахоДящаясяр анализируемом растворе глюкоза, диффундирует е слой глюкозооксидазы, где в {реакции с кислородом образуется перекись водорода, которая электрохимически окисляется на поверхности электрода. Количество образовавшейся перекиси водорода опреде ляется концентрацией глюкозы и таким образом измеряемый ток зависит от ее конц ентрации. Однако известный способ не позволяет определить концентрацию аденозин трифосфата. Цель изобретения - определение концентрации аденозинтрифосфата.. Поставленная цель достигается тем, что согласно способу определения концентрации физиологически активных веществ, заключающемуся в электролизе исследуемого раствора в присутствии глюкозооксидазы, содержащейся в приэлектродном слое мембраны, измерении тока и определении концентрации по изменению тока, в приэлектродныи слои мембраны дополнительно вводят иммобилизованную гексокиназу в буферном растворетрцс -НСР , содержащем сульфат магния и глюкозу, а концентрацию аденозинтрифосфаТа определяют по уменьшению анодного тока. С целью повышения чувствительности определения глюкозооксидазу вводят в количестве (1,5-3,0)-10 ед/см, а Иммобилизованную гексокиназу - в количестве (3-6)МО ед/см в 0,009 0,011 М буферном растворе Трис-НСС, содержащем 2- мМ сульфата магния и 0,1-0,2 мМ глюкозы. Приведенный нижний предел концентрации гексокиназы является существенным, если аденозинтрифосфат присутствует в небольших концентрациях. Так, например, при уменьшении концентрации гексокиназы до 2 «10 ед/см чувствительность устройства уменьшается и нижнюю концентрацию АТФ - 0,035 мМ определить невозможно. При выходе из верхнего предела концентрации гексокиназы увеличивается толщина мембранного слоя, чувствительность электрода уменьшается и определить минимальную концентрацию аденозинтрифос.фата невозможно. По аналогичным причинам нельзя выходить за указанные пределы концентраций глюкозооксидазы. От Р|Н зависит активность ферментов, а соответственно и чувствительность электрода. Выход за пределы данного интервала значений рН приводит к уменьшению активности электрода и определить нижний предел концентрации АТФ невозможно. Так, уменьшение концентрации буферного раствора ниже 0,01 М не обеспечивает стабильного рН всей системы, что уменьшает стабильность чувствительности электрода. Увеличение концентрации буферного раствора ведет к образованию значительного остаточного тока, что приводит к нестабильной работе электрода. Не обеспечивается точное определение аденозинтрифосфата в минимальных конц гнтрацкях. По аналогичным причинам даны оптимальные интервалы концентраций суль фата магния и глюкозы. Большие концентрации аденозинтрифосфета возможно определить и не в оптимальных количествах ферментов, т.е. допустимо любое соотношение веществ, но тогда не обеспечивается точ ное определение аденозйнтр.ифосфата
глюкозооксидаза
глюкоза + О,
При наличии гексокиназы и аденозин- трифосфата параллельно протекает фосгексокиназа люкозо-6-фосфат + АДФ
глюкоза + АТФ
В результате фосфорилирования глюкозы анодный ток падает. Степень уменьшения тока пропорциональна концентрации АТФ.
Для осуществления способа приме-, няется электрод,.содержащий глюкозооксидазную и гексокиназную.мембраны, т.е. ферменты захвачены в приэлектродном слое. Активность используемой, иммобилизованной глюкозооксидазы составляет (1,5-3)10 ед/см (толщина слоя 0,1 мм), а гексокиназы - (3-6) 10 ед/см (толщина слоя задана капроновой сеткой из нитей диаметром 0,1 мм).
При погружении электрода в буферный раствор, содержащий глюкозу, генерируется анодный ток в результате окисления . При наличии АТФ количество ) уменьшается из-за паI д, мкА/см
мМ
АТф 1
сГ-глюконолактон +
форилирование глюкозы с образованием аденозиндифосфата (АДФ) пд.
раллельного фосфорилирования глюкозы, и, следовательно, наблюдается уменьшение анодного тока. Способ включает следующие операции: электролиз ис5следуемого раствора, измерение тока иопределение концентраций аденозинтрифосфата (АТФ).
Пример 1. Электролиз исследуемого раствора проводят в присуТстВИИ 1,510 ед/см глюкозооксидазы, ЗЮ ед/см гексокиназы а 0,01 М трос-НС буфере (рН 7,0), содержащем 2 мМ сульфата магния и 0,1 мН глюко- ; зы. Определяют стационарный ток электрода в зависимости от концентрации аденозинтрифосфата при.рН 7,0, 25°С, +0,6 В.
Зависимость анодного тока электрода от концентрации АТФ приведена в табл. .1.
Таблица 1
Сд.уф, мМ I Al, мкА/см 8 во всех концентрациях (не созданы оптимальные условия действия ферментов) . Способ определения обоснован следующими ферментативными превращениями.. . Под действием глюкозооксидазы окисляется глюкоза, образовывается , а электрохимическое окисление последг.с ней при +0,6 В от электрода сравнения (насыщенный Ag/AgC) генерирует анодг ный ток

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения активности ферментов,синтезирующих или разлагающих аденозинтрифосфат | 1982 |
|
SU1070166A1 |
| Способ получения ферментных электродов чувствительных к метаболитам | 1979 |
|
SU891774A1 |
| Ферментный датчик для определения лактозы | 1987 |
|
SU1502995A1 |
| БИОСЕНСОР С ПОВЫШЕННЫМ КОЭФФИЦИЕНТОМ ЧУВСТВИТЕЛЬНОСТИ | 2019 |
|
RU2731411C1 |
| Электрохимический датчик для определения концентрации веществ в растворах | 1979 |
|
SU1034618A3 |
| Способ приготовления инкубационной среды для потенциометрического определения активности @ -АТФ-азы | 1982 |
|
SU1133534A1 |
| РЕАГЕНТ ДЛЯ ОПРЕДЕЛЕНИЯ АДЕНОЗИН-5'-ТРИФОСФАТА | 2004 |
|
RU2268944C2 |
| БИОСЕНСОР ДЛЯ ОДНОВРЕМЕННОГО ОПРЕДЕЛЕНИЯ ГЛЮКОЗЫ И ЛАКТАТА В КРОВИ | 2018 |
|
RU2696499C1 |
| Способ получения иммобилизованной люциферазы светляков | 1986 |
|
SU1341189A1 |
| МЕЧЕННОЕ ЛЮЦИФЕРАЗОЙ АНТИТЕЛО И СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ОСУЩЕСТВЛЕНИЯ АНАЛИЗА НА СПЕЦИФИЧЕСКОЕ СВЯЗЫВАНИЕ И НАБОР ДЛЯ ПРИМЕНЕНИЯ В АНАЛИЗЕ НА СПЕЦИФИЧЕСКОЕ СВЯЗЫВАНИЕ | 1995 |
|
RU2199125C2 |
1. СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ФИЗИОЛОГИЧЕСКИ. АКТИВНЫХ ВЕЩЕСТВ, заключающийся в электролизе исследуемого раствора в присутствии глюкозооксидазы, содержащейся в приэлёктродном слое мембраны, измерении тока и определении концентрации по изменению тока, отличающийся тем, что, с целью обеспе- чения возможности определения концентрации аденозинтрифосфата, в призлектродный слой мембраны дополнительно вводят иммобилизованную гексокиназу в буферном растворе трис-НСР, , содержащем сульфат магния и тгйокозу, а концентрацию аденозинтрифосфата определяют по уменьшению анодного тока. 2. Способ по п. 1, о т л и ч а ю щ и и с я тем, что, с целью повышения чувствительности определения, глюкозооксидазу уводят в количестве g 
Коэффициент чувствительности 3,06 мкА/см мМ АТФ, предел обнаружения АТФ - 2,.
Пример 2. Электролиз исследуемого раствора проводят в присутствии 3, ед/см глюкозооксидазы и 610 ед/си гексокиназы в 0,01 М
Трис-НСе буфере (рН 7,2), содержащем Ц мМ сульфата магния и 0,2 мН глюкозы. Снимают показания электрода во время его эксплуатации при рН 7,2, , +0,6 В. .
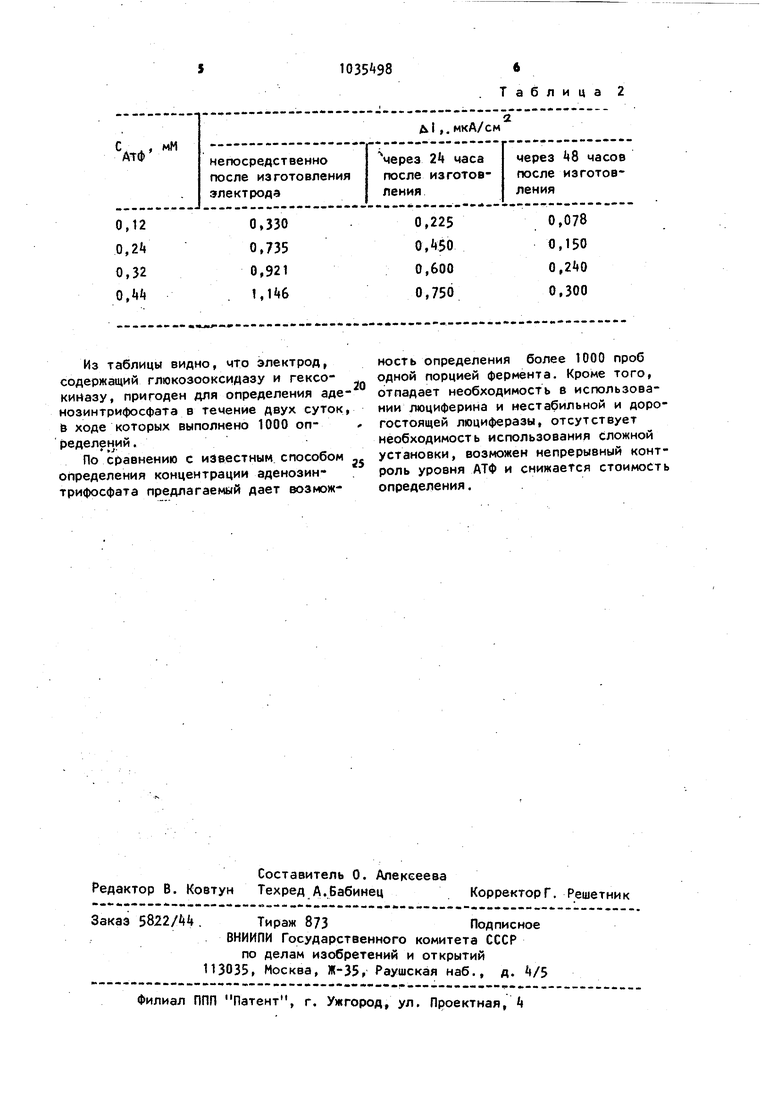
Изменение чувствительности электрода при его эксплуатации показано в т абл. 2. Из таблицы видно, что электрод, содержащий глюкозооксидазу и гексокийазу, пригоден для определения аде нозинтрифосфата в течение двух суток 6 ходе которых выполнено 1000 определений . По сравнению с известным способом определения концентрации аденозинтрифосфата предлагаемый дает возможТаблица 2 ноеть определения более 1000 проб одной порцией фермента. Кроме того, отпадает необходимость в использовании люциферина и нестабильной и дорогостоящей люциферазы, отсутствует необходимость использования сложной установки, возможен непрерывный контроль уровня АТФ и снижается стоимость определения.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Имшенецкий А.А | |||
| и др | |||
| Оптимальные условия | |||
| определения АТФ микробного происхождения | |||
| - Микробиология, 1977, т | |||
| X-vr, вып | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ПАРОПЕРЕГРЕВАТЕЛЬ ДЛЯ ЛОКОМОБИЛЬНЫХ КОТЛОВ | 1912 |
|
SU277A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент США (Г , кл | |||
| , опублик | |||
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
Авторы
Даты
1983-08-15—Публикация
1981-12-08—Подача