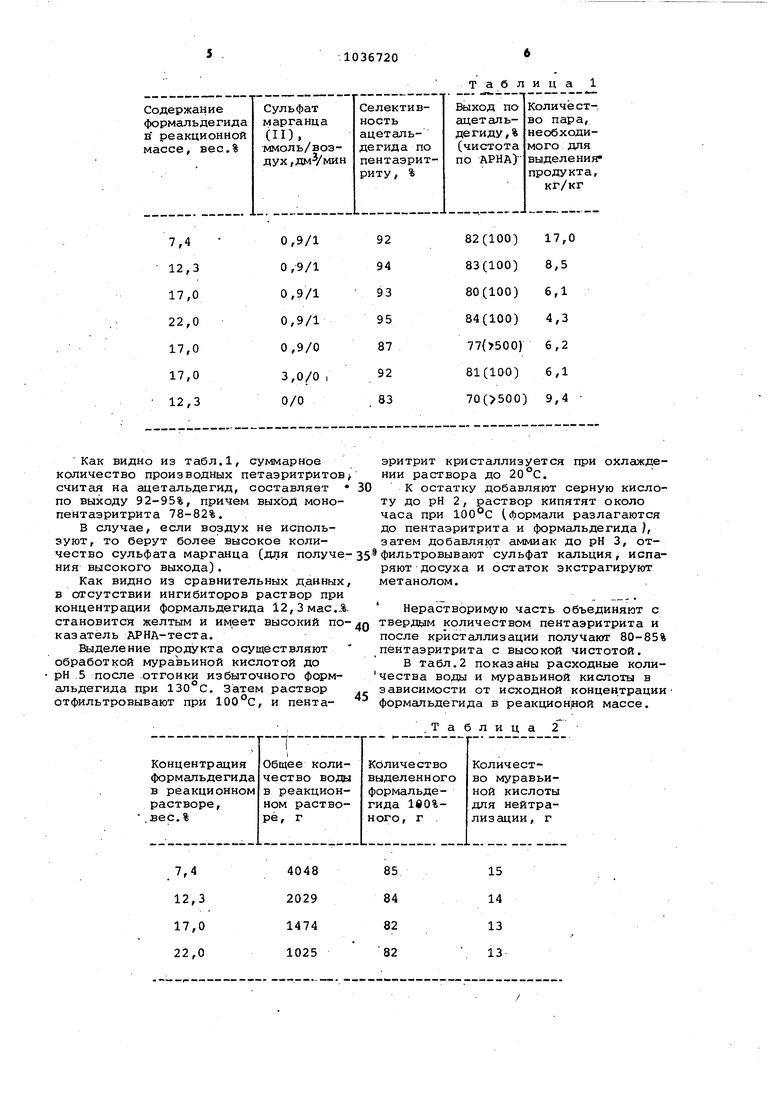
Изобретение относится к усоверше ствованному способу получения диили полиоксисоединений, которые используются в производстве лаков. Известен- с.пособ получения ди- ил полиоксисоединений конденсацией фор сшьдегида с другим альдегидом и/или кетоном в разбавленных водных раств рах, при этом оптим альными условиям получения пентаэритрита является ис пользование концентрации формальдеги да в реакционной смеси, равной 6,3 вес.% fl или 6-10 вес.% 2 с достижением выхода целевого продукта 80%, Такие разбавленные растворы форм альдегида используют в случае применения слабых оснований, т.е. гидроокиси кальция или других щелочно-земельных металлов. Однако, хотя в этих случаях и получшот хорошие выходы целевого продукта, но из-за большой растворимости его в воде требуется большое коли честв.о тепла для упаривания и выделения. Разделение остатка (образованного продуктами реакции муравьиной кислоты с основным катализатором, ди-. или полиоксисоединениями и побочными продуктами) возможно на-основании различной растворимости их в органических растворителях или в воде. Известен способ получения диили полиоксисоединений, для снижения себестоимости продукта используют большие концентрации формальдегида 3. Однако протекание реакции становится более чувствительным к реакционному теплу, в результате чего изме няется качество продукта, особенно АРНА-теста, который для приготовления транспате 1тных лаков является ре . Известен также способ получения пентаэритрита взаимодействием избыт- 45 ка формальдегида с ацетальдегидом в водном растворе щелочи при 30-50 С в присутствии гидроокиси кальция и преимущественном весовом соотношении СНОСНО:НСНО:Н20; Са(ОН)2 равном 14:й20:1196:58, причем ацетальдегид добавляют в течение 2 ч, а затем воду - 1,5 ч. Время выдержки 7 ч, выхо 88% (при избытке Формальдегида 320 вес.% . Однако длительность процесса огра ничивает его использование. Наиболее близким к предложенному является способ получения ди- или полиоксисоединений конденсацией избытка формальдегида -с други 1 альдегидом и/или кетоном в присутствии гидроокиси щелочно-земельного металл в начале процесса и гидроокиси щелоч ного металла в конце при температуре больше 30 С. Замену гидроокисью щелочного металла ведут после достижения конверсии другого альдегида и/или кетона не менее 50%, преимущественно 90%, с помощью добавления растворимых в воде солей щелочных металлов. Общее количество оснований для даЬной реакции должно быть выше теоретического, так как нужно учитывать наличие параллельных реакций, имеющихся в данном процессе. После достижения содержания формальдегида в реакционной смеси равного 1-0,1 % вес. Начинают выделение целевого продукта. Так, в случае получения 2,2,6,бтетраметилциклогексанола используют 15%-ный формалин, циклогексанон и водную суспензию Са(ОН)2, которые берут в мольном соотношении 6:1:0,7, соответственно. Процесс ведут в течение 20 мин при 35°С. Затем к смеси добавляют оксалат калия в количестве, эквивалентном Са(ОН)2.Смесь отфильтровывают и затем нагревают до 65°С и выдерживают 4 ч. Содержание целевого продукта в растворе соответствует выходу целевого продукта 83%. Общее содержание формальдегида в реакционной смеси составляет 6,6 вес.% 5. Однако невысокое содержание формальдегида предусматривает дополнительные расходы тепла на выпаривание. Целью изобретения является получение ди- или полиоксисоединений общей формулы C H2n+1 Om, где п 5-20; t 0 или 2; m 2-7,. с меньшими энергетическими затратами. Поставленная цель достигается тем, что согласно способу получения диили полиоксисоединений конденсацией избытка формальдегида с другим альдегидом и/или кетоном, имеющим 2-10 атомов углерода в присутствии щелочи и/или гидроокиси щелочно-земельного металла, взятой в количестве моль-эквивсшентов из интервала, рассчитываемого по формуле ,5 (F-Ax)J, . где А - количество другого альдегида и/или кетона,моль; F - количество формальдегида, X - теоретическое количество формальдегида, реагирующего с одним молем другого альдегида и/или кетона, моль, при 30-100°С, формальдегид берут в количестве 10-33 мас.%, считая на исходную реакционную смесь, и процесс ведут в присутствии кислородсодержащего газа и ингибитора автоконденсации формальдегида - соединения, выбранного из группы: нитротолуол, хлорид или сульфат марганца (II) или железа (II) муравьинокислый или азотнокислый марганец (IT), тетраборат натрия, хлорид олова (IV) , висмута (III) или церия, ацетат свинца (II) сульфат сурьмы (II), перманганат () или манганат () калия, причем выделение целевого продукта ведут после удаления непрореагировав шего формальдегида физическим методом - дистилляцией или ректификацией , и/или химическим методом - обработкой аммиаком, с последукщим концентрированием раствора и кристаллизацией. Это обеспечивает полу.чение проду та с хорошим выходом при меньших затратах. В качестве другого альдегида и/ил кетона целесообразно использовать ацетальдегид, пропионовый, н- или изобутироальдегид, циклогексанон, в качестве оснований - гидроокись кал ция в виде ч одных раствсров или в твердой форме. Количество используемого основания обычно составляет более теоретического, т.е. не менее 1 моль (эквивалента), считая на моль другого ал дегида и/или кетона. В этом случае катализатор расходуется на восстановление окисей по реакции Каницарро При этом для .восстановления одной мо лекулы оС-MOHo-ot, о -гексаметилолальдегида и/или кетона требуется одна молекула формальдегида. Образующаяся при этом муравьиная кислота в резуль тате нейтрализации основанием дает соответствующую соль муравьиной кислоты, за счет чего катализатор конденсации удаляется из реакционной среда. Таким образом, необходимо применять количество основания в моль-экБивалентах из интервала, расчитываемого по формуле ,5(F-Ax|. Для «получения монопентаэритрита используют 50-100%-ный избыток формс1льдегида от теоретического, так как при применении меньшего количест ва получаются ди- и трипентаэритриты Для снижения количества побочных пр дуктов используют ингибиторы автоконденсации формальдегида. Наиболее предпочтительными являются соединени марганца или железа, например сульфат, в количестве 0,0003 вес.% на реакционный раствор. Исходный формальдегид применяют виде 15-25%-ных растворов, при этом должен обеспечиваться максимальный контакт с кислородсодержащим газом. Это контролируется наблюдением за окраской реакционного раствора. При использовании рульфата марганца (II) активная форма дает розовое окрагиивание, а не активная - бесцветная. Наличие розовой окраски свидетельствует об отсутствии продуктов автоконденсации. Выделение непрореагировавшего формальдегида можно вести физическими или химическими методами, например дистилляцией при использовании большого избытка формальдегида, или обработкой пииакрм за счет различной растворимости формиата аммония и целевого продукта. Преимуществом изобретения является снижение расхсзда энергии на выпаривание и концентрирование продукта. Так, при использовании 18,3 вес.%. содержания формальдегида в реакционной смеси вместо 8,8 вес.% для получения. 1 т пентаэритрита требуется понижение количества тепла для испарения 9000 кг воды, т.е. на 5-10 кал снижение энергетических затрат. Пример 1. Получение пентаэритрита проводят в трехгорлой колбе (6л), снабженной мешалкой, обратным холодильником, термометром и дозирующей воронкой, причем.термометр вставляют в горло с помощью V-образной трубки, во второе горло которой вставляют холодильник. Через обратный холодильник в раствор подают воздух со скоростью 4 л/ч. Температуру поддерживают около 40°С. В/реакцию вводят 4 моль ацетальдегида; 24 моль формальдегида, 3,2 моль окиси кальция и необходимое количество воды. Выли исследованы 7,4-22,0%-ные концентрации формальдегида в исходной реакционной массе, причем загрузка формальдегида составляет 4 550 г во всех случаях, а ацетальдегида - 1,5 и 2,5 моль. В качестве ингибитора применяют сульфат марганца (11) в количестве 0,9 ммоль (0,15 г) на одну порцию. Дозирование ацетальдегида в реакционный раствор ведут в течение 40 мин, затем перемешивают при постоянных условиях 30 мин.1 В табл.1 показаны зависимость выхода, чистоты целевого продукта, а также расход пара, необходимого для выделения целевого продукта, от условий процесса и концентрации формальдегида.
таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения ди-или полиоксисоединений | 1974 |
|
SU905225A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИ- И ТРИПЕНТАЭРИТРИТА | 1973 |
|
SU387959A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНЗАЭРИТРИТА | 1992 |
|
RU2054409C1 |
| Способ получения пентаэритрита | 1974 |
|
SU533230A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАЭРИТРИТА С ИСПОЛЬЗОВАНИЕМ ПАРАФОРМАЛЬДЕГИДА | 2010 |
|
RU2440324C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАЭРИТРИТА И ДИПЕНТАЭРИТРИТА | 2008 |
|
RU2402519C2 |
| Способ получения диспергирующей добавки для белитсодержащих шламов | 1976 |
|
SU658126A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАЭРИТРИТА | 2010 |
|
RU2445303C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАЭРИТРИТА С СОДЕРЖАНИЕМ ОСНОВНОГО ВЕЩЕСТВА БОЛЕЕ 98 МАС.% И ПЕНТАЭРИТРИТА, ОБОГАЩЕННОГО ДИПЕНТАЭРИТРИТОМ В КОЛИЧЕСТВЕ 5-20 МАС.% | 2002 |
|
RU2208009C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАЭРИТРИТА | 2000 |
|
RU2181353C2 |
СПОСОБ ПОЛУЧЕНИЯ ДИ- ИЛИ ПОЛИОКСИСОЕДИНЕНИЙ общей формулы C H2n+1tOm где п 5,20; 1 0 или 2/ гг. 2-7, путем конденсации избытка формальдегида с другим альдегидом и/или кетоноМ с числом атомов углерода 2-10 в присутствии щёлоки и/или гидроокиси щелочно-эемельного металла,взятой в количестве моль-эквивалентов из интервала, рассчитываемого по формуле ,5(F-Ax)|, где А - количество Другого альдегида и/или кетона,моль; F - количество формальдегида, моль ; X - теоретическое количество формальдегида, реагирующего с одним молем другого апьдегидй и/или кетона,моль при ЗО-ЮО С, отличаю щийся тем, что, с целью снижения энергетических затрат, процесс ведут в присутствии кислородсодержащего газа и g автоконденсации формаль(Л дегида - соединения, выбранного из i группы итротолуол, хлорид или суль-; фат марганца (II) или железа (II), муравьинокислый или азотнокислый марганец СП), тетраборат натрия,хлорид олова (IV) или висмута (III) или це-. рия, ацетат свинца (II), сульфат сурьмл (II), перманганат (Мп) или марганат (ЬЬг) калия, причем содероо жание формальдегида в реакционной смеси составляет 10-33 мас.% и выдеа ление целевого продукта ведут после удаления непрорёагировавшего форм 4i альдегида физическим методом - даюю тилляцией или ректификацией, и/или химическим методом - обработкой аммиаком, с последуквдим концентрированием pacifsopa и кристаллизгщией.1 .
Как видно из табл,1, суммарное количество производных петаэритритов считая на ацетальдегид, составляет по выходу 92-95%, причем выход монопентаэритрита 78-82%. В случае, если воздух не используют, то берут более высокое количество сульфата маргш1ца (для получе ния высокого выхода). Как видно из сравнительных данных в отсутствии ингибиторов раствор при концентрации формальдегида 12,3мас...% становится желтым и имеет высокий показатель АРНА-теста, Выделение продукта осуществляют обработкой муравьиной кислотой до рН .5 после .отгонки избыточного формальдегида при 130°С. Затем раствор отфильтровывают при 100°С, и пента40482029 1474 1025
85 84 82 82
15 14 13 13 эритрит кристаллизуется при охлаждении раствора до 20°С. К остатку добавляют серную кислоту до рН 2, раствор кипятят около часа при 100°С (формали разлагаются до пентаэритрита и формальдегида ), затем добавляют аммиак до рН 3, отфильтровывают сульфат кгшьция, испаряют досуха и остаток экстрагируют метанолом. Нерастворимую часть объединяют с твердым количеством пентаэритрита и после кристаллизации получают 80-85% пентаэритрита с высокой чистотой. В табл.2 показаны расходные количества воды и муравьиной кислоты в зависимости от исходной концентрации формальдегида в реакционной массе. .Таблица 2
Авторы
Даты
1983-08-23—Публикация
1978-01-23—Подача