4
Изобретение отно;;ится к повьет химическим соединениям, а (,; к имидазоД, 5-g|HHAOJ H3H-aM обптй фопМ ЛЫ I
Г R - 6
где R,
R, - Н, R,,.
которые могут быть испол аопапы для синтеза белаз-тлиденпроизво; пых -INUE;.-зо А , 5-g индолизинор ,, o6jia;iaKViiHx Оя;
5РИ{. ID О
И фуи; ,; г:;- -;г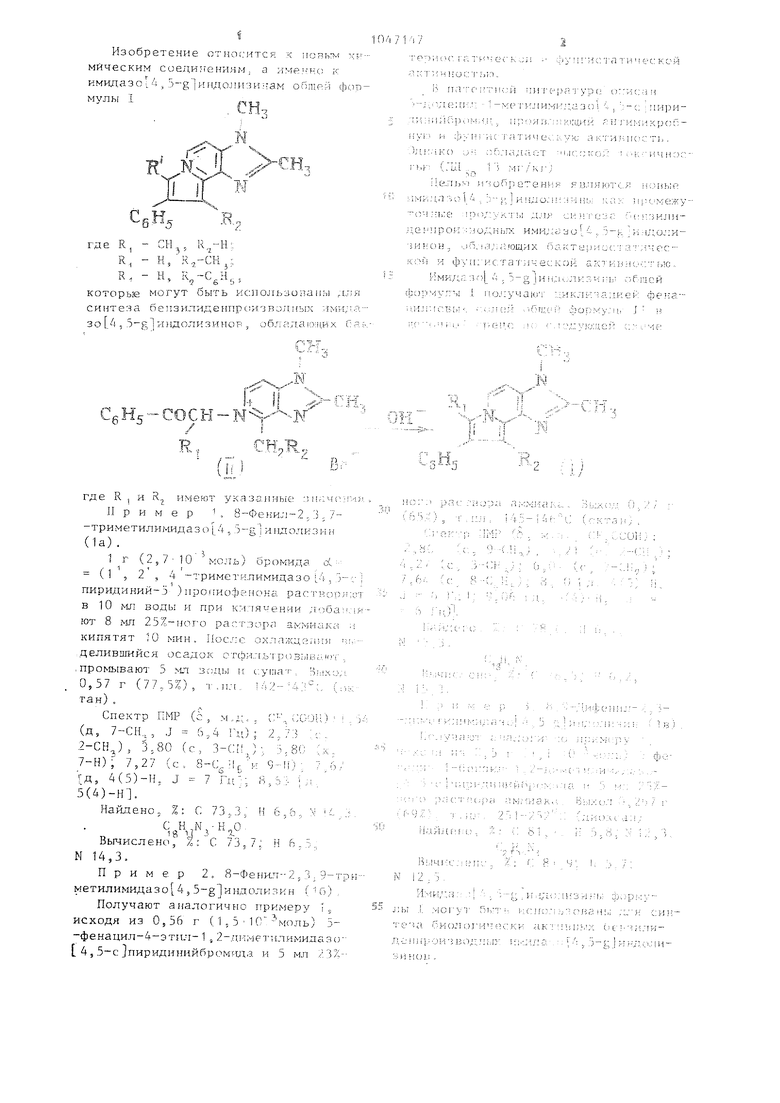

Имидазо 4,5-§ индолизины общей формулы где R , - CHj,R,j-H; R, R, - Н, R-C,H,, как промежуточные продукты для синтеза бензилиденпроизводных имидазо Д,5-g индoлизинoв, обладающих бактериостатической и фунгистатической сл активноетью.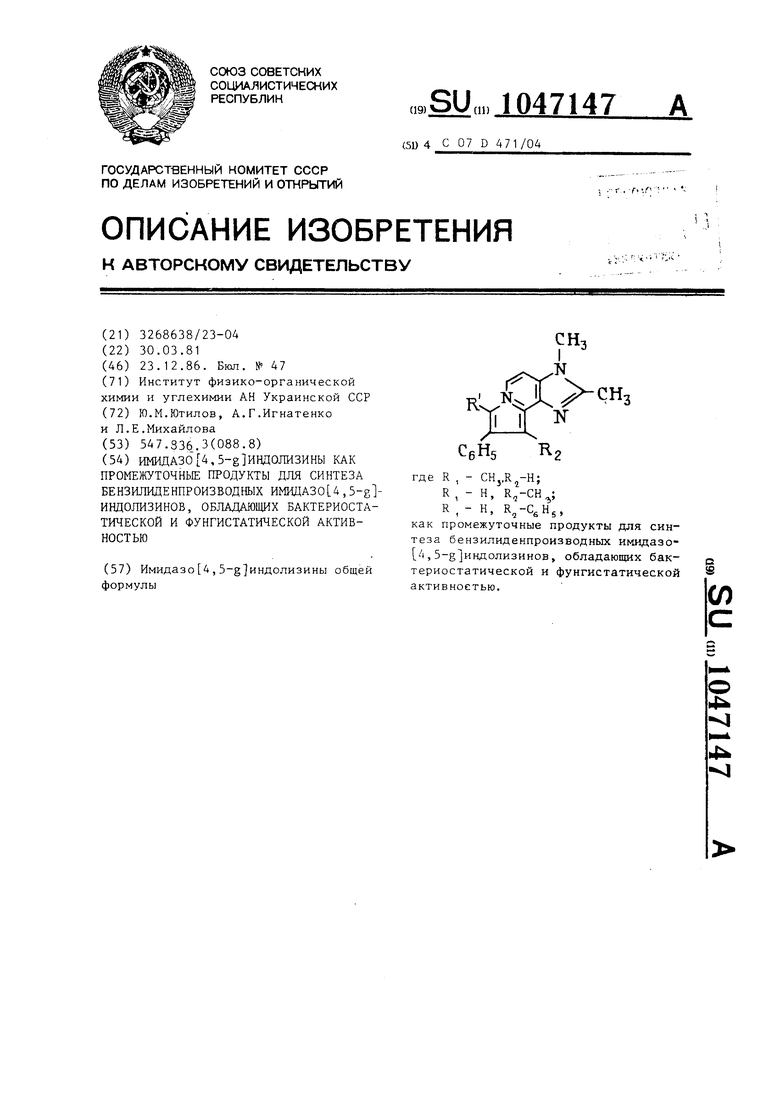
--
п
:6H5-COCH- NV --N R...CHR,,
где R I и Rj имеют указа)1нь;е inuiMi-;;Пример ч 8-Фе}5Ил-2, 3 , 7-три; 1етилимидазо1 3-;-1 ицдочизнн (1а).
1 г (2,710 моль) бромица d / 1 т
V 5 - 5 + риметилимидазо -f - пиридиний-5 ) проииофенока растт ог я:
в 1 О мл ВОДЬ и при КМЛЯггенИИ .
ют 8 мл 25%-ifor-o ра Гз;1ра аммиака ; кипятят 10 мин. После охлаждзаю . деливпшйся осадок стфильчрозынаJOT.
промывают 5 мл воды и суша-г )::
0,57 г (77,5%) , ТЛ1Л, i 0,v тан) .
Спектр ПМР (с , M,z;, . Гл СООН (д, 7-СН, , J 6,4 Il.) ; 2.73 лл 2-Cfi) , 3,80 (с, 3-Сл J 3;8(: :K 7-Н) , 7,27 (с, 3-( 7 о/ ГД, 4(5)-Н. J 7 ГгГ: Я л i:i 5(4)-Н.
Найдено. %: С 73 „3 i 6 о v i.
Sg4iN,-H
Вычислено, % С 73,7; Н п.N 14,3.
Пример 2, 8-ФеЕ1И.л-2 S 3 , 9-гр метилнмидазо 4, 5-§ индолизкн ) ,
Получают аналогично примеру ., исходя из 0,56 г ( 1, 5 10 моль) 5 фенацил-4-эти;1-1 , 2-л,имет;-:лимидазо- 4,5-с пиридиннйбромсща и 5 мл /3/;-3|i
Актив но с т I, 6 ензилиденпроиз водных имидазо 4,5-glиндолизинов изучали методом двукратных разведений на жидкой срелте. Для культивирования бактерий использовали бульон Хоттингера (рН 7,2-7,4). Микробная нагрузка для бактерий 5-10 кдеток агаровой 18-Ч. культуры в 1 мл среды. Максимальная из испытанных концентраций 200 мкг/мл.
Для вьфащивания грибов использовали среду Сабуро (рН 6,0-6,8). Нагрузка 500 тыс. репродуктивных телец в 1 мл. Максимальная из испытанных концентраций 200 мкг/мл. Антимикробную активность соединений оценивали по
Штаммы микроорганизмов Минимальная бактериостатическая
и грибов
Staphylococcus aureus 20YP
Bacillus antracoides 1312
Escherichia coli 675 B. pyocyaneum Shigella Flexneri
Trichophyton mentag. IMJ 124768
Microsporum lanos ura 257
минимальной бактериостатической или мнкростатической концентрации соединений ,
Результаты испытаний приведены в таблице.
LDgQ соединений 1 а-1 в составляет 1040±76, 1120159, 65101377 мг/кг соответственно .
Таким образом, из предлагаемых соединений простьм доступным способом можно получать продукты, которы проявляют бактериостатическую и фунгистатическую активность и могут быть использованы в химико-фармацетической промышленности.
|или микостатическая концентрация, Iмкг/мл
200
200
6,25 12,5 100 100
Более200 Более 200 , 6,25 200
Более 20C
25
25
25
50
To же
Авторы
Даты
1986-12-23—Публикация
1981-03-30—Подача