б)6-Окси-1,4-диметилкарбазол. Нагревают при мягком кипяче1ши с обратным холодильником При 180-190с в течение 5 ч раствор 30 г 6-метокси-1,4диметилкарбазола с 300 г абсолютно 5 безводного хлористоводородного пиридина. После охлаждение выливают смесь на лед и подщелачивают концентрированным раствором аммиака до рН б6,5, .затем сушат, промывают несколько tO раз водой и снова кристаллизуют из смеси этанол/вода.
Получают тонкие бесцветные кристалль (молекулярная масса 211,26), вькод 22 г, т.пл. .15
Элементный анализ для (.
Еычислено, %: С 77,84; Н 5,60; N 4,32; О 12,35.,
Найдено, %: С 77,41; Н 5,64; N 3,97-3,92, О 13.20
в)6-Бензоштоксо-1,4-диметш1кар- базол. Растворяют 21 г(О,10 моль).
6-ОКСИ-1,4-диметилкарбазола в смеси 200 мл безводного ацетона в 50 мл тризтиламина, высушенного над таб- 25 летками едкого кали.
Прибавляют по каплям 17 г (0,12 моль) перегнанного бензоилхлорш да при постоянном перемешивании смеси магнитной мешалкой. Длительность ЗО реакции составляет 2ч.
Наблюдается осаждение солянокислого триэтиламина. Удаляют избыток ацетона и остаточный триэтиламин при нагревании, на водяной бане. Сно- 35 ва растворяют продукт в воду и несколько раз экстрагируют хлороформом. Хлороформный раствор промывают водой, потом 5%-ным раствором бикарбоната натрия и снова водой, затем сушат 0 над хлористым кальцием, фильтруют . и отгоняют избыток хлороформа.Продукт снова кристаллизуют из мини- мального количества хлороформа. Про-г дукт имеет т.пл. 315+9®С.
Элементный анализ для Q, + + 0,5 НуО
Вычислено, %: С 77,84; Н 5,60; N 4,32; О 12,35.
Найдено, %: С 77,41; Н 5,64;50
N 3,97-3,92; О 13.
г) 9-Этил-6-бензоилоксо-1,4-диметилкарбазол. В аппарате, снабженном ловушкой с хлористым кальцием, растворяют в 120 мл ДМФ, высушенного над 55 молекулярными ситами, 16 г (0,05 моль) 6-бензоилоксо-1,4-диметилкарбазола. Прибавляют туда при перемешивании
магнитной мешалкой 1,35 г 100%-ного гидрида натрия. Примерно через I ч образуется мононатриевое производное
При полном наружном охлаждегаш ледяной водой прибавляют по каплям п течение 30 мин 9 г йод1 стого этила. Смесь оставляют на ночь без перемешивания. После этого в течение 1 ч нагревают на водяной бане.
Удаляют основную часть ДГ1Ф в глубоком ва.кууме. После охлаждения повторйо растворяют продукт в ледяной воде и несколько раз экстрагируют хлроформом. Промывают хлороформный расвор водой, сушат над хлористым кальцем, фильтруют и удаляют избыток х.пороформа.
Продукт молекулярной массы 143,4 имеет формулу (L JL NO .
д)9-Этил-6-6ензоилоксо-3-формил1,4-диметилкарбазол. В 200 мл сухого ортодихлорбензола растворяют 4 г (0,12 моль) полученного продукта, затем прибавляют 22 г (0,7 моль) свежеперегнанного N-метилформанилида и поциями прибавляют 22 г (0,14 моль) хлорокиси фосфора.
; Всю смесь нагревают в течегаге 3 ч на кипящей водяной бане. После охлаждения осторожно вьшивают реакционный продукт в холодный раствор 50 г ацетата натрия в 300 мл воды.
Отдаляют бензольнь1й слой деканта1щей и используют экстракцию с паром для удаления ортодихлорбензола и избытка М-метилформанил1 да. Остаток растворяют, в толуоле при нагревании и очищают на угле.
Продукт молекулярной массы 371,436 имеет формулу Q, ILNO-.
е)0-Этил-6-бензош10ксо-3-(, /Э диметилоксиэтилиминометш) -1,4-диметилкарбазол.
1 .
На кипящей водяной бане в течегше
12 ч нагревают смесь 18,60 г (0,05 мол полученного продута (альдегида) и 50 мл диметилацеталя аминоацетальдегида. Затем прибавляют 100 мп безводного бензола и удаляют азеотропной перегонкой смеси воду, образующуюся во время реакции. Остаток перекристаллизовывают из бензола (или толуола) .Получают продукт молекулярной массы 458,56, который имеет форму«yWA; ж) 9-Вензоилоксо-6-этилзллиптицин
(основание). В раствор 600 г ортофосфорной кислоты и 20 г пятиокиси S1 фосфора вводят 22 г (0,05 моль) полученного продукта (азеометина), Осторожно нагревают смесь до 125 1 и выдерживают при этой темпер туре 20 мин. После пдследующе1 о охлаяаде шя реакционную смесь выливают в 3 л ледяной воды и проводят осторолшую нейтрализацию аммиаком до рН примерно 7. Получают смесь 9 бензоилоксо-6этияэллиптицина и 9-оксо-6-этилэлли тицина, которую можно разделить хро матографией на колонке. МлО Сцеле Молекулярная масса С, вое соединение) равна 394,48. з) 9-Окси-6-этилэллиптицин (осно ваьше). Нагревают при слабом кипении на водяной бане в течение 30 мин 10 г смеси полученных 2 эллиптицинов в 100 мл.95%-ного этанола и 10 мл кон центрированной соляной кислоты. После охпалсдения. и сушки получают цепевое соединение, которое пере кристаллизовьшают из этанола. , Молекулярная масса равна 290,37. и). Йодистый 9- окси-2,6-диэтилэллиптициний (или йодэтилат-9-ОКСО-6этилэллиптициния),. Растворяют в 100 мл ДМФ, предвар )тельно высушенного над молекулярными ситами, 10 г 9-ОКСО-6-ЭТИЛЗЛЛНПТ цина и после охлаждения прибавля-, ют еще 5 мл йодистого этила. Смесь перемешивают с помощью магнитной ме шалки в течение нескольких часов,чт способствует осаждению максимальног количества гапогенида. Продукт cyiuaT и прогЛ.шают безвод эфиром, а затем перекристаллизовывают из абсолютного этанола. Молекулярная масса С Н N.01 равt I f 5 jib на 446. Элементный анализ: Вычислено,%: С 56,55; Н 5,20; N 6,28; О 3,59; I 28,45. , Ншщейо, %: С 55,77-55;73; И 5,2 5,18; N 6,11-6,25; О 3,85-4,10; 28,96-28,89, Тонкослойная хроматография с силикагелем Мерк F-254 и растворителем смесью бутанрл-уксусная кислота вода (4:1:5). R.g3iO,33. к) Ацетат 9-окси-2,6-эллиптицини В ДМФ растворяют полученный продукт, добавляя все время воду порци ми, чтобы образовать растворитель. 6 состоящий из ДМФ и воды (в равных частях) , и получить конечную концентрацию около 2-10 мг/нмл. Затем тЕ.;ательно дегазируют этот раствор. Готовят колонку из анатштическогосорта анионообменнор смолы Бис-Рэд (ацетатная форма). Обменная емкость этой смолы составляет 1,4 мэк/мл смолы или 3,2 мэк/г сухого веса смолыj т.е. 0,78 г смолы/г продукта. Соответственно, тсоличество использованной смолы равно .троекратному от точно необходимого количества, В качестве элюента использу}от смесь ДМФ и (50:50), В этой смеси суспендируют смолу. Затем заполняют колонку и уравновешивают ее, элюируют йо.цистое производное на этой колонке, получая раствор ацетата 9 оксо-2,6-диэтилэллиптици11ИЯ. Из него полностью удаляют воду и частично ,Ц11Ф Проводят осалодег-ше эфиром и после фильтрования, осалоденный и отфильтрованный продукт- сушат эфиром и сушат в вакуух е и эксикаторе. Получают оранжевый порошок, хорошо растворимый в воде (выход 95 вёс.%), из которого легко мохию приготовить водш,1Й раствор, ссцержащий 4 мг/мл . этого ацетата. Молекулярная масса .NiQA рав„ „.Ъ 2Ь i 3 на 378. Прим ер 2,. Работает по методике примера 15 но исключают необязательную стадию металлировал-шя , ш один из продуктов , полученных на этапах g-k, не содерлсит алкильной группы у атома азота в поло) 9 карбазольного цикла (или в положении 6 эллиптицинового цикла), Продукт этапа 5 имеет т,пл, 200С. С помощью тонкослойной хроматографии (тех) при элюировада1и смесью гшористый метилен-этанол (ЗО:1) получают одно пятно, доказывающее чистоту продукта; продукт этапа Э имеет т.пл. 264°С; тех (бензол-этилацетат 5:1)-одно пятно; продукт этапа е имеет т.пл. 238°С, ТСХ (хлористый метилен-этанол 20:1)-одно пятно; продукт этапа Ж имеет т.пл. 245 С. ТСХ (хлористый метиленэтанол 20:10) одно пятно. Полученшлй 9-оксиэллиптицин имеет молекулярную массу 262. Его анализ соответствует теоретическому, допуская наличие половины молекулы присоединенной воды. %1стота 97-98%. П р и м е р 3. Получение 9-оксиэл липтицина из 6-бензилокси-1,4-димепшкарбазола. Сначала готовят 6-окси-1,4-днмети карбазол по методике примера 1. Затем проводят синтез 9-оксиэл гапти1Ш на. П р и м е р 4. 1,4-Диметил-6-окси карбазол. В трехгорлую колбу загружают 790 (10 моль) пиридина, потом через погр женную трубку барботируют II 2-, 5 г (5, моль) газообразного хлористого водорода. Отгоняют головную фракцию до получения температуры массы 192195°С. Охлаждают до и вводят 112,5 г (0,5 моль) 1,4-диметил-б-метоксикарбазола. Повьшают температуру до 192-195 с и выдерживают эту температуру в течение 0,5 ч. Гидроли зуют 1000 г ледяной воды. Экстрагиру ют трижды 300 см серного эфира. Про мывают объединенные эфирные слои дваж ды 100 см воды, потом сушат над без водным сульфатом натрия. Удаляют эфи концентрированием при атмосферном давлении .Собирают 99 г сырого продукта , выход 94%. Церекристаллизовывают сырой продук из 10 объемов смеси дихлорэтан-п-гептан (50:50 по объему). Выход, при очистке 65%i т.пл. 167с Тонкослойняя хроматография - на пластинке Мерк F 254 с элюентом бензолом. Проявление: ближний УФ. Rf 0,10-0,12. Деметилирование 1,4-диметил-6метоксикарбазола в противоположность демётилированню 9-метоксиэллиптицина ;не вызывает проблемы чистоты для полу ченного 1,4-диметил-6-оксикарбазола, потому что последний является стабиль ным продуктом в рабочих условиях, имеющихся в этой реакции. П р и м е р 5. 1,4-Диметил-6-бензилоксикарбазол. В трехгорлую колбу загружают 12,6 1,4-диметил-6-оксикарбазола; 100 г N, М-диметилформамида; 16,0 г хлористого бензила и 16,8 г безводного ка боната калия. Перемешивают 20 ч при комнатной температуре. Реакционную среду гидролизуют 500 г воды. Двадцы экстрагируют 100 см серного эфира и промывают объединенные эфирные слои два раза 50 см воды, потом сушат над б.езводным сульфатом натрия. Удал ют эфир концентрированием при атмосферном давлею. Остаток обрабатывают 30 см пентанас Отсасывают ося-док. Перекристлллнзовывают его из 40 см смеси -гептана и дих.11Орэта}1а (60:40 по объему) .Вес гюлучеююгО) продукта 12,4 г; выход 60%, т.пл. То Н1С о алойная хрсматография на плафиике Лерк F 25 с элюентом бепзолом. Проявлелше : ближш1Й УФ. R 0,60. П р И М е р 6. i54-Диметил-З-формил 6-бензилоксикарбазол. В трехгорлую колбу загружают 6,02 г 1,4-диметил-6-бепзилоксикарбазола; 20 см дихлорэтана и 3,7 г М-диметилформаьшлида. В эту среду вводят в течение 0,5 ч 3,7 г оксихлорида фосфора. Выдерживают реакционную массу на водяной бане в течеш е 5 ч npi- Te.isnepaType массы 50 С. Реакционн ю среду гидролизуют раствором 12,3 г тригидрата ацетата натрия в. 350 г 15ОДЫ. Отфильтровывают осадок, промывают его обильно водой, потрм обрабатывают при перемешивании 50 см серного эфира. Снова отсасывают и сушат. Вес полученного продукта 5, 25 г; выход 80%; т.пл. . Тонкослойная хроматография на плястипке Мерк 254 с элюетггом бензолом (60 см) и ацетоном (20 смЗ) . Проявле1ше: ближщп 5Ф. Rf D,80. П р и м е р 7 , ., - Диметил-З-(N, М-диметокс1-1:Этилпминометтш) -6-бензилоксикарбазол. В трехгорлую колбу загружают 6,6 г 154 диметил-3-формш1-6-бензилоксикарбазола; 50 г бензола и 2,4 г диметилацеталя a шнoaцeтaльдeгидa. Нагревают до кипения с обратным холодильником и удаляют р«акцион гую воду азеотропной отгонкой в течение 2 ч. Охлаждают сре,цу до 10 С и отсасывают осадок. Промывают полученные кристаллы 50 см н-гептана и сушат. Вес полученного 6,6 г; выход 79%; т.пл. 1-30 С. Прим ер 8. 9-Бенз1 локсиэллиптицип. В трехгорлую колбу захружают A3 г 85%-ной фосфорной кислоты и 5,7 i фосфорного ангидрида. Нагревают при перемешивании до 80-90 С, потом при- ливают раствор 3,7 г I,4-диметил-З(jb, fb -диметоксиэтилиминометил) 6бензилоксикарбазола в 25 см бензола. Гидролизуют реакциоир1ую среду с помощью 100 г воды, потом нейтрали1зуют до рН 9 jtyreM медленного добавл ния 50%-ногд аствора гидроокиси натрия. Отсасывают .осадок, обильно промывают его водой и сушат. Вес полученного продукта 3,0 г; выход 95 Тонкослойная -хроматография на пластинке Мерк 254 с элюентом бензолом (72 см) и этанолом (18 см ) . Проявление: ближний УФ. Kf-0,50 (С Н5-СН20Н) и ,35 (НО). Сырой продукт представляет собой смесь 70% бензильного производного и 30% гидроксильного производного из-за недостаточной кислотности среды. Он может быть перекристаллнзован- из 200 объемов ацетона, что приводит к продукту, содержащему менее 5% гидроксильного производного, которое не представляет собой загрязнение, поскольку речь идет о продукте, получаемом на следующей стадии. П р и м е р 8 . 9-Оксиэллиптицин В колбу Эрленмейера загружают 500 см этанола; 0,5 г палладированного угля, содержащего 10% палладия, потом 3.О 5 г 9-бензш1оксиэллиптицина. После продувки азотом проводят гидрогенолиз при давлении 150 г и комнатной температуре . После поглощения теоретического количества водорода удаляют палладированный уголь. Выпаривают досуха на роторном испарителе при остаточном давлении, создаваемом водоструйным насосом. Вес полученного продукта 3„7 г. Выход 100%.. Очищают продукт в 100 объемах этанола при удалении нерастворимого продукта при нагреве. Выход после очистки 85%; т.пл. . Ангидро-гтитриметрический титр не менее 98%. Процентное содержание димера ке более 2%, (жидкостная хроматография). Предлагаемый способ позволяет получать целевые продукты с высокими выходом и степенью чистоты, которые могут быть использованы для приготовления композиций с противораковой активностью или в качестве промехсуточных продуктов для получе1шя таких соединений.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения N-ацетилмурамилпептидов | 1979 |
|
SU1326197A3 |
| Способ выделения углеводородов, имеющих подвижные атомы водорода,из углеводородных смесей | 1972 |
|
SU460612A3 |
| Способ получения н-бутиловых эфиров производных N-ацетилмурамилпептидов | 1982 |
|
SU1346046A3 |
| Способ получения 2-метил-1,4-дихлорбутена-2 | 1973 |
|
SU499797A3 |
| Способ получения солей ангидридов кислот фосфора | 1976 |
|
SU615861A3 |
| Способ получения карбоцепных полимеров | 1977 |
|
SU676174A3 |
| Муфта свободного хода | 1973 |
|
SU561524A3 |
| Способ получения @ -аминоамидов | 1979 |
|
SU1220568A3 |
| Способ получения сопряженных соединений гаптенов и мурамилпептидов | 1983 |
|
SU1331433A3 |
| Способ получения привитых сополимеров | 1971 |
|
SU475784A3 |
Способ получения 9-оксиэллиптицина или его производных общей формулы СН, БоО l Щ или их солей, кватернизированных по атому азота в положении 2, общей формулы «Hj в,о. J.jr% о -Л. :; :BI сщ где R - водород или ннзши -алкил; R - водород, бензил, бензоил или низший алкил; R - низший алкил; X - кватерьшзирующпй amton, о т л и ч а ю щ и и с я тем, что 5;Метоксиивдол подвергают взаимодействию с 2,5-гександ1 опом, деметилируют полученньц 6-метокси-1 .4--диметилкар базол, защищают гидроксильную группу бензилированием или бензоилированнем б-окси-1,4 диметилкарбазола, потом, если необходимо, осуществляют.металлирование продуктами обработку иодис- ть1м алкилом, форми.1шроваш1е,ко1-щеисацию .с диметилацеталем аминоацетальдегида, циклизацию полученного продукта, оь5ыле1ше 9-бензоилоксоэллиптицина.или гидрогенолиз 9-бензилоксоэллиптицина или 9-бемзилоксо-6-алкилэллиатицина с вьщеленпем целевого продукта или послед тпиюн реакцией lltMK с галоидалкилом и вьщелеталем продуклГЯЭ Vss та в свободном виде или после анионСД ного обмена в виде соли, соответстоо венно кватернизированной по атоъту азота в положегши 2. СД ОО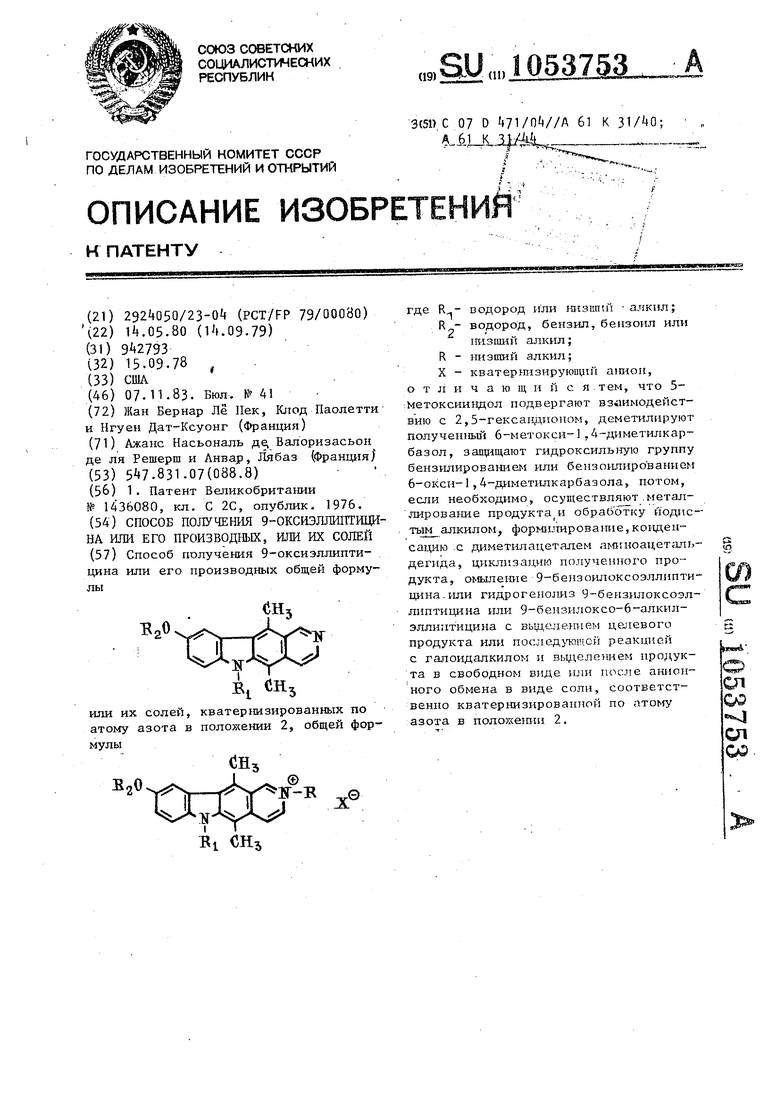
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ изготовления упругого элемента подвеса сейсмометра | 1987 |
|
SU1436080A1 |
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
Авторы
Даты
1983-11-07—Публикация
1980-05-14—Подача