Изобретение относится к химии фосфорорганических соединений с С-Р-связью, а именно к новым О-этил-S-[(N-карбалкокси-N-карбалкоксиалкил)аминометил] метилтио- или дитиофосфонатам общей формулы I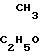



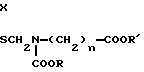 где при X = S, n = 1
где при X = S, n = 1
R = R′ = CH3; R = CH3, R′ = C2H5; R = = C2H5, R′ = CH3;
R = R′ = C2H5; R = CH3, R′ = изо - C4H9; R = изо - C4H9, R′= CH3;
при Х = S, n = 2
R = R′ = CH3; R = CH3, R′ = C2H5; R = R′ = C2H5;
при X = O, n = 1
R = R′ = CH3; R = CH3, R′ = C2H5; R = CH3, R′ = изо - C4H9;
при X= O, n = 2
R = CH3, R′ = C2H5, которые проявляют акарицидную активность.
Известно использование в сельском хозяйстве в качестве акарицидов таких препаратов, как метафос и рогор.
Наиболее близкими к описываемым соединениям по структуре и назначению являются O, O-диалкил-S-[(N-карбэтокси-N-метил)аминометил] дитиофосфаты формулы II
(RO)2P(S)-SCH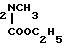 где R - CH3, C2H5, C4H9, которые обладают акарицидной активностью.
где R - CH3, C2H5, C4H9, которые обладают акарицидной активностью.
Однако акарицидная активность соединений общей формулы II недостаточно высокая.
Целью изобретения является расширение ассортимента акарицидов и повышение их эффективности.
Поставленная цель достигается описываемыми O-этил-S-[(N-карбалкокси-N-карбалкоксиалкил)аминометил] метилтио- или дитиофосфонатами общей формулы I, которые проявляют акарицидную активность выше, чем аналоги общей формулы II.
Соединения формулы общей I получают взаимодействием калиевых, натриевых или аммониевых солей O-этилметилтио- или дитиофосфоновых кислот с эфирами N-хлорметил-N-карбалкоксиглицина или N-хлорметил-N-карбалкокси- β -аланина в ацетоне при 20-25оС в течение 2-6 ч.
Известно использование в сельском хозяйстве в качестве инсектицидов метафоса, хлорофоса и карбофоса. Наиболее близким к описываемым соединениям по структуре является O, O-диметил-S-[(N-карбэтокси-N-изопропил)аминометил] дитиофосфат формулы
(CH3O)2P(S)-SCH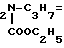 изо который проявляет инсектицидную активность в отношении комнатной мухи и который в концентрации 0,1% вызывает 100% -ную гибель насекомых и не активен в отношении рисового долгоносика и черной свекловичной тли.
изо который проявляет инсектицидную активность в отношении комнатной мухи и который в концентрации 0,1% вызывает 100% -ную гибель насекомых и не активен в отношении рисового долгоносика и черной свекловичной тли.
Целью изобретения является расширение ассортимента и спектра действия инсектицидов.
Поставленная цель достигается описываемыми соединениями общей формулы I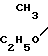


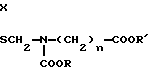 где при X= S, n = 1
где при X= S, n = 1
R = R′ = CH3; R = CH3, R′= C2H5; R = C2H5, R′ = CH3;
R = R′ = C2H5; R = CH3, R′ = изо - C4H9;
при X= О, n = 1
R = R′ = CH3; R = CH3, R′ = C2H5; R = CH3; R′ = изо - C4H9;
при Х = О, n = 2
R = CH3, R′ = C2H5, которые обладают инсектоакарицидной активностью как в отношении комнатных мух, так и в отношении рисового долгоносика и черной свекловичной тли.
Чистота веществ подтверждена элементным анализом и данными ТСХ (SiO2Л100/160μ , гексан-ацетон 3: 2). Строение полученных соединений подтверждено ИК-спектрами (характерные полосы поглощения С = O при 1730 и 1760 см-1, а для монотиоаналогов - Р = О-поглощение при 1260-1265 см-1).
П р и м е р 1. О-Этил-S- [(N-карбметокси-N-карбметоксиметил)аминометил] метил- дитиофосфонат (I).
К раствору 35,17 г (0,181 моль) О-этилметилдитиофосфоната калия в 180 мл сухого ацетона при 20-25оС добавляют по каплям при перемешивании 34,44 г (0,176 моль) метилового эфира N-хлорметил-N-карбметоксиглицина и выдерживают смесь в тех же условиях 4 ч. Осадок хлористого калия отфильтровывают и промывают на фильтре ацетоном, фильтрат выпаривают в вакууме, остаток растворяют в 200 мл эфира, промывают 50 мл ледяной воды, 30 мл охлажденного насыщенного раствора NaHCO3, 50 мл воды и сушат над Na2SO4. Эфир удаляют в вакууме и получают 51,05 г (91,9% ) чистого соединения I (R = R ′= CH3 X = S, n = 1).
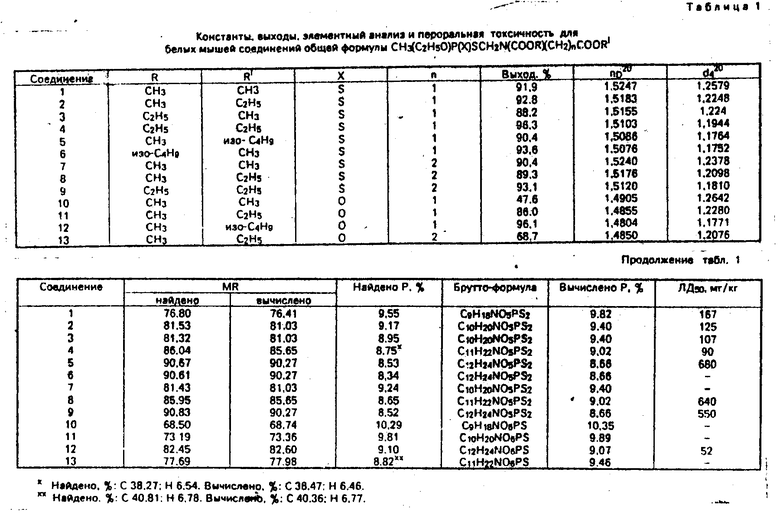
Аналогично получены соединения общей формулы I, где R = CH3, R′ = C2H5; X = = S, n = 1 (2); R = C2H5, R ′= CH3, X = S, n = 1 (3); R = R ′= C2H5, X = S, n = 1 (4); R = CH3, R= = изо - C4H9, X = S, n = 1 (5); R = изо - C4H9, R ′= CH3, X = S, n = 1 (6); R = R′= CH3, X = S, n= = 2 (7); R = CH3, R′ = C2H5, X = S, n = 2 (8); R = = R′ = C2H5, X = S, n = 2 (9). Константы, выходы и данные элементного анализа соединений 1-9 приведены в табл. 1.
П р и м е р 2. О-Этил-S-[(N-карбметокси-N-карбэтоксиметил)аминометил] метилти-офосфонат (11).
К раствору 4,38 г (0,027 моль) О-этилметилтиофосфоната натрия в 25 мл сухого ацетона при перемешивании медленно добавляют 5,24 г (0,025 моль) этилового эфира N-хлорметил-N-карбметоксиглицина (температура смеси 20-25оС) и выдерживают смесь в тех же условиях 6 ч. Осадок хлористого натрия отфильтровывают и промывают на фильтре ацетоном. Фильтрат выпаривают в вакууме, остаток растворяют в 30 мл эфира, промывают 10 мл ледяной воды, 10 мл охлажденного насыщенного раствора NaHCO3, 10 мл воды и эфирный раствор сушат над Na2SO4. Эфир удаляют в вакууме и получают 6,73 г (86,0% ) чистого соединения 11 (R = CH3, R′ = C2H5, X = O, n = = 1).
Аналогично получены соединения формулы общей I с Х = О, где R = R′ = CH3, n = = 1 (10); R = CH3, R′ = изо - C4H9, n = 1 (12); R = CH3, R′ = C2H5, n = 2 (13).
Константы, выходы и данные элементного анализа соединений 10-13 приведены в табл. 1.
Токсичность и инсектоакарицидная активность предлагаемых соединений.
Токсичность соединений общей формулы (I) для теплокровных животных исследовали при введении их в желудок белым мышам в виде равномерных эмульсий, приготовленных разведением препаратов в дистиллированной воде с использованием минимального количества ОП-7. В опыт отбирали животных обоего пола, которых подвергали воздействию различных доз веществ. Каждая доза испытывалась не менее чем на 6 животных. Наблюдения над животными проводили в течение 14-30 дней после введения веществ. Основным критерием оценки токсичности являлись дозы, вызывающие гибель 50% животных (ЛД50), которые рассчитывали методом пробит-анализа. Данные токсичности соединений общей формулы I для белых мышей приведены в табл. 1.
Испытания соединений общей формулы I на инсектоакарицидную активность проводили в лабораторных, тепличных и полевых условиях.
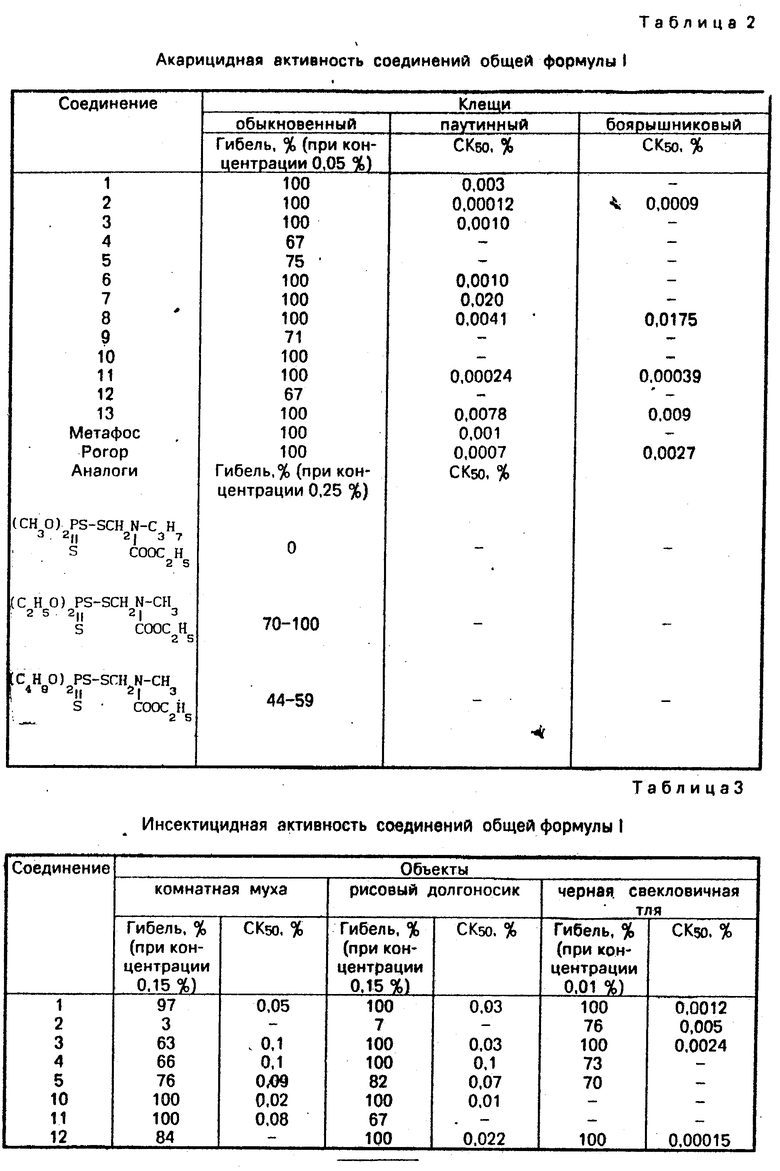
Черную свекловичную тлю Aphis fabe подсаживали в чашки, предварительно обработанные водно-ацетоновыми растворами предлагаемых соединений в концентрации 0,01% . Учет вели через 24 ч. (Результаты приведены в табл. 2. ).
Обыкновенного паутинного клеща Tetranychus urticae подсаживали на диски, вырезанные из листьев фасоли, и подвергали опрыскиванию. Учет гибели проводили через 48 ч. Данные приведены в табл. 2.
В лабораторных опытах инсектицидную активность определяли методом опрыскивания в стационарном опрыскивателе (расход жидкости 37 мл/м2) водно-ацетоновыми растворами соединений с добавлением эмульгатора Имаго комнатных мух Musca domestica L и рисового долгоносика Calendra oryzae в стеклянных емкостях. Концентрация 0,15% . Учет гибели вели через 24 и 48 ч. Полученные данные приведены в табл. 3.
При проведении испытаний в теплице и в полевых условиях растения опрыскивали различными концентрациями водных эмульсий, приготовленных из 20% -ных КЭ соединений. Параллельно растения опрыскивали эталонными препаратами. Тепличные и мелкоделяночные опыты проводили на разных видах тлей (см. табл. 4), боярышниковом клеще Tetranychus vienuensis (см. табл. 2) и оранжерейной белокрылке Myzus persicae (см. табл. 5).
Большинство соединений обладает высокой акарицидной активностью (см. табл. 2), близкой к эталонам, а соединения 2 и 11 в отношении обыкновенного паутинного и боярышникового клещей превосходят по активности эталон рогор в 3-7 раз.
Как видно из табл. 3, соединения общей формулы I обладают инсектицидной активностью, интенсивность которой зависит от строения соединений. Соединения 1, 2 и 3 близки по активности к эталонам, а соединение 12 значительно превосходит эталон по действию на черную свекловичную тлю.
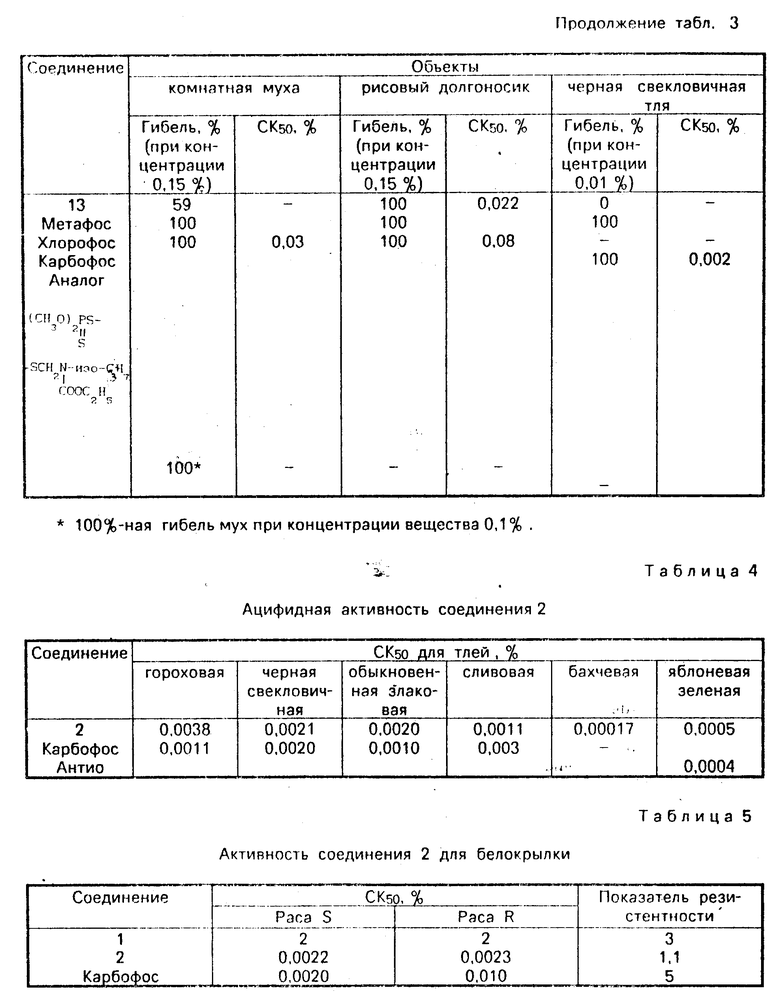
Афицидность соединений была изучена в теплице и в полевых условиях для различных видов тлей, в том числе резистентных к фосфорорганическим соединениям, путем опрыскивания водными эмульсиями, приготовленными из 20% -ных КЭ соединения 2. Как видно из табл. 4, соединение 2 проявляет высокую активность на уровне эталонов карбофоса и антио.
При испытаниях на оранжерейной тле, резистентной к фосфорорганическим соединениям, соединение 2 также проявило высокую активность (СК50 0,0072% ).
В условиях теплиц определена активность соединения 2 в отношении чувствительной и резистентной к фосфорорганическим соединениям расы оранжерейной белокрылки. Из данных, приведенных в табл. 5, видно, что соединение 2 активно как для резистентной, так и для чувствительной белокрылок. К этому соединению не индуцируется кросс-резистентность.
Соединение 1, испытанное в полевых условиях на зеленой персиковой тле, проявило высокую афицидную активность, СК50 0,00016% , что в 10 раз превосходит активность эталона карбофоса.
Таким образом, соединения общей формулы I обладают высокой инсектоакарицидной активностью, в том числе к членистоногим, выработавшим устойчивость к фосфорорганическим пестицидам, а предлагаемый способ их получения позволяет выделять целевые вещества в чистом виде с высоким выходом. (56) Краткий справочник по ядохимикатам. /Под ред. Н. Н. Юхтина, М. : Колос, 1973, с. 20.
Мельников Н. Н. Химия и технология пестицидов. М. : Химия, 1974, с. 542.
Органические инсектофунгициды и гербициды. Государственное научно-технологическое издательство химической литературы. М. , 1958, с. 344-345.
Мельников Н. Н. Химия и технология пестицидов. М. : Химия, 1974, с. 568.
Патент Франции N 1318314, кл. A 01 N, 1963.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 0-АЛКИЛ-S-[(N-АЦИЛ-N-КАРБАЛКОКСИАЛКИЛ) АМИНОМЕТИЛ] МЕТИЛДИТИОФОСФОНАТОВ | 1989 |
|
SU1616103A1 |
| ФОСФОРИЛИРОВАННЫЕ N-АЛКИЛБЕНЗАМИДОКСИМЫ, ОБЛАДАЮЩИЕ ИНСЕКТИЦИДНОЙ И ИНСЕКТОАКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1983 |
|
SU1189067A1 |
| 2-АЛКОКСИ-2-ТИО-5-(N-ФЕНИЛКАРБАМОИЛ)-6-МЕТИЛ-1,4,2-ОКСАТИАФОСФОРИНЫ | 1996 |
|
RU2105771C1 |
| S-(2,2,5-Триметилоксазолидинил-3-карбонилметил)-0,0-диалкилтио-, или дитиофосфаты, или О-диалкилтиофосфонаты, обладающие афицидной активностью | 1988 |
|
SU1530629A1 |
| 1-( ДИЭТИЛТИОФОСФОРИЛТИО )МЕТИЛ -5- МЕТИЛ - 4,5 - ДИГИДРО -6- ОКСО - 1,2,4 - ТРИАЗИНЫ, ОБЛАДАЮЩИЕ ИНСЕКТИЦИДНОЙ И АКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1989 |
|
SU1621453A1 |
| ДИЭТИЛОВЫЙ ЭФИР ОКСИ[(1-МЕТИЛ-2-МОРФОЛИНОКАРБОНИЛ)ВИНИЛ]-ФОСФОРНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ИНСЕКТОАКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2007412C1 |
| N @ -(фосфонато)-диазен-N-оксиды | 1990 |
|
SU1747450A1 |
| Функционально замещенные бутиновые эфиры проявляющие инсектоакарицидную активность | 1976 |
|
SU630860A1 |
| Фосфорилированные триметилизомочевины, обладающие инсектоакарицидной активностью | 1978 |
|
SU707233A1 |
| N-4-(1-ОКСИ-1-АМИНО)- ИЛИ ЭТОКСИ(КАРБОНИЛ)-2,2,2-ТРИФТОРЭТИЛ)ФЕНИЛ-N-АЛКИЛ- N' -АЛКИЛ( α -НАФТИЛ)МОЧЕВИНЫ, ПРОЯВЛЯЮЩИЕ РОСТОРЕГУЛИРУЮЩУЮ АКТИВНОСТЬ | 1991 |
|
SU1822133A1 |
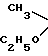
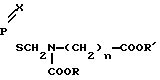
где при X = S, n = 1
R = R' = CH3;
R = CH3, R' = C2H5;
R = C2H5, R' = CH3;
R = R' = C2H5;
R = CH3, R' = изо-C4H9;
R = изо-C4H9, R' = CH3;
при X = S, n = 2;
R = R' = CH3;
R = CH3, R' = C2H5;
R = R' = C2H5;
при X = 0, n = 1
R = R' = CH3;
R = CH3, R' = C2H5; R = CH3, R' = изо-C4H9;
при X = 0, n = 2
R = CH3, R' = C2H5,
обладающие акарицидной активностью.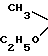
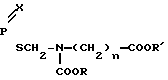
где при x = S, n = 1
R = R' = CH3;
R = CH3, R' = C2H5;
R = C2H5, R' = CH3;
R = R' = C2H5;
R = CH3, R' = изо-C4H9;
при X = 0, n = 1
R = R' = CH3;
R = CH3, R' = C2H5;
R = CH3, R' = изо-C4H9;
при X = 0, n = 2
R = CH3, R' = C2H5,
обладающие инсектоакарицидной активностью.
Авторы
Даты
1994-02-15—Публикация
1982-01-22—Подача