4
00
оо со
95 № Вреця мин Изобретение относится к микробиологической промышшнности, а именно к способу получения производных фенилглицина, в частности N-карбамилфенилглицина и карбамилпараметоксифенилглицина, используемых в фармацевтической промышленности. Известен способ получегшя производных фенилглицнна, в том числе N-карбамилфенилглицина, заключающийся в проведении ферментативного гидролиза 5-(D,L)-фенилгидантоина пггаммом Pseudomonas sp. 942 и.пи 945 при в течение 24 ч 13. Выход целевого продукта составляет 57-90% от теоретического при максимальной концентрации 20 мм/мл. Цель изобретения - обеспечение возможности использова шя концентрированных растворов гидантоинов при высоком выходе целевых продуктов. Поставленная цель достигается тем что согласно способу получения производных Ы-карбамилфея1шглицина, предусматривающему ферментативньш гидролиз растворов соответствующий производных гидантоинов, ферментатив ный гидролиз осуществляют штаммом Bacillus brevis NRRL 1286 или Bacillus bcearothermophilus NRKL 1287 при 40-50°C. Способ осуществляется следующим образом. Бактериапьные штаммы, вьщеленные из почвы, овощей и мусора, инокулируют при 50°С со скошенного агара в колбы Эрленмейера объемом 250 мл, содержащие каждая по 50 мл следующей питательной среды, при рН 7,2, г/л: Мясной пептон10 Дрожжевой экстракт 10 NaCI3 5-В,Ь-метил.гидантион1 Среду стерилизуют при 110 С в течение 30 мин. Инкубирование проводят ч течение 18-20 ч при 50°С при пере4еш1вании. В колбу Эрленмейера объем 500 МП помещают 100 мл той же среды с добавлением 2 мл предварительно приготовленной культуры. После 1618 ч дополнительной вьщержки проводят ферментативную реакцию, для чего в пробирку, содержащую 10 мл 0,07 М фосфатного буфера при рН 8,5 и 20 мкмоль/мл 5-В,Ь-фенилгидантоина, вносят 1 мл бактериальной суспензии (сухой вес 40 мг/мл). По прошествии 15 мин инкубирования при 40 С проводят реакцию с Ь -диметиламинобензаль .1 9 дегидом для количественного определения полученного таким путем карбамилпроизводного, В способе используют культуры Bacillus brevis и Bacillus stefrothermophilus, которые были переданы на хранение в 1977 г. в Северный региональный исследовательский центр г. Пеория, штат Иллинойс, США. Им были присвоены номера NRRL 11079 для штамма 1286 и NRRL-B 11080 для штамма 1287. Характеристика штаммов представлена в табл. 1. Во время протекания ферментативного гидролиза D -гидантоина при рН 7-10 установлено, что в результате получающиеся карбаминпроизводные находятся в D-форме. Химическая структура и его .идентичность N -карбамилфенилглицину и М-карбамилпараметоксифенилглицину подтверждена после перектристаллизации продукта реакции с помощью ИК-спектров N.M.R., массспектрометрии и элементарного анализа. Постоянные оптического вращения составляют соответственно ( в 1 н. растворе ) 140° ( в 1 н. растворе ), что соответствует литературным данным. Гидролиз может протекать при использовании целых клеток микроорганизмов, спор .или экстрактов вышеназванных микроорганизмов с помощью так называемых покоящихся клеток, для чего выделенные из культуральной среды бактериальные клетки после тп5ательной промывки суспендируют в буфере с добавлением рацемического гидантоина. Могут быть использованы препараты, содержащее гидролазу, такие как ее экстракты или концентраты очищенные гидролазы, полученные с использованием вьшеназванных микроорганизмов. Пример 1. Готовят среду для бактериального штамма В.brevis 1286 следующего состава, г/л: Мясной пептон10 Дрожжевой экстракт10 NaCl3 5-В,.тилгидантоин1 РН среды доводят до 7,2, стерилизуют при в течение 30 мин и инкубируют. Отбирают 100 кп культуральной .жидкости, помещают в колбу Эрленмейера объемом 500 мл и добавляют на 18 часу инкубирова шя (с использованием планетарной мешалки) при 100 мл 0,14 М фосфатного буфера (рН 8,5) содержащего 40 мкмоль/мп 5-(В,Ь)-фенилг1щантоин По прошествии еще 4 ч инкубирования при тех же условиях определяют коли чество полученноготаким путем Nкарбамилфенилглицина. Из 705 мг 5-(0,Ь)-фенилгидантоин получают 700 мг N-карбамилфенилглицина, что соответствует выходу приблизительно 90%. Пример 2. Так же, как в при мере 1, но по прошествии 4 ч при и с помощью штамма В. stearothermophilus NRRI. 1287 из 705 мг 5-(П,Ь)-фенилгидактиона получают 600 мг Ы-карбамш1фенилглицина, что соответствует выходу около 85%. . П р и м е р 3. Готовят среду, имеющую приведенный выше состав и содержащую 1 г/л 5-(В,Ь)-метш1гидан тоина. Добавлением соды рН доводят до 7,5 и культуральную жидкость распределяют порциями по 50 мл в Эрленмейера объемом 250 мл. После стерилизации в течение 30 мин при 110°С колбы инокулируют штаммом Bacillus brevis NRKL 1286 со скошенно го агара, содержащего ту же твердую среду с агаром (фирма ДИФКО) при 2%-ной концентрации, и инкубируют в течение 22 ч при с.использованием планетарной мешалки со скоростью 220 об./мин. Используя полученную культуру (оптическая плотность 0,4 при 550 н разбавление 1:10) в количестве 2 мп для инокулирования 100 мл той же ер ды в 500-миллш1итровых колбах Эрлен мейера, полученную культуру инкубируют при 40°С с использованием планетарной мешалки (220 o6.), в течение 18 ч. Клетки отделяют от бульона центрифугированием при g-500 (g - ускорение силы тяжести) в течение 20 мин, промывают трижды изотоническим раствором при рН 8,0 суспендируют в 0,07 М фосфатном буфере (рН 8,5), получая тем самым по коящиеся клетки. Для проведения реакции ферментативного гидролиза при 40°С и переме шивании (220 об/мин) в 250-миллилит ровых колбах Эрленмейера инкубируют 64 мл реакционной смеси, содержащей 200 мг бактерий (сухой вес) и 20 мкмоль/мл 5-(В,Ь)-фенилгидантоин (3,52 мг/мп). В подходящие моменты 9Л времени проводят измерения содержания продукта Г1здролиза т.е. D-карбамилфенилглицина, с использованием колориметр1{ческого метода на 438 ммкм. Ка чертеже дана кривая зависимости, выражающая процент теоретического выхода получаемого карбамилпроизводного. Пример4. Бактериальные клет ки штамма В. brevis NRRL 1286 получают описанным в примере 3 путем. Суспензию клеток (41,5 мг/мл сухих бактериальных клеток) помещают в буфер фосфатных солей при рН 8,5, подвергают механическому измельчению в гомоге шзаторе типа Manton laulin при температуре ниже 35°С и давлении 650 кгс/см. Клеточньй мусор отделяют от экстракта в с помощью центрифугирования (25000-кратное ускорение силы тяжести в течение 30 мин). К 970 мл 0,2 М буфера фосфатных солей (рП 8,5), содержащего 4,7 г 5-(В,Ь)-феиилг1щантоина, добавляют 30 мл экстракта, содержащего 280 ед. фермента (одна единица соответствует количеству фермента, которое обеспечивает преобразование 1 мкмоль/мл в минуту субстрата в 0,2 М фосфатном буфере, рН 8,5, при 50С, причем буфер содержит 20 мкмоль/мл 5-(В,Ь)-фенилгидантоина). По прошествии одного часа образуется 3,2 г N-кapбa iилфeшшглицина, что соответствует приблизительно 63% полного гидролиза. Пример 5. Готовят полусинтетическую среду, имуюшью следуюЕДгй состав, г/л: NH4Ci5 NajPO 7,05 КН2Р042,72 Мясной пептон5 Др.ожжевой экстракт 0,5 5-(D,L)-Нетнлгвдак . тонн1,0 Среду распределяют порциями по 50 мл в колбы Эрленмейера емкостью 250 МП и-по 100 ьш в колбы Эрленмейера емкостью 500 мл и стерилизуют в течение 30 t-nm при . Посевную культуру получают инокулированием в 250-миллш1итровых колбах со скошенного- агара культурой штамма В.brevis и инкубируют, как в примере 4, при 40°С в течение 22 ч. Для итокулировет.ния эту культуру (оптическая плотность 0,105 при 550 нм, разбавление 1:10) отбирают в количестве 2,5 мл
в колбы Эрленмейера объемом 500 мл, содержащие ту же среду. По прошествии 15ч инкубирования при 40°С реакционная смесь содержит в 64 мл буфера 100 мг бактерий (в пересчете на сухой вес и эквивалент 100 мл бульонной культуры) и 20 мкмоль/мл 5(D,Ъ)-фенилгидантиона.
По прошествии 5, 10 и 15 мин проводят определение количества полученного N-карбамилфенилглицина, которое соответственно равно 0,6; 1,0 и 1,4 мкмоль/мл.
Пример 6. Готовят питательную среду, состоящую из воды от замачивания кукурузы в количестве 2,6% (в пересчете на сухой вес). Среду доводят до рН 7,5 с помощью КОН, распределяют порциями по 50 мл в колбы емкостью 250 мл, а также порциями по 100 мл в колбы емкостью 250 и 500 мл с последующей стерилизацией в течение 30 мин при . Для получения посевной культуры производят инокулирование в колбах по 250 мл со скошенного агара с культурой штамма B.brevis NRRL 1286 с последующим инкубированием, как в примере 4, лри 40°С в течение 22 ч.
Для инокулйрования среды в колбах по 500 мл отбирают по 2,5 мл полученной посевной культуры, По прошествии 18 ч инкубирования при получают покоящиеся клетки аналогично примеру 3.
Ферментативный гидролиз проводят при 40°С в реакционной смеси, содержащей в 64 МП 0,07 М фосфатного буфера (рН 9,5) бактериальные клетки, полученные из 100 мл бульонной культуры, и 20 мкмоль/мл 5-(N,L)-фенилгидантиона; в реакционной смеси, содержащей в 64 МП 0,07 -М фосфатного буфера (рН 8,5) бактериальные клетки полученные из 100 мл бульонной культуры, и 20 мкмоль/мл 5-(N,L)-napaметоксифенилгидантиона.
По прошествии 5, 10, 15 и 60 мин определяют количество полученного таким путем N-карбамилфенилглицина и N-карбамилпараметоксифенилглицина;
Результаты представлены в табл.2.
Пример 7. Получают, ацетоновый порошок клеток штамма Bacillius brevis NRRL 1286, и 80 мг этого порошка содержащего 420 ед. фермента, суспендируют в 1 л 0,2 М фосфатного солевого буфера (рН 8,5), содержащего 5,0 г 5-(D,L)-фенилгидантиона. По прошествии одного часа при получают 4,8 г Ы-карбамилфенилглидина, что соответствует приблизительно 87% полного гидролиза.
Пример 8. С использованием штамма Bacillus brevis NRRL 1286 получают биомассу в 20-литровом ферментаторе Fomel, содержащем 16 л культурной среды рН 7,8, имеющей состав, г/л:
Дрожжевой экстракт 10 Мясной пептон . 10 NaCi3
0,56
5-(D,L)-Метилгидантоин1
Культур3 в ферментаторе инокулируют с использованием 16- мл посевной культуры (оптическая плотность О,360 при 550 нм, разбавление 1:10), выращенной в 50-миллш1итровых колбах содержащих 100 мл той же питательной -среды, и инкубированной в течение 16 ч при 40 С при перемешивании (220 об/мин). Ферментацию проводят при рН 7,8 с добавлением 2н.НСВ, при поддержании коэффициента О.А.Р. порядка 0,45. К 16-му часу ферментации (оптическая плотность 0,350 при 550 нм. разбавление 1:10) биомассу отделяют от культуральной жидкости с помощью центрифугирования в сеператоре фирмы Альфа Лаваль при комнатной температуре.
Клетки промывают изотоническим раствором при рН 8,0. Ферментативный гидролиз осуществляют при 40С в реакционной смеси, содержащей в 64 мл 0,07 М фосфатного солевого буфера (рН 8,5) 0,5 г бактериальной суспензии (эквивалентно 0,120 г сухих клеток) и 20 мкмоль/ют 5-(D,L)-гидaнтоина, и в реа кционной смеси, аналогичной вьш1еуказанной,но содержащей 20 мкмоль/мл 5-(D,L)-н-мeтoкcифeнилгидантоина. По прошествии 5, 10, 15 и 60 мин определяют количество полученного N-карбамилфенилглицина и N-карбаминпараметоксифенилглицина.
Результаты представлены .в табл.3.
Наименование показателей
Таблица 1
Характеристика штамма



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения оптически активных АМиНОКиСлОТ | 1976 |
|
SU810082A3 |
| Способ получения д-фенилглицина и его производных | 1979 |
|
SU884576A3 |
| Штамм бактерий RноDососсUS RноDоснRоUS - продуцент нитрилгидратазы | 1990 |
|
SU1731814A1 |
| Способ получения глюкозоизомеразы | 1973 |
|
SU655327A3 |
| СПОСОБ БИОТРАНСФОРМАЦИИ СОЕДИНЕНИЙ КОЛХИЦИНОИДОВ В СООТВЕТСТВУЮЩИЕ 3-ГЛИКОЗИЛПРОИЗВОДНЫЕ | 1997 |
|
RU2196826C2 |
| СПОСОБ БИОТРАНСФОРМАЦИИ КОЛХИКОНОВОГО СОЕДИНЕНИЯ В СООТВЕТСТВУЮЩЕЕ 3-0-ГЛИКОЗИЛЬНОЕ ПРОИЗВОДНОЕ | 1998 |
|
RU2218409C2 |
| Штамм АсINетовастеR @ р.-продуцент гидролазы N-карбамоил-5-фенилглицина | 1988 |
|
SU1599433A1 |
| ШТАММ БАКТЕРИЙ RHODOCOCCUS ERYTHROPOLIS - ПРОДУЦЕНТ НИТРИЛГИДРАТАЗЫ | 2001 |
|
RU2196822C1 |
| ШТАММ БАКТЕРИЙ BACILLUS СEREUS-ПРОДУЦЕНТ НИТРИЛГИДРАТАЗЫ | 1999 |
|
RU2160778C1 |
| ШТАММ БАКТЕРИЙ rhodococcus ruber - ПРОДУЦЕНТ НИТРИЛГИДРАТАЗЫ | 2001 |
|
RU2223316C2 |
СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ Ы-КАРБАМШ1ФЕНШ1ГЛИ1ЩНА путем ферментативного гидролиза растворов соответствуюпщх производных гидантионов, отличающийся тем, что, с целью обеспечения возможности использования концентрированных растворов 1гидантоинов при высоком выходе целевых продуктов, ферментативный гидролиз осуществляют штаммом Bacillus brevis NRRL 1286 или Bacillus stearothermophilus NRRL 1287 при 40-50 0. О)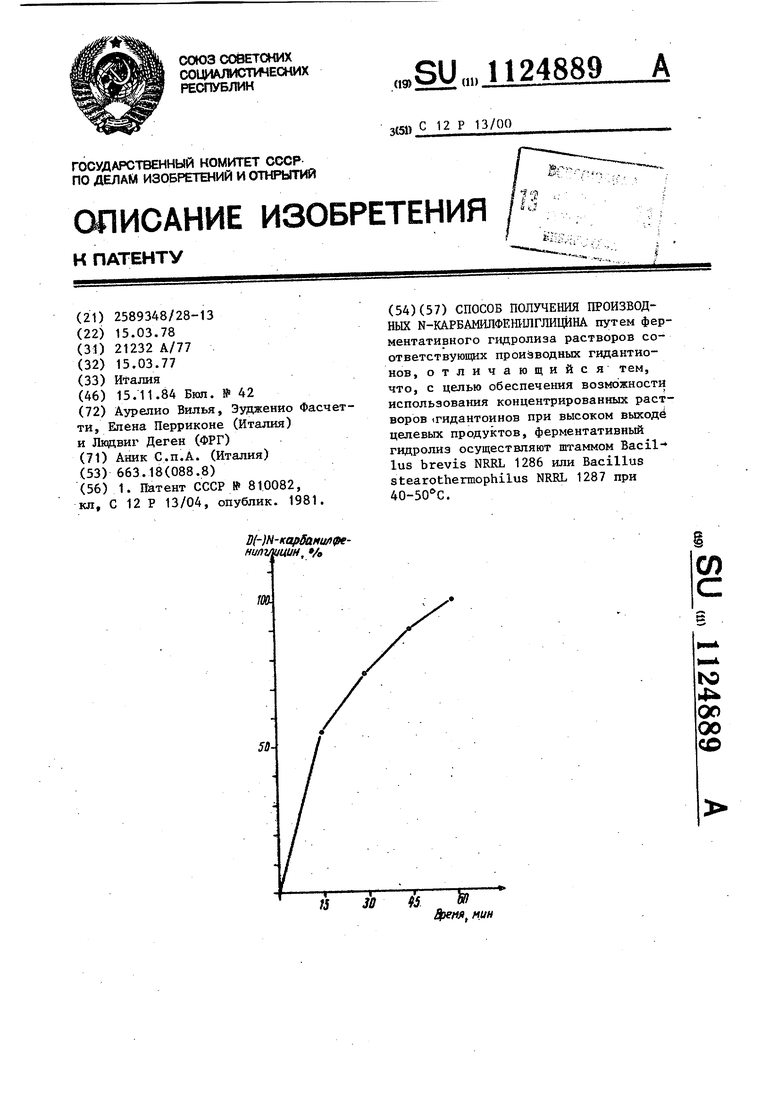
Bacillus brevis NRRL 1286 , а
в
там O)
атрия:
Bacillus stearothermophilusNRRL 1287
0,6-1
0,6-0,9 2,0-3,5
1,5-4
t
+ f
+ Эллипсоидная Эллипсоидная
СубтерминальСубтерминальное-ное
40-50
40-50
30
+ +
+
+ +
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения оптически активных АМиНОКиСлОТ | 1976 |
|
SU810082A3 |
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1984-11-15—Публикация
1978-03-15—Подача