Изобретение относится к количествениому определению ди-П-метокси. тpитил-N-aцилдeзoкcиpибoнyклeoзидов, которые являются исходными соединениями для синтеза олигонуклеотидов и представляют актуальное значение в генной инженерии. Для оценки пригодности препаратов для дальнейших синтезов полинуклеотидов необходимо охарактеризовать их как по основанию нуклеозида, так и .по количеству ди-П-метокситритильных трупп. Известен метод потенциометрическо го титрования пиримидиновых и пуриновых оснований в метилцеплозольве {. Метод имеет ограниченное применение для анализа N-ацилдезоксирибонук леозидов вследствие слабо выраженных основных свойств последних в метклцеллозольве,. Метилцеллозольв также неприменим для проведений титрования ди-П-метокситритнльных групп. Известен метод спектрофотометрыческого определения дезоксирибонукле зидов.по цветной реакции дезоксирибозы с дифениламином 2 . Недостатком указанного метода является то, что он дает характеристику анализируемого вещества только по дезоксирибозной .части молекулы. Наиболее близким по достигаемому результату к предлагаемому является спектрофотометрический способ количественного определения ди-П-метокси тритил-М-ацилдезоксирибонуклеозидов путем раздельного определения основания нуклеозида и ди-г -метокситритильных групп.Для определения основания нуклеозида навеску вещества ра створяют в этиловом или метиловом спирте и измеряют оптическую плотность раствора в УФ-области спектра Для определения содержания ди-п-метокситритильных групп навеску растворяют в смеси этанола с 70%-ной хлорной кислотой (при объемных соот ношениях 1:1) и измеряют оптическую плотность при 500 нм. Количество оп ределяемых групп находят по калибро вочному графику з2 . Недостатками способа являются ни I кая точность, трудоемкость и длиi тельноеть анализа. Цель изобрет ения - повьшение точ ности и упрощений способа. Поставленная цель достигается тем, что, проводят раздельное определение основания нуклеоэида и ди-р-метокситритильных групп дифференцированнмм потенциометрическим нeвoдны f титрованием в среде нитрометана хлорной или хлористоводородной кислотой, причем после оттитровывания основания нуклеозида в анализируемьй раствор добавляют органическую кислоту или хлорид тяжелого металла, Упрощение процесса и сокращение его длительности достигается дифференцированным потенциометрическим титрованием основания нуклеозида и ди-П-метокситритильных групп. Это позволяет определить оба компонента в одной навеске образца. В среде нитрометана основания ди-л-метокситpитшI-N-aцилдeзoкcиpибoнyклeoзидoвпроявляют довольно вьфаженные основные свойства и титруются неводным раствором сильной кислоты. Ди-п-метокситритильные группы в нитрометане основных свойств не проявляют, однако после добавления к раствору бензойной кислоты, уксусной кислоты или солей тяжелых металлов группы титруются с довольно выраженным скачком потенциала. По-видимому, в присутствии названных веществ происходит разлсжение ди-п метокситритилN-ацилдезоксирибонуклеозидов с образованием ди-п-метокситритилкарбинола, который в данной среде под действием этих соединений проявляет основные свойства. Использование других органических растворителей, применяемых для дифференцированного потенциометрического титрования очень слабых органических оснований, например ацетона, метилэтклкетона и ацетонитрила позволяет провести титрование основания нуклеозида, но не дает возможности осуществить потенциометрическое определение ди-П-метокситритильных групп. Для обеспечения дифференцированного .потенциометрического титрования основания нуклеозида и ди-П-метокситритильных групп органическую кислоту или хлорид тяжелого металла вводят только после оттитрования основания нуклеозида., так как добавление реагента в начале титрования приводит к нивелированию основных свойств определяемьк компонентов и их совместному титрованию. Способ осуществляют следующим образом. Навеску анализируемого вещества 7 10 мг растворяют в 5-10 мл очищенного нитрометана, в раствор погружаю пару электродов (стеклянный и каломельный) и потенциометрически титруют из бюретки емкостью 2,5 мл 0,020,03 н, неводным раствором хлорной или хлористоводородной кислоты до появления скачка потенциала на кривой титрования. Затем в раствор вводят приблизительно 0,01-0,1 г органической кислоты или хлорида тяжелого металла, перемешивают 1-2 мин И продолжают титрование до появления второго скачка потенциала на кривой. Первый скачок потенциала соответствует оттитрованию основания нуклеозида, а второй - оттитрованию ди -YT-метокситритильных групп. При . анализе чистого образца объемы титранта на титрование каждого компонента одинаковы. Различия объемов израсходованного титранта на титрование основания нуклеозида и ди-Пметокситритильных групп свидетельствует о несоответствии качества трегбованиям однородного препарата. Например, если на титрование основания нуклеозида израсходовано больше титранта, чем на титрование ди-п-меток тритильных групп, образец содержит свободный нуклеозид и, следовательно, препарат не может быть применен для синтеза олигонуклеозидов. Пример 1. Количественное оп ределение ди-Л-метокситритил-К-бензоилдезоксицитидина. 7.435 мг ди-П-метокситритил-Nбензоилдезоксицитидина растворяют в 5 мл нитрометана, в раствор погружа ют пару электродов (стеклянный и каломельньй) и потенциометрически титруют 0,0215 н, раствором хлороводородной кислоты в диоксане до появ ления скачка потенциала на кривой т рования, затем к раствору добавляют ,01 г хлорида цинка, перемещивают 2 мин и продолжают титрование до по явления второго скачка потенциала. На титрование основания нуклеозида израсходовано 0,466 мл (V) титрант а на титрование ди-п-метокситритиль ных групп 0,468 МП (V,). Поскольку можно считать, что препарат не содержит свободного N -ацилдезокси ;нуклеозида и ди-п-метокситритилкарбинола. По данным титрования рассчитывают либо содержание основания нуклеозида и тритилгрупп, либо содержание основного вещества. Рассчитывают содержание ди-п-метокситритилN-бензоилдезоксицитидина.66:0,0 215:634, .-69l5.0215,,, Пример 2. Количественное определение ди-п-метокситритип-М-изобутирилдезоксигуанозина. 8,516 мг ди-п-метокситритил-Nизобутирилдезоксигуанозина растворяют в 10 мл нитрометана и потенциометрически титруют 0,0289 н,раствором хлористоводородной кислоты в ацетонит.риле до появления скачка потенциала на кривой титрования. Затем к раствору добавляют 0,1 г уксусной , перемешивают 1 мин и продолжают титрование до появления второго скачка потенциала на кривой. На титрование основания нуклеозида израсходовано 0,419 мл (V,) титранта, а на титрование ди-п-метокситритильных групп 0,452 МП ( V) . Как видно, что свидетельствует о наличии примеси ди-п-метокситритилкарбинола. Поэтому для расчета со; ержания ди-Пметокситритил-Ч- изобутирилдезокснгуанозина используют V, 0,419.0 289:653 .,00 92,8% о,ЬID Содержание примесей ди-П-метокситритилкарбинола рассчитывают по разнице V, и У .. (0 452-0,419). 0 0289-320 . X .100. 3,6%. П р и м е р 3. Количественное определение ди-п-метокситритил-Ы-бензоил-2 -дезоксиаденозина. 9,885 мг ди-П-метокситритш1-Мбензоил-2-дезоксиаденозина растворяют в 8 МП нитрометана и потенциометрически титруют 0,0258 н.раствором хлорной кислоты в диоксане до появления скачка потенциала на кривой титрования. Затем к раствору добавляют 0,1 г бензойной кислоты, перемешивают 1,5 мин и продолжают титрование до появления второго скачка потенциала на кривой. На титрование основания нуклеозида израсходовано 0,543мл (V ) титранта, а на титрование ди- -метокситритильных групп 0,463 мл (Уя),Как видно, V4 V, что свидительствует о наличии примеси нуклеозида. Поэтому для расчета содержания ди-п-метокситритш1-М-бензоил-2 -дезоксиаденозина используют V X 0.-§M|P8.65J.,, Содержание примесей W-безоил-2 дезоксиаденозина рассчитывают по разнице V и Vg .513зО,,, П р и м .е р 4. Количественное оп ределение ди-П-метокситритил-N-изобутирилдезоксигуанозина,. 9.630 мг ди-П-метокситритш1-Низобутирилдезоксигуанозина растворяю в 10 мл нитрометана и потенциометрически титруют 0,0229 н,. раствором хлорной кислоты в ацетонитриле до по явления скачка потенциала на кривой титрования. Затем к раствору добавляют А- О, 01 г хлорида никеля, перемешивают - 1 мин и продолжают титрование до появления второго скачка по тенциала на кривой титрования. На титрование основания нуклеозида израсходовано 0,647 мл (V) титранта, а на титрование ди-п-метокситритильньк групп 0,650 мл С) Содержание дн-п-метокснтритил-И-изобутирилгуа;нозинаX 5i° p9lв53,,„„.,,„ хДЙ|-.0.0229-,653.,.,„„, Пример 5. Количественное оп ределение ди-П-метокситритил-Н-бензо.илдезоксиаденозина. 1 506 7,532 мг анализируемого образца растворяют в 10 мл нитрометана и потенциометрически титруют 0,0241 н, раствором хлорной кислоты в дисксане до появления скачка потенциала на кривой титрования. Затем к раствору добавляют 0,01 г хлорида кобальта, перемешивают л/1 мин и продолжают титрование до появления второго скачка потенциала на кривой титрования. На титрование основания нуклеозида израсходовано 0,420 ьш титранта (V), а на титрование ди-П-метокситритильных групп 0,422 мл (|). Содержание ди-г -метокси-М-бензоилдезоксиаденозина.20.0 0241, , 2i 24: 0 0241:. В таблице приведены сравнительные метрологические характеристики предлагаемого и известного способов определения ди-п-метокситритил-М-ацилдезоксирибонуклеозидов. Таким образом, предлагаемый способ точнее, значительно проще в сравнении с известным сокращена длительность. По известному способу необходимо проводить два параллельных определения, причем для определения дип-метокситритильных групп необходимо строить калибровочный график, поэтоь«у определение занимает 1,52 ч рабочего времени и требует наличия стандартного вещества в виде чистого препарата ди-п-метокситритилN- ацилдезоксинуклеозида. Определение по предлагаемому способу занимает всего 15-20 мин и не требует применения в качестве стандартных веществ препаратов тритилдезоксинуклеозидов. Кроме того, способ позволяет проводить анализы в микромасштабе, поэтому.на анализ рас1содуется несколько миллиграммов дорогостоящего анализируемого вещества.
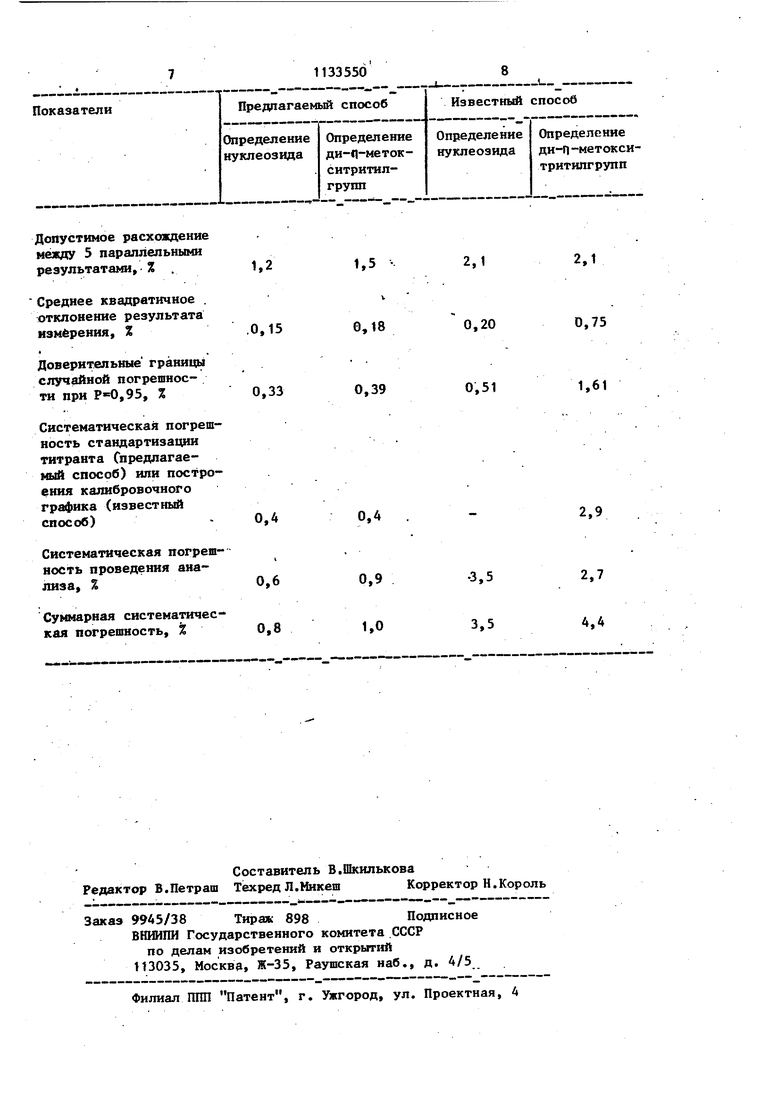
Допустимое расхождение между 5 параллельными результатами, % .
Среднее квадратичное . отклонение результата измерения, %
«
Доверительные границы случайной погрешности при Р-Ю,95, %
Систематическая погрешность стандартизации титранта Спредлагаемый способ) или построения калибровочного графика (известный способ)Систематическая погрешность проведения ана2.1
2,1
0,18
0,20
0,75
1,61
0,51
0,39
2,9


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения ди-п-метокситритилкарбинола | 1983 |
|
SU1133549A1 |
| Способ определения трифенилхлорметана и его замещенных | 1983 |
|
SU1129519A1 |
| Способ количественного определения аде-НОзиНА и иНОзиНА или пРОизВОдНыХ АдЕНОзи-HA и пРОизВОдНыХ иНОзиНА пРи иХ СОВМЕСТНОМпРиСуТСТВии B СМЕСи | 1979 |
|
SU805167A1 |
| Способ раздельного определения формальдегида и оксиметилсодержащих соединений в их смеси | 1981 |
|
SU968754A1 |
| Способ количественного определения рибонуклеозидов | 1976 |
|
SU641341A1 |
| Способ количественного определения солей нуклеозидфосфорных кислот | 1976 |
|
SU577459A1 |
| Способ количественного определения оксиметилсоединений | 1976 |
|
SU577458A1 |
| Способ количественного определения @ -аланина | 1980 |
|
SU941898A1 |
| Способ количественного определения производных оксипуринов и их смесей | 1974 |
|
SU499529A1 |
| Способ раздельного определения компонентов смеси 2- @ -/карбометоксиаминобензолсульфамидо/-5-этил-1,3,4-тиадиазола с 2-ди-/ @ -карбометоксиаминобензолсульфамидо/-5-этил-1,3,4-тиадиазолом | 1984 |
|
SU1247745A1 |
СПОСОБ ОПРЕДЕЛЕНИЯ ДИ-П-МЕТОКСИТРИТИЛ-N -АЦИПДЕЗОКСИРИБОНУКЛЕО|ЗИДОВ с использованием раздельного определения основания нуклеозида и диП-метокситритнльных групп в среде органического растворителя, отличающийся тем, что, с целью повьшения точности и упрощения способа, проводят раздельное определение основания нуклеозида и ди-гт-метркситритильных групп дифференцированным потенхщометрнческим неводным титрованием в среде нитрометана хлорнойг или хлористоводородной кислотой, причем после оттитровывания основания нуклеозида в анализируемый раствор добавляют органическую кислоту или хлорид тяжелого металла.
Авторы
Даты
1985-01-07—Публикация
1983-06-01—Подача