;О 0)
1I
Изобретение относится к химии фосфороргапических срединений с С-Р связью, а именно к новым соединениям - эфирам моно- и дифенил-(4-гидрокси-3,5-ди-трет-бутилфенил)метил фосфоновой кислоты общей формулы
С(СНз).
С&Н5
/гл
с- р(о){ов)5
Б
С(СНз)
-%
R фенил; ,R- метил или этил; R-- водород; R - метил, которые могут быть иснользованы в качестве терМОстабилизаторов ударопрочного полистирола.
Известно использование три(п-нонилфенил)фосфита (фосфит НФ) в качестве термостабилизатора ударопрочното полистирола ij.
Однако это соединение обладает невысоким термостабилизирующим эффектом и гидролизуется в процессе хранения.
Наиболее близким к изобретению по структуре является диметиловый эфир 4-гндрокси-355-ди-трет бутилбензилфосфоновой кислоты, который может быть использован для стабилизадни органических полимерных материалов 2.
Однако известное соединение обладает невысоким .термостабилизирующим эффектом.
Целью изобретения является повышение эффективности термостабилизаторов ударопрочного полистирола.
Поставленная цель достигается новыми соединениями - эфирами монои дифе1н-ш- (4гидрокси-3,5-ди третбутнлфенил)метилфосфоновой кислоты общей формулы ll, которые могут быть иснользованы в качестве термостабилизаторов ударопрочного полистирола.
Указа1Н ые соединения обладают высокой термостабилизирующей активностью и но всей эффективности значительно превосходят известный ста билизатор фосфит ПФ.
Эфиры моно- н дифенил(4-гидрокс3,5-ди-трет-бутилфенил)метилфосфоновой кислоты () получают взаимодействием соответствующего метиленхинона
10962
с диалкилфосфитом в присутствии минера. кислоты в качестве катализатора.
Новые соединен1ш представляют 5 собой бесцветные кристаллические вещества с четкими температурнами плавления, нерастворимые в воде, петролейном эфире и растворимые в ацетоне, спиртах, бензоле. Строение
10 полученных соедипений однозначно подтверлодают данные ИК- и ГМР-спектроскопии, а таклсе элементного анализа, В ИК-спектрах полученных соединений присутствуют полосы поглощения
15 группы ОН (3400-3600 ) , Р О .(1220-1250 см) и СОР (10301070 см ), Положение и иптенсивность сигналов протонов в ПМР-спектрах описываемых соединений соответствует приведенным структурным формулам. Пример 1, Получение диметилового эфира дифенил-(4-гидрокси3,5-дн-трет-бутилфенил)метилфосфоновой кислоты,
5 В колбу емкостью 0,25 л, снабженную механической мешалкой и обратным холодильником загружают 24,8 г (0,067 мол1) 4-дифенил-метилен-2,6-ди-трет-бутил--2 ,5-циклогек0 садиен-1-она и 27,2 г (0,25 моль) ,диметилфосфита. По окончании загрузки включают перемешивание и нагревают реакциомную смесь до полного растворения, ме иленхинона, после чего прибавляют через обратный холодильник 10-20 капель кондентрированной серной кислоты. Смесь выдерживают при .температуре бани 130. 140 С до обесцвечивания (6 - 8 ч) Q и охлаждают до , Избыток фосфита отгоняют в вакууме. Остаток кристаллизуют из петролейного эфр ра и ацетона. Получают 21,3 диметилового эфира дифенил-(4-гидрокси5 3,5 ди-трет-бутилфенил)метилфосфоновой кислоты (1, R - ,, ) , Выход 68%,
I- v и
ИК-спектр (табл,КВг, v , см ):
1050 (СОР); 1240 (); 3480 (ОН), 0ПМР-спектр (раствор в В ацетоне;
СГ, м,д,):1,25, с, (C-CHj); 3,4 д, (О-СН-з), 1(нсоР) 10,5 Гц; 4,9 м, (ОН); 7,1 м, ароматические протоны, Т,пл, 187-187,, 5Найдено,%: С 71,88; И 7,18;
Р 6,34,
Вы.числено,%: С 72,48; IJ 7,76; Р 6,44,
Пример 2, Получение диэтило вого эфира дифенил-(4-гидроксн3,5-ди-трет-бутилфенил) метилфосфоновой кислоты.
В .условиях примера 1 из 25,9 г (0,07 моль) 4-дифенш1метилен-25б- . ди-трет-бутил-255-циклогексадиен-1она и 20 г (0,3 моль) диэтилфосфита получают 25,0 г диэтилового эфира дифенил-(4-гидрокси-З,5-дитрет-бетш1фергил)метилфосфоновой кислоты (1, R CgHj, R С2Н) в виде бесцветных кристаллов с т.пл. 213-214°С (из ацетона). Выход 54%.
ИК-спектр (табл.КВг; , см ): 1050 (СОР); 1230 (Р О); 3560 (ОН)
ПМР-спектр (раствор в СС14, м.д.):0,99, т, (СЫ), 1(нссн1 , 7 Гц| 1,25, с, ((С11з)з -С); 3,72,м, (); .7,13, м, ароматические цро,тоны.
Найдено,%: С 72,10; Ы 8,26; Р 6,15.
Вычислено,%: С 72,20; Н 8,12; Р 6,08.
Пример 3. Получение диметилового эфира фенил-(4-гидрокси-З,5ди-трет-бутилфенил)метилфосфон6вой кислоты.
В условиях примера 1 из 3,0 г (0,01 моль) 4-бензилиден-2,6-дитрет-бутил-2,5-циклогексадиен-1она и 3,3 г (0,03 моль)диметилфос(1)ита получают 3,1 г диметилового эфира фенил-(4-гидрокси-З,5-дитрет-бутилфенил) метилфосфоновой кислоты (I,R Н, R СПр в виде бесцветных кристаллов с т.пл. 132-. 133 С (из смеси гексан:ацетон 10:1). Выход 75%.
11410964
ИК-спектр (табл.КВг-;
см-М:
1040-1070 (СОР) 1250 (); 3450 (ОН).
ПМР-спектр раствор в D-ацетоне; с, м.д.)1 1,33, с, (С-СН); 3,4 д (0-СНз), ) 10 Гц; 4,4 д, (PrCHj, 1 (HOP) 25 Гц; 6,0, с, (он); 7,2, м, ароматические протоны. Найдено,%: С 67,82; Н 8,03; Р 8,00.
Вычислено,%: С 68,29; Н 8,22; Р 7,66.
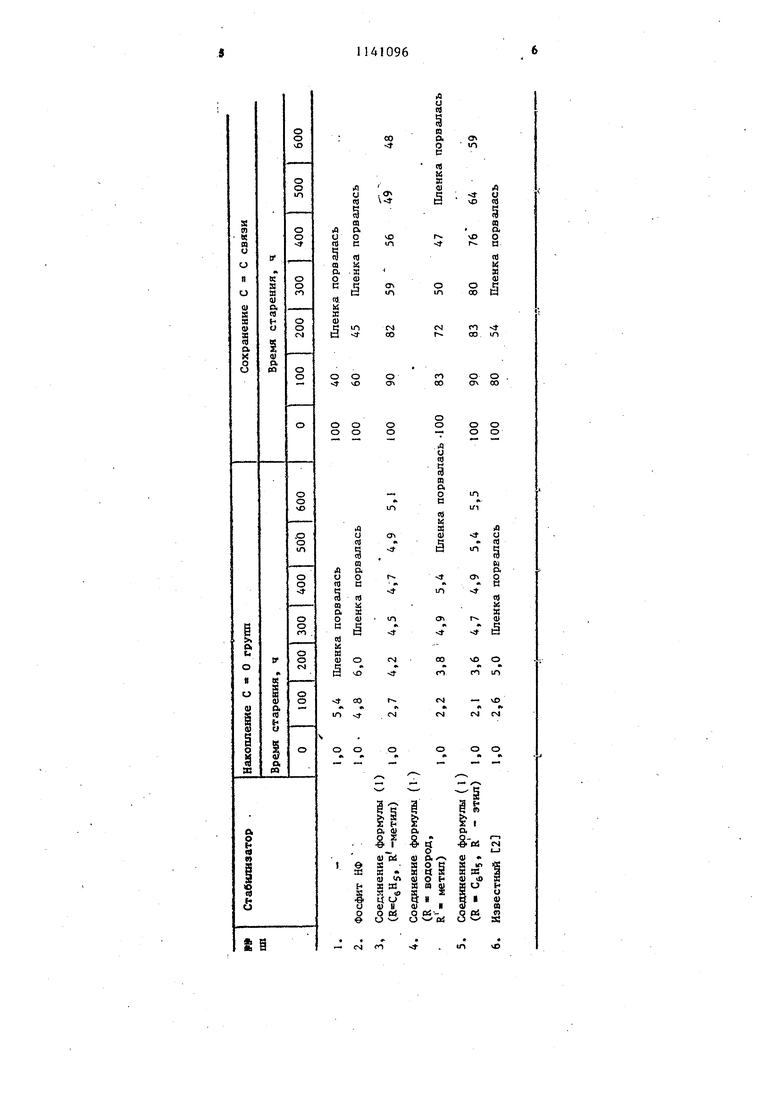
Синтезированные соединения испытаны в качестве термостабилизаторов ударопрочного полистирола марки УШ1-0503.
Готовят композицию, состоящую из ударопрочного полистирола марки УПМ-0503 и стабилизирующей добавки в количестве 0,5 мае.ч.
Из полученной композиции готовят 5%-ный бензольный раствор, После полного растворения полимера и стабилизатора в бензоле отливают пленки методом полива на целлофановую подложку, ограниченную стеклянным кругом.
Пленки толщиной 70 мкм подвергают термостарению при , среда воздушная, с последующим отбором проб и снятием ИК-спектров, поглощения в области 1600-1900 см характеристическая полоса поглощения групп при I720 см и в области 800-1000 см (характеристическая полоса поглощения связей при 967 см) .
Полученные данные приведены в таблице.
- cs 7 Таким образом, по сравнению о применяемым на практике стабилизатором фосфитом НФ, а также структурным1аналогом новых соединений, последние обладают существенно бо1141096. 8 лее высокой термостабйлизирующей активностью. Пленки полимеров в iпроцессе старения не окрашиваются и сохраняют первоначальную эластичность.


| название | год | авторы | номер документа |
|---|---|---|---|
| Восьмичленные циклические фосфиты в качестве ингибиторов коксообразования и способ их получения | 1980 |
|
SU929645A1 |
| 2,2,6,6-Тетраметилпиперидиламиды насыщенных карбоновых кислот в качестве свето-,термостабилизаторов ударопрочного полистирола | 1980 |
|
SU871487A1 |
| 2,2,6,6-Тетраметилпиперидиламиды замещенных окси- или тиоуксусных кислот в качестве светотермостабилизаторов полимерных материалов | 1981 |
|
SU976649A1 |
| Производные 2-(3,5-ди-трет.бутил-4оксифенил)-1,3-диоксацикланов в качестве термостабилизаторов органического стекла на основе метилметакрилата | 1978 |
|
SU753848A1 |
| Способ получения диалкиловых эфиров @ -фенил- @ -(1,2-диметилциклопропенил)-этилиденоксивинилфосфоновой кислоты | 1988 |
|
SU1549958A1 |
| АМОРФНАЯ ТВЕРДАЯ МОДИФИКАЦИЯ 2,2',2''-НИТРИЛ[ТРИЭТИЛ-ТРИС-(3,3',5,5'-ТЕТРА-ТРЕТ.БУТИЛ-1,1'-БИФЕНИЛ-2,2' -ДИИЛ)ФОСФИТА], СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СТАБИЛИЗИРОВАННАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОТИВООКИСЛИТЕЛЬНОЙ СТАБИЛИЗАЦИИ | 1993 |
|
RU2118327C1 |
| Способ получения поли-N-хлорированных бициклических мочевин | 1989 |
|
SU1675300A1 |
| Бис-(О,О-ди(пара-трет.бутилфенил)дитиофосфонилметилизопропионато)ди(н-бутилкарбонилоксиметилен)метан в качестве противоизносной присадки к синтетическому смазочному маслу | 1987 |
|
SU1609789A1 |
| Способ получения (S)-3Z-додецен-11-олида | 1990 |
|
SU1773913A1 |
| Способ получения производных 1,2- дигидРОпиРиМидиНА | 1979 |
|
SU833964A1 |
Эфиры МОНО- и дифенил-( 4-гид рокси-3, 5-ди-трет-бутилфенил)метилфосфоновой кислоты общей формулы Чед. t- P
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Справочник | |||
| М., Химия, 1981, С.74 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление к комнатным печам для постепенного сгорания топлива | 1925 |
|
SU1963A1 |
Авторы
Даты
1985-02-23—Публикация
1983-05-20—Подача