Изобретение относится к усовершенствованному способу получения 1,2,3,6-тетрагидроникотиновой кислоты (гувацина-алкалоида арековой пальмы), которая обладает способностью ингибировать действие гамма-аминомасляной кислоты (тормозного медиатора ЦНС в синапсах мозга), т.е. является антидепрессантом, и может быть использовано в медицинской практике, а также к 1-(4'-метоксифенацил)-3-этоксикарбонилпиридинийбромиду и 1-(3',4'-диметоксифенацил)-3-этоксикарбонилпиридинийбромиду в качестве промежуточных продуктов для его получения.
Алкалоид гувацин выделен наряду с другими алкалоидами арекалином, гуваколином и арекаидином из плодов арековой или бетелевой пальмы, произрастающей на Цейлоне, в Индии, Малайских и Филиппинских островах. Главный алкалоид арекалин широко применяется в качестве лекарственного средства в ветеринарной практике [1]
Известен способ [2] получения гувацина, исходным соединением в котором служит этилакрилат: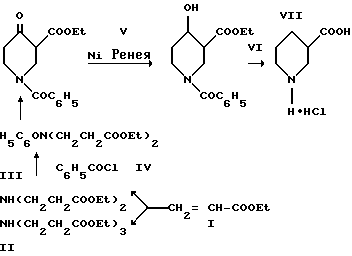
Известный способ является многостадийным, трудоемким, включает большое количество операций, связанных с очисткой и выделением промежуточных соединений (например, разгонка в глубоком вакууме продуктов II и Ш). При этом используются пожаро- и взрывоопасные реагенты: металлический натрий, никель Ренея и др. Общий выход гувацина составляет всего 14%
Целью изобретения является увеличение выхода целевого продукта, упрощение технологии, а также новые исходные соединения в синтезе 1,2,3,6-тетрагидроникотиновой кислоты.
Указанная цель достигается предлагаемым способом получения 1,2,3,6-тетрагидроникотиновой кислоты, заключающимся в том, что на 1-(4'-метоксифенацил)-3-этоксикарбонилпиридинийбромид или 1-(3', 4'-диметоксифенацил)-3-этоксикарбонилпиридинийбромид действуют боргидридом натрия в водно-метанольной среде, а затем концентрированной соляной кислоте по следующей схеме: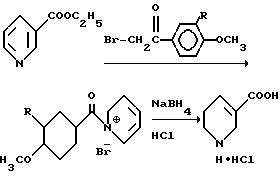
где
R H, CH3.
1-(4'-Метоксифенацил)-3-этоксикарбонилпиридинийбромид общей формулы
где R-H или R-OCH3, предлагается в качестве промежуточных продуктов для синтеза 1,2,3,6-тетрагидроникотиновой кислоты.
Указанные соединения приведенной общей формулы получают в одну стадию взаимодействием этилникотината и соответствующего фенацилбромида в ацетоне с высоким выходом (до 88%). Использование этих соединений в синтезе 1,2,3,6-тетрагидроникотиновой кислоты позволяет получить последнюю с выходом 86-88% в одну стадию, что значительно упрощает способ и повышает выход целевого продукта.
Пример 1. Растворяют 4,8 г (0,021 моль) 4-метоксифенацилбромида в 50 мл ацетона и смешивают с 3,15 г (0,021 моль) этилового эфира никотиновой кислоты, через 5 ч выделившийся осадок отфильтровывают, промывают ацетоном, эфиром. Выход 6,7 г (85%). Т.пл. 195-197oC (изопропанол).
Найдено, C 53,4; H 5,0; N 3,4; Br 20,6.
Вычислено, C 53,7; H 4,7; N 3,7; Br 21,0.
ИК-спектр, см-1: 1710-1685 (C=O), 1620-1570 (C=C).
Пример 2. Растворяют 6 г (0,023 моль) 3,4-диметоксифенацилбромида в 70 мл ацетона и прибавляют 3,48 г (0,023 моль) этилового эфира никотиновой кислоты, через 5 ч выделившийся осадок отфильтровывают, промывают ацетоном, эфиром. Выход 8,3 (88%). Т.пл. 183-186oC (изопропанол).
Найдено, C 52,4; H 4,7; N 3,2; Br 19,0.
Вычислено, C 52,7; H 4,4; N 3,4; Br 19,5.
ИК-спектр, см-1: 1710-1685 (C=O), 1620-1570 (C=C).
Пример 3. В 150 мл смеси метанола и воды (1:1) растворяют 7,6 г (0,02 моль) 1-(4'-метоксифенацил)-3-этоксикарбонилпиридинийбромида и частями при перемешивании прибавляют 4,5 г (1,2 моль) боргидрида натрия, затем реакционную массу выдерживают 2 ч при 60-70oC, растворитель отгоняют в вакууме водоструйного насоса. Остаток светло-оранжевую густую массу -промывают водой (2х30 мл), прибавляют 30 мл концентрированной соляной кислоты и упаривают досуха. Гувацин хлоргидрат белый кристаллический порошок отмывают от смолы ацетоном. Выход 2,7 г (88%). Т.пл. 316oC (разл. метанол).
Найдено, C 44,3; H 6,5; N 8,4; Cl 21,2.
Вычислено, C 44,0; H 6,15; N 8,55; Cl 21,7.
ИК-спектр, см-1: 3150 (С-N), 1700 (С=O), 1580 (С=С).
Пример 4. Растворяют 4,1 г (0,01 моль) 1-(3',4'-диметоксифенацил)-3-этоксикарбонилпиридинийбромида в 100 мл водно-метанольного раствора (1:1), прибавляли частями 2,27 г (0,06 моль) боргидрида натрия и выдерживают смесь при 60-70oC. Затем растворитель упаривают досуха в вакууме водоструйного насоса, остаток промывают водой (2х30 мл), растворяют в 25 мл концентрированной соляной кислоты и упаривают досуха, отмывают целевой продукт ацетоном. Выход гувацина хлоргидрата 1,4 г (86%). Температура плавления смешанной пробы не дает депрессии с образцом, приготовленным по методу, описанному в примере 1.
В результате фармакологических испытаний установлено, что гувацин, полученный предлагаемым способом, в опытах на изолированных суперфузируемых срезах коры полушарий мозга крыс в концентрациях 10-6 10-3 моль/л уменьшает поглощение срезами 3H-гамма-аминомасляной кислоты (3H-ГАМК). Концентрация, ингибирующая захват 3H-ГАМК на 50% (LC50), составляет 48 мкМ. Соответствующая концентрация для (-)-нипекотиновой кислоты, известной в качестве ингибитора нейтрального захвата ГАМК, составляет 5 мкМ. Гувацин в концентрациях до 10-4 не проявляет ГАМК-миметической активности, но усиливает влияние ГАМК на нейрон спинного мозга.
В опытах на белых мышах найдено, что гувацин обладает умеренно выраженным угнетающим центральную нервную систему действием. В дозах 20-80 мг/кг он уменьшает спонтанную двигательную активность и ориентировочное поведение животных, но в тех же дозах не обнаруживает гексаналопотенцирующего и противосудорожного (антикоразолового) действия. Он мало токсичен и не вызывает видимых признаков отравления и гибели мышей при внутрибрюшинном введении в дозе до 400 мг/кг.
Таким образом, гувацин оказывает выраженное влияние на ГАМК-органические синапсы центральной нервной системы, обладая свойствами ингибитора нейронального захвата гамма-аминомасляной кислоты тормозного медиатора ЦНС в синапсах мозга, и может найти применение в экспериментальной биологии и медицине.
Использование предлагаемых промежуточных соединений позволяет упростить способ получения гувацина, достигая при этом высокого выхода (86-88%).
1. Способ получения 1,2,3,6-тетрагидроникотиновой кислоты, отличающийся тем, что, с целью увеличения выхода целевого продукта и упрощения технологии его получения, на 1-(4'-метоксифенацил)- или 1-(3',4-диметоксифенацил)-3-этоксикарбонилпиридинийбромид действуют боргидридом натрия в водно-метанольной среде, а затем концентрированной соляной кислоте.
2. 1-(4'-Метоксифенацил)-3-этоксикарбонилпиридинийбромид или 1-(3',4'-диметоксифенацил)-3-этоксикарбонилпиридинийбромид общей формулы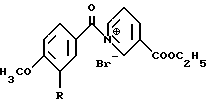
где R - водород или -ОСН3,
в качестве промежуточных продуктов для получения 1,2,3,6-тетрагидроникотиновой кислоты.
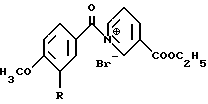
где R водород или -ОСН3,
в качестве промежуточных продуктов для получения 1,2,3,6-тетрагидроникотиновой кислоты.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Yonston J.A.R., Krogsgaard - Larsen P., Stephanson A | |||
| Physiologic pharmacology of GABA and its antagonists in Vertebrate neroous system | |||
| - "Nature", 1975, 258, p | |||
| ПНЕВМАТИЧЕСКИЙ ДВИГАТЕЛЬ | 1923 |
|
SU627A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Mc | |||
| Elvain S.M., Stork Y | |||
| Piperidine derivatives XV, Synthesis of guvacine - Journ | |||
| of amer | |||
| Chem | |||
| Soc., 1946, 68, N 6, p | |||
| УСТРОЙСТВО ОРГАНОВ СТАБИЛИЗАЦИИ И УПРАВЛЕНИЯ В АЭРОПЛАНАХ, СНАБЖЕННЫХ НЕСКОЛЬКИМИ РЯДОМ УСТАНОВЛЕННЫМИ МОТОРАМИ | 1924 |
|
SU1049A1 |
Авторы
Даты
1997-12-10—Публикация
1983-08-30—Подача