Изобретение относится к новым хи мическим соединениям, конкретно к галогеноалкилпроизводным 7-окси5,6-бензо-0 -пирона общей формулы { I) где при (СН)зС1, Нг - водород или метил или при (СН )Вг, R,j метил, в качестве флуоресцентной метки для определения третичных аминосоединений. Соединения формулы (J) обладают высокой флуоресценцией и содержат д статочно реакционноспособные функци нальные группы, что позволяет испол зовать их в качестве флуоресцентных меток для количественного флуорометрического определения различных лекарственных препаратов и токсических веществ в объектах судебно-медицинской экспертизы и в водных растворах. Известен 4-метил-8-ацетнп-7-{3хлорпропокси)-5,6-бензо-о -пирон формулы (П) J-0-CH2-CH2-CH2-Ci Однако соединение формулы П имеет слабую флуоресценцию (чувствительность определения 10 мг/мл) Известны также в качестве флуоресцентных реагентов некоторые производные 5,6-бензо-0 -пирона, в частности 7-окси-3-карбокси-5,6бензо-(/-пирон формулы (Ш) чувствительность определения 10 мг/мл и 7-метокси-4-бромметшт-5,6-бензоct-пирон формулы (1У) (чувствительность определения 10 мг/мп), на основе которых разработаны спектрофлуорометрические методы количественного определения производных амфетамина и простагландинов СН ОТ т Нзсо- :х о Недостатком известных соединений формул (Ш)и.(1У) является то, что они имеют слабую флуоресценцию чувствительность определения до 10 мг/мл. Целью изобретения является изыскание новых реакционных галогеноалкилпроизводных 7-окси-5,6-бензо-о пирона, обладающих свойством придавать третичным аминосоединениям повышенную флуоресценцию. Цель достигается использованием в качестве флуоресцентной метки для определения третичных аминосоединений галогенойлкилпроизводных 7-окси-5,6-бензо- о -пирона общей формулы ( 1 ) где при (CH,,)jCI, R .3- водород или метил или при (СН2)2Вг, R2 - метил. Соединения формулы (1) получают путем взаимодействия умбеллиферона ( V, R -Н) или 4-метилумбеЛлиферона (У1, R.-CH,j) с дибромэтаном или I,3-хлорбромпропаном в среде абсолютно сухого органического растворителя, такого, как ацетон, в присутствий , при температуре кипения реакционной смеси. Соединения формулы (1) обладают высокой флуоресценцией (чувствительность определения до 10мг/мл), причем последняя зависит от строения и расположения заместителей в ядре 5,б-бензо-oi-пирона. Реакция их синтеза протекает всего в одну стадию, основана на использовании доступных реагентов, технологически проста и открьшает возможность расширения числа флуоресцентных реагентов, применяемых в спектрофлуорометрии. Получение соединений формулы I иллюстрируется примерами 1-3.
Пример 1. 7-(3-Хлорпропокси)-5,6-бензо-о -пирон R -CCH) R - Hj. 16,2 Г умбеллиферона растворяют в 15б мл .ацетона, добавляют 15 мл 1,3-хлорбромпропана и 14 г КjCO-, Реакционную смесь помещают в круглодонную колбу, которую соединяют с обратным холодильником, и кипятят в течение 24 ч. Затем фильтруют, растворитель концентрируют до небольшого объема и хроматографируют на колонке (5x150 см) с нейтральной окисью алюминия (800 г акт. П ст.). Элюирование проводят смесью хлороформа и петролейного эфира. Получают 7-(3 -хлорпропокси)-5,6-бензо- oi-пирон состава , Т.Ш1. 107-109°С (из бензола ) с выходом 7,0г(31%).
П р и м е р 2. 4-Метш1-7-(2 -бро этокси )-5,6-бензо-oi-пирон CRl-(CH2)Br, Rj -CH,.
17,6 г 4-метилумбеллиферона растворяют в 150 мл ацетона, добавляю эико-химические харвктеристнкн производных формулы I
18 мл дибромэтана и 14 г KjCO Далее процесс ведут, как в примере 1. Получают 4-метил-7-(2 чбромэтокси)-. 5,6-бензо-oi-пирон состава , т. пл. 106-106,(из бензола). Выход 13 г (46%)
Пример 3. 4-Метил-7-(3--хлорпропокси)-5,6-бензо-of-пирон (R(CHJ3 С1, Rj-CHj)..
17,6 г 4-метилумбеш1иферона растворяют в 150 мл ацетона, добавляют 15 мл 1,3-хлорбромпропана и 14 г KjCOj. Далее процесс ведут, как в примере 5. Получают 4- 1етш1-7-(3хлорпропокси)-5,6-бенэо-«/-пирон состава Cj H jOjCl, т. пл. 79-80 0 (из бензола) с выходом 12 г (53%).
Соединения формулы 1 - кристаллические вещества белого цвета, растворимЁ в хлороформе, спирте, ацетоне, бензоле, нерастворимы в воде, их химико-физические характеристики приведены в табл. I.
ПНР-спектр (НХ-90, в CDCfj 0-ГМДС), г, м,д. Т 9 л и ц « I 7--окси 5,6-бензо-пв(-пиров«



| название | год | авторы | номер документа |
|---|---|---|---|
| ХЛОРПРОПОКСИПРОИЗВОДНЫЕ 7-ОКСИ-КУМАРИНА, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ И ГЕПАТОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 2010 |
|
RU2452732C2 |
| Сополимеры @ -винилпирролидона с производными 5,6-бензо- @ -пирона,обладающие антигенными свойствами | 1981 |
|
SU1034383A1 |
| Способ получения производных @ 4-(4н)-оксо-8-бензопиранил @ -уксусной кислоты | 1982 |
|
SU1250171A3 |
| Способ получения производных 1,3-пропилендифосфоновых кислот | 1985 |
|
SU1375141A3 |
| Способ получения сульфинилхлоридов | 1975 |
|
SU644383A3 |
| Способ получения производных бензо/с/хинолина или их фармацевтически приемлемых солей | 1981 |
|
SU1098520A3 |
| Способ получения производных 5-оксибензофурана | 1986 |
|
SU1416489A1 |
| Способ получения производных бензо/с/-хинолинов или их солей | 1977 |
|
SU940646A3 |
| Способ получения 3-метиленце-фАМСульфОКСидОВ | 1975 |
|
SU799667A3 |
| Способ получения производных 2-фенил-5,6-дигидро-4-пирона | 1979 |
|
SU919595A3 |
Галогеноалкнппроизводные 7-ок-си-5,6-бензо-ed-пирона общей формулы где при R,- -(он 2), водород или метип или при R,-(СН ) Вг, RJ - метил,g в качестве флуоресцентной метки для определения третичных аминосоединений. 4 СО О1 со Од
С1 14,65, С1 14,70 ««ольце/ 15,00 1720/С Оа -пирона 52,65; С 52,74 1675, 1560 52,55 . 1515/-СН-СН-связ Н 4,0 в ароматическом кольце/ Вч 29,34 Вч 29 ,-15 С 61,90 1715 /С-0 et-пиро С 61,65; на/, 1680, 1650, 61,79 1530, J510 /-СНН 5,15; Н s 1 ч в арокатическом 4,95 CI 13,80 кольце/ CJ 14,0 7,58/д, Э- 9,5 Гц, Н-3 и Н-4/ 6,77; 7,33 /д, 3-9 Гц, Н-6 и Н-5/, 6,73/с, Н-8/, 2,20 /к, J П Гц, 3-6 Гц, -CHf/, 3,62, 4,11/т, :- 7 Гц, -CHi-Ct и соответственно/ 6,05 /с,Н-3/, 6,79, 7,38/д, Э- 9 Гц, Н-6 я Н-5/, 6,72 /с,Н-8/ 3,61, 4,27 /т, 3-7 Гц, -O-CHj-СНг-Вч/, 2,34 /с, С-СНз/ 6,60 /с, Н-3/, 6,73; 7,38 /д. Э9 Гц, Н-6 и Н-5/, 6,67 /с, Н-8/, 3,71, 4,11 /т, J- 7,5 Гц, и соответственно/ 2,25 /к, J- П Гц, - 6 Гц, -CHj-/, 2,31 /с, - С-СНз/
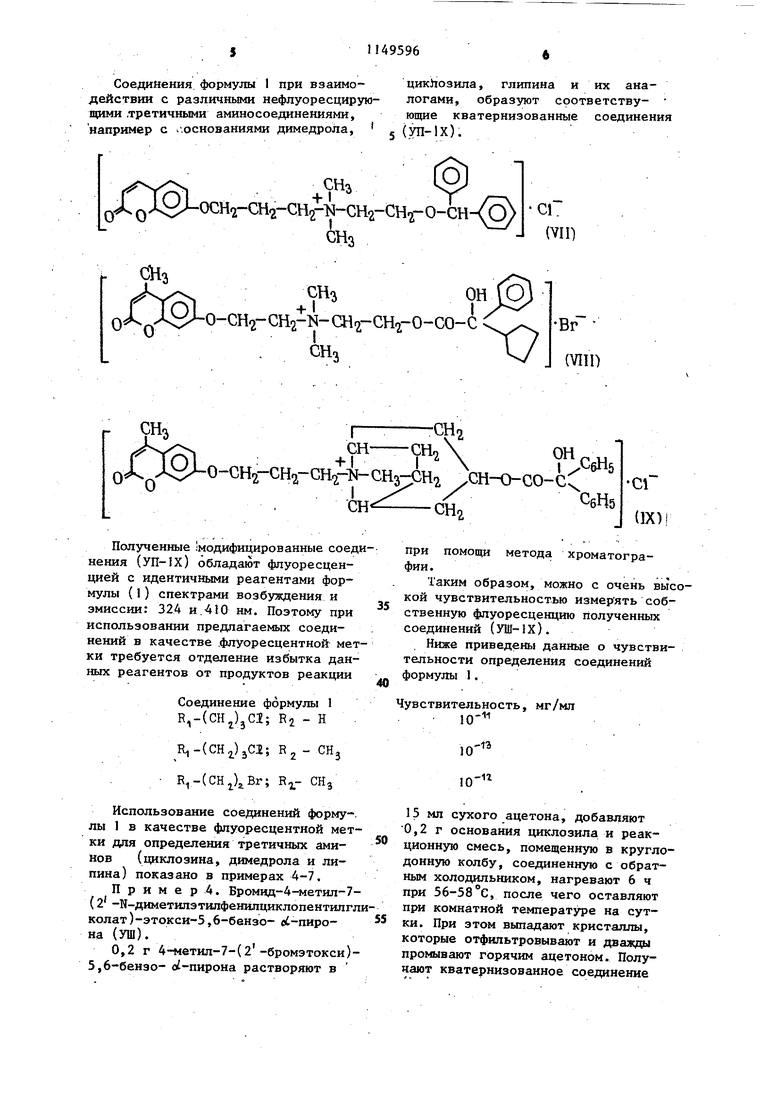
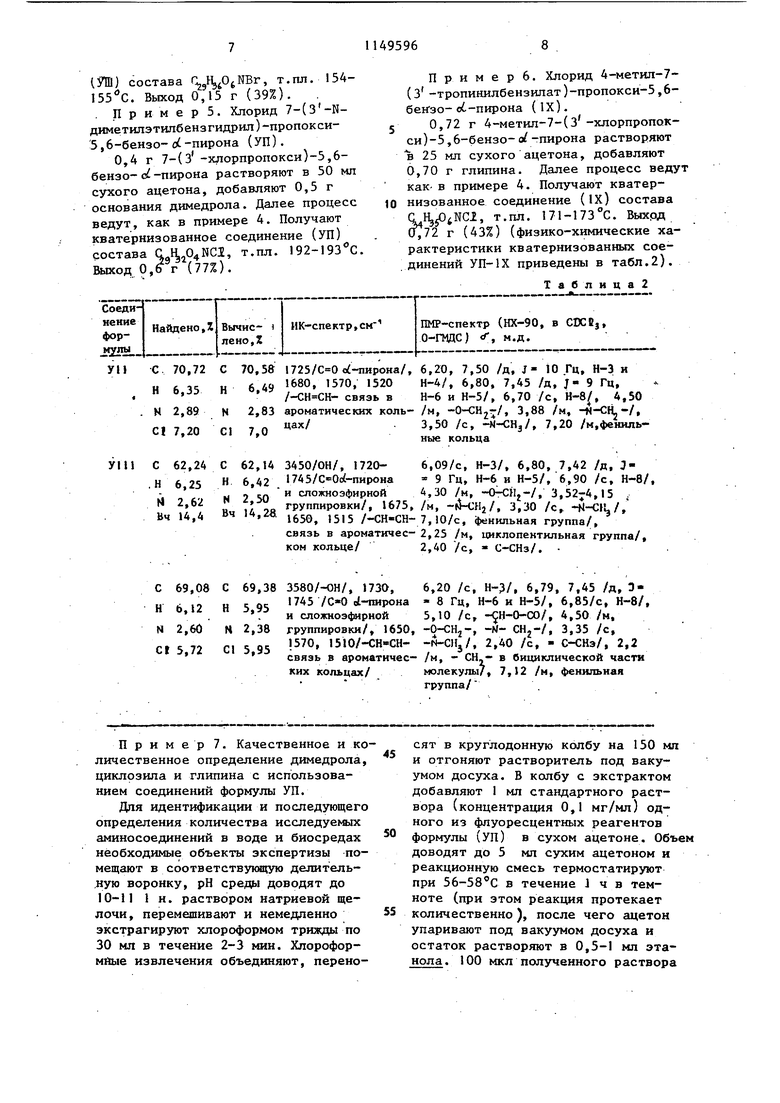
Соединения формулы 1 при взаимодействии с различными нефлуоресцирующими .третичными аминосоединениями, например с ..основаниями димедрола,
цикЛозила, глипина и их аналогами, образуют соответству- ющие кватернизованные соединения 5 (УП-1Х).
Шз
ОСН2-СН2-Ш2--Ъ1-СН2-СН2-0-СН- О
сш
С1.
(VI п
Вг
{VIII) -CHrr-CH2-CHrrN-CH3;HiH2 .CH-Q-CO-C
СН2
снI ..СйНз
сГ
СН
СбЧэ
СНг
(IX)
Полученные модифицированные соединения (УП-1Х) обладают флуоресценцией с идентичными реагентами формулы (1) спектрами возбуждения и эмиссии: 324 и.410 нм. Поэтому при использовании предпагаемых соединений в качестве .флуоресцентной метки требуется отделение избытка данных реагентов от продуктов реакции
Соединение формулы 1
Н,-(СН)зС1; R2 - Н
11,-(СН)зС1; Rj - CHj R,-(CHj)Br; СНз Использование соединений форму-, лы 1 в качестве флуоресцентной метки для определения третичных аминов (циклозина, димедрола и липина) показано в примерах 4-7, П р и м е р 4. Бромид-4-метил-7(2 -N-диметилэтилфенилциклопентилгл колат)-этокси-5,6-бензо- оС-пирона (УШ). 0,2 г 4-«етш1-7-(2 -бромэтокси)5,6-бензо- oi-пирона растворяют в
при помощи метода хроматографии.
Таким образом, можно с очень выской чувствительностью измерять собственную флуоресценцию полученных соединений (УШ-1Х).
Ниже приведены данные о чувствительности определения соединений формулы I.
Чувствительность, мг/мл
-11
10
-13
10 15 мл сухого ацетона, добавляют 0,2 г основания циклозила и реакционную смесь, помещенную в круглодонную колбу, соединенную с обратным холодильником, нагревают 6 ч при 56-58 С, после чего оставляют при комнатной температуре на сутки. При этом выпадают кристаллы, которые отфильтровывают и дважды промывают горячим ацетоном. Получают кватернизованное соединение
(ЯП) состава т.пл. 154ISS C. Выход 0,15 г (39%).
Примерз. Хлорид 7-(3-Nдиметш1этилбензгидрил)-пропокси5,б-бензо-ci-пирона (УП).
0,4 г 7-{3 -хлорпропокси)-5,6бензо- с -пирона растворяют в 50 мл сухого ацетона, добавляют 0,5 г основания димедрола. Далее процесс ведут, как в примере 4. Получают кватернизованное соединение (УП) состава СД 04НС1, т.пл. 192-193 С. Выход 0, г (77%). УП С. 70,72С70,5а1725/С 0 о -пирона/, н А ч-iн6 , 1570, 1520 . /-СН СН- связь в . N 2,89N2,83ароматических кольС 7,20С17,0 У1П С 62,24 С 62,14 3450/ОН/, 1720Н 6,25 6,42 . 745/С« Ос(-пирона 2 CQ и сложноэфирной М 2,62 Г Вч 14 28 группировки/, 1675, Вч 14,4 вч 14, jg50, 1515 /-СН«СНсвязь в ароматическом кольце/ 69,08 С 69,38 3580/-ОН/, 1730, 1745 /С«0 dt-пирона Н 5,95 Н 6,12 и сложноэфирной N 2,60 2,38 группировки/, 1650, 1570, 1510/-СН«СНС1 5,95 СГ 5,72 связь в аронатических кольцах/
Пример 7. Качественное и количественное определение димедрола, циклозила и глипина с использованием соединений формулы УП.
Для идентификации и последующего определения количества исследуеьалх аминосоединений в воде и биосредах необходимые объекты экспертизы помещают в соответствукнцую делитель,ную воронку, рН среды доводят до 10-11 1 Н. раствором натриевой щелочи, перемешивают и немедленно экстрагируют хлороформом трижды по 30 мл в течение 2-3 мин. Хлороформйые извлечения объединяют, переноП р и м е р 6. Хлорид 4-метил-7(З -тропинилбензилат)-пропокси-5,6бекзо-ot-пирона (1Х).
0,72 г 4-метил-7-(3-хлорпропокси)-5,6-бензо-о -пирона растворяют Ъ 25 мл сухого ацетона, добавляют 0,70 г глипина. Далее процесс веду как- в примере 4. Получают кватернизованное соединение (1Х) состава С t 5°tNCl, т.пл. 171-173°С. Выход г (43%) (физико-химические характеристики кватернизованШ)ПС соединений УП-1Х приведены в табл.2).
Таблица2
сят в круглодонную колбу на 150 мл и отгоняют растворитель под вакуумом досуха. В колбу с экстрактом добавляют 1 мл стандартного раствора (концентрация 0,1 мг/мл) одного из флуоресцентных реагентов формулы (УП) в сухом ацетоне. Объ доводят до 5 мл сухим ацетоном и реакционную смесь термостатируют при 56-58С в течение i ч в темноте (при этом реакция протекает количественно), после чего ацетон упаривают под вакуумом досуха и остаток растворяют в 0,5-1 мл этанола. 100 мкл полученного раствора 6,20, 7,50 /д, J- 10 Гц, Н-3 и Н-4/, 6,80, 7,45 /д, - 9 Гц, Н-6 и Н-5/, 6,70 /с, Н-8(, 4,50 /м, -О-СН г;/, 3,88 /м, -N-CH,,-/, 3,50 /с, -N-CHj/, 7,20 /м,фенильные кольца 6,09/с, Н-3/, 6,80, 7,42 /д, J- 9 Гц, Н-6 и Н-5/, 6,90 /с, Н-8/, 4,30 /м, -О-СН -/, 3,52-4,15 . /м, -Й-СНг/, 3,30 /с, -H-C1L/, 7,10/с, фенильная группа/, 2,25 /м, циклопектильная группа/, 2,40 Ус, - С-СНз/. 6,20 /с, Н-3/, 6,79, 7,45 /д, Э- 8 Гц, Н-6 и Н-5/, 6,В5/с, Н-8/, 5,10 /с, - Н-О-СО/, 4,50 /м, -О-СН -, -N- , 3,35 /с, -N-CHj/, 2,40 /с, « С-СНэ/, 2,2 /м, - СН,- в бициклической части молекулы/, 7,12 /м, феинльная группа/
с помощью микропипетки наносят на стартовую линию (1,5 см от нижнего края) пластины силуфол (20 смх х20 см). После улетучивания растворителя в местах нанесения проб хроматограмму помещают в предварительно (10-15 мин) насыщенную камеру с системой метанол-НС1 в соотношении 1:0,05. Нижний край пластины погружают в систему растворителей примерно на 1 см так, чтобы уровень растворителя бьш ниже стартовой линии. Когда фронт растворителя находится на расстоянии 0,5 см от верхнего края пластины, ее извлекают из камеры и отмечают линию фронта. Xpoмaтoгpa y сушат в вытяжном шкафу в течение 5-10 мин, затем обнаруживают пятна, рассматривая хроматограмму в УФ-свете. При этом кватернизованные соединения (Х-ХП) проявляются в виде ярко-голубых пятен со следз ющими значениями ,43 ,38, ,50, что позволяет иден тифицировать их среди, многочисленш 1Х природных соединений, содержащихся в исследуемых объектах зкспертизы. После этого соответствующие пятна обводят, вырезают и вещества смывают с пластины в мерную колбу на 25 мл трижда по 5 мл дистиллированно водой через,.складчатый бумажный
Растворено циклозила, мг/мп
Найдено, мг/мл
Результаты определения димедрола в сыворотке крови кроликов (опыты in vivo) с применением 7-(3 хлоропропокси) -5,6-бензо- oi-пнрона (I).
Доза димедрола,мг/кг Найдено,мг/м
303-10
Определение димедрола производят через 30 мин после внутрибрюшинного введения препарата цельному животному.
Результаты определения глипина в сыворотке крови крыс (опыты in vivo) с применением 4-метил-7-(3хлорпропокси)-5,6-бензо-е -пирона (3). . Доза глипнна,мг/кг Найдено,мг/мл
108-10
фипьтр. Объем доводят до -метки, перемепшвают и флуоресценцию раствора измеряют, например на спектрофлуорометре фирмы Hitachi MPF-2A при длине волны 410 нм, возбуждая свечение светом длиной волны 324 нм. Количественное содержание исследуемых соединений определяют по калибровочным графикам или методом сравнения интенсивности флуоресценции стандартных растворов кватернизованных соединений (УП-1Х) с таковыми изучае1« 1х проб.
Минимальное визуально открьгоаемое в пробе (в пятне на пластине) количество вещества при использовании для хроматографии пластин - силуфол в системе метанол-HCj (1:0,05) и при освещении ультрафиолетовьйч осветителем типа ВИО-1, УФС-2 равно для циклозила 10 мг (из вода|), для димедрола 10 мг (in vivo, из сыворотки крови кролика), для глипина Ю мг (in vivo, из сыворотки крови и из печени крыс), что иллюстрируется приведенными ниже данными. Результаты определения циклозила в воде с применением 4-метил-7-(2бромэтокси)-5,6-бензо- ot-пирона (2) (приведенные здесь и далее данные являются средними из 5 измерений),.
IlO
i
-5
I -10
1 -10 .940
-(,
8-10
8-10
Определение глипина производят через 30 мин после внутрибрюшинного :. введения препарата цельному животному.,
Соединения формулы (Г) и разработанный на их основе спектрофлуорометрический метод качественного и количественного определения различных лекарственных препаратов и токсических веществ могут найти применение для микроаналитических исследований в области фармако- и токсикокинетики, в контроле за производством лекарственных препаратов, при решении задач судебно-медицинской экспертизы.
Соединения формулы (Г) обладают повышенной чувствительностью по сравПнению с известными BeinecTBahm, применяемыми для этой же цели (1.(Г 1{Г1мг/мл против 10 мр/мл соответ114959612ственно, при их использовании в качестве флуоресцентной метки.
| Malik M.S., Rastogi 5.Ы | |||
| Indian J | |||
| Chem., 1981, V.20B, № 6, p.171174 | |||
| Goodwin R.H., Kavanagh F | |||
| Arch | |||
| Bioch., 1950, V.27, 1, p.152-173 | |||
| Stewart J.T., Lotti D.M., Anol | |||
| Chem | |||
| Acta., 1970, v.52, № 2, p.390393 | |||
| Stewart J.T., Lotti D.M., J.Phartn | |||
| Sci, 1971, V.60, № 3, p.461-463 | |||
| Turk J.., Weiss S.J., Davis J.E., et | |||
| al | |||
| Prostagl d,, 1978, v.l6, p.291-309 | |||
| Алексеев C.M., Помойницкий В.Д., Сарычева И.К., Евстигнеева P.П., Хим | |||
| фарм | |||
| ж., 1981, 11, с | |||
| Ударно-долбежная врубовая машина | 1921 |
|
SU115A1 |
Авторы
Даты
1985-12-15—Публикация
1983-07-07—Подача