1 Изобретение относится к новьм производным 2-(3-метил-2-бутенил)-циклопентанона общей формулы (I) О , Rjj « где R и R образуют двойную связь (1а) или Я,-Н; R -СН N0 (t6), являющимся полупродуктами в синтезе . простагландинов , Аналогами предлагаемых соединений по структуре и назначению явля ются производные 2-(2-пропенш1)-1и1клопентанона общей формулы (II) Лхч СНзПОа Л..-х L-Л/ио, юо-А AiX где Rj и Rj образуют двойную связь (На) или R,-H; R,.CHjNO (116). Соединение формулы На получают из этилового эфира 4-пентеновой кислоты в 8 стадий с суммарным выходом 2%. Соединения формулы II используют в синтезе простагландинов по эффективной схеме, позволяющей избежать применение элементоорганических соединений при введении60-цепи. Данная схема приводит к простагландинам ряда Н-дезокси Е и Fj . в частности к простагланднну Н-дезокси-Рг (X) V ,Ни , 4f%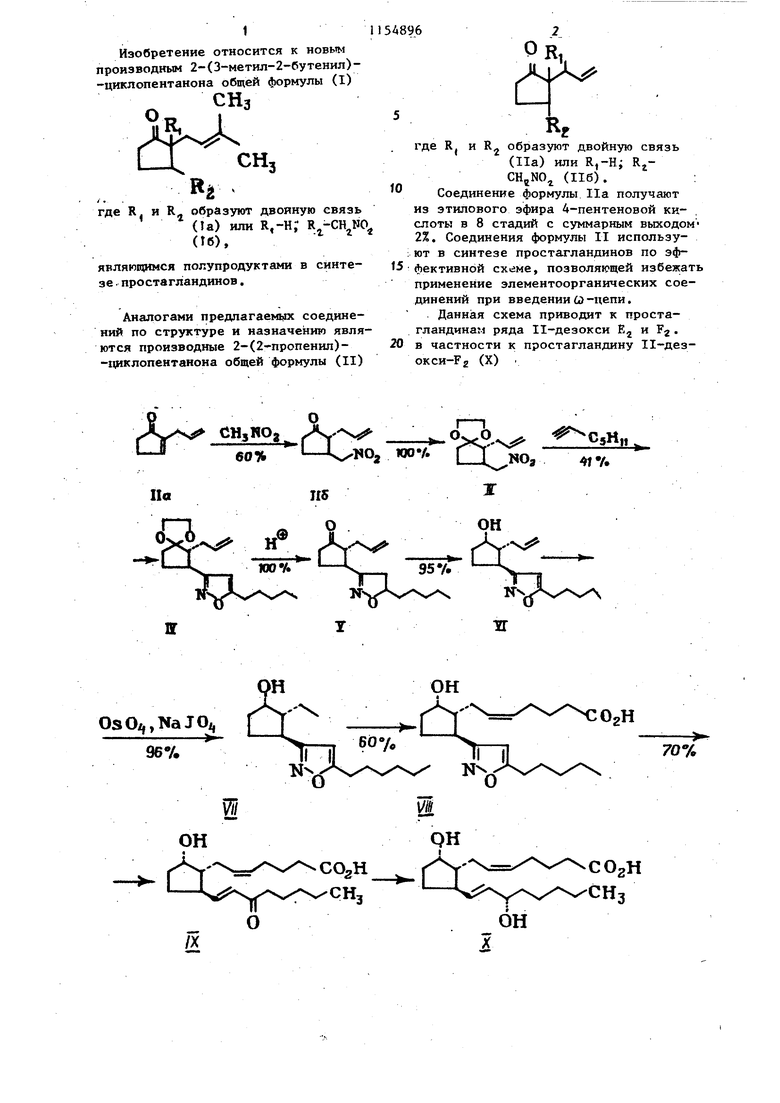



| название | год | авторы | номер документа |
|---|---|---|---|
| Производные 3-изоксазолилциклопентанона в качестве полупродуктов полного синтеза простагландинов | 1981 |
|
SU989850A1 |
| Способ получения 1-формил-2-ацил3-оксициклопентанов | 1976 |
|
SU639854A1 |
| Способ получения 2-/6-карбметокси (этокси)-гексил/-циклопентен2-она-1 | 1978 |
|
SU789510A1 |
| Способ получения производных 3-пропенил-7- @ 2-(2-аминотиазолил-4)-2-гидроксииминоацетамидо @ -3-цефем-4-карбоновой кислоты или ее сложных эфиров в виде Z- или Е-изомеров или их смесей | 1986 |
|
SU1428204A3 |
| Способ получения вторичных ацетиленовых аминов | 1978 |
|
SU739065A1 |
| Способ получения производных 2-(тиенил-2)- или 2-(тиенил-3) этиламина | 1982 |
|
SU1148563A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 3-АРИЛ-5-ХЛОРИЗОКСАЗОЛОВ | 2015 |
|
RU2637927C2 |
| Способ получения 2-(6-карбалкоксигек-Сил) циКлОпЕНТЕН-2-OHOB-1 | 1978 |
|
SU806672A1 |
| Способ получения аналогов простагландинов @ | 1979 |
|
SU1104134A1 |
| Пиримидо/1,2-а/индол-2-оны в качестве промежуточных продуктов для синтеза 10а-стирилпиримидо/1,2-а/индол-2-онов | 1983 |
|
SU1145021A1 |
Производные 2-
OsO/,NaJOi,
96V.
Wi
OH
70%
0
Ш
Использование аналогов как полупродуктов в описанной схеме приводит к недостаточно высоким выходам на стадиях присоединения нитрометана (60%) и присоединения гептина (41%), что снижает выход целевого продукта.
Целью изобретения является изыскание новых полупродуктов, позволяюл О CHj СНзКО, , ОН СН,о„
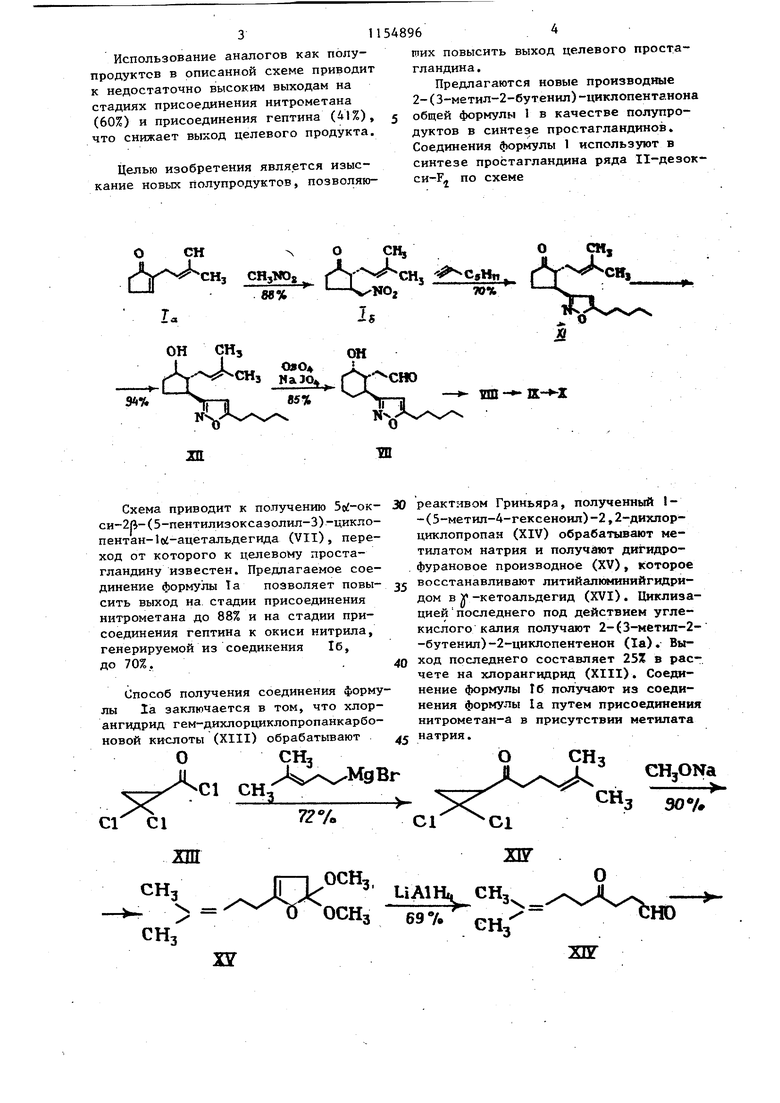
Ж Схема приводит к получению 5с -окси-2й-(5-пентилизоксазолил-3)-циклопентан-1ы-ацетальдегида (VII), переход от которого к целевому простагландину известен. Предлагаемое соединение формулы Та позволяет повысить выход на стадии присоединения нитрометана до 88% и на стадии присоединения гептина к окиси нитрила, генерируемой из соединения 1б, до 70%.. Способ получения соединения форму лы 1а заключается в том, что хлорангидрид гем-дихлорциклопропанкарбоновой кислоты (XIII) обрабатывают .MgB С1 СН С1 С1
Zffl
,, ЛГ(
осн.
СН.
хг
ших повысить выход целевого простагландина.
Предлагаются новые производные 2-(З-метил-2-бутенил)-циклопентанона общей формулы 1 в качестве полупродуктов в синтезе простагландинов. Соединения формулы 1 используют в синтезе простагландина ряда 11-дезокси-F., по схеме
хпг
UA1
хпг О СН, СдНп. (СН, реактивом Гриньяра, полученный 1-(5-метил-4-гексеноил)-2,2-дихлорциклопропан (XIV) обрабатывают метилатом натрия и получают дигидрофурановое производное (XV), которое восстанавливают литийалюминийгидридом в у-кетоальдегид (XVI). Циклизацией последнего под действием углекислого калия получают 2-(3-метил-2-бутенил)-2-циклопентенон (1а). Выход последнего составляет 25% в рас-. чете на хлорангидрид (XIII). Соединение формулы 1б получают из соединения формулы 1а путем присоединения нитрометан-а в присутствии метилата натрия. ОСНз Д. CHjONa 90%
КгСОд 57%
Исходный хлорангидрид гем-дихлорциклопропанкарбоновой кислоты получают из диаллилацеталя уксусного альдегида в 4 стадии с выходом 61%. Дишшилацеталь уксусного альдегида, в свою очередь, получают из аллилового спирта в одну стадию с выходом 68%. Таким образом, переход от аллилового спирта к соединению 1а осуществляется в 9 стадий с суммарным выходом 11%. Пример 1. Получение 2-(3-метип-2-бутеиип)-2-циклопентенона (1а) К охлажденному до раствору реактива Гриньяра, полученному из 3,12 г (0,13 г-атом) Mg и 19,56 г (0,122 моль) 5-6ром-2-метилпентенав I70 мл абсолютного тетрагидрофурана, добавляют по каплям при перемешивании раствор 17,33 г (0,1 моль хлорангидрида гем-дихлорциклопропан карЭоновой кислоты (XIII) в 30 мл абсолютного тетрагидрофурана с такой скоростью, чтобы температура не под нималась вьпае -75 С. После перемеши вания при этой температуре в течени 30 мин реакционную смесь оставляют нагреваться до комнатной температуры, затем добавляют 100 мл насыщенного раствора хлористого аммония Тетрагидрофуран упаривают в вакууме остаток экстрагируют эфиром ( м эфирные экстракты промывают раствором соды и сушат сульфатом натрия. После удаления растворителя остаток перегоняют. Получают 15,91 г (72%) 1-(5-метш1-4-гексеноил)-2,2-дихлорциклопропана (XIV), т.кип. 104105 с/2 мм рт.ст. ,4925. Найдено, %: С 54,54; Н 6,14 Ск,н„сч Вычислено, %: С 54,29; Н 6,33. К охлажденному до 10С раствору метилата натрия в метаноле, получен ному при растворении 5,06 г (0,22 ) Na в 150 мл метанола, добавляют по каплям при перемешивании раствор 22,1 V (0,1 моль) 1-(5-метил-4-гексеноил)-2,2-дихлорциклопропана (XIV) в 50 мл метанола с такой скоростью, чтобы температура раствора была 10-15°С. Реакционную массу перемешивают при комнатной температуре в течение 15 мин, разбавляют 200 мл воды и экстрагируют гексаном (3 100 мп). Экстракты сушат сульфатом натрия, растворитель удаляют в вакууме и остаток перегоняют. Получают 19,08 г (90%) 5-(4-метил-3-пентенил)-2,2-диметокси-2,3-дигидрофурана (XV), т.кип. 9597°С/2 мм рт.ст., ,4617. Найдено, %: С 67,75-, Н 10,07. С HJ/Y Вычислено, %: С 67,92; Н 9,91. К суспензии 0,95 -г (0,025 моль) литийалюминийгидрида в 40 мл абсолютного диоксана добавляют раствор 10,6 г (0,05 моль) 5-(4-метил-3-пентенил)-2,2-диметокси-2,3-дигидрофурана (XV) в 10 мл абсолютного диоксана. Смесь кипятят при перемешива- НИИ в течение 15 мин, затем охлаждают, добавляют по каплям раствор 6 мл ацетона в 50 мл абсолютного эфира. Реакционную массу разлагают добавлением 50 мл 10%-ной HCI .с перемешиванием при комнатнрй температуре в течение 30 мин. Органический слой отделяют, водный слой экстрагируют эфиром (3 50 мл). Объединенные органические экстракты сушат сульфатом натрия, растворитель удаляют в вакууме, остаток перегоняют. Получают 5,8 г (69%) 8-метил-7-нонен-4-он-1-аля (XVI), т.кип. 97-100°С/3 мм рт.ст. п 1,4647. Найдено, %: С 71,65; Н 9,39 ю(б 2 Вычислено, %: С 71,43; Н 9,52. Раствор 5,04 г (0,03 моль) 8-метил-7-нонен-4-он-1-аля в 60 мл метаиола добавляют по каплям при перемешивании к кипяшей смеси 60 мл 5%-ной KjCO и 120 мл метанола в течение I ч. Реакционную смесь кипятят 1,5 ч, охлаждают, прйбавля лт к ней разбавленную HCl до кислой среды и экстрагируют эфиром. Растворитель удаляют в вакууме, остаток разбавл ют эфиро, оставшуюся воду отделяю и дополнительно экстрагируют эфиром Объединенные эфирные экстракты сушат сульфатом натрия, растворител удаляют в вакууме, остаток перегон ют. Получают 2,57 г (57%) 2-(3-ме тил-2-бутенил)-2-ииклопентенона (1а), т.кип. 78-80с/2 мм рт.ст.. ° 1,489 5. Найдено, %: С 80,23 Н 9,45, Вычислено, %: С 80,00; Н 9,33. П р и м е р.2. Получение 2-(3-метил-2-бутенил)-3-нитрометилцикл пентанона (16). К раствору 1,05 г (0,007 моль) 2-(3-метил-2-бутенил)-2-циклопентанона (1а) в 10 мл абсолютного мета нола добавляют по каплям при Перемешивании раствор метилата натрия, полученного из 0,22 г (0,0096 г-ато Na в 20 мл метанола. Затем добавляют раствор 0,61 г (0,1 моль) нитрометана в 10 мл абсолютного метанола. Реакционную смесь перемешивают в течение 3ч, добавляют 3 г сухого хлористого аммония, осадок отфильтровывают. Растворитель удаляют в вакууме, остаток хроматографируют на колонке с 30 г силикагеля (Chemapol 40/100). Элюирование проводят смесью эфир-гексан переменного состава. Получают 1,3 г (88%) 2-(З-метил-2-бутенил)-3-нитрометилциклопентанона (1б). ИК-спектр, , см(пленка): 1550, 1735. С„НпКОз. Вычислено: мол.вес.. 211,26. Масс-спектр: N 211. ПМР-спектр (CDC1,,S): 1,61 (СН,, с, ЗН); 1,69 (СН,, с, ЗН); 4,52 (Ciyi02,M, 2Н); 5,0 (, м, 1Н) Далее из соединения формулы 1б пЬлучают соединение VII, которое по .спектральным характеристикам идентично соединению VII, получаемому на основе аналогов. П р и м -е р 3. Получение 5(6-окси-2р-(5-пентилизоксазолш1-3)-циклопентан-1о6-ацетальдегида (VII) К смеси 0,633 г (0,003 моль) 2-(3-метил-2-бутенил)-3-нитрометилциклопентанона, 0,864 г (0,009моль) гептина-1 (16) и 1,071 г (0,009 моль) феншшзоцианата в 20 мл абсолютного бензола добавляют 5 капель триэтиламина (до помутн ения раствора). Реакционную смесь перемешивают 2 сут, осадок отфильтровывают, растворитель упаривают. Остаток хроматографируют последовательно на колонке, с (Reanal), элюэнт г смесь эфир-гексан переменного состава, затем хроматографируют на колонке с силикагелем (Chemapol 40/100), элюент - смесь эфиргексан переменного состава. Получают 0,605 г (69%) 2-(3-метип-2-бутенип)-3-(5-пентилизоксазолш1-Э)-циклопентанона (XI). ИК-спектр,-, см (п.пенка): 1540. 1600, 1745. Вычислено: мол.вес. 289,43. Масс-спектр: . ПМР-спектр (CDC1, ,5): 0,86 (СН,, м, ЗН); 1,50 (СИ,, с, ЗН); ,1,57 (СН , с, ЗН); 4,92 (СН-С, м, JH); 5,81 (, с, 1Н). К суспензий 0,82 (0,00322 моль) LiAlH (0-t-Bu) 3 в 15 МП тетрагидрофурана при О С прибавляют по каплям при перемешивании раствор 0,467 г (0,00161 моль) 2-(3-метил 2-бутенил)-3-(5-пентилизоксазолил-3)-циклопентанона (XI) в 5 мл тетрагидрофурана. Перемешивание продолжают при ОС в течение 1 ч, реакционную смесь выливают в 50 МП воды, подкисляют 0%-ной соляной кислотой до рН 2, экстрагируют эфиром. Экстракты сушат над сульфатом магния, растворитель упаривают в вакууме, остаток хр оматографируют в колонке с силикагелем (Chemapol 40/100). Элюент - смесь эфир-гексан переменного состава.. Получают 0,444 г (94%) 2-(3-метил-2-бутенш1)-3-(5-пентилизоксазолил-3)-циклопентанола. ИК-спектр, (пленка): 1595, 3400. . Вычислено: мол., вес, 291,43. Масс-спектр: . ПМР-спектр (CDC1,,): 0,86 (СН,, т. ЗН); 1,56 (СН,, с, ЗН); 1,62 (СН,, с, ЗН); 5,10 (, н, 1Н); 5,86 (СН, с, 1Н). К раствору 0,233 г (0,0008 моль) 2-(3-метил-2-бутенил)-3-(5-пентилизоксазолил-3)-циклопентанола (XII) в 10,4 мл диоксана и 3,36 кп воды добавляют маленький, кристалл Os04.
9II
Реакционную смесь перемешивают в токе аргона до образования коричневой окраски, затем добавляют 0,442 г (0,00197 моль) метаперйодата натрия. Перемешивают в ночи, осадок отфильтровывают, растворитель удаляют в вакууме, остаток экстрагируют эфиром, пропускают через небольшой слой селикагеля (Chemapol 40/100), растворитель удаляют в вакууме. Получают 0,180 г (85%) 5л-1-окси-2р-(5-пентилизоксазолил-3)-циклопентан-1е6-ацетапьдегида (VII).
ИК-спектр, , см (пленка): 1595, 1720, 3400.
5489610
ПМР-спектр (CDCl,): 0,9-(CHj, т, ЗН); 5,8 (СН , с, 1Н); 9,76 (СНО, т, 1Н).
Преимущество предлагаемых соединений заключается в том, что их использование в синтезе простагландина ряда 11-дезокси-Р (X) позволяет повысить выход на стадии присоединения нитрометана до 88% и на стадии присоединения гептина до 70%. Выходы на указанных стадиях при использовании соединений-аналогов составляют 60 и 41% соответственно.
| А.Вагсо, S.Benetti, G.Pollini, P.Baraldi u.a | |||
| Elaboration of the W-chain of Il-deoxyprostanoid derivatives throunp isoxazole intennediates - I | |||
| Org | |||
| Chem., v | |||
| Способ изготовления звездочек для французской бороны-катка | 1922 |
|
SU46A1 |
| Гидравлические рычажные ножницы для разрезания металлических листов | 1925 |
|
SU4518A1 |
| LiNovak, G.-Baan, I.Marosfalvi, Cs | |||
| Szantay, Application of carbonyl ищю1ип§ to prostaglatidin sinthesis | |||
| III | |||
| Synthesis of ll-deoxyprostaglandln synthons - Chem | |||
| Ber | |||
| V | |||
| Способ обработки грубых шерстей на различных аппаратах для мериносовой шерсти | 1920 |
|
SU113A1 |
| Конденсационное устройство для больших количеств пара и высокого вакуума | 1925 |
|
SU2939A1 |
| A.Khusid, G.Krystal, V.Kuchetov, L.Yanovskaya | |||
| A simple syntesis of gem-dichlorocyclopropyl - and cyclopropylmethanol | |||
| Sinthesis, 1977, p | |||
| Способ получения сульфокислот из нефтяных масел | 1911 |
|
SU428A1 |
| C.Hurd, M.Pollack, The rearrangement of vinyl allyl ethers | |||
| I | |||
| Amer | |||
| Chem, Soc., 60, 1938, p | |||
| Дисковая машина для резки капусты и прочих овощей | 1924 |
|
SU1905A1 |
Авторы
Даты
1987-02-28—Публикация
1983-09-09—Подача