Данные элементного анализа: Найдено, %: С 86,i, Н 8,00. Вычислено для С,Н2.бО, %: С 86,79, Н 8,18. Индивидуальность полученного продукта подтверждена методом тонкослойной хроматографии на пластинах Silufol. Строение 2-(-фенилбензилиден)-1-ментона подтверждено ИК-спектроскопически; - l673, 1590 (в таблетках КВг). Пример 2. Получение 2-(kэтоксибензйлиден)-1-ментона. В двухгорлую колбу, снабженную Meшалкой, помещают 4 г порошкообразного едкого кали и быстро вливают раствор 17,3 мл (0.1 моль) 1-ментона и 13,г (0,1 моль) -этоксибензальдегида в 25 мл диметилсульфоксида. Реакционную смесь перемешивают в течение 20 ч при 20-25С и вливают в стакан, содержащий 500 мл ледяной воды и t мл уксусной кислоты. Выпавшее масло отделяют, водный слой экстрагируют эфиром. Эфирные вытяжки соединяют с масляным слоем, промывают водой и высушивают над сульфатом магния. Эфир отгоняют. Из полученного жидкого продукта под.вакуумом отгоняют непрореа гировавший 1-ментон. Остаток растворяют в 75 мл этанола и обрабатывают избытком насыщенного водного раствора бисульфита натрия. Осадок бисульфитного производного непрореагировав шего -этоксибензальдегида отфильтро вывают, из маточника эфиром извлекают продукт, эфирный раствор сушат над сульфатом магния. Эфир отгоняют. Полученное масло пропускают через хроматографическую колонку,, содержащую силохром С-120. В качестве элюента используют гексан. Гексановый раствор упаривают и выделяют 1,28 г кристаллического 2-(этоксибензилиден)-1-ментона (выход очищенного про дукта ,5% от теоретического). Т.пл. 60,5-62,5°С. 2-(-этоксибензилиден)1-ментон в литературе не описан. Данные элементного анализа, ; Найдено, %: С 79,4, Н 9,3. Вычислено для , %: С 79,72 Н 9,09. Индивидуальность полученного продукта подтверждена газохроматографическим анализом. Строение 2-(4-этоксибензилиден)1 ментона подтверждено ИК-спектроскопи чески: 168 ( таблетках КВг)„ . Для синтеза ОАД этого типа, содер жащих в молекуле нитрогруппу (R R-z Н; R П; NOj,) разработан вариант проведения кротоновой конденсации 1-ментона с соотт ветствующими нитрозамещенными бензальдегида в присутствии щелочного катализатора с использованием в качестве среды смесей апротоиного (диметилформамид) и гидроксилсодержащего (метанол) растворителей. Пример 3. Получение 2-(4нитробензилиден)-1-ментона. В двухгорлую колбу, снабженную мешалкой, помещают 1 г порошкообразного едкого кали и быстро вливают раствор 8,6 мл (0,05 моль) 1-ментона и 7,5б г (0,05 моль) и нитрсбензальдегида в 20 глп смеси растворителей, состоящей из Н,Ы-диметилформамида и ; метанола, взятых в соотношении А:1. Реакционную смесь охлаждают в бане с водой, поддерживая 20-25 0. Перемешивание продолжают в течение Т ч. Реакционную смесь выливают при энергичном перемешивании в АОО мл с небольшим количеством льда и 1 мл уксусной кислоты. Через 12 ч выпавший осадок отфильтровывают, промывают двумя .порциями гексана по 30 мл, затем небольшим количеством воды. Продукт высушивают в вакуум-эксикаторе и перекристаллизовывают из метанола. Получают ,45 г (выход очищенного продукта 33 от теоретического) крупных игольчатых кристаллов светло-желтого цве- , та. Т.пл. 129-130С. Данные элементного анализа. Найдено, %; N k,S Вычислено для 047 , %:N,88.. Индивидуальность полученного продукта подтверждена методом тонкослойной хроматографии на пластинках Silufol. Строение 2-(4-нитррбензилиден)-1-ментона подтверждено ИК-спектроскопически: ..(3 1б80 ,0с«с - 1б2б (в таблетках КВг). Пример k. Получение 2-(3нитробензилиден)-1-ментона. Получение и. выделение 2-(3-нитрЬбензилиден)-1-ментона аналогичны .операциям, описанным в примере 3. 2-(3 Нитробензилиден)-1-ментон представляет собой кристаллическое вещество светло-желтого цвета. Т.пл. 93,5-9tC.
Таблица 1

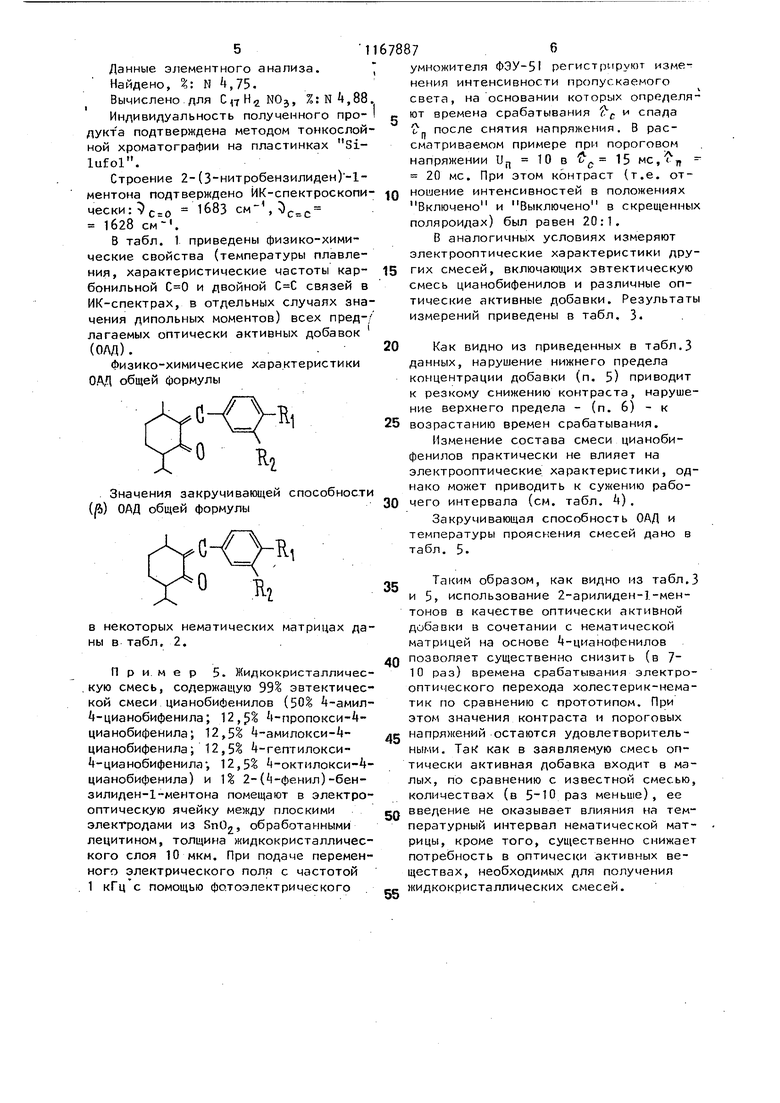
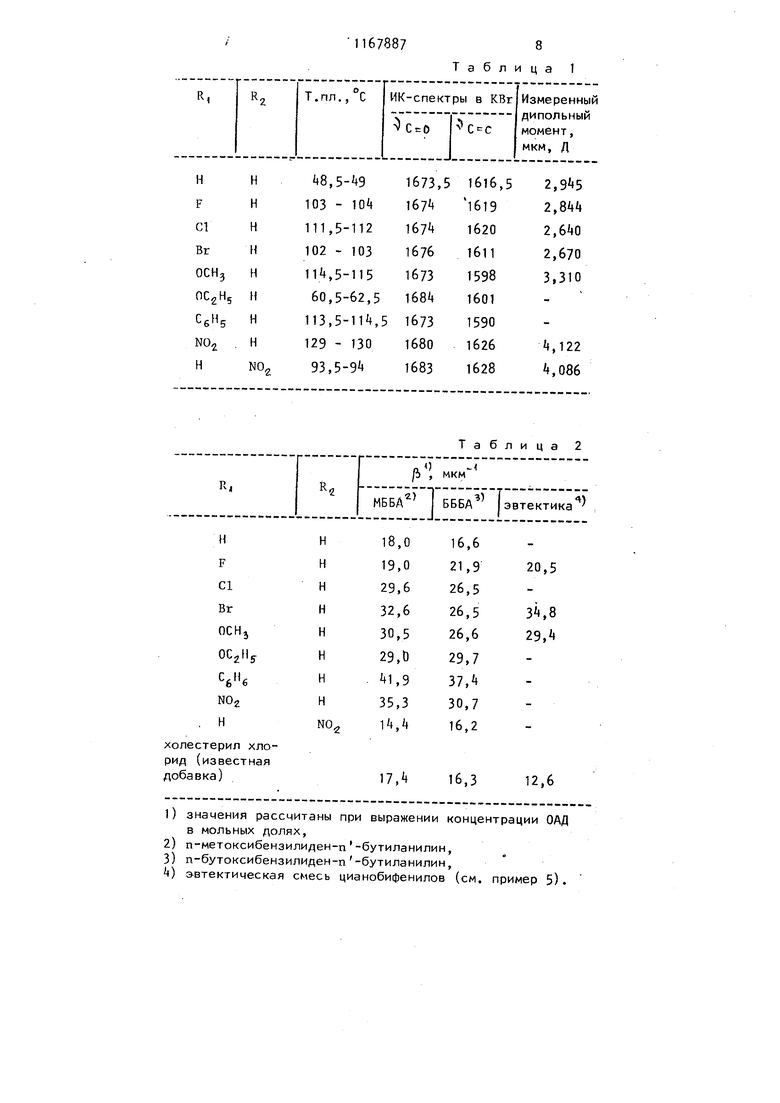
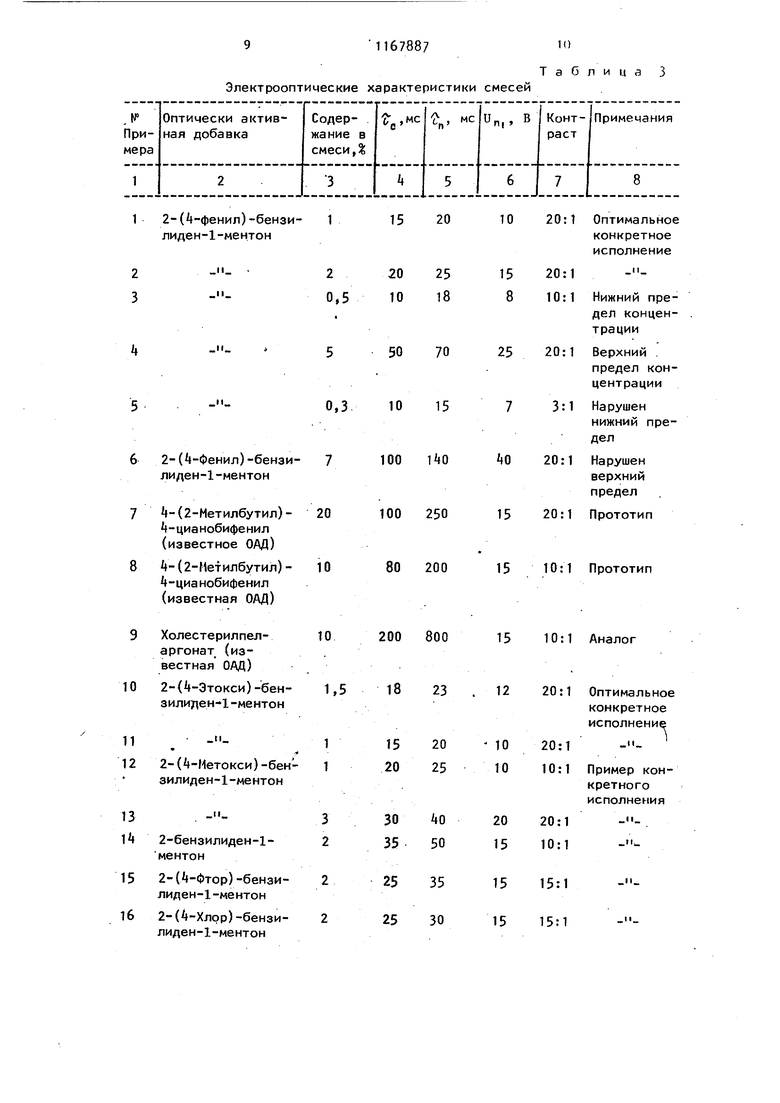
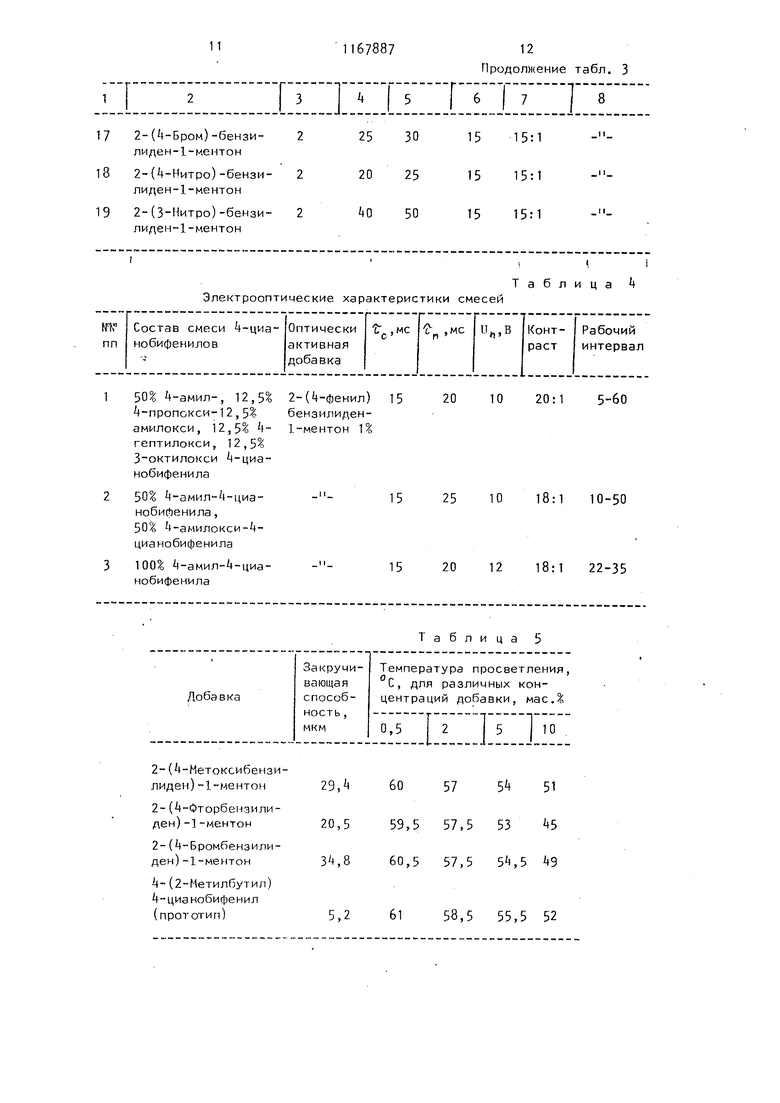

холестерил хлорид (известная добавка)
1)значения рассчитаны при выражении концентрации ОАД в мольных долях,
2)п-метоксибензилиден-п-бутиланилин,
3)п-бутоксибензилиден-п-бутиланилин,
) эвтектическая смесь цианобифенилов (см. пример 5).
Таблица 2
17,4
12,6
16,3
Электрооптические характеристики смесей
2-(А-фенил)-бензилиден-1-ментон
2 3
2-(-Фенил)-бензи6лиден-1-ментон
l- (2-Метилбутил) -цианобифенил(известное ОАД)
А-(2-Метилбутил) -цианобифенил(известная ОАД)
Холестерилпеларгонат (известная ОАД)
2-(4-Этокси)-бен0зилиден-1-ментон
|
1
2-(А-Метокси)-бен- 1 зилиден-1-ментон
2-бензилиден-1 ментон
2-(|-Фтор)-бензилиден-1-ментон
2-(4-Хлрр)-бензилиден-1-ментон
Таблица 3
15 20 10 20:1 Оптимальное
конкретное исполнение 172-(4-Бром)-бензи- 2 25 30 лиден-1-меитон 182-{ 1-Нитро)-бензи- 2 20 25 лиден-1-ментон 192-(3-Нитро)-бензи- 2 kO 50 лиден-1-ментон
Электрооптические характеристики смесей 1501 А-амил-, 12,5%2-({-фенил) -пропокси-12,5 бензилиденаммлокси, 12,5% -1-ментон ° гептилокси, 12,5% 3 октилокси 4-цианобифенила250% -амил-А-цианобифенила, 50% t-амилокси-Ацианобифенила3100% А-амил- -цианобифенила
Таблица t
Таблица 5 15 15:1 15:1 15:1 10 20:15-60 25 10 18:1 10-50 20 12 18:1 22-35
Авторы
Даты
1993-02-28—Публикация
1984-01-06—Подача