Изобретение относится к способу получения новых производных пиримидина, которые могут найти применение в синтезе биологически активных веществ.
Цель изобретения - селективный способ получения сложных эфиров (4-пиримидинилокси)уксусных кислот, .пример 1. Получение метиловых эфиров (4-пиримидиниЛокси уксусных кислот (соединение 1) и метиловых эфиров (3,4-дигидро-4-оксо-3-пиримидинил )уксусных кислот ; соединение 11),
Перемешивают при кипячении 0,1 мбль соответствующего 4-гидроксипиримидина и эквимолекулярное количество метилата натрия в метаноле, Затем по каплям прибавляют 18,4 г (0,12 моль I метилового эфира бромуксусной кислоты. Смесь кипятят до нейтральной реакции (3-4 ч ). Растворитель удаляют в вакууме. После охладения остаток обрабатывают водой для удаления бромида натрия и сушат, Продукты разделяют с помощью хроматографии на колонке, используя в качестве адсорбента силикагель, а в качестве элюента - смесь хлороформ: этиладетат (5:). ,
Пример 2, Получение этило вого эфира (б-метш1-2-метш1тйо-4-пиримидинилокси )уксусной кислоты и этиловый эфир (3,4-дигидро-6-метил-2-метилтио-4-оксо-3-пиримидинш1 уксусной кислоты.
в условиях, аналогичных примеру 1, из г (0,1 моль) 4-гидрокси-6-метил-2-метилтиопиримидина, 6,8 г (0,1 моль) этилата натрия в этаноле, 18,4 г (0,12 моль ) метилового эфира бромуксусной кислоты получают этиловьй эфир (б-метил-2-метилтио-4-пиримидинилокси)уксусной кислоты и этиловый эфир (3,4-дигидро-6-ме тил-2-метилтио-4-оксо-З-пиримидиншт) уксусной кислоты. Выходы 7,3 г (30%) и 6,1 г С25%), Т.Ш1. 52-53 и 72-73с найдено N 11,34 и 11,73%, вычислено N 11,56%, УФ Л„о(кс253 и 291 нм соответственно. .
I
Пример 3. Получение метиловых эфиров 4-пиримидинилокси уксусных кислот (соединение 1 ).
К суспензии 0,1 моль соответствующего 4-гидроксипиримидина, 3,2 г (о,01 моль ) тетрабутиламмонийбромида
в 40 мл триэтиламина, перемешиваемой в случае соединения I , при 0-10 С, а в случае соединений I «-г- при 50-60°С, прибавляют по каплям 18,4 г (0,12 моль) метилового эфира бромуксусной кислоты и перемешивают при указанной температуре в случае соединений I д ,е 34, а в случае соединений 1 «- г - 5 мин. После этого смесь охлаждают и разбавляют 1,5 л воды. Выделившийся кри таллический (Ге , жидкий) продукт отфильтровывают (в случае соединения Г е отделяют), промывают водой (в сл чае 1 -растворяют в эфире, сушат хлористым кальцием, эфир отгоняют) И перекристаллизовывают из гексана (в случае соединения Г е перегоняют в вакууме).
Пример 4, Получение метилового эфира (б-метш1-2-метилтио-4-пиримидинилокси уксусной кислоты (16)
К перемешиваемой при 60°С суспензии ISj.6 г (0,1 моль 4-гидрокси-6-метил-2-метилтиопиримидина в 40 мл триэтйламина прибавляют по каплям 18,4 г (0,12 моль) метилового эфира бромуксусной кислоты и перемешивают при указанной температуре, 3ч. Вьщеляют метиловый эфир (б-метил-2-метилтио-4-пиримидинилокси)уксусной кислоты аналогично примеру 3. Выход 7,3 г 32% .
Пример 5. Получение метилового эфира (б-метил-2-этилтио-4-пиримидинилокси)уксусной кислоты
(1 В) .
в условиях ,аналогичных примеру 3, из 17,1 г (0,1 моль) 4-гидрокси-б-метил-2-этилтиопиримидина, 1,64 г (0,002 моль) тетрабутиламмонийбромида и 18,4 г (0,12 моль) метилового эфира бромуксусной кислоты в 40 мл триэтйламина получают метиловый эфир (6-метил-2-этилтио-4-пиримидинилокси)уксусной кислоты. Выход 13,9 г (57%).
Пример 6. Получение метилового эфира (б-метил-2-этилтио-4пиримидинилокси)уксусной кислоты
(16) .
Из 17,1 г (о,1 моль) 4-гидрокси--6-метил-2-этилтиопиримидина, 6,4 г (0,02 моль) тeтpaбyтилa rмoний бромида и 18,4 г (0,12 моль) метилового эфира бромуксусной кислоты в 40 мл триэтйламина в условиях примера 3 получают метиловый эфир (6-метил-2-этилтио-4 - пиримидинилокси) уксусной кислоты. Выход 19,4 г (8(Г%)
Пример 7. Получение метилового эфира (2-бензш1Тио-6-метил-4-пиримидинилокси)уксусной кислоты (it).
Из 23,2 г (0,1 моль) 2-6ензилтио-4-гидрокси-6-метилпиримидина, 3,2 г (0,01 моль) тетрабутиламмонийбромида и 15,3 г (О,1 моль) метилового эфира бромуксусной кислоты в 40 мл триэтиламина в условиях примера 3 получают метиловый эфир (2-бензилтио-6-метил-4-пиримидинилокси)уксусной кислоты. Выход 11,6 г (38% ).
Пример 8. Метиловый эфир (2-б-ензилтио-6-метил-4-пиримидинилокси)уксусной кислоты (1 г) получают аналогично примеру 3 из 23,2 г (0,1 моль) 2-бензилтио-4-гидрокси-6-метилпиримидина, 3,2 г (0,01 моль тетрабутиламмонийбромида и 30,6 г (0,2 моль ) метилового эфира бромуксусной кислоты в 40 мл триэтиламина. Выход 20,1 г (66% )i
Пример 9. Метиловый эфир (6-метил-2-этилтио-4-пиримидинилокси)уксусной кислоты (,1 В ) получают аналогично примеру 3 из 17,1 г (0,1 моль) 4-гидрокси-6-метил-2-этитиопиримидина, 3,2 г (0,01 моль) тетрабутиламмонийбромида и 13,0 г (0,12 моль) метилового эфира хлоруксусной кислоты в 40 мл триэтиламина.Выход 18,2 г (75%).
Пример 10. Получение метилового эфира (6-метил-2-метилтио-5-этил-4-пиримидинилокси)уксусной кислоты (1 Э ) и метилового эфира Сз,4-дигидро-6-метил-2-метилтио-4-оксо-5-этил-З-пиримидинил )уксусной кислоты ( 1 1 (3 ) .
Из 18,4 г (0,1 моль) 4-гидрокси-6-метил-2-метилтио-5-этилпиримидина, 3,2 г (0,01 моль) тетрабутиламмонийбромида и 18,4 г (0,12 моль) метилового эфира бромуксусной кислоты в 40 мл триэтиламина, перемешивая 3 ч при , получают метиловый эфир (6-метил-2-метилтио-5-этил-4-пиримидинилокси)уксусной кислоты и метиловый эфир (3,4-дигидро-6-метш-2-метилтио-4-оксо-5-этил-3-пири- . мидинил)уксусной кислоты вьщеляют по примеру 1 ), Выходы 15,4 г (60%) и 2,3 г (9%) соответственно ,
Пример 11. Получение метилового эфира (2-бензилтио-6-метил-4-пиримидинилокси)уксусной кислоты (1) и метилового эфира (2-бензилтио-3,4-дигидро-6-метил-4-оксо-3-пиримидиншт)уксусной кислоты (Иг).
Из 23,2 г (0,1 моль) 2-бензилтио-4-гидрокси-6--метилпиримидина, 3,2 г (0,01 моль) тетрабутиламмонийбромида и 18,4 г (0,12 моль) метилового эфира бромуксусной кислоты в 40 нп триэтиламина при 70°С в условиях примера 3 получают метиловый эфир (2-бензилтио-6-метил-4-пиримидинилокси)уксусной кислоты и метиловый эфир (2-бензилтио-З,4-дигидро-6-метил-4-оксо-3-пиримидинил)уксусной кислоты (выделяют ПО примеру 1). Выходы 17,3 г (57%) и 2,4 г (8%) соответственно.
В табл.1 приведены данные синтезов метиловых ;эфиров (4-пиримидинилокси)уксусных кислот (1) и метиловых эфиров (3,4-дигидро-4-оксо-3-пиримидинил)уксусных кислот (П).
в табл.2 приведены данные УФ- и н-ЯМР-спектров метиловых эфиров (4-пиримидинилокси)уксусных кислот (1) и метиловых эфиров (3,4-дигидро-4-оксо-З-пиримидинил)уксусных кислот (П), при этом все Н-ЯМР-спектры сняты в CFgCOOH.
я я
X
ч «)
л и
Соединение Н-ЯМР-спектр относительно
гексаметилдисилоксана, сЛ, м,д. 2,25(SCH, ЗН, с) 3,45(OCHj, ЗН, с) 4,83(ОСН2, 2Н, с) 6,58(5-Н, 1Н, д-J 7 Гц) 7,95(6-Н, Ш, д-J 7 Гц) 2,14(CHj, ЗН, с) 2,21(SCHj, ЗН, с) 3,41(OCHj, ЗН, с) 4,79(ОСНг, 2Н, с) 6,38(5-Н, 1Н, с) 0,98(2-СНз, ЗН, т - J 7 Г 2,13(6-СНз, ЗН, j:) 2,85(SCH, 2Н, к - J 7 Гц 3,45(ОСН, ЗН, с) 4,78(ОСН, 2Н, с) 6,34(5-Н, Ш, с) 2,18(CHj, ЗН,:с) . 3,43(OCHj, ЗН, с) 4,10(SCHj, 2Н, с) 4,73(ОСН, 2Н, с) 6,38(5-Н, 1Н, с) 6,88(, 5Н, с) 0,78(5-CHj, ЗН,-т - J « 7 2,18(б-СН, ЗН, с) 2,20(СН, 2Н, к - J 7Г)
Таблица 2
УФ-спектр в этаноле
Ig
.ксИ
Мин 04 52 204 256 204 254 203
н-да -спектр относйтельно
Соединение гексаматилдисилоксана, (, м.д.
2,21(5СНз, З.Н, с)
3,46(ОСНз, ЗН, с)
4,85(OCHi, 2Н, с)
0,90С(СНз)2С, 6Н, 6Н, Mj
c
0,90(2-СНз, ЗН, т- J 8 Гц)
2,18(б-СНд. ЗН, с)
2,80(СН, 1Н, м)
2,80(SCH, 2Н, к -J 8 Гц)
3.46(OCHj, ЗН, с)
4,82(OCHj, 2Н, с)
2,58(ЗСНз, ЗН, с)
и
3.47(ОСНз, ЗН, с) 4,66(НСН-,, 2Н, с)
6,28(5-Н, 1Н,д - J 8 Гц)
7,51(6-Н, 1Н,д - J 8 Гц)
2,2(СНз, ЗН, с)
Б
2,63 (SCHj, ЗН, с)
3,1(OCHj, ЗН, с)
4,72(NCHj, 2Н, с)
р,15(5-Н, 1Н, с)
1,07(2-СНз, ЗН, т - J - 8 Гц)
ie
2,06(б-СН,, ЗН, с)
3,31(SCH, 2Н, к - J - 8 Гц)
3,47(ОСН, ЗН, с)
4,69(NCHj, 2Н, с)
6,09(5-Н, 1Н, с)
Продолжение табл.2
учн-спектр в этаноле
Ig f
.нм
МИН.
.a..i.
204
3,96 254
4,24
2243,73
240 (плечо)
2923,89
2263,71
241 (плечо)
2903,88
2263,74
240 (плечо)
2923,95

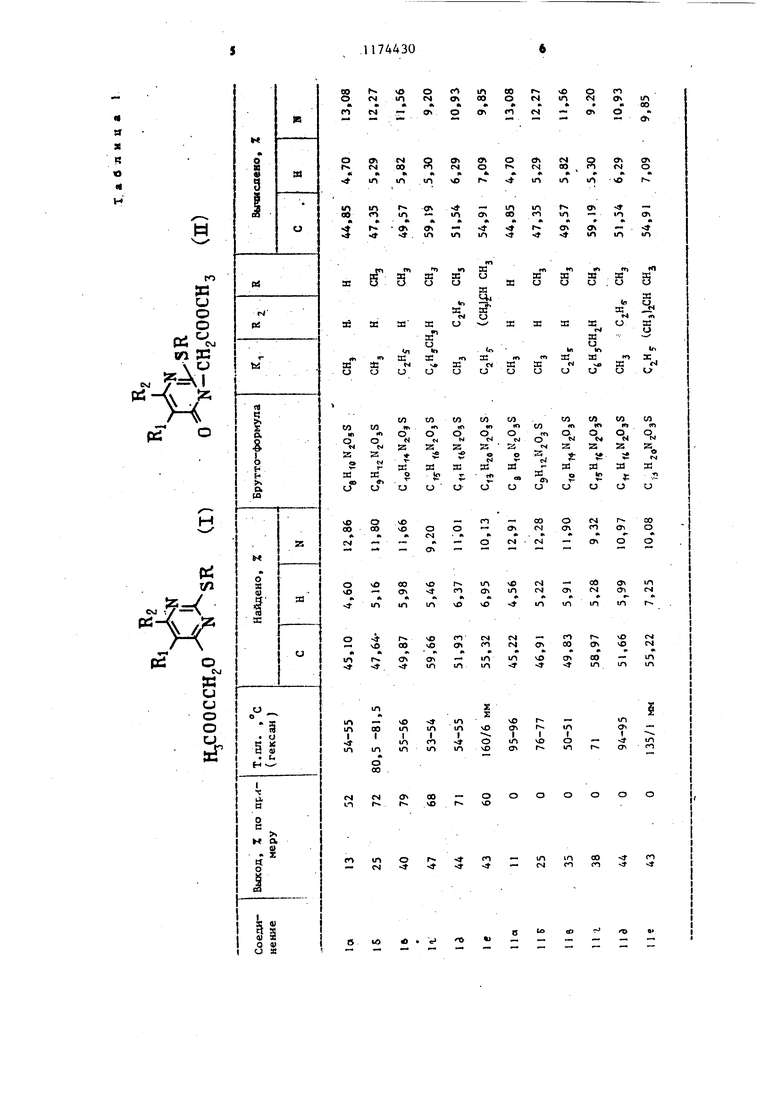
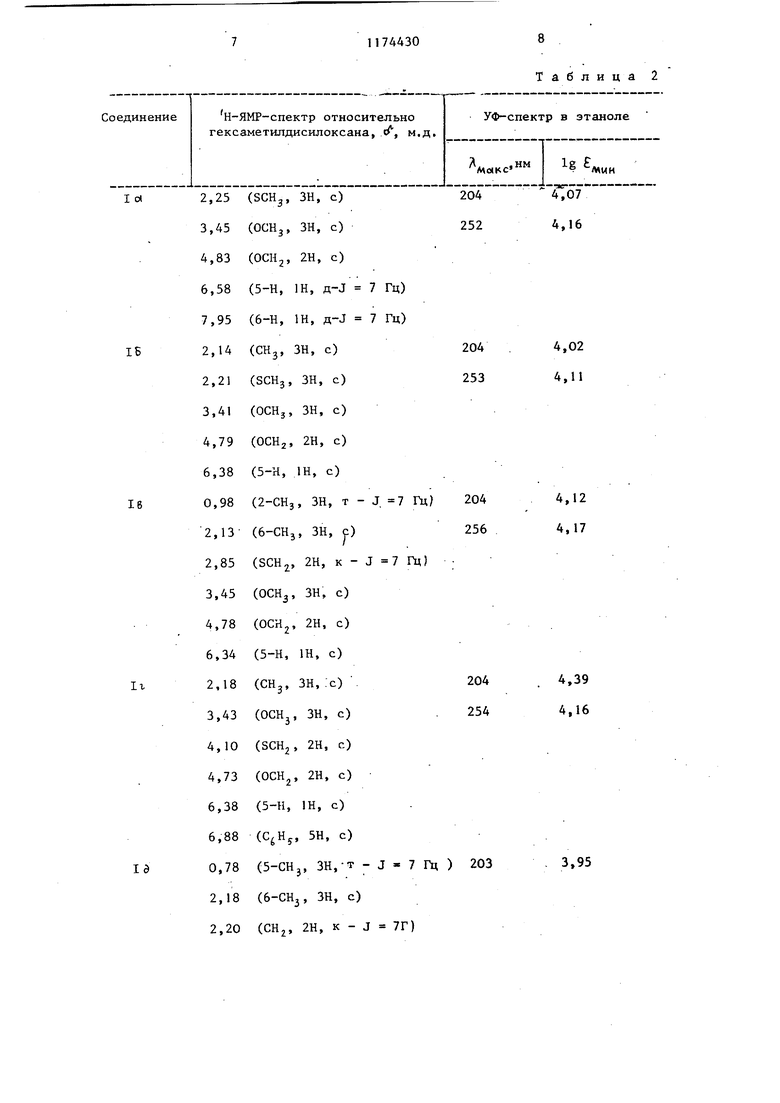


1. СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВЫХ ЭФИРОВ С2-АЛКШ1САРАЛКШ1)ТИО-4-ПИРИМИДИНИЛОКСИЗУКСУСНЫХ кислот- общей формулыR IY HjCOOCCHpCrSf SR где R - метил, этил или бензилj R - водород, этил или изопропил; Е.2 водород, или метил, отличающийся тем, что соответствующий 4-гидроксипиримидин подвергают взаимодействию с метиловым эфиром галогенуксусньпс кислот общей формулы ХСН СООСНд где X - бром или хлор, в триэтиламине в присутствии тетрабутиламмонийбромида. 2. Способ по п. 1, о т л и ч а ющ и и с я тем, что процесс проводят при молярном соотношении 4-гид(Л роксипиримидина,метилового эфира га логеноуксусной кислоты и тетрабутиламмонийбромида 1:1,2:0,1. со
| Вайнилавичюс П.И | |||
| и др | |||
| Синтез и сцинтилляционные свойства 0-гидразонов на основе 4-метил-2-тиоурадила | |||
| - Науч.труды вузов ЛитССР, Химия и хин.техн, 1972, т | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Способ приготовления строительного изолирующего материала | 1923 |
|
SU137A1 |
Авторы
Даты
1985-08-23—Публикация
1984-03-29—Подача