H2N--C-1SHв ацетоне при температуре кипения реакционной смеси с вьщелением целевого продукта в свободном виде или в виде кристаллической бромистоводородной соли.
2, Способ получения ацетилимидазола формулы Ш
н
N0 Y).
СНз
где R - группа формулы NHR2 или
NR3R4;
lRJ()-aлкил, (С4-С5)-пиридилалкил или (Ст-Ц)-фенилалкил, возможно замещенный хлором;
1195907
Rj и R - каждый независимо - ()-алкил
или взятые вместе с атомом азота, к которому они присоединены, образуют пиррспидиновое, пиперидиновое или морфолиновое кольцо, отличающ и я тем , что оксазол формулы //
N
. H.,N 0 5
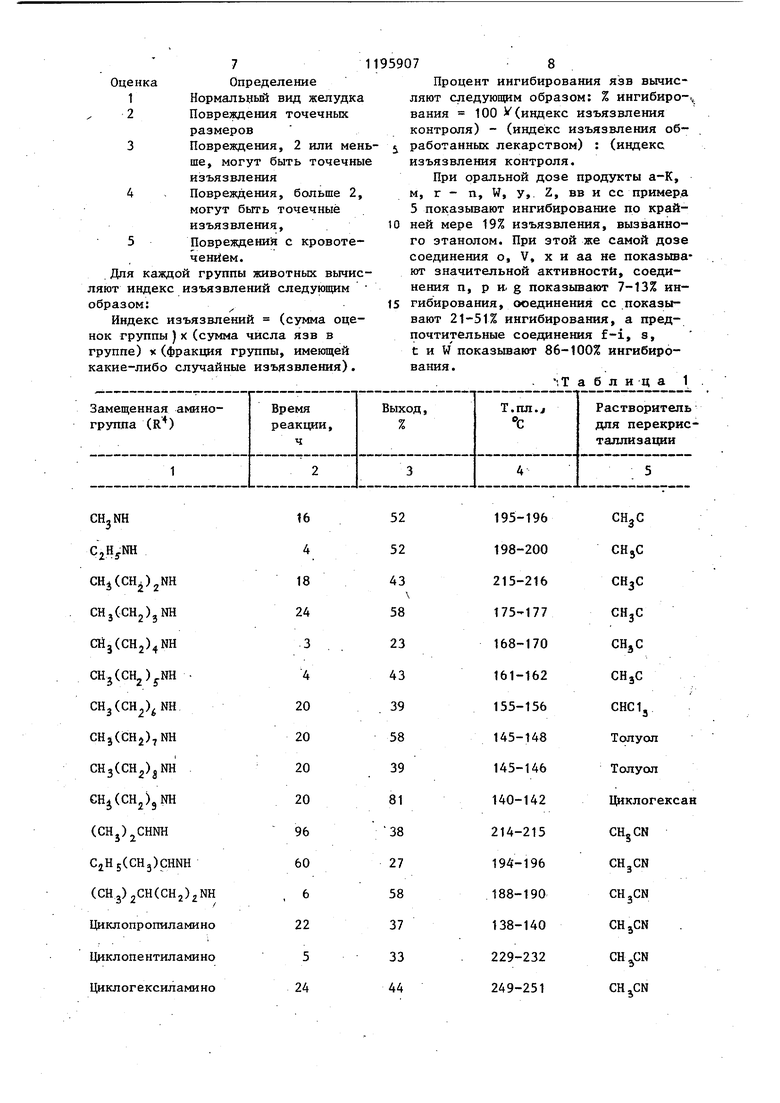
подвергают взаимодействию с избытком амина формулы
HjNR2 или HNRgR
в воде или а смеси воды и изопропанола при температуре кипения реакционной смеси с вьщелением целевого продукта.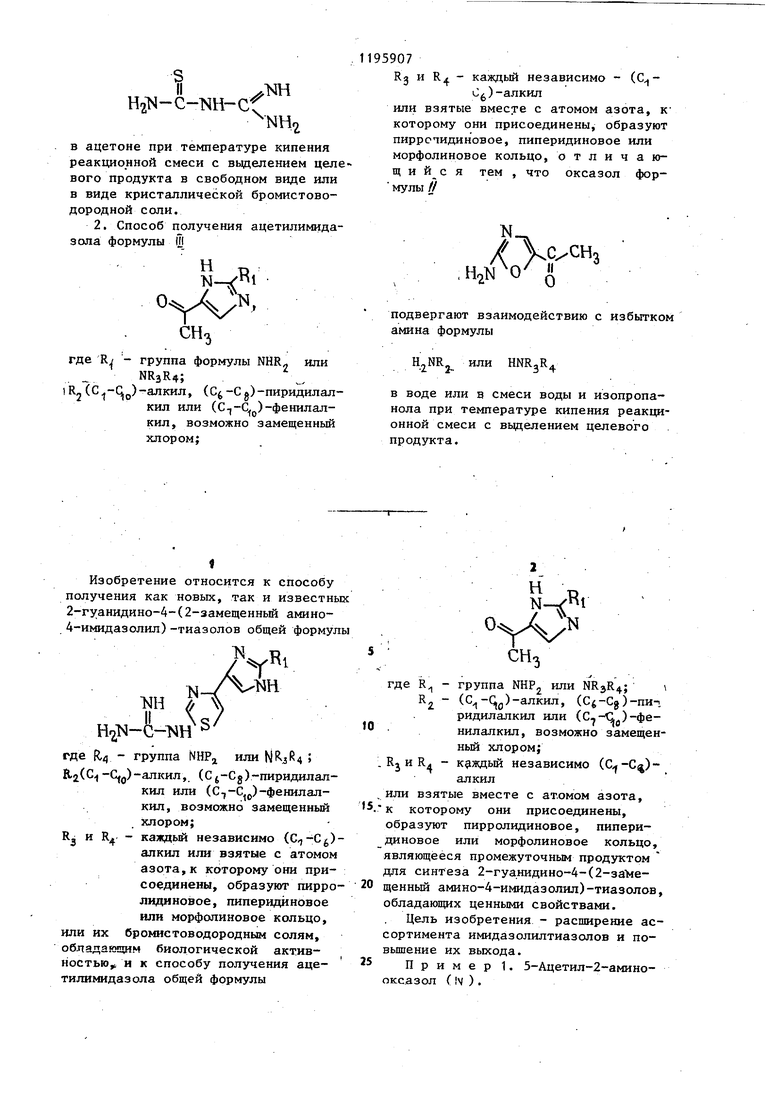







1. Способ получения 2-гуанидино-4-

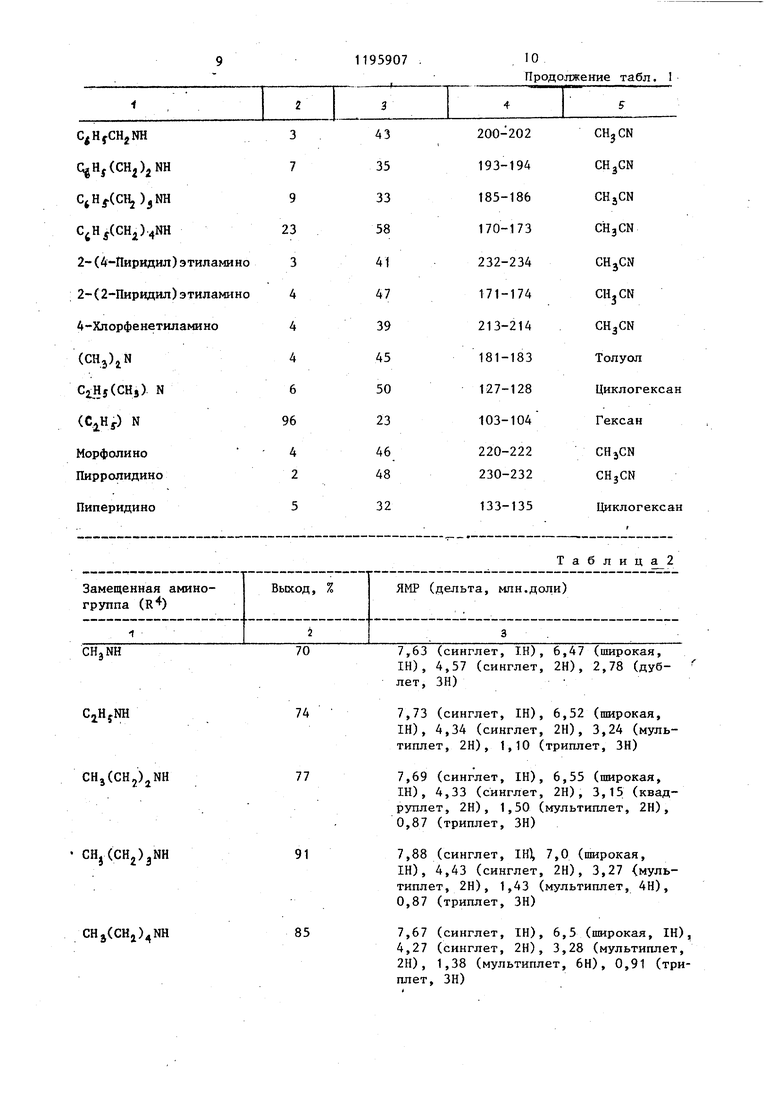
Изобретение относится к способу получения как новых, так и известных 2-гуанидино-4-(2-замещенный амино4-имидазолил)-тиазолов общей формулы
N.
/V
,/VKH
л
{
NH
NS/
H N-С- 1Н
где R/5 - группа NHPj или 5 К(С -C)-алкал, (С4-Сд)-пиридилалкил или (С-,)-фенилалкил, возможно замещенный хпором;
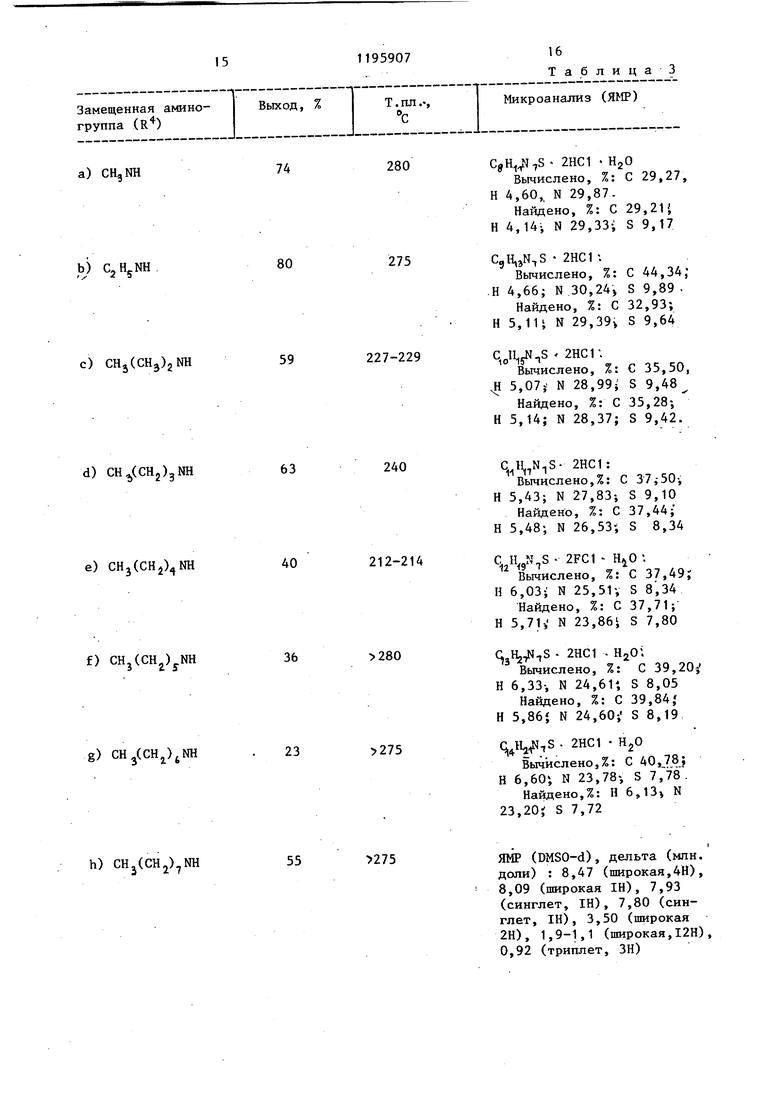
Rj и R - каждьй независимо ()алкил или взятые с атомом азота,к которому они присоединены, образуют пирролидиновое, пиперидиновое или морфолиновое кольцо, или их бромистоводородным солям, обладающим биологической активностью и к способу получения ацетилимидазола общей формулы
2
Н NRt
/
X .N
CHr
где R - группа NHP или NRsR.; R - ()-алкшт, (С4-С8)-пи-1 ридилалкил или (C--G )-фенилалкил, возможно замещенный хлором; . RJи R - каждый независимо ()алкил
, или взятые вместе с атомом азота, к которому они присоединены, образуют пирролидиновое, пиперидиновое или морфолиновое кольцо, являющееся промежуточным продуктом для синтеза 2-гуанидино-4-(2-за 1ещенный амино-4-имидазолил)-тиазолов, обладающих ценными свойствами.
Цель изобретения - расширение ассортимента имидазолилтиазолов и повьшение их выхода.
Пример 1. 5-Ацетил-2-аминооксазол ( IV ) . Смесь 132,2 г (0,80 моль) 2-бром 1-окси-3-оксо-1-бутена, 120,1 г (2,0 моль) мочевины и 1,85 л ацетона кипятят с обратным холодильником при верхнем перемешивании в течение 1 ч. Смесь концентрируют и масляный остаток обрабатывают 600 мл воды, затем подщелачивают концентрированной гидроокисью аммония. После пере мешивания при комнатной температуре в течение 0,5 ч образуется осадок. Его собирают и сушат в вакууме, получают 61,1 г сырого продукта.Фильт рат Снова концентрируют и маслянис тый. осадок обрабатывают 50 мп воды снова подщелачивают концентрированной гидроокисью аммония. После выстаивания в течение ночи вьщеляют второй сбор сырого продукта в количестве 17,6 г. Оба сбора объединяют и перекристаллизовывают из метанола получают 50,3 г (50%) 5-ацетил-2аминооксазола, т.пл. 214-215 С. И р и м е р 2. Общая процедура д 2-замещенных-амин з-5-ацетш1имидазолов (V). Смесь 2,0 г (16 ммоль) 5-ацетил2-аминооксазола, 20 мл соответствую щего амина и 30 мл воды кипятят с обратным холодильником в течение 396 ч (в случае некоторых липофильных аминов необходимо добавлять изо пропанол для получения гомогенной реакционной смеси). Смесь концентрируют (при необходимости отгоняют для удаления всех следов амина), а остаток затем хроматографируют на 60 г силикагеля, используя в качест ве элюента смесь 4:1 этилацетат/гек сан. Сразу, как только элюируется весь менее полярный материал (пиримидиновый побочньй продукт), колонк злюируют смесью 9:1 хлороформ/метанол для того, чтобы получить более полярный имидазольный продукт. Аналитически чистый имидазол получают при перекристаллизации из подходяще го растворителя. Таким образом,полу чают 2-замещенные амино-5-ацетилими дазолы, представленные в табл. 1. И р и м е р 3..Общая процедура для 2-замещенных амино-5-(2-бромацетил)-имидазолов (VI). Раствор 1,0 г подходящего кетона в 25 мл концентрированной бромистрводородной кислоты перемешивают при комнатной температуре и прибавляют по каплям 5%-ный молярный избыток брома по каплям в течение 2 мин. Затем смесь нагревают при 80°С (внешний нагрев) в течение 1 ч, за это время окраска, придаваемая бромом,исчезает. Смесь охлаждают, затем концентрируют. Осадок тщательно растирают с. насьш5енным раствором бикар- .боната натрия и собирают осадок, образовавшийся в этой основной среде, промывают его водой, атем сушат в вакууме и получают 2-амино-5(2-бромацетил) имидазолы (см.табл.2) в виде твердых продуктов, котоые охарактеризованы ЯМР-спктрами в ДМСр-dt. П р и м е р 4. Общая процедура для 2-гуанидино-4-(2-замещенный амино-4-имидазолил)-тиазол гидробромидов ( Ш.Вг). Смесь 1 г бромацетилимидазола примера 3, зквимолярного количества амидинотиомочевины и 50 мп ацетона кипятят с обратным холодильником в течение 1 ч, за это время продукт осаждается в виде его монобромистоводородной соли. Этот твердый продукт собирают, промывают ацетоном и сушат в вакууме. Затем его превращают в его дихлоргидрат, как описано в примере 5. П р и м е р 5. Общая процедура для получения дихлоргидратов-2-гуанидино-4-(2-замещенный амино-4-имидазолил)-тиазолов (Щ(НС1)). Бромистоводородную соль перемешивают в 50 мл насьш1енного раствора бикарбоната натрия в течение 1530 мин. Твердый продукт в виде свободного основания собирают, промывают водой, затем сушат в вакууме. Этот твердый продукт растворяют в минимальном количестве метанола. Метанольный раствор насьш ают газообразным НС1, затем медленно разбавляют эфиром. Собирают полученный осадок, промьтают эфиром, затем сушат в , получают дихлоргидрат, которьш характеризуют элементным анализом (сожжение) и/или спектральными данными. Выход дихлоргидрата, полз енного по примерам 4-5, результаты его элементного анализа и/или спектральные данные приведены в табл. 3. П р и м е р 6. Антисекреторная ктивность к вьщелению желудочного
S
Антисекреторная активность к выделению желудочного сока соединений изобретения была определена на некормленных в течение ночи и находящихся в сознании сумчатых собаках Хейденхайна. Пентагастрин (Пентаволон-Айерст) используют для стимуляции вьщеления кислоты при непрерывной инфузии в поверхностную ножную вену заранее определенными дозами, чтобы стимулировать близкое к максимальному вьщелению желудочного сока из жедудочного мешка. Желудочный сок собирают с интервалами 30.мин от начала инфузии пентагастрина и измеряют с точностью до 0,1 мл. За время эксперимента делают 10 сборов у каждой собаки. Концентрацию кислоты определяют титрованием 1,0 МП желудочного сока до рН 7,4 0,1 N гидроокисью натрия, используя автоматическую бюретку и рН-метр со стеклянным электродом (Радометр).
Лекарство или носитель вводят внутривенно через 90 мин после начала инфузий пентагастрина в дозе 1 мг/кг или менее. Антисекреторное действие на выделение желудочного сока вычисляют при сравнении самого низкого выделения сока после введения лекарства со средним вьщелением сока непосредственно перед введением лекарства.
Продукты h,, п, г, и ее примера 3 в дозе 1 мг/кг ингибируют желудочную секрецию по крайней мере на 21% Предпочтительные продукты f - h и W ингибируют желудочную секрецию по крайней мере на 97% при такой же или меньшей дозе. При дозе 3 мг/кг соединение дает 42% ингибирования. При дозе 0,1 мг/кг соединение ее дает 72% ингибирования.
Пример 7. Hj-Антагонистическая активность по отношению к гистамину.
Ня-Антагонистическую активност.ь по отношению к гистамину соединений изобретения определяют следующим образом.
Морских свинок быстро убивают ударом по голове, извлекают сердце и правое предсердие рассекают. Предсердие суспендируют изотермически в 10 мл тканевой ванны с контролируемой температурой (32+2 С),содержащей оксигенированный (95% Oi, 5%
959076
СО) буфер Кребса-Хензелейта (рН 7,4) дают стабилизироваться в течение приблизительно 1 ч, в течение этого времени тканевую ванну несколько раз 5 промьзают сильным напором струи. Индивидуальные сокращения предсердия следуют за перемещаемым под действием силы трансдуктором, соединенным с кардиотахометром и регистрирующим О полиграфом Грасса. После получения кривой доза-ответ для гистамина ванну, содержащую каждое предсердие, несколько раз промывают сильной струей свежего буфера, и предсердие сно5 ва уравновешивается до основной интенсивности. После возвращения к основной интенсивности прибавляют испытуемые соединения в выбранных конечных концентрациях и снова определяют кривую доза гистамина-ответ в присутствии антагониста. Результаты выражены как доза-соотношение концентраций гистамина, требуемых для получения половины максимального стимулирования в присутствии и в отсутствие антагониста, и кажущаяся константа диссоциации Н -рецептора антагониста рЛ2 определена.
Продукты а- t, п, ои§-вв примера 5 величины pAj по крайней мере 5,9. Предпочтительные продукты f, i, п, S, t и W дают рА 7,0 и выше.
П р и м е р 8. Ингибирование вызванных этанолом язв у крыс.
5 Противоязвенная активность продуктов изобретения также быпа определена при испытании на язве, вызванной этанолом, у крысы. В этом испытании некормленным в течение ночи
0 крысам дают лекарство (5 мг/кг) или воду орально за 15 мин до орального введения дозы абсолютного этанола (1,0 мл). Час спустя после введения этанола животных убивают и желудки
5 исследуют на наличие повреждений. После умерщвления вскрывают брюшную полость, помещают в пилорус запирающий гемостат. Инжектируют 6 мл 4%-ного раствора формальдегида в желудок
0 с желудочной питающей трубкой и используют второй запирающий гемостат для закрытия пищевода. Желудок удаляют, открывают вдоль наибольшей кривизны и исследуют на изъязвление.
Система оценки, использованная для количества повреждений, вызванных этанолом, следующая: 7 Оценка Определение 1Нормальный вид желудка 2Повреждения точечных размеров 3Повреждения, 2 или мен ше, могут быть точечны изъязвления 4- Повреждения, больше 2, могут быть точечные изъязвления, 5Повреждений с кровотечением. Для каждой группы животных вычис ляют индекс изъязвлений следующим образом: Индекс изъязвлений (сумма оценок группы ) X (cjTMMa числа язв в группе) X(фракция группы, имеющей какие-либо случайные изъязвления).
CHjNH
CHj(CH,)2NH
СНз(СН2)зШ
Cti3(CH2)4NH
ск(СЕ)т
CE(
СН()Н
CE.)Ntt
CHj(CH2)gNH
(CHj)CHNH
С2Н5(СНз)СНЫН
(СНз)2СН(СН2)2МН
Циклопропиламино
Циклопентиламино
Циклогексиламино 78 Процент ингибирования язв вычисляют следуюпщм образом: % ингибиро-ч, вания 100 V(индекс изъязвления контроля) - (индекс изъязвления обработанных лекарством) : (индекс изъязвления контроля. При оральной дозе продукты а-К, м, г - п, W, у, Z, вв и ее пример.а 5 показывают ингибирование по крайней мере 19% изъязвления, вызванного этанолом. При этой же самой дозе соединения о, V, х и аа не показывают значительной активности, соединения п, р и. g показывают 7-13% ингибирования, ооединения ее показывают 21-51% ингибирования, а предпочтительные соединения f-i, s, t и W показывают 86-100% ингибирования . ,Т а б л и ц а 1
CHjCCHp NH
91
CHj(CHj)NH
85
IH), 4,33 (синглет, 2H), 3,15 (квадруплет, 2Н), 1,50 (мультиплет, 2Н), 0,87 (триплет, ЗН)
7,88 (синглет, 1Н 7,0 (широкая, IH), 4,43 (синглет, 2Н), 3,27 (мультиплет, 2Н), 1,43 (мультиплет, 4Н), 0,87 (триплет, ЗН)
7,67 (синглет, IH), 6,5 (широкая, IH), 4,27 (синглет, 2Н), 3,28 (мультиплет, 2Н), 1,38 (мультиплет, 6Н), 0,91 (триплет, ЗН)
11
Выход,
Замещенная аминогруппа (R)
CHjCCH -NH
75
СН j(CH2)iNH
97
СНз(СН),Ш
98
CHgCCH gNH
90
СНз(СН2)эКН
99
:CH3)iCHNH
63
C,H5j(CHj)CHNH
60
(СНэ)оСН(СН,)1Ш
80
45
Циклопропиламино
81
Циклoneнтиламино
83
Циклогексиламино
92
12
1195907 Продолжение табл.2
ЯМР (дельта, млн. доли)
7,65 (синглет, IH), 6,5 (широкая, IH), 4,32 (синглет, 2Н), 3,17 (мультшшет, 2Н), 1,31 (мультиш1ет,8Н), 0,83 (триЗН)
плет,
8,23 (синглет, IH), 4,56 (синглет, 2Н), 3,30 (мультиплет, 2Н), 1,21 (широкий синглет, ЮН), 0,80 (триплет, ЗН)
8,06 (синглет, IH), 4,46 (синглет, 2Н), 3,20 (широкая, 2Н), 1,26 (широкий синглет 16Н), 0,80 (триплет,ЗН)
7,75 (синглет, IH), 6,43 (широкий дублет, IH), 4,38 (синглет, 2Н), 3,90 (мультиплет, IH), 1,19 (дублет, 6Н)
7,50 (синглет, IH), 5,4 (широкая, IH 4,11 (синглет, 2Н), 3,75 (мультиплет 2н), 1,48 (мультиплет, 2Н), 1,2 (дyблет, ЗН), 0,90 (триплет, ЗН)
7,87 (синглет, IH), 6,9 (широкая, IH), 4,42 (синглет, 2Н), 3,28 (мультиплет, 2Н), 1,9-1,3 (мультиплет, ЗН), 0,92 (дублет, 6Н)
7,97 (синглет, IH), 7,0 (широкая, IH), 4,46 (синглет, 2Н), 4,1 (широкая, IH), 2,0-1,4 (широкая, 8Н)
7,87 (синглет, IH), 6,9 (широкая, IH), 4,42 (синглет, 2Н), 3,5 (широкая, IH), 2,0-1,0 (мультиплет, ЮН)
(CH2)NH
84
C(iif(cH)m
76
C(,l{(CE2)m
75
2-(4-Пиридил)91этиламино
2-(2-Пиридил)
94 этиламино
4-Хлорфенетил100амино
(
53
60
62
100
47
71
7,73 (синглет, IH), 7,23 (синглет, 5Н), 6,63 (широкая, IH), 4,36 (синглет,2Н), 3,42 (триплет, 2Н), 2,80 (триплет, 2Н)
7,67 (синглет, IH), 7,20 (синглет, 5Н), 6,64 (широкая, IH), 4,37 (синглет, 2Н), 3,18 (триплет, 2Н), 2,60 (триплет, 2Н), 1,83 (мультиплет, 2Н)
7,79 (синглет. III), 7,37 (синглет, 5Н), 6,77 (широкая, IH),, 4,42 (сииглет, 2Н), 3,33 (мультиплет, 2Н), 1,9-1,6 (мультиплет, 6Н)
8,45 (дублет, 2Н), 7,72 (синглет, IH), 7,23 (дублет, IH), 6,6 (широкая, IH), 4,38 (синглет, 2Н), 3,56 (мультиплет, 2Н), 2,85 (триплет, 2Н)
8,43 (дублет, IH), 7,951-7,6 (синглет и мультиплет, 2Н), 7,4-7,2 (мультиплет, 2Н), 6,75 (широкая, IH), 4,34 (синглет, 2Н), 3,60 (мультиплет, 2Н), 2,97 (триплет, 2Н)
(СС1) - 7,64 (синглет, IH), 4,13 (синглет, 2Н), 3,20 (синглет, 6Н)
7,63 (синглет, IH), 4,23 (синглет, 2Н), 3,29 (квадруплет, 2Н), 2,86 (синглет, ЗН), 0,93 (триплет, ЗН)
7,87 (синглет, .IH), 4,42 (синглет, 2Н),,3,50 (квадруплет , 4Н), 1,13 (триплет, 6Н)
7,83 (синглет, IH), 4,41 (синглет, 2Н), 4,0-3,3 (мультиплет, 8Н)
7,81 (синглет, IH), 4,37 (синглет, 2Н), 3,40 (мультиплет, 4Н), 1,89 (мультиплет, 4Н)
7,70 (синглет, IH), 4,28 (синглет, 2Н), 3,3 (широкая, 4Н, 1,4 (широкая, 6Н)
74
а) CHgNH
b) C,H-NH
80
X Э
c) CHj(CH5)2NH
59 d) CH,(CH2)3NH е) CHjCCH NH f) CHj(CH)yNH g) CH(CH)NH
h) CHj(CH)NH
55
2HC1 HgO
280
Вычислено, %:С 29,27, Н 4,60,, N 29,87.
Найдено, %: С29,21,
Н 4,14- N 29,33-,S 9,17
2НС1 -.
275
Вьиислено, %:С 44,34J
.Н 4,66; N 30, 9,89 ,
Найдено, %: С32,93;
Н 5,1U N 29,39iS 9,64
C,oV-.S.2HCr.
27-229
Вычислено, %:С 35,50,
5,07j N 28,99-S 9,48
Найдено, %: С35,28-,
Н 5,14; N 28,37;S 9,42.
ЯМР (DMSO-d), дельта (млн. доли) : 8,47 (широкая,4Н), 8,09 (широкая IH), 7,93 (синглет, IH), 7,80 (синглет, IH), 3,50 (широкая 2Н), 1,9-1,1 (широкая,I2H), 0,92 (триплет, ЗН) 2HC1 : Вычислено,%: С , Н 5,43; N 27,83-, S 9,10 Найдено, %: С 37,44; Н 5,48; N 26,53; S 8,34 C, . 2FC1 Вычислено, %: С 37,49; Н 6,03-; N 25,51v S 8,34 Найдено, %: С 37,71; Н 5,71V N 23,86 S 7,80 - 2НС1 . H-iO; Вычислено, %: С 39,20V Н 6,33-, N 24,61, S 8,05 Найдено, %: С 39,84, Н 5,865 N 24,60; S 8,19 . 2НС1 HjO Вычислено,%: С 40,78; Н 6,60i N 23,78-, S 7,78. Найдено,%: Н 6,13 N 23,20J S 7,72
i) CHg(CHj)gNH
43
j) СН,(СН2)э№1
k)(CHj)2CHNH42
6) C,H5(CH5)CHNH
60
m) (CHj), CH(CH2)2NH18
n) Циклопропиламино
42
о) Циклопентиламино
21
p) Циклогексиламино
38
275
2HC1 « %0 ;
Вычислено, %; С 43,63j Н 7,09,- N 22,26; S 7,28.
Найдено, %: С 43, 73; Н 6,48; N 21,60, S 7,04 ,
ЯМР. (DMSO-dj),дельта (млн.
275 доли) : 8,47 (широкая, 4Н); 8,06 (широкая, IH), 7,93 (синглет, IH); 7,77 (синглет, IH), 3,46 (широкая. 2Н), 1,9-1,1 (широкая,I6H) 0,90 (триплет, ЗН)
ЯМР (DMSO-d), дельта (млн.
07-210 доли): 8,38 (широкая, 4Н), 8,00 (широкая, IH), 7,89 (синглет, IH), 7,67 (синглет IH), 3,9 (широкая, IH), 1,26. (дублет, 6Н)
ЯМР (DMSO-dб), дельта (млн.
93-294 доли): 8,37 (широкая, 4Н), 7,90 (синглет, IH), 7,80 (широкая, IH), 7,66 (синглет IH), 4,0 (широкая, IH), 1,56 (мультиплет, 2Н), 1,23 (дублет, ЗН), 0,98 (триплет, ЗН).
, : 2НС1- HjO
275
Вычислено, %: С 37,50-,
Н 6,03 N 25,51; S 8,34
Найдено, %: С 37,83; Н 5,75;
N 25,17; S 8,00
275
2НС1
Вычислено, %: С 35,72; Н 4,50; N 9,53
Найдено, %: С 35,91; Н 4,81; S 8,60.
275
C;j,,H.,,N,S,- 2НС1
Вычислено, %: С 37,70; Н 5,54; N 25.,65; S 8,38,
Найдено, %: С 37,28; Н 5,30 N 24,89; S 8,08, -.
ЯГ-1Р (DMSO-d), дельта .(млн.
40
q) C4%CH2NH
r) (CH2)2NH
58
s) ,г(СН2)зШ
58
t) C HjCCH NH
44
u) 2-(4-Пиридип)48этиламино
v) 2-(2-1Ь1ридил)- 52 этиламино
w) 4 Хлорфенетил- 60 амино
х) (CH)jN66
. 2НС1
275
Вычислено, %:С 43,53i
Н 4,44i N 25,28JS 8,30.Найдено, %: С42,95{
Н 4,75; N 24,59j5,8,25
ЯМР (DMSO-d), дельта (млн.
275 доли): 8,40 (широкая, 4Н), 8,04(пшрокая, IH), 7,83 (синглет, IH), 7,69 (синглет, IH), 7,30 (синглет, 5Н), 3,7 (широкая, 2Н), 2,91 (триплет,
2Н) j
53-255 ,jN7S ;2НС1 - HjO
Вычислено, %: С 44,44| Н 4,90i N 22,67i S 7,42.
Найдено, %: С 44,00) Н 4,64} N 21,83v S 7,14
ЯМР (DMSO-d,), дельта (млн.
69-270 доли):.8,41 (широкая, 4Н)., 8,08 (широкая, IH), 7,86 (синглет, IH), 7,70 (синглет, IH), 7,14 (синглет, 5Н), 3,5 (широкая, 2Н), 2,66 (мультиплет, 2Н), 1,9-1,5 (широкая, 4Н)
ЯМР (DMSO-d), дельта (млн. доли): 8,89 (дублет, 2Н), 8,43 (широкая, 4Н), 8,17 (дублет, 2Н), 7,98 (синглет, IH), 7,73 (синглет, IH), 4,0 (широкая, 2Н), 3,36 (мультиплет, 2Н)
05-209
%%NgS - 3HCt
Вычислено, : С 38,41 Н 4,37-, N 25,60, S 7,32.
Найдено, %: С 38,38; Н 4,65; N 24,78; S 7,08qjH,SC1 -2НС1«1/2Н20 Вычислено, %: С 40,60j
Н 4,32| N 22.,09;.S 7,23Найдено,%: С 40,74; Н 4,32$
N 21,90i S 7,16
285
CjHijN S - 2НС1 Н20
Вычислено,%: С 31,58;
Н 5,01; N 28,64i S 9,37..
Найдено, %: С 31,20-, Н 5,22-,
N 27,86i S 8,91
у) C HjfCCHpN.
61
z) (
61
aa) Морфолино
45
68
BB) Пирролидино
38
cc) Пиперидине
dd) (CHj)jNH
Приготовлен из С, Н ) j-NH по методикам примеров 2-5,
275
;j-S 2HC1 - HjO Вычислено, %: С 33,71,
Н 5,38i N 27,52j S 9,00
Найдено, %: С 33,92-; Н 4,90}
N 27,45; S 9,19
2HC1
275
Вычислено, %: С 37,50; Н 5,44; N 27,83 S 9,10.
Найдено, %: С 37,37 Н 5,41; N 26,43; S 8,80
270
. SiV-S 2НС1 .
. Вычислено, %: С 36,07; Н 4,68 N 26,77} S 8,75 .
Найдено, % : С 35,97; Н 5,06; N 25,95;. S 8,62
2НС1 - 1/2Н2.0
280
Вычислено, %: С 36,77;
Н 5,05; N 27,29$ S 8,92 Найдено, %: С 37,145,
Н 4,98; N 27,02; S 8,38.
2НС1 . 1/2h2.0
250
Вычислено, %: С 38,61,
Н 5,40i N 26,27; S 8,59 Найдено, %: С 38,67;
Н N 26,05; S 8,71
,S Hbr HC1
.
вычислено, %: С 44,40 Н 5,18; N 20,14; S 5,49.
Найдено, %: С 44,00; Н 4,97-, N 19,73; S 6,51
| Эльдерфильд Р | |||
| Гетероциклические соединения | |||
| Т | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Ступка | 1922 |
|
SU536A1 |
Авторы
Даты
1985-11-30—Публикация
1983-05-03—Подача