12
Изобретение относится к биохимичес кому получению пищевых и кормовых Сахаров из растительного сырья и преимущественно может быть использовано в гидролизной и микробиологической промьшшенности.
Цель изобретения - упрощение процесса и повышение качества целевого продукта.
Способ осуществляют следующим об- разом.
Качество буфера определяют буферной емкостью j5 которая характеризует способность раствора сохранять постоянное значение рН при добавлении к нему кислоты или основания, 0,1 М раствор, состоящий из смеси бензоата натрия и уксусной кислоты, имеет высокое значение |j (максимальное значение по отношению к НС1 при рН 4,8 составляет 0,051, а по отношению к NaOH при рН буфера 4,2 значение равно 0,047)j что приравнивают предлагаемый буфер к широко употребляемому буферу, состоящему из аце- тата натрия и уксусной кислоты. Кроме того, 0,1 М и тем более 0,05 М раствор буфера, состоящий из бензоата натрия и уксусной кислоты, при значении рН 4-5 не снижает активности геми целлншазных и целлюлазных ферментов,. имеющих оптимальные значения рН-дей- ствия в этом интервале. Это окределя- ет°возможность использования предлагаемого буфера для поддержания зна- чения при рН при ферментативном гидролизе полисахаридов. Бензоат натрия является консервактом, что предохраняет реакционную среду, в которой
проходит ферментативный гидролиз рас- тительног о сырья, от микробного заражения.
Для получения буферного раствора берут от 0,05 до 0,1 М раствор уксус- яой кислоты и бензоата натрия, так как.при употреблении буфера ниже этой концентрации он не проявляет стабильное консервирующее действие, а выше нестабилен ввиду вьшадения бензойной кислоты при низких значениях рН,
Для определения объемньтх соотношений растворов выбранной молярности Компонентов буфера и получения требуемого значения рН, которое определяется применяемь1м для гидролиза ком- гшексом фермента, компоненты взаимно титруют До получения требуемого рН буферного раствора. Такчм образом,
0 5 о
Q
0
5
12а
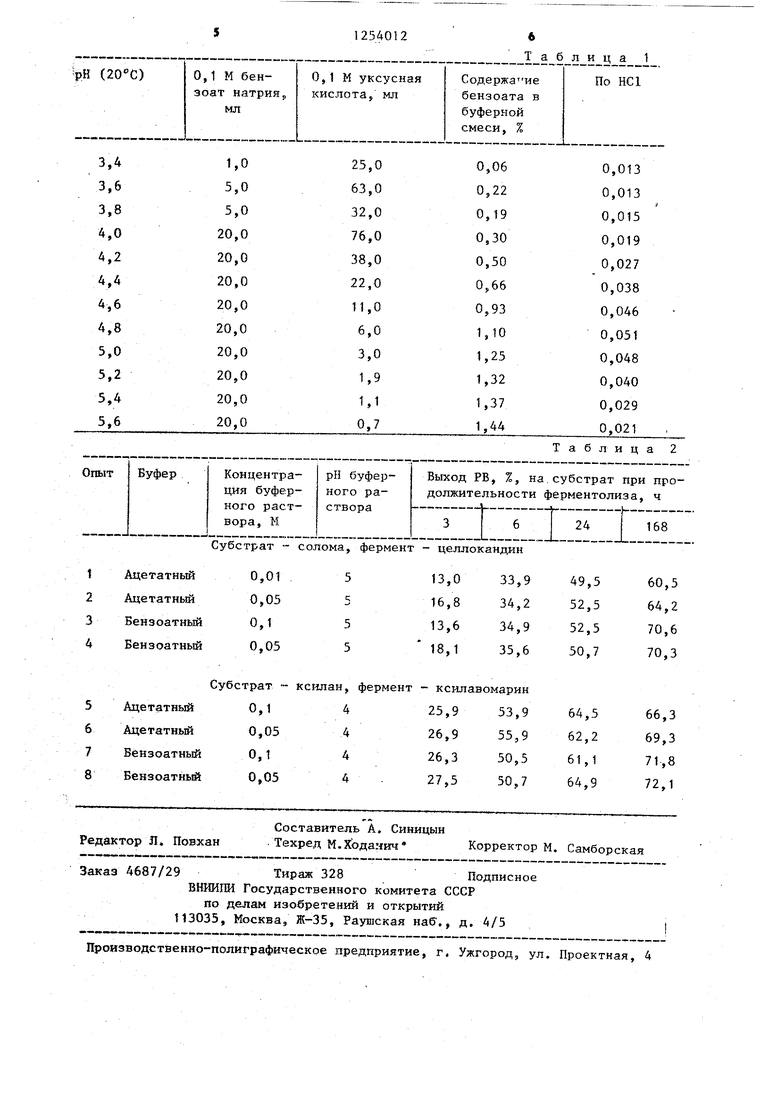
можно составить таблицу для определения взаимных соотношений молярных растворов бензоата натрия и уксусной кислоты, обеспечивающих Любые искомые значения рН (см, табл. 1).
Дальнейшим этапом подготовки реакционной среды к ферментативному гидролизу является включение в буферный раствор фермента и субстрата, количество которых I определяют l конкретным случаем„ Ферментативный гидролиз проводят в ферментерах в статических условиях, в реакторах, снабженных ди- ализирующей мембраной для отвода низкомолекулярных продуктов реакции,или в ферментерах колоночного типа с не- ограниченной продолжительностью без опасности заражения реакционной среды или отобранных растворов Сахаров микроорганизмами.
Пример 1, 1,0г соломы с размерами частиц меньше 2 мм и влажностью 6%, обрабатанной 1,0%-ным раствором NaOH, помещают в колбу на 200 in с резиновой пробкой. Дли осахаривания этого субстрата используют ферментный комплекс деллокандин, имеющий оп- т1-1мальное действие при значении рН5,0,
Сначала приготавливают буферный раствор, состоящий из 43,5 мл 0,1 М раствора бензоата натрия и 6,5 мл . О,Ш уксусной кислоты. Для перевода 0,1 М раствора в 0,05 М к приготовленному раствору прибавляют равное количество (50 мл) дистиллированной воды, имеющей значение рН 6,5| 1,0 г фермента растворяют в приготовленном буфере путем медленного переменшвания в течение 10 мин магнитной мешалкой, потом нерастворимую часть фермента отделяют на стеклянном фильтре. Приготовленный ферментный раствор,имеющий значение рН 5,0, наливают на субстрат, колбу закрывают и помещают в термостат при 40°С. В начале и в конце опыта измеренное значение рН реак- аионной соепы равно 5,,0+0,2. Через 3, 6, 24 и 168 ч колбу вручную встряхи- в4к5Т и отбирают пробы в количестве 1 мл, которые немедленно прибавляют к 2 мл дисктиллированной воды, нагретой до , и вьщерживают 10 мин на .водяной бане для инактивации фермента. В такой пробе, учитывая трехкратное ее разбавление, определяют количество редуцирующих веществ методом Шо- модьи и подсчитывают их количество на абсолютно сухой исходный субстрат.
соответственно
значение опыта
Пример
Л
Таким образом параллельно ставят тр опыта. Количество РВ после 3 ч составляет в параллельных опытах 14,2 18,6 и 21,4%; после 6 ч - 35,9, 33 и 37,3%; после 24 ч - 52,9, 46,8 и 52,4%; 168 ч - 68,9, 71,6 и 70,3%
(см. табл. 2,среднее 4). 2. Осуществляется
1, концентрация используемого бензоатного буфера составляет 0,1 М. Выход РВ через 3, 6, 24 и 168 ч гидролиза составил соответственно 13,6, 34,9, 52,5 и 70,6% (приведено среднее значение, см табл. 2, опыт 3).
Пример 3. Субстратом являеся ксилан, выделенный из овса, а ферментом - кси: авомарин Г-ЮХ,имеющий оптимум действия при рН среда, равном 4. Приготавливают 100 мл 0,1 М буферного раствора, имеющего рН 4,0, смешиванием 79,2 мл 0,1 М раствора уксусной кислоты и 20,8 мл 0,1 М раствора бензоата натрия, добавляют 0,1 г фермента и 0,1 г субстрата, перемешивая все компоненты 10 мин магнитной мешалкой. Приготовленная реакционная среда имеет рН 4,0. Аналогичным образом, как в при мере 1, закрытая колба помещается в термостат при 40°С. Через 3, 6, 24 и 168 ч отбирают пробы для анализа и измеряют рН среды. Значения рН в тр параллельных опытах во время непре- рывного гидролиза составляет 4,0+0, Количество РВ после 3 ч составляет в трех, параллельных опытах 21,1, 29 и 28,1%; через 6 ч - 46,8, 49,6 и 55,2%; 24 ч - 56,9, 62,4 и 63,9%; 168 ч - 73,6, 67,6 и 74,2% соответсвенно (см. табл. 2, среднее значени опыта 7).
Пример 4. Осутдествляется аналогично примеру 3, концентрация используемого ацетатного буфера составляет 0,05 М. Выход РВ (средние значения) через 3, 6, 24 и 168 ч составляют соответственно 27,5; 50,7; 64,9 и 72,1% (см. табл. 2, опыт 8).
Примеры 5-6. Проводят фер ментативный гидролиз в 0,05 М ацетаном буфере, приготовленном известны способом,со значением рН 5. Субстра и фермент, а также их концентрация
5
54012
5
О 5
20 0
4
такие же, как в примере 1. Опыт проводится по примеру 1, но как консервант применяется толуол. Расход толуола на 100 мл реакционной среды - 5 мм.Выход РВ в трех параллельных опытах после 3 ч составляет 15,3, 19,t и 16,0%; 6 4-33,2, 36,6 и32,9%. 24 ч - 59,4, 51,3 и 46,8%; 168 ч - 64,8, 67,4 и 60,1% (см. табл. 2, средние значения опыта 2).
Аналогичный эксперимент осуществляют в 0,1 М ацетатном буфере.Выход РВ (средние значения) через 3, 6, 24 и 16,8 ч Составил соответственно 13,0, 33,9, 49,5 и 60,5% (см. табл. 2, опыт 1).
Примеры 7-8. Осуществляются аналогично примеру 3. Согласно прототипу гидролиз проводят в 0,1 М ацетатном буфере (рН 4) с добавлением толуола (5 мл/100 мл реакционной смеси). Выход РВ (средние значения) через 3, 6, 24 и 168 ч состаЬи.п соответственно 25,9, 53,9, 64,5 и 66,3% (см. табл. 2, опыт 5).
Аналогичный эксперимент осуществляют в 0,05 М ацетатном буфере. Выход РВ (средние значения) через 3, 6, 24 и 168 ч составил соответственно 26,9, 55,9, 62,2 и 69,3% (см. табл. 2, . опыт 6).
Таким образом, для составления реакционной среды создания требуемого значения рН среды и ее консервирования по предлагаемому способу требуются только компоненты буфера, что обеспечивает упрощение процесса гидролиза.
Присутствие бензоата натрия в среде ферментативного гидролиза полиса- харидсодержащих субстратов не снижает активности ферментов, а в некоторых случаях даже способствует .повьшению выхода РВ по сравнению со средами, содержащими ацетатный буфер и толуол.
Полученные растворы Сахаров в при- . сутствии бензоата натрия не содержат токсичное соединение - толуол, что повьшает их качество, и поэтому могут быть использованы для кормовых и пищевых целей без особой очистки, так как бензоат натрия допущен, как консервант, в пищевой и кормовой про- мьшшённости.
Редактор Л. Повхан
Составитель А, Синицын
Техред М.Ходаяич Корректор М. Самборская
Заказ 4687/29Тираж 328Подписное
ВНЙИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская на5., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения видовой принадлежности водных организмов | 1980 |
|
SU1001898A1 |
| Способ получения 7-( - -аминофенилацетамидо)-дезацетоксицефалоспорановой кислоты (цефалексина) | 1972 |
|
SU579901A3 |
| Способ получения гетерогенного биокатализатора на основе целлюлазы, иммобилизованной на катионообменном волокне ВИОН КН-1 в Н-форме | 2024 |
|
RU2834720C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧЕСКОГО ЗАГРЯЗНЕНИЯ СТОЧНЫХ И ПРИРОДНЫХ ПРЕСНЫХ ВОД | 2006 |
|
RU2308719C1 |
| Способ определения таксономической принадлежности кальмаров | 1983 |
|
SU1142079A1 |
| ВЫСОКОЧУВСТВИТЕЛЬНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ ИММУНОГЛОБУЛИН-ПРОТЕИНАЗНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕРНЫХ МАТРИЦ | 2013 |
|
RU2519071C1 |
| Способ определения активности аминоацилазы | 1980 |
|
SU968070A1 |
| ФЕРМЕНТ КАРБОКСИПЕПТИДАЗА КПSВ, ШТАММ Streptomyces bikiniensis - ПРОДУЦЕНТ КАРБОКСИПЕПТИДАЗЫ КПSВ, ФРАГМЕНТ ДНК SB27-995, КОДИРУЮЩИЙ СИНТЕЗ ЗРЕЛОЙ ФОРМЫ ЭТОГО ФЕРМЕНТА, И СПОСОБ МИКРОБИОЛОГИЧЕСКОГО СИНТЕЗА КАРБОКСИПЕПТИДАЗЫ КПSВ | 2008 |
|
RU2388825C1 |
| Ферментативный способ определения концентрации антибиотика с бета-лактамным кольцом | 1983 |
|
SU1313353A3 |
| Способ определения активности х-пролилдипептидиламинопептидазы | 1976 |
|
SU786853A3 |


| 0 |
|
SU155081A1 | |
| Насос | 1917 |
|
SU13A1 |
| Toyama N., Ogawa К, - Biotechnol | |||
| Bioeng | |||
| Symp | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
Авторы
Даты
1986-08-30—Публикация
1984-08-15—Подача