N3
СО
ел
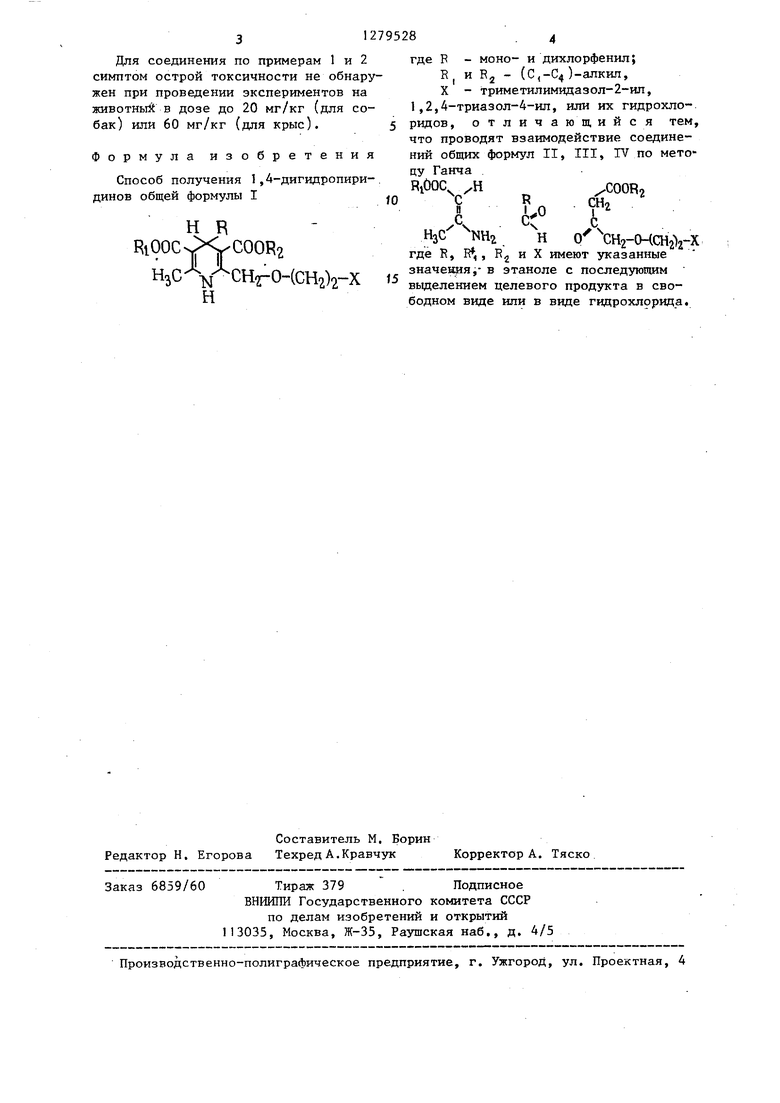
о 112 Изобретение относится к способам получения новых производных 1,4-дигидропиридинов общей формулы Н R RlOOCs :.cOOR2 НзС СН2-0-(СН2)2-Х Н где R - моно- и дихлорфенил; R и R - (С,-С4.)-алкил; X - триметилимидазол-;2гид, 1,2,4-триазол-4-ил, или их гидрохлоридов, обладающих свойствами антагонистов кальция. , Цель изобретения - разработка на основе известного метода способа получения новых производных 1,4-дигидропиридиНов, обладающих ценными фармакологическими свойствами. П р и м-е р 1. 4-(2-Хлорфенил)-З-этоксикарбонил-5-метоксикарбонил-6-метил-2- 2-(2,4,5-триметил-1-имидазолил)этоксиметил -1,4-дигидропиридин, гидрохлоридная соль. Этил 4- 2- ( 2,4,5-7 трнметил- 1 -имида золил)этокси ацетоацетат (6,4 г1 , 2-хлорбенэапьдегил (3,2 г), метил-3-аминокротонат (2,6 г) и уксусную кислоту (31 мл) в этаноле (15 мл) смешивают и кипятят с обратным холодильником в течение 4,4 ч. Затем охлажденную реакционную смесь выпарива ют досуха и остаток распределяют меж ду 2 Н.соляной кислотой (100 мл) и толуолом (50 мл) Слой кислоты отделяют, экстрагируют метиленхлоридом (З X 20 мл) и экстракты промывают на .сьщенным водным раствором карбоната натрия (30 мл), сущат над карбонатом натрия, отфильтровывают и выпаривают Остаток в небольшом количестве толуо ла хроматографируют на силикагеле,. элюируют метиленхлоридом с 30 об.% петролейного эфира. Соответствующие фракции объединяют, выпаривают досух и вновь растворяют в этилацетате. До бавление эфирного раствора хлористог водорода приводят к осаждению гидрохлористой соли, которую перекристаллизовывают из этилацетата с получени ем целевого соединения (ls2 г), т„пл 167-168°С. Найдено, %: С 57,30; Н 6,07; N 7,7Г,. C HjjClN O J НС1. Вычислено, %: С 57,99; Н 6.18; N 7.80. 8 Пример 2. ((Д-( 3-Ди- хлорфенил)-4-этоксикарбонил-5-метоксикарбонил-6-метил-1,4-дигидропирид ,-2-nni) метокси),2,4-триазол, Раствор этиловогоэфира (1,2,4-триазол-4-ил)этокси ацетоуксусной кислоты (4,8 г), 2,3-дихлорбензальдегида (3,4 г).,метилового эфира 3-аминокротоновой кислоты (2,3 г) и уксусной кислоты (1,0 мл) в 30 мл этилового спирта нагревают с обратньм холодильником в течение 16 ч и выпаривают. Остаток распределяют между этилацетатом и водой, и органический слой двалч ы промывают водой, сушат над сульфатом натрия и выпаривают. Остаток очищают хроматографически на силикагеле (60 г), используя в качестве элюента толуол с добавкой 0-100% этилацетата,, Соответствующие фракции объединяют и вьтаривают, остаток подвергают кристаллизации из эфира, получают целевое соединение примера: (1,3 г), т.лл. 86-88 С. Найдено, %г С 53,17; Н 5,20; N 10,91. С,,Н,,С1гН,05 Вычислено, %: С 53,34;Н 4,85, N 11,31. Для оценки действия кальциевых антагонистов (соединения примеров 1 и 2) исследуют их влияние на коронарное кровообращение анестезированной собаки, Для оценки длительности действия собакам, анестезированным хлоралозойуретаном, внутривенно вводят дозы 150 мг/кг (позволяющие достичь примерно 60% максимального расширения коронарных сосудов) и регистрируют время, которое необходимо для снижения на 50% максимального эффекта резистентности коронарных сосудов. Получены следуюшр е данные: Соединение Полупериод 5-3 ч По примеру 1 6,5 ч По примеру 2 5-10 мин Нифедипин Определяют величину IC - молярную концентрацию соединения, необходнмую для .снижения чувствительности изолированной аорты крыс к ионам кальция на 50%. Для соединения по примеру ICjo составляет 5,01- х X , по примеру 2 - 2,63«10м. Для соединения по примерам 1 и 2 симптом острой токсичности не обнару жен при проведении экспериментов на животный в дозе до 20 мг/кг (для собак) или 60 мг/кг (для крыс). Формула изобретения Способ получения 1,4-дигидропиридинов общей формулы I Н R RlOOCx.COOR2 (СН2)2-Х Н где R - моно- и дихлорфенил; RI и ЕЗ - (С,-С4)-алкил, X - триметилимидазол-2-ш1, 1,2,4-триазол-4-ил, или их гидрохло-. РИДОВ, отличающийся тем, что проводят взаимодействие соединений общих формул II, III, IV по методу Ганча /COORo СН2 С 0 H2-(HCH2VX где R, R,, R, X имеют указанные значетая,- в этаноле с последзтощим выделением целевого продукта в свободном виде или в виде гидрохлорида.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производного 1,4-дигидропиридина | 1984 |
|
SU1391499A3 |
| Способ получения производных 1,4-дигидропиридина | 1984 |
|
SU1303025A3 |
| Способ получения производных 2-аминокарбонилоксиалкил-1,4-дигидропиридина | 1982 |
|
SU1097195A3 |
| Способ получения производных 1,4-дигидропиридина | 1985 |
|
SU1417795A3 |
| Способ получения производных 2-аминоалкилтиометил-1,4-дигидропиридина или их энантиомеров | 1988 |
|
SU1816282A3 |
| Способ получения производных 1,4-дигидропиридина или их гидрохлоридов | 1983 |
|
SU1364237A3 |
| Способ получения 2-замещенных или незамещенных аминокарбонилоксиалкил-1,4-дигидропиридинов | 1983 |
|
SU1169531A3 |
| ПРОИЗВОДНЫЕ 1,4-ДИГИДРОПИРИДИНА ИЛИ ИХ ГИДРОХЛОРИДЫ, ОБЛАДАЮЩИЕ АНТАГОНИСТИЧЕСКИМИ СВОЙСТВАМИ ПО ОТНОШЕНИЮ К ИОНАМ КАЛЬЦИЯ | 1992 |
|
RU2036922C1 |
| Способ получения производных 1,4-дигидропиридина или их кислотно-аддитивных солей | 1983 |
|
SU1238730A3 |
| ПРОИЗВОДНЫЕ 1,4-ДИГИДРОПИРИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, ОБЛАДАЮЩАЯ ВАЗОАКТИВНЫМ ДЕЙСТВИЕМ | 1991 |
|
RU2081869C1 |
Изобретение касается замещенных дигидропиридинов, в частности 1,4дигидропиридинов общей формулы CHR-CX CY-NH-C(CH) CZ (l), где X -C

| Me Alester J | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Cardiovoscular form, 1980, s | |||
| Способ отопления гретым воздухом | 1922 |
|
SU340A1 |
| Элдерфильд P | |||
| Гетероциклические соединения | |||
| Приспособление для строгания деревянных полов, устраняющее работу на коленях | 1925 |
|
SU1956A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| УСТРОЙСТВО ДЛЯ РАСФАСОВКИ ПОРОШКООБРАЗНОГО МАТЕРИАЛА В МЕШКИ | 0 |
|
SU351356A1 |
Авторы
Даты
1986-12-23—Публикация
1983-07-19—Подача