Изобретение относится к биотехно- огии, в частности к генной инженеии, и представляет собой фагово- лазмидный вектор (ФПВ) / pMYF 131 для рямого отбора рекомбинантных молекул НК, их генетического анализа и спооб его конструирования.
Целью изобретения является создание вектора с повышенной эффективное-fQ тью клонирования, позволяющего упростить процесс получения банков генов и облегчить физический и генетический анализ рекомбинантных клонов.
Поставленная цель достигается тем, f5 что из предшественника ФПВ удалили части молекулы ДОК, не содержащей генов, существенных для развития фага, Размер векторной молекулы ,ЦНК в результате Удаления этого фрагмента дол- 20 жен быть меньше критического размера, необходимого для упаковки з фаговый капсид. Полученный вектор не способен осуществлять литический цикл развития фага. Поэтому для поддержания вектор-25 ной молекулы ДНК в клетке фрагмент, содержащий все гены и участки. ДНК, существенные для развития фага, соединен с фрагмейтом плазмидной ДНК. Этот фрагмент обеспечивает автономную 30 репликацию (ФПВ) в клетке, возможность селекции клеток, содержащие: векторную молекулу в плазмидной форме: по маркеру устойчивости к ампицилл1-шу плазми- ды pUC19. Фрагменты ДНК, содержащие 5 существенные гены для фагового развития, участок инициации Ш1азми,цной репликации и ген устойчивости к антибиотику, выбраны таким образом, что не содержат сайтов расщепления для ряда 40 рестриктаз. Введение уникальных сайтов расщепления для этих рестриктаз сообщает полученной молекуле ДНК свойства вектора для ФПВ А pMYF 131.
ФПВ состоит из следующих элементов.45
Гены и регуляторные области, необходимые и достаточные для литического цикла развития фага И , в том числе левое плечо .ЦНК фага j 47АВ от участка m (координата О т.п.н) до сайта 50 рас1т епления рестриктазой Sma I (координата 19,3 т.п.н), правое плечо ДНК вегетативного фага/ gtWES от сайта расщепления Ваш HI (координата 34,5 т.п.н.) до участка т (координа-55 га 48,5 т.п.н.), координаты приведены по ДНК фага Д дикого типа,
Ген С1, кодирующий тepмo ryвcтви- тельный белок-репрессор фага/ , с мутацией 857. Присут(::твие ts-мутации в гене репрессора С1 позволяет индуцировать фаговуго репликацию при повышении температуры. обеспечивает простой и эффективный способ амплификации как векторной ДНК, так и ДНК рекомбинантньпс на с-снове ФПВ. Упомянутая ак:плификация увеличивает копий ;ность ДНК в 20-50 раз. Такая амплификация может быть прш- енена для облегчения выделения дак-вектора и гибридов на его основе.
Присутствие ts-мутации в гене С1 обеспечивает большув безопасность при работе с рекомбинантными ДНК на основе ФПВ, поскольку при температуре выше 37 с невозможно поддержание ФПВ в плазмидной форме, и клетки, содержащие 1 шазми;1У5 гибнут
Chi - сайт 3 гене J фагаД , необ- ходимый для по,лучения высокого титра фага в отсутствие п : одуктов генов red и gam.
Гены А,В и S в амбер-форме, что позвол51ет литическое развитие ФПВ на основе/, pMYF 131 только на штаммах E.coli, содержащих с1мбер-супрессор SUP Наличие гмбер--мутаций ограничивает литическое развитие рекомбинантных ФПВ Б подавляющем большинстве природных , чувствительных к фагут . Мутация в гене S удлиняет период репликации ДНК ФПВ после индукции фагоспецифической репликации, что позволяет увеличить количество выделяемой ДНК ФПВ, и рекомбинантных молекул ДНК на его основе. Мутация в гене А препятствует надрезанию сверх- скрученньгх молекул ДНК, накапливающихся после индукции фагоспецифической репликации, что позволяет использовать для выделения ДНК методы выделения плазмидной ДНК,
Участок индикации репликации (ori) плазмиды pUCIQ, исходно содержащийся в плазмиде рШГ, размером 0,6 т.п.н,. Присутствие ori обеспечи- ваег поддержание век орной молекулы в плазмидной форме, эффективное установление лизогенного (плазмидного) состояния при инфицировании клеток фаговыми частицами, содержащими гибридный ФПВ. ПрисутстЕие такого репли- кона, кроме того, обеспечивает большую безопасность при работе с рекомбинантными ДНК на оскове ФПВ при по- вьшенной температуре, поскольку присутствие резистентного гомоиммунного
профага в индуцированной клетке не способно репрессировать литическое развитие ДНК ФПВ. Это приводит к гибели индуцированных лйзогенных клеток.
Генр - лактамазы (размер 1,1т. п.н), обеспечивающий устойчивость клеток к ампициллину (маркер Ар ) плазмиды pUC19, исходно содержавшийся в транспозе ТпЗ. Присутствие в фазмиде маркера Ар позволяет использовать данный маркер в качестве селективного или контрольного при ком- плементационном анализе рекомбинант- ного ФПВ.
Полилинкер - последовательность молекулы ДНК, имеющую набор близко расположенных участков расщепления ряда рестриктаз: Hind III, Sph I, Pst I, Sal GI, Xba I, Bam HI, Sma I, Kpn I, Sac I, ECO RI, в том числе уникальные участки рестрикции Есо RI Sac I, SalGI, Xba 1.
Уникальные участки рестрикции, помимо полилинкера, имеются также в несущественных для литического развития област51х молекулы ДНК ФПВ. Это участки расщепления для рестриктаз ЕсоА7Ш ХтаШ.
Рекомбинантные ФПВ со вставками ДНК размером не менее А т. п.н. по сайтам Есо R1, Sac I, SalGI, ХЪа I, Есо 47 III и Xasa III способны развиваться подобно недефектному фагу/ или могут поддерживаться в клетке, содержащей рекомбинантный ФПВ, в плаз- мидной форме.
При расщеплении рестриктазой SalGI возможна встройка в ФПВ фрагментов ДНК, расщепленной рестриктазами SalGI, Xho I.
При расщеплении вектора рестриктазой Xba I возможна встройка в ФПВ фрагментов ДНК, расщепленной рестриктазами Xba I и Avr II. При расщепле- НИИ вектора рестриктазой Есо 47 III возможна встройка в ФПВ фрагментов
ДНК, расщепленной рестриктазами с пол ностью спаренными (тупыми) концами, которые образуются под действием раз- личных рестриктаз.
Уникальные участки расщепления для рестриктаз Nru I, Sna BI, Sac II и Asu II в областях ДНК ФПВ, существенных для ее развития по литическому пути.
Вставка фрагментов ДНК по указанным участкам расщепления обеспечивает большую безопасность при работе с
5
O
0
рекомбинантными ФПВ благодаря блоку литического развития гибридных ФПВ. Гибридный ФПВ, полученный подобным образом, способен поддерживаться в клетке лишь в форме плазмиды. При использовании рестриктазы Nru I и Sna BI возможна встройка в ФПВ фрагментов ДНК с тупыми концами. При использовании рестриктазы Asu II возможно клонирование фрагментов ДНК, полученных под действием рестриктаз ASU II, Nar I, Mlu I, Bse PI, Асу I, Tag I, Msp I, Hin PI, Mae II.
Суммарный размер ФПВ/i pMYF 131 32 т.п.н. (65% от размера ДНК фага/ дикого типа).
Клонирующая емкость сконструированного вектора одинакова для каждой из указанных рестриктаз и составляет 4-21 т.п.н.
Анализ векторных свойств/|. pMYF 1 31 приведен в табл.1.
Таблица Рестриктазы, которые могут быть использованы при клонировании в / р MYF 131
Ферменты, имеющие уникальный участок расщепления на ДНК pMYF 131
. В несущественной зоне
Есо RI Sal GI
Xba I Sac I Xma III
ECO 47 III
ECO RI
Cal GI, Xho I
Xba I, Avr II
Sac I
Xma III, Cfr I, Not I
Bee, ферменты, образующие фрагменты ДНК с тупыми концами
45
50
55
II. В существенной зоне
Nru I Sna BI Sac II
Asu II
То же it
Sac II, Bdc II, Нас II
Asu II, Nar I, Mlu I, Bse PI, Asy 1, Tag I, Msp I, Hinc PI, Mac II
Пример 1. Конструирование ФИВ, обладающего требуемой структу- рой, проводится в два этапа.
На первом этапе совместили в составе одной молекулы фаговой ДНК все перечисленные элементы тгисим образом, чтобы все необходимые участки фаговой ДНК можно было легко присоединить к плазмидной части. В качестве исходного материала для конструирования использовали ДНК фагового вектора gt WES (jl Warn Earn Sam nin 5) и сконструированного нами ранее ФПВ J р MYF 15 (Л 47АВ::ЛМ7).
Предполагалось соединить в составе одной молекулы левый EcoRI - фрагмент /ipMYFtS и правый EcoRI - фрагмент фагаЛ gt WES./ pMYF 131 представляет собой гибридную молекулу ДНК ФПВ, содержащего плаэмиду ЗТ AN7, которая утрачивается при дальнейшем конструировании. ИзД р MYF 15 в конструируемую молекулу переходит chi- сайт из фага /( gt WES - область иммунитета фага с геном Cl, содержащим мутацию с1857.
25 MYF 17, выделень:ой в фаговой форм расщепленной рестр эстазой Ват HI, л гировалк с 0,01 мкг плазмиды pUC 19 расщепленной этой же рестриктазой. Смесь лигированньгх фрагментов ДНК
В процессе конструирования 1 мкг ДНК )|gt WES и 0,1 мкг ДНК, р MYF 15, расщепленных рестриктазой Есо RI, ли- ЗО использовали для трансформации комгиров али в объеме 3 мкл, паковали in vitro в капсид фага А и высевали на газон бактерий E.coli W3350, не содержащих амбер-супрессора. На этом газоне могли образовать негативные колонии/1 р MIfF 15 и гибрид, получивший левое плечо ФПВ и правое плечо фага, так как в левом плече ФПВ в составе плазмиды Я AN7 содержится ген Sup F, супрессирующий амбер-м - тации, присутствующая в геномах фага и/ р MYF 15. Фаг Х gt WES и гибрид, содержащий правое плечо ФШ5 и левое плечо фг.га, не может расти на газоне бактерий W 3350, так как содержит в своем составе амбер-мутации и не содержит амбер-супрессора. Маркером для обнаружения правого плеча фага Дgt WES в составе гибридной молекулы является признак иммунности к фагу jH, Правое плечо Лр MYF 15 определяет иммунитет к фагу 434, Чтобы различит два типа фаговых частиц, выросших на газоне бактерий W 3350, их иммунитет проверяли с помощью спот-теста. Из фаговых частитд, способных к росту на бактериях Q 358/Д i 434 и не способных к росту на бактериях Q 358 () при , т.е. содержащих область
00096
иммунитета фага у gt WES, выделили ДНК. По данным расщепления рестрикта- зой Есо RI эта ДНр; соответствовала искомому гибриду между фагами /( gt 5 WES и/( р МУР 15. Один из полученных
клонов обозначенных/ р MYF 17, использовали для дальнейшего конструирования.
j(3На втором этапе конструирования
Ват HI плечо фазмицы р MYF 17, содержащее все гены, необходимые для лити- ческого развития фага :СЬ -сайт и ген С1, кодирующий тер;чолабильный распресJ5 сор (С1, ), соединили с плазмидой
pUC19.j расщепленн(эй этой, же рестрик- тазой. Плазмида pUC19 представляет собой делеционньгй зариант плазмиды pBR322, содержащий фрагмент lac- опе20 рона E.coli. Этот фрагмент обеспечивает ot - комплементацию ферментативной активности р галя.ктозидазы в штаммах, содержшцих делецию йМ15, таких как например E.coli TG-1. 1 мкг ДНК
25 MYF 17, выделень:ой в фаговой форме, расщепленной рестр эстазой Ват HI, ли- гировалк с 0,01 мкг плазмиды pUC 19, расщепленной этой же рестриктазой. Смесь лигированньгх фрагментов ДНК
ЗО использовали для трансформации компетентных клеток E.coli TG1 (/), которые высевали на среду с пенициллином, содержшдую хромогенный субстрат X-gal и ИПТГ. Из неокрашенных колоний
выделили гибридные 1лазмиды. Гибридную плаз МИД н;/то ДНК одного из клонов обозначили/ р MYF 131. Для получения больших количеств вэкторной ДНК р MYF 131 (до 30% от всей клеточной
НК) осуществляют а1-1Ш1Ификацию ДНК фазмиды путем термолндукции фаговой репликации.
ФПВ/1 р MYF 131, конструирование которого описано в примере 1, используют для полз чения векторной ДНК и для создания банки генов.
П р и м е р 2. ФГ1Б ДНК трансформировали компетентные клетки штамма E.coli НВ101, являю11;егося гесА, Sup° .
Ф11В содержит амбер-кутации в генах А и S. Мутация в гене S позволяет увеличить время фаге специфической репликации ФПВ. Мутация в гене А и отсутствие в ФПВ генов red и gam позволяет выделять ФПВ, пользуясь методами выделения сверхскрученных ДНК, поскольку в клетке отсутствуют ферменты гее, red систем и белок А, которые могут релаксирэнать реплицирующийся ФПВ ДНК.,В логарифмической куль-. туре клеток E.coli НВ101, содержа- щих-ФПВ, индуцировали фаговую репликацию, повышая температуру инкубации с 30 до 45 С, и инкубировали при 5 в течение 15 мин. Затем культуры растили 2 ч при . Из выросших клеток выделяли плазмидную ДНК в количестве 1 мкг из 1-2-10 бактериальных клеток, что соответствует 25-50- кратной амплификации плазмиды.
П р и м е р 3. Хромосомную ДНК выделяли из ночной культуры клеток
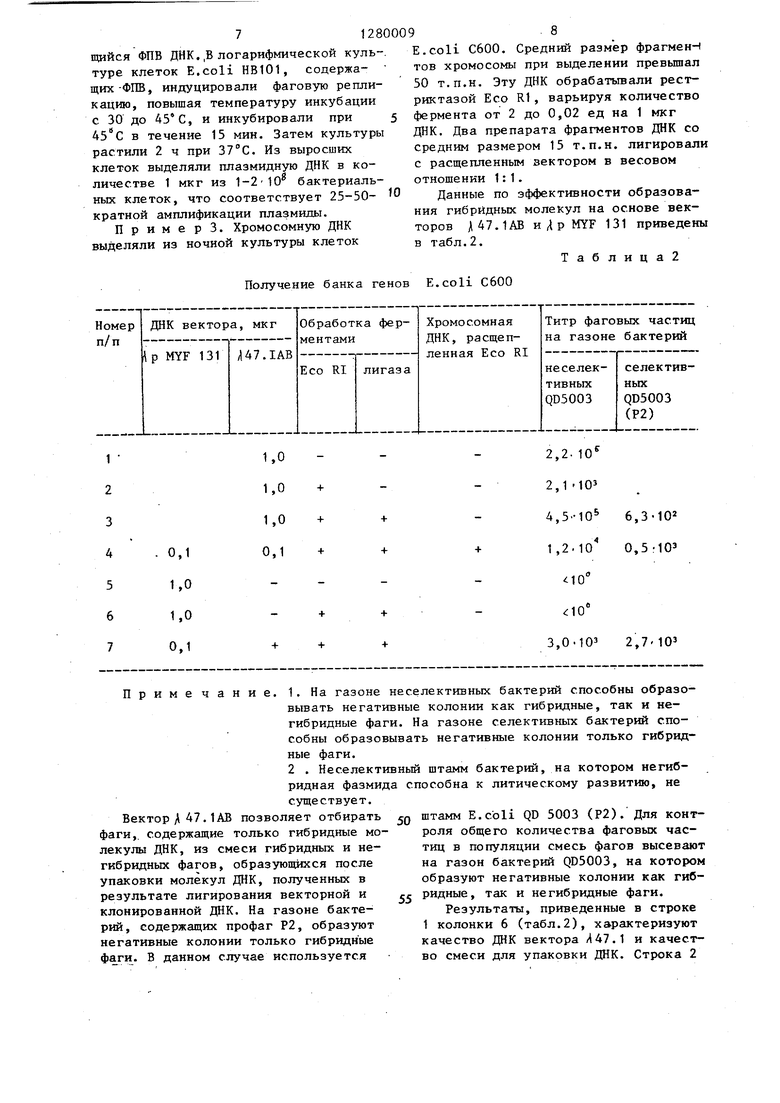
Получение банка генов E.coli СбОО
Примечание. 1.На газоне неселективных бактерий способны образовывать негативные колонии как гибридные, так и негибридные фаги. На газоне селективных бактерий способны образовывать негативные колонии только гибридные фаги.
2 . Неселективный штамм бактерий, на котором негибридная фазмида способна к литическому развитию, не существует.
50
Вектор А 47.1АВ позволяет отбирать фаги,, содержащие только гибридные молекулы ДНК, из смеси гибридных и негибридных фагов, образующихся после упаковки молекул ДНК, полученных в результате лигирования векторной и клонированной ДНК. На газоне бактерий, содержащих профаг Р2, образуют негативные колонии только гибридные фаги. В данном случае используется
штамм E.coli QD 5003 (Р2). Для контроля общего количества фаговых частиц в популяции смесь фагов высеваю на газон бактерий QD5003, на котором образуют негативные колонии как гиб- ридные, так и негибридные фаги.
Результаты, приведенные в строке 1 колонки 6 (табл.2), характеризуют качество ДНК вектора .1 и качество смеси для упаковки ДНК. Строка 2
E.coli С600. Средний размер фрагменН тов хромосомы при выделении превышал 50 т.п.н. Эту ДНК обрабатьшали рест- риктазой Есо R1, варьируя количество фермента от 2 до 0,02 ед на 1 мкг ДНК. Два препарата фрагментов ДНК со средним размером 15 т.п.н. лигировали с расщепленным вектором в весовом отношении 1:1.
Данные по эффективности образования гибридных молекул на основе векторов H.IAB и Д р MYF 131 приведены в табл.2.
Таблица2
штамм E.coli QD 5003 (Р2). Для контроля общего количества фаговых частиц в популяции смесь фагов высевают на газон бактерий QD5003, на котором образуют негативные колонии как гиб- ридные, так и негибридные фаги.
Результаты, приведенные в строке 1 колонки 6 (табл.2), характеризуют качество ДНК вектора .1 и качество смеси для упаковки ДНК. Строка 2
колонки б характеризует э(|)фективность расщепления молекул ДНК вектора ре- стриктазой EcoRI. Эффективность упаковки составляет после расщепления 2,1-1055 т.е. падает на три порядка по сравнента с эффективностью упаковки нативной ДНК.
Строка 3 Колонки 6 характеризует качество векторной молекуж. ДНК и
25
использованных ферментов - рестрилкта- О тивной векторной молекулы ДНК /1 р
зы и лигазы. Титр фаговых частиц пусле лигировакия молекул ДНК вектора
Х47 1АВ составляет 4,5. 10 (строка 3
колонки б). Тов. поднимается в
200 раз и составляет пpи «;pнo 20 % 5
от титра при упаковке нерасщепленной
ДНК (2,210, строка 1 колонки 6). Колонка 7 строка 3 харгжтеризует
уровень фона - титр не гибридных час-- .тиц, гюлученкых после упаковки рас- щепленной и .пигированной ДНК вектора
М7.1АБ и способных образовывать негативные колонии на газоне селективных бактерий QD 5003 (Р2), В данном
примере фон составил 6,310.
Из строки 3 колонки 6 следует, что одна из примерно 700 (0,150) расщеп-ленных и лигированяых молекул векторной ДНК /|47.ШЗ способна образовывать негативную колонию на селективном газоне несмотря на отсутствие в лигируемой смеси чужеродной ДНК.
Строка 4 характеризует эффективность образования гибридных молекул ДНК при использовании вектора М7.1АВ, На селективном газоне титр фаговых частиц составил О.,510 (колонка 7), что соответс Гвует эффективности клонирования 5-10 гибр1едных фагов на 1 мкг ДНК вектора Д47.1АВ. Отношение титров на селективном газоне (колонка 7, титр 0,,5-10) и неселективном газоне (колонка 6j титр 1,2-10) характеризует долю гибридных молекул 5 ДНК в лигированной смеси молекул векторной и клонируемой ДНК Доля гибридных молекул составляет около 4% от всех упагсованных молекул ли иро-MYF 131, Титр фагов, образуемых.пр упаковке нативной плазмидной формы ФПВ составляет менее 10 на 1 мкг упаковьгааемой ДНК вектора. Контрол качества упаковочнэй смеси являетс определенный параллельно титр упак ванной нативной вектора А47,1А (строка 1 колонки 6, 2,210), Так образом,, менее чем 1 из 10 молеку нативного ФГШ А р MYF 131 способна упаковке и образовгшию негативной лонии,
Строка 6 характеризует уровень фона - титр не гибридных частиц, по ченных после упакоики расщепленной лигированкой ДНК вб:ктора А р fYF 13 способных образовать негативные ко нии на газоне бактерий. Титры не ги ридных частиц сост,свляют менее 1 н 1 мкг упакованной, расщепленной и гированной ДНК ФПВ ,1 р MYF 131 (стр 6 колонки 6, титр ,i 10 ). Аналогич показатель фона для вектора прото па и базового образца .1АВ (с 15 ка 3 колонки 7, ти1р 6,3--10) выше показателя фона для заявляемого ФП более чем в 630 раз. Таким образом ФПВ по сравнению с вектором-прото пом и базовым образцом характеризу ся в 630 раз более низким фоном.
30
40
Строка 7 характеризует эффектив ность образования гибридных молеку ДНК с помощью заявл«;нного ФПВ Д р M 131. После упаковки смеси расщепле ной и лигированнор ДНК ФПВ и клони емой ДНК титр фаговых частиц соста вил 3,0 ; 10 (строка 7 колонки 6), что соответствует образованию 3,0х
ванной смеси. Качество бапка, полу- 50 0 Фаговых частиц на 1 мкг ФПБ.
Качество банка, полученного на основе ФПВ I i р MYF 131, характеризуется долей не гибридных молекул в лигированкой смеси, способных образовывать
ченного на основе вектора прототипа М7.1АВ, характеризуется долей негибридных молекул в лигированной смеси, способных образовывать негативные колонии после упаковки и высева на негативные ко,понии после упаковки и газон селективных бактерий. В данном высева на газон бактерий. В данном примере доля негибридных фз:гов, обра- npHivfepe доля негибрицных Д р MYF 131, зующих негативные колонии Е селектив- образующи с негативны - колонии на га- ных условиях (строка 3 колонки 7, зоне бактерий (строка 6 колонки 6,
титр 6,310 при мкг),.от всех фагов, полученных при упаковке лигиро- ванной смеси ДНК, образующих колонии в селективных услсвиях (строка 4 ко- лонки 7s 0,510 г:ри,0,1 мкг) составляет 12 %.
Свойства предлагаемого ФПВ р MYF 131 характеризуются строками 5,6 и 7, Строка 5 характеризует качество нао
5
5
5
MYF 131, Титр фагов, образуемых.при упаковке нативной плазмидной формы ФПВ составляет менее 10 на 1 мкг упаковьгааемой ДНК вектора. Контролем качества упаковочнэй смеси является определенный параллельно титр упакованной нативной вектора А47,1АВ (строка 1 колонки 6, 2,210), Таким образом,, менее чем 1 из 10 молекул нативного ФГШ А р MYF 131 способна к упаковке и образовгшию негативной колонии,
Строка 6 характеризует уровень фона - титр не гибридных частиц, полученных после упакоики расщепленной и лигированкой ДНК вб:ктора А р fYF 131, способных образовать негативные колонии на газоне бактерий. Титры не гибридных частиц сост,свляют менее 1 на 1 мкг упакованной, расщепленной и лигированной ДНК ФПВ ,1 р MYF 131 (строка 6 колонки 6, титр ,i 10 ). Аналогичный показатель фона для вектора прототипа и базового образца .1АВ (стро- 15 ка 3 колонки 7, ти1р 6,3--10) выше показателя фона для заявляемого ФПВ, более чем в 630 раз. Таким образом ФПВ по сравнению с вектором-прототипом и базовым образцом характеризуется в 630 раз более низким фоном.
0
40
Строка 7 характеризует эффективность образования гибридных молекул ДНК с помощью заявл«;нного ФПВ Д р MYF 131. После упаковки смеси расщеплен - ной и лигированнор ДНК ФПВ и клонируемой ДНК титр фаговых частиц составил 3,0 ; 10 (строка 7 колонки 6), что соответствует образованию 3,0х
0 Фаговых частиц на 1 мкг ФПБ.
Качество банка, полученного на основе ФПВ I i р MYF 131, характеризуется долей не гибридных молекул в лигированкой смеси, способных образовывать
негативные ко,понии после упаковки и высева на газон бактерий. В данном npHivfepe доля негибрицных Д р MYF 131, образующи с негативны - колонии на га- зоне бактерий (строка 6 колонки 6,
11
титр .10 на 1 мкг ДНК), от всех ФПВ, полученных при упаковке лигиро- ванной смеси ДНК и образующих негативные колонии (строка 7 колонки 6, титр 3, на 0,1 мкг ДНК), состав- 5
ляет менее 10(0,003%).
Сравнение качества банка, полученного на основе вектора-прототипа и 47.1АВ (доля негибридных фагов 12%),
12800
с качеством банка, полученного на ос-Ш ФПВ клетки высевали на селективные
нове предлагаемого у р MYF 131 (доля негибридных фазмид менее 0,003%), показьшает, что качество банка на основе предлагаемого вектора значительно вьше - доля негибридных частиц в банке, полученном на основе ФПВ IP MYF 131, по крайней мере в 4000 раз меньше, чем в банке, полученном на основе вектора-прототипа.
Таким образом, по двум взаимосвязанным параметрам (уровню фона и качеству банка) предлагаемьй ФПВ Др MYF 131 значительно превосходит вектор-прототип 47.1.АВ. В плане
среды, содержащие пенициллин, а такж стрептомицин, являющийся селективным маркером реципиентного штамма, и не содержащие либо пролин, либо аромати
15 ческие аминокислоты - триптофан, тирозин и фенилаланин.
Титр популяции ФПВ составлял 3,1х х10 фаговьос частиц. Титр трансдук- тантов, выросших на полной среде с
20 пенициллином, равнялся 4,5-10 при множественности инфекции при трансду ции 1 фаговая частица на 10 бактерий Эффективность трансдукции пеницилли- нового маркера популяцией гибридных
практической работы по конструирова- фаговых частиц составила 15 %. Доля
нию банков генов это превосходство выражается в гораздо меньшей вероятности получения ложного банка - популяции негибридных бляшкообразующих частиц, полученных после упаковки смеси расщепленной и лигированной ДНК вектора и клонируемой ДНК.
Сравнение эффективности образования гибридных молекул ДНК на основе
предлагаемого ФПВ MYF 131 (строка 35 высеяли на газон чувствительных бак3,0-10 на 0,1 мкг основе вектора- го образца А47.1АВ 7, титр 0,5,-10 на а) показьгеает, что 40 Ар зования гибридных редлагаемого веканном примере в
тер пол ти ке
фа де 45 явл ис то но
В плане практической работы по конструированию банков генов это превосходство предлагаемого вектора выражается в большем количестве гибридных
молекул, получаемых в расчете на одй- 50 Р° дополнению генома фазмиды до наковре количество клонируемой ДНК.
П р и м е р 4. Использование гибридного ФПВ /(Р MYF 131 для генетического анализа. Проведен поиск генов комплементирующих мутаций аго G и pro А E.coli. Обнаружение указанных генов необходимо для конструирования микроорганизмов - продуцентов аминокислот.
55
пакуемого размера.
Формула изобретени
1. Фагово-плазмидный вектор, пре назначенный для получения и анализа банка генов, имеет размер молекулы 33 т.п.н. и состоит из следующих эл ментов:
912
Банк генов E.coli получен для обнаружения в нем ФПВ, несущих ген аго G. Одновременно определяет частоту встречаемости ФПВ, несущих гены пролиново- го оперона. Поиск ФПВ, содержащих искомые гены, проводили с помощью комплементации соответствующих ауксотроф- ных мутаций бактерий штамма E.coli АВ3252 pro А, аго G. Инфицированные
среды, содержащие пенициллин, а также стрептомицин, являющийся селективным маркером реципиентного штамма, и не содержащие либо пролин, либо аромати-
ческие аминокислоты - триптофан, тирозин и фенилаланин.
Титр популяции ФПВ составлял 3,1х х10 фаговьос частиц. Титр трансдук- тантов, выросших на полной среде с
пенициллином, равнялся 4,5-10 при множественности инфекции при трансдук- ции 1 фаговая частица на 10 бактерий. Эффективность трансдукции пеницилли- нового маркера популяцией гибридных
Ар колоний, прототрофных по пролину, среди всех Ар колоний состав,ила 1,7х . Для колоний, прототрофных по триптофану, тирозину и фенилаланину, УЗ эта величина составляла О.З-Ю.- Из колоний Ар , аго G. выделили плазмидную ДНК, как описано в примере 3. ДНК упаковали in Vitro в капсид фагаД , как описано в примере 3, и
Ар
терий. Из отдельных фаговых колоний получили препараты фагов высокого титра, которые трансдуцировали маркер аго С сцепленно (100%) с маркером
Ар
Таким образом, получены гибридные фазмиды, производныеД р MYF 131, содержащие искомый ген аго G. Предлагаемый векторД р MYF 131 является первым ФПВ, котор 1й можно использовать для получения популяции . только гибридных молекул благодаря новому принципу для фаговых вектоР° дополнению генома фазмиды до
пакуемого размера.
Формула изобретения
1. Фагово-плазмидный вектор, предназначенный для получения и анализа банка генов, имеет размер молекулы 33 т.п.н. и состоит из следующих элементов:
Гены и регуляторные области, необходимые и достаточные для литкчес- кого цикла развития фага А , в том числе левое плечо ДНК вегетативного фагау 47.1АВ от участка m (координа- та О т.п.н,) до сайта расщепления рестриктазой Sma I (координата 19.3 т..), правое плечо ДНК вегетативного f gt WES о т сайта расщепления Ваш HI (координата 34,5 т.п.н.) до участка т (координата 48,5 т,, п. и.), координаты приведены по .ДНК фага/| дикого типа.
Участок инициации репликации (ori) из ппазмиды pUC 19 размером О, 6 т.п.н
Ген J3-лгистамазы, обеспечивающий устойчивость клеток к ампициллину
(маркер Ар , размер 1,1 т.п.н.) из плазмиды pUC 19.
Полилинкер - последовательность молекулы ДНК, имеющая набор близко расположенных участков расщепления ряда рестриктаз: Hind III, Sph I, Pst I, Sal GI, Xba I, Bam HI, Sma I, Kpn I, Sac I, ECO RI, в том числе уникального участка рестрикции: Есо RI, Sac I, Sal GI, Xba I,
Уникальные участки рестрикции в несущественных для литического развития областях фагово-плазмидного вектора: Есо 47 III, Хта III.
Уникальные участки расщепления для рестриктаз Nru I, Sna BI,, Sac II Asu II в областях фагово-плазмидного
вектора, существенных для ее развития 35 17, расщепляют рестриктазой Ват HI и
по литическому пути,
Ген с 1, кодирзтощий термочувствительный белок-реп рессор фаг, с мутацией 857.
Chi - сайт в гене J фага /I , необходимый для получения высокого титра
Составитель Н.Кузенкова Редактор Л.Веселовская Техред л,Сердюкова Корректор А.Тяско
Заказ 268Тираж 490Подписное
ВНРШПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
ПроизводстЕ1енно-полиграфическое предприятие, г, Ужгород, уп. Проектная, 4
фага в отсутствие продуктов гена red и gam.
Гены А, В и S в амбер-форме, что позволяет литическое развитие фагово- плазмидного вектора и его гибридов только на штамма : E.coli, содержащих амбер-супрессор Sup .
Емкость вектора одинакова для каждой из указанных рестриктаз и составляет 7-21 т. п,ь;.
Возможными хозяевами для плазмид- ного размножения фагово-плазмидного вектора yt Р MYF 131 являются, штаммы E.coli, адсорбирующие фаг, в которых может происходить- репликация coli-no- добных плазмид; Сактерии TG 1 ( ).
2, Способ конструирования фагово- плазмидного вектора/ р MYF 131, предназначенного для юлучения и анализа банков генов, зак:1ючающийся в том, что ДНК фага 47, 1А13 и плазмиды JfaN 7 расщепляют 1:1естриктазой Cfr 91 , лигируюТг упаковыпают in vitro и вы- севают на пермиссивный газон E.coli W 3350, полученный гибрид Лр MYF 15, содержащий встройку плазмиды в левый сайт расщепления C fr 91 , гидролизуют эндон:уклеазой Есо RI и лигируют с расщепленным этой же эндонуклеазой фагом }, gt WES, упе.ковывают in vitro, отбирают по маркерам правого плеча фага Д gt WES (imm /1 ) и плазмиды IfaN7 (sup F) , этот гибрид названный/ р MYF
лигируют с плазми ой pUC195 расщепленной этой же рестриктазой, трансформируют бактерии E.coli TG 1 (2) и отбирают по маркеру Ар и термочувствительности (ts), из которых выделяют фагово-плазмидный гибрид Ар MYF 131.




Изобретение относится к биотехнологии, в частности к генной инженерии, и представляет собой фагово-пла- змидный вектор (ФПВ)А pMYF 131 для прямого отбора рекомбинатных молекул ДНК, их генетического анализа и способ его конструирования. Цель изобретения - создание ФПВ с повьшенной эффективностью клонирования, позволяющего упростить процесс получения банков генов и облегчить физический и генетический анализ рекомбинатных клонов. Для этого из предшественника ФПВ удаляют часть молекулы ДНК, не содержащей генов, существенных для развития фага. В результате размер векторной молекулы ДНК становится меньше критического размера, необходимого для упаковки в фаговый капсид. Для поддержания векторной молекулы дак в клетке фрагмент, содержащий все гены и участки ДНК, существенные для развития фага, соединен с фрагментом плазмидной ДНК. Этот фрагмент обеспечивает автономную репликацию ФПВ в клетке, возможность селекции клеток. Фрагменты ДНК, содержащие существенные гены для фагового развития, участок инициации плазмидной репликации и ген устойчивости к антибиотику, не содержат сайтов расщепления для ряда рестриктаз. Введение уникальных сайтов расщепления для этих рестриктаз сообщает полученной молекуле ДНК свойства вектора для ФВПАрМУР 131. 2 с.п. ф-лы; 2 табл. § О) to 00


| Loenen W | |||
| А.М, Brammar W.T | |||
| А bactcriophage lambda vector for cloning large DNA fragments made with several restriction ensymes | |||
| Gene, 1980, 10(3),249 | |||
| Brenner S.T, Cesareni T, Karn T | |||
| Phasmids hibrids between COSEI plas- mids and E | |||
| coli bacteriopkage lanib- da | |||
| Gene, 1982.17,27 | |||
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
Авторы
Даты
1986-12-30—Публикация
1985-07-09—Подача