Изобретение относится к области медицины, а именно клинической биохимии.
Целью изобретения является создание активированной матрицы для иммобилизации белков, более устойчивой и специфичной в сравнении с известной.
Для достижения поставленной цели используют новые полисахаридные матрицы, которые получают в три стадии: активация полисахаридного носителя эпихлоргидрином; раскрытие эпоксидного цикла аминокислотной, т. е. введение карбоксильной группы; этерификация N-оксисукцинимидом карбоксильной группы.
Схема получения активной матрицы I. П-OH 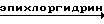 П-O-CH2-
П-O-CH2-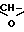 CH2
CH2
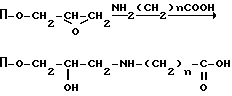 III. П-O-CH2-
III. П-O-CH2-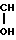 -CH2-NH-(CH2)n-
-CH2-NH-(CH2)n-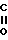 -OH
-OH 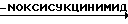 П-O-CH2-
П-O-CH2-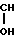 -CH2-NH-(CH2)n-
-CH2-NH-(CH2)n-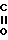 -ON
-ON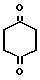
Матрицы, полученные по этой схеме на основе сефарозы 4Б, содержат 5-10 мкмоль активных эфирных групп в 1 мл сорбента. Использование целлюлозы и сефадекса G - 200 в качестве полисахаридного носителя приводит к получению матрицы с содержанием эфирных групп 2-4 мкмоль в 1 мл сорбента.
Все эти сорбенты могут применяться для иммобилизации белков, в частности транскортина, секстероидсвязывающего глобулина, бычьего сывороточного альбумина, иммоноглобулинов, а также других лигандов, содержащих первичную аминогруппу.
Ниже приведены примеры получения активных матриц на основе различных полисахаридных носителей с применением различных аминокислот (n = 2,3).
П р и м е р 1. Получение матрицы на основе агарозы с применением
γ - аминомасляной кислоты.
I стадия. Получение эпоксиагарозы.
К суспензии 10 мл сефарозы 4Б (Pharmacia Fine Chemicals, Sweden) в 60 мл 0,4 М едкого натра, нагретой до 40оС, при перемешивании прибавляют 4 мл эпихлоргидрина. Суспензию перемешивают 2 ч при 40оС, после чего на стеклянном фильтре отмывают от избытков реагентов.
Найдено: 1 мл геля содержит 30-40 мкмоль эпоксидных групп.
II стадия. Получение карбоксильного производного агарозы.
К раствору 1 г γ -аминомасляной кислоты в 20 мл 1 М раствора едкого натра прибавляют 10 мл полученной эпоксиагарозы. Смесь перемешивают 2 ч при 40оС. Полученное производное агарозы промывают сначала 0,2 М соляной кислотой, затем дистиллированной водой.
Найдено: 1 мл геля содержит 28-35 мкмоль карбоксильных групп.
III стадия. Этерификация карбоксильных групп.
Для связывания лабильных карбоксильных групп производное агарозы 30-40 мин перемешивают в 0,1 М раствора едкого натра, затем отмывают дистиллированной водой до нейтральной реакции промывных вод (рН 7). Агарозу постепенно переводят в диоксан. К суспензии 10 мл карбоксиагарозы в 30 мл диоксана прибавляют 0,35 г N-оксисукцинимида и после его полного растворения 0,62 г дициклогексилкарбодиимида. Смесь перемешивают 18-20 ч при комнатной температуре. Сорбент отфильтровывают и промывают диоксаном (80 мл), метанолом (40 мл) и снова диоксаном (40 мл).
Найдено: 1 мл геля содержит 7-10 мкмоль активных N-оксисукцинимидных эфирных групп.
П р и м е р 2. Получение активированной матрицы на основе целлюлозы с использованием β -аланина.
Активированную β -аланинцеллюлозную матрицу получают, как описано в примере 1, только в стадии 1 при получении эпоксицеллюлозы реакцию проводят в 1 М растворе едкого натра. При этом получают продукт, содержащий 16-18 мкмоль эпоксидных групп в 1 мл сорбента. В стадии II вместо γ -аминомасляной кислоты используют β -аланин. Продукт реакции содержит 13-15 мкмоль карбоксильных групп в 1 мл сорбента. Стадию III проводят без изменения. Получают активированную матрицу с содержанием 2-4 мкмоль эфирных групп в 1 мл сорбента.
П р и м е р 3. Получение активированной матрицы на основе сефадекса с использованием γ -аминомасляной кислоты.
Матрицу на основе сефадекса получают, как описано в примере 1, только вместо агарозы берут сефадекс G - 200 (Pharmacia Fine Chemicals, Sweden).
Найдено: содержание эпоксидных групп 13-16 мкмоль/мл, содержание карбоксильных групп 11-14 мкмоль/мл геля, содержание эфирных групп 1-3 мкмоль/мл геля. (56) Cuatrecasas P. and Parikh I. Adsorbents for Affinity Chromatography. Use of N - Hydroxysuccinimid Esters of Agarose. - Biochemistry, 1972, v. 11, p. 2291-2299.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОРБЕНТ ДЛЯ СВЯЗЫВАНИЯ ТИРОКСИНА | 1981 |
|
SU1281005A1 |
| КОНЪЮГАТ ПОЛИСАХАРИДНОГО АНТИГЕНА С ПОЛИЭТИЛЕНИМИНОМ В КАЧЕСТВЕ ИММУНОСОРБЕНТА ДЛЯ ВЫЯВЛЕНИЯ СТРЕПТОКОККОВЫХ И ПНЕВМОКОККОВЫХ ИНФЕКЦИЙ | 1990 |
|
RU2027190C1 |
| СОРБЕНТ ДЛЯ ХРОМАТОГРАФИИ | 2009 |
|
RU2451544C2 |
| 2- -Бензоил амидогептиламино-4-окси -триазинилагароза,как сорбент для гидрофобной хроматографии гликозидаз | 1977 |
|
SU660975A1 |
| N-ОКСИСУКЦИНИМИДНЫЕ ЭФИРЫ N-АЦЕТИЛТИРОНИНОВ В КАЧЕСТВЕ ПОЛУПРОДУКТОВ ДЛЯ СИНТЕЗА КОНЪЮГАТОВ ТИРЕОИДНЫХ ГОРМОНОВ С АЛЬБУМИНОМ | 1983 |
|
SU1100846A1 |
| СОРБЕНТ ДЛЯ УДАЛЕНИЯ ИММУНОГЛОБУЛИНОВ | 2008 |
|
RU2389022C2 |
| ПРОИЗВОДНОЕ КОРИЧНОЙ КИСЛОТЫ, ПРОИЗВОДНОЕ КОРИЧНОЙ КИСЛОТЫ И ПОЛИСАХАРИДА, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО КОРИЧНОЙ КИСЛОТЫ И ГЛИКОЗАМИНОГЛИКАНА, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО КОРИЧНОЙ КИСЛОТЫ И ПОЛИАМИНОСАХАРИДА, СПОСОБ ПОЛУЧЕНИЯ СШИТОГО ПРОИЗВОДНОГО КОРИЧНОЙ КИСЛОТЫ И ПОЛИСАХАРИДА | 1995 |
|
RU2169136C2 |
| Способ получения иммобилизованных нуклеофильных соединений | 1983 |
|
SU1690544A3 |
| Производное сефарозы 4 @ с аффинантом- @ (11 @ ,17 @ )-11,17-дигидрокси-3,20-диоксопрегн-4-ен-21-ил @ тио @ уксусной кислоты,как биоспецифический сорбент для аффинной хроматографии | 1983 |
|
SU1162815A1 |
| Способ получения адсорбентов,содержащих аминогруппы | 1982 |
|
SU1054353A1 |
Изобретение относится к клинической биохимии. Цель изобретения - создание активированной матрицы для иммобилизации белков, более устойчивой и специфичной. К суспензии сефарозы 4B в 60 мл едкого натра при перемешивании прибавляют 4 мл эпихлоргидрина. Затем на стеклянном фильтре отмывают от избытков реагентов. К раствору γ-аминомасляной кислоты в растворе едкого натра прибавляют 10 мл полученной эпоксиагарозы. Смесь перемешивают 2 ч при 40С. Полученное производное агарозы промывают соляной кислотой, а затем дистиллированной водой. Производное агарозы перемешивают в растворе едкого натра, затем отмывают дистиллированной водой до нейтральной реакции. Агарозу постепенно переводят в диоксан. К суспензии карбоксиагарозы в 30 мл диоксана прибавляют N-оксисукцинимид и после его полного растворения дициклогексилкарбодиимид. Сорбент отфильтровывают и промывают диоксаном, метанолом и снова диоксаном.
Активированная матрица формулы
П-O-CH2-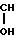 -CH2-NH-(CH2)n-
-CH2-NH-(CH2)n-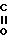 -ON
-ON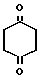
где П - остаток агарозы, сефадекса или целлюлозы,
n = 2 или 3, для иммобилизации белков.
Авторы
Даты
1994-01-30—Публикация
1981-11-02—Подача