Изобретение относится к способу получения новых производных гидразин- угольной кислоты формулы
R, N - NH - COOR,
(1)
где R,- циклоалкилиден Cg- С,2 , инданилиден или группа формуль
А - С в которой А - фенильная груп«2 0
па, которая может быть замещена одним или несколькими заместителями, выбранными из галоген-, нитро-, амино-, гидрокси-, низшей алкокси-групп, или А обозначает индолил, низший алкил, циклогексшц
R - водород, низший алкил, ал-, кил С,
f5
R, - С,М5
С алкил.
25
Указанные соединения обладают свойствами повышать прирост веса полезных животных.
Целью изобретения является разработка способа получения новых производных гидразинугольной кислоты, обладающих более высокой эффективностью в повьш1ении прироста веса животных.
Пример 1. Получение метилового эфира 3-(о6-изопропил-бензилиден)- гидразинугольной кислоты.
К раствору 44,46 г (0,3 моль) изо- бутирофенона и 200 мл метанола сначала добавляют 3 мл уксусной кислоты и после этого 27 г метилкарбазата
К раствору 39,65 г (0,3 моль) 1-ин- 5 данона и 300 мл метанола сначала добавляют 3 мл уксусной кислоты и после этого 27 г (0,3 моль) метилкарбазата. Реакционную смесь нагревают в течение 1 ч до температуры кипения, после этого осветляют кипячением с углем и фильтруют. Фильтрат охлаждают водой со льдом. Получают 43,7 г целевого соединения. Полученные белые кристал-i лы плавятся при 155-156°С. В результате упаривания маточника приблизитель но до четверти первоначального объема получают еще дополнительное количество (12,3 г) целевого соединения. Выход 91,5%.
П р и м.е р 4. Получение метилового эфира 3-(о-амино-бензилиден)-гид- разинугольной кислоты.
Опыт проводят, как описано в примере 3, с той лишь разницей, что в качестве исходного вещества берут 36,35 г (0,3 моль) 2-аминобензапьде- гида. Получают 50 г целевого соединения. Вькод 86,35%. Т.пл. 149-150°С.
Пример 5. Получение метилового эфира З-циклооктилиден-гидразин- угольной кислоты.
Опыт проводят, как описано в примере 1, с той лишь разницей, что в качестве исходного соединения исполь20
1 .f i I iw i±,iiiV4 4 -«- -..-.n-ir /- хл V
Реакционную смесь нагревают в течение 5 зуют 37,86 г (0,3 моль) циклооктанона. Получают 49 г целевого соединения.
, о ,
1 ч до температуры кипения, после этого осветляют и при пониженном давлении испаряют до половины первоначального объема. Остаток охлазсдают. Осаждается белое маслообразное вещество. Получают 64,2 г целевого соединения. Выход 97,3%., Т.пл. 78-80 С. Продукт можно очистить перекристаллизацией из бензина.
Пример 2. Получение метилового эфира Э-(3 -индолил-метилен)7 гидразинугольлой кислоты.
К раствору 36,29 г (0,25 моль) инВыход 82,5%. Т.пл. 93-94 С.
Пример 6. Получение метилового эфира 3-(п-нитро-бензилиден)-гид О разинугольной кислоты.
Опыт проводят, как описано в примере 3, с тем различием, что в качестве исходного соединения применяют 45,34 г (0,3 моль) п-нитро-бензальде 5 гида. Получан т 61,5 г целевого соединения. Зыход 91,9%. Т.пл. 212-213 с.
Пример 7. Получение метилового эфира 3-(t -фенил-гексадецилиден)- дол-З-альдепада и 300 мл метанола . гидразинугольной кислоты, чала добавляют 3 мл уксусной кислоты 47,48 г (0,15 моль) пальмитофено- и после этого 0,25 моль метилкарбаза- „а и 13,5 г (0,15 моль) метилкарбазата . Реакционную смесь в течение 1 ч подвергают взаимодействию аналогично нагревают до температуры кипения, пос- примеру 1. Получают 47,3 г (81,3%) ле этого осветляют. Из фильтрата при 55 целевого соединения. Выход 81,3%.
добавлении 50 мл воды выпадают рово- вые кристаллы. Получают 51,5 г целевого соединения. Выход 94,9%. Т.ш1.144-145 с.
Т.пл. 68-69°С.
Пример 8. Получение метилового эфира 3-(1 -бензил-пропилиден)- гидразинугольной кислоты.
Пример 3. Получение метилового эфира 3-(1 -инданилиден-гидразин- угольной кислоты.
К раствору 39,65 г (0,3 моль) 1-ин- данона и 300 мл метанола сначала добавляют 3 мл уксусной кислоты и после этого 27 г (0,3 моль) метилкарбазата. Реакционную смесь нагревают в течение 1 ч до температуры кипения, после этого осветляют кипячением с углем и фильтруют. Фильтрат охлаждают водой со льдом. Получают 43,7 г целевого соединения. Полученные белые кристал-i лы плавятся при 155-156°С. В результате упаривания маточника приблизитель но до четверти первоначального объема получают еще дополнительное количество (12,3 г) целевого соединения. Выход 91,5%.
П р и м.е р 4. Получение метилового эфира 3-(о-амино-бензилиден)-гид- разинугольной кислоты.
Опыт проводят, как описано в примере 3, с той лишь разницей, что в качестве исходного вещества берут 36,35 г (0,3 моль) 2-аминобензапьде- гида. Получают 50 г целевого соединения. Вькод 86,35%. Т.пл. 149-150°С.
Пример 5. Получение метилового эфира З-циклооктилиден-гидразин- угольной кислоты.
Опыт проводят, как описано в примере 1, с той лишь разницей, что в качестве исходного соединения исполь
, о ,
Выход 82,5%. Т.пл. 93-94 С.
Пример 6. Получение метилового эфира 3-(п-нитро-бензилиден)-гид О разинугольной кислоты.
Опыт проводят, как описано в примере 3, с тем различием, что в качестве исходного соединения применяют 45,34 г (0,3 моль) п-нитро-бензальде 5 гида. Получан т 61,5 г целевого соединения. Зыход 91,9%. Т.пл. 212-213 с.
Пример 7. Получение метилово го эфира 3-(t -фенил-гексадецилиден)- гидразинугольной кислоты, 47,48 г (0,15 моль) пальмитофено- „а и 13,5 г (0,15 моль) метилкарбазат подвергают взаимодействию аналогично примеру 1. Получают 47,3 г (81,3%) целевого соединения. Выход 81,3%.
Т.пл. 68-69°С.
Пример 8. Получение метилового эфира 3-(1 -бензил-пропилиден)- гидразинугольной кислоты.
Опыт проводят аналогично примеру 1 с тем различием, что в качестве исходного соединения используют 44,46 г (0,3 моль) этилбензилкетона. Получают 66 г целевого соединения. Выход г 99,9%. Т.пл. SiD c.
Пример 9. Получение метилового эфира 3-(2, 4 -дигидрокси-бензили- ден)-гидразинугольной кислоты.
К раствору 34,5 г (0,25 моль) 2,4-10 дигидроксибензальдегида и 300 мл метанола сначала добавляют 3 мл уксусной кислоты и после этого 22,5 г (0,25 моль) метилкарбазата. Реакционную смесь нагревают в течение 2 ч до t5 температуры кипения, после этого раствор осветляют кипячением с углем, фильтруют и фильтрат охлаждают. Получают 49,2 г целевого соединения. Выход 93,4%. Т.пл. 205°С.20
Пример 10. Получение метилового эфира 3-(3, 4 , 5 -триметокси- бензилиден)-гидразинугольной кислоты.
30,86 г (0,2 моль) 3,4,5-триметок- си-бензальдегида и 18 г (0,2 моль) 25 метилкарбацата подвергают взаимодействию аналогично примеру 1. Получают 48,6 г целевого соединения. Выход 86%. Белые кристаллы плавятся при 140-141°С.30
Пример 11. Получение метилового эфира 3-(l -этил-пpoпилидeн)- гидpaзинyгoльнoй кислоты.
Опыт проводят, как описано в примере 9, с тем различием, что в ка- 35 честве исходного соединения используют 34,4 г (0,4 моль) диэтилкетона. Получают 57,15 г целевого соединения в виде белых кристаллов. Выход 90,4%. Т.пл. 66-67 С (после перекристалли- 40 зации из бензола).
Пример 12. Получение метилового эфира 3-(3 -этокси-4-гидрокси- бензилиден)-гидразинугольной кислоты.
Опыт проводят, как описано в приме-45 ре 9, с тем различием, что в качестве исходного соединения используют 41,6 г .(0,25 моль) З-этокси-4-гидрокси-бенз- альдегида. Получают 56,3 г целевого соединения в виде белых кристаллов. . О Выход 94,6%. Т.пл. 172-173°С.
П р и м .е р 13. Получение метилового эфира 3-(1 -этил-пентилиден)-гидразинугольной кислоты. 55
Опыт проводят, как описано в примере 9, с тем различием, что в качестве исходного соединения используют 34,25 -г (0,3 моль) этил-(н-бутил)кетона. Получают 35,4 г целевого соединения. Выход 63,4%. Т.пл. 67-68°С.
Пример 14. Получение метилового эфира З-(циклопентилиден)-гидразинугольной кислоты.
Опыт проводят, как описано в примере 1, с тем различием, что в качестве исходного соединения используют 33,6 г (0,3 моль) циклопентанона. Целевое соединение в виде белых кристаллов получают в количестве 49,25 г. Выход 89,1%. Т.пл. 75°С.
Прим е- р 15. Получение метилового эфира 3-((Л-этил)-п-гидрокси-бен- зилиден)-гидразинугольной кислоты.
Опыт проводят, как описано в примере 1 , с тем различием, что в качестве исходного соединения используют 37,54 г (0,25 моль) п-гидрокси-иро- пиофенона. Получают 43,8 г целевого соединения в виде белых кристаллов. Выход 78,85%. Т.пл. 167°С.
Пример 16. Получение метилового эфира 3-(циклододецш1иден)-гидразинугольной кислоты.
Опыт проводят, как описано в примере 9, с тем различием, что в качестве исходного соединения используют 45,6 г (0,25 моль) циклододеканона. Целевое соединение получают в виде белых кристаллов в количестве 52,5 г. Выход 83,2%. Т.пл. 141-142 с.
Пример 17. Получение метило.вого эфира 3-(циклогексш1-метил)-гидр.зинугольной кислоты,
К растору 11,2 г (0,1 моль) цикло- гексанкарбоналя и 100 мл метанола сначала добавляют 2 мл .уксусной кислоты и после этого 9,0 г (0,1 моль) метилкарбацата. Реакционную смесь нагревают в течение 2 ч до температуры кипения, затем осветляют, фильтруют и фильтрат испаряют при пониженном давлении. Получают 15,6 г целевого соединения в виде бе.пых кристаллов. Выход 84,8%. Т.пл. 103°С.
Пример 18. Получение метилового эфира 3-(4 -гидрокси-3 -ннтро- бензилиден)-гидразинугольной кислоты.
Опыт проводят, как описано.в примере 3, с тем различием, что в качестве исходного соединения использую 33,4 г (0,2 моль) 4-гидрокси-З-нитро- бензальдегида. Получают 41,65 г целевого соединения. Выход 87,1%. . Т.пл. ПЗ-Пб С.
.Пример 19. Получение метилового эфира 3-(2 -нитро-бензилиден)- гидразинугольной кисло-х Ы.
Опыт проводят, как описано в примере 9, с тем различием, что в качест-5 ве исходного соединения используют 30,2 г (0,2 моль) 2-нитро-бензаль- дегида. Получают 36,85 г целевого соединения в виде желтоватых кристаллов. Выход 82,6%. Т.пл. 152°С Ш
Пример 20. Получение метилового эфира 3-(4,5 -диметокси-2 -нит- робензилиден)-г1щразинугольной кислоты.
указанного
Опыт проводят, как описано в при- f5 Т.пл. . мере 9, с тем различием, что в качестве исходного соединения используют 52,8 г (0,25 моль) 2-нитро-4,5-диме- токси-бензальдегида. Получают 57,6 г
(92,4%) указанного в заголовке со динения. Т.пл. .
Пример 25. Метиловый эфи 3-(2 -циклогексшщиклогексилиден) карбазиновой кислоты.
35,66 г (0,2 моль) 2- циклогекс циклогексанона растворяют в 250 м метанола и прибавляют 18 г (0,2 м метилкарбазата и 3 мл уксусной ки ты. Через 2 ч осветляют, выпарива и из полученного масла выделяют б лые кристаллы. После суспендирова в бензине получают 46,4 г (87,2%) в названии соединения.
Пример 26. Метиловьм эфи (2,4-дихлорбензнлиден)карбазиново кислоты.
Исходя из 43,75 г (0,25 моль)
целевого соединения. Выход 81,5%. Жел-20 2,4-дихлорбензальдегида и 22,5 г
тый продукт плавится при 230-231 С.
Пример 21. Получение метилового эфира 3-(3 -хлор-5 -нитро-бен- зилиден) -гидразинугольной кислоты .
Опыт проводят, как описано в при- мере 3, с тем различием, что в качестве исходного соединения используют 3-хлор-5-нитро-бензальдегида.
Пример 22. Получение метило(0,25 моль) метилкарбазата, как описано в примере 1.,и получают 53,2 г (86,2%) указанного в названии соединения. Т.пл. 156-157°С.
Пример 27. Метиловый эфир 3-(3 4 -дихлорбензилиден)-карбазино- вой кислоты.
Исходят из 43,75 г (0,25 моль) 3,4-дихлорбензальдегида и 22,5 г
вого эфира 3-(о -этил)-п-хлор-бензили-30 (0,25 моль) метилкарбазата и получаден)-карбационовой кислоты.ют 57,25 г (92,7%) указанного в назОпыт проводят, как описано в примере 1 с тем различием, что в качестве исходного соединения используют
35
п-хлор-пропиофенон.
Пример 23. Метиловьй эфир . 3- (о4-циклопропил-4 -метокси)-бензи- лиден-карбазиновой кислоты.
К раствору 17,6 г (0,1 моль) цик- лопропил-4-метоксифенилкетона в 100 мл метанола прибавляют 3 мл уксусной кисло.ты и затем еще 9,0 г (0,1 моль) метилкарбазата.
Реакционную смесь кипятят в течение 5 ч, затем осветляют и фильтруют в горячем состоянии. Фильтрат выпаривают под разряжением, обрабатывают 10 мл эфира к выделившиес,я белые кристаллы отфильтровывают. Получают
вании соединения« Т.пл. 154-155 С.
П р-и м е р 28. Метиловый эфир 3-(2 -хлор-б -фторбензилиден)-карба- зиновой киспоты.
Исходят из 47,65 г (0,3 моль) 2- хлор-6-фторбензальдегида и 27 г (0,3 моль) метилкарбазата, как описано в примере 1, и получают 45 г 40 (65,2%) указанного в названии соединения. Т.пл. 152-153 с.
Эффективность соединений общей
формулы (Т), способствунлцая увеличению прироста веса животныхj доказана 45 следующими опытами.
А. В качестве испытуемых животных использовали свиней. Для каждого теста использовали группы животных по шесть шт. и каждый опыт повторяли с каждой группой животных по три раза
18,3 г (73,7%) соединения, указанного-50 11/11 с Г Тля кормления опытной группы свиней
в заголовке. Т.пл, С.применяли корм, содержащий 50 мг/кг
Пример 24. Метиловьш эфир « к
(4 хлор-3 -нитробензилиден)-карба- кислоты.
Исходят из 18,55 г (0,1 моль) 4- хлор-3-нитробензальдегида и 9 г (0,1 моль) метилкарбазата и, как описано в примере 1, получают 23,8 г
испытуемых соединений. Откорм животных осуществляли при одинаковых усло- 55 ВИЯХ и все :группы животных откармлива ли одинаковым количеством корма одинакового состава. Сравнительная группа получала корм в таком же количестве, однако с содержанием флавомицина.
указанного
Т.пл. .
(92,4%) указанного в заголовке соединения. Т.пл. .
Пример 25. Метиловый эфир 3-(2 -циклогексшщиклогексилиден)- карбазиновой кислоты.
35,66 г (0,2 моль) 2- циклогексил- циклогексанона растворяют в 250 мл метанола и прибавляют 18 г (0,2 моль метилкарбазата и 3 мл уксусной кислоты. Через 2 ч осветляют, выпаривают и из полученного масла выделяют белые кристаллы. После суспендирования в бензине получают 46,4 г (87,2%) в названии соединения.
Т.пл. .
Пример 26. Метиловьм эфир (2,4-дихлорбензнлиден)карбазиновой кислоты.
Исходя из 43,75 г (0,25 моль)
(0,25 моль) метилкарбазата, как описано в примере 1.,и получают 53,2 г (86,2%) указанного в названии соединения. Т.пл. 156-157°С.
Пример 27. Метиловый эфир 3-(3 4 -дихлорбензилиден)-карбазино- вой кислоты.
Исходят из 43,75 г (0,25 моль) 3,4-дихлорбензальдегида и 22,5 г
вании соединения« Т.пл. 154-155 С.
П р-и м е р 28. Метиловый эфир 3-(2 -хлор-б -фторбензилиден)-карба- зиновой киспоты.
Исходят из 47,65 г (0,3 моль) 2- хлор-6-фторбензальдегида и 27 г (0,3 моль) метилкарбазата, как описано в примере 1, и получают 45 г (65,2%) указанного в названии соединения. Т.пл. 152-153 с.
Эффективность соединений общей
формулы (Т), способствунлцая увеличению прироста веса животныхj доказана следующими опытами.
А. В качестве испытуемых животных использовали свиней. Для каждого теста использовали группы животных по есть шт. и каждый опыт повторяли с каждой группой животных по три раза.
ля кормления опытной группы свиней
« к
испытуемых соединений. Откорм животных осуществляли при одинаковых усло- 55 ВИЯХ и все :группы животных откармливали одинаковым количеством корма одинакового состава. Сравнительная группа получала корм в таком же количестве, однако с содержанием флавомицина.
Контрольная группа получала корм в таком же количестве, но без испытуемого соединения.
Ежедневно регистрировали увеличение 5 веса и рассчитывали ежедневный средний прирост веса в весовых процентах по следующей формуле:
Средний дневной прирост веса
в опытной группе .
Средний дневной прирост веса
в контрольной группе
fO
X 100
Количество корма, скармливаемое в соответствукицей опытной группе, де- лили на прирост веса, достигнутый в этом опыте, и полученный таким образом критерий относили к критерию, рассчитанному аналогичным образом для контрольной rpynnbf. Это значение есть количество корма, которое в соответствующей опытной группе дает увеличение веса 1 кг, считая на количество корма, которое в контрольной групт пе дает увеличение веса 1 кг, в весо- вых процентах.
Полученные результаты приведены в табл.1.
По примеру:
6.
21
22 Флавомицин
Карбадокс (структурный
аналог)
8
Таблица 1
463 345
336
82 95
100,,.
i Б. Опыт, описанньй в пункте А, проводили с группой свиней по 50 mt,. Период откорма 60 дн. Доза испытуемого соединения 50 мг/кг. Результаты сравнивали с результатами опытов, полученными с кормами, содержащими фла- вомицин. Результаты, полученные с фла- вомицином, были приняты за 100%.
Полученные результаты представлены в табл.2.
Таблица 2
2,23
96,2
91299503
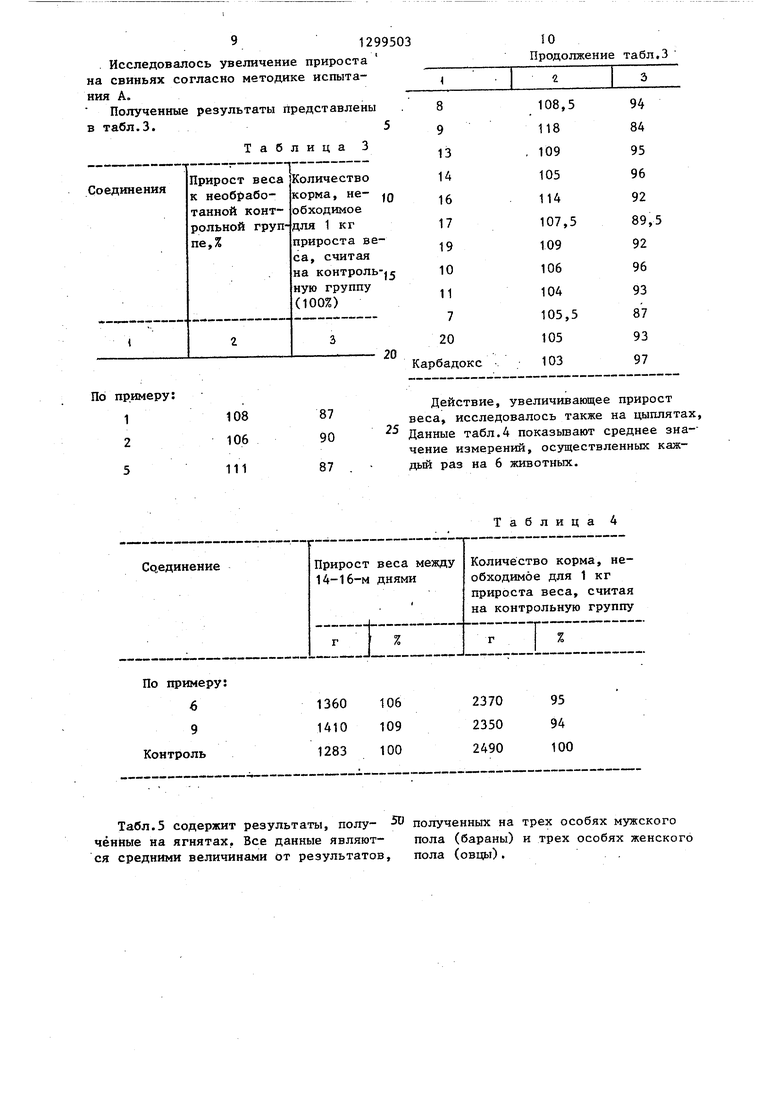
Исследовалось увеличение прироста на свиньях согласно методике испытания А„-
Полученные результаты представлены в табл.3.5
Таблица 3
Табл.З содержит результаты, полу- - полученных на трех особях мужского чённые на ягнятах. Все данные являют- пола (бараны) и трех особях женского ся средними величинами от результатов, пола (овцы).
10 Продолжение табл.З
8 9 13 14 16 17 19 10 11 7
20 арбадокс
108,5
118
109
105
114
107,5
109
106
104
105,5
105
103
94
84
95
96
92
89,5
92
96
93
87
93
97
Действие, увеличивающее прирост веса, исследовалось также на цыплятах, Данные табл.4 показьгоают среднее зна-- чение измерений, осуществленных каждый раз на 6 животных.
Таблица 4
Из результатов опытов табл.5 видно, что животные, которых откармлива ли с применением новых производных гидразинугольной кислоты в соответст ВИИ с изобретением, показали значительно более высокий прирост веса, чем животные контрольной и сравнительной групп. Одновременно такого же прироста веса можно достигнуть со значительно меньшим количеством корма, что указьгоает на существенно лучшую реализацию кормов (усваивае- мость).
Формула изобретения
Способ получения производных гидразинугольной кислоты общей формулы
R, N - NH - COORj,
Редактор Н. Марголина
Составитель Л. Иоффе
Техред Л.Сердюкова Корректор А. Обручар
Заказ 905/63Тираж 372 Подписное
ВНИШШ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная,4
Таблица 5
25
30
35
40
где R, - циклоалкилиден Cg- С,г , ин- данилиден или группа формуль ; Д -
RI
в которой А - фенильная группа, которая может быть замещена одним или несколькими заместителями, выбранными из галоген-, нитро-, амино-, гидрокси- низшей алкокси-групп или А - индолил, низший алкил, циклогексил;
RJ- водород, низший алкил, алкил
15
С,- С алкил, о тличающийся тем, что карбонильное соединение общей формулы R,0, где имеет ука:занное значение, подвергают взаимодействию с метилкарбазатом с последующим выделением целевого продукта.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных пиридазино @ 4,5- @ хиноксалин-5,10-диоксида | 1981 |
|
SU1165235A3 |
| Способ получения производных хиноксалиндиоксида | 1976 |
|
SU1220570A3 |
| Способ получения производных хиноксалин-1,4-диоксида | 1982 |
|
SU1233800A3 |
| Способ получения производных хиноксалин-1,4-диоксида | 1982 |
|
SU1230468A3 |
| Способ получения производных дигидроарилокси алкиламино-1,2,4-триазола или их фармацевтически пригодных солей присоединения кислот | 1984 |
|
SU1480767A3 |
| Способ получения производных циклоалкилиденгидразина | 1983 |
|
SU1274620A3 |
| Способ получения производных пиридо-(3,2-е)-асимм-триазина или их солей | 1975 |
|
SU576941A3 |
| Способ получения производных нитроалканола | 1980 |
|
SU1264838A3 |
| Способ получения производных 2.4-диамино-5-бензилпиримидина | 1983 |
|
SU1222194A3 |
| Способ получения 1-изопропиламино-3-(4-ацетамидофенокси)-2-пропанола | 1972 |
|
SU489308A3 |
Изобретение касается производных кислот, в частности производных гид- разинугольной кислоты (ГК) общей формулы: R, N - NH - C(0)-OR, где R Cg- С, - циклоалкилиден, инда- нилиден, группа формулы А - С(Кг) , в которой А - фенильная , . не- или замещенная одним или н есколь- кими заместителями, галоген; NHjJ ОН, низший алкоксил или А-индо- лил, низший алкил, циклогексил, г низший алкил или С -алкил, алкил, которые влияют на прирост веса животных и поэтому могут быть использованы в сельском хозяйстве. Для выявления полезных свойств среди соединений указанного класса были получены новые ГК из карбонильного соединения, и метилкарбазата в присутствии при кипении. Выход до 97,3%. Испытание ГК показьтает, что они влияют на прирост веса животных лучше известного карбадокса или Алавомицина, при одинаковом составе и количестве кормов. В этой связи нужный привес возможно достигнуть при меньшем расходе кормов за счет их лучшей усвояемости. 5 табл1. § О) tsD СО QO сд сн

| Преобразователь кодов | 1982 |
|
SU1058047A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление к индикатору для определения момента вспышки в двигателях | 1925 |
|
SU1969A1 |
Авторы
Даты
1987-03-23—Публикация
1983-05-04—Подача