Изобретение относится к области органической химий, а именгю к выделению 3-метил- 2К -алкенилхлорпроиз- водных из смеси с изомерными алкенил хлорпроизводными.
3-МеТил- 2Е |-алкенипхлорпроизвод- ные, напри мер гераннпхлорид-1-хлор- f-3, 7-диметил- 2Ej, 6-октадиен (I) и фарнезилхлорид-1-хлор-3,7,11-триме- , 6Е , 10-додекатриен (II) и их четвертичные (ЛМФА) аммониевые соли с Ы,К-диметиланилином (ДНА) соответственно хлористый геранилдиме- тилфенкпаммоний - ХГДМФА (1а) и хлористый фарнезилдиметилфениламмо- НИИ .(Па) - ХФДМФА используют в качестве полупродукта для синтеза сложны эфиров гераниола и фарнезола, которы являются феромонами-аттрактантами дл различных видов жука-щелкуна. Актив- ность аттрактантов в силовой мере зависит от ст-епени их чистоты. Кроме того, гераниол, фарнезол и их сложные зфиры, получаемые из вышеприведенных хлорпроизводных I (1а и На), являются ценными душистыми вещества- ми для парфюмерии, качество которых также зависит от степени их чистоты.
Во фракции хлоридов С,, являющейся исходной для синтеза производных гераниола, присутствуют также: . I 58,9-59,2%; т.кип. 60-62°С (2 мм рт.ст.)I
I хлор-3,7-диметил- 2г, 6-октадиен (III) 1,9-2,2%; т.кип. 58-60°С (2 мм рт.ст.)i
1-хлор-2,7-диметил- 2Е 6-октади- ей (IV) 6,0-6,6%; т.кип. 59°С (2 мм рт.ст.).
Как видно из „приведенных темпера- тур кипения, эти хлориды практически неразделимы при помощи ректифи- кации.
Целью данного изобретения явля .ется повышение качества и выхода це- левых продуктов, упрощение процесса Загружено, г
1. Исходная смесь,в том числе: 120 ДМФА I 90,9
ЛМФА III и IV 9,1 . Толуол20 ..
Петролейный эфир (5.00 мл) 335
5
0
5
и получение в препаративных количествах хлорпроизводных 3,7,11-триме- , бк , I 0-додекатриена (фар- незила).
П р и м е р 1. В качестве исход- Ч.9,со... вещества используют фракцию С,g Н,, СI содержащую 79% I; 3% III и 5% IV, а также 13% хлоридов непервичных, главным образом линалил- и терпенилхлоридов. Из 200 г фракции (158 г или 0,92 моль I) и 133.т ДМА получают смесь ДМФА I, III и IV, которую извлекают воцой и разделяют слои непрореагировавших С Н,С1 и ДМА, Водный раствор промывают петролейньгм эфиром, затем насьпцают поташом для высаливания ДМФА I, III и IV,К полученной смеси ДМФА I, III и IV прибав ляют 300 мл толуола. Для окончательного высушивания отгоняют влагу с азеотропом толуол - вода при умеренном вакууме и температуре ниже . Получают 338 г остатка, который со- держит 282 г ДМФА I, III и IV (из них 256 г или 0,87 моля ДМФА I). Вы-, ход 94,5% ДМФА I в перерасчете на I, . ос.тальное - толуол. I 20 г полученной остаточной смеси, содержащей 100 г ДМФА I, III и IV (из них 90,9 г ДМФА или 0,31 моль), загружают в колбу, куда добавляют 500 мл пегролейного. эфира и перемеимвают 6 часов при температуре 50 С. Затем отделяют, ра- створ петролейного эфира, который .- содержит I, III и IV, а также ДНА. Остаток дважды промывают петролейным эфиром и cyDjaT cjocHM-аргоном, чтобы удалить следы растворителя. Сушка требуется только для уточнения анализа.
Получают 82 г ХГДМФА (1а)| 99% (81,2 г или 0,277 моль ДМФА I). Выход 89,4% на исходный ДМФА I или 84,5% на исходный I, .
Материальный баланс процесса очн стки приведен Ниже. Получего, г
i . ХГДМА 9.9%, в том числе: .ДМФА I ДМФА III и IV Петролейный эфир .
2. Раствор,
в том числе:
Петролейный
эфир
3. Петролейный эфир для промывки (2 раза по 40 мп)
Итого: 509
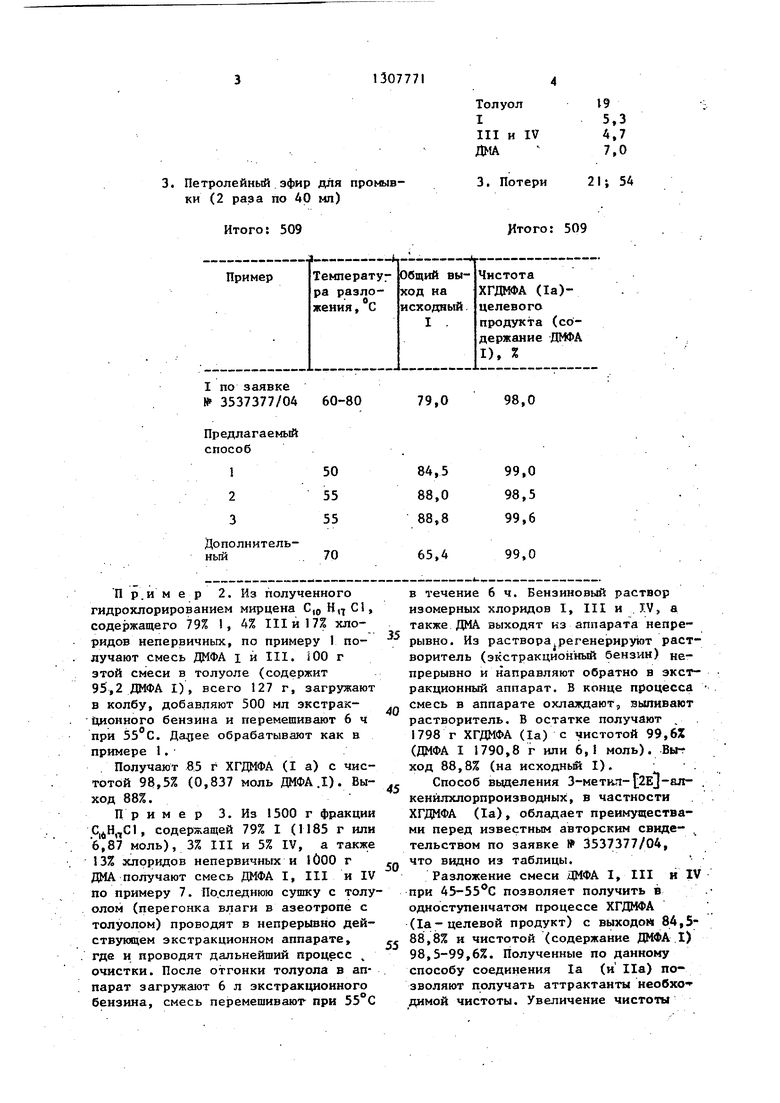
60-80 79,0 98,0
50 84,5 99,0
55 88,0 98,5
55 88,8 99,6
70 65,4 99,0
П р.и м е р 2. Из полученного гидрохлорированием мирцена С,(,Н,7С, содержащего 79% , 4% III и 17% хлоридов непервичньпс, по примеру 1 получают смесь ДМФА I и III. 100 г этой смеси в толуоле (содержит 95,2 ДМФА I), всего 127 г, эагружают в колбу, добавляют 500 мл экстракционного бензина и перемешивают 6 ч при 55 С. Дадее обрабатывают как в примере 1.
Получают 85 г ХГДМФА (I а) с чистотой 98,5% (0,837 моль ДМФА Д). Выход 88%.
Пример 3. Из 1500 г фракции , содерл;ащей 79% I (1185 г или 6,87 моль), 3% III и 5% IV, а также 13% хлоридов непервичных и lOOO г ДМА получают смесь ДМФА I, III и IV по примеру 7. По.следнюю сушку с толуолом (перегонка влаги в азеотропе с толуолом) проводят в непрерывно действующем экстракционном аппарате, где и проводят дальнейший процесс , очистки. После отгонки толуола в аппарат загружают 6 л экстракционного беизина, смесь перемешивают при 55°С
19 5.3 А,7 7,0
21; 54
Итого: 509
5
0
5
в течение 6 ч. Бензиновый раствор изомерных хлоридов I, III и IV, а также ДМА выходят кз аппарата непрерывно. Из раствора регенерируют растворитель (экстракционный бензин) непрерывно и направляют обратно в экстракционный аппарат. В конце процесса смесь в аппарате охлаждают, выпивают растворитель. В остатке получают , . 1798 г ХГДМФА (1а) с чистотой 99,6Z (ДМФА I 1790,8 г или 6,1 моль). Быт ход 88,8% (на исходньй I),
Способ выделения 3-MeTHn- 2Ej-an- . кенйлхлорпроизводных, в частности ХГДМФА (1а), обладает преимуществами перед известным авторским свидетельством по заявке № 3537377/04, что видно из таблицы.
Разложение смеси ДМФА I, III и IV при 45-55 С позволяет получить в одноступепчатом процессе ХГДМФА (1а-целевой продукт) с выходом 84,5- 88,8% и чистотой (содержание ДМФА I) 98,5-99,6%. Полученные по данному способу соединения 1а (и На) позволяют получать аттрактанты необхо ДИМОЙ чистоты. Увеличение чистоты
0
51
аттрактанта с 98 до 98,5% повьппает эффективность феромона-аттрактанта до 2 раз, а до 99,6 - уже в 10 раз.
Пример 4. В качестве исходного вещества используют фракцию CijHjpCl ,в Kon iecTse 240 г (содержит 43,5%),11, или 104,4 г, или , 0,434 моль и 49,0% хлоридов непервичных) ; 3,5% 1-хлор 3,7,11-триме- , 6Е , 10-додекатриен (V) и 4,0% 1-хлор-З,7,11-триметил- 2Z бЕ, 10-додекатриен (VI). Добавля- ioT 160 г ДМА, который образует 00-7 ответственно ДМФА II, V и VI. К по-- лученной смеси добавляют петролей- ный эфир и метанол, перемешивают и разделяют слои. Образующийся мета- нольный раствор, содержащий ДМФЛ II, V и VI, промывают петролейным эфиром. В петролейном эфире остаются непрореагировавшие ингредиенты, главным образом, хлориды непервичные и избыток ДМА. Затем добавляют дихлорэтан и раэбавляют 40%-ным раствором CaCl до образования двух слоев. Отделенный дихлорэтановый раствор (содержит ДМФА II, V и VI) Промывают несколько раз 40%-ным раствором CaCl. За тем отгоняют дихлорэтан при пониженном давлении. Получают 198 Т
Составитель Н. Гозалова
Редактор Л. Герасимова Техред м.Моргентал Корректор И. Эрдейи
Заказ 4337Тираж 342 Подписное
ВНИИЛИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб. , д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Г1роектная, 4
10
077716
остатка, содержащего 182 г ДМФА II, V и VI (ДМФА II 155 г), остальное дихлорэтан.
100 г ДМФА il, V и VI (содержит 5 ДМФА Си 85,з),, всего с дихлорэтаном 109 г загружают в колбу, добавляют 500 мл петролейного эфира и перемешивают при в течение 6 ч После отделения раствора, промывки и сушки сухим аргоном получают 71 г ХФДМФА (На) t чистотой 95% (ДМФА II 67,5 г или 0,19 моль). Выход со- с.тавляет 79,1%.
Формула изобретения Способ выделения 3-метил- 23-ал- кенилхлорпроизводных из смеси с изомерными 2-метил- 2ЕЗ-алкенил и (или) 3-метил- 22 -алкенилхлорпроизводными путем обработки смеси диметилани- лином с последуюп ш разложением сме- . си четвертичных аммониевых солей при повьшенной температуре, отличающийся тем, что, с целью повышения качества и выхода целевых продуктов и упрощения процесса, разложе- ние проводят при 45--55°С,с одновременной экстракцией образующихся при разложении изомерных хлорпроизводных углеводородным органическим растворн15
20
30
тел ем.

Изобретение относится к галоид- углеводородам, в частности выделению 3-метил- 2ЕЗ-алкенилхлорпроиэводных 

| Способ выделения первичных замещенных аллильных галоидопроизводных из смеси с изомерными соединениями | 1959 |
|
SU128860A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| , Авторское свидетельство СССР № 1225224, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
Авторы
Даты
1990-12-07—Публикация
1985-03-26—Подача