Изобретение относится к новым соединениям с ценными фармакологическими свойствами, в частности к способу получения производных 1,4-ди- гидропиридинлактона общей формулы
R R.
Ro Rx 25
30
де R - галоид, метил, метилтио,
трифторметил, диано,нитро; водород, хлор, фтор; С -С -алкил, С -Сд-алкил, прерванный атомом кислорода или серы или сульфинилом, фенетилом;
метил, метоксиметил, диме- тиламиноэтил; ,-алкил, аллил, окси- карбонилметил, этоксикар- бонршметил, оксиэтил, ди- этиламиноэтнл,
ричем R не означает трифторметил, если Rj этил, которые понижают со- N 3 7 ержание глюкозы в крови.
Цель изобретения - способ полуения производных 1,4-дигидропири- инлактона, которые проявляют более высокую активность по снижению содержания глюкозы в крови.
В качестве растворителей для де- протонизации и последующего алкили- рования пригодны все обычные инертные растворители, предпочтительно амиды кислоты, такие как диметилфор- мамид, триамид гексаметилфосфорной кислоты, простые эфиры, такие как тетрагидрофуран, диоксан, сульфокси- ды, такие как диметилсульфоксиды, такие как диметилсульфоксид или суль- фолан. В качестве оснований можно использовать, например, гидриды метал- 50 лов, такие как гидрид натрия, гидрид калия или амиды,такие как амид натрия, 4-диизопропиламид,диэтиламид калия или алкилы металлов,такие как бутиллитий, фениллитий или гидроксиды, такие как j гидроксид калия, гидроксид натрия; или спирты, такие как трет-бутанолят калия, метилат калия или карбонаты, такие как карбонат калия.
50 м ра 2-ме 5-оксо20 Ь)пирид воряют рофуран да натр комнатн 55 ммол с обрат щения п водой, лизовыв т.пл. 1
Расс
С,, H Найд 35 N 3,8.
П р эфир 1ти.пфени
40 фУРо-( лоты.
Пов что в зуют д
45 алкили ли.пбром т.пло
Н 2,4 (с 4,7 (с (м, 1Н
Рас N 3,6.
C,,,
Най N 3,4.
П р эфир 4
N 3 7
Алкилирование осуществляют при -20-ISO C .(предпочтительно при комнатной температуре и до температуры кипения используемого растворителя).
Алкилирование обычно проводят при нормальном давлении, но при необходимости давление можно повысить. Реагенты можно использовать в любом количественном соотношении, предпочтительно их используют в молярном количественном соотношении.
Пример 1. Сложный метиловый эфир 1-этрш-2-метил-4-(2-трифторме- тилфенил)-5-оксо-1,4,5,7-тетрагидрофуро-(3,4-Ь)пиридин-3-карбоновой кислоты.
50 ммоль сложного метилового эфира 2-метил-4-(2-трифторметилфенил)- 5-оксо1,4,5,7-тетрагидрофуро-(3,4Ь)пиридин-3-карбоновой кислоты растворяют в 100 мл безводного тетрагид- рофурана и добавляют 50 ммоль гидрида натрия. По истечении 10 мин при комнатной температуре добавляют 55 ммоль этилйодида и кипятят 1 ч с обратным холодильником. После сгущения поглошс1ют ,, промывают водой, сушат, сгущают и перекристал- лизовывают. Выход 4,9 г (2 6% теории), т.пл. 150-152°С.
Рассчитано,%: С 59,8; Н 4,8;
3 7
С,, H,g . Найдено, %,: С 3,8.
59,7; Н 4,6;
50 j
П р и м е р 2. Сложньш метиловый эфир 1аллил-2-метил-4-(2-трифторме- ти.пфенил)-5-оксо-1,4,5,7-тетрагидро40 фУРо-(3,4-Ь)пиридин-3-карбоновой кислоты.
Повторяют пример. 1 с той разницей что в качестве растворителя используют диметилформамид,. а в качестве
45 алкилирующего агента используют ал- ли.пбромид. Вькод 5,3 г (27% теории), т.пло аморфное вещество.
Н - ЯМ (CDC1,), , ч./млн: 2,4 (с,ЗН), 3,5 (с, ЗН), 4,1 (м,2Н), 4,7 (с, 2Н), 5,4 (д, 2Н), 5,8-6,0 (м, 1Н), 7,3-7,7 (м,, 4Н).
Рассчитано,%« С 61,1; Н 4,6; N 3,6.
C,,,H|gF,N04.
Найдено, %: С 61,4; Н 4,4; N 3,4.
П р и м е р 3. Сложный этиловый эфир 4-(2-хлорфенил)-1-этил-2-метил3 13 5-ОКСО-1,4,5,7-тетрагидрофуро-(3,4- Ь)пиридин-3-карбоновой кислоты.
50 ммоль сложного этилового эфира 4-(2-хлорфенил)-2-метил-5-оксо- 1,4,5,7-тетрагидрофуро-(3,4-Ъ)пири- дин-3-карбоновой кислоты растворяют в тетрагидрофуране,добавляют 50 ммоль диизопропиламида лития при -78 С и последовательно добавляют 50 ммоль этилйо дида. Затем нагревают до комнатной температуры, перемешивают 1 ч аналогично примеру 1 осуществляют дальнейшую переработку. Выход 9,6 г (53% теории), т.пл. 140-141°С.
Рассчитано, %: С 63,0; Н 5,6; N 9,8.
С,, Н,„С1М04.
Найдено, %: С 62,4; Н 5,9; N 9,8.
П р и м е р 4. Сложный пропиловый эфир 4-(2-хлорфенил)-1,2-диметил-5- оксо-1,4,5,7-тетрагидрофуро-(3,4-Ь) пиридин-З-карбоновой кислоты.
50 ммоль сложного пропилового эфира 4-(2-хлорфенил)-2-метил-5-ок- со-1,4,5,7-тетрагидрофуро-(3,4-Ь) пиридин-З-карбоновой кислоты растворяют в 150 мл диметилсульфоксида, затем добавляют 7 г порошкового гидро- ксида калия и 50 ммоль метилйодида. По истечении 2 ч при комнатной температуре наливают на ледяную воду, экстрагируют , сушат, сгущают и перекристаллизовывают. Выход 10,8 г (60% теории), т.пл. 173-177°С.
Рассчитано,%: С 63,0; Н 5,6; N 9,8.
С,,Н,„С1ЫО,.
Найдено,%: С 62,8; Н 5,9; N 10,0.
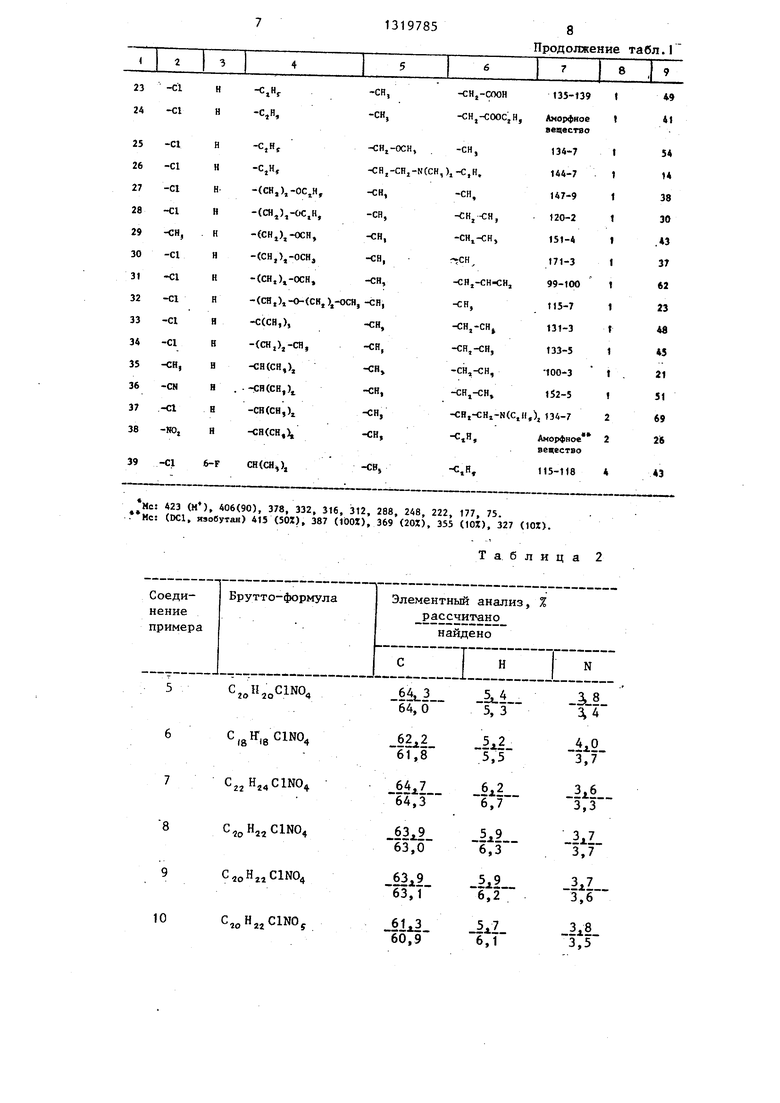
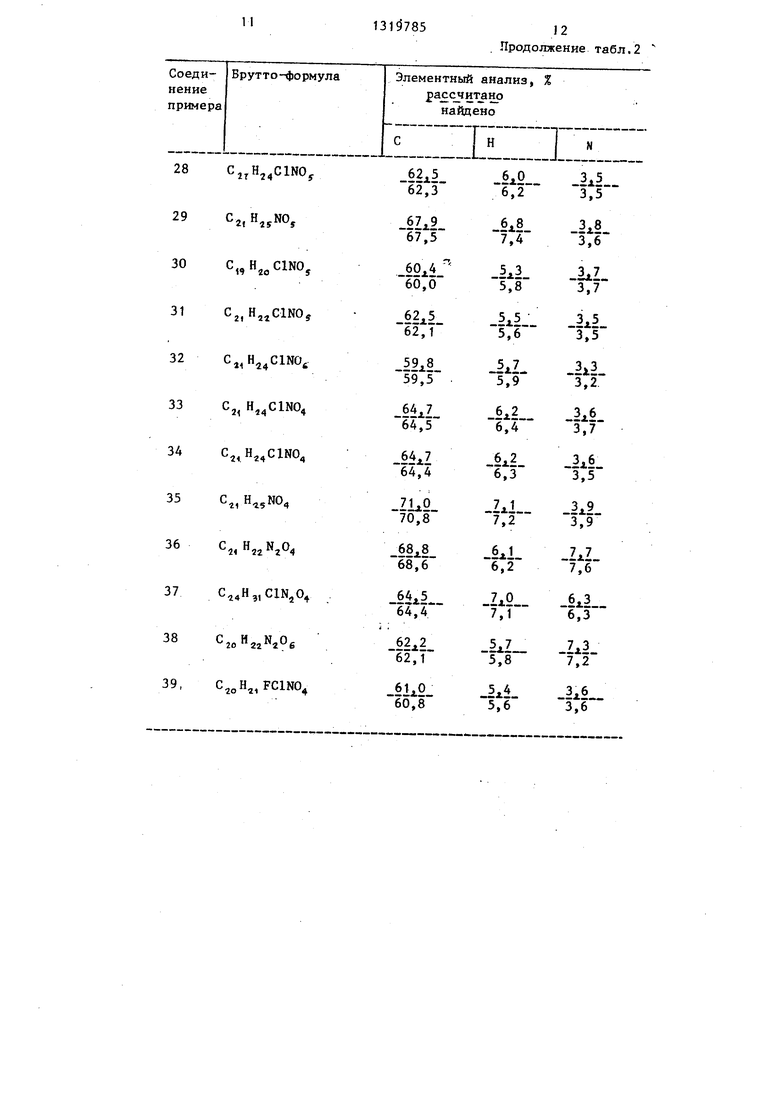
Аналогично получают соединения по примерам 5-39 (табл. 1), данные по брутто-формуле и элементному анализу этих соединений даны в табл. 2.
П р и м е р 40. Сложный изопропи- ловый эфир 4-(2-xлopфeнил)-1-oкcи- этил-2-мeтил-5-oкco- 1,4,5,7-тетрагидрофуро- (3, 4-Ь) пиридин-З-карбоновой кислоты.
50 ммоль сложного изопропилового эфира 4-(2-хлорфенил)-2-метил-5-ок- со-1,4,5,7-тетрагидрофуро-{3,4-Ь) пиридин-З-карбоновой кислоты растворяют в диметилформамиде, депротони- руют 50 ммолями гидрида натрия и затем добавляют 100 ммоль ацетальде- гид-этил-(2-бромэтил)-кеталя, нагревают 1 ч до , сгущают, добавляют
54
соляную кислоту и осаждают- зодой. Выход 9,8 г, т.пл. 140-143 С (из метанола).
Рассчитано,%: С 61,3; Н 5,7; N 3,6.
C,,H,,C1NO,.
Найдено,%: С 61,0; Н 5,9; N 3,6. Биологический опыт. Снижающее глюкозу в крови действие испытывается на крысах-самцах вистар весом 140- 190 г. Для этого крыс за 18 ч до аппликации исследуемых веществ взвешивают, разделяют на группы по 6 животных и держат натощак. Непосредствен- но пе ред аппликацией исследуемые вещества суспендируют в водной 0,75%- ной трагантной суспензии. Аппликацию трагантной суспензии (на контрольных животных) или суспендированных в траганте исследуемых веществ осуществляют посредством желудочного зонда.
Взятие проб крови из ретроорби- тального венозного сплетения осуществляют у каждой крысы через 30, 60 и 120 мин после аппликации.
Каждый раз берут по 30 мкл крови и при помощи 0,3 мл уранилацетата (0,16%-го) удаляют из нее белок.После центрифугирования фотометрически определяют содержание глюкозы в над- осадочной жидкости с использованием 4-амино-феназона в качестве красочного реагента.
Оценку результатов осуществляют методом по Студенту, в качестве предела значимости берут р :0,05.
Вещества, вызвавшие у крыс в какой-то момент значимое снижение концентрации глюкозы в крови по меньшей мере на 10% в сравнении с контрольной группой, получившей только тра- гантную суспензию, признают действующими.
В табл. 3 приведены данные по изменению концентрации глюкозы в крови в процентах к контролыюй группе животных в дозе 30 мг/кг, оральная дача.
Данные табл. 3 свидетельствуют о том, что новые соединения проявляют лучшую активность, чем известное, являются нетоксичными - ЛДу(орально;, крысы) составляет 5 г/кг.
Формулаиз обретения
Способ получения производньсх 1,4- дигидропиридинлактона общей формулы
де R - галоид, метил, метилтио,
трифторметил, циано, нитро;
R, - водород, хлор, фтор;
R - С,-С -алкил, С,-Су-алкил, прерванньй атомом кислорода или серы или сульфини- лом, фенетилом;
R - метил, метоксиметил, диме тиламиноэтил;
Rj - С,-С5 алкш1, аллил, оксикар- бонилметил, этоксикарбонил- метил, оксиэтил, диэтипами- ноэтил, причем R не трифторметил, если Rj. - этил.
1319785 6
отличающийся тем, что, соединение общей формулы
R,OOC
где, R, R, , Rj , R имеют указанные значения, подвергают депротонизации основанием в среде инертного растворителя с последующим алкилированием соединением общей формулы
4
где R имеет указанные значения;
Hal - означает галоид, и выделением целевого продукта.
Таблица 1
Me: 423 (М ), 406(90), 378, 332, 316, 312, 288, 248, 222, 177, 75. Mcs (DCl, изовутая) 415 (50Z), 387 (iDOZ), 369 (20X), 355 (10X), 327 (101).
Таблица 2
29 С, Н„КО,
30 ,
31 Cj, Hj ClNOj
32 C,H,j ClNOt
33 Cj
ЗА C.2,H C1N04
35 C, ,
36 C,,,0,
37 ,СШ,0
38 C,H,,
39, ,,FC1NO
Заказ 2537/59 Тираж 371 . Подписное ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д.4/5
Производственно-полиграфическое предприятие, г.Ужгород, ул.Проектная,4




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 4-(полиалкоксифенил)2-пирролидонов | 1975 |
|
SU649312A3 |
| Способ получения производных дигидропиридинлактола | 1986 |
|
SU1440345A3 |
| Способ получения пиразолонов-5 или их солей | 1974 |
|
SU668600A3 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА | 1993 |
|
RU2126378C1 |
| Способ получения замещенных 1,4-дигидропиридинов | 1983 |
|
SU1360585A3 |
| Способ получения производных 2-иминоимидазолидина или их солей | 1979 |
|
SU910119A3 |
| ПРОИЗВОДНЫЕ 1,4-ДИГИДРОПИРИДИНА С ЦИКЛИЧЕСКИМ МОСТИКОМ В ПОЛОЖЕНИЯХ 1,2 В ФОРМЕ СМЕСИ ИХ ИЗОМЕРОВ | 1995 |
|
RU2155765C2 |
| Способ получения производных 1,6-нафтиридина в виде рацематов или энантиомеров,или их кислотно-аддитивных солей | 1985 |
|
SU1395143A3 |
| ПРОИЗВОДНЫЕ 1-АЛКИЛ-3,5-ДИАЦИЛ-1,4-ДИГИДРОПИРИДИНА В ФОРМЕ СМЕСИ ИХ ИЗОМЕРОВ | 1995 |
|
RU2158259C2 |
| Способ получения 1,4-дигидро-пиридинов или их солей | 1974 |
|
SU509221A3 |
Изобретение касается производных 1,4-дигидропиридинлактона (ПЛ), в частности соединений общей формулы (ObC-CK- С- С О . II И /о R -C-TSlR/i-C-CH где к - -C CR-CH CH-(R,) С--алкил или -Сд-Су-алкил,прерванньм атомом кислорода и серы или сульфинилом, или фенетил; Rj-CH ,метоксиметил,диме- тиламиноэтил; R С,-С -алкил, аплил, оксикарбонилметил, этоксикарбонилме-. тил, оксиэтил, диэтиламиноэтил, причем R не означает CF, если R. что вызьгоает снижение глюкозы в крови. Цель - создание более активных веществ указанного класса. Их получение ведут введением группы в соответствующий 1,4-дигидропиридинлактон, который сначала протонизируют в среде инертного растворителя, а затем ал- килируют соответствующим галоидал- килом с последующим выделением целевого продукта. Испытания ПЛ показывают, что они практически не токсичны и эффективнее, чем известный елож- ньй эфир 4-(2-хлорфенил)-2-метил-5- оксо-1,4,5,7-тетрагидрофуро-3,4- Ь пиридин-3-карбоновой кислоты. 3 табл. W CN

| Европейский патент № 071819, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Гребенчатая передача | 1916 |
|
SU1983A1 |
Авторы
Даты
1987-06-23—Публикация
1985-03-15—Подача