Изобретение относится к биотехнологии, в.частности к производству антибиотиков.
Целью изобретения является разработка способа получения новых анти- биотиков-макролидов, активных в отношении широкого спектра микроорганизмов,
Макролидные антибиотики (PTL-448- производные) получают путем аэробного культивирования штамма StreptO myces arabofaciens АТСС 15154. При этом получают два основных продукта ферментации - PTL-448 А и В, и два дополнительных - PTL-448 С и D, которые получают гидролитическим отщеплением микарозного сахара от основных продуктов. Эти демикарозиловые продукты наиболее активны,
PTL-448-производные представляют сабой стабильные белые порошки,
Продукты PTL-448 А, В, С и D предположительно имеют следующую структуру:
С
СНз
CHj
СНО но (СНэ)г
о- ;-o-R
O-RI снз
Величина химического сдвига С- -ЯМР-спектра (в CDClj) продукта PTL-448A, млн- : 202,3; 171,1; 170,8; 137,1; 135,9; 133,0; 128,8; 104,2; 101,1; 96,4; 80,5; 79,1; 76,4; 74,8; 73,8; 73,3; 71,7; 70,1; 69.4; 68,8; 66,1; 44,0; 42,0; 41,0; 40,7; 38,9; 37,8; 34,3; 31,3; 30,7; 25,4; 25,0; 21,4; 19,1; 19,0; 18,5; 18,3; 16,8; 12,7; 10,0; 9,5,,j
Величина химического сдвига С- -ЯМР-спектра (в CDClj) продукта PTL-448B, млн 202,7; 174,9; 135,1; 134,8; 133,9; 129,5; 105,0; 102,4; 96,3; 82,6; 79,4; 76,5; 74,6; 73,8; 71,4; 69,4; 69,0; 66,6; 64,8; 44,1; 42,0; 40,7; 39,0; 38,0; 37,3; 33,2; 31,2; 30,5; 25,4; 24,8; 19,3; 19,1; 18,5; 18,3; 16,7; 16,6; 12,9; 9,6; 8,3.
Следующие характеристики являются общими для PTL-448 А, С и D, Растворимость: в метаноле, этаноле, ацетоне, этилацетате, хлороформе, бензоле.
10
15
20
25
; ;
;
я ое.
слаборастворимы в эфире, н-гексане, немного растворимы в воде. Цветовая проба: положительная - Драгендорфа, анисовый альдегид-серная кислота, 2,4-динитрофенилгидразин, отрицательная - нингидрин, FeClj , Рейдона-Сми- та,
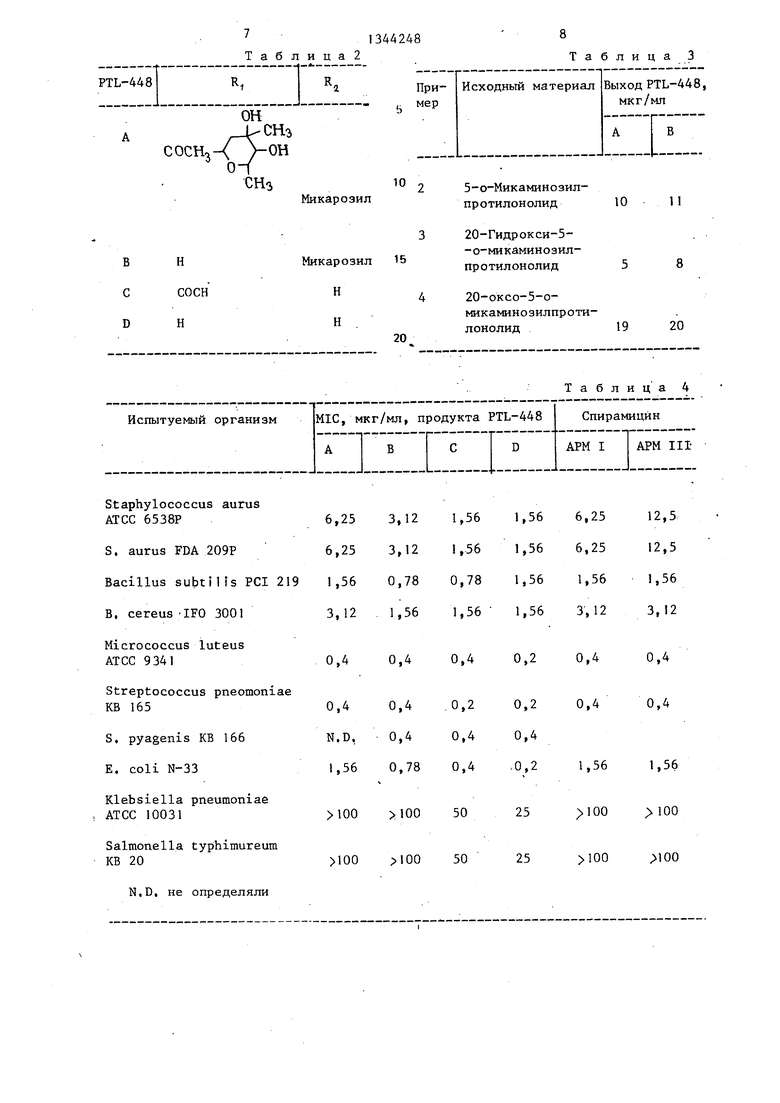
В табл, 1 дана физико-химическая характеристика антибиотиков А, В, С и D,
PTL-448-производные приведены в табл, 2,
В приведенной структурной формуле стереохимия не показана, но предполагается, что различные составляющие части молекулы имеют ту же стереохи- мическую конфигурацию, что и протило- нолид (лактон в центре), форозамин (лактон слева), микаминоза (сахар справа). Протилонолид-форозамино- вая связь предположительно имеет сте- реохимическую конфигурацию -форозаминила.
Наличие аминовых функций в структуре формулы (I) .означает, что свободные основания способны образовывать соли. Подобные соли, если они достаточно нетоксичны при употребле- И 30 НИИ для хемотерапии теплокровных животных, могут использоваться в качестве антибиотиков, К их числу относятся СОЛИ;,, образованные в реакциях как с -органическими, так и. с неор35 ганическими солями, такими как серная, хлористоводородная, фосфорная, уксусная, янтарная, лимонная, молочная, малеиновая, фумаровая, пальмитиновая, холевая, памоевая, слизевая,
40 D-глютаминовая, d-камфорная, глу- таровая, гликолевая, фталевая, винная, муравьиная, лауриновая, стеариновая, салициловая, метансульфоно- вая, бензолсульфоновая, сорбиновая,
45 пикриновая, бензойная и коричная Кислота,
Пример 1, Штамм Streptomy- ces ambofaciens АТСС 15154 (NRRL 2420) выращивают в 100 мл среды, со50 дерясащей, %: глюкоза 2; мясной экстракт 0,5; пептон 0,5; сухие дрожжи 0,3; хлористый натрий 0,5; углекислый кальций 0,3, при рН 7,0 в колбе Сакагучи на 500 мл при 27 С в течение 48 ч при встряхивании. Полученный посевной материал переносят в 100 мл ферментационной среды, содержащей, %: глюкоза 1,0; сухие дрожжи 1,0; хлористый натрий 0,5;
55
углекислый кальций 1,0; азотнокислый натрий О,1 J рН 7,5 в колбе Сакагучи . ria 500 мл. Культивирование осуществляют при 27 С в условиях встряхивания.
В начале культивирования и спустя 24 и 48 ч в колбу добавляют церу- ленин в растворе и небольшом количестве этанола по норме 4 мг в колбу. Через .24 ч после начала культивирования в колбу добавляют проти- лонолид в растворе в небольшом количестве этанола по норме 10 мл на колбу. Культивирование продолжают в течение 72 ч, на протяжении которых рН среды не регулируют.
Мицелий и осадок отфильтровывают от. культуральной среды 100 колб Сакагучи с получением 8,5. л фильтрата. Фильтрат доводят до рН 8,5 добавлением 6н. раствора гидроокиси натрия и дважды экстрагируют тем же количе-, ством бензола. Бензольный слой концентрируют до сухого остатка с получением 1,3 г желтого порошка. Этот порошковый продукт после суспендиро- вания в хлороформе добавляют в колонку, набитую силикагелем (продукт № 7734, выпускаемый фирмой Мерк), и элюируют смесью хлороформ(метанол) концентрированный водный аммиак (10/1/0,05). Каждую фракцию (20 кп) анализируют с помощью тонкослойной хроматографии на силикагеле( продукт
сутки после начала культивирования заменяют 5-о-микаминозилпротилоно- лидом, 20-гидрокси-5-о-микаминозил протилонолидом или 20-оксо-5-о-мик минозилпротилонолидом, и каждое ве щество добавляют по норме 15 мг на колбу. Спустя 3 сут после начала культивирования PTL-448A и PTL-448
10 образуются и накапливаются в культ ральной среде в количествах, указа ных в табл. 3. Выходы определяют э страгированием культуральной среды бензолом, концентрированием экстра
15 та, растворением культуральной сре ды бензолом, концентрированием экстракта, растворением осадка в метаноле, а затем по методике примера 1 - разделением и очисткой осад
20 ка тонкослойной хроматографией на геле окись алюминия / двуокись крем .ния и сканированием (УФ-диапазон) на 232 нм.
Пример 5. В5мл метанола
25 подкисленного хлористоводородной кислотой (рН 2) растворяют 100 мг PTL-448A и перемешивают при 42 С в течение 2 ч. Добавлением гидроокис натрия рН реакционного раствора до
30 водят до 9, и после этого раствор экстрагируют бензолом. Осадок раст воряют в небольшом количестве мета нола и подвергают тонкослойной хро матографии (силикагель, проявление смесью хлороформ(метанол)концентри
- f.l i4CV-OnJ AJlWp JlJlkJi/iM V. t- - Л-У i-
№ 5554 фирмы Мерк, проявляющий рас- рованный водный аммиак 10/1/0,05). творитель - смесь хлороформ(метанол) Продукт со значением Rf около 0,4 концентрированный водный аммиак
собирают и концентрируют с получен 45 мг продукта PTL-448 С в виде бе
15/1/0,05) для выявления тех фракций которые содержат соединение, имеющее значение Rf около 0,26. Эти фракции собирают и концентрируют при пониженном давлении с получением 96 мг смеси PTL-448A и PTL-448B в виде белого порошка.
Для дальнейшего разделения этих веществ проводят тонкослойную хроматографию окиси алюминия (продукт № 5550 фирмы Мерк, проявляющий растворитель - смесь этилацетат/бен- зол 6/1). Полосы со значениями Rf 0,6 и 0,4 собирают, элюируют этилацета- том и концентрируют с получением 37 мг PTL-448A и 45 мг PTL-448B в виде белых порошков.
Примеры 2-4. Пример 1 повторяют с тем отличием, что протило- нолид - вещество, добавляемое в качестве исходного материала спустя
сутки после начала культивирования, заменяют 5-о-микаминозилпротилоно- лидом, 20-гидрокси-5-о-микаминозил- протилонолидом или 20-оксо-5-о-мика- минозилпротилонолидом, и каждое вещество добавляют по норме 15 мг на колбу. Спустя 3 сут после начала культивирования PTL-448A и PTL-448B
образуются и накапливаются в культуральной среде в количествах, указанных в табл. 3. Выходы определяют экстрагированием культуральной среды бензолом, концентрированием экстрак-
та, растворением культуральной среды бензолом, концентрированием экстракта, растворением осадка в метаноле, а затем по методике примера 1 - разделением и очисткой осадка тонкослойной хроматографией на геле окись алюминия / двуокись крем- .ния и сканированием (УФ-диапазон) на 232 нм.
Пример 5. В5мл метанола,
подкисленного хлористоводородной кислотой (рН 2) растворяют 100 мг PTL-448A и перемешивают при 42 С в течение 2 ч. Добавлением гидроокиси натрия рН реакционного раствора доводят до 9, и после этого раствор экстрагируют бензолом. Осадок растворяют в небольшом количестве метанола и подвергают тонкослойной хроматографии (силикагель, проявление смесью хлороформ(метанол)концентриl i4CV-OnJ AJlWp JlJlkJi/iM V. t- - Л-У i-
рованный водный аммиак 10/1/0,05). Продукт со значением Rf около 0,4
рованный водный аммиак 10/1/0,05). Продукт со значением Rf около 0,4
собирают и концентрируют с получением 45 мг продукта PTL-448 С в виде белого порошка. Физико-химическая характеристика этого вещества приведена в табл. 1.
Пример 6. При комнатной температуре на протяжении ночи перемешивают 5 мл раствора 01н. хлористоводородной кислоты/метанол (1/3), содержащего 20 мг PTL-448A, После экстрагирования бензолом повторяют методику примера 5 с получением 8,4 мг PTL-448C.
Пример 7. Методику примера 5 повторяют с тем отличием, что 100 мг продукта PTL-448B растворяют в 5 мл метанола, подкисленного хлористоводородной кислотой до рН 2. Таким о.бразом получают 41 мг продукта PTL-448D в виде белого порошка. Физико-химическая характеристика этого вещества приведена в табл. 1.
Антимикробная активность антибио- тиков-макролидов в сравнении со спи- рамицином представлена в табл. 4.
Кроме того, изучают активность в отношении Mycoplasraa с использованием известных методов (бумажный диск диаметром 8 мм, 37 С, около 48 ч).
Активность антибиотиков в отношении Macoplasma приведена в табл. 5. ю
Полученные соединения могут быть использованы для лечения или борьбы с бактериальными или микоплазменными инфекциями теплокровных животных, а также людей.-15
С этой целью новые активные ингредиенты смешивают со вспомогательными веществами и носителями, обычно применяемыми в фармакологии и ветерина- . рии. Подобные носители и вспомога- 20 тельные вещества могут быть аналогичными применяемым для приготовления спирамицина или тилозина. Режимы дозировки также могут быть аналогичными используемьш в отношении описан- 25 ных антибиотиков.
Формула изобретения
Способ получения антибиотика-мак- ролида общей формулы (I)
СНО НО(СНзН
0-( оЧ-,,
O-RI
сн.
где RI - водород или ацетил;
R - водород или микарозил, заключающийся в том, что штамм Strep- torayces ambofaciens АТСС 15154 культивируют в жидкой питательной среде, содержащей источники азота и углерода и минеральные соли, в аэробных условиях, затем через 24 ч от начала культивирования в культуральную среду вводят протилонолид, 5-о-микамино- -зилпротилонолид, 20-оксо-5-о-микамино- зйлпротилонолид или 20-ГИДРОКСИ-5- -о-миканозилпрртилонолид в концентрации ID-15 мг/100 мл культуральной жидкости и выделяют целевой продукт общей формулы (I), где Rj - микарозил, далее, при необходимости, целевой продукт подвергают гидролизу и получают целевой продукт общей формулы (I), где R. - водород.



Изобретение относится к области биотехнологии и касается получения антибиотика-макролида, называемого PTL-448. Цель изобретения - создание способа получения новых антибиотиковг макролидов, активных в отношении широкого спектра микроорганизмов, в т.ч. mycoplasma. Для получения антибиотика и его производных формулы VCHO HONCCHo.) , Ъ О в S О) где R - водород или ацетил; R - водород ИЛИ микарозил, используют известный штамм Streptomy- ces ambofaciens АТСС 15154, который выращивают в жидкой питательной ере- де, содержащей источники углерода, азота и минеральные соли, в аэробных условиях. Через 24 ч и более после начала культивирования в культураль- ную среду вводят протилонолид, 5-о- микаминозилпротилонолид, 20-оксо-5- -о-микаминозилпротилонолид или 20-гидрокси-5-о-миканозилпротилонолид в концентрации 10-15 мг/100 мл куль- туральной жидкости. Отделяют фильтрованием жидкую фракцию,экстрагируют целевой продукт и подвергают колоночной хроматографии. Выделяют фракции, содержащие целевой продукт указанной формулы, где RJ - микарозил, и при ; необходимости подвергают гидролизу с получением целевого продукта, где R - водород. 5 табл. (
4,4 (, CHCl) (C-I, CHClj)
Таблица 1
-15,9+23,2
(,5, СНСЦ) (, СНСЦ)
Таблица2
PTL-448
ОН
СНэ
СОСНо-Ч У-ОН
0-f
СНз
Микарозил
Н
СОСН
Н
Микарозил 1В Н
Н
20
Staphylococcus aurus АТСС 6538Р
S. aurus FDA 209Р Bacillus subtills PCI B. cereus -IFO 3001
Micrococcus luteus ATCC 9341
Streptococcus pneomoni KB 165
S, pyagenis KB 166 E. coli N-33
Klebsiella pneumoniae ATCC 10031
Salmonella typhimureum KB 20
N,D, He определяли
Таблица 3
5-о-Микаминозил- протилонолид 10 11
20-Гидрокси-5- -о-микаминозил- протилонолид 5 8
20-ОКСО-5-Омикаминозилпротилонолид1920
Таблица 4
Mycoplasraa gallisepti- cum KP-13
Achoieplasma laidlacou PG
Редактор С. Пекарь
Составитель Г. Смирнова
Техред А.Кравчук Корректор А, Зимокосов
Заказ 4840/59 Тираж 499Подписное
ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-полиграфическое предприятие, г, Ужгород, ул. Проектная, 4
Таблица 5
29,2 30,1
31,4 . 33,1 32,0
| Chem | |||
| pharm | |||
| Bull.,1980, 29,1963 | |||
| Antimicrob | |||
| Agents Chemother | |||
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| Biochem | |||
| Biophys | |||
| Res | |||
| Commun | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| СНз (СНз) | |||
| СБ | |||
Авторы
Даты
1987-10-07—Публикация
1984-03-28—Подача