Штамм получен в Северном исследовательском отделе Министерства земледелия США, Приория, Штат Иллинойс, США и хранитс 1 в 1 оллекции микроорганизмов под номером NR.RL 2486.
Основные xapaKjepiibie н)нзиак 1 штамма btreptomyces Kitasalocnsis NRiRL2486.
Воздушный мицелий от серовато-белого до желтого илн светло-коричневого, слабо развитый, тонкий, иногда нушистый или хлоньевидный. Иногда можно наблюдать сиирально закрученные гифы.
Агар Чанека. Культура от желтого до желГ1)вато-кор11чиевого цвета, нроннкающая в среду. Воздун1ный мицелий серовато-белый. Растиоримый нигмеит желтоватый.
Aiap KpaHiicKoio. Колонии желтовато-белого lUiCTa, центр 1риподнят, ироипкают в агар, l;acTMi,yibiii тошчий край.
Воздушный мьцелий тонкий, серовато-белого цвета. Во время инкубации образуются нушистые образования, которые иревращаются из белых в рыжевато-коричневые и иокрывают всю иоверхность.
Растворимый ннгме1гг светло-желтый.
Пищевой агар. Колонии ограниченные коричневого цвета с прииоднятым центром и складками от центра к краю. Воздушный мнцелий отсутствует. Растворимый нигмеит коричневого цвета.
Глюкозный агар. Культура - от коричневой до темно-коричневой, нроникает в агар.
Воздушный мицелий очень слабый, серого или мышиного цвета. Растворимый иигмент коричневого цвета.
Крахмальный агар. Культура - от бесцветной до желтоватой или желтовато-коричневой, нроникает в среду; центр колоний коричневого цвета, нрииоднят.
Воздушный мицелий тонкий. В ироцессе культивирования быстро растет иушнстый или хлоньевидный воздушный мицелий белого цвета, разрастаясь но всей поверхности среды и окрашивая ее в желтоватый цвет.
Растворимый ннгмеит отсутствует или образуется в незначительном количестве.
Агар с тирозином. Культура - от. коричневой до темно-коричневой, проникает в среду.
Воздушный мицелий серовато-белого цвета, тонкий, со временем нушнстый. Реакция на тирозиназу ноложнтельная. Р1ногда реакция на тирозиназу бывает отрицательной для некоторых штаммов, что обусловливает слабожелтую окраску среды. В других случаях - обильное образование серовато-черного пигмента.
Картофельная пробка. Культура желтоватокоричневая и морщинистая.
Воздушный мицелий отсутствует или тонкий, белого цвета, иногда пушистый и желтоватокоричневый. Цвет цробки нензмениый или светло-коричневый, иногда черный.
Морковная пробка. Культура - от коричневой до темно-коричиевой. Воздушный мицелий
отсутствует илн бледно-серый. Цвет нробки неизменный.
Среда с желатиной. При носеве уколом культура слабо развитая, темно-коричневого цвета. 1 азжижеиие медленное, полное.
Молоко. Коагуляция слабая или отрицательная. Цеитонизация иоложительная. Кольцо от желтого до коричневато-желтого или темнокоричневого цвета.
Яичная среда. Культура желтовато-коричневая. Воздушный мицелий тонкий, разбросанный, светло-желтый, со временем пушистый. Среда фиолетового цвета.
Сыворотка. Культура коричневато-желтая. Возду пный мицелий отсутствует.
Кровь. Культура темно-коричневого цвета. Воздуишый мицелий отсутствует. Гемолиз ноложитсльный.
Нитратное восстановление положительное. Гидролиз крахмала ноложнтельный. Разложение целлюлозы отрицательное. Образование сероводорода иоложительное.
Описанная выше морфологическая характеристика Str. Kitasatoensis соответствует четырем типам формы колоний; AjBidD.
Тин D имеет неправильную форму. Толшина колоний: тип А больше типа В, больше типа С.
Воздушный мицелий: отсутствует у типа А и С, слаборазвитый у типа В.
Цвет поверхности колоний: тип А - желтоватый блестяший, типы В и С - коричневый.
Диаметр колоний: тина В больше типа А,
типа С - очень маленький. Складки, тип А -
менее трех, В - более трех, С - отсутствуют.
Способ получения комплекса антибиотиков осуществляют следующим образом.
Культуру Streptomyces Kitasatoensis NRRL 2486 выращивают в глубинных условиях в ферментационном аэробном процессе на питательной среде, содержашей нсточники углерода, азота, .минеральные соли и микроэлементы.
В качестве источника углерода могут быть использованы лактоза, мальтоза, декстрин, меласса, крахмал, глюкоза, кукурузная патока, сахар, глицерин, жирные кислоты - стеариновая, нальмитиновая, уксусная, пронионовая и т. д.
В качестве источника азота могут быть использованы жидкость при вымачивании кукурузы, дрожжи или дрожжевой экстракт, мясной сок, пентон, молоко, хлопковое масло, гидролизат казеина, аминокислоты, соевое масло и т. д., а также неорганический нитрат, соли аммония и т. д.
Из неорганических солей питательная среда
может содержать калий, натрий, кальций в
виде фосфатов, карбонатов, хлоридов и т. д.,
а также активаторы роста - соли бора, молибдена, меди, никеля, железа и т. д.
Ферментацию проводят при 25-35°С, рН среды 7,0 при постоянном перемешивании и аэрации. Для выделения и очистки антибиотического комплекса используют известные способы, например экстракцию растворителем.
обработку адсорбентом, распределительную хроматографию, кристаллизацию из растворителя и т. д.
Полученный антибиотический комплекс обладает следующими свойствами.
Элементарный анализ, %: С 60,0; Н 8,80; N 1,68. Мол. вес около 800.
Физические свойства
Порошок белого цвета, т. пл. 128-145°С. Спектр поглощения УФ-лучей:
ГкГ -231нм, Ei;t, 353.
Оптическое вращение: ( -53° (с 1; хлороформ).
Растворим в низших спиртах, таких как метанол, этанол и т. д.; эфирах - этилацетате, бутилацетате; кетонах - ацетоне, метилизобутилкетоне; бензоле, хлороформе и т. п. Трудно растворим в воде и нерастворим в петролейном эфире.
Химические свойства
Новые антибиотические композиции дают следуюшие цветные реакции:
отрицательные: реакция Адамкевича, реакция с биуретом, реакция Милона, реакция с ксантопротеином;
положительные: реакция с антроном, реакция Шриванова, реакция Молиша и реакция с концентрированной серной кислотой.
Для выделения отдельных антибиотиков АЗ, А4, AS, AS, АГ, AS и Ад из указанного комплекса его дополнительно обрабатывают методом хроматографии с применением силикагеля, целлюлозного материала, активированной окиси алюминия и т. п. При дальнейшей обычной обработке системой растворителей можно выделить каждый из компонентов в виде призм белого цвета (Аз-Ае, Ag), кристаллического порошка белого цвета (А и Ад).
Анализ антибиотических соединений АЗ-C42H69NOi5; радикалы
Сн
i
J rC-dH,, Т1 е-снгсн
сн.
о
о
Молекулярный вес 835+15; т. пл. 120-121°С. Оптическое вращение -55,4° (с 1, хлороформ).
Величина рК (50% -этанол) -6,70. Спектр поглощения УФ-лучей, нм:
fc° 231-232, - 351.
Кроме вышеуказанных цветных реакций для антибиотического комплекса, АЗ - соединение дает отрицательные реакции Шиффа и Эрлиха.
А4-C4iH67NOi5; радикалы
R,-C-CH,, Нг-С-СН,-СН,-СНз II
ОО
Мол. вес 820±15; т. пл. 120-127°С.
Оптическое вращение:
/а/25д 50° (с 1, хлороформ),
Величина рК (50% этанол) -6,71. Спектр поглощения УФ-лучей. нм:
метанол - 32
%акс. - icM
Кроме выщеуказанных цветных реякций дает отрицательные реакции Шиффа и Эплиха. Aj-СзэНбсЛ01 л: радикалы
R,-C-CH,, R,-C-CH.-CH,-CH,
IIИ
оо
Мол. вес 780+ 10; т. пл. 120-123°С. Оптическое вращение: /(х/25п -52° (с 1, хлороформ). Величина рК (50% этанол) -6,69. Спектр поглощения УФ-лучей, нм:
ч метанол 949 Р °Ч7П
макс , .Cl см - О/и.
Дает отригательную реакцию Шиффа. Аб-CjoHesNOi.,; радикалы
Н,-С-СНз, R,-C-CH,-CH,
П11
оо
Мол. вес 801 гЫО; т. пл. 135-137°С. Оптическое в.ращение -56°С (с 1. хлороформ).
Величина рК (50% этанол) -6.72. Спектр поглотления УФ-лучей, нм:
Х ГкГ- 231, 5 „-405.
Дает отрицательные реакции Шиффа, Эрлиха и Сякагухи н положительную реакцию с тетразолиумом.
Av-C,sH«iNOb, радикалы R,-Н. 1,с-СНо-СНз. Мол. вес 770+15: т. пл. 111 -113°С.
Оптическое вращение /п/,)-. -65.3° (с 1, хлороформ).
Величина рК (50% этанол - 6,73.
Спектр полгощенпя УФ-лучей, нм:
, метанол QQO Pl 4Т5 iO.i, ;i CM - T-iO.
Дает те же реакции, что и сое.аинеиие .А.6. AS-CjoHfisNOis; радикалы Ri-С-СНз
О
R,-С-СНз. II О
Мол. вес 790+10; т. пл. 147-149°С. Оптическое вращение -58,3° (с 1,8, хлороформ). Величина рК (50 %этанол) -6,75. Спектр поглощения УФ-лучей, нм:
.,метанол поо с- ЧОП
макс oZ, Cl см - OOU.
Дает те же реакции, что н соединение Ае. АО-C3vH6iNOi.. радикалы Ri-Н, Rg-С-СНз
11 О
Мол. вес 760+:10.
Оптическое,- вращение --65,1° (с - - 1,3, хлороформ). Величина рК (50% этанол) -6,75. 7 Спектр поглощения УФ-лучей, метанол -)оо р1-.опп; макс iu, jCi (.j, - ОУО. Дает те же реакции, что и еоединение Ае. Антибиотики обладают большой продолжительностью действия и слабой токсичностью. Пример 1. Водную питательную среду, содержащую, %: пентон 0,5; мясной экстракт 0,5; глюкоза 2; хлористый натрий 0,5; сухие дрожжи 0,3 и карбонат кальция 0,3, разбавляют водой до 100 мл, помещают в колбу Сакагуки емкостью 500 мл, устанавливают рН , 7, стерилизуют, засевают культурой Str. Kitasatoensis и инкубируют при 27°С в течение 72 ч ири взбалтывании. 20 л ферментационной среды, содержащей, %: соевая мука 3, крахмал 2; глюкоза 1; хлористый натрий 0,5; сульфат аммония 0,3; су.хие дрожл и 0,5, карбонат кальция 0,3; двухоеновиый фосфат калия 0,1 и мочевина 0,01, помеи.1ают в стерильную склянку емкостью 30 л и засевают в асептических условиях инокулятом. Ферментацию осуществляют при 27°С в течение 50 ч при перемещивании мешалкой (250 об/мии) и скорости аэрации 20 л/мин. Зател культуральную жидкость асептически переносят в бродильный чан из нержавеющей стали емкостью 400 л п тщательно смешивают с 200 л бродильной среды того же состава. Смесь дополнительно инкубируют при 27°С в течение 85ч при перемешивании (200об/мин) и аэрации стерильным воздухом (200л/мин). В конце инкубационного пернода культуральная жидкость содержит 1200 мкг/мл смеси антибиотиков АЗ-АЭ в пересчете на соответствующее количество обычиого стандартного лейком ицина. В 160 л фильтрата, полученного после удаления мицелия центрифугированием, устанавливают рН 9, экстрагируют дважды 50 л бутилацетата. Устанавливают рН 9 в бутилацетатной фазе добавлением разбавленной соляной кислоты (рН 3), хорошо перемешивают и устанавливают рН 8,5 в отделенной водяной фазе, а затем дважды экетрагируют 8 л бутилацетата. Бутилацетатную фазу экстрагируют 6 л разбавленной соляной кислоты (рН 3,5). Водную фазу после установления рН 9 экстрагируют 6 л бензола. Бензольные экстракты объединяют и концентрируют под вакуумом. Получают 130 г смеси антибиотиков в виде порошкообразного свободного основания белого цвета. Активность 1150 мкг/мг. П р н м е р 2. Выделение соединения АЗ. 250 г порошкообразного иродукта белого цвета (пример 1) растворяют в I мл бензола и раствор выливают через верхний конец в хроматографическую колонку диаметром 1 см и наполненную 10 г селикагеля в бензоле. Затем колонку тщательно промывают бензолом и ппопускают через нее смесь бензола с ацетоном (5:1) со скоростью 1/4 об./об.-ч. Элю(1Т собирают в большое число пробирок по 1 мл в каждую, пользуясь сборником фракций. При исследовании состава содержимого каждой пробирки методом хроматографии в тонком слое было установлено, что пробирки 15-25 содержат значительные количества соединения АЗ. Содержимое указанных пробирок объединяют и в вакууме удаляют растворитель. Остаток растворяют в бензоле при 60°С и выдерживают в течение 10-15 ч в камере, охлаждае.мой льдом. Получают свободное основание в виде белых призм. Выход АЗ 30 мг. Пример 3. 4 г продукта, получаемого в примере 2, подвергают распределению но принципу противотока, применяя систему растворителя бензол - хлороформ - метанол - 1/15 моля лимонной кислоты (буфер) при рН 4,4 (соотношение растворителей 20 : 6 : :20:8), и помещают в 300 пробирок, каждая из которых содержит 10 мл обработанного растворителя. При исследовании содержимого пробирок методом хроматографии в тонком слое с силикагелем установлено, что пробирки 65-80 содержат значительные количества соединения АЗ. Содержимое этих пробирок объединяют и обрабатывают, как указано выше. Выход 350 мг АЗ в виде порошка белого цвета. Полученное соединение растворяют в 5 мл этилового эфира и по каплям при перемешивании выливают в 5 мл 2%-ного раствора винной кислоты в этиловом эфире. Образовавшийся осадок соединения АЗ промывают этиловым эфиром и после выделения высуиншают. Выход 400 мг. П р и .м е р 4. Получение соединения .. Содержимое пробирок 28-35 после обработки его, как описано в примере 2, объединяют и удаляют растворитель путем перегонки под вакуумом. Оставшийся белый порошок растворяют в 1 мл бензола и выливают в хроматографическую колонку диаметром 6 мм, наполненную 5 г силикагеля, смешанного с требуемым количеством бензола. Затем колонку элюируют смесью бензола с ацетоном (4:1). Из элюата удаляют растворитель путем перегонки и остаток церекристаллизовывают из бензола. Получают свободное основание А4 в виде кристаллов в форме призм белого цвета. Выход 20 мг. Пример 5. Содержимое пробирок 95- 115, полученное, как описано в примере 3. объединяют и обрабатывают, как описано выше. Получают соединение А.) в виде порошка белого цвета. Выход 294 мг. П р и м е р 6. Получение соединения АЗ. Содержимое пробирок 45-68. полученное, как описано в примере 2, объединяют и обрабатывают методом хроматографии (элюируют смесью бензол : ацетон 4:1). Получают свободное основание соединения в виде порошка белого цвета. Выход 35 мг. Пример 7. Содержимое пробирок 171 - 195, полученное, как описано в примере 3, объединяют и обрабатывают, как ранее, Выход AS 480 мг,
Пример 8. Получение соединения Ае.
250 мг белого порошкообразного продукта, полученного по примеру 1, растворяют в 1 мл бензола и раствор выливают в хроматографическую колонку диаметром 1 см, наполненную 10 г силикагеля в бензоле. Затем колонку элюируют бензолом и пропускают через нее смесь бензола с ацетоном (4:1) со скоростью 1/4 об./об. ч. Элюат собирают в большое число пробирок в количестве 1 мл в каждой, пользуясь колектором фракций.
Содержимое пробирок 26-40 объединяют п удаляют растворитель перегонкой. Оставшийся порошок белого цвета растворяют в 1 мл бензола и выливают в верхний конец хроматографической колонки диаметром 6 мм, наполненной 5 г активированной окиси алюминия в смеси с необходимым количеством бензола. Затем через колонку пропускают смесь бензола с этилацетатом (2 : 3) на второй стадии хроматографирования. Элюат перегоняют в вакууме и остаток перекристаллизовывают из бензола. Получают продукт в виде белых призм. Выход соединения Ад в форме свободного основания 15 мг.
Пример 9. 35 мг белого порошка, полученного по примеру 1, растворяют в 70 мл бензола и раствор выливают в хроматографическую колонку диаметром 10 см, наполненную 900 г силикагеля в бензоле. Колонку тщательно промывают бензолом, а затем через нее пропускают смесь бензола с ацетоном (4: 1) со скоростью 1/4 об./об. ч. Элюат собирают в пробирки по 20 мл в каждой. Содержимое пробирок 130-170 объединяют и удаляют растворитель иерегонкой под вакуумом. Оставшийся порошок белого цвета растворяют в 20 мл бензола и выливают во вторую хроматографическую колонку диаметром 3 см, содержащую 100 г активированной окиси алюминия в смеси с требуемым количеством бензола. Затем через колонку пропускают смесь бензола с этилацетатом (2:3). Элюат собирают, перегоняют под вакуумом и остаток перекристаллизовывают из горячего бензола. Получают чистый продукт в виде кристаллов белого цвета. Выход AS 800 мг.
Пример 10. Получение соединения Ау.
250мг белого порошка, полученного,по примеру 1 , растворяют в 1 мл бензола, и раствор выливают в хроматографическую колонку диаметром 1 см, наполненную 10 г силпкагеля в бензоле. Затем колонку промывают бензолом и пропускают через нее смесь бензола с ацетоном (3:1) со скоростью 1/4 об./об. ч. Элюат собирают в пробирки по 1 мл в каждую.
Содержимое пробирок 35-55 объединяют и иод вакуумом отгоняют растворитель. Полученный остаток в виде порошка белого цвета растворяют в небольшом количестве бензола и обрабатывают хроматографическим методом, как ранее. Получают соединение А в виде кристаллического порошка белого цвета, Выход 10 мг.
Пример 11. Содержимое пробирок 220- 245, полученное по примеру 3, объединяют и обрабатывают, как описано выше. Получают 200 мг сырого порошка белого цвета. Этот продукт дополнительно хроматографируют, как в примере 10. Получают свободпое основание соединения А в виде кристаллического порошка белого цвета. Выход 100 мг. Пример 12. Получение соединения AS.
Содержимое пробирок 30-40, полученное по примеру 10, объединяют и удаляют растворитель перегонкой под вакуумом. Полученный порошок белого цвета растворяют в небольшом количестве бензола и раствор обрабатывают путем повторного хроматографирования, как описано выше. Получают свободное основание соединення AS в виде кристаллов белого цвета. Выход 5 мг. Пример 13. 35 г белого порошка, полученного по примеру 1, растворяют в 70 мл бензола и раствор выливают в хроматографическую колонку диаметром 6 см, наиолнеииую 700 г активированной окиси алюминия в бензоле. После иромывки бензолом через колонку пропускают смесь бензола с этилацетатом (1:2) со скоростью 1/4 об./об. ч. Элюат собирают в пробирки порциями по 20 мл. Содержимое каждой пробирки обрабатывают методом хроматографии в тонком слое. Установлено, что соединение AS содерл ится в пробирках 13-40. Содержимое этих пробирок объединяют 1 перегоняют под вакуумом. Остаток растворяют в 30 мл бензола, и раствор выливают хроматографическую 1ч4)лоику диаметром
5 см, наполненную 375 мл смеси силикагеля в требуемом количестве бензола. Затем колонку элюируют смесью бензола и ацетона (3:1) и содержимое иробирок 150-170 объединяют и высушивают под вакуумом. Полученный остаток перекристаллизовывают из горячего бензола. Получают соединение AS в виде иглообразных кристаллов белого цвета. Выход 500 мг. Пример 14. Получение соединения Ад.
Содержимое пробирок 60-70, полученпое по прпмеру 10, объединяют и высушивают под вакуумом. Получеппый порошок белого цвета растворяют в беизоле и обрабатывают повторно хроматографическим методом, как описано
выше. Выделяют соедтшенпе Адв виде кристаллического порошка белого цвета. Выход 20 мг. Прпмер 15. 35 г порошка белого цвета, полученного по примеру I. растворяют в 70 мл бензола. Раствор выливают в хроматографическую колонку диаметром 6 см, наполненную 700 г смеси активированной окиси алюминия с бензолом. Затем колонку промывают бензолом и пропускают через нее смесь бензола с этилацетатом (1:2) со скоростью 1/4 об./об. ч.
Элюат собирают R пробирки по 20 мл в каждой и содержимое каждой пробирки анализируют методом хроматографии в тонком слое, применяя активированную окись алюминия. Установлеиа, что в ппобирках 60-80 содержится соедииснис Ад. Содержимое этих пробирок объединяют, высушивают под вакуумом и полученный остаток растворяют в 30 мл бензола. Раствор выливают в хроматографическую колонку диаметром 5 см, наполненную 350 г смеси силикагеля с бензолом. Колонку злюируют системой растворителей бензол, ацетон (3:1), содержимое пробирок 150-170 объединяют н высушивают под вакуумом. ПоСК
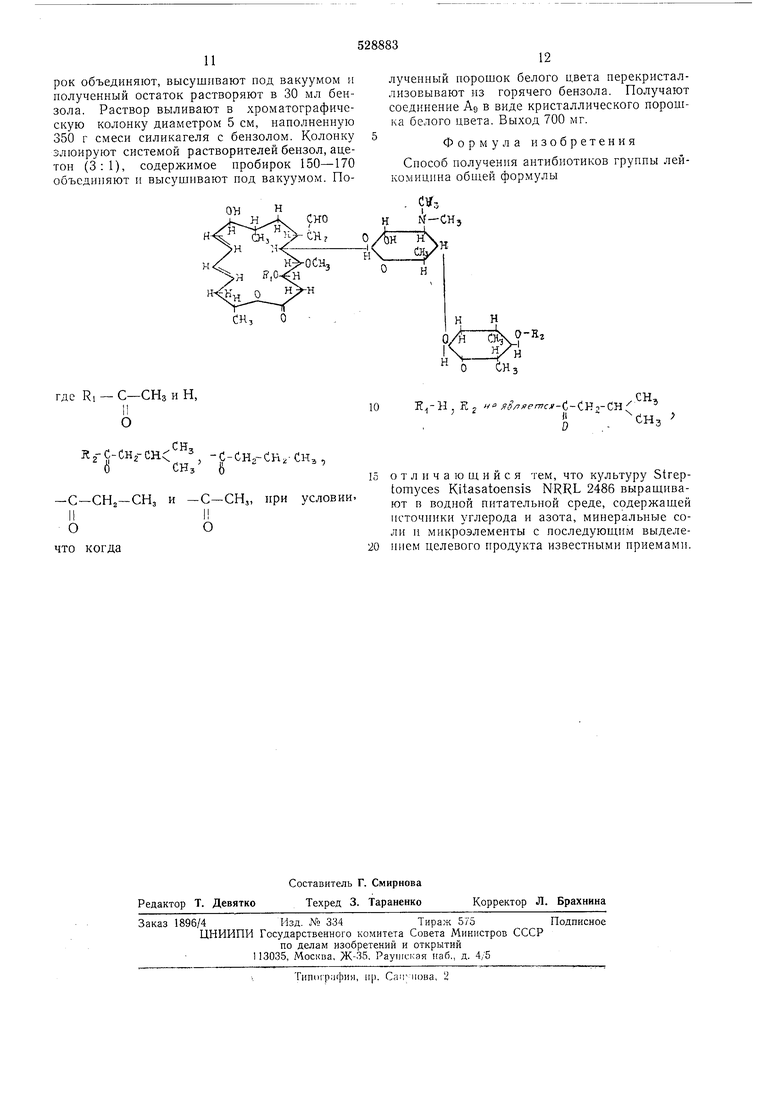
где R, -С-СНзиН,
11 О
rvT
R,
ИСН,
-С-СНг-СНз и -С-
О
о
что когда
Г1-Т
, Кг jV f c -C-CHn-CH/
D .- 3
отличающийся тем, что культуру Streptomyces Kitasatoensis NRRL 2486 выращивают в водной питательной среде, содержащей источники углерода и азота, минеральные соли и микроэлементы с последующим выделеиием целевого продукта известными приемами. лученный порошок белого цвета перекристаллизовывают из горячего бензола. Получают соединение Ад в виде кристаллического порошка белого цвета. Выход 700 мг. Формула изобретения Способ получения антибиотиков группы лейкомицпна обшей формулы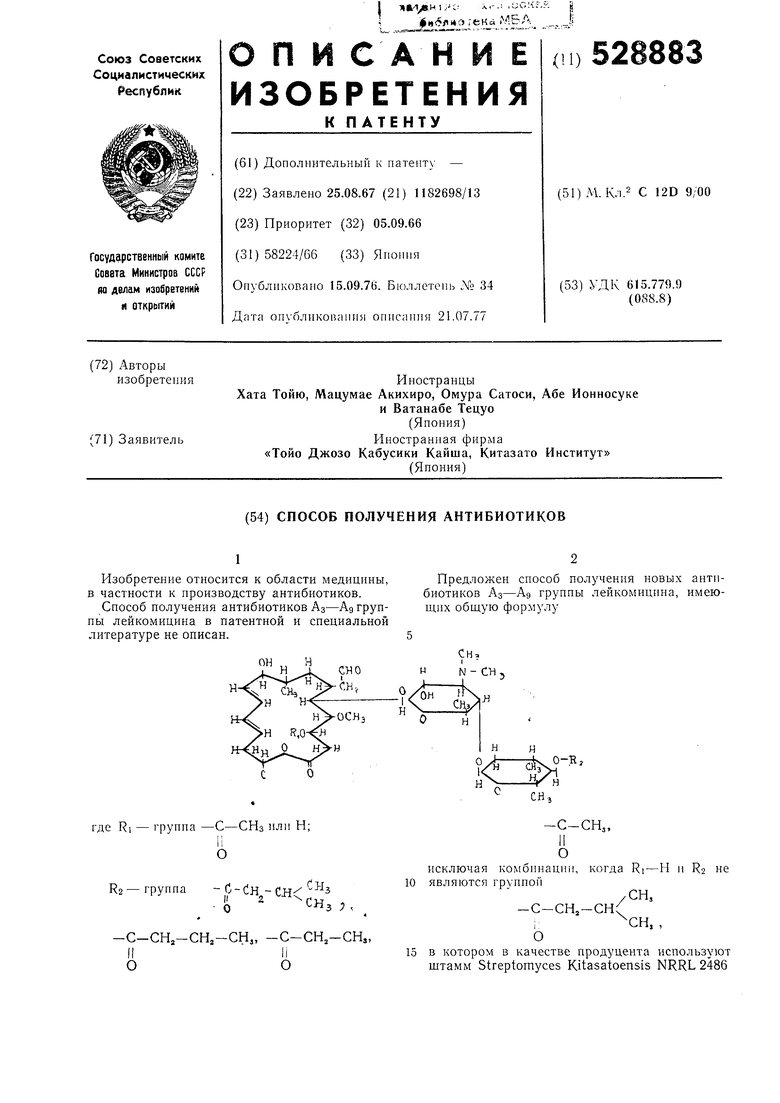




| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА | 1970 |
|
SU420187A3 |
| СПОСОБ ПОЛУЧЕНИЯ АВЕРМЕКТИНА | 1994 |
|
RU2109057C1 |
| Способ получения баумицина а и в | 1977 |
|
SU867318A3 |
| Способ получения компонентов А @ ,А @ ,А @ ,А @ ,В @ или В @ антибиотического комплекса ВВМ-1675 , обладающих антимикробным и противоопухолевым действием, штамм актиномицета АстINомаDURа VeRRUcoSoSpoRa АТСС 39334 и штамм актиномицета АстINомаDURа VeRRUcoSoSpoRa АТСС 39638, используемый для получения компонентов А @ ,А @ ,А @ ,А @ ,В @ или В @ антибиотического комплекса ВВМ-1675 , обладающих антимикробным и противоопухолевым действием | 1984 |
|
SU1344249A3 |
| Способ получения веществ, обладающих антипаразитарной активностью | 1977 |
|
SU716524A3 |
| Способ получения антибиотического комплекса | 1977 |
|
SU786914A3 |
| Штамм @ @ 12/3а-продуцент аклациномицинов @ и @ | 1982 |
|
SU1069433A1 |
| Антибиотик тавримицин и способ егопОлучЕНия | 1977 |
|
SU677497A1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИЧЕСКОГО КОМПЛЕКСА | 1972 |
|
SU352469A1 |
| Способ получения антибиотического комплекса а-35512 | 1977 |
|
SU751332A3 |


Авторы
Даты
1976-09-15—Публикация
1967-08-25—Подача